Енантіоселективне одержання похідних бензімідазолу та їх солей
Номер патенту: 92050
Опубліковано: 27.09.2010
Автори: Ван Вань-Цзюнь, Чжао Сяо-Лун, Цзян Бяо, Дун Цзя-Цзя
Формула / Реферат
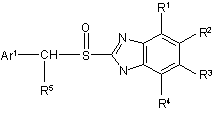
1. Спосіб одержання оптично активного енантіомера або збагаченої цим енантіомером форми сполуки формули (І)
 , (I)
, (I)
у якій залишки R1, R2, R3 і R4 незалежно один від одного являють собою водень, алкіл, алкоксигрупу, галоген, галогеналкоксигрупу, алкілкарбоніл, алкоксикарбоніл, оксазоліл або трифторалкіл, або сусідні залишки R1, R2, R3 і R4 можуть утворювати необов'язково заміщені циклічні структури, R5 являє собою атом водню або з'єднаний із залишком Аr1 з утворенням конденсованої циклічної системи, а Аr1 являє собою залишок формули
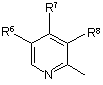 або
або 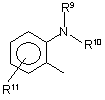 ,
,
у якій залишки R6, R7 і R8 незалежно один від одного являють собою водень, алкіл, алкілтіогрупу, алкоксигрупу, галогензаміщену алкоксигрупу, алкоксіалкоксигрупу, діалкіламіногрупу, піперидиногрупу, морфоліногрупу, галоген, фенілалкіл або фенілалкоксигрупу, або один із цих залишків з'єднаний із залишком R5 з утворенням конденсованої циклічної системи, залишки R9 і R10 незалежно один від одного являють собою водень, галоген або алкіл, а залишок R11 являє собою водень, галоген, трифторметил, алкіл або алкоксигрупу,
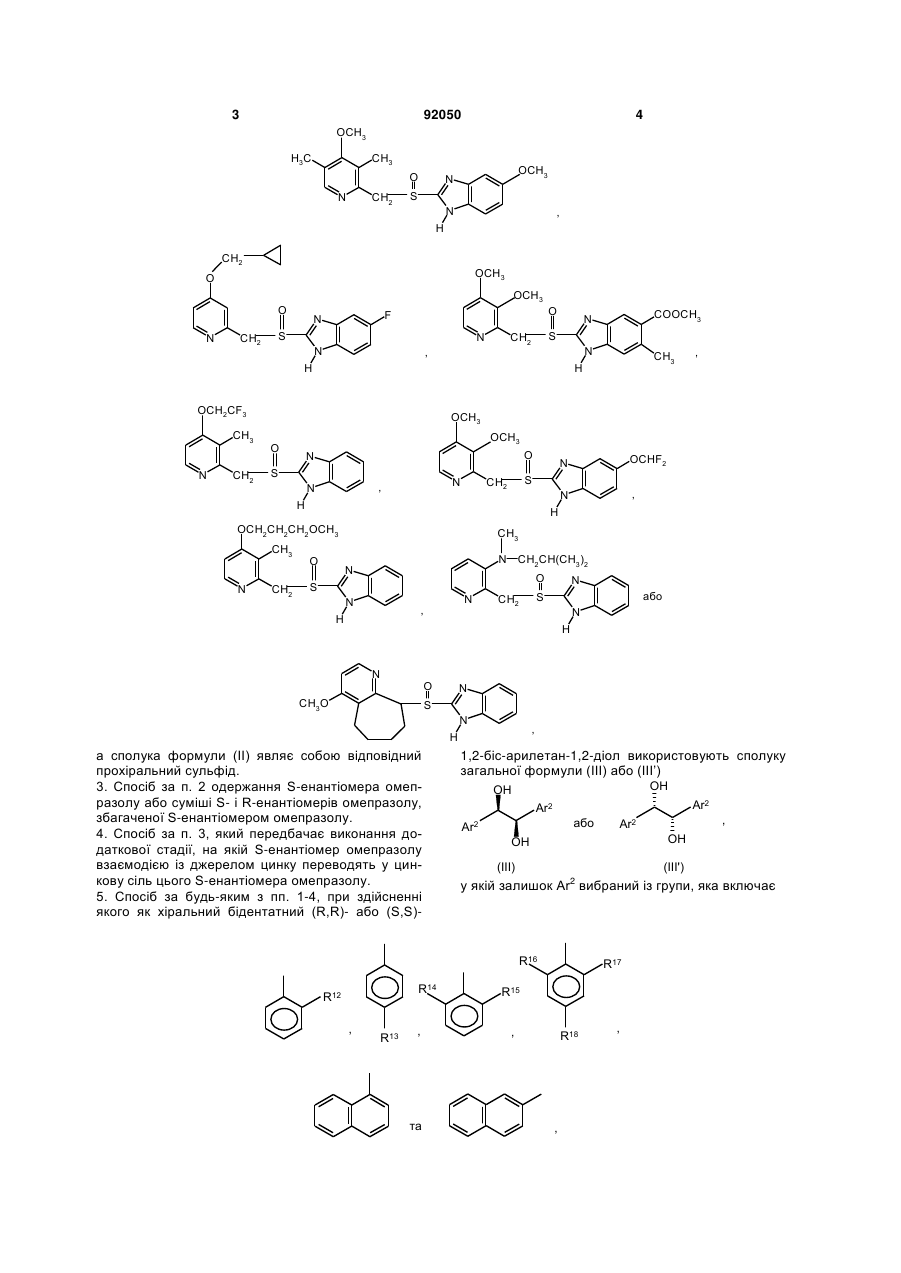
який полягає в тому, що прохіральний сульфід формули (II)
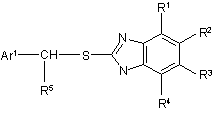 , (II)
, (II)
у якій залишки R1, R2, R3, R4, R5 та Аr1 мають зазначені вище значення,
окиснюють в органічному розчиннику відповідним окисником у присутності каталізатора, який відрізняється тим, що каталізатором є комплекс титану(ІV), одержуваний взаємодією сполуки титану(ІV) з хіральним бідентатним (R,R)- або (S,S)-1,2-біс-арилетан-1,2-діолом.
2. Спосіб за п. 1, який відрізняється тим, що сполука формули (І) являє собою будь-яку зі сполук з формулами
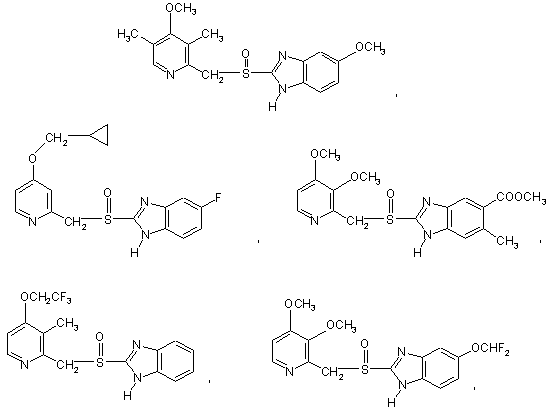
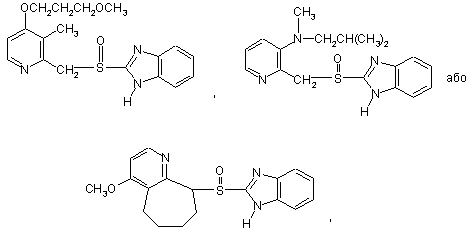
а сполука формули (II) являє собою відповідний прохіральний сульфід.
3. Спосіб за п. 2 одержання S-енантіомера омепразолу або суміші S- і R-енантіомерів омепразолу, збагаченої S-енантіомером омепразолу.
4. Спосіб за п. 3, який передбачає виконання додаткової стадії, на якій S-енантіомер омепразолу взаємодією із джерелом цинку переводять у цинкову сіль цього S-енантіомера омепразолу.
5. Спосіб за будь-яким з пп. 1-4, при здійсненні якого як хіральний бідентатний (R,R)- або (S,S)-1,2-біс-арилетан-1,2-діол використовують сполуку загальної формули (III) або (ІІI’)
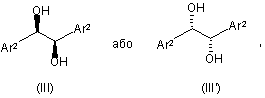
у якій залишок Аr2 вибраний із групи, яка включає
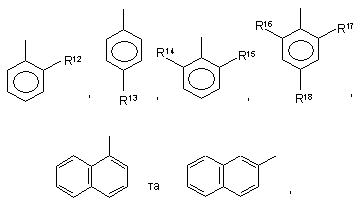
де залишки R12-R18 незалежно один від одного вибрані із групи, яка включає водень, алкіл, алкоксигрупу, карбоксилатний залишок, галоген, феніл, трифторметил та NO2.
6. Спосіб за п. 5, де залишки R14 і R15 незалежно один від одного вибирають із групи, яка включає водень, алкіл, алкоксигрупу й галоген, а залишки R16, R17 і R18 незалежно один від одного вибирають із групи, яка включає водень і алкіл.
7. Спосіб за п. 6, де залишки R14 і R15 є ідентичними, а залишки R16, R17 і R18 також мають ідентичні значення.
8. Спосіб за п. 7, де залишок R12 являє собою атом брому.
9. Спосіб за п. 8, при здійсненні якого як (R,R)- або (S,S)-1,2-біс-арил-1,2-діол використовують сполуку формули
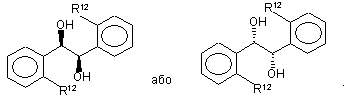
10. Спосіб за будь-яким з пп. 1-9, при здійсненні якого як сполуку титану(IV) використовують алкоксид титану(IV).
11. Спосіб за п. 10, при здійсненні якого як титанову сполуку використовують ізопропоксид титану(IV).
12. Спосіб за будь-яким з попередніх пунктів, при здійсненні якого хіральний бідентатний ліганд і прохіральний сульфід формули (II) використовують у співвідношенні між ними, що дорівнює 0,1:1.
13. Спосіб за будь-яким з попередніх пунктів, при здійсненні якого алкоксид титану(ІV) і прохіральний сульфід формули (II) використовують у молярному співвідношенні між ними, що дорівнює 0,05:1.
14. Спосіб за будь-яким з попередніх пунктів, при здійсненні якого реакцію проводять у присутності води.
15. Спосіб за будь-яким з попередніх пунктів, при здійсненні якого як окисник використовують пероксид водню, гідропероксид алкілу або гідропероксид арилалкілу.
16. Спосіб за будь-яким з попередніх пунктів, при здійсненні якого спочатку приготовляють каталізатор взаємодією хірального ліганду з алкоксидом титану(ІV) в органічному розчиннику, а потім до реакційної суміші додають прохіральний сульфід формули (ІІ).
17. Спосіб за будь-яким з попередніх пунктів, при здійсненні якого окиснення проводять при температурі близько -20 °С протягом 12-18 год.
18. Спосіб за будь-яким з попередніх пунктів, який полягає в тому, що
а) у реактор завантажують суміш хірального бідентатного (R,R)- або (S,S)-1,2-біс-арилетан-1,2-діолу й алкоксиду титану(ІV) у присутності органічного розчинника,
б) до реакційної суміші, одержаної на стадії а), додають воду,
в) до реакційної суміші, яка утворилася на стадії б), додають прохіральний сульфід формули (II),
г) до реакційної суміші, одержаної на стадії в), додають окисник,
д) до реакційної суміші, одержаної на стадії г), додають водний розчин аміаку,
е) до водної суміші, одержаної на стадії д), додають кислоту,
є) водну суміш екстрагують органічним розчинником,
ж) органічний розчин охолоджують і відфільтровують енантіомер сполуки формули (І), який випав в осад, та
з) при необхідності необхідний ізомер сполуки формули (І) переводять у цинкову сіль.
Текст
1. Спосіб одержання оптично активного енантіомера або збагаченої цим енантіомером форми сполуки формули (І) 3 92050 4 OCH3 H3C CH3 O N CH2 OCH3 N S N , H CH2 OCH3 O OCH3 O N CH2 O N S N N OCH2CF3 N CH2 , OCH3 OCH3 O O N S N , N N N CH2 , H OCH2CH2CH2OCH3 CH3 OCHF2 S CH2 H N CH3 H H CH3 COOCH3 S CH2 , N N F O CH3 N CH2CH(CH3)2 N O S N N , H N або S CH2 N H N O CH3O N S N , H а сполука формули (II) являє собою відповідний прохіральний сульфід. 3. Спосіб за п. 2 одержання S-енантіомера омепразолу або суміші S- і R-енантіомерів омепразолу, збагаченої S-енантіомером омепразолу. 4. Спосіб за п. 3, який передбачає виконання додаткової стадії, на якій S-енантіомер омепразолу взаємодією із джерелом цинку переводять у цинкову сіль цього S-енантіомера омепразолу. 5. Спосіб за будь-яким з пп. 1-4, при здійсненні якого як хіральний бідентатний (R,R)- або (S,S) 1,2-біс-арилетан-1,2-діол використовують сполуку загальної формули (III) або (ІІI’) OH OH Ar2 Ar2 або Ar2 OH OH (III) (III') у якій залишок Аr2 вибраний із групи, яка включає R16 R14 R12 , R13 , та , Ar2 R17 R15 , R18 , , 5 92050 де залишки R12-R18 незалежно один від одного вибрані із групи, яка включає водень, алкіл, алкоксигрупу, карбоксилатний залишок, галоген, феніл, трифторметил та NO2. 14 15 6. Спосіб за п. 5, де залишки R і R незалежно один від одного вибирають із групи, яка включає водень, алкіл, алкоксигрупу й галоген, а залишки R16, R17 і R18 незалежно один від одного вибирають із групи, яка включає водень і алкіл. 7. Спосіб за п. 6, де залишки R14 і R15 є ідентичними, а залишки R16, R17 і R18 також мають ідентичні значення. 8. Спосіб за п. 7, де залишок R12 являє собою атом брому. 9. Спосіб за п. 8, при здійсненні якого як (R,R)- або (S,S)-1,2-біс-арил-1,2-діол використовують сполуку формули 6 10. Спосіб за будь-яким з пп. 1-9, при здійсненні якого як сполуку титану(IV) використовують алкоксид титану(IV). 11. Спосіб за п. 10, при здійсненні якого як титанову сполуку використовують ізопропоксид титану(IV). 12. Спосіб за будь-яким з попередніх пунктів, при здійсненні якого хіральний бідентатний ліганд і прохіральний сульфід формули (II) використовують у співвідношенні між ними, що дорівнює 0,1:1. 13. Спосіб за будь-яким з попередніх пунктів, при здійсненні якого алкоксид титану(ІV) і прохіральний сульфід формули (II) використовують у молярному співвідношенні між ними, що дорівнює 0,05:1. 14. Спосіб за будь-яким з попередніх пунктів, при здійсненні якого реакцію проводять у присутності води. 15. Спосіб за будь-яким з попередніх пунктів, при здійсненні якого як окисник використовують пероксид водню, гідропероксид алкілу або гідропероксид арилалкілу. 16. Спосіб за будь-яким з попередніх пунктів, при здійсненні якого спочатку приготовляють каталізатор взаємодією хірального ліганду з алкоксидом титану(ІV) в органічному розчиннику, а потім до реакційної суміші додають прохіральний сульфід формули (ІІ). 17. Спосіб за будь-яким з попередніх пунктів, при здійсненні якого окиснення проводять при температурі близько -20 °С протягом 12-18 год. 18. Спосіб за будь-яким з попередніх пунктів, який полягає в тому, що а) у реактор завантажують суміш хірального бідентатного (R,R)- або (S,S)-1,2-біс-арилетан-1,2-діолу й алкоксиду титану(ІV) у присутності органічного розчинника, б) до реакційної суміші, одержаної на стадії а), додають воду, в) до реакційної суміші, яка утворилася на стадії б), додають прохіральний сульфід формули (II), г) до реакційної суміші, одержаної на стадії в), додають окисник, д) до реакційної суміші, одержаної на стадії г), додають водний розчин аміаку, е) до водної суміші, одержаної на стадії д), додають кислоту, є) водну суміш екстрагують органічним розчинником, ж) органічний розчин охолоджують і відфільтровують енантіомер сполуки формули (І), який випав в осад, та з) при необхідності необхідний ізомер сполуки формули (І) переводять у цинкову сіль. Даний винахід стосується нового способу одержання похідних бензімідазолу з хіральною сульфоксидною групою у формі чистих енантіомерів або у формі, збагаченій одним з обох енантіомерів у порівнянні з іншим з них. Винахід стосується також способу одержання солей індивідуальних енантіомерів похідних бензімідазолу з хіральною сульфоксидною групою. Винахід стосується насамперед способу одержання S-енантіомеру омепразолу (відомого також за назвою езомепразол) і його солей, насамперед цинкової солі Sенантіомеру омепразолу. Поняття "S-снантіомер омепразолу" і "езомепразол" використовується в даному описі як синоніми. Похідні бензімідазолу з хіральною сульфоксидною групою належать до відомих інгібіторів секреції кислоти шлункового соку, і багато сполук із цієї групи застосовуються як лікарські засоби для лікування захворювань шлунково-кишкового тракту, насамперед виразки шлунка. Як приклад таких відомих діючих речовин можна назвати омепразол, пантопразол, лансопразол і рабепразол. Ці діючі речовини завдяки наявності у них сульфок сидної групи є хіральними, і тому інтерес являє одержання подібних сполук у формі чистих енаптіомерів. У даний час на ринку широко пропонується насамперед S-енаптіомер омепразолу, тобто езомепразол, у вигляді його магнієвої солі. Розділення заміщених 2-(2піридинілметилсульфініл)-1Н-бензімідазолів на окремі енантіомери описано, наприклад, в DE 4035455, WO 94/27988 і WO 2004/002982. Дані публікації стосуються, зокрема, також розділення омепразолу на обидва його енантіомери. При розділенні енантіомерів описаними в цих публікаціях способами виходять із рацемата зазначених сполук, який взаємодією з відповідною оптично активною сполукою переводять у пару діастереомерів, які потім можна розділяти відомим шляхом. Виділення одного енантіомеру зі збагаченої ним суміші двох енантіомерів хіральних бензімідазольних сполук описано також в WO 97/02261. Подібним способам розділення рацемічної суміші властивий цілий ряд недоліків, які полягають у тому, що, поперше, непотрібний енантіомер доводиться звичайно направляти у відходи, а по-друге, розділен R12 OH R12 OH OH R12 або OH R12 . 7 92050 8 ня рацемічної суміші пов'язане із проведенням У даному винаході пропонується спосіб одерскладних та таких, що знижують вихід цільового жання оптично активного енантіомеру або збагапродукту, операцій. ченої цим енантіомером форми сполуки формули Відповідно до цього в даній галузі є цілий ряд (І) пропозицій, спрямованих на одержання індивідуальних енантіомерів похідних бензімідазолу з хіральною сульфоксидною групою шляхом хірального синтезу. Відносно цього можна послатися, наприклад, на публікацію WO 96/17076, у якій описане окиснення відповідних прохіральних сульфідів під дією мікроорганізмів до індивідуальних енантіомерів необхідних сульфідних сполук, або на публікацію у якій залишки R1, R2, R3 і R4 незалежно один WO 96/17077, у якій описане відновлення рацемічвід одного являють собою водень, алкіл, алкоксигних сульфонів під дією мікроорганізмів до необхідрупу, галоген, галогеналкоксигрупу, алкілкарбоніл, них стереоізомерів сульфоксидів. В обох зазначеалкоксикарбоніл, оксазоліл або галогеналкіл або них публікаціях мова йде, однак, про способи, які сусідні залишки R1, R2, R3 і R4 можуть утворювати передбачають використання мікроорганізмів, тоді необов'язково заміщені циклічні структури, R5 явяк відповідні індивідуальні енантіомери похідних ляє собою атом водню або з'єднаний із залишком бензімідазолу з хіральною сульфоксидною групою Аr1 з утворенням конденсованої циклічної системи, представляється більш доцільним одержувати а Аr1 являє собою залишок формули хімічним способом асиметричного синтезу. Подібний спосіб описаний у публікації WO 96/002535 і полягає в тому, що прохіральний сульфід піддають взаємодії з окисником у присутності каталізатора. Такий каталізатор являє собою титановий комплекс із діетилтартратом як бідентатний ліганд. Цьому способу, однак, властивий істотний недолік, який полягає в необхідності проведення реакції в дуже специфічних умовах. Так, у якій залишки R6 , R7 і R8 незалежно один від зокрема, реакцію звичайно необхідно проводити в одного являють собою водень, алкіл, алкілтіогруприсутності основи й у строго визначеній послідопу, алкоксигрупу, галогензаміщену алкоксигрупу, вності. Для перетворення титанового комплексу, алкоксіалкоксигрупу, діалкіламіногрупу, піперидинаприклад, обов'язкова присутність прохірального ногрупу, морфоліногрупу, галоген, фенілалкіл або сульфіду, а реакція повинна протікати при підвифенілалкоксигрупу або один із цих залишків з'єдщеній температурі і/або при підвищеній тривалоснаний із залишком R5 з утворенням конденсованої ті. Крім того, при здійсненні описаного в зазначеній циклічної системи, залишки R9 і R10 незалежно публікації способу використовують дуже специфіодин від одного являють собою водень, галоген чний окисник, а саме: гідропероксид кумолу. або алкіл, а залишок R11 являє собою водень, гаБільш новий спосіб асиметричного синтезу пологен, трифторметил, алкіл або алкоксигрупу. хідних бензімідазолу з хіральною сульфоксидною При здійсненні пропонованого у винаході спогрупою описаний у публікації WO 03/089408. Відсобу прохіральний сульфід формули (II) повідно до цієї публікації реакцію проводять у присутності основи й титанового або ванадієвого каталізатора з хіральним монодентатним лігандом. В принципі з рівня техніки відома множина способів асиметричного окиснення сульфідів до оптично активних сульфоксидів, і відносно цього можна послатися, наприклад, на публікацію в Journal of Organic Chemistry 63, 1998, ее. 93929395. Однак заздалегідь не можна передбачити, чи придатний будь-який із багатьох описаних загау якій залишки R1, R2, R3, R4, R5 і Ar1 мають залом способів асиметричного окиснення сульфідів значені вище значення, окислюють в органічному до оптично активних сульфоксидів і для одержанрозчиннику відповідним окисником у присутності ня необхідних заміщених бензімідазолів з хіралькаталізатора. Такий спосіб відрізняється тим, що ною сульфоксидною групою і чи буде він мати пекаталізатором є комплекс титану(ІV), одержуваний реваги перед відомими способами. Сказане взаємодією сполуки титану(ІV) з хіральним біденстосується насамперед асиметричного синтезу татним (R,R)- або (S,S)-1,2-бiс-арилетан-1,2індивідуальних енантіомерів омепразолу, насамдіолом. перед езомепразолу. Хіральний бідентатний (R,R)- або (S,S)-1,2-бiсВиходячи з вищевикладеного, у даній галузі арилетан-1,2-діол переважно являє собою сполуку зберігається потреба в розробці інших способів загальної формули (III) або (III') одержання індивідуальних енантіомерів похідних бензімідазолу з хіральною сульфоксидною групою без недоліків, властивим відомим з рівня техніки способам. 9 92050 10 атомами галогену. Атоми галогену можуть бути ідентичними або різними й розташовуватися біля одного або біля декількох атомів вуглецю. Кращі ідентичні атоми галогену, які (якщо це можливо з хімічної точки зору) зв'язані з одним і тим самим атомом вуглецю, як це має місце, наприклад, у випадку СF3-групи. Відповідно до даного винаходу під алкілкарбо2 у якій залишок Аr вибраний із групи, яка нільним залишком переважно мається на увазі включає алкіл, який має зазначені вище значення та містить функціональну карбонільну групу С=О. Відповідно до даного винаходу під алкоксикарбонілом мається на увазі алкоксигрупа, яка мас зазначені вище значення та містить карбонільну групу С=О. Відповідно до даного винаходу під арилом переважно мається на увазі фенільна або 1- або 2нафтильна група. Арил необов'язково може бути заміщений одним-трьома замісниками, насамперед зазначеними вище атомами галогену, нітрогрупою, алкілом і зазначеною вище алкоксигрупою. 12 18 де залишки R –R незалежно один від одного Відповідно до даного винаходу під алкілтіогрувибрані із групи, яка включає водень, алкіл, алкокпою переважно мається на увазі алкіл, який має сигрупу, карбоксилатний залишок, галоген, феніл, зазначені вище значення та містить тіогрупу. трифторметил і NO2. Відповідно до даного винаходу під алкоксіалВідповідно до даного винаходу під алкілом пекоксигрупою переважно мається на увазі алкоксигреважно мається на увазі С1-С20 алкільний залирупа, яка має зазначені вище значення та заміщешок, більш краще С1-С10 алкільний залишок, особна зазначеною вище алкоксигрупою. ливо краще С1-С6 алкільний залишок, такий як Відповідно до даного винаходу під діалкіламіметильна, етильна, ізопропільна, н-пропільна, нногрупою мається на увазі аміногрупа, заміщена бутильна, ізобутильна та трет-бутильна група. двома зазначеними вище алкільними групами. Відповідно до даного винаходу під алкоксигруВідповідно до даного винаходу під фенілалкіпою переважно мається на увазі алкоксильний лом, відповідно фснілалкоксигрупою маються на залишок з 1-20, більш краще з 1-10, насамперед з увазі алкіл, відповідно алкоксигрупа, які мають 1-6, атомами вуглецю, такий як метокси-, етокси-, зазначені вище значення та заміщені фенільною ізопропокси-, н-пропокси-, н-бутокси-, ізобутоксигрупою. та трет-бутоксигрупа. Відповідно до даного винаходу під карбоксиВідповідно до даного винаходу під галогеном латним залишком переважно мається на увазі замається на увазі атом галогену, насамперед атом лишок карбонової кислоти з 1-10, більш краще з 1фтору, хлору, брому або йоду, особливо кращі з 6, особливо краще з 1-4, атомами вуглецю. яких атоми фтору. Відповідно до даного винаходу під арилалкіВідповідно до даного винаходу під галогеналлом переважно мається на увазі алкіл, який має коксигрупою переважно мається на увазі алкоксигзазначені вище значення та заміщений зазначерупа, яка має зазначені вище значення та заміщеним вище арилом. на одним або декількома, насамперед 1-5, більш Оскільки відповідно до даного винаходу заликраще 1-3, особливо краще 1, 2 або 3, зазначенишки можуть утворювати циклічні структури або ми вище атомами галогену. Атоми галогену моконденсовані циклічні системи, такі залишки пережуть бути ідентичними або різними й розташовуважно замикають вуглецевий цикл із 5-10, більш ватися біля одного або біля декількох атомів краще з 5, 6 або 7, атомами вуглецю, який необовуглецю. Кращі ідентичні атоми галогену, які (якщо в'язково може бути заміщений. це можливо з хімічної точки зору) зв'язані з одним і Оскільки відповідно до винаходу відповідна тим самим атомом вуглецю, як це має місце, наструктурна одиниця може бути заміщена, як її заприклад, у випадку СF3-групи. місник кращий, якщо не зазначено інше, зазначеВідповідно до даного винаходу під галогеналний вище атом галогену С1-С6 алкільної групи або кілом переважно мається на увазі алкіл, який має С1-С6 алкоксигрупи. зазначені вище значення, заміщений одним або Особливо кращою сполукою формули (І) є віддекількома, насамперед 1-5, більш краще 1-3, повідно до винаходу сполука формули особливо краще 1, 2 або 3, зазначеними вище 11 Особливо кращою сполукою формули (І) є відповідно до винаходу омепразол, пантопразол, лансопразол або рабепразол. Найбільш кращий з них омепразол. Відповідно до цього відповідно до одного з особливо кращих варіантів здійснення винаходу, він стосується способу одержання енантіомеру омепразолу і його солей або суміші обох енантіомерів омепразолу, у якій один енантіомер є присутнім у більшій кількості, ніж інший з них. Винахід стосується насамперед способу одержання езомепразолу і його солей, насамперед цинкової солі езомепразолу. Надалі винахід більш докладно розглянуто в основному на прикладі омепразолу. Однак такі пояснення рівною мірою справедливі й відносно інших сполук формули (І). У залишках Аr2 залишок R12 особливо краще являє собою алкіл, який має зазначені вище значення або галоген, який має зазначені вище значення, насамперед атом брому. Залишок R13 являє собою насамперед алкіл, який мас зазначені вище значення, галоген, який має зазначені вище значення, насамперед атом брому, або алкоксигрупу, яка має зазначені вище значення, особливо краще алкільний залишок з 14 атомами вуглецю або атом брому. Залишки R14 і R15 переважно ідентичні й вибрані із групи, яка включає атом водню та галоген, алкіл і алкоксигрупу, які мають зазначені вище значення. 92050 12 Залишки R16, R17 і R18 також переважно ідентичні й більш краще являють собою атом водню або алкіл, який має зазначені вище значення. Особливо кращий (R,R)- або (S,S)-1,2-бiсарилетил-1,2-діол, тобто сполука формули (R,R)- або (S,S)-1,2-бiс-арилетил-1,2-діол, використовуваний відповідно до винаходу як хіральний ліганд титанової сполуки, можна одержувати відомим шляхом, відповідно ця сполука є у продажу. Зазначені сполуки можна одержувати насамперед асиметричним дигідроксилуванням (Е)стильбену або відповідних похідних стильбену методом, описаним, наприклад, в Chem. Rev. 94, 1994, с. 2483, або в Chirality 13, 2001, ее. 258-265. Обидві ці публікації в частині, яка стосується одержання діолів, включені в даний опис як посилання. Відповідно до винаходу каталізатор приготовляють in situ взаємодією відповідної титанової сполуки, насамперед алкоксиду титану(ІV), переважно ізопропоксиду титану(ІV) (Ті(і-РrО)4), з відповідним хіральним діолом формули (III), відповід 13 92050 14 0,4:1, більш краще біля 0,1:1. Молярне ж співвідно (III ). Взаємодію сполуки титану(ІV) з діолом ношення між титановою сполукою й сульфідом проводять в органічному розчиннику, переважно в формули (II) відповідно до винаходу переважно присутності води, а більш краще використовувати повинно становити від 0,01:1 до 0,2:1, більш краще для приготування каталізатора той же розчинник, біля 0,05:1. що пізніше використовують для окиснення. При Відповідно до винаходу переважно приготовцьому мова йде насамперед про галогензаміщені ляти каталізатор, так само як і проводити наступне або незаміщені алкіл- і арилвуглеводні, такі як меенантіоселективне каталітичне окиснення в присутиленхлорид, хлороформ, чотирихлористий вугтності води при молярному співвідношенні між лець, гексан і толуол. Найбільш кращий як органіводою та прохіральним сульфідом формули (II) чний розчинник толуол. Каталізатор бажано переважно від 0,01:1 до 2:1, більш краще біля 1:1. приготовляти при температурі в інтервалі від 20 до Кількість використовуваного окисника не відіг50°С, насамперед від 20 до 25°С. Тривалість прорає істотної ролі, однак переважно використовувацесу одержання каталізатора становить від 1 до ти окисник у кількості, при якому співвідношення 60 хв, переважно від 10 до 20 хв. між ним і прохіральним сульфідом формули (II) Відповідно до винаходу переважно спочатку становить від 0,5:1 до 3:1, більш краще біля 2:1. приготовляти in situ каталізатор, а потім додавати Після завершення процесу енантіоселективнодо реакційної суміші, яка містить каталізатор, прого окиснення прохірального сульфіду формули (II) хіральний сульфід формули (II), насамперед сподо хірального сульфоксиду формули (І) реакційну луку формули суміш в принципі можна піддавати будь-якій прийнятній переробці, однак при створенні винаходу було встановлено, що при переробці реакційної суміші особливим способом сульфоксид формули (І), насамперед езомепразол, утворюється у вигляді основи, яку потім можна особливо простим шляхом переводити в його солі. Після завершення процесу енантіоселективного каталітичного окиснення сполуки формули (II) і на завершення додавати окисник. до сполуки формули (І) реакційну суміш краще В іншому кращому варіанті каталізатор приговідповідно до винаходу обробляти водним основтовляють у присутності прохірального сульфіду ним розчином. Як такий водний основний розчин формули (II), тобто, наприклад, спочатку в реактор краще використовувати водний розчин аміаку. завантажують титанову сполуку, потім додають Після додавання розчину аміаку додають кислоту, прохіральний сульфід формули (II) і на завершеняк таку можна використовувати неорганічну кислоня додають хіральний діол. У цьому варіанті окисту у вигляді водного розчину або органічну кислоник також переважно додавати в останню чергу. ту, краще органічну кислоту, особливо краще оцНаступне окиснення краще проводити в тій же тову кислоту. Величину pH водного розчину краще суміші розчинників, яку використовували для припри цьому встановлювати на значення в межах від готування каталізатора, тобто також у присутності 5 до 8, особливо краще від 6 до 7,5. Одержаний води в органічному розчиннику, переважно вибратаким шляхом водний розчин екстрагують органічному із групи галогензаміщених або незаміщених ним розчинником, як такий краще використовувати алкіл- і арилвуглеводнів, таких як метиленхлорид, галогензаміщені або незаміщені алкіл- або арилвухлороформ, чотирихлористий вуглець, гексан і глеводні й кетони, такі як метиленхлорид, хлоротолуол, кращий з яких толуол. форм, чотирихлористий вуглець, гексан, толуол, Енантіоселективну каталітичну реакцію краще ацетон, бутанон і метилізобутилкетон. Можливе проводити при температурі в інтервалі від -78 до використання й інших звичайних органічних екст25°С, більш краще в інтервалі від біля -20 до 0°С, рагентів. Кращим розчинником для екстрагування насамперед при температурі біля -20°С. Тривас метилізобутилкетон. лість енантіоселективного каталітичного окисненПри створенні винаходу несподівано було ня становить, як правило, від 2 до 24 год, перевавстановлено, що сполука формули (І), насамперед жно від 12 до 18 год. (6)-омепразол (езомепразол), при охолодженні Відповідно до винаходу можна застосовувати органічного екстрагента випадає в осад у чистому будь-який придатний для цієї мети окисник, однак вигляді. Переважно при цьому охолоджувати екстособливо краще використовувати як окисник перорагуючий розчин до температури в інтервалі від ксид водню, гідропероксид алкілу або арилалкілу, 78 до 25 °С, більш краще в інтервалі від -20 до найбільш краще гідропероксид трет-бутилу. Краще 0°С, наприклад, до температури біля -10°С, у реж у кожному разі не використовувати як окисник зультаті чого необхідний енантіомер сполуки форгідропероксид кумолу. мули (І) випадає при цьому у вигляді твердої реПропоноване у винаході енантіоселективне човини у формі вільної основи. каталітичне окиснення доцільно проводити без Таким у принципі простим шляхом вдається додавання будь-якої основи. одержувати насамперед S-енантіомер омепразолу При здійсненні пропонованого у винаході споз дуже гарним виходом і високою оптичною чистособу кількості каталізатора й прохірального сультою. При наявності в одержаному зазначеним фіду формули (II) краще вибирати з таким розрашляхом продукті залишків небажаного енантіомехунком, щоб молярне співвідношення між ру сполуки формули (І), їх для підвищення ступеня хіральним бідентатним лігандом і прохіральним сульфідом формули (II) становило від 0,02:1 до 15 92050 16 оптичної чистоти продукту можна відокремлювати звичайним способом. Звичайно необхідний енантіомер, насамперед при одержанні езомепразолу, утворюється у вигляді твердої речовини, яка являє собою суміш аморфного й кристалічного продуктів. Оскільки пропонований у винаході спосіб з пег) до цієї суміші додають окисник, насамперед редбаченою при його здійсненні кращою процедугідропероксид алкілу або арилалкілу, найбільш рою переробки реакційної суміші дозволяє одеркраще гідропероксид дибутилу, жувати необхідний ізомер сполуки формули (І) у д) додають водний основний розчин, насампеформі вільної основи у вигляді твердої речовини, ред водний розчин аміаку, може виявитися найбільш кращим таку основу е) до цієї суміші додають кислоту, насамперед переводити в її сіль. У цьому полягає особлива органічну кислоту, таку як оцтова кислота, переперевага пропонованого у винаході способу перед важно до досягнення значення pH у межах від 5 до відомими з рівня техніки способами, якими одер8, особливо краще від 6 до 7,5, жання визначеної солі езомепразолу, описане, є) водну суміш екстрагують відповідним органаприклад, в WO 98/28294, можливо лише за умонічним розчинником, ви високих витрат і, зокрема, полягає в розчиненні ж) органічний розчин охолоджують і відфільтутвореної з лужним металом солі езомепразолу у ровують енантіомер сполуки формули (І), який воді, екстракції нейтрального езомепразолу оргавипав в осад, насамперед езомепразол, і нічним розчинником шляхом зниження значення з) при необхідності зазначений енантіомер пеpH додаванням водорозчинної кислоти, випарюреводять у сіль, насамперед цинкову сіль. ванням розчинника до одержання висококонцентНижче винахід більш докладно пояснюється рованого розчину та додаванні речовини, яка не є на прикладах. розчинником, з одержанням у результаті езомепПриклад 1 разолу у формі основи у вигляді твердої речовини. Одержання S-омепразолу Пропонований же у винаході спосіб дозволяє проДо розчину (R,R)-1,2-бiс-(2-бромфеніл)етанстим шляхом безпосередньо одержувати в ре1,2-діолу (12 мг, 0,032 ммоль) у толуолі (2 мл) при зультаті відповідної переробки реакційної суміші 25°С додавали тетраізопропоксид титану (4,5 мг, після завершенні енантіоселективного каталітич0,016 ммоль). Розчин перемішували протягом 10 ного окиснення відповідного сульфіду до сульфокхв, додавали воду (5,7 мг, 0,32 ммоль) і перемішусиду вільну основу у вигляді твердої речовини. вання продовжували ще протягом 10 хв. Потім до Потім таку вільну основу можна звичайним шлярозчину додавали 5-метокси-2-[[(4-метокси-3,5хом переводити в одну з необхідних солей, на кондиметил-2-піридиніл)метил]тіо]-1Н-бензімідазол кретний тип яких у принципі не накладається ні(105 мг, 0,32 моль) і температуру встановлювали яких особливих обмежень. При цьому можна на рівні -20°С. Далі повільно додавали гідроперокнасамперед назвати натрієву, магнієву, літієву, сид трет-бутилу (70%-вий, 96 мкл, 0,064 ммоль). калієву, кальцієву й четвертинну амонієву солі, а Після витримування протягом 12 год при -20°С також піперидинову сіль і насамперед цинкову розчин тричі екстрагували водним гідроксидом сіль. Цинкову сіль езомепразолу відповідно до амонію (12,5%-вий NH3, 3 5 мл). Потім до об'єднавинаходу особливо краще одержувати шляхом них водних екстрактів додавали метилізобутилкеобробки езомепразолу відповідним джерелом цинтон (5 мл). Після цього pH водної фази встановку. До таких кращих джерел цинку належать ацелювали на необхідне значення додаванням тат цинку, бромід цинку, гідроксид карбонату циноцтової кислоти, водну фазу відокремлювали й ку, хлорид цинку, трифторметансульфонат цинку, екстрагували її додатковою кількістю метилізобунітрат цинку, діетилцинк і сульфат цинку, з яких тилкетону (5 мл). Органічний розчин залишали найбільш кращі діетилцинк і хлорид цинку, насамстояти на ніч в охолодженому до -10°С стані, осаперед діетилцинк. джуючи таким шляхом зазначену в заголовку нейВідповідно до цього в найбільш кращому варітральну форму S-омепразолу у твердому вигляді анті здійснення винаходу в ньому пропонується (99 мг, вихід 90%). Енантіомерний надлишок Sспосіб одержання езомепразолу або солі езомепомепразолу складав 94%. Після очищення метиліразолу, насамперед цинкової солі езомепразолу, зобутилкетоном одержали S-омепразол з енантіоякий полягає в тому, що мерним надлишком більше 99%. а) у реактор завантажують (R,R)-1,2-бісПриклад 2 арилетил-1,2-діол, насамперед (R,R)-1,2-біс-(2Одержання R-омепразолу бромфеніл)етан-1,2-діол, разом з алкоксидом тиДо розчину (S,S)-1,2-біс-(2-бромфеніл)етантану(ІV), насамперед з тетраізопропоксидом тита1,2-діолу (12 мг, 0,032 ммоль) у толуолі (2 мл) при ну, в органічному розчиннику, 25°С додавали тетраізопропоксид титану (4,5 мг, б) до цієї реакційної суміші додають воду, 0,016 ммоль). Розчин перемішували протягом 10 в) до одержаної на стадії б) реакційної суміші хв, додавали воду (5,7 мг, 0,32 ммоль) і перемішудодають відповідний сульфід загальної формули вання продовжували ще протягом 10хв. Потім до (II), насамперед сполуку формули розчину додавали 5-метокси-2-[[(4-метокси-3,5диметил-2-піридиніл)метил]тіо]-1Н-бензімідазол (105 мг, 0,32 моль) і температуру встановлювали на рівні -20°С. Далі повільно додавали гідроперок 17 92050 18 сид трет-бутилу (70%-вий, 96 мкл, 0,064 ммоль). тним холодильником. Охолоджену реакційну суПісля витримування протягом 12 год при -20°С міш зливали в 1-молярну розведену водну соляну розчин тричі екстрагували водним гідроксидом кислоту й продукт екстрагували гексаном. Об'єдамонію (12,5%-вий NH3, 3x5 мл). Потім до об'єднанані екстракти промивали водою й розчином (куних водних екстрактів додавали метилізобутилкехонної) солі, сушили над сульфатом натрію, фільтон (5 мл). Після цього pH водної фази встановтрували й фільтрат упарювали на ротаційному лювали на необхідне значення додаванням випарнику з одержанням у результаті 6,2 г (97%) оцтової кислоти, водну фазу відокремлювали й сполуки 2. Після перекристалізації із суміші, що екстрагували її додатковою кількістю метилізобумістила 5% толуолу й 95% етанолу, одержали тилкетону (5 мл). Органічний розчин залишали сполуку 2 у вигляді голчастих кристалів білого костояти на ніч в охолодженому до -10°С стані, осальору. джуючи таким шляхом зазначену в заголовку ней(1R,2R)-1,2-бiс(2-бромфеніл)етан-1,2-діол тральну форму R-омепразолу у твердому вигляді. Енантіомерний надлишок R-омепразолу складав 93%. Приклад 3 Одержання цинкової солі езомепразолу В 10 мл тетрагідрофурану при 5-годинному перемішуванні розчиняли езомепразол (1г, 2,9 ммоль) і повільно додавали 2,9 мл діетилцинку (1молярний розчин в гексані). Одержану суміш заВ 1-літрову тригорлу колбу спочатку поміщали лишали перемішуватися на ніч при температурі воду (180 мл) і 2-метилпропан-2-ол (180 мл), а навколишнього середовища. Потім додавали 10 потім додавали метансульфонамід (3,39 г, 0,0419 мл дистильованої води, осад, що випав відфільтмоль) і суміш каталізаторів асиметричного дигідровували й промивали дистильованою водою. роксилування AD-mix- (50,2 г). Суміш, що утвориТаким шляхом одержували 1 г (91%) зазначеної в лася, перемішували механічною мішалкою до повзаголовку сполуки. ного розчинення всіх твердих речовин. Потім Приклад 4 (Одержання лігандів каталізатора) колбу охолоджували до 0°С і додавали до її вмісту (Е)-2,2-дибромстильбен дибромстильбен 2 (12,0 г, 32,3 ммоль). Далі реакційну суміш протягом 72 год інтенсивно перемішували з витримуванням при температурі в інтервалі від 0 до 3°С. Потім додавали сульфід натрію (54 год, 0,439 моль) і суміш залишали перемішуватися на ніч. Після цього додавали дихлорметан (350 мл) і фази розділяли. Водний шар екстрагували дихлорметаном (3x175 мл), об'єднані органічні шари промивали 2-молярним розчином КОН (30 мл), сушили (MgSO4) і леткі речовини випарювали 4,4 мл (7,4 г, 40 ммоль) жовтої суспензії хлопри зниженому тиску. Залишок очищали експресриду титану (ІV) в 150мл тетрагідрофурану перехроматографією шляхом елюювання сумішшю мішували магнітною мішалкою на льодяній бані в діетиловий ефір/гексан і потім перекристалізовуатмосфері азоту. Потім обережно додавали 5 г (77 вали (із суміші гексан/дихлорметан у співвідноммоль) пилоподібного цинку. Після цього додавашенні 1,1:1, 92 мл) з одержанням у результаті діоли 7 г (38 ммоль) альдегіду 1 в 50 мл тетрагідролу 3 (12,5 г, 94 %) у вигляді голчастих кристалів. фурану й суміш протягом 8 год нагрівали зі зворо Комп’ютерна верстка В. Мацело Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюEnantioselective preparation of benzimidazole derivatives and their salts
Автори англійськоюJiang Biao, Zhao Xiao-Long, Dong Jia-Jia, Wang Wan-Jun
Назва патенту російськоюЭнантиоселективное получение производных бензимидазола и их солей
Автори російськоюЦзян Бяо, Чжао Сяо-Лун, Дун Цзя-Цзя, Ван Вань-Цзюнь
МПК / Мітки
МПК: C07D 235/28, C07D 401/12
Мітки: солей, енантіоселективне, одержання, похідних, бензимідазолу
Код посилання
<a href="https://ua.patents.su/9-92050-enantioselektivne-oderzhannya-pokhidnikh-benzimidazolu-ta-kh-solejj.html" target="_blank" rel="follow" title="База патентів України">Енантіоселективне одержання похідних бензімідазолу та їх солей</a>
Попередній патент: Спосіб безперервного розливання тонких металевих штаб і установка безперервного розливання
Наступний патент: Спосіб одержання колективного концентрату для вилучення благородних металів
Випадковий патент: Спосіб виготовлення порошкового дроту