Спосіб одержання празугрелю
Формула / Реферат
1. Спосіб одержання празугрелю, 5-[2-циклопропіл-1-(2-фторфеніл)-2-оксоетил]-4,5,6,7-тетрагідротієно[3,2-с]піридин-2-ілацетат, формули І
 , I
, I
який відрізняється тим, що сполука формули IV
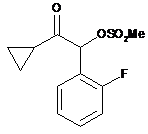 IV
IV
взаємодіє із сполукою формули III
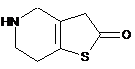 III
III
у формі солі з хлорводневою кислотою або п-толуолсульфоновою кислотою, з утворенням сполуки формули II
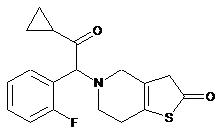 , II
, II
яку потім перетворюють на сполуку формули І шляхом ацилювання безпосередньо у реакційній суміші без виділення, одержаний празугрель потім кристалізують безпосередньо з реакційної суміші і потім очищають кристалізацією з органічного розчинника з доданим ацилювальним агентом.
2. Спосіб за п. 1, який відрізняється тим, що неочищений празугрель розчиняють у полярному апротонному розчиннику при температурі від 10 до 50 °C, до розчину додають ацилювальний агент і потім кристалізують празугрель, додаючи водний розчин дигідрофосфату калію.
3. Спосіб за п. 2, який відрізняється тим, що полярний апротонний розчинник вибирають з нітрилів органічних кислот, етерів та циклічних етерів.
Текст
Реферат: Винахід належить до способу одержання празугрелю, використовуючи метансульфонат 3циклопропіл-1-(2-фторфеніл)-3-оксопропілу для алкілування 2-оксо-тієнотетрагідропіридину, який може знаходитись у формі солі, наприклад, з хлорводневою кислотою або птолуолсульфоновою кислотою. Отриману сполуку формули II ацилювали, бажано ацетангідридом, бажано безпосередньо у реакційній суміші без виділення, та одержаний празугрель формули І після цього кристалізували безпосередньо у реакційній суміші. O N O F S O I UA 106595 C2 (12) UA 106595 C2 O N O F S II UA 106595 C2 5 10 15 20 Галузь винаходу Винахід стосується нового способу виготовлення 5-[2-циклопропіл-1-(2-фторфеніл)-2оксоетил]-4,5,6,7-тетрагідротієно[3,2-с]піридин-2-іл ацетату, відомого під незареєстрованою назвою празугрель, високої чистоти. Празугрель є добре відомою сполукою формули I, яка зменшує коагуляцію крові: Попередній рівень техніки Празугрель, спосіб його одержання та його застосування як сполуки проти агрегації для пацієнтів з ризиком обструкції кров'яних судин внаслідок згортання крові, вперше було описано у патенті EP 542411. Виготовлення празугрелю згідно з цим патентом показано на Схемі 1. Згідно з цим документом реагент Грігнарда, одержаний з 2-фторбензилброміду, (Xl), реагує у ефірі з циклопропілціанідом (X) з утворенням сполуки (IX). Сполука (IX) реагує з бромом у CCI4 або з N-бромсукцинімідом (NBS) в присутності дибензоїлпероксиду до бромпохідної (VIII), яку приєднують в присутності поташу до атому азоту сполуки (III), з утворенням сполуки (II). Сполука (II) перетворюється на вихідний празугрель (І) шляхом реагування з ацетангідридом в присутності NaH у DMF. Подібний спосіб можна вивести з більш раннього патенту EP 192 535, який показано на Схемі 2. 1 UA 106595 C2 5 10 15 Реакція тієнопіридин-2-ону (III) з трет-бутилдиметилсилілхлоридом (TBDMS-CI) у дихлорметані в присутності триетиламіну забезпечує одержання силілованого енолетеру (XII), який реагує зі сполукою (XIII), знову в присутності триетиламіну у дихлорметані, з утворенням сполуки (XIV). Кінцевий празугрель формули І після цього одержують з сполуки (XIV), починаючи з додаткового захисту використовуючи Et3N та наступне ацетилування ацетангідридом в присутності диметиламінопіридину. Окрім -галокетонів (VIII) та (XIII), іншою ключовою проміжною сполукою є 2-оксотієнотетрагідропіридин (III), який використовують у формі гідрохлориду на Схемі 1 та у формі тозилату на Схемі 2. Його одержання було описано фірмою Sanofi Company та починається з наявного на ринку 4,5,6,7-тетрагідротієно[3,2-с]піридину (XX); дивись Схему 3. Спочатку, атом азоту блокується реакцією трифенілметилхлориду у дихлорметані в присутності Et3N (96%) з одержанням захищеної сполуки (XIX). Цю сполуку (XIX) перетворюють на літієву сіль (XVIII), яка шляхом реагування з три-н-бутилборатом забезпечує одержання похідної (XVII), яку окислюють in-situ 30% перекисом водню до сполуки (XVI), яка миттєво гідролізується до тритільованого тієнопіридону (XV) (64 %). Цю стадію здійснюють у суміші THF та гексану при температурі від -40 °С до -20 °С. На останній стадії з тритільної групи знімають захист 98% мурашиною кислотою (90 °C, 1 година) (81%) та одержують бажану сполуку (III). 2 UA 106595 C2 5 10 15 У порівнянні з відомими способами спосіб винаходу представляє технологічно виконувану методику одержання, яка забезпечує одержання основи празугрелю високої чистоти. Він має простий підхід без використання захисних груп. Основа празугрелю формули І є нестійкою сполукою; вона перетворюється на сполуку формули Il за Схемою 5 при нагріванні, наприклад, під час кристалізації, тільки внаслідок її присутності у розчині. Одержання празугрелю формули І високої чистоти є основною передумовою промислової придатності способу одержання. Опис винаходу Винахід стосується нового способу одержання високочистого ацетату 5-[2-циклопропіл-1-(2фторфеніл)-2-оксоетил]-4,5,6,7-тетрагідротієно[3,2-с]піридин-2-ілу формули I, відомого під незареєстрованою назвою празугрель. Вихідна сполука формули IV взаємодіє зі сполукою формули III 3 UA 106595 C2 у формі солі, такої як гідрохлорид або n-толуолсульфонат, з одержанням сполуки формули II, 5 10 15 20 яку потім перетворюють, ацетилюючий агент. не виділяючи, на сполуку формули І, використовуючи Винахід також стосується очистки продукту формули І кристалізацією у розчиннику з додаванням ацетангідриду. Як розчинник використовують нітрили органічних кислот, етери та циклічні етери. Після додавання води або водного розчину неорганічної солі до цієї суміші, одержують високочистий празугрель формули І із вмістом сполуки формули Il до 0,2 %. Детальний опис винаходу Синтез винаходу коротко описано на наступній Схемі 4. Винахід стосується одержання празугрелю за способом, який використовує 3-циклопропіл-1(2-фторфеніл)-3-оксопропілметансульфонат (IV) для алкілування 2-оксотієнотетрагідропіридину (III), який може знаходитись у формі солі, наприклад, з хлорводневою або n-толуолсульфоновою кислотою. Отриману сполуку формули Il після цього ацилюють ацилувальним агентом безпосередньо у реакційній суміші не виділяючи, та після цього отриманий празугрель формули І кристалізують безпосередньо з реакційної суміші. 4 UA 106595 C2 5 10 15 20 25 30 35 40 45 50 Ацетангідрид або ацетилхлорид, наприклад, використовують як ацилувальні агенти. Ацетангідрид є найбільш бажаним. Празугрель є нестійкою сполукою; вона перетворюється на сполуку формули Il згідно з Схемою 5 при нагріванні, наприклад, протягом кристалізації, тільки внаслідок її присутності у розчині. Винахід також стосується очистки кристалізацією отриманого продукту формули I, у розчиннику з додаванням ацилувального агента, наприклад, ацетангідриду або ацетилхлориду. Ацетангідрид є найбільш бажаним. Полярні апротонні розчинники використовують як розчинники, наприклад, нітрили органічних кислот, етери та циклічні етери. Процес бажано здійснюють при температурі від -20 до +50 °С. Після додавання води або водного розчину неорганічної солі (наприклад, розчин гідрофосфату калію) до цієї суміші, одержують празугрель формули І високої чистоти. Додавання ацилувального агента зсуває рівновагу в сторону бажаного продукту (І) та попереджує утворення небажаного продукту деацилування. Вміст небажаного продукту формули Il становить менше ніж 0,2%, бажано менше ніж 0,1%, що є рівнем чистоти прийнятним для фармацевтичної сполуки. Цей спосіб очистки безперечно представляє значну технологічну перевагу, з огляду на те, що попередні способи забезпечували одержання продукту із значним вмістом домішок, особливо продукту деацилування формули II, вміст якого зазвичай становив більше ніж 3,4%. Спроби використання різних умов реакції, наприклад, різних температур та часу реакції. А також спроби використання різних розчинників для реакції та кристалізація не давали прийнятних результатів, як вказано особливо у прикладах 9, 10 та 11. Приклади Чистоту празугрелю у нижченаведених прикладах оцінювали за ВЕРХ хроматографії, використовуючи спосіб наведений у прикладі 6. Приклад 1 У тригорлу колбу ємністю 250 мл, оснащену магнітною мішалкою та термометром, закриту трубкою з хлоридом кальцію, додавали 12,22 г п-толуолсульфонату сполуки формули III та 40 мл ацетонітрилу. Протягом перемішування, 13,6 мл діізопропілетиламіну виливали у в'язку суспензію та суміш перемішували при кімнатній температурі до одержання розчину (5-10 хв.). Після цього, до колби додавали метансульфонат 3-циклопропіл-1-(2-фторфеніл)-3-оксопропілу + (сполука формули IV) (9,68 г) та 7,84 г Et4N Br. Після цього, отриману суміш перемішували при температурі від +22 до +25 °C протягом 4 -5 годин. Реакцію контролювали за допомогою ТШХ. Після зникнення вихідної сполуки до реакційної суміші додавали 10 мл Ac 2O та 50 мг диметиламінопіридину. Після цього реакційну суміш перемішували при температурі від +22 до +25 °C протягом ще 1,5-2 годин. Реакцію контролювали за допомогою ТШХ у такій самій системі. Після перетворення проміжної сполуки (II) реакційну суміш охолоджували до температури від -12 до -15 °C, додавали 25 мл 20 мM водного розчину KH2PO4. Суміш інокулювали та продукт залишали кристалізуватись перемішуючи при температурі від -12 до -15 °C протягом 1,5 години. Відділений продукт фільтрували з відсмоктуванням крізь скляний фільтр та скляний фільтр промивали 20 мл охолодженого етанолу. Продукт вільно висушували при кімнатній температурі. Одержували 4,06 г неочищеного продукту з чистотою 96,11% (ВЕРХ). 1 H ЯМР (250 МГц, CDCI3) (млн.ч.): 7,47 (ддд, J=14,7, 7,4, 1,7 Гц, 1Н), 7,31 (м, 1Н), 7,14 (м, 2Н), 6,26 (с, 1Н), 4,82 (с, 1Н), 3,51 (м, 2Н), 2,89 (м, 1Н), 2,79 (м, 3H), 4,30 (м, 1Н), 2,25 (с, 3H), 13 1,03 (м, 2H), 0,85 (м, 2Н); C ЯМР (250 МГц, CDCI3) (млн.ч.): 207,7, 167,7, 161.3 (д, JCF = 247,6 Гц), 149,5, 130,6 (д, JCF = 3,5 Гц), 129,9 (д, JCF = 8,4 Гц), 129,4, 125,8, 124.4 (д, JCF = 3,5 Гц), 122,1 (д, JCF =14,1 Гц), 115,8 (д, JCF = 22,9 Гц), 112,0, 71,6, 50,5, 48,4,25,0,20,6, 18,3,12,0, 11,4. Приклад 2 Празугрель, одержаний за прикладом 1 (4,06 г), розчиняли у 60 мл ацетонітрилу при кімнатній температурі. 2 мл Ac2O додавали до розчину та розчин перемішували при температурі від +22 до +25 °С протягом 1,5 години. Після цього, розчин охолоджували до температури від 5 UA 106595 C2 5 10 15 20 25 30 35 40 45 50 55 60 12 до -15 °С та додавали 30 мл 20 мМ водного розчину KH2PO4. Протягом перемішування продукт залишали для кристалізації при температурі від -12 до -15 °Спротягом 2,5 годин. Відділений продукт фільтрували крізь скляний фільтр та промивали сумішшю ацетонітрил:вода; 1:1. Продукт вільно висушували повітрям до одержання стійкої маси - 3,19 г очищеного празугрелю (78,6%); ВЕРХ 99,5%; сполука формули II: 0,07%. Приклад 3 Празугрель, одержаний за прикладом 1 (0,8 г), розчиняли у 11,8 мл ацетонітрилу при кімнатній температурі. 1 мл Ac2O додавали до розчину та розчин перемішували при кімнатній температурі протягом 10 хв. Після цього розчин охолоджували до температури від -10 до -15 °С, та додавали 6,5 мл 20 мМ водного розчину KH2PO4. Продукт залишали кристалізуватись перемішуючи при температурі від -12 до -15 °С протягом 1,5 години. Відділений продукт фільтрували крізь скляний фільтр та промивали сумішшю ацетонітрил:вода; 1:1. Продукт вільно висушували повітрям до одержання стійкої маси - 0,55 г очищеного празугрелю (68,75%); ВЕРХ 99,11%; сполука формули II: 0,60%. Приклад 4 Празугрель одержаний за прикладом 1 (0,373 г) розчиняли у 5,5 мл ацетонітрилу при кімнатній температурі. Прозорий розчин охолоджували до температури -5 °С. 3 мл 20 мМ водного розчину KH2PO4 додавали до розчину та продукт кристалізували при цій температурі протягом 1,5 години. Відділену фракцію фільтрували крізь скляний фільтр та промивали мінімальною кількістю суміші ацетонітрил:вода; 1:1. Одержували 310,7 мг (83,3%) очищеного празугрелю з вмістом 98,07%; сполука формули II: 1,7%. Приклад 5 Празугрель, одержаний за прикладом 1 (0,373 г), розчиняли у 3,0 мл ацетону при кімнатній температурі. Прозорий розчин охолоджували до температури -3 °C. 1 мл 20мМ водного розчину KH2PO4 додавали до розчину та продукт кристалізували при температурі від -5 до 0 °С протягом 1,5 години. Відділену фракцію фільтрували крізь скляний фільтр та промивали мінімальною кількістю суміші ацетонітрил:вода; 1:1. Одержували 336 мг (90,1%) очищеного празугрелю з вмістом 98,127%; сполука формули II: 1,61%. Приклад 6 ВЕРХ здійснювали на октадециловій колонці (250x4,6 мм; 5 мкм) при температурі 30 °С з УФ виявленням при 228 нм. Для розділення використовували градієнт елюювання фосфатним буфером (0,01 M KH2PO4 рН 2,2) з ацетонітрилом, зі швидкістю потоку 1,0 мл/хв. з наступним градієнтом: 0 хв. 80% буфера; 40 хв. 10% буфера (лінійний градієнт); 45 хв. 10% буфера. Час урівноваження колонки становив 10 хв. Об'єм ін'єкції становив 10 мкл. Фактор ємності празугрелю становив 4,3. Зразок готовили шляхом розчинення відповідної сполуки у ацетонітрилі до концентрації 1 мг/мл. Приклад 7 Празугрель, одержаний за прикладом 1 (200 мг), розчиняли у 2 мл тетрагідрофурану при кімнатній температурі. 0,25 мл Ac2O додавали до розчину та розчин перемішували при температурі від +22 до +25 °C протягом 2 годин. Після цього розчин охолоджували до температури від -5 до -2 °С; додавали 1 мл 20 мМ водного розчину KH 2PO4. Продукт залишали кристалізуватись перемішуючи при температурі від -5 до -2 °С протягом 2 годин. Відділений продукт фільтрували крізь скляний фільтр та промивали розчином THF:вода; 1:1. Продукт вільно висушували повітрям до досягнення постійної маси - одержували 75 мг очищеного празугрелю з вмістом 99,45%. Приклад 8 Празугрель, одержаний за прикладом 1 (200 мг), розчиняли у 2 мл 1,4-діоксану при кімнатній температурі. 0,25 мл Ac2O додавали до розчину та розчин перемішували при температурі від +22 до +25 °C протягом 2 годин. Після цього розчин охолоджували до температури від -5 до -2 °C; додавали 1 мл 20 мМ водного розчину KH 2PO4. Продукт залишали кристалізуватись перемішуючи при температурі від -5 до -2 °С протягом 2 годин. Відділений продукт фільтрували крізь скляний фільтр та промивали розчином діоксан:вода; 1:1. Продукт вільно висушували повітрям до досягнення постійної маси - одержували 142 мг очищеного празугрелю з вмістом 99,80%. Приклад 9 Празугрель, одержаний за прикладом 1 (1,56 г), розчиняли, перемішуючи при температурі від 60 °С у 22 мл метанолу з додаванням водного розчину KH 2PO4 у пропорції 20 мл метанолу та 0,5 мл цього розчину. Після розчинення миттєво припиняли нагрівання та протягом 0,5 години залишали для охолодження до кімнатної температури. Кристали починали розділятись. Отриману суміш охолоджували у воді + крижана баня ще протягом 1 години. Відділений продукт 6 UA 106595 C2 5 10 15 фільтрували та промивали метанолом. Продукт вільно висушували повітрям до досягнення постійної маси - одержували 1,25 г очищеного празугрелю з вмістом 97,65%; сполука формули II: 1,48%. Приклад 10 Празугрель, одержаний за прикладом 1 (373 мг), розчиняли у 3 мл ацетону при кімнатній температурі. Протягом перемішування розчин охолоджували до -3 °С та додавали 1 мл 20 мМ розчину KH2PO4. Продукт залишали кристалізуватись при температурі бані -5 °C - 0 °C. Відділений продукт фільтрували крізь скляний фільтр та промивали ацетоном. Продукт вільно висушували повітрям до досягнення постійної маси - одержували 336 мг очищеного празугрелю з вмістом 98,12%; сполука формули II: 1,64%. Приклад 11 Празугрель, одержаний за прикладом 1 (204 мг), розчиняли у 2 мл ацетону при кімнатній температурі. Протягом перемішування розчин охолоджували до -5 °C та додавали 2 мл метанолу. Продукт залишали кристалізуватись при температурі бані від -5 °C до -10 °С, потім при -22 °C протягом години. Відділений продукт фільтрували крізь скляний фільтр та промивали ацетоном. Продукт вільно висушували повітрям до досягнення постійної маси - одержували 96,2 мг очищеного празугрелю з вмістом 96,34%; сполука формули II: 3,42%. ФОРМУЛА ВИНАХОДУ 20 1. Спосіб одержання празугрелю, 5-[2-циклопропіл-1-(2-фторфеніл)-2-оксоетил]-4,5,6,7тетрагідротієно[3,2-с]піридин-2-ілацетат, формули І O N O S F O ,I 25 який відрізняється тим, що сполука формули IV O OSO2Me F IV 30 взаємодіє із сполукою формули III HN O S 35 III у формі солі з хлорводневою кислотою або п-толуолсульфоновою кислотою, з утворенням сполуки формули II 7 UA 106595 C2 O N O F 5 10 S , II яку потім перетворюють на сполуку формули І шляхом ацилювання безпосередньо у реакційній суміші без виділення, одержаний празугрель потім кристалізують безпосередньо з реакційної суміші і потім очищають кристалізацією з органічного розчинника з доданим ацилювальним агентом. 2. Спосіб за п. 1, який відрізняється тим, що неочищений празугрель розчиняють у полярному апротонному розчиннику при температурі від 10 до 50 °C, до розчину додають ацилювальний агент і потім кристалізують празугрель, додаючи водний розчин дигідрофосфату калію. 3. Спосіб за п. 2, який відрізняється тим, що полярний апротонний розчинник вибирають з нітрилів органічних кислот, етерів та циклічних етерів. Комп’ютерна верстка А. Крулевський Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 8
ДивитисяДодаткова інформація
Автори російськоюStepankova, Hana, Hajicek, Josef, Dousa, Michal
МПК / Мітки
МПК: C07D 495/04
Мітки: празугрелю, одержання, спосіб
Код посилання
<a href="https://ua.patents.su/10-106595-sposib-oderzhannya-prazugrelyu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання празугрелю</a>
Попередній патент: Пакувальний матеріал для фармацевтичного продукту
Наступний патент: Нове застосування фібратів
Випадковий патент: Спосіб лікування опісторхозної інвазії