Гетероциклічні інгібітори мек, їх застосування та фармацевтична композиція, що їх містить
Номер патенту: 100007
Опубліковано: 12.11.2012
Автори: Сео Дзеонбеоб, Воллес Ілай, Ян Гон Вун, Леонард Джон, Філдінг Марк Річард, Ліссікатос Джозеф П., Марлоу Еллісон Л., Піттам Джон Девід, Блейк Джім, Сторі Річард Ентоні, Бус Ребекка Джейн
Формула / Реферат
1. Сполука, а також її таутомери, метаболіти, розділені енантіомери, діастереоізомери, сольвати та фармацевтично прийнятні солі, вказана сполука має формулу І
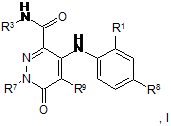
де:
R1 - Сl або F;
R3 - Н, метил, етил, ОН, МеО-, ЕtO-, НОСН2СН2О-, HOCH2C(Me)2O-, (S)-МеСН(ОН)СН2О-, (R)-HOCH2CH(OH)CH2O-, циклопропіл-СН2O-, НOСН2СН2-,
![]() ,
, 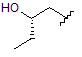 ,
, ![]() ,
,  ,
, ![]() або
або ![]() ;
;
R7 - циклопропіл-СН2- або С1-С4алкіл, де вказаний алкіл є необов'язково заміщеним одним або більше атомами F;
R8 - Вr, І або SMe; та
R9 - СН3, CH2F, CHF2, CF3, F або Сl.
2. Сполука, а також її таутомери, метаболіти, розділені енантіомери, діастереоізомери, сольвати та фармацевтично прийнятні солі, де вказана сполука має формулу ІА:
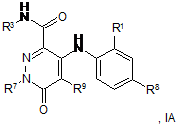
де:
R1 - Сl або F;
R3 - H, метил, ОН, МеО, ЕtO-, НОСН2СН2О, МеОСН2СН2О, НОСН2СН2СН2,
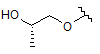 ,
, ![]() ,
, 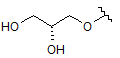 ,
, ![]() ,
, 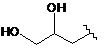 ,
, ![]() або
або ![]() ;
;
R7 - циклопропіл-СН2- або С1-С4алкіл, де вказаний алкіл є необов'язково заміщеним одним або більше атомами F;
R8 - Вr, І або SMe; та
R9 - СН3, CH2F, CHF2, CF3, F або Сl.
3. Сполука за пп. 1 або 2, де R7 - циклопропіл-СН2- або метил.
4. Сполука за пп. 1 або 2, де R9 - СН3, F або Сl.
5. Сполука, що має формулу II:

або її фармацевтично прийнятна сіль, де:
R3 - Н, МеО, НОСН2СН2О, МеОСН2СН2О, НОСН2СН2СН2,
![]() ,
, 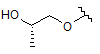 або
або 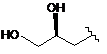 ; та
; та
R9 - H, СН3, F або Сl.
6. Сполука за п. 5 або її фармацевтично прийнятна сіль, де сполука є вибраною з групи:
4-(2-флуор-4-(метилтіо)феніламіно)-N-(2-гідроксіетокси)-1-метил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
4-(2-флуор-4-(метилтіо)феніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,б-дигідропіридазин-3-карбоксамід;
N-(циклопропілметокси)-4-(2-флуор-4-(метилтіо)феніламіно)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
4-(2-флуор-4-(метилтіо)феніламіно)-N-(2-метоксіетокси)-1,5-диметил-6-оксо-1,б-дигідропіридазин-3-карбоксамід;
4-(2-флуор-4-(метилтіо)феніламіно)-N-метокси-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
(S)-4-(2-флуор-4-(метилтіо)феніламіно)-N-(2-гідроксипропокси)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
4-(2-флуор-4-(метилтіо)феніламіно)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
5-флуор-4-(2-флуор-4-(метилтіо)феніламіно)-N-(2-гідроксіетокси)-1-метил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
(S)-5-флуор-4-(2-флуор-4-(метилтіо)феніламіно)-N-(2-гідроксипропокси)-1-метил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
5-хлор-4-(2-флуор-4-(метилтіо)феніламіно)-N-(2-гідроксіетокси)-1-метил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
(S)-5-хлор-4-(2-флуор-4-(метилтіо)феніламіно)-N-(2-гідроксипропокси)-1-метил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
4-(2-флуор-4-(метилтіо)феніламіно)-N-(3-гідроксипропіл)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід та
(S)-N-(2,3-дигідроксипропіл)-4-(2-флуор-4-(метилтіо)феніламіно)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід.
7. Сполука, що має формулу III:

або її фармацевтично прийнятна сіль, де:
R1 - Сl або F;
R3- Н, метил, МеО, НОСН2СН2О, НОСН2СН2СН2, НОСН2СН2,
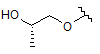 ,
, ![]() ,
, 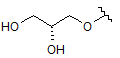 ,
, ![]() ,
, 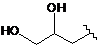 ,
, ![]() або
або ![]() ;
;
R8 - Br або I; та
R9 - СН3, F, Сl або Вr.
8. Сполука за п. 7 або її фармацевтично прийнятна сіль, де сполука є вибраною з групи:
5-бром-4-(4-бром-2-флуорфеніламіно)-N-(циклопропілметокси)-1-метил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
4-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
(R)-N-(2,3-дигідроксипропокси)-4-(2-флуор-4-йодфеніламіно)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
4-(2-флуор-4-йодфеніламіно)-N-метокси-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
N-(циклопропілметокси)-4-(2-флуор-4-йодфеніламіно)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
(S)-4-(2-флуор-4-йодфеніламіно)-N-(2-гідроксипропокси)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
4-(2-хлор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
(S)-4-(2-хлор-4-йодфеніламіно)-N-(2-гідроксипропокси)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
4-(4-бром-2-хлорфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
(S)-4-(4-бром-2-хлорфеніламіно)-N-(2-гідроксипропокси)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
4-(4-бром-2-флуорфеніламіно)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
(R)-4-(4-бром-2-флуорфеніламіно)-N-(2,3-дигідроксипропокси)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
4-(4-бром-2-флуорфеніламіно)-N-(1-гідрокси-2-метилпропан-2-ілокси)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
4-(2-флуор-4-йодфеніламіно)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
4-(4-бром-2-флуорфеніламіно)-5-флуор-N-(2-гідроксіетокси)-1-метил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
4-(2-флуор-4-йодфеніламіно)-N,1,5-триметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
N-(циклопропілметил)-4-(2-флуор-4-йодфеніламіно)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
4-(2-флуор-4-йодфеніламіно)-N-(3-гідроксипропіл)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
5-флуор-4-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1-метил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
4-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетил)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
N-(2,3-дигідроксипропіл)-4-(2-флуор-4-йодфеніламіно)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
5-хлор-4-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1-метил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
(S)-5-хлор-4-(2-флуор-4-йодфеніламіно)-N-(2-гідроксипропокси)-1-метил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
5-хлор-4-(2-флуор-4-йодфеніламіно)-1-метил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
5-хлор-N-(2,3-дигідроксипропіл)-4-(2-флуор-4-йодфеніламіно)-1-метил-6-оксо-1,6-дигідропіридазин-3-карбоксамід;
(S)-N-(2,3-дигідроксипропіл)-4-(2-флуор-4-йодфеніламіно)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід та
(S)-5-хлор-N-(2,3-дигідроксипропіл)-4-(2-флуор-4-йодфеніламіно)-1-метил-6-оксо-1,6-дигідропіридазин-3-карбоксамід.
9. Сполука за пп. 1 або 7 або її фармацевтично прийнятна сіль, де сполука є вибраною з групи:
4-(4-бром-2-флуорфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід та
(S)-4-(4-бром-2-флуорфеніламіно)-N-(2-гідроксипропокси)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід.
10. Сполука за будь-яким з пп. 1, 2, 5, 7, 9 для застосування як медикаменту.
11. Сполука за будь-яким з пп. 1, 2, 5, 7, 9 для застосування як медикаменту для лікування гіперпроліферативного розладу або запального стану.
12. Застосування сполуки за будь-яким з пп. 1, 2, 5, 7, 9 у виробництві медикаменту для лікування гіперпроліферативного розладу або запального стану.
13. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1, 2, 5, 7, 9 в асоціації з фармацевтично прийнятним носієм.
Текст
Реферат: Розкритими є МЕК-інгібітори загальної формули R3 H N O H N N R7 N R9 O R1 R8 ,I корисні у лікуванні гіперпроліферативних хвороб, як-то раку та запалення, у ссавців та запальних станів. Також розкритими є застосування таких сполук у лікуванні гіперпроліферативних хвороб у ссавців та фармацевтичні композиції, що містять так сполуки. UA 100007 C2 (12) UA 100007 C2 UA 100007 C2 5 10 15 20 25 30 35 40 45 50 55 Заявлений винахід стосується серії нових гетероциклічних сполук, котрі є корисними у лікуванні гіперпроліферативних хвороб, як-то рак та запалення, у ссавців. Цей винахід також стосується способу застосування таких сполук у лікуванні гіперпроліферативних хвороб у ссавців, особливо людей, та фармацевтичних композицій, що містять такі сполуки. Передача сигналу у клітинах через рецептори фактора росту та білкові кінази є важливим регулятором росту, проліферації та диференціації клітин. При нормальному рості клітин, фактори росту за допомогою активації рецепторів (тобто PDGF або EGF та інших), активують шляхи метаболізму МАР-кінази. Одним найбільш важливих та найбільш добре зрозумілих шляхів метаболізму МАР-кінази, що приймають участь у нормальному та неконтрольованому рості клітин, є шляхи метаболізму Ras/Raf-кінази. Активна GTP-зв'язана Ras-кіназа приводить до активації та непрямого фосфорилування Raf-кінази. Raf-кіназа тоді фосфорилує МЕК1 та 2 на двох серинових залишках (S218 та S222 для МЕК1 та S222 та S226 для МЕК2) (Ahn et al., Methods in Enzymology, 2001, 332, 417-431). Активована МЕК тоді фосфорилує тільки свої відомі субстрати, МАР-кінази, ERK1 та 2. Фосфорилування ERK за допомогою МЕК відбувається на Y204 та Т202 для ERK1 та Y185 та Т183 для ERK2 (Ahn et al., Methods in Enzymology, 2001, 332, 417-431). Фосфорилована ERK димеризується та тоді переміщується до ядра, де вона накопичується (Khokhlatchev et al., Cell, 1998, 93, 605-615). В ядрі ERK приймає участь у кількох важливих клітинних функціях, охоплюючи, але без обмеження, ядерний транспорт, трансдукцію сигналу, репарацію ДНК, комплектування та транслокацію нуклеосом та процесинг та трансляцію мРНК (Ahn et al., Molecular Cell, 2000, 6, 1343-1354). Взагалі, обробка клітин факторами росту приводить до активації ERK1 та 2, котра приводить до проліферації, а у деяких випадках, диференціації (Lewis et al., Adv. Cancer Res., 1998, 74, 49-139). У проліферативних хворобах генетичні мутації та/або надекспресія рецепторів фактора росту, униз по ходу передачі сигналу білків, або білкових кіназ, що приймають участь у шляху метаболізму ERK-кінази, призводять до нерегульованої проліферації клітин та, кінець кінцем, утворення пухлин. Наприклад, деякі типи раку мають мутації, котрі призводять до безперервної активації цього шляху метаболізму внаслідок безперервного продукування факторів росту. Інші мутації можуть призводити до дефектів у дезактивації активованого GTP-зв'язаного Rasкомплексу, знов утвореного при активації шляху метаболізму МАР-кінази. Мутовані онкоангіогенні форми Ras-кінази знайдені у 50 % типів раку ободової кишки та >90 % підшлункової залози, а також багатьох інших типах раку (Kohl et al., Science, 1993, 260, 18341837). Нещодавно, ідентифіковано мутації bRaf у більше ніж 60 % злоякісної меланом (Davies, Н. et al., Nature, 2002, 417, 949-954). Ці мутації у bRaf призводять до конститутивно активного каскаду МАР-кінази. Дослідження зразків первинних пухлин та ліній клітин також показали конститутивність або надактивацію шляху метаболізму МАР-кінази у типах раку підшлункової залози, ободової кишки, легень, яєчника та нирок (Hoshino, R. et al., Oncogene, 1999, 18, 813822). Звідси, існує сильна кореляція між типами раку та надактивним шляхом метаболізму МАРкінази, утвореним від генетичних мутацій. Оскільки конститутивний або надактиваційний каскад МАР-кінази грає кардинальну роль у проліферації та диференціації клітин, інгібування цього шляху метаболізму, можна вважати, буде корисним при гіперпроліферативних хворобах. МЕК є ключовим гравцем у цьому шляху метаболізму, оскільки вона знаходиться униз по ходу стосовно Ras та Raf. Додатково, вона є привабливою терапевтичною метою внаслідок того, що відомими субстратами для фосфорилування МЕК є тільки МАР-кінази, ERK1 та 2. Інгібування МЕК, як показано у кількох дослідженнях, має потенційну терапевтичну корисність. Наприклад, інгібітори невеликої молекулярної маси МЕК показані для інгібування росту пухлин людини у ксенотрансплантатах голих мишей (Sebolt-Leopold et al., Nature-Medicine, 1999, 5 (7), 810-816; Trachet et al., AACR 6nd 10, 04 2002, Poster #5426; Tecle, H., IBC 2 International Conference of Protein Kinases, September 9-10, 2002), блокування статичної алодинії у тварин (WO 01/05390) та інгібування росту клітин при гострій мієлоїдній лейкемії (Milella et al., J. Clin. Invest., 2001, 108 (6), 851-859). Інгібітори МЕК невеликої молекулярної маси є розкритими, їх охоплюють патентні публікації США №№ 2003/0232869, 2004/0116710 та 2003/0216460, та заявки на патент США №№ 10/654,580 та 10/929,295, кожну з котрих уведено тут як посилання. Принаймні п'ятнадцять додаткових патентних заявках з'явилися у останні кілька років. Дивись, наприклад,: патент США № 5,525,625; WO 98/43960; WO 99/01421; WO 99/01426; WO 00/41505; WO 00/42002; WO 00/42003; WO 00/41994; WO 00/42022; WO 00/42029; WO 00/68201; WO 01/68619; WO 02/06213; WO 03/077914 та WO 03/077855. Цей винахід стосується нових гетероциклічних сполук та їх фармацевтично прийнятних солей та проліків, котрі є корисними у лікуванні гіперпроліферативних хвороб. Виявлено, що 1 UA 100007 C2 5 сполуки 6-оксо-1,6-дигідропіридазину та 6-оксо-1,6-дигідропіридину, що мають певні замісники, які описано тут, є потужними інгібіторами ферменту МЕК. Більш конкретно, згідно з одним аспектом заявлений винахід стосується сполук, охоплюючи їх таутомери, метаболіти, розділені енантіомери, діастереоізомери, сольвати та фармацевтично прийнятні солі, вказані сполуки мають формулу І: R3 H N O H N N R7 R1 N R9 R8 O 10 ,I де: 1 R - Сl або F; 3 R - H, метил, етил, ОН, МеО-, ЕtO-, НОСН2СН2О-, НОСН2С(Ме)2О-, (S)-МеСН(ОН)СН2О-, (R)-HOCH2CH(OH)CH2O-, циклопропіл-СН2О-, НОСН2СН2-, HO HO HO HO , , O OH , або , ; 15 7 20 R - циклопропіл-СН2- або C1-C4алкіл, де вказаний алкіл є необов'язково заміщеним одним або більше атомами F; 8 R - Вr, І або SMe; та 9 R - СН3, CH2F, CHF2, CF3, F або Сl. Згідно з ще одним аспектом заявлений винахід стосується сполук, охоплюючи їх таутомери, метаболіти, розділені енантіомери, діастереоізомери, сольвати та фармацевтично прийнятні солі, вказані сполуки мають формулу IV: R3 H N O N R9 R7 R8 O 25 30 R1 H N , IV де: 1 R - Сl або F; 3 R - Н, метил, етил, ОН, МеО-, ЕtO-, НОСН2СН2О-, НОСН2С(Ме)2О-, (S)-МеСН(ОН)СН2О-, (R)-HOCH2CH(OH)CH2O-, циклопропіл-СН2O-, НOСН2СН2-, HO HO , 35 HO HO , O OH , , або ; 7 R - метил або етил, де вказані метил та етил є необов'язково заміщеними одним або більше атомами F; 8 R - Вr, І або SMe; та 9 R - Н, C1-C4алкіл, Сl або CN, де вказаний алкіл є необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: F або CN, 2 UA 100007 C2 5 за умови, що: 1 8 9 3 7 a) коли R - F, R - Br, R - Н та R - НОСН2СН2О, тоді R не може бути метилом або етилом; 1 8 9 3 7 b) коли R - F, R є І, R - Н та R - МеО, тоді R не може бути метилом; 1 8 9 3 7 c) коли R - F, R - метил, R - Н та R - НОСН2СН2О, тоді R не може бути метилом, та 1 8 9 3 7 d) коли R - F, R - Br, R - Н та R - циклопропіл-СН2О, тоді R не може бути метилом. У наступному аспекті заявлений винахід стосується двох кристалічних форм сполуки формули XI HO O H N O H N N O F I , XI 10 15 20 25 30 35 40 45 50 де дві кристалічні форм позначені як Форма 1, 2-(2-флуор-4-йодфеніламіно)-N-(2гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридин-3-карбоксамід, та Форма 2, 2-(2-флуор-4йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридин-3-карбоксамід. Також запропонованими є способи отримання Форми 1 та Форми 2 сполуки формули XI. У наступному аспекті заявлений винахід стосується композицій, що інгібують МЕК, які містять одну або більше сполук заявленого винаходу. Винахід також стосується способів одержання сполуки заявленого винаходу. У наступному аспекті заявлений винахід стосується способу застосування сполуки цього винаходу як медикаменту для лікування хвороби або медичного стану, опосередкованого МЕК. Наприклад, цей винахід стосується сполуки цього винаходу як медикаменту для лікування гіперпроліферативного розладу або запального стану у ссавця, що полягає у призначенні вказаному ссавцю однієї або більше сполук заявленого винаходу або їх фармацевтично прийнятних солей або проліків у кількості, ефективній для лікування вказаного гіперпроліферативного розладу. У ще одному аспекті цей винахід стосується сполуки цього винаходу у виробництві медикаменту для лікування гіперпроліферативного розладу або запального стану. У наступному аспекті заявлений винахід стосується способу продукування МЕК-інгібіторної дії у теплокровної тварини, як-то людини, яка має необхідність у такому лікуванні, котрий полягає у призначенні вказаній тварині ефективної кількості сполуки цього винаходу. У наступному аспекті заявлений винахід стосується лікування або попередження МЕКопосередкованого стану, що полягає у призначенні людині або тварині, яка має необхідність у цьому, фармацевтичної композиції, що містить сполуку заявленого винаходу або її фармацевтично прийнятну сіль або in vivo здатні до розщеплення проліки у кількості, ефективній для лікування або попередження вказаного МЕК-опосередкованого стану. Патентоздатні сполуки можна також застосовувати переважно у комбінації з іншими відомими терапевтичними засобами. Винахід також стосується фармацевтичних композицій, що інгібують МЕК, що містить ефективну кількість сполуки, вибраної згідно із заявленим винаходом, або її фармацевтично прийнятних проліків, фармацевтично активних метаболітів або фармацевтично прийнятних солей, вибраних згідно із заявленим винаходом. Додатковим аспектом винаходу є застосування заявленого винаходу в отриманні медикаменту для лікування або попередження хвороби або медичного стану, опосередкованих МЕК, у теплокровної тварини, переважно ссавця, більш переважно людини, яка потерпає від такого розладу. Більш конкретно, винахід стосується застосування сполуки винаходу в отриманні медикаменту для лікування або попередження гіперпроліферативного розладу або запального стану у ссавця. Додаткові переваги та нові особливості цього винаходу будуть представлені частково в нижченаведеному описі та частково повинні стати зрозумілі спеціалістам з наступного опису або можуть бути зрозумілі при виконанні винаходу на практиці. Переваги винаходу можуть бути реалізовані та досягнуті за допомогою інструментарію, комбінацій, композицій та способів, особливо представлених у доданій формулі винаходу. Короткий опис креслень. Додані креслення, котрі уведені тут та утворюють частину опису, ілюструють необмежувальні втілення заявленого винаходу та разом з описом пояснюють основи винаходу. 3 UA 100007 C2 5 10 15 20 25 30 35 На кресленнях: Фіг. 1 показує схему реакцій для синтезу сполуки формули 96. Фіг. 2 показує схему реакцій для синтезу сполук 96, 100, 101 та 102. Фіг. 3 показує схему реакцій для синтезу сполук 109, 110 та 111. Фіг. 4 показує альтернативну схему реакцій для синтезу сполук 109, 110 та 111. Фіг. 5 показує схему реакцій для синтезу сполук 119, 120 та 121. Фіг. 6 показує схему реакцій для синтезу сполук 124 та 125. Фіг. 7 показує схему реакцій для синтезу сполук 128, 129 та 130. Фіг. 8 показує схему реакцій для синтезу сполук 145 та 146. Фіг. 9 показує альтернативну схему реакцій для синтезу сполуки формули 145. Фіг. 10 показує картину рентгенівської дифракції від порошку для форми 2, 2-(2-флуор-4йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридин-3-карбоксаміду, отриманого згідно з прикладом 16А, етап 3. Фіг. 11 показує картину рентгенівської дифракції від порошку для форми 1, 2-(2-флуор-4йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридин-3-карбоксаміду, отриманого згідно з прикладом 16А, етап 4. Фіг. 12 показує картину рентгенівської дифракції від порошку для форми 1, 2-(2-флуор-4йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридин-3-карбоксаміду, отриманого згідно з прикладом 16В. Фіг. 13 показує картину рентгенівської дифракції від порошку для форми 1, 2-(2-флуор-4йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридин-3-карбоксаміду, отриманого згідно з прикладом 16D. Фіг. 14 показує термограму диференційної сканувальної калориметрії для форми 2, 2-(2флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридин-3карбоксаміду. Фіг. 15 показує термограму диференційної сканувальної калориметрії для форми 1, 2-(2флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридин-3карбоксаміду. Патентоздатні сполуки заявленого винаходу та їх таутомери, метаболіти, розділені енантіомери, діастереоізомери, сольвати та фармацевтично прийнятні солі та проліки є корисними у лікуванні гіперпроліферативних хвороб. Загалом, згідно з ще одним аспектом заявлений винахід стосується сполуки заявленого винаходу, що діє як МЕК-інгібітори. Більш конкретно, згідно з одним аспектом заявлений винахід стосується сполук, охоплюючи їх таутомери, метаболіти, розділені енантіомери, діастереоізомери, сольвати та фармацевтично прийнятні солі, вказані сполуки мають формулу І: R3 H N O H N N R7 R1 N R9 R8 O 40 ,I де: 1 R - Сl або F; 3 R - H, метил, етил, ОН, МеО-, ЕtO-, НОСН2СН2О-, НОСН2С(Ме)2О-, (S)-МеСН(ОН)СН2О-, (R)-HOCH2CH(OH)CH2O-, циклопропіл-СН2О-, НОСН2СН2-, HO HO , 45 HO HO , , O OH , або ; 7 R - циклопропіл-СН2- або С1-C4алкіл, де вказаний алкіл є необов'язково заміщеним одним або більше атомами F; 8 R - Вr, І або SMe; та 9 R - СН3, CH2F, CHF2, CF3, F або Сl. 4 UA 100007 C2 В одному втіленні винахід стосується сполук, охоплюючи їх таутомери, метаболіти, розділені енантіомери, діастереоізомери, сольвати та фармацевтично прийнятні солі, що мають формулу ІА: R3 H N O H N N R7 R1 N R9 R8 O 5 , ІА де: 1 R - Сl або F; 3 R - Н, метил, ОН, МеО, ЕtO, НОСН2СН2О, МеОСН2СН2О, НОСН2СН2СН2, HO O HO HO O , 10 OH , OH O O , HO , , OH HO 15 або ; 7 R - циклопропіл-СН2- або С1-С4алкіл, де вказаний алкіл є необов'язково заміщеним одним або більше атомами F; 8 R - Вr, І або SMe; та 9 R - СН3, CH2F, CHF2, CF3, F або Сl. 7 В одному втіленні у сполуках формул І або ІА, R - циклопропіл-СН2- або метил. У ще 9 одному втіленні R - СН3, F або Сl. У ще одному втіленні запропоновано сполуку формули II R3 H N O N N 20 F H N R9 SMe O II або її фармацевтично прийнятну сіль, де: 3 R - Н, МеО, НОСН2СН2О, МеОСН2СН2О, НОСН2СН2СН2, HO O 25 30 35 O OH HO , або ; та 9 R -H, СН3, F або Сl. 3 Сполуки формули II, що мають метильний замісник у N1-положенні та специфічні групи R 9 та R , є потужними МЕК-інгібіторами. Конкретні нові сполуки винаходу охоплюють будь-яку одну з групи: 4-(2-флуор-4-(метилтіо)феніламіно)-N-(2-гідроксіетокси)-1-метил-6-оксо-1,6дигідропіридазин-3-карбоксамід; 4-(2-флуор-4-(метилтіо)феніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6дигідропіридазин-3-карбоксамід; N-(циклопропілметокси)-4-(2-флуор-4-(метилтіо)феніламіно)-1,5-диметил-6-оксо-1,6дигідропіридазин-3-карбоксамід; 4-(2-флуор-4-(метилтіо)феніламіно)-N-(2-метоксіетокси)-1,5-диметил-6-оксо-1,6дигідропіридазин-3-карбоксамід; 4-(2-флуор-4-(метилтіо)феніламіно)-N-метокси-1,5-диметил-6-оксо-1,6-дигідропіридазин-3карбоксамід; 5 UA 100007 C2 5 10 15 (S)-4-(2-флуор-4-(метилтіо)феніламіно)-N-(2-гідроксипропокси)-1,5-диметил-6-оксо-1,6дигідропіридазин-3-карбоксамід; 4-(2-флуор-4-(метилтіо)феніламіно)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід; 5-флуор-4-(2-флуор-4-(метилтіо)феніламіно)-N-(2-гідроксіетокси)-1-метил-6-оксо-1,6дигідропіридазин-3-карбоксамід; (S)-5-флуор-4-(2-флуор-4-(метилтіо)феніламіно)-N-(2-гідроксипропокси)-1-метил-6-оксо-1,6дигідропіридазин-3-карбоксамід; 5-хлор-4-(2-флуор-4-(метилтіо)феніламіно)-N-(2-гідроксіетокси)-1-метил-6-оксо-1,6дигідропіридазин-3-карбоксамід; (S)-5-хлор-4-(2-флуор-4-(метилтіо)феніламіно)-N-(2-гідроксипропокси)-1-метил-6-оксо-1,6дигідропіридазин-3-карбоксамід; 4-(2-флуор-4-(метилтіо)феніламіно)-N-(3-гідроксипропіл)-1,5-диметил-6-оксо-1,6дигідропіридазин-3-карбоксамід та (S)-N-(2,3-дигідроксипропіл)-4-(2-флуор-4-(метилтіо)феніламіно)-1,5-диметил-6-оксо-1,6дигідропіридазин-3-карбоксамід. У ще одному втіленні запропоновано сполуку формули III R3 H N O R1 H N N N R9 R8 O 20 III або її фармацевтично прийнятну сіль, де: 1 R - Сl або F; 3 R - Н, метил, МеО, НОСН2СН2О, НОСН2СН2СН2, НОСН2СН2, HO O HO , HO O , OH O OH O , HO , , OH HO 25 30 35 40 45 або ; 8 R - Br aбo І; та 9 R - СН3, F, Сl або Вr. 1 Сполуки формули III, що мають метильний замісник у N1-положенні та специфічні групи R , 3 8 9 R -R та R , є потужними МЕК-інгібіторами. Конкретні нові сполуки винаходу охоплюють будь-яку одну з групи: 5-бром-4-(4-бром-2-флуорфеніламіно)-N-(циклопропілметокси)-1-метил-6-оксо-1,6дигідропіридазин-3-карбоксамід; 4-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридазин3-карбоксамід; (R)-N-(2,3-дигiдpoкcипpoпoкcи)-4-(2-флyop-4-йoдфeнiлaмiнo)-1,5-димeтил-6-oкco-1,6дигідропіридазин-3-карбоксамід; 4-(2-флуор-4-йодфеніламіно)-N-метокси-1,5-диметил-6-оксо-1,6-дигідропіридазин-3карбоксамід; N-(циклопропілметокси)-4-(2-флуор-4-йодфеніламіно)-1,5-диметил-6-оксо-1,6дигідропіридазин-3-карбоксамід; (S)-4-(2-флуор-4-йодфеніламіно)-N-(2-гідроксипропокси)-1,5-диметил-6-оксо-1,6дигідропіридазин-3-карбоксамід; 4-(2-хлор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3карбоксамід; (S)-4-(2-хлор-4-йодфеніламіно)-N-(2-гідроксипропокси)-1,5-диметил-6-оксо-1,6дигідропіридазин-3-карбоксамід; 4-(4-бром-2-хлорфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридазин3-карбоксамід; 6 UA 100007 C2 5 10 15 20 25 30 35 40 (S)-4-(4-бром-2-хлорфеніламіно)-N-(2-гідроксипропокси)-1,5-диметил-6-оксо-1,6дигідропіридазин-3-карбоксамід; 4-(4-бром-2-флуорфеніламіно)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід; (R)-4-(4-бром-2-флуорфеніламіно)-N-(2,3-дигідроксипропокси)-1,5-диметил-6-оксо-1,6дигідропіридазин-3-карбоксамід; 4-(4-бром-2-флуорфеніламіно)-N-(1-гідрокси-2-метилпропан-2-ілокси)-1,5-диметил-6-оксо1,6-дигідропіридазин-3-карбоксамід; 4-(2-флуор-4-йодфеніламіно)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід; 4-(4-бром-2-флуорфеніламіно)-5-флуор-N-(2-гідроксіетокси)-1-метил-6-оксо-1,6дигідропіридазин-3-карбоксамід; 4-(2-флуор-4-йодфеніламіно)-N,1,5-триметил-6-оксо-1,6-дигідропіридазин-3-карбоксамід; N-(циклопропілметил)-4-(2-флуор-4-йодфеніламіно)-1,5-диметил-6-оксо-1,6дигідропіридазин-3-карбоксамід; 4-(2-флуор-4-йодфеніламіно)-N-(3-гідроксипропіл)-1,5-диметил-6-оксо-1,6-дигідропіридазин3-карбоксамід; 5-флуор-4-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1-метил-6-оксо-1,6дигідропіридазин-3-карбоксамід; 4-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетил)-1,5-диметил-6-оксо-1,6-дигідропіридазин-3карбоксамід; N-(2,3-дигідроксипропіл)-4-(2-флуор-4-йодфеніламіно)-1,5-диметил-6-оксо-1,бдигідропіридазин-3-карбоксамід; 5-хлор-4-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1-метил-6-оксо-1,6дигідропіридазин-3-карбоксамід; (S)-5-хлор-4-(2-флуор-4-йодфеніламіно)-N-(2-гідроксипропокси)-1-метил-6-оксо-1,6дигідропіридазин-3-карбоксамід; 5-хлор-4-(2-флуор-4-йодфеніламіно)-1-метил-6-оксо-1,6-дигідропіридазин-3-карбоксамід; 5-хлор-N-(2,3-дигідроксипропіл)-4-(2-флуор-4-йодфеніламіно)-1-метил-6-оксо-1,6дигідропіридазин-3-карбоксамід; (S)-N-(2,3-дигідроксипропіл)-4-(2-флуор-4-йодфеніламіно)-1,5-диметил-6-оксо-1,6дигідропіридазин-3-карбоксамід та (S)-5-хлор-N-(2,3-дигідроксипропіл)-4-(2-флуор-4-йодфеніламіно)-1-метил-6-оксо-1,6дигідропіридазин-3-карбоксамід. Конкретні нові сполуки винаходу також охоплюють нижченаведені сполуки: 4-(4-бром-2-флуорфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6дигідропіридазин-3-карбоксамід та (S)-4-(4-бром-2-флуорфеніламіно)-N-(2-гідроксипропокси)-1,5-диметил-6-оксо-1,6дигідропіридазин-3-карбоксамід. Згідно з ще одним аспектом заявлений винахід стосується сполук, охоплюючи їх таутомери, метаболіти, розділені енантіомери, діастереоізомери, сольвати та фармацевтично прийнятні солі, вказані сполуки мають формулу IV: H R3 N O R1 H N N R9 R7 R8 O 45 , IV де: 1 R - Сl або F; 3 R - H, метил, етил, ОН, МеО-, ЕrO-, НОСН2СН2О-, НОСН2С(Ме)2О-, (S)-МеСН(ОН)СН2О-, (R)-HOCH2CH(OH)CH2O-, циклопропіл-СН2O-, НOСН2СН2-, HO HO HO HO , , O OH , 7 , або UA 100007 C2 5 10 ; 7 R - метил або етил, де вказані метил та етил є необов'язково заміщеними одним або більше атомами F; 8 R - Вr, І або SMe; та 9 R - Н, С1-С4алкіл, Сl або CN, де вказаний алкіл є необов'язково заміщеним одним або більше замісниками, незалежно вибраними з групи: F або CN, за умови, що, коли: 1 8 9 7 3 a) R - F, R - Br, R - Н та R - метил або етил, тоді R не може бути НОСН2СН2О; 1 8 9 3 7 b) R - F, R є І, R - Н та R - МеО, тоді R не може бути метилом; 1 8 9 3 7 c) R - F, R - метил, R - Н та R - НОСН2СН2О, тоді R не може бути метилом; та 1 8 9 3 7 d) R - F, R - Br, R - H та R - циклопропіл-СН2О, тоді R не може бути метилом. В одному 9 втіленні у сполуках формул IV, R - Н, метил, етил, Сl або CN. В одному втіленні запропоновано сполуки згідно з винаходом, що мають формулу V: H R3 N O F H N N R9 SMe O V 15 20 25 30 35 або їх фармацевтично прийнятні солі, де: 3 R - НОСН2СН2О або (S)-MeCH(OH)CH2O; та 9 R - H, СН3, F або Сl, 1 8 9 7 3 за умови, що, коли R - F, R - SMe, R - Сl та R - метил, тоді R не може бути НОСН2СН2О. 3 Сполуки формули V, де R - НОСН2СН2О або (S)-MeCH(OH)CH2O, є потужними МЕКінгібіторами. Конкретні нові сполуки винаходу охоплюють будь-яку одну з групи: 2-(2-флуор-4-(метилтіо)феніламіно)-N-(2-гідроксіетокси)-1-метил-6-оксо-1,6-дигідропіридин3-карбоксамід; (S)-2-(2-флуор-4-(метилтіо)феніламіно)-N-(2-гідроксипропокси)-1-метил-6-оксо-1,6дигідропіридин-3-карбоксамід; 2-(2-флуор-4-(метилтіо)феніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6дигідропіридин-3-карбоксамід; (S)-2-(2-флуор-4-(метилтіо)феніламіно)-N-(2-гідроксипропокси)-1,5-диметил-6-оксо-1,6дигідропіридин-3-карбоксамід; 5-флуор-2-(2-флуор-4-(метилтіо)феніламіно)-N-(2-гідроксіетокси)-1-метил-6-оксо-1,6дигідропіридин-3-карбоксамід; (S)-5-флуор-2-(2-флуор-4-(метилтіо)феніламіно)-N-(2-гідроксипропокси)-1-метил-6-оксо-1,6дигідропіридин-3-карбоксамід та (S)-5-хлор-2-(2-флуор-4-(метилтіо)феніламіно)-N-(2-гідроксипропокси)-1-метил-6-оксо-1,6дигідропіридин-3-карбоксамід. В одному втіленні запропоновано сполуки згідно з винаходом, що мають формулу VI: H R3 N O R1 H N N R9 O I VI 40 або їх фармацевтично прийнятні солі, де: 1 R - Сl або F; 3 R - Н, НОСН2СН2О або (S)-MeCH(OH)CH2O; та 8 UA 100007 C2 9 5 10 15 20 25 30 35 R - H, метил, F або Сl. 1 3 9 Сполуки формули VI, де R - Сl, R - НОСН2СН2О або (S)-MeCH(OH)CH2O та R - Н, є потужними МЕК-інгібіторами. 1 3 9 Сполуки формули VI, де R - F, R - Н та R - метил, є потужними МЕК-інгібіторами. 3 Сполуки формули VI, де R - НОСН2СН2О або (S)-MeCH(OH)CH2O, є потужними МЕКінгібіторами. 1 3 9 Сполука формули VI, де R - F, R - НОСН2СН2О та R - метил, є потужним МЕК-інгібітором та також має гарну розчинність. Як застосовано тут, термін "гарна розчинність" стосується сполуки, що має розчинність більше 50 мкг/мл, наприклад розчинність приблизно від 50 до 270 мкг/мл, як визначено способом прикладу С. Конкретні нові сполуки формули VI згідно з винаходом охоплюють будь-яку одну з групи: 2-(2-хлор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1-метил-6-оксо-1,6-дигідропіридин-3карбоксамід; (S)-2-(2-хлор-4-йодфеніламіно)-N-(2-гідроксипропокси)-1-метил-6-оксо-1,6-дигідропіридин-3карбоксамід; 2-(2-флуор-4-йодфеніламіно)-1,5-диметил-6-оксо-1,6-дигідропіридин-3-карбоксамід; 2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1-метил-6-оксо-1,6-дигідропіридин-3карбоксамід; (S)-2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксипропокси)-1-метил-6-оксо-1,6-дигідропіридин3-карбоксамід; (S)-2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксипропокси)-1,5-диметил-6-оксо-1,6дигідропіридин-3-карбоксамід; 2-(2-хлор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридин-3карбоксамід; 5-хлор-2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1-метил-6-оксо-1,6-дигідропіридин3-карбоксамід; (S)-2-(2-хлор-4-йодфеніламіно)-N-(2-гідроксипропокси)-1,5-диметил-6-оксо-1,6дигідропіридин-3-карбоксамід; (S)-5-хлор-2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксипропокси)-1-метил-6-оксо-1,6дигідропіридин-3-карбоксамід; 5-флуор-2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1-метил-6-оксо-1,6дигідропіридин-3-карбоксамід та (S)-5-флуор-2-(2-флуор-4-йодфеніламiно)-N-(2-гідроксипропокси)-1-метил-6-оксо-1,6дигідропіридин-3-карбоксамід. 1 3 9 У ще одному втіленні запропоновано сполуку формули VI, де R - F, R - НОСН2СН2О та R метил, або її фармацевтично прийнятну сіль. Було знайдено, що сполука формули XI HO O H N O H N N 40 45 50 O F I XI може існувати у двох кристалічних формах, позначених далі як Форма 1, 2-(2-флуор-4йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридин-3-карбоксамід, та Форма 2, 2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6дигідропіридин-3-карбоксамід, та Форму 2 можна перетворювати у Форму 1. Зразки конкретної кристалічної форми сполуки формули XI були проаналізовані, застосовуючи комбінацію аналізу рентгенівською дифракцією від порошку та аналізу диференційною сканувальною калориметрією (ДСК), як описано у прикладах 16Е та 16F. Там, де встановлено, що заявлений винахід стосується кристалічної форми сполуки формули XI, ступінь кристалічності, як визначено за допомогою даних рентгенівської дифракції від порошку, є придатно більше приблизно 60 %, більш придатно більше приблизно 80 %, переважно більше приблизно 90 % та більш переважно більше приблизно 95 %. 9 UA 100007 C2 5 10 15 Згідно з наступним аспектом винаходу запропоновано кристалічну форму сполуки формули XI по суті у стані форми 2, 2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6оксо-1,6-дигідропіридин-3-карбоксаміду. Згідно з наступним аспектом винаходу запропоновано кристалічну форму сполуки формули XI по суті у стані форми 1, 2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6оксо-1,6-дигідропіридин-3-карбоксаміду. Сполука формули XI у стані форми 2, 2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5диметил-6-оксо-1,6-дигідропіридин-3-карбоксамід, має картину рентгенівської дифракції, що має характеризувальні піки на шкалі 2-тета () приблизно при 9,5 та 12,6. Згідно з наступним аспектом винаходу сполука формули XI у стані форми 2, 2-(2-флуор-4-йодфеніламіно)-N-(2гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридин-3-карбоксамід, має картину рентгенівської дифракції, що має характеризувальні піки на шкалі 2-тета () приблизно при 9,5, 12,6, 14,7 та 19,6. Форма 2, 2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6дигідропіридин-3-карбоксамід, має картину рентгенівської дифракції, яку по суті показано на Фіг. 10 тут далі, що має характеризувальні піки [на шкалі 2-тета ()] приблизно при положеннях, показаних у таблиці А. Таблиця А Два-тета 9,54 10,24 12,62 13,86 14,67 15,65 16,62 17,15 17,36 17,54 17,86 18,72 19,00 19,63 20,04 20,47 22,02 22,40 22,97 23,54 20 25 30 Відносна інтенсивність ДС С ДC C ДС С С С С С ДС С С ДС С ДС ДС C ДС ДС Два-тета 23,78 24,54 25,13 25,60 27,95 28,72 29,19 29,67 30,40 30,65 31,44 31,75 32,39 33,48 33,77 34,94 36,20 38,70 39,62 Відносна інтенсивність ДС С ДС С С ДС С С С ДС С ДС С С ДС С С С П Сполука формули XI у стані форми 1, 2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5диметил-6-оксо-1,6-дигідропіридин-3-карбоксамід, має картину рентгенівської дифракції, що має характеризувальні піки на шкалі 2-тета () приблизно при 9,2 та 13,0. Згідно з наступним аспектом винаходу сполука формули XI у стані форми 1, 2-(2-флуор-4-йодфеніламіно)-N-(2гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридин-3-карбоксамід, має картину рентгенівської дифракції, що має характеризувальні піки на шкалі 2-тета () приблизно при 9,2, 13,0, 18,3, 21,0 та 21,7. Форма 1, 2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6дигідропіридин-3-карбоксамід, має картину рентгенівської дифракції по суті таку, як показано тут далі на Фіг. 11 або 12, що має характеризувальні піки [на шкалі 2-тета ()] приблизно при положеннях, показаних у таблиці В. 10 UA 100007 C2 Таблиця В Два-тета 2,29 2,44 9,24 10,25 13,01 14,85 17,17 17,70 18,30 19,47 20,35 20,98 21,69 22,14 23,02 23,70 24,15 25,15 25,58 5 Відносна інтенсивність П П С С С П П П С П ДС П С П П П С С П 15 20 25 30 Відносна інтенсивність П П П П С С П С п П П П П П П П П С П Як згадано вище, інтенсивності піків у рентгенівській дифрактограмі від порошку можуть виявляти деяку непостійність, залежно від застосовуваних умов вимірювання. Відповідно, у Таблицях А та В, на які будуть посилання тут далі, відносні інтенсивності не є встановленими чисельно. Правильніше, застосовувані наступні визначення для інтенсивності: % Відносна інтенсивність 25-100 10-25 3-10 1-3 10 Два-тета 25,86 26,32 27,08 27,49 28,17 28,61 29,20 30,65 32,15 32,61 34,26 34,90 35,51 35,94 36,74 37,71 38,20 38,71 39,78 Визначення ДС (дуже сильно) С (сильно) П (помірно) Сл (слабко) де відносні інтенсивності є похідними від картини рентгенівської дифракції, виміряної з перемінними щілинами. Фіг. 13 показує картину рентгенівської дифракції від порошку для форми 1, 2-(2-флуор-4йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридин-3-карбоксаміду, отриманого згідно з прикладом 16D. Як треба розуміти, деякі з більш другорядних піків, присутніх у картинах рентгенівської дифракції на Фіг. від 10 до 13, видалено Таблиць А та В. Сполука формули Х1 у стані форми 2, 2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5диметил-6-оксо-1,6-дигідропіридин-3-карбоксамід, має картину рентгенівської дифракції по суті таку, як показано на Фіг. 10. Сполука формули Х1 у стані форми 1, 2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5диметил-6-оксо-1,6-дигідропіридин-3-карбоксамід, має картину рентгенівської дифракції по суті таку, як показано на Фіг. 11 або 12. У попередніх розділах визначення піків рентгенівської дифрактограми від порошку для кристалічної форми 2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6дигідропіридин-3-карбоксаміду, термін "при приблизно" застосовано у експрессії "...на шкалі 2тета () при приблизно.." свідчить, що точне положення піків (тобто перелічені значення кутів два-тета) не слід сприймати як абсолютні значення внаслідок того, як треба розуміти спеціалістам, що точне положення піків може слабко варіювати від однієї апаратури до іншої, від одного зразка до іншого, або у результаті слабких варіацій в використовуваних умовах вимірювання. Також встановлено у попередніх розділах, що кристалічна форма 2-(2-флуор-4йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридин-3-карбоксаміду дає картини рентгенівської дифракції від порошку "по суті" такі ж, як картини рентгенівської дифракції від порошку, як показані на Фіг. від 10 до 13, та мають по суті найбільш визначувані 11 UA 100007 C2 5 10 15 20 25 30 35 40 45 50 55 піки (значення кутів два-тета), показані у таблицях А та В, відповідно. Потрібно розуміти, що застосування терміна "по суті" у цьому контексті задумано також для позначення, що значення кутів два-тета картин рентгенівської дифракції від порошку можуть слабко варіювати від однієї апаратури до іншої, від одного зразка до іншого, або у результаті слабких варіацій в використовуваних умовах вимірювання, такі положення піків показані на Фігурах або представлені у таблицях А та В, знов не слід сприймати як абсолютні значення. Способи отримання сполук формули XI у будь-якій з Форм 1 або 2 є тут розкритими. В одному аспекті запропоновано спосіб отримання сполуки формули XI по суті у стані форми 1, 2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6дигідропіридин-3-карбоксаміду, який включає: a) контактування 2-(2-флуор-4-йодфеніламіно)-1,5-диметил-6-оксо-1,6-дигідропіридин-3карбонової кислоти (2-вінілоксіетоксі)-аміду з кислотною сумішшю протягом часу, достатнього для перетворення сполуки у 2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6оксо-1,6-дигідропіридин-3-карбоксамід; b) дозволяння матеріалу з етапу а) кристалізуватися з органічного розчинника, що містить кристали затравки форми 1, 2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6оксо-1,6-дигідропіридин-3-карбоксаміду; та c) виділення форми 1, 2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо1,6-дигідропіридин-3-карбоксаміду. В одному аспекті кислотна суміш на етапі а) може бути сумішшю неорганічних або органічних кислот. У ще одному аспекті етап а) може бути проведений у двофазній системі розчинників водна кислота-етилацетат. В одному аспекті органічним розчинником на етапі b) є етилацетат. У ще одному аспекті запропоновано отримання сполуки формули XI по суті у стані форми 1, 2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридин-3карбоксаміду, що включає: a) перемішування форми 2, 2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил6-оксо-1,6-дигідропіридин-3-карбоксаміду із невеликою кількістю форми 1, 2-(2-флуор-4йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридин-3-карбоксаміду, в органічному розчиннику; та b) виділення форми 1, 2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо1,6-дигідропіридин-3-карбоксаміду. В одному аспекті кількість матеріалу форми 1, застосовуваного на етапі а), є приблизно 5 % за масою. У ще одному аспекті етап а) є проведеним в етилацетаті при температурі трохи вище температури довкілля, як-то приблизно від 50 до 60 °С. У ще одному аспекті винахід стосується способу отримання сполуки формули Х1 по суті у стані форми 2, 2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6дигідропіридин-3-карбоксаміду, за пунктом 1, який включає: a) контактування 2-(2-флуор-4-йодфеніламіно)-1,5-диметил-6-оксо-1,6-дигідропіридин-3карбонової кислоти (2-вінілоксіетоксі)-аміду з кислотною сумішшю протягом часу, достатнього для перетворення сполуки у 2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6оксо-1,6-дигідропіридин-3-карбоксамід; b) дозволяння матеріалу з етапу а) кристалізуватися з органічного розчинника; та c) виділення форми 2, 2-(2-флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо1,6-дигідропіридин-3-карбоксаміду. В одному аспекті органічний розчинник на етапі b) містить кристали затравки форми 2, 2-(2флуор-4-йодфеніламіно)-N-(2-гідроксіетокси)-1,5-диметил-6-оксо-1,6-дигідропіридин-3карбоксаміду. Кислотна суміш на етапі а) може бути сумішшю неорганічних або органічних кислот, та етап а) може бути проведений в органічному розчиннику, як-то тетрагідрофуран. В одному аспекті органічний розчинник на етапі b) може бути вибраний з етилацетату та метилізобутилкетону, в обох випадках необов'язково у присутності ізогексану. Деякі сполуки цього винаходу можуть існувати як дві або більше таутомерних форм. "Таутомер" є одним з двох або більше структурних ізомерів, що існують у рівновазі та легко перетворюються від однієї ізомерної форми до іншої, як-то структури, утвореної внаслідок переходу гідрогену від однієї ділянки до іншої у межах тієї ж молекули. Інші таутомери, що утворюють сполуки, можуть переходити один в одний, наприклад, внаслідок енолізації/деенолізації тощо. Відповідно, заявлений винахід стосується отримання усіх таутомерних форм сполук цього винаходу. 12 UA 100007 C2 5 10 15 20 25 30 35 40 45 50 55 60 Сполуки цього винаходу можуть виявляти один або більше асиметричних центрів; такі сполуки можуть внаслідок цього бути отримані як індивідуальні (R)- або (S)-стереоізомери або як їх суміші. Якщо не вказане інше, опис або назву конкретної сполуки в описі та формулі винаходу використано для позначення обох індивідуальних енантіомерів, суміші їх діастереоізомерів, рацемічної або інакше. Відповідно, цей винахід також стосується усіх таких ізомерів, охоплюючи діастереоізомерні суміші та відокремлені енантіомери сполук цього винаходу. Діастереоізомерні суміші можуть бути розділені на їх індивідуальні діастереоізомери на основі їх фізико-хімічних відмінностей способами, відомими спеціалістам, наприклад хроматографією або фракційною кристалізацією. Енантіомери можуть бути відокремлені перетворенням енантіомерної суміші у діастереоізомерну суміш реакцією з прийнятною оптично активною сполукою (наприклад, спиртом), розділенням діастереоізомерів та перетворенням (наприклад, гідролізуванням) індивідуальних діастереоізомерів до відповідних чистих енантіомерів. Способи визначення стереохімії та відокремлення стереоізомерів добре відомі у попередньому рівні техніки (дивись обговорення у Chapter 4 of "Advanced Organic Chemistry", 4th edition, J. March, John Wiley та Sons, New York, 1992). Цей винахід також стосується фармацевтичних композицій, що містять сполуку заявленого винаходу, та способів лікування проліферативних розладів або анормального росту клітин за допомогою призначення сполуки заявленого винаходу. Сполуки заявленого винаходу, що мають вільні аміногрупи, амідогрупи, гідроксильні або карбоксильні групи, можна перетворювати у фармацевтично прийнятні проліки. "Проліками" є сполука, що може перетворюватися у фізіологічних умовах або внаслідок сольволізу у визначену сполуку або у фармацевтично прийнятну сіль такої сполуки. Проліки охоплюють сполуки, де амінокислотний залишок або поліпептидний ланцюг двох або більше (наприклад, двох, трьох або чотирьох) амінокислотних залишків є ковалентно приєднаний через амідний або естерний зв'язок до вільної аміногрупи, гідроксигрупи або групи карбонової кислоти сполуки заявленого винаходу. Амінокислотні залишки охоплюють, але без обмеження, 20 існуючих у природі амінокислот, звичайно позначених за допомогою трилітерних символів, та також охоплюють 4-гідроксипролін, гідроксилізин, демозин, ізодемозин, 3-метилгістидин, норвалін, бета-аланін, гамма-аміномасляну кислоту, цитрулін, гомоцистеїн, гомосерин, орнітин та метіонінсульфон. Одними кращими проліками цього винаходу є сполука заявленого винаходу, ковалентно приєднана до залишку валіну. Додаткові типи проліків є охопленими також. Наприклад, вільні карбоксильні групи можуть бути дериватизовані як аміди або алкілові естери. Як ще один приклад, сполуки цього винаходу, що містять вільні гідроксильні групи, можуть бути дериватизовані як проліки перетворенням гідроксильної групи у фосфатний естер, гемісукцинат, диметиламіноацетат або фосфорилоксиметилоксикарбоніл, як показано у A dvanced Drug Delivery R eviews, 1996, 19, 115. Карбаматні проліки гідроксилу та аміногрупи є охопленими також, ними є карбонатні проліки, сульфонатні естери та сульфатні естери гідроксильної групи. Дериватизація гідроксильної групи, як (ацилокси)метиловим та (ацилоксі)етиловим етерами, де ацильна група може бути алкіловим естером, необов'язково заміщеним групами, охоплюючи, але без обмеження, етерні, амін та карбоновокислотні функціональні групи, або ті, де ацильна група є амінокислотним естером, як описано вище, є охопленими також. Проліки цього типу описані у J. Med. Chem., 1996, 39, 10. Більш конкретні приклади охоплюють заміщення атома гідрогену спиртової групи такою групою, як (С1-С6)алканоїлоксиметил, 1-((С1-С6)алканоїлоксі)етил, 1метил-1-((С1-С6)алканоїлоксі)етил, (С1-С6)алкоксикарбонілоксиметил, N-(С1С6)алкоксикарбоніламінометил, сукциноїл, (С1-С6)алканоїл, -аміно(С1-С4)алканоїл, арилацил та -аміноацил або -аміноацил--аміноацил, де кожна -аміноацильна група є незалежно вибраною з існуючих у природі L-амінокислот, Р(О)(ОН)2, -Р(О)(О(С1-С6)алкіл)2 або глікозилу (радикала, утвореного від усунення гідроксильної групи геміацетальної форми вуглеводу). Вільні аміни можуть також бути дериватизовані як аміди, сульфонаміди або фосфонаміди. Наприклад, проліки можуть бути утворені за допомогою заміщення атома гідрогену в аміногрупі групою, як-то R-карбоніл, RO-карбоніл, NRR'-карбоніл, де R та R', кожний незалежно, представляють (С1-С10)алкіл, (С3-С7)циклоалкіл, бензил, або R-карбоніл є природним аміноацилом або природним альфа-аміноацилом-природним -аміноацилом, -C(OH)C(O)OY, де Y - Н, (С1-C6)алкіл або бензил, -C(OY0)Y1, де Y0 - (С1-С4)алкіл та Y1 - (С1-С6)алкіл, карбоксі(C1С6)алкіл, аміно(С1-С4)алкіл або моно-N- або ді-N,N-(С1-С6)алкіламіноалкіл, -C(Y2)Y3, де Y2 - Н або метил та Y3 - моно-N- або ді-N,N-(С1-С6)алкіламіно, морфоліно, піперидин-1-іл або піролідин-1-іл. Усі з цих частин проліків можуть охоплювати групи, охоплюючи, але без обмеження, етерні групи, аміногрупи та карбоновокислотні функціональні групи. 13 UA 100007 C2 5 10 15 20 25 30 35 40 45 50 55 Проліки сполук заявленого винаходу можуть бути ідентифіковані, застосовуючи звичайні способи, відомі у попередньому рівні техніки. Різні форми проліків відомі у попередньому рівні техніки. Як приклади таких похідних проліків, дивись, наприклад, а) Design of Prodrugs, edited by H. Bundgaard, (Elsevier, 1985) and Methods in Enzymology, Vol. 42, p. 309-396, edited by K. Widder, et al. (Academic Press, 1985); b) A Textbook of Drug Design and Development, edited by Krogsgaard-Larsen and H. Bundgaard, Chapter 5 "Design and Application of Prodrugs," by H. Bundgaard p. 113-191 (1991); с) Н. Bundgaard, Advanced Drug Delivery Reviews, 8, 1-38 (1992); d) H. Bundgaard, et al., Journal of Pharmaceutical Sciences, 77:285 (1988); та е) N. Kakeya, et al., Chem. Pharm. Bull., 32: 692 (1984), кожне з котрих уведено тут як посилання. На додаток, винахід також стосується сольватів, метаболітів та фармацевтично прийнятних солей сполук заявленого винаходу. Термін "сольват" стосується агрегації молекули з одною або більше молекулами розчинника. "Метаболіт" є фармакологічно активним продуктом, отриманим внаслідок in vivo метаболізму в організмі визначеної сполуки або її солі. Такі продукти можуть утворюватися, наприклад, від окиснення, відновлення, гідролізу, амідування, дезамідування, естерифікаці, дезестерифікаці, ферментного розщеплення, тощо, застосовуваної сполуки. Відповідно, винахід стосується метаболітів сполук заявленого винаходу, охоплюючи сполуки, отримані способом, що включає контактування сполук цього винаходу з ссавцем протягом періоду часу, достатнього для утворення продукту їх метаболізму. 14 3 Метаболіти звичайно ідентифікують отриманням радіомічених (наприклад, С або Н) ізотопами сполук винаходу, призначення їх парентерально у дозі, яку можна визначити (наприклад, більше приблизно 0,5 мг/кг), тварині, як-то щуру, миші, морській свинці, мавпі або людині, даючи достатній час для того, щоб відбувся метаболізм (звичайно приблизно 30 секунд - 30 годин) та виділення продуктів його перетворювання з сечі, крові або інших біологічних зразків. Ці продукти легко виділяти, оскільки вони є міченими (інші є виділеними застосуванням антитіл, здатних до зв'язування епітопів, що зберігаються як метаболіт). Метаболітні структури визначають звичайним чином, наприклад, за допомогою аналізів МС, РХ/МС або ЯМР. Загалом, аналіз метаболітів роблять тим же шляхом, як дослідження метаболізму звичайних ліків, добре відомі спеціалістам. Метаболіти, оскільки їх інакше не знайти in vivo, є корисними у діагностичних дослідженнях для терапевтичного дозування сполук винаходу. "Фармацевтично прийнятна сіль", як застосовано тут, якщо не вказане інше, охоплює солі, що зберігають біологічну ефективність вільної кислоти та основи визначеної сполуки та при цьому не є біологічно або інакше небажаними. Сполука винаходу може мати достатньо кислотні, достатньо основні або обидві функціональні групи та відповідно реагувати з будь-якою з ряду неорганічних або органічних основ та неорганічних або органічних кислот для утворення фармацевтично прийнятних солей. Приклади фармацевтично прийнятних солей охоплюють солі, що отримані реакцією сполуки заявленого винаходу із мінеральною або органічною кислотою або неорганічною основою, такі солі включають сульфати, піросульфати, гідросульфати, сульфіти, гідросульфіти, фосфати, моногідрогенфосфати, дигідрогенфосфати, метафосфати, пірофосфати, хлориди, броміди, йодиди, ацетати, пропіонати, деканоати, каприлати, акрилати, форміати, ізобутирати, капроати, гептаноати, пропіолати, оксалати, малонати, сукцинати, суберати, себацинати, фумарати, малеати, бутин-1,4-діоати, гексин-1,6діоати, бензоати, хлорбензоати, метилбензоати, динітробензоати, гідроксибензоати, метоксибензоати, фталати, сульфонати, ксиленсульфонати, фенілацетати, фенілпропіонати, фенілбутирати, цитрати, лактати, -гідроксибутирати, гліколяти, тартрати, метансульфонати, пропансульфонати, нафталін-1-сульфонати, нафталін-2-сульфонати та манделати. Оскільки одинична сполука заявленого винаходу може містити більше однієї кислотної або основної частини, сполуки заявленого винаходу можуть містити моно-, ди- або трисолі у одиничній сполуці. Якщо патентоздатною сполукою є основа, потрібна фармацевтично прийнятна сіль може бути отримана будь-яким придатним способом, доступним у попередньому рівні техніки, наприклад обробкою вільної основи кислотною сполукою, особливо неорганічною кислотою, якто гідрохлоридна кислота, гідробромідна кислота, сульфатна кислота, нітратна кислота, фосфатна кислота тощо, або органічною кислотою, як-то оцтова кислота, малеїнова кислота, бурштинова кислота, мигдальна кислота, фумарова кислота, малонова кислота, пірувинна кислота, щавлева кислота, гліколева кислота, саліцилова кислота, піранозидилкислотою, як-то глюкуронова кислота або галактуронова кислота, альфа-гідроксикислотою, як-то лимонна кислота або винна кислота, амінокислотою, як-то аспарагінова кислот або глутамінова кислота, 14 UA 100007 C2 5 10 15 20 25 30 35 40 45 50 55 60 ароматичною кислотою, як-то бензойна кислота або корична кислота, сульфоновою кислотою, як-то пара-толуолсульфонова кислота або етансульфонова кислота, тощо. Якщо патентоздатною сполукою є кислота, потрібну фармацевтично прийнятну сіль можна отримувати будь-яким придатним способом, наприклад обробкою вільної кислоти неорганічною або органічною основою. Кращі неорганічні солі є тими, які утворені з лужними та лужноземельними металами, як-то літій, натрій, калій, барій та кальцій. Кращі солі органічних основ охоплюють, наприклад, солі, вибрані з групи: амоній, дибензиламоній, бензиламоній, 2гідроксіетиламоній, біс(2-гідроксіетил)амоній, фенілетилбензиламін, дибензилетилендіамін, тощо. Інші солі кислотних частин можуть містити, наприклад, такі солі, утворені з прокаїном, хініном та N-метилглюкозаміном, а також солі, утворені з основними амінокислотами, як-то гліцин, орнітин, гістидин, фенілгліцин, лізин та аргінін. Способи виробництва сполук заявленого винаходу запропоновані як подальші особливості винаходу. Патентоздатні сполуки можуть бути отриманими, застосовуючи реакційні шляхи та схеми синтезу, які описано нижче, застосовуючи способи, доступні у попередньому рівні техніки, застосовуючи вихідні матеріали, котрі є легко доступними або їх можна синтезувати, застосовуючи способи, відомі у попередньому рівні техніки. Ілюстрації отримання сполук заявленого винаходу є показаними на Фіг. 1-7. Отримання сполуки формули 96 показане на Фіг. 1. Заміщений гідразин 28 можна перетворювати у гідразонопропаноат 29 за допомогою двостадійної процедури. На першому етапі, гідразин 28 конденсують з етилпіруватом у стандартних умовах дегідрування, як-то у присутності магнію сульфату у придатному органічному розчиннику, як-то хлороформ або метиленхлорид, при температурах у межах від 0 °С до температури довкілля. На другому етапі ацилування досягають обробкою основи при низькій температурі у придатному органічному розчиннику, як-то тетрагідрофуран, диметилформамід, діоксан або ацетонітрил, а потім додаванням метилмалонілхлориду. В одному втіленні гідразон обробляють LiH у тетрагідрофурані при 0 °С з наступним додаванням метилмалонілхлориду та нагріванням до кімнатної температури. Гідроксипіридазинон 31 отримують від гідразонопропаноату 29 за допомогою циклізації у сильно основних умовах, а потім декарбоксилуванням. Циклізації можна досягти обробкою гідразонопропаноату 29 сильною основою, як-то DBU, LDA або натрію гідрид, у придатному органічному розчиннику, як-то тетрагідрофуран або ацетонітрил, при кімнатній температурі. В одному втіленні циклізації досягають за допомогою DBU в ацетонітрилі при кімнатній температурі. Декарбоксилування для утворення гідроксипіридазинону 31 можна досягти нагріванням частини метилового естеру піразинону у придатному органічному розчиннику, як-то діоксан або декалін або суміш діоксан/декалін, до високої температури у присутності концентрованої НСl. Карбонова кислота 94 може бути отримана з гідроксипіридазинону 31 двостадійним способом, тобто хлоруванням а потім окисненням. Хлорування можна досягти обробкою РОСl3, тіонілхлоридом, оксалілхлоридом або РСl5. В одному втіленні цього перетворювання досягають за допомогою бездомішкового РОСl 3 при підвищеній температурі (приблизно 85 °С). Після етапу хлорування карбонова кислота 94 може бути отримана окисненням у стандартних умовах, охоплюючи, але без обмеження, КМnО 4 у воді, SeO2 в органічному розчиннику, як-то діоксан, ксилен або піридин, NaOCl/RuCl3, CrO3 у водній сульфатній кислоті, калію дихромат та натрію дихромат у воді. В одному втіленні цього перетворювання досягають за допомогою суміші калію дихромат-сульфатна кислота. Карбонову кислоту 94 можна перетворювати у піридазиноновий естер 95 двостадійною процедурою, котра охоплює естерифікацію піридазинонової кислоти 94 а потім паладійопосередковану реакцію перехресного сполучення. Естерифікація може бути проведена у стандартних умовах, охоплюючи, але без обмеження, концентровану НСl у метанолі, TMSCl у метанолі або TMSCHN2 у придатному органічному розчиннику, як-то етер/метанол, тетрагідрофуран/метанол або толуол/метанол. Паладій-опосередковану реакцію перехресного сполучення можна досягти стандартними способами, охоплюючи, але без обмеження, обробку піридазинонового естеру аніліном, паладієвим каталізатором, як-то Pd(OAc)2, PdCl2(dppf), Pd(Ph3P)4 або Pd2dba3, фосфіновим лігандом та основою у придатному органічному розчиннику, як-то тетрагідрофуран, диметилформамід, толуол, ДМЕ або ацетонітрил, при підвищеній температурі. В одному втіленні реакція перехресного сполучення полягає у обробці естеру 94 Pd(OAc)2, рац-2,2-біс(дифенілфосфіно)-1,1'-бінафтилом та цезію карбонатом у толуолі при 709 100 °С. У втіленні сполуки формули 95, де є потрібним R =Вr, бромозамісник може бути уведений після реакції перехресного сполучення. Бромування піридазинону можна досягти за допомогою NBS у придатному органічному розчиннику, як-то диметилформамід, ацетонітрил або змішані системи розчинників, при кімнатній температурі. В одному втіленні бромування проводиться у диметилформаміді. Гідроксамат 96 може бути отриманий обробкою 15 UA 100007 C2 5 10 15 20 25 30 35 40 45 50 55 60 піридазинонового естеру 95 прийнятним гідроксиламіном та амідною основою, як-то LDA, LiHMDS або NaHMDS, у придатному органічному розчиннику, як-то тетрагідрофуран, при низькій температурі. В одному втіленні розчин LiHMDS додають до розчину піридазинонового естеру 95 та гідроксиламіну у тетрагідрофурані при 0 °С. Реакційну суміш тоді нагрівають до кімнатної температури для утворення потрібного гідроксамату 96. У деяких обставинах гідроксиламін, застосовуваний у реакції сполучення, містить стандартну захисну групу. У цих випадках захисна група може бути видалена у стандартних умовах, відомих у попередньому рівні техніки. Фіг. 2 відображує синтез сполук 96, 100, 101 та 102. Заміщений гідразин 28 можна перетворювати у гідразономалонат 97 за допомогою однієї з двох процедур. В одному втіленні конденсація заміщеного гідразину 28, а потім ацилування є особливо корисними для аналогів, 9 де R - алкіл або галоген. У цьому втіленні гідразин 28 може бути конденсований із діетил-2оксомалонатом у стандартних умовах дегідратування, застосовуючи пастку Діна-Старка, у придатному органічному розчиннику, як-то бензол або толуол, при температурах у межах від 80 до 120 °С. Ацилування за допомогою реагенту, що поставляє ацильну групу для забезпечення гідразономалонату 97, досягають обробкою основою при прийнятній температурі у придатному органічному розчиннику, як-то тетрагідрофуран, диметилформамід, діоксан або ацетонітрил, а потім додаванням реагенту ацилування. Приклади реагентів ацилування добре відомі спеціалістам та охоплюють, але без обмеження, хлорангідриди кислоти, ангідриди кислот та активовані естери. В одному втіленні гідразон обробляють LiH у тетрагідрофурані при 0 °С з наступним додаванням хлорангідриду кислоти та перемішуванням при 25 до 60 °С для 9 забезпечення сполук 97. Альтернативний спосіб синтезу сполук 97, де R не є галогеном, полягає в ацилуванні гідразину 28 за допомогою реагенту, що поставляє ацильну групу, а потім конденсації із діетил-2-оксомалонатом для забезпечення гідразономалонату 97. Згідно з цим способом, заміщений гідразин 28 можна перетворювати у гідразид стандартними способами ацилування. В одному втіленні цього перетворювання досягають за допомогою прийнятного хлорангідриду кислоти у метиленхлориді при від 0 °С до температури довкілля. Отриманий гідразид конденсують з діетилкетомалонатом у стандартних умовах дегідратування, застосовуючи пастку Діна-Старка, у придатному органічному розчиннику, як-то бензол або толуол, при температурі від 80 до 130 °С. Піридазинон 99 отримують з гідразономалонату 97 за допомогою циклізації в основних умовах для забезпечення проміжної кислоти або естеру 98, а потім хлорування для забезпечення піридазинону 99. Циклізації можна досягти обробкою гідразономалонату 7 амідною основою, як-то LiHMDS, NaHMDS, KHMDS або LDA, у придатному органічному розчиннику, як-то тетрагідрофуран або етер, при низькій температурі. В одному втіленні циклізації досягають за допомогою LiHMDS у тетрагідрофурані при низькій температурі (від -78 до -40 °С), з наступною обробкою концентрованою НСl для утворення естерного похідного 98 (R=етил). У ще одному втіленні кислотне похідне 98 (R=Н) отримують за допомогою омилення на місці піридазинонового естеру 98. Після завершення циклізації, реакційну суміш гасять водою при низьких температурах (від -78 до -40 °С), тоді нагрівають до температури довкілля із перемішуванням, а потім підкисляють. Піридазинон 99 тоді отримують з піридазинонової кислоти або естеру 98 обробкою РОСl3, тіонілхлоридом, оксалілхлоридом або РСl5. В одному втіленні цього перетворювання досягають за допомогою бездомішкового РОСl3 9 при підвищеній температурі (приблизно 85 °С). Коли R не є атомом F, піридазинонову кислоту 99 (коли R=Н) можна тоді перетворювати у піридазинон 101. Уведення анілінової частини досягають за допомогою реакції SNAR у придатному органічному розчиннику, як-то тетрагідрофуран, застосовуючи амідну основу, як-то LDA, LiHMDS, NaHMDS або KHMDS, при прийнятній температурі (від -78 °С до кімнатної температури). В одному втіленні анілін додають до LDA або LiHMDS у тетрагідрофурані при низькій температурі (-20 до -80 °С). Піридазинонову кислоту 99 (R=Н) тоді додають та реакційну суміш нагрівають до кімнатної температури для утворення карбонової кислоти 101. Гідроксамати 96 та аміди 102 можуть тоді бути отриманими з кислоти 101, застосовуючи стандартний реагент сполучення, як-то, але без обмеження, 1-(3диметиламінопропіл)-3-етилкарбодіімід гідрохлориду (EDCl), 1-гідроксибензотриазол-6сульфонамідометил гідрохлориду (HOBt) або бензотриазол-1-ілокситрипіролідинофосфоній гексафлуорфосфату (РуВОР), та прийнятний амін або гідроксиламін у придатному органічному розчиннику, як-то диметилформамід, тетрагідрофуран або метиленхлорид. У деяких обставинах амін або гідроксиламін містить стандартну захисну групу. У цих випадках захисна група може бути видалена у стандартних умовах, відомих у попередньому рівні техніки. Альтернативно, естер піридазинону 99 (R=етил) можна перетворювати у гідроксамат 96 через піридазиноновий естер 100 стандартними способами, описаними на Фіг. 1. Коли є потрібним 8 R =Вr або І, потрібний галоген може бути уведений, застосовуючи NBS або NIS у придатному 16 UA 100007 C2 5 10 15 20 25 30 35 40 45 50 55 60 органічному розчиннику або змішаній системі розчинників, як-то диметилформамід, тетрагідрофуран-метанол, або АсОН-тетрагідрофуран, у присутності прийнятного кислотного каталізатора. На Фіг. 3 наведено синтез сполук 109, 110 та 111, де застосовано 2,6-дихлорнікотинову кислоту як вихідний матеріал. Нікотинову кислоту 103 перетворюють у монохлоркислоту 104 кип'ятінням із зворотним холодильником у 2 Н водному розчині натрію гідроксиду виконанням процедури, описаної у патенті США № 3,682,932. Алкілування 104 для забезпечення 105 можна досягти за допомогою стандартних основних умов алкілування, уводячи алкілгалогеніди з двома еквівалентами прийнятного алкілгалогеніду та основою з утворенням суміші Nалкілпіридонового естеру 105 та регіоізомерного О-алкілпіридинового естеру, котрі легко відокремлювати хроматографією на колонці. Ці умови охоплюють, але без обмеження, калію карбонат в ацетоні або диметилформаміді при кімнатній температурі або підвищеній температурі або натрію гідрид у тетрагідрофурані при температурі довкілля або підвищеній температурі та тоді додавання алкілгалогеніду. У деяких втіленнях такого алкілування досягають за допомогою LiH у диметилформаміді при 0 °С, з наступним додаванням алкілброміду або алкілйодиду та нагрівання до кімнатної температури. Бромування піридонового естеру 105 можна досягти з Вr2 та оцтовою кислотою або NBS у придатному органічному розчиннику, як-то диметилформамід. У деяких втіленнях NBS додають до розчину піридонового естеру 105 у диметилформаміді для утворення 106. Перетворювання броміду 106 у сполуку 107 можна досягти, застосовуючи опосередковані паладієм умови перехресного 9 сполучення. Коли R =алкеніл або алкініл, вони можуть бути далі відновленими, застосовуючи 9 прийнятний відновник для забезпечення алкільних замісників при R . Загалом, цього хімічного перетворення можна досягти, застосовуючи широку різноманітність паладієвих каталізаторів та лігандів, з додаванням основи або без неї, у придатному органічному розчиннику, як-то диметилформамід, толуол, ДМЕ, тетрагідрофуран, ацетонітрил, при підвищеній температурі. 9 9 Партнер сполучення залежатиме від природи R . Наприклад, якщо потрібний R =CN, партнером сполучення є Zn(CN)2. Ця реакція може бути проведена за допомогою Pd2dba3 та dppf у Nметилпіролідоні при 120 °С. Ці опосередковані паладієм реакції перехресного сполучення є добре задокументованими у літературі та добре відомі спеціалістам. Уведення належним чином заміщеної анілінової частини для забезпечення 108 досягають за допомогою реакції SNAR. Це може бути виконано у придатному органічному розчиннику, як-то тетрагідрофуран, застосовуючи амідну основу, як-то LDA, LiHMDS, NaHMDS або KHMDS, при прийнятних температурах (від -78 °С до кімнатної температури). У деяких втіленнях анілін додають до LDA або LiHMDS у тетрагідрофурані при низькій температурі (від -20 до -80 °С). Піридон 105 тоді додають та суміш перемішують при низькій температурі для утворення естеру 108. Карбонова кислота 109 може тоді бути отримана, застосовуючи стандартні умови омилення, як-то LiOH або натрію гідроксид, у стандартних змішаних системах водноорганічних розчинників. Гідроксамат 110 та амід 111 можуть бути отримані, застосовуючи стандартні процедури сполучення, за допомогою, але без обмеження, EDCl, HOBt або РуВОР та прийнятного аміну або гідроксиламіну у придатному органічному розчиннику, як-то диметилформамід, тетрагідрофуран або метиленхлорид. У деяких втіленнях, сполучення досягають за допомогою HOBt та EDCl у диметилформаміді. У деяких обставинах амін або гідроксиламін, застосовувані у реакції сполучення, містять стандартні захисні групи. У цих випадках захисна група може бути видалена у стандартних умовах, відомих у попередньому рівні техніки. Фіг. 4 показує альтернативну схему реакцій для синтезу сполук 109, 110 та 111. Цей шлях є 7 особливо корисним для аналогів, де R не представляє метил або етил. Нікотинову кислоту 103 можна перетворювати у метиловий естер N-алкілпіридону 114 за допомогою процедури з семи етапів, де 2,6-дихлорнікотинову кислоту 103 спершу перетворюють у метоксипіридинову кислоту, котру естерифікують з утворенням метилового естеру, та тоді позбавляють захисту для утворення монохлорестеру 112. У деяких втіленнях перетворювання у метоксипіридинову кислоту проводять додаванням калію трет-бутоксиду до розчину кислоти 103 у метанолі та цю суміш тоді нагрівають до температури кипіння зі зворотним холодильником протягом кількох діб. Естерифікація з утворенням метилового естеру може бути проведена у стандартних умовах, охоплюючи, але без обмеження, естерифікацію за Фішером (метанол, сульфатна кислота), TMSCl у метанолі або TMSCHN2 у придатному органічному розчиннику, як-то толуол/метанол. Деметилування метоксипіридину можна тоді досягти стандартними умовами, охоплюючи, але без обмеження, розчин НСl при підвищеній температурі, розчин n-TsOH в оцтовій кислоті при підвищеній температурі та водний розчин НВr у метанолі при підвищеній температурі. Кращого деметилування з утворенням піридону 112 досягають обробкою метоксипіридину водним розчином НВr в оцтовій кислоті при підвищеній температурі (від 80 до 120 °С). Алкілування 112 17 UA 100007 C2 5 10 15 20 25 30 35 40 45 50 55 60 можна досягти за допомогою стандартних основних умов алкілування, уводячи алкілгалогеніди, з одним еквівалентом прийнятного алкілгалогеніду та основою з утворенням суміші Nалкілпіридонового естеру 113 та регіоізомерного О-алкілпіридинового естеру, котрі є легко відокремлюваними хроматографією на колонці. Ці умови охоплюють, але без обмеження, калію карбонат в ацетоні або диметилформаміді при кімнатній температурі або підвищеній температурі або натрію гідрид у тетрагідрофурані при температурі довкілля або підвищеній температурі, та тоді додавання алкілгалогеніду. У деяких втіленнях такого алкілування досягають за допомогою LiH у диметилформаміді при 0 °С, з наступним додаванням алкілброміду або алкілйодиду та нагріванням до кімнатної температури. Бромування піридонового естеру 113 можна досягти за допомогою Вr 2 та оцтової кислоти або NBS у придатному органічному розчиннику, як-то диметилформамід. У деяких втіленнях NBS додають до розчину піридонового естеру 113 у диметилформаміді для утворення 114. Перетворювання броміду 114 у сполуку 115 можна досягти, застосовуючи опосередковані паладієм умови 9 перехресного сполучення. Коли R =алкеніл або алкініл, вони можуть бути далі відновлені, 9 застосовуючи прийнятний відновник для забезпечення алкільних замісників при R . Загалом, цього хімічного перетворення можна досягти, застосовуючи широку різноманітність паладієвих каталізаторів та лігандів, з додаванням основи або без неї, у придатному органічному розчиннику, як-то диметилформамід, толуол, ДМЕ, тетрагідрофуран, ацетонітрил, при 9 підвищеній температурі. Партнер сполучення залежатиме від природи R . Ці опосередковані паладієм реакції перехресного сполучення є добре задокументованими у літературі та добре відомі спеціалістам. Уведення належним чином заміщеної анілінової частини для забезпечення 116 досягають за допомогою реакції SNAR. Це може бути виконано у придатному органічному розчиннику, як-то тетрагідрофуран, застосовуючи амідну основу, як-то LDA, LiHMDS, NaHMDS або KHMDS, при прийнятних температурах (від -78 °С до кімнатної температури). У деяких втіленнях анілін додають до LDA або LiHMDS у тетрагідрофурані при низькій температурі (від 20 до -80 °С). Піридон 115 тоді додають та суміш перемішують при низькій температурі для утворення естеру 116. Перетворювання 116 у карбонову кислоту 109, а також гідроксамат 110 та амід 111 можна досягти, як описано для Фіг. 3. Альтернативно, гідроксамат 110 може бути отриманий безпосередньо з метилового естеру 116 у придатному органічному розчиннику, як-то тетрагідрофуран, застосовуючи прийнятний гідроксиламін та амідну основу, як-то LDA, LiHMDS, NaHMDS або KHMDS, при прийнятних температурах (від -78 °С до кімнатної температури). У деяких втіленнях, розчин LiHMDS додають до розчину естеру 116 та гідроксиламіну у тетрагідрофурані при 0 °С. Реакційну суміш тоді нагрівають до кімнатної температури для утворення потрібного гідроксамату 110. У деяких обставинах гідроксиламін, застосовуваний у реакції сполучення, містить стандартні захисні групи. У цих випадках захисна група може бути видалена у стандартних умовах, відомих у попередньому рівні техніки. Фіг. 5 показує схему реакцій для синтезу сполук 119, 120 та 121, де метиловий естер Nалкілпіридону 112 застосований як вихідний матеріал. Утворення 117 можна досягти за допомогою уведення належним чином заміщеної анілінової частини за допомогою реакції SNAR. Це може бути виконано у придатному органічному розчиннику, як-то тетрагідрофуран, застосовуючи амідну основу, як-то LDA, LiHMDS, NaHMDS або KHMDS, при прийнятних температурах (від -78 °С до кімнатної температури). У деяких втіленнях анілін додають до LDA або LiHMDS у тетрагідрофурані при низькій температурі (від -20 до -80 °С). Піридон 112 тоді додають та суміш перемішують при низькій температурі для утворення естеру 117. Це може бути виконано у придатному органічному розчиннику, як-то тетрагідрофуран, застосовуючи амідну основу, як-то LDA, LiHMDS, NaHMDS або KHMDS, при прийнятних температурах (від -78 °С до кімнатної температури). Хлорування піридону 117 з утворенням піридону 118 можна досягти, застосовуючи стандартні умови, як-то NCS, у придатному органічному розчиннику, якто диметилформамід. Перетворювання 118 у карбонову кислоту 119, а також гідроксамат 120 та амід 121 можна досягти, як описано для Фіг. 3 та 4. Фіг. 6 показує схему реакцій для синтезу сполук 124 та 125. 4-Флуорпіридазинон 123 може бути отриманий з 4-хлорпіридазинону 122 обробкою KF або HF з основою, як-то Et3N або Me3N, або без неї у придатному органічному розчиннику, як-то ацетонітрил, тетрагідрофуран, диметилформамід, N-метилпіролідон або ДМСО. В одному втіленні цього перетворювання досягають за допомогою KF у ДМСО при підвищеній температурі (наприклад, 160 °С). Піридазиноновий естер 123 (коли R=етил) можна перетворювати у піридазинон 124, де уведення анілінової частини досягають за допомогою реакції SNAR. Це може бути виконано у придатному органічному розчиннику, як-то диметилформамід, етанол, ізопропанол, ацетонітрил або тетрагідрофуран, застосовуючи основу, як-то цезію карбонат, натрію гідрокарбонат, калію карбонат або натрію карбонат при температурі від 80 до 160 °С. В одному втіленні анілін та 18 UA 100007 C2 5 10 15 20 25 30 35 40 45 50 55 60 цезію карбонат додають до розчину піридазинону 123 у диметилформаміді та реакційну суміш нагрівають до 80 °С. Альтернативно, піридазинонову кислоту 123 (R=Н) можна перетворювати у піридазинон 125 стандартними способами, як-то тими, що описані на Фіг. 2. Піридазинон 124 або 125 можна перетворювати у гідроксамати або аміди, як описано на Фіг. 1 або 2. Фіг. 7 показує схему реакцій для синтезу сполук 128, 129 та 130, де метиловий естер піридону 117 застосовано як вихідний матеріал. Бромування піридонового естеру 117 можна досягти за допомогою Вr2 та оцтової кислоти або NBS у придатному органічному розчиннику, якто диметилформамід. Переважно NBS додають до розчину піридонового естеру 117 у 9 диметилформаміді для утворення 126. Перетворювання броміду 126 у сполуку 127, де R ціаногрупа, можна досягти, застосовуючи опосередковані паладієм умови перехресного сполучення. Загалом, цього хімічного перетворення можна досягти, застосовуючи широку різноманітність паладієвих каталізаторів та лігандів, з додаванням основи або без неї, у придатному органічному розчиннику, як-то диметилформамід, толуол, ДМЕ, тетрагідрофуран, ацетонітрил або N-метилпіролідон, при підвищеній температурі. Переважно, цю реакцію проводять за допомогою Zn(CN)2, Pd2dba3 та dppf у диметилформаміді при 120 °С. Перетворювання 127 у карбонову кислоту 128, а також гідроксамат 129 та амід 130 можна досягти, як описано для Фіг. 3 та 4. 9 На Фіг. 8 представлено синтез сполук формули V, де R =Н або F, у котрому застосовано як вихідний матеріал 2,6-дихлорнікотинову кислоту або 2,6-дихлор-5-флуорнікотинову кислоту. 7 Цей шлях є особливо корисним для аналогів, де R - метил. Нікотинову кислоту 140 перетворюють у монохлоркислоту 141 кип'ятінням зі зворотним холодильником у 2 Н водному розчині натрію гідроксиду виконанням процедури, описаної у патенті США 3682932 (1972). Алкілування 141 можна досягти за допомогою стандартних основних умов алкілування, уводячи алкілгалогеніди з двома еквівалентами прийнятного алкілгалогеніду та основою з утворенням суміші N-алкілпіридонового естеру та регіоізомерного О-алкілпіридонового естеру, котрі є легко відокремлюваними хроматографією на колонці. Ці умови охоплюють але без обмеження, додавання калію карбонату в ацетоні або диметилформаміді при кімнатній температурі або підвищеній температурі або натрію гідриду у тетрагідрофурані при температурі довкілля або підвищеній температурі, та тоді додавання алкілгалогеніду. Переважно такого алкілування досягають за допомогою LiH у диметилформаміді при 0 °С, з наступним додаванням алкілброміду або алкілйодиду та нагріванням до кімнатної температури. Уведення належним чином заміщеної анілінової частини для забезпечення 143 досягають за допомогою реакції SNAR. Це може бути виконано у придатному органічному розчиннику, як-то тетрагідрофуран, застосовуючи амідну основу, як-то LDA, LiHMDS, NaHMDS або KHMDS, при прийнятних температурах (від -78 °С до кімнатної температури). Переважно анілін додають до LDA або LiHMDS у тетрагідрофурані при низькій температурі (від -20 до -80 °С). Піридон тоді додають та суміш перемішують при низькій температурі для утворення естеру 143. Карбонова кислота 144 може тоді бути отримана, застосовуючи стандартні умови омилення, як-то LiOH або натрію гідроксид у стандартних змішаних системах водноорганічних розчинників. Гідроксамат 145 та амід 146 можуть бути отримані, застосовуючи стандартні процедури сполучення, охоплюючи, але без обмеження, EDCl, HOBt або РуВОР та прийнятний амін або гідроксиламін у придатному органічному розчиннику, як-то диметилформамід, тетрагідрофуран або метиленхлорид. Переважно, сполучення досягають за допомогою HOBt та EDCl у диметилформаміді. У деяких обставинах амін або гідроксиламін, застосовуваний у реакції сполучення, містить стандартні захисні групи. У цих випадках захисна група може бути видалена у стандартних умовах, відомих у попередньому рівні техніки. 9 На Фіг. 9 представлено альтернативний синтез сполук формули V, де R =Н або F, у котрому застосовано як вихідний матеріал 2,6-дихлорнікотинову кислоту або 2,6-дихлор-5флуорнікотинову кислоту. Нікотинову кислоту 140 можна перетворювати у метиловий естер Nалкілпіридону 149 після процедури з п'яти етапів, де 2,6-дихлорнікотинову кислоту 140 спершу перетворюють у метоксипіридинову кислоту, котру естерифікують з утворенням метилового естеру та тоді позбавляють захисту для утворення монохлорестеру 147. Перетворювання у метоксипіридинову кислоту переважно проводять додаванням калію трет-бутоксиду до розчину кислоти 140 у метанолі, та цю суміш тоді нагрівають до температури кипіння зі зворотним холодильником протягом кількох діб. Естерифікація з утворенням метилового естеру може бути проведена у стандартних умовах, охоплюючи, але без обмеження, естерифікацію за Фішером (метанол, сульфатна кислота), TMSCl у метанолі або TMSCHN 2 у придатному органічному розчиннику, як-то толуол/метанол. Деметилування метоксипіридину можна тоді досягти стандартними умовами, охоплюючи, але без обмеження, НСl при підвищеній температурі, nTsOH в оцтовій кислоті при підвищеній температурі та водний розчин НВr у метанолі при 19 UA 100007 C2 5 10 15 20 25 підвищеній температурі. Кращого деметилування з утворенням піридону 147 досягають обробкою метоксипіридину водним розчином НВr в оцтовій кислоті при підвищеній температурі (від 80 до 120 °С). Алкілування 147 для забезпечення 148 можна досягти за допомогою стандартних основних умов алкілування, уводячи алкілгалогеніди з одним еквівалентом прийнятного алкілгалогеніду та основою з утворенням суміші N-алкілпіридонового естеру та регіоізомерного О-алкілпіридонового естеру, котрі є легко відокремлюваними хроматографією на колонці. Ці умови охоплюють але без обмеження, калію карбонат в ацетоні або диметилформаміді при кімнатній температурі або підвищеній температурі або натрію гідрид у тетрагідрофурані при температурі довкілля або підвищеній температурі та тоді додавання алкілгалогеніду. Переважно такого алкілування досягають за допомогою LіН у диметилформаміді при 0 °С, з наступним додаванням алкілброміду або алкілйодиду та нагріванням до кімнатної температури. Уведення належним чином заміщеної анілінової частини досягають за допомогою реакції SNAR. Це може бути виконано у придатному органічному розчиннику, як-то тетрагідрофуран, застосовуючи амідну основу, як-то LDA, LiHMDS, NaHMDS або KHMDS, при прийнятних температурах (від -78 °С до кімнатної температури). Переважно анілін додають до LDA або LiHMDS у тетрагідрофурані при низькій температурі (від -20 до -80 °С). Піридон тоді додають та суміш перемішують при низькій температурі для утворення естеру 149. Гідроксамат 145 може бути отриманий безпосередньо з метилового естеру 149 у придатному органічному розчиннику, як-то тетрагідрофуран, застосовуючи прийнятний гідроксиламін та застосовуючи амідну основу, як-то LDA, LiHMDS, NaHMDS або KHMDS, при прийнятних температурах (від -78 °С до кімнатної температури). Переважно, розчин LiHMDS додають до розчину метилового естеру 149 та гідроксиламіну у тетрагідрофурані при 0 °С. Реакційну суміш тоді нагрівають до кімнатної температури для утворення потрібного гідроксамату 145. У деяких обставинах гідроксиламін, застосовуваний у реакції сполучення, містить стандартні захисні групи. У цих випадках захисна група може бути видалена у стандартних умовах, відомих у попередньому рівні техніки. У наступному аспекті цей винахід стосується способу отримання сполуки формули ІА, вказаний спосіб полягає у наступному: реакція сполуки формули 100 або 101 30 O O HO R1 H N N O R1 H N N N N R7 R7 R8 R9 O R8 R9 O 100 101 3 35 3 з R NH2 у присутності (і) реагенту сполучення, коли R є таким, як визначено у формулі ІА, 3 3 або (іі) амідної основи, коли R є таким, як визначено у формулі ІА, за винятком того, що R не представляє Н або метил, для забезпечення отримання вказаної сполуки формули ІА. У наступному аспекті цей винахід стосується способу отримання сполуки формули IV, вказаний спосіб полягає у наступному: реакція сполуки формули 108 або 109 O R O HO R1 O H N H N N R9 O 3 45 N R7 40 R1 R8 R9 108 R7 O R8 109 3 з R NH2, де R є таким, як визначено у формулі IV, у присутності (і) реагенту сполучення або 3 3 (іі) амідної основи, коли R є таким, як визначено у формулі IV, за винятком того, що R не представляє Н або метил. У наступному аспекті цей винахід стосується способу отримання сполуки формули VI, вказаний спосіб полягає у наступному: (a) бромування сполуки, що має формулу 105 20 UA 100007 C2 O RO Cl N O , де R - алкіл, для забезпечення отримання сполуки формули 106 O RO Cl N Br O 5 , (b) реакція сполуки формули 106 з Zn(Me)2 у присутності паладієвого каталізатора та ліганду та необов'язково у присутності основи, для забезпечення отримання сполуки формули 107 O RO Cl N R9 O 10 , (c) реакція сполуки формули 107 з аніліном, що має формулу R1 H2N I, 15 у присутності паладієвого каталізатора, фосфінового ліганду та амідної основи, для забезпечення отримання сполуки формули 108 CH3O O R1 H N N R9 O I , 20 (d) необов'язково гідролізування сполуки формули 108 в основних умовах для забезпечення отримання сполуки формули 109 21 UA 100007 C2 HO O R1 H N N R9 I O , та 3 (e) реакція сполуки 108 або сполуки 109 з R NH2 у присутності (і) реагенту сполучення, коли 3 R є таким, як визначено у формулі VI, або (іі) амідної основи, коли R є таким, як визначено у 3 формулі VI, за винятком того, що R не представляє Н, для забезпечення отримання вказаної сполуки формули VI. В одному втіленні сполуку 105 отримують способом, що полягає у наступному: (a) реакція сполуки формули 103 3 5 O HO Cl N Cl 10 з водним розчином натрію гідроксиду для забезпечення отримання сполуки формули 104 O HO Cl NH N O , та 15 20 25 (b) реакція сполуки формули 104 з RX, де R - метил та X - галогенід, у присутності основи для забезпечення отримання сполуки формули 105. У наступному аспекті цей винахід стосується способу отримання сполуки формули II, вказаний спосіб полягає у наступному: (a) реакція гідразину, що має формулу Me-NH-NH2, із: (і) діетил-2-оксомалонатом, з наступною обробкою реагентом ацилування, що поставляє 9 9 ацильну групу, що має формулу C(=O)CH2R , де R є таким, як визначено у формулі II, або 9 9 (іі) реагентом ацилування, що поставляє ацильну групу, що має формулу C(=O)CH 2R , де R є таким, як визначено у формулі II, з наступною обробкою діетилкетомалонатомом, для забезпечення отримання сполуки формули 97 CO2Et N CO2Et N R9 O 30 , (b) обробка сполуки формули 97 амідною основою при температурі нижче -40 °С, з наступною обробкою концентрованою НСl, для забезпечення отримання формули 98 22 UA 100007 C2 CO2Et OH N N R9 O , (c) хлорування сполуки формули 98 для забезпечення отримання сполуки формули 99 CO2Et Cl N N R9 O 5 , (d) реакція сполуки формули 99 з аніліном, що має формулу F H2 N SMe , 10 у присутності паладієвого каталізатора, ліганду, та амідної основи, для забезпечення отримання сполуки формули 100 O O F H N N N R9 SMe O , та 15 20 25 3 3 (e) реакція сполуки формули 100 із R NH2 у присутності (і) реагенту сполучення, коли R є 3 таким, як визначено у формулі II, або (іі) амідної основи, коли R є таким, як визначено у 3 формулі II, за винятком того, що R не представляє Н, для забезпечення отримання вказаної сполуки формули II. 9 У наступному аспекті цей винахід стосується способу отримання сполуки формули II, де R Н, метил або Сl, вказаний спосіб полягає у наступному: (a) реакція гідразину, що має формулу Me-NH-NH2, із: (і) діетил-2-оксомалонатом, з наступною обробкою реагентом ацилування, що поставляє 9 9 ацильну групу, що має формулу C(=O)CH2R , де R - Н, метил або Сl; або 9 9 (іі) реагентом ацилування, що поставляє ацильну групу, що має формулу C(=O)CH 2R , де R - Н, метил або Сl, з наступною обробкою діетилкетомалонатом, для забезпечення отримання сполуки формули 97 CO2Et CO2Et N N R9 O , 30 23 UA 100007 C2 (b) обробка сполуки формули 97 амідною основою при температурі нижче -40 °С з утворенням сполуки формули 98 CO2H OH N N R9 O , 5 (c) хлорування сполуки формули 98 для забезпечення отримання сполуки формули 99 CO2H Cl N HN N R9 O 10 , (d) реакція сполуки формули 99 з аніліном, що має формулу F H2 N SMe , у присутності амідної основи, для забезпечення отримання сполуки формули 101 15 O HO O F H N N N R9 SMe O , та 3 20 3 (e) реакція сполуки формули 101 із R NH2 у присутності (і) реагенту сполучення, коли R є 3 таким, як визначено у формулі II, або (іі) амідної основи, коли R є таким, як визначено у 3 формулі II, за винятком того, що R не представляє Н, для забезпечення отримання вказаної сполуки формули II. 9 У наступному аспекті цей винахід стосується способу отримання сполуки формули V, де R метил, вказаний спосіб полягає у наступному: (a) бромування сполуки, що має формулу 105 25 R O O Cl N O , де R - алкіл, для забезпечення отримання сполуки формули 106 24 UA 100007 C2 R O O Cl N Br O 5 , (b) реакція сполуки формули 106 із Zn(Me) 2 у присутності паладієвого каталізатора та ліганду, та необов'язково у присутності основи, для забезпечення отримання сполуки формули 107 R O O Cl N R9 O , (c) реакція сполуки формули 107 з аніліном, що має формулу 10 F H2 N SMe , у присутності амідної основи, для забезпечення отримання сполуки формули 108 R O O F H N N R9 SMe O 15 , (d) необов'язково гідролізування сполуки формули 108 в основних умовах для забезпечення отримання сполуки формули 109 O HO O F H N N R9 20 SMe O , та 3 25 3 (e) реакція сполуки формули 108 або сполуки формули 109 із R NH2, де R є таким, як визначено у формулі V, у присутності реагенту сполучення або амідної основи, для забезпечення отримання вказаної сполуки формули V. 9 У наступному аспекті цей винахід стосується способу отримання сполуки формули V, де R Сl, вказаний спосіб полягає у наступному: (а) реакція сполуки формули 112 25 UA 100007 C2 O O Cl N O з аніліном, що має формулу F H2 N SMe , 5 у присутності амідної основи для забезпечення отримання сполуки формули 117 O O F H N N SMe O , 10 (b) хлорування сполуки формули 117 для забезпечення отримання сполуки формули 118 O O F H N N Cl SMe O 15 , та (с) необов'язково гідролізування сполуки формули 118 для забезпечення отримання сполуки формули 118А O HO O F H N N Cl SMe O 20 25 , 118А (d) реакція сполуки формули 118 або 118А із (S)-MeCH(OH)CH2ONH2 або HOCH2CH2ONH2 у присутності реагенту сполучення або амідної основи, для забезпечення отримання вказаної сполуки формули V. 9 У наступному аспекті цей винахід стосується способу отримання сполуки формули V, де R Н або F, вказаний спосіб полягає у наступному: (а) обробка сполуки формули 140 26 UA 100007 C2 O HO O Cl N R9 Cl , 9 де R - Н або F, водним розчином натрію гідроксиду для забезпечення отримання сполуки формули 141 5 O HO O Cl N NH R9 O , (b) реакція сполуки формули 141 із СН 3Х, де X - галогенід, у присутності основи для забезпечення отримання сполуки формули 142 10 CH3O O Cl N NH R9 O , (c) реакція сполуки формули 142 з аніліном, що має формулу F H2 N SMe , 15 у присутності амідної основи для забезпечення отримання сполуки формули 143 CH3O O F H N N R9 SMe O , 20 (d) необов'язково гідролізування сполуки формули 143 для забезпечення отримання сполуки формули 144 27 UA 100007 C2 O HO O F H N N R9 SMe O , та 3 5 10 15 20 25 30 35 40 45 50 3 (e) реакція сполуки формули 143 або 144 із R NH2, де R є таким, як визначено у формулі V, у присутності реагенту сполучення або амідної основи, для забезпечення отримання вказаної сполуки формули V. В одному втіленні вищезазначених способів, засобом сполучення є 1-(3диметиламінопропіл)-3-етилкарбодіімід гідрохлориду, 1-гідроксибензотриазол-6сульфонамідометил гідрохлориду або бензотриазол-1-ілокситрипіролідинофосфоній гексафлуорфосфату. У наступному аспекті заявлений винахід стосується способу застосування сполуки цього винаходу як медикаменту для лікування хвороб або медичних станів, опосередкованих МЕК. Наприклад, цей винахід стосується сполуки цього винаходу як медикаменту для лікування гіперпроліферативного розладу або запального стану у ссавця, що полягає у призначенні вказаному ссавцю однієї або більше сполук заявленого винаходу або їх фармацевтично прийнятних солей або проліків у кількості, ефективній для лікування вказаного гіперпроліферативного розладу. У ще одному аспекті цей винахід стосується сполуки цього винаходу у виробництві медикаменту для лікування гіперпроліферативного розладу або запального стану. У наступному аспекті заявлений винахід стосується способу продукування МЕК-інгібіторної дії у теплокровної тварини, як-то людини, яка має необхідність у такому лікуванні, котрий полягає у призначенні вказаній тварині ефективної кількості сполуки цього винаходу. У наступному аспекті заявлений винахід стосується лікування або попередження МЕКопосередкованого стану, що полягає у призначенні людині або тварині, яка має необхідність у цьому, фармацевтичної композиції, що містить сполуку заявленого винаходу або її фармацевтично прийнятну сіль або in vivo здатні до розщеплення проліки у кількості, ефективній для лікування або попередження вказаного МЕК-опосередкованого стану. Винахід також стосується фармацевтичної композиції, що інгібує МЕК, що містить ефективну кількість сполуки, вибраної згідно із заявленим винаходом, або її фармацевтично прийнятних проліків, фармацевтично активних метаболітів або фармацевтично прийнятних солей. Винахід також стосується фармацевтичної композиції для лікування гіперпроліферативного розладу у ссавця, котра містить терапевтично ефективну кількість сполуки заявленого винаходу або її фармацевтично прийнятних солі, проліків або гідрату та фармацевтично прийнятний носій. В одному втіленні вказана фармацевтична композиція є призначеною для лікування раку, як-то раку мозку, раку легень, сквамозних клітин, раку сечового міхура, раку шлунка, раку підшлункової залози, раку молочних залоз, раку голови, раку шиї, раку нирок, ренального раку, раку яєчника, раку простати, раку ободової та прямої кишки, раку стравоходу, раку яєчок, гінекологічного раку або раку щитовидної залози. У ще одному втіленні вказана фармацевтична композиція є призначеною для лікування незлоякісного гіперпроліферативного розладу, як-то доброякісна гіперплазія шкіри (наприклад, псоріаз), рестеноз, або простати (наприклад, доброякісна простатична гіпертрофія (ВРН)). Винахід також стосується фармацевтичної композиції для лікування панкреатиту або хвороби нирок (охоплюючи проліферативний гломерулонефрит та індуковану діабетом хворобу нирок) або лікування болю у ссавця, котра містить терапевтично ефективну кількість сполуки заявленого винаходу або її фармацевтично прийнятних солі, проліків або гідрату та фармацевтично прийнятний носій. Винахід також стосується фармацевтичної композиції для попередження бластоцитної імплантації у ссавця, котра містить терапевтично ефективну кількість сполуки заявленого винаходу або її фармацевтично прийнятних солі, проліків або гідрату та фармацевтично прийнятний носій. Винахід також стосується фармацевтичної композиції для лікування хвороби, спорідненої з утворенням та розвитком судин або ангіогенез у ссавця, котра містить терапевтично ефективну кількість сполуки заявленого винаходу або її фармацевтично прийнятних солі проліків або гідрату та фармацевтично прийнятний носій. В одному втіленні вказана фармацевтична композиція є призначеною для лікування хвороби, вибраної з групи, що складається з 28
ДивитисяДодаткова інформація
Назва патенту англійськоюHeterocyclic inhibitors of mek, use thereof and pharmaceutical composition containing thereof
Автори англійськоюMarlow Allison L., Wallace Eli, Seo Jeongbeob, LYSSIKATOS JOSEPH P., YANG HONG WOON, Blake Jim, Storey Richard Anthony, Booth Rebecca Jane, Pittam John David, Leonard John, Fielding Mark Richard
Назва патенту російськоюГетероциклические ингибиторы мек, их применение и фармацевтическая композиция, которая их содержит
Автори російськоюМарлоу Эллисон Л., Воллес Илай, Сео Дзеонбеоб, Лиссикатос Джозеф П., Ян Гон Вун, Блейк Джим, Стори Ричард Энтони, Бус Ребекка Джейн, Питтам Джон Девид, Леонард Джон, Филдинг Марк Ричард
МПК / Мітки
МПК: A61P 35/00, A61K 31/50, C07D 237/24
Мітки: інгібітори, застосування, містить, гетероциклічні, фармацевтична, композиція, мек
Код посилання
<a href="https://ua.patents.su/105-100007-geterociklichni-ingibitori-mek-kh-zastosuvannya-ta-farmacevtichna-kompoziciya-shho-kh-mistit.html" target="_blank" rel="follow" title="База патентів України">Гетероциклічні інгібітори мек, їх застосування та фармацевтична композиція, що їх містить</a>
Попередній патент: Світлодіодна лампа для транспортного засобу
Наступний патент: Комбіноване лікування інгібіторами sglt-2 (натрійзалежний співпереносник глюкози 2) і фармацевтичною композицією, що їх містить
Випадковий патент: Ванна для гарячого цинкування металу