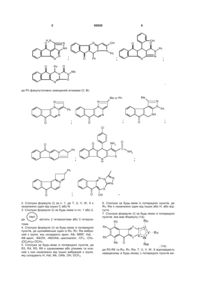
Інгібітори цистеїнпротеаз, фармацевтична композиція, яка їх містить, та їх терапевтичне застосування
Номер патенту: 95930
Опубліковано: 26.09.2011
Автори: Жак Ксав'є, Гюдо Філіпп, Буассі Гійом, Бор-Капра Катрін, Коллан Фредерік, Рен Жан-Крістоф, Дав'є Лоран, Перетто Іларія, Віньяндо Стефано, Формстеше Етьєнн, Делансорн Ремі
Формула / Реферат
1. Сполуки формули (І)
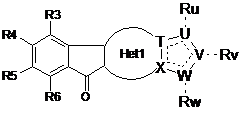 , (I)
, (I)
де:
![]() є або одинарний, або подвійний зв'язок, за обставинами;
є або одинарний, або подвійний зв'язок, за обставинами;
![]() відсутній або одинарний зв'язок, за обставинами;
відсутній або одинарний зв'язок, за обставинами;
![]() є 5-, 6- або 7-членний гетероцикл, за варіантом, якому віддається перевага, гетероарил, який містить 1-5 гетероатомів, факультативно заміщений одним або декількома замісниками, вибраними з групи, яку складають Н, CN, Hal, Alk, OAlk, OH, NRCN, C(CN)=C(OH)(OAlk), SR, NRR', C(O)NRR', гетероцикл, арил, гетероарил, де Alk, арил, гетероарил, гетероцикл факультативно заміщені однією або декількома Hal, NRR', CN, OH, CF3, арил, гетероарил, OAlk;
є 5-, 6- або 7-членний гетероцикл, за варіантом, якому віддається перевага, гетероарил, який містить 1-5 гетероатомів, факультативно заміщений одним або декількома замісниками, вибраними з групи, яку складають Н, CN, Hal, Alk, OAlk, OH, NRCN, C(CN)=C(OH)(OAlk), SR, NRR', C(O)NRR', гетероцикл, арил, гетероарил, де Alk, арил, гетероарил, гетероцикл факультативно заміщені однією або декількома Hal, NRR', CN, OH, CF3, арил, гетероарил, OAlk;
де ![]() та
та
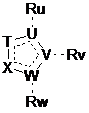 є конденсованими між собою за допомогою Т та X;
є конденсованими між собою за допомогою Т та X;
Т, U, V, W, X є однаковими або різними та можуть бути вибрані з-посеред С, N, О, S;
Ru, Rv, Rw є однаковими або різними та можуть бути вибрані з групи, яку складають Н, CN, =O, Hal, Alk, OAlk, ОН, пергалогеналкіл, NRCN, C(CN)=C(OH)(OAlk), SR, NRR', C(O)NRR' гетероцикл, арил, гетероарил, циклоалкіл, де Alk, арил, гетероарил, гетероцикл, циклоалкіл факультативно заміщені однією або декількома з таких груп, як Hal, NRR', CN, OH, CF3, арил, гетероарил, OAlk або полі(алкіленокси)група,
за умови, що щонайменше один із Ru, Rv, Rw є наявним та іншим ніж Н;
R3, R4, R5, R6 є однаковими або різними та кожний з них незалежно від інших вибраний з групи, яку складають Н, OAlk, Alk, Hal, NRR', CN, OH, OCF3, CF3, арил, гетероарил;
R та R' є однаковими або різними та кожний з них незалежно від інших вибраний з групи, яку складають Н, Alk, де Alk факультативно заміщений однією або декількома групами Hal, NRR', CN, OH, CF3, арил, гетероарил;
"алкіл" або "Alk" є аліфатичною вуглеводневою групою, нерозгалуженоюабо розгалуженою, яка має у ланцюгу 1-20 атомів вуглецю;
"гетероцикл" є насиченою, частково ненасиченою або ненасиченою, неароматичною стабільною 3-14-членною моно-, бі- або поліциклічною системою, де щонайменше одним членом циклу є гетероатом;
"арил" є ароматичною моноциклічною або поліциклічною вуглеводневою системою із 6-14 атомів вуглецю;
"гетероарил" є 5-14-членною ароматичною гетероциклічною моно-, бі- або поліциклічною системою;
"Hal" є атомом фтору, хлору, брому або йоду;
полі(алкіленокси)група містить 1-20 атомів вуглецю,
або фармацевтично прийнятні солі, гідрати або гідратовані солі, або поліморфні кристалічні структури цих сполук, або їхні оптичні ізомери, рацемати, діастереомери або енантіомери,
за винятком перелічених нижче сполук:
1-аміно-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он;
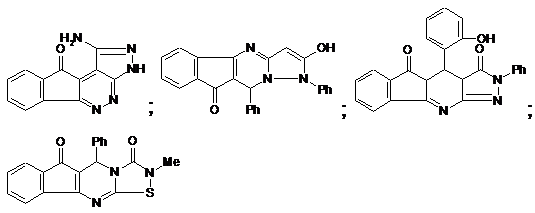 ,
,
де Ph факультативно заміщений атомами Сl, Вr;

2. Сполука формули (І) за п. 1, де Т, U, V, W, X є незалежно один від інших С або N.
3. Сполуки формули (І) за будь-яким із пп. 1 або 2, де ![]() містить 2 гетероатоми або 3 гетероатоми.
містить 2 гетероатоми або 3 гетероатоми.
4. Сполуки формули (І) за будь-яким із попередніх пунктів, де щонайменше один із Ru, Rv, Rw вибраний з групи, яку складають арил, Alk, NRR', Hal, -Alk-арил, -AlkOH, -AlkOAlk, циклоалкіл, -CF3, -CH2-(OC2H4)2-OCH3.
5. Сполука за будь-яким із попередніх пунктів, де R3, R4, R5, R6 є однаковими або різними та кожний з них незалежно від інших вибраний з групи, яку складають Н, Hal, Alk, OAlk, OH, OCF3.
6. Сполука за будь-яким із попередніх пунктів, де Rv, Rw є незалежно один від інших або Н, або відсутні.
7. Сполука формули (І) за будь-яким із попередніх пунктів, яка має Формулу (1а):
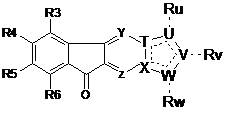 , (1а)
, (1а)
де R3-R6 та Ru, Rv, Rw, T, U, V, W, X відповідають наведеному в будь-якому з попередніх пунктів визначенню та Y, Z, однакові або різні, незалежно один від одного вибрані з-посеред С та N.
8. Сполука формули (І) за будь-яким із попередніх пунктів, яка має Формулу (Іb):
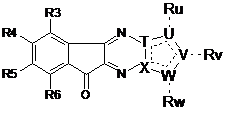 , (Іb)
, (Іb)
де R3-R6 та Ru, Rv, Rw, T, U, V, W, X відповідають наведеному в будь-якому з попередніх пунктів визначенню.
9. Сполука формули (І) за будь-яким із попередніх пунктів, де Rv=Rw=H та Ru вибраний з групи, яку складають арил, Alk, NRR', Hal, -Alk-арил, -AlkOH, -AlkOAlk, циклоалкіл, -CF3, -CH2-(OC2H4)2-OCH3.
10. Сполука формули (І) за будь-яким із попередніх пунктів, де R4=R5=H та R3, R6 незалежно один від одного вибрані з групи, яку складають Н, Hal, Alk, OAlk, OH, OCF3.
11. Сполука за будь-яким із попередніх пунктів, вибрана з групи, яку складають:
1-метил-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-метил-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
3-аміно-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-етил-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-етил-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-пропіл-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-пропіл-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-бутил-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-бутил-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-ізобутил-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-ізобутил-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-гідроксиметил-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-гідроксиметил-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-метоксиметил-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-метоксиметил-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-циклопропіл-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-циклопропіл-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-бензил-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-бензил-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-хлор-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
1-бром-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-бром-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
6-(7)-хлор-1-метил-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
7-хлор-3-метил-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
2-метил-2Н-1,2,3,4,10-пентаазациклопента[b]флуорен-9-он,
2-бензил-2Н-1,2,3,4,10-пентаазациклопента[b]флуорен-9-он,
1-ізопропіл-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-ізопропіл-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-трифторметил-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-трифторметил-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-[2-(2-метоксіетоксі)етоксиметил]-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
6,7-диметокси-1-метил-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
6,7-диметокси-3-метил-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-етил-6,7-диметокси-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-етил-6,7-диметокси-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
6,7-диметокси-1-пропіл-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
6,7-диметокси-3-пропіл-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-етил-5,8-диметокси-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-етил-5,8-диметокси-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
6,7-дигідрокси-1-метил-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он
або фармацевтично прийнятні солі, гідрати або гідратовані солі, або поліморфні кристалічні структури цих сполук, або їхні оптичні ізомери, рацемати, діастереомери або енантіомери.
12. Спосіб виготовлення сполуки формули (І) за будь-яким із попередніх пунктів, який включає стадію проведення реакції відповідної сполуки Формули (I'):
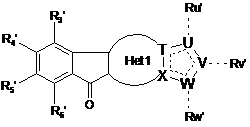 , (I')
, (I')
де Het1, T, U, V, W, X відповідають визначенням за будь-яким із пп. 1-7, та де щонайменше один із R3', R4', R5', R6', Ru', Rv', Rw' є групою-попередником відповідного R3, R4, R5, R6, Ru, Rv, Rw, а інші є подібними до бажаних R3, R4, R5, R6, Ru, Rv, Rw, в одну або кілька стадій, які уможливлюють перетворення групи-попередника у бажану групу R3, R4, R5, R6, Ru, Rv або Rw, та факультативно виділення сполуки формули (І).
13. Спосіб отримання сполуки за будь-яким із попередніх пунктів, який включає стадію проведення реакції відповідних сполук формули (II) та формули (III):
 ,
, ,
,
де R3, R4, R5, R6, Т, U, V, W, X, Ru, Rv, Rw відповідають визначенням за будь-яким із пп. 1-7,
причому реакцію здійснюють у присутності спирту та оцтової кислоти.
14. Спосіб за п. 13, де реакцію здійснюють у органічному протонному розчиннику у присутності кислоти.
15. Фармацевтична композиція, яка містить сполуку формули (І)
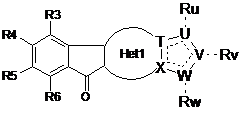 , (I)
, (I)
де:
![]() є або одинарний або подвійний зв'язок, за обставинами;
є або одинарний або подвійний зв'язок, за обставинами;
![]() відсутній або одинарний зв'язок, за обставинами;
відсутній або одинарний зв'язок, за обставинами;
![]() є 5-, 6- або 7-членний гетероцикл, за варіантом, якому віддається перевага, гетероарил, який містить 1-5 гетероатомів, факультативно заміщений одним або декількома замісниками, вибраними з групи, яку складають Н, CN, Hal, Alk, OAlk, OH, NRCN, C(CN)=C(OH)(OAlk), SR, NRR', C(O)NRR', гетероцикл, арил, гетероарил, де Alk, арил, гетероарил, гетероцикл факультативно заміщені однією або декількома Hal, NRR', CN, OH, CF3, арил, гетероарил, OAlk;
є 5-, 6- або 7-членний гетероцикл, за варіантом, якому віддається перевага, гетероарил, який містить 1-5 гетероатомів, факультативно заміщений одним або декількома замісниками, вибраними з групи, яку складають Н, CN, Hal, Alk, OAlk, OH, NRCN, C(CN)=C(OH)(OAlk), SR, NRR', C(O)NRR', гетероцикл, арил, гетероарил, де Alk, арил, гетероарил, гетероцикл факультативно заміщені однією або декількома Hal, NRR', CN, OH, CF3, арил, гетероарил, OAlk;
де ![]() та
та
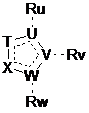 є конденсованими між собою за допомогою Т та X;
є конденсованими між собою за допомогою Т та X;
Т, U, V, W, X є однаковими або різними та можуть бути вибрані з-посеред С, N, О, S;
Ru, Rv, Rw є однаковими або різними та можуть бути вибрані з групи, яку складають Н, CN, =O, Hal, Alk, OAlk, ОН, пергалогеналкіл, NRCN, C(CN)=C(OH)(OAlk), SR, NRR', C(O)NRR' гетероцикл, арил, гетероарил, циклоалкіл, де Alk, арил, гетероарил, гетероцикл, циклоалкіл факультативно заміщені однією або декількома з таких груп, як Hal, NRR', CN, OH, CF3, арил, гетероарил, OAlk або полі(алкіленокси)група, за умови, що щонайменше один із Ru, Rv, Rw є наявним та іншим ніж Н;
R3, R4, R5, R6 є однаковими або різними та кожний з них незалежно від інших вибраний з групи, яку складають Н, OAlk, Alk, Hal, NRR', CN, OH, OCF3, CF3, арил, гетероарил;
R та R' є однаковими або різними та кожний з них незалежно від інших вибраний з групи, яку складають Н, Alk, де Alk факультативно заміщений однією або декількома групами Hal, NRR', CN, OH, CF3, арил, гетероарил;
"алкіл" або "Alk" є аліфатичною вуглеводневою групою, нерозгалуженою або розгалуженою, яка має у ланцюгу 1-20 атомів вуглецю;
"гетероцикл" є насиченою, частково ненасиченою або ненасиченою, неароматичною стабільною 3-14-членною моно-, бі- або поліциклічною системою, де щонайменше одним членом циклу є гетероатом;
"арил" є ароматичною моноциклічною або поліциклічною вуглеводневою системою із 6-14 атомів вуглецю;
"гетероарил" є 5-14-членною ароматичною гетероциклічною моно-, бі- або поліциклічною системою;
"Hal" є атомом фтору, хлору, брому або йоду;
полі(алкіленокси)група містить 1-20 атомів вуглецю,
або фармацевтично прийнятні солі, гідрати або гідратовані солі, або поліморфні кристалічні структури цих сполук, або їхні оптичні ізомери, рацемати, діастереомери або енантіомери та фармацевтично прийнятний носій.
16. Фармацевтична композиція за п. 15, де Формула (І) відповідає визначенню за будь-яким із пп. 2-10.
17. Фармацевтична композиція за п. 15 або п. 16, де згадана сполука Формули (І) вибрана з групи, яку складають:
1-метил-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-метил-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-аміно-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-аміно-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-етил-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-етил-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-пропіл-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-пропіл-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-бутил-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-бутил-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-ізобутил-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-ізобутил-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-гідроксиметил-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-гідроксиметил-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-метоксиметил-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-метоксиметил-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-циклопропіл-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-циклопропіл-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-бензил-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-бензил-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-хлор-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
1-бром-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-бром-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
6-(7)-хлор-1-метил-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
7-хлор-3-метил-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
2-метил-2Н-1,2,3,4,10-пентаазациклопента[b]флуорен-9-он,
2-бензил-2Н-1,2,3,4,10-пентаазациклопента[b]флуорен-9-он,
1-ізопропіл-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-ізопропіл-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-трифторметил-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-трифторметил-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-[2-(2-метоксіетоксі)етоксиметил]-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
6,7-диметокси-1-метил-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
6,7-диметокси-3-метил-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-етил-6,7-диметокси-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-етил-6,7-диметокси-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
6,7-диметокси-1-пропіл-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
6,7-диметокси-3-пропіл-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
1-етил-5,8-диметокси-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он,
3-етил-5,8-диметокси-1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он,
6,7-дигідрокси-1-метил-2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он
або фармацевтично прийнятні солі, гідрати або гідратовані солі, або поліморфні кристалічні структури цих сполук, або їхні оптичні ізомери, рацемати, діастереомери або енантіомери та фармацевтично прийнятний носій.
18. Застосування сполуки формули (І), яка відповідає визначенню за будь-яким із пп. 15-17, для виготовлення лікарського засобу для інгібування однієї або декількох цистеїнпротеаз.
19. Застосування за п. 18, причому згадані цистеїнпротеази належать до однієї або декількох груп ензимів деубіквітинації, каспаз, катепсинів, кальпаїнів, а також вірусних, бактеріальних, грибкових або паразитарних циснеїнпротеаз.
20. Застосування сполуки формули (І), яка відповідає визначенню за будь-яким з пп. 15-17, для виготовлення лікарського засобу для лікування та/або попередження раку та метастазів, нейродегенеративних захворювань, наприклад хвороби Альцгеймера та хвороби Паркінсона, запальних розладів, серцево-судинних захворювань та/або вірусних інфекцій та прихованих патологічних станів, зокрема вірусу-1 простого герпесу, вірусу Епштейна-Барра або коронавірусу SARS.
21. Застосування за п. 20, причому згадані сполуки інгібують один або декілька ензимів деубіквітинації.
22. Застосування сполуки формули (І), яка відповідає визначенню за будь-яким з пп. 15-17, для виготовлення лікарського засобу для лікування та/або попередження запальних розладів, нейродегенеративних захворювань, за варіантом, якому віддається перевага, ушкоджень нервових клітин, спричинених інсультом, ушкодження печінки та печінкової недостатності, які є наслідком гострої або хронічної інфекції, ішемічного або хімічного ушкодження печінки, ушкодження нирок та ниркової недостатності, які є наслідком гострої або хронічної інфекції, ішемічного або хімічного ушкодження нирок, ушкодження серця та серцевої недостатності, які є наслідком гострої або хронічної інфекції, ішемічного або хімічного ушкодження серця, діабету, спричиненого гострим або хронічним аутоімунним, хімічним, окиснювальним або метаболічним ушкодженням Інсулінових бета-клітин острівців підшлункової залози.
23. Застосування за п. 22, причому згадані сполуки інгібують одну або декілька каспаз.
24. Застосування сполуки формули (І), яка відповідає визначенню за будь-яким із пп. 15-17, для виготовлення лікарського засобу для лікування та/або попередження раку та метастазів, серцево-судинних захворювань, імунологічних розладів, захворювань кісток та суглобів, остеопорозу та артриту.
25. Застосування за п. 24, причому згадані сполуки інгібують один або декілька катепсинів.
26. Застосування сполуки формули (І), яка відповідає визначенню за будь-яким із пп. 15-17, для виготовлення лікарського засобу для лікування та/або попередження вікових розладів, пізніх нападів діабету та катаракти.
27. Застосування за п. 26, причому згадані сполуки інгібують один або декілька кальпаїнів.
28. Застосування сполуки формули (І), яка відповідає визначенню за будь-яким із пп. 15-17, для виготовлення лікарського засобу для лікування та/або попередження вірусних інфекцій та захворювань.
29. Застосування за п. 28, причому згадані вірусні інфекції та захворювання вибрані з-посеред гепатиту А, гепатиту С, інфекції та захворювань, спричинених коронавірусом SARS, риновірусних інфекцій та захворювань, аденовірусних інфекцій та захворювань, поліомієліту.
30. Застосування за п. 28 або п. 29, причому згадані сполуки інгібують одну або декілька вірусних цистеїнпротеаз.
31. Застосування сполуки формули (І), яка відповідає визначенню за будь-яким із пп. 15-17, для виготовлення лікарського засобу для лікування та/або попередження бактеріальних інфекцій та захворювань.
32. Застосування за п. 31, причому згадані бактеріальні інфекції та захворювання вибрані з-посеред стрептококових інфекцій та захворювань, інфекцій та захворювань, спричинених бактеріями роду Clostridium sp. Genus, стафілококових інфекцій та захворювань, гінгівіту та періодонтальних захворювань.
33. Застосування за п. 31 або п. 32, причому згадані сполуки інгібують одну або декілька бактеріальних цистеїнпротеаз.
34. Застосування за будь-яким із пп. 31-33, причому згадана сполука інгібує одну або декілька бактеріальних цистеїнпротеаз, вибраних з-посеред стрептопаїну, клострипаїну, стафілококових цистеїнпротеаз, гінгіпаїну.
35. Застосування сполуки Формули (І), яка відповідає визначенню за будь-яким із пп. 15-17, для виготовлення лікарського засобу для лікування та/або попередження грибкових інфекцій та захворювань.
36. Застосування за п. 34, причому згадані сполуки інгібують одну або декілька грибкових цистеїнпротеаз.
37. Застосування сполуки формули (І), яка відповідає визначенню за будь-яким із пп. 15-17, для виготовлення лікарського засобу для лікування та/або попередження інфекцій та захворювань, викликаних протозойними паразитами.
38. Застосування за п. 37, причому згадані сполуки інгібують одну або декілька цистеїнпротеаз, які продукуються протозойними паразитами.
39. Застосування сполуки формули (І), яка відповідає визначенню за будь-яким із пп. 15-17, для виготовлення лікарського засобу для лікування та/або попередження інфекцій та захворювань, викликаних паразитами - плоскими черв'яками.
40. Застосування за п. 39, причому згадані сполуки інгібують одну або декілька цистеїнпротеаз, які продукуються паразитами - плоскими черв'яками.
41. Застосування сполуки формули (І), яка відповідає визначенню за будь-яким із пп. 15-17, для виготовлення лікарського засобу для лікування та/або попередження інфекцій та захворювань, викликаних паразитами - круглими черв'яками.
42. Застосування за п. 41, причому згадані сполуки інгібують одну або декілька цистеїнпротеаз, які продукуються паразитами - круглими черв'яками.
Текст
1. Сполуки формули (І) Ru R3 R4 Het1 T X R5 R6 O U V Rv W Rw , (I) де: є або одинарний, або подвійний зв'язок, за обставинами; відсутній або одинарний зв'язок, за обставинами; Het1 є 5-, 6- або 7-членний гетероцикл, за ва ріантом, якому віддається перевага, гетероарил, який містить 1-5 гетероатомів, факультативно заміщений одним або декількома замісниками, вибраними з групи, яку складають Н, CN, Hal, Alk, OAlk, OH, NRCN, C(CN)=C(OH)(OAlk), SR, NRR', C(O)NRR', гетероцикл, арил, гетероарил, де Alk, арил, гетероарил, гетероцикл факультативно за 4 міщені однією або декількома Hal, NRR', CN, OH, CF3, арил, гетероарил, OAlk; де Het1 та Ru T X U V Rv W Rw є конденсованими між собою за допомогою Т та X; Т, U, V, W, X є однаковими або різними та можуть бути вибрані з-посеред С, N, О, S; Ru, Rv, Rw є однаковими або різними та можуть бути вибрані з групи, яку складають Н, CN, =O, Hal, Alk, OAlk, ОН, пергалогеналкіл, NRCN, C(CN)=C(OH)(OAlk), SR, NRR', C(O)NRR' гетероцикл, арил, гетероарил, циклоалкіл, де Alk, арил, гетероарил, гетероцикл, циклоалкіл факультативно заміщені однією або декількома з таких груп, як Hal, NRR', CN, OH, CF3, арил, гетероарил, OAlk або полі(алкіленокси)група, за умови, що щонайменше один із Ru, Rv, Rw є наявним та іншим ніж Н; R3, R4, R5, R6 є однаковими або різними та кожний з них незалежно від інших вибраний з групи, яку складають Н, OAlk, Alk, Hal, NRR', CN, OH, OCF3, CF3, арил, гетероарил; R та R' є однаковими або різними та кожний з них незалежно від інших вибраний з групи, яку складають Н, Alk, де Alk факультативно заміщений однією або декількома групами Hal, NRR', CN, OH, CF3, арил, гетероарил; "алкіл" або "Alk" є аліфатичною вуглеводневою групою, нерозгалуженою або розгалуженою, яка має у ланцюгу 1-20 атомів вуглецю; "гетероцикл" є насиченою, частково ненасиченою або ненасиченою, неароматичною стабільною 314-членною моно-, бі- або поліциклічною системою, де щонайменше одним членом циклу є гетероатом; "арил" є ароматичною моноциклічною або поліциклічною вуглеводневою системою із 6-14 атомів вуглецю; "гетероарил" є 5-14-членною ароматичною гетероциклічною моно-, бі- або поліциклічною системою; "Hal" є атомом фтору, хлору, брому або йоду; полі(алкіленокси)група містить 1-20 атомів вуглецю, або фармацевтично прийнятні солі, гідрати або гідратовані солі, або поліморфні кристалічні структури цих сполук, або їхні оптичні ізомери, рацемати, діастереомери або енантіомери, за винятком перелічених нижче сполук: 1-аміно-2,3,4,10,10апентаазациклопента[b]флуорен-9-он; 5 95930 H2N O N N NH N O N 6 OH N ; O N OH O O N Ph ; Ph N N Ph ; O Ph N Me N S N , де Ph факультативно заміщений атомами Сl, Вr; Me Me or Ph N N Ph N ; Ph NH N N O N N N ; O ; O Cl O NH2 O O C Ph N NH2 ; S N H ; Ph N N N N N S O ; O 2. Сполука формули (І) за п. 1, де Т, U, V, W, X є незалежно один від інших С або N. 3. Сполуки формули (І) за будь-яким із пп. 1 або 2, де Het1 містить 2 гетероатоми або 3 гетероа томи. 4. Сполуки формули (І) за будь-яким із попередніх пунктів, де щонайменше один із Ru, Rv, Rw вибраний з групи, яку складають арил, Alk, NRR', Hal, Alk-арил, -AlkOH, -AlkOAlk, циклоалкіл, -CF3, -CH2(OC2H4)2-OCH3. 5. Сполука за будь-яким із попередніх пунктів, де R3, R4, R5, R6 є однаковими або різними та кожний з них незалежно від інших вибраний з групи, яку складають Н, Hal, Alk, OAlk, OH, OCF3. . CN 6. Сполука за будь-яким із попередніх пунктів, де Rv, Rw є незалежно один від інших або Н, або відсутні. 7. Сполука формули (І) за будь-яким із попередніх пунктів, яка має Формулу (1а): Ru R3 Y R4 z R5 R6 O T X U V Rv W Rw , (1а) де R3-R6 та Ru, Rv, Rw, T, U, V, W, X відповідають наведеному в будь-якому з попередніх пунктів ви 7 95930 значенню та Y, Z, однакові або різні, незалежно один від одного вибрані з-посеред С та N. 8. Сполука формули (І) за будь-яким із попередніх пунктів, яка має Формулу (Іb): Ru R3 R4 N R5 N X W R6 O T U V Rw Rv , (Іb) де R3-R6 та Ru, Rv, Rw, T, U, V, W, X відповідають наведеному в будь-якому з попередніх пунктів визначенню. 9. Сполука формули (І) за будь-яким із попередніх пунктів, де Rv=Rw=H та Ru вибраний з групи, яку складають арил, Alk, NRR', Hal, -Alk-арил, -AlkOH, AlkOAlk, циклоалкіл, -CF3, -CH2-(OC2H4)2-OCH3. 10. Сполука формули (І) за будь-яким із попередніх пунктів, де R4=R5=H та R3, R6 незалежно один від одного вибрані з групи, яку складають Н, Hal, Alk, OAlk, OH, OCF3. 11. Сполука за будь-яким із попередніх пунктів, вибрана з групи, яку складають: 1-метил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-метил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 3-аміно-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-етил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-етил-1,2,3а,4,10-пентаазациклопента[b]флуорен9-он, 1-пропіл-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-пропіл-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-бутил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-бутил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-ізобутил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-ізобутил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-гідроксиметил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-гідроксиметил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-метоксиметил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-метоксиметил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-циклопропіл-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-циклопропіл-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-бензил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-бензил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-хлор-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 8 1-бром-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-бром-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 6-(7)-хлор-1-метил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 7-хлор-3-метил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 2-метил-2Н-1,2,3,4,10пентаазациклопента[b]флуорен-9-он, 2-бензил-2Н-1,2,3,4,10пентаазациклопента[b]флуорен-9-он, 1-ізопропіл-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-ізопропіл-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-трифторметил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-трифторметил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-[2-(2-метоксіетоксі)етоксиметил]-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 6,7-диметокси-1-метил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 6,7-диметокси-3-метил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-етил-6,7-диметокси-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-етил-6,7-диметокси-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 6,7-диметокси-1-пропіл-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 6,7-диметокси-3-пропіл-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-етил-5,8-диметокси-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-етил-5,8-диметокси-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 6,7-дигідрокси-1-метил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он або фармацевтично прийнятні солі, гідрати або гідратовані солі, або поліморфні кристалічні структури цих сполук, або їхні оптичні ізомери, рацемати, діастереомери або енантіомери. 12. Спосіб виготовлення сполуки формули (І) за будь-яким із попередніх пунктів, який включає стадію проведення реакції відповідної сполуки Формули (I'): Ru' R3' R4' Het1 T X R5 ' R6' U V Rv' W O Rw' , (I') де Het1, T, U, V, W, X відповідають визначенням за будь-яким із пп. 1-7, та де щонайменше один із R3', R4', R5', R6', Ru', Rv', Rw' є групою-попередником відповідного R3, R4, R5, R6, Ru, Rv, Rw, а інші є подібними до бажаних R3, R4, R5, R6, Ru, Rv, Rw, в одну або кілька стадій, які уможливлюють перетворення групи-попередника у бажану групу R3, R4, 9 95930 R5, R6, Ru, Rv або Rw, та факультативно виділення сполуки формули (І). 13. Спосіб отримання сполуки за будь-яким із попередніх пунктів, який включає стадію проведення реакції відповідних сполук формули (II) та формули (III): R3 R3 Rw Rw O O Rv Rv R4 R4 OH OH W W V V OH OH R5 R5 R6 R6 O O X XU U H2NH2N T T Ru Ru NH2NH2 (II) (II) (III) (III) , , де R3, R4, R5, R6, Т, U, V, W, X, Ru, Rv, Rw відповідають визначенням за будь-яким із пп. 1-7, причому реакцію здійснюють у присутності спирту та оцтової кислоти. 14. Спосіб за п. 13, де реакцію здійснюють у органічному протонному розчиннику у присутності кислоти. 15. Фармацевтична композиція, яка містить сполуку формули (І) Ru R3 R4 Het1 T X R5 R6 O U V Rv W Rw , (I) де: є або одинарний або подвійний зв'язок, за обставинами; відсутній або одинарний зв'язок, за обставинами; Het1 є 5-, 6- або 7-членний гетероцикл, за ва ріантом, якому віддається перевага, гетероарил, який містить 1-5 гетероатомів, факультативно заміщений одним або декількома замісниками, вибраними з групи, яку складають Н, CN, Hal, Alk, OAlk, OH, NRCN, C(CN)=C(OH)(OAlk), SR, NRR', C(O)NRR', гетероцикл, арил, гетероарил, де Alk, арил, гетероарил, гетероцикл факультативно заміщені однією або декількома Hal, NRR', CN, OH, CF3, арил, гетероарил, OAlk; де Het1 та Ru T X U V Rv W Rw є конденсованими між собою за допомогою Т та X; 10 Т, U, V, W, X є однаковими або різними та можуть бути вибрані з-посеред С, N, О, S; Ru, Rv, Rw є однаковими або різними та можуть бути вибрані з групи, яку складають Н, CN, =O, Hal, Alk, OAlk, ОН, пергалогеналкіл, NRCN, C(CN)=C(OH)(OAlk), SR, NRR', C(O)NRR' гетероцикл, арил, гетероарил, циклоалкіл, де Alk, арил, гетероарил, гетероцикл, циклоалкіл факультативно заміщені однією або декількома з таких груп, як Hal, NRR', CN, OH, CF3, арил, гетероарил, OAlk або полі(алкіленокси)група, за умови, що щонайменше один із Ru, Rv, Rw є наявним та іншим ніж Н; R3, R4, R5, R6 є однаковими або різними та кожний з них незалежно від інших вибраний з групи, яку складають Н, OAlk, Alk, Hal, NRR', CN, OH, OCF3, CF3, арил, гетероарил; R та R' є однаковими або різними та кожний з них незалежно від інших вибраний з групи, яку складають Н, Alk, де Alk факультативно заміщений однією або декількома групами Hal, NRR', CN, OH, CF3, арил, гетероарил; "алкіл" або "Alk" є аліфатичною вуглеводневою групою, нерозгалуженою або розгалуженою, яка має у ланцюгу 1-20 атомів вуглецю; "гетероцикл" є насиченою, частково ненасиченою або ненасиченою, неароматичною стабільною 314-членною моно-, бі- або поліциклічною системою, де щонайменше одним членом циклу є гетероатом; "арил" є ароматичною моноциклічною або поліциклічною вуглеводневою системою із 6-14 атомів вуглецю; "гетероарил" є 5-14-членною ароматичною гетероциклічною моно-, бі- або поліциклічною системою; "Hal" є атомом фтору, хлору, брому або йоду; полі(алкіленокси)група містить 1-20 атомів вуглецю, або фармацевтично прийнятні солі, гідрати або гідратовані солі, або поліморфні кристалічні структури цих сполук, або їхні оптичні ізомери, рацемати, діастереомери або енантіомери та фармацевтично прийнятний носій. 16. Фармацевтична композиція за п. 15, де Формула (І) відповідає визначенню за будь-яким із пп. 210. 17. Фармацевтична композиція за п. 15 або п. 16, де згадана сполука Формули (І) вибрана з групи, яку складають: 1-метил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-метил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-аміно-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-аміно-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-етил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-етил-1,2,3а,4,10-пентаазациклопента[b]флуорен9-он, 1-пропіл-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 11 3-пропіл-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-бутил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-бутил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-ізобутил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-ізобутил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-гідроксиметил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-гідроксиметил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-метоксиметил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-метоксиметил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-циклопропіл-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-циклопропіл-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-бензил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-бензил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-хлор-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 1-бром-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-бром-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 6-(7)-хлор-1-метил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 7-хлор-3-метил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 2-метил-2Н-1,2,3,4,10пентаазациклопента[b]флуорен-9-он, 2-бензил-2Н-1,2,3,4,10пентаазациклопента[b]флуорен-9-он, 1-ізопропіл-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-ізопропіл-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-трифторметил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-трифторметил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-[2-(2-метоксіетоксі)етоксиметил]-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 6,7-диметокси-1-метил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 6,7-диметокси-3-метил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-етил-6,7-диметокси-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 3-етил-6,7-диметокси-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 6,7-диметокси-1-пропіл-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 6,7-диметокси-3-пропіл-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 1-етил-5,8-диметокси-2,3,4,10,10апентаазациклопента[b]флуорен-9-он, 95930 12 3-етил-5,8-диметокси-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он, 6,7-дигідрокси-1-метил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он або фармацевтично прийнятні солі, гідрати або гідратовані солі, або поліморфні кристалічні структури цих сполук, або їхні оптичні ізомери, рацемати, діастереомери або енантіомери та фармацевтично прийнятний носій. 18. Застосування сполуки формули (І), яка відповідає визначенню за будь-яким із пп. 15-17, для виготовлення лікарського засобу для інгібування однієї або декількох цистеїнпротеаз. 19. Застосування за п. 18, причому згадані цистеїнпротеази належать до однієї або декількох груп ензимів деубіквітинації, каспаз, катепсинів, кальпаїнів, а також вірусних, бактеріальних, грибкових або паразитарних циснеїнпротеаз. 20. Застосування сполуки формули (І), яка відповідає визначенню за будь-яким з пп. 15-17, для виготовлення лікарського засобу для лікування та/або попередження раку та метастазів, нейродегенеративних захворювань, наприклад хвороби Альцгеймера та хвороби Паркінсона, запальних розладів, серцево-судинних захворювань та/або вірусних інфекцій та прихованих патологічних станів, зокрема вірусу-1 простого герпесу, вірусу Епштейна-Барра або коронавірусу SARS. 21. Застосування за п. 20, причому згадані сполуки інгібують один або декілька ензимів деубіквітинації. 22. Застосування сполуки формули (І), яка відповідає визначенню за будь-яким з пп. 15-17, для виготовлення лікарського засобу для лікування та/або попередження запальних розладів, нейродегенеративних захворювань, за варіантом, якому віддається перевага, ушкоджень нервових клітин, спричинених інсультом, ушкодження печінки та печінкової недостатності, які є наслідком гострої або хронічної інфекції, ішемічного або хімічного ушкодження печінки, ушкодження нирок та ниркової недостатності, які є наслідком гострої або хронічної інфекції, ішемічного або хімічного ушкодження нирок, ушкодження серця та серцевої недостатності, які є наслідком гострої або хронічної інфекції, ішемічного або хімічного ушкодження серця, діабету, спричиненого гострим або хронічним аутоімунним, хімічним, окиснювальним або метаболічним ушкодженням Інсулінових бетаклітин острівців підшлункової залози. 23. Застосування за п. 22, причому згадані сполуки інгібують одну або декілька каспаз. 24. Застосування сполуки формули (І), яка відповідає визначенню за будь-яким із пп. 15-17, для виготовлення лікарського засобу для лікування та/або попередження раку та метастазів, серцевосудинних захворювань, імунологічних розладів, захворювань кісток та суглобів, остеопорозу та артриту. 25. Застосування за п. 24, причому згадані сполуки інгібують один або декілька катепсинів. 26. Застосування сполуки формули (І), яка відповідає визначенню за будь-яким із пп. 15-17, для виготовлення лікарського засобу для лікування 13 95930 14 та/або попередження вікових розладів, пізніх нападів діабету та катаракти. 27. Застосування за п. 26, причому згадані сполуки інгібують один або декілька кальпаїнів. 28. Застосування сполуки формули (І), яка відповідає визначенню за будь-яким із пп. 15-17, для виготовлення лікарського засобу для лікування та/або попередження вірусних інфекцій та захворювань. 29. Застосування за п. 28, причому згадані вірусні інфекції та захворювання вибрані з-посеред гепатиту А, гепатиту С, інфекції та захворювань, спричинених коронавірусом SARS, риновірусних інфекцій та захворювань, аденовірусних інфекцій та захворювань, поліомієліту. 30. Застосування за п. 28 або п. 29, причому згадані сполуки інгібують одну або декілька вірусних цистеїнпротеаз. 31. Застосування сполуки формули (І), яка відповідає визначенню за будь-яким із пп. 15-17, для виготовлення лікарського засобу для лікування та/або попередження бактеріальних інфекцій та захворювань. 32. Застосування за п. 31, причому згадані бактеріальні інфекції та захворювання вибрані зпосеред стрептококових інфекцій та захворювань, інфекцій та захворювань, спричинених бактеріями роду Clostridium sp. Genus, стафілококових інфекцій та захворювань, гінгівіту та періодонтальних захворювань. 33. Застосування за п. 31 або п. 32, причому згадані сполуки інгібують одну або декілька бактеріальних цистеїнпротеаз. 34. Застосування за будь-яким із пп. 31-33, причому згадана сполука інгібує одну або декілька бак теріальних цистеїнпротеаз, вибраних з-посеред стрептопаїну, клострипаїну, стафілококових цистеїнпротеаз, гінгіпаїну. 35. Застосування сполуки Формули (І), яка відповідає визначенню за будь-яким із пп. 15-17, для виготовлення лікарського засобу для лікування та/або попередження грибкових інфекцій та захворювань. 36. Застосування за п. 34, причому згадані сполуки інгібують одну або декілька грибкових цистеїнпротеаз. 37. Застосування сполуки формули (І), яка відповідає визначенню за будь-яким із пп. 15-17, для виготовлення лікарського засобу для лікування та/або попередження інфекцій та захворювань, викликаних протозойними паразитами. 38. Застосування за п. 37, причому згадані сполуки інгібують одну або декілька цистеїнпротеаз, які продукуються протозойними паразитами. 39. Застосування сполуки формули (І), яка відповідає визначенню за будь-яким із пп. 15-17, для виготовлення лікарського засобу для лікування та/або попередження інфекцій та захворювань, викликаних паразитами - плоскими черв'яками. 40. Застосування за п. 39, причому згадані сполуки інгібують одну або декілька цистеїнпротеаз, які продукуються паразитами - плоскими черв'яками. 41. Застосування сполуки формули (І), яка відповідає визначенню за будь-яким із пп. 15-17, для виготовлення лікарського засобу для лікування та/або попередження інфекцій та захворювань, викликаних паразитами - круглими черв'яками. 42. Застосування за п. 41, причому згадані сполуки інгібують одну або декілька цистеїнпротеаз, які продукуються паразитами - круглими черв'яками. Цей винахід стосується нових інгібіторів цистеїнпротеаз, способів їх виготовлення та їх терапевтичного застосування. Протеази можна класифікувати на основі їхньої специфічності до субстратів або механізмів каталізу. Відомі п'ять головних класів протеаз, що розрізняються за механізмами гідролізу пептидів: серинпротеази, цистеїнпротеази, аспартатпротеази, треонінпротеази та металопротеази. До цистеїнпротеаз належать, поряд з іншими, ензими деубіквітинації, каспази, катепсини, кальпаїни, а також вірусні, бактеріальні або паразитарні цистеїнпротеази. До ензимів деубіквітинації належать убіквітинспецифічні протеази (USP) та убіквітинкарбоксигідролази (UCH). Загалом кажучи, убіквітиновий провідний шлях регулює деградацію протеїнів і, більш конкретно, бере участь у процесах розвитку раку, нейродегенеративних захворювань, наприклад, хвороби Альцгеймера, хвороби Паркінсона, запалень, вірусних інфекцій та прихованих патологічних станів (зокрема, це стосується вірусу1 простого герпесу, вірусу Епштейна-Барра, коронавірусу SARS), та серцево-судинних захворювань (Chem. Rev. 1997, 97, p. 133-171; Chem. Rev. 2002, 102, p. 4459_4488; J. Biochem. 2003, 134, p. 9-18; J. Virology, 2005, 79(7), p. 4550-4551; Cardiovasc. Res. 2004, 61, p. 11-21). Показано, що каспази беруть участь в апоптозі і, отже, є мішенями при гепатиті, печінковій недостатності, запаленнях, серцевій ішемії та серцевій недостатності, нирковій недостатності, нейродегенерації, глухоті, діабеті та інсульті (J. Pharmacol Exp. Ther., 2004, 308(3), p. 1191-1196, J. Cell. Physiol, 2004, 200(2), p. 177-200; Kidney Int, 2004, 66(2), p. 500-506; Am. J. Pathol, 2004, 165(2), p. 353-355; Mini Rev. Chem., 2004, 4(2), p. 153-165; Otol. Neurotol, 2004, 25(4), p. 627-632; Ref. 7, 21, 22, 23, 24, 25). Показано, що катепсини, як правило, беруть участь у розвитку раку та метастазів, запалень, імунологічних процесів та імунорегуляції (Eur. Respir. J., 2004, 23(4), p. 620-628) та атеросклерозу (Ageing Res. Rev.. 2003, 2(4), p. 407-418). Більш конкретно, до катепсинів належать катепсин-В та В-подібні катепсини, які відіграють роль у розвитку раку та метастазів, а також артриту (Cancer Metastasis Rev., 2003, 22(2-3), p. 271-286; Вiol. Chem., 2003, 384(6), p. 845-854 та Biochem. Soc. Symp., 2003, 70, p. 263-276); катепсин-D, який бере 15 участь, зокрема, у розвитку раку та метастазів (Clin. Exp. Metastasis, 2004, 21(2), p. 91-106); катепсин-K, який відіграє певну роль при остеопорозі та артриті (Int. J. Pharm., 2004, 277(1-2), p. 73-79): катепсин-S, який відіграє певну роль при презентації антигенів в імунології (Drug News Perspective, 2004, 17(6), p. 357-363). Кальпаїни відіграють певну роль взагалі при старінні (Ageing Res. Rev. 2003, 2(4), p. 407-418), а також, більш конкретно, при діабеті (Моl. Cell. Biochem., 2004, 261(1), p. 161-167) та катаракті (Trends Моl. Med., 2004, 10(2), p. 78-84). Вірусні цистеїнпротеази ідентифіковано у риновірусах, вірусі поліомієліту, вірусі гепатиту А, вірусі гепатиту С, аденовірусі та коронавірусі SARS (Chem. Rev. 1997, 97, p. 133-171; Chem. Rev. 2002, 102, p. 4459-4488; J. Virology, 2005, 79(7), p. 4550-4551; Acta Microbiol. Immunol. Hung., 2003, 50(1), p. 95-101). До бактеріальних цистеїнпротеаз належать стрептопаїн, стафілококова цистеїнпротеаза, клострипаїн та гінгіпаїни; показано також, що дріжджі, наприклад, Aspergillus flavus, також експресують цистеїнпротеази, які можуть бути вірулентним фактором (Chem. Rev. 1997, 97, p. 133-171). Огляд паразитарних цистеїнпротеаз подано, наприклад, у Molecular & Biochemical Parasitology (2002, 120, p. 1-21) та у Chem. Rev. (2002, 102, p. 4459-4488). Слід зазначити, що паразитарні організми, відповідальні за більшість головних паразитарних захворювань, використовують власні цистеїнпротеази на тій чи іншій стадії інфекційного, живильного або репродуктивного циклу; до таких захворювань належать малярія, хвороба Шагаса, африканський трипаносомоз, лейшманіоз, лямбліоз, трихомоноз, амебіоз, криптоспоридіоз, токсоплазмоз, шистозоматоз, фасціольоз, онхоцеркоз та інші інфекції, що викликаються деякими іншими плоскими або круглими черв'яками. Отже, віднайдення нового класу інгібіторів цистеїнпротеаз має важливе значення для лікування широкого різноманіття захворювань та патологічних станів. Абдельбасат Гассанейн та ін. (Abd el Basat Hassanein et al., Synthetic communications, 30(21), 3883-3895, 2000); Гассан та ін. (Hassan et al., Monatshefte fuer Chemie, 128(1), 61-70, 1997); Дослідний Інститут хімії Бейльштейна (Beilstein Crossfire Institut zur Foerderung der Chemischen Wissenschaften, DE, BRN 7227978, 1993); Метуаллі та ін. (Metwally et al., Zeitschrift fuer Naturforschung, Teil B: Anorganische Chemie, Organische Chemie, 41B(4), 486-488, 1986); Алі та ін. (Аli et al., Phosphorus and Sulfur and the related elements, 39(3-4), 211-216, 1988); Гассанін та ін. (Hassaneen et al., Heteroatom Chemistry, 14(6), 491-497, 2003); Фішер-Колбрі та ін. (Fischer-Colbrie et al., Monatshefte fuer Chemie, 106(3), 743-53, 1975); Простаков та ін. (Химия гетероциклических соединений, (6), 794-798, 1979); Краузе та ін. Химия гетероциклических соединений, (1), 115-119, 1990; Простаков та ін. (Химия гетероциклических соединений, (2), 252-255, 1983; Дослідний Інститут хімії Бейлыптейна (Beilstein Crossfire Institut zur Foerderung der Chemischen Wissenschaften, DE, 95930 16 Citation No. 5846828, 1993); US 6,514,972; WO01/79209 та WO02/02562 розкривають сполуки, які містять 4 конденсовані цикли. Однак на їхнє застосування як інгібіторів цистеїнпротеаз не вказується. За першим аспектом, цей винахід стосується сполуки формули (І): де: є або одинарний або подвійний зв'язок, за обставинами; відсутній або одинарний зв'язок, за обставинами; є 5-, 6- або 7-членний гетероцикл, за варіантом, якому віддається перевага, гетероарил, який містить 1-5 гетероатомів, факультативно заміщений одним або кількома замісниками, вибраними з групи, яку складають Н, CN, Hal, Alk, OAlk, OH, NRCN, C(CN)=C(OH)(OAlk), SR, NRR', C(O)NRR', гетероцикл, арил, гетероарил, де Alk, арил, гетероарил, гетероцикл факультативно заміщені однією або кількома групами Hal, NRR, CN, ОН, CF3, арил, гетероарил, OAlk; де та є конденсованими між собою через посередництво Τ та X; Т, U, V, W, X є однаковими або різними та можуть бути вибрані з-посеред С, Ν, О, S; Ru, Rv, Rw є однаковими або різними та можуть бути вибрані з групи, яку складають Н, CN, =O, Hal, Alk, OAlk, ОН, пергалогеналкіл (повністю галогенований алкіл), NRCN, C(CN)=C(OH)(OAlk), SR, NRR', C(O)NRR', гетероцикл, арил, гетероарил, циклоалкіл, де Alk, арил, гетероарил, гетероцикл, циклоалкіл факультативно заміщені однією або кількома з таких груп, як Hal, NRR', CN, OH, CF3, арил, гетероарил, OAlk або полі(алкіленокси)група, за умови, що щонайменше один із Ru, Rv, Rw є наявним та відрізняється від Н; R3, R4, R5, R6 є однаковими або різними та кожний з них незалежно від інших вибраний з групи, яку складають Н, OAlk, Alk, Hal, NRR', CN, OH, OCF3, CF3, арил, гетероарил; R та R' є однаковими або різними та кожний з них незалежно від інших вибраний з групи, яку складають Н, Alk, де Alk факультативно заміщений 1 однією або кількома групами Hal, NRR , CN, OH, CF3, арил, гетероарил; 17 95930 або фармацевтично прийнятних солей, гідратів або гідратованих солей, або поліморфних кристалічних структур цих сполук, або їхніх оптичних ізомерів, рацематів, 18 діастереомерів або енантіомерів, за винятком перелічених нижче сполук: 1-аміно-2,3,4,10,10апентаазациклопента[b]флуорен-9-он; де Ph факультативно заміщений атомами Cl, Br За варіантом, якому віддається перевага, За варіантом, якому віддається перевага, містить 2 гетероатоми або 3 гетероатоми; за варіантом, якому віддається більша перевага, 2 атоми N або 3 атоми N. За варіантом, якому віддається найбільша перевага, є є або або , за варіантом, якому віддається більша . За варіантом, якому віддається перевага, є незаміщеним. За варіантом, якому віддається перевага, X, Т, U, V, W вибрані з-посеред С та N. перевага, або , де Rv, Rw або Ru є наявним та іншим ніж Н. За варіантом, якому віддається перевага, щонайменше один із Ru, Rv, Rw вибраний з групи, яку складають арил, Alk, NRR', Hal, -Alk-арил, AlkOH, -AlkOAlk, циклоалкіл, -CF3, -СН2-(ОС2Н4)2ОСН3. 19 За варіантом, якому віддається перевага, R3, R4, R5, R6 є однаковими або різними та кожний з них незалежно від інших вибраний з групи, яку складають Н, Hal, Alk, OAlk, OH, OCF3. За варіантом, якому віддається перевага, R та R' є однаковими або різними та кожний з них незалежно від інших вибраний з групи, яку складають Н, Alk. За варіантом, якому віддається перевага, Rv, Rw є Η або відсутні. До сполук формули (І), яким віддається перевага, належать сполуки формули (Іа): де R3-R6 та Ru, Rv, Rw, T, U, V, W, X відповідають наведеним вище визначенням та Υ, Z, однакові або різні, незалежно один від одного вибрані з-посеред С та N. За варіантом, якому віддається більша перевага, сполуки формули (І) відповідають формулі (Іb): де R3-R6 та Ru, Rv, Rw, T, U, V, W, X відповідають наведеним вище визначенням. За аспектами, яким віддається перевага: - Rv=Rw=H та Ru вибраний з групи, яку складають арил, Alk, NRR', Hal, -Alk-арил, -AlkOH, AlkOAlk, циклоалкіл, -CF3, -СН2-(ОС2Н4)2-ОСН3; та/або - R4=R5=H та R3, R6 незалежно один від одного вибрані з групи, яку складають Н, Hal, Alk, OAlk, OH, OCF3, за варіантом, якому віддається більша перевага, OAlk. Сполуки за цим винаходом, яким віддається перевага, вибирають із групи, яку складають: 1-метил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-метил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 3-аміно-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-етил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-етил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-пропіл-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-пропіл-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 95930 20 1-бутил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-бутил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-ізобутил-2,3,4,10Д0апентаазациклопента[b]флуорен-9-он 3-ізобутил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-гідроксиметил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-гідроксиметил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-метоксиметил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-метоксиметил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-циклопропіл-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-циклопропіл-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-бензил-2,3,4Д0,10апентаазациклопента[b]флуорен-9-он 3-бензил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-хлор-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 1-бром-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-бром-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 6-(7)-хлор-1-метил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 7-хлор-3-метил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 2-метил-2Н-1,2,3,4,10пентаазациклопента[b]флуорен-9-он 2-бензил-2Н-1,2,3,4,10пентаазациклопента[b]флуорен-9-он 1-ізопропіл-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-ізопропіл-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-трифторметил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-трифторметил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-[2-(2-метокси-етокси)етоксиметил]2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он 6,7-диметокси-1-метил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 6,7-диметокси-3-метил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-етил-6,7-диметокси-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-етил-6,7-диметокси-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 6,7-диметокси-1-пропіл-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 6,7-диметокси-3-пропіл-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-етил-5,8-диметокси-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-етил-5,8-диметокси-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 21 6,7-дигідрокси-1-метил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он або фармацевтично прийнятні солі, гідрати або гідратовані солі, або поліморфні кристалічні структури цих сполук, або їхні оптичні ізомери, рацемати, діастереомери або енантіомери. При вживанні вище або нижче: Alk означає алкіл, алкеніл або алкініл. Термін "алкіл" означає аліфатичну вуглеводневу групу, яка може бути нерозгалуженою або розгалуженою та мати у ланцюгу 1-20 атомів вуглецю. Алкільні групи, яким віддається перевага, мають у ланцюгу 1-12 атомів вуглецю. Термін "розгалужений" означає, що до нерозгалуженого алкільного ланцюга приєднані одна або декілька нижчих алкільних груп, наприклад, метил, етил або пропіл. Прикладами алкільних груп є метил, етил, н-пропіл, ізопропіл, н-бутил, трет-бутил, н-пентил, 3-пентил, октил, ноніл, децил. Термін "алкеніл" означає аліфатичну вуглеводневу групу, яка містить вуглець-вуглецевий подвійний зв'язок, може бути нерозгалуженою або розгалуженою та має у ланцюгу 2-15 атомів вуглецю. Алкенільні групи, яким віддається перевага, мають у ланцюгу 2-12 атомів вуглецю; та за варіантом, якому віддається більша перевага, мають у ланцюгу приблизно 2-4 атоми вуглецю. Прикладами алкенільних груп є етеніл, пропеніл, н-бутеніл, ізобутеніл, 3-метилбут-2-еніл, н-пентеніл, гептеніл, октеніл, ноненіл, деценіл. Термін "алкініл" означає аліфатичну вуглеводневу групу, яка містить вуглець-вуглецевий потрійний зв'язок, може бути нерозгалуженою або розгалуженою та має у ланцюгу 2-15 атомів вуглецю. Алкінільні групи, яким віддається перевага, мають у ланцюгу 2-12 атомів вуглецю; а за варіантом, якому віддається більша перевага, мають у ланцюгу 2-4 атоми вуглецю. Прикладами алкінільних груп є етиніл, пропініл, н-бутиніл, 2-бутиніл, 3метилбутиніл, н-пентиніл, гептиніл, остиніл та дециніл. Термін "атом галогену" означає атоми фтору, хлору, брому або йоду; за варіантом, якому віддається перевага, атоми фтору та хлору. Термін "арил" означає ароматичну моноциклічну або поліциклічну вуглеводневу систему із 6-14 атомів вуглецю, за варіантом, якому віддається перевага, із 6-10 атомів вуглецю. Прикладами арильних груп є феніл або нафтил. При вживанні у цьому описі терміни "гетероцикл" або "гетероциклічний" означають насичені, частково ненасичені або ненасичені, неароматичні стабільні 3-14-, за варіантом, якому віддається перевага, 5-10-членні моно-, бі- або поліциклічні системи, де щонайменше одним членом циклу є гетероатом. У типових випадках до гетероатомів належать, проте без обмеження ними, атоми кисню, азоту, сірки, селену та фосфору. До гетероатомів, яким віддається перевага, належать кисень, азот та сірка. Придатні гетероцикли також описані у довідниth ку The Handbook of Chemistry and Physics, 76 Edition, CRC Press, Inc., 1995-1996, стор. з 2-25 до 2-26, зміст якого включено до цього опису шляхом посилання. 95930 22 До неароматичних гетероциклів, яким віддається перевага, належать, проте без обмеження ними, піролідиніл, піразолідиніл, імідазолідиніл, оксираніл, тетрагідрофураніл, діоксоланіл, тетрагідропіраніл, діоксаніл, діоксоланіл, піперидил, піперазиніл, морфолініл, піраніл, імідазолініл, піролініл, піразолініл, тіазолідиніл, тетрагідротіопіраніл, дитіаніл, тіоморфолініл, дигідропіраніл, тетрагідропіраніл, дигідропіраніл, тетрагідропіридил, дигідропіридил, тетрагідропіринідиніл, дигідротіопіраніл, азепаніл, а також конденсовані системи, які утворюються при конденсації з фенільною групою. При вживанні у цьому описі, терміни "гетероарил" або «ароматичний гетероцикл» означають 514-, за варіантом, якому віддається перевага, 5-10членну ароматичну моно-, бі- або поліциклічну гетероциклічну систему. Прикладами є піроліл, піридил, піразоліл, тієніл, піримідиніл, піразиніл, тетразоліл, індоліл, хінолініл, пуриніл, імідазоліл, тієніл, тіазоліл, бензотіазоліл, фураніл, бензофураніл, 1,2,4-тіадіазоліл, ізотіазоліл, триазоліл, тетразоліл, ізохіноліл, бензотієніл, ізобензофурил, піразоліл, карбазоліл, бензимідазоліл, ізоксазоліл, піридил-N-оксид, а також конденсовані системи, одержані шляхом конденсування із фенільною групою. Терміни "алкіл", "циклоалкіл", "алкеніл", "алкініл", "арил", "гетероарил", "гетероцикл" тощо стосуються також відповідних "алкілену", "циклоалкілену", "алкенілєну", "алкінілену", "арилену", "гетероарилєну", "гетероциклену" тощо, які утворюються при видаленні двох атомів водню. При вживанні у цьому описі, термін "пацієнт" стосується як тварини, наприклад, тварини, корисної для розплодження, спілкування або збереження, або, за варіантом, якому віддається перевага, людини чи дитини, які страждають на одне або декілька захворювань та хворобливих станів, описаних у цьому документі, або можуть захворіти на них. При вживанні у цьому описі, термін "терапевтично ефективна кількість" означає кількість сполуки за цим винаходом, ефективну для попередження, послаблення, усунення, лікування або регулювання розвитку симптомів вищезгаданих захворювань та хворобливих станів. Термін "регулювання" призначений для позначення процесів, якими можуть бути сповільнення, припинення, затримання або припинення розвитку захворювань та хворобливих станів, описаних у цьому документі, але необов'язково означає повне усунення всіх симптомів захворювань та хворобливих станів, та охоплює профілактичне лікування. При вживанні у цьому описі, термін "фармацевтично прийнятний" стосується тих сполук, матеріалів, наповнювачів, композицій або лікарських форм, які є, в межах логічних медичних міркувань, придатними для контактування з тканинами людей та тварин без надмірної токсичності, подразнення, алергічної реакції або інших ускладнень, порівнянних із прийнятним співвідношенням корисність/ризик. При вживанні у цьому описі, термін "фармацевтично прийнятні солі" стосується похідних розк 23 ритих сполук, в яких вихідна сполука модифікована шляхом одержання солей цієї сполуки із кислотою або основою. Фармацевтично прийнятні солі охоплюють звичайні нетоксичні солі або четвертинні амонієві солі вихідної сполуки, утворені, наприклад, із нетоксичними неорганічними або органічними кислотами. Наприклад, такі звичайні нетоксичні солі охоплюють похідні неорганічних кислот, наприклад, хлористоводневої, бромистоводневої, сірчаної, сульфамінової, фосфорної, азотної тощо; та солі, одержані із застосуванням органічних кислот, наприклад, оцтової, пропіонової, бурштинової, винної, лимонної, метансульфонової, бензолсульфонової, глюкоронової, глутамінової, бензойної, саліцилової, толуолсульфонової, щавлевої, фумарової, малеїнової, молочної тощо. Крім того, до таких солей належать амонієві солі, наприклад, трометаміну, меглуміну, еполаміну тощо, солі металів, наприклад, натрію, калію, кальцію, цинку або магнію. Фармацевтично прийнятні солі за цим винаходом можуть бути синтезовані з вихідної сполуки, яка містить основні або кислотні фрагменти, звичайними хімічними способами. Взагалі, такі солі можуть бути одержані шляхом проведення реакції цих сполук у формах вільної кислоти або основи із стехіометричною кількістю прийнятної основи або кислоти у воді або у органічному розчиннику, або ж у їх суміші. Як правило, перевага віддається неводним розчинникам, наприклад, таким як діетиловий ефір, етилацетат, етанол, ізопропанол або ацетонітрил. Перелік придатних солей можна знайти у довіднику Remington's Pharmaceutical th Sciences, 17 ed., Mack Publishing Company, Easton, PA, 1985, cтop. 1418, зміст якого включено до цього опису шляхом посилання. Сполуки загальної формули (І), які мають геометричні та стереоізомери, також є частиною цього винаходу. За подальшим аспектом, цей винахід також стосується способу одержання сполук формули (І). Сполуки та спосіб за цим винаходом можуть бути реалізовані численними шляхами, відомими фахівцю в галузі. Сполуки можуть бути синтезовані, наприклад, шляхом застосування або адаптації способів, описаних нижче, або їх варіюванням, що зрозуміло фахівцю в галузі. Прийнятні модифікації та заміни є очевидними та добре відомими або можуть бути легко запозичені фахівцем у галузі з наукової літератури. Зокрема, такі способи можна знайти у монографії Ларока (R.C. Larock, Comprehensive Organic Transformations, Wiley-VCH Publishers, 1999). Мається на увазі, що сполуки за цим винаходом можуть містити один або кілька асиметрично заміщених атомів вуглецю, та можуть бути виділені в оптично активних або рацемічних формах. Таким чином, маються на увазі усі хіральні, діастереомерні, рацемічні форми та ізомерні форми, якщо спеціально не вказано конкретну стереохімічну конфігурацію або ізомерну форму. Способи одержання та виділення таких оптично активних форм добре відомі в галузі. Наприклад, суміші стереоізомерів можна розділяти стандартними способами, необмежувальними прикладами яких є 95930 24 розділення рацемічних форм, хроматографія на нормальній фазі, з оберненою фазою та на хіральній фазі, переважне солеутворення тощо, або методами хірального синтезу із хіральних вихідних матеріалів чи цілеспрямованого синтезу цільових хіральних центрів. Крім того, за способом за цим винаходом можуть бути одержані різні регіоізомери, всі з яких охоплюються цим винаходом. Регіоізомери, як правило, виділяють шляхом хроматографування. Сполуки за цим винаходом можна одержувати різноманітними синтетичними методами. Реагенти та вихідні матеріали є наявними на ринку або можуть бути легко синтезовані фахівцем у галузі добре відомими способами. Усі замісники відповідають поданим вище визначенням, якщо не вказано інше. У реакціях, описаних нижче, може видатися необхідним захист реакційноздатних функціональних груп, наприклад, гідрокси-, аміно-, іміно-, тіоабо карбоксигруп, якщо бажаною є їх присутність у кінцевих продуктах, із метою запобігання їх небажаної участи в реакціях. Для цього можна застосовувати звичайні групи захисту згідно зі стандартною практикою. Приклади таких процесів можна знайти у монографіях Гріні та Вутса (T.W. Greene, P.G.M. Wuts, Protective Groups in Organic rd Chemistry, 3 ed., John Wiley and Sons, 1999) та Мак-Омі (J.F.W. McOmie, Protective Groups in Organic Chemistry, Plenum Press, 1973). Деякі реакції можна виконувати у присутності основи. Конкретних обмежень стосовно природи основ, які слід використовувати у таких реакціях, не існує, і будь-яка основа, звичайно застосовувана в реакціях цього типу, є придатною також у даному разі, за умови, що вона не впливає негативно на інші фрагменти молекули. Прикладами придатних основ є: гідроксид натрію, карбонат калію, триетиламін, гідриди лужних металів, наприклад, гідрид натрію та гідрид калію; алкіллітієві сполуки, наприклад, метиллітій та бутиллітій; та алкоголяти лужних металів, наприклад, метилат натрію та етилат натрію. Реакції звичайно проводять у придатному розчиннику. Можна застосовувати різноманітні розчинники за умови, що вони не впливають негативно на хід реакцій або на застосовані реагенти. Прикладами придатних розчинників є: вуглеводні, які можуть бути ароматичними, аліфатичними або циклоаліфатичними вуглеводнями, наприклад, гексан, циклогексан, бензол, толуол та ксилол; аміди, наприклад, диметилформамід; спирти, наприклад, етанол та метанол, та прості ефіри, наприклад, діетиловий простий ефір та тетрагідрофуран. Реакції можна проводити у широкому діапазоні температур. З'ясовано, що, як правило, зручно проводити реакції при температурі від 0°С до 150°С (за варіантом, якому віддається більша перевага, від температури, близької до кімнатної, до 100°С). Час, необхідний для протікання реакції, також може варіювати у широких межах, залежно від численних факторів, особливо від температури реакції та природи реагентів. Однак за умови, що реакція здійснюється у вказаних 25 вище умовах, яким віддається перевага, достатнім, як правило, є період від 3 год до 20 год. Одержану таким чином сполуку можна виділити з реакційної суміші звичайними способами. Наприклад, сполуку можна виділити шляхом видалення з реакційної суміші розчинника шляхом дистиляції або, в разі необхідності, видалення розчинника з реакційної суміші, виливання залишку у воду з подальшим екстрагуванням органічним розчинником, що не змішується з водою, та видалення розчинника з екстракту. Крім того, продукт за бажанням можна додатково очистити різноманітними добре відомими способами, наприклад, перекристалізацією, переосадженням або різноманітними хроматографічними способами, зокрема, хроматографією на колонці або препаративною хроматографією в тонкому шарі. Спосіб одержання сполук формули (І) за цим винаходом є додатковим предметом цього винаходу. За першим аспектом, сполуки за цим винаходом формули (І) можуть бути одержані шляхом проведення реакції відповідних сполук формули (II) та формули (III): де R3, R4, R5, R6, Т, U, V, W, X, Ru, Rv, Rw відповідають визначенням для формули (І). Як правило, реакція може бути здійснена у органічному протонному розчиннику, наприклад, спирті (за варіантом, якому віддається перевага, етанолі), у присутності кислоти, наприклад, оцтової кислоти. Альтернативно або додатково, сполуки формули (І) можуть бути одержані з відповідних сполук формули (І'): де Het1, T, U, V, W, X відповідають визначенням за будь-яким із пп. 1-7 формули винаходу, та де щонайменше один із R3', R4', R5', R6', Ru', Rv', Rw' є групою-попередником відповідного R3, R4, R5, R6, Ru, Rv, Rw, а інші є подібними до бажаних R3, R4, R5, R6, Ru, Rv, Rw, в одну або кілька стадій, які уможливлюють перетворення групипопередника у бажану групу R3, R4, R5, R6, Ru, Rv або Rw, та факультативно виділення сполуки формули (І). Згідно із цим винаходом, вираз «попередник» стосовно до функціональної групи означає будьяку групу, яка може бути із застосуванням однієї або кількох реакцій під впливом одного або кількох відповідних реагентів перетворена у бажану функ 95930 26 ціональну групу. До таких реакцій належать відщеплення групи захисту, а також звичайні реакції приєднання, заміщення або фукнціоналізації. Сполуки формули (l') можуть бути одержані з відповідних сполук формули (II) та формули (III), як описано вище. Вищезазначені реакції можуть бути здійснені фахівцем шляхом застосування або адаптації способів, ілюстрованих у поданих нижче прикладах. Крім того, спосіб за цим винаходом може також включати додаткову стадію виділення сполуки формули (І). Ця стадія може бути здійснена фахівцем будь-яким відомим звичайним шляхом, наприклад, способами виділення, описаними вище. Вихідні продукти формули (II) та формули (III) є наявними на ринку або можуть бути одержані шляхом застосування або адаптації будь-яких відомих способів або способів, описаних у прикладах. Синтез може бути також проведений в одному реакторі у формі багатокомпонентної реакції. За подальшим аспектом, цей винахід також стосується фармацевтичних композицій, які містять сполуку формули (І), яка відповідає наведеному вище визначенню: де: є або одинарний або подвійний зв'язок, за обставинами; відсутній або одинарний зв'язок, за обставинами; є 5-, 6- або 7-членний гетероцикл, за варіантом, якому віддається перевага, гетероарил, який містить 1-5 гетероатомів, факультативно заміщений одним або декількома замісниками, вибраними з групи, яку складають Н, CN, Hal, Alk, OAlk, OH, NRCN, C(CN)=C(OH)(OAlk), SR, NRR', C(O)NRR', гетероцикл, арил, гетероарил, де Alk, арил, гетероарил, гетероцикл факультативно заміщені однією або декількома групами Hal, NRR', CN, ОН, CF3, арил, гетероарил, OAlk; де та є конденсованими між собою через посередництво Τ та X; Т, U, V, W, X є однаковими або різними та можуть бути вибрані з-посеред С, Ν, О, S. Ru, Rv, Rw є однаковими або різними та можуть бути вибрані з групи, яку складають Н, CN, =O, Hal, Alk, OAlk, ОН, пергалогеналкіл, NRCN, C(CN)=C(OH)(OAlk), SR, NRR', C(O)NRR', гетероцикл, арил, гетероарил, циклоалкіл, де Alk, арил, гетероарил, гетероцикл, циклоалкіл факультативно заміщені однією або декількома з таких груп, як 27 Hal, NRR', CN, OH, CF3, арил, гетероарил, OAlk або полі(алкіленокси)група, за умови, що щонайменше один із Ru, Rv, Rw є наявним та відрізняється від Н; R3, R4, R5, R6 є однаковими або різними та кожний з них незалежно від інших вибраний з групи, яку складають Н, OAlk, Alk, Hal, NRR', CN, OH, OCF3, CF3, арил, гетероарил; R та R' є однаковими або різними та кожний з них незалежно від інших вибраний з групи, яку складають Н, Alk, де Alk факультативно заміщений однією або декількома групами Hal, NRR', CN, OH, CF3, арил, гетероарил; або фармацевтично прийнятних солей, гідратів, або гідратованих солей, або поліморфних кристалічних структур цих сполук або їхніх оптичних ізомерів, рацематів, діастереомерів або енантіомерів. Варіанти сполук формули (І), яким віддається перевага, відповідають наведеним вище визначенням, що стосуються сполук за цим винаходом. Сполуки, яким віддається перевага, для терапевтичного застосування за винаходом вибирають із групи, яку складають: 1-метил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-метил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-аміно-2,3,4,10,10апентаазациклопента[b]флуорен-9-он. 3-аміно-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-етил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-етил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-пропіл-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-пропіл-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-бутил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-бутил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-ізобутил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-ізобутил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-гідроксиметил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-гідроксиметил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-метоксиметил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-метоксиметил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-циклопропіл-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-циклопропіл-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-бензил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-бензил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 95930 28 1-хлор-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 1-бром-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-бром-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 6-(7)-хлор-1-метил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 7-хлор-3-метил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 2-метил-2Н-1,2,3,4,10пентаазациклопента[b]флуорен-9-он 2-бензил-2Н-1,2,3,4,10пентаазациклопента[b]флуорен-9-он 1-ізопропіл-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-ізопропіл-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-трифторметил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-трифторметил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-[2-(2-метокси-етокси)етоксиметил]2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он 6,7-диметокси-1-метил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 6,7-диметокси-3-метил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-етил-6,7-диметокси-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-етил-6,7-диметокси-1,2,3а,4,10пентаазацикиопента[b]флуорен-9-он 6,7-диметокси-1-пропіл-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 6,7-диметокси-3-пропіл-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 1-етил-5,8-диметокси-2,3,4,10,10апентаазациклопента[b]флуорен-9-он 3-етил-5,8-диметокси-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он 6,7-дигідрокси-1-метил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он або фармацевтично прийнятні солі, гідрати або гідратовані солі, або поліморфні кристалічні структури цих сполук, або їхні оптичні ізомери, рацемати, діастереомери або енантіомери. За ще одним аспектом, даний винахід стосується застосування сполуки формули (І), визначеної вище стосовно до фармацевтичної композиції за цим винаходом, для виготовлення лікарського засобу для інгібування цистеїнпротеази. Сполуки за цим винаходом корисні для інгібування цистеїнпротеаз, зокрема, ензимів деубіквітинації (нариклад, USP та UCH), каспаз, катепсинів (зокрема, катепсинів В, D, K, S тощо), кальпаїнів, а також вірусних, бактеріальних або паразитарних цистеїнпротеаз у пацієнтів, які потребують такого інгібування. Сполуки за цим винаходом, зокрема, корисні для лікування та/або попередження раку та метастазів, більш конкретно, рак простати та/або ободової кишки, нейродегенеративних захворювань, наприклад, хвороби Альцгеймера та хвороби Паркінсона, глухоти, розладів, пов'язаних із віком, запальних розладів, артриту, остеопорозу, гепатиту, 29 печінкової недостатності, серцевої ішемії та недостатності, інсульту, атеросклерозу, ниркової недостатності, діабету, катаракти; гострих або латентних вірусних інфекцій, спричинених вірусом-1 простого герпесу, вірусом Епштейна-Барра, коронавірусом SARS, риновірусами, вірусом поліомієліту, вірусом гепатиту А, вірусом гепатиту С, аденовірусами тощо; бактеріальних або грибкових інфекцій, спричинених патогенними агентами, що належать до груп Streptococcus sp., Staphylococcus sp., Clostidium sp., Aspergillus sp. тощо; протозойних інфекцій, спричинених видами, що належать до груп Trypanosoma sp., Plasmodium sp., Leishmania sp., Trichomonas sp., Entamoeba sp., Giardia sp., Toxoplasma sp., Cryptosporidium sp. тощо; інфекцій плоскими або круглими черв'яками видів, які належать до груп Fasciola sp., Schistosoma sp., Onchocerca sp., Ascaris sp., Taenia sp., Caenorhabitis sp., Toxocara sp., Haemonchus sp., Ancylostoma sp., Trichuris sp., Trichinella sp., Strongyloides sp., Brugia sp. тощо; а також розладів імунологічного, імунорегуляторного або антигенного походження. Цей винахід стосується також відповідних способів лікування, які включають введення сполуки за цим винаходом спільно із фармацевтично прийнятним носієм або наповнювачем в організм пацієнта, який потребує такого лікування. Ідентифікація суб'єктів, які потребують лікування описаних у цьому документі захворювань та патологічних станів, лежить у межах компетенції та знань фахівця у галузі. Кваліфікований ветеринар або медик може без утруднень визначити суб'єктів, які потребують такого лікування, шляхом застосування клінічних тестів, фізичного дослідження, анамнезу та родинного анамнезу або біологічних та діагностичних тестів. Терапевтично ефективну кількість може без утруднень визначити, будучи фахівцем, лікаркуратор, шляхом застосування звичайних способів та спостереження за результатами, одержаними за аналогічних обставин. При визначенні терапевтично ефективної кількості лікар-куратор бере до уваги численні фактори, до яких належать (але якими не обмежуються): біологічний вид суб'єкта; його маса тіла, вік та загальний стан здоров'я; конкретне захворювання; ступінь ураження або тяжкості захворювання; індивідуальна реакція суб'єкта; конкретна застосовувана сполука; спосіб введення; характеристика біодоступності застосовуваного препарату; обраний режим дозування; застосування супутньої терапії; та інші релевантні обставини. Кількість сполуки формули (І), необхідна для досягнення бажаного біологічного ефекту, варіює залежно від численних факторів, в тому числі від хімічних характеристик (наприклад, гідрофобності) застосовуваних сполук, ефективності сполук, типу захворювання, біологічного виду пацієнта, стану захворювання пацієнта, способу застосування, біодоступності сполуки при обраному шляху введення, усіх факторів, які визначають необхідну величину дози, спосіб постачання та режим дозування. 95930 30 Терміни "фармацевтичний" або "фармацевтично прийнятний" стосуються сполук та композицій, які не викликають шкідливих, алергічних або інших несприятливих реакцій при введенні в організм тварини або людини за відповідних обставин. При вживанні у цьому описі, термін "фармацевтично прийнятний наповнювач" охоплює будь-які носії, розріджувачі, допоміжні речовини або носії, наприклад, консерванти або антиоксиданти, наповнювачі, розпушувальні речовини, зволожувачі, емульгатори, суспензатори, розчинники, дисперсійні середовища, покриття, антибактеріальні та антигрибкові засоби, ізотонічні засоби та засоби, що уповільнюють абсорбцію, тощо. Застосування таких середовищ та засобів для фармацевтично активних речовин добре відоме в галузі. За винятком випадків, коли будь-який звичайний засіб або середовище є несумісним з активним інгредієнтом, застосування таких засобів у терапевтичних композиціях мається на увазі. До складу композицій можуть бути введені також додаткові активні інгредієнти у відповідних терапевтичних комбінаціях. У контексті цього винаходу термін "лікування" або "лікувати", при вживанні у цьому описі, означає обернення напрямку розвитку, полегшення, пригнічення розвитку або попередження розладу або патологічного стану, якого стосується даний термін, або одного або кількох симптомів такого розладу або патологічного стану. Термін "терапевтично ефективна кількість" означає кількість сполуки або лікарського засобу за цим винаходом, ефективну з точки зору попередження або лікування патологічного стану, при якому необхідним є інгібування активної цистеїнпротеази, яка бере участь у патогенезі цього стану. Згідно із цим винаходом, терміни "пацієнт" або "пацієнт, що потребує такого лікування", означає тварину або людину, уражену або можливо уражену патологічним станом, у патогенезі якого бере участь активна цистеїнпротеаза. За варіантом, якому віддається перевага, пацієнтом є людина. У загальному випадку сполуки за цим винаходом можуть застосовуватися у формі розчину у водному буферованому фізіологічному розчині для парентерального застосування, який містить від 0,1% до 10% (маси на об'єм) сполуки. Типова доза лежить у межах від 1 мкг/кг до 0,1 г/кг маси тіла на добу; перевага віддається дозам у межах від 0,01 мг/кг до 10 мг/кг маси тіла на добу або еквівалентним дозам для дітей. Дози застосовуваного лікарського засобу, яким віддається перевага, залежать від таких змінних параметрів, як тип та ступінь розвитку захворювання або розладу, загальний стан здоров'я конкретного пацієнта, відносна біологічна ефективність обраної сполуки, форма композиції, яка включає сполуку, спосіб введення в організм (внутрішньовенний, внутрішньом'язовий або інший), фармакокінетичні характеристики сполуки при обраному способі постачання та швидкість введення (наприклад, у вигляді болюсу або шляхом безперервної інфузії) та режиму застосування (кількість повторних застосувань за даний період часу). Сполуки за цим винаходом можуть застосовуватися також у формі одиничних доз, де термін 31 "одинична доза" означає одиничну дозу, яка може бути застосована до пацієнта та є зручною для маніпулювання та пакування, залишаючись фізично та хімічно стабільною одиничною дозою, що містить або активну сполуку як таку, або фармацевтично прийнятну композицію, як описано нижче. У таких випадках типові добові дози лежать у межах 0,01-100 мг/кг маси тіла. Як загальну рекомендацію можна вказати на одиничні дози для людей в межах від 1 мг на добу до 3000 мг на добу. За варіантом, якому віддається перевага, одинична доза лежить у межах від 1 мг до 500 мг і застосовується 1-6 разів на добу, а за варіантом, якому віддається більша перевага - у межах від 10 мг до 500 мг і застосовується один раз на добу. Сполуки, що пропонуються цим винаходом, можна вводити до складу фармацевтичних композицій шляхом змішування з одним або кількома фармацевтично прийнятними наповнювачами. Такі композиції у формі одиничних доз можуть бути виготовлені для перорального застосування, зокрема, у формі таблеток, твердих або м'яких гелевих капсул; або для назального введення, зокрема, у формі порошків, крапель для носа або аерозолів; або для черезшкірного введення, наприклад, для місцевого застосування, у вигляді мазей, кремів, лосьйонів, гелів або спреїв, або у формі нашкірних пластирів. Згадані композиції зручно застосовувати у формі одиничних дозованих форм та виготовляти будь-яким зі способів, добре відомих у фармацевтичній галузі, наприклад, як описано у монографії Ремінгтона (Remington: The Science and Practice of th Pharmacy, 20 ed.; Gennaro A.R., Ed.; Lippincott Williams & Wilkins: Philadelphia, PA, 2000). Перевага віддається лікарським формам фармацевтичних композицій, у яких сполука за цим винаходом знаходиться у формі, призначеній для перорального або парентерального застосування. У лікарських формах для перорального застосування таблетки, пігулки, порошки, капсули, пастилки тощо можуть містити один або кілька перелічених нижче інгредієнтів або сполук аналогічної природи: в'яжуче, наприклад, мікрокристалічну целюлозу або трагантову камедь; розріджувач, наприклад, крохмаль або лактозу; розпушувач, наприклад, крохмаль та похідні целюлози; змащувач, наприклад, стеарат магнію; ковзний агент, наприклад, колоїдний діоксид кремнію; підсолоджувач, наприклад, сахарозу або сахарин; або смакоароматичну домішку, наприклад, м'яту або метилсаліцилат. Капсули можуть мати форму твердих або м'яких капсул, які звичайно виготовляються з желатинвмісних сумішей, факультативно змішаних із пластифікаторами, а також із крохмалю. Крім того, дозовані одиничні форми можуть містить різноманітні інші матеріали, які модифікують фізичну форму одиничної дозованої форми, наприклад, покриття із цукру, шелаку або ентеричних засобів. Інші лікарські форми для перорального застосування, наприклад, сиропи або еліксири, можуть містити підсолоджувачі, консерванти, барвники, пігменти та ароматизатори. Крім того, активні сполуки можуть бути введені до складу 95930 32 препаратів та лікарських форм швидкого розчинення, модифікованого вивільнення або тривалого вивільнення, причому такі лікарські форми тривалого вивільнення за варіантом, якому віддається перевага, є бімодальними. Перевага віддається таблеткам, які містять лактозу, кукурудзяний крохмаль, силікат, магнію, натрієву кроскармелозу, повідон, стеарат магнію або тальк у будь-яких комбінаціях. До рідких препаратів для парентерального застосування належать стерильні водні або неводні розчини, суспензії та емульсії. Рідкі композиції можуть також включати в'яжучі, буфери, консерванти, комплексоутворювальні засоби, підсолоджувачі, ароматизатори та забарвлювальні засоби тощо. До неводних розчинників належать спирти, пропіленгліколь, поліетиленгліколь, рослинні олії, наприклад, оливкову олію, та органічні складні ефіри, наприклад, етилолеат. До водних носіїв належать суміші спиртів із водою, буферовані середовища та фізіологічний розчин. Наповнювачами, корисними для регулювання вивільнення активних сполук, можуть бути, зокрема, біосумісні полімери лактидів, співполімери лактидів із гліколідами або співполімери поліоксіетиленів із поліоксипропіленами, які піддаються біорозкладу. До наповнювачів для внутрішньовенних препаратів можуть належати домішки для регулювання плинності та поживні домішки, електроліти, наприклад, на основі декстрози Рінгера, тощо. Інші потенціально корисні системи для парентерального постачання цих активних сполук містять частинки співполімеру етилену з вінілацетатом, осмотичні насоси, імплантувальні інфузійні системи та ліпосоми. Альтернативні способи введення в організм забезпечуються лікарськими формами для інгаляції, до яких належать такі форми, як сухі порошки, аерозолі або краплі. Такі форми можуть являти собою водні розчини, які містять, наприклад, поліоксіетилен-9-лауриловий простий ефір, глікохолат та деоксихолат, або розчини на олійній основі для застосування у формі назальних крапель або гелю для назального введення. До лікарських форм для букального введення належать, наприклад, таблетки або пастилки, які можуть містити також смакоароматичну основу, наприклад, сахарозу та аравійську камедь, та інші наповнювачі, наприклад, глікохолат. Лікарські форми, придатні для ректального введення, за варіантом, якому віддається перевага, являють собою супозиторії з одиничними дозами на основі твердого носія, наприклад, какаової олії, та можуть містити саліцилат. Лікарські форми для місцевого нанесення на шкіру за варіантом, якому віддається перевага, мають вигляд мазей, кремів, лосьйонів, паст, гелів, спреїв, аерозолів або олій. До носіїв, які можуть бути використані в таких випадках, належать вазелін, ланолін, поліетиленгліколі, спирти та їх комбінації. Лікарські форми, придатні для черезшкірного введення, можуть мати вигляд окремих пластирів та містити ліпофільні емульсії або буферовані водні розчини, розчинені та/або дисперговані у полімерах або клейких основах. 33 Подані нижче приклади ілюструють винахід, але не обмежують його обсяг. 95930 34 Приклади сполук за цим винаходом представлено у поданій нижче таблиці: 35 95930 36 37 95930 38 39 95930 40 41 95930 42 Експериментальна частина Типові сполуки за цим винаходом можуть бути синтезовані за наведеними нижче методиками: Загальна методика А: синтез пентаазациклопента[b]флуорен-9-ону: Суміш заміщеного (1,2,4)-триазол-3,4-діаміну (8,8 ммоль) та нінгідрину (1,57 г, 8,8 ммоль) у EtOH (10 мл) та АсОН (1,5 мл) нагрівали зі зворотним холодильником протягом 2-16 год. Розчинник видаляли під зниженим тиском, а одержаний залишок розчиняли у EtOAc, промивали насиченим K2СО3 та розсолом. Органічну фазу сушили над Na2SO4, фільтрували, та розчинники видаляли шляхом випарювання під зниженим тиском. Неочищений продукт очищали таким чином: флешхроматографія на силікагелі (градієнт толуол/МеОН від 95:5 до 8:2 або CH2Cl2/EtOAc від 9:1 до 1:1) для очищення регіоізомерної суміші, після чого флеш-хроматографія на нейтральному оксиді алюмінію (гатунок II) (градієнт від СН2СІ2/ЕtOАc 7:3 до СН2СІ2/МeОН 1:1 + 5% НСООН або АсОН) для розділення регіоізомерів. 1-метил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он (1b/А) Одержували за загальною методикою А (вихід 13%) у вигляді жовтої твердої речовини. 1 H ЯМР (300 МГц, DMSO d6): δ 8,23 (d, 1H), + 8,02 (m, 2H), 7,89 (ddd, 1H), 2,72 (s, 3H). ESI MS: обчислено для C12H7N5O: 237,22; знайдено: 238,2 + (MH ). 43 95930 44 + 3-метил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он (1b/B) Одержували за загальною методикою А (вихід 30%) у вигляді жовтої твердої речовини. 1 H ЯМР (300 МГц, DMSO d6): δ 8,16 (d, 1H), 8,05-7,95 (m, 2H), 7,85 (ddd, 1H), 2,77 (s, 3H). ESI MS: обчислено для C12H7N5O: 237,22; знайде+ но: 238,2 (MH ). Синтез аміно-пентаазациклопента[b]флуорен9-ону (1c): Суміш (1,2,4)-триазол-3,4,5-триаміну (2,5 г, 21,9 ммоль) у АсОН/Н2О (1:1, 80 мл) нагрівали до 70°С. Нінгідрин (3,9 г, 21,9 ммоль) розчиняли у АсОН/Н2О (1:1, 80 мл), нагрівали до 50°С, після чого додавали до одержаного розчину триаміну. Реакційну суміш нагрівали при 70°С протягом 3 год, після чого перемішували протягом ночі при кімнатній температурі. Одержану суміш охолоджували до 0°С та перемішували протягом 1 год. Осад збирали шляхом фільтрування, промивали холодною водою та сушили у вакуумі, одержуючи 3,9 г сполуки 1с у вигляді суміші регіоізомерів (співвідношення 6:4, вихід 82%). Регіоізомери розділяли за загальною методикою А. 1-аміно-2,3,4,10,10апентаазациклопента[b]флуорен-9-он (1с/А) 1 Червона тверда речовина. H ЯМР (300 МГц, DMSO d6): δ 8,15 (d, 1H), 8,01-7,95 (m, 2H), 7,83 + (ddd, 1H), 6,98 (s, 2H). ESI MS: обчислено для + C11H6N6O: 238,21; знайдено: 239,1 (МН ). 3-аміно-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он (1с/В) 1 Коричнева тверда речовина. H ЯМР (300 МГц, DMSO d6): δ 8,05-7,93 (m, 3Н), 7,82 (ddd, 1H), + 7,14 (s, 2H). ESI MS: обчислено для C11H6N6O: + 238,21; знайдено: 239,1 (МН ). Загальна методика В: синтез пентаазациклопента[b]флуорен-9-ону: Одержання діамінотриазолів за методикою, описаною у Eur. J. Med. Chem.-Chim. Ther. 1986, 27, 235 Суміш гідрохлориду діаміногуанідину (1 г, 8 ммоль) із надлишком (10 г) відповідної карбонової кислоти перемішували та нагрівали при 120-130°С протягом 12-24 год. Одержаний розчин охолоджували до кімнатної температури та" додавали НСI (37%, 10 мл). Одержану суміш нагрівали зі зворотним холодильником протягом 2-3 год, після чого випарювали досуха у вакуумі. Одержаний неочищений продукт промивали Et2O (хЗ) та використовували без додаткового очищення. Технологію конденсації неочищеного діамінотриазолу з нінгідрином дивись Загальну методику А. 1-етил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он (1d/A) Одержували за загальною методикою В (вихід 48%) у вигляді жовтої твердої речовини. 1 H ЯМР (300 МГц, CDCI3): δ 8,21 (d, 1H), 8,00 (d, 1H), 7,90 (ddd, 1H), 7,77 (ddd, 1H), 3,21 (q, 2H), + 1,49 (t, 3H). ESI MS: обчислено для C13H9N5O: + 251,25; знайдено: 252,1 (MH ). 3-етил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он (1d/B) Одержували за загальною методикою В (вихід 32%) у вигляді жовтої твердої речовини. 1 H ЯМР (300 МГц, CDCI3): δ 8,12 (d, 1H), 8,02 (d, 1H), 7,88 (ddd, 1H), 7,75 (ddd, 1H), 3,25 (q, 2H), + 1,53 (t, 3H). ESI MS: обчислено для C13H9N5O: + 251,25; знайдено: 252,1 (MH ). 45 1-пропіл-2,3,4,10,10апентаазациклопента[b]флуорен-9-он (1e/A) Одержували за загальною методикою В (вихід 14%) у вигляді жовтої твердої речовини. 1 Н ЯМР (300 МГц, CDCI3): δ 8,18 (d, 1H), 7,97 (d, 1H), 7,87 (ddd, 1H), 7,75 (ddd, 1H), 3,12 (dd, 2H), 1,91 (m, 2H), 1,01 (t, 3H). ESI+MS: обчислено для + C14H11N5O: 265,28; знайдено: 266,2 (MH ). 3-пропіл-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он (1е/В) Одержували за загальною методикою В (вихід 12%) у вигляді жовтої твердої речовини. 1 Н ЯМР (300 МГц, CDCI3): δ 8,10 (ddd, 1H), 8,00 (ddd, 1H), 7,86 (ddd, 1H), 7,74 (ddd, 1H), 3,19 + (dd, 2H), 1,96 (m, 2H), 1,06 (t, 3H). ESI MS: обчислено для C14H11N5O: 265,28; знайдено: 266,2 + (MH ). 1-бутил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он (1f/A) Одержували за загальною методикою В (вихід 6%) у вигляді жовтої твердої речовини. 1 Н ЯМР (300 МГц, DMSO d6): δ 8,23 (d, 1H), 8,02 (m, 2H), 7,89 (ddd, 1H), 3,10 (dd, 2H), 1,81 (m, + 2H), 1,42 (m, 2H), 0,94 (t, 3H). ESI MS: обчислено + для C15H13N5O: 279,30; знайдено: 280,2 (MH ). 3-бутил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он (1f/B) Одержували за загальною методикою В (вихід 10%) у вигляді жовтої твердої речовини. 1 H ЯМР (300 МГц, DMSO d6): δ 8,16 (d, 1H), 7,99 (m, 2H), 7,85 (dd, 1H), 3,16 (dd, 2H), 1,87 (m, + 2H), 1,44 (m, 2H), 0,96 (t, 3H). ESI MS: обчислено + для C15H13N5O: 279,30; знайдено: 280,3 (MH ). 1-ізобутил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он (1g/A) Одержували за загальною методикою В (вихід 17%) у вигляді жовтої твердої речовини. 1 H ЯМР (300 МГц, CDCI3): δ 8,20 (d, 1H), 7,99 (d, 1H), 7,89 (ddd, 1H), 7,76 (ddd, 1H), 3,06 (d, 2H), + 2,34 (m, 1H), 1,00 (d, 6H). ESI MS: обчислено для + C15H13N5O: 279,30; знайдено: 280,2 (MH ). 3-ізобутил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он (1g/B) Одержували за загальною методикою В (вихід 12%) у вигляді жовтої твердої речовини. 1 H ЯМР (300 МГц, CDCI3): δ 8,10 (d, 1H), 7,99 (d, 1H), 7,86 (ddd, 1H), 7,74 (ddd, 1H), 3,11 (d, 2H), + 2,38 (m, 1H), 1,04 (d, 6H). ESI MS: обчислено для + C15H13N5O: 279,30; знайдено: 280,2 (MH ). 1-гідроксиметил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он (1h/A) Одержували за загальною методикою В (вихід 10%) у вигляді жовтої твердої речовини. 1 Н ЯМР (300 МГц, DMSO d6): δ 8,24 (d, 1H), 8,02 (m, 2H), 7,90 (ddd, 1H), 5,85 (t, 1H), 4,92 (d, + 2H). ESI MS: обчислено для C12H7N5O2: 253,22; + знайдено: 254,1 (MH ). 3-гідроксиметил-1,2,3a,4,10пентаазациклопента[b]флуорен-9-он (1h/Β) Одержували за загальною методикою В (вихід 1%) у вигляді коричневої твердої речовини. 1 Н ЯМР (300 МГц, DMSO d6): δ 8,15 (d, 1H), 8,06-7,96 (m, 2H), 7,86 (ddd, 1Н), 5,84 (t, 1H), 4,98 + (d, 2H). ESI MS: обчислено для C12H7N5O2: 253,22; + знайдено: 254,2 (МН ). 95930 46 1-метоксиметил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он (1i/A) Одержували за загальною методикою В (вихід 2%) у вигляді жовтої твердої речовини. 1 Н ЯМР (300 МГц, CDCI3): δ 8,18 (ddd, 1H), 7,96 (ddd, 1H), 7,87 (ddd, 1H), 7,75 (ddd, 1H), 4,92 + (s, 2H), 3,42 (s, 3H). ESI MS: обчислено для + C13H9N5O2: 267,25; знайдено: 268,1 (MH ). 3-метоксиметил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он (1i/B) Одержували за загальною методикою В (вихід 2%) у вигляді коричневої твердої речовини. 1 Н ЯМР (300 МГц, CDCI3): δ 8,13 (d, 1H), 8,01 (d, 1H), 7,87 (ddd, 1H), 7,76 (ddd, 1H), 5,02 (s, 2H), + 5,49 (s, 3H). ESI MS: обчислено для C13H9N5O2: + 267,25; знайдено: 268,1 (MH ). 1-циклопропіл-2,3,4,10,10апентаазациклопента[b]флуорен-9-он (1j/Α) Одержували за загальною методикою В (вихід 6%) у вигляді жовтої твердої речовини. 1 Н ЯМР (300 МГц, CDCI3): δ 8,25 (dd, 1H), 8,04 (dd, 1H), 7,93 (ddd, 1H), 7,80 (ddd, 1H), 2,51 (m, 1H), + 1,44 (m, 2H), 1,26 (m, 2H). ESI MS: обчислено для + C14H9N5O: 263,26; знайдено: 264,2 (MH ). 3-циклопропіл-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он (1j/B) Одержували за загальною методикою В (вихід 4%) у вигляді жовтої твердої речовини. 1 Н ЯМР (300 МГц, CDCI3): δ 8,14 (dd, 1H), 8,05 (dd, 1H), 7,90 (ddd, 1H), 7,78 (ddd, 1H), 2,55 (m, 1H), + 1,52 (m, 2H), 1,31 (m, 2H). ESI MS: обчислено для + C14H9N5O: 263,26; знайдено: 264,1 (MH ). 1-бензил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он (Ik/A) Одержували за загальною методикою В (вихід 12%) у вигляді яскраво-жовтої твердої речовини. 1 Н ЯМР (300 МГц, CDCI3): δ 8,23 (dd, 1H), 8,03 (dd, 1H), 7,92 (ddd, 1H), 7,79 (ddd, 1H), 7,46 (m, 2H), + 7,31 (m, 2H), 7,24 (m, 1H), 4,56 (s, 2H). ESI MS: обчислено для C18H11N5O: 313,32; знайдено: 314,2 + (MH ). 3-бензил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он (1k/B) Одержували за загальною методикою В (вихід 6%) у вигляді жовтої твердої речовини. 1 Н ЯМР (300 МГц, CDCI3): δ 8,11 (dd, 1H), 8,04 (dd, 1H), 7,90 (ddd, 1H), 7,77 (ddd, 1H), 7,45 (m, 2H), + 7,32 (m, 2H), 7,25 (m, 1H), 4,62 (s, 2H). ESI MS: обчислено для C18H11N5O: 313,32; знайдено: 314,1 + (MH ). 1-ізопропіл-2,3,4,10,10апентаазациклопента[b]флуорен-9-он (1l/А) Одержували за загальною методикою В (вихід 39%) у вигляді жовтої твердої речовини. 1 Н ЯМР (300 МГц, CDCI3): δ 8,19 (d, 1H), 7,99 (d, 1H), 7,89 (ddd, 1H), 7,76 (ddd, 1H), 3,62 (m, 1H), + 1,51 (d, 6H). ESI MS: обчислено для C14H11N5O: + 265,28; знайдено: 266,2 (MH ). 3-ізопропіл-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он (1l/В) Одержували за загальною методикою В (вихід 10%) у вигляді жовто-коричневої твердої речовини. 1 Н ЯМР (300 МГц, CDCI3): δ 8,16 (dd, 1H), 8,07 (dd, 1H), 7,93 (ddd, 1H), 7,80 (ddd, 1H), 3,73 (dq, 47 95930 + 48 1H), 1,62 (d, 6H). ESI MS: обчислено для + C14H11N5O: 265,28; знайдено: 266,2 (MH ). 1-трифторметил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он (1m/A) Одержували за загальною методикою В (вихід 21%) у вигляді жовтої твердої речовини. 1 Н ЯМР (300 МГц, CDCI3): δ 8,39 (dd, 1H), 8,12 + (dd, 1H), 8,03 (ddd, 1H), 7,92 (ddd, 1H). ESI MS: обчислено для C12H4F3N5O: 291,19; знайдено: + 292,3 (МН ). 3-трифторметил1,2,3а,4,10пентаазациклопента[b]флуорен-9-он (1m/В) Одержували за загальною методикою В (вихід 14%) у вигляді жовто-зеленої твердої речовини. 1 Н ЯМР (300 МГц, CDCI3): δ 8,25 (dd, 1H), 8,13 + (dd, 1H), 7,99 (ddd, 1H), 7,88 (ddd, 1H). ESI MS: обчислено для C12H4F3N5O: 291,19; знайдено: + 292,2 (MH ). 1-[2-(2-метоксі-етоксі)етоксиметил]2,3,4,10,10а-пентаазациклопента[b]флуорен-9-он (In/А) Одержували за загальною методикою В (вихід 14%, по 2 стадіях) у вигляді жовтої твердої речовини. 1 Н ЯМР (300 МГц, CDCI3): δ 8,29 (dd, 1H), 8,07 (dd, 1H), 7,97 (ddd, 1H), 7,84 (ddd, 1H), 5,16 (s, 2H), 3,88 (m, 2H), 3,71 (m, 2H), 3,65 (m, 2H), 3,53 (m, + 2H), 3,34 (s, 3H). ESI MS: обчислено для + C17H17N5O4: 355,36; знайдено: 356,2 (MH ). Загальна методика С: синтез галогенпентаазациклопента[b]флуорен-9-ону: Регіоізомерну суміш амінів 1с (400 мг, 1,68 ммоль) додавали частинами до розчину третбутилнітриту (300 мкл, 2,52 ммоль) та галогеніду міді(ІІ) (2,52 ммоль) у ацетонітрилі (8 мл) при 60°С. Одержану суміш нагрівали при 80°С протягом 2 год, після чого її охолоджували, та випарювали розчинники. Одержаний неочищений продукт очищали флеш-хроматографією (ЕtOАс/МеОН 99:1 або СН2Сl2/ацетон 95:5). 1-хлор-2,3,4,10,10апентаазациклопента[b]флуорен-9-он (2а/А) Одержували за загальною методикою С (вихід 49%) у вигляді жовтої твердої речовини у вигляді єдиного регіоізомера. 1 Н ЯМР (300 МГц, DMSO d6): δ 8,29 (d, 1H), 8,07 (m, 2H), 7,95 (dd, 1H). ESI+MS: обчислено для + C11H4ClN5O: 257,64; знайдено: 258,1 (МН ). 1-бром-2,3,4,10,10апентаазациклопента[b]флуорен-9-он та 3-бром1,2,3а,4,10-пентаазациклопента[b]флуорен-9-он (2b) Одержували за загальною методикою С (вихід 69%) у вигляді жовтої твердої речовини у формі суміші регіоізомерів (6:4). 1 Н ЯМР (300 МГц, DMSO d6) (суміш ізомерів): δ + 8,28 та 8,23 (d, 1H), 8,10-7,86 (m, 3H). ESI MS: обчислено для C11H4BrN5O: 302,09; знайдено: 302,0 + (МН ). Синтез 6-(7)хлорметилпентаазациклопента[b]флуорен-9-ону (3): Розчин 5-хлор-1-інданону (0,97 г, 5,8 ммоль) та N-бромсукциніміду (2,1 г, 11,6 ммоль) у DMSO (23 мл) перемішували 16 год при 40°С та 4 год при 80°С у вакуумі. Додавали розсіл (25 мл), та одержану суміш екстрагували СН2Сl2 (4×25 мл). Зібрані органічні шари сушили над Na2SO4, фільтрували та випарювали. Одержаний неочищений продукт використовували без додаткового очищення. Технологію конденсації неочищеного діамінотриазолу з нінгідрином дивись Загальну методику А. 6-(7)-хлор-1-метил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он (3/А) Вихід: 13%, жовта тверда речовина, суміш ре1 гіоізомерів (1:1): Н ЯМР (300 МГц, CDCI3) (суміш 49 95930 50 1 ізомерів): δ 8,19 (d, 1Н), 7,96 (d, 1H), 7,74 (dd, 1H), 2,84 (s, 3H). 8,17 (d, 1H), 7,97 (d, 1H), 7,86 (dd, 1H), + 2,83 (s, 3H). ESI MS: обчислено для C12H6ClN5O: + 271,67; знайдено: 272,0 (MH ). 7-хлор-3-метил-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он (3/В) Вихід: 3%, коричнювата тверда речовина: Н ЯМР (300 МГц, CDCI3): δ 8,03 (d, 1H), 7,90 (d, 1H), + 7,65 (dd, 1H), 2,79 (s, 3H). ESI MS: обчислено для + C12H6ClN5O: 271,67; знайдено: 272,0 (MH ). Загальна методика D: синтез 2-алкіл-2Н1,2,3,4,10-пентааза-циклопента[b]1флуорен-9-ону: 1-метил-3,4-діаміно-1,2,5-триазол та 1-бензил3,4-діаміно-1,2,5 триазол виготовляють за методикою, описаною у Chem. Heterocycl. Compel. 1992, 803, використовуючи дитіооксамід як вихідний продукт. Технологію конденсації неочищеного діамінотриазолу з нінгідрином дивись Загальну методику А. Одержаний неочищений продукт очищали флеш-хроматографією на силікагелі (СН2Сl2/МеOН, 95:5). 2-метил-2Н-1,2,3,4,10пентаазациклопента[b]флуорен-9-он (4а) Одержували за загальною методикою D (вихід 1 12%) у вигляді коричневої твердої речовини. Н ЯМР (300 МГц, DMSO d6): δ 8,09 (d, 1H), 7,88 (m, + 2H), 7,72 (ddd, 1H), 4,59 (s, 3H). ESI MS: обчислено + для C12H7N5O: 237,22; знайдено: 238,1 (MH ). 2-бензил-2Н-1,2,3,4,10пентаазациклопента[b]флуорен-9-он (4b) Одержували за загальною методикою D (вихід 1 7%) у вигляді коричневої твердої речовини. Н ЯМР (300 МГц, DMSO d6): δ 8,07 (d, 1H), 7,88 (m, 2H), 7,73 (ddd, 1Н), 7,51-7,33 (m, 5H), 6,05 (s, 2H). + ESI MS: обчислено для C18H11N5O: 313,32; знай+ дено: 314,1 (MH ). Загальна методика Е: синтез 6,7диметоксипентааза-циклопента-[b]флуорен-9-ону: Суміш 5,6-диметокси-1-інданону (2,23 г, 11,6 ммоль) та N-бромсукциніміду (4,13 г, 23,2 ммоль) у DMSO (46 мл) перемішували протягом ночі при 40°С та 5 год при 80°С у вакуумі. Додавали воду (46 мл), та одержану суміш екстрагували СН2Сl2 (1×10 мл). Водний шар насичували твердим NaCl, після чого екстрагували СН2СІ2 (3×80 мл). Об'єднані органічні фази другої екстракції сушили над Na2SO4, та розчинник випарювали. Одержаний неочищений продукт використовували без додаткового очищення. Конденсацію 5,6-диметокси1,2,3-індантріону із заміщеним гідрохлоридом (1,2,4)-триазол-3,4-діаміну виконували за загальною методикою В. 6,7-диметокси-1-метил-2,3,4,10,10апентаазациклопента[b]флуорен-9-он (5а/А) Одержували за загальною методикою Ε (вихід 35%) у вигляді оранжевої твердої речовини. 1 Н ЯМР (300 МГц, CDCI3): δ 7,55 (s, 1H), 7,40 (s, 1H), 4,10 (s, 3H), 4,03 (s, 3H), 2,78 (s, 3H). ESI MS: обчислено для С14Н11N5О3: 297,28; знай+ дено: 298,3 (MH ). 6,7-диметокси-3-метил-1,2,3а,4,10пентаазациклопента[h]флуорен-9-он (5а/В) Одержували за загальною методикою Ε (вихід 15%) у вигляді червоної твердої речовини. 1 Н ЯМР (300 МГц, CDCI3): δ 7,42 (s, 1H), 7,41 (s, 1H), 4,11 (s, 3H), 4,03 (s, 3H), 2,82 (s, 3H). + ESI MS: обчислено для C14H11N5O3: 297,28; знай+ дено: 298,3 (MH ). 1-етил-6,7-диметокси-2,3,4,10,10апентаазациклопента[b]флуорен-9-он (5b/A) Одержували за загальною методикою Ε (вихід 27%, по 2 стадіях) у вигляді жовто-оранжевої твердої речовини. 1 Н ЯМР (300 МГц, CDCI3): δ 7,57 (s, 1H), 7,42 (s, 1H), 4,12 (s, 3H), 4,06 (s, 3H), 3,20 (q, 2H), 1,51 + (t, 3H). ESI MS: обчислено для C15H13N5O3: 311,30; + знайдено: 312,2 (MH ). 3-етил-6,7-диметокси-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он (5b/B). + 51 95930 52 + Одержували за загальною методикою Ε (вихід 15%, по 2 стадіях) у вигляді оранжевої твердої речовини. 1 Н ЯМР (300 МГц, CDCI3): δ 7,44 (s, 1H), 7,42 (s, 1H), 4,15 (s, 3H), 4,06 (s, 3Н), 3,24 (q, 2H), 1,54 + (t, 3H). ESI MS: обчислено для C15H13N5O3: 311,30; + знайдено: 312,2 (МН ). 6,7-диметокси-1-пропіл-2,3,4,10,10апентаазациклопента[b]флуорен-9-он (5с/А) Одержували за загальною методикою Ε (вихід 33%) у вигляді оранжевої твердої речовини. 1 Н ЯМР (300 МГц, CDCI3): δ 7,56 (s, 1H), 7,41 (s, 1H), 4,11 (s, 3H), 4,05 (s, 3H), 3,14 (dd, 2H), 1,95 (m, 2H), 1,07 (t, 3H). ESI MS: обчислено для + C16H15N5O3: 325,33; знайдено: 326,3 (MH ). 6,7-диметокси-3-пропіл-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он (5c/B) Одержували за загальною методикою Ε (вихід 13%) у вигляді червоно-коричневої твердої речовини. 1 Н ЯМР (300 МГц, CDCI3): δ 7,42 (s, 1H), 7,41 (s, 1H), 4,13 (s, 3H), 4,03 (s, 3H), 3,17 (dd, 2H), 1,98 + (m, 2H), 1,09 (t, 3H). ESI MS: обчислено для + C16H15N5O3: 325,33; знайдено: 326,3 (MH ). Синтез етил-5,8-диметоксипентаазациклопента[b]флуорен-9-ону: Етил-5,8диметоксипентаазациклопента[b]флуорен-9-онів одержували за загальною методикою Е, використовуючи як вихідний матеріал 4,7-диметокси-1інданон та відповідний діамінотриазол. 1-етил-5,8-диметокси-2,3,4,10,10апентаазациклопента[b]флуорен-9-он (6/А). Вихід: 20% (по 2 стадіях), оранжево-червона 1 тверда речовина. Н ЯМР (300 МГц, CDCI3): δ 7,37 (d, 1H), 7,24 (d, 1H), 4,06 (s, 3H), 4,03 (s, 3H), 3,21 (q, 2H), 1,50 (t, 3H). ESI MS: обчислено для + C15H13N5O3: 311,30; знайдено: 312,3 (MH ). 3-етил-5,8-диметокси-1,2,3а,4,10пентаазациклопента[b]флуорен-9-он (6/В). Вихід: 11% (по 2 стадіях), червона тверда ре1 човина. Н ЯМР (300 МГц, DMSO d6): δ 7,33 (d, 1H), 7,18 (d, 1H), 4,02 (s, 3H), 3,99 (s, 3H), 3,23 (q, + 2H), 1,51 (t, 3H). ESI MS: обчислено для + C15H13N5O3: 311,30; знайдено: 312,5 (MH ). Синтез 6,7-дигідрокси-1-метил-2,3,4,10,10апентааза-циклопента-[b]флуорен-9-ону (7): До суспензії сполуки 6/А (97 мг, 0,32 ммоль) у СН2СІ2 (3,2 мл) додавали 1 Μ розчин ВВr3 у СН2СІ2 (0,96 мл), та одержану суміш перемішували 2 год при кімнатній температурі. Розчинник випарювали під зниженим тиском, та одержаний залишок промивали EtOH та СН2СІ2. Одержаний неочищений продукт розчиняли у DMSO, та очікуваний продукт осаджували шляхом додавання Н2О. Після сушіння одержували сполуку 7 у вигляді коричневої твердої речовини (вихід 79%, 68 мг). 1 Н ЯМР (300 МГц, DMSO d6): δ 7,37 (s, 1Η), + 7,24 (s, 1H), 2,63 (s, 3H). ESI MS: обчислено для + C12H7N5O3: 269,22; знайдено: 270,1 (MH ). Типові цистеїнпротеази Випробування активності USP5 USP5 розводили у буфері USP (50 мМ Tris HCI; 0,5 мМ EDTA; 5 мМ DTT; 0,01% Triton Х-100; бичачий сироватковий альбумін 0,05 мг/мл, рН 7,6). Вихідні розчини сполук у DMSO (100 мМ) збе рігали при -20°С. Сполуки випробовували у таких кінцевих концентраціях: 100 мкМ; 33,3 мкМ; 11,1 мкМ; 3,7 мкМ; 1,23 мкМ; 412 нМ; 137 нМ; 45,7 нМ; 15,2 нМ; 5 нМ. Реакції проводили у двох паралельних пробах, використовуючи 96-лункові планшети Black LJL (мікропланшети НЕ, фірма Molecular Devices; кінцевий об'єм реакційних сумішей 20 мкл). Концентрація субстрату для USP5 становила 400 нМ UbAMC (фірма Boston Bidchem). Концентрація ензиму (USP5) при випробуваннях специфічності становила 300 пМ. Концентрації визначали з метою виконання випробувань специфічності при початкових швидкостях в умовах фіксованої концентрації субстрату. Сполуки попередньо інкубували з ензимами протягом 30 хв при 25°С. Реакції ініціювали додаванням субстрату у планшети, що містили ензими (у присутності або за відсутності сполук), розведені у випробувальному буфері. + 53 Реакційні суміші інкубували протягом 60 хв при 37°С. Реакції припиняли доданням оцтової кислоти (кінцева концентрація 100 мМ). Сканування виконували із застосуванням приладу Pherastar Fluorescent Reader (фірма BMG) (збудження 380 нм; випромінювання =460 нм). Дані (середні значення ± стандартне відхилення) виражали у відсотках від контролю (у відсутності сполуки) та графічно відображали як залежність відсотка ефекту від логарифма концентрації сполуки, застосовуючи програму GraphPad (фірма Prism). Результати апроксимували за сігмоїдною моделлю (змінний нахил). Клонування та очищення USP7 Одержували кДНК, що кодує USP7, шляхом ампліфікації із застосуванням PCR з м-РНК плаценти. Субклонували кДНК USP7 із застосуванням PCR у вектор експресії бакуловіруса (pFastBac-HT; фірма Invitrogen). Генерували кДНК, що кодує мутантну USP7, застосовуючи мутагенний PCR. Відповідний протеїн кодує заміну цистеїну на аланін у залишку 223. Послідовності оцінювали шляхом визначення послідовностей усього відкритого для сканування діапазону. Бакміди, які кодують USP7, генерували відповідно до транспозиції DHIObac. Відповідні бакміди трансфікували у клітини комах (Sf9). Віруси добували з надосадової рідини культури та двічі ампліфікували. Клітини комах (Sf9 або High Five; Invitrogen) інфікували протягом 72 год. Збирали загальні лізати клітин та лізували у лізисному буфері (Tris HCI 50 мМ рН 7,6; 0,75% NP40; 500 мМ NaCl; 10% гліцерин; 1 мМ DTT; 10 мМ імідазол; суміш інгібіторів протеаз Protease Inhibitor Cocktail; AEBSF 20 мкг/мл; апротинін 10 мкг/мл). Протеїни очищали афінним способом на афінних смолах з іонами металів (Talon Metal affinity resin; фірма BD Biosciences). Зв'язані матеріали промивали великою кількістю промивального буфера (50 мМ фосфат натрію, рН 7,0; 300 мМ NaCl; 10 мМ імідазол; 0,5% Triton Х-100; 10% гліцерин) та елюювали зі смоли промивальним буфером із концентрацією імідазолу 250 мМ. Протеши піддавали діалізу у діалізувальному буфері (Tris HCI, рН 7,6 20 мМ; NaCl 200 мМ; DTT 1 мМ; EDTA 1 мМ; 10% гліцерин). Очищені протеши аналізували, застосовуючи 4-12% NuPAGE (фірма Invitrogen). Випробування активності USP7 USP7 розводили у буфері USP (50 мМ Tris HCI; 0,5 мМ EDTA; 5 мМ DTT; 0,01% Triton X-100; бичачий сироватковий альбумін 0,05 мг/мл, рН 7,6). Вихідні розчини сполук у DMSO (100 мМ) зберігали при -20°С. Сполуки випробовували у таких кінцевих концентраціях: 100 мкМ; 33,3 мкМ; 11,1 мкМ; 3,7 мкМ; 1,23 мкМ; 412 нМ; 137 нМ; 45,7 нМ; 15,2 нМ; 5 нМ. Реакції проводили у двох паралельних пробах, використовуючи 96-лункові планшети Black LJL (мікропланшети НЕ, фірма Molecular Devices; кінцевий об'єм реакційних сумішей 20 мкл). Концентрація субстрату для USP7 становила 400 нМ UbAMC (Chem. Biol, 2003, 10, p. 837-846) (фірма Boston Biochem). Концентрація ензиму (USP7) при випробуваннях специфічності становила 152 пМ. Концентрації визначали з метою виконання випро 95930 54 бувань специфічності при початкових швидкостях в умовах фіксованої концентрації субстрату. Сполуки попередньо інкубували з ензимами протягом 30 хв при 25°С. Реакції ініціювали додаванням субстрату у планшети, що містили ензими (у присутності або за відсутності сполук), розведені у випробувальному буфері. Реакційні суміші інкубували протягом 60 хв при 37°С. Реакції припиняли доданням оцтової кислоти (кінцева концентрація 100 мМ). Сканування виконували із застосуванням приладу Pherastar Fluorescent Reader (фірма BMG) ( збудження 380 нм; випромінювання =460 нм). Дані (середні значення ± стандартне відхилення) виражали у відсотках від контролю (у відсутності сполуки) та графічно відображали як залежність відсотка ефекту від логарифма концентрації сполуки, застосовуючи програму GraphPad (фірма Prism). Результати апроксимували за сігмоїдною моделлю (змінний нахил). Клонування та очищення USP8 Одержували кДНК, що кодує USP8, шляхом ампліфікації із застосуванням PCR з м-РНК плаценти. Субклонували кДНК USP8 із застосуванням PCR у вектор експресії бакуловіруса (pFastBac-HT; фірма Invitrogen). Генерували кДНК, що кодує мутантну USP8, застосовуючи мутагенний PCR. Відповідний протеїн кодує заміну цистеїну на аланін у залишку 786. Послідовності оцінювали шляхом визначення послідовностей усього відкритого для сканування діапазону. Бакміди, які кодують USP8, генерували відповідно до транспозиції DHIObac. Відповідні бакміди трансфікували у клітини комах (Sf9). Віруси добували з надосадової рідини культури та двічі ампліфікували. Клітини комах (Sf9 або High Five; Invitrogen) інфікували протягом 72 год. Збирали загальні лізати клітин та лізували у лізисному буфері (Tris HCI 50 мМ рН 7,6; 0,75% NP40; 500 мМ NaCl; 10% гліцерин; 1 мМ DTT; 10 мМ імідазол; суміш інгібіторів протеаз Protease Inhibitor Cocktail; AEBSF 20 мкг/мл; апротинін 10 мкг/мл). Протеши очищали афінним способом на афінних смолах з іонами металів (Talon Metal affinity resin; фірма BD Biosciences). Зв'язані матеріали промивали великою кількістю промивального буфера (50 мМ фосфат натрію, рН 7,0; 300 мМ NaCl; 10 мМ імідазол; 0,5% Triton X-100; 10% гліцерин) та елюювали зі смоли промивальним буфером із концентрацією імідазолу 250 мМ. Протеши піддавали діалізу у діалізувальному буфері (Tris HCI, рН 7,6 20 мМ; NaCl 200 мМ; DTT 1 мМ; EDTA 1 мМ; 10% гліцерин). Очищені протеїни аналізували, застосовуючи 4-12% NuPAGE (фірма Invitrogen). Випробування активності USP8 USP8 розводили у буфері USP (50 мМ Tris HCI; 0,5 мМ EDTA; 5 мМ DTT; 0,01 % Triton X-100; бичачий сироватковий альбумін 0,05 мг/мл, рН 7,6). Вихідні розчини сполук у DMSO (100 мМ) зберігали при -20°С. Сполуки випробовували у таких кінцевих концентраціях: 100 мкМ; 33,3 мкМ; 11,1 мкМ; 3,7 мкМ; 1,23 мкМ; 412 нМ; 137 нМ; 45,7 нМ; 15,2 нМ; 5 нМ. Реакції проводили у двох паралельних пробах, використовуючи 96-лункові планшети Black LJL (мікропланшети НЕ, фірма Molecular Devices; кін 55 цевий об'єм реакційних сумішей 20 мкл). Концентрація субстрату для USP7 становила 400 нМ UbAMC (Chem. Biol, 2003, 10, p. 837-846) (фірма Boston Biochem). Концентрація ензиму (USP8) при випробуваннях специфічності становила 630 пМ. Концентрації визначали з метою виконання випробувань специфічності при початкових швидкостях в умовах фіксованої концентрації субстрату. Сполуки попередньо інкубували з ензимами протягом 30 хв при 25°С. Реакції ініціювали додаванням субстрату у планшети, що містили ензими (у присутності або за відсутності сполук), розведені у випробувальному буфері. Реакційні суміші інкубували протягом 60 хв при 37°С. Реакції припиняли доданням оцтової кислоти (кінцева концентрація 100 мМ). Сканування виконували із застосуванням приладу Pherastar Fluorescent Reader (фірма BMG) ( збудження 380 нм; випромінювання =460 нм). Дані (середні значення істандартне відхилення) виражали у відсотках від контролю (у відсутності сполуки) та графічно відображали як залежність відсотка ефекту від логарифма концентрації сполуки, застосовуючи програму GraphPad (фірма Prism). Результати апроксимували за сігмоїдною моделлю (змінний нахил). Випробування активності UCH-L3 UCH-L3 розводили у буфері USP (50 мМ Tris HCI; 0,5 мМ EDTA; 5 мМ DTT; 0,01 % Triton X-100; бичачий сироватковий альбумін 0,05 мг/мл, рН 7,6). Вихідні розчини сполук у DMSO (100 мМ) зберігали при -20°С. Сполуки випробовували у таких кінцевих концентраціях: 100 мкМ; 33,3 мкМ; 11,1 мкМ; 3,7 мкМ; 1,23 мкМ; 412 нМ; 137 нМ; 45,7 нМ; 15,2 нМ; 5 нМ. Реакції проводили у двох паралельних пробах, використовуючи 96-лункові планшети Black LJL (мікропланшети НЕ, фірма Molecular Devices; кінцевий об'єм реакційних сумішей 20 мкл). Концентрація субстрату для USP7 становила 400 нМ UbAMC (фірма Boston Biochem). Концентрація ензиму (UCH-L3) при випробуваннях специфічності становила 13 пМ. Концентрації визначали з метою виконання випробувань специфічності при початкових швидкостях в умовах фіксованої концентрації субстрату. Сполуки попередньо інкубували з ензимами протягом 30 хв при 25°С. Реакції ініціювали додаванням субстрату у планшети, що містили ензими (у присутності або за відсутності сполук), розведені у випробувальному буфері. Реакційні суміші інкубували протягом 60 хв при 37°С. Реакції припиняли доданням оцтової кислоти (кінцева концентрація 100 мМ). Сканування виконували із застосуванням приладу Pherastar Fluorescent Reader (фірма BMG) ( збудження 380 нм; випромінювання =460 нм). Дані (середні значення ± стандартне відхилення) виражали у відсотках від контролю (у відсутності сполуки) та графічно відображали як залежність відсотка ефекту від логарифма концентрації сполуки, застосовуючи програму GraphPad (фірма Prism). Результати апроксимували за сігмоїдною моделлю (змінний нахил). Клонування та очищення SENP1 Одержували кДНК, яка кодує SENP1, шляхом ампліфікації із застосуванням PCR з м-РНК плаце 95930 56 нти. Субклонували кДНК SENP1 із застосуванням PCR у бактеріальний вектор експресії (pMAL-C2X; фірма New England BioLabs, Inc). Послідовності оцінювали шляхом визначення послідовностей усього відкритого для сканування діапазону. pMAL-C2-SENPl трансформували у клітини BL21 та вирощували у LB-ампіциліновому середовищі, доповненому глюкозою (2 г/л). Експресію конденсувального протеїну індукували за допомогою IPTG (0,5 мМ). Збирали лізати бактеріальних клітин та лізували у лізисному буфері (Tris HCI 20 мМ, рН 7,4; 1 мМ EDTA; 200 мМ NaCI; 0,5% Triton X-100; 10% гліцерину; суміш інгібіторів протеаз Protease Inhibitor Cocktail) з подальшим обробленням ультразвуком. Протеїни очищали афінним способом на афінній смолі з амілозою (фірма New England BioLabs, Inc). Зв'язані матеріали промивали великою кількістю промивального буфера (20 мМ Tris HCI, рН 7,4; 200 мМ NaCI; 1 мМ EDTA; 0,5% Triton X-100; 10% гліцерину) та елюювали зі смоли промивальним буфером із концентрацією мальтози 10 мМ. Протеши піддавали діалізу у діалізувальному буфері (Tris HCI, рН 7,6 20 мМ; NaCI 200 мМ; DTT 1 мМ; EDTA 1 мМ; 10% гліцерин). Очищені протеїни аналізували, застосовуючи 412% NuPAGE (фірма Invitrogen). Випробування активності SENP1 MBP-SENP1 розводили у буфері SENP1 (50 мМ Tris HCI; 0,5 мМ EDTA; 5 мМ DTT; 0,01% Triton X-100; бичачий сироватковий альбумін 0,05 мг/мл, рН 7,6). Вихідні розчини сполук у DMSO (100 мМ) зберігали при -20°С. Сполуки випробовували у таких кінцевих концентраціях: 100 мкМ; 33,3 мкМ; 11,1 мкМ; 3,7 мкМ; 1,23 мкМ; 412 нМ; 137 нМ; 45,7 нМ; 15,2 нМ; 5 нМ. Реакції проводили у двох паралельних пробах, використовуючи 96-лункові планшети Black LJL (мікропланшети НЕ, фірма Molecular Devices; кінцевий об'єм реакційних сумішей 20 мкл). Концентрація субстрату для SENP1 становила 200 нМ SUMO-AMC (Chem. ВЫ., 2003, 10, p. 837-846) (Boston Biochem). Концентрація ензиму (SENP1) при випробуваннях специфічності становила 1,8 нМ. Концентрації визначали з метою виконання випробувань специфічності при початкових швидкостях в умовах фіксованої концентрації субстрату. Сполуки попередньо інкубували з ензимами протягом 30 хв при 25°С. Реакції ініціювали додаванням субстрату у планшети, які вміщували ензими (у присутності або за відсутності сполук), розведені у випробувальному буфері. Реакційні суміші інкубували протягом 60 хв при 37°С. Реакції припиняли доданням оцтової кислоти (кінцева концентрація 100 мМ). Сканування виконували із застосуванням приладу Pherastar Fluorescent Reader (фірма BMG) ( збудження 380 нм; випромінювання =460 нм). Дані (середні значення ± стандартне відхилення) виражали у відсотках від контролю (у відсутності сполуки) та графічно відображали як залежність відсотка ефекту від логарифма концентрації сполуки, застосовуючи програму GraphPad (фірма Prism). Результати апроксимували за сігмоїдною моделлю (змінний нахил). 57 Випробування активності каспази-3 Каспазу-3 розводили у буфері каспази-3 (100 мМ HEPES, рН 7,5; 10% сахарози; 0,1% CHAPS). Вихідні розчини сполук у DMSO (100 мМ) зберігали при -20°С. Сполуки випробовували у таких кінцевих концентраціях: 100 мкМ; 33,3 мкМ; 11,1 мкМ; 3,7 мкМ; 1,23 мкМ; 412 нМ; 137 нМ; 45,7 нМ; 15,2 нМ; 5нМ. Реакції проводили у двох паралельних пробах, використовуючи 96-лункові планшети Black LJL (мікропланшети НЕ, фірма Molecular Devices; кінцевий об'єм реакційних сумішей 20 мкл). Концентрація субстрату для випробувань специфічності каспази-3 становила 500 нМ (Ac-DEVD-AMC; фірма Promega). Концентрація ензиму (каспази-3) при випробуваннях специфічності становила 3,2 нМ. Концентрації визначали з метою виконання випробувань специфічності при початкових швидкостях в умовах фіксованої концентрації субстрату. Сполуки попередньо інкубували з ензимами протягом 30 хв при 25°С. Реакції ініціювали додаванням субстрату у планшети, що містили ензими (у присутності або за відсутності сполук), розведені у випробувальному буфері. Реакційні суміші інкубували протягом 60 хв при 37°С. Реакції припиняли доданням оцтової кислоти (кінцева концентрація 100 мМ). Сканування виконували із застосуванням приладу Pherastar Fluorescent Reader (фірма BMG) ( збудження 380 нм; випромінювання =460 нм). Дані (середні значення ± стандартне відхилення) виражали у відсотках від контролю (у відсутності сполуки) та графічно відображали як залежність відсотка ефекту від логарифма концентрації сполуки, застосовуючи програму GraphPad (фірма Prism). Результати апроксимували за сігмоїдною моделлю (змінний нахил). Випробування активності катепсину-В Катепсин-В розводили у буфері катепсину-В (20 мМ Tris HCI, рН 6,8; 1 мМ EDTA; 1 мМ DTT). Вихідні розчини сполук у DMSO (100 мМ) зберігали при -20°С. Сполуки випробовували у таких кінцевих концентраціях: 100 мкМ; 33,3 мкМ; 11,1 мкМ; 3,7 мкМ; 1,23 мкМ; 412 нМ; 137 нМ; 45,7 нМ; 15,2 нМ; 5нМ. Реакції проводили у двох паралельних пробах, використовуючи 96-лункові планшети Black LJL (мікропланшети НЕ, фірма Molecular Devices; кінцевий об'єм реакційних сумішей 20 мкл). Концентрація субстрату для випробувань специфічності катепсину-В становила 36 мкМ (z-RR-AMC; фірма Calbiochem). Концентрація ензиму (катепсину-В) при випробуваннях специфічності становила 3,6 нМ. Концентрації визначали з метою виконання випробувань специфічності при початкових швидкостях в умовах фіксованої концентрації субстрату. Сполуки попередньо інкубували з ензимами протягом 30 хв при 25°С. Реакції ініціювали додаванням субстрату у планшети, що містили ензими (у присутності або за відсутності сполук), розведені у випробувальному буфері. Реакційні суміші інкубували протягом 60 хв при 37°С. Реакції припиняли доданням оцтової кислоти (кінцева концентрація 100 мМ). Сканування виконували із застосуванням приладу Pherastar Fluorescent Reader (фірма BMG). збудження 380 нм; випроміню 95930 58 вання =460 нм. Дані (середні значення ± стандартне відхилення) виражали у відсотках від контролю (у відсутності сполуки) та графічно відображали як залежність відсотка ефекту від логарифма концентрації сполуки, застосовуючи програму GraphPad (фірма Prism). Результати апроксимували за сігмоїдною моделлю (змінний нахил). Методики випробування життєздатності та проліферації клітин Випробування життєздатності та проліферації клітин НСТ116 Клітини раку товстої кишки НСТ116 одержували з Американської колекції типових культур (АТСС, American Type Culture Collection) та культивували у середовищі Мак-Коя 5А, яке містило 10% FBS, 3 мМ глутамін та 1% пеніциліну/стрептоміцину. Клітини інкубували при 37°С у зволоженій атмосфері із вмістом СО2 5%. Життєздатність клітин випробовували із застосуванням способу MTS у 96-лункових культивува® льних планшетах (CellTiter 96 , проба на проліферацію клітин без радіоактивності у водному середовищі - Aqueous Non-Radioactive Cell Proliferation Assay, фірма Promega) згідно зі вказівками виробника. MTS (3-(4,5-диметилтіазол-2-іл)5-(3-карбоксиметоксифеніл)-2-(4-сульфофеніл)2Н-тетразолій) являє собою тетразолій - похідне МTT, який у метаболічно активних клітинах відновлюється у розчинний клітинно-проникний формазан. Кількість формазану, яка визначається за поминальною здатністю на довжині хвилі 492 нм, пропорційна кількості живих метаболічно активних клітин. 3 Висівали по 10 клітин НСТ116 у кожну лунку. Через 24 год середовище змінювали, і клітини обробляли у трьох паралельних дослідах такими концентраціями кожної сполуки: 10 мкМ, 3,33 мкМ, 1,11 мкМ, 370 нМ, 123 нМ, 41 нМ, 14 нМ та 5 нМ. Сполуки розводили у 100% DMSO, кінцева концентрація якого у кільтурах клітин підтримувалася на рівні 0,5%. Клітини інкубували зі сполуками протягом 72 год, після чого їхню життєздатність випробовували шляхом додавання MTS протягом 2 год. Поглинання на довжині хвилі 492 нм вимірювали безпосередньо у 96-лункових культивувальних планшетах. Обчислювали значення концентрацій GI50 (50% інгібування росту) для кожної сполуки із застосуванням апроксимації сігмощного змінного нахилу (програмне забезпечення Prism 4.0, Graphpad). Визначали середні значення для трьох незалежних дослідів. Випробування життєздатності та проліферації клітин РС3 Клітини раку простати PC-3 одержували з АТСС та культивували в середовищі F-12K, яке містило 7% FBS та 1% пеніциліну/стрептоміцину. Клітини інкубували при 37°С у зволоженій атмосфері зі вмістом СО2 5%. Життєздатність клітин випробовували із застосуванням способу MTS у 96-лункових культивува® льних планшетах (CellTiter 96 , проба на проліферацію клітин без радіоактивності у водному середовищі - Aqueous Non-Radioactive Cell Proliferation Assay, фірма Promega) згідно із вказівками виробника. MTS (3-(4,5-диметилтіазол-2-іл) 59 5-(3-карбоксиметоксифеніл)-2-(4-сульфофеніл)2Н-тетразолій) являє собою тетразолій - похідне МТТ, який у метаболічно активних клітинах відновлюється у розчинний клітинно-проникний формазан. Кількість формазану, яка визначається за поглинальною здатністю на довжині хвилі 492 нм, пропорційна кількості живих метаболічно активних клітин. 3 Висівали по 2×10 клітин РС3 у кожну лунку. Через 24 год середовище змінювали, і клітини обробляли у трьох паралельних дослідах такими концентраціями кожної сполуки:: 10 мкМ, 3,33 мкМ, 1,11 мкМ, 370 нМ, 123 нМ, 41 нМ, 14 нМ та 5 нМ. Сполуки розводили у 100% DMSO, кінцева концеРезультати 1. Інгібування активності цистеїнпротеаз USP 95930 60 нтрація якого у кільтурах клітин підтримувалася на рівні 0,5%. Клітини інкубували зі сполуками протягом 72 год, після чого їхню життєздатність випробовували шляхом додавання MTS протягом 2 год. Поглинання на довжині хвилі 492 нм вимірювали безпосередньо у 96-лункових культивувальних планшетах. Обчислювали значення концентрацій GI50 (50% інгібування росту) для кожної сполуки із застосуванням апроксимації сігмоїдного змінного нахилу (програмне забезпечення Prism 4.0, Graphpad). Визначали середні значення для трьох незалежних дослідів.
ДивитисяДодаткова інформація
Назва патенту англійськоюInhibitors of cysteine proteases, the pharmaceutical compositions thereof and their therapeutic applications
Автори англійськоюGuedat, Philippe, Boissy Guillaume, Borg-Capra Catherine, Colland, Frederic, Daviet, Laurent, Formstecher, Etienne, Jacq, Xavier, Rain, Jean-Christophe, Delansorne Remi, Peretto Ilaria, Vignando Stefano
Назва патенту російськоюИнгибиторы цистеинпротеаз, фармацевтическая композиция, которая их содержит, и их терапевтическое применение
Автори російськоюГюдо Филипп, Буасси Гийом, Бор-Капра Катрин, Коллан Фредерик, Давье Лоран, Формстеше Этьенн, Жак Ксавье, Рен Жан-Кристоф, Делансорн Реми, Перетто Илария, Виньяндо Стефано
МПК / Мітки
МПК: C07D 487/04, A61P 37/02, A61K 31/4192
Мітки: яка, інгібітори, цистеїнпротеаз, містить, терапевтичне, композиція, застосування, фармацевтична
Код посилання
<a href="https://ua.patents.su/34-95930-ingibitori-cistenproteaz-farmacevtichna-kompoziciya-yaka-kh-mistit-ta-kh-terapevtichne-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Інгібітори цистеїнпротеаз, фармацевтична композиція, яка їх містить, та їх терапевтичне застосування</a>
Попередній патент: Спосіб безперервного контролю процесу подрібнення у кульовому млині
Наступний патент: Самохідна косарка-подрібнювач
Випадковий патент: Пристрій для профілактики і лікування захворювань хребта