Діамінопіридинові, піримідинові і піридазинові модулятори гістамінового рецептора h4
Номер патенту: 106046
Опубліковано: 25.07.2014
Автори: Савалль Бред М., Турмонд Робін Л., Тайс Кевін Л., Грінспан Ендрю Дж., Куіроз Джордж А., Вей Дзяньмей, Данфорд Пол Дж., Цай Хой, Чавез Франк, Медуна Стівен П., Чжан Сяоху, Волін Рональд Л.
Формула / Реферат
1. Сполука, вибирана зі сполук формули (І)
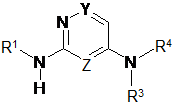 ,
,
Формула (I)
де
Ζ являє собою СН або Ν;
Υ являє собою СН або Ν;
Ζ і Υ визначаються незалежно один від одного, і кільце, що містить згадані Υ і Ζ, має не більше двох атомів азоту; за умови, що
і) коли Υ являє собою СН і Ζ являє собою СН або Ν, то
R1 являє собою:
а) -(СН2)2ОСН3, -(CH2)2SCH3 або С1-8алкіл, кожний з яких незалежно не заміщений або заміщений -ОН або CF3;
б) -(CH2)0-2-Аr1, -CHR2-Аr1 або -(СН2)0-2-Аr2, причому кожний зі згаданих Аr1 і Аr2 незалежно не заміщений або заміщений галогеном, -СН3 або -ОСН3,
Аr1 являє собою 6-членне ароматичне карбоциклічне кільце,
Аr2 являє собою 5- або 6-членне гетероароматичне кільце, що містить N, S або О; або
в) циклоалкіл, -(СН2)-(моноциклічний циклоалкіл), -(СН2)-(місточковий поліциклічний циклоалкіл)0-1, -(СНR2)-(моноциклічний циклоалкіл), -(СН2)-(конденсований циклоалкіл), -(СН2)-(місточковий моноциклічний циклоалкіл), -(СН2)0-1-тетрагідрофураніл або -(СН2)0-1-тетрагідропіраніл, причому кожний зі згаданих фрагментів незалежно не заміщений або заміщений одним, двома або трьома С1-4алкільними замісниками;
R2 являє собою -С1-4алкіл;
![]() являє собою
являє собою 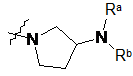 ,
, 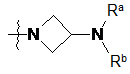 ,
, 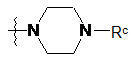 ,
, 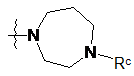 ,
, 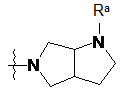 або
або 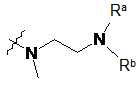 ;
;
де Ra, Rb і Rc, кожен незалежно, являють собою Η або С1-3алкіл;
за умови, що:
якщо R1 являє собою ізопропіл, то Rc являє собою метил;
якщо R1 являє собою 4-метилфеніл, то Rc являє собою метил;
коли Ζ являє собою Ν, Υ являє собою СН і R1 являє собою бензил, не заміщений або заміщений галогеном, то Rc являє собою метил;
іі) коли Υ являє собою N і Ζ являє собою СН, то
R1 являє собою:
а) -(СН2)2ОСН3, -(CH2)2SCH3 або С1-8алкіл, кожний з яких незалежно не заміщений або заміщений -CF або -CF3;
б) -(CH2)0-2-Ar1, -CHR2-Ar1, -(CH2)0-2-Ar2, причому кожний зі згаданих Аr1 і Аr2 незалежно не заміщений або заміщений галогеном, -СН3, -ОСН3,
Аr1 являє собою 6-членне ароматичне карбоциклічне кільце,
Аr2 являє собою 5- або 6-членне гетероароматичне кільце, що містить N, S або О; або
в) циклоалкіл, -(СН2)-(моноциклічний циклоалкіл), -(СН2)-(місточковий поліциклічний циклоалкіл)0-1, -(CHR2)-(моноциклічний циклоалкіл), -(СН2)-(конденсований циклоалкіл), -(СН2)-(місточковий моноциклічний циклоалкіл), -(СН2)0-1-тетрагідрофураніл і -(СН2)0-1-тетрагідропіраніл, причому кожний зі згаданих фрагментів не заміщений або заміщений одним, двома або трьома С1-4алкільними замісниками;
R2 являє собою -С1-4алкіл;
![]() являє собою
являє собою 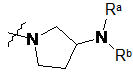 ,
, 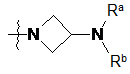 ,
, 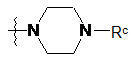 ,
, 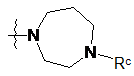 ,
, 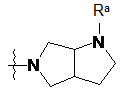 або
або 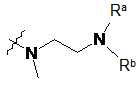 ;
;
де Ra, Rb і Rc, кожен незалежно, являють собою Η або С1-3алкіл;
або їх фармацевтично прийнятних солей.
2. Сполука за п. 1, у якій Υ являє собою СН і Ζ являє собою СН або N.
3. Сполука за п. 1, у якій Υ являє собою N і Ζ являє собою СН.
4. Сполука за п. 2, у якій R1 вибирають із групи, що включає:
а) С1-8алкіл, не заміщений або заміщений -ОН або -CF3;
б) феніл, піридил, бензил, піридин-2-ілметил, фенілетил, 1-фенілетил, кожний з яких незалежно не заміщений або заміщений галогеном, -СН3, -ОСН3; і
в) циклоалкіл, -(СН2)-моноциклічний циклоалкіл), -(CHR2)-(моноциклічний циклоалкіл), -(СН2)-(конденсований циклоалкіл), -(СН2)-(місточковий поліциклічний циклоалкіл), -(СН2)0-1-тетрагідрофураніл і -(CH2)0-1-тетрагідропіраніл, кожний з яких незалежно не заміщений або заміщений одним, двома або трьома С1-4алкільними замісниками.
5. Сполука за п. 2, у якій R1 вибирають із групи, що включає:
а) 2,2-диметилпропанол, 2,2-диметилпропан-1-ол, 2,2-диметилпропіл, 2-метил-1-пропан-2-ол, 2-метилпропан-2-ол, 3-пропанол, 1-метилетил, 2,2-диметилпропіл, 2-метоксіетил, 2-метипропіл, 4,4,4-трифторбутил, пропіл, бутил, трет-бутил, пропан-1-ол, 2-(метилсульфаніл)етил;
б) 2-фенілетил, фуран-3-ілметил, піридин-2-ілметил, (1R)-1-фенілетил, бензил, феніл, 4-фторбензил, 4-метоксибензил, 4-метилбензил; і
в) біцикло[2.2.1]гепт-2-илметил, тетрагідро-2Н-піран-4-іл, тетрагідрофуран-2-ілметил, (1R,2R,3R,5S)-2,6,6-тpимeтилбiциклo[3.1.1]гепт-3-ил, (1R,2S,4R)-1,7,7-триметилбіцикло[2.2.1]гепт-2-ил, (1S,2S,3S,5R)-2,6,6-триметилбіцикло[3.1.1]гепт-3-ил, (1S,2S,4R)-бiциклo[2.2.1]гeпт-2-ил, (1S,5R)-2,6,6-триметилбіцикло[3.1.1]гепт-3-ил, (2R)-тeтpaгiдpoфypaн-2-iлмeтил, (2S)-біцикло[2.2.1]гепт-2-ил, (2S)-тетрагідрофуран-2-ілметил, (3R)-тeтpariдpoфypaн-3-іл, (6,6-диметилбіцикло[3.1.1]гепт-2-ил)метил, біцикло[2.2.1]гепт-2-ил, циклобутил, циклогексил, циклопентил, циклопропіл, циклогексилметил, циклопентилметил, циклопропілметил, адамантан-1-іл, 2-адамантил, біцикло[2.2.1]гепт-2-ил і (6,6-диметилбіцикло[3.1.1]гепт-2-ил)-метил.
6. Сполука за п. 2, у якій R1 вибирають із групи, що складається з:
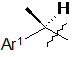 і
і  .
.
7. Сполука за п. 2, у якій ![]() вибирають із групи, що складається з:
вибирають із групи, що складається з:
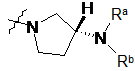 і
і 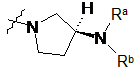 .
.
8. Сполука за п. 2, у якій ![]() являє собою
являє собою 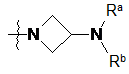 .
.
9. Сполука за п. 2, у якій ![]() являє собою
являє собою 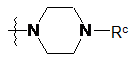 .
.
10. Сполука за п. 2, у якій ![]() являє собою
являє собою 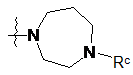 .
.
11. Сполука за п. 2, у якій ![]() являє собою
являє собою 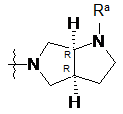 .
.
12. Сполука за п. 2, у якій ![]() являє собою
являє собою 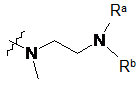 .
.
13. Сполука за п. 2, у якій Ra являє собою Н.
14. Сполука за п. 2, у якій Rb являє собою Η або метил.
15. Сполука за п. 2, у якій Rc являє собою Η або метил.
16. Сполука за п. 2, у якій R2 являє собою метил.
17. Сполука за п. 2, у якій Ζ являє собою СН.
18. Сполука за п. 2, у якій Ζ являє собою N.
19. Сполука за п. 3, у якій R1 вибирається з групи, що включає:
а) С1-8алкіл, не заміщений або заміщений -ОН або -CF3;
б) феніл, піридил, бензил, піридин-2-ілметил, фенілетил, 1-фенілетил, кожний з який незалежно не заміщений або заміщений галогеном, -СН3, -ОСН3; і
в) циклоалкіл, -(СН2)-(моноциклічний циклоалкіл), -(CHR2)-(моноциклічний циклоалкіл), -(СН2)-(конденсований циклоалкіл), -(СН2)-(місточковий поліциклічний циклоалкіл), -(СН2)0-1-тетрагідрофураніл і -(СН2)0-1-тетрагідропіраніл, кожний з яких незалежно не заміщений або заміщений одним, двома або трьома С1-4алкільними замісниками.
20. Сполука за п. 3, у якій R1 вибирається з групи, що включає:
а) 2,2-диметилпропанол, 2,2-диметилпропан-1-ол, 2,2-диметилпропіл, 2-метил-1-пропан-2-ол, 2-метилпропан-2-ол, 3-пропанол, 1-метилетил, 2,2-диметилпропіл, 2-метоксіетил, 2-метипропіл, 4,4,4-трифторбутил, пропіл, бутил, трет-бутил, пропан-1-ол, 2-(метилсульфаніл)етил;
б) 2-фенілетил, фуран-3-ілметил, піридин-2-ілметил, (1R)-1-фенілетил, бензил, феніл, 4-фторбензил, 4-метоксибензил, 4-метилбензил; і
в) біцикло[2.2.1]гепт-2-илметил, тетрагідро-2Н-піран-4-іл, тетрагідрофуран-2-ілметил, (1R,2R,3R,5S)-2,6,6-тpимeтилбiциклo[3.1.1]гeпт-3-ил, (1R,2S,4R)-1,7,7-триметилбіцикло[2.2.1]гепт-2-ил, (1S,2S,3S,5R)-2,6,6-триметилбіцикло[3.1.1]гепт-3-ил, (1S,2S,4R)-біциклo[2.2.1]гeпт-2-ил, (1S,5R)-2,6,6-триметилбіцикло[3.1.1]гепт-3-ил, (2R)-тeтpaгiдpoфypaн-2-iлмeтил, (2S)-біцикло[2.2.1]гепт-2-ил, (2S)-тетрагідрофуран-2-ілметил, (3R)-тeтpaгiдpoфypaн-3-іл, (6,6-диметилбіцикло[3.1.1]гепт-2-ил)метил, біцикло[2.2.1]гепт-2-ил, циклобутил, циклогексил, циклопентил, циклопропіл, циклогексилметил, циклопентилметил, циклопропілметил, адамантан-1-іл, 2-адамантил, біцикло[2.2.1]гепт-2-ил і (6,6-диметилбіцикло[3.1.1]гепт-2-ил)метил.
21. Сполука за п. 3, у якій R1 вибирається з групи, що включає:
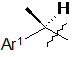 і
і  .
.
22. Сполука за п. 3, у якій ![]() вибирається з групи, що включає:
вибирається з групи, що включає:
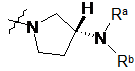 і
і 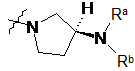 .
.
23. Сполука за п. 3, у якій ![]() являє собою
являє собою 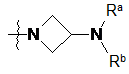 .
.
24. Сполука за п. 3, у якій ![]() являє собою
являє собою 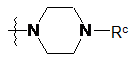 .
.
25. Сполука за п. 3, у якій ![]() являє собою
являє собою 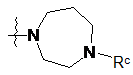 .
.
26. Сполука за п. 3, у якій![]() являє собою
являє собою  .
.
27. Сполука за п. 3, у якій ![]() являє собою
являє собою 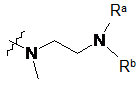 .
.
28. Сполука за п. 3, у якій Ra являє собою Н.
29. Сполука за п. 3, у якій Rb являє собою Η або метил.
30. Сполука за п. 3, у якій Rc являє собою Η або метил.
31. Сполука за п. 3, у якій R2 являє собою метил.
32. Сполука за п. 3, у якій Ζ являє собою СН.
33. Сполука, вибирана з групи, що включає:
біцикло[2.2.1]гепт-2-ил-[4-((3R)-3-метиламінопіролідин-1-іл)-піридин-2-іл]-аміну дигідрохлорид;
N-циклoпeнтил-4-[(3R)-3-(мeтилaмiнo)піpoлiдин-1-iл]пipидин-2-aмiн;
4-[(3R)-3-(мeтилaмінo)піpoлiдин-1-іл]-N-пpoпілпipидин-2-aмiнy дигідрохлорид;
N-(циклoпpoпiлмeтил)-4-[(3R)-3-(мeтилaмiнo)пipoлiдин-1-iл]пipидин-2-аміну дитрифторацетат;
4-[(3R)-3-(мeтилaмiнo)пipoлiдин-1-iл]-N-[(3R)-тeтpaгiдpoфypaн-3-іл]піридин-2-аміну дигідрохлорид;
4-[(3R)-3-(мeтилaмiнo)пipoлiдин-1-iл]-N-[тeтpaгiдpoфypaн-2-ілметил]піридин-2-аміну дигідрохлорид;
N-(4-фторбензил)-4-[(3R)-3-(метиламіно)піролідин-1-іл]піридин-2-аміну дигідрохлорид;
N-циклопропіл-4-[(3R)-3-(метиламіно)піролідин-1-іл]піридин-2-аміну дигідрохлорид;
4-[(3R)-3-(метиламіно)піролідин-1-іл]-N-[(1S,2S,3S,5R)-2,6,6-триметилбіцикло[3.1.1]гепт-3-ил]піридин-2-амін;
4-[(3R)-3(метиламіно)піролідин-1-іл]-N-[(1R,2R,3R,5S)-2,6,6-триметилбіцикло[3.1.1]гепт-3-ил]піридин-2-амін;
N-бензил-4-[(3R)-3(метиламіно)піролідин-1-іл]піридин-2-амін;
4-[(3R)-3(метиламіно)піролідин-1-іл]-N-(1-метилетил)піридин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-(1-метилетил)піридин-2-амін;
4-[(3S)-3-амінопіролідин-1-іл]-N-(2-метилпропіл)піридин-2-амін;
4-[(3S)-3-(метиламіно)піролідин-1-іл]-N-(2-метилпропіл)піридин-2-амін;
N-циклопентил-4-піперазин-1-ілпіридин-2-амін;
4-піперазин-1-іл-N-пропілпіридин-2-аміну дигідрохлорид;
N-бензил-4-піперазин-1-ілпіридин-2-амін;
N-(2-метилпропіл)-4-піперазин-1-ілпіридин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-(2-метилпропіл)піридин-2-амін;
4-(4-метилпіперазин-1-іл)-N-(2-метилпропіл)піридин-2-амін;
4-[(3R)-3-(метиламіно)піролідин-1-іл]-N-(2-метилпропіл)піридин-2-амін;
4-[(3R)-3-(метиламіно)піролідин-1-іл]-N-фенілпіридин-2-амін;
4-[3-(метиламіно)азетидин-1-іл]-N-(2-метилпропіл)піридин-2-амін;
N-(циклопропілметил)-4-піперазин-1-ілпіридин-2-амін;
N-бутил-4-піперазин-1-ілпіридин-2-амін;
N-(2-метоксіетил)-4-піперазин-1-ілпіридин-2-амін;
N-феніл-4-піперазин-1-ілпіридин-2-амін;
4-піперазин-1-іл-N-(тетрагідрофуран-2-ілметил)піридин-2-амін;
N-(4-фторбензил)-4-піперазин-1-ілпіридин-2-амін;
N-(2,2-диметилпропіл)-4-[(3R)-3-(метиламіно)піролідин-1-іл]піридин-2-амін;
N-(2-метоксіетил)-4-[(3R)-3-(метиламіно)піролідин-1-іл]піридин-2-амін;
4-[(3S)-3-(метиламіно)піролідин-1-іл]-N-[(1R,2S,4R)-1,7,7-триметилбіцикло[2.2.1]гепт-2-ил]піридин-2-амін;
адамантан-2-іл-[4-(4-метилпіперазин-1-іл)-піридин-2-іл]амін;
адамантан-2-іл-[4-(3R)-(3-метиламінопіролідин-1-іл)-піридин-2-іл]амін;
N-[(1R)-1-циклогексилетил]-4-[(3R)-3-(метиламіно)піролідин-1-іл]піридин-2-амін;
адамантан-1-іл-[4-(3S)-(3-метиламінопіролідин-1-іл)-піридин-2-іл]амін;
N-(циклогексилметил)-4-[(3R)-3-(метиламіно)піролідин-1-іл]піридин-2-амін;
N-(циклогексилметил)-4-(4-метилпіперазин-1-іл)піридин-2-амін;
N-[(1R)-1-циклогексилетил]-4-[(3S)-3-(метиламіно)піролідин-1-іл]піридин-2-амін;
N-[(1R)-1-циклогексилетил]-4-(4-метилпіперазин-1-іл)піридин-2-амін;
адамантан-2-іл-[4-(3S)-(3-метиламінопіролідин-1-іл)-піридин-2-іл]амін;
3-{[4-(4-метилпіперазин-1-іл)піридин-2-іл]аміно}пропан-1-ол;
N-{[(1S,2S,5S)-6,6-диметилбіцикло[3.1.1]гепт-2-ил]метил}-4-[(3R)-3-(метиламіно)піролідин-1-іл]піридин-2-амін;
aдaмaнтaн-1-iл-[4-(3R)-(3-мeтилaмiнoпipoлiдин-1-iл)-пipидин-2-iл]aмiн;
адамантан-1-іл-[4-(4-метилпіперазин-1-іл)-піридин-2-іл]амін;
aдaмaнтaн-1-iлмeтил-[4-(3R)-(3-мeтилaмiнoпipoлiдин-1-iл)-пipидин-2-iл]амін;
N-{[(1S,2S,5S)-6,6-диметилбіцикло[3.1.1]гепт-2-ил]метил}-4-(4-метилпіперазин-1-іл)піридин-2-амін;
4-[(3R)-3-(метиламіно)піролідин-1-іл]-N-(тетрагідро-2Н-піран-4-іл)піридин-2-амін;
4-(4-метилпіперазин-1-іл)-N-(тетрагідро-2Н-піран-4-іл)піридин-2-амін;
N-{[(1S,2S,5S)-6,6-диметилбіцикло[3.1.1]гепт-2-ил]метил}-4-[(3S)-3-(метиламіно)піролідин-1-іл]піридин-2-амін;
N-(циклoгeкcилмeтил)-4-[(3S)-3-(мeтилaмiнo)пipoлiдин-1-iл]піридин-2-амін;
N-(циклoпeнтилмeтил)-4-[(3R)-3-(мeтилaмiнo)пipoлiдин-1-iл]пipидин-2-амін;
N-(циклопентилметил)-4-[(3S)-3-(метиламіно)піролідин-1-іл]піридин-2-амін;
N-циклопентил-4-[(3S)-3-(метиламіно)піролідин-1-іл]піридин-2-амін;
4-[(3S)-3-(метиламіно)піролідин-1-іл]-N-(піридин-2-ілметил)піридин-2-амін;
4-[(3S)-3-(метиламіно)піролідин-1-іл]-N-[(1S,5R)-2,6,6-триметилбіцикло[3.1.1]гепт-3-ил]піридин-2-амін;
N-біцикло[2.2.1]гепт-2-ил-4-[(3S)-3-(метиламіно)піролідин-1-іл]піридин-2-амін;
4-(4-метилпіперазин-1-іл)-N-[(1S,5R)-2,6,6-триметилбіцикло[3.1.1]гепт-3-ил]піридин-2-амін;
N-трет-бутил-4-[(3S)-3-(метиламіно)піролідин-1-іл]піридин-2-амін;
3-({4-[(3S)-3-(метиламіно)піролідин-1-іл]піридин-2-іл}аміно)пропан-1-ол;
N-циклопропіл-4-[(3S)-3-(метиламіно)піролідин-1-іл]піридин-2-амін;
N-(циклопентилметил)-4-(4-метилпіперазин-1-іл)піридин-2-амін;
N-бензил-4-[(3S)-3-(метиламіно)піролідин-1-іл]піридин-2-амін;
N-(2-метоксіетил)-4-[(3S)-3-(метиламіно)піролідин-1-іл]піридин-2-амін;
N-(2-метоксіетил)-4-(4-метилпіперазин-1-іл)піридин-2-амін;
2-метил-1-({4-[(3R)-3-(метиламіно)піролідин-1-іл]піридин-2-іл}аміно)пропан-2-ол;
2-метил-1-{[4-(4-метилпіперазин-1-іл)піридин-2-іл]аміно}пропан-2-ол;
2-метил-1-({4-[(3S)-3-(метиламіно)піролідин-1-іл]піридин-2-іл}аміно)пропан-2-ол;
N-бутил-4-[(3S)-3-(метиламіно)піролідин-1-іл]піридин-2-амін;
4-(4-метилпіперазин-1-іл)-N-(піридин-2-ілметил)піридин-2-амін;
4-[(3S)-3-(метиламіно)піролідин-1-іл]-N-(2-фенілетил)піридин-2-амін;
N-(4-фторбензил)-4-[(3S)-3-(метиламіно)піролідин-1-іл]піридин-2-амін;
4-[(3R)-3-(метиламіно)піролідин-1-іл]-N-[(1R,2S,4R)-1,7,7-триметилбіцикло[2.2.1]гепт-2-ил]піридин-2-амін;
N-циклопентил-4-(4-метилпіперазин-1-іл)піридин-2-амін;
N-(4-фторбензил)-4-(4-метилпіперазин-1-іл)піридин-2-амін;
4-(4-метилпіперазин-1-іл)-N-(2-фенілетил)піридин-2-амін;
адамантан-1-ілметил-[4-(3S)-(3-метиламінопіролідин-1-іл)-піридин-2-іл]амін;
4-(4-метилпіперазин-1-іл)-N-[(1R,2S,4R)-1,7,7-триметилбіцикло[2.2.1]гепт-2-ил]піридин-2-амін;
N-(біцикло[2.2.1]гепт-2-илметил)-4-[(3R)-3-(метиламіно)піролідин-1-іл]піридин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-бутилпіридин-2-амін;
адамантан-1-ілметил-[4-(4-метилпіперазин-1-іл)-піридин-2-іл]амін;
N-(циклогексилметил)-4-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]піридин-2-амін;
4-[(3aR,6aR)-гексагідропіроло[3,4-b]пірол-5(1H)-іл]-N-(2-метилпропіл)піридин-2-амін;
4-[(3S)-3-амінопіролідин-1-іл]-N-(піридин-2-ілметил)піридин-2-амін;
N-циклопентил-4-[3-(метиламіно)азетидин-1-іл]піридин-2-амін;
4-піперазин-1-іл-N-(піридин-2-ілметил)піридин-2-амін;
N-(циклопентилметил)-4-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1H)-іл]піридин-2-амін;
N-циклопентил-4-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]піридин-2-амін;
4-[(3S)-3-амінопіролідин-1-іл]-N-(4-фторбензил)піридин-2-амін;
4-[(3S)-3-амінопіролідин-1-іл]-N-(2-метоксіетил)піридин-2-амін;
N-біцикло[2.2.1]гепт-2-ил-4-(1,4-діазепан-1-іл)піридин-2-амін;
адамантан-2-іл-[4-(3аR,6аR)-(гексагідропіроло[3,4-b]пірол-5-іл)-піридин-2-іл]амін;
4-[(3S)-3-амінопіролідин-1-іл]-N-бензилпіридин-2-амін;
4-[(3S)-3-амінопіролідин-1-іл]-N-циклопентилпіридин-2-амін;
4-піперазин-1-іл-N-[(1S,5R)-2,6,6-триметилбіцикло[3.1.1]гепт-3-ил]піридин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-біцикло[2.2.1]гепт-2-илпіридин-2-амін;
N-[(1R)-1-циклогексилетил]-4-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]піридин-2-амін;
4-[(3S)-3-амінопіролідин-1-іл]-N-[(1S,5R)-2,6,6-триметилбіцикло[3.1.1]гепт-3-ил]піридин-2-амін;
1-({4-[(3S)-3-амінопіролідин-1-іл]піридин-2-іл}аміно)-2-метилпропан-2-ол;
4-[(3R)-3-амінопіролідин-1-іл]-N-циклогексилпіридин-2-амін;
N-(циклопентилметил)-4-[3-(метиламіно)азетидин-1-іл]піридин-2-амін;
4-[(3S)-3-амінопіролідин-1-іл]-N-(2-фенілетил)піридин-2-амін;
4-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]-N-(тетрагідро-2Н-піран-4-іл)піридин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-(циклопентилметил)піридин-2-амін;
1-({4-[(3R)-3-амінопіролідин-1-іл]піридин-2-іл}аміно)-2-метилпропан-2-ол;
N-трет-бутил-4-[3-(метиламіно)азетидин-1-іл]піридин-2-амін;
N-циклопропіл-4-[3-(метиламіно)азетидин-1-іл]піридин-2-амін;
2-метил-1-({4-[3-(метиламіно)азетидин-1-іл]піридин-2-іл}аміно)пропан-2-ол;
3-({4-[3-(метиламіно)азетидин-1-іл]піридин-2-іл}аміно)пропан-1-ол;
4-[3-(метиламіно)азетидин-1-іл]-N-[(1S,5R)-2,6,6-триметилбіцикло[3.1.1]гепт-3-ил]піридин-2-амін;
N-бензил-4-[3-(метиламіно)азетидин-1-іл]піридин-2-амін;
N-(2-метоксіетил)-4-[3-(метиламіно)азетидин-1-іл]піридин-2-амін;
4-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]-N-[(1S,5R)-2,6,6-триметилбіцикло[3.1.1]гепт-3-ил]піридин-2-амін;
N-трет-бутил-4-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]піридин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-(2-метоксіетил)піридин-2-амін;
2-метил-1-[(4-піперазин-1-ілпіридин-2-іл)аміно]пропан-2-ол;
N-{[(1S,2S,5S)-6,6-диметилбіцикло[3.1.1]гепт-2-ил]метил}-4-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1H)-іл]піридин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-циклопентилпіридин-2-амін;
N-(2,2-диметилпропіл)-4-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]піридин-2-амін;
4-[3-(метиламіно)азетидин-1-іл]-N-(2-фенілетил)піридин-2-амін;
N-(4-фторбензил)-4-[3-(метиламіно)азетидин-1-іл]піридин-2-амін;
адамантан-1-іл-[4-(3аR,6аR)-(гексагідропіроло[3,4-b]пірол-5-іл)-піридин-2-іл]амін;
4-[3-(метиламіно)азетидин-1-іл]-N-(піридин-2-ілметил)піридин-2-амін;
N-(циклопентилметил)-4-піперазин-1-ілпіридин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-(2-метилпропіл)піримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-(циклопропілметил)піримідин-2-амін;
4-[(3R)-3-амінопіролідин-і-іл]-N-циклопентилпіримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-(2,2-диметилпропіл)піримідин-2-амін;
1-({4-[(3R)-3-амінопіролідин-1-іл]піримідин-2-іл}аміно)-2-метилпропан-2-ол;
4-[(3R)-3-амінопіролідин-1-іл]-N-циклобутилпіримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-[(3R)-тетрагідрофуран-3-іл]піримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-(тетрагідро-2Н-піран-4-іл)піримідин-2-амін;
ізобутил-[4-(4-метилпіперазин-1-іл)-піримідин-2-іл]-амін;
4-[(3R)-3-(метиламіно)піролідин-1-іл]-N-(2-метилпропіл)піримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-[біцикло[2.2.1]гепт-2-ил]піримідин-2-амін;
N-[біцикло[2.2.1]гепт-2-ил]-4-(4-метилпіперазин-1-іл)піримідин-2-амін;
N-(циклопропілметил)-4-(4-метилпіперазин-1-іл)піримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-бутилпіримідин-2-амін;
N-бутил-4-(4-метилпіперазин-1-іл)піримідин-2-амін;
N-циклопентил-4-(4-метилпіперазин-1-іл)піримідин-2-амін;
N-(2,2-диметилпропіл)-4-(4-метилпіперазин-1-іл)піримідин-2-амін;
4-(4-метилпіперазин-1-іл)-N-(тетрагідрофуран-2-ілметил)піримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-(тетрагідрофуран-2-ілметил)піримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-(1-метилетил)піримідин-2-амін;
N-(1-метилетил)-4-(4-метилпіперазин-1-іл)піримідин-2-амін;
N-циклобутил-4-(4-метилпіперазин-1-іл)піримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-циклопропілпіримідин-2-амін;
N-циклопропіл-4-(4-метилпіперазин-1-іл)піримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-(4-фторбензил)піримідин-2-амін;
N-(4-фторбензил)-4-(4-метилпіперазин-1-іл)піримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-(2-метоксіетил)піримідин-2-амін;
N-(2-метоксіетил)-4-(4-метилпіперазин-1-іл)піримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-(піридин-2-ілметил)піримідин-2-амін;
4-(4-метилпіперазин-1-іл)-N-(піридин-2-ілметил)піримідин-2-амін;
циклопентил-(4-піперазин-1-ілпіримідин-2-іл)амін;
(2,2-диметилпропіл)-(4-піперазин-1-ілпіримідин-2-іл)амін;
ізобутил-(4-піперазин-1-ілпіримідин-2-іл)амін;
циклопропілметил-(4-піперазин-1-ілпіримідин-2-іл)амін;
ізопропіл-(4-піперазин-1-ілпіримідин-2-іл)амін;
бутил-(4-піперазин-1-ілпіримідин-2-іл)амін;
(R)-(4-піперазин-1-ілпіримідин-2-іл)-(тетрагідрофуран-2-ілметил)амін;
біцикло[2.2.1]гепт-2-ил-(4-піперазин-1-ілпіримідин-2-іл)амін;
(4-піперазин-1-ілпіримідин-2-іл)-(2,6,6-триметилбіцикло[3.1.1]гепт-3-ил)амін;
N-(2-метоксіетил)-4-піперазин-1-ілпіримідин-2-амін;
бутил-[4-(3R)-(3-метиламінопіролідин-1-іл)-піримідин-2-іл]амін;
біцикло[2.2.1]гепт-2-ил-[4-(3R)-(3-метиламінопіролідин-1-іл)-піримідин-2-іл]амін;
циклопентил-[4-(3R)-(3-метиламінопіролідин-1-іл)-піримідин-2-іл]амін;
(2,2-диметилпропіл)-[4-(3R)-(3-метиламінопіролідин-1-іл)-піримідин-2-іл]амін;
циклопропілметил-[4-(3R)-(3-метиламінопіролідин-1-іл)-піримідин-2-іл]амін;
ізопропіл-[4-(3R)-(3-метиламінопіролідин-1-іл)-піримідин-2-іл]амін;
(4-фторбензил)-[4-(3R)-(3-метиламінопіролідин-1-іл)-піримідин-2-іл]амін;
циклопропіл-[4-(3R)-(3-метиламінопіролідин-1-іл)-піримідин-2-іл]амін;
[4-(3R)-(3-метиламінопіролідин-1-іл)-піримідин-2-іл]-(тетрагідрофуран-2-ілметил)амін;
(2-метоксіетил)-[4-(3R)-(3-метиламінопіролідин-1-іл)-піримідин-2-іл]амін;
[4-(3R)-(3-метиламінопіролідин-1-іл)-піримідин-2-іл]-піридин-2-ілметиламін;
[4-(3-аміноазетидин-1-іл)-піримідин-2-іл]бутиламін;
4-(3-аміноазетидин-1-іл)-N-циклопентилпіримідин-2-амін;
4-(3-аміноазетидин-1-іл)-N-(циклопропілметил)піримідин-2-амін;
4-(3-аміноазетидин-1-іл)-N-біцикло[2.2.1]гепт-2-илпіримідин-2-амін;
4-(3-аміноазетидин-1-іл)-N-(2,2-диметилпропіл)піримідин-2-амін;
4-(3-аміноазетидин-1-іл)-N-(2-метилпропіл)піримідин-2-амін;
4-(3-аміноазетидин-1-іл)-N-(1-метилетил)піримідин-2-амін;
4-(3-аміноазетидин-1-іл)-N-циклопропілпіримідин-2-амін;
4-(3-аміноазетидин-1-іл)-N-(4-фторбензил)піримідин-2-амін;
4-(3-аміноазетидин-1-іл)-N-[(3R)-тетрагідрофуран-3-іл]піримідин-2-амін;
4-(3-аміноазетидин-1-іл)-N-[(2R)-тетрагідрофуран-2-ілметил]піримідин-2-амін;
N-(циклогексилметил)-4-[3-(метиламіно)азетидин-1-іл]піримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-[(1R)-1-циклогексилетил]піримідин-2-амін;
N-{[(1S,2S,5S)-6,6-диметилбіцикло[3.1.1]гепт-2-ил]метил}-4-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]піримідин-2-амін;
N-[(6,6-диметилбіцикло[3.1.1]гепт-2-ил)метил]-4-[3-(метиламіно)азетидин-1-іл]піримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-[(6,6-диметилбіцикло[3.1.1]гепт-2-ил)метил]піримідин-2-амін;
N-(циклогексилметил)-4-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]піримідин-2-амін;
4-[3-(метиламіно)азетидин-1-іл]-N-(тетрагідро-2Н-піран-4-іл)піримідин-2-амін;
4-[(3S)-3-амінопіролідин-1-іл]-N-(циклопропілметил)піримідин-2-амін;
1-({4-[(3S)-3-амінопіролідин-1-іл]піримідин-2-іл}аміно)-2-метилпропан-2-ол;
4-[(3S)-3-амінопіролідин-1-іл]-N-(2,2-диметилпропіл)піримідин-2-амін;
N-циклопропіл-4-піперазин-1-ілпіримідин-2-амін;
N-[(1R)-1-циклогексилетил]-4-[3-(метиламіно)азетидин-1-іл]піримідин-2-амін;
2-метил-1-({4-[(3R)-3-(метиламіно)піролідин-1-іл]піримідин-2-іл}аміно)пропан-2-ол;
N-[(1R)-1-циклогексилетил]-4-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]піримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-[(1S,2S,3S,5R)-2,6,6-триметилбіцикло[3.1.1]гепт-3-ил]піримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-(2-фенілетил)піримідин-2-амін;
4-[(3S)-3-амінопіролідин-1-іл]-Н-(піридин-2-ілметил)піримідин-2-амін;
N-(циклопентилметил)-4-(4-метилпіперазин-1-іл)піримідин-2-амін;
2-метил-1-{[4-(4-метилпіперазин-1-іл)піримідин-2-іл]аміно}пропан-2-ол;
N-(циклопeнтилмeтил)-4-[(3R)-3-(мeтилaмiнo)пipoлiдин-1-iл]пipимiдин-2-амін;
2-метил-1-({4-[3-(метиламіно)азетидин-1-іл]піримідин-2-іл}аміно)пропан-2-ол;
4-[(3R)-3-aмiнoпipoлiдин-1-iл]-N-(циклoпeнтилмeтил)пipимiдин-2-aмiн;
N-[2-(мeтилcyльфaнiл)eтил]-4-пiпepaзин-1-iлпipимiдин-2-aмiн;
4-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]-N-[(1R,2S,4R)-1,7,7-триметилбіцикло[2.2.1]гепт-2-ил]піримідин-2-амін;
4-[3-(метиламіно)азетидин-1-іл]-N-[(1R,2S,4R)-1,7,7-триметилбіцикло[2.2.1]гепт-2-ил]піримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-[(1R,2S,4R)-1,7,7-триметилбіцикло[2.2.1]гепт-2-ил]піримідин-2-амін;
4-[(3S)-3-амінопіролідин-1-іл]-N-(2-метоксіетил)піримідин-2-амін;
4-[(3S)-3-амінопіролідин-1-іл]-N-циклогексилпіримідин-2-амін;
3-({4-[(3S)-3-амінопіролідин-1-іл]піримідин-2-іл}аміно)-2,2-диметилпропан-1-ол;
N-бензил-4-піперазин-1-ілпіримідин-2-амін;
N-(2-фенілетил)-4-піперазин-1-ілпіримідин-2-амін;
N-біцикло[2.2.1]гепт-2-ил-4-піперазин-1-ілпіримідин-2-амін;
4-піпepaзин-1-iл-N-[(1S,2S,3S,5R)-2,6,6-тpимeтилбiциклo[3.1.1.]гeпт-3-ил]піримідин-2-амін;
3-({4-[3-(метиламіно)азетидин-1-іл]піримідин-2-іл}аміно)пропан-1-ол;
2,2-диметил-3-({4-[3-(метиламіно)азетидин-1-іл]піримідин-2-іл}аміно)пропан-1-ол;
3-[(4-піперазин-1-ілпіримідин-2-іл)аміно]пропан-1-ол;
4-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]-N-(2-метилпропіл)піримідин-2-амін;
N-циклопентил-4-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]піримідин-2-амін;
4-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]-N-(2-метоксіетил)піримідин-2-амін;
4-[(3aR,6aR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]-N-[(1R)-1-фенілетил]піримідин-2-амін;
N-[-(4-фторбензил)-4-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]піримідин-2-амін;
N-циклопропіл-4-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]піримідин-2-амін;
N-(4-метоксибензил)-4-піперазин-1-ілпіримідин-2-амін;
N-циклопропіл-4-[(3S)-3-(метиламіно)піролідин-1-іл]піримідин-2-амін;
4-[(3S)-3-амінопіролідин-1-іл]-N-біцикло[2.2.1]гепт-2-илпіримідин-2-амін;
N-біцикло[2.2.1]гепт-2-ил-4-[3-(метиламіно)азетидин-1-іл]піримідин-2-амін;
3-({4-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1H)-іл]піримідин-2-іл}аміно)-2,2-диметилпропан-1-ол;
4-[(3S)-3-амінопіролідин-1-іл]-N-(циклопентилметил)піримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-(4,4,4-трифторбутил)піримідин-2-амін;
3-{[4-(3-аміноазетидин-1-іл)піримідин-2-іл]аміно}-2,2-диметилпропан-1-ол;
3-({4-[(3S)-3-(метиламіно)піролідин-1-іл]піримідин-2-іл}аміно)пропан-1-ол;
3-({4-[(3R)-3-амінопіролідин-1-іл]піримідин-2-іл}аміно)-2,2-диметилпропан-1-ол;
3-({4-[(3R)-3-амінопіролідин-1-іл]піримідин-2-іл}аміно)пропан-1-ол;
3-{[4-(3-аміноазетидин-1-іл)піримідин-2-іл]аміно}пропан-1-ол;
N-(4-метилбензил)-4-піперазин-1-ілпіримідин-2-амін;
4-піперазин-1-іл-N-(піридин-2-ілметил)піримідин-2-амін;
2,2-диметил-3-({4-[(3S)-3-(метиламіно)піролідин-1-іл]піримідин-2-іл}аміно)пропан-1-ол;
3-({4-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]піримідин-2-іл}аміно)пропан-1-ол;
4-[(3S)-3-амінопіролідин-1-іл]-N-циклопентилпіримідин-2-амін;
3-{[4-(4-метилпіперазин-1-іл)піримідин-2-іл]аміно}пропан-1-ол;
N-біцикло[2.2.1]гепт-2-ил-4-[(3S)-3-(метиламіно)піролідин-1-іл]піримідин-2-амін;
N-(4-метилбензил)-4-(4-метилпіперазин-1-іл)піримідин-2-амін;
4-(4-метилпіперазин-1-іл)-N-[2-(метилсульфаніл)етил]піримідин-2-амін;
N-бензил-4-(4-метилпіперазин-1-іл)піримідин-2-амін;
2,2-диметил-3-[(4-піперазин-1-ілпіримідин-2-іл)аміно]пропан-1-ол;
3-({4-[(3R)-3-(метиламіно)піролідин-1-іл]піримідин-2-іл}аміно)пропан-1-ол;
4-(4-метилпіперазин-1-іл)-Ν-[(1S,2S,3S,5R)-2,6,6-триметилбіцикло[3.1.1]гепт-3-ил]піримідин-2-амін;
2,2-диметил-3-({4-[(3R)-3-(метиламіно)піролідин-1-іл]піримідин-2-іл}аміно)пропан-1-ол;
4-[(3R)-3-(метиламіно)піролідин-1-іл]-N-(4-метилбензил)піримідин-2-амін;
4-[3-(метиламіно)азетидин-1-іл]-N-(2-метилпропіл)піримідин-2-амін;
N-циклoпeнтил-4-[3-(мeтилaмiнo)aзeтидин-1-iл]пipимiдин-2-aмін;
4-(4-метилпіперазин-1-іл)-N-(2-фенілетил)піримідин-2-амін;
N-бензил-4-[(3R)-3-(метиламіно)піролідин-1-іл]піримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-[(1R)-1-фенілетил]піримідин-2-амін;
N-(4-метоксибензил)-4-[(3R)-3-(метиламіно)піролідин-1-іл]піримідин-2-амін;
2-метил-1-[(4-піперазин-1-ілпіримідин-2-іл)аміно]пропан-2-ол;
N-(4-фторбензил)-4-[3-(метиламіно)азетидин-1-іл]піримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-бензилпіримідин-2-амін;
4-[(3R)-3-(метиламіно)піролідин-1-іл]-N-[(1R)-1-фенілетил]піримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-циклогексилпіримідин-2-амін;
N-(2-метоксіетил)-4-[3-(метиламіно)азетидин-1-іл]піримідин-2-амін;
4-[(3R)-3-(метиламіно)піролідин-1-іл]-N-(2-фенілетил)піримідин-2-амін;
4-[(3R)-3-(метиламіно)піролідин-1-іл]-N-[(1S,2S,3S,5R)-2,6,6-триметилбіцикло[3.1.1]гепт-3-ил]піримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-(4-метоксибензил)піримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-(4-метилбензил)піримідин-2-амін;
N-(циклопентилметил)-4-піперазин-1-ілпіримідин-2-амін;
4-[3-(метиламіно)азетидин-1-іл]-N-(піридин-2-ілметил)піримідин-2-амін;
4-[(3R)-3-(метиламіно)піролідин-1-іл]-N[(3S,5S,7S)-трицикло[3.3.1.1.3.7]дец-1-илметил]піримідин-2-амін;
4-[(3R)-3-(метиламіно)піролідин-1-іл]-N-[(1R,2S,4R)-1,7,7-триметилбіцикло[2.2.1]гепт-2-ил]піримідин-2-амін;
N-(циклогексилметил)-4-[(3R)-3-(метиламіно)піролідин-1-іл]піримідин-2-амін;
N-циклогексил-4-[(3R)-3-(метиламіно)піролідин-1-іл]піримідин-2-амін;
N-{[(1S,2S,5S)-6,6-диметилбіцикло[3.1.1]гепт-2-ил]метил}-4-[(3R)-3-(метиламіно)піролідин-1-іл]піримідин-2-амін;
4-(1,4-діазепан-1-іл)-N-(2,2-диметилпропіл)піримідин-2-амін;
N-біцикло[2.2.1]гепт-2-ил-4-(1,4-діазепан-1-іл)піримідин-2-амін;
4-[(3S)-3-амінопіролідин-1-іл]-N-бутилпіримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-(циклогексилметил)піримідин-2-амін;
4-[(3S)-3-амінопіролідин-1-іл]-N-(2-метилпропіл)піримідин-2-амін;
4-[(3S)-3-амінопіролідин-1-іл]-N-(4-фторбензил)піримідин-2-амін;
4-[(3S)-3-(метиламіно)піролідин-1-іл]-N-(піридин-2-ілметил)піримідин-2-амін;
N-циклопентил-4-[(3S)-3-(метиламіно)піролідин-1-іл]піримідин-2-амін;
4-[(3S)-3-(метиламіно)піролідин-1-іл]-N-(2-метилпропіл)піримідин-2-амін;
N-(2,2-диметилпропіл)-4-[(3S)-3-(метиламіно)піролідин-1-іл]піримідин-2-амін;
N-бензил-4-[(3S)-3-(метиламіно)піролідин-1-іл]піримідин-2-амін;
4-[(3R)-3-амінопіролідин-1-іл]-N-[(1R,5R,7S)-трицикло[3.3.1.1.3.7]дец-2-ил]піримідин-2-амін, а також їх фармацевтично прийнятні солі і фармацевтично прийнятні проліки.
34. Сполука, вибирана з групи, що включає:
5-[(3R)-3-(метиламіно)піролідин-1-іл]-N-(2-метилпропіл)піридазин-3-амін;
N-біцикло[2.2.1]гепт-2-ил-5-[(3R)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
5-[(3R)-3-(метиламіно)піролідин-1-іл]-N-[(1S,2S,3S,5R)-2,6,6-триметилбіцикло[3.1.1]гепт-3-ил]піридазин-3-амін;
N-циклогексил-5-[(3R)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
N-(циклопропілметил)-5-[(3R)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
N-бутил-5-[(3R)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
5-(4-метилпіперазин-1-іл)-N-(2-метилпропіл)піридазин-3-амін;
5-[(3R)-3-амінопіролідин-1-іл]-N-(2-метоксіетил)піридазин-3-амін;
5-[3-(метиламіно)азетидин-1-іл]-N-(4,4,4-трифторбутил)піридазин-3-амін;
N5-(2-аміноетил)-N3-(2,2-диметилпропіл)-N5-метилпіридазин-3,5-діамін;
5-[3-(метиламіно)азетидин-1-іл]-N-[(1S,5R)-2,6,6-триметилбіцикло[3.1.1]гепт-3-ил]піридазин-3-амін;
N5-(2-аміноетил)-N3-біцикло[2.2.1]гепт-2-ил-N5-метилпіридазин-3,5-діамін;
N5-(2-аміноетил)-N3-(циклопентилметил)-N5-метилпіридазин-3,5-діамін;
5-[(3S)-3-амінопіролідин-1-іл]-N-(біцикло[2.2.1]гепт-2-илметил)піридазин-3-амін;
3-({5-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]піридазин-3-іл}аміно)пропан-1-ол;
5-(3-аміноазетидин-1-іл)-N-{[(1S,2S,5S)-6,6-диметилбіцикло[3.1.1]гепт-2-ил]метил}піридазин-3-амін;
5-(1,4-діазепан-1-іл)-N-(2,2-диметилпропіл)піридазин-3-амін;
N-біцикло[2.2.1]гепт-2-ил-5-(1,4-діазепан-1-іл)піридазин-3-амін;
N-циклопропіл-5-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]піридазин-3-амін;
N-бутил-5-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]піридазин-3-амін;
5-[(3R)-3-амінопіролідин-1-іл]-N-(біцикло[2.2.1]гепт-2-илметил)піридазин-3-амін;
3-({5-[(3R)-3-амінопіролідин-1-іл]піридазин-3-іл}аміно)пропан-1-ол;
3-[(5-піперазин-1-ілпіридазин-3-іл)аміно]пропан-1-ол;
N-циклопропіл-5-піперазин-1-ілпіридазин-3-амін;
N-(циклопентилметил)-5-(1,4-діазепан-1-іл)піридазин-3-амін;
5-[(3S)-3-амінопіролідин-1-іл]-N-(циклопентилметил)піридазин-3-амін;
5-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]-N-(2-метилпропіл)піридазин-3-амін;
5-[3-(метиламіно)азетидин-1-іл]-N-(2-метилпропіл)піридазин-3-амін;
N-(2-метоксіетил)-5-[3-(метиламіно)азетидин-1-іл]піридазин-3-амін;
5-[(3R)-3-амінопіролідин-1-іл]-N-[(1R)-1-фенілетил]піридазин-3-амін;
5-(3-аміноазетидин-1-іл)-N-біцикло[2.2.1]гепт-2-илпіридазин-3-амін;
5-(3-аміноазетидин-1-іл)-N-(2,2-диметилпропіл)піридазин-3-амін;
N-(2,2-диметилпропіл)-5-[3-(метиламіно)азетидин-1-іл]піридазин-3-амін;
N-цииклогексил-5-[3-(метиламіно)азетидин-1-іл]піридазин-3-амін;
5-(3-аміноазетидин-1-іл)-N-циклопентилпіридазин-3-амін;
N-(циклопропілметил)-5-[3-(метиламіно)азетидин-1-іл]піридазин-3-амін;
5-(3-аміноазетидин-1-іл)-N-(2-метилпропіл)піридазин-3-амін;
5-(3-аміноазетидин-1-іл)-N-бензилпіридазин-3-амін;
N-бензил-5-[3-(метиламіно)азетидин-1-іл]піридазин-3-амін;
N-біцикло[2.2.1]гепт-2-ил-5-[3-(метиламіно)азетидин-1-іл]піридазин-3-амін;
N-циклопентил-5-[3-(метиламіно)азетидин-1-іл]піридазин-3-амін;
5-(3-аміноазетидин-1-іл)-N-циклопропілпіридазин-3-амін;
3-({5-[3-(метиламіно)азетидин-1-іл]піридазин-3-іл}аміно)пропан-1-ол;
5-(3-аміноазетидин-1-іл)-N-(2-метоксіетил)піридазин-3-амін;
5-[(3S)-3-амінопіролідин-1-іл]-N-циклопропілпіридазин-3-амін;
5-[(3R)-3-амінопіролідин-1-іл]-N-(піридин-2-ілметил)піридазин-3-амін;
3-({5-[(3S)-3-амінопіролідин-1-іл]піридазин-3-іл}аміно)пропан-1-ол;
5-[(3S)-3-амінопіролідин-1-іл]-N-(2-метилпропіл)піридазин-3-амін;
5-[(3R)-3-амінопіролідин-1-іл]-N-бензилпіридазин-3-амін;
5-[(3R)-3-амінопіролідин-1-іл]-N-(4-метоксибензил)піридазин-3-амін;
5-[(3R)-3-амінопіролідин-1-іл]-N-(4-фторбензил)піридазин-3-амін;
5-[(3R)-3-амінопіролідин-1-іл]-N-(4-метилбензил)піридазин-3-амін;
N-(4-метилбензил)-5-піперазин-1-ілпіридазин-3-амін;
N-циклопентил-5-[(3аR,6аR)-гексагідропіроло[3,4-b]пірол-5(1H)-іл]піридазин-3-амін;
N-(4-фторбензил)-5-піперазин-1-ілпіридазин-3-амін;
N-(4-метоксибензил)-5-піперазин-1-ілпіридазин-3-амін;
N-бензил-5-піперазин-1-ілпіридазин-3-амін;
N-[(1R)-1-фенілетил]-5-піперазин-1-ілпіридазин-3-амін;
3-({5-[(3R)-3-амінопіролідин-1-іл]піридазин-3-іл}аміно)-2,2-диметилпропан-1-ол;
N-циклопропіл-5-[3-(метиламіно)азетидин-1-іл]піридазин-3-амін;
5-[3-(метиламіно)азетидин-1-іл]-N-(піридин-2-ілметил)піридазин-3-амін;
5-[(3R)-3-амінопіролідин-1-іл]-N-(2-метилпропіл)піридазин-3-амін;
N-циклопентил-5-піперазин-1-ілпіридазин-3-амін;
N-циклогексил-5-піперазин-1-ілпіридазин-3-амін;
N-бутил-5-піперазин-1-ілпіридазин-3-амін;
N-(2,2-диметилпропіл)-5-піперазин-1-ілпіридазин-3-амін;
5-(3-аміноазетидин-1-іл)-N-(циклопентилметил)піридазин-3-амін;
5-[(3R)-3-амінопіролідин-1-іл]-N-(циклопентилметил)піридазин-3-амін;
N-(циклопентилметил)-5-[(3АR,6аR)-гексагідропіроло[3,4-b]пірол-5(1Н)-іл]піридазин-3-амін;
N-(циклопропілметил)-5-піперазин-1-ілпіридазин-3-амін;
N-(2-фенілетил)-5-піперазин-1-ілпіридазин-3-амін;
N-(циклопентилметил)-5-піперазин-1-ілпіридазин-3-амін;
5-[(3R)-3-амінопіролідин-1-іл]-N-(2-фенілетил)піридазин-3-амін;
5-[(3R)-3-амінопіролідин-1-іл]-N-циклогексилпіридазин-3-амін;
2,2-диметил-3-[(5-піперазин-1-ілпіридазин-3-іл)аміно]пропан-1-ол;
5-[(3R)-3-амінопіролідин-1-іл]-N-бутилпіридазин-3-амін;
5-[(3R)-3-амінопіролідин-1-іл]-N-циклопентилпіридазин-3-амін;
5-[(3R)-3-амінопіролідин-1-іл]-N-(циклопропілметил)піридазин-3-амін;
N-(циклопентилметил)-5-[3-(метиламіно)азетидин-1-іл]піридазин-3-амін;
5-[(3R)-3-амінопіролідин-1-іл]-N-(2,2-диметилпропіл)піридазин-3-амін;
5-[(3R)-3-(метиламіно)піролідин-1-іл]-N-(2-фенілетил)піридазин-3-амін;
N-[(1R)-1-циклогексилетил]-5-[(3S)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
N-(біцикло[2.2.1]гепт-2-илметил)-5-[(3S)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
N-(біцикло[2.2.1]гепт-2-илметил)-5-[(3R)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
N-(2-метоксіетил)-5-[(3S)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
N-циклопропіл-5-[(3R)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
N-[(1R)-1-циклогексилетил]-5-[(3R)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
5-[(3S)-3-(метиламіно)піролідин-1-іл]-N-(2-метилпропіл)піридазин-3-амін;
N-циклопентил-5-[(3S)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
N-біцикло[2.2.1]гепт-2-ил-5-[(3S)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
N-(циклопентилметил)-5-[(3S)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
2,2-диметил-3-({5-[(3S)-3-(метиламіно)піролідин-1-іл]піридазин-3-іл}аміно)пропан-1-ол;
5-[(3R)-3-(метиламіно)піролідин-1-іл]-N-(4-метилбензил)піридазин-3-амін;
N-(2,2-диметилпропіл)-5-[(3S)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
5-[(3R)-3-(метиламіно)піролідин-1-іл]-N-(4,4,4-трифторбутил)піридазин-3-амін;
N-(фуран-3-ілметил)-5-[(3R)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
N-[(6,6-диметилбіцикло[3.1.1]гепт-2-ил)метил]-5-[(3R)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
5-[(3S)-3-(метиламіно)піролідин-1-іл]-N-(4,4,4-трифторбутил)піридазин-3-амін;
3-({5-[(3R)-3-(метиламіно)піролідин-1-іл]піридазин-3-іл}аміно)пропан-1-ол;
N-(циклогексилметил)-5-[(3R)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
N-(2,2-диметилпропіл)-5-[(3R)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
N-(2-метоксіетил)-5-[(3R)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
N-[(6,6-диметилбіцикло[3.1.1]гепт-2-ил)метил]-5-[(3S)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
N-циклопропіл-5-[(3S)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
N-(циклогексилметил)-5-[(3S)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
N-бензил-5-[(3R)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
N-(4-фторбензил)-5-[(3R)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
N-(4-фторбензил)-5-[(3S)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
N-(4-метоксибензил)-5-[(3R)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
5-[(3R)-3-(метиламіно)піролідин-1-іл]-N-[(1R)-1-фенілетил]піридазин-3-амін;
5-[(3S)-3-(метиламіно)піролідин-1-іл]-N-(піридин-2-ілметил)піридазин-3-амін;
3-({5-[(3S)-3-(метиламіно)піролідин-1-іл]піридазин-3-іл}аміно)пропан-1-ол;
N-(2,2-диметилпропіл)-5-(4-метилпіперазин-1-іл)піридазин-3-амін;
N-(2-метоксіетил)-5-(4-метилпіперазин-1-іл)піридазин-3-амін;
N-біцикло[2.2.1]гепт-2-ил-5-(4-метилпіперазин-1-іл)піридазин-3-амін;
N-циклопентил-5-(4-метилпіперазин-1-іл)піридазин-3-амін;
N-(циклопентилметил)-5-(4-метилпіперазин-1-іл)піридазин-3-амін;
5-(4-метилпіперазин-1-іл)-N-(2-фенілетил)піридазин-3-амін;
N-бензил-5-(4-метилпіперазин-1-іл)піридазин-3-амін;
5-(4-метилпіперазин-1-іл)-N-(піридин-2-ілметил)піридазин-3-амін;
N-циклопентил-5-[(3R)-3-(метиламіно)піролідин-1-іл]піридазин-3-амін;
(R)-5-(3-(метиламіно)піролідин-1-іл)-N-(1-адамантил)піридазин-3-аміну дигідрохлорид;
(R)-5-(3-(метиламіно)піролідин-1-іл)-N-(2-адамантил)піридазин-3-аміну дигідрохлорид;
(S)-5-(3-(метиламіно)піролідин-1-іл)-N-(2-адамантил)піридазин-3-аміну дигідрохлорид;
(S)-5-(3-(метиламіно)піролідин-1-іл)-N-(1-адамантил)піридазин-3-аміну дигідрохлорид або їх фармацевтично прийнятні солі.
35. Фармацевтична композиція, яка містить ефективну кількість щонайменше однієї зі сполук формули (І)
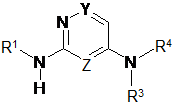 ,
,
Формула (I)
де
Ζ являє собою СН або Ν;
Υ являє собою СН або Ν;
Ζ і Υ визначаються незалежно один від одного, і кільце, що містить згадані Υ і Ζ, має не більше двох атомів азоту; за умови, що
і) коли Υ являє собою СН і Ζ являє собою СН або Ν, то R1 являє собою:
а) -(СН2)2ОСН3, -(СН2)2СН3 або С1-8алкіл, кожний з яких незалежно не заміщений або заміщений -ОН або -CF3;
б) -(CH2)0-2-Ar1, -CHR2-Ar1 або -(СН2)0-2-Аr2, причому кожний зі згаданих Аr1 і Аr2 незалежно не заміщений або заміщений галогеном, -СН3 або -ОСН3,
Аr1 являє собою 6-членне ароматичне карбоциклічне кільце,
Аr2 являє собою 5- або 6-членне гетероароматичне кільце, що містить N, S або О; або
в) циклоалкіл, -(СН2)-(моноциклічний циклоалкіл), -(СН2)-(місточковий поліциклічний циклоалкіл)0-1, -(СHR2)-(моноциклічний циклоалкіл), -(СН2)-(конденсований циклоалкіл), -(СН2)-(місточковий моноциклічний циклоалкіл), -(СН2)0-1-тетрагідрофураніл або -(СН2)0-1-тетрагідропіраніл, причому кожний зі згаданих фрагментів незалежно не заміщений або заміщений одним, двома або трьома С1-4алкільними замісниками;
R2 являє собою -С1-4алкіл;
![]() являє собою
являє собою 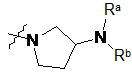 ,
, 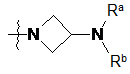 ,
, 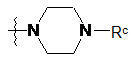 ,
, 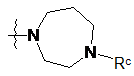 ,
, 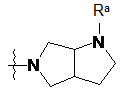 або
або 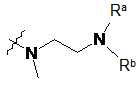 ;
;
де Ra, Rb і Rc, кожен незалежно, являють собою Η або С1-3алкіл; за умови, що:
якщо R1 являє собою ізопропіл, то Rc являє собою метил;
якщо R1 являє собою 4-метилфеніл, то Rc являє собою метил;
коли Ζ являє собою Ν, Υ являє собою СН і R1 являє собою бензил, не заміщений або заміщений галогеном, то Rc являє собою метил;
іі) коли Υ являє собою N і Ζ являє собою СН, то R1 являє собою:
а) -(СН2)2ОСН3, -(CH2)2SCH3 або С1-8алкіл, кожний з яких незалежно не заміщений або заміщений -CF або -CF3;
б) -(СН2)0-1-Аr1, -CHR2-ArI, -(СН3)0-2-Аr2, причому кожний зі згаданих Аr1 і Аr2 незалежно не заміщений або заміщений галогеном, -СН3, -ОСН3,
Аr1 являє собою 6-членне ароматичне карбоциклічне кільце,
Аr2 являє собою 5- або 6-членне гетероароматичне кільце, що містить N, S або О; або
в) циклоалкіл, -(СН2)-(моноциклічний циклоалкіл), -(СН2)-(місточковий поліциклічний циклоалкіл)0-1, -(СHR2)-(моноциклічний циклоалкіл), -(СН2)-(конденсований циклоалкіл), -(СН2)-(місточковий моноциклічний циклоалкіл), -(СН2)0-1-тетрагідрофураніл або -(СН2)0-1-тетрагідропіраніл, причому кожний зі згаданих фрагментів незалежно не заміщений або заміщений одним, двома або трьома С1-4алкільними замісниками;
R2 являє собою -С1-4алкіл;
![]() являє собою
являє собою 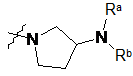 ,
, 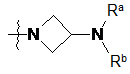 ,
, 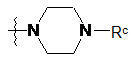 ,
, 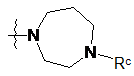 ,
, 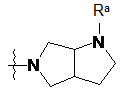 або
або 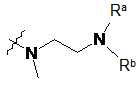 ;
;
де Ra, Rb і Rc, кожен незалежно, являють собою Η або С1-3алкіл; або їх фармацевтично прийнятних солей.
36. Фармацевтична композиція за п. 35, де Υ являє собою СН і Ζ являє собою СН або N.
37. Фармацевтична композиція за п. 35, де Υ являє собою N і Ζ являє собою СН.
38. Фармацевтична композиція, яка містить ефективну кількість щонайменше однієї з хімічних сполук за п. 33.
39. Фармацевтична композиція, яка містить ефективну кількість щонайменше однієї з хімічних сполук за п. 34.
40. Спосіб лікування пацієнта, що страждає від або у якого діагностовано захворювання, розлад або медичний стан, опосередкований активністю гістамінового рецептора Н4, в якому потребуючому подібного лікування пацієнту вводять ефективну кількість щонайменше однієї з хімічних сполук, вибираних зі сполук формули (І)
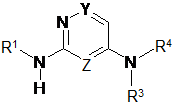 ,
,
Формула (I)
де
Ζ являє собою СН або Ν;
Υ являє собою СН або Ν;
Ζ і Υ визначаються незалежно один від одного, і кільце, що містить згадані Υ і Ζ, має не більше двох атомів азоту; за умови, що
і) коли Υ являє собою СН і Ζ являє собою СН або Ν, то R1 являє собою:
а) -(СН2)2ОСН3, -(CH2)2SCH3 або С1-8алкіл, кожний з яких незалежно не заміщений або заміщений -ОН або -CF3;
б) -(СН2)0-2-Аr1, -СНR2-Аr1 або -(СН2)0-2-Аr2, причому кожний зі згаданих Аr1 і Аr2 незалежно не заміщений або заміщений галогеном, -СН3 або -ОСН3,
Аr1 являє собою 6-членне ароматичне карбоциклічне кільце,
Аr2 являє собою 5- або 6-членне гетероароматичне кільце, що містить N, S або О; або
в) циклоалкіл, -(СН2)-(моноциклічний циклоалкіл), -(СН2)-(місточковий поліциклічний циклоалкіл)0-1, -(СНR2)-(моноциклічний циклоалкіл), -(СН2)-(конденсований циклоалкіл), -(СН2)-(місточковий моноциклічний циклоалкіл), -(СН2)0-1-тетрагідрофураніл або -(СН2)0-1-тетрагідропіраніл, причому кожний зі згаданих фрагментів не заміщений або заміщений одним, двома або трьома С1-4алкільними замісниками;
R2 являє собою -С1-4алкіл;
![]() являє собою
являє собою 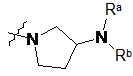 ,
, 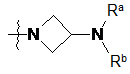 ,
, 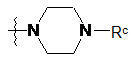 ,
, 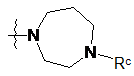 ,
, 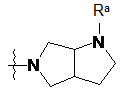 або
або 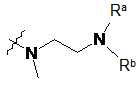 ;
;
де Ra, Rb і Rc, кожен незалежно, являють собою Η або С1-3алкіл; за умови, що:
якщо R1 являє собою ізопропіл, то Rc являє собою метил;
якщо R1 являє собою 4-метилфеніл, то Rc являє собою метил;
коли Ζ являє собою Ν, Υ являє собою СН і R1 являє собою бензил, не заміщений або заміщений галогеном, то Rc являє собою метил;
іі) коли Υ являє собою N і Ζ являє собою СН, то R1 являє собою:
а) -(СН2)2ОСН3, -(СН2)2SСН3 або С1-8алкіл, кожний з яких незалежно не заміщений або заміщений -CF або -CF3;
б) -(СН2)0-2-Аr1, -CHR2-Ar1, -(СН2)0-2-Аr2, причому кожний зі згаданих Аr1 і Аr2 незалежно не заміщений або заміщений галогеном, -СН3, -ОСН3,
Аr1 являє собою 6-членне ароматичне карбоциклічне кільце,
Аr2 являє собою 5- або 6-членне гетероароматичне кільце, що містить N, S або О; або
в) циклоалкіл, -(СН2)-(моноциклічний циклоалкіл), -(СH2)-(місточковий поліциклічний циклоалкіл)0-1, -(CHR2)-(моноциклічний циклоалкіл), -(СН2)-(конденсований циклоалкіл), -(СН2)-(місточковий моноциклічний циклоалкіл), -(СН2)0-1-тетрагідрофураніл або -(СН2)0-1-тетрагідропіраніл, причому кожний зі згаданих фрагментів незалежно не заміщений або заміщений одним, двома або трьома С1-4алкільними замісниками;
R2 являє собою -С1-4алкіл;
![]() являє собою
являє собою 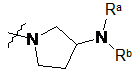 ,
, 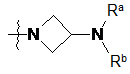 ,
, 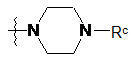 ,
, 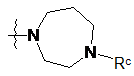 ,
, 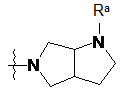 або
або 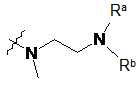 ;
;
де Ra, Rb і Rc, кожен незалежно, являють собою Η або С1-3алкіл;
або їх фармацевтично прийнятних солей.
41. Спосіб за п. 40, у якому Υ являє собою Η і Ζ являє собою СН або N.
42. Спосіб за п. 40, у якому Υ являє собою N і Ζ являє собою СН.
43. Спосіб лікування пацієнта, що страждає від або у якого діагностовано захворювання, розлад або медичний стан, опосередкований активністю гістамінового рецептора H4, в якому потребуючому подібного лікування пацієнту вводять ефективну кількість щонайменше однієї з хімічних сполук за п. 33.
44. Спосіб лікування пацієнта, що страждає від або у якого діагностовано захворювання, розлад або медичний стан, опосередкований активністю гістамінового рецептора Н4, в якому потребуючому подібного лікування пацієнту вводять ефективну кількість щонайменше однієї з хімічних сполук за п. 34.
45. Спосіб за п. 40, у якому згадані захворювання, розлад або медичний стан являють собою запалення.
46. Спосіб за п. 40, у якому згадані захворювання, розлад або медичний стан вибирають з групи, що включає запальні розлади, алергічні розлади, дерматологічні розлади, аутоімунні захворювання, лімфатичні розлади і імунодефіцитні розлади.
47. Спосіб за п. 40, у якому згадані захворювання, розлад або медичний стан вибирають з групи, що включає наступні захворювання: алергію, астму, синдром сухого ока, хронічне обструктивне захворювання легень (COPD), атеросклероз, ревматоїдний артрит, розсіяний склероз, запальні захворювання кишечнику, коліт, хворобу Крона, виразковий коліт, псоріаз, прурит, шкірний свербіж, атопічний дерматит, алергічну висипку, кропивницю, запалення очей, кон'юнктивіт, носові поліпи, алергічний риніт, носовий свербіж, склеродермію, аутоімунні захворювання щитовидної залози, післяопераційні спайки, імуноопосередкований цукровий діабет (1 типу), цукровий діабет 2 типу, хронічну ниркову недостатність, гепатичний холестаз, вовчак, важку псевдопаралітичну міастенію (Myasthenia gravis), аутоімунні нейропатії, синдром Гійєна-Барре (Guillain-Barre), аутоімунний увеїт, аутоімунну гемолітичну анемію, злоякісну анемію, аутоімунну тромбоцитопенію, скроневий артеріїт, антифосфоліпідний синдром, васкулітиди, гранулематоз Вегенера, хворобу Бехчета, герпетиформний дерматит, пухирчатку звичайну, вітиліго, первинний біліарний цироз печінки, аутоімунний гепатит, аутоімунний оофорит, аутоімунний орхіт, аутоімунне захворювання надниркових залоз, поліміозит, дерматоміозит, спондилоартропатії, анкілозуючий спондилоартрит, синдром Сьєргена, великий депресивний розлад, біполярний афективний розлад, великий депресивний розлад, що не піддається лікуванню, біполярний афективний розлад, що не піддається лікуванню, генералізований тривожний розлад, соціофобії, посттравматичний стресовий розлад і больовий синдром.
48. Спосіб за п. 40, у якому згадані захворювання, розлад або медичний стан вибирають з групи, що включає наступні захворювання: алергію, астму, ревматоїдний артрит, аутоімунні захворювання і шкірний свербіж.
49. Спосіб модуляції активності гістамінового рецептора Н4, в якому на гістаміновий рецептор Н4 впливають ефективною кількістю щонайменше однієї з хімічних сполук, вибираних зі сполук формули (І)
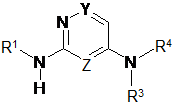 ,
,
Формула (I)
де
Ζ являє собою СН або Ν;
Υ являє собою СН або Ν;
Ζ і Υ визначаються незалежно один від одного, і кільце, що містить згадані Υ і Ζ, має не більше двох атомів азоту; за умови, що
і) коли Υ являє собою СН і Ζ являє собою СН або Ν, то R1 являє собою:
а) -(СН2)2ОСН3, -(СН2)2SСН3 або С1-8алкіл, кожний з яких незалежно не заміщений або заміщений -ОН або -CF3;
б) -(СН2)0-2-Аr1, -CHR2-Ar1 або -(СН2)0-2-Аr2, причому кожний зі згаданих Аr1 і Аr2 незалежно не заміщений або заміщений галогеном, -СН3 або -ОСН3,
Аr1 являє собою 6-членне ароматичне карбоциклічне кільце,
Аr2 являє собою 5- або 6-членне гетероароматичне кільце, що містить N, S або О; або
в) циклоалкіл, -(СН2)-(моноциклічний циклоалкіл), -(СН2)-(місточковий поліциклічний циклоалкіл)0-1, -(СНR2)-(моноциклічний циклоалкіл), -(СН2)-(конденсований циклоалкіл), -(СН2)-(місточковий моноциклічний циклоалкіл), -(СН2)0-1-тетрагідрофураніл або -(СН2)0-1-тетрагідропіраніл, причому кожний зі згаданих фрагментів незалежно не заміщений або заміщений одним, двома або трьома С1-4алкільними замісниками;
R2 являє собою -С1-4алкіл;
![]() являє собою
являє собою 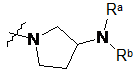 ,
, 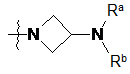 ,
, 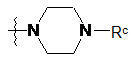 ,
, 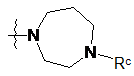 ,
, 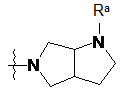 або
або 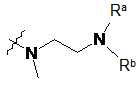 ;
;
де Ra, Rb і Rc, кожен незалежно, являють собою Η або С1-3алкіл;
за умови, що:
якщо R1 являє собою ізопропіл, то Rc являє собою метил;
якщо R1 являє собою 4-метилфеніл, то Rc являє собою метил;
коли Ζ являє собою Ν, Υ являє собою СН і R1 являє собою бензил, не заміщений або заміщений галогеном, то Rc являє собою метил;
іі) коли Υ являє собою N і Ζ являє собою СН, то R1 являє собою:
а) -(СН2)2ОСН3, -(СН2)2SСН3 або С1-8алкіл, кожний з яких незалежно не заміщений або заміщений -ОН або -CF3;
б) -(CH2)0-2-Ar1, -CHR2-Аr1, -(СН2)0-2-Аr2, причому кожний зі згаданих Аr1 і Аr2 незалежно не заміщений або заміщений галогеном, -СН3, -ОСН3,
Аr1 являє собою 6-членне ароматичне карбоциклічне кільце,
Аr2 являє собою 5- або 6-членне гетероароматичне кільце, що містить N, S або О; або
в) циклоалкіл, -(СН2)-(моноциклічний циклоалкіл), -(СН2)-(місточковий поліциклічний циклоалкіл)0-1, -(СHR2)-(моноциклічний циклоалкіл), -(СH2)-(конденсований циклоалкіл), -(СН2)-(місточковий моноциклічний циклоалкіл), -(СH2)0-1-тетрагідрофураніл або -(СН2)0-1-тетрагідропіраніл, причому кожний зі згаданих фрагментів не заміщений або заміщений одним, двома або трьома С1-4алкільними замісниками;
R2 являє собою -С1-4алкіл;
![]() являє собою
являє собою 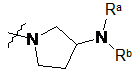 ,
, 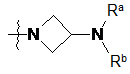 ,
, 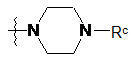 ,
, 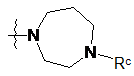 ,
, 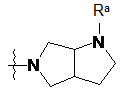 або
або 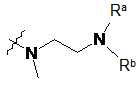 ;
;
де Ra, Rb і Rc, кожен незалежно, являють собою Η або С1-3алкіл; фармацевтично прийнятних солей сполук формули (І) і фармацевтично прийнятних проліків сполук формули (І).
50. Спосіб за п. 49, у якому Υ являє собою СН і Ζ являє собою СН або N.
51. Спосіб за п. 49, у якому Υ являє собою N і Ζ являє собою СН.
52. Спосіб модуляції активності гістамінового рецептора Н4, в якому на гістаміновий рецептор Н4 впливають ефективною кількістю щонайменше однієї зі сполук за п. 33.
53. Спосіб модуляції активності гістамінового рецептора Н4, в якому на гістаміновий рецептор Н4 впливають ефективною кількістю щонайменше однієї зі сполук за п. 34.
54. Спосіб за п. 49, у якому згаданий гістаміновий рецептор H4 знаходиться в тілі пацієнта (людини).
55. Спосіб за п. 54, у якому згаданий пацієнт страждає від або у нього діагностовано захворювання, розлад або медичний стан, опосередкований активністю гістамінового рецептора Н4.
56. Спосіб за п. 55, у якому згадані захворювання, розлад або медичний стан вибирають з групи, що включає наступні розлади і захворювання: алергія, ревматоїдний артрит, астма, аутоімунні захворювання і шкірний свербіж.
57. Спосіб за п. 40, у якому згадане введення являє собою місцеве застосування.
58. Спосіб за п. 57, у якому згаданий розлад або медичний стан являє собою запалення.
59. Спосіб за п. 57, у якому згаданий розлад або медичний стан являє собою щонайменше один з наступних розладів: шкірний свербіж, алергічна висипка або атопічний дерматит.
Текст
Реферат: Діамінопіридинові, піримідинові і піридазинові сполуки, що можуть використовуватися як модулятори рецептора Н4, а також у складі фармацевтичних композицій й у способах лікування захворювань, розладів або патологічних станів, опосередкованих активністю рецептора Н4, таких як алергія, астма, аутоімунні захворювання і шкірний свербіж. UA 106046 C2 (12) UA 106046 C2 UA 106046 C2 5 10 15 20 25 30 35 40 45 50 55 60 Галузь винаходу Даний винахід стосується деяких діамінопіридинових, піримідинових і піридазинових сполук, фармацевтичних композицій, що їх містять, способів одержання даних сполук і способів їх застосування для модулювання гістамінового рецептора H 4 і для лікування хворобливих і патологічних станів, а також розладів, опосередкованих активністю гістамінового рецептора H 4. Передумови створення винаходу Гістаміновий рецептор H4 (H4R), іноді просто позначуваний "H4" або "H4", є найбільш останнім з виявлених рецепторів гістаміну (огляди можна знайти в роботах: Fung-Leung W.-P. et al., Curr. Opin. Invest. Drugs 2004, 5(11), 1174-1183; de Esch I.J.P. et al., Trends Pharmacol. Sci. 2005, 26(9), 462-469; Zhang M. et al. Pharmacol. Ther. 2007, 113, 594-606; Thurmond R.L. et al. Nat. Rev. Drug Disc. 2008, 7, 41-53; Zhang M. et al. Expert Opin. Investig. Drugs 2006, 15(11), 14431452). Даний рецептор локалізується в кістковому мозку і селезінці і експресується еозинофілами, базофілами, тучними клітинами (Liu C. et al., Mol. Pharmacol. 2001, 59(3), 420426; Morse K.L. et al., J. Pharmacol. Exp. Ther. 2001, 296(3), 1058-1066; Hofstra C.L. et al., J. Pharmacol. Exp. Ther. 2003, 305(3), 1212-1221; Lippert U. et al., J. Invest. Dermatol. 2004, 123(1), + 116-123; Voehringer D. et al., Immunity 2004, 20(3), 267-277), Т-клітинами CD8 (Gantner F. et al., J. Pharmacol. Exp. Ther. 2002, 303(1), 300-307), дендритними клітинами і людськими синовіальними клітинами пацієнтів, що страждають ревматоїдним артритом (Ikawa Y. et al., Biol. Pharm. Bull. 2005, 28(10), 2016-2018). Підвищений рівень експресії гістамінового рецептора H 4 також спостерігається в тканинах носових поліпів людини (Jókúti A. et al. Cell. Biol. Int. 2007, 31, 1367-1370). Однак експресія в нейтрофілах і моноцитах виражена не настільки явно (Ling P. et al., Br. J. Pharmacol. 2004, 142(1), 161-171; Damaj B.B. et al. J. Immunol. 2007, 179, 7907-7915). Рівень експресії рецептора, щонайменше частково, контролюється різними запальними стимулами (Coge F. et al., Biochem. Biophys. Res. Commun. 2001, 284(2), 301-309; Morse et al., 2001), тим самим підтримуючи гіпотезу, що активація рецептора H 4 впливає на запальну реакцію. Через переважну експресію на імунокомпетентних клітинах рецептор H 4 тісно пов'язаний з регуляторними функціями гістаміну в ході імунної відповіді. Біологічна активність гістаміну в контексті імунології й аутоімунних захворювань тісно пов'язана з алергічною реакцією і її шкідливим впливом, таким як запалення. Явища, що викликають запальну реакцію, включають фізичне подразнення (у тому числі травмування), хімічне подразнення, інфікування і вторгнення стороннього тіла. Запальна реакція характеризується наявністю болю, підвищеною температурою, почервонінням, набряканням або порушенням функції органа або тканини, а також сполученням зазначених симптомів. Дегрануляція тучних клітин (екзоцитоз) супроводжується вивільненням гістаміну і приводить до запальної реакції, яка початково може бути охарактеризована модульованою гістаміном шкірною алергічною реакцією. До активації, міграції і дегрануляції тучних клітин може приводити широкий спектр імунологічних (наприклад, алергенів або антитіл) і неімунологічних (наприклад, хімічних) стимулів. Активація тучних клітин ініціює алергічну запальну реакцію, яка у свою чергу викликає міграцію інших ефекторних клітин, що приводить до подальшого розвитку запальної реакції. Було показано, що гістамін індукує хемотаксис тучних клітин миші (Hofstra et al., 2003), причому хемотаксис не спостерігається при використанні тучних клітин, одержаних з мишей з виключеним геном рецептора H4. Крім того, зазначена реакція блокується H4-специфічним антагоністом, але не блокується антагоністами рецепторів H1, H2 і H3 (Hofstra et al., 2003; Thurmond R.L. et al., J. Pharmacol. Exp. Ther. 2004, 309(1), 404-413). Дослідження in vivo також показали, що викликана гістаміном міграція тучних клітин залежить від рецептора H 4 (Thurmond et al., 2004). Зазначена міграція тучних клітин може відігравати роль у розвитку алергічного риніту й алергії, де виявлене підвищення чисельності тучних клітин (Kirby J.G. et al., Am. Rev. Respir. Dis. 1987, 136(2), 379-383; Crimi E. et al., Am. Rev. Respir. Dis. 1991, 144(6), 1282-1286; Amin K. et al., Am. J. Resp. Crit. Care Med. 2000, 162(6), 2295-2301; Gauvreau G.M. et al., Am. J. Resp. Crit. Care Med. 2000, 161(5), 1473-1478; Kassel O. et al., Clin. Exp. Allergy 2001, 31(9), 14321440). Крім того, відомо, що у відповідь на вплив алергену відбувається перерозподіл тучних клітин зі збільшенням їх кількості в епітеліальному шарі слизової оболонки носа (Fokkens W.J. et al., Clin. Exp. Allergy 1992, 22(7), 701-710; Slater A. et al., J. Laryngol. Otol. 1996, 110, 929-933). Ці результати показують, що хемотаксичний відгук тучних клітин на гістамін опосередкований гістаміновими рецепторами H4. Було показано, що гістамін також може викликати хемотаксис еозинофілів (О'Rеіllу M., et al., J. Recept. Signal Transduction 2002, 22(1-4), 431-448; Buckland K.F. et al., Br. J. Pharmacol. 2003, 140(6), 1117-1127; Ling et al., 2004). З використанням H4-селективних лігандів було показано, що індукований гістаміном хемотаксис еозинофілів опосередкований рецептором H 4 (Buckland et al., 2003; Ling et al., 2004). Рівень експресії молекул адгезії CD11b/CD18 (LFA-1) і CD54 (ICAM-1) 1 UA 106046 C2 5 10 15 20 25 30 35 40 45 50 55 60 на клітинній поверхні еозинофілів після обробки гістаміном зростає (Ling et al., 2004). Цей ріст блокується антагоністами рецептора H4, але не блокується антагоністами рецепторів H1, H2 і H3. Рецептор H4 також важливий для дендритних клітин і T-клітин. У похідних від моноцитів дендритних клітинах людини стимулювання рецептора H 4 пригнічує продукцію IL-12p70 і викликає індукований гістаміном хемотаксис (Gutzmer R. et al., J. Immunol. 2005, 174(9), 5224+ 232). Також указувалося на роль рецептора H4 у T-клітинах типу CD8 . У роботі Gantner, et al., (2002) було показано, що як рецептор H4, так і рецептор H2 контролюють індуковане гістаміном + вивільнення IL-16 з людських T-клітин типу CD8 . IL-16 виявляється в бронхоальвеолярній рідини пацієнтів із бронхіальною астмою після алергенної або гістамінової провокації (Mashikian V.M. et al., J. Allergy Clin. Immunol. 1998, 101 (6, Part 1), 786-792; Krug N. et al., Am. J. Resp. Crit. + Care Med. 2000, 162(1), 105-111) і вважається важливим фактором у міграції клітин типу CD4 . Активність рецептора H4 у клітинах перерахованих типів указує на його важливу роль в адаптивних імунних відповідях, наприклад відповідях, активних при аутоімунних захворюваннях. In vivo антагоністи рецептора H4 виявилися здатні блокувати нейтрофілію в моделях індукованого цимозаном перитоніту і плевриту (Takeshita K. et al., J. Pharmacol. Exp. Ther. 2003, 307(3), 1072-1078; Thurmond, et al., 2004). Крім того, антагоністи рецептора H4 показують активність і в широко використовуваній і добре охарактеризованій моделі коліту (Varga C. et al., Eur. J. Pharmacol. 2005, 522(1-3), 130-138). Ці результати підтверджують висновок, що антагоністи рецептора H4 мають протизапальну активність in vivo. Ще однією фізіологічною функцією гістаміну є опосередкування шкірного свербежу, і антагоністи рецептора H1 не показують тут повної клінічної ефективності. Нещодавно було вказано на можливу участь рецептора H4 в індукованому гістаміном свербежі у мишей (Bell J.K. et al., Br. J. Pharmacol. 2004, 142(2), 374-380). Антагоністи рецептора H4 блокували ці ефекти гістаміну. Перераховані результати підтверджують гіпотезу про участь рецептора H 4 в індукованому гістаміном шкірному свербежі і про можливий позитивний ефект антагоністів рецептора H4 при лікуванні шкірного свербежу. Було показано, що антагоністи гістамінового рецептора H4 приводять до полегшення свербежу в експериментальних моделях (Dunford P.J. et al. J. Allergy Clin. Immunol. 2007, 119(1), 176-183). Модулювання рецепторів H4 контролює вивільнення медіаторів запалення і інгібує міграцію лейкоцитів, тим самим даючи можливість профілактики і (або) лікування опосередкованих рецептором H4 захворювань і патологічних станів, включаючи негативний вплив алергічних реакцій, таких як запалення. Сполуки, які складають предмет даного винаходу, мають властивості, що модулюють рецептор H4. Сполуки, які складають предмет даного винаходу, мають властивості, інгібуючі міграцію лейкоцитів. Сполуки, які складають предмет даного винаходу, мають протизапальні властивості. Модулювання гістамінового рецептора H 4 також обговорювалося в контексті зняття больового синдрому (Міжнародна патентна заявка WO 2008/060766 (Abbott). У постійно зростаючій кількості публікацій повідомляється про підвищені рівні експресії багатьох прозапальних цитокінів у пацієнтів, що страждають великою депресією (Frommberger et al., European Archives of Psychiatry & Clinical Neuroscience. 1997, 247(4), 228-33; Sluzewska A. et al., Psychiatry Research, 1996, 64(3), 161-7; Ortiz-Dominguez et al., Bip. Disporder 9, 2007; O'Brien et al., J. Affective Disorders, 2006, 90, 263-267; Anisman H. et al., Biological Psychiatry, 1999, 46(12),1649-55) (у порівнянні з недепресивними або суб'єктами, у ряді випадків, у кореляції зі ступенем тяжкості симптому). Останні включають в себе білки гострої фази (Kling et al., Biol. Phychiatry, 2007, 62, 309-313; Kim et al., Progress in Neuro-Psychopharmacology & Biological Psychiatry, 2007, 31, 1044-1053; (C-реактивний білок, альфа-1 кислий глікопротеїн, альфа-1 антихімотрипсин і гаптоглобін), підвищений рівень експресії хемокінів і молекул клітинної адгезії (включаючи людський хемоатрактантний білок-1 макрофагів (MCP-1), розчинну внутрішньоклітинну молекулу адгезії-1 (sICAM-1) і E-селектин), підвищені концентрації інтерлейкіну (IL)-1-β, IL-6 і фактора некрозу пухлин (TNF)-α у сироватці і (або) плазмі, як у периферичному кровотоці, так і в центральній нервовій системі (особливо в спинномозковій рідині) з більш високим рівнем консистенції при вимірюванні TNF-α і IL-6 (О'Вrіеn et al., Journal of Psychiatric Research, 2007, 41, 326-331; Moorman et al., J. of Cardiac Failure, 2007, 13(9), 738-43; Soygur et al., Progress in Neuro-Psychopharmacology & Biolofical Psychiatry, 2007, 31, 1242-1247). Крім того, алельні варіанти генів для білків IL-1β і TNF-α підвищують ризик депресії й асоціюються зі зниженою сприйнятливістю до антидепресантної терапії. Нарешті, результати ряду доклінічних досліджень підтверджують гіпотезу про участь деяких цитокінів у моделях депресії, є також клінічні дані про залучення антагонізму цитокінів у лікування симптомів депресії у пацієнтів, що страждають гострими запальними захворюваннями (Kim et al., Progress in Neuro-Psychopharmacology & Biological Psychiatry, 2007, 31, 1044-1053). 2 UA 106046 C2 5 10 15 20 25 30 35 40 45 50 55 60 [5-(4,6-Диметил-1H-бензоімідазол-2-іл)-4-метилпіримідин-2-іл]-[3-(1-метилпіперидин-4-іл)пропіл]-амін (Патент США № 7507737, Приклад 2) є ефективним антагоністом рецептора H 4 (H4R) з величиною Ki 8,4 нМ і більше ніж 25-кратною селективністю відносно інших гістамінових рецепторів in vitro. Зазначений амін інгібував індуковані гістаміном зміни форми еозинофілів, хемотаксис тучних клітин і продукування IL-6 у тучних клітинах. В експериментах in vivo [5-(4,6диметил-1H-бензоімідазол-2-іл)-4-метилпіримідин-2-іл]-[3-(1-метилпіперидин-4-іл)-пропіл]-амін приводив до зниження запалення в мишачих моделях астми, артриту і дерматиту. Зазначена сполука також інгібувала індуковане ліпополісахаридами (LPS) вироблення фактора некрозу пухлин альфа (TNF-α) і інших цитокінів in vivo. На основі цих спостережень і ефектів антагонізму до H4R передбачається, що [5-(4,6диметил-1H-бензоімідазол-2-іл)-4-метилпіримідин-2-іл]-[3-(1-метилпіперидин-4-іл)-пропіл]-амін і сімейство хімічно споріднених йому сполук мають антидепресантні і (або) анксіолітичні властивості, що дозволяють використовувати їх для терапії афективних розладів (включаючи, крім іншого, великий депресивний розлад, біполярний афективний розлад, великий депресивний розлад, що не піддається лікуванню, і біполярний афективний розлад, що не піддається лікуванню), тривожних розладів (включаючи, крім іншого, генералізований тривожний розлад, стресовий і посттравматичний стресовий розлад). Передбачається, що антагоністи рецептора H4 також будуть мати подібні властивості, які дозволяють використовувати їх для лікування зазначених розладів. Пов'язані з ожирінням запалення і інсулінорезистентність пов'язані з розвитком цукрового діабету 2 типу, жирового гепатиту й атеросклерозу. Макрофаги мігрують у жирову тканину й атеросклеротичні бляшки й активуються, вивільняючи запальні цитокіни і хемокіни. Пов'язані з розвитком подібних станів раціони з високим вмістом жирів можуть приводити до підвищеної проникності кишечнику і дисліпідемії. Наступна активація толлподібних рецепторів 2 і 4 (TLR2, TLR4) адипоцитів і макрофагів бактеріями і підвищеним рівнем вільних жирних кислот приводить до запального фенотипу і резистентності до інсуліну. Більш конкретно, ефективність опосередкованих інсуліном каскадів передачі сигналів може бути ослаблена такими цитокінами, як TNF-α і IL-6, і активацією кіназ, включаючи c-jun-кіназу, NKkВ або PKCӨ, далі по каскаду після стимулювання рецепторів TLR2/4. Ефекти модуляції опосередкованих інсуліном каскадів передачі сигналів підсилюються підвищеним припливом моноцитів/макрофагів у тканину через вивільнення таких хемокінів, як MCP-1. H4R являє собою рецептор з високою спорідненістю до гістаміну, експресований на популяціях моноцитів/макрофагів і інших гематопоетичних клітинах. Було показано, що антагонізм до H4R знижує ефективність сигнального каскаду TLR4 in vitro і знижує опосередковане TLR2 і TLR4 вироблення запальних цитокінів in vitro і in vivo. Було неодноразово показано, що експресія прозапальних медіаторів, включаючи TNF-α, IL-6 і LTB4, у TLR-залежних системах інгібується антагонізмом до H4R. Одержані в контексті даного винаходу дані підтверджують заяву, що антагоністи H4R можуть бути корисні при лікуванні цукрового діабету 2 типу і споріднених метаболічних порушень завдяки їх здатності знімати запалення. Антагоністи гістамінового рецептора H4 при систематичному прийомі демонструють протизапальну і протисвербіжну активність у моделях тварин. Даний винахід також стосується використання композицій для місцевого застосування, що містять антагоністи до рецептора H4, для місцевого лікування шкірного запалення і свербежу. Місцеве лікування при терапії шкірних розладів, таких як алергічна висипка й атопічний дерматит, може виявитися більш переважним у порівнянні із системним введенням препарату через більш сприятливі показники безпеки. У контексті даного винаходу було перевірене місцеве застосування антагоніста рецептора H 4, (5хлор-1H-індол-2-іл)-(4-метилпіперазин-1-іл)-метанону (Патент США № 6803362, Приклад 1) на мишачій моделі шкірного свербежу. Одержані результати підтверджують заяву, що місцеве застосування антагоніста рецептора H4 може бути корисне при місцевому лікуванні шкірного свербежу і передбачувано може також бути корисне при місцевому протизапальному лікуванні. Композиції для місцевого застосування, що містять подібні антагоністи, можуть бути корисні як в охороні здоров'я людини, так і у ветеринарії. Приклади англомовних підручників в сфері запалення включають наступні книги: 1) Gallin J.I.; Snyderman R., Inflammation: Basic Principles and Clinical Correlates, 3rd ed.; Lippincott Williams & Wilkins: Philadelphia, 1999; 2) Stvrtinova V. et al., Inflammation and Fever. Pathophysiology Principles of Diseases (підручник для студентів медичних спеціальностей); Academic Press: New York, 1995; 3) Cecil et al. Textbook of Medicine, 18th ed.; W.B. Saunders Co., 1988; і 4) Stеdmаn's Medical Dictionary. Оглядову і базову інформацію по запаленнях і пов'язаних з ними станах можна знайти в наступних роботах: Nathan C., Nature 2002, 420(6917), 846-852; Tracey K.J., Nature 2002, 3 UA 106046 C2 5 10 15 20 25 30 35 40 45 420(6917), 853-859; Coussens L.M. et al., Nature 2002, 420(6917), 860-867; Libby P., Nature 2002, 420, 868-874; Benoist C. et al., Nature 2002, 420(6917), 875-878; Weiner H.L. et al., Nature 2002, 420(6917), 879-884; Cohen J., Nature 2002, 420(6917), 885-891; Steinberg D., Nature Med. 2002, 8(11), 1211-1217. Таким чином, низькомолекулярні модулятори гістамінового рецептора H 4 відповідно до даного винаходу контролюють вивільнення медіаторів запалення і інгібують міграцію лейкоцитів, і можуть знайти застосування в терапії запалень різної етіології, включаючи наступні захворювання і патологічні стани: запальні розлади, алергічні розлади, дерматологічні розлади, аутоімунні захворювання, лімфатичні розлади, шкірний свербіж і імунодефіцитні розлади. Опосередковані активністю гістамінового рецептора H4 захворювання, розлади і патологічні стани включають захворювання, розлади і патологічні стани, зазначені в даній заявці. Ряд діамінозаміщених піридинів наведений у наступних публікаціях: міжнародна патентна заявка WO 2008/122378 (UCB Pharma, 16 жовтня 2008 р.); міжнародна патентна заявка WO 1991/09849 (Upjohn, 11 липня 1991 р.); міжнародна патентна заявка WO 2006/063718 (Hoffmann La Roche, 22 червня 2006 р.); патент США № 4788196 (Pfizer, 29 листопада 1988 р.); і патент США № 4806536 (Pfizer, 21 люте 1989 р.). Ряд амінозаміщених 2-амінопіримідинів наведений у наступних публікаціях: Becker I. J., Het. Chem. 2005, 42(7), 1289-1295; європейська патентна заявка № EP 1437348 (14 липня 2004 р.); патент США 3907801 (23 вересня 1975 р.); Lespagnol A. et al., Chim. Therap. 1971, 6(2), 105-108; Willecomme B., Annales de Chimie 1969, 4(6), 405-428; Lespagnol A. et al. Chim. Therap. 1965, 1, 26-31; міжнародна патентна заявка WO 2001/62233 (30 серпня 2007 р.); міжнародна патентна заявка WO 2001/47921 (5 липня 2001 р.); заявка на патент США 2007/0167459 (Ono Pharmaceutical Co., 19 липня 2007 р.); заявка на патент США 2003/0105106 (Pfizer, 5 червня 2003 р.); заявка на патент США 2002/0147200 (Nilsson, 10 жовтня 2002 р.); і патент США № 5147876 (Mitsui, 15 вересня 1992 р.). Ряд амінозаміщених 2-амінопіридазинів розкритий у наступних публікаціях: Heinisch G., Heterocycles 1999, 51(5), 1035-1050; заявка на патент США 2005182067 (Amgen Inc., 18 серпня 2005 р.) і міжнародна патентна заявка WO 2002/022605 (Vertex Pharmaceuticals Inc., 21 березня 2002 р.). Крім того, комерційно доступний (5-піперазин-1-ілпіридазин-3-іл)-п-толіламін (CAS № 1092336-93-0). Ряд заміщених 2-амінопіримідинів як антагоністів гістамінового рецептора H4 розкритий у наступних публікаціях: міжнародна патентна заявка WO 2008/074445 (UCB Pharma, 26 червня 2008 р.); WO 2005/054239 (Bayer Healthcare AG; 16 червня 2005 р.) і EP 1505064 (Bayer Healthcare AG; 9 лютого 2005 р.; що має рівну силу з міжнародною патентною заявкою WO 2005/014556). Заміщені піримідини описані як ліганди до гістамінового рецептора H4 у наступних публікаціях: заявка на патент США 2007/0185075 (Pharmacia Corp.; 9 серпня 2007 р.), міжнародна патентна заявка WO 2007/031529 (Palau Pharma S.A.; 22 березня 2007 р.) і заявка на патент США Рег. № 12/070051 (14 лютого 2008 р.). Застосування амінопіримідинів як лігандів гістамінового рецептора H4 додатково розкрите в наступних публікаціях: міжнародні патентні заявки №№ WO 2007/090852, WO 2007/090853 і WO 2007/090854 (16 серпня 2007 р.) і EP 1767537 (28 березня 2007 р.), усі подані компанією Cellzome Ltd., міжнародні патентні заявки №№ WO 2008/031556 (UCB Pharma; 20 березня 2008 р.), WO 2006/050965 (Argenta; 18 травня 2006 р.) і WO 2007/072163 (Pfizer; 28 червня 2007 р.). Однак залишається потреба в ефективних модуляторах гістамінового рецептора H4 з бажаними фармацевтичними властивостями. У контексті даного винаходу було виявлено, що ряд діамінопіридинових, піримідинових і піридазинових похідних має модулюючу активність відносно гістамінового рецептора H4. Короткий опис винаходу Один аспект даного винаходу стосується сполук формули (I) , 50 де Z являє собою CH або N; Y являє собою CH або N; 4 UA 106046 C2 5 10 15 Z і Y визначаються незалежно один від одного, і кільце, що містить згадані Y і Z, має не більше двох атомів азоту; за умови, що i) коли Y являє собою CH і Z являє собою CH або N, то 1 R являє собою: а) -(CH2)2OCH3, -(CH2)2SCH3 або C1-8алкіл, кожний з який незалежно не заміщений або заміщений -OH або -CF3; 1 2 1 2 1 2 б) -(CH2)0-2-Ar , -CHR -Ar або -(CH2)0-2-Ar , причому кожний зі згаданих Ar і Ar незалежно не заміщений або заміщений галогеном, -CH3 або -OCH3, 1 Ar являє собою 6-членне ароматичне карбоциклічне кільце, 2 Ar являє собою 5- або 6-членне гетероароматичне кільце, що містить N, S або O; або в) циклоалкіл, -(CH2)-(моноциклічний циклоалкіл), -(CH2)-(місточковий поліциклічний 2 циклоалкіл)0-1, -(CHR )-(моноциклічний циклоалкіл), -(CH2)-(конденсований циклоалкіл), -(CH2)(місточковий моноциклічний циклоалкіл), -(CH2)0-1-тетрагідрофураніл або -(CH2)0-1тетрагідропіраніл, причому кожний зі згаданих фрагментів незалежно не заміщений або заміщений одним, двома або трьома C1-4алкільними замісниками; 2 R являє собою -C1-4алкіл; a 25 30 35 40 45 c a 20 b b c де R , R і R , кожен незалежно, являють собою H або C1-3алкіл; за умови, що: 1 c якщо R являє собою ізопропіл, то R являє собою метил; 1 c якщо R являє собою 4-метилфеніл, то R являє собою метил; 1 коли Z являє собою N, Y являє собою CH і R являє собою бензил, не заміщений або c заміщений галогеном, то R являє собою метил; ii) коли Y являє собою N і Z являє собою CH, то 1 R являє собою: а) -(CH2)2OCH3, -(CH2)2SCH3 або C1-8алкіл, кожний з який незалежно не заміщений або заміщений -О або -CF3; 1 2 1 2 1 2 б) -(CH2)0-2-Ar , -CHR -Ar , -(CH2)0-2-Ar , причому кожний зі згаданих Ar і Ar незалежно не заміщений або заміщений галогеном, -CH3, -OCH3, 1 Ar являє собою 6-членне ароматичне карбоциклічне кільце, 2 Ar являє собою 5- або 6-членне гетероароматичне кільце, що містить N, S або O; або в) циклоалкіл, -(CH2)-(моноциклічний циклоалкіл), -(CH2)-(місточковий поліциклічний 2 циклоалкіл)0-1, -(CHR )-(моноциклічний циклоалкіл), -(CH2)-(конденсований циклоалкіл), -(CH2)(місточковий моноциклічний циклоалкіл), -(CH2)0-1-тетрагідрофураніл, -(CH2)0-1-тетрагідропіраніл, причому кожний зі згаданих фрагментів не заміщений або заміщений одним, двома або трьома C1-4алкільними замісниками; 2 R являє собою -C1-4алкіл; де R , R і R , кожен незалежно, являють собою H або C1-3алкіл. В інших здійсненнях даний винахід стосується сполук формули (I), де Y являє собою CH і Z являє собою CH або N. У подальших здійсненнях даний винахід стосується сполук формули (I), де Y являє собою N і Z являє собою CH. У подальших здійсненнях даний винахід стосується фармацевтично прийнятних солей сполук формули (I), фармацевтично прийнятних проліків і фармацевтично активних метаболітів. 5 UA 106046 C2 5 10 15 20 25 30 35 40 45 50 У ряді варіантів здійснення даного винаходу сполука формули (I) являє собою сполуку, вибирану зі сполук, описаних або проілюстрованих у наведеному нижче докладному описі. Надалі аспекті даний винахід стосується фармацевтичних композицій для лікування захворювання, розладу або патологічного стану, опосередкованого активністю гістамінового рецептора H4, до складу яких входить ефективна кількість щонайменше однієї з хімічних сполук, вибираних зі сполук формули (I), фармацевтично прийнятних солей, фармацевтично прийнятних проліків і фармацевтично активних метаболітів. До складу відповідних цілям даного винаходу фармацевтичних композицій може також входити фармацевтично прийнятний наповнювач. В іншому аспекті даний винахід спрямований на спосіб лікування пацієнта, який страждає від або у якого діагностовано захворювання, розлад або патологічний стан, опосередкований активністю гістамінового рецептора H4, який включає введення потребуючому подібного лікування пацієнту ефективної кількості щонайменше однієї з хімічних сполук, вибираних зі сполук формули (I), фармацевтично прийнятних солей, фармацевтично прийнятних проліків і фармацевтично активних метаболітів. У ряді переважних здійснень способу, що складає предмет даного винаходу, згадані захворювання, розлад або патологічний стан являють собою запалення. Використовуваний у даній заявці термін "запалення" стосується реакції, яка розвивається у відповідь на вивільнення гістаміну, що у свою чергу викликається щонайменше одним стимулом. Прикладами подібних стимулів є імунологічні стимули і неімунологічні стимули. В іншому аспекті хімічні здійснення даного винаходу можуть знайти застосування як модулятори гістамінового рецептора H4. Таким чином, даний винахід спрямований на спосіб модуляції активності гістамінового рецептора H4, включаючи ситуації, коли подібний рецептор знаходиться в організмі пацієнта, який включає вплив на гістаміновий рецептор H 4 ефективні кількості щонайменше однієї з хімічних сполук, вибираних зі сполук формули (I), фармацевтично прийнятних солей, фармацевтично прийнятних проліків і фармацевтично активних метаболітів. Метою даного винаходу є подолання або пом'якшення щонайменше одного з недоліків стандартних методологій і (або) відомих способів або надання корисних альтернатив для останніх. Додаткові варіанти здійснення винаходу, особливості і переваги винаходу стануть зрозумілі з наведеного далі докладного опису і практичного здійснення винаходу. Докладний опис винаходу і переважні варіанти його здійснення Зміст усіх цитованих по ходу письмового викладу заявки джерел, включаючи, крім іншого, патенти і заявки на патенти, повністю включений в дану заявку шляхом посилання. Терміни "який включає", "який містить", "який складається" використовуються в даному документі в їх відкритому, необмеженому значенні. Використовуваний у даній заявці термін "алкіл" стосується алкільної групи з лінійним або розгалуженим ланцюгом, що містить від 1 до 12 атомів вуглецю. Приклади алкільних груп включають наступні групи: метил (Me), етил (Et), н-пропіл, ізопропіл, бутил, ізобутил, вторбутил, трет-бутил (tBu), пентил, ізопентил, трет-пентил, гексил, ізогексил, а також групи, що у світлі загальноприйнятих знань, очікуваних від фахівця в даній галузі, і наведених у даній заявці описів можуть вважатися еквівалентними одному з вищенаведених прикладів. Використовуваний у даній заявці термін "циклоалкіл" стосується насиченого або частково насиченого карбоциклу, такого як моноциклічний, конденсований поліциклічний, місточковий моноциклічний, місточковий поліциклічний або спірополіциклічний карбоцикл, що містить від 3 до 12 атомів вуглецю на карбоцикл. Якщо термін "циклоалкіл" уточнюється конкретним модифікатором, таким як "моноциклічний", "конденсований поліциклічний", "місточковий поліциклічний" або "спірополіциклічний", то використовуваний термін "циклоалкіл" стосується тільки охарактеризованого таким чином карбоциклу. Типові приклади циклоалкільних груп включають наступні фрагменти, у вигляді відповідним чином зв'язаних фрагментів: 6 UA 106046 C2 5 10 15 20 25 30 Використовуваний у даній заявці термін "гетероциклоалкіл" стосується моноциклічної або конденсованої, місточкової або спірополіциклічної кільцевої структури, яка є насиченою або частково насиченою і містить від 3 до 12 кільцевих атомів на кільцеву структуру, вибираних з атомів вуглецю, і до трьох гетероатомів, вибираних з азоту, кисню і сірки. Згадана кільцева структура може також містити до двох оксогруп на вуглецевих або сірчаних членах кільця. Типові приклади у вигляді відповідним чином зв'язаних фрагментів включають в себе: Використовуваний у даній заявці термін "гетероарил" означає моноциклічний, конденсований біциклічний або конденсований поліциклічний ароматичний гетероцикл (кільцеву структуру, що має в кільці атоми, вибирані з атомів вуглецю, і до чотирьох гетероатомів, вибираних з азоту, кисню і сірки), що містить від 3 до 12 кільцевих атомів на гетероцикл. Типові приклади гетероарильних груп включають в себе наступні фрагменти, у вигляді відповідним чином зв'язаних фрагментів: Фахівці в даній галузі визначать, що перераховані або проілюстровані вище гетероарильні, циклоалкільні і гетероциклоалкільні групи не вичерпують усі можливості, і в рамках цілей даного винаходу можуть бути вибрані й інші групи зазначених типів. Використовуваний у даній заявці термін "галоген" означає хлор, фтор, бром або йод. Використовуваний у даній заявці термін "гало" означає хлор-, фтор-, бром- або йод-. Використовуваний у даній заявці термін "заміщений" означає, що зазначена функціональна група або фрагмент заміщені одним або декількома замісниками. Використовуваний у даній заявці термін "не заміщений" означає, що зазначена група не має замісників. Використовуваний у даній заявці термін "додатково заміщений" означає, що зазначена група або не має замісників, або заміщена одним або декількома замісниками. Якщо термін "заміщений" використовується для опису структурної системи, це означає, що заміщення здійснюється по будь-якому положенню системи, яке допускається валентністю. Кожна формула з наведених у даній заявці формул представляє як сполуки зі структурами, показаними даною структурною формулою, так і деякі варіації або форми подібних структур. Зокрема, сполуки за будь-якою із наведених у даній заявці формул можуть мати асиметричні центри і тому існувати в різних енантіомерних формах. Всі оптичні ізомери і стереоізомери сполук за наведеною загальною формулою, а також будь-які їх суміші, вважаються представленими в рамках даної формули. Таким чином, будь-яка формула, що наводиться в даній заявці, представляє рацемат, одну або декілька енантіомерних форм, одну або декілька діастереомерних форм, одну або декілька атропоізомерних форм зазначеної сполуки, а також їх 7 UA 106046 C2 5 10 15 20 25 30 35 40 45 50 55 суміші. Крім того, деякі структури можуть існувати у формі геометричних ізомерів (наприклад, цис- і транс-ізомери), у формі таутомерів або у формі атропоізомерів. Крім того, кожна наведена в даній заявці формула, крім власне сполуки, також стосується її гідратів, сольватів і поліморфів, а також їх сумішей, навіть якщо такі форми не зазначені явно. У ряді здійснень розчинник являє собою воду, а сольвати є гідратами. Для більшої стислості опису ряд кількісних виразів, що наводяться в даній заявці, дається без модифікатора "приблизно". Мається на увазі, що незалежно від того, вказується модифікатор "приблизно" явно чи ні, кожне числове значення, що наводиться в даній заявці, стосується конкретного наведеного значення, а також наближення до даного наведеного значення, що може бути розумним чином оцінено будь-яким фахівцем, включаючи еквіваленти і наближення, пов'язані з умовами проведення експерименту і (або) вимірювання для подібного наведеного значення. При указанні виходу сполуки у відсотках вихід, що наводиться, стосується маси сполуки, для якої указується вихід, стосовно максимально досяжної кількості даної сполуки в конкретних стехіометричних умовах. Якщо не зазначене інше, концентрації, що наводяться у відсотках, стосуються масових співвідношень. Згадування хімічної сполуки в даній заявці означає відсилання до будь-якого з наступного: (а) буквально зазначеній формі даної сполуки, і (б) будь-якій формі згаданої сполуки в тому середовищі, де дана сполука знаходиться на момент згадування. Наприклад, згадування в даній заявці такої сполуки, як R-COOH, включає відсилання до будь-якої з, наприклад, наступних форм: R-COOH(s), R-COOH(sol) і R-COO (sol). У наведеному прикладі R-COOH(s) стосується твердої сполуки, наприклад, у вигляді таблетки або іншої твердої фармацевтичної форми або композиції; R-COOH(sol) стосується недисоційованої форми сполуки в розчиннику; і R-COO (sol) стосується дисоційованої форми сполуки в розчиннику, такої як дисоційована форма сполуки у водному середовищі, незалежно від того, одержана дана дисоційована форма з RCOOH, з її солі або з будь-якої іншої структурної одиниці, що дають R-COO при дисоціації в розглянутому середовищі. В іншому прикладі такий вираз, як "дія на хімічну сполуку сполукою за формулою R-COOH", означає дію на згадану хімічну сполуку формою або формами сполуки R-COOH, яка існує або які існують у тому середовищі, де здійснюється описуваний вплив. У цьому зв'язку, якщо подібна хімічна сполука знаходиться, наприклад, у водному середовищі, мається на увазі, що згадана сполука R-COOH знаходиться в тому ж середовищі і тому на згадану хімічну сполуку діють такі реагенти, як R-COOH(aq) і (або) R-COO (aq), де нижній індекс "(aq)" означає "водний" відповідно до його загальноприйнятого значення в хімії і біохімії. В описаних прикладах використовуваної номенклатури застосовується карбоксильна функціональна група, однак цей вибір ні в якій мірі не є обмеженням і був зроблений тільки для ілюстрації. Мається на увазі, що аналогічні приклади можуть бути наведені і для інших функціональних груп, включаючи, крім іншого, такі групи, як гідроксильна група, азотна основна група, наприклад, в амінах, а також будь-які інші групи, що відомим чином взаємодіють або перебудовуються в середовищі, що містить дану сполуку. Подібні взаємодії і перебудови включають, крім іншого, дисоціацію, асоціацію, таутомеризм, сольволіз, включаючи гідроліз, сольватацію, включаючи гідратацію, протонування і депротонування. У даній заявці не наводиться подальших прикладів у цьому зв'язку, оскільки можливі взаємодії і перебудови в кожному конкретному середовищі добре відомі фахівцям у даній галузі. Кожна з наведених у даній заявці формул також представляє як немічені, так і ізотопномічені форми відповідних сполук. Ізотопно-мічені сполуки мають структури, що відповідають представленим у даній заявці формулам, за винятком того, що один або більше атомів у них замінені атомом, що має визначену атомну масу або масове число. Приклади ізотопів, що можуть бути введені в сполуки даного винаходу, включають ізотопи водню, вуглецю, азоту, 2 3 11 13 14 15 18 17 31 32 35 18 кисню, фосфору, фтору, хлору і йоду, такі як H, H, C, C, C, N, O, O, P, P, S, F, 36 125 Cl і I, відповідно. Подібні ізотопно-мічені сполуки корисні при вивченні метаболізму 14 2 3 (переважно з використанням C), кінетики реакцій (наприклад, з використанням H або H), для способів детектування або одержання зображень [таких як позитронно-емісійна томографія (PET) або однофотонна емісійна комп'ютерна томографія (SPECT)], включаючи аналіз розподілу ліків або субстрату по тканинах, або при радіотерапії пацієнтів. Зокрема, сполуки, 18 11 мічені F або C, можуть виявитися особливо переважними для досліджень способами PET 2 або SPECT. Крім того, заміщення більш важкими ізотопами, такими як дейтерій (тобто H), може дати визначені терапевтичні переваги, як наслідок більшої метаболічної стабільності сполук, наприклад підвищений період напіввиведення in vivo або зниження необхідного дозування. Ізотопно-мічені сполуки за даним винаходом і їх проліки можуть бути, як правило, одержані шляхом здійснення процедур відповідно до схем або прикладів і способів одержання, описаних 8 UA 106046 C2 5 10 15 20 25 30 35 40 45 50 55 60 нижче, шляхом заміни реагенту, що не містить мічених атомів, на легкодоступний реагент із міченими атами. При обговоренні будь-якої наведеної в даній заявці формули вибір конкретного фрагмента зі списку можливих варіантів для конкретної хімічної змінної не означає фіксування такого вибору фрагмента для даної змінної в інших формулах. Іншими словами, якщо яка-небудь хімічна змінна присутня у формулі більше ніж в одному місці, вибір варіанта для неї зі списку можливих в одному місці не залежить від вибору варіанта для тієї ж змінної в іншому місці формули, якщо не зазначене інше. Як перший приклад по використовуваній для позначення замісників термінології, якщо 1 2 замісник S приклад являє собою один з S1 і S2 і замісник S приклад являє собою один з S3 і S4, то зазначені вибори замісників стосуються здійснень даного винаходу з наступними наборами 1 2 1 2 замісників: S приклад являє собою S1 і S приклад являє собою S3; S приклад являє собою S1 і S приклад 1 2 1 являє собою S4; S приклад являє собою S2 і S приклад являє собою S3; S приклад являє собою S2 і 2 S приклад являє собою S4; а також еквіваленти кожного з перерахованих наборів замісників. Тому для стислості викладу без обмеження спільності в даній заявці використовується скорочена 1 2 термінологія: "S приклад являє собою один з S1 і S2, а S приклад являє собою один з S3 і S4". Наведений вище перший приклад по використовуваній для позначення замісників термінології, наданий у загальних термінах, ілюструє різні варіанти позначення замісників, описані в даній заявці. Описаний вище спосіб позначення замісників поширюється, якщо застосовно, на такі 1-4 a-c групи, як R , R і Z, а також на будь-які інші загальні позначення замісників, використовуваних у даній заявці. Крім того, якщо для будь-якого учасника хімічної структури або замісника наводиться більше ніж один варіант, варіанти здійснення даного винаходу включають різні незалежні сполучення варіантів зі списків можливих замісників, а також їх еквіваленти. Як другий приклад по використовуваній для позначення замісників термінології, якщо в даній заявці зазначено, що замісник Sприклад являє собою один з S1, S2 і S3, даний перелік включає варіанти здійснення даного винаходу, у яких Sприклад являє собою S1; Sприклад являє собою S2; Sприклад являє собою S3; Sприклад являє собою один з S1 і S2; Sприклад являє собою один з S1 і S3; Sприклад являє собою один з S2 і S3; Sприклад являє собою один з S1, S2 і S3; і Sприклад являє собою будь-який еквівалент кожного з перерахованих варіантів. Тому для стислості викладу без обмеження спільності в даній заявці використовується скорочена термінологія: "S приклад являє собою один з S1, S2 і S3". Наведений вище другий приклад по використовуваній для позначення замісників термінології, наданий у загальних термінах, ілюструє різні варіанти позначення замісників, описані в даній заявці. Описаний вище спосіб позначення замісників поширюється, якщо застосовно, на такі 1-4 a-c групи, як R , R і Z, а також на будь-які інші загальні позначення замісників, використовуваних у даній заявці. Номенклатура "Ci-j", де j>i, використовувана в даній заявці для позначення класу замісників, включає варіанти здійснення даного винаходу, для яких індивідуально реалізована кожна і всі можливі кількості атомів вуглецю, від i до j, включаючи i і j. Як приклад термін "C 1-3" стосується незалежно варіантів здійснення, у яких наявний один атом вуглецю (C 1), варіантів здійснення, у яких наявні два атоми вуглецю (C2), і варіантів здійснення, у яких наявні три атоми вуглецю (C 3). Використовуваний у даній заявці термін "C n-mалкіл" означає лінійний або розгалужений аліфатичний ланцюг з повною кількістю N вуглецевих центрів у ланцюзі, що задовольняє умові n ≤ N ≤ m, де m > n. Будь-яке згадування в даній заявці дивалентного замісника включає різні варіанти приєднання згаданого замісника, якщо є більше однієї такої можливості. Наприклад, згадування дивалентного замісника -A-B-, де A≠B, у даній заявці стосується такого дивалентного замісника -A-B-, де фрагмент A приєднується до першого заміщуваного центра і фрагмент B приєднується до другого заміщуваного центра, а також до такого дивалентного замісника -A-B-, де фрагмент A приєднується до другого заміщуваного центра і фрагмент B приєднується до першого заміщуваного центра. Відповідно до наведених вище міркувань по позначенню замісників і використовуваній номенклатурі мається на увазі, що в даній заявці явне згадування деякого набору можливостей означає, при наявності хімічного змісту і якщо не зазначене інше, незалежне відсилання до всіх можливих варіантів здійснення даного набору, а також відсилання до всіх і кожного можливого варіанта здійснення підмножин явно зазначеного набору можливих варіантів. Деякі здійснення даного винаходу надаються сполуками формули (I), де Y являє собою CH, 1 Z являє собою CH або N, і R являє собою C1-8алкіл (не заміщений або заміщений -OH або CF3), феніл, піридил, бензил, піридин-2-ілметил, фенілетил, 1-фенілетил (кожний з який незалежно не заміщений або заміщений галогеном, -CH3, -OCH3), циклоалкіл, -(CH2) 9 UA 106046 C2 2 5 10 15 20 (моноциклічний циклоалкіл), -(CHR )-(моноциклічний циклоалкіл), -(CH2)-(конденсований циклоалкіл), -(CH2)-(місточковий поліциклічний циклоалкіл), -(CH2)0-1-тетрагідрофураніл або (CH2)0-1-тетрагідропіраніл (кожний з який незалежно не заміщений або заміщений одним, двома 1 або трьома C1-4алкільними замісниками). У ряді таких здійснень R являє собою 2,2-диметилпропанол, 2,2-диметилпропан-1-ол, 2,2-диметилпропіл, 2-метил-1-пропан-2-ол, 2-метилпропан-2-ол, 3-пропанол, (1-метилетил), 2,2-диметилпропіл, 2-метоксіетил, 2метилпропіл, 4,4,4-трифторбутил, пропіл, бутил, трет-бутил, пропан-1-ол, 2(метилсульфаніл)етил, 2-фенілетил, фуран-3-ілметил, піридин-2-ілметил, (1R)-1-фенілетил, бензил, феніл, 4-фторбензил, 4-метоксибензил, 4-метилбензил, біцикло[2.2.1]гепт-2-илметил, тетрагідро-2H-піран-4-іл, тетрагідрофуран-2-ілметил, (1R, 2R, 3R, 5S)-2,6,6триметилбіцикло[3.1.1]гепт-3-ил, (1R, 2S, 4R)-1,7,7-триметилбіцикло[2.2.1]гепт-2-ил, (1S, 2S, 3S, 5R)-2,6,6-триметилбіцикло[3.1.1]гепт-3-ил, (1S, 2S, 4R)-біцикло[2.2.1]гепт-2-ил, (1S, 5R)-2,6,6триметилбіцикло[3.1.1]гепт-3-ил, (2R)-тетрагідрофуран-2-ілметил, (2S)-біцикло[2.2.1]гепт-2-ил, (2S)-тетрагідрофуран-2-ілметил, (3R)-тетрагідрофуран-3-іл, (6,6-диметилбіцикло[3.1.1]гепт-2ил)метил, біцикло[2.2.1]гепт-2-ил, циклобутил, циклогексил, циклопентил, циклопропіл, циклогексилметил, циклопентилметил, циклопропілметил, адамантан-1-іл, 2-адамантил, біцикло[2.2.1]гепт-2-ил або (6,6-диметилбіцикло[3.1.1]гепт-2-ил)-метил. У ряді здійснень даного винаходу, де Y являє собою фрагмент CH і Z являє собою CH або 1 N, R являє собою У ряді здійснень даного винаходу, де Y являє собою CH і Z являє собою CH або N, N(R3)R4 являє собою У ряді здійснень даного винаходу, де Y являє собою CH і Z являє собою CH або N, 25 являє собою . У ряді здійснень даного винаходу, де Y являє собою CH і Z являє собою CH або N, являє собою . У ряді здійснень даного винаходу, де Y являє собою CH і Z являє собою CH або N, являє собою 30 . У ряді здійснень даного винаходу, де Y являє собою CH і Z являє собою CH або N, являє собою . У ряді здійснень даного винаходу, де Y являє собою CH і Z являє собою CH або N, являє собою . a 35 У ряді здійснень даного винаходу, де Y являє собою CH і Z являє собою CH або N, R являє собою H. b У ряді здійснень даного винаходу, де Y являє собою CH і Z являє собою CH або N, R являє собою H або метил. c У ряді здійснень даного винаходу, де Y являє собою CH і Z являє собою CH або N, R являє собою H або метил. 10 UA 106046 C2 2 5 10 15 20 25 У ряді здійснень даного винаходу, де Y являє собою CH і Z являє собою CH або N, R являє собою -CH3. У ряді здійснень даного винаходу Y і Z являють собою CH. У ряді здійснень даного винаходу Y і Z являють собою атоми N. Деякі подальші здійснення даного винаходу представлені сполуками формули (I), де Y 1 являє собою N, Z являє собою CH, і R являє собою C1-8алкіл (не заміщений або заміщений -OH або -CF3), феніл, піридил, бензил, піридин-2-ілметил, фенілетил, 1-фенілетил (кожний з який незалежно не заміщений або заміщений галогеном, -CH3, -OCH3), циклоалкіл, -(CH2)2 (моноциклічний циклоалкіл), -(CHR )-(моноциклічний циклоалкіл), -(CH2)-(конденсований циклоалкіл), -(CH2)-(місточковий поліциклічний циклоалкіл), -(CH2)0-1-тетрагідрофураніл або -(CH2)0-1-тетрагідропіраніл (кожний з який незалежно не заміщений або заміщений одним, двома 1 або трьома C1-4алкільними замісниками). У ряді таких здійснень R являє собою 2,2диметилпропанол, 2,2-диметилпропан-1-ол, 2,2-диметилпропіл, 2-метил-1-пропан-2-ол, 2метилпропан-2-ол, 3-пропанол, (1-метилетил), 2,2-диметилпропіл, 2-метоксіетил, 2метилпропіл, 4,4,4-трифторбутил, пропіл, бутил, трет-бутил, пропан-1-ол, 2(метилсульфаніл)етил, 2-фенілетил, фуран-3-ілметил, піридин-2-ілметил, (1R)-1-фенілетил, бензил, феніл, 4-фторбензил, 4-метоксибензил, 4-метилбензил, біцикло[2.2.1]гепт-2-илметил, тетрагідро-2H-піран-4-іл, тетрагідрофуран-2-ілметил, (1R, 2R, 3R, 5S)-2,6,6триметилбіцикло[3.1.1]гепт-3-ил, (1R, 2S, 4R)-1,7,7-триметилбіцикло[2.2.1]-гепт-2-ил, (1S, 2S, 3S, 5R)-2,6,6-триметилбіцикло[3.1.1]гепт-3-ил, (1S, 2S, 4R)-біцикло[2.2.1]гепт-2-ил, (1S, 5R)2,6,6-триметилбіцикло[3.1.1]гепт-3-ил, (2R)-тетрагідрофуран-2-ілметил, (2S)-біцикло[2.2.1]гепт2-ил, (2S)-тетрагідрофуран-2-ілметил, (3R)-тетрагідрофуран-3-іл, (6,6диметилбіцикло[3.1.1]гепт-2-ил)метил, біцикло[2.2.1]гепт-2-ил, циклобутил, циклогексил, циклопентил, циклопропіл, циклогексилметил, циклопентилметил, циклопропілметил, адамантан-1-іл, 2-адамантил, біцикло[2.2.1]гепт-2-ил або (6,6-диметилбіцикло[3.1.1]гепт-2-ил)метил. 1 У ряді здійснень даного винаходу, де Y являє собою N і Z являє собою фрагмент CH, R являє собою У ряді здійснень даного винаходу, де Y являє собою N і Z являє собою CH, собою 30 У ряді здійснень даного винаходу, де Y являє собою N і Z являє собою CH, собою собою являє . У ряді здійснень даного винаходу, де Y являє собою N і Z являє собою CH, собою являє . У ряді здійснень даного винаходу, де Y являє собою N, і Z являє собою CH, собою являє . У ряді здійснень даного винаходу, де Y являє собою N і Z являє собою CH, 35 являє . 11 являє UA 106046 C2 У ряді здійснень даного винаходу, де Y являє собою N і Z являє собою CH, собою являє . a У ряді здійснень даного винаходу, де Y являє собою N і Z являє собою CH, R являє собою H. 5 10 15 20 25 30 35 40 45 50 55 b У ряді здійснень даного винаходу, де Y являє собою N і Z являє собою CH, R являє собою H або метил. c У ряді здійснень даного винаходу, де Y являє собою N і Z являє собою CH, R являє собою H або метил. 2 У ряді здійснень даного винаходу, де Y являє собою N і Z являє собою CH, R являє собою CH3. У ряді здійснень даного винаходу, де Y являє собою N, і Z являє собою CH. Даний винахід також включає фармацевтично прийнятні солі сполук, представлених формулою (I), переважно сполук, описаних вище, і тих конкретних сполук, які перераховані в даній заявці, а також способи застосування згаданих солей. Термін "фармацевтично прийнятна сіль" означає сіль вільної кислоти або основу сполуки, представленої формулою (I), що є нетоксичною, біологічно переносимою або іншим способом біологічно відповідною для призначення пацієнту. Для загальної інформації див. роботу Paulekuhn G.S. et al., "Trends in Active Pharmaceutical Ingredient Salt Selection based on Analysis of the Orange Book Database" (Полекун Дж.С. і ін. "Тенденції у виборі активних фармацевтичних інгредієнтів солей на основі аналізу бази даних "Оранжевої книги"), J. Med. Chem., 2007, 50:6665-72, Berge S.M. et al., "Pharmaceutical Salts" (Берг С.М. і ін. "Фармацевтичні солі"), J. Pharm Sci., 1977, 66:1-19, і Довідник фармацевтичних солей, властивості, вибір і застосування, Stahl and Wermuth, Eds., Wiley-VCH and VHCA, Zurich, 2002. Прикладами фармацевтично прийнятних солей є солі, що мають фармакологічний ефект і відповідні для контакту з тканинами пацієнтів без надмірної подразливої, токсичної або алергічної реакції. Сполука формули (I) може мати в достатній мірі кислу групу, у достатній мірі основну групу або обидва типи функціональних груп і вступати у відповідні реакції з рядом неорганічних або органічних основ, а також неорганічних або органічних кислот з утворенням фармацевтично прийнятних солей. Приклади фармацевтично прийнятних солей включають наступні солі: сульфати, піросульфати, бісульфати, сульфіти, бісульфіти, фосфати, моногідрогенфосфати, дигідрогенфосфати, метафосфати, пірофосфати, хлориди, броміди, йодиди, ацетати, пропіонати, деканоати, каприлати, акрилати, форміати, ізобутирати, капроати, гептаноати, пропіолати, оксалати, малонати, сукцинати, суберати, себакати, фумарати, малеати, бутин-1,4діоати, гексин-1,6-діоати, бензоати, хлорбензоати, метилбензоати, динітробензоати, гідроксибензоати, метоксибензоати, фталати, сульфонати, ксиленсульфонати, фенілацетати, фенілпропіонати, фенілбутирати, цитрати, лактати, γ-гідроксибутирати, гліколяти, тартрати, метансульфонати, пропансульфонати, нафталін-1-сульфонати, нафталін-2-сульфонати і манделати. Якщо сполука формули (I) містить основний атом азоту, то бажана фармацевтично прийнятна сіль може бути одержана за будь-якою відповідною відомою фахівцям методикою, наприклад, обробкою вільної основи неорганічною кислотою, такою як хлористоводнева кислота, бромистоводнева кислота, сірчана кислота, сульфамінова кислота, азотна кислота, борна кислота, фосфорна кислота і ним подібні, або органічною кислотою, такою як оцтова кислота, фенілоцтова кислота, пропіонова кислота, стеаринова кислота, молочна кислота, аскорбінова кислота, малеїнова кислота, гідроксималеїнова кислота, ізетіонова кислота, бурштинова кислота, валеріанова кислота, фумарова кислота, малонова кислота, піровиноградна кислота, щавлева кислота, гліколева кислота, саліцилова кислота, олеїнова кислота, пальмітинова кислота, лауринова кислота, піранозидиловою кислотою, такою як глюкуронова кислота або галактуронова кислота, альфа-гідроксикислотою, такою як мигдальна кислота, лимонна кислота або винна кислота, амінокислотою, такою як аспарагінова кислота, глутарова або глутамінова кислота, ароматичною кислотою, такою як бензойна кислота, 2ацетоксибензойна кислота, нафтойна кислота або корична кислота, сульфоновою кислотою, такою як лаурилсульфонова кислота, п-толуолсульфонова кислота, метансульфонова кислота, етансульфонова кислота, будь-якою сумісною сумішшю кислот, таких як наведені в прикладах даного документа, і будь-якою іншою кислотою або сумішшю кислот, що розглядаються як еквівалентні або прийнятні замінники у світлі даної технології. 12 UA 106046 C2 5 10 15 20 25 30 35 40 45 50 55 60 Якщо сполука формули (I) містить більше одного основного атома азоту, фахівець у даній галузі визначить, що придатні для цілей даного винаходу солі включають в себе солі, утворені з одним або більше еквівалентами неорганічної або органічної кислоти. У переважних здійсненнях формули (I) подібні солі включають в себе бісгідрохлоридні солі. Якщо сполука формули (I) є кислотою, такою як карбонова кислота або сульфонова кислота, то бажана фармацевтично прийнятна сіль може бути одержана будь-яким придатним способом, наприклад, обробкою вільної кислоти неорганічною або органічною основою, такою як амін (первинний, вторинний або третинний), гідроксид лужного металу, гідроксид лужноземельного металу, будь-якою сумісною сумішшю основ, таких як наведені в прикладах даного документа, і будь-якою іншою основою і сумішшю основ, що розглядаються як еквівалентні або прийнятні замінники у світлі даної технології. Характерні приклади відповідних солей включають в себе органічні солі (похідні амінокислот), таких як N-метил-D-глюкамін, лізин, холін, гліцин і аргінін, амонієві солі, карбонати, бікарбонати, первинні, вторинні і третинні аміни і циклічні аміни, такі як трометамін, бензиламіни, піролідини, піперидин, морфолін і піперазин, і неорганічні солі похідні натрію, кальцію, калію, магнію, марганцю, заліза, міді, цинку, алюмінію і літію. Даний винахід також стосується фармацевтично прийнятних проліків сполук формули (I) і способів з використанням подібних фармацевтично прийнятних проліків. Використовуваний у даній заявці термін "проліки" означає попередника зазначеної сполуки, який після призначення пацієнту дає сполуку in vivo за допомогою хімічного або фізіологічного процесу, такого як сольволіз або ферментативне розщеплення, або при фізіологічних умовах (наприклад, проліки, приведені до визначеного фізіологічного значення pН, перетворюються в сполуку формули (I)). "Фармацевтично прийнятні проліки" означають проліки, що є нетоксичними, біологічно переносимими і іншим способом біологічно відповідними для призначення пацієнту. Характерні процедури вибору й одержання відповідних цілям даного винаходу похідних-проліків описані, наприклад, у книзі "Design of Prodrugs", ed. H. Bundgaard, Elsevier, 1985. Приклади проліків включають сполуки, що мають амінокислотний залишок або поліпептидний ланцюжок із двох або більше (наприклад, двох, трьох або чотирьох) амінокислотних залишків, ковалентно зв'язаних через амідний або ефірний зв'язок з вільною аміногрупою, гідроксигрупою або карбоксильною групою сполуки формули (I). Приклади амінокислотних залишків включають в себе двадцять існуючих у природі амінокислот, що звичайно позначаються трьома буквами, а також 4-гідроксипролін, гідроксилізин, демозин, ізодемозин, 3-метилгістидин, норвалін, бета-аланін, гамма-аміномасляна кислота, цитрулін гомоцистеїн, гомосерин, орнітин і метіонінсульфон. Додаткові типи проліків можуть бути одержані, наприклад, при використанні вільних карбоксильних груп структур формули (I) для одержання амідних або алкілефірних похідних. Приклади амідів включають похідні амонію, первинних C1-6алкіламінів і вторинних ді(C1-6алкіл)амінів. Вторинні аміни включають 5- або 6-членні циклічні гетероциклоалкільні або гетероарильні фрагменти. Приклади амідів включають похідні амонію, первинних C1-3алкіламінів і ді(C1-2алкіл)амінів. Приклади ефірів для цілей даного винаходу включають C 1-7алкіл, C5-7циклоалкіл, феніл і феніл(C1-6алкіл)ефіри. Переважні ефіри включають в себе метилові ефіри. Проліки також можуть бути одержані функціоналізацією вільних гідроксильних груп з використанням груп, що включають гемісукцинати, фосфатні ефіри, диметиламіноацетати і фосфорилоксиметилоксикарбоніли, відповідно до процедур, описаних в роботі Fleisher et al., Adv. Drug Delivery Rev. 1996, 19, 115-130. Карбаматні похідні гідрокси- і аміногруп можуть також давати проліки. Карбонатні похідні, сульфонатні ефіри і сульфатні ефіри гідроксигруп можуть також давати проліки. Також для одержання проліків можлива функціоналізація гідроксигруп до (ацилокси)метил- і (ацилоксі)етилефірів, де ацильна група може бути алкілефіром, можливо, заміщеним однією або більше ефірними, аміно або карбоксильними функціональними групами, або де згадана ацильна група являє собою ефір амінокислоти, як описано вище. Проліки цього типу можна одержати, додержуючись процедур, описаних у роботі Robinson et al., J. Med. Chem. 1996, 39, 10-18. Вільні аміногрупи можуть також бути використані для одержання амідних, сульфонамідних або фосфонамідних похідних. Усі перераховані фрагменти проліків можуть мати у своїй структурі додаткові функціональні групи, такі як ефірні, аміно і карбоксильні групи. Даний винахід також стосується фармацевтично активних метаболітів сполук формули (I) і можливостей використання подібних метаболітів у способах, що складають предмет даного винаходу. "Фармацевтично активний метаболіт" означає фармакологічно активний продукт метаболізму в організмі сполуки формули (I) або її солі. Проліки й активні метаболіти сполуки можуть бути визначені за допомогою звичайних способів, відомих і доступних фахівцям у даній галузі. Див, наприклад, роботи Bertolini et al., J. Med. Chem. 1997, 40, 2011-2016; Shan et al., J. Pharm. Sci. 1997, 86 (7), 765-767; Bagshawe, Drug Dev. Res. 1995, 34, 220-230; Bodor, Adv. Drug 13 UA 106046 C2 5 10 15 20 25 30 35 40 45 50 55 60 Res. 1984, 13, 255-331; книги Bundgaard, Design of Prodrugs (Elsevier Press, 1985); and Larsen, Design and Application of Prodrugs, Drug Design and Development (Krogsgaard-Larsen et al., eds., Harwood Academic Publishers, 1991). Сполуки формули (I) і їх фармацевтично прийнятні солі, фармацевтично прийнятні проліки і фармацевтично активні метаболіти, окремо або в будь-яких сполученнях (збірно іменовані "активні агенти"), що складають предмет даного винаходу, можуть знайти застосування як модулятори гістамінового рецептора H4 у способах даного винаходу. Подібні способи модуляції активності гістамінового рецептора H4 включають вплив на гістаміновий рецептор H 4 ефективної кількості щонайменше однієї з хімічних сполук, вибираних зі сполук формули (I), фармацевтично прийнятних солей, фармацевтично прийнятних проліків і фармацевтично активних метаболітів. За допомогою здійснень даного винаходу інгібують активність гістамінового рецептора H4. У ряді здійснень даного винаходу, таких як описані в даній заявці, згаданий гістаміновий рецептор H4 знаходиться в тілі пацієнта з захворюванням, розладом або медичним станом, опосередкованим активністю гістамінового рецептора H4. Симптоми або хворобливі стани також охоплюються термінами "медичні стани, розлади або захворювання". Відповідно, даний винахід стосується способів застосування описуваних у даній заявці активних агентів для лікування пацієнтів, що страждають від або у яких діагностовано захворювання, розлад або медичний стан, опосередкований активністю гістамінового рецептора H4, такий як запалення. Таким чином, активні агенти відповідно до даного винаходу можуть застосовуватися як протизапальні агенти. Активні агенти відповідно до даного винаходу можуть також застосовуватися для лікування больового синдрому. У ряді варіантів здійснення активний агент відповідно до даного винаходу вводиться для лікування запалення. Запалення може бути пов'язане з різними захворюваннями, розладами і станами, такими як запальні розлади, алергічні розлади, дерматологічні розлади, аутоімунні захворювання, лімфатичні розлади і імунодефіцитні розлади, включаючи більш конкретні стани і захворювання, перераховані нижче. У плані виникнення і розвитку запалення, до запальних або опосередкованих запаленням захворювань і станів крім іншого належать гостре запалення, алергічне запалення і хронічне запалення. Лікування запалення відповідно до даного винаходу включає місцеве лікування, наприклад місцеве лікування таких станів, як шкірний свербіж, алергічна висипка й атопічний дерматит. Типові приклади запалень, для лікування яких може застосовуватися модулюючий гістаміновий рецептор H4 агент, включають в себе запалення, пов'язані з одним або декількома з таких станів, як алергія, астма, синдром сухого ока, хронічне обструктивне захворювання легень (COPD), атеросклероз, ревматоїдний артрит (див. Ohki E. et al. Biol. Pharm. Bull. 2007, 30(11), 2217-2220), множинний склероз, запальні захворювання кишечнику (включаючи коліт, хворобу Крона і виразковий коліт), псоріаз, прурит, короста, шкірний свербіж, атопічний дерматит, алергічна висипка (кропивниця), запалення очей (наприклад, постхірургічне запалення очей), кон'юнктивіт, носові поліпи, алергічний риніт, носовий свербіж, склеродермія, аутоімунні захворювання щитовидної залози, післяопераційні спайки (див. заявку на патент США 2007/0185163), імуноопосередкований (1 типу) цукровий діабет і вовчак, які характеризуються надлишковим або затягнутим в часі запаленням на одній зі стадій захворювання. У рамках даного винаходу також передбачається можливість лікування розладів метаболізму, таких як цукровий діабет 2 типу. Можливість лікування інших розладів метаболізму, передбачувана в рамках даного винаходу, включає лікування хронічної ниркової недостатності, гепатичного холестазу і цукрового діабету. Інші аутоімунні захворювання, що ведуть до запалення, включають наступні захворювання: важку псевдопаралітичну міастенію (Myasthenia gravis), аутоімунні нейропатії, такі як синдром Гійєна-Барре (Guillain-Barré), аутоімунний увеїт, аутоімунну гемолітичну анемію, злоякісну анемію, аутоімунну тромбоцитопенію, скроневий артеріїт, антифосфоліпідний синдром, васкулітиди, такі як гранулематоз Вегенера, хворобу Бехчета (Behcet), герпетиформний дерматит, пухирчатку звичайну, вітиліго, первинний біліарний цироз печінки, аутоімунний гепатит, аутоімунний оофорит і орхіт, аутоімунне захворювання надниркових залоз, поліміозит, дерматоміозит, спондилоартропатії, такі як анкілозуючий спондилоартрит, і синдром Сьєргена. Свербіж, для лікування якого може застосовуватися агент, модулюючий гістаміновий рецептор H4 відповідно до даного винаходу, включає свербіж, що є симптомом алергічних шкірних захворювань (таких як атопічний дерматит і кропивниця). У рамках даного винаходу також передбачається можливість лікування афективних і тривожних розладів. Приклади подібних афективних розладів включають великий депресивний розлад, біполярний афективний розлад, великий депресивний розлад, що не піддається 14 UA 106046 C2 5 10 15 20 25 30 35 40 45 50 55 лікуванню, і біполярний афективний розлад, що не піддається лікуванню. Приклади подібних тривожних розладів включають генералізований тривожний розлад, соціофобії і посттравматичний стресовий розлад. В інших здійсненнях активний агент відповідно до даного винаходу вводиться для лікування таких захворювань, як алергія, ревматоїдний артрит, астма, аутоімунні захворювання або свербіж. Таким чином, згадані активні агенти можуть застосовуватися для лікування пацієнтів, що страждають від або у яких діагностовано захворювання, розлад або медичний стан, опосередкований активністю гістамінового рецептора H4. Використовуваний у даній заявці термін "лікувати" або "лікування" стосується призначення активного агента або композиції відповідно до даного винаходу пацієнту для одержання бажаного терапевтичного або профілактичного ефекту за допомогою модуляції активності гістамінового рецептора H4. Лікування включає в себе обертання перебігу, поліпшення, полегшення, уповільнення прогресування, зменшення чутливості або запобігання захворюванню, розладу або стану, або одного або більше симптомів такого захворювання, розладу або стану, обумовленого активністю гістамінового рецептора H4. Використовуваний у даній заявці термін "пацієнт" стосується представника ссавців, що потребують обговорюваного лікування, наприклад людини. Передбачається застосування деяких здійснень даного винаходу у ветеринарії. "Модулятори" включають одночасно і інгібітори, і активатори, де термін "інгібітори" стосується сполук, що знижують, блокують, інактивують, послабляють чутливість або знижують рівень експресії або активність гістамінового рецептора H4, а "активатори" являють собою сполуки, що підвищують, активують, полегшують, підсилюють чутливість або підвищують рівень експресії або активність гістамінового рецептора H4. У способах лікування відповідно до даного винаходу пацієнтам, що страждають від або у яких діагностовано захворювання, розлад або медичний стан, вводять ефективну кількість щонайменше одного активного агента відповідно до даного винаходу. "Ефективна кількість" означає кількість або дозування, достатні для досягнення загалом бажаного терапевтичного або профілактичного ефекту для пацієнта, що потребує такого лікування при зазначеному захворюванні, розладі або стані. Ефективні кількості або дозування активних агентів відповідно до даного винаходу можуть бути визначені стандартними способами, такими як моделювання, дослідження зі збільшенням дози або клінічні випробування, а також шляхом взяття до уваги стандартних факторів, таких як спосіб або шлях введення або доставки ліків, фармакокінетика агента, ступінь тяжкості і характер перебігу хвороби, розладу або стану, поточна або попередня терапії пацієнта, стан здоров'я і реакція на ліки пацієнта, а також здоровий глузд лікуючого спеціаліста. Типова доза може знаходитися в діапазоні від приблизно 0,001 до приблизно 200 мг активного агента на кг ваги тіла пацієнта на день, переважно від приблизно 0,05 до приблизно 100 мг/кг/день або від приблизно 0,1 до приблизно 35 мг/кг/день, або від приблизно 0,1 до приблизно 10 мг/кг/день у вигляді однократного дозування або дробового введення (наприклад, два, три або чотири рази на день). Для пацієнта вагою 70 кг типовий діапазон відповідних дозувань складає від приблизно 1 до приблизно 200 мг/день або від приблизно 5 до приблизно 50 мг/день. Після поліпшення стану пацієнта, полегшення симптомів захворювання або розладу дозування може бути скоректоване для профілактичного або підтримуючого лікування. Наприклад, дозування, частота введення або і те, і інше можуть бути знижені залежно від симптомів до рівня, при якому підтримується бажаний терапевтичний або профілактичний ефект від прийому препарату. Зрозуміло, якщо симптоми полегшені до прийнятного рівня, лікування можна припинити. Однак при наявності рецидивів симптомів пацієнту може знадобитися довгострокове періодичне лікування. Крім того, активні агенти відповідно до даного винаходу можуть застосовуватися в сполученні з додатковими активними компонентами для лікування перерахованих вище станів. Згадані додаткові активні компоненти можуть вводитися пацієнту окремо від активного агента формули (I) або вводитися одночасно з подібним агентом у складі фармацевтичної композиції згідно з даним винаходом. В одному з прикладів здійснення згадані активні компоненти являють собою компоненти, для яких відома або виявлена ефективність у лікуванні станів, розладів або хвороб, опосередкованих активністю гістамінового рецептора H4, такі як інший модулятор гістамінового рецептора H4 або сполука з активністю проти іншої мішені, пов'язаної з даним конкретним станом, розладом або захворюванням. Згадане сполучення компонентів може служити для підвищення ефективності (наприклад, шляхом включення до складу даної комбінації сполуки, що підвищує ефективність або активність агента відповідно до даного 15 UA 106046 C2 5 10 15 20 25 30 35 40 45 50 55 60 винаходу), ослаблення одного або декількох побічних ефектів або зниження необхідного дозування активного агента відповідно до даного винаходу. Стосовно модулювання цільового рецептора "ефективна кількість" означає кількість, достатню для впливу на активність подібного рецептора. Вимірювання активності цільового рецептора може бути виконане стандартними аналітичними способами. Модуляція цільового рецептора може бути корисна в ряді обставин, включаючи проведення аналізів. Активні агенти за даним винаходом використовуються, самостійно або в сполученні з одним або декількома додатковими активними компонентами, для приготування фармацевтичних композицій, що відповідають цілям даного винаходу. До складу придатної для цілей даного винаходу фармацевтичної композиції входить (а) ефективна кількість щонайменше одного активного агента відповідно до даного винаходу; і, можливо, додатково (б) фармацевтично прийнятний наповнювач. Термін "фармацевтично прийнятний наповнювач" означає нетоксичну, біологічно переносиму і по інших параметрах біологічно відповідну для введення пацієнту речовину, таку як інертна речовина, яка додається у фармакологічну композицію або іншим способом використовується як засіб доставки, носій або розріджувач для полегшення введення агента і сумісна з останнім. Приклади наповнювачів включають в себе карбонат кальцію, фосфат кальцію, різні цукри і типи крохмалів, похідні целюлози, желатин, рослинні олії і поліетиленгліколі. Форми доставки фармацевтичних композицій, що містять одну або більше одиниць дозування активних агентів, можуть бути приготовлені з використанням відповідних фармацевтичних наповнювачів і способів приготування, відомих фахівцям сьогодні або доступних у майбутньому. Описувані композиції можуть відповідно до цілей даного винаходу вводитися будь-яким придатним шляхом, наприклад перорально, парентерально, ректально, місцево, в очі або через інгалятор. Композиція може бути приготовлена у формі таблеток, капсул, саше, драже, порошків, гранул, пастилок, порошків для відновлення, рідких препаратів або супозиторіїв. Переважно композиції формулюються для внутрішньовенного вливання, місцевого застосування або перорального введення. Для перорального введення активні агенти відповідно до даного винаходу можуть бути приготовлені у формі таблеток або капсул, а також у формі розчину, емульсії або суспензії. Для приготування композицій для перорального введення активні компоненти можуть вводитися в композиції в кількостях, що забезпечують дозування, наприклад, від приблизно 0,05 до приблизно 50 мг/кг/день або від приблизно 0,05 до приблизно 20 мг/кг/день, або від приблизно 0,1 до приблизно 10 мг/кг/день. Таблетки для перорального введення можуть включати активні компоненти, змішані із сумісними фармацевтично прийнятними наповнювачами, такими як розріджувачі, речовини для поліпшення розпаду таблеток, зв'язуючі агенти, мастильні речовини, підсолоджувачі, смакові добавки, барвники і консерванти. Відповідні інертні наповнювачі включають карбонати натрію і кальцію, фосфати натрію і кальцію, лактозу, крохмаль, цукор, глюкозу, метилцелюлозу, стеарат магнію, маніт, сорбіт і т. п. Приклади рідких наповнювачів для орального введення включають етанол, гліцерин, воду і т. п. Типові компоненти для поліпшення розпаду таблеток включають крохмаль, полівінілпіролідон (PVP), крохмалю натрію гліколят, мікрокристалічну целюлозу й альгінову кислоту. Зв'язуючі агенти можуть включати крохмаль і желатин. Функції мастильного агента, якщо він присутній, може виконувати стеарат магнію, стеаринова кислота або тальк. При необхідності таблетки можуть бути покриті таким матеріалом, як гліцерилмоностеарат або гліцерилдистеарат, для уповільнення всмоктування в шлунково-кишковому тракті або можуть мати ентеросолюбільну оболонку. Капсули для перорального застосування включають тверді і м'які желатинові капсули. Для приготування твердих желатинових капсул активні компоненти можуть бути змішані з твердим, напіврідким або рідким розріджувачем. М'які желатинові капсули можуть бути приготовлені шляхом змішування активного компонента з водою, олією, такою як арахісова або маслинова олія, вазеліновим маслом, сумішшю моно- і дигліцеридів коротколанцюжкових жирних кислот, поліетиленгліколем 400 або пропіленгліколем. Можливі рідини для перорального застосування включають суспензії, розчини, емульсії або сиропи або можуть бути ліофілізовані і постачатися в сухому вигляді для відновлення водою або іншим відповідним носієм перед використанням. До складу подібних рідких композицій можуть входити наступні компоненти: фармацевтично прийнятні наповнювачі, такі як суспендуючі агенти (наприклад, сорбіт, метилцелюлоза, альгінат натрію, желатин, гідроксіетилцелюлоза, карбоксиметилцелюлоза, гелеподібний стеарат алюмінію і т. д.); неводні 16 UA 106046 C2 5 10 15 20 25 30 35 40 45 50 носії, наприклад олії (наприклад, мигдальна олія або фракціонована кокосова олія), пропіленгліколь, етиловий спирт або вода; консерванти (наприклад, метил- або пропіл-пгідроксибензоат або сорбінова кислота); змочувальні агенти, такі як лецитин; а також, при необхідності, ароматизатори або барвники. Активні агенти, що складають предмет даного винаходу, можуть також вводитися пацієнту непероральними шляхами. Наприклад, композиції можуть бути приготовлені у вигляді супозиторіїв для ректального застосування. У випадку композицій для парентерального введення, включаючи внутрішньовенне, внутрішньом'язове, внутрішньоочеревинне або підшкірне введення, агенти відповідно до даного винаходу можуть бути приготовлені у формі стерильних водних розчинів або суспензій, з додаванням відповідних розчинів до одержання необхідних значень pН і ізотонічності, або у вигляді парентерально прийнятного масла. Відповідні рідкі носії включають розчин Рінгера і ізотонічний розчин хлориду натрію. Подібні лікарські форми можуть бути приготовлені у вигляді однодозової форми, такої як ампула або одноразове пристосування для ін'єкцій, у вигляді багатодозової форми, такої як флакони, з яких може бути відібрана необхідна кількість препарату, або у твердій формі або у формі первинного концентрату, що може бути використаний для приготування сполук для ін'єкцій. Характерні дози для ін'єкцій знаходяться в діапазоні від приблизно 1 до 1000 мкг/кг/хв. активного агента у вигляді суміші з фармацевтичним носієм протягом проміжку часу від декількох хвилин до декількох днів. Для місцевого застосування агенти можуть бути змішані з фармацевтичним носієм у концентрації від приблизно 0,1 % до приблизно 10 % препарату в носії. Інший спосіб введення агентів, що складають предмет даного винаходу, може включати використання пластирів для трансдермальної доставки препарату. Альтернативно з метою даного винаходу активні агенти можуть вводитися шляхом інгаляції, через ніс або рот, наприклад, у вигляді спрею, що містить також відповідний носій. Далі типові хімічні сполуки, які можуть застосовуватися в способах, що складають предмет даного винаходу, будуть описані з посиланням на наведені нижче типові синтетичні схеми для їх загального одержання і представлені далі конкретні приклади. Як визначать фахівці в даній галузі, для одержання різних сполук, що розкриваються в даній заявці, можуть бути відповідним чином вибрані вихідні матеріали, так щоб необхідні в кінцевій сполуці замісники могли бути проведені через схему реакції за наявності або за відсутності захисту, залежно від ситуації, з утворенням бажаного продукту. Як альтернатива може виявитися необхідним або бажаним ввести замість бажаного замісника відповідну групу, що може бути проведена через схему реакції і потім замінена відповідним чином на необхідний замісник. Кожна з наведених на Схемі A реакцій переважно проводиться при температурі від приблизно кімнатної до температури кипіння використовуваного органічного розчинника. Якщо не зазначене інше, усі хімічні змінні у формулах визначаються відповідно до наданого вище опису формули (I). Як показано на Схемі A, сполуки формули (I) одержують шляхом послідовного введення 1 сполук (X) у реакцію з амінами (XI) і потім амінами (XIII). Якщо Y і Z являють собою CH, Hal 2 являє собою хлор, і Hal являє собою хлор, бром або йод, приєднання амінів (XI) у каталізованій паладієм реакції амінування дає сполуки (XII). Реакції амінування проводять у присутності каталізатора, що містить паладій(0), такого як трис(дибензиліденацетон)-дипаладій(0) (Pd2(dba)3) або тетракис(трифенілфосфин)паладій, ліганду, такого як 4,5-біс(дифенілфосфіно)9,9-диметилксантен (Xantphos), 2-дициклогексилфосфіно-2',4',6'-триізопропілбіфеніл (X-Phos), 1,1'-біс(дифенілфосфіно)фероцен (dppf), 2,2'-біс(дифенілфосфіно)-1,1'-бінафтил (BINAP), CyMAP [(2'-дициклогексилфосфанілбіфен-2-іл)диметиламін], Cy2P(Ph-Ph) (дициклогексил-2біфенілфосфан), tBu2P(Ph-Ph) (ди-трет-бутил-2-біфенілфосфан), tBu3P або IPr•HCl (IPr=1,4біс(2,6-діізопропіл)імідазол-2-іліден), і основи, такої як трет-бутоксид натрію, трет-бутоксид калію, біс(триметилсиліл)амід літію або натрію або Cs 2CO3, у розчиннику, такому як толуол, тетрагідрофуран (THF), диметилацетамід (DMA), диметоксіетан (DME) або трет-бутанол, або їх суміші, при температурі від приблизно 50 °C до приблизно 140 °C (Ji et al. J. Org. Chem. 2003, 24, 4611–4614). Переважно реакції проводять з використанням Pd2(dba)3, Xantphos і третбутоксиду натрію в толуолі при температурі від приблизно 70 °C до приблизно 110 °C. 17 UA 106046 C2 1 5 10 15 20 25 30 35 40 Потім сполуки (XII), у яких Y і Z являють собою CH, і Hal являє собою хлор, перетворюють у піридини формули (I) у каталізованій паладієм реакції амінування з амінами (XIII), як описано вище. Переважно реакції проводять з використанням ацетату паладію(II) (Pd(OAc)2), BINAP і трет-бутоксиду натрію в толуолі, DMA або трет-бутанолі (або їх суміші) при температурі від приблизно 50 °C до приблизно 110 °C. 1 2 Якщо Y являє собою CH і Z являє собою N, Hal являє собою хлор і Hal являє собою хлор, бром або йод, сполуки (X) вводять у реакцію заміщення з амінами (XI), у присутності або за відсутності основного третинного аміну (такого як діізопропілетиламін або триетиламін), в органічному розчиннику, такому як метанол, етанол, ізопропанол, трет-аміловий спирт, пентан1-ол, THF або ацетонітрил, або їх суміші, при температурі від приблизно 0 °C до приблизно 180 °C, при традиційному нагріванні або в умовах мікрохвильового нагрівання, з одержанням 1 сполук формули (XII). Потім сполуки (XII), у яких Y являє собою CH і Z являє собою N, і Hal являє собою хлор, вводять у реакцію з амінами (XIII) в умовах реакції заміщення, як описано вище, одержуючи піримідини формули (I). Додатково сполуки формули (I) одержують шляхом послідовного введення сполук (X) у реакцію з амінами (XI) і потім амінами (XIII). Сполуки (X), у яких Y являє собою N і Z являє 1 2 собою CH, Hal і Hal являють собою атоми хлору, вводять у реакцію з амінами, у присутності або за відсутності основного третинного аміну (такого як діізопропілетиламін або триетиламін), у такому розчиннику, як THF, DMF або їм подібному, при температурі від приблизно 23 °C до приблизно 110 °C, з одержанням сполук (XII). Потім приєднанням амінів (XIII), або в описаній вище реакції каталізованого паладієм амінування, або шляхом заміщення атома хлору аміном (XIII), чистим або в полярному розчиннику, такому як DME, у присутності або за відсутності основного третинного аміну (такого як діізопропілетиламін або триетиламін), при температурах у діапазоні від 100 °C до 250 °C в умовах традиційного або мікрохвильового нагрівання, одержують піридазини формули (I). Як показано на схемі B, сполуки формули (I) одержують шляхом послідовного введення сполук (XIV) у реакцію з амінами (XIII) і потім амінами (XI). Сполуки (XIV), у яких Y і Z являють 3 4 собою CH, Hal являє собою фтор і Hal являє собою йод або бром, вводять у реакцію з амінами (XIII) у полярному розчиннику, такому як N-метилпіролідинон (NMP), N, N-диметилформамід, DMA, диметилсульфоксид або їх суміш, при температурі від приблизно 50 °C до приблизно 110 °C, в умовах традиційного або мікрохвильового нагрівання й одержують сполуки (XV). Потім приєднанням амінів (XI), або в реакції каталізованого паладієм амінування (як описано для схеми A), або в реакції ароматичного нуклеофільного заміщення в присутності кислоти Льюїса, такої як трифторметансульфонат ітербію (Yb(OTf)3), у полярному розчиннику, такому як DMA або NMP, при температурі від приблизно 150 °C до приблизно 250 °C в умовах традиційного або мікрохвильового нагрівання одержують піридини формули (I). 3 4 Сполуки (XIV), у яких Y являє собою CH і Z являє собою N, Hal являє собою хлор і Hal являє собою хлор, вводять у реакцію заміщення з амінами (XIII), даючи сполуки (XV), і потім з амінами (XI), даючи піримідини формули (I). Реакції заміщення проводять способом, описаним для схеми A. 18 UA 106046 C2 1 5 10 15 20 25 30 Як показано на схемі C, сполуки (XVII), у яких Y являє собою N, Z являє собою C і Hal являє собою хлор, одержують хлоруванням сполук (XVI) з використанням умов, відомих фахівцям у даній галузі, наприклад у реакції з хлористим фосфорилом, при температурах у діапазоні від 65 °C до приблизно 120 °C, з одержанням сполук (XVII). Одержані сполуки (XVII) вводять у реакцію заміщення з амінами (XI) у присутності основного третинного аміну (наприклад, діізопропілетиламіну або триетиламіну) в органічному розчиннику, такому як метанол, етанол, ізопропанол, трет-аміловий спирт, пентан-1-ол, THF або ацетонітрил, або їх суміші, при температурі від приблизно 23 °C до 180 °C, при традиційному нагріванні або в умовах мікрохвильового нагрівання. Потім сполуки (XVIII) вводять у реакцію з амінами (XIII) в описаних вище умовах реакції заміщення, одержуючи піридазини (XIX). Реакцією галопіридазинів (XIX) з відновником, таким як 10 % паладій на вуглеці, у присутності форміату амонію в полярному розчиннику, такому як метанол, при температурах у діапазоні від 65 °C до 85 °C, потім одержують сполуки формули (I). 1 Як показано на схемі D, сполуки (XVI), у яких Y являє собою N, Z являє собою C і Hal являє собою хлор, вводять у реакцію з йодистоводневою кислотою (57 %) при температурах у діапазоні від 100 °C до 150 °C з одержанням проміжного продукту (XXI), 5-йод-4H-піридазин-3ону. Потім реакцією проміжного продукту (XXI) з амінами (XI) в умовах реакції заміщення в органічному розчиннику, такому як метанол, етанол, ізопропанол, трет-аміловий спирт, пентан1-ол, THF або ацетонітрил, або їх суміші, при температурі від 23 °C до 180 °C, при традиційному нагріванні або в умовах мікрохвильового нагрівання, одержують сполуки формули (XXII). Потім хлоруванням сполук (XXII) з використанням умов, відомих фахівцям у даній галузі, наприклад у реакції з хлористим фосфорилом, при температурах у діапазоні від 65 °C до приблизно 120 °C, одержують сполуки (XXIII). Одержані сполуки (XXIII) вводять у реакцію з амінами (XIII) в умовах реакції заміщення в органічному розчиннику, такому як метанол, етанол, ізопропанол, третаміловий спирт, пентан-1-ол, THF або ацетонітрил, або їх суміші, при температурі від приблизно 23 °C до 200 °C, при традиційному нагріванні або в умовах мікрохвильового нагрівання, і одержують сполуки формули (I). 3 4 В описаних вище схемах, якщо діамін HNR R (XIII) містить захисну групу для атома азоту, a c таку як трет-бутоксикарбонільну групу (Boc) або бензильну групу, замість замісника R або R , 19 UA 106046 C2 5 10 15 20 25 30 35 40 45 50 55 захисна група потім знімається у відомих фахівцям у даній галузі умовах з одержанням сполук, a c у яких замісники R або R являють собою H. Наприклад, трет-бутоксикарбонільна група знімається з використанням органічної кислоти, такої як TFA (чистої або в розчиннику, такому як CH2Cl2), або неорганічної кислоти, такої як HCl (у такому розчиннику, як 1,4-діоксан, ефір, метанол, ізопропанол, мурашина кислота або їх суміш). Для перетворення сполук, у яких c c замісник R являє собою H, у сполуки, де R являє собою C1-3алкіл, можуть використовуватися процедури відновного амінування або алкілування. Сполуки формули (I) можуть бути перетворені у відповідні солі з використанням відомих у даній галузі способів. Наприклад, обробка аміну формули (I) трифтороцтовою кислотою, HCl або лимонною кислотою в розчиннику, такому як Et2O, CH2Cl2, THF, MeOH, хлороформ або ізопропанол, дає відповідну сольову форму. Альтернативно солі трифтороцтової або мурашиної кислоти можуть бути одержані в результаті очищення сполук в умовах високоефективної рідинної хроматографії з оберненими фазами. Кристалічні форми фармацевтично прийнятних солей сполук формули (I) можуть бути одержані в кристалічній формі шляхом перекристалізації з полярних розчинників (включаючи суміші полярних розчинників і водні суміші полярних розчинників) або з неполярних розчинників (включаючи суміші неполярних розчинників). Сполуки, одержані відповідно до описаних вище схем, можуть бути одержані як окремо узяті енантіомери, діастереомери або регіоізомери шляхом енантіо-, діастерео- або регіоспецифічного синтезу або шляхом поділу. Сполуки, одержані відповідно до описаних вище схем, можуть альтернативно бути одержані як рацемічні (1:1) або нерацемічні (не 1:1) суміші або як суміші діастереомерів або регіоізомерів. При одержанні рацемічних і нерацемічних сумішей енантіомерів, індивідуальні енантіомери можуть бути виділені за допомогою відомих фахівцям у даній галузі традиційних способів поділу, таких як хіральна хроматографія, перекристалізація, утворення діастереомерної солі, перетворення в діастереомерні аддукти, біотрансформація або ферментативна трансформація. При одержанні сумішей регіоізомерів або діастереомерів індивідуальні ізомери можуть бути виділені з використанням традиційних способів, таких як хроматографія або кристалізація. Наведені нижче конкретні приклади більш докладно ілюструють даний винахід і його різні переважні здійснення. ПРИКЛАДИ Якщо не зазначене інше, для одержання описаних у наведених нижче прикладах сполук і відповідних аналітичних даних використовувалися наступні експериментальні й аналітичні процедури. Якщо інше не зазначено особливо, реакційні суміші перемішували на магнітній мішалці при кімнатній температурі в атмосфері азоту. Якщо розчини були "осушені", для цього, як правило, використовували осушувальний агент, такий як Na2SO4 або MgSO4. Якщо суміші, розчини й екстракти були "концентровані", то їх звичайно концентрували на роторному випарнику при зниженому тиску. Для очищення з використанням колонкової флеш-хроматографії використовували силікагель (SiО2) і зазначений у дужках елюент. TM Мікрохвильове нагрівання виконували на системі Emrys Optimizer компанії Personal Chemistry, використовуючи пробірки для мікрохвильового синтезу Biotage. Аналітичну високоефективну рідинну хроматографію (HPLC) з оберненими фазами виконували на аналізаторі HPLC Series 1100 компанії Hewlett Packard, використовуючи монолітні колонки ONYX® C18 (5 мкм, 4,6×100 мм) компанії Phenomenex. Детектування виконували на довжинах хвиль λ=230, 254 і 280 нм. Використовували швидкість потоку 1 мл/хв. і градієнт від 10 до 90 % ацетонітрил/вода (20 мМ NH4OH) за період 5,0 хв. Препаративну високоефективну рідинну хроматографію з оберненими фазами проводили на системі Dionex з колонками YMC Pack ODS 250×30 мм і градієнтом від 10 до 50 % NH4OH в ацетонітрилі (0,05 % води) за період 15 хв. при швидкості потоку 70 мл/хв. Альтернативно сполуки очищали на рідинному хроматографі з мас-спектроскопічним детектуванням Waters LC/MS з колонкою Waters XBridge C18 (100×30 мм), використовуючи градієнт від 1 до 25 % ацетонітрил/вода (0,05 % трифтороцтової кислоти (TFA)) за період 15 хв. при швидкості потоку 44 мл/хв. Аналітичну високоефективну рідинну хроматографію з оберненими фазами виконували на аналізаторі Agilent з колонкою C18 (5 мкм, 4,6×150 мм). Детектування виконували на довжинах хвиль λ=214 і 254 нм. Використовували швидкість потоку 1 мл/хв. і градієнт від 10 до 90 % ацетонітрил/вода (0,1 % мурашиної кислоти) за період 10 хв. Препаративну тонкошарову хроматографію (TLC/ТШХ) проводили на пластинках розміром 20×20 см із силікагелем 60 F254, товщина шару 0,5 мм. 20 UA 106046 C2 5 10 15 20 25 30 35 40 45 50 Препаративну високоефективну рідинну хроматографію з оберненими фазами проводили на колонці Gemini C18 (150×21,2 мм) із градієнтом від 5 до 60 % ацетонітрил/вода (0,1 % трифтороцтової кислоти або 0,1 % мурашиної кислоти) за період 14 хв. при швидкості потоку 20 мл/хв. із контролем на довжині хвилі 214 нм. Сполуки аналізували у формі вільної основи, гідрохлоридної або трифторацетатної солі. Гідрохлоридні солі одержували або 1) у процесі видалення трет-бутилкарбамоїльної групи (Boc); або 2) шляхом обробки розчину очищеної вільної основи в THF, CHCl 3 або CH2Cl2 (DCM) щонайменше двома еквівалентами розчину HCl у 1,4-діоксані з наступною концентрацією. Трифторацетатні солі одержували безпосередньо в процесі хроматографічного очищення. Спектри ядерного магнітного резонансу (ЯМР) одержували на спектрометрах Bruker DRX (400 МГц або 500 МГц) або Varian (300 МГц). Далі використовується наступний формат 1 представлення даних H ЯМР: хімічний зсув в мільйонних частках у бік слабкого поля від сигналу, використовуваного як стандарт тетраметилсилану (мультиплетність, константа спінспінової взаємодії J у Гц, інтеграція). Мас-спектри (МС) одержували на аналізаторі Agilent серії 1100 MSD або 1200 MSD при електророзпилювальній іонізації (ЕРІ) у позитивному або негативному режимах, як зазначено при характеризації сполуки. Мас-спектрометричні дані представлені у формі одержаних значень + m/z (як правило, [M+H] ) для молекулярного іона. Хімічні назви генерували за допомогою програмного пакета ACD/Name версії 10 (Advanced Chemistry Development, Торонто, Онтаріо, Канада) або ChemDraw версії 6.0.2 (CambridgeSoft, Кембридж, Массачусетс, США). Приклад 1: Біцикло[2.2.1]гепт-2-ил-[4-((3R)-3-метиламінопіролідин-1-іл)-піридин-2-іл]-аміну дигідрохлорид (3R)-[1-(2-хлорпіридин-4-іл)-піролідин-3-іл]-метиламін До розчину 2-хлор-4-бромпіридину (4,3 г, 22,1 ммоль) у толуолі (100 мл) при перемішуванні додавали (R)-метилпіролідин-3-іламін (1,7 г, 17,0 ммоль) і трет-бутоксид натрію (2,5 г, 26,0 ммоль). Колбу відкачували і двічі продували газоподібним N 2. Потім в один прийом додавали суміш 4,5-біс(дифенілфосфіно)-9,9-диметилксантену (Xantphos; 590 мг, 1,0 ммоль) і трис(дибензиліденацетон)-дипаладію(0) (Pd2(dba)3; 310 мг, 0,34 ммоль) і витримували одержану суміш при температурі 85 °C протягом 20 годин. Одержану суміш охолоджували до кімнатної температури, розбавляли H2O (75 мл) і екстрагували етилацетатом (EtOAc; 3x). Об'єднані органічні фази висушували і концентрували, одержуючи прозоре масло коричневого кольору. Одержане масло очищали (флеш-хроматографія, 0-5 % 2 M розчину NH3 у MeOH/CH2Cl2) і одержували шукану сполуку у вигляді твердої речовини коричневого кольору (1,1 г, 30 %). МС 1 (ЕРІ): розраховано для C10H14ClN3: 211,09; одержано m/z: 212,1 [M+H]. H ЯМР (DMSO-d6): 7,86 (д, J=5,9, 1H); 6,47-6,38 (м, 2H); 3,45-3,17 (м, 4H); 3,11-3,01 (м, 1H); 2,29 (с, 3H); 2,15-2,00 (м, 1H); 1,82 (уш.с, 1H); 1,79-1,65 (м, 1H). Біцикло[2.2.1]гепт-2-ил-[(3R)-4-(3-метиламінопіролідин-1-іл)-піридин-2-іл]-амін До поміщеної в сцинтиляційний флакон суміші [(3R)-1-(2-хлорпіридин-4-іл)-піролідин-3-іл]метиламіну (97 мг, 0,46 ммоль), екзо-2-амінонорборнану (164 мкл, 1,4 ммоль) у диметиловому ефірі етиленгліколю (DME; 4 мл) при перемішуванні додавали трет-бутоксид натрію (245 мг, 2,6 ммоль). До одержаної суміші при перемішуванні в один прийом додавали Pd(OAc) 2 (16 мг, 0,024 ммоль) і рацемічний 2,2'-біс(дифенілфосфіно)-1,1'-бінафтил (BINAP; 19 мг, 0,031 ммоль). Одержану суміш витримували при температурі 65 °C протягом 20 годин, охолоджували до кімнатної температури і фільтрували через пробку з діатомової землі. Потім пробку промивали MeOH (2 мл) і очищали безпосередньо фільтрат (флеш-хроматографія, 5 % 2 M розчину NH3 у MeOH/CH2Cl2), одержуючи прозоре масло золотавого кольору (70 мг, 54 %). Біцикло[2.2.1]гепт-2-ил-[(3R)-4-(3-метиламінопіролідин-1-іл)-піридин-2-іл]-амін До розчину біцикло[2.2.1]гепт-2-ил-[(3R)-4-(3-метиламінопіролідин-1-іл)-піридин-2-іл]-аміну в 1:1 суміші Et2O/CH2Cl2 (8 мл) при перемішуванні додавали 1 H розчин HCl у Et2O (1 мл). Органічні фази розділяли і концентрували, одержуючи шуканий продукт (89 мг, 100 %) у вигляді твердої речовини бежевого кольору. МС (ЕРІ): розраховано для C 17H26N4: 286,2; одержано m/z: + 1 287,3 [M+H] . H ЯМР (DMSO-d6): 12,07 (с, 1H); 9,57 (уш.с, 1H); 9,46 (уш.с, 1H); 7,81 (д, J=5,1, 21 UA 106046 C2 5 1H); 7,66 (д, J=4,6, 1H); 6,28 (д, J=7,4, 1H); 5,64 (с, 1H); 3,89 (уш.с, 1H); 3,85-3,61 (м, 3H); 3,49 (уш.с, 2H); 2,60 (с, 3H); 2,35-2,20 (м, 3H); 2,18 (с, 1H); 1,95-1,85 (м, 1H); 1,55-1,46 (м, 3H); 1,371,25 (м, 2H); 1,21-1,09 (м, 2H). Сполуки в прикладах 2-15 одержували за допомогою способів, аналогічних описаним для прикладу 1. Приклад 2: N-циклопентил-4-[(3R)-3-(метиламіно)піролідин-1-іл]піридин-2-амін + 1 10 МС (ЕРІ): розраховано для C15H24N4: 260,2; одержано m/z: 261,3 [M+H] . H ЯМР (DMSO-d6): 7,57 (д, J=5,9, 1H); 5,77 (дд, J=5,9; 2,1, 1H); 5,72 (д, J=7,1, 1H); 5,42 (с, 1H); 4,05-3,96 (м, 1H); 3,36-3,29 (м, 2H); 3,28-3,15 (м, 2H); 2,99-2,91 (м, 1H); 2,29 (с, 3H); 2,06-1,98 (м, 1H); 1,90-1,81 (м, 2H); 1,81-1,72 (м, 2H); 1,71-1,62 (м, 2H); 1,55-1,46 (м, 2H); 1,45-1,35 (м, 2H). Приклад 3: 4-[(3R)-3-(метиламіно)піролідин-1-іл]-N-пропілпіридин-2-аміну дигідрохлорид + 1 15 20 25 МС (ЕРІ): розраховано для C13H22N4: 260,2; одержано m/z: 235,2 [M+H] . H ЯМР (DMSO-d6): 12,12 (с, 1H); 9,46-9,26 (м, 2H); 7,71 (д, J=5,2, 1H); 7,65 (д, J=6,9, 1H); 6,29 (д, J=7,4, 1H); 5,68 (с, 1H); 3,90 (уш.с, 1H); 3,78-3,61 (м, 3H); 3,37 (уш.с, 1H); 3,28-3,16 (м, 2H); 2,61 (с, 3H); 2,46-2,21 (м, 2H); 1,58 (кв, J=7,3, 2H); 0,95 (т, J=7,4, 3H). Приклад 4: N-(циклопропілметил)-4-[(3R)-3-(метиламіно)піролідин-1-іл]піридин-2-аміну дитрифторацетат + 1 МС (ЕРІ): розраховано для C14H22N4: 246,2; одержано m/z: 247,2 [M+H] . H ЯМР (DMSO-d6): 12,00 (с, 1H); 8,96 (с, 2H); 7,74 (д, J=5,1, 1H); 7,66 (д, J=4,3, 1H); 6,30 (д, J=7,4, 1H); 5,71 (с, 1H); 3,94 (уш.с, 2H); 3,60 (уш.с, 2H); 3,12 (д, J=6,8, 2H); 2,67 (с, 3H); 2,51-2,42 (м, 2H); 2,42-2,36 (м, 1H); 1,58-1,46 (м, 1H); 0,53 (д, J=8,0, 2H); 0,27 (д, J=6,1, 2H). Приклад 5: 4-[(3R)-3-(метиламіно)піролідин-1-іл]-N-[(3R)-тетрагідрофуран-3-іл]піридин-2аміну дигідрохлорид + 30 35 1 МС (ЕРІ): розраховано для C14H22N4O: 262,2; одержано m/z: 263,2 [M+H] . H ЯМР (DMSOd6): 12,14 (с, 1H); 9,55 (уш.с, 1H); 9,48 (с, 1H); 7,99 (д, J=7,1, 1H); 7,68 (д, J=7,1, 1H); 7,48 (с, J=8,0, 0,5H); 7,12 (д, J=8,4, 0,5H); 6,32 (д, J=7,4, 1H); 5,73 (с, 1H); 4,35-4,21 (м, 1H); 3,95-3,79 (м, 3H); 3,82-3,70 (м, 2H); 3,66-3,50 (м, 2H); 2,61 (т, J=5,1, 3H); 2,45-2,21 (м, 4H); 1,88-1,74 (м, 1H). Приклад 6: 4-[(3R)-3-(метиламіно)піролідин-1-іл]-N-[тетрагідрофуран-2-ілметил]піридин-2аміну дигідрохлорид Шукану сполуку одержували у вигляді суміші діастереомерів. МС (ЕРІ): розраховано для + 1 C15H24N4O: 276,2; одержано m/z: 277,2 [M+H] . H ЯМР (DMSO-d6): 12,34 (с, 1H); 9,63 (уш.с, 1H); 9,60 (с, 1H); 7,75-7,61 (м, 2H); 6,27 (д, J=7,4, 1H); 5,77 (с, 1H); 4,05-3,96 (м, 1H); 3,96-3,83 (м, 1H); 3,82-3,61 (м, 6H); 3,38-3,30 (м, 2H); 2,58 (с, 3H); 2,48-2,38 (м, 2H); 2,04-1,85 (м, 3H); 1,78-1,72 (м, 1H). 22 UA 106046 C2 Приклад дигідрохлорид 7: N-(4-фторбензил)-4-[(3R)-3-(метиламіно)піролідин-1-іл]піридин-2-аміну + 5 10 15 1 МС (ЕРІ): розраховано для C17H21FN4: 300,2; одержано m/z: 301,2 [M+H] . H ЯМР (DMSOd6): 12,39 (с, 1H); 9,38 (уш.с, 2H); 8,15 (т, J=6,0, 1H); 7,68 (д, J=7,1, 1H); 7,48-7,38 (м, 2H); 7,257,13 (м, 2H); 6,29 (д, J=7,4, 1H); 5,73 (с, 1H); 4,52 (д, J=6,0, 2H); 3,96 (уш.с, 1H); 3,92-3,38 (м, 4H); 2,59 (с, 3H); 2,42-2,21 (м, 2H). Приклад 8: N-циклопропіл-4-[(3R)-3-(метиламіно)піролідин-1-іл]піридин-2-аміну дигідрохлорид + 1 МС (ЕРІ): розраховано для C13H20N4: 232,2; одержано m/z: 233,2 [M+H] . H ЯМР (DMSO-d6): 12,21 (с, 1H); 9,58 (уш.с, 2H); 8,28 (д, J=5,4, 0,35H); 8,19 (с, 1H); 7,70 (с, 0,65H); 6,90 (д, J=7,4, 0,65H); 6,35 (д, J=7,4, 0,65H); 5,78 (с, 1H); 4,02-3,33 (м, 6H); 2,60 (с, 3H); 2,43-2,25 (м, 2H); 0,880,86 (м, 2H); 0,56-0,50 (м, 2H). Приклад 9: 4-[(3R)-3-(метиламіно)піролідин-1-іл]-N-[(1S, 2S, 3S, 5R)-2,6,6триметилбіцикло[3.1.1]гепт-3-ил]піридин-2-амін + 25 30 35 + 1 + 20 1 1 МС (ЕРІ): розраховано для C20H32N4: 328,5; одержано m/z: 329,3 [M+H] . H ЯМР (CD3OD): 7,56 (д, J=6,2, 1H); 5,93 (дд, J=6,2; 2,2, 1H); 5,56 (д, J=2,1, 1H); 4,80 (с, 4H); 3,99 (дт, J=9,4; 6,3, 1H); 3,52 (дд, J=10,0; 6,4, 1H); 3,49-3,40 (м, 1H); 3,38-3,27 (м, 4H); 3,11 (дд, J=10,0; 5,2, 1H); 2,712,61 (м, 1H); 2,46-2,37 (м, 1H); 2,23 (тд, J=13,6; 5,9, 1H); 2,01-1,77 (м, 4H); 1,58 (ддд, J=13,8; 5,6; 2,4, 1H); 1,24 (д, J=8,9, 3H); 1,13 (т, J=7,4, 3H); 1,10 (с, 3H); 1,03 (д, J=9,7, 1H). Приклад 10: 4-[(3R)-3-(метиламіно)піролідин-1-іл]-N-[(1R, 2R, 3R, 5S)-2,6,6триметилбіцикло[3.1.1]гепт-3-ил]піридин-2-амін МС (ЕРІ): розраховано для C20H32N4: 328,5; одержано m/z: 329,3 [M+H] . H ЯМР (CD3OD): 7,56 (д, J=6,2, 1H); 5,95 (дд, J=6,3; 2,2, 1H); 5,57 (д, J=2,1, 1H); 3,99 (дт, J=9,4; 6,3, 1H); 3,52 (дд, J=10,0; 6,3, 1H); 3,46 (дд, J=14,7; 8,9, 1H); 3,39-3,28 (м, 6H); 3,13 (дд, J=10,0; 5,1, 1H); 2,67 (т, J=11,6, 1H); 2,47-2,37 (м, 1H); 2,23 (тд, J=13,7; 5,9, 1H); 2,02-1,78 (м, 4H); 1,58 (ддд, J=13,8; 5,6; 2,4, 1H); 1,26 (с, 3H); 1,14 (д, J=7,2, 3H); 1,10 (с, 3H); 1,03 (д, J=9,7, 1H). Приклад 11: N-бензил-4-[(3R)-3-(метиламіно)піролідин-1-іл]піридин-2-амін МС (ЕРІ): розраховано для C17H22N4: 282,4; одержано m/z: 283,3 [M+H] . H ЯМР (CD3OD): 7,57 (д, J=6,1, 1H); 7,36-7,32 (м, 2H); 7,31-7,26 (м, 2H); 7,20 (т, J=7,2, 1H); 5,93 (дд, J=6,2; 2,2, 1H); 5,51 (д, J=2,1, 1H); 4,41 (с, 2H); 3,44 (дд, J=10,0; 6,4, 1H); 3,41-3,32 (м, 1H); 3,28-3,19 (м, 1H); 3,04 (дд, J=10,0; 5,1, 1H); 2,27-2,10 (м, 1H); 1,93-1,76 (м, 1H). Приклад 12: 4-[(3R)-3-(метиламіно)піролідин-1-іл]-N-(1-метилетил)-піридин-2-амін 23 UA 106046 C2 + + 10 15 20 25 30 35 40 1 + 5 1 1 + 1 МС (ЕРІ): розраховано для C13H22N4: 234,4; одержано m/z: 235,3 [M+H] . H ЯМР (CD3OD): 7,56 (д, J=6,2, 1H); 5,92 (дд, J=6,2; 2,2, 1H); 5,53 (д, J=2,1, 1H); 3,82 (гепт, J=6,4, 1H); 3,51 (дд, J=10,0; 6,4, 1H); 3,48-3,40 (м, 1H); 3,38-3,26 (м, 2H); 3,10 (дд, J=10,0; 5,2, 1H); 2,27-2,17 (м, 1H); 1,96-1,79 (м, 1H); 1,18 (д, J=6,4, 6H). Приклад 13: 4-[(3R)-3-амінопіролідин-1-іл]-N-(1-метилетил)піридин-2-амін МС (ЕРІ): розраховано для C12H20N4: 220,3; одержано m/z: 221,2 [M+H] . H ЯМР (CD3OD): 7,55 (д, J=7,4, 1H); 6,35 (дд, J=7,4; 2,4, 1H); 5,74 (д, J=2,3, 1H); 4,12 (с, 1H); 3,83 (дт, J=12,7; 6,4, 2H); 3,78-3,66 (м, 1H); 3,66-3,54 (м, 2H); 3,40-3,24 (м, 4H); 2,53 (дд, J=14,9; 6,5, 1H); 2,26 (д, J=5,3, 1H); 1,28 (д, J=6,4, 6H). Приклад 14: 4-[(3S)-3-амінопіролідин-1-іл]-N-(2-метилпропіл)піридин-2-амін МС (ЕРІ): розраховано для C13H22N4: 234,4; одержано m/z: 235,2 [M+H] . H ЯМР (CD3OD): 7,49 (д, J=7,3, 1H); 6,23 (дд, J=7,3; 2,4, 1H); 5,64 (д, J=2,3, 1H); 3,78-3,69 (м, 1H); 3,66-3,56 (м, 2H); 3,51-3,41 (м, 1H); 3,33-3,27 (м, 1H); 3,20 (дд, J=10,8; 4,5, 1H); 3,06 (д, J=6,9, 2H); 2,32-2,20 (м, 1H); 1,97-1,85 (м, 2H); 1,01 (д, J=6,7, 6H). Приклад 15: 4-[(3S)-3-(метиламіно)піролідин-1-іл]-N-(2-метилпропіл)-піридин-2-амін МС (ЕРІ): розраховано для C14H24N4: 248,4; одержано m/z: 249,2 [M+H] . H ЯМР (CD3OD): 7,55 (д, J=6,4, 1H); 6,02 (дд, J=6,5; 2,2, 1H); 5,57 (д, J=2,1, 1H); 3,56 (дд, J=10,2; 6,3, 1H); 3,533,46 (м, 1H); 3,42-3,34 (м, 2H); 3,16 (дд, J=10,2; 5,1, 1H); 3,03 (д, J=6,9, 2H); 2,34-2,18 (м, 1H); 1,91 (м, 2H); 0,99 (д, J=6,7, 6H). Приклад 16: N-циклопентил-4-піперазин-1-ілпіридин-2-амін 4-(2-Хлорпіридин-4-іл)-піперазин-1-карбонової кислоти трет-бутиловий ефір До розчину 2-хлор-4-бромпіридину (4,3 г, 22,5 ммоль) у толуолі (100 мл) при перемішуванні додавали трет-бутиловий ефір піперазин-1-карбонової кислоти (3,2 г, 17,2 ммоль) і третбутоксид натрію (2,5 г, 26,0 ммоль). Колбу відкачували і двічі продували газоподібним N 2. Потім в один прийом додавали суміш Xantphos (600 мг, 1,0 ммоль) і Pd2(dba)3 (318 мг, 0,35 ммоль) і витримували одержану суміш при температурі 85 °C протягом 20 годин. Одержану суміш охолоджували до кімнатної температури, розбавляли H2O (75 мл) і екстрагували EtOAc (3x). Об'єднані органічні фази висушували і концентрували, одержуючи прозоре масло золотавого кольору. Одержане масло очищали (флеш-хроматографія, 0-5 % 2 M розчину NH3 у MeOH/CH2Cl2) і одержували шукану сполуку у вигляді твердої речовини бежевого кольору (5,1 г, + 1 100 %). МС (ЕРІ): розраховано для C14H20ClN3O2: 297,1; одержано m/z: 298,2 [M+H] . H ЯМР (DMSO-d6): 7,95 (д, J=5,9, 1H); 6,88-6,78 (м, 2H); 3,46-3,32 (м, 8H); 1,42 (с, 9H). Трет-бутил-4-[2-(циклопентиламіно)піридин-4-іл]піперазин-1-карбоксилат До поміщеного у флакон розчину трет-бутилового ефіру 4-(2-хлорпіридин-4-іл)-піперазин-1карбонової кислоти (163 мг, 0,55 ммоль) у толуолі (2 мл) при перемішуванні додавали циклопентиламін (136 мкл, 1,38 ммоль) і трет-бутоксид натрію (161 мг, 1,68 ммоль). До одержаної суміші при перемішуванні в один прийом додавали суміш рацемічного BINAP (20 мг, 24 UA 106046 C2 5 10 15 20 25 30 35 40 0,032 ммоль) і Pd(OAc)2 (18 мг, 0,027 ммоль) і витримували її при температурі 85 °C протягом 20 годин. Одержану суміш охолоджували до кімнатної температури і безпосередньо очищали (флеш-хроматографія, 0-5 % 2 M розчину NH3 у MeOH/CH2Cl2), одержуючи шукану сполуку у вигляді твердої речовини білого кольору (34 мг, 17 %). МС (ЕРІ): розраховано для C19H30N4O2: + 1 346,2; одержано m/z: 347,3 [M+H] . H ЯМР (DMSO-d6): 7,65 (д, J=6,0, 1H); 6,10 (д, J=6,0, 1H); 5,92 (д, J=7,1, 1H); 5,78 (с, 1H) 4,08-4,02 (м, 1H); 3,41 (т, J=5,4, 4H); 3,16 (т, J=5,4, 4H); 1,89-1,82 (м, 2H); 1,67-1,61 (м, 2H); 1,59-1,48 (м, 2H); 1,42 (с, 9H); 1,43-1,35 (м, 2H). N-циклопентил-4-піперазин-1-ілпіридин-2-аміну дигідрохлорид До розчину трет-бутил-4-[2-(циклопентиламіно)піридин-4-іл]піперазин-1-карбоксилату (34 мг, 0,1 ммоль) у 96 % мурашиній кислоті (4 мл) при перемішуванні додавали 6 Н водний розчин HCl (2 краплі). Одержану суміш перемішували протягом 2 годин і концентрували, одержуючи шуканий продукт у вигляді твердої речовини білого кольору (26 мг, 93 %). МС (ЕРІ): + 1 розраховано для C14H22N4: 246,2; одержано m/z: 247,2 [M+H] . H ЯМР (DMSO-d6): 9,32 (с, 2H); 7,89 (д, J=7,1, 1H); 7,69 (д, J=7,5, 1H); 6,58 (д, J=7,6, 1H); 6,04 (с, 1H); 4,03-3,96 (м, 1H); 3,73 (т, J=4,9, 4H); 3,20 (т, J=5,0, 4H); 2,03-1,95 (м, 2H); 1,73-1,68 (м, 2H); 1,64-1,52 (м, 2H); 1,50-1,42 (м, 2H). Сполуки в прикладах 17-20 одержували за допомогою способів, аналогічних описаним для прикладу 16. Приклад 17: 4-піперазин-1-іл-N-пропілпіридин-2-аміну дигідрохлорид + 1 МС (ЕРІ): розраховано для C12H20N4: 220,2; одержано m/z: 221,2 [M+H] . H ЯМР (DMSO-d6): 9,35 (уш.с, 2H); 7,87-7,82 (м, 1H); 7,69 (д, J=7,5, 1H); 6,57 (дд, J=7,5; 2,4, 1H); 6,05 (с, 1H); 3,793,69 (м, 4H); 3,32-3,13 (м, 6H); 1,63-1,51 (м, 2H); 0,94 (т, J=7,3, 3H). Приклад 18: N-бензил-4-піперазин-1-ілпіридин-2-аміну дигідрохлорид + 1 МС (ЕРІ): розраховано для C16H20N4: 268,4; одержано m/z: 269,2 [M+H] . H ЯМР (CD3OD): 7,62 (д, J=7,5, 1H); 7,46-7,24 (м, 5H); 6,65 (дд, J=7,5; 2,1, 1H); 6,13 (д, J=2,0, 1H); 4,55 (с, 2H); 3,90-3,74 (м, 4H); 3,41-3,33 (м, 4H). Приклад 19: N-(2-метилпропіл)-4-піперазин-1-ілпіридин-2-аміну дигідрохлорид + 1 МС (ЕРІ): розраховано для C13H22N4: 234,4; одержано m/z: 235,3 [M+H] . H ЯМР (CDCl3): 7,81 (д, J=6,1, 1H); 6,11 (дд, J=6,1; 2,3, 1H); 5,69 (д, J=2,0, 1H); 4,47 (с, 1H); 3,43-3,18 (м, 4H); 3,03 (т, J=6,2, 2H); 3,02-2,84 (м, 4H); 1,88 (квінт, J=6,7, 1H); 0,99 (д, J=6,7, 6H). Приклад 20: 4-[(3R)-3-амінопіролідин-1-іл]-N-(2-метилпропіл)піридин-2-аміну дигідрохлорид + 1 МС (ЕРІ): розраховано для C13H22N4: 234,4; одержано m/z: 235,3 [M+H] . H ЯМР (CD3OD): 7,54 (д, J=6,3, 1H); 5,97 (дд, J=6,4; 2,2, 1H); 5,53 (д, J=2,1, 1H); 3,67-3,60 (квінт, J=5,5, 1H); 3,563,45 (м, 2H); 3,39-3,32 (м, 1H); 3,06 (дд, J=10,0; 4,9, 1H); 3,01 (д, J=6,9, 2H); 2,28-2,14 (м, 1H); 1,94-1,78 (м, 2H); 0,98 (д, J=6,7, 6H). Приклад 21: 4-(4-метилпіперазин-1-іл)-N-(2-метилпропіл)піридин-2-амін Спосіб A: 25 UA 106046 C2 5 10 15 20 25 30 35 40 45 50 55 (4-Йодпіридин-2-іл)-ізобутиламін Розчин 2-фтор-4-йодпіридину (2,2 г, 1,0 ммоль) у N-метилпіролідиноні (10 мл) при кімнатній температурі обробляли ізобутиламіном (2,5 мл, 2,5 ммоль) і витримували одержану суміш при температурі 100 °C протягом 6 годин. Потім суміш охолоджували до кімнатної температури, розбавляли EtOAc (50 мл) і промивали водою (2×10 мл). Об'єднані водні екстракти знову екстрагували EtOAc, і об'єднані органічні фази висушували і концентрували, одержуючи густе масло, яке при стоянні перетворювалося у тверду речовину (2,6 г, 95 %). Одержану тверду 1 речовину використовували без подальшого очищення. H ЯМР (CDCl3): 7,72 (д, J=5,3, 1H); 6,89 (дд, J=5,3; 1,4, 1H); 6,77 (д, J=1,1, 1H); 4,58 (с, 1H); 3,04 (дд, J=6,8; 5,9, 2H); 1,87 (дквінт, J=13,4; 6,7, 1H); 0,98 (д, J=6,7, 6H). 4-(4-Метилпіперазин-1-іл)-N-(2-метилпропіл)піридин-2-амін Суспензію (4-йодпіридин-2-іл)-ізобутиламіну (78 мг, 0,3 ммоль), N-метилпіперазину (0,04 мл, 0,4 ммоль), 2-дициклогексилфосфіно-2',4',6'-триізопропілбіфенілу (X-phos) (5,4 мг, 4 мольних %), Pd2dba3 (3,2 мг, 2 мольних %) у THF (1 мл) обробляли біс(триметилсиліл)амідом літію (1,0 M розчин у THF; 0,8 мл, 0,8 ммоль) і витримували одержану суміш при температурі 65 °C протягом 16 годин. Одержаний розчин охолоджували до кімнатної температури і концентрували до мінімального об'єму, а потім безпосередньо очищали (флеш-хроматографія, 0-10 % 2 M розчину NH3 у MeOH/CH2Cl2), одержуючи шуканий продукт (29 мг, 41 %). МС (ЕРІ): + 1 розраховано для C14H24N4: 248,4; одержано m/z: 249,3 [M+H] . H ЯМР (CDCl3): 7,79 (д, J=6,1, 1H); 6,12 (дд, J=6,2, 2,3, 1H); 5,69 (д, J=2,2, 1H); 4,62 (с, 1H); 3,54-3,23 (м, 4H); 3,03 (дд, J=6,7; 5,8, 2H); 2,59-2,22 (м, 7H); 1,89 (дквінт, J=13,4; 6,7, 1H); 1,19-0,78 (м, 6H). Спосіб B: 4-Бром-N-ізобутилпіридин-2-амін Розчин 4-бром-2-фторпіридину (352 мг, 2 ммоль) і 2-метилпропан-1-аміну (584 мг, 8 ммоль) у N-метил-2-піролідиноні (NMP, 10 мл) протягом 1 години перемішували при температурі 100ºC. Потім суміші давали охолонути до кімнатної температури, розбавляли її DCM (50 мл) і промивали водою (10 мл ×2). Відділений органічний шар висушували над Na 2SO4, фільтрували і концентрували. Одержаний залишок очищали колонковою хроматографією (0-20 % градієнтне елюювання сумішшю EtOAc/петролейний ефір) і одержували шуканий продукт у вигляді масла 1 (382 мг, 83 %). H ЯМР (300 МГц, CDCl3): 7,86 (д, J=5,1, 1H); 6,98 (д, J=5,4, 1H); 6,53 (с, 1H); 4,75 (с, 1H); 3,03 (дд, J=6,6; 6,0, 2H); 1,88-1,86 (м, 1H); 0,98 (с, 3H); 0,96 (с, 3H); РХ-МС: m/z=229,2; + 231,2 [M+H] . N-ізобутил-4-(4-метилпіперазин-1-іл)піридин-2-амін Суміш 4-бром-N-ізобутилпіридин-2-аміну (153 мг, 0,7 ммоль), 1-метилпіперазину (80 мг, 0,8 ммоль), Pd2(dba)3 (6,1 мг, 0,007 ммоль) і X-phos (12,7 мг, 0,028 ммоль) у безводному THF (4 мл) обробляли LiHMDS (1,0 M, 2,0 мл, 2 ммоль) в атмосфері азоту. Одержану реакційну суміш перемішували протягом 3 годин при температурі 65ºC, потім давали їй охолонути до кімнатної температури, розбавляли DCM (20 мл) і промивали водою (4 мл). Відділений органічний шар висушували над Na2SO4, фільтрували і концентрували. Одержаний залишок очищали колонковою хроматографією (0-10 % градієнтне елюювання сумішшю MeOH/DCM) і одержували 1 шуканий продукт (60 мг, 34 %). H ЯМР (300 МГц, CDCl3): 7,74 (д, J=6,6, 1H); 6,12 (д, J=6,3, 1H); 5,66 (с, 1H); 3,31 (т, J=5,4, 4H); 3,01 (д, J=6,0, 2H); 2,51 (т, J=5,4, 4H); 2,34 (с, 3H); 1,90-1,88 (м, + 1H); 1,00 (с, 3H); 0,98 (с, 3H); РХ-МС: m/z=249,1 [M+H] . N-ізобутил-4-(4-метилпіперазин-1-іл)піридин-2-аміну дигідрохлорид N-ізобутил-4-(4-метилпіперазин-1-іл)піридин-2-амін (60 мг, 0,24 ммоль) розчиняли в MeOH (1 мл) і додавали в одержаний розчин водну HCl (6 Н, 0,5 мл). Одержану реакційну суміш перемішували протягом 2 годин при температурі 30ºC. Потім суміш концентрували при 1 зниженому тиску й одержували шуканий продукт (80 мг, 93 %). H ЯМР (300 МГц, DMSO-d6): 12,59 (с, 1H); 11,49 (уш.с, 1H); 7,97 (с, 1H); 7,72 (м, 1H); 6,60 (д, J=6,9, 1H); 6,12 (с, 1H); 4,20 (д, J=14,0, 2H); 4,00 (уш.с, 2H); 3,50-3,42 (м, 2H); 3,10 (м, 4H); 2,77 (с, 3H); 1,88-1,79 (м, 1H); 0,94 (д, + J=6,6, 6H); РХ-МС, m/z=249,2 [M+H] , tR=0,1 хв.; HPLC: 96 % (214 нм), 96 % (254 нм), tR=4,5 хв. Приклад 22: 4-[(3R)-3-(метиламіно)піролідин-1-іл]-N-(2-метилпропіл)-піридин-2-амін Розчин (4-йодпіридин-2-іл)-ізобутиламіну (96 мг, 0,4 ммоль), (3R)-(метиламіно)піролідину (0,08 мл, 0,8 ммоль) і Yb(OTf)3 (215 мг, 0,4 ммоль) у DMA (2 мл) витримували протягом 2 годин при температурі 200 °C в умовах мікрохвильового нагрівання. Одержаний розчин охолоджували до кімнатної температури і концентрували до мінімального об'єму, потім безпосередньо 26 UA 106046 C2 5 10 15 20 25 30 35 40 очищали (флеш-хроматографія, 0-10 % 2 M розчину NH3 у MeOH/CH2Cl2). Одержаний таким чином матеріал (58 мг) очищали далі з використанням високоефективної рідинної хроматографії з оберненими фазами (умови Dionex), одержуючи в підсумку шукану сполуку (10 + 1 мг, 11 %). МС (ЕРІ): розраховано для C14H24N4: 248,4; одержано m/z: 249,3 [M+H] . H ЯМР (CDCl3): 7,73 (д, J=6,0, 1H); 5,86 (дд, J=6,1, 2,0, 1H); 5,38 (д, J=2,0, 1H); 4,70-4,45 (м, 1H); 3,51 (дд, J=9,8; 6,2, 1H); 3,44 (дд, J=14,7; 8,7, 1H); 3,39-3,29 (м, 2H); 3,10 (дд, J=9,7; 4,9, 1H); 3,03-2,97 (м, 2H); 2,48 (с, 3H); 2,20 (дд, J=12,6; 7,6, 1H); 1,96-1,77 (м, 2H); 0,99 (д, J=6,7, 7H). Приклад 23: 4-[(3R)-3-амінопіролідин-1-іл]-N-(2-метилпропіл)піримідин-2-амін [(3R)-1-(2-хлорпіримідин-4-іл)-піролідин-3-іл]-карбамінової кислоти трет-бутиловий ефір До кашки з 2,4-дихлорпіримідину (2,05 г, 13,7 ммоль) і N, N-діізопропілетиламіну (3,60 мл, 20,6 ммоль) у i-PrOH (12 мл) додавали (R)-3-N-Boc-амінопіролідин (2,69 г, 14,4 ммоль). Одержану суміш витримували протягом 2 годин при температурі 160 °C в умовах мікрохвильового нагрівання. Потім реакційну суміш охолоджували до кімнатної температури, концентрували й очищали сирий залишок (флеш-хроматографія, 0-50 % суміші EtOAc/гексани), одержуючи тверду речовину білого кольору (2,10 г, 51 %). МС (ЕРІ): розраховано для + 1 C13H19ClN4O2: 298,1; одержано m/z: 299,1 [M+H] . H ЯМР (CDCl3): 8,02 (д, J=6,0, 1H); 6,19 (д, J=6,0, 1H); 4,85-4,47 (м, 1H); 4,40-4,16 (м, 1H); 3,94-3,08 (м, 4H); 2,46-2,17 (м, 1H); 2,12-1,78 (м, 1H); 1,45 (с, 9H). [(3R)-1-(2-ізобутиламінопіримідин-4-іл)-піролідин-3-іл]-карбамінової кислоти трет-бутиловий ефір До кашки з трет-бутилового ефіру [(3R)-1-(2-хлорпіримідин-4-іл)-піролідин-3-іл]-карбамінової кислоти (103 мг, 0,35 ммоль) і N,N-діізопропілетиламіну (0,09 мл, 0,52 ммоль) у i-PrOH (1,5 мл) додавали ізопропіламін (30 мг, 0,41 ммоль). Одержану суміш витримували протягом 6 годин при температурі 140 °C в умовах мікрохвильового нагрівання. Одержану реакційну суміш охолоджували до кімнатної температури і концентрували. Сирий залишок очищали (флешхроматографія, 0-10 % суміші MeOH/CH2Cl2), одержуючи шуканий продукт (93 мг, 80 %). МС + 1 (ЕРІ): розраховано для C17H29N5O2: 335,2; одержано m/z: 336,3 [M+H] . H ЯМР (CDCl3): 7,83 (д, J=5,9, 1H); 5,64 (д, J=5,9, 1H); 4,98-4,80 (м, 1H); 4,78-4,61 (м, 1H); 4,38-4,20 (м, 1H); 3,79-3,26 (м, 4H); 3,23-3,11 (м, 2H); 2,32-2,09 (м, 1H); 1,99-1,77 (м, 2H); 1,45 (с, 9H); 0,95 (д, J=6,7, 6H). 4-[(3R)-3-амінопіролідин-1-іл]-N-(2-метилпропіл)піримідин-2-амін До розчину трет-бутилового ефіру [(3R)-1-(2-ізобутиламінопіримідин-4-іл)-піролідин-3-іл]карбамінової кислоти (93 мг, 0,28 ммоль) у MeOH (0,5 мл) додавали HCl (4,0 M розчин у 1,4діоксані; 1,0 мл). Реакційну суміш перемішували протягом 2 годин при кімнатній температурі, потім концентрували й очищали сирий залишок (флеш-хроматографія, 0-20 % 2 M розчину NH3 у MeOH/CH2Cl2), одержуючи шуканий продукт (65 мг, 100 %). МС (ЕРІ): розраховано для + 1 C12H21N5: 235,2; одержано m/z: 236,2 [M+H] . H ЯМР (CDCl3): 7,82 (д, J=5,9, 1H); 5,65 (д, J=5,9, 1H); 4,87 (с, 1H); 3,75-3,51 (м, 3H); 3,48-3,38 (м, 1H); 3,20 (дд, J=6,7; 6,1, 3H); 2,16 (д, J=6,3, 1H); 1,87 (дт, J=13,4; 6,7, 1H); 1,81-1,71 (м, 1H); 1,47 (с, 2H); 0,95 (д, J=6,7, 6H). Сполуки в прикладах 24-30 одержували за допомогою способів, аналогічних описаним для прикладу 23. Приклад 24: 4-[(3R)-3-амінопіролідин-1-іл]-N-(циклопропілметил)-піримідин-2-амін + 45 1 МС (ЕРІ): розраховано для C12H19N5: 233,2; одержано m/z: 234,2 [M+H] . H ЯМР (CDCl3): 7,83 (д, J=5,9, 1H); 5,66 (д, J=5,9, 1H); 4,89 (с, 1H); 3,76-3,37 (м, 4H); 3,23 (дд, J=7,0; 5,6, 2H); 3,20-3,11 (м, 1H); 2,21-2,10 (м, 1H); 1,82-1,70 (м, 1H); 1,40 (с, 2H); 1,16-0,97 (м, 1H); 0,59-0,39 (м, 2H); 0,32-0,14 (м, 2H). 27 UA 106046 C2 Приклад 25: 4-[(3R)-3-амінопіролідин-1-іл]-N-циклопентилпіримідин-2-амін + + 25 30 1 + 20 1 + 15 1 + 10 1 + 5 1 1 МС (ЕРІ): розраховано для C13H21N5: 247,2; одержано m/z: 248,2 [M+H] . H ЯМР (CDCl3): 7,83 (д, J=5,9, 1H); 5,65 (д, J=5,9, 1H); 4,74 (д, J=6,6, 1H); 4,33-4,11 (м, 1H); 3,80-2,93 (м, 5H); 2,22-2,10 (м, 1H); 2,08-1,96 (м, 2H); 1,82-1,54 (м, 5H); 1,51-1,17 (м, 4H). Приклад 26: 4-[(3R)-3-амінопіролідин-1-іл]-N-(2,2-диметилпропіл)-піримідин-2-амін МС (ЕРІ): розраховано для C13H23N5: 249,2; одержано m/z: 250,2 [M+H] . H ЯМР (CDCl3): 7,82 (д, J=5,9, 1H); 5,64 (д, J=5,9, 1H); 4,96-4,66 (м, 1H); 3,80-3,33 (м, 4H); 3,23 (д, J=6,4, 2H); 3,20-3,08 (м, 1H); 2,27-2,04 (м, J=6,2, 1H); 1,85-1,63 (м, 1H); 1,26 (с, 2H); 0,95 (с, 9H). Приклад 27: 1-({4-[(3R)-3-амінопіролідин-1-іл]піримідин-2-іл}аміно)-2-метилпропан-2-ол МС (ЕРІ): розраховано для C12H21N5O: 251,2; одержано m/z: 252,2 [M+H] . H ЯМР (CDCl3): 7,79 (д, J=6,0, 1H); 5,93 (уш.с, 1H); 5,69 (д, J=6,0, 1H); 5,23 (с, 1H); 3,77-3,30 (м, 6H); 3,28-2,93 (м, 1H); 2,24-2,05 (м, 1H); 1,86-1,71 (м, 1H); 1,66-1,33 (м, 2H); 1,23 (с, 6H). Приклад 28: 4-[(3R)-3-амінопіролідин-1-іл]-N-циклобутилпіримідин-2-амін МС (ЕРІ): розраховано для C12H19N5: 233,2; одержано m/z: 234,2 [M+H] . H ЯМР (CDCl3): 7,82 (д, J=5,9, 1H); 5,65 (д, J=5,9, 1H); 5,00-4,83 (м, 1H); 4,51-4,35 (м, 1H); 3,76-3,32 (м, 4H); 3,252,96 (м, 1H); 2,47-2,30 (м, 2H); 2,23-2,06 (м, 1H); 1,94-1,60 (м, 5H); 1,57-1,31 (м, 2H). Приклад 29: 4-[(3R)-3-амінопіролідин-1-іл]-N-[(3R)-тетрагідрофуран-3-іл]піримідин-2-амін МС (ЕРІ): розраховано для C12H19N5O: 249,2; одержано m/z: 250,2 [M+H] . H ЯМР (CDCl3): 7,83 (д, J=5,9, 1H); 5,69 (д, J=5,9, 1H); 4,98-4,84 (м, 1H); 4,61-4,47 (м, 1H); 4,05-3,88 (м, 2H); 3,883,77 (м, 1H); 3,73-3,32 (м, 5H); 3,26-3,02 (м, 1H); 2,35-2,22 (м, 1H); 2,20-2,10 (м, 1H); 1,92-1,69 (м, 2H); 1,54-1,16 (м, 2H). Приклад 30: 4-[(3R)-3-амінопіролідин-1-іл]-N-(тетрагідро-2H-піран-4-іл)піримідин-2-амін МС (ЕРІ): розраховано для C13H21N5O: 263,2; одержано m/z: 264,2 [M+H] . H ЯМР (CDCl3): 7,83 (д, J=5,9, 1H); 5,68 (д, J=5,9, 1H); 4,71 (д, J=7,5, 1H); 4,09-3,84 (м, 3H); 3,75-3,34 (м, 6H); 3,26-2,99 (м, 1H); 2,24-2,09 (м, 1H); 2,03 (д, J=12,3, 2H); 1,86-1,69 (м, 1H); 1,60-1,19 (м, 4H). Приклад 31: ізобутил-[4-(4-метилпіперазин-1-іл)-піримідин-2-іл]-амін 28
ДивитисяДодаткова інформація
Назва патенту англійськоюDiamino-pyridine, pyrimidine, and pyridazine modulators of the histamine h4 receptor
Автори російськоюCai, Hui, Chavez, Frank, Dunford, Paul, J., Greenspan, Andrew, J., Meduna, Steven, P/, Quiroz, Jorge, A., Savall, Brad, M., Tays, Kevin, L., Thurmond, Robin, L., Wei, Jianmei, Wolin, Ronald, L., Zhang, Xiaohu
МПК / Мітки
МПК: A01N 43/58
Мітки: модулятори, піридазинові, гістамінового, рецептора, діамінопіридинові, піримідинові
Код посилання
<a href="https://ua.patents.su/126-106046-diaminopiridinovi-pirimidinovi-i-piridazinovi-modulyatori-gistaminovogo-receptora-h4.html" target="_blank" rel="follow" title="База патентів України">Діамінопіридинові, піримідинові і піридазинові модулятори гістамінового рецептора h4</a>
Попередній патент: Трициклічні сполуки
Наступний патент: Спосіб отримання високої щільності життєздатних клітин в культурі клітин ссавців
Випадковий патент: Енергозберігаючий спосіб виробництва спирту ректифікованого високоякісного












