Похідні сульфонових кислот, фармацевтична композиція та спосіб лікування запалень та інших розладів імунної системи
Формула / Реферат
1. Сполука формули
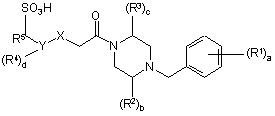
або її фармацевтично прийнятні солі та проліки; в якій
a означає 0-5,
b означає 0-2,
c означає 0-2,
d означає 0-4,
Х означає -O-, -S-, -CH2-, -NR6-,
Y означає (C6-C10)арил або (C2-C9)гетероарил,
кожний R1 незалежно вибраний з групи, що складається з: H-, HO-, галогену, (C1-С8)алкілу, необов‘язково заміщеного 1-3 атомами фтору, (C1-C8)алкіл-O-, де алкільна група необов‘язково заміщена 1-3 атомами фтору, HO-(C1-C8)алкілу, NC-, H2N-, H2N-(C1-C8)алкілу, HO-(C=O)-, (C1-C8)алкіл-(C=O)-, (C1-C8)алкіл-(C=O)-(C1-C8)алкілу, H2N-(C=O)-, H2N-(C=O)-(C1-C8)алкілу;
кожний R2 та R3 незалежно вибрані з групи, що складається з: H-, оксо, (C1-C8)алкілу, необов‘язково заміщеного 1-3 атомами фтору, (C1-C8)алкілу, (C6-C10)арилу, (C6-C10)арил-(C1-C8)алкілу, HO-(C1-C8)алкілу, (C1-C8)алкіл-O-(C1-C8)алкілу, H2N-(C1-C8)алкілу, (C1-C8)алкіл-NH-(C1-C8)алкілу, [(C1-C8)алкіл]2N-(C1-C8)алкілу, (C2-C9)гетероцикліл-(C1-C8)алкілу, (C1-C8)алкіл-(C=O)-NH-(C1-C8)алкілу, (C1-C8)алкіл-O-(C=O)-NH-(C1-C8)алкілу, H2N-(C=O)-NH-(C1-C8)алкілу, (C1-C8)алкіл-SO2-NH-(C1-C8)алкілу, (C2-C9)гетероарил-(C1-C8)алкілу, H2N-(C=O)-, H2N-(C=O)-(C1-C8)алкілу;
кожний R4 незалежно вибраний з групи, що складається з: H-, HO-, галогену, NC, HO-(C=O)-, H2N-, (C1-C8)алкіл-NH-, [(C1-C8)алкіл]2N-, (C1-C8)алкілу, необов‘язково заміщеного 1-3 атомами фтору, (C1-C8)алкіл-O-, де алкільна група необов‘язково заміщена 1-3 атомами фтору, HO-(C1-C8)алкілу, (C1-C8)алкіл-O-(C1-C8)алкілу, H2N-(C1-C8)алкілу, (C1-C8)алкіл-NH-(C1-C8)алкілу, [(C1-C8)алкіл]2N-(C1-C8)алкілу, (C1-C8)алкіл-(С=O)- (C1-C8)алкіл-(C=O)-(C1-C8)алкілу, (C6-C10)арилу, (C2-C9)гетероарилу, (C6-C10)арилoкси, H2N-(C=O)-, H2N-(C=O)-(C1-C8)алкілу, (C1-C8)алкіл-NH-(C=O)-, (C1-C8)алкіл-NH-(C=O)-(C1-C8)алкіл-, [(C1-C8)алкіл]2N-(C=O)-, [(C1-C8)алкіл]2-N-(C=O)-(C1-C8)алкілу, (C3-C8)циклоалкілу, (C1-C8)алкіл-SO2-, NC-(C1-C8)алкілу, (C1-C8)алкіл-(C=O)-NH-, H2N-(C=O)-NH-, H2N-(C=O)-NH-(C1-C8)алкілу;
R5 означає (C1-C8)алкіл-.
2. Сполука за п. 1, в якій R1 вибраний з групи, що складається з: H-, HO-, галогену, NC-(C1-С8)алкілу, необов‘язково заміщеного 1-3 атомами фтору, та (C1-C8)алкіл-O-, в якому алкільна група необов‘язково заміщена 1-3 атомами фтору.
3. Сполука за п. 1 або 2, в якій кожний R2 та R3 незалежно вибраний з групи, що складається з: H-, (C1-С8)алкілу, (С3-С8)циклоалкілу, (С3-С8)циклоалкілу-(C1-С8)алкілу, (C6-C10)арилу, (C6-C10)арил-(C1-C8)алкілу, HO-(C1-C8)алкілу, H2N-(C1-C8)алкілу, (C2-C9)гетероарил-(C1-C8)алкілу, (C1-C8)алкіл-O-(C=O)-NH-(C1-C8)алкілу, H2N-(C=O)-NH-(C1-С8)алкілу, (C1-C8)алкіл-SO2-NH-(C1-C8)алкілу, (C2-C9)гетероарил-(C1-C8)алкілу, H2N-(C=O), H2N-(C=O)-(C1-С8)алкілу.
4. Сполука за п. 1 або 2, в якій Х означає -О- і Y означає (C6-C10)арил або (C2-C9)гетероарил.
5. Сполука за п. 1, 2 або 4, в якій R4 вибраний з групи, що складається з: H-, HO-, NC, (C1-С8)алкілу, (C1-С8)алкіл-О-, (C1-С8)алкіл-(C=O)- або галогену.
6. Сполука за п. 5, в якій, коли Y означає (C6-C10)арил, R4 вибраний з групи, що складається з: H-, HO-, NC, (C1-С8)алкілу, де алкільна група необов‘язково заміщена 1-3 атомами фтору, (C1-С8)алкіл-О-, де алкільна група необов‘язково заміщена 1-3 атомами фтору, (C1-С8)алкіл-(C=O) або галогену, а коли Y означає (C2-C9)гетероарил, R4 вибраний з групи, що складається з: H-, HO-, NC, (C1-С8)алкілу, де алкільна група необов‘язково заміщена 1-3 атомами фтору, (C1-С8)алкіл-О-, де алкільна група необов‘язково заміщена 1-3 атомами фтору, (C1-С8)алкіл-(C=O) або галогену.
7. Сполука за п. 6, в якій R5 означає С1-С3алкіл, якщо Y означає (C6-C10)арил, та в якій R5 означає С1-С3алкіл, якщо Y означає (C2-C9)гетероарил.
8. Сполука за п. 1, в якій згадана сполука вибрана з групи, що складається з:
(5-бром-2-{2-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота;
(5-хлор-2-{2-[4-(4-хлорбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота;
2-(5-бром-2-{2-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)етансульфокислота;
2-(5-хлор-2-{2-[4-(4-хлорбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)етансульфокислота;
(4-бром-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота;
(3-хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота;
(5-бром-2-{2-[4-(4-хлорбензил)-2R,2S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)метансульфокислота;
(5-хлор-2-{2-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)метансульфокислота;
(5-бром-2-{2-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)метансульфокислота;
(5-хлор-2-{2-[4-(3,4-дифторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота;
(5-бром-2-{2-[4-(3,4-дифторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота;
(5-хлор-2-{2-[4-(4-хлорбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота;
(5-бром-2-{2-[4-(4-хлорбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота;
(5-хлор-2-{2-[4-(3,4-дифторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота;
(5-бром-2-{2-[4-(3,4-дифторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота;
2-(5-хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)етансульфокислота;
(5-бром-2-{2-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)етансульфокислота;
(4-хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота;
(3-бром-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота;
(2-хлор-6-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота;
(5-бром-2-{2-[2R-етил-4-(4-фторбензил)-5S-метилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота;
2-(5-бром-2-{2-(4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)етансульфокислота;
(5-хлор-2-{2-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота;
2-(5-бром-2-{2-(4-(4-хлорбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)етансульфокислота;
2-(5-хлор-2-{2-[4-(3,4-дифторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)етансульфокислота;
2-(5-хлор-2-{2-(4-(4-хлорбензил)-2R-метилпіперазин-1-іл)-2-оксоетокси}феніл)етансульфокислота;
2-(5-бром-2-{2-[4-(4-хлорбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)етансульфокислота;
(5-хлор-2-{2-(4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл)-2-оксоетокси}феніл)метансульфокислота;
2-(5-хлор-2-{2-(4-(3,4-дифторбензил)-2R-метилпіперазин-1-іл)-2-оксоетокси}феніл)етансульфокислота;
(5-бром-2-{2-(4-(4-хлорбензил)-2R-метилпіперазин-1-іл)-2-оксоетокси}піридин-3-іл)етансульфокислота;
3-(5-бром-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)пропан-1-сульфонова кислота;
3-(5-хлор-2-{2-(4-(4-фторбензил)-2R-метилпіперазин-1-іл)-2-оксоетокси}феніл)пропан-1-сульфонова кислота;
3-(5-бром-2-{2-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)пропан-1-сульфонова кислота;
(2-бром-6-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота;
(5-хлор-2-{2-[2E-етил-4-(4-фторбензил)-5S-метилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота;
3-(5-хлор-2-{2-[4-(4-хлорбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)пропан-1-сульфонова кислота;
2-(5-хлор-2-{2-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)етансульфокислота;
3-(5-бром-2-{2-[4-(4-хлорбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)пропан-1-сульфонова кислота;
2-(5-бром-2-{2-[4-(3,4-дифторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)етансульфокислота;
3-(5-хлор-2-{2-[4-(3,4-дифторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)пропан-1-сульфонова кислота;
3-{5-хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)пропан-1-сульфонова кислота;
(5-бром-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)метансульфокислота;
3-(5-хлор-2-{2-[4-(4-хлорбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)пропан-1-сульфонова кислота;
(5-бром-2-{2-[4-(3,4-дифторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)етансульфокислота;
(5-бром-2-{2-[2R-етил-4-(4-фторбензил)-5S-метилпіперазин-1-іл]-2-оксоетокси}феніл)етансульфокислота;
3-(5-бром-2-{2-[4-(4-хлорбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)пропан-1-сульфонова кислота;
3-(5-хлор-2-{2-[4-{3,4-дифторбензил}-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)пропан-1-сульфонова кислота;
(5-бром-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)етансульфокислота;
{3-(5-бром-2-{2-[4-(3,4-дифторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)пропан-1-сульфонова кислота;
(2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}-5-метилфеніл)метансульфокислота;
2-(5-бром-2-{2-[4-(3,4-дифторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)етансульфокислота;
3-{5-хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)пропан-1-сульфонова кислота;
(5-хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)метансульфокислота;
(5-бром-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота;
(5-хлор-2-{2-[4-(3,4-дифторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)метансульфокислота;
(5-хлор-2-{2-[4-(4-хлорбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)метансульфокислота;
(5-бром-2-{2-[4-(4-хлорбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)метансульфокислота;
(5-хлор-2-{2-[4-(3,4-дифторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)метансульфокислота;
(5-бром-2-{2-[4-(3,4-дифторбензил)-2R-мeтилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)метансульфокислота;
(5-хлор-2-{2-[4-(4-хлорбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)метансульфокислота;
(5-бром-2-{2-[4-(4-хлорбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)метансульфокислота;
2-(5-хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)етансульфокислота;
(5-хлор-2-{2-[4-(3,4-дифторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)етансульфокислота;
(5-бром-2-{2-[4-(3,4-дифторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)етансульфокислота;
(5-хлор-2-{2-[4-(4-хлорбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)етансульфокислота;
(5-бром-2-{2-[4-(4-хлорбензил)-2R,5S-диметилпіперазин-1-іл)-2-оксоетокси}піридин-3-іл)етансульфокислота;
3-(5-бром-2-{2-[4-(3,4-дифторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)пропан-1-сульфонова кислота;
(5-хлор-2-{2-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)етансульфокислота;
(5-бром-2-{2-[4-(3,4-дифторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)метансульфокислота;
(5-хлор-2-{2-[4-(4-хлорбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)етансульфокислота;
3-(5-хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)пропан-1-сульфонова кислота;
2-(5-хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)пропан-2-сульфонова кислота;
2-(5-бром-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)пропан-2-сульфонова кислота;
2-(5-хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)-2-метилпропан-1-сульфонова кислота;
2-(5-бром-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)-2-метилпропан-1-сульфонова кислота;
1-(5-хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)-2-метилпропан-2-сульфонова кислота;
(2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}-5-трифторметилфеніл)метансульфокислота;
(2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}-5-трифторзаміщений метилфеніл)метансульфокислота;
(2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}-5-метилфеніл)метансульфокислота;
(5-хлор-2-{2-[2R-етил-4-(4-фторбензил)-5S-метилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота;
(5-бром-2-{2-[2R-етил-4-(4-фторбензил)-5S-метилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота;
(5-хлор-2-{2-[2R-етил-4-(4-фторбензил)-5S-метилпіперазин-1-іл]-2-оксоетокси}феніл)етансульфокислота;
(5-хлор-2-{2-[2R-етил-4-(4-фторбензил)піперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота;
(5-бром-2-{2-[2R-етил-4-(4-фторбензил)піперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота;
(5-хлор-2-{2-[2R-етил-4-(4-фторбензил)піперазин-1-іл]-2-оксоетокси}феніл)етансульфокислота;
(5-бром-2-{2-[2R-етил-4-(4-фторбензил)піперазин-1-іл]-2-оксоетокси}феніл)етансульфокислота;
1-(5-бром-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)-2-метилпропан-2-сульфонова кислота;
2-(5-хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетиламіно}феніл)етансульфокислота і
(5-хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетиламіно}феніл)метансульфокислота.
9. Фармацевтична композиція для лікування розладу або стану, вибраного з аутоімунних хвороб, туберкульозу шкіри, гострих і хронічних запалень, алергії, інфікування, пов’язаного з запаленням, вірусного і хронічного бронхіту, ксеногенної трансплантації, відторгнення трансплантованої тканини, атеросклерозу, рестенозу, ВІЛ інфікування і грануломатозних хвороб у ссавців, яка містить кількість сполуки за п. 1, що є ефективною для лікування або запобігання таким розладам або станам, та фармацевтично прийнятний носій.
10. Фармацевтична композиція для лікування розладу або стану, які можна лікувати шляхом інгібування зв‘язування МІР-1![]() та/або RANTES з рецептором CCR1 у ссавців, яка містить кількість сполуки за п. 1 або її фармацевтично прийнятну сіль, що є ефективною для лікування або запобігання таким розладам або станам, та фармацевтично прийнятний носій.
та/або RANTES з рецептором CCR1 у ссавців, яка містить кількість сполуки за п. 1 або її фармацевтично прийнятну сіль, що є ефективною для лікування або запобігання таким розладам або станам, та фармацевтично прийнятний носій.
11. Спосіб лікування розладу або стану, вибраного з аутоімунних хвороб, туберкульозу шкіри, гострих і хронічних запалень, алергії, інфікування пов’язаного з запаленням, вірусного і хронічного бронхіту, ксеногенної трансплантації, відторгнення трансплантованої тканини, атеросклерозу, рестенозу, ВІЛ інфікування і грануломатозних хвороб у ссавців, при якому здійснюють введення ссавцеві, який потребує такого лікування або запобігання, сполуки за п. 1 або її фармацевтично прийнятної солі, у кількості, що є ефективною для лікування або запобігання таким розладам або станам.
12. Спосіб лікування або запобігання розладу або стану, який можна лікувати або запобігти шляхом антагоністичної дії на ССR1 рецептор у ссавців, при якому здійснюють введення ссавцеві, який потребує такого лікування або запобігання, сполуки за п. 1 або її фармацевтично прийнятної солі, у кількості, що є ефективною для лікування або запобігання таким розладам або станам.
13. Фармацевтична композиція для лікування розладу або стану, що можна лікувати або попереджувати шляхом антагоністичної дії на ССR1 рецептор у ссавців, яка містить сполуку за п. 1 або її фармацевтично прийнятну сіль, у кількості, яка є ефективною для антагоністичної дії на рецептор CCR1, та фармацевтично прийнятний носій.
Текст
Даний винахід стосується нових похідних сульфонової кислоти, способів їх використання і композицій, що їх містять. Сполуки винаходу є ефективними і селективними інгібіторами МІР-1a (CCL3), що зв'язані з їх рецептором CCR1, виявленим в запальних та імуномодулюючих клітинах (переважно лейкоцитах і лімфоцитах). CCR1 рецептор також інколи називають рецептором CCCКR1. Ці сполуки також інгібують індукований МІР-1a (і пов'язаними з ним хемокінами, що, як показано взаємодіють з CCR1 (наприклад, RANTES (CCL5), МСР-2 (CCL8), МСР-3 (CCL7), НСС-1 (CCL14) і НСС-2 (CCL15))) хемотаксис клітин ТНР-1 і лейкоцитів людини і є потенційно корисними для лікування і запобігання аутоімунних хвороб, ревматичного артриту, початкових стадій діабету І тип у, туберкульозу шкіри, запалення кишечнику, невриту зорового нерву, псоріазу, розсіяного склерозу, ревматоїдної поліміалгії, увеїту, васкуліту, гострих і хронічних запалень, остеоартриту, синдрому дихальної недостатності у дорослих, синдрому дихальної недостатності у дітей, ішемічного реперфузійного ураження, гломерунефриту, алергії, астми, атопічного дерматиту, інфікування пов'язаного з запаленням, вірусних запалень, грипу, гепатиту, хвороби Гійєна-Барре, хронічного бронхіту, ксеногенної трансплантації, хронічного та гострого відторгнення трансплантованої тканини, хронічного і гострого відторгнення трансплантованого органу, атеросклерозу, рестенозу (включаючи, але не обмежуючись ним, рестеноз, викликаний імплантацією балону та/або стенту), ВІЛ інфікування (використання ко-рецепторів) і грануломатозних хвороб (включаючи саркоїдоз, лепру та туберкульоз), а також ускладнень, що пов'язані з певними раковими захворюваннями, такими як, розсіяна мієлома. Сполуки цієї серії можуть також бути використані для запобігання розвитку метастазів раку. Сполуки цієї серії можуть також обмежувати утворення цитокинів в сайтах запалення, включаючи, але не обмежуючись ними, TNF і IL-1, як наслідок зменшення інфільтрації клітин, що може бути корисним при хворобах, пов'язаних з TNF і IL-1, включаючи застійну серцеву недостатність, легеневу емфізему або задишку, пов'язану з нею, емфізему, ВІЛ-1, ВІЛ-2, ВІЛ-3, цитомегаловірус, аденовіруси, віруси герпесу (Herpes zoster та Herpes simplex). Вони також можуть бути корисними при ускладненнях, пов'язаних з інфікуванням, яке призводить до утворення шкідливих запальних цитокинів, таких як TNF, наприклад, грибковий менінгіт, ушкодження з'єднувальної тканини, гіперплазія, утворення паннуса, і резорбція кісток, псоріатичний артрит, печінкова недостатність, бактеріальний менінгіт, синдром Кавасакі, інфаркт міокарду, гостра печінкова недостатність, хвороба Ліма, септичний шок, рак, травмування і малярія тощо. МІР-1a і RANTES є розчинними пептидами (хемокінами), що викликають хемотаксис, які продукуються запаленими клітинами, а саме лімфоцитами CD8+, поліморфно-ядерними лейкоцитами (PMN) та макрофагами J.Biol Chem.. 270 (30) 29671-29675 (1995). Ці хемокіни спричиняють міграцію і активізацію основних клітин запалення та імуномодулюючих клітин. Підвищений рівень хемокінів був виявлений в синовіальній рідині пацієнта, хворого на ревматоїдний артрит, хронічних і відторгнених тканинах пацієнтів з трансплантантами та в носових секретах пацієнтів, що хворіють на алергічний риніт, після контакту з алергеном (Teran, et al. J. Immunol 1806-1812 (1996), and Kuna etal. J. Allergy Clin. Immunol 321 (1994)). Антитіла, що перешкоджають взаємодії хемокінів з рецепторами, шляхом нейтралізації МІР-1a або руйнування гену, представили прямий доказ ролі МІР-1a і RANTES під час хвороби шляхом поповнення моноцитів і лейкоцитів CD8+ (Smith et al. .J. Immunol. 153. 4704 (1994) and Cook et al. Science. 269. 1583 (1995)). Разом ці дані вказують на те, що антагоністи рецепторів CCR1 були би б ефективним засобом лікування деяких імунних хвороб. Сполуки, описані в цьому винаході є ефективними та вибірковими антагоністами рецептора CCR1. Сполука формули або фармацевтично прийнятні солі і її проліки; в яких а означає 0-5, b означає 0-2, с означає 0-2, d означає 0-4 X означає -Ο-, -S-, -CH 2-, -NR6Y означає (С6-С10)арил, або (С2-С9)гетероарил кожний R1 незалежно вибраний з групи, що складається з: Н-, НО-, галогену, (C1-С8)алкілу, необов'язково заміщеного 1-3 атомами фтору, (C1-С8)алкіл-О-, де алкільна група необов'язково заміщена 13 атомами фтору, НО-(C1-С8)алкілу, NC-, H 2N-, H2N-(C1-С8)алкілу, Н О-(С=О )-, (C1-С 8)алкіл-(С=О )-, (С1С8)алкіл-(С= О)-(С1-С8)алкілу, H2N-(C=O)-, H 2N-(C=O)-(C1-С8)алкілу; кожний R2 і R3 незалежно вибраний з групи, що складається з: Н-, оксо, (C1-С8)алкілу, необов'язково заміщеного 1-3 атомами фтору, (С1-С8)алкілу, (С6-С 10)арилу, (С6-С10)арил-(С1-С8)алкілу, НО-(С1-С8)алкілу, (C1-С8)алкіл-О-(С1-С8)алкілу, Н2N-(C1-С8)алкілу, (C1-С8)алкіл-NН-(C1-С8)алкілу, [(С1-С8)алкіл]2N-(C1-С8)алкілу, (С2-С9)гетероцикліл-(C1-С8)алкілу, (С1-С8)алкіл-(С О)-NН-(C1-С8)алкілу, = (С1-С8)алкіл-О-(С О)-NН-(С1= С8)алкілу, Н2N-(С= О)-NН-(С1-С8)алкілу, (C1-С8)алкіл-SО2-NН-(С1-С8)алкілу, (С2-С9)гетероарил-(C1-С8)алкілу, H2N-(C=O)-, Н2N-(С=О)-(С1-С8)алкілу; кожний R4 незалежно вибраний з групи, що складається з: Н-, НО-, галогену, NC, НО-(С=О)-, H2N-, (С1С8)алкіл-NН-, [(С1-С8)алкіл]2N-, (C1-С8)алкілу, необов'язково заміщеного 1-3 атомами фтору, (C1-С8)алкіл-О-, де алкільна група необов'язково заміщена 1-3 атомами фтору, НО-(C1-С8)алкілу, (C1-С8)алкіл-О-(С1С8)алкілу, H2N-(C1-С8)алкілу, (С1-С8)алкіл-NH-(C1-С8)алкілу, [(С1-С8)алкіл]2N-(C1-С8)алкілу, (C1-С8)алкіл(C=О)-, (С1-С8)алкіл-(С= О)-(C1-С8)алкілу, (С6-С10)арилу, (С2-С 9)гетероарилу, (С6-С10)арилокси, -SO2NH2, NHSO2-(C1-C8)алкілу, H2N-(C=O)-, Н2N-(С= О)-(С1-С8)алкілу, (C1-С8)алкіл-NН-(С=О )-, (С1-С8)алкіл-NН-(С= О)(С1-С8)алкіл-, [(С1-С8)алкіл]2N-(С=О)-, [(С1-С8)алкіл]2-N-(С=О)-(C1-С8)алкілу, (С3-С8)циклоалкілу, (С1-С8)алкілSО2-, NС-(C1-С8)алкілу, (С1-С 8)алкіл-(C=O)-NH-, H 2N-(C=O)-NH-, H2N-(C=O)-NH-(C 1-С8)anKmy; R5 означає (C1-С8)алкіл-. Даний винахід також стосується фармацевтичноприйнятних кислотно-адитивних солей сполук формули І. Кислоти, що використовуються для одержання фармацевтичноприйнятних кислотно-адитивних солей вищезазначених основних сполук цього винаходу є такими, що утворюють нетоксичні кислотно-адитивні солі, а саме, солі, що включають, але не обмежуються ними, фармакологічноприйнятні аніони, такі як гідрохлорид, гідробромід, гідройодид, нітрат, сульфат, бісульфа т, фосфат, кислий фосфат, ацетат, лактат, цитрат, кислий цитрат, тартрат, бітартрат, сукцинат, малеат, фумарат, глюконат, сахарат, бензоат, метансульфонат, етансульфонат, бензолсульфонат, п-толуолсульфонат і памоат (а саме, солі 1,1'метилен-біс-(2-гідрокси-3-нафтоату)). Винахід також стосується основно-адитивних солей формули І. Хімічні основи, які можуть бути використані як реагенти для одержання фармацевтичноприйнятних основно-адитивних солей тих сполук формули І, що є кислотними за природою, являються такими, що утворюють нетоксичні основні солі з такими сполуками. Такі нетоксичні основні солі включають, але не обмежуються ними, солі, що походять від таких фармакологічноприйнятних катіонів, як катіони лужних металів (наприклад, калій і натрій) і катіони лужноземельних металів (наприклад, кальцій і магній), амоній або водорозчинні аміно-адитивні солі такі як N-метилглюкамін-(меглумін), (нижчий алканол)амонієві та інші основні солі фармацевтичноприйнятних органічних амінів. Сполуки цього винаходу можуть містити олефіноподібні подвійні зв'язки. У разі присутності таких зв'язків, сполуки винаходу існують у вигляді цис- та транс-конфігураційних ізомерів та їх суміші. Даний винахід також стосується сполук формули І, в якій деякі з воднів можуть бути необов'язково заміщені дейтерієм. Якщо вони не вказано інакше, зазначені тут алкільні групи, можуть бути нерозгалуженими або розгалуженими, а також циклічними (наприклад, циклопропіл, циклобутил, циклогексил, циклогептил) або біциклічними (наприклад, норбоманіл, біцикло[3.2.1]октан) або містити циклічні групи. Вони також можуть не містити або містити до двох ненасичених зв'язків і можуть бути необов'язково заміщені 1-3 замісниками, незалежно вибраними з групи, що складається з галогену, HO-, NC-, Н2Ν-, НО-(С=О)-, включаючи, але не обмежуючись ними. Якщо не вказано нічого іншого, галоген включає фтор, хлор, бром і йод. (С2-С9)гетероцикліл- в даному контексті включає, але не обмежується ними, піролідиніл, тетрагідрофураніл, дигідрофураніл, тетрагідропіраніл, піраніл, тіопіраніл, азиридиніл, оксираніл, метилендіоксил, хроменил, барбітурил, ізоксазолідиніл,1,3-оксазолідин-3-іл, ізотіазолідиніл, 1,3-тіазолідин3-іл, 1,2-піразолідин-2-іл, 1,3-піразолідин-1-ілпіперидиніл, тіоморфолініл, 1,2-тетрагідротіазин-2-іл, 1,3тетрагідротіазин-3-іл, тетрагідротіадіазинілморфолініл, 1,2-тетрагідродіазин-2-іл, 1,3-тетрагідродіазин-1-іл, тетрагідроацепініл, піперазиніл і хроманіл. Зазначене (С2-С9)кільце приєднується через атом вуглецю або азоту. (С2-С9)гетероарил в даному контексті включає, але не обмежується ними, фурил, тієніл, тіазоліл, піразоліл, ізотіазоліл, оксазоліл, ізоксазоліл, піроліл, триазоліл, тетразоліл, імідазоліл, 1,3,5-оксадіазоліл, 1,2,4-оксадіазоліл, 1,2,3-оксадіазоліл, 1,3,5-тіадіазоліл, 1,2,3-тіадіазоліл, 1,2,4-тіадіазоліл, піридил, піримідил, піразиніл, піридазиніл, 1,2,4-триазиніл, 1,2,3-триазиніл, 1,3,5-триазиніл, піразоло[3,4-b]піридиніл, цинолініл, птеридиніл, пуриніл, 6,7-дигідро-5Н-[1]піриндиніл, бензо[b]тіофеніл, 5,6,7,8-тетрагідрохінолін-3-іл, бензоксазоліл, бензотіазоліл, бензізотіазоліл, бензізоксазоліл, бензімідазоліл, тіанафтеніл, ізотіанафтеніл, бензофураніл, ізобензофураніл, ізоіндоліл, індоліл, індолізиніл, індазоліл, ізохіноліл, хіноліл, фталазиніл, хіноксалініл, хіназолініл і бензоксазиніл, які можуть бути необов'язково заміщені 1-3 замісниками, що незалежно вибрані з групи, що складається з: Н, НО, галогену, (C1-С8)алкілу, необов'язково заміщеного 1-3 атомами фтору, (C1-С8)алкіл-О, де алкільна група необов'язково заміщена 1-3 атомами фтору, НО-(С1С8)алкілу, NC-, H2N-, Н2N-(С1-С8)алкілу, НО-(С=О )-, (C1-С8)алкіл-(С=О )-, (С1-С8)алкіл-(С= О)-(С1-С8)алкілу, H2N-(C=O)-, Н2N-(С=О)-(С1-С8)алкіл-, H2NSO2-, (C1-C8)алкіл-SO2-NH-. Арил в даному контексті стосується фенілу або нафтилу, що може бути заміщений 1-3 замісниками, що незалежно вибрані з групи, яка складається Н-, НО-, галогену, (C1-С8)алкілу, необов'язково заміщеного 1-3 атомами фтору, (C1-С8)алкіл-О-, де алкільна група необов'язково заміщена 1-3 атомами фтору, НО-(С1С8)алкілу, NC-, H2N-, H2N-(C1-С8)алкілу, НО-(С=О )-, (С1-С8)алкіл-(С=О )-, (С1-С8)алкіл-(С= О)-(C1-С8)алкілу, H2N-(C=O)-, Н2N-(С=О)-(С1-С8)алкілу, H2NSO2-, (C1-С8)алкіл-SO2-NH-; Сполуки цього винаходу включають всі конформаційні ізомери (наприклад, цис- і транс-ізомери) і всі оптичні ізомери сполук формули І (наприклад, енантіомери і діастереомери) а також рацемічні, діастереомерні та інші суміші таких ізомерів. Прикладами переважно використовуваних сполук формули І є наступні: (5-Бром-2-{2-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)-метансульфокислота; (5-Хлор-2-{2-[4-(4-хлорбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}-феніл)метансульфокислота; 2-(5-Бром-2-{2-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}-феніл)етансульфокислота; 2-(5-Хлор-2-{2-[4-(4-хлорбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)етансульфокислота; (4-Бром-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота; (3-Хлор-2-{2-[4-(4-хлорбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}-феніл)метансульфокислота; (5-Бром-2-{2-[4-(4-хлорбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}-піридин-3іл)метансульфокислота; (5-Хлор-2-{2-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}-піридин-3іл)метансульфокислота; (5-Бром-2-{2-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}-піридин-3іл)метансульфокислота; (5-Хлор-2-{2-[4-(3,4-дифторбензил)-2R,5S-диметилпіперазин-1-іл]-2 оксоетокси}феніл)метансульфокислота; (5-Бром-2-{2-[4-(3,4-дифторбензил)-2R,5S-диметилпіперазин-1-іл]-2оксоетокси}феніл)метансульфокислота; (5-Хлор-2-{2-[4-(4-хлорбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)-метансульфокислота; (5-Бром-2-{2-[4-(4-хлорбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)-метансульфокислота; (5-Хлор-2-{2-[4-(3,4-дифторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}-феніл)метансульфокислота; (5-Бром-2-{2-[4-(3,4-дифторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)-метансульфокислота; 2-(5-Хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2оксоетокси}феніл)етансульфокислота; (5-Бром-2-{2-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}-піридин-3-іл)етансульфокислота; (4-Хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота; (3-Бром-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота; (2-Хлор-6-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота; (5-Бром-2-{2-[2R-етил-4-(4-фторбензил)-5S-метилпіперазин-1-іл]-2оксоетокси}феніл)метансульфокислота; 2-(5-Бром-2-{2-(4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2оксоетокси}феніл)етансульфокислота; (5-Хлор-2-{2-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)-метансульфокислота; 2-(5-Бром-2-{2-(4-(4-хлорбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)етансульфокислота; 2-(5-Хлор-2-{2-[4-(3,4-дифторбензил)-2R,5S-диметилпіперазин-1-іл]-2оксоетокси}феніл)етансульфокислота; 2-(5-Хлор-2-{2-(4-(4-хлорбензил)-2R-метилпіперазин-1-іл)-2-оксоетокси}-феніл)етансульфокислота; 2-(5-Бром-2-{2-[4-(4-хлорбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}-феніл)етансульфокислота; (5-Хлор-2-{2-(4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл)-2-оксоетокси}феніл)метансульфокислота; 2-(5-Хлор-2-{2-(4-(3.4-дифторбензил)-2R-метилпіперазин-1-іл)-2-оксоетокси}-феніл)етансульфокислота; (5-Бром-2-{2-(4-(4-хлорбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}-піридин-3-іл)етансульфокислота; 3-(5-Бром-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)пропан-1сульфонова кислота; 3-(5-Хлор-2-{2-(4-(4-фторбензил)-2R-метилпіперазин-1-іл)-2-оксоетокси}-феніл)пропан-1-сульфонова кислота; 3-(5-Бром-2-{2-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}-феніл)пропан-1-сульфонова кислота; (2-Бром-6-{2-(4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота; (5-Хлор-2-{2-[2Е-етил-4-(4-фторбензил)-5S-метилпіперазин-1-іл]-2оксоетокси}феніл)метансульфокислота; 3-(5-Хлор-2-{2-[4-(4-хлорбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)пропан-1сульфонова кислота; 2-(5-Хлор-2-{2-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}-феніл)етансульфокислота; 3-(5-Бром-2-{2-[4-(4-хлорбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)пропан-1сульфонова кислота; 2-(5-Бром-2-{2-[4-(3,4-дифторбензил)-2R,5S-диметилпіперазин-1-іл]-2оксоетокси}феніл)етансульфокислота; 3-(5-Хлор-2-{2-[4-(3,4-дифторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)пропан-1сульфонова кислота; 3-{5-Хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)пропан-1сульфонова кислота; (5-Бром-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}-піридин-3іл)метансульфокислота; 3-(5-Хлор-2-{2-[4-(4-хлорбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}-феніл)пропан-1-сульфонова кислота; (5-Бром-2-{2-[4-(3,4-дифторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}-піридин-3іл)етансульфокислота; (5-Бром-2-{2-[2R-етил-4-(4-фторбензил)-5S-метилпіперазин-1-іл]-2оксоетокси}феніл)етансульфокислота; 3-(5-Бром-2-{2-[4-(4-хлорбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}-феніл)пропан-1-сульфонова кислота; 3-(5-Хлор-2-{2-[4-{3,4-дифторбензил}-2R-метилпіперазин-1-іл]-2-оксоетокси}-феніл)пропан-1сульфонова кислота; (5-Бром-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}-піридин-3іл)етансульфокислота; 3-(5-Бром-2-(2-[4-(3,4-дифторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)пропан-1сульфонова кислота; (2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}-5метилфеніл)метансульфокислота; 2-(5-Бром-2-{2-[4-(3,4-дифторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)етансульфокислота; 3-{5-Хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)пропан-1сульфонова кислота; (5-Хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл)-2-оксоетокси}піридин-3 іл)метансульфокислота; (5-Бром-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)метансульфокислота; (5-Хлор-2-{2-[4-(3,4-дифторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3іл)метансульфокислота; (5-Хлор-2-{2-[4-(4-хлорбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3іл)метансульфокислота; (5-Бром-2-{2-[4-(4-хлорбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3іл)метансульфокислота; (5-Хлор-2-{2-[4-(3,4-дифторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}піридин-3іл)метансульфокислота; (5-Бром-2-{2-[4-(3,4-дифторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}піридин-3іл)метансульфокислота; (5-Хлор-2-{2-[4-(4-хлорбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)метансульфокислота; (5-Бром-2-{2-[4-(4-хлорбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)метансульфокислота; 2-(5-Хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3іл)етансульфокислота; (5-Хлор-2-{2-[4-(3,4-дифторбензил)-2R,5S-диметилпіперазин-1-іл-2-оксоетокси}піридин-3іл)етансульфокислота; (5-Бром-2-{2-[4-(3,4-дифторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3іл)етансульфокислота; (5-Хлор-2-{2-[4-(4-хлорбензил)-2R,5S-диметилпіперазин-1-іл)-2-оксоетокси}піридин-3іл)етансульфокислота; (5-Бром-2-{2-[4-(4-хлорбензил)-2R,5S-диметилпіперазин-1-іл)-2-оксоетокси}піридин-3іл)етансульфокислота; 3-(5-Бром-2-{2-[4-(3,4-дифторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)пропан-1сульфонова кислота; (5-Хлор-2-{2-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}-піридин-3-іл)етансульфокислота; (5-Бром-2-{2-[4-{3,4-дифторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3іл)метансульфокислота; (5-Хлор-2-{2-[4-{4-хлорбензил)-2R-метилпіперазин-1-іл)-2-оксоетокси}піридин-3-іл)етансульфокислота; 3-(5-Хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3-іл)пропан-1сульфонова кислота; 2-(5-Хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)пропан-2сульфонова кислота; 2-(5-Бром-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)пропан-2сульфонова кислота; 2-(5-Хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)-2-метилпропан-1сульфонова кислота; 2-(5-Бром-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)-2-метилпропан-1сульфонова кислота; 1-(5-Хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)-2-метилпропан-2сульфонова кислота; (2-{2-[4-(4-Фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}-5трифторметилфеніл)метансульфокислота; (2-{2-[4-(4-Фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}-5-трифторзаміщенийметил-феніл)метансульфокислота; (2-{2-[4-(4-Фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}-5метилфеніл)метансульфокислота; (5-Хлор-2-{2-[2R-етил-4-(4-фторбензил)-5S-метилпіперазин-1-іл]-2оксоетокси}феніл)метансульфокислота; (5-Бром-2-{2-[2R-етил-4-(4-фторбензил)-5S-метилпіперазин-1-іл]-2оксоетокси}феніл)метансульфокислота; (5-Хлор-2-{2-[2R-етил-4-(4-фторбензил)-5S-метилпіперазин-1-іл]-2оксоетокси}феніл)етансульфокислота; (5-Хлор-2-{2-[2R-етил-4-(4-фторбензил)піперазин-1-іл]-2-оксоетокси}феніл)-метансульфокислота; (5-Бром-2-{2-[2R-етил-4-(4-фторбензил)піперазин-1-іл]-2-оксоетокси}феніл)-метансульфокислота; (5-Хлор-2-{2-[2R-етил-4-(4-фторбензил)-піперазин-1-іл]-2-оксоетокси}-феніл)-етансульфокислота; (5-Бром-2-{2-[2R-етил-4-(4-фторбензил)піперазин-1-іл]-2-оксоетокси}феніл)-етансульфокислота; 1-(5-Бром-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)-2-метилпропан-2сульфонова кислота; 2-(5-Хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2оксоетиламіно}феніл)етансульфокислота і (5-Хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2оксоетиламіно}феніл)метансульфокислота; Даний винахід також стосується фармацевтичної композиції для лікування або запобігання розладу або стану, вибраного з аутоімунних хвороб, ревматичного артриту, початкових стадій діабету І типу, туберкульозу шкіри, запалення кишечнику, невриту зорового нерву, псоріазу, розсіяного склерозу, ревматоїдної поліміалгії, увеїту, васкуліту, гостри х і хронічних запалень, остеоартриту, синдрому дихальної недостатності у дорослих, синдрому дихальної недостатності у дітей, ішемічного реперфузійного ураження, гломерунефриту, алергії, астми, атопічного дерматиту, інфікування пов'язаного з запаленням, вірусних запалень, грипу, гепатиту, хвороби Гійєна-Барре, хронічного бронхіту, ксеногенної трансплантації, хронічного та гострого відторгнення трансплантованої тканини, хронічного і гострого відторгнення трансплантованого органу, атеросклерозу, рестенозу (включаючи, але не обмежуючись ним, рестеноз, викликаний імплантацією балону та/або стенту), ВІЛ інфікування (використання ко-рецепторів) і грануломатозних хвороб (включаючи саркоїдоз, лепра і туберкульоз), а також ускладнень, що пов'язані з певними раковими захворюваннями, такими як, розсіяна мієлома. Сполуки цієї серії можуть також бути використані для запобігання розвитку метастаз раку. Сполуки цієї серії можуть також обмежувати утворення цитокинів в сайтах запалення, включаючи, але не обмежуючись ними, TNF і IL-1, як наслідок зменшення інфільтрації клітин, що може бути корисним при хворобах, пов'язаних з TNF і IL-1, включаючи застійну серцеву недостатність, легеневу емфізему або задишку, пов'язану з нею, емфізему, ВІЛ-1, ВІЛ-2, ВІЛ-3, цитомегаловірус, аденовіруси, віруси герпесу (оперезуючий лишай та звичайний герпес). Вони також можуть бути корисними при ускладненнях, пов'язаних з інфікуванням, яке призводить до утворення шкідливих запальних цитокинів, таких як TNF, наприклад, грибковий менінгіт, ушкодження з'єднувальної тканини, гіперплазія, утворення паннуса, і резорбція кісток, псоріатичний артрит, печінкова недостатність, бактеріальний менінгіт, синдром Кавасакі, інфаркт міокарду, гостра печінкова недостатність, хвороба Ліма, септичний шок, рак, травмування і малярія у ссавців, переважно людей, яка містить сполуку формули І або її фармацевтично прийнятну сіль у кількості, ефективній для лікування таких розладів або станів, та фармацевтично прийнятний носій. Даний винахід також стосується фармацевтичної композиції для лікування або запобігання розладів або станів, що можна лікувати або попереджувати шля хом інгібування зв'язування хемокіну з CCR1 рецептором у ссавців, переважно людей, яка містить сполуку формули І або її фармацевтично прийнятну сіль у кількості, ефективній для лікування таких розладів або станів, та фармацевтично прийнятний носій. Приклади таких розладів і станів наведені в попередньому абзаці. Даний винахід також стосується способу лікування або запобігання розладу або стану, вибраного з аутоімунних хвороб, ревматичного артриту, початкових стадій діабету І типу, туберкульозу шкіри, запалення кишечнику, невриту зорового нерву, псоріазу, розсіяного склерозу, ревматоїдної поліміалгії, увеїту, васкуліту, гострих і хронічних запалень, остеоартриту, синдрому дихальної недостатності у дорослих, синдрому дихальної недостатності у дітей, ішемічного реперфузійного ураження, гломерунефриту, алергії, астми, атопічного дерматиту, інфікування пов'язаного з запаленням, вірусних запалень, грипу, гепатиту, хвороби Гійєна-Барре, хронічного бронхіту, ксеногенної трансплантації, хронічного та гострого відторгнення трансплантованої тканини, хронічного і гострого відторгнення трансплантованого органу, атеросклерозу, рестенозу (включаючи, але не обмежуючись ним, рестеноз, викликаний імплантацією балону та/або стенту), ВІЛ інфікування (використання ко-рецепторів) і грануломатозних хвороб (включаючи саркоїдоз, лепра і туберкульоз), а також ускладнень, що пов'язані з певними раковими захворюваннями, такими як, розсіяна мієлома. Сполуки цієї серії можуть також бути використані для запобігання розвитку метастаз раку. Сполуки цієї серії можуть також обмежувати утворення цитокинів в сайтах запалення, включаючи, але не обмежуючись ними, TNF і IL-1, як наслідок зменшення інфільтрації клітин, що може бути корисним при хворобах, пов'язаних з TNF і IL-1, включаючи застійну серцеву недостатність, легеневу емфізему або задишку, пов'язану з нею, емфізему, ВІЛ-1, ВІЛ-2, ВІЛ-3, цитомегаловірус, аденовіруси, віруси герпесу (оперезуючий лишай та звичайний герпес). Вони також можуть бути корисними при ускладненнях, пов'язаних з інфікуванням, яке призводить до утворення шкідливих запальних цитокинів, таких як TNF, наприклад, грибковий менінгіт, ушкодження з'єднувальної тканини, гіперплазія, утворення паннуса, і резорбція кісток, псоріатичний артрит, печінкова недостатність, бактеріальний менінгіт, синдром Кавасакі, інфаркт міокарду, гостра печінкова недостатність, хвороба Ліма, септичний шок, рак, травмування і малярія у ссавців, переважно у людей, який полягає в уведенні ссавцеві, який потребує такого лікування або запобігання, сполуки формули І або її фармацевтично прийнятної солі, у кількості, що є ефективною для лікування або запобігання таких розладів або станів. Даний винахід також стосується способу лікування або запобігання розладу або стану, який можна лікувати або запобігти шляхом антагоністичної дії на CCR1 рецептор у ссавця, переважно, у людини, який полягає в уведенні ссавцю, який потребує такого лікування або запобігання, сполуки формули І або її фармацевтично прийнятної солі, у кількості, що є ефективною для лікування або запобігання такого розладу або стану. Даний винахід також стосується фармацевтичної композиції для лікування або запобігання розладу або стану, вибраного з аутоімунних хвороб, ревматичного артриту, початкових стадій діабету І типу, туберкульозу шкіри, запалення кишечнику, невриту зорового нерву, псоріазу, розсіяного склерозу, ревматоїдної поліміалгії, увеїту, васкуліту, гостри х і хронічних запалень, остеоартриту, синдрому дихальної недостатності у дорослих, синдрому дихальної недостатності у дітей, ішемічного реперфузійного ураження, гломерунефриту, алергії, астми, атонічного дерматиту, інфікування пов'язаного з запаленням, вірусних запалень, грипу, гепатиту, хвороби Гійєна-Барре, хронічного бронхіту, ксеногенної трансплантації, хронічного та гострого відторгнення трансплантованої тканини, хронічного і гострого відторгнення трансплантованого органу, атеросклерозу, рестенозу (включаючи, але не обмежуючись ним, рестеноз, викликаний імплантацією балону та/або стенту), ВІЛ інфікування (використання ко-рецепторів) і грануломатозних хвороб (включаючи саркоїдоз, лепра і туберкульоз), а також ускладнень, що пов'язані з певними раковими захворюваннями, такими як, розсіяна мієлома. Сполуки цієї серії можуть також бути використані для запобігання розвитку метастаз раку. Сполуки цієї серії можуть також обмежувати утворення цитокинів в сайтах запалення, включаючи, але не обмежуючись ними, TNF і IL-1, як наслідок зменшення інфільтрації клітин, що може бути корисним при хворобах, пов'язаних з TNF і IL-1, включаючи застійну серцеву недостатність, легеневу емфізему або задишку, пов'язану з нею, емфізему, ВІЛ-1, ВІЛ-2, ВІЛ-3, цитомегаловірус, аденовіруси, віруси герпесу (оперезуючий лишай та звичайний герпес). Вони також можуть бути корисними при ускладненнях, пов'язаних з інфікуванням, яке призводить до утворення шкідливих запальних цитокинів, таких як TNF, наприклад, грибковий менінгіт, ушкодження з'єднувальної тканини, гіперплазія, утворення паннуса, і резорбція кісток, псоріатичний артрит, печінкова недостатність, бактеріальний менінгіт, синдром Кавасакі, інфаркт міокарду, гостра печінкова недостатність, хвороба Ліма, септичний шок, рак, травмування і малярія у ссавців, переважно людей, яка містить сполуку формули І або її фармацевтично прийнятну сіль, у кількості, яка є ефективною для антагоністичної дії на рецептор CCR1, та фармацевтично прийнятний носій. Даний винахід також стосується фармацевтичної композиції для лікування або запобігання розладу або стану, що який можна лікувати або запобігати шляхом протидії проти CCR1 рецептора у ссавців, переважно людей, яка містить сполуку формули І або її фармацевтично прийнятну сіль, у кількості, яка є ефективною для антагоністичної дії на рецептор CCR1, та фармацевтично прийнятний носій. Даний винахід також стосується способу лікування або запобігання розладу або стану, вибраного з аутоімунних хвороб, ревматичного артриту, початкових стадій діабету І типу, туберкульозу шкіри, запалення кишечнику, невриту зорового нерву, псоріазу, розсіяного склерозу, ревматоїдної поліміалгії, увеїту, васкуліту, гострих і хронічних запалень, остеоартриту, синдрому дихальної недостатності у дорослих, синдрому дихальної недостатності у дітей, ішемічного реперфузійного ураження, гломерунефриту, алергії, астми, атонічного дерматиту, інфікування пов'язаного з запаленням, вірусних запалень, грипу, гепатиту, хвороби Гійєна-Барре, хронічного бронхіту, ксеногенної трансплантації, хронічного та гострого відторгнення трансплантованої тканини, хронічного і гострого відторгнення трансплантованого органу, атеросклерозу, рестенозу (включаючи, але не обмежуючись ним, рестеноз, викликаний імплантацією балону та/або стенту), ВІЛ інфікування (використання ко-рецепторів) і грануломатозних хвороб (включаючи саркоїдоз, лепра і туберкульоз), а також ускладнень, що пов'язані з певними раковими захворюваннями, такими як, розсіяна мієлома. Сполуки цієї серії можуть також бути використані для запобігання розвитку метастаз раку. Сполуки цієї серії можуть також обмежувати утворення цитокинів в сайтах запалення, включаючи, але не обмежуючись ними, TNF і IL-1, як наслідок зменшення інфільтрації клітин, що може бути корисним при хворобах, пов'язаних з TNF і IL-1, включаючи застійну серцеву недостатність, легеневу емфізему або задишку, пов'язану з нею, емфізему, ВІЛ-1, ВІЛ-2, ВІЛ-3, цитомегаловірус, аденовіруси, віруси герпесу (оперезуючий лишай та звичайний герпес). Вони також можуть бути корисними при ускладненнях, пов'язаних з інфікуванням, яке призводить до утворення шкідливих запальних цитокинів, таких як TNF, наприклад, грибковий менінгіт, ушкодження з'єднувальної тканини, гіперплазія, утворення паннуса, і резорбція кісток, псоріатичний артрит, печінкова недостатність, бактеріальний менінгіт, синдром Кавасакі, інфаркт міокарду, гостра печінкова недостатність, хвороба Ліма, септичний шок, рак, травмування і малярія у ссавців, переважно людей, який полягає у введенні ссавцеві, який потребує такого лікування або запобігання, сполуки формули І або її фармацевтично прийнятної солі, у кількості, яка є ефективною для антагоністичної дії на рецептор CCR1, та фармацевтично прийнятного носія. Наступні схеми реакцій зображують одержання сполук даного винаходу. Якщо не вказано інакше, a, b, c, d та R1 до R6 і структурна формула в Схемі реакцій та в наступному обговоренні, є такими, як визначено вище. Реакції в препаративних прикладах і схемах описані в заявках на тимчасовий патент, що розглядаються одночасно і за якими діловодство не закінчено, а саме, реєстраційний номер 60/193789, яку подано 31 березня 2000 року, реєстраційний номер 60/241084, яку подано 19 жовтня 2000 року і реєстраційний номер 09/821322, яку подано 29 березня 2001 року, розкриття яких включено сюди як посилання. В реакції 1 Препаративного прикладу А сполуку формули II, де b дорівнює 0, 1 або 2, перетворюють у відповідну сполуку формули III шляхом взаємодії сполуки формули II з бензальдегідом формули в присутності основи, такої як триетиламін, і відновлювального агента, такого як, триацетоксиборогідрид натрію, в апротонному розчиннику, такому як 1,2-дихлоретан. Реакційну суміш перемішують при кімнатній температурі протягом від приблизно 1 до приблизно 4 годин, переважно близько 2 годин. В реакції 2 Препаративного прикладу А сполуку формули III перетворюють у відповідну сполуку формули IV спочатку шля хом реакції зі сполукою формули де с дорівнює 0, 1 або 2, з 4-метилморфоліном і ізобутилхлорформіатом в присутності полярного апротонного розчиника, такого як тетрагідрофуран, з наступною взаємодією з проміжною сполукою, що таким чином утворилася зі сполукою формули III. Реакційну суміш, що таким чином утворилася, перемішують протягом ночі при температурі навколишнього середовища. В реакції 3 Препаративного прикладу А сполуку формули IV перетворюють у відповідний піперазин-2,5діон формули V шляхом обробки сполуки IV трифтороцтовою кислотою у присутності полярного апротонного розчинника, такого як метиленхлорид. Реакційну суміш перемішують при кімнатній температурі протягом від приблизно 1 до приблизно 4 годин, переважно приблизно 2 години. В реакції 4 Препаративного прикладу А сполуку формули V перетворюють у відповідну сполуку формули VI шляхом відновлення сполуки V відновлювальним агентом, таким як літійалюмінійгідрид. Реакцію проводять при температурі між приблизно -10°С і 10°С, переважно біля 0°С, протягом від приблизно 10 до приблизно 90 хвилин, переважно приблизно 40 хвилин. В реакції 5 Препаративного прикладу А сполуку формули VI перетворюють у відповідну сполуку формули VII шля хом взаємодії сполуки VI з хлорацетилхлоридом в присутності основи, такої як триетиламін, в полярному апротонному розчиннику, такому як метиленхлорид, при температурі навколишнього середовища протягом від приблизно 15 хвилин до приблизно 3 годин, переважно приблизно 30 хвилин. В реакції 6 Препаративного прикладу А сполуку формули VI перетворюють у відповідну сполуку формули VIII шляхом взаємодії сполуки VI з ацетоксиацетилхлоридом в присутності основи, такої як триетиламін, в полярному апротонному розчиннику, такому як метиленхлорид, при температурі навколишнього середовища протягом від приблизно 15 хвилин до приблизно 4 годин, переважно протягом приблизно 1 години. Утворений ацетил-захищений спирт піддають взаємодії з гідратом гідроксиду літію в суміші розчинника, що містить воду, тетрагідрофуран і метанол, при температурі навколишнього середовища протягом від приблизно 1 години до приблизно 8 годин, переважно протягом приблизно 2 годин. В реакції 1 Препаративного прикладу В сполуку формули IX перетворюють у відповідну сполуку формули X шля хом обробки сполуки формули IX відновлювальним агентом, такім як лійтійалюмініягідрид в апротонному розчиннику, такому як тетрагідрофуран. Реакційну суміш нагрівають до кипіння протягом від приблизно 1 години до приблизно 6 годин, переважно протягом приблизно 2 годин. В реакції 2 Препаративного прикладу В сполуку формули X перетворюють у відповідну сполуку формули XI шляхом перетворення спочатку гідроксильної групи у хлоридну шляхом взаємодії сполуки X з тіонілхлоридом у присутності апротонного розчинника такого як метиленхлорид. Реакційну суміш нагрівають до кипіння протягом від приблизно 1 до приблизно 10 годин, переважно приблизно 3 години. Далі на алкілхлорид, що утворився в результаті, впливають джерелом ціанід-іонів, таким як ціанід калію, у присутності апротонного розчинника, такого як ацетонітрил, і краун-естера, такого як 18-краун-6. Реакційну суміш перемішують при температурі навколишнього середовища протягом від приблизно 1 години до приблизно 10 годин, переважно приблизно 3 години. В реакції 3 Препаративного прикладу В сполуку формули XI перетворюють у сполуку формули XII шляхом обробки сполуки XI спочатку джерелом гідроксильних іонів, таким як гідроксид калію, в суміші з етанолом і водою. Реакційну суміш нагрівають до кипіння протягом від приблизно 1 години до приблизно 10 годин, переважно приблизно 8 годин. В реакції 4 Препаративного прикладу В сполуку формули XII перетворюють у сполуку формули XIII шляхом обробки етанолом у присутності кислоти, такої як соляна кислота, при температурі навколишнього середовища протягом від приблизно 8 години до приблизно 16 годин, переважно 12 годин. В реакції 5 Препаративного прикладу В сполуку формули XIII перетворюють у відповідну сполуку формули XIV шля хом обробки сполуки XIII спочатку відновлювальним агентом, таким як вказаний вище в реакції 1 Препаративного прикладу В. Спирт, що утворився в результаті, може бути перетворений у сполуку XIV за допомогою окислювача, такого як перйодинан Деса-Мартіна, в присутності апротонного розчинника, такого як тетрагідрофуран, при температурі навколишнього середовища протягом від приблизно 1 години до приблизно 16 годин, переважно 4 годин. В реакції 6 Препаративного прикладу В сполуку формули X перетворюють у відповідну сполуку формули XV шля хом обробки сполуки X спочатку окислювачем, таким як перйодинан Деса-Мартіна, в присутності апротонного розчинника, такого як тетрагідрофуран, при температурі навколишнього середовища протягом від приблизно 1 години до приблизно 16 годин, переважно приблизно 4 години. В реакції 7 Препаративного прикладу В сполуку формули XV перетворюють у відповідну сполуку формули XVI, де є може дорівнювати 2-7, шляхом обробки сполуки XV спочатку фосфонілідом, отриманого з солі фосфонію формули: де f може бути (С1-6)-алкілом, де алкіл є таким, як визначено вище, в присутності апротонного розчинника, такого як тетрагідрофуран. Реакцію проводять при температурі від -78°С до температури кипіння, переважна температура залежить від того, який фосфонілід використовується, протягом від приблизно 4 годин до приблизно 16 годин, переважно приблизно 10 годин (для аналогічних перетворень див. J. Am. Cem. Soc. 1985, 107, 217). Олефіновий естер, що утворився в результаті, гідрують шляхом збовтування під тиском водню, що перевищує атмосферний, у присутності каталізатору, такого як діоксид платини, в присутності апротонного розчинника, такого як етилацетат. Далі естер відновлюють і окислюють повторно відповідно до методики, що описана в реакції 5 Препаративного прикладу В для отримання сполуки формули XVI. В реакції 8 Препаративного прикладу С сполуки формули XIV, XV, XVI перетворюють у відповідну сполуку формули XVIII, де g може дорівнювати 0-7, шляхом деметилування метилового естеру кислотою, такою як 47% водний розчину гідроброміду. Реакційну суміш нагрівають до кипіння протягом від приблизно 10 годин до приблизно 30 годин, переважно приблизно 24 години. В реакції 1 Схеми 1, сполуку формули VII перетворюють у відповідну сполуку формули XVIII, де g дорівнює 0-7, шляхом взаємодії сполуки VII зі сполукою формули XVII в присутності карбонату калію, йодиду калію і апротонного розчинника, такого як диметилформамід. Продукт реакції нагрівають до кипіння протягом від приблизно 4 годин до приблизно 8 годин, переважно приблизно 6 годин. В реакції 2 Схеми 1, сполуку формули XVIII перетворюють у відповідну сполуку формули XIX, де g дорівнює 0-7, шляхом взаємодії сполуки XVIII з відновлювальним агентом, таким як борогідрид натрію, в апротонному розчиннику, такому як тетрагідрофуран, при температурі від -10°С до температури навколишнього середовища, переважно при температурі навколишнього середовища, протягом від приблизно 15 хвилин до приблизно 90 хвилин, переважно приблизно 60 хвилин. В реакції 3 Схеми 1, сполуку формули XIX перетворюють у відповідну сполук у формули XX, де g дорівнює 0-7, як описано в реакції 2 Препаративного прикладу B. В реакції 4 Схеми 1, сполуку формули XIX перетворюють у відповідну сполуку формули І, шляхом взаємодії сполуки XX з сульфа том натрію у воді при температурі від 70 до 100°С, переважно 100°С, протягом від приблизно 1 години до приблизно 5 годин, переважно протягом приблизно 1 години. Корисним може бути додавання каталітичного йодиду натрію. В реакції 1 Схеми 2, сполуку формули VIII перетворюють у відповідну сполуку формули XXI, шляхом взаємодії сполуки VIII зі сполукою формули CI-Y[(R4) d]-(CH2)h-CHO де Υ є (С2-С9) гетероарил, де хлор приєднаний до атому вуглецю, що є суміжним з гетероатомом (наприклад, 2-піридил) і де h дорівнює 0-7. Реагенти перемішують в полярному апротонному розчиннику, такому як ацетонітріл, в присутності основи, такої як триетиламін, при температурі кипіння протягом від приблизно 4 годин до приблизно 24 годин, переважно приблизно 12 годин. В реакції 2 Схеми 2, сполука формули XXI, де Υ є (С2-С9) гетероарил, може бути перетворена у сполуку формули І, використовуючи методики, що описані вище в С хемі 1. В реакції 1 Схеми 3, сполука формули VII може бути перетворена у відповідну сполуку формули XXII, де Υ є (С2-С9) гетероарил, шляхом взаємодії сполуки VII з трет-бутоксикарбоніламінооцтовою кислотою в апротонному розчиннику, такому як метиленхлорид, з карбодіімідом, таким як дициклогексилкарбодіімід, в присутності основи, такої як триетиламін, при кімнатній температурі протягом від приблизно 1 години до приблизно 24 годин, переважно приблизно 3 години. Таким чином, сполука формули XXII може бути отримана з карбамату шляхом дії трифтороцтової кислоти при кімнатній температурі протягом від приблизно 1 години до приблизно 12 годин, переважно приблизно 4 години. В реакції 2 Схеми 3, сполука формули XXII може бути перетворена у відповідну сполуку формули XXIII, де Υ є (С2-С9) гетероарил, використовуючи методику, викладену в реакції 1 Схеми 2. В реакції 3 Схеми 3, сполука формули XXIII може бути перетворена у відповідну сполуку формули XXIV, де Υ є (С2-С9) гетероарил, відновлюючи спочатку естер до відповідного спирту відновлювальним агентом, таким як борогідрид натрію, в трет-бутанолі і метанолі при температурі від 20°С до кипіння, переважно при температурі кипіння, протягом від приблизно 1 години до приблизно 6 годин, переважно приблизно 1 годину. Спирт, що утворився в результаті, може бути перетворений у сполуку формули XXIV шляхом обробки окисником, таким як перйодинан Деса-Мартіна, в присутності апротонного розчинника, такого як тетрагідрофуран, при температурі навколишнього середовища протягом від приблизно 1 години до приблизно 16 годин, переважно приблизно 4 години. В реакції 4 Схеми 3, сполука формули XXIV, де Υ є (С2-С9) ге тероарил, може бути перетворена у сполуку формули І, використовуючи методики, вказані вище в С хемі 1. Якщо не вказано інакше, тиск для кожної з реакцій, що вказані вище, не є важливим параметром. Загалом, реакції проводяться при тиску від однієї до трьох атмосфер, переважно при тиску навколишнього середовища (приблизно одна атмосфера). Сполуки формули І, що є основними за природою, здатні утворювати велику кількість різноманітних солей з різними неорганічними і органічними кислотами. Хоча такі солі повинні бути фармацевтично прийнятними для введення тваринам, часто на практиці бажано початково виділити сполуку формули І з реакційної суміші як фармацевтично неприйнятну сіль і тоді просто перетворити останню назад у вільну основу шляхом обробки лужним реагентом і надалі перетворити вільну основу у фармацевтично прийнятну кислотно-адитивну сіль. Кислотно-адитивні солі основних сполук даного винаходу легко отримуються шляхом обробки основної сполуки суттєво еквівалентною кількістю вибраного мінеральної або органічної кислоти в середовищі водного розчинника або в придатному органічному розчиннику, такому метанол або етанол. Шляхом обережного випаровування розчинника отримується сіль в твердому стані. Кислоти, що використовуються для отримання фармацевтично прийнятних кислотно-адитивних солей основних сполук даного винаходу є такі, що утворюють нетоксичні кислотно-адитивні солі, а саме, солі, що містять фармакологічно прийнятні аніони, такі як гідрохлоридні, гідробромідні, гідройодидні, нітратні, сульфатні або бісульфатні, фосфа тні або кислі фосфатні, ацетатні, лактатні, цитратні або кислі цитратні, тартратні або бітартратні, сукцинатні, малеатні, фумаратні, глюконатні, сахаратні, бензоатні, метансульфонатні і памоатні (а саме, 1,1'-метилен-біс-(2-гідрокси-3-нафтоатні)) солі. Ті сполуки формули І, також є кислотними за природою, здатні утворювати основні солі з різноманітними фармакологічно прийнятними катіонами. Прикладами таких солей є солі лужних металів або лужноземельних металів і, зокрема, солі натрію і калію. Всі ці солі отримуються звичайними способами. Хімічними основами, що використовуються як реагенти для отримання фармацевтично прийнятних основних солей даного винаходу, є такі, що утворюють нетоксичні основні солі з кислотними сполуками формули І, що описані тут. До цих нетоксичних основних солей відносять солі, що були отримані з таких фармакологічно прийнятних катіонів, як натрій, калій, кальцій і магній тощо. Ці солі можна легко отримати шляхом обробки відповідної кислотної сполуки водним розчином, що містить бажані фармакологічно прийнятні катіони, і надалі випарюванням одержаного розчину до сухого стан у, переважно при зниженому тиску. Альтернативним способом, ці солі можна також отримати шляхом змішування нижчих алканових розчинів кислотних сполук і бажаного алкоксиду лужного металу з наступним випарюванням одержаного розчину до сухого стану тим же способом, що вказаний раніше. В будь-якому випадку переважно застосовуються стехіометричні кількості реагентів для того, щоб забезпечити завершення реакції і отримати максимальну кількість продукту на ви ході. Сполуки формули І і їх фармацевтично прийнятні солі (надалі також згадуються разом, як "активні сполуки") є ефективними антагоністами CCR1 рецептора. Активні сполуки також є корисними при лікуванні або запобіганні аутоімунних хвороб, ревматичного артриту, початкових стадій діабету І типу, туберкульозу шкіри, запалення кишечнику, невриту зорового нерву, псоріазу, розсіяного склерозу, ревматоїдної поліміалгії, увеїту, васкуліту, гостри х і хронічних запалень, остеоартриту, синдрому дихальної недостатності у дорослих, синдрому дихальної недостатності у дітей, ішемічного реперфузійного ураження, гломерунефриту, алергії, астми, атопічного дерматиту, інфікування пов'язаного з запаленням, вірусних запалень, грипу, гепатиту, хвороби Гійена-Барре, хронічного бронхіту, ксеногенної трансплантації, хронічного та гострого відторгнення трансплантованої тканини, хронічного і гострого відторгнення трансплантованого органу, атеросклерозу, рестенозу (включаючи, але не обмежуючись ним, рестеноз, викликаний імплантацією балону та/або стенту), ВІЛ інфікування (використання ко-рецепторів) і грануломатозних хвороб (включаючи саркоїдоз, лепра і туберкульоз), а також ускладнень, що пов'язані з певними раковими захворюваннями, такими як, розсіяна мієлома. Сполуки цієї серії можуть також бути використані для запобігання розвитку метастаз раку. Сполуки цієї серії можуть також обмежувати утворення цитокинів в сайтах запалення, включаючи, але не обмежуючись ними, TNF і IL-1, як наслідок зменшення інфільтрації клітин, що може бути корисним при хворобах, пов'язаних з TNF іIL-1, включаючи застійну серцеву недостатність, легеневу емфізему або задишку, пов'язану з нею, емфізему, ВІЛ-1, ВІЛ-2, ВІЛ-3, цитомегаловірус, аденовіруси, віруси герпесу (оперезуючий лишай та звичайний герпес). Вони також можуть бути корисними при ускладненнях, пов'язаних з інфікуванням, яке призводить до утворення шкідливих запальних цитокинів, таких як TNF, наприклад, грибковий менінгіт, ушкодження з'єднувальної тканини, гіперплазія, утворення паннуса, і резорбція кісток, псоріатичний артрит, печінкова недостатність, бактеріальний менінгіт, синдром Кавасакі, інфаркт міокарду, гостра печінкова недостатність, хвороба Ліма, септичний шок, рак, травмування і малярія тощо. Активність сполук винаходу може бути оцінена згидно з методиками, що відомі спеціалістам в цій області. Приклади визнаних способів визначення індукованої CCR1 міграції можна знайти в Coligan, J.Ε., Kruisbeek, A.M., Margulies, D.H., Shevach, E.M., Strober, W. Редактори: Current Protocols In Immunology. 6.12.1-6.12.3. (John Wiley and Sons, NY, 1991). Один конкретний приклад того, як визначити активність сполуки на інгібування міграції, описаний детально нижче. Аналіз хемотаксису: Здатність сполук пригнічувати хемотаксис різноманітних хемокинів може бути оцінена шляхом використання стандарних камер Boyden з 48 або 96 лунками з полікарбонатним фільтром в 5 мікрон. Усі реагенти і клітини можуть бути отримані зі стандартного культурального середовища тканини RPMI (BioWhitikker Inc.) з додаванням 1мг/мл бичачого сироваткового альбуміну. Коротко, МІР-1a (Peprotech, Inc., P.O. Bo x 275, Rocky Hill NJ) або інші досліджувані агоністи поміщають в нижню частину камери Бойдена. Далі встановлюють полікарбонатний фільтр і прикріплюють верхню частину камери. Кількість вибраного агоністу є такою, яка визначена, як така, що викликає максимальний ефект хемотаксису в цій системі (наприклад, для МІР-1a ця кількість повинна дорівнювати 1нМ). Клітини ТНР-1 (АТСС ТІВ-202), первинні людські моноцити, або первинні лімфоцити, відділені стандартним способом, можуть потім додаватись в верхню частину камери в трикратній повторюваності разом з різними концентраціями сполуки, що досліджується. Розведення сполуки можуть бути отримані шляхом стандартної серологічної методики і змішані з клітинами перед додаванням у камеру. Після відповідного періоду інкубації при 37 градусах за Цельсієм (наприклад, 3,5 години для клітин ТНР-1, 90 хвилин для первинних моноцитів), камеру знімають, клітини в верхній частині відсмоктують, верхню частину фільтру вичищають і визначають кількість мігруючих клітин відповідно до наступної методики. Для клітин ТНР-1 камера (96 луночна серія виготовлена Neuroprobe) може бути центрифугована для того, щоб витіснити клітини з нижчої камери і таким чином проаналізувати кількість клітин у порівнянні зі стандартною кривою шляхом зміни кольору діацетатного флуоресцентного барвника. Для первинних людських моноцитів або лімфоцитів фільтр може бути пофарбований фарбою Dif Quik (American Scientific Products) і тоді кількість мігруючих клітин може бути визначена під мікроскопом. Кількість клітин, що мігрують в присутності сполуки, ділять на кількість клітин, що мігрують в контрольних лунках (без сполуки). Ця величина є % інгібування для сполуки, який, з використанням стандартної графічної методики, може бути зображений у вигляді кривої залежності від концентрації сполуки, що була використана. Потім визначається точка 50% інгібування з використанням відповідного лінійного аналізу для всіх концентрацій тестування. Лінійний аналіз для всіх точок даних повинен мати коефіцієнт кореляції (R в квадраті) >90%, щоб розглядатися як надійний аналіз. Всі сполуки винаходу, наведені в наступних прикладах, мали ІС 50 менше 10мкМ в аналізі хемотаксису. Композиції даного винаходу можуть бути сформульовані звичайним способом, використовуючи один або більше фармацевтично прийнятних носіїв. Таким чином, активні сполуки винаходу можуть бути сформульовані для орального, буккального, інтраназального, парентерального (наприклад, внутрішньовенного, внутрішньом'язового або підшкірного) або ректального уведення або у формі, придатній для уведення шляхом інгаляції або інсуфляції. Активні сполуки винаходу можуть бути також сформульовані у лікарські форми довготривалого вивільнення. Для орального уведення фармацевтичні композиції можуть бути у вигляді, наприклад, таблеток або капсул приготовлених звичайними способами з фармацевтично прийнятними екціпієнтами, такими як з'вязуюча речовина (наприклад, пептизований маїсовий крохмаль, полівінілпіролідон або гідроксипропілметилцелюлоза); наповнювачі (наприклад, лактоза, мікрокристалічна целюлоза або фосфат кальцію); змащувачі (наприклад, стеарат магнію, тальк або силікат); дезінтегранти (наприклад, картопляний крохмаль або натрій крохмальгліколят); або зволожувачі (наприклад, лаурилсульфат натрію). Таблетки можуть бути вкриті оболонкою відповідно до добре відомих способів. Рідкі препарати для орального уведення можуть бути в вигляді, наприклад, розчинів, сиропів або суспензій, або також можуть бути представлені як сухий продукт для розчинення у воді або іншій відповідній речовині перед вживанням. Такі рідкі препарати можуть бути отримані звичайними способами з додаванням фармацевтично прийнятних добавок, таких як суспендувальні агенти (наприклад, сироп сорбіту, метилцелюлоза або гідрогенізовані жири); емульгатори (наприклад, лецитин або гуміарабік); неводні носії (наприклад, міндальне масло, масляні естери або етиловий спирт); і консерванти (наприклад, метил або пропіл п-гідроксибензоати або сорбінова кислота). Для буккального уведення композиція може бути представлена у вигляді таблеток, сформульованих звичайним способом. Активні сполуки винаходу можуть бути сформульовані для парентерального уведення шляхом ін'єкцій, в тому числі використовуючи звичайний спосіб катетеризації або вливання. Рецептури для ін'єкцій можуть бути представлені в формі одиничних доз, наприклад, в ампулах або в багатодозових контейнерах з додаванням консерванту. Композиції можуть бути у вигляді суспензій, розчинів або емульсій в масляних або водних носіях, а також можуть містити агенти рецептування, такі як суспендувальні агенти, стабілізатори і/або диспергатори. Як альтернатива, активний інгредієнт може бути у формі порошку для змішування з відповідним носієм наприклад, стерильною апірогенною водою, перед вживанням. Активні сполуки винаходу можуть також бути сформульовані в ректальних композиціях таких як супозиторії або утримуючі клізми, наприклад, що містять звичайні основи супозиторіїв, такі як масло какао або інші гліцериди. Для інтраназального введення або введення шляхом інгаляції активні сполуки винаходу вводяться звичайним способом у вигляді розчину або суспензії з накачного або аерозольного розпилювача, де речовина попередньо знаходиться під тиском, з використанням придатного пропелента, наприклад, дихлордифторметану, трихлор фторметану, дихлортетра фторетану, двоокису вуглецю або іншого відповідного газу. У випадку аерозолю під тиском одинична доза може бути визначена шляхом встановлення клапану для введення відміряної кількості. Контейнер із речовиною під тиском або розпилювач може містити розчин або суспензію активної сполуки. Капсули і картріджі (виготовлені, наприклад, з желатину) для використання в інгаляторі або інсуфляторі можуть містити суміш порошку сполуки винаходу і відповідної порошкової основи, такої як лактоза або крохмаль. Запропонованою дозою активних сполук винаходу для орального, парентерального або буккального введення для дорослої людини середнього віку для лікування станів, вказаних вище (наприклад, ревматичного артриту), є від 0,1 до 1000мг активного інгредієнту на одиничну дозу, що може бути введена, на приклад, 1-4 рази на день. Аерозольні рецептури для лікування станів, вказаних ви ще (наприклад, ревматичного артриту) для дорослої людини середнього віку створені таким чином, що кожна відміряна доза або "пшик" аерозолю містить від 20мкг до 1000мкг сполуки винаходу. Загальна денна доза при використанні аерозолю буде складати від 0,1мг до 1000мг. Введення може бути здійснене декілька раз за день, на приклад, 2, 3, 4 або 8 раз, при введенні, наприклад, 1, 2 або 3 дози кожного разу. Активні агенти можуть бути сформульовані для довготривалого вивільнення відповідно до способів, добре відомих фахівцям. Приклади таких рецептур можна знайти в патентах США №№ 3,538,214, 4,060,598, 4,173,626, 3,119,742 і 3,492,397. Сполуки винаходу можуть також бути використані в комбінованій терапії з використанням імунодепресантних агентів, включаючи, але не обмежуючись ними, рапаміцин, циклоспорін A, FK-506, CellceptÒ; імуран і IL-2R інгібіторні антитіла, або з використанням класичних антизапальних агентів (наприклад, інгібіторів циклооксигенази/ліпоксигенази), включаючи, але не обмежуючись ними, аспірин, ацетамінофен, напроксен і піроксикам, або з використанням агентів, що інгібують цитокін, включаючи, але не обмежуючись ним, ENBREL. Наступні приклади ілюструють отримання сполук даного винаходу. Використовувалися реагенти, що є наявними в продажу, без подальшого очищення. Під хроматографією розуміється колонкова хроматографія, здійснювана з використанням 32-63мм колонки з силікагелем і під тиском азоту (флешхроматографія). Променеві мас-спектри часток реєстрували або на Hewlett Packard 5989Ò, з використанням хімічної іонізації (амонію), або на Fisons (або MicroMass) платформі хімічної іонізації при атмосферному тиску, при якій використовується суміш 50/50 ацетонітрил/вода. Кімнатна або температура навколишнього середовища відповідає 20-25°С. Усі неводні реакції проводились в атмосфері азоту для зручності і для отримання максимально ефективного результату. Концентрування у вакуумі вказує на те, був використаний роторний випарювач. Назви сполук винаходу були створені Autonom 2.0 версії PC-batch з Bellstein Informationssysteme GmbH (ISBN 3-89536-976-4). Приклад 1 (5-Хлор-2-{2-[4-(4-фторбензил)-(2R,5S)-2,5-диметилпіперазин-1-іл]-2оксоетокси}феніл)метансульфокислота. Метиловий естер (S)-2-(4-Фторбензиламін)пропіонової кислоти До розчину гідрохлориду метилового естеру (S)-2-амінпропіонової кислоти (25г, 179ммоль) і 4 фторбензальдегіду (23мл, 215ммоль) в 1,2-дихлоретані (200мл) додавали триетиламін (25мл, 179ммоль). Суміш, що утворюється в результаті, перемішують протягом двох годин при температурі навколишнього середовища. Далі до неї додають натрій триацетоксиборогідрид (57г, 268ммоль) чотирма порціями. Суміш, що утворюється в результаті, перемішують протягом ночі при температурі навколишнього середовища. Реакційну суміш нейтралізують за допомогою розведеного водного розчину гідроксиду натрію і екстрагують за допомогою дихлорметану. Органічний шар висушують сульфа том магнію, відфільтровують і концентрують у вакуумі. Хроматографією на силікагелі одержують сполуку, вказану в назві винаходу (34,4г). Метиловий естер (2S)-2-[(2R)-(2-трет-бутоксикарбоніламінопропіоніл)-(4-фторбензил)амін]пропіонової кислоти До розчину (R)-2-трет-бутоксикарбонілпропіонової кислоти (37г, 195ммоль) в сухому тетрагідрофурані (250мл) при температурі 0°С додають 4-метилморфолін (21,5мл, 195ммоль), а далі ізобутилформіат (25,3мл, 195ммоль). Реакційну суміш залишають нагріватися до температури навколишнього середовища і перемішують протягом двох годин. Далі додають метиловий естер (S)-2-(4-фторбензиламін)пропіонової кислоти (34,4г, 162ммоль). Суміш, що утворилася в результаті, перемішують протягом ночі при температурі навколишнього середовища. Реакційну суміш фільтрують через целітову прокладку, а осад на фільтрі промивають етилацетатом. Фільтрат концентрують у вакуумі, розводять етилацетатом і промивають водою і насиченим розчином солі. Органічний шар висушують над сульфа том магнію, фільтрують і концентрують в вакуумі. Хроматографією на силікагелі, одержують сполуку, вказану в назві винаходу (43,2г). (3R,6S)-1-(4-Фторбензил)-3,6-диметилпіперазин-2,5-діон До розчину метилового естеру (2S)-2-[(2R)-(2-третбутоксикарбоніламінпргопіоніл)-(4фторлбензил)амін]пропіонової кислоти (43г, 382ммоль) в дихлорметані (120мл) при температурі 0°С додають трифтороцтову кислоту (60мл). Реакційну суміш залишають нагріватися до температури навколишнього середовища і перемішують протягом двох годин. Реакційну суміш охолоджують до 0°С і повільно гасять шляхом додавання 3N розчину гідроксиду натрію до тих пір, поки вона не стане основною. Суміш, що утворилася в результаті, екстрагують за допомогою дихлорметану. Органічний шар висушують над сульфатом магнію, фільтрують і концентрують в вакуумі для отримання сполуки, вказаної в назві винаходу (22г). (2R,5S)-1-(4-фторбензил)-2,5-диметилпіперазин До розчину (3R,6S)-1-(4-фторбензил)-3,6-диметилпіперазин-2,5-діон (22г, 87,9ммоль) в сухому тетрагідрофурані (160мл) при температурі 0°С додають розчин літійалюмінійгідриду (1M в тетрагідрофурані, 373мл, 373ммоль) по краплям протягом 40 хвилин. Реакційну суміш далі доводять до кипіння протягом 4 годин, охолоджують до температури навколишнього середовища і повільно гасять за допомогою води. Суміш, що утворилася, фільтрують через целітову прокладку, а осад на фільтрі промивають етилацетатом. Потім фільтрат концентрують, розводять етилацетатом і промивають насиченим водним розчином гідрокарбонату натрію. Органічний шар відокремлюють, висушують над сульфатом магнію, фільтрують і концентрують в вакуумі для отримання сполуки, вказаної в назві винаходу (17,7г). 2-Хлор-1-[4-(4-фторбензил)-(2R,5S)-2,5-диметилпіперазин-1-іл]етанон До розчину (2R,5S)-1-(4-фторбензил)-2,5-диметилпіперазину (2,5г, 11,2ммоль) в сухому ди хлорметані (11мл) при температурі 0°С додають триетиламін (1,57мл, 11,2ммоль) потім хлорацетилхлорид (0,86мл, 11,2ммоль). Реакційну суміш, що утворилася в результаті, перемішують протягом 30 хвилин. Потім реакційну суміш фільтрують через целітову прокладку, промивають дихлорметаном і фільтрат, що утворився в результаті, концентрують. Хроматографією на силікагелі одержують сполуку, вказану в назві винаходу (2,84г). 5-Хлор-2-(2-[4-(4-фторбензил)-(2R,5S)-2,5-диметилпіперазин-1-іл]-2-оксоетокси)-бензальдегід До розчину 2-хлор-1-[4-(4-фторбензил)-(2R,5S)-2,5-диметилпіперазин-1-іл]етанон (2,87г, 9,6ммоль) в диметилформаміді (20мл) додають 5-хлорсаліцилальдегід (1,65г, 10,5ммоль), карбонат калію (2,64г, 19,2ммоль) і йодид калію (1,59г, 9,6ммоль). Суміш, що утворилася в результаті, нагрівають до 100°С протягом 12 годин. Потім реакційну суміш охолоджують, розводять насиченим водним сольовим розчином і екстрагують за допомогою етилацетату. Органічний шар висушують над сульфа том магнію і фільтрують. Фільтрат концентрують в вакуумі для отримання неочищеного продукту. Очи щенням шляхом хроматографії на силікагелі одержують сполуку, вказану в назві винаходу (3,40г). 2-(4-Хлор-2-гідроксиметилфенокси)-1-[4-(4-фторбензил)-(2R,5S)-2,5-диметилпіперазин-1-іліетанон До розчину 5-хлор-2-{2-[4-(4-фторбензил)-(2R,5S)-2,5-диметилпіперазин-1-іл]-2оксоетокси}бензальдегід (0,99г, 2,36ммоль) в сухому метанолі (25мл) додають борогідрид натрію (0,19г, 4,92ммоль). Через 1 годину реакційну суміш підкислюють до рН 2 шляхом додавання 1N соляної кислоти. Через 5 хвилин реакційну суміш нейтралізують 1N гідроксидом натрію, а метанол видаляють шляхом випарювання. Водну суспензію, що утворилася в результаті, екстрагують за допомогою етилацетату. Органічний шар промивають сольовим розчином, висушують над сульфатом магнію, фільтрують і випаровують для отримання сполуки, вказаної в назві винаходу (0,98г). 2-(4-Хлор-2-хлорметилФенокси)-1-[4-(4-фторбензил)-2,5-диметилпіперазин-1-іл]етанон До 2-(4-хлор-2-гідроксиметилфенокси)-1-[4-(4-фторбензил)-2,5-диметилпіперазин-1-іл]етанону (0,55г, 1,3ммоль) в метиленхлориді (6мл) додають тіонілхлорид (0,26г, 3,58ммоль). Реакційну суміш доводять до кипіння протягом 2 годин. Після охолодження реакційну суміш гасять шляхом додавання води. Органічний шар промивають насиченим розчином бікарбонату натрію а далі водним розчином хлориду натрію. Потім органічний шар концентрують для отримання сполуки, вказаної в назві винаходу, у вигляді жовтого масла (0,52г). (5-хлор-2-{2-[4-(4-фторбензил)-(2R,5S)-2,5-диметилпіперазин-1-іл]-2-оксоетокси)феніл)метансульФокислота До 2-(4-хлор-2-хлорметилфенокси)-1-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]етанону (0,52г, 1,2ммоль) в співвідношенні 1:1 етанол:вода (6мл) додають сульфат натрію (0,75г, 5,97ммоль). Реакційну суміш доводять до кипіння протягом 12 годин. Після охолодження реакційну суміш концентрують і очищують шля хом хроматографії на силікагелі, для отримання сполуки, вказаної в назві винаходу (0,39г) у вигляді солі натрію. Приклад 2 (5-Хлор-2-{2-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}феніл)-метансульфокислота (3R)-1-(4-фторбензил)-3-метилпіперазин До розчину (2R)-2-метилпіперазину (4,5г, 45ммоль) в етанолі (80мл) додають 4-фторбензилхлорид (5,38мл, 45,0ммоль) і гідрокарбонат натрію (11,3г, 135ммоль). Реакційну суміш протягом ночі доводять до кипіння, охолоджують і концентрують. Осад, що залишився, розводять дихлорметаном і промивають водою. Органічний шар відокремлюють і концентрують для отримання чистого масла. Шляхом хроматографії на силікагелі, отримують сполуку, вказану в назві винаходу (5,0г). 2-Хлор-1-(2-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]етанон До розчину (3R)-1-(4-фторбензил)-3-метилпіперазину (3г, 14,4ммоль) в дихлорметані (40мл) додають триетиламін (2,0мл, 14,4ммоль). Реакційну суміш охолоджують до 0°С і додають хлорацетилхлорид (1,1мл, 14,4ммоль). Реакційну суміш залишають нагріватися до температури навколишнього середовища і перемішують протягом 2 годин. Реакційну суміш розводять дихлорметаном і промивають 10% лимонною кислотою. Органічний шар відокремлюють, висушують над сульфатом магнію, фільтрують і концентрують у вакуумі. Шляхом хроматографії на силікагелі, отримують сполуку, вказану в назві винаходу (3,9г). 5-Хлор-2-(2-[4-(4-фторбензил)-(2R,5S)-2R-метилпіперазин-1-іл1-2-оксоетокси)бензальгід До розчину 2-хлор-1-[4-(4-фторбензил)-(2R,5S)-2,5-метилпіперазин-1-іл]етанону (0,1г, 0352ммоль) в диметилформаміді (5мл) додають 5-хлорсаліцилальдегід (60мг, 0,387ммоль), карбонат калію (97мг, 0,704ммоль) і йодид калію (58мг, 0,352ммоль). Суміш, що утворилась в результаті, нагрівають до 65°С протягом 2 годин. Реакційну суміш охолоджують і в вакуумі видаляють диметилформамід. Неочищену реакційну суміш розводять етилацетатом, промивають насиченим водним розчином солі, а органічний шар висушують над сульфатом магнію і фільтрують. Фільтрат концентрують у вакуумі для отримання сполуки, вказаної в назві винаходу (140мг), що безпосередньо використовують на наступній стадії. (5-Хлор-2-(2-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси)феніл)-метансульфокислота До розчину 5-хлор-2-{2-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]-2-оксоетокси}-бензальгіду (90мг, 0,223ммоль) в тетрагідрофурані (2мл) додають борогідрид натрію (25мг, 0,667ммоль). Через 1 годину реакційну суміш розводять етилацетатом і промивають спочатку водою, а потім сольовим розчином. Органічний шар висушують над сульфатом магнію, фільтрують і концентрують в вакуумі для отримання відповідного спирту, що використовують на наступній стадії. До 2-(4-хлор-2-гідроксиметилфенокси)-1-[4-(4-фторбензил)-(2R,5S)-2R-метилпіперазин-1-іл]етанону (0,223ммоль) в метиленхлориді (3мл) додають тіонілхлорид (0,04мл, 0,558ммоль). Реакційну суміш доводять до кипіння протягом 1 години. Після охолодження реакційну суміш розводять додатковою кількістю метиленхлориду, промивають насиченим водним розчином бікарбонату натрію, а потім сольовим розчином. Потім органічний шар висушують над сульфатом магнію і концентрують в вакуумі для отримання відповідного хлориду у вигляді жовтого масла, що використовують в на наступній стадії. До 2-(4-хлор-2-гідроксиметилфенокси)-1-[4-(4-фторбензил)-2R-метилпіперазин-1-іл]етанону (0,223ммоль) в співвідношенні 1:1 етанол:вода (2мл) додають сульфат натрію (0,75г, 5,97ммоль). Реакційну суміш доводять до кипіння протягом 12 годин. Після охолодження реакційну суміш концентрують у вакуумі і очищують шляхом хроматографії на силікагелі для отримання сполуки, вказаної в назві винаходу (приклад 2) у вигляді натрієвої солі (10мг). Приклад 3 2-(5-Хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}феніл)етансульфокислота (5-Хлор-2-метоксифеніл)метанол До розчину метилового естеру 5-хлор-2-метоксибензойної кислоти (20г, 9,97ммоль) в THF (100мл) при температурі 0°С додають по краплям розчин літійалюмінійгідриду (210мл, 210ммоль, 1М розчин в THF). Далі розчин доводять до кипіння протягом 2 годин. Реакційну суміш охолоджують до 0°С і обережно гасять шляхом додавання холодної води. Суміш фільтрують через целіт, а осад на фільтрі промивають діетиловим етером. Фільтрат промивають насиченим водним розчином гідрокарбонату натрію потім висушують над сульфатом магнію. Шляхом концентрування в вакуумі отримують сполуку, вказану в назві винаходу (17,2г). (5-Хлор-2-метоксифеніл)аиетонітрил До розчину (5-хлор-2-метоксифеніл)метанолу (17,1г, 99,1ммоль) в метиленхлориді (100мл) додають тіонілхлорид (14,5мл, 198ммоль). Реакційну суміш перемішують при температурі кипіння протягом 3 годин, охолоджують до кімнатної температури і концентрують в вакуумі. Неочищений продукт розчиняють в метиленхлориді і промивають насиченим водним розчином гідрокарбонату натрію, потім висушують над сульфатом магнію. Шляхом концентрування в вакуумі отримують 4-хлор-2-хлорметил-1-метоксибензол (18,4г). До розчину 4-хлор-2-хлорметил-1-метоксибензолу (18,4г, 96,4ммоль) в ацетонітрилі (100мл) додають ціанід калію (12,5г, 193ммоль) і 18-краун-6 (2,54г, 9,64ммоль). Реакційну суміш перемішують протягом 12 годин при температурі навколишнього середовища, розводять етилацетатом і промивають насиченим водним розчином гідрокарбонату натрію. Органічний шар висушують над сульфатом магнію і концентрують у вакуумі. Неочищений продукт очищають шляхом пропускання його через силікагель, елююючи метиленхлоридом для отримання сполуки, вказаної в назві винаходу (17,2г). (5-Хлор-2-метоксифеніл)оитова кислота До розчину (5-хлор-2-метоксифеніл)ацетонітрилу (17,2г, 96,3ммоль) в етанолі (200мл) і воді (20мл) додають гідроксид калію (27г, 481ммоль). Реакційну суміш доводять до кипіння протягом 12 годин, охолоджують і видаляють етанол шляхом концентрування в вакуумі. Розчин, що лишився, підкислюють водним розчином соляної кислоти (3М) і екстрагують діетиловим етером. Органічний шар висушують над сульфатом магнію і концентрують в вакуумі для отримання сполуки, вказаної в назві винаходу (15,6г). Етиловий естер (5-хлор-2-метоксиФеніл)оитової кислоти Розчин (5-хлор-2-метоксифеніл)оцтової кислоти (15,5г, 77,5ммоль) в 48% водному розчині броміду водню доводять до кипіння протягом 20 годин. Розчин охолоджують, розводять водою і екстрагують діетиловим етером. Органічний шар висушують над сульфатом магнію і концентрують в вакуумі. Неочищений продукт очищають шляхом розтирання в суміші 2:1 метиленхлорид : гексан для отримання (5хлор-2-гідроксифеніл)-оцтової кислоти (12,8г). Її розчиняють в розчині етанолу, насиченого соляною кислотою і перемішують протягом 12 годин. Реакційну суміш концентрують в вакуумі, потім сирий продукт розчиняють в діетиловому етері і промивають насиченим водним розчином гідрокарбонату натрію. Органічний шар висушують над сульфатом магнію, фільтрують і концентрують в вакуумі для отримання сполуки, вказаної в назві винаходу (12,7г). Етиловий естер (5-хлор-2-(2-[4-(4-фтообензил)-2,5-диметилпіперазин-1-іл]-2-оксоетокси}-феніл)оцтової кислоти До розчину 2-хлор-1-[4-(4-фторбензил)-(2R,5S)-2,5-диметилпіперазин-1-іл]етанону (3,3г, 11,0ммоль) в 2бутаноні (100мл) додають етиловий естер (5-хлор-2-гідроксифеніл)оцтової кислоти (2,3г, 11,0ммоль), карбонат калію (3,05г, 22,1ммоль) і йодид калію (1,83г, 11,0ммоль). Реакційну суміш доводили до кипіння протягом 48 годин. Розчин охолоджують, розводять етилацетатом і промивають сольовим розчином. Органічний шар висушують над сульфа том магнію, фільтрують і концентрують в вакуумі. Неочищений продукт очищають шляхом розчинення в дихлорметані і пропускання через шар силікагелю. Шляхом концентрування в вакуумі отримують сполуку, вказану в назві винаходу (5,13г). 2-[4-хлор-2-(2-гідроксиетил)фенікси]-1-[4-(4-фторбензил)-2R,5S-диметилпіпеоазин-1-іл]-етанон До розчину етилового естеру (5-хлор-2-{2-[4-(4-фторбензил)-2,5-диметилпіперазин-1-іл]-2оксоетокси}феніл)оцтової кислоти (0,05г, 0,1ммоль) в трет-бутанолі (1мл) додають борогідрид літію (0,01г, 0,26ммоль). Реакційну суміш доводять до кипіння і через годину додають метанол (0,2мл). Через 1 годину реакційну суміш промивають сольовим розчином, висушують над сульфатом магнію, фільтрують і концентрують в вакуумі і очищають хроматографією на силікагелі для отримання сполуки, вказаної в назві винаходу (0,04г). 2-(5-Хлор-2-[2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл1-2-оксоетокси)феніл)етансульфокислота До 2-[4-хлор-2-(2-гідроксиетил)фенокси]-1-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]етанону (0,072г, 0,166ммоль) в метиленхлориді (2мл) додають тіонілхлорид (0,1мл, 0,83ммоль). Реакційну суміш перемішують при кімнатній температурі протягом 14 годин і доводять до кипіння протягом ще 3 годин. Після охолодження реакційну суміш гасять шляхом додавання води і розбавляють додатковою кількістю метиленхлориду. Органічний шар промивають насиченим розчином бікарбонату натрію, а потім насиченим водним розчином хлориду натрію. Органічний шар потім концентрують для отримання відповідного хлориду у вигляді коричневого масла (0,075г). До 2-[4-хлор-2-(2-хлоретил)фенокси]-1-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]етанону (0,075г, 0,166ммоль) в суміші 1:1 етанол:вода (5мл) додають сульфат натрію (0,1г, 0,79ммоль) і йодид натрію (0,024г, 0,16ммоль). Реакційну суміш доводять до кипіння протягом 20 годин. Після охолодження реакційну суміш концентрують і очищують хроматографією на силікагелі для отримання сполуки, вказаної в назві винаходу (6,0мг) у вигляді солі натрію. (5-Хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин-3іл)метансульфокислота 2-[4-(4-Фторбензил)-2R,5S-диметилпіперазин-1іл]-20оксоетиловий естер оцтової кислоти До 2-[4-(4-фторбензил)-2R,5S-диметилпіперазину (2г, 9ммоль) в метиленхлориді (45мл) при температурі 0°С додають триетиламін (1,36мл, 9,9ммоль) і потім хлоркарбонілметиловий естер оцтової кислоти (1,06мл, 9,9ммоль). Через три години реакційну суміш промивають насиченим розчином бікарбонату натрію. Органічний шар висушують над сульфа том магнію, фільтрують, концентрують і очищують хроматографією на силікагелі для отримання сполуки, вказаної в назві винаходу (2,6мг). 1-[4-(4-фторбензил)-(2R,5S)-2,5-диметипіперазин-1-іл]-2-гідроксиетанон До 2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетилового естеру оцтової кислоти (2,6г, 8ммоль) в суміші тетрагідрофуран/метанол/вода (2:2:1, 40мл) додають гідроксидгідрат літію (0,5г, 12ммоль). Через 2 години реакційну суміш концентрують до сухого залишку і переносять в етилацетат. Органічний шар промивають насиченим розчином бікарбонату натрію, висушують над сульфатом магнію, фільтрують і концентрують для отримання сполуки, вказаної в назві винаходу (2,12г). Метиловий естер 5-хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}нікотинової кислоти До 1-[4-(4-фторбензил)-2R,5S-2,5-диметипіперазин-1-іл]-2-гідроксиетанону (0,05г, 0,178ммоль) в тетрагідрофурані (1мл) при температурі 0°С додають гідрид натрію (11мг, 0,275ммоль) і потім 18-краун-6 (26мг, 0,10ммоль). Чере15 хвилин реакційну суміш залишають нагріватися до температури навколишнього середовища і повільно додають метиловий естер 2,5-дихлорнікотинової кислоти (55мг, 0,267ммоль) (з модифікацією J. Med. Chem., 1997, 40, 2674) в тетрагідрофурані (0,25мл). Через дві години реакційну суміш гасять насиченим водним розчином бікарбонату натрію і екстрагують тричі етилацетатом. Об'єднані органічні шари промивають сольовим розчином, висушують над сульфатом магнію, фільтрують і концентрують в вакуумі. Шляхом хроматографії на силікагелі отримують сполуку, вказану в назві винаходу (25мг). 2-(5-Хлор-3-гідроксиметилпіридин-2-ілокси)-1-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]етанон До метилового естеру 5-хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2оксоетокси}нікотинової кислоти (24мг, 0,053ммоль) і борогідриду натрію (5мг, 0132ммоль) в трет-бутанолі (1мг) при температурі кипіння додають метанол (0,04мл, 1,06ммоль). Через 90 хвилин реакційну суміш охолоджують до температури навколишнього середовища і видаляють розчинник в вакуумі. Реакційну суміш поміщають в воду і тричі екстрагують метиленхлоридом. Об'єднані органічні шари промивають сольовим розчином, висушують над сульфатом магнію, фільтрують і концентрують в вакуумі. Шляхом хроматографії на силікагелі отримують сполуку, вказану в назві винаходу (22мг). (5-Хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}-піридин-3-іл)метансульфокислота До 2-(5-хлор-3-гідроксиметилпіридин-2-ілокси)-1-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1іл]етанону (0,067г, 0159ммоль) в метиленхлориді (1,5мл) додають тіонілхлорид (0,04мл, 0,49ммоль). Реакційну суміш перемішують при кімнатній температурі протягом однієї години. Реакційну суміш гасять додаванням води і розбавляють додатковою кількістю метиленхлориду. Органічний шар промивають насиченим водним розчином хлориду натрію і висушують над сульфатом магнію. Потім органічний шар концентрують для отримання відповідного хлориду у вигляді коричневого масла. (0,07г). До сполуки 2-(5-хлор-3-гідроксиметилпіридин-2-ілокси)-1-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1іл]етанону (0,05г, 0,161ммоль) в суміші 1:1 етанол:вода (1мл) додають сульфат натрію (0,07г, 0,58ммоль). Реакційну суміш доводять до кипіння протягом 20 годин. Після охолодження реакційну суміш концентрують і очищують шляхом хроматографії на силікагелі для отримання сполуки, вказаної в назві винаходу (46мг) у вигляді солі натрію. Приклади 1-5 Сполуки в Таблиці 1 отримані відповідно до способів, що описані вище № прикладу 1 2 3 4 5 6 ІЮПАК НРМС 5-Хлор-2-{2-[4-(4-фторбензил)-2R,5S-2,5-диметилпіперазин-1-іл]-2485,3 оксоетокси}феніл)метансульфокислота (5-Хлор-2-{2-[4-(4-фторбензил)-2Н-метилпіперазин-1-іл]-2469,1 оксоетокси}феніл)метансульфокислота 2-(5-Хлор-2-{2-[4-(4-фторбензил)-2,5S-диметилпіперазин-1-іл]-2499,4 оксоетокси}феніл)етансульфокислота (5-Хлор-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2-оксоетокси}піридин486,4 3-іл)метансульфокислота 5-Бром-2-{2-[4-(4-фторбензил)-2R,5S-диметилпіперазин-1-іл]-2529,1 оксоетокси}феніл)метансульфокислота 5-Бром-2-{2-[4-(4-фторбензил)-2R-диметилпіперазин-1-іл]-2513,2 оксоетокси}феніл)метансульфокислота
ДивитисяДодаткова інформація
Назва патенту англійськоюSulfonic acids derivatives, pharmaceutical composition and a method for the treatment of inflammations and other disorders of immune system
Назва патенту російськоюПроизводные сульфоновых кислот, фармацевтическая композиция и способ лечения воспалений и других расстройств имунной системы
МПК / Мітки
МПК: A61K 31/496, A61P 9/10, A61P 9/08, A61K 31/495, A61P 31/18, A61P 43/00, A61P 37/00, C07D 401/12, A61P 35/00, C07D 213/64, A61P 19/00, A61P 11/00, A61P 9/00, A61P 31/00, C07D 295/185, A61P 31/12, A61P 37/02, A61P 29/00, A61P 37/08, C07D 241/04
Мітки: розладів, кислот, сульфонових, спосіб, інших, системі, композиція, імунної, запалень, фармацевтична, лікування, похідні
Код посилання
<a href="https://ua.patents.su/19-74266-pokhidni-sulfonovikh-kislot-farmacevtichna-kompoziciya-ta-sposib-likuvannya-zapalen-ta-inshikh-rozladiv-imunno-sistemi.html" target="_blank" rel="follow" title="База патентів України">Похідні сульфонових кислот, фармацевтична композиція та спосіб лікування запалень та інших розладів імунної системи</a>
Попередній патент: Високотеплостійка штампова сталь
Наступний патент: Спосіб перероблення і утилізації відходів буріння під час спорудження свердловин на нафту і газ
Випадковий патент: Транспортний засіб для перевезення молодняку птиці та яєць на інкубацію