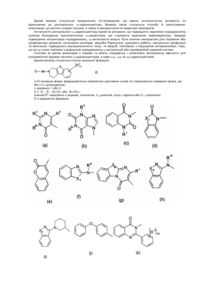
Вторинні аміноанілінові піперидини як антагоністи mch1 та їх застосування
Номер патенту: 77536
Опубліковано: 15.12.2006
Автори: Ветзель Джон, Делеон Джон, Джианг Ю, Чен Чіен-Ан, Лу Кай, Марзабаді Мохамед
Формула / Реферат
1. Сполуки, що мають структуру:
 ,
,
де кожний А являє собою незалежно -Н, -F, -Сl, -Br, -I, -CN, -NO2, -ОR3 або С1-С7 алкіл з прямим або розгалуженим ланцюгом;
де кожний В являє собою незалежно N або СН;
де Z являє собою CO або SO2;
де кожний R являє собою незалежно -Н, -F або С1-С7 алкіл, монофторалкіл або поліфторалкіл з прямим або розгалуженим ланцюгом;
де R4 являє собою незалежно -ОR3, -NНR3, -SR3, -СОR3, С1-С7 алкіл, монофторалкіл або поліфторалкіл з прямим або розгалуженим ланцюгом, арил або гетероарил, де арил або гетероарил необов'язково заміщений одним або більше -F, -Сl, -Br, -I, -OR2 або С1-С7 алкілом з прямим або розгалуженим ланцюгом;
де кожний R3 являє собою незалежно -Н, С1-C7 алкіл, монофторалкіл або поліфторалкіл з прямим або розгалуженим ланцюгом, арил або гетероарил, де арил або гетероарил необов'язково заміщений одним або більше -F, -Сl, -Br, -I, -NO2, -CN, -OR2 або -NHR2;
де кожний R2 являє собою незалежно -Н, С1-C7 алкіл з прямим або розгалуженим ланцюгом, арил або гетероарил, де арил або гетероарил необов'язково заміщений одним або більше - F, -Сl, -Br, -I, -NO2, -CN;
та де n являє собою ціле число від 1 до 6 включно;
або їх фармацевтично прийнятні солі.
2. Сполука за п. 1, де сполука має структуру:
 ,
,
де А, В, Z, n та R4 є такими, як визначено у п. 1.
3. Сполука за п. 2, де сполука має структуру:
 ,
,
де А та Z є такими, як визначено у п. 1;
де R4 являє собою арил або гетероарил, де арил або гетероарил необов'язково заміщений одним або більше -F, -Сl, -Вr, -І, -ОR3 або С1-C7 алкілом з прямим або розгалуженим ланцюгом;
де кожний R3 являє собою С1-С7 алкіл з прямим або розгалуженим ланцюгом, арил або гетероарил, де арил або гетероарил необов'язково заміщений одним або більше -F, -Сl, -Br, -I, -NO2, -CN або -OR2;
де кожний R2 являє собою -H, С1-С7 алкіл з прямим або розгалуженим ланцюгом, арил або гетероарил, де арил або гетероарил необов'язково заміщений одним або більше -F, -Сl, -Br, -І, -NO2, -CN; та
де n є таким, як визначено у п. 1.
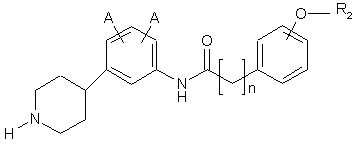
4. Сполука за п. 3, де сполука має структуру:
 ,
,
де А є таким, як визначено у п. 1;
де R2 являє собою -H, С1-С7 алкіл з прямим або розгалуженим ланцюгом, арил або гетероарил, де арил або гетероарил необов'язково заміщений одним або більше -F, -Сl, -Br, -І, -NO2 або -CN; та
де n є таким, як визначено у п. 1.
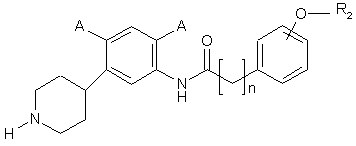
5. Сполука за п. 4, де сполука має структуру:
 ,
,
де А є таким, як визначено у п. 1;
де R2 являє собою С1-С7 алкіл з прямим або розгалуженим ланцюгом, та
де n являє собою ціле число від 3 до 6 включно.
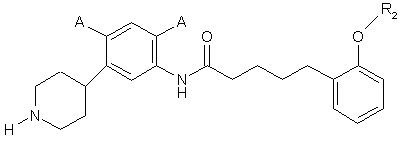
6. Сполука за п. 5, де сполука має структуру:
 ,
,
де кожний А являє собою незалежно -H, -F, -Сl, -Вr або -І, та
R2 є таким, як визначено у п. 5.
7. Сполука за п. 6, де сполука має структуру:
 ,
,
де кожний А являє собою незалежно -H, -F або -Сl, та
де R2 являє собою С1-С3 алкіл з прямим або розгалуженим ланцюгом.
8. Сполука за п. 7, де сполука має структуру:
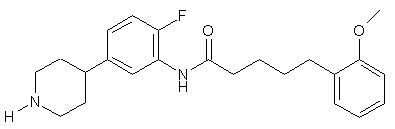 .
.
9. Сполука за п. 7, де сполука має структуру:
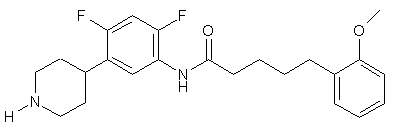 .
.
10. Сполука за п. 2, де сполука має структуру:
 ,
,
де А є таким, як визначено у п. 1, та
де R2 являє собою арил, де арил необов'язково заміщений одним або більше -F, -Сl, -Вr, -І, -NO2 або -CN, та
де n являє собою ціле число від 1 до 6 включно.
11. Сполука за п. 10, де сполука має структуру:
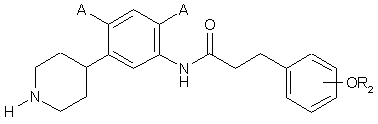 ,
,
де кожний А являє собою незалежно -Н, -F, -Сl, -Вr або -І, та
де R2 є таким, як визначено у п. 10.
12. Сполука за п. 11, де сполука має структуру:
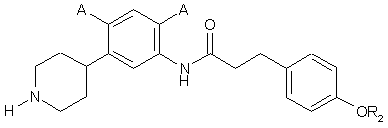 ,
,
де кожний А являє собою незалежно -Н, -F або -Сl, та
де R2 являє собою арил, необов'язково заміщений одним або більше -Н, -F, -Сl або -Вr.
13. Сполука за п. 12, де сполука має структуру:
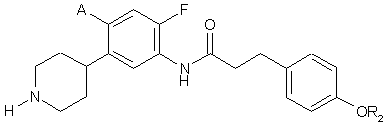 ,
,
де кожний А являє собою незалежно -Н, -F або -Сl, та
де R2 являє собою арил, необов'язково заміщений одним або більше -F.
14. Сполука за п. 13, де сполука має структуру:
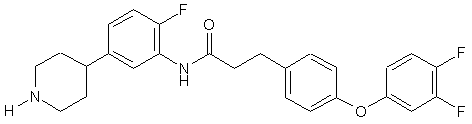 .
.
15. Сполука за п. 2, де сполука має структуру:
 ,
,
де A, Z, n та R4 є такими, як визначено у п. 1.
16. Сполука за п. 15, де сполука має структуру:
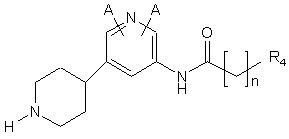 ,
,
де А є таким, як визначено у п. 1, та
де R4 являє собою арил, необов'язково заміщений одним або більше -F, -Сl, -Вr, -І, -ОR3 або С1-С7 алкілом з прямим або розгалуженим ланцюгом;
де кожний R3 являє собою незалежно С1-C7 алкіл з прямим або розгалуженим ланцюгом, арил або гетероарил, де арил або гетероарил необов'язково заміщений одним або більше -F, -Сl, -Вr, -І, -NO2, -CN або -OR2;
де кожний R2 являє собою незалежно С1-С7 алкіл з прямим або розгалуженим ланцюгом; та
де n є таким, як визначено у п. 1.
17. Сполука за п. 2, де сполука має структуру:
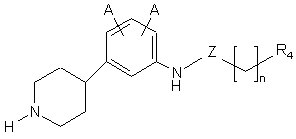 ,
,
де А є таким, як визначено у п. 1;
де Z є таким, як визначено у п. 1;
де R4 являє собою незалежно -OR3, -NHR3, -СОR3 або -SR3;
де кожний R3 являє собою незалежно С1-C7 алкіл з прямим або розгалуженим ланцюгом, арил або гетероарил, де арил або гетероарил необов'язково заміщений одним або більше -F, -Сl, -Br, -I, -NO2, -CN, -OR2 або -NHR2;
де R2 являє собою -Н, С1-С7 алкіл з прямим або розгалуженим ланцюгом або арил, де арил необов'язково заміщений одним або більше - F, -Сl, -Br, -I, -NO2, -CN; та
де n являє собою ціле число від 1 до 6 включно.
18. Сполука за п. 17, де сполука має структуру:
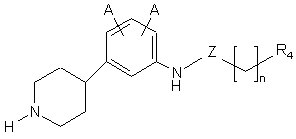 ,
,
де Z є таким, як визначено у п. 1;
де кожний А являє собою незалежно -Н, -F, -Сl, -Br або -І;
де R4 являє собою незалежно -ОR3, -NHR3 або -СОR3;
де R3 являє собою арил, необов'язково заміщений одним або більше -F, -Сl, -Br, -І, -NO2, -CN, -OR2 або -NHR2;
де кожний R2 являє собою незалежно -Н, С1-С7 алкіл з прямим або розгалуженим ланцюгом або арил, необов'язково заміщений одним або більше -F, -Сl, -Br, -І, -NO2, -CN; та
де n являє собою ціле число від 1 до 6 включно.
19. Сполука за п. 18, де сполука має структуру:
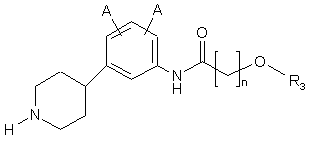 ,
,
де кожний А являє собою незалежно -Н або -F;
де R3 являє собою арил, необов'язково заміщений одним або більше -F, -Сl, -Вr, -І, -NO2, -CN, -OR2 або -NHR2;
де R2 являє собою незалежно С1-С7 алкіл з прямим або розгалуженим ланцюгом або арил, необов'язково заміщений одним або більше -F, -Сl, -Вr або -І, та
де n являє собою ціле число від 1 до 6 включно.
20. Сполука за п. 17, де сполука має структуру:
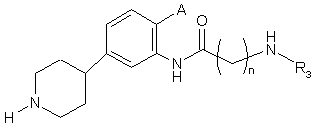 ,
,
де А являє собою незалежно -Н, -F, -Сl, -Вr або -І;
де R3 являє собою арил, необов'язково заміщений -NHR2; та
де R2 являє собою арил, необов'язково заміщений одним або більше -F, -Сl, -Вr, -І.
21. Сполука за п. 20, де сполука має структуру:
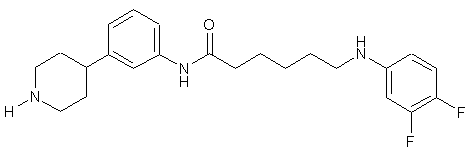 .
.
22. Сполука за п. 18, де сполука має структуру:
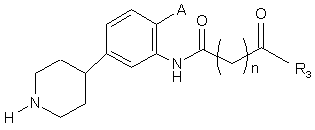 .
.
23. Сполука за п. 18, де сполука має структуру:
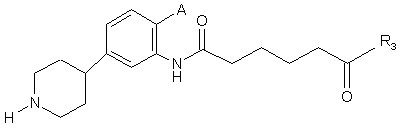 ,
,
де А являє собою незалежно -Н, -F, -Сl, -Вr або -І;
де R3 являє собою арил, необов'язково заміщений одним або більше -F, -Сl, -Вr або -І.
24. Сполука за п. 23, де сполука має структуру:
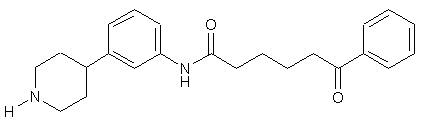 .
.
25. Сполука за п. 23, де сполука має структуру:
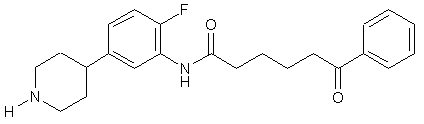 .
.
26. Фармацевтична композиція, що містить сполуку за п. 1 та фармацевтично прийнятний носій.
27. Фармацевтична композиція, виготовлена шляхом змішування сполуки за п. 1 та фармацевтично прийнятного носія.
28. Спосіб виготовлення фармацевтичної композиції, який включає змішування сполуки за п. 1 з фармацевтично прийнятним носієм.
29. Спосіб лікування суб'єкта, що страждає на розлад, опосередкований рецептором МСН1, який включає введення суб'єктові терапевтично ефективної кількості сполуки за п. 1.
30. Спосіб за п. 29, де терапевтично ефективна кількість становить кількість від приблизно 0,03 до приблизно 300 мг.
31. Спосіб за п. 29, де розлад являє собою депресію.
32. Спосіб за п. 29, де розлад являє собою тривожний стан.
33. Спосіб за п. 29, де розлад являє собою ожиріння.
34. Спосіб за п. 29, де розлад являє собою нетримання сечі.
35. Спосіб лікування суб'єкта, що страждає на депресію, тривожний стан, нетримання сечі або ожиріння, який включає введення суб'єктові терапевтично ефективної кількості сполуки за п. 1.
36. Спосіб за п. 35, де терапевтично ефективна кількість становить від приблизно 0,03 до приблизно 300 мг.
37. Спосіб за п. 35, де суб'єкт страждає на депресію.
38. Спосіб за п. 35, де суб'єкт страждає на тривожний стан.
39. Спосіб за п. 35, де суб'єкт страждає на ожиріння.
40. Спосіб за п. 35, де суб'єкт страждає на нетримання сечі.
Текст
УКРАЇНА (19) UA 77536 (11) (13) C2 (51) МПК A61K 31/451 (2006.01) A61K 31/4545 (2006.01) A61K 31/506 (2006.01) A61P 3/04 (2006.01) A61P 13/02 (2006.01) A61P 25/22 (2006.01) A61P 25/24 (2006.01) A61P 43/00 (2006.01) C07D 211/26 (2006.01) C07D 401/12 (2006.01) МІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ ДЕРЖАВНИЙ ДЕПАРТАМЕНТ ІНТЕЛЕКТУАЛЬНОЇ ВЛАСНОСТІ ОПИС ДО ПАТЕНТУ НА ВИНАХІД (54) ВТОРИННІ АМІНОАНІЛІНОВІ ПІПЕРИДИНИ ЯК АНТАГОНІСТИ MCH1 ТА ЇХ ЗАСТОСУВАННЯ B H N N H Z * B A N H R4 R n R , де кожний А являє собою незалежно -Н, -F, -Сl, Br, -I, -CN, -NO2, -ОR3 або С1-С7 алкіл з прямим або розгалуженим ланцюгом; де кожний В являє собою незалежно N або СН; де Z являє собою CO або SO2; де кожний R являє собою незалежно -Н, -F або С1С7 алкіл, монофторалкіл або поліфторалкіл з прямим або розгалуженим ланцюгом; де R4 являє собою незалежно -ОR3, -NНR3, -SR3, СОR3, С1-С7 алкіл, монофторалкіл або поліфторалкіл з прямим або розгалуженим ланцюгом, арил H Z * R4 n C2 (13) N , де А, В, Z, n та R4 є такими, як визначено у п. 1. 3. Сполука за п. 2, де сполука має структуру: A A N H H 77536 B A A Z * R4 n N , де А та Z є такими, як визначено у п. 1; де R4 являє собою арил або гетероарил, де арил або гетероарил необов'язково заміщений одним UA A або гетероарил, де арил або гетероарил необов'язково заміщений одним або більше -F, -Сl, -Br, -I, OR2 або С1-С7 алкілом з прямим або розгалуженим ланцюгом; де кожний R3 являє собою незалежно -Н, С1-C7 алкіл, монофторалкіл або поліфторалкіл з прямим або розгалуженим ланцюгом, арил або гетероарил, де арил або гетероарил необов'язково заміщений одним або більше -F, -Сl, -Br, -I, -NO2, -CN, OR2 або -NHR2; де кожний R2 являє собою незалежно -Н, С1-C7 алкіл з прямим або розгалуженим ланцюгом, арил або гетероарил, де арил або гетероарил необов'язково заміщений одним або більше - F, -Сl, -Br, -I, NO2, -CN; та де n являє собою ціле число від 1 до 6 включно; або їх фармацевтично прийнятні солі. 2. Сполука за п. 1, де сполука має структуру: (19) (21) 20041210489 (22) 03.07.2003 (24) 15.12.2006 (86) PCT/US2003/021391, 03.07.2003 (31) 10/189,145 (32) 03.07.2002 (33) US (46) 15.12.2006, Бюл. № 12, 2006 р. (72) Марзабаді Мохамед , US, Джианг Ю , US, Лу Кай , US, Чен Чіен-Ан , US, Делеон Джон , US, Ветзель Джон, US (73) Х. ЛУННБЕК А/С, DK (56) WO 2004/005257 A1 Borowsky, et al., Nature Medicine, 2003 Takekawa, S., et al., " T-226296: a novel, orally active and selective melanin-concentrating hormone receptor antagonist " Eur J Pharmacol 438 (3) :12935 (2002) (57) 1. Сполуки, що мають структуру: 2 (11) 1 3 77536 4 або більше -F, -Сl, -Вr, -І, -ОR3 або С1-C7 алкілом з F O O прямим або розгалуженим ланцюгом; де кожний R3 являє собою С1-С7 алкіл з прямим N або розгалуженим ланцюгом, арил або гетероаH N рил, де арил або гетероарил необов'язково заміH . щений одним або більше -F, -Сl, -Br, -I, -NO2, -CN 9. Сполука за п. 7, де сполука має структуру: або -OR2; F F де кожний R2 являє собою -H, С1-С7 алкіл з пряO O мим або розгалуженим ланцюгом, арил або гетероарил, де арил або гетероарил необов'язково N H заміщений одним або більше -F, -Сl, -Br, -І, -NO2, N H CN; та . де n є таким, як визначено у п. 1. 10. Сполука за п. 2, де сполука має структуру: 4. Сполука за п. 3, де сполука має структуру: R2 O A A A R2 O A O O N H H N H n N , де А є таким, як визначено у п. 1; де R2 являє собою -H, С1-С7 алкіл з прямим або розгалуженим ланцюгом, арил або гетероарил, де арил або гетероарил необов'язково заміщений одним або більше -F, -Сl, -Br, -І, -NO2 або -CN; та де n є таким, як визначено у п. 1. 5. Сполука за п. 4, де сполука має структуру: A A O H , де А є таким, як визначено у п. 1, та де R2 являє собою арил, де арил необов'язково заміщений одним або більше -F, -Сl, -Вr, -І, -NO2 або -CN, та де n являє собою ціле число від 1 до 6 включно. 11. Сполука за п. 10, де сполука має структуру: A H H n N , де А є таким, як визначено у п. 1; де R2 являє собою С1-С7 алкіл з прямим або розгалуженим ланцюгом, та де n являє собою ціле число від 3 до 6 включно. 6. Сполука за п. 5, де сполука має структуру: A A R2 O N , де кожний А являє собою незалежно -H, -F, -Сl, -Вr або -І, та R2 є таким, як визначено у п. 5. A R2 O O N H H N , де кожний А являє собою незалежно -H, -F або -Сl, та де R2 являє собою С1-С3 алкіл з прямим або розгалуженим ланцюгом. 8. Сполука за п. 7, де сполука має структуру: N H N A OR2 A O N H N OR2 , де кожний А являє собою незалежно -Н, -F або -Сl, та де R2 являє собою арил, необов'язково заміщений одним або більше -Н, -F, -Сl або -Вr. 13. Сполука за п. 12, де сполука має структуру: A 7. Сполука за п. 6, де сполука має структуру: A O , де кожний А являє собою незалежно -Н, -F, -Сl, -Вr або -І, та де R2 є таким, як визначено у п. 10. 12. Сполука за п. 11, де сполука має структуру: H O N H H A R2 O N H n N H F O N H N OR 2 , де кожний А являє собою незалежно -Н, -F або -Сl, та де R2 являє собою арил, необов'язково заміщений одним або більше -F. 14. Сполука за п. 13, де сполука має структуру: F H N O F N H O F . 15. Сполука за п. 2, де сполука має структуру: 5 A N A Z * N H H R4 n 77536 6 арил, необов'язково заміщений одним або більше -F, -Сl, -Br, -І, -NO2, -CN; та де n являє собою ціле число від 1 до 6 включно. 19. Сполука за п. 18, де сполука має структуру: A A N O , де A, Z, n та R4 є такими, як визначено у п. 1. 16. Сполука за п. 15, де сполука має структуру: A A N O R4 N H H n N , де А є таким, як визначено у п. 1, та де R4 являє собою арил, необов'язково заміщений одним або більше -F, -Сl, -Вr, -І, -ОR3 або С1-С7 алкілом з прямим або розгалуженим ланцюгом; де кожний R3 являє собою незалежно С1-C7 алкіл з прямим або розгалуженим ланцюгом, арил або гетероарил, де арил або гетероарил необов'язково заміщений одним або більше -F, -Сl, -Вr, -І, NO2, -CN або -OR2; де кожний R2 являє собою незалежно С1-С7 алкіл з прямим або розгалуженим ланцюгом; та де n є таким, як визначено у п. 1. 17. Сполука за п. 2, де сполука має структуру: A A N H H R4 Z * n N , де А є таким, як визначено у п. 1; де Z є таким, як визначено у п. 1; де R4 являє собою незалежно -OR3, -NHR3, -СОR3 або -SR3; де кожний R3 являє собою незалежно С1-C7 алкіл з прямим або розгалуженим ланцюгом, арил або гетероарил, де арил або гетероарил необов'язково заміщений одним або більше -F, -Сl, -Br, -I, NO2, -CN, -OR2 або -NHR2; де R2 являє собою -Н, С1-С7 алкіл з прямим або розгалуженим ланцюгом або арил, де арил необов'язково заміщений одним або більше - F, -Сl, -Br, I, -NO2, -CN; та де n являє собою ціле число від 1 до 6 включно. 18. Сполука за п. 17, де сполука має структуру: A H R3 n N , де кожний А являє собою незалежно -Н або -F; де R3 являє собою арил, необов'язково заміщений одним або більше -F, -Сl, -Вr, -І, -NO2, -CN, -OR2 або -NHR2; де R2 являє собою незалежно С1-С7 алкіл з прямим або розгалуженим ланцюгом або арил, необов'язково заміщений одним або більше -F, -Сl, Вr або -І, та де n являє собою ціле число від 1 до 6 включно. 20. Сполука за п. 17, де сполука має структуру: A O N H H H N R3 n N , де А являє собою незалежно -Н, -F, -Сl, -Вr або -І; де R3 являє собою арил, необов'язково заміщений -NHR2; та де R2 являє собою арил, необов'язково заміщений одним або більше -F, -Сl, -Вr, -І. 21. Сполука за п. 20, де сполука має структуру: O H N H N N H F F . 22. Сполука за п. 18, де сполука має структуру: A N H H O O n R3 N . 23. Сполука за п. 18, де сполука має структуру: A O R3 A N H H O N H N H R4 Z * n N , де Z є таким, як визначено у п. 1; де кожний А являє собою незалежно -Н, -F, -Сl, -Br або -І; де R4 являє собою незалежно -ОR3, -NHR3 або СОR3; де R3 являє собою арил, необов'язково заміщений одним або більше -F, -Сl, -Br, -І, -NO2, -CN, -OR2 або -NHR2; де кожний R2 являє собою незалежно -Н, С1-С7 алкіл з прямим або розгалуженим ланцюгом або H O N , де А являє собою незалежно -Н, -F, -Сl, -Вr або -І; де R3 являє собою арил, необов'язково заміщений одним або більше -F, -Сl, -Вr або -І. 24. Сполука за п. 23, де сполука має структуру: O H N N H O . 25. Сполука за п. 23, де сполука має структуру: 7 77536 8 32. Спосіб за п. 29, де розлад являє собою тривоO жний стан. 33. Спосіб за п. 29, де розлад являє собою ожиN H ріння. N O H . 34. Спосіб за п. 29, де розлад являє собою нетри26. Фармацевтична композиція, що містить сполумання сечі. ку за п. 1 та фармацевтично прийнятний носій. 35. Спосіб лікування суб'єкта, що страждає на де27. Фармацевтична композиція, виготовлена шляпресію, тривожний стан, нетримання сечі або ожихом змішування сполуки за п. 1 та фармацевтично ріння, який включає введення суб'єктові терапевприйнятного носія. тично ефективної кількості сполуки за п. 1. 28. Спосіб виготовлення фармацевтичної компо36. Спосіб за п. 35, де терапевтично ефективна зиції, який включає змішування сполуки за п. 1 з кількість становить від приблизно 0,03 до приблифармацевтично прийнятним носієм. зно 300 мг. 29. Спосіб лікування суб'єкта, що страждає на ро37. Спосіб за п. 35, де суб'єкт страждає на депрезлад, опосередкований рецептором МСН1, який сію. включає введення суб'єктові терапевтично ефек38. Спосіб за п. 35, де суб'єкт страждає на тривожтивної кількості сполуки за п. 1. ний стан. 30. Спосіб за п. 29, де терапевтично ефективна 39. Спосіб за п. 35, де суб'єкт страждає на ожикількість становить кількість від приблизно 0,03 до ріння. приблизно 300 мг. 40. Спосіб за п. 35, де суб'єкт страждає на нетри31. Спосіб за п. 29, де розлад являє собою депремання сечі. сію. F Ця заявка подана з проханням про встановлення пріоритету за заявкою США №10/189,145, поданої 3 липня 2002p., зміст якої включено в цю заявку шляхом посилання. У даній заявці приведені шляхом посилання різні публікації, у дужках зазначені автор і рік. Повну бібліографію стосовно цих посилань можна знайти наприкінці опису винаходу безпосередньо перед формулою винаходу. Опис цих публікацій у їхньому повному обсязі включено в цю заявку для більш докладного опису стану сучасного рівня галузі, до якого відноситься даний винахід. Меланін-концентрувальний гормон (МСН) є циклічним пептидом, що спочатку був виділений зі слизистої лосося (гольця) [Kawauchi et al., 1983]. Пептид, що складається з 17 амінокислот, викликав у риби агрегаціюмеланіну в меланофорах та інгібував вивільнення АКТГ, діючи як функціональний антагоніст -МСГ. У пацюків, мишей і людини МСН ссавців (19 амінокислот) високо консервативний, має 100% амінокислотну ідентичність, але його фізіологічна роль чітко не визначена. Повідомлялося, що МСН бере участь у різних процесах, включаючи харчування, водний баланс, енергетичний метаболізм, стан загального порушення ЦНС і уваги, пам'ять і когнітивні функції і психічні розлади [як огляд дивіться Baker, 1991, Baker, 1994, Nahon, 1994, Knigge et al., 1996]. Його роль у харчуванні або регуляції маси тіла була підтверджена в останній публікації в журналі Nature [Qu et al., 1996], у якій було показано, що МСН дуже сильно експресується в гіпоталамусі мишей ob/ob у порівнянні з мишами ob/+ та що голодування сприяло підвищенню мРНК МСН як у нормальних мишей, так і в мишей, що страждають на ожиріння, під час голодування. При введенні в бокові шлуночки МСН також стимулює прийом їжі у нормальних пацюків [Rossi et al., 1997]. Також повідомлялося, що МСН викликає фун кціональний антагонізм поведінкових ефектів МСГ [Miller et al., 1993, Gonzalez et al, 1996, Sanchez et al., 1997]; крім того, було показано, що стрес збільшує рівні мРНК ПОМК поряд зі зменшенням рівнів мРНК препроМСН попередника МСН (ррМСН) [Presse et al., 1992]. Таким чином, МСН може служити інтегративним нейропептидом, залученим до стресових реакцій, а також до регуляції харчування і сексуальної активності [Baker, 1991, Knigge et al., 1996]. Вважають, що біологічні ефекти МСН викликаються за допомогою специфічних рецепторів. Повідомлялося, що ліганд, мічений тритієм ([3Н]МСН), має специфічне зв'язування у відношенні мембран мозку, але був невідповідним для аналізу насичування, тому ні афінність, ні Вmах не були визначені [Drozdz and Eberle, 1995]. Введення радіоактивного йоду в 13 положенні тирозину приводить до істотного зниження біологічної активності ліганду [дивіться Drozdz and Eberle, 1995]. Навпроти, введення радіоактивного йоду в аналог МСН [Phe13, Tyr19]-MCH дало позитивний результат [Drozdz et al., 1995]; ліганд залишився біологічно активним і мав специфічне зв'язування з різноманітними клітинними лініями, включаючи меланому миші (B16-F1, G4F і G4F-7), клітини PC12 і COS. Для клітин G4F-7, КD=0,118нМ і Вmах~1100сайтів/клітину. Важливо, що зв'язування не інгібувалось -МСГ, але слабко інгібувалось ANF пацюка (Кі=116нМ у порівнянні з 12нМ природного МСН) [Drozdz et al., 1995]. Недавно було описано специфічне зв'язування МСН у трансформованих кератиноцитах [Burgaud et al., 1997] і в клітинах меланоми [Drozdz et al., 1998], у результаті дослідження фотозшиванням було зроблено припущення про те, що рецептором є мембранний білок із середньою молекулярною масою 45-50кД, який можна порівняти з діапазоном молекулярної маси суперродини рецепторів GPCR. Дотепер не проводилися радіоавтографічні дослідження лока 9 77536 10 лізації рецептора МСН за допомогою цього ліга(SCA2) [Auburger et al., 1992, Twells et al., 1992]. Це нду. захворювання полягає в нейродегенеративних Локалізація і біологічна активність пептиду розладах, включаючи олівопонтоцеребелярну атМСН наводить на думку, що модуляція активності рофію. рецептора МСН може бути ефективною для багаБільш того, ген хвороби Дар'є на генетичній тьох терапевтичних використань. Для можливого карті розташований у локусі 12q23-24 [Craddock et клінічного використання самою описаною є роль al., 1993]. Хвороба Дар'є характеризується патолоМСН у харчуванні. МСН експресується в бічній гічною адгезією кератиноцитів І і, у деяких родичастині гіпоталамуса, ділянці мозку, залученій до нах, психічними захворюваннями. Маючи на увазі регуляції спраги і голоду [Grillon et al., 1997]; функціональні та нейроанатомічні особливості останнім часом було показано, що орексини А і В, МСН нервової системи головного мозку пацюка і що є сильними орексигенними агентами, дуже людини, ген МСН може бути прекрасним рішенням схожі за розташовуванням з МСН у бічній частині у випадку захворювань SCA2 або Дар'є. Цікаво, гіпоталамуса [Sakurai et al., 1998]. Рівні мРНК МСН що в даному локусі на генетичній карті розташовау цій ділянці мозку збільшуються в пацюків після ні захворювання високого соціального значення. 24 годин відсутності харчування [Herve і Fellman, Дійсно, використовуючи дослідження зв'язування 1997]; після ін'єкції інсуліну спостерігали значне генів, ген, відповідальний за хронічну або гостру збільшення відносної кількості й інтенсивності фаформи спінальних м'язових атрофій, був співвідрбування імунореактивного МСН перикаріону і несений із хромосомою 5ql2-13 [Melki et al., 1990, волокон поряд зі значним збільшенням рівня мРНК Westbrook et al., 1992]. Крім того, незалежний ряд МСН [Bahjaoui-Bouhaddi et al., 1994]. свідчень підтвердив перебування головного локуЗі здатністю МСН стимулювати потребу в їжі у су шизофренії на хромосомі 5ql 1,2-13,3 пацюків [Rossi et al., 1997] узгоджується спостере[Sherrington et al., 1988, Bassett et al., 1988, Gilliam ження, що рівні мРНК МСН у гіпоталамусі миші et al., 1989]. На підставі вищевказаних досліджень ob/ob, що страждає на ожиріння, регулювалися на було припущено, що МСН може відігравати роль у підвищення [Qu et al., 1996] і знижувалися в гіпонейродегенеративних захворюваннях і емоційних таламусі пацюків, які одержували лептин, позитирозладах. вний вплив якого на прийом їжі й масу тіла також Припускають, що додатковим терапевтичним був описаний [Sahu, 1998]. МСН можливо діє як застосуванням сполук, пов'язаних з МСН, є ефекти функціональний антагоніст меланокортинової сисМСН, що спостерігаються в інших біологічних системи у випадку його впливу на прийом їжі та на темах. Наприклад, МСН може регулювати репрогормональну секрецію ΗΡΑ (гіпоталамодуктивні функції у самців і самок пацюків. Транскгіпофізано-адреналова система) [Ludwig et al., рипти МСН і пептиди МСН були виявлені в 1998]. Усі ці дані наводять на думку щодо ролі енембріональних клітинах яєчок дорослих пацюків, догенного МСН у регуляції енергетичного балансу що дало припущення про те, що МСН може брати та відповіді на стрес і дають підставу для розвитку участь у відновленні стовбурних клітин і/або диспецифічних сполук, які діють на рецептори МСН, ференціації ранніх сперматоцитів [Hervieu et al., для використання при лікуванні ожиріння і пов'яза1996]. Ін'єкція МСН безпосередньо в серединну них зі стресами розладів. предзорову ділянку (МРОА) або вентромедіальне В усіх видах досліджень, проведених дотепер, ядро (VMN) стимулювало сексуальну активність головна частина нейронів групи клітин МСН має в самок пацюків [Gonzalez et al., 1996]. У пацюків з значній мірі постійну локалізацію в ділянках бічної вилученими яєчниками, яким вводили естрадіол, частини гіпоталамуса і субталамуса, де вони розМСН стимулювали вивільнення лютеїнзувального ташовуються, і може бути частиною деяких, так гормону (LH), тоді як анти-МСН антисироватка званих "екстрапірамідних" рухових ділянок. До них інгібувала вивільнення LH [Gonzalez et al., 1997]. відносяться основні стриато- і палідофугальні Зона інцерта, що містить велику популяцію тіл шляхи, що включають таламус і кору головного клітин МСН, спочатку була ідентифікована як ремозку, гіпоталамічні ділянки і реципрокні зв'язки із гуляторний сайт передовуляційного збільшення субталамічним ядром, чорною субстанцією і LH [MacKenzie et al., 1984]. центрами серединного мозку [Bittencourt et al., Повідомлялося, що МСН впливає на вивіль1992]. За своєю локалізацією групи клітин МСН нення пітуітарних гормонів, включаючи АСТН і ймовірно можуть бути мостом або механізмом для окситоцин. Аналоги МСН також можуть використовстановлення зв'язку гіпоталамічної вісцеральної вуватися при лікуванні епілепсії. На моделі епілепактивності з відповідною і погодженою руховою тичних припадків, викликаних PTZ, ін'єкція МСН до активністю. Клінічно це може мати деяке значення початку припадку запобігала активності судорожпри розгляді можливості залучення цієї системи ного припадку, як у пацюків, так і у морських свиМСН у рухові розлади, такі як хвороба Паркінсона і нок, що означало, що нейрони, що містять МСН, хорея Ґентінґтона, у які, як відомо, залучені екстможуть брати участь у нейрональному ланцюзі, рапірамідні ділянки. що лежить в основі припадку, викликаного PTZ Дослідження зв'язування генів у людини пока[Knigge and Wagner, 1997]. Також були зроблені зали, що автентичний локус МСН, розташований спостереження про те, що МСН впливає на повена 12 хромосомі (12q23-24), і варіантний локус дінкові зв'язки когнітивних функцій. Введення МСН МСН, розташований на 5 хромосомі (5ql2-13) прискорює вгасання реакції пасивного уникнення в [Pedeutour et al., 1994]. Локус 12q23-24 збігається з пацюків [McBride et al., 1994], що збільшує можлилокусом, щодо якого на генетичній карті показана вість того, що антагоністи рецептора МСН можуть аутосомно-домінантна церебелярна атаксія II типу мати корисний вплив на механізми збереження в 11 77536 12 пам'яті та/або утримування в пам'яті. Можлива заним з G-білком. Описується спроможність інгібуроль МСН у модуляції або сприйнятті болю підтвати активацію клонального рецептора, що визнаримується щільною іннервацією періакведуктальчено шляхом аналізів in vitro. ної сірої речовини (PAG) МСН-позитивними волокБільш того, сполуки за цим винаходом також нами. Нарешті, МСН може брати участь у регуляції можуть використовуватися при лікуванні патологіспоживання рідини. ICV інфузія МСН бадьорій вівчних станів, опосередкованих інактивацією рецепці давала діуретичні, натрійуретичні і калійуретичні торів МСН-1, таких як розлади харчування (ожизміни у відповідь на збільшення об'єму плазми ріння, булімія і нейрогенна булімія), [Parkes, 1996]. Разом з анатомічними даними про сексуальні/репродуктивні розлади, депресія, триприсутність МСН в ділянках мозку, що регулюють вожний стан, депресія з тривожним станом, епілегомеостаз рідини, результати показали, що МСН птичні припадки, підвищений кровоносний тиск, може бути важливим пептидом, залученим у геморагічний інсульт, застійна серцева недостатцентральний контроль гомеостазу рідини у ссавність, порушення сну або будь-які стани, при яких ців. може бути ефективний антагонізм до рецептора Недавно була опублікована інформація про МСН1. ідентифікацію рецептора МСН, пов'язаного з GДо того ж, сполуки за цим винаходом можуть білком [Chambers et al., 1999, Saito et al., 1999]. Ці бути ефективними для зниження маси тіла суб'єкгрупи ідентифікували МСН як ендогенний ліганд у та. Крім того, сполуки за цим винаходом можуть відношенні людського рецептора-сироти SLC-1, використовуватися при лікуванні сечових розладів. пов'язаного з G-білком [Lakaye et al., 1998]. ПовіЦим винаходом пропонуються сполуки, що домлялося, що гомологічний йому рецептор у памають структуру. цюка (який зараз називають "МСН-1") локалізований в ділянках головного мозку пацюка, пов'язаних з харчовою поведінкою (наприклад, дорсомедіальний і вентромедіальний гіпоталамус). Зв'язок між МСН-1 і впливом МСН на харчову поведінку був підсилений останніми даними, отриманими на мишах з подавленим МСН-1. Двома групами незалежно було показано [Marsh et al., 2002, Chen et де кожний А являє собою незалежно -Н, -F, al., 2002], що задане руйнування гена рецептора СІ, -Br, -I, -CN, -NO2, -OR3 або С1-С7 алкіл з прямим МСН-1 (нокаут МСН-1) у мишей, приводило до або розгалуженим ланцюгом; того, що тварини страждали на гіперфагію, але де кожний В являє собою незалежно N або були худими і мали знижену масу тіла, у порівнянСН; ні з диким типом того ж приплоду. Зниження маси де Ζ являє собою CO або SO2; тіла зв'язували з підвищенням метаболізму. У коде кожний R являє собою незалежно -Н, -F жній групі було показано, що миші з нокаутом або С1-С7 алкіл, монофторалкіл або поліфторалкіл МСН-1 стійкі до ожиріння, викликаному режимом з прямим або розгалуженим ланцюгом; харчування, і що вони мають ту ж масу, що і миші де R4 являє собою незалежно -OR3, -NHR3, того ж приплоду, які знаходяться на звичайному SR3, -COR3, С1-С7 алкіл, монофторалкіл або полірежимі харчування. фторалкіл з прямим або розгалуженим ланцюгом, Нарешті, у літературі були описані синтетичні арил або гетероарил, де арил або гетероарил неантагоністи рецептора МСН-1. [Bednarek et al. обов'язково заміщений одним або більше -F, -СІ, (2002)] описали синтез високоафінних пептидних Br, -I, -OR2 або С1-С7 алкілом з прямим або розгаантагоністів МСН-1. Більш того, низькомолекулярлуженим ланцюгом; ні антагоністи МСН-1 були описані [Takekawa et al. де кожний R3 являє собою незалежно -Н, С1-С7 (Takekawa et al., 2002)]. Ця сполука, Т-226296, має алкіл, монофторалкіл або поліфторалкіл з прямим високу афінність у відношенні рецептора МСН-1 або розгалуженим ланцюгом, арил або гетероа(~5-9нМ для МСН-1 пацюка і людини), і, як був рил, де арил або гетероарил необов'язково заміпоказано, інгібує прийом їжі, викликаний інтрацещений одним або більше -F, -СІ, -Br, -I, -NO2, -CN, ребровентрикулярним введенням МСН. Ці дані OR2 або -NHR2; підтверджують стратегію використання антагоніста де кожний R2 являє собою незалежно -Н, С1-С7 рецептора МСН-1 для лікування ожиріння. алкіл з прямим або розгалуженим ланцюгом, арил Крім того, у власних дослідженнях заявників або гетероарил, де арил або гетероарил необов'ябули випробувані антагоністи МСН1 на декількох зково заміщений одним або більше -F, -СІ, -Br, -I, тваринних моделях, добре відомих як моделі, що NO2, -CN; прогнозують ефективність сполук у людини та де n являє собою ціле число від 1 до 6 [Borowsky, et al., Nature Medicine 2003)]. Ці експевключно; рименти показують, що антагоністи МСН1 ефектиабо їх фармацевтично прийнятні солі. вні для лікування ожиріння, депресії, тривожного У подальшому варіанті здійснення вищезазнастану, а також сечових розладів. ченого винаходу сполука є енантіомерно та діасТут ми повідомляємо про синтез вторинних теріомерно чистою. В іншому варіанті здійснення аміноанілінових піперидинів, що зв'язуються з клосполука є енантіомерно або діастеріомерно чиснальним рецептором меланін-концентрувального тою. В одному варіанті здійснення сполука являє гормону-1 (МСН1) людини. Крім того, ці сполуки собою (+)-енантіомер. В одному варіанті здійсненселективно зв'язуються з рецептором МСН-1 у ня сполука являє собою (-)-енантіомер. порівнянні з іншим клональним рецептором, зв'яІлюстрацією винаходу є фармацевтична ком 13 77536 14 позиція, що включає фармацевтично прийнятний Br, -I, -OR2 або С1-С7 алкілом з прямим або розганосій та терапевтично ефективну кількість будьлуженим ланцюгом; якої сполуки винаходу. де кожний R3 являє собою незалежно -Н, С1-С7 Ілюстрацією винаходу є фармацевтична комалкіл, монофторалкіл або поліфторалкіл з прямим позиція, виготовлена шляхом змішування будьабо розгалуженим ланцюгом, арил або гетероаякої сполуки, описаної вище, з фармацевтично рил, де арил або гетероарил необов'язково заміприйнятним носієм. щений одним або більше -F, -СІ, -Br, -I, -NO2, -CN, Ілюстрацією винаходу є спосіб виготовлення OR2 або -NHR2; фармацевтичної композиції, який включає змішуде кожний R2 являє собою незалежно -Н, С1-С7 вання будь-якої сполуки винаходу та фармацевтиалкіл з прямим або розгалуженим ланцюгом, арил чно прийнятного носія. або гетероарил, де арил або гетероарил необов'яІлюстрацією винаходу є спосіб синтезу для зково заміщений одним або більше -F, -СІ, -Br, -I, одержання будь-якої сполуки винаходу. NO2, -CN; Прикладом винаходу є спосіб лікування розта де n являє собою ціле число від 1 до 6 ладу, опосередкованого рецептором МСН1 у сувключно; б'єкта, якому це необхідно, який включає введення або їх фармацевтично прийнятні солі. суб'єктові терапевтично ефективної кількості будьВ одному варіанті здійснення сполука має якої сполуки або фармацевтичної композиції винаструктуру: ходу та фармацевтично прийнятного носія. В одному варіанті здійснення терапевтично ефективна кількість становить між приблизно 0,03 та приблизно 300мг. В одному варіанті здійснення розлад являє собою депресію. В одному варіанті здійснення розлад являє собою тривожний стан. В одному варіанті здійснення винаходу розлад являє собою В одному варіанті винаходу сполука має струожиріння. В одному варіанті здійснення винаходу ктуру: розлад являє собою нетримання сечі. Один варіант здійснення винаходу являє собою спосіб лікування суб'єкта, який страждає від розладу, вибраного з депресії, тривожного стану, ожиріння або нетримання сечі, та якому це потрібно, що включає введення суб'єктові терапевтично , ефективної кількості сполуки винаходу. В одному варіанті здійснення терапевтично де R4 являє собою арил або гетероарил, де ефективна кількість становить між приблизно 0,03 арил або гетероарил необов'язково заміщений та приблизно 300мг. одним або більше -F, -Сl, -Вr, -І, -OR3 або С1-С7 В одному варіанті здійснення розлад являє алкілом з прямим або розгалуженим ланцюгом, собою депресію. В одному варіанті здійснення де кожний R3 являє собою С1-С7 алкіл з прярозлад являє собою тривожний стан. В одному мим або розгалуженим ланцюгом, арил або гетеваріанті здійснення винаходу розлад являє собою роарил, де арил або гетероарил необов'язково ожиріння. В одному варіанті здійснення винаходу заміщений одним або більше -F, -СІ, -Br, -I, -NO2, розлад являє собою нетримання сечі. CN або -OR2; та Винаходом пропонуються сполуки, що мають де кожний R2 являє собою -Н, С1-С7 алкіл з структуру: прямим або розгалуженим ланцюгом, арил або гетероарил, де арил або гетероарил необов'язково заміщений одним або більше -F, -СІ, -Вr, -І, NO2, -CN. В одному варіанті здійснення винахід являє собою сполуки, що мають структуру: , де кожний А являє собою незалежно -Н, -F, СІ, -Br, -I, -CN, -NO2, -OR3 або С1-С7 алкіл з прямим або розгалуженим ланцюгом; де кожний В являє собою незалежно N або СН; де Ζ являє собою CO або SO2; де кожний R являє собою незалежно -Н, -F або С1-С7 алкіл, монофторалкіл або поліфторалкіл з прямим або розгалуженим ланцюгом; де R4 являє собою незалежно -OR3, -NHR3, SR3, -COR3, С1-С7 алкіл, монофторалкіл або поліфторалкіл з прямим або розгалуженим ланцюгом, арил або гетероарил, де арил або гетероарил необов'язково заміщений одним або більше -F, -СІ, , де R2 являє собою -Н, С1-С7 алкіл з прямим або розгалуженим ланцюгом або арил, де арил необов'язково заміщений одним або більше -F, СІ, -Br, -I, -NO2 або -CN. В одному варіанті здійснення сполука має структуру. 15 77536 16 , , де R2 являє собою С1-С7 алкіл з прямим або розгалуженим ланцюгом, та де n являє собою ціле число від 3 до 6 включно. Сполука винаходу, де сполука має структуру: де кожний А являє собою незалежно -Н, -F, СІ, -Вr або -І. В одному варіанті здійснення сполука має структуру: , де кожний А являє собою незалежно -Н, -F,-Cl, -Br або -І. В одному варіанті сполука має структуру: де кожний А являє собою незалежно -Н, -F або -СІ; та де R2 являє собою арил, що необов'язково заміщений одним або більше -F, -СІ або -Вr. В одному варіанті здійснення сполука має структуру: , де кожний А являє собою незалежно -Н, -F або -СІ; та де R2 являє собою С1-С3 алкіл з прямим або розгалуженим ланцюгом. Сполука, що має структуру: , де кожний А являє собою незалежно -Н, -F або -СІ; та де R2 являє собою арил, необов'язково заміщений одним або більше -F. В одному варіанті сполука має структуру: Сполука, що має структуру: . В одному варіанті сполука має структуру: . В одному варіанті здійснення сполука має структуру: . В одному варіанті сполука має структуру: , де R2 являє собою арил, де арил необов'язково заміщений одним або більше -F, -СІ, -Br, -I, NO2 або -CN, та де n являє собою ціле число від 1 до 6 включно. В одному варіанті здійснення сполука має структуру: де R4 являє собою арил, необов'язково заміщений одним або більше -F, -СІ, -Вr, -І, -OR3 або С1-С7 алкілом з прямим або розгалуженим ланцюгом; де кожний R3 являє собою незалежно С1-С7 алкіл з прямим або розгалуженим ланцюгом, арил або гетероарил, де арил або гетероарил необов'язково заміщений одним або більше -F, -СІ, -Br, -I, 17 77536 NO2, -CN або -OR2; ка має структуру: де кожний R2 являє собою незалежно С1-С7 алкіл з прямим або розгалуженим ланцюгом. Цим винаходом далі пропонуються сполуки, що мають структуру: 18 , де А являє собою -Н, -F, -СІ, -Вr або -І; де арил необов'язково заміщений одним або більше -F, -СІ, -Вr, -І. Сполука, що має структуру: , де R4 являє собою незалежно -OR3, -NHR3, COR3 або -SR3; де кожний R3 являє собою незалежно С1-С7 алкіл з прямим або розгалуженим ланцюгом, арил або гетероарил, де арил або гетероарил необов'язково заміщений одним або більше -F,-Cl, -Br, -I, NO2, -CN, -OR2 або -NHR2; де R2 являє собою -Η, С1-С7 алкіл з прямим або розгалуженим ланцюгом або арил, де арил необов'язково заміщений одним або більше -F, СІ, -Вr, -І, -NO2, -CN; та де n являє собою ціле число від 1 до 6 включно. В одному варіанті здійснення сполука має структуру: . В одному варіанті здійснення сполука має структуру: . В одному варіанті здійснення сполука має структуру: , де кожний А являє собою незалежно -Н, -F, СІ, -Вr або -І; де R4 являє собою незалежно -OR3, -NHR3 або -COR3; де R3 являє собою арил, необов'язково заміщений одним або більше -F, -СІ, -Вr, -І, -NO2, -CN, OR2 або -NHR2; де кожний R2 являє собою незалежно -Н, С1-С7 алкіл з прямим або розгалуженим ланцюгом або арил, необов'язково заміщений одним або більше -F, -СІ, -Вr, -І, -NO2, -CN; та де n являє собою ціле число від 1 до 6 включно. В одному варіанті здійснення сполука має структуру: , де кожний А являє собою незалежно -Н або -F; де R3 являє собою арил, необов'язково заміщений одним або більше -F, -СІ, -Вr, -І, -NO2, -CN, OR2 або -NHR2; де R2 являє собою незалежно С1-С7 алкіл з прямим або розгалуженим ланцюгом або арил, необов'язково заміщений одним або більше -F, СІ, -Вr або -І; та де n являє собою ціле число від 1 до 6 включно. В одному варіанті здійснення винаходу сполу де А являє собою -Н, -F, -СІ, -Вr або -І; де R3 являє собою арил, необов'язково заміщений одним або більше -F, -СІ, -Вr або -І. Сполука, що має структуру: . Сполука, що має структуру: Цим винаходом також пропонуються сполуки, що мають структуру: , де кожний Q незалежно являє собою водень; 19 77536 20 ло від 0 до 1 включно; де n являє собою ціле число від 0 до 6 включно; де q являє собою ціле число від 1 до 3 включно; або їх фармацевтично прийнятні солі. де X являє собою арил або гетероарил, де Цим винаходом також пропонуються сполуки, арил або гетероарил необов'язково заміщений що мають структуру: одним або більше -F, -СІ, -Вr, -І, -ZR3, -ZOR3, OZR3, -ZN(R3)2, -N(R3)ZR3, -N(R3)ZN(R3)2, -CN, NO2, -SR3, -(CH2)qOR3, -(CH2)qSR3, арилом, фенокси або гетероарилом, С1-С7 алкілом, монофторалкілом або поліфторалкілом з прямим або розгалуженим ланцюгом, С2-С7 алкенілом або алкінілом з прямим або розгалуженим ланцюгом або С3-С7 , циклоалкілом, монофторциклоалкілом, поліфторциклоалкілом або циклоалкенілом; де кожний Q являє собою незалежно водень; де кожний Ζ являє собою незалежно CO, CS, SO2 або може бути відсутнім; де кожний R являє собою незалежно -Н, -F, С1-С7 алкіл, монофторалкіл або поліфторалкіл з прямим або розгалуженим ланцюгом, С2-С7 алкеніл або алкініл з прямим або розгалуженим ланцюгом, -N(R3)2, -NO2, -CN, -CO2R3, -OCOR3, -OR3, де X являє собою арил або гетероарил, де N(R3)COR3 або -CON(R3)2; арил або гетероарил необов'язково заміщений де кожний R2 являє собою незалежно -Η, С1-С7 одним або більше -F, -СІ, -Br, -I, -ZR3, -ZOR3, алкіл з прямим або розгалуженим ланцюгом, арил OZR3, -ZN(R3)2, -N(R3)ZR3, -N(R3)ZN(R3)2, -CN, або гетероарил, де арил або гетероарил необов'яNO2, -SR3, -(CH2)qOR3, -(CH2)qSR3, арилом, фенокзково заміщений одним або більше -F, -СІ, -Br, -I, си або гетероарилом, С1-С7 алкілом, монофторалNO2, -CN, С1-С7 алкілом, монофторалкілом або кілом або поліфторалкілом з прямим або розгалуполіфторалкілом з прямим або розгалуженим ланженим ланцюгом, С2-С7 алкенілом або алкінілом з цюгом або С2-С7 алкенілом або алкінілом з прямим прямим або розгалуженим ланцюгом або С3-С7 або розгалуженим ланцюгом; циклоалкілом, монофторциклоалкілом, поліфторде кожний R3 являє собою незалежно -Н, С1-С7 циклоалкілом або циклоалкенілом; алкіл, монофторалкіл або поліфторалкіл з прямим де кожний Ζ являє собою незалежно CO, CS, або розгалуженим ланцюгом, С2-С7 алкеніл або SO2 або може бути відсутнім; алкініл з прямим або розгалуженим ланцюгом, С3де кожний R являє собою незалежно -Н, -F, С7 циклоалкіл, монофторциклоалкіл, поліфторцикС1-С7 алкіл, монофторалкіл або поліфторалкіл з лоалкіл або циклоалкеніл, арил або гетероарил, прямим або розгалуженим ланцюгом, С2-С7 алкеде арил або гетероарил необов'язково заміщений ніл або алкініл з прямим або розгалуженим ланцюодним або більше -F, -СІ, -Вr, -І, -N(R2)2, -NO2, -CN, гом, -N(R3)2, -NO2, -CN, -CO2R3, -OCOR3, -OR3, -COR2, -CO2R2, -OCOR2, -OR2, -N(R2)COR2, N(R3)COR3 або -CON(R3)2; N(R2)CON(R2)2, -CON(R2)2, арилом, гетероарилом, де кожний R2 являє собою незалежно -Η, С1-С7 фенокси, С1-С7 алкілом, монофторалкілом або алкіл з прямим або розгалуженим ланцюгом, арил поліфторалкілом з прямим або розгалуженим ланабо гетероарил, де арил або гетероарил необов'яцюгом, С2-С7 алкенілом або алкінілом з прямим зково заміщений одним або більше -F, -СІ, -Br, -I, або розгалуженим ланцюгом, С3-С7 циклоалкілом, NO2, -CN, С1-С7 алкілом, монофторалкілом або монофторциклоалкілом, поліфторциклоалкілом поліфторалкілом з прямим або розгалуженим ланабо циклоалкенілом; цюгом або С2-С7 алкенілом або алкінілом з прямим де кожний R4 являє собою незалежно -H,-ZR3, або розгалуженим ланцюгом; -ZOR3, -OZR3, -ZN(R3)2, -N(R3)ZR3; -N(R3)ZN(R3)2, де кожний R3 являє собою незалежно -Н, С1-С7 С1-С7 алкіл, монофторалкіл або поліфторалкіл з алкіл, монофторалкіл або иоліфторалкіл з прямим прямим або розгалуженим ланцюгом, арил, бенабо розгалуженим ланцюгом, С2-С7 алкеніл або зил або гетероарил, де арил, бензил або гетероаалкініл з прямим або розгалуженим ланцюгом, С3рил необов'язково заміщений одним або більше С7 циклоалкіл, монофторциклоалкіл, поліфторцикF, -СІ, -Br, -I, -ZR3, -ZOR3, -OZR3, -ZN(R3)2, лоалкіл або циклоалкеніл, арил або гетероарил, N(R3)ZR3, -N(R3)ZN(R3)2, -CN, -NO2, -SR3, де арил або гетероарил необов'язково заміщений (CH2)qOR3, -(CH2)qSR3, арилом, бензилом, гетероодним або більше -F, -СІ, -Br, -I, -N(R2)2, -NO2, -CN, арилом, С1-С7 алкілом, монофторалкілом або по-COR2, -CO2R2, -OCOR2, -OR2, -N(R2)COR2, ліфторалкілом з прямим або розгалуженим ланцюN(R2)CON(R2)2, -CON(R2)2, арилом, гетероарилом, гом, С2-С7 алкенілом або алкінілом з прямим або фенокси, С1-С7 алкілом, монофторалкілом або розгалуженим ланцюгом або С3-С7 циклоалкілом, поліфторалкілом з прямим або розгалуженим ланмонофторциклоалкілом, поліфторциклоалкілом цюгом, С2-С7 алкенілом або алкінілом з прямим або циклоалкенілом; або розгалуженим ланцюгом, С3-С7 циклоалкілом, де кожний k являє собою незалежно ціле чисмонофторциклоалкілом, поліфторциклоалкілом ло від 1 до 3 включно; або циклоалкенілом; де кожний m являє собою незалежно ціле чис 21 77536 22 де кожний R4 являє собою незалежно -Н, -ZR3, (CH2)qOR3, -(CH2)qSR3, арилом, фенокси або гете-ZOR3, -OZR3, -ZN(R3)2, -N(R3)ZR3, -N(R3)ZN(R3)2, роарилом, С1-С7 алкілом, монофторалкілом або С1-С7 алкіл, монофторалкіл або поліфторалкіл з поліфторалкілом з прямим або розгалуженим ланпрямим або розгалуженим ланцюгом, арил, бенцюгом, С2-С7 алкенілом або алкінілом з прямим зил або гетероарил, де арил, бензил або гетероаабо розгалуженим ланцюгом або С3-С7 циклоалкірил необов'язково заміщений одним або більше лом, монофторциклоалкілом, поліфторциклоалкіF, -СІ, -Br, -I, -ZR3, -ZOR3, -OZR3, -ZN(R3)2, лом або циклоалкенілом; N(R3)ZR3, -N(R3)ZN(R3)2, -CN, -NO2, -SR3, де кожний Ζ являє собою незалежно CO, CS, (CH2)qOR3, -(CH2)qSR3, арилом, бензилом, гетероSO2 або може бути відсутнім; арилом, С1-С7 алкілом, монофторалкілом або поде кожний R являє собою незалежно -Н, -F, ліфторалкілом з прямим або розгалуженим ланцюС1-С7 алкіл, монофторалкіл або поліфторалкіл з гом, С2-С7 алкенілом або алкінілом з прямим або прямим або розгалуженим ланцюгом, С2-С7 алкерозгалуженим ланцюгом або С3-С7 циклоалкілом, ніл або алкініл з прямим або розгалуженим ланцюмонофторциклоалкілом, поліфторциклоалкілом гом, -N(R3)2, -NO2, -CN, -CO2R3, -OCOR3, -OR3, або циклоалкенілом; N(R3)COR3 або -CON(R3)2; де кожний k являє собою незалежно ціле чисде кожний R2 являє собою незалежно -Η, С1-С7 ло від 1 до 3 включно; алкіл з прямим або розгалуженим ланцюгом, арил де n являє собою ціле число від 0 до 6 вклюабо гетероарил, де арил або гетероарил необов'ячно; зково заміщений одним або більше -F, -СІ, -Вr, -І, де q являє собою ціле число від 1 до 3 вклюNO2, -CN, С1-С7 алкілом, монофторалкілом або чно; поліфторалкілом з прямим або розгалуженим ланабо їх фармацевтично прийнятні солі. цюгом або С2-С7 алкенілом або алкінілом з прямим Ілюстрацією винаходу є фармацевтична комабо розгалуженим ланцюгом; позиція, що включає фармацевтично прийнятний де кожний R3 являє собою незалежно -Н, С1-С7 носій та фармацевтично ефективну кількість будьалкіл, монофторалкіл або поліфторалкіл з прямим якої сполуки, описаної вище. або розгалуженим ланцюгом, С2-С7 алкеніл або Ілюстрацією винаходу є фармацевтична комалкініл з прямим або розгалуженим ланцюгом, С3позиція, виготовлена шляхом змішування будьС7 циклоалкіл, монофторциклоалкіл, поліфторцикякої сполуки, описаної вище, та фармацевтично лоалкіл або циклоалкеніл, арил або гетероарил, прийнятного носія. де арил або гетероарил необов'язково заміщений Ілюстрацією винаходу є спосіб виготовлення одним або більше -F, -СІ, -Br, -I, -N, (R2)2, -NO2, фармацевтичної композиції, який включає змішуCN, -COR2, -CO2R2, -OCOR2, -OR2, -N(R2)COR2,вання будь-якої сполуки, описаної вище, та фарN(R2)CON(R2)2, -CON(R2)2, арилом, гетероарилом, мацевтично прийнятного носія. фенокси, С1-С7 алкілом, монофторалкілом або Ілюстрацією винаходу є спосіб синтезу для виполіфторалкілом з прямим або розгалуженим ланготовлення будь-якої сполуки, описаної вище. цюгом, С2-С7 алкенілом або алкінілом з прямим Прикладом винаходу є спосіб лікування стану, або розгалуженим ланцюгом, С3-С7 циклоалкілом, опосередкованого рецептором МСН1, у суб'єкта, монофторциклоалкілом, поліфторциклоалкілом якому це необхідно, який включає введення суабо циклоалкенілом; б'єктові терапевтично ефективної кількості будьде кожний R4 являє собою незалежно -Н, -ZR3, якої сполуки або фармацевтичної композиції, опи-ZOR3, -OZR3, ZN(R3)2, -N(R3)ZR3, -N(R3)ZN(R3)2, саної вище, та фармацевтично прийнятного носія. С1-С7 алкіл, монофторалкіл або поліфторалкіл з Цим винаходом також пропонуються сполуки, прямим або розгалуженим ланцюгом, арил, бенщо мають структуру: зил або гетероарил, де арил, бензил або гетероарил необов'язково заміщений одним або більше F, -СІ, -Br, -I, -ZR3, -ZOR3, -OZR3, -ZN(R3)2, N(R3)ZR3, N(R3)ZN(R3)2, -CN, -NO2, -SR3, (CH2)qOR3, -(CH2)qSR3, арилом, бензилом, гетероарилом, С1-С7 алкілом, монофторалкілом або поліфторалкілом з прямим або розгалуженим ланцюгом, С2-С7 алкенілом або алкінілом з прямим або розгалуженим ланцюгом або С3-С7 циклоалкілом, де кожний Q являє собою незалежно водень; монофторциклоалкілом, поліфторциклоалкілом або циклоалкенілом; де кожний k являє собою незалежно ціле число від 1 до 3 включно; де n являє собою ціле число від 0 до 6 включно; де q являє собою ціле число від 1 до 3 включно; де X являє собою феніл або гетероцикл, що або їх фармацевтично прийнятні солі. містить азот, де феніл або гетероцикл, що містить Цим винаходом також пропонуються сполуки, азот, необов'язково заміщений одним або більше що мають структуру: F, -СІ, -Br, -I, -ZR3, -ZOR3, -OZR3, -ZN(R3)2, N(R3)ZR3, -N(R3)ZN(R3)2, -CN, -NO2, -SR3, 23 77536 24 арилом, C1-C7 алкілом, монофторалкілом або поліфторалкілом з прямим або розгалуженим ланцюгом, С2-С7 алкенілом або алкінілом з прямим або розгалуженим ланцюгом або С3-С7 циклоалкілом, монофторциклоалкілом, поліфторциклоалкілом або циклоалкенілом; де кожний k являє собою незалежно ціле чисде кожний Q являє собою незалежно водень; ло від 1 до 3 включно; де n являє собою ціле число від 0 до 6 включно; де q являє собою ціле число від 1 до 3 включно, , або їх фармацевтично прийнятні солі. В одному варіанті здійснення кожний А являє де кожний А являє собою незалежно -Н, -F, собою незалежно -Н, -F, -СІ, -Вr, -І, -ZR3, -ZOR3, СІ, -Вr, -І, -ZR3, -ZOR3, -OZR3, -ZN(R3)2, -N(R3)ZR3, OZR3, -ZN(R3)2, -N(R3)ZR3, -N(R3)ZN(R3)2, -N(R3)2, N(R3)ZN(R3)2, -CN, -NO2, -N(R3)2, -OR3, -SR3, OR3, -SR3, -(CH2)qOR3, -(CH2)qSR3, С1-С7 алкіл, мо(CH2)qOR3, -(CH2)qSR3, С1-С7 алкіл, монофторалкіл нофторалкіл або поліфторалкіл з прямим або розабо поліфторалкіл з прямим або розгалуженим галуженим ланцюгом; ланцюгом, С2-С7 алкеніл або алкініл з прямим або де кожний Ζ являє собою незалежно CO, CS розгалуженим ланцюгом, С3-С7 циклоалкіл, моноабо може бути відсутнім; фторциклоалкіл, поліфторциклоалкіл або циклоаде кожний R являє собою незалежно -Н, -F лкеніл; або С1-С7 алкіл з прямим або розгалуженим ланде кожний В являє собою незалежно N або цюгом; СН; де кожний R2 являє собою незалежно -Н, С1-С7 де кожний Ζ являє собою незалежно CO, CS, алкіл з прямим або розгалуженим ланцюгом, арил SO2 або може бути відсутнім; або гетероарил, де арил або гетероарил необов'яде кожний R являє собою незалежно -Н, -F, зково заміщений одним або більше -F, -Cl, -Br, -I, С1-С7 алкіл, монофторалкіл або поліфторалкіл з NO2, -CN, С1-С7 алкілом, монофторалкілом або прямим або розгалуженим ланцюгом, С2-С7 алкеполіфторалкілом з прямим або розгалуженим ланніл або алкініл з прямим або розгалуженим ланцюцюгом або С2-С7 алкенілом або алкінілом з прямим гом, -N(R3)2, -NO2, -CN, -CO2R3, -OCOR3, -OR3, або розгалуженим ланцюгом; N(R3)COR3 або -CON(R3)2; де кожний R3 являє собою незалежно -Н, С1-С7 де кожний R2 являє собою незалежно -Η, С1-С7 алкіл з прямим або розгалуженим ланцюгом, арил алкіл з прямим або розгалуженим ланцюгом, арил або гетероарил, де арил або гетероарил необов'яабо гетероарил, де арил або гетероарил необов'язково заміщений одним або більше -F, -СІ, -Br, -I, зково заміщений одним або більше -F, -СІ, -Br, -I, N(R2)2, -NO2, -CN, -COR2, -CO2R2, -OCOR2, -OR2, NO2, -CN, С1-С7 алкілом, монофторалкілом або N(R2)COR2, -N(R2)CON(R2)2, -CON(R2)2, арилом, поліфторалкілом з прямим або розгалуженим лангетероарилом, фенокси, С1-С7 алкілом, монофтоцюгом, С2-С7 алкенілом або алкінілом з прямим ралкілом або поліфторалкілом з прямим або розабо розгалуженим ланцюгом; галуженим ланцюгом, С2-С7 алкенілом або алкініде кожний R3 являє собою незалежно -Н, С1-С7 лом з прямим або розгалуженим ланцюгом, С3-С7 алкіл, монофторалкіл або поліфторалкіл з прямим циклоалкілом, монофторциклоалкілом, поліфторабо розгалуженим ланцюгом, С2-С7 алкеніл або циклоалкілом або циклоалкенілом. алкініл з прямим або розгалуженим ланцюгом, С3В одному варіанті здійснення сполука має С7 циклоалкіл, монофторциклоалкіл, поліфторцикструктуру: лоалкіл або циклоалкеніл, арил або гетероарил, де арил або гетероарил необов'язково заміщений одним або більше -F, -СІ, -Br, -I, -N(R2)2, -NO2, -CN, -COR2, -CO2R2, -OCOR2, -OR2, -N(R2)COR2, N(R2)CON(R2)2, -CON(R2)2, арилом, гетероарилом, фенокси, С1-С7 алкілом, монофторалкілом або поліфторалкілом з прямим або розгалуженим ланцюгом, С2-С7 алкенілом або алкінілом з прямим або розгалуженим ланцюгом, С3-С7 циклоалкілом, В одному варіанті здійснення сполука має монофторциклоалкілом, поліфторциклоалкілом структуру: або циклоалкенілом; де кожний R4 являє собою незалежно -Н, -ZR3, -ZOR3, -OZR3, -ZN(R3)2, -N(R3)ZR3, -N(R3)ZN(R3)2, С1-С7 алкіл, монофторалкіл або поліфторалкіл з прямим або розгалуженим ланцюгом, арил, бензил або гетероарил, де арил, бензил або гетероарил необов'язково заміщений одним або більше . F, -СІ, -Br, -I, -ZR3, -ZOR3, -OZR3, -ZN(R3)2, N(R3)ZR3, -N(R3)ZN(R3)2, -CN, -NO2, -SR3, В одному варіанті здійснення сполука має (CH2)qOR3, -(CH2)qSR3, арилом, бензилом, гетеро 25 77536 26 структуру: . В одному варіанті здійснення сполука має структуру: . В одному варіанті здійснення сполука має структуру: , де R4 являє собою арил, де арил необов'язково заміщений одним або більше -F, -СІ, -Вr, -І, С1С7 алкілом, монофторалкілом або поліфторалкілом з прямим або розгалуженим ланцюгом, С2-С7 алкенілом або алкінілом з прямим або розгалуженим ланцюгом або С3-С7 циклоалкілом, монофторциклоалкілом, поліфторциклоалкілом або циклоалкенілом. В одному варіанті здійснення сполука має структуру: . В одному варіанті здійснення сполука має структуру: . В одному варіанті здійснення сполука має структуру: де R3 являє собою арил або гетероарил, де арил або гетероарил необов'язково заміщений одним або більше -F, -СІ, -Br, -I, -N(R2)2, -NO2, -CN, -COR2, -CO2R2, -OCOR2, -OR2, -N(R2)COR2, N(R2)CON(R2)2, -CON(R2)2, арилом, гетероарилом, фенокси, С1-С7 алкілом з прямим або розгалуженим ланцюгом. В одному варіанті здійснення сполука має структуру: . Як застосовується в описаних вище винаходах, термін "гетероарил" позначає п'яти- і шестичленні ненасичені кільця, що можуть містити один або більше атомів кисню, сірки або азоту. Приклади гетероарильних груп включають, проте не обмежуються лише ними, карбазол, фураніл, тієніл, піроліл, оксазоліл, тіазоліл, імідазоліл, піразоліл, ізокдазоліл, ізотіазоліл, оксадіазоліл, триазоліл, тіадіазоліл, піридил, піридазиніл, піримідиніл, піразиніл та триазиніл. Крім того, використовуваний тут термін "гетероарил" позначає сконденсовані біциклічні кільцеві системи, що можуть містити один або декілька гетероатомів, таких як кисень, сірка й азот. До прикладів таких гетероарильних груп належать, але не обмежуються тільки ними, індолізиніл, індоліл, ізоіндоліл, бензо[b]фураніл, бензо[b]тіофеніл, індазоліл, бензімідазоліл, пуриніл, бензоксазоліл, бензізоксазоліл, бензо[b]тіазоліл, імідазо[2,1b]тіазоліл, циннолініл, хіназолініл, хіноксалініл, 1,8нафтиридиніл, птеридиніл, хінолініл, ізохінолініл, фталіміділ та 2,1,3-бензотіазоліл. Термін "гетероарил" також позначає ті перелічені вище хімічні групи, що можуть бути заміщені однією або декількома наступними групами: -F, СІ, -Br, -I, -CN, -NO2, C1-С7 алкілом з прямим або розгалуженим ланцюгом, С1-С7 монофторалкілом з прямим або розгалуженим ланцюгом, С1-С7 поліфторалкілом з прямим або розгалуженим ланцюгом, С2-С7 алкенілом з прямим або розгалуженим ланцюгом, С2-С7 алкінілом з прямим або розгалуженим ланцюгом, С3-С7 циклоалкілом, С3-С7 монофторциклоалкілом, С3-С7 поліфторциклоалкілом, С5-С7 циклоалкенілом. Термін "гетероарил" далі включає N-оксиди тих хімічних груп, які перелічені вище, що включають принаймні один атом азоту. У цьому винаході термін "арил" позначає феніл або нафтил. У подальшому варіанті здійснення вищезгаданого винаходу сполука є енантіомерно та діастеріомерно чистою. В іншому варіанті здійснення сполука є енантіомерно або діастеріомерно чистою. В одному варіанті здійснення сполука являє собою (+)-енантіомер. В одному варіанті здійснення сполука являє собою (-)-енантіомер. Даний винахід відноситься до кожного чистого стереоізомера будь-якої сполуки, описаної тут. Такі стереоізомери можуть включати енантіомери, діастереомери або Ε або Ζ алкенові або імінові ізомери. Винахід також відноситься до стереоізомерних сумішей, включаючи рацемічні суміші, діа 27 77536 28 стереоізомерні суміші або Ε/Ζ ізомерні суміші. фармацевтичної композиції, який включає змішуСтереоізомери можуть бути синтезовані в чистому вання будь-якої сполуки винаходу та фармацевтивиді [Nogradi, Μ.; Stereoselective Synthesis, (1987) чно прийнятного носія. VCH Editor Ebel, H. та Asymmetric Synthesis, Твердий носій може містити одну або декілька Volumes З В 5, (1983) Academic Press, Editor речовин, що можуть діяти як ендогенні носії (наMorrison, J.] або вони можуть бути виділені за приклад, поживні речовини або поживні мікроелебудь-яким з численних способів, таких як кристаліменти), ароматизатори, змащувальні агенти, созація і методи хроматографії [Jaques, J.; Collet, Α.; любілізатори, суспендувальні агенти, наповнювачі, Wilen, S.; Enantiomer, Racemates, and Resolutions, ковзні агенти, ущільнювальні добавки, зв'язувальні 1981, John Wiley and Sons and Asymmetric агенти або дезінтегратори таблеток; ним також Synthesis, Vol. 2, 1983, Academic Press, Editor може бути інкапсулювальний матеріал. У порошMorrison, J.]. ках носій є дрібнодиспергованою твердою речовиКрім того, сполуки за цим винаходом можуть ною, що знаходиться в суміші з дрібнодисперговабути отримані у виді енантіомерів, діастереомерів, ним активним інгредієнтом. У таблетках активний ізомерів або дві або декілька сполук можуть існуінгредієнт змішаний з носієм, який має необхідні вати у виді рацемічної або діастереомерної суміші. властивості щодо пресування, у придатних пропоСполуки за цим винаходом є переважно на рціях і спресований до потрібної форми та розмі80% чистими, більш переважно на 90% чистими і ру. Порошки і таблетки переважно містять до 99% найбільш переважно на 95% чистими. До цього активного інгредієнта. Придатні тверді носії місвинаходу відносяться фармацевтично прийнятні тять, наприклад, фосфат кальцію, стеарат магнію, солі та комплекси усіх сполук, описаних тут. Кистальк, сахари, лактозу, декстрин, крохмаль, желалоти і основи, з яких одержують ці солі, включатин, целюлозу, полівінілпіролідин, віск з низькою ють, але не обмежуються тільки ними, перелічені температурою плавлення та іонно-обмінні політут кислоти і основи. Кислоти включають, але не мери. обмежуються тільки ними, наступні неорганічні Рідкі носії використовуються для одержання кислоти: хлористоводневу кислоту, бромистоводрозчинів, суспензій, емульсій, сиропів, еліксирів і неву кислоту, йодистоводневу кислоту, сірчану герметичних композицій. Активний інгредієнт може кислоту і борну кислоту. Кислоти включають, але бути розчинений або суспендований у фармацевне обмежуються тільки ними, наступні органічні тично прийнятному рідкому носії, такому як вода, кислоти: оцтову кислоту, малонову кислоту, буршорганічний розчинник, їх суміш або фармацевтичтинову кислоту, фумарову кислоту, винну кислоту, но прийнятні олії або жири. Рідкий носій може місмалеїнову кислоту, лимонну кислоту, метансультити інші придатні фармацевтичні добавки, такі як фонову кислоту, бензойну кислоту, гліколеву киссолюбілізатори, емульгатори, буфери, консерванлоту, молочну кислоту і мигдалеву кислоту. Осноти, підсолоджувачі, ароматизатори, суспендувальви включають, але не обмежуються тільки ними, ні агенти, загусники, барвники, регулятори в'язкосамоній, метиламін, етиламін, пропіламін, диметиті, стабілізатори або осморегулятори. Придатні ламін, діетиламін, триметиламін, триетиламін, приклади рідких носіїв для перорального та пареетилендіамін, гідроксіетиламін, морфолін, піперантерального введення включають воду (яка частзин і гуанідин. Цей винахід також відноситься до ково містить добавки, описані вище, наприклад, гідратів і поліморфів усіх описаних тут сполук. похідні целюлози, переважно розчин карбоксимеВ обсяг цього винаходу входять проліки сполук тилцелюлози натрію), спирти (включаючи одноаданого винаходу. Звичайно такими проліками явтомні спирти та багатоатомні спирти, наприклад, ляються функціональні похідні сполук за цим вигліколі) та їхні похідні та олії (наприклад, фракціонаходом, які легко перетворяться in vivo на необновані кокосову олію й арахісову олію). Для паренхідну сполуку. Таким чином, у цьому винаході терального введення носій також може бути склатермін "введення" охоплює лікування різних опидним ефіром жирної кислоти, таким як етилолеат саних станів конкретно описаною сполукою або або ізопропілміристат. Стерильні рідкі носії викосполукою, яка може бути конкретно не описаною, ристовуються в стерильних рідких композиціях для але яка перетвориться на конкретну сполуку in парентерального введення. Рідкий носій для герvivo після введення пацієнту. Звичайні способи метичних композицій може бути галогенованим вибору й одержання придатних пролікових похідвуглеводнем або іншим фармацевтично прийнятних описані, наприклад, у [Design of Prodrugs, ed. ним диспергатором. Bungaard, Elsevier, 1985]. Рідкі фармацевтичні композиції, які є стерильЦей винахід далі відноситься до метаболітів ними розчинами або суспензіями, можуть викориссполук за цим винаходом. Метаболіти включають товуватися, наприклад, за допомогою внутрішньоактивні типи сполук, одержувані при введенні спом'язової, інтратекальної, епідуральної, лук за цим винаходом в біологічне середовище. інтраперитонеальної або підшкірної ін'єкції. СтеІлюстрацією винаходу є фармацевтична комрильні розчини можуть також вводитися внутріпозиція, що включає фармацевтично прийнятний венно. Сполуки можуть бути приготовані у виді носій та терапевтично ефективну кількість будьстерильної твердої композиції, яку можна розчиняякої сполуки винаходу. ти або суспендувати під час введення, використоІлюстрацією винаходу є фармацевтична комвуючи стерильну воду, фізіологічний розчин або позиція, виготовлена шляхом змішування будьінше придатне стерильне ін'єкційне середовище. якої сполуки, описаної вище, та фармацевтично Носії призначені для включення до них необхідних прийнятного носія. та інертних зв'язувальних агентів, суспендувальІлюстрацією винаходу є спосіб виготовлення них агентів, змащувальних речовин, ароматизато 29 77536 30 рів, підсолоджувачів, консервантів, барвників й ссавець або людина. покривних речовин. Сполуки можуть вводитися Цей винахід відноситься до способу лікування перорально у формі стерильного розчину або сусуб'єкта з патологією, яка зменшується при зниспензії, що містить інші розчинені речовини або женні активності рецептора МСН1, який полягає у суспендувальні агенти (наприклад, достатню кільвведенні суб'єкту кількості сполуки за цим винахокість фізіологічного розчину або глюкози для надом, яка є антагоністом рецептора МСН1, для лідання розчину ізотонічності), солі жовчних кислот, кування патології суб'єкта. гуміарабік, желатин, сорбітанмонолеат, полісорбат У конкретних варіантах здійснення патологією 80 (олеатні естери сорбіту та його ангідриди, соє порушення регуляції стероїдного гормону або полімеризовані з етиленоксидом) тощо. гормону гіпофіза, порушення вивільнення епінефСполука також може вводитися перорально у рину, шлунково-кишковий розлад, серцевоформі рідкої або твердої композиції. Композиції, судинне захворювання, порушення електролітного що підходять для перорального введення вклюбалансу, підвищений тиск, діабет, порушення дичають тверді форми, такі як пігулки, капсули, грахання, астма, порушення репродуктивної функції, нули, таблетки і порошки, й рідкі форми, такі як порушення імунної системи, порушення ендокринрозчини, сиропи, еліксири і суспензії. Форми, приної системи, скелетно-м'язове порушення, нейродатні для парентерального введення, включають ендокринні порушення, когнітивний розлад, розлад стерильні розчини, емульсії та суспензії. пам'яті, такий як хвороба Альцгеймера, порушення Оптимальна доза введення може бути визнасенсорної модуляції й передачі, порушення коорчена фахівцем у даній галузі та може змінюватися динації руху, порушення сенсорної інтеграції, пов залежності від конкретної використовуваної спорушення моторної інтеграції, порушення дофамілуки, концентрації лікарського засобу, шляху ввенергічної функції, таке як хвороба Паркінсона, дення та від тяжкості захворювання. Додаткові порушення сенсорної передачі, порушення нюху, фактори, що залежать від певного хворого, якого порушення симпатичної інервації, афективний лікують, можуть призводити до необхідності додарозлад, такий якдепресія й тривожний стан, розткових доз і включають вік хворого, масу, стать, лад, пов'язаний зі стресом, порушення водного режим харчування і час введення. балансу, судорожні припадки, біль, психотична Ілюстрацією винаходу є спосіб синтезу для поведінка, така як шизофренія, пристрасть до одержання будь-якої сполуки винаходу. морфіну й опіатів, мігрень або сечовий розлад, Прикладом винаходу є спосіб лікування розтакий як нетримання сечі. ладу, опосередкованого рецептором МСН1, у суУ кращому варіанті здійснення цей винахід віб'єкта, якому це необхідно, який включає введення дноситься до способу лікування наступного: десуб'єктові терапевтично ефективної кількості будьпресії, тривожного стану, порушення харчуванякої сполуки або фармацевтичної композиції винаня/маси тіла й сечових розладів. Прикладами ходу та фармацевтично прийнятного носія. порушення харчування/маси тіла є ожиріння, буліВ одному варіанті здійснення терапевтично мія або нейрогенна булімія. Приклади сечових ефективна кількість становить від приблизно 0,03 розладів включають, але не обмежуються тільки до приблизно 300мг. ними, нетримання сечі при напрузі, гіперактивний В одному варіанті здійснення розлад являє сечовий міхур, невідкладне нетримання сечі, часті собою депресію. В одному варіанті здійснення сечовипускання, невідкладний позив до сечовипурозлад являє собою тривожний стан. В одному скання, ніктурію або енурез. Гіперактивний сечоваріанті здійснення розлад являє собою ожиріння. вий міхур і невідкладний позив до сечовипускання В одному варіанті здійснення розлад являє собою можуть бути як пов'язані, так і не пов'язані із добнетримання сечі. роякісною гіперплазією простати. Один варіант здійснення являє собою спосіб Цей винахід відноситься до способу модифікулікування суб'єкта, який страждає на розлад, вибвання харчової поведінки суб'єкта, який полягає у раний з депресії, тривожного стану, ожиріння та введенні суб'єкту кількості сполуки за цим винахонетримання сечі, та якому це необхідно, що вклюдом, ефективної для зменшення споживання їжі чає введення суб'єктові терапевтично ефективної суб'єктом. кількості сполуки винаходу. Цей винахід також відноситься до способу ліВ одному варіанті здійснення терапевтично кування харчових порушень у суб'єкта, який поляефективна кількість становить від приблизно 0,03 гає у введенні суб'єкту кількості сполуки за цим до приблизно 300мг. винаходом, ефективної для зменшення споживанВ іншому варіанті здійснення розлад являє соня їжі суб'єктом. В одному з варіантів здійснення бою депресію. В одному варіанті здійснення розцього винаходу харчовим порушенням є булімія, лад являє собою тривожний стан. В одному варіаожиріння або нейрогенна булімія. В одному з варінті здійснення розлад являє собою ожиріння. В антів здійснення даного винаходу суб'єктом є хреодному варіанті здійснення розлад являє собою бетне, ссавець, людина або собака. У ще одному нетримання сечі. варіанті здійснення сполука вводиться з їжею. В предметі винаходу за даною заявкою, "тераЦей винахід також відноситься до способу певтично ефективною кількістю" є будь-яка кільзниження маси тіла у суб'єкта, який полягає у ввекість сполуки, яка при введенні хворому, що страденні суб'єкту кількості сполуки за цим винаходом, ждає захворюванням, у відношенні якого ці ефективної для зниження маси тіла у суб'єкта. сполуки є ефективними, викликає зниження, реміЦей винахід також відноситься до способу лісію або регресію захворювання. В предметі винакування суб'єкта, що страждає на депресію, який ходу за даною заявкою, "суб'єктом" є хребетне, полягає у введенні суб'єкту кількості сполуки за 31 77536 32 цим винаходом, ефективної для лікування депресії ньо покритих силікагелем 60 F254 (0,25мм, EM у суб'єкта. Цей винахід також відноситься до споSeparations Tech.). Препаративну тонкошарову собу лікування суб'єкта з тривожним станом, який хроматографію виконували на скляних пластинах, полягає у введенні суб'єкту кількості сполуки за попередньо покритих силікагелем GF (2мм, цим винаходом, ефективної для лікування тривоAnaltech). Флеш-хроматографію на колонках викожного стану у суб'єкта. Цей винахід також віднонували на силікагелі Merck 60 (230-400меш). Точки ситься до способу лікування суб'єкта з депресією і плавлення (mр) визначали на відкритих капілярних тривожним станом, який полягає у введенні суб'єктрубках на апараті Mel-Temp та їх не коректували. ту кількості сполуки за цим винаходом, ефективної Наступні схеми ілюструють способи синтезу для лікування депресії та тривожного стану у сусполук цього винаходу б'єкта. Цей винахід також відноситься до способу лікування суб'єкта, що страждає великим депресивним розладом, дистимічним розладом, біполярними розладами І і II, шизоафективним розладом, когнітивним розладом з депресивним настроєм, розладом особистості, інсомнією, гіперсомнією, нарколепсією, порушенням циркадного ритму, стражданнями на кошмари, приступами інтенсивного страху під час сну, сомнамбулізмом, обсесивно-компульсивним розладом, панічним розладом з агорафобією або без неї, посттравматичним стресовим розладом, соціальним тривожним розладом, соціальною фобією і генералізованим тривожним розладом. Цей винахід також відноситься до способу лікування суб'єкта, що страждає сечовим розладом, який полягає у введенні суб'єкту кількості сполуки (a) LDA/PhNTf2/THF/ -78°С, потім 0°С протягом за цим винаходом, ефективної для лікування сеночі. (b) Амінофенілборонова кислочового розладу у суб'єкта. У деяких варіантах та/Рd(PPh)4/LiCI/Na2СО3/DМЕ-Н2О/ кип'ятили у здійснення, сечовим розладом є нетримання сечі колбі зі зворотним холодильником протягом 3 гопри напрузі, гіперактивний сечовий міхур, невіддин, (с) 10% Pd/C/H2/EtOH/ кімнатна температура кладне нетримання сечі, часті сечовипускання, протягом 24-48 годин, (d) Хлорангідрид кислоневідкладний позив до сечовипускання, ніктурію ти/триетиламін/THF/ 0°С, потім кімнатна темпераабо енурез. тура протягом 2-3 годин або карбонова кислоЦей винахід буде краще зрозумілим з розділу та/EDC/DMAP/CH2CI2/DMF/ кімнатна температура "Експериментальна частина", наведеного далі. протягом 12 годин, (e) 4М НСl у 1,4-діоксані/ кімнаПроте фахівцю в даній галузі без зусиль буде зротна температура протягом 1 години або зуміло, що розглянуті конкретні способи й резульTFA/CH2CI2/ кімнатна температура протягом 10 тати, є просто ілюстративними для даного винахохвилин. ду, як описано більш докладно у формулі винаходу, що додана до цього опису винаходу. Експериментальна частина І. Синтез хімічних сполук Загальні способи: Усі реакції здійснювали в атмосфері аргону та реагенти, без розчинника або у відповідних розчинниках, переносили у реакційну судину за допомогою шприца та канюлі. Дослідження паралельних реакцій синтезу проводили в пробірках (без інертної атмосфери), застосовуючи нагрівальні шейкери J-KEM (Saint Louis, МО). Безводні розчинники були придбані у Aldrich Chemical Company (Milwaukee, WI) і використовувалися такими, якими вони були одержані. Якщо не вказано інше, спектри 1H записували при 400МГц (Bruker, Model: Avance) з тетраметилсиланом як внутрішній стандарт, с = синглет, д = дублет, т = триплет, кв. = квартет, квін. = квінтет, секстет, септет, ушир. = уширений, м = мультиплет. Елементні аналізи проводили Robertson Microlit Laboratories, Inc. Якщо не зазначено іншого, мас-спектри одержували на приладі VG Patform II, застосовуючи електророзпилювач (ESI-MS) і вказували МН+. Тонкошарову хроматографію (а) Біс(пінаколато)дибор/КОАс/РdСІ2dррf/dррf/ (ТШХ) виконували на скляних пластинах, поперед 33 77536 34 80°С протягом ночі, (b) K2CO3/PdCl2 dppf/DMF/ чого отримали бажаний продукт (16,5г), забрудне80°C протягом ночі, (с) 10% Pd/C /H2/EtOH/ кімнатний деякою кількістю початкового матеріалу на температура протягом 24-72 годин, (d) 4М НСl у Tf2NPh: 1H ЯМР (400МГц, CDCl3) 5,77 (с, 1Н), 1,4-діоксані/ кімнатна температура протягом 1 го4,05 (дм, 2Н, J=3,0Гц), 3,63 (т, 2Н, J=5,7Гц), 2,45 дини або TFA/CH2CI2/ кімнатна температура про(м, 2Н), 1,47 (с, 9Н). тягом 10 хвилин, (e) Карбонова кислота/EDC/DMAP/CH2CI2/DMF/ кімнатна температура протягом 12 годин, (f) H2SO4/HNO3, 0°С, 10 хвилин, (g) Fe/NH4Cl/THF/H2O/EtOH/ 95°C протягом 1,5 години, (h) Сhz-Сl/NаНСО3/СН3СN/ кімнатна температура протягом 12 годин. (b) K2CO3/PdCl2dppf/DMF/ 85°C 24 години, (с) 10% Pd/C/H2 (200psi (фунтів на квадратний дюйм))/ЕtOАс/МеОН/ кімнатна температура протягом 24 годин - 72 годин, (d) 4М НСI у 1,4-діоксані/ кімнатна температура протягом 1 години або TFA/CH2CI2/ кімнатна температура протягом 0,2 години, (e) Карбонова кислота/ЕDС/DМАР/CH2CI2/DMF/ кімнатна температура протягом 12 годин. Загальна процедура синтезу піперидину (схема 1) Трeт-бутил 4{[(трифторметил)сульфоніл]окси}-3,6-дигідро1(2Н)-піридинкарбоксилат: n-бутиллітій (17,6мл, 44,2ммоль, 2,5Μ у гексанах) додали до розчину діізопропіламіну (96,2мл, 44,2ммоль) у безводному THF (40,0мл) при температурі 0°С та одержану суміш перемішували протягом 20 хвилин. Реакційну суміш охолодили до -78°С та трет-бутиk 4-оксо1-піперидинкарбоксилат [Aldrich Chemical Company, 7,97г, 40,0ммоль] у THF (40,0мл) додавали краплями до реакційної суміші, яку потім перемішували протягом 30 хвилин. Tf2NPh (42,0ммоль, 15,0г) у THF (40,0мл) додавали краплями до реакційної суміші та реакційну суміш перемішували при 0°С протягом ночі. Реакційну суміш концентрували в умовах вакууму, знову розчинили у гексанах: ЕtOАс (9:1), пропустили крізь шар оксиду алюмінію та шар оксиду алюмінію промили гексанами:EtOAc (9:1). Об'єднані екстракти концентрували в умовах вакууму, внаслідок Трет-бутил 4-(3-амінофеніл)-3,6-дигідро-1(2н)піридинкарбоксилат: Дегазовану суміш 2,0Μ водного розчину Na2CO3 (4,20мл), трет-бутил 4{[(трифторметил)сульфоніл]окси}-3,6-дигідро1(2Н)-піридинкарбоксилату (0,500г, 1,51ммоль), гемісульфату 3-амінофенілкарбонової кислоти (0,393г, 2,11ммоль), хлориду літію (0,191г, 4,50ммоль) та тетракістрифенілфосфінпаладію (0,080г, 0,075ммоль) у диметоксіетані (5,00мл) нагрівали при температурі дефлегмації протягом 3 годин в атмосфері аргону. Органічний шар охолодженої реакційної суміші відокремили та водний шар промили етилацетатом (3х50мл). Об'єднані органічні розчини висушили та концентрували в умовах вакууму. Сирий продукт піддали хроматографії (силікагель, гексани:ЕtOАс:дихлорметан 6:1:1 з 1% ізопропіламіном), внаслідок чого отримали бажаний продукт (0,330г, 81%). 1H ЯМР (400МГц, CDCl3) 7,12 (т, 1Н, J=7,60Гц), 6,78 (д, 1Н, J=8,4Гц), 6,69 (т, 1Η, J=2,0Гц), 6,59 (дд, 1Н, J=2,2, 8,0Гц), 6,01 (ушир, 1Н), 4,10-4,01 (д, 2Н, J=2,4Гц), 3,61 (т, 2Η, J=5,6Гц), 2,52 - 2,46 (м, 2Н), 1,49 (с, 9Н), ESMS m/e: 275,2 (М+Н)+. Розраховано для C16H24N2O2: С, 70,04; Н, 8,08; N, 10,21. Знайдено: С, 69,78; Н, 7,80; N, 9,92. Трет-бутил 4-[3-(аміно)феніл]-1піридинкарбоксилат: Суміш трет-бутил 4-(3амінофеніл)-3,6-дигідро-1(2Н)піридинкарбоксилату (3,10г, 11,3ммоль) та 10% Pd/C (1,00г) в етанолі (100мл) гідрували при кімнатній температурі, застосовуючи балонний спосіб протягом 2 днів. Реакційну суміш профільтрували крізь Celite (броунмілерит) та промили етанолом. Об'єднані етанолові екстракти концентрували в умовах вакууму та залишок піддали хроматографії на силікагелі (дихлорметан:метанол:ізопропіламін 95:5:1), внаслідок чого отримали бажаний продукт (2,63г, 84%). 1H ЯМР (400МГц, CDCl3) 7,10 (т, 1Η, J=7,6Гц), 6,62 (д, 1Н, J=8,4Гц), 6,60-6,59 (м, 2Н), 4,27-4,18 (м, 2Η), 3,62-3,58 (м, 2Н), 2,80-2,72 (м, 2Н), 2,62-2,59 (м, 1Н), 1,89-1,52 (м, 4Н), 1,49 (с, 9Н), ESMS m/e: 277,2 (Μ+Н)+. 35 Трет-бутил 4-{3-[(6бромгексаноїл)аміно]феніл}-1піперидинкарбоксилат. 25-мл круглодонну колбу, наповнену трет-бутил-4-[3-(аміно)феніл]-1піперидинкарбоксилатом (2,00ммоль, 0,553г), 6бромогексаноїлхлоридом (0,427г, 2,00ммоль, 1,0екв.), триетиламіном (0,404г, 4,00ммоль) та THF (8,00мл), перемішували при кімнатній температурі протягом 4 годин. Реакційну суміш розбавили хлороформом (50мл) та промили водою (100мл), сольовим розчином, висушили над MgSО4 та концентрували в умовах вакууму. Залишок очистили шляхом хроматографії (силікагель, гексани/EtOAc 10:1), внаслідок чого отримали бажаний продукт (0,921г, 95,8%). 1H ЯМР (400МГц, CDCl3) 7,47 (с, 1Н), 7,28-7,22 (м, 2Н), 7,11 (с, 1Н), 6,5 (д, 1Н, J=7,0Гц), 3,45-3,39 (м, 2Н), 2,85-2,70 (м, 2Н), 2,68-2,58 (м, 1Н), 2,37 (т, 2Н, J=7,4Гц), 1,961,71 (м, 7Н), 1,68-1,50 (м, 5Н), 1,48 (с, 9Н), ESMS m/e: 355,4, 476,6. Трет-бутил 4-(3-{[6-(3,4дифтораніліно)гексаноїл]аміно}-феніл)-1піперидинкарбоксилат. 5-мл круглодонну колбу, наповнену трет-бутил-4-{3-[(6бромгексаноїл)аміно]феніл}-1піперидинкарбоксилатом (40,9мг, 0,100ммоль), 3,4-дифтораніліном (0,100ммоль, 12,9мг), К2СО3 (0,100ммоль, 13,8мг), Nal (22,5мг, 0,150ммоль) та DMF (1,00мл), нагрівали при 120°С протягом 12 годин. Реакцію розвели водою (10мл). Водний шар екстрагували хлороформом (3х10мл) та об'єднані екстракти промили сольовим розчином, висушили над MgSО4 та концентрували в умовах вакууму. Залишок очистили шляхом хроматографії (гексани/EtOAc 10:1), внаслідок чого отримали бажаний продукт у вигляді світло-жовтої олії (7,14мг, 14,3%). 1H ЯМР (400МГц, CDCl3) 7,47 (с, 1Н), 7,31-7,18 (м, 1Н), 6,98-6,90 (м. 3Н), 6,50-6,43 (м, 1 Η), 6,40-6,30 (м, 2Η), 6,26-6,20 (м, 1Н), 4,28-4,18 (м, 2Н), 3,06 (т, 2Н, J=7,2Гц), 2,97-2,87 (м, 1Н), 2,842,72 (м, 2Н), 2,68-2,58 (м, 2Н), 2,38 (т, 2Н, J=7,4Гц), 1,85-1,73 (м, 4Н), 1,7-1,54 (м, 4Н), 1,48 (с, 9Н) ESMS m/e: 502,2 (Μ + Н)+. 77536 36 Приклад 6: 6-(3,4-дифтораніліно)-N-[3-(4піперидиніл)феніл]-гексанамід. До розчину третбутил 4-(3-{[6-(3,4-дифтораніліно)гексаноїл]аміно}феніл)-1-піперидинкарбоксилату (11,2мг, 0,0224ммоль) в дихлорметані (0,500мл) при 0°С повільно додавали трифторооцтову кислоту (25,5мг, 2,24ммоль). Реакційну суміш перемішували при кімнатній температурі протягом 10 хвилин та концентрували у вакуумі. Залишок розчинили у i-РrОН/СНСl3 (1:3; 10мл) і підлужували до рН 11 10% КОН, промили водою, потім соляним розчином. Органічний шар висушили над MgSO4 та концентрували в умовах вакууму, одержуючи бажаний продукт (8,98мг, 99%): 1H ЯМР (400МГц, CDCl3) 7,39-7,08 (м, 5Н), 7,06-6,94 (м, 2Н), 6,916,81 (м, 1Н), 6,77-6,67 (м, 1Н), 3,54-3,42 (м, 2Н), 3,25-3,04 (м, 3Н), 2,91-2,80 (м, 1Н), 2,45-2,32 (м, 2Н), 2,11-1,99 (м, 2Н), 1,98-1,83 (м, 2Н), 1,80-1,62 (м, 4Н), 1,55-1,40 (м, 2Н), 1,34-1,23 (м, 1Н), ESMS т/е: 402,2 (М+Н)+. Наступні сполуки були одержані у відповідності зі схемою І. Приклад 1 5-(2-метоксифеніл)-N-[3-(4піперидиніл)феніл]пентанамід: трет-бутил 4-(3-{[5(2-метоксифеніл)пентаноїл]аміно}феніл)-1піперидинкарбоксилат зазнав процедури згідно зі схемою І, внаслідок чого отримали продукт: 1H ЯМР (400МГц, CD3CI3) 7,52-6,68 (м, 8Н), 3,74 (с, 3Н), 3,61-3,35 (м, 2Н), 3,14-2,90 (м, 2Н), 2,88-2,56 (м, 3Н), 2,52-2,27 (м, 2Н), 2,10-1,51 (м, 8Н), ESIMS + m/e: 367,2 [М + Н] . Приклад 2 5-феніл-N-(3-(4-піперидиніл)феніл]пентанамід: трет-бутил 4-{3-[(5-фенілпентаноїл)аміно]феніл}-1піперидинкарбоксилат зазнав процедури згідно зі схемою І, внаслідок чого отримали продукт: 1H ЯМР (400МГц, CD3CI3) 7,51-6,83 (м, 9Н), 3,663,40 (м, 2Н), 3,08-2,80 (м, 2Н), 2,78-2,45 (м, 3Н), 2,43-2,28 (м, 2Н), 2,08-1,60 (м, 8Н); ESIMS m/e: 337,2 [М + Н]+. Приклад 3 6-оксо-6-феніл-N-[3-(4піперидиніл)феніл]гексанамід: трет-бутил 4-{3-[(6оксо-6-фенілгексаноїл)аміно]феніл}-1піперидинкарбоксилат зазнав процедури згідно зі схемою І, внаслідок чого отримали продукт: 1H ЯМР (400МГц, CD3OD) 7,98-7,83 (м, 2Н), 7,607,31 (м, 4Н), 7,28-7,12 (м, 2Н), 6,97-6,87 (м, 1Н), 3,48-3,31 (м, 2Н), 3,10-2,68 (м, 5Н), 2,40-2,26 (м, 2Н), 2,05-1,63 (м, 8Н), ESIMS m/e: 365,2 [М+Н]+. Приклад 4 2-фенокси-N-[3-(4піперидиніл)феніл]нікотинамід: Суміш трет-бутил 4-[3-(аміно)феніл]-1-піперидинкарбоксилату (0,15ммоль), 2-феноксинікотиноїлхлориду 37 77536 38 (0,23ммоль) та триетиламіну (0,30ммоль) у 3мл хроматографії (силікагель, гексани/ЕtOАс/Еt3N розчинника (CH2CI2:THF, 1:3) перемішували при 50:50:0,1), внаслідок чого отримали суміш таутокімнатній температурі протягом 12 годин. Реакціймерів (4:1, 33,0г, 53,9%). 1H ЯМР (CDCl3) 7,32ну суміш очистили шляхом препаративної тонко7,24 (м, 2Н), 7,04-6,95 (м, 2Н), 5,81 (с, 1Н), 5,38 (д, шарової хроматографії (ТШХ) (силакагель, 1Н, J=2,9Гц), 4,00 (с, 3Н), 3,63 (с, 3Н), 2,34 (с, 3Н). ЕtOАс:гексан, 1:1), внаслідок чого отримали бажаний продукт, трет-бутил 4-(3-{[(2-фенокси-3піридиніл)карбоніл]аміно}феніл)-1піперидинкарбоксилат. Трифторооцтову кислоту (1,0мл) додали в очищений продукт, розчинений у 1,0мл CH2CI2 та розчин перемішували при кімнатній температурі протягом 1 хвилини. Реакційну суміш концентрували в умовах вакууму, внаслідок чого отримали сіль TFA бажаного продукту. 1H 5-метил 1-(4-нітрофеніл)-6-(4-фторфеніл)-2ЯМР (400МГц, CDCl3) 9,85 (с, 1Н), 8,76-8,64 метокси-4-метил-1,5(6Н)-піримідиндикарбоксилат. (ушир, 1Н), 8,30-8,14 (ушир, 1Н), 7,67 (с, 1Н), 7,49 До розчину метил 6-(4-фторфеніл)-2-метокси-4(т, 2Η, J=7,8Гц), 7,42-7,29 (м, 3Н), 7,24 (т, 3Н, метил-1,6-дигідро-5-піримідинкарбоксилату (1,76г, J=5,2Гц), 7,03 (д, 1Н, J=7,2Гц), 3,59 (ушир д, 2Н, 6,34ммоль) та 4-диметиламінопіридину J=11,5), 3,16-3,02 (м, 2Н), 2,9-2,79 (м, 1Н), 2,14(12,7ммоль, 1,55г) у безводному СН2СІ2 (20,0мл) 2,01 (м, 4Н), ESIMS m/e: 374,1 [Μ+Н]+. додали розчин 4-нітрофенілхлорформіату (4,47г, Приклад 5 22,2ммоль) у CH2CI2 (20,0мл) при 23°С. Реакційну 5-(4-метоксифеніл)-N-[3-(4суміш перемішували протягом 2 годин при кімнатппіеридиніл)феніл]пентанамід: Приготували згідно ній температурі. Реакційну суміш розбавили з процедурою, наведеною на Схемі І CH2CI2 (50мл), промили водою, сольовим розчином, висушили над сульфатом натрію та концентрували в умовах вакууму. Залишок очистили шляхом колончастої флеш-хроматографії (гексани/етилацетат 4:1). Продукт отримали у вигляді жовтого сиропу, який після розтирання у порошок гексанами перетворився на білий порошок (2,40г, 84,3%). Сирий продукт застосовували на наступному етапі без подальшого очищення. Метил (2Z)-2-ацетил-3-(4-фторфеніл)-2пропеноат. Суміш 4-фторбензальдегіду (25,5г, 0,220моль), метил 3-оксобутаноату (21,80г, 0,220моль) та піперидину (1,0мл) у безводному бензолі (250мл) перемішували протягом 10 хвилин при кімнатній температурі з наступним нагріванням при температурі дефлегмації протягом ночі у апараті Dean-Stark. Реакційну суміш потім охолодили до кімнатної температури та розчинник виМетил 1-{[(4-трет-бутокси-4далили в умовах вакууму, внаслідок чого отримаоксобутил)аміно]карбоніл}-6-(4-фторфенiл)-2ли метил (2Z)-2-ацетил-3-(4-фторфеніл)-2метокси-4-метил-1,6-дигідро-5пропеноат у вигляді чорної твердої речовини піримідинкарбоксилат. До розчину 5-метил-1-(4(48,6г, 99%), який застосовували на наступному нітрофеніл) 6-(4-фторфеніл)-2-метокси-4-метилетапі без очищення. 1,5(6Н)-піримідинкарбоксилату (88,7мг, 0,200ммоль) та К2СО3 (41,5мг, 0,300ммоль) у СН3ОН/CH2CI2 (0,1/2,0мл) додали трет-бутил 4амінобутаноат (31,8мг, 0,200ммоль). Після перемішування при кімнатній температурі протягом 1 години, суміш промили насиченим Nа2СО3 та сольовим розчином. Органічний шар висушили над MgSO4 та концентрували в умовах вакууму. Сирий матеріал очистили шляхом флеш-хроматографії (5%-10% 2Μ NH3/MeOH у 50% EtOАс/гексанах), Метил 6-(4-фторфеніл)-2-метокси-4-метил-1,6внаслідок чого отримали продукт (92,2г, 99%). Тодигідро-5-піримідинкарбоксилат. Суміш метил чка плавлення 135-138°С, 1H ЯМР (CD3OD) 7,29(2Z)-2-ацетил-3-(4-фторфеніл)-2-пропеноату 7,23 (м, 2Н), 6,97-6,88 (м, 2Н), 6,65 (с, 1Н), 3,98 (с, (0,220моль, 48,8г), О-метилізосечовини гідро3Н), 3,66 (с, 3Н), 3,38-3,30 (м, 2Н), 2,43 (с, 3Н), 2,28 сульфату (53,40г, 0,310моль, 1,5екв.), NaHCO3 (т, 2Н, J=7,2Гц), 1,89-1,78 (м, 2Н), 1,43 (с, 9Н), (61,74г, 0,74моль, 3,5екв.) та етанолу (1,2л) нагріESMS m/e: 464,1 (М+Н)+. вали при температурі дефлегмації протягом 24 годин, охолодили до кімнатної температури та профільтрували. Тверду речовину промили етанолом (200мл) та об'єднаний фільтрат концентрували в умовах вакууму. Залишок очистили шляхом 39 4-{[(6-(4-фторфеніл)-5-(метоксикарбоніл)-4метил-2-оксо-3,6-дигідро-1(2н)шримідишл)карбошл]аміно}бутанова кислота. До розчину метил 1-{[(4-яірет-бутокси-4оксобутил)аміно]карбоніл}-6-(4-фторфеніл)-2метокси-4-метил-1,6-дигідро-5піримідинкарбоксилату (77,3мг, 0,166ммоль) у дихлорметані (2,00мл) при 0°С повільно додавали трифторооцтову кислоту (189мг, 1,66ммоль). Реакційну суміш перемішували при кімнатній температурі протягом 10 хвилин та концентрували в умовах вакууму. Залишок розчинили у ізо-РrOН/СНСI3 (1:3, 10мл) та підлужили до рН 11 10% розчином КОН, промили Н2О, потім сольовим розчином. Органічний Шар висушили над MgSO4 та концентрували в умовах вакууму, внаслідок чого отримали бажаний продукт (58,1мг, 88,9%). ESMS m/e: 394,1 (Μ+Н)+. Метил 3-{[(4-{3-[1-(трет-бутоксикарбонiл)-4ппіеридиніл]аніліно}-4-оксобутил)аміно]карбоніл}4-(4-фторфеніл)-6-метил-2-оксо-1,2,3,4-тетрагідро5-піперидинкарбоксилат. 10-мл круглодонну колбу наповнили 4-{[(6-(4-фторфеніл)-5(метоксикарбоніл)-4-метил-2-оксо-3,6-дигідро1(2Н)-піримідиніл)карбоніл]аміно}бутановою кислотою (77,0мг, 0,189ммоль), трет-бутил-4-[3(аміно)феніл]-1-піперидинкарбоксилатом (52,2мг, 0,189ммоль), 1-[3-(диметиламіно)пропіл]-3етилкарбодіміду гідрохлоридом (0,567ммоль, 87,8мг), 4-диметиламінопіридином (11,5мг, 0,0945ммоль) у DMF:DCM (0,2:2,0мл) при кімнатній температурі. Реакційну суміш перемішували протягом 12 годин та додали воду (10,0мл) до реакційної суміші. Органічний шар видалили та водний шар екстрагували СНСl3 (3x10мл). Об'єднані органічні екстракти промили сольовим розчином, висушили над MgSO4, профільтрували та концентрували в умовах вакууму. Залишок піддали хроматографії (сілікагель, гексани: EtOAc 9:1), внаслідок чого отримали бажаний продукт (40,9мг, 33,2%): 1H ЯМР (400МГц, CDCl3) 8,03 (м, 3Н), 7,57 (с, 1Н), 7,36-7,28 (м, 3Н), 7,27-7,22 (м, 1Н), 6,97-6,89 (м, 3Н), 6,72 (с, 1Н), 3,72 (с, 3Н), 3,473,37 (м, 2Н), 2,42 (с, 3Н), 2,37-2,29 (м, 2Н), 1,981,91 (м, 2Н), 1,86-1,75 (м, 2Н), 1,72-1,54 (м, 7Н), 1,48 (с, 9Н), ESMS m/e: 652,2 (М+Н)+. 77536 40 Приклад 7: Метил 4-(4-фторфенiл)-6-метил-2оксо-3-[({4-оксо-4-[3-(4піперидиніл)аніліно]бутил}аміно)карбоніл]-1,2,3,4тетрагідро-5-піримідинкарбоксилат. До розчину метил 3-{[(4-{3-[1-(трет-бутоксикарбоніл)-4піперидиніл]аніліно}-4-оксобутил)аміно]карбоніл}4-(4-фторфеніл)-6-метил-2-оксо-1,2,3,4-тетрагідро5-піримідинкарбоксилату (40,9мг, 0,0628ммоль) у дихлорметані (2,00мл) при 0°С повільно додавали трифторооцтову кислоту (71,6мг, 0,628ммоль). Реакційну суміш перемішували при кімнатній температурі протягом 10 хвилин та концентрували в умовах вакууму. Залишок розчинили в (ізоPrOH/CHCl3 (1:3, 10мл) та підлужили до рН 11 10% розчином КОН, промили Н2О, а потім сольовим розчином. Органічний шар висушили над MgSO4 та концентрували в умовах вакууму, внаслідок чого отримали бажаний продукт (34,6мг, 99%): 1H ЯМР (400МГц, CDCl3) 8,00 (м, 3Н), 7,67 (с, 1Н), 7,35-7,27 (м, 4Н), 7,04-6,98 (м, 3Н), 6,65 (с, 1Н), 3,72 (с, 3Н), 3,5-3,48 (м, 2Н), 3,20-3,11 (м, 3Н), 2,42 (т, 2Н, J=7,5Гц), 2,36 (с, 3Н), 2,13-2,06 (м, 2Н), 1,97-1,88 (м, 4Н), ESMS т/е: 552,3 (М+Н)+. Трет-бутил-4-{3-[(4-{[(5-метоксилкарбонiл-6(3,4-дифторфенiл)-4-метил-2-оксо-3,6-дигідро1(2Н)-піперидиніл)карбоніл]аміно}бутаноїл)аміно]феніл}піперидинкарбоксилат. 50мл круглодонну колбу заповнили 4-{[(5-ацетил-6(3,4-дифторфеніл)-4-метил-2-оксо-3,6-дигідро1(2Н)-піримідиніл)карбоніл]аміно}бутановою кислотою (313мг, 0,854ммоль), трет-бутил-4-[3(аміно)феніл]-1-піперидинкарбоксилатом (235мг, 0,857ммоль), 1-[3-(диметиламіно)пропіл]-3етилкарбодіміду гідрохлоридом (7,71ммоль, 265мг), 4-диметиламінопіридином (10,4мг, 0,0854ммоль) у DMF:DCM (0,8:8,0мл) при кімнатній температурі. Реакційну суміш перемішували протягом 12 годин та додали воду (20,0мл) до реакційної суміші. Органічний шар видалили та водний шар екстрагували СНСl3 (3x10мл). Об'єднані органічні екстракти промили сольовим розчином, висушили над MgSO4, профільтрували та концентрували в умовах вакууму. Залишок піддали хроматографії (силікагель, гексани:ЕtOАс 9:1), внаслідок чого отримали бажаний продукт (378мг, 67,8%): 1H ЯМР (400МГц, CDCl3) 8,03 (м, 2Н), 7,57 (с, 1Н), 7,36-7,28 (м, 3Н), 7,27-7,22 (м, 1Н), 6,97-6,89 (м, 3Н), 6,72 (с, 1Н), 3,72 (с, 3Н), 3,473,37 (м, 2Н), 2,42 (с, 3Н), 2,37-2,29 (м, 2Н), 1,98 41 77536 42 1,91 (м, 2Н), 1,86-1,75 (м, 2Н), 1,72-1,54 (м, 7Н), тетраметил-1,3,2-діоксаборолан-2-іл)-3,6-дигідро1,48 (с, 9Н), ESMS m/e: 554,3 (М-100). 1(2Н)-піридинкарбоксилат (355мг, 76%): 1H ЯМР (400МГц, CDCl3) 6,60-6,34 (ушир, 1Н), 4,06-3,86 (ушир, 2Н), 3,55-3,34 (ушир, 2Н), 2,35-2,09 (ушир, 2Н), 1,46 (с, 9Н), 1,26 (с, 12Н), ESMS m/e: 310,4 + (М+Н) . Приклад 8: 5-метоксилкарбонiл-6-(3,4дифторфенiл)-4-метил-2-оксо-N-{4-оксо-4-[3-(4піперидиніл)аніліно]бутил}-3,6-дигідро-1(2Н)піперидинкарбоксамід. До розчину трет-бутил 4-{3[(4-{[(5-метоксилкарбоніл-6-(3,4-дифторфеніл)-4метил-2-оксо-3,6-дигідро-1(2Н)піримідиніл)карбоніл]аміно}-бутаноїл)аміно]феніл}1-піперидинкарбоксилату (378мг, 0,579ммоль) у дихлорметані (5,00мл) при 0°С повільно додавали трифторооцтову кислоту (659мг, 5,79ммоль). Реакційну суміш перемішували при кімнатній температурі протягом 10 хвилин та концентрували в умовах вакууму. Залишок розчинили в ізо-РrOН/СНСI3 (1:3, 10мл) та підлужили до рН 11 10% розчином КОН, промили Н2О, потім сольовим розчином. Органічний шар висушили над MgSO4 та концентрували в умовах вакууму. Залишок очистили шляхом флеш-хроматографії (дихлорметан:метанол 5:1), внаслідок чого отримали бажаний продукт (93,8мг, 29,3%): 1H ЯМР (400МГц, CDCl3) 7,46-7,43 (м, 3Н), 7,35-7,29 (м, 2Н), 7,12-7,06 (м, 3Н), 6,63-6,60 (м, 1Н), 6,56-6,52 (м, 2Н), 3,26 (с, 3Н), 3,22 (с, 3Н), 2,72 (дт, 6Н, J=2,3, 12,3Гц), 2,66 (тт, 2Н, J=3,6, 11,9Гц), 2,55 (тт, 1Н, J=3,8, 11,9Гц), 1,88-1,82 (м, 1Н), 1,75-1,63 (м, 6Н), ESMS m/e: 554,3 (Μ+Н)+. Загальна процедура синтезу піперидину (схема 2) Трет-бутил 4-(4,4,5,5-тетраметил-1,3,2діоксаборолан-2-іл)-3,6-дигідро-1(2Н)піридинкарбоксилат : У 50-мл круглодонну колбу, наповнену біс(пінаколато)дибором (422мг, 1,66ммоль), КОАс (444мг, 4,53ммоль), PdCl2dppf (37,0мг, 3,00мол %) та dppf (25,0мг, 3,00мол%), додали розчин трет-бутил 4{[(трифторметил)сульфоніл]окси}-3,6-дигідро1(2Н)-піридинкарбоксилату (500мг, 1,51ммоль) у 1,4-діоксані (10,0мл) при кімнатній температурі в атмосфері аргону. Суміш нагрівали при 80°С протягом ночі. Після охолодження до кімнатної температури суміш профільтрували крізь Celite та Celite промили EtOAc (3х20мл). Об'єднані фільтрати промили Н2О та сольовим розчином, висушили над MgSO4, профільтрували та концентрували в умовах вакууму. Сирий продукт очистили шляхом флеш-хроматографії (EtOAc:гексани 1:9), внаслідок чого одержали трет-бутил 4-(4,4,5,5 5-бром-2,4-дифторнітробензол. До суспензії 1бром-2,4-дифторбензолу (53,0ммоль, 6,00мл) у концентрованій H2SO4 (38,5мл) при 0°С додавали краплями концентровану ΗΝΟ3 (34,0мл), підтримуючи внутрішню температуру нижче 20°С. Одержану суміш перемішували протягом 10 хвилин при 0°С, потім вилили у лід/воду, при цьому сильно перемішуючи. Суміш екстрагували Et2O (3х100мл). Об'єднані органічні екстракти промили водним розчином NаНСО3 (3x100мл) та сольовим розчином, висушили над MgSO4, профільтрували та концентрували в умовах вакууму. Сирий продукт очистили шляхом флеш-хроматографії (EtOAc:гексани 1:9), внаслідок чого отримали 5бром-2,4-дифторнітробензол у вигляді жовтої олії (12,2г, 97%). 1H ЯМР (400МГц, CDCl3) 8,45 (т, 1Η, J=7,5Гц), 7,16 (дд, 1Н, J=11,0, 8,6Гц), ESMS m/e: 240, 238, 223, 221, 112. 5-бром-2,4-дифторанілін. 250-мл круглодонну колбу, наповнену 5-бром-2,4дифторнітробензолом (5,04г, 21,3ммоль), насиченим NH4CI (25,0мл), порошком заліза (5,00г, 89,5ммоль), етанолом (100мл), THF (50,0мл) та водою (25,0мл), нагрівали у колбі зі зворотним холодильником при 95°С протягом 1,5 години. Після охолодження до кімнатної температури додали насичений NаНСО3 (100мл) та суміш профільтрували крізь Celite та Celite промили EtOAc (3x50 мл). Об'єднані фільтрати промили Н2О та сольовим розчином, висушили над MgSO4, профільтрували та концентрували в умовах вакууму. Сирий продукт очистили шляхом флеш-хроматографії (ЕtOАс:гексани 1:9), внаслідок чого отримали 5бром-2,4-дифторанілін (2,61г, 59,1%). 1H ЯМР (400МГц, CDCl3) 6,97 (дд, 1Н, J=7,2, 6,7Гц), 6,85 (т, 1Η, J=8,2Гц), 3,63 (ушир, 2Н). Бензил 5-бром-2,4-дифторфенілкарбамат. До 250-мл круглодонної колби додали 5-бром-2,4дифторанілін (5,00г, 24,2ммоль), хлорбензилфор 43 77536 44 міат (4,10мл, 29,0ммоль), NаНСО3 (6,10г, лацетаті (25,0мл) та метанолі (25,0мл) гідрували 72,6ммоль) та ацетонітрил (100мл). Реакційну супри кімнатній температурі протягом 72 годин, заміш перемішували при 25°С протягом 12 годин, стосовуючи водневу бомбу (200 фунтів на квадрапотім профільтрували крізь крупно спечене скло, тний дюйм). Реакційну суміш профільтрували крізь фриттовану лійку, промили ЕtOАс (3x20мл) та Celite та промили ЕtOАс/МеОН (1:1, 3х50мл). Фільконцентрували в умовах вакууму. Фільтрат промитрат концентрували в умовах вакууму, внаслідок ли Н2О та сольовим розчином, висушили над чого отримали трет-бутил 4-(5-аміно-2,4MgSO4, профільтрували та концентрували в умодифторфеніл)-1-піперидинкарбоксилат (1,39г, вах вакууму. Сирий продукт очистили шляхом 100%). 1H ЯМР (400МГц, CDCl3) 6,73 (т, 1Н, флеш-хроматографії (ЕtOАс:гексани 1:9), внасліJ=10,6Гц), 6,60-6,54 (дд, 1Н, J=7,6, 6,57Гц), 4.20 док чого отримали бензил 5-бром-2,4(ушир, 2Н), 3,55 (с, 2Н), 2,96-2,72 (м, 3Н), 1,79-1,71 дифторфенілкарбамат (5,05г, 61,0%): 1H ЯМР (м, 2Н), 1,58-1,52 (м, 2Н), 1,47 (с, 9Н), ESMS m/e: (400МГц, CDCl3) 8,38 (с, 1Н), 7,49-7,31 (м, 5Н), 257,3 (Μ-56). 6,94-6,89 (м, 1Н), 6,81-6,77 (м, 1Н), 5,22 (с, 2Н), ESMS m/e: 340,1 (М-Н+). Трет-бутил 4-(5-{[(бензилокси)карбонiл]аміно}2,4-дифторфенiл)-3,6-дигiдро-1(2Н)піридинкарбоксилат. До 250-мл круглодонної колби, що містила трет-бутил 4-(4,4,5,5-тетраметил1,3,2-діоксаборолан-2-іл)-3,6-дигідро-1(2Н)піридинкарбоксилат (4,58г, 14,8ммоль), К2СО3 (6,14г, 44,4ммоль) та PdChdppf (1,48ммоль, 1,21г), додали розчин бензил 5-бром-2,4дифторфенілкарбамату (5,05, 14,8ммоль) у DMF (150мл) при кімнатній температурі в атмосфері аргону. Суміш нагрівали до 80°С в атмосфері аргону протягом ночі. Після охолодження до кімнатної температури суміш профільтрували крізь Celite та Celite промили ЕtOАс (3х100мл). Фільтрати промили Н2О (3х200мл), сольовим розчином (100мл), висушили над MgSO4, профільтрували та концентрували в умовах вакууму. Сирий матеріал очистили шляхом флеш-хроматографії (ЕtOАс/гексани 1:9), внаслідок чого отримали третбутил 4-(5-{[(бензилокси)карбоніл]аміно}-2,4дифторфеніл)-3,6-дигідро-1(2Н)піридинкарбоксилат (1,60г, 24,5%): 1H ЯМР (400МГц, CDCl3) 8,08 (с, 1Н), 7,45-7,35 (м, 5Н), 6,85-6,70 (м, 1Η), 5,95-5,85 (м, 1Н), 5,20 (с, 2Н), 4,05 (м, 2Н), 3,6-3,5 (м, 2Н), 2,5-2,4 (м, 2Н), 1,50 (с, 9Н), ESMS m/e: 443,3 (М-Н+). Трет-бутил 4-(5-аміно-2,4-дифторфеніл)-1піперидинкарбоксилат. Суміш трет-бутил 4(5{[(бензилокси)карбоніл]аміно}-2,4-дифторфеніл)3,6-дигідро-1(2Н)-піридинкарбоксилату (1,60г, 3,60ммоль) та 5% Pd/C (320мг, 0,100ммоль) в ети Етил (4Е)-5-(2-метоксифеніл)-4-пентеноат. До 200-мл круглодонної колби додали 2-йодоанізол (5,00г, 21,4ммоль), етил 4-пентеноат (3,30г, 25,6ммоль), тетракістрифенілфосфінпаладій(0) (0,740г, 0,600ммоль), триетиламін (6,00мл, 42,7ммоль) та суміш CH3CN (45,0мл) та THF (15,0мл). Реакційну суміш нагрівали при температурі дефлегмації протягом ночі та потім охолодили до кімнатної температури. Після того, як видалили розчинники в умовах вакууму, одержаний темнокоричневий залишок розчинили у 5% НСІ (водн.) та екстрагували CH2CI2 тричі. Об'єднані екстракти промили насиченим розчином NaHCО3, висушили над MgSO4, концентрували в умовах вакууму. Темно-коричневу олію очистили шляхом хроматографії (силікагель, ЕtOАс/Гексани 1:10), внаслідок чого отримали продукт у вигляді світло-жовтої олії (3,40г, 68%). Етил 5-(2-метоксифеніл)пентаноат. До розчину етил (4Е)-5-(2-метоксифеніл)-4-пентеноату (3,40г, 14,5ммоль) у суміші EtOAc та МеОН (40,0/10,0мл) додавали дрібними порціями Pd/C (паладій на вуглецю 10%, 0,700г), щоб запобігти спалахуванню. Реакційну суміш потім перемішували протягом ночі при кімнатній температурі під тиском 300 фунтів на кв. дюйм в атмосфері водню. Після зняття тиску суміш профільтрували крізь Celite та Celite промили EtOAc (3х50мл). Фільтрат концентрували в умовах вакууму, внаслідок чого отримали сирий продукт у вигляді світло-жовтої олії (3,40г, 100%), який потім застосовували без подальшого очищення. 5-(2-метоксифеніл)пентанова кислота. 250-мл круглодонну колбу наповнили етил 5-(2 45 77536 46 метоксифеніл)пентаноатом (3,40г, 14,5ммоль), трифторооцтову кислоту (707мг, 6,20мл). РеакційNaOH (1,74г, 42,8ммоль), тетрагідрофураном ну суміш перемішували при кімнатній температурі (25,0мл) та водою (25,0мл). Реакційну суміш нагріпротягом 10 хвилин та концентрували в умовах вали при температурі дефлегмації протягом 2 говакууму. Залишок розчинили у і-РrOН/СНСI3 (1:3, дин та охолодили до кімнатної температури. Реак10мл) та підлужили до рН 11 10% розчином КОН, ційну суміш концентрували в умовах вакууму та промили Н2О, а потім сольовим розчином. Органіодержаний водний розчин підкислили 6Μ НСІ до чний шар виділили, висушили над MgSO4 та конрН
ДивитисяДодаткова інформація
Назва патенту англійськоюSecondary aminoaniline piperidines as mch1 antagonists and their use
Автори англійськоюJIANG YU, LU KAI, CHEN CHIEN AN
Назва патенту російськоюВторичные аминоанилиновые пиперидины в качестве антагонистов mch1 и их применение
Автори російськоюДжианг Ю, Лу Кай, Чен Чиен-Ан
МПК / Мітки
МПК: A61P 3/04, A61P 25/22, C07D 211/26, A61P 25/24, A61K 31/506, A61P 13/02, A61K 31/4545, A61K 31/451, C07D 401/12, A61P 43/00
Мітки: застосування, аміноанілінові, піперидини, антагоністи, вторинні
Код посилання
<a href="https://ua.patents.su/32-77536-vtorinni-aminoanilinovi-piperidini-yak-antagonisti-mch1-ta-kh-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Вторинні аміноанілінові піперидини як антагоністи mch1 та їх застосування</a>
Попередній патент: Технологічне мастило для металевих форм
Наступний патент: Пристрій для швидкої оцінки механічних характеристик пружних матеріалів
Випадковий патент: Спосіб отримання ембріонів свиней in vitro з використанням наноматеріалу