Сполуки хіноліну для лікування порушень, які реагують на модуляцію рецептора серотоніну 5-ht6
Номер патенту: 97837
Опубліковано: 26.03.2012
Автори: Вікке Карстен, Майрер Маттіас, Дрешер Карла, Мецлер Маріо, Тернер Шон Кольм, Вернет Вольфганг, Ланге Удо, УНГЕР Ліліане, Хаупт Андреас, Брайє Вілфрід
Формула / Реферат
1. Сполука хіноліну формули (І)
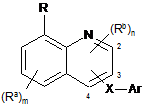 , (I)
, (I)
де R являє собою радикал формули
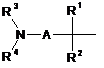 , (R)
, (R)
де А являє собою хімічний зв'язок, CHR5 або CH2CHR5;
R1 являє собою водень, С1-С4-алкіл, С1-С4-галогеналкіл, С1-С4-алкокси або С1-С4-галогеналкокси;
R2 являє собою водень, С1-С4-алкіл, С1-С4-галогеналкіл, С1-С4-алкокси або С1-С4-галогеналкокси;
R3 являє собою водень або С1-С4-алкіл;
R1 і R3 разом можуть також являти собою лінійний С1-С4-алкілен, який може містити 1 або 2 радикали R6;
R4 являє собою водень, С1-С6-алкіл, С1-С6-гідроксіалкіл, С1-С6-галогеналкіл, С1-С6-алкоксі-С1-С4-алкіл, С1-С6-галогеналкоксі-С1-С4-алкіл, С3-С6-циклоалкіл, С3-С6-галогенциклоалкіл, С3-С6-циклоалкіл-С1-С4-алкіл, арил-С1-С4-алкіл, гетероарил-С1-С4-алкіл, С3-С6-алкеніл, С3-С6-галогеналкеніл, форміл, С1-С4-алкілкарбоніл або С1-С4-алкоксикарбоніл;
R5 являє собою водень, С1-С4-алкіл, С1-С4-галогеналкіл, С1-С4-алкокси або С1-С4-галогеналкокси;
R1 і R5 разом можуть також являти собою одинарний зв'язок або лінійний С1-С4-алкілен, який може містити 1 або 2 радикали R7; або
R3 і R5 разом можуть також являти собою лінійний С1-С4-алкілен, який може містити 1 або 2 радикали R8;
R6 являє собою С1-С4-алкіл, С1-С4-галогеналкіл, С1-С4-алкокси або С1-С4-галогеналкокси; або
R5 і R6 разом можуть також являти собою лінійний С1-С4-алкілен, який може містити 1 або 2 радикали R9;
R7, R8 і R9 незалежно вибирають з групи, що складається з С1-С4-алкілу, С1-С4-галогеналкілу, С1-С4-алкокси і С1-С4-галогеналкокси;
n являє собою 0, 1 або 2;
m являє собою 0, 1, 2 або 3;
Ra, Rb незалежно вибирають з групи, що складається з галогену, CN, С1-С4-алкілу, С1-С4-галогеналкілу, С1-С4-алкокси, С1-С4-галогеналкокси, C(O)Raa, C(O)NRccRbb і NRccRbb; при цьому Raa являє собою водень, С1-С4-алкіл, С1-С4-галогеналкіл, С1-С4-алкокси або С1-С4-галогеналкокси, a Rcc, Rbb незалежно вибирають з групи, що складається з водню і С1-С4-алкілу;
X являє собою СН2, С(О), S, S(O) або S(O)2; який знаходиться в 3 або 4 положенні хінолінового кільця;
Аr являє собою радикал Аr1, Аr2-Аr3 або Аr2-О-Аr3, при цьому кожний з Аr1, Аr2 і Аr3 незалежно вибирають з групи, що складається з арилу або гетероарилу, при цьому арильний або гетероарильний радикал може бути незаміщеним або може містити 1, 2, 3 замісники Rx, при цьому
Rx являє собою галоген, CN, NO2, С1-С6-алкіл, С1-С6-галогеналкіл, С1-С6-гідроксіалкіл, С1-С6-алкоксі-С1-С4-алкіл, С2-С6-алкеніл, С2-С6-галогеналкеніл, С3-С6-циклоалкіл, С3-С6-галогенциклоалкіл, С1-С6-алкокси, С1-С6-гідроксіалкокси, С1-С6-алкоксі-С1-С4-алкокси, С1-С6-галогеналкокси, С1-С6-алкілтіо, С1-С6-галогеналкілтіо, С1-С6-алкілсульфініл, С1-С6-галогеналкілсульфініл, С1-С6-алкілсульфоніл, С1-С6-галогеналкілсульфоніл, С1-С6-алкілкарбоніл, С1-С6-галогеналкілкарбоніл, С1-С6-алкілкарбоніламіно, С1-С6-галогеналкілкарбоніламіно, карбокси, NH-C(O)-NRx1Rx2, NRx1Rx2, NRx1Rx2-С1-С6-aлкiлeн, O-NRx1Rx2, при цьому Rx1 i Rx2 в останніх 4 із згаданих радикалів являють собою незалежно один від одного водень, С1-С6-алкіл, С1-С6-галогеналкіл або С1-С6-алкокси, або Rx1 і Rx2 в останніх 4 із згаданих радикалів утворюють разом з атомом азоту N-зв'язаний 5-, 6- або 7-членний насичений гетероцикл, який є незаміщеним або містить 1, 2, 3 або 4 радикали, вибрані з С1-С4-алкілу, С1-С4-галогеналкілу, С1-С4-гідроксіалкілу і С1-С4-алкокси, і при цьому 2 радикали Rx, які зв'язані з сусідніми атомами вуглецю Аr, можуть утворювати насичене або ненасичене 5- або 6-членне карбоциклічне або гетероциклічне кільце, яке саме по собі може містити радикал Rx;
при умові, що X являє собою S(O)2 і щонайменше один з радикалів R1, R2 і, якщо присутній, R5 відрізняється від водню і С1-С4-алкілу;
її фізіологічно прийнятні кислотно-адитивні солі і її N-оксиди.
2. Сполука за п.1, в яких радикал R являє собою радикал формули:
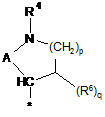 ,
, 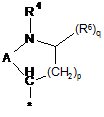 ,
, 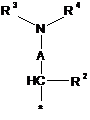 ,
, 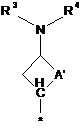 ,
,
в яких A, R2, R3, R4 і R6 визначені в п. 1, * показує місце зв'язування з хіноліновим радикалом, р являє собою 0, 1, 2 або 3, q являє собою 0 або 1, і в яких А являє собою одинарний зв’язок, СН2, СН2СН2, CHR7 або CH2CHR7, при цьому R7 визначений в п. 1.
3. Сполука за п. 1, в яких радикал R являє собою радикал формули:
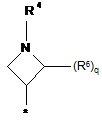 ,
, 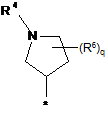 ,
, 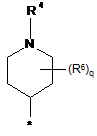 ,
, 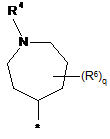 ,
,
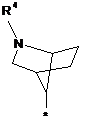 ,
,  ,
, 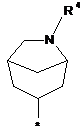 ,
,
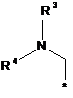 ,
, 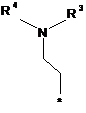 ,
, 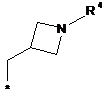 ,
,
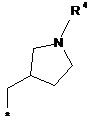 ,
,  ,
, 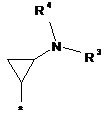 ,
,
в якій R3, R4 і R6 визначені в п. 1, * показує місце зв'язування з хіноліновим радикалом, і в яких q являє собою 0 або 1.
4. Сполука за п. 1, в яких радикал R являє собою радикал формули:
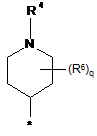 ,
,
в якій R4 і R6 визначені в п. 1, * показує місце зв'язування з хіноліновим радикалом, і в якій q являє собою 0 або 1.
5. Сполука за будь-яким з попередніх пунктів, в яких R4 являє собою водень.
6. Сполука за будь-яким з попередніх пунктів, в яких X являє собою SO2.
7. Сполука за будь-яким з пп. 1-5, в яких X являє собою СН2.
8. Сполука за будь-яким з пп. 1-5, в яких X являє собою С(О).
9. Сполука за будь-яким з попередніх пунктів, в яких X знаходиться в 3 положенні хінолінового радикала.
10. Сполука за будь-яким з пп. 1-8, в яких X знаходиться в 4-положенні хінолінового радикала.
11. Сполука за будь-яким з попередніх пунктів, в яких Аr являє собою феніл, нафтил, тієніл, піридил, піримідил, піразоліл, імідазоліл, оксазоліл, ізоксазоліл, тіазоліл, триазоліл, тіадіазоліл, хінолініл, ізохінолініл, тетрагідроізохінолініл, бензофураніл, бензотієніл, бензоксазиніл, бензотіазоліл, бензоксадіазоліл, бензотіадіазоліл, бензоморфолініл або інданіл, при цьому циклічний радикал Аr є незаміщеним або може містити 1, 2 або 3 замісники Rx, визначені в п. 1.
12. Сполука за п. 11, в яких Аr являє собою феніл, який є незаміщеним або може містити 1, 2 або 3 замісники Rx, визначені в п. 1.
13. Сполука за будь-яким з попередніх пунктів, в яких Rx вибирають з галогену, CN, С1-С4-алкілу, С1-С4-галогеналкілу, С1-С4-алкокси, С1-С4-галогеналкокси, С3-С6-циклоалкілу і групи NRx1Rx2.
14. Сполука за будь-яким з попередніх пунктів, в яких m являє собою 0.
15. Сполука за будь-яким з попередніх пунктів, в яких n являє собою 0.
16. Фармацевтична композиція, що містить щонайменше одну сполуку за будь-яким з попередніх пунктів, необов'язково разом щонайменше з одним фізіологічно прийнятним носієм або допоміжною речовиною.
17. Спосіб лікування медичного порушення, вибраного із захворювань центральної нервової системи, захворювань, пов'язаних із звиканням, або ожиріння, при якому вводять ефективну кількість щонайменше однієї сполуки за будь-яким з пп. 1-15 пацієнту, який в цьому має потребу.
18. Спосіб за п. 17, в якому медичне порушення являє собою захворювання центральної нервової системи.
19. Спосіб за п. 17 для лікування когнітивних дисфункцій.
20. Спосіб за п. 17 для лікування когнітивних дисфункцій, пов'язаних з хворобою Альцгеймера.
21. Спосіб за п. 17 для лікування когнітивних дисфункцій, пов'язаних з шизофренією.
22. Спосіб за п. 17, в якому медичне порушення являє собою захворювання, пов'язане із звиканням.
23. Спосіб за п. 17, в якому медичне порушення являє собою ожиріння.
24. Застосування сполуки за будь-яким з пп. 1-15 для отримання фармацевтичної композиції.
25. Застосування сполуки за будь-яким з пп. 1-15 для отримання фармацевтичної композиції для лікування медичного порушення, визначеного в будь-якому одному з пп. 17-23.
26. Сполука за будь-яким з пп. 1-15 для застосування як лікарського засобу.
27. Сполука за будь-яким з пп. 1-15 для застосування як лікарського засобу для лікування медичного порушення, визначеного в будь-якому одному з пп. 17-23.
Текст
Реферат: Даний винахід стосується хінолінових сполук. Сполуки мають цінні терапевтичні властивості і особливо придатні для лікування захворювань, які реагують на модуляцію серотонінового рецептора 5-НТ6. 1 4 Сполуки формули (І), в яких R являє собою радикал формули (R), в якій А, з R по R визначені a b в формулі винаходу і описі, n являє собою 0, 1 або 2; m являє собою 0, 1, 2 або 3; R , R незалежно вибирають з групи, що складається з галогену, CN, С 1-С4-алкілу, С1-С4aa cc bb cc bb галогеналкілу, С1-С4-алкокси, С1-С4-галогеналкокси, C(O)R , C(O)NR R і NR R ; X являє собою СН2, С(О), С, S(O) або S(O)2; яка знаходиться в 3 або 4 положенні хінолінового кільця; Аr 1 2 3 2 3 1 2 3 являє собою радикал Аr , Аr -Аr або Аr -О-Аr , в якому Аr , Аr і Аr , кожний незалежно, вибирають з групи, що складається з арилу або гетероарилу, при цьому арильний або UA 97837 C2 (12) UA 97837 C2 x гетероарильний радикал може бути незаміщеним або може містити 1, 2, 3 замісники R , і їх фізіологічно прийнятні кислотно-адитивні солі і їх N-оксиди. UA 97837 C2 5 10 15 20 25 30 35 40 45 50 Рівень техніки даного винаходу Даний винахід стосується нових хінолінових сполук. Дані сполуки мають цінні терапевтичні властивості і особливо придатні для лікування захворювань, які реагують на модуляцію 5-НТ6 рецептора серотоніну. Серотонін (5-гідрокситриптамін, 5-НТ), моноаміновий нейротрансмітер і місцевий гормон, утворюється при гідроксилюванні і декарбоксилуванні триптофану. Найвищу його концентрацію виявляють в ентерохромафіноцитах шлунково-кишкового тракту, при цьому інший серотонін переважно знаходиться в тромбоцитах і в центральній нервовій системі (ЦНС). 5-НТ бере участь у безлічі фізіологічних і патофізіологічних шляхах. На периферії 5-НТ скорочує ряд гладеньких м'язів і спричиняє ендотелій-залежне розширення кровоносних судин. Вважається, що в ЦНС 5-НТ бере участь в широкому діапазоні функцій, в тому числі в контролі апетиту, настрою, тривожності, галюцинацій, сну, блювоти і сприйняття болю. Нейрони, які секретують 5-НТ, називаються серотонінергічними. На функціонування 5-НТ впливає його взаємодія зі специфічними (серотонінергічними) нейронами. У даний час виділяють сім типів рецепторів 5-НТ: 5-НТ1 (з підтипами 5-НТ1А, 5-НТ1B, 5-НТ1D, 5-НТ1Е і 5-HT1F), 5-HT2 (з підтипами 5-НТ2A, 5-НТ2B і 5-НТ2C), 5-НТ3, 5-НТ4, 5-НТ5 (з підтипами 5-НТ5A і 5-НТ5B), 5НТ6 і 5-НТ7. Більшість даних рецепторів зв'язана з G-білками, які чинять вплив на активність або аденілатциклази, або фосфоліпази С. Людські 5-НТ6 рецептори позитивно зв'язані з аденілатциклазою. Вони розподілені по всіх лімбічній, стріарній і кортикальній областях півкуль головного мозку проявляють високу спорідненість до нейролептичних препаратів. Чекають, що модуляція рецептора 5-НТ6 відповідними речовинами поліпшить стан при деяких порушеннях, в тому числі при когнітивних дисфункціях, таких як порушення пам'яті, когнітивності і здатності до навчання, особливо пов'язаних з хворобою Альцгеймера, віковим погіршенням когнітивності і помірними когнітивними порушеннями, синдромом порушення уваги/синдрому гіперактивності, при особистісних порушеннях, таких як шизофренія, особливо когнітивні розлади, пов'язані з шизофренією, при афективних розладах, таких як депресія, тривожність і обсесивно-компульсивні розлади, при рухових або моторних порушеннях, таких як хвороба Паркінсона і епілепсія, при гемікранії, порушеннях сну (в тому числі порушеннях циркадіанного ритму), при порушеннях харчової поведінки, таких як анорексія і булімія, при деяких шлунково-кишкових розладах, таких як синдром подразненої кишки, при захворюваннях, пов'язаних з нейродегенерацією, таких як інсульт, травма спинного або головного мозку, і при пошкодженнях головного мозку, таких як гідроцефалія, при лікарському звиканні і ожирінні. Хінолінові сполуки, що мають спорідненість до рецептора 5-НТ6, описані у відомому рівні техніки, наприклад, в US 20070027161, WO 05026125 і WO 03080580. Сполуки, розкриті в цих документах, несуть піперазин-1-ільний радикал в 8 положенні хінолінового фрагмента. Згадується, що дані сполуки застосовують для лікування розладів, пов'язаних з 5-НТ6 рецептором. WO 05113539 описує хінолінові сполуки, які несуть N-зв'язаний гетероциклічний радикал в 8 положенні, що має спорідненість до рецептора 5-НТ6. Проміжна опублікована заявка WO 07039219 описує хінолінові сполуки формули (1), IIX IX IIX IX де В являє собою -(СH2)m- або -(CR R )-, при цьому m являє собою від 2 до 4, a R і R являють собою Η або С1-С3-алкіл, що мають спорідненість до рецептора 5-НТ6. Однак все ще існує постійна необхідність в створенні сполук, що мають високу спорідненість до рецептора 5-НТ6 і, які проявляють високу селективність до даного рецептора. Зокрема, дані сполуки повинні мати низьку спорідненість до адренергічних рецепторів, таких як 1адренергічний рецептор, гістамінових рецепторів, таких як H 1-рецептор, і дофамінергічних рецепторів, таких як D2-рецептор, для того щоб уникнути або зменшити значні побічні ефекти, пов'язані з модуляцією даних рецепторів, такі як постуральна гіпотензія, рефлекторна тахікардія, потенціювання гіпотензивного ефекту празозину, теразозину, доксазозину і лабеталолу або запаморочення, пов'язані з блокадою 1-адренергічного рецептора, додавання 1 UA 97837 C2 5 10 15 20 у вазі, седативний ефект, сонливість або потенціювання заспокійливих засобів, що діють на ЦНС, пов'язані з блокадою Н1-рецептора, або екстрапірамідальне рухове порушення, таке як дистонія, паркінсонізм, акатизія, пізня дискінезія або синдром кролика, або ендокринні ефекти, такі як збільшення рівня пролактину (галакторея, гінекомастія, менструальні зміни, статева дисфункція у чоловіків), пов'язані з блокадою D2-рецептора. Задачею даного винаходу є створення сполук, які мають високу спорідненість і селективність по відношенню до рецептора 5-НТ6, таким чином, даючи можливість лікувати порушення, пов'язані або опосередковані рецептором 5-НТ6. Сполуки також повинні мати хороший фармакологічний профіль, наприклад, хороше співвідношення вмісту в плазмі і мозку, хорошу біодоступність, хорошу метаболічну стійкість або знижене інгібування мітохондріального дихання. Суть винаходу На даний момент встановлено, що хінолінові сполуки формули (І), визначені в контексті даного документа, їх фізіологічно переносимі кислотно-адитивні солі і їх N-оксиди показують дивний і несподіваний ступінь селективного зв'язування з рецептором 5-НТ6. Отже, даний винахід стосується сполук формули (І) де R являє собою радикал формули 5 25 30 35 40 45 50 5 де А являє собою хімічний зв'язок, CHR або CH2CHR ; С1-С3 1 R являє собою водень, С1-С4-алкіл, С1-С4-галогеналкіл, С1-С4-алкокси або С1-С4галогеналкокси; 2 R являє собою водень, С1-С4-алкіл, С1-С4-галогеналкіл, С1-С4-алкокси або С1-С4галогеналкокси; 3 R являє собою водень або С1-С4-алкіл; 1 3 R і R разом можуть також являти собою лінійний С1-С4-алкілен, який може містити 1 або 2 6 радикали R ; 4 R являє собою водень, С1-С6-алкіл, С1-С6-гідроксіалкіл, С1-С6-галогеналкіл, С1-С6-алкоксіС1-С4-алкіл, С1-С6-галогеналкоксі-С1-С4-алкіл, С3-С6-циклоалкіл, С3-С6-галогенциклоалкіл, С3-С6циклоалкіл-С1-С4-алкіл, арил-С1-С4-алкіл, гетероарил-С1-С4-алкіл, С3-С6-алкеніл, С3-С6галогеналкеніл, форміл, С1-С4-алкілкарбоніл або С1-С4-алкоксикарбоніл; 5 R являє собою водень, С1-С4-алкіл, С1-С4-галогеналкіл, С1-С4-алкокси або С1-С4галогеналкокси; 1 5 R і R разом можуть також являти собою ординарний зв'язок або лінійний С 1-С4-алкілен, 7 який може містити 1 або 2 радикали R ; або 3 5 R і R разом можуть також являти собою лінійний С1-С4-алкілен, який може містити 1 або 2 8 радикали R ; 6 R являє собою С1-С4-алкіл, С1-С4-галогеналкіл, С1-С4-алкокси або С1-С4-галогеналкокси; або 5 6 R і R разом можуть також являти собою лінійний С1-С4-алкілен, який може містити 1 або 2 9 радикали R ; 7 8 9 R , R і R незалежно вибирають з групи, що складається з С 1-С4-алкілу, С1-С4галогеналкілу, С1-С4-алкокси і С1-С4-галогеналкокси; n являє собою 0, 1 або 2; m являє собою 0, 1, 2 або 3; a b R , R незалежно вибирають з групи, що складається з галогену, CN, С 1-С4-алкілу, С1-С4aa cc bb cc bb галогеналкілу, С1-С4-алкокси, С1-С4-галогеналкокси, C(O)R , C(O)NR R і NR R ; при цьому aa R являє собою водень, С1-С4-алкіл, С1-С4-галогеналкіл, С1-С4-алкокси або С1-С4cc bb галогеналкокси, a R , R незалежно вибирають з групи, що складається з водню і С1-С4-алкілу; 2 UA 97837 C2 5 10 15 20 25 30 35 40 45 50 55 60 X являє собою СН2, С(О), С, S(O) або S(O)2; який знаходиться в 3 або 4 положенні хінолінового кільця; 1 2 3 2 3 1 2 3 Ar являє собою радикал Ar , Ar -Ar або Ar -О-Ar , при цьому кожний з Ar , Ar і Ar незалежно вибирають з групи, що складається з арилу або гетероарилу, при цьому арильний або гетероарильний радикали можуть бути незаміщеними або можуть містити 1, 2, 3 замісники x R , при цьому x R являє собою галоген, CN, NO2, С1-С6-алкіл, С1-С6-галогеналкіл, С1-С6-гідроксіалкіл, С1-С6алкоксі-С1-С4-алкіл, С2-С6-алкеніл, С2-С6-галогеналкеніл, С3-С6-циклоалкіл, С3-С6галогенциклоалкіл, С3-С6-алкокси, С1-С6-гідроксіалкокси, С1-С6-алкоксі-С1-С4-алкокси, С1-С6галогеналкокси, С1-С6-алкілтіо, С1-С6-галогеналкілтіо, С1-С6-алкілсульфініл, С1-С6галогеналкілсульфініл, С1-С6-алкілсульфоніл, С1-С6-галогеналкілсульфоніл, С1-С6алкілкарбоніл, С1-С6-галогеналкілкарбоніл, С1-С6-алкілкарбоніламіно, С1-С6x1 x2 x1 x2 x1 x2 галогеналкілкарбоніламіно, карбокси, NH-C(O)-NR R , NR R , NR R -С1-С6-алкілен, Ox1 x2 x1 x2 NR R , при цьому R і R в останніх 4 із згаданих радикалів являють собою незалежно один x1 x2 від одного водень, С1-С6-алкіл, С1-С6-галогеналкіл або С1-С6-алкокси, або R і R в останніх 4 із згаданих радикалів утворюють разом з атомом азоту N-зв'язаний 5-, 6-або 7-членний, насичений гетероцикл, який є незаміщеним або містить 1, 2, 3 або 4 радикали, вибрані з С 1-С4x алкілу, С1-С4-галогеналкілу, С1-С4-гідроксіалкілу і С1-С4-алкокси і при цьому 2 радикали R , які зв'язані з сусідніми атомами вуглецю Ar, можуть утворювати насичене або ненасичене 5- або 6x членне карбоциклічне або гетероциклічне кільце, яке саме по собі може містити радикал R ; і їх фізіологічно переносимих кислотно-адитивних солей і їх N-оксидів. Сполука формули (І), в якій X являє собою S(O) 2, переважно вибирають із сполук, в яких, 1 2 5 щонайменше, один з радикалів R , R і, якщо присутній, R не є воднем і С1-С4-алкілом. Даний винахід також стосується фармацевтичної композиції, яка містить, щонайменше, одну хінолінову сполуку формули (І) і/або, щонайменше, одну фізіологічно переносиму кислотноадитивну сіль (І) і/або щонайменше, один N-оксид (І), при необхідності разом з фізіологічно прийнятними носіями і/або допоміжними речовинами. Крім того, даний винахід стосується застосування хінолінової сполуки формули (І) і/або її фізіологічно переносимих кислотно-адитивних солей і/або, щонайменше, одного N-оксиду (І) для отримання фармацевтичної композиції, необов'язково разом, щонайменше, з одним фізіологічно прийнятним носієм або допоміжною речовиною. Дані сполуки є селективними лігандами 5-НТ6 рецептора. Таким чином, дані сполуки особливо підходять для лікування порушень центральної нервової системи, захворювань пов'язаних зі звиканням, або ожиріння, оскільки дані порушення і захворювання, очевидно, реагують на вплив лігандів рецептора 5-НТ6. Отже, даний винахід також забезпечує спосіб лікування у ссавців порушень, при цьому вище згаданий спосіб включає введення пацієнту, який в цьому має потребу, ефективної кількості, щонайменше, однієї сполуки формули (І) і/або, щонайменше, однієї фізіологічно переносимої кислотно-адитивної солі (І) і/або, щонайменше, одного N-оксиду (І). Докладний опис винаходу Захворювання, які піддаються лікуванню хіноліновою сполукою формули І, включають, наприклад, порушення і захворювання центральної нервової системи, зокрема, когнітивні дисфункції, такі як порушення пам'яті, когнітивної діяльності і здатності до навчання, зокрема, пов'язані з хворобою Альцгеймера, віковий когнітивний спад і помірні когнітивні порушення, синдром дефіциту уваги/синдрому гіперактивності (СДУГ), особистісні порушення, такі як шизофренія, зокрема, когнітивні розлади, пов'язані з шизофренією, афективні розлади, такі як депресія, тривожність і обсесивно-компульсивні розлади, рухові або моторні порушення, такі як хвороба Паркінсона і епілепсія, гемікранія, порушення сну (в тому числі порушення циркадіанного ритму), порушення харчової поведінки, такі як анорексія і булімія, деякі шлунково-кишкові порушення, такі як синдром подразненої кишки, захворювання, пов'язані з нейродегенерацією, такі як інсульт, травма спинного або головного мозку, і пошкодження головного мозку, такий як гідроцефалія, лікарське звикання і ожиріння. Згідно з даним винаходом, щонайменше, одну хінолінову сполуку загальної формули (І), що має радикали, згадані спочатку, застосовують для лікування вище згаданих показів. При умові, що сполуки формули (І) даної структури можуть існувати в різних просторових конфігураціях, наприклад, якщо вони мають один або більше центрів асиметрії, полізаміщені кільця або подвійні зв'язки, або у вигляді різних таутомерів, можна також застосовувати енантіомерні суміші, зокрема, рацемати, діастереомерні суміші і таутомерні суміші, переважні, однак, відповідні по суті чисті енантіомери, діастереомери і таутомери сполук формули (І) і/або їх солі і/або їх N-оксиди. 3 UA 97837 C2 5 10 15 20 25 30 35 40 45 50 55 60 Також можна застосовувати фізіологічно переносимі солі даних сполук формули (І), особливо кислотно-адитивні солі фізіологічно переносимих кислот. Прикладами відповідних фізіологічно переносимих органічних і неорганічних кислот є соляна кислота, бромистоводнева кислота, фосфорна кислота, сірчана кислота, С1-С4-алкілсульфонові кислоти, така як метансульфонова кислота, ароматичні сульфонові кислоти, така як бензолсульфонова кислота і толуолсульфонова кислота, щавлева кислота, малеїнова кислота, фумарова кислота, молочна кислота, винна кислота, адипінова кислота і бензойна кислота. Інші кислоти, що застосовуються, описані в Fortschritte der Arzneimittelforschung [Advances in drug research], Volume 10, pages 224 ff., Birkhauser Verlag, Basel and Stuttgarr, 1966. Також можна застосовувати N-оксиди даних сполук формули (І), якщо дані сполуки містять основний атом азоту, такий як атом азоту хінолінового радикала. Органічні радикали, згадані у вище вказаних визначеннях радикалів, є - подібно до поняття галоген - загальним поняттям для позначення конкретного списку окремих членів групи. Префікс Cn-Cm вказує в кожному конкретному випадку можливе число атомів вуглецю в групі. Поняття "галоген" означає в кожному конкретному випадку фтор, бром, хлор або йод, особливо фтор, хлор або бром. Поняття "С1-С6-алкіл", що застосовується в контексті даного документа і в алкільних радикалах С1-С6-гідроксіалкілу, С1-С6-алкоксі-С1-С4-алкілу, С1-С66-алкілтіо, С1-С6алкілсульфінілу, С1-С6-алкілсульфонілу, С1-С6-алкілкарбонілу, С1-С6-алкілкарбоніламіно, С3-С6циклоалкіл-С1-С4-алкілу, арил-С1-С4-алкілу або гетероарил-С1-С4-алкілу, означає в кожному конкретному випадку лінійну або розгалужену алкільну групу, що має від 1 до 6 атомів вуглецю, переважно від 1 до 4 атомів вуглецю. Прикладами алкільної групи є метил, етил, n-пропіл, ізопропіл, н-бутил, 2-бутил, ізобутил, трет-бутил, пентил, 1-метилбутил, 2-метилбутил, 3метилбутил, 2,2-диметилпропіл, 1-етилпропіл, гексил, 1,1-диметилпропіл, 1,2-диметилпропіл, 1метилпентил, 2-метилпентил, 3-метилпентил, 4-метилпентил, 1,1-диметилбутил, 1,2диметилбутил, 1,3-диметилбутил, 2,2-диметилбутил, 2,3-диметилбутил, 3,3-диметилбутил, 1етилбутил, 2-етилбутил, 1,1,2-триметилпропіл, 1,2,2-триметилпропіл, 1-етил-1-метилпропіл і 1етил-2-метилпропіл. Поняття "С1-С6-галогеналкіл", що застосовується в контексті даного документа і в галогеналкільних радикалах С1-С6-галогеналкілтіо, С1-С6-галогеналкілсульфінілу, С1-С6галогеналкілсульфонілу, С1-С6-галогеналкілкарбонілу, С1-С6-галогеналкілкарбоніламіно, означає в кожному конкретному випадку лінійну або розгалужену алкільну групу, що має від 1 до 6 атомів вуглецю, в якій атоми водню даної групи частково або повністю заміщені атомами галогену. Переважні галогеналкільні радикали вибирають з С 1-С4-галогеналкілу, особливо переважно з С1-С2-галогеналкілу, такого як хлорметил, бромметил, дихлорметил, трихлорметил, фторметил, дифторметил, трифторметил, хлорфторметил, дихлорфторметил, хлор дифторметил, 1-хлоретил, 1-брометил, 1-фторетил, 2-фторетил, 2,2-дифторетил, 2,2,2трифторетил, 2-хлор-2-фторетил, 2-хлор-2,2-дифторетил, 2,2-дихлор-2-фторетил, 2,2,2трихлоретил, пентафторетил і тому подібні. Поняття "С1-С4-алкілен", що застосовується в контексті даного документа, означає лінійну або розгалужену бівалентну алкандіїльну групу, що має від 1 до 4 атомів вуглецю, при цьому приклади включають метилен, 1,1-етилєн (1,1-етандіїл), 1,2-етилен (1,2-етандіїл), 1,1пропандіїл, 1,2-пропандіїл, 2,2-пропандіїл, 1,3-пропандіїл, 1,1-бутандіїл, 1,2-бутандіїл, 1,3бутандіїл, 1,4-бутандіїл, 2,3-бутандіїл, 2,2-бутандіїл. Поняття "лінійний С1-С4-алкілен", що застосовується в контексті даного документа, означає лінійну бівалентну алкандіїльну групу, що має від 1 до 4 атомів вуглецю, при цьому приклади включають метилен, 1,2-етилен, 1,3пропандіїл і 1,4-бутандіїл. Поняття "С1-С6-алкокси", що застосовується в контексті даного документа і в алкоксильних радикалах С1-С6-алкоксі-С1-С4-алкілу, означає в кожному конкретному випадку лінійну або розгалужену алкоксильну групу, що має від 1 до 6 атомів вуглецю, переважно від 1 до 4 атомів вуглецю. Прикладами алкоксильної групи є метокси, етокси, н-пропокси, ізопропокси, нбутилокси, 2-бутилокси, ізобутилокси, трет-бутилокси, пентилокси, 1-метилбутилокси, 2метилбутилокси, 3-метилбутилокси, 2,2-диметилпропілокси, 1-етилпропілокси, гексилокси, 1,1диметилпропілокси, 1,2-диметилпропілокси, 1-метилпентилокси, 2-метилпентилокси, 3метилпентилокси, 4-метилпентилокси, 1,1-диметилбутилокси, 1,2-диметилбутилокси, 1,3диметилбутилокси, 2,2-диметилбутилокси, 2,3-диметилбутилокси, 3,3-диметилбутилокси, 1етилбутилокси, 2-етилбутилокси, 1,1,2-триметилпропілокси, 1,2,2-триметилпропілокси, 1-етил-1метилпропілокси і 1-етил-2-метилпропілокси. Поняття "С1-С6-галогеналкокси", що застосовується в контексті даного документа і в галогеналкоксильних радикалах С1-С6-галогеналкоксі-С1-С4-алкілу, означає в кожному 4 UA 97837 C2 5 10 15 20 25 30 35 40 45 50 55 60 конкретному випадку лінійну або розгалужену алкоксильну групу, що має від 1 до 6 атомів вуглецю, в якій атоми водню даної групи частково або повністю заміщені атомами галогену, особливо атомами фтору. Переважні галогеналкоксильні радикали включають С1-С4галогеналкокси, особливо С1-С2-фторалкокси, такий як фторметокси, дифторметокси, трифторметокси, 1-фторетокси, 2-фторетокси, 2,2-дифторетокси, 2,2,2-трифторетокси, 2-хлор2-фторетокси, 2-хлор-2,2-дифтор-етокси, 2,2-дихлор-2-фторетокси, 2,2,2-трихлоретокси, пентафторетокси і тому подібне. Поняття "С1-С6-гідроксіалкіл" являє собою лінійну або розгалужену алкільну групу, що має від 1 до 6, особливо від 1 до 4 атомів вуглецю (=С 1-С4 гідроксіалкіл), особливо від 1 до 3 атомів вуглецю (=С1-С3 гідроксіалкіл), в якій один з атомів водню заміщений на гідроксильну групу, як наприклад, в 2-гідроксіетилі або 3-гідроксипропілі. Поняття "С1-С6-алкоксі-С1-С4-алкіл" являє собою лінійну або розгалужену алкільну групу, що має від 1 до 4 атомів вуглецю, в якій один з атомів водню заміщений на С1-С6-алкоксильну групу, як наприклад, в метоксиметилі, етоксиметилі, пропоксиметилі, 1-метоксіетилі, 1етоксіетилі, 2-метоксіетилі, 2-етоксіетилі, 2-метоксипропілі, 2-етоксипропілі, 3-метоксипропілі або 3-етоксипропілі. Поняття "С1-С6-галогеналкоксі-С1-С4-алкіл" являє собою лінійну або розгалужену алкільну групу, що має від 1 до 4 атомів вуглецю, в якій один з атомів водню заміщений на С 1-С6галогеналкоксильну групу. Поняття "С3-С6-циклоалкіл", що застосовується в контексті даного документа і в циклоалкільних радикалах С3-С6-циклоалкіл-С1-С4-алкілу і С3-С6-галогенциклоалкілу, означає в кожному конкретному випадку циклоаліфатичний радикал, що має від 3 до 6 атомів вуглецю С, наприклад, циклопропіл, циклобутил, циклопентил і циклогексил. Циклоалкільний радикал може бути незаміщеним або може містити 1, 2, 3 або 4 С 1-С4-алкільних радикали, переважно один метильний радикал. Поняття "С3-С6-галогенциклоалкіл", що застосовується в контексті даного документа і в галогенциклоалкільних радикалах С3-С6-галогенциклоалкіл-С1-С4-алкілу, означає в кожному конкретному випадку циклоаліфатичний радикал, що має від 3 до 6 атомів вуглецю С, наприклад, циклопропіл, циклобутил, циклопентил і циклогексил, в якому, щонайменше, один водневий радикал, наприклад, 1, 2, 3, 4 або 5 водневі радикали заміщені на галоген, особливо на фтор. Приклади включають 1-фторциклопропіл, 2-фторциклопропіл, 2,2-дифторциклопропіл, 1-фторциклобутил, 2-фторциклобутил, 2,2-дифторциклобутил, 3-фторциклобутил, 3,3дифторциклобутил, 1, 3-дифторциклобутил і т.д. Поняття "С2-С6-алкеніл", що застосовується в контексті даного документа і в алкенільних радикалах С3-С6-галогеналкенілу і арил-С2-С4-алкенілу, означає в кожному конкретному випадку однократно ненасичений вуглеводневий радикал, що має 2, 3, 4, 5 або 6 атомів вуглецю С, наприклад, вініл, аліл (2-пропен-1-іл), 1-пропен-1-іл, 2-пропен-2-іл, металіл (2-метилпроп-2-ен-1іл), 2-бутен-1-іл, 3-бутен-1-іл, 2-пентен-1-іл, 3-пентен-1-іл, 4-пентен-1-іл, 1-метилбут-2-ен-1-іл, 2етилпроп-2-ен-і-іл і тому подібне. Поняття "арил", що застосовується в контексті даного документа, означає в кожному конкретному випадку карбоциклічний радикал, вибраний з групи, що складається з фенілу і фенілу, конденсованого з насиченим або ненасиченим 5- або 6-членним карбоциклічним кільцем, такого як нафтил, 1,2-дигідронафтил, 1,2,3,4-тетрагідронафтил, інденіл або інданіл, при умові, що в конденсованих кільцях арил зв'язаний через фенільний фрагмент конденсованих кілець. Поняття "гетероарил", що застосовується в контексті даного документа, означає в кожному конкретному випадку гетероциклічний радикал, вибраний з групи, що складається з моноциклічних 5- або 6-членних гетероароматичних радикалів, що містять як кільцеві члени 1, 2 або 3 гетероатоми, вибрані з N, О і С, і 5- або 6-членного гетероароматичного кільця, конденсованого з фенільним кільцем або з 5- або 6-членним гетероароматичним радикалом, при цьому гетероциклічне кільце містить як кільцеві члени 1, 2 або 3 гетероатоми, вибрані з Ν, Ο і S. Приклади 5- або 6-членних гетероароматичних радикалів включають піридил, тобто 2-, 3-, або 4-піридил, піримідиніл, тобто 2-, 4- або 5-піримідиніл, піразиніл, піридазиніл, тобто 3- або 4піридазиніл, тієніл, тобто 2- або 3-тієніл, фурил, тобто 2- або 3-фурил, піроліл, тобто 2- або 3піроліл, оксазоліл, тобто 2-, 3-або 5-оксазоліл, ізоксазоліл, тобто 3-, 4- або 5-ізоксазоліл, тіазоліл, тобто 2-, 3- або 5-тіазоліл, ізотіазоліл, тобто 3-, 4- або 5-ізотіазоліл, піразоліл, тобто 1-, 3-, 4- або 5-піразоліл, тобто 1-, 2-, 4- або 5-імідазоліл, оксадіазоліл, наприклад, 2- або 5[1,3,4]оксадіазоліл, 4- або 5-(1,2,3-оксадіазол)іл, 3- або 5-(1,2,4-оксадіазол)іл, 2- або 5-(1,3,4тіадіазол)іл, тіадіазоліл, наприклад, 2- або 5-(1,3,4-тіадіазол)іл, 4- або 5-(1,2,3-тіадіазол)іл, 3 5 UA 97837 C2 5 10 15 20 25 30 35 40 або 5-(1,2,4-тіадіазол)іл, триазоліл, наприклад, 1Н-, 2Н- або 3Н-1,2,3-триазол-4-іл, 2Н-триазол3-іл, 1Н-, 2Н- або 4Н-1,2,4-триазоліл і тетразоліл, тобто 1Н- або 2Н-тетразоліл. Приклади 5- або 6-членного гетероароматичного кільця, конденсованого з фенільним кільцем або з 5- або 6-членним гетероароматичним радикалом включають бензофураніл, бензотієніл, індоліл, індазоліл, бензімідазоліл, бензоксатіазоліл, бензоксадіазоліл, бензотіадіазоліл, бензоксазиніл, хінолініл, ізохінолініл, пуриніл, 1,8-нафтиридил, птеридил, піридо[3,2-d]піримідил або піридоімідазоліл і тому подібне. Дані конденсовані гетероарильні радикали можуть бути сполучені з іншою частиною молекули (точніше з X групою) через будьякий кільцевий атом 5- або 6-членного гетероароматичного кільця або через атом вуглецю конденсованого фенільного радикала. x Приклади кілець Ar, в яких 2 радикали R , які зв'язані з сусідніми атомами вуглецю в Ar, утворюють насичене або ненасичене 5- або 6-членне карбоциклічне або гетероциклічне кільце, включають 2,3-дигідробензофураніл, 2,3-дигідроіндоліл, дигідроізоіндоліл, дигідробензоксазиніл, тетрагідроізохінолініл, бензоморфолініл, хроменіл, хроманіл, 1,2дигідронафтил, 1,2,3,4-тетрагідронафтил, інденіл і інданіл. Поняття "насичене або ненасичене гетероциклічне кільце" в кожному конкретному випадку означає від 3- до 7-членний циклічний радикал, що містить, щонайменше, один гетероатом, вибраний з групи, що складається з Ν, Ο і S. Приклади подібних насичених або ненасичених від 3- до 7-членних гетероциклічних кілець включають насичені або ненасичені, ароматичні або неароматичні гетероциклічні кільця. Отже, приклади включають, крім вище згаданих 5- або 6членних гетероароматичних радикалів, азиридил, діазиридиніл, оксираніл, азетидиніл, азетиніл, ди- і тетрагідрофураніл, піролініл, піролідиніл, оксопіролідиніл, піразолініл, піразолідиніл, імідазолініл, імідазолідиніл, оксазолініл, оксазолідиніл, оксо-оксазолідиніл, ізоксазолініл, ізоксазолідиніл, піперидиніл, піперазиніл, морфолініл, тіоморфолініл, оксотіоморфолініл, діоксотіоморфолініл і тому подібне. Прикладами "N-зв'язаного 5-7-членного насиченого гетероциклу" є піролідин-1-іл, піперидин1-іл, піперазин-1-іл, морфолін-4-іл, імідазолідин-1-іл, оксазолідин-3-іл, тіазолідин-3-іл або гексагідродіазепін-1-іл, особливо піперидин-1-іл і морфолін-4-іл. Що стосується здатності сполук зв'язуватися 5-НТ6 рецептором, то перевага віддається 1 2 3 4 a b сполукам формули (І), в яких радикали Ar, А, X, n, m, R , R , R , R , R і R мають значення, наведені нижче. Зроблені нижче примітки відносно переважних аспектів даного винаходу, наприклад, відносно переважних значень радикалів сполуки (І), відносно переважних сполук (І) і відносно переважних варіантів здійснення способу або застосування відповідно до даного винаходу, посилаються в кожному конкретному випадку на них же або їх комбінації. Перший переважний варіант здійснення даного винаходу стосується сполук формули (І), в 1 3 яких R являє собою циклічну групу, тобто R і R разом є лінійним С1-С4-алкіленом, який може 6 1 5 містити 1 або 2 радикали R ; R і R разом являють собою ординарний зв'язок або лінійну С1-С47 3 5 алкілен, який може містити 1 або 2 радикали R ; або R і R разом є лінійним С1-С4-алкіленом, 8 який може містити 1 або 2 радикали R . 1 3 Більш переважними є сполуки формули (І), в яких радикали R і R разом утворюють лінійну 6 6 С1-С4-алкіленову групу, яка може містити 1 або 2 радикали R , особливо 0 або 1 радикал R . Серед даних сполук перевага віддається таким сполукам формули І, в яких радикал R 45 A B являє собою радикал формул R або R : , 50 4 6 в яких A, R і R визначені вище, * показує місце зв'язування з хінолініловим радикалом, p являє собою 0, 1, 2 або 3, a q являє собою 0 або 1. p переважно являє собою 1 або 2. В A B 5 5 формулі R і R радикал А, зокрема, являє собою метилен, 1,2-етилен або CH2-CHR . R 6 UA 97837 C2 6 5 6 переважно являє собою метил. R переважно являє собою метил або R і R разом являють 4 A B собою 1,2-етандіїл. R переважно являє собою водень. Приклади радикалів R і R включають A1 A2 A3 A4 A5 A6 A7 радикали формул R , R , R , R ,R ,R i R : 5 4 10 15 6 в яких R і R визначені вище, * показує місце зв'язування з хінолініловим радикалом, a q 6 4 являє собою 0 або 1. R переважно являє собою метил. R переважно являє собою водень. Особлива перевага віддається хіноліновим сполукам формули І, в яких радикал R являє A2 A3 A4 4 6 собою групу формул R , R або R , в яких R і R визначені вище, a q являє собою 0 або 1. В A2 A3 A4 6 A2 A3 формулах R , R і R радикал R , якщо є, переважно являє собою метил. У формулах R , R A4 4 і R радикал R переважно являє собою водень. Крім того, особлива перевага надається хіноліновим сполукам формули І, в яких радикал R A1 A2 A3 4 6 являє собою групу формул R , R або R , в яких R і R визначені вище, a q являє собою 0 A1 A2 A3 6 або 1. В формулах R , R і R радикал R , якщо є, переважно являє собою метил. У A1 A2 A3 4 формулах R , R і R радикал R переважно являє собою водень. Особливо переважний варіант здійснення даного винаходу стосується сполук формули І, в A3 якій радикал R являє собою радикал формули R : 20 4 25 30 35 6 в якій R і R визначені вище, * показує місце зв'язування з хінолініловим радикалом, a q 6 4 являє собою 0 або 1. R переважно являє собою метил. R переважно являє собою водень. 1 Другий варіант здійснення даного винаходу стосується сполук формули А, в якій радикал R являє собою водень. Серед даних сполук, перевага віддається таким сполукам формули І, в c яких радикал R являє собою радикал формули R : 2 3 4 в якій A, R , R і R визначені вище, * показує місце зв'язування з хінолініловим радикалом. У c 2 c формулі R радикал R переважно являє собою водень. У формулі R радикал А являє собою, 5 5 зокрема, ординарний зв'язок СН2 або CH2CHR , в якій R визначений вище або переважно 3 5 являє собою водень, або R і R разом являють собою СН2, 1,2-етандіїл або 1,3-пропандіїл. У c 3 c 4 формулі R R переважно являє собою водень або С1-С4-алкіл. У формулі R R переважно c C1 C2 C3 C4 являє собою водень. Приклади радикалів R включають радикали формул R , R , R і R : 7 UA 97837 C2 3 5 4 4 в яких R і R визначені вище. У даних формулах R переважно являє собою водень або С1С4-алкіл, особливо водень. 2 Третій варіант здійснення даного винаходу стосується сполук формули І, в якій радикал R 5 1 5 являє собою водень, А являє собою бівалентний радикал CH 2CHR , і в якій R і R разом 7 являють собою лінійний С1-С4-алкілен, який може містити 1 або 2 радикали R . Серед даних сполук третього варіанту здійснення перевага віддається таким сполукам формули І, в яких D радикали R являють собою радикал формули R : 10 7 15 7 7 в якій А' являє собою ординарний зв'язок, СН2, CH2CH2, CHR або CH2CHR , в якій R 7 D визначений вище, і в якій R , зокрема, являє собою водень. У формулі R радикал А', зокрема, D 3 являє собою ординарний зв'язок СН2 або СН2СН2. У формулі R R переважно являє собою D 4 водень або С1-С4-алкіл, особливо водень. У формулі R R переважно являє собою водень. D D1 D2 Приклади радикалів R включають радикали формул R і R : , 20 25 30 3 4 в яких R і R визначені вище, * показує місце зв'язування з хінолініловим радикалом. Особливо переважний варіант здійснення даного винаходу стосується сполук формули І, в якій X являє собою SO2. Ще один варіант здійснення даного винаходу стосується сполук формули І, в якій X являє собою СН2. Додатковий варіант здійснення даного винаходу стосується сполук формули І, в якій X являє собою карбонільну групу, тобто X являє собою С(=О). В одному переважному варіанті здійснення даного винаходу X знаходиться в 3 положенні хінолінілового радикала, тобто даний варіант здійснення стосується сполук наступної формули Іа: . 35 У ще одному варіанті здійснення даного винаходу X знаходиться в 4 положенні хінолінілового радикала, тобто даний варіант здійснення стосується сполук наступної формули Іb: 8 UA 97837 C2 . 5 10 15 Серед сполук Іа і Іb перевага віддається таким сполукам, в яких X являє собою SO 2. Серед сполук Іа і Іb перевага віддається таким сполукам, в яких радикал R являє собою A B A2 A3 A4 A3 радикал формули R або R , особливо радикал R , R або R , і більш переважно радикал R , 4 6 в якій q, R і R визначені вище. Серед сполук Іа і Іb перевага також віддається таким сполукам, в яких радикал R являє c C1 C2 C3 C4 3 4 собою радикал формули R , особливо радикал R , R , R або R , в якій R і R визначені вище. Серед сполук Іа і Іb перевага також віддається таким сполукам, в яких радикал R являє D D1 D2 4 собою радикал формули R , особливо радикал R або R , в якій R і R визначені вище. Серед сполук Іа і Іb, особлива перевага віддається таким сполукам Іа і Іb, в яких X являє A B A2 A3 собою SO2 і в яких R являє собою радикал формули R або R , особливо радикал R , R або A4 A3 4 6 R , і більш переважно радикал R , в якій q, R і R визначені вище. Самий переважний варіант здійснення даного винаходу стосується сполук наступної формули Іа.а: a b a 20 b a b в якій n, m, Ar, R і R визначені в контексті даного документа і в якій R визначений вище і A B C D A являє собою, наприклад, радикал формули R , R , R або R , більш переважно радикал R або B A2 A3 A4 A3 R , особливо радикал R , R або R , і найбільш переважно радикал R . Ще один переважний варіант здійснення даного винаходу стосується сполук наступної формули Іа.b: 25 30 35 в якій n, m, Ar, R і R визначені в контексті даного документа і в якій R визначений вище і A B C D A являє собою, наприклад, радикал формули R , R , R або R більш переважно радикал R або B A2 A3 A4 A3 R , особливо радикал R , R або R і найбільш переважно радикал R . Додатковий переважний варіант здійснення даного винаходу стосується сполук наступної формули Іа.с: в якій n, m, Ar, R і R визначені в контексті даного документа і в якій R визначений вище і A B C D A являє собою, наприклад, радикал формули R , R , R або R більш переважно радикал R або B A2 A3 A4 A3 R , особливо радикал R , R або R і найбільш переважно радикал R . 9 UA 97837 C2 Особливо переважний варіант здійснення даного винаходу стосується сполук наступної формули Іа.а1: 5 4 6 a b 4 4 6 a b 4 4 6 a b 4 4 6 a b 4 в якій n, m, q, Ar, R , R , R і R визначені в контексті даного документа. R , зокрема, являє собою водень. Змінна q, зокрема, являє собою 0. Ще один особливо переважний варіант здійснення даного винаходу стосується сполук наступної формули Іа.а2: 10 15 20 в якій п, m, q, Ar, R , R , R і R визначені в контексті даного документа. R , зокрема, являє собою водень. Змінна q, зокрема, являє собою 0. Додатковий особливо переважний" варіант здійснення даного винаходу стосується сполук наступної формули Іа.а3: в якій n, m, q, Ar, R , R , R і R визначені в контексті даного документа. R , зокрема, являє собою водень. Змінна q, зокрема, являє собою 0. Додатковий особливо переважний варіант здійснення даного винаходу стосується сполук наступної формули Іа.а4: 25 30 в якій n, m, q, Ar, R , R , R і R визначені в контексті даного документа. R , зокрема, являє собою водень. Змінна q, зокрема, являє собою 0. У сполуках формули І, так само як і в формулах la, Ib, Ia.a, Ia.b, Ia.c, Ia.a1, Іа.а2, Іа.а3 і Іа.а4, 1 Ar переважно являє собою радикал Ar , зокрема, радикал, вибраний з фенілу, нафтилу, тієнілу, піридилу, піримідилу, піразолілу, імідазолілу, оксазолілу, ізоксазолілу, тіазолілу, триазолілу, тіадіазолілу, хінолінілу, ізохінолінілу, тетрагідроізохінолінілу, бензофуранілу, бензотіофенілу, бензоксазинілу, бензотіазолілу, бензоксадіазолілу, бензотіадіазолілу, бензоморфолінілу або 10 UA 97837 C2 1 5 10 15 20 25 30 35 40 інданілу, в якому циклічний радикал Ar є незаміщеним або може містити 1, 2 або 3 замісники x R , які визначені в контексті даного документа. Також переважними є сполуки формули І, в якій 2 3 2 3 Ar являє собою радикал Ar -Ar , в якій Ar і Ar незалежно один від одного вибирають з групи, що складається з фенілу, тієнілу, піридилу, піримідилу, піразолілу, імідазолілу, оксазолілу, 1 2 ізоксазолілу, тіазолілу, триазолілу, тіадіазолілу, в якій Ar і Ar є незаміщеними або можуть x 2 3 містити 1, 2 або 3 замісники R , які визначені в контексті даного документа. У радикалах Ar -Ar 2 3 радикал Ar переважно вибирають з фенілу, піридилу і тієнілу, а радикал Ar переважно являє собою феніл, тієніл, піридил, піримідил, піразоліл, імідазоліл, оксазоліл, ізоксазоліл, тіазоліл, 2 3 триазоліл або тіадіазоліл, при цьому Ar і Ar є незаміщеними або можуть містити 1, 2 або 3 x замісники R , які визначені в контексті даного документа. Також переважними є сполуки 2 3 2 3 формули І, в якій Ar являє собою радикал Ar -О-Ar , в якому Ar і Ar незалежно один від одного вибирають з групи, що складається з фенілу, тієнілу, піридилу, піримідилу, піразолілу, 2 3 імідазолілу, оксазолілу, ізоксазолілу, тіазолілу, триазолілу або тіадіазолілу, в якому Ar і Ar є x незаміщеними або можуть містити 1, 2 або 3 замісники R , які визначені в контексті даного 2 3 2 документа. У радикалах Ar -Ar радикал Ar переважно вибирають з фенілу, піридилу і тієнілу, а 3 2 3 радикал Ar переважно являє собою феніл, при цьому Ar і Ar є незаміщеними або можуть x містити 1, 2 або 3 замісники R , які визначені в контексті даного документа. У сполуках формули І, так само як і в формулах la, Ib, Ia.a, Ia.b, Ia.c, Ia.a1, Іа.а2, Іа.а3 і Іа.а4, Ar більш переважно являє собою феніл, який незаміщений або може містити 1, 2 або 3 x замісники R , які визначені в контексті даного документа. x x Якщо R присутній, то R переважно вибирають з галогену, CN, С1-С4-алкілу, С1-С4x1 x2 галогеналкілу, С1-С4-алкокси, С1-С4-галогеналкокси, С3-С6-циклоалкілу і групи NR R . x Більш переважно R вибирають з галогену, С1-С4-галогеналкілу, С1-С4-галогеналкокси і групи x1 x2 x NR R . Найбільш переважно R вибирають з галогену, С1-С4-галогеналкілу або С1-С4галогеналкокси. x 2 В одному варіанті здійснення R являє собою феніл або фенокси (тобто Ar являє собою Ar 3 2 3 3 Ar або Ar -О-Ar , при цьому Ar являє собою феніл), в якому фенільний радикал у 2 вище згаданих радикалах є незаміщеним або може містити 1, 2 або 3 замісники, вибраних з галогену, CN, NO2, С1-С4-алкілу, С1-С4-галогеналкілу, С1-С4-алкокси, С1-С4-галогеналкокси. У сполуках формули І, так само як і в формулах la, Ib, Ia.a, Ia.b, Ia.c, Ia.a1, Іа.а2, Іа.а3 і Іа.а4, a m переважно являє собою 0. Якщо m відрізняється від 0, то R переважно вибирають з галогену, CN, С1-С4-алкілу, особливо метилу, ОСН3, CF3, CHF2, OCHF2 і OCF3. У сполуках формули І, так само як і в формулах la, Ib, Ia.a, Ia.a1, Іа.а2 і Іа.а3, n переважно b являє собою 0. Якщо m відрізняється від 0, то R переважно вибирають з галогену, CN, С1-С4алкілу, особливо метилу, ОСН3, CF3, CHF2, OCHF2 і OCF3. Приклади переважних сполук формули І наведені в наступних таблицях з 1 по 6. Таблиця 1 Сполуки формули І.а.а, в якій m і n являють собою 0, a R являє собою радикал формули A3 4 R , при цьому q являє собою 0, а радикали Ar і R мають значення, наведені в одному з рядів з 1 по 110 таблиці А (сполуки з Ia.a1-1 по Ia.a1-110). Таблиця А 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 феніл 2-фторфеніл 3-фторфеніл 2,3-дифторфеніл 2,4-дифторфеніл 2,5-дифторфеніл 2,6-дифторфеніл 3,4-дифторфеніл 3,5-дифторфеніл 2-хлорфеніл 3-хлорфеніл 2-толіл 3-толіл 2-ізопропілфеніл 3-ізопропілфеніл 2-дифторметилфеніл Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η 11 UA 97837 C2 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 68 69 70 71 72 3-дифторметилфеніл 2-трифторметилфеніл 3-трифторметилфеніл біфеніл-2-іл біфеніл-3-іл 2-метоксифеніл 3-метоксифеніл 2-дифторметоксифеніл 3-дифторметоксифеніл 2-трифторметоксифеніл 3-трифторметоксифеніл 2-феноксифеніл 3-феноксифеніл 4-(оксазол-5-іл)феніл 3-(піролідин-1-іл)феніл 1-нафтил 2-нафтил піридин-2-іл піридин-3-іл піридин-4-іл 2-(піролідин-1-іл)піридин-4-іл 6-морфолінілпіридин-3-іл 6-феноксипіридин-3-іл тієн-2-іл 5-мeтилтіeн-2-іл 5-(піридин-2-іл)тієн-2-іл 5-(2-метилтіазол-4-іл)тієн-2-іл 5-хлор-3-метилбензо[b]тієн-2іл 2-метилтіазол-5-іл 2,4-диметилтіазол-5-іл 4-метилтіазол-2-іл 5-метилтіазол-2-іл 3,5-диметилізоксазол-4-іл 1-метилімідазол-4-іл бензотіазол-7-іл 4-метилбензоморфолін-8-іл хінолін-8-іл ізохінолін-4-іл 2,1,3-бензоксдіазол-4-іл феніл 2-фторфеніл 3-фторфеніл 2,3-дифторфеніл 2,4-дифторфеніл 2,5-дифторфеніл 2,6-дифторфеніл 3,4-дифторфеніл 3,5-дифторфеніл 2-хлорфеніл 3-хлорфеніл 2-толіл 3-толіл 2-ізопропілфеніл 3-ізопропілфеніл 2-дифторметилфеніл 3-дифторметилфеніл Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η Η н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл 12 UA 97837 C2 73 74 75 76 77 78 79 80 81 82 83 84 85 86 87 88 89 90 91 92 93 94 95 96 97 98 99 100 101 102 103 104 105 106 107 108 109 110 5 10 15 2-трифторметилфеніл 3-трифторметилфеніл біфеніл-2-іл біфеніл-3-іл 2-метоксифеніл 3-метоксифеніл 2-дифторметоксифеніл 3-дифторметоксифеніл 2-трифторметоксифеніл 3-трифторметоксифеніл 2-феноксифеніл 3-феноксифеніл 4-(оксазол-5-іл)феніл 3-(піролідин-1-іл)феніл 1-нафтил 2-нафтил піридин-2-іл піридин-3-іл піридин-4-іл 2-(піролідин-1-іл)піридин-4-іл 6-морфолінілпіридин-3-іл 6-феноксипіридин-3-іл тієн-2-іл 5-метилтієн-2-іл 5-(піридин-2-іл)тієн-2-іл 5-(2-метилтіазол-4-іл)тієн-2-іл 5-хлор-3-метилбензо[b]тієн-2іл 2-метилтіазол-5-іл 2,4-диметилтіазол-5-іл 4-метилтіазол-2-іл 5-метилтіазол-2-іл 3,5-диметилізоксазол-4-іл 1-метилімідазол-4-іл бензотіазол-7-іл 4-метилбензоморфолін-8-іл хінолін-8-іл ізохінолін-4-іл 2,1,3-бензоксдіазол-4-іл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл н-пропіл Таблиця 2. Сполуки формули І.а.а, в якій m і n являють собою 0, a R являє собою радикал формули A3 6 R , при цьому q являє собою 1, a R являє собою метил, який знаходиться у 2 положенні 4 піперидинового кільця, а радикали Ar і R мають значення, наведені в одному з рядів з 1 по 110 таблиці А (сполуки з Іа.а1-111 по Іа.а1-220). Таблиця 3. Сполуки формули І.а.а, в якій m і n являють собою 0, a R являє собою радикал формули A3 6 R , при цьому q являє собою 1, a R являє собою метил, який знаходиться в 3 положенні 4 піперидинового кільця, а радикали Ar і R мають значення, наведені в одному з рядів з 1 по 110 таблиці А (сполуки з Іа.а1-221 по Іа.а1-330). Таблиця 4. Сполуки формули І.а.а, в якій m і n являють собою 0, a R являє собою радикал формули A2 4 R , при цьому q являє собою 0, а радикали Ar і R мають значення, наведені в одному з рядів з 1 по 110 таблиці А (сполуки з Іа.а2-1 по Іа.а2-110). Таблиця 5. Сполуки формули І.а.а, в якій m і n являють собою 0, a R являє собою радикал формули A1 4 R , при цьому q являє собою 0, а радикали Ar і R мають значення, наведені в одному з рядів з 1 по 110 таблиці А (сполуки з Іа.а3-1 по Іа.а3-110). 13 UA 97837 C2 5 10 Таблиця 6. Сполуки формули І.а.а, в якій m і n являють собою 0, a R являє собою радикал формули A4 4 R , при цьому q являє собою 0, а радикали Ar і R мають значення, наведені в одному з рядів з 1 по 110 таблиці А (сполуки з Іа.а4-1 по Іа.а4-110). Сполуки формули І відповідно до даного винаходу можна отримати, як викладено в синтетичних підходах нижче. 1. Основні синтетичні шляхи Сполуки формули І можна отримати, наприклад, виходячи з відповідних 8-галогензаміщених хінолінових сполук формули II і амінів III за допомогою реакції крос-поєднання, каталізованої перехідним металом, як зображено на схемі 1: Схема 1: 15 20 25 30 35 40 45 50 1 2 3 a b У схемі 1 радикали R , R , R , A, R , R , X, Ar, m і п визначені в контексті даного документа. 4 R має одне із значень, наведених для R , що відрізняється від водню або відповідної Nзахисної групи, наприклад, Вос, a Hal і Наl' являють собою Br або І. Згідно зі схемою 1 галогеновану сполуку III перетворюють в цинкорганічну сполуку IIIa у відповідності зі стандартними способами, наприклад, за допомогою способу, описаного в Tetrahedron 1987, 43, 2203-2212; J. Org. Chem. 1988, 53, 2390-2392. Далі цинкорганічна сполука вступає в реакцію крос-поєднання Негіші, що каталізується Pd(0), з відповідною 8-галогенхіноліновою сполукою II і дає в результаті 8-заміщену сполуку I' аналогічно зі способом, описаним в Synlett 1998, 4, 379380; J. Am. Chem. Soc. 2003, 125, 12527-12530. Як альтернатива проміжну цинкорганічну сполуку IIIa, що утворилася, можна трансметалізувати, наприклад, при допомозі CuCN*2LiCl, а потім піддати реакції з 8-галогенхіноліновою сполукою формули II. 4' 4 Якщо R являє собою відповідну N-захисну групу, то сполуки формули І, в якій R являє 4' собою водень, можна отримати із сполук формули I' за допомогою розщеплення N-RR -зв'язку. 4' У випадку якщо R являє собою Вос, розщеплення можна добитися обробкою трифтороцтовою кислотою. 4' 4 Якщо в отриманій хіноліновій сполуці I' радикал R не є цільовим радикалом R , а лише його попередником, то сполуку можна модифікувати, як викладено нижче, для того щоб отримати 4 цільовий замісник R . Попередник являє собою радикал, який можна легко видалити або 4 4 замістити на цільову групу R або який можна модифікувати, для того щоб отримати R . Попередник може також являти собою N-захисну групу (ЗГ), таку як бутилоксикарбоніл (Вос), бензилоксикарбоніл (Cbz), 9-флуоренілметоксикарбоніл (Fmoc), трифенілметил (Trt), нітробензолсульфеніл (Nps), аліл або бензил. 4' Якщо R являє собою аліл, то алільну групу можна розщепити з отриманням сполуки 4 формули І, в якій R являє собою водень. Розщеплення алільної групи домагаються, наприклад, 4' за допомогою реакції сполуки I' з R =аліл і агента, що захоплює алільну групу, такого як меркаптобензойна кислота або 1,3-диметилбарбітурова кислота, в присутності каталітичних кількостей сполук паладію (0) або сполук паладію, які здатні утворювати сполуки паладію (0) в реакційних умовах, наприклад, дихлорид паладію, тетракис(трифенілфосфін)паладій(0) або трис(дибензиліденацетон)дипаладій(0), переважно в комбінації з фосфіновими лігандами, наприклад, триарилфосфіни, такі як трифенілфосфін, триалкілфосфіни, такі як трибутилфосфін, і циклоалкілфосфіни, такі як трициклогексилфосфін, а особливо з фосфіновими хелатними лігандами, такими як 2,2'-біс(дифенілфосфіно)-1,1'-бінафтил або 1,4-біс(дифенілфосфіно)бутан, застосовуючи способи, відомі фахівцеві (що стосується видалення N-алілу в присутності меркаптобензойної кислоти, дивись WO 9424088; що стосується видалення N-алілу в присутності 1,3-диметилбарбітурової кислоти, дивись J. Am. Chem. Soc. 2001, 123(28), pp. 68016808 і J. Org. Chem. 2002, 67(11) pp. 3718-3723). Як альтернатива розщеплення N-алілу також 4' можна здійснити за допомогою реакції сполуки I' з R , що являє собою аліл, в присутності сполук родію, таких як трис(трифенілфосфін)хлорродій(І), аналогічно зі способами, описаними в 4' 14 UA 97837 C2 5 10 15 20 25 30 35 40 J. Chem. Soc, Perkin Transaction I: Organic and Bio-Organic Chemistry 1999 (21) pp. 3089-3104 і Tetrahedron Asymmetry 1997, 8(20), pp. 3387-3391). 4' Якщо R являє собою бензил, то цей замісник можна також розщепити з отриманням 4 сполуки І, в якій R являє собою Н. Умови реакції розщеплення відомі на даному рівні техніки. Звичайно бензильну групу видаляють за допомогою реакції гідрогенізації в присутності відповідного Pd каталізатора, такого як Pd на вуглеці або гідроксид паладію. 4' R також може являти собою захисну групу. Захисну групу можна видалити і отримати 4' сполуку І, в якій R являє собою водень. Відповідні захисні групи відомі на даному рівні техніки, і їх, наприклад, вибирають з трет-бутоксикарбонілу (Вос), бензилоксикарбонілу (Cbz), 9флуоренілметоксикарбонілу (Fmoc), трифенілметилу (Trt) і нітробензолсульфеніл (Nps). Переважною захисною групою є Вос. Захисні групи можна видалити відомими способами, такими як обробка захищеного аміну кислотою, наприклад, галоїдоводневою кислотою, такою як НСl або НBr, мурашиною кислотою або трифтороцтовою кислотою, або гідрогенізацією, необов'язково в присутності Pd каталізатора. 4 Отримана сполука І, в якій R являє собою Н, може потім реагувати, відомим чином, по 4 4 реакції алкілування, із сполукою R -X. У даній сполуці R являє собою С1-С4-алкіл, С3-С6циклоалкіл, С1-С4-галогеналкіл, С1-С4-алкоксі-С1-С4-алкіл, арил-С1-С4-алкіл, гетероарил-С1-С4алкіл або С3-С6-циклоалкіл-С1-С4-алкіл, а X являє собою нуклеофільно відхідну групу, що заміняється, наприклад, галоген, трифторметилсульфонат, алкілсульфонат, арилсульфонат, алкілсульфат і тому подібне. Умови реакції, які необхідні для алкілування, розкриті, наприклад, в Bioorganic and Medicinal Chemistry Lett. 2002, 12(7), pp. 2443-2446, а також 2002, 12(5), pp. 1917-1919. Алкілування також можна добитися, по шляху відновного амінування, за допомогою реакції 4 сполуки І, в якій R =Н, з відповідним кетоном або альдегідом в присутності відновлювального агента, наприклад, в присутності борогідриду, такого як борогідрид натрію, ціаноборогідрид натрію або триацетоксиборогідрид натрію. Фахівець знає умови реакції, які необхідні для відновного амінування, наприклад, з Bioorganic and Medicinal Chemistry Lett. 2002, 12(5), pp. 795798 і 12(7) pp. 1269-1273. 4 У випадку якщо R являє собою водень, сполуку І можна також піддавати реакції з 4 ацилгалогенідом, для того щоб отримати сполуку формули І, в якій R являє собою форміл або С1-С4-алкілкарбоніл. Карбонільну групу в даних сполуках можна відновити при допомозі 4 диборану, для того щоб отримати сполуку загальної формули І, в яких R являє собою С2-С5алкіл. Карбонільна група також може зазнавати реакції з фторуючим агентом з отриманням 4 сполуки І, в якій R являє собою 1,1-дифторалкіл. Ацилювання і відновлення можна здійснити за допомогою стандартних способів, які обговорюються в Jerry March, Advanced Organic Chemistry, 3rd ed J. Wiley & Sonc, New York 1985, p.370 і 373 (ацилювання) і p. 1099 f. і в літературі, що цитується в даній публікації (що стосується ацилювання, дивись також Synth. Commun. 1986, 16, p. 267, а що стосується відновлення, дивись також J. Heterocycl. Chem. 1979, 16, p. 1525). A B Сполуки формули І, в якій радикал R являє собою радикал формули R або R , при цьому 4 R являє собою водень, можна отримати, наприклад, виходячи з відповідних 8галогензаміщених хінолінових сполук формули II за допомогою реакції крос-поєднання, що каталізується перехідним металом, з бороновою сполукою IIIa і подальшої гідрогенізації і видалення захисної групи, як зображено на схемі 2: 15 UA 97837 C2 Схема 2: 5 10 15 6 a b У схемі 2 радикали R , A, p, q, R , R , X, Ar, m і n визначені в контексті даного документа. ЗГ являє собою відповідну N-захисну групу, наприклад, ВОС, а Hal і Hal' являють собою Br або І. 8хінолінову сполуку II піддають реакції з бороновою кислотою IIIb в умовах реакції поєднання Сузукі в присутності паладієвого каталізатора, для того, щоб отримати проміжну сполуку IV. Потім сполуку IV можна відновити в умовах каталітичної гідрогенізації, для того, щоб отримати сполуку V. Якщо гідрогенізацію проводять в хіральних умовах, наприклад, за допомогою застосування хіральних каталізаторів, то можна отримати енантіомерно чисті фенілпіролідинові сполуки. Каталізатори хіральної гідрогенізації добре відомі на даному рівні техніки і описані, наприклад, в Jerry March, Advanced Organic Chemistry, John Wiley, 3rd edition. В залежності від 4 вибору захисної групи ЗГ, можна отримати вільну аміносполуку І (R =H) за допомогою подальшого зняття захисної групи (наприклад, TFA для ВОС). A2 Сполуки формули І, в якій радикал R являють собою радикал формули R , можна отримати у відповідності зі способом, зображеним на схемі 3: Схема 3: 20 6 25 a b У схемі 3 радикали R , q, R , R , X, Ar, m і п визначені в контексті даного документа. Ζ являє 3 4a 4 собою радикал SnR , при цьому R являє собою С1-С4-алкіл. R має одне із значень R , що відрізняється від Н, або являє собою відщеплювану групу, наприклад, бензил, а Hal' являє собою Br або І. Ключовою стадією є [3+2] диполярне циклоприєднання нестабілізованого азометинового іліду до 8-алкенілхінолінового похідного VI з виходом сполуки V. Даний спосіб, загалом, описаний в J. Org. Chem 1987, 52, 235. Попередник іліду, амін VII, є комерційно доступним або його можна синтезувати з NH2(PG), (СН3)зSіСН2Сl і НСНО в присутності метанолу. 16 UA 97837 C2 5 10 15 20 8-Алкенілхінолінову сполуку (VI) можна синтезувати, наприклад, за допомогою поєднання Стілле 8-галогенохіноліну II, наприклад, йодо, з відповідним алкенілтрибутилстаннатом, таким як вініл або ізобутенілтрибутилстаннат, в присутності відповідного Pd каталізатора реакції поєднання, наприклад, тетракистрифенілфосфінпаладію(0) (дивись, наприклад, Tetrahedron, 2003, 59(34), 6545 і Bioorg. Med. Chem. 1999, 7(5), 665). Вибравши цільовий ізомер Стілле (наприклад, цис- або транс-ізобутенілтрибутилстаннат), можна селективно отримати відповідний цис- або транс-алкілфенілпіролідин. Як альтернатива, 8-алкенілароматичну сполуку (VI) можна отримати за допомогою реакції Віттіга відповідного 8-формілхінолінового похідного з реагентом Віттіга, таким як PPh3=CHR (R являє собою Η або С1-С3-алкіл). Умови для реакції Віттіга добре відомі на даному рівні техніки і обговорюються, наприклад, в Jerry March, Advanced Organic Chemistry, John Wiley, 3rd edition, page 845 ff. 4a 4 Група R попередника аміну VII переважно відповідає або цільовій групі R кінцевої сполуки І, або являє собою, як альтернатива, групу, що розщеплюється, таку як бензил, яку можна A2 видалити за допомогою каталітичної гідрогенізації, для того, щоб отримати сполуку І з R=R і 4 R =H. A2 Сполуку формули І, в якій радикал R являє собою радикал формули R , можна також отримати у відповідності зі способом, зображеним на схемі 4: Схема 4: a 25 30 35 χ b У схемі 4 радикали R , R , X, Ar, m і n визначені в контексті даного документа. Ζ являє 3 4a собою водень, С1-С4-алкіл або SiR , при цьому R являє собою С1-С4-алкіл. R має одне із 4 значень R , що відрізняється від Η або являє собою групу, що розщеплюється, наприклад, бензил, а Hal' являє собою Br або І. Ключовою стадією є [3+2] диполярне циклоприєднання нестабілізованого азометинового іліду до 8-алкінілхінолінового похідного VIII з виходом сполуки IVa (дивись, наприклад, Tetrahedron 1996, 52, 59). Потім IVa гідрогенізують до відповідної A2 x піролідинової сполуки І (R=R ). Радикал Z необов'язково видаляють. Якщо гідрогенізацію проводять в хіральних умовах, наприклад, за допомогою застосування хіральних каталізаторів, то можна отримати енантіомерно чисті фенілпіролідинові сполуки. Хіральні каталізатори гідрогенізації добре відомі на даному рівні техніки, і описані, наприклад, в Jerry March, Advanced Organic Chemistry, John Wiley, 3rd edition. Сполуки формули І, в якій радикал R являє собою радикал формули RC 2, можна отримати виходячи із сполуки VI у відповідності зі способом, зображеним на схемі 5: Схема 5: 17 UA 97837 C2 6 5 a b 4b У схемі 5 радикали R , q, R , R , X, Ar, m і n визначені в контексті даного документа. R має 4 одне із значень R , що відрізняється від Η або являє собою Ν-захисну групу, наприклад, бензил або Воc. У відповідності зі схемою 5 8-алкенілхінолінову сполуку VI обробляють відповідним 3 4b аміном HNR R в присутності сильної основи, такої як н-бутиллітій (BuLi) або гідрид натрію в апротонному полярному розчиннику, такому як тетрагідрофуран (ТГФ) або Ν,Νдиметилформамід (ДМФА) з отриманням після обробки цільового продукту І реакції Міхаеля. C1 Сполуки формули І, в якій радикал R являє собою радикал формули R , можна отримати виходячи із сполуки II у відповідності зі способом, зображеним на схемі 6: 10 Схема 6: 3 20 a a 15 4 b b У схемі 6 радикали R , R , R , R , X, Ar, m і n визначені в контексті даного документа. Hal' являє собою бром або йод. У відповідності зі схемою 6 8-галоген-хінолінову сполуку II піддають реакції з ДМФА і відповідною основою, такою як BuLi або NaH в апротонному розчиннику, такому як ТГФ або ДМФА, для того, щоб отримати формільну сполуку IX. Потім сполуку IX 3 4 піддають відновному амінуванню аміном HNR R , для того щоб отримати цільову амінометилхінолінову сполуку. Відновне амінування звичайно проводять в присутності відповідної основи (наприклад, Na2CO3), а відновлення можна здійснити за допомогою різноманіття способів хімічного відновлення або каталітичної гідрогенізації, відомого фахівцям в даній галузі техніки. Сполуки формули І, в якій X являє собою СН2, можна також отримати, виходячи з 3- або 4галогенхінолінових сполук формули X, як зображено на схемі 7: 25 Схема 7: 30 35 40 У схемі 7 радикали R, R , R , Ar, m і n визначені в контексті даного документа. Hal і Hal' являють собою бром або йод. R' являє собою алкіл. Μ являє собою літій або Mg-Hal. У відповідності зі схемою 7, 3- або 4-галогенхінолінову сполуку X обробляють алкіл метальною сполукою M-R, такою як BuLi або MeMgBr в апротонному ефірному розчиннику, такому як діетиловий ефір, метил-трет-бутиловий ефір, ТГФ або діоксан, для того щоб отримати проміжну метальовану сполуку XI. Потім сполуку XI піддають алкілуванню відповідним арилметилгалогенідом ArСН2Наl, для отримання цільового 3- або 4-заміщеного хіноліну. Дану реакційну послідовність можна також завершити раніше в синтетичному підході перед введенням 8-алкіламінозамісника. Сполуку X можна отримати за допомогою перестановки хімічних перетворень, викладених на схемах з 1 по 6 у відповідності з добре відомим фахівцеві в даній галузі техніки способом. Сполуки формули І, в якій X являє собою С(=О), можна також отримати, виходячи з 3- або 4галогенхінолінових сполук формули X, як зображено на схемі 8: 18 UA 97837 C2 Схема 8: a 5 10 15 b У схемі 8, радикали R, R , R , Ar, m і п визначені в контексті даного документа. Hal' являє собою бром або йод. R' являє собою алкіл. Μ являє собою літій або Mg-Hal. L являє собою відповідну відхідну групу, наприклад, галоген (ароїлгалогенід), О-алкіл (ароїлефір) або амідний залишок Вайнреба. У відповідності зі схемою 8 3- або 4-галогенхінолінову сполуку X обробляють алкіл метальною сполукою M-R, такою як BuLi або MeMgBr в апротонному ефірному розчиннику, такому як діетиловий ефір, метил-трет-бутиловий ефір, ТГФ або діоксан, для того щоб отримати проміжну метальовану сполуку XI. Потім сполуку XI піддають ацилюванню відповідною ароїльною сполукою Ar-C(=O)-L, для того щоб отримати цільовий 3або 4-заміщений хінолін. Дану реакційну послідовність можна також завершити раніше в синтетичному підході перед введенням 8-алкіламінозамісника. 8-галогенхінолінові сполуки формули II є комерційно доступними або їх можна отримати відповідно до загальноприйнятих способів органічного синтезу, які добре відомі фахівцеві в даній галузі техніки. Сполуки формули II, в якій X являє собою S(O) 2, можна отримати, наприклад, виходячи з 8-нітрохінолінових сполук формули XII, як зображено на схемі 9. Схема 9: 20 25 30 35 Комерційно доступні нітрохіноліни, такі як XII, можна перетворити в 3-йодопохідні XIII за допомогою обробки йодуючим реагентом, таким як N-йодосукцинімід в розчиннику, такому як оцтова кислота з отриманням 3- або 4-йодохінолінової сполуки XIII. 3- і 4-ізомери можна розділити на цій же стадії або на подальшій стадії. Потім сполуку XIII піддають реакції з сіллю лужного металу сульфінової кислоти Ar-S(O)OH, наприклад, натрієвою сіллю Ar-S(O)2Na, в присутності солі міді (І), такої як Сu(І) трифлат в полярному розчиннику, такому як Ν,Νдиметилацетамід (ДМА) або ДМФА. Відновлення нітрогрупи XIV дає аміносполуку XV. Відновлення можна здійснити за допомогою різноманіття способів, включаючи відновлення "неводневим" відновлювальним агентом, таким як SnCl2, або за допомогою способів каталітичної гідрогенізації, відомих фахівцям в даній галузі техніки. Потім аміногрупу XV перетворюють в йодогрупу за допомогою реакції Зандмейєра, застосовуючи джерело нітрозонію (наприклад, NaNO2, n-BuNO2) і йодид (наприклад, Cul або h-Bu4NI) у відповідному розчиннику, такому як вода або CH3CN. Сполуки формули IIIb, 19 UA 97837 C2 особливо сполуки формули IIIb, в яких p являє собою 0, а А являє собою СН 2, можна отримати по реакційній послідовності, зображеній на схемі 10. Схема 10: 5 10 15 20 25 30 35 40 45 50 Виходячи з бензгідрильної сполуки XVI, наприклад, 1-бензгідрил-азетидин-3-ольної сполуки, проводять Pd-каталізоване зняття захисної групи з отриманням вільного аміну (Tetrahedron 2002, 58, 9865-9870). Потім вводять захисну групу ЗГ (наприклад, утворення карбамату, якщо ЗГ являє собою ВОС) з отриманням сполуки XVII. Подальше галогенування дає йодовану сполуку ІIIb, яка легко зазнає впровадження Zn (Tetrahedron 1987, 43, 2203-2212; J. Org. Chem. 1988, 53, 2390-2392). Таким чином, цинкорганічну сполуку, що отримується, можна застосовувати в синтетичних підходах, як викладено вище в схемі 1. Синтез азетидин-3-ольних сполук описаний, наприклад, в J. Med. Chem. 1994, 37, 4195-4210 або Helvetica Chimica Acta 1995, 78, 1238-1246. Якщо не вказано інше, вище описані реакції звичайно проводять в розчиннику при температурах між кімнатною температурою і температурою кипіння розчинника, що застосовується. Як альтернатива, активаційну енергію, яка необхідна для реакції, можна підводити в реакційну суміш, застосовуючи мікрохвилі, що виявилося вельми важливим, особливо у разі реакцій, що каталізуються перехідними металами (що стосується реакцій із застосуванням мікрохвиль, дивись Tetrahedron 2001, 57, p. 9199 ff. p. 9225 ff., а також звичайним способом, "Microwaves in Organic Synthesis", Andre Loupy (Ed.), Wiley-VCH 2002. Кислотно-адитивні солі сполук І отримують звичайним способом за допомогою змішування вільної основи з відповідною кислотою, якщо необхідно в розчині в органічному розчиннику, наприклад, в ацетонітрилі, нижчому спирті, такому як метанол, етанол або пропанол, ефірі, такому як діетиловий ефір, метил-трет-бутиловий ефір або діізопропіловий ефір, кетон, такому як ацетон або метилетил кетон, складному ефірі, такому як етилацетат, в їх сумішах, а також в їх сумішах з водою. Сполука даного винаходу може бути агоністом 5-НТ6 рецептора, включаючи часткову агоністичну активність, або антагоністом 5-НТ6 рецептора, включаючи активність зворотного агоніста. Сполуки формули І відповідно до даного винаходу мають дивно високу спорідненість до 5НТ6 рецепторів. Висока спорідненість сполук відповідно до даного винаходу до 5-НТ6 рецепторів відбивається в дуже низьких константах зв'язування з рецептором in-vitro (Ki(5-HT6) значення), як правило, менше за 50 пМ (нмоль/л), переважно менше за 10 пМ і особливо менше за 5 пМ. Заміщення 3Н-ЛСД можна застосовувати, наприклад, в дослідженнях рецепторного зв'язування для визначення зв'язувальної спорідненості до 5-НТ6 рецепторів. Більш того, сполуки формули І є високо селективними лігандами рецептора 5-НТ6, які, завдяки своїй низькій спорідненості до інших рецепторів, таких як дофамінові рецептори, адренергічні рецептори, мускаринові рецептори, гістамінові рецептори, опіатні рецептори, особливо дофаміновий D2, 1-адренергічний і гістаміновий Н1 рецептори, приводять до менших побічних ефектів, ніж інші, менш селективні 5-НТ6 ліганди. Наприклад, 5-НТ6/D2, 5-НТ6/1-адренергічний або 5-НТ6/Н1 селективності сполук відповідно до даного винаходу, тобто співвідношення констант зв'язування з рецепторами K i(D2)/Ki(5-HT6), Ki(1-адренергічний)/Ki(5-НТ6) або Ki(H1)/Ki(5-НТ6), складають, як правило, щонайменше, 25, переважно, щонайменше, 50, а краще, щонайменше, 100. 3 125 Заміщення [ H]SCH23390 або [ І]спіперон можна застосовувати, наприклад, для проведення досліджень рецепторного зв'язування на D1, D2 і D4 рецепторах. Більш того, сполуки формули І, завдяки своїм структурним особливостям, схильні проявляти підвищену мозкову проникність в порівнянні з іншими відомими лігандами 5-НТ6 рецептора. Завдяки їх профілю зв'язування, дані сполуки можна застосовувати для лікування захворювань, які реагують на вплив лігандів рецептора 5-НТ6 (або які піддаються лікуванню лігандом рецептора 5-НТ6), тобто вони є ефективними в лікуванні таких медичних порушень або захворювань, в яких здійснення впливу на (модулювання) рецептори 5-НТ6 приводить до 20 UA 97837 C2 5 10 15 20 25 30 35 40 45 50 55 60 поліпшення клінічної картини або до того, що захворювання виліковується. Прикладами таких захворювань є порушення або захворювання центральної нервової системи. Під порушеннями або захворюваннями центральної нервової системи розуміються значні порушення, які уражають спинний мозок і особливо головний мозок. По визначенню даного винаходу поняття "порушення" означає патологічні відхилення і/або аномалії, які, як, як правило, вважається, є патологічними станами або функціями і які можуть виявлятися у вигляді особливих ознак, симптомів і/або дисфункцій. Лікування відповідно до даного винаходу можна направити не тільки на окремі порушення, тобто аномалії або патологічні стани, але також можна і на декілька аномалій, які можуть бути причинно пов'язані одна з одною, будучи об'єднані в картинах хвороби, тобто синдроми, які можна лікувати відповідно до даного винаходу. Порушення, які можна лікувати відповідно до даного винаходу являють собою, зокрема, порушення, які реагують на модуляцію рецептора 5-НТ6. Вони включають когнітивні дисфункції, такі як порушення пам'яті, когнітивності і здатності до навчання, особливо пов'язаних з хворобою Альцгеймера, віковим когнітивним спадом і помірними когнітивними порушеннями, синдром дефіциту уваги/синдрому гіперактивності (СДУГ), особистісні порушення, такі як шизофренія, зокрема, когнітивні розлади, пов'язані з шизофренією, афективні розлади, такі як депресія, тривожність і обсесивно-компульсивні розлади, рухові або моторні порушення, такі як хвороба Паркінсона і епілепсія, гемікранія, порушення сну (в тому числі порушення циркадіанного ритму), порушення харчової поведінки, такі як анорексія і булімія, деякі шлунково-кишкові порушення, такі як синдром подразненої кишки, захворювання, пов'язані з нейродегенерацією, такі як інсульт, травма спинного або головного мозку, і пошкодження головного мозку, таке як гідроцефалія, лікарське звикання і ожиріння. Захворювання, пов'язані із звиканням, включають психічні розлади і поведінкові порушення, які викликаються зловживанням психотропними речовинами, такими як лікарські препарати або наркотичні речовини, а також інші захворювання, пов'язані із звиканням, такі як пристрасть до азартної гри (розлади контролю над спонуками ще не класифіковані). Прикладами речовин, що спричиняють звикання, є: опіоїди (наприклад, морфін, героїн і кодеїн), кокаїн; нікотин; алкоголь; речовини, які взаємодіють з ГАМК хлоридіонним канальним комплексом, седативні засоби, снотворні засоби і транквілізатори, наприклад, бензодіазепіни; ЛСД; каннабіноїди; психомоторні стимулятори, такі як 3,4-метилендіокси-N-метиламфетамін (екстазі); амфетамін і амфетаміноподібні речовини, такі як метилфенідат і інші стимулятори, в тому числі кофеїн. Речовинами, що спричиняють звикання, яким приділяють особливу увагу, є опіоїди, кокаїн, амфетамін або амфетаміноподібні речовини, нікотин і алкоголь. Що стосується лікування захворювань, пов'язаних із звиканням, особлива перевага віддається таким сполукам відповідно до даного винаходу формули І, які самі по собі не мають ніякого психотропного ефекту. Можна також спостерігати, що у щурів, що застосовуються для досліджень, які після введення їм сполук, які можна застосовувати відповідно до даного винаходу, знижується їх самовведення психотропних речовин, наприклад, кокаїну. Відповідно до ще одного аспекту даного винаходу, сполуки згідно з даним винаходом підходять для лікування порушень, причини яких можна, щонайменше, частково пояснити аномальною активністю рецепторів 5-НТ6. Відповідно до ще одного аспекту даного винаходу, лікування направляють особливо на такі порушення, на які можна вплинути, шляхом належного медичного лікування, зв'язуванням переважно екзогенно зв'язувальних партнерів (лігандів), що вводяться з рецепторами 5-НТ6. Захворювання, які можна лікувати сполукою згідно з даним винаходом, часто характеризуються прогресивним розвитком, тобто зміною вище описаних патологічних станів протягом часу; як правило, тяжкість захворювання посилюється, і патологічні стани можуть об'єднуватися один з одним і на додаток до патологічних станів, що вже є, можуть з'явитися нові. Сполуки формули І можна застосовувати для лікування великої кількості ознак, симптомів і/або дисфункцій, які пов'язані з порушеннями центральної нервової системи, а особливо вище описаних патологічних станів. Дані ознаки, симптоми і/або дисфункції включають, наприклад, порушений зв'язок з реальністю, відсутність адекватної самооцінки і здатності відповідати загальноприйнятим соціальним нормам або життєвим вимогам, зміни темпераменту, зміни індивідуальних потреб, таких як голод, сон, спрага, і т.д., і настрої, порушення здатності спостерігати і комбінувати, зміни особистості, особливо емоційна нестійкість, галюцинації, порушення его, безумство, амбівалентність, аутизм, деперсоналізація і помилкове сприйняття, маревні ідеї, співуча мова, відсутність синкінезії, хода короткими кроками, зігнене положення торса і кінцівок, тремор, відсутність міміки, монотонна мова, депресії, апатія, утруднена 21 UA 97837 C2 5 10 15 20 25 30 35 40 45 50 55 60 спонтанність і рішучість, знижена здатність об'єднання з іншими людьми, тривожність, нервове збудження, заїкання, соціофобія, панічні хвилювання, симптоми відміни в зв'язку із залежністю, маніформні синдроми, стани збудження і потьмарення свідомості, дисфорія, дискінетичні синдроми і тикові розлади, наприклад, хорея Гентінгтона і синдром Жіля де ла Туретта, синдроми вертиго, наприклад, периферичний позиційний, ротаційний і коливний вертиго, меланхолія, істерія, іпохондрія і тому подібне. За визначенням даного винаходу лікування також включає профілактичне лікування (профілактику), особливо у вигляді профілактики, що повторюється, або фазової профілактики, а також лікування гострих або хронічних ознак, симптомів і/або дисфункцій. Лікування може бути орієнтоване симптоматично, наприклад, у вигляді пригнічення симптомів. Воно може діяти протягом короткого періоду, бути направленим на дію протягом середнього терміну або може бути довгодіючим лікуванням, наприклад, в рамках підтримуючої терапії. Сполуки згідно з даним винаходом переважно підходять для лікування захворювань центральної нервової системи, більш переважно для лікування когнітивних дисфункцій, а особливо для лікування когнітивних дисфункцій, пов'язаних з шизофренією або з хворобою Альцгеймера. Відповідно до ще одного аспекту даного винаходу сполуки формули (І) особливо підходять для лікування захворювань, пов'язаних із звиканням, викликані, наприклад зловживанням психотропними речовинами, такими як лікарські препарати, наркотичні речовини, нікотин або алкоголь, в тому числі психічних розладів і поведінкових порушень, пов'язаних з цим. Відповідно до ще одного аспекту даного винаходу сполуки формули (І) особливо підходять для лікування порушень харчування, таких як ожиріння, а також пов'язаних з цим захворювань, таких як серцево-судинні захворювання, порушення травлення, респіраторні захворювання, рак або діабет 2-го типу. Застосування відповідно до даного винаходу описаних сполук в рамках лікування має на увазі спосіб. У даному способі ефективна кількість однієї або більше сполук, як правило, сформульованих відповідно до фармацевтичної і ветеринарної практики, вводять індивіду, якого необхідно лікувати, переважно ссавцеві, особливо людській істоті, продуктивній тварині або домашній тварині. Чи потрібне подібне лікування, і в якій формі воно повинно протікати, залежить від конкретного випадку і підлягає медичній оцінці (діагностиці), яка бере до уваги ознаки, симптоми і/або дисфункції, які спостерігаються, небезпеку розвитку окремих ознак, симптомів і/або дисфункції і інших чинників. Як правило, лікування здійснюється за допомогою однократного або щоденного введення, що повторюється, при необхідності разом, або навперемінно з іншими активними сполуками або препаратами, що містять активну сполуку, при якому добова доза переважно від близько 0,1 до 1000 мг/кг маси тіла, у разі перорального введення, або від близько 0,1 до 100 мг/кг маси тіла, у разі парентерального введення, дається індивіду, який потребує лікування. Даний винахід також стосується отримання фармацевтичних композицій для лікування індивіда, переважно ссавця, особливо людської істоти, продуктивної тварини або домашньої тварини. Таким чином, сполуку формули І звичайно вводять у вигляді фармацевтичних композицій, які містять фармацевтично прийнятний носій разом, щонайменше, з однією сполукою відповідно до даного винаходу і, при необхідності, іншими активними сполуками. Дані композиції можна, наприклад, вводити перорально, ректально, трансдермально, підшкірно, внутрішньовенно, внутрішньом'язово або інтраназально. Прикладами відповідних фармацевтичних складів є тверді лікарські форми, такі як порошки, гранули, таблетки, особливо таблетки, покриті оболонкою, пастилки, пакетики, крохмальні капсули, таблетки з цукровим покриттям, капсули, такі як тверді желатинові капсули і м'які желатинові капсули, супозиторії або вагінальні лікарські форми, напівтверді лікарські форми, такі як мазі, креми, гідрогелі, пасти або пластири, а також рідкі медичні форми, такі як розчини, емульсії, особливо емульсії масло у воді, суспензії, наприклад, лосьйони, ін'єкційні препарати і інфузійні препарати, і очні краплі і вушні краплі. Для введення інгібіторів відповідно до даного винаходу можна також застосовувати імплантовані пристрої для вивільнення. Крім того, також можна застосовувати ліпосоми або мікросфери. При отриманні композицій сполуку відповідно до даного винаходу необов'язково змішують або розбавляють одним або більше наповнювачами. Наповнювачі можуть бути твердими, напівтвердими або рідкими речовинами, які служать як наповнювачі, носії або середовища для активної сполуки. Відповідні наповнювачі перераховані в спеціальних медичних фармакопейних статтях. Крім того, склади можуть містити фармацевтично прийнятні носії або звичайні допоміжні речовини, такі як гліданти; змочувальні реагенти; емульгуючі і суспендуючі реагенти; консерванти; 22 UA 97837 C2 5 10 15 20 25 30 35 40 45 50 55 антиоксиданти; антиіританти; хелатуючі агенти; допоміжні речовини покриття; стабілізатори емульсії; плівкоутворювачі; гелеутворювачі; речовини, що коригують запах лікарського засобу; коригенти смаку; смола; гідроколоїди; розчинники; солюбілізатори; нейтралізуючі компоненти; прискорювачі дифузії; пігменти; четвертинні амонієві сполуки; пережирювальні добавки; сировина для мазей, кремів або масел; силіконові похідні; розширювальні допоміжні речовини; стабілізатори; стерилізуючі засоби; основи для супозиторіїв; допоміжні засоби для формування таблеток, такі як зв'язувальні речовини, наповнювачі, гліданти, розрихлювачі або покриття; пропеленти; осушувальні реагенти; замутнювачі; загусники; віск; пом'якшувачі і світлі мінеральні масла. У зв'язку з цим склад засновується на спеціальних даних, описаних, наприклад, в Fiedler, Η. P., Lexikon der Hilfsstoffe fur Pharmazie, Kosmetik und angrenzende Gebiete [Encyclopedia of auxiliary substances for pharmacy, cosmetics and related fields], 4th edition, Aulendorf: ECV-EditioKantor-Verlag, 1996. Наступні приклади служать, для того, щоб пояснити даний винахід, не обмежуючи його об'єму. 1 Сполуки були охарактеризовані або Н-ЯМР в d6-димeтилcyльфoкcидi або d-хлороформі на 400 МГц або 500 МГц ЯМР приладі (Bruker AVANCE), або мас-спектрометричним аналізом, що звичайно реєструється за допомогою ВЕРХ-МС при швидкому градієнті на матеріалі С18 (електроспрей-іонізаційний (ESI) тип), або визначенням температури плавлення. Спектральні властивості ядерного магнітного резонансу (ЯМР) співвідносяться з хімічними 1 зсувами (), вираженими в мільйонних частках (м.ч.). Відносна область зсувів в Н-ЯМР спектрі відповідає ряду атомів водню для конкретного радикала в молекулі. Природа зсуву, відносно мультиплетності, проявляється у вигляді синглету (с), уширеного синглету (уш.с), дублету (д), уширеного дублету (уш.д), триплету (т), уширеного триплету (уш.т), квартету (кв.), квінтету (квінт.) і мультиплету (м). Приклади отримання І. Отримання сполук Приклад 1 8-(Азетидин-3-іл)-3-(фенілсульфоніл)хінолінгідрохлорид 1.1 Трет-бутиловий ефір 3-гідроксі-азетидин-1-карбонової кислоти До дегазованого розчину 1-бензгідрил-азетидин-3-олу (4,75 г, 19,84 ммоль)в метанолі (МеОН) (150 мл) додавали форміат амонію (8,76 г, 138,91 ммоль), 10% Pd/C (450 мг) і Вос 2О (ди-трет-бутилдикарбонат) (13 г, 59,56 ммоль). Отриману суспензію нагрівали до температури дефлегмування в атмосфері N2 протягом 1 год. Потім її охолоджували до кімнатної температури, фільтрували через шар целіту і концентрували. Залишок розбавляли в СН 2Сl2 і промивали водою. Органічний шар сушили над Na2SO4, фільтрували і концентрували під вакуумом. Залишок очищали за допомогою колонкової флеш-хроматографії на силікагелі (гептан:етилацетат (EtOAc), 1:1) з отриманням цільової сполуки (3,30 г, 96 %) у вигляді білих кристалів. + 1 MS(ESI+): m/z=118,1 [M-tBu+H] ; Н-ЯМР (400 МГц, CDCl3): =1,43 (с, 9Н), 2,35 (д, J=6,2 Гц, 1Н), 3,80 (дд, J=10,4, 4,4 Гц, 2Н), 4,15 (дд, J=9,6, 6,7 Гц, 2Н), 4,58 м.ч. (м, 1Н). 1.2 Трет-бутиловий ефір 3-йодо-азетидин-1-карбонової кислоти Розчин трет-бутилового ефіру 3-гідроксі-азетидин-1-карбонової кислоти (3,35 г, 19,34 ммоль) в толуолі (200 мл) обробляли імідазолом (3,95 г, 58,01 ммоль), трифенілфосфіном (10,14 г, 38,65 ммоль) і І2 (7,36 г, 28,99 ммоль). Отриману суміш нагрівали при 100°С протягом 1 год., охолоджували до кімнатної температури, а потім вливали в насичений водний розчин NaHCO3 (30 мл). Надлишок трифенілфосфіну прибирали за допомогою додавання йоду доти, поки І2 забарвлення продовжувало зберігатися в органічному шарі. Останній промивали водним розчином Na2S2O3 (5% міцності), сушили над Na2SO4, фільтрували і концентрували під вакуумом. Отриманий залишок очищали за допомогою колонкової флеш-хроматографії на силікагелі (гептан:EtOAc, 2:1) з отриманням цільової сполуки (5,19 г, 95 %) у вигляді ясножовтого масла. + 1 MS(ESI+): m/z=227,9 [M-tBu+H] ; Н-ЯМР (400 МГц, CDCl3): =1,44 (с, 9Н), 4,29 (дд, J=10,4, 5,4 Гц, 2Н), 4,47 (м, 1Н), 4,64 м.д. (дд, J=9,5, 8,0 Гц, 2Н). 1.3 Йодид (1-(трет-бутоксикарбоніл)азетидин-3-іл)цинку(II) Zn пил (1,80 г, 27,5 ммоль) енергійно перемішували в ДМА (11 мл) в атмосфері азоту, і отриману суспензію нагрівали при 65°С. Додавали триметилсилілхлорид (0,37 г, 3,39 ммоль) і 1,2-диброметан (0,64 г, 3,39 ммоль) і продовжували перемішувати протягом 40 хв. Потім до даного розчину додавали по краплях розчин трет-бутилового ефіру 3-йодо-азетидин-1карбонової кислоти (6,00 г, 21,2 ммоль) в диметилацетаміді (ДМА, 10 мл) протягом 30 хв., а 23 UA 97837 C2 5 10 15 20 25 30 35 40 45 50 55 потім реакційну суміш охолоджували до кімнатної температури протягом 16 год. Отриманий розчин застосовували на наступній стадії без будь-якого очищення. 1.4 Трет-бутил-3-(3-(фенілсульфоніл)хінолін-8-іл)азетидин-1-карбоксилат До розчину 8-йодо-3-(фенілсульфоніл)хіноліну (200 мг, 0,51 ммоль, отриманому у відповідності з WO 2003080580) в ДМА (1 мл) додавали PdCl 2 (dppf) (8,3 мг, 0,10 ммоль; dррf=1,1'-біс(дифенілфосфіно)ферроцен) і Cul (11,6 мг, 0,06 ммоль), після чого додавали по краплях йодид (1-(трет-бутоксикарбоніл)азетидин-3-іл)цинку(ll) (317 мг, 0,91 ммоль) в ДМА (1 мл) протягом 10 хв. Потім суміш нагрівали при 80°С протягом 6 год., потім перемішували при кімнатній температурі протягом 150 год. і гасили насиченим водним розчином NaCl. Отриману реакційну суміш екстрагували трет-бутилметиловим ефіром (МТВЕ). Органічні фази сушили над Na2SO4, фільтрували і концентрували під вакуумом. Залишок очищали за допомогою флешхроматографії з отриманням цільової сполуки (54 мг, 25%) у вигляді ясно-жовтого масла. + + MS(ESI+): m/z=425,1 (M+H) , 370,1 (M-tBu+H) . 1.5 Гідрохлорид 8-(азетидин-3-іл)-3-(фенілсульфоніл)хінолін Розчин трет-бутил-3-(3-(фенілсульфоніл)хінолін-8-іл)азетидин-1-карбоксилату (54 мг, 0,13 ммоль) в СН2Сl2 (3 мл) обробляли соляною кислотою (1М в ефірі, 0,3 мл) при 0°С, а потім перемішували при кімнатній температурі протягом 16 год. Після концентрації отриманий продукт промивали ЕtOАс і сушили під вакуумом, для того щоб отримати цільову сполуку (45 мг, 98 %) у вигляді білої твердої речовини. + 1 MS(ESI+): m/z=325,1 (М+Н) ; Н-ЯМР (400 МГц, d6-ДМСО): =3,32 (м, 1Н), 3,47 (м, 1Н), 4,58 (м, 1Н), 5,38 (м, 1Н), 5,47 (м, 1Н), 7,72 (м, 2Н), 7,80 (м, 1Н), 8,16 (м, 3Н), 8,42 (м, 2Н), 8,73 (с, 3Н), 9,92 (с, 1Н), 10,38 м.ч. (с, 1Н). Приклад 2 3-(Фенілсульфоніл)-8-(піперидин-4-іл)хінолін гідрохлорид Цільову сполуку отримували способом, аналогічним описаному для прикладу отримання 1. 2.1 Трет-бутил-4-(3-(фенілсульфоніл)хінолін-8-іл)піперидин-1-карбоксилат + Вихід: 45%; MS(ESI+): m/z=453,1 (M+H)+, 397,1 (M-tBu+H) . 2.2 Гідрохлорид 3-(фенілсульфоніл)-8-(піперидин-4-іл)хінолін + 1 Вихід: 62%; MS(ESI+): m/z=353,1 (М+Н) ; Н-ЯМР (400 МГц, ДМСО): =2,00 (м, 4Н), 3,09 (м, 2Н), 4,58 (м, 1Н), 5,38 (м, 1Н), 5,47 (м, 1Н), 7,72 (м, 2Н), 7,80 (м, 1Н), 8,16 (м, 3Н), 8,42 (м, 2Н), 8,73 (с, 3Н), 9,92 (с, 1Н), 10,38 м.д. (с, 1Н). Приклад 3 8-(1-Бензилпіролідин-3-іл)-3-(фенілсульфоніл)хінолін 3-(Фенілсульфоніл)-8-вінілхінолін (210 мг, 0,71 ммоль, отриманий у відповідності з WO 2007039219) піддавали реакції з бензилметоксиметилтриметилсилілметиламіном (253 мг, 1,07 ммоль) в дихлорметані (2 мл) в присутності трифтороцтової кислоти протягом 20 хвилин. Отриманий розчин промивали насиченим водним розчином NaHCO 3, сушили над MgSO4, фільтрували і концентрували під вакуумом. Залишок очищали за допомогою хроматографії (100% дихлорметан), для того, щоб отримати цільову сполуку у вигляді безбарвного масла (100 мг, 33%). + 1 MS(ESI+): m/z=429,1 (М+Н) ; Н-ЯМР (400 МГц, dб-ДМСО): =2,22 (м, 1Н), 3,00 (м, 1Н), 3,22 (м, 1Н), 3,35 (м, 1Н), 3,60 (м, 1Н), 3,75 (м, 2Н), 4,00 (м, 1Н), 5,26 (д, 1Н), 5,72 (д, 1Н), 7,11 (м, 2Н), 7,32 (м, 11Н), 7,50 (м, 1Н), 7,68 (д, 2Н), 7,77 м.ч. (с, 1Н). Приклад 4 8-(Піперидин-4-іл)-3-(3-(трифторметил)фенілсульфоніл)хінолін Цільову сполуку отримували способом, аналогічним описаному для прикладу отримання 1. 4.1 Трет-бутил-4-(3-(3-(трифторметил)фенілсульфоніл)хінолін-8-іл)піперидин-1-карбоксилат 1 Вихід: 26%; Н-ЯМР (400 МГц, d6-ДМСО): =1,43 (с, 9Н), 1,60 (м, 2Н), 1,82 (м, 2Н), 2,90 (м, 2Н), 4,10 (м, 3Н), 7,81 (м, 2Н), 5,47 (м, 1Н), 7,92 (м, 1Н), 8,19 (м, 2Н), 8,47 (м, 3Н), 8,67 (уш. м, 1Н), 9,30 (с, 1Н), 9,43 м.ч. (с, 1Н). 4.2 8-(Піперидин-4-іл)-3-(3-(трифторметил)фенілсульфоніл)хінолін + 1 Вихід: 98%; MS(ESI+): m/z=421,1 (M+H) ; Н-ЯМР (400 МГц, d6-ДМСО): =2,00 (м, 4Н), 3,17 (м, 2Н), 4,20 (м, 1Н), 7,81 (м, 2Н), 5,47 (м, 1Н), 7,92 (м, 1Н), 8,19 (м, 2Н), 8,47 (м, 3Н), 8,67 (уш.м, 1Н), 9,30 (с, 1Н), 9,43 м.ч. (с, 1Н). Приклад 5 3-(4-Фторфенілсульфоніл)-8-(піперидин-4-іл)хінолін Цільову сполуку отримували способом, аналогічним описаному для прикладу отримання 1. 5.1 Трет-бутил-4-(3-(4-фторфенілсульфоніл)хшолін-8-іл)піперидин-1-карбоксилат 24 UA 97837 C2 Вихід: 41%; MS(ESI+): m/z=415,1 (M+H-tBu) ; Н-ЯМР (400 МГц, d6-ДМСО): =1,42 (с, 9Н), 1,67 (м, 2Н), 1,82 (м, 2Н), 2,90 (м, 2Н), 4,10 (м, 3Н), 7,49 (м, 2Н), 7,73 (м, 1Н), 7,86 (м, 1Н), 8,15 (м, 3Н), 9,15 (с, 1Н), 9,36 м. ч. (с, 1Н). 5.2 3-(4-Фторфенілсульфоніл)-8-(піперидин-4-іл)хінолін + 1 Вихід: 96%; MS (ESI+): m/z=371,1 (M+H) ; Н-ЯМР (400 МГц, d6-ДМСО): =2,02 (м, 4Н), 3,10 (м, 2Н), 3,39 (м, 2Н), 4,16 (м, 1Н), 7,49 (м, 2Н), 7,79 (м, 2Н), 8,16 (м, 3Н), 9,15 (с, 1Н), 9,34 м. ч. (с, 1Н). Приклад 6 3-(3-Бромфенілсульфоніл)-8-(піперидин-4-іл)хінолін Цільову сполуку отримували способом, аналогічним описаному для прикладу отримання 1. 6.1 3-(3-Бромфенілсульфоніл)-8-йодохінолін + 1 MS(ESI+): m/z=473,8, 475,8 (М+Н) ; Н-ЯМР (400 МГц, d6-ДМСО): =7,59 (м, 2Н), 7,95 (д, 1Н), 8,12 (д, 1Н), 8,30 (д, 1Н), 8,62 (д, 1Н), 9,35 (с, 1Н), 9,48 м. ч. (с, 1Н). 6.2 Трет-бутил-4-(3-(3-бромфенілсульфоніл)хінолін-8-іл)піперидин-1-карбоксилат + 1 Вихід: 54%; MS(ESI+): m/z=475,0, 477,0 (M+H-tBu) ; Н-ЯМР (400 МГц, d6-ДМСО): =1,48 (с, 9Η), 1,67 (м, 2Н), 1,82 (м, 2Н), 2,90 (м, 2Н), 4,10 (м, 3Н), 7,62 (т, 2Н), 7,73 (т, 1Н), 7,86 (д, 1Н), 7,89 (д, 1Н), 8,13 (м, 3Н), 8,30 (с, 1Н), 9,18 (с, 1Н), 9,38 м. ч. (с, 1Н). 6.3 3-(3-Бромфенілсульфоніл)-8-(піперидин-4-іл)хінолін + 1 Вихід: 91%; MS(ESI+): m/z=431,0, 433,0 (M+H) ; Н-ЯМР (400 МГц, d6-ДМСО): =2,02 (м, 4Η), 3,10 (м, 2Н), 3,39 (м, 2Н), 4,16 (м, 1Н), 7,60 (т, 1Н), 7,79 (м, 2Н), 7,90 (м, 1Н), 8,14 (м, 2Н), 8,30 (с, 1Н), 9,25 (с, 1Н), 9,39 м. ч. (с, 1Н). Приклад 7 8-(Піперидин-4-іл)-3-(3-(піролідин-1-іл)фенілсульфоніл)хінолін 7.1 Трет-бутил-4-(3-(3-(піролідин-1-іл)фенілсульфоніл)хінолін-8-іл)піперидин-1-карбоксилат Розчин трет-бутил-4-(3-(3-бромфенілсульфоніл)хінолін-8-іл)піперидин-1-карбоксилату (100 мг, 0,19 ммоль), піролідину (40 мг, 0,564 ммоль), Na трет-бутаноляту (32 мг, 0,34 ммоль), хлороформного адукта трис(дибензиліденацетон)дипаладію(0) (19 мг, 0,019 ммоль) і [1,1'бінафтален]-2,2'-діїлбіс(дифенілфосфіну) (BINAP, 23 мг, 0,038 ммоль) в 10 мл тетрагідрофурану (ТГФ) нагрівали при температурі дефлегмування протягом 2 годин. Охолоджений розчин після стандартної водної обробки і хроматографії дав 60 мг (61%) ВОС-захищеного продукту у вигляді жовтої твердої речовини. + 1 MS(ESI+): m/z=422,3 (M+H-tBu) ; Н-ЯМР (400 МГц, d6-ДМСО): =0,87 (д, 1Н), 1,28 (м, 2Н), 1,48 (с, 9Η), 1,63 (м, 2Н), 1,82 (м, 2Н), 1,98 (м, 4Н), 2,90 (м, 2Н), 4,10 (м, 3Н), 6,70 (м, 2Н), 7,07 (с, 1Н), 7,20 (д, 1Н), 7,38 (м, 1Н), 7,73 (м, 1Н), 7,84 (д, 1Н), 8,13 (м, 1Н), 9,18 (с, 1Н), 9,38 м. ч. (с, 1Н). 7.2 8-(Піперидин-4-іл)-3-(3-(піролідин-1-іл)фенілсульфоніл)хінолін Цільову сполуку отримували способом, аналогічним описаному для прикладу отримання 1. + 1 Вихід: 88%; MS(ESI+): m/z-431,0 (M+H) ; Н-ЯМР (400 МГц, ДМСО): =2,02 (м, 8Н), 3,16 (м, 2Н), 3,27 (м, 4Н), 3,40 (м, 2Н), 4,22 (м, 1Н), 6,80 (д, 1Н), 7,09 (с, 2Н), 7,22 (д, 1Н), 7,40 (м, 1Н), 7,80 (м, 2Н), 8,14 (м, 12Н), 8,30 (с, 1Н), 9,15 (с, 1Н), 9,35 м. ч. (с, 1Н). II. Біологічні дослідження Заміщення радіолігандів, що зв'язуються з нижче описаними клонованими людськими рецепторами 1. Отримання мембран за допомогою ультразвукової обробки і диференціального центрифугування Клітини стійких клональних клітинних ліній, що експресують відповідний рецептор (5-НТ6, 1адренергічний, дофаміновий D2 або гістаміновий Н1 рецептори) промивали ФБР (без Са++, Mg++) і збирали з культури в ФБР з 0,02% ЕДТА. Клітини збирали за допомогою центрифугування при 500 g протягом 10 хв. при 4°С, промивали ФБР і центрифугували (500 g, 10 хв. 4°С). Осад зберігали при -80°С до застосування. Для отримання мембран розморожений клітинний осад ресуспендували в крижаному сахарозному буфері (0,25 Μ сахароза, 10 мМ Hepes (рН 7,4), 1 мМ фенілметилсульфонілфторид (ФМСФ) в ДМСО, 5 мкг/мл перстатину-А, 3 мМ ЕДТА, 0,025% бацитрацин) і гомогенізували при допомозі ультразвукового дезінтегратора Branson Sonifier W-250 (Настройки: таймер 4; вихідний контроль 3; робочий цикл постійний; від 2 до 3 циклів). Руйнування клітин перевіряли за допомогою мікроскопа. Клітки, що залишилися незруйнованими, осаджували при 1,000 g протягом 10 хв. при 4°С. Потім центрифугували при 60,000 g протягом 1 год. при 4°С супернатант сахарозного буфера (Beckman Ultrazentrifuge XL 80). Отриманий осад ресуспендували в 30 мл крижаного буфера Тріс (20 мМ Тріс (рН 7,4), 5 мкг/мл перстатину А, 0,1 мМ ФМСФ, 3 мМ ЕДТА) за допомогою піпетування через 10 мл серологічну піпетку і центрифугували протягом 1 год. при 4°С при 60,000 g. Кінцеву повторну + 5 10 15 20 25 30 35 40 45 50 55 60 25 1 UA 97837 C2 5 10 15 20 25 30 35 40 45 50 55 60 суспензію вмістили в невеликий об'єм крижаного буфера Тріс (дивись вище) за допомогою продавлювання через серологічну піпетку, після чого слідувала ультразвукова обробка при допомозі ультразвукового дезінтегратора Branson Sonifier W-250 (Настройки: таймер 1; вихідний контроль 3; робочий цикл постійний; 1 цикл). Визначали концентрацію білка (BCA-Kit; Pierce) і зберігали аліквоти при -80°С або в рідкому азоті для тривалого зберігання. 2. Експерименти по зв'язуванню з рецептором Всі експерименти по зв'язуванню з рецептором проводили у відповідному буфері для аналізу в загальному об'ємі 200 мкл в присутності різних концентрацій сполуки, що -5 -9 досліджується (від 10 М до 10 М, десятиразове послідовне розведення, подвійні визначення). Аналізи завершували фільтрацією на заздалегідь вимочених в поліетиленіміні (ΠΕΘ 0,1% або 0,3%) фільтрувальних планшетах Packard Unifilter (GF/C або GF/B) за допомогою 96-ямкового планшета для збору клітин Tomtec Machlll U. Після того, як планшети сушили протягом 2 год. при 55°С в сушильній камері, додавали сцинтиляційний коктейль (BetaPlate Scint; PerkinElmer). Радіоактивність вимірювали сцинтиляційним лічильником Microbeta Trilux через дві години після додавання сцинтиляційної суміші. Дані, отримані за допомогою рідинно-сцинтиляційного вимірювання активності, аналізували посередництвом ітеративного аналізу нелінійної регресії із застосуванням системи статистичного аналізу (ССА): програми подібній програмі "LIGAND", описаній в Munson and Rodbard (Analytical Biochemistry 107,220-239 (1980). a) Аналіз зв'язування з рецептором 5-НТб Клітини НEK293, що стійко експресують h-5-НТ6 рецептор (Контрольна послідовність NCBI ХМ 001435), культивували в середовищі RPMI1640 з додаванням 25 мМ НЕРЕС, 10% ембріональної сироватки теляти і 1-2 мМ глутаміну. Отримання мембран здійснювали, як 3 описано в розділі 1. Для отриманих мембран KD 1,95 нМ для [ Н]-ЛСД (діетиламід лизергінової кислоти; AmershaM, TRK1038) визначали за допомогою експериментів по зв'язуванню при насиченні. У день аналізу мембрани розморожували, розбавляли в буфері для аналізу (50 мМ Трис-НСІ, 5 мМ СаСl2, 0,1 % аскорбінова кислота, 10 мкМ паргілін, рН 7,4) до концентрації 8 мкг білка в пробі і гомогенізували за допомогою слабкого струшування. Для дослідження 3 інгібування, 1 нМ [ Н]-лізергінової кислоти діетиламід інкубували в присутності різних концентрацій сполуки, що досліджується, в буфері для аналізу. Неспецифічне зв'язування визначали при допомозі 1 мкМ метіотепіну. Реакцію зв'язування проводили протягом 3,5 год. при кімнатній температурі. Під час інкубації планшети трусили на планшетному шейкері при 100 об./хв. і завершували інкубацію фільтрацією на фільтрувальних планшетах Packard Unifilter GF/C (0,1% ΠΕΘ), після чого слідувало 2 цикли промивання крижаним 50 мМ Трис-НСІ, 5 мМ СаСl2. b) Аналіз зв'язування з дофаміновим рецептором D2 Клітини НEK293, що стійко експресують дофаміновий рецептор D 2 (Контрольна послідовність NCBI NM_000795), культивували в середовищі RPMI1640 з додаванням 25 мМ НЕРЕС, 10% ембріональної сироватки теляти і 1-2 мМ глутаміну. Отримання мембран 125 здійснювали, як описано в розділі 1. Для отриманих мембран Κ D 0,22 нМ для [ І]йодоспіперону (PerkinElmer Life Sciencec, NEX284) визначали за допомогою експериментів по зв'язуванню при насиченні. У день аналізу мембрани розморожували, розбавляли в буфері для аналізу (50 мМ Трис-НСІ, 120 мМ NaCl, 5 мМ MgCl2, 5 мМ KСI, 1,5 мМ СаСI2, рН 7,4) до концентрації 15 мкг білка в пробі і гомогенізували за допомогою слабкого струшування. Для 125 дослідження інгібування, 0,01 нМ [ І]-йодоспіперон (PerkinElmer Life Sciencec, NEX284) інкубували в присутності різних концентрацій сполуки, що досліджується, в буфері для аналізу. Неспецифічне зв'язування визначали при допомозі 1 мкМ галоперидолу. Реакцію зв'язування проводили протягом 1 год. при кімнатній температурі і завершували фільтрацією на фільтрувальних планшетах Packard Unifilter GF/B (0,1% ΠΕΘ), після чого слідувало 6 циклів промивання крижаним 7% розчином поліетиленгліколю. c) Аналіз зв'язування з 1-адренергічним рецептором Клітини СНО-K1, що стійко експресують 1-адренергічний рецептор (Контрольна послідовність NCBI NM_033303), культивували в середовищі RPMI1640 з додаванням 25 мМ НЕРЕС, 10% ембріональної сироватки теляти і 1-2 мМ глутаміну. Отримання мембран 3 здійснювали, як описано в розділі 1. Для отриманих мембран KD 0,12 нМ для [ Н]-празозину (PerkinElmer Life Sciencec, NET823) визначали за допомогою експериментів по зв'язуванню при насиченні. У день аналізу мембрани розморожували, розбавляли в буфері для аналізу (50 мМ Трис-НСІ, рН 7,4) до концентрації 4 мкг білка в пробі і гомогенізували за допомогою слабкого 3 струшування. Для дослідження інгібування, 0,1 нМ [ Н]-празозин (PerkinElmer Life Sciencec, NET823) інкубували в присутності різних концентрацій досліджуваної сполуки в буфері для аналізу. Неспецифічне зв'язування визначали за допомогою 1 мкМ фентоламіну. Реакцію 26 UA 97837 C2 5 10 15 20 25 30 35 зв'язування проводили протягом 1 год. при кімнатній температурі і завершували фільтрацією на фільтрувальних планшетах Packard Unifilter GF/C (0,1% ΠΕΘ), після чого слідувало 3 цикли промивання крижаним буфером для аналізу. d) Аналіз зв'язування з рецептором Н1 Клітини СНО-K1, що стійко експресують гістаміновий рецептор Н 1 (Euroscreen-ES-390-C, Контрольна послідовність NCBI NM_000861), культивували в середовищі RPMI1640 з додаванням 25 мМ НЕРЕС, 10% ембріональної сироватки теляти і 1-2 мМ глутаміну. Отримання 3 мембран здійснювали, як описано в розділі 1. Для отриманих мембран K D 0,83 нМ для [ Н]піриламіну (PerkinElmer Life Sciencec, NET594) визначали за допомогою експериментів по зв'язуванню при насиченні. У день аналізу мембрани розморожували, розбавляли в буфері для аналізу (50 мМ Na2HPO4, 50 мМ KН2РО4, рН 7,4) до концентрації 6 мкг білка в пробі і 3 гомогенізували за допомогою слабкого струшування. Для дослідження інгібування 1 нМ [ Н]піриламін (PerkinElmer Life Sciencec, NET594) інкубували в присутності різних концентрацій досліджуваної сполуки в буфері для аналізу. Неспецифічне зв'язування визначали при допомозі 1 мкМ піриламіну. Реакцію зв'язування проводили протягом 50 хвилин при кімнатній температурі і завершували фільтрацією на фільтрувальних планшетах Packard Unifilter GF/C (0,3% ΠΕΘ), після чого слідувало 2 цикли промивання крижаним буфером для аналізу. 3. Аналіз отриманих даних Дані, отримані за допомогою рідинно-сцинтиляційного вимірювання активності, аналізували шляхом ітеративного аналізу нелінійної регресії із застосуванням системи статистичного аналізу (ССА): програми подібної програмі "LIGAND", описаній в Munson and Rodbard (Anal. Biochem. 1980, 107, 220-239). Фітинг здійснювали відповідно до формул, описаних в Feldman (Anal. Biochem. 1972, 48, 317-338). Величини ІС50, nH і Ki виражали у вигляді середнього геометричного. Для рецепторів з низькою спорідненістю до сполуки, що досліджується, притому, що найвища концентрація досліджуваної сполуки інгібувала менше за 30% специфічного зв'язування радіоліганду, величини Ki визначали відповідно до рівняння ЧенгаПрусофа (Biochem. Pharmacol. 1973, 22, 2099-2108) і виражали у вигляді знаку більше (>). Результати досліджень зв'язування з рецептором виражають у вигляді констант зв'язування з рецептором Ki(5-НТ6), Ki(D2), Ki(1-адренергічний) і Ki(H1), відповідно, як описано вище в контексті даного документа, і наводять в таблиці 1. У даних дослідженнях сполуки згідно з даним винаходом проявляють дуже хорошу спорідненість до рецептора 5-НТ6 (Ki1 мкМ, (++) в кожному конкретному випадку означає, що величина Ki становить 100 нМ-1 мкМ, і (+++) в кожному конкретному випадку означає, що величина Ki
ДивитисяДодаткова інформація
Назва патенту англійськоюQuinoline compounds suitable for treating diseases that respond to modulation of the serotonin 5-ht6 receptor
Автори англійськоюTurner, Sean Colm, Haupt, Andreas, Braje, Wilfried, Lange, Udo, Drescher, Karla, Wicke, Karsten, Unger, Liliane, Mezler, Mario, Wernet, Wolfgang, Mayrer, Matthias
Назва патенту російськоюСоединения хинолина для лечения нарушений, которые реагируют на модуляцию рецептора серотонина 5-ht6
Автори російськоюТернер Шон Кольм, Хаупт Андреас, Брайе Вильфрид, Лангэ Удо, Дрэшэр Карла, Виккэ Карстэн, Унгер Лилиане, Мецлер Марио, Вернет Вольфганг, Майрер Маттиас
МПК / Мітки
МПК: C07D 401/14, C07D 413/14, A61K 31/4709, C07D 401/04, A61P 25/00, C07D 417/14
Мітки: 5-ht6, сполуки, хіноліну, серотоніну, рецептора, лікування, модуляцію, порушень, реагують
Код посилання
<a href="https://ua.patents.su/32-97837-spoluki-khinolinu-dlya-likuvannya-porushen-yaki-reaguyut-na-modulyaciyu-receptora-serotoninu-5-ht6.html" target="_blank" rel="follow" title="База патентів України">Сполуки хіноліну для лікування порушень, які реагують на модуляцію рецептора серотоніну 5-ht6</a>
Попередній патент: Похідні плевромутиліну для лікування захворювань, викликаних мікробами
Наступний патент: Термопластичний пінопласт з частинок та спосіб його одержання
Випадковий патент: Спосіб одержання мембрани іоноселективного електрода для визначення осмію












