Похідні індолу як антагоністи рецептора crth2
Номер патенту: 105039
Опубліковано: 10.04.2014
Автори: Колуччі Джон, Вілльнєв Карін, Метот Джоі, Бертелетт Карл, Бойд Майкл
Формула / Реферат
1. Сполука формули І
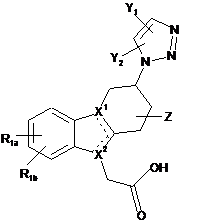 І
І
і її фармацевтично прийнятні солі, де:
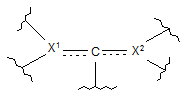 є або
є або 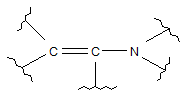 , або
, або 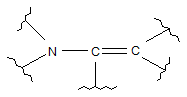 ;
;
Υ1 вибирають з необов'язково заміщеного арилу і -C(R2)(R3)(R4);
Y2 вибирають з Η і -С1-6алкілу;
Ζ вибирають з Η і -С1-6алкілу;
R1a і Rlb незалежно вибирають з Н, галогену, -ОС1-6алкілу, -О-галоС1-6алкілу, -С1-6алкілу, галоС1-6алкілу, необов'язково заміщеного арилу і арилу, необов'язково заміщеного -(С1-3алкіленом);
R2 вибирають з Н; -С1-6алкілу, необов'язково заміщеного галогеном, -ОН або -NHSO2CH3; -ОН; -ОС1-6алкілу; -S(O)nС1-6алкілу; -CN; необов'язково заміщеного арилу; необов'язково заміщеного -О-арилу і необов'язково заміщеного гетероарилу; де n дорівнює 0, 1 або 2;
R3 вибирають з Н, -С1-6алкілу, С1-6галоалкілу, необов'язково заміщеного арилу і необов'язково заміщеного гетероарилу; і
R4 вибирають з Н, -С1-6алкілу, С1-6галоалкілу, необов'язково заміщеного арилу і необов'язково заміщеного гетероарилу; або
R3, R4 і атом вуглецю, до якого вони приєднані, разом утворюють -С3-6циклоалкіл, флуореніл або -С3-6гетероцикліл, що має гетероатом в кільці, вибраний з -N(Ra)-, -О- і -S-; або
R3, R4 разом є С1-6алкіліденом;
Ra є Н, С1-6алкілом або -С(О)С1-6алкілом; і
необов'язковий замісник для арилу і гетероарилу являє собою від 1 до 4 груп, незалежно вибраних з галогену, -С1-3алкокси, -С1-3галоалкілу, гідроксі-С1-3алкілу, аміно, -S(О)n-С1-3алкілу і моно- і ді(С1-3алкіл)аміно.
2. Сполука за п. 1, де R1b, Y2 і Ζ кожний є Н.
3. Сполука за п. 1, що має формулу Іа, і її фармацевтично прийнятні солі:
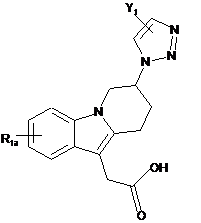 , Ia
, Ia
де Υ1 і R1a такі, як визначені в п. 1.
4. Сполука за п. 1, що має формулу Іb, і її фармацевтично прийнятна сіль:
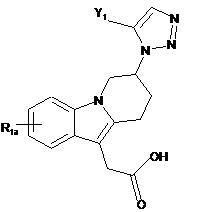 , Ib
, Ib
де Υ1 і R1a такі, як визначені в п. 1.
5. Сполука за п. 3, де Y1 є фенілом, необов'язково заміщеним -C(R3)(R4), або фенілом, необов'язково заміщеним -СН2О; і (і) один з R3 і R4 є Н і інший є Н, -С1-3алкілом або необов'язково заміщеним фенілом; або (іі) R3, R4 і атом вуглецю, до якого вони приєднані, разом утворюють -С3-6циклоалкіл; або (ііі) R3 і R4 разом утворюють -С1-3алкіліден.
6. Сполука за п. 5, де Υ1 є -С(R3)(R4)-фенілом, необов'язково заміщеним 1 або 2 атомами галогену.
7. Сполука за п. 6, де один з R3 і R4 є Н і інший є Н, С1-3алкілом або фенілом, необов'язково заміщеним 1 або 2 атомами галогену.
8. Сполука за п. 6, де R3, R4 і атом вуглецю, до якого вони приєднані, разом утворюють -С3-6циклоалкіл.
9. Сполука за п. 6, де R3 і R4 разом утворюють -С1-3алкіліден.
10. Сполука, вибрана з групи, що включає:
[7-(4-бензил-[1,2,3]триазол-1-іл)-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл]оцтову кислоту;
{7-[4-(4-метоксифеніл)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
[7-(5-бензил-[1,2,3]триазол-1-іл)-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл]оцтову кислоту;
(7-{5-[(2,6-дихлорфенокси)метил]-1Н-1,2,3-триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл)оцтову кислоту;
(7-{5-[1-(4-фторфеніл)-1-гідроксіетил]-[1,2,3]триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл)оцтову кислоту;
{7-[5-(1-фенілциклопентил)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
[7-(5-бензил-[1,2,3]триазол-1-іл)-4-фтор-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл]оцтову кислоту;
{4-фтор-7-[5-(4-фторбензил)-1Н-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
{(7R)-4-фтор-7-[5-(4-фторбензил)-1Н-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]-індол-10-іл}оцтову кислоту;
[3-(5-бензил-[1,2,3]триазол-1-іл)-1,2,3,4-тетрагідрокарбазол-9-іл]оцтову кислоту;
{7-[4-(4-фторфеніл)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
{7-[4-(4-метансульфоніламінобутил)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
{7-[4-(1-гідрокси-2-метилпропіл)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
{7-[4-(1-гідрокси-1-фенілетил)-[1,2,3]-триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
[7-(4-феноксиметил-[1,2,3]триазол-1-іл)-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл]оцтову кислоту;
{7-[4-(4-метансульфонілфеніл)-[1,2,3]-триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
(7-{4-[4-(1-гідрокси-1-метилетил)феніл]-[1,2,3]триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл)оцтову кислоту;
{7-[4-(4-трифторметилфеніл)-[1,2,3]-триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
[7-(4-нафталін-1-іл-[1,2,3]триазол-1-іл)-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл]оцтову кислоту;
{7-[4-(4-диметиламінофеніл)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
{7-[5-(4-фторфеніл)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
[7-(5-феноксиметил-[1,2,3]триазол-1-іл)-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл]оцтову кислоту;
(7-{5-[(4-бромфеніл)гідроксиметил]-[1,2,3]триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл)оцтову кислоту;
трет-бутиловий ефір 4-[3-(10-карбоксиметил-6,7,8,9-тетрагідропіридо[1,2-а]індол-7-іл)-3Н-[1,2,3]триазол-4-іл]піперидин-1-карбонової кислоти;
[7-(5-циклогексил-[1,2,3]триазол-1-іл)-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл]оцтову кислоту;
{7-[5-(9-гідрокси-9Н-флуорен-9-іл)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
(7-{5-[1-(4-фторфеніл)вініл]-[1,2,3]триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл)оцтову кислоту;
(7-{(R)-5-[біс-(4-фторфеніл)гідроксиметил]-[1,2,3]триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл)оцтову кислоту;
{(R)-7-[5-(4-фторбензил)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
{(R)-7-[5-(1-фенілетил)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
((R)-7-{5-[біс-(4-фторфеніл)метил]-[1,2,3]триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл)оцтову кислоту;
((R)-7-{5-[1-(4-фторфеніл)-1-гідроксіетил]-[1,2,3]триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл)оцтову кислоту;
{4-фтор-7-[5-(1-фенілетил)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
{7-[5-(3,4-дифторбензил)-1Н-1,2,3-триазол-1-іл]-4-фтор-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
{7-[5-(4-хлорбензил)-1Н-1,2,3-триазол-1-іл]-4-фтор-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту і
{7-[5-(2,2,2-трифтор-1-гідрокси-1-фенілетил)-1Н-1,2,3-триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
і їх фармацевтично прийнятні солі.
11. Сполука, вибрана з групи, що включає:
[7-(5-бензил-[1,2,3]триазол-1-іл)-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл]оцтову кислоту;
(7-{5-[1-(4-фторфеніл)-1-гідроксіетил]-[1,2,3]триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл)оцтову кислоту;
{7-[5-(1-фенілциклопентил)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
[7-(5-бензил-[1,2,3]триазол-1-іл)-4-фтор-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл]оцтову кислоту;
{4-фтор-7-[5-(4-фторбензил)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
{(7R)-4-фтор-7-[5-(4-фторбензил)-1Н-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
(7-{5-[1-(4-фторфеніл)вініл]-[1,2,3]триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл)оцтову кислоту;
(7-{(R)-5-[біс-(4-фторфеніл)гідроксиметил]-[1,2,3]триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл)оцтову кислоту;
{(R)-7-[5-(4-фторбензил)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
{(R)-7-[5-(1-фенілетил)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
((R)-7-{5-[біс-(4-фторфеніл)метил]-[1,2,3]триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл)оцтову кислоту;
((R)-7-{5-[1-(4-фторфеніл)-1-гідроксіетил]-[1,2,3]триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл)оцтову кислоту і
{4-фтор-7-[5-(1-фенілетил)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту;
і їх фармацевтично прийнятні солі.
12. Фармацевтична композиція, яка містить терапевтично ефективну кількість сполуки за п. 1 і фармацевтично прийнятний носій.
13. Фармацевтична композиція за п. 12, що додатково містить другий активний інгредієнт.
14. Фармацевтична композиція за п. 13, де вказаним другим інгредієнтом є модифікатор лейкотриєну.
15. Фармацевтична композиція за п. 13, де вказаним другим інгредієнтом є антагоніст рецептора лейкотриєну, вибраний з монтелукасту, пранлукасту і зафірлукасту і фармацевтично прийнятної солі кожного.
16. Застосування сполуки за п. 1 для приготування лікарського засобу для лікування або попередження захворювань, опосередкованих CRTH2.
17. Сполука за п. 1 або її фармацевтично прийнятна сіль, де сполука являє собою: [7-(5-бензил-[1,2,3]триазол-1-іл)-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл]оцтову кислоту.
18. Сполука за п. 1 або її фармацевтично прийнятна сіль, де сполука являє собою: {4-фтор-7-[5-(4-фторбензил)-1Н-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-a]індол-10-іл}оцтову кислоту.
19. Сполука за п. 1 або її фармацевтично прийнятна сіль, де сполука являє собою:{(7R)-4-фтор-7-[5-(4-фторбензил)-1H-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]-індол-10-іл}оцтову кислоту.
20. Сполука за п. 1 або її фармацевтично прийнятна сіль, де сполука являє собою: {(R)-7-[5-(4-фторбензил)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту.
21. Сполука за п. 1 або її фармацевтично прийнятна сіль, де сполука являє собою: ((R)-7-{5-[1-(4-фторфеніл)-1-гідроксіетил]-[1,2,3]триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл)оцтову кислоту.
22. Сполука за п.1 або її фармацевтично прийнятна сіль, де сполука являє собою:{4-фтор-7-[5-(1-фенілетил)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-а]індол-10-іл}оцтову кислоту.
23. Фармацевтична композиція за п. 15, де антагоніст рецептора лейкотриєну являє собою монтелукаст або його фармацевтично прийнятну сіль.
24. Застосування сполуки за будь-яким з пп. 1-11 і 17-22 або її фармацевтично прийнятної солі для приготування лікарського засобу для лікування або попередження астми.
25. Застосування за п. 24, де астма являє собою алергійну астму.
Текст
Реферат: Сполуки формули (І) є антагоністами рецептора PGD2, CRTH2 і як такі застосовуються при лікуванні і/або попередженні захворювань, опосередкованих CRTH2, таких як астма. UA 105039 C2 (12) UA 105039 C2 UA 105039 C2 5 10 15 20 25 30 Рівень техніки Простагландин D2 (PGD2) являє собою метаболіт циклооксигенази арахідонової кислоти. Він виділяється з мастоцитів і клітин TH2 у відповідь на імунологічний виклик, і залучений до різних фізіологічних процесів, таких як сон і алергічні реакції. Рецептори для PGD2 включають рецептор "DP", рецептор-хемоатрактант - гомологічну молекулу, яка експресується на клітинах TH2 ("CRTH2"), і рецептор типу "FP". Ці рецептори є зв'язаними з G-білком рецепторами, активованими PGD2. Рецептор CRTH2 і його експресія на різних клітинах, включаючи Т-хелперні клітини людини, базофіли і еозинофіли, описані в Abe, et al., Gene 227:71-77, 1999, Nagata, et al., FEBS Letters 459:195-199, 1999, і Nagata, et al., The Journal of Immunology 762:1278-1286, 1999, де описаний рецептор CRTH2. Hirai, et al., J. Exp. Med. 193:255-261, 2001, повідомляють, що CRTH2 є рецептором для PGD 2. У WO2007019675 описані антагоністи CRTH2 формули: Суть винаходу У даному винаході представлені нові сполуки, які є антагоністами рецептора CRTH2. Сполуки відповідно до даного винаходу застосовують для лікування різних опосередкованих простагландином захворювань і розладів; отже, в даному винаході представлений спосіб лікування опосередкованих простагландином захворювань із застосуванням описаних тут нових сполук, а також фармацевтичні композиції, що містять їх. Короткий опис малюнків На фігурі 1 зображена порошкова рентгенограма кристалічної форми В сполуки з прикладу 8A. На фігурі 2 зображена порошкова рентгенограма кристалічної форми С сполуки з прикладу 8A. На фігурі 3 зображена крива диференціальної скануючої калориметрії (ДСК) кристалічної форми В сполуки з прикладу 8A. На фігурі 4 зображена крива диференціальної скануючої калориметрії (ДСК) кристалічної форми С сполуки з прикладу 8A. Докладний опис винаходу Даний винахід належить до сполук формули I: і їх фармацевтично прийнятних солей, де: є або , або 1 ; UA 105039 C2 5 10 15 20 25 Y1 вибирають з необов'язково заміщеного арилу і -C(R2)(R3)(R4); Y2 вибирають з Н і -C1-6алкілу; Z вибирають з Н і -C1-6алкілу; R1a і R1b незалежно вибирають з Н, галогену, -OC1-6алкілу, -O-галоC1-6алкілу, -C1-6алкілу, галоC1-6алкілу, необов'язково заміщеного арилу і арилу, необов'язково заміщеного -(C13алкіленом); R2 вибирають з Н, -C1-6алкілу, необов'язково заміщеного галогеном, -OH або -NHSO2CH3, OH, -OC1-6алкілу, -S(O)nC1-6алкілу, -CN, необов'язково заміщеного арилу, необов'язково заміщеного -O-арилу і необов'язково заміщеного гетероарилу, де n дорівнює 0, 1 або 2; R3 вибирають з Н, -C1-6алкілу, C1-6галоалкілу, необов'язково заміщеного арилу і необов'язково заміщеного гетероарилу; і R4 вибирають з Н, -C1-6алкілу, C1-6галоалкілу, необов'язково заміщеного арилу і необов'язково заміщеного гетероарилу; або R3, R4 і атом вуглецю, до якого вони приєднані, разом утворюють -C3-6циклоалкіл, флуореніл a або -C3-6гетероцикліл, що має гетероатом в кільці, вибраний з -N(R )-, -O- і -S-; або R3, R4 разом є C1-6алкіліденом; a R є Н, C1-6алкілом або -C(O)C1-6алкілом; і необов'язковий замісник для арилу і гетероарилу являє собою від 1 до 4 груп, незалежно вибраних з галогену, -C1-3алкокси, -C1-3галоалкілу, гідроксі-C1-3алкілу, -S(O)n-C1-3алкілу, аміно і моно- і ді(C1-3алкіл)аміно. В одному варіанті формули I представлені сполуки, де R1b, Y2 і Z кожний є Н. В одному варіанті формули I представлені сполуки формули Ia і їх фармацевтично прийнятні солі: . В іншому варіанті формули I представлені сполуки формули Ib і їх фармацевтично прийнятні солі: . В іншому варіанті формули I представлені сполуки формули Ic і їх фармацевтично прийнятні солі: 2 UA 105039 C2 5 10 15 20 25 30 35 40 45 . В одній групі формул I, Ia, Ib і Ic представлені сполуки, де R 1a є Н або галогеном. В одному варіанті R1a є H. В іншому варіанті, R1a є F. В іншій групі формул I, Ia, Ib і Ic представлені сполуки, де Y1 є необов'язково заміщеним арилом. В одному варіанті, Y1 є фенілом, необов'язково заміщеним від 1 до 3 групами, незалежно вибраними з галогену, -C1-3алкокси, -C1-3галоалкілу; гідроксі-C1-3алкілу, -S(O)n-C13алкілу, аміно і моно- і ді-(C1-3алкіл)аміно. В іншій групі формул I, Ia, Ib і Ic представлені сполуки, де Y 1 є фенілом, необов'язково заміщеним -C(R3)(R4), або фенілом, необов'язково заміщеним -CH2O. В одному варіанті, R3 і R4 кожний є H. В другому варіанті, один з R3 і R4 є OH і інший є Н, C1-3алкілом або необов'язково заміщеним фенілом. У третьому варіанті, R3, R4 і атом вуглецю, до якого вони приєднані, разом утворюють -C3-6циклоалкіл. У четвертому варіанті, один з R3 і R4 є Н і інший є C1-3алкілом або необов'язково заміщеним фенілом. У п'ятому варіанті, R3 і R4 разом утворюють -C1-3алкіліден. У цій групі необов'язковими замісниками для фенілу є від 1 до 3 груп, незалежно вибраних з галогену, -C1-3алкокси, -C1-3галоалкілу, гідроксі-C1-3алкілу, -S(O)n-C1-3алкілу, аміно і моно- і ді-(C13алкіл)аміно; більш переважно, необов'язковими замісниками є 1 або 2 атоми галогену. В іншій групі формул Ia і Ib представлені сполуки, де R 1a є Н або F, і Y1 вибирають з необов'язково заміщеного фенілу, фенілу, необов'язково заміщеного -C(R3)(R4), і фенілу, необов'язково заміщеного -CH2O. У цю групу включені сполуки формули Ib, де Y1 є фенілом, необов'язково заміщеним -C(R3)(R4), і (i) один з R3 і R4 є Н або OH, і інший є Н, -C1-3алкілом або необов'язково заміщеним фенілом; або (ii) R3, R4 і атом вуглецю, до якого вони приєднані, разом утворюють -C3-6циклоалкіл; або (iii) R3 і R4 разом утворюють -C1-3алкіліден. В іншій групі формул Ib представлені сполуки, де R 1a є Н або F, і Y1 є -CH2-фенілом, необов'язково заміщеним 1 або 2 групами, незалежно вибраними з галогену, -C1-3алкокси, -C13галоалкілу, гідроксі-C1-3алкілу, -S(O)n-C1-3алкілу, аміно і моно- і ді-(C1-3алкіл)аміно; більш переважно, необов'язковим замісником є 1 або 2 атоми галогену. Типовими сполуками відповідно до даного винаходу (включаючи їх фармацевтично прийнятні солі) є: [7-(4-бензил-[1,2,3]триазол-1-іл)-6,7,8,9-тетрагідропіридо[1,2-α]індол-10-іл]оцтова кислота; {7-[4-(4-метоксифеніл)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-α]індол-10-іл}оцтова кислота; [7-(5-бензил-[1,2,3]триазол-1-іл)-6,7,8,9-тетрагідропіридо[1,2-α]індол-10-іл]оцтова кислота; (7-{5-[(2,6-дихлорфенокси)метил]-1H-1,2,3-триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2-α]індол10-іл)оцтова кислота; (7-{5-[1-(4-фторфеніл)-1-гідроксіетил]-[1,2,3]триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2α]індол-10-іл)оцтова кислота; {7-[5-(1-фенілциклопентил)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-α]індол-10іл}оцтова кислота; [7-(5-бензил-[1,2,3]триазол-1-іл)-4-фтор-6,7,8,9-тетрагідропіридо[1,2-α]індол-10-іл]оцтова кислота; {4-фтор-7-[5-(4-фторбензил)-1H-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-α]індол-10іл}оцтова кислота; {(7R)-4-фтор-7-[5-(4-фторбензил)-1H-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-α]індол-10-іл}оцтова кислота; [3-(5-бензил[1,2,3]триазол-1-іл)-1,2,3,4-тетрагідрокарбазол-9-іл]оцтова кислота; 3 UA 105039 C2 5 10 15 20 25 30 35 40 45 50 55 60 {7-[4-(4-фторфеніл)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-α]індол-10-іл}оцтова кислота; {7-[4-(4-метансульфоніламінобутил)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-α]індол10-іл}оцтова кислота; {7-[4-(1-гідрокси-2-метилпропіл)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-α]індол-10іл}оцтова кислота; {7-[4-(1-гідрокси-1-фенілетил)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-α]індол-10іл}оцтова кислота; [7-(4-феноксиметил-[1,2,3]триазол-1-іл)-6,7,8,9-тетрагідропіридо[1,2-α]індол-10-іл]оцтова кислота; {7-[4-(4-метансульфонілфеніл)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-α]індол-10іл}оцтова кислота; (7-{4-[4-(1-гідрокси-1-метилетил)феніл]-[1,2,3)триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2α]індол-10-іл)оцтова кислота; {7-[4-(4-трифторметилфеніл)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-α]індол-10іл}оцтова кислота; [7-(4-нафталін-1-іл-[1,2,3]триазол-1-іл)-6,7,8,9-тетрагідропіридо[1,2-α]індол-10-іл]оцтова кислота; {7-[4-(4-диметиламінофеніл)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-α]індол-10іл}оцтова кислота; {7-[5-(4-фторфеніл)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-α]індол-10-іл}оцтова кислота; [7-(5-феноксиметил-[1,2,3]триазол-1-іл)-6,7,8,9-тетрагідропіридо[1,2-α]індол-10-іл]оцтова кислота; (7-{5-[(4-бромфеніл)гідроксиметил]-[1,2,3]триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2-α]індол10-іл)оцтова кислота; трет-бутиловий ефір 4-[3-(10-карбоксиметил-6,7,8,9-тетрагідропіридо[1,2-α]індол-7-іл)-3H[1,2,3]триазол-4-іл]піперидин-1-карбонової кислоти; [7-(5-циклогексил-[1,2,3]триазол-1-іл)-6,7,8,9-тетрагідропіридо[1,2-α]індол-10-іл]оцтова кислота; {7-[5-(9-гідрокси-9H-флуорен-9-іл)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-α]індол10-іл}оцтова кислота; (7-{5-[1-(4-фторфеніл)вініл]-[1,2,3]триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2-α]індол-10іл)оцтова кислота; (7-{(R)-5-[біс-(4-фторфеніл)гідроксиметил]-[1,2,3]триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2α]індол-10-іл)оцтова кислота; {(R)-7-[5-(4-фторбензил)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-α]індол-10іл}оцтова кислота; {(R)-7-[5-(1-фенілетил)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-α]індол-10-іл}оцтова кислота; ((R)-7-{5-[біс-(4-фторфеніл)метил]-[1,2,3]триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2-α]індол10-іл)оцтова кислота; ((R)-7-{5-[1-(4-фторфеніл)-1-гідроксіетил]-[1,2,3]триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2α]індол-10-іл)оцтова кислота; {4-фтор-7-[5-(1-фенілетил)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-α]індол-10іл}оцтова кислота; {7-[5-(3,4-дифторбензил)-1H-1,2,3-триазол-1-іл]-4-фтор-6,7,8,9-тетрагідропіридо[1,2-α]індол10-іл}оцтова кислота; {7-[5-(4-хлорбензил)-1H-1,2,3-триазол-1-іл]-4-фтор-6,7,8,9-тетрагідропіридо[1,2-α]індол-10іл}оцтова кислота; і {7-[5-(2,2,2-трифтор-1-гідрокси-1-фенілетил)-1H-1,2,3-триазол-1-іл]-6,7,8,9тетрагідропіридо[1,2-α]індол-10-іл}оцтова кислота. Даний винахід також охоплює фармацевтичні композиції, що містять сполуки формули I, і способи лікування або попередження опосередкованих простагландином захворювань із застосуванням сполук формули I. Даний винахід описаний за допомогою наступних визначень, якщо не вказане інакше. Термін "галоген" або "гало" включає F, Cl, Br і I. Термін "алкіл" належить до лінійних або розгалужених алкільних ланцюгів, що мають вказану кількість атомів вуглецю. Не обмежувальні приклади алкільних груп включають метил, етил, пропіл, ізопропіл, бутил, втор- і трет-бутил, пентил, гексил і подібні. 4 UA 105039 C2 5 10 15 20 25 30 35 40 45 50 55 60 "Галоалкіл" означає алкільну групу, описану вище, де один або більше атомів водню заміщені атомами галогену, аж до повного заміщення всіх атомів водню групами галогену. C 16галоалкіл, наприклад, включає -CF3, -CF2CF3, CHFCH3 і подібні. "Алкокси" означає алкоксигрупи з лінійним або розгалуженим алкільним ланцюгом, що мають вказану кількість атомів вуглецю. C1-6алкокси, наприклад, включає метокси, етокси, пропокси, ізопропокси і подібні. "Арил" означає 6-14-членне карбоциклічне ароматичне кільце, що містить 1-3 бензольних кілець. Якщо присутні два або більше ароматичних кілець, тоді кільця конденсовані разом так, щоб сусідні кільця мали загальний зв'язок. Приклади включають феніл і нафтил. "Необов'язково заміщений арил" означає арильну групу, яка не заміщена або заміщена як описано. Термін "гетероарил" (Het) в даному описі представляє 5-10-членну ароматичну систему кілець, що містить одне кільце або два конденсованих кільця, 1-4 гетероатоми, вибрані з О, S і N. Het включає, але не обмежений ними, фураніл, імідазоліл, ізоксазоліл, ізотіазоліл, оксадіазоліл, оксазоліл, піразоліл, піридил, піроліл, тетразоліл, тіазоліл, тіадіазоліл, тієніл, триазиніл, триазоліл, 1H-пірол-2,5-діоніл, 2-пірон, 4-пірон, піролопіридин, фуропіридин і тієнопіридин. "Необов'язково заміщений гетероарил" означає гетероарильну групу, яка не заміщена або заміщена як визначено вище. "Терапевтично ефективна кількість" означає кількість лікарської речовини або фармацевтичного засобу, яка викликає біологічну або медичну реакцію в тканинах, системі, у тварини або людини, що досліджується експериментатором, ветеринаром, лікарем або іншим клініцистом. Термін "лікування" або "лікувати" включає полегшення, послаблення, зменшення або інше зниження ознак і симптомів, пов'язаних із захворюванням або розладом. Термін "композиція", наприклад, фармацевтична композиція, охоплює продукт, що містить активний інгредієнт і інертний інгредієнт (фармацевтично прийнятні наповнювачі), які складають носій, а також будь-який продукт, який одержують, прямо або непрямо, при поєднанні, з'єднанні або об'єднанні будь-яких двох або більше з цих інгредієнтів, або при розчиненні одного або більше інгредієнтів, або при проведенні інших реакцій або взаємодій одного або більше інгредієнтів. Отже, композиції відповідно до даного винаходу охоплюють будь-яке поєднання, одержане змішуванням сполуки формули I і фармацевтично прийнятних наповнювачів. Термін "необов'язково заміщений" означає "не заміщений або заміщений", і тому загальні структурні формули, представлені тут, охоплюють сполуки, що містять вказаний необов'язковий замісник, а також сполуки, які не містять необов'язковий замісник. Кожна змінна незалежно визначена кожний раз, коли вона присутня у визначенні загальної структурної формули. Наприклад, якщо є більше одного замісника для арилу/гетероарилу, кожний замісник незалежно вибирають в кожному випадку, і кожний замісник може бути однаковим або відмінним від інших. Оптичні ізомери - Діастереомери - Геометричні ізомери - Таутомери Сполуки формули I містять один або більше асиметричних центрів і, тому, можуть існувати у вигляді рацематів і рацемічних сумішей, окремих енантіомерів, діастереомерних сумішей і окремих діастереомерів. Даний винахід охоплює всі такі ізомерні форми сполук формули I, або у вигляді окремих видів, або у вигляді їх сумішей. Деякі сполуки, описані тут, містять олефінові подвійні зв'язки і, якщо не вказано інакше, включають обидва Е і Z геометричні ізомери. Деякі сполуки, описані тут, можуть існувати з різними місцями приєднання водню, їх позначають як таутомери. Прикладом може служити кетон і його енольна форма, відомі як кетоенольні таутомери. Окремі таутомери, а також їх суміші, включені в сполуки формули I. Сполуки формули I можуть бути розділені на діастереоізомерні пари енантіомерів, наприклад, фракційною кристалізацією з відповідного розчинника, наприклад, метанолу або етилацетату, або їх суміші. Пара енантіомерів, одержаних таким чином, може бути розділена на окремі стереоізомери звичайними методами, наприклад, із застосуванням оптично активної кислоти як розділювального агента. Альтернативно, будь-який енантіомер сполуки загальної формули I може бути одержаний стереоспецифічним синтезом із застосуванням оптично чистих вихідних матеріалів, проміжних сполук або реагентів відомої конфігурації. Солі Термін "фармацевтично прийнятні солі" належить до солей, одержаних з фармацевтично прийнятних не токсичних основ, включаючи неорганічні основи і органічні основи. Солі, одержані з неорганічних основ, включають солі алюмінію, амонію, кальцію, міді, заліза, двовалентного заліза, літію, магнію, марганцю, двовалентного марганцю, калію, натрію, цинку і 5 UA 105039 C2 5 10 15 20 25 30 35 40 45 50 55 60 подібних. Особливо переважними є солі амонію, кальцію, магнію, калію і натрію. Солі, одержані з органічних не токсичних основ, включають солі первинних, вторинних і третинних амінів, заміщених амінів, включаючи природні заміщені аміни, циклічних амінів і лужних іонообмінних смол, таких як аргінін, бетаїн, кофеїн, холін, N, N’-дибензилетилендіамін, діетиламін, 2діетиламіноетанол, 2-диметиламіноетанол, етаноламін, етилендіамін, N-етилморфолін, Nетилпіперидин, глюкамін, глюкозамін, гістидин, гідрабамін, ізопропіламін, лізин, метилглюкамін, морфолін, піперазин, піперидин, поліамінові смоли, прокаїн, пурини, теобромін, триетиламін, триметиламін, трипропіламін, трометамін і подібні. Якщо сполука відповідно до даного винаходу є лужною, солі можуть бути одержані з фармацевтично прийнятних не токсичних кислот, включаючи неорганічні кислоти і органічні кислоти. Такі кислоти включають оцтову, бензолсульфонову, бензойну, камфорсульфонову, лимонну, етансульфонову, фумарову, глюконову, глутамінову, бромистоводневу, хлористоводневу, ізетіонову, молочну, малеїнову, яблучну, мигдалеву, метансульфонову, слизову, азотну, памову, пантотенову, фосфорну, сукцинову, сірчану, винну, птолуолсульфонову і подібні. Особливо переважними є лимонна, бромистоводнева, хлористоводнева, малеїнова, фосфорна, сірчана і винна кислоти. Зрозуміло, що, якщо не вказано інакше, посилання на сполуки формули I, Ia, Ib, Ic і Id, їх підтипи, їх варіанти, а також конкретні сполуки також включають їх фармацевтично прийнятні солі. Більш того деякі кристалічні форми сполук відповідно до даного винаходу можуть існувати у вигляді поліморфів, і всі такі форми включені в даний винахід. Крім того, деякі сполуки відповідно до даного винаходу можуть утворювати сольвати з водою (гідрати) або звичайними органічними розчинниками. Такі сольвати включені в обсяг даного винаходу. Мічені сполуки У сполуках відповідно до даного винаходу загальної формули I атоми можуть мати їх природні ізотопні надлишки, або один або більше атомів можуть бути штучно збагачені конкретним ізотопом, що має таке ж атомне число, але атомна маса або масове число якого відрізняються від атомної маси або масового числа, переважно існуючої в природі. Даний винахід включає всі придатні ізотопні варіанти сполук загальної формули I. Наприклад, різні 1 2 ізотопні форми водню (Н) включають протій ( Н) і дейтерій ( H). Протій є переважним ізотопом водню, що знаходиться в природі. Збагачення до дейтерію може давати певні терапевтичні переваги, такі як збільшення періоду напіврозпаду in vivo або зниження дози, або можуть давати сполуку, корисну як стандарт для одержання характеристик біологічних зразків. Збагачені ізотопами сполуки загальної формули I можуть бути одержані без зайвого експериментування звичайними методиками, добре відомими фахівцям в даній галузі техніки, або способами, аналогічними тим, які описаних в схемах і прикладах нижче, із застосуванням відповідних збагачених ізотопами реагентів і/або проміжних сполук. Застосування Здатність сполук формули I взаємодіяти з рецепторами простагландину робить їх корисними для попередження або зниження небажаних симптомів, викликаних простагландинами, у ссавців, особливо у людини. Така імітація або антагонізм до дії простагландинів показує, що сполука і її фармацевтична композиція можуть бути використані для лікування, попередження або полегшення у ссавців, особливо у людини: респіраторних станів, алергічних станів, болю, запальних станів, розладів секреції слизової, кісткових розладів, розладів сну, розладів здібності до відтворення потомства, розладів коагуляції крові, проблем із зором, а також імунних і аутоімунних захворювань. Крім того, така сполука може інгібувати неопластичні трансформації клітин і ріст метастазів пухлини і, отже, може застосовуватися при лікуванні раку. Сполуки формули I також можуть застосовуватися при лікуванні і/або попередженні опосередкованих простагландином розладів проліферації, які можуть виникнути при діабетичній ретинопатії і ангіогенезі пухлини. Сполуки формули I також інгібують викликане простаноїдом скорочення гладких м'язів через антагонізм до скорочувальних простаноїдів або імітацію послаблюючих простаноїдів і, отже, можуть застосовуватися при лікуванні менструального болю, передчасних пологів і розладів, пов'язаних з еозинофілами. Більш конкретно, сполуки формули I є антагоністами рецептора простагландину D 2, CRTH2. Отже, інший аспект даного винаходу належить до способу лікування або попередження опосередкованих простагландином захворювань, що включає введення ссавцеві пацієнту, при необхідності такого лікування, сполуки формули I в кількості, яка ефективна для лікування або попередження вказаного опосередкованого простагландином захворювання. Опосередковані простагландином захворювання включають, але не обмежені ними, алергічний риніт, закладання носа, ринорею, хронічний алергічний риніт, запалення носа, астму, що викликає 6 UA 105039 C2 5 10 15 20 25 30 35 40 45 50 55 60 алергічну астму, хронічне обструктивне захворювання легенів і інші форми запалення легенів; розлади сну і розлади циклу сну-неспання; викликане простаноїдом скорочення гладких м'язів, пов'язане з менструальними болями і передчасними родами; викликані еозинофілами захворювання; тромбоз; глаукому і розлади зору; оклюзійні захворювання судин; застійну серцеву недостатність; захворювання або стани, що потребують лікування антикоагулянтами, такі як посттравматичне або післяопераційне лікування; запалення; гангрену; хворобу Рейно; розлади секреції слизової, включаючи цитопротекцію; біль і мігрень; захворювання, що потребують контролю утворення і резорбції кісток, таких як, наприклад, остеопороз; шок; теплове регулювання, включаючи лихоманку; і імунні розлади або стани, в яких бажане імунорегулювання. Більш конкретно, захворюванням, яке можна лікувати запропонованим способом, є захворювання, опосередковане простагландином D 2, таке як закладання носа, легенева гіперемія і астма, включаючи алергічну астму. В одному варіанті даного винаходу представлений спосіб лікування або попередження опосередкованого простагландином захворювання, що включає введення ссавцеві, потребуючому такого лікування, сполуки формули I в кількості, яка є ефективною для лікування або попередження опосередкованого простагландином захворювання, де опосередкованим простагландином захворюванням є закладання носа, риніт, включаючи алергічний риніт, і астма, включаючи алергічну астму. В іншому варіанті даного винаходу представлений спосіб лікування або попередження опосередкованого простагландином D2 захворювання, що включає введення ссавцеві, потребуючому такого лікування, сполуки формули I в кількості, яка є ефективною для лікування або попередження опосередкованого простагландином D2 захворювання, де опосередкованим простагландином D2 захворюванням є закладання носа або астма. В іншому варіанті даного винаходу представлений спосіб лікування закладання носа у пацієнта, потребуючого такого лікування, який включає введення вказаному пацієнту терапевтично ефективної кількості сполуки формули I. У ще одному варіанті даного винаходу представлений спосіб лікування астми, включаючи алергічну астму, у пацієнта, потребуючого такого лікування, який включає введення вказаному пацієнту терапевтично ефективної кількості сполуки формули I. Дозування Інтервал профілактичної або терапевтичної дози сполуки формули I, зазвичай, залежить від природи і тяжкості стану і конкретної сполуки формули I і способу її введення. Також він варіюється залежно від таких факторів як вік, маса тіла, загальний стан здоров'я, стать, режим харчування, час введення, швидкість виведення, поєднання лікарських засобів і реакція конкретного пацієнта. Загалом, добова доза складає від близько 0,001 мг до близько 100 мг на кг масу тіла ссавця, переважно, від 0,01 мг до близько 10 мг на кг. З іншого боку, може бути необхідно застосовувати дози, що виходять за вказані межі, в деяких випадках. Кількості активного інгредієнта, яка може бути об'єднана з носіями для одержання стандартної лікарської форми, варіюється залежно від пацієнта, що лікується, і конкретного способу введення. Наприклад, композиція для перорального введення людині може містити від 0,05 мг до 5 г активного агента, об'єднаного з відповідною і зручною кількістю носія, який може складати від близько 5 до близько 99,95 процентів від загальної композиції. Стандартні лікарські форми зазвичай містять від близько 0,1 мг до близько 0,4 г активного інгредієнта, зазвичай 0,5 мг, 1 мг, 2 мг, 5 мг, 10 мг, 25 мг, 50 мг, 100 мг, 200 мг або 400 мг. Фармацевтичні композиції В іншому аспекті даного винаходу представлені фармацевтичні композиції, що містять сполуки формули I з фармацевтично прийнятним носієм. Для лікування будь-якого з опосередкованих простаноїдом захворювань сполуки формули I можуть вводитися перорально, інгаляцією, місцево, парентерально або ректально в стандартних лікарських формах, що містять звичайні не токсичні фармацевтично прийнятні носії, ад'юванти і наповнювачі. Термін "парентеральне" в даному описі включає підшкірні, внутрішньовенні, внутрішньом'язові, надчеревинні ін'єкції або вливання. На додаток до лікування теплокровних тварин, таких як миші, щури, коні, худоба, вівці, собаки, кішки і т. д., сполука відповідно до даного винаходу ефективна для лікування людини. Фармацевтичні композиції, що містять активний інгредієнт, можуть бути в формі, придатній для перорального застосування, наприклад, у вигляді таблеток, коржиків, пастилок, водних або масляних суспензій, диспергованих порошків або гранул, емульсій, жорстких або м'яких капсул або сиропів або еліксирів. Композиції, призначені для перорального застосування, можуть бути одержані будь-яким способом, відомим в даній галузі техніки для одержання фармацевтичних композицій, і такі композиції можуть містити один або більше агентів, вибраних з групи, що 7 UA 105039 C2 5 10 15 20 25 30 35 40 45 50 55 60 включає підсолоджувачі, смакові добавки, барвники і консерванти для одержання фармацевтично чудового і приємного на смак препарату. Таблетки містять активний інгредієнт в суміші з не токсичними фармацевтично прийнятними наповнювачами, які придатні для виробництва таблеток. Ці наповнювачі можуть включати, наприклад, інертні розріджувачі, такі як карбонат кальцію, карбонат натрію, лактоза, фосфат кальцію або фосфат натрію; гранулюючі і диспергуючі агенти, наприклад, кукурудзяний крохмаль або альгінову кислоту; зв'язувальні агенти, наприклад, крохмаль, желатин або аравійська камедь, і мастильні агенти, наприклад, стеарат магнію, стеаринову кислоту або тальк. Таблетки можуть бути без оболонки або покриті оболонкою із застосуванням відомих методик для затримки руйнування і абсорбції в шлунковокишковому тракті, тим самим забезпечуючи уповільнену дію протягом більш тривалого періоду часу. Наприклад, може застосовуватися затримуючий матеріал, такий як моностеарат гліцерилу або дистеарат гліцерилу. Вони також можуть бути покриті із застосуванням методики, описаної в патенті США 4256108; 4166452; і 4265874 з одержанням осмотичних терапевтичних таблеток з контрольованим виділенням. Препарати для перорального застосування також можуть бути представлені у вигляді твердих желатинових капсул, де активний інгредієнт змішаний з інертним твердим розріджувачем, наприклад, карбонатом кальцію, фосфатом кальцію або каоліном, або у вигляді м'яких желатинових капсул, де активні інгредієнти змішують з розчинниками, що змішуються з водою, такими як пропіленгліколь, ПЕГ і етанол, або з масляним середовищем, наприклад, арахісовим маслом, рідким парафіном або оливковою олією. Водні суспензії містять активний інгредієнт в суміші з наповнювачами, придатними для виробництва водних суспензій. Такі наповнювачі включають суспендувальні агенти, наприклад, карбоксиметилцелюлозу натрію, метилцелюлозу, гідроксипропілметилцелюлозу, альгінат натрію, полівінілпіролідон, трагакант і аравійську камедь; диспергуючі або змочувальні агенти можуть бути природними фосфатидами, наприклад, лецитином, або продуктами конденсації алкіленоксиду і жирними кислотами, наприклад, стеаратом поліоксіетилену, або продуктами конденсації етиленоксиду з довголанцюжковими аліфатичними спиртами, наприклад, гептадекаетиленоксицетанолом, або продуктами конденсації етиленоксиду з неповним ефіром, одержаним з жирних кислот і гекситу, таких як моноолеат поліоксіетиленсорбіту, або продуктами конденсації етиленоксиду з неповним ефіром, одержаним з жирних кислот і ангідридів гекситу, наприклад, моноолеатом поліетиленсорбітану. Водні суспензії також можуть містити одинабо більше консервантів, наприклад, етил або н-пропіл, п-гідроксибензоат, один або більше барвників, одну або більше смакових добавок, і один або більше підсолоджувачів, таких як сахароза, сахарин або аспартам. Масляні суспензії можуть бути складені суспендуванням активного інгредієнта в рослинній олії, наприклад, арахісовому маслі, оливковій олії, кунжутній олії або кокосовій олії, або в мінеральному маслі, такому як рідкий парафін. Масляні суспензії можуть містять загусник, наприклад, бджолиний віск, твердий парафін або цетиловий спирт. Підсолоджувачі, такі як вказані вище, і смакові добавки можуть бути додані для одержання приємної на смак пероральної композиції. Ці композиції можуть зберігатися додаванням антиоксиданту, такого як аскорбінова кислота. Дисперговані порошки і гранули, придатні для одержання водної суспензії додаванням води, включають активний інгредієнт в суміші з диспергуючим або змочувальним агентом, суспендувальним агентом і одним або більше консервантами. Придатні диспергуючі або змочувальні агенти представлені тими, які вказані вище. Також можуть бути присутніми додаткові наповнювачі, наприклад, підсолоджувачі, смакові добавки і барвники. Фармацевтичні композиції відповідно до даного винаходу також можуть бути у вигляді емульсії масло у воді. Масляною фазою може бути рослинна олія, наприклад, оливкова олія або арахісова олія, або мінеральне масло, наприклад, рідкий парафін, або їх суміші. Придатні емульгувальні агенти можуть включати природні фосфатиди, наприклад, соєві боби, лецитин, і складні ефіри або неповні ефіри, одержані з жирних кислот і ангідридів гекситу, наприклад, моноолеат сорбітану, і продукти конденсації вказаного неповного ефіру з етиленоксидом, наприклад, моноолеат поліоксіетиленсорбітану. Емульсії також можуть містити підсолоджувачі і смакові добавки. Сиропи і еліксири можуть бути складені з підсолоджувачами, наприклад, гліцерином, пропіленгліколем, сорбітом або сахарозою. Такі композиції також можуть містити пом'якшувачі, консервант і барвники. Фармацевтичні композиції можуть бути у вигляді стерильної водної або масляної суспензії для ін'єкцій. Ця суспензія може бути складена методами відомого рівня техніки із застосуванням придатних диспергуючих або змочувальних агентів і суспендувальних агентів, які вказані вище. Стерильний препарат для ін'єкцій також може бути стерильним 8 UA 105039 C2 5 10 15 20 25 30 35 40 45 50 55 60 розчином або суспензією для ін'єкцій в не токсичному, прийнятному для парентерального введення розріджувачі або розчиннику, наприклад, розчином в 1,3-бутандіолі. Застосовувані прийнятні носії і розчинники включають воду, розчин Рінгера і ізотонічний розчин хлориду натрію. Також можуть застосовуватися співрозчинники, такі як етанол, пропіленгліколь або поліетиленгліколі. Крім того, стерильні нелеткі масла також зазвичай застосовують як розчинник або суспендувальне середовище. Для цієї мети може застосовуватися будь-яке м'яке нелетке масло, включаючи синтетичні моно- і дигліцериди. Крім того, в препаратах для ін'єкцій застосовують жирні кислоти, такі як олеїнова кислота. Лікарські форми для інгаляцій можуть бути складені у вигляді аерозолів або сухих порошків. Для композицій, придатних і/або адаптованих для інгаляцій, переважно, щоб активна речовина була в формі із зменшеним розміром частинок, і більш переважно, в формі із зменшеним розміром частинок, що одержуються або одержаних мікронізацією. Переважний розмір частинок сполуки, солі або сольвату із зниженим розміром частинок (тобто мікронізованої) визначається значенням D50 від близько 0,5 до близько 10 мікрон (наприклад, за вимірюваннями із застосуванням лазерної дифракції). В одному варіанті, медичний препарат адаптований для застосування в дозуючому інгаляторі під тиском (pMDI), який виділяє певну дозу лікарського засобу при кожному натисненні. Композиція для рMDI може бути у вигляді розчинів або суспензій в галогенованих вуглеводневих газах-витисниках. Як газ-витисник, що застосовується в pMDI, частіше застосовують гідрофторалкани (ГФА), також відомі як гідрофторвуглеводні (ГФВ), оскільки застосування хлорфторвуглеводнів (також відомих як фреони або ХФВ) було припинене. Зокрема, 1,1,1,2-тетрафторетан (ГФА 134a) і 1,1,1,2,3,3,3-гептафторпропан (ГФА 227) застосовують в декількох фармацевтичних інгальованих продуктах, що продаються в даний час. Композиція може включати іншу фармацевтично прийнятні наповнювачі для інгаляцій, такі як етанол, олеїнова кислота, полівінілпіролідон і подібні. Інгалятори типу pMDI зазвичай мають два компоненти. По-перше, є каністра, в якій під тиском зберігаються частинки лікарського засобу у вигляді суспензії або розчину. По-друге, є сховище, що застосовується для утримування і приведення в дію каністри. Зазвичай каністра містить множину доз композиції, хоча існують каністри з однією дозою. Каністра зазвичай включає випускний клапан, з якого виприскується вміст каністри. Аерозольний лікарський засіб виприскується з pMDI при застосуванні сили до каністри, при втисненні її в приймаючий компонент, тим самим відкриваючи випускний клапан і викликаючи перехід частинок лікарського засобу з випускного клапана через сховище і випускання частинок через вихідний отвір сховища. При випусканні з каністри частинки лікарського засобу "розпилюються", утворюючи аерозоль. Вважають, що пацієнт координує випускання аерозольного лікарського засобу з його або її вдиханням так, щоб частинки лікарського засобу попадали в дихальний шлях пацієнта і переносилися в легені. Зазвичай в pMDI застосовують гази-витиснювачі для стискання вмісту каністри і для виштовхування частинок лікарського засобу з виходу сховища. У pMDI композиція представлена в рідкій або суспендованій формі, і знаходиться всередині контейнера разом з газом-витиснювачем. Газ-витиснювач може мати множину форм. Наприклад, газ-витиснювач може містити стиснений газ або зріджений газ. Інший варіант лікарського препарату адаптований для застосування з інгалятором для сухих порошків (DРI). Композиція для інгаляції, застосовна в DРI, зазвичай містить частинки активного інгредієнта і частинки фармацевтично прийнятного носія. Розмір частинок активного матеріалу складає від близько 0,1 мкм до близько 10 мкм; однак для ефективної доставки у віддалені частини легенів принаймні 95 процентів частинок активних агентів повинні мати розмір 5 мкм або менше. Кожний активний агент може бути присутнім в концентрації 0,01-99 %. Зазвичай кожний з активних агентів присутній в концентрації від близько 0,05 до 50 %, більш переважно, близько 0,2-20 % від загальної маси композиції. Як відмічено вище, на додаток до активних інгредієнтів інгальований порошок переважно включає фармацевтично прийнятний носій, який може бути складений з будь-якого фармакологічно прийнятного інертного матеріалу або поєднання матеріалів, які прийнятні для інгаляції. Переважно, частинки носія складаються з одного або більше кристалічного цукру; частинки носія можуть бути складені з одного або більше цукрових спиртів або багатоатомних спиртів. Переважно, частинки носія включають частинки декстрози або лактози, особливо лактози. У варіантах даного винаходу, в яких застосовуються звичайні інгалятори сухих порошків, такі як Handihaler, Rotohaler, Diskhaler, Twisthaler і Turbohaler, розмір частинок носія може варіюватися від близько 10 мікрон до близько 1000 мікрон. У певних варіантах такий розмір частинок носія може варіюватися від близько 20 мікрон до близько 120 мікрон. У певних варіантах, розмір принаймні 90 % мас. частинок носія складає менше 1000 мікрон і, переважно, 9 UA 105039 C2 5 10 15 20 25 30 35 40 45 50 55 60 від 60 мікрон до 1000 мікрон. Відносно великий розмір частинок носія забезпечує хороші характеристики потоку і захоплення. Якщо він присутній, кількість носія зазвичай складає аж до 95 %, наприклад, аж до 90 %, переважно, аж до 80 % і, більш переважно, аж до 50 % мас. по відношенню до загальної маси порошку. Кількість будь-якого тонкоподрібненого наповнювача, якщо присутня, може складати аж до 50 % і, переважно, аж до 30 %, особливо, аж до 20 % мас. по відношенню до загальної маси порошку. Порошок може необов'язково містити модифікатор дії, такий як L-лейцин або інша амінокислота, і/або металеві солі стеаринової кислоти, такі як стеарат магнію або кальцію. Сполуки формули I також можуть вводитися в формі супозиторіїв для ректального введення лікарського засобу. Ці композиції можуть бути одержані змішуванням лікарського засобу з придатним не подразнюючим наповнювачем, який є твердим при температурі навколишнього середовища, але рідким при ректальній температурі і, отже, плавиться в прямій кишці з виділенням лікарського засобу. Такі матеріали включають олію какао і поліетиленгліколі. Для місцевого застосування використовуються креми, мазі, гелі, розчини або суспензії, наприклад, що містять сполуки формули I. (Для цілей даного винаходу місцеве введення включає полоскання для рота і полоскання для горла). Місцеві композиції зазвичай містять фармацевтичний носій, співрозчинник, емульгатор, агент, поліпшуючий проникнення, систему консервантів і пом'якшувач. Поєднання з іншими лікарськими засобами Для лікування і попередження захворювань, опосередкованих простагландином, сполука формули I може вводитися спільно з іншими терапевтичними засобами. Таким чином, в іншому аспекті даного винаходу представлені фармацевтичні композиції для лікування захворювань, опосередкованих простагландином, що містять терапевтично ефективну кількість сполуки формули I і один або більше терапевтичний засіб. Придатні терапевтичні засоби для комбінованої терапії зі сполукою формули I включають: (1) антагоніст рецептора DP, такий як S5751; (2) кортикостероїд, такий як триамцинолон ацетонід, будезонід, беклометазон, мометазон фуроат, флутиказон пропіонат і циклезонід; (3) β-агоніст, такий як сальметерол, формотерол, тербуталін, метапротеренол, альбутерол і подібні; (4) модифікатор лейкотриєну, включаючи антагоніст рецептора лейкотриєну, такий як монтелюкаст, зафірлюкаст, пранлюкаст, або інгібітор ліпооксигенази, включаючи інгібітори 5-ліпооксигенази і інгібітори FLAP (активуючого білка 5-ліпооксигенази), такі як зилейтон; (5) антигістамін, такий як бромфенірамін, хлорфенірамін, дексхлорфенірамін, трипролідин, клемастин, дифенгідрамін, дифенілпіралін, трипеленнамін, гідроксизин, метдилазин, прометазин, тримепразин, азатадин, ципрогептадин, антазолін, фенірамін, піриламін, астемізол, терфенадин, лоратадин, цетиризин, фексофенадин, дескарбоетоксилоратадин і подібні; (6) протинабряковий засіб, включаючи фенілефрин, фенілпропаноламін, псевдоефедрин, оксиметазолін, епінефрин, нафазолін, ксилометазолін, пропілгекседрин або ліво-дезоксіефедрин; (7) протикашльовий засіб, включаючи кодеїн, гідрокодон, караміфен, карбетапентан або декстраметорфан; (8) інший ліганд простагландину, включаючи агоніст простагландину F, такий як латанопрост; мізопростол, енпростил, ріопростил, орнопростол або розапростол; (9) діуретик; (10) нестероїдні протизапальні засоби (НСПЗЗ), такі як похідні пропіонової кислоти (алмінопрофен, беноксапрофен, буклоксова кислота, карпрофен, фенбуфен, фенопрофен, флупрофен, флурбіпрофен, ібупрофен, індопрофен, кетопрофен, міропрофен, напроксен, оксапрозин, пірпрофен, пранопрофен, супрофен, тіапрофенову кислоту і тиоксапрофен), похідні оцтової кислоти (індометацин, ацеметацин, алклофенак, кліданак, диклофенак, фенклофенак, фенклозинова кислота, фентіазак, фурофенак, ібуфенак, ізоксепак, окспінак, суліндак, тіопінак, толметин, зидометацин і зомепірак), похідні фенамінової кислоти (флуфенамінова кислота, меклофенамінова кислота, мефенамінова кислота, ніфлумінова кислота і толфенамінова кислота), похідні біфенілкарбонової кислоти (дифлунізал і флуфенізал), оксиками (ізоксикам, піроксикам, судоксикам і теноксикан), саліцилати (ацетилсаліцилова кислота, сульфасалазин) і піразолони (апазон, безпіперилон, фепразон, мофебутазон, оксифенбутазон, фенілбутазон); (11) інгібітори циклооксигенази-2 (COX-2), такі як целекоксиб і рофекоксиб; (12) інгібітори фосфодіестерази типу IV (PDE-IV), наприклад, Ariflo, рофлуміласт; (13) антагоністи рецепторів хемокіну, особливо CCR-1, CCR-2 і CCR-3; (14) засоби, що знижують холестерин, такі як інгібітори HMG-CoA редуктази (ловастатин, симвастатин і правастатин, флувастатин, аторвастатин і інші статини), секвестранти (холестирамін і колестипол), нікотинову кислоту, похідні фенофібринової кислоти (гемфіброзил, клофібрат, фенофібрат і бензафібрат), і пробукол; (15) антидіабетичні засоби, такі як інсулін, сульфонілсечовини, бігуаніди (метформін), інгібітори α-глюкозидази (акарбоза) і глітазони (троглітазон, піоглітазон, енглітазон, розиглітазон і подібні); (16) препарати інтерферону бета (інтерферон бета-1a, інтерферон бета-1b); (17) антихолінергічні засоби, такі 10 UA 105039 C2 5 10 15 20 25 30 35 40 як мускаринові антагоністи (бромід іпратропію, бромід тіотропію, хлорид троспію, бромід аклідинію і глікопіролят, включаючи R, R-гліколпіролят), а також селективні мускаринові антагоністи M3; (18) стероїди, такі як беклометазон, метилпреднізолон, бетаметазон, преднізон, дексаметазон і гідрокортизон; (19) триптани, що зазвичай застосовуються для лікування мігрені, такі як сумітриптан і ризатриптан; (20) алендронат і інше лікування остеопорозу; (21) інші сполуки, такі як 5-аміносаліцилова кислота і її проліки, антиметаболіти, такі як азатіоприн і 6меркаптопурин, цитотоксичні засоби для хіміотерапії раку, антагоністи брадикініну (BK2), такі як FK-3657, антагоністи TP рецептора, такі як сератродаст, антагоністи нейрокініну (NK1/NK2), антагоністи VLA-4, такі як описані в US 5510332, WO97/03094, WO97/02289, WO96/40781, WO96/22966, WO96/20216, WO96/01644, WO96/06108, WO95/15973 і WO96/31206. Крім того, даний винахід включає спосіб лікування захворювань, опосередкованих простагландином D2, що включає: введення пацієнту, потребуючому такого лікування, не токсичної терапевтично ефективної кількості сполуки формули I, необов'язково спільно з одним або більше інгредієнтів, перерахованих вище. Сполуки синтезу Сполуки формули I відповідно до даного винаходу можуть бути одержані відповідно до методів синтезу, вказаних на наступних схемах і способах, описаних тут. Застосовувані абревіатури включають: Ac=ацетил; Bu=бутил; COD=1,5-циклооктадієн; Cp*=пентаметилциклопентадієніл; МЕЦП=метиловий ефір циклопропілу; ДХМ=дихлорметан; ДІПЕА=діізопропілетиламін; ДМФ=диметилформамід; ЕА/EtOAc=етилацетат; Et=етил; Гекс=гексан; HMDS=гексаметилдисилазан; ІПА=ізопропанол; ІПАц=ізопропілацетат; iPr=ізопропіл; Me=метил; Ms=метансульфоніл (мезил); MTBE=Метил трет-бутиловий ефір; Pr=пропілати; КТ=кімнатна температура; t-bu=трет-бутил; ТЕА=триетиламін; ТГФ=тетрагідрофуран; ТМС=триметилсиліл; р-ТСК=п-толуолсульфонова кислота. Як показано на схемі 1, заміщені азиди VIII можуть бути одержані в сім послідовних стадій. Конденсація 4-оксопімелату I із заміщеними гідразинами II в киплячому при температурі рефлюксу толуолі дає проміжні сполуки етилового ефіру III. Обробка сполуки III метансульфоновою кислотою в пропанолі дає відповідні індоли IV. Регіоселективне додавання аніону йодиду триметилсульфонію в складний ефір в положенні 2 індолу дає іліди V. Циклізація сполуки V в присутності каталітичної кількості димеру хлор(1,5-циклооктадієн)іридію(I) дає бажані кетоіндоли VI. Перетворення кетонової групи на азид VIII може бути проведене із застосуванням стандартного тристадійного протоколу, що включає відновлення з боргідридом натрію, мезилювання з хлоридом метансульфонілу і заміщення з азидом натрію. Схема 1: Синтез азидів Недоступні комерційно алкіни можуть бути одержані взаємодією триметилсилілацетилену і відповідного галогеніду бензилу IX із застосуванням броміду етилмагнію і броміду міді (Схема 2, Gazz. Chim. Ital. 1990, 120, 783). Видалення групи ТМС в сполуці X може бути досягнуте із застосуванням водного KF в ДМФ з одержанням бажаних заміщених алкінів XI. Схема 2: Синтез алкінів 11 UA 105039 C2 5 10 15 Триазол, такий як сполуки XIII і XV, може бути одержаний із застосуванням клік-хімії. Циклододавання (3+2) азидів VIII і алкінів XI в присутності йодиду міді дає виключно 1,4-триазол XII (Angew. Chem. Int. Ed. 2002, 41, 2596). 1,5-Триазол, такий як сполука XIV, може бути одержаний із застосуванням комплексу рутенію (J. Am. Chem. Soc. 2005, 127, 15998). Гідроліз сполук XII або XIV у водній основі дає кінцевий продукт XIII або XV. Схема 3: Синтез 1,4-триазолів (частина А) і 1,5-триазолів (частина В) Кетон XVI вже описаний в J. Med. Chem. 2005, 48, 897. Перетворення кетонової групи XVI на азид XVIII може бути проведене із застосуванням стандартного тристадійного протоколу, що включає відновлення боргідридом натрію, мезилювання з хлоридом метансульфонілу і заміщення з азидом натрію. Азид XVIII можна поєднувати з алкіном XI із застосуванням або міді, або рутенію з одержанням триазолу XIX. Стандартний гідроліз дає бажану кислоту XX. Схема 4 Альтернативний метод одержання не доступних комерційно алкінів включає застосуванням умов Соногаширі для одержання ТМС-алкіну, з якого може бути знятий захист з одержанням 12 UA 105039 C2 5 ацетилену XXII із застосуванням каталітичної кількості тетрагідрату фториду тетраметиламонію, буферованого оцтовою кислотою. Внутрішні алкіни можуть бути одержані алкілуванням кінцевого алкіну XXIII метилйодидом з одержанням алкіну XXIV (Схема 5, Knobloch, K.; Keller, M.; Eberbach, W. Eur. J. Org. Chem. 2001, 3313-23332). Приєднані до одного і того ж атому диметилу α-заміщені алкіни можуть бути одержані депротонуванням складного ефіру XXV з гідридом натрію з подальшим алкілуванням метилйодидом. Відновлення складного ефіру XXVI з подальшим окисленням в умовах Сверна дає альдегід XXVII. Обробка реагентом Бестманна дає бажаний, приєднаний до одного і того ж атому диметилу заміщений алкін XXVIII. Схема 5 10 15 Індол XXXI може бути одержаний через утворення кеталю (XXIX) і іміну (XXX) з подальшою циклізацією Хека і утворенням іліду. Каталізована іридієм циклізація дає кетон XXXII. Перетворення кетону на хіральний спирт XXXIII може бути проведене через ферментне відновлення для встановлення необхідного стереоцентру. Схема 6 20 Алкілування кетону VI з йодметаном дає заміщений кетон XXXIV. Перетворення кетонової групи XXXIV на триазол XXXVII проводять, дотримуючись протоколу, аналогічного протоколу для неметильованого кетону, показаного на Схемі 1 і Схемі 3. Схема 7 13 UA 105039 C2 5 10 15 20 25 Дизаміщені алкіни також можуть бути зв'язані з азидом VIII із застосуванням рутенієвого каталізатора, з одержанням регіоізомерної суміші 1,4,5-триазолів. Після розділення ізомерів і гідролізу відповідного складного ефіру одержують карбонові кислоти XXXVIII і XXXIX. Схема 8 Сполуки формули I можуть бути одержані способами, зображеними на Схемах і в прикладах, із застосуванням відповідних матеріалів, і конкретні приклади сполук показані нижче. Представлені сполуки, однак, не обмежують обсяг даного винаходу. Представлені нижче приклади ілюструють деталі одержання сполук відповідно до даного винаходу. Фахівці в даній галузі техніки легко зрозуміють, що відомі варіанти захисних груп, реагентів, а також умов і процесів в представлених нижче методиках одержання можуть застосовуватися для одержання цих сполук. Також зрозуміло, що якщо хімічний реагент не є комерційно доступним, такий хімічний реагент може бути легко одержаний фахівцем в даній галузі техніки із застосуванням або адаптацією відомих способів, описаних в літературі. Всі температури дані в градусах Цельсія, якщо не вказано інакше. Мас спектр (МС) вимірюють або мас спектроскопією з електророзпиленням іонів (МСЕІ), або мас спектроскопією з хімічною іонізацією при атмосферному тиску (ХІАТ). Приклад 1 [7-(4-Бензил-[1,2,3]триазол-1-іл)-6,7,8,9-тетрагідропіридо[1,2-a]індол-10-іл]оцтова кислота Стадія 1: пропіл[7-(4-бензил-1Н-1,2,3-триазол-1-іл)-6,7,8,9-тетрагідропіридо[1,2-a]індол-10іл]ацетат До перемішуваного розчину пропіл(7-азидо-6,7,8,9-тетрагідропіридо[1,2-a]індол-10іл)ацетату (1 екв.) (синтез описаний в WO07019675 A1) і проп-2-ін-1-ілбензолу (2 екв.) в тетрагідрофурані (ТГФ) (0,1 M) при кімнатній температурі додають діізопропілетиламін (ДІПЕА) 14 UA 105039 C2 5 10 15 20 25 30 35 40 45 (5 екв.) і CuI (5 екв.). Реакційну суміш перемішують протягом ночі, потім гасять насиченим NH 4Cl і екстрагують етилацетатом (ЕА), промивають насиченим розчином солі, сушать над Na2SO4 і випарюють. Очищення комбі-флеш ЕА/Гекс 0-100 % дає бажану сполуку, яку застосовують без подальшого очищення. Стадія 2: До перемішуваного розчину пропіл[7-(4-бензил-1Н-1,2,3-триазол-1-іл)-6,7,8,9тетрагідропіридо[1,2-a]індол-10-іл]ацетату (1 екв.) в ТГФ/MeOH (2:1, 0,1 M) при кімнатній температурі додають 2M розчин гідроксиду калію (10 екв.) Реакційну суміш перемішують при кімнатній температурі протягом 2 год., потім гасять додаванням HCl 10 % до кислого pH і розбавляють дихлорметаном (ДХМ). Фільтрація через фазовий сепаратора з подальшим 1 випарюванням дає бажаний продукт у вигляді білої твердої речовини. H ЯМР (400 МГц, ДМСOd6): δ 12,13 (с, 1Н), 8,05 (с, 1Н), 7,46 (д, 1Н), 7,40 (д, 1Н), 7,34-7,17 (м, 5Н), 7,12-7,00 (м, 2Н), 5,35-5,18 (м, 1Н), 4,67 (дд, 1Н), 4,32 (дд, 1Н), 4,02 (с, 2Н), 3,69-3,50 (м, 2Н), 3,07-2,92 (м, 2Н), 2,52-2,30 (м, 2Н). МС (+ІЕР) m/z: 387,2. Приклад 2 {7-[4-(4-Метоксифеніл)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-a]індол-10-іл}оцтова кислота Вказану в заголовку сполуку одержують із застосуванням методик, описаних в Прикладі 1 з пропіл(7-азидо-6,7,8,9-тетрагідропіридо[1,2-a]індол-10-іл)ацетату і 1-етиніл-4-метоксибензолу. 1 H ЯМР (400 МГц, ДМСO-d6): δ 12,14 (с, 1Н), 8,67 (с, 1Н), 7,78 (д, 2Н), 7,48 (д, 1Н), 7,42 (д, 1Н), 7,13-6,99 (м, 4Н), 5,40-5,30 (м, 1Н), 4,74 (дд, 1Н), 4,40 (дд, 1Н), 3,80 (с, 3Н), 3,61 (с, 2Н), 3,12-3,01 (м, 2Н). МС (+ІЕР) m/z: 403,1. Приклад 3 [7-(5-Бензил-[1,2,3]триазол-1-іл)-6,7,8,9-тетрагідропіридо[1,2-a]індол-10-іл]оцтова кислота Стадія 1: пропіл[7-(5-бензил-1H-1,2,3-триазол-1-іл)-6,7,8,9-тетрагідропіридо[1,2-a]індол-10іл]ацетат До перемішуваного розчину пропіл(7-азидо-6,7,8,9-тетрагідропіридо[1,2-a]індол-10іл)ацетату (синтез описаний в WO07019675 A1) і проп-2-ін-1-ілбензолу (1,5 екв.) в бензолі (0,3 M) при кімнатній температурі додають хлор(1,5-циклооктадієн)(пентаметилциклопентадієніл)рутеній(II) (0,1 екв.). Реакційну суміш промивають азотом, потім нагрівають до 80 °C протягом ночі, охолоджують до кімнатної температури, фільтрують через силікагель, промивають EtOAc і концентрують. Залишок очищають хроматографією на колонці з силікагелем, елююючи EtOAc/Гексаном (від 0 до 50 %) з одержанням бажаних рацемічних складних ефірів, які розділяють СРХ із застосуванням колонки 10×250 мм Chiralpak AD, елююючи 40 % MeOH при 5 мл/хв при 150 бар і 254 нм (час утримування = 7,5 і 9,8 хв). Стадія 2: Одержані хіральні складні ефіри (1 екв.) (час утримування = 7,5 і 9,8 хв) гідролізують окремо при кімнатній температурі із застосуванням 2M розчину гідроксиду калію (10 екв.) в ТГФ/MeOH (2:1, 0,1 M). Реакційну суміш перемішують при кімнатній температурі протягом 2 год., потім гасять додаванням HCl 10 % до кислого pH і розбавляють ДХМ. Фільтрація через фазовий 1 сепаратор з подальшим випарюванням дає Приклад 3.1 і 3.2, відповідно. Η ЯМР (400 МГц, ДМСO-d6): δ 12,14 (с, 1Н), 7,57 (с, 1Н), 7,46 (д, 1Н), 7,43-7,28 (м, 2Н), 7,40-7,22 (м, 3Н), 7,29-7,19 (м, 1Н), 7,05 (т, 2Н), 5,14 (с, 1Н), 4,53-4,28 (м, 1Н), 4,28 (с, 2Н), 4,18 (т, 1Н), 3,81-3,36(м, 2Н), 3,09 (д, 1Н), 3,02-2,73 (м, 1Н), 2,50-2,07 (м, 1Н), 2,22-1,94 (м, 1Н). МС (+ІЕР) m/z: 387,2. Приклад 4 15 UA 105039 C2 (7-{5-[(2,6-дихлорфенокси)метил]-1H-1,2,3-триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2-a]індол10-іл)оцтова кислота 5 10 15 20 25 30 35 . Вказану в заголовку сполуку одержують із застосуванням методик, описаних в Прикладі 3 з пропіл(7-азидо-6,7,8,9-тетрагідропіридо[1,2-a]індол-10-іл)ацетату і проп-2-ін-1-ілового ефіру 2,61 дихлорфенілу. H ЯМР (400 МГц, ДМСO-d6): δ 12,14 (с, 1Н), 7,91 (с, 1Н), 7,54 (д, 2Н), 7,49 (д, 1Н), 7,35 (д, 1Н), 7,25 (т, 1Н), 7,11-7,00 (м, 2Н), 5,48-5,32 (м, 3Н), 4,78 (дд, 1Н), 4,37 (т, 1Н), 3,62 (д, 2Н), 3,43-3,34 (м, 1Н), 3,24-3,09 (м, 1Н), 3,09-2,97 (м, 1Н). МС (+ІЕР) m/z: 471,1. Приклад 5 (7-{5-[1-(4-Фторфеніл)-1-гідроксіетил]-[1,2,3]триазол-1-іл}-6,7,8,9-тетрагідропіридо[1,2a]індол-10-іл)оцтова кислота Вказану в заголовку сполуку одержують із застосуванням методик, описаних в Прикладі 3 з пропіл(7-азидо-6,7,8,9-тетрагідропіридо[1,2-a]індол-10-іл)ацетату і 2-(4-фторфеніл)бут-3-ин-2олу. Розділення одержаних діастереоізомерів проводять на стадії складного ефіру флешхроматографією із застосуванням градієнта 10-70 % ЕА/Гекс з одержанням двох енантіомерних сумішей. Більш швидко елюйовану енантіомерну суміш розділяють на хіральній ВЕРХ із застосуванням колонки 50×400 мм Chiralcel OD, елююючи 8 % iPrOH, 8 % EtOH, 83,75 % гексанами і 0,25 % Et3N при 60 мл/хв і 254 нм. Одержаний складний ефір (час утримування = 18,4 і 22,1 хв) гідролізують окремо в ТГФ/MeOH (2:1, 0,1 M) при кімнатній температурі із застосуванням 1M розчину гідроксиду натрію (10 екв.). Реакційну суміш перемішують при кімнатній температурі протягом 2 год., потім гасять додаванням HCl 10 % до кислого pH і розбавляють ДХМ. Фільтрація через фазовий сепаратора з подальшим випарюванням дає бажані Приклад 5.1 і 5.2, відповідно. Повільно елюйовану енантіомерну суміш розділяють на хіральній ВЕРХ із застосуванням колонки 50×400 мм Chiralcel OD, елююючи 30 % iPrOH, 70 % гексанами при 60 мл/хв і 254 нм. Одержаний складний ефір (час утримування = 18,3 і 34 хв) 1 гідролізують так само, як описано вище, з одержанням Прикладу 5.3 і 5.4, відповідно. H ЯМР (400 МГц, ДМСO-d6): δ 12,13 (с, 1Н), 7,97 (с, 1Н), 7,45 (д, 1Н), 7,36 (дд, 2Н), 7,31 (д, 1Н), 7,20 (т, 2Н), 7,11-7,00 (м, 2Н), 6,68 (с, 1Н), 5,03 (с, 1Н), 4,54 (дд, 1Н), 4,24 (т, 1Н), 3,60-3,48 (м, 2Н), 3,012,91 (м, 1Н), 2,37-2,26 (м, 1Н), 2,02-1,93 (м, 1Н), 1,90 (с, 3Н), 1,36-1,24 (м, 1Н). МС (+ІЕР) m/z: 435,1. Приклад 6 {7-[5-(1-Фенілциклопентіл)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-a]індол-10іл}оцтова кислота . Вказану в заголовку сполуку одержують із застосуванням методик, описаних в Прикладі 3 з (1-етинілциклопентил)бензолу і енантіомерно чистого пропіл (7-азидо-6,7,8,9тетрагідропіридо[1,2-a]індол-10-іл)ацетату, одержаного розділенням рацемічного азиду на 16 UA 105039 C2 5 10 15 20 25 30 35 40 45 50 колонці 4,6×250 мм ChiralCel OD, елююючи 15 % MeOH, 15 % iPrOH, 69,75 % гексанами і 0,25 % Et3N при 1 мл/хв і 254 нм. Час утримування = 10,3 і 11,5 мн. Приклади 6.1 і 6.2 одержують з 1 хірального азиду з часом утримування 10,3 і 11,5 хв, відповідно. H ЯМР (400 МГц, ДМСO-d6): δ 12,13 (с, 1Н), 7,93 (с, 1Н), 7,42 (д, 1Н), 7,36 (дд, 2Н), 7,31-7,23 (м, 3Н), 7,13 (д, 1Н), 7,07-6,97 (м, 2Н), 4,59 (с, 1Н), 3,98-3,89 (м, 1Н), 3,58-3,46 (м, 2Н), 3,03-2,92 (м, 1Н), 2,29-2,20 (м, 1Н), 2,10-2,01 (м, 1Н), 1,54-1,43 (м, 1Н). МС (+ІЕР) m/z: 441,2. Приклад 7 [7-(5-Бензил-[1,2,3]триазол-1-іл)-4-фтор-6,7,8,9-тетрагідропіридо[1,2-a]індол-10-іл]оцтова кислота Стадія 1: Етил 3-[1-(2-фторфеніл)-6-оксо-1,4,5,6-тетрагідропіридазин-3-іл]пропаноат У колбі, обладнаній пасткою Старка, гідрохлорид 2-фторгідразину (1 екв.) і 4-оксопимелат діетилу (1 екв.) об'єднують в толуолі (1M). Суспензію вистоюють протягом 24 годин при кипінні із зворотним холодильником. Реакційну суміш охолоджують до кімнатної температури і концентрують у вакуумі. Неочищений продукт очищають на шарі силікагелю, елююючи EtOAc/гексаном (від 10 до 50 %) з одержанням бажаного матеріалу у вигляді оранжевокоричневого масла, яке застосовують як є на наступній стадії. Стадія 2: пропіл 3-[7-фтор-3-(2-оксо-2-пропоксіетил)-1Н-індол-2-іл]пропаноат Метансульфонову кислоту (1,2 екв.) додають до перемішуваного розчину етил 3-[1-(2фторфеніл)-6-оксо-1,4,5,6-тетрагідропіридазин-3-іл]пропаноату (1 екв.) в н-пропанолі (1M). Суміш нагрівають протягом 48 год. при 80 °C. Суміш охолоджують до кімнатної температури і нейтралізують водним розчином гідроксиду натрію (1,2 екв.) і екстрагують метил третбутиловим ефіром (МТБЕ). Органічний шар сушать над сульфатом натрію і концентрують. Залишок очищають на короткому шарі силікагелю, елююючи EtOAc/Гексаном (від 0 до 60 % за 30 хв) з одержанням бажаного продукту у вигляді коричневого масла. Стадія 3: пропіл(2-(4-[диметил(оксидо)-1-сульфаніліден]-3-оксобутил}-7-фтор-1Н-індол-3іл)ацетат Йодид триметилсульфоксонію (2 екв.) частково розчиняють в ТГФ (9M) і додають розчин трет-бутоксиду калію в ТГФ (2,4 екв.). Суміш нагрівають до 67 °C протягом 2 год. і потім охолоджують до 0 °C. До охолодженого розчину додають розчин пропіл 3-[7-фтор-3-(2-оксо-2пропоксіетил)-1Н-індол-2-іл]пропаноату (1 екв.) в ТГФ (5M) протягом більше 15 хв. Суміш нагрівають до кімнатної температури і перемішують протягом 24 годин. Реакційну суміш виливають в суміш води і EtOAc, і шари розділяють. Водний шар знов екстрагують EtOAc. Об'єднані органічні шари промивають послідовно насиченим розчином NaHCO3 і насиченим розчином солі, сушать (MgSO4), фільтрують і концентрують з одержанням бажаного продукту у вигляді оранжево-коричневої твердої речовини, яку застосовують як є на наступній стадії. Стадія 4: пропіл(4-фтор-7-оксо-6,7,8,9-тетрагідропіридо[1,2-a]індол-10-іл)ацетат Дегазований розчин пропіл(2-{4-[диметил(оксидо)-1-сульфаніліден]-3-оксобутил}-7-фтор-1Ніндол-3-іл)ацетату (1 екв.) в диметилформаміді (ДМФ) (0,2 M) додають протягом більш 15 хвилин із застосуванням канюлі до попередньо нагрітого (105 °C) дегазованого розчину димеру хлор(1,5-циклооктадієн)іридію(I) (0,02 екв.) в толуолі (0,01 M). Суміш вистоюють при 105 °C протягом 45 хв, охолоджують до кімнатної температури і виливають в насичений розчин солі і розбавляють Et2O. Шари розділяють, і органічний шар знов промивають насиченим розчином солі. Органічний шар сушать (Na2SO4), фільтрують і концентрують при зниженому тиску. Залишок очищають хроматографією на колонці з силікагелем, елююючи EtOAc/Гексаном (від 0 до 30 % за 30 хв) з одержанням бажаного продукту у вигляді жовтого масла. Стадія 5: пропіл{4-фтор-7-[(метилсульфоніл)окси]-6,7,8,9-тетрагідропіридо[1,2-a]індол-10іл}ацетат До перемішуваного розчину пропіл(4-фтор-7-оксо-6,7,8,9-тетрагідропіридо[1,2-a]індол-10іл)ацетату (1 екв.) і MeOH (3 екв.) в ТГФ (0,07 M) при 0 °C додають NaBH4 (1 екв.). Реакційну суміш перемішують при 0 °C протягом 60 хв. Додають насичений розчин хлориду амонію і 17 UA 105039 C2 5 10 15 20 25 30 35 40 45 50 EtOAc, і шари розділяють. Органічний шар промивають насиченим розчином солі, сушать (Na2SO4), фільтрують і концентрують з одержанням бажаного спирту у вигляді твердої речовини, яку застосовують як є на наступній стадії. До переміщуваного розчину неочищеного спирту (1 екв.) в CH2Cl2 (0,33 M) при 0 °C додають хлорид метансульфонілу (1,05 екв.), потім триетиламін (1,1 екв.). Реакційну суміш перемішують при 0 °C протягом 30 хв, потім протягом ночі при кімнатній температурі. Реакцію гасять додаванням розчину насиченого NH 4Cl, екстрагують етилацетатом, промивають насиченим розчином солі, сушать і випарюють. Залишок очищають хроматографією на колонці з силікагелем, елююючи EtOAc/Гексаном (від 0 до 100 %) з одержанням бажаного продукту у вигляді блідо-жовтого масла. Стадія 6: пропіл(7-азидо-4-фтор-6,7,8,9-тетрагідропіридо[1,2-a]індол-10-іл)ацетат До перемішуваного розчину пропіл{4-фтор-7-[(метилсульфоніл)окси]-6,7,8,9тетрагідропіридо[1,2-a]індол-10-іл}ацетату (1 екв.) в ДМФ (0,15 M) при 0 °C додають азид натрію (1,2 екв.). Реакційну суміш перемішують при 60 °C протягом 6 год. Реакційну суміш гасять додаванням води і NH4Cl, екстрагують EtOAc, промивають водою, насиченим розчином солі, сушать і випарюють. Залишок очищають хроматографією на колонці з силікагелем, елююючи EtOAc/Гексанами (від 0 до 50 %) з одержанням бажаного продукту у вигляді жовтого масла. Стадія 7: пропіл[7-(5-бензил-1H-1,2,3-триазол-1-іл)-4-фтор-6,7,8,9-тетрагідропіридо[1,2a]індол-10-іл]ацетат До перемішуваного розчину пропіл(7-азидо-4-фтор-6,7,8,9-тетрагідропіридо[1,2-a]індол-10іл)ацетату (1 екв.) і проп-2-ін-1-ілбензолу (1,5 екв.) в бензолі (0,3 M) при кімнатній температурі додають хлор(1,5-циклооктадієн)(пентаметилциклопентадієніл)рутеній(II) (0,1 екв.). Реакційну суміш промивають азотом, потім вистоюють при 80 °C протягом ночі, охолоджують до кімнатної температури, фільтрують через силікагель, промивають EtOAc і концентрують. Залишок очищають хроматографією на колонці з силікагелем, елююючи EtOAc/Гексаном (від 0 до 50 %) з одержанням бажаного продукту у вигляді коричневого масла. Рацемічну суміш розділяють ВЕРХ із застосуванням колонки 50×400 мм Chiralpak AD, елююючи 15 % MeOH, 15 % EtOH, 69,75 % Гексанами і 0,25 % Et3N при 50 мл/хв і 254 нм з одержанням бажаного хірального складного ефіру з часом утримування 9,6 і 11,6 хв, відповідно. Стадія 8: Два хіральні складні ефіри зі стадії 7 омилюють окремо таким чином. До перемішуваного розчину пропіл[7-(5-бензил-1Н-1,2,3-триазол-1-іл)-4-фтор-6,7,8,9-тетрагідропіридо[1,2-a]індол10-іл]ацетату (1 екв.) в ТГФ:MeOH (2:1 0,3M) при кімнатній температурі додають 1M розчин гідроксиду натрію (12 екв.). Реакційну суміш перемішують при кімнатній температурі протягом 2 год., потім гасять додаванням HCl 10 % до кислого pH і розбавляють EtOAc. Шари розділяють і водну фазу знов екстрагують EtOAc. Об'єднані органічні фракції сушать (MgSO4), фільтрують, і розчинник випарюють при зниженому тиску з одержанням бажаної хіральної кислоти 7.1 і 7.2 у 1 вигляді білої твердої речовини після спільного випаровування з ефіром/гексанами. H ЯМР (400 МГц, aцeтoн-d6) δ 7,54 (с, 1Н), 7,23-7,39 (м, 5Н), 6,98 (дт, 1Н), 6,81 (дд, 1Н), 5,15-5,22 (м, 1Н), 4,71-4,76 (м, 1Н), 4,61 (м, 1Н), 4,37 (т, 2Н), 3,68 (кв, 2Н), 3,21 (дт, 1Н), 2,94 (ддд, 1Н), 2,43 (дкв, 1Н), 2,14-2,18 (м, 1Н). МС (+ІЕР) m/z: 405,2. Приклад 8 {4-Фтор-7-[5-(4-фторбензил)-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-a]індол-10іл}оцтова кислота Вказану в заголовку сполуку одержують із застосуванням методик, описаних в Прикладі 3 з пропіл(7-азидо-4-фтор-6,7,8,9-тетрагідропіридо[1,2-a]індол-10-іл)ацетату (Приклад 7, стадія 6) і 1-фтор-4-проп-2-ін-1-ілбензолу, одержаного за наступною методикою (Gazz. Chim. Ital. 1990, 120, 783). До суміші етинілтриметилсилану (1 екв.) в ТГФ (0,6 M) при кімнатній температурі додають бромід етилмагнію (1 екв.). Суміш перемішують при кімнатній температурі протягом 30 хв, потім додають бромід міді (I) (0,1 екв.). Після перемішування протягом 30 хв. додають 1М розчин броміду 4-фторбензилу (1 екв.) в ТГФ, і суміш нагрівають до кипіння із зворотним холодильником протягом ночі. Реакційну суміш гасять додаванням холодного насиченого розчину NH4Cl, перемішують протягом 30 хв, потім екстрагують Et2O, промивають насиченим розчином солі, сушать і випарюють. Очищення комбі-флеш із застосуванням градієнта 0-100 % 18 UA 105039 C2 5 10 15 20 25 30 35 40 45 50 ЕА/Гекс дає бажаний ТМС алкін. ТМС алкін відразу змішують з фторидом калію (1,2 екв.) в ДМФ (0,2 M, містить 1 % води). Суміш перемішують при кімнатній температурі протягом ночі, потім гасять додаванням HCl 3N, перемішують протягом 1 год., потім екстрагують пентаном, промивають насиченим NaHCO3, насиченим розчином солі, сушать і випарюють. Неочищену сполуку алкіну застосовують одразу ж для клік-хімії, описаної в Прикладі 3. Одержані рацемічні складні ефіри розділяють ВЕРХ із застосуванням колонки 4,6×250 мм Chiralpak AS, елююючи 60 % EtOH, 39,75 % гексаном і 0,25 % Et3N при 0,8 мл/хв і 254 нм. Одержані хіральні складні ефіри (час утримування = 10,3 і 13,3 хв) гідролізують з одержанням Прикладу 8.1 і 8.2, 1 1 відповідно. H ЯМР Прикладу 8.1: H ЯМР (400 МГц, ДМСO-d6): δ 12,20 (с, 1Н), 7,55 (с, 1Н), 7,33 (дд, 2Н), 7,27 (д, 1Н), 7,17 (т, 2Н), 6,96 (тд, 1Н), 6,85 (дд, 1Н), 5,23-5,09 (м, 1Н), 4,58 (дд, 1Н), 4,44 (дд, 1Н), 4,25 (с, 2Н), 3,65-3,52 (м, 2Н), 3,12-3,02 (м, 1Н), 2,89 (ддд, 1Н), 2,32-2,19 (м, 1Н), 2,14-2,02 (м, 1Н). МС (+ІЕР) m/z: 423,1. Приклад 8A {(7R)-4-Фтор-7-[5-(4-фторбензил)-1H-[1,2,3]триазол-1-іл]-6,7,8,9-тетрагідропіридо[1,2-a]індол-10-іл}оцтова кислота Стадія 1: діетил 4,4-діетоксигептандіоат ("кеталь") До EtOH (27,8 л), ортоформіату триетилу (9,26 л, 55,6 моль) і 4-оксопимелату діетилу (5,93 л, 27,8 моль) додають моногідрат п-толуолсульфонової кислоти (0,053 кг, 0,278 моль), і реакційну суміш нагрівають до 77,0 °C при перемішуванні протягом 20 год. Нагрівання припиняють, і етанол видаляють дистиляцією у вакуумі, починаючи з порції при 63 °C. Оранжевий розчин кеталю, що залишився, розчиняють в толуолі (32 л) і переносять в 100-л екстрактор, в який завантажують 2 % NaHCO3 (24 л), при перемішуванні. Шари розділяють, і шар толуолу промивають водою (19,2 л), потім переносять через вбудований фільтр в 50-л круглодонну колбу, приєднану до колбонагрівача. Толуол видаляють у вакуумі, включаючи додаткове промивання (5 л) для азеотропного видалення води. Кеталь виділяють у вигляді жовтого масла. Стадія 2: 4-[(2-бром-6-фторфеніл)іміно]гептандіоат діетилу ("імін") До кеталю зі стадії 1 (8,46 кг, 24,31 моль), завантажують 2-бром-6-фторанілін (2,509 л, 22,10 моль) і оцтову кислоту (0,253 л, 4,42 моль) в азоті. Суміш нагрівають до 145 °C і етанол видаляють дистиляцією. Продукт застосовують в наступній реакції. Стадія 3: етил 3-[3-(2-етоксі-2-оксоетил)-7-фтор-1H-індол-2-іл]пропаноат ("діефір індолу") Метиловий ефір циклопропілу (МЕЦП, 27 л) дегазують протягом 20 хвилин, потім додають трис(дибензиліденацетон)дипаладій(0) (0,504 кг, 0,551 моль) і тетрафторборат три-третбутилфосфонію (0,639 кг, 2,203 моль), потім МЕЦП (3,2 л). Суміш дегазують і додають Nметилдициклогексиламін (2,336 л, 11,01 моль) при дегазації, що продовжується протягом 100 хв. Імін зі стадії 2 (8,86 кг, 22,03 моль) розчиняють в МЕЦП (28 л) при активній дегазації. Додають N-метилдициклогексиламін (7,01 л, 33,0 моль), і суміш дегазують протягом 75 хв. У безперервному потоці азоту розчин іміну переносять у вакуумі в розчин каталізатора, і всю реакційну посудину точно дегазують протягом 20 хв. МЕЦП (2,2 л) промивку, після дегазації, переносять в реакційну посудину у вакуумі. Реакційну суміш дегазують знов протягом 35 хв і нагрівають при ~108 °C протягом 18 год. Порцію промивають 2×2N HCl (18 л), 1×5 % NaHCO3 (18 л), 1×H2O (12 л). Об'єднані МЕЦП шари фільтрують через 2 вбудовані фільтри (1 звичайний, 1 вугільний), і МЕЦП видаляють до низького об'єму вакуумною дистиляцією, з одержанням темно-жовтого розчину. Толуол (12 л) завантажують і видаляють у вакуумі для вимивання додаткового МЕЦП. Додають гептан (18 л), і гетерогеннусуміш перемішують, засівають кристалами діефіру індолу і продовжують охолоджувати, але кристалізація не відбувається. Додають толуол (500 мл) і ТГФ (5 л) до повного розчинення порції; реакційний розчин охолоджують на сухій бані лід/ацетон. При -6,8 °C порція стає злегка каламутною, додають невелику кількість затравки, порція перетворюється на кристали. Охолоджування продовжують до -10 °C протягом більше 30 хвилин. При цій температурі додають гептан (30 л), зберігаючи температуру
ДивитисяДодаткова інформація
Назва патенту англійськоюIndole derivatives as crth2 peceptor antagonists
Автори англійськоюBerthelette, Carl, Boyd, Michael, Colucci, John, Villeneuve, Karine, Methot, Joey
Автори російськоюБертелетт Карл, Бойд Майкл, Колуччи Джон, Вилльнев Карин, Метот Джои
МПК / Мітки
МПК: C07D 403/04, A61K 31/4192, A61K 31/405, A61P 11/06, A61K 31/435, C07D 471/04
Мітки: crth2, рецептора, похідні, антагоністи, індолу
Код посилання
<a href="https://ua.patents.su/42-105039-pokhidni-indolu-yak-antagonisti-receptora-crth2.html" target="_blank" rel="follow" title="База патентів України">Похідні індолу як антагоністи рецептора crth2</a>
Попередній патент: Система для утворення аерозолю нікотину, одержаного з тютюну
Наступний патент: Похідні бензотіазинів, їх одержання та застосування як ліків
Випадковий патент: Спосіб відображення інформації роботи торгового агента із застосуванням електронних карт місцевості












