(піридин-4-іл)бензиламіди як алостеричні модулятори альфа-7 nachr
Номер патенту: 109803
Опубліковано: 12.10.2015
Автори: МакДональд Грегор Джеймс, Ромбутс Гірт, де Бек Бенойт Крістіан Альберт Гіслейн, Лінаертс Джозеф Елизабет
Формула / Реферат
1. Сполука, що характеризується формулою (І)
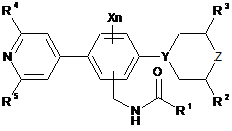 , (І)
, (І)
або її стереоізомер, де
n дорівнює 0, 1 або 2;
X являє собою фтор або хлор;
Y являє собою N або СН;
Z являє собою О або СН2;
R1 являє собою С1-8алкіл; С1-8алкіл, заміщений 1, 2 або 3 галогеновими замісниками; С3-6циклоалкіл; (С3-6циклоалкіл)С1-6алкіл; (С1-6алкілоксі)С1-6алкіл; (тригалогенС1-4алкілоксі)С1-6алкіл; тетрагідрофурил; тетрагідропіраніл; феніл або феніл, заміщений 1, 2 або 3 замісниками, вибраними з галогену, трифторметилу, трифторметокси, ціано, С1-6алкілу та С1-4алкілокси; або моноциклічний ароматичний гетероциклічний радикал, що містить щонайменше один гетероатом, вибраний з N, О і S, необов'язково заміщений 1, 2 або, якщо можливо, 3 замісниками, вибраними з галогену, С1-4алкілу, С1-4алкілокси, С3-6циклоалкілу та трифторметилу;
R2 і R3 незалежно являють собою Н, С1-4алкіл або трифторметил;
або R2 і R3 узяті разом з утворенням 1,2-етандіїлу або 1,3-пропандіїлу;
R4 і R5 незалежно являють собою Н, С1-4алкіл, трифторметил, С3-6циклоалкіл або С1-4алкілокси;
або її кислотно-адитивна сіль, або сольват.
2. Сполука за п. 1, де
R1 являє собою С1-6алкіл; С1-4алкіл, заміщений 3 фторзамісниками; С3-6циклоалкіл; (С3-6циклоалкіл)С1-2алкіл; метоксиметил; метоксіетил; тетрагідропіраніл; феніл; феніл, заміщений 1, 2 або 3 замісниками, вибраними із фтору, хлору, трифторметилу, трифторметокси, ціано, метилу та метокси; або фураніл, оксазоліл, ізоксазоліл, оксадіазоліл, піроліл, піразоліл, імідазоліл, піридиніл, піридимініл, піразиніл, піридазиніл, тієніл, 1,2,3-тіадіазоліл, тіазоліл або бензізоксазоліл, кожний з яких незаміщений або заміщений 1, 2 або, якщо можливо, 3 замісниками, вибраними з метилу, етилу, пропілу, ізопропілу, бутилу, ізобутилу, трет-бутилу, циклопропілу, метокси або трифторметилу.
3. Сполука за п. 1, де R2 являє собою водень, метил або трифторметил.
4. Сполука за п. 1, де R3 являє собою водень, метил або трифторметил.
5. Сполука за п. 1, де R4 являє собою водень або метил.
6. Сполука за п. 1, де R5 являє собою водень або метил.
7. Сполука за п. 1, де R1 являє собою метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, втор-бутил, трет-бутил, 2,2,2-трифторетил, 3,3,3-трифторпропіл, 2-метоксіетил, циклопропіл, циклобутил, циклопентил, 1-(циклопропіл)етил, (циклопропіл)метил, (циклобутил)метил, 4-фтор-2-метилфеніл, 3-мeтилізоксазол-5-іл, 3-метилізоксазол-4-іл, 5-метилізоксазол-3-іл, 2-метил-5-трифторметилоксазол-4-іл, 2-метилоксазол-4-іл.
8. Сполука за п. 1, де R2 і R3 являють собою метил або трифторметил і характеризуються цис-конфігурацією.
9. Сполука за п. 1, де R4 і R5 являють собою метил.
10. Сполука за п. 1, де сполука являє собою N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)феніл]метил]-2-метилпропанамід.
11. Фармацевтична композиція, що містить як активний інгредієнт сполуку за будь-яким з пп. 1-10.
12. Продукт, що містить
(a) сполуку формули (І) за п. 1 і
(b) агоніст a7 нікотинового рецептора, вибраний з
1,4-діазабіцикло[3.2.2]нонан-4-карбонової кислоти 4-бромфенілового складного ефіру моногідрохлориду (SSR180711А);
(-)-спіро[1-азабіцикло[2.2.2]октан-3,5'-оксазолідин]-2'-ону;
(+)-N-(1-азабіцикло[2.2.2]окт-3-ил)бензо[b]фуран-2-карбоксаміду;
3-[(2,4-диметокси)бензиліден]-анабазеїну дигідрохлориду (GTS-21);
[N-[(3R)-1-азабіцикло[2.2.2]окт-3-ил]-4-хлорбензаміду гідрохлориду] PNU-282987;
нікотину; варенікліну; А-582941; AR-R17779; ТС-1698: PHA-709829; тропісетрону; WAY-317538; МЕМ3454; EVP-6124; ТС-5619; МЕМ-63908 і AZD-0328,
як комбінований препарат для одночасного, роздільного або послідовного застосування при попередженні або лікуванні психічних розладів, розумових розладів або запальних захворювань.
13. Сполука за будь-яким з пп. 1-10 для застосування як лікарського препарату.
14. Сполука за будь-яким з пп. 1-10 для застосування при лікуванні хвороби Альцгеймера, деменції, що розвивається при хворобі дифузійних тілець Леві, синдрому гіперактивності з дефіцитом уваги, тривоги, шизофренії, манії, біполярної депресії, хвороби Паркінсона, хвороби Гентінгтона, синдрому Туретта, травми головного мозку, синдрому зміни годинних поясів, нікотинової залежності, болю; ендотоксикозу, ендотоксинового шоку, сепсису, ревматоїдного артриту, астми, розсіяного склерозу, псоріазу, уртикарії, запального захворювання кишечнику, запального захворювання жовчних проток, хвороби Крона, виразкового коліту, післяопераційного ілєусу, панкреатиту, серцевої недостатності, гострого ушкодження легенів або відторгнення алотрансплантата; когнітивного порушення при шизофренії, когнітивного порушення при хворобі Альцгеймера, комірного когнітивного порушення, хвороби Паркінсона, синдрому гіперактивності з дефіцитом уваги, виразкового коліту, панкреатиту, артриту, сепсису, післяопераційного ілєусу або гострого ушкодження легенів.
15. Спосіб одержання фармацевтичної композиції за п. 11, що передбачає етап, на якому ретельно змішують фармацевтично прийнятний носій з терапевтично ефективною кількістю сполуки за будь-яким з пп. 1-10.
Текст
Реферат: Даний винахід стосується (піридин-4-іл)бензиламідних похідних та їх фармацевтично прийнятних солей, способів їх одержання, фармацевтичних композицій, що містять їх, і їх застосування в терапії. UA 109803 C2 ДЕРЖАВНА СЛУЖБА ІНТЕЛЕКТУАЛЬНОЇ ВЛАСНОСТІ УКРАЇНИ UA 109803 C2 Даний винахід, зокрема, стосується позитивних алостеричних модуляторів нікотинових ацетилхолінових рецепторів, причому такі позитивні алостеричні модулятори мають здатність підвищувати ефективність агоністів нікотинових рецепторів. UA 109803 C2 5 10 15 20 25 30 35 40 45 50 55 60 Даний винахід відноситься до (піридин-4-іл)бензиламідів та їх фармацевтично прийнятних солей, способів їх одержання, фармацевтичних композицій, що містять їх, та до їх застосування в терапії. Даний винахід, зокрема, відноситься до алостеричних модуляторів нікотинових ацетилхолінових рецепторів, такі алостеричні модулятори мають здатність підвищувати ефективність агоністів нікотинових рецепторів. Відомий рівень техніки Алостеричні модулятори нікотинових ацетилхолінових альфа 7 рецепторів були розкриті в WO-2007/031440, WO-2007/118903, WO-2009/050186, WO-2009/050185, WO-2009/115547 і WO2009/135944. В WO-2006/096358 розкриваються азабіциклоалканові похідні як агоністи нікотинових ацетилхолінових рецепторів. Передумови винаходу Холінергічні рецептори в нормі зв'язують ендогенний нейротрансмітер ацетилхолін (ACh), тим самим запускаючи відкривання іонних каналів. Рецептори ACh у центральній нервовій системі ссавців можуть бути розділені на мускаринові (mAChR) та нікотинові (nAChR) підтипи на основі агоністичних активностей по відношенню до мускарину та нікотину, відповідно. Нікотинові ацетилхолінові рецептори представляють керовані лігандом іонні канали, що містять п'ять субодиниць. Представники сімейства генів субодиниці nAChR розділили на дві групи на основі їх амінокислотних послідовностей; при цьому одна група містить так звані альфа субодиниці, а друга група містить бета субодиниці. Було показано, що три види альфа субодиниць, альфа 7, альфа 8 і альфа 9, утворюють функціональні рецептори, якщо експресовані окремо, і передбачається, що таким чином утворюють гомоолігомерні пентамерні рецептори. Була розроблена модель алостеричного перехідного стану nAChR, яка передбачає щонайменше стан спокою, активований стан і десенситизований стан закритого каналу, процес, завдяки якому рецептори стають нечутливими до агоніста. Різні ліганди nAChR можуть стабілізувати конформаційний стан рецептора, з яким вони переважно зв'язуються. Наприклад, агоністи ACh і (-)-нікотину стабілізують, відповідно, активні та десенситизовані стани. Зміни активності нікотинових рецепторів були відзначені в ряді захворювань. Деякі з них, наприклад, міастенія гравіс і аутосомно-домінантна нічна лобова епілепсія (ADNFLE), асоційовані зі зниженнями активності нікотинової передачі або внаслідок зменшення числа рецепторів, або внаслідок підвищення десенситизації. Передбачається, що зниження числа нікотинових рецепторів опосередковує когнітивні розлади, що спостерігаються при захворюваннях, таких як хвороба Альцгеймера та шизофренія. Ефекти нікотину з тютюну також опосередковуються нікотиновими рецепторами, і оскільки дія нікотину полягає в стабілізації рецепторів у десенситизованому стані, підвищена активність нікотинових рецепторів може послабити бажання курити. Сполуки, що зв'язуються з nAChR, були запропоновані для лікування ряду захворювань, зв'язаних зі зниженням холінергічної функції, таких як дефіцит навчання, дефіцит когнітивних функцій, дефіцит уваги та втрата пам’яті. Модуляція активності 7-нікотинових рецепторів, як вважається, виявить сприятливий вплив у ряді захворювань, що включають хворобу Альцгеймера, деменцію, що розвивається при хворобі дифузійних тілець Леві, синдром гіперактивності з дефіцитом уваги, тривогу, шизофренію, манію, біполярний aфективний розлад, хворобу Паркінсона, хворобу Гентингтона, синдром Туретта, травму головного мозку або інші неврологічні, дегенеративні та психіатричні розлади, при яких відбувається втрата холінергічних синапсів, що включають синдром зміни годинних поясів, нікотинову залежність, біль. Однак лікування агоністами нікотинових рецепторів, які діють на ту саму ділянку, що і ACh, є проблематичним, оскільки ACh не тільки активує, але й блокує активність рецепторів за допомогою процесів, що включають десенситизацію та неконкурентне блокування. Крім того, тривала активація, очевидно, викликає тривалу інактивацію. Тому можна припустити, що агоністи ACh втрачають ефективність при постійному введенні. У цілому, у нікотинових рецепторів і особливо у альфа 7 нікотинового рецептора десенситизація обмежує тривалість дії використовуваного агоніста. Опис винаходу Було виявлено, що деякі нові (піридин-4-іл)бензиламіди можуть збільшувати ефективність агоністів у нікотинових ацетилхолінових рецепторів (nAChR). Сполуки, що характеризуються зазначеним типом дії (які далі називають «позитивними алостеричними модуляторами»), імовірно, придатні для лікування станів, асоційованих зі зниженнями нікотинової передачі. При терапевтичному призначенні такі сполуки можуть відновлювати нормальний міжнейронний зв'язок без впливу на тимчасовий профіль активації. Крім того, позитивні алостеричні 1 UA 109803 C2 5 10 15 модулятори, як вважається, не викликають тривалої інактивації рецепторів, як можна побачити після повторного або пролонгованого застосування агоністів. Позитивні модулятори nAChR згідно з даним винаходом придатні для лікування та профілактики психічних розладів, розумових розладів та захворювань, запальних захворювань і станів, при яких модуляція альфа 7 нікотинового рецептора виявляється сприятливою. Даний винахід відноситься до (піридин-4-іл)бензиламідів, що проявляють властивості позитивних алостеричних модуляторів, зокрема, що збільшують ефективність агоністів у альфа 7 нікотинового рецептора. Даний винахід також відноситься до способів їх одержання та фармацевтичних композицій, що містять їх. Даний винахід також відноситься до застосування цих похідних для виробництва лікарського препарату для лікування та профілактики психічних розладів, розумових розладів і захворювань, запальних захворювань і станів, при яких модуляція альфа 7 нікотинового рецептора виявляє сприятливий вплив. Даний винахід, крім того, відноситься до таких похідних для застосування при лікуванні й профілактиці психічних розладів, розумових розладів і захворювань, запальних захворювань і станів, при яких модуляція альфа 7 нікотинового рецептора виявляється сприятливою. У першому аспекті даний винахід відноситься до сполуки, що характеризується формулою (I), R4 R3 Xn N R5 20 25 30 35 40 45 50 Y O N H Z R1 R2 (I), або її стереоізомеру, де n рівняється 0, 1 або 2; X являє собою фтор або хлор; Y являє собою N або CH; Z являє собою О або CH2; 1 R являє собою C1-8алкіл; C1-8алкіл, заміщений 1, 2 або 3 галогеновими замісниками; C 3(C3-6циклоалкіл)C1-6алкіл; (C1-6алкілокси)C1-6алкіл; (тригалогенС1-4алкілокси)C16циклоалкіл; 6алкіл; тетрагідрофурил; тетрагідропіраніл; феніл; феніл, заміщений 1, 2 або 3 замісниками, вибраними з галогену, трифторметилу, трифторметоксі, ціано, C 1-6алкілу та C1-4алкілокси; або моноциклічний ароматичний гетероциклічний радикал, що містить щонайменше один гетероатом, вибраний з N, O і S, необов'язково заміщений 1, 2 або, якщо можливо, 3 замісниками, вибраними з галогену, C1-4алкілу, C1-4алкілоксі, C3-6циклоалкілу та трифторметилу; 2 3 R і R незалежно являють собою H, C1-4алкіл або трифторметил; 2 3 або R і R узяті разом з утворенням 1, 2-етандіїлу або 1, 3-пропандіїлу; 4 5 R і R незалежно являють собою H, C1-4алкіл, трифторметил, C3-6циклоалкіл або C14алкілокси; або її кислотно-адитивної солі або їх сольвату. 1 В одному варіанті здійснення R являє собою C1-6алкіл; C3-6циклоалкіл; циклопропіл, заміщений 1, 2, 3, або 4 метильними групами; (C3-6циклоалкіл)C1-2алкіл; метоксиметил; феніл, заміщений 1, 2, або 3 замісниками, вибраними із фтору, хлору, метилу, метоксі, трифторметилу, трифторметоксі, ціано та аміносульфонілу; або фураніл, оксазоліл, ізоксазоліл, оксадіазоліл, піроліл, піразоліл, імідазоліл, піридиніл, піридимініл, піразиніл, піридазиніл або бензізоксазоліл, кожний з яких незаміщений або заміщений 1, 2 або, якщо можливо, 3 замісниками, вибраними з метилу, етилу, пропілу, ізопропілу, бутилу, ізобутилу, трет-бутилу, циклопропілу, метоксі та трифторметилу. 1 В іншому варіанті здійснення R являє собою C1-6алкіл; C1-4алкіл, заміщений 3 замісниками фторами; C3-6циклоалкіл; (C3-6циклоалкіл)C1-2алкіл; метоксиметил; метоксіетил, (2,2,2трифторетокси)метил; тетрагідропіраніл; феніл або феніл, заміщений 1, 2 або 3 замісниками, вибраними із фтору, хлору, трифторметилу, трифторметоксі, ціано, метилу та метоксі; або фураніл, оксазоліл, ізоксазоліл, оксадіазоліл, піроліл, піразоліл, імідазоліл, піридиніл, піридимініл, піразиніл, піридазиніл, тієніл, 1,2,3-тіадіазоліл, тіазоліл або бензізоксазоліл, кожний з яких незаміщений або заміщений 1, 2 або, якщо можливо, 3 замісниками, вибраними з метилу, етилу, пропілу, ізопропілу, н-бутилу, ізобутилу, втор-бутилу, трет-бутилу, циклопропілу, метоксі та трифторметилу. 2 UA 109803 C2 1 5 10 15 20 25 В іншому варіанті здійснення R являє собою фураніл, оксазоліл, ізоксазоліл, піразоліл, піридиніл, піразиніл, тієніл, 1,2,3-тіадіазоліл, тіазоліл або бензізоксазоліл, кожний з яких незаміщений або заміщений 1, 2 або, якщо можливо, 3 замісниками вибраними з метилу, ізопропілу, трет-бутилу, циклопропілу, метоксі та трифторметилу. 2 В іншому варіанті здійснення R являє собою водень, метил або трифторметил. 3 В іншому варіанті здійснення R являє собою водень, метил або трифторметил. 4 В іншому варіанті здійснення R являє собою водень або метил. 5 В іншому варіанті здійснення R являє собою водень або метил. 1 В іншому варіанті здійснення R являє собою метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, втор-бутил, трет-бутил, циклопропіл, циклобутил, циклопентил, (циклопропіл)етил, (циклопропіл)метил, (циклобутил)метил, (циклогексил)метил, 3-метил-ізоксазол-5-іл, 3-метилізоксазол-4-іл, 5-метил-ізоксазол-3-іл, 2-метил-5-трифторметил-оксазол-4-іл або 2-метилоксазол-4-іл. 1 В іншому варіанті здійснення R являє собою метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, втор-бутил, трет-бутил, 2,2,2-трифторетил, 3,3,3-трифторпропіл, 2-метоксіетил, циклопропіл, циклобутил, циклопентил, 1-(циклопропіл)етил, (циклопропіл)метил, (циклобутил)метил, 4-фтор-2-метилфеніл, 3-метил-ізоксазол-5-іл, 3-метил-ізоксазол-4-іл, 5метил-ізоксазол-3-іл, 2-метил-5-трифторметил-оксазол-4-іл або 2-метил-оксазол-4-іл. 1 В іншому варіанті здійснення R являє собою ізопропіл, циклопропіл (циклопропіл)метил, (циклобутил)метил, 3-метил-4-ізоксазоліл або 5-метил-ізоксазол-3-іл. 2 3 В іншому варіанті здійснення R і R являють собою метил або трифторметил та характеризуються цис-конфігурацією. 2 3 В іншому варіанті здійснення R і R являють собою метил та характеризуються трансконфігурацією. У переважному варіанті здійснення сполука вибрана з N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)феніл]метил]циклопропанацетаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)феніл]метил]-5метил-3-ізоксазолкарбоксаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)феніл]метил]-3метил-4-ізоксазолкарбоксаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)феніл]метил]-4фтор-2-метил-бензаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)феніл]метил]-2метил-пропанаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)феніл]метил]циклопропанкарбоксаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)феніл]метил]3,3,3-трифтор-пропанаміду, N-[[3-[(2R,6S)-2,6-диметил-4-морфолініл]-6-(2,6-диметил-4-піридиніл)-2фторфеніл]метил]-циклопропанацетаміду, N-[[3-[(2R,6S)-2,6-диметил-4-морфолініл]-6-(2,6-диметил-4-піридиніл)-2фторфеніл]метил]-2-метил-пропанаміду, N-[[3-[(2R,6S)-2,6-диметил-4-морфолініл]-6-(2,6-диметил-4-піридиніл)-2фторфеніл]метил]-5-метил-3-ізоксазолкарбоксаміду, N-[[3-[(2R,6S)-2,6-диметил-4-морфолініл]-6-(2,6-диметил-4-піридиніл)-2фторфеніл]метил]-3-метил-4-ізоксазолкарбоксаміду, N-[[3-[(2R,6S)-2,6-диметил-4-морфолініл]-6-(2,6-диметил-4-піридиніл)-2фторфеніл]метил]-4-фтор-2-метил-бензаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)-3фторфеніл]метил]-циклопропанацетаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)-3фторфеніл]метил]-5-метил-3-ізоксазолкарбоксаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)-3фторфеніл]метил]-3-метил-4-ізоксазолкарбоксаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)-3фторфеніл]метил]-3,3,3-трифтор-пропанаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(4-піридиніл)феніл]метил]-2-метилпропанаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)-3 3 UA 109803 C2 фторфеніл]метил]-2-метил-пропанаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(4-піридиніл)феніл]метил]циклопропанацетаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2-метил-4-піридиніл)феніл]метил]-2метил-пропанаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2-метил-4-піридиніл)феніл]метил]-5метил-3-ізоксазолкарбоксаміду, N-[[5-[(3R,5S)-3,5-диметил-1-піперидиніл]-2-(2,6-диметил-4-піридиніл)феніл]метил]-5метил-3-ізоксазолкарбоксаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2-метил-4-піридиніл)феніл]метил]-4фтор-2-метил-бензаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(4-піридиніл)феніл]метил]-3-метил-4ізоксазолкарбоксаміду, N-[[2-(2,6-диметил-4-піридиніл)-5-(4-морфолініл)феніл]метил]циклопропанацетаміду, N-[[2-(2,6-диметил-4-піридиніл)-5-(4-морфолініл)феніл]метил]-5-метил-3ізоксазолкарбоксаміду, N-[[2-(2,6-диметил-4-піридиніл)-5-(4-морфолініл)феніл]метил]-3-метил-4ізоксазолкарбоксаміду, N-[[2-(2,6-диметил-4-піридиніл)-5-(4-морфолініл)феніл]метил]-4-фтор-2-метилбензаміду, N-[[2-(2,6-диметил-4-піридиніл)-5-(4-морфолініл)феніл]метил]-3,3,3-трифторпропанаміду, N-[[2-(2,6-диметил-4-піридиніл)-5-(4-морфолініл)феніл]метил]-2-метил-пропанаміду, N-[[2-(2,6-диметил-4-піридиніл)-5-(4-морфолініл)феніл]метил]циклопропанкарбоксаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2-метил-4-піридиніл)феніл]метил]циклопропанацетаміду, 4-фтор-2-метил-N-[[2-(2-метил-4-піридиніл)-5-(4-морфолініл)феніл]метил]-бензаміду, N-[[5-[(3R,5S)-3,5-біс(трифторметил)-1-піперидиніл]-2-(2,6-диметил-4піридиніл)феніл]метил]-3-метил-4-ізоксазолкарбоксаміду, N-[[5-[(3R,5S)-3,5-біс(трифторметил)-1-піперидиніл]-2-(2,6-диметил-4піридиніл)феніл]метил]-4-фтор-2-метил-бензаміду, N-[[5-[(3R,5S)-3,5-біс(трифторметил)-1-піперидиніл]-2-(2,6-диметил-4піридиніл)феніл]метил]-5-метил-3-ізоксазолкарбоксаміду, N-[[5-[(3R,5S)-3,5-біс(трифторметил)-1-піперидиніл]-2-(2,6-диметил-4піридиніл)феніл]метил]-циклопропанацетаміду, N-[[5-[(3R,5S)-3,5-біс(трифторметил)-1-піперидиніл]-2-(2,6-диметил-4піридиніл)феніл]метил]-2-метил-пропанаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)-3фторфеніл]метил]-альфа-метил-циклопропанацетаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)-3фторфеніл]метил]-циклопропанкарбоксаміду, N-[[2-(2,6-диметил-4-піридиніл)-5-[3-(трифторметил)-1-піперидиніл]феніл]метил]-3метил-4-ізоксазолкарбоксаміду, N-[[2-(2,6-диметил-4-піридиніл)-5-[3-(трифторметил)-1-піперидиніл]феніл]метил]-4фтор-2-метил-бензаміду, N-[[2-(2,6-диметил-4-піридиніл)-5-[3-(трифторметил)-1-піперидиніл]феніл]метил]-5метил-3-ізоксазолкарбоксаміду, N-[[2-(2,6-диметил-4-піридиніл)-5-[3-(трифторметил)-1-піперидиніл]феніл]метил]циклопропанацетаміду, N-[[2-(2,6-диметил-4-піридиніл)-5-[3-(трифторметил)-1-піперидиніл]феніл]метил]-2метил-пропанаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-[3-(трифторметил)-1піперидиніл]феніл]метил]-альфа-метил-циклопропанацетаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-[3-(трифторметил)-1піперидиніл]феніл]метил]-5-метил-3-ізоксазолкарбоксаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-[3-(трифторметил)-1піперидиніл]феніл]метил]-циклопропанацетаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-[3-(трифторметил)-1 4 UA 109803 C2 піперидиніл]феніл]метил]-2-метил-пропанаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-[3-(трифторметил)-1піперидиніл]феніл]метил]-циклопропанкарбоксаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-[3-(трифторметил)-1піперидиніл]феніл]метил]-3-метил-4-ізоксазолкарбоксаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)-3фторфеніл]метил]-циклобутанацетаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)-3фторфеніл]метил]-4,4,4-трифтор-бутанаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)-3фторфеніл]метил]-2-(2,2,2-трифторетокси)-ацетаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)-3фторфеніл]метил]-3-метил-бутанаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)-3фторфеніл]метил]-3,3-диметил-бутанаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)-3фторфеніл]метил]-циклобутанкарбоксаміду, N-[[3-[(2R,6S)-2,6-диметил-4-морфолініл]-6-(2,6-диметил-4-піридиніл)-2фторфеніл]метил]-циклопропанкарбоксаміду, N-[[3-[(2R,6S)-2,6-диметил-4-морфолініл]-6-(2,6-диметил-4-піридиніл)-2фторфеніл]метил]-3-метил-бутанаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-3-фтор-2-(2-метил-4піридиніл)феніл]метил]-циклопропанацетаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-3-фтор-2-(2-метил-4піридиніл)феніл]метил]-циклопропанкарбоксаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-3-фтор-2-(2-метил-4піридиніл)феніл]метил]-2-метил-пропанаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-3-фтор-2-(2-метил-4піридиніл)феніл]метил]-5-метил-3-ізоксазолкарбоксаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-3-фтор-2-(2-метил-4піридиніл)феніл]метил]-3-метил-4-ізоксазолкарбоксаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-3-фтор-2-(2-метил-4піридиніл)феніл]метил]-3-метил-бутанаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)-3фторфеніл]метил]тетрагідро-2H-піран-4-карбоксаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2-метил-4-піридиніл)феніл]метил]циклопропанкарбоксаміду, N-[[6-(2,6-диметил-4-піридиніл)-2-фтор-3-[(2R,6S)-тетрагідро-2,6-диметил-2H-піран-4ил]феніл]метил]-циклопропанацетаміду, N-[[6-(2,6-диметил-4-піридиніл)-2-фтор-3-[(2R)-2-(трифторметил)-4морфолініл]феніл]метил]-2-метил-пропанаміду, N-[[6-(2,6-диметил-4-піридиніл)-2-фтор-3-[(2R)-2-(трифторметил)-4морфолініл]феніл]метил]-5-метил-3-ізоксазолкарбоксаміду, N-[[6-(2,6-диметил-4-піридиніл)-2-фтор-3-[(2R)-2-(трифторметил)-4морфолініл]феніл]метил]-3-метил-4-ізоксазолкарбоксаміду, N-[[6-(2,6-диметил-4-піридиніл)-2-фтор-3-[(2R)-2-(трифторметил)-4морфолініл]феніл]метил]-циклопропанацетаміду, N-[[6-(2,6-диметил-4-піридиніл)-2-фтор-3-(тетрагідро-2,6-диметил-2H-піран-4іл)феніл]метил]-циклобутанацетаміду, N-[[6-(2,6-диметил-4-піридиніл)-2-фтор-3-(тетрагідро-2,6-диметил-2H-піран-4іл)феніл]метил]-2-метил-пропанаміду, N-[[6-(2,6-диметил-4-піридиніл)-2-фтор-3-(тетрагідро-2,6-диметил-2H-піран-4іл)феніл]метил]-5-метил-3-ізоксазолкарбоксаміду, N-[[6-(2,6-диметил-4-піридиніл)-2-фтор-3-(тетрагідро-2,6-диметил-2H-піран-4іл)феніл]метил]-3-метил-4-ізоксазолкарбоксаміду, N-[[6-(2,6-диметил-4-піридиніл)-2-фтор-3-[(2R,6S)-тетрагідро-2,6-диметил-2H-піран-4ил]феніл]метил]-циклопропанкарбоксаміду, N-[[6-(2,6-диметил-4-піридиніл)-2-фтор-3-[(2S)-2-(трифторметил)-4морфолініл]феніл]метил]-циклопропанацетаміду, N-[[6-(2,6-диметил-4-піридиніл)-2-фтор-3-[(2R)-2-(трифторметил)-4 5 UA 109803 C2 морфолініл]феніл]метил]-циклобутанацетаміду, N-[[6-(2,6-диметил-4-піридиніл)-2-фтор-3-[(2R)-2-(трифторметил)-4морфолініл]феніл]метил]-3-метил-бутанаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-[(2R)-2-(трифторметил)-4морфолініл]феніл]метил]-2-метил-пропанаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-[(2R)-2-(трифторметил)-4морфолініл]феніл]метил]-5-метил-3-ізоксазолкарбоксаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-[(2R)-2-(трифторметил)-4морфолініл]феніл]метил]-3-метил-бутанаміду, N-[[6-(2,6-диметил-4-піридиніл)-2-фтор-3-[(2R,6S)-тетрагідро-2,6-диметил-2H-піран-4ил]феніл]метил]-3-метил-бутанаміду, N-[[6-(2,6-диметил-4-піридиніл)-2-фтор-3-[(2S)-2-(трифторметил)-4морфолініл]феніл]метил]-2-метил-пропанаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-[(2R)-2-(трифторметил)-4морфолініл]феніл]метил]-циклопропанкарбоксаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-[(2R)-2-(трифторметил)-4морфолініл]феніл]метил]-3-метил-4-ізоксазолкарбоксаміду, N-[[6-(2,6-диметил-4-піридиніл)-2-фтор-3-[(2R)-2-(трифторметил)-4морфолініл]феніл]метил]-циклопропанкарбоксаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2-метил-4-піридиніл)феніл]метил]-3метил-4-ізоксазолкарбоксаміду 1,7 HCl, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-[(2R)-2-(трифторметил)-4морфолініл]феніл]метил]-циклопропанацетаміду, N-[[6-(2,6-диметил-4-піридиніл)-2-фтор-3-[(2S)-2-(трифторметил)-4морфолініл]феніл]метил]-3-метил-4-ізоксазолкарбоксаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)-4фторфеніл]метил]-циклопропанкарбоксаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)-4фторфеніл]метил]-циклопропанацетаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)-4фторфеніл]метил]-5-метил-3-ізоксазолкарбоксаміду, N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)-4фторфеніл]метил]-2-метил-пропанаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-[(2S)-2-(трифторметил)-4морфолініл]феніл]метил]-циклобутанацетаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-(2-метил-4-морфолініл)феніл]метил]циклобутанацетаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-(2-метил-4-морфолініл)феніл]метил]-3метил-4-ізоксазолкарбоксаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-[(2S)-2-(трифторметил)-4морфолініл]феніл]метил]-3-метил-4-ізоксазолкарбоксаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-[(2S)-2-(трифторметил)-4морфолініл]феніл]метил]-5-метил-3-ізоксазолкарбоксаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-(2-метил-4-морфолініл)феніл]метил]-5метил-3-ізоксазолкарбоксаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-(2-метил-4-морфолініл)феніл]метил]-2метил-пропанаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-[(2S)-2-(трифторметил)-4морфолініл]феніл]метил]-2-метил-пропанаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-(2-метил-4-морфолініл)феніл]метил]циклопропанацетаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-[(2S)-2-(трифторметил)-4морфолініл]феніл]метил]-циклопропанацетаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-(2-метил-4-морфолініл)феніл]метил]циклопропанкарбоксаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-[(2S)-2-(трифторметил)-4морфолініл]феніл]метил]-циклопропанкарбоксаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-(2-метил-4-морфолініл)феніл]метил]-3метил-бутанаміду, N-[[2-(2,6-диметил-4-піридиніл)-3-фтор-5-[(2S)-2-(трифторметил)-4 6 UA 109803 C2 морфолініл]феніл]метил]-3-метил-бутанаміду, N-[[3-[(2R,6S)-2,6-диметил-4-морфолініл]-6-(2,6-диметил-4-піридиніл)-2,5дифторфеніл]метил]-циклопропанкарбоксаміду, N-[[3-[(2R,6S)-2,6-диметил-4-морфолініл]-6-(2,6-диметил-4-піридиніл)-2,5дифторфеніл]метил]-5-метил-3-ізоксазолкарбоксаміду, N-[[3-[(2R,6S)-2,6-диметил-4-морфолініл]-6-(2,6-диметил-4-піридиніл)-2,5дифторфеніл]метил]-циклопропанацетаміду, N-[[3-[(2R,6S)-2,6-диметил-4-морфолініл]-6-(2,6-диметил-4-піридиніл)-2фторфеніл]метил]-5,5,5-трифтор-пентанаміду, N-[[3-[(2R,6S)-2,6-диметил-4-морфолініл]-6-(2,6-диметил-4-піридиніл)-2фторфеніл]метил]-циклобутанацетаміду, N-[[3-[(2R,6S)-2,6-диметил-4-морфолініл]-6-(2,6-диметил-4-піридиніл)-2фторфеніл]метил]-циклогексанкарбоксаміду, N-[[3-[(2R,6S)-2,6-диметил-4-морфолініл]-6-(2,6-диметил-4-піридиніл)-2фторфеніл]метил]-3-метокси-пропанаміду, N-[[3-[(2R,6S)-2,6-диметил-4-морфолініл]-6-(2,6-диметил-4-піридиніл)-2фторфеніл]метил]-3,3-диметил-бутанаміду, N-[[3-[(2R,6S)-2,6-диметил-4-морфолініл]-6-(2,6-диметил-4-піридиніл)-2фторфеніл]метил]-циклобутанкарбоксаміду, N-[[3-[(2R,6S)-2,6-диметил-4-морфолініл]-6-(2,6-диметил-4-піридиніл)-2фторфеніл]метил]-альфа-метил-циклопропанацетаміду, 4,6-дихлор-N-[[3-[(2R,6S)-2,6-диметил-4-морфолініл]-6-(2,6-диметил-4-піридиніл)-2фторфеніл]метил]-3-піридинкарбоксаміду, 3-хлор-N-[[3-[(2R,6S)-2,6-диметил-4-морфолініл]-6-(2,6-диметил-4-піридиніл)-2фторфеніл]метил]-2-фтор-бензаміду, N-[[6-(2,6-диметил-4-піридиніл)-2-фтор-3-[(2S)-2-(трифторметил)-4морфолініл]феніл]метил]-5-метил-3-ізоксазолкарбоксаміду, N-[[6-(2,6-диметил-4-піридиніл)-2-фтор-3-[(2S)-2-(трифторметил)-4морфолініл]феніл]метил]-3-метил-бутанаміду, N-[[6-(2,6-диметил-4-піридиніл)-2-фтор-3-[(2S)-2-(трифторметил)-4морфолініл]феніл]метил]-циклопропанкарбоксаміду, N-[[6-(2,6-диметил-4-піридиніл)-2-фтор-3-[(2S)-2-(трифторметил)-4морфолініл]феніл]метил]-циклобутанацетаміду, N-[[3-хлор-5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4піридиніл)феніл]метил]-2-метил-пропанаміду, N-[[3-хлор-5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4піридиніл)феніл]метил]-циклопропанацетаміду, N-[[3-хлор-5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4піридиніл)феніл]метил]-5-метил-3-ізоксазолкарбоксаміду, N-[[2-[(2R,6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)феніл]метил]циклопропанацетаміду, N-[[2-[(2R,6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)феніл]метил]-5метил-3-ізоксазолкарбоксаміду, N-[[2-[(2R,6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)феніл]метил]-2метил-пропанаміду, N-[[2-[(2R,6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)феніл]метил]-4фтор-2-метил-бензаміду, N-[[2-[(2R,6S)-2,6-диметил-4-морфолініл]-5-(2,6-диметил-4-піридиніл)феніл]метил]-3метил-4-ізоксазолкарбоксаміду, N-[[2-(2,6-диметил-4-піридиніл)-5-(8-окса-3-азабицикло[3.2.1]окт-3-ил)феніл]метил]2-метил-пропанаміду, N-[[2-(2,6-диметил-4-піридиніл)-5-(8-окса-3-азабицикло[3.2.1]окт-3-ил)феніл]метил]циклопропанацетаміду, N-[[2-(2,6-диметил-4-піридиніл)-5-(8-окса-3-азабицикло[3.2.1]окт-3-ил)феніл]метил]циклопропанкарбоксаміду, 2-метил-N-[[2-(2-метил-4-піридиніл)-5-(4-морфолініл)феніл]метил]-пропанаміду, N-[[2-(2-метил-4-піридиніл)-5-(4-морфолініл)феніл]метил]-циклопропанацетаміду, 5-метил-N-[[2-(2-метил-4-піридиніл)-5-(4-морфолініл)феніл]метил]-3ізоксазолкарбоксаміду, 3-метил-N-[[2-(2-метил-4-піридиніл)-5-(4-морфолініл)феніл]метил]-4 7 UA 109803 C2 5 10 15 20 25 30 35 40 45 50 55 ізоксазолкарбоксаміду. Конкретною сполукою є N-[[5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4піридиніл)феніл]метил]-2-метил-пропанамід. Передбачається, що всі можливі комбінації вищезгаданих варіантів здійснення, що представляють інтерес, попадають в об'єм даного винаходу. При описі сполук згідно з даним винаходом використовувані терміни пояснюються згідно з наступними визначеннями, якщо в контексті не вказується інше. Термін «галоген» як група або частина групи є загальним для фтору, хлору, брому, йоду, якщо в контексті явно не зазначене інше. Термін «C1-8алкіл» як група або частина групи означає гідрокарбільний радикал формули CnH2n+1, де n є числом, що варіює від 1 до 8. C1-8алкільні групи містять від 1 до 8 атомів вуглецю, переважно від 1 до 6 атомів вуглецю, більш переважно від 1 до 4 атомів вуглецю, ще більш переважно 1-2 атомів вуглецю. Алкільні групи можуть бути лінійними або розгалуженими, а також можуть бути заміщеними, як зазначено в даному документі. Якщо в даному документі після атома вуглецю використовується нижній індекс, то нижній індекс означає число атомів вуглецю, яке згадана група може містити. Таким чином, наприклад, C 1-8алкіл включає всі лінійні або розгалужені алкільні групи з 1-8 атомами вуглецю та, таким чином, включає, наприклад, метил, етил, н-пропіл, ізопропіл, бутил і його ізомери (наприклад, н-бутил, ізобутил і третбутил), пентил, гексил, гептил, октил та їх ізомери. Термін «C1-4алкіл» як група або частина групи означає гідрокарбільний радикал формули CnH2n+1, де n є числом, що варіює від 1 до 4. C1-4алкільні групи містять від 1 до 4 атомів вуглецю, переважно від 1 до 3 атомів вуглецю, більш переважно 1-2 атома вуглецю. C1-4алкіл включає всі лінійні або розгалужені алкільні групи з 1-4 атомами вуглецю та, таким чином, включає, наприклад, метил, етил, н-пропіл, ізопропіл, бутил і його ізомери, наприклад, н-бутил, ізобутил, втор-бутил і трет-бутил. Термін «C1-6алкілокси» як група або частина групи означає радикал, що характеризується a a формулою -OR , де R являє собою C1-6алкіл. Необмежувальні приклади прийнятних алкілоксі включають метилоксі, етилоксі, пропілоксі, ізопропілоксі, бутилоксі, ізобутилоксі, втор-бутилоксі, трет-бутилоксі, пентилоксі та гексилоксі. Термін «C1-4алкілокси» як група або частина групи означає радикал, що характеризується b b формулою -OR , де R являє собою C1-4алкіл. Необмежувальні приклади прийнятних C14алкілоксі включають метилоксі (також метоксі), етилоксі (також етоксі), пропілоксі, ізопропілоксі, бутилоксі, ізобутилоксі, втор-бутилоксі та трет-бутилоксі. Термін «галогенC1-4алкілокси» як група або частина групи означає радикал C1-4алкілоксі, де зазначень радикал C1-4алкілоксі далі заміщений 1, 2 або 3 атомами галогену. Необмежувальні приклади прийнятних радикалів галогенC1-4алкілоксі включають трифторметилоксі, трифторетилоксі, трифторпропілоксі та трифторбутилоксі. Термін «C3-6циклоалкіл» окремо або в комбінації означає циклічний насичений вуглеводневий радикал з 3-6 атомами вуглецю. Необмежувальні приклади прийнятного циклоC3-6алкілу включають циклопропіл, циклобутил, циклопентил і циклогексил. Вище та нижче термін «сполука формули (I)» припускає включення його адитивних солей, сольватів та стереоізомерів. Терміни «стереоізомери» або «стереохімічно ізомерні форми» вище або нижче застосовуються взаємозамінно. Даний винахід включає всі стереоізомери сполуки формули (I) або у вигляді чистого стереоізомера, або у вигляді суміші двох або більше стереоізомерів. Енантіомери являють собою стереоізомери, які є незбіжними при накладенні дзеркальними відображеннями один одного. Суміш 1:1 пари енантіомерів являє собою рацемат або рацемічну суміш. Діастереомери (або діастереоізомери) являють собою стереоізомери, які не є енантіомерами, тобто вони не є дзеркальними відображеннями один одного. Якщо сполука містить подвійний зв'язок, заступники можуть бути в E- або Z-конфігурації. Якщо сполука містить двохзаміщену циклоалкільну групу, заступники можуть бути в цис- або транс-конфігурації. Тому даний винахід включає енантіомери, діастереомери, рацемати, E-ізомери, Z-ізомери, цисізомери, транс-ізомери та їх суміші. Абсолютна конфігурація визначається згідно із системою Кана-Інгольда-Прелога. Конфігурація при асиметричному атомі визначається або як R, або як S. Аналізовані сполуки, абсолютна конфігурація яких невідома, можуть бути позначені як (+) або (-) залежно від напрямку, в якому вони обертають площину поляризованого світла. Якщо ідентифікується певний стереоізомер, це означає, що зазначений стереоізомер практично не містить, тобто зв’язаний з менш 50%, переважно менш 20%, більш переважно 8 UA 109803 C2 5 10 15 20 25 30 35 менш 10%, ще більш переважно менш 5%, зокрема менш 2% і найбільше переважно менш 1% інших ізомерів. Таким чином, якщо сполука формули (I) визначається, наприклад, як (R), це означає, що сполука практично не містить (S) ізомер; якщо сполука формули (I) визначається, наприклад, як E, це означає, що сполука практично не містить Z-ізомер; якщо сполука формули (I) визначається, наприклад, як цис, це означає, що сполука практично не містить транс-ізомер. Солями сполук формули (I) для терапевтичного застосування є такі, у яких протиіон є фармацевтично прийнятним. Однак солі кислот та основ, які не є фармацевтично прийнятними, також можуть знайти застосування, наприклад, в одержанні або очищенні фармацевтично прийнятної сполуки. Усі солі, що являються або не являються фармацевтично прийнятними, включені в об’єм даного винаходу. Вищезгадані та нижчезгадані фармацевтично прийнятні кислотно- і основно-адитивні солі містять терапевтично активні нетоксичні форми кислотно- і основно-адитивних солей, які можуть утворювати сполуки формули (I). Фармацевтично прийнятні кислотно-адитивні солі можна легко одержати обробкою форми основи цією відповідною кислотою. Відповідні кислоти включають, наприклад, неорганічні кислоти, такі як галогенводневі кислоти, наприклад, хлористоводнева або бромистоводнева кислота, сірчана, азотна, фосфорна та подібні кислоти; або органічні кислоти такі як, наприклад, оцтова, пропанова, гідроксіоцтова, молочна, піровіноградна, щавлева (тобто етандіова), малонова, бурштинова (тобто бутандіова кислота), малеїнова, фумарова, яблучна, винна, лимонна, метансульфонова, етансульфонова, бензолсульфонова, п-толуолсульфонова, цикламова, саліцилова, п-аміносаліцилова, памоєва та подібні кислоти. У свою чергу форми зазначених солей можуть бути перетворені обробкою відповідною основою у форму вільної основи. Термін «сольвати» означає гідрати та алкоголяти, які можуть утворювати сполуки формули (I), а також їх солі. Хімічні назви сполук згідно з даним винаходом були отримані згідно із правилами номенклатури, прийнятими Хімічної реферативною службою з використанням номенклатурного програмного забезпечення Advanced Chemical Development, Inc., (ACD/Name версія продукту 10.01; Build 15494, 1 Dec 2006). Деякі зі сполук формули (I) також можуть існувати у своїй таутомерній формі. Такі форми, хоча чітко не зазначені у вищенаведеній формулі, призначені для включення в об'єм даного винаходу. Одержання сполук Залежно від положення ациламінометиленової групи на фенільному фрагменті, і від того, чи представляє Y N або CH, можуть бути виділені три підгрупи формул (Ia), (Ib) і (Ic), для синтезу кожної з яких існує власна методика. R4 R2 Xn N N Z R5 HN O R1 R4 (Ia) R3 R2 Xn N N Z (Ib) R 5 O R 3 NH R1 9 UA 109803 C2 R4 R2 Xn N Z (Ic) R 5 HN R 3 O R1 Сполуки формули (Ia) можуть бути отримані реагуванням сполуки формули (II), R4 R2 Xn N 5 10 N Z R5 H2N R3 (II), 2 3 4 5 1 1 де R , R , R , R , Z і Xn визначені формулою (I), зі сполукою формули R -CO2H (III), де R визначений формулою (I), у присутності прийнятного амідного зв’язувального реагенту, такого як HBTU, прийнятної основи, такої як DIPEA, у прийнятному розчиннику, такому як DCM, і при прийнятній температурі, такій як кімнатна температура. У якості альтернативи, реакція ацилювання (II) може бути проведена із симетричним або асиметричним ангідридом або ацилгалогенідом карбонової кислоти (III). Сполуки формули (II) можуть бути отримані реагуванням сполуки формули (IV), R4 R2 Xn N N Z R5 15 R3 N (IV), 2 3 4 5 де R , R , R , R , Z і Xn визначені формулою (I), із прийнятним відновним засобом, таким як водень, у присутності прийнятного каталізатора, такого як нікель Ренея, у прийнятному розчиннику, такому як 7 M аміаку в метанолі, при прийнятній температурі, такій як кімнатна температура. Сполуки формули (IV) можуть бути отримані реагуванням сполуки формули (V), R2 Xn Hal1 N Z R3 20 25 N (V), 2 3 1 де R , R , Z і Xn визначені формулою (I), і Hal являє собою атом галогену, такого як йод, бром або хлор, зі сполукою формули (VI), R4 O N B O R5 (VI), 4 5 де R і R визначені формулою (I), у присутності прийнятного каталізатора, такого як Pd(PPh3)4, із прийнятною основою, такою як карбонат натрію, у прийнятному розчиннику, такому як 1,4-діоксан та етанол/вода (1:1), і при прийнятній температурі, такій як 120 °C, у закупореній пробірці, у прийнятній інертній атмосфері, такій як атмосфера азоту. Сполуки формули (V) можуть бути отримані реагуванням сполуки формули (VII), 10 UA 109803 C2 Xn Hal2 Hal1 N (VII), 1 2 де Hal і Xn визначені формулою (V), а Hal являє собою атом галогену, такий як фтор, зі сполукою формули (VIII), R2 H N R3 5 10 Z (VIII), 2 3 де R , R і Z визначені формулою (I), у присутності прийнятної основи, такої як карбонат калію, у прийнятному розчиннику, такому як DMSO, при прийнятній температурі, такій як 100 °C. У якості альтернативи, сполуки формули (V) можуть бути отримані реагуванням сполуки формули (IX), R2 Xn N Z R3 15 N (IX), 2 3 де R , R , Z і Xn визначені формулою (V), із прийнятною основою, такою як 1 тетраметилпіперидид літію, і галогеном (Hal )2, таким як йод, у прийнятному розчиннику, такому як THF, при прийнятній температурі, такій як -78 °C, і в прийнятній інертній атмосфері, такій як атмосфера азоту. Сполуки формули (IX) можуть бути отримані реагуванням сполуки формули (X), Xn Hal3 20 25 N (X), 3 де Xn визначений формулою (IX), і Hal являє собою атом галогену, такий як бром, зі сполукою формули (VIII) у присутності прийнятного каталізатора, такого як Pd 2(dba)3 або каталізатор Nolan [478980-01-7], прийнятного ліганда, такого як ксантфос, і прийнятної основи, такої як трет-бутанолат натрію, у прийнятному розчиннику, такому як толуол або моноглім, при прийнятній температурі, такій як 120 °C, у закупореній пробірці та у прийнятній інертній атмосфері, такій як атмосфера азоту. У якості альтернативи, сполуки формули (IV) можуть бути отримані реагуванням сполуки формули (XI), R4 Xn N Hal4 R5 30 N (XI), 4 5 4 де R , R і Xn визначені формулою (I), і Hal являє собою атом галогену, такий як хлор або бром, зі сполукою формули (VIII) у присутності прийнятного каталізатора, такого як Pd 2(dba)3 або каталізатор Nolan [478980-01-7], прийнятного ліганда, такого як ксантфос, і прийнятної основи, такої як трет-бутанолат натрію, у прийнятному розчиннику, такому як толуол або 11 UA 109803 C2 моноглім, при прийнятній температурі, такій як 120 °C, у закупореній пробірці та у прийнятній інертній атмосфері, такій як атмосфера азоту. Сполуки формули (XI) можуть бути отримані реагуванням сполуки формули (XII), Xn Hal4 Hal5 5 10 N (XII), 4 5 де Hal і Xn визначені формулою (XI), і Hal являє собою атом галогену, такий як бром або йод, зі сполукою формули (VI) у присутності прийнятного каталізатора, такого як Pd(PPh 3)4, із прийнятною основою, такою як карбонат натрію або карбонат калію, у прийнятному розчиннику, такому як 1,4-діоксан або диметоксіетан і вода, та при прийнятній температурі, такій як 100 °C, у закупореній пробірці та у прийнятній інертній атмосфері, такій як атмосфера азоту. У якості альтернативи, сполуки формули (IV) можуть бути отримані реагуванням сполуки формули (XIII), R4 R2 Xn N 15 20 N R5 Hal6 R3 (XIII), 2 3 4 5 6 де R , R , R , R , Z і Xn визначені формулою (I), і Hal являє собою атом галогену, такий як бром, з прийнятною ціанідною сіллю, такою як ціанід цинку, у присутності прийнятного каталізатора, такого як Pd(PPh3)4, і в присутності прийнятного ліганда, такого як трифенілфосфін, у прийнятному розчиннику, такому як ацетонітрил, і при прийнятній температурі, такій як 150 °C, у закупореній пробірці та у прийнятній інертній атмосфері, такій як атмосфера азоту. Сполуки формули (XIII) можуть бути отримані реагуванням сполуки формули (XIV), R4 Xn Hal7 N 25 Z R5 Hal6 (XIV), 4 5 6 7 де R , R , Xn і Hal визначені формулою (XIII), і Hal являє собою атом галогену, такий як бром, зі сполукою формули (VIII) у присутності прийнятного каталізатора, такого як Pd 2(dba)3, прийнятного ліганда, такого як ксантфос, і прийнятної основи, такої як трет-бутанолат натрію, у прийнятному розчиннику, такому як толуол, при прийнятній температурі, такій як 120 °C, у закупореній пробірці та у прийнятній інертній атмосфері, такій як атмосфера азоту. Сполуки формули (XIV) можуть бути отримані реагуванням сполуки формули (XV), Xn 7 Hal8 Hal Hal6 30 35 (XV), 6 7 8 де Xn, Hal і Hal визначені формулою (XIV), а Hal являє собою атом галогену, такий як йод, зі сполукою формули (VI) у присутності прийнятного каталізатора, такого як Pd(PPh 3)4, у присутності прийнятної основи, такої як карбонат калію, у прийнятному розчиннику, такому як диметоксіетан, і при прийнятній температурі, такій як 100 °C, у закупореній пробірці та у прийнятної інертній атмосфері, такій як атмосфера азоту. Сполуки формули (Ib) можуть бути отримані реагуванням сполуки формули (XVI), 12 UA 109803 C2 R4 R2 Xn N N Z R5 R3 H2N 5 (XVI), 2 3 4 5 де R , R , R , R , Z і Xn визначені формулою (Ib), зі сполукою формули (III) у присутності прийнятного амідного зв’язувального реагенту, такого як HBTU, прийнятної основи, такої як DIPEA, у прийнятному розчиннику, такому як DCM, і при прийнятній температурі, такій як кімнатна температура. У якості альтернативи, реакція ацилювання (XVI) може бути проведена із симетричним або aсиметричним ангідридом або ацилгалогенідом карбонової кислоти (III). Сполуки формули (XVI) можуть бути отримані реагуванням сполуки формули (XVII), R4 R2 Xn N N Z R5 10 15 R3 N (XVII), 2 3 4 5 де R , R , R , R , Z і Xn визначені формулою (Ib), із прийнятним засобом, що відновлює, таким як водень, у присутності прийнятного каталізатора, такого як нікель Ренея, у прийнятному розчиннику, такому як 7 M аміаку в метанолі, при прийнятній температурі, такій як кімнатна температура. Сполуки формули (XVII) можуть бути отримані реагуванням сполуки формули (XVIII), R2 Xn Hal9 N Z R3 20 N (XVIII), 2 3 9 де R , R , Z і Xn визначені формулою (Ib), і Hal являє собою атом галогену, такий як хлор, зі сполукою формули (VI), у присутності прийнятного каталізатора, такого як Pd(PPh 3)4 або PdCl2(dppf), із прийнятною основою, такою як карбонат натрію, у прийнятному розчиннику, такому як суміш діоксану, етанолу та води, або ацетонітрил, при прийнятній температурі, такій як 130 °C, у закупореній пробірці та у прийнятній інертній атмосфері, такій як атмосфера азоту. Сполуки формули (XVIII) можуть бути отримані реагуванням сполуки формули (XIX), Xn Hal9 25 30 Hal10 N (XIX), 9 10 де Hal і Xn визначені формулою (XVIII), і Hal являє собою атом галогену, такий як бром, зі сполукою формули (VIII) у присутності прийнятного каталізатора, такого як Pd 2(dba)3, у присутності прийнятного ліганда, такого як ксантфос, із прийнятною основою, такою як карбонат цезію, у прийнятному розчиннику, такому як діоксан, при прийнятній температурі, такій як 145 °C, у закупореній пробірці та у прийнятній інертній атмосфері, такій як атмосфера азоту. Сполуки формули (Ic) можуть бути отримані реагуванням сполуки формули (XX), 13 UA 109803 C2 R4 R2 Xn N 5 10 Z R5 H2N R3 (XX), 2 3 4 5 де R , R , R , R , Z і Xn визначені формулою (I), зі сполукою формули (III), 1 R -CO2H (III), 1 де R визначений формулою (I), у присутності прийнятного амідного зв’язувального реагенту, такого як HBTU, у прийнятній основі, такій як DIPEA, у прийнятному розчиннику, такому як DCM, і при прийнятній температурі, такій як кімнатна температура. У якості альтернативи, реакція ацилювання (XX) може бути проведена із симетричним або aсиметричним ангідридом або ацилгалогенідом карбонової кислоти (III). Сполуки формули (XX) можуть бути отримані реагуванням сполуки формули (XXI), R4 R2 Xn N 15 Z R5 H2N R3 (XXI), 2 3 4 5 де R , R , R , R , Z і Xn визначені формулою (I), із прийнятним засобом, що відновлює, таким як водень, у присутності прийнятного каталізатора, такого як платина на вугіллі, у прийнятному розчиннику, такому як THF, при прийнятній температурі, такій як 50 °C. Сполуки формули (XXI) можуть бути отримані реагуванням сполуки формули (XXII), R4 R2 Xn N R5 20 25 30 Z R3 N (XXII), 2 3 4 5 де R , R , R , R , Z і Xn визначені формулою (I), із прийнятним засобом, що відновлює, таким як водень, у присутності прийнятного каталізатора, такого як нікель Ренея, у прийнятному розчиннику, такому як 7 M аміаку в метанолі, при прийнятній температурі, такій як кімнатна температура. Сполуки формули (XXII) можуть бути отримані реагуванням сполуки формули (XXIII), R2 R6 O B Z R6 O R3 (XXIII), 2 3 6 6 де R , R і Z визначені формулою (I), і R являє собою C1-6алкіл, або обидва R разом утворюють C2-8алкандіїл, зі сполукою формули (XI) у присутності прийнятного каталізатора, такого як Pd(PPh3)4, із прийнятною основою, такою як карбонат калію, у прийнятному розчиннику, такому як диметоксіетан, при прийнятній температурі, такій як 100 °C, в прийнятній інертній атмосфері, такій як атмосфера азоту. Сполуки формули (XXIII) можуть бути отримані реагуванням сполуки формули (XXIV), F3C (CF2)3 R2 S O O O Z R3 (XXIV), 14 UA 109803 C2 2 5 3 де R , R і Z визначені формулою (I), із прийнятним похідним бору, таким як біс(пінаколато)дибор, у присутності прийнятного каталізатора, такого як PdСl 2(dppf), у присутності прийнятного ліганда, такого як dppf, із прийнятною основою, такою як ацетат калію, у прийнятному розчиннику, такому як диметоксіетан, при прийнятній температурі, такій як 80 °C, у прийнятній інертній атмосфері, такій як атмосфера азоту. Сполуки формули (XXIV) можуть бути отримані реагуванням сполуки формули (XXV), R2 O Z R3 10 15 20 25 30 35 40 45 50 55 (XXV), 2 3 де R , R і Z визначені формулою (I), із прийнятною основою, такою як LDA, і із прийнятним сульфонілувальним засобом, таким як перфторбутансульфонілфторид, у прийнятному розчиннику, такому як THF, при прийнятній температурі, такій як -78 °C, у прийнятній інертній атмосфері, такій як атмосфера азоту. Фармакологія Було виявлено, що сполуки згідно з даним винаходом є позитивними алостеричними модуляторами альфа 7 нікотинового рецептора. Альфа 7 нікотиновий рецептор (альфа 7 nAChR) належить до надсімейства цис-петельних, іонотропних керованих лігандом іонних каналів, які включають сімейства рецепторів 5-HT3, GABAA і сімейство гліцинового рецептора. Він активується ацетилхоліном і його продуктом деградації холіном, та головною особливістю альфа 7 nAChR є його швидка десенсибілізація в постійній присутності агоніста. Він є другим найбільш широким підтипом нікотинових рецепторів у головному мозку, а також є важливим регулятором вивільнення багатьох нейротрансмітерів. Він характеризується дискретним розподілом у деяких структурах головного мозку, що мають відношення до процесів уваги та когнітивних процесів, таких як гіпокамп і префронтальна кора, та залучається до ряду психіатричних і неврологічних розладів у людей. Він також залучається до холінергічного запального шляху. Генетичний доказ його зв'язку із шизофренією проявляється у формі міцного зв'язку між маркером шизофренії (дефіцитом фільтрації сенсорної інформації) і локусом альфа 7 на 15q13-14 і поліморфізмів у коровій промоторній області гена альфа 7. Патологічні дані вказують на втрату альфа 7 імунореактивності та зв'язування α-бунгаротоксину (Btx) у гіпокампі, лобній і передній поясній корі головного мозку хворих шизофренією, при хворобі Паркінсона та хворобі Альцгеймера, а також у паравентрикулярному ядрі та в nucleus reuniens при аутизмі. Фармакологічні дані, такі як відмічена звичка до паління хворих шизофренією в порівнянні з нормою, були інтерпретовані як спроба пацієнтів займатися самолікуванням, щоб компенсувати дефіцит альфа 7 нікотинергічної передачі. Тимчасова нормалізація дефектів фільтрації сенсорної інформації (преімпульсне інгібування, PPI) і на тваринних моделях, і у людини при введенні нікотину та тимчасове відновлення нормальної фільтрації сенсорної інформації у хворих шизофренією, коли холінергічна активність переднього мозку низька (наприклад, 2 етап сну), були інтерпретовані як результат тимчасової активації альфа 7 нікотинового рецептора з наступною десенсибілізацією. Таким чином, є підстави вважати, що активація альфа 7 nAChR буде виявляти терапевтично сприятливий вплив на ряд розладів CNS (психіатричних і неврологічних). Як уже згадувалося, альфа 7 nAChR легко десенсибілізує у постійній присутності природного трансмітерного ацетилхоліну, а також екзогенних лігандів, таких як нікотин. У десенсибілізованому стані рецептор залишається зв'язаним з лігандом, але функціонально неактивним. Це не є проблемою для природних трансмітерів, таких як ацетилхолін і холін, оскільки вони є субстратами для дуже потужних механізмів руйнування (ацетилхолінестераза) і кліренсу (холіновий транспортер). Ці трансмітерні механізми руйнування/кліренсу, імовірно, підтримують баланс між активованими та десенсибілізованому альфа 7 nAChR у фізіологічно прийнятному діапазоні. Однак синтетичні агоністи, які не є субстратами для природних механізмів руйнування та кліренсу, як виявлено, мають потенційну здатність як до надстимуляції, так і до зсуву популяційної рівноваги альфа 7 nAChR убік цілеспрямовано десенсибілізованого стану, що небажано при розладах, при яких відіграє роль недостатність експресії або функції альфа 7 nAChR. Агоністи по своїй природі повинні бути спрямовані на «кишеню», що зв’язує ACh, яка є високо консервативною для всіх різних підтипів нікотинових рецепторів, що веде до можливості побічних реакцій через неспецифічну активацію інших 15 UA 109803 C2 5 10 15 20 25 30 35 40 45 50 55 60 підтипів нікотинових рецепторів. Тому, для запобігання таких потенційних перешкод існує альтернативна терапевтична стратегія щодо агонізму альфа 7, що полягає в посиленні реагування рецепторів на природних агоністів з позитивним алостеричним модулятором (PAM). PAM визначається як засіб, який зв'язується з ділянкою, відмінною від ділянки зв'язування агоніста, і тому передбачається, що він не має агоністичних або десенсибілізувальних властивостей, але підсилює чутливість альфа 7 nAChR до природного трансмітера. Цінність цієї стратегії в тому, що для даної кількості трансмітера інтенсивність реакції альфа 7 nAChR зростає в присутності PAM щодо рівня передачі, можливої в його відсутність. Крім того, PAM також може підсилювати ефективність природного трансмітера. Так для розладів, при яких спостерігається дефіцит білка альфа 7 nAChR, може бути корисним індуковане PAM посилення альфа 7 нікотинергічної передачі. Оскільки PAM залежить від присутності природного трансмітера, можливість надстимуляції обмежується механізмами руйнування/кліренсу для природного трансмітера. Сполуки згідно з даним винаходом класифікуються на типи 1-4 на основі якісних кінетичних властивостей, як визначено за допомогою реєстрації фіксації напруги на цілих клітинах. Ця класифікація ґрунтується на впливі сполуки альфа 7 PAM, як описано вище, на сигнал, викликаний застосуванням агоніста. Зокрема, зазначений агоніст являє собою холін у концентрації 1 мМ. У переважній постановці експерименту зазначена сполука альфа 7 PAM і холін одночасно застосовуються до клітини, як описано нижче. Десенсибілізація визначається як закриття рецептора при активації під час застосування агоніста при електрофізіологічних вимірах фіксації напруги на цілих клітинах, що спостерігається як зниження вихідного струму після початкової активації агоністом. Нижче описано визначення типів 1-4 PAM. Тип 0 сполуки мінімально змінюють величину ефекту струму, викликаного 1 мM холіну. Тип 1 сполуки підвищують величину ефекту струму, викликаного 1 мM холіну, але мінімально змінюють кінетичні показники рецептора. Зокрема, не впливають на швидкість і ступінь десенсибілізації та деактивації рецептора, викликаних агоністом. Модульована сполукою реакція на 1 мМ холіну, тому, близька до лінійного масштабування реакції на 1 мМ холіну у відсутності сполуки альфа 7 PAM. Тип 2 сполуки підвищують величину ефекту струму, викликаного 1 мM холіну, при цьому знижують швидкість і/або ступінь десенсибілізації. Деактивація рецептора, як правило, не зачіпається. Тип 3 сполуки підвищують величину ефекту струму, викликаного 1 мM холіну. При тестуванні при більш високих концентраціях до 10 мкM вони повністю інгібують десенсибілізацію, зокрема, застосування 1 мM холіну за 250 мілісекунд. Деактивація рецептора може бути вповільнена. Тип 4 сполуки забезпечують початкову десенсибілізацію рецептора з наступним повторним відкриттям рецептора під час застосування агоніста. При низькоефективних концентраціях сполуки альфа 7 PAM індукована агоністом активація, за якою іде десенсибілізація, все ще може бути відділена від індукованого сполукою повторного відкриття як максимум початкового вхідного струму. При більш високих ефективних концентраціях сполуки альфа 7 PAM повторне відкриття відбувається швидше, ніж закриття через десенсибілізацію так, що максимум початкового струму зникає. Сполуку розглядали, як таку, що має подібну PAM активність, що представляє інтерес, якщо потенціювання пікового струму становило щонайменше 200% у порівнянні з контрольною реакцією на холін (= 100%). Такі сполуки класифікуються як належні до певного типу PAM в експериментальній частині. Сполуки, які не відповідають умові, не класифікуються як належні до певного типу PAM. Можна підтвердити активність ряду сполук згідно з даним винаходом за допомогою тесту потенціалу, викликаного слуховим подразненням. Лінія інбредних мишей DBA/2, використовувана в цьому тесті, показала дефіцит обробки сенсорної інформації, подібний такому у пацієнтівіз шизофренією, що також корелює зі зменшенням нікотинових альфа 7 рецепторів у гіпокампі. Підтвердили, що миша DBA/2 є застосовуваною моделлю подібних шизофренії дефіцитів обробки сенсорної інформації. Дослідження на людині ефектів нікотину на обробку сенсорної інформації прогнозували результати, отриманні на миші DBA/2, а дослідження селективного альфа 7 агоніста GTS-21 на мишах DBA/2 прогнозували ефекти на людях. Тому ця модель здатності фільтрації сенсорної інформації має високу перехідну релевантність. Отже, метою даного винаходу є забезпечення способів лікування, які передбачають або введення позитивного алостеричного модулятора в якості єдиної активної речовини, що, таким 16 UA 109803 C2 5 10 15 20 25 30 35 40 45 50 55 60 чином, модулює активність агоністів ендогенного нікотинового рецептора, такого як ацетилхолін або холін, або введення позитивного алостеричного модулятора разом з агоністом нікотинового рецептора. У конкретній формі цього аспекту даного винаходу спосіб лікування передбачає лікування позитивним алостеричним модулятором альфа 7 нікотинового рецептора, як описано в даному документі, і агоністом альфа 7 нікотинового рецептора або частковим агоністом. Приклади прийнятних сполук з агоністичною активністю щодо альфа 7 нікотинового рецептора включають - 1,4-діазабіцикло[3.2.2]нонан-4-карбонової кислоти 4-бромфенілового складного ефіру моногідрохлорид (SSR180711A); - (-)-спіро[1-азабіцикло[2.2.2.]октан-3,5’-оксазолідин]-2’-он; - 3-[(2,4-диметокси)бензиліден]-анабазеїну дигідрохлорид (GTS-21); - [N-[(3R)-1-азабіцикло[2.2.2]окт-3-ил]-4-хлорбензаміду гідрохлорид] PNU-282987; - нікотин; - вареніклін; - MEM3454; - AZD-0328; - MEM63908; - (+)-N-(1-азабіцикло[2.2.2]окт-3-ил)бензo[b]фуран-2-карбоксамід; - A-582941; - AR-R17779; - TC-1698; - PHA-709829; - тропісетрон; - WAY-317538; - EVP-6124 і - TC-5619. Зокрема, приклади прийнятних сполук з агоністичною активністю щодо α7 нікотинового рецептора включають 1,4-діазабіцикло[3.2.2]нонан-4-карбонової кислоти 4-бромфенілового складного ефіру моногідрохлорид (SSR180711A); (-)-спіро[1-азабіцикло[2.2.2.]октан-3,5’оксазолідин]-2’-он; 3-[(2,4-диметокси)бензиліден]-анабазеїну дигідрохлорид (GTS-21); [N-[(3R)-1азабіцикло[2.2.2] окт-3-ил]-4-хлорбензаміду гідрохлорид] PNU-282987; нікотин; вареніклін; MEM3454; AZD-0328 і MEM63908. Позитивні модулятори nAChR згідно з даним винаходом є застосовними для лікування або профілактики психічних розладів, розумових розладів або захворювань, або станів, при яких корисна модуляція активності альфа 7 нікотинового рецептора. Конкретним аспектом способу згідно з даним винаходом є спосіб лікування дефіциту навчання, дефіциту когнітивних функцій, дефіциту уваги або втрати пам'яті, вважається, що модуляція активності альфа 7 нікотинового рецептора корисна при ряді захворювань, у тому числі при хворобі Альцгеймера, деменції, що розвивається при хворобі дифузійних тілець Леві, синдромі гіперактивності з дефіцитом уваги, тривозі, шизофренії, манії, біполярній депресії, хворобі Паркінсона, хворобі Гентингтона, синдромі Туретта, травми головного мозку або інших неврологічних, дегенеративних або психіатричних розладах, при яких відбувається втрата холінергічних синапсів, у тому числі при синдромі зміни годинних поясів, нікотиновій залежності, болі. Сполуки також можуть знайти терапевтичне застосування в якості протизапальних лікарських препаратів, оскільки субодиниця альфа 7 нікотинового ацетилхолінового рецептора є необхідною для інгібування синтезу цитокінів холінергічним шляхом запалення. Прикладами показань, які можна лікувати сполуками, є ендотоксикоз, ендотоксиновий шок, сепсис, ревматоїдний артрит, астма, розсіяний склероз, псоріаз, уртикарія, запальне захворювання кишечнику, запальне захворювання жовчних проток, хвороба Крона, виразковий коліт, післяопераційний ілєус, панкреатит, серцева недостатність, гостре ушкодження легенів та відторгнення алотрансплантата. Сполуки згідно з даним винаходом можуть знайти терапевтичне застосування при таких показаннях як когнітивне порушення при шизофренії, когнітивне порушення при хворобі Альцгеймера, помірне когнітивне порушення, хвороба Паркінсона, синдром гіперактивності з дефіцитом уваги, виразковий коліт, панкреатит, артрит, сепсис, післяопераційний ілєус та гостре ушкодження легенів. У світлі описаних вище фармакологічних властивостей сполуки формули (I) або будь-яка їх підгрупа, їх фармацевтично прийнятні адитивні солі, сольвати та стереохімічні ізомерні форми можуть бути використані в якості лікарського препарату. Зокрема, сполуки відповідно до даного винаходу можуть бути використані для виготовлення лікарського препарату для лікування або 17 UA 109803 C2 5 10 15 20 25 30 35 40 45 50 55 профілактики психічних розладів, розумових розладів, або захворювань, або станів, при яких корисна модуляція альфа 7 нікотинового рецептора. У варіанті здійснення даний винахід відноситься до сполук формули (I) для застосування в лікуванні або профілактиці, зокрема, лікуванні психічних розладів, розумових розладів або захворювань, або станів, при яких корисна модуляція альфа 7 нікотинового рецептора. У варіанті здійснення даний винахід відноситься до сполук формули (I) для застосування в лікуванні або профілактиці, зокрема, у лікуванні психічних розладів, розумових розладів або запальних захворювань. У варіанті здійснення даний винахід відноситься до сполук формули (I) для лікування або попередження, зокрема, лікування зазначених захворювань або станів. Що стосується застосовності сполук формули (I), представлений спосіб лікування або профілактики у теплокровних тварин, включаючи людей, що страждають від захворювань, при яких корисна модуляція альфа 7 нікотинового рецептора, таких як шизофренія, манія та біполярна депресія, тривога, хвороба Альцгеймера, дефіцит навчання, дефіцит когнітивних функцій, дефіцит уваги, втрата пам'яті, деменція, що розвивається при хворобі дифузійних тілець Леві, синдром гіперактивності з дефіцитом уваги, хвороба Паркінсона, хвороба Гентингтона, синдром Туретта, травма головного мозку, синдром зміни годинних поясів, нікотинова залежність, біль. Зазначені способи передбачають введення, а саме системне або місцеве введення, переважно пероральне введення, ефективної кількості сполуки формули (I), його стереохімічно ізомерної форми, фармацевтично прийнятної адитивної солі або їх сольвату теплокровним тваринам, включаючи людей. Фахівцеві в даній області буде зрозуміло, що терапевтично ефективною кількістю PAM згідно з даним винаходом є кількість, достатня для модуляції активності альфа 7 нікотинового рецептора, і що ця кількість варіює inter alia залежно від типу захворювання, концентрації сполуки в терапевтичному складі та стану пацієнта. Як правило, кількість PAM, що підлягає введенню в якості терапевтичного засобу для лікування захворювань, при яких корисна модуляція альфа 7 нікотинового рецептора, таких як шизофренія, манія та біполярна депресія, тривога, хвороба Альцгеймера, дефіцит навчання, дефіцит когнітивних функцій, дефіцит уваги, втрата пам'яті, деменція, що розвивається при хворобі дифузійних тілець Леві, синдром гіперактивності з дефіцитом уваги, хвороба Паркінсона, хвороба Гентингтона, синдром Туретта, травма головного мозку, синдром зміни годинних поясів, нікотинова залежність та біль, буде визначатися лікарем у кожному конкретному випадку. Як правило, прийнятною дозою є доза, яка дає в результаті концентрацію PAM на ділянці лікування в діапазоні від 0,5 нM до 200 мкM і більш типово від 5 нM до 50 мкM. Для одержання таких терапевтичних концентрацій пацієнтові, що потребує такого лікуванні, буде введено від 0,01 мг/кг до 2,50 мг/кг ваги тіла, зокрема, від 0,1 мг/кг до 0,50 мг/кг ваги тіла. Кількість сполуки відповідно до даного винаходу, також названої в даному документі активним інгредієнтом, яка необхідна для досягнення терапевтичного ефекту, звичайно, варіює у кожному конкретному випадку, варіює залежно від конкретної сполуки, шляху введення, віку та стану реципієнта та конкретного розладу або захворювання, що підлягає лікуванню. Спосіб лікування також може передбачати введення активного інгредієнта з режимом від одного до чотирьох прийомів на добу. У цих способах лікування сполуки відповідно до даного винаходу переважно складаються перед прийманням. Як описано в даному документі нижче, прийнятні фармацевтичні сполуки одержують згідно з відомими процедурами з використанням добре відомих і легкодоступних інгредієнтів. Фармацевтичні композиції Даний винахід також відноситься до композицій для попередження або лікування захворювань, при яких корисна модуляція альфа 7 нікотинового рецептора, таких як шизофренія, манія та біполярна депресія, тривога, хвороба Альцгеймера, дефіцит навчання, дефіцит когнітивних функцій, дефіцит уваги, втрата пам'яті, деменція, що розвивається при хворобі дифузійних тілець Леві, синдром гіперактивності з дефіцитом уваги, хвороба Паркінсона, хвороба Гентингтона, синдром Туретта, травма головного мозку, синдром зміни годинних поясів, нікотинова залежність та біль. Зазначені композиції містять терапевтично ефективну кількість сполуки формули (I) і фармацевтично прийнятного носія або розріджувача. Хоча можна активний інгредієнт вводити окремо, бажаною є присутність його у вигляді фармацевтичної композиції. Отже, даний винахід, крім того, відноситься до фармацевтичної композиції, що містить сполуку відповідно до даного винаходу разом з фармацевтично прийнятним носієм або розріджувачем. Носій або розріджувач має бути «прийнятним» у сенсі сумісності з іншими інгредієнтами композиції та має бути нешкідливим для його реципієнтів. 18 UA 109803 C2 5 10 15 20 25 30 35 40 45 50 55 60 Фармацевтичні композиції відповідно до даного винаходу можуть бути отримані будь-якими способами, добре відомими в рівні техніки фармації, наприклад, з використанням способів, th таких як описані в Gennaro et al. Remington’s Pharmaceutical Sciences (18 ed., Mack Publishing Company, 1990, зокрема див. Part 8: Pharmaceutical preparations and their Manufacture). Терапевтично ефективна кількість конкретної сполуки у формі основи або у формі адитивної солі в якості активного інгредієнта комбінується в однорідній суміші з фармацевтично прийнятним носієм, який може приймати форми в широкому діапазоні залежно від форми препарату, бажаного для введення. Такі фармацевтичні композиції бажано мають одиничну дозовану форму, прийнятну переважно для системного введення, такого як пероральне, черезшкірне або парентеральне введення; або для місцевого введення, такого як шляхом інгаляції, назального аерозолю, очних крапель або шляхом крему, гелю, шампуню або подібного. Наприклад, при одержанні композицій у пероральній дозованій формі може бути використано кожне зі звичайних фармацевтичних середовищ, таких як, наприклад, вода, гліколі, масла, спирти та подібне, у випадку пероральних рідких препаратів, таких як суспензії, сиропи, еліксири та розчини, або тверді носії, такі як крохмалі, цукор, каолін, засоби, що змазують, зв’язувальне, засоби, що дезінтегрують, та подібне, у випадку порошків, пігулок, капсул і таблеток. Оскільки їх легко вводити, таблетки та капсули представляють найбільш переважну пероральну дозовану одиничну форму, у випадку якої, звичайно, використовуються тверді фармацевтичні носії. Для парентеральних композицій носій, як правило, буде містити стерильну воду, щонайменше в значній мірі, хоча можуть бути включені інші інгредієнти, наприклад, для розчинності. Можуть бути отримані, наприклад, ін'єкційні розчини, у яких носій включає сольовий розчин, розчин глюкози або суміш сольового розчину та розчину глюкози. Також можуть бути отримані ін'єкційні суспензії, у випадку яких можуть використовуватися відповідні рідкі носії, засоби, що суспендують, та подібне. У композиціях, прийнятних для черезшкірного введення, носій необов'язково містить засіб, що посилює проникність, і/або прийнятний змочувальний засіб, необов'язково комбінований з прийнятними допоміжними засобами будьякої природи в малих кількостях, причому допоміжні засоби не виявляють жодних значних шкідливих ефектів на шкіру. Зазначені допоміжні засоби можуть полегшувати введення на шкіру і/або можуть використовуватися для одержання бажаних композицій. Ці композиції можуть бути введені різними шляхами, наприклад, як трансдермальний пластир, як краплинне нанесення або як мазь. Особливо переважно складати вищезгадані фармацевтичні композиції в дозовані одиничні форми для простоти введення та рівномірності дозування. Дозована одинична форма, як використано в описі та формулі винаходу в даному документі, означає фізично дискретні одиниці, прийнятні як одиничні дозування, причому кожна одиниця містить певну кількість активного інгредієнта, розраховану для одержання бажаного терапевтичного ефекту, разом з потрібним фармацевтичним носієм. Прикладами таких дозованих одиничних форм є таблетки (у тому числі з насічкою або покриті таблетки), капсули, пігулки, пакети з порошком, облатки, ін'єкційні розчини або суспензії, повні чайні ложки, повні столові ложки та подібне, а також їх розділені множинні форми. Точне дозування та частота введення залежить від конкретної використовуваної сполуки формули (I), конкретного стану, що підлягає лікуванню, тяжкості стану, що підлягає лікуванню, віку, ваги, статі, ступеню розладу та загального фізичного стану конкретного пацієнта, а також від іншого медичного препарату, який індивідуум може приймати, як добре відомо фахівцеві в даній галузі. Крім того, очевидно, що зазначену ефективну добову кількість можна знижувати або підвищувати залежно від реакції суб'єкта, що одержує лікування, і/або залежно від оцінювання призначених лікарем сполук відповідно до даного винаходу. Залежно від шляху введення фармацевтична композиція буде містити від 0,05 до 99 ваг. %, переважно від 0,1 до 70 ваг. %, більш переважно від 0,1 до 50 ваг. % активного інгредієнта, і від 1 до 99,95 ваг. %, переважно від 30 до 99,9 ваг. %, більш переважно від 50 до 99,9 ваг. % фармацевтично прийнятного носія, причому всі процентні співвідношення засновані на загальній вазі композиції. Кількість сполуки формули (I), яку можна об'єднати з матеріалом-носієм з одержанням одиночної дозованої форми, буде варіювати залежно від захворювання, яке лікують, видів ссавців і конкретного способу введення. Однак, у якості загальної вказівки, прийнятні одиничні дози для сполук згідно з даним винаходом можуть, наприклад, переважно становити від 0,1 мг до приблизно 1000 мг активної сполуки. Переважна одинична доза становить від 1 мг до приблизно 500 мг. Більш переважна одинична доза становить від 1 мг до приблизно 300 мг. Ще більш переважна одинична доза становить від 1 мг до приблизно 100 мг. Такі одиничні дози можуть вводитися більш одного разу на добу, наприклад, 2, 3, 4, 5 або 6 раз на добу, але 19 UA 109803 C2 5 10 15 20 25 30 35 40 45 50 55 60 переважно 1 або 2 рази на добу, так, що загальне дозування для дорослого вагою 70 кг знаходиться в діапазоні від 0,001 до приблизно 15 мг на кг ваги суб'єкта на введення. Переважне дозування становить від 0,01 до приблизно 1,5 мг на кг ваги суб'єкта на введення, і така терапія може тривати протягом кількох тижнів або місяців, а в деяких випадках, років. Буде зрозуміло, однак, що конкретний рівень дози для будь-якого конкретного пацієнта буде залежати від ряду факторів, у тому числі від активності конкретної використовуваної сполуки; віку, ваги тіла, загального стану здоров'я, статі та дієти підлягаючого лікуванню індивідуума; часу та шляху введення; швидкості виведення; інших лікарських засобів, які були введені раніше; і тяжкості конкретного захворювання, що підлягає лікуванню, як добре відомо фахівцям у даній галузі. Типове дозування може становити одну таблетку від 1 мг до приблизно 100 мг або від 1 мг до приблизно 300 мг, прийняту один раз на добу або кілька разів на добу, або одну капсулу або таблетку пролонгованого дії, яка приймається один раз на добу та містить пропорційно більш високий вміст активного інгредієнта. Ефект пролонгованого дії може бути забезпечений матеріалами капсули, які розчиняються при різних значеннях pH, капсулами, які повільно вивільняють за допомогою осмотичного тиску, або будь-яким іншим відомим засобом контрольованого вивільнення. В деяких випадках може бути необхідним застосування дозувань, що виходять за ці діапазони, як буде очевидно фахівцям у даній галузі. Крім того, слід зазначити, що клініцисту або лікарю добре відомо, як і коли почати, перервати, відрегулювати або припинити терапію в залежності від індивідуальної реакції пацієнта. Сполуки відповідно до даного винаходу можуть бути використані для системного введення, такого як пероральне, черезшкірне або парентеральне введення; або для місцевого введення, такого як шляхом інгаляції, назального аерозолю, очних крапель або за допомогою крему, гелю, шампуню або подібного. Сполуки переважно вводяться перорально. Точне дозування та частота введення залежить від конкретної використовуваної сполуки формули (I), конкретного стану, що підлягає лікуванню, тяжкості стану, що підлягає лікуванню, віку, ваги, статі, ступені розладу та загального фізичного стану конкретного пацієнта, а також іншого медичного препарату, який може приймати індивідуум, як добре відомо фахівцям у даній галузі. Крім того, очевидно, що зазначена ефективна добова кількість може бути знижена або підвищена залежно від реакції суб'єкта, що приймає лікування, і/або залежно від оцінки лікаря, що прописав сполуку відповідно до даного винаходу. Сполуки формули (I) також можуть бути використані в комбінації з іншими загальноприйнятими агоністами α7 нікотинового рецептора, наприклад, 1,4-діазабіцикло[3.2.2]нонан-4-карбонової кислоти 4-бромфенілового складного ефіру моногідрохлорид (SSR180711A); (-)-спіро[1-азабіцикло[2.2.2.]октан-3,5’-оксазолідин]-2’-он; 3-[(2,4диметокси)бензиліден]-анабазеїну дигідрохлорид (GTS-21); [N-[(3R)-1-азабіцикло[2.2.2]окт-3ил]-4-хлорбензаміду гідрохлорид] PNU-282987; нікотин; вареніклін; MEM3454; AZD-0328; MEM63908; (+)-N-(1-азабіцикло[2.2.2]окт-3-ил)бензo[b]фуран-2-карбоксамід; A-582941; ARR17779; TC-1698; PHA-709829; тропісетрон; WAY-317538; EVP-6124 і TC-5619. Таким чином, даний винахід також відноситься до комбінації сполуки формули (I) і агоніста альфа 7 нікотинового рецептора. Зазначена комбінація може бути використана в якості лікарського препарату. Даний винахід також відноситься до продукту, що містить (a) сполуку формули (I) і (b) агоніст альфа 7 нікотинового рецептора, як комбінованого препарату для одночасного, роздільного або послідовного застосування в лікуванні захворювань, при яких корисна модуляція альфа 7 нікотинового рецептора. Різні лікарські засоби можуть бути комбіновані в один препарат разом з фармацевтично прийнятними носіями. Експериментальна частина Деякі способи одержання сполук відповідно до даного винаходу ілюструються в наступних прикладах. Якщо не зазначене інше, усі вихідні матеріали одержували від комерційних постачальників і використовували без додаткового очищення. Нижче або вище, «хв.» означає хвилини; «MeOH» означає метанол; «EtOH» означає етанол; «Et2O» означає діетиловий ефір; «TFA» означає трифтороцтову кислоту «NH 4OAc» означає ацетат амонію, «HBTU» означає O-(бензoтриазол-1-іл)-N,N,N’,N’-тетраметилуронію гексафторфосфат; «DIPEA» означає діізопропілетиламін; «LDA» означає літію діізопропіламін; «DCM» означає дихлорметан; «VCD» означає коливальний круговий дихроїзм. Реакції за допомогою мікрохвиль виконували в однорежимному реакторі: мікрохвильовий TM реактор Initiator Sixty EXP (Biotage AB), або у багаторежимному реакторі: MicroSYNTH Labstation (Milestone, Inc.). Наступні приклади призначені для ілюстрації, а не для обмеження об'єму даного винаходу. 20 UA 109803 C2 A. Одержання проміжних сполук 5-Хлор-2-(2,6-диметил-4-піридиніл)-бензoнітрил (проміжна сполука 1) Cl CN N 5 10 15 (Проміжна сполука 1) Суміш 2-бром-5-хлорбензoнітрилу (10,03 г, 46,33 ммоль), 2,6-диметилпіридин-4-боронової кислоти пінаколового складного ефіру ([325142-95-8], 16,20 г, 69,50 ммоль), тетракіс(трифенілфосфін)паладію (3,21 г, 2,78 ммоль), 1,4-діоксану (50 мл) і карбонату натрію (14,73 г, 139,00 ммоль) у воді (50 мл) збовтували та нагрівали в атмосфері азоту при 100 °C протягом 2 годин. Реакційну суміш розбавляли за допомогою CH2Cl2 і води та шари розділяли. Органічний шар сушили з MgSO4, фільтрували та випарювали. Залишок очищали колонковою хроматографією на силікагелі (градієнт елюенту від 100% DCM до 98/2 DCM/MeOH). Бажані фракції збирали та випарювали, одержуючи 8,73 г (77%) проміжної сполуки 1 після сушіння протягом ночі під вакуумом при 50 °C. 5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)-бензoнітрил (проміжна сполука 2) O N CN N 20 25 (Проміжна сполука 2) Суміш проміжної сполуки 1 (2,64 г, 10,88 ммоль), цис-2,6-диметилморфоліну (1,35 мл, 10,88 ммоль), натрію трет-бутоксиду (1,57 г, 16,33 ммоль) і сухого толуолу (15 мл) ввели в пробірку для проведення реакцій під тиском та дегазували азотом протягом 5 хвилин. Додавали ксантфос [161265-03-8] (378 мг, 0,65 ммоль) і Pd2(dba)3 (199 мг, 0,22 ммоль) і додатково дегазували суміш протягом 5 хвилин. Пробірку закривали та реакційну суміш збовтували при 120 °C протягом 1,5 години. Реакційну суміш розбавляли CH 2Cl2 і промивали водою. Водний шар двічі екстрагували CH2Cl2. Об'єднані органічні шари промивали водою, сушили над MgSO 4, фільтрували та випарювали. Залишок очищали колонковою хроматографією на силікагелі (градієнт елюенту від 100% DCM до 99/1 DCM/MeOH), одержуючи 2,69 г проміжної сполуки 2 (77%) у вигляді білої твердої речовини після сушіння у вакуумній печі при 50 °C протягом ночі. 5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)-бензолметанамін (проміжна сполука 3) O NH2 N N 30 35 (Проміжна сполука 3) Проміжну сполуку 2 (3,26 г, 10,14 ммоль) додавали в суспензію нікелю Ренея (1 г) в 7 н розчині аміаку в MeOH (200 мл). Реакційну суміш збовтували при 14 °C в атмосфері водню до абсорбції 2 еквівалентів водню. Каталізатор видаляли фільтрацією через діатомову землю. Розчинник випарювали, одержуючи проміжну сполуку 3 кількісно. Проміжну сполуку 3 використовували без додаткового очищення. 3,5-Біс(трифторметил)піперидин (проміжна сполука 4) 21 UA 109803 C2 CF3 NH F3C 5 (Проміжна сполука 4) 3,5-Біс(трифторметил)піридин [20857-47-0] (10 г, 46,49 ммоль) і 6 н HCl в ізопропанолі (7,75 мл, 46,49 ммоль) додавали в суспензію Pt на вугіллі 5% (1 г) в EtOH (150 мл). Реакційну суміш збовтували при 25 °C в атмосфері водню до абсорбції 3 еквівалентів водню. Каталізатор видаляли фільтрацією через діатомову землю. Розчинник випарювали, одержуючи проміжну сполуку 4 кількісно у вигляді суміші 50:50 цис- і транс-ізомерів. Проміжну сполуку 4 використовували без додаткового очищення. Таблиця 1 Наступні проміжні сполуки одержували згідно із процедурами, використовуваними для проміжної сполуки 3 (починаючи із проміжної сполуки 1 через проміжну сполуку 2). Проміжна сполука Структура O Починаючи з NH2 N проміжної сполуки 1 і морфоліну 5 N O NH2 проміжної сполуки 1 і 8-окса-3азабіцикло[3.2.1]октану гідрохлориду [54745-74-3] N 6 N NH2 N проміжної сполуки 1 і цис-3,5диметилпіперидину 7 N CF3 NH2 N 8 проміжної сполуки 1 і 4 з розділенням цис- і транс-ізомерів F 3C N CF3 NH2 N проміжної сполуки 1 і 3-(трифторметил)піперидину 9 N 10 22 UA 109803 C2 Таблиця 2 Наступні проміжні сполуки одержували згідно із процедурами, використовуваними для проміжної сполуки 3 (починаючи з 2-бром-5-хлорбензoнітрилу). Проміжна сполука Структура O Починаючи з 2-бром-5-хлорбензoнітрилу та піридин-4боронової кислоти ([1692-15-5]) замість 2,6диметилпіридин-4-боронової кислоти пінаколового складного ефіру NH2 N 10 N O 2-бром-5-хлорбензoнітрилу та піридин-4боронової кислоти ([1692-15-5]) замість 2,6диметилпіридин-4-боронової кислоти пінаколового складного ефіру та з морфоліном замість цис-2,6диметилморфоліну NH2 N 11 N O 2-бром-5-хлорбензoнітрилу та 2метилпіридин-4-боронової кислоти пінаколового складного ефіру ([660867-801]) замість 2,6-диметилпіридин-4-боронової кислота пінаколового складного ефіру NH2 N 12 N 2-Бром-5-(4-морфолініл)-бензoнітрил (проміжна сполука 10) O N CN Br 5 10 (Проміжна сполука 10) Суміш 2-бром-5-фторбензoнітрилу (10 г, 50 ммоль), морфоліну (4,37 мл, 50 ммоль) і карбонату калію (6,91 г, 50 ммоль) в DMSO (100 мл) збовтували при 100 °C протягом 48 годин. Реакційну суміш вливали у воду (200 мл) і збовтували протягом 1 години. Осад фільтрували та очищали колонковою хроматографією на силікагелі (градієнт елюенту від 50/50 до 100/0 DCM/гептан). Бажані фракції збирали та випарювали, одержуючи 4,1 г (30%) проміжної сполуки 10 після сушіння протягом ночі під вакуумом при 50 °C. 2-(2-Метил-4-піридиніл)-5-(4-морфолініл)-бензoнітрил (проміжна сполука 11) O N CN N 15 20 (Проміжна сполука 11) Суміш проміжної сполуки 10 (4,1 г, 15,35 ммоль), 2-метилпіридин-4-боронової кислоти пінаколового складного ефіру ([660867-80-1], 3,70 г, 16,88 ммоль), тетракіс(трифенілфосфін)паладію (0,88 г, 0,77 ммоль), 1,4-діоксану (50 мл) і карбонату натрію (3,58 г, 33,67 ммоль) розчиняли у воді (20 мл) і EtOH (30 мл), дегазували та посудину закривали. Реакційну суміш збовтували та нагрівали в атмосфері азоту при 120 °C протягом 2 годин. Розчинник випарювали. Залишок поглинали в DCM і промивали водою. Органічний шар сушили з MgSO4 і випарювали. Залишок очищали колонковою хроматографією на силікагелі (градієнт елюенту від 100% DCM до 99/1 DCM/MeOH). Бажані фракції збирали та випарювали, 23 UA 109803 C2 одержуючи 3,7 г (86%) проміжної сполуки 11 після сушіння протягом ночі під вакуумом при 50 °C. 2-(2-Метил-4-піридиніл)-5-(4-морфолініл)-бензолметанамін (проміжна сполука 12) O NH2 N N 5 (Проміжна сполука 12) Проміжну сполуку 12 одержували згідно із процедурою, використовуваною для проміжної сполуки 3, починаючи із проміжної сполуки 11 замість проміжної сполуки 2. 3-[(2R,6S)-2,6-диметил-4-морфолініл]-5-фтор-бензoнітрил (проміжна сполука 13) O N CN F 10 15 20 (Проміжна сполука 13) Суміш 3-бром-5-фторбензoнітрилу (55,56 г, 277,80 ммоль), цис-2,6-диметилморфоліну (34,40 мл, 277,80 ммоль), натрію трет-бутоксиду (40,05 г, 416,70 ммоль) і сухого толуолу (300 мл) ввели в пробірку для проведення реакцій під тиском та дегазували азотом протягом 5 хвилин. Додавали ксантфос [161265-03-8] (9,64 г, 16,67 ммоль) і Pd2(dba)3 (5,09 г, 5,55 ммоль) і додатково дегазували суміш протягом 5 хвилин. Пробірку закривали та реакційну суміш збовтували при 120 °C протягом 2 годин. Реакційну суміш розбавляли CH 2Cl2 і промивали водою. Водний шар екстрагували CH2Cl2. Об'єднані органічні шари промивали водою, сушили над MgSO4, фільтрували та випарювали. Залишок очищали колонковою хроматографією на силікагелі (градієнт елюенту від 100% DCM до 99/1 DCM/MeOH). Бажані фракції випарювали. Залишок розтирали в Et2O і фільтрували, одержуючи 33 г проміжної сполуки 13 (51%) у вигляді білої твердої речовини після сушіння у вакуумній печі при 50 °C протягом ночі. 5-[(2R,6S)-2,6-диметл-4-морфолініл]-3-фтор-2-йод-бензoнітрил (проміжна сполука 14) O N CN I F 25 30 35 40 (Проміжна сполука 14) Розчин 2,2,6,6-тетраметилпіперидину (18,82 мл, 110,58 ммоль) в THF (1 л) охолоджували до 0 °C. Краплинами додавали н-бутиллітій (2,5 M у гексанах, 44,23 мл, 110,58 ммоль) при збовтуванні при 0 °C. Потім реакційну суміш збовтували протягом 15 хвилин при 0 °C. Отриманий у результаті розчин охолоджували до -78 °C і розчин проміжної сполуки 13 (29,44 г, 100,53 ммоль), розчинений в THF (200 мл), додавали краплинами протягом 20 хвилин. Темножовтий розчин збовтували при -78 °C протягом 30 хвилин перед додаванням краплинами за 15 хвилин розчину йоду (30,62 г, 120,64 ммоль), розчиненого в THF (250 мл). Суміш збовтували протягом 30 хвилин при -78 °C перед забезпеченням нагрівання до кімнатної температури. Збовтування продовжували протягом 1 години. Реакцію гасили водним NH4Cl. Суміш розбавляли водою та Et2O, а шари розділяли. Водний шар екстрагували з Et 2O. Об'єднаний органічний шар знову промивали водним Na2S2O3 і сушили над MgSO4, фільтрували та випарювали. Залишок розтирали в теплому DCM і фільтрували, одержуючи 31,28 гпроміжної сполуки 14 (86%) у вигляді білої твердої речовини після сушіння у вакуумній печі при 50 °C протягом ночі. 5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)-3-фтор-бензoнітрил (проміжна сполука 15) 24 UA 109803 C2 O N CN F 5 10 N (Проміжна сполука 15) Суміш проміжної сполуки 14 (12,09 г, 33,57 ммоль), 2,6-диметилпіридин-4-боронової кислоти пінаколового складного ефіру ([325142-95-8], 11,74 г, 50,35 ммоль), тетракіс(трифенілфосфін)паладію (2,33 г, 2,01 ммоль), 1,4-діоксану (100 мл) і карбонату натрію 1 M (100 мл, 100 ммоль) дегазували азотом. Реакційну суміш збовтували та нагрівали в атмосфері азоту при 140 °C протягом 12 годин. Реакційну суміш розбавляли DCM і водою, а шари розділяли. Водний шар екстрагували з DCM. Об'єднаний органічний шар сушили з MgSO4, фільтрували та випарювали. Залишок очищали колонковою хроматографією на силікагелі (градієнт елюенту від 100% DCM до 99/1 DCM/MeOH). Бажані фракції збирали та випарювали, одержуючи 8,37 г (73%) проміжної сполуки 15 після сушіння протягом ночі під вакуумом при 50 °C. 5-[(2R,6S)-2,6-диметил-4-морфолініл]-2-(2,6-диметил-4-піридиніл)-3-фтор-бензолметанамін (проміжна сполука 13) O NH2 N F 15 20 N (Проміжна сполука 16) Проміжну сполуку 16 одержували згідно із процедурою, використовуваною для проміжної сполуки 3, починаючи із проміжної сполуки 15 замість проміжної сполуки 2. 5-[(2R,6S)-2,6-диметил-4-морфолініл]-3-фтор-2-(2-метил-4-піридиніл)-бензолметанамін (проміжна сполука 17) O NH2 N F 25 N (Проміжна сполука 17) Проміжну сполуку 17 одержували згідно із процедурами, використовуваними для проміжної сполуки 13, починаючи із проміжної сполуки 14, і з використанням 2-метилпіридин-4-боронової кислоти пінаколового складного ефіру ([660867-80-1] замість 2,6-диметилпіридин-4-боронової кислоти пінаколового складного ефіру. 2-Бром-N-(фенілметил)-N-(3,3,3-трифтор-2-гідроксипропіл)-ацетамід (проміжна сполука 18) Br O OH N F3C 30 (Проміжна сполука 18) Розчин 1,1,1-трифтор-3-бензиламінопропан-2-олу ([178218-36-5], 11,64 г, 53,12 ммоль) і триетиламіну (7,38 мл, 53,12 ммоль) в DCM (150 мл) охолоджували до 0 °C в атмосфері азоту. Бромацетилхлорид (5,41 мл, 58,43 ммоль), розчинений в DCM (50 мл), додавали краплинами і реакційну суміш збовтували протягом 30 хвилин. Реакційну суміш розбавляли DCM, промивали 25 UA 109803 C2 з HCl 1 н, а потім водним натрію гідрокарбонатом і сольовим розчином. Органічний шар сушили з MgSO4, фільтрували та випарювали, одержуючи 18,07 г проміжної сполуки 18 (кількісно), яку використовували без додаткового очищення. 4-(Фенілметил)-6-(трифторметил)-3-морфолінон (проміжна сполука 19) O O N 5 10 15 F3C (Проміжна сполука 19) Проміжну сполуку 18 (123 г, 361,61 ммоль) розчиняли в сухому THF (500 мл), додавали краплинами у суспензію гідриду натрію (60% дисперсія у мінеральному маслі, 17,35 г, 433,94 ммоль) у сухому THF (500 мл), охолоджували до -5 °C в атмосфері азоту. Після додавання реакційну суміш нагрівали до кімнатної температури та збовтували протягом 30 хвилин. Реакцію гасили обережним додаванням MeOH при 0 °C. Потім реакційну суміш вливали в 1 н HСl (100 мл) і водний шар екстрагували з EtOAc. Органічний шар промивали водним гідрокарбонатом і сольовим розчином перед сушінням з MgSO 4, фільтрацією та випарюванням, одержуючи 90 г проміжної сполуки 19 (96%) у вигляді масла, яку використовували без додаткового очищення. 4-(Фенілметил)-2-(трифторметил)-, (2S)-морфолін (проміжна сполука 20) і 4-(фенілметил)-2(трифторметил)-, (2R)-морфолін (проміжна сполука 21) O S O R N F3C 20 25 30 N F3C (Проміжна сполука 20) (Проміжна сполука 21) Розчин комплексу борану/THF 1 M ([14044-65-6], 868 мл, 868,96 ммоль) додавали краплинами у розчин проміжної сполуки 19 (90 г, 347,18 ммоль) розчиняли в сухому THF (850 мл) при кімнатній температурі в атмосфері азоту. Суміш збовтували протягом 2,5 годин при 70 °C (доки газ вже більше не виділявся). Потім краплинами додавали MeOH (70,32 мл, 1735,92 ммоль), а потім HCl (3 M у воді, 578 мл, 1735,92 ммоль) і суміш збовтували при 70 °C ще годину. Потім реакційну суміш гасили карбонатом калію (239,91 г, 1735,92 ммоль) і розчиняли у воді (250 мл). Реакційну суміш екстрагували діетиловим ефіром. Органічний шар промивали сольовим розчином, сушили з MgSO4, фільтрували та випарювали. Отримане в результаті масло очищали колонковою хроматографією на силікагелі (елюент: DCM), одержуючи прозоре масло, яке потім розділяли на його чисті енантіомери колонковою хроматографією на Chiralcel OJ 1000 Å 20 мкм (Daicel) (елюент: гептан/iPrOH 99/1), одержуючи 27 г проміжної сполуки 21 (32%) і 25 г проміжної сполуки 20 (29%), обидві у вигляді прозорого масла. Визначали абсолютну стереохімію цих двох енантіомерів за допомогою VCD. 2-(Трифторметил)-(2S)-морфоліну гідрохлорид (проміжна сполука 22) O S NH .HCl F3C 35 40 (Проміжна сполука 22) Проміжну сполуку 20 (25 г, 101,94 ммоль) додавали в суспензію Pd на вугіллі 10% (2 г) в MeOH (150 мл). Реакційну суміш збовтували при 25 °C в атмосфері водню до абсорбції 1 еквівалента водню. Каталізатор видаляли фільтрацією через діатомову землю. Фільтрат обробляли водною HCl 5,5 M (18,5 мл, 101,94 ммоль). Розчинник випарювали, одержуючи 18,46 г проміжної сполуки 22 (95%) у вигляді білої твердої речовини. 2-(Трифторметил)-(2R)-морфоліну гідрохлорид (проміжна сполука 23) O R NH .HCl F3C 45 (Проміжна сполука 23) Проміжну сполуку 21 (27 г, 110,09 ммоль) додавали в суспензію Pd на вугіллі 10% (2 г) в MeOH (150 мл). Реакційну суміш збовтували при 25 °C в атмосфері водню до абсорбції 1 еквівалента водню. Каталізатор видаляли фільтрацією через діатомову землю. Фільтрат обробляли водною HCl 5,5 M (20,0 мл, 110,09 ммоль). Розчинник випарювали, одержуючи 16,4 г проміжної сполуки 23 (78%) у вигляді білої твердої речовини. 26 UA 109803 C2 3-Фтор-5-[(2S)-2-(трифторметил)-4-морфолініл]-бензoнітрил (проміжна сполука 24) O S N CN F3C F 5 10 (Проміжна сполука 24) Суміш проміжної сполуки 22 (4,94 г; 25 ммоль) і натрію трет-бутоксиду (6 г, 62,5 ммоль) у моноглімі (50 мл) дегазували протягом 15 хвилин з азотом. Додавали каталізатор Нолана ([478980-01-7], 718 мг, 1,25 ммоль), а потім 3-бром-5-фторбензoнітрил (5 г, 25 ммоль). Реакційну суміш збовтували при 50 °C протягом 48 годин. Реакційну суміш вливали у лід/воду. Суміш нейтралізували 1 н HCl і двічі екстрагували з EtOAc. Об'єднаний органічний шар промивали сольовим розчином, сушили над MgSO4, фільтрували та випарювали. Залишок очищали колонковою хроматографією на силікагелі (елюент 50/50 DCM/гептан). Бажані фракції випарювали та залишок кристалізували в iPr2O/гептані 1/10, одержуючи 3 г проміжної сполуки 24 (44%) після сушіння у вакуумній печі при 50 °C протягом ночі. 2-Йод-3-фтор-5-[(2S)-2-(трифторметил)-4-морфолініл]-бензoнітрил (проміжна сполука 25) O S N CN F3C I F 15 (Проміжна сполука 25) Проміжну сполуку 25 одержували згідно із процедурою, використовуваною для проміжної сполуки 14, починаючи із проміжної сполуки 24 замість проміжної сполуки 13. 2-(2,6-Диметил-4-піридиніл)-3-фтор-5-[(2S)-2-(трифторметил)-4-морфолініл]-бензoнітрил (проміжна сполука 26) O S N CN F3C F 20 25 30 35 N (Проміжна сполука 26) Суміш проміжної сполуки 25 (4,03 г, 10,07 ммоль), 2,6-диметилпіридин-4-боронової кислоти пінаколового складного ефіру ([325142-95-8], 2,82 г, 12,09 ммоль), тетракіс(трифенілфосфін)паладію (582 мг, 0,50 ммоль), диметоксіетану (100 мл) і карбонату калію 2 M (10,07 мл, 20,14 ммоль) дегазували азотом. Реакційну суміш збовтували в закритій посудині та нагрівали в атмосфері азоту при 145 °C протягом 3 годин. Після випарювання розчинника реакційну суміш розбавляли DCM і водою, а шари розділяли. Водний шар екстрагували з DCM. Об'єднаний органічний шар промивали сольовим розчином, сушили з MgSO4, фільтрували та випарювали. Залишок очищали колонковою хроматографією на силікагелі (градієнт елюенту від 10/90 до 50/50 EtOAc/гептану). Бажані фракції збирали та випарювали, одержуючи 2,05 г (54%) проміжної сполуки 26 у вигляді білої твердої речовини після сушіння протягом ночі під вакуумом при 50 °C. 2-(2,6-Диметил-4-піридиніл)-3-фтор-5-[(2S)-2-(трифторметил)-4-морфолініл]бензолметанамін (проміжна сполука 27) і 2-(2,6-диметил-4-піридиніл)-3-фтор-5-[2-(метил)-4морфолініл]-бензолметанамін (проміжна сполука 28) O S NH2 O RS N NH2 N F3C F N F 27 N UA 109803 C2 5 (Проміжна сполука 27) (Проміжна сполука 28) Проміжні сполуки 27 і 28 одержували згідно із процедурою, використовуваною для проміжної сполуки 3, починаючи із проміжної сполуки 26 замість проміжної сполуки 2. Рацемічну проміжну сполуку 28 одержували як побічний продукт у цьому етапі (співвідношення 27:28 = 64:36). Дві проміжні сполуки використовували як суміш для синтезу кінцевих сполук 64-70 і 112-118, які розділяли за допомогою хроматографії. 2-(2,6-диметил-4-піридиніл)-3-фтор-5-[(2R)-2-(трифторметил)-4-морфолініл]бензолметанамін (проміжна сполука 29) O R NH2 N F3C F 10 15 N (Проміжна сполука 29) Проміжна сполука 29 одержували згідно із процедурами, використовуваними для проміжної сполуки 27, з використанням проміжної сполуки 23 замість проміжної сполуки 22. Рацемічну проміжну сполуку 28 також одержували як побічний продукт у цьому етапі (співвідношення 29:28 = 88:12). Дві проміжні сполуки використовували як суміш для синтезу кінцевих сполук 56-59, 7173 і 112-118, які розділяли за допомогою хроматографії. 3-Фтор-5-[3-(трифторметил)-1-піперидиніл]-бензoнітрил (проміжна сполука 30) N CN F3C F 20 25 (Проміжна сполука 30) Суміш 3,5-дифторбензoнітрилу (1,38 г, 9,9 ммоль), 3-трифторметилпіперидину (1,82 г, 11,88 ммоль) і діізопропілетиламіну (2,56, 14,85 ммоль) в ацетонітрилі (20 мл) збовтували в пробірці для проведення реакцій під тиском при 150 °C протягом 72 годин. Реакційну суміш випарювали, поглинали водою/DCM і підлужували з K2CO3. Органічний шар розділяли, а водний шар екстрагували ще раз із DCM. Об'єднані органічні шари сушили над MgSO 4, фільтрували та випарювали. Залишок очищали колонковою хроматографією на силікагелі (елюент: градієнт гептан/DCM 30/70 - 70/30) у якості елюенту. Бажані фракції випарювали, одержуючи 2,5 г проміжної сполуки 30 (93%) після сушіння у вакуумній печі при 50 °C протягом ночі. 2-(2,6-Диметил-4-піридиніл)-3-фтор-5-[3-(трифторметил)-1-піперидиніл]-бензолметанамін (проміжна сполука 31) NH2 N F3C F 30 N (Проміжна сполука 31) Проміжну сполуку 31 одержували згідно із процедурами, використовуваними для проміжної сполуки 27, починаючи із проміжної сполуки 30 замість проміжної сполуки 24. 28
ДивитисяДодаткова інформація
Назва патенту англійською(pyridin-4-yl)benzylamides as allosteric modulators of alpha 7 nachr
Автори англійськоюde Boeck, Benoit, Christian, Albert, Ghislain, Rombouts, Geert, Leenaerts, Joseph, Elisabeth, Macdonald, Gregor, James
Автори російськоюде Бек Бенойт Кристиан Альберт Гислейн, Ромбутс Гирт, Линаертс Джозеф Элизабет, Макдональд Грегор Джеймс
МПК / Мітки
МПК: A61P 25/14, A61K 31/44, C07D 413/10, C07D 405/12, C07D 413/12, C07D 213/82, A61P 1/00, A61P 25/28, A61P 17/06, A61P 25/16, C07D 401/12, C07D 213/40, C07D 413/14, A61P 25/18, A61P 25/34
Мітки: піридин-4-іл)бензиламіди, nachr, модулятори, алостеричні, альфа-7
Код посилання
<a href="https://ua.patents.su/59-109803-piridin-4-ilbenzilamidi-yak-alosterichni-modulyatori-alfa-7-nachr.html" target="_blank" rel="follow" title="База патентів України">(піридин-4-іл)бензиламіди як алостеричні модулятори альфа-7 nachr</a>
Попередній патент: Похідні біцикло[3.2.1]октиламіду та їх застосування
Наступний патент: 2-метоксипіридин-4-ільні похідні
Випадковий патент: Установка для водопостачання міського населення смт комиш-зоря












