Похідні піролопіридину та їх застосування як модуляторів ppar-рецепторів
Номер патенту: 92026
Опубліковано: 27.09.2010
Автори: Бубіа Бенаїсса, Барт Мартін, Пупарден-Олів'є Олівія, Лєжондр Крістіан, Бене Жан, Доде П'єр
Формула / Реферат
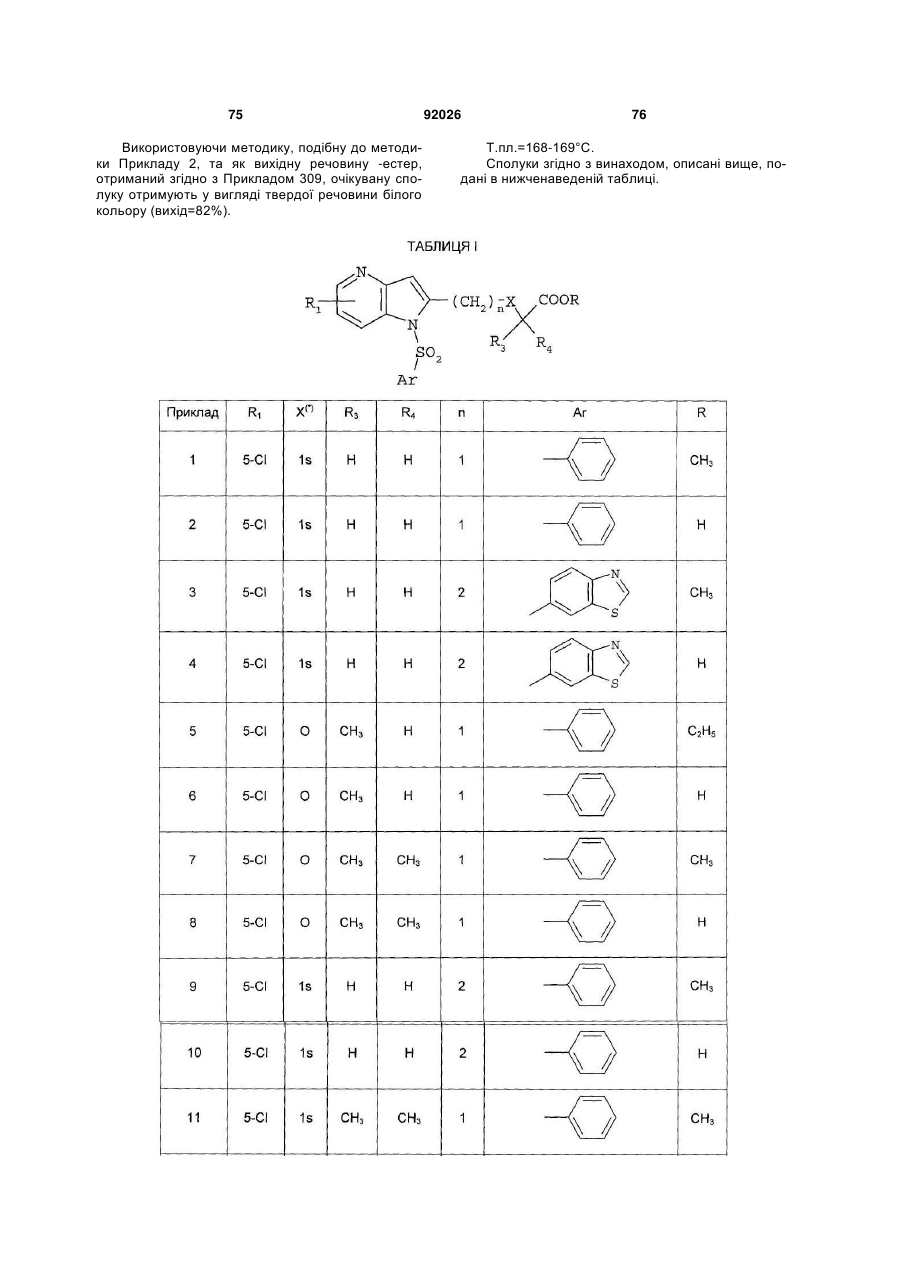
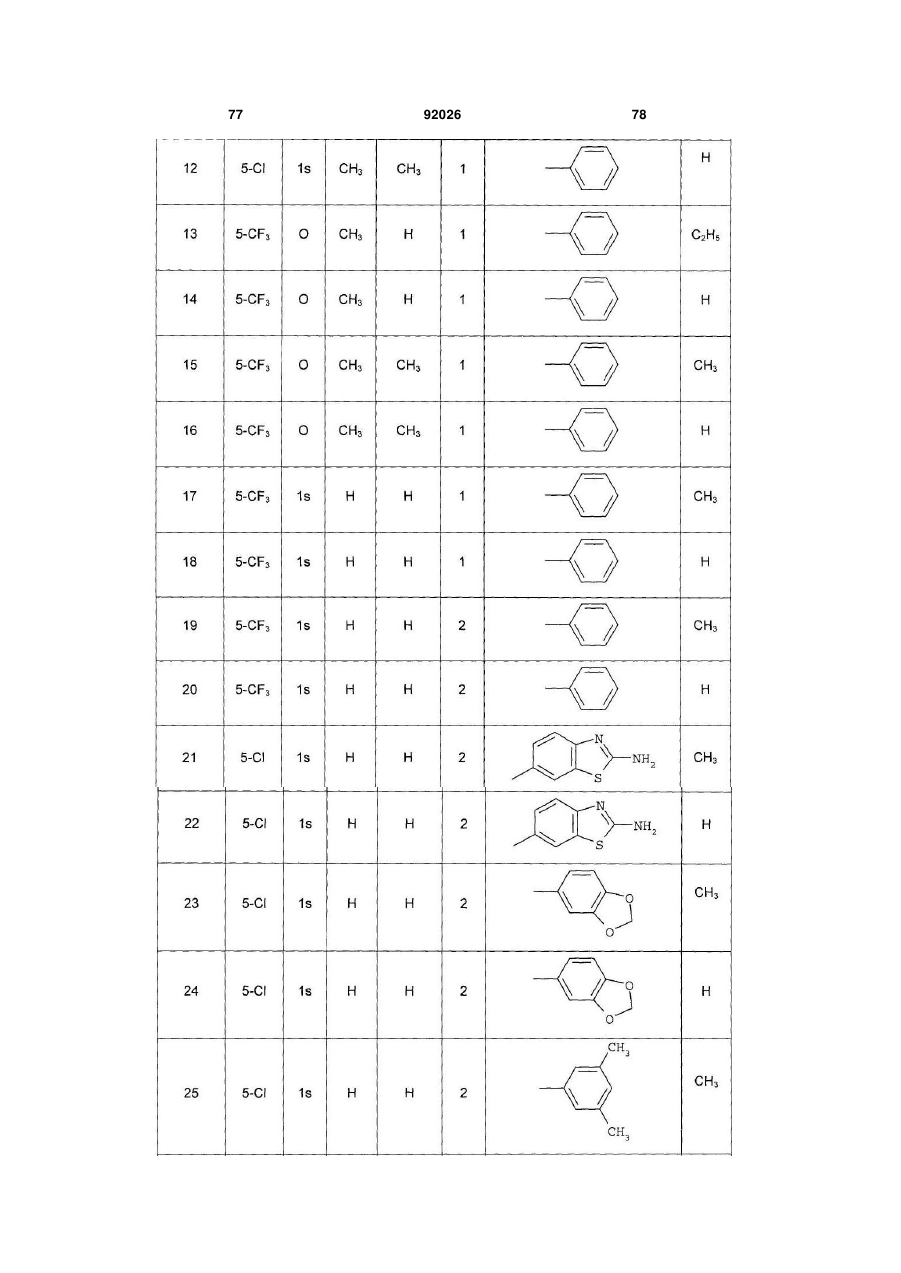
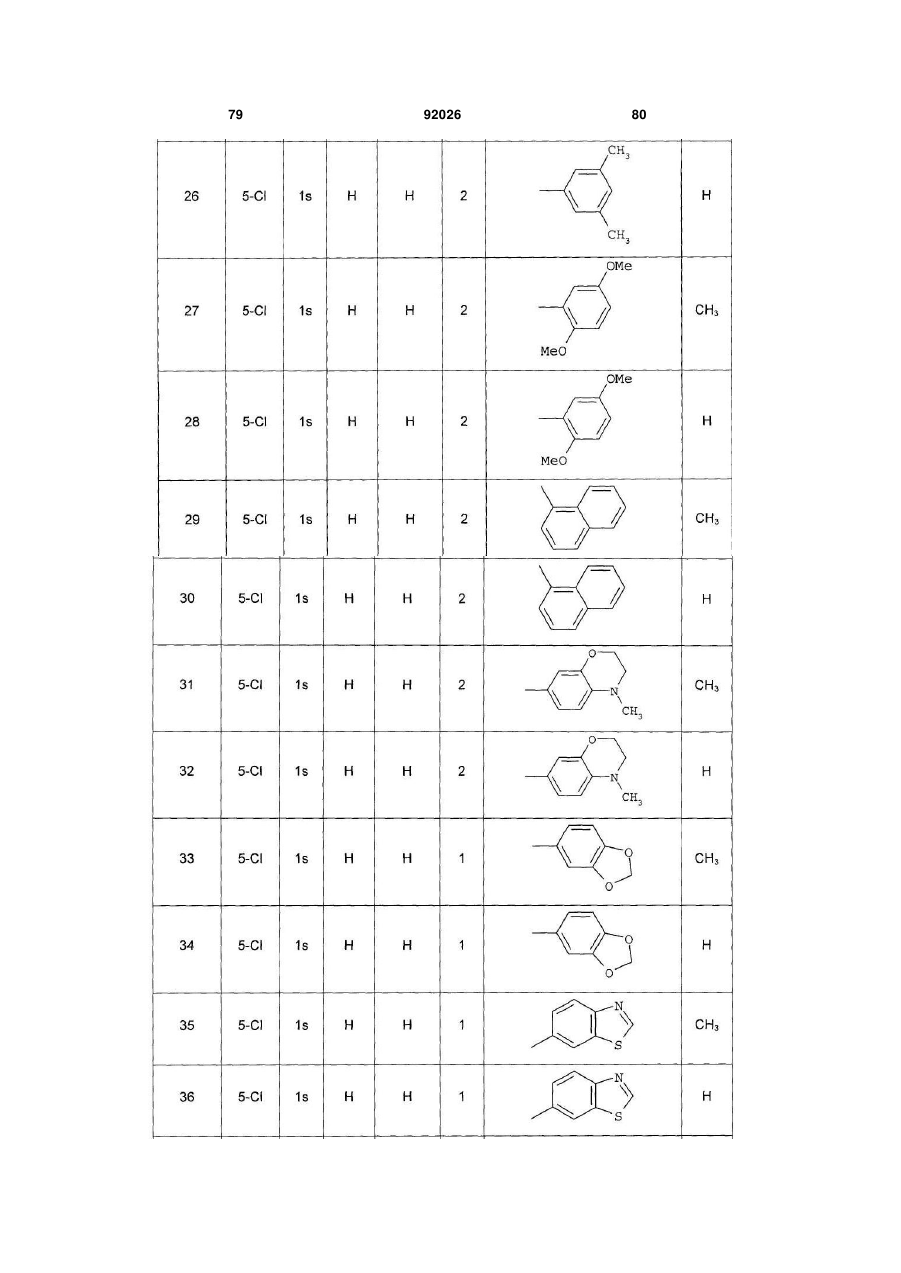
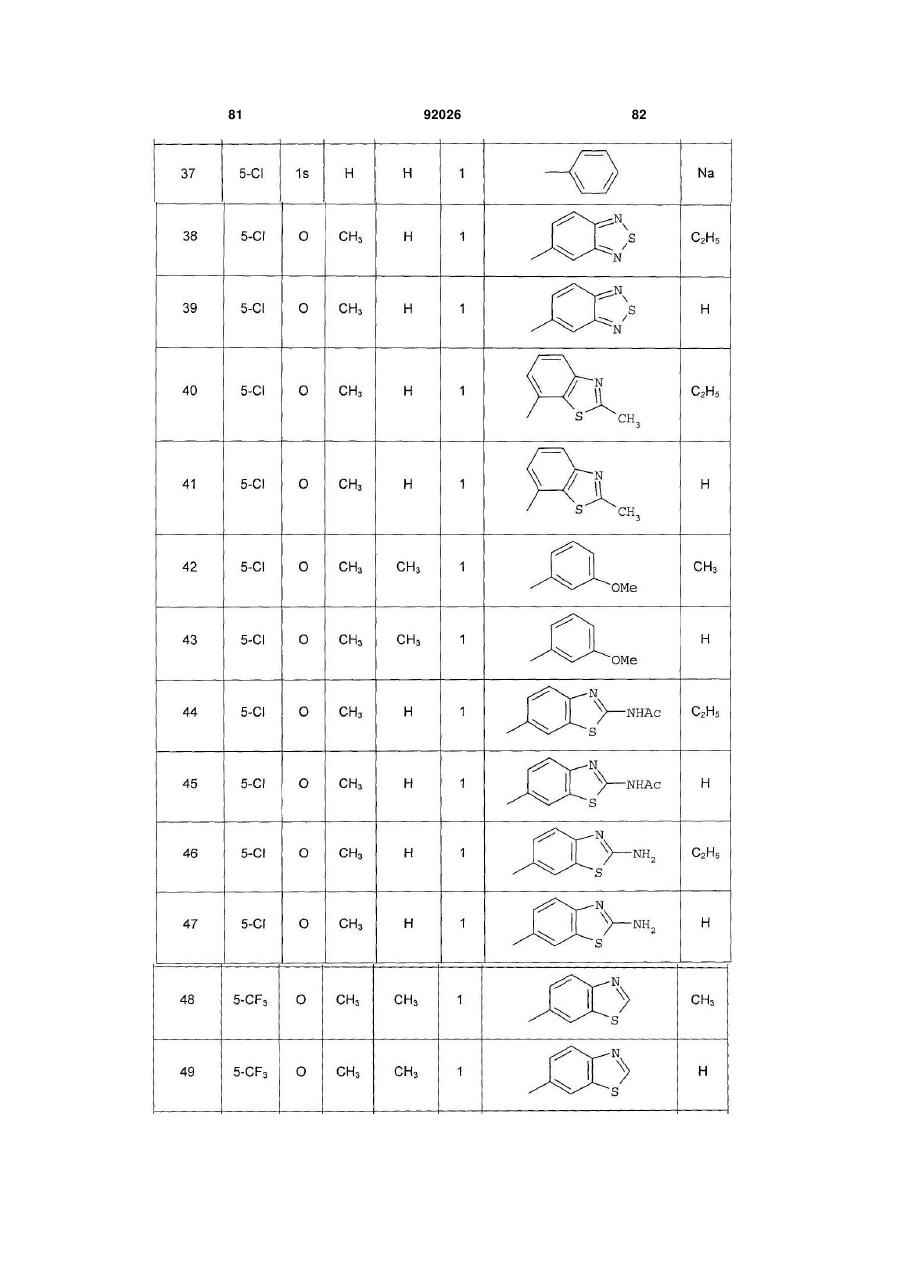
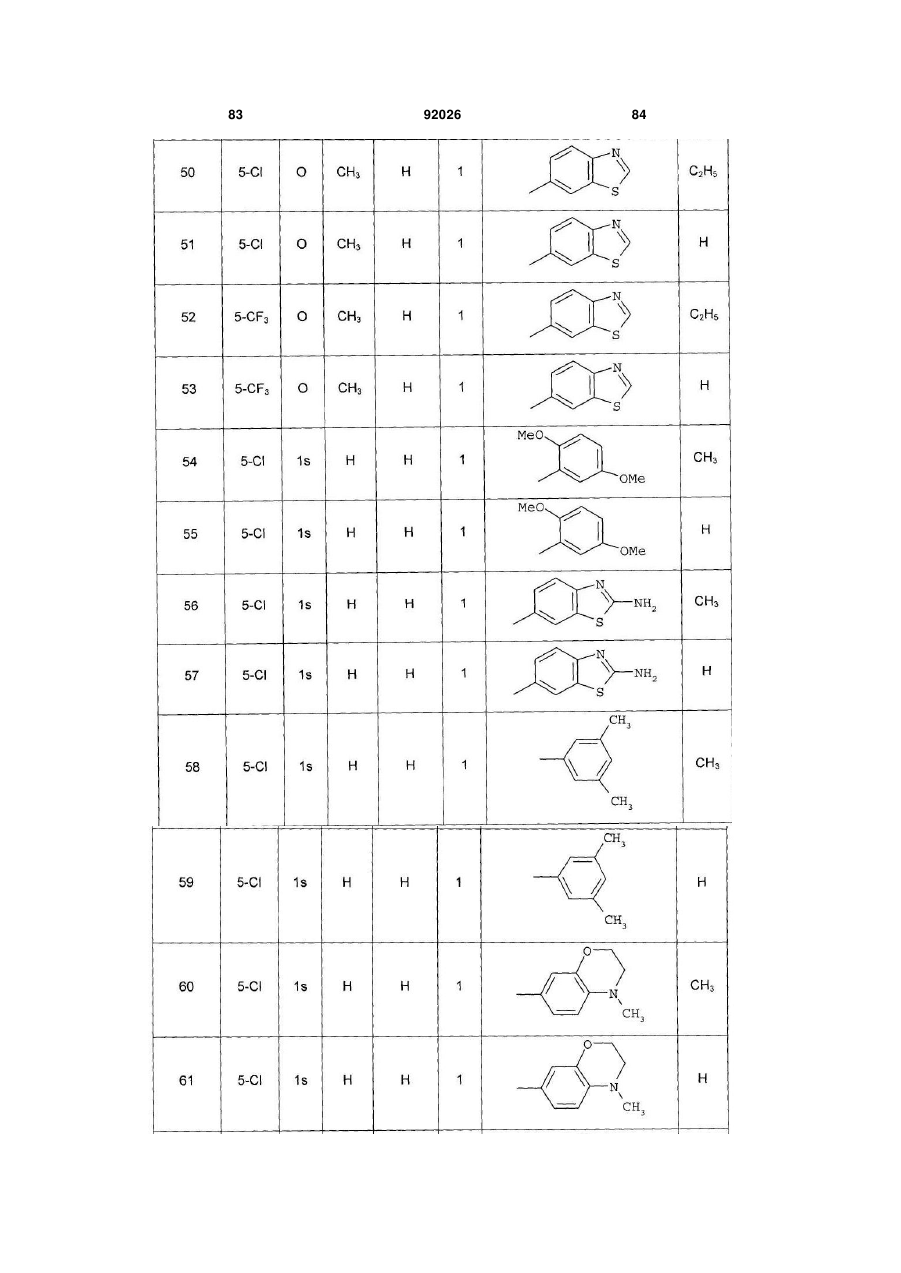
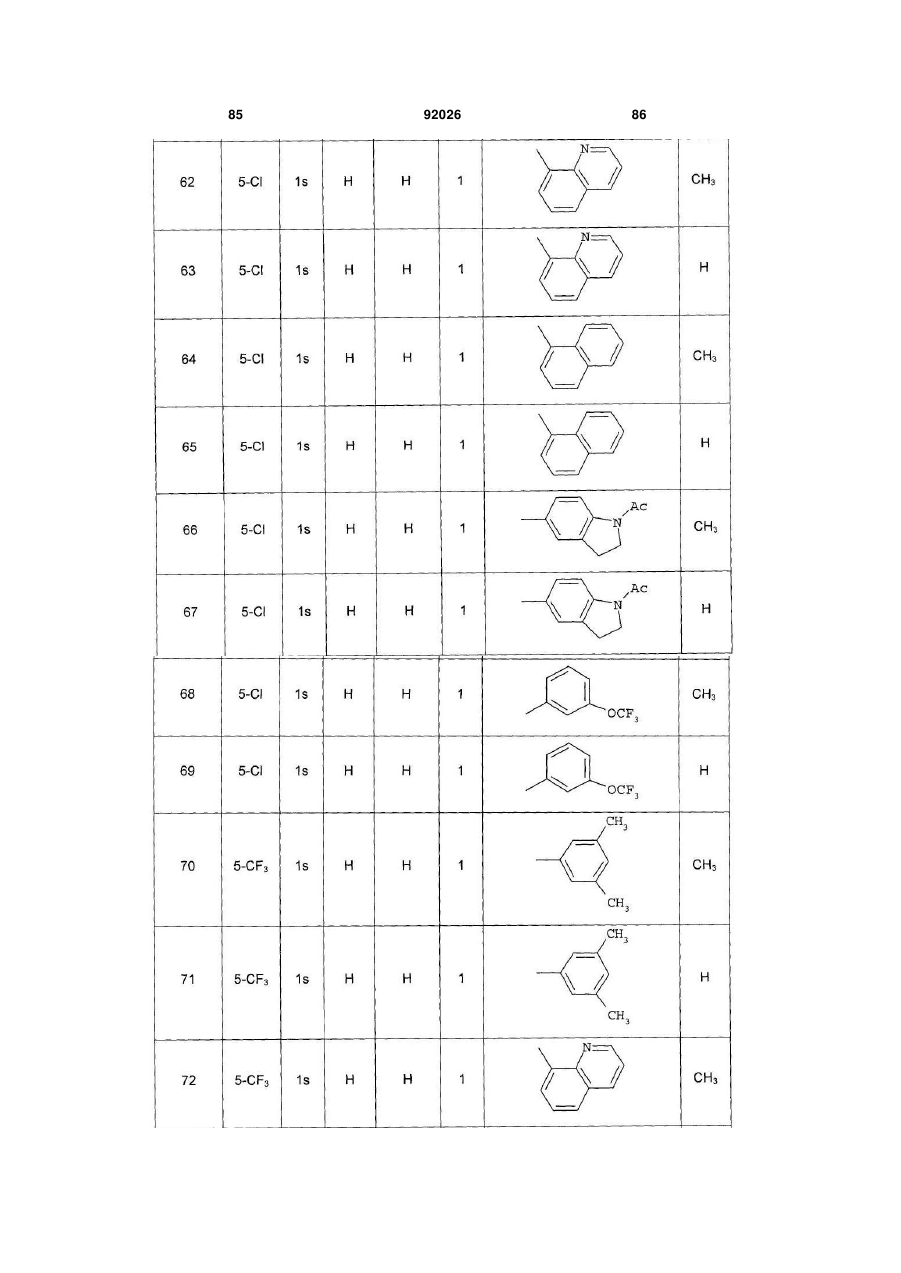
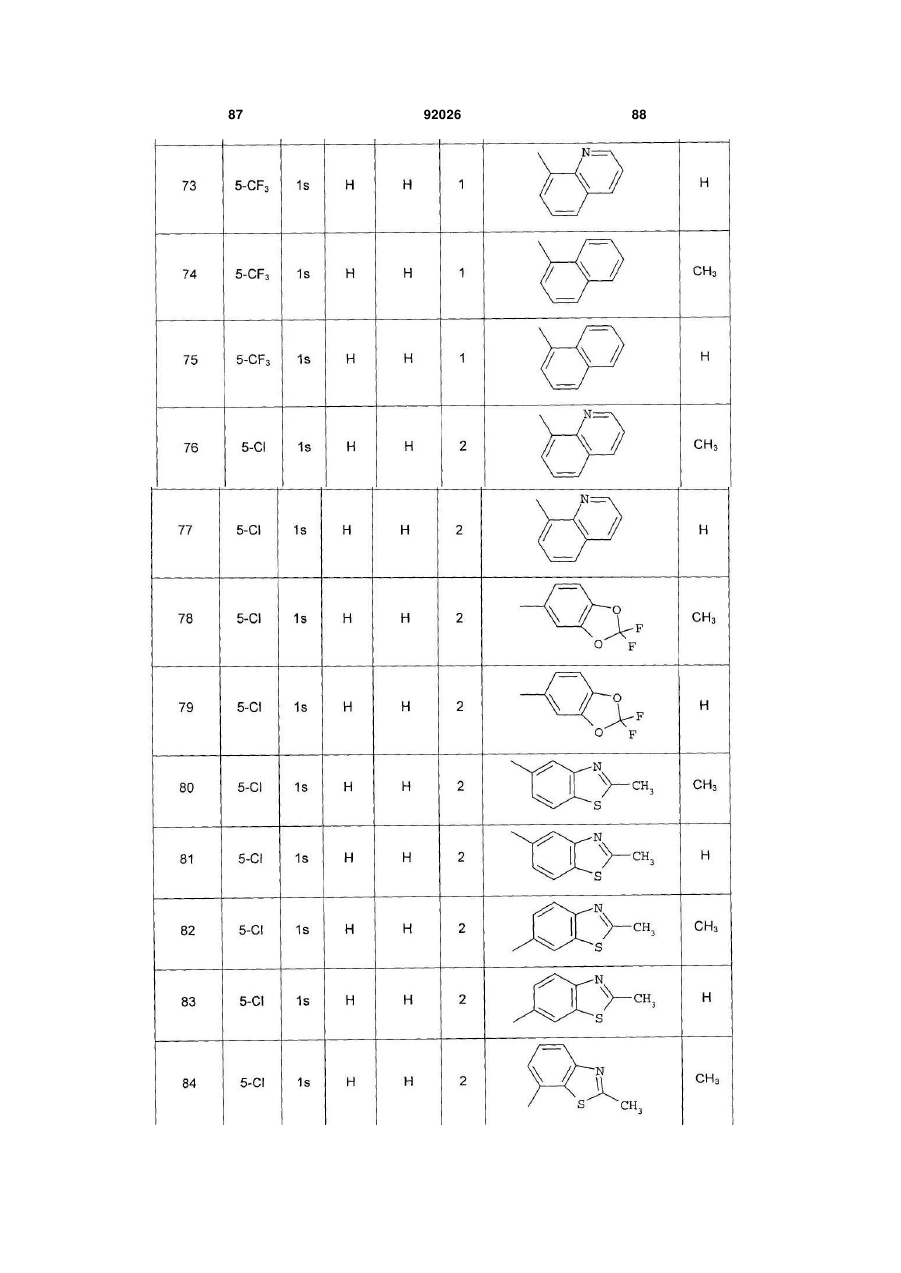
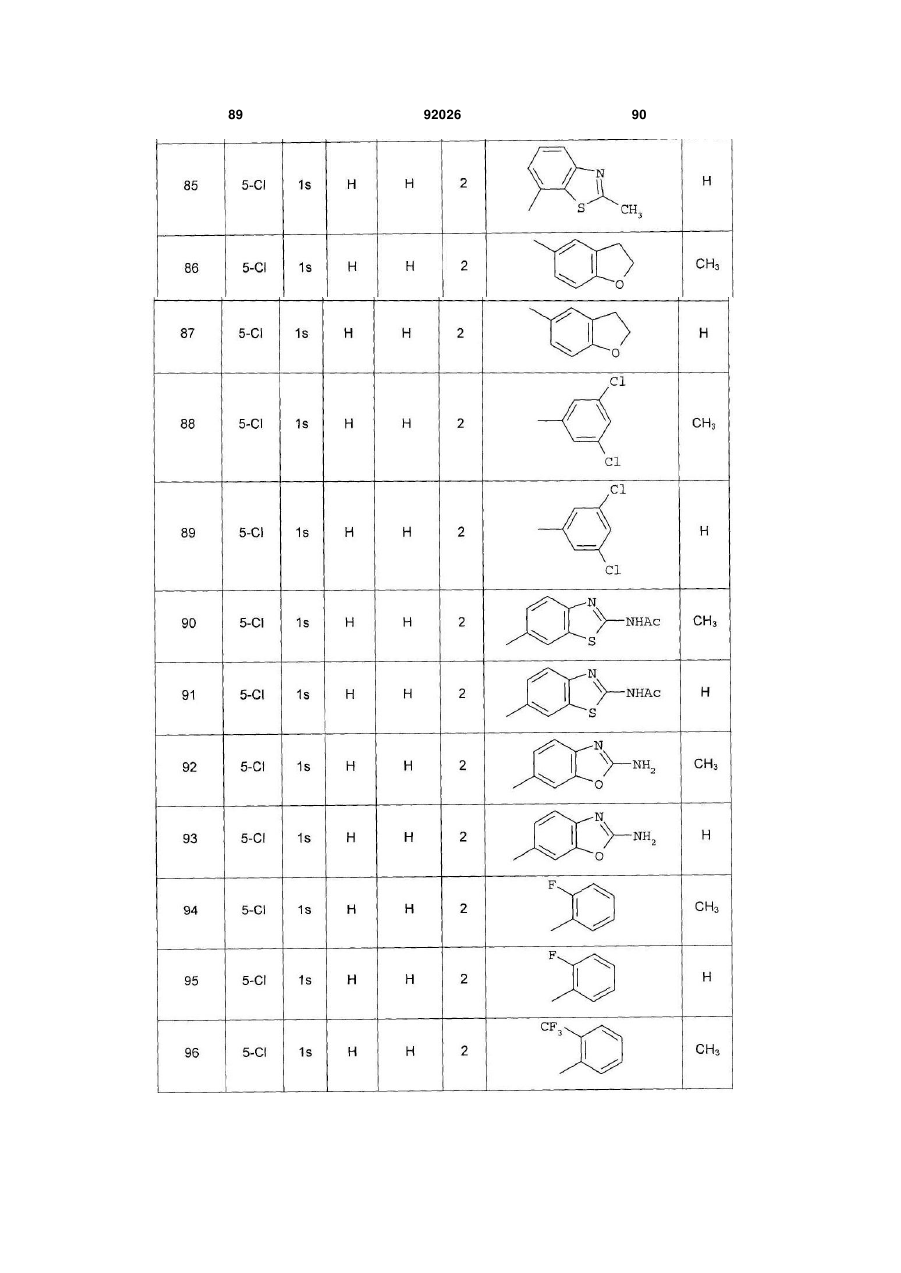
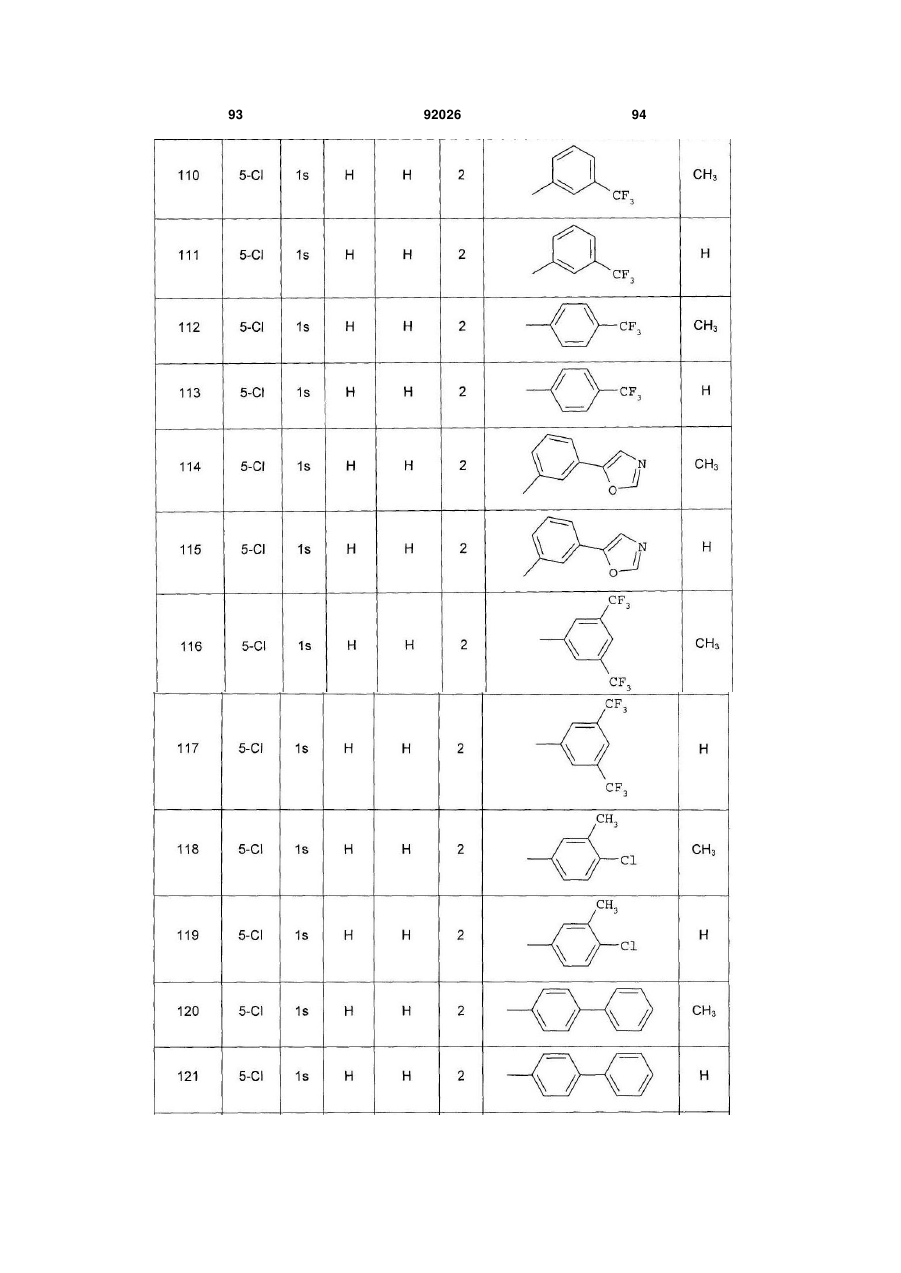
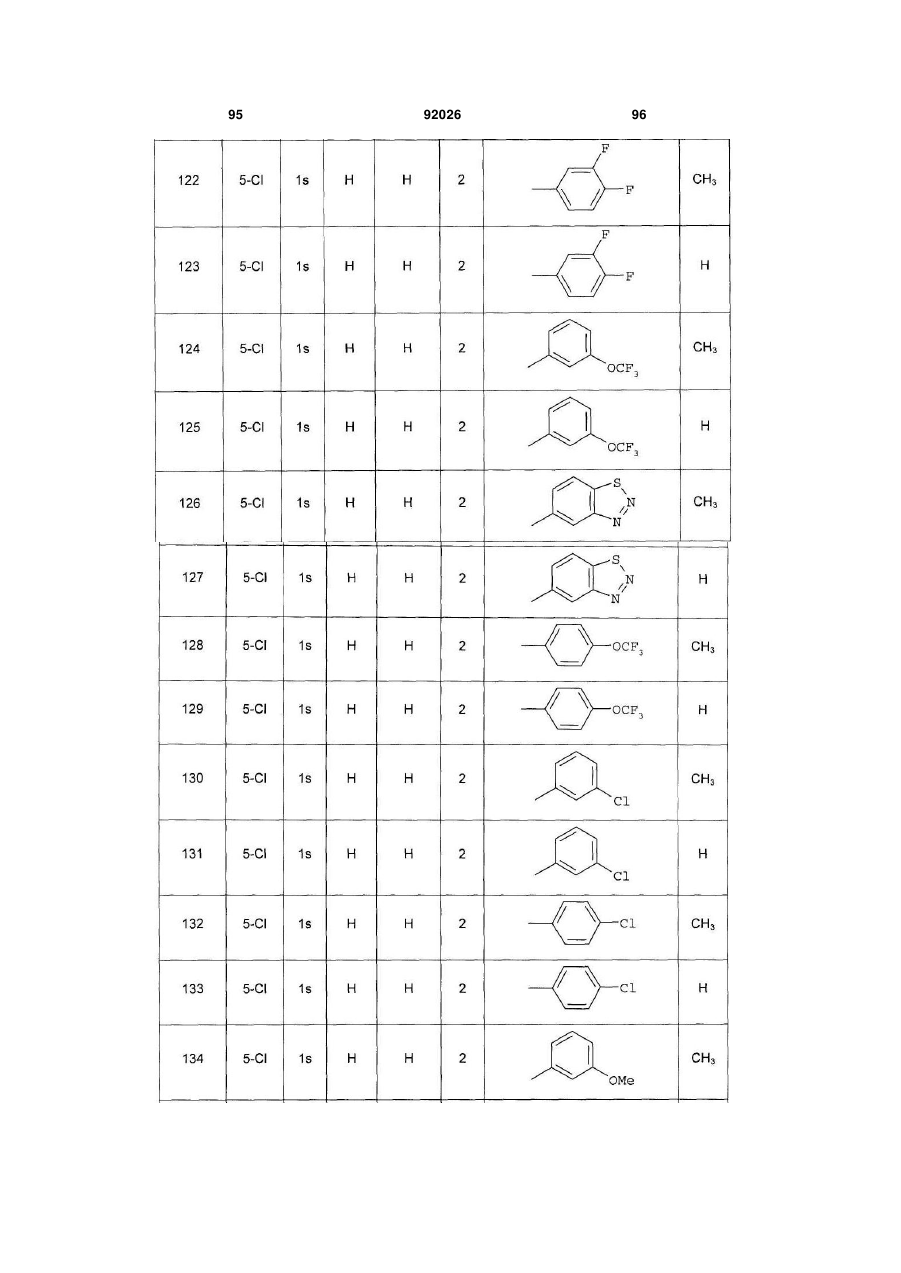
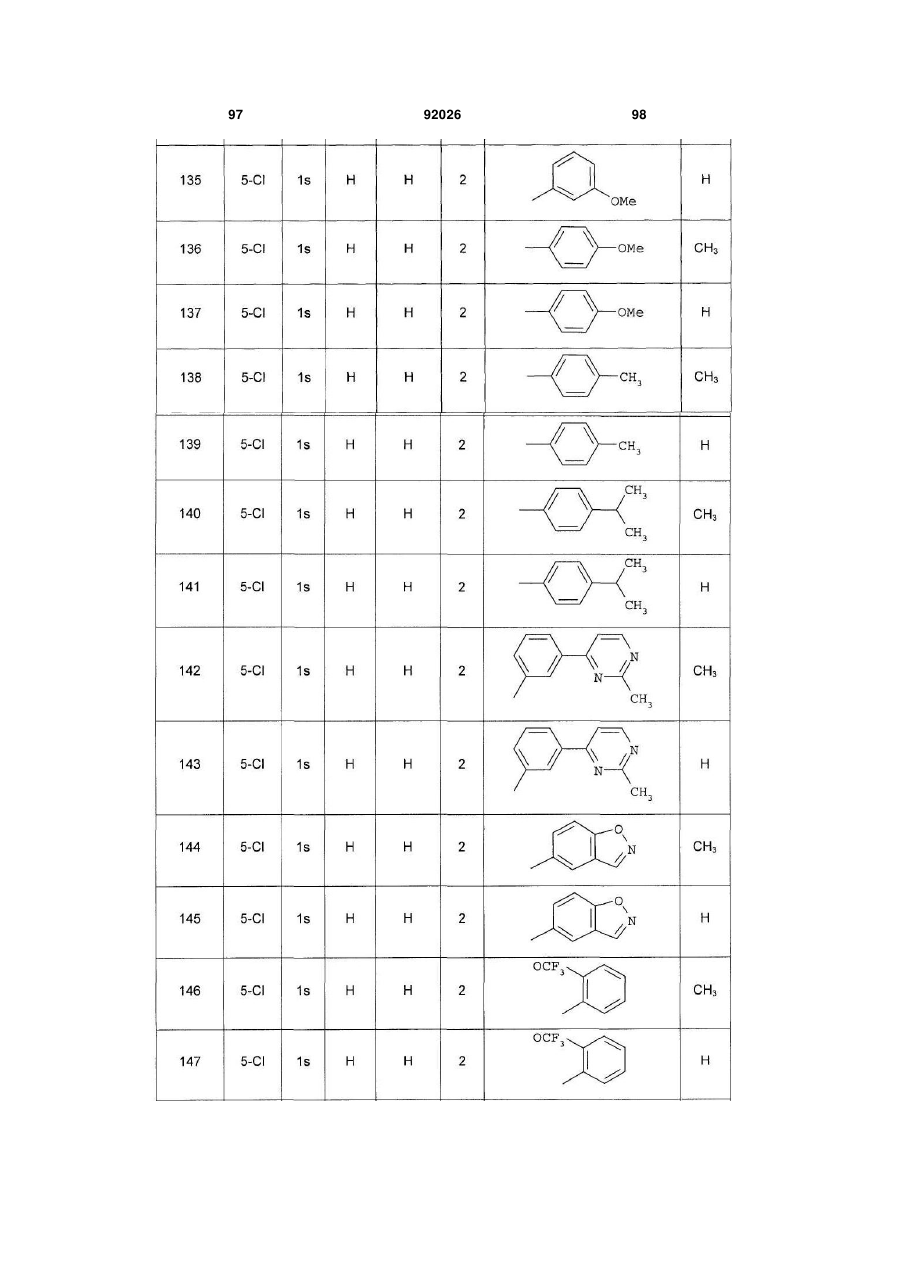
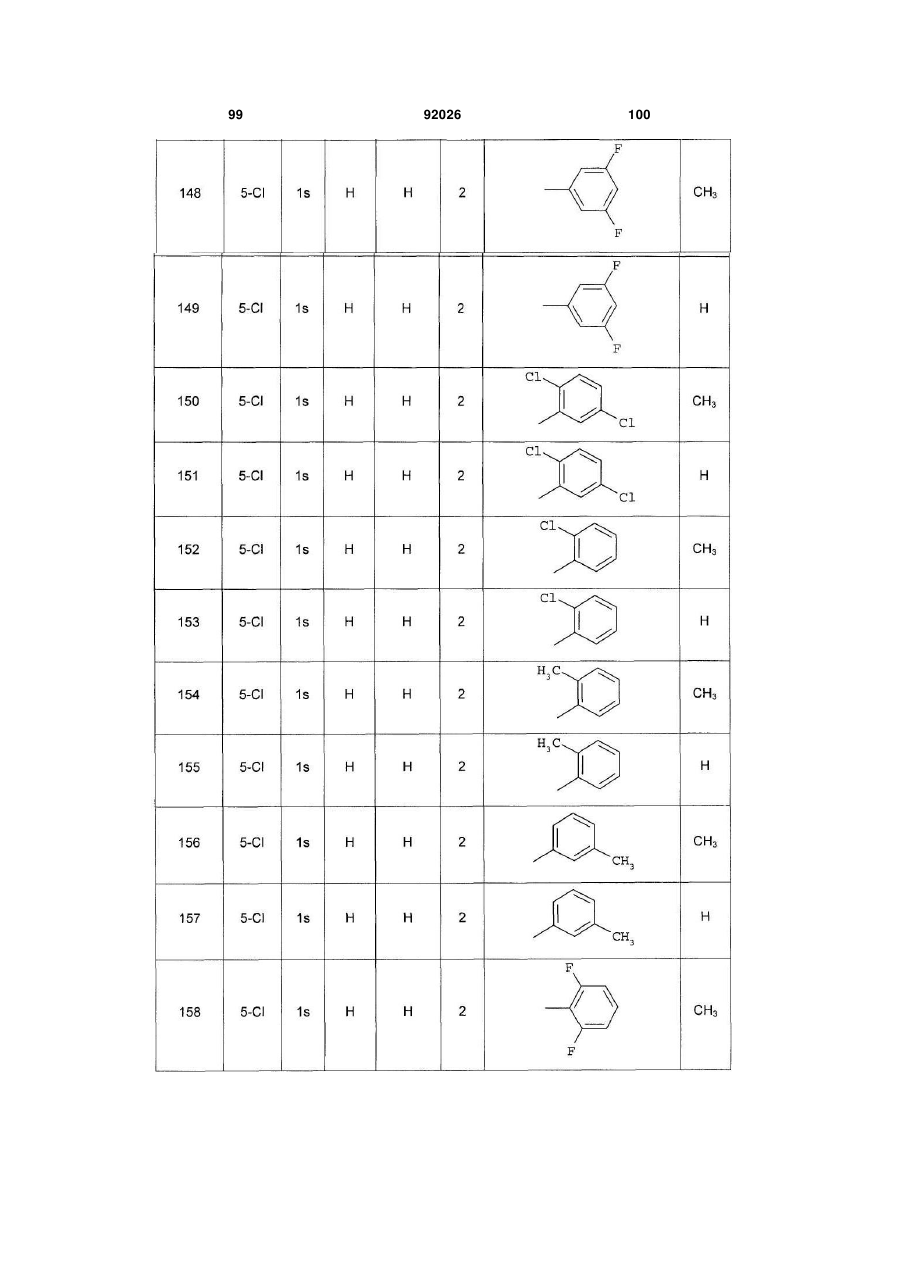
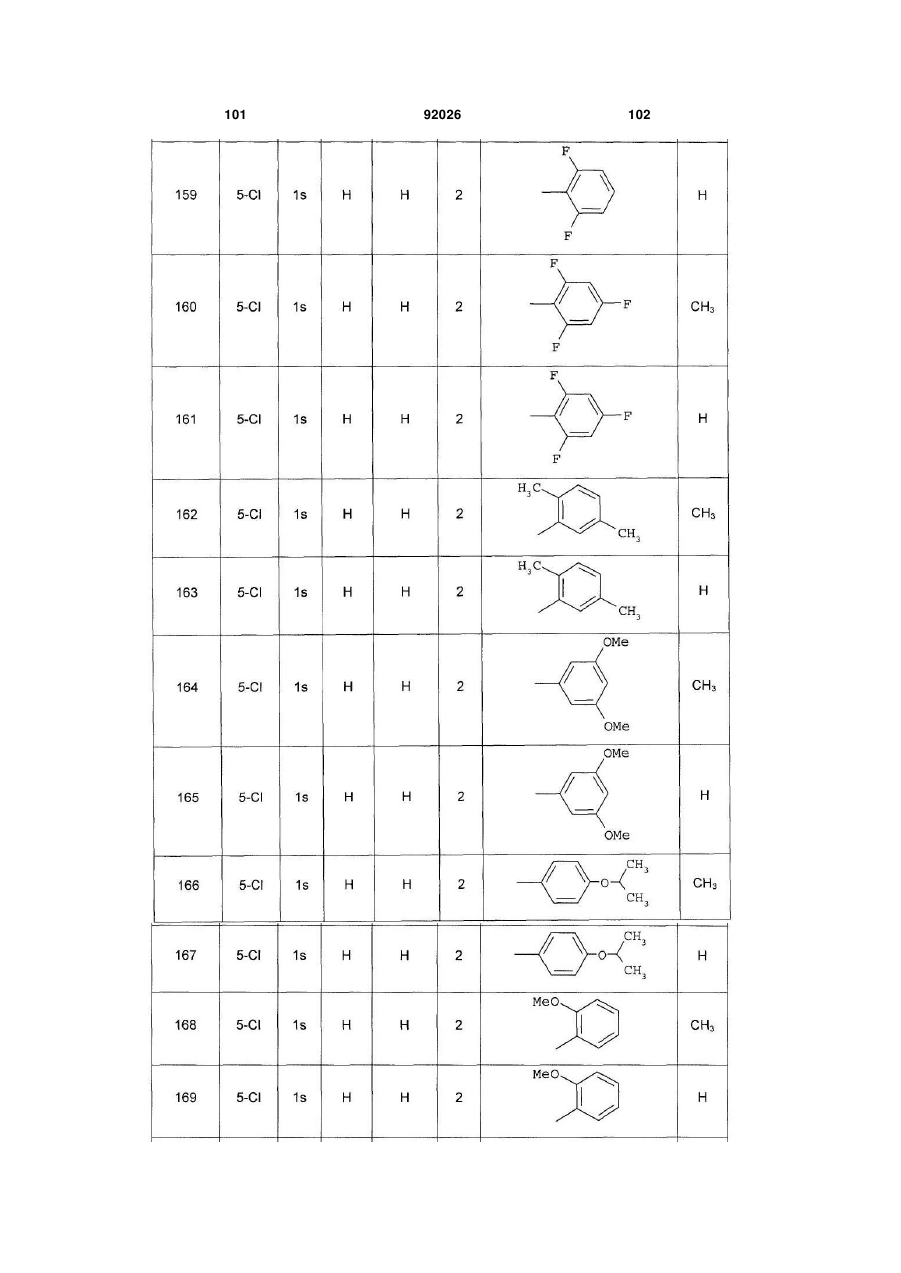
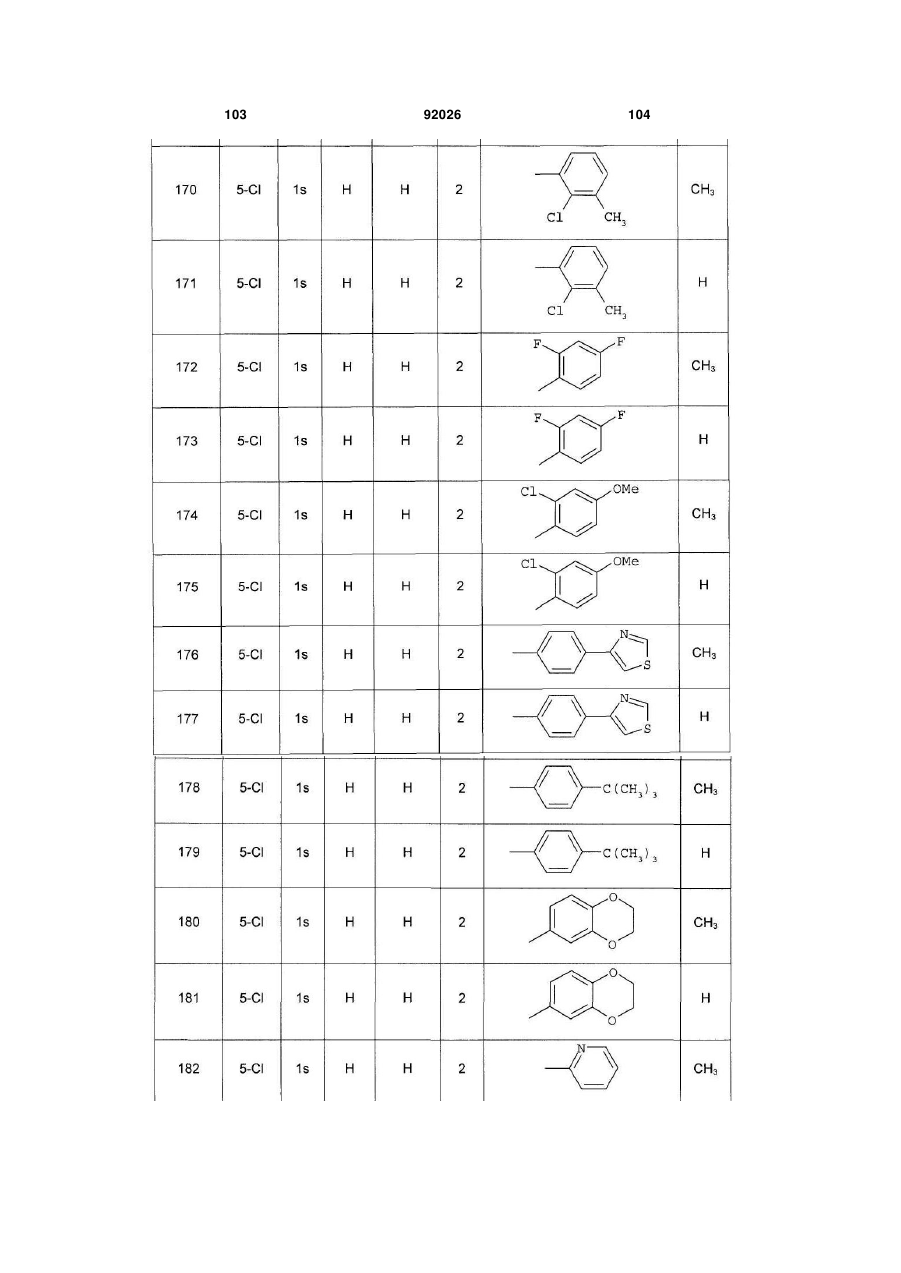
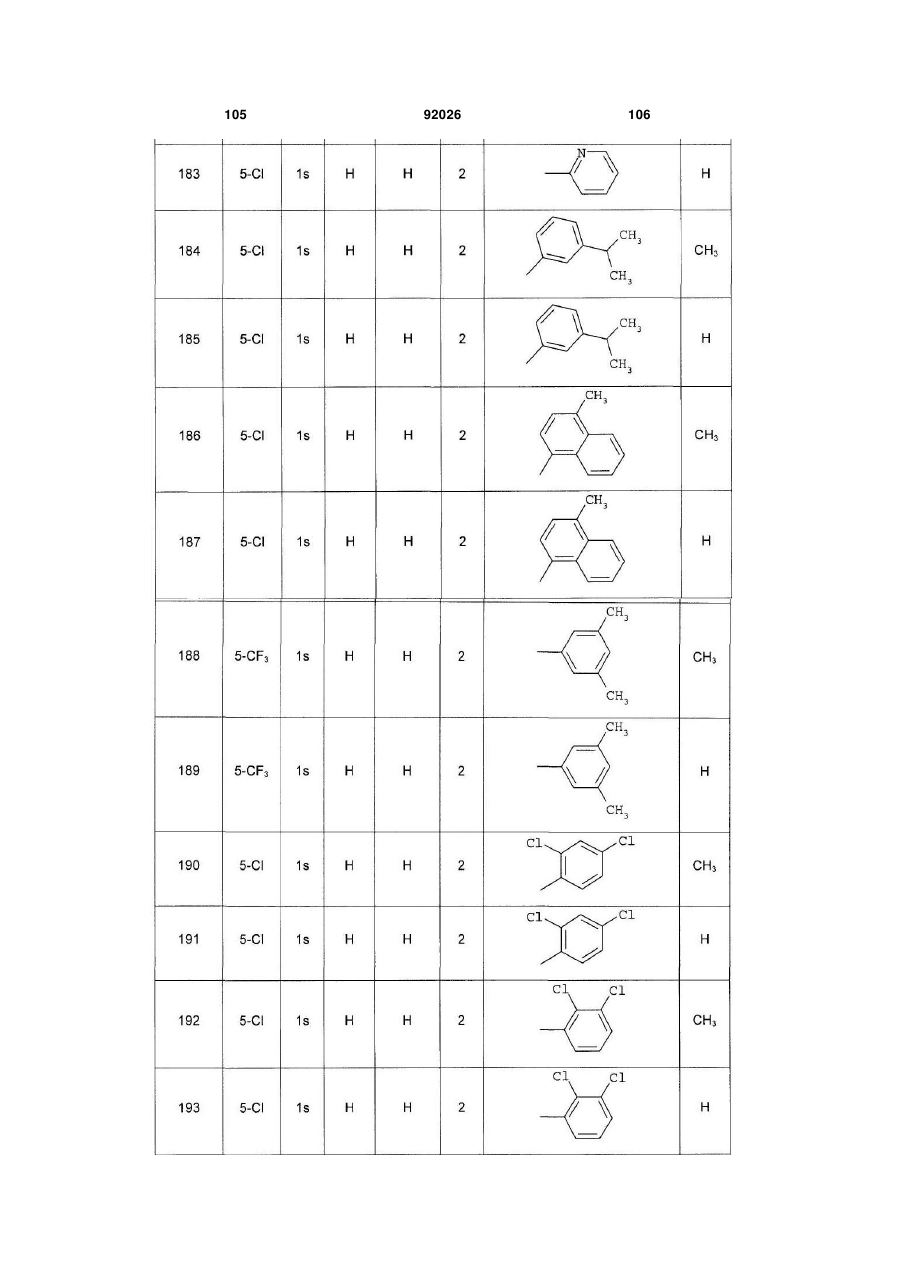
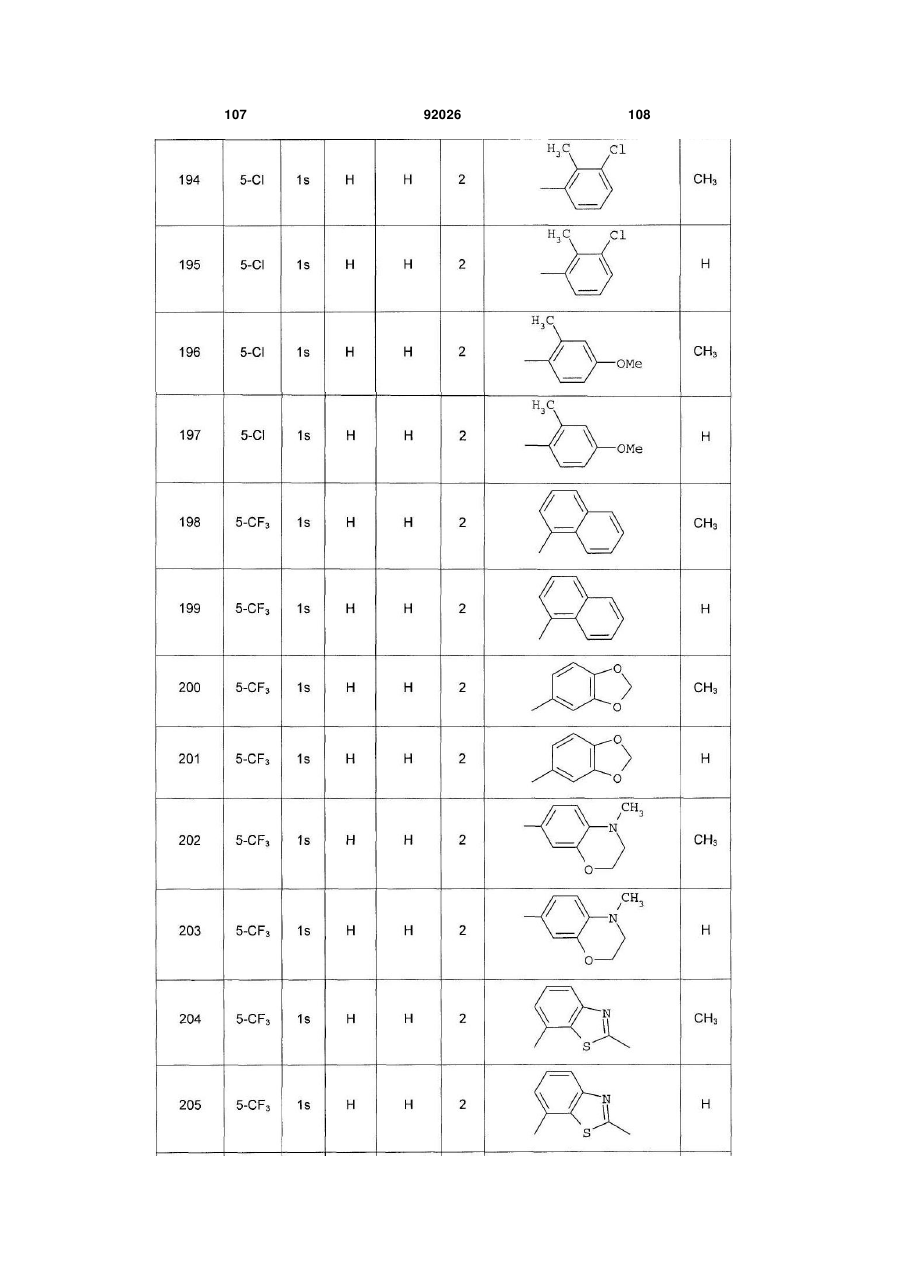
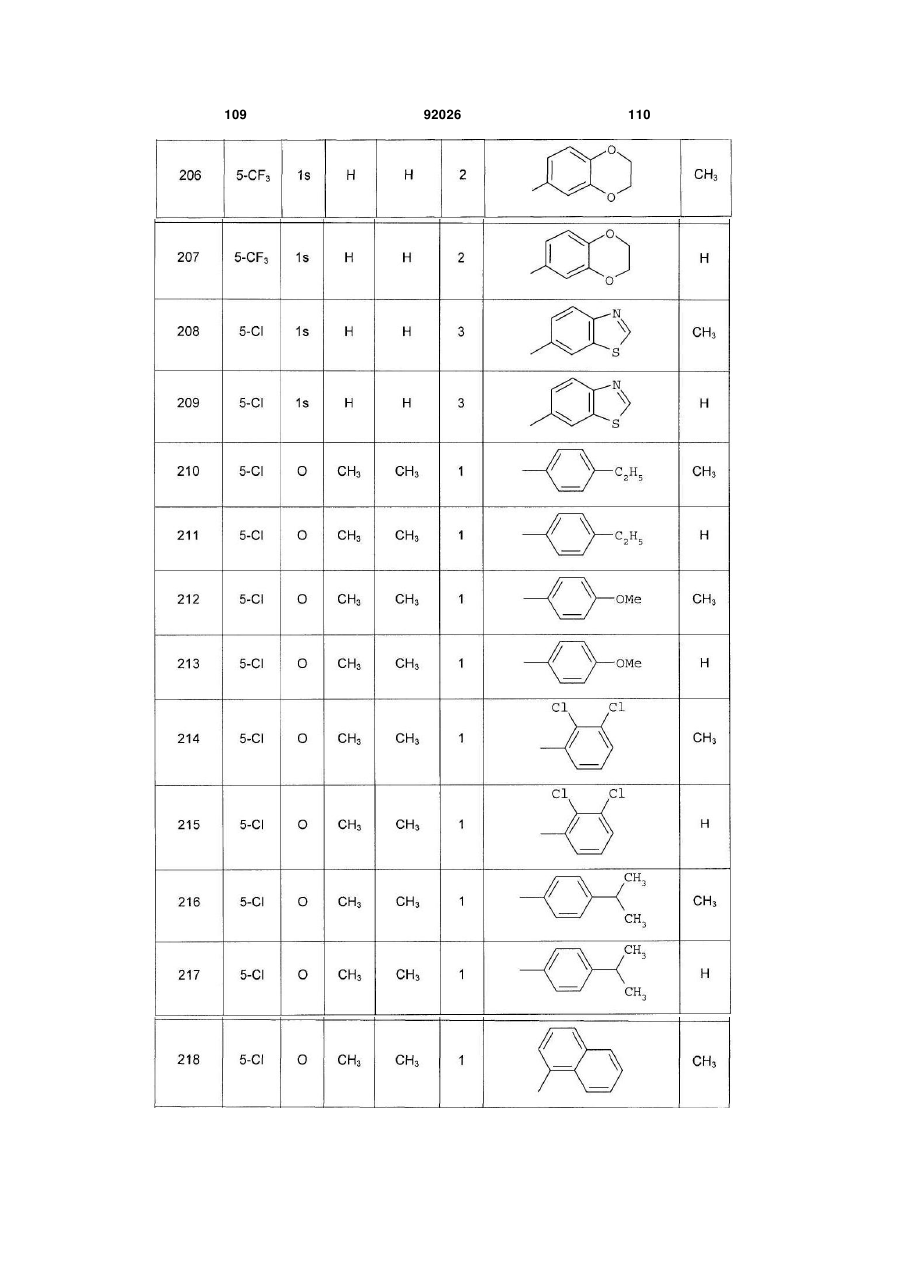
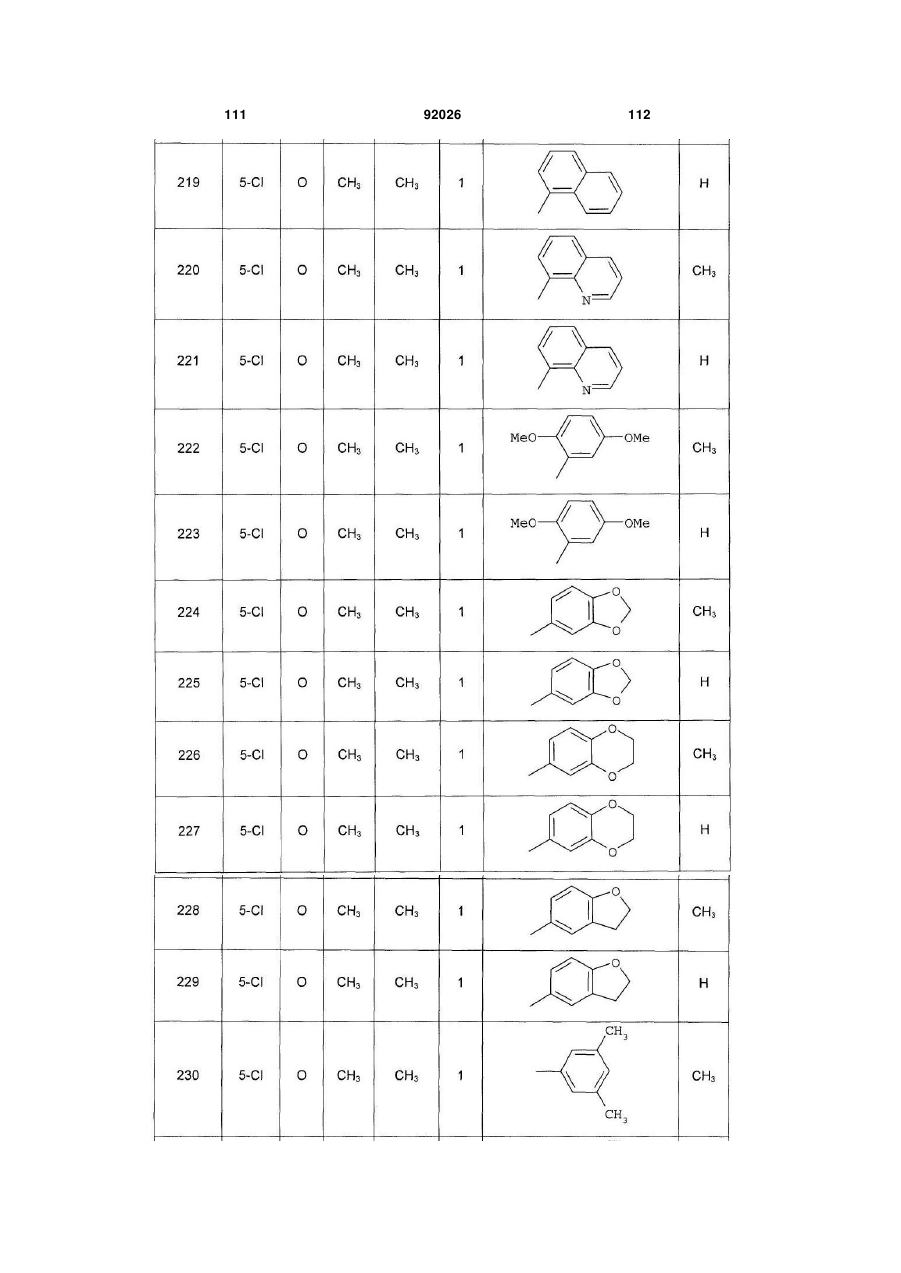
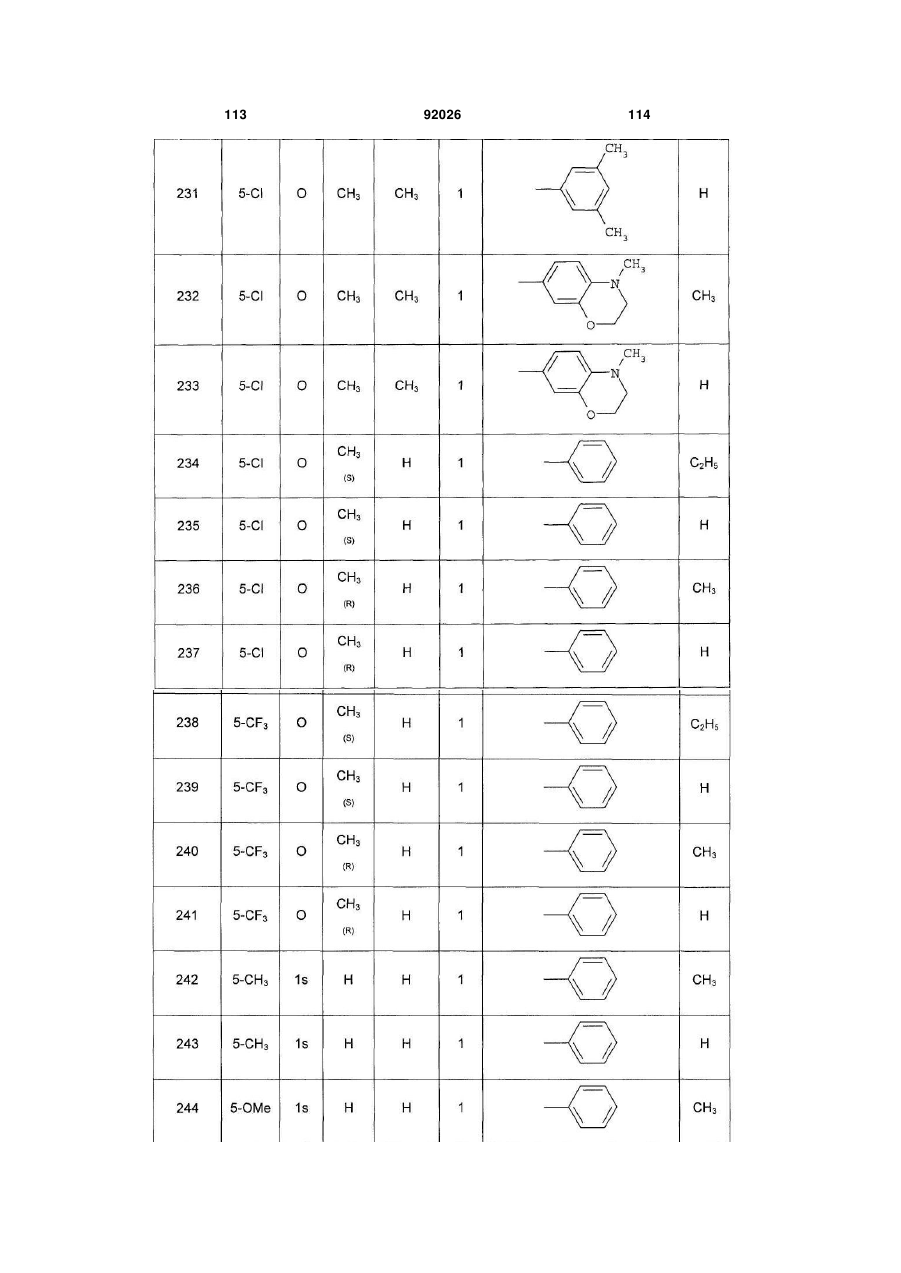
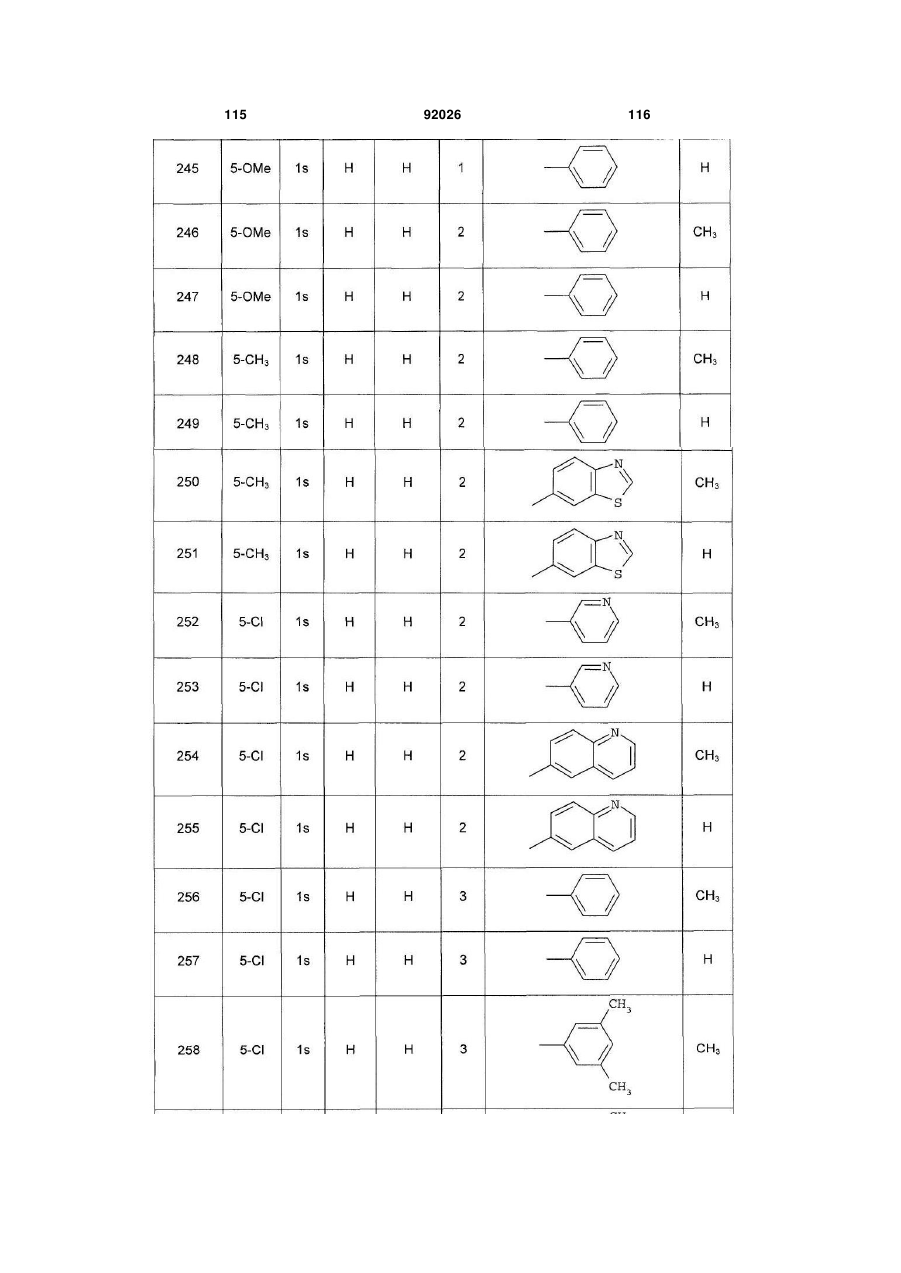
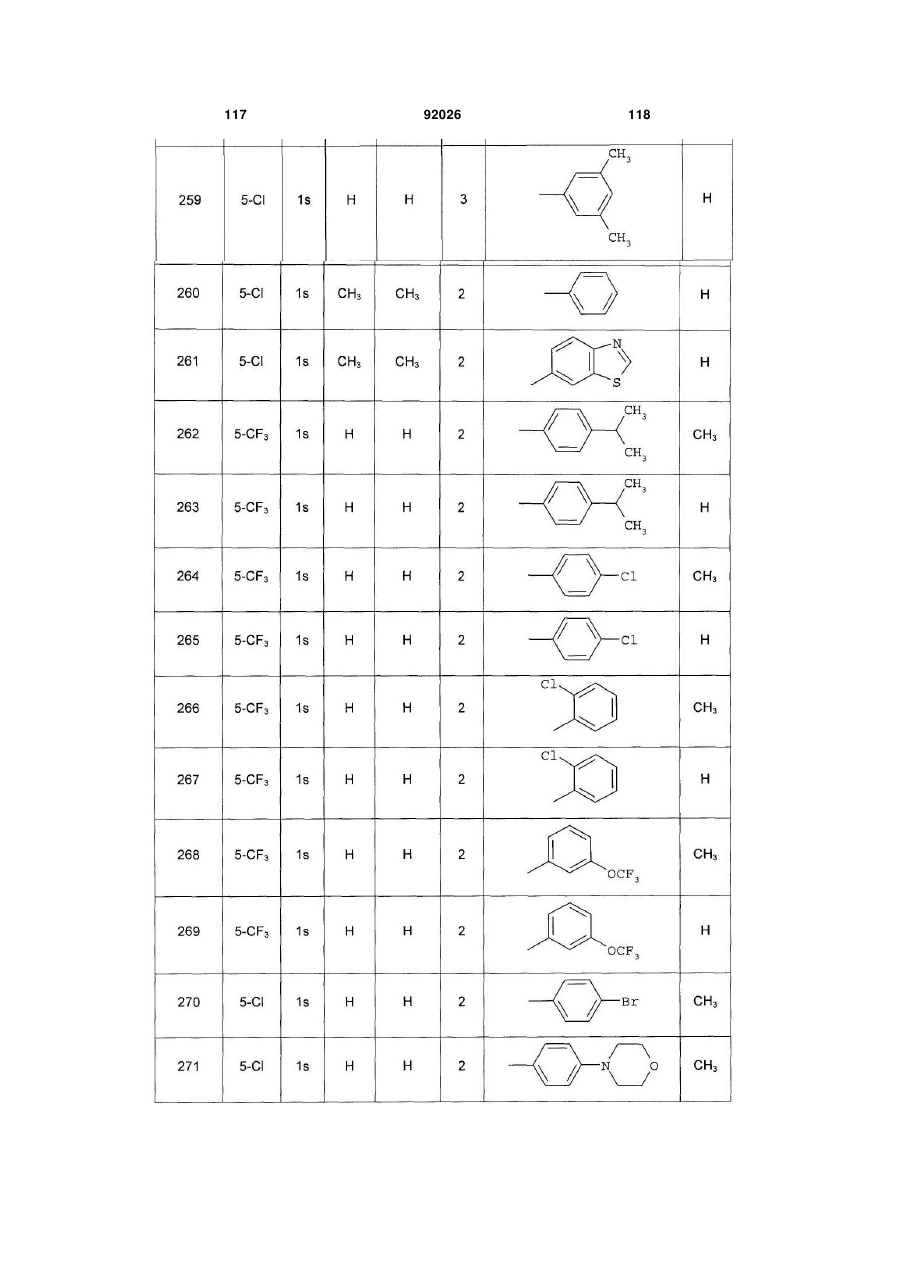
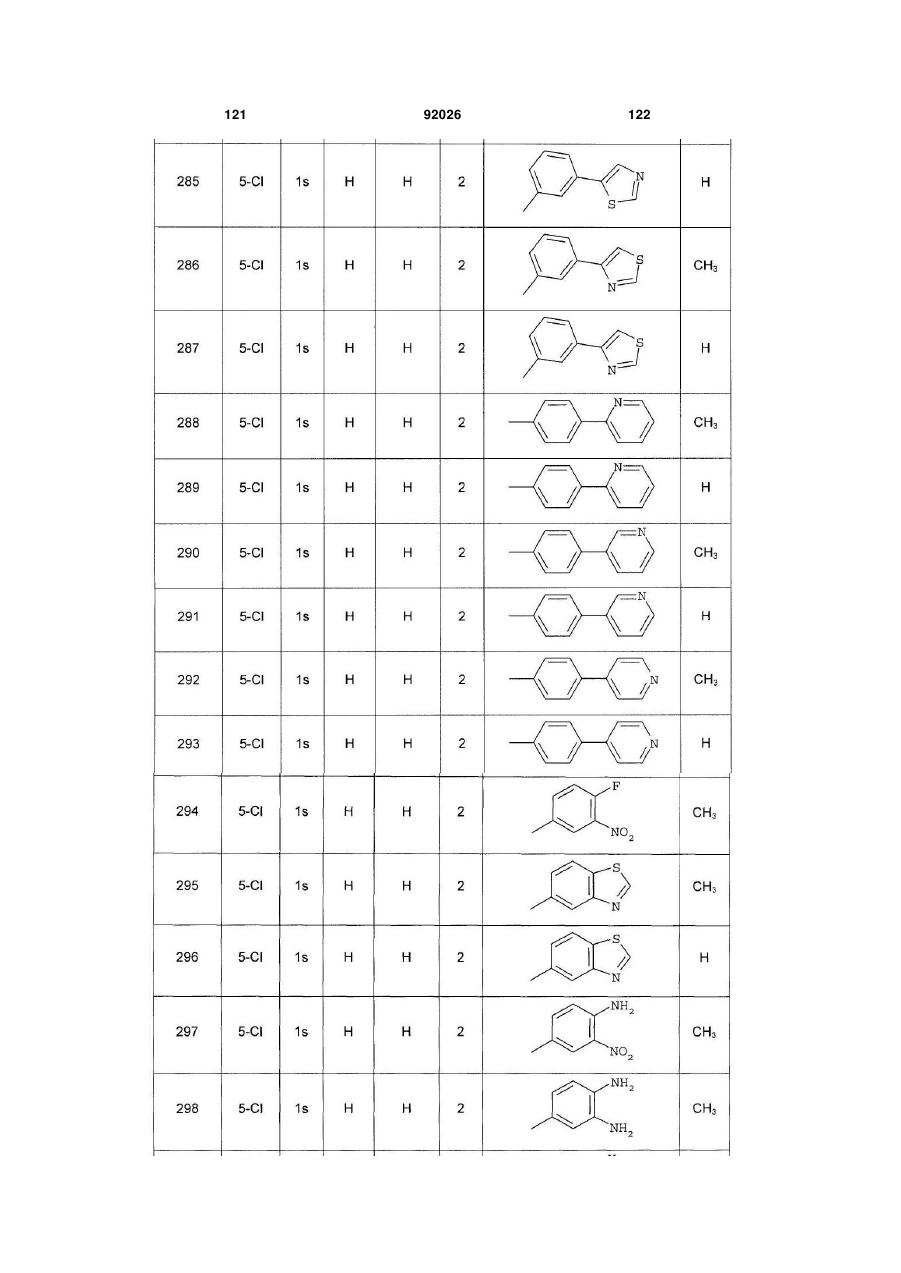
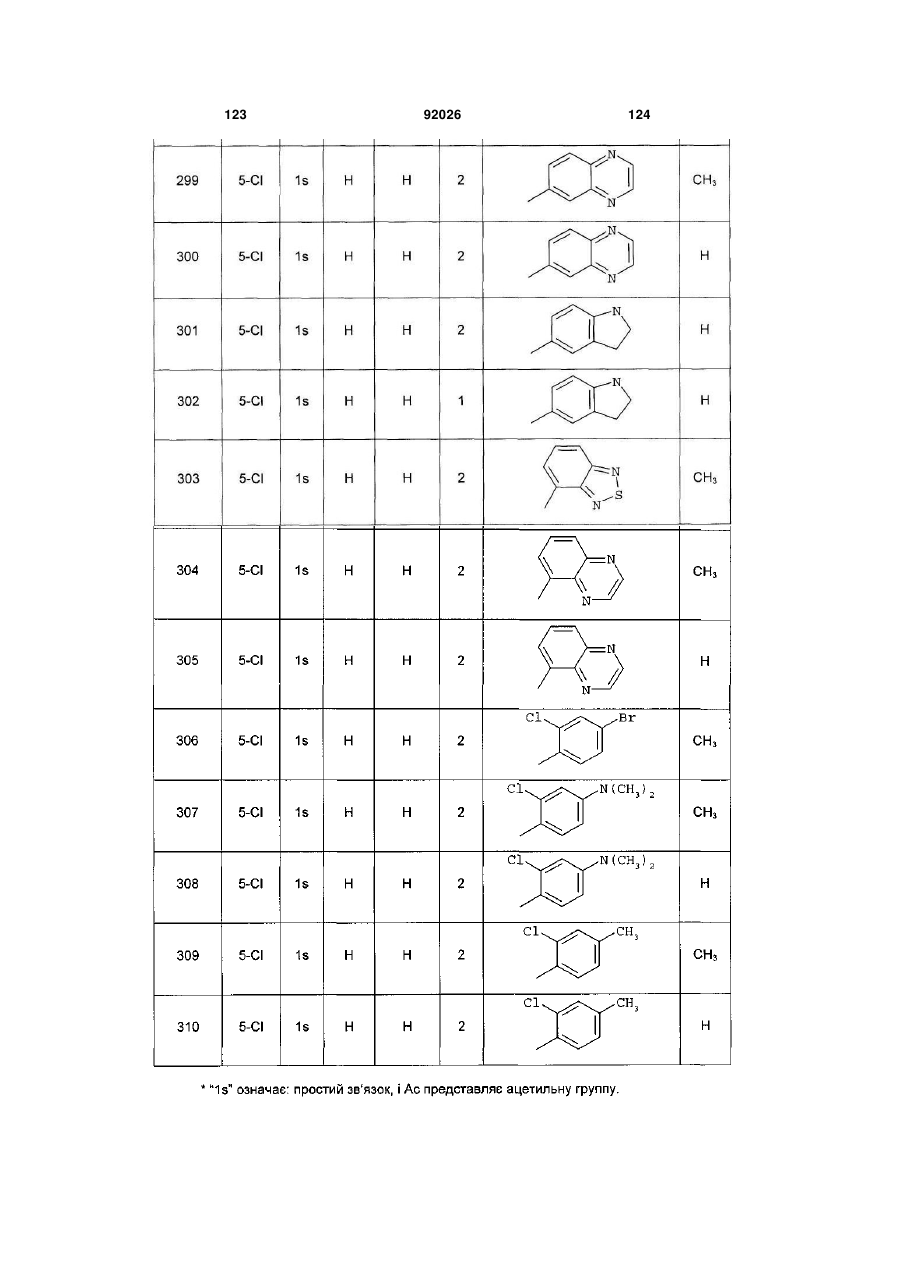
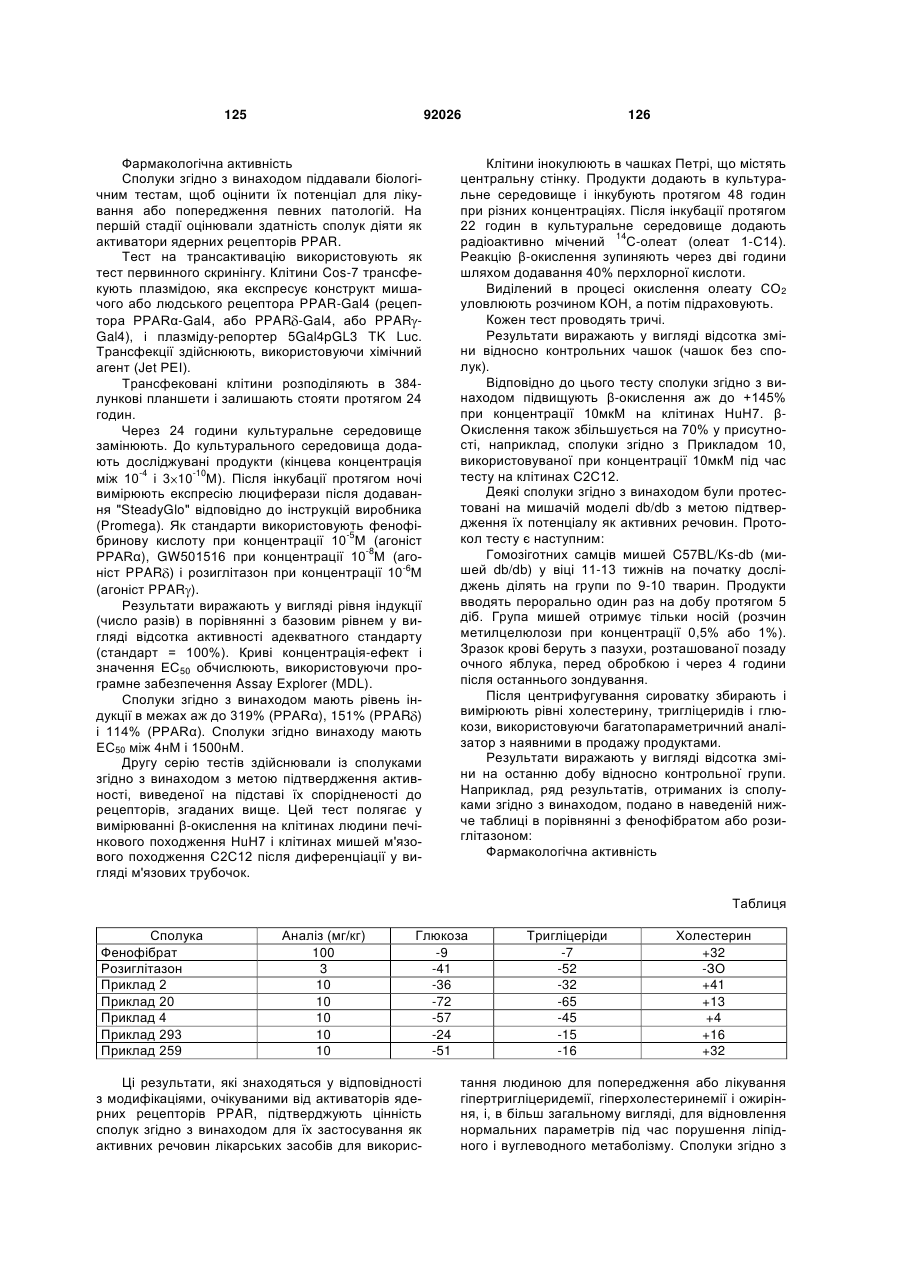
1. Похідне піролопіридину, яке відрізняється тим, що воно вибране із:
і) сполук формули:
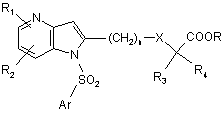 , (I)
, (I)
в якій:
R1 і R2 кожен незалежно є атомом водню, атомом галогену, С1-С4алкільною групою або С1-С4алкоксигрупою, або групою CF3;
R3 і R4 кожен незалежно є атомом водню або С1-С4алкільною групою;
R є атомом водню або С1-С3алкільною групою;
n=1, 2 або 3;
X є одинарним зв'язком або атомом кисню;
Аr є ароматичним або гетероароматичним ядром, вибраним з групи, яку складають феніл, піразоліл, імідазоліл, тіазоліл, оксазоліл, ізоксазоліл, фурил, тієніл, піроліл, піридил, дифеніл, нафтил, 1,2,3,4-тетрагідронафтил, ізохіноліл, хіноліл, 1,2,3,4-тетрагідрохіноліл, бензімідазоліл, бензопіразиніл, індоліл, 2,3-дигідроіндоліл, бензофурил, 2,3-дигідробензофурил, бензотіазоліл, бензотіадіазоліл, бензізоксазоліл, 3,4-дигідро-1,4-бензоксазиніл, 1,3-бензодіоксоліл, 2,3-дигідробензодіоксиніл, імідазотіазоліл і бензоксазоліл, необов'язково заміщені одним або кількома (наприклад, 2 або 3) замісниками, вибраними з атомів галогену і С1-С6алкільної групи, С1-С4алкоксильної групи, трифторметильної групи, трифторметоксильної групи, нітрогрупи, ацетильної групи, ацетиламіногрупи і діалкіламіногрупи або аміногрупи, або гетероциклів оксазолілу, тіазолілу, піразолілу, піролідинілу, піридилу, піримідинілу, метилпіримідинілу або морфолінілу.
іі) їх фармацевтично прийнятних солей.
2. Сполука за п. 1, яка відрізняється тим, що Аr є ароматичним або гетероароматичним ядром, вибраним з групи, яку складають феніл, піридил, дифеніл, нафтил, хіноліл, бензопіразиніл, індоліл, 2,3-дигідроіндоліл, бензофурил, 2,3-дигідробензофурил, бензотіазоліл, бензотіадіазоліл, бензізоксазоліл, 3,4-дигідро-1,4-бензоксазиніл, 1,3-бензодіоксоліл, 2,3-дигідробензодіоксиніл, імідазотіазоліл і бензоксазоліл, необов'язково заміщені одним або кількома (наприклад, 2 або 3) замісниками, вибраними з атомів галогену і С1-С6алкільної групи, С1-С4алкоксильної групи, трифторметильної групи, трифторметоксильноїгрупи, нітрогрупи, ацетильної групи, ацетиламіногрупи і діалкіламіногрупи або аміногрупи, або гетероциклів оксазолілу, тіазолілу, піразолілу, піролідинілу, піридилу, піримідинілу, метилпіримідинілу або морфолінілу.
3. Сполука за п. 1 або 2, яка відрізняється тим, що R1 є атомом хлору або трифторметильною групою.
4. Сполука за будь-яким з пп. 1-3 для застосування як фармакологічно активної речовини.
5. Застосування сполуки за будь-яким з пп. 1-3 для виготовлення лікарського засобу для лікування гіпертригліцеридемії, гіперліпідемії, гіперхолестеринемії, дисліпідемії, інсулінорезистентності, діабету і ожиріння.
6. Застосування сполуки за будь-яким з пп. 1-3 для виготовлення лікарського засобу для лікування дисфункції ендотелію.
7. Застосування сполуки за будь-яким з пп. 1-3 для виготовлення лікарського засобу для лікування серцево-судинних захворювань, запальних захворювань і нейродегенеративних захворювань, зокрема, таких як хвороба Альцгеймера або хвороба Паркінсона.
8. Фармацевтична композиція, яка відрізняється тим, що містить щонайменше одну сполуку за будь-яким з пп. 1-3 як активну речовину.
9. Спосіб отримання сполуки за п. 1, який відрізняється тим, що проводять:
а) реакцію галогенування, переважно реакцію йодування, амінопіридину формули
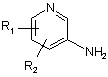 , (II)
, (II)
в якій:
R1 і R2 кожен незалежно є атомом водню, атомом фтору, брому або хлору або С1-С4алкільною групою, С1-С4алкоксигрупою або трифторметильною групою,
використовуючи галогенувальний агент, наприклад йод, у присутності сульфату срібла або дихлорйодату бензилтриметиламонію, в розчиннику при кімнатній температурі протягом 5-24 годин з отриманням сполуки формули
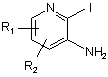 , (III)
, (III)
в якій:
R1 і R2 зберігають такі ж значення, як у вихідних сполуках;
б) взаємодію, відповідно до реакції Соногашири, сполуки формули III з похідним ацетилену формули
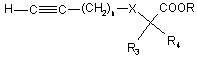 , (IV)
, (IV)
в якій:
n=1, 2 або 3;
R3 і R4 кожен незалежно є атомом водню або С1-С4алкільною групою;
R є С1-С3алкільною групою;
X є одинарним зв'язком або атомом кисню;
у присутності йодиду міді, каталізатора на основі паладію, наприклад тетракис(трифенілфосфін)паладію або дихлорбіс(трифенілфосфін)паладію, і органічної основи в розчиннику при температурі між 0 і 60 °С протягом 2-24 годин з отриманням сполуки формули
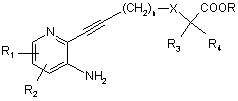 , (V)
, (V)
в якій:
R1, R2, n, X, R3, R4 і R зберігають такі ж значення, як у вихідних сполуках;
в) взаємодію сполуки формули V з арилсульфонілхлоридом формули
![]() , (VI)
, (VI)
в якій:
Аr є ароматичним або гетероароматичним ядром, вибраним з групи, яку складають феніл, піразоліл, імідазоліл, тіазоліл, оксазоліл, ізоксазоліл, фурил, тієніл, піроліл, піридил, дифеніл, нафтил, 1,2,3,4-тетрагідронафтил, хіноліл, ізохіноліл, 1,2,3,4-тетрагідрохіноліл, бензімідазоліл, бензопіразиніл, індоліл, 2,3-дигідроіндоліл, бензофурил, 2,3-дигідробензофурил, бензотіазоліл, бензотіадіазоліл, бензізоксазоліл, 3,4-дигідро-1,4-бензоксазиніл, 1,3-бензодіоксоліл, 2,3-дигідробензодіоксиніл, імідазотіазоліл і бензоксазоліл, необов'язково заміщені одним або кількома (наприклад, 2 або 3) замісниками, вибраним з атомів галогену і С1-С6алкільної групи, С1-С4алкоксильної групи, трифторметильної групи, трифторметоксильної групи, нітрогрупи, ацетильної групи, ацетиламіногрупи і діалкіламіногрупи або аміногрупи, або гетероциклів оксазолілу, тіазолілу, піразолілу, піролідинілу, піридилу, піримідинілу, метилпіримідинілу або морфолінілу,
у присутності піридину, необов'язково в розчиннику при кімнатній температурі протягом 10-120 хвилин з отриманням сполуки формули
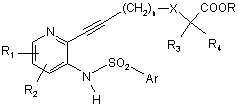 , (VII)
, (VII)
в якій:
R1, R2, n, X, R3, R4, R і Аr зберігають такі ж значення, як у вихідних сполуках;
г) циклізацію сполуки формули VII, наприклад, шляхом дії ацетату міді II, в розчиннику при температурі, близькій до температури кипіння розчинника, протягом 4-24 годин з отриманням сполуки формули
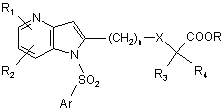 , (Ia)
, (Ia)
в якій:
R1, R2, n, X, R3, R4, R і Аr зберігають такі ж значення, як у вихідних сполуках;
д) якщонеобхідно, гідроліз естерної функціональної групи сполуки формули Іа, наприклад, шляхом дії неорганічної основи, з отриманням після обробки кислотою сполуки формули І у формі вільної кислоти:
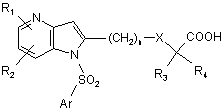 (Ib).
(Ib).
10. Спосіб отримання сполуки за п. 1, який відрізняється тим, що проводять:
а) взаємодію сполуки формули (III)
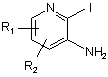 , (III)
, (III)
в якій R1 і R2 кожен незалежно є атомом водню, хлору або фтору або С1-С4алкільною групою, С1-С4алкоксильною групою або трифторметильною групою, з арилсульфонілхлоридом формули
![]() , (VI)
, (VI)
в якій:
Аr є ароматичним або гетероароматичним ядром, вибраним з групи, яку складають феніл, піразоліл, імідазоліл, тіазоліл, оксазоліл, ізоксазоліл, фурил, тієніл, піроліл, піридил, дифеніл, нафтил, 1,2,3,4-тетрагідронафтил, хіноліл, ізохіноліл, 1,2,3,4-тетрагідрохіноліл, бензімідазоліл, бензопіразиніл, індоліл, 2,3-дигідроіндоліл, бензофурил, 2,3-дигідробензофурил, бензотіазоліл, бензотіадіазоліл, бензізоксазоліл, 3,4-дигідро-1,4-бензоксазиніл, 1,3-бензодіоксоліл, 2,3-дигідробензодіоксиніл, імідазотіазоліл і бензоксазоліл, необов'язково заміщені одним або кількома (наприклад, 2 або 3) замісниками, вибраним з атомів галогену і С1-С6алкільної групи, С1-С4алкоксильної групи, трифторметильної групи, трифторметоксильної групи, нітрогрупи, ацетильної групи, ацетиламіногрупи і діалкіламіногрупи або аміногрупи, або гетероциклів оксазолілу, тіазолілу, піразолілу, піролідинілу, піридилу, піримідинілу, метилпіримідинілу або морфолінілу,
у розчиннику при кімнатній температурі протягом 1-12 годин з отриманням сполуки формули (VIII)
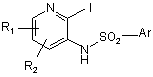 , (VIII)
, (VIII)
в якій:
R1, R2 і Аr зберігають такі ж значення, як у вихідних сполуках;
б) взаємодію сполуки формули VIII з похідним ацетилену формули
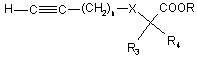 , (III)
, (III)
в якій:
n=1, 2 або 3;
R3 і R4 кожен незалежно є атомом водню або С1-С4алкільною групою;
R є С1-С3алкільною групою;
X є одинарним зв'язком або атомом кисню;
у присутності йодиду міді, каталізатора на основі паладію, наприклад тетракис(трифенілфосфін)паладію або дихлорбіс(трифенілфосфін)паладію, і органічної основи в розчиннику при температурі між 0 і 60 °С протягом 2-24 годин з отриманням сполуки формули
 , (Ia)
, (Ia)
в якій R1, R2, n, X, R3, R4, R і Аr зберігають такі ж значення, як у вихідних сполуках;
в) якщо необхідно, гідроліз естерної функціональної групи сполуки формули Іа, наприклад, шляхом дії неорганічної основи, з отриманням після обробки кислотою сполуки формули І у формі вільної кислоти:
 .
.
Текст
1. Похідне піролопіридину, яке відрізняється тим, що воно вибране із: і) сполук формули: 2 (19) 1 3 92026 рювань і нейродегенеративних захворювань, зокрема, таких як хвороба Альцгеймера або хвороба Паркінсона. 8. Фармацевтична композиція, яка відрізняється тим, що містить щонайменше одну сполуку за будь-яким з пп.1-3 як активну речовину. 9. Спосіб отримання сполуки за п.1, який відрізняється тим, що проводять: а) реакцію галогенування, переважно реакцію йодування, амінопіридину формули N R1 NH2 R2 , (II) в якій: R1 і R2 кожен незалежно є атомом водню, атомом фтору, брому або хлору або С1-С4алкільною групою, С1-С4алкоксигрупою або трифторметильною групою, використовуючи галогенувальний агент, наприклад йод, у присутності сульфату срібла або дихлорйодату бензилтриметиламонію, в розчиннику при кімнатній температурі протягом 5-24 годин з отриманням сполуки формули Аr є ароматичним або гетероароматичним ядром, вибраним з групи, яку складають феніл, піразоліл, імідазоліл, тіазоліл, оксазоліл, ізоксазоліл, фурил, тієніл, піроліл, піридил, дифеніл, нафтил, 1,2,3,4тетрагідронафтил, хіноліл, ізохіноліл, 1,2,3,4тетрагідрохіноліл, бензімідазоліл, бензопіразиніл, індоліл, 2,3-дигідроіндоліл, бензофурил, 2,3дигідробензофурил, бензотіазоліл, бензотіадіазоліл, бензізоксазоліл, 3,4-дигідро-1,4-бензоксазиніл, 1,3-бензодіоксоліл, 2,3-дигідробензодіоксиніл, імідазотіазоліл і бензоксазоліл, необов'язково заміщені одним або кількома (наприклад, 2 або 3) замісниками, вибраним з атомів галогену і С1С6алкільної групи, С1-С4алкоксильної групи, трифторметильної групи, трифторметоксильної групи, нітрогрупи, ацетильної групи, ацетиламіногрупи і діалкіламіногрупи або аміногрупи, або гетероциклів оксазолілу, тіазолілу, піразолілу, піролідинілу, піридилу, піримідинілу, метилпіримідинілу або морфолінілу, у присутності піридину, необов'язково в розчиннику при кімнатній температурі протягом 10-120 хвилин з отриманням сполуки формули NH2 в якій: R1 і R2 зберігають такі ж значення, як у вихідних сполуках; б) взаємодію, відповідно до реакції Соногашири, сполуки формули III з похідним ацетилену формули C C (CH2)n X R3 COOR R4 , (IV) в якій: n=1, 2 або 3; R3 і R4 кожен незалежно є атомом водню або С1С4алкільною групою; R є С1-С3алкільною групою; X є одинарним зв'язком або атомом кисню; у присутності йодиду міді, каталізатора на основі паладію, наприклад тетракис(трифенілфосфін)паладію або дихлорбіс(трифенілфосфін)паладію, і органічної основи в розчиннику при температурі між 0 і 60 °С протягом 2-24 годин з отриманням сполуки формули N R2 X COOR R3 (CH2)n R1 R4 R4 Ar H , (VII) в якій: R1, R2, n, X, R3, R4, R і Аr зберігають такі ж значення, як у вихідних сполуках; г) циклізацію сполуки формули VII, наприклад, шляхом дії ацетату міді II, в розчиннику при температурі, близькій до температури кипіння розчинника, протягом 4-24 годин з отриманням сполуки формули R1 N X COOR R3 (CH2)n R4 N R2 SO2 Ar , (Ia) в якій: R1, R2, n, X, R3, R4, R і Аr зберігають такі ж значення, як у вихідних сполуках; д) якщо необхідно, гідроліз естерної функціональної групи сполуки формули Іа, наприклад, шляхом дії неорганічної основи, з отриманням після обробки кислотою сполуки формули І у формі вільної кислоти: R1 N (CH2)n NH2 , (V) в якій: R1, R2, n, X, R3, R4 і R зберігають такі ж значення, як у вихідних сполуках; в) взаємодію сполуки формули V з арилсульфонілхлоридом формули Ar SO2 Cl , (VI) в якій: N R2 , (III) SO2 COOR R3 N R1 R2 X (CH2)n I N R1 H 4 X COOH R3 R4 N R2 SO2 Ar (Ib). 10. Спосіб отримання сполуки за п.1, який відрізняється тим, що проводять: а) взаємодію сполуки формули (III) 5 N 92026 I R1 NH2 R2 , (III) в якій R1 і R2 кожен незалежно є атомом водню, хлору або фтору або С1-С4алкільною групою, С1С4алкоксильною групою або трифторметильною групою, з арилсульфонілхлоридом формули Ar SO2 Cl , (VI) в якій: Аr є ароматичним або гетероароматичним ядром, вибраним з групи, яку складають феніл, піразоліл, імідазоліл, тіазоліл, оксазоліл, ізоксазоліл, фурил, тієніл, піроліл, піридил, дифеніл, нафтил, 1,2,3,4тетрагідронафтил, хіноліл, ізохіноліл, 1,2,3,4тетрагідрохіноліл, бензімідазоліл, бензопіразиніл, індоліл, 2,3-дигідроіндоліл, бензофурил, 2,3дигідробензофурил, бензотіазоліл, бензотіадіазоліл, бензізоксазоліл, 3,4-дигідро-1,4-бензоксазиніл, 1,3-бензодіоксоліл, 2,3-дигідробензодіоксиніл, імідазотіазоліл і бензоксазоліл, необов'язково заміщені одним або кількома (наприклад, 2 або 3) замісниками, вибраним з атомів галогену і С1С6алкільної групи, С1-С4алкоксильної групи, трифторметильної групи, трифторметоксильної групи, нітрогрупи, ацетильної групи, ацетиламіногрупи і діалкіламіногрупи або аміногрупи, або гетероциклів оксазолілу, тіазолілу, піразолілу, піролідинілу, піридилу, піримідинілу, метилпіримідинілу або морфолінілу, у розчиннику при кімнатній температурі протягом 1-12 годин з отриманням сполуки формули (VIII) N I R1 R2 N H 6 R1, R2 і Аr зберігають такі ж значення, як у вихідних сполуках; б) взаємодію сполуки формули VIII з похідним ацетилену формули H (CH2)n C X R1 N R2 SO2 COOR R4 Ar , (Ia) в якій R1, R2, n, X, R3, R4, R і Аr зберігають такі ж значення, як у вихідних сполуках; в) якщо необхідно, гідроліз естерної функціональної групи сполуки формули Іа, наприклад, шляхом дії неорганічної основи, з отриманням після обробки кислотою сполуки формули І у формі вільної кислоти: N X COOH R3 R4 N R2 SO2 Ar Представлений винахід відноситься до нових сполук піролопіридину, до способу їх отримання і до їх терапевтичного застосування для попередження або лікування патологій, в які залучені ядерні рецептори типу PPAR (рецептори активаторів проліферації пероксисом). У терапії відомо, що захворювання серцевосудинної системи представляють важливий чинник ризику для здоров'я. Ці захворювання часто є наслідком високого рівня холестерину та/або тригліцеридів, і, отже, важливо підтримувати ці рівні нижче за значення, широко визнані професійною медициною. У випадку холестерину особливо необхідно оцінювати кількості холестерину, пов'язаного з різними ліпопротеїнами, в цілях адаптації лікування таким чином, щоб знижувати рівні холестерину ЛПНГ (ліпопротеїнів низької густини), в той же час, зберігаючи рівні холестерину ЛПВГ (ліпопротеїнів високої густини). Серед відомих сімейств сполук, X R3 (CH2)n N (CH2)n , (VIII) R4 , (III) в якій: n=1, 2 або 3; R3 і R4 кожен незалежно є атомом водню або С1С4алкільною групою; R є С1-С3алкільною групою; X є одинарним зв'язком або атомом кисню; у присутності йодиду міді, каталізатора на основі паладію, наприклад тетракис(трифенілфосфін)паладію або дихлорбіс(трифенілфосфін)паладію, і органічної основи в розчиннику при температурі між 0 і 60 °С протягом 2-24 годин з отриманням сполуки формули Ar в якій: COOR R3 R1 SO2 C . що використовуються для регуляції цих параметрів, можна назвати статини, які є інгібіторами HMG СоА-редуктази і дають можливість по суті лікувати надмірно високі рівні холестерину ЛПНГ, і сполуки сімейства фібратів, які діють за допомогою активації ядерних рецепторів PPARα (що активуються проліфератором пероксисом рецепторів альфа) і дають можливість понизити рівні тригліцеридів і холестерину. Дослідження ядерних рецепторів PPAR привело до ідентифікації трьох підтипів, відомих як PPARα, PPAR і PPAR . Ці різні рецептори шляхом зв'язування з певними специфічними фрагментами ДНК регулюють експресію генів-мішеней, які кодують білки, залучені в механізми регуляції метаболізму ліпідів (див., наприклад, Current Topics in Medicinal Chemistry, 2003, 3, (14), 1649-1661). Таким чином: - PPARα експресуються по суті в печінці і залучені в катаболізм жирних кислот шляхом регу 7 ляції β- і ω-окислення (J. Lipid. Res. (1996) 37, 907925); - PPAR експресуються головним чином в жировій тканині і залучені в механізми регуляції глікемії; - PPAR експресуються повсюдно, але, в основному, присутні в нирках, скелетних м'язах, серці і кишечнику. Подібно до інших рецепторів типа PPAR, PPAR утворюють гетеродимер з RXR (рецептором ретиноїду X), і тоді вони здатні до зв'язування з певними елементами генів-мішеней ядра і регулюючими факторами транскрипції. Серед різних досліджень, присвячених даному ядерному рецептору, продемонстровано, наприклад, що активація PPAR дає можливість підвищити рівень холестерину ЛПВГ у мишей db/db (FEBS Letters (2000), 473, 333-336) і інсулінозалежних макакрезусів з ожирінням, а також стимулює виділення холестерину через Аро А1 в людських клітинах ТНР-1 (Proc. Nat. Ac. Sci. USA (2001), 98, 53065311). Лікування інсулінонезалежного діабету типу 2 залишається незадовільним, не зважаючи на надходження в продаж різних пероральних гіпоглікемізуючих похідних для полегшення секреції інсуліну і для стимуляції його дії на периферичні тканини-мішені. Агоністи PPAR в цілому описані для поліпшення чутливості до інсуліну, як вже спостерігали з тіазолідиндіонами (ТЗД). Нові агоністи PPAR розроблені для лікування діабету типу 2 та/або дисліпідемії. Серед нових агоністів PPAR деякі є активаторами щонайменше двох з трьох підтипів PPARα, і . Зростання частоти виявлення даних патологій вимагає розробки нових терапевтичних агентів, які є активними у випадку цих захворювань: отже, сполуки, що мають відмінну гіпоглікемічну активність і гіполіпідемічну активність, при цьому уникаючи побічних ефектів, що спостерігаються у випадку з тіазолідиндіонами, є вельми корисними при лікуванні та/або профілактиці інсулінонезалежного діабету типу 2 для зниження периферичної стійкості до інсуліну і нормалізації глікемії. В результаті дослідження різних ядерних рецепторів виявилось, що сполуки, які є агоністами одночасно двох і переважно трьох підтипів рецепторів PPAR, можуть мати вкрай сприятливий фармакологічний профіль для одночасного лікування патологій, таких як гіперліпідемія, гіперхолестеринемія і діабет, а також різних захворювань серцево-судинної системи, які є наслідком метаболічного синдрому. Даний винахід відноситься до активаторів або модуляторів рецепторів PPAR. Ці сполуки задовольняють фармакологічним критеріям, згаданим вище. Серед документів попереднього рівня техніка, в якій згадані подібні сполуки, відомі приклади включають документи WO 97/28149, WO 04/060871, WO 05/016335 і WO 05/016881, в яких описані агоністи рецептора PPAR , документ WO 01/60807, в якому описані агоністи PPARα, або документи WO 05/009958 і WO 05/056522, в яких запропоновані сполуки індолу, які є активними на рецепторах PPAR. 92026 8 Слід також згадати документи WO 02/071827 і Bioorganic and Med. Chem. Letter, Vol. 14 (11) стор.259-2763 (06/2004), де описані похідні, які є модуляторами рецепторів RXR, та їх терапевтичне застосування для лікування патологій, залучених в метаболічний синдром. Крім того, в попередньому рівні техніки описані різні сполуки піролопіридину, наприклад, в документі WO 98/25611 розкриті деякі проміжні сполуки, заявлені сполуки є активними проти тромбозу. Представлений винахід відноситься до нових похідних піролопіридину, які є активаторами PPAR і вибрані із і) сполук формули: (I) в якій: R1 і R2 кожен незалежно є атомом водню, атомом галогену, С1-С4 алкільною групою або С1-С4 алкоксигрупою, або групою CF3; R3 і R4 кожен незалежно є атомом водню або С1-С4 алкільною групою; R є атомом водню або С1-С3 алкільною групою; n=1, 2 або 3; X є одинарним зв'язком або атомом кисню. Аr є ароматичним або гетероароматичним ядром, вибраним з групи, яку складають феніл, піразоліл, імідазоліл, тіазоліл, оксазоліл, ізоксазоліл, фурил, тієніл, піроліл, піридил, дифеніл, нафтил, 1,2,3,4-тетрагідронафтил, ізохіноліл, хіноліл, 1,2,3,4-тетрагідрохіноліл, бензімідазоліл, бензопіразиніл, індоліл, 2,3-дигідроіндоліл, бензофурил, 2,3-дигідробензофурил, бензотіазоліл, бензотіадіазоліл, бензізоксазоліл, 3,4-дигідро-1,4бензоксазиніл, 1,3-бензодіоксоліл, 2,3дигідробензодіоксиніл, імідазотіазоліл і бензоксазоліл, необов'язково заміщені одним або кількома (наприклад, 2 або 3) замісниками, вибраними з атомів галогену і С1-С6 алкільної групи, С1-С4 алкоксильної групи, трифторметильної групи, трифторметоксильної групи, нітрогрупи, ацетильної групи, ацетиламіногрупи і діалкіламіногрупи, де кожна алкільна група містить від 1 до 3 атомів вуглецю, або аміногрупи, або гетероциклів оксазолілу, тіазолілу, піразолілу, піролідинілу, піридилу, піримідинілу, метилпіримщинілу або морфолінілу. її) їх фармацевтично прийнятних солей Згідно з другим аспектом винахід стосується вищезазначених сполук для їх застосування як фармакологічно активних речовин, а також фармацевтичних композицій, що містять їх. Крім того, винахід відноситься до застосування щонайменше однієї сполуки формули (І) або м фармацевтично прийнятних солей як активної речовини для виготовлення лікарського засобу, призначеного для терапевтичного застосування, зокрема, для боротьби з гіперхолестеринемією, гіперліпідемією, гіпертригліцеридемією, дисліпідеемією, інсулінорезистентністю, діабетом або ожирінням, а також з серцево-судинними захворюван 9 нями, які є наслідком дисбалансу сироваткових ліпопротеїнів. Сполуки згідно з винаходом є також придатними як активні речовини для лікарських засобів для попередження або лікування захворювань, обумовлених дисфункцією ендотелію, атеросклерозу, інфаркту міокарда, гіпертензії, проблем судин головного мозку, деяких запальних захворювань, наприклад, ревматоїдного артриту, і нейродегенеративних захворювань, зокрема, таких як хвороба Альцгеймера або хвороба Паркінсона. У даному описі термін "С1-Сn алкільна група" (де n є цілим числом) означає лінійний, розгалужений, або частково або повністю циклічний ланцюг на основі вуглеводню, що містить від 1 до n атомів вуглецю, де циклічна частина містить щонайменше 3 атоми вуглецю. Наприклад, і без обмеження, С1-С6 алкільною групою може бути метил, етил, пропіл, бутил, пентил, гексил, 1метилетил, 1-метилпропіл, 2-метилпропіл, 1,1метилетил, 1-метилбутил, 1,1-диметилпропіл, 1метилпентіл, 1,1-диметилбутил, циклопропіл, циклобутил, циклопентил, циклогексил або циклопентилметил. Термін " С1-Сn алкоксильна група" (де n є цілим числом) означає групу RO-, в якій R є алкільною групою, що містить від 1 до n атомів вуглецю, як визначено вище. Термін "галоген" означає атом фтору, хлору, брому або йоду, де перевага надається атомам фтору і хлору. Сполуками формули (І), в яких R є атомом водню, є карбонові кислоти, які можна використовувати у формі вільних кислот або у формі солей, де вказані солі отримують шляхом поєднання кислоти з фармацевтично прийнятною нетоксичною неорганічною або органічною основою. Серед неорганічних основ, які можна використовувати, можна назвати, наприклад, гідроксид натрію, гідроксид калію, гідроксид магнію і гідроксид кальцію. Серед органічних основ, які можна використовувати, можна назвати, наприклад, аміни, аміноспирти, основні амінокислоти, такі як лізин або аргінін, або сполуки, що несуть функціональну групу четвертинного амонію, наприклад, бетаїн або холін. Сполуки формули (І), в яких замісники R3 і R4 є різними, мають асиметричний центр. Для цих сполук винахід охоплює як рацемічні сполуки, так і кожний з оптичних ізомерів, розглянутий окремо. Одне конкретне сімейство сполук згідно винаходу включає сполуки вищезазначеної формули І, в якій: R1 і R2 кожен незалежно є атомом водню, атомом галогену або групою CF3; R3 і R4 кожен незалежно є атомом водню або С1-С4 алкільною групою; R є атомом водню або С1-С3 алкільною групою; n=1 або 2; X є одинарним зв'язком або атомом кисню; Аг є ароматичним або гетероароматичним ядро, вибраним з групи, яку складають феніл, нафтил, бензотіазоліл, 3,4-дигідро-1,4-бензоксазиніл, 1,3-бензодіоксоліл, 2,3-дигідробензодіоксиніл і бензоксазоліл, необов'язково заміщені одним або 92026 10 кількома замісниками, вибраними з С1-С6 алкільної групи, С1-С4 алкоксильної групи і аміногрупи. Серед сполук формули І згідно винаходу переважними сполуками є ті, в яких: R1 і R2 кожен незалежно є атомом водню, атомом галогену, С1-С4 алкільною групою або С1-С4 алкоксильною групою або групою CF3; R3 і R4 кожен незалежно є атомом водню або С1-С4 алкільною групою; R є атомом водню або С1-С3 алкільною групою; n=1, 2 або 3; X є одинарним зв'язком або атомом кисню; Аг є ароматичним або гетероароматичним ядром, вибране з групи, яку складають феніл, піридил, дифеніл, нафтил, хіноліл, бензопіразиніл, індоліл, 2,3-дигідроіндоліл, бензофурил, 2,3дигідробензофурил, бензотіазоліл, бензотіадіазоліл, бензізоксазоліл, 3,4-дигідро-1,4-бензоксазиніл, 1,3-бензодіоксоліл, 2,3-дигідробензодіоксиніл, імідазотіазоліл і бензоксазоліл, необов'язково заміщені одним або кількома (наприклад, 2 або 3) замісниками, вибраними з атомів галогену і С1-С6 алкільної групи, С1-С4 алкоксильної групи, трифторметильної групи, трифторметоксильної групи, нітрогрупи, ацетильної групи, ацетиламіногрупи і діалкіламіногрупи, в яких кожна алкільна група містить від 1 до 3 атомів вуглецю, або аміногрупи, або гетероциклів оксазолілу, тіазолілу, піразолілу, піролідинілу, піридилу, піримідинілу, метилпіримідинілу або морфолінілу. Серед сполук згідно винаходу перевага також надається сполукам, в яких Аr є фенільною групою. Також перевага надається сполукам, в яких R1 є атомом хлору або трифторметильною групою. Сполуки згідно з винаходом можуть бути отримані відповідно до першого способу, який полягає в: а) проведенні реакції галогенування, переважно реакції йодування, амінопіридину формули (Il) в якій: R1 і R2 кожен незалежно є атомом водню, атомом хлору, брому або фтору, С1-С4 алкільною групою або (С1-C4 алкоксильною групою або трифторметильною групою; використовуючи галогенувальний агент, наприклад, йод, у присутності сульфату срібла або дихлорйодату бензилтриметиламонію, в розчиннику, такому як дихлорметан або аліфатичний спирт, при кімнатній температурі протягом 5-24 годин з отриманням сполуки формули (Ill) в якій: R1 і R2 зберігають такі ж значення, як і у вихідних сполуках; б) взаємодії у відповідності з реакцією Соногашири (див., наприклад: Tet. Lett., 1975, 4467) 11 92026 сполуки формули III з похідним ацетилену формули (IV) в якій: n=1, 2 або 3; R3 і R4 кожен незалежно є атомом водню або С1-С4 алкільною групою; R є С1-С3 алкільною групою; X є одинарним зв'язком або атомом кисню; у присутності йодиду міді, каталізатора на основі паладію, наприклад, тетракис(трифенілфосфін)паладію або дихлорбіс(трифенілфосфін)паладію, і органічної основи, наприклад, триетиламіну, в розчиннику, наприклад, в диметилформаміді (ДМФ), при температурі між 0 і 60°С протягом 2-24 годин з отриманням сполуки формули (V) в якій: R1, R2, n, X, R3, R4 і R зберігають такі ж значення, як у вихідних сполуках; в) взаємодії сполуки формули V з арилсульфонілхлоридом формули (VI) в якій: Аr є ароматичним або гетероароматичним ядром, вибраним з групи, яку складають феніл, піразоліл, імідазоліл, тіазоліл, оксазоліл, ізоксазоліл, фурил, тієніл, піроліл, піридил, дифеніл, нафтил, 1,2,3,4-тетрагідронафтил, хіноліл, ізохіноліл, 1,2,3,4-тетрагідрохіноліл, бензімідазоліл, бензопіразиніл, індоліл, 2,3-дигідроіндоліл, бензофурил, 2,3-дигідробензофурил, бензотіазоліл, бензотіадіазоліл, бензізоксазоліл, 3,4-дигідро-1,4бензоксазиніл, 1,3-бензодіоксоліл, 2,3дигідробензодіоксиніл, імідазотіазоліл і бензоксазоліл, необов'язково заміщені одним або кількома (наприклад, 2 або 3) замісниками, вибраними з атома галогену і С1-С6 алкільної групи, С1-С4 алкоксильної групи, трифторметильної групи, трифторметоксильної групи, нітрогрупи, ацетильної групи, ацетиламіногрупи і діалкіламіногрупи, або аміногрупи, або гетероциклів оксазолілу, тіазолілу, піразолілу, піролідинілу, піридилу, піримідинілу, метилпіримідинілу або морфолінілу, у присутності піридину, необов'язково у розчиннику, такому як дихлорметан, при кімнатній температурі протягом 10-120 хвилин з отриманням сполуки формули (VII) в якій: 12 R1, R2, n, X, R3, R4, R і Аr зберігають такі ж значення, як у вихідних сполуках; г) проведенні циклізації сполуки формули VII, наприклад, за допомогою дії ацетату міді II (див., наприклад, J. Org. Chem., 2004, 69 (4), 1126-1136), в розчиннику, такому як 1,2-дихлоретан, при температурі, близькій до температури кипіння розчинника, протягом 4-24 годин, з отриманням сполуки формули (Ia) в якій: R1, R2, n, X, R3, R4, R і Аr зберігають такі ж значення, як у вихідних сполуках; д) якщо необхідно, гідролізі ефірної функціональної групи сполуки формули Іа, наприклад, під дією неорганічної основи, такої як гідроксид натрію або гідроксид літію, згідно з методиками, які добре відомі фахівцям в даній галузі техніки, з отриманням після обробки кислотою сполуки формули І у формі вільної кислоти: (Ib) Відповідно до першого варіанту способу отримання, сполуки формули І можуть бути отримані шляхом послідовності реакцій, яка складається із: а) взаємодії сполуки формули (III) (Ill) яку отримано вище, з арилсульфонілхлоридом формули (VI) в якій: Аr є ароматичним або гетероароматичним ядром, вибраним з групи, яку складають феніл, піразоліл, імідазоліл, тіазоліл, оксазоліл, ізоксазоліл, фурил, тієніл, піроліл, піридил, дифеніл, нафтил, 1,2,3,4-тетрагідронафтил, хіноліл, ізохіноліл, 1,2,3,4-тетрагідрохіноліл, бензімідазоліл, бензопіразиніл, індоліл, 2,3-дигідроіндоліл, бензофурил, 2,3-дигідробензофурил, бензотіазоліл, бензотіадіазоліл, бензізоксазоліл, 3,4-дигідро-1,4бензоксазиніл, 1,3-бензодіоксоліл, 2,3дигідробензодіоксиніл, імідазотіазоліл і бензоксазоліл, необов'язково заміщені одним або кількома (наприклад, 2 або 3) замісниками, вибраними з атомів галогену і С1-С6 алкільної групи, С1-С4 алкоксильної групи, трифторметильної групи, трифторметоксильної групи, нітрогрупи, ацетильної групи, ацетиламіногрупи і діалкіламіногрупи, або аміногрупи, або гетероциклів оксазолілу, тіазолілу, піра 13 92026 золілу, піролідинілу, піридилу, піримідинілу, метилпіримідинілу або морфолінілу, у розчиннику, наприклад, в диметилформаміді, переважно у присутності апротонної основи, наприклад, піридину, при кімнатній температурі протягом 1-12 годин з отриманням сполуки формули (VIII) (VIIl) в якій: R1, R2 і Аr зберігають такі ж значення, як у вихідних сполуках; б) взаємодії сполуки формули VIII з похідним ацетилену формули (llI) в якій: n=1, 2 або 3; R3 і R4 кожен незалежно є атомом водню або С1-С4 алкільною групою; R є С1-С3 алкільною групою; X є одинарним зв'язком або атомом кисню; в умовах, аналогічних описаним для стадії б) наведеного вище загального способу з отриманням сполуки формули (Ia) в якій R1, R2, n, X, R3, R4, R і Аr зберігають такі ж значення, як у вихідних сполуках; в) якщо необхідно, гідролізу ефірної функціональної групи сполуки формули Іа, наприклад, шляхом дії неорганічної основи, такої як гідроксид натрію або гідроксид літію, згідно з методиками, які добре відомі фахівцям в даній галузі техніки, з отриманням після обробки кислотою сполуки формули І у формі вільної кислоти: (Ib) Сполуки за винаходом у формі солей кислоти формули Іb з неорганічною або органічною основою можуть бути отримані загальноприйнятим шляхом, використовуючи способи, які добре відомі фахівцям в даній галузі техніки, наприклад, шляхом змішування стехіометричних кількостей кислоти і основи в розчиннику, наприклад, у воді або у водно-спиртовій суміші, а потім ліофілізації отриманого розчину. На деяких із стадій вищеописаних реакцій переважно можливою є заміна традиційних методів нагрівання мікрохвильовим нагріванням з використанням реакторів, пристосованих до даного виду 14 реакції. В даному випадку фахівцеві в даній галузі техніки повинно бути зрозумілим, що час "нагрівання" буде значно зменшуватися порівняно з часом, необхідним для стандартного нагрівання. Приклади, в яких описано отримання сполук формули (І), дозволяють ясніше зрозуміти винахід. У даних прикладах, які не обмежують об'єм винаходу, терміном "Підготовчий приклад" позначають Приклади, в яких описано синтез проміжних сполук, а терміном "Приклади" позначено Приклади, в яких описано синтез сполук формули (І) згідно з винаходом. Серед скорочень "мМ" означає мілімолі, ТГФ означає тетрагідрофуран, ДМФ означає диметилформамід, ДМЕ означає 1,2диметоксиетан, ДХМ означає дихлорметан і PdCI2dppf означає дихлор-1,1'біс(дифенілфосфіно)фероценпаладій (II). Температури плавлення вимірюють на установці Kofler, або з використанням апарату Mettler, а спектральні значення ядерного магнітного резонансу характеризуються хімічним зсувом, обчисленим відносно ТМС (тетраметилсилану), числом протонів, пов'язаних із сигналом, і формою сигналу (с для синглету, д для дублету, дд для подвійного дублету, τ для триплету, к для квартету, квін. для квінтету і м для мультиплету). Робоча частота і використовуваний розчинник вказані для кожної сполуки. Кімнатна температура складає 20°С±5°С. Підготовчий приклад І 3-Аміно-6-хлор-2-йодопіридин 23,2г (180,5мМ) 5-Аміно-2-хлорпіридину перемішують в 70мл дихлорметану (ДХМ) і 180мл метанолу, і додають 21,6г (216мМ) карбонату кальцію і 75,3г (226мМ) дихлорйодату бензилтриметиламонію. Реакційну суміш перемішують при кімнатній температурі протягом 16 годин і потім фільтрують для видалення мінеральних солей. Фільтрат розбавляють водою й екстрагують ДХМ. Отриману органічну фазу промивають розчином хлориду натрію і потім насиченим розчином тіосульфату натрію, сушать над сульфатом магнію і концентрують при зниженому тиску. Отримують масло, яке очищають хроматографією на силікагелі, елююючи сумішшю циклогексан/етилацетат (80/20 і потім 70/30; об./об.). Таким чином отримують 13,9г очікуваного продукту у вигляді твердої речовини оранжевого кольору (вихід =30%). Т.пл.=148°С. Підготовчий приклад II 3-[Ди(бензолсульфоніл)аміно]-6-хлор-2йодопіридин Суміш 13,75г (54мМ) сполуки згідно з Підготовчим прикладом І і 27,6мл (216мМ) бензолсульфонілхлориду в 30мл піридину перемішують протягом 60 годин при кімнатній температурі. Реакційну суміш потім розбавляють водою і екстрагують декілька разів етилацетатом. Органічну фазу промивають N розчином соляної кислоти і потім розчином хлориду натрію, сушать над сульфатом магнію і концентрують при зниженому тиску. Очікувану сполука отримують у вигляді твердої речовини бежевого кольору (вихід=96%). Т.пл.=231°С. Підготовчий приклад III 15 N-(6-Хлор-2-йодо-3піридил)бензолсульфонамід 15,46г (29мМ) Сполуки згідно з Підготовчим прикладом II перемішують в 170мл діоксану і додають 77мл водного 3Μ розчину гідроксиду калію. Реакційну суміш перемішують при слабкому кипінні розчинника із зворотним холодильником протягом 1 години і потім концентрують при зниженому тиску. Отримують тверду речовину бежевого кольору, яку суспендують в 200мл води. Суміш підкислюють до приблизно рН4 шляхом додавання соляної кислоти і потім екстрагують дихлорметаном (ДХМ). Органічну фаза сушать над сульфатом магнію і потім концентрують при зниженому тиску. Таким чином отримують 10,32г очікуваного продукту у вигляді твердої речовини бежевого кольору (вихід=91%). Т.пл.=132°С. Приклад 1 Метиловий естер 5-хлор-1-(фенілсульфоніл)1Н-піроло[3,2-b]піридин-2-пропанової кислоти 10,32г (26,2мМ) Сполуки згідно з Підготовчим прикладом III, 30мл диметилформаміду, 460мг (0,65мМ) дихлорбіс(трифенілфосфін)паладію, 250мг (1,3мМ) йодиду міді і 20мл діетиламіну змішують разом. Потім при кімнатній температурі при перемішуванні додають 3,5г (31,25мМ) метил 4пентиноату, і реакційну суміш перемішують протягом 1 години при слабкому кипінні розчинника із зворотним холодильником. Реакційну суміш потім розбавляють водою й екстрагують декілька разів етилацетатом. Органічну фаза промивають розчином хлориду натрію, сушать над сульфатом магнію і концентрують при зниженому тиску. Отримане масло коричневого кольору очищають хроматографією на силікагелі, елююючи сумішшю циклогексан/етилацетат (8/2; об./об.). Таким чином отримують 8,02г очікуваного продукту у вигляді твердої речовини жовтого кольору (вихід: 81%). Т.пл.=108-115°С. Приклад 2 5-Хлор-1-(фенілсульфоніл)-1Н-піроло[3,2b]піридин-2-пропанова кислота 1,5г (4мМ) Естеру, отриманого згідно з Прикладом 1, перемішують в 5мл тетрагідрофурану і додають розчин 332мг (7,9мМ) гідроксиду літію (LiΟΗ·H2Ο) в 4мл води. Реакційне середовище перемішують протягом 2 годин при кімнатній температурі і потім підкислюють до рН3 соляною кислотою й екстрагують за допомогою ДХМ. Органічну фазу сушать над сульфатом магнію і концентрують при зниженому тиску. Отримують масло злегка жовтого кольору, яке кристалізується у вигляді білого твердої речовини (вихід=77%). Т.пл.=185-187°С. Підготовчий приклад IV 3-Аміно-2-йодо-6-(трифторметил)піридин 3,85г (12.3мМ) Сульфату срібла додають при перемішуванні і при кімнатній температурі до розчину 2г (12,3мМ) 5-аміно-2(трифторметил)піридину в 100мл етанолу. Потім додають 3,13г йоду і реакційну суміш перемішують при кімнатній температурі протягом 24 годин. Тверду речовину у вигляді суспензії в розчиннику видаляють фільтрацією і фільтрат концентрують при 92026 16 зниженому тиску. Залишок після випарювання переносять в 200мл дихлорметану і промивають 5% розчином гідроксиду натрію, а потім водою і сушать над сульфатом магнію. Отриманий розчин концентрують при зниженому тиску і таким чином отримують 3,42г очікуваної сполуки у вигляді твердої речовини рожевого кольору (вихід=96%). Т.пл.=127°С. Підготовчий приклад V Метиловий естер 6-(3-аміно-6-хлор-2-піридил)5-гексинової кислоти 5г (19,6мМ) Сполуки згідно з Підготовчим прикладом І, 20мл диметилформаміду, 345мг (0,49мМ) дихлорбіс(трифенілфосфін)паладію, 187мг (0,98мМ) йодиду міді і 10мл діетиламіну змішують разом. Потім при кімнатній температурі при перемішуванні додають 2,97г (23,5мМ) метил 5-гексиноату, і реакційну суміш перемішують протягом 1 години при слабкому кипінні розчинника із зворотним холодильником. Потім реакційну суміш розбавляють водою й екстрагують декілька разів етилацетатом. Органічну фазу промивають розчином хлориду натрію, сушать над сульфатом магнію і концентрують при зниженому тиску. Отриману масляну сполуку очищають хроматографією на силікагелі, елююючи сумішшю циклогексан/етилацетат (9/1; об./об.). Таким чином 4.15г отримують очікуваного продукту у вигляді масла (вихід: 84%). 1 Н ЯМР (300МГц, ДМСО) δ: 1,83 (квінт., 2Н); 2,47 (т, 2Н); 2,54 (т, 2Н); 3,60 (с, 3Н); 5,63 (с, 2Н); 7,10 (с, 2Н). Підготовчий приклад VI Метиловий естер 6-[3-[(6бензотіазолілсульфоніл)аміно]-6-хлор-2-піридил]5-гексинової кислоти Отримують розчин 1г (4мМ) сполуки згідно з Підготовчим прикладом V в 10мл піридину і додають 1,1г (4,7мМ) 6-бензотіазолсульфонілхлориду. Суміш перемішують протягом 3 годин при кімнатній температурі і потім розбавляють водою й екстрагують етилацетатом. Органічну фазу промивають двічі N розчином соляної кислоти і потім водою, сушать над сульфатом магнію і концентрують при зниженому тиску. Залишкове масло очищають хроматографією на силікагелі, елююючи сумішшю циклогексан/етилацетат (7/3; об./об.). Таким чином отримують 1,07г очікуваної сполуки у вигляді твердої речовини жовтого кольору (вихід=60%). Т.пл.=134°С. Приклад 3 Метиловий естер 1-(6бензотіазолілсульфоніл)-5-хлор-1Н-піроло[3,2b]піридин-2-бутанової кислоти Отримують в мікрохвильовій реакторній трубці суміш 1г (2,22мМ) естеру згідно з Підготовчим прикладом VI в 3мл 1,2-дихлоретану і додають 403мг (2,22мМ) ацетату міді. Суміш нагрівають мікрохвилями при 150°С протягом 30 хвилин і потім охолоджують, розбавляють 6мл дихлорметану і фільтрують через ватманський папір. Фільтрат концентрують при зниженому тиску і сирий продукт очищають хроматографією на силікагелі, елююючи сумішшю циклогексан/етилацетат (8/2; об./об.). 17 Таким чином отримують 500мг очікуваної сполуки у вигляді твердої речовини жовтого кольору (вихід=50%). Т.пл.=55°С. Приклад 4 1-(6-Бензотіазолілсульфоніл)-5-хлор-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та вихідну сполуку, отриману згідно з Прикладом 3, очікуваний продукт отримують у вигляді твердої речовини бежевого кольору (вихід=95%). Т.пл.=178°С. Підготовчий приклад VII N-[2-Йод-6-(трифторметил)-3піридил]бензолсульфонамід 7г (40мМ) Бензолсульфонілхлориду потрохи додають при перемішуванні і при кімнатній температурі до розчину 2,88г (10мМ) сполуки згідно з Підготовчим прикладом IV в 25мл піридину. Реакційну суміш перемішують при кімнатній температурі протягом 24 годин і потім виливають в 300мл охолодженої льодом N соляної кислоти. Отриманий осад відокремлюють фільтрацією і промивають водою на фільтрі, і потім перемішують у колбі з 40мл діоксану та 10мл водного розчину 3Μ гідроксиду калію при слабкому кипінні розчинника із зворотним холодильником, протягом 2 годин. Цю реакційну суміш охолоджують, розбавляють 300мл води, підкислюють приблизно до рН1,5 концентрованою соляною кислотою і потім екстрагують дихлорметаном. Отриману органічну фазу промивають водою і потім сушать над сульфатом магнію і концентрують при зниженому тиску. Таким чином отримують 3,7г очікуваного продукту у вигляді твердої речовини білого кольору (вихід=89%). Т.пл.=131°С. Підготовчий приклад VIII Метиловий естер 5-[3-аміно-6-хлор-2-піридил]4-пентинової кислоти, Використовуючи методику, подібну до методики Підготовчого прикладу V, та як вихідну речовину - метиловий естер 4-пентинової кислоти, очікуваний продукт отримують у вигляді твердої речовини жовтого кольору (вихід=77%). Т.пл.=96-100°С. Використовуючи методику, подібну до методики Підготовчого прикладу VI, та як вихідні речовини - відповідні сульфонілхлориди, отримують наступні сполуки: Підготовчий приклад IX Метиловий естер 6-[3-[(1,3-бензодіоксол-5ілсульфоніл)аміно]-6-хлор-2-піридил]-5-гексинової кислоти Тверда речовина коричневого кольору, вихід=91%. Т.пл.=123°С. Підготовчий приклад X Метиловий естер 6-[3-[(2-аміно-5бензотіазолілсульфоніл)аміно]-6-хлор-2-піридил]5-гексинової кислоти Біла тверда речовина, вихід=37%. Т.пл.=66-72°С. Підготовчий приклад XI 92026 18 Метиловий естер 6-[6-хлор-3-[(3,5диметилфеніл)сульфоніламіно]-2-піридил]-5гексинової кислоти Масло оранжевого кольору, вихід=98%. 1 Н ЯМР (300МГц, ДМСО) δ: 1,74 (квінт., 2Н); 2,30 (с, 6Н); 2,40 (т, 2Н); 2,42 (т, 2Н); 3,61 (с, 3Н); 7,28 (с, 1Н); 7,33 (с, 2Н); 7,45 (д, 1Н); 7,70 (д, 2Н); 10,07 (с, 1Н). Підготовчий приклад XII Метиловий естер 6-[6-хлор-3-[(2,5диметоксифеніл)сульфоніламіно]-2-піридил]-5гексинової кислоти Тверда речовина оранжевого кольору, вихід=84%. Т.пл.=78-82°С. Підготовчий приклад XIII Метиловий естер 6-[6-хлор-3-[(1нафталеніл)сульфоніламіно]-2-піридил]-5гексинової кислоти Тверда речовина оранжевого кольору, вихід=98%. Т.пл.=117°С. Підготовчий приклад XIV Метиловий естер 6-[6-хлор-3-[(3,4-дигідро-4метил-2Н-1,4-бензоксазин-7-іл)сульфоніламіно]-2піридил]-5-гексинової кислоти Масло коричневого кольору, вихід=74%. 1 Н ЯМР (300МГц, ДМСО-d6) δ: 1,75 (квінт., 2Н); 2,41 (м, 4Н); 2,78 (с, 3Н); 3,28 (м, 2Н); 3,61 (с, 3Н); 4,27 (м, 2Н); 6,78 (д, 1Н); 6,88 (с, 1Н); 6,89 (д, 1Н); 7,44 (д, 1Н); 7,71 (д, 1Н); 9,80 (с, 1Н). Використовуючи методику, подібну до методики Підготовчого прикладу VI, та як вихідні речовини - естер згідно з Підготовчим прикладом VIII та відповідні сульфонілхлориди, отримують наступні сполуки: Підготовчий приклад XV Метиловий естер 5-[3-[(5бензодіоксолілсульфоніл)аміно]-6-хлор-2-піридил]4-пентинової кислоти Тверда речовина коричневого кольору, вихід=92%. Т.пл.=133°С. Підготовчий приклад XVI Метиловий естер 5-[3-[(6бензотіазолілсульфоніл)аміно]-6-хлор-2-піридил]4-пентинової кислоти Тверда речовина жовтого кольору, вихід=49%. Т.пл.=137°С. Підготовчий приклад XVII Етиловий естер 2-[[3-(3-аміно-6-хлор-2піридил)-2-пропініл]окси]пропанової кислоти Використовуючи методику, подібну до методики Підготовчого прикладу V, та як вихідну речовину - етиловий естер 2-(2-пропінілокси)пропанової кислоти, очікуваний продукт отримують у вигляді твердої речовини коричневого кольору (вихід=73%). Т.пл.=70°С. Підготовчий приклад XVIII N-(6-Хлор-2-йодо-3піридил)-3-метоксибензолсульфонамід Використовуючи методику, подібну до методики Підготовчого прикладу VII, та як вихідні речовини - сполуку згідно з Підготовчим прикладом І і 3метоксибензолсульфонілхлорид, очікуваний про 19 дукт отримують у вигляді твердої речовини білого кольору (вихід=96%). Т.пл.=154°С. Підготовчий приклад XIX Метиловий естер 2-[[3-[3-аміно-6(трифторметил)-2-піридил]-2-пропініл]окси]-2метилпропанової кислоти Використовуючи методику, подібну до методики Підготовчого прикладу V, та як вихідні речовини - сполуку згідно з Підготовчим прикладом IV і метиловий естер 2-метил-2-(2пропінілокси)пропанової кислоти, очікуваний продукт отримують у вигляді масла жовтого кольору (вихід=56%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 7,50 (д, 1Н); 7,18 (д, 1Н); 6,23 (с, 2Н); 4,44 (с, 2Н); 3,68 (с, 3Н); 1,42 (с, 6Н). Підготовчий приклад XX Етиловий естер 2-[[3-[3-аміно-6(трифторметил)-2-піридил]-2пропініл]окси]пропанової кислоти Змішують разом 800мг (2,78мМ) сполуки згідно з Підготовчим прикладом IV, 78мг (0,28мМ) трициклогексилфосфіну, 20мл диметилформаміду, 97мг (0,14мМ) дихлорбіс(трифенілфосфін)паладію, 26мг (0,14мМ) йодиду міді і 8мл трeт-бутиламіну. Потім при кімнатній температурі при перемішуванні додають 1,09г (7мМ) етилового естеру 2-(2пропінілокси)пропанової кислоти і реакційну суміш перемішують протягом 20 годин при 45-50°С. Реакційну суміш потім охолоджують, розбавляють водою й екстрагують декілька разів етилацетатом. Об'єднані органічні фази промивають розчином хлориду натрію, сушать над сульфатом магнію і концентрують при зниженому тиску. Отриманий сирий продукт очищають хроматографією на силікагелі, елююючи сумішшю толуол/етилацетат (9/1 і потім 8/2; об./об.). Очікуваний продукт отримують у вигляді масла (вихід: 76%). 1Н ЯМР (300МГц, ДМСО-d6) δ: 7,51 (д, 1Н); 7,18 (д, 1Н); 6,27 (с, 2Н); 4,58 (д, 1Н); 4,48 (д, 1Н); 4,23 (к, 1Н); 4,12 (к, 2Н); 1,31 (д, 3Н); 1,20 (т, 3Н). Підготовчий приклад XXI Метиловий естер 5-[3-аміно-6-(трифторметил)2-піридил]-4-пентинової кислоти Використовуючи методику, подібну до методики Підготовчого прикладу V, та як вихідні речовини - сполуку згідно з Підготовчим прикладом IV і метиловий естер 4-пентинової кислоти, очікуваний продукт отримують у вигляді твердої речовини кольору охри (вихід=81%). Т.пл.=90°С. Підготовчий приклад XXII Метиловий естер 6-[3-аміно-6-(трифторметил)2-піридил]-5-гексинової кислоти Використовуючи методику, подібну до методики Підготовчого прикладу XXI, та як вихідну сполуку - метиловий естер 5-гексинової кислоти, очікуваний продукт отримують у вигляді твердої речовини коричневого кольору (вихід=94%). Т.пл.=49°С. Підготовчий приклад XXIII Метиловий естер 6-(3-аміно-6-хлор-2-піридил)6-гептинової кислоти 92026 20 Використовуючи методику, подібну до методики Підготовчого прикладу V, та як вихідну сполуку метиловий естер 6-гептинової кислоти, очікуваний продукт отримують у вигляді масла жовтого кольору (вихід=85%). 1 Н ЯМР (300МГц, ДМСО-d6) δ: 7,09 (с, 2Н); 5,60 (с, 2Н); 3,60 (с, 3Н); 2,50 (м, 2Н); 2,37 (т, 2Н); 1,63 (м, 4Н). Використовуючи методику, подібну до методики Підготовчого прикладу VII, та як вихідні сполуки - сполуку згідно з Підготовчим прикладом І і придатні сульфонілхлориди, отримують наступні арил- або гетероарилсульфонаміди: Підготовчий приклад XXIV N-(6-Хлор-2-йод-3-піридил)-4етилбензолсульфонамід Тверда речовина жовтого кольору, вихід=88%. Т.пл.=141°С. Підготовчий приклад XXV N-(6-Хлор-2-йод-3-піридил)-4метоксибензолсульфонамід Тверда речовина коричневого кольору, вихід=98%. Т.пл.=93°С. Підготовчий приклад XXVI N-(6-Хлор-2-йод-3-піридил)-2,3дихлорбензолсульфонамід Тверда речовина бежевого кольору, вихід=99%. Т.пл.>260°С. Підготовчий приклад XXVII N-(6-Хлор-2-йод-3-піридил)-4-(1метилетил)бензолсульфонамід Тверда речовина жовтого кольору, вихід=93%. Т.пл.=132°С. Підготовчий приклад XXVIII N-(6-Хлор-2-йод-3-піридил)-1нафталінсульфонамід Тверда речовина білого кольору, вихід=54%. Т.пл.=135°С. Підготовчий приклад XXIX N-(6-Хлор-2-йод-3-піридил)-8хінолінсульфонамід Тверда речовина рожевого кольору, вихід=14%. Т.пл.=199°С. Підготовчий приклад XXX N-(6-Хлор-2-йод-3-піридил)-2,5диметоксибензолсульфонамід Тверда речовина бежевого кольору, вихід=99%. Т.пл.=147°С. Підготовчий приклад XXXI N-(6-Хлор-2-йод-3-піридил)-1,3-бензодіоксол5-сульфонамід Тверда речовина білого кольору, вихід=95%. Т.пл.=187°С. Підготовчий приклад XXXII N-(6-Хлор-2-йод-3-піридил)-2,3-дигідро-1,4бензодіоксин-6-сульфонамід Тверда речовина жовтого кольору, вихід=94%. Т.пл.=122°С. Підготовчий приклад XXXIII N-(6-Хлор-2-йод-3-піридил)-2,3-дигідро-5бензофурансульфонамід 21 Тверда речовина білого кольору, вихід=94%. Т.пл.=187°С. Підготовчий приклад XXXIV N-(6-Хлор-2-йод-3-піридил)-3,5диметилбензолсульфонамід Тверда речовина бежевого кольору, вихід=99%. Т.пл.=138°С. Підготовчий приклад XXXV N-(6-Хлор-2-йод-3-піридил)-3,4-дигідро-4метил-2Н-1,4-бензоксазин-7-сульфонамід Тверда речовина білого кольору, вихід=99%. Т.пл.=139°С. Підготовчий приклад XXXVI N-(2-Бром-6-метил-3піридил)бензолсульфонамід Використовуючи методику, подібну до методики Підготовчого прикладу VII, та як вихідну сполуку - 3-аміно-2-бром-6-метилпіридин, очікуваний продукт отримують у вигляді твердої речовини бежевого кольору (вихід=95%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 10,05 (с, 1Н); 7,70 (м, 3Н); 7,61 (д, 2Н); 7,47 (д, 1Н); 7,25 (д, 1Н); 2,39 (с, 3Н). Підготовчий приклад XXXVII 3-Аміно-2-бром-6-метоксипіридин Отримують суміш 1,83г (14,7мМ) 5-аміно-2метоксипіридину і 1,21г (14,7мМ) ацетату натрію в 12мл оцтової кислоти і обережно при перемішуванні додають 0,75мл (14,7мМ) брому, підтриуючи кімнатну температуру. Реакційну суміш залишають перемішуватися протягом 30 хвилин при кімнатній температурі, і потім додають 200мл насиченого розчину тіосульфату натрію. Отриману водну фазу екстрагують двічі етилацетатом. Об'єднані органічні фази сушать над сульфатом магнію і концентрують при зниженому тиску. Отримують 3г очікуваної сполуки у вигляді твердої речовини фіолетового кольору (кількісний вихід). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 7,18 (д, 1Н); 6,64 (д, 1Н); 4,91 (с, 2Н); 3,71 (с, 3Н). Підготовчий приклад XXXVIII (2-Бромо-6-метокси-3піридил)бензолсульфонамід Використовуючи методику, подібну до методики Підготовчого прикладу VII, та як вихідну сполуку - 3-аміно-2-бромо-6-метоксипіридин, очікуваний продукт отримують у вигляді твердої речовини коричневого кольору (вихід=50%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 9.92 (с, 1Н); 7,67 (м, 3Н); 7,57 (м, 2Н); 7,45 (д, 1Н); 6,84 (д, 1Н); 3,80 (с, 3Н). Підготовчий приклад XXXIX 3-Аміно-2-йод-6-метоксипіридин Використовуючи методику, подібну до методики Підготовчого прикладу IV, та як вихідну сполуку - 5-аміно-2-метоксипіридин, очікуваний продукт отримують у вигляді масла коричневого кольору (вихід=6%). 1 Н ЯМР (300МГц, ДМСО-d6) δ: 7,08 (д, 1Н); 6,62 (д, 1Н); 4,81 (с, 2Н); 3,71 (с, 3Н). Підготовчий приклад XL (2-Йод-6-метокси-3піридил)бензолсульфонамід 92026 22 Використовуючи методику, подібну до методики Підготовчого прикладу VII, та як вихідну сполуку - 3-аміно-2-йод-б-метоксипіридин, отримують очікуваний продукт у вигляді твердої речовини коричневого кольору (вихід=91%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 9,84 (с, 1Н); 7,65 (м, 5Н); 7,17 (д, 1Н); 6,77 (д, 1Н); 3,79 (с, 3Н). Підготовчий приклад XLI N-(2-Бром-6-метил-3-піридил)-6бензотіазолсульфонамід Використовуючи методику, подібну до методики Підготовчого прикладу VII, та як вихідні сполуки 3-аміно-2-бром-6-метилпіридин і 6бензотіазолсульфонілхлорид, отримують очікуваний продукт у вигляді пасти бежевого кольору (вихід=35%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 10,20 (с, 1Н); 9,63 (с, 1Н); 8,61 (д, 1Н); 8,25 (д, 1Н); 7,85 (дд, 1Н); 7,49 (д, 1Н); 7,26 (д, 1Н); 2,39 (с, 3Н). Підготовчий приклад XLII N-(6-Хлор-2-йод-3-піридил)-3піридинсульфонамід Використовуючи методику, подібну до методики Підготовчого прикладу XVIII, та як вихідну сполуку - 3-піридинсульфонілхлорид, очікуваний продукт отримують у вигляді пастоподібної сполуки, яку використовують без подальшого очищення для одержання сполуки згідно з Прикладом 252. Підготовчий приклад XLIII N-(6-Хлор-2-йод-3-піридил)-6хінолінсульфонамід Використовуючи методику, подібну до методики Підготовчого прикладу XVIII, та як вихідну сполуку - 6-хінолінсульфонілхлорид, очікуваний продукт отримують у вигляді твердої речовини білого кольору (вихід=99%) Т.пл.>250°С. Підготовчий приклад XLIV N-(2-Йод-6-хлор-3-піридил)-6бензотіазолсульфонамід Використовуючи методику, подібну до методики Прикладу 50, та як вихідні сполуки - 3-аміно-2йод-6-хлорпіридин і 6бензотіазолсульфонілхлорид, отримують очікуваний продукт у вигляді твердої речовини оранжевого кольору (вихід=33%). Т.пл.=191°С. Підготовчий приклад XLV Метиловий естер 5-(трифторметил)-1Hпіроло[3,2-b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 3, та як вихідну сполуку - метиловий естер згідно з Підготовчим прикладом XXII, отримують очікуваний продукт у вигляді твердої речовини бежевого кольору (вихід=66%). Т.пл.=137°С. Підготовчий приклад XLVI Метиловий естер 6-[6-хлор-3-[[(4-фтор-3нітрофеніл)сульфоніл]аміно]-2-піридил]-5гексинової кислоти Використовуючи методику, подібну до методики Підготовчого прикладу VI, та як вихідну сполуку - 4-фтор-3-нітробензолсульфонілхлорид, отримують очікуваний продукт у вигляді масла жовтого кольору (вихід=31%). 23 1 Н ЯМР (300МГц, ДМСО-d6) δ: 10,63 (с, 1Н); 8,41 (дд, 1Н); 8,06 (м, 1Н); 7,75 (м, 2Н); 7,46 (д, 1Н); 3,61 (с, 3Н); 2,39 (м, 4Н); 1,72 (квінт., 2Н). Підготовчий приклад XLVII Метиловий естер 6-[3-[[(2,1,3-бензотіадіазол-4іл)сульфоніл]аміно]-6-хлор-2-піридил]-5-гексинової кислоти Використовуючи методику, подібну до методики Підготовчого прикладу VI, та як вихідну сполуку - 2,1,3-бензотіадіазол-4-сульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=64%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 10,36 (с, 1Н); 8,40 (д, 1Н); 8,18 (д, 1Н); 7,84 (м, 2Н); 7,48 (д, 1Н); 3,62 (с, 3Н); 2,26 (т, 2Н); 2,01 (т, 2Н); 1,47 (квінт., 2Н). Приклад 5 Етиловий естер 2-[[5-хлор-1-(фенілсульфоніл)1Н-піроло[3,2-b]пірид-2-іл]-метокси]пропанової кислоти Використовуючи методику, подібну до методики Прикладу 1, та як вихідну сполуку - етиловий естер 2-(2-пропінілокси)пропанової кислоти, очікувану сполуку отримують у вигляді масла жовтого кольору (вихід=62%). 1 Н ЯМР (300МГц, ДМСО-d6) δ: 1,18 (т, 3Н); 1,31 (д, 3Н); 4,12 (к, 2Н); 4,24 (к, 1Н); 4,92 (д, 1Н); 5,05 (д, 1Н); 6,95 (с, 1Н); 7,43 (д, 1Н); 7,60 (т, 2Н); 7,74 (т, 1Н); 8,02 (д, 2Н); 8,42 (д, 1Н). Приклад 6 2-[[5-Хлор-1-(фенілсульфоніл)-1Н-піроло[3,2b]пірид-2-іл]метокси]пропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 5, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=57%). Т.пл.=153-155°С. Приклад 7 Метиловий естер 2-[[5-хлор-1(фенілсульфоніл)-1Н-піроло[3,2-b]пірид-2-іл]метокси]-2-метилпропанової кислоти Використовуючи методику, подібну до методики Прикладу 1, та як вихідну сполуку - метиловий естер 2-метил-2-(2-пропінілокси)пропанової кислоти, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=20%). Т.пл.=8487°С. Приклад 8 2-[[5-Хлор-1-(фенілсульфоніл)-1Н-піроло[3,2b]пірид-2-іл]-метокси]-2-метилпропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 7, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=57%). Т.пл.=183-185°С. Приклад 9 Метиловий естер 5-хлор-1-(фенілсульфоніл)1N-піроло[3,2-b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 1, та як вихідну сполуку - метиловий естер 5-гексинової кислоти, очікувану сполуку отримують у вигляді твердої речовини жовтого кольору (вихід=38%). 92026 24 Т.пл.=85-90°С. Приклад 10 5-Хлор-1-(фенілсульфоніл)-1Н-піроло[3,2b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 9, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=38%). Т.пл.=160-164°С. Приклад 11 Метиловий естер 3-(1-бензолсульфоніл-5хлор-1Н-піроло[3,2-b]пірид-2-іл)-2,2диметилпропанової кислоти Використовуючи методику, подібну до методики Прикладу 1, та як вихідну сполуку - метиловий естер 2,2-диметил-4-пентинової кислоти, очікувану сполуку отримують у вигляді масла жовтого кольору (вихід=82%). 1 Н ЯМР (300МГц, ДМСО-d6) δ: 1,22 (с, 6Н); 3,41 (с, 2Н); 3,62 (с, 3Н); 6,58 (с, 1Н); 7,40 (д, 1Н); 7,59 (т, 2Н); 7,72 (т, 1Н); 7,82 (д, 2Н); 8,42 (д, 1Н). Приклад 12 3-(1-Бензолсульфоніл-5-хлор-1Н-піроло[3,2b]пірид-2-іл)-2,2-диметилпропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 11, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=18%). Т.пл.==208-211°С. Приклад 13 Етиловий естер 2-[[1-(фенілсульфоніл)-5(трифторметил)-1Н-піроло[3,2-b]пірид-2іл]метокси]пропанової кислоти Використовуючи методику, подібну до методики Прикладу 1, та як вихідні сполуки - сполуку згідно з Підготовчим прикладом VII та етиловий естер 2-(2-пропінілокси)пропанової кислоти, очікувану сполуку отримують у вигляді безбарвного масла (вихід=63%). 1 Н ЯМР (300МГц, ДМСО-d6) δ: 1,17 (т, 3Н); 1,31 (д, 3Н); 4,11 (к, 2Н); 4,23 (к, 1Н); 4,97 (д, 1Н); 5,10 (д, 1Н); 7,12 (с, 1Н); 7,61 (т, 2Н); 7,75 (т, 1Н); 7,80 (д, 1Н); 8,06 (д, 2Н); 8,63 (д, 1Н). Приклад 14 2-[[1-(Фенілсульфоніл)-5-(трифторметил)-1Hпіроло[3,2-b]пірид-2-іл]метокси]пропанова кислота Використовуючи методику, подібну до методики Приклад 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 13, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=56%). Т.пл.=53-57°С. Приклад 15 Метиловий естер 2-[[1-(фенілсульфоніл)-5(трифторметил)-1H-піроло[3,2-b]пірид-2іл]метокси]-2-метилпропанової кислоти Використовуючи методику, подібну до методики Прикладу 13, та як вихідні сполуки - сполуку згідно з Підготовчим прикладом VII і метиловий естер 2-метил-2-(2-пропінілокси)пропанової кислоти, очікувану сполуку отримують у вигляді масла жовтого кольору (вихід=30%). 25 1 Н ЯМР (300МГц, ДМСО-d6) δ: 1,44 (с, 6Н); 3,65 (с, 3Н); 4,93 (с, 2Н); 7,10 (с, 1Н); 7,63 (т, 2Н); 7,76 (т, 1Н); 7,83 (д, 1Н); 8,05 (д, 2Н); 8,64 (д, 1Н). Приклад 16 2-[[1-(Фенілсульфоніл)-5-(трифторметил)-1Нпіроло[3,2-b]пірид-2-іл]метокси]-2-метилпропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 15, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=45%). Т.пл.=122-125°С. Приклад 17 Метиловий естер 1-(фенілсульфоніл)-5(трифторметил)-1H-піроло[3,2-b]піридин-2пропанової кислоти Використовуючи методику, подібну до методики Прикладу 13, та як вихідну сполуку - метиловий естер 4-пентинової кислоти, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=91%). Т.пл.=119°С. Приклад 18 1-(Фенілсульфоніл)-5(трифторметил)-1Н-піроло[3,2-b]піридин-2пропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 17, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=53%). Т.пл.=180°С. Приклад 19 1-(Фенілсульфоніл)-5-(трифторметил)-1Nпіроло[3,2-b]піридин-2-бутанова кислота, метиловий естер Використовуючи методику, подібну до методики Прикладу 13, та як вихідну сполуку - метиловий естер 5-гексинової кислоти, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=88%). Т.пл.=95°С. Приклад 20 1-(Фенілсульфоніл)-5(трифторметил)-1H-піроло[3,2-b]піридин-2бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 19, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=58%). Т.пл.=168°С. Приклад 21 Метиловий естер 1-[(2-аміно-6бензотіазоліл)сульфоніл]-5-хлор-1Н-піроло[3,2b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 3, та як вихідну сполуку - сполуку згідно з Підготовчим прикладом X, очікувану сполуку отримують у вигляді твердої речовини жовтого кольору (вихід=63%). Т.пл.=85-90°С. Приклад 22 1-[(2-Аміно-6-бензотіазоліл)сульфоніл]-5-хлор1Н-піроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - сполуку, 92026 26 отриману згідно з Прикладом 21, очікуваний продукт отримують у вигляді твердої речовини білого кольору (вихід=82%). Т.пл.>250°С. Приклад 23 Метиловий естер 1-(1,3-бензодіоксол-5ілсульфоніл)-5-хлор-1H-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Прикладу 3, та як вихідну сполуку - сполука згідно з Підготовчим прикладом IX, очікувану сполуку отримують у вигляді твердої речовини жовтого кольору (вихід=74%). Т.пл.=120°С. Приклад 24 1-(1,3-Бензодіоксол-5-ілсульфоніл)-5-хлор-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - сполуку, отриману згідно з Прикладом 23, очікуваний продукт отримують у вигляді твердої речовини бежевого кольору (вихід=95%). Т.пл.=160°С. Приклад 25 Метиловий естер 5-хлор-1-[(3,5диметилфеніл)сульфоніл]-1Н-піроло[3,2-b]піридин2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 3, та як вихідну сполуку - сполуку згідно з Підготовчим прикладом XI, очікувану сполуку отримують у вигляді твердої речовини коричневого кольору (вихід=99%). Т.пл.=138°С. Приклад 26 5-Хлор-1-[(3,5-диметилфеніл)сульфоніл]-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - сполуку, отриману згідно з Прикладом 25, очікуваний продукт отримують у вигляді твердої речовини бежевого кольору (вихід=88%). Т.пл.=200°С. Приклад 27 Метиловий естер 5-хлор-1-[(2,5диметоксифеніл)сульфоніл]-1H-піроло[3,2b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 3, та як вихідну сполуку - сполуку згідно з Підготовчим прикладом XII, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=94%). Т.пл.=102°С. Приклад 28 5-Хлор-1-[(2,5-диметоксифеніл)сульфоніл]-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - сполуку, отриману згідно з Прикладом 27, очікуваний продукт отримують у вигляді твердої речовини білого кольору (вихід=95%). Т.пл.=227-231°С. Приклад 29 Метиловий естер 5-хлор-1-(1нафталенілсульфоніл)-1Н-піроло[3,2-b]піридин-2бутанової кислоти 27 Використовуючи методику, подібну до методики Прикладу 3, та як вихідну сполуку - сполуку згідно з Підготовчим прикладом XIII, отримують очікувану сполуку у вигляді масла жовтого кольору (вихід=86%). 1 Н ЯМР (300МГц, ДМСО-d6) δ: 1,83 (квінт., 2Н); 2,34 (т, 2Η); 2,88 (т, 2Η); 3,52 (с, 3Н); 6,83 (с, 1Н); 7,39 (д, 1Н); 7,71 (м, 4Н); 8,14 (м, 1Н); 8,30 (м, 1Н); 8,37 (м, 2Н). Приклад 30 5-Хлор-1-(1-нафталенілсульфоніл)-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - сполуку, отриману згідно з Прикладом 29, очікуваний продукт отримують у вигляді твердої речовини білого кольору (вихід=96%). Т.пл.=202-206°С. Приклад 31 Метиловий естер 5-хлор-1-[(3,4-дигідро-4метил-2H-1,4-бензоксазин-7-іл)сульфоніл]-1Нпіроло[3,2-b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 3, та як вихідну сполуку - сполуку згідно з Підготовчим прикладом XIV, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=78%). Т.пл.=106-110°С. Приклад 32 5-Хлор-1-[(3,4-дигідро-4-метил-2Н-1,4бензоксазин-7-іл)сульфоніл]-1Н-піроло[3,2b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - сполуку, отриману згідно з Прикладом 31, очікуваний продукт отримують у вигляді твердої речовини білого кольору (вихід=98%). Т.пл.=180-183°С. Приклад 33 Метиловий естер 1-(1,3-бензодіоксол-5ілсульфоніл)-5-хлор-1Н-піроло[3,2-b]піридин-2пропанової кислоти Використовуючи методику, подібну до методики Прикладу 3, та як вихідну сполуку - сполуку згідно з Підготовчим прикладом XV, очікувану сполуку отримують у вигляді масла жовтого кольору (вихід=76%). 1 Н ЯМР (300МГц, ДМСО-d6) δ: 2,84 (т, 2Η); 3,31 (т, 2Η); 3,47 (т, 2Η); 3,62 (с, 3Н); 6,16 (с, 2Н); 6,72 (с, 1Н); 7,09 (д, 1Н); 7,37 (д, 1Н); 7,38 (с, 1Н); 7,51 (дд, 1Н); 8,40 (с, 1Н). Приклад 34 1-(1,3-Бензодіоксол-5-ілсульфоніл)-5-хлор-1Нпіроло[3,2-b]піридин-2-пропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - сполуку, отриману згідно з Прикладом 33, очікуваний продукт отримують у вигляді твердої речовини коричневого кольору (вихід=98%). Т.пл.=186°С. Приклад 35 Метиловий естер 1-(6бензотіазолілсульфоніл)-5-хлор-1H-піроло[3,2b]піридин-2-пропанової кислоти 92026 28 Використовуючи методику, подібну до методики Прикладу 3, та як вихідну сполуку - сполуку згідно з Підготовчим прикладом XVI, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=57%). Т.пл.=146°С. Приклад 36 1-(6-Бензотіазолілсульфоніл)-5-хлор-1Hпіроло[3,2-b]піридин-2-пропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - сполуку, отриману згідно з Прикладом 35, очікуваний продукт отримують у вигляді твердої речовини білого кольору (вихід=90%). Т.пл.=248°С. Приклад 37 Натрієва сіль 5-хлор-1-(фенілсульфоніл)-1Hпіроло[3,2-b]піридин-2-пропанової кислоти 1,46г (4мМ) Кислоти, отриманої згідно з Прикладом 2, перемішують в 12мл тетрагідрофурану і додають 8мл (4мМ) 0,5N розчину гідроксиду натрію у воді. Реакційне середовище перемішують протягом 2 годин при кімнатній температурі і потім концентрують при зниженому тиску. Маслянистий залишок розтирають з метанолом і утворений білий осад відокремлюють фільтрацією та сушать у вакуумі. Очікувану сіль отримують у вигляді порошкоподібної твердої речовини білого кольору (вихід=98%). Т.пл.=200°С. Приклад 38 Етиловий естер 2-[[1-(2,1,3-бензотіадіазол-5ілсульфоніл)-5-хлор-1Н-піроло[3,2-b]пірид-2іл]метокси]пропанової кислоти Використовуючи методику, подібну до методики Підготовчого прикладу VI, та як вихідні сполуки естер згідно з Підготовчим прикладом XVII і 1,2,3бензотіадіазол-5-сульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини оранжевого кольору (вихід=46%). Т.пл.=77-79°С. Приклад 39 2-[[1-(2,1,3-Бензотіадіазол-5-ілсульфоніл)-5хлор-1Н-піроло[3,2-b]пірид-2-іл]метокси]пропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 38, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=16%). Т.пл.=192-194°С. Приклад 40 Етиловий естер 2-[[5-хлор-1-[(2-метил-7бензотіазоліл)сульфоніл]-1Н-піроло[3,2-b]пірид-2іл]метокси]пропанової кислоти Використовуючи методику, подібну до методики Підготовчого прикладу VI, та як вихідні сполуки естер згідно з Підготовчим прикладом XVII і 2метил-7-бензотіазолсульфонілхлорид, очікувану сполуку отримують у вигляді безбарвного масла (вихід=50%). 1 Н ЯМР (300МГц, ДМСО-d6) δ: 8,32 (д, 1Н); 8,27 (д, 1Н); 7,94 (д, 1Н); 7,67 (т, 1Н); 7,43 (д, 1Н); 7,00 (с, 1Н); 5,02 (д, 1Н); 4,88 (д, 1Н); 4,13 (к, 1Н); 4,07 (к, 2Н); 2,85 (с, 3Н); 1,15 (м, 6Н). 29 Приклад 41 2-[[5-Хлор-1-[(2-метил-7бензотіазоліл)сульфоніл]-1Н-піроло[3,2-b]пірид-2іл]метокси]пропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 40, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=28%). Т.пл.=203-205°С. Приклад 42 Метиловий естер 2-[[5-хлор-1-[(3метоксифеніл)сульфоніл]-1Н-піроло[3,2-b]пірид-2іл]метокси]-2-метилпропанової кислоти Використовуючи методику, подібну до методики Прикладу 1, та як вихідні сполуки - сполуку згідно з Підготовчим прикладом XVIII і метиловий естер 2-метил-2-(2-пропінілокси)пропанової кислоти, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=33%). Т.пл.=153°С. Приклад 43 2-[[5-Хлор-1-[(3-метоксифеніл)сульфоніл]-1Нпіроло[3,2-b]пірид-2-іл]метокси]-2-метилпропанова кислота Готують розчин 186мг (0,41мМ) естеру, отриманого згідно з Прикладом 42, в 7,5мл оцтової кислоти і при перемішуванні та при кімнатній температурі додають 0,75мл концентрованої соляної кислоти. Реакційну суміш підтримують при слабкому кипінні із зворотним холодильником протягом 18 годин і потім концентрують при зниженому тиску. Залишок після випарювання переносять у воді й екстрагують дихлорметаном. Органічну фазу промивають водою, сушать над сульфатом магнію і концентрують при зниженому тиску. Сирий продукт очищають хроматографією на силікагелі, елююючи сумішшю дихлорметан/метанол (градієнт від 99/1 до 90/10, об./об.). Таким чином отримують цільову кислоту у вигляді твердої речовини бежевого кольору (вихід=70%). Т.пл.=130°С. Приклад 44 Етиловий естер 2-[[1-[(2-ацетиламіно-6бензотіазоліл)сульфоніл]-5-хлор-1Н-піроло[3,2b]пірид-2-іл]метокси]пропанової кислоти Використовуючи методику, подібну до методики Підготовчого прикладу VI, та як вихідні сполуки естер згідно з Підготовчим прикладом XVII та 2ацетиламіно-6-бензотіазолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=25%). Т.пл.=100-102°С. Приклад 45 2-[[1-[(2-Ацетиламіно-6бензотіазоліл)сульфоніл]-5-хлор-1Н-піроло-[3,2b]пірид-2-іл]метокси]пропанова кислота Використовуючи методику, подібну до методики Прикладу 43, та як вихідну сполуку - естер, отриманий згідно з Прикладом 44, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=25%). Т.пл.=257-260°С. Приклад 46 92026 30 Етиловий естер 2-[[1 -[(2-аміно-6бензотіазоліл)сульфоніл]-5-хлор-1Н-піроло[3,2b]пірид-2-іл]метокси]пропанової кислоти Використовуючи методику, подібну до методики Підготовчого прикладу VI, та як вихідні сполуки естер згідно з Підготовчим прикладом XVII та 2аміно-6-бензотіазолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини жовтого кольору (вихід=25%). Т.пл.=86-88°С. Приклад 47 2-[[1-[(2-Аміно-6-бензотіазоліл)сульфоніл]-5хлор-1Н-піроло[3,2-b]пірид-2-іл]метокси]пропанова кислота Використовуючи методику, подібну до методики Прикладу 43, та як вихідну сполуку - естер, отриманий згідно з Прикладом 46, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=65%). Т.пл.=218-220°С. Приклад 48 Метиловий естер 2-[[1-(6бензотіазолілсульфоніл)-5-(трифторметил)-1Нпіроло[3,2-b]пірид-2-іл]метокси]-2метилпропанової кислоти Використовуючи методику, подібну до методики Підготовчого прикладу VI, та як вихідні сполуки сполуку згідно з Підготовчим прикладом XIX і 6бензотіазолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=13%). Т.пл.=124-127°С. Приклад 49 2-[[1-(6-Бензотіазолілсульфоніл)-5(трифторметил)-1Н-піроло[3,2-b]пірид-2іл]метокси]-2-метилпропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 48, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=16%). Т.пл.=180-182°С. Приклад 50 Етиловий естер 2-[[1-(6бензотіазолілсульфоніл)-5-хлор-1H-піроло[3,2b]пірид-2-іл]-метокси]пропанової кислоти Готують розчин 350мг (1,24мМ) естеру згідно з Підготовчим прикладом XVII в 8мл піридину і при 0°С при перемішуванні додають 550мг (2,35мМ) 6бензотіазолсульфонілхлориду. Реакційне середовище перемішують при кімнатній температурі протягом 24 годин і потім розбавляють етилацетатом. Цю органічну фазу промивають 2N розчином соляної кислоти і потім водою, сушать над сульфатом магнію і концентрують при зниженому тиску. Отримане масло переносять в 10мл ТГФ і поступово до цього розчину, охолодженого до 0°С, додають 2,6мл (2,6мМ) тетрабутиламонійфториду у вигляді 1Μ розчину в ТГФ. Реакційну суміш перемішують протягом 24 годин при 4°С, і потім розчиняють в ДХМ. Отриману органічну фазу промивають N розчином соляної кислоти і потім водою, сушать над сульфатом магнію і концентрують при зниженому тиску. Сирий продукт очищають хроматографією на силікагелі, елююючи сумішшю толу 31 ол/етилацетат (95/5 і потім 9/1; об./об.). Таким чином отримують цільовий продукт у вигляді масла жовтого кольору (вихід=31%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 9,68 (с, 1Н); 9,11 (д, 1Н); 8,50 (д, 1Н); 8,23 (д, 1Н); 8,10 (дд, 1Н); 7,43 (д, 1Н); 6,96 (с, 1Н); 5,08 (д, 1Н); 4,96 (д, 1Н); 4,25 (к, 1Н); 4,12 (к, 2Н); 1,28 (д, 3Н); 1,19 (т, 3Н). Приклад 51 2-[[1-(6-Бензотіазолілсульфоніл)-5-хлор-1Нпіроло[3,2-b]пірид-2-іл]метокси]пропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 50, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=40%). Т.пл.=179°С. Приклад 52 Етиловий естер 2-[[1-(6бензотіазолілсульфоніл)-5-(трифторметил)-1Hпіроло[3,2-b]пірид-2-іл]метокси]пропанової кислоти Готують розчин 140мг (0,443мМ) сполуки згідно з Підготовчим прикладом XX в 2мл піридину і додають 228мг (0,98мМ) 6бензотіазолсульфонілхлориду. Реакційну суміш перемішують при кімнатній температурі протягом 48 годин і потім розбавляють етилацетатом. Отриману органічну фазу промивають послідовно водою, N соляною кислотою, знову водою, розчином бікарбонату натрію і нарешті розчином хлориду натрію. Після висушування над сульфатом магнію і концентрування отримують 242мг етилового естеру 2-[[3-[3-(6-бензотіазолілсульфоніламіно)-6(трифторметил)-2-піридил]-2пропініл]окси]пропанової кислоти, який переносять в 5мл ДХМ в реакторній трубці, адаптованій до нагрівання мікрохвилями. Додають 100мг (0,5мМ) моногідрату ацетаміді і цю суміш нагрівають при 150°С протягом 15 хвилин. Реакційне середовище охолоджують, фільтрують і концентрують при зниженому тиску. Після очищення хроматографією на колонці з діоксидом кремнію з елююванням сумішшю толуол/етилацетат (9/1; об./об.), очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=42%). Т.пл.=96°С. Приклад 53 2-[[1-(6-Бензотіазолілсульфоніл)-5(трифторметил)-1Н-піроло[3,2-b]пірид-2іл]метокси]пропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 52, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=50%). Т.пл.=124°С. Приклад 54 Метиловий естер 5-хлор-1-[(2,5диметоксифеніл)сульфоніл]-1H-піроло[3,2b]піридин-2-пропанової кислоти Використовуючи методику, подібну до методики Прикладу 52, та як вихідні сполуки - сполуку згідно з Підготовчим прикладом VIII і 2,5диметоксибензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=77%). 92026 32 Т.пл.=127°С. Приклад 55 5-Хлор-1-[(2,5-диметоксифеніл)сульфоніл]-1Hпіроло[3,2-b]піридин-2-пропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 54, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=71%). Т.пл.=204-209°С. Приклад 56 Метиловий естер 1-[(2-аміно-6бензотіазоліл)сульфоніл]-5-хлор-1H-піроло[3,2b]піридин-2-пропанової кислоти Використовуючи методику, подібну до методики Прикладу 52, та як вихідні сполуки - естер згідно з Підготовчим прикладом VIII і 2-аміно-6бензотіазолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини жовтого кольору (вихід=38%). Т.пл.=205-215°С. Приклад 57 1-[(2-Аміно-6-бензотіазоліл)сульфоніл]-5-хлор1Н-піроло[3,2-b]піридин-2-пропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 56, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=57%). Т.пл.>260°С. Приклад 58 Метиловий естер 5-хлор-1-[(3,5диметилфеніл)сульфоніл]-1H-піроло[3,2-b]піридин2-пропанової кислоти Використовуючи методику, подібну до методики Прикладу 52, та як вихідні сполуки - сполуку згідно з Підготовчим прикладом VIII і 3,5диметилбензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=86%). Т.пл.=182-185°С. Приклад 59 5-Хлор-1-[(3,5-диметилфеніл)сульфоніл]-1Нпіроло[3,2-b]піридин-2-пропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 58, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=99%). Т.пл.=181-186°С. Приклад 60 Метиловий естер 5-хлор-1-[(3,4-дигідро-4метил-2Н-1,4-бензоксазин-7-іл)сульфоніл]-1Нпіроло[3,2-b]піридин-2-пропанової кислоти Використовуючи методику, подібну до методики Прикладу 52, та як вихідні сполуки - сполуку згідно з Підготовчим прикладом VIII і 3,4-дигідро-4метил-2H-1,4-бензоксазин-7-сульфонілхлорид, очікувану сполуку отримують у вигляді масла жовтого кольору (вихід=87%). 1 Н ЯМР (300МГц, ДМСО-d6) δ: 8,43 (д, 1Н); 7,37 (д, 1Н); 7,07 (дд, 1Н); 6,94 (д, 1Н); 6,81 (д, 1Н); 6,69 (с, 1Н); 4,25 (м, 2Н); 3,62 (с, 3Н); 3,26 (м, 4Н); 2,86 (м, 2Н); 2,82 (с, 3Н). Приклад 61 33 5-Хлор-1-[(3,4-дигiдро-4-метил-2Н-1,4бензоксазин-7-іл)сульфоніл]-1Н-піроло[3,2b]піридин-2-пропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 60, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=98%). Т.пл.=175-185°С. Приклад 62 Метиловий естер 5-хлор-1-(8хінолілсульфоніл)-1Н-піроло[3,2-b]піридин-2пропанової кислоти Використовуючи методику, подібну до методики Прикладу 52, та як вихідні сполуки - сполуку згідно з Підготовчим прикладом VIII і 8хінолінсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=59%). Т.пл.=120°С. Приклад 63 5-Хлор-1-(8-хінолілсульфоніл)-1Н-піроло[3,2b]піридин-2-пропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 62, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=98%). Т.пл.=183°С. Приклад 64 Метиловий естер 5-хлор-1-(1нафталенілсульфоніл)-1H-піроло[3,2-b]піридин-2пропанової кислоти Використовуючи методику, подібну до методики Прикладу 52, та як вихідні сполуки - сполуку згідно з Підготовчим прикладом VIII і 1нафталінсульфонілхлорид, очікувану сполуку отримують у вигляді масла жовтого кольору (вихід=66%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 8,34 (м, 3Н); 8,15 (м, 1Н); 7,69 (м, 4Н); 7,39 (д, 1Н); 6,81 (с, 1Н); 3,56 (с, 3Н); 3,12 (т, 2Η); 2,74 (т, 2Η). Приклад 65 5-Хлор-1-(1-нафталенілсульфоніл)-1Hпіроло[3,2-b]піридин-2-пропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 64, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=86%). Т.пл.=93°С. Приклад 66 Метиловий естер 1-[(1-ацетил-2,3-дигідро-1Ніндол-5-іл)сульфоніл]-5-хлор-1Н-піроло[3,2b]піридин-2-пропанової кислоти Використовуючи методику, подібну до методики Прикладу 52, та як вихідні сполуки - сполуку згідно з Підготовчим прикладом VIII і 1-ацетил-2,3дигідро-1H-індол-5-сульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини коричневого кольору (вихід=93%). Т.пл.=66°С. Приклад 67 92026 34 1-[(1-Ацетил-2,3-дигідро-1Н-індол-5іл)сульфоніл]-5-хлор-1Н-піроло-[3,2-b]піридин-2пропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 66, очікувану сполуку отримують у вигляді твердої речовини жовтого кольору (вихід=37%). Т.пл.=216°С Приклад 68 Метиловий естер 5-хлор-1-[3(трифторметокси)фенілсульфоніл]-1Н-піроло[3,2b]піридин-2-пропанової кислоти Використовуючи методику, подібну до методики Прикладу 52, та як вихідні сполуки - сполуку згідно з Підготовчим прикладом VIII і 3(трифторметокси)бензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини оранжевого кольору (вихід=71%). Т.пл.=102°С. Приклад 69 5-Хлор-1-[3(трифторметокси)фенілсульфоніл]-1Н-піроло[3,2b]піридин-2-пропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 68, очікувану сполуку отримують у вигляді твердої речовини жовтого кольору (вихід=9%). Т.пл.=146°С. Приклад 70 Метиловий естер 1-[(3,5диметилфеніл)сульфоніл]-5-(трифторметил)-1Hпіроло[3,2-b]піридин-2-пропанової кислоти Використовуючи методику, подібну до методики Прикладу 52, та як вихідні сполуки - сполуку згідно з Підготовчим прикладом XXI і 3,5диметилбензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=51%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 8,60 (д, 1Н); 7,79 (д, 1Н); 7,57 (с, 2Н); 7,39 (с, 1Н); 6,90 (с, 1Н); 3,63 (с, 3Н); 3,33 (т, 2Н); 2,87 (т, 2Н); 2,31 (с, 6Н). Приклад 71 1-[(3,5-Диметилфеніл)сульфоніл]-5(трифторметил)-1Н-піроло[3,2-b]піридин-2пропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 70, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=91%). Т.пл.=185-189°С. Приклад 72 Метиловий естер 1-(8-хінолілсульфоніл)-5(трифторметил)-1Н-піроло[3,2-b]піридин-2пропанової кислоти Використовуючи методику, подібну до методики Прикладу 52, та як вихідні сполуки - сполуку згідно з Підготовчим прикладом XXI і 8хінолінсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=51%). 35 1 Н ЯМР (300МГц, ДМСО-d6) δ: 8,72 (м, 2Н); 8,45 (м, 3Н); 7,88 (т, 1Н); 7,72 (д, 1Н); 7,62 (дд, 1Н); 6,76 (с, 1Н); 3,60 (с, 3Н); 3,54 (т, 2Η); 2,88 (т, 2Η). Приклад 73 1-(8-Хінолілсульфоніл)-5-(трифторметил)-1Нпіроло[3,2-b]піридин-2-пропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 72, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=56%). Т.пл.=216-217°С. Приклад 74 Метиловий естер 1-(1-нафталенілсульфоніл)5-(трифторметил)-1Н-піроло[3,2-b]піридин-2пропанової кислоти Використовуючи методику, подібну до методики Прикладу 52, та як вихідні сполуки - сполуку згідно з Підготовчим прикладом XXI і 1нафталінсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=63%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 8,56 (д, 1Н); 8,36 (м, 2Н); 8,17 (м, 1Н); 7,72 (м, 5Н); 6,98 (с, 1Н); 3,56 (с, 3Н); 3,15 (т, 2Η); 2,77 (т, 2Η). Приклад 75 1-(1-Нафталенілсульфоніл)-5-(трифторметил)1Н-піроло[3,2-b]піридин-2-пропанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 74, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=42%). Т.пл.=116-117°С. Приклад 76 Метиловий естер 5-хлор-1-(8хінолілсульфоніл)-1H-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Прикладу 52, та як вихідні сполуки - сполуку згідно з Підготовчим прикладом V і 8хінолінсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=25%). Т.пл.=64°С. Приклад 77 5-Хлор-1-(8-хінолілсульфоніл)-1Н-піроло[3,2b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 76, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=99%). Т.пл.=186-189°С. Приклад 78 Метиловий естер 5-хлор-1-[(2,2-дифтор-1,3бензодіоксол-5-іл)сульфоніл]-1Н-піроло-[3,2b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 2,2дифтор-1,3-бензодіоксол-5-сульфонілхлорид, очікувану сполуку отримують у вигляді безбарвного масла (вихід=95%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 8,43 (д, 1Н); 8,09 (д, 1Н); 7,83 (дд, 1Н); 7,60 (д, 1Н); 7,38 (д, 1Н); 92026 36 6,77 (с, 1Н); 3,59 (с, 3Н); 3,07 (т, 2Н); 2,45 (т, 2Н); 1,97 (м, 2Н). Приклад 79 5-Хлор-1-[(2,2-дифтор-1,3-бензодіоксол-5іл)сульфоніл]-1Н-піроло-[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 78, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=78%). Т.пл.=216°С. Приклад 80 Метиловий естер 5-хлор-1-[(2-метил-5бензотіазоліл)сульфоніл]-1H-піроло[3,2-b]піридин2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 2-метил-5бензотіазолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=79%). Т.пл.=114°С. Приклад 81 5-Хлор-1-[(2-метил-5бензотіазоліл)сульфоніл]-1Н-піроло[3,2-b]піридин2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 80, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=98%). Т.пл.=173°С. Приклад 82 Метиловий естер 5-хлор-1-[(2-метил-6бензотіазоліл)сульфоніл]-1H-піроло[3,2-b]-піридин2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 2-метил-6бензотіазолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=69%). Т.пл.=117°С. Приклад 83 5-Хлор-1-[(2-метил-6бензотіазоліл)сульфоніл]-1H-піроло[3,2-b]піридин2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 82, очікувану сполуку отримують у вигляді твердої речовини жовтого кольору (вихід=99%). Т.пл.=184°С. Приклад 84 Метиловий естер 5-хлор-1-[(2-метил-7бензотіазоліл)сульфоніл]-1H-піроло[3,2-b]піридин2-бутанової кислоти Використовуючи методику, подібну до методики Підготовчого прикладу VI, та як вихідні сполуки сполуку згідно з Підготовчим прикладом V і 2метил-7-бензотіазолсульфоніл-хлорид, очікувану сполуку отримують у вигляді твердої речовини жовтого кольору (вихід=48%). Т.пл.=138°С. Приклад 85 37 5-Хлор-1-[(2-метил-7бензотіазоліл)сульфоніл]-1Н-піроло[3,2-b]піридин2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 84, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=90%). Т.пл.=225°С. Приклад 86 Метиловий естер 5-хлор-1-[(2,3-дигідро-5бензофурил)сульфоніл]-1Н-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 2,3дигідро-5-бензофурансульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини жовтого кольору (вихід=82%). Т.пл.=201°С. Приклад 87 5-Хлор-1-[(2,3-дигідро-5бензофурил)сульфоніл]-1Н-піроло[3,2-b]піридин-2бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 86, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=98%). Т.пл.=225°С. Приклад 88 Метиловий естер 5-хлор-1-[(3,5дихлорфеніл)сульфоніл]-1H-піроло[3,2-b]піридин2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 3,5дихлорбензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=66%). Т.пл.=112-114°С. Приклад 89 5-Хлор-1-[(3,5-дихлорфеніл)сульфоніл]-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 88, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=28%). Т.пл.=164-165°С Приклад 90 Метиловий естер 1-[(2-ацетиламіно-6бензотіазоліл)сульфоніл]-5-хлор-1H-піроло[3,2b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 2ацетиламіно-6-бензотіазолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини жовтого кольору (вихід=35%). Т.пл.=274°С. Приклад 91 1-[(2-Ацетиламіно-6-бензотіазоліл)сульфоніл]5-хлор-1H-піроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 90, очікувану спо 92026 38 луку отримують у вигляді твердої речовини білого кольору (вихід=87%). Т.пл.=270°С. Приклад 92 Метиловий естер 1-[(2-аміно-6бензоксазоліл)сульфоніл]-5-хлор-1H-піроло[3,2b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 2-аміно-6бензоксазолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=35%). Т.пл.=241°С. Приклад 93 1-[(2-Аміно-6-бензоксазоліл)сульфоніл]-5хлор-1H-піроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 92, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=96%). Т.пл.=273°С. Приклад 94 Метиловий естер 5-хлор-1-[(2фторфеніл)сульфоніл]-1Н-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 2фторбензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини коричневого кольору (вихід=87%). Т.пл.=83°С. Приклад 95 5-Хлор-1-[(2-фторфеніл)сульфоніл]-1Hпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 94, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=92%). Т.пл.=176°С. Приклад 96 Метиловий естер 5-хлор-1-[[2(трифторметил)феніл]сульфоніл]-1Н-піроло[3,2b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Підготовчого прикладу VI, та як вихідні сполуки сполуку згідно з Підготовчим прикладом V і 2(трифторметил)-бензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини жовтого кольору (вихід=39%). Т.пл.=127°С. Приклад 97 5-Хлор-1-[[2-(трифторметил)феніл]сульфоніл]1Н-піроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 96, очікувану сполуку отримують у вигляді твердої речовини жовтого кольору (вихід=89%). Т.пл.=171°С. Приклад 98 Метиловий естер 1-([1,1'-біфеніл]-3ілсульфоніл)-5-хлор-1Н-піроло[3,2-b]піридин-2бутанової кислоти 39 Використовуючи методику, подібну до методики Підготовчого прикладу VI, та як вихідні сполуки сполуку згідно з Підготовчим прикладом V і [1,1'біфеніл]-3-сульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=68%). 1 Н ЯМР (300МГц, ДМСО-d6) δ: 8,49 (д, 1Н); 8,03 (м, 2Н); 7,78 (д, 1Н); 7,66 (м, 3Н); 7,47 (м, 3Н); 7,39 (д, 1Н); 6,79 (с, 1Н); 3,55 (с, 3Н); 3,11 (т, 2Н); 2,44 (т, 2Н); 2,01 (м, 2Н). Приклад 99 1-([1,1'-Біфеніл]-3-ілсульфоніл)-5-хлор-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 98, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=23%). Т.пл.=147-149°С. Приклад 100 Метиловий естер 5-хлор-1-[(4фторфеніл)сульфоніл]-1Н-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Підготовчого прикладу VI, та як вихідні сполуки сполуку згідно з Підготовчим прикладом V і 4фторбензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини жовтого кольору (вихід=29%). Т.пл.=119°С. Приклад 101 5-Хлор-1-[(4-фторфеніл)сульфоніл]-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 100, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=66%). Т.пл.=180°С. Приклад 102 Метиловий естер 5-хлор-1-[(3фторфеніл)сульфоніл]-1Н-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 3фторбензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини коричневого кольору (вихід=76%). Т.пл.=104°С. Приклад 103 5-Хлор-1-[(3-фторфеніл)сульфоніл]-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 102, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=75%). Т.пл.=163°С. Приклад 104 Метиловий естер 1-[(1-ацетил-2,3-дигідро-1Ніндол-5-іл)сульфоніл]-5-хлор-1Н-піроло[3,2b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 1-ацетил2,3-дигідро-1H-індол-5-сульфонілхлорид, очікувану 92026 40 сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=91%). Т.пл.=123°С. Приклад 105 1-[(1-Ацетил-2,3-дигідро-1H-індол-5іл)сульфоніл]-5-хлор-1Н-піроло[3,2-b]піридин-2бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 104, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=54%). Т.пл.=226°С. Приклад 106 Метиловий естер 5-хлор-1-[(6-хлорімідазо[2,1b]тіазол-5-іл)сульфоніл]-1H-піроло-[3,2-b]піридин2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 6хлорімідазо[2,1-b]тіазол-5-сульфонілхлорид, очікувану сполуку отримують у вигляді безбарвного масла (вихід=70%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 8,55 (с, 1Н); 8,43 (д, 1Н); 7,95 (м, 5Н); 7,39 (д, 1Н); 6,78 (с, 1Н); 3,58 (с, 3Н); 3,07 (т, 2Н); 2,44 (т, 2Н); 1,97 (м, 2Н). Приклад 107 5-Хлор-1-[(6-хлорімідазо[2,1-b]тіазол-5іл)сульфоніл]-1H-піроло-[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 106, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=99%). Т.пл.=186°С. Приклад 108 Метиловий естер 5-хлор-1-[[4-(1H-піразол-1іл)феніл]сульфоніл]-1Н-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Підготовчогоприкладу VI, та як вихідні сполуки сполуку згідно з Підготовчим прикладом V і 4-(1Hпіразол-1-іл)-бензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=10%). Т.пл.=122-124°С. Приклад 109 5-Хлор-1-[[4-(1H-піразол-1іл)феніл]сульфоніл]-1Н-піроло[3,2-b]піридин-2бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 108, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=58%). Т.пл.=196-207°С. Приклад 110 Метиловий естер 5-хлор-1-[[3(трифторметил)феніл]сульфоніл]-1Н-піроло[3,2b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Підготовчого прикладу VI, та як вихідні сполуки сполуку згідно з Підготовчим прикладом V і 3(трифторметил)-бензолсульфонілхлорид, очікува 41 ну сполуку отримують у вигляді твердої речовини жовтого кольору (вихід=11%). Т.пл.=97°С. Приклад 111 5-Хлор-1-[[3-(трифторметил)феніл]сульфоніл]1Н-піроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 110, очікувану сполуку отримують у вигляді твердої речовини жовтого кольору (вихід=41%). Т.пл.=188°С. Приклад 112 Метиловий естер 5-хлор-1-[[4(трифторметил)феніл]сульфоніл]-1Н-піроло[3,2b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Підготовчого прикладу VI, та як вихідні сполуки сполуку згідно з Підготовчим прикладом V і 4(трифторметил)бензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=27%). Т.пл.=99°С. Приклад 113 5-Хлор-1-[[4-(трифторметил)феніл]сульфоніл]1Н-піроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 112, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=27%). Т.пл.=185°С. Приклад 114 Метиловий естер 5-хлор-1-[[4-(5оксазоліл)феніл]сульфоніл]-1Н-піроло[3,2b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 4-(5оксазоліл)бензолсульфонілхлорид, очікувану сполуку отримують у вигляді безбарвного масла (вихід=50%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 8,55 (с, 1Н); 8,43 (д, 1Н); 7,95 (м, 5Н); 7,39 (д, 1Н); 6,78 (с, 1Н); 3,58 (с, 3Н); 3,07 (т, 2Н); 2,44 (т, 2Н); 1,97 (м, 2Н). Приклад 115 5-Хлор-1-[[4-(5-оксазоліл)феніл]сульфоніл]-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 114, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=27%). Т.пл.=169-176°С. Приклад 116 Метиловий естер 1-[[3,5біс(трифторметил)феніл]сульфоніл]-5-хлор-1Нпіроло[3,2-b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 3,5біс(трифторметил)бензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=62%). Т.пл.=134-144°С. Приклад 117 92026 42 1-[[3,5-Біс(трифторметил)феніл]сульфоніл]-5хлор-1Н-піроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 116, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=6%). Т.пл.=155-164°С. Приклад 118 Метиловий естер 5-хлор-1-[(4-хлор-3метилфеніл )сул ьфоніл]-1H-піроло[3,2-b]піридин2-бутановлї кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 4-хлор-3метилбензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=78%). Т.пл.=111-114°С Приклад 119 5-Хлор-1-[(4-хлор-3-метилфеніл)сульфоніл]1Н-піроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 118, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=42%). Т.пл.=175-183°С. Приклад 120 Метиловий естер 1-([1,1'-біфеніл]-4ілсульфоніл)-5-хлор-1H-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - [1,1'біфеніл]-4-сульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=85%). Т.пл.=122-124°С. Приклад 121 1-([1,1'-Біфеніл]-4-ілсульфоніл)-5хлор-1Н-піроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 120, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=55%). Т.пл.=186-190°С. Приклад 122 Метиловий естер 5-хлор-1-[(3,4дифторфеніл)сульфоніл]-1Н-піроло[3,2-b]піридин2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 3,4дифторбензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=61%). Т.пл.=96-98°С. Приклад 123 5-Хлор-1-[(3,4-дифторфеніл)сульфоніл]-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 122, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=59%). Т.пл.=180-190°С. Приклад 124 43 Метиловий естер 5-хлор-1-[3(трифторметокси)фенілсульфоніл]-1H-піроло[3,2b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 3(трифторметокси)бензолсульфонілхлорид, очікувану сполуку отримують у вигляді масла коричневого кольору (вихід=84%). 1 Н ЯМР (300МГц, ДМСО-d6) δ: 8,44 (д, 1Н); 7,89 (м, 2Н); 7,77 (м, 2Н); 7,39 (д, 1Н); 6,80 (с, 1Н); 3,58 (с, 3Н); 3,06 (т, 2Н); 2,44 (т, 2Н); 1,96 (квінт., 2Н). Приклад 125 5-Хлор-1-[3(трифторметокси)фенілсульфоніл]-1Н-піроло[3,2b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 124, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=37%). Т.пл.=176°С. Приклад 126 Метиловий естер 1-(1,2,3-бензотіадіазол-5ілсульфоніл)-5-хлор-1Н-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Підготовчого прикладу VI, та як вихідні сполуки сполуку згідно з Підготовчим прикладом V і 1,2,3бензотіадіазол-5-сульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=9%). Т.пл.=219°С. Приклад 127 1-(1,2,3-Бензотіадіазол-5-ілсульфоніл)-5-хлор1Н-піроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 126, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=58%). Т.пл.=227°С. Приклад 128 Метиловий естер 5-хлор-1-[4(трифторметокси)фенілсульфоніл]-1Н-піроло[3,2b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 4(трифторметокси)бензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=52%). Т.пл.=109°С. Приклад 129 5-Хлор-1-[4(трифторметокси)фенілсульфоніл]-1Н-піроло[3,2b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 128, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=88%). Т.пл.=168°С. Приклад 130 92026 44 Метиловий естер 5-хлор-1-[(3хлорфеніл)сульфоніл]-1Н-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 3хлорбензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=14%). Т.пл.=107°С. Приклад 131 5-Хлор-1-[(3-хлорфеніл)сульфоніл]-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 130, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=83%). Т.пл.=174°С. Приклад 132 Метиловий естер 5-хлор-1-[(4хлорфеніл)сульфоніл]-1Н-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 4хлорбензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=35%). Т.пл.=108°С. Приклад 133 5-Хлор-1-[(4-хлорфеніл)сульфоніл]-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 132, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=81%). Т.пл.=174°С. Приклад 134 Метиловий естер 5-хлор-1-[(3метоксифеніл)сульфоніл]-1Н-піроло[3,2-b]піридин2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 3метоксибензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини жовтого кольору (вихід=45%). Т.пл.=90°С. Приклад 135 5-Хлор-1-[(3-метоксифеніл)сульфоніл]-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 134, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=94%). Т.пл.=139°С. Приклад 136 Метиловий естер 5-хлор-1-[(4метоксифеніл)сульфоніл]-1Н-піроло[3,2-b]піридин2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 4метоксибензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=66%). 45 Т.пл.=96°С. Приклад 137 5-Хлор-1-[(4-метоксифеніл)сульфоніл]-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 136, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=78%). Т.пл.=189°С. Приклад 138 Метиловий естер 5-хлор-1-[(4метилфеніл)сульфоніл]-1Н-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 4метилбензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини сірого кольору (вихід=37%). Т.пл.=106°С. Приклад 139 5-Хлор-1-[(4-метилфеніл)сульфоніл]-1Hпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 138, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=87%). Т.пл.=172°С. Приклад 140 Метиловий естер 5-хлор-1-[[4-(1метилетил)феніл]сульфоніл]-1H-піроло[3,2b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 4-(1метилетил)бензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=51%). Т.пл.=75°С. Приклад 141 5-Хлор-1-[[4-(1-метилетил)феніл]сульфоніл]1Н-піроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 140, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=88%). Т.пл.=155°С. Приклад 142 Метиловий естер 5-хлор-1-[[3-(2-метил-4піримідиніл)феніл]сульфоніл]-1H-піроло-[3,2b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 3-(2-метил4-піримідиніл)бензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини жовтого кольору (вихід=78%). Т.пл.=140-144°С. Приклад 143 5-Хлор-1-[[3-(2-метил-4піримідиніл)феніл]сульфоніл]-1Н-піроло-[3,2b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 142, очікувану спо 92026 46 луку отримують у вигляді твердої речовини білого кольору (вихід=38%). Т.пл.=178-188°С. Приклад 144 Метиловий естер 1-(1,2-бензізоксазол-5ілсульфоніл)-5-хлор-1H-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Підготовчого прикладу VI, та як вихідні сполуки сполуку згідно з Підготовчим прикладом V і 1,2бензізоксазол-5-сульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=7%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 8,42 (д, 1Н); 8,32 (д, 1Н); 7,98 (дд, 1Н); 7,36 (д, 1Н); 7,10 (д, 1Н); 6,75 (с, 1Н); 3,58 (с, 3Н); 3,05 (т, 2Н); 2,45 (т, 2Н); 1,95 (квінт., 2Н). Приклад 145 1-(1,2-Бензізоксазол-5-ілсульфоніл)-5-хлор1Н-піроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 144, очікувану сполуку отримують у вигляді твердої речовини жовтого кольору (вихід=33%). Т.пл.=226°С. Приклад 146 Метиловий естер 5-хлор-1-[2(трифторметокси)фенілсульфоніл]-1Н-піроло[3,2b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Підготовчого прикладу VI, та як вихідні сполуки сполуку згідно з Підготовчим прикладом V і 2(трифторметокси)бензолсульфонілхлорид, очікувану сполуку отримують у вигляді пастоподібної твердої речовини білого кольору. Приклад 147 5-Хлор-1-[2(трифторметокси)фенілсульфоніл]-1Н-піроло[3,2b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 146, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=50%). Т.пл.=138°С. Приклад 148 Метиловий естер 5-хлор-1-[(3,5дифторфеніл)сульфоніл]-1Н-піроло[3,2-b]піридин2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 3,5дифторбензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=83%). Т.пл.=90°С. Приклад 149 5-Хлор-1-[(3,4-дифторфеніл)сульфоніл]-1Hпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 148, очікувану сполуку отримують у вигляді твердої речовини сірого кольору (вихід=24%). 47 1 Н ЯМР (300МГц, ДМСО-d6) δ: 12,11 (с, 1Н); 8,44 (д, 1Н); 7,75 (м, 3Н); 7,38 (д, 1Н); 6,80 (с, 1Н); 3,08 (т, 2Н); 2,37 (м, 2Н); 1,94 (м, 2Н). Приклад 150 Метиловий естер 5-хлор-1-[(2,5дихлорфеніл)сульфоніл]-1H-піроло[3,2-b]піридин2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 2,5дихлорбензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=65%). Т.пл.=95-105°С. Приклад 151 5-Хлор-1-[(2,5дихлорфеніл)сульфоніл]-1Н-піроло[3,2-b]піридин2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 150, очікувану сполуку отримують у вигляді твердої речовини сірого кольору (вихід=43%). Т.пл.=86-89°С. Приклад 152 Метиловий естер 5-хлор-1-[(2хлорфеніл)сульфоніл]-1H-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 2хлорбензолсульфонілхлорид, отримують очікувану сполуку, яку зразу ж піддають реакції для одержання кислоти. Приклад 153 5-Хлор-1-[(2-хлорфеніл)сульфоніл]-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 152, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=48%). Т.пл.=139°С. Приклад 154 Метиловий Естер 5-хлор-1-[(2метилфеніл)сульфоніл]-1Н-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 2метилбензолсульфонілхлорид, отримують очікувану сполуку, яку зразу ж піддають реакції для одержання відповідної кислоти. Приклад 155 5-Хлор-1-[(2-метилфеніл)сульфоніл]-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 154, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=66%). Т.пл.=161°С. Приклад 156 Метиловий естер 5-хлор-1-[(3метилфеніл)сульфоніл]-1Н-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 3метилбензолсульфонілхлорид, отримують очіку 92026 48 вану сполуку, яку зразу ж піддають реакції для одержання відповідної кислоти. Приклад 157 5-Хлор-1-[(3-метилфеніл)сульфоніл]-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 156, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=38%). Т.пл.=165°С. Приклад 158 Метиловий естер 5-хлор-1-[(2,6дифторфеніл)сульфоніл]-1Н-піроло[3,2-b]піридин2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 2,6дифторбензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=76%). Т.пл.=107-109°С. Приклад 159 5-Хлор-1-[(2,6-дифторфеніл)сульфоніл]-1Hпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 158, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=38%). Т.пл.=192-195°С. Приклад 160 Метиловий естер 5-хлор-1-[(2,4,6трифторфеніл)сульфоніл]-1H-піроло[3,2-b]піридин2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 2,4,6трифторбензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=71%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 8,20 (д, 1Н); 7,56 (м, 2Н); 7,41 (д, 1Н); 6,84 (с, 1Н); 3,57 (с, 3Н); 2,94 (т, 2Н); 2,41 (т, 2Н); 1,94 (квінт., 2Н). Приклад 161 5-Хлор-1-[(2,4,6-трифторфеніл)сульфоніл]-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 160, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=27%). Т.пл.=135-150°С. Приклад 162 Метиловий естер 5-хлор-1-[(2,5диметилфеніл)сульфоніл]-1Н-піроло[3,2-b]піридин2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 2,5диметилбензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=87%). Т.пл.=92-103°С. Приклад 163 5-Хлор-1-[(2,5-диметилфеніл)сульфоніл]-1Нпіроло[3,2-b]піридин-2-бутанова кислота 49 Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 162, очікувану сполуку отримують у вигляді твердої речовини жовтого кольору (вихід=72%). Т.пл.=106-117°С. Приклад 164 Метиловий естер 5-хлор-1-[(3,5диметоксифеніл)сульфоніл]-1Н-піроло[3,2b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 3,5диметоксибензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=75%). Т.пл.=109-111°С. Приклад 165 5-Хлор-1-[(3,5-диметоксифеніл)сульфоніл]-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 164, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=27%). Т.пл.=136-138°С. Приклад 166 Метиловий естер 5-хлор-1-[4-(1метилетокси)фенілсульфоніл]-1Н-піроло[3,2b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 4-(1метилетокси)бензолсульфонілхлорид, очікувану сполуку отримують у вигляді безбарвного масла (вихід=88%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 8,41 (д, 1Н); 7,77 (д, 2Н); 7,38 (д, 1Н); 7,05 (д, 2Н); 6,73 (с, 1Н); 4,70 (септ., 1Н); 3,59 (с, 3Н); 3,04 (т, 2Н); 2,43 (т, 2Н); 1,95 (квінт., 2Н); 1,24 (д, 6Н). Приклад 167 5-Хлор-1-[4-(1-метилетокси)фенілсульфоніл]1H-піроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 166, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=97%). Т.пл.=171°С. Приклад 168 Метиловий естер 5-хлор-1-[(2метоксифеніл)сульфоніл]-1H-піроло[3,2-b]піридин2-бутанової кислоти Використовуючи методику, подібну до методики Підготовчого прикладу VI, та як вихідні сполуки сполуку згідно з Підготовчим прикладом V і 2метоксибензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=41%). Т.пл.=115°С. Приклад 169 5-Хлор-1-[(2-метоксифеніл)сульфоніл]-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 168, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=89%). 92026 50 Т.пл.=197°С. Приклад 170 Метиловий естер 5-хлор-1-[(2-хлор-3метилфеніл)сул ьфоніл]-1Н-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 2-хлор-3метилбензолсульфонілхлорид, очікувану сполуку отримують у вигляді масла зеленого кольору (вихід=57%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 8,18 (д, 1Н); 7,87 (д, 1Н); 7,79 (д, 1Н); 7,55 (т, 1Н); 7,34 (д, 1Н); 6,81 (с, 1Н); 3,55 (с, 3Н); 2,86 (т, 2Н); 2,35 (м, 5Н); 1,85 (квінт., 2Н). Приклад 171 5-Хлор-1-[(2-хлор-3-метилфеніл)сульфоніл]1Н-піроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 170, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=16%). Т.пл.=171-174°С. Приклад 172 Метиловий естер 5-хлор-1-[(2,4дифторфеніл)сульфоніл]-1Н-піроло[3,2-b]піридин2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 2,4дифторбензолсульфонілхлорид, очікувану сполуку отримують у вигляді масла жовтого кольору (вихід=82%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 8,26 (д, 1Н); 8,17 (м, 1Н); 7,59 (м, 1Н); 7,40 (м, 2Н); 6,81 (с, 1Н); 3,57 (с, 3Н); 2,94 (т, 2Н); 2,40 (т, 2Н); 1,89 (квінт., 2Н). Приклад 173 5-Хлор-1-[(2,4-дифторфеніл)сульфоніл]-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 172, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=8%). Т.пл.=172-177°С. Приклад 174 Метиловий естер 5-хлор-1-[(2-хлор-4метоксифеніл)сульфоніл]-1H-піроло[3,2-b]піридин2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 2-хлор-4метоксибензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=75%). Т.пл.=116-118°С. Приклад 175 5-Хлор-1-[(2-хлор-4-метоксифеніл)сульфоніл]1H-піроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 174, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=78%). Т.пл.=154-156°С. Приклад 176 51 Метиловий естер 5-хлор-1-[[4-(4тіазоліл)феніл]сульфоніл]-1Н-піроло[3,2-b]піридин2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 4-(4тіазоліл)бензолсульфонілхлорид, очікувану сполуку отримують у вигляді пасти білого кольору (вихід=78%). 1 Н ЯМР (300МГц, ДМСО-d6) δ: 9,23 (д, 1Н); 8,43 (м, 2Н); 8,18 (д, 2Н); 7,95 (д, 2Н); 7,40 (д, 1Н); 6,77 (с, 1Н); 3,58 (с, 3Н); 3,09 (т, 2Н); 2,45 (т, 2Н); 1,98 (квінт., 2Н). Приклад 177 5-Хлор-1-[[4-(4-тіазоліл)феніл]сульфоніл]-1Нпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 176, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=62%). Т.пл.=211-217°С. Приклад 178 Метиловий естер 5-хлор-1-[[4-(1,1диметилетил)феніл]сульфоніл]-1Н-піроло[3,2-b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 4-(1,1диметилетил)бензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=98%). Т.пл.=107°С. Приклад 179 5-Хлор-1-[[4-(1,1диметилетил)феніл]сульфоніл]-1Н-піроло[3,2b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 178, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=89%). Т.пл.=168°С. Приклад 180 Метиловий естер 5-хлор-1-[(2,3-дигідро-1,4бензодіоксин-6-іл)сульфоніл]-1Н'-піроло-[3,2b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Підготовчого прикладу VI, та як вихідні сполуки сполуку згідно з Підготовчим прикладом V і 2,3дигідро-1,4-бензодіоксин-6-сульфонілхлорид, очікувану сполуку отримують у вигляді масла коричневого кольору (вихід=23%). 1 Н ЯМР (300МГц, ДМСО-d6) δ: 8,41 (д, 1Н); 7,35 (м, 3Н); 7,03 (д, 1Н); 6,74 (с, 1Н); 4,28 (м, 4Н); 3,59 (с, 3Н); 3,05 (т, 2Н); 2,44 (т, 2Н); 1,94 (квінт., 2Н). Приклад 181 5-Хлор-1-[(2,3-дигідро-1,4-бензодіоксин-6іл)сульфоніл]-1Н-піроло-[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 180, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=95%). Т.пл.=166°С. 92026 52 Приклад 182 Метиловий естер 5-хлор-1-[(2піридил)сульфоніл]-1H-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 2піридинсульфонілхлорид, очікувану сполуку отримують у вигляді безбарвного масла (вихід=50%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 8,61 (д, 1Н); 8,24 (м, 3Н); 7,74 (м, 1Н); 7,34 (д, 1Н); 6,77 (с, 1Н); 3,58 (с, 3Н); 3,08 (т, 2Н); 2,41 (т, 2Н); 1,94 (квінт., 2Н). Приклад 183 5-Хлор-1-[(2-піридил)сульфоніл]-1H-піроло[3,2b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 182, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=30%). Т.пл.=187°С. Приклад 184 Метиловий естер 5-хлор-1-[[3-(1метилетил)феніл]сульфоніл]-1H-піроло[3,2b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 3-(1метилетил)бензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини коричневого кольору (вихід=73%). Т.пл.=92°С. Приклад 185 5-Хлор-1-[[3-(1-метилетил)феніл]сульфоніл]1Н-піроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 184, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=37%). Т.пл.=119°С. Приклад 186 Метиловий естер 5-хлор-1-[(4-метил-1нафталеніл)сульфоніл]-1Н-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 4-метил-1нафталінсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=85%). Т.пл.=118-120°С. Приклад 187 5-Хлор-1-[(4-метил-1-нафталеніл )сульфоніл]1H-піроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 186, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=13%). Т.пл.=199-204°С. Приклад 188 Метиловий естер 1-[(3,5диметилфеніл)сульфоніл]-5-(трифторметил)-1Hпіроло[3,2-b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 52, та як вихідні сполуки - сполуку 53 згідно з Підготовчим прикладом XXII і 3,5диметилбензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=51%). Т.пл.=156-160°С. Приклад 189 1-[(3,5-Диметилфеніл)сульфоніл]-5(трифторметил)-1Н-піроло[3,2-b]піридин-2бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 188, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=33%). Т.пл.=227-231°С. Приклад 190 Метиловий естер 5-хлор-1-[(2,4дихлорфеніл)сульфоніл]-1Н-піроло[3,2-о]піридин2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 2,4дихлорбензолсульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=22%). Т.пл.=100-101°С. Приклад 191 5-Хлор-1-[(2,4-дихлорфеніл)сульфоніл]-1Hпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 190, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=96%). Т.пл.=154-155°С. Приклад 192 Метиловий естер 5-хлор-1-[(2,3дихлорфеніл)сульфоніл]-1Н-піроло[3,2-b]піридин2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 2,3дихлорбензолсульфонілхлорид, очікувану сполуку отримують у вигляді масла рожевого кольору (вихід=40%). 1 Н ЯМР (250МГц, CDCI3) δ: 8,18 (д, 1Н); 7,83 (д, 1Н); 7,74 (д, 1Н); 7,41 (т, 1Н); 7,18 (д, 1Н); 6,61 (с, 1Н); 3,66 (с, 3Н); 2,90 (т, 2Н); 2,39 (т, 2Н); 2,03 (квінт., 2Н). Приклад 193 5-Хлор-1-[(2,3-дихлорфеніл)сульфоніл]-1Hпіроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 192, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=79%). Т.пл.=173-174°С. Приклад 194 Метиловий естер 5-хлор-1-[(3-хлор-2метилфеніл)сульфоніл]-1Н-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 3-хлор-2метилбензолсульфонілхлорид, очікувану сполуку отримують у вигляді безбарвної пасти (вихід=84%). 92026 54 1 Н ЯМР (250МГц, CDCI3) δ: 8,21 (д, 1Н); 7,61 (д, 1Н); 6,98 (м, 2Н); 6,95 (д, 1Н); 6,65 (с, 1Н); 3,66 (с, 3Н); 2,87 (т, 2Н); 2,55 (с, 3Н); 2,38 (т, 2Н); 2,02 (квінт., 2Н). Приклад 195 5-Хлор-1-[(3-хлор-2-метилфеніл)сульфоніл]1Н-піроло[3,2-b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 194, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=93%). Т.пл.=127-128°С. Приклад 196 Метиловий естер 5-хлор-1-[(4-метокси-2метилфеніл)сул ьфоніл]-1Н-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Прикладу 76, та як вихідну сполуку - 4-метокси2-метилбензолсульфонілхлорид, очікувану сполуку отримують у вигляді пасти білого кольору (вихід=38%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 8,23 (д, 1Н); 7,71 (д, 1Н); 7,35 (д, 1Н); 6,98 (м, 2Н); 6,78 (с, 1Н); 3,82 (с, 3Н); 3,55 (с, 3Н); 2,81 (т, 2Н); 2,33 (т, 2Н); 2,22 (с, 3Н); 1,83 (квінт., 2Н)). Приклад 197 5-Хлор-1-[(4-метокси-2метилфеніл)сульфоніл]-1Н-піроло[3,2-b]піридин-2бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 196, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=40%). Т.пл.=134-140°С. Приклад 198 Метиловий естер 1-[(1-нафталеніл)сульфоніл]5-(трифторметил)-1Н-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Прикладу 188, та як вихідну сполуку - 1нафталінсульфонілхлорид, очікувану сполуку отримують у вигляді безбарвного масла (вихід=49%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 8,57 (д, 1Н); 8,36 (м, 2Н); 8,15 (м, 1Н); 7,82 (м, 2Н); 7,69 (м, 3Н); 7,00 (с, 1Н); 3,52 (с, 3Н); 2,92 (т, 2Н); 2,35 (т, 2Н); 1,88 (квінт., 2Н). Приклад 199 1-[(1-Нафталеніл)сульфоніл]-5(трифторметил)-1Н-піроло[3,2-b]піридин-2бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 198, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=97%). Т.пл.=195°С. Приклад 200 Метиловий естер 1-(1,3-бензодіоксол-5ілсульфоніл)-5-(трифторметил)-1Н-піроло[3,2b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 188, та як вихідну сполуку - 1,3 55 бензодіоксол-5-сульфонілхлорид, очікувану сполуку отримують у вигляді безбарвного масла (вихід=45%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 8,82 (д, 1Н); 7,78 (д, 1Н); 7,54 (дд, 1Н); 7,42 (д, 1Н); 7,08 (д, 1Н); 6,91 (с, 1Н); 6,15 (с, 2Н); 3,59 (с, 3Н); 3,11 (т, 2Н); 2,47 (т, 2Н); 1,96 (квінт., 2Н). Приклад 201 1-(1,3-Бензодіоксол-5-ілсульфоніл)-5(трифторметил)-1H-піроло[3,2-b]піридин-2бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 200, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=44%). Т.пл.=161°С. Приклад 202 Метиловий естер 1-[(3,4-дигідро-4-метил-2H1,4-бензоксазин-7-іл)сульфоніл]-5(трифторметил)-1H-піроло[3,2-b]піридин-2бутанової кислоти Використовуючи методику, подібну до методики Прикладу 188, та як вихідну сполуку - 3,4дигідро-4-метил-2H-1,4-бензоксазин-7сульфонілхлорид, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=27%). Т.пл.=118°С. Приклад 203 1-[(3,4-Дигідро-4-метил-2H-1,4-бензоксазин-7іл)сульфоніл]-5-(трифторметил)-1Н-піроло[3,2b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 202, очікувану сполуку отримують у вигляді твердої речовини рожевого кольору (вихід=39%). Т.пл.=134°С. Приклад 204 Метиловий естер 1-[(2-метил-7бензотіазоліл)сульфоніл]-5-(трифторметил)-1Нпіроло[3,2-b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Прикладу 188, та як вихідну сполуку - 2-метил7-бензотіазолсульфонілхлорид, очікувану сполуку отримують у вигляді масла жовтого кольору (вихід=9%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 8,60 (д, 1Н); 8,30 (д, 1Н); 7,91 (д, 1Н); 7,83 (д, 1Н); 7,70 (т, 1Н); 6,98 (с, 1Н); 3,54 (с, 3Н); 2,99 (т, 2Н); 2,83 (с, 3Н); 2,38 (т, 2Н); 1,90 (квінт., 2Н). Приклад 205 1-[(2-Метил-7-бензотіазоліл)сульфоніл]-5(трифторметил)-1Н-піроло[3,2-b]піридин-2бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 204, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=48%). Т.пл.=187°С. Приклад 206 92026 56 Метиловий естер 5-(трифторметил)-1-[(2,3дигідро-1,4-бензодіоксин-6-іл)сульфоніл]-1Нпіроло[3,2-b]піридин-2-бутанової кислоти Використовуючи методику, подібну до методики Підготовчого прикладу VI, та як вихідні сполуки сполуку згідно з Підготовчим прикладом XXII і 2,3дигідро-1,4-бензодіоксин-6-сульфонілхлорид, очікувану сполуку отримують у вигляді безбарвного масла (вихід=13%). 1 Н ЯМР (300МГц, ДМСО-d6) δ: 8,63 (д, 1Н); 7,79 (д, 1Н); 7,39 (м, 2Н); 7,04 (д, 1Н); 6,92 (с, 1Н); 4,28 (м, 4Н); 3,60 (с, 3Н); 3,10 (т, 2Н); 2,47 (т, 2Н); 1,99 (квінт., 2Н). Приклад 207 5-(Трифторметил)-1-[(2,3-дигідро-1,4бензодіоксин-6-іл)сульфоніл]-1Н-піроло[3,2b]піридин-2-бутанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 206, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=88%). Т.пл.=158°С. Приклад 208 Метиловий естер 1-(6бензотіазолілсульфоніл)-5-хлор-1Н-піроло[3,2b]піридин-2-пентанової кислоти Використовуючи методику, подібну до методики Підготовчого прикладу VI, та як вихідні сполуки сполуку згідно з Підготовчим прикладом XXIII і бензотіазол-6-сульфонілхлорид, очікувану сполуку отримують у вигляді безбарвної пасти (вихід=36%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 9,68 (с, 1Н); 9,02 (д, 1Н); 8,46 (д, 1Н); 8,23 (д, 1Н); 7,92 (дд, 1Н); 7,39 (д, 1Н); 6,75 (с, 1Н); 3,58 (с, 3Н); 3,06 (т, 2Н); 2,34 (т, 2Н); 1,66 (м, 4Н). Приклад 209 1-(6-Бензотіазолілсульфоніл)-5-хлор-1Нпіроло[3,2-b]піридин-2-пентанова кислота Використовуючи методику, подібну до методики Прикладу 2, та як вихідну сполуку - естер, отриманий згідно з Прикладом 208, очікувану сполуку отримують у вигляді твердої речовини сірого кольору (вихід=43%). Т.пл.=169°С. Приклад 210 Метиловий естер 2-[[5-хлор-1-[(4етилфеніл)сульфоніл]-1H-піроло[3,2-b]пірид-2-іл]метокси]-2-метилпропанової кислоти Використовуючи методику, подібну до методики Прикладу 42, та як вихідну сполуку - сполуку згідно з Підготовчим прикладом XXIV, очікувану сполуку отримують у вигляді масла жовтого кольору (вихід=74%). 1 Н ЯМР (300МГц, ДМСО-d6) δ: 8,42 (д, 1Н); 7,92 (д, 2Н); 7,45 (д, 1Н); 7,42 (д, 2Н); 6,90 (с, 1Н); 4,87 (с, 2Н); 3,66 (с, 3Н): 2,65 (к, 2Н); 1,45 (с,6Н); 1,13 (т, 3Н). Приклад 211 2-[[5-Хлор-1-[(4-етилфеніл)сульфоніл]-1Нпіроло[3,2-b]пірид-2-іл]метокси]-2-метилпропанова кислота Використовуючи методику, подібну до методики Прикладу 43, та як вихідну сполуку - естер, 57 отриманий згідно з Прикладом 210, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=14%). Т.пл.=172°С. Приклад 212 Метиловий естер 2-[[5-хлор-1-[(4метоксифеніл)сульфоніл]-1Н-піроло[3,2-b]пірид-2іл]метокси]-2-метилпропанової кислоти Використовуючи методику, подібну до методики Прикладу 42, та як вихідну сполуку - сполуку згідно з Підготовчим прикладом XXV, очікувану сполуку отримують у вигляді пасти жовтого кольору (вихід=27%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 8,41 (д, 1Н); 7,96 (д, 2Н); 7,40 (д, 1Н); 7,10 (д, 2Н); 6,88 (с, 1Н); 4,87 (с, 2Н); 3,81 (с, 3Н); 3,67 (с, 3Н); 1,47 (с, 6Н). Приклад 213 2-[[5-Хлор-1-[(4-метоксифеніл)сульфоніл]-1Нпіроло[3,2-b]пірид-2-іл]метокси]-2-метилпропанова кислота Використовуючи методику, подібну до методики Прикладу 43, та як вихідну сполуку - естер, отриманий згідно з Прикладом 212, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=57%). Т.пл.=199°С. Приклад 214 Метиловий естер 2-[[5-хлор-1-[(2,3дихлорфеніл)сульфоніл]-1H-піроло[3,2-b]пірид-2іл]метокси]-2-метилпропанової кислоти Використовуючи методику, подібну до методики Прикладу 42, та як вихідну сполуку - сполуку згідно з Підготовчим прикладом XXVI, очікувану сполуку отримують у вигляді безбарвної пасти (вихід=41%). 1 Н ЯМР (300МГц, ДМСО-d6) δ: 8,20 (д, 1Н); 8,06 (дд, 1Н); 7,72 (дд, 1Н); 7,62 (т, 1Н); 7,41 (д, 1Н); 7,01 (с, 1Н); 4,75 (с, 2Н); 3,61 (с, 3Н); 1,24 (с, 6Н). Приклад 215 2-[[5-Хлор-1-[(2,3-дихлорфеніл)сульфоніл]-1Нпіроло[3,2-b]пірид-2-іл]метокси]-2-метилпропанова кислота Використовуючи методику, подібну до методики Прикладу 43, та як вихідну сполуку - естер, отриманий згідно з Прикладом 214, очікувану сполуку отримують у вигляді твердої речовини жовтого кольору (вихід=16%). Т.пл.=174°С. Приклад 216 Метиловий естер 2-[[5-хлор-1-[[4-(1метилетил)феніл]сульфоніл]-1Н-піроло[3,2b]пірид-2-іл]метокси]-2-метилпропанової кислоти Використовуючи методику, подібну до методики Прикладу 42, та як вихідну сполуку - сполуку згідно з Підготовчим прикладом XXVII, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=87%). Т.пл.=120°С. Приклад 217 2-[[5-Хлор-1-[[4-(1метилетил)феніл]сульфоніл]-1Н-піроло[3,2b]пірид-2-іл]метокси]-2-метилпропанова кислота Використовуючи методику, подібну до методики Прикладу 43, та як вихідну сполуку - естер, 92026 58 отриманий згідно з Прикладом 216, очікувану сполуку отримують у вигляді твердої речовини жовтого кольору (вихід=39%). Т.пл.=190°С. Приклад 218 Метиловий естер 2-[[5-Хлор-1-(1нафталенілсульфоніл)-1Н-піроло[3,2-b]пірид-2-іл]метокси]-2-метилпропанової кислоти Використовуючи методику, подібну до методики Прикладу 42, та як вихідну сполуку - сполуку згідно з Підготовчим прикладом XXVIII, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=54%). Т.пл.=108°С. Приклад 219 2-[[5-Хлор-1-(1-нафталенілсульфоніл)-1Hпіроло[3,2-b]пірид-2-іл]метокси]-2-метилпропанова кислота Використовуючи методику, подібну до методики Прикладу 43, та як вихідну сполуку - естер, отриманий згідно з Прикладом 218, очікувану сполуку отримують у вигляді твердої речовини голубуватого кольору (вихід=36%). Т.пл.=209°С. Приклад 220 Метиловий естер 2-[[5-хлор-1-(8хінолілсульфоніл)-1Н-піроло[3,2-b]пірид-2-іл]метокси]-2-метилпропанової кислоти Використовуючи методику, подібну до методики Прикладу 42, та як вихідну сполуку - сполуку згідно з Підготовчим прикладом XXIX, очікувану сполуку отримують у вигляді піни коричневого кольору (вихід=66%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 8,77 (дд, 1Н); 8,67 (дд, 1Н); 8,51 (дд, 1Н); 8,42 (дд, 1Н); 8,24 (д, 1Н); 7,65 (т, 1Н); 7,28 (м, 1Н); 7,20 (д, 1Н); 6,76 (с, 1Н); 5,11 (с, 2Н); 3,63 (с, 3Н); 1,39 (с, 6Н). Приклад 221 2-[[5-Хлор-1-(8-хінолілсульфоніл)-1Hпіроло[3,2-b]пірид-2-іл]метокси]-2-метилпропанова кислота Використовуючи методику, подібну до методики Прикладу 43, та як вихідну сполуку - естер, отриманий згідно з Прикладом 220, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=14%). Т.пл.=223°С. Приклад 222 Метиловий естер 2-[[5-хлор-1-[(2,5диметоксифеніл)сульфоніл]-1Н-піроло[3,2-b]пірид2-іл]метокси]-2-метилпропанової кислоти Використовуючи методику, подібну до методики Прикладу 42, та як вихідну сполуку - сполуку згідно з Підготовчим прикладом XXX, очікувану сполуку отримують у вигляді масла коричневого кольору (вихід=37%). 1 Н ЯМР (250МГц, ДМСО-d6) δ: 8,20 (д, 1Н); 7,52 (д, 1Н); 7,36 (д, 1Н); 7,32 (дд, 1Н); 7,14 (д, 1Н); 6,81 (с, 1Н); 4,77 (с, 2Н); 3,82 (с, 3Н); 3,64 (с, 3Н); 3,48 (с, 3Н); 1,37 (с, 6Н). Приклад 223 2-[[5-Хлор-1-[(2,5-диметоксифеніл)сульфоніл]1Н-піроло[3,2-b]пірид-2-іл]метокси]-2метилпропанова кислота 59 Використовуючи методику, подібну до методики Прикладу 43, та як вихідну сполуку - естер, отриманий згідно з Прикладом 222, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=23%). Т.пл.=200°С. Приклад 224 Метиловий естер 2-[[1-(1,3-бензодіоксол-5ілсульфоніл)-5-хлор-1Н-піроло[3,2-b]пірид-2іл]метокси]-2-метилпропанової кислоти Використовуючи методику, подібну до методики Прикладу 42, та як вихідну сполуку - сполуку згідно з Підготовчим прикладом XXXI, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=99%). Т.пл.=131°С. Приклад 225 2-[[1-(1,3-Бензодіоксол-5-ілсульфоніл)-5-хлор1H-піроло[3,2-b]пірид-2-іл]метокси]-2метилпропанова кислота Використовуючи методику, подібну до методики Прикладу 43, та як вихідну сполуку - естер, отриманий згідно з Прикладом 224, очікувану сполуку отримують у вигляді твердої речовини білого кольору (вихід=39%). Т.пл.=172°С. Приклад 226 Метиловий естер 2-[[5-хлор-1-[(2,3-дигідро-1,4бензодіоксин-6-іл)сульфоніл]-1H-піроло[3,2b]пірид-2-іл]метокси]-2-метилпропанової кислоти Використовуючи методику, подібну до методики Прикладу 42, та як вихідну сполуку - сполуку згідно з Підготовчим прикладом XXXII, очікувану сполуку отримують у вигляді масла коричневого кольору (вихід=91%). 1 Н ЯМР (500МГц, ДМСО-d6) δ: 8,41 (д, 1Н); 7,58 (м, 2Н); 7,41 (д, 1Н); 7,13 (д, 1Н); 6,87 (с, 1Н); 4,87 (с, 2Н); 4.30 (м, 4Н); 3,67 (с, 3Н); 1,47 (с, 6Н). Приклад 227 2-[[5-Хлор-1-[(2,3-дигідро-1,4-бензодіоксин-6іл)сульфоніл]-1Н-піроло[3,2-b]пірид-2-іл]метокси]2-метилпропанова кислота Використовуючи методику, подібну до методики Прикладу 43, та як вихідну сполуку - естер, отриманий згідно з Прикладом 226, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=59%). Т.пл.=213°С. Приклад 228 Метиловий естер 2-[[5-хлор-1-(2,3-дигідро-5бензофурансульфоніл)-1Н-піроло[3,2-b]пірид-2іл]метокси]-2-метилпропанової кислоти Використовуючи методику, подібну до методики Прикладу 42, та як вихідну сполуку - сполуку згідно з Підготовчим прикладом XXXIII, очікувану сполуку отримують у вигляді масла жовтого кольору (вихід=99%). 1 Н ЯМР (300МГц, ДМСО-d6) δ: 8,40 (д, 1Н); 7,91 (д, 1Н); 7,83 (дд, 1Н); 7,40 (д, 1Н); 6,93 (д, 1Н); 6,87 (с, 1Н); 4,89 (с, 2Н); 4,62 (т, 2Н); 3,67 (с, 3Н); 3,20 (т, 2Н); 1,47 (с, 6Н). Приклад 229 2-[[5-Хлор-1-(2,3-дигідро-5бензофурансульфоніл)-1H-піроло[3,2-b]пірид-2іл]метокси]-2-метилпропанова кислота 92026 60 Використовуючи методику, подібну до методики Прикладу 43, та як вихідну сполуку - естер, отриманий згідно з Прикладом 228, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=26%). Т.пл.=169°С. Приклад 230 Метиловий естер 2-[[5-хлор-1-[(3,5диметилфеніл)сульфоніл]-1H-піроло[3,2-b]пірид-2іл]метокси]-2-метилпропанової кислоти Використовуючи методику, подібну до методики Прикладу 42, та як вихідну сполуку - сполуку згідно з Підготовчим прикладом XXXIV, очікувану сполуку отримують у вигляді масла коричневого кольору (вихід=99%). 1 Н ЯМР (300МГц, ДМСО-d6) δ: 8,40 (д, 1Н); 7,64 (с, 2Н); 7,40 (д, 1Н); 7,38 (с, 1Н); 6,89 (с, 1Н); 4,90 (с, 2Н); 3,66 (с, 3Н); 2,31 (с, 6Н); 1,45 (с, 6Н). Приклад 231 2-[[5-Хлор-1-[(3,5-диметилфеніл)сульфоніл]1Н-піроло[3,2-b]пірид-2-іл]метокси]-2метилпропанова кислота Використовуючи методику, подібну до методики Прикладу 43, та як вихідну сполуку - естер, отриманий згідно з Прикладом 230, очікувану сполуку отримують у вигляді твердої речовини бежевого кольору (вихід=40%). Т.пл.=154°С. Приклад 232 Метиловий естер 2-[[5-хлор-1-[(3,4-дигідро-4метил-2H-1,4-бензоксазин-7-іл)-сульфоніл]-1Hпіроло[3,2-b]пірид-2-іл]метокси]-2метилпропанової кислоти Використовуючи методику, подібну до методики Прикладу 42, та як вихідну сполуку - сполуку згідно з Підготовчим прикладом XXXV, очікувану сполуку отримують у вигляді масла коричневого кольору (вихід=99%). 1 Н ЯМР (300МГц, ДМСО-d6) δ: 8,44 (д, 1Н); 7,39 (д, 1Н); 7,15 (дд, 1Н); 6,98 (д, 1Н); 6,82 (м, 2Н); 4,87 (с, 2Н); 4,25 (т, 2Н); 3,66 (с, 3Н); 3,26 (т, 2Н); 2,83 (с, 3Н); 1,45 (с, 6Н). Приклад 233 2-[[5-Хлор-1-[(3,4-дигідро-4-метил-2H-1,4бензоксазин-7-іл)сульфоніл]-1H-піроло[3,2-b]пірид2-іл]метокси]-2-метилпропанова кислота Використовуючи методику, подібну до методики Прикладу 43, та як вихідну сполуку - естер, отриманий згідно з Прикладом 232, очікувану сполуку отримують у вигляді твердої речовини рожевого кольору (вихід=37%). Т.пл.=229°С. Приклад 234 Етиловий естер (2S)-2-[[5-хлор-1(фeнілсульфоніл)-1Н-піроло[3,2-b]пірид-2іл]метокси]пропанової кислоти а) Етиловий естер (2S)-2-(2пропінілокси)пропанової кислоти: цю сполуку отримують з виходом 24%, шляхом взаємодії пропаргілброміду з етиловим естером (S)-(-)-молочної кислоти, заздалегідь обробленим гідридом натрію в ТГФ (безбарвна рідина; т.кип.=70-73°С при 13гПа). b) - Використовуючи методику, подібну до методики Прикладу 1, та як вихідну сполуку - естер,
ДивитисяДодаткова інформація
Назва патенту англійськоюPyrrolopyridine derivatives and use of same as ppar receptor modulators
Автори англійськоюBoubia, Benaissa, Barth Martine, Binet Jean, Dodey Pierre, Legendre Christiane, Poupardin-Olivier, Olivia
Назва патенту російськоюПроизводные пирролопиридина и их применение в качестве модуляторов ppar-рецепторов
Автори російськоюБарт Мартин, Бен Жан, Доде Пьер, Лежондр Кристиан, Пупарден-Оливье Оливия
МПК / Мітки
МПК: A61P 3/06, C07D 471/04, A61K 31/437
Мітки: модуляторів, піролопіридину, ppar-рецепторів, похідні, застосування
Код посилання
<a href="https://ua.patents.su/64-92026-pokhidni-pirolopiridinu-ta-kh-zastosuvannya-yak-modulyatoriv-ppar-receptoriv.html" target="_blank" rel="follow" title="База патентів України">Похідні піролопіридину та їх застосування як модуляторів ppar-рецепторів</a>
Попередній патент: Індольні сполуки
Наступний патент: Застосування ін’єкційного композиційного матеріалу як замінника кістки
Випадковий патент: Лікувально-профілактична мазь "алагор"