Сполука 2-(2,4,5-заміщеного аніліно)піримідину та її застосування для лікування раку
Номер патенту: 106710
Опубліковано: 25.09.2014
Автори: Муруґан Андіппан, Фінлі Мауріс Реймонд Вершоіл, Баттерворс Сем, Чуакуй Клаудіо Едмундо, Ворд Річард Ендрю, Редфеарн Хізер Мері, Кадамбар Васанта Крішна, Чінтакунтла Чандрасекхара Редді
Формула / Реферат
1. Сполука N-(2-{2-диметиламіноетилметиламіно}-4-метокси-5-{[4-(1-метиліндол-3-іл)піримідин-2-іл]аміно}феніл)проп-2-енаміду:
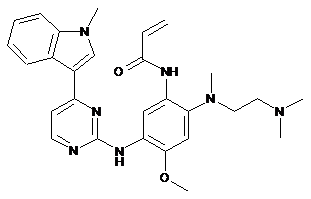 ,
,
або її фармацевтично прийнятна сіль.
2. Сполука N-(2-{2-диметиламіноетилметиламіно}-4-метокси-5-{[4-(1-метиліндол-3-іл)піримідин-2-іл]аміно}феніл)проп-2-енаміду за п. 1.
3. Фармацевтично прийнятна сіль за п. 1, якою є сіль мезилату N-(2-{2-диметиламіноетилметиламіно}-4-метокси-5-{[4-(1-метиліндол-3-іл)піримідин-2-іл]аміно}феніл)проп-2-енаміду.
4. Фармацевтична композиція, яка містить сполуку або фармацевтично прийнятну сіль за будь-яким з пп. 1-3 разом з фармацевтично прийнятним розріджувачем або носієм.
5. Сполука або її фармацевтично прийнятна сіль за будь-яким з пп. 1-3 для застосування як медикаменту.
6. Сполука або її фармацевтично прийнятна сіль за будь-яким з пп. 1-3 для застосування в лікуванні раку.
7. Сполука або її фармацевтично прийнятна сіль за будь-яким з пп. 1-3 для застосування в лікуванні недрібноклітинного раку легенів.
8. Застосування сполуки або її фармацевтично прийнятної солі за будь-яким з пп. 1-3 для виготовлення медикаменту для лікування раку.
9. Застосування за п. 8, де рак - недрібноклітинний рак легенів.
Текст
Реферат: Заявлений винахід стосується певних сполук 2-(2,4,5-заміщений аніліно)піримідину та її фармацевтично прийнятних солей, які можуть бути корисними в лікуванні або попередженні хвороби або медичного стану, опосередкованого через певні мутантні форми рецептора фактора росту епідермісу (наприклад, як-то активувальний мутант L858R, мутант делеції Ехоn19 та резистентнтний мутант Т790М). Такі сполуки та їх солі можуть бути корисними в лікуванні або попередженні кількості різних видів раку. Винахід також стосується фармацевтичних композицій, які містять названі сполуки та їх солі, зокрема придатні поліморфні форми цих сполук та солей, проміжних сполук, придатних для виготовлення названих сполук, та способів лікування хвороб, опосередкованих різними відмінними формами EGFR, застосовуючи названі сполуки та їх солі. UA 106710 C2 (12) UA 106710 C2 G O NH 3 1 R R N N N H 2 R UA 106710 C2 5 10 15 20 25 30 35 40 45 50 55 Заявлений винахід стосується певних сполук 2-(2,4,5-заміщеного-аніліно)піримідину та його фармацевтичних солей, які можуть бути корисними в лікуванні або попередженні хвороби, або медичного стану, опосередкованого через певні мутантні форми рецептору фактору росту епідерміс (наприклад, мутант, який активує L858R-, мутант, який активує делецію Exon19 та мутант резистентності T790M). Такі сполуки та їх солі можуть бути корисними в лікуванні або попередженні численних видів раку. Винахід також стосується фармацевтичних композицій, які містять названі сполуки та їх солі, зокрема, придатних поліморфних форм цих сполук та солей, проміжних сполук, придатних для виготовлення названих сполук, та способів лікування хвороб, опосередкованих різними відмінними формами EGFR, застосовуючи названі сполуки та їх солі. EGFR − член трансмембранного білку тирозинкінази сімейства рецептору erbB. Стосовно зв'язування ліганду фактору росту, як-то фактор росту епідермісу (EGF), рецептор може гомодимеризуватися із ще одною молекулою EGFR або гетеро- димеризуватися з ще одним членом сімейства, як-то erbB2 (HER2), erbB3 (HER3) або erbB4 (HER4). Гомо- та/або гетеро-димеризація рецепторів erbB має наслідком фосфорилування ключових залишків тирозину у внутрішньоклітинному домені та призводить до стимулювання численних шляхів внутрішньоклітинної сигнальної трансдукції, охопленої в проліферації клітини та виживанні. Дерегулювання сигналізації сімейства erbB стимулює проліферацію, інвазію, метастазування, ангіогенез та виживання клітини пухлини, та описано для багатьох захворювань раком людей, охоплюючи рак легенів, голови та шиї й грудної залози. Отже, сімейство erbB являє собою доцільну мету для розробки лікарських засобів проти раку, та ряд засобів, спрямованих щодо EGFR або erbB2 зараз є клінічно доступними, як-то такі: TM TM TM TM гефітиніб (IRESSA ), ерлотиніб (TARCEVA ) та лапатиніб (TYKERB , TYVERB ). Детальний огляд сигналізації рецептору erbB та їх залучення до створення пухлин передбачено в New England Journal of Medicine (2008) Vol. 358,1160-74 та Biochemical and Biophysical Research Communications (2004) Vol. 319, 1-11. В 2004 було повідомлено (Science [2004] Vol, 304, 1497–500 та New England Journal of Medicine [2004] Vol. 350, 2129-39), що активувальні мутації в EGFR пов'язано з відгуком на терапію гефітинібом у немалоклітинному раку легенів (NSCLC). Найбільш загальні активувальні мутації EGFR, L858R та delE746_A750 призводять до підвищення в спорідненості до інгібіторів малої молекули тирозинкінази, як-то гефітиніб та ерлотиніб, та зменшенні спорідненості до аденозин-трифосфату (ATP) стосовно дикого типу (WT) EGFR. Зрештою, набута резистентність до лікування гефітинібом або ерлотинібом виникає, наприклад, мутацією контролеру залишку T790M, яка, як повідомляють, виявлено в 50 % клінічно резистентних пацієнтів. Вважають, що ця мутація на заважає зв'язуванню гефітинібу або ерлотинібу стерично до EGFR, а тільки для зміни спорідненості до ATP до рівнів, порівнянних до WT EGFR. Зважаючи на важливість цієї мутації в резистентності щодо існуючих лікувань, спрямованих на EGFR, ми вважаємо, що засоби, які можуть інгібувати мутації контролеру притулку EGFR, зокрема, можуть бути придатними в лікуванні раку. Це зберігає потребу в сполуках, які можуть виявляти сприятливу активність проти WT EGFR стосовно активувальних мутантних форм EGFR (наприклад, мутанту L858R EGFR, або мутанту delE746_A750, або Exon19-делеції мутанту EGFR), та/або резистентних мутантних форм EGFR (наприклад, мутанту T790M EGFR), та/або селективність через інші рецептори ферменту, які можуть робити сполуки, зокрема, надаючи надію щодо створення нових матеріалів як терапевтичних засобів. Щодо цього, залишається потреба в сполуках, які виявляють вище інгібування певних активувальних або резистентних форм мутанту EGFR у той же час демонструючи низьке інгібування WT EGFR. Можна сподіватися, що такі сполуки більш придатні як терапевтичні засоби, конкретною для лікування раку, обумовленого зменшенням токсикології, асоційованої з інгібуванням WT EGFR. Відомо, що такі токсикології виявляють себе в людини як висипи на шкірі та/або діарея. Заявники несподівано знайшли, що ця одна або більша сполук 2-(2,4,5-заміщений-аніліно)піримідину мають високу ефективність проти кількох мутантних форм EGFR, у той час показуючи відносно низьке інгібування WT EGFR. Сполуки винаходу також можуть виявляти сприятливі фізичні властивості (наприклад, наступне: висока розчинність у воді, висока проникність, та/або слабке зв'язування білку плазми), та/або сприятливі профілі токсичності (наприклад, зменшення hERG блокування перешкод) та/або сприятливі метаболічні профілі в порівняні з іншими відомими EGFR / EGFRмутантними інгібіторами… Отже, такими сполуками можуть бути, зокрема, придатні для лікування хворобливих станів, у яких EGFR та/або активувальні мутації EGFR, та/або резистентнтні мутації EGFR залучено, наприклад, у лікуванні раку. У першому аспекті винаходу запропоновано сполуку формули (I): 1 UA 106710 C2 G O R 10 15 20 25 30 35 40 45 R N N 5 NH 1 N H R 3 2 (I) де: G вибрано з наступного: 4,5,6,7-тетрагідропіразоло[1,5-a]піридин-3-іл, 1H-індол-3-іл, 1-метил-1H-індол-3-іл та піразоло[1,5-a]піридин-3-іл; 1 R вибрано з наступного: гідроген, флуоро, хлоро, метил та ціано; 2 R вибрано з наступного: метоксил та метил; та 3 R вибрано з наступного: (3R)-3-(диметиламіно)піролідин-1-іл, (3S)-3-(диметиламіно)піролідин-1-іл, 3-(диметиламіно)азетидин-1-іл, [2-(диметиламіно)етил]-(метил)аміно, [2(метиламіно)етил](метил)аміно, 5-метил-2,5-діазаспіро[3,4]окт-2-іл, (3aR,6aR)-5-метилгексагідро-піроло[3,4-b]пірол-1(2H)-іл, 1-метил-1,2,3,6-тетрагідропіридин-4-іл, 4-металпіперазин-1-іл, 4-[2-(диметиламіно)-2-оксоетил]піперазин-1-іл, метил[2-(4-метилпіперазин-1-іл)етил]аміно, метил[2-(морфолін-4-іл)етил]аміно, 1-аміно-1,2,3,6-тетрагідропіридин-4-іл та 4-[(2S)-2амінопропаноіл]піперазин-1-іл; або їх фармацевтично прийнятна сіль. В одному втіленні запропоновано сполуку формули (I), як показано вище, де: G вибрано з наступного: 4,5,6,7-тетрагідропіразоло[1,5-a]піридин-3-іл, 1H-індол-3-іл, 1-метил-1H-індол-3-іл та піразоло[1,5-a]піридин-3-іл; 1 R вибрано з наступного: гідроген, флуоро, хлоро, метил та ціано; 2 R вибрано з наступного: метоксил та метил; та 3 R вибрано з наступного: (3R)-3-(диметиламіно)піролідин-1-іл, (3S)-3-(диметиламіно)піролідин-1-іл, 3-(диметиламіно)азетидин-1-іл, [2-(диметиламіно)етил]-(метил)аміно, 5метил-2,5-діазаспіро[3,4]окт-2-іл, (3aR,6aR)-5-метилгекса-гідро-піроло[3,4-b]пірол-1(2H)-іл, 1метил-1,2,3,6-тетрагідропіридин-4-іл, 4-металпіперазин-1-іл, 4-[2-(диметиламіно)-2оксоетил]піперазин-1-іл, метил[2-(4-метилпіперазин-1-іл)етил]аміно, метил[2-(морфолін-4іл)етил]аміно, 1-аміно-1,2,3,6-тетрагідропіридин-4-іл та 4-[(2S)-2-амінопропаноіл]піперазин-1-іл; або їх фармацевтично прийнятна сіль. В одному втіленні запропоновано сполуку формули (I), як показано вище, де: G вибрано з наступного: 1H-індол-3-іл, 1-метил-1H-індол-3-іл та піразоло[1,5-a]-піридин-3-іл; 1 R вибрано з наступного: гідроген, флуоро, хлоро, метил та ціано; 2 R вибрано з наступного: метоксил та метил; та 3 R вибрано з наступного: (3R)-3-(диметиламіно)піролідин-1-іл, (3S)-3-(диметиламіно)піролідин-1-іл, 3-(диметиламіно)азетидин-1-іл, [2-(диметиламіно)етил]-(метил)аміно, 5метил-2,5-діазаспіро[3,4]окт-2-іл, (3aR,6aR)-5-метилгекса-гідро-піроло[3,4-b]пірол-1(2H)-іл, 1метил-1,2,3,6-тетрагідропіридин-4-іл, 4-метилпіперазин-1-іл, 4-[2-(диметиламіно)-2оксоетил]піперазин-1-іл, метил[2-(4-метилпіперазин-1-іл)етил]аміно, метил[2-(морфолін-4іл)етил]аміно, 1-аміно-1,2,3,6-тетрагідропіридин-4-іл and4-[(2S)-2-амінопропаноіл]піперазин-1-іл; або їх фармацевтично прийнятна сіль. Придатною фармацевтично прийнятною сіллю сполуки формули (I), наприклад, є кислотноадитивна сіль. Наприклад, кислотно-адитивну сіль можна отримувати, застосовуючи неорганічну або органічну кислоту. Кислотно-адитивну сіль можна отримувати, застосовуючи неорганічну кислоту, вибрану з наступного: хлоридна кислота, бромідна кислота, сульфатна кислота та фосфатна кислота. Кислотно-адитивну сіль можна отримувати, застосовуючи органічну кислоту, вибрану з наступного: трифлуорооцтова кислота, лимонна кислота, малеінова кислота, щавлева кислота, оцтова кислота, мурашина кислота, бензойна кислота, фумарова кислота, бурштинова кислота, винно-кам'яна кислота, молочна кислота, піровиноградна кислота, метансульфокислота, бензолсульфонова кислота та птолуолсульфонова кислота. В одному втіленні тут запропоновано мезилатну сіль N-(2-{2-диметиламіно-етилметиламіно}-4-метокси-5-{[4-(1-метиліндол-3-іл)піримідин-2-іл]аміно}феніл)-проп-2-енаміду. 2 UA 106710 C2 5 10 15 20 25 30 35 40 45 50 55 60 Слід розуміти, що сполука формули (I), та її фармацевтично прийнятні солі, можуть існувати в сольватованих і несольватованих формах. Наприклад, сольватована форма може бути гідратною формою. Зрозуміло, що заявлений винахід охоплює всі такі сольватовані й несольватовані форми. Сполуку формули (I) можна застосовувати у форм проліків, які розкладаються в організмі людини або тварини, що дають сполуку формули (I). Приклади проліків охоплюють здатні до гідролізу in-vivo естери сполуки формули (I). Здатні до гідролізу In-vivo естери можна отримувати естерифікацією групи гідроксилу в сполуці формули (I). Різні форми проліків відомі в рівні техніки. Приклад таких похідних проліків, дивись: a) Design of Prodrugs, edited by H. Bundgaard, (Elsevier, 1985) та Methods in Enzymology, Vol. 42, p. 309-396, edited by K. Widder, et al. (Academic Press, 1985); b) A Textbook of Drug Design та Development, edited by Krogsgaard-Larsen та H. Bundgaard, Chapter 5 "Design та Application of Prodrugs", by H. Bundgaard p. 113-191 (1991); c) H. Bundgaard, Advanced Drug Delivery Reviews, 8, 1-38 (1992); d) H. Bundgaard, et al., Journal of Pharmaceutical Sciences, 77, 285 (1988); та N. Kakeya, et al., Chem Pharm Bull, 32, 692 (1984). Згідно з одним аспектом винаходу запропоновано сполуки формули (I), які інгібують одну або більше активувальних або резистентних мутацій EGFR, наприклад, активувальний мутант L858R, активувальний мутант EGFR делеції Exon19 та резистентний мутант T790M. Переважно такі сполуки можуть бути придатними для лікування розвитого раку в пацієнта, або може бути при ризику розвитку рівня резистентності до існуючого лікування, базованого на інгібіторі EGFR. Згідно з одним аспектом винаходу запропоновано сполуки формули (I), які демонструють більш високе інгібування активувальних або резистентних форм мутанту EGFR ніж WT EGFR. Вважають, що такі сполуки більш придатні як терапевтичні засоби, конкретно для лікування раку, обумовленого зменшенням токсикології, асоційованої з інгібуванням WT EGFR. Такі токсикології відомі при їх виявленні в людей як висипи на шкірі та/або діарея. В одному втіленні запропоновано сполуку формули (I), як показано вище, де: G − селективна форма наступного 1H-індол-3-ілу; 1 R вибрано з наступного: гідроген, хлоро, метил та ціано; 2 R − метоксил; та 3 R вибрано з наступного: (3R)-3-(диметиламіно)піролідин-1-іл, (3S)-3-(диметиламіно)піролідин-1-іл, 3-(диметиламіно)азетидин-1-іл, [2-(диметиламіно)-етил](метил)аміно, 5метил-2,5-діазаспіро[3,4]окт-2-іл, (3aR,6aR)-5-метилгексагідропіролo[3,4-b]пірол-1(2H)-іл, 1метил-1,2,3,6-тетрагідро-піридин-4-іл; 4-металпіперазин-1-іл, 4-[2-(диметиламіно)-2оксоетил]піперазин-1-іл, метил[2-(4-метилпіперазин-1-іл)етил]аміно, метил[2-(морфолін-4іл)етил]аміно, 1-аміно-1,2,3,6-тетрагідропіридин-4-іл та 4-[(2S)-2-аміно-пропаноіл]піперазин-1-іл; або їх фармацевтично прийнятна сіль. Згідно з наступним утіленням запропоновано сполуку формули (I), як показано вище, де: G − селективна форма 1H-індол-3-ілу; 1 R вибрано з наступного: гідроген, хлоро, метил та ціано; 2 R − метоксил; та 3 R вибрано з наступного: (3R)-3-(диметиламіно)піролідин-1-іл, 3-(диметиламіно)-азетидин-1іл, [2-(диметиламіно)етил](метил)аміно, 1-метил-1,2,3,6-тетрагідропіридин-4-іл та 4метилпіперазин-1-іл; або їх фармацевтично прийнятна сіль. Згідно з наступним утіленням запропоновано сполуку формули (I), як показано вище, де: G - 1-метил-1H-індол-3-іл; 1 R вибрано з наступного: гідроген, хлоро, метил та ціано; 2 R - метоксил; та 3 R вибрано з наступного: (3R)-3-(диметиламіно)піролідин-1-іл, (3S)-3-(диметиламіно)піролідин-1-іл, 3-(диметиламіно)азетидин-1-іл, [2-(диметиламіно)етил]-(метил)аміно, 5метил-2,5-діазаспіро[3,4]окт-2-іл, (3aR,6aR)-5-метил-гексагідро-піролo[3,4-b]пірол-1(2H)-іл, 1метил-1,2,3,6-тетрагідропіридин-4-іл, 4-металпіперазин-1-іл, 4-[2-(диметиламіно)-2оксоетил]піперазин-1-іл, метил[2-(4-метилпіперазин-1-іл)етил]аміно, метил[2-(морфолін-4іл)етил]аміно, 1-аміно-1,2,3,6-тетрагідро-піридин-4-іл та 4-[(2S)-2-амінопропаноіл]піперазин-1-іл; або їх фармацевтично прийнятна сіль. Згідно з наступним утіленням запропоновано сполуку формули (I), як показано вище, де: G − 1-метил-1H-індол-3-іл; 1 R вибрано з наступного: гідроген, хлоро, метил та ціано; 2 R − метоксил; та 3 UA 106710 C2 3 5 10 15 20 25 30 35 40 45 50 55 60 R вибрано з наступного: (3R)-3-(диметиламіно)піролідин-1-іл, 3-(диметиламіно)-азетидин-1іл, [2-(диметиламіно)етил](метил)аміно та 4-метилпіперазин-1-іл; або їх фармацевтично прийнятна сіль. У наступному втіленні запропоновано сполуку формули (I), як показано вище, де: G − піразоло[1,5-a]піридин-3-іл; 1 R вибрано з наступного: гідроген, хлоро, метил та ціано; 2 R − метоксил; та 3 R вибрано з наступного: (3R)-3-(диметиламіно)піролідин-1-іл, (3S)-3-(диметиламіно)піролідин-1-іл, 3-(диметиламіно)азетидин-1-іл, [2-(диметиламіно)етил]-(метил)аміно, 5метил-2,5-діазаспіро[3,4]окт-2-іл, (3aR,6aR)-5-метилгекса-гідропіролo[3,4-b]пірол-1(2H)-іл, 1метил-1,2,3,6-тетрагідропіридин-4-іл, 4-металпіперазин-1-іл, 4-[2-(диметиламіно)-2оксоетил]піперазин-1-іл, метил[2-(4-метилпіперазин-1-іл)етил]аміно, метил[2-(морфолін-4іл)етил]аміно, 1-аміно-1,2,3,6-тетрагідро-піридин-4-іл та 4-[(2S)-2-амінопропаноіл]піперазин-1-іл; або їх фармацевтично прийнятна сіль. У наступному втіленні запропоновано сполуку формули (I), як показано вище, де: G − піразоло[1,5-a]піридин-3-іл; 1 R вибрано з наступного: гідроген, хлоро, метил та ціано; 2 R − метоксил; та 3 R вибрано з наступного: (3R)-3-(диметиламіно)піролідин-1-іл, (3S)-3-(диметиламіно)піролідин-1-іл, 3-(диметиламіно)азетидин-1-іл, [2-(диметиламіно)-етил](метил)аміно, 5метил-2,5-діазаспіро[3,4]окт-2-іл, (3aR,6aR)-5-метил-гексагідропіролo[3,4-b]пірол-1(2H)-іл, 1метил-1,2,3,6-тетрагідропіридин-4-іл, 4-металпіперазин-1-іл, 4-[2-(диметиламіно)-2оксоетил]піперазин-1-іл, метил[2-(4-метилпіперазин-1-іл)етил]аміно, метил[2-(морфолін-4іл)етил]аміно, 1-аміно-1,2,3,6-тетрагідропіридин-4-іл та 4-[(2S)-2-амінопропаноіл]піперазин-1-іл; або їх фармацевтично прийнятна сіль. Згідно з наступним утіленням запропоновано сполуку формули (I), як показано вище, де: G − 4,5,6,7-тетрагідропіразоло[1,5-a]піридин-3-іл; 1 R вибрано з наступного: гідроген, хлоро, метил та ціано; 2 R − метоксил; та 3 R вибрано з наступного: [2-(диметиламіно)-етил](метил)аміно, (3aR,6aR)-5-метилгексагідропіролo[3,4-b]пірол-1(2H)-іл, (3R)-3-(диметиламіно)піролідин-1-іл, 1-метил-1,2,3,6тетрагідропіридин-4-іл, 3-(диметиламіно)азетидин-1-іл, 5-метил-2,5-діазаспіро[3,4]окт-2-іл; або їх фармацевтично прийнятна сіль. Згідно з наступним утіленням запропоновано сполуку формули (I), як показано вище, де: G − 4,5,6,7-тетрагідропіразоло[1,5-a]піридин-3-іл; 1 R − гідроген; 2 R − метоксил; та 3 R вибрано з наступного: [2-(диметиламіно)-етил](метил)аміно, (3aR,6aR)-5-метилгексагідропіролo[3,4-b]пірол-1(2H)-іл, (3R)-3-(диметиламіно)піролідин-1-іл, 1-метил-1,2,3,6тетрагідропіридин-4-іл, 3-(диметиламіно)азетидин-1-іл, 5-метил-2,5-діазаспіро[3,4]окт-2-іл; або їх фармацевтично прийнятна сіль. В одному втіленні запропоновано сполуку формули (I), як показано вище, де: G − 1H-індол-3-іл або 1-метил-1H-індол-3-іл; 1 R − гідроген; 2 R − метоксил; та 3 R − [2-(диметиламіно)етил]-(метил)аміно або [2-(метиламіно)етил](метил)аміно; або їх фармацевтично прийнятна сіль. Деякі величини змінних груп є наступними. Такі величини можна застосовувати в комбінації з будь-якими визначеннями, формулою винаходу, аспектами або втіленнями, визначеними тут для передбачення подальших втілень винаходу: G − 1H-індол-3-іл. G − 1-метил-1H-індол-3-іл. G − піразоло[1,5-a]піридин-3-іл. G − 4,5,6,7-тетрагідропіразоло[1,5-a]піридин-3-іл. 1 R − гідроген. 1 R − хлоро. 1 R − метил. 1 R − ціано. 2 R − метоксил. 3 R − (3R)-3-(диметиламіно)піролідин-1-іл. 4 UA 106710 C2 3 5 10 15 20 25 30 35 40 45 50 55 R − (3S)-3-(диметиламіно)піролідин-1-іл. 3 R − (диметиламіно)азетидин-1-іл. 3 R − [2-(диметиламіно)етил](метил)аміно. 3 R − [2-(метиламіно)етил](метил)аміно. 3 R − 5-метил-2,5-діазаспіро[3,4]окт-2-іл. 3 R − (3aR,6aR)-5-метилгексагідропіролo[3,4-b]пірол-1(2H)-іл. 3 R − 1-метил-1,2,3,6-тетрагідропіридин-4-іл. 3 R − 4-метилпіперазин-1-іл. 3 R − 4-[2-(диметиламіно)-2-оксоетил]піперазин-1-іл. 3 R − метил[2-(4-метилпіперазин-1-іл)етил]аміно. 3 R − метил[2-(морфолін-4-іл)етил]аміно. 3 R − 1-аміно-1,2,3,6-тетрагідропіридин-4-іл. 3 R − 4-[(2S)-2-амінопропаноіл]піперазин-1-іл. У наступному втіленні винаходу, стосовно будь-якого п. формули винаходу або втілення формули (I), описаних або отриманих тут, або їх фармацевтично прийнятної солі, тут запропоновано як формула винаходу або втілення, де один із прикладів сполук цього застосування не визнано. Для відхилення від сумнівів приклад сполук в експериментальному розділі нижче описано як Приклад 1, Приклад 2, т.д. Отже, наприклад, в одному втіленні запропоновано сполуку формули (I), як показано вище, де: G − селективна форма 4,5,6,7-тетрагідропіразоло[1,5-a]піридин-3-іл, 1H-індол-3-іл, 1-метил1H-індол-3-іл та піразоло[1,5-a]піридин-3-ілу; 1 R вибрано з наступного: гідроген, флуоро, хлоро, метил та ціано; 2 R вибрано з наступного: метоксил та метил; та 3 R вибрано з наступного: (3R)-3-(диметиламіно)піролідин-1-іл, (3S)-3-(диметиламіно)піролідин-1-іл, 3-(диметиламіно)азетидин-1-іл, [2-(диметиламіно)етил]-(метил)аміно, [2(метиламіно)етил](метил)аміно, 5-метил-2,5-діазаспіро[3,4]окт-2-іл, (3aR, 6aR)-5-метилгексагідро-піроло[3,4-b]пірол-1(2H)-іл, 1-метил-1,2,3,6-тетрагідропіридин-4-іл, 4-металпіперазин-1-іл, 4-[2-(диметиламіно)-2-оксоетил]піперазин-1-іл, метил[2-(4-метилпіперазин-1-іл)етил]аміно, метил[2-(морфолін-4-іл)етил]аміно, 1-аміно-1,2,3,6-тетрагідропіридин-4-іл та 4-[(2S)-2амінопропаноіл]піперазин-1-іл; або їх фармацевтично прийнятна сіль, де сполука формули (I) є іншою ніж N-(2-{2-диметиламіноетил-метиламіно}-4-метокси-5-{[4(1-метил-індол-3-іл)піримідин-2-іл]аміно}феніл)проп-2-енамід. Отже, в одному втіленні запропоновано сполуку формули (I), як показано вище, де: G − селективна форма 4,5,6,7-тетрагідропіразоло[1,5-a]піридин-3-іл, 1H-індол-3-іл, 1-метил1H-індол-3-іл та піразоло[1,5-a]піридин-3-ілу; 1 R вибрано з наступного: гідроген, флуоро, хлоро, метил та ціано; 2 R вибрано з наступного: метоксил та метил; та 3 R вибрано з наступного: (3R)-3-(диметиламіно)піролідин-1-іл, (3S)-3-(диметиламіно)піролідин-1-іл, 3-(диметиламіно)азетидин-1-іл, [2-(диметиламіно)етил]-(метил)аміно, 5метил-2,5-діазаспіро[3,4]окт-2-іл, (3aR,6aR)-5-метилгекса-гідро-піроло[3,4-b]пірол-1(2H)-іл, 1метил-1,2,3,6-тетрагідропіридин-4-іл, 4-металпіперазин-1-іл, 4-[2-(диметиламіно)-2оксоетил]піперазин-1-іл, метил[2-(4-метилпіперазин-1-іл)етил]аміно, метил[2-(морфолін-4іл)етил]аміно, 1-аміно-1,2,3,6-тетрагідропіридин-4-іл та 4-[(2S)-2-амінопропаноіл]піперазин-1-іл; або їх фармацевтично прийнятна сіль, де сполука формули (I) є іншою ніж N-(2-{2-диметиламіноетил-метиламіно}-4-метокси-5-{[4(1-метил-індол-3-іл)піримідин-2-іл]аміно}феніл)проп-2-енамід. Отже, у наступному втіленні запропоновано сполуку формули (I), як показано вище, де: G вибрано з наступного: 1H-індол-3-іл, 1-метил-1H-індол-3-іл та піразоло[1,5-a]-піридин-3-іл; 1 R вибрано з наступного: гідроген, флуоро, хлоро, метил та ціано; 2 R вибрано з наступного: метоксил та метил; та 3 R вибрано з наступного: (3R)-3-(диметиламіно)піролідин-1-іл, (3S)-3-(диметиламіно)піролідин-1-іл, 3-(диметиламіно)азетидин-1-іл, [2-(диметиламіно)етил]-(метил)аміно, 5метил-2,5-діазаспіро[3,4]окт-2-іл, (3aR,6aR)-5-метилгекса-гідро-піроло[3,4-b]пірол-1(2H)-іл, 1метил-1,2,3,6-тетрагідропіридин-4-іл, 4-металпіперазин-1-іл, 4-[2-(диметиламіно)-2оксоетил]піперазин-1-іл, метил[2-(4-метилпіперазин-1-іл)етил]аміно, метил[2-(морфолін-4іл)етил]аміно, 1-аміно-1,2,3,6-тетрагідропіридин-4-іл та 4-[(2S)-2-амінопропаноіл]піперазин-1-іл; або їх фармацевтично прийнятна сіль, 5 UA 106710 C2 5 10 15 20 25 30 35 40 45 50 55 60 де сполука формули (I) є іншою ніж N-(2-{2-диметиламіноетил-метиламіно}-4-метокси-5-{[4(1-метил-індол-3-іл)піримідин-2-іл]аміно}феніл)проп-2-енамід. У наступних утіленнях винаходу тут запропоновано будь-яку одну зі сполук прикладу, (яку названо нижче в експериментальному розділі у формі ї вільної основи). У наступних утіленнях винаходу тут запропоновано будь-яку одну зі сполук прикладу (яку названо нижче в експериментальному розділі у формі ї вільної основи), або їх фармацевтично прийнятну сіль. Отже, приклади з деяких згаданих вище втілень надано нижче: В одному втіленні тут запропоновано N-(5-{[5-хлоро-4-(1H-індол-3-іл)піримідин-2-іл]аміно}-2{(3R)-3-диметиламінопіролідин-1-іл}-4-метоксифеніл)проп-2-енамід. В одному втіленні тут запропоновано N-(5-{[5-хлоро-4-(1H-індол-3-іл)піримідин-2-іл]аміно}-2{2-диметил-аміноетил-метиламіно}-4-метоксифеніл)проп-2-енамід або його фармацевтично прийнятна сіль. В одному втіленні тут запропоновано N-(5-{[5-хлоро-4-(1-метиліндол-3-іл)піримідин-2іл]аміно}-2-{2-диметиламіноетил-метиламіно}-4-метоксифеніл)-проп-2-енамід. В одному втіленні тут запропоновано N-(5-{[5-ціано-4-(1H-індол-3-іл)піримідин-2-іл]аміно}-4метокси-2-{4-метилпіперазин-1-іл}феніл)проп-2-енамід або його фармацевтично прийнятна сіль. В одному втіленні тут запропоновано N-(5-{[5-ціано-4-(1H-індол-3-іл)піримідин-2-іл]аміно}-4метокси-2-{4-метилпіперазин-1-іл}феніл)проп-2-енамід. В одному втіленні тут запропоновано N-(2-{2-диметиламіноетил-метиламіно}-4-метокси-5{[4-(1-метиліндол-3-іл)піримідин-2-іл]аміно}феніл)проп-2-енамід або його фармацевтично прийнятна сіль. В одному втіленні тут запропоновано N-(2-{2-диметиламіноетил-метиламіно}-4-метокси-5{[4-(1-метиліндол-3-іл)піримідин-2-іл]аміно}феніл)проп-2-енамід. В одному втіленні тут запропоновано N-(5-{[5-ціано-4-(1-метиліндол-3-іл)піримідин-2іл]аміно}-2-{2-диметиламіноетил-метиламіно}-4-метоксифеніл)проп-2-енамід або його фармацевтично прийнятна сіль. В одному втіленні тут запропоновано N-(5-{[5-ціано-4-(1-метиліндол-3-іл)піримідин-2іл]аміно}-2-{2-диметиламіноетил-метиламіно}-4-метоксифеніл)проп-2-енамід. В одному втіленні тут запропоновано N-{5-[(5-ціано-4-піразоло[1,5-a]піридин-3-ілпіримідин-2іл)аміно]-2-[2-диметиламіноетил-метиламіно]-4-метоксифеніл}проп-2-енамід або його фармацевтично прийнятна сіль. В одному втіленні тут запропоновано N-{5-[(5-ціано-4-піразоло[1,5-a]піридин-3-ілпіримідин-2іл)аміно]-2-[2-диметиламіноетил-метиламіно]-4-метоксифеніл}проп-2-енамід. В одному втіленні тут запропоновано N-{5-[(5-ціано-4-піразоло[1,5-a]піридин-3-ілпіримідин-2іл)аміно]-2-[3-диметиламіноазетидин-1-іл]-4-метоксифеніл}проп-2-енамід або його фармацевтично прийнятна сіль. В одному втіленні тут запропоновано N-{5-[(5-ціано-4-піразоло[1,5-a]піридин-3-ілпіримідин-2іл)аміно]-2-[3-диметиламіноазетидин-1-іл]-4-метоксифеніл}проп-2-енамід. В одному втіленні тут запропоновано N-(2-{2-диметиламіноетил-метиламіно}-4-метокси-5{[4-(4,5,6,7-тетрагідропіразоло[1,5-a]піридин-3-іл)піримідин-2-іл]аміно}феніл)проп-2-енамід. В одному втіленні тут запропоновано N-(2-{2-диметиламіноетил-метиламіно}-4-метокси-5{[4-(4,5,6,7-тетрагідропіразоло[1,5-a]піридин-3-іл)піримідин-2-іл]аміно}феніл)проп-2-енамід або його фармацевтично прийнятна сіль. В одному втіленні тут запропоновано N-{2-[2-диметиламіноетил-метиламіно]-4-метокси-5[(4-піразоло[1,5-a]піридин-3-ілпіримідин-2-іл)аміно]феніл}проп-2-енамід. В одному втіленні тут запропоновано N-{2-[2-диметиламіноетил-метиламіно]-4-метокси-5[(4-піразоло[1,5-a]піридин-3-ілпіримідин-2-іл)аміно]феніл}проп-2-енамід або його фармацевтично прийнятна сіль. В одному втіленні тут запропоновано N-(2-[2-диметиламіноетил-метиламіно]-5-{[4-(1H-індол3-іл)піримідин-2-іл]аміно}-4-метоксифеніл)проп-2-енамід. В одному втіленні тут запропоновано N-(2-[2-диметиламіноетил-метиламіно]-5-{[4-(1H-індол3-іл)піримідин-2-іл]аміно}-4-метоксифеніл)проп-2-енамід або його фармацевтично прийнятна сіль. В одному втіленні тут запропоновано N-(4-метокси-5-{[4-(1-метиліндол-3-іл)піримідин-2іл]аміно}-2-[метил-(2-метиламіноетил)аміно]феніл)проп-2-енамід або його фармацевтично прийнятна сіль. В одному втіленні тут запропоновано N-(4-метокси-5-{[4-(1-метиліндол-3-іл)піримідин-2іл]аміно}-2-[метил-(2-метиламіноетил)аміно]феніл)проп-2-енамід. Сполуки формули (I) можна отримувати реакцією сполуки формули (II): 6 UA 106710 C2 G NH2 3 1 R N N 5 10 15 20 25 30 35 40 45 50 R N H 2 R (II) 1 2 3 або її солі, (де G, R , R та R розкрито тут) з похідним активованої акрилової кислоти (наприклад, з акрилоілхлоридом або відповідним активованим естером), у розчиннику, як-то CH2Cl2, тетрагідрофуран, N,N-диметилформамід або N,N-диметилацетамід. Отже, проміжна сполука сполуки формули (II) запропоновано згідно з подальшим аспектом заявленого винаходу. Отже, згідно з подальшим аспектом винаходу запропоновано сполуку формули (II), (як показано вище) де: G вибрано з наступного: 1H-індол-3-іл, 1-метил-1H-індол-3-іл та піразоло[1,5-a]-піридин-3-іл; 1 R вибрано з наступного: гідроген, хлоро, метил та ціано; 2 R − метоксил; та 3 R вибрано з наступного: (3R)-3-(диметиламіно)піролідин-1-іл, (3S)-3-(диметиламіно)піролідин-1-іл, 3-(диметиламіно)азетидин-1-іл, [2-(диметиламіно)етил]-(метил)аміно, 5метил-2,5-діазаспіро[3,4]окт-2-іл, (3aR,6aR)-5-метилгекса-гідропіролo[3,4-b]пірол-1(2H)-іл, 1метил-1,2,3,6-тетрагідропіридин-4-іл, 4-металпіперазин-1-іл, 4-[2-(диметиламіно)-2оксоетил]піперазин-1-іл, метил[2-(4-метилпіперазин-1-іл)етил]аміно, метил[2-(морфолін-4іл)етил]аміно, 1-аміно-1,2,3,6-тетрагідропіридин-4-іл та 4-[(2S)-2-(трет-бутоксикарбоніл)амінопропаноіл]піперазин-1-іл; або її солі. В одному втіленні запропоновано сполуку формули (II), (як показано вище) де: G вибрано з наступного: 4,5,6,7-тетрагідропіразоло[1,5-a]піридин-3-іл, 1H-індол-3-іл, 1метил-1H-індол-3-іл та піразоло[1,5-a]піридин-3-іл; 1 R вибрано з наступного: гідроген, хлоро, метил та ціано; 2 R − метоксил; та 3 R вибрано з наступного: (3R)-3-(диметиламіно)піролідин-1-іл, (3S)-3-(диметиламіно)піролідин-1-іл, 3-(диметиламіно)азетидин-1-іл, [2-(диметиламіно)етил]-(метил)аміно, 5метил-2,5-діазаспіро[3,4]окт-2-іл, (3aR,6aR)-5-метилгекса-гідропіролo[3,4-b]пірол-1(2H)-іл, 1метил-1,2,3,6-тетрагідропіридин-4-іл, 4-металпіперазин-1-іл, 4-[2-(диметиламіно)-2оксоетил]піперазин-1-іл, метил[2-(4-метилпіперазин-1-іл)етил]аміно, метил[2-(морфолін-4іл)етил]аміно, 1-аміно-1,2,3,6-тетрагідропіридин-4-іл та 4-[(2S)-2-(трет-бутоксикарбоніл)амінопропаноіл]піперазин-1-іл; або її солі. У наступному втіленні запропоновано сполуку формули (II), (як показано вище) де: G вибрано з наступного: 4,5,6,7-тетрагідропіразоло[1,5-a]піридин-3-іл, 1H-індол-3-іл, 1метил-1H-індол-3-іл та піразоло[1,5-a]піридин-3-іл; 1 R вибрано з наступного: гідроген, хлоро, метил та ціано; 2 R − метоксил; та 3 R вибрано з наступного: (3R)-3-(диметиламіно)піролідин-1-іл, (3S)-3-(диметиламіно)піролідин-1-іл, 3-(диметиламіно)азетидин-1-іл, [2-(диметиламіно)етил]-(метил)аміно, [2(метиламіно)етил](метил)аміно, 5-метил-2,5-діазаспіро[3,4]окт-2-іл, (3aR,6aR)-5-метилгексагідро-піроло[3,4-b]пірол-1(2H)-іл, 1-метил-1,2,3,6-тетрагідропіридин-4-іл, 4-металпіперазин-1-іл, 4-[2-(диметиламіно)-2-оксоетил]піперазин-1-іл, метил[2-(4-метилпіперазин-1-іл)етил]аміно, метил[2-(морфолін-4-іл)етил]аміно, 1-аміно-1,2,3,6-тетрагідропіридин-4-іл та 4-[(2S)-2амінопропаноіл]піперазин-1-іл; або її солі. У наступних утіленнях винаходу тут запропоновано будь-який один із проміжних сполук, (яку названо в експериментальному розділі у формі її вільної основи). У наступних утіленнях винаходу тут запропоновано будь-яку одну із проміжних сполук (яку названо нижче в експериментальному розділі у формі його вільної основи) або його фармацевтично прийнятної солі. 7 UA 106710 C2 5 1015 Отже, приклади деяких названих вище втілень надано нижче: В одному втіленні тут запропоновано проміжна сполука 100 або його солі. 1 1 4 Отже, у цьому випадку, тут запропоновано N -(2-диметиламіноетил)-5-метокси-N -метил-N [4-(1-метиліндол-3-іл)піримідин-2-іл]бензол-1,2,4-триамін або його солі. 1 1 4 В одному втіленні тут запропоновано N -(2-диметиламіноетил)-5-метокси-N -метил-N -[4-(1метиліндол-3-іл)піримідин-2-іл]бензол-1,2,4-триамін. В одному втіленні тут запропоновано проміжна сполука 168 або його солі. 1 4 Отже, у цьому випадку тут запропоновано N -(2-диметиламіноетил)-N -[4-(1H-індол-31 іл)піримідин-2-іл]-5-метокси-N -метилбензол-1,2,4-триамін або його солі. 1 4 В одному втіленні тут запропоновано N -(2-диметиламіноетил)-N -[4-(1H-індол-31 іл)піримідин-2-іл]-5-метокси-N -метилбензол-1,2,4-триамін. Сполуки аміну формули (II) можна отримувати відновленням відповідних нітро-сполук. Якщо G − індол-3-іл, тоді атом нітрогену групи індолу можна захищати придатною захисною групою нітрогену, наприклад, захисною групою фенілсульфонілу. Приклади захисних груп, охоплюючи захисні групи, придатні для захисту атомів нітрогену (а також засоби створення та зняття захисту), дивись T.W. Greene та P.G.M. Wuts, "Protective Groups in Organic Synthesis", Second Edition, John Wiley & Sons, New York, 1991. Такі подальші проміжні сполуки передбачено в подальшому аспекті винаходу. Отже, згідно з подальшим аспектом винаходу запропоновано сполуку формули (III): G NO2 3 1 R N N 20 25 30 35 40 45 50 R N H 2 R (III) де: G вибрано з наступного: 1H-індол-3-іл, 1-метил-1H-індол-3-іл та 1-(N-захисна група)-індол-3іл та піразоло[1,5-a]піридин-3-іл; 1 R вибрано з наступного: гідроген, хлоро, метил та ціано; 2 R − метоксил; та 3 R вибрано з наступного: (3R)-3-(диметиламіно)піролідин-1-іл, (3S)-3-(диметиламіно)піролідин-1-іл; 3-(диметиламіно)азетидин-1-іл, [2-(диметиламіно)етил]-(метил)аміно, 5-метил2,5-діазаспіро[3,4]окт-2-іл, (3aR,6aR)-5-метилгекса-гідропіролo[3,4-b]пірол-1(2H)-іл, 1-метил1,2,3,6-тетрагідропіридин-4-іл, 4-металпіперазин-1-іл, 4-[2-(диметиламіно)-2-оксоетил]піперазин1-іл, метил[2-(4-метилпіперазин-1-іл)етил]аміно, метил[2-(морфолін-4-іл)етил]аміно, 1-аміно1,2,3,6-тетрагідропіридин-4-іл та 4-[(2S)-2-(трет-бутоксикарбоніл)аміно-пропаноіл]піперазин-1-іл; або її солі. В одному втіленні цього аспекту винаходу запропоновано сполуку формули (III), яку показано вище, де: G вибрано з наступного: 4,5,6,7-тетрагідропіразоло[1,5-a]піридин-3-іл, 1H-індол-3-іл, 1метил-1H-індол-3-іл та 1-(N-захисна група)-індол-3-іл та піразоло[1,5-a]піридин-3-іл; 1 R вибрано з наступного: гідроген, хлоро, метил та ціано; 2 R − метоксил; та 3 R вибрано з наступного: (3R)-3-(диметиламіно)піролідин-1-іл, (3S)-3-(диметиламіно)піролідин-1-іл; 3-(диметиламіно)азетидин-1-іл, [2-(диметиламіно)етил]-(метил)аміно, 5-метил2,5-діазаспіро[3,4]окт-2-іл, (3aR,6aR)-5-метилгекса-гідропіролo[3,4-b]пірол-1(2H)-іл, 1-метил1,2,3,6-тетрагідропіридин-4-іл, 4-металпіперазин-1-іл, 4-[2-(диметиламіно)-2-оксоетил]піперазин1-іл, метил[2-(4-метилпіперазин-1-іл)етил]аміно, метил[2-(морфолін-4-іл)етил]аміно, 1-аміно1,2,3,6-тетрагідропіридин-4-іл та 4-[(2S)-2-(трет-бутоксикарбоніл)аміно-пропаноіл]піперазин-1-іл; або її солі. У наступному втіленні цього аспекту винаходу запропоновано сполуку формули (III), як показано вище, де: G вибрано з наступного: 4,5,6,7-тетрагідропіразоло[1,5-a]піридин-3-іл, 1H-індол-3-іл, 1метил-1H-індол-3-іл та 1-(N-захисна група)-індол-3-іл та піразоло[1,5-a]піридин-3-іл; 1 R вибрано з наступного: гідроген, хлоро, метил та ціано; 8 UA 106710 C2 2 5 10 15 20 25 30 R − метоксил; та 3 R вибрано з наступного: (3R)-3-(диметиламіно)піролідин-1-іл, (3S)-3-(диметиламіно)піролідин-1-іл, 3-(диметиламіно)азетидин-1-іл, [2-(диметиламіно)етил]-(метил)аміно, [2(метиламіно)етил](метил)аміно, 5-метил-2,5-діазаспіро[3,4]окт-2-іл, (3aR,6aR)-5-метилгексагідро-піроло[3,4-b]пірол-1(2H)-іл, 1-метил-1,2,3,6-тетрагідропіридин-4-іл, 4-металпіперазин-1-іл, 4-[2-(диметиламіно)-2-оксоетил]піперазин-1-іл, метил[2-(4-метилпіперазин-1-іл)етил]аміно, метил[2-(морфолін-4-іл)етил]аміно, 1-аміно-1,2,3,6-тетрагідропіридин-4-іл та 4-[(2S)-2амінопропаноіл]піперазин-1-іл; або її солі. Одним прикладом "N-захисної групи" в "1-(N-захисній групі)-індол-3-іл" є фенілсульфоніл. В одному втіленні тут запропоновано проміжна сполука 101 або його солі. Отже, у цьому випадку, тут запропоновано N'-(2-диметиламіноетил)-2-метокси-N'-метил-N[4-(1-метиліндол-3-іл)піримідин-2-іл]-5-нітробензол-1,4-діамін або його солі. В одному втіленні тут запропоновано N'-(2-диметиламіноетил)-2-метокси-N'-метил-N-[4-(1метиліндол-3-іл)піримідин-2-іл]-5-нітробензол-1,4-діамін. В одному втіленні тут запропоновано проміжна сполука 169 або його солі. Отже, у цьому випадку тут запропоновано N'-(2-диметиламіноетил)-N-[4-(1H-індол-3іл)піримідин-2-іл]-2-метокси-N'-метил-5-нітробензол-1,4-діамін або його солі. В одному втіленні тут запропоновано N'-(2-диметиламіноетил)-N-[4-(1H-індол-3-іл)піримідин2-іл]-2-метокси-N'-метил-5-нітробензол-1,4-діамін. В одному втіленні тут запропоновано проміжна сполука 175 або його солі. 4 4 1 Отже, у цьому випадку тут запропоновано N -(2-диметиламіноетил)-2-метокси-N -метил-N [4-(1-метиліндол-3-іл)піримідин-2-іл]-5-нітро-бензол-1,4-діамін або його солі. 4 4 1 В одному втіленні тут запропоновано N -(2-диметиламіноетил)-2-метокси-N -метил-N -[4-(1метиліндол-3-іл)піримідин-2-іл]-5-нітро-бензол-1,4-діамін. 3 Деякі сполуки формули (III) мають групу R , приєднану до фенільного кільця формули (III) 3 через атом нітрогену групи R : Ці сполуки можна отримувати реакцією придатного аміну із придатною флуоро-сполукою. Такі проміжні сполуки запропоновано згідно з подальшим аспектом винаходу. Отже, згідно з подальшим аспектом винаходу запропоновано сполуку формули (IV): G NO2 1 R N 35 40 45 F N N H 2 R (IV) де: G вибрано з наступного: 1H-індол-3-іл, 1-метил-1H-індол-3-іл та піразоло[1,5-a]піридин-3-іл; 1 R вибрано з наступного: гідроген, хлоро, метил та ціано; та 2 R − метоксил; або її солі. В одному втіленні цього аспекту винаходу запропоновано сполуку формули (IV), яку показано вище, де: G вибрано з наступного: 4,5,6,7-тетрагідропіразоло[1,5-a]піридин-3-іл, 1H-індол-3-іл, 1-метил-1H-індол-3-іл та піразоло[1,5-a]піридин-3-іл; 1 R вибрано з наступного: гідроген, хлоро, метил та ціано; та 2 R − метоксил; або її солі. В одному втіленні тут запропоновано проміжна сполука 68 або його солі. Отже, у цьому випадку тут запропоновано N-(4-флуоро-2-метокси-5-нітрофеніл)-4-(1H-індол3-іл)піримідин-2-амін або його солі. В одному втіленні тут запропоновано N-(4-флуоро-2-метокси-5-нітрофеніл)-4-(1H-індол-3іл)піримідин-2-амін. В одному втіленні тут запропоновано проміжна сполука 129 або його солі. 9 UA 106710 C2 5 10 15 Отже, у цьому випадку тут запропоновано N-(4-флуоро-2-метокси-5-нітрофеніл)-4-(1метиліндол-3-іл)піримідин-2-амін або його солі. В одному втіленні тут запропоновано N-(4-флуоро-2-метокси-5-нітрофеніл)-4-(1-метиліндол3-іл)піримідин-2-амін. В одному втіленні тут запропоновано проміжна сполука 176 або його солі. Отже, у цьому випадку тут запропоновано N-(4-флуоро-2-метокси-5-нітро-феніл)-4-(1метиліндол-3-іл)-піримідин-2-амін або його солі. В одному втіленні тут запропоновано N-(4-флуоро-2-метокси-5-нітро-феніл)-4-(1метиліндол-3-іл)-піримідин-2-амін. 3 Деякі сполуки формули (III) мають групу R , приєднану до фенільного кільця формули (III) 3 через атом карбону групи R . Ці сполуки можна отримувати реакцією придатної борорганічної сполуки (наприклад, сполуки боронат-естеру) із придатним арил-бромідом або арил-хлоридом сполуки. Наприклад, борорганічною сполукою може бути (4,4,5,5-тетраметил-1,3,23 діоксаборолан-2-іл)-R . Ці проміжні сполуки запропоновано згідно з подальшим аспектом заявленого винаходу. Отже, згідно з подальшим аспектом винаходу запропоновано сполуку формули (V): G NO2 1 R N 20 25 30 35 40 X N N H 2 R (V) де: X − бромо або хлоро; G вибрано з наступного: 4,5,6,7-тетрагідропіразоло[1,5-a]піридин-3-іл, 1H-індол-3-іл, 1-метил-1H-індол-3-іл та піразоло[1,5-a]піридин-3-іл; 1 R вибрано з наступного: гідроген, хлоро, метил та ціано; та 2 R − метоксил; або її солі. В одному втіленні для сполука формули (V), X − бромо. В одному втіленні для сполука формули (V), X − хлоро. В одному втіленні тут запропоновано проміжна сполука 145. Отже, у цьому випадку тут запропоновано N-(4-бромо-2-метокси-5-нітрофеніл)-4-(1метиліндол-3-іл)піримідин-2-амін або його солі. В одному втіленні тут запропоновано N-(4-бромо-2-метокси-5-нітрофеніл)-4-(1-метиліндол-3іл)піримідин-2-амін. Переважно сполуки заявленого винаходу можна отримувати реакцією сполуки формули (II) з 3-хлоропропаноіл хлоридом у присутності основи (наприклад, основи лужного металу карбонату, наприклад, калій карбонату, у придатному розчиннику, наприклад, ацетон. Утворена сполука проміжна сполуці формули (VI) можна виділити твердому вигляді (у формі вільної основи або як сіль), або її можна залишати в розчині та обробляти основою (наприклад, гідроксидом лужного металу, наприклад, NaOH), для перетворення сполуки формули (VI) до відповідної сполуки формули (I). Отже, сполуки формули (VI), та їх солі є придатними хімічними проміжними сполуками для створення сполук формули (I). Отже, згідно з подальшим аспектом винаходу запропоновано сполуку формули (VI): 10 UA 106710 C2 Cl G HN R 1 R N N O N H R 3 2 (VI) 1 2 3 або його солі, де G, R , R та R розкрито тут. В одному втіленні тут запропоновано сполуку формули (VI), як показано вище, або її солі, де: 5 10 15 20 25 30 35 40 45 G вибрано з наступного: 4,5,6,7-тетрагідропіразоло[1,5-a]піридин-3-іл, 1H-індол-3-іл, 1-метил-1H-індол-3-іл та піразоло[1,5-a]піридин-3-іл; 1 R вибрано з наступного: гідроген, флуоро, хлоро, метил та ціано; 2 R вибрано з наступного: метоксил та метил; та 3 R вибрано з наступного: (3R)-3-(диметиламіно)піролідин-1-іл, (3S)-3-(диметиламіно)піролідин-1-іл, 3-(диметиламіно)азетидин-1-іл, [2-(диметиламіно)етил]-(метил)аміно, [2(метиламіно)етил](метил)аміно, 5-метил-2,5-діазаспіро[3,4]окт-2-іл, (3aR,6aR)-5-метилгексагідро-піроло[3,4-b]пірол-1(2H)-іл, 1-метил-1,2,3,6-тетрагідропіридин-4-іл, 4-металпіперазин-1-іл, 4-[2-(диметиламіно)-2-оксоетил]піперазин-1-іл, метил[2-(4-метилпіперазин-1-іл)етил]аміно, метил[2-(морфолін-4-іл)етил]аміно, 1-аміно-1,2,3,6-тетрагідропіридин-4-іл та 4-[(2S)-2амінопропаноіл]піперазин-1-іл. Згідно з подальшим утіленням тут запропоновано сполуку формули (VI), яку показано вище, або її солі, де: G вибрано з наступного: 1H-індол-3-іл, 1-метил-1H-індол-3-іл та піразоло[1,5-a]-піридин-3-іл; 1 R вибрано з наступного: гідроген, флуоро, хлоро, метил та ціано; 2 R вибрано з наступного: метоксил та метил; та 3 R вибрано з наступного: (3R)-3-(диметиламіно)піролідин-1-іл, (3S)-3-(диметиламіно)піролідин-1-іл, 3-(диметиламіно)азетидин-1-іл, [2-(диметиламіно)етил]-(метил)аміно, 5метил-2,5-діазаспіро[3,4]окт-2-іл, (3aR,6aR)-5-метилгекса-гідро-піроло[3,4-b]пірол-1(2H)-іл, 1метил-1,2,3,6-тетрагідропіридин-4-іл, 4-металпіперазин-1-іл, 4-[2-(диметиламіно)-2оксоетил]піперазин-1-іл, метил[2-(4-метилпіперазин-1-іл)етил]аміно, метил[2-(морфолін-4іл)етил]аміно, 1-аміно-1,2,3,6-тетрагідропіридин-4-іл та 4-[(2S)-2-амінопропаноіл]піперазин-1-іл. У наступному втіленні тут запропоновано проміжна сполука 174 або його солі. Отже, у цьому випадку запропоновано 3-хлоро-N-[2-[2-диметиламіноетил-(метил)аміно]-4метокси-5-[[4-(1-метиліндол-3-іл)піримідин-2-іл]аміно]феніл]-пропанамід або його солі. В одному втіленні тут запропоновано 3-хлоро-N-[2-[2-диметиламіноетил-(метил)аміно]-4метокси-5-[[4-(1-метиліндол-3-іл)піримідин-2-іл]аміно]феніл]-пропанамід. Інші проміжні сполуки є корисними для отримання деяких сполук формули (I). Отже, наприклад, в одному втіленні тут запропоновано проміжна сполука 170 або його солі. У наступному втіленні тут запропоновано проміжна сполука 171 або його солі. У наступному втіленні тут запропоновано проміжна сполука 172 або його солі. В одному втіленні тут запропоновано проміжна сполука 144 або його солі. Згідно з подальшим аспектом винаходу тут запропоновано фармацевтичну композицію, яка містить сполуку формули (I) або їх фармацевтично прийнятну сіль, яку розкрито вище, в асоціації з фармацевтично прийнятним розріджувачем або носієм. Композиції винаходу можуть бути у формі, придатній для перорального застосування (наприклад, як таблетки, пілюлі, тверді або м'які капсули, водні або олійні суспензії, емульсії, дисперсні порошки або гранули, сиропи або еліксири), для місцевого застосування (наприклад, як креми, мазі, гелі, або водні або олійні розчини або суспензії), для застосування інгаляцією (наприклад, як тонко диспергований порошок або рідинний аерозоль), для застосування вдуванням (наприклад, як тонко диспергований порошок) або для парентерального застосування (наприклад, як стерильний водний або олійний розчин для внутрішньовенного, підшкірного, внутрішньом'язового, або внутрішньом'язового дозування, або як супозиторій для ректального дозування). 11 UA 106710 C2 5 10 15 20 25 30 35 40 45 50 55 Композиції винаходу можна отримувати стандартними процедурами, застосовуючи традиційні фармацевтичні наповнювачі, добре відомі в рівні техніки. Отже, призначені для перорального застосування композиції можуть містити, наприклад, один або більше барвників, підсолоджувачів, ароматизаторів та/або консервантів. Сполука формули (I) звичайно слід застосовувати до теплокровної тварини при одиничній 2 дозі в діапазоні 5-5000 мг/м площі тіла тварини, тобто, приблизно, 0,1-100 мг/кг, та це звичайно постачає терапевтично ефективну дозу. Формі одиничної дози, як-то таблетка або капсула, зазвичай слід містити, наприклад, 1-250 мг активного інгредієнту. Добову дозу обов'язково слід змінювати залежно від реципієнта, якого лікують, особливості шляху застосування та тяжкості хвороби, яку лікують. Відповідно, практикуючий лікар, який лікує конкретного пацієнта, може визначати оптимальне дозування. У розумінні наявної специфікації термін "лікування" також охоплює "профілактику" якщо конкретно не вказано протилежне. Терміни "терапевтичний" та "терапевтично" слід тлумачити відповідно. Як тут застосовано, термін "лікування" призначено означати звичайне значення щоденних учинків щодо хвороби щоб повністю або частково полегшувати один, деякі або всі із цих симптомів, або регулювати, або компенсувати головну патологію. Як тут застосовано, термін "профілактика" призначено для звичайного щоденного призначення та охоплювання первинної профілактики, яка попереджує розвиток хвороби та вторинної профілактики, коли хвороба вже розвинута та пацієнт тимчасово або перманентно захищений проти загострення або погіршення хвороби або розвитку нових симптомів, асоційованих із хворобою. Як результат її інгібіторної активності проти мутанту L858R EGFR, мутанту T790M мутант активувальної делеції EGFR та Exon19 вважають, що сполука формули (I) та її фармацевтично прийнятні солі є придатними для лікуванні хвороб або медичних станів, опосередкованих виключно або частково активністю мутанту EGFR, наприклад, раком. Типи раків, які можуть бути чутливими до лікування при застосування сполуки формули (I) або її фармацевтично прийнятних солей, охоплюють, але без обмеження, рак яєчнику, рак шейки матки, рак кишечнику, рак молочно залози, рак підшлункової залози, гліома, гліобластома, меланома, рак простати, лейкемія, лімфома, неходкінсова лімфома, рак шлунку, рак легенів, гепатоцеллюлярний рак, рак шлунку, шлунково-кишкова пухлина (GIST), рак щитоподібної залози, рак жовчної протоки, ендометріальний рак, рак нирок, анапластична великоклітинна лімфома, гостра мієлоїдна лейкемія (AML), множинна мієлома, меланома та мезотеліома. Як передбачено для способів лікування згаданого тут раку, сполуку формули (I) слід застосовувати до ссавця, конкретніше − до людини. Так само для застосувань сполуки формули (I) для лікування згаданого тут раку, передбачено, що сполуку формули (I) слід застосовувати до ссавця, конкретніше − людини. Отже, згідно із ще одним аспектом винаходу, запропоновано сполуку формули (I), яку визначено вище, або їх фармацевтично прийнятну сіль для застосування як медикаменту. Згідно з подальшим аспектом винаходу тут запропоновано сполуку формули (I), яку визначено вище, або їх фармацевтично прийнятну сіль для застосування в лікуванні хвороби, опосередкованої через мутант L858R EGFR та/або T790M EGFR, та/або мутант активувальної делеції Exon19. В одному втіленні винаходу названа хвороба, опосередкована через мутант L858R EGFR та/або T790M EGFR мутант та/або Exon19 мутант активувальної делеції − рак. Згідно з подальшим аспектом винаходу тут запропоновано застосування сполуки формули (I), яку визначено вище, або її фармацевтично прийнятної солі для виготовлення медикаменту для лікування хвороби, опосередкованої через мутант L858R EGFR та/або мутант T790M EGFR, та/або мутант активувальної делеції Exon19. В одному втіленні винаходу, названою хворобою, опосередкованою через мутант L858R EGFR та/або мутант T790M EGFR, та/або мутант активувальної делеції Exon19 є рак. Згідно з подальшим аспектом винаходу тут запропоновано застосування сполуки формули (I), яку визначено вище, або її фармацевтично прийнятої солі для виготовлення медикаменту для лікування раку. Згідно з подальшим аспектом винаходу тут запропоновано спосіб застосування сполуки формули (I), яку визначено вище, або її фармацевтично прийнятної солі для лікування раку. Згідно із цим аспектом винаходу тут запропоновано спосіб, який полягає в дії проти раку в теплокровної тварини, як-то людина, яка потребує такого лікування, який полягає в застосуванні до названої тварини ефективної кількості сполуки формули (I) або її фармацевтично прийнятної солі, яку тут визначено. 12 UA 106710 C2 5 10 15 20 25 30 35 40 45 50 55 Згідно з подальшим аспектом винаходу тут запропоновано спосіб лікування людини, яка потерпає від хвороби, при якій інгібування мутанту L858R EGFR та/або мутанту T790M EGFR та/або мутанту активувальної делеції Exon19 є корисним, який полягає в застосуванні до персони, яка цього потребує, терапевтично ефективної кількості сполуки формули (I), яку визначено вище, або їх фармацевтично прийнятної солі. В одному втіленні винаходу хворобою, у якій є корисним інгібування мутанту L858R EGFR та/або мутанту T790M EGFR, та/або мутанту активувальної делеції Exon19, є рак. У будь-яких із приведених тут аспектів або утілень, де рак згадано в загальному сенсі, названий рак можна вибирати з наступного: рак яєчнику, рак шийки матки, рак кишечнику, рак молочної залози, рак підшлункової залози, гліома, гліобластома, меланома, рак простати, лейкемія, лімфома, неходкінсова лімфома, рак шлунку, рак легенів, гепатоцеллюлярний рак, рак шлунку, шлунково-кишкова пухлина (GIST), рак щитоподібної залози, рак жовчної протоки, ендометріальний рак, рак нирок, анапластична великоклітинна лімфома, гостра мієлоїдна лейкемія (AML), множинна мієлома, меланома та мезотеліома. У будь-якому аспекті або утіленні винаходу, де рак згадано в загальному сенсі можна застосовувати наступні утілення: В одному втіленні рак − рак яєчнику. В одному втіленні рак − рак шийки матки. В одному втіленні рак − рак кишечнику. В одному втіленні рак − рак молочно залози. В одному втіленні рак − рак підшлункової залози. В одному втіленні рак є гліома. В одному втіленні рак є гліобластома. В одному втіленні рак є меланома. В одному втіленні рак − рак простати. В одному втіленні рак є лейкемія. В одному втіленні рак є лімфома. В одному втіленні рак є неходкінсова лімфома. В одному втіленні рак − рак шлунку. В одному втіленні рак − рак легенів. В одному втіленні рак є немалими клітинами раку легенів. В одному втіленні рак є гепатоцеллюлярний рак. В одному втіленні рак − рак шлунку. В одному втіленні рак є шлунково-кишкова пухлина (GIST). В одному втіленні рак − рак щитоподібної залози. В одному втіленні рак − рак жовчної протоки. В одному втіленні рак є ендометріальний рак. В одному втіленні рак − рак нирок. В одному втіленні рак є анапластична великоклітинна лімфома. В одному втіленні рак є гостра мієлоїдна лейкемія (AML). В одному втіленні рак є множинна мієлома. В одному втіленні рак є меланома. В одному втіленні рак є мезотеліома. Описане вище протиракове лікування моне застосовувати як єдине лікування або може охоплювати додатково до сполуки винаходу, звичайну хірургію або радіотерапію або хіміотерапію, або імунотерапію. Таку хіміотерапію можна застосовувати спільно, одночасно, послідовно або роздільно до лікування сполукою винаходу та може охоплювати одну або більше з наступних протипухлинних засобів: (i) антипроліферативні/протипухлинні ліки та їх комбінації, які застосовано в медичній онкології, як-то алкілувальні засоби (наприклад, цис-платин, оксаліплатин, карбоплатин, циклофосфамід, нітроген-мустард, мелфалан, хлорамбуцил, бусульфан, темозоламід та нітросоуреаз); антиметаболіти (наприклад, гемоцитабін та антифолати, як-то флуоропіримідино-подібні 5-флуороурацил та тегафур, ралтитресед, метотрексат, цитозин арабінозид, та гідроксисечовина); протипухлинні антибіотики (наприклад, антрацикліно-подібні адріаміцин, блеоміцин, доксорубіцин, дауноміцин, епірубіцин, ідарубіцин, мітоміцин-C, дактиноміцин та мітраміцин); антимітотичні засоби (наприклад, вінка-алкалоідо-подібні вінкристин, вінбластин, віндесин та вінорелбін, та таксо ідо-подібні таксол та таксотер, та інгібітори полокінази); та інгібітори топоізомерази (наприклад, епіподофілотоксино-подібні етопосид та теніпосид, амсакрин, топотекан та камптотецин); 13 UA 106710 C2 5 10 15 20 25 30 35 40 45 50 55 60 (ii) цитостатичні засоби, як-то антіоестрогени (наприклад, тамоксифен, фулвестрант, тореміфен, ралоксифен, дролоксифен та іодоксифен), антиандрогени (наприклад, бікалутамід, флутамід, нілутамід та ципротерон ацетат), антагоністи LHRH або агоністи LHRH (наприклад, госерелін, лейпрорелін та буцерелін), прогестогени (наприклад, мегестрол ацетат), інгібітори ароматази (наприклад, як анастрозол, летрозол, воразол та ексеместан) та інгібітори 5αредуктази, як-то фінастерид; (iii) антиінвазивні засоби [,наприклад, подібні до сімейства інгібіторів c-Src-кинази 4-(6хлоро-2,3-метилендіоксианіліно)-7-[2-(4-метилпіперазин-1-іл)етокси]-5-тетрагідропіран-4ілоксихіназолін [AZD0530 (саракатиніб); WO01/94341], N-(2-хлоро-6-метилфеніл)-2-{6-[4-(2гідроксиетил)піперазин-1-іл]-2-метилпіримідин-4-іламіно}тіазол-5-карбоксамід (дасатиніб, BMS354825; J. Med. Chem., 2004, 47, 6658-6661) та босутиніб (SKI-606), та подібні інгібіторам металопротеінази маримастат, інгібітори функції рецептору активатору плазминогену урокінази або антитіла до гепаранази]; (iv) інгібітори функції фактору: росту, наприклад, такі інгібітори охоплюють антитіла фактору росту та антитіла рецептору фактору росту (наприклад, анти-erbB2-антитіло трастузумаб [Herceptin™], анти-EGFR-антитіло панітумумаб, анти-erbB1-антитіло цетуксимаб [Erbitux, C225] та будь-який фактор росту або антитіла рецептору фактору росту, розкриті в Stern et al. Critical reviews. Critical reviews in oncology/haematology Vol. 54, pp11-29); такі інгібітори також охоплюють інгібітори тирозинкінази, наприклад, інгібітори фактору росту сімейства епідерміса (наприклад, інгібітори EGFR-сімейства тирозинкінази, як-то N-(3-хлоро-4-флуорофеніл)-7-метокси-6-(3морфолінoпропокси)-хіназолін-4-амін (гефітиніб, ZD1839), N-(3-етинілфеніл)-6,7-біс(2метоксиетокси)хіназолін-4-амін (ерлотиніб, OSI-774) та 6-акриламідо-N-(3-хлоро-4флуорофеніл)-7-(3-морфолінoпропокси)-хіназолін-4-амін (CI 1033), інгібітори erbB2тирозинкінази, як-то лапатиніб); інгібітори сімейства фактору росту гепатоциту; інгібітори сімейства фактору росту інсуліну; інгібітори сімейства тромбоцитарного фактору росту, як-то іматиніб та/або нілотиніб (AMN107); інгібітори серин/треонін-кінази (наприклад, інгібітори сигнального Ras/Raf, як-то інгібітори фармезил-трансферази, наприклад, сорафеніб (BAY 439006), типіфаміб (R115777) та лонафаміб (SCH66336)), інгібітори сигналізації клітини через MEK- та/або AKT-кіназу, інгібітори c-kit, інгібітори абл-кинази, інгібітори PI3-кинази, інгібітори Plt3-кинази, інгібітори CSF-1R-кинази, інгібітори IGF-рецептору (подібний фактору росту інсуліну) кинази; інгібітори аврора-кинази (наприклад, AZD1152, PH739358, VX-680, MLN8054, R763, MP235, MP529, VX-528 ТА AX39459) та інгібітори циклін-залежної кинази, як-то інгібітори CDK2 та/або CDK4; (v) анти-ангіогенні засоби, як-то які інгібують дії васкулярного ендотеліального фактору росту, [наприклад, антитіло анти-васкулярного ендотеліального фактору росту клітини бевацизумаб (Avastin™) та, наприклад, інгібітор VEGF-рецептору тирозинкінази, як-то вандетаніб (ZD6474), ваталаніб (PTK787), сунітиніб (SU11248), акситиніб (AG-013736), пазопаніб (GW 786034) та 4-(4-флуоро-2-метиліндол-5-ілокси)-6-метокси-7-(3-піролідин-1ілпропокси)хіназолін (AZD2171; Приклад 240 у WO 00/47212), сполуки, як-то розкриті в WO97/22596, WO97/30035, WO97/32856 та WO98/13354, та сполуки, які працюють за іншими механізмами (наприклад, ліномід, інгібітори αvβ3-функції інтегрину та ангіостатин)]; (vi) засоби, які ушкоджують судини, як-то Комбретастатин A4 та сполуки, розкриті в WO99/02166, WO00/40529, WO00/41669, WO01/92224, WO02/04434 та WO02/08213; (vii) антагоніст рецептору ендотеліну, наприклад, зиботентан (ZD4054) або атрасентан; (viii) антисенсорні лікування, наприклад, які спрямовано щодо цілей згаданих раніше, як-то ISIS 2503, антиi-рас-антисенс; (ix) способи генного лікування, які охоплюють, наприклад, способи для заміщення аберантних генів, як-то аберантний p53 або аберантний BRCA1 або BRCA2, GDEPT (ген-спрямована ферментна проліскова терапія), способи, як-то застосування наступного: цитозиндезаміназа, тимідинкіназа або фермент бактеріальної нітроредуктази, та способи підвищення толерантності пацієнта до хіміотерапії або радіотерапії, як-то багатолікова терапія резистентності гену; та (x) способи імунотерапії, які охоплюють, наприклад, способи ex-vivo та in-vivo підвищення імуногенності пухлинних клітин пацієнта, як-то трансфекція цитокінами, як-то інтерлейкін 2, інтерлейкін 4 або фактор стимулювання колонії гранулоциту-макрофагу, способи зменшення анергії T-клітини, способи застосування трансфектованих імунних клітин, як-то цитокін-трансфектовані дендритні клітини, способи застосування ліній цитокін-трансфектованих пухлинних клітин, способи застосування антиідіотипових антитіл, способи зменшення функції імунних супресивних клітин, як-то регуляторних T клітин, похідні від мієлоїду супресорні клітини або IDO (індоламін 2,3,-деоксигеназа)-експресувальні дендритні клітини, та способи 14 UA 106710 C2 5 10 15 20 25 30 35 40 45 50 55 застосування вакцин, які містять білки або пептиди, які походять із антигенів, пов'язаних з пухлинами, як-то NY-ESO-1, MAGE-3, WT1 або Her2/neu. Отже, згідно з подальшим аспектом винаходу тут запропоновано фармацевтичний продукт, який містить сполуку формули (I), яку визначено вище, та додаткову протипухлинну субстанцію, яку визначено вище, для спільного лікування раку. Згідно з таким аспектом винаходу тут запропоновано фармацевтичний продукт, який містить сполуку формули (I), або їх фармацевтично прийнятну сіль, яку визначено тут, та додаткову протипухлинну речовину, яку визначено вище, для спільного лікування раку. Тут, де термін "спільне лікування" застосовано стосовно комбінованого лікування, зрозуміло, що, це може стосуватися одночасного, роздільного або послідовного застосування. Посилання на "сумісне застосування" слід означати теж саме. В одному аспекті винаходу "спільне лікування" стосується одночасного застосування. У ще одному аспекті винаходу "спільне лікування" стосується роздільного застосування. Згідно з подальшим аспектом винаходу "спільне лікування" стосується послідовного застосування. Де застосування є послідовним або роздільним, затримка в застосуванні другого компоненту не слід бути втратою вигоди від появи дії від застосування комбінації. Отже, в одному втіленні послідовне лікування охоплює застосування комбінації кожного компоненту за період 11 діб. У ще одному втіленні цей період дорівнює 10 діб. У ще одному втіленні цей період дорівнює 9 діб. У ще одному втіленні цей період дорівнює 8 діб. У ще одному втіленні цей період дорівнює 7 діб. У ще одному втіленні цей період дорівнює 6 діб. У ще одному втіленні цей період дорівнює 5 діб. У ще одному втіленні цей період дорівнює 4 діб. У ще одному втіленні цей період дорівнює 3 діб. У ще одному втіленні цей період дорівнює 2 діб. У ще одному втіленні цей період дорівнює 24 годинам. У ще одному втіленні цей період дорівнює 12 годинам. Отже, в одному втіленні винаходу тут запропоновано застосування сполуки формули (I) або її фармацевтично прийнятної солі, яку тут визначено, та додаткову протипухлинну речовину для спільного лікування раку. В одному втіленні винаходу тут запропоновано застосування сполуки формули (I) або її фармацевтично прийнятної солі, яку тут визначено, та додаткову протипухлинну речовину для одночасного, роздільного або послідовного лікування раку. В одному втіленні тут запропоновано спосіб продукування дії проти раку в теплокровної тварини, як-то людина, яка потребує такого лікування, яке містить застосування до названого ссавця сполуки формули (I) або її фармацевтично прийнятної солі, та спільного застосування додаткової протипухлинної речовини до названого ссавця, де кількості сполуки формули (I) або її фармацевтичної прийнятної солі та додаткової протипухлинної речовини є сукупно ефективною в продукування дії проти раку. В одному втіленні тут запропоновано спосіб продукування дії проти раку в теплокровної тварини, як-то людина, яка потребує такого лікування, яке містить застосування до названого ссавця сполуки формули (I) або її фармацевтично прийнятної солі та одночасного, роздільного або послідовного застосування додаткової протипухлинної речовини до названого ссавця, де кількості сполуки формули (I) або її фармацевтичної прийнятної солі та додаткової протипухлинної речовини є спільно ефективною в продукуванні дії проти раку. При створенні композицій ліків важливим для субстанції ліків бути у формі придатній для застосування та обробки. Отже, важливим є не тільки, щоб технологія була комерційно рентабельною, але також, щоб таким було подальше вироблення фармацевтичних композицій (наприклад, форм перорального дозування, як-то таблетки), які містять активну сполуку. Різні фізичні властивості кристалічних форм стосовно щодо кожної іншої та стосовно щодо некристалічного стану можуть значно впливати на хімічне та фармацевтичне обробляння сполуки, конкретно, коли сполуку отримано або застосовано в промисловому масштабі. Далі, у виробництві композицій пероральних ліків є важливим, що надійний та відтворюваний профіль концентрації плазми ліків запропоновано подальше застосування пацієнта. Мінливість пацієнта щодо профілю абсорбції ліків у шлунку, кишечнику або кровотоку може мати дію на безпеку та дієвість ліків. Хімічна стабільність, стабільність твердого стану та "строк придатності при зберіганні" активних інгредієнтів також є дуже важливими факторами. Субстанціям ліків, та композицій, які їх містять, слід залежати від значних періодів часу їх зберігання без значних змін активних фізико-хімічних характеристик компонентів (наприклад, їх хімічної композиції, густоти, гігроскопічності та розчинності). Крім того, також є важливим здатність постачати ліки у формі, яка є хімічно чистою як припустимо. 15 UA 106710 C2 5 10 15 20 25 30 35 40 45 50 55 Аморфні матеріали можуть надавати проблеми щодо цього. Наприклад, такі матеріали типово є вимогливими щодо обробки та розробки рецептури, постачання щодо ненадійної розчинності, та часто знайдено їх нестабільність та наявність хімічних домішок. Спеціалісту слід розуміти, щоб легко отримати ліки в стабільній кристалічній формі, треба вирішити зазначені вище проблеми. Отже, для виробництва комерційно рентабельних та фармацевтичних прийнятних композицій ліків важливим по можливості передбачати ліки в кристалічній та стабільній формі. Однак, слід підкреслити, що такої мети неможливо досягти. Дійсно, типово, неможливо передрікати тільки з молекулярної структури, якою слід бути поведінка кристалізації сполуки, як такої або у формі солі. Це можна визначати тільки емпірично. У подальшому аспекті винаходу певні сполуки та їх солі можна отримувати в кристалічних формах. Ці кристалічні форми можна охарактеризувати в конкретній поліморфній формі. Коли це заявлено, що заявлений винахід стосується кристалічної форми із придатним ступенем кристалічності більшим, приблизно, 60 %, краще − більш придатним, приблизно, 80 %, найкраще − більш придатним, приблизно, 90 % та найкраще − більш придатним, приблизно, 95 %. Найбільш придатна ступінь кристалічності − більше ніж, приблизно, 98 %. Конкретні описані тут тверді форми передбачають рентгенівську дифракцію на порошках, по суті, таку як рентгенівська дифракція на порошках, показана на фігурах, та які мають різні величини 2-тета, які показано в таблицях, розміщених тут. Слід розуміти, що величини 2-тета рентгенівської дифракції на порошку можуть злегка відрізнятися від одного приладу до іншого, або від одного зразку до іншого, та, таким чином, цитовані величини не слід уважати абсолютними. Відомо, що рентгенівську дифракцію на порошку можна отримувати при наявності одної або більш помилок вимірів залежно від способів вимірювання (таких як застосоване оснащення або апаратура). Взагалі відомо, що напруженості рентгенівської дифракції на порошку може коливатися залежно від способів вимірювання. Отже, слід розуміти, що тверді форми заявленого винаходу не обмежені кристалами, які передбачає рентгенівська дифракція на порошках, які є ідентичними рентгенівській дифракції на порошку, показаними на фігурах, та будь-які кристали, для яких передбачена рентгенівська дифракція на порошках, по суті, такі ж, як показані на фігурах, є в межах заявленого винаходу. Спеціаліст у рівні техніки рентгенівської дифракції на порошку є здатним уважати істотну ідентичність рентгенівської дифракції на порошках. Спеціалістам у рівні техніки рентгенівської дифракції на порошку зрозуміло, що на відносну інтенсивність піків може впливати, наприклад, розміри кристалів більші 30 мкм та неодиничні характеристичні співвідношення, які можуть впливати на аналіз зразків. Спеціалісту також слід розуміти, що позиція відбиттів може вражатися межею точності для зразка в дифрактометрі та калібруванням нуля дифрактометру. Площинність поверхні зразку також може мати невелику дію. Отже, дані рентгенограми дифракційної смуги не слід сприймати як абсолютні величини. (Jenkins, R & Snyder, R.л. "Introduction to X-Ray Powder Diffractometry" John Wiley & Sons 1996; Bunn, C.W. (1948), Chemical Crystallography, Clarendon Press, London; Klug, H. P. & Alexander, L. E. (1974), X-Ray Diffraction Procedures). Взагалі, погрішність виміру куту дифракції в рентгенівській дифрактограмі на порошку приблизно дорівнює плюс або мінус 0,2° 2-тета, і такий ступінь виміру погрішності слід брати до уваги щодо рентгенівської дифракції на порошку на фігурах та при розгляді даних у розміщених тут таблицях. Крім того, слід розуміти, що, інтенсивності можуть коливатися залежно від способів експерименту та приготування зразку (привілейована орієнтація). У цих технічних вимогах N-(2-{2-диметиламіноетил-метиламіно}-4-метокси-5-{[4-(1метиліндол-3-іл)піримідин-2-іл]аміно}феніл)проп-2-енамід стосується "Сполуки X". Знайшли, що спочатку вироблена сполука X була аморфною твердою. Декілька придатних кристалічних поліморфних форм потім можна було отримати, застосовуючи умови, описані нижче в експериментальному розділі. В усіх утіленнях наведених тут твердих форм піки рентгенівської дифракції на порошках вимірювали, застосовуючи радіовипромінювання CuKa. Поліморфна форма A сполуки X Отже, згідно з подальшим аспектом винаходу тут запропоновано поліморфну форму A сполуки X. Цю поліморфну форму можна охарактеризувати тим, що вона постачає, принаймні, одну з наступних 2θ величин, визначених, застосовуючи радіацію CuKa: 7,8 та 21,8. Поліморфну форму A сполуки X охарактеризовано при забезпеченні рентгенівської дифракції на порошку, по суті, як показано на фігурі 1. 16 UA 106710 C2 5 10 15 20 25 30 35 40 45 50 55 60 Десять піків рентгенівської дифракції на порошку для цієї поліморфної форми [кут 2-тета (2θ), інтенсивність (%)] дорівнює 7,8 (100 %), 21,8 (73,4 %), 13,3 (59,4 %), 6,6 (49,5 %), 23,9 (40,5 %), 9,6 (38,1 %), 14,5 (35,3 %), 15,6 (33,2 %), 22,7 (31,2 %) та 19,1 (29,8 %). Згідно із заявленим винаходом тут запропоновано поліморфну форму A сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком, приблизно, при 2тета = 7,8°. Згідно із заявленим винаходом тут запропоновано поліморфну форму A сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком, приблизно, при 2тета = 21,8°. Згідно із заявленим винаходом тут запропоновано поліморфну форму A сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, із двома конкретними піками, приблизно, при o o 2-тета = 7,8 та 21,8 . Згідно із заявленим винаходом тут запропоновано поліморфну форму A сполуки X, яка має рентгенівську дифракцію на порошку з конкретними піками, приблизно, при 2-тета = 7,8, 21,8, o 13,3, 6,6, 23,9, 9,6, 14,5, 15,6, 22,7 та 19,1 . Згідно із заявленим винаходом тут запропоновано поліморфну форму A сполуки X, яка має рентгенівську дифракцію на порошку, по суті, таку як рентгенівська дифракція на порошку показано на фігурі 1. Згідно із заявленим винаходом тут запропоновано поліморфну форму A сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком при 2-тета = 7,8° полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано a Поліморфну форму A сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком при 2-тета = 21,8° полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму A сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, із двома конкретними піками при 2-тета = 7,8° та 21,8°, де названі величини можуть бути полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано Поліморфну форму A сполуки X, яка має рентгенівську дифракцію на порошку з конкретними піками при 2-тета = 7,8, 21,8, 13,3, 6,6, 23,9, 9,6, 14,5, 15,6, 22,7 та 19,1° де названі величини можуть бути полюс або мінус 0,2° 2-тета. Поліморфна форма B сполуки X Згідно з подальшим аспектом винаходу тут запропоновано поліморфну форму B сполуки X. Цю поліморфну форму можна охарактеризувати тим, що вона постачає, принаймні, одну з наступних 2θ величин, визначених, застосовуючи радіацію CuKa: 9,3 та 23,4. Поліморфну форму B сполуки X охарактеризовано при забезпеченні рентгенівської дифракції на порошку, по суті, як показано на фігурі 3. Десять піків рентгенівської дифракції на порошку для цієї поліморфної форми [кут 2-тета (2θ), інтенсивність (%)] дорівнює 9,3 (100 %), 23,4 (75,0 %), 10,5 (63,6 %), 17,7 (54,3 %), 21,0 (48,1 %), 16,1 (46,4 %), 26,1 (44,2 %), 18,6 (41,8 %), 26,7 (32,2 %) та 20,6 (30,9 %). Згідно із заявленим винаходом тут запропоновано поліморфну форму B сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком, приблизно, при 2тета = 9,3°. Згідно із заявленим винаходом тут запропоновано поліморфну форму B сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком, приблизно, при 2тета = 23,4°. Згідно із заявленим винаходом тут запропоновано поліморфну форму B сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, із двома конкретними піками, приблизно, при 2-тета = 9,3° та 23,4°. Згідно із заявленим винаходом тут запропоновано поліморфну форму B сполуки X, яка має рентгенівську дифракцію на порошку з конкретними піками, приблизно, при 2-тета = 9,3, 23,4, 10,5, 17,7, 21,0, 16,1, 26,1, 18,6, 26,7 та 20,6°. Згідно із заявленим винаходом тут запропоновано поліморфну форму B сполуки X, яка має рентгенівську дифракцію на порошку, по суті, таку як рентгенівська дифракція на порошку, показана на фігурі 3. Згідно із заявленим винаходом тут запропоновано поліморфну форму B сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком при 2-тета = 9,3° полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму B сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком при 2-тета = 23,4° полюс або мінус 0,2° 2-тета. 17 UA 106710 C2 5 10 15 20 25 30 35 40 45 50 55 Згідно із заявленим винаходом тут запропоновано поліморфну форму B сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, із двома конкретними піками при 2-тета = 9,3° та 23,4°, де названі величини можуть бути полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму B сполуки X, яка має рентгенівську дифракцію на порошку з конкретним піком при 2-тета = 9,3, 23,4, 10,5, 17,7, 21,0, 16,1, 26,1, 18,6, 26,7 та 20,6°, де названі величини можуть бути полюс або мінус 0,2° 2-тета. Поліморфна форма C сполуки X Згідно з подальшим аспектом винаходу тут запропоновано поліморфну форму C сполуки X. Цю поліморфну форму можна охарактеризувати тим, що вона постачає, принаймні, одну з наступних 2θ величин, визначених, застосовуючи радіацію CuKa: 6,0 та 11,3. Поліморфну форму C сполуки X охарактеризовано при забезпеченні рентгенівської дифракції на порошку, по суті, як показано на фігурі 5. Десять піків рентгенівської дифракції на порошку для цієї поліморфної форми [кут 2-тета (2θ), інтенсивність (%)] дорівнює 6,0 (100 %), 11,3 (58,2 %), 7,5 (40,5 %), 10,3 (21,9 %), 12,0 (20,1 %), 24,9 (19,4 %), 13,0 (16,9 %), 14,5 (13,5 %), 16,5 (13,5 %) та 18,3 (11,8 %). Згідно із заявленим винаходом тут запропоновано поліморфну форму C сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком, приблизно, при 2тета = 6,0°. Згідно із заявленим винаходом тут запропоновано поліморфну форму C сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком, приблизно, при 2тета = 11,3°. Згідно із заявленим винаходом тут запропоновано поліморфну форму C сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, із двома конкретними піками, приблизно, при 2-тета = 6,0° та 11,3°. Згідно із заявленим винаходом тут запропоновано поліморфну форму C сполуки X, яка має рентгенівську дифракцію на порошку з конкретними піками, приблизно, при 2-тета = 6,0, 11,3, 7,5, 10,3, 12,0, 24,9, 13,0, 14,5, 16,5, та 18,3°.Згідно із заявленим винаходом тут запропоновано поліморфну форму C сполуки X, яка має рентгенівську дифракцію на порошку, по суті, таку як рентгенівська дифракція на порошку, показана на фігурі 5. Згідно із заявленим винаходом тут запропоновано поліморфну форму C сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком при 2-тета = 6,0° полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму C сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком при 2-тета = 11,3° полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму C сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, із двома конкретними піками при 2-тета = 6,0° та 11,3°, де названі величини можуть бути полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму C сполуки X, яка має рентгенівську дифракцію на порошку з конкретним піком при 2-тета = 6,0, 11,3, 7,5, 10,3, 12,0, 24,9, 13,0, 14,5, 16,5, та 18,3°, де названі величини можуть бути полюс або мінус 0,2° 2-тета. Поліморфна форма D сполуки X Згідно з подальшим аспектом винаходу тут запропоновано поліморфну форму D сполуки X, яку вважають моногідратною кристалічною формою. Цю поліморфну форму можна охарактеризувати тим, що вона постачає, принаймні, одну з наступних 2θ величин, визначених, застосовуючи радіацію CuKa: 9,3 та 10,5. Поліморфну форму D сполуки X охарактеризовано при забезпеченні рентгенівської дифракції на порошку, по суті, як показано на фігурі 7. Десять піків рентгенівської дифракції на порошку для цієї поліморфної форми [кут 2-тета (2θ), інтенсивність (%)] дорівнює 9,3 (100 %), 10,5 (90,6 %), 16,1 (75,8 %), 26,1 (75,2 %), 21,0 (70,9 %), 20,6 (56,9 %), 16,8 (56,5 %), 17,7 (53,3 %), 14,7 (41,3 %) та 9,7 (38,3 %). Згідно із заявленим винаходом тут запропоновано поліморфну форму D сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком, приблизно, при 2тета = 9,3°. Згідно із заявленим винаходом тут запропоновано поліморфну форму D сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком, приблизно, при 2тета = 10,5°. 18 UA 106710 C2 5 10 15 20 25 30 35 40 45 50 55 Згідно із заявленим винаходом тут запропоновано поліморфну форму D сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, із двома конкретними піками, приблизно, при 2-тета = 9,3° та 10,5°. Згідно із заявленим винаходом тут запропоновано поліморфну форму D сполуки X, яка має рентгенівську дифракцію на порошку з конкретними піками, приблизно, при 2-тета = 9,3, 10,5, 16,1, 26,1, 21,0, 20,6, 16,8, 17,7, 14,7, та 9,7°. Згідно із заявленим винаходом тут запропоновано поліморфну форму D сполуки X, яка має рентгенівську дифракцію на порошку, по суті, таку як рентгенівська дифракція на порошку, показана на фігурі 7. Згідно із заявленим винаходом тут запропоновано поліморфну форму D сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком при 2-тета = 9,3° полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму D сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком при 2-тета = 10,5° полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму D сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, із двома конкретними піками при 2-тета = 9,3° та 10,5°, де названі величини можуть бути полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму D сполуки X, яка має рентгенівську дифракцію на порошку з конкретним піком при 2-тета = 9,3, 10,5, 16,1, 26,1, 21,0, 20,6, 16,8, 17,7, 14,7, та 9,7°, де названі величини можуть бути полюс або мінус 0,2° 2-тета. Поліморфна форма E сполуки X Згідно з подальшим аспектом винаходу тут запропоновано поліморфну форму E сполуки X, яку вважають 1,25 стехіометрично гідратованою формою сполуки X. Цю поліморфну форму можна охарактеризувати тим, що вона постачає, принаймні, одну з наступних 2θ величин, визначених, застосовуючи радіацію CuKa: 9,2 та 22,9. Поліморфну форму E сполуки X охарактеризовано при забезпеченні рентгенівської дифракції на порошку, по суті, як показано на фігурі 10. Десять піків рентгенівської дифракції на порошку для цієї поліморфної форми [кут 2-тета (2θ), інтенсивність (%)] є: 9,2 (100 %), 22,9 (84,0 %), 14,6 (80,3 %), 12,7 (77,8 %), 16,5 (66,4 %), 26,9 (60,3 %), 9,7 (95,6 %), 14,0 (52,3 %), 10,4 (49,9 %) та 19,5 (48,3 %). Згідно із заявленим винаходом тут запропоновано поліморфну форму E сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком, приблизно, при 2тета = 9,2°. Згідно із заявленим винаходом тут запропоновано поліморфну форму E сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком, приблизно, при 2тета = 22,9°. Згідно із заявленим винаходом тут запропоновано поліморфну форму E сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, із двома конкретними піками, приблизно, при 2-тета = 9,2° та 22,9°. Згідно із заявленим винаходом тут запропоновано поліморфну форму E сполуки X, яка має рентгенівську дифракцію на порошку з конкретними піками, приблизно, при 2-тета = 9,2, 22,9, 14,6, 12,7, 16,5, 26,9, 9,7, 14,0, 10,4 та 19,5°. Згідно із заявленим винаходом тут запропоновано поліморфну форму E сполуки X, яка має рентгенівську дифракцію на порошку, по суті, таку як рентгенівська дифракція на порошку, показана на фігурі 10. Згідно із заявленим винаходом тут запропоновано поліморфну форму E сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком при 2-тета = 9,2° полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму E сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком при 2-тета = 22,9° полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму E сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, із двома конкретними піками при 2-тета = 9,2° та 22,9°, де названі величини можуть бути полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму E сполуки X, яка має рентгенівську дифракцію на порошку з конкретним піком при 2-тета = 9,2, 22,9, 14,6, 12,7, 16,5, 26,9, 9,7, 14,0, 10,4, та 19,5°, де названі величини можуть бути полюс або мінус 0,2° 2-тета. Поліморфна форма F сполуки X 19 UA 106710 C2 5 10 15 20 25 30 35 40 45 50 55 60 Згідно з подальшим аспектом винаходу тут запропоновано поліморфну форму F сполуки X, яку вважають 0,25 стехіометрично гідратованою формою сполуки X. Цю поліморфну форму можна охарактеризувати тим, що вона постачає, принаймні, одну з наступних 2θ величин, визначених, застосовуючи радіацію CuKa: 18,7 та 8,9. Поліморфну форму F сполуки X охарактеризовано при забезпеченні рентгенівської дифракції на порошку, по суті, як показано на фігурі 13. Десять піків рентгенівської дифракції на порошку для цієї поліморфної форми [кут 2-тета (2θ), інтенсивність (%)] є: 18,7 (100 %), 8,9 (87,7 %), 15,1 (80,3 %), 25,4 (74,6 %), 14,5 (72,3 %), 22,9 (69,6 %), 9,9 (51,1 %), 28,2 (42,0 %), 8,2 (24,2 %) та 11,9 (22,3 %). Згідно із заявленим винаходом тут запропоновано поліморфну форму F сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком, приблизно, при 2тета = 18,7°. Згідно із заявленим винаходом тут запропоновано поліморфну форму F сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком, приблизно, при 2тета = 8,9°. Згідно із заявленим винаходом тут запропоновано поліморфну форму F сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, із двома конкретними піками, приблизно, при 2-тета = 18,7° та 8,9°. Згідно із заявленим винаходом тут запропоновано поліморфну форму F сполуки X, яка має рентгенівську дифракцію на порошку з конкретними піками, приблизно, при 2-тета = 18,7, 8,9, 15,1, 25,4, 14,5, 22,9, 9,9, 28,2, 8,2 та 11,9°. Згідно із заявленим винаходом тут запропоновано поліморфну форму F сполуки X, яка має рентгенівську дифракцію на порошку, по суті, таку як рентгенівська дифракція на порошку, показана на фігурі 13. Згідно із заявленим винаходом тут запропоновано поліморфну форму F сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком при 2-тета = 18,7° полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму F сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком при 2-тета = 8,9° полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму F сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, із двома конкретними піками при 2-тета = 18,7° та 8,9°, де названі величини можуть бути полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму F сполуки X, яка має рентгенівську дифракцію на порошку з конкретним піком при 2-тета = 18,7, 8,9, 15,1, 25,4, 14,5, 22,9, 9,9, 28,2, 8,2 та 11,9°, де названі величини можуть бути полюс або мінус 0,2° 2-тета. Поліморфна форма K сполуки X Згідно з подальшим аспектом винаходу тут запропоновано поліморфну форму K сполуки X. Цю поліморфну форму можна охарактеризувати тим, що вона постачає, принаймні, одну з наступних 2θ величин, визначених, застосовуючи радіацію CuKa: 8,4 та 9,7. Поліморфну форму F сполуки X охарактеризовано при забезпеченні рентгенівської дифракції на порошку, по суті, як показано на фігурі 16. Десять піків рентгенівської дифракції на порошку для цієї поліморфної форми [кут 2-тета (2θ), інтенсивність (%)] є: 8,4 (100 %), 9,7 (37,7 %), 12,2 (32,4 %), 15,1 (25,2 %), 24,7 (20,7 %), 9,0 (16,8 %), 21,9 (13,9 %), 19,5 (13,9 %), 24,2 (13,8 %) та 18,3 (11,8 %). Згідно із заявленим винаходом тут запропоновано поліморфну форму K сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком, приблизно, при 2тета = 8,4°. Згідно із заявленим винаходом тут запропоновано поліморфну форму K сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком, приблизно, при 2тета = 9,7°. Згідно із заявленим винаходом тут запропоновано поліморфну форму K сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, із двома конкретними піками, приблизно, при 2-тета = 8,4° та 9,7°. Згідно із заявленим винаходом тут запропоновано поліморфну форму K сполуки X, яка має рентгенівську дифракцію на порошку з конкретними піками, приблизно, при 2-тета = 8,4, 9,7, 12,2, 15,1, 24,7, 9,0, 21,9, 19,5, 24,2 та 18,3°. Згідно із заявленим винаходом тут запропоновано поліморфну форму K сполуки X, яка має рентгенівську дифракцію на порошку, по суті, таку як рентгенівська дифракція на порошку, показана на фігурі 16. 20 UA 106710 C2 5 10 15 20 25 30 35 40 45 50 55 Згідно із заявленим винаходом тут запропоновано поліморфну форму K сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком при 2-тета = 8,4° полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму K сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком при 2-тета = 9,7° полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму K сполуки X, яка має рентгенівську дифракцію на порошку, принаймні, із двома конкретними піками при 2-тета = 8,4° та 9,7°, де названі величини можуть бути полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму K сполуки X, яка має рентгенівську дифракцію на порошку з конкретним піком при 2-тета = 8,4, 9,7, 12,2, 15,1, 24,7, 9,0, 21,9, 19,5, 24,2 та 18,3°, де названі величини можуть бути полюс або мінус 0,2° 2-тета. У цій специфікації мезилат солі N-(2-{2-диметиламіноетил-метиламіно}-4-метокси-5-{[4-(1метиліндол-3-іл)піримідин-2-іл]аміно}феніл)проп-2-енаміду стосується "Мезилату солі Y". Поліморфна форма A солі мезилату Y Згідно з подальшим аспектом винаходу тут запропоновано поліморфну форму A солі мезилату Y. Цю поліморфну форму можна охарактеризувати тим, що вона постачає, принаймні, одну з наступних 2θ величин, визначених, застосовуючи радіацію CuKa: 5,6 та 6,5. Поліморфна форма A солі мезилату Y охарактеризовано при забезпеченні рентгенівської дифракції на порошку, по суті, як показано на фігурі 18. Десять піків рентгенівської дифракції на порошку для цієї поліморфної форми [кут 2-тета (2θ), інтенсивність (%)] є: 5,6 (100 %), 6,5 (66,7 %), 10,2 (97,2 %), 21,0 (96,2 %), 13,5 (91,7 %), 22,7 (89,6 %), 19,3 (80,6 %), 27,3 (75,7 %), 15,7 (71,2 %) та 19,9 (66,7 %). Згідно із заявленим винаходом тут запропоновано поліморфну форму A солі мезилату Y, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком, приблизно, при 2-тета = 5,6°. Згідно із заявленим винаходом тут запропоновано поліморфну форму A солі мезилату Y, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком, приблизно, при 2-тета = 6,5°. Згідно із заявленим винаходом тут запропоновано поліморфну форму A солі мезилату Y, яка має рентгенівську дифракцію на порошку, принаймні, із двома конкретними піками, приблизно, при 2-тета = 5,6° та 6,5°. Згідно із заявленим винаходом тут запропоновано поліморфну форму A солі мезилату Y, яка має рентгенівську дифракцію на порошку з конкретними піками, приблизно, при 2-тета = 5,6, 6,5, 10,2, 21,0, 13,5, 22,7, 19,3, 27,3, 15,7 та 19,9°. Згідно із заявленим винаходом тут запропоновано поліморфну форму A солі мезилату Y яка має рентгенівську дифракцію на порошку, по суті, таку як рентгенівська дифракція на порошку, показана на фігурі 18. Згідно із заявленим винаходом тут запропоновано поліморфну форму A солі мезилату Y, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком при 2-тета = 5,6° полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму A солі мезилату Y, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком при 2-тета = 6,5° полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму A солі мезилату Y, яка має рентгенівську дифракцію на порошку, принаймні, із двома конкретними піками при 2тета = 5,6° та 6,5°, де названі величини можуть бути полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму A солі мезилату Y, яка має рентгенівську дифракцію на порошку з конкретним піком при 2-тета = 5,6, 6,5, 10,2, 21,0, 13,5, 22,7, 19,3, 27,3, 15,7 та 19,9° де названі величини можуть бути полюс або мінус 0,2° 2-тета. Поліморфна форма B солі мезилату Y Згідно з подальшим аспектом винаходу тут запропоновано поліморфну форму B солі мезилату Y. Цю поліморфну форму можна охарактеризувати тим, що вона постачає, принаймні, одну з наступних 2θ величин, визначених, застосовуючи радіацію CuKa: 7,2 та 8,6. Поліморфна форма A солі мезилату Y охарактеризовано при забезпеченні рентгенівської дифракції на порошку, по суті, як показано на фігурі 20. Десять піків рентгенівської дифракції на порошку для цієї поліморфної форми [кут 2-тета (2θ), інтенсивність (%)] є: 7,2 (50,2 %), 8,6 (55,2 %), 15,3 (100 %), 10,4 (92,6 %), 25,7 (74,0 %), 26,1 (63,9 %), 16,4 (55,2 %), 9,5 (47,5 %), 22,1 (46,9 %) та 18,8 (47,7 %). 21 UA 106710 C2 5 10 15 20 25 30 35 Згідно із заявленим винаходом тут запропоновано поліморфну форму B солі мезилату Y, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком, приблизно, при 2-тета = 7,2°. Згідно із заявленим винаходом тут запропоновано поліморфну форму B солі мезилату Y, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком, приблизно, при 2-тета = 8,6°. Згідно із заявленим винаходом тут запропоновано поліморфну форму B солі мезилату Y, яка має рентгенівську дифракцію на порошку, принаймні, із двома конкретними піками, приблизно, при 2-тета = 7,2° та 8,6° Згідно із заявленим винаходом тут запропоновано поліморфну форму B солі мезилату Y, яка має рентгенівську дифракцію на порошку з конкретними піками, приблизно, при 2-тета = 7,2, 8,6, 15,3, 10,4, 25,7, 26,1, 16,4, 9,5, 22,1 та 18,8°. Згідно із заявленим винаходом тут запропоновано поліморфну форму B солі мезилату Y, яка має рентгенівську дифракцію на порошку, по суті, таку як рентгенівська дифракція на порошку, показана на фігурі 20. Згідно із заявленим винаходом тут запропоновано поліморфну форму B солі мезилату Y, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком при 2-тета = 7,2° полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму B солі мезилату Y, яка має рентгенівську дифракцію на порошку, принаймні, з одним конкретним піком при 2-тета = 8,6° полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму B солі мезилату Y, яка має рентгенівську дифракцію на порошку, принаймні, із двома конкретними піками при 2тета = 7,2° та 8,6°, де названі величини можуть бути полюс або мінус 0,2° 2-тета. Згідно із заявленим винаходом тут запропоновано поліморфну форму B солі мезилату Y, яка має рентгенівську дифракцію на порошку з конкретним піком при 2-тета = 7,2, 8,6, 15,3, 10,4, 25,7, 26,1, 16,4, 9,5, 22,1 та 18,8°, де названі величини можуть бути полюс або мінус 0,2° 2-тета. Перелік фігур Усі фігури стосуються твердих форм сполуки: N-(2-{2-диметиламіноетил-метиламіно}-4метокси-5-{[4-(1-метиліндол-3-іл)піримідин-2-іл]аміно}феніл)проп-2-енаміду ("Сполука X") або її сіль мезилату, де позначено ("Сіль мезилату Y"). Фігура 1: Рентгенівська дифракція на порошку - Форма A Фігура 2: Термограма ДСК - Форма A Фігура 3: Рентгенівська дифракція на порошку - Форма B Фігура 4: Термограма ДСК - Форма B Фігура 5: Рентгенівська дифракція на порошку - Форма C Фігура 6: Термограма ДСК - Форма C Фігура 7: Рентгенівська дифракція на порошку - Форма D (Моногідрат) Фігура 8: Термограма ДСК - Форма D Моногідрат Фігура 9: Термограма ТГА - Форма D Моногідрат Фігура 10: Рентгенівська дифракція на порошку - Форма E (Гідратована форма) Фігура 11: Термограма ДСК - Форма E (Гідратована форма) Фігура 12: Термограма ТГА - Форма E (Гідратована форма) Фігура 13: Рентгенівська дифракція на порошку - Форма F (Гідратована форма) Фігура 14: Термограма ДСК - Форма F (Гідратована форма) Фігура 15: Термограма ТГА - Форма F (Гідратована форма) Фігура 16: Рентгенівська дифракція на порошку - Форма K Фігура 17: Термограма ДСК - Форма K Фігура 18: Рентгенівська дифракція на порошку - сіль мезилату Форми A Фігура 19: Термограма ДСК – Сіль мезилату Форм A Фігура 20: Рентгенівська дифракція на порошку - сіль мезилату Форми B Фігура 21: Термограма ДСК - Сіль мезилату Форм B Способи хімічного синтезу та біологічного аналізу Застосовано наступні скорочення: ТГФ = тетрагідрофуран; DIPEA = діізопропілетиламін; насич. = насичений водний розчин; FCC = флеш-хроматографія на колонці, застосовуючи діоксид силіцію; ТФОК = трифлуорооцтова кислота; к.т. = кімнатна температура; ДМФ = N,N-диметилформамід; ДМСО = диметилсульфоксид; ДМА = N,N-диметилацетамід; EtOAc = 1 етилацетат; год. = години; протонний ЯМР: ( H ЯМР) визначали, застосовуючи дейтерований диметилсульфоксид при 400 або 500 МГц у діапазоні 20-30 °C, якщо не встановлено інакше. Застосовано стандартні скорочення ЯМР, (s = синглет; d = дублет; dd = подвійний із дублетів; t 22 UA 106710 C2 5 10 15 20 25 30 35 40 45 50 55 60 = триплет; q = квартет; p = пентет; m = мультиплет; br = широкий; т.д.). Де залізо згадують як реагент, це – порошок заліза, 325 меш та відновлений гідрогеном. Величини аналізу (мкM), надані в прикладі, − це величини ІК50. Рентгенівську дифракцію на порошку (XRPD) робили, застосовуючи прилад Bruker D4. Рентгенівську дифрактограму на порошку визначали встановленням зразку кристалічного матеріалу на Bruker single silicon crystal (SSC), змонтованому на кристалічній пластині, та розгортанням зразку до тонкого шару на мікроскопічному склі. Зразок повертали при 30 обертах за хвилину (для поліпшення статистичного підрахунку) та опромінювали рентгенівським промінням, генерованим із довготонкофокусної електронної мідної лампи, яка працює при 40 кВ та 40 мA із довжиною хвилі 1,5418 ангстремів (радіовипромінювання CuKa). Колімоване джерело рентгенівського випромінювання пропускали через систему автоматичної змінної дивергентної щілини при V20 та відбитим радіовипромінюванням, спрямованим через 5,89 мм щілину, яка антирозсіює, та 9,55 мм детекторну щілину. Зразок експонували протягом 0,03 секунд через 0,00570° 2-тета інкремент (суцільний спосіб сканування) протягом діапазону 2 ступенів − 40 ступенів 2-тета в способі тета-тета. Перебіг часу дорівнював 3 хвилинам та 36 секундам. Прилад обладнано позитивним чутливим детектором (Lynxeye). Контроль та збір даних робили засобом Dell Optiplex 686 NT 4,0 Workstation, що оперує програмою Diffrac+software. Диференціальну сканувальну калориметрію (ДСК) робили, застосовуючи диференціальний сканувальний калориметр "TA Instruments Q1000. Типово менше ніж 5 мг матеріалу в стандартному алюмінієвому резервуарі із кришкою нагрівали при температурі 25°C - 300°C при постійній швидкості нагрівання 10°C за хвилину. Пропускали газ азот при швидкості потоку 50 мл за хвилину. Будь-яка дифрактограма XRPD або ДСК термограма кристалічної форми, по суті, ідентична розкритій тут, є в межах заявленого винаходу. Кожен спеціаліст у рівні техніки здатен визначати реальні тотожності дифрактограм та термограм. Аналіз 1: Аналіз клітинного фосфорилування Exon19-делеції EGFR (активувальний прямий мутант) Лінію клітин легенів людини PC9 (Exon 19-делеції EGFR) отримували від американської колекції типових культур American type Culture Collection. PC9 утримували в RPMI 1640, яке містить 10 % фетальну телячу сироватку та 2 мМ глутаміну. Клітини вирощували в зволоженому інкубаторі при 37 °C з 5 % CO2. Аналіз вимірювання клітинного фосфорилування ендогенного pEGFR в клітинах лізатів робили згідно із протоколом, описаним у R&D Systems DuoSet IC Human Phospho-EGF R ELISA (R&D Systems catalogue number #DYC1095). 40 мкл клітин засівали (10000 клітин/лунку) у середовище росту в чорні чистодонні 384лункові планшети Corning та інкубували при 37 °C з 5 % CO2 протягом ночі. Клітини акустично дозували, застосовуючи Echo 555, зі сполуками послідовно розбавленими в 100 % ДМСО. Планшети інкубували протягом наступних 2 год., тоді − наступна аспірація середовища, до кожної лунки додавали 40 мкл 1x буферу лізису. Чорні високі поєднані 384-лункові планшети Greiner покривали імобілізованим антитілом і тоді блокували 3 % BSA. Потім блок видаляли й 15 мкл лізату переносили до чорних високих поєднаних 384-лункових планшетів Greiner та інкубували протягом 2 годин. Після аспірації та промивання планшетів PBS додавали 20 мкл антитіла виявлення та інкубували протягом 2 годин. Після аспірації та промивання планшетів PBS додавали 20 мкл субстрату флуорогенної пероксидази QuantaBlu (каталог Thermo Fisher Scientific catalogue number 15169) та інкубували протягом 1 години. До планшетів додавали 20 мкл стоп-розчину QuantaBlu та флуоресценцію визначали на планшет-рідері Envision, застосовуючи довжину хвилі збудження 352 нм та довжину хвилі випромінювання 460 нм. Отримані дані для кожної сполуки передавали до придатного пакету програм (як-то Origin) для аналізу визначеної кривої. Із цих даних визначали величину ІК50 обчисленням концентрації сполуки, яка потрібна для отримання 50 % ефекту. Аналіз 2: Аналіз клітинного фосфорилування L858R/T790M EGFR (подвійний мутант) Лінії клітин легенів людини NCI-H1975 отримували від американської колекції типових культур American type Culture Collection. NCI-H1975 утримували в RPMI 1640, яка містить 10 % фетальну телячу сироватку та 2 мМ глутаміну. Клітини вирощували в зволоженому інкубаторі при 37 °C з 5 % CO2. Аналіз вимірювання клітинного фосфорилування ендогенного p-EGFR в клітинах лізатів робили згідно із протоколом, описаним у R&D Systems DuoSet IC Human Phospho-EGF R ELISA (R&D Systems catalogue number #DYC1095). 40 мкл клітин засівали (10000 клітин/лунку) у середовище зростання в чорні чистодонні 384лункові планшети Corning, та інкубували при 37°C з 5 % CO2 протягом ночі. Клітини акустично дозували, застосовуючи Echo 555, зі сполуками послідовно розбавленими в 100 % ДМСО. Планшети інкубували протягом наступних 2 годин, і тоді − наступна аспірація середовища, до 23 UA 106710 C2 5 10 15 20 25 30 35 кожної лунки додавали 40 мкл 1x буферу лізису. Чорні високі поєднані 384-лункові планшети Greiner покривали імобілізованим антитілом і тоді блокували 3 % BSA. Потім блок видаляли й 15 мкл лізату переносили до чорних високих поєднаних 384-лункових планшетів Greiner та інкубували протягом 2 годин. Після аспірації та промивання планшетів PBS додавали 20 мкл антитіла виявлення та інкубували протягом 2 годин. Після аспірації та промивання планшетів PBS додавали 20 мкл субстрату флуорогенної пероксидази QuantaBlu (каталог Thermo Fisher Scientific catalogue number 15169) та інкубували протягом 1 години. До планшетів додавали 20 мкл стоп-розчину QuantaBlu та флуоресценцію визначали на планшеті-рідері Envision, застосовуючи довжину хвилі збудження 352 нм та довжину хвилі випромінювання 460 нм. Отримані дані для кожної сполуки передавали до придатного пакету програм (як-то Origin) для аналізу визначеної кривої. Із цих даних визначали величину ІК 50 обчисленням концентрації сполуки, яка потрібна для отримання 50 % ефекту. Аналіз 3: аналіз клітинного фосфорилування Wild-тип EGFR Лінії клітин легенів людини LoVo отримували від американської колекції типових культур. LoVo утримували в RPMI 1640, яка містить 3 % фетальну телячу сироватку та 2 мМ глутаміну. Клітини вирощували в зволоженому інкубаторі при 37 °C з 5 % CO2. 40 мкл клітин засівали (15000 клітин/лунку) у середовище зростання в чорні чистодонні 384лункові планшети Corning, та інкубували при 37°C з 5 % CO2 протягом ночі. Клітини акустично дозували, застосовуючи Echo 555, зі сполуками послідовно розбавленими в 100 % ДМСО. Планшети інкубували протягом наступних 2 годин, тоді стимулювали 100 нг/мл протягом 10 хвилин, при наступній аспірації середовища, до кожної лунки додавали 40 мкл 1x буферу лізису. Чорні високі поєднані 384-лункові планшети Greiner покривали імобілізованим антитілом і тоді блокували 3 % BSA. Потім блок видаляли й 15 мкл лізату переносили до чорних високих поєднаних 384-лункових планшетів Greiner та інкубували протягом 2 годин. Після аспірації та промивання планшетів PBS додавали 20 мкл антитіла виявлення та інкубували протягом 2 годин. Після аспірації та промивання планшетів PBS додавали 20 мкл субстрату флуорогенної пероксидази QuantaBlu (каталог Thermo Fisher Scientific catalogue number 15169) та інкубували протягом 1 години. До планшетів додавали 20 мкл стоп-розчину QuantaBlu та флуоресценцію визначали на планшет-рідері Envision, застосовуючи довжину хвилі збудження 352 нм та довжину хвилі випромінювання 460 нм. Отримані дані для кожної сполуки передавали до придатного пакету програм (як-то Origin) для аналізу визначеної кривої. Із цих даних визначали величину ІК 50 обчисленням концентрації сполуки, яка потрібна для отримання 50 % ефекту. Приклад даних аналізу (мкM) цієї заявки показано нижче в таблиці. Тоді як дані аналізу встановлено згідно з певним числом значущих цифр, що не слід приймати як твердження, що ці дані визначають точне число значущих цифр Прикл. No. 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 Аналіз 1 0,007614 0,001291 0,01054 0,01273 0,02059 0,002183 0,003262 0,02239 0,009959 0,07377 0,02854 0,03613 0,1388 0,05328 0,01399 0,1437 0,02344 0,06644 0,002149 0,007487 0,002948 Аналіз 2 0,004956 0,001504 0,01549 0,0016 0,003402 0,0006695 0,0006825 0,005481 0,002818 0,03998 0,01871 0,005821 0,01926 0,01912 0,05524 0,07052 0,005644 0,03138 0,001463 0,005276 0,002339 24 Аналіз 3 0,4744 0,04122 0,5222 0,5099 0,8225 0,1959 0,1606 1,17 0,8744 8,427 1,599 1,393 11,91 12,48 1,067 >18,92 0,772 2,696 0,07081 0,1929 0,1283 UA 106710 C2 Прикл. No. 22 23 24 25 26 27 28 28A 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 5 10 15 Аналіз 1 0,002137 0,01694 0,001327 0,0005811 0,002289 0,00561 0,01292 0,01975 0,001228 0,07375 0,03746 0,138 0,8916 0,009044 0,008571 0,04329 0,002112 0,005092 0,002336 0,0124 0,02863 0,005192 0,01817 0,03329 0,1102 0,1289 0,1939 0,03988 0,0742 0,1145 0,01296 0,02603 0,03537 0,003217 0,006433 0,04433 0,006455 0,007085 0,002266 0,0146 Аналіз 2 0,001524 0,01759 0,0008856 0,000238 0,001925 0,01142 0,01144 0,01271 0,0008846 0,05211 0,00734 0,02378 1,158 0,003767 0,006772 0,03272 0,001814 0,004405 0,001005 0,01477 0,0295 0,005161 0,01055 0,0256 0,041 0,09293 0,1192 0,03098 0,05097 0,1297 0,007713 0,01501 0,02824 0,002803 0,002863 0,02922 0,01452 0,01683 0,003021 0,04886 Аналіз 3 0,07336 3,018 0,03567 0,01092 0,05831 0,3177 0,4938 1,443 0,04652 1,613 2,506 10,53 11,86 0,1526 0,2623 1,051 0,04859 0,5384 0,2484 >30 1,841 0,4542 1,34 3,64 7,396 7,091 15,45 1,579 3,093 7,626 0,4622 1,4 2,638 0,1832 0,5066 3,504 0,08931 0,1786 0,02816 0,6241 Приклад 1: N-{4-Метокси-2-[1-метил-3,6-дигідро-2H-піридин-4-іл]-5-[(5-метил-4-піразоло[1,5α]піридин-3-ілпіримідин-2-іл)аміно]феніл}проп-2-енамід Акрилоілхлорид (0,331 мл, 1M в ТГФ, 0,33 ммол) додавали краплями до розчину 6-метокси4-(1-метил-1,2,3,6-тетрагідропіридин-4-іл)-N1-[5-метил-4-(піразоло[1,5-а]-піридин-3-іл)піримідин2-іл]бензол-1,3-діаміну (проміжної сполуки 1, 146 мг, 0,33 ммол) та DIPEA (0,086 мл, 0,50 ммол) у ТГФ (4 мл) при -10 °C протягом 1 хвилини під N2. Отриману суміш перемішували при 0 °C протягом 15 хвилин і тоді концентрували у вакуумі. Залишок розчиняли в CH 2Cl2 (5 мл) плюс мала кількість CH3OH. Тоді цей розчин промивали насич. NaHCO 3 (2 мл), сушили (MgSO4) і тоді концентрували у вакуумі. Очищення FCC, елюювання 5-25 % CH3OH в CH2Cl2 та концентрацію придатних фракцій у вакуумі постачали матеріалом, який розчиняли в CH 2Cl2:7N метанольному аміаку 100:8 (1 мл) та фільтрували через 1 г прокладку діоксиду силіцію. Концентрування 1 отриманого розчину дало заголовну сполуку (70 мг, 38 %) як бліду оранжеву піну; H ЯМР: 2,27 (3H, s), 2,37 (2H, m), 2,42 (3H, s), 2,53-2,57 (2H, m), 2,97 (2H, m), 3,87 (3H, d), 5,66 (2H, d), 6,14 (1H, d), 6,39 (1H, d), 6,86 (1H, s), 7,07 (1H, t), 7,42 (1H, m), 7,98 (1H, s), 8,17 (1H, s), 8,32 (1H, s), + + 8,48 (1H, d), 8,58 (1H, s), 8,81 (1H, d), 9,29 (1H, s); m/z: ES MH 496. Приклад 2: N-(5-{[5-Хлоро-4-(1H-індол-3-іл)піримідин-2-іл]аміно}-4-метокси-2-[1-метил-3,6дигідро-2H-піридин-4-іл]феніл)проп-2-енамід 25 UA 106710 C2 5 10 15 20 25 30 35 40 45 50 55 60 Акрилоілхлорид (0,217 мл, 1M в ТГФ, 0,22 ммол) додавали краплями до кашки N'-[5-хлоро-4(1H-індол-3-іл)піримідин-2-іл]-4-метокси-6-(1-метил-3,6-дигідро-2H-піридин-4-іл)бензол-1,3діаміну (проміжної сполуки 7, 100 мг, 0,22 ммол) та DIPEA (0,057 мл, 0,33 ммол) у ТГФ (3 мл) при -5 °C протягом 1 хвилини під N2. Отриману суміш перемішували при 0 °C протягом 15 хвилин і тоді концентрували у вакуумі. Залишок розчиняли в CH 2Cl2 (5 мл) плюс кілька крапель CH3OH, та промивали насич. NaHCO3 (2 мл). Тоді органічний розчин сушили (MgSO 4) та завантажували на діоксид силіцію у вакуумі. Очищення FCC, елюювання 5-25 % CH3OH в CH2Cl2 та концентрування придатних фракцій у вакуумі дало залишок, який промивали CH 3OH (0,3 мл) та сушили на повітрі, що дало заголовну сполуку (37 мг, 31 %) як бежеву кристалічну 1 тверду речовину. H ЯМР: 2,28 (3H, s), 2,38 (2H, m), 2,55 (2H, m), 2,98 (2H, d), 3,85 (3H, s), 5,65,72 (2H, m), 6,15 (1H, m), 6,41 (1H, m), 6,88 (1H, s), 7,10 (1H, t), 7,18 (1H, t), 7,47 (1H, d), 7,98 (1H, + + s), 8,33 (1H, s), 8,36 (1H, d), 8,42 (1H, s), 8,49 (1H, s), 9,29 (1H, s), 11,86 (1H, s); m/z: ES MH 515. Приклад 3: N-(5-{[4-(1H-Індол-3-іл)-5-метилпіримідин-2-іл]аміно}-4-метокси-2-[4метилпіперазин-1-іл]феніл)проп-2-енамід Акрилоілхлорид (0,025 мл, 0,30 ммол) додавали краплями до N'-[4-(1H-індол-3-іл)-5метилпіримідин-2-іл]-4-метокси-6-(4-метилпіперазин-1-іл)бензол-1,3-діаміну (проміжної сполуки 12, 135 мг, 0,30 ммол) та DIPEA (0,090 мл, 0,33 ммол) в CH 2Cl2 (10 мл) та ДМФ (2 мл) при 0 °C під N2. Отриману суспензію перемішували при 0 °C протягом 2 год. тоді дозволяли нагріватися до к.т. Тоді суміш розбавляли водою (15 мл) та екстрагували СH 2Cl2 (40 мл). Отриманий органічний розчин промивали насич. Na2CO3 (20 мл) і тоді насич. розсолом (20 мл). Розчин тоді сушили (MgSO4) та концентрували у вакуумі. Очищення FCC, елюювання 1-5 % 7M метанольним аміаком в CH2Cl2 дало сирий продукт. Подальше очищення препаративною ВЕРХ (колонка Waters SunFire, 5 мк діоксид силіцію, 19 мм діаметр, 100 мм довжина), елюювання зниженими полярними сумішами води (яка містить 0,1 % мурашиної кислоти) та CH3CN, а потім − ВЕРХ (колонка Waters XBridge Prep C18 OBD, 5 мк діоксиду силіцію, 19 мм діаметр, 100 мм довжина), елюювання зниженими полярними сумішами води (яка містить 1 % NH3) та CH3CN, 1 що дало заголовну сполуку (23 мг, 15 %) як білу тверду речовину; H ЯМР: 2,26 (3H, s), 2,37 (3H, s), 2,48-2,57 (4H, m), 2,87 (4H, t), 3,84 (3H, s), 5,70 (1H, d), 6,18 (1H, dd), 6,59 (1H, dd), 6,87 (1H, s), 7,05 (1H, dd), 7,15 (1H, t), 7,44 (1H, d), 7,83 (1H, s), 7,98 (1H, d), 8,22 (1H, s), 8,34 (1H, d), 8,49 + + (1H, s), 8,97 (1H, s), 11,68 (1H, s); m/z: ES MH 498,60. Приклад 4: N-{5-[(5-Хлоро-4-піразоло[1,5-α]піридин-3-ілпіримідин-2-іл)аміно]-2-[(3R)-3диметиламінопіролідин-1-іл]-4-метоксифеніл}проп-2-енамід Розчин акрилоілхлориду (0,042 мл, 0,51 ммол) в CH 2Cl2 (1 мл) додавали краплями до суміші N-(5-хлоро-4-піразоло[1,5-a]піридин-3-ілпіримідин-2-іл)-4-[(3R)-3-диметиламіно-піролідин-1-іл]-6метоксибензол-1,3-діаміну (проміжної сполуки 18, 245 мг, 0,51 ммол) та DIPEA (0,097 мл, 0,56 ммол) в CH2Cl2 (10 мл), який охолоджували в льодяній бані. Суміш перемішували протягом 2 год. і тоді промивали розсолом, сушили (Na2SO4) та концентрували у вакуумі. Очищення FCC, елюювання 2 % 7N метанольним аміаком в CH2Cl2 дало піну після концентрації у вакуумі. Цю піну розтирали до порошку, застосовуючи CH 2Cl2 та діетилетер, та отримане тверде збирали фільтруванням та сушили, що дало заголовну сполуку (157 мг, 58 %) як жовту тверду речовину; 1 H ЯМР: 1,68-1,83 (1H, m), 2,05-2,16 (1H, m), 2,18 (6H, s), 2,64-2,76 (1H, m), 3,18-3,29 (3H, m), 3,36-3,47 (1H, m), 3,77 (3H, s), 5,67 (1H, dd), 6,16 (1H, dd), 6,48 (1H, dd), 6,54 (1H, s), 7,12 (1H, t), 7,37 (1H, t), 7,43 (1H, s), 8,28-8,46 (2H, m), 8,55 (1H, s), 8,83 (1H, d), 8,94 (1H, s), 9,37 (1H, s); m/z: + + ES MH 533,5. Приклад 5: N-{5-[(5-Хлоро-4-піразоло[1,5-a]піридин-3-ілпіримідин-2-іл)аміно]-2-[3диметиламіноазетидин-1-іл]-4-метоксифеніл}проп-2-енамід Розчин акрилоілхлориду (0,038 мл, 0,47 ммол) в CH 2Cl2 (1 мл) додавали краплями до перемішуваного розчину N-(5-хлоро-4-піразоло[1,5-a]піридин-3-ілпіримідин-2-іл)-4-(3диметиламіно-азетидин-1-іл)-6-метоксибензол-1,3-діаміну проміжної сполуки 24, 220 мг, 0,47ммол) та DIPEA (0,090 мл, 0,52 ммол) в CH2Cl2 (5 мл), що охолоджували в бані лід/вода. Суміш перемішували протягом 3 год. і тоді промивали розсолом, сушили (Na2SO4) та концентрували у вакуумі. Очищення FCC, елюювання 0-5 % 7N метанольним аміаком у CH2Cl2 дало заголовну 1 сполуку (221 мг, 90 %) як (проміжна сполука 24; H ЯМР: 2,09 (6H, s), 3,08 (1H, p), 3,55-3,62 (2H, m), 3,76 (3H, s), 3,97 (2H, t), 5,66 (1H, dd), 6,16 (1H, dd), 6,25 (1H, s), 6,45 (1H, dd), 7,10 (1H, dd), 7,35 (1H, s), 7,39 (1H, dd), 8,25-8,40 (1H, m), 8,35 (1H, s), 8,45 (1H, s), 8,81 (1H, d), 8,92 (1H, s), + + 9,24 (1H, s); m/z: ES MH 519,56. Приклад 6: N-{5-[(5-Хлоро-4-піразоло[1,5-a]піридин-3-ілпіримідин-2-іл)аміно]-2-[2диметиламіноетил-метиламіно]-4-метоксифеніл}проп-2-енамід 4 Акрилоілхлорид (1,248 мл, 1M в ТГФ, 1,25 ммол) додавали краплями до N -[5-хлоро-41 1 (піразоло[1,5-a]піридин-3-іл)піримідин-2-іл]-N -[2-(диметиламіно)етил]-5-метокси-N 26 UA 106710 C2 5 10 15 20 25 30 35 40 45 50 55 60 метилбензол-1,2,4-триаміну (проміжної сполуки 33, 530 мг, 1,13 ммол) та DIPEA (0,244 мл, 1,36 ммол) у ТГФ (20 мл), який охолоджували до 0 °C. Суміш перемішували при 0 °C протягом 2 год. Тоді суміш концентрували у вакуумі. Отримане розчиняли в CH2Cl2 (100 мл), потім промивали послідовно насич. NaHCO3 (25 мл), водою (25 мл) та насич. розсолом (25 мл). Органічний розчин концентрували у вакуумі, Подальше очищення в FCC Подальшу спробу очищення FCC елююванням 0-20 % 2М метанольним аміаком в CH2Cl2 та подальше очищення FCC елююванням 0-20 % CH3OH в CH2Cl2 дало коричневу камедь. РХМС ще показав наявність домішок. Подальшу спробу очищення FCC робили елююванням 0-20 % CH3OH в CH2Cl2, Придатні фракції концентрували, що дало коричневу камедь, яка містить сполуку заголовну Спроби переробити цю камедь до твердого стану розтиранням до порошку були невдалими Ліофілізація з CH3CN/вода також були невдалими, але ліофілізація з CH 3OH/вода коричневу напівтверду речовину. Розтирання її з диетилетером, а потім випаровування етеру дало 1 заголовну сполуку (191 мг, 32 %) як світлу жовту сипучу тверду сполуку; H ЯМР: (CDCl3) 2,28 (6H, s), 2,32 (2H, t), 2,71 (3H, s), 2,84-2,92 (2H, m), 3,87 (3H, s), 5,67 (1H, dd), 6,29 (1H, dd), 6,37 (1H, dd), 6,80 (1H, s), 6,89 (1H, td), 7,23-7,33 (1H, m), 7,46 (1H, s), 8,45 (1H, s), 8,52 (1H, d), 8,56 + + (1H, d), 8,94 (1H, s), 9,39 (1H, s), 10,09 (1H, s); m/z: ES MH 521,29. Приклад 7: N-{2-[(3aR, 6aR)-5-Метил-2,3,3a, 4,6,6a-гексагідропіролo[3,2-c]пірол-1-іл]-5-[(5хлоро-4-піразоло[1,5-a]піридин-3-ілпіримідин-2-іл)аміно]-4-метоксифеніл}проп-2-енамід Акрилоілхлорид (1M в ТГФ, 0,225 мл, 0,22 ммол) в CH2Cl2 (1 мл) додавали краплями до суміші 4-[(3aR, 6aR)-5-метил-2,3,3a, 4,6,6a-гексагідропіролo[3,2-c]пірол-1-іл]-N-(5-хлоро-4піразоло[1,5-a]піридин-3-ілпіримідин-2-іл)-6-метоксибензол-1,3-діаміну (проміжна сполука 35, 105 мг, 0,21 ммол) та DIPEA (0,041 мл, 0,24 ммол) в CH2Cl2 (3 мл), який охолоджували в бані лід/вода. Суміш перемішували протягом 0,5h, промивали розсолом і тоді концентрували у вакуумі. Очищення FCC, елюювання 0-2,5 % 7N метанольним аміаком в CH2Cl2 дало заголовну 1 сполуку (60 мг, 52 %) як світлу жовту тверду речовину; H ЯМР: 1,77-1,81 (1H, m), 1,95-2,16 (5H, m), 2,24-2,35 (1H, m), 2,38-2,48 (1H, m), 2,86-2,90 (1H, m), 3,18-3,22 (1H, m), 3,37-3,45 (1H, m), 3,76 (3H, s), 4,33-4,37 (1H, m), 5,68 (1H, dd), 6,18 (1H, dd), 6,51 (1H, dd), 6,66 (1H, s), 7,10 (1H, dt), 7,33-7,41 (1H, m), 7,65 (1H, s), 8,3-8,4 (2H, m), 8,56 (1H, s), 8,81 (1H, d), 8,94 (1H, s), 9,38 (1H, s); + + m/z: ES , MH 545,57. Приклад 8: N-{5-[(5-Хлоро-4-піразоло[1,5-a]піридин-3-ілпіримідин-2-іл)аміно]-4-метокси-2-[5метил-2,5-діазаспіро[3,4]октан-2-іл]феніл}проп-2-енамід Розчин акрилоілхлориду (5,71 мг, 0,06 ммол) в CH2Cl2 (1 мл) додавали краплями до суміші N'-(5-хлоро-4-піразоло[1,5-a]піридин-3-ілпіримідин-2-іл)-4-метокси-6-(5-метил-2,5діазаспіро[3,4]октан-2-іл)бензол-1,3-діамін (проміжна сполука 45, 31 мг, 0,06 ммол) в CH2Cl2 (5 мл), який охолоджували в бані лід/вода. Суміш перемішували протягом 3 год. і тоді промивали розсолом, сушили (Na2SO4) та концентрували у вакуумі. Очищення FCC, елюювання 0-2 % 7N 1 метанольним аміаком в CH2Cl2 дало заголовну сполуку (21 мг, 61 %) як жовту піну; H ЯМР: 1,70 (2H, dd), 1,98-2,11 (2H, m), 2,37 (3H, s), 2,62 (2H, t), 3,65 (2H, d), 3,76 (3H, s), 3,95 (2H, d), 5,67 (1H, d), 6,09-6,27 (2H, m), 6,43 (1H, dd), 7,10 (1H, t), 7,30 (1H, s), 7,34-7,45 (1H, m), 8,35 (2H, s), + + 8,44 (1H, s), 8,81 (1H, d), 8,92 (1H, s), 9,20 (1H, s); m/z: ES MH 545,5. Приклад 9: N-{5-[(5-Хлоро-4-піразоло[1,5-a]піридин-3-ілпіримідин-2-іл)аміно]-4-метокси-2-[1метил-3,6-дигідро-2H-піридин-4-іл]феніл}проп-2-енамід Розчин акрилоілхлориду (0,026 мл, 0,32 ммол) в CH 2Cl2 (1 мл) додавали краплями до суміші N'-(5-хлоро-4-піразоло[1,5-a]піридин-3-ілпіримідин-2-іл)-4-метокси-6-(1-метил-3,6-дигідро-2Hпіридин-4-іл)бензол-1,3-діаміну (проміжна сполука 55, 150 мг, 0,32 ммол) та DIPEA (0,062 мл, 0,36 ммол) в CH2Cl2 (5 мл), який охолоджували в бані лід/вода. Суміш перемішували протягом 3 год. і тоді промивали розсолом, сушили (Na2SO4) та концентрували у вакуумі. Очищення FCC, елюювання 2,5 % 7N метанольним аміаком в CH 2Cl2 дало заголовну сполуку (120 мг, 72 %) як 1 жовту піну; H ЯМР: 2,28 (3H, s), 2,38 (2H, s), 2,54 (2H, t), 2,98 (2H, d), 3,81 (3H, s), 5,62-5,73 (2H, m), 6,14 (1H, dd), 6,43 (1H, dd), 6,88 (1H, s), 7,12 (1H, dt), 7,39-7,47 (1H, m), 7,83 (1H, s), 8,41-8,50 + + (2H, m), 8,63 (1H, s), 8,85 (1H, d), 8,95 (1H, s), 9,36 (1H, s); m/z: ES MH 516,25. Приклад 10: N-{5-[(5-Хлоро-4-піразоло[1,5-a]піридин-3-ілпіримідин-2-іл)аміно]-2-[4-(2диметиламіно-2-оксоетил)піперазин-1-іл]-4-метоксифеніл}проп-2-енамід Розчин акрилоілхлориду (0,030 мл, 0,37 ммол) в CH 2Cl2 (1 мл) додавали краплями до перемішуваного розчину 2-(4-{2-аміно-4-[(5-хлоро-4-піразоло[1,5-a]піридин-3-ілпіримідин-2іл)аміно]-5-метоксифеніл}піперазин-1-іл)-N,N-диметилацетаміду (проміжна сполука 57, 0,19 г, 0,35 ммол) та DIPEA (0,067 мл, 0,39 ммол) в CH 2Cl2 (5 мл). Суміш перемішували протягом 0,5 год., тоді розбавляли CH2Cl2 (20 мл) та промивали насич. розсолом (2 × 25 мл). Органічний розчин сушили (MgSO4), та концентрували у вакуумі. Очищення FCC, елюювання 5 % CH3OH в 1 CH2Cl2 дало заголовну сполуку (0,157 г, 75 %) як жовту тверду речовину; H ЯМР: (CDCl3) 2,76 27 UA 106710 C2 5 10 15 20 25 30 35 40 45 50 55 (4H, s), 2,90-2,96 (4H, m), 2,98 (3H, s), 3,12 (3H, s), 3,30 (2H, s), 3,87 (3H, s), 5,65-5,77 (1H, m), 6,18-6,37 (2H, m), 6,80 (1H, s), 6,90 (1H, t), 7,28 (1H, d), 7,42 (1H, s), 8,44 (1H, s), 8,46-8,59 (3H, + + m), 8,93 (1H, s), 9,33 (1H, s); m/z: ES MH 590,52. Приклад 11: (S)-N-{2-[4-(2-Амінопропаноіл)піперазин-1-іл]-5-[(5-хлоро-4-піразоло[1,5a]піридин-3-ілпіримідин-2-іл)аміно]-4-метоксифеніл}проп-2-енамід Розчин акрилоілхлориду (10,2 мкл, 0,13 ммол) в CH 2Cl2 (3 мл) додавали краплями до перемішуваного розчину (S)-трет-бутил N-[1-(4-{2-аміно-4-[(5-хлоро-4-піразоло[1,5-a]піридин-3ілпіримідин-2-іл)аміно]-5-метоксифеніл}піперазин-1-іл)-1-оксопропан-2-іл]карбамату (проміжна сполука 59, 65 мг) та DIPEA (0,75 мл) в CH2Cl2 (10 мл), який охолоджували в бані лід/вода. Суміш перемішували протягом 0,75 год. тоді гасили водою (10 мл) та 2M Na 2CO3 (5 мл). Фази відокремлювали та органічний розчин сушили (MgSO 4) та концентрували у вакуумі. Отриманий залишок розчиняли в CH2Cl2 (3 мл) та толі обробляли ТФОК (0,1 мл). Після стояння протягом 0,25 год. додавали. другу порцію ТФОК (0,2 мл). Після подальших 0,25 год. розчин концентрували у вакуумі та очищали препаративною ВЕРХ (колонка Waters SunFire, 5 мк діоксид силіцію, 19 мм діаметр, 100 мм довжина), елюювання зниженими полярними сумішами води (яка містить 0,1 % мурашиної кислоти) та CH3CN. Фракції, які містять бажану сполуку концентрували у вакуумі, що дало заголовну сполуку (17 мг, 6 % від 5-хлоро-N-(4-флуоро-2метокси-5-нітрофеніл)-4-піразоло[1,5-a]піридин-3-ілпіримідин-2-аміну) як білу тверду речовину; 1 H ЯМР: 1,25 (3H, s), 2,83-2,96 (4H, m), 3,65-3,82 (7H, m), 4,14-4,23 (1H, m), 5,73 (1H, d), 61,9 (1H, d), 6,64-6,70 (1H, m), 6,69 (1H, s), 7,08-7,12 (1H, m) 7,30-7,37 (1H, m), 8,20-8,28 (2H, m), 8,35-8,41 + + (2H, m), 8,68 (1H, s), 8,80-8,84 (1H, m), 8,95 (1H, s), 9,11-9,15 (1H, m); m/z: ES MH 576,60. Приклад 12: N-{5-[(5-Хлоро-4-піразоло[1,5-a]піридин-3-ілпіримідин-2-іл)аміно]-2-[(3S)-3диметиламінопіролідин-1-іл]-4-метоксифеніл}проп-2-енамід Розчин акрилоілхлориду (0,042 мл, 0,52 ммол) в CH 2Cl2 (1 мл) додавали краплями до суміші 1 (S)-N -[5-хлоро-4-(піразоло[1,5-a]піридин-3-іл)піримідин-2-іл]-4-[3-(диметиламіно)піролідин-1-іл]6-метоксибензол-1,3-діаміну (проміжна сполука 61, 250 мг, 0,52 ммол) та DIPEA (0,099 мл, 0,57 ммол) в CH2Cl2 (5 мл), яку охолоджували в бані лід/вода. Суміш перемішували протягом 3 год. і тоді промивали розсолом, сушили (Na2SO4) та концентрували у вакуумі. Очищення FCC, елюювання 2 % 7N метанольним аміаком в CH2Cl2 дало заголовну сполуку (194 мг, 70 %) як 1 жовту тверду речовину; H ЯМР: 1,69-1,83 (1H, m), 2,05-2,16 (1H, m), 2,19 (6H, s), 2,65-2,78 (1H, m), 3,18-3,29 (3H, m), 3,35-3,46 (1H, m), 3,77 (3H, s), 5,67 (1H, dd), 6,16 (1H, dd), 6,48 (1H, dd), 6,54 (1H, s), 7,12 (1H, t), 7,37 (1H, t), 7,43 (1H, s), 8,3-8,46 (2H, m), 8,55 (1H, s), 8,83 (1H, d), 8,94 + + (1H, s), 9,37 (1H, s); m/z: ES MH 533,5. Приклад 13: N-{5-[(5-Хлоро-4-піразоло[1,5-a]піридин-3-ілпіримідин-2-іл)аміно]-4-метокси-2-[4метилпіперазин-1-іл]феніл}проп-2-енамід Розчин акрилоілхлориду (0,092 мл, 1,14 ммол) в CH 2Cl2 (1 мл) додавали краплями до суміші N'-(5-хлоро-4-піразоло[1,5-a]піридин-3-ілпіримідин-2-іл)-4-метокси-6-(4-метилпіперазин-1іл)бензол-1,3-діамін (проміжна сполука 63, 480 мг, 1,03 ммол) та DIPEA (0,214 мл, 1,24 ммол) в CH2Cl2 (18 мл) при к.т. Після 0,25 год., додавали додатковий акрилоілхлорид (15 мг в 0,15 мл CH2Cl2). Суміш перемішували протягом 0,5 год. і тоді промивали розсолом, сушили (Na 2SO4) та концентрували у вакуумі. Очищення FCC, елюювання 2,5 % 7N метанольним аміаком в CH2Cl2 дало заголовну сполуку (390 мг, 73 %) як жовту тверду речовину після розтирання до порошку з 1 CH3OH; H ЯМР: 2,27 (3H, s), 2,53-2,61 (4H, m), 2,84-2,97 (4H, m), 3,77 (3H, s), 5,70 (1H, d), 6,17 (1H, d), 6,61 (1H, dd), 6,89 (1H, s), 7,11 (1H, t), 7,3-7,42 (1H, m), 8,10 (1H, s), 8,26-8,47 (2H, m), + + 8,70 (1H, s), 8,83 (1H, d), 8,96 (1H, s), 9,02 (1H, s); m/z: ES MH 519. Приклад 14: N-{5-[(5-Ціано-4-піразоло[1,5-a]піридин-3-ілпіримідин-2-іл)аміно]-4-метокси-2-[4метилпіперазин-1-іл]феніл}проп-2-енамід Розчин акрилоілхлориду (0,017 мл, 0,21 ммол) в CH 2Cl2 (0,6 мл) додавали до суміші 2-{[5аміно-2-метокси-4-(4-метилпіперазин-1-іл)феніл]аміно}-4-піразоло[1,5-a]піридин-3-ілпіримідин-5карбонітрилу (проміжна сполука 65, 87 мг, 0,19 ммол) та DIPEA (0,063 мл, 0,38 ммол) в CH 2Cl2 (1,5 мл) при 0 °C. Суміш тоді перемішували при 0 °C протягом 4 год. (протягом цього часу далі додавали 0,5 екв. акрилоілхлориду). Суміш тоді розбавляли CH 2Cl2, промивали двічі насич. NaHCO3, тоді − водою і тоді сушили (MgSO4). Очищення FCC, елюювання 0-6 % метанольним 1 аміаком в CH2Cl2 дало заголовну сполуку (67 мг, 69 %) як жовту тверду речовину; H ЯМР: (102 °C) 2,30 (3H, s), 2,56-2,59 (4H, m), 2,93-2,96 (4H, m), 3,78 (3H, s), 5,67-5,7 (1H, m), 6,16 (1H, d), 6,44-6,51 (1H, m), 6,95 (1H, s), 7,11 (1H, t), 7,35 (1H, t), 8,20 (1H, s), 8,32 (1H, d), 8,66 (1H, s), + + 8,72 (1H, br s), 8,76 (1H, d), 8,91 (1H, s), 8,96 (1H, br s); m/z: ES MH 510,5. Приклад 15: N-(5-{[4-(1H-індол-3-іл)піримідин-2-іл]аміно}-4-метокси-2-{4-метилпіперазин-1іл}феніл)проп-2-енамід 28
ДивитисяДодаткова інформація
Автори англійськоюButterworth, Sam, Finlay, Maurice, Raymond, Verchoyle, Ward, Richard, Andrew, Kadambar, Vasantha, Krishna, Chintakuntla, Chandrasekhara, Reddy, Murugan, Andiappan, Redfearn,Heather, Marie, Chuaqui, Claudio Edmundo
Автори російськоюБаттерворс Сем, Финли Маурис Реймонд Вершоил, Ворд Ричард Ендрю, Кадамбар Васанта Кришна, Чинтакунтла Чандрасекхара Редди, Муруган Андиппан, Редфеарн Хизер Мери, Чуакуй Клаудио Эдмундо
МПК / Мітки
МПК: A61K 31/506, A61P 35/00, C07D 401/02, C07D 471/04, A61K 31/437
Мітки: сполука, застосування, лікування, анілінопіримідину, 2-(2,4,5-заміщеного, раку
Код посилання
<a href="https://ua.patents.su/96-106710-spoluka-2-245-zamishhenogo-anilinopirimidinu-ta-zastosuvannya-dlya-likuvannya-raku.html" target="_blank" rel="follow" title="База патентів України">Сполука 2-(2,4,5-заміщеного аніліно)піримідину та її застосування для лікування раку</a>
Попередній патент: Спосіб одержання біметалевих наночастинок паладій-золото
Наступний патент: З’єднувач для механічного стикування конвеєрних стрічок
Випадковий патент: Пристрій для вимірювання податливості слизової оболонки ротової порожнини