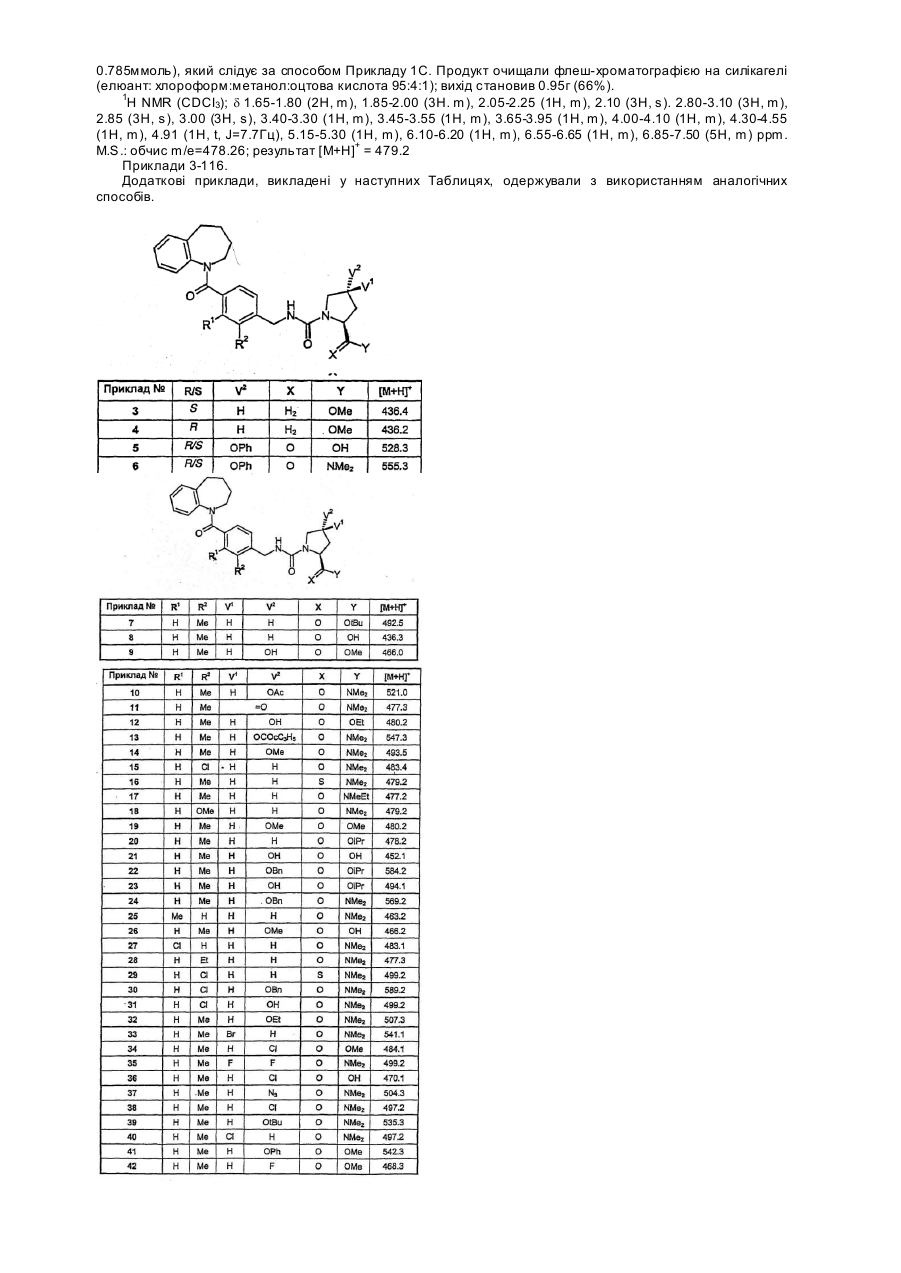
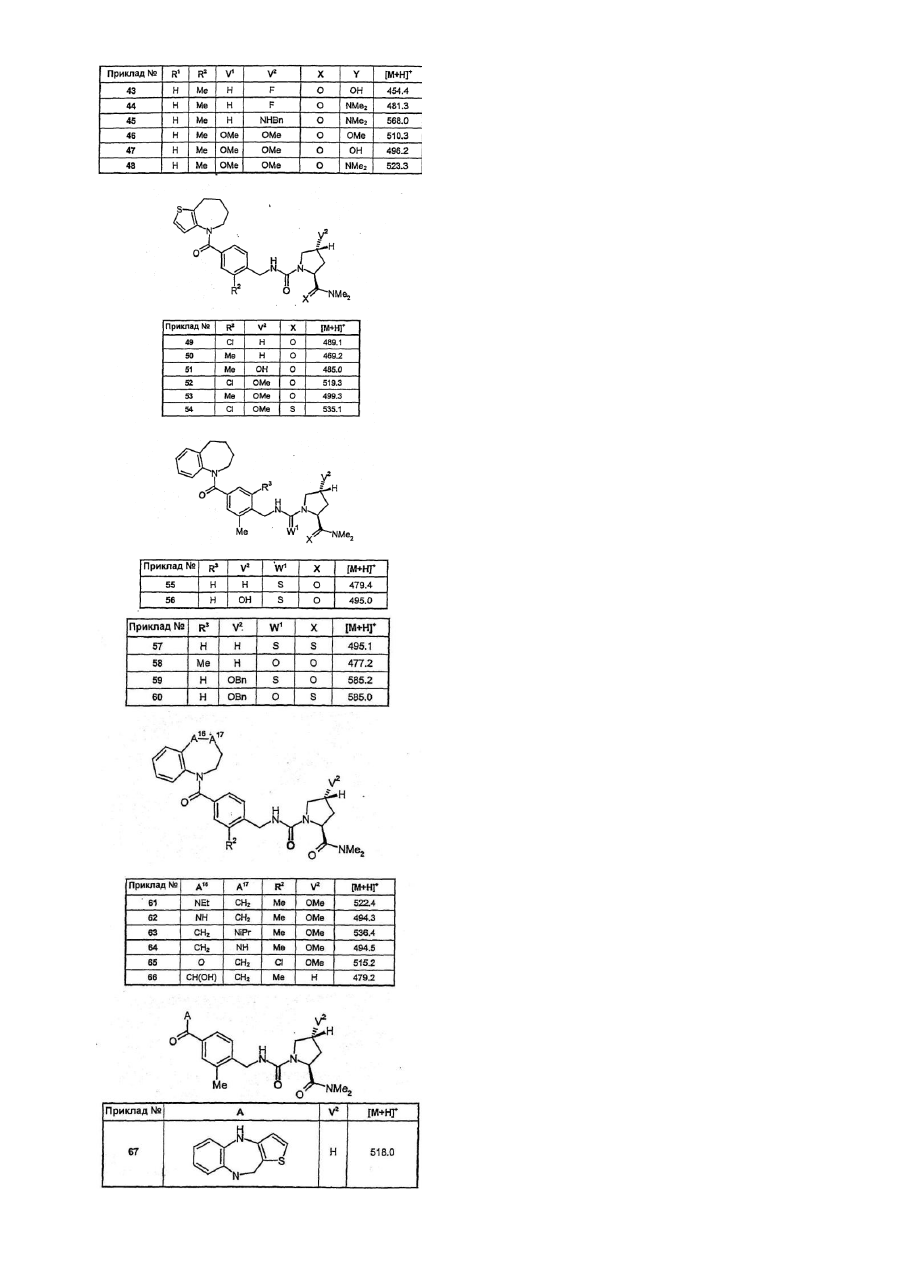
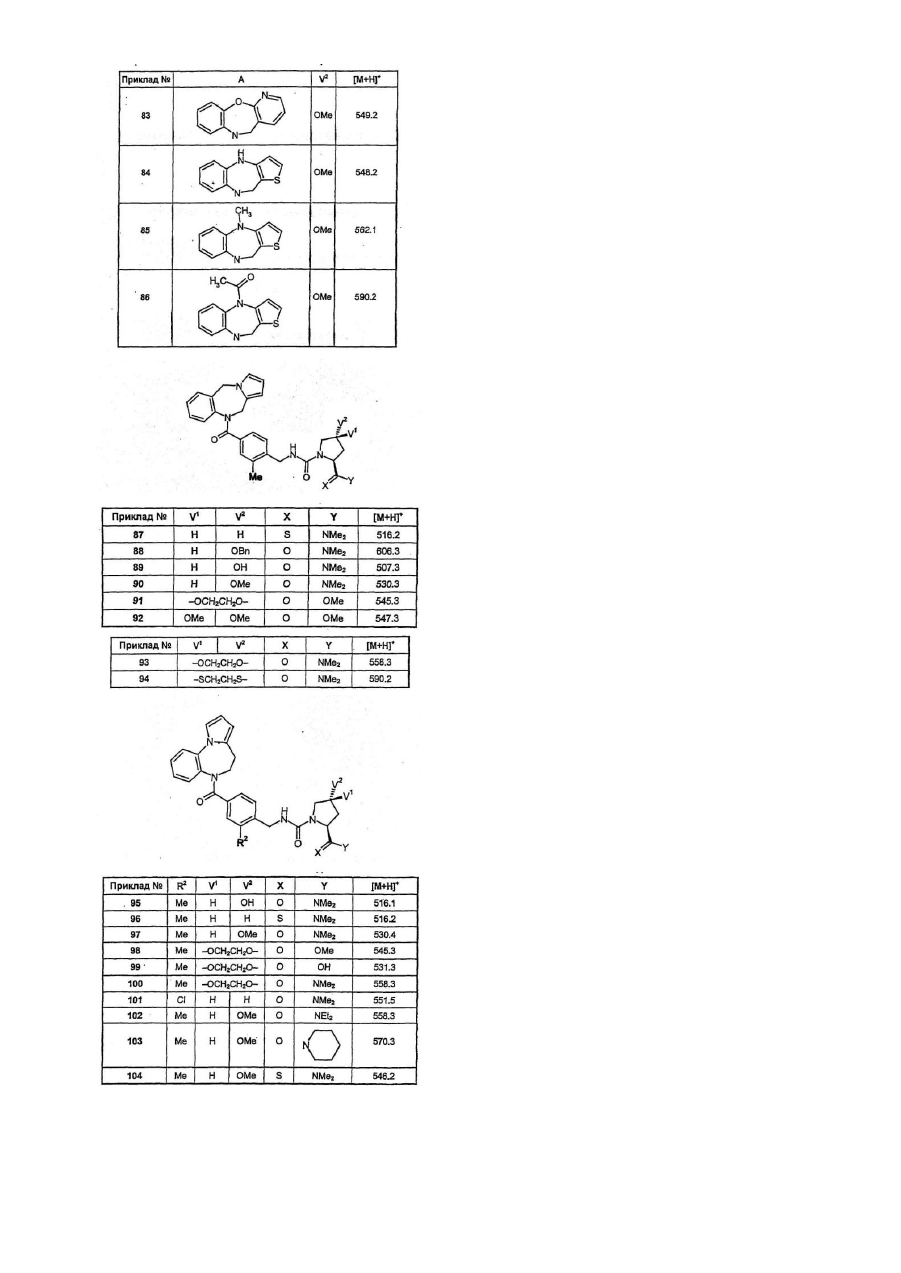
Конденсовані азепіни як агоністи вазопресину
Номер патенту: 73152
Опубліковано: 15.06.2005
Автори: Пітт Гарі Роберт Уільям, Ешворт Дорін Мері, Йі Крістофер Мартін, Хадсон Пітер, Франклін Річард Джеремі
Формула / Реферат
1. Сполука згідно із загальною формулою 1 або її фармацевтично прийнятна сіль,
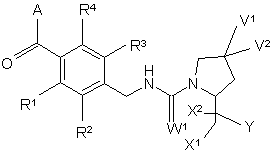 , 1
, 1
у якій:
А є біциклічною або трициклічною похідною азепіну, вибраною із загальних формул 2 - 7
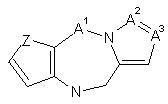 , 2
, 2 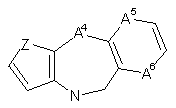 , 3
, 3 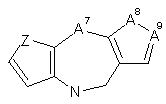 , 4
, 4
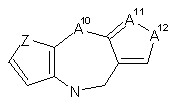 , 5
, 5 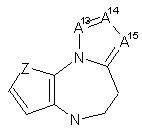 , 6
, 6 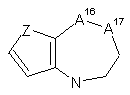 , 7
, 7
де A1, A4, A7 або А10 кожен незалежно вибраний з СН2, О та NR8;
А2, А3, А9, А11, А13, А14 та А15 кожен незалежно вибраний з СН та N;
або А5 є ковалентним зв'язком, а А6 - S, або А5 є N=CH, а А6 є ковалентним зв'язком;
А8 та А12 кожен незалежно вибраний з NH та S;
обидва А16 та А17 є СН2, або один з А16 та А17 є СН2, а інший вибраний з СН(ОН), CF2, О, SOx та NR8,
обидва V1 та V2 є Н, ОМе або F, або один з V1 та V2 є ОН, ОМе, OBn, OPh, О-ацилом, Вr, Сl, F, N3, NH2, NHBn або NH-ацилом, а інший є Н, або V1 та V2 разом є =О, -S(СН2)рS- або -O(СН2)рО-;
W1 є або О або S;
обидва X1 та X2 є Н або разом є =О або =S;
Y є OR5 або NR6R7;
Z є S або -СН=СН-;
R1, R2, R3 та R4 кожен незалежно вибраний з Н, нижчого алкілу, нижчого алкілокси, F, Сl та Вr;
R5 вибраний з Н та нижчого алкілу;
R6 та R7 незалежно вибрані з Н та нижчого алкілу або разом є -(СН2)n-;
R8 є Н або нижчим алкілом;
n = 3, 4, 5 або 6;
р = 2 або 3; і х є 0, 1 або 2.
2. Сполука за п. 1 або її фармацевтично прийнятна сіль, у якій А є група згідно із загальною формулою 2.
3. Сполука за п. 1 або її фармацевтично прийнятна сіль, у якій А є групою згідно із загальною формулою 3.
4. Сполука за п. 1 або її фармацевтично прийнятна сіль, у якій А є групою згідно із загальною формулою 4.
5. Сполука за п. 1 або її фармацевтично прийнятна сіль, у якій А є групою згідно із загальною формулою 5.
6. Сполука за п. 1 або її фармацевтично прийнятна сіль, у якій А є групою згідно із загальною формулою 6.
7. Сполука за п. 1 або її фармацевтично прийнятна сіль, у якій А є групою згідно із загальною формулою 7.
8. Сполука за п. 1 або 7 або її фармацевтично прийнятна сіль, у якій А є групою згідно із загальною формулою 7, Z є -СН=СН- і обидва А16 та А17 є -CH2-.
9. Сполука за будь-яким із пп. 1 - 8 або її фармацевтично прийнятна сіль, у якій один із R1 та R2 є Сl або Me, а інший є Н і обидва R3 та R4 є Н.
10. Сполука за будь-яким із пп. 1 - 9 або її фармацевтично прийнятна сіль, у якій один з V1 та V2 є ОМе або ОВn, а інший є Н.
11. Сполука за будь-яким із пп. 1 - 10 або її фармацевтично прийнятна сіль, у якій X1 та X2 разом є =O, a Y є NR6R7.
12. Сполука за будь-яким із пп. 1 або 7 - 11 або її фармацевтично прийнятна сіль, яка є
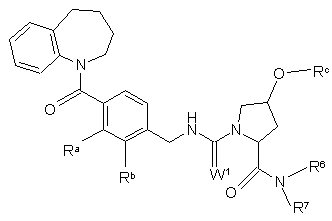 ,
,
де W1 є або О або S;
один з Ra та Rb є Сl або метилом, а інший є Н;
Rc є метилом або бензилом;
R6 та R7 незалежно вибрані з Н та нижчого алкілу або разом є -(СН2)n-, а n дорівнює 3, 4, 5 або 6.
13. Сполука за будь-яким із пп. 1 або 7 - 12 або її фармацевтично прийнятна сіль, яка є
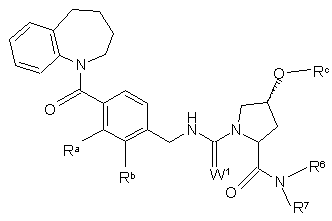 ,
,
де W1 є або О або S;
один з Ra та Rb є Сl або метилом, а інший є Н;
Rc є метилом або бензилом; і
R6 та R7 незалежно вибрані з Н та нижчого алкілу або разом є -(СН2)n-; і
n дорівнює 3, 4, 5 або 6.
14. Сполука за будь-яким із пп. 1 - 9 або її фармацевтично прийнятна сіль, у якій обидва V1 та V2 є Н.
15. Сполука за п. 14 або її фармацевтично прийнятна сіль, у якій X1 та X2 разом є =О, a Y є NR6R7.
16. Сполука за будь-яким із пп. 1 або 7 - 9 або 14, або 15, або її фармацевтично прийнятна сіль, яка є
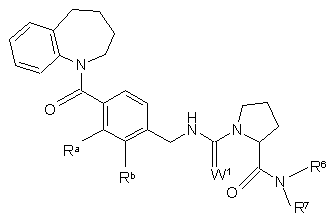 ,
,
де W1 є або О або S;
один із Ra та Rb є Сl або метилом, а інший є Н;
R6 та R7 незалежно вибрані з Н та нижчого алкілу або разом є -(СН2)n-; і n дорівнює 3, 4, 5 або 6.
17. Сполука за будь-яким із пп. 1 або 7 – 9, або 14 - 16, або її фармацевтично прийнятна сіль, яка є
 ,
,
де W1 є або О або S;
один з Ra та Rb є Сl або метилом, а інший є Н;
R6 та R7 незалежно вибрані з Н та нижчого алкілу або разом є -(СН2)n-; і
n дорівнює 3, 4, 5 або 6.
18. Сполука за будь-яким з попередніх пунктів, яка вибрана з
1-(2-метил-4-(2,3,4,5-тетрагідро-1-бензазепін-1-ілкарбоніл)бензилкарбамоїл)-L-пролін-N,N-диметиламіду,
(4R)-4-гідрокси-1-(2-метил-4-(2,3,4,5-тетрагідро-1-бензазепін-1-ілкарбоніл)бензилкарбамоїл)-L-пролін-N,N-диметиламіду,
(4R)-1-(3-хлор-4-(2,3,4,5-тетрагідро-1-бензазепін-1-ілкарбоніл)бензилкарбамоїл)-4-метокси-L-пролін-N,N-диметиламіду,
(4R)-1-(2-хлор-4-(2,3,4,5-тетрагідро-1-бензазепін-1-ілкарбоніл)бензилкарбамоїл)-4-метокси-L-пролін-N,N-диметиламіду,
(4R)-4-бензилокси-1-(2-метил-4-(2,3,4,5-тетрагідро-1-бензазепін-1-ілкарбоніл)бензилкарбамоїл)-L-пролін-N,N-диметиламіду,
(4R)-4-метокси-1-(2-метил-4-(2,3,4,5-тетрагідро-1-бензазепін-1-ілкарбоніл)бензилкарбамоїл)-L-пролін-N,N-диметиламіду,
(4R)-4-метокси-1-(3-метил-4-(2,3,4,5-тетрагідро-1-бензазепін-1-ілкарбоніл)бензилкарбамоїл)-L-пролін-N,N-диметиламіду,
(4R)-1-(2-хлор-4-(5,6,7,8-тетрагідро-4Н-тієно[3,2-b]азепін-4-ілкарбоніл)бензилкарбамоїл)-4-метокси-L-пролін-N,N-диметиламіду,
(4R)-1-(4-(10,11-дигідро-5Н-піроло[2,1-с](1,4)бензодіазепін-10-ілкарбоніл)-2-метил-бензилкарбамоїл)-4-метокси-L-пролін-N,N-диметиламіду,
(4R)-1-(2-хлор-4-(10,11-дигідро-5Н-піроло[2,1-с](1,4)бензодіазепін-10-ілкарбоніл)-бензилкарбамоїл)-4-метокси-L-пролін-N,N-диметиламіду та
(4R)-1-(4-(10,11-дигідро-5Н-піроло[2,1-с](1,4)бензодіазепін-10-ілкарбоніл)-2-метил-бензилкарбамоїл)-4-метокси-L-пролін-N,N-диметилтіоаміду
або її фармацевтично прийнятної солі.
19. Фармацевтична композиція, яка містить активний агент, вибраний зі сполук та фармацевтично прийнятних солей за будь-яким із пп. 1 - 18.
20. Фармацевтична композиція за п. 19, яка призначена для лікування поліурії.
21. Фармацевтична композиція за п. 19, яка призначена для регулювання нетримання сечі.
22. Фармацевтична композиція за п. 19, яка призначена для затримки спорожнення.
23. Фармацевтична композиція за п. 19, яка призначена для лікування кровотеч.
24. Спосіб лікування нічного енурезу, ніктурії та центрального нецукрового діабету, при якому особі, що потребує такого лікування, призначають ефективну кількість композиції за п. 19.
25. Спосіб регулювання нетримання сечі, при якому особі, що потребує такого лікування, призначають ефективну кількість композиції за п. 19.
26. Спосіб лікування за п. 25, у якому лікування призводить до затримки спорожнення.
27. Спосіб лікування кровотеч, при якому особі, що потребує такого лікування, призначають ефективну кількість композиції за п. 19.
Текст
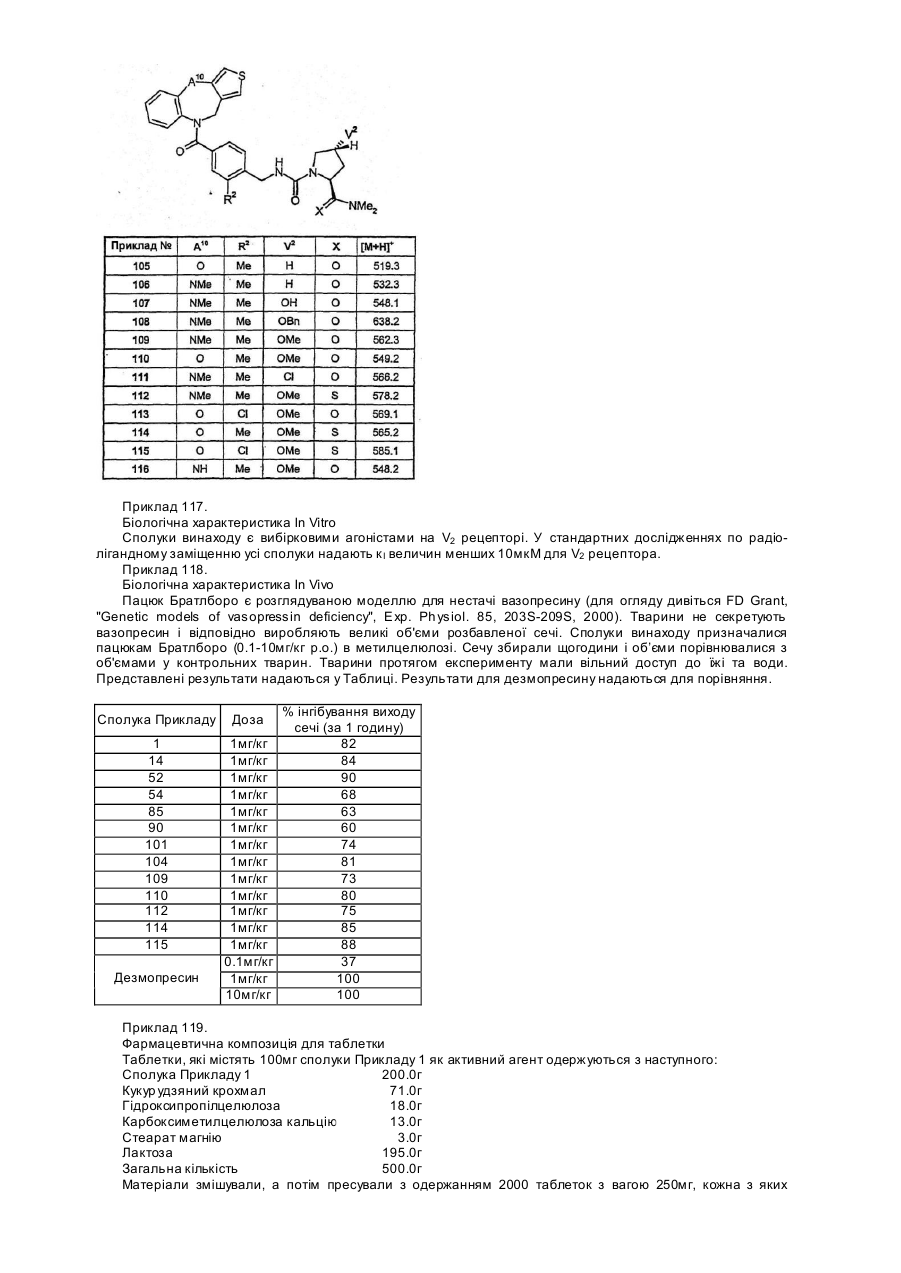
Представлений винахід стосується класу нових хімічних сполук, які діють як агоністи пептидного гормонного вазопресину. Вони зменшують вихід сечі з нирок і, таким чином, є корисними у лікуванні деяких людських захворювань, які характеризуються поліурією. Вони також корисні у регулюванні нетримання сечі та кровотечах. Вазопресин є пептидним гормоном, секретованим нейрогіпофізом. Він діє на нирку з підсиленням затримки води і, таким чином, зменшує вихід сечі. З цієї причини вазопресин, з іншого боку, відомий як "антидіуретичний гормон". Він також діє на судинну сітку, де він створює гіпертензійний ефект. Клітинні рецептори, що опосередковують ці дві дії, о характеризовані та відображені як відмінні. Антидіуретична дія опосередковується вазопресиновим рецептором типу 2, зазвичай названому V2 рецептором. Агенти, що можуть взаємодіяти з V2 рецептором та активують його тим же шляхом що й вазопресин називаються агоністами V2 рецептора (або просто V2 агоністами). Такі агенти будуть мати антидіуретичну дію. Якщо ці агенти вибірково взаємодіють з V2 рецептором і не взаємодіють з іншими підтипами вазопресинового рецептора, то вони не будуть мати вазопресинового гіпертензійного ефекту. Це повинно бути важливим з точки зору безпеки і повинно робить такі агенти привабливими для лікування станів людської хвороби, яка характеризується поліурією (що взято тут для позначення непомірного виділення сечі). Насправді такий агент вже застосовується у людській терапії. Дезмопресин (інакше кажучи [1-дезаміно, О-Аrg8 ]вазопресин, Minirin™, DDAVP™) є пептидним аналогом вазопресину, який вибірково є агоністом на V2 рецепторі. Він використовується у лікуванні центрального нецукрового діабету, який є станом, що є результатом недостатньої секреції вазопресину. Він також використовується у регулюванні нічного енурезу і може також використовува тися у регулюванні ніктурії. Тим не менше, в усіх відношеннях дезмопресин не є ідеальним агентом. Навіть найкращий поточний синтез агенту є дуже довгим і дезмопресин не піддається найбільш зручним способам очищення, як наприклад кристалізації. Відповідно, дезмопресин є відносно дорогим. Він має дуже низьку пероральну біологічну придатність і існує деяка непостійність у цьому параметрі. Окрім цього, тут повсюдно існує потреба у вибірковому агоністі вазопресинового V2 рецептора, який легко одержати та очистити і, що має високу та передбачувану пероральну біологічну придатність. Такі властивості найкраще досягаються з непептидною сполукою. Ці роздуми привели інші групи до дослідження непептидних вазопресинових V2 агоністів і їх результати розкриваються , наприклад, у міжнародних заявках на патент WO97/22591, WO99/06403, WO99/06409, WO00/46224. WO00/46225, WO00/46227 та WO00/46228. Сполуки, розкриті у цих документах є, тим не менше, менш ніж ідеальними. Зокрема, вони мають слабку пероральну біологічну придатність, можливо частково завдяки їх низькій водній розчинності. Представлений винахід надає сполуки з покращеною розчинністю та біологічною придатністю. Окрім їх антидіуретични х дій дезмопресин використовується для підвищення концентрації коагуляційних протеїнів у крові, відомих як Фактор VIII та фактор фон Вілебранда. В клінічному контексті це робить дезмопресин корисним у лікуванні гемофілії А та хвороби фон Вілебранда. Подібні застосування повинні бути загальнодоступними для непептидних агоністів представленого винаходу. Як тут розкрито, представлений винахід стосується серій сполук, що є непептидними агоністами вазопресину і, які є вибірковими для підтипу V2 рецептора. Сполуки описуються загальною формулою 1 у якій: А є біциклічною або трициклічною похідною азепіну, вибраною із загальних формул 2-7 А1 , А4, А7 та А10 кожен незалежно вибраний серед СН2, О та NR8; А2 , А3, А9, А11 , А13, А14 та А15 кожен незалежно вибраний серед СН та N; або А5 є ковалентним зв’язком, а А6 є S, або А5 є N=CH, а А6 є ковалентним зв'язком; А8 та А12 кожен незалежно вибраний серед NH та S; Обидва А16 та А17 є СН 2, або один з А16 та А17 є СН2 , а інший вибраний серед О, SO x тa NR8, Обидва V1 та V2 є Н, ОМе або F, або один з V1 та V2 є Вr, СІ, F, OH, OMe, OBn, OPh, О-ацилом, N3, NH2, NHBn або NH-ацилом, а інший є Н, або V1 та V2 разом є =O, -О(СН 2)Р О- або -S(CH2)PS-; W1 є або О або S; Обидва X1 та X2 є Н або разом є =O або =S; Y є OR5 або NR6R7; Z є S або -СН=СН-; R1, R2, R3 та R4 незалежно вибрані серед Н, нижчого алкілу, нижчого алкілокси, F, СІ та Вr, R5 вибраний серед Н та нижчого алкілу; R6 та R7 незалежно вибрані серед Н та нижчого алкілу або разом є -(СН2)n-; R8 є Н або нижчим алкілом; n=3, 4, 5 або 6; р дорівнює 2 або 3; а х дорівнює 0, 1 або 2. Окрім цього, винахід включає фармацевтичні композиції, які містять у собі ці вазопресинові агоністи, композиції, які особливо корисні у лікуванні центрального нецукрового діабету, нічного енурезу та ніктурії. Представлений винахід включає похідні N-бензилкарбаміл піролідину, визначені загальною формулою 1. У цій формулі, А представляє біциклічну або трициклічну азепінову групу згідно з однією із загальних формул 2-7. А1 , А4 , А7 та А10 представляють двовалентні групи, вибрані серед метилену (-СН2-), кисню (-О-) та заміщеного азоту (-NR8-). А2 , А3, А9, А11 , А13, А14 та А15 представляють або атом азоту (-N=) або метанову груп у (-СН=). А5 може представляти ковалентний зв'язок, у випадку якого А6 представляє атом сірки (-S-) так, що кільце, яке містить ці дві групи є тіофеновим кільцем. Альтернативно, А5 може представляти групу N=CH-, у випадку якої А6 представляє ковалентний зв'язок так, що кільце, яке містить ці дві групи є піридиновим кільцем. А8 та А12 представляють або -NH- або атом сірки (-S-). А16 та А17 представляють двовалентні групи. Обидва можуть бути метиленовими групами (-СН2- ) або один є . метиленовою групою, а інший вибраний серед гідроксиметилену (-СН(ОН)-), дифторметилену (-CF2-), кисню (-О-), заміщеного азоту (-NR8-) та сірки або окисленої сірки (-S-, -SO-, або -SO2-). Обидва V та V2 можуть бути воднем, метокси або фтором, або один може бути вибраним серед брому, хлору, фтору, гідрокси, нижчого алкокси, бензилокси, фенокси, ацилокси, азидо, аміно, бензиламіно та ациламіду (Вr, СІ, F, ОН, О-нижчого алкілу, OBn, OPh, Оацилу, NH2, NHBn та NH-ацилу), забезпечуючи те, що інший є воднем, або V1 та V2 разом можуть представляти атом кисню так, що фрагмент CV1 V2 є карбонільною групою (С =О). V1 та V2 можуть також бути е тиленом або пропілендіокси або дитіовим ланцюгом (-О(СН2)2О-, -О(СН2) 3О-, -S(CH 2)2S-, -S(CH2)3S-) так, що C V1 V2 є 1,3-діоксоланом, 1,3-діоксаном, 1,3-дитіоланом або 1,3 дитіановим кільцем. W1 є або киснем або атомом сірки. Обидва X1 та X2 можуть бути або воднем або разом можуть представляти кисень, або атом сірки так, що фрагмент СХ1 Х2 є карбонільною або тіокарбонільною групою (С=О або C=S). Y є або гр упою -OR5 або групою -NR6 R7. Z представляє або атом сірки так, що кільце, яке містить його є тіофеновим кільцем або він представляє групу -СН=СН- так, що кільце є бензольним кільцем. R1, R2, R3 та R4 кожен незалежно вибраний серед водню, нижчих алкільних груп, нижчих алкілоксильних груп та галогенів: фтору, хлору та брому. R5 може бути або атомом водню або нижчою алкільною групою. R6 та R7 кожен незалежно може бути атомами водню або нижчими алкільними групами, або разом вони можуть утворювати ланцюг між 3 та 6 метиленовими групами так, що разом з атомом азоту, з яким вони зв'язані, вони утворюють азетидин, піролідин, піперидин або пергідроазепінове кільце. R8 може бути воднем або нижчою алкільною групою. В контексті представленого опису термін "нижчий алкіл" розглядається як той, що містить прямий ланцюг і розгалужені алкільні групи та циклоалкільні групи між 1 та 6 атомами вуглецю. Наприклад, метил, етил, ізопропіл, трет-бутил, неопентил та циклогексил усі включені в об'єм терміну нижчий алкіл. Термін "ацил" позначає нижчі алкілкарбонільні групи, як наприклад ацетилову, півалоїлову, циклопропілкарбонільну і т.п. Форміл також розглядається як ацилова група. Деякі сполуки загальної формули 1 здатні утворювати солі з кислотами або основами. Наприклад, сполуки, які містять один або більше атомів азоту, можуть утворювати додаткові солі з мінеральними та органічними кислотами, як наприклад соляною кислотою, сірчаною кислотою, фосфорною кислотою, оцтовою кислотою, трифтороцтовою кислотою, метансульфоновою кислотою, лимонною кислотою та бензойною кислотою. Сполуки, які містять кислі групи, можуть утворювати солі з основами. Приклади таких солей включають натрієві, калієві, кальцієві солі, солі триетиламіаку та тетраетиламіаку. Окрім того, сполуки, що мають обидві кислі та основні групи, можуть утворювати внутрішні солі (цвітеріони). Постільки поскільки ці солі є фармацевтично прийнятними, то вони включені в об’єм винаходу. Сполуки згідно із загальною формулою 1 усі мають щонайменше один стереогенний центр (тетраєдний атом вуглецю, який містить чотири різних замісники) і також можуть існувати як оптичні ізомери, як наприклад енантіомери та діастереомери. Такі ізомери та їх суміші усі включені в об'єм представленого винаходу. У переважному варіанті реалізації представленого винаходу А є групою згідно із загальною формулою 2. В іншому переважному варіанті реалізації представленого винаходу А є гр упою згідно із загальною формулою 3. В іншому переважному варіанті реалізації представленого винаходу А є групою згідно із загальною формулою 4. В іншому переважному варіанті реалізації представленого винаходу А є гр упою згідно із загальною формулою 5. В іншому переважному варіанті реалізації представленого винаходу А є групою згідно із загальною формулою 6. В іншому переважному варіанті реалізації представленого винаходу А є гр упою згідно із загальною формулою 7. У найбільш переважному варіанті реалізації А є тетрагідро-1-бензазепін-1-іловою групою, тобто, гр упою згідно із загальною формулою 7, у якій Z є -СН =СН- і обидва А16 та А17 є метиленовими групами. В іншому переважному варіанті реалізації один з R1 та R2 є хлором або метиловою групою, а інший є воднем з двома R3 та R4, які також є воднем. В іншому переважному варіанті реалізації один з V1 та V2 є метокси aбо бензилокси групою, а інший є воднем. У ще іншому переважному варіанті реалізації X1 та X2 разом представляють атом кисню, a Y є -NR 6R7. Особливо переважними варіантами реалізації представленого винаходу є ті, що поєднують дві або більше вищезгаданих переважних ознак. Все ще найбільш переважним варіантом реалізації представленого винаходу є сполука згідно із загальною формулою 8. У загальній формулі 8, W1, R5 та R6 є тими, як визначено вище для 1. Один з R a та Rb є воднем, а інший - або хлором aбо метиловою групою. Rc є або метиловою групою або бензильною групою. Ще найбільш переважним варіантом реалізації є сполука загальної формули 8А, у якій стереохімія є як зображена. Іншим переважним варіантом реалізації представленого винаходу є сполука згідно із загальною формулою 1, у якій обидва V1 та V2 є воднем. У найбільш переважному варіанті реалізації X1 та X2 разом є атомом кисню, a Y є NR8R7 . Найбільш переважною все ще є сполука згідно із загальною формулою 9. У загальній формулі 9, W1, R5 та R6 є як визначені вище для 1. Один з Ra та Rb є воднем, а інший - або хлором або метиловою групою. Ще найбільш переважним варіантом реалізації є сполука згідно із загальною формулою 9А, у якій стереохімія є як зображена. Індивідуальні переважні сполуки у представленому винаході включають (але не обмежуються) наступні: 1-(2-метил-4-(2,3,4.5-тетрагідро-1-бензазепін-1-ілкарбоніл)бензилкарбамоїл)-L-пролін-N,N-диметиламід, (4R)-4-гідрокси-1-(2-метил-4-(2,3,4,5-тетрагідро-1-бензазепін-1-ілкарбоніл)бензил-карбамоїл)-L-пролiнN,N-диметиламід, (4R)-1-(3-хлор-4-(2,3,4,5-тетрагідро-1-бензазепін-1-ілкарбоніл)бензилкарбамоїл)-4-метокси-L-пролінN,N-диметиламід, (4R)-1-(2-хлор-4-(2,3,4,5-тетрагідро-1-бензазепін-1-ілкарбоніл)бензилкарбамоїл)-4-метокси-L-пролінN,N-диметиламід, (4В)-4-бензилокси-1-(2-метил-4-(2,3,4,5-тетрагідро-1-бензазепін-1-ілкарбоніл)бензил-карбамоїл)-Lпролін-N,N-диметиламід, (4R)-4-метокси-1-(2-метил-4-(2,3,4,5-тетрагідро-1-бензазепін-1-ілкарбоніл)бензил-карбамоїл)-L-пролінN,N-диметиламід (4R)-4-метокси-1-(3-метил-4-(2,3,4,5-трагідро-1-бензазепін-1-ілкарбоніл)бензил-карбамоїл)-L-пролінN,N-диметиламід, (4R)-1-(2-хлор-4-(5,6,7,8-тетрагідро-4Н-тіено[3,2-b]азепін-4-ілкарбоніл)бензил-карбамоїл)-4-метокси-Lпролін-N,N-диметиламід, (4R)-1-(4-(10,11-дигідро-5Н-піроло]2,1-с](1,4)бензодиазепін-10-ілкарбоніл)-2-метил-бензилкарбамоїл)-4метокси-L-пролін-N,N-диметиламід, (4R)-1-(2-хлор-4-(10,11-дигідро-5Н-піроло[2,1-с](1,4)бензодиазепін-10-ілкарбоніл)-бензилкарбамоїл)-4метокси-L-пролін-N,N-диметиламід,і (4R)-1-(4-(10,11-дигідро-5Н-піроло[2,1-с](1,4)бензодіазепін-10-ілкарбоніл)-2-метил-бензилкарбамоїл)-4метокси-L-пролін-N,N-диметилтіоамід. Сполуки представленого винаходу можуть одержуватися, використовуючи способи, головним чином відомі з рівня техніки. Сполуки загальної формули 1 можуть розглядатися утвореними з трьох зв'язаних фрагментів (А-С). Три фрагменти будуть, головним чином, одержуватися окремо і потім об'єднуватися на останній стадії в синтезі. Деякі приклади різних груп (R1-R 4, V1, V2, X1, X2 і т.д.) можуть бути несумісними з цим складом і тому будуть вимагати використання захисних груп. Використання захисних груп добре відоме в рівні техніки (дивіться наприклад "Protective Groups in Organic Synthesis", T.W. Greene, Wiley-lnterscience, 1981). Окремі групи, що можуть вимагати захисту, є амінами (захищеними як аміди або карбамати), спиртами (захищені як естери або етери) та карбоновими кислотами (захищеними як естери). Для цілей цієї дискусії буде припущено, що такі захисні групи є замість необхідних. Фрагменти А, В та С можуть поєднуватися згідно з двома стратегіями з наданням сполуки формули 1. По-перше, фрагменти А та В зв'язуються для одержання фрагменту, що відповідає AB, який потім об'єднується з фрагментом С. По-друге, фрагменти В та С зв'язуються для надання фрагменту, який відповідає ВС, який потім об'єднується з фрагментом А. Хімія, задіяна у конденсації фрагмента А з В, а потім задіяна у конденсації фрагмента В з фрагментом С, буде однаковою, в залежності від стратегії яка слідує. Ми виявили, що перша стратегія більш гнучка при роботі на малій шкалі та для одержання вибірки сполук. Тим не менше, можливо, що друга стратегія могла б бути вигідною для одержання вибраної сполуки на великій шкалі. Формування фрагменту AB Тут {А} та {В} представляють частину структур відповідно фрагментів А та В. Формування амідів шляхом конденсації карбонових кислот амінами є добре відомим. Головним чином, кислота та амін змішуються в апротонному розчиннику, як наприклад дихлорметані або диметилформаміді у присутності конденсуючого агента, як наприклад карбодиіміду (наприклад "водорозчинний карбодиімід", який є N-етил-N-(3-диметиламінопропіл)-карбодиімідом) або реакційної похідної фосфору (наприклад "ВОР", яка є (бензотріазол-1-ілокси)тріс(диметиламіно)фосфоній гексафторфосфатом). Реакція може необов'язково каталізуватися третинним аміном, як наприклад триетиламіном або 4-диметиламінопіридином. Альтернативно, карбонова кислота може перетворюватися на більш реакційну похідну, як наприклад на кислий хлорид. Така похідна може потім реагувати з аміном як описано вище, але без потреби в конденсуючому агенті. Формування фрагменту ВС Формування сечовинного або тіосечовинного зв'язку між фрагментами В та С може найлегше досягатися наданням можливості первинному аміну, який відповідає фрагменту В, реагувати з похідною карбонової кислоти, як наприклад фогеном (у якому LG вище є хлором) або карбонілдиімідазолом (у якому LG є 1-імідазолілом) з одержанням проміжної похідної карбамінової кислоти. Коли W1 є скоріше сіркою, а ніж киснем, то використовується тіофосген або тіокарбонілдиімідазол. Реакція вдало проводиться в апротонному розчиннику, як наприклад у дихлорметані або в диметилформаміді у присутності третинного аміну, як наприклад триетиламіну або N,N-диізопропілетиламіну. Після надання достатньої кількості часу для формування проміжної сполуки до реакційної суміші може додаватися вторинний амін, який відповідає фрагменту С. В ізоляції проміжної похідної карбамату немає необхідності. Як варіацію цього процесу можна поміняти порядок додавання амінів, які відповідають фрагментам В та С так, що похідна карбамату одержується з вторинного аміну, а первинний амін додається потім. Потім, в цілому, потребуються наступні проміжні сполуки для синтезу сполук представленого винаходу і) Для фрагменту А Розчинені азепіни згідно з цими загальними формулами можуть одержуватися згідно зі способами, наведеними в літературі. Дивіться наприклад: Aranapakam et al., Bioorg. Med. Chem. Lett-1993, 1733; Artico et al., Farmaco. Ed. Sei. 24, 1969, 276; Artico et al., Farmaco. Ed. Sei. 32, 1977, 339; Chakrabarti et al., J. Med. Chem. 23, 1980, 878; Chakrabarti et al., J. Med. Chem. 23. 1980, 884; Chakrabarti et al., J. Med. Chem. 32, 1989, 2573; Chimirri et al., Heterocycles 36,1993, 601; Grunewald et al., J. Med. Chem. 39,1996. 3539; Klunder et al., J. Med. Chem. 35,1992,1887; Liegeois et al., J. Med. Chem. 37,1994, 519; Olagbemiro et al., J. Het Chem. 19, 1982,1501; Wright et al., J. Med. Chem. 23.1980. 462; Yamamoto et al., Tet. Lett. 24, 1983, 4711; та міжнародну заявку на патент номер публікації якої WO99/06403. Деякі з них є комерційними товарами. іі) Для фрагменту В Через те, що первинний амін та групи карбонової кислоти є несумісними, вони повинні окремо формуватися та захищатися. Заміщені бензойні кислоти є добре відомими, а карбонова кислота вдало захищається як її метиловий естер. Первинний амін може вироблятися з відповідного нітрилу (відновленням) або спирту (шля хом заміщення азотним нуклеофілом). Найкращий спосіб буде залежати від природи замісників R1-R4. ііі) Для фрагменту С Похідні піролідину цього типу одержуються згідно зі способами, описаними в літературі. Дивіться наприклад: Dugave et al., Tet. Lett. 39, 1998,1169; Petrillo et al., J. Med. Chem. 31,1988, 1148; та Smith et al., J. Med. Cnem. 31,1988, 875. Похідні проліну та гідроксипроліну визначеної стереохімії є комерційними товарами і, щонайменше таким чином, є зручними сировинними матеріалами. Представлений винахід, окрім цього, включає фармацевтичні композиції, що містять у собі одну сполуку згідно із згаданим вище описом як активний компонент. Композиція може також містити другий фармакологічний агент, як наприклад спазмолітичний або калієвий канальний блокатор, які відомі у рівні техніки для послаблення дисфункції сечового міхура. Переважно, композиція містить тільки один активний компонент. Композиція буде містити ексципієнти, вибрані серед зв’язуючих агентів, наповнювачів, диспергаторів, розчинників, стабілізуючих агентів і т.п, такі ексципієнти, які головним чином відомі з рівня техніки. Використовувані ексципієнти будуть залежати від встановленої природи складу, який буде у свою чергу залежати від встановленого способу приймання. Приймання може бути пероральним, трансмукозальним (як наприклад підязиковим, трансбукальним, інтраназальним, вагінальним та ректальним), трансдермальним або шляхом ін'єкції (як наприклад підшкірної, внутрішньом'язової та внутрішньовенної). Головним чином надається перевага пероральному прийманню. Для перорального приймання склад буде мати форму таблетки або капсули. Решта складів містять сухі порошки, розчини, суспензії, супозиторії і т.п. У подальшому аспекті представлений винахід є способом лікування або регулювання деяких людських фізіологічних дисфункцій. Цей спосіб включає призначення особі, яка потребує такого лікування, ефективної кількості фармацевтичної композиції, яка містить сполуку згідно із вищезгаданим описом як активний компонент. Сполуки діють із зменшенням виходу сечі і, таким чином, спосіб винаходу може застосовуватися до всіх станів, у яких підвищений вихід сечі є сприятливим фактором. Сполуки також підвищують формування коагуляційних протеїнів крові, відомих як Фактор VIII та фактор фон Віллебранда і, таким чином, може здійснюватися лікування кровотеч. У переважному варіанті реалізації стан, який лікується, є нецукровим діабетом. Це є стан, спричинений нездатністю тіла виробляти та секретувати фізіологічно активний вазопресин, в результаті чого, повторне поглинання води значно зменшується і створюються великі об'єми сечі. В іншому переважному варіанті реалізації стан, який лікується, є нічним енурезом. Це визначається як спорожнення сечового міхура під час сну особи. Цей стан, що головним чином вражає дітей, і ряд факторів може втягуватися в його етіологію. В іншому переважному варіанті реалізації стан, який лікується, є ніктурією. Це визначається як вироблення протягом ночі достатньої кількості сечі, необхідної для пробудження персони та спорожнення його (або її) сечового міхура. Знову цей стан може бути результатом ряду факторів. В іншому переважному варіанті реалізації стан, який лікується, є нетримання. Цей стан частково характеризується зменшенням об'єму сечового міхура і регулювання так, що відбувається ненавмисне сечовипускання, якщо сечовий міхур не спорожнюється часто. Нетримання розділене на два стани: нетримання сечі при напруженні та спричинене нетримання. Вважається, що тут втягнуто ряд етіологічних факторів. Лікування згідно з винаходом особливо корисне для вилучення потреби спорожнення сечового міхура ("затримка спорожнення") для того, щоб надати об'єкту нетримання сухий період в декілька годин (як наприклад до чотирьох годин). Така затримка спорожнення може також бути корисною для людей, які не страждають нетриманням, наприклад для людей, зобов’язаних залишатися на зустрічах на довгі періоди часу. В іншому переважному варіанті реалізації стан, який лікується, є гемофілія А або хвороба фон Віллебранда. Це є стани, у яких Фактор VIII або формування фактору фон Віллебранда знижується і персона страждає від тривалої кровотечі. В іншому переважному варіанті реалізації композиція приймається до хірургічного втручання (включаючи зубну хір ургію) для підвищення коагулювальності крові і, таким чином, для зменшення втрати крові під час операції. Приймання композицій представленого винаходу буде, головним чином, під контролем лікаря. Лікар буде визначати кількість композиції, яку необхідно прийняти та графік дозування, беручи до уваги фізичний стан пацієнта та терапевтичні цілі. Для дорослого пацієнта з нецукровим діабетом типова доза повинна бути між 50мг та 1г на день активної сполуки, взятої як одна таблетка або як до чотирьох таблеток на протязі дня. Для способів приймання, відмінних від перорального, кількість сполуки буде зменшуватися, оскільки непероральні способи вважаються більш ефективними в показниках введення терапевтичних агентів в систематичну циркуляцію. Для лікування гемофілії А та хвороби фон Вілебранда може бути потрібною більша кількість сполуки ніж для лікування нецукрового діабету. Вищезгаданий основний опис буде тепер додатково ілюструватися з рядом необмежуючих Прикладів. ПРИКЛАДИ Абревіатури. Використані наступні абревіатури. Ac AIBN Ацетил Азо-біс-(ізобутиронітрил) Bn BOC (BOC)2O DMF Et EtOAc IPA iPr M.S. Me NBS Бензил Трет-бутилоксикарбоніл Дітрет-бутилдікарбонат Діметилформамід Етил Етилацетат Ізопропанол Ізопропіл мас спектрометрія Метил N-Бромосукцинимід pet. ether нафтовий етер, фракція, яка кипить при 60-80°С Ph Феніл tBu Трет-бутил THF Тетрагідрофуран WSCDI Водорозчинний карбодиімід Одержання проміжних сполук. Реагенти, які відповідають фрагменту А та С були комерційно доступними або одержаними згідно з опублікованими процедурами за виключенням деталізованих в особливих Прикладах. Реагенти, які відповідають фрагменту В одержувалися як деталізовано нижче. Приклад А. 4-(трет-бутилоксикарбоніламінометил)-3-хлорбензойна кислота А1. Ме тил 4-бромметил-3-хлорбензоат До розчину метил 3-хлор-4-метилбензоату (5.0г, 27.1ммоль) у тетрахлориді вуглецю (50мл) додавали NBS (5.8г, 32.0ммоль) та AIBN (0.442г, 2.70ммоль). Суміш розмішували зі зворотним холодильником протягом 18 годин. Суміші надавали можливість охолонути до кімнатної температури і потім випарювали у вакуумі. Осад очи щали фле ш-хроматографією на силікагелі (елюант ЕtOАс:нафт. етер 0:100-5:95); вихід 5.96г (84%). А2. 4-(трет-бутилоксикарбоніламінометил)-3-хлорбензойна кислота До насиченого розчину аміаку в етанолі (170мл) додавали метил 4-бромметил-3-хлорбензоат з Прикладу А1 (5 .5г, 20.9ммоль). Суміш розмішували при кімнатній температурі протягом 1 години і потім випарювали у вакуумі. Осад розтирали з діетиловим етером і білі кристали, що одержувалися в результаті, фільтрували та знову промивали діетиловим етером. До розчину цієї твердої речовини у воді (100мл) додавали розчини (ВОС)2О (5.0г, 23.0ммоль) у діоксані (100мл) та гідроксиду натрію (1.86г, 46.0ммоль) у воді (100мл). Суміш розмішували при кімнатній температурі протягом 18 годин і потім випарювали у вакуумі. Водний осад підкислювали лимонною кислотою та екстрагували з добавлянням хлороформу/IРА. Органічний шар промивали водою, просушували MgSO4 та випарювали у вакуумі з одержанням білої твердої речовини; вихід становив 2.8г (67%). Приклад В. 4-Ціано-3-метилбензойна кислота До розчину 4-бром-2-метилбензонітрилу (2.0г, 10.2ммоль) у THF (100мл) при -78°С в атмосфері азоту додавали по краплі 2.5М розчину n-бутил літію (4.48мл, 11.2ммоль). Суміш розмішували при -78°С протягом 1 години і потім виливали на твердий двоокис вуглецю (5г) у THF (50мл). Суміші надавали можливість нагріватися до кімнатної температури. Додавали воду (200мл) і суміш екстрагували з добавлянням діетилового етеру (3 рази). Водний шар підкислювали додаванням концентрованої НСІ та екстрагували з добавлянням хлороформу (3 рази). Змішані екстракти хлороформу промивали водою, просушували MgSO4 та випарювали у вакуумі з одержанням білої твердої речовини; вихід становив 1.2г (73%). Приклад С 4-Ціано-2-метилбензойна кислота 4-Бром-3-метилбензонітрил (2.0г, 10.2ммоль) вводили у взаємодію наступним способом Прикладу В для одержання жовтої твердої речовини, яку розтирали з гексаном і фільтрували; вихід становив 0.96г (59%). Реагенти, які відповідають фрагментам А, В та С об'єдн ували для одержання особливих Прикладів як деталізовано нижче. Приклад 1. 1-(2-Метил-4-(2,3,4,5-тетрагідро-1-бензазепін-1-ілкарбоніл)бензилкарбамоїл)-L-пролін-N,N-диметиламід 1А. 2-Метил-4-((2,3,4,5-тетрагідро-1Н-бензо[b]азепін)-1-карбоніл)-бензонітрил. До розчину 2,3,4,5-тетрагідро-1Н-бензо[b]азепіну (0.80г, 5.44ммоль) у дихлорметані (50мл) додавали 4циано-3-метилбензойну кислоту (0.96г, 5.95ммоль), триетиламін (0.60г, 5.95ммоль), 4(диметиламіно)піридин (0.73г, 5.95ммоль) та WSCDI (1.24г, 6.48ммоль). Суміш розмішували зі зворотним холодильником протягом 18 годин, охолоджували та випарювали у вакуумі. Осад розділяли між EtOAc та 1М KHSO4. Органічний шар промивали насиченим розчином бікарбонату натрію та розсолом, просушували MgSO4 , та випарювали у вакуумі. Неочищений матеріал очищали флеш-хроматографією на силікагелі (елюант ЕtOАс:нафт. етер 30:70); ви хід 1.10г (70%). 1В. Гідро хлорид 1-(4-(Амінометил)-3-метилбензоїл)-2,3,4,5-тетрагідро-1Н-бензо[b]азепіну До дегазованого розчину ціанобензазепіну Прикладу 1А (1.10г, 3.79ммоль) у метанолі (50мл) додавали концентровану соляну кислоту (0.98мл, 11.3ммоль) та 10% паладію на вуглеці (0.80г). Газоподібний водень барботували крізь суміш протягом 5 годин при кімнатній температурі. Каталізатор видаляли фільтруванням крізь прокладку з целіту, а фільтрат випарювали; вихід становив 1.23г (98%). 1С. 1-(2-Метил-4-(2,3,4,5-тетрагідро-1-бензазепін-1-ілкарбоніл)бензилкарбамоїл)-Lпролін-N,Nдиметиламід До розчину аміну Прикладу 1В (0.10г, 0.302ммоль) у DMF (10мл) в атмосфері азоту додавали N,Nдиізопропілетиламін (43мг, 0.332ммоль) та карбонілдиімідазол (0.074г, 0.453ммоль). Суміш розмішували при кімнатній температурі протягом 40 хвилин. Додавали розчин пролін-N,N-диметиламіду (0.107г, 0.756ммоль) у D MF (1мл). Суміш розмішували при кімнатній температурі протягом додаткових 16 годин. Розчинник видаляли у вакуумі, а неочищений матеріал очищали флеш-хроматографією на силікагелі (елюант метанол:дихлорметан 5:95); вихід становив 0.115г (82%). 1 NMR (CDCI3): d 1.35-1.55 (1Н, m), 1.74-2.10 (3Н, m), 2.11 (3Н, s), 2.17-2.35 (1Н, m), 2.60-2.82 (2Н, m), 2.86 (3Н, s), 2.90-3.14 (2Н, m), 3.05 (3Н, s), 3.26 (1Н, dd, J=14.9 & 7.2Гц), 3.40-3.53 (1Н, m), 3.64-3.84 (1Н, m), 4.03-4.19 (1Н, m), 4.29-4.42 (1Н, m), 4.55-4.68 (1Н. m), 4.74-4.81 (1Н, m), 4.85-4.98 (1Н, m), 6.58 (1Н, d, J=7.7Гц), 6.75-6.89 (2Н, m). 6.91-7.06 (3Н, m), 7.16 (1Н, d. J=6.5Гц), 7.93-8.03 (1Н, m) ррm. M.S.: обчис m/e=462.26; результат [М+Н]+= 463.2 Приклад 2. (4R)-4-Гідрокси-1-(2-метил-4-(2,3,4.5-тетрагідро-1-бензазепін-1-ілкарбоніл)бензил-карбамоїл)-L-пролінN,N-диметиламід 2А. Гідрохлорид L-транс-4-Гідроксипролін-N,N-диметиламід До розчину ВОС-гідроксипроліну (2.99г, 13.89ммоль) у дихлорметані (100мл) додавали N,Nдиізопропілетиламін (3.7мл, 21.24ммоль), 4-(диметиламіно)піридин (1.74г, 14.24ммоль), гідрохлорид диметиламіну (1.72г, 21.09ммоль) та WSCDI (3.17г, 16.68ммоль). Суміш розмішували при кімнатній температурі протягом 30 годин. Суміш розбавляли дихлорметаном (100мл) та промивали 0.3М KHSO4 насиченим розчином бікарбонату натрію та розсолом, просушували MgSO 4 та випарювали у вакуумі з одержанням безкольорової смоли. Цей неочищений матеріал вилучали в 4N НСІ/діоксані (50мл) та розмішували при кімнатній температурі протягом 1 години, а потім випарювали у вакуумі. Осад азеотропували толуолом та діетиловим етером з одержанням білої твердої речовини; вихід становив 0.45г (17%). 2В. (4R)-4-Гідрокси-1-(2-метил-4-(2,3,4,5-тетрагідро-1-бензазепін-1-ілкарбоніл)бензил-карбамоїл)-Lпролін-N,N-диметиламід. Амін Прикладу 1В (0.10г, 0.302ммоль) вводили у взаємодію з аміном Прикладу 2А (0.153мг, 0.785ммоль), який слідує за способом Прикладу 1С. Продукт очищали флеш-хроматографією на силікагелі (елюант: хлороформ:метанол:оцтова кислота 95:4:1); вихід становив 0.95г (66%). 1 Н NMR (CDCI3); d 1.65-1.80 (2Н, m), 1.85-2.00 (3Н. m), 2.05-2.25 (1Н, m), 2.10 (3Н, s). 2.80-3.10 (3Н, m), 2.85 (3Н, s), 3.00 (3Н, s), 3.40-3.30 (1Н, m), 3.45-3.55 (1Н, m), 3.65-3.95 (1Н, m), 4.00-4.10 (1Н, m), 4.30-4.55 (1Н, m), 4.91 (1Н, t, J=7.7Гц), 5.15-5.30 (1H, m), 6.10-6.20 (1H, m), 6.55-6.65 (1H, m), 6.85-7.50 (5H, m) ppm. M.S.: обчис m/e=478.26; результат [М+Н]+ = 479.2 Приклади 3-116. Додаткові приклади, викладені у наступних Таблицях, одержували з використанням аналогічних способів. Приклад 117. Біологічна характеристика In Vitro Сполуки винаходу є вибірковими агоністами на V2 рецепторі. У стандартних дослідженнях по радіолігандному заміщенню усі сполуки надають к I величин менших 10мкМ для V2 рецептора. Приклад 118. Біологічна характеристика In Vivo Пацюк Братлборо є розглядуваною моделлю для нестачі вазопресину (для огляду дивіться FD Grant, "Genetic models of vasopressin deficiency", Exp. Ph ysiol. 85, 203S-209S, 2000). Тварини не секретують вазопресин і відповідно виробляють великі об'єми розбавленої сечі. Сполуки винаходу призначалися пацюкам Братлборо (0.1-10мг/кг р.о.) в метилцелюлозі. Сечу збирали щогодини і об’єми порівнювалися з об'ємами у контрольних тварин. Тварини протягом експерименту мали вільний доступ до їжі та води. Представлені результати надаються у Таблиці. Результати для дезмопресину надаються для порівняння. Сполука Прикладу 1 14 52 54 85 90 101 104 109 110 112 114 115 Дезмопресин % інгібування виходу сечі (за 1 годину) 1мг/кг 82 1мг/кг 84 1мг/кг 90 1мг/кг 68 1мг/кг 63 1мг/кг 60 1мг/кг 74 1мг/кг 81 1мг/кг 73 1мг/кг 80 1мг/кг 75 1мг/кг 85 1мг/кг 88 0.1мг/кг 37 1мг/кг 100 10мг/кг 100 Доза Приклад 119. Фармацевтична композиція для таблетки Таблетки, які містять 100мг сполуки Прикладу 1 як активний агент одержуються з наступного: Сполука Прикладу 1 200.0г Кукур удзяний крохмал 71.0г Гідроксипропілцелюлоза 18.0г Карбоксиметилцелюлоза кальцію 13.0г Стеарат магнію 3.0г Лактоза 195.0г Загальна кількість 500.0г Матеріали змішували, а потім пресували з одержанням 2000 таблеток з вагою 250мг, кожна з яких містить 100мг сполуки Прикладу 5. Вищенаведені Приклади демонструють те, що сполуки в об'ємі винаходу легко одержуються, використовуючи стандартні хімічні способи і те, що ці сполуки мають біологічні властивості, що слід очікувати від агоністів V2 рецептора. Зокрема, сполуки є сильнодіючими антидіуретиками у моделі тварини із нестачею вазопресину. Таким чином, ясно, що вони можуть бути корисними у лікуванні людських хвороб, що лікуються в наш час дезмопресином, як наприклад центральний нецукровий діабет, нічний енурез та ніктурія. Надалі припущено, що антидіуретики, як наприклад дезмопресин, можуть бути корисними для деяких типів нетримання сечі. Ці аргументи слід також поширювати на сполуки представленого винаходу. Дезмопресин також використовується у лікуванні деяких розладів коагуляції. Є очевидним припустити, що ця дія також опосередковується за допомогою V2 рецептора (дивіться наприклад JE Kaufmann et al., "Vasopressin-induced von Willebrand factor secretion from endothelial cells involves V2 receptors and cAMP", J. Clin. Invest. 106, 107-116, 2000; A Bemat et al.. "V2 receptor antagonism of DDAVP-induced release of hemostasis factors in conscious dogs", J. Pharmacol, exp. Ther. 282, 597-602, 1997), і тому слід очікувати, що сполуки представленого винаходу повинні бути корисними прокоагулянтами. Об’єм представленого винаходу надалі визначається у наступній формулі винаходу.
ДивитисяДодаткова інформація
Назва патенту англійськоюCondensed azepins as agonists of vasopressin
Назва патенту російськоюКонденсированные азепины как агонисты вазопресcина
Автори російськоюFranklin, Richard Jeremy
МПК / Мітки
МПК: A61P 7/12, A61K 31/55, A61K 31/553, C07D 487/04, C07D 519/00, C07D 471/04, A61P 13/00, A61K 31/551, C07D 413/12, C07D 498/04, A61P 7/04, A61P 5/10, A61K 31/5513, C07D 495/04, C07D 403/12, A61P 43/00, A61K 31/5517
Мітки: агоністи, конденсовані, азепіни, вазопресину
Код посилання
<a href="https://ua.patents.su/14-73152-kondensovani-azepini-yak-agonisti-vazopresinu.html" target="_blank" rel="follow" title="База патентів України">Конденсовані азепіни як агоністи вазопресину</a>
Наступний патент: Спосіб оцінки токсичності водного середовища
Випадковий патент: Адаптивний пристрій фільтрації параметрів траєкторії маневруючої цілі