Тетрагідропіранілциклопентилтетрагідропіридопіридинові модулятори активності хемокінового рецептора, фармацевтична композиція на їх основі та спосіб лікування розладу або захворювання (варіанти)
Номер патенту: 75828
Опубліковано: 15.05.2006
Автори: Янг Ліху, Дзіао Річард, Мойєс Крістофер, Морріелло Грегорі
Формула / Реферат
1. Сполука формули І
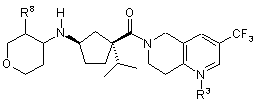 , I
, I
де:
R3 є киснем або відсутній;
R8 вибирають з:
(a) водню,
(b) С1-3алкілу, який є незаміщеним або заміщений 1-6 атомами фтору,
(c) -O-С1-3алкілу,
(d) фтору і
(e) гідрокси;
і її фармацевтично прийнятні солі і окремі діастереомери.
2. Сполука за п.1, в якій R3 відсутній.
3. Сполука за п.1, в якій R3 є киснем.
4. Сполука за п. 1, в якій R8 вибирають з:
(a) водню,
(b) трифторметилу,
(c) метилу,
(d) метокси,
(e) етокси,
(f)етилу,
(g) фтору і
(h) гідрокси.
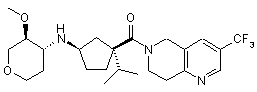
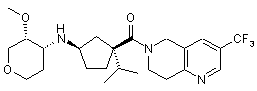
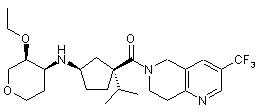
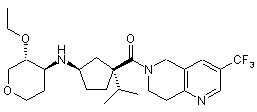
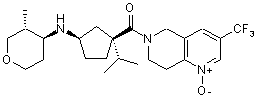
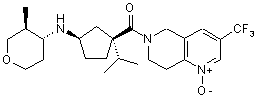
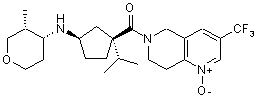
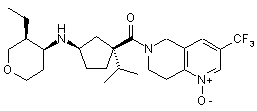
5. Сполука, яку вибирають з групи, що включає:
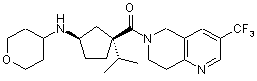 ,
,
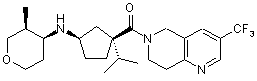 ,
,
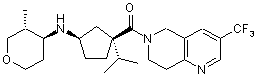 ,
,
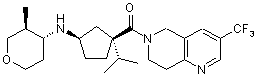 ,
,
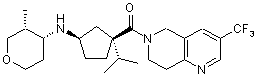 ,
,
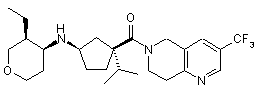 ,
,
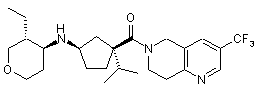 ,
,
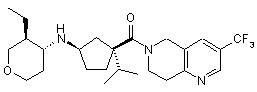 ,
,
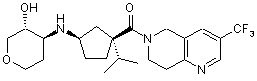 ,
,
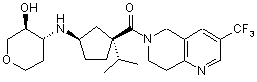 ,
,
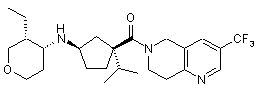 ,
,
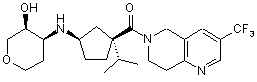 ,
,
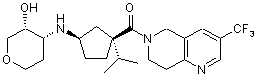 ,
,
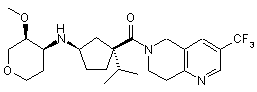 ,
,
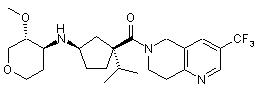 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
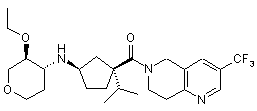 ,
,
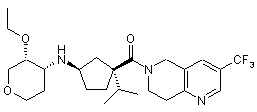 ,
,
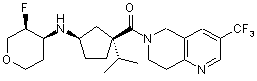 ,
,
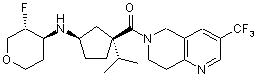 ,
,
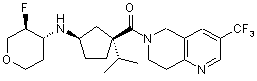 ,
,
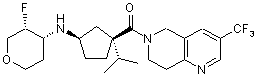 ,
,
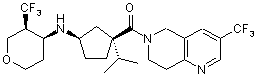 ,
,
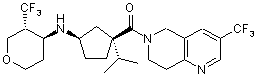 ,
,
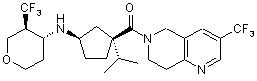 ,
,
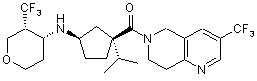 ,
,
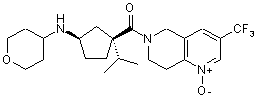 ,
,
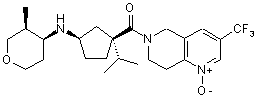 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
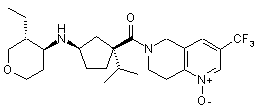 ,
,
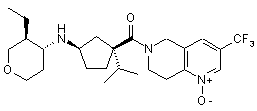 ,
,
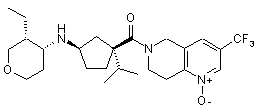 ,
,
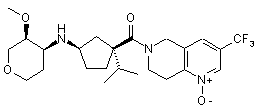 ,
,
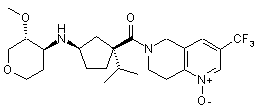 ,
,
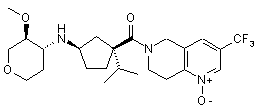 ,
,
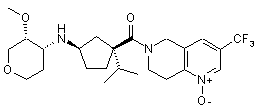 ,
,
і їх фармацевтично прийнятні солі і окремі діастереомери.
6. Фармацевтична композиція, яка містить інертний носій і сполуку за п. 1.
7. Спосіб модулювання активності рецептора хемокіну у ссавців, при якому здійснюють введення ефективної кількості сполуки за п. 1.
8. Спосіб одержання лікарського засобу для модулювання активності рецептора хемокіну у людини і тварин, при якому здійснюють об'єднання сполуки за п. 1 з фармацевтично прийнятним носієм або розріджувачем.
9. Спосіб лікування, поліпшення, контролю або зниження ризику запального та імунорегуляторного розладу або захворювання, при якому здійснюють введення пацієнту ефективної кількості сполуки за п. 1.
10. Спосіб лікування, поліпшення, контролю або зниження ризику ревматоїдного артриту, при якому здійснюють введення пацієнту ефективної кількості сполуки за п. 1.
Текст
1. Сполука формули І 2 3 F H N F CF3 N O H N O CF3 N H N CF3 N H N H N O CF3 N H N CF3 N O CF3 N O N+ O O CF3 N O H N O O O CF3 N N+ N+ O O CF3 N O H N O O O CF3 N N+ N+ O H N O CF3 N O H N O O O CF3 N N+ N+ O H N O CF3 N N+ O CF3 N O N+ O H N O CF3 N N+ O N H N O H N O O O H N O O N O H N O O O N O N+ CF3 N CF3 N O N CF3 H N O O O O CF3 O CF3 N O N CF3 H N 4 O N CF3 O H N O N F 75828 O O CF3 N H N N+ O O O CF3 N і їх фармацевтично прийнятні солі і окремі діастереомери. 6. Фармацевтична композиція, яка містить інертний носій і сполуку за п.1. 7. Спосіб модулювання активності рецептора хемокіну у ссавців, при якому здійснюють введення ефективної кількості сполуки за п.1. 8. Спосіб одержання лікарського засобу для модулювання активності рецептора хемокіну у людини і тварин, при якому здійснюють об'єднання сполуки за п.1 з фармацевтично прийнятним носієм або розріджувачем. 9. Спосіб лікування, поліпшення, контролю або зниження ризику запального та імунорегуляторного розладу або захворювання, при якому здійснюють введення пацієнту ефективної кількості сполуки за п.1. 10. Спосіб лікування, поліпшення, контролю або зниження ризику ревматоїдного артриту, при якому здійснюють введення пацієнту ефективної кількості сполуки за п.1. N+ O Хемокіни являють собою сімейство невеликих (70-120 амінокислот), прозапальних цитокінів з могутньою хемотактичною дією. Хемокіни являють собою хемотактичні цитокіни, які виділяються широким спектром клітин для залучення різних клітин, таких як моноцити, макрофаги, Τ клітини, еозинофіли, базофіли і нейтрофіли до місць запалення [описано в Schall, Cytokine, 3, 165-183 (991) і Murphy, Rev. Immun., 12, 593-633 (1994)]. Ці молекули спочатку були визначені чотирма збереженими цистеїнами і діляться на дві підродини на основі розташування першої цистеїнової пари. У сімействі СХС-хемокінів, яке включає IL-8, GROα, NAP-2 і IP-10, ці два цистеїни розділені однією амінокислотою, в той час як в сімействі ССхемокінів, яке включає RANYES, МСР-1, МСР-2, МСР-3, МІР-1α, ΜΙΡ-1β і еотаксин, ці два залишки є сусідніми. Хемокіни секретуються широким спектром клітин і зв'язуються зі специфічними рецепторами, зв'язаними з G-білком (GPCR) [описано в Horuk, Trends Pharm. Sci., 15, 159-165 (1994)), присутніми в лейкоцитах та інших клітинах. Такі рецептори хемокіну утворюють підродину GPCR, яка в цей час складається з п'ятнадцяти охарактеризованих членів і деякої кількості окремих членів. На відміну від рецепторів для різнорідних хемоатрактантів, таких як С5а, fMLP, PAF і LTB4, рецептори хемокіну більш селективно експресуються на підмножині лейкоцитів. Таким чином, утворення специфічних хемокінів забезпечує механізм для поповнення певних підмножин лейкоцитів. При зв'язуванні зі своїми спорідненими лігандами, рецептори хемокіну перетворюють внутрішньоклітинний сигнал через пов'язаний з ним тривимірний G білок, що приводить до швидкого збільшення концентрації внутрішньоклітинного кальцію. Існує, принаймні, сім рецепторів хемокіну людини, які зв'язуються або реагують на βхемокіни за наступною характерною схемою: CCR1 (або "CKR-1" або "CC-CKR-1") [МІР-1α, ΜΙΡ-1β, МСР-3, RANTES] (Ben-Barruch, et al., J. Biol. Chem., 270, 22123-22128 (1995); Beote, et al., Cell, 72, 415-425 (1993)); CCR-2A і CCR-2B (або "CKR2A"/"CKR-2A" або "CC-CKR-2A"/"CC-CKR-2A") [MCP-1, МСР-2, МСР-3, МСР-4]; CCR-3 (або "CKR3" або "CC-CKR-3") [Еотаксин, Еотаксин 2, RANTES, МСР-2, МСР-3] (Rollins, et al., Blood, 90, 908-928 (1997)); CCR-4 (або "CKR-4" або "CC-CKR4") [МІР-1α, RANTES, MCP-1] (Rollins, et al., Blood, 90, 908-928 (1997)); CCR-5 (або "CKR-5" або "CCCKR-5") [ΜΙΡ-1α, RANTES, MIP-1β] (Sanson, et al., Biochemistry, 35, 3362-3367 (1996)); і антиген групи крові Даффі [RANTES, MCP-1] (Chaudhun, et al., J. Biol. Chem.. 269, 7835-7838 (1994)). β-хемокіни включають еотаксин, МІР («запальний білок макрофагу»), МСР («білок хемоатрактант моноциту») і RANTES («регульований при активації, експресо 5 75828 6 ваний і секретований нормальними Т») серед інal., J. Clin Invest.. 103, 773-778 (1999)]. Таким чиших цитокінів. ном, антагоністи CCR2 можуть інгібувати утворенРецептори хемокіну, такі як CCR-1, CCR-2, ня атеросклеротичних пошкоджень і патологічного CCR-2A, CCR-2B, CCR-3, CCR-4, CCR-5, CXCR-3, розвитку за допомогою зменшення поповнення CXCR-4, вважаються важливими медіаторами моноцитів і диференціації в стінку артерії. запальних та імунорегуляторних захворювань і Даний винахід представляє сполуки, які є морозладів, включаючи астму, риніт і алергічні задуляторами активності рецептора хемокіну, і корихворювання, а також аутоімунних патологій, таких сні для профілактики або лікування певних запаяк ревматоїдний артрит і атеросклероз. Вважаєтьльних і імунорегуляторних розладів і захворювань, ся, що люди, які є гомозиготними для делеції 32алергічних захворювань, атонічних станів, вклюосновної пари в гені CCR-5, менш сприйнятливі до чаючи алергічний риніт, дерматит, кон'юнктивіт і ревматоїдного артриту [Gomez, et al., Arthritis & астму, а також аутоімунних патологій, таких як Rheumatism, 42, 989-992 (1999)]. Огляд ролі еозиревматоїдний артрит і атеросклероз. Даний винанофілів в алергічному запаленні представлений хід також представляє фармацевтичні композиції, [Kita, Η., et al., у J. Exp. Med. 183, 2421-2426 що містять такі сполуки, і застосування даних спо(1996)]. Загальний огляд ролі хемокінів в алергічлук і композицій для профілактики і лікування таному запаленні представлений [Lugster, A.D., у ких захворювань, в які залучені рецептори хеNew England J. Med., 338(7), 426-445 (1998)]. Підмокіну. множина хемокінів являє собою могутні хемоатраДаний винахід відноситься до сполук форктанти для моноцитів і макрофагів. Найбільш охамули І рактеризованими з них є МСР-1 (білок хемоатрактант моноциту-1), первинним рецептоl ром якого є CCR2. МСР-1 виробляється в багатьох типах клітин у відповідь на запальну стимуляцію у різних видів, включаючи гризунів і людину, і стиде: мулює хемотаксис в моноцитах і підмножині лімR3 є киснем або відсутній; фоцитів. Зокрема, вироблення МСР-1 співвідноR8 вибирають з: ситься з інфільтрацією моноцитів і макрофагів в (a) водню, місце запалення. Делеція або МСР-1, або CCR2 (b) С1-3алкілу, який є незаміщеним або замігомогенною рекомбінацією у мишей дає значне щений 1-6 атомами фтору, ослаблення поповнення моноцитів у відповідь на (c) - О-С1-3алкілу, ін'єкцію тіогліколяту та інфекцію Listeria (d) фтору і monocytogenes [Lu et al., J. Exp. Med.. 187, 601-608 (e) гідрокси; (1998); Kurihara et al., J. Exp. Med., 186, 1757-1762 і їх фармацевтично прийнятних солей і окре(1997); Boring et al., J. Clin. Invest., 100, 2552-2561 мих діастереомерів. (1997); Kuziel et al, Proc. Natl. Acad. Sci., 12053В одному з варіантів даного винаходу R3 від12058 (1997)]. Більш того ці тварини показують сутній. знижену інфільтрацію моноцитів в гранулематозні В одному з варіантів даного винаходу R3 є вопошкодження, викликані ін'єкцією шистосомалу днем. або мікобактеріальних антигенів [Boring et al., J. В даному винаході переважно, коли R вибиClin. Invest., 100, 2552-2561 (1997); Warmington et рають з: al., Am. J. Path.. 154, 1407-1416 (1999)]. Ці дані (a) водню, підтверджують, що викликана МСР-1 активація 2 (b) трифторметилу, CCR грає основну роль у поповненні моноцитів в (c) метилу, місцях запалення, і що антагонізм цієї активності (d) метокси, дасть значне придушення імунної відповіді з оде(e) етокси, ржанням терапевтичної користі при імунозапаль(f) етилу, них і аутоімунних захворюваннях. Отже, агенти, які (g) фтору і модулюють рецептори хемокіну, такі як рецептор (h) гідрокси. CCR-2, будуть корисні при таких розладах і захвоПриклади сполук відповідно до даного винарюваннях. Крім того, поповнення моноцитів в заходу включають ті сполуки, які представлені у припалених пошкодженнях стінок судин є основним кладах і їх фармацевтично прийнятні солі і окремі компонентом патогенезу і утворення атерогенних діастереомери. бляшок. МСР-1 виробляється і секретується ендоСполуки відповідно до даного винаходу мателіальними клітинами і клітинами інтимальних ють, принаймні, два асиметричних центри в пологладких м'язів після пошкодження стінки судини женнях 1 і 3 циклопентильного кільця, один асимепри гіперхолестеринемічних станах. Моноцити, що тричний центр в положенні 4 морфолінового поповнюються в місці пошкодження, інфільтрукільця і, необов'язково, один асиметричний центр ються в стінку судини і диференціюються в пінисті в положенні 3 морфолінового кільця. Додаткові клітини у відповідь на виділення МСР-1. Деякі груасиметричні центри можуть бути присутніми в запи продемонстрували, що розмір пошкодження лежності від природи різних замісників в молекулі. аорти, вміст макрофагів і некроз ослаблені у МСРКожний такий асиметричний центр буде незалеж1 -/- або CCR2-/-мишей, обернено схрещених з но давати два оптичних ізомери, і мається на уваАРО-Е -/-, LDL-R -/- або Аро В трансгенними мизі, що всі можливі оптичні ізомери і діастереомери шами, які одержують їжу з високим рівнем жиру в сумішах і як чисті або частково очищені сполуки [Boring et al., Nature, 394, 894-897 (1998); Gosling et 7 75828 8 включені в об'єм даного винаходу. Незалежний Сполуки відповідно до даного винаходу кориссинтез діастереомерів і енантіомерів або їх хромані в способі модулювання активності рецептора тографічне розділення можуть бути проведені мехемокіну у пацієнта, за необхідності такої модулятодами, відомими в даній галузі техніки, відповідції, де спосіб включає введення ефективної кільконою модифікацією методики, описаною нижче. їх сті сполуки. Даний винахід призначений для застоабсолютна стереохімія може бути визначена рентсування наступних сполук як модулятори генівською кристалографією кристалічних продукактивності рецептора хемокіну. Зокрема, ці сполутів або кристалічних проміжних сполук, які одерки корисні як модулятори рецепторів хемокіну, жують, за необхідності, з реагентом, що містить зокрема, CCR-2. асиметричний центр відомої абсолютної конфігуЗастосування сполук відповідно до даного вирації. находу як модуляторів активності рецептора хемоЯк зрозуміло фахівцям в даній галузі техніки, кіну може бути продемонстроване методом, відоС1-3алкіл включає групу, що має 1, 2 або 3 атоми мим в даній галузі техніки, таким як дослідження вуглецю в лінійному або розгалуженому розташузв'язування хемокіну, [описані Van Riper, et al., в J. ванні, так, що С1-3алкіл включає метил, етил, нExp. Med., 177, 851-865 (1993)], які можуть бути пропіл та ізопропіл. легко адаптовані для вимірювання зв'язування Фраза «фармацевтично прийнятні» відноситьCCR-2. ся до сполук, матеріалів, композицій і/або дозоваСпорідненість рецептора в дослідженні на них форм, які, з точки зору медицини, підходять зв'язування CCR-2 визначають вимірюванням інгідля застосування в контакті з тканинами людини і бування 125І-МСР-1 до ендогенного рецептора тварин без зайвої токсичності, пошкодження, алеCCR-2 в різних клітинах, включаючи моноцити, ргічної реакції або інших проблем або ускладнень, клітини ТНР-1, або після гетерологічної експресії і мають розумне співвідношення користь/ризик. В клонованого рецептора в еукаріотні клітини. Клітиданому описі термін «фармацевтично прийнятні ни суспендують у зв'язувальному буфері (50мМ солі» відноситься до похідних, в яких вихідну споHEPES, рН7,2, 5мМ MgCl2, 1мМ СаСl2 і 0,50% луку модифікують перетворенням в її кислотну або BSA) і додають до сполуки, що тестується, або основну сіль. Приклади фармацевтично прийнятДМСО і 125І-МСР-1 при кімнатній температурі проних солей включають, але не обмежені ними, мітягом 1 години для зв'язування. Потім клітини збинеральні або органічні кислотні солі основних зарають "на фільтри GBF, промивають 25мМ HEPES лишків, таких як аміни; лужні або органічні солі буфером, що містить 500мМ NaCl, і розраховують кислих залишків, таких як карбонові кислоти; і поклітини, пов'язані з 1251-МСР-1. дібні. Фармацевтично прийнятні солі включають У хемотаксичному дослідженні, хемотаксис звичайні нетоксичні солі або четвертинні амонієві проводять із застосуванням РВМС, збідненого Тсолі вихідної сполуки, утворені, наприклад, з нетоклітинами з цільної венозної крові або лейкофорексичних неорганічних або органічних кислот. Назної крові, і очищають центрифугуванням Фіколлприклад, такі звичайні нетоксичні солі включають Гіпак з подальшим розетингом з обробленими солі, одержані з неорганічних кислот, таких як хлонейрамінідазом еритроцитами овець. Після видіристоводнева, бромистоводнева, сірчана, сульлення клітини промивають HBSS, що містить фамінова, фосфорна, азотна і подібна; і солі, оде0,1мг/мл BSA, і суспендують при 1 107клітин/мл. ржані з органічних кислот, таких як оцтова, Клітини мітять в темряві флуоресцентом з 2мкМ пропіонова, янтарна, гліколева, стеаринова, молоCalcien-AM (молекулярні проби) протягом 30 хвична, яблучна, винна, лимонна, аскорбінова, памолин при температурі 37°С. Мічені клітини двічі ва, малеїнова, гідроксималеїнова, фенілоцтова, промивають і суспендують при 5 106клітин/мл в глутамінова, бензойна, саліцилова, сульфаніліноRPMI 1640 з L-глутаміном (без червоного фенолу), ва, 2-ацетоксибензойна, фумарова, толуолсульщо містить 0,1мг/мл BSA. MCP-1 (Petrotech) при фонова, метансульфонова, етандисульфонова, 10нг/мл розводять в тому ж середовищі або тільки щавлева, ізетіонова і подібні. середовище додають на дно ямок (27мкл). У верхФармацевтично прийнятні солі відповідно до ню частину фільтра додають моноцити (150000 даного винаходу можуть бути одержані з вихідних клітин) (30мкл) з подальшим 15 хвилинним попесполук, які містять основну або кислотну групу, реднім інкубуванням з ДМСО або з різними концезвичайними хімічними методами. Звичайно такі нтраціями сполуки, що тестується. У рівних концесолі можуть бути одержані взаємодією вільної кинтраціях сполуку, що тестується, або ДМСО слої або основної форми вказаних сполук зі стехідодають на дно ямок для запобігання розбавленометричною кількістю відповідної основи або кисню дифузією. Після 60хв. інкубації при температурі лоти у воді або органічному розчиннику, або в 37°С, 5% СО2, фільтр видаляють і верхню частину суміші обох; переважно в неводному середовищі, промивають HBSS, що містить 0,1мг/мл BSA для такому як простий ефір, етилацетат, етанол, ізопвидалення клітин, які не перейшли на фільтр. ропанол або ацетонітрил. Відповідні солі описані, Спонтанну міграцію (хемокінез) визначають за [наприклад, в Remington's Pharmaceutical Sciences, відсутності хемоатрактанту. 17th ed., Mack Publishing Company, Easton, PA, Зокрема, сполуки з представлених нижче при1985, стор.1418]. кладів володіють активністю при зв'язуванні з Визначені сполуки відповідно до даного винаCCR-2 рецептором у вказаному вище дослідженні, ходу включають сполуки, які вибирають з групи, звичайно з ІС50 приблизно нижче 1мкМ. Такі рещо включає: сполуки, вказані в заголовках приклазультати показують активність, властиву сполукам дів; і їх фармацевтично прийнятні солі і окремі при застосуванні їх як модуляторів активності редіастереомери. цептора хемокіну. 9 75828 10 Рецептори хемокіну ссавців являють собою льні хвороби кишечнику, такі як хвороба Крона і мішень для втручання або стимулювання функції виразковий коліт; спондилоартропатії; склеродереозинофілу і/або лімфоцитів у ссавців, таких як ма; псоріаз (включаючи псоріаз, медійований Тлюдина. Сполуки, які інгібують або стимулюють клітинами) і запальні шкірні хвороби, такі як дерфункцію рецептора хемокіну, особливо корисні матит, екзема, атопічний дерматит, алергічний для модулювання функції еозинофілу і/або лімфоконтактний дерматит, кропивниця; васкуліт (нациту для терапевтичних цілей. Отже, сполуки, які приклад, некротизований, 1Нкірний і гіперчутливий інгібують або стимулюють функцію рецептора хеваскуліт); еозинофільний міозит, еозинофільний мокіну, можуть бути корисні для лікування, профіфасцит; рак шкіри або органів з інфільтрацією лактики, поліпшення, контролю або зниження рилейкоцитів. Інші захворювання або стани, при яких зику широкого спектра запальних і можуть лікуватись небажані інгібовані запальні імунорегуляторних розладів і захворювань, алергіреакції, включають, але не обмежені ними, реперчних захворювань, атонічних станів, включаючи фузійні пошкодження, атеросклероз, певні гематоалергічний риніт, дерматит, кон'юнктивіт і астму, а логічні злоякісні утворення, викликана цитокіном також аутоімунних патологій, таких як ревматоїдтоксична реакція (наприклад, септичний шок, енний артрит і атеросклероз. Наприклад, сполука дотоксичний шок), поліміозит, дерматоміозит. миттєвої дії, яка інгібує одну або більше функцій Захворювання або стани людей або інших вирецептора хемокіну ссавця (наприклад, рецептора дів, які можуть лікуватись модуляторами дії рецепхемокіну людини), може вводитись для інгібування тора хемокіну, включають, але не обмежені ними: (наприклад, зниження або профілактик) запаленімунодепресію, таку як у пацієнтів з синдромом ня. В результаті інгібується один або більше запаімунодефіциту, таким як СНІД або інші вірусні інльних процесів, таких як еміграція лейкоцитів, хефекції, у пацієнтів, що приймають променеве лікумотаксис, екзоцитоз (наприклад, ферментів, вання, хіміотерапію, терапію для аутоімунних загістаміну) або виділення медіатора запалення. хворювань або лікарську терапію (наприклад, В доповнення до приматів, таких як людина, терапію кортикостероїдами), які викликають імунометод відповідно до даного винаходу може застодепресію; імунодепресію внаслідок природженого совуватись для лікування різних інших ссавців. дефіциту функції рецептора або інших причин; та Наприклад, можна лікувати ссавців, що включаінфекційні захворювання, такі як паразитичні зають, але не обмежених ними, корів, овець, кіз, кохворювання, включаючи, але, не обмежуючись ней, собак, кішок, морських свинок, щурів або інними, гельмінтні інфекції, такі як нематоди (круглі ших коров'ячих, овечих, конячих, собачих, котячих, черв'яки), (Trichuriasis, Enterobiasis, Ascariasis, щурячих або мишачих видів. Однак метод також Hookworm, Strongylodiasis, Trichinosis, Filariasis), може застосовуватись до інших видів, таких як трематоди (плоскі черв'яки) (Schistosomiasis, пернаті (наприклад, кури). Clonorchiasis), цестоди (стрічкові черв'яки) Захворювання і стани, пов'язані із запаленням (Echinococcosis, Taeniasis saginata, Cysticercosis), та інфекцією, можуть лікуватись із застосуванням вісцеральні черв'яки, мігрені від вісцеральних лисполук відповідно до даного винаходу. У переважчинок (наприклад, Тохосага), еозинофільні гастроному варіанті захворюванням або станом є таке, в ентерити (наприклад, Anisaki sp., Phocanema sp.) і якому дія лімфоцитів інгібується або стимулюється мігрені від шкірних личинок (Ancylostona для модулювання запальної реакції. brazilience, Ancylostoma caninum). Крім того, лікуЗахворювання і стани людини та інших видів, вання вказаних вище запальних, алергічних і аутоякі можуть лікуватись інгібіторами функції рецепімунних захворювань може проводитись для протора хемокіну, включають, але не обмежені ними: моторів функції рецептора хемокіну, якщо вони запальні або алергічні захворювання і стани, забезпечують доставку достатньої кількості сполувключаючи респіраторні алергічні захворювання, ки для припинення експресії рецептора в клітинах такі як астма, особливо бронхіальна астма, алергічерез індукування інтерналізації рецептора хемочний риніт, гіперчутливість легень, гіперчутливий кіну, або доставку сполуки способом, який додає пульмоніт, еозинофільна пневмонія (наприклад, неправильний напрям міграції клітин. синдром Леффлера, хронічна еозинофільна пневСполуки відповідно до даного винаходу корисмонія), гіперчутливість уповільненого типу, проміні для лікування, профілактики, поліпшення, контжна хвороба легень (ПХЛ) (наприклад, ідіопатичролю або зниження ризику широкого спектра заний фіброз легень або ПХЛ, пов'язана з пальних та імунорегуляторних розладів і ревматоїдним артритом, системний червоний вовзахворювань, алергічних станів, атонічних станів, чак, анкілозуючий спондиліт, системний склероз, а також аутоімунних патологій. У певному варіанті, синдром Сйоргена, поліміозит або дерматоміозит); даний винахід відноситься до застосування сполук системна анафілаксія або реакція гіперчутливості, відповідно до даного винаходу для лікування, алергії до лікарських засобів (наприклад, до пеніпрофілактики, поліпшення, контролю або зниженциліну, цефалоспоринів), алергія до укусів комах; ня ризику аутоімунних захворювань, таких як реваутоімунні захворювання, такі як ревматоїдний матоїдний артрит або псоріазний артрит. артрит, псоріазний артрит, розсіяний склероз, сисВ іншому варіанті, даний винахід може застотемний червоний вовчак, бульбоспінальний парасовуватись для оцінки передбачуваних специфічліч, дитячий початковий діабет; гломерулонефрит, них агоністів або антагоністів рецепторів хемокіну, аутоїмунний тироїдит, хвороба Беккета; відторгвключаючи CCR-2. Отже, даний винахід віднонення трансплантату (наприклад, при транспланситься до застосування таких сполук для одертації), включаючи відторгнення алотранспланту жання і проведення скринінгових досліджень споабо реакцію «трансплантат проти хазяїна»; запалук, які модулюють активність рецепторів 11 75828 12 хемокіну. Наприклад, сполуки відповідно до даного Термін «композиція», що використовується в винаходу корисні для виділення мутантів рецептоданому описі, відноситься до продукту, який місра, які є чудовими інструментами для скринінгу тить певні інгредієнти в певних кількостях, а також більш могутніх сполук. Більш того, сполуки відподо будь-якого продукту, який одержують, прямо відно до даного винаходу корисні для встановленабо опосередковано, з поєднання певних інгредієня або визначення місця зв'язування інших сполук нтів у певних кількостях. Під «фармацевтично з рецепторами хемокіну, наприклад, за допомогою прийнятним» розуміють носій, розріджувач або конкурентного інгібування. Сполуки відповідно до ексципієнт, який повинен бути сумісний з іншими даного винаходу також корисні для оцінки передінгредієнтами препаративної форми, і не завдавабачуваних специфічних модуляторів рецепторів ти шкоди пацієнту. Під термінами «введення» і/або хемокіну, включаючи CCR-2. Як визнано в даній «сполука, що вводиться» розуміють забезпечення галузі техніки, всебічній оцінці специфічних агоніссполукою відповідно до даного винаходу пацієнта тів і антагоністів вказаних вище рецепторів хемокіза необхідності лікування. У цьому випадку термін ну перешкоджає відсутність доступності не«лікування» означає як лікування, так і профілакпептидних (метаболічно стійких) сполук з високою тику або профілактичну терапію вказаних вище спорідненістю зв'язування до таких рецепторів. станів. Таким чином, сполуки відповідно до даного винаКомбінована терапія для модулювання активходу є комерційними продуктами, які можуть проності рецептора хемокіну для лікування, профілакдаватись в цих цілях. тики, поліпшення, контролю або зниження ризику Даний винахід також відноситься до способу запальних і імунорегуляторних розладів і захвоодержання медикаменту для модулювання активрювань, включаючи астму і алергічні хвороби, а ності рецептора хемокіну у людини і тварин, що також аутоімуні патології, такі як ревматоїдний включає об'єднання сполуки відповідно до даного артрит і атеросклероз, і патології, вказані вище, винаходу з фармацевтичним носієм або розріджуілюструється поєднанням сполук відповідно до вачем. даного винаходу та інших сполук, які відомі для Даний винахід також відноситьсядо застосутаких цілей. вання даних сполук для лікування, профілактики, Наприклад, при лікуванні, профілактиці, пополіпшення, контролю або зниження ризику інфекліпшенні, контролі або зниженні ризику запалення, ції ретровірусом, зокрема, вірусом герпеса або сполука даного винаходу може застосовуватись в вірусом імунодефіциту людини (ВІЛ), або лікуванпоєднанні з протизапальними або аналгезуючими ня і затримання настання подальших патологічних агентами, такими як агоніст опіату, інгібітор ліпокстанів, таких як СНІД. Лікування СНІД або профісигенази, такий як інгібітор 5-ліпоксигенази, інгібілактика або лікування інфекції ВІЛ визначено як тор циклооксигенази, такий як інгібітор циклоокситаке, що включає, але не обмежене ними, лікувангенази-2, інгібітор інтерлейкіну, такий як інгібітор ня широкого спектра станів ВІЛ інфекцій: СНІД, інтерлейкіну-1, антагоніст NMDA, інгібітор оксиду СПК (СНІД-пов'язаний комплекс), симптоматичний азоту або інгібітор синтезу оксиду азоту, нестероїі безсимптомний, і гострий або потенційний кондний протизапальний засіб або цитокінтакт з ВІЛ. Наприклад, сполуки відповідно до данопереважний протизапальний засіб, наприклад, зі го винаходу корисні для лікування інфекції ВІЛ сполукою, такою як ацетамінофен, аспірин, кодеїн, після передбачуваного контакту з ВІЛ через, наембрел, фентаніл, ібупрофен, індометацин, кетоприклад, переливання крові, трансплантації оргаролак, морфін, напроксен, фенацетин, піроксикам, нів, обміну рідинами тіла, укусів, випадкових уколів стероїдний аналгетик, суфентаніл, санліндак, теголкою або контакту з кров'ю пацієнта під час хірунідап і подібні. Також, сполуки відповідно до даноргічних операцій. го винаходу можуть вводитись із знеболюючими; У переважному варіанті даного винаходу спопотенціюючими засобами, такими як кофеїн, анталука відповідно до даного винаходу може застосогоністом Н2, симетиконом, гідроксидом алюмінію вуватись у способі інгібування зв'язування хемокіабо магнію; протизастійним засобом, таким як фену з рецептором хемокіну, таким як CCR-2 клітини нілефрин, фенілпропаноламін, псевдофедрин, мішені, який включає взаємодію клітини мішені з оксиметазолін, ефінефрин, нафазолін, ксилометакількістю сполуки, яка є ефективною для інгібуваннолін, пропілгексендрин або ліво-дезоксиня зв'язування хемокіну з рецептором хемокіну. ефедрин; засобом проти кашлю, таким як кодеїн, Об'єктом лікування у вказаному вище способі гідрокодон, караміфен, карбетапентан або декє ссавець, переважно людина, чоловічої або жіностраметофан; сечогінним; і седативним або несечої статі, для якої бажано модулювання активності дативним антигістаміном. рецептора хемокіну. «Модулювання» в даному Також сполуки відповідно до даного винаходу контексті має на увазі антагонізм, агонізм, часткоможуть застосовуватись в поєднанні з іншими лівий антагонізм, обернений агонізм і/або частковий карськими засобами, які застосовуються для лікуагонізм. У переважному варіанті даного винаходу вання/профілактики/придушення або зменшення модулювання відноситься до антагонізму відносно інтенсивності симптомів захворювань або станів, активності рецептора хемокіну. Термін «терапевдля яких корисні сполуки відповідно до даного тично ефективна кількість» означає таку кількість винаходу. Такі інші лікарські засоби можуть вводисполуки відповідно до даного винаходу, яка виклитись способом і в кількості, що застосовується кає біологічну або медичну реакцію тканини, сисзвичайно, одночасно або послідовно зі сполукою теми, тварини або людини, яка очікується дослідвідповідно до даного винаходу. Якщо сполуку відником, ветеринаром, лікарем або іншим повідно до даного винаходу застосовують одночаклініцистом. сно з одним або декількома лікарським засобами, 13 75828 14 переважно застосовувати фармацевтичну компостатини), секвестра™ (холестирамін і колестипол), зицію, що містить такі інші лікарські засоби в допоінгібітори абсорбції холестерину (езитиміб), похідні внення до сполуки відповідно до даного винаходу. нікотинової і фенофібрової кислоти (гемфіброзил, Отже, фармацевтичні композиції відповідно до клофібрат, фенофібрат і бензафібрат) і пробукол; даного винаходу являють собою такі композиції, (k) протидіабетичні агенти, такі як інсулін, сульфоякі також містять один або декілька інших активних нілсечовини, бігуаніди (метформін), інгібітори аінгредієнтів, в доповнення до сполуки відповідно глюкозидази (акарбоза) і глітазони (троглітазон і до даного винаходу. піоглітазон); (1) препарати інтерферону бета (інтеПриклади інших активних інгредієнтів, які морферон бета-1α, інтерферон бета-1β); (m) інші жуть об'єднуватись зі сполукою відповідно до дасполуки, такі як 5-аміносаліцилова кислота і її проного винаходу, і вводитись окремо або в тій же ліки, антиметаболіти, такі як азатіоприн і 6фармацевтичній композиції, включають, але не меркаптопурин і цитотоксичні хіміотерапевтичні обмежені ними: (а) антагоністи VLA-4, такі як [опиагенти для лікування ракових захворювань. сано в US 5510332, WO 95/15973, WO 96/01644, Масове співвідношення сполуки відповідно до WO 96/06108, WO 96/20216, WO 96/22966, WO даного винаходу до другого активного інгредієнта 96/31206, WO 96/40781, WO 97/03094, WO може варіюватись і залежить від ефективної дози 97/02289, WO 98/42656, WO 98/53814, WO кожного інгредієнта. Загалом, застосовується ефе98/53817, WO 98/53818, WO 98/54207 і WO ктивна доза кожного інгредієнта. Таким чином, 98/58902], (b) стероїди, такі як беклометазон, менаприклад, якщо сполуку відповідно до даного тилпреднізолон, бетаметазон, преднізолон, деквинаходу об'єднують з NSAID, масове співвідносаметазон і гідрокортизон; (с) імунодепресанти, шення сполуки відповідно до даного винаходу до такі як циклоспорин, такролімус, рапаміцин та інші NSAID звичайно варіюється від близько 1000:1 до імунодепресанти типу FK-506; (d) антигістаміни близько 1:1000, переважно від близько 200:1 до (антагоністи Н1-гістаміну), такі як бромфенірамін, 1:200. Поєднання сполуки відповідно до даного хлорфенірамін, дексхлорфенірамін, трипролідин, винаходу та інших активних інгредієнтів звичайно клемастин, дифенгідрамін, дифенілпіралін, трипетакож знаходиться у вказаних вище межах, але в ленамін, гідроксизин, метдилазин, прометазин, кожному випадку повинна застосовуватись ефектримепразин, азатадин, ципрогептадин, антазолін, тивна доза кожного інгредієнта. У таких комбінаціфенірамін, піриламін, астемізол, терфенадин, лоях сполуки відповідно до даного винаходу та іншоратадин, дезлоратадин, цетиризин, фексофенаго активного інгредієнта можуть вводитись окремо дин, дезкарбоетоксилоратадин і подібні; (e) нестеабо в поєднанні. Крім того, введення одного елероїдні протиастматичні засоби, такі як β2-агоністи мента може здійснюватись перед, під час або піс(тербуталін, метапротеренол, фенотерол, ізоеталя введення іншого агента (агентів). рин, альбутерол, бітолтерол і пірбутерол), теофіСполуки відповідно до даного винаходу молін, кромолін натрію, атропін, іпратропію бромід, жуть вводитись пероральним, парентеральним антагоністи лейкотриєну (зафірлукаст, монтелушляхами (наприклад, внутрішньом'язовим, внуткаст, пранлукаст, іралукаст, побілукаст, SKB-106, рішньочеревинним, внутрішньовенним, інтрецере203), інгібітори біосинтез лейкотриєну (зилеутон, бровентрикулярним шляхами, інтрацистернальBAY-1005); (f) нестероїдні протизапальні засоби ними ін'єкціями або інфузіями, підшкірним (NSAID), такі як похідні пропіонової кислоти (альін'єкціями або імплантатами), інгаляцією, інтранамінопрофен, беноксапрофен, буклоксова кислота, зальним, ректальним, вагінальним, під'язиковим капрофен, фенбуфен, фенопрофен, флупрофен, або місцевими шляхами введення і можуть бути флурбіпрофен, ібупрофен, індопрофен, кетопросформульовані, по одному або разом, у відповідні фен, міропрофен, напроксен, оксапрозин, пірпростандартні лікарські форми, що містять звичайні, фен, пранопрофен, супрофен, тіарофенова кислонетоксичні, фармацевтично прийнятні носії, ад'юта і тіоксапрофен), похідні оцтової кислоти ванти і наповнювачі, відповідні для кожного шляху (індометацин, ацеметацин, алклофенак, кліданак, ведення. Крім лікування теплокровних тварин, диклофенак, фенклофенак, фенклозова кислота, таких як миші, щури, коні, худоба, вівці, собаки, фентіазак, фурофенак, ібуфенак, ізоксепак, окспікішки, мавпи і т.д., сполуки відповідно до даного нак, зуліндак, тіопінак, толметин, зидометацин і винаходу є ефектними для лікування людей. зомепірак), похідні фенамінової кислоти (флуфеФармацевтичні композиції для введення спонамінова кислота, меклофенамінова кислота, мелук відповідно до даного винаходу можуть бути у фенамінова кислота, ніфлумінова кислота і толзручних стандартних лікарських формах і можуть фенамінова кислота), похідні біфенілкарбонової бути одержані будь-яким методом, добре відомим кислоти (дифлунізал і флуфенізал), оксиками (ізов галузі фармацевтики. Всі методи включають ксикам, піроксикам, судоксикам і теноксикам), састадію об'єднання активного інгредієнта з носієм, ліцилати (ацетилсаліцилова кислота, сульфазалаякий складається з одного або декількох додаткозин) і піразолони (апазон, безпіперилон, фепразон, вих інгредієнтів. Загалом, фармацевтичні компомофебутазон, оксифенбутазон, фенілбутазон); (g) зиції одержують однорідним і ретельним з'єднанінгібітори циклооксигенази-2 (СОХ-2); (h) інгібітори ням активного інгредієнта з рідким носієм або фосфодіестерази типу IV (PDE-IV); (і) інші антаготонкоподрібненим твердим носієм, або обома, і ністи рецепторів хемокіну, особливо CCR-1, CCRпотім, за необхідності, формуванням продукту в 2, CCR-3, CXCR-3 і CCR-5; (j) агенти, понижувальбажану лікарську форму. У фармацевтичній комні холестерин, такі як інгібітори HMG-СоА редуктапозиції активна сполука міститься в кількості, досзи (ловастатин, симвастатин і правастатин, флутатній для одержання бажаного ефекту в наявновастатин, аторвастатин, розувастатин та інші му процесі або стані захворювання. У даному 15 75828 16 контексті термін "композиція" відноситься до проефірів, одержаних з жирних кислот і гекситолу, такі дукту, що містить певні інгредієнти в певних кільяк поліоксіетилен сорбітолмоноолеат, або продуккостях, а також до будь-якого продукту, який одети конденсації етиленоксиду і часткових ефірів, ржують прямо або опосередковано, з поєднання одержаної з жирних кислот і ангідридів гекситолу, певних інгредієнтів в певних кількостях. наприклад; поліетиленсорбітанмоноолеат. Водні Фармацевтичні композиції, що містять активсуспензії також можуть містити один або більше ний інгредієнт, можуть бути у формі, відповідній консервант, наприклад, етил або н-пропіл, ндля перорального застосування, наприклад, у вигідроксибензоат, один або більше барвник, один гляді таблеток, пастилок, водних або масляних або більше смаковий агент, один або більше підсуспензій, диспергованих порошків або гранул, солоджувач, такий як сахароза або сахарин. Масемульсій, жорстких або м'яких капсул, або сиропів ляні суспензії можуть бути одержані суспендуванабо еліксирів. Композиції, призначені для перораням активного інгредієнта в олії, наприклад, льного застосування, можуть бути одержані будьарахісовій олії, оливковій олії, конопляній олії або яким методом, відомим в галузі одержання фаркокосовій олії, або в мінеральному маслі, такому мацевтичних композицій, і такі композиції можуть як рідкий парафін. Масляні суспензії можуть містимістити один або більше агентів, вибраних з групи, ти загущувальний агент, наприклад, бджолиний що складається з підсолоджувачів, смакових агенвіск, твердий парафін або цетиловий спирт. Для тів, барвників і консервантів, для одержання фародержання приємних пероральних композицій момацевтично чудових і смачних композицій. Таблежуть бути додані підсолоджувачі, такі, як описано тки містять активний інгредієнт в "суміші з вище, і смакові агенти. Ці композиції можуть зберінетоксичними фармацевтично прийнятними ексгатись за допомогою додавання антиокислювача, ципієнтами, які підходять для одержання таблеток. такого як аскорбінова кислота. Дисперговані поЦі ексципієнти можуть бути, наприклад, інертними рошки і гранули, відповідні для одержання водної розріджувачами, такими як карбонат кальцію, карсуспензії додаванням води, містять активний інгбонат натрію, лактоза, фосфат кальцію або фосредієнт в суміші з диспергуючим або зволожуючим фат натрію; гранулюючими і розпушуючими агенагентом, суспендуючим агентом і одним або більтами, наприклад, кукурудзяним крохмалем або ше консервантами. Відповідні диспергуючі або альгіновою кислотою; зв'язувальними агентами, зволожуючі агенти і суспендуючі агенти представнаприклад, крохмалем, желатином або акацією, і лені тими, які вказані вище. Також можуть бути змащувальними агентами, наприклад, стеаратом присутніми додаткові наповнювачами, такі як підмагнію, стеариновою кислотою або тальком. Табсолоджувачі, смакові агенти і барвники. Фармацелетки можуть не мати оболонки або можуть бути втичні композиції відповідно до даного винаходу покриті відомими методами для того, щоб відкластакож можуть бути у вигляді емульсій масло у воти розкладання і абсорбцію в шлунково-кишковому ді. Масляна фаза може являти собою олію, напритракті і, тим самим, забезпечити пролонговану дію клад, оливкову олію або арахісову олію, або мінепротягом більш тривалого періоду. Наприклад, як ральне масло, наприклад, рідкий парафін або їх уповільнююча речовина може застосовуватись суміш. Відповідні емульгуючі агенти можуть бути така як гліцерилмоностеарат або гліцерилдистеаприродними смолами, наприклад, аравійською рат. Вони також можуть бути покриті із застосукамеддю або трагакантом, природними фосфативанням методик, [описаних в патентах США дами, наприклад, соєвими бобами, лецитином і 4256108, 4166452 і 4265874], з одержанням, осмоскладними ефірами або частковими ефірами, одетичних терапевтичних таблеток для вивільнення, ржаними з жирних кислот і ангідридів гекситолу, що контролюється. наприклад, моноолеатом сорбітану, і продуктами Композиції для перорального застосування конденсації вказаних часткових ефірів і етиленокможуть бути представлені в твердих желатинових сиду, наприклад, поліоксіетиленсорбітанмоноокапсулах, в яких активні інгредієнти змішані з інерлеатом. Емульсії також можуть містити підсолотним твердим розріджувачем, наприклад, карбоджувачі і смакові агенти, наприклад, гліцерин, натом кальцію, фосфатом кальцію або каоліном, пропіленгліколь, сорбіт або сахарозу. Такі компоабо в м'яких желатинових капсулах, в яких активні зиції також можуть містити болезаспокійливі засоінгредієнти змішані з водним або масляним сереби, консерванти і смакові агенти і барвники. довищем, наприклад, арахісовою олією, рідким Фармацевтичні композиції можуть бути у випарафіном або оливковою олією. Водні суспензії гляді стерильних водних або масляних суспензій містять активні матеріали в суміші з ексципієнтадля ін'єкцій. Ці суспензії можуть бути одержані ми, відповідними для одержання водних суспензій. відповідно до методів, відомих в даній галузі, із Такі ексципієнти включають суспендуючі агенти, застосуванням відповідних диспергуючих або змонаприклад, натрійкарбоксиметилцелюлозу, метичувальних агентів і суспендуючих Агентів, які вкалцелюлозу, гідроксипропілметилцелюлозу, альгізані вище. Стерильні лікарські форми для ін'єкцій нат натрію, полівінілпіролідон, трагакантову смолу також можуть бути стерильними розчинами або і аравійську камедь; диспергуючі або змочувальні суспензіями для ін'єкцій в нетоксичному парентеагенти являють собою природні фосфатиди, нарально прийнятному розріджувачі або розчиннику, приклад, лецитин або продукти конденсації алкінаприклад, в розчині 1,3-бутандіолу. Серед прийнленоксиду і жирних кислот, наприклад, поліоксіеятних носіїв і розчинників, які можуть застосовуватиленстеарат, або продукти конденсації тись, можна відмітити воду, розчин Рінгера та ізоетиленоксиду і довголанцюгових аліфатичних тонічний розчин хлориду натрію. Крім того, як спиртів, наприклад, гептадекаетиленоксицетанол, розчинник або суспендуюче середовище можуть або продукти конденсації етиленоксиду і часткових застосовуватись стерильні, жирні масла. Для цієї 17 75828 18 мети може застосовуватись будь-яке м'яке жирне що розкривається. Нижче представлені приклади масло, включаючи синтетичні моно- або дигліцеметодів одержання сполук, що використовуються у риди. Крім того, для одержання форм для ін'єкцій представлених нижче прикладах, або які можуть можуть застосовуватись жирні кислоти, такі як бути замісниками сполук, представлених у приколеїнова кислота. Сполуки відповідно до даного ладах, які можуть не бути комерційно дос-тупними. винаходу також можуть вводитись у вигляді супоКонцентрування розчинів звичайно здійснюзиторіїв для ректального введення лікарського ють на роторному випарнику при зниженому тиску. засобу. Такі композиції можуть бути одержані зміФлеш-хроматографію проводять на силікагелі шуванням лікарського засобу з відповідним непод(230-400меш). РХСТ - рідинну хроматографію серазнювальним ексципієнтом, який є твердим при реднього тиску, проводять в нерухомій фазі силізвичайних температурах, але рідким при ректалькагелю, якщо не указано інакше. ЯМР спектр оденій температурі і, отже, плавиться в прямій кишці ржують в розчині CDCl3, якщо не указано інакше. для вивільнення лікарського засобу. Такими матеКонстанти взаємодії (J) дані в герцах (Гц). Абревіріалами є кокосова олія і поліетиленгліколі. Для атури: діетиловий ефір (ефір), триетиламін (TEA), місцевого застосування використовують креми, Ν,Ν-діізопропілетиламін (ДІЕА), насичений водний мазі, желе, розчини або суспензії, і т.д., що містять (нас), кімнатна температура (кт), години (год.), сполуки відповідно до даного винаходу. (Для цілей хвилини (хв.). даного винаходу композиції для місцевого застоУ деяких випадках порядок проведення предсування включають полоскання для рота і полосставлених нижче реакцій може бути змінений, щоб кання для горла). сприяти реакції або уникнути небажаних продуктів Фармацевтичні композиції і спосіб відповідно реакції. Приклади представлені тільки для ілюстдо даного винаходу можуть також включати інші рації і не обмежують винахід, що розкривається. терапевтично активні сполуки, як указано вище, які Нижче представлені приклади методик одерзвичайно застосовують для лікування вказаних жання сполук, що використовуються у представпатологічних станів. При лікуванні, профілактиці, лених нижче прикладах, або які можуть бути заміполіпшенні, контролі і зниженні ризику станів, які сниками сполук, представлених у прикладах, які вимагають модулювання рецептора хемокіну, відможуть не бути комерційно доступними. повідне дозування звичайно складає від близько Проміжна сполука 1 0,01 до 500мг на кілограма маси тіла пацієнта на день і може вводитись однією або декількома дозами. Переважно, рівень дозування складає від близько 0,1 до 250мг/кг на день, більш переважно Проміжну сполуку 1 одержують за методикою, від близько 0,5 до близько 100мг/кг на день. Від[описаною в J. Am. Chem. Soc, 1991, 113,2079повідні дози складають від близько 0,01 до 2089]. 250мг/кг на день, від близько 0,05 до 100мг/кг на Проміжна сполука 2 день, від близько 0,1 до 50мг/кг на день. У цьому інтервалі доза може становити 0,05-0,5, 0,5-5 або 5-50мг/кг на день. Для перорального введення композиції переважно мають форму таблеток, що До розчину тетрагідро-4Н-піран-4-ону (5,0г, містять 1,0-1000 міліграм активного інгредієнта, 50ммоль) і гексаметилфосфораміду (8,70мл) в переважно 2,0-500, більш переважно 3,0-200, осотетрагідрофурані (150мл) повільно додають розбливо 1, 5, 10, 15, 20, 25, 30, 50, 75, 100, 125, 150, чин діізопропіламіду літію (31,25мл, 3М розчин) в 175, 200, 250, 300, 400, 500, 600, 750, 800, 900 і 125мл тетрагідрофурану при температурі -78°С. 1000 міліграм активного інгредієнта для доведення Реакційну суміш перемішують протягом 5хв. і подози в залежності від пацієнта, що піддається літім додають етилйодид (16,0мл, 200ммоль). Суміш куванню. Сполуки можуть вводитись в режимі від 1 поступово нагрівають до температури 0°С протядо 4 разів на день, переважно один або два рази гом більше 2год. Реакційну суміш гасять насичена день. ним розчином NH4Cl і потім екстрагують простим Повинно бути зрозуміло, що певний рівень доефіром (4 100мл). Ефірний шар промивають назування і частота дозування для будь-якого конксиченим розчином солі, сушать (безводний сульретного пацієнта може варіюватись і залежить від фат магнію), концентрують і очищають флешмножини факторів, включаючи активність певної хроматографією на колонці, елююючи сумішшю сполуки, що застосовується, метаболічну стійкість гексан/етилацетат (4:1) з одержанням проміжної і тривалість дії даної сполуки, віку, маси тіла, загасполуки 2 (1,20г, 20%). льного стану здоров'я, статі, дієти, способу і часу Проміжна сполука 3 введення, 1Нвидкості вивільнення, комбінації лікарського засобу, тяжкості певного стану і терапії, що приймається пацієнтом. Декілька способів одержання сполуки відповіСтадія А дно до даного винаходу проілюстровані в представлених нижче прикладах. Сполуки відповідно до даного винаходу можуть бути одержані модифікацією методик, описаних у прикладах. Вихідні До суміші 5,6-дигідро-4-метокси-2Н-пірану речовини одержують відомими методами або як (10,0г, 87,5ммоль) в метанолі (200мл.) при темпепоказано у прикладах. Представлені нижче прикратурі 0°С краплями додають розчин 3лади дані для ілюстрації і не обмежують винахід, хлорпероксибензойної кислоти (30,2г, 175ммоль) в 19 75828 20 метанолі (50мл) через додаткову лійку. ОдержаJ=5,95, 8,7Гц, 1Н), 3,74 (ддд, J=5,5, 8,5, 13,6Гц, ний розчин перемішують протягом 5год., даючи 1Н), 3,56 (дд, J=8,8, 11,3Гц, 1Н), 3,50 (с, ЗН), 2,61 йому нагріватись до кімнатної температури. Мета(арр дд, J=5,0, 8,9Гц, 2Н). нол видаляють при зниженому тиску з одержанням Проміжна сполука 4 білої твердої речовини. Речовину розчиняють в 500мл дихлорметану і охолоджують до температури 0°С. До суміші, що енергійно перемішується, порціями додають надлишок твердого гідроксиду кальцію (50-60г). Після перемішування протягом До суміші 5,6-дигідро-4-метокси-2Н-пірану ще 30хв. суміш фільтрують через шар целіту і фі(0,5г, 4ммоль) в суміші ацетонітрил/вода (15мл, льтрат випаровують при зниженому тиску з одер1:1) при кімнатній температурі додають жанням 11,62г (82%) бажаного продукту у вигляді біс(тетрафторборат) 1-(хлорметил)-4-фтор-1,4прозорої олії. діазоніабіцикло[2.2.2]октану (1,5г, 4,4ммоль, 1 Н ЯМР (500МГц, CDCl3) δ 3,88-3,80 (м, 2Н), SELECTFLUOR™) однією порцією і одержану реа3,73-3,68 (м, 2Н), 3,54-3,48 (м, 1H), 3,28 (с, 3Н), кційну суміш перемішують при кімнатній темпера3,27 (с, 3Н), 2,00-1,93 (м, 1H), 1,82-1,77 (м, 1Н). турі до завершення реакції. Потім додають тверСтадія В дий NaCl і реакційну суміш екстрагують простим ефіром (4 50мл). Ефірний шар сушать (безводний сульфат магнію) і концентрують з одержанням 0,34г (65%) вказаної в заголовку сполуки, яка не вимагає подальшого очищення. До охолодженого (0°С) розчину продукту зі 1 Н ЯМР(500МГц, CDCI3) δ 4,95 (м, -1Н), 4,4стадії А, проміжної сполуки 3 (9,40г, 58,0ммоль) в 4,21 (м, 2Н), 3,72-3,65 (м, 2Н), 2,75 (м, 2Н). тетрагідрофурані (200 мл) в атмосфері азоту повіПроміжна сполука 6 льно додають NaH (2,32г, 58,0ммоль) і одержану суспензію перемішують протягом 1год. при температурі 0°С. Потім до суспензії через шприц додають йодметан (7,22мл, 116ммоль) і одержану суміш перемішують протягом ночі, даючи їй Стадія А нагріватись до кімнатної температури. Реакцію гасять насиченим розчином хлориду амонію (200мл) і органічний шар потім видаляють, використовуючи ділильну лійку. Водний шар екстрагують простим ефіром (3 150мл) і всі органічні шари об'єднують, сушать над безводним сульфатом Суміш тетаргідро-4Н-піран-4-ону (10,0г, натрію, фільтрують і випаровують у вакуумі. Очи100ммоль) і піролідину (11г, 150ммоль) перемішущення проводять флеш-хроматографією на колоють при кімнатній температурі протягом 1год. нці, використовуючи градієнтне елюювання суміНадлишок піролідину видаляють у вакуумі і залишшю 10-60% простий ефір/гексан з одержанням шок сушать протягом ночі у високому вакуумі. 8,46г (83%) бажаного продукту у вигляді прозорої Енамін одержують у вигляді жовтої рідини (14,7г), олії. 1 яку використовують на наступній стадії без подаН ЯМР(500МГц, CDCI3) δ 3,98 (дд, J=2,5, льшого очищення. 12,4Гц, 1Н), 3,77 (ддд, J=3,5, 7,1, 10,8Гц, 1Н), 3,57 Стадія В (дд; J=l,4, 12,4Гц, 1Н), 3,50 (дд, J=2,5, 11,7Гц, 1Н), 3,46 (с, 3Н), 3,25 (с, 3Н), 3,22 (с, 3Н), 3,22-3,20 (м, 1Н), 1,96 (ддд, J=4,7, 11,8, 16,5Гц, 1Н), 1,75 (уш.дд,а=1,7, 14,2Гц, 1Н). Стадія С Енамін, одержаний на стадії А, проміжну сполуку 6 (1,54г, 10ммоль) і 4-Ν,Ν-диметилпіридин (1,22г) обробляють Ν,Ν-диметилформамідом (25мл). Суміш охолоджують до температури 0°С і додають твердий трифторметансульфонат 5Розчин продукту зі стадії В, проміжної сполуки (трифторметил)дибензотіофенію (4,0г, 10ммоль). 3 (3,0г, 17,04ммоль) в суміші тетрагідрофуОдержану суміш перемішують при температурі ран/вода (60мл/10мл) обробляють концентрова0°С протягом 1год., потім гасять 30мл концентроною хлористоводневою кислотою (6мл) і одержаваної водної НСl. Одержану суміш перемішують ний розчин перемішують при кімнатній протягом 2год. і потім екстрагують простим ефіром температурі протягом 1год. Суміш концентрують у (4 70мл). Об'єднані ефірні шари промивають вовакуумі для видалення тетрагідрофурану і потім дою (50мл) і насиченим розчином солі (50мл), суводний шар екстрагують простим ефіром (6x50 шать над Na2SO4, фільтрують і випаровують. Замл). Органічні шари об'єднують, сушать над сульлишок очищають на силікагелі (елюент: 10% фатом натрію, фільтрують і випаровують при зниефір/гексан) з одержанням двох компонентів. женому тиску з одержанням проміжної сполуки 24 Більш полярний компонент (200мг) є бажаним (1,75г, 79%) у вигляді прозорої олії. 1 продуктом. 1Н-ЯМР показав, що продукт може ісН ЯМР(500МГц, CDCI3) δ 4,23 (ддд, J=1,2, нувати у формі напівкеталю. 11,4, 12,4Гц, 1Н), 4,15-4,09 (м, 1Н), 3,82 (дд, 21 75828 22 Н ЯМР (500МГц, CDCI3) δ 4,43-3,38 (м, 5Н), тним холодильником протягом ночі. Реакційну су3,24, 3,18 (сс, 3Н) 2,52 (м, 1Н), 1,82 (м, 1Н). міш охолоджують і дають вистоюватись при кімнаМенш полярний продукт (100мг) підтверджутній температурі протягом 7 днів. Реакційну суміш ють* як альфа-альфа'-дитрифторметилтетрагідровиливають у воду і екстрагують етилацетатом (3х). 4Н-піран-4-он. Об'єднані органічні шари промивають водою (2х), 1 H ЯМР (500МГц, CDCI3) δ 4,59 (дд, 2Η), 3,24, насиченим NaHCO3 і насиченим розчином солі, 3,80 (τ, J=l 1,3Гц, 2H), 3,42 (м, 2Н). сушать над Na2SO4, фільтрують і концентрують у Проміжна сполука 7 вакуумі з одержанням бажаного продукту у вигляді коричневого порошку (17,84г, 90%). 1 HЯМР (400 МГц, CD3OD) δ 8,37 (д, J=2,7Гц, 1Н), 8,19 (кв, J=0,7Гц, 0,3Гц, 1Н). Стадія А Стадія D 1 До розчину 5-трифторметил-2-піридиналю (51г, 310ммоль) і ацетату натрію (26,2г, 319ммоль) в крижаній оцтовій кислоті (200мл) додають бром (16,7мл, 325ммоль) і одержану суміш нагрівають до температури 80°С протягом 2,5год. Реакційну суміш охолоджують до кімнатної температури і потім випаровують при зниженому тиску. Залишок нейтралізують насиченим NaHCO3 розчином і екстрагують етилацетатом (3 200мл). Органічні шари об'єднують, сушать над MgSO4, фільтрують і випаровують у вакуумі з одержанням 74,45г (98%) неочищеного продукту. 1 Н ЯМР(400МГц, CDCI3) δ 8,04 (д, J=2,6Гц, 1Н), 7,89 (м, 1Н). Стадія В В атмосфері азоту заміщений піридин, описаний на стадії А, проміжну сполуку 7 (48,8г, 202ммоль) додають невеликими порціями до суспензії NaH (8,9г, 220ммоль) в безводному тетрагідрофурані (500мл). Після завершення додавання проміжної сполуки реакційну суміш охолоджують до температури -78°С і обробляють третбутиллітієм (260мл, 444ммоль), який додають краплями через шприц. Після перемішування протягом 5хв. повільно додають Ν,Ν-диметилформамід (50мл, 707ммоль) для підтримки температури розчину нижче - -50°С. Одержану суміш потім перемішують протягом 10год., даючи їй нагріватись до кімнатної температури. Суміш гасять 2н НСl і потім розбавляють етилацетатом (1000мл). Органічний шар відділяють, промивають насиченим розчином солі, сушать над MgSO4 і випаровують у вакуумі. Бажаний продукт осаджують з етилацетату і гексану і фільтрують з одержанням світло-коричневої твердої речовини (28,55г, 74%). 1 Н ЯМР(500МГц, CD3OD) δ 10,13 (с, 1Н), 8,21 (с, 2Н). Стадія C Суміш проміжної сполуки зі стадії В, проміжної сполуки 7 (18г, 95ммоль), форміату натрію (7,1г, 110ммоль), гідрохлориду гідроксиламіну (7,3г, 110ммоль) і мурашиної кислоти (150мл) перемішують при кімнатній температурі протягом 2год. і потім нагрівають до температури кипіння зі зворо До суміші оксихлориду фосфору (13.4мл, 144ммоль) і хіноліну (8,7мл, 73ммоль) додають продукт зі стадії С, проміжну сполуку 8 (24,6г, 131ммоль) і одержану суміш нагрівають до температури кипіння зі зворотним холодильником протягом 3год. Реакційну суміш охолоджують до температури 100°С перед повільним додаванням води (70мл). Потім суміш охолоджують до кімнатної температури і обережно нейтралізують насиченим NaHCO3 розчином. Водний шар екстрагують етилацетатом (3х) і органічні шари об'єднують, сушать над MgSO4, фільтрують і випаровують у вакуумі. Неочищений продукт очищають флешхроматографією з одержанням (23,5г, 87%) бажаної сполуки. 1 Н ЯМР(500МГц, CDCI3) δ 8,88 (д, J=2,0Гц, 1Н), 8,26 (д, J=2,5Гц, 1Н). Стадія E До суспензії NaH (7,8г, 200ммоль) в тетрагідрофурані (100мл) в атмосфері азоту краплями додають розчин трет-бутилметилмалонату (20мл, 120ммоль) в безводному тетрагідрофурані (100мл) через шприц. Реакційну суміш перемішують протягом 0,5год., потім повільно додають розчин проміжної сполуки, одержаної на стадії D, проміжну сполуку 8 (20,1г, 97,6ммоль) в тетрагідрофурані (200мл), через шприц. Реакційну суміш перемішують при кімнатній температурі протягом ночі, потім гасять насиченим розчином NH4Cl. Органічний шар відділяють і водний шар екстрагують етилацетатом (3х). Об'єднані органічні шари промивають водою (3х), сушать над Na2SO4, фільтрують і випаровують у вакуумі. Флеш-хроматографія дає 31,76г (95%) чистого бажаного продукту. 1 Н ЯМР(500МГц, CDCI3) δ 9,03 (д, J=1,5Гц, 1Н), 8,25 (д, J=2,0Гц, 1Н), 5,25 (с, 1Н), 3,86 (с, 3Н), 1,52 (с, 9Н). Стадія F Суспензію Ni Ренея (1г) і продукту зі стадії Ε, проміжну сполуку 7 (18,2г, 52,9ммоль) в етанолі (130мл) вміщують на апарат Парра і гідрують при 40ф/д2 Н2 протягом ночі. Суспензію фільтрують через целіт і фільтрат випаровують у вакуумі з 23 75828 одержанням 16,35г (98%) неочищеного продукту. 1 Н ЯМР(500МГц, CDCI3) δ 8,83 (с, 1Н), 7,89 (с, 1Н), 7,82 (с, 1Н), 4,83 (д, J=16Гц, 1Н), 4,72 (с, 1Н), 4,49 (д, J=16Гц, 1Н), 1,45 (с, 9Н). Стадія G До суміші продукту зі стадіїJ, проміжної сполуки 7 (16г, 51ммоль) в-дихлорметані (60мл) додають ТФОК (30мл) і одержану суміш перемішують при кімнатній температурі протягом 0,5год. Розчин випаровують при зниженому тиску і залишок розчиняють в дихлорметані. Суміш нейтралізують повільним додаванням розчину насиченого бікарбонату натрію і органічний шар видаляють. Водний шар екстрагують дихлорметаном (4х) і об'єднані органічні шари сушать над Na2SO4, фільтрують і випаровують у вакуумі з одержання 10,42г (95%) бажаного продукту. 1 Н ЯМР(500МГц, CDCI3) δ 8,81 (с, 1Н), 7,78 (с, 1Н), 7,30 (с, 1Н), 4,63 (с, 2Н), 3,90 (с, 2Н). Стадія H До розчину продукту зі стадії G, проміжної сполуки 7 (18,0г, 83,3ммоль) в тетрагідрофурані (50 мл) додають 1,0М борану в тетрагідрофурані (417мл, 420ммоль) і одержаний розчин перемішують при кімнатній температурі протягом ночі. Розчин випаровують при зниженому тиску і залишок обробляють розчином 1% НСІ/метанол. Одержану суміш нагрівають до температури 50°С протягом ночі для розкладання комплексу борану. Обробку кислим метанолом повторюють двічі для того, щоб пересвідчитись у видаленні комплексу борану. Розчин такого неочищеного продукту (83,3ммоль, приблизно 100% перетворення) і діізопропілетиламіну (43мл, 250ммоль) в дихлорметані обробляють ди-трет-бутилдикарбонатом (35,4г, 167ммоль) і одержану суміш перемішують при кімнатній температурі протягом ночі. Розчин промивають насиченим водним розчином бікарбонату натрію, водою і насиченим розчином солі. Водні шари об'єднують і знову промивають дихлорметаном (2х). Потім об'єднані органічні шари сушать над Na2SO4, фільтрують і випаровують досуха. Неочищений продукт очищають флешхроматографією і РХСТ з одержанням (11,89г, 47%) у вигляді жовтої твердої речовини. 1 Н ЯМР(500МГц, CDCI3) δ 8,69 (с, 1Н), 7,66 (с, 1Н), 4,67 (с, 2Н), 3,79 (τ, J=6,0Гц, 2Н), 3,08 (τ, J=5,5Гц, 2Н), 1,51 (с, 9Н). Стадія I Продукт, описаний на стадії Η, проміжну сполуку 8 (11,89г) обробляють розчином 4н НСl в діоксані. Розчин перемішують при кімнатній температурі протягом 2год. і потім випаровують у вакуумі з одержанням проміжної сполуки 8 (10,85г, 99%) у вигляді жовтого порошку. РХ-МС для C9H10F3N2 розраховано 202,07, знайдено [М+Н]+ 203,0. Проміжна сполука 8 24 Методика А Стадія А Суміш (1S)-(+)-2-азабіцикло[2.2.1]гепт-5-ен-3ону (10,3г, 94,4ммоль) в етилацетаті (200мл) і 10% Pd/C (0,5г) гідрують при кімнатній температурі. Через 24 години реакційну суміш фільтрують і випаровують, залишаючи менше 10,4г (100%) продукту, який вміщують в 250мл метанолу і НСl (12М, 6мл). Одержану суміш перемішують при кімнатній температурі доти, доки реакція не завершиться (72год.). Випаровування метанолу з подальшим сушінням у високому вакуумі дає вказану в заголовку сполуку у вигляді не зовсім білої твердої речовини (16,0г, 96%.). 1 H ЯМР (500МГц, D2O): δ 3,70 (с, 3Н), 3,01 (м, 1Н), 2,38 (м, 1Н), 2,16-1,73 (м, 6Н). Стадія В До суспензії проміжної сполуки зі стадії А (10,2г, 56,8ммоль) в сухому дихлорметані (200мл) додають бензофенонімін (10,2г, 56,8ммоль) при кімнатній температурі і одержану суміш перемішують протягом 24год. Реакційну суміш фільтрують і фільтрат випаровують з одержанням жовтого масла, яке розтирають з простим ефіром (100мл), фільтрують і випаровують. Цю операцію повторюють двічі, щоб пересвідчитися, що продукт не містить домішки хлориду амонію. Одержану олію ретельно сушать у вакуумі з одержанням вказаної в заголовку сполуки (18,03г, >100%) і вона не вимагає подальшого очищення. 1 H ЯМP (500МГц, CDCI3): δ 7,5-7,18 (м, 10Н), 3,75 (м, 1Н), 3,7 (с, ЗН), 2,78 (м, 1Н), 2,26-1,71 (м,6Н). Стадія С До розчину діізопропіламіду літію (одержаного з діізопропіламіну (7,7г, 76ммоль) і н-бутиллітію (30,4мл, 2,5Μ в гексані, 76ммоль) в тетрагідрофурані (120мл) при температурі -78°С додають простий ефір зі стадії В (18,0г, 56,8ммоль). Одержаний розчин червоного кольору перемішують протягом 20хв., потім гасять 2-йодпропаном (14,9мг, 88ммоль). Реакційну суміш поступово нагрівають протягом 3 годин до температури 0°С і таку температуру підтримують протягом ще 3 годин. Реакцію гасять водою і екстрагують етилацетатом. Органічний шар промивають водою, насиченим розчином солі, сушать (безводний сульфат магнію) і концентрують з одержанням олії. До розчину неочищеної основи Шиффа (20,0г) в тетрагідрофурані (100мл) додають НСl (5,0мл, 12М). Одержану реакційну суміш перемішують при кімнатній температурі протягом 3год. Після видалення всіх 25 75828 26 летких речовин гідрохлоридну сіль вміщують в дихлорметан (250мл), додають насичений розчин бікарбонату натрію (250мл) і ди-третбутилдикарбонат (26,0г, 1,4екв.). Одержану суміш До розчину біс(триметилсиліл)аміду літію відділяють і промивають водою, насиченим розчи(10,4г, 62,1ммоль) в тетрагідрофурані (100мл) доном солі, сушать (безводний сульфат магнію) і дають розчин проміжної сполуки зі стадії В (6,71г, концентрують з одержанням олії. Очищення 27,8ммоль) в тетрагідрофурані (10мл) протягом флеш-хроматографією на колонці (елюент: гек10хв. при температурі -78°С. Одержаний розчин сан/етилацетат 19:1) дає бажаний продукт (4,91г, перемішують при температурі -78°С протягом 30%). 30хв., потім додають однією порцією ізопропілйо1 H ЯМP (500МГц, CDCI3): 4,79 (уш., 1Н), 4,01 дид (3,3мл, 33ммоль). Реакційну суміш нагрівають (м, 1Н), 3,71 (с, 3Н), 2,18-1,60 (м, 6Н), 1,44 (с, 9Н), до температури -25°С і цю температуру підтриму0,87 (д, J=6, 9Гц, 3Н), 0,86 (д, J=6,9Гц, 3Н). ють протягом ночі. Потім реакцію гасять насичеСтадія D ним водним розчином NH4Cl (250мл). Органічний шар відділяють і водний шар далі екстрагують діетиловим ефіром (3 100мл). Об'єднані органічні шари потім промивають насиченим розчином солі (1 100мл), сушать над безводним Na2SO4, фільтДо розчину складного ефіру зі стадії С (4,91г, рують, концентрують і очищають флеш17; 2ммоль) в метанолі (100мл) додають розчин хроматографією (5-10% етилацетат/гексан) з одеLiOH (3,6г, 85ммоль) у воді (20мл) і тетрагідрофуржанням продукту (5,66г, 72%) у вигляді прозорої рані (10мл). Одержану суміш нагрівають до темпеолії (цис/транс=4,3/1). ратури 80°С до завершення реакції (18год). Мета1 Н ЯМР(500МГц, CDCI3) цис-ізомер: δ 5,79 (с, нол видаляють у вакуумі і неочищений продукт 2Н), 4,75 (м, 1Н), 3,72 (с, 3Н), 2,28-2,20 (м, 2Н), 2,0 вміщують в суміш вода/етилацетат (200мл, 1:4) і (дд, J=15, 4Гц, 1Н), 1,45 (с, 9Н), 0,85 (д, J=6, 6Гц, охолоджують до температури 0°С. Кислотність 3Н), 0,81 (д, J=7Гц, 3Н). суміші доводять до рН6. Шар етилацетату віддіСтадія D ляють, промивають водою, насиченим розчином солі, сушать (безводний сульфат магнію) і концентрують з одержанням олії. Очищення флешхроматографією на колонці (елюент: гекДо розчину продукту зі стадії С (1,6г, сан/етилацетат 1:1+2% АсОН) дає проміжну спо5,7ммоль) в тетрагідрофурані (50мл), метанолі луку 8 (3,9г, 84%). 1 (50мл) і воді (10мл) додають моногідрат LiOH Н ЯМР(500МГц, CDCI3): 11,36 (уш., 1Н), 6,49 (400мг) і реакційну суміш нагрівають до темпера(уш., 1Н), 4,83 (м, 1Н), 3,71 (с, 3Н), 2,30-1,55 (м, тури кипіння зі зворотним холодильником доти, 6Н), 1,46 (с, 9Н), 0,94 (д, J=6,9Гц, 3Н), 0,933 (д, доки ТШХ не покаже завершення реакції. Органічні J=6,9Гц, 3Н). розчинники видаляють у вакуумі і водний шар Методика В промивають простим ефіром (1х) і потім повільно Стадія А підкисляють концентрованою НСl до досягнення рН4. Одержану суспензію екстрагують СН2Сl2 (3х). Об'єднані органічні шари сушать над безводним MgSO4, фільтрують і концентрують з одержанням Комерційно доступну (1R,4S)-4продукту у вигляді суміші двох цис/транс/ізомерів аміноциклопент-2-ен-1-карбонову кислоту перет(1,5г) у вигляді пінистої твердої жовтої речовини. ворюють в гідрохлорид метилового ефіру класичЦю тверду речовину розчиняють в етилацетаті ним методом. (2мл) при нагріванні і розбавляють гексаном Стадія В (50мл) з одержанням прозорого розчину. Розчин охолоджують до кімнатної температури протягом 1год. і потім витримують при температурі -25°С в холодильнику протягом ночі. Транс-ізомер кристаДо суспензії аміну зі стадії А (6,31г, 35,5ммоль) лізується разом з деякою кількістю бажацого цисв ацетоні (40мл), воді (20мл) порціями додають ізомеру (500 мг всі). Маточний розчин збирають і твердий NaHCO3 (6,6г, 78ммоль). Через 5хв. доконцентрують з одержанням вказаної в заголовку дають розчин ди-трет-бутилдикарбонату (8,5г, сполуки (1г, 66%, тільки цис-ізомер). 39ммоль) в ацетоні (60мл) і реакційну суміш пере1 H ЯМP (500МГц, CDCI3) цис-ізомер: δ 5,80 (м, мішують при кімнатній температурі. Через 3год. 2Η), 4,80 (м, 11-1), 2,40-2,20 (м, 2Н), 2,15-2,0 (м, ацетон видаляють у вакуумі і залишок розділяють 1Н), 1,5 (м, 9Н), 1,0-0,8 (м, 3Н). між простим ефіром (500мл) і насиченим водним Стадія E розчином NaHCO3 (120мл). Ефірний шар додатково промивають водним розчином NaHCO3 (1 100мл), насиченим розчином солі (1 100мл), сушать над безводним Na2SO4, концентрують і очищають флеш-хроматографією (15% етилацетат/гексан) з одержанням продукту (7,25г, 85%). Стадія С До розчину продукту зі стадії D (1г) в етанолі (30мл) додають 10% Pd/C (100мг) і одержану суміш перемішують в апараті Парра при тиску 50ф Н2 протягом ночі. Суміш фільтрують через целіт і концентрують у вакуумі з одержанням вказаної в 27 75828 28 заголовку сполуки (1г, 99%). мішують протягом ночі при кімнатній температурі. 1 Н ЯМР(500МГц, CDCI3): 11,36 (уш., 1Н), 6,49 Суміш охолоджують до температури 0°С і, при (уш., 1Н), 4,83 (м, 1Н), 3,71 (с, 3Н), 2,30-1,55 (м, енергійному перемішуванні, порціями додають 6Н), 1,46 (с, 9Н), 0,94 (д, J=6,9Гц, 3Н), 0,933 (д, твердий гідроксид кальцію (близько 6г). Суспензію J=6,9Гц, 3Н). перемішують протягом ще 30хв., потім фільтрують Проміжна сполука 9 через целіт для видалення всіх твердих речовин. Фільтрат випаровують у вакуумі і залишок очищають РХСТ (градієнтне елюювання 40-100% етилацетат/гексан) з одержанням 1,32г (64%) бажаної сполуки. Стадія А 1 Н ЯМР(500МГц, CDCI3) δ 8,46 (с, 1Н), 7,28 (с, 1Н), 4,88 (уш.д, J=17,2Гц, 1H), 4,78 (д, J=17,7Гц, 1Н), 4,05-3,84 (м, 2Н), 3,12 (уш.с, 1Н), 2,34-2,06 (м, Проміжну сполуку 8 (4,6г, 16ммоль) і проміжну 3Н), 1,88-1,70 (м, 4Н), 1,62-1,54 (м, 1Н), 1,43 (с, сполуку 11 (4,0г, 14ммоль) спочатку сушать азеот9Н), 0,90-0,85 (м, 6Н). РХ-МС для C23H32F3N3O5 ропною перегонкою з толуолом (3 50мл) і вміщурозраховано 471,20, знайдено [М+Н]+ 472,2. ють у високий вакуум на 30хв. В атмосфері азоту Стадія В послідовно додають 4-диметиламінопіридин (1,08г, 8,60ммоль), безводний дихлорметан (40мл) і діізопропілетиламін (7,0мл, 40ммоль). Після перетворення проміжної сполуки 8 в розчин додають гексафторфосфат бром-трис-піролідинофосфонію Продукт зі стадії В, проміжну сполуку 20 (1,32г, (6,80г, 14,3ммоль), з негайним додаванням ще 2,82ммоль) розчиняють в 4н НСl в діоксані (50мл) і діізопропілетиламіну (7,0мл, 40ммоль). Реакційну одержаний розчин перемішують при кімнатній тесуміш перемішують при кімнатній температурі промпературі протягом 1год. Реакційну суміш випаротягом ночі і потім гасять насиченим NаНСО3. Водвують у вакуумі з одержанням продукту (1,10г, ний шар знову промивають дихлорметаном 98%) у вигляді білого порошку. РХ-МС для С18Н24F3N3О2 розраховано 371,20, знайдено (3 50мл) і органічні шари об'єднують, сушать над [М+Н]+ 372,2. Na2SO4, фільтрують і випаровують у вакуумі. НеПриклад 1 очищений продукт очищають флешхроматографією на колонці (ступінчастий градієнт 0-60% етилацетат/гексан) з одержанням продукту (4,80г, 74%) у вигляді жовтої піни. 1 Розчин проміжної сполуки 9 (980мг, Н ЯМР(500МГц, CDCI3) δ 8,72 (с, 1Н), 7,70 (с, 2,08ммоль), тетрагідро-4Н-піран-4-ону (320мг, 1Н), 4,88 (уш.д, J=17,0Гц, 1Н), 4,78 (д, J=17,6Гц, 3,13ммоль), діізопропілетиламіну (1,10мл, 1Н), 4,04-3,84 (м, 2Н), 3,52 (уш.с, 1Н), 3,12 (уш.т, 6,24ммоль) і дроблених молекулярних сит (4А, J=5, 6Гц, 1Н), 2,32-2,06 (м, 3Н), 1,98-1,70 (м, 4Н), 500мг) в дихлорметані (50мл) обробляють триаце1,64-1,54 (м, 1Н), 1,44 (с, 9Н), 0,92-0,82 (м, 6Н). токсиборгідридом натрію (2,20г, 10,4ммоль) і пеРХ-МС для C23H32F3N3O розраховано 4555,24, ремішують при кімнатній температурі протягом знайдено [М+Н]+ 456,2. ночі. Реакцію гасять насиченим розчином бікарбоСтадія В нату натрію (50мл) і розбавляють 25мл дихлорметану. Органічний шар відділяють і водний шар промивають дихлорметаном (2 25мл). Органічні шари об'єднують, сушать над безводним сульфаПродукт зі стадії В, проміжну сполуку 19 (1,2г, том натрію, фільтрують і випаровують при зниже2,6ммоль) розчиняють з 4н НСl в діоксані (50мл) і ному тиску. Неочищений продукт очищають ВЕРХ одержаний розчин перемішують при кімнатній тез оберненою фазою з одержанням сполуки Прикмпературі протягом 1год. Реакційну суміш випароладу 1 (915мг, 86,0%). РХ-МС для C23H31F3N3O2 вують у вакуумі з одержанням продукту (904мг, розраховано 439,24, знайдено [М+Н]+ 440,2. 97%) у вигляді білого порошку. РХ-МС для + Приклад 2 C18H24F3N3O розраховано 355,20, знайдено [М+Н] 356,2. Проміжна сполука 10 Стадія А До розчину продукту, описаного на стадії А, проміжної сполуки 19 (2,0г, 4,4ммоль) в дихлорметані (80мл) додають 3-хлорпероксибензойну кислоту (2,11г, 8,83ммоль) і одержаний розчин пере Розчин проміжної сполуки 9 (304мг, 0,712ммоль), проміжної сполуки 1 (160мг, 1,42ммоль), діізопропілетиламіну (370мкл, 2,14ммоль) і дроблених молекулярних сит (4Å, 150мг) в дихлорметані (25мл) обробляють триацетоксиборгідридом натрію (755мг, 3,56ммоль) і перемішують при кімнатній температурі протягом ночі. Реакцію гасять насиченим розчином бікарбонату натрію (25мл) і розбавляють 25мл дихлорметану. Органічний шар відділяють і водний шар промивають дихлорметаном (2 20мл). Органічні шари об'єднують, сушать над безводним сульфа 29 75828 30 том натрію, фільтрують і випаровують при знижеремішують при кімнатній температурі протягом ному тиску. Залишок очищають препаративною ночі. Реакцію гасять насиченим розчином бікарбоТШХ (елюент: 0,5% NH4OH/5% метанол/94,5% нату натрію (25мл) і розбавляють 25мл дихлормеСН2Сl2) з одержанням 239мг (74%) кінцевого протану. Органічний шар відділяють і водний шар дукту у вигляді суміші діастереомерів. Цис- і транспромивають дихлорметаном (2 20мл). Органічні рацемати відносно піранового кільця розділяють шари об'єднують, сушать над безводним сульфаВЕРХ на колонці з Preparative ChiralCel OD (елютом натрію, фільтрують і випаровують при знижеент: 5% етанол/95% гексан). Цис- рацемат далі ному тиску. Залишок очищають препаративною відділяють на колонці з Preparative ChiralCel AD ТШХ (елюент: 1,0% ΝΗ4ΟΗ/10% метанол/89% (елюент: 5% етанол/95% гексан). РХ-МС для СН2Сl2) з одержанням 210мг (86%) кінцевого проC24H35F3N3O2 розраховано 453,26, знайдено дукту у вигляді суміші чотирьох діастереомерів. [М+Н]+ 52 454,30. Окремі ізомери одержують ВЕРХ на колонці з Приклад 3 Preparative ChiralCel OD, елююючи 20% етанолом і 80% гексаном при швидкості потоку 9 мл/хв. РХМС для С24Н34F3N3О3 розраховано 469,21, знайдено [М+Н]+ 470,2 для всіх 4 ізомерів. 3-й ізомер з колонки ChiralCel OD: 1Η ЯМР Продукт одержують за методикою прикладу 2 (500МГц, CDCI3) δ 8,72 (с, 1Н), 7,69 (с, 1Н), 4,87 за виключенням того, що проміжну сполуку 1 замі(уш.д, J=17,2Гц, 1Н), 4,75 (д, J=17,4Гц, 1Н), 4,12 нюють проміжною сполукою 2. Очистка препара(дд, J=3,1, 12,4Гц, 1Н), 3,99-3,86 (м, 3Н), 3,47-3,39 тивною ТШХ (елюент: 0,5% NH4OH/5% мета(м, 1Н), 3,41 (с, накладення, 3Н), 3,35-3,30 (м, 2Н), нол/94,5% СН2Сl2) дає 203мг (92%) у вигляді суміш 3,20-3,08 (м, 3Н), 2,87-2,80 (м, 1Н), 2,62-2,54 (м, чотирьох діастереомерів. Окремі ізомери одержу1Н), 2,16-2,02 (м, 2Н), 1,95 (уш.с, 1Н), 1,88-1,81 (м, ють очищенням ВЕРХ на колонці з Preparative 1Н), 1,78-1,57 (м, 6Н), 1,41-1,32 (м, 1Н), 0,96 (д, ChiralCel OD, елююючи 5% етанол/95% гексаном J=6,7Гц, 3Н),0,84(д,1=6,6Гц, 3Н). при швидкості потоку 9мл/хв. РХ-МС для 4-й ізомер з колонки ChiralCel OD: 1H ЯМР C25H36F3N3O2 розраховано 467,28, знайдено + (500МГц, CDCI3) δ 8,72 (с, 1Н), 7,69 (с, 1Н), 4,87 [М+Н] 468,3 для всіх 4 ізомерів. (уш.д, J=17,6Гц, 1Н), 4,75 (д, J=17,5Гц, 1Н), 4,10 Приклад 4 (дд, J=3,1, 12,3Гц, 1Н), 3,99-3,88 (м, 3Н), 3,46-3,39 (м, 1Н), 3,41 (с, накладення, 3Н), 3,35-3,30 (м, 2Н), 3,17-3,09 (м, 3Н), 2,86-2,80 (м, 1Н), 2,64-2,55 (м, 1Н), 2,16-2,10 (м, 1Н), 2,05 (уш.с, 1Н), 1,95-1,82 (м, 2Н), 1,76-1,55 (м, 6Н), 1,33-1,24 (м, 1Н), 0,95 (д, J=6,7Гц, 3Н),0,83 (д, J=6,6Гц, 3Н). Продукт одержують за методикою прикладу 2 Приклад 7 за винятком того, що проміжну сполуку 1 замінюють проміжною сполукою 5. Очищення дає 312мг (88%) продукту у вигляді суміші чотирьох діастереомерів. РХ-МС для C30H36CIF3N3O4 розраховано Продукт одержують за методикою прикладу 2 593,23, знайдено [М+Н]+ 594,3. за винятком того, що проміжну сполуку 1 замінюПриклад 5 ють проміжною сполукою 4. Окремі ізомери одержують очищенням ВЕРХ на колонці з Preparative ChiralCel OD, елююючи 15% етанолом і 85% гексаном при швидкості потоку 9мл/хв. РХ-МС для До розчину продукту, описаного в прикладі 4 C25H36F3N3O3 розраховано 483,23, знайдено (286мг, 0,482ммоль), в метанолі додають 0,5Μ [М+Н]+ 484,2 для всіх 4 ізомерів. розчин метоксиду натрію в метанолі (1,2мл, Приклад 8 0,58ммоль) і одержану суміш перемішують при кімнатній температурі протягом 2год. Після завершення реакції суміш випаровують у вакуумі і очищають препаративною ТШХ (елюент: 1,0% ΝΗ4ΟΗ/10% метанол/89% СН2Сl2) з одержанням сполуки прикладу 21 (201мг, 91,6%) у вигляді суміші чотирьох діастереомерів. РХ-МС для C23H33F3N3O3 розраховано 455,24, знайдено [М+Н]+ 456,25. Приклад 6 Продукт одержують за методикою прикладу 2 за винятком того, що проміжну сполуку 1 замінюють проміжною сполукою 5. РХ-МС для C24H34F3N3O3 розраховано 457,23, знайдено [М+Н]+ 458,2 для всіх 4 ізомерів. Приклад 9 Розчин проміжної сполуки 9 (500мг, 1,17ммоль), проміжної сполуки 3 (458мг, 3,51ммоль), діізопропілетиламіну (407мкл, 2,34ммоль) і дроблених молекулярних сит (4Å, 250мг) в дихлорметані (25мл) обробляють триацетоксиборгідридом натрію (1,24г, 5,85ммоль) і пе Продукт одержують за методикою прикладу 2 за винятком того, що проміжну сполуку 1 замінюють проміжною сполукою 6. Окремі ізомери одержують очищенням ВЕРХ на колонці з Preparative ChiralCel OD, елююючи 5% етанолом і 95% гексаном при швидкості потоку 9мл/хв. РХ-МС для 31 C24H31F6N3O2 розраховано 507,23, [М+Н]+ 508,2 для всіх 4 ізомерів. Приклад 10 75828 знайдено Розчин проміжної сполуки 10 (641мг, 1,60ммоль), тетрагідро-4Н-піран-4-ону (220мг, 2,24ммоль), діізопропілетиламіну (279мкл, 1,60ммоль) і дроблених молекулярних сит (4Å, 320мг) в дихлорметані (20мл) обробляють триацетоксиборгідридом натрію (1,70г, 8,00ммоль) і перемішують при кімнатній температурі не більше 5год. Реакцію гасять насиченим розчином бікарбонату натрію (50мл) і розбавляють 30мл дихлорметану. Органічний шар відділяють і водний шар промивають дихлорметаном (2 30мл). Органічні шари об'єднують, сушать над безводним сульфатом натрію, фільтрують і випаровують при зниженому тиску. Неочищений продукт очищають препаративною ТШХ (елюент: 0,75% NH4OH/7,5% метанол/91,75% СН2Сl2) з одержанням 626мг (86%) кінцевого продукту. 1 H ЯМР (500МГц, CDCI3) δ 8,45, (с, 3Н), 7,25 (с, 1Н), 4,88 (уш.д, J=17,4Гц, 1Н), 4,77 (д, J=17,6Гц, 1Н), 4,00-3,85 (м, 4Н), 3,41 (арр т, J=11,7Гц, 2Н), 3,22, (р, J=6,8Гц, 1Н), 3,13-3,07 (м, 2Н), 2,82-2,74 (м, 1Н), 2,54-2,47 (м, 1Н), 2,14 (дд, J=6,8, 12,8Гц, 1Н), 2,07-2,00 (м, 1Н), 1,94-1,86 (м, 2Н), 1,84-1,77 (м, 3Н), 1,65-1,57 (м, 2Н), 1,46-1,26 (м, 3Н), 0,93 (д, J=6,8Гц, 3Н), 0,83 (д, J=6,8Гц, 3Н). РХ-МС для C23H32F3N3O3 розраховано 455,24, знайдено [М+Н]+ 456,20. Приклад 11 Продукт одержують за методикою прикладу 10 за винятком того, що тетрагідро-4Н-піран-4-он замінюють проміжною сполукою 1. Окремі ізомери одержують очищенням ВЕРХ на колонці з Preparative ChiralCel OD, елююючи 7% етанолом і 93% гексаном при швидкості потоку 9мл/хв. РХ-МС для C24H34F3N3O3 розраховано 469,24, знайдено [М+Н]+ 470,20 для всіх 4 ізомерів. Комп’ютерна верстка Т. Чепелева 32 Приклад 12 Продукт одержують за методикою прикладу 10 за винятком того, що тетрагідро-4Н-піран-4-он замінюють проміжною сполукою 2. Окремі ізомери одержують очищенням ВЕРХ на колонці з Preparative ChiralCel OD, елююючи 5% етанолом і 95% гексаном при швидкості потоку 9 мл/хв. РХМС для C25H36F3N3O3 розраховано 483,24, знайдено [М+Н]+ 484,20 для всіх 4 ізомерів. Приклад 13 Продукт одержують за методикою прикладу 10 за винятком того, що тетрагідро-4Н-піран-4-он замінюють проміжною сполукою 3. Окремі ізомери одержують очищенням ВЕРХ на колонці з Preparative ChiralCel OD, елююючи 21% етанолом і 79% гексаном при швидкості потоку 9мл/хв. ЖХМС для C24H34F3N3O4 розраховано 485,25, знайдено [М+Н]+ 486,30 для всіх 4 ізомерів. Хоча дана сполука описана і проілюстрована конкретними варіантами, фахівцеві в даній галузі техніки буде зрозуміло, що різна адаптація, зміни, модифікації, заміщення, видалення або додавання можуть бути зроблені не виходячи за рамки і об'єм даного винаходу. Наприклад, можуть застосовуватись ефективні дози, які відрізняються від визначених доз, вказаних вище, внаслідок зміни реакції ссавця, що лікується, за будь-якою з показань сполукою, вказаною вище. Фармакологічні реакції, що також спостерігаються, можуть змінюватись згідно і в залежності від певної вибраної активної сполуки, або присутніх фармацевтичних носіїв, а також типу лікарської форми і способу введення, і такі очікувані варіації або відмінності в результатах розглядаються в об'єктах і практиці даного винаходу. Тому мається на увазі, що даний винахід визначений представленою нижче формулою винаходу, і пункти вказаної формули винаходу трактуються так широко, наскільки це розумно. Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюTetrahydropyranyl cyclopentyl tetrahydropyridopyridine modulators of chemokine receptor activity, pharmaceutical composition based thereon and method for treatment of disorder or disease (variants)
Назва патенту російськоюТетрагидропиранилциклопентилтетрагидропиридопиридиновые модуляторы активности хемокинового рецептора, фармацевтическая композиция на их основе и способ лечения расстройства или заболевания (варианты)
Автори російськоюYang, Lihu
МПК / Мітки
МПК: A61P 29/00, C07D 471/04, A61P 37/04
Мітки: розладу, хемокінового, спосіб, рецептора, варіанти, фармацевтична, основі, активності, модулятори, лікування, захворювання, тетрагідропіранілциклопентилтетрагідропіридопіридинові, композиція
Код посилання
<a href="https://ua.patents.su/16-75828-tetragidropiranilciklopentiltetragidropiridopiridinovi-modulyatori-aktivnosti-khemokinovogo-receptora-farmacevtichna-kompoziciya-na-kh-osnovi-ta-sposib-likuvannya-rozladu-abo-zakhv.html" target="_blank" rel="follow" title="База патентів України">Тетрагідропіранілциклопентилтетрагідропіридопіридинові модулятори активності хемокінового рецептора, фармацевтична композиція на їх основі та спосіб лікування розладу або захворювання (варіанти)</a>
Попередній патент: Бемітний матеріал, полімерний матеріал, що його містить, та спосіб формування продукту
Наступний патент: Спосіб вакуум-плазмової обробки кольорових сплавів
Випадковий патент: Система автоматичного регулювання продуктивності компресорної станції зиф-55












