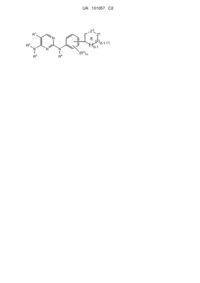
Похідні піримідину як інгібітори кінази
Номер патенту: 101057
Опубліковано: 25.02.2013
Автори: Марсіл'є ІІІ Томас Х., Чен Бей, Лі Крістіан Чо-Хуа, Джіанг Сонгчун, Хі Ксяогуй, Лу Уеншуо, Янг Кунйонг
Формула / Реферат
1. Сполука Формули (1):
 , (1)
, (1)
або її фізіологічно прийнятна сіль;
у якій кільце Е може необов'язково містити подвійний зв'язок;
один з Z1, Z2 та Z3 являє собою NR6, N(R6)+-O- або S(O)1-2 та інші являють собою CR2;
R1 являє собою галогрупу або необов'язково галогенований С1-6алкіл;
R2 являє собою піридин-2-оніл, азепан-2-оніл або моноциклічний 5-6-членний гетероарил, що має 1-3 гетероатоми, що вибирають з N, О та S; кожен з яких необов'язково заміщений за допомогою R9, де R9 являє собою С1-6алкіл, С1-6галоалкіл або С3-7циклоалкіл;
R3 та R4 кожен являє собою Н;
R5 являє собою галогрупу, гідроксил, С1-6алкіл, С1-6алкоксигрупу, галозаміщений С1-6алкіл, галозаміщену С1-6алкоксигрупу, ціаногрупу або C(O)O0-1R8;
R6 являє собою Н, С1-6алкіл, С2-6алкеніл або С2-6алкініл, кожен з яких може бути необов'язково заміщений за допомогою гало та/або гідроксильних груп; -(CR2)р-OR7, -(CR2)p-CH(OH)CtF2t+1, у якій t являє собою 1-3, (CR2)p-CN; (CR2)p-NR(R7), -(CR2)p-C(O)OR7, (CR2)pNR(CR2)pOR7, (CR2)pNR-L-C(O)R8, C(O)(CR2)qOR8, -C(O)O-(CR2)p-NRR7, -C(O)-(CR2)p-OR7, L-Y, -L-C(O)R7, -L-C(O)-NRR7, -L-C(O)-NR-(CR2)p-NRR7,-L-C(O)NR(CR2)pOR7, -L-C(O)-(CR2)q-NR-C(O)-R8, -L-C(O)NR(CR2)pSR7, -L-C(O)NR(CR2)pS(O)1-2R8, -L-S(O)2R8, -L-S(O)2-(CR2)q-NRR7, -L-S(O)2NR(CR2)pNR(R7) або -L-S(O)2NR(CR2)pOR7;
альтернативно, R6 являє собою радикал, вибраний з формули (а), (b), (с) або (d):
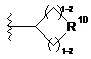 ,
, 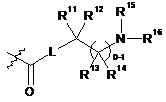 ,
, 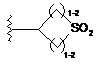 ,
, 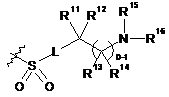 ,
,
(a)
(b)
(c)
(d)
R10 являє собою О, S, NR17, де R17 являє собою Н, С1-6алкіл, SO2R8a або CO2R8a;
R11, R12, R13, R14, R15 та R16 незалежно вибирають з таких як: Н, С1-6алкоксигрупа; С1-6алкіл, С2-6алкеніл або С2-6алкініл, кожен з яких може бути необов'язково заміщений за допомогою гало, аміно або гідроксильних груп; або
R11 та R12, R12 та R15, R15 та R16, R13 та R14 або R13 та R15 разом з атомами, до яких вони приєднані, можуть утворювати 3-7-членне насичене, ненасичене або частково ненасичене кільце, що містить 1-3 гетероатоми, вибрані з N, О та S, та необов'язково заміщене за допомогою оксо та 1-3 R5 груп;
L являє собою (CR2)1-4 aбo зв'язок;
Y являє собою С3-7карбоциклічне кільце, С6-10арил або 5-10-членне гетероарильне або 4-10-членне гетероциклічне кільце, кожне з яких необов'язково заміщене за допомогою 1-3 R5 груп;
R7, R8 та R8a являють собою незалежно С1-6алкіл, С2-6алкеніл або С2-6алкініл, кожен з яких може бути необов'язково заміщений за допомогою галогрупи, аміногрупи, гідроксилу або ціаногрупи; (CR2)qY або С1-6алкокси; або R7 являє собою Н;
кожен R незалежно являє собою Н або С1-6алкіл;
R та R7 разом з N у кожній NRR7 можуть утворювати 5-6-членне кільце, що містить 1-3 гетероатоми, вибрані з N, О та S, та необов'язково заміщене за допомогою оксо та 1-3 R5 груп;
m являє собою 2-4;
n являє собою 1-3;
р являє собою 1-4; та
q являє собою 0-4.
2. Сполука за п. 1, де зазначена сполука має Формулу (2):
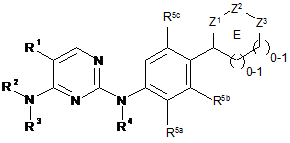 , (2)
, (2)
у якій один з R5a, R5b та R5c являє собою Н та інші являють собою незалежно галогрупу, С1-6алкіл, С1-6алкоксигрупу, галозаміщений С1-6алкіл, ціаногрупу або C(O)O0-1R8, де R8 являє собою С1-6алкіл; та
R1, R2, R3, R4, Е, Z1, Z2 та Z3 приймають значення, визначені у п. 1.
3. Сполука за п. 2, у якій Z3 являє собою NR6 або N(R6)+-O-; та Z1 та Z2 являють собою СН2.
4. Сполука за п. 3, у якій R6 являє собою Н, С1-6алкіл, необов'язково заміщений за допомогою гало та/або гідроксильних груп; -(CR2)р-OR7, -(CR2)p-CH(OH)CtF2t+1, де t являє собою 1-3, (CR2)p-CN, (CR2)p-NR(R7), -(CR2)p-C(O)OR7, C(O)(CR2)qOR8, -C(O)O-(CR2)p-NRR7, L-Y, -L-C(O)R7, -L-C(O)-NRR7, -L-C(O)-NR-(CR2)p-NRR7,-L-C(O)-(CR2)q-NR-C(O)-R8, -L-S(O)2R8, -L-S(O)2-(CR2)q-NRR7 або радикал, вибраний з формули (а), (b), (с) або (d):
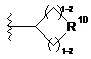 ,
, 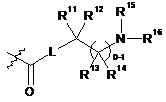 ,
, 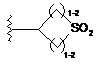 ,
, 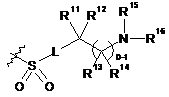 ,
,
(a)
(b)
(c)
(d)
R10 являє собою О, S, NR17, де R17 являє собою Н, С1-6алкіл, SO2R8a або CO2R8a та R8a являє собою С1-6алкіл; та
R7, R8, R11, R12, R13, R14, R15, R16, R, L, Y, р та q приймають значення, визначені у п. 1.
5. Сполука за будь-яким з пп. 1-4, у якій R2 являє собою піразоліл, ізоксазоліл, піридин-2-оніл або азепан-2-оніл, кожен з яких заміщений за допомогою С1-6алкілу, С1-6галоалкілу або С3-7циклоалкілу.
6. Сполука за п. 1, де зазначена сполука має Формулу (3):
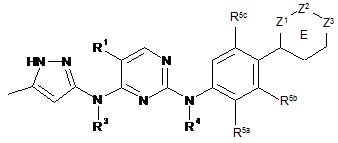 , (3)
, (3)
або її таутомер;
у якій R5b являє собою Н; та R5a та R5c незалежно являють собою галогрупу, С1-6алкіл, С1-6алкоксигрупу, галозаміщений С1-6алкіл, ціаногрупу або C(O)O0-1R8, де R8 являє собою С1-6алкіл;
Z1 та Z2 являють собою СН2;
Z3 являє собою NR6 або N(R6)+-O-;
R6 являє собою Н, С1-6алкіл, необов'язково заміщений за допомогою гало та/або гідроксильних груп; -(CR2)р-OR7, -(CR2)p-CH(OH)CtF2t+1, де t являє собою 1-3, (CR2)p-CN, (CR2)p-NR(R7), -(CR2)p-C(O)OR7, C(O)(CR2)qOR8, -C(O)O-(CR2)p-NRR7, L-Y, -L-C(O)R7, -L-C(O)-NRR7, -L-C(O)-NR-(CR2)p-NRR7,-L-C(O)-(CR2)q-NR-C(O)-R8, -L-S(O)2R8, -L-S(O)2-(CR2)q-NRR7 або радикал, вибраний з формули (а), (b), (с) або (d):
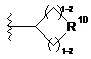 ,
, 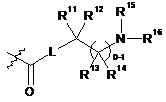 ,
, 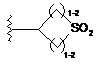 ,
, 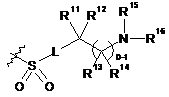 ,
,
(a)
(b)
(c)
(d)
R10 являє собою О, S, NR17, де R17 являє собою H, С1-6алкіл, SO2R8a або CO2R8a та R8a являє собою С1-6алкіл; та
R1, R3, R4, R7, R8, R11, R12, R13, R14, R15, R16, R, L, Y, p, q та Е приймають значення, визначені у п. 1.
7. Сполука за п. 6, у якій R5a являє собою галогрупу та R5c являє собою С1-6алкіл.
8. Сполука за п. 6, у якій R6 являє собою С1-6алкіл або радикал формули (а) або (с); та R10 являє собою О.
9. Сполука за будь-яким з пп. 1-8, у якій R1 являє собою галогрупу.
10. Сполука за п. 1, де зазначену сполуку вибирають з групи, що включає такі як:

5-хлор-N2-(2-фтор-5-метил-4-(1-метилпіперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
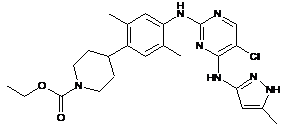
етил 4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-карбоксилат
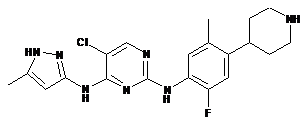
5-хлор-N2-(2-фтор-5-метил-4-(піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(S)-2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)пропанамід

5-хлор-N2-(2-ізопропокси-5-метил-4-(1-метилпіперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(S)-2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)-N-метилпропанамід

N2-(2-фтор-5-метил-4-(піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)-5-(трифторметил)піримідин-2,4-діамін

(R)-2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)пропанамід

N2-(2-iзoпpoпoкcи-5-мeтил-4-(1-метилпіперидин-4-іл)феніл)-5-метил-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(S)-2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)пропанамід
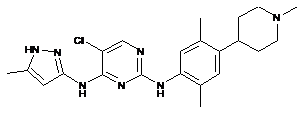
5-хлор-N2-(2,5-диметил-4-(1-метилпіперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(R)-2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)пропанамід
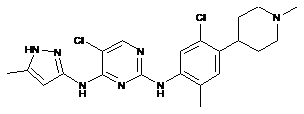
5-хлор-N2-(5-хлор-2-метил-4-(1-метилпіперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
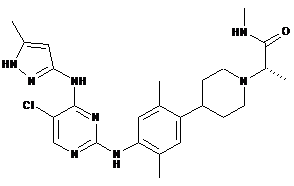
(S)-2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-iл)-N-метилпропанамід

5-хлор-N2-(4-фтор-2-метил-5-(піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(1-(етиламіно)циклопропіл)метанон

3-(5-хлор-2-(2-фтор-5-метил-4-(1-метилпіперидин-4-іл)феніламіно)-піримідин-4-іламіно)азепан-2-он

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)(1-(етиламіно)циклопропіл)метанон

(S)-3-(5-хлор-2-(2-фтор-5-метил-4-(1-метилпіперидин-4-іл)феніламіно)-піримідин-4-іламіно)азепан-2-он

5-хлор-N2-(2-фтор-5-метил-4-(піперидин-4-іл)феніл)-N4-(5-(трифторметил)-1Н-піразол-3-іл)піримідин-2,4-діамін

(R)-3-(5-хлор-2-(2-фтор-5-метил-4-(1-метилпіперидин-4-іл)феніламіно)-піримідин-4-іламіно)азепан-2-он

2-(4-(4-(5-хлор-4-(5-(трифторметил)-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-iл)-N-метилацетамід

5-хлор-N2-(4-(1-ізопропілпіперидин-4-іл)-2,5-диметилфеніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
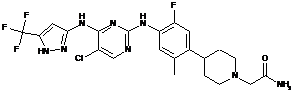
2-(4-(4-(5-хлор-4-(5-(трифторметил)-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)ацетамід

5-хлор-N2-(4-фтор-5-(1-ізопропілпіперидин-4-іл)-2-метилфеніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

5-хлор-N2-(2,5-диметил-4-(1-(тетрагідро-2Н-тіопіран-4-іл)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
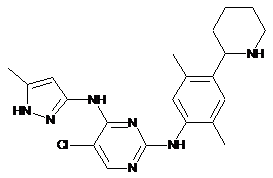
5-хлор-N2-(2,5-диметил-4-(піперидин-2-іл)феніл)-N4-(5-метил-1H-піразол-3-іл)піримідин-2,4-діамін

1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-2-(етиламіно)-2-метилпропан-1-он

5-хлор-N2-(2,5-диметил-4-(піперидин-3-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(1-(етиламіно)циклобутил)метанон
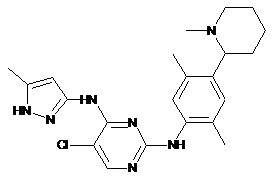
5-хлор-N2-(2,5-диметил-4-(1-метилпіперидин-2-іл)феніл)-N4-(5-метил-1H-піразол-3-іл)піримідин-2,4-діамін

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(1-(метиламіно)циклобутил)метанон

5-хлор-N4-(5-циклопропіл-1Н-піразол-3-іл)-N2-(2-фтор-5-метил-4-(піперидин-4-іл)феніл)піримідин-2,4-діамін

N2-(2,5-диметил-4-(піперидин-4-іл)феніл)-5-метил-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

5-хлор-N4-(5-циклопропіл-1Н-піразол-3-іл)-N2-(2,5-диметил-4-(піперидин-4-іл)феніл)піримідин-2,4-діамін

(S)-3-(4-(2,5-диметил-4-(5-метил-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)феніл)піперидин-1-іл)-1,1,1-трифторпропан-2-ол
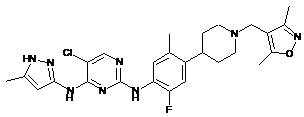
5-хлор-N2-(4-(1-((3,5-диметилізоксазол-4-іл)метил)піперидин-4-іл)-2-фтор-5-метилфеніл)-N4-(5-метил-1H-піразол-3-іл)піримідин-2,4-діамін

1-(3-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-2-(диметиламіно)етанон
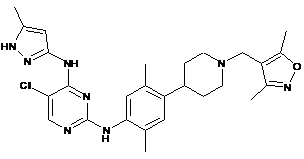
5-хлор-N2-(4-(1-((3,5-диметилізоксазол-4-іл)метил)піперидин-4-іл)-2,5-диметилфеніл)-N4-(5-метил-1H-піразол-3-іл)піримідин-2,4-діамін

2-(2-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)ацетамід

5-хлор-N2-(2,5-диметил-4-(1-(піридазин-4-ілметил)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
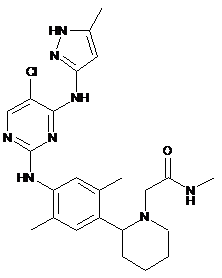
2-(2-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-N-метилацетамід
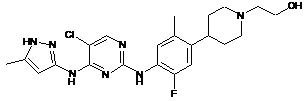
2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)етанол
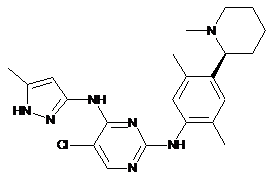
(S)-5-хлор-N2-(2,5-диметил-4-(1-метилпіперидин-2-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
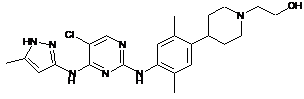
2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)етанол
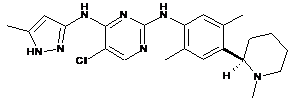
(R)-5-хлор-N2-(2,5-диметил-4-(1-метилпіперидин-2-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
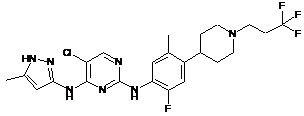
5-хлор-N2-(2-фтор-5-метил-4-(1-(3,3,3-трифторпропіл)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)бутанамід

5-хлор-N2-(2,5-диметил-4-(1-(3,3,3-трифторпропіл)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

1-(4-(4-(5-хлор-4-(5-циклопропіл-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-2-(диметиламіно)етанон

5-хлор-N2-(2-фтор-5-метил-4-(1-(2,2,2-трифторетил)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(1-аміноциклопропіл)(3-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)метанон
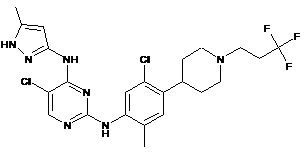
5-хлор-N2-(5-хлор-2-метил-4-(1-(3,3,3-трифторпропіл)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(1-аміноциклопропіл)(4-(4-(5-хлор-4-(5-циклопропіл-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)метанон
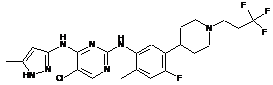
5-хлор-N2-(4-фтор-2-метил-5-(1-(3,3,3-трифторпропіл)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
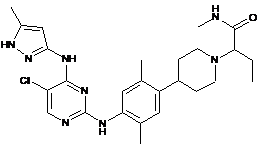
2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-N-метилбутанамід

3-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-1,1,1-трифторпропан-2-ол

2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-N-етилбутанамід

3-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)-1,1,1-трифторпропан-2-ол

5-хлор-N2-(4-(1-((3,5-диметилізоксазол-4-іл)метил)піперидин-2-іл)-2,5-диметилфеніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
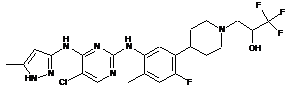
3-(4-(5-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2-фтор-4-метилфеніл)піперидин-1-іл)-1,1,1-трифторпропан-2-ол

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(1-гідроксициклопропіл)метанон

2-(4-(4-(5-хлор-4-(5-циклопропіл-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)-N-метилацетамід

(2-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)(1-гідроксициклопропіл)метанон

2-(4-(4-(5-хлор-4-(5-циклопропіл-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-N-метилацетамід

5-хлор-N2-(2,5-диметил-4-(1-(3-морфолінопропілсульфоніл)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
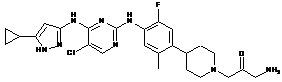
2-(4-(4-(5-хлор-4-(5-циклопропіл-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)ацетамід
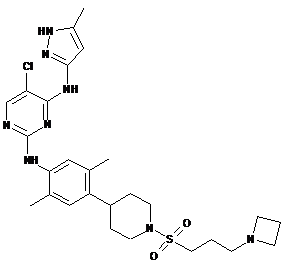
N2-(4-(1-(3-(азетидин-1-іл)пропілсульфоніл)піперидин-4-іл)-2,5-диметилфеніл)-5-хлор-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
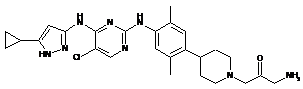
2-(4-(4-(5-хлор-4-(5-циклопропіл-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)ацетамід

(3R,4R)-1-(3-(4-(4-(5-хлор-4-(5-метил-1H-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-ілсульфоніл)пропіл)піролідин-3,4-діол

2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-(трифторметил)феніл)піперидин-1-іл)ацетамід

(2S)-3-(2-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-1,1,1-трифторпропан-2-ол

2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)ацетамід

1-((4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)метил)циклопропанкарбонітрил

2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-N-метилацетамід

2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)ацетонітрил
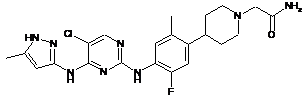
2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)ацетамід

3-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)пропаннітрил
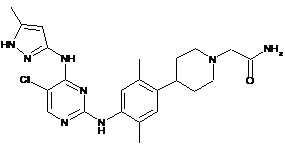
2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)ацетамід
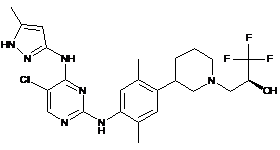
(2S)-3-(3-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-1,1,1-трифторпропан-2-ол
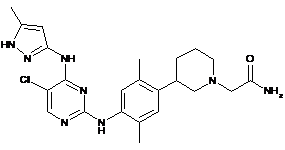
2-(3-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)ацетамід

2-(4-(2,5-диметил-4-(4-(5-метил-1H-піразол-3-іламіно)-5-(трифторметил)-піримідин-2-іламіно)феніл)піперидин-1-іл)ацетамід
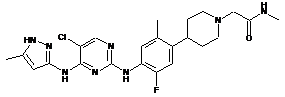
2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)-N-метилацетамід
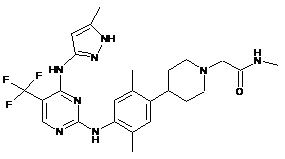
2-(4-(2,5-диметил-4-(4-(5-метил-1Н-піразол-3-іламіно)-5-(трифторметил)-піримідин-2-іламіно)феніл)піперидин-1-іл)-N-метилацетамід

2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-N-метилацетамід
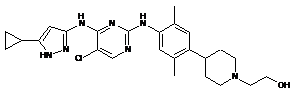
2-(4-(4-(5-хлор-4-(5-циклопропіл-1H-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)етанол

2-(3-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-N-метилацетамід
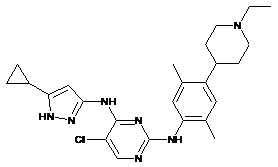
5-хлор-N4-(5-циклопропіл-1Н-піразол-3-іл)-N2-(4-(1-етилпіперидин-4-іл)-2,5-диметилфеніл)піримідин-2,4-діамін
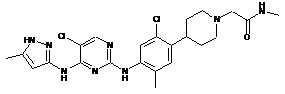
2-(4-(2-хлор-4-(5-хлор-4-(5-метил-1H-піразол-3-іламіно)піримідин-2-іламіно)-5-метилфеніл)піперидин-1-іл)-N-метилацетамід

4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-карбальдегід
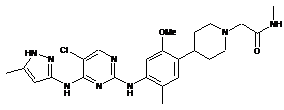
2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2-метокси-5-метилфеніл)піперидин-1-іл)-N-метилацетамід
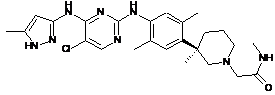
(R)-2-(3-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-N-метилацетамід

2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-метил-2-(трифторметил)феніл)піперидин-1-іл)ацетамід
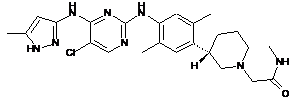
(S)-2-(3-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-N-метилацетамід
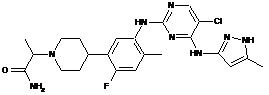
2-(4-(5-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2-фтор-4-метилфеніл)піперидин-1-іл)пропанамід

5-хлор-N2-(2-фтор-5-метил-4-(1-(тетрагідро-2Н-піран-4-іл)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)пропанамід

5-хлор-N2-(4-(1-циклопропілпіперидин-4-іл)-2-фтор-5-метилфеніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)-N-метилпропанамід

5-хлор-N2-(4-(1-етилпіперидин-4-іл)-2,5-диметилфеніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)пропанамід

5-хлор-N2-(4-(1-(2-метоксіетил)-піперидин-4-іл)-2,5-диметилфеніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-N-метилпропанамід

(S)-3-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2-метокси-5-метилфеніл)піперидин-1-іл)-1,1,1-трифторпропан-2-ол

2-(4-(5-фтор-2-метил-4-(4-(5-метил-1Н-піразол-3-іламіно)-5-(трифторметил)-піримідин-2-іламіно)феніл)піперидин-1-іл)пропанамід

N2-(4-(1-(3-(азетидин-1-ілсульфоніл)-пропіл)піперидин-4-іл)-2,5-диметил-феніл)-5-хлор-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)пропанової кислоти

5-хлор-N2-(2,5-диметил-4-(пiперидин-4-іл)феніл)N4-(5-(трифторметил)-1H-піразол-3-іл)піримідин-2,4-діамін

5-хлор-N2-(2-фтор-5-метил-4-(1-(2-(метилсульфоніл)етил)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
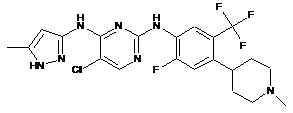
5-хлор-N2-(2-фтор-4-(1-метилпiперидин-4-іл)-5-(трифторметил)-феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

5-хлор-N2-(2,5-диметил-4-(1-(2-(метилсульфоніл)етил)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
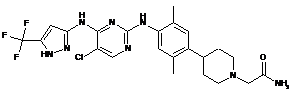
2-(4-(4-(5-хлор-4-(5-(трифторметил)-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)ацетамід

5-хлор-N2-(4-(1-(2-(етилсульфоніл)етил)піперидин-4-іл)-2-фтор-5-метилфеніл)-N4-(5-метил-1H-піразол-3-іл)піримідин-2,4-діамін

5-хлор-N4-(5-метил-1Н-піразол-3-іл)-N2-(2-метил-4-(1-метилпіперидин-4-іл)-5-(трифторметил)феніл)піримідин-2,4-діамін

2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)-N,N-диметилетансульфонамід

5-хлор-N2-(5-метокси-2-метил-4-(1-метилпіперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)етансульфонамід

2-(4-(4-(5-хлор-4-(5-(трифторметил)-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-N-метилацетамід

N2-(4-(1-(2-(азетидин-1-ілсульфоніл)етил)піперидин-4-іл)-5-хлор-2-метилфеніл)-5-хлор-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

N2-(4-(1-етилпіперидин-4-іл)-2,5-диметилфеніл)-N4-(5-метил-1Н-піразол-3-іл)-5-(трифторметил)піримідин-2,4-діамін

N2-(4-(1-(2-(азетидин-1-ілсульфоніл)етил)піперидин-4-іл)-2-фтор-5-метилфеніл)-5-хлор-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
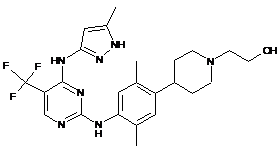
2-(4-(2,5-диметил-4-(4-(5-метил-1H-піразол-3-іламіно)-5-(трифторметил)-піримідин-2-іламіно)феніл)піперидин-1-іл)етанол

5-хлор-N2-(2-фтор-5-метил-4-(1-(метилсульфоніл)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

1-(4-(4-(5-хлор-4-(5-(трифторметил)-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-2-(диметиламіно)етанон

5-хлор-N2-(2,5-диметил-4-(1-(метилсульфоніл)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-4-морфолінобутан-1-он
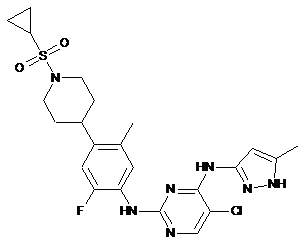 5-хлор-N2-(4-(1-(циклопропілсульфоніл)піперидин-4-іл)-2-фтор-5-метилфеніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
5-хлор-N2-(4-(1-(циклопропілсульфоніл)піперидин-4-іл)-2-фтор-5-метилфеніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-3-морфолінопропан-1-он

5-хлор-N2-(2-фтор-5-метил-4-(1-(піридин-3-ілсульфоніл)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
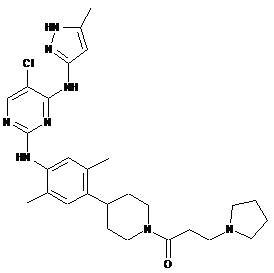
1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-3-(піролідин-1-іл)пропан-1-он

етил-4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-карбоксилат

1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-4-(піролідин-1-іл)бутан-1-он
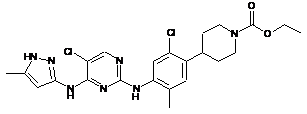 етил-4-(2-хлор-4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-метилфеніл)піперидин-1-карбоксилат
етил-4-(2-хлор-4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-метилфеніл)піперидин-1-карбоксилат

(R)-3-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2-метокси-5-метилфеніл)піперидин-1-іл)-1,1,1-трифторпропан-2-ол
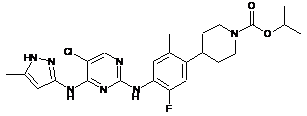
ізопропіл-4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-карбоксилат

(2R)-3-(2-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-1,1,1-трифторпропан-2-ол

4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)-N,N-диметилпіперидин-1-карбоксамід

5-хлор-N2-(4-(1-етилпіперидин-4-іл)-2-фтор-5-метилфеніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
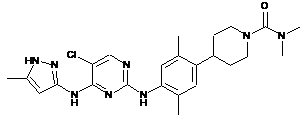
4-(4-(5-хлор-4-(5-метил-1H-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)-N,N-диметилпіперидин-1-карбоксамід

5-хлор-N2-(2,5-диметил-4-(1-(3-(піролідин-1-іл)пропілсульфоніл)-піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
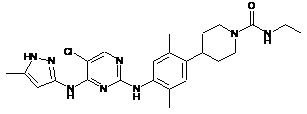
4-(4-(5-хлор-4-(5-метил-1H-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)-N-етилпіперидин-1-карбоксамід

(R)-1-(3-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-ілсульфоніл)пропіл)піролідин-3-ол
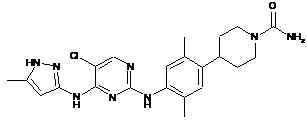
4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-карбоксамід

5-xлop-N2-(4-(l-((2,2-дифторциклопропіл)метил)піперидин-4-іл)-2-фтор-5-метилфеніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
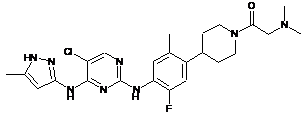
1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)-2-(диметиламіно)етанон

3-(4-(4-(5-хлор-4-(5-метил-1H-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)пропанамід
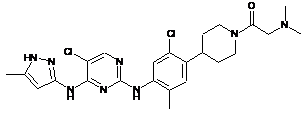
1-(4-(2-хлор-4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-метилфеніл)піперидин-1-іл)-2-(диметиламіно)етанон

N2-(4-(азетидин-3-іл)-2,5-диметилфеніл)-5-хлор-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
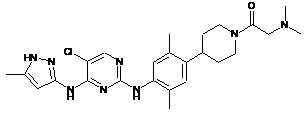
1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-2-(диметиламіно)етанон

3-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-1-(піролідин-1-іл)пропан-1-он
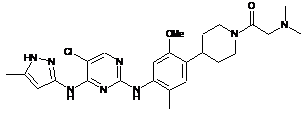
1-(4-(4-(5-хлор-4-(5-метил-1H-піразол-3-іламіно)піримідин-2-іламіно)-2-метокси-5-метилфеніл)піперидин-1-іл)-2-(диметиламіно)етанон

1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-3-(диметиламіно)пропан-1-он
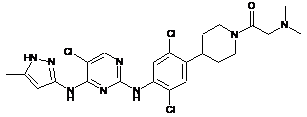
1-(4-(2,5-дихлор-4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)феніл)піперидин-1-іл)-2-(диметиламіно)етанон
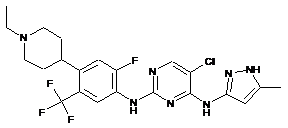
5-хлор-N2-(4-(1-етилпіперидин-4-іл)-2-фтор-5-(трифторметил)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)-3-(диметиламіно)пропан-1-он

5-хлор-N2-(4-(1-етилпіперидин-4-іл)-2-метил-5-(трифторметил)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

2-аміно-1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)етанон

3-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)-1-(піролідин-1-іл)пропан-1-он

1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)-2-(метиламіно)етанон
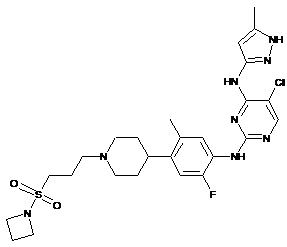
N2-(4-(1-(3-(азетидин-1-ілсульфоніл)-пропіл)піперидин-4-іл)-2-фтор-5-метилфеніл)-5-хлор-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
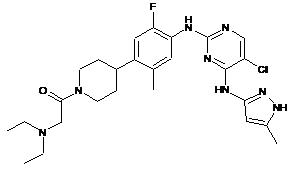
1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)-2-(діетиламіно)етанон

5-хлор-N2-(2-фтор-5-метил-4-(1-(3-(піролідин-1-ілсульфоніл)пропіл)-піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)-2-(метиламіно)етанон

5-хлор-N2-(2-фтор-5-метил-4-(1-(3-(морфоліносульфоніл)пропіл)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

1-(2-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-2-(диметиламіно)етанон

4-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)-1-морфолінобутан-1-он
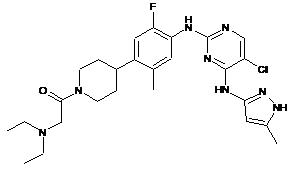
1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)-2-(діетиламіно)етанон

3-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)-N-циклопропілпропанамід

1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)-2-(метиламіно)пропан-1-он

3-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)пропанамід

2-аміно-1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)пропан-1-он
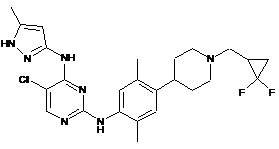
5-xлop-N2-(4-(1-((2,2-дифторциклопропіл)метил)піперидин-4-іл)-2,5-диметилфеніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
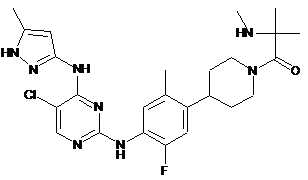
1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)-2-метил-2-(метиламіно)пропан-1-он

5-хлор-N2-(4-(1-циклопропілпіперидин-4-іл)-2,5-диметилфеніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

1-(4-(2-хлор-4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-метилфеніл)піперидин-1-іл)-2-метил-2-(метиламіно)пропан-1-он

N2-(4-(1-((2,2-дифторциклопропіл)-метил)піперидин-4-іл)-2-фтор-5-метилфеніл)-N4-(5-метил-1Н-піразол-3-іл)-5-(трифторметил)-піримідин-2,4-діамін

2-аміно-1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-2-метилпропан-1-он

5-хлор-N2-(2,5-диметил-4-(1-(тетрагідро-2Н-піран-4-іл)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)(1-(метиламіно)циклопропіл)метанон

5-хлор-N2-(2-фтор-4-(піперидин-4-іл)-5-(трифторметил)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
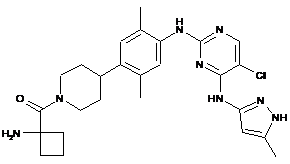
(1-аміноциклобутил)(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)метанон
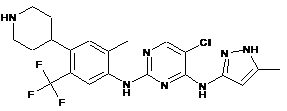
5-хлор-N4-(5-метил-1Н-піразол-3-іл)-N2-(2-метил-4-(піперидин-4-іл)-5-(трифторметил)феніл)піримідин-2,4-діамін
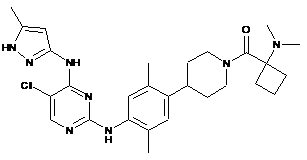
(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)(1-(диметиламіно)циклобутил)метанон

5-хлор-N4-(5-циклопропіл-1Н-піразол-3-іл)-N2-(4-(1-циклопропілпіперидин-4-іл)-2-фтор-5-метилфеніл)піримідин-2,4-діамін

(1-аміноциклопропіл)(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)метанон
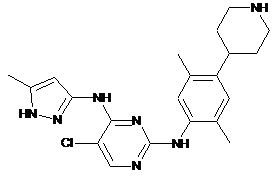
5-хлор-N2-(2,5-диметил-4-(піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(1-(диметиламіно)циклопропіл)метанон

N2-(2,5-диметил-4-(піперидин-4-іл)феніл)-N4-(5-мeтил-1H-пipaзoл-3-iл)-5-(трифторметил)піримідин-2,4-діамін

1-(4-(2-хлор-4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-метилфеніл)піперидин-1-іл)-2-морфоліноетанон
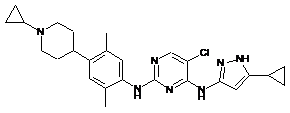
5-хлор-N4-(5-циклопропіл-1Н-піразол-3-iл)-N2-(4-(1-циклопропілпіперидин-4-іл)-2,5-диметилфеніл)піримідин-2,4-діамін
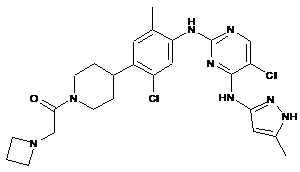
2-(азетидин-1-іл)-1-(4-(2-хлор-4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-метилфеніл)піперидин-1-іл)етанон

5-хлор-N2-(2-фтор-4-(1-((3-ізопропіл-1,2,4-оксадіазол-5-іл)метил)піперидин-4-іл)-5-метилфеніл)-N4-(5-метил-1H-піразол-3-іл)піримідин-2,4-діамін

1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)-2-морфоліноетанон

5-хлор-N2-(4-(1-((3-ізопропіл-1,2,4-оксадіазол-5-іл)метил)піперидин-4-іл)-2,5-диметилфеніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

2-(азетидин-1-іл)-1-(4-(4-(5-хлор-4-(5-метил-1H-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)етанон

2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2-етил-5-метилфеніл)піперидин-1-іл)ацетамід

1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)-2-(піролідин-1-іл)етанон

2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2-метокси-5-метилфеніл)піперидин-1-іл)ацетамід

1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)-2-(1Н-пірол-1-іл)етанон

2-(4-(4-(5-хлор-4-(5-етил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)ацетамід
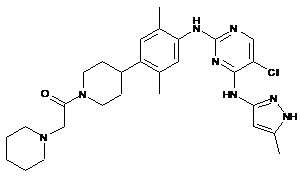
1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-2-(піперидин-1-іл)етанон

5-хлор-N2-{4-[1-(1,1-діоксо-1l,6-тіетан-3-іл)-піперидин-4-іл]-2-фтор-5-метилфеніл}-N4-(5-етил-1Н-піразол-3-іл)-піримідин-2,4-діамін

1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-2-морфоліноетанон

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(3-ізопропіл-1,2,4-оксадіазол-5-іл)метанон

1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-2-(2,6-диметилпіперидин-1-іл)етанон
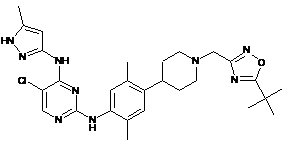
N2-(4-(1-((5-трет-бутил-1,2,4-оксадіазол-3-іл)метил)піперидин-4-іл)-2,5-диметилфеніл)-5-хлор-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
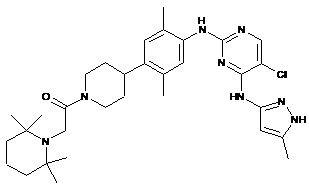
1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-2-(2,2,6,6-тетраметилпіперидин-1-іл)етанон

N2-(4-(1-((5-трет-бутил-1,2,4-оксадіазол-3-іл)метил)піперидин-4-іл)-2-фтор-5-метилфеніл)-5-хлор-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)-2-(4-метилпіперазин-1-іл)етанон

5-хлор-N4-(5-етил-1Н-пiразол-3-іл)-N2-(4-(1-етилпіперидин-4-іл)-2-фтор-5-метилфеніл)піримідин-2,4-діамін
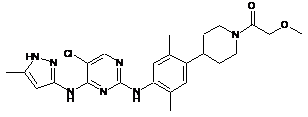 1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-2-метоксіетанон
1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-2-метоксіетанон

5-хлор-N2-(4-(1-(2-(3-ізопропіл-1,2,4-оксадіазол-5-іл)етил)піперидин-4-іл)-2,5-диметилфеніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

N-(2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)-2-оксоетил)ацетамід

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)(3-ізопропіл-1,2,4-оксадіазол-5-іл)метанон

2-(диметиламіно)етил-4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-карбоксилат
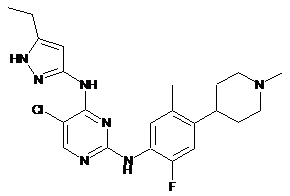
5-хлор-N4-(5-етил-1Н-піразол-3-іл)-N2-(2-фтор-5-метил-4-(1-метилпіперидин-4-іл)феніл)піримідин-2,4-діамін
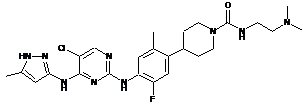
4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)-N-(2-(диметиламіно)етил)-піперидин-1-карбоксамід

5-хлор-N2-(4-(1-циклобутилпіперидин-4-іл)-2-фтор-5-метилфеніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
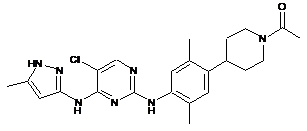
1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)етанон

5-хлор-N2-(2-фтор-5-метил-4-(2-метилпіперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
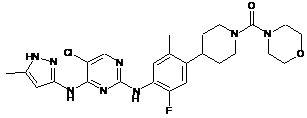
(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(морфоліно)метанон

2-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)-2-метилпіперидин-1-іл)ацетамід

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(4-метилпіперазин-1-іл)метанон

5-хлор-N2-(4-(1,2-диметилпіперидин-4-іл)-2-фтор-5-метилфеніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

1-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-карбоніл)імідазолідин-2-он

N2-(4-(1,4'-біпіперидин-4-іл)-2-фтор-5-метилфеніл)-5-хлор-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
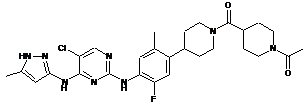
(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)-2-метоксіетанон

5-хлор-N2-(2-фтор-5-метил-4-(1-(6-метилпіридазин-3-іл)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(піперидин-4-іл)метанон

5-хлор-N2-(2-фтор-5-метил-4-(1'-(метилсульфоніл)-1,4'-біпіперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(S)-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(піролідин-2-іл)метанон
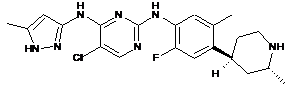
5-хлор-N2-(2-фтор-5-метил-4-((транс)-2-метилпіперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(1-метилазетидин-3-іл)метанон
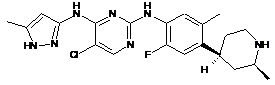
5-хлор-N2-(2-фтор-5-метил-4-((цис)-2-метилпіперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(1-метилпіперидин-4-іл)метанон

5-хлор-N2-(2-фтор-5-метил-4-(1-(піридин-2-ілметил)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

3-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-карбоніл)азетидин-2-он

3-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)циклопент-2-енон

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)(1-метилазетидин-3-іл)метанон

N2-(4-(1-(1,4-діоксаспіро[4,5]декан-8-іл)піперидин-4-іл)-2-фтор-5-метилфеніл)-5-хлор-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
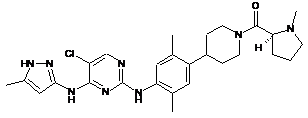
(S)-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)(1-метилпіролідин-2-іл)метанон

5-хлор-N2-(4-(1-((3-етил-1,2,4-оксадiазол-5-іл)метил)піперидин-4-іл)-2-фтор-5-метилфеніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(4-(4-(5-хлор-4-(5-метил-1H-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)(1-метилпіперидин-4-іл)метанон

5-хлор-N2-(2-фтор-4-(1-((5-ізопропіл-1,2,4-оксадіазол-3-іл)метил)піперидин-4-іл)-5-метилфеніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-iл)((2R,4R)-4-гідрокси-1-метилпіролідин-2-іл)метанон

5-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-4-метил-2-(1-метилпіперидин-4-іл)бензонітрил

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(1Н-пірол-2-іл)метанон

метил-5-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-4-метил-2-(1-метилпіперидин-4-іл)бензоат

(S)-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(1-ізопропілпіперидин-2-іл)метанон
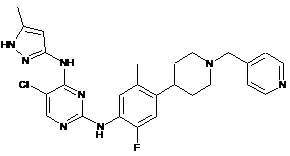
5-хлор-N2-(2-фтор-5-метил-4-(1-(піридин-4-ілметил)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(S)-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(4-ізопропілморфолін-3-іл)метанон

4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)-1-етилпіперидин 1-оксид

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(2,4-диметилоксазол-5-іл)метанон

4-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)циклогексанон

(4-(4-(5-хлор-4-(5-метил-1H-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)((2S)-4-гідрокси-1-метилпіролідин-2-іл)метанон

трет-бутил-3-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)-піперидин-1-іл)піролідин-1-карбоксилат
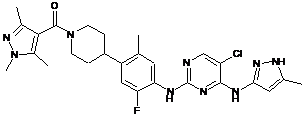
(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(1,3,5-триметил-1Н-піразол-4-іл)метанон

5-хлор-N2-(2-фтор-5-метил-4-(1-((5-метил-1,2,4-оксадіазол-3-іл)метил)-піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(1-метил-5-(трифторметил)-1Н-піразол-4-іл)метанон

5-хлор-N2-(2-фтор-5-метил-4-(1-((3-метил-1,2,4-оксадіазол-5-іл)метил)-піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

азетидин-3-іл(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)метанон

4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)-1-(тетрагідро-2Н-піран-4-іл)піперидин 1-оксид

(S)-азетидин-2-іл(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)метанон
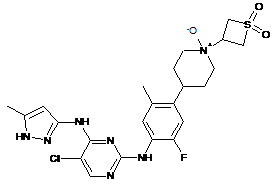
5-хлop-N2-{4-[1-(1,1-діоксо-1l,6-тіетан-3-іл)-1-оксидпіперидин-4-іл]-2-фтор-5-метилфеніл}-N4-(5-етил-1Н-піразол-3-іл)-піримідин-2,4-діамін

(R)-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-2,5-диметилфеніл)піперидин-1-іл)(1-метилпіролідин-2-іл)метанон

N2-(4-(l-(азетидин-3-іл)4-iл)-2-фтор-5-метилфеніл)-5-хлор-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(R)-(4-(4-(5-хлор-4-(5-метил-1H-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(1-метилпіролідин-2-іл)метанон

5-хлор-N2-(2-фтор-5-метил-4-(1-(піридин-3-ілметил)піперидин-N4-іл)феніл)-4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(R)-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(1-ізопропілпіролідин-2-іл)метанон

4-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)циклогексанол

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(4-метилоксазол-5-іл)метанон
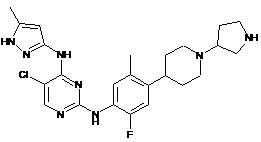
5-хлор-N2-(2-фтор-5-метил-4-(1-(піролідин-3-іл)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(3,5-диметилізоксазол-4-іл)метанон

5-хлор-N2-(2-фтор-5-метил-4-(1-(1-(метилсульфоніл)азетидин-3-іл)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
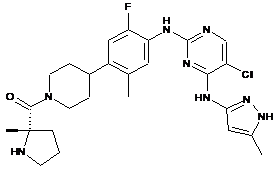
(S)-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(2-метилпіролідин-2-іл)метанон

5-хлор-N2-(2-фтор-5-метил-4-(1-(1-(метилсульфоніл)піролідин-3-іл)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)((2S,3R)-3-гідрокси-1-метилпіролідин-2-іл)метанон

5-хлор-N2-(2,5-диметил-4-(1-((3-метил-1,2,4-оксадіазол-5-іл)метил)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(1Н-тетразол-1-іл)метанон

5-хлор-N2-(4-(1-((3-етил-1,2,4-оксадіазол-5-іл)метил)піперидин-4-іл)-2,5-диметилфеніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(2-метил-5-(трифторметил)оксазол-4-іл)метанон
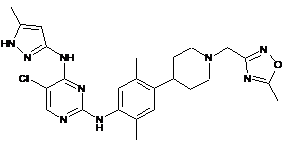
5-хлор-N2-(2,5-диметил-4-(1-((5-метил-1,2,4-оксадіазол-3-іл)метил)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

6-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-карбоніл)-піперидин-2-он

5-xлop-N2-(4-(1-((5-ізопропіл-1,2,4-оксадіазол-3-іл)метил)піперидин-4-іл)-2,5-диметилфеніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

(S)-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)(морфолін-3-іл)метанон

5-хлор-N2-(2-фтор-5-метил-4-(1-(оксетан-3-іл)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
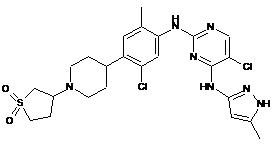
5-хлор-N2-(2-метил-5-хлор-4-(1-(тетрагідро-1,1-діоксидо-3-тієніл)піперидин-4-іл)феніл)-N4-(5-метил-1H-піразол-3-іл)піримідин-2,4-діамін

5-хлор-N2-(2,5-диметил-4-(1-(піридин-2-ілметил)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

5-хлор-N2-(2-фтор-5-метил-4-(1-(тетрагідро-1,1-діоксидо-3-тієніл)піперидин-4-іл)феніл)-N4-(5-метил-1H-піразол-3-іл)піримідин-2,4-діамін
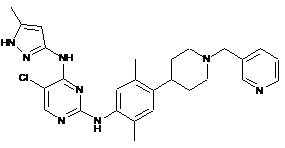
5-хлор-N2-(2,5-диметил-4-(1-(піридин-3-ілметил)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
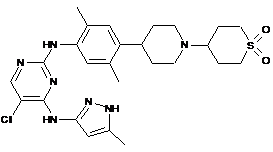
5-хлор-N2-(2,5-диметил-4-(1-(тетрагідро-1,1-діоксидо-2H-тіопіран-4-іл))піперидин-4-іл)феніл)-N4-(5-метил-1H-піразол-3-іл)піримідин-2,4-діамін
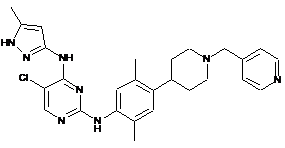 5-хлор-N2-(2,5-диметил-4-(1-(піридин-4-ілметил)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
5-хлор-N2-(2,5-диметил-4-(1-(піридин-4-ілметил)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

5-хлор-N2-(2-хлор-5-метил-4-(1-(1,1-діоксидо-3-тіетаніл)піперидин-4-іл)феніл)-N4-(5-метил-1H-піразол-3-іл)піримідин-2,4-діамін

транс-4-(4-(4-(5-хлор-4-(5-метил-1H-піразол-3-іламіно)піримідин-2іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)циклогексанол

5-хлор-N2-(2-хлор-5-метил-4-(1-(1,1-діоксидо-3-тіетаніл)піперидин-4-іл)феніл)-N4-(5-мeтил-1Н-піразол-3-іл)піримідин-2,4-діамін

цис-4-(4-(4-(5-хлор-4-(5-метил-1Н-піразол-3-іламіно)піримідин-2-іламіно)-5-фтор-2-метилфеніл)піперидин-1-іл)циклогексанол

5-хлор-N2-(4-(1-(5-етилпіримідин-2іл)піперидин-4-іл)-2-фтор-5метилфеніл)-N4-(5метил-1H-піразол-3іл)піримідин-2,4-діамін

(R)-5-хлор-N2-(2-фтор-5-метил-4-(1-(1-(метилсульфоніл)піролідин-3-іл)піперидин-4-іл)феніл)-N4-(5-метил-1H-піразол-3-іл)піримідин-2,4-діамін
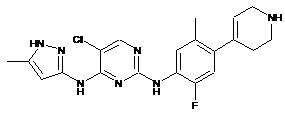
5-хлор-N2-(2-фтор-5-метил-4-(1,2,3,6-тетрагідропіридин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
 (S)-5-хлор-N2-(2-фтор-5-метил-4-(1-(1-(метилсульфоніл)піролідин-3-іл)піперидин-4-іл)феніл)-N4-(5-метил-1H-піразол-3-іл)піримідин-2,4-діамін
(S)-5-хлор-N2-(2-фтор-5-метил-4-(1-(1-(метилсульфоніл)піролідин-3-іл)піперидин-4-іл)феніл)-N4-(5-метил-1H-піразол-3-іл)піримідин-2,4-діамін
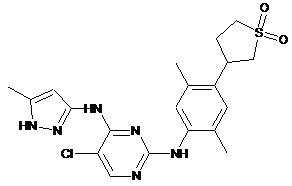
5-хлор-N2-[4-(1,1-діоксотетрагідро-1l6-тіофен-3-іл)-2,5-диметилфеніл]-N4-(5-метил-1H-піразол-3-іл)-піримідин-2,4-діамін

5-хлор-N2-(2-фтор-5-метил-4-(1-(піримідин-5-ілметил)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
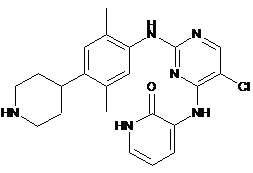
3-(5-хлор-2-(2,5-диметил-4-(піперидин-4-іл)феніламіно)піримідин-4-іламіно)піридин-2(1Н)-он

5-хлор-N2-(2-фтор-5-метил-4-(1-(піразин-2-ілметил)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін

5-хлор-N2-(2-фтор-5-метил-4-(1-метилпіперидин-4-іл)феніл)-N4-(5-метилізоксазол-3-іл)піримідин-2,4-діамін

5-хлор-N2-(2-фтор-5метил-4-(1-піридазин-4-ілметил)піперидин-4-іл)феніл)-N4-(5-метил-1H-піразол-3іл)піримідин-2,4-діамін

3-(5-хлор-2-(2,5-диметил-4-(піперидин-4-іл)феніламіно)піримідин-4-іламіно)піридин-2(1Н)-он

5-хлор-N2-(2,5-диметил)-4-(1-(піримідин-5-ілметил)піперидин-4-іл)феніл)-N4-(5-метил-1H-піразол-3-іл)піримідин-2,4-діамін
 5-хлор-N2-(2-ізопропокси-5-метил-4-(1-метилпіперидин-4-іл)феніл)-N4-(1Н-піразол-3-іл)піримідин-2,4-діамін
5-хлор-N2-(2-ізопропокси-5-метил-4-(1-метилпіперидин-4-іл)феніл)-N4-(1Н-піразол-3-іл)піримідин-2,4-діамін
 5-хлор-N2-(2,5-диметил-4-(1-(піразин-2-ілметил)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
5-хлор-N2-(2,5-диметил-4-(1-(піразин-2-ілметил)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін
11. Сполука за будь-яким з пп. 1-10, де зазначена сполука вибрана з-поміж:
5-хлор-N2-(2-фтор-5-метил-4-(1-(1,1-діоксидо-3-тіетаніл)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін;
5-хлор-N2-(2-фтор-5-метил-4-(1-(тетрагідро-2Н-піран-4-іл)піперидин-4-іл)феніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін або
5-хлор-N2-(4-(1-етилпіперидин-4-іл)-2-фтор-5-метилфеніл)-N4-(5-метил-1Н-піразол-3-іл)піримідин-2,4-діамін; або
їх фармацевтично прийнятні солі.
12. Сполука за будь-яким з пп. 1-11 для застосування, необов'язково у комбінації з другим терапевтичним агентом, який необов'язково являє собою хіміотерапевтичний агент, у лікуванні IGF-1R-опосередкованого стану у ссавця, що страждає від нього, де зазначений стан являє собою аутоімунну хворобу, реакцію "трансплантат проти хазяїна", інфекційну хворобу або клітинно-проліферативний розлад.
13. Сполука за п. 12, де стан являє собою клітинно-проліферативний розлад, який являє собою мієломну хворобу, нейробластому, синовіальну, гепатоцелюлярну, саркому Юінга або солідну пухлину, вибрану з таких як: остеосаркома, меланома та пухлина молочної залози, нирки, передміхурової залози, колоректальної області, щитовидної залози, яєчника, підшлункової залози, легені, матки або шлунково-кишкового тракту.
14. Фармацевтична композиція, що містить терапевтично ефективну кількість сполуки за будь-яким з пп. 1-11 та фізіологічно прийнятний носій.
15. Фармацевтична композиція за п. 14, необов'язково у комбінації з другим терапевтичним агентом, який необов'язково являє собою хіміотерапевтичний агент, для застосування у лікуванні IGF-1R-опосередкованого стану у ссавця, що страждає від нього, де зазначений стан являє собою аутоімунну хворобу, реакцію "трансплантат проти хазяїна", інфекційну хворобу або клітинно-проліферативний розлад.
16. Фармацевтична композиція за п. 15, де стан являє собою клітинно-проліферативний розлад, який являє собою мієломну хворобу, нейробластому, синовіальну, гепатоцелюлярну, саркому Юінга або солідну пухлину, вибрану з таких як: остеосаркома, меланома та пухлина молочної залози, нирки, передміхурової залози, колоректальної області, щитовидної залози, яєчника, підшлункової залози, легені, матки або шлунково-кишкового тракту.
17. Застосування сполуки за будь-яким з пп. 1-11 або її фармацевтичної композиції для виробництва лікарського засобу для лікування стану, опосередкованого IGF-1R або кіназою анапластичної лімфоми, та необов'язково у комбінації з другим терапевтичним агентом, де зазначений стан являє собою аутоімунну хворобу, реакцію "трансплантат проти хазяїна", інфекційну хворобу або клітинно-проліферативний розлад.
18. Застосування фармацевтичної композиції за п. 14 для виробництва лікарського засобу для лікування стану, опосередкованого IGF-1R або кіназою анапластичної лімфоми, та необов'язково у комбінації з другим терапевтичним агентом, де зазначений стан являє собою аутоімунну хворобу, реакцію "трансплантат проти хазяїна", інфекційну хворобу або клітинно-проліферативний розлад.
Текст
Реферат: Даний винахід забезпечує нові похідні піримідину, їх фармацевтичні композиції та застосування таких сполук. Наприклад, похідні піримідину даного винаходу можуть бути використані для лікування, полегшення симптомів або профілактики стану, який реагує на інгібування інсуліноподібного фактора росту (IGF-1R) або кінази анапластичної лімфоми (ALK). UA 101057 C2 (12) UA 101057 C2 R1 Z1 N R3 N Z3 E R2 N Z2 N R4 0-1 (R 5)m 0-1 (1) UA 101057 C2 5 10 15 20 25 Перехресні посилання до споріднених заявок Дана заявка заявляє пріоритет до Попередніх Патентних Заявок США серійні номери 61/075,583, поданої 25 червня 2008 року, та 61/155,434, поданої 25 лютого 2009 року, розкриття кожної з яких включене у даний опис шляхом посилання у їх повноті. Галузь винаходу Даний винахід відноситься до інгібіторів протеїнкінази, особливо до нових похідних піримідину та їх фармацевтичних композицій, та їх застосування як фармацевтичних препаратів. Передумови створення винаходу Сигналювання інсуліно-подібного фактору росту (IGF-1) високо залучене у рак, з IGF-1 рецептором (IGF-1R) як домінуючим фактором. IGR-1R є важливим для трансформації пухлини та виживання злоякісних клітин, але тільки частково залучений у ріст нормальних клітин. Націлювання IGF-1R запропоноване як багатообіцяючий варіант терапії раку. (Larsson et al., Br. J. Cancer 92:2097-2101 (2005)). Кіназа анапластичної лімфоми (ALK), член суперсімейства інсулінових рецепторів рецепторних тирозин-кіназ, залучена у онкогенез у гематопоетичних та негематопоетичних пухлинах. Аберантна експресія непроцессованих ALK рецепторних білків описана у нейробластомах та гліобластомах; та ALK білки злиття зустрічаються у анапластичній великоклітинній лімфомі. Дослідження ALK білків злиття також збільшило можливість нових терапевтичних лікувань для пацієнтів з ALK-позитивними злоякісними утвореннями. (Pulford et al., Cell. Mol. Life Sci. 61: 2939-2953 (2004)). Через пов’язані з хворобами ролі IGF-1R та ALK, існує постійна необхідність у сполуках, які можуть бути корисними для лікування та профілактики хвороби, яка чутлива до інгібування IGF1R та ALK. Розкриття даного винаходу Даний винахід відноситься до нових похідних піримідину та їх фармацевтичних композицій, та їх застосування як фармацевтичних препаратів. У одному аспекті, даний винахід забезпечує сполуку Формули (1): R1 Z1 N 30 35 40 45 N Z3 E R2 N Z2 0-1 N 0-1 (1) (R 5)m R3 R4 або її фізіологічно прийнятну сіль; у якій кільце E може необов’язково містити подвійний зв’язок; 1 2 3 6 6 + один з Z , Z та Z являє собою NR , N(R ) -O або S(O)1-2 та інші являють собою CR2; 1 R являє собою гало групу або необов’язково галогенований C1-6 алкіл; 2 R являє собою піридин-2-оніл, азепан-2-оніл або моноциклічний 5-6-членний гетероарил, що має 1-3 гетероатоми, що вибирають з N, O та S; кожен з яких необов’язково заміщений за 9 9 допомогою R , де R являє собою C1-6 алкіл, C1-6 галоалкіл або C3-7 циклоалкіл; 3 4 R та R кожен являє собою H; 5 R являє собою гало групу, гідроксил, C1-6 алкіл, C1-6 алкокси, гало-заміщений C1-6 алкіл, 8 гало-заміщену C1-6 алкокси групу, ціано групу або C(O)O0-1R ; 6 R являє собою H; C1-6 алкіл, C2-6 алкеніл або C2-6 алкініл, кожен з яких може бути 7 необов’язково заміщений за допомогою гало та/або гідроксильних груп; -(CR2)p-OR , -(CR2)p7 7 CH(OH)CtF2t+1, де t являє собою 1-3, (CR2)p-CN; (CR2)p-NR(R ), -(CR2)p–C(O)OR , 7 8 8 7 7 (CR2)pNR(CR2)pOR , (CR2)pNR-L-C(O)R , C(O)(CR2)qOR , -C(O)O-(CR2)p-NRR , –C(O) -(CR2)p-OR , 7 7 7 7 L-Y, -L-C(O)R , -L–C(O)-NRR , -L–C(O)-NR-(CR2)p-NRR ,-L-C(O)NR(CR2)pOR , -L–C(O)-(CR2)q-NR8 7 8 8 7 C(O)-R , -L-C(O)NR(CR2)pSR , -L-C(O)NR(CR2)pS(O)1-2R , -L-S(O)2R , -L-S(O)2-(CR2)q-NRR , -L7 7 S(O)2NR(CR2)pNR(R ) або -L-S(O)2NR(CR2)pOR ; 6 альтернативно, R являє собою радикал, вибраний з формули (a), (b), (c) або (d): 15 R11 R12 R N R16 L 1-2 R10 15 R11 R12 R N R16 L 1-2 SO2 0-1 1-2 (a) O R13 R14 (c) (b) 1 0-1 S 1-2 O O R13 R14 (d) UA 101057 C2 10 5 10 15 20 17 17 8a R5c Z1 Z2 Z3 E 0-1 1 R N R N N 30 R5b N R4 R3 5a (2) 0-1 2 25 5b R5a 5c у якій один з R , R та R являє собою H та інші являють собою незалежно гало групу, C 1-6 8 8 алкіл, C1-6 алкокси групу, гало-заміщений C1-6 алкіл, ціано групу або C(O)O0-1R , де R являє собою C1-6 алкіл; та 1 2 3 4 1 2 3 R , R , R , R , E, Z , Z та Z приймають значення, визначені у Формулі (1). 3 6 6 + У деяких прикладах, Z у представленій вище Формулі (2) являє собою NR або N(R ) -O ; та 1 2 6 Z та Z являють собою CH2. У інших прикладах, R являє собою H, C1-6 алкіл, необов’язково 7 заміщений за допомогою гало та/або гідроксильних груп; -(CR2)p-OR , -(CR2)p-CH(OH)CtF2t+1, де t 7 7 8 являє собою 1-3, L-Y, (CR2)p-CN; (CR2)p-NR(R ), -(CR2)p–C(O)OR , C(O)(CR2)qOR , -C(O)O-(CR2)p7 7 7 7 8 8 NRR , -L-C(O)R , -L–C(O)-NRR , -L–C(O)-NR-(CR2)p-NRR , -L–C(O)-(CR2)q-NR-C(O)-R , -L-S(O)2R , 7 -L-S(O)2-(CR2)q-NRR , або радикал, вибраний з формули (a), (b), (c) або (d): 15 R11 R12 R N R16 L 1-2 R10 15 R11 R12 R N R16 L 1-2 SO2 0-1 R13 R14 1-2 (a) 35 40 8a R являє собою O, S, NR , де R являє собою H, C1-6 алкіл, SO2R або CO2R ; 11 12 13 14 15 16 R , R , R , R , R та R незалежно вибирають з таких як: H; C1-6 алкокси група; C1-6 алкіл, C2-6 алкеніл або C2-6 алкініл, кожен з яких може бути необов’язково заміщений за допомогою 11 12 12 15 15 16 13 14 13 15 гало, аміно або гідроксильних груп; або R та R , R та R , R та R , R та R , або R та R разом з атомами, до яких вони приєднані, можуть утворювати 3-7-членне насичене, ненасичене або частково ненасичене кільце, що містить 1-3 гетероатоми, вибрані з N, O та S, та 5 необов’язково заміщене за допомогою оксо та 1-3 R груп; L являє собою (CR2)1-4 або зв’язок; Y являє собою C3-7 карбоциклічне кільце, C6-10 арил, або 5-10-членне гетероарильне або 45 10-членне гетероциклічне кільце, кожне з яких необов’язково заміщене за допомогою 1-3 R груп; 7 8 8a R , R та R незалежно являють собою C1-6 алкіл, C2-6 алкеніл або C2-6 алкініл, кожен з яких може бути необов’язково заміщений за допомогою гало, аміно, гідроксильних або ціано груп; 7 (CR2)qY або C1-6 алкокси групу; або R являє собою H; кожен R незалежно являє собою H або C1-6 алкіл; 7 7 R та R разом з N у кожному NRR можуть утворювати 5-6 членне кільце, що містить 1-3 5 гетероатоми, вибрані з N, O та S, та необов’язково заміщене за допомогою оксо та 1-3 R груп; m являє собою 2-4; n являє собою 1-3; p являє собою 1-4; та q являє собою 0-4. У одному варіанті втілення, даний винахід забезпечує сполуку Формули (2): 10 O (c) (b) 17 17 0-1 S 1-2 O 8a O R13 R14 (d) 8a R являє собою O, S, NR , де R являє собою H, C1-6 алкіл, SO2R або CO2R ; 8a R являє собою C1-6 алкіл; та 7 8 10 11 12 13 14 15 16 R , R , R , R , R , R , R , R , R , R, L, Y, p та q приймають значення, визначені у Формулі (1). 2 У представленій вище Формулі (1) та (2), R може являти собою піразоліл, ізоксазоліл, піридин-2-оніл або азепан-2-оніл, кожен з яких заміщений за допомогою C1-6 алкілу, C1-6 галоалкілу або C3-7 циклоалкілу. У іншому варіанті втілення, даний винахід забезпечує сполуку Формули (3): 2 UA 101057 C2 R5c R HN N N 10 Z2 Z3 E 1 N N (3) R5b N R5a R4 R3 5 Z1 або її таутомер; 5b 5a 5c у якій R являє собою H; та R та R незалежно являють собою гало групу, C 1-6 алкіл, C1-6 8 8 алкокси групу, гало-заміщений C1-6 алкіл, ціано групу або C(O)O0-1R , де R являє собою C1-6 алкіл; 1 2 2 Z та Z являють собою CH ; 3 6 6 + Z являє собою NR або N(R ) -O ; 6 R являє собою H, C1-6 алкіл, необов’язково заміщений за допомогою гало та/або гідроксильних груп; 7 7 -(CR2)p-OR , -(CR2)p-CH(OH)CtF2t+1, де t являє собою 1-3, (CR2)p-CN; (CR2)p-NR(R ), 7 8 7 7 -(CR2)p–C(O)OR , C(O)(CR2)qOR , -C(O)O-(CR2)p-NRR , L-Y, -L-C(O)R , 7 7 8 8 -L–C(O)-NRR , -L–C(O)-NR-(CR2)p-NRR , -L–C(O)-(CR2)q-NR-C(O)-R , -L-S(O)2R , 7 -L-S(O)2-(CR2)q-NRR , або радикал, вибраний з формули (a), (b), (c) або (d): 15 R11 R12 R N R16 L 1-2 R10 15 R11 R12 R N R16 L 1-2 SO2 0-1 R13 R14 1-2 (a) 15 20 25 30 35 10 O (c) (b) 17 17 0-1 S 1-2 O 8a O R13 R14 (d) 8a R являє собою O, S, NR , де R являє собою H, C1-6 алкіл, SO2R або CO2R ; 8a R являє собою C1-6 алкіл; та 1 3 4 7 8 10 11 12 13 14 15 16 R , R , R , R , R , R , R , R , R , R , R , R , R, L, Y, p, q та E приймають значення, визначені у Формулі (1). 5a 5c У представленій вище Формулі (3), R може являти собою гало групу та R являє собою C16 10 6 алкіл. У деяких прикладах, R являє собою C1-6 алкіл або радикал формули (a) або (c); та R являє собою O. 1 У представленій вище Формулі (1), (2) та (3), R може являти собою гало групу. У 1 3 4 специфічних прикладах, R являє собою хлор. У інших прикладах, R та R являють собою H. У іншому аспекті, даний винахід забезпечує сполуку Формули (4): R1 HN N N X (4) N N N (R 5 )m 3 4 R R або її фізіологічно прийнятну сіль; у якій X являє собою моноциклічне 5-6 членне гетероциклічне кільце, що містить 1-3 гетероатоми, вибрані з N, O та S, та необов’язково заміщене на кільцевому атомі вуглецю, що може бути заміщений, за допомогою оксо групи та на будь-якому кільцевому атомі азоту, що 6 може бути заміщений, за допомогою R ; 1 R являє собою гало групу; 3 4 R та R кожен являє собою H; 5 R являє собою гало групу, гідроксил, C1-6 алкіл, C1-6 алкокси групу, гало-заміщений C1-6 8 алкіл, гало-заміщену C1-6 алкокси групу, ціано групу або C(O)O0-1R ; 6 R являє собою H; C1-6 алкіл, C2-6 алкеніл або C2-6 алкініл, кожен з яких може бути 7 необов’язково заміщений за допомогою гало та/або гідроксильних груп; -(CR2)p-OR , -(CR2)p7 7 CH(OH)CtF2t+1, де t являє собою 1-3, (CR2)p-CN; (CR2)p-NR(R ), -(CR2)p–C(O)OR , 7 (CR2)pNR(CR2)pOR , 8 8 7 7 (CR2)pNR-L-C(O)R , C(O)(CR2)qOR , -C(O)O-(CR2)p-NRR , –C(O) -(CR2)p-OR , L-Y, 3 UA 101057 C2 7 5 7 7 7 -L-C(O)R , -L–C(O)-NRR , -L–C(O)-NR-(CR2)p-NRR ,-L-C(O)NR(CR2)pOR , 8 7 8 -L-C(O)-(CR2)q-NR-C(O)-R , -L-C(O)NR(CR2)pSR , -L-C(O)NR(CR2)pS(O)1-2R , 8 7 7 -L-S(O)2R , -L-S(O)2-(CR2)q-NRR , -L-S(O)2NR(CR2)pNR(R ) або 7 -L-S(O)2NR(CR2)pOR ; 6 альтернативно, R являє собою радикал, вибраний з формули (a), (b), (c) або (d): 15 R11 R12 R N R16 L 1-2 R10 15 R11 R12 R N R16 L 1-2 SO2 0-1 R13 R14 1-2 (a) 10 10 15 20 25 30 35 40 45 50 55 O (c) (b) 17 17 0-1 S 1-2 O 8a O R13 R14 (d) 8a R являє собою O, S, NR , де R являє собою H, C1-6 алкіл, SO2R або CO2R ; 11 12 13 14 15 16 R , R , R , R , R та R незалежно вибирають з таких як: H; C1-6 алкокси група; C1-6 алкіл, C2-6 алкеніл або C2-6 алкініл, кожен з яких може бути необов’язково заміщений за допомогою 11 12 12 15 15 16 13 14 13 15 гало, аміно або гідроксильних груп; або R та R , R та R , R та R , R та R , або R та R разом з атомами, до яких вони приєднані, можуть утворювати 3-7-членне насичене, ненасичене або частково ненасичене кільце, що містить 1-3 гетероатоми, вибрані з N, O та S, та5 необов’язково заміщене за допомогою оксо та 1-3 R груп; L являє собою (CR2)1-4 або зв’язок; Y являє собою C3-7 карбоциклічне кільце, C6-10 арил, або 5-10-членне гетероарильне або 45 10-членне гетероциклічне кільце, кожне з яких необов’язково заміщене за допомогою 1-3 R груп; 7 8 8a R , R та R незалежно являють собою C1-6 алкіл, C2-6 алкеніл або C2-6 алкініл, кожен з яких може бути необов’язково заміщений за допомогою гало групи, аміно групи, гідроксилу або ціано 7 групи; (CR2)qY або C1-6 алкокси групу; або R являє собою H; кожен R незалежно являє собою H або C1-6 алкіл; 7 7 R та R разом з N у кожній NRR можуть утворювати 5-6 членне кільце, що містить 1-3 5 гетероатоми, вибрані з N, O та S, та необов’язково заміщене за допомогою оксо та 1-3 R груп; m являє собою 2-4; n являє собою 1-3; p являє собою 1-4; та q являє собою 0-4. У представленій вище Формулі (4), X може являти собою морфолініл, піперазиніл, піперазин-2-оніл, оксазолідин-2-оніл або піперидин-2-оніл, кожен з яких є заміщеним на будьякому кільцевому атомі азоту, що може бути заміщений, за допомогою C 1-6 алкілу; або X являє 1 собою тетрагідро-2H-піран-2-оніл; та R являє собою хлор. У іншому аспекті, даний винахід забезпечує фармацевтичні композиції, що включають сполуку, яка має Формулу (1), (2), (3) та (4), та a фізіологічно прийнятний наповнювач. У ще одному іншому аспекті, даний винахід забезпечує способи інгібування IGF-1R у клітині, що включає контактування клітини з ефективною кількістю сполуки, що має Формулу (1), (2), (3) та (4), або її фармацевтичної композиції. Даний винахід також забезпечує способи лікування, полегшення симптомів або профілактики стану, який реагує на інгібування IGF-1R або кінази анапластичної лімфоми (ALK) у ссавця, що страждає від зазначеного стану, що включає введення ссавцю терапевтично ефективної кількості сполуки, що має Формулу (1), (2), (3) та (4), або її фармацевтичної композиції, та необов’язково у комбінації з другим терапевтичним агентом. Альтернативно, даний винахід забезпечує застосування сполуки, що має Формулу (1), (2), (3) та (4), та необов’язково у комбінації з другим терапевтичним агентом, у виробництві лікарського засобу для лікування стану, опосередкованого IGF-1R або ALK. Сполуки даного винаходу можуть бути введені, наприклад, ссавцю, що страждає від аутоімунної хвороби, реакції «трансплантат проти хазяїна», інфекційної хвороби або клітинно-проліферативного розладу. У специфічних прикладах, сполуки даного винаходу можуть бути використані окремо або у комбінації з хіміотерапевтичним агентом для лікування клітинно-проліферативного розладу, включаючи, не обмежуючись наведеними, такі як: мієломна хвороба, нейробластома, синовіальна, гепатоцелюлярна саркома Юінга або солідна пухлина, яку вибирають з таких як: остеосаркома, меланома, та пухлина молочної залози, нирки, передміхурової залози, коло ректальної області, щитовидної залози, яєчнику, підшлункової залози, легені, матки або шлунково-кишкового тракту. 4 UA 101057 C2 5 10 15 20 25 30 35 40 45 50 55 60 Визначення “Алкіл” відноситься до залишку та як структурний елемент інших груп, наприклад, галозаміщений-алкіл та алкокси група, та може бути лінійно-ланцюговим або розгалуженим. Необов’язково заміщений алкіл, алкеніл або алкініл, як використано у цьому описі, може бути необов’язково галогенований (наприклад, CF3), або може мати один або більшу кількість вуглеців, які є заміщеними або заміненими гетероатомом, таким як NR, O або S (наприклад, – OCH2CH2O–, алкілтіоли, тіоалкокси, алкіламіни, тощо). “Арил” відноситься до моноциклічного або сконденсованого біциклічного ароматичного кільця, що містить вуглецеві атоми. “Арилен” являє собою двовалентний радикал, одержаний з арильної групи. Наприклад, арильна група може являти собою феніл, інденіл, інданіл, нафтил, або 1,2,3,4-тетрагідронафталеніл, який може бути необов’язково заміщений у орто, мета або пара положенні. “Гетероарил”, як використано у цьому описі, визначається як описано вище для арилу, де один або більша кількість кільцевих членів являє собою гетероатом. Наприклад, гетероарильний замісник для використання у сполуках даного винаходу може являти собою моноциклічний або біциклічний 5-10 членний гетероарил, що містить 1-4 гетероатоми, які вибирають з N, O, та S. Приклади гетероарилів включають, не обмежуючись наведеними, піридил, піразиніл, індоліл, індазоліл, хіноксалініл, хінолініл, бензофураніл, бензопіраніл, бензотіопіраніл, бензо[1,3]діоксол, імідазоліл, бензо-імідазоліл, піримідиніл, фураніл, оксазоліл, ізоксазоліл, триазоліл, бензотриазоліл, тетразоліл, піразоліл, тієніл, піроліл, ізохінолініл, пуриніл, тіазоліл, тетразиніл, бензотіазоліл, оксадіазоліл, бензоксадіазоліл, тощо. “Карбоциклічне кільце”, як використано у цьому описі, відноситься до насиченого або частково ненасиченого, моноциклічного, сконденсованого біциклічного або місткового поліциклічного кільця, що містить атоми вуглецю, які можуть бути необов’язково заміщені, наприклад, за допомогою =O. Приклади карбоциклічних кілець включають, не обмежуючись наведеними, циклопропіл, циклобутил, циклопентил, циклогексил, циклопропілен, циклогексанон, тощо. “Гетероциклічне кільце”, як використано у цьому описі, визначається як описано вище для карбоциклічного кільця, де один або більша кількість кільцевих атомів вуглецю являють собою гетероатом. Наприклад, гетероциклічне кільце для застосування у сполуках даного винаходу може являти собою 4-7 членне гетероциклічне кільце, що містить 1-3 гетероатоми, вибрані з N, O та S, або їх комбінацію, таку як -S(O) або -S(O)2-. Приклади гетероциклічних кілець включають, не обмежуючись наведеними, азетидиніл, морфоліно, піролідиніл, піролідиніл-2-он, піперазиніл, піперидиніл, піперидинілон, 1,4-діокса-8-аза-спіро[4.5]дец-8-ил, 1,2,3,4тетрагідрохінолініл тощо. Гетероциклічні кільця, як використано у цьому описі, можуть включати біциклічні аміни та біциклічні діаміни. Як використано у цьому описі, H атом у будь-яких групах - замісниках (наприклад, CH2) 2 3 включає всі прийнятні ізотопні варіанти, наприклад, H, H та H. Термін “фармацевтична комбінація”, як використано у цьому описі, означає продукт, який одержують після змішування або об’єднання активних інгредієнтів та включає як фіксовані, так і нефіксовані комбінації активних інгредієнтів. Термін “фіксована комбінація” означає, що активні інгредієнти, наприклад, сполуку Формули (1) та спів-агент, обидва вводять пацієнту одночасно у формі однієї одиниці або дози. Термін “нефіксована комбінація” означає, що активні інгредієнти, наприклад, сполуку Формули (1) та спів-агент, обидва вводять пацієнту як окремі одиниці або одночасно, паралельно або послідовно без специфічних обмежень часу, де таке введення забезпечує терапевтично ефективні рівні активних інгредієнтів у організмі пацієнта. Останню також застосовують для лікування сумішами, наприклад, введення трьох або більшої кількості активних інгредієнтів. “Ссавець” відноситься до будь-якої тварини, що класифікується як ссавець, включаючи людей, домашніх та сільськогосподарських тварин, та тварин, що утримуються у зоопарках, тварин, що пов’язані із спортом, або тварин - домашній улюбленців, таких як собаки, коти, велика рогата худоба, коні, вівці, свині, кози, кролики, тощо. У специфічних прикладах, ссавцем є людина. Термін "введення" або "що вводять" сполуки даного винаходу означає забезпечення доставки сполуки даного винаходу та її проліків суб’єкту, якому необхідне таке лікування. Введення “у комбінації з” одним або більшою кількістю додаткових терапевтичних агентів включає одночасне (паралельне) та послідовне введення у будь-якому порядку, та будь-яким шляхом введення. “Ефективна кількість” сполуки являє собою кількість, достатню для досягнення специфічно встановленої цілі. “Ефективна кількість” може бути визначена емпірично та рутинним способом 5 UA 101057 C2 5 10 15 20 25 30 35 40 45 50 55 60 відносно встановленої цілі. Термін “терапевтично ефективна кількість” відноситься до кількості сполуки (наприклад, IGF1R антагоністу), ефективної для “лікування” IGF-1R-опосередкованого розладу суб’єкта або ссавця. У випадку раку, терапевтично ефективна кількість лікарського засобу може зменшувати кількість ракових клітин; зменшувати розмір пухлини; інгібувати (тобто уповільнювати до деякого ступеню та переважно зупиняти) інфільтрацію ракових клітин у периферичні органи; інгібувати (тобто уповільнювати до деякого ступеню та переважно зупиняти) метастази пухлин; інгібувати, до деякого ступеню, ріст пухлини; та/або полегшувати до деякого ступеню один або більшу кількість симптомів, пов’язаних з раком. Дивись визначення “лікування” у даному описі. Наскільки можливо лікарський засіб може запобігати росту та/або знищувати існуючі ракові клітини, він може бути цитостатичним та/або цитотоксичним. Термін “рак” відноситься до фізіологічного стану у ссавців, що, як правило, характеризується нерегульованим ростом/проліферацією клітин. Приклади раку включають, не обмежуючись наведеними, такі як: карцинома, лімфома, бластома, та лейкемія. Більш типові приклади раку включають, не обмежуючись наведеними, такі як: хронічний лімфоцитарний лейкоз (CLL) легенів, включаючи недрібноклітинний лімфоцитарний лейкоз (NSCLC), рак молочної залози, яєчнику, шийки матки, ендометрію, передміхурової залози, коло ректальної області, шлунковокишкова карциноїдна пухлина, сечового міхура, шлунку, підшлункової залози, печінки (печінково-клітинний рак), гепатобластома, стравоходу, легенева аденокарцинома, мезотеліома, синовіальна саркома, остеосаркома, плоскоклітинна карцинома голови та шиї, ювенільні носоглоткові ангіофіброми, ліпосаркома, щитовидної залози, меланома, базальноклітинна карцинома (BCC), медулобластома та десмоїдна пухлина. “Виліковування” або “лікування” або “полегшення симптомів” відноситься як до терапевтичного лікування, так і до профілактичних або запобіжних заходів, де ціль полягає у запобіганні або уповільненні (зменшенні) цільової патологічної хвороби або стану або розладу. Ті, що потребують такого лікування, включають тих, що вже мають розлад, а також тих, які схильні мати розлад, або тих, у яких намагаються запобігти появі цього розладу (профілактика). Коли IGF-1R-опосередкований розлад являє собою рак, суб’єкт або ссавець успішно “лікується” або показує зменшене пухлинне навантаження, якщо, після отримання терапевтичної кількості IGF-1R антагоністу відповідно до способів даного винаходу, пацієнт показує помітне та/або вимірне зниження у або відсутність однієї або більшої кількості наступних ознак: зменшення кількості ракових клітин або відсутність ракових клітин; зменшення розміру пухлини; інгібування (тобто уповільнення до деякого ступеня та переважно зупинення) інфільтрації ракових клітин у периферичні органи, включаючи розповсюдження раку у м’які тканини та кістки; інгібування (тобто уповільнення до деякого ступеня та переважно зупинення) метастаз пухлин; інгібування (тобто уповільнення до деякого ступеня) росту пухлини; та/або полегшення до деякого ступеня, одного або більшої кількості симптомів, пов’язаних із специфічним раком; знижена захворюваність та смертність, та покращення якості життя. Наскільки можливо IGF-1R антагоніст може запобігати росту та/або знищувати існуючі ракові клітини, він може бути цитостатичним та/або цитотоксичним. Зменшення цих ознак або симптомів також може відчувати пацієнт. “Носії”, як використано у цьому описі, включають фармацевтично прийнятні носії, наповнювачі, або стабілізатори, які є нетоксичними для клітин або ссавця, які піддаються його дії, у використовуваних дозах та концентраціях. Часто фізіологічно прийнятний носій являє собою водний pH забуферений розчин. Приклади фізіологічно прийнятних носіїв включають буфери, такі як фосфат, цитрат та інші органічні кислоти; антиоксиданти, включаючи аскорбінову кислоту; поліпептиди з низькою молекулярною масою (менше, ніж приблизно 10 залишків); білки, такі як сироватковий альбумін, желатин, або імуноглобуліни; гідрофільні полімери, такі як полівінілпіролідон; амінокислоти, такі як гліцин, глутамін, аспарагін, аргінін або лізин; моносахариди, дисахариди, та інші карбогідрати, включаючи глюкозу, манозу або декстрини; хелатуючі агенти, такі як ЕДТА; цукрові спирти, такі як маніт або сорбіт; солеутворюючі протиіони, такі як натрій; та/або неіонні поверхнево-активні речовини, такі як TWEEN®, поліетиленгліколь (PEG), та PLURONICS®. “Хіміотерапевтичний агент” являє собою хімічну сполуку, яка є корисною у лікуванні раку. Приклади хіміотерапевтичних агентів включають такі як: алкілуючі агенти, такі як тіотепа та CYTOXAN® циклофосфамід; алкіл-сульфонати, такі як бусульфан, імпросульфан та піпосульфан; азиридини, такі як бензодопа, карбоквон, метуредопа, та уредопа; етиленіміни та метиламельаміни, включаючи альтретамін, триетиленемельамін, триетиленфосфорамід, триетиїлентіофосфорамід та триметилоломеламін; ацетогеніни (особливо буллатацин та буллатацинон); дельта-9-тетрагідроканнабінол (дронабінол, MARINOL®); бета-лапахон; 6 UA 101057 C2 5 10 15 20 25 30 35 40 45 50 55 60 лапахол; колхіцини; бетулінова кислота; камптотецин (включаючи синтетичний аналог топотекан (HYCAMTIN®), CPT-11 (іринотекан, CAMPTOSAR®), ацетилкамптотецин, скополектин, та 9-амінокамптотецин); бріостатин; каллістатин; CC-1065 (включаючи його синтетичні аналоги - адозелесин, карзелесин та бізелесин); подофілотоксин; подофілінова кислота; теніпозид; криптофіцини (особливо криптофіцин 1 та криптофіцин 8); доластатин; дуокарміцин (включаючи синтетичні аналоги, KW-2189 та CB1-TM1); елеутеробін; панкратистатин; саркодиктиїн; спонгістатин; азотистий іприт, такий як хлорамбуцил, хлорнафазин, холофосфамід, естрамустин, іфосфамід, мехлоретамін, мехлоретаміну оксид гідрохлорид, мелфалан, новембіхін, фенестерин, преднімустин, трофосфамід, урамустин; нітрозсечовини, такі як кармустин, хлорзотоцин, фотемустин, ломустин, німустин, та ранімнустин; антибіотики, такі як енедіінові антибіотики (наприклад, каліхеаміцин, особливо каліхеаміцин гама та каліхеаміцин омегаI1 (дивись, наприклад, Agnew, Chem Intl. Ed. Engl., 33: 183-186 (1994)); динеміцин, включаючи динеміцин A; еспераміцин; а також неокарзиностатин хромофор та зв’язані хромопротеїн енедіінові антибіотичні хромофори), аклациномізини, актиноміцин, аутраміцин, азасерін, блеоміцини, кактиноміцин, карабіцин, каміноміцин, карзинофілін, хромоміцини, дактиноміцин, даунорубіцин, деторубіцин, 6-діазо-5-оксо-Lнорлейцин, АДРІАМІЦИН® доксорубіцин (включаючи морфоліно-доксорубіцин, ціаноморфолінодоксорубіцин, 2-піроліно-доксорубіцин та деоксидоксорубіцин), епірубіцин, езорубіцин, ідарубіцин, марцелломіцин, мітоміцини, такі як мітоміцин C, мікофенольна кислота, ногаламіцин, олівоміцини, пепломіцин, потфіроміцин, пуроміцин, квеламіцин, родорубіцин, стрептонігрін, стрептозоцин, туберцидин, убенімекс, зиностатин, зорубіцин; анти-метаболіти, такі як метотрексат та 5-фторурацил (5-FU); аналоги фолієвої кислоти, такі як деноптерин, метотрексат, птероптерин, триметрексат; аналоги пурину, такі як флударабін, 6-меркаптопурин, тіаміприн, тіогуанін; аналоги піримідину, такі як анцитабін, азацитидин, 6-азауридин, кармофур, цитарабін, дидеоксиуридин, доксифлуридин, еноцитабін, флоксуридин; андрогени, такі як калустерон, дромостанолон пропіонат, епітіостанол, мепітіостан, тестолактон; анти-адренали, такі як аміноглутетимід, мітотан, трилостан; поповнювач фолієвої кислоти, такий як фролінова кислота; ацеглатон; альдофосфамід глікозид; амінолевулінова кислота; енілурацил; амсакрин; бестрабуцил; бізантрен; едатраксат; дефофамін; демеколцин; діазиквон; елфомітин; елліптиніум ацетат; епотилон; етоглюцид; нітрат галію; гідроксисечовина; лентінан; лонідаінін; мейтанзиноїди, такі як мейтанзин та ансамітоцини; мітогуазон; мітоксантрон; мопіданмол; нітраерин; пентостатин; фенамет; пірарубіцин; лозоксантрон; 2-етилгідразид; прокарбазин; PSK® полісахаридний комплекс (JHS Natural Products, Eugene, Oreg.); разоксан; різоксин; сизофуран; спірогерманій; тенуазонова кислота; триазиквон; 2,2′,2″-трихлортриетиламін; трихотецени (особливо T-2 токсин, верракурин A, роридин A та ангуідин); уретан; віндезин (ELDISINE®, FILDESIN®); дакарбазин; манномустин; мітобронітол; мітолактол; піпоброман; гацитозин; арабінозид (“Ara-C”); тіотепа; таксоїди, наприклад, TAXOL® паклітаксел (Bristol-Myers Squibb Oncology, Princeton, N.J.), ABRAXANE™ вільний від кремофору, альбумін-спроектована наночасткова композиція паклітакселу (American Pharmaceutical Partners, Schaumberg, Ill.), та TAXOTERE® доксетаксел (Rhône-Poulenc Rorer, Antony, France); хлоранбуцил; гемцитабін (GEMZAR®); 6-тіогуанін; меркаптопурин; метотрексат; аналоги платини, такі як цисплатин та карбоплатин; вінбластин (VELBAN®); платина; етопозид (VP-16); іфосфамід; мітоксантрон; вінкристин (ONCOVIN®); оксаліплатин; лейкововін; вінорелбін (NAVELBINE®); новантрон; едатрексат; дауноміцин; аміноптерин; ібандронат; інгібітор топоізомерази RFS 2000; дифторметилорнітин (DMFO); ретиноїди, такі як ретиноєва кислота; капецитабін (XELODA®); фармацевтично прийнятні солі, кислоти або похідні будь-якого з описаних вище; а також комбінації двох або більшої кількості описаних вище, такі як CHOP, абревіатура для комбінованої терапії циклофосфаміду, доксорубіцину, вінкристину, та преднізолону, та FOLFOX, абревіатура для лікувального режиму з оксаліплатином (ELOXATIN™), об’єднаним з 5-FU та лейкововіном. Більш того, “хіміотерапевтичний агент” може включати проти-гормональні агенти, які діють для регулювання, зменшення, блокування, або інгібування ефектів гормонів, які можуть промотувати ріст раку, та часто знаходиться у формі системного, або загального лікування. Вони самі можуть бути гормонами. Приклади включають анти-естрогени та селективні модулятори естрогенових рецепторів (SERMs), включаючи, наприклад, тамоксифен (включаючи NOLVADEX® тамоксифен), EVISTA® ралоксифен, дролоксифен, 4-гідрокситамоксифен, тріоксифен, кеоксифен, LY117018, онапрістон, та FARESTON® тореміфен; анти-прогестерони; даун-регулятори естрогенових рецепторів (ERDs); агенти, які функціонують для пригнічення або зупинення роботи яєчників, наприклад, агоністи лейтинізуючого гормон-вивільнюючого гормону (LHRH), такі як LUPRON® та ELIGARD® лейпролід ацетат, госерелін ацетат, бусерелін ацетат 7 UA 101057 C2 5 10 15 20 та триптерелін; інші анти-андрогени, такі як флутамід, нілутамід та бікалутамід; та інгібітори ароматази, які інгібують фермент ароматазу, яка регулює вироблення естрогену у надниркових залозах, такі як, наприклад, 4(5)-імідазоли, аміноглутетимід, MEGASE® мегестрол ацетат, AROMASIN® екземестан, форместан, фадрозол, RIVISOR® ворозол, FEMARA® летрозол, та ARIMIDEX® анастрозол. Крім того, таке визначення хіміотерапевтичних агентів включає бісфосфонати, такі як клодронат (наприклад, BONEFOS® або OSTAC®), DIDROCAL® етидронат, NE-58095, ZOMETA® золедронова кислота/золедронат, FOSAMAX® алендронат, AREDIA® памідронат, SKELID® тилудронат, або ACTONEL® різедронат; а також троксацитабін (1,3-діоксолан нуклеозид цитозиновий аналог); антисмислові олігонуклеотиди, особливо ті, які інгібують експресію генів сигнальних шляхах, залучених у проліферацію адгезивних клітин, такі як, наприклад, PKC-альфа, Raf, H-Ras, та рецептор епідермального фактору росту (EGF-R); вакцини, такі як THERATOPE® вакцина та вакцини генної терапії, наприклад, ALLOVECTIN® вакцина, LEUVECTIN® вакцина, та VAXID® вакцина; LURTOTECAN® інгібітор топоізомерази 1; ABARELIX® rmRH; лапатиніб дитозилат (ErbB-2 та EGFR подвійний тирозин-кіназний дрібноклітинний інгібітор, також відомий як GW572016); та фармацевтично прийнятні солі, кислоти або похідні будь-якого з описаних вище. Способи здійснення винаходу Даний винахід забезпечує нові похідні піримідину та їх фармацевтичні композиції, та способи застосування таких сполук. У одному аспекті, даний винахід забезпечує сполуку Формули (1): R1 Z1 N 25 30 35 N Z3 E R2 N Z2 0-1 N 0-1 (1) (R 5)m R3 R4 або її фізіологічно прийнятну сіль; у якій кільце E може необов’язково містити подвійний зв’язок; 1 2 3 6 6 + один з Z , Z та Z являє собою NR , N(R ) -O або S(O)1-2 та інші являють собою CR2; 1 R являє собою гало групу або необов’язково галогенований C1-6 алкіл; 2 R являє собою піридин-2-оніл, азепан-2-оніл або моноциклічний 5-6-членний гетероарил, що має 1-3 гетероатоми, що вибирають з N, O та S; кожен з яких необов’язково заміщений за 9 9 допомогою R , де R являє собою C1-6 алкіл, C1-6 галоалкіл або C3-7 циклоалкіл; 3 4 R та R кожен являє собою H; 5 R являє собою гало групу, гідроксил, C1-6 алкіл, C1-6 алкокси групу, гало-заміщений C1-6 8 алкіл, гало-заміщену C1-6 алкокси групу, ціано групу або C(O)O0-1R ; 6 R являє собою H; C1-6 алкіл, C2-6 алкеніл або C2-6 алкініл, кожен з яких може бути 7 необов’язково заміщений за допомогою гало та/або гідроксильних груп; -(CR2)p-OR , -(CR2)p7 7 CH(OH)CtF2t+1, де t являє собою 1-3, (CR2)p-CN; (CR2)p-NR(R ), -(CR2)p–C(O)OR , 7 8 8 7 7 (CR2)pNR(CR2)pOR , (CR2)pNR-L-C(O)R , C(O)(CR2)qOR , -C(O)O-(CR2)p-NRR , –C(O) -(CR2)p-OR , 7 7 7 7 L-Y, -L-C(O)R , -L–C(O)-NRR , -L–C(O)-NR-(CR2)p-NRR ,-L-C(O)NR(CR2)pOR , -L–C(O)-(CR2)q-NR8 7 8 8 7 C(O)-R , -L-C(O)NR(CR2)pSR , -L-C(O)NR(CR2)pS(O)1-2R , -L-S(O)2R , -L-S(O)2-(CR2)q-NRR , -L7 S(O)2NR(CR2)pNR(R ) або 7 -L-S(O)2NR(CR2)pOR ; 6 альтернативно, R являє собою радикал, вибраний з формули (a), (b), (c) або (d): 40 15 R11 R12 R N R16 L 1-2 R10 15 R11 R12 R N R16 L 1-2 SO2 0-1 R13 R14 1-2 (a) 10 45 O (c) (b) 17 17 0-1 S 1-2 O 8a O R13 R14 (d) 8a R являє собою O, S, NR , де R являє собою H, C1-6 алкіл, SO2R або CO2R ; 11 12 13 14 15 16 R , R , R , R , R та R незалежно вибирають з таких як: H; C1-6 алкокси група; C1-6 алкіл, C2-6 алкеніл або C2-6 алкініл, кожен з яких може бути необов’язково заміщений за допомогою 11 12 12 15 15 16 13 14 13 15 гало, аміно або гідроксильних груп; або R та R , R та R , R та R , R та R , або R та R разом з атомами, до яких вони приєднані, можуть утворювати 3-7-членне насичене, ненасичене або частково ненасичене кільце, що містить 1-3 гетероатоми, вибрані з N, O та S, та 8 UA 101057 C2 5 5 10 15 необов’язково заміщене за допомогою оксо та 1-3 R груп; L являє собою (CR2)1-4 або зв’язок; Y являє собою C3-7 карбоциклічне кільце, C6-10 арил, або 5-10 членне гетероарильне або 45 10 членне гетероциклічне кільце, кожне з яких необов’язково заміщене за допомогою 1-3 R груп; 7 8 8a R , R та R незалежно являють собою C1-6 алкіл, C2-6 алкеніл або C2-6 алкініл, кожен з яких може бути необов’язково заміщений за допомогою гало групи, аміно групи, гідроксилу або ціано 7 групи; (CR2)qY або C1-6 алкокси групу; або R являє собою H; кожен R незалежно являє собою H або C1-6 алкіл; 7 7 R та R разом з N у кожній NRR можуть утворювати 5-6 членне кільце, що містить 1-3 5 гетероатоми, вибрані з N, O та S, та необов’язково заміщене за допомогою оксо та 1-3 R груп; m являє собою 2-4; n являє собою 1-3; p являє собою 1-4; та q являє собою 0-4. У одному варіанті втілення, даний винахід забезпечує сполуку Формули (2): Z2 Z1 R5c Z3 E 0-1 1 R N R N N 20 R5b N R4 R3 5a 5b R5a 5c у якій один з R , R та R являє собою H та інші являють собою незалежно гало групу, C 1-6 8 8 алкіл, C1-6 алкокси групу, гало-заміщений C1-6 алкіл, ціано групу або C(O)O0-1R , де R являє собою C1-6 алкіл; та 1 2 3 4 1 2 3 R , R , R , R , E, Z , Z та Z приймають значення, визначені у Формулі (1). У іншому варіанті втілення, даний винахід забезпечує сполуку Формули (3): R5c R HN N N Z2 Z3 E N N (3) R5b N R5a R4 R 30 Z1 1 3 25 (2) 0-1 2 або її таутомер; 5b 5a 5c у якій R являє собою H; та R та R незалежно являють собою гало групу, C 1-6 алкіл, C1-6 8 8 алкокси групу, гало-заміщений C1-6 алкіл, ціано групу або C(O)O0-1R , де R являє собою C1-6 алкіл; 1 2 2 Z та Z являють собою CH ; 3 6 6 + Z являє собою NR або N(R ) -O ; 6 R являє собою H, C1-6 алкіл, необов’язково заміщений за допомогою гало та/або гідроксильних груп; 7 7 -(CR2)p-OR , -(CR2)p-CH(OH)CtF2t+1, де t являє собою 1-3, (CR2)p-CN; (CR2)p-NR(R ), 7 8 7 7 -(CR2)p–C(O)OR , C(O)(CR2)qOR , -C(O)O-(CR2)p-NRR , L-Y, -L-C(O)R , 7 7 8 8 -L-C(O)-NRR , -L–C(O)-NR-(CR2)p-NRR , -L–C(O)-(CR2)q-NR-C(O)-R , -L-S(O)2R , 7 -L-S(O)2-(CR2)q-NRR , або радикал, вибраний з формули (a), (b), (c) або (d): 15 R11 R12 R N R16 L 1-2 R10 15 R11 R12 R N R16 L 1-2 SO2 0-1 1-2 35 (a) O R13 R14 (c) (b) 9 0-1 S 1-2 O O R13 R14 (d) UA 101057 C2 10 5 10 15 20 17 17 8a 8a R являє собою O, S, NR , де R являє собою H, C1-6 алкіл, SO2R або CO2R ; 8a R являє собою C1-6 алкіл; та 1 3 4 7 8 10 11 12 13 14 15 16 R , R , R , R , R , R , R , R , R , R , R , R , R, L, Y, p, q та E приймають значення, визначені у Формулі (1). У іншому аспекті, даний винахід забезпечує сполуку Формули (4): R1 HN N N X (4) N N N (R 5 )m 3 4 R R або її фізіологічно прийнятну сіль; у якій X являє собою моноциклічне 5-6 членне гетероциклічне кільце, що містить 1-3 гетероатоми, вибрані з N, O та S, та необов’язково заміщене на кільцевому атомі вуглецю, що може бути заміщений, за допомогою оксо групи та на будь-якому кільцевому атомі азоту, що 6 може бути заміщений, за допомогою R ; 1 R являє собою гало групу; 3 4 R та R кожен являє собою H; 5 R являє собою гало групу, гідроксил, C1-6 алкіл, C1-6 алкокси групу, гало-заміщений C1-6 8 алкіл, гало-заміщену C1-6 алкокси групу, ціано групу або C(O)O0-1R ; 6 R являє собою H; C1-6 алкіл, C2-6 алкеніл або C2-6 алкініл, кожен з яких може бути 7 необов’язково заміщений за допомогою гало та/або гідроксильних груп; -(CR2)p-OR , -(CR2)p7 7 CH(OH)CtF2t+1, де t являє собою 1-3, (CR2)p-CN; (CR2)p-NR(R ), -(CR2)p–C(O)OR , 7 (CR2)pNR(CR2)pOR , 8 8 7 7 (CR2)pNR-L-C(O)R , C(O)(CR2)qOR , -C(O)O-(CR2)p-NRR , –C(O) -(CR2)p-OR , L-Y, 7 7 7 7 -L-C(O)R , -L–C(O)-NRR , -L–C(O)-NR-(CR2)p-NRR ,-L-C(O)NR(CR2)pOR , 8 7 8 -L–C(O)-(CR2)q-NR-C(O)-R , -L-C(O)NR(CR2)pSR , -L-C(O)NR(CR2)pS(O)1-2R , 8 7 7 -L-S(O)2R , -L-S(O)2-(CR2)q-NRR , -L-S(O)2NR(CR2)pNR(R ) або 7 -L-S(O)2NR(CR2)pOR ; 6 альтернативно, R являє собою радикал, вибраний з формули (a), (b), (c) або (d): 25 15 R11 R12 R N R16 L 1-2 R10 15 R11 R12 R N R16 L 1-2 SO2 0-1 R13 R14 1-2 (a) 10 30 35 40 45 O (c) (b) 17 17 0-1 S 1-2 O 8a O R13 R14 (d) 8a R являє собою O, S, NR , де R являє собою H, C1-6 алкіл, SO2R або CO2R ; 11 12 13 14 15 16 R , R , R , R , R та R незалежно вибирають з таких як: H; C1-6 алкокси група; C1-6 алкіл, C2-6 алкеніл або C2-6 алкініл, кожен з яких може бути необов’язково заміщений за допомогою 11 12 12 15 15 16 13 14 13 15 гало, аміно або гідроксильних груп; або R та R , R та R , R та R , R та R , або R та R разом з атомами, до яких вони приєднані, можуть утворювати 3-7-членне насичене, ненасичене або частково ненасичене кільце, що містить 1-3 гетероатоми, вибрані з N, O та S, та 5 необов’язково заміщене за допомогою оксо та 1-3 R груп; L являє собою (CR2)1-4 або зв’язок; Y являє собою C3-7 карбоциклічне кільце, C6-10 арил, або 5-10 членне гетероарильне або 45 10 членне гетероциклічне кільце, кожне з яких необов’язково заміщене за допомогою 1-3 R груп; 7 8 8a R , R та R незалежно являють собою C1-6 алкіл, C2-6 алкеніл або C2-6 алкініл, кожен з яких може бути необов’язково заміщений за допомогою гало групи, аміно групи, гідроксилу або ціано 7 групи; (CR2)qY або C1-6 алкокси групу; або R являє собою H; кожен R незалежно являє собою H або C1-6 алкіл; 7 7 R та R разом з N у кожній NRR можуть утворювати 5-6 членне кільце, що містить 1-3 5 гетероатоми, вибрані з N, O та S, та необов’язково заміщене за допомогою оксо та 1-3 R груп; m являє собою 2-4; n являє собою 1-3; p являє собою 1-4; та q являє собою 0-4. 10 UA 101057 C2 У ще одному іншому аспекті, даний винахід забезпечує сполуки Формули (5): R1 N X R2 N N (5) N (R5 )m R3 R4 або їх фізіологічно прийнятні солі; ON+ R6 , O або S, та 6 5 10 15 20 у якій X являє собою 4-7 членне гетероциклічне кільце, що містить NR , 5 необов’язково заміщене за допомогою 1-3 R груп; 1 у якій R являє собою гало групу, C1-6 алкіл, або гало-заміщений C1-6 алкіл; 2 R являє собою необов’язково заміщене 5-6 членне гетероарильне або 5-7 членне гетероциклічне кільце, кожне з яких має 1-3 гетероатоми, що вибирають з N, O та S, та 9 необов’язково заміщене за допомогою 1-3 R груп; 3 4 8 R та R незалежно являють собою H, C(O)R , C1-6 алкіл або гало-заміщений C1-6 алкіл; 5 9 R та R незалежно являють собою C1-6 алкіл, C2-6 алкеніл або C2-6 алкініл, кожен з яких може 5 9 бути необов’язково заміщений за допомогою гало, аміно або гідроксильних груп; або R та R незалежно являють собою C1-6 алкокси групу, гало-заміщену C1-6 алкокси групу, гало групу, нітро 7 7 7 7 7 7 7 7 групу, ціано групу, CR(OR )R , OR , O(CR2)p-OR , NR(R ), CR(R )NRR , (CR2)1-6NR(CR2)pOR , 8 8 7 7 7 (CR2)1-6NR(CR2)qC(O)R , –C(O)-(CR2)q-NR-C(O)-R , (CR2)qY, C(O)O0-1R , C(O)NR(R ), C(O)CRR 7 7 7 7 8 NR(R ), C(O)NR(CR2)pNR(R ), C(O)NR(CR2)pOR , C(O)NR(CR2)pSR , C(O)NR(CR2)pS(O)1-2R , 8 7 7 7 S(O)0-2R , S(O)2NRR , S(O)2NR(CR2)pNR(R ), або S(O)2NR(CR2)pOR ; 6 R являє собою H; C1-6 алкіл, C2-6 алкеніл або C2-6 алкініл, кожен з яких може бути необов’язково заміщений за допомогою гало групи, аміно групи, гідроксилу або алкокси групи; 7 7 7 7 7 7 (CR2)p-CN; C(O)H, CR(OR )R , (CR2)p-OR , (CR2)p-NR(R ), CR(R )NRR , -L-Y, -L–C(O)O0-1-(CR2)q8 7 7 7 7 7 R , -(CR2)p–C(O)O0-1-R , -L–C(O)-NRR, -L–C(O)O0-1-CR(R )-NRR , -L–C(O)-NR-(CR2)p-NRR , -L7 8 7 8 C(O)NR(CR2)pOR , -L–C(O)-(CR2)q-NR-C(O)-R , -L-C(O)NR(CR2)pSR , -L-C(O)NR(CR2)pS(O)1-2R , 8 7 8 7 7 L-S(O)2R , (CR2)pNR(CR2)pOR , (CR2)pNR-L-C(O)R , -L-S(O)2NRR , -L-S(O)2NR(CR2)pNR(R ) або 7 L-S(O)2NR(CR2)pOR ; 6 альтернативно, R являє собою радикал, вибраний з формули (a), (b), (c) або (d): 25 15 R11 R12 R N R16 L 1-2 O R13 30 35 40 45 R14 1-2 (a) 11 12 R17 SO2 0-1 1-2 (c) (b) 13 14 15 15 R11 R12 R N R16 L 1-2 16 0-1 S O R13 R14 O (d) у якій R , R , R , R , R та R незалежно вибирають з таких як: H або C1-6 алкіл, C1-6 алкокси група, C2-6 алкеніл або C2-6 алкініл, кожен з яких може бути необов’язково заміщений за 11 12 12 15 15 16 13 14 допомогою гало, аміно або гідроксильних груп; або R та R , R та R , R та R , R та R , 13 15 або R та R разом з атомами вуглецю та/або азоту, до яких вони прикріплені, можуть утворювати 3-7-членне насичене, ненасичене або частково ненасичене кільце, що необов’язково містить до 3 атомів або груп, що вибирають з C(O), N, O та S(O) 0-2; 17 8 R являє собою O або SO2R ; L являє собою (CR2)1-4 або зв’язок; Y являє собою C3-7 карбоциклічне кільце, C6-10 арил, або 5-10 членне гетероарильне або 45 10 членне гетероциклічне кільце, кожне з яких необов’язково заміщене за допомогою 1-3 R груп; 7 8 R та R незалежно являють собою C1-6 алкіл, C2-6 алкеніл або C2-6 алкініл, кожен з яких може бути необов’язково заміщений за допомогою гало групи, аміно групи, гідроксилу або ціано 7 групи; (CR2)qY або C1-6 алкокси групу; або R являє собою H; кожен R являє собою H або C1-6 алкіл; m являє собою 2-4; n являє собою 1-3; p являє собою 1-4; та q являє собою 0-4. У представленій вище Формулі (5), приклади 5-6 членних гетероарильних або 5-7 членних 2 гетероциклічних кільцевих R груп включають, не обмежуючись наведеними, піразоліл, піроліл, 11 UA 101057 C2 5 10 15 20 25 30 35 40 45 50 55 60 тіофеніл, піримідиніл, ізоксазоліл, піридил, азепан-2-оніл, 2H-тіопіран, 3H-тіопіран, 4H-тіопіран, тетрагідротіопіран, 2H-піран, 4H-піран, тетрагідропіран, піперидин, 1,2-дитіін, 1,2-дитіан, 1,3дитіін, 1, 3-дитіан, 1,4-дитіін, 1,4-дитіан, 1,2-діоксин, 1,2-діоксан, 1,3-діоксин, 1,3-діоксан, 1,4діоксин, 1,4-діоксан, піперазин, 1,2-оксатіін, 1,2-оксатіан, 4H-1,3-оксатіін, 1,3-оксатіан, 1,4оксатіін, 1,4-оксатіан, 2H-1,2-тіазин, тетрагідро-1,2-тіазин, 2H-1,3-тіазин, 4H-1,3-тіазин, 5,6дигідро-4H-тіазин, 4H-1,4-тіазин, тетрагідро-1,4-тіазин, 2H-1,2-оксазин, 4H-1,2-оксазин, 6H-1,2оксазин, 2H-1,3-оксазин, 4H-1,3-оксазин, 4H-1, 4-оксазин, морфолін, тріоксан, 4H-1,2,3-тритіін, 1,2,3-тритіан, 1,3,5-тритіан, гексагідро-1,3,5-триазин, тетрагідротіофен, тетрагідрофуран, піролін, піролідин, піролідон, піролідіон, піразолін, піразолідин, імідазолін, імідазолідин, 1,2діоксол, 1,2-діоксолан, 1,3-діоксол, 1, 3-діоксолан, 3H-1,2- дитіол, 1, 2-дитіолан, 1,3-дитіол, 1,3дитіолан, ізоксазолін, ізоксазолідин, оксазолін, оксазолідин, тіазолін, тіазолідин, 3H-1,2-оксатіол, 1,2-оксатіолан, 5H-1,2-оксатіол, 1,3-оксатіол, 1,3-оксатіолан, 1,2,3-тритіол, 1,2,3-тритіолан, 1,2,4тритіолан, 1,2,3-триоксол, 1,2,3-триоксолан, 1,2,4-триоксолан, 1,2,3-триазолін та 1,2,3триазолідин. У кожній з описаних вище формул, будь-які асиметричні атоми вуглецю можуть бути присутніми у (R)-, (S)- або (R,S)-конфігурації. Таким чином, сполуки можуть бути присутніми у вигляді сумішей ізомерів або у вигляді чистих ізомерів, наприклад, як чисті енантіомери або діастереомери. Даний винахід додатково включає можливі таутомери сполук за винаходом. Будь-яка формула, показана у цьому описі, також призначена для представлення немічених форм, а також ізотопно мічених форм цих сполук. Ізотопно мічені сполуки мають структури, показані формулами, даними у цьому описі, за винятком того, що один або більша кількість атомів замінена атомом, що має вибрану атомну масу або масове число. Приклади ізотопів, які можуть бути включені у сполуки даного винаходу, включають ізотопи водню, вуглецю, азоту, 2 3 11 13 14 15 18 31 32 35 36 125 кисню, фосфору, фтору, та хлору, такі як H, H, C, C, C, N, F P, P, S, Cl, I, відповідно. Даний винахід включає різні ізотопно мічені сполуки, визначені у даному описі, наприклад, 3 13 14 ті, у яких присутні радіоактивні ізотопи, такі як H, C, та C. Такі ізотопно мічені сполуки є 14 корисними у метаболічних дослідженнях (наприклад, з C), дослідженнях кінетики реакції 2 3 (наприклад, з H або H), способах детектування або отримання зображення, таких як позитронно-емісійна хроматографія (PET) або однофотонна емісійна комп’ютерна томографія (SPECT), включаючи дослідження розподілення у тканинах лікарського засобу або субстрату, 18 або у променевій терапії пацієнтів. У інших прикладах, F або мічена сполука може бути використана для PET або SPECT досліджень. Ізотопні варіанти сполук мають потенціал змінювати метаболічний шлях сполуки та/або створювати невеликі зміни у фізичних властивостях, таких як гідрофобність, та подібні. Ізотопні варіанти також мають потенціал підвищувати ефективність та безпеку, підвищувати біодоступність та період напіввиведення, змінювати зв’язування білків, змінювати біорозподілення, підвищувати частину активних метаболітів та/або зменшувати утворення реакційно-здатних або токсичних метаболітів. Ізотопно мічені сполуки даного винаходу та їх проліки в основному можуть бути одержані шляхом проведення процедур, розкритих у схемах або у прикладах та одержаннях, описаних нижче, шляхом заміщення легко доступного ізотопно міченого реагенту на не-ізотопно мічений реагент. У кожній з описаних вище формул, кожен необов’язково заміщений залишок може бути заміщений за допомогою C1-6 алкілу, C2-6 алкенілу або C3-6 алкінілу, кожен з яких може бути необов’язково галогенований або що необов’язково має вуглець, який може бути замінений або заміщений за допомогою таких як: N, S, O, або їх комбінації (наприклад, гідроксилC1-C8алкіл, C1C8алкоксиC1-C8алкіл); гало група, аміно група, амідино група, C 1-6 алкокси група; гідроксил, метилендіокси група, карбокси група; C1-8 алкілкарбоніл, C1-8 алкоксикарбоніл, карбамоїл, C1-8 алкілкарбамоїл, сульфамоїл, ціано група, оксо група, нітро група, або необов’язково заміщене карбоциклічне кільце, гетероциклічне кільце, арил або гетероарил, як описано вище. Фармакологія та застосування Сполуки даного винаходу та їх фармацевтично прийнятні солі показують цінні фармакологічні властивості при дослідженні in vitro у вільних від клітин кіназних дослідженнях та у клітинних дослідженнях, та, тому, є корисними як фармацевтичні засоби. У одному аспекті, сполуки даного винаходу також можуть інгібувати рецептор інсуліноподібного фактору росту 1 (IGF-1R), та можуть бути корисними у лікуванні IGF-1R опосередкованих хвороб. Приклади IGF-1R опосередкованих хвороб включають, не обмежуючись наведеними, проліферативні хвороби, такі як пухлини, наприклад, молочної залози, нирки, передміхурової залози, колоректальної області, щитовидної залози, яєчнику, підшлункової залози, нервових клітин, легені, матки та шлунково-кишкового тракту, а також 12 UA 101057 C2 5 10 15 20 25 30 35 40 45 50 55 60 остеосаркоми та меланоми. Ефективність сполук даного винаходу як інгібіторів активності IGF1R тирозин-кінази може бути показана, використовуючи спосіб клітинного захоплення ELISA. У цьому дослідженні визначають активність сполук даного винаходу проти (IGF-1)-викликаного аутофосфорилювання IGF-1R. У іншому аспекті, сполуки даного винаходу можуть інгібувати тирозин-кіназну активність кінази анапластичої лімфоми (ALK) та білку злиття NPM-ALK. Ця протеїн-тирозин-кіназа походить з генного злиття нуклеофозміну (NPM) та ALK, роблячи протеїн-тирозин-кіназну активність незалежною від ALK ліганду. NPM-ALK відіграє ключову роль у передачі сигналу у цілому ряді гематопоетичних та інших клітин людини, що веде до гематологічних та непластичних хвороб, наприклад, у анапластичній великоклітинній лімфомі (ALCL) та неходжкінівських лімфомах (NHL), особливо при ALK+NHL або Alkomas, у запальних міофібробластичних пухлинах (IMT) та нейробластомах. (Duyster et al. 2001 Oncogene 20, 56235637). Окрім NPM-ALK, інші генні злиття були знайдені у гематологічних та непластичних хворобах людини; наприклад, TPM3-ALK (злиття нем’язового тропоміозину з ALK). Інгібування ALK тирозин-кіназної активності може бути продемонстровано, використовуючи відомі способи, наприклад, використовуючи рекомбінантний кіназний домен ALK по аналогії до VEGF-R кіназного дослідження, описаного у J. Wood et al. Cancer Res. 60, 2178-2189 (2000). Загалом, in vitro ферментативні дослідження, використовуючи GST-ALK протеїн-тирозин-кіназу, проводять у 96-лункових планшетах як спосіб зв’язування на фільтрах у 20 мM Tris HCl, pH = 33 7,5, 3 мM MgCl2, 10 мM MnCl2, 1 мM DTT, 0,1 мкКi/дослідж. (=30 мкл) [- P]-ATP, 2 мкM ATP, 3 мкг/мл полі (Glu, Tyr 4:1) Poly-EY (Sigma P-0275), 1 % ДМСО, 25 нг ALK ферменту. Дослідні планшети інкубують впродовж 10 хвилин при кімнатній температурі. Реакції закінчують додаванням 50 мкл 125 мM EDTA, та реакційну суміш переносять на MAIP Multiscreen планшет (Millipore, Bedford, MA, USA), попередньо зволожений метанолом, та регідрований впродовж 5 хвилин за допомогою H2O. Після промивання (0,5 % H3PO4), планшети зчитують у рідинному сцинтиляційному лічильнику. IC50 значення розраховують за допомогою аналізу лінійної регресії відсотку інгібування. Сполуки даного винаходу можуть сильно інгібувати ріст людських NPM-ALK надекспресуючих мишиних BaF3 клітин (DSMZ Deutsche Sammiung von Mikroorganismen und Zelikulturen GmbH, Germany). Експресія NPM-ALK може бути досягнута трансфікуванням BaF3 TM клітинної лінії з вектором експресії pClneo (Promega Corp., Madison WI, USA), кодуючи NPMALK, та наступним вибором G418 стійких клітин. Не-трансфектовані BaF3 клітини залежать від IL-3 для виживання клітини. На противагу, NPM-ALK експресуючі BaF3 клітини (що нижче називають BaF3-NPM-ALK) можуть проліферувати за відсутності IL-3, так як вони одержують проліферативний сигнал через NPM-ALK кіназу. Тому, передбачувані інгібітори NPM-ALK кінази анулюють сигнал росту та можуть приводити до антипроліферативної активності. Антипроліферативна активність передбачуваних інгібіторів NPM-ALK кінази, однак, може перемогти додаванням IL-3, що забезпечує сигнали росту через NPM-ALK незалежний механізм. Аналогічна клітинна система, використовуючи FLT3 кіназу також була описана (дивись, E Weisberg et al. Cancer Cell; 1, 433-443 (2002)). Інгібіторна активність сполук даного винаходу може бути визначена наступним чином. Загалом, BaF3-NPM-ALK клітини (15,000/лунку мікротитрового планшету) переносять у 96лункові мікротитрові планшети. Тестові сполуки, розчинені у диметил-сульфоксиді (ДМСО), додають серіями концентрацій (серійне розведення) таким способом, що кінцева концентрація ДМСО є не більшою ніж 1 % (об’єм/об’єм). Після додавання, планшети інкубують впродовж двох днів, протягом яких контрольні культури без тестової сполуки можуть піддаватися двом циклам TM клітинного ділення. Ріст BaF3-NPM-ALK клітин вимірюють за допомогою YOPRO забарвлення [T Idziorek et al. J. Immunol. Methods; 185: 249-258 (1995)]: 25 мкл лізисного буферу, що включає 20 мM цитрат натрію, pH 4,0, 26,8 мM хлорид натрію, 0,4 % NP40, 20 мM EDTA та 20 мM, додають до кожної лунки. Клітинний лізис закінчують впродовж 60 хвилин при кімнатній TM температурі та загальну кількість YOPRO , прикріпленого до ДНК, визначають вимірюванням, використовуючи Cytofluor II 96-лунковий рідер (PerSeptive Biosystems) з наступними параметрами настроювання: збудження (нм) 485/20 та випромінювання (нм) 530/25. Сполуки даного винаходу також можуть бути корисними при лікуванні та/або профілактиці таких хвороб як: гостра або хронічна запальні хвороби або розлади або аутоімунні хвороби, наприклад, такі як ревматоїдний артрит, остеоартрит, системний червоний вовчак, хронічний лімфоматозний тиреоідит Хасімото, розсіяний склероз, міастенія, діабет (типу I та II) та розлади, пов’язані з ним, респіраторні хвороби, такі як астма, або запальне ураження печінки, запальне гломерулярне ураження, шкірні прояви імунологічно-зв’язаних хвороб або захворювань, запальні та гіперпроліферативні хвороби шкіри (такі як псоріаз, атопічний 13 UA 101057 C2 5 10 15 20 25 30 35 40 45 50 55 60 дерматит, алергічний контактний дерматит, подразнюючий контактний дерматит та подальший екзематозний дерматит, себорейний дерматит), запальні хвороби ока, наприклад, синдром Гужеро - Шегрена, кератоконьюнктивіт або увеіт, запальна хвороба кишок, хвороба Крона або виразковий коліт. Відповідно до описаного вище, даний винахід забезпечує: (1) сполуку даного винаходу для застосування як фармацевтичний засіб; (2) сполуку даного винаходу для застосування як IGF-1R інгібітор, наприклад, для застосування при будь-яких певних показаннях, розкритих у цьому описі вище; (3) фармацевтичну композицію, наприклад, для застосування при будь-яких певних показаннях, розкритих у цьому описі вище, що включає сполуку даного винаходу як активний інгредієнт разом з одним або декількома фармацевтично прийнятними розріджувачами або носіями; (4) спосіб для лікування будь-якого певного показання, розкритого у цьому описі вище, у суб’єкта, якому це необхідно, що включає введення ефективної кількості сполуки даного винаходу або фармацевтичної композиції, що включає її; (5) застосування сполуки даного винаходу для виробництва лікарського засобу для лікування або профілактики хвороби або стану, у яких IGF-1R активація грає роль або залучена; (6) спосіб, як визначено вище у (4), що включає спів-введення, наприклад, супутньо або послідовно, терапевтично ефективної кількості сполуки даного винаходу та однієї або декількох додаткових лікарських речовин, де зазначена додаткова лікарська речовина є корисною при будь-якому з певних показань, розкритих у цьому описі вище; (7) комбінацію, що включає терапевтично ефективну кількість сполуки даного винаходу та одну або декілька додаткових лікарських речовин, де зазначена додаткова лікарська речовина є корисною при будь-якому з певних показань, розкритих у цьому описі вище; (8) застосування сполуки даного винаходу для виробництва лікарського засобу для лікування або профілактики хвороби, яка чутлива до інгібування кінази анапластичної лімфоми; (9) застосування за (8), у якому хворобу, яку необхідно лікувати, вибирають з анапластичної великоклітинної лімфоми, неходжкінівських лімфом, запальних міофібробластичних пухлин, нейробластом та непластичних хвороб; (10) застосування за (8) або (9), у якому сполука являє собою будь-яку одну сполуку з прикладів, або її фармацевтично прийнятну сіль; (11) спосіб лікування хвороби, яка чутлива до інгібування кінази анапластичної лімфоми, особливо хвороби, що вибирають з анапластичної великоклітинної лімфоми, неходжкінівських лімфом, запальних міофібробластичних пухлин, нейробластом та непластичних хвороб, що включає введення ефективної кількості сполуки даного винаходу або її фармацевтично прийнятної солі. Введення та фармацевтичні композиції Загалом, сполуки даного винаходу будуть вводитися у терапевтично ефективних кількостях через будь-який із звичайних та прийнятних способів, відомих у даній галузі техніки, або окремо або у комбінації з одним або більшою кількістю терапевтичних агентів. Терапевтично ефективна кількість може змінюватися у широких межах в залежності від серйозності хвороби, віку та відносного стану здоров’я суб’єкта, ефективності використовуваної сполуки та інших факторів, відомих спеціалістам, звичайно кваліфікованим у даній галузі техніки. Наприклад, для лікування неопластичних хвороб та розладів імунної системи, необхідна доза буде також змінюватися в залежності від способу введення, певного стану, який необхідно лікувати, та бажаного ефекту. Загалом, показано, що задовільні результати отримують систематично при щоденних дозах від приблизно 0,01 до 100 мг/кг маси тіла, або особливо від приблизно 0,03 до 2,5 мг/кг маси тіла. Показана щоденна доза у великого ссавця, наприклад, людей, знаходиться у інтервалі від приблизно 0,5 мг до приблизно 2000 мг, або більш особливо, від приблизно 0,5 мг до приблизно 100 мг, при зручному введенні, наприклад, у розділених дозах до чотирьох разів на день або у формі уповільненого вивільнення. Прийнятні одиничні лікарські форми для перорального введення включають від приблизно 1 до 50 мг активного інгредієнту. Сполуки даного винаходу можуть бути введені як фармацевтичні композиції будь-яким зручним шляхом, зокрема ентерально, наприклад, перорально, наприклад, у формі таблеток або капсул, або парентерально, наприклад, у формі ін’єкційних розчинів або суспензій, місцево, наприклад, у формі лосьйонів, гелів, мазей або кремів, або у назальній формі або у формі супозиторію. Фармацевтичні композиції, що включають сполуку даного винаходу у вільній формі або у формі фармацевтично прийнятної солі у поєднанні з щонайменше одним фармацевтично прийнятним носієм або розріджувачем, можуть бути вироблені звичайним способом шляхом 14 UA 101057 C2 5 10 15 20 25 30 35 40 45 50 55 60 змішування, гранулювання, нанесення покриття, розчинення або ліофілізування. Наприклад, фармацевтичні композиції, що включають сполуку даного винаходу у поєднанні з щонайменше одним фармацевтично прийнятним носієм або розріджувачем, можуть бути вироблені звичайним способом шляхом змішування з фармацевтично прийнятним носієм або розріджувачем. Одиничні лікарські форми для перорального введення містять, наприклад, від приблизно 0,1 мг до приблизно 500 мг активної речовини. У одному варіанті втілення, фармацевтичні композиції являють собою розчини активного інгредієнту, включаючи суспензії або дисперсії, такі як ізотонічні водні розчини. У випадку ліофілізованих композицій, що включають активний інгредієнт окремо або разом з носієм, таким як маніт, дисперсії або суспензії можуть бути одержані безпосередньо перед застосуванням. Фармацевтичні композиції можуть бути стерилізовані та/або можуть містити допоміжні речовини, такі як консерванти, стабілізатори, зволожуючі або емульгуючі агенти, прискорювачі розчинення, солі для регулювання осмотичного тиску та/або буфери. Прийнятні консерванти включають, не обмежуючись наведеними, антиоксиданти, такі як аскорбінова кислота, або бактерицидні засоби, такі як сорбінова кислота або бензойна кислота. Розчини або суспензії можуть додатково включати підвищуючи в’язкість агенти, включаючи, не обмежуючись наведеними, карбоксиметилцелюлозу натрію, карбоксиметилцелюлозу, декстран, полівінілпіролідон, желатини, або солюбілізатори, наприклад, Твін 80 (поліоксиетилен(20)сорбіту моно-олеат). Суспензії у маслі можуть включати як масляний компонент рослинні, синтетичні або напівсинтетичні масла, звичайні для ін’єкційних цілей. Приклади включають рідкі складні ефіри жирних кислот, які містять як кислий компонент довго ланцюгову жирну кислоту, що має від 8 до 22 атомів вуглецю, або у деяких варіантах втілення, від 12 до 22 атомів вуглецю. Прийнятні рідкі складні ефіри жирних кислот включають, не обмежуючись наведеними, лауринову кислоту, тридецилову кислоту, міристилову кислоту, пентадецилову кислоту, пальмітинову кислоту, маргаринову кислоту, стеаринову кислоту, арахідонову кислоту, бегенову кислоту або відповідні ненасичені кислоти, наприклад, такі як олеїнова кислота, елаідинова кислота, ерукова кислота, брассидинова кислота та лінолева кислота, та при бажанні, можуть містити антиксиданти, наприклад, вітамін E, 3-каротин або 3,5-ди-трет-бутил-гідрокситолуол. Спиртовий компонент цих складних ефірів жирних кислот може мати шість атомів вуглецю та може бути моновалентним або полівалентним, наприклад, моно-, ди- або тривалентний спирт. Прийнятні спиртові компоненти включають, не обмежуючись наведеними, метанол, етанол, пропанол, бутанол або пентанол або їх ізомери; гліколь та гліцерин. Інші прийнятні складні ефіри жирних кислот включають, не обмежуючись наведеними, етилолеат, ізопропіл-міристат, ізопропіл-пальмітат, LABRAFIL®M2375, (поліоксиетиленгліцерин), LABRAFIL® M 1944 CS (ненасичені поліглікозильовані гліцериди, одержані спиртовим гідролізом кісточкового абрикосового масла, та що включають гліцериди та складний ефір TM поліетиленгліколю), LABRASOL (насичені поліглікозильовані гліцериди, одержані спиртовим гідролізом TCM, та що включають гліцериди та складний ефір поліетиленгліколю; всі доступні з GaKefosse, France), та/або MIGLYOL® 812 (тригліцерид насичених жирних кислот з довжиною ланцюга C8-C12 від Hüls AG, Germany), та рослинні масла, такі як бавовняна олія, мигдалева олія, оливкова олія, касторова олія, сезамова олія, соєва олія або арахісове масло. Фармацевтичні композиції для перорального введення можуть бути одержані, наприклад, шляхом об’єднання активного інгредієнта з одним або декількома твердими носіями, та, при бажанні, гранулювання отриманої суміші, та обробки зазначеної суміші або гранул включенням додаткових наповнювачів, з утворенням таблеток або ядер таблеток. Прийнятні носії включають, не обмежуючись наведеними, наповнювачі, такі як цукри, такі як лактоза, сахароза, маніт або сорбіт, целюлозні препарати, та/або фосфати кальцію, наприклад, трикальцію фосфат або гідрофосфат кальцію, та також зв’язуючі речовини, такі як крохмалі, наприклад, кукурудзяний, пшеничний, рисовий або картопляний крохмаль, метилцелюлоза, гідроксипропіл-метилцелюлоза, натрію карбоксиметилцелюлоза, та/або полівінілпіролідон, та/або, при бажанні, дезінтегратори, такі як описані вище крохмалі, карбоксиметил-крохмаль, перехресно-зв’язаний полівінілпіролідон, альгінова кислота або її солі, такі як альгінат натрію. Додаткові наповнювачі включають регулятори потоку та любриканти, наприклад, кремнієва кислота, тальк, стеаринова кислота або її солі, такі як стеарат магнію або кальцію, та/або поліетиленгліколь, або їх похідні. Ядра таблеток можуть бути одержані з прийнятними, необов’язково ентеросолюбільними, покриттями шляхом застосування, серед інших, концентрованих цукрових розчинів, які можуть включати гуміарабік, тальк, полівінілпіролідон, поліетиленгліколь та/або діоксид титану, або покриваючих розчинів у прийнятних органічних розчинниках або сумішах розчинників, або, для 15 UA 101057 C2 5 10 15 20 25 30 35 40 45 50 55 60 одержання ентеросолюбільних покриттів, розчини прийнятних целюлозних препаратів, таких як фталат ацетилцелюлози або фталат гідроксипропілметилцелюлози. Барвники або пігменти можуть бути додані до таблеток або покриттів таблеток, наприклад, з метою ідентифікації або для показання різних доз активного інгредієнту. Фармацевтичні композиції для перорального введення також можуть включати тверді капсули, що містять желатин, або м’які капсули, що містять желатин та пластифікатор, такий як гліцерин або сорбіт. Тверді капсули можуть містити активний інгредієнт у формі гранул, наприклад, у суміші з такими як: наповнювачі, такі як кукурудзяний крохмаль, зв’язуючі речовини, та/або гліданти, такі як тальк або стеарат магнію, та необов’язково стабілізатори. У м’яких капсулах, активний інгредієнт може бути розчинений або суспендований у прийнятних рідких наповнювачах, таких як жирні масла, керосин або рідкі поліетилен-гліколі або складні ефіри жирних кислот етилен або пропілен гліколю, до яких можуть бути додані стабілізатори та детергенти, наприклад, типу складних ефірів поліоксиетилен-сорбіту та жирних кислот. Фармацевтичні композиції, прийнятні для ректального застосування, являють собою, наприклад, супозиторії, що включають комбінацію активного інгредієнту та основи для супозиторію. Прийнятні основи для супозиторію являють собою, наприклад, природні або синтетичні тригліцериди, парафінові вуглеводні, поліетилен-гліколі або вищі алканоли. Фармацевтичні композиції, прийнятні для парентерального введення, можуть включати водні розчини активного інгредієнту у водорозчинній формі, наприклад, водорозчинній солі, або водні ін’єкційні суспензії, які містять речовини, що підвищують в’язкість, наприклад, карбоксиметилцелюлоза натрію, сорбіт та/або декстран, та, при бажанні, стабілізатори. Активний інгредієнт, необов’язково разом із наповнювачами, також може бути у формі ліофілізату та може бути переведений у розчин перед парентеральним застосуванням шляхом додавання прийнятних розчинників. Розчини, які використовують, наприклад, для парентерального введення, також можуть бути використані як інфузійні розчини. Виробництво ін’єкційних препаратів зазвичай проводять за стерильних умов, наприклад, воно являє собою наповнення, наприклад, у ампули або склянки, та запечатування контейнерів. Сполуки даного винаходу можуть бути введені як єдиний активний інгредієнт, або разом з іншими лікарськими засобами, корисними проти непластичних хвороб або корисними у імуномоделюючих режимах. Наприклад, сполуки даного винаходу можуть бути використані відповідно до винаходу у комбінації з фармацевтичними композиціями, ефективними при різних хворобах, як описано вище, наприклад, з такими як: циклофосфамід, 5-фторурацил, флударабін, гемцитабін, цисплатинум, карбоплатин, вінкристин, вінбластин, етопозид, іринотекан, паклітаксел, доцетаксел, ритуксан, доксорубіцин, гефітиніб або іматиніб; або також з такими як: циклоспорини, рапаміцини, аскоміцини або їх імунопригнічуючі аналоги, наприклад, циклоспорин A, циклоспорин G, FK-506, сіролімус або еверолімус, кортикостероїди, наприклад, преднізон, циклофосфамід, азатіопрен, метотрексат, солі золота, сульфасалазин, протималярійні засоби, бреквінар, лефлуномід, мізорибін, мікофенольна кислота, мікофенолят, мофетил, 15-деоксиспергуалін, імунопригнічуючі моноклональні антитіла, наприклад, моноклональні антитіла до рецепторів лейкоцитів, наприклад, MHC, CD2, CD3, CD4, CD7, CD25, CD28, I CD40, CD45, CD58, CD80, CD86, CD152, CD137, CD154, ICOS, LFA-1, VLA-4 або їх лігандів, або інші імуномоделюючі сполуки, наприклад, CTLA41g. Даний винахід також забезпечує фармацевтичні комбінації, наприклад, набір, що включає a) перший агент, який являє собою сполуку даного винаходу як розкрито у цьому описі, у вільній формі або у формі фармацевтично прийнятної солі, та b) щонайменше один спів-агент. Зазначений набір може включати інструкції для його введення. Способи одержання сполук даного винаходу Загальні процедури одержання сполук даного винаходу описані у Прикладах, представлених нижче. У описаних реакціях, реакційно-здатні функціональні групи, наприклад, гідрокси, аміно, іміно, тіо або карбокси групи, коли вони є бажаними у кінцевому продукті, можуть бути захищені для уникнення їх небажаної участі у реакціях. Звичайні захисні групи можуть бути використані у відповідності до стандартної практики (дивись, наприклад, T.W. Greene та P. G. M. Wuts у “Protective Groups in Organic Chemistry”, John Wiley and Sons, 1991). Сполуки даного винаходу, включаючи їх солі, також можуть бути одержані у формі гідратів, або їх кристали можуть включати, наприклад, розчинник, що використовують для кристалізації (у цьому описі - сольвати). Солі, як правило, можуть бути перетворені у сполуки у вільній формі, наприклад, шляхом обробки з прийнятними основними агентами, наприклад, з карбонатами лужних металів, гідрокарбонатами лужних металів, або гідроксидами лужних металів, такими як карбонат калію або гідроксид натрію. Сполука даного винаходу у формі солі приєднання основи може бути перетворена у відповідну вільну кислоту шляхом обробки підходящою кислотою 16 UA 101057 C2 5 10 15 20 25 30 35 40 45 50 55 60 (наприклад, соляною кислотою, тощо). Приймаючи до уваги тісний зв’язок між новими сполуками у вільній формі та сполуками у формі їх солей, включаючи ті солі, які можуть бути використані як проміжні сполуки, наприклад, у очищенні або ідентифікації нових сполук, будьяке посилання на вільні сполуки у цьому описі вище та нижче слід розуміти як посилання також на відповідні солі, якщо прийнятно. Солі сполук даного винаходу з солеутворюючими групами можуть бути одержані за способом, відомим per se. Солі приєднання кислоти сполук Формули (1), (2), (3) та (4), таким чином, можуть бути одержані шляхом обробки кислотою або прийнятним аніонообмінним реагентом. Фармацевтично прийнятні солі сполук даного винаходу можуть бути утворені, наприклад, як солі приєднання кислоти, з органічними або неорганічними кислотами, зі сполук Формули (1), (2), (3) та (4), з основним атомом азоту. Прийнятні неорганічні кислоти включають, не обмежуючись наведеними, галогенові кислоти, такі як соляна кислота, сірчана кислота, або фосфорна кислота. Прийнятні органічні кислоти включають, не обмежуючись наведеними, такі як карбонова, фосфорна, сульфонова або сульфамінова кислоти, наприклад, оцтова кислота, пропіонова кислота, каприлова кислота, капринова кислота, додеканова кислота, гліколева кислота, молочна кислота, фумарова кислота, бурштинова кислота, адипінова кислота, пімелінова кислота, суберинова кислота, азелаїнова кислота, яблучна кислота, винна кислота, лимонна кислота, аміно кислоти, такі як глутамінова кислота або аспарагінова кислота, малеїнова кислота, гідроксималеїнова кислота, метилмалеїнова кислота, циклогексанкарбонова кислота, адамантанкарбонова кислота, бензойна кислота, саліцилова кислота, 4-аміносаліцилова кислота, фталева кислота, фенілоцтова кислота, мигдальна кислота, корична кислота, метан- або етан-сульфонова кислота, 2-гідроксиетансульфонова кислота, етан-1,2-дисульфонова кислота, бензолсульфонова кислота, 2-нафталінсульфонова кислота, 1,5-нафталін-дисульфонова кислота, 2-, 3- або 4 метилбензолсульфонова кислота, метилсірчана кислота, етилсірчана кислота, додецилсірчана кислота, N-циклогексилсульфамінова кислота, N-метил-, N-етил- або N-пропіл-сульфамінова кислота, або інші органічні протонні кислоти, такі як аскорбінова кислота. Для виділення та очищення, також можна використовувати фармацевтично неприйнятні солі, наприклад, пікрати або перхлорати. Для терапевтичного застосування використовують тільки фармацевтично прийнятні солі або вільні сполуки (де прийнятно у формі фармацевтичних препаратів). Сполуки даного винаходу у неокисленій формі можуть бути одержані з N-оксидів сполук даного винаходу шляхом обробки відновлюючим агентом (наприклад, таким як сірка, діоксид сірки, трифеніл-фосфін, боргідрид літію, боргідрид натрію, фосфору трихлорид, трибромід, або подібні) у прийнятному інертному органічному розчиннику (наприклад, ацетонітрил, етанол, водний діоксан, або подібні) при 0 – 80 °C. Похідні проліків сполук даного винаходу можуть бути одержані за способами, відомими спеціалістам, кваліфікованим у даній галузі техніки (наприклад, для більш детального опису дивись Saulnier et al., (1994), Bioorganic and Medicinal Chemistry Letters, том 4, стор. 1985). Наприклад, відповідні пролікарські засоби можуть бути одержані шляхом введення у реакцію недериватизованої сполуки даного винаходу з прийнятним карбамілізуючим агентом (наприклад, 1,1-ацилоксиалкіл-карбано-хлоридат, пара-нітрофеніл карбонат, або подібні). Захищені похідні сполук даного винаходу можуть бути одержані за допомогою засобів, відомих спеціалістам, кваліфікованим у даній галузі техніки. Детальний опис технологій, застосовних для створення захисних груп та їх видалення, може бути знайдений у T. W. Greene, тє “Protecting Groups in Organic Chemistry”, 3 видання, John Wiley and Sons, Inc., 1999. Сполуки даного винаходу можуть бути одержані у вигляді їх окремих стереоізомерів шляхом введення у реакцію рацемічної суміші сполуки з оптично активним розділюючим агентом з утворенням пари діастереоізомерних сполук, розділення діастереоізомерів та відновлення оптично чистих енантіомерів. Розділення енантіомерів може бути виконане, використовуючи ковалентні діастереомерні похідні сполук даного винаходу або комплекси, що дисоціюються (наприклад, кристалічні діастереомерні солі). Діастереомери мають відмінні фізичні властивості (наприклад, точки плавлення, точки кипіння, розчинності, реакційну здатність, тощо) та можуть бути легко розділені, приймаючи до уваги перевагу цих відмінностей. Діастереомери можуть бути розділені за допомогою фракційної кристалізації, хроматографії або за допомогою технологій розділення/відділення, основаних на різницях у розчинності. Оптично чистий енантіомер потім відновлюють, з відновлюючим агентом, шляхом будь-яких практичних засобів, які не будуть приводити до рацемізації. Більш детальний опис технологій, застосовний для розділення стереоізомерів сполук з їх рацемічної суміші, може бути знайдений у Jean Jacques, Andre Collet, Samuel H. Wilen, “Еnantіоmеrs, Racemates and Resolutions”, John Wiley and Sons, 17 UA 101057 C2 5 10 15 20 25 30 Inc., 1981. Коротко, сполуки даного винаходу можуть бути одержані за способом, як описано у Прикладах, та (a) необов’язково перетворюючи сполуки даного винаходу у фармацевтично прийнятну сіль; (b) необов’язково перетворюючи сольову форму сполуки даного винаходу у несольову форму; (c) необов’язково перетворюючи неокислену форму сполуки даного винаходу у фармацевтично прийнятний N-оксид; (d) необов’язково перетворюючи N-оксидну форму сполуки даного винаходу у її неокислену форму; (e) необов’язково відділюючи окремий ізомер сполуки даного винаходу від суміші ізомерів; (f) необов’язково перетворюючи недериватизовану сполуку даного винаходу у фармацевтично прийнятну пролікарську похідну; та (g) необов’язково перетворюючи пролікарську похідну сполуки даного винаходу у її недериватизовану форму. Оскільки вироблення вихідних матеріалів особливо не описане, сполуки є відомими або можуть бути одержані аналогічно до способів, відомих у даній галузі техніки або як розкрито у Прикладах, представлених нижче. Спеціаліст, кваліфікований у даній галузі техніки, зрозуміє, що описані вище перетворення є тільки типовими прикладами способів для одержання сполук даного винаходу, та що інші добре відомі способи можуть бути використані аналогічно. Даний винахід додатково описаний, але не обмежується, наступним та Прикладами, які ілюструють одержання сполук даного винаходу. Проміжна сполука 1 2,5-дихлор-N-(5-метил-1H-піразол-3-іл)піримідин-4-амін HN N Cl N N N Cl H Суміш 5-метил-1H-піразол-3-аміну (3,00 г, 30,9 ммоль), 2,4,5-трихлорпіримідину (5,67 г, 30,9 ммоль, 1 еквів.) та Na2CO3 (3,60 г, 34,0 ммоль, 1,1 еквів.) у EtOH (100 мл) нагрівають при 40 C впродовж 24 год.. Розчинник видаляють у вакуумі. Отриманий залишок розподіляють між EtOAc (350 мл) та водою (100 мл). EtOAc шар промивають водою (3x), насиченим водним розчином NaCl (1x) та сушать над Na2SO4. Отриманий EtOAc розчин концентрують у вакуумі, забезпечуючи одержання продукту 2,5-дихлор-N-(5-метил-1H-піразол-3-іл)піримідин-4-аміну; + ESMS m/z 244,0 (M + H ). Проміжна сполука 2 2-хлор-N-(5-метил-1H-піразол-3-іл)-5-(трифторметил)піримідин-4-амін F F F N HN 35 40 45 N Cl N HN Суміш 2,4-дихлор-5-(трифторметил)піримідину (1,06 г, 4,86 ммоль), 5-метил-1H-піразол-3аміну (472,2 мг, 4,86 ммоль) та карбонату натрію (2,06 г, 19,4 ммоль) у 100 мл EtOH перемішують при кімнатній температурі впродовж ночі. Реакційну суміш концентрують у вакуумі. Сиру тверду речовину розподіляють між EtOAc та водою. Об’єднані органічні екстракти сушать (Na2SO4), концентрують у вакуумі, та очищують за допомогою хроматографії на кремнеземі (EtOAc/ гексани: 1/1), що забезпечує одержання 2-хлор-N-(5-метил-1H-піразол-3-іл)-5+ (трифторметил)піримідин-4-аміну; ESMS m/z 278,0 (M + H ). Проміжна сполука 3 2-хлор-5-метил-N-(5-метил-1H-піразол-3-іл)піримідин-4-амін H3 C N HN N N N Cl H Суміш 5-метил-1H-піразол-3-аміну (3,00 г, 30,9 ммоль), 2,4-дихлор-5-метилпіримідину (5,03 18 UA 101057 C2 5 г, 30,9 ммоль, 1 еквів.) та Na2CO3 (3,60 г, 34,0 ммоль, 1,1 еквів.) у EtOH (100 мл) нагрівають при 40 C впродовж 24 год. Розчинник видаляють у вакуумі. Отриманий залишок розподіляють між EtOAc (350 мл) та водою (100 мл). EtOAc шар промивають водою (3x), насиченим водним NaCl (1x), сушать над Na2SO4, та концентрують у вакуумі. Отриманий сирий продукт обробляють ультразвуком у Et2O (200 мл) та отриманий осад збирають фільтруванням. Цей порошок далі промивають за допомогою Et2O, забезпечуючи одержання продукту 2-хлор-5-метил-N-(5-метил+ 1H-піразол-3-іл)піримідин-4-аміну; ESMS m/z 224,1 (M + H ). Проміжна сполука 4 N-(2,5-дихлорпіримідин-4-іл)-5-метилізоксазол-3-амін Cl N HN N Cl N O 10 15 Суміш 5-метилізоксазол-3-аміну (98 мг, 1,0 ммоль), 2,4,5-трихлорпіримідину (344 мкл, 3,0 ммоль), та карбонату натрію (106 мг, 1,0 ммоль) у 3 мл EtOH нагрівають при 60 °C впродовж ночі. Реакційну суміш концентрують та потім розподіляють між EtOAc та сольовим розчином. Зібрані органічні екстракти сушать (Na2SO4), концентрують у вакуумі, та очищують за допомогою хроматографії на силікагелі (MeOH/DCM: 1/9), що забезпечує одержання N-(2,5+ дихлорпіримідин-4-іл)-5-метилізоксазол-3-аміну; ESMS m/z 245,0 (M + H ). Проміжна сполука 5 2,5-дихлор-N-(5-циклопропіл-1H-піразол-3-іл)піримідин-4-амін Cl N HN N Cl N HN 20 25 Суміш 5-циклопропіл-1H-піразол-3-аміну (246 мг, 2,00 ммоль), 2,4,5-трихлорпіримідину (367 мг, 2,00 ммоль, 1 еквів.) та Na2CO3 (233 мг, 2,20 ммоль, 1,1 еквів.) у EtOH (10 мл) нагрівають при 40 C впродовж 16 год. Сиру реакційну суміш розбавляють за допомогою EtOAc та послідовно промивають за допомогою: води (3x) та насиченого водного розчину NaCl (1x). Отриманий EtOAc шар сушать над Na2SO4 та потім концентрують у вакуумі, забезпечуючи одержання 2,5+ дихлор-N-(5-циклопропіл-1H-піразол-3-іл)піримідин-4-аміну; ESMS m/z 270,0 (M + H ). Проміжна сполука 6 3-(2,5-дихлорпіримідин-4-іламіно)азепан-2-он Cl N HN 30 35 N H N Cl O Суміш (±)-α-аміно-ε-капролактаму (256 мг, 2,0 ммоль), 2,4,5-трихлорпіримідину (366 мг, 2,0 ммоль, 1 еквів.) та NaHCO3 (168 мг, 2 ммоль, 1 еквів.) у суміші MeOH (12 мл) та H2O (6 мл) перемішують при кімнатній температурі впродовж 15 год.. Отриманий осад збирають шляхом вакуумного фільтрування та промивають невеликими кількостями MeOH та води, забезпечуючи + одержання продукту 3-(2,5-дихлорпіримідин-4-іламіно)азепан-2-ону; ESMS m/z 275,0 (M + H ). Проміжна сполука 7 3-(2,5-дихлорпіримідин-4-іламіно)піридин-2(1H)-он Cl N HN N N Cl H O Суміш 3-амінопіридин-2(1H)-ону (99 мг, 0,90 ммоль), 2,4,5-трихлорпіримідину (165 мг, 0,90 ммоль, 1 еквів.) та NaHCO3 (76 мг, 0,90 ммоль, 1 еквів.) у суміші MeOH (6 мл) та H2O (3 мл) перемішують при кімнатній температурі впродовж 24 год.. Отриманий осад збирають шляхом 19 UA 101057 C2 5 10 15 20 25 30 35 40 вакуумного фільтрування та промивають невеликими кількостями MeOH та води, забезпечуючи одержання продукту 3-(2,5-дихлорпіримідин-4-іламіно)піридин-2(1H)-ону; ESMS m/z 257,0 (M + + H ). Проміжна сполука 8 2,5-Дихлор-N-(5-метил-1-(тетрагідро-2H-піран-2-іл)-1H-піразол-3-іл)піримідин-4-амін THP N N Cl N N N Cl H До суміші 2,5-дихлор-N-(5-метил-1H-піразол-3-іл)піримідин-4-аміну (2,44 г, 10 ммоль) та 4толуолсульфонової кислоти моногідрат (1,9 г, 10 ммоль) у THF (200 мл), додають DHP (4,25 г, 50 ммоль). Після перемішування впродовж ночі, реакційна суміш стає прозорою. Після концентрування, залишок розчиняють у етилацетаті та промивають за допомогою Na 2CO3 насиченого водного розчину. Органічний шар потім промивають за допомогою сольового розчину, сушать над сульфатом натрію та концентрують у вакуумі, що забезпечує одержання 2,5-дихлор-N-(5-метил-1-(тетрагідро-2H-піран-2-іл)-1H-піразол-3-іл)піримідин-4-аміну у вигляді світло-жовтої твердої речовини, яку використовують у наступних реакціях без додаткового + очищення; ESMS m/z 244 (M-THP+H ); ТШХ Rf=0,6 (кремнезем; 1:1 етилацетат/гексани; вихідний матеріал Rf=0,2). Проміжна сполука 9 2,5-Дихлор-N-(5-(трифторметил)-1H-піразол-3-іл)піримідин-4-амін HN N Cl N F3C N N Cl H Стадія 1: 5-(Трифторметил)-1H-піразол-3-амін Суміш (E)-4-аміно-4-етокси-1,1,1-трифторбут-3-ен-2-ону (5,00 г, 27 ммоль) та гідразину (1,05 г) у безводному EtOH (20 мл) перемішують при 80 C у запечатаній пробірці впродовж ночі. Реакцію гасять водою (50 мл), та екстрагують за допомогою EtOAc (100 мл, потім 250 мл). EtOAc шари об’єднують та послідовно промивають водою (25 мл), сольовим розчином (25 мл), сушать над Na2SO4 та випарюють з одержанням світло-коричневого маслянистого залишку. Сирий продукт очищують за допомогою хроматографії на кремнеземі (30-100% градієнт EtOAc у гексанах) з одержанням 5-(трифторметил)-1H-піразол-3-аміну у вигляді майже білої твердої + речовини; ESMS m/z 152,0 (M+H ). Стадія 2: 2,5-Дихлор-N-(5-(трифторметил)-1H-піразол-3-іл)піримідин-4-амін Суміш 5-(трифторметил)-1H-піразол-3-аміну (500 мг, 3,3 ммоль), 2,4,5-трихлорпіримідину (607 мг, 3,3 ммоль) та карбонату натрію (525 мг, 5 ммоль) у безводному EtOH (10 мл) перемішують при кімнатній температурі. Через один день, РХМС показала, що реакція не закінчилася. Додають додатковий 2,4,5-трихлорпіримідин (0,15 мл) та карбонат натрію (525 мг) та реакція продовжується протягом ще двох днів. Розчинник випарюють, та залишок екстрагують за допомогою DCM (3 20 мл). Об’єднані DCM шари промивають за допомогою сольового розчину (10 мл), сушать над Na2SO4 та випарюють. Сирий продукт очищують за допомогою хроматографії на кремнеземі (0-50% градієнт EtOAc у гексанах) з одержанням 2,5дихлор-N-(5-(трифторметил)-1H-піразол-3-іл)піримідин-4-аміну у вигляді світло-жовто+ коричневої твердої речовини; ESMS m/z 297,9 (M+H ). Проміжна сполука 10 2,5-Дихлор-N-(5-етил-1H-піразол-3-іл)піримідин-4-амін HN N Cl 45 N N N Cl H Суміш 5-етил-1H-піразол-3-аміну (1,00 г, 6,77 ммоль), 2,4,5-трихлорпіримідину (1,24 г, 6,77 ммоль) та Na2CO3 (1,79 г, 16,9 ммоль) у ізо-пропанолі (15 мл) перемішують у запечатаній пробірці при кімнатній температурі впродовж двох днів. Додають воду (10 мл). Тверду речовину збирають фільтруванням, промивають за допомогою води (10 мл) та сушать з одержанням 2,5дихлор-N-(5-етил-1H-піразол-3-іл)піримідин-4-аміну у вигляді світло-жовтої твердої речовини; + ESMS m/z 258,0 (M+H ). Проміжна сполука 11 20 UA 101057 C2 1-хлор-5-метил-4-нітро-2-(трифторметил)бензол CF3 Cl O2N 5 10 До розчину 2-хлор-4-метил-1-(трифторметил)бензолу (6,65 г, 34,1 ммоль) у конц. сірчаній кислоті (25 мл) при 0 C додають нітрат калію (3,46 г, 34,1 ммоль) у сірчаній кислоті (15 мл). Після перемішування при 0 C впродовж 1,5 год., реакційну суміш виливають у 500 мл льодяної води. Осад збирають фільтруванням та промивають за допомогою надмірних кількостей води, що приводить до одержання 1-хлор-5-фтор-4-нітро-2-(трифторметил)бензолу у вигляді 1 помаранчевої твердої речовини; H ЯМР (400 MГц, хлороформ-d) 8,356 (s, 1H), 7,543 (s, 1H), 2,660 (s, 3H). Проміжна сполука 12 2-Бром-4-метил-5-нітробензонітрил CN Br O2 N 15 Слідуючи тій же процедурі, що описана для Проміжної сполуки 11, виходячи з 2-бром-4метилбензонітрилу, 2-бром-4-метил-5-нітробензонітрил отримують у вигляді жовтої твердої 1 речовини; H ЯМР (400 MГц, хлороформ-d) 8,290 (s, 1H), 7,742 (s, 1H), 2,683 (s, 3H). Проміжна сполука 13 5-Аміно-2-бром-4-метилбензонітрил CN Br H 2N 20 25 До розчину 2-бром-4-метил-5-нітробензонітрилу (500 мг, 2,07 ммоль) у етанолі (20 мл) додають хлорид олова (785 мг, 4,14 ммоль). Суміш нагрівають при зрошенні впродовж 5 годин. Після охолодження до кімнатної температури, додають триетиламін (1,01 г, 10 ммоль). Суміш концентрують та очищують за допомогою хроматографії на кремнеземі (30-50% градієнт етилацетату у гексанах), що забезпечує одержання 5-аміно-2-бром-4-метилбензонітрилу у + вигляді бежевої твердої речовини; ESMS m/z 211 (M + H ). Проміжна сполука 14 Метил 2-бром-4-метил-5-нітробензоат COOMe Br O2 N 30 Слідуючи тій же процедурі, що описана для Проміжної сполуки 11, виходячи з метил 2-бром1 4-метилбензоату, заголовну сполуку отримують у вигляді білої твердої речовини; H ЯМР (400 MГц, хлороформ-d) 8,505 (s, 1H), 7,711 (s, 1H), 3,967 (s, 3H), 2,640 (s, 3H). Проміжна сполука 15 Метил 5-аміно-2-бром-4-метилбензоат COOMe Br H 2N 35 Слідуючи тій же процедурі, що описана для Проміжної сполуки 13, заголовну сполуку + отримують у вигляді бежевої твердої речовини; ESMS m/z 244 (M + H ). Проміжна сполука 16 4-Бром-5-метокси-2-метиланілін 21 UA 101057 C2 OMe Br H 2N 5 10 15 20 25 Стадія 1: N-(5-метокси-2-метилфеніл)ацетамід До розчину триетиламіну (2,9 г, 14,4 ммоль) та 5-метокси-2-метиланіліну (1,0 г, 7,2 ммоль) у DCM (30 мл) при 0 C, додають ацетилхлорид (0,57 г, 7,2 ммоль) краплинним способом. Суміш перемішують при кімнатній температурі впродовж 1 години. Реакцію гасять насиченим водним розчином хлориду амонію, та екстрагують за допомогою DCM. Органічний шар сушать над Na2SO4 та концентрують, що забезпечує одержання N-(5-метокси-2-метилфеніл)ацетаміду у вигляді кристалів голкоподібної форми. Сирий продукт використовують на наступній стадії без додаткового очищення. Стадія 2: N-(4-бром-5-метокси-2-метилфеніл)ацетамід До розчину N-(5-метокси-2-метилфеніл)ацетаміду у оцтовій кислоті (40 мл) повільно додають Br2 (3 г, 19 ммоль). Суміш закривають кришкою та перемішують при 50 C впродовж 5 годин. Реакційну суміш охолоджують до кімнатної температури, потім реакцію гасять водним розчином сульфіту натрію, та екстрагують за допомогою етилацетату (3 50 мл). Об’єднаний органічний шар сушать над Na2SO4 та концентрують, що забезпечує одержання сирого N-(4бром-5-метокси-2-метилфеніл)ацетаміду у вигляді коричневого масла, яке використовують на наступній стадії без додаткового очищення. Стадія 3: 4-бром-5-метокси-2-метиланілін N-(4-бром-5-метокси-2-метилфеніл)ацетамід розчиняють у метанолі (15 мл) та концентрованій HCl (30 мл). Суміш нагрівають при зрошенні при 95 C впродовж ночі. Після охолодження до кімнатної температури, суміш виливають у льодяну воду, та підлужують до pH = 12 за допомогою конц. NaOH водного розчину. Суміш потім екстрагують за допомогою етилацетату (3 50 мл). Об’єднаний органічний шар сушать над Na 2SO4 та концентрують. Сирий продукт очищують за допомогою хроматографії на кремнеземі (15% етилацетат у гексанах), що приводить до одержання 4-бром-5-метокси-2-метиланіліну у вигляді бежевої 1 твердої речовини; H ЯМР (400 МГц, CDCl3) 7,20 (s, 1H), 6,37 (s, 1H), 4,6 (br, 2H), 3,82 (s, 3H), 2,12 (s, 3H). Проміжна сполука 17 2-Фтор-5-метил-4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)анілін O B O H2 N 30 35 40 F Суміш 4-бром-2-фтор-5-метиланіліну (2,0 г, 9,8 ммоль), біс(пінаколато)дибору (2,74 г, 10,8 ммоль), трициклогексилфосфін (274,8 мг, 0,98 ммоль), Pd2(dba)3 (448,9 мг, 0,49 ммоль), та ацетат калію (1,92 г, 19,6 ммоль) у 60 мл 1,4-діоксану дегазують та продувають азотом. Реакційну суміш нагрівають при 80 °C впродовж ночі та потім охолоджують до кімнатної температури. Суміш розподіляють між EtOAc та водою та зібрані органічні екстракти сушать (Na2SO4), концентрують у вакуумі, та очищують за допомогою хроматографії на кремнеземі (EtOAc / гексани: 20/ 80), що забезпечує одержання 2-фтор-5-метил-4-(4,4,5,5-тетраметил-1,3,2+ діоксаборолан-2-іл)аніліну; ESMS m/z 252,2 (M + H ). Проміжна сполука 18 2-Ізопропокси-5-метил-4-(1-метил-піперидин-4-іл)-феніламін H2N N O Стадія 1: 1-бром-5-фтор-2-метил-4-нітробензол До розчину 2-бром-4-фтор-1-метилбензолу (5 г, 26,4 ммоль), розчиненого у конц. сірчаній кислоті (20 мл), додають нітрат калію (2,67 г, 26,4 ммоль) у сірчаній кислоті (5 мл) при 0 C. 22 UA 101057 C2 5 10 15 20 25 30 35 40 45 50 Після перемішування при 0 C впродовж 1 години, реакційну суміш розбавляють за допомогою води, екстрагують за допомогою етилацетату (3 40 мл). Об’єднані органічні фази промивають за допомогою насиченого розчину бікарбонату натрію та сольового розчину послідовно, та потім сушать над Na2SO4. Сирий продукт, отриманий після концентрування, отримують за допомогою силікагелевої колонкової хроматографії із змішаним розчинником гексани/EtOAc (95/5), що забезпечує одержання 1-бром-5-фтор-2-метил-4-нітробензолу у вигляді помаранчевої 1 твердої речовини. H ЯМР (400 MГц, хлороформ-d) 7,93 (d, 1H, J = 7,6 Гц), 7,50 (d, 1H, J = 10 Гц), 2,43 (s, 3H). Стадія 2: 1-бром-5-ізопропокси-2-метил-4-нітробензол До розчину 1-бром-5-фтор-2-метил-4-нітробензолу (Стадія 1, 1,5 г, 6,4 ммоль) у 2-пропанолі (30 мл) додають карбонат цезію (5,3 г, 16 ммоль). Суміш нагрівають при 50 C впродовж ночі. Суміш концентрують та розподіляють між етилацетатом та водою. Органічний шар концентрують та залишок очищують за допомогою силікагелевої колонкової хроматографії з 5% етилацетатом у гексанах, що забезпечує одержання 1-бром-5-ізопропокси-2-метил-4нітробензолу у вигляді жовтої твердої речовини. Стадія 3: 4-(5-Ізопропокси-2-метил-4-нітрофеніл)піридин До суміші 1-бром-5-ізопропокси-2-метил-4-нітробензолу (Стадія 2, 1 г, 3,65 ммоль), піридин4-боронової кислоти (490 мг, 4 ммоль), 2-дициклогексилфосфіно-2’,6’-диметоксибіфеніл (300 мг, 0,73 ммоль) та фосфат калію (1,55 г, 7,3 ммоль) у змішаному розчиннику діоксану (15 мл) та води (7,5 мл) додають тріс(дибензиліден-ацетон)дипаладій (0) (334 мг, 0,36 ммоль). Цю суміш герметично закривають та продувають азотом впродовж 3 хвилин та потім нагрівають при 120 C впродовж 5 годин. Суміш охолоджують до кімнатної температури, фільтрують, та фільтрат концентрують. Після концентрування, сирий продукт очищують за допомогою силікагелевої флеш колонкової хроматографії (60% етилацетат у гексанах), що забезпечує одержання 4-(5ізопропокси-2-метил-4-нітрофеніл)піридину у вигляді жовтої твердої речовини: ESMS m/z 273,2 + (M + H ). Стадія 4: 4-(5-Ізопропокси-2-метил-4-нітро-феніл)-1-метил-піридиній йодид 4-(5-Ізопропокси-2-метил-4-нітро-феніл)-піридин (Стадія 3, 217 мг, 0,797 ммоль) розчиняють у безводному THF (9 мл). Додають йодметан (0,10 мл, 1,61 ммоль, 2 еквів.), та реакційну суміш перемішують при 40 C у запаяній пробірці впродовж 2 днів. Леткі речовини видаляють у вакуумі, забезпечуючи одержання 4-(5-ізопропокси-2-метил-4-нітро-феніл)-1-метил-піридиній йодиду у вигляді коричневої твердої речовини: ESMS m/z 287,1 (M+). Стадії 5 та 6: 2-Ізопропокси-5-метил-4-(1-метил-піперидин-4-іл)-феніламін 4-(5-Ізопропокси-2-метил-4-нітро-феніл)-1-метил-піридиній йодид (Стадія 4, 0,697 ммоль) розчиняють у CH3OH (20 мл) та охолоджують до 0 C. Повільно додають NaBH4 (264 мг, 6,97 ммоль, 10 еквів.). Після закінчення цього додавання, охолоджуючу баню видаляють та реакційну суміш перемішують при кімнатній температурі впродовж 1 годин. Реакцію гасять шляхом повільного додавання 1N водного розчину HCl (14 мл). CH 3OH частково видаляють у вакуумі. Отриманий залишок розподіляють між EtOAc та 1 N водним розчином NaOH. Додатковий 50 % водний розчин NaOH додають поки водний шар не буде мати pH >12. EtOAc шар промивають за допомогою 1 N водного розчину NaOH (2x), органічний шар потім сушать над сульфатом натрію, фільтрують, та концентрують у вакуумі. Після концентрування, сирий продукт (175 мг) розчиняють у оцтовій кислоті (10 мл). TFA (0,15 мл, 3 еквів.) та PtO 2 (53 мг, 30% мас./мас.) додають та реакційну суміш поміщають під 50 псі газоподібного H 2 у шейкері Пара впродовж 14 годин. Реакційну суміш фільтрують та фільтрат концентрують у вакуумі. Отриманий залишок розподіляють між EtOAc та 1 N водним розчином NaOH. Додатковий 50% водний розчин NaOH додають поки водний шар не буде мати pH >12. EtOAc шар промивають за допомогою 1 N водного розчину NaOH (2x), органічний шар потім сушать над сульфатом натрію, фільтрують, та концентрують у вакуумі, що приводить до одержання 2-ізопропокси-5-метил-4(1-метил-піперидин-4-іл)-феніламіну, який використовують у наступних стадіях без додаткового очищення: ESMS m/z 263,2 (M + H+). Проміжна сполука 19 трет-бутил 4-(4-аміно-5-фтор-2-метилфеніл)піперидин-1-карбоксилат O N O H 2N F 23 UA 101057 C2 5 10 15 20 25 30 35 40 45 Стадія 1: 4-Трифторметансульфонілокси-3,6-дигідро-2H-піридин-1-карбонової кислоти третбутиловий складний ефір Розчин N-трет-бутоксикарбоніл-4-піперидону (10,17 г, 0,05 моль) у THF (100 мл) додають краплинним способом у охолоджений (-78 C), енергійно перемішуваний розчин LDA (40 мл 1,5 M розчин у циклогексанах, 0,06 моль) у THF (100 мл), у атмосфері N2. Реакційну суміш залишають стояти при -78 C впродовж 30 хвилин перед додаванням розчину фенілтрифторсульфоніміду (19,85 г, 0,055 моль) у THF (50 мл). Потім реакційну суміш нагрівають до кімнатної температури та перемішують впродовж 3 годин. Реакцію гасять при 0 C за допомогою 100 мл насиченого водного NH4Cl та фільтрують через Целіт. Фільтрат додають до 100 мл EtOAc, та шари розділяють. Органічний шар промивають за допомогою H 2O, сушать над MgSO4 та концентрують. Сирий продукт очищують за допомогою хроматографії на силікагелі (030% EtOAc у гексанах як елюенті та контролюють за допомогою ТШХ, на яку наносять точкою 2% KMnO4 у EtOH), що забезпечує одержання 4-трифторметансульфонілокси-3,6-дигідро-2Hпіридин-1-карбонової кислоти трет-бутилового складного ефіру у вигляді жовтого масла. Стадія 2: Трет-бутил 4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)-5,6-дигідропіридин1(2H)-карбоксилат Розчин трет-бутил 4-(трифторметилсульфонілокси)-5,6-дигідропіридин-1(2H)-карбоксилату (16,0 г, 48,2 ммоль) у ДМСО (200 мл) обробляють за допомогою біс(пінаколато)дибору (12,6 г, 49,6 ммоль), ацетату калію (14,65 г, 149 ммоль) та Pd(dppf)Cl2 (790 мг, 0,96 ммоль). Цей розчин продувають N2 (г.) впродовж 5 хвилин, та потім запечатують та нагрівають при 80 C впродовж 15 год. Реакційну суміш охолоджують до кімнатної температури та виливають у льодяну воду. Суміш екстрагують за допомогою етилацетату (3 100 мл). Об’єднану органічну фазу промивають за допомогою сольового розчину, сушать над сульфатом натрію, та концентрують у вакуумі. Сирий продукт очищують за допомогою хроматографії на силікагелі (15% етилацетат у гексанах), що забезпечує одержання трет-бутил 4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2іл)-5,6-дигідропіридин-1(2H)-карбоксилату у вигляді білої твердої речовини. Стадії 3 та 4: Трет-бутил 4-(4-аміно-5-фтор-2-метилфеніл)піперидин-1-карбоксилат До суміші 5'-хлор-N,2'-диметил-4'-нітробіфеніл-4-карбоксаміду (204 мг, 1 ммоль), трет-бутил 4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)-5,6-дигідропіридин-1(2H)-карбоксилату (370 мг, 1,2 ммоль) та карбонату натрію (742 мг, 7 ммоль) у ДМФА/H 2O (12/3 мл) додають тетракіс(трифенілфосфін)паладій (0) (58 мг, 5% ммоль). Реакційну пробірку запечатують, суміш продувають N2 впродовж 3 хвилин та потім нагрівають при 90 C у N2 впродовж ночі. Реакційну суміш охолоджують до кімнатної температури, та виливають у насичений водний розчин хлориду амонію. Сиру реакційну суміш екстрагують за допомогою етилацетату (3 15 мл). Органічні екстракти об’єднують, промивають за допомогою сольового розчину та концентрують. Сирий продукт очищують за допомогою хроматографії на силікагелі (20% етилацетат у гексанах), що забезпечує одержання трет-бутил 4-(4-аміно-5-фтор-2-метилфеніл)-5,6дигідропіридин-1(2H)-карбоксилату у вигляді жовтого масла. Отримане масло розчиняють у метанолі (20 мл). До цього розчину додають Pd/C (10%). Реакційну суміш дегазують та продувають H2 декілька разів та перемішують у атмосфері H2 (1 атм.) впродовж ночі. Суміш фільтрують та концентрують, що забезпечує одержання трет-бутил 4-(4-аміно-5-фтор-2метилфеніл)піперидин-1-карбоксилату у вигляді білої твердої речовини. ESMS m/z 207 (M -Boc+ + H ). Проміжна сполука 20 2,5-Диметил-4-(піперидин-2-іл)анілін N H H 2N 50 55 До суміші 1-бром-2,5-диметил-4-нітробензолу (185 мг, 1 ммоль) та 2(трибутилстаніл)піридину (202 мг, 1,1 ммоль) у ДМФА (4 мл) додають тетракіс(трифенілфосфін) паладій (0) (58 мг, 5% ммоль). Реакційну пробірку запечатують, суміш продувають N 2 впродовж 3 хвилин та потім нагрівають при 120 C у атмосфері N2 впродовж ночі. Реакційну суміш охолоджують до кімнатної температури та виливають у насичений водний розчин хлориду амонію. Сиру реакційну суміш екстрагують за допомогою етилацетату (3 15 мл). Органічні екстракти об’єднують, промивають за допомогою сольового розчину та концентрують. Сирий продукт очищують за допомогою силікагелевої колонкової хроматографії (60% етилацетату у гексанах), що забезпечує одержання 2-(2,5-диметил-4-нітрофеніл)піридину у вигляді білої 24 UA 101057 C2 5 10 15 твердої речовини. Отриману тверду речовину розчиняють у оцтовій кислоті/TFA (15 мл/200 мкл). До цього розчину додають PtO2 (10% мас./мас.). Реакційну суміш дегазують та продувають H2 декілька разів та перемішують у 1 атм. Газоподібного водню впродовж ночі. Суміш фільтрують та концентрують, що забезпечує одержання 2,5-диметил-4-(піперидин-2-іл)аніліну у + вигляді жовтого масла. ESMS m/z 205 (M + H ). Проміжна сполука 21 трет-бутил 3-(4-аміно-2,5-диметилфеніл)азетидин-1-карбоксилат Стадія 1: трет-бутил 3-(2,5-диметил-4-нітрофеніл)азетидин-1-карбоксилат Отримують з трет-бутил 3-йодазетидин-1-карбоксилату та 1-бром-2,5-диметил-4нітробензолу слідуючи загальному протоколу як описано у Billotte, S. Synlett 1998, 379. Стадія 2: трет-бутил 3-(4-аміно-2,5-диметилфеніл)азетидин-1-карбоксилат трет-Бутил 3-(2,5-диметил-4-нітрофеніл)азетидин-1-карбоксилат відновлюють до трет-бутил 3-(4-аміно-2,5-диметилфеніл)азетидин-1-карбоксилату за допомогою стандартного гідрогенування на нікелі Ренея при кімнатній температурі, використовуючи MeOH як розчинник. Проміжна сполука 22 5-Етил-2-метил-4-(піперидин-4-іл)анілін NH H 2N 20 25 30 35 40 45 Стадія 1: трет-бутил 4-(4-аміно-5-метил-2-вінілфеніл)-5,6-дигідропіридин-1(2H)-карбоксилат До суміші 4-бром-5-хлор-2-метиланіліну (500 мг, 2,27ммоль), трет-бутил 4-(4,4,5,5тетраметил-1,3,2-діоксаборолан-2-іл)-5,6-дигідропіридин-1(2H)-карбоксилату (840 мг, 3,73 ммоль) та карбонату натрію (2,52 г, 15,9 ммоль) у ДМФА/H 2O (20/5 мл) додають тетракіс(трифенілфосфін) паладій (0) (131 мг, 5 моль%). Реакційну пробірку запечатують, суміш продувають N2 впродовж 3 хвилин та потім нагрівають при 100 C у атмосфері N2 впродовж ночі. Реакційну суміш охолоджують до кімнатної температури та виливають у насичений водний розчин хлориду амонію. Сиру реакційну суміш екстрагують за допомогою етилацетату (3 15 мл). Органічні екстракти об’єднують, промивають за допомогою сольового розчину та концентрують. Сирий продукт очищують за допомогою кремнеземової хроматографії (80% етилацетат у гексанах), що забезпечує одержання трет-бутил 4-(4-аміно-2-хлор-5-метилфеніл)5,6-дигідропіридин-1(2H)-карбоксилату у вигляді жовтої твердої речовини. Цей отриманий продукт (322 мг, 1 ммоль) розчиняють у суміші діоксан/NMP (безводна, 4 мл, 3/1). До цього розчину додають трибутил(вініл)станан (380 мг, 1,2 ммоль), фторид цезію (304 мг, 2 ммоль) та паладій біс(три-трет-бутил-фосфін) (51 мг, 10 моль%). Цю суміш продувають N2 впродовж 3 хвилин та потім нагрівають у запаяній пробірці при 120 C впродовж ночі. Суміш охолоджують до кімнатної температури та розбавляють етилацетатом. Отриману суміш послідовно промивають насиченим водним розчином хлориду амонію та сольовим розчином, та нарешті сушать над сульфатом натрію. Після концентрування, сирий продукт очищують за допомогою хроматографії на кремнеземі (10% етилацетат у гексанах), що забезпечує одержання третбутил 4-(4-аміно-5-метил-2-вінілфеніл)-5,6-дигідропіридин-1(2H)-карбоксилату у вигляді світло+ жовтого масла; ESMS m/z 215,2 (M -Boc + H ). Стадія 2: 5-Етил-2-метил-4-(піперидин-4-іл)анілін Продукт, отриманий з попередньої стадії, розчиняють у метанолі (20 мл). До цього розчину додають конц. водний розчин HCl (200 мкл) та оксид паладію (23 мг, 0,1 ммоль). Реакційну суміш дегазують та продувають H2 декілька разів та енергійно перемішують у 1 атм. H2 впродовж 3 годин. Суміш фільтрують та концентрують, що забезпечує одержання 5-етил-2+ метил-4-(піперидин-4-іл)аніліну у вигляді жовтої твердої речовини. ESMS m/z 219,2 (M + H ). Проміжна сполука 23 25 UA 101057 C2 2,5-Диметил-4-(піперидин-3-іл)анілін H N H 2N 5 10 15 20 Стадія 1: 2,5-Диметил-4-(піридин-3-іл)анілін Суспензію 4-бром-2,5-диметиланіліну (4,00 г, 20 ммоль), піридин-3-ілбборонової кислоти (2,70 г, 11 ммоль), Pd2(dba)3 (0,55 г, 0,6 ммоль), 2-дициклогексилфосфіно-2’,6’диметоксибіфенілу (0,98 г, 1,2 ммоль) та Na2CO3 (10,6 г, 100 ммоль) у n-BuOH (50 мл) дегазують струменем газоподібного аргону впродовж 15 хвилин. Реакційну колбу запечатують та поміщають у попередньо нагріту масляну баню (115 C). Після перемішування впродовж ночі, реакційну суміш охолоджують та фільтрують. Осад на фільтрі промивають за допомогою DCM та фільтрат концентрують у вакуумі. Отриманий залишок розчиняють у EtOAc (150 мл). EtOAC послідовно промивають водою (20 мл), сольовим розчином (20 мл), сушать над Na2SO4 та випарюють. Сирий продукт очищують за допомогою хроматографії на кремнеземі (градієнт 050% EtOAC у гексанах), що приводить до одержання 2,5-диметил-4-(піридин-3-іл)аніліну у + вигляді жовтої твердої речовини; ESMS m/z 199,1 (M+H ). Стадія 2: 2,5-Диметил-4-(піперидин-3-іл)анілін 2,5-Диметил-4-(піридин-3-іл)анілін (403 мг, 2,03 ммоль) розчиняють у MeOH (5 мл) та конц. водному розчині HCl (1 мл), що супроводжують додаванням PtO 2 (40 мг). Колбу продувають H 2 та реакційну суміш енергійно перемішують при кімнатній температурі у атмосфері H 2 (1 атм). Через два дні, РХМС показує закінчення реакції. Каталізатор видаляють фільтруванням та розчин, що залишився, концентрують у вакуумі, що приводить до одержання 2,5-диметил-4(піперидин-3-іл)аніліну у вигляді білої твердої речовини, яка може бути використана у наступних + реакціях без додаткового очищення; ESMS m/z 205,2 (M+H ). Проміжна сполука 24 1-(трет-бутоксикарбоніл(метил)аміно)циклопропанкарбонова кислота OH O 25 30 35 40 45 N Boc До розчину 1-(трет-бутоксикарбоніламіно)циклопропанкарбонової кислоти (201 мг, 1,0 ммоль) у ДМФА (2 мл) додають NaH (120 мг, 3,0 ммоль) при 0 C. Отриману суміш перемішують при 0 C впродовж 10 хвил. перед додаванням MeI (568 мг, 4,0 ммоль). Суміш потім нагрівають до кімнатної температури та перемішують впродовж 2 годин. Насичений NH 4Cl водний розчин (20 мл) додають у суміш, та цей розчин екстрагують за допомогою EtOAc (3 10 мл). Об’єднані органічні шари концентрують та залишок розчиняють у MeOH (3 мл) з NaOH (3 N, 1 мл). Цю суміш перемішують при 80 C впродовж 1 години та охолоджують до кімнатної температури. Прозорий розчин очищують безпосередньо на препаративній ОФ-ВЕРХ, що забезпечує одержання 1-(трет-бутоксикарбоніл(метил)аміно)циклопропанкарбонової кислоти. ESMS m/z + 238,2 (M + Na ). Проміжна сполука 25 (R)-2-бромпропанамід Br NH 2 O Стадія 1: (R)-2-бромпропаноїл хлорид У атмосфері азоту, до розчину (R)-2-бромпропанової кислоти (5,0 г, 32,68 ммоль) у 100 мл DCM додають тіоніл-хлорид (7,1 мл, 98,04 ммоль) та 1 мл ДМФА послідовно при 0 C. Реакційну суміш перемішують при кімнатній температурі впродовж ночі, та концентрують у вакуумі. Отриманий сирий продукт безпосередньо використовують у наступній стадії без додаткового очищення. Стадія 2: (R)-2-бромпропанамід (R)-2-бромпропаноїл хлорид повільно додають до 37% водного розчину гідроксиду амонію, охолодженого до 0 C. Реакційній суміші дають нагрітися до кімнатної температури та 26 UA 101057 C2 5 10 15 20 25 30 35 40 45 50 перемішують впродовж 2 годин. Продукт екстрагують за допомогою EtOAc та зібрані органічні екстракти сушать (Na2SO4) та концентрують у вакуумі, що забезпечує одержання (R)-2бромпропанаміду. Проміжна сполука 26 (R)-2-бром-N-метилпропанамід Br H N O (R)-2-бромпропаноїл хлорид повільно додають до водного розчину метиламіну, охолодженого до 0 C. Реакційній суміші дають нагрітися до кімнатної температури та перемішують впродовж 2 годин. Цей продукт екстрагують за допомогою EtOAc та зібрані органічні екстракти сушать (Na2SO4) та концентрують у вакуумі, що забезпечує одержання (R)-2бром-N-метилпропанаміду. Проміжна сполука 27 1-(трет-бутоксикарбоніл(етил)аміно)циклопропанкарбонова кислота O Boc N HO Стадія 1: Етил 1-(трет-бутоксикарбоніл(етил)аміно)циклопропанкарбоксилат У атмосфері азоту, до розчину 1-(трет-бутоксикарбоніламіно)циклопропанкарбонової кислоти (201,2 мг, 1,0 ммоль) у 4 мл ДМФА додають NaH (120,0 мг, 3,0 ммоль) при 0 C. Після 30 хвилин перемішування, йодетан (0,4 мл, 5,0 ммоль) додають до цієї реакційної суміші. Цю реакційну суміш нагрівають поступово до кімнатної температури та перемішують впродовж ночі. Реакційну суміш розподіляють між EtOAc та водою. Об’єднані органічні екстракти сушать (Na2SO4), та концентрують у вакуумі, що забезпечує одержання сирого етил 1-(третбутоксикарбоніл(етил)аміно)циклопропан-карбоксилату, який використовують на наступній стадії без додаткового очищення. Стадія 2: 1-(трет-бутоксикарбоніл(етил)аміно)циклопропанкарбонова кислота Сирий продукт зі Стадії 1 розчиняють у суміші EtOH (4,0 мл) та води (1,0 мл). LiOH (82,0 мг, 2,0 ммоль) додають до реакційної суміші. Реакційну суміш нагрівають при 120 °C у мікрохвильовому реакторі впродовж 10 хвилин. Реакційну суміш концентрують у вакуумі, та сирий продукт розподіляють між EtOAc та водою. Водний шар нейтралізують з 4N водн. HCl до pH 4 та потім екстрагують за допомогою EtOAc. Об’єднані органічні екстракти сушать (Na 2SO4), та концентрують у вакуумі, що забезпечує одержання 1-(третбутоксикарбоніл(етил)аміно)циклопропанкарбонової кислоти. Проміжна сполука 28 1-(трет-бутоксикарбоніл(етил)аміно)циклобутанкарбонова кислота O Boc N HO Стадія 1: Етил 1-(трет-бутоксикарбоніл(етил)аміно)циклобутанкарбоксилат У атмосфері азоту, до розчину 1-(трет-бутоксикарбоніламіно)циклобутанкарбонової кислоти (430,0 мг, 2,0 ммоль) у 4 мл ДМФА додають NaH (240,0 мг, 6,0 ммоль) при 0 °C. Після перемішування впродовж 30 хвил., до реакційної суміші додають йодетан (0,8 мл, 10,0 ммоль). Реакційну суміш нагрівають до кімнатної температури поступово та перемішують впродовж ночі. Реакційну суміш розподіляють між EtOAc та водою. Об’єднані органічні екстракти сушать (Na2SO4), та концентрують у вакуумі, що забезпечує одержання сирого етил 1-(третбутоксикарбоніл(етил)аміно)-циклобутан-карбоксилату. Стадія 2: 1-(трет-бутоксикарбоніл(етил)аміно)циклобутанкарбонова кислота Сирий продукт зі Стадії 1 розчиняють у EtOH (4,0 мл) та воді (1,0 мл). LiOH (164,0 мг, 4,0 ммоль) додають до цієї реакційної суміші. Реакційну суміш нагрівають при 120°C у мікрохвильовому реакторі впродовж 10 хвилин. Реакційну суміш концентрують у вакуумі, та сирий продукт розподіляють між EtOAc та водою. Водний шар нейтралізують з 4N водн. HCl до pH 4 та потім екстрагують за допомогою EtOAc. Об’єднані органічні екстракти сушать (Na 2SO4), та концентрують у вакуумі, що забезпечує одержання 1-(третбутоксикарбоніл(етил)аміно)циклобутанкарбонової кислоти. Проміжна сполука 29 27 UA 101057 C2 1-(трет-бутоксикарбоніл(метил)аміно)циклобутанкарбонова кислота O Boc N HO 5 10 15 20 25 30 35 40 45 Стадія 1: Метил 1-(трет-бутоксикарбоніл(етил)аміно)циклобутанкарбоксилат У атмосфері азоту, до розчину 1-(трет-бутоксикарбоніламіно)циклобутанкарбонової кислоти (430,0 мг, 2,0 ммоль) у 4 мл ДМФА додають NaH (240,0 мг, 6,0 ммоль) при 0 °C. Після перемішування впродовж 30 хвил., до реакційної суміші додають йодметан (0,62 мл, 10,0 ммоль). Реакційну суміш нагрівають до кімнатної температури поступово та перемішують впродовж ночі. Реакційну суміш розподіляють між EtOAc та водою. Об’єднані органічні екстракти сушать (Na2SO4), та концентрують у вакуумі, що забезпечує одержання сирого метил 1-(трет-бутоксикарбоніл(етил)аміно)-циклобутан-карбоксилату. Стадія 2: 1-(трет-бутоксикарбоніл(метил)аміно)циклобутанкарбонової кислоти Сирий продукт зі Стадії 1 розчиняють у MeOH (4,0 мл) та воді (1,0 мл). LiOH (164,0 мг, 4,0 ммоль) додають до реакційної суміші. Реакційну суміш нагрівають при 120 °C у мікрохвильовому реакторі впродовж 10 хвилин. Реакційну суміш концентрують у вакуумі, та сирий продукт розподіляють між EtOAc та водою. Водний шар нейтралізують за допомогою 4N водн. HCl до pH 4, та потім екстрагують за допомогою EtOAc. Об’єднані органічні екстракти сушать (Na2SO4), та концентрують у вакуумі, що забезпечує одержання 1-(третбутоксикарбоніл(метил)аміно)циклобутанкарбонової кислоти. Проміжна сполука 30 2-бромбутанамід O Br NH2 У атмосфері азоту, до розчину 2-броммасляної кислоти (2,0 г, 12,0 ммоль) у DCM (50 мл) при 0 °C поступово додають тіоніл-хлорид (2,6 мл, 35,9 ммоль) та 0,5 мл ДМФА. Реакційній суміші дають нагрітися до кімнатної температури та перемішують впродовж ночі. Реакційну суміш концентрують у вакуумі та потім охолоджують до 0 °C. Повільно додають тридцять (30) мл 37% водного розчину гідроксиду амонію. Реакційній суміші дають нагрітися до кімнатної температури та перемішують впродовж 2 годин, що супроводжують екстракцією з EtOAc. Об’єднані органічні екстракти сушать (Na 2SO4), та концентрують у вакуумі, що забезпечує одержання 2-бромбутанаміду. Проміжна сполука 31 2-бром-N-метилбутанамід O Br NH У атмосфері азоту, до розчину 2-броммасляної кислоти (2,0 г, 12,0 ммоль) у DCM (50 мл) при 0 °C поступово додають тіоніл-хлорид (2,6 мл, 35,9 ммоль) та 0,5 мл ДМФА. Реакційній суміші дають нагрітися до кімнатної температури та перемішують впродовж ночі. Реакційну суміш концентрують у вакуумі та потім охолоджують до 0 °C. Повільно додають тридцять (30) мл 40% водного розчину метиламіну. Реакційній суміші дають нагрітися до кімнатної температури та перемішують впродовж 2 годин, що супроводжують екстракцією з EtOAc. Об’єднані органічні екстракти сушать (Na 2SO4), та концентрують у вакуумі, що забезпечує одержання 2-бром-N-метилбутанаміду. Проміжна сполука 32 2-бром-N-етилбутанамід O Br N H У атмосфері азоту, до розчину 2-броммасляної кислоти (2,0 г, 12,0 ммоль) у DCM (50 мл) при 0 °C поступово додають тіоніл-хлорид (2,6 мл, 35,9 ммоль) та 0,5 мл ДМФА. Реакційній суміші дають нагрітися до кімнатної температури та перемішують впродовж ночі. Реакційну суміш концентрують у вакуумі та потім охолоджують до 0 °C. Повільно додають тридцять (30) 28
ДивитисяДодаткова інформація
Назва патенту англійськоюPyrimidine derivatives as kinase inhibitors
Автори англійськоюMarsilje III, Thomas H., Lu, Wenshuo, Chen, Bei, He, Xiaohui, Lee, Christian Cho-Hua, Jiang, Songchun, Yang, Kunyong
Назва патенту російськоюПроизводные пиримидина как ингибиторы киназы
Автори російськоюМарсилье ИИИ Томас Х., Лу Уэншуо, Чен Бей, Хи Ксяогуй, Ли Кристиан Чо-Хуа, Джианг Сонгчун, Янг Кунйонг
МПК / Мітки
МПК: C07D 403/12, A61K 31/506, C07D 413/14, C07D 403/14, C07D 401/14, C07D 409/14
Мітки: інгібітори, похідні, піримідину, кінази
Код посилання
<a href="https://ua.patents.su/178-101057-pokhidni-pirimidinu-yak-ingibitori-kinazi.html" target="_blank" rel="follow" title="База патентів України">Похідні піримідину як інгібітори кінази</a>
Попередній патент: Інгаляційний пристрій і спосіб дозованої подачі медикаменту
Наступний патент: Спосіб і пристрій для облагороджування деревинно-стружкової плити
Випадковий патент: Піддон двигуна внутрішнього згоряння