Бензолсульфонамідні сполуки, придатні для лікування розладів, які сприйнятливі до модуляції дофамінового рецептора d3
Номер патенту: 99628
Опубліковано: 10.09.2012
Автори: Бєспалов Антон, Брайє Вілфрід, Дрешер Карла, Ланге Удо, Хаупт Андреас, Йонген-Рело Ана Люсія, Тернер Шон Кольм, УНГЕР Ліліане
Формула / Реферат
1. N-(6-піперазин-1-ілпіридин-3-іл)бензолсульфонамідні сполуки формули І
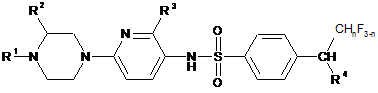 , (I)
, (I)
де
R1 вибраний із групи, яка складається з водню, лінійного С1-С3алкілу й фторованого лінійного С1-С3алкілу;
R2 являє собою водень або метил;
R3 вибраний із групи, яка складається з водню, галогену, С1-С2алкілу, фторованого С1-С2алкілу, С1-С2алкокси й фторованого С1-С2алкокси,
R4 являє собою С1-С2алкіл або фторований С1-С2алкіл;
n являє собою 0, 1 або 2;
і фізіологічно стійкі солі цих сполук і їх N-оксиди.
2. Сполука за п. 1, де R1 являє собою водень.
3. Сполука за п. 1 або 2, де R2 являє собою метил.
4. Сполука за п. 3, де атом вуглецю, який несе R2, має S-конфігурацію.
5. Сполука за п. 3, де атом вуглецю, який несе R2, має R-конфігурацію.
6. Сполука за п. 1 або 2, де R2 являє собою водень.
7. Сполука за будь-яким з попередніх пунктів, де R3 являє собою метил.
8. Сполука за будь-яким з попередніх пунктів, де R4 являє собою метил.
9. Сполука за п. 8, де атом вуглецю, який несе R4, має S-конфігурацію.
10. Сполука за п. 8, де атом вуглецю, який несе R4, має R-конфігурацію.
11. Сполука за будь-яким з попередніх пунктів, де n являє собою 1.
12. Сполука за будь-яким з попередніх пунктів, де n являє собою 2.
13. Сполука за п. 1, вибрана із групи, яка складається з:
4-(2-фтор-1-метилетил)-N-[2-метил-6-(3-метилпіперазин-1-іл)-піридин-3-іл]-бензолсульфонаміду,
4-((R)-2-фтop-1-метилетил)-N-[2-метил-6-((R)-3-метилпіперазин-1-іл)-піридин-3-іл]-бензолсульфонаміду,
4-((S)-2-фтор-1-метилетил)-N-[2-метил-6-((S)-3-метилпіперазин-1-іл)-піридин-3-іл]-бензолсульфонаміду,
4-((R)-2-фтор-1-метилетил)-N-[2-метил-6-((S)-3-метилпіперазин-1-іл)-піридин-3-іл]-бензолсульфонаміду,
4-((S)-2-фтор-1-метилетил)-N-[2-метил-6-((R)-3-метилпіперазин-1-іл)-піридин-3-іл]-бензолсульфонаміду,
4-(2-фтор-1-метилетил)-N-[2-метил-6-піперазин-1-ілпіридин-3-іл]-бензолсульфонаміду,
4-((R)-2-фтop-1-метилетил)-N-[2-метил-6-піперазин-1-ілпіридин-3-іл]-бензолсульфонаміду,
4-((S)-2-фтор-1-метилетил)-N-[2-метил-6-піперазин-1-ілпіридин-3-іл]-бензолсульфонаміду
і фізіологічно стійких солей цих сполук.
14. Сполука за п. 1, вибрана із групи, яка складається з:
4-(2,2-дифтор-1-метилетил)-N-(2-метил-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонаміду,
4-((S)-2,2-дифтор-1-метилетил)-N-(2-метил-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонаміду,
4-((R)-2,2-дифтор-1-метилетил)-N-(2-метил-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонаміду
і фізіологічно стійких солей цих сполук.
15. Сполука за п. 1, вибрана із групи, яка складається з:
4-(2,2,2-трифтор-1-метилетил)-N-(2-метил-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонаміду,
4-((R)-2,2,2-трифтор-1-метилетил)-N-(2-метил-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонаміду,
4-((S)-2,2,2-трифтор-1-метилетил)-N-(2-метил-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонаміду
і фізіологічно стійких солей цих сполук.
16. Сполука за п. 1, вибрана із групи, яка складається з:
4-(2-фтор-1-метилетил)-N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонаміду,
4-((R)-2-фтор-1-метилетил)-N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонаміду,
4-((S)-2-фтоp-l-метилетил)-N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонаміду,
4-(2,2-дифтор-1-метилетил)-N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонаміду,
4-((S)-2,2-дифтор-1-метилетил)-N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонаміду,
4-((R)-2,2-дифтор-1-метилетил)-N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонаміду,
N-(2-метокси-6-піпepaзин-1-ілпіридин-3-іл)-4-(2,2,2-трифтор-1-метилетил)-бензолсульфонаміду,
N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)-4-((S)-2,2,2-трифтор-1-метилетил)-бензолсульфонаміду,
N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)-4-((R)-2,2,2-трифтор-1-метилетил)-бензолсульфонаміду
і фізіологічно стійких солей цих сполук.
17. Фармацевтична композиція, яка містить щонайменше одну сполуку за будь-яким з пп. 1-16, необов'язково разом зі щонайменше одним фізіологічно прийнятним носієм або допоміжною речовиною.
18. Застосування сполуки за будь-яким з пп. 1-16 для одержання лікарського засобу.
19. Сполука за будь-яким з пп. 1-16 для застосування як лікарського засобу.
20. Застосування сполуки за будь-яким з пп. 1-16 для лікування медичного захворювання, що піддається лікуванню за допомогою ліганду дофамінового рецептора D3.
21. Застосування сполуки за будь-яким з пп. 1-16 для одержання лікарського засобу для лікування медичного захворювання, що піддається лікуванню за допомогою ліганду дофамінового рецептора D3.
22. Спосіб лікування медичних захворювань, що піддаються лікуванню за допомогою ліганду дофамінового рецептора D3, що включає введення ефективної кількості щонайменше однієї сполуки за будь-яким з пп. 1-16 суб'єкту, який потребує цього.
23. Спосіб лікування захворювання центральної нервової системи, що включає введення ефективної кількості щонайменше однієї сполуки за будь-яким з пп. 1-16 суб'єкту, який потребує цього.
24. Спосіб за п. 22 або 23, де медичне захворювання являє собою шизофренію.
25. Спосіб за п. 22 або 23, де медичне захворювання являє собою наркотичну залежність.
26. Спосіб за п. 22, де медичне захворювання являє собою діабетичну нефропатію.
27. Спосіб за п. 22 або 23, де медичне захворювання являє собою біполярний розлад.
28. Сполука формули IV
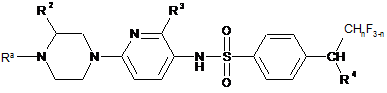 , (IV)
, (IV)
де Ra являє собою N-захисну групу, і де n, R2, R3 і R4 є такими, як визначено в пунктах 1-12.
Текст
Реферат: Винахід стосується сполук формули R 2 R 3 O N R 1 N N N H S O CHnF3-n CH R 4 , (I) 1 де R вибраний із групи, яка складається з водню, лінійного С 1-С3алкілу й фторованого 2 3 лінійного С1-С3алкілу; R являє собою водень або метил; R вибраний із групи, яка складається з водню, галогену, С1-С2алкілу, фторованого С1-С2алкілу, С1-С2алкокси й фторованого С14 С2алкокси, R являє собою С1-С2алкіл або фторований С1-С2алкіл; n являє собою 0, 1 або 2; і фізіологічно стійкі солі цих сполук і їх N-оксиди. Винахід також стосується фармацевтичної композиції, що містить щонайменше одну сполуку формули (І) і/або щонайменше одну її фізіологічно стійку кислотно-адитивну сіль, і способу лікування захворювань, які сприйнятливі до впливу антагоністів дофамінового рецептора D3 або UA 99628 C2 агоністів дофаміну D3, що включає введення ефективної кількості щонайменше однієї сполуки або фізіологічно стійкої кислотно-адитивної солі формули І суб'єкту, який потребує цього. UA 99628 C2 5 10 15 20 25 30 35 40 45 50 55 Даний винахід належить до нових N-(6-піперазин-1-ілпіридин-3-іл)бензолсульфонамідних сполук, зокрема, до сполук формули I, описаних у даному документі. Сполуки мають корисні терапевтичні властивості й придатні, зокрема, для лікування захворювань, які сприйнятливі до модуляції дофамінового рецептора D3. Нейрони одержують свою інформацію за допомогою, серед іншого, рецептора, сполученого з G-білком. Велика кількість речовин проявляє свій вплив за допомогою цих рецепторів. Одним з них є дофамін. Існують підтверджені дані щодо присутності дофаміну і його фізіологічного призначення як нейромедіатора. Розлади в дофамінергічній системі передачі приводять до захворювань центральної нервової системи, які включають, наприклад, шизофренію, депресію й хворобу Паркінсона. Ці захворювання й інші лікують за допомогою лікарських засобів, які взаємодіють із дофаміновими рецепторами. Аж до 1990 року, було чітко визначено фармакологічно два підтипи дофамінового рецептора, названі рецепторами D1 і D2. Пізніше, третій підтип був знайдений, а саме, рецептор D3, який, очевидно, опосередковує деякі ефекти нейролептичних і антипаркінсонічних лікарських засобів (J. C. Schwartz et al., "The Dopamine D3 Receptor as a Target for Antipsychotics" in Novel Antipsychotic Drugs, H. Y. Meltzer, ed., Raven Press, New York 1992, pages 135-144; M. Dooley et al., Drugs and Aging 1998, 12:495-514; J.N. Joyce, Pharmacology and Therapeutics 2001, 90:231-59, "The Dopamine D3 Receptor as a Therapeutic Target for Antipsychotic and Antiparkinsonian Drugs"). Після цього, дофамінові рецептори були розділені на два сімейства. З одного боку, існує група D2, що складається з рецепторів D2, D3 і D4, і, з іншого боку, група D1, що складається з рецепторів D1 і D5. У той час, як рецептори D1 і D2 широко розподілені, рецептори D3, очевидно, експресуються регіоселективно. Таким чином, ці рецептори переважно варто шукати в лімбічній системі й проекційних областях мезолімбічної дофамінової системи, особливо в прилеглому ядрі, але так само в інших областях, таких як мигдалевидна залоза. Завдяки цій відносно регіоселективній експресії, рецептори D3 розглядають як мета, що має декілька побічних ефектів, і допускають, що в той час, коли селективний ліганд D3 мав би властивості відомих нейролептичних лікарських засобів, він би не мав їх побічних неврологічних ефектів, опосередкованих дофаміновим рецептором D2 (P. Sokoloff et al., Arzneim. Forsch./Drug Res. 42(1):224 (1992), "Localization and Function of the D3 Dopamine Receptor"; P. Sokoloff et al., Nature, 347:146 (1990), "Molecular Cloning and Characterization of a Novel Dopamine Receptor (D 3) as a Target for Neuroleptics"). N-(6-Піперазин-1-ілпіридин-3-іл)бензолсульфонамідні сполуки, які мають афінність до дофамінового рецептора D3, були описані раніше на різних подіях, як, наприклад, в WO2004/089905. Ці сполуки мають високі афінності відносно дофамінового рецептора D 3, і, отже, були запропоновані як придатні для лікування захворювань центральної нервової системи. На жаль, їх селективність відносно рецептора D 3 не завжди є задовільною. Більш того, деякі із цих сполук мають незадовільний профіль DMPK (DMPK: метаболічна стабільність і/або фармакокінетика), і/або можуть проявляти серцево-судинні взаємодії. Отже, існує постійна потреба в забезпеченні новими сполуками, які мають поліпшену селективність відносно рецепторів D3 або поліпшений фармакологічний профіль, такий як профіль DMPK і/або можуть проявляти менші серцево-судинні взаємодії. В цей час було знайдено, що певні N-(6-піперазин-1-ілпіридин-3-іл)бензолсульфонамідні сполуки проявляють, з дивним і несподіваним ступенем, достатньо селективне зв'язування з дофаміновим рецептором D3, а так само задовільний профіль DMPK, зокрема, відносно метаболічної стабільності, і/або задовільний серцево-судинний профіль, тобто сполуки проявляють менші серцево-судинні взаємодії. Такими сполуками є сполуки, що мають загальну формулу I, їх фізіологічно стійкі солі і їх N-оксиди: , де 1 R вибраний із групи, яка складається з водню, лінійного C1-C3 алкілу й фторованого лінійного C1-C3 алкілу; 2 R являє собою водень або метил; 3 R вибраний із групи, яка складається з водню, галогену, C 1-C2-алкілу, фторованого C1-C2алкілу, C1-C2-алкокси й фторованого C1-C2-алкокси, 1 UA 99628 C2 4 5 10 15 20 25 30 35 40 45 50 55 R являє собою C1-C2-алкіл або фторований C1-C2-алкіл; і n являє собою 0, 1 або 2. Отже, даний винахід належить до N-(6-піперазин-1-ілпіридин-3-іл)бензолсульфонамідних сполук загальної формули I, а так само до їх фізіологічно стійких солей і до N-оксидів сполук I і їх фізіологічно стійких солей. Даний винахід так само належить до фармацевтичної композиції, що включає щонайменше одну N-(6-піперазин-1-ілпіридин-3-іл)бензолсульфонамідну сполуку формули I і/або щонайменше одну фізіологічно стійку сіль I і/або її N-оксид, де прийнятно разом з фізіологічно прийнятними носіями і/або допоміжними речовинами. Даний винахід так само належить до способу лікування розладів, які сприйнятливі до впливу антагоністів дофамінового рецептора D3 або агоністів дофаміну D3, що включає введення ефективної кількості щонайменше однієї N-(6-піперазин-1-ілпіридин-3-іл)бензолсульфонамідної сполуки формули I і/або щонайменше однієї фізіологічно стійкої кислотно-адитивної солі I і/або її N-оксиду суб'єкту, який потребує цього. Докладний опис даного винаходу Захворювання, які сприйнятливі до впливу антагоністів дофамінового рецептора D 3 або агоністів, включають розлади й захворювання центральної нервової системи, зокрема, емоційні потрясіння, нервові потрясіння, стресові потрясіння й соматоформні порушення й психози, і особливо шизофренію, депресію, біполярний розлад, наркотичну залежність і токсикоманію (яка так само називається наркоманією), слабоумство, великий депресивний розлад, занепокоєння, аутизм, дефіцитарний розлад уваги з або без підвищеної активності й розладом особистості. Крім того, D3-опосередковані захворювання можуть включати порушення функції нирки, зокрема, порушення функції нирки, які викликані діабетом, таким як цукровий діабет, який так само називається діабетичною нефропатією (дивися WO 00/67847). Відповідно до винаходу, одна або більше сполук загальної формули I, що мають значення, згадані спочатку, можуть бути використані для лікування вищезгаданих показань. У випадку, якщо сполуки формули I мають один або більше центрів асиметрії, так само можна використовувати енантіомерні суміші, зокрема, рацемічні, діастереомерні суміші й таутомерні суміші; переважними, однак, є відповідні по суті чисті енантіомери, діастереомери й таутомери. Подібним чином можна використовувати фізіологічно стійкі солі сполук формули I, особливо кислотно-адитивні солі з фізіологічно стійкими кислотами. Прикладами прийнятних фізіологічно стійких органічних і неорганічних кислот є хлористоводнева кислота, бромистоводнева кислота, фосфорна кислота, азотна кислота, сірчана кислота, органічні сульфонові кислоти, що мають від 1 до 12 атомів вуглецю, наприклад, C1-C4-алкілсульфонові кислоти, такі як метансульфонова кислота, циклоаліфатичні сульфонові кислоти, такі як S-(+)-10-камфорсульфонові кислоти й ароматичні сульфонові кислоти, такі як бензолсульфонова кислота й толуолсульфонова кислота, ди- і трикарбонові кислоти й гідроксикарбонові кислоти, що мають від 2 до 10 атомів вуглецю, такі як щавлева кислота, малонова кислота, малеїнова кислота, фумарова кислота, муцинова кислота, молочна кислота, винна кислота, лимонна кислота, гліколієва кислота й адипінова кислота, а так само цис- і транс-корична кислоти, фуранкарбонова кислота й бензойна кислота. Інші використовувані кислоти описані в Fortschritte der Arzneimittelforschung [Advances in Drug Research], Volume 10, pages 224 ff., Birkhauser Verlag, Basel and Stuttgart, 1966. Фізіологічно стійкі солі сполук формули I можуть бути присутніми у вигляді моно-, біс-, трис- і тетракіс-солей, тобто вони можуть містити 1, 2, 3 або 4 вищезгаданих молекул кислоти на молекулу формули I. Молекули кислоти можуть знаходитися у своїй кислотній формі або у вигляді аніону. Використовуваний у даному описі C1-C3 алкіл являє собою розгалужену або з нерозгалуженим ланцюгом алкільну групу, що містить 1, 2 або 3 атоми вуглецю. Прикладами таких груп є метильна, етильна, н-пропільна й ізопропільна. Використовуваний у даному описі фторований C 1-C3 алкіл являє собою розгалужену або з нерозгалуженим ланцюгом алкільну групу, що містить 1, 2 або 3 атоми вуглецю, де щонайменше один, наприклад, 1, 2, 3, 4 або 5, атом водню або всі атоми водню замінені атомами фтору. Прикладами таких груп є фторметильна, дифторметильна, трифторметильна, 2-фторетильная, 2,2-дифторетильна, 2,2,2-трифторетильна, 1,1,2,2-тетрафторетильна, 3,3,3трифторпропільна, 1-метил-2-фторетильна, 1-метил-2,2-дифторетильна, 1-метил-2,2,2трифторетильна і 1,1,1,3,3,3-гексафторпропан-2-ільна. Використовуваний у даному описі C1-C2 алкокси являє собою алкільну групу з нерозгалуженим ланцюгом, що містить 1 або 2 атоми вуглецю, який приєднаний до іншої молекули через атом кисню. Прикладами таких груп є метокси й етокси. 2 UA 99628 C2 5 10 15 20 25 30 35 40 45 50 55 60 Використовуваний у даному описі фторований C1-C2 алкокси являє собою алкоксигрупу як визначено вище, де щонайменше один, наприклад, 1, 2, 3, 4 або 5 атомів водню, замінений атомами фтору. Прикладами таких груп є фторметокси, дифторметокси, трифторметокси, 2фторетокси, 2,2-дифторетокси, 2,2,2-трифторетокси і 1,1,2,2-тетрафторетокси. Перший переважний варіант здійснення даного винаходу належить до сполук формули I, до 1 їх фармакологічно стійких солей і до їх N-оксидів, де R являє собою водень. Інший переважний варіант здійснення даного винаходу належить до сполук формули I, до їх 1 фармакологічно стійких солей і до їх N-оксидів, де R являє собою етил або н-пропіл. Додатковий переважний варіант здійснення даного винаходу належить до сполук формули I, 2 2 2 де R являє собою метил. У сполуках, де R являє собою метил, атом вуглецю, який несе R , створює хіральний центр. Таким чином, конкретний варіант здійснення даного винаходу 2 належить до сполук формули I, до їх фармакологічно стійких солей і до їх N-оксидів, де R являє 2 собою метил і де атом вуглецю, який несе R , має S-конфігурацію. Інший конкретний варіант здійснення даного винаходу належить до сполук формули I, до їх фармакологічно стійких солей 2 2 і до їх N-оксидів, де R являє собою метил і де атом вуглецю, який несе R , має R-конфігурацію. 2 Подібним чином переважними є суміші сполук, де атом вуглецю, який несе R , має Sконфігурацію або R-конфігурацію, відповідно. Ці суміші можуть містити однакові кількості або 2 неоднакові кількості сполуки I, що має R-конфігурацію щодо групи CH-R , і сполуки, що має S2 конфігурацію відносно CH-R . 2 Переважні суміші містять S-ізомер у надлишку або є енантіомерно чистими відносно CH-R . Термін "енантіомерно чистий" означає, що суміш містить відповідну сполуку в енантіомерному надлишку щонайменше 80 %, зокрема щонайменше 90 % (ee). Додатковий переважний варіант здійснення даного винаходу належить до сполук формули I, 2 до їх фармакологічно стійких солей і до їх N-оксидів, де R являє собою водень. Перевага віддана сполукам формули I, їх фармакологічно стійким солям і їх N-оксидам, де 3 R вибраний із групи, яка складається з водню, фтору, хлору, метилу, фторованого C1-алкілу, такого як трифторметил, метокси й фторованого C1-алкокси, такого як дифторметокси й 3 трифторметокси. Зокрема, R вибирають із водню, метилу або метокси. Особливо переважний варіант здійснення даного винаходу належить до сполук формули I, до їх фармакологічно 3 стійких солей і до їх N-оксидів, де R являє собою метил. Додатковий особливо переважний варіант здійснення даного винаходу належить до сполук формули I, до їх фармакологічно 3 стійких солей і до їх N-оксидів, де R являє собою метокси. Перевага віддана сполукам формули I, їх фармакологічно стійким солям і їх N-оксидам, де n являє собою 1. Особлива перевага віддана сполукам формули I, їх фармакологічно стійким солям і їх Nоксидам, де n являє собою 2. Перевага віддана сполукам формули I, їх фармакологічно стійким солям і їх N-оксидам, де 4 R являє собою C1-C2-алкіл, зокрема метил. У сполуках за даним винаходом атом вуглецю, який 4 несе R , створює хіральний центр. Таким чином, конкретний варіант здійснення даного винаходу належить до сполук формули I, до їх фармакологічно стійких солей і до їх N-оксидів, 4 4 де R являє собою C1-C2-алкіл, зокрема метил, і де атом вуглецю, який несе R , має Sконфігурацію. Інший конкретний варіант здійснення даного винаходу належить до сполук 4 формули I, до їх фармакологічно стійких солей і до їх N-оксидів, де R являє собою C1-C2-алкіл, 4 зокрема метил, і де атом вуглецю, який несе R , має R-конфігурацію. 4 Подібним чином переважними є суміші сполук, де атом вуглецю, який несе R , має Sконфігурацію або R-конфігурацію, відповідно. Ці суміші можуть містити однакові кількості або 2 неоднакові кількості сполуки I, що має R-конфігурацію щодо групи CH-R , і сполуки, що має S4 конфігурацію відносно CH-R . Переважні суміші містять один S-ізомер у надлишку або є 4 енантіомерно чистими відносно CH-R . Термін "енантіомерно чистий" означає, що суміш містить відповідну сполуку в енантіомерному надлишку щонайменше 80 %, зокрема щонайменше 90 % (ee). Особливо переважний варіант здійснення Ia винаходу належить до сполук формули I, до їх фармакологічно стійких солей і до їх N-оксидів, де 1 R являє собою водень; 2 R являє собою метил; 3 R вибраний із групи, яка складається із фтору, хлору, метилу, фторованого C 1-алкілу, такого як трифторметил, метокси й фторованого C1-алкокси, такого як дифторметокси й 3 трифторметокси, і де R являє собою, зокрема метил; 4 R являє собою C1-C2-алкіл, зокрема метил; і де змінна n являє собою 1. 3 UA 99628 C2 5 10 15 20 25 30 35 40 45 50 55 Додатковий особливо переважний варіант здійснення Ib винаходу належить до сполук формули I, до їх фармакологічно стійких солей і до їх N-оксидів, де 1 R являє собою водень; 2 R являє собою метил; 3 R вибраний із групи, яка складається із фтору, хлору, метилу, фторованого C 1-алкілу, такого як трифторметил, метокси й фторованого C1-алкокси, такого як дифторметокси й 3 трифторметокси, і де R являє собою, зокрема метил; 4 R являє собою C1-C2-алкіл, зокрема метил; і де змінна n являє собою 2. Додатковий особливо переважний варіант здійснення Ic винаходу належить до сполук формули I, до їх фармакологічно стійких солей і до їх N-оксидів, де 1 R являє собою водень; 2 R являє собою метил; 3 R вибраний із групи, яка складається із фтору, хлору, метилу, фторованого C 1-алкілу, такого як трифторметил, метокси й фторованого C1-алкокси, такого як дифторметокси й 3 трифторметокси, і де R являє собою, зокрема метил; 4 R являє собою C1-C2-алкіл, зокрема метил; і де змінна n являє собою 0. Сполуки варіантів здійснення Ia, Ib і Ic мають два хіральних центри й, таким чином, можуть існувати в чотирьох різних стереоізомерних формах, а саме у формі: 4 1. RR-сполуки, де обидва атом вуглецю, який несе радикал R , і атом вуглецю, який несе 2 радикал R , мають R-конфігурацію, 4 2. SS-сполуки, де обидва атом вуглецю, який несе радикал R , і атом вуглецю, який несе 2 радикал R , мають S-конфігурацію, 4 3. RS-сполуки, де атом вуглецю, який несе радикал R , має R-конфігурацію, у той час, коли 2 атом вуглецю, який несе радикал R , має S-конфігурацію, і 4 4. SR-сполуки, де атом вуглецю, який несе радикал R , має S-конфігурацію, у той час, як 2 атом вуглецю, який несе радикал R , має R-конфігурацію. Сполуки варіантів здійснення Ia, Ib і Ic можуть бути присутніми у вигляді діастереомерних сумішей, де RR-, SS-, RS- і SR-сполуки можуть бути присутніми у однакових або неоднакових кількостях, як енантіомерні (рацемічні або нерацемічні) суміші, тобто у вигляді суміші RRсполуки зі SS-сполукою або у вигляді суміші RS-сполуки зі SR-сполукою, а так само у формі чистих діастереомерів. Термін "чистий діастереомер" означає, що відповідний діастереомер складається зі щонайменше на 80 %, і особливо щонайменше на 90 % відповідної сполуки I, тобто інші діастереомери присутні в кількостях, менших ніж 20 %, зокрема, менших ніж 10 %, з розрахунку на загальну кількість сполуки I. Приклади сполук варіанта здійснення Ia включають 4-(2,2-Дифтор-1-метилетил)-N-[2-метил6-(3-метил-піперазин-1-іл)-піридин-3-іл]-бензолсульфонамід і їх фармакологічно стійкі солі. Ця сполука може бути присутньою у вигляді чистих стереоізомерів, а саме: 4-((R)-2,2-Дифтор-1-метилетил)-N-[2-метил-6-((R)-3-метил-піперазин-1-іл)-піридин-3-іл]бензолсульфонамід, 4-((S)-2,2-Дифтор-1-метилетил)-N-[2-метил-6-((S)-3-метил-піперазин-1-іл)-піридин-3-іл]бензолсульфонамід, 4-((R)-2,2-Дифтор-1-метилетил)-N-[2-метил-6-((S)-3-метил-піперазин-1-іл)-піридин-3-іл]бензолсульфонамід, або 4-((S)-2,2-Дифтор-1-метилетил)-N-[2-метил-6-((R)-3-метил-піперазин-1-іл)-піридин-3-іл]бензолсульфонамід, або як діастереомерні суміші RR-, SS-, RS- і SR-сполуки або у вигляді енантіомерної (рацемічної або нерацемічної) суміші RR-сполуки зі SS-сполукою або як суміш RS-сполуки зі SR-сполукою. Приклади сполук варіанта здійснення Ib включають 4-(2-Фтор-1-метилетил)-N-[2-метил-6-(3метил-піперазин-1-іл)-піридин-3-іл]-бензолсульфонамід і їх фармакологічно стійкі солі. Ця сполука може бути присутньою у вигляді чистих стереоізомерів, а саме: 4-((R)-2-Фтор-1-метилетил)-N-[2-метил-6-((R)-3-метил-піперазин-1-іл)-піридин-3-іл]бензолсульфонамід, 4-((S)-2-Фтор-1-метилетил)-N-[2-метил-6-((S)-3-метил-піперазин-1-іл)-піридин-3-іл]бензолсульфонамід, 4-((R)-2-Фтор-1-метилетил)-N-[2-метил-6-((S)-3-метил-піперазин-1-іл)-піридин-3-іл]бензолсульфонамід, або 4 UA 99628 C2 5 10 15 20 25 30 35 40 45 50 55 60 4-((S)-2-Фтор-1-метилетил)-N-[2-метил-6-((R)-3-метил-піперазин-1-іл)-піридин-3-іл]бензолсульфонамід, або у вигляді діастереомерних сумішей RR-, SS-, RS- і SR-сполуки або у вигляді енантіомерної (рацемічної або нерацемічної) суміші RR-сполуки зі SS-сполукою або як суміш RS-сполуки зі SR-сполукою. Приклади сполук варіанта здійснення Ic включають 4-(2,2,2-Трифтор-1-метилетил)-N-[2метил-6-(3-метил-піперазин-1-іл)-піридин-3-іл]-бензолсульфонамід і їх фармакологічно стійкі солі. Ця сполука може бути присутньою у вигляді чистих стереоізомерів, а саме: 4-((R)-2,2,2-Трифтор-1-метилетил)-N-[2-метил-6-((R)-3-метил-піперазин-1-іл)-піридин-3-іл]бензолсульфонамід, 4-((S)-2,2,2-Трифтор-1-метилетил)-N-[2-метил-6-((S)-3-метил-піперазин-1-іл)-піридин-3-іл]бензолсульфонамід, 4-((R)-2,2,2-Трифтор-1-метилетил)-N-[2-метил-6-((S)-3-метил-піперазин-1-іл)-піридин-3-іл]бензолсульфонамід, або 4-((S)-2,2,2-Трифтор-1-метилетил)-N-[2-метил-6-((R)-3-метил-піперазин-1-іл)-піридин-3-іл]бензолсульфонамід, або у вигляді діастереомерних сумішей RR-, SS-, RS- і SR-сполуки або у вигляді енантіомерної (рацемічної або нерацемічної) суміші RR-сполуки зі SS-сполукою або у вигляді суміші RS-сполуки зі SR-сполукою. Додатковий особливо переважний варіант здійснення Id винаходу належить до сполук формули I, до їх фармакологічно стійких солей і до їх N-оксидів, де 1 R являє собою водень; 2 R являє собою водень; 3 R вибраний із групи, яка складається із фтору, хлору, метилу, фторованого C 1-алкілу, такого як трифторметил, метокси й фторованого C1-алкокси, такого як дифторметокси й 3 трифторметокси, і де R являє собою, зокрема метил; 4 R являє собою C1-C2-алкіл, зокрема метил; і де змінна n являє собою 1. Додатковий особливо переважний варіант здійснення Ie винаходу належить до сполук формули I, до їх фармакологічно стійких солей і до їх N-оксидів, де 1 R являє собою водень; 2 R являє собою водень; 3 R вибраний із групи, яка складається із фтору, хлору, метилу, фторованого C 1-алкілу, такого як трифторметил, метокси й фторованого C1-алкокси, такого як дифторметокси й 3 трифторметокси, і де R являє собою, зокрема метил; 4 R являє собою C1-C2-алкіл, зокрема метил; і де змінна n являє собою 2. Додатковий особливо переважний варіант здійснення If винаходу належить до сполук формули I, до їх фармакологічно стійких солей і до їх N-оксидів, де 1 R являє собою водень; 2 R являє собою водень; 3 R вибраний із групи, яка складається із фтору, хлору, метилу, фторованого C 1-алкілу, такого як трифторметил, метокси й фторованого C1-алкокси, такого як дифторметокси й 3 трифторметокси, і де R являє собою, зокрема метил; 4 R являє собою C1-C2-алкіл, зокрема метил; і де змінна n являє собою 0. Сполуки варіантів здійснення Id, Ie і If можуть бути присутніми у вигляді рацемічних або нерацемічних сумішей R-енантіомера з S-енантіомером, а так само у формі чистого енантіомера. Термін "чистий енантіомер" означає, що відповідний енантіомер складається щонайменше на 80 %, і особливо щонайменше на 90 % відповідної сполуки I, тобто інший енантіомер є присутнім у кількостях, менших ніж 20 %, зокрема, менших ніж 10 %, з розрахунку на загальну кількість сполуки I. Приклади сполук варіанта здійснення Id включають 4-(2,2-Дифтор-1-метилетил)-N-[2-метил6-піперазин-1-ілпіридин-3-іл]-бензолсульфонамід і їх фармакологічно стійкі солі. Ця сполука може бути присутньою у вигляді чистих енантіомерів, а саме: 4-((R)-2,2-Дифтор-1-метилетил)-N-[2-метил-6-піперазин-1-ілпіридин-3-іл]бензолсульфонамід, 4-((S)-2,2-Дифтор-1-метилетил)-N-[2-метил-6-піперазин-1-ілпіридин-3-іл]бензолсульфонамід, або у вигляді суміші R- і S-енантіомера. 5 UA 99628 C2 5 10 15 20 25 30 35 40 45 Приклади сполук варіанта здійснення Id додатково включають 4-(2,2-Дифтор-1-метилетил)N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонамід і їх фармакологічно стійкі солі. Ця сполука може бути присутньою у вигляді чистих енантіомерів, а саме: 4-((R)2,2-Дифтор-1-метилетил)-N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)бензолсульфонамід, 4-((S)2,2-Дифтор-1-метилетил)-N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)бензолсульфонамід, або у вигляді суміші R- і S-енантіомера. Приклади сполук варіанта здійснення Ie включають 4-(2-Фтор-1-метилетил)-N-[2-метил-6піперазин-1-ілпіридин-3-іл]-бензолсульфонамід і їх фармакологічно стійкі солі. Ця сполука може бути присутньою у вигляді чистих енантіомерів, а саме: 4-((R)-2-Фтор-1-метилетил)-N-[2-метил-6-піперазин-1-ілпіридин-3-іл]-бензолсульфонамід, 4-((S)-2-Фтор-1-метилетил)-N-[2-метил-6-піперазин-1-ілпіридин-3-іл]-бензолсульфонамід, або у вигляді суміші R- і S-енантіомера. Приклади сполук варіанта здійснення Ie додатково включають 4-(2-Фтор-1-метилетил)-N-(2метокси-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонамід-бензолсульфонамід і їх фармакологічно стійкі солі. Ця сполука може бути присутньою у вигляді чистих енантіомерів, а саме: 4-((R)-2-Фтор-1-метилетил)-N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонамід, 4-((S)-2-Фтор-1-метилетил)-N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонамід, або у вигляді суміші R- і S-енантіомера. Приклади сполук варіанта здійснення If включають 4-(2,2,2-Трифтор-1-метилетил)-N-(2метил-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонамід і їх фармакологічно стійкі солі. Ця сполука може бути присутньою у вигляді чистих енантіомерів, а саме: 4-((R)-2,2,2-Трифтор-1-метилетил)-N-(2-метил-6-піперазин-1-ілпіридин-3-іл)бензолсульфонамід, 4-((S)-2,2,2-Трифтор-1-метилетил)-N-(2-метил-6-піперазин-1-ілпіридин-3-іл)бензолсульфонамід або у вигляді суміші R- і S-енантіомера. Приклади сполук варіанта здійснення If додатково включають N-(2-Метокси-6-піперазин-1ілпіридин-3-іл)-4-(2,2,2-трифтор-1-метилетил)-бензолсульфонамід і їх фармакологічно стійкі солі. Ця сполука може бути присутньою у вигляді чистих енантіомерів, а саме: N-(2-Метокси-6-піперазин-1-ілпіридин-3-іл)-4-((R)-2,2,2-трифтор-1-метилетил)бензолсульфонамід, N-(2-Метокси-6-піперазин-1-ілпіридин-3-іл)-4-((S)-2,2,2-трифтор-1-метилетил)бензолсульфонамід. Сполуки I за винаходом одержують за аналогією зі способами, відомими з літератури. Важливий підхід до сполук за винаходом пропонується реакцією 2-(піперазин-1-іл)-5амінопіридинової сполуки II з похідним бензолсульфонової кислоти III, як показано на схемі 1. Схема 1: 2 3 4 a На схемі 1, n, R , R і R мають раніше вказані значення. R являє собою захисну групу азоту або вибрана з лінійного C1-C3 алкілу й фторованого лінійного C1-C3 алкілу. Прийнятні N-захисні nd групи описані, наприклад, в PJ. Kocienski "Protecting Groups", 2 ed., Georg Thieme Verlag, Stuttgart 2000, pp 186-237 і у вказаній у даному документі літературі. Переважними прикладами N-захисних груп є, наприклад, оксикарбонільні групи, такі як C 1-C6-алкоксикарбонільна, наприклад, метоксикарбонільна, етоксикарбонільна й Boc (третбутоксикарбонільна) і інші оксикарбонільні групи, такі як бензилоксикарбонільна (Cbz), алілоксикарбонільна, 9 6 UA 99628 C2 5 10 15 20 25 30 35 40 флуоренілметоксикарбонільна (Fmoc) і 2-триметилсилілетоксикарбонільна (Teoc), або 2пропенільна (аліл). X являє собою нуклеофільно заміщувану відхідну групу зокрема, атом галогену й, особливо, хлору або брому. a Сполука формули IV, де R являє собою захисну групу азоту, зокрема, C1-C6алкоксикарбонільну групу, таку як метоксикарбонільну, етоксикарбонільну й Boc (третбутоксикарбонільна), є новими й таким чином так само утворюють частину даного винаходу. a Сполука формули IV, де R являє собою лінійний C1-C3 алкіл або фторований лінійний C1-C3 1 алкіл, належать до сполук I, де R являє собою лінійний C1-C3 алкіл або фторований лінійний C1-C3 алкіл. Реакція, вказана на схемі 1, проходить при умовах реакції, які загальноприйняті для одержання арилсульфонамідних сполук або арилсульфонових складних ефірів, відповідно, і, які описані, наприклад, в J. March, Advanced Organic Chemistry, 3rd edition, John Wiley & Sons, New York, 1985, p 444 і вказаної в даному документі літературі, European J. Org. Chem. 2002 (13), pp. 2094-2108, Tetrahedron 2001, 57 (27) pp. 5885-5895, Bioorganic and Medicinal Chemistry Letters, 2000, 10(8), pp. 835-838 and Synthesis 2000 (1), pp. 103-108. Реакцію звичайно проводять в інертному розчиннику, наприклад у простому ефірі, такому як діетиловий ефір, діізопропіловий ефір, метил-трет-бутиловий ефір або тетрагідрофуран, галогеновуглеводні, такому як дихлорметан, аліфатичному або циклоаліфатичному вуглеводні, такому як пентан, гексан або циклогексан, або ароматичному вуглеводні, такому як толуол, ксилен, кумол і подібних, або в суміші вищезгаданих розчинників. Реакцію сполуки II зі сполукою III звичайно проводять у присутності допоміжної основи. Прийнятними основами є неорганічні основи, такі як карбонат натрію або карбонат калію, або гідрокарбонат натрію або гідрокарбонат калію, і органічні основи, наприклад триалкіламіни, такі як триетиламін, або піридинові сполуки, такі як піридин, диметилпіридин і подібні. Останні зі згаданих сполук можна, у той же час, використовувати як розчинники. Допоміжні основи звичайно застосовують щонайменше в еквімолярних кількостях, з розрахунку на сполуку аміну II. a Реакція сполуки II зі сполукою III приводить до сполуки IV, з якої, у випадку, якщо R являє собою N-захисну групу, знімають захисну групу з одержанням сполуки загальної формули I, де 1 R являє собою водень. Зняття захисної групи сполуки IV може бути досягнуте за допомогою стандартними способами, наприклад, за допомогою способів описаних в PJ. Kocienski "Protecting Groups", 2nd ed., Georg Thieme Verlag, Stuttgart 2000, pp 186-237 і в вказаній у даному документі літературі. Загальноприйняті способи можуть бути потім використані для реакції цих 1 1 сполук із алкілуючим агентом R '-Z, в, якому R ' являє собою C1-C3-алкіл або фторований C1-C3алкіл, і Z являє собою нуклеофільно заміщувану відхідну групу (наприклад, галоген, такий як 1 хлор, бром або йод), з одержанням сполуки I, у якій R являє собою C1-C3-алкіл або фторований C1-C3-алкіл. Умови реакції, необхідні для цього, розкриті, наприклад, в WO 02/83652, Tetrahedron 2000, 56(38) pp. 7553-7560 і Synlett. 2000 (4), pp. 475-480. Сполуки загальної формули II самі по собі відомі або можуть бути отримані способом, показаним на схемі 2. Схема 2: a 45 50 55 2 3 На схемі 2, R , R , і R мають раніше вказані значення. Y являє собою нуклеофільно заміщувану відхідну групу зокрема, атом галогену, наприклад, хлор або бром, або алкілсульфонільну групу, наприклад, метилсульфоніл. Реакція, показана на стадії a) схеми 2, проходить при умовах реакції, які є загальноприйнятими для нуклеофільного заміщення на ароматичний радикал й, які описані, наприклад, в Tetrahedron 1999, 55(33), pp. 10243-10252, J. Med. Chem. 1997, 40(22), pp. 36793686 і Synthetic Communications, 1993, 23(5), pp. 591-599. За необхідністю, може бути вигідним перетворити кільцевий атом азоту в піридиновому кільці в його N-оксид (дивися, наприклад, Angew. Chem. Int. Ed. Engl., 2002 41(11), pp. 1937-1940, J. Med. Chem. 1985, 28(2), pp. 248-252 і Tetrahedron Lett. 2002 43(17) pp. 3121-3123). У зв'язку з наступним відновленням нітрогрупи в VII (стадія b), N-оксидна група так само відновлюється. Для цього, відновлення проводять, наприклад, у присутності солей індію. 7 UA 99628 C2 5 10 15 20 25 30 35 40 45 50 55 Якщо Y у сполуці VI являє собою бром, сполучення на стадії a) схеми 2 може так само бути досягнуте при каталізі на паладії в присутності допоміжної основи, наприклад карбонату лужного металу, такого як карбонат цезію. Особливо прийнятними паладієвими каталізаторами в цьому зв'язку є сполуки паладію (0) або сполуки паладію, які здатні утворити сполуки паладію (0) при умовах реакції, наприклад, дихлорид паладію, тетракіс(трифенілфосфін)паладій (0), трис(дибензиліденацетон)дипаладій (0), переважно в комбінації з фосфіновими лігандами, наприклад, триарилфосфіни, такі як трифенілфосфін, триалкіл-фосфіни, такі як трибутилфосфін, і циклоалкілфосфіни, такі як трицикло-гексилфосфін, і, особливо, використовуючи фосфінові хелатні ліганди, такі як 2,2'-біс(дифенілфосфіно)-1,1'-бінафтил. Умови, які є необхідними для реакцій цієї природи, описані, наприклад, в Tetrahedron Lett. 2001, 42(22), p. 3681 і Tetrahedron Lett. 2002, 43(12), pp. 2171-2173. На стадії b) нітрогрупу в сполуці VII відновлюють до NH 2 групи з одержанням сполуки II. Умови реакції, які є необхідними для стадії b), належать до загальноприйнятих умов для відновлення ароматичних нітрогруп, які широко були описані в літературі (дивися, наприклад, J. March, Advanced Organic Chemistry, 3rd ed., J. Wiley & Sons, New-York, 1985, p. 1183 і літературу, вказану в цьому посиланні). Відновлення може бути досягнуто, наприклад, за допомогою взаємодії нітросполуки VII за допомогою металу, такого як залізо, цинк або олово, при кислотних умовах реакції, тобто використовуючи водень, що утворюється, або використовуючи складний гідрид, такий як літійалюмогідрид або боргідрид натрію, переважно в присутності сполук перехідного металу нікелю або кобальту, таких як NiCl 2(P(феніл)3)2, або CoCl2,(дивися Ono et al. Chem. Ind. (London), 1983 p.480), або використовуючи NaBH 2S3 (дивися Lalancette et al. Can. J. Chem. 49, 1971, p. 2990), уможливлюючи проведення цих відновлень, залежно від конкретного реагенту, у речовині або в розчиннику або розріджувачі. З іншого боку, відновлення VII до II може бути проведене за допомогою водню в присутності каталізатора перехідного металу, наприклад, використовуючи водень у присутності каталізаторів, основаних на платині, паладію, нікелі, рутенії або родії. Каталізатори можуть містити перехідний метал в елементарній формі або у формі складної сполуки, солі або оксиду перехідного металу, уможливлюючи, для мети зміни активності, використання загальноприйнятих со-лігандів, наприклад, органічних фосфінових сполук, таких як трифенілфосфін, трициклогексилфосфін або три-н-бутилфосфіни або фосфіти. Каталізатор звичайно застосовують у кількостях від 0,001 до 1 моль на моль сполуки VII, розраховані на метал каталізатора. У переважному варіанті, відновлення здійснюють, використовуючи хлорид олова (II) за аналогією зі способами, описаними в Bioorganic and Medicinal Chemistry Letters, 2002, 12(15), pp. 1917-1919 і J. Med. Chem. 2002, 45(21), pp. 4679-4688. Реакцію VII із хлоридом олова (II) переважно проводять в інертному органічному розчиннику, переважно спирті, такому як метанол, етанол, ізопропанол або бутанол. N-оксиди сполуки формули I можуть бути отримані за допомогою обробки сполуки формули I окиснювальним агентом, зокрема, неорганічним або органічним пероксидом або гідропероксидом, таким як пероксид водню, або перкарбоновими кислотами, такими як надоцтова кислота, надбензойна кислота або м-хлорпербензойна кислота. Якщо не вказано іншого, вищеописані реакції в основному проводять у розчиннику при температурах між кімнатною температурою й температурою кипіння використовуваного розчинника. З іншого боку, енергія активації, що необхідна для реакції, може бути уведена в реакційну суміш, використовуючи мікрохвилі, деякі з яких, виявляється, мають значення, зокрема, у випадку, якщо реакції каталізуються за допомогою перехідних металів (щодо реакцій, що використовують мікрохвилі, дивися Tetrahedron 2001, 57, p. 9199 ff. p. 9225 ff., а так само, у загальному випадку, "Microwaves in Organic Synthesis", Andre Loupy (Ed.), Wiley-VCH 2002). Прикладами розчинників, які можуть бути використані, є прості ефіри, такі як діетиловий ефір, діізопропіловий ефір, метил-трет-бутиловий ефір або тетрагідрофуран, апротонні полярні розчинники, такі як диметилформамід, диметилсульфоксид, диметоксіетан і ацетонітрил, ароматичні вуглеводні, такі як толуол і ксилен, кетони, такі як ацетон або метилетилкетон, галогенвуглеводні, такі як дихлорметан, трихлорметан і дихлоретан, складні ефіри, такі як етилацетат і метилбутират, карбонові кислоти, такі як оцтова кислота або пропіонова кислота, і спирти, такі як метанол, етанол, н-пропанол, ізопропанол і бутанол. Якщо необхідно, можлива присутність основи, щоб нейтралізувати протони, які вивільняються в реакціях. Прийнятними основами включають неорганічні основи, такі як карбонат натрію, карбонат калію, гідрокарбонат натрію або гідрокарбонат калію, алкоксиди, такі як метоксид натрію або етоксид натрію, гідриди лужних металів, такі як гідрид натрію, органометалічні сполуки, такі як бутиллітієві сполуки або алкілмагнієві сполуки, і органічні азотні 8 UA 99628 C2 5 10 15 20 25 30 35 40 45 50 55 60 основи, такі як триетиламін або піридин. Останні зі згаданих сполук можна в той же час використовувати як розчинники. Сирий продукт виділяють загальноприйнятим способом, як, наприклад, за допомогою фільтрування, дистиляції розчинника або екстракцією з реакційної суміші, і т. д. Отримані сполуки можуть бути очищені загальноприйнятим способом, як, наприклад, за допомогою перекристалізації з розчинника, за допомогою хроматографії або за допомогою перетворення в кислотно-адитивну сіль. Кислотно-адитивні солі одержують загальноприйнятим способом за допомогою змішування вільної основи з відповідною кислотою, де прийнятно в розчині в органічному розчиннику як, наприклад, нижчому спирті, такому як метанол, етанол, н-пропанол або ізопропанол, простому ефірі, такому як метил-трет-бутиловий ефір або діізопропіловий ефір, кетоні, такому як ацетон або метилетилкетон, або складному ефірі, такому як етилацетат. Наприклад, вільна основа формули I і прийнятні кількості відповідної кислоти, такі як від 1 до 4 молів на моль формули I, розчинні в прийнятному розчиннику, переважно в нижчому спирті, такому як метанол, етанол, нпропанол або ізопропанол. Нагрівання може бути застосоване для розчинення твердих речовин, якщо необхідно. Розчинники, де кислотно-адитивна сіль I нерозчинна (антирозчинники), можуть бути додані для осадження солі. Прийнятні анти-розчинники включають C1C4-алкіл-складні ефіри C1-C4-аліфатичні кислоти, такі як етилацетат, аліфатичні й циклоаліфатичні вуглеводні, такі як гексан, циклогексан, гептан, і т. д., ді-C1-C4-алкіл-складні ефіри, такі як метил-трет-бутиловий ефір або діізопропіловий ефір. Частина або весь антирозчинник може бути доданий до гарячого розчину солі, і в такий спосіб отриманий розчин охолоджують; залишок анти-розчинника потім додають доти, поки концентрація солі в маточному розчині не буде низькою як приблизно 10 мг/л або нижче. Сполуки за винаходом формули I є вражаюче достатньо селективними лігандами дофамінового рецептора D3. Завдяки своїй низькій афінності стосовно інших рецепторів, таких як D1 рецептори, D4 рецептори, α1-адренорецептор і/або α2-адренорецептор, мускаринові рецептори, гістамінові рецептори, опіатні рецептори й, особливо, дофамінові рецептори D 2, можна очікувати, що сполуки викличуть менше побічних ефектів, ніж класичні нейролептики, які є антагоністами рецептора D2. Висока афінність сполук за винаходом відносно рецептора D3 виражається в дуже низьких значеннях Ki in-vitro в, як правило, менше ніж 60 нМ (нмоль/л), переважно менше ніж 30 нМ і, 125 зокрема, менше ніж 20 нМ. Заміщення [ I]йодосульпридом може, наприклад, бути використане у вивченнях зв'язування рецептора для визначення афінності зв'язування для рецептора D3. Селективність сполук за винаходом відносно D2 рецептора щодо рецептора D 3, виражена як Ki(D2)/Ki(D3), дорівнює, як правило щонайменше 20, переважно щонайменше 40. Заміщення 3 125 125 [ H]SCH23390, [ I]йодосульпридом або [ I]спіпероном може бути використане, наприклад, при проведенні досліджень зв'язування рецептора на D1, D2 і D4 рецепторах. Завдяки своєму профілю зв'язування дані сполуки можуть бути використані для лікування захворювань або розладів, які сприйнятливі до лігандів дофаміну D 3, тобто можна чекати, що вони повинні бути ефективними для лікування тих медичних розладів або захворювань, у яких прояв впливу (модулювання) на дофамінові рецептори D3 приводить до поліпшення клінічної картини або захворювання, яке лікується. Прикладами цих захворювань є розлади або захворювання центральної нервової системи. Під розладами або захворюваннями центральної нервової розуміються розлади, які діють на спинний мозок і, зокрема мозок. У межах значення винаходу, термін "розладів" означає порушення і/або аномалії, які, як правило, розглядають як патологічні стани або функції й, які можуть виявляти себе у вигляді особливих знаків, симптомів і/або дисфункцій. У той час, як лікування за винаходом може бути спрямоване на індивідуальний розлад, тобто аномалії або патологічні стани, так само можливо для деяких аномалій, які можуть бути причиною хвороби одне для одного, об'єднання в моделі хвороби або синдроми, які можуть бути вилікувані відповідно до винаходу. Розладами, які можуть бути вилікувані відповідно до винаходу, є, зокрема, психіатричні й неврологічні порушення. Ці порушення включають, зокрема, органічні порушення, включаючи симптоматичні порушення, такі як психози гострого екзогенного типу реакції або супутні психози органічної або екзогенної причини, як, наприклад, у зв'язку з метаболічними порушеннями, інфекціями й патологіями ендокринної системи; екзогенні психози, такі як шизофренія й шизотипні й ілюзорні порушення; емоційні потрясіння, такі як депресії, великий депресивний розлад, манія і/або маніакально-депресивні стани; змішані форми вищеописаних порушень; невропатичні й соматоформні порушення й так само порушення у зв'язку зі стресом; дисоційовані порушення, такі як втрата свідомості, потьмарення свідомості, роздвоєння 9 UA 99628 C2 5 10 15 20 25 30 35 40 45 50 55 свідомості й особистісні порушення; аутизм; порушення уваги й режиму неспання/сну, такі як поведінкові порушення й емоційні порушення, чия поява належить до дитинства і юності, як, наприклад, підвищена активність у дітей, розумові порушення, такі як порушення уваги (розлади, пов'язані з дефіцитом уваги з або без підвищеної активності), порушення пам'яті й когнітивні порушення, такі як порушення навчання й пам'яті (порушена когнітивна функція), слабоумство, наркоманія й порушення сну, такі як синдром втомлених ніг; порушення розвитку; стану занепокоєння; маревний стан; сексуальні порушення, такі як імпотенція в чоловіків; порушення харчування, такі як анорексія або булемія; залежність; біполярний розлад; і інші точно не встановлені психіатричні порушення. Розлади, які можуть бути вилікувані відповідно до винаходу, так само включають хворобу Паркінсона й епілепсію й, зокрема, емоційні потрясіння, пов'язані з нею. Так само лікуванню піддаються захворювання, що викликають залежність (наркотичну залежність і токсикоманію), тобто психічні розлади й поведінкові порушення, які викликані зловживанням психотропними речовинами, такими як фармацевтичні препарати або наркотики, і так само інші залежні поводження, такі як ігорна залежність і/або розлади контролю над спонуканнями, не віднесені до інших категорій. Приклади речовин, що викликають залежність, включають опіоїди, такі як морфін, героїн і кодеїн: кокаїн; нікотин; спирт; речовини, які взаємодіють із комплексом ГАМК - канал-переносник для іонів хлору; седативні засоби, снотворні засоби й транквілізатори, як, наприклад, бензодіазепіни; ЛСД; канабіноїди; психомоторні стимулятори, такі як 3,4-метилендіокси-N-метиламфетамін (екстазі); амфетамін і амфетамінподобні речовини, такі як метилфенідат; і інші стимулятори, включаючи кофеїн. Речовини, що викликають залежність, які особливо беруть до уваги, являють собою опіоїди, кокаїн, амфетамін або амфетаміноподібні речовини, нікотин і спирт. Щодо лікування захворювань, пов'язаних із залежністю, особлива перевага віддана тим сполукам за винаходом формули I, які самі по собі не мають який-небудь психотропний вплив. Це так само можна спостерігати в дослідженні, використовуючи щурів, які, після введення їм сполук, які можуть бути використані відповідно до винаходу, зменшили самостійне споживання психотропних речовин, наприклад кокаїну. Відповідно до іншого аспекту даного винаходу, сполуки за винаходом є придатними для лікування розладів, чиї причини можна щонайменше частково віднести до аномальної активності дофамінових рецепторів D3. Відповідно до іншого аспекту даного винаходу, лікування спрямоване, зокрема, на ті розлади, які можуть знаходитися під впливом, як раціональне медичне лікування, зв'язування партнерів (лігандів), що переважно вводяться екзогенно, які зв'язуються з дофаміновими рецепторами D3. Захворювання, які можуть бути вилікувані за допомогою сполук за винаходом, часто характеризують за допомогою прогресивного розвитку, тобто вищеописані стани міняються із часом; як правило, тяжкість зростає, і умови можуть, імовірно, накладатися одна на одну, або інші умови можуть з'являтися на додаток до уже існуючих. Сполуки за винаходом можуть бути використані для лікування великої кількості явищ, симптомів і/або дисфункцій, які пов'язані з розладами центральної нервової системи й, зокрема, з вищезгаданими станами. Ці явища, симптоми і/або дисфункції включають, наприклад, порушені відношення до реальності, відсутність адекватної самооцінки й здатності прийняти загальноприйняті суспільні норми або вимоги, поставлені життям, зміни темпераменту, зміни в самоврядуванні, такі як голод, сон, спрага й т. д., і в настрої, порушення в здатності спостерігати й поєднувати, зміни в особистості, зокрема, емоційна нестійкість, галюцинації, порушення еґо, стривоженість, роздвоєння почуттів, аутизм, деперсоналізація й помилкове сприйняття, ілюзорні ідеї, бубніння, відсутність спільного рефлекторного руху, ходьбу короткими кроками, вигнуте положення тулуба й кінцівок, тремор, відсутність міміки, монотонну мову, депресії, апатію, стиснуту безпосередність і рішучість, убогу асоціативну здатність, занепокоєння, нервове порушення, заїкуватість, суспільні фобії, панічні порушення, синдроми скасування у зв'язку із залежністю, експансивні синдроми, стани порушення й потьмарення свідомості, подавлений настрій, дискінетичні синдроми й тикові розлади, такі як хорея Гентінгтона й Синдром Жиля де ла Туретта, синдроми запаморочення, такі як периферичне позиційне, ротаційне й осцилююче запаморочення, меланхолію, істеричний невроз, іпохондрію й подібні. У межах значення винаходу, лікування так само включає профілактичне лікування (профілактику), зокрема, у вигляді повторної профілактики або періодичної профілактики, а так само лікування гострих або хронічних явищ, симптомів і/або дисфункцій. Лікування може бути зорієнтоване симптоматично, як, наприклад, для придушення симптомів. Воно може мати ефект 10 UA 99628 C2 5 10 15 20 25 30 35 40 45 50 55 60 протягом короткого періоду, бути зорієнтоване протягом середнього строку або може являти собою лікування протягом тривалого періоду, як, наприклад, у рамках підтримуючої терапії. Отже, сполуки за винаходом переважно придатні для лікування захворювань центральної нервової системи, зокрема, для лікування афективних розладів; нервових потрясінь, стресових потрясінь і соматоформних порушень і психозів, і, зокрема, для лікування шизофренії й біполярного розладу. Завдяки свій високій селективності відносно рецептора D 3, сполуки I за винаходом є так само придатними для лікування порушень функції нирки, зокрема, порушень функції нирки, які викликані діабетом (дивися WO 00/67847) і, особливо, діабетичною нефропатією. Крім того, сполуки за даним винаходом можуть мати інші фармакологічні і/або токсикологічні властивості, які роблять їх особливо придатними для розробки як фармацевтичних препаратів. Як приклад, очікується, що сполуки формули I, які мають низьку афінність відносно HERG рецептора, мають знижену ймовірність стимулювання QT-пролонгації (розглядають як один показник ризику, що викликає аритмію серця) (для обговорення QT-пролонгації дивися, наприклад, A. Cavalli et al., J. Med. Chem. 2002, 45:3844-3853 і вказану в даному документі літературу; аналіз HERG доступний платно в GENION Forschungsgesellschaft mbH, Hamburg, Germany). У рамках лікування, застосування відповідно до винаходу описаних сполук включає спосіб. У цьому способі ефективна кількість однієї або більше сполук, як правило, складена відповідно до фармацевтичної й ветеринарної практики, уводять індивідууму, якого необхідно лікувати, переважно ссавцеві, зокрема, людині, продуктивній тварині або свійській тварині. Чи показане таке лікування й у якій формі воно повинне мати місце, залежить від індивідуального випадку і являє собою предмет медичного обстеження (діагноз), що бере до уваги явища, симптоми і/або дисфункції, які присутні, ризики розвитку конкретних явищ, симптомів і/або дисфункцій, і інші фактори. Як правило, лікування здійснюють за допомогою однократного або повторюваного щодня введення, де прийнятно спільно, або при чергуванні, з іншими активними сполуками або препаратами, що містять активну сполуку, таким чином, щоб щоденну дозу переважно від приблизно 0,01 до 1000 мг/кг, більш переважно від 0,1 до 1000 мг/кг ваги тіла, у випадку перорального введення, або від приблизно 0,01 до 100 мг/кг, більш переважно від 0,1 до 100 мг/кг ваги тіла, у випадку парентерального введення, уводили індивідууму, якого необхідно лікувати. Винахід так само належить до одержання фармацевтичних композицій для лікування індивідуума, переважно ссавця й зокрема, людини, сільськогосподарської тварини або свійської тварини. Таким чином, сполуки звичайно вводять у формі фармацевтичної композиції, які включають фармацевтично прийнятний ексципієнт разом зі щонайменше однією сполукою за винаходом й, де прийнятно, іншими активними сполуками. Ці композиції можна, наприклад, уводити перорально, ректально, вагінально, трансдермально, підшкірно, внутрішньовенно, внутрішньом'язово або через ніс. Прикладами прийнятних фармацевтичних складів є тверді медичні форми, такі як порошки, гранули, таблетки (зокрема, таблетки, покриті плівковою оболонкою), таблетки для розсмоктування, саше, капсули для прийому ліків, таблетки, покриті цукром, капсули, такі як тверді желатинові капсули й м'які желатинові капсули; супозиторії або вагінальні медичні форми; напівтверді медичні форми, такі як мазі, креми, гідрогелі, пасти або гіпс; і так само рідкі медичні форми, такі як розчини, емульсії (зокрема, емульсії масло-в-воді), суспензії, такі як лосьйони, препарати для введення й препарати для інфузії, і краплі в ніс і краплі для вух. Імплантовані спускові пристрої так само можуть бути використані для введення інгібіторів за винаходом. Крім того, так само можна використовувати ліпосоми або мікросфери. При одержанні композицій, сполуки за винаходом звичайно змішують або розбавляють ексципієнтом. Ексципієнти можуть являти собою тверді, напівтверді або рідкі матеріали, які використовують як засоби для перенесення, носіїв або середовища для активної сполуки. Прийнятні ексципієнти перераховані в медичних монографіях фахівців. Крім того, склади можуть включати фармацевтично прийнятні носії або загальноприйняті допоміжні речовини, такі як речовини, що сприяють ковзанню; змочувальні агенти; емульгуючі й суспендуючі агенти; консерванти; антиоксиданти; антиподразники; хелатуючі агенти; покривні допоміжні речовини; стабілізатори емульсії; плівкоутворювачі; гелеутворювачі; агенти, що маскують запах; поліпшувачі смаку; смолу; гідроколоїди; розчинники; солюбілізатори; нейтралізуючі агенти; прискорювачі дифузії; пігменти; сполуки четвертинного амонію; повторно знежирювальні і пережирювальні агенти; сирі матеріали для мазей, кремів або масел; силіконові похідні; допоміжні речовини, що розподіляються; стабілізатори; стерилізуючі засоби; супозиторні 11 UA 99628 C2 5 10 15 20 25 30 35 40 45 основи; допоміжні речовини для таблетки, такі як зв'язувальні речовини, наповнювачі, речовини, що сприяють ковзанню, розпушувачі або покриття; пропеленти; осушувальні речовини; замутнювачі; загусники; воски; пластифікатори й білі мінеральні масла. Склад у цьому зв'язку оснований на знанні фахівця, як описано, наприклад, в Fiedler, H. P., Lexikon der Hilfsstoffe fur Pharmazie, Kosmetik und angrenzende Gebiete [Encyclopedia of auxiliary substances for pharmacy, cosmetics and related fields], 4th edition, Aulendorf: ECV-Editio-Kantor-Verlag, 1996. Наступні приклади служать для пояснення винаходу без його обмеження. Сполуки характеризували або через протонний ЯМР в d6-диметилсульфоксиді або dхлороформі на ЯМР приладі (Bruker AVANCE) при 400 MHz або 500 MHz, або за допомогою мас-спектрометрії, в основному записаній через ВЕРХ-МС у швидкому градієнті на C18матеріалі (режим електророзпилювальної іонізації (ESI)), або по температурі плавлення. Спектральні властивості магнітного ядерного резонансу (ЯМР) належать до хімічних 1 зрушень (δ), виражених у мільйонних частках (м. ч.). Відносна площа зрушень в H ЯМР спектрі відповідає числу атомів водню для конкретного функціонального типу в молекулі. Природа зрушення, що стосується мультиплетності, вказана як синглет (с), уширений синглет (уш.с), дублет (д), уширений дублет (уш.д), триплет (т), уширений триплет (уш.т), квартет (кв), квінтет (квін) і мультиплет (м). Приклади одержання: I. Одержання проміжної сполуки IV Приклад одержання 1: третбутиловий ефір ((R)-4-{5-[4-((S)-2-Фтор-1-метилетил)бензолсульфоніл-аміно]-6-метилпіридин-2-іл}-2-метилпіперазин-1-карбонової кислоти 1.1 (R)-2-Метил-4-(6-метил-5-нітропіридин-2-іл)-піперазин 0,72 г (R)-2-метилпіперазину (4,17 ммоль) розчиняли в 10 мл N, N-диметилформаміду. Додавали 1,165 г карбонату калію (8,43 ммоль) і 0,44 г 6-хлор-2-метил-3-нітропіридину, і суміш перемішували протягом 16 год. при кімнатній температурі. Розчинник упарювали при зниженому тиску, і залишок розділяли між водою й діетиловим ефіром. Водний шар екстрагували за допомогою діетилового ефіру, і об'єднані органічні фази промивали водою, сушили над сульфатом натрію, фільтрували, і фільтрат упарювали досуха з одержанням 0,85 г вказаної в заголовку сполуки. + ESI-МС: 237,1 [M+Н] 1.2 Третбутиловий ефір (R)-2-метил-4-(6-метил-5-нітропіридин-2-іл)-піперазин-1-карбонової кислоти 0,85 г (R)-2-метил-4-(6-метил-5-нітропіридин-2-іл)-піперазину (3,6 ммоль) розчиняли в 12 мл тетрагідрофурану. Додавали розчин 0,775 г дитретбутилдикарбонату (0,355 ммоль) в 3 мл тетрагідрофурану й 1,5 мл триетиламіну. Суміш перемішували протягом 3 год. при кімнатній температурі, розчинник упарювали, і залишок повторно розчиняли в діетиловому ефірі, і розчин промивали двічі за допомогою розведеного водного розчину хлориду амонію. Органічну фазу сушили над сульфатом натрію, фільтрували, і фільтрат упарювали досуха з одержанням 1,2 г вказаного в заголовку продукту. + ESI-МС: 337,1 [M+Н] 1.3 третбутиловий ефір (R)-2-метил-4-(6-метил-5-амінопіридин-2-іл)-піперазин-1-карбонової кислоти 1,2 г третбутилового ефіру (R)-2-метил-4-(6-метил-5-нітропіридин-2-іл)-піперазин-1карбонової кислоти (3,57 ммоль) розчиняли в 20 мл етилацетату. Додавали 10 % Pd на вуглеці 12 UA 99628 C2 5 10 15 20 25 30 35 40 й 3 мл оцтової кислоти, і суміш гідрували протягом 4 год. при 50ºC до завершення. Каталізатор відфільтровували, і фільтрат упарювали досуха. Залишок обробляли водою, і pH доводили до pH 8-9 за допомогою 1 N водного розчину гідроксиду натрію. Водну фазу екстрагували двічі за допомогою дихлорметану, органічні екстракти сушили над сульфатом натрію, фільтрували, і фільтрат упарювали досуха. Сирий продукт очищали за TM допомогою хроматографії на силікагелі, використовуючи прилад ISCO Companion (дихлорметан-етилацетат 0-50 %) з одержанням 0,88 г вказаного в заголовку продукту. + ESI-МС: 307,2 [M+Н] 1.4 третбутиловий ефір (R)-4-{5-[4-((S)-2-Фтор-1-метилетил)-бензолсульфоніламіно]-6метилпіридин-2-іл}-2-метилпіперазин-1-карбонової кислоти 0,105 г третбутилового ефіру (R)-2-метил-4-(6-метил-5-амінопіридин-2-іл)-піперазин-1карбонової кислоти (0,34 ммоль) і 0,085 г ((S)-2-фтор-1-метилетил)-бензолсульфонілхлориду (0,36 ммоль) розчиняли в 5 мл піридину, і розчин перемішували протягом 1 год. при кімнатній температурі. Розчинник упарювали при зниженому тиску, залишок обробляли за допомогою діетилового ефіру. Органічні фази згодом промивали двічі за допомогою розведеного водного хлориду амонію й водою. Органічну фазу сушили над сульфатом натрію, фільтрували, і розчинник упарювали при зниженому тиску. Сирий продукт очищали за допомогою хроматографії на силікагелі, використовуючи хроматографічну систему ISCO Companion (циклогексан-етилацетат 15-40 %) з одержанням 0,162 г продукту. + ESI-МС: 507,2 [M+Н] Приклад одержання 2: третбутиловий ефір (S)-4-{5-[4-((S)-2-фтор-1-метилетил)бензолсульфоніламіно]-6-метилпіридин-2-іл}-2-метилпіперазин-1-карбонової кислоти 2.1 (S)-2-Метил-4-(6-метил-5-нітропіридин-2-іл)-піперазин 0,72 г (S)-2-метил-4-(6-метил-5-нітропіридин-2-іл)-піперазин одержували як описано в прикладі одержання 1,1 для синтезу (R)-2-метил-4-(6-метил-5-нітропіридин-2-іл)-піперазину. + ESI-МС: 237,1 [M+Н] 1 H-ЯМР (CDCl3, 400 Гц): δ [м.ч.] 8,2 (д, 1Н), 6,45 (д, 1Н), 4,3-4,45 (м, 2H), 3,1 (м, 1Н), 3,0 (м, 1Н), 2,7-2,95 (м, 2H), 2,75 (с, 3H), 2,65 (м, 1Н), 1,15 (с, 3H). 2.2 Третбутиловий ефір (S)-2-метил-4-(6-метил-5-нітропіридин-2-іл)-піперазин-1-карбонової кислоти 1,13 г третбутилового ефіру (S)-2-метил-4-(6-метил-5-нітропіридин-2-іл)-піперазин-1карбонової кислоти одержували як описано в прикладі одержання 1,2 для синтезу третбутилового ефіру (R)-2-метил-4-(6-метил-5-нітропіридин-2-іл)-піперазин-1-карбонової кислоти. + ESI-МС: 337,2 [M+Н] 2.3 третбутиловий ефір (S)-2-метил-4-(6-метил-5-амінопіридин-2-іл)-піперазин-1-карбонової кислоти 13 UA 99628 C2 5 10 15 20 1,13 г третбутилового ефіру (S)-2-метил-4-(6-метил-5-нітропіридин-2-іл)-піперазин-1карбонової кислоти (3,36 ммоль) розчиняли в 65 мл метанолу й 5 мл етилацетату, і розчин TM піддавали гідруванню в H-cube (Thalos Ltd.) при 40ºC (швидкість потоку 1 мл/хв). Розчинники видаляли при зниженому тиску, і залишок очищали за допомогою хроматографії на силікагелі, TM використовуючи прилад ISCO Companion (дихлорметан-етилацетат 0-45 %) з одержанням 0,58 г вказаного в заголовку продукту. + ESI-МС: 307,2 [M+Н] 2.4 Третбутиловий ефір (S)-4-{5-[4-((S)-2-фтор-1-метилетил)-бензолсульфоніламіно]-6метилпіридин-2-іл}-2-метилпіперазин-1-карбонової кислоти 0,105 г третбутилового ефіру (S)-2-метил-4-(6-метил-5-амінопіридин-2-іл)-піперазин-1карбонової кислоти (0,34 ммоль) і 0,085 г ((S)-2-фтор-1-метилетил)-бензолсульфонілхлориду (0,36 ммоль) розчиняли в 5 мл піридину, і розчин перемішували протягом 1 год. при кімнатній температурі. Розчинник упарювали при зниженому тиску, залишок обробляли за допомогою діетилового ефіру. Органічні фази згодом промивали двічі за допомогою розведеного водного хлориду амонію й водою. Органічну фазу сушили над сульфатом натрію, фільтрували, і розчинник упарювали при зниженому тиску. Сирий продукт очищали за допомогою хроматографії на силікагелі, використовуючи хроматографічну систему ISCO Companion (циклогексан-етилацетат 15-40 %) з одержанням 0,162 г продукту. + ESI-МС: 507,2 [M+Н] Приклад одержання 3: третбутиловий ефір (S)-4-{5-[4-((R)-2-фтор-1-метилетил)бензолсульфоніламіно]-6-метилпіридин-2-іл}-2-метилпіперазин-1-карбонової кислоти 30 Сполуку одержували як описано для синтезу третбутилового ефіру (S)-4-{5-[4-((S)-2-фтор-1метилетил)-бензолсульфоніламіно]-6-метилпіридин-2-іл}-2-метилпіперазин-1-карбонової кислоти в прикладі одержання 2,4 з одержанням 0,194 г продукту. + ESI-МС: 507,2 [M+Н] Приклад одержання 4: третбутиловий ефір ефір 4-{5-[4-((S)-2-фтор-1-метилетил)бензолсульфоніламіно]-6-метилпіридин-2-іл}-піперазин-1-карбонової кислоти 4.1 третбутиловий ефір 4-(6-метил-5-амінопіридин-2-іл)-піперазин-1-карбонової кислоти 35 Вказану в заголовку сполуку одержували за аналогією зі способами, описаними в прикладах одержання з 1.1 по 1.3 4.2 третбутиловий ефір 4-{5-[4-((S)-2-фтор-1-метилетил)-бензолсульфоніламіно]-6метилпіридин-2-іл}-піперазин-1-карбонової кислоти 25 40 Сполуку одержували як описано для синтезу третбутилового ефіру (S)-4-{5-[4-((S)-2-фтор-1метилетил)-бензолсульфоніламіно]-6-метилпіридин-2-іл}-2-метилпіперазин-1-карбонової кислоти в прикладі одержання 2.4. + ESI-МС: 493,2 [M+Н] Приклад одержання 5: третбутиловий ефір 4-{5-[4-((R)-2-фтор-1-метилетил)бензолсульфоніламіно]-6-метилпіридин-2-іл}-піперазин-1-карбонової кислоти 14 UA 99628 C2 5 10 15 20 25 30 35 40 Сполуку одержували як описано для синтезу третбутилового ефіру (S)-4-{5-[4-((S)-2-фтор-1метилетил)-бензолсульфоніламіно]-6-метилпіридин-2-іл}-2-метилпіперазин-1-карбонової кислоти в прикладі одержання 2.4. + ESI-МС: 493,2 [M+Н] Приклад одержання 6: третбутиловий ефір (R)-4-{5-[4-((R)-2-фтор-1-метилетил)бензолсульфоніламіно]-6-метилпіридин-2-іл}-2-метилпіперазин-1-карбонової кислоти. Сполуку одержували як описано для синтезу третбутилового ефіру (S)-4-{5-[4-((S)-2-фтор-1метилетил)-бензолсульфоніламіно]-6-метилпіридин-2-іл}-2-метилпіперазин-1-карбонової кислоти в прикладі одержання 2,4. + ESI-МС: 507,2 [M+Н] Приклад одержання 7: третбутиловий ефір 4-{5-[4-(2,2-дифтор-1-метилетил)бензолсульфоніламіно]-6-метилпіридин-2-іл}-піперазин-1-карбонової кислоти 450 мг, вихід 86 %. II. Одержання сполук I Приклад 1: 4-((S)-2-Фтор-1-метилетил)-N-[2-метил-6-((S)-3-метилпіперазин-1-іл)-піридин-3іл]-бензолсульфонамід 0,162 г третбутилового ефіру (S)-4-{5-[4-((S)-2-фтор-1-метилетил)-бензолсульфоніламіно]-6метилпіридин-2-іл}-2-метилпіперазин-1-карбонової кислоти (0,32 ммоль) розчиняли в 5 мл дихлорметану. До розчину додавали 1,5 мл 6N хлористоводневої кислоти в ізопропанолі. Суміш перемішували протягом 16 год. при кімнатній температурі, і розчинник упарювали. Залишок розбавляли водою, і розчин доводили до pH 8-9 за допомогою насиченого водного бікарбонату натрію. Суміш екстрагували три рази за допомогою діетилового ефіру. Об'єднані органічні шари промивали водою, сушили над сульфатом натрію, фільтрували, і розчинник упарювали при зниженому тиску. Сирий продукт обробляли за допомогою 0,3 мл ацетонітрилу (що містить 0,1 % трифтороцтової кислоти) і 0,3 мл ацетонітрил/вода (що містить 0,1 % трифтороцтової кислоти). Осад, що утворився, збирали, промивали за допомогою ацетонітрил/вода 1:1 і сушили з одержанням 0,025 г вказаного в заголовку продукту. + ESI-МС: 407,2 [M+Н] 1 H-ЯМР (CDCl3, 400 Гц): δ [м.ч.] 7,7 (д, 2H), 7,4 (д, 2H), 7,3 d, 1Н), 6,4 (д, 1Н), 4,55 (м, 1Н), 4,4, (м, 1Н), 4,1 (т, 2H), 3,15 (м, 1Н), 3,1 (м, 1Н), 2,7-2,95 (небагато м, 3H), 2,4 (т, 1Н), 2,0 (с, 3H), 1,3 (д, 3H), 1,1 (д, 3H). Приклад 2: 4-((R)-2-Фтор-1-метилетил)-N-[2-метил-6-((S)-3-метилпіперазин-1-іл)-піридин-3іл]-бензолсульфонамід 0,194 г третбутилового ефіру (S)-4-{5-[4-((R)-2-фтор-1-метилетил)-бензолсульфоніламіно]-6метилпіридин-2-іл}-2-метилпіперазин-1-карбонової кислоти (0,38 ммоль) розчиняли в 5 мл дихлорметану. До розчину додавали 1,5 мл 6N хлористоводневої кислоти в ізопропанолі. Суміш перемішували протягом 16 год. при кімнатній температурі, і розчинник упарювали. Залишок розбавляли водою, і розчин доводили до pH 8-9 за допомогою насиченого водного бікарбонату натрію. Суміш екстрагували три рази за допомогою діетилового ефіру. Об'єднані органічні шари 15 UA 99628 C2 5 10 15 20 25 30 35 40 45 50 55 60 промивали водою, сушили над сульфатом натрію, фільтрували, і розчинник упарювали при зниженому тиску з одержанням 0,128 г вказаного в заголовку продукту. + ESI-МС: 407,2 [M+Н] 1 H-ЯМР (CDCl3, 400 Гц): δ [м.ч.] 7,7 (д, 2H), 7,4 (д, 2H), 7,3 д, 1Н), 6,4 (д, 1Н), 4,55 (м, 1Н), 4,4, м, 1Н), 4,1 (т, 2H), 3,15 (м, 1Н), 3,1 (м, 1Н), 2,7-2,95 (трохи м, 3H), 2,4 (т, 1Н), 2,0 (с, 3H), 1,3 (д, 3H), 1,1 (д, 3H). Якщо не вказано іншого, сполуки наступних прикладів з 3 по 18 одержували за допомогою за аналогією зі способами, розкритими в прикладах 1 і 2. Приклад 3: 4-((R)-2-Фтор-1-метилетил)-N-[2-метил-6-((R)-3-метилпіперазин-1-іл)-піридин-3іл]-бензолсульфонамід Приклад 4: 4-((S)-2-Фтор-1-метилетил)-N-[2-метил-6-((R)-3-метилпіперазин-1-іл)-піридин-3іл]-бензолсульфонамід Приклад 5: 4-((R)-2-Фтор-1-метилетил)-N-[2-метил-6-піперазин-1-ілпіридин-3-іл]бензолсульфонамід + 100 мг, вихід 99 %.ESI-МС: 393,1 [M+Н] 1 H-ЯМР (ДМСО-d6, 400 Гц): δ [м.ч.] 1,24 (д, 3H), 1,98 (с, 3H), 3,16 (м, 4H), 3,23 (м, 1Н), 3,67 (м, 4H), 4,48 (д, 1Н), 4,60 (д, 1Н), 6,66 (д, 1Н), 7,12 (д, 1Н), 7,50 (д, 2H), 7,60 (д, 2H), 9,00 (уш. с, 1Н), 9,43 (с, 1Н). Приклад 6: 4-((S)-2-Фтор-1-метилетил)-N-[2-метил-6-піперазин-1-ілпіридин-3-іл]бензолсульфонамід + 460 мг, вихід 99 %.ESI-МС: 393,1 [M+Н] 1 H-ЯМР (ДМСО-d6, 400 Гц): δ [м.ч.] 1,24 (д, 3H), 1,98 (с, 3H), 3,16 (м, 4H), 3,23 (м, 1Н), 3,67 (м, 4H), 4,48 (д, 1Н), 4,60 (д, 1Н), 6,66 (д, 1Н), 7,12 (д, 1Н), 7,50 (д, 2H), 7,60 (д, 2H), 9,00 (уш. с, 1Н), 9,43 (с, 1Н). Приклад 7 (порівняльний): N-(5-Бром-2-метил-6-піперазин-1-ілпіридин-3-іл)-4-((S)-2-фтор-1метилетил)-бензолсульфонамід Третбутиловий ефір 4-{5-[4-((S)-2-фтор-1-метилетил)-бензолсульфоніламіно]-6метилпіридин-2-іл}-піперазин-1-карбонової кислоти (370 мг, 0,754 ммоль) розбавляли в ацетонітрилі (3 мл) і додавали N-бромсукцинімід (201 мг, 1,13 ммоль). Отриманий розчин нагрівали при 80ºC при мікрохвильовому випромінюванні протягом 35 хвилин. Охолоджений розчин потім розділяли між розчином NaHCО3 і дихлорметаном. Органічний шар відділяли, сушили (MgSO4), фільтрували й очищали за допомогою колонкової хроматографії з одержанням бажаного продукту. Жовта тверда речовина. Кількість 135 мг. Вихід 38 %. Характеризували у вигляді солі НСl: + ESI-МС: 473,1, 471,1 [M+Н] 1 H-ЯМР (CDCl3, 400 Гц): δ [м.ч.] 1,24 (д, 3H), 2,02 (с, 3H), 3,18 (м, 4H), 3,25 (м, 1Н), 3,40 (м, 4H), 4,52 (дд, 2H), 7,39 (с, 1Н), 7,54 (д, 2H), 7,67 (д, 2H), 9,15 (уш. с, 2H), 9,85 (с, 1Н). Приклад 8: 4-(2,2-Дифтор-1-метилетил)-N-(2-метил-6-піперазин-1-ілпіридин-3-іл)бензолсульфонамід + 420 мг, вихід 99 %. ESI-МС: 41 1,1 [M+Н] 1 H-ЯМР (CD3OD, 400 Гц): δ [м.ч.] 1,38 (д, 3H), 2,00 (с, 3H), 3,28 (м, 5H), 3,79 (м, 4H), 5,97 (тд, 1Н), 6,63 (д, 1Н), 7,22 (д, 1Н), 7,50 (д, 2H), 7,64 (д, 2H). Приклад 9: 4-((S)-2,2-Дифтор-1-метилетил)-N-(2-метил-6-піперазин-1-ілпіридин-3-іл)бензолсульфонамід + 181 мг, вихід 99 %.ESI-МС: 411,1 [M+Н] 1 H-ЯМР (CD3OD, 400 Гц): δ [м.ч.] 1,38 (д, 3H), 2,00 (с, 3H), 3,28 (м, 5H), 3,79 (м, 4H), 5,97 (тд, 1Н), 6,63 (д, 1Н), 7,22 (д, 1Н), 7,50 (д, 2H), 7,64 (д, 2H). Приклад 10: 4-((R)-2,2-Дифтор-1-метилетил)-N-(2-метил-6-піперазин-1-ілпіридин-3-іл)бензолсульфонамід + 230 мг, вихід 99 %.ESI-МС: 41 1,1 [M+Н] 1 H-ЯМР (CD3OD, 400 Гц): δ [м.ч.] 1,38 (д, 3H), 2,00 (с, 3H), 3,28 (м, 5H), 3,79 (м, 4H), 5,97 (тд, 1Н), 6,63 (д, 1Н), 7,22 (д, 1Н), 7,50 (д, 2H), 7,64 (д, 2H). Приклад 11: 4-(2,2,2-Трифтор-1-метилетил)-N-(2-метил-6-піперазин-1-ілпіридин-3-іл)бензолсульфонамід + Характеризували у вигляді солі НСl: ESI-МС: 430,1 [M+Н] 1 H-ЯМР (ДМСО-d6, 400 Гц): δ [м.ч.] 1,45 (д, 3H), 1,90 (с, 3H), 3,14 (м, 4H), 3,67 (м, 4H), 4,98 (м, 1Н), 6,68 (д, 1Н), 7,12 (д, 1Н), 7,63 (д, 4H), 8,93 (с, 2H), 9,55 (с, 1Н). Приклад 12: 4-((R)-2,2,2-Трифтор-1-метилетил)-N-(2-метил-6-піперазин-1-ілпіридин-3-іл)бензолсульфонамід 420 мг, вихід 99 %. Характеризували у вигляді солі НСl: 16 UA 99628 C2 + 5 10 15 20 25 30 35 40 45 50 55 60 ESI-МС: 430,1 [M+Н] 1 H-ЯМР (ДМСО-d6, 400 Гц): δ [м.ч.] 1,45 (д, 3H), 1,90 (с, 3H), 3,14 (м, 4H), 3,67 (м, 4H), 4,98 (м, 1Н), 6,68 (д, 1Н), 7,12 (д, 1Н), 7,63 (д, 4H), 8,93 (с, 2H), 9,55 (с, 1Н). Приклад 13: 4-((S)-2,2,2-Трифтор-1-метилетил)-N-(2-метил-6-піперазин-1-ілпіридин-3-іл)бензолсульфонамід 62 мг, вихід 47 %. Характеризували у вигляді солі НСl: + ESI-МС: 430,1 [M+Н] 1 H-ЯМР (ДМСО-d6, 400 Гц): δ [м.ч.] 1,45 (д, 3H), 1,90 (с, 3H), 3,14 (м, 4H), 3,67 (м, 4H), 4,98 (м, 1Н), 6,68 (д, 1Н), 7,12 (д, 1Н), 7,63 (д, 4H), 8,93 (с, 2H), 9,55 (с, 1Н). Приклад 14: 4-((R)-2-Фтор-1-метилетил)-N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)бензолсульфонамід 160 мг, вихід 80 %. Характеризували у вигляді солі НСl: + ESI-МС: 409,1 [M+Н] 1 H-ЯМР (ДМСО-d6, 400 Гц): δ [м.ч.] 1,23 (д, 3H), 3,12 (м, 4H), 3,18 (м, 1Н), 3,35 (с, 3H), 3,67 (м, 4H), 4,52 (дд, 2H), 6,37 (д, 1Н), 7,34 (д, 1Н), 7,45 (д, 2H), 7,59 (д, 2H), 9,28 (м, 3H). Приклад 15: 4-((S)-2-Фтор-1-метилетил)-N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)бензолсульфонамід 24 мг, вихід 18 %. Характеризували у вигляді солі НСl: + ESI-МС: 409,1 [M+Н] 1 H-ЯМР (ДМСО-d6, 400 Гц): δ [м.ч.] 1,23 (д, 3H), 3,12 (м, 4H), 3,18 (м, 1Н), 3,35 (с, 3H), 3,67 (м, 4H), 4,52 (дд, 2H), 6,37 (д, 1Н), 7,34 (д, 1Н), 7,45 (д, 2H), 7,59 (д, 2H), 9,28 (м, 3H). Приклад 16: 4-(2,2-Дифтор-1-метилетил)-N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)бензолсульфонамід 57 мг, вихід 28 %. Характеризували у вигляді солі НСl: + ESI-МС: 427,1 [M+Н] 1 H-ЯМР (CD3OD, 400 Гц): δ [м.ч.] 1,38 (д, 3H), 3,28 (м, 4H), 3,42 (с, 3H), 3,48 (м, 1Н), 3,74 (м, 4H), 5,97 (дт, 1Н), 6,39 (д, 1Н), 7,43 (д, 2H), 7,60 (д, 1Н), 7,65 (д, 2H). Приклад 17: N-(2-Метокси-6-піперазин-1-ілпіридин-3-іл)-4-(2,2,2-трифтор-1-метилетил)бензолсульфонамід 42 мг, вихід 31 %. + ESI-МС: 445,1 [M+Н] 1 H-ЯМР (CDCl3, 400 Гц): δ [м.ч.] 1,48 (д, 3H), 3,10 (м, 4H), 3,38 (с, 3H), 3,43 (м, 1Н), 3,59 (м, 4H), 5,20 (уш. с, 2H), 6,17 (д, 1Н), 7,37 (д, 2H), 7,63 (м, 3H). Приклад 18: N-(2-Метокси-6-піперазин-1-ілпіридин-3-іл)-4-((S)-2,2,2-трифтор-1-метилетил)бензолсульфонамід 45 мг, вихід 62 %. + ESI-МС: 445,1 [M+Н] 1 H-ЯМР (CDCl3, 400 Гц): δ [м.ч.] 1,48 (д, 3H), 3,10 (м, 4H), 3,38 (с, 3H), 3,43 (м, 1Н), 3,59 (м, 4H), 5,20 (уш. с, 2H), 6,17 (д, 1Н), 7,37 (д, 2H), 7,63 (м, 3H). III. Приклади форм введення, отримані обробкою рослинної й тваринної сировини A) Таблетки Таблетки наступних композицій пресували на таблетковому пресі загальноприйнятим способом: 40 мг речовини із прикладу 1 120 мг кукурудзяного крохмалю 13,5 мг желатину 45 мг лактози 2,25 мг Aerosil® (хімічно чиста кремнієва кислота в ультрамікроскопічній тонкій дисперсії) 6,75 мг картопляний крохмаль (у вигляді 6 % пасти) B) Таблетки, покриті цукром 20 мг речовини із прикладу 1 60 мг основної композиції 70 мг цукроутворювальної композиції Основна композиція складається з 9 частин кукурудзяного крохмалю, 3 частин лактози й 1 частини співполімеру вінілпіролідон/вінілацетат 60:40. Цукроутворювальна композиція складається з 5 частин тростинного цукру, 2 частин кукурудзяного крохмалю, 2 частин карбонату кальцію й 1 частини тальку. Таблетки, покриті цукром, які одержували цим способом, згодом надають із покриттям, стійким до шлункового соку. IV. Біологічні дослідження Вивчення зв'язування рецептора: 17 UA 99628 C2 5 10 15 20 25 30 35 Речовина, яку необхідно досліджувати, або розчиняли в метанол/Chremophor® (BASF-AG) або в диметилсульфоксиді й потім розбавляли водою до бажаної концентрації. a) Дофаміновий рецептор D3: 6 Аналізована суміш (0,250 мл) складалася з мембран, що походять з ~10 HEK-293 клітин, які 125 мають людські дофамінові рецептори D3, які стабільно експресуються, 0,1 нМ [ I]йодосульприду й інкубаційного буфера (повне зв'язування) або, крім того, досліджуваної речовини (крива інгібування) або 1 μM спіперону (неспецифічне зв'язування). Кожну аналізовану суміш використовували тричі. Інкубаційний буфер містив 50 мМ тріс, 120 мМ NaCl, 5 мМ KCl, 2 мМ CaCl2, 2 мМ MgCl2 і 0,1 % бичачого сироваткового альбуміну, 10 μM хінолону й 0,1 % аскорбінової кислоти (одержували свіжу щодня). Буфер доводили до pH 7,4 за допомогою НCl. b) Дофаміновий рецептор D2L: 6 Аналізована суміш (1 мл) складалася з мембран, що походять з ~10 HEK-293 клітин, які мають людські дофамінові рецептори D2L (довга ізоформа), які стабільно експресуються, і 0,01 125 нМ [ I]йодоспіперону й інкубаційного буфера (повне зв'язування) або, крім того, досліджуваної речовини (крива інгібування) або 1 μM галогенперидолу (неспецифічне зв'язування). Кожну аналізовану суміш використовували тричі. Інкубаційний буфер містив 50 мМ тріс, 120 мМ NaCl, 5 мМ KCl, 2 мМ CaCl 2, 2 мМ MgCl2 і 0,1 % бичачого сироваткового альбуміну. Буфер доводили до pH 7,4 за допомогою НCl. c) Вимірювання і аналіз: Після інкубування при 25ºC протягом 60 хвилин, аналізовані суміші фільтрували через Whatman GF/B скловолоконний фільтр під вакуумом, використовуючи пристрій для збирання клітин. Фільтри переносили на сцинтиляційні віали, використовуючи систему для перенесення фільтрів. Після додавання 4 мл Ultima Gold® (Packard) зразки струшували протягом години й потім вираховували радіоактивність у Бета-лічильнику (Packard, Tricarb 2000 або 2200CA). Значення cpm (число імпульсів за хвилину) переводили в dpm (число розпадів за хвилину), використовуючи стандартний порядок гасіння й програму, що належить приладу. Криві інгібування аналізували за допомогою циклічного аналізу криволінійної регресії, використовуючи Статистичну Аналізуючу Систему (SAS), яка аналогічна програмі "Ligand", описаній Munson і Rodbard. У цих дослідженнях сполуки за винаходом проявляють дуже гарні афінності відносно рецептора D3 (50 >50 >50 >50 >50 >50 >50 >50 >50 >50 >50 UA 99628 C2 ФОРМУЛА ВИНАХОДУ 1. N-(6-піперазин-1-ілпіридин-3-іл)бензолсульфонамідні сполуки формули І R 2 R 3 R 1 N N CHnF3-n O N N H S CH R O 5 10 15 20 25 30 35 40 45 50 55 4 , (I) де 1 R вибраний із групи, яка складається з водню, лінійного С 1-С3алкілу й фторованого лінійного С1-С3алкілу; 2 R являє собою водень або метил; 3 R вибраний із групи, яка складається з водню, галогену, С 1-С2алкілу, фторованого С1-С2алкілу, С1-С2алкокси й фторованого С1-С2алкокси, 4 R являє собою С1-С2алкіл або фторований С1-С2алкіл; n являє собою 0, 1 або 2; і фізіологічно стійкі солі цих сполук і їх N-оксиди. 1 2. Сполука за п. 1, де R являє собою водень. 2 3. Сполука за п. 1 або 2, де R являє собою метил. 2 4. Сполука за п. 3, де атом вуглецю, який несе R , має S-конфігурацію. 2 5. Сполука за п. 3, де атом вуглецю, який несе R , має R-конфігурацію. 2 6. Сполука за п. 1 або 2, де R являє собою водень. 3 7. Сполука за будь-яким з попередніх пунктів, де R являє собою метил. 4 8. Сполука за будь-яким з попередніх пунктів, де R являє собою метил. 4 9. Сполука за п. 8, де атом вуглецю, який несе R , має S-конфігурацію. 4 10. Сполука за п. 8, де атом вуглецю, який несе R , має R-конфігурацію. 11. Сполука за будь-яким з попередніх пунктів, де n являє собою 1. 12. Сполука за будь-яким з попередніх пунктів, де n являє собою 2. 13. Сполука за п. 1, вибрана із групи, яка складається з: 4-(2-фтор-1-метилетил)-N-[2-метил-6-(3-метилпіперазин-1-іл)-піридин-3-іл]бензолсульфонаміду, 4-((R)-2-фтop-1-метилетил)-N-[2-метил-6-((R)-3-метилпіперазин-1-іл)-піридин-3-іл]бензолсульфонаміду, 4-((S)-2-фтор-1-метилетил)-N-[2-метил-6-((S)-3-метилпіперазин-1-іл)-піридин-3-іл]бензолсульфонаміду, 4-((R)-2-фтор-1-метилетил)-N-[2-метил-6-((S)-3-метилпіперазин-1-іл)-піридин-3-іл]бензолсульфонаміду, 4-((S)-2-фтор-1-метилетил)-N-[2-метил-6-((R)-3-метилпіперазин-1-іл)-піридин-3-іл]бензолсульфонаміду, 4-(2-фтор-1-метилетил)-N-[2-метил-6-піперазин-1-ілпіридин-3-іл]-бензолсульфонаміду, 4-((R)-2-фтop-1-метилетил)-N-[2-метил-6-піперазин-1-ілпіридин-3-іл]-бензолсульфонаміду, 4-((S)-2-фтор-1-метилетил)-N-[2-метил-6-піперазин-1-ілпіридин-3-іл]-бензолсульфонаміду і фізіологічно стійких солей цих сполук. 14. Сполука за п. 1, вибрана із групи, яка складається з: 4-(2,2-дифтор-1-метилетил)-N-(2-метил-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонаміду, 4-((S)-2,2-дифтор-1-метилетил)-N-(2-метил-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонаміду, 4-((R)-2,2-дифтор-1-метилетил)-N-(2-метил-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонаміду і фізіологічно стійких солей цих сполук. 15. Сполука за п. 1, вибрана із групи, яка складається з: 4-(2,2,2-трифтор-1-метилетил)-N-(2-метил-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонаміду, 4-((R)-2,2,2-трифтор-1-метилетил)-N-(2-метил-6-піперазин-1-ілпіридин-3-іл)бензолсульфонаміду, 4-((S)-2,2,2-трифтор-1-метилетил)-N-(2-метил-6-піперазин-1-ілпіридин-3-іл)бензолсульфонаміду і фізіологічно стійких солей цих сполук. 16. Сполука за п. 1, вибрана із групи, яка складається з: 4-(2-фтор-1-метилетил)-N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонаміду, 4-((R)-2-фтор-1-метилетил)-N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонаміду, 4-((S)-2-фтоp-l-метилетил)-N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонаміду, 19 UA 99628 C2 5 10 15 20 25 30 4-(2,2-дифтор-1-метилетил)-N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)-бензолсульфонаміду, 4-((S)-2,2-дифтор-1-метилетил)-N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)бензолсульфонаміду, 4-((R)-2,2-дифтор-1-метилетил)-N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)бензолсульфонаміду, N-(2-метокси-6-піпepaзин-1-ілпіридин-3-іл)-4-(2,2,2-трифтор-1-метилетил)-бензолсульфонаміду, N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)-4-((S)-2,2,2-трифтор-1-метилетил)бензолсульфонаміду, N-(2-метокси-6-піперазин-1-ілпіридин-3-іл)-4-((R)-2,2,2-трифтор-1-метилетил)бензолсульфонаміду і фізіологічно стійких солей цих сполук. 17. Фармацевтична композиція, яка містить щонайменше одну сполуку за будь-яким з пп. 1-16, необов'язково разом зі щонайменше одним фізіологічно прийнятним носієм або допоміжною речовиною. 18. Застосування сполуки за будь-яким з пп. 1-16 для одержання лікарського засобу. 19. Сполука за будь-яким з пп. 1-16 для застосування як лікарського засобу. 20. Застосування сполуки за будь-яким з пп. 1-16 для лікування медичного захворювання, що піддається лікуванню за допомогою ліганду дофамінового рецептора D3. 21. Застосування сполуки за будь-яким з пп. 1-16 для одержання лікарського засобу для лікування медичного захворювання, що піддається лікуванню за допомогою ліганду дофамінового рецептора D3. 22. Спосіб лікування медичних захворювань, що піддаються лікуванню за допомогою ліганду дофамінового рецептора D3, що включає введення ефективної кількості щонайменше однієї сполуки за будь-яким з пп. 1-16 суб'єкту, який потребує цього. 23. Спосіб лікування захворювання центральної нервової системи, що включає введення ефективної кількості щонайменше однієї сполуки за будь-яким з пп. 1-16 суб'єкту, який потребує цього. 24. Спосіб за п. 22 або 23, де медичне захворювання являє собою шизофренію. 25. Спосіб за п. 22 або 23, де медичне захворювання являє собою наркотичну залежність. 26. Спосіб за п. 22, де медичне захворювання являє собою діабетичну нефропатію. 27. Спосіб за п. 22 або 23, де медичне захворювання являє собою біполярний розлад. 28. Сполука формули IV R 2 R 3 Ra N N CHnF3-n O N N H S CH R O 4 , (IV) a 2 3 4 де R являє собою N-захисну групу, і де n, R , R і R є такими, як визначено в пунктах 1-12. 35 Комп’ютерна верстка Л. Купенко Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 20
ДивитисяДодаткова інформація
Назва патенту англійськоюBenzenesulfonamide compounds suitable for treating disorders that respond to modulation of the dopamine d3 receptor
Автори англійськоюTurner, Sean, Colm, Haupt, Andreas, Braje, Wilfried, Lange, Udo, Drescher, Karla, Unger, Liliane, Jongen-Relo, Ana Lucia, Bespalov, Anton
Назва патенту російськоюБензолсульфонамидные соединения, пригодные для лечения расстройств, восприимчивых к модуляции дофаминового рецептора d3
Автори російськоюТернер Шон Кольм, Хаупт Андреас, Брайе Вильфрид, Ланге Удо, Дрешер Карла, Унгер Лилиане, Йонген-Рело Ана Люсия, Беспалов Антон
МПК / Мітки
МПК: A61P 25/00, C07D 213/76, A61K 31/444, C07D 401/04
Мітки: придатні, сприйнятливі, дофамінового, розладів, сполуки, бензолсульфонамідні, рецептора, лікування, модуляції
Код посилання
<a href="https://ua.patents.su/22-99628-benzolsulfonamidni-spoluki-pridatni-dlya-likuvannya-rozladiv-yaki-sprijjnyatlivi-do-modulyaci-dofaminovogo-receptora-d3.html" target="_blank" rel="follow" title="База патентів України">Бензолсульфонамідні сполуки, придатні для лікування розладів, які сприйнятливі до модуляції дофамінового рецептора d3</a>
Попередній патент: Термодинамічно стабільна кристалічна модифікація 2-({2-хлор-4-(метилсульфоніл)-3-[(2,2,2-трифторетокси)метил]феніл}карбоніл)циклогексан-1,3-діону
Наступний патент: Ароматично-смакова приправочна основа для підсилення смаку і спосіб її приготування
Випадковий патент: Пристрій для контролю ресурсу комутаційних апаратів