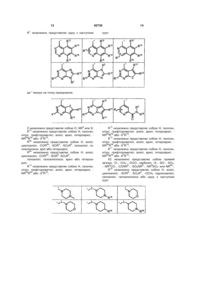
Аналоги бензазолу і їх застосування
Номер патенту: 92730
Опубліковано: 10.12.2010
Автори: Таслер Стефан, Куббутат Майкл, Краусс Рольф, Ланг Мартін, Герц Томас, Тотцке Франк, Шехтеле Крістоф
Формула / Реферат
1. Сполука за загальною формулою (І) або її сіль, або її фізіологічно функціональне похідне
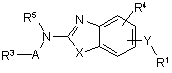 , (I)
, (I)
в якій:
замісник -Y-R1 приєднано до 5-або 6-позиції бензазолу;
Х незалежно являє собою S, О, SO або SO2;
Y незалежно являє собою S, О, NR2, SO або SO2;
А незалежно являє собою ¬СО-, ¬CS-, ¬SO-, ¬SO2-, ¬СO2-, ¬CONR8-, ¬NR8CO-, ¬NR8CONR9-, -¬NR8COO-, ¬NR8NR9CO-, ¬NR8OCO-, -¬ONR8CO-, ¬NR8SO2-, де ¬ указує точку приєднання до R3;
R2 незалежно являє собою Н, алкіл, циклоалкіл, -COR6, -SOR6, -SO2R6, -CN, гідроксіалкіл, галоалкіл або галоалкілокси;
R3 незалежно являє собою Н, алкіл, циклоалкіл, арил, гетероарил;
R4 незалежно являє собою Н, -COR6, -CO2R6, -SOR6, -SO2R6, -SO3R6, -NO2, -CN, -CF3, -ОСН3, -ОСF3, алкіл, циклоалкіл, алкокси, -NH2, алкіламіно, -NR7COR6, галоген, -ОН, -SH, алкілтіо, галоалкіл, галоалкілокси, арил або гетероарил;
R5 незалежно являє собою Н, алкіл, циклоалкіл, -COR6, -SOR6, -SO2R6, -CN, гідроксіалкіл, галоалкіл, галоалкілокси, арил або гетероарил;
R6a незалежно являє собою Н, алкіл, циклоалкіл, -NR8NR2R9, -ONR8R9, -NR8OR9, арил або гетероарил;
R6 незалежно являє собою Н, алкіл, циклоалкіл, -NR8R9, -NR8NR2R9, -ONR8R9, -NR8OR9, арил або гетероарил;
R7 незалежно являє собою Н, алкіл, циклоалкіл, або алкокси;
R8 незалежно являє собою Н, алкіл, циклоалкіл, -COR6, -SOR6, -SO2R6, галоалкіл, галоалкілокси, арил або гетероарил;
R9 незалежно являє собою Н, алкіл, циклоалкіл, -COR6, -SOR6, -SO2R6,
галоалкіл, галоалкілокси, арил або гетероарил;
R1 незалежно являє собою одну з наступних груп:
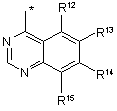
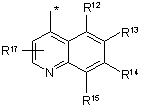
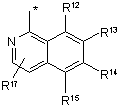
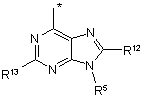
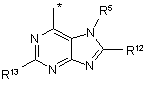
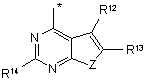
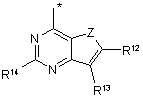
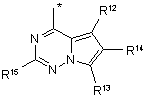
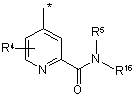
де * вказує на точку приєднання;
Z незалежно являє собою О, NR8 или S;
R12 незалежно являє собою H, галоген, нітро, трифторометил, алкіл, арил, гетероарил, -NR8aR9a або -Х2R16;
R8a незалежно являє собою H, алкіл, циклоалкіл, -COR6a, -SOR6, -SO2R6, галоалкіл, галоалкілокси, арил або гетероарил;
R9a незалежно являє собою H, алкіл, циклоалкіл, -COR6a, -SOR6 -SO2R6, галоалкіл, галоалкілокси, арил або гетероарил;
R13 незалежно являє собою H, галоген, нітро, трифторометил, алкіл, арил, гетероарил, -NR8aR9a або -Х2R16;
R14 незалежно являє собою H, галоген, нітро, трифторометил, алкіл, арил, гетероарил, -NR8aR9a або -Х2R16;
R15 незалежно являє собою H, галоген, нітро, трифторометил, алкіл, арил, гетероарил, -NR8aR9a або -Х2R16;
R17 незалежно являє собою H, галоген, нітро, трифторометил, алкіл, арил, гетероарил, -NR8aR9a або -Х2R16;
X2 незалежно являє собою прямий зв'язок, -O-, -CH2-, -OCO-, карбоніл, -S-, -SO-, -SO2-, -NR8CO-, -CONR8-, -SO2NR8-, -NR8SO2- або NR8a-;
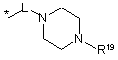
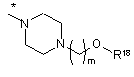
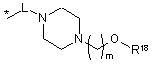
R16 незалежно являє собою Н, алкіл, циклоалкіл, -SOR6, -SO2R6, -ОСН3 гідроксіалкіл, галоалкіл, галоалкілокси або одну з наступних груп:


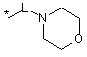
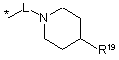
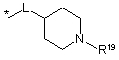
![]()
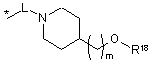
![]()

![]()
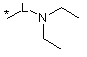
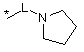
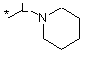
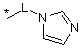



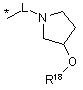
де * указує на точку приєднання;
m незалежно являє собою ціле з 1-3;
L відсутній або являє собою групу двовалентного зв'язку, вибрану з алкілену, циклоалкілену, гетероциклілену, арилену або гетероарилену, в якій одна або декілька груп (-СН2-) можуть заміщатися киснем або NR8, і в якій один або декілька атомів вуглецю можуть незалежно заміщатися одним або двома замісниками, вибраними з галогену, гідрокси, алкокси, галоалкілокси, фосфоноокси або фосфонооксіалкілу;
X3 незалежно являє собою -СООН, -СООалкіл, -ОН, -SH, -SО3Н або -SO2NR8R9;
R18 незалежно являє собою Н, фосфоноокси або фосфонооксіалкіл;
R19 незалежно являє собою Н, алкіл, циклоалкіл, алкіламіно або алкокси;
при умові, що наступні сполуки відсутні:
N-[6-(6,7-диметоксихінолін-4-ілокси)-5-фторобензотіазол-2-іл]-2-фенілацетамід,
N-[6-(6,7-диметоксихінолін-4-ілокси)-бензотіазол-2-іл]-2-фенілацетамід,
N-[6-(6,7-диметоксихінолін-4-ілокси)-5-фторобензотіазол-2-іл]-3-фенілпропіонамід,
N-[6-(6,7-диметоксихінолін-4-ілокси)-5-фторобензотіазол-2-іл]-2-(3-трифторометилфеніл)-ацетамід,
2-(3,5-біс-трифторометилфеніл)-N-[6-(6,7-диметоксихінолін-4-ілокси)-5-фторобензотіазол-2-іл]-ацетамід,
2-(2-хлоро-5-трифторометилфеніл)-N-[6-(6,7-диметоксихінолін-4-ілокси)-5-фторобензотіазол-2-іл]-ацетамід;
в якій алкільна група, якщо не передбачено інше, означає лінійний або розгалужений С1-С6-алкіл, переважно лінійний або розгалужений ланцюг, що складається з від одного до п'яти атомів вуглецю, лінійний або розгалужений С2-С6-алкеніл або лінійну або розгалужену групу С2-С6-алкінілу, які можуть заміщатися одним або декількома замісниками R';
де R' незалежно являє собою Н, -CO2R", -CONHR", -CR"O, -SO2NR", -NR"-СО-галоалкіл, -NO2, -NR"-SO2-галоалкіл, -NR"-SO2-алкіл, -SO2-алкіл, -NR"-CO-алкіл, -CN, алкіл, циклоалкіл, аміноалкіл, алкіламіно, алкокси, -ОН, -SH, алкілтіо, гідроксіалкіл, гідроксіалкіламіно, галоген, галоалкіл, галоалкілокси, арил, арилалкіл або гетероарил;
де R" незалежно являє собою Н, галоалкіл, гідроксіалкіл, алкіл, циклоалкіл, арил, гетероарил або аміноалкіл;
де циклоалкільна група являє собою циклічну неароматичну систему, що містить від трьох до восьми атомів вуглецю, переважно від чотирьох до восьми атомів вуглецю, в якій один або декілька атомів вуглецю в циклі можуть заміщатися групою Е, причому група Е може бути представлена О, S, SO, SO2, N або NR", R", визначеними вище;
де група алкокси являє собою О-алкільну групу, причому алкільна група відповідає групі, описаній вище; переважно групою алкокси є група метокси, етокси, ізопропокси, t-бутокси або пентокси;
де група алкілтіо являє собою S-алкільну групу, причому алкільна група відповідає групі, визначеній вище;
де галоалкільна група являє собою алкільну групу, яка заміщається від одного до п'яти атомами галогену, причому алкільна група відповідає групі, визначеній вище;
де гідроксіалкільна група являє собою НО-алкільну групу, причому алкільна група відповідає групі, визначеній вище;
де галоалкілоксильна група являє собою алкоксильну групу, яка заміщається від одного до п'яти атомами галогену, причому алкільна група відповідає групі, визначеній вище;
де гідроксіалкіламіновою групою є (НО-алкіл)2-N-група або НО-алкіл-NН-група, причому алкільна група відповідає групі, визначеній вище;
де алкіламінова група являє собою HN-алкільну або N-діалкільну групу, причому алкільна група відповідає групі, визначеній вище;
де галогенова група являє собою фтор, хлор, бром або йод;
де арильна група являє собою ароматичну групу, що містить від п'яти до п'ятнадцяти атомів вуглецю, які можуть заміщатися одним або декількома замісниками R';
де R' визначено вище,
де гетероарильна група являє собою 5- або 6-елементну гетероциклічну групу, яка складається принаймні з одного гетероатома, подібного О, N, S, при цьому гетероциклічна група може бути зконденсована з іншим ароматичним циклом, крім того, гетероциклічна група може заміщатися одним або декількома замісниками R', при цьому R' визначено вище.
2. Сполука за п. 1 або її сіль, або її фізіологічно функціональне похідне, в якій:
R' являє собою
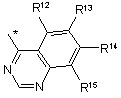 ,
,
(* вказує на точку приєднання).
3. Сполука за п. 1 або її сіль, або фізіологічно функціональне похідне, в якій Х незалежно являє собою S або О; Y являє собою NH; А являє собою -CO; R5 являє собою Н.
4. Сполука за п. 1 або її сіль, або фізіологічно функціональне похідне, в якій Х незалежно являє собою S або О; Y являє собою NH; R5 являє собою Н, А являє собою ¬NНСО-, де ¬ вказує на точку приєднання до R3.
5. Сполука за будь-яким з пп. 1-4 або її сіль, або фізіологічно функціональне похідне, в якій замісник -Y-R1 приєднаний до 6-ї позиції бензазолу.
6. Сполука за п. 5 або її сіль, або фізіологічно функціональне похідне, в якій R12 і R15 являються Н, а R13 і R14 незалежно являють собою -О-алкіл, який може бути заміщеним.
7. Сполука за загальною формулою (Іа) або її сіль, або її фізіологічно функціональне похідне
 , (Ia)
, (Ia)
де:
замісник -Ya-R1a приєднаний до 5-ї-або 6-ї позиції бензазолу;
Xа незалежно являє собою S, О, SO або SO2;
Ya незлежно являє собою S, NR2, SO або SO2;
Аa незалежно являє собою ¬СО-, ¬CS-, ¬SO-, ¬SO2-, ¬CO2-, ¬CONR8-, ¬NR8CO-, ¬NR8CONR9-, ¬NR8COO-, ¬NR8NR9CO-, ¬NR8OCO-, ¬ONR8CO-, ¬NR8SO2-, де ¬ вказує точку приєднання до R3;
R1a незалежно являє собою одну з наступних груп:

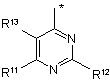
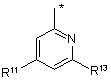
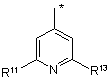
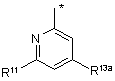
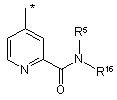
де * указує на точку приєднання;
R11 незалежно являє собою Н, NHR8a або одну з наступних груп:
 або
або 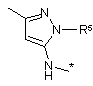 ,
,
де * вказує на точку приєднання;
R13a незалежно являє собою Н, галоген, нітро, трифторометил, алкіл, -NR8aR9a або Х2R16; причому R2, R3, R4, R5, R6, R6a, R7, R8, R8a, R9, R9a, R12, R13, R16 або X2 є елементами за пп. 1-6.
8. Сполука за загальною формулою (II) або її сіль, або її фізіологічно функціональне похідне
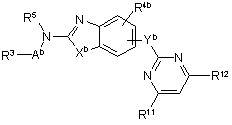 , (II)
, (II)
де:
замісник -Yb приєднаний до 5-ї - або 6-ї позиції бензазолу;
Xb незалежно являє собою S, О, SO або SO2;
Yb незалежно являє собою S, NR2, SO або SO2;
Аb незалежно являє собою ¬СО-, ¬CS-, ¬SO-, ¬SO2-, ¬CO2-, ¬CONR8-, ¬NR8CO-, ¬NR8CONR9-, ¬NR8COO-, ¬NR8NR9CO-, ¬NR8OCO-, ¬ONR8CO-, ¬NR8SO2-, де ¬ вказує точку приєднання до R3;
R4b незалежно являє собою Н, -SOR6, -SO2R6, -SO3R6, -NO2, -CN, -CF3, -ОСН3, -OCF3, алкіл, циклоалкіл, алкокси, оксіалкіл, алкоксіалкіл, -NH2, алкіламіно, аміноалкіл, алкіламіноалкіл, -NR7 COR6, галоген, -ОН, -SH, алкілтіо, гідроксіалкіл, галоалкіл, галоалкілокси, арил або гетероарил;
причому, R2, R3, R5, R6, R6a, R7, R8, R8a, R9, R9a, R11, R12, R16 або Х2 є елементами за пп. 1-6;
9. Сполука за будь-яким з пп. 1-8 або її сіль, або фізіологічно функціональне похідне, призначені для використання як медикаменту.
10. Сполука за будь-яким з пп. 1-8 або її сіль, або фізіологічно функціональне похідне, призначені для використання у терапії.
11. Композиція, що містить сполуку за будь-яким з пп. 1-8 або її сіль, або фізіологічно функціональне похідне та фармацевтично прийнятний носій або розчинник .
12. Композиція за п. 11, що містить ад’ювант та/або добавку.
13. Застосування сполуки за будь-яким з пп. 1-10 або її солі, або її фізіологічно функціонального похідного для одержання фармацевтичної композиції для лікування хвороб, які виліковуються або тяжкість яких знижується у результаті інгібування одної або декількох кіназ.
14. Застосування композиції за будь-яким з пп. 11-12 для лікування хвороб, які виліковуються або тяжкість яких знижується у результаті інгібування одної або декількох кіназ.
15. Застосування сполуки за будь-яким з пп. 1-10 або її солі, або її фізіологічно функціонального похідного для приготування медикаменту для лікування, зниження тяжкості протікання та/або профілактики раку.
16. Застосування композиції за будь-яким з пп. 11-12 для приготування медикаменту для лікування, зниження тяжкості протікання та/або профілактики раку.
Текст
1. Сполука за загальною формулою (І) або її сіль, або її фізіологічно функціональне похідне R4 R5 N N Y 3 X A R R1 , (I) в якій: замісник -Y-R1 приєднано до 5-або 6-позиції бензазолу; Х незалежно являє собою S, О, SO або SO2; Y незалежно являє собою S, О, NR2, SO або SO2; А незалежно являє собою СО-, CS-, SO-, SO2-, СO2-, CONR8-, NR8CO-, NR8CONR9-, - NR8COO-, NR8NR9CO-, 2 (19) 1 3 92730 R12 * 4 R12 * R13 R13 N N R14 R14 * * N N * N N R12 N R12 N R13 R15 R5 N R12 N R13 R14 R17 R15 R15 N R13 N R17 N R12 * R13 Z N R14 R5 * * Z N N R14 R5 N R12 N R15 * R12 R14 N R13 R4 N N R16 O R13 де * вказує на точку приєднання; Z незалежно являє собою О, NR8 или S; R12 незалежно являє собою H, галоген, нітро, трифторометил, алкіл, арил, гетероарил, -NR8aR9a або -Х2R16; R8a незалежно являє собою H, алкіл, циклоалкіл, COR6a, -SOR6, -SO2R6, галоалкіл, галоалкілокси, арил або гетероарил; R9a незалежно являє собою H, алкіл, циклоалкіл, COR6a, -SOR6 -SO2R6, галоалкіл, галоалкілокси, арил або гетероарил; R13 незалежно являє собою H, галоген, нітро, трифторометил, алкіл, арил, гетероарил, -NR8aR9a або -Х2R16; * * N L R14 незалежно являє собою H, галоген, нітро, трифторометил, алкіл, арил, гетероарил, -NR8aR9a або -Х2R16; R15 незалежно являє собою H, галоген, нітро, трифторометил, алкіл, арил, гетероарил, -NR8aR9a або -Х2R16; 17 R незалежно являє собою H, галоген, нітро, трифторометил, алкіл, арил, гетероарил, -NR8aR9a або -Х2R16; X2 незалежно являє собою прямий зв'язок, -O-, CH2-, -OCO-, карбоніл, -S-, -SO-, -SO2-, -NR8CO-, CONR8-, -SO2NR8-, -NR8SO2- або NR8a-; R16 незалежно являє собою Н, алкіл, циклоалкіл, SOR6, -SO2R6, -ОСН3 гідроксіалкіл, галоалкіл, галоалкілокси або одну з наступних груп: * N N N N L * * N L * N O L O O * * N O m * L N N N m N L R19 * * O R19 L * * N N R18 O m * L N L R18 X3 N N R18 * R19 L N R19 5 92730 6 * * L L * N N L N N O R18 * L * N L N * L N O R18 O R18 де * указує на точку приєднання; m незалежно являє собою ціле з 1-3; L відсутній або являє собою групу двовалентного зв'язку, вибрану з алкілену, циклоалкілену, гетероциклілену, арилену або гетероарилену, в якій одна або декілька груп (-СН2-) можуть заміщатися киснем або NR8, і в якій один або декілька атомів вуглецю можуть незалежно заміщатися одним або двома замісниками, вибраними з галогену, гідрокси, алкокси, галоалкілокси, фосфоноокси або фосфонооксіалкілу; X3 незалежно являє собою -СООН, -СООалкіл, ОН, -SH, -SО3Н або -SO2NR8R9; R18 незалежно являє собою Н, фосфоноокси або фосфонооксіалкіл; R19 незалежно являє собою Н, алкіл, циклоалкіл, алкіламіно або алкокси; при умові, що наступні сполуки відсутні: N-[6-(6,7-диметоксихінолін-4-ілокси)-5фторобензотіазол-2-іл]-2-фенілацетамід, N-[6-(6,7-диметоксихінолін-4-ілокси)-бензотіазол-2іл]-2-фенілацетамід, N-[6-(6,7-диметоксихінолін-4-ілокси)-5фторобензотіазол-2-іл]-3-фенілпропіонамід, N-[6-(6,7-диметоксихінолін-4-ілокси)-5фторобензотіазол-2-іл]-2-(3трифторометилфеніл)-ацетамід, 2-(3,5-біс-трифторометилфеніл)-N-[6-(6,7диметоксихінолін-4-ілокси)-5-фторобензотіазол-2іл]-ацетамід, 2-(2-хлоро-5-трифторометилфеніл)-N-[6-(6,7диметоксихінолін-4-ілокси)-5-фторобензотіазол-2іл]-ацетамід; в якій алкільна група, якщо не передбачено інше, означає лінійний або розгалужений С1-С6-алкіл, переважно лінійний або розгалужений ланцюг, що складається з від одного до п'яти атомів вуглецю, лінійний або розгалужений С2-С6-алкеніл або лінійну або розгалужену групу С2-С6-алкінілу, які можуть заміщатися одним або декількома замісниками R'; де R' незалежно являє собою Н, -CO2R", -CONHR", -CR"O, -SO2NR", -NR"-СО-галоалкіл, -NO2, -NR"SO2-галоалкіл, -NR"-SO2-алкіл, -SO2-алкіл, -NR"CO-алкіл, -CN, алкіл, циклоалкіл, аміноалкіл, алкіламіно, алкокси, -ОН, -SH, алкілтіо, гідроксіалкіл, гідроксіалкіламіно, галоген, галоалкіл, галоалкілокси, арил, арилалкіл або гетероарил; m O R18 де R" незалежно являє собою Н, галоалкіл, гідроксіалкіл, алкіл, циклоалкіл, арил, гетероарил або аміноалкіл; де циклоалкільна група являє собою циклічну неароматичну систему, що містить від трьох до восьми атомів вуглецю, переважно від чотирьох до восьми атомів вуглецю, в якій один або декілька атомів вуглецю в циклі можуть заміщатися групою Е, причому група Е може бути представлена О, S, SO, SO2, N або NR", R", визначеними вище; де група алкокси являє собою О-алкільну групу, причому алкільна група відповідає групі, описаній вище; переважно групою алкокси є група метокси, етокси, ізопропокси, t-бутокси або пентокси; де група алкілтіо являє собою S-алкільну групу, причому алкільна група відповідає групі, визначеній вище; де галоалкільна група являє собою алкільну групу, яка заміщається від одного до п'яти атомами галогену, причому алкільна група відповідає групі, визначеній вище; де гідроксіалкільна група являє собою НОалкільну групу, причому алкільна група відповідає групі, визначеній вище; де галоалкілоксильна група являє собою алкоксильну групу, яка заміщається від одного до п'яти атомами галогену, причому алкільна група відповідає групі, визначеній вище; де гідроксіалкіламіновою групою є (НО-алкіл)2-Nгрупа або НО-алкіл-NН-група, причому алкільна група відповідає групі, визначеній вище; де алкіламінова група являє собою HN-алкільну або N-діалкільну групу, причому алкільна група відповідає групі, визначеній вище; де галогенова група являє собою фтор, хлор, бром або йод; де арильна група являє собою ароматичну групу, що містить від п'яти до п'ятнадцяти атомів вуглецю, які можуть заміщатися одним або декількома замісниками R'; де R' визначено вище, де гетероарильна група являє собою 5- або 6елементну гетероциклічну групу, яка складається принаймні з одного гетероатома, подібного О, N, S, при цьому гетероциклічна група може бути зконденсована з іншим ароматичним циклом, крім того, гетероциклічна група може заміщатися од 7 92730 ним або декількома замісниками R', при цьому R' визначено вище. 2. Сполука за п. 1 або її сіль, або її фізіологічно функціональне похідне, в якій: R' являє собою R12 R13 6. Сполука за п. 5 або її сіль, або фізіологічно функціональне похідне, в якій R12 і R15 являються Н, а R13 і R14 незалежно являють собою -О-алкіл, який може бути заміщеним. 7. Сполука за загальною формулою (Іа) або її сіль, або її фізіологічно функціональне похідне R4 R5 N N Ya Xa R3 Aa R1a , (Ia) де: замісник -Ya-R1a приєднаний до 5-ї-або 6-ї позиції бензазолу; Xа незалежно являє собою S, О, SO або SO2; Ya незлежно являє собою S, NR2, SO або SO2; Аa незалежно являє собою СО-, CS-, SO-, SO2-, CO2-, CONR8-, NR8CO-, NR8CONR9-, NR8COO-, NR8NR9CO-, 8 8 8 NR OCO-, ONR CO-, NR SO2-, де вказує точку приєднання до R3; R1a незалежно являє собою одну з наступних груп: * R14 N N R15 , (* вказує на точку приєднання). 3. Сполука за п. 1 або її сіль, або фізіологічно функціональне похідне, в якій Х незалежно являє собою S або О; Y являє собою NH; А являє собою CO; R5 являє собою Н. 4. Сполука за п. 1 або її сіль, або фізіологічно функціональне похідне, в якій Х незалежно являє собою S або О; Y являє собою NH; R5 являє собою Н, А являє собою NНСО-, де вказує на точку приєднання до R3. 5. Сполука за будь-яким з пп. 1-4 або її сіль, або фізіологічно функціональне похідне, в якій замісник -Y-R1 приєднаний до 6-ї позиції бензазолу. * R11 R13 R13a N * * R12 N 8 R11 N N N * R13 R11 R12 * * R5 N R11 N R13 N N R13a R11 R16 O де * указує на точку приєднання; R11 незалежно являє собою Н, NHR8a або одну з наступних груп: R5 N N H N R5 N * H або , де * вказує на точку приєднання; R13a незалежно являє собою Н, галоген, нітро, трифторометил, алкіл, -NR8aR9a або Х2R16; причому R2, R3, R4, R5, R6, R6a, R7, R8, R8a, R9, R9a, R12, R13, R16 або X2 є елементами за пп. 1-6. 8. Сполука за загальною формулою (II) або її сіль, або її фізіологічно функціональне похідне * N N R3 N N R5 Ab Xb R4b Yb N N R11 R12 , (II) де: замісник -Yb приєднаний до 5-ї - або 6-ї позиції бензазолу; Xb незалежно являє собою S, О, SO або SO2; Yb незалежно являє собою S, NR2, SO або SO2; Аb незалежно являє собою СО-, CS-, SO-, SO2-, CO2-, CONR8-, NR8CO-, 8 9 8 8 9 NR CONR -, NR COO-, NR NR CO-, 8 8 8 2 NR OCO-, ONR CO-, NR SO -, де вказує точку приєднання до R3; R4b незалежно являє собою Н, -SOR6, -SO2R6, SO3R6, -NO2, -CN, -CF3, -ОСН3, -OCF3, алкіл, циклоалкіл, алкокси, оксіалкіл, алкоксіалкіл, -NH2, алкіламіно, аміноалкіл, алкіламіноалкіл, -NR7 COR6, 9 92730 10 галоген, -ОН, -SH, алкілтіо, гідроксіалкіл, галоалкіл, галоалкілокси, арил або гетероарил; причому, R2, R3, R5, R6, R6a, R7, R8, R8a, R9, R9a, R11, R12, R16 або Х2 є елементами за пп. 1-6; 9. Сполука за будь-яким з пп. 1-8 або її сіль, або фізіологічно функціональне похідне, призначені для використання як медикаменту. 10. Сполука за будь-яким з пп. 1-8 або її сіль, або фізіологічно функціональне похідне, призначені для використання у терапії. 11. Композиція, що містить сполуку за будь-яким з пп. 1-8 або її сіль, або фізіологічно функціональне похідне та фармацевтично прийнятний носій або розчинник . 12. Композиція за п. 11, що містить ад’ювант та/або добавку. 13. Застосування сполуки за будь-яким з пп. 1-10 або її солі, або її фізіологічно функціонального похідного для одержання фармацевтичної композиції для лікування хвороб, які виліковуються або тяжкість яких знижується у результаті інгібування одної або декількох кіназ. 14. Застосування композиції за будь-яким з пп. 1112 для лікування хвороб, які виліковуються або тяжкість яких знижується у результаті інгібування одної або декількох кіназ. 15. Застосування сполуки за будь-яким з пп. 1-10 або її солі, або її фізіологічно функціонального похідного для приготування медикаменту для лікування, зниження тяжкості протікання та/або профілактики раку. 16. Застосування композиції за будь-яким з пп. 1112 для приготування медикаменту для лікування, зниження тяжкості протікання та/або профілактики раку. Даний винахід відноситься до бензазолів за загальною формулою (І) або до їх солей, або до їх фізіологічно функціонуючих похідних, або до їх стереоізомерів, які використовуються як лікарські препарати. Сполуки за даним винаходом виключно корисні для лікування захворювань, пов'язаних з порушенням процесів, що протікають в клітині, і її надмірним розростанням (гіперпроліферацією) у ссавців, особливо у людини. Зокрема вони використовуються для лікування різних форм раку. Крім того, розкритий спосіб приготування похідних бензазола. Протеїнкінази відіграють основну роль в регулюванні клітинних функцій. Це поняття включає процеси, подібні росту і поділу клітини, клітинній диференціації і припиненню життєдіяльності клітини, а також багато які інші види клітинної активності. Протеїнкинази каталізують перенесення фосфатних залишків від АТР (аденозин-5'трифосфату) на протеїни-мішені, які унаслідок даного протеинкіназа-опосередкованого фосфорилування, змінюють їх тримірну структуру і, як результат, їх фізіологічну функцію. Залежно від амінокислоти, яка стає фосфорилуваною протеїнкіназою, дані ензими групуються з утворенням двох сімейств, так звані серин/треонінові протеїнкінази і тирозинові протеїнкінази. Ґрунтуючись на концепції людського геному, зроблено висновок, що людина має в своєму розпорядженні 518 ДНК-послідовностей, які кодують протеїнкіназа-подібну протеїнову послідовність. За останні 20 років для деяких з цих 518 протеїнів можна показати, що модифікації генних послідовностей (наприклад, точкових мутацій, делецій або генної ампліфікації), що відносяться до них, приводять до патологічних змін клітинної активності відповідної протеїн кінази. Зокрема, це справедливо для протеїнкіназ, які залучені в процес контролю за ростом клітини (проліферацією клітини), контролю за клітинною циклічністю, процесом життєдіяльності клітини і процесом відмирання кліти ни, а також в процес ангіогенезу пухлини і формування пухлинних метастазів. Деякі так звані онкогени являють собою модифіковані гени, які в своїй протоонкогенній формі кодують протеїн кінази, залучені в нормальне фізіологічне регулювання росту і поділу клітини. Оскільки протеїнкінази є ключовими регуляторами клітинних функцій і оскільки вони можуть проявляти ензиматичну активність, що розрегулювана, в клітинах, вони є об'єктами, на основі яких можуть бути створені лікарські речовини. У фармацевтичній промисловості існує велика кількість проектів створення лікарських речовин, здатних забезпечити ідентифікацію модуляторів протеїнкіназ. В даний час щонайбільший інтерес викликають протеїнкінази, які мають відношення до запалень і ракових новоутворень, проте, окрім цього, вказані протеїнкінази є предметом обговорення в зв'язку з їх використовуванням як лікувальних засобів для лікування майже всіх видів захворювань. В області лікування пухлинних новоутворень ринок вже отримав перші інгібітори протеїнкінази (Gleevec, Iressa). Крім того, велика кількість інгібіторів протеїнкінази знаходиться в різних фазах клінічних досліджень. В більшості випадків дані сполуки є або коньюгіруючими підтипами рецептора EGF (чинника епідермального росту) або рецептора VEGF (чинника судинного ендотеліального росту). Всі ці сполуки були розроблені, з метою специфічного придушення кожної окремої протеїнкінази, щодо якої існує очевидність, що вона протидіє одному з чотирьох основних молекулярних процесів розвитку пухлини. Цими чотирма процесами є: (1) контроль клітинного розростання (проліферації)/клітинного циклу; (2) регулювання запрограмованого процесу відмирання клітини (апоптозу) і виживання клітини; (3) ангіогенез пухлини і (4) метастазів пухлини. Даний винахід відноситься до похідних бензазолу, які можуть бути використані для пригнічення протеїнкіназ, залучених до патологічного процесу, викликаного різними захворюваннями, окрім раку, 11 при цьому, похідні бензазолу особливо доцільно використовувати як протипухлинні речовини. Перелік даних похідних включає інгібітори моноспецифічних протеїнкіназ, які, переважно, інгібірують одну протеїнкіназу, що у результаті хвороби залучена до процесу прогресування пухлини, а також так звані багатоцільові інгібітори протеїнкіназ, які поглинають, принаймні, дві різні протеїнкінази, відіграючи істотну роль в двох або більш різних молекулярних механізмах розвитку пухлини. Наприклад, така сполука може бути інгібітором пухлинного ангіогенезу і, крім того, стимулятором апоптозу. Концепція багатоцільових інгібіторів протеїнкіназ є новим підходом до вирішення проблеми, хоча ідея створення «інгібіторів множинних протеїнкіназ» вже була описана в роботі J. Adams et al., Current Option in Chemical Biology 6, 486-492, 20002. В даній роботі описані сполуки, які одночасно пригнічують життєдіяльність декількох протеїнкіназ, хоч всі вони залучені до одного молекулярного механізму розвитку пухлини, а саме, до процесу пухлинного ангіогенезу. В публікації WO 2004085425 описані бензазоли, які відіграють роль інгібіторів кіназ. В публікації WO 9924035 2 описані амінобензотіазоли. Ці сполуки вже були розкриті в роботі Das et al., Biogr. Med.Chem. Lett 13, 2003, 2587-2590 і в роботі Das et al., Biogr. Med.Chem. Lett 13, 2145-2149. В публікації WO 2000061580 описані бензимідазоліл- та бензоксазолілцетиламінопіридилбутирати, використовувані як антагоністи інтегріну. В публікації WO 9940072 описані п'ятикомпонентні бензоконденсовані гетероцикли, використовувані як антитромботики. Технічна задача, поставлена в даному винаході, розв'язується, завдяки використовуванню істотних ознак, висловлених в незалежних пунктах формули винаходу. Додаткові позитивні ефекти, ознаки і подробиці по даному винаходу розкриваются в залежних пунктах формули, опису винаходу, малюнках і прикладах здійснення винаходу. Беручи до уваги той факт, що в даний час не існує надійної системи лікування більшості захворювань, пов'язаних з такими протеїнкіназами, як ABL1, ACV-R1, АКТІ, АКТ2, АКТ3, ART5, Aurora-Α, Aurora-B, Aurora-C, B-RAF, BRK, CDC42BPB, CDK1, CDK2, CDK3, CDK4, CDK5, CDK6, CDK7, CDK8, CDK9, CNK1, CK2, COT, CSK1, DAPK1, EGF-R, EPHA1, EPHA2, EPHA3, EPHA4, EPHB1, EPHB2, ЕРНВЗ, ЕРНВ4, ERBB2, ERBB4, FAK, FGF-R3, FGF-R4, FGR, FLT3, GSK3-beta, HCK, IGF1-R, IKK-beta, IKK-epsilon, INS-R, IRAK4, ITK, JAK2, JAK3, JNK3, KIT, LCK, LYN, MARKAPK5, MET, MST4, MUSK, NEK2, NEK6, NLK, PAK1, PAK2, PAK4, PBK, PCTAIRE1, PDGFR-alpha, PDGFR-beta, PDK1, PIM1, PIM2, PKC-alpha, PKCbeta1, PKC-beta2, PKC-delta, PKC-epsilon, PKC-eta, PKC-gamma, PKC-iota, PKC-mu, PKC-theta, PKCzeta, PLK1, PRK1, RET, ROCK2, S6K, SAK, SGK1, SGK3, SNK, SRC, SRPK2, SYK, TGFB-R1, TIE2, TSF1, TSK2, TTK, VEGF-R1, VEGF-R2, VEGF-R3, VRK1, WEE1, YES, ZAP70 особливо з такими протеїнкіназами, як, наприклад, EGF-R (клітинна про 92730 12 ліферація), ERBB2 (клітинна проліферація), PDGFR (клітинна проліферація), FLT3 (клітинна проліферація), Aurora-A (контроль циклічності клітини ), Aurora-B (контроль циклічності клітини), IGF1-R (апоптоз), VEGF-R2 (ангіогенез), VEGF-R3 (ангіогенез), ТІЕ2 (ангіогенез), ЕРНВ4 (ангіогенез), FAK (метастаз), SRC-киназа (метастаз), існує великий попит на лікарські речовини, що мають здатність до поглинання згаданих вище протеїнових мішеней. Описані в даній заявці похідні бензазолу - це нова група інгібіторів протеїнкінази, які проявляють здібність до диференційованого поглинання протеїнкіназ, при цьому кожен з них може мати відношення до одного з чотирьох молекулярних механізмів розвитку пухлини. Даний винахід відноситься до сполук по формулі (І) або до їх солі, або до їх фізіологічно функціонуючого похідного або стереоізомеру. В якій: замісник (заступник) -Y-R1 приєднано до 5-або 6-позиції бензазолу; X незалежно являє собою S, О, SO або SO2; В незалежно являє собою S, О, NR2, SO або SO2; А незалежно являє собою CO- CS- SOSO2- СО2- CONR8- NR8CO- NR8CONR9NR8COO- NR8NR9CO- NR8OCO- ONR8CONR8SO2-, де 4- указує точку приєднання до R3; R2 незалежно представляє собою Н, алкіл, циклоалкіл, -COR6, -SOR6, -SO2R6, -CN, гідроксиалкіл, галоалкіл або галоалкілокси; R3 незалежно представляє собою Н, алкіл, циклоалкіл, арил, гетероарил; R4 незалежно представляє собою Н, -COR6, -CO2R6, -SOR6, -SO2R6, SO3R6, -NO2; -CN, -CF3, -OCH3, -OCF3, алкіл, циклоалкіл, алкокси, -NH2, алкіламіно, -NR7COR6, галоген, -ОН, SH, алкілтіо, галоалкіл, галоалкілокси, арил або гетероарил; R5 незалежно представляє Н, алкіл, циклоалкіл, -COR6, -SOR6, -SO2R6, -CN, гідроксиалкіл, галоалкіл, галоалкілокси, арил або гетероарил; R6a незалежно представляє собою Н, алкіл, циклоалкіл, -NR8NR2R9, -ONR8R9, -NR8OR9, арил, гетероарил; R6 незалежно представляє Н, алкіл, циклоалкіл, -NR8R9, -NR8NR2R9, -ONR8R9, -NR8OR9, арил, гетероарил; R7 незалежно представляє Η, алкіл, циклоалкіл, або алкокси; 8 R незалежно представляє Н, алкіл, циклоалкіл, -COR6, -SOR6, -SO2R6, галоалкіл, галоалкілокси, арил або гетероарил; R9 незалежно представляє Η, алкіл, циклоалкіл, -COR6, -SOR6, -SO2R6, галоалкіл, галоалкілокси, арил або гетероарил; 13 R1 незалежно представляє одну з наступних 92730 14 груп: де * вказує на точку приєднання; Ζ незалежно представляє собою О, NR8 или S; R12 незалежно представляє собою Н, галоген, нітро, трифторометил, алкіл, арил, гетероарил, NR8aR9a або -X2R16; R8a незалежно представляє собою Η, алкіл, циклоалкіл, -COR6a, -SOR6, -SO2R6, галоалкіл, галоалкілокси, аріл або гетероаріл; R9a незалежно представляє собою Н, алкіл, циклоалкіл, -COR6a, -SOR6 -SO2R6, галоалкіл, галоалкілокси, арил або гетероарил; R13 незалежно представляє собою Н, галоген, нітро, трифторометил, алкіл, арил, гетероарил, NR8aR9a або -X2R16; R14 незалежно представляє собою Н, галоген, нітро, трифторометил, алкіл, арил, гетероарил, NR8aR9a або -X2R16; R15 незалежно представляє собою Н, галоген, нітро, трифторометил, алкіл, арил, гетероарил, NR8aR9a або -X2R16; R17 незалежно представляє собою Н, галоген, нітро, трифторометил, алкіл, арил, гетероарил, NR8aR9a або -X2R16; Х2 незалежно представляє собою прямий зв'язок, -О-, -СН2-, -ОСО-, карбоніл, -S-, -SO-, -SO2, -NR8CO-, -CONR8-, -SO2NR8-, -NR8SO2- или NR8a-; R16 незалежно представляє собою Н, алкіл, циклоалкіл, -SOR6, -SO2R6, -OCH3 гідроксиалкіл, галоалкіл, галоалкілокси або одну з наступних груп: 15 де * вказує на точку приєднання; m незалежно представляє ціле з 1-3; L відсутній або представляє групу двовалентного зв'язку, вибрану з алкілену, циклоалкілену, гетероциклілену, арилену або гетероарилену, в якій одна або декілька груп (-СН2-) можуть замінятися киснем або NR8 і в якій один або декілька атомів вуглецю можуть незалежно замінятися одним або двома замісниками, вибраними з групи компонентів, що включають галоген, гідрокси, алкокси, галоалкілокси, фосфоноокси або фосфонооксиалкіл; X3 незалежно представляє -СООН, -СООалкіл, -ОН, -SH, -SO3H або -SO2NR8R9; R18 незалежно представлено Н, фосфоноокси або фосфонооксиалкілом; R19 незалежно представляє собою Н, алкіл, циклоалкіл, алкіламіно або алкокси; При умові, що наступні сполуки відсутні: N-[6-(6,7-Диметоксихінолін-4-ілокси)-5фторобензотіазол-2-іл]-2-фенілацетамід, N-[6-(6,7Диметоксихінолін-4-ілокси)-бензотіазол-2-іл]-2фенілацетамід, N-[6-(6,7-Диметоксихінолін-4ілокси)-5-фторобензотіазол-2-іл]-3фенілпропіонамід, N-[6-(6,7-Диметоксихінолін-4ілокси)-5-фторобензотіазол-2-іл]-2-(3трифторометилфеніл)-ацетамід, 2-(3,5-Бістрифторометилфеніл)-N-[6-(6,7-диметоксихінолін4-ілокси)-5-фторобензотіазол-2-іл]-ацетамід, 2-(2Хлоро-5-трифторометилфенiл)-N-[6-(6,7диметоксихінолін-4-ілокси)-5-фторобензотіазол-2іл]-ацетамід; алкільна група, якщо не передбачено інше, означає лінійний або розгалужений С1-С6-алкіл, переважно, лінійний або розгалужений ланцюг, що складається з від одного до п'яти атомів вуглецю, лінійний або розгалужений С2-С6-алкенілу або лі 92730 16 нійну або розгалужену групу С2-С6-алкінілу, які можуть замінятися одним або декількома замісниками R'; С1-С6-Алкіл, С2-С6-алкеніл, С2-С6-алкініл - залишок можуть бути вибрані з групи, що містить СН3, -С2Н5, -СН=СН2, -С СН, -С3Н7, -СН(СН3)2, СН2-СН=СН2, -С(СН3)=СН2, -СН=СН-СН3, -С СН3, СН2-С СН, -С4Н9, -СН2-СН(СН3)2, -СН(СН3)-С2Н5, С(СН3)3-С5Н11, -С6Н13, -C(R')3, -C2(R')5, -CH2-C(R')3, -C3(R')7, -C2H4-C(R')3, -C2H4-CH=CH2, -CH=CH-C2H5, -CH=C(CH3)2, -СН2-СН=СН-СН3, -СН=СН-СН=СН2, -С2Н4-С СН, -С С-С2Н5, -СН2-С С-СН3, -С ССН=СН2, -СН=СН-С СН, -С2Н4-СН(СН3)2, СН(СН3)-С3Н7, -СН2-СН(СН3)-С2Н5, -СН(СН3)СН(СН3)2, -С(СН3)2-С2Н5, -СН2-С(СН3)3, -С3Н6СН=СН2, -СН=СН-С3Н7, -С2Н4-СН=СН-СН3, -СН2СН=СН-С2Н5, -СН2-СН=СН-СН=СН2, -СН=СНСН=СН-СН3, -СН=СН-СН2-СН=СН2, -С(СН3)=СНСН=СН2, -СН=С(СН3)-СН=СН2, -СН=СНС(СН3)=СН2, -СН2-СН=С(СН3)2, -С(СН3)=С(СН3)2, С3Н6-С СН, -С С-С3Н7, -С2Н4-С С-СН3, -СН2-С СС2Н5, -СН2-С С-СН=СН2, -СН2-СН=СН-С СН, СН2-С С-С СН, -С С-СН=СН-СН3, -СН=СН-С ССН3, -С С-С С-СН3, -С С-СН2-СН=СН2, -СН=СНСН2-С СН, -С С-СН2-С СН, -С(СН3)=СН-СН=СН2, -СН=С(СН3)-СН=СН2, -СН=СН-С(СН3)=СН2, С(СН3)=СН-ОСН,, -СН=С(СН3)-С СН, -С СС(СН3)=СН2, -С3Н6-СН(СН3)2, -С2Н4-СН(СН3)-С2Н5, -СН(СН3)-С4Н9, -СН2-СН(СН3)-С3Н7, -СН(СН3)-СН2СН(СН3)2, -СН(СН3)-СН(СН3)-С2Н5, -СН2-СН(СН3)СН(СН3)2, -СН2-С(СН3)2-С2Н5, -С(СН3)2-С3Н7, С(СН3)2-СН(СН3)2, -С2Н4-С(СН3)3, -СН(СН3)С(СН3)3, -С4Н8-СН=СН2, -СН=СН-С4Н9, -С3Н6СН=СН-СН3, -СН2-СН=СН-С3Н7, -С2Н4-СН=СНС2Н5, -СН2-С(СН3)=С(СН3)2, -С2Н4-СН=С(СН3)2, С4Н8-С СН, -С С-С4Н9, -С3Н6-С С-СН3, -СН2-С СС3Н7, -C2H4-C C-C2H5. 17 R' незалежно представляє собою Η, -CO2R", CONHR", -CR"O, -SO2NR", -NR"-CO-галоалкіл, NO2, -NR"-SO2-галоалкіл, -NR"-SO2-алкіл, -SО2алкіл, -NR"-CO-алкіл, -CN, алкіл, циклоалкіл, аміноалкіл, алкіламіно, алкокси, -ОН, -SH, алкілтіо, гідроксиалкіл, гідроксиалкіламіно, галоген, галоалкіл, галоалкілокси, арил, арилалкіл або гетероарил; R" незалежно представляє собою Н, галоалкіл, гідроксиалкіл, алкіл, циклоалкіл, арил, гетероарил або аміноалкіл; алкіленова група є двовалентним лінійним або розгалуженим С1-С6-алкіленом, переважно, лінійним або розгалуженим ланцюгом, що включає від одного до п'яти атомів вуглецю, лінійним або розгалуженим С2-С6-алкеніленом або лінійною або розгалуженою С2-С6-алкініленовою групою, яка може замінятися одним або декількома заступниками R'; циклоалкіленова група представляє собою двовалентну циклічну не ароматичну систему, що містить від трьох до восьми атомів вуглецю, переважно, від чотирьох до восьми атомів вуглецю, в якій один або декілька атомів вуглецю в циклі можуть замінятися групою Е, причому група Ε може бути представлена О, S, SO, SO2, N або NR", R", описаними вище; гетероцикпіленова група є двовалентною гетероциклічною не ароматичною групою з 3 до 8 елементів, що містить, принаймні, один гетероатом, вибраний з групи, що включає О, N і S, причому гетероцикліленова група може бути вплавлена в інший не ароматичний цикл і може замінятися одним або декількома заступниками R', при цьому R' є елементами, описаними вище; ариленова група представляєсобою двовалентну ароматичну групу, що містить від п'яти до п'ятнадцяти атомів вуглецю, які можуть замінятися одним або декількома заступниками R' і можуть бути спаяні з іншим ароматичним циклом, при цьому R' є елементами, описаними вище; гетероариленова група представляє собою двовалентну 5-або 6-елементну гетероциклічну групу, яка містить, принаймні, один гетероатом, вибраний з групи, що включає О, N і S, причому гетероцикліленова група може бути вплавлена в інший ароматичний цикл і може замінятися одним або декількома заступниками R', при цьому R' є елементами, описаними вище; циклоалкільна група представляє собою циклічну не ароматичну систему, що містить від трьох до восьми атомів вуглецю, переважно, від чотирьох до восьми атомів вуглецю, в якій один або декілька атомів вуглецю в циклі можуть замінятися групою Е, причому група Ε може бути представлена О, S, SO, SO2, N або NR", R", описаними вище; залишок С3-С8-циклоалкілу може бути вибраний з групи, що включає -цикло-С3Н5, цикло-С4Н7, циклоС5Н9, цикло-С6Н11, цикло-С7Н13, цикло-С8Н15, морфолін-4-іл, піперазиніл, 1-алкілпіперазин-4-іл; група алкокси представляє собою О-алкільну групу, причому алкільна група відповідає групі, описаній вище; переважно, групою алкокси є група метокси, етокси, ізопропокси, t-бутокси або пентокси; 92730 18 група алкілтіо представляє собою S-алкільну групу, причому алкільна група відповідає групі, описаній вище; галоалкільна група представляє собою алкільну групу, яка заміняється від одного до п'яти атомами галогену, причому алкільна група відповідає групі, описаній вище; галоалкільною групою, переважно, є -C(R10)3, -CR10(R10')2, -CR10(R10')R10'', C2(R10)5, -CH2-C(R10)3, -CH2-CR10(R10')2, -CH2CR10(R10')R10", -C3(R10)7, або C2H4-C(R10)3, де R10,R10', і R10'' уявлені у вигляді F, СІ, Br, І, переважно, F; гідроксиалкільна група представляє собою НО-алкільну групу, причому алкільна група відповідає групі, описаній вище; галоалкілоксильною група представляє собою алкоксильну групу, яка заміняється від одного до п'яти атомами галогену, причому алкільна група відповідає групі, описаній вище; галоалкілоксильною групою, переважно, є OC(R10)3, -OCR10(R10')2, OCR10(R10')R10'', -OC2(R10)5, -OCH2-C(R10)3, -OCH2CR10(R10')2, -OCH2-CR10(R10')R10", -OC3(R10)7, або OC2H4-C(R10)3, де R10,R10', і R10" уявлені у вигляді F, СІ, Br, I, переважно, F; гидроксиалкіламіновою групою є (НО-алкт)2-Nгрупа або НО-алкіл-NH-групa, причому алкільна група відповідає групі, описаній вище; алкіламінова група представляє собою HNалкілову або N-диалкільну групу, причому алкільна група відповідає групі, описаній вище; галогенова група представляє собою фтор, хлор, бром або йод; арильна група представляє собою ароматичну групу, що містить від п'яти до п'ятнадцяти атомів вуглецю, які можуть замінятися одним або декількома заступниками R'; де R' є елементами, показаними вище, арильною групою є, переважно, фенільна група, o-C6H4-R', m-C6H4-R', p-C6H4-R', 1нафтил, 2-нафтил, 1-антраценіл або 2-антраценіл; гетероарильна група представляє собою 5або 6-елементну гетероциклічну групу, яка містить, принаймні один гетероатом, подібний О, N, S. Гетероциклічна група може бути спаяна з іншим ароматичним циклом. Наприклад, дана група може бути вибрана з переліку, що включає такі групи, як: тіадiазол, тіазол-2-іл, тіазол-4-іл, тіазол-5-іл, ізотіазол-3-іл, ізотіазол-4-іл, ізотіазол-5-іл, оксазол-2іл, оксазол-4-іл, оксазол-5-іл, ізооксазол-3-іл, ізооксазол-4-iл, ізооксазол-5-іл, 1,2,4-оксадіазол-3-іл, 1,2,4-оксадiазол-5-iл, 1,2,5-оксадiазол-3-iл, 1,2,5оксадiазол-4-iл, 1,2,4-тіадіазол-3-іл, 1,2,4тіадіазол-5-іл, 1,2,5-тіадіазол-3-іл, 1,2,5-тіадіазол4-іл, ізотіазол-3-іл, ізотіазол-4-іл, iзотiазол-5-iл, 1,2,5-тiадiазол-3-iл, 1-iмiдазолил, 2-iмiдазолил, 1,2,5-тіадіазол-4-іл, 4-імідазоліл, 1-піроліл, 2піроліл, 3-піроліл, 2-фураніл, 3-фураніл, 2-тієнил, 3-тієніл, 2-піридил, 3-піридил, 4-піридил, 2-піраніл, 3-піраніл, 4-піраніл, 2-піримідиніл, 4-піримідиніл, 5піримідиніл, пірид-2-iл, пірид-3-iл, пірид-4-iл, пірид5-iл, пірид-6-iл, 3-піридазиніл, 4-піридазиніл, 2піразиніл, 1-піразоліл, 3-піразоліл, 4-піразоліл, 1,2,3-триазол-4-іл, 1,2,3-триазол-5-іл, 1,2,4триазол-3-іл, 1,2,4-триазол-5-іл, 1Н-тетразол-2-іл, 1Н-тетразол-3-іл, тетразоліл, акридил, феназиніл, карбазоліл, феноксазиніл, індолізин, 2-індоліл, 3 19 92730 20 індоліл, 4-індоліл, 5-індоліл, 6-індоліл, 7-індоліл, 1ізоіндоліл, 3-ізоіндоліл, 4-ізоіндоліл, 5-ізоіндоліл, 6-ізоіндоліл, 7-ізоіндоліл, 2-індолініл, 3-індолініл, 4індолініл, 5-індолініл, 6-індолініл, 7-індолініл, бензо[b]фураніл, бензофуразан, бензотіофуразан, бензотриазол-1-іл, бензотриазол-4-іл, бензотриазол-5-іл, бензотриазол-6-іл, бензотриазол-7-іл, бензотриазин, бензо[b]тіофеніл, бензімідазоліл, бензотіазоліл, хіназолініл, хіноксазолініл, цинолін, хінолініл, тетрагідрохінолініл, ізохінолініл, тетрагідроізохінолініл, пурин, фталазин, птеридин, тіатетраазаінден, тіатриазаінден, ізотіазолопиразин, ізотіазолопіримідин, піразолотриазин, піразолопіримідин, імідазопіридазин, імідазопіримідин, імідазопіридин, імідазолотриазин, тріазолотриазин, триазолопіридин, триазолопіразин, триазолопіримідин, триазолопіридазин. Гетероциклічна група може замінятися одним або декількома заступниками R', при цьому R' є елементами, описаними вище; фосфонооксигрупою є О-Р(=О)(ОН)2 або її сіль; фосфонооксиалкільна група є групою -алкіл-ОР(=О)(ОН)2 або її сіллю, при цьому алкіл є елементом, описаним вище. Даний винахід відноситься також до сполук за загальною формулою (Іа) або до їх солей або до їх фізіологічно функціонуючих похідних, або до їх стереоізомерів де * указує на точку приєднання; R11 незалежно є Н, NHR8a або одну з наступних груп: СН3, -СН2-С СН, -С4Н9, -СН2-СН(СН3)2, -СН(СН3)С2Н5, -С(СН3)3-С5Н11, -С6Н13, -C(R')3, -C2(R')5, -CH2C(R')3, C3(R')7, -C2H4-C(R')3, -C2H4-CH=CH2, CH=CH-C2H5, -СН=С(СН3)2, -СН2-СН=СН-СН3, СН=СН-СН=СН2, -С2Н4-С СН, -С C-С2Н5, -СН2С С-СН3, -С С-СН=СН2, -СН=СН-С СН, -С2Н4СН(СН3)2, -СН(СН3)-С3Н7, -СН2-СН(СН3)-С2Н5, СН(СН3)-СН(СН3)2, -С(СН3)2-С2Н5, -СН2-С(СН3)3, С3Н6-СН=СН2, -СН=СН-С3Н7, -С2Н4-СН=СН-СН3, СН2-СН=СН-С2Н5, -СН2-СН=СН-СН=СН2, -СН=СНСН=СН-СН3, -СН=СН-СН2-СН=СН2, -С(СН3)=СНСН=СН2, -СН=С(СН3)-СН=СН2, -СН=СНС(СН3)=СН2, -СН2-СН=С(СН3)2, -С(СН3)=С(СН3)2, С3Н6-С СН, -С С-С3Н7, -С2Н4-С С-СН3, -СН2-С СС2Н5, -СН2-С С-СН=СН2, -СН2-СН=СН-С СН, СН2-С С-С СН, -С С-СН=СН-СН3, -СН=СН-С ССН3, -С С-С С-СН3, -С С-СН2-СН=СН2, -СН=СНСН2-С=СН, -С С-СН2-С СН, -С(СН3)=СН-СН=СН2, -СН=С(СН3)-СН=СН2, -СН=СН-С(СН3)=СН2, С(СН3)=СН-С СН, -СН=С(СН3)-С СН, -С СС(СН3)=СН2, -С3Н6-СН(СН3)2, -С2Н4-СН(СН3)-С2Н5, -СН(СН3)-С4Н9, -СН2-СН(СН3)-С3Н7, -СН(СН3)-СН2СН(СН3)2, -СН(СН3)-СН(СН3)-С2Н5, -СН2-СН(СН3)СН(СН3)2, -СН2-С(СН3)2-С2Н5, -С(СН3)2-С3Н7, С(СН3)2-СН(СН3)2, -С2Н4-С(СН3)3, -СН(СН3) де * указує на точку приєднання; R13a незалежно є Н, галоген, нітро, трифторометил, алкіл, -NR8aR9a або X2R16; при цьому, R2, R3, R4, R5, R6, R6a, R7, R8, R8a, R9, R9a, R12, R13, R16, або X2 є елементами, описаними вище; алкільна група, якщо не передбачено інше, означає лінійний або розгалужений С1-С6-алкіл, переважно, лінійний або розгалужений ланцюг, що включає від одного до п'яти атомів вуглецю, лінійний або розгалужений С2-С6-алкеніл або лінійну або розгалужену групу С2-С6-алкінілу, які можуть замінятися одним або декількома заступниками R'; С1-С6-алкіл, С2-С6-алкеніл, С2-С6-алкініл - залишок можуть бути вибрані з групи, що містить СН3, -С2Н5, -СН=СН2, -C CH, -С3Н7, -СН(СН3)2, СН2-СН=СН2, -С(СН3)=СН2, -СН=СН-СН3, -С С Де: заступник -Ya-R1a приєднаний до 5-або 6позиції бензазолу; Xа незалежно представляє S, О, SO або SO2; Уа незалежно представляє S, NR2, SO або SO2; Аа незалежно представляє СО- CS- SOSO2- СО2- CONR8- NR8CO- NR8CONR9NR8COO- NR8NR9CO- NR8OCO- ONR8CO8 3 NR SO2-, де указує точку приєднання до R ; 1a R незалежно є однією з наступних груп: 21 С(СН3)3, -С4Н8-СН=СН2, -СН=СН-С4Н9, -С3Н6СН=СН-СН3, -СН2-СН=СН-С3Н7, -С2Н4-СН=СНС2Н5, -СН2-С(СН3)=С(СН3)2, -С2Н4-СН=С(СН3)2, С4Н8-С СН, -С С-С4Н9, -С3Н6-С С-СН3, -СН2-С СС3Н7, -Ο2Η4-C C-C2Η5· R' незалежно представляє Н, -CO2R", CONHR", -CR'O, -SO2NR", -NR"-CO-галоалкіл, NO2, -NR"-SO2-гaлoaлкiл, -NR"-SO2-алкілm, -SО2алкіл, -NR"-CO-алкіл, -CN, алкіл, циклоалкіл, аміноалкіл, алкіламіно, алкокси, -ОН, -SH, алкілтіо, гідроксиалкіл, гідроксиалкіламіно, галоген, галоалкіл, галоалкілокси, арил, арилалкіл або гетероарил; R" незалежно представляє Н, галоалкіл, гідроксиалкіл, алкіл, циклоалкіл, арил, гетероарил або аміноалкіл; алкіленова група є двовалентним лінійним або розгалуженим С1-С6-алкіленом, переважно, лінійним або розгалуженим ланцюгом, що включає від одного до п'яти атомів вуглецю, лінійним або розгалуженим С2-С6-алкеніленом або лінійною або розгалуженою С2-С6-алкініленовою групою, яка може замінятися одним або декількома заступниками R'; циклоалкіленова група представляє собою двовалентну циклічну не ароматичну систему, що містить від трьох до восьми атомів вуглецю, переважно, від чотирьох до восьми атомів вуглецю, в якій один або декілька атомів вуглецю в циклі можуть замінятися групою Е, причому група Ε може бути представлена О, S, SO, SO2, N або NR", R", описаними вище; гетероцикліленова група є двовалентною гетероциклічною не ароматичною групою з 3 до 8 елементів, що містить, принаймні, один гетероатом, вибраний з групи, що включає О, N і S, причому гетероцикліленова група може бути вплавлена в інший не ароматичний цикл і може заміщатися одним або декількома заступниками R', при цьому R' є елементами, описаними вище; ариленова група представляє собою двовалентну ароматичну групу, що містить від п'яти до п'ятнадцяти атомів вуглецю, які можуть заміщатися одним або декількома заступниками R' і можуть бути спаяні з іншим ароматичним циклом, при цьому R' є елементами, описаними вище; гетероариленова група представляє собою двовалентну 5-або 6-елементну гетероциклічну групу, яка містить, принаймні, один гетероатом, вибраний з групи, що включає О, N і S, причому гетероцикліленова група може бути вплавлена в інший ароматичний цикл і може заміщатися одним або декількома заступниками R', при цьому R' є елементами, описаними вище; циклоалкільна група представляє собою циклічну не ароматичну систему, що містить від трьох до восьми атомів вуглецю, переважно, від чотирьох до восьми атомів вуглецю, в якій один або декілька атомів вуглецю в циклі можуть замінятися групою Е, причому група Ε може бути представлена О, S, SO, SO2, N або NR", R", описаними вище; залишок С3-С8-циклоалкілу може бути вибраний з групи, що включає -цикло-С3Н5, цикло-С4Н7, циклоС6Н9, цикло-С6Н11, цикло-С7Н13, цикло-С8Н15, морфолін-4-іл, піперазиніл, 1-алкілпіперазин-4-іл; 92730 22 група алкокси представляє собою О-алкільну групу, причому алкільна група відповідає групі, описаній вище; переважно, групою алкокси є група метокси, етокси, ізопропокси, t-бутокси або пентокси; група алкілтіо представляє собою S-алкільну групу, причому алкільна група відповідає групі, описаній вище; галоалкільна група представляє собою алкільну групу, яка заміняється від одного до п'яти атомами галогену, причому алкільна група відповідає групі, описаній вище; галоалкільною групою, переважно, є -C(R10)3, -CR10(R10')2, -CR10(R10')R10'', C2(R10)5, -CH2-C(R10)3, -CH2-CR10(R10')2, -CH2CR10(R10')R10", -C3(R10)7, або C2H4-C(R10)3, де R10,R10', і R10'' уявлені у вигляді F, СІ, Br, І, переважно, F; гідроксиалкільна група представляє собою НО-алкілову групу, причому алкільна група відповідає групі, описаній вище; галоалкілоксилова група представляє собою алкоксильну групу, яка заміняється від одного до п'яти атомами галогену, причому алкільна група відповідає групі, описаній вище; галоалкілоксильною групою, переважно, є -OC(R10)3, -OCR10(R10')2, -OCR10(R10')R10", -OC2(R10)5, -OCH2-C(R10)3, -OCH2CR10(R10')2, -OCH2-CR10(R10')R10", -OC3(R10)7- або OC2H4-C(R10)3, де R10, R10', і R10" уявлені у вигляді F, СІ, Br, I, переважно, F; гідроксиалкіламіновою групою є (НО-алкіл)2-Nгрупа або НО-алкіл-NH-групa, причому алкільна група відповідає групі, описаній вище; алкіламінова група представляє собою HNалкільну або N-диалкільну групу, причому алкільна група відповідає групі, описаній вище; галогенова група представляє собою фтор, хлор, бром або йод; арильна група представляє собою ароматичну групу, що містить від п'яти до п'ятнадцяти атомів вуглецю, які можуть замінятися одним або декількома заступниками R'; де R' є елементами, показаними вище, арильною групою є, переважно, фенільна група, o-C6H4-R', m-C6H4-R', p-C6H4-R', 1нафтил, 2-нафтил, 1-антраценіл або 2-антраценіл; гетероарильна група представляє собою 5або 6-елементну гетероциклічну групу, яка містить, принаймні один гетероатом, подібний О, N, S. Гетероциклічна група може бути спаяна з іншим ароматичним циклом. Наприклад, дана група може бути вибрана з переліку, що включає такі групи, як: тіадiазол, тіазол-2-іл, тіазол-4-іл, тіазол-5-іл, ізотіазол-3-іл, ізотіазол-4-іл, ізотіазол-5-іл, оксазол-2іл, оксазол-4-іл, оксазол-5-іл, ізооксазол-3-іл, ізооксазол-4-iл, ізооксазол-5-іл, 1,2,4-оксадіазол-3-іл, 1,2,4-оксадiазол-5-iл, 1,2,5-оксадiазол-3-iл, 1,2,5оксадiазол-4-iл, 1,2,4-тіадіазол-3-іл, 1,2,4тіадіазол-5-іл, 1,2,5-тіадіазол-3-іл, 1,2,5-тіадіазол4-іл, ізотіазол-3-іл, ізотіазол-4-іл, iзотiазол-5-iл, 1,2,5-тiадiазол-3-iл, 1-iмiдазолил, 2-iмiдазолил, 1,2,5-тіадіазол-4-іл, 4-імідазоліл, 1-піроліл, 2піроліл, 3-піроліл, 2-фураніл, 3-фураніл, 2-тієнил, 3-тієніл, 2-піридил, 3-піридил, 4-піридил, 2-піраніл, 3-піраніл, 4-піраніл, 2-піримідиніл, 4-піримідиніл, 5піримідиніл, пірид-2-iл, пірид-3-iл, пірид-4-iл, пірид5-iл, пірид-6-iл, 3-піридазиніл, 4-піридазиніл, 2 23 піразиніл, 1-піразоліл, 3-піразоліл, 4-піразоліл, 1,2,3-триазол-4-іл, 1,2,3-триазол-5-іл, 1,2,4триазол-3-іл, 1,2,4-триазол-5-іл, 1Н-тетразол-2-іл, 1Н-тетразол-3-іл, тетразоліл, акридил, феназиніл, карбазоліл, феноксазиніл, індолізин, 2-індоліл, 3індоліл, 4-індоліл, 5-індоліл, 6-індоліл, 7-індоліл, 1ізоіндоліл, 3-ізоіндоліл, 4-ізоіндоліл, 5-ізоіндоліл, 6-ізоіндоліл, 7-ізоіндоліл, 2-індолініл, 3-індолініл, 4індолініл, 5-індолініл, 6-індолініл, 7-індолініл, бензо[b]фураніл, бензофуразан, бензотіофуразан, бензотриазол-1-іл, бензотриазол-4-іл, бензотриазол-5-іл, бензотриазол-6-іл, бензотриазол-7-іл, бензотриазин, бензо[Ь]тіофеніл, бензімідазоліл, бензотіазоліл, хіназолініл, хіноксазолініл, цинолін, хінолініл, тетрагідрохінолініл, ізохінолініл, тетрагідроізохінолініл, пурин, фталазин, птеридин, тіатетраазаінден, тіатриазаінден, ізотіазолопиразин, ізотіазолопіримідин, піразолотриазин, піразолопіримідин, імідазопіридазин, імідазопіримідин, імідазопіридин, імідазолотриазин, тріазолотриазин, триазолопіридин, триазолопіразин, триазолопіримідин, триазолопіридазин. Гетероциклічна група може заміщатися одним або декількома заступниками R', при цьому R' є елементами, описаними вище; фосфонооксигрупою є О-Р(=О)(ОН)2 або її сіль; фосфонооксиалкільна група є групою -алкіл-ОР(=О)(ОН)2 або її сіллю, при цьому алкіл є елементом, описаним вище. Даний винахід відноситься також до сполук за загальною формулою (II) або до їх солей або до фізіологічно фунціонуючого похідного, або до його стереоізомеру де: заступник -Yb приєднаний до 5-або 6-позиції бензазолу; Хb незалежно представляє S, О, SO або SO2; Yb незалежно представляє S, NR2, SO або SO2; Ab незалежно представляє СО- CS- SOSO2- CO2- CONR8- NR8CO- NR8CONR9NR8COO- NR8NR9CO- NR8OCO- ONR8CONR8SO2-, де указує точку приєднання до R3; b R4 незалежно є Н, -SOR6, -SO2R6, -SO3R6, NO2, -CN, -CF3, -OCH3, -OCF3, алкіл, циклоалкіл, алкокси, -NH2, алкіламіно, -NR7 COR6, галоген, ОН, -SH, алкілтіо, галоалкіл, галоалкілокси, арил або гетероарил; при цьому, R2, R3, R5, R6, R6a, R8, R8a, R9, R9a, R11, R12, R16, X2 є елементами, описаними вище; алкільна група, якщо не передбачено інше, означає лінійну або розгалужену групу С1-С6алкілу, переважно, лінійний або розгалужений ла 92730 24 нцюг, що складається з від одного до п'яти атомів вуглецю, лінійний або розгалужений С2-С6-алкеніл або лінійну або розгалужену групу С2-С6-алкінілу, які можуть заміщатися одним або декількома заступниками R'; С1-С6-Алкіл, С2-С6-алкеніл, С2-С6-алкініл - залишок можуть бути вибрані з групи, що містить СН3, -С2Н5, -СН=СН2, -С СН, -С3Н7, -СН(СН3)2, СН2-СН=СН2, -С(СН3)=СН2, -СН=СН-СН3, -С ССН3, -СН2-С СН, -С4Н9, -СН2-СН(СН3)2, -СН(СН3)С2Н5, -С(СН3)3-С5Н11, -С6Н13, -C(R')3, -C2(R')5, -CH2C(R')3, -C3(R')7, -C2H4-C(R')3, -C2H4-CH=CH2, CH=CH-C2H5, -СН=С(СН3)2, -СН2-СН=СН-СН3, СН=СН-СН=СН2, -С2Н4-С СН, -С С-С2Н5, -СН2С С-СН3, -С С-СН=СН2, -СН=СН-С СН, -С2Н4СН(СН3)2, -СН(СН3)-С3Н7, -СН2-СН(СН3)-С2Н5, СН(СН3)-СН(СН3)2, -С(СН3)2-С2Н5, -СН2-С(СН3)3, С3Н6-СН=СН2, -СН=СН-С3Н7, -С2Н4-СН=СН-СН3, СН2-СН=СН-С2Н5, -СН2-СН=СН-СН=СН2, -СН=СНСН=СН-СН3, -СН=СН-СН2-СН=СН2, -С(СН3)=СНСН=СН2, -СН=С(СН3)-СН=СН2, -СН=СНС(СН3)=СН2, -СН2-СН=С(СН3)2, -С(СН3)=С(СН3)2, С3Н6-С СН, -С С-С3Н7, -С2Н4-С С-СН3, -СН2-С СС2Н5, -СН2-С С-СН=СН2, -СН2-СН=СН-С СН, СН2-С С-С СН, -С С-СН=СН-СН3, -СН=СН-С ССН3, -С С-С С-СН3, -С С-СН2-СН=СН2, -СН=СНСН2-С СН, -С С-СН2-С СН, -С(СН3)=СН-СН=СН2, -СН=С(СН3)-СН=СН2, -СН=СН-С(СН3)=СН2, С(СН3)=СН-С СН2, -СН=С(СН3)-С СН, -С СС(СН3)=СН2, -С3Н6-СН(СН3)2, -С2Н4-СН(СН3)-С2Н5, -СН(СН3)-С4Н9, -СН2-СН(СН3)-С3Н7, -СН(СН3)-СН2СН(СН3)2, -СН(СН3)-СН(СН3)-С2Н5, -СН2-СН(СН3)СН(СН3)2, -СН2-С(СН3)2-С2Н5, -С(СН3)2-С3Н7, С(СН3)2-СН(СН3)2, -С2Н4-С(СН3)3, -СН(СН3)С(СН3)3, -С4Н8-СН=СН2, -СН=СН-С4Н9, -С3Н6СН=СН-СН3, -СН2-СН=СН-С3Н7, -С2Н4-СН=СНС2Н5, -СН2-С(СН3)=С(СН3)2, -С2Н4-СН=С(СН3)2, С4Н8-С СН, -С С-С4Н9, -С3Н6-C C-СН3, -СН2-С СС3Н7, -С2Н4-С С-С2Н5. R' незалежно представляє Η, -CO2R", CONHR", -CR"O, -SO2NR", -NR"-CO-галоалкіл, NO2, -NR"-SО2-галоалкіл, -NR"-SO2-алкіл, -SО2алкіл, -NR"-CO-алкіл, -CN, алкіл, циклоалкіл, аміноалкіл, алкіламіно, алкокси, -ОН, -SH, алкілтіо, гідроксиалкіл, гідроксиалкіламіно, галоген, галоалкіл, галоалкілокси, арил, арилалкіл або гетероарил; R" незалежно представляє Н, галоалкіл, гідроксиалкіл, алкіл, циклоалкіл, арил, гетероарил або аміноалкіл; алкіленова група є двовалентним лінійним або розгалуженим С1-С6-алкіленом, переважно, лінійним або розгалуженим ланцюгом, що включає від одного до п'яти атомів вуглецю, лінійним або розгалуженим С2-С6-алкеніленом або лінійною або розгалуженою С2-С6-алкініленовою групою, яка може замінятися одним або декількома заступниками R'; циклоалкіленова група представляє собою двовалентну циклічну не ароматичну систему, що містить від трьох до восьми атомів вуглецю, переважно, від чотирьох до восьми атомів вуглецю, в якій один або декілька атомів вуглецю в циклі можуть замінятися групою Е, причому група Ε може 25 бути представлена О, S, SO, SO2, N або NR", R", описаними вище; гетероцикліленова група є двовалентною гетероциклічною не ароматичною групою з 3 до 8 елементів, що містить, принаймні, один гетероатом, вибраний з групи, що включає О, N і S, причому гетероцикліленова група може бути синтезована в інший не ароматичний цикл і може заміщатися одним або декількома заступниками R', при цьому R' є елементами, описаними вище; ариленова група представляє собою двовалентну ароматичну групу, що містить від п'яти до п'ятнадцяти атомів вуглецю, які можуть заміщатися одним або декількома заступниками R' і можуть бути спаяні з іншим ароматичним циклом, при цьому R' є елементами, описаними вище; гетероариленова група представляє собою двовалентну 5-або 6-елементну гетероциклічну групу, яка містить, принаймні, один гетероатом, вибраний з групи, що включає О, N і S, причому гетероцикліленова група може бути вплавлена в інший ароматичний цикл і може заміщатися одним або декількома заступниками R', при цьому R' є елементами, описаними вище; циклоалкільна група представляє собою циклічну не ароматичну систему, що містить від трьох до восьми атомів вуглецю, переважно, від чотирьох до восьми атомів вуглецю, в якій один або декілька атомів вуглецю в циклі можуть замінятися групою Е, причому група Ε може бути представлена О, S, SO, SO2, N або NR", R", описаними вище; залишок С3-С8-цикпоалкілу може бути вибраний з групи, що включає -цикло-С3Н5, цикло-С4Н7, циклоС5Н9, цикло-С6Н11, цикло-С7Н13, цикло-С8Н15, морфолін-4-іл, піперазиніл, 1-алкілпіперазин-4-іл; група алкокси представляє собою О-алкілову групу, причому алкілова група відповідає групі, описаній вище; переважно, групою алкокси є група метокси, етокси, ізопропокси, t-бутокси або пентокси; група алкілтіо представляє собою S-алкільну групу, причому алкільна група відповідає групі, описаній вище; галоалкільна група представляє собою алкільну групу, яка заміняється від одного до п'яти атомами галогену, причому алкільна група відповідає групі, описаній вище; галоалкільною групою, переважно, є -C(R10)3, -CR10(R10')2, -CR10(R10')R10", C2(R10)5, -CH2-C(R10)3, -CH2-CR10(R10')2, -CH2CR10(R10')R10", -C3(R10)7, або C2H4-C(R10)3, де R10,R10', і R10'' уявлені у вигляді F, СІ, Вr, І, переважно, F; гідрокси алкільна група представляє собою НО-алкілову групу, причому алкільна група відповідає групі, описаній вище; галоалкілоксильна група представляє собою алкоксильну групу, яка заміняється від одного до п'яти атомами галогену, причому алкільна група відповідає групі, описаній вище; галоалкілоксильною групою, переважно, є -OC(R10)3, -OCR10(R10')2, -OCR10(R10')R10", -OC2(R10)5, -OCH2-C(R10)3, -OCH2CR10(R10')2, -OCH2-CR10(R10')R10", -OC3(R10)7, або OC2H4-C(R10)3, де R10, R10', і R10" уявлені у вигляді F, СІ, Вr, І, переважно, F; 92730 26 гідроксиалкіламіновою групою є (НО-алкіл)2-Nгрупа або НО-алкіл-NH-групa, причому алкільна група відповідає групі, описаній вище; алкіламінова група представляє собою HNалкілову або N-диалкілову групу, причому алкільна група відповідає групі, описаній вище; галогенова група представляє собою фтор, хлор, бром або йод; арильна група представляє собою ароматичну групу, що містить від п'яти до п'ятнадцяти атомів вуглецю, які можуть замінятися одним або декількома заступниками R'; де R' є елементами, показаними вище, арильною групою є, переважно, фенільна група, o-C6H4-R', m-C6H4-R', p-C6H4-R', 1нафтил, 2-нафтил, 1-антраценіл або 2-антраценіл; гетероарильна група представляє собою 5або 6-елементну гетероциклічну групу, яка містить, принаймні один гетероатом, подібний О, N, S. Гетероциклічна група може бути спаяна з іншим ароматичним циклом. Наприклад, дана група може бути вибрана з переліку, що включає такі групи, як: тіадiазол, тіазол-2-іл, тіазол-4-іл, тіазол-5-іл, ізотіазол-3-іл, ізотіазол-4-іл, ізотіазол-5-іл, оксазол-2іл, оксазол-4-іл, оксазол-5-іл, ізооксазол-3-іл, ізооксазол-4-iл, ізооксазол-5-іл, 1,2,4-оксадіазол-3-іл, 1,2,4-оксадiазол-5-iл, 1,2,5-оксадiазол-3-iл, 1,2,5оксадiазол-4-iл, 1,2,4-тіадіазол-3-іл, 1,2,4тіадіазол-5-іл, 1,2,5-тіадіазол-3-іл, 1,2,5-тіадіазол4-іл, ізотіазол-3-іл, ізотіазол-4-іл, iзотiазол-5-iл, 1,2,5-тiадiазол-3-iл, 1-iмiдазолил, 2-iмiдазолил, 1,2,5-тіадіазол-4-іл, 4-імідазоліл, 1-піроліл, 2піроліл, 3-піроліл, 2-фураніл, 3-фураніл, 2-тієнил, 3-тієніл, 2-піридил, 3-піридил, 4-піридил, 2-піраніл, 3-піраніл, 4-піраніл, 2-піримідиніл, 4-піримідиніл, 5піримідиніл, пірид-2-iл, пірид-3-iл, пірид-4-iл, пірид5-iл, пірид-6-iл, 3-піридазиніл, 4-піридазиніл, 2піразиніл, 1-піразоліл, 3-піразоліл, 4-піразоліл, 1,2,3-триазол-4-іл, 1,2,3-триазол-5-іл, 1,2,4триазол-3-іл, 1,2,4-триазол-5-іл, 1Н-тетразол-2-іл, 1Н-тетразол-3-іл, тетразоліл, акридил, феназиніл, карбазоліл, феноксазиніл, індолізин, 2-індоліл, 3індоліл, 4-індоліл, 5-індоліл, 6-індоліл, 7-індоліл, 1ізоіндоліл, 3-ізоіндоліл, 4-ізоіндоліл, 5-ізоіндоліл, 6-ізоіндоліл, 7-ізоіндоліл, 2-індолініл, 3-індолініл, 4індолініл, 5-індолініл, 6-індолініл, 7-індолініл, бензо[b]фураніл, бензофуразан, бензотіофуразан, бензотриазол-1-іл, бензотриазол-4-іл, бензотриазол-5-іл, бензотриазол-6-іл, бензотриазол-7-іл, бензотриазин, бензо[b]тіофеніл, бензімідазоліл, бензотіазоліл, хіназолініл, хіноксазолініл, цинолін, хінолініл, тетрагідрохінолініл, ізохінолініл, тетрагідроізохінолініл, пурин, фталазин, птеридин, тіатетраазаінден, тіатриазаінден, ізотіазолопиразин, ізотіазолопіримідин, піразолотриазин, піразолопіримідин, імідазопіридазин, імідазопіримідин, імідазопіридин, імідазолотриазин, тріазолотриазин, триазолопіридин, триазолопіразин, триазолопіримідин, триазолопіридазин. Гетероциклічна група може заміщатися одним або декількома заступниками R', при цьому R' є елементами, описаними вище; фосфонооксигруппою є О-Р(=О)(ОН)2 або її сіль; 27 фосфонооксиалкільна група є групою -алкіл-ОР(=О)(ОН)2 або її сіллю, при цьому алкіл є елементом, описаним вище. Даний винахід також направлений на створення фармацевтичної композиції, що містить сполуку за формулою (І) в незв'язаному вигляді або у вигляді фармацевтично прийнятних солей і фізіологічно функціонуючих похідних разом з фармацевтично прийнятним розчинником або наповнювачем. Термін «фізіологічно функціонуюче похідне» в контексті даного опису відноситься до сполук, які не є фармацевтично активними самі по собі, але які перетворюються на свою фармацевтично активну форму in vivo, тобто в організмі, в який дана сполука вводиться. Прикладами фізіологічно функціонуючих похідних є проліки, описані нижче в матеріалах даної заявки. Проліки сполук за даним винаходом включають, не обмежуючись прерахованим нижче, ефіри, які трансформуються in vivo у відповідний активний спирт, ефіри, які трансформуються in vivo у відповідну активну кислоту, іміни, які трансформуються in vivo у відповідні аміни, іміни, які метаболізуються in vivo у відповідне активне похідне карбонілу (наприклад, альдегід або кетон), 1карбоксиаміни, які декарбоксилізуються in vivo в активний амін, фосфорилокси-сполуки, які дефосфорилуються in vivo фосфатазою в активні спирти, і аміди, які метаболізуються у відповідний активний амін або кислоту, відповідно. Термін «стереоізомери» в контексті даного опису відноситься до сполук, принаймні, з одним стереогенним центром, що має R- або Sконфігурацію. Слід зауважити, що в сполуках більш, ніж з одним стереогенним центром, кожний з них, незалежно один від одного, може мати Rабо S-конфігурацію. Термін «стереоізомер» в контексті даного опису відноситься також до солей сполук, описаних в даному документі, з оптично активними кислотами або основами. Крім того, даний винахід забезпечує способи приготування сполук за винаходом, наприклад, сполук у відповідності до формули (І). Сполуки за формулою (І), формулою (Іа), формулою (II) можуть бути приготовані з використанням різних способів. Однією з можливостей синтезу сполук за формулою (І) є забезпечення реакції сполуки за формулою (VII), де R2, R4, R5, А, X, Υ визначені у формулі (І), формулі (Іа), формулі (II), зі сполукою за формулою (VIII), де R1, відповідає наведеному вище визначенню, a LG містить групу, що залишилася, наприклад, СІ, Вr, І. Може бути використане або нуклеофільне заміщення або каталізоване паладієм перехресне з'єднання. Якщо Υ=NR2, R2 може бути доданий до або після додавання R1. 92730 28 Інший спосіб синтезу сполук за формулою (І), формулою (Іа), формулою (II) включає операцію додавання R5 до сполуки за формулою (IX), причому R1, R4, X і Υ визначені у формулі (І), формулі (Іа), формулі (II), з подальшою реакцією з кислотним хлоридом, карбоновою кислотою, хлоридом сульфонової кислоти або ізоціанатом (ефіром ізоціанової кислоти), або навпаки. Сполуки за формулою (IX) можуть бути синтезовані шляхом забезпечення реакції сполуки за формулою (X), причому R4, X і Υ визначені у формулі (І), формулі (Іа), формулі (II), із сполукою за формулою (VIII), де R1, відповідає приведеному вище визначенню по формулі (І), формулі (Іа), формулі (II), a LG містить групу, що залишилася, наприклад, СІ, Вr, І. Може бути використано або нуклеофільне заміщення або каталізоване паладієм перехресне з'єднання. Може виникнути потреба в захисті (наприклад, Вос. protection) 2-аміно-групи бензазолу. Якщо Υ=NR2, R2 може бути доданий до або після додавання R1. Сполуки за формулою (VII), де Υ=ΝΗ, можуть бути синтезовані шляхом відновлення сполуки за формулою (XI), де R3, R4, R5, А і X визначені вище у формулі (І), формулі (Іа), формулі (II). Наприклад, може бути застосована гетерогенна каталітична гідрогенізація. 29 92730 30 Сполуки за формулою (XI) можуть бути синтезовані шляхом додавання R5 до сполуки за формулою (XII), де R4 і X відповідають компонентам, визначеним вище, із забезпеченням подальшої реакції з кислотним хлоридом, карбоновою кислотою, хлоридом сульфонової кислоти або iзоціанатом, або навпаки. де Υ приєднано в 5-й або 6-й позиції бензазоПереважним прикладом здійснення винаходу є сполука за формулою (III) лу; А, X, Y, R3, R4, R5, R12, R13 ,R14, R15 відповідають компонентам, визначеним для формули (І). Ще одним переважним прикладом здійснення винаходу є сполука за формулою (VI) де Υ приєднано в 5-й або 6-й позиції бензазолу; А, Φ, Υ, R3, R4, R5, R12, R13, R14, R15 відповідають компонентам, визначеним для формули (І). Іншим переважним прикладом здійснення винаходу є сполука за формулою (III), де R12 і R15 є Η і R13 і R14, незалежно один від одного, являють собою О-алкіл, який може заміщатися. Більш переважним прикладом здійснення винаходу є сполуки за формулою (III), де X незалежно представлено S або О; Υ представлено ΝΗ; А незалежно представлено -CO або NHCO, де вказує точку приєднання до R3; R3 представляє собою довільно заміщену арильну або гетероарильну групу, R5, R12 і R15, є Н; R13 і R14 представляють собою О-алкіл, який може заміщатися. Ще одним переважним прикладом здійснення винаходу є сполука за формулою (IV) де Υ приєднано в 5-й або 6-й позиції бензазолу; А, X, Y, R3, R4, R5, R12, R13 відповідають компонентам, визначеним для формули (І). Ще одним переважним прикладом здійснення винаходу є сполука за формулою (V) де Υ приєднано в 5-й або 6-й позиції бензазолу; А, X, Y, R3, R4, R5, R16 відповідають компонентам, визначеним для формули (І). Ще одним переважним прикладом здійснення винаходу є сполука за формулою (І) де X представлено S; Υ представлено ΝΗ; А представлено CO-; R5 є Н. Ще одним переважним прикладом здійснення винаходу є сполука за формулою (І), де X представлено S; Υ представлено ΝΗ; А представлено NHCO-, де вказує точку приєднання до R3; R5 є Н. Ще одним переважним прикладом здійснення винаходу є сполука за формулою (І) де X представлено О; Υ представлено ΝΗ; А представлено CO-; R5 є Н. Ще одним переважним прикладом здійснення винаходу є сполука за формулою (І) де X представлено О; Υ представлено ΝΗ; А представлено NHCO-, де указує точку приєднання до R3; R5 є Н. Ще одним переважним прикладом здійснення винаходу є сполука за формулою (І) де X представлено О; Υ представлено ΝΗ; А представлено CO-; R3 представляє собою довільно заміщену арильну або гетероарильну групу; R5 є Н. Більш переважним прикладом здійснення винаходу авляються сполуки за формулою (III), де заступник -Y-R1 приєднаний до 5-ї позиції бензазолу, X незалежно представляє собою S або О; Υ є ΝΗ; А незалежно представляє собою -CO- або NHCO-, де указує точку приєднання до R3; R3 представляє собою довільно заміщену арильну або гетероарильну групу, R5, R12 і R15 є Н; R13 і R14 представляють собою О-алкіл, який може бути заміщеним. Більш переважним прикладом здійснення винаходу авляються сполуки за формулою (III), де заступник -Y-R1 приєднаний до 6-ї позиції бенза 31 золу, X незалежно представляє собою S або О; Υ є ΝΗ; А незалежно представляє собою -CO- або NHCO-, де указує точку приєднання до R3; R3 представляє собою довільно заміщену арильну 5 12 15 13 14 або гетероарильну групу, R , R і R є Н; R і R представляють собою О-алкіл, який може бути заміщеним. Більш переважним прикладом здійснення винаходу авляються сполуки за формулою (III), де заступник -Y-R1 приєднаний до 5-ї позиції бензазолу, X незалежно представляє собою S або О; Υ є ΝΗ; А незалежно представляє собою -CO- або NHCO-, де указує точку приєднання до R3; R3 представляє собою довільно заміщений феніл, R5, R12 і R15 є Н; R13 і R14 представляють собою Оалкіл, який може бути заміщеним. Більш переважним прикладом здійснення винаходу являються сполуки за формулою (III), де заступник -Y-R1 приєднаний до 6-ї позиції бензазолу, X незалежно представляє собою S або О; Υ є ΝΗ; А незалежно представляє собою -CO- або NHCO-, де указує точку приєднання до R3; R3 представляє собою довільно заміщену феніларилову абр гетероарилову групу, R5, R12 і R15 є Н; R13 і R14 представляють собою О-алкіл, який може бути заміщеним. Іншим переважним прикладом здійснення винаходу являются сполуки за формулою (І), де R3; представляє собою довільно заміщену арильну або гетероарильну групу. Ще одним переважним прикладом здійснення винаходу являються сполуки за формулою (І), де R3; представляє собою довільно заміщену фенільну групу. Ще одним переважним прикладом здійснення винаходу являються сполуки за формулою (І), де заступник -Y-R1 приєднаний до 5-ї позиції бензазолу. Ще одним переважним прикладом здійснення винаходу являються сполуки за формулою (І), де заступник -Y-R1 приєднаний до 6-ї позиції бензазолу. Іншим переважним прикладом здійснення винаходу являються сполуки за формулою (III), де R3 представляє собою довільно заміщену арильну або гетероарильну групу. Ще одним переважним прикладом здійснення винаходу являються сполуки за формулою (III), де R3; представляє собою довільно заміщену фенільну групу. Ще одним переважним прикладом здійснення винаходу являються сполуки за формулою (III), де заступник -Y-R1 приєднаний до 5-ї позиції бензазолу. Ще одним переважним прикладом здійснення винаходу являються сполуки за формулою (III), де заступник -Y-R1 приєднаний до 6-ї позиції бензазолу. Ще одним переважним прикладом здійснення винаходу являються сполуки за формулою (III), де де X представляє собою S; Υ представляє собою ΝΗ; А є -CO-; R5 є Н. Ще одним переважним прикладом здійснення винаходу являються сполуки за формулою (III), де де X представляє собою S; Υ представляє собою 92730 32 ΝΗ; А є NHCO-, де указує точку приєднання до R3; R5 є Н. Ще одним переважним прикладом здійснення винаходу являються сполуки за формулою (III), де де X представляє собою О; Υ представляє собою ΝΗ; А є -CO-; R5 є Н. Ще одним переважним прикладом здійснення винаходу являються сполуки за формулою (III), де де X представляє собою О; Υ представляє собою ΝΗ; А є NHCO-, де указує точку приєднання до R3; R5 є Н. Ще одним переважним прикладом здійснення винаходу є сполуки за формулою (III) де X представлено О; Υ представлено ΝΗ; А є -CO-; R3 представляє собою довільно заміщену арильну або гетероарильну групу; R5 є Н. Ще одним переважним прикладом здійснення винаходу є сполуки за формулою (Іа) де Xа представлено S; Ya представлено NH; Аа представлено -CO-; R5 є Н. Ще одним переважним прикладом здійснення винаходу є сполуки за формулою (Іа) де Xа представлено S; Ya представлено NH; Аа представлено NHCO-, де указує точку приєднання до R3; R5 є Н. Іншим переважним прикладом здійснення винаходу є сполуки за формулою (Іа), де R3; представляє собою довільно заміщену арильну або гетероарильну групу. Ще одним переважним прикладом здійснення винаходу є сполуки за формулою (Іа), де заступa 1a ник -Y -R приєднаний до 5-ї позиції бензазолу. Ще одним переважним прикладом здійснення винаходу авляються сполуки за формулою (Іа), де заступник -Ya-R1a приєднаний до 6-ї позиції бензазолу. Ще одним переважним прикладом здійснення винаходу є сполуки за формулою (II) де Хb представлено S; Yb представлено NH; Аb представлено -CO-; R5 є Н. Ще одним переважним прикладом здійснення винаходу є сполуки за формулою (II) де Хb представлено S; Yb представлено NH; Аb представлено NHCO-, де указує точку приєднання до R3; R5 є Н. Іншим переважним прикладом здійснення винаходу є сполуки за формулою (II), де R3 представляє собою довільно заміщену арильну або гетероарильну групу. Іншим переважним прикладом здійснення винаходу є сполуки за формулою (II), де R3 представляє собою довільно заміщену фенільну групу. Ще одним переважним прикладом здійснення винаходу є сполуки за формулою (II), де заступник -Yb- приєднаний до 5-ї позиції бензазолу. Ще одним переважним прикладом здійснення винаходу є сполуки за формулою (II), де заступник -Yb- приєднаний до 6-ї позиції бензазолу. Ще одним переважним прикладом здійснення даного винаходу є композиції, що містять одну або декілька сполук по даному винаходу і фармацевтично прийнятний носій або розчинник. Сполуки за даним винаходом можуть формувати солі з неорганічними або органічними кислотами або основами. Перелік прикладів фармацев 33 тично прийнятних солей включає, не обмежуючись перерахованим, нетоксичні неорганічні або органічні солі, наприклад, ацетат, похідне від оцтової кислоти, аконітат, похідне від аконітової кислоти, аскорбат, похідне від аскорбінової кислоти, бензоат, похідне від бензойної кислоти, цинамат, похідне від коричної кислоти, цитрат, похідне від лимонної кислоти, ембонат, похідне від ембонової кислоти, енантат, похідне від гептанової кислоти, форміат, похідне від мурашиної кислоти, фумарат, похідне від фумарової кислоти, глутамат, похідне від глутамінової кислоти, гліколат, похідне від гліколевої кислоти, хлорид, похідне від хлористоводородної кислоти, бромід, похідне від бромистоводородної кислоти, лактат, похідне від молочної кислоти, малеат, похідне від малеїнової кислоти, малонат, похідне від малонової кислоти, манделат, похідне від мигдалевої кислоти, метансульфонат, похідне від метансульфокислоти, нафталін-2-сульфонат, похідне від нафталін-2сульфокислоти, нітрат, похідне від азотної кислоти, перхлорат, похідне від хлорної кислоти, фосфат, похідне від фосфорної кислоти, фталат, похідне від фталевої кислоти, саліцилат, похідне від саліцилової кислоти, сорбат, похідне від сорбінової кислоти, стеарат, похідне від стеаринової кислоти, сукцинат, похідне від бурштинової кислоти, сульфат, похідне від сірчаної кислоти, тартрат, похідне від винної кислоти, толуол-р-сульфат, похідне від толуол-р-сульфокислоти і інші. Солі фосфонокси- і фосфоноксиалкіловіх груп можуть бути представлені солями, які формуються з використанням іонів лужних металів, наприклад, натрію або калію, або солями, які формуються з використанням іонів лужноземельних металів, наприклад, кальцію або магнію, а також солями, які формуються з використанням іонів цинку. Такими солями сполук за даним винаходом можуть бути безводні солі або сольватовані солі. Вказані солі можуть бути отримані способами, відомими кваліфікованим фахівцям з описів рівня техніки. Інші солі, подібні оксалатам, похідним щавлевої кислоти, які не вважаються фармацевтично придатними, можуть бути використані як посередники або проміжні продукти, що використовуються для виробництва сполук за даним винаходом або їх фармацевтично придатних солей, або їх фізіологічно функціонуючих похідних, або їх стереоізомерів. Сполуки за даним винаходом або лікарські препарати, приготовані з їх використовуванням, в основному, застосовуються для лікування розладів, пов'язаних з клітинною проліферацією (розростанням клітини), для лікування або профілактики імунологічних захворювань і станів (наприклад, запальних процесів, нейроімунологічних захворювань, аутоімунних хвороб і інших хворобливих станів). Сполуки за даним винаходом використовуються для лікування хвороб, які викликаються злоякісним розростанням клітини, наприклад, всіх видів твердих пухлин, лейкемії і лімфом. Тому сполуки за винаходом і лікарські засоби, приготовані з їх використовуванням, в основному, застосовуються 92730 34 для регулювання життєдіяльності клітини, росту клітини, терміну життєздатності клітини, клітинної диференціації, клітинного циклу, дозрівання клітини і її відмирання, а також для введення системних змін в процес метаболізму, наприклад, змін в процес цукрового, ліпідного або протеїнового метаболізму. Вони також можуть бути використані для забезпечення умов розмноження клітин, включаючи ріст і поділ клітин крові (прогематопоіетичний ефект) після виснаження або руйнування клітин, викликаних, наприклад, дією токсичних речовин, радіацією, імунотерапією, порушеннями росту, недостатнім живленням, порушеннями в процесах всмоктування живильних речовин, порушеннями в процесах імунного регулювання, анемією і подібними їй чинниками, або для забезпечення терапевтичного контролю за ростом і відмиранням тканин і терапевтичного поліпшення процесу життєдіяльності клітин і тканин, а також гомеостазу клітин крові. Дані хвороби і хворобливі стани включають, не обмежуючись перерахованим, такі злоякісні захворювання, як гематологічні хвороби (наприклад, лейкемія, мієлома) або лімфоми (наприклад, лімфоми Ходкіна і нон-Ходкін лімфоми), або тверді пухлини (наприклад, молочної залози, простати, печінки, сечового пухиря, легенів, стравоходу, шлунку, кишково-ректальної системи, сечостатевої системи, шлунково-кишкового тракту, шкіри), підшлункової залози, мозку, матки, товстої кишки, голови і шиї, яєчників, меланоми, астроцитоми, дрібноклітинного раку легенів, гліоми, базальної і сквамозно-клітинної карциноми, таких типів сарком, як саркома Капозі і остеосаркома). Інші аспекти даного винаходу відносяться до похідних бензазолу, що представляють собою нові фармацевтично активні речовини, зокрема, використовувані для приготування фармацевтичної композиції для лікування захворювань, які піддаються лікуванню або ослабінню, завдяки iнгібуванню однієї або декількох кіназ і/або фосфатаз. В одному з більш переважних прикладів здійснення винаходу сполуки за даним винаходом можуть бути використані для лікування і/або попередження захворювань шляхом iнгібування однієї або декількох кіназ, наприклад, таких як: Aurora A, Aurora В, EGF-R, ERBB2, IGF-R, PDGFR, FLT3 VEGF-R2, VEGF-R3, ЕРНВ4, Тіе2, FAK і SRC. Сполуки за даним винаходом або їх фармацевтично прийнятні солі, або фізіологічно функціонуючі похідні, або стереоізомери, при необхідності, з відповідними адьювантами і добавками, використовуваними для приготування лікарських препаратів, застосовуються для лікування або попередження хвороб, що характеризуються надмірним розростанням кератиноцитів та/або Т-клітин, зокрема, запальних процесів і захворювань імунної системи, переважно, вибраних з переліку захворювань, що включає такі захворювання як: хвороба Аддісона, осередкова алопеція, анкілоспондильоз, гемолітична анемія (anemia haemolitica), пернициозна анемія (anemia perniciosa) афти, афтозний стоматит, артрит, атерослеротичні захворювання, остеоартрит, ревматоїдний артрит, ас 35 пермогенез, бронхіальна астма, аутоімунна астма, аутоімунний гемоліз, хвороба Бехчета, хвороба Бека, запалення кишкового тракту, лімфома Буркита, хвороба Крону, хоріоїдит, улцирозний коліт, хвороби, що відносяться до черевної порожнини, криоглобулінемія, герпетиформний дерматит, дерматоміозит, діабет інсулін-залежного типу 1, ювенільний діабет, iдеопатичний нецукровий діабет, цукровий інсулін-залежний діабет, аутоімунні демієлініючі захворювання, контрактура Дюпюітрена, eнцефаломіеліт, алергічний eнцефаломіеліт, факоанафілактична ендофталмія, алергічний ентерит, аутоімунний eнтеропатичний синдром, лепрозна вузликова еритема, ідиопатичний лицьовий параліч, синдром хронічної втоми, ревматична лихоманка, гломерулярний нефрит, синдром Гудпастера, хвороба Грейвса, хвороба ГарнманаРіча, хвороба Хашимото, тиреоїдит Хашимото, раптова втрата слуху, сенсоневральна втрата слуху, хронічний гепатит, хвороба Ходкіна, пароксизмальна гемоглобінурія, гіпогонадизм, регіональний ілеїт, ірит, лейкопенія, лейкемія, дисемінуючий червоний вовчак (люпус), системний червоний вовчак, шкірний червоний вовчак, хронічний злоякісний лімфоматоз, інфекційний мононуклеоз, міастенія гравіс, первинна iдеопатична мікседема, нефроз, симпатична офтальмія, грануломатозний орхіт, панкреатит, пухирчатка, звичайна пухирчатка, вузликовий поліартерит, первинний хронічний поліартрит, поліміозит, гострий полірадикуліт, псоріаз, пурпура, гангренозна піодерма, тиреоїдит Хервейна, синдром Рейтера, саркоїдоз, атаксичний склероз, прогресуючий системний склероз, склерит, склеродермія, розсіяний склероз, множинний склероз, придбана spenic атрофія, безплідність через наявність антисперматозоїдальних антитіл, тромбоцитопенія, ідиопатическая тромбоцитопенійна пурпура, тимома, гострий передній увеїт, вітиліго, AIDS(CHIД), HIV(BIЧ), SCID і Epstein Barr-вірус-асоційовані хвороби, наприклад синдром Шегрена, вірус (AIDS або ЕВ\/)-асоційована Вклітинна лімфома, хвороби, викликані паразитами, наприклад, лейшманіоз, хвороби, викликані пригнобленням імунної системи, наприклад, вірусними інфекціями після алогенних трансплантацій, AIDS, раку, хронічного активного гепатитного діабету, токсичного шокового синдрому і харчового отруєння. Термін «лікування» в контексті даного винаходу означає повне або часткове вилікування хвороби, попередження захворювання або полегшення хворобливого стану, або припинення прогресування вказаного захворювання. Сполуки за даним винаходом можуть бути використані для лікування хвороб, викликаних інвазіями найпростіших паразитів, у тварин і людини. Сполуки за даним винаходом можуть бути використані для лікування хвороб, викликаних вірусними інфекціями або іншими інфекціями, викликаними, наприклад, Pneumocystis carinii. Крім того, винахід відноситься до способу лікування і попередження захворювань, який включає прийом ефективної кількості сполуки за формулою (І) фармацевтично прийнятної солі, або її 92730 36 фізіологічно функціонуючого похідного, або стереоізомеру. Сполуки за даним винаходом і їх фармакологічно прийнятні солі можуть призначатися тваринам, переважно, ссавцям, зокрема, людині, як терапевтичні засоби, безпосередньо у вигляді сумішей або у вигляді лікувальних препаратів, які можуть вводитися як ентерально, так і парентерально, і які у вигляді активного компоненту містять ефективну дозу, принаймні, одної сполуки за даним винаходом або її солі на додаток до традиційного фармацевтично нешкідливого наповнювача і добавок. Приготування медикаментів, що включають сполуки за даним винаходом, і їх застосування можуть відбуватися у відповідності з добре відомими фармацевтичними способами. В тих випадках, коли сполуки за даним винаходу для використовування при лікуванні можуть призначатися у вигляді сировинної хімічної сполуки, переважним є введення активного інгредієнта, по вибору, у вигляді фізіологічно прийнятної солі у фармацевтичній композиції разом з одним або декількома адьювантами, наповнювачами, носіями, буферними розчинами, розчинниками та/або іншими звичайно вживаними додатковими фармацевтичними компонентами. Такими солями сполук можуть бути обезводнені або сольватовані солі. В переважному прикладі здійснення винаходу представлені медикаменти, що містять сполуки, відповідні винаходу або фармацевтично прийнятна сіль, або фізіологічно функціонуюче похідне, або їх стереоізомер разом з одним або декількома фармацевтично прийнятними носіями і, по вибору, іншими лікувальними або профілактичними інгредієнтами. Носій (носії) може бути «прийнятним» в сенсі сумісності з іншими інгредієнтами сполуки і не завдавати шкоди приймаючому її пацієнту. Медикамент відповідно до винаходу може бути придатний для орального, ректального, бронхіального, носового, зовнішнього, трансбуккального, підщелепного, трансдермального, вагінального, парентерального(включаючи шкірну, підшкірну, внутрішньом'язову, внутрішньоочеревинну, внутрівенну, внутрішньоартеріальну, внутрішньоцеребральну, внутрішньоочну ін'єкцію або інфузію) введення, або він може бути представлений у формі, придатній для введення у вигляді інгаляції або інсуфляції (вдування), включаючи порошки, рідкі аерозолі або системи для введення по краплям. Відповідними прикладами таких систем можуть бути системи, які включають напівпроникні матриці з гідрофобних полімерів, що містять сполуки за винаходом, при цьому, дані матриці можуть бути виконані у вигляді виробів певної форми, наприклад, у вигляді плівок або мікрокапсул. Медикамент, виготовлений із сполук за даним винаходом і фармацевтично прийнятних носіїв, може бути або в твердому, або в рідкому стані. Тверді форми препаратів включають порошки, таблетки, пілюлі, капсули, крохмальні капсули, свічки, здатні до змішування гранули. Твердим носієм можуть бути одна або декілька речовин, які також можуть функціонувати як розчинники, ароматизатори, солюбілізатори, суспендуючі речови 37 ни, мастила, зв'язуючі речовини, консерванти, розпушувачі таблеток або капсулюючі матеріали. В порошках носій присутній у вигляді твердої речовини, остаточно розкладеної на дрібні частинки, які змішані з активним компонентом, також остаточно розкладеним на дрібні частинки. В таблетках активний компонент у відповідних пропорціях змішаний з носієм, що має необхідну зв'язуючу здатність, і спресований в елементи заданої форми і розмірів. Відповідними носіями є карбонат магнію, стеарат магнію, тальк, цукор, лактоза, пектин, декстрин, крохмаль, желатин, трагакант, метилцелюлоза, натрійкарбоксиметилцелюлоза, низькоплавкий віск (парафін), масло какао і інші компоненти. Термін «препарат» включає поняття композиції, яка містить активну сполуку разом з капсулюючим матеріалом, як носієм, що забезпечує виготовлення капсули в яку вкладений активний компонент разом з носієм або без нього, при цьому активний компонент оточений носієм, який таким способом зв'язаний з даним активним компонентом. За таким принципом приготовані крохмальні облатки (крохмальні капсули) і коржики. Таблетки, порошки, капсули, пілюлі, крохмальні облатки і коржики можуть бути використані в твердій формі, придатній для орального призначення. Для приготування свічок спочатку низькотемпературний віск, наприклад, суміш гліцериду жирної кислоти або масла какао, розплавляють, після чого в розплаві в процесі перемішування гомогенно диспергують активний компонент. Потім розплавлену гомогенну суміш вливають в спеціально підготовлені форми, суміші дають можливість охолодитися і затвердіти. Композиції, придатні для вагінального застосування, можуть бути представлені у вигляді вагінальних супозиторіїв, тампонів, кремів, гелів, паст, пінок або спреїв, що містять на додаток до активного інгредієнта такі носії, які відомі з рівня техніки як придатні для даного використання. Рідкі препарати представлено розчинами, суспензіями і емульсіями, наприклад, водними і водо-пропіленгліколевими розчинами. Наприклад, рідкі препарати для парентеральної ін'єкції можуть бути приготовані у вигляді розчинів у водному поліетиленгліколевому розчині. Сполуки за даним винаходом можуть, таким чином, готуватися для парентерального введення (наприклад, шляхом ін'єкції, зокрема ін'єкції ударної дози речовини, або шляхом безперервного вливання). Окрім, того, вони можуть бути рекомендовані у формі дозованої одиниці в ампулах, у вигляді заздалегідь наповнених шприців, в контейнерах малих об'ємів, або з множинним дозуванням з додаванням консерванту. Композиції можуть приймати форми суспензій, розчинів або емульсій в масляному або водному носії, а також можуть містити формоутворювальні речовини, наприклад, суспендуючі, стабілізуючі та/або розсіюючі речовини. По вибору, активний інгредієнт може бути присутній у вигляді порошку, отриманого шляхом асептичного виділення стерильного твердого продукту або шляхом ліофілізації з розчину для отримання сполуки в поєднанні з відповідним носієм, наприклад, стерильною во 92730 38 дою, що не містить пірогену, безпосередньо перед використовуванням. Водні розчини, придатні для орального використовування, можуть бути приготовані шляхом розчинення активного компоненту у воді і додавання, за потребою, відповідних фарбників, ароматизаторів, стабілізуючих речовин і загусників. Водні суспензії, придатні для орального використовування можуть бути приготовані шляхом диспергування розділеного на тонкі частинки активного компоненту у воді з в'язким матеріалом, наприклад, натуральними і синтетичними гумами, смолами, метилцелюлозою, натрійкарбоксиметилцелюлозою або іншими добре відомими суспендуючими речовинами. Крім того, застосовуються тверді препарати, призначені для перетворення в рідкі препарати для орального введення безпосередньо перед використовуванням. Такими рідкими формами є розчини, суспензії і емульсії. Дані препарати можуть містити на додаток до активного компоненту фарбники, ароматизатори, стабілізатори, буферні розчини, штучні і натуральні дезодоруючі речовини, диспергатори, загусники, солюбілізуючі речовини і тому подібне. В найбільш переважному прикладі здійснення винаходу представлено медикамент, призначений для зовнішнього застосування. Це знижує побічні ефекти і обмежує заданий процес лікування тією ділянкою, на яку нанесено лікарський засіб. Переважно, такий медикамент готують у вигляді мазі, гелю, пластиру, емульсії, лосьйону, пінки, крему в змішаному стані або у вигляді амфіфільної емульсивної системи (в змішаній фазі: масло/вода-вода/масло), ліпосоми, трансферсоми, пасти або порошка. Мазі і креми можуть, наприклад, можуть бути приготовані на водній або масляній основі з додаванням відповідного загусника та/або желеутворюючої речовини. Лосьйони можуть бути приготовані на водній або масляній основі і, як правило, містять одну або декілька эмульгуючих речовин, стабілізуючих речовин, диспегуючих речовин, суспендуючих речовин, загусників, або барвників. Композиції, придатні для зовнішнього застосування в порожнині рота, включають коржики, що містять активну речовину в ароматизованій основі, для чого, звичайно, використовують сахарозу і гуміарабік (акацію) або трагакант; пастили, що містять активний інгредієнт в інертній основі, наприклад, желатині і гліцерині або сахарозі і гуміарабіку (акації); рідини для полоскання рота, що містять активний інгредієнт у відповідному рідкому носії. Розчини або суспензії вводяться безпосередньо в носову порожнину традиційним способом, наприклад, за допомогою крапельниці, піпетки або розпилювача. Композиції можуть бути приготовані для введення одиночної дози або декількох доз. Застосовуючи в останньому випадку крапельницю або піпетку, пацієнт одержує відповідний, наперед заданий об'єм розчину або суспензії. Якщо використовують розпилювач, заданий результат може бути досягнутий, наприклад, за допомогою дозуючого насосу тонкого розпилювання. 39 Введення в респіраторний тракт може бути забезпечено за допомогою аерозолі, в якій під тиском активний інгредієнт упакований з відповідним носієм, таким, як, хлорофторвуглець (CFC), наприклад, дихлородифторометан, трихлорофторометан або дихлоротетрафтороетан, двоокис вуглецю або інший придатний для даної мети газ. Аерозоль може також містити поверхнево-активну речовину, наприклад, лецитин. Доза ліків може контролюватися за допомогою дозуючого клапана. За бажанням, активний інгредієнт може бути використаний у вигляді сухого порошку, наприклад у вигляді порошкової суміші сполуки з відповідною порошковою основою, представленою у вигляді лактози, крохмалю, похідних крохмалю, наприклад, гідроксипропілметилцелюлози і полівінілпіролідону (PVP). Звичайно, порошковий носій формує гель в носовій порожнині. Порошкова композиція може бути представлена в дозованій формі по типу одна доза на один прийом, наприклад, в капсулах або картриджах, наприклад, із желатину, або у вигляді упаковок у формі балонів з яких порошок може вводитися за допомогою ингалятора. В композиціях для введення в респіраторний тракт, включаючи інтраназальні композиції, сполука повинна містити дрібні частинки розміром, наприклад, біля 5 мікронів або менше. Такий розмір частинок може бути забезпечений, завдяки використовуванню технологій, відомих з рівня техніки, наприклад, технологій дуже тонкого подрібнення. При необхідності, можуть бути використані композиції, пристосовані для забезпечення тривалого безперервного секретування активного інгредієнта. Фармацевтичні препарати представлені, переважно, в дозованому вигляді. Приготовані таким чином препарати підрозділяються на окремі дози, що містять відповідну кількість активного компоненту. Дозована лікарська форма може мати вид упакованого препарату, при цьому упаковка містить дискретні кількості препарату, наприклад, у вигляді таблеток, капсул, і порошків в пухирцях або ампулах. Крім того, дозована лікарська форма може існувати у вигляді окремої капсули, таблетки, крохмальної капсули або коржика або у вигляді упаковки, що містить задану кількість названих вище компонентів упаковану в окремі дозовані форми. Таблетки або капсули для орального прийому і рідини для внутрішньовенного введення і безперервного вливання є переважними дозованими лікарськими формами композицій. Додаткову інформацію про технічні засоби для приготування і введення препаратів в організм можна знайти в останньому виданні Remington's Pharmaceutical Science (Maack Publishing Co. Easton, Pa.). Фармацевтичні композиції можуть також містити дві або більш сполук за даним винаходом або їх фармацевтично прийнятні солі, а також інші терапевтично активні речовини. Таким чином, сполуки за даним винаходом можуть бути використані у вигляді тільки одної сполуки або в комбінації з іншими активними сполуками - наприклад, з медикаментами, які вже 92730 40 відомі як засіб для лікування перерахованих вище захворювань, і завдяки яким в останньому випадку наголошується досягнення додаткового позитивного підсилюючого ефекту. Для приготування фармацевтичних препаратів можуть бути використані фармацевтично інертні неорганічні або органічні наповнювачі. Для приготування пілюль, таблеток, таблеток в оболонці і твердих желатинових капсул, можуть бути застосовані, наприклад, лактоза, кукурудзяний крохмаль або їх похідні, тальк, стеаринова кислота або її солі і інші речовини. Носіями для м'яких желатинових капсул і свічок є, наприклад, жири, віск, напівтверді і рідкі поліоли, натуральні і отверджені масла і інші речовини. Відповідними наповнювачами для приготування розчинів і сиропів є, наприклад, вода, сахароза, інвертований цукор, глюкоза, поліоли і інші речовини. Відповідними наповнювачами для виробництва розчинів для ін'єкцій є, наприклад, вода, спирти, гліцерол, поліол або рослинні масла. Дозування може мінятися в широких діапазонах і повинне призначатися у кожному окремому випадку відповідно до індивідуальних особливостей стану пацієнта. Для позначених вище цілей відповідні дозування повинні змінюватися залежно від способу введення, особливостей стану, потребуючого лікування і від передбачуваного ефекту. Проте, в основному, задовільні результати досягаються при дозуваннях в діапазоні від 1 до 100мг/кг ваги тварини, переважно, від 1 до 50мг/кг. Відповідним діапазоном дозувань для крупних ссавців, наприклад, людини, є діапазон, порядку, від 10мг до 3г/сутки, які, як правило, приймаються окремими підрозділеними кількостями на один прийом від 2 до 4 разів на добу, або в лікарській формі, що забезпечує безперервне виділення ефективного компоненту з лікарської речовини. Наступні приклади і числові показники включені в даний опис для того, щоб продемонструвати переважні приклади здійснення винаходу. Кваліфікованим фахівцям в даній області техніки слід мати на увазі, що технічні засоби, розкриті в подальших прикладах, представляють собою технічні засоби, відкриті авторами даного винаходу для здійснення свого винаходу на практиці і тому вважаються переважними засобами для здійснення даного винаходу. Проте, кваліфіковані фахівці в даній області техніки повинні розуміти, виходячи з об'єму даного розкриття винаходу, що в окремі приклади здійснення винаходу, розкриті в даному документі, можуть бути внесені зміни, які не виходять за межі об'єму захисту, визначені набором істотних ознак, висловлених в незалежних пунктах прикладеної формули винаходу. Вся інформація, приведена як аргументи, включена в дану заявку методом посилань. Приклади Скорочення: min., хвилина (хвилини); h., година (години); r.t., кімнатна температура; Rt- час утримання ; ψ, псевдо; s, синглет; t, триплет; quint., група з п'яти об'єктів; br., широкий; J, коефіцієнт зв'язку; pTLC, препаративна тонкошарова хроматографія; DMAP, 4-диметиламінопіридин; IМ, проміжний. 41 NMR spectra (спектри): Bruker Avance 300МНz (Мгц). Спектри 1Н NMR були зареєстровані при 300МНz (Мгц), використовуючи пік залишкового розчинника як внутрішнього стандарту (CDCL3 δH=7,26). Аналітична LC/ESI-MS: 2x Water 600, система доставки з множинним розчинником (2 Water 600 Multisolvent Delivery System). Петля (трубка для введення проб) 50мкл. Колонка, Хромолітична швидкість (Column, Chromolith Speed) ROD RP18e (Merck, Darmstadt), 50 4,6мм, з попереднім фільтром, 2мкм (Merck). Елюент А, Н2О+0,1%НСО2Н; елюент В, MeCN. Градієнт, від 5% В до 100% В в межах 5 хвилин; витрата, 3мл/хв. Waters LCZ одиночний квадрупольний масспектрометр з джерелом електророзпиленості. Метод MS, MS8минPM80-800-20V; позитивний/негативний іонний спосіб сканування, m/z 80-800 в 1 з; капілярність, 3,5kV; напруга на конусі, 20V; вольтаж мультиплікатора, 400V; температура проби і десольватації газу, 120°С і 350°С, відповідно. Waters 2487 Детектор γспектральної поглинальної здатності подвійної дії, сет до 254нм. Препаративна високоефективна рідинна хроматографія HPLC-MC: Waters 600, система доставки з множинним розчинником (Waters 600 Multisolvent Delivery System) з препаративними распилювальними головками. Петля (трубка для введення проб) 2000мкл і 5000мкл. Колонка, Waters X-Terra RP18, 7мкм, 19 150мм з X-Terra RP18 із захисним картріджом 7мкм, 19 10мм; використовували при витраті 20мл/хв. або YMC ODSA, 120 А, 40 150мм з X-Terra RP18 із захисним картріджом 7мкм, 19 10мм; використовували при витраті 50мл/хв. Приготування розчинника: MeCNH2O-HCO2H 80:20:0,05(v:v:v). Елюент А, Н2О+0,1%НСО2Н; елюент В, MeCN. Диференціальні лінійні градієнти від 5-100% елюента В, пристосованого до зразка. Об'єм ін'єкції: 500мкл2000мкл залежно від зразка. Waters ZQ одиночний квадрупольний масспектрометр з джерелом електророзпиленості. Позитивний або негативний іонний спосіб сканування, m/z 80-800 в 1 с; капілярність, 3,5kV або 3,0kV ; напруга на конусі, 20V; вольтаж мультиплікатора, 400V; температура проби і газу десольватації, 120°С і 350°С, відповідно. Waters Fraction Collector II (колектор фракцій) з масс-ініційованим збором фракцій. Waters 996 детектор випромінювання фотодіода. Синтез проміжних сполук Проміжна сполука 1: N-(6-Амінобензоксазол-2іл)бензамід. Операція 1. Розчин ціаногенброміду (3,50г, 33ммол; попередження: надзвичайно токсичний! Ліквідація відпрацьованих відходів: додавання надлишку NaOCI до базового водного розчину ціаногенброміду) в тетрагідрофурані (3мл) додавали до розчину 2-аміно-5-нітрофенолу (4,62г, 30ммол) в тетрагідрофурані (20мл). Після перемішування протягом доби при кімнатній температурі утворювався осад, який розчиняли шляхом додавання води (5мл). Після перемішування протягом трьох діб при кімнатній температурі додавали воду (10мл), а також додавали NaOH до тих пір, доки суміш не набувала властивостей основи. Тетрагі 92730 42 дрофуран видаляли in vacuo, a осад, сформований в водній фазі, що залишилася, відділяли методом фільтрації, промивали водою і рекристалізовували з метанолу (100мл). Після додаткової фракційної кристалізації маточної рідини в цілому було отримано 3,80г (21,2ммол, 71%) 2-аміно-6нітробензоксазолу у вигляді твердої речовини коричневого кольору. LC/ESI-MS: m/z=180[M+H]+; m/z=178[M-H]-; Rt=2,52xв. Операція 2. Бензолхлорид (1,17мл, 10,0ммол) додавали до суспензії 2-аміно-6-нітробензоксазолу (1,50г, 8,37ммол) в піридині (10мл). Після перемішування протягом 24 годин при 80°С розчин вливали у воду (250мл). Суміш відразу ж перемішували протягом 12 годин (протягом ночі) при кімнатній температурі і отриманий осад відділяли методом фільтрації. Таким чином, був отриманий N-(6Нітробензоксазол-2-іл)бензамід (2,08г, 7,32ммол, 88%) у вигляді твердої речовини жовтого кольору. LC/ESI-MS: m/z=284[M+H]+; m/z=282[M-H]-; Rt=3,13xв. Операція 3. До розчину N-(6-нітробензоксазол2-іл)бензаміду (2,03г, 7,17ммол) в диметилформаміді (60мл) додавали паладій на рослинному або тваринному вугіллі (1,52г, 10% Pd, 1,43ммол Pd), а повітря замінювали воднем (1бар). Суміш перемішували протягом 2 годин при 60°С, а потім протягом 12 годин при кімнатній температурі. Паладій видаляли шляхом фільтрації через м'яку прокладку з целіту. Після концентрації до 20мл додавали воду, а отриманий осад відділяли методом фільтрації для отримання N-(6-амінобензоксазол-2іл)бензаміду (0,823г,3,25ммол, 45%) у вигляді твердої речовини коричневого кольору. LC/ESI-MS: m/z=254[M+H]+; m/z=252[M-H]-; Rt=1,92хв. Проміжна речовина 2: N-(6-Амінобензотіазол2-іл)бензамід. Операція 1. До суспензії 2-аміно-6нітробезотіазолу (Sigma Aldrich, 2,93г, 15ммол) в піридині (20мл) додавали бензоїлхлорид (1,74мл, 15ммол) і суміш перемішували при 60°С. Після завершення реакції суміш вливали у воду (250мл) і перемішували протягом 12 годин при кімнатній температурі. Після відділення осаду, що утворився, одержували N-(6-нітробензотіазол-2іл)бензамід (3,87г, 12,9ммол, 86%) у вигляді твердої речовини жовтого кольору. LC/ESI-MS: m/z=300[M+H]+; m/z=298[М-Н]-; Rt=3,93xв. Операція 2. Суміш N-(6-нітробензотіазол-2іл)бензаміду (3,77г, 12,6ммол), паладію на рослинному або тваринному вугіллі (2г, 10% Pd, 1,88ммол Pd), диметилформаміду (80мл) і етилацетату (20мл) гідрогенізували (1бар) протягом 2 годин при 60°С. Паладій видаляли шляхом фільтрації через м'яку прокладку з целіту. Після концентрації до 20мл додавали воду, а отриманий осад відділяли методом фільтрації для отримання N-(6амінобензотіазол-2-іл)бензаміду (3,15г, 11,7ммол, 93%) у вигляді твердої речовини сірого кольору. LC/ESI-MS: m/z=270[M+H]+; m/z=268[М-Н]-; Rt=2,27xв. Проміжна речовина 3: N-(6-Амінобензотіазол2-іл)ізонікотинамід. Операція 1: До суміші 2-аміно-6нітробезотіазолу (Sigma Aldrich, 1,95г, 10ммол) і 43 піридину (40мл) додавали бензоїлхлорид (2,1мл, 18ммол). Після перемішування протягом 5 годин при 80°С додавали воду (10мл). Суміш перемішували протягом 0,5 години при кімнатній температурі, після чого додавали метанол (30мл) і воду (50мл). Осад N-(6-нітробензотіазол-2-іл)ізонікотинаміда відділяли методом фільтрації. Сировинний продукт витримували в диметилформаміді і знову осаджували шляхом додавання метанолу і води (2,53г, 8,42ммол, 84%). LC/ESI-MS: m/z=301[M+H]+; m/z=299[М-Н]-; Rt=3,48xв. Операція 2. N-(6-Нітробензотіазол-2-іл)ізонікотинамід (2,42г, 8,04ммол) суспендували в етилацетаті (150мл) і додавали диметилформамід до повного розчинення. Після додавання паладію на рослинному або тваринному вугіллі (4,25г, 10% Pd, 4ммол Pd) суміш гідрогенізували (1бар) при 60°С до завершення реакції. Паладій видаляли шляхом фільтрації через м'яку прокладку з целіту, а розчинник випаровували. Залишок витримували в невеликій кількості метанолу і осаджували шляхом додавання води для отримання N-(6амінобензотіазол-2-іл)ізонікотинаміду (1,73г, 6,4ммол, 80%). LC/ESI-MS: m/z=271[M+H]+; m/z=269[M-H]-; Rt=1,43хв. Проміжна речовина 4: N-(6-Амінобензотіазол2-іл)нікотинамід. Операція 4. Суміш 2-аміно-6-нітробензотіазолу (0,976г, 5ммол), нікотиноілхлоридгідрохлориду (1,07г, 6ммол), триетиламіну (1,9мл, 13,8ммол), DMAP (каталітична кількість) і диоксану (50мл) нагрівали до температури зворотного повернення (у флегму) протягом 7 годин. Після додавання нікотиноілхлоридгідрохлориду (0,89г, 5ммол) і триетиламіну (1,8мл, 12,5ммол) нагрівання продовжували протягом 5 годин. Після охолоджування до кімнатної температури осад видаляли методом фільтрації. Тверду речовину обробляли киплячим метанолом (25мл) для видалення розчинних забруднюючих включень. Таким чином одержували N-(6-нітробензотіазол-2-іл)нікотинамід (1,36г, 4,53ммол, 91%). LC/ESI-MS: m/z=301[M+H]+; m/z=299[М-Н]-; Rt=3,54xв. Операція 2. N-(6-Нітробензотіазол-2іл)нікотинамід (0,50г, 1,67ммол) розчиняли в диметилсульфоксиді (50мл) шляхом нагріву. Після додавання паладію на рослинному або тваринному вугіллі (0,089г, 10% Pd, 0,08ммол Pd) суміш гідрогенізували протягом 5,5 годин при 80°С. Палладій видаляли шляхом гарячої фільтрації через м'яку прокладку з целіту. Після видалення розчинника одержували N-(6-амінобензотіазол-2іл)нікотинамід (0,45г, 1,67ммол, 100%) у вигляді твердої речовини коричневого кольору. LC/ESIMS: m/z=271[M+H]+; m/z=269[M-H]-; Rt=1,67xв. Проміжна речовина 5: N-(5-Амінобензотіазол2-іл)бензамід. Операція 1. Амонійтіоціанат (8,55г, 112,5ммол) розчиняли в ацетоні (80мл) і краплями додавали ацетилхлорид (8,83г, 112,5ммол). Після перемішування протягом 1 години при кімнатній температурі тверду фазу фільтрували, а фільтрат додавали до розчину 2-фторо-5-нітроаніліну в ацетоні (45мл). Суміш витримували в умовах зворотного повернення (у флегму) протягом 6 годин, після 92730 44 чого розчин концентрували і витримували протягом 12 годин при кімнатній температурі. Осад 1ацетил-3-(2-фторо-5-нітрофеніл)тіокарбаміда (тіомочевина) фільтрували, промивали ацетоном і висушували. Маточний розчин концентрували і ви кристал ізовувал і з ацетону для отримання іншої порції продукту. В цілому, отримано 12,55г (48,8ммол, 43%) твердої речовини сірого кольору. LC/ESI-MS: m/z=258[M+H]+; Rt=3,42xв. Операція 2. Розчин 1-ацетил-3-(2-фторо-5нітрофеніл)тіокарбаміду (тіомочевини) (9,63г, 37,4ммол) в метанолі (400мл) швидко вливали в розчин натрійметанолату (концентрацією 0,5мол/л) в метанолі (100мл). Розчин витримували протягом 12 годин (всю ніч) без перемішування. Осаджений 2-аміно-5-нітробензотіазол фільтрували, промивали метанолом і висушували (жовті кристали, 6,87г, 35,2ммол, 94%). LC/ESI-MS: m/z=196[M+H]+; m/z=194[M-H]-; Rt=2,71хв. Операція 3. Суміш 2-аміно-5-нітробензотіазолу (1,52г, 7,8ммол), бензоїлхлориду (1,36мл, 11,7ммол) і піридину (15мл) нагрівали до 60°С протягом 24 годин. Суміш вливали у воду (250мл), а отриманий осад відділяли методом фільтрації для отримання N-(5-нітробензотіазол-2іл)бензаміду у вигляді твердої речовини жовтого кольору (1,83г, 6,12ммол, 78%). Операція 4. Суміш N-(5-нітробензотіазол-2іл)бензаміду (1,79г, 6,0ммол) і паладію на рослинному або тваринному вугіллі (0,95г, 10% Pd, 0,9ммол Pd) в диметилформаміді (40мл) гідрогенізували (1бар) протягом 2 годин при температурі 100°С. Паладій видаляли шляхом гарячої фільтрації через м'яку прокладку з целіту і фільтрат концентрували до придбання малого об'єму. Після додавання води (200мл) формували осад, який відділяли методом фільтрації. Таким чином, одержували N-(5-амінобензотіазол-2-іл)бензамід (1,39г, 5,14ммол, 86%) у вигляді твердої речовини сірого кольору. LC/ESI-MS: m/z=300[M+H]+; m/z=298[MH] ; Rt=4,2xв. Проміжна речовина 7: 4-Хлоро-6-метокси-7-[3(4-метилпіперазин-1-іл)пропокси]хіназолін. Операція 1. До розчину метилванілату (4,79г, 40ммол) в диметилформаміді (25мл), додавали калійкарбонат (8,29г, 60ммол) і бензилбромід (5,26мл, 44ммол). Суміш нагрівали до 100°С протягом 3 годин. Після охолоджування до кімнатної температури додавали воду і продукт кілька разів екстрагували за допомогою етилацетату. Сполучені органічні фази промивалися водою і соляним розчином. Після висушування в Na2SO4 розчинник видаляли для отримання Метил 4-бензилокси-3метоксибензоату (10,8г, 39,7ммол, 99%) у вигляді твердої речовини сірого кольору, яку використовували для подальшого очищення. LC/ESI-MS: m/z=273[M+H]+; Rt=3,82xв. Операція 2. Метил 4-бензилокси-3метоксибензоат (10,9г, 40,0ммол) конвертували в метил 4-бензилокси-5-метокси-2-нітробензоат (11,6г, 36,6ммол, 91%) за способом, описаним в документі US 02/0026052 А1, стр.51, приклад для посилання 15. LC/ESI-MS: m/z=318[М+Н]+; Rt=3,85xв. 45 Операція 3. Колбу Schlenk, наповнену аргоном, метил 4-бензилокси-5-метокси-2нітробензоатом (11,60г, 36,6ммол), і паладій на рослинному або тваринному вугіллі (1,17г, 10% Pd, 1,1ммол Pd) об'єднували і додавали тетрагідрофуран (250мл). Аргон замінювали воднем (1бар) і суміш інтенсивно перемішували при кімнатній температурі до завершення реакції. Паладій відділяли методом фільтрації через м'яку прокладку з целіту, а розчинник видаляли для отримання метил 2-аміно-4-гідрокси-5-метоксибензоату (6,56г, 36,0ммол, 98%), який використовували для подальшого очищення. LC/ESI-MS: m/z=166[MCH4O+H]+; Rt=2,17xв. Операція 4. Суміш формаміду (29мл), амонійформату (3,41г, 54ммол) і метил 2-аміно-4гідрокси-5-метоксибензоату (6,56г, 36,0ммол) нагрівали до 140°С протягом 4 годин. Після охолоджування до кімнатної температури додавали воду (75мл). Після перемішування протягом години осад 7-гідрокси-6-метокси-3,4-дигідрохіназолін-4он фільтрували, промивали водою і висушували (тверда речовина сірого кольору, 5,86г, 30,5ммол, 85%). LC/ESI-MS: m/z=193[M+H]+; m/z=191[Μ-Η]-; Rt=1,53xв. Операція 5. Суміш 7-гідрокси-6-метокси-3,4дигідрохіназолін-4-ону (5,86г, 30,5ммол) і оцтового ангідриду (21,5мл, 229ммол) в піридині (4,9мл, 61ммол) нагрівали до 100°С протягом 4 годин. Після охолоджування до кімнатної температури додавали крижану воду (200мл) і суміш інтенсивно перемішували протягом 1 години. Осад 7ацетокси-6-метокси-3,4-дигідрохіназолін-4-она фільтрували, промивали водою і висушували (сіра тверда речовина, 6,64г, 28,3ммол, 93%). LC/ESIMS: m/z=235[М+Н]+; m/z=233[Μ-Η]-; Rt=2,88мин. Див. також WO 04/043472, стор.32. Операція 6. 7-Ацетокси-6-метокси-3,4дигідрохіназолін-4-он (2,34г, 10,0ммол) конвертували в 4-хлоро-7-гідрокси-6-метоксихіназолін (1,22г, 5,79ммол, 58%) відповідно до опису в WO 04/043472, стор.32. LC/ESI-MS: m/z=211[M(35CI)+H]+; m/z=209[М(35СІ)-Н]-; Rt=2,45xв. Операція 7. Ди-терт-бутилазодикарбоксилат (0,478г, 2,8ммол) порціями додавали до суміші 4хлоро-7-гидрокси-6-метоксихіназоліну (0,350г, 1,66ммол), 3-(4-метил-пиперазин-1-ил)-пропан-1ола (проміжна речовина 9, 0,276г, 1,74ммол) і трифенілфосфіну (0,544г, 2,08ммол) в дихлорометані (20мл) при кімнатній температурі. При необхідності додавали додатково спирт. Після перемішування протягом 2 годин розчин концентрували до 10мл, укладали на силіка і хроматографували (градієнт, дихлорометан до дихлорометану:метанол =3:2 в межах 1 години) для отримання 4-хлоро-6-метокси-7-[3-(4-метилпіперазин-1іл)пропокси]хіназоліну (коричнева тверда речовина, 0,431г, 1,23ммол, 74%). LC/ESI-MS: m/z=351[M(35CI)+H]+; Rt=1,88xв. Див. також WO 04/043472, стор.32. Проміжна речовина 8: 4-Хлоро-7-метокси-6-[3(4-метилпіперазин-1-іл)пропокси]хіназолін. Операція 1. Метилізованілат (2,73г, 15ммол) конвертували в метил 3-бензилокси-4метоксибензоат (3,91г, 14,4ммол, 96%) аналогічно 92730 46 приготуванню проміжної речовини 7, операція 1. LC/ESI-MS: m/z=273[M+H]+; Rt=3,90xв. Операція 2. Метил 3-бензилокси-4метоксибензоат (2,83г, 10,4ммол) конвертували в Метил 5-бензилокси-4-метокси-2-нитробензоат (3,08г, 9,71ммол, 94%) аналогічно приготуванню проміжної речовини 7, операція 2. LC/ESI-MS: m/z=318[M+H]+; Rt=4,00xв. Операція 3. Метил 5-бензилокси-4-метокси-2нітробензоат (4,11г, 13,0ммол) конвертували в метил 2-аміно-5-гідрокси-4-метоксибензоат (2,56г, 13,0ммол, 100%) аналогічно приготуванню проміжної речовини 7, операція 3. LC/ESI-MS: m/z=166[M-СН4О+Н]+; Rt=1,95xв. Операція 4. 2-Аміно-5-гідрокси-4метоксибензоат (2,56г, 13,0ммол) конвертували в 6-гідрокси-7-метокси-3,4-дигідрохіназолін-4-он (1,91г, 9,94ммол, 76%) аналогічно приготуванню проміжної речовини 7, операція 4. LC/ESI-MS: m/z=193[M+H]+; m/z=191 [M-H]-; Rt=1,77хв. Операція 5. 6-Гідрокси-7-метокси-3,4дигідрохіназалін-4-он (1,90г, 9,86ммол) конвертували в 6-ацетокси-7-метокси-3,4-дигідрохіназолін4-он (2,22г, 9,48ммол, 96%) аналогічно приготуванню проміжної речовини 7, операція 5. LC/ESIMS: m/z=235[М+Н]+; m/z=233[M-H]-; Rt=2,20xв. Операція 6. 6-Ацетокси-7-метокси-3,4дигідрохіназалін-4-он (0,468г, 2,00ммол) конвертували в 4-хлоро-6-гідрокси-7-метоксихіназолін (0,398г, 1,89ммол, 95%) аналогічно приготуванню проміжної речовини 7, операція 6. LC/ESI-MS: 35СІ + 35СІ m/z=211[М( )+Н] ; m/z=209[М( )-Н] ; Rt=2,40xв. Операція 7. 4-Хлоро-6-гідрокси-7метоксихіназолін (0,373г, 1,77ммол) конвертували в 4-хлоро-7-метокси-6-[3-(4-метилпіперазин-1іл)пропокси]хіназолін (0,451г, 1,29ммол, 73%) аналогічно приготуванню проміжної речовини 7, операція 7. LC/ESI-MS: m/z=351 [M(35CI)+H]+; Rt=1,82хв. Проміжна речовина 9: 3-(4-Метилпіперазин-1іл)-пропан-1-ол. 1-Метилпіперазин (6,99мл, 63мол) розчиняли в толуолі (30мл). Поволі додавали 3Бромопропанол (2,62мл, 30ммол) і суміш перемішували протягом 12 годин при кімнатній температурі. Після нагріву до 80°С протягом 2 годин і охолоджування до кімнатної температури суміш фільтрували, а фільтрувальний коржик ретельно промивали толуолом. Після видалення розчинника залишок піддавали дистиляції (b.р.(барометричний тиск ), 180°С/2мбар) для отримання безбарвного масла (4,08г, 25,8ммол, 86%). 1Н NMR (CDCI3):δ=1,70 (ψ-quint, J≈5,8Hz, 2Н), 2,26 (s, 3Н), 2,35-2,6 (m,8H), 2,60 (ψ-t, J 5,8Hz, 2H), 3,77 (ψ-t, J≈5,3Hz, 2H), 4,09 (s,br., 1H). Проміжна речовина 10: 2-хлоро-4-(4метилпіперазин1-іл)-піримідин. Суміш 2,4-дихлоропіримідину (0,967г, 6,49ммол), 1-метилпіперазину (0,65г, 6,40ммол) і етилдиізопропіламіну (2,8мл, 16,22ммол) в етанолі (13мл) перемішували при -10°С протягом 2 годин і потім при кімнатній температурі - протягом 12 годин. Суміш розділяли між Н2О/солевим розчином (3:1; 100мл) і хлороформом (3 70мл). Об'єднані органічні фази промивалися один раз сольовим 47 розчином (50мл) і висушувалися в MgSO4. Видалення розчинника давало можливість отримати світло-бежеву тверду речовину, яку промивали етилацетатом/ обробляли ультразвуком для отримання необхідного продукту у вигляді безбарвного порошка, що згодом промивали Et2O. Додатковий продукт одержували після фракційної кристалізації промивального розчину. В цілому отримали 0,741г (3,48ммол, 54%) 2-хлоро-4-(4-метилпіперазин1-іл)піримідину. LC/ESI-MS: m/z=213[М(35СІ)+Н]+; Rt=0,5xв. Проміжна речовина 11: (2-Хлоропіримідин-4іл)-(5-метилпіразол-3-іл)амін. Суміш 2,4-дихлоропіримідину (0,967г, 6,49ммол), 3-аміно-5-метилпіразолу (0,63г, 6,40ммол) і етилдиізопропіламіну (2,8мл, 16,22ммол) в етанолі (13мл) перемішували при 10°С протягом 2 годин, потім при кімнатній температурі протягом 12 годин і остаточно при температурі 50°С протягом 3,5 годин. Суміш концентрували до загального об'єму, приблизно, 10мл. Після повторного додавання диетилового ефіру одержували (2-хлоропіримідин-4-іл)-(5-метилпіразол-3іл)амін (0,258г, 1,23ммол, 19%) у вигляді безбарвних кристалів. LC/ESI-MS: m/z=210[M(35CI)+H]+; m/z=208[М(35СІ)-Н]-; Rt=2,30xв. Проміжна речовина 12: N6-{6-метокси-7-[3-(4метилпіперазин-1-іл)-пропокси]-хіназолін-4-ил}бензотіазол-2,6-диамінгідрохлорид. Проміжна речовина 7 (0,285ммол) і бензотіазол-2,6-діамін (47мг, 0,285ммол) розчиняли в бутанолі (5мл). Додавали НСІ в діоксані (0,214мл, розчин 4М). Реакція завершувалася через 6 годин при 100°С. Отриманий осад фільтрували, промивали дихлорометаном і висушували у вакуумі (вихід склав 97%). LC/ESI-MS: m/z=480[М+Н]+. Проміжна речовина 13: N6-{6-метокси-7-[3-(4метилпіперазин-1-іл)-пропокси]-хіназолін-4-іл}бензотіазол-2,5-диамінгідрохлорид. Проміжна речовина 7 (0,285ммол) і бензотіазол-2,5-диамін (47мг, 0,285ммол) розчиняли в бутанолі (5мл). Додавали НСІ в діоксані (0,214мл, розчин 4М). Реакція завершувалася через 6 годин при 100°С. Отриманий осад фільтрували, промивали дихлорометаном і висушували у вакуумі (вихід склав 97%). LC/ESI-MS: m/z=480[М+Н]+. Проміжна речовина 14: 1- [6-(6-Хлоропіримідин-4-іламіно)-бензотіазол-2-іл]-3-(2метокси-5-метилфеніл)-мочевина. Суміш 4,6-дихлоропіримідину (180мг, 1,21ммол), бензотіазол-2,6-диаміну (200мг, 1,21ммол), іодиду натрію (216мг, 1,45ммол), eтилдиізопропіламину (0,25мл, 1,45ммол) і DMF (10мл) нагрівали при 85°С протягом 3 годин. Додавали 2-метокси-5-метилфенилізоціанат (0,20мл, 1,33ммол), і продовжували нагрівання при 85°С протягом 3 годин. Видаляли розчинник, а залишок обробляли СН2Сl2. Осад відділяли (0,57г, 85%). LC/ESI-MS: m/z=441 [М+Н]+; m/z=439[M-H]-; Rt=3,64xв. Синтез прикладів Приклад 1: N-[6-(6,7-Диметоксихіназолін-4іламіно)бензоксазол-2-іл]-бензамід був приготований шляхом нагріву суміші N-(6-амінобензоксазол2-іл)бензаміду (lМ 1,30мг, 0,118ммол) і 4-хлоро 92730 48 6,7-диметоксихіназоліну (Fluorochem, 26,5мг, 0,118ммол) в етанолі (3мл) до 80°С протягом 2 годин. Отриманий осад був відокремлений методом фільтрації, промитий етанолом і висушений (твердий продукт жовтого кольору, 38мг, 85мкмол, 72%). LC/ESI-MS: m/z=442[M+H]+; m/z=440[М-Н]-; Rt=2,43xв. Приклад 2: N-[6-(6,7-Диметоксихіназолін-4іламіно)бензотіазол-2-іл]-бензамід був приготований шляхом нагріву суміші N-(6-аминобензотіазол2-іл)бензамідау (lМ 2,30мг, 0,118ммол) і 4-хлоро6,7-диметоксихіназоліну (Fluorochem, 25мг, 0,111ммол) в eтиленгліколі (0,7мл) до 100°С протягом 2 годин. Додавали сольовий розчин (25мл) і насичений розчин гідрокарбонату натрія (25мл) і продукт екстрагували хлороформом (3 40мл). Після висушування в Na2So4 розчинник видаляли, а залишок очищали за допомогою pTLC (петролейний ефір:дихлорометан:метанол =12:14:3) для отримання твердого продукту жовтого кольору (19мг, 41мкмол, 37%). LC/ESI-MS: m/z=458[М+Н]+; m/z=456[M-H]-; Rt=2,88xв. Приклад 3: N-[6-(6,7-Диметоксихіназолін-4іламіно)бензотіазол-2-іл]ізонікотинамід був приготований шляхом нагріву суміші N-(6амінобензотіазол-2-іл)ізонікотинаміду (проміжна речовина 3, 50мг, 0,185ммол) і 4-хлоро-6,7диметоксихіназоліну (Fluorochem, 42мг, 0,185ммол) в етанолі (3мл) до 80°С протягом 2 годин. Отриманий осад був відокремлений методом фільтрації, промитий етанолом і висушений (твердий продукт жовтого кольору, 82мг, 0,179ммол, 97%). LC/ESI-MS: m/z=459[M+H]+; m/z=457[М-Н]-; Rt=2,65xв. Приклад 4: N-[6-(6,7-Диметоксихіназолін-4іламіно)бензотіазол-2-іл]нікотинамід був приготований шляхом нагріву суміші N-(6амінобензотіазол-2-іл)нікотинаміду (IМ 4, 30мг, 0,111ммол) і 4-хлоро-6,7-диметоксихіназоліну (Fluorochem, 25мг, 0,111ммол) в етанолі (3мл) до 80°С протягом 2 годин. Отриманий осад був відокремлений методом фільтрації, промитий етанолом і висушений (твердий продукт жовтого кольору, 44мг, 96мкмол, 87%). LC/ESI-MS: m/z=459[M+H]+; m/z=457[M-H]-; Rt=2,60xв. Приклад 5: N-(6-{6-Метокси-7-[3-(-4метилпіперазин-1-іл)пропокси]хіназолін-4-іламіно}бензотіазол-2-іл)бензамід був приготований шляхом нагріву суміші N-(6-амінобензотіазол-2іл)бензаміду (IМ 2,30мг, 0,111ммол), 4-хлоро-6метокси-7-[3-(-4-метилпіперазин-1іл)пропокси]хіназоліну (проміжна речовина 7,39мг, 0,111ммол), eтилдиізопропіламіну (40мкл, 0222ммол) і соляної кислоти (НСІ) (84мкл, розчин 4М в діоксані, 0,333ммол) в n-бутанолі (3мл) до 110°С протягом 2 годин. Додавали насичений розчин гідрокарбонату натрію і продукт екстрагували хлороформом. Після промивки водою і висушування в Na2So4 розчинник видаляли, а залишок витримували в невеликій кількості метанолу, після чого поволі додавали воду. В результаті перемішування суміші протягом 12 годин одержували твердий продукт коричневого кольору (38мг, 65мкмол, 59%). LC/ESI-MS: m/z=584[M+H]+; m/z=582[M-H]-; Rt=2,27xв. 49 Приклад 6: N-(6-{7-Метокси-6-[3-(-4-метил піперазин-1-іл)пропокси]хіназолін-4-іламіно}бензотіазол-2-іл)бензамід був приготований шляхом нагріву суміші N-(6-амінобензотіазол-2іл)бензаміду (проміжна речовина 2,40мг, 0,148ммол), 4-хлоро-7-метокси-6-[3-(-4метилпіперазин-1-іл)пропокси]хіназоліну (IМ 8,52мг, 0,148ммол) i соляної кислоти (НСІ) (112мкл, розчин 4М в диоксані, 0,444ммол) в nбутанолі (6мл) до 110°С на протязі 5 годин. Додавали насичений розчин гідрокарбонату натрію і продукт екстрагували хлороформом. Після промивки водою і висушування в Na2So4 розчинник видаляли, а залишок витримували в невеликій кількості метанолу, після чого поволі додавали воду. В результаті перемішування суміші протягом 12 годин одержували твердий продукт сірого кольору (39мг, 66мкмол, 45%). LC/ESI-MS: m/z=584[М+Н]+; m/z=582[М-Н]-; Rt=2,26xв. Приклад 7: N-[6-(Пурін-6-іламіно)бензотіазол2-іл]-бензамід був приготований шляхом нагріву суміші N-(6-амінобензотіазол-2-іл)бензаміду (IМ 2,50мг, 0,86ммол) і 6-хлоропурину (29мг, 0,186ммол) в етанолі (3мл) до 80°С протягом 4 годин. Отриманий осад було відділено методом фільтрації і промито етанолом (69мг, 0,178ммол, 96%). LC/ESI-MS: m/z=388[M+H]+; m/z=386[М-Н]-; Rt=3,07xв. Приклад 8: Ν-{6-[4-(-4-метилпіперазин-1іл)піримідин-2-іламіно]бензотіазол-2-іл}бензамід був приготований шляхом нагріву суміші N-(6амінобензотіазол-2-іл)бензаміду (IМ 2,50мг, 0,186ммол) і 2-хлоро-4-(4-метилпіперазин1іл)піримідину (IМ 10, 40мг, 0,186ммол) в етанолі (3мл) до 80°С протягом 4 діб. Після розчинення осаду шляхом додавання диметилформаміду pTLC (дихлорометан:метанол =4:1) одержували твердий продукт жовтого кольору (44мг, 0,100ммол, 54%). LC/ESI-MS: m/z=446[M+H]+; m/z=444[M-H]-; Rt=2,12xв. Приклад 9: N-{6-[4-(5-Метилпіразол-3іламіно)піримідин-2-іламіно]бензотіазол-2іл}бензамід був приготований шляхом нагріву суміші N-(6-амінобензотіазол-2-іл)бензаміду (IМ 2,35мг, 0,13ммол) і (2-хлоропіридин-4-іл)-(5метилпіразол-3-іл)аміну (IМ 11,30мг, 0,143ммол) в етанолі (3мл) до 80°С протягом 9 годин. Осад відділяли методом фільтрації, промивали етанолом і висушували (38мг, 85мкмол, 66%). LC/ESI-MS: m/z=443[M+H]+; m/z=441 [М-Н]-; Rt=2,80xв. Приклад 10: N-[5-(6,7-Диметоксихіназолін-4іламіно)бензотіазол-2-іл]-бензамід був приготований шляхом нагріву суміші N-(5-амінобензотіазол2-іл)бензаміду (IМ 5,30мг, 0,111ммол) і 4-хлоро6,7-диметоксихіназоліну (Fluorochem, 25мг, 0,111ммол) в етиленгліколі (0,7мл) до 100°С протягом 2 годин. Додавали сольовий розчин (25мл) і насичений розчин гідрокарбонату натрію (25мл) і продукт екстрагували хлороформом (3 40мл). Після висушування в Na2So4 розчинник видаляли і до осаду додавали етилацетат і петролейний ефір. У результаті фільтрації одержували твердий продукт жовтого кольору (28мг, 60мкмол, 55%). LC/ESI-MS: m/z=458[M+H]+; m/z=456[M-H]-; Rt=3,20xв. 92730 50 Приклад 11: N-[5-(Пурин-6іламіно)бензотіазол-2-іл]-бензамід був приготований шляхом нагрівання суміші N-(5амінобензотіазол-2-іл)бензаміду (IМ 5,50мг, 0,186ммол) і 6-хлоропурину (29мг, 0,186ммол) в етанолі (3мл) до 80°С протягом 4 годин. Отриманий осад був відділений методом фільтрації і промитий етанолом (68мг, 0,174ммол, 94%). LC/ESIMS: m/z=388[M+H]+; m/z=386[M-H]-; Rt=3,13xв. Приклад 12: N-{5-[4-(-4-метилпіперазин-1іл)піримідин-2-іламіно]бензотіазол-2-іл}бензамід був приготований шляхом нагрівання суміші N-(5амінобензотіазол-2-іл)бензаміду (IМ 5,50мг, 0,186ммол) і 2-хлоро-4-(4-метилпіперазин1іл)піримідину (IМ 10, 40мг, 0,186ммол) в етанолі (3мл) до 80°С протягом 4 діб. Додавали сольовий розчин (25мл) і насичений розчин гідрокарбонату натрію (25мл) і продукт екстрагували хлороформом (3 40мл) і етилацетатом (40мл). Комбіновану органічну фазу висушували в Na2So4, а розчинник видаляли. Осад очищували за допомогою pTLC (дихлорометан:метанол =4:1). У результаті, отримували твердий продукт жовтого кольору (44мг, 99мкмол, 53%). LC/ESI-MS: m/z=446[M+H]+; m/z=444[M-H]-; Rt=2,38xв. Приклад 13: N-{5-[4-(5-Метилпіразол-3іламіно)піримідин-2-іламіно]бензотіазол-2іл}бензамід був приготований шляхом нагрівання суміші N-(5-амінобензотіазол-2-іл)бензаміду (IМ 5,35мг, 0,13ммол) і (2-хлоропіридин-4-іл)-(5метилпіразол-3-іл)аміну (IМ 11, 30мг, 0,143ммол) в етанолі (3мл) до 80°С протягом 9 годин. Осад відділяли методом фільтрації, промивали етанолом і висушували (32мг, 72мкмол, 56%). LC/ESI-MS: m/z=443[M+H]+; m/z=441 [М-Н]-; Rt=2,92xв. Приклад 15: N-(6-{6-Метокси-7-[3-(-4метилпіперазин-1-іл)пропокси]-хіназолін-4іламіно}-бензооксазол-2-іл)бензамід був приготований у результаті проведення реакції проміжної речовини 1 (0,138мМ) з проміжною речовиною 7 (0,138мМ) в бутанолі в умовах кислотного каталізу (3,0eкв., 0,105мл, 4М НСІ в Диоксані) при 110°С. Реакцію завершували через 5 годин. Після охолодження реакцийну суміш розподіляли між насиченим водним розчином NaHCO3 і етилацетатом. Шари розділяли, водяний шар екстрагували етилацетатом. Комбіновані органічні шари промивали нейтральною водою, висушували в Na2So4. Після фільтрації і видалення розчинника в умовах вакууму продукт очищали, використовуючи препаративну HPLC. Приклад 16: N-(5-{7-Метокси-6-[3-(-4метилпіперазин-1-іл)пропокси]хіназолін-4іламіно}бензотіазол-2-іл)бензамід був приготований шляхом нагрівання суміші N-(5амінобензотіазол-2-іл)бензаміду (IМ 5,35мг, 0,13ммол), 4-хлоро-7-метокси-6-[3-(-4метилпіперазин-1-іл)пропокси]хіназоліну (IМ 8,46мг, 0,13ммол) і 4Μ НСІ в діаксані (0,09мл, 0,39ммол) в n-бутанолі (3мл) до 110°С протягом 5 годин. Сіль продукта НСІ випадала в осад. Вона була відділена фільтрацією, два рази промита СН2НСІ2. Подальше очищення не потрібне (65мг, 0,11ммол, 94%). LC/ESI-MS: m/z=620[M+H]+; m/z=618[М-Н]-; Rt=2,43xв. 51 Приклад 17: N-(5-{6-Метокси-7-[3-(-4метилпіперазин-1-іл)пропокси]хіназолін-4іламіно}бензотіазол-2-іл)бензамід був приготований у відповідності до процедури, описаної для приклада 15, із проміжної речовини 5 і проміжної речовини 7. Приклад 18: 3-Хлоро-N-(6-{6-Метокси-7-[3-(-4метилпіперазин-1-іл)пропокси]хіназолін-4іламіно}бензотіазол-2-іл)бензамід був приготований у результаті забезпечення реакції проміжної речовини 12 (30мг, 58мкмол) з 3хлоробензоілхлоридом (8мкл, 63мкмол) в суміші піридину і DMF (1:1, 4мл всього) в присутності триетиламіну (100мкл, 0,71ммол) при 60°С. Реактивну суміш розподіляли між насиченим водним розчином NаНСО3 і DMF. Після екстрагування за допомогою дихлорометану комбіновані органічні шари висушували в Na2So4. Після фільтрації розчинника видаляли в умовах вакууму і продукт очищали, використовуючи препаративну HPLC (20мг, виход 55%). Приклад 19: 3-Хлоро-N-(5-{6-Метокси-7-[3-(-4метилпіперазин-1-іл)-пропокси]-хіназолін-4іламіно}бензотіазол-2-іл)бензамід був приготований за методикою процедури, описаної для приклада 18, починаючи від проміжної речовини 13. Приклад 20: 1-(4-Хлоро-3трифторометилфеніл)-3-(6-{6-метокси-7-[3-(-4метилпіперазин-1-іл)пропокси]хіназолін-4-іламіно}бензотіазол-2-іл)-мочевина була приготована у результаті забезпечення реакції проміжної речовини 12 (30мг, 58мкмол) з 1-хлоро-4-ізоціанато-2трифторометилбензолом (13мг, 58мкмол) в дихлорометані в присутності триетиламіну (5 крапель). Продукт очищали, використовуючи препаративну HPLC (5мг, виход 15%). Приклад 21: 1-(4-Хлоро-3-трифторометил феніл)-3-(5-{6-метокси-7-[3-(-4-метилпіперазин-1іл)пропокси]хіназолін-4-іламіно}-бензотіазол-2-іл)мочевина була приготована у відповідності до 92730 52 процедури, описаної для приклада 20, починаючи з проміжної речовини 13. Приклад 22: 1-(2-Метокси-5-метилфеніл)-3-(6{6-метокси-7-[3-(-4-метилпіперазин-1-іл)-пропокси]хіназолін-4-іламіно}-бензотіазол-2-іл)-мочевина була приготована у відповідності до процедури, описаної для приклада 20, починаючи від проміжної речовини 12, і 2-ізоціанато-1-метокси-4метилбензолу. Приклад 23: 1-(6-{6-Метокси-7-[3-(-4метилпіперазин-1-іл)-пропокси]-хіназолін-4іламіно}-бензотіазол-2-іл)-3-(2-метоксифеніл)мочевина була приготована у відповідності до процедури, описаної для приклада 20, починаючи від проміжної речовини 12, і 1-ізоціанато-2метоксибензолу. Приклад 24: 1-{6-[6-(2-Гідроксиетиламіно)піримідин-4-іламіно]-бензотіазол-2-іл}-3-(2метокси-5-метилфеніл)-мочевина була приготована шляхом нагрівання суміші lМ 14(100мг, 0,227ммол) і 3-амінометанолу (1мл) при 85°С протягом 3 годин. Продукт був осаджений додаванням води (47мг, 45%). Приклад 24: 1-{6-[6-(2-Гідроксиетиламіно)піримідин-4-іламіно]-бензотіазол-2-іл}-3-(2метокси-5-метилфеніл)-мочевина була приготована шляхом нагрівання суміші lМ 14(100мг, 0,227ммол) і 3-амінометанолу (1мл) при 85°С протягом 3 годин. Продукт був осаджений додаванням води (47мг, 45%). Приклад 25: 1-{6-[6-(3-Гідроксипропіламіно)піримидин-4-іламіно]-бензотіазол-2-іл}-3-(2метокси-5-метилфеніл)-мочевина бyла приготовлена шляхом нагрівання суміші 14(100мг, 0,227ммол) і 3-амінопропанола (1мл) при 85°С протягом 3 годин. Продукт був осаджений додаванням води (42мг, 39%). Аналітичні дані сполук за формулою (І) даного винаходу. 53 92730 54 55 92730 56 57 Аналітичні дані сполук за формулою (Іа) даного винаходу. 92730 58 59 Аналітичні дані сполук за формулою (ІI) даного винаходу. 92730 60
ДивитисяДодаткова інформація
Назва патенту англійськоюBenzazole analogues and use thereof
Автори англійськоюHerz Thomas, Krauss Rolf, Kubbutat Michael, Lang Martin, Schaechtele Christoph, Tasler Stefan, Totzke Frank
Назва патенту російськоюАналоги бензазола и их применение
Автори російськоюГерц Томас, Краусс Рольф, Куббутат Майкл, Ланг Мартин, Шехтеле Кристоф, Таслер Стефан, Тотцке Франк
МПК / Мітки
МПК: A61K 31/52, C07D 417/12, C07D 417/14, A61P 35/00, C07D 413/12, C07D 473/34, A61K 31/505, C07D 403/12
Мітки: застосування, бензазолу, аналоги
Код посилання
<a href="https://ua.patents.su/32-92730-analogi-benzazolu-i-kh-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Аналоги бензазолу і їх застосування</a>
Попередній патент: Спосіб та установка для виробництва титанового шлаку з ільменіту
Наступний патент: Лікарський засіб для гігієнічної обробки вуха
Випадковий патент: Хопер-вагон для перевезення сипких вантажів