Фосфонатні аналоги сполук, що інгібують віл протеази, фармацевтична композиція на їх основі та їх застосування
Номер патенту: 80819
Опубліковано: 12.11.2007
Автори: Уанг Джіан'їнг, Ю Ричард Х., Дестгех Азар, Пьюн Хьюнг-Джунг, Уільямс Метью А., Спарасіно Марк, Роув Таніша Д., Ксу Ліанхонг, Суамінатан Сандарамурті, Чен Ксяову, Янг Женг-Ю, Бекер Марк М., Макмен Річард Л., Брайант Кліффорд, Джін Хаолюн, Таріо Джеймс Д., Лі Уільям А., Чен Джеймс М., Лі Крістофер П., Кім Чоунг У., Ліу Хонгтао, Жанг Джіанкун, Хі Гонг-Ксін, Фардіс Марія, Жанг Ліджун, Лін Куей-Їнг, Аріміллі Мерті Н., Мітчелл Майкл Л., Нельсон Пітер Х.
Формула / Реферат
1. Сполука, що має формулу:
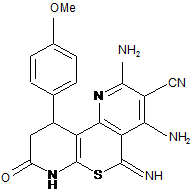 ,
,
у якій
А3 являє собою
a) -OCH2P(O)R1R2;
b) -P(O)R1R2;
c) -CH2P(O)R1R2;
де в радикалах а), b), с) R1 та R2 незалежно вибрані з групи, яка включає гідрокси, метокси, етокси, трифторетокси, ізопропокси, фенокси, бензилокси та O-півалоїлоксиметил;
d) -OCH2P(O)R1R2, де R1 та R2 незалежно вибрані з групи, яка включає Gly-Et, Ala-Et, Aba-Et, Val-Et, Leu-Et, Phe-Bu та Phe-Et;
e) -OCH2P(O)R1R2,
f) -OCH2CH2OCH2P(O)R1R2,
де в радикалах e), f) R1 являє собою гідрокси, метокси, етокси, трифторетокси, ізопропокси, фенокси або бензилокси, та R2 являє собою Gle-Et, Lac-Me, Lac-Et, Lac-iPr, Lac-Bu, Lac-EtMor, Lac-Me, Lac-Et, Lac-Bn, Lac-OH, Hba-Et, Hba-tBu, Hba-OH, MeBut-Et або DiMePro-Me;
g) -OCH2P(O)R1R2,
де R1 являє собою фенокси, бензилокси, етокси, трифторетокси або гідроксил, та R2 вибраний з Gly-Bu, Аlа-Ме, Ala-Et, Ala-iPr, (D)Ala-iPr, Ala-Bu, Aba-Et, Aba-Bu та Ala-OH;
h) -CH2NHCH2CH2P(O)R1R2,
де R1 являє собою гідрокси, метокси, етокси, трифторетокси, ізопропокси, фенокси або бензилокси, та R2 вибраний з Gle-Et, Lac-Me, Lac-Et, Lac-iPr, Lac-Bu, Lac-EtMor, Lac-Bn, Lac-OH, Hba-Et, Hba-tBu, Hba-OH, MeBut-Et, DiMePro-Me, Gly-Bu, Alа-Ме, Ala-Et, Ala-iPr, (D)Ala-iPr, Ala-Bu, Aba-Et, Aba-Bu та Alа-ОН; та
їх енантіомери і діастереомери, а також їх фізіологічно прийнятні солі, гідрати та проліки.
2. Сполука за п. 1, у якій А3 являє собою -OCH2P(O)R1R2 або
-ОСН2СН2ОСН2Р(O)R1R2 (радикали е) та f)) та у якій лактатні складноефірні групи мають (R)-конфігурацію.
3. Сполука за п. 1, у якій А3 являє собою -OCH2P(O)R1R2 або -OCH2CH2OCH2P(O)R1R2 (радикали е) та f)) та лактатні складноефірні групи мають (S)-конфігурацію.
4. Сполука за п. 1, у якій А3 являє собою -OCH2P(O)R1R2 та R1 і R2 незалежно вибрані з групи, яка включає гідрокси та етокси.
5. Сполука за п. 4, у якій R1 і R2 являють собою гідрокси або етокси.
6. Сполука, що має формулу:
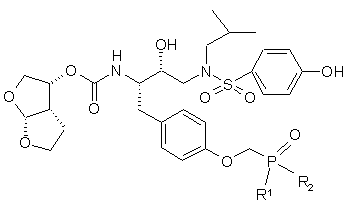 ,
,
у якій R1 та R2 незалежно вибрані з групи, яка включає гідрокси, метокси, етокси, трифторетокси, ізопропокси, фенокси, бензилокси та O-півалоїлоксиметил.
7. Застосування сполуки за будь-яким з пп. 1-6 у виробництві лікарського засобу для лікування ВІЛ-інфекції.
8. Застосування сполуки за будь-яким з пп. 1-6 у виробництві лікарського засобу для лікування захворювань, що впливають на білі кров’яні клітини.
9. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-6 та звичайні носії і наповнювачі.
Текст
1. Сполука, що має формулу: 80819 2 C2 ФАРМАЦЕВТИЧНА (11) (21) 20041109372 (22) 25.04.2003 (24) 12.11.2007 (86) PCT/US03/12901, 25.04.2003 (31) 60/375,622 (32) 26.04.2002 (33) US (31) 60/375,665 (32) 26.04.2002 (33) US (31) 60/375,779 (32) 26.04.2002 (33) US (31) 60/375,834 (32) 26.04.2002 (33) US (72) АРІМІЛЛІ МЕРТІ Н., US/US, БЕКЕР МАРК М., US/US, БРАЙАНТ КЛІФФОРД, US/US, ЧЕН ДЖЕЙМС М., US/US, ЧЕН КСЯОВУ, US/US, ДЕСТГЕХ АЗАР, US/US, ФАРДІС МАРІЯ, US/US, ХІ ГОНГ-КСІН, CN/US, ДЖІН ХАОЛЮН, CA/US, КІМ ЧОУНГ У., US/US, ЛІ УІЛЬЯМ А., US/US, ЛІ КРІСТОФЕР П., US/US, ЛІН КУЕЙ-ЇНГ, US/US, ЛІУ ХОНГТАО, CN/US, МАКМЕН РІЧАРД Л., GB/US, МІТЧЕЛЛ МАЙКЛ Л., US/US, НЕЛЬСОН ПІТЕР Х., ПРОТЕАЗИ, UA 1 ВІЛ (19) (54) ФОСФОНАТНІ АНАЛОГИ СПОЛУК, ЩО ІНГІБУЮТЬ КОМПОЗИЦІЯ НА ЇХ ОСНОВІ ТА ЇХ ЗАСТОСУВАННЯ 3 80819 4 їх енантіомери і діастереомери, а також їх фізіологічно прийнятні солі, гідрати та проліки. OH 2. Сполука за п. 1, у якій А3 являє собою H OCH2P(O)R1R2 або O N N OCH3 -ОСН2СН2ОСН2Р(O)R1R2 (радикали е) та f)) та у S O O O якій лактатні складноефірні групи мають (R)O конфігурацію. 3. Сполука за п. 1, у якій А3 являє собою O OCH2P(O)R1R2 або -OCH2CH2OCH2P(O)R1R2 A3 (радикали е) та f)) та лактатні складноефірні групи , мають (S)-конфігурацію. у якій 4. Сполука за п. 1, у якій А3 являє собою А3 являє собою OCH2P(O)R1R2 та R1 і R2 незалежно вибрані з a) -OCH2P(O)R1R2; групи, яка включає гідрокси та етокси. b) -P(O)R1R2; 5. Сполука за п. 4, у якій R1 і R2 являють собою c) -CH2P(O)R1R2; гідрокси або етокси. де в радикалах а), b), с) R1 та R2 незалежно 6. Сполука, що має формулу: вибрані з групи, яка включає гідрокси, метокси, етокси, трифторетокси, ізопропокси, фенокси, бензилокси та O-півалоїлоксиметил; OH H d) -OCH2P(O)R1R2, де R1 та R2 незалежно вибрані O N N OH з групи, яка включає Gly-Et, Ala-Et, Aba-Et, Val-Et, S Leu-Et, Phe-Bu та Phe-Et; O O O O e) -OCH2P(O)R1R2, f) -OCH2CH2OCH2P(O)R1R2, O O де в радикалах e), f) R1 являє собою гідрокси, P O метокси, етокси, трифторетокси, ізопропокси, фенокси або бензилокси, та R2 являє собою GleR2 R1 Et, Lac-Me, Lac-Et, Lac-iPr, Lac-Bu, Lac-EtMor, Lac, Me, Lac-Et, Lac-Bn, Lac-OH, Hba-Et, Hba-tBu, Hbaу якій R1 та R2 незалежно вибрані з групи, яка OH, MeBut-Et або DiMePro-Me; включає гідрокси, метокси, етокси, трифторетокси, g) -OCH2P(O)R1R2, ізопропокси, фенокси, бензилокси та Oде R1 являє собою фенокси, бензилокси, етокси, півалоїлоксиметил. трифторетокси або гідроксил, та R2 вибраний з 7. Застосування сполуки за будь-яким з пп. 1-6 у Gly-Bu, Аlа-Ме, Ala-Et, Ala-iPr, (D)Ala-iPr, Ala-Bu, виробництві лікарського засобу для лікування ВІЛAba-Et, Aba-Bu та Ala-OH; інфекції. h) -CH2NHCH2CH2P(O)R1R2, 8. Застосування сполуки за будь-яким з пп. 1-6 у де R1 являє собою гідрокси, метокси, етокси, виробництві лікарського засобу для лікування трифторетокси, ізопропокси, фенокси або захворювань, що впливають на білі кров’яні бензилокси, та R2 вибраний з Gle-Et, Lac-Me, Lacклітини. Et, Lac-iPr, Lac-Bu, Lac-EtMor, Lac-Bn, Lac-OH, 9. Фармацевтична композиція, що містить сполуку Hba-Et, Hba-tBu, Hba-OH, MeBut-Et, DiMePro-Me, за будь-яким з пп. 1-6 та звичайні носії і Gly-Bu, Alа-Ме, Ala-Et, Ala-iPr, (D)Ala-iPr, Ala-Bu, наповнювачі. Aba-Et, Aba-Bu та Alа-ОН; та Винахід в цілому стосується сполук з антивірусною активністю, а саме - з властивостями проти ВІЛ. СНІД є головною проблемою охорони здоров'я в усьому світі. Хоча ліки, спрямовані проти вірусів ВІЛ, широко застосовуються і виявилися ефективними, токсичність та розвиток резистентних штамів обмежують їх корисність. Способи аналізу, які дозволяють визначити присутність, відсутність або кількість вірусів ВІЛ мають практичне застосування для пошуків інгібіторів, а також для діагностування присутності ВІЛ. Інфекція вірусу імунодефіциту людини (ВІЛ) та пов'язана з нею хвороба є головною проблемою для охорони здоров'я в усьому світі. Ретровірус вірус імунодефіциту людини 1-го типу (ВІЛ-1), який належить до родини лентивірусів приматів [DeClercq Ε (1994) Annals of the New York Academy of sciences, 724:438-456; Barre-Sinoussi F (1996) Lancet, 348:31-35], всіма визнано збудником синдрому набутого імунодефіциту (СНІД) [Tarrago et al., FASEB Journal 1994, 8:497-503]. СНІД є результатом повторної реплікації ВІЛ-1 та зниження імунної здатності, насамперед, різкого зниження кількості CD4+ лімфоцитів. Зрілий вірус має геном одноланцюгової РНК, який кодує 15 білків [Frankel et al. (1998) Annual Review of Biochemistry, 67:1-25; Katz et al. (1994) Annual Review of Biochemistry, 63:133-173], включаючи три головні ферменти: (і) протеазу (Prt) [von der Helm К (1996) Biological Chemistry, 377:765-774]; (ii) зворотну транскриптазу (RT) [Hottiger et al. (1996) Biological Chemistry Hoppe-Seyler, 377:97-120], фермент, унікальний для ретровірусів; та (ііі) інтегразу [Asante et al. (1999) Advances in Virus 5 80819 6 Research 52:351-369; Wlodawer A (1999) Advances [див., наприклад, P.L.Darke, et al., J.Biol. Chem., in Virus Research 52:335-350; Esposito et al. (1999) 264:2307-2312 (1989)] і синтезується хімічним Advances in Virus Research 52:319-333]. Протеаза шляхом [J.Schneider and S.B.Kent, Cell, 54:363-368 відповідає за процесинг прекурсорів вірусних (1988); і R.F.Nutt, et al., Proc. Natl. Acad. Sci., USA, поліпротеїнів, інтеграза відповідає за включення 85:7129-7133 (1988)]. Сайт - специфічний форми дволанцюгової ДНК вірусного геному у ДНК мутагенез [P.L.Darke, et al., above; і Ν.Ε.Kohl, et al., хазяїна, a RT є головним ферментом у реплікації Proc. Natl. Acad. Sci., USA, 85:4686-4690 (1988)] та вірусного геному. У вірусній реплікації RT діє як інгібування пепстатином [P.L.Darke, et al., J.Biol. РНК- та ДНК-залежна ДНК полімераза для Chem., 264:2307-2312 (1989); S.Seelmeier, et al., перетворення геному одноланцюгової РНК на Proc. Natl. Acad. Sci., USA, 85:6612-6616 (1988); C.дволанцюгову ДНК. Оскільки кодована вірусом Z.Giam and I.Borsos, J.Biol. Chem., 263:14617зворотна транскриптаза (RT) опосередковує 14720 (1988); і J.Hansen, et al., EMBO J., 7:1785специфічні реакції під час природного відтворення 1791 (1988)] підтвердили механічну функцію вірусу, інгібування RT ВІЛ є важливим протеази ВІЛ як аспартил-протеази. Дослідження терапевтичним об'єктом для лікування ВІЛпродемонструвало, що протеаза розщеплюється у інфекції та пов'язаної з нею хвороби. місцях, передбачених у пептидах, змодельованих Аналіз послідовностей повних геномів з після фактичного розщеплення ділянок кількох інфекційних і неінфекційних ВІЛ-ізолятів ферментом у gag- та роl-білків-прекурсорів під час значною мірою пояснює структуру вірусу та типи вірусного визрівання. [P.L. Darke, et al., Biochem. молекул, які є суттєвими для його реплікації та Biophys. Res. Communs., 156:297-303 (1988)]. визрівання до інфекційних видів. Протеаза ВІЛ є Рентгенівський кристалографічний аналіз ВІЛсуттєвою для процесингу вірусних gag та gag-pol протеази [Μ.A.Navia, et al., Nature, 337:615-620 поліпептидів до зрілих віріонних білків. [L.Ratner, et (1989)] та спорідненого ретровірусного ферменту з al., Nature, 313:277-284 (1985); L.Η.Pearl and вірусу саркоми Рауса [М.Miller, et al., Nature, W.R.Taylor, Nature, 329:351 (1987)]. ВІЛ має таку 337:576-579 (1989)] виявили активний сайт у саму організацію gag/pol/env, що й в інших димері протеази, який є ідентичним тому, який ретровірусах [L.Ratner, et al., above; S.Wainспостерігається в інших аспартил-протеазах, Hobson, et al., Cell, 40:9-17 (1985); R.Sanchezтаким чином, підтверджуючи припущення Pescador, et al., Science, 227:484-492 (1985); і [L.Н.Pearl and W.R.Taylor, див. вище], що фермент Μ.A.Muesing, et al., Nature, 313:450-458 (1985)]. ВІЛ є активним як димер. [Див. також Joseph Терапевтичною метою у разі СНІД є A.Martin, "Recent Advances in the Design of HIV інгібування вірусної протеази (або протеїнази), яка Proteinase Inhibitors", Antiviral Research, 17 (1992) є суттєвою для процесингу прекурсорів ВІЛ-злитих 265-278]. поліпептидів. Було виявлено, що у ВІЛ та кількох Інгібітори ВІЛ-протеази застосовують для інших ретровірусах протеолітичне визрівання gag обмеження утворення та прогресування інфекції та gag/pol злитих поліпептидів (процес, необхідний шляхом терапевтичного введення, а також у для утворення інфекційних вірусних частинок) діагностичних аналізах на ВІЛ. До інгібіторів опосередковується протеазою, яка й сама протеази, ухвалених Управлінням з контролю за кодується pol-ділянкою вірусного геному продуктами та ліками (FDA), належать: [Y.Yoshinaka, et al., Proc. Natl. Acad. Sci. USA, - саквінавір (Invirase®, Fortovase®, Hoffman-La 82:1618-1622 (1985); Y.Yoshinaka, et al., J.Virol., Roche, EP-00432695 та EP-00432694) 55:870-873 (1985); Y.Yoshinaka, et al., J.Virol., - ритонавір (Norvir®, Abbott Laboratories) 57:826-832 (1986); і К. von der Helm, Proc. Natl. - індинавір (Crixivan®, Merck & Co.) Acad. Sci., USA, 74:911-915 (1977)]. Було - нелфінавір (Viracept®, Pfizer) виявлено, що інгібування протеази інгібує - ампренавір (Agenerase®, GlaxoSmithKline, процесинг HIV р55 у клітині ссавця та реплікацію Vertex Pharmaceuticals) ВІЛ у Т-лімфоцитах [Т.J.McQuade, et al., Science, лопінавір/ритонавір (Kaletra®, Abbott 247:454 (1990)]. Laboratories) Медикаменти, ухвалені у Сполучених Штатах Експериментальними інгібіторами протеази є: для терапії при СНІД, включають нуклеозидні - фозампренавір (GlaxoSmithKline, Vertex інгібітори RT [Smith et al. (1994) Clinical Investigator, Pharmaceuticals) 17:226-243], інгібітори протеази та ненуклеозидні - типанавір (Boehringer Ingelheim) інгібітори RT (NNRTI), [Johnson et al. (2000) - атазанавір (Bristol-Myers Squibb). Advances in Internal Medicine, 45 (1-40) Porche DJ Існує потреба у терапевтичних засобах проти (1999) Nursing Clinics of North America, 34:95-112]. ВІЛ, тобто ліках, які мають поліпшені антивірусні Протеаза (або протеїназа), яка складається та фармакокінетичні властивості, з підвищеною лише з 99 амінокислот, належить до найменших з активністю проти розвитку резистентності до ВІЛ, відомих ферментів, і продемонстрована нею поліпшеною біодоступністю при пероральному гомологія з аспартил-протеазами, такими як введенні, більшою ефективністю та подовженим пепсин та ренін [L.Н.Pearl and W.R.Taylor, Nature, ефективним півперіодом in vivo. Нові інгібітори 329:351-354 (1987); і I.Katoh, et al., Nature, 329:654ВІЛ-протеази (РІ) повинні бути активними проти 656 (1987)], дозволила дійти висновку щодо мутантних штамів ВІЛ, мати індивідуальні профілі тривимірної структури та механізму ферменту резистентності, менше побічних ефектів, менш [L.Н. Pearl and W.R.Taylor, див. вище], яку з того складний режим дозування, і бути активними при часу було підтверджено експериментально. пероральному введенні. Зокрема, існує потреба у Активна протеаза ВІЛ експресується у бактеріях менш обтяжливому режимі дозування, наприклад, 7 80819 8 одна пігулка раз на день. Хоча ліки, спрямовані вірусу. Вони є корисними для лікування людей, проти ВІЛ-протеази, широко застосовуються і інфікованих людським ретровірусом, таким як виявили свою ефективність, зокрема, при вірус імунодефіциту людини (штами ВІЛ-1 або ВІЛзастосуванні у комбінації, токсичність та розвиток 2) або вірусами Т-клітинної лейкемії (HTLV-I або резистентних штамів обмежують їх корисність HTLV-II), що призводить до синдрому набутого [Palella, et al. N.Engl. J. Med. (1998) 338:853-860; імунодефіциту (СНІД) та/або пов'язаних з ним Richman, D. D. Nature (2001) 410:995-1001]. хвороб. Даний винахід охоплює нові сполуки Комбінована терапія з інгібіторами РІ та RT фосфонатного інгібітора ВІЛ-протеази (РІ) та виявилися високоефективною у пригніченні фосфонатні аналоги відомих ухвалених та вірусної реплікації до неквантифікованих рівнів експериментальних інгібіторів протеази. Сполуки протягом тривалого періоду часу. Крім того, згідно з винаходом необов'язково забезпечують комбінована терапія з інгібіторами RT та протеази накопичення в клітинах (клітинну акумуляцію), як продемонструвала синергічний ефект у викладено нижче. пригніченні реплікації ВІЛ. На жаль, для багатьох Даний винахід в цілому стосується пацієнтів у даний час комбінована терапія накопичення або утримання терапевтичних сполук виявляється марною через розвиток всередині клітин. Більш конкретно винахід резистентності до ліків, недотримання складних стосується досягнення високих концентрацій режимів дозування, фармакокінетичну взаємодію, фосфонат-вмісних молекул у ВІЛ-інфікованих токсичність та брак ефективності. Отже, існує клітинах. Внутрішньоклітинного спрямування потреба у нових інгібіторах ВІЛ-протеази, які є досягають завдяки способам та композиціям, які синергічними у комбінації з іншими інгібіторами забезпечують накопичення або утримання ВІЛ. біологічно активних агентів всередині клітин. Таке На поліпшенні доставлення ліків та інших ефективне спрямування може застосовуватися до агентів для спрямування на клітини та тканини вже різних терапевтичних композицій та процедур. багато років зосереджено значні дослідження. Композиції згідно з винаходом включають нові Хоча робилося багато спроб розробки ефективних РІ-сполуки, які мають принаймні одну фосфонатну способів введення біологічно активних молекул у групу. Винахід охоплює всі нові ухвалені та клітини, як in vivo, так і in vitro, жодна з них не експериментальні інгібітори протеази з принаймні виявилася повністю задовільною. Оптимізація однією фосфонатною групою. зв'язування інгібіторних ліків з їх В одному аспекті винахід охоплює сполуки, які внутрішньоклітинною мішенню, з мінімізацією мають Формули І, II, lII, lV, V, VI, Vll тa VIIIa-d: міжклітинного перерозподілу медикаменту, наприклад, до сусідніх клітин, часто буває важкою або неефективною. Більшість агентів, які нині вводять пацієнтові парентерально, не є спрямованими, що веде до системного доставлення агента до клітин та тканин організму, коли це не є необхідним, а часто буває й небажаним. Це може призвести до негативних побічних ефектів ліків і часто обмежує дозу ліків (наприклад, цитотоксичних агентів та інших протиракових або противірусних ліків), які можуть бути введені. Для порівняння, хоча пероральне введення ліків в цілому визнається як зручний і економічний спосіб введення, пероральне введення в результаті дає або (а) поглинання ліків крізь клітинні та тканинні бар'єри, наприклад, кров/мозок, епітеліальну, клітинну мембрану, призводячи до небажаного системного розподілу, або (б) тимчасове перебування ліків у шлунково-кишковому тракті. Відповідно, головною метою є розробка способів специфічного спрямування агентів до клітин та тканин. До переваг такого лікування належать уникнення загального фізіологічного впливу непотрібного доставлення таких агентів до інших клітин та тканин, наприклад, неінфікованих клітин. Внутрішньоклітинного спрямування можна досягти завдяки способам та композиціям, які дозволяють накопичувати або утримувати біологічно активні агенти всередині клітин. Даний винахід забезпечує нові сполуки з активністю ВІЛ-протеази, тобто нові інгібітори ретровірусної протеази людини. Отже, сполуки де хвиляста лінія означає інші структурні згідно з винаходом можуть інгібувати ретровірусні компоненти сполук. протеази і, таким чином, інгібують реплікацію 9 80819 10 Формули І-VIII є заміщеними однією або що вони не обмежують винахід цими варіантами кількома ковалентно приєднаними групами, втілення. Навпаки, винахід охоплює всі включаючи принаймні одну фосфонатну групу. альтернативні варіанти, модифікації та Формули І-VIII є "каркасами", тобто еквіваленти, які можуть охоплюватись обсягом підструктурами, які є спільними для конкретних даного винаходу, визначеного формулою. сполук, які ними охоплюються. Якщо не вказано іншого, представлені нижче Інший аспект винаходу передбачає терміни та фрази, вжиті авторами, мають такі фармацевтичну комбінацію, яка включає значення: ефективну кількість сполуки, вибраної з-поміж Терміни "фосфонат" та "фосфонатна група" Формул І-VIII, та другу сполуку, яка має означають функціональну групу або компонент у властивості проти ВІЛ. межах молекули, що включає принаймні один Інший аспект винаходу передбачає спосіб фосфорно-вуглецевий зв'язок та принаймні один лікування або профілактики симптомів або впливу фосфорно-кисневий подвійний зв'язок. Атом ВІЛ-інфекції у інфікованої тварини, який включає фосфору далі заміщують кисневим, сірчаним та введення, тобто лікування вищезгаданої тварини азотним замісниками. Ці замісники можуть фармацевтичною комбінацією, яка включає складати частину компонента проліків. Як ефективну кількість сполуки, вибраної з-поміж визначено авторами, до "фосфонатів" та Формул І-VIII, та другу сполуку, яка має "фосфонатних груп" належать молекули з властивості проти ВІЛ. фосфоновою кислотою, фосфоновим Винахід забезпечує фармацевтичну моноестером, фосфоновим діестером, композицію, яка включає ефективну кількість фосфонамідатною, фосфондіамідатною та сполуки, вибраної з-поміж Формул І-VIII, або її фосфонтіоатною функціональними групами. фармацевтично прийнятної солі, у комбінації з Вжитий авторами термін "проліки" стосується фармацевтично прийнятним розріджувачем або будь-якої сполуки, яка при введенні до біологічної носієм. системи утворює лікарську речовину, тобто Цей винахід стосується способу збільшення активний інгредієнт, в результаті спонтанної(их) накопичення та утримання у клітинах лікарських хімічної(их) реакції (реакцій), каналізованої(их) сполук, таким чином, збільшуючи їх терапевтичну ферментами хімічної(их) реакції (реакцій), та діагностичну цінність. фотолізу та/або метаболічної(их) хімічної(их) Винахід також забезпечує спосіб інгібування реакції (реакцій). Таким чином, проліки є ВІЛ, який включає введення ссавцеві, ковалентно модифікованим аналогом або інфікованому ВІЛ (ВІЛ-позитивному), кількості латентною формою терапевтично активної сполуки Формул І-VIII, ефективної для інгібування сполуки. росту вищезгаданих ВІЛ-інфікованих клітин. Термін "фармацевтично прийнятні проліки" Винахід також забезпечує сполуку, вибрану зстосується сполуки, яка метаболізується в поміж Формул І-VIII, для застосування у медичній організмі-хазяїні, наприклад, гідролізується або терапії (в оптимальному варіанті - для окиснюється, або під дією ферментів, або шляхом застосування у лікуванні від раку, наприклад, загального сольволізу за допомогою кислот та твердих пухлин), а також застосування сполуки основ, для утворення активного інгредієнта. Типові Формул І-VIII для виробництва медикаменту, приклади проліків сполук згідно з винаходом корисного для лікування від раку, наприклад, мають біологічно нестійкі захисні групи на твердих пухлин. функціональному компоненті сполуки. До проліків Винахід також забезпечує способи та нові належать сполуки, які можуть бути окиснені, описані авторами проміжні сполуки, які є відновлені, аміновані, деаміновані, естерифіковані, корисними для одержання сполук згідно з деестерифіковані, алкіловані, деалкіловані, винаходом. Деякі зі сполук Формул І-VIII є ациловані, деациловані, фосфориловані, корисними для одержання інших сполук Формул Ідефосфориловані, або піддані зміні чи VIII. перетворенню функціональної групи іншим чином, В іншому аспекті винаходу активність ВІЛвключаючи утворення або розривання хімічних протеази інгібується способом, який включає етап зв'язків на проліках. обробки зразка, який, за припущенням, містить "Компонент проліків" означає нестійку вірус ВІЛ, сполукою або композицією згідно з функціональну групу, яка відокремлюється від винаходом. активної інгібуючої сполуки під час метаболізму, Інший аспект винаходу передбачає спосіб системно, всередині клітини, шляхом гідролізу, інгібування активності ВІЛ-протеази, який включає ферментного розщеплення, або шляхом інших етап контактування зразка, який, за припущенням, процесів [Bundgaard, Hans, "Design and Application містить вірус ВІЛ, з композицією згідно з of Prodrugs", Textbook of Drue Design and винаходом. Development (1991), P.Krogsgaard-Larsen and В інших аспектах забезпечуються способи H.Bundgaard, Eds. Harwood Academic Publishers, синтезу сполук згідно з цим винаходом. pp.113-191]. До ферментів, здатних до ферментної Нижче детально буде розглянуто певні активації зі сполуками фосфонатних проліків варіанти втілення винаходу, приклади яких згідно з винаходом, належать, крім інших, амідази, пояснено у супровідних описах, структурах та естерази, мікробні ферменти, фосфоліпази, формулах. холінестерази та фосфази. Компоненти, які є Хоча винахід описується у зв'язку з проліками, можуть підвищувати розчинність, переліченими варіантами втілення, слід розуміти, абсорбцію та ліпофільність для оптимізації 11 80819 12 кислоту та епісульфід [Puech et al. (1993) Antiviral доставлення ліків, біоакумуляції та ефективності. Res., 22:155-174; Benzaria et al. (1996) / Med. Прикладами компонентів, які є проліками, є Chem. 39:4958]. Циклічні фосфонатаі естери також гідролітично чутливі або нестійкі ацилоксиметилові було описано як проліки фосфоровмісних сполук естери -CH2OC(=O)R9 та ацилоксиметилкарбонати [Erion et al., Патент США №6312662]. -CH2OC(=O)OR9, де R9 є С1-С6 алкілом, С1-С6 Термін "захисна група" стосується компонента заміщеним алкілом, С6-С20 арилом або С6-С20 заміщеним арилом. Ацилоксіалкіловий естер сполуки, який маскує або змінює властивості спочатку застосовували як проліки для карбонових функціональної групи або властивості сполуки в кислот, а потім застосовували до фосфатів та цілому. Захисні групи можуть мати різну хімічну фосфонатів, як описано у [публікації Farquhar et структуру у широких межах. Одна з функцій al., (1983) J. Pharm. Sd. 72:324; а також у патентах захисної групи полягає в тому, що вона служить як США №№4816570, 4968788, 5663159 та 5792756]. посередник у синтезі вихідної лікарської речовини. Згодом ацилоксіалкіловий естер застосовували Хімічні захисні групи та способи для доставлення фосфорних кислот крізь клітинні захисту/депротекції добре відомі спеціалістам. мембрани і для підвищення біоакумуляції при [Див.: "Protective Groups in Органічн Chemistry", пероральному введенні. Подібний варіант Theodora W. Greene (John Wiley & Sons, Inc., New ацилоксіалкілового естеру, York, 1991)]. Захисні групи часто застосовують для алкоксикарбонілоксіалкіловий естер (карбонат), маскування реактивності певних функціональних також може підвищувати біоакумуляцію при груп, для сприяння ефективності потрібних пероральному введенні як компонент проліків у хімічних реакцій, наприклад, створення та сполуках комбінацій згідно з винаходом. розривання хімічних зв'язків упорядкованим і Прикладом ацилоксиметилового естеру є запланованим чином. Захист функціональних груп півалоїлоксиметокси, (РОМ) -СН2ОС(=О)С(СН3)3. сполуки змінює інші фізичні властивості, крім Прикладом ацилоксиметилкарбонатного реактивності захищеної функціональної групи, компонента проліків є півалоїлоксиметилкарбонат наприклад, полярність, ліпофільність (РОС) -СН2ОС(=О)ОС(СН3)3. (гідрофобність), та інші властивості, які можуть Фосфонатна група може бути компонентом бути виміряні загальними засобами аналізу. фосфонатних проліків. Компонентом проліків може Хімічно захищені проміжні сполуки самі можуть бути чутлива до гідролізу група, якою може бути, бути біологічно активними або неактивними. крім інших, півалоїлоксиметилкарбонатна (РОС) Захищені сполуки також можуть виявляти або РОМ-група. В альтернативному варіанті змінені, а у деяких випадках оптимізовані компонент проліків може бути чутливим до властивості in vitro та in vivo, такі як проходження посиленого ферментами розщеплення, таким як крізь клітинні мембрани та резистентність до лактатний естер або фосфонамідат-естерна група. ферментного розпаду або секвестру. У цій ролі Повідомлялося, що арилові естери захищені сполуки з запланованим терапевтичним фосфорних груп, зокрема, фенілові естери, впливом можуть називатися проліками. Іншою підвищують біодоступність при пероральному функцією захисної групи є перетворення вихідного введенні [DeLambert et al. (1994) J. Med. Chem. медикаменту на проліки, причому вихідний 37:498]. Також було описано фенілові естери, які медикамент вивільнюється після перетворення містять карбоновий естер в ортопозиції до проліків in vivo. Оскільки активні проліки можуть фосфату [Khamnei and Torrence, (1996) J. Med. абсорбуватися ефективніше, ніж вихідний Chem. 39:4109-4115]. Повідомлялося, що медикамент, проліки можуть мати більшу бензилові естери виробляють вихідну фосфонову ефективність in vivo, ніж вихідний медикамент. кислоту. У деяких випадках замісники в орто- або Захисні групи видаляють або in vitro, у разі пара-позиції можуть прискорювати гідроліз. хімічних проміжних сполук, або in vivo, у разі Бензилові аналоги з ацилованим фенолом або проліків. У разі хімічних проміжних сполук алкілованим фенолом можуть утворювати фізіологічна прийнятність одержаних в результаті фенольну сполуку через дію ферментів, депротекції продуктів, наприклад, спиртів не має наприклад, естераз, оксидаз та ін., яка, у свою особливого значення, хоча взагалі більш бажано, чергу, зазнає розщеплення у бензильному С-О щоб продукти були фармакологічно безпечними. зв'язку для утворення фосфорної кислоти та Будь-яке посилання на будь-які сполуки згідно хінонметидної проміжної сполуки. Приклади цього з винаходом також включає посилання на їх класу проліків описано у публікаціях [Mitchell et al. фізіологічно прийнятні солі. Прикладами (1992) J. Chem. Soc. Perkin Trans. I 2345; Brook et фізіологічно прийнятних солей сполук згідно з al. WO 91/19721]. Було описано інші бензилові винаходом є солі, похідні від відповідної основи, проліки, які містять групу, що містить карбоновий наприклад, лужного металу (такого як натрій), естер, приєднану до бензильного метилену лужноземельного (такого як магній), амонію та [Glazier et al. WO 91/19721]. Повідомлялося, що NX4+ (де X є С1-С4 алкілом). До фізіологічно тіо-вмісні проліки є корисними для прийнятних солей атома водню або аміногрупи внутрішньоклітинного доставлення фосфонатних належать солі органічних карбонових кислот, таких ліків. Ці проестери містять етилтіо-групу, в якій як оцтова, бензойна, молочна, фумарова, винна, тіолова група або естерифікується ацильною малеїнова, малонова, яблучна, ізетіонова, групою, або комбінується з іншою тіоловою групою лактобіонова та бурштинова кислоти; органічні для утворення дисульфіду. Деестерифікація або сильфонові кислоти, такі як метансульфонова, відновлення дисульфіду утворює вільну проміжну етансульфонова, бензолсульфонова та ртіо-сполуку, яка згодом розпадається на фосфорну толуолсульфонова кислоти; і неорганічні кислоти, 13 80819 14 такі як хлористоводнева, сірчана, фосфорна та вуглеводневого радикала з 2-18 атомів вуглецю, сульфамінова кислоти. До фізіологічно прийнятних що має два центри моновалентного радикала, солей сполуки гідроксигрупи належать аніон одержані шляхом видалення двох атомів водню з вищезгаданої сполуки у комбінації з придатним однакових або двох різних атомів вуглецю катіоном, таким як Na+ та NX4+ (де X незалежно вихідного алкену. До типових алкеніленових вибирають з-поміж Η або С1-С4 алкільної групи). радикалів належить, крім інших, 1,2-етилен (Для терапевтичного застосування солі СН= СН-). активних інгредієнтів сполук винаходу мають бути "Алкінілен" стосується ненасиченого, фізіологічно прийнятними, тобто, вони мають бути розгалуженого або лінійного або циклічного солями, які походять від фізіологічно прийнятної вуглеводневого радикала з 2-18 атомів вуглецю, кислоти або основи. Однак солі кислот або основ, що має два центри моновалентного радикала, які не є фізіологічно прийнятними, також можуть одержані шляхом видалення двох атомів водню з застосовуватися, наприклад, у приготуванні або однакових або двох різних атомів вуглецю очищенні фізіологічно прийнятної сполуки. Усі вихідного алкіну. До типових алкініленових солі, незалежно від того, чи походять вони від радикалів належать, крім інших: ацетилен (-С С-), фізіологічно прийнятної кислоти або основи, пропаргіл (-СН2С С-) та 4-пентиніл (-СН2СН2СН2С охоплюються обсягом даного винаходу. CH-). "Алкіл" є С1-С18 вуглеводнем, який містить "Арил" означає моновалентний ароматичний нормальні, вторинні, третинні або циклічні атоми вуглеводневий радикал з 6-20 атомів вуглецю, вуглецю. Прикладами є метил (Me, -СН3), етил (Et, одержаний шляхом видалення одного атома -СН2СН3), 1-пропіл (n-Рr, n-пропіл, -СН2СН2СН3), 2водню з єдиного атома вуглецю вихідної пропіл (і-Рr, і-пропіл, -СН(СН3)2), 1-бутил (n-Bu, nароматичної кільцевої системи. До типових бутил, -СН2СН2СН2СН3), 2-метил-1-пропіл (і-Bu, іарильних груп належать, крім інших, радикали, бутил, -СН2СН(СН3)2), 2-бутил (s-Bu, s-бутил, одержані з бензолу, заміщеного бензолу, СН(СН3)СН2СН3), 2-метил-2-пропіл (t-Bu, t-бутил, нафталіну, антрацену, біфенілу та інші. С(СН3)3), 1-пентил (n-пентил, -СН2СН2СН2СН2СН3), "Арилалкіл" стосується ациклічного алкільного 2-пентил (-СН(СН3)СН2СН2СН3), 3-пентил (радикала, в якому один з атомів водню, зв'язаних з СН(СН2СН3)2), 2-метил-2-бутил (-С(СН3)2СН2СН3), атомом вуглецю, як правило, кінцевим або sp3 3-метил-2-бутил (-СН(СН3)СН(СН3)2), 3-метил-1атомом вуглецю, є заміщеним арильним бутил (-СН2СН2СН(СН3)2), 2-метил-1-бутил (радикалом. До типових арилалкільних груп СН2СН(СН3)СН2СН3), 1-гексил (належать, крім інших, бензил, 2-фенілетан-1-іл, 2СН2СН2СН2СН2СН2СН3), 2-гексил (фенілетен-1-іл, нафтилметил, 2-нафтилетан-1-іл, СН(СН3)СН2СН2СН2СН3), 3-гексил (2-нафтилетен-1-іл, нафтобензил, 2СH(СН2СН3)(СН2СН2СН3)), 2-метил-2-пентил (нафтофенілетан-1-іл та інші. Арилалкільна група С(СН3)2СН2СН2СН3), 3-метил-2-пентил (включає від 6 до 20 атомів вуглецю, наприклад, СН(СН3)СН(СН3)СН2СН3), 4-метил-2-пентил (алкільний компонент, включаючи алканільну, СН(СН3)СН2СН(СН3)2), 3-метил-3-пентил (алкенільну або алкінільну групи, арилалкільної С(СН3)(СН2СН3)2), 2-метил-3-пентил (групи включає від 1 до 6 атомів вуглецю, і СН(СН2СН3)СН(СН3)2), 2,3-диметил-2-бутил (арильний компонент включає від 5 до 14 атомів С(СН3)2СН(СН3)2), 3,3-диметил-2-бутил (вуглецю. СН(СН3)С(СН3)3. "Заміщений алкіл", "заміщений арил" та "Алкеніл" є С2-С18 вуглеводнем, який містить "заміщений арилалкіл" означає алкіл, арил та нормальні, вторинні або третинні циклічні атоми арилалкіл, відповідно, у якому один або кілька вуглецю з принаймні одним сайтом ненасиченості, атомів водню є незалежно заміщеними тобто вуглець-вуглець, sp2 подвійного зв'язку. замісником. До типових замісників належать, крім Прикладами, крім інших, є: етилен або вініл (інших, -X, -R, -О-, -OR, -SR, -S-, -NR2, -NR3, =NR, СН= СН2), аліл (-СН2СН= СН2), циклопентеніл (СХ3, -CN, -OCN, -SCN, -N=C=O, -NCS, -NO, -NO2, С5Н7) та 5-гексеніл (-СН2СН2СН2СН2СН=СН2). =N2, -N3, NC(=O)R, -C(=O)R, -C(=O)NRR -S(=O)2O-, "Алкініл" є С2-С18 вуглеводнем, який містить -S(=O)2OH, -S(=O)2R, -OS(=O)2OR, -S(=O)2NR, нормальні, вторинні або третинні циклічні атоми S(=O)R, -OP(=O)O2RR -P(=O)O2RR -P(=O)(O-)2, вуглецю з принаймні одним сайтом ненасиченості, P(=O)(OH)2, -C(=O)R, -C(=O)X, -C(S)R, -C(O)OR, тобто вуглець-вуглець, sp потрійний зв'язок. C(O)O-, -C(S)OR, -C(O)SR, -C(S)SR, -C(O)NRR, Прикладами, крім інших, є: ацетиленовий (-С СН) C(S)NRR, -C(NR)NRR, де кожен Х незалежно є та пропаргіл (-СН2С СН). галогеном: F, СІ, Вr або І; і кожен R незалежно є "Алкілен" стосується насиченого, Н, алкілом, арилом, гетероциклом або розгалуженого або лінійного або циклічного компонентом проліків. Алкіленова, алкеніленова вуглеводневого радикала з 1-18 атомів вуглецю, та алкініленова групи також можуть бути подібним що має два центри моновалентного радикала, чином заміщені. одержані шляхом видалення двох атомів водню з Вжитий авторами термін "гетероцикл", крім однакових або двох різних атомів вуглецю інших, охоплює, наприклад, гетероцикли, описані у вихідного алкану. До типових алкіленових [публікаціях Paquette, Leo Α.; "Principles of Modern радикалів належать, крім інших: метилен (-СН2-) Heterocyclic Chemistry" (W.A. Benjamin, New York, 1,2-етил (-СН2СН2-), 1,3-пропіл (-СН2СН2СН2-), 1,41968), зокрема, Розділи 1, 3, 4, 6, 7 та 9; "The бутил (-СН2СН2СН2СН2-) та інші. Chemistry of Heterocyclic Compounds, A series of "Алкенілен" стосується ненасиченого, monographs" (John Wiley & Sons, New York, 1950 to розгалуженого або лінійного або циклічного present), зокрема, томи 13, 14, 16, 19 та 28; і J. Am. 15 80819 16 Chem. Soc. (1960) 82:5566]. піразоліл та 1-піперидиніл. Прикладами гетероциклів, крім інших, є, "Карбоцикл" означає насичене, ненасичене наприклад, піридил, дигідропіридил, або ароматичне кільце, яке має від 3 до 7 атомів тетрагідропіридил (піперидил), тіазоліл, вуглецю як моноцикл або від 7 до 12 атомів тетрагідротіофеніл, окиснений сіркою вуглецю як біцикл. Моноциклічні карбоцикли тетрагідротіофеніл, піримідиніл, фураніл, тієніл, мають від 3 до 6 атомів кільця, ще більш типово піроліл, піразоліл, імідазоліл, тетразоліл, 5 або 6 атомів кільця. Біциклічні карбоцикли мають бензофураніл, тіанафталініл, індоліл, індоленіл, від 7 до 12 атомів кільця, наприклад, розташовані хінолініл, ізохінолініл, бензімідазоліл, піперидиніл, як біцикло [4,5], [5,5], [5,6] або [6,6] система, або 9 4-піперидоніл, піролідиніл, 2-піролідоніл, піролініл, або 10 атомів кільця, розташовані як біцикло [5,6] тетрагідрофураніл, тетрагідрохінолініл, або [6,6] система. Прикладами моноциклічних тетрагідроізохінолініл, декагідрохінолініл, карбоциклів є циклопропіл, циклобутил, октагідроізохінолініл, азоциніл, триазиніл, 6Н-1,2,5циклопентил, 1-циклопент-1-еніл, 1-циклопент-2тіадіазиніл, 2Н,6Н-1,5,2-дитіазиніл, тієніл, еніл, 1-циклопент-3-еніл, циклогексил, 1-циклогекстіантреніл, піраніл, ізобензофураніл, хроменіл, 1-еніл, 1-циклогекс-2-еніл, 1-циклогекс-3-еніл, ксантеніл, феноксантиніл, 2Н-піроліл, ізотіазоліл, феніл, спірил та нафтил. ізоксазоліл, піразиніл, піридазиніл, індолізиніл, "Лінкер" або "зв'язок" означає хімічний ізоіндоліл, 3Н-індоліл, 1H-індазоліл, пуриніл, 4Нкомпонент, який включає ковалентний зв'язок або хінолізиніл, фталазиніл, нафтиридиніл, ланцюг атомів, який ковалентно зв'язує хіноксалініл, хіназолініл, цинолініл, птеридиніл, фосфонатну групу з медикаментом. До лінкерів належать частини замісників А1 та А3, перелічені у 4аН-карбазоліл, карбазоліл, b-карболініл, Формулі І, або замісники А1 та А3, перелічені у фенантридиніл, акридиніл, піримідиніл, Формулі II, які включають такі компоненти, як: фенантролініл, феназиніл, фенотіазиніл, повторювані елементи алкілокси (наприклад, фуразаніл, феноксазиніл, ізохроманіл, хроманіл, поліетиленокси, PEG, поліметиленокси) та імідазолідиніл, імідазолініл, піразолідиніл, алкіламіно (наприклад, поліетиленаміно, піразолініл, піперазиніл, індолініл, ізоіндолініл, Jeffamine™); і двоатомний естер та аміди, хінуклідиніл, морфолініл, оксазолідиніл, включаючи сукцинат, сукцинамід, дигліколят, бензотриазоліл, бензізоксазоліл, оксіндоліл, малонат та капроамід. бензоксазолініл та ізатиноїл. Термін "хіральний" стосується молекул, які Одним варіантом втілення бісмають властивість не накладатися на дзеркальний тетрагідрофуранільної групи є: відповідник, а термін "ахіральний" стосується молекул, які накладаються на дзеркальний відповідник. Термін "стереоізомери" стосується сполук, які мають ідентичний хімічний склад, але Як необмежувальний приклад, зв'язані відрізняються просторовим розташуванням атомів вуглецем гетероцикли є зв'язаними у позиції 2, 3, або груп. 4, 5 або 6 піридину, позиції 3, 4, 5 або 6 "Діастереомер" стосується стереоізомера з піридазину, позиції 2, 4, 5 або 6 піримідину, позиції двома або кількома центрами хіральності, і ці 2, 3, 5 або 6 піразину, позиції 2, 3, 4 або 5 фурану, молекули не є дзеркальними відображеннями тетрагідрофурану, тіофурану, тіофену, піролу або одна одної. Діастереомери мають різні фізичні тетрагідропіролу, позиції 2, 4 або 5 оксазолу, властивості, наприклад, точки плавлення, точки імідазолу або тіазолу, позиції 3, 4 або 5 ізоксазолу, кипіння, спектральні властивості та реактивність. піразолу або ізотіазолу, позиції 2 або 3 азиридину, Суміші діастереомерів можуть відокремлюватися позиції 2, 3 або 4 азетидину, позиції 2, 3, 4, 5, 6, 7 при застосуванні аналітичних процедур високої або 8 хіноліну або позиції 1, 3, 4, 5, 6, 7 або 8 роздільної здатності, таких як електрофорез та ізохіноліну. Ще більш типово, до зв'язаних хроматографія. вуглецем гетероциклів належать 2-піридил, 3Термін "енантіомери" стосується двох піридил, 4-піридил, 5-піридил, 6-піридил, 3стереоізомерів сполуки, які не є взаємними піридазиніл, 4-піридазиніл, 5-піридазиніл, 6дзеркальними відображеннями, що накладаються піридазиніл, 2-піримідиніл, 4-піримідиніл, 5одне на одне. піримідиніл, 6-піримідиніл, 2-піразиніл, 3-піразиніл, Вжиті авторами стереохімічні визначення та 5-піразиніл, 6-піразиніл, 2-тіазоліл, 4-тіазоліл або позначення здебільшого відповідають вжитим у 5-тіазоліл. [публікаціях S.P.Parker, Ed., McGraw-Hill Dictionary Як необмежувальний приклад, зв'язані азотом of Chemical Terms (1984) McGraw-Hill Book гетероцикли є зв'язаними у позиції 1 азиридину, Company, New York; and Eliel, E. and Wilen, S., азетидину, піролу, піролідину, 2-піроліну, 3Стереохімію of Organic Compounds (1994) John піроліну, імідазолу, імідазолідину, 2-імідазоліну, 3Wiley & Sons, Inc., New York]. Багато органічних імідазоліну, піразолу, піразоліну, 2-піразоліну, 3сполук існують в оптично активних формах, тобто, піразоліну, піперидину, піперазину, індолу, вони мають здатність повертати площину індоліну, 1Н-індазолу, позиції 2 ізоіндолу або плоскополяризованого світла. В описі оптично ізоіндоліну, позиції 4 морфоліну та позиції 9 активної сполуки префікси D та L або R та S карбазолу або b-карболіну. Ще більш типово, до вживаються для позначення абсолютної зв'язаних азотом гетероциклів належать 1конфігурації молекули відносно її хорального(их) азиридил, 1-азетедил, 1-піроліл, 1-імідазоліл, 1центра(ів). Префікси d та 1, D та L або (+) та (-) 17 80819 18 вжито для позначення повертання плоскополяризованого світла сполукою, де (-) або 1 означає, що сполука є лівообертальною. Сполука з префіксом (+) або d є правообертальною. Для даної хімічної структури ці сполуки, які називаються стереоізомерами, є ідентичними, за винятком того, що вони є дзеркальними відображеннями одна одної. Конкретний стереоізомер також може називатися енантіомером, і суміш таких ізомерів часто називають енантіомерною сумішшю. Суміш 50:50 енантіомерів називають рацемічною сумішшю або рацематом, який може траплятися за відсутності у хімічній реакції або процесі стереоселекції або стереоспецифічності. Терміни "рацемічна суміш" та "рацемат" стосуються еквімолярної суміші двох енантіомерних різновидів, позбавлених оптичної активності. Сполуки-інгібітори ВІЛ-протеази До сполук згідно з винаходом належать ті, що мають інгібіторну активність проти ВІЛ-протеази. Зокрема, до цих сполук належать інгібітори ВІЛпротеази. Сполуки згідно з винаходом мають фосфонатну групу, яка може бути компонентом проліків. У різних варіантах втілення винаходу розпізнають сполуки, які можуть охоплюватися загальним обсягом наведених документів під визначенням термінів ILPPI (Індинавір-подібні фосфонатні інгібітори протеази, Формула І); AMLPPI (Ампренавір-подібні фосфонатні інгібітори протеази, Формула II); KNELPPI (KNI-подібні де хвиляста лінія означає інші структурні фосфонатні інгібітори протеази, Формула III); компоненти сполук. RLPPI (Ритонавір-подібні фосфонатні інгібітори Сполуки Формули І мають 3-гідрокси-5-амінопротеази, Формула IV); LLPPI (Лопінавір-подібні пентамідне ядро. Сполуки Формули II мають 2фосфонатні інгібітори протеази, Формула IV); гідрокси-1, 3-аміно-пропіламідний або 2-гідроксиNLPPI (Нелфінавір-подібні фосфонатні інгібітори 1,3-аміно-пропіламіносульфонове ядро. Сполуки протеази, Формула V); SLPPI (Саквінавір-подібні Формули III мають 2-гідрокси-3-аміно-пропіламідне фосфонатні інгібітори протеази, Формула V); ядро. Сполуки Формули IV мають 2-гідрокси-4ATLPPI (Атанзавір-подібні фосфонатні інгібітори аміно-бутиламінове ядро. Сполуки Формули V протеази, Формула VI); TLPPI (Типанавір-подібні мають ацилований 1,3-діамінопропанове ядро. фосфонатні інгібітори протеази, Формула VII); і Сполуки Формули VI мають 2-гідрокси-3-діазаCCLPPI (Циклокарбонілоподібні фосфонатні пропіламідне ядро. Сполуки Формули VII мають інгібітори протеази, Формула VIIIa-d), які всі сульфонамід 5,6-дигідро-4-гідрокси-2-піронове включають фосфонатну групу, наприклад, ядро. Сполуки Формули VIIIa-d мають шести- або фосфонатний діестер, фосфонамідат-естерні семичленне кільце та циклічний карбонільний, проліки або фосфондіамідат-естер [Jiang et al, US сульфгідрильний, сульфоксидний або сульфонове 2002/0173490 Α1]. ядро, де Y1 є киснем, сіркою або заміщеним Якщо описана авторами сполука є заміщеною азотом, і m2 є 0,1 або 2. більш ніж однією з однаково позначених груп, Формули І, II, III, IV, V, VI, VII та VIIIa-d є 1 6a наприклад, "R " або "R ", то слід розуміти, що заміщеними однією або кількома ковалентно групи можуть бути однаковими або різними, тобто, приєднаними групами, включаючи принаймні одну кожна група є вибраною незалежно. Хвилясті лінії фосфонатну групу. Формули І, II, III, IV, V, VI, VII та вказують на місце приєднання ковалентних VIIIa-d є заміщеними однією або кількома зв'язків до сусідніх груп, компонентів або атомів. ковалентно приєднаними А0 групами, включаючи Сполуки згідно з винаходом представлено одночасні заміщення у будь-якому або всіх А0. А0 є нижче на схемах, прикладах, в описах та пунктах A1, А2 або W3. Сполуки Формул І, II, III, IV, V, VI, VII формули, і винахід охоплює сполуки, які мають та VIIIa-d включають принаймні один А1. Формули І, II, III, IV, V, VI, VII тa VIIIa-d: A1 є: 19 80819 20 принаймні один із m1b та m1c є 0; і якщо m1d є 0, і m1a та m12с не є 0, то принаймні один із m1c та m1e є 0. R1 незалежно є Η або алкілом з 1-18 атомами вуглецю. R2 незалежно є Н, R3 або R4, де кожен R4 незалежно є заміщеним 0-3 R3 групами. В 2 альтернативному варіанті взяті разом на атомі А є: вуглецю, дві R2 групи утворюють кільце, тобто кільце вуглецю. Кільце може бути, наприклад, циклопропілом, циклобутилом, циклопентилом або циклогексилом. Кільце може бути заміщене 0-3 R3 групами. R3 є R3a, R3b, R3c або R3d, за умови, що у разі, коли R3 є зв'язаним з гетероатомом, то R3 є R3c aбo R3d. А3 є: R3a є F, СІ, Br, I, -CN, N3 або -NO2. R3b e Y1. R3c є -RХ, -N(RX)(RX), -SRX, -S(O)RX, -S(O)2RX, S(O)(ORX), -S(O)2(ORX), -OC(Y1)RX, -OC(Y1)ORX, OC(Y1)(N(RX)(RX)), -SC(Y1)RX, -SC(Y1)ORX, 1 X X X 1 X SC(Y )(N(R )(R )), -N(R )C(Y )R , -N(RX)C(Y1)ORX або -N(RX)C(Y1)(N(RX)RX)). R3d є -C(Y1)RX, -C(Y1)ORX або -C(Y1)N(RX)(RX)). Y1 незалежно є О, S, N(RX), N(O)(RX), N(ORX), X X X R4 є алкілом з 1-18 атомами вуглецю, N(O)(OR ) або N(N(R )(R )). алкенілом з 2-18 атомами вуглецю, або алкінілом з Υ2 незалежно є зв'язком, О, N(RX), N(O)(RX), 2-18 атомами вуглецю. N(ORX), N(O)(ORX), N(N(RX)(RX)), -S(O)М2- або R5 є R4, де кожен R4 є заміщеним 0-3 R3 S(O)М2-S(O)М2-. Х 3 групами. R незалежно є Η, W , захисною групою або R5a незалежно є алкіленом з 1-18 атомами формулою: вуглецю, алкеніленом з 2-18 атомами вуглецю або алкініленом з 2-18 атомами вуглецю, і кожен з цих алкілену, алкенілену або алкінілену є заміщеним 0-3 R3 групами. W3 є W4 aбo W 5. W4 є R5, -C(Y1)R5, -C(Y1)W5, -SO2R5 або SO2W5. де: W5 є карбоциклом або гетероциклом, де W5 M1a, М1с та m1d незалежно є 0 або 1; незалежно є заміщеним 0-3 R2 групами. М12с є 0,1,2,3,4, 5,6,7,8,9,10,11 або 12; і y 3 2 W3а є W4а aбo W5а. R незалежно є Н, W , R або захисною W4а є R5a, -C(YХ)R5a, -C(Y1)W5a, -SO2R5a або групою. Х SO2W5a. В альтернативному варіанті R є групою W5a є багатовалентним заміщеним формули: карбоциклом або гетероциклом, де W5a незалежно є заміщеним 0-3 R2 групами. W6 є W3, незалежно заміщеним 1, 2 або 3 А3 групами. М2 є 0,1 або 2; М12а є 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 або 12; і М12b є 0, 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 або 12. де: W5 та W5a карбоцикли і W5 та W5a гетероцикли m1a, m1b, m1c, m1d та m1e незалежно є 0 або незалежно можуть бути заміщені 0-3 R2 групами. 1; W5 може бути насиченим, ненасиченим або m12c є 0,1,2,3,4, 5,6, 7,8,9,10,11 або 12; ароматичним кільцем, яке включає моно- або Ry є Н, W 3, R2 або захисною групою; біциклічний карбоцикл або гетероцикл. W5 може за умови, що: мати від 3 до 10 атомів кільця, наприклад, від 3 до якщо m1a, m12c та m1d є 0, то m1b, m1c та 7 атомів кільця. Кільця W 5 є насиченими, коли m1e є 0; містять 3 атоми кільця, насиченими або моноякщо m1a та m12с є 0, і m1d не є 0, то m1b та ненасиченими, коли містять 4 атоми кільця, m1c є 0; насиченими або моно- або ди-ненасиченими, коли якщо m1a та m1d є 0, і m12с не є 0, то m1b і містять 5 атомів кільця, і насиченими, моно- або принаймні один із m1c та m1e є 0; ди-ненасиченими або ароматичними, коли містять якщо m1a є 0, і m12с та m1d не є 0, то m1b є 0; 6 атомів кільця. якщо m12с та m1d є 0, і m1a не є 0, то W5 або W5a гетероцикл може бути принаймні два з m1b, m1c та m1e є 0; моноциклом, який має від 3 до 7 членів кільця (від якщо m12с є 0, і m1a та m1d не є 0, то 2 до 6 атомів вуглецю і від 1 до 3 гетероатомів, 21 80819 вибраних з-поміж Ν, Ο, Ρ та S) або біциклом, який має 7 до 10 членів кільця (від 4 до 9 атомів вуглецю і від 1 до 3 гетероатомів, вибраних зпоміж Ν, Ο, Ρ та S). W 5 та W5a гетероциклічні моноцикли можуть мати від 3 до 6 атомів кільця (від 2 до 5 атомів вуглецю і від 1 до 2 гетероатомів, вибраних з-поміж N, О та S); або 5 або 6 атомів кільця (від 3 до 5 атомів вуглецю і від 1 до 2 гетероатомів, вибраних з-поміж N та S). W5 та W 5a гетероциклічні біцикли мають від 7 до 10 атомів кільця (від 6 до 9 атомів вуглецю і від 1 до 2 гетероатомів, вибраних з-поміж Ν, Ο та S), розташованих як біцикло [4,5], [5,5], [5,6] або [6,6] система; або від 9 до 10 атомів кільця (від 8 до 9 атомів вуглецю і від 1 до 2 гетероатомів, вибраних з-поміж N та S), розташованих як біцикло [5,6] або [6,6] система. W5 гетероцикл може бути зв'язаний з Y2 через вуглець, азот, сірку або інший атом стійким ковалентним зв'язком. W5 та W5a гетероцикли включають, наприклад, піридил, ізомери дигідропіридилу, піперидин, піридазиніл, піримідиніл, піразиніл, s-триазиніл, оксазоліл, імідазоліл, тіазоліл, ізоксазоліл, піразоліл, ізотіазоліл, фураніл, тіофураніл, тієніл та піроліл. W 5 також включає, крім інших, такі приклади, як: 22 Варіанти втілення А1 включають: де один або кілька Y2 є зв'язком, таким, як: W5 та W5a карбоцикли та гетероцикли незалежно можуть бути заміщені 0-3 R2 групами, як визначено вище. Наприклад, заміщені W5 карбоцикли включають: де W5a є карбоциклом або гетероциклом, і W5a незалежно є заміщеним 0 або 1 R2 групою. Варіанти втілення А1 також включають: де n є цілим числом від 1 до 18. Варіанти втілення А3 включають ті, в яких М2 є 0, наприклад: Прикладами заміщених фенільних карбоциклів є: 23 і в яких М12b є 1, Υ1 є киснем, і Y2b є киснем (О) або азотом (N(RX)), наприклад: Варіант втілення А3 включає: де Y2c є О, N(Ry) або S. Наприклад, R1 може бути Н, і n може бути 1. Інший варіант втілення А3 включає: де W 5 є карбоциклом, таким як феніл або заміщений феніл. Такі варіанти втілення включають: 80819 24 де Y2b є О або N(RX); M12d є 1, 2, 3, 4, 5, 6, 7 або 8; і фенільний карбоцикл є заміщеним 0-3 R2 групами. Такі варіанти втілення А3 включають фенілфосфонамідатну амінокислоту, наприклад, аланатні естери та фенілфосфонат-лактатні естери: Хіральний водень амінокислотного та лактатного компонентів може мати R- або Sконфігурацію або бути рацемічною сумішшю. Варіанти втілення RX включають естерні, карбаматні, карбонатні, тіоестерні, амідні, тіоамідні та сечовинні групи: Варіанти втілення А2 включають ті, в яких W3 є W5, наприклад: В альтернативному варіанті А є фенілом, заміщеним фенілом, бензилом, заміщеним бензилом, піридилом або заміщеним піридином. Прикладами варіантів втілення сполук Формули І є, крім інших, структури: де А1 означає місце ковалентного приєднання фосфонатної групи. Прикладами варіантів втілення сполук Формули II є, крім інших, структури: 25 де А1 означає місце ковалентного приєднання фосфонатної групи. Прикладами варіантів втілення сполук Формули III є, крім інших, структури: 80819 26 де А1 означає місце ковалентного приєднання фосфонатної групи. Прикладами варіантів втілення сполук Формули VI є, крім інших, структури: де А1 означає місце ковалентного приєднання фосфонатної групи. Прикладами варіантів втілення сполук Формули IV є, крім інших, структури: де А1 означає місце ковалентного приєднання фосфонатної групи. Прикладами варіантів втілення сполук Формули VII є, крім інших, структури: де А1 означає місце ковалентного приєднання фосфонатної групи. Прикладами варіантів втілення сполук Формули V є, крім інших, структури: де А1 означає місце ковалентного приєднання фосфонатної групи. Прикладами варіантів втілення сполук Формули Vllla є структури: Прикладами варіантів втілення сполук 27 Формули VllIb є структури: 80819 28 метаболіт, як правило, генерується внутрішньоклітинно, більш типово, він генерується у людських РВМС. Ще більш типово, метаболіт є продуктом розщеплення фосфонатних проліків у людських РВМС. Ще більш типово, фосфонатні проліки розщеплюються для утворення метаболіту, що має принаймні один негативний заряд за фізіологічного рівня рН. Більш типово, фосфонатні проліки ферментно розщеплюються у людських РВМС для утворення фосфонату, що має принаймні один активний атом водню форми Р-ОН. Незважаючи на інші представлені авторами описи, в яких описано роль або представлено фосфонати у сполуках згідно з винаходом, в іншому варіанті втілення винаходу А3 є А3а, який має формулу: Прикладами варіантів Формули VIIIc є структури: втілення сполук Прикладами варіантів Формули Vllld є структури: втілення сполук де А1 означає місце ковалентного приєднання фосфонатної групи. Здійснення клітинної акумуляції Інший варіант втілення винаходу спрямовано на інгібітор ВІЛ-протеази, здатний накопичуватися в людських РВМС. Накопичення у людських РВМС описано авторами у прикладах. Як правило, сполуки цього варіанта втілення також включають фосфонат або фосфонатні проліки. Більш типово, фосфонат або фосфонатні проліки мають структуру А3, як описано авторами. Кожен з оптимальних варіантів втілення А3, описаних авторами, є оптимальним варіантом втілення А3 у представленому варіанті втілення. Необов'язково сполуки цього варіанта втілення виявляють поліпшений внутрішньоклітинний півперіод сполук або внутрішньоклітинних метаболітів сполук у людських РВМС порівняно з аналогами сполук, які не мають фосфонату або фосфонатних проліків. Як правило, півперіод поліпшується принаймні приблизно на 50%, більш типово - принаймні на 50-100%, ще більш типово - принаймні приблизно на 100%, ще більш типово - більше, ніж приблизно на 100%. В оптимальному варіанті втілення внутрішньоклітинний півперіод метаболіту сполуки у людських РВМС поліпшується порівняно з аналогом сполуки, що не має фосфонату або фосфонатних проліків. У таких варіантах втілення У цьому варіанті втілення винаходу будь-яка А3 група може бути А3а. В іншому аспекті винаходу А3 має формулу: Μ12а не є 0, і принаймні одна фосфонатна група, присутня у сполуці, не є безпосередньо зв'язаною з W3. Більш типово, фосфонат не є безпосередньо зв'язаним з W 5. У такому варіанті втілення атом фосфору фосфонату не є безпосередньо зв'язаним з атомом вуглецю кільця. В іншому аспекті винаходу Ампренавірподібний фосфонатний інгібітор протеази, як описано вище в описі і нижче у формулі, містить А3 групу формули: Μ12а не є 0, і принаймні одна фосфонатна група, присутня у сполуці, не є безпосередньо зв'язаною з W3. Більш типово, фосфонат не є безпосередньо зв'язаним з W 5. У такому варіанті втілення атом фосфору фосфонату не є безпосередньо зв'язаним з атомом вуглецю кільця. Один варіант втілення Ампренавір-подібних 29 80819 30 фосфонатних інгібіторів протеази, як описано фосфонатних інгібіторів протеази, як описано вище в описі і нижче у формулі, не включає сполук вище в описі і нижче у формулі, стосується сполук формул: формул: В іншому аспекті винаходу А3 має формулу: Μ12а є 0, і принаймні одна фосфонатна група, присутня у сполуці, є безпосередньо зв'язаною з W3. Більш типово, фосфонат є безпосередньо зв'язаним з W5. У такому варіанті втілення атом фосфору фосфонату є безпосередньо зв'язаним з атомом вуглецю кільця. В іншому аспекті винаходу Ампренавірподібний фосфонатний інгібітор протеази, як описано вище в описі і нижче у формулі, містить А3 групу формули: Μ12а є 0, і принаймні одна фосфонатна група, присутня у сполуці, є безпосередньо зв'язаною з W3. Більш типово, фосфонат є безпосередньо зв'язаним з W5. У такому варіанті втілення атом фосфору фосфонату є безпосередньо зв'язаним з атомом вуглецю кільця. Один варіант втілення Ампренавір-подібних Приклади перелічених сполук. Як необмежувальний приклад, варіанти втілення винаходу названо нижче у формі таблиці (Таблиця 100). Ці варіанти втілення мають загальну формулу "MBF": Кожен варіант втілення MBF описано як заміщене ядро (Sc), причому ядро позначено номером, в кожен замісник позначено порядковою літерою або числом. У Таблицях з 1.1 по 1.5 представлено перелік ядер, які застосовують при утворенні варіантів втілення з Таблиці 100. Кожне ядро (Sc) має числове позначення з Таблиць з 1.1 по 1.5, і це позначення вказано першим у назві кожного варіанта втілення. Так само, у Таблицях з 10.1 по 10.19 і з 20.1 по 20.36 представлено перелік вибраних зв'язувальних груп (Lg) та замісників пролінів (Pd1 та Pd2), так само за літерним або числовим позначенням, відповідно. Відповідним чином, кожен названий варіант втілення з Таблиці 100 описано числом, яке позначає ядро з Таблиці 1.1-1.5, а потім літерою, яка позначає зв'язувальну групу (Lg) з Таблиці 10.1-10.19, та двома числами, які позначають дві групи проліків (Pd1 та Pd2) з Таблиці 20.1-20.36. У графічній формі таблиці кожен варіант втілення з Таблиці 100 позначено як назву, що має синтакс: Sc.Lg.Pd1.Pd2 31 80819 Таким чином, якщо не враховувати стереохімію, структуру 10, Схема 2, Розділ Схеми А, представляють як 12.АН.247.247. Кожну Sc груну показано з тильдою ("~"). Тильда означає точку ковалентного приєднання Sc до Lg. Слід розуміти, що Q1 та Q2 зв'язувальних груп (Lg) не представляють групи або атоми, а просто є позначеннями можливості зв'язування. Q1 є місцем ковалентного зв'язку з ядром (Sc), і Q2 є місцем ковалентного зв'язку з атомом фосфору формули MBR. Кожна група проліків (Pd1 та Pd2) є ковалентно зв'язаною з атомом фосфору MBF у місці тильди ("~"). Деякі варіанти втілення з Таблиць 10.1-10.19 та 20.1-20.36 можуть бути позначені комбінацією літер та чисел (Таблиця 10.1-10.19) або числа та літери (Таблиця 20.120.36). Наприклад, у Таблиці 10 є записи для BJ1 та BJ2. У будь-якому разі, записи в Таблиці 10.110.19 завжди починаються з літери, а у Таблиці 20.1-20.36 завжди починаються з числа. Якщо ядро (Sc) показано у квадратних дужках ("[ ]"), а ковалентний зв'язок вказано за межами дужок, то точка ковалентного приєднання Sc до Lg може бути у будь-якому придатному місці на SC. Вибір точки приєднання описується авторами. Як необмежувальний приклад, точку приєднання вибирають з-поміж описаних на схемах та прикладах. 32 33 80819 34 35 80819 36 37 80819 38 39 80819 40 41 80819 42 43 80819 44 45 80819 46 47 80819 48 49 80819 50 51 80819 52 53 80819 54 55 80819 56 57 80819 58 59 80819 60
ДивитисяДодаткова інформація
Назва патенту англійськоюPhosphonate analogs of compounds inhibiting hiv proteases, pharmaceutical composition on their basis and their use
Автори англійськоюArimilli Merti N., Becker Marc M., Brayant Klifford, Chen James M., Chen Ksiaovu, Destheh Azar, Fardis Maria, He Gong-Xin, Jin Haoliun, Kim, Choung, U., Kim Choung U., Lee William A., Li Cristophere P., Lin Kuei-Ing, Liu, Hongtao, Makmen Richard L., Mitchell Michael L., Nelson Peter H., Piun Hiung-Jung, Rouve Tanisha D., Sparacino Mark, Suamnatan Sandaramurti, Tario James D., Wang Jianning, Williams Mathew A., Ksu Lianhong, Xu, Lianhong, Yang, Zheng-Yu, Yang Zheng-Yu, Yu Richard H., Jang Jiankun, Zhang Lijun, Zhang, Lijun
Назва патенту російськоюФосфонатные аналоги соединений, которые ингибируют вич протеазы, фармацевтическая композиция на их основе и их применение
Автори російськоюАримилли Мерти Н., Бекер Марк М., Брайант Клиффорд, Чен Джеймс М., Чен Ксяову, Дестгех Азар, Фардис Мария, Хи Гонг-Ксин, Джин Хаолюн, Ким Чоунг У., Ли Уильям А., Ли Кристофер П., Лин Куэй-Инг, Макмен Ричард Л., Митчелл Майкл Л., Нельсон Питер Х., Пьюн Хьюнг-Джунг, Роув Таниша Д., Спарасино Марк, Суаминатан Сандарамурти, Тарио Джеймс Д., Уанг Джианинг, Уильямс Мэтью А., Ксу Лианхонг, Янг Женг-Ю, Ю Ричард Х., Жанг Джианкун, Жанг Лиджун
МПК / Мітки
МПК: C07F 9/655, C07F 9/653, A61K 31/675, A61P 31/18, C07F 9/6506, C07F 9/6533, C07F 9/40, C07F 9/44, A61K 31/665, C07F 9/62, C07F 9/6509, A61P 43/00, C07F 9/6561, C12N 9/16, C07F 9/58, C07F 9/6558, C07F 9/6584, C12N 9/99, C07D 403/06, C07F 9/6512, C12Q 1/44, C07F 9/645, C07D 243/04
Мітки: інгібують, сполук, фармацевтична, застосування, віл, протеази, фосфонатні, основі, композиція, аналоги
Код посилання
<a href="https://ua.patents.su/33-80819-fosfonatni-analogi-spoluk-shho-ingibuyut-vil-proteazi-farmacevtichna-kompoziciya-na-kh-osnovi-ta-kh-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Фосфонатні аналоги сполук, що інгібують віл протеази, фармацевтична композиція на їх основі та їх застосування</a>
Попередній патент: Суднова силова установка, що живиться паливом, одержаним з відходів, та спосіб її застосування
Наступний патент: N-заміщені трициклічні 3-амінопіразоли як інгібітори pdgf-рецепторів
Випадковий патент: Підвіска керованого колеса велосипеда, мотоцикла












