Похідні хіноліну як антагоністи nk3 рецептора, спосіб їх одержання, фармацевтична композиція на їх основі та спосіб лікування захворювань
Номер патенту: 51623
Опубліковано: 16.12.2002
Автори: Равеглія Люка Франческо, Гругні Маріо, Джардіна Джузеппе Арнальдо Марія, Фаріна Карло
Формула / Реферат
1. Производные хинолина формулы (I), его сольваты или соли
, (I)
в которой
Аr представляет необязательно замещенную фенильную, нафтильную или С5-7 циклоалкдиенильную группу или необязательно замещенную одинарную или сконденсированную кольцевую гетероциклическую группу, имеющую ароматический характер, содержащую от 5 до 12 кольцевых атомов и включающую до четырех гетероатомов в кольце или каждом кольце, выбранных из S, О, N;
R представляет линейный или разветвленный C1-8 алкил, С3-7 циклоалкил, С4-7 циклоалкилалкил, необязательно замещенный фенил или фенил С1-6 алкил, необязательно замещенное пятичленное гетероароматическое кольцо, включающее до четырех гетероатомов, выбранных из О и N, гидрокси С1-6 алкил, амино С1-6 алкил, С1-6 алкиламиноалкил, ди С1-6 алкиламиноалкил, С1-6 ациламиноалкил, С1-6 алкоксиалкил, С1-6 алкилкарбонил, карбокси, С1-6 алкоксикарбонил, С1-6 алкоксикарбонил С1-6 алкил, аминокарбонил, С1-6 алкиламинокарбонил, ди С1-6 алкиламинокарбонил, галоид С1-6 алкил; или представляет группу -(CH2)p-, когда он циклизован с Аr, где p представляет 2 или 3,
R1 и R2, которые могут быть одинаковыми или различными, представляют независимо водород или С1-6 линейный, или разветвленный алкил, или вместе образуют группу -(CH2)n-, в которой n представляет 3, 4 или 5; или R1 вместе с R образует группу -(CH2)q-, в которой q представляет 2, 3, 4 или 5,
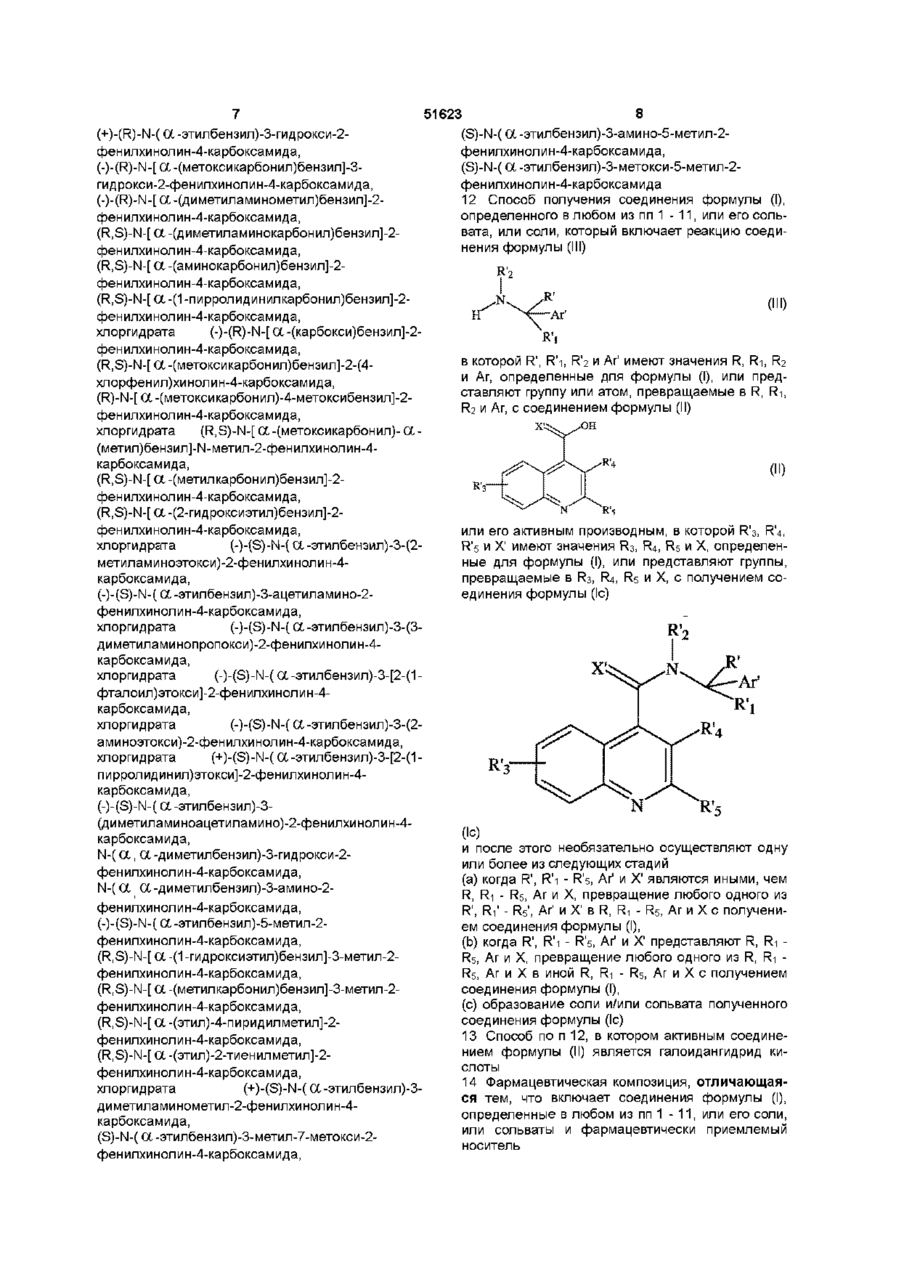
R3 и R4, которые могут быть одинаковыми или различными, представляют независимо водород, С1-6 линейный или разветвленный алкил, С1-6 алкенил, арил, С1-6 алкокси, гидрокси, галоген, нитро, циано, карбокси, карбоксамидо, сульфонамидо, С1-6 алкоксикарбонил, трифторметил, ацилокси, фталимидо, амино, моно- или ди-С1-6 алкиламино, -O(CH2)r-NT2, в которой r представляет 2, 3 или 4, и Т представляет водород или С1-6 алкил, или он образует с соседним азотом группу:
или
,
в которой V и V1 представляют независимо водород или кислород, и u представляет 0, 1 или 2; -O(CH2)s-OW, в которой s представляет 2, 3 или 4, и W представляет водород или С1-6 алкил; гидроксиалкил, аминоалкил, моно- или ди-алкиламиноалкил, ациламино, алкилсульфониламино, аминоациламино, моно- или ди-алкиламиноациламино; причем в хинолиновом ядре присутствует до четырех R3 заместителей; или R4 представляет группу -(CH2)t, когда он циклизован с R5 в виде арила, в которой t представляет 1, 2 или 3;
R5 представляет линейный или разветвленный С1-6 алкил, С3-7 циклоалкил, С4-7 циклоалкилалкил, необязательно замещенный арил или необязательно замещенную одинарную или сконденсированную кольцевую гетероциклическую группу, имеющую ароматический характер, содержащую от 5 до 12 кольцевых атомов и включающую до четырех гетероатомов в кольце или в каждом кольце, выбранных из S, О, N;
Χ представляет О, S или .
2. Соединение по п. 1, в котором
Аr представляет фенил, необязательно замещенный С1-6 алкилом или галогеном; тиенильную или С5-7 циклоалкдиенильную группу.
3. Соединение по п. 1 или 2, в котором
R представляет С1-6 алкил, С1-6 алкоксикарбонил, С1-6 алкилкарбонил или гидрокси С1-6 алкил.
4. Соединение по любому из пп. 1 - 3, в котором R1 и R2 каждый представляет водород или С1-6 алкил.
5. Соединение по любому из пп. 1 - 4, в котором R3 представляет водород, гидрокси, галоген, С1-6 алкокси или С1-6 алкил.
6. Соединение по любому из пп. 1 - 5, в котором R4 представляет водород, С1-6 алкил, С1-6 алкокси, гидрокси, амино, галоген, аминоалкокси, моно- или ди-алкиламиноалкокси, моно- или ди-алкиламиноалкил, фталоилалкокси, моно- или ди-алкиламиноациламино или ациламино.
7. Соединение по любому из пп. 1 - 6, в котором R5 представляет фенил, тиенил, фурил, пиррил или тиазолил.
8. Соединение формулы (I) по п. 1 или его соль или сольват, в котором:
Аr представляет фенил, 2-хлорфенил, 2-тиенил или циклогексадиенил;
R представляет метил, этил, н-пропил, -СООМе или -СОМе;
R1 и R2 каждый представляет водород или метил;
R3 представляет водород, метокси или гидрокси;
R4 представляет водород, метил, этил, метокси, гидрокси, амино, хлор, бром, диметиламиноэтокси, 2-(1-фталоил)этокси, аминоэтокси, 2-(1-пирролидинил)этокси, диметиламинопропокси, диметиламиноацетиламино, ацетиламино или диметиламинометил;
R5 представляет фенил, 2-тиенил, 2-фурил, 2-пиррил, 2-тиазолил или 3-тиенил; и
Χ представляет кислород.
9. Соединение по любому из пп. 1 - 7 или его соль, или сольват, имеющее формулу (Iа):
, (Iа)
в которой
R, R2, R3 и R4 имеют значения, определенные для формулы (І) в любом из пп. 1 - 7, и Υ и Z, которые могут быть одинаковыми или различными, каждый представляет Аr, как он определен для формулы (І) в п. 1 или 2.
10. Соединение по п. 9 формулы (Ib):
, (Ib)
в которой R, R2, R3 и R4, Υ и Ζ имеют значения, определенные в п. 9.
11. Соединение по п. 1, выбранное из группы, состоящей из:
(R,S)-N-(-метилбензил)-2-фенилхинолин-4-карбоксамида,
(+)-(S)-N-(-метилбензил)-2-фенилхинолин-4-карбоксамида,
(-)-(R)-N-(-метилбензил)-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-2-фенилхинолин-4-карбоксамида,
(+)-(S)-N-[-(метоксикарбонил)бензил]-2-фенилхинолин-4-карбоксамида,
(-)-(R)-N-[-(метоксикарбонил)бензил]-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-7-метокси-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(мeтoкcикapбoнил)бeнзил]-7-гидpoкcи-2-фeнилxинoлин-4-карбоксамида,
хлоргидрата(R,S)-N-[-(карбокси)бензил]-7-метокси-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метиламинокарбонил)бензил]-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-2-(2-тиенил)хинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-2-(2-фурил)хинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-2-(4-пиридил)хинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)-2-тиенилметил]-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонилметил)бензил]-2-фенилхинолин-4-карбоксамида,
(-)-(R)-N-[-(метоксикарбонил)-1,4-циклогексадиенилметил]-2-фенилхинолин-4-карбоксамида,
индивидуального диастереомера (R,S)-N-[-(1-гидроксиэтил)бензил]-2-фенилхинолин-4-карбоксамида,
(R,S)-N-(-этилбензил)-3-метокси-2-фенилхинолин-4-карбоксамида,
(R,S)-N-(-этилбензил)-3-н-бутил-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]бензо-1,3-циклогептадиено[1,2-b]хинолин-8-карбоксамида,
(R,S)-N-(-этилбензил)-3-гексил-2-фенилхинолин-4-карбоксамида,
(-)-(S)-N-(-этилбензил)-3-метил-2-фенилхинолин-4-карбоксамида,
(+)-(R)-N-(-этилбензил)-3-метил-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-2-(2-метоксифенил)хинолин-4-карбоксамида,
(R,S)-N-(-этилбензил)-3-фенил-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-2-(2-фторфенил)хинолин-4-карбоксамида,
(R,S)-N-[-(этил)-3,4-дихлорбензил]-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(гидроксиметил)бензил]-2-фенилхинолин-4-карбоксамида,
(R,S)-N-(-этилбензил)-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-3-метил-2-фенилхинолин-4-карбоксамида,
(R,S)-N-(-этилбензил)-3-метил-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-7-хлор-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-6-метил-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксиметил)бензил]-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-6-хлор-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-3-этил-2-фенилхинолин-4-карбоксамида,
(R,S)-N-(-н-пропилбензил)-2-фенилхинолин-4-карбоксамида,
(R,S)-N-(-этилбензил)-3-этил-2-фенилхинолин-4-карбоксамида,
(R,S)-N-(-этилбензил)-3-фталимидо-2-фенилхинолин-4-карбоксамида,
(R,S)-N-(-этилбензил)-3-н-пропил-2-фенилхинолин-4-карбоксамида,
(-)-(S)-N-(-этилбензил)-6-бром-3-метил-2-(4-бромфенил)хинолин-4-карбоксамида,
(-)-(S)-N-(-этилбензил)-6-бром-3-метил-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-6-метокси-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-2-(2-бензофурил)хинолин-4-карбоксамида,
(R,S)-N-[(1,2-дифенил)этил]-2-фенилхинолин-4-карбоксамида,
(R,S)-N-(-трифторметилбензил)-2-фенилхинолин-4-карбоксамида,
(-)-(S)-N-(-этилбензил)-3-метокси-2-фенилхинолин-4-карбоксамида,
(-)-(S)-N-(-этилбензил)-3-этил-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(этил)-4-хлорбензил]-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-N-метил-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-2-(3-тиенил)хинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-5,6-дигидробензо[а]-акридин-7-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-2-(2-пиррил)хинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-2-(2-тиазолил)хинолин-4-карбоксамида,
(R,S)-N-(1-инданил)-2-фенилхинолин-4-карбоксамида,
(R,S)-N-(-н-бутилбензил)-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-2-(4-метилфенил)хинолин-4-карбоксамида,
(R,S)-N-(-гептилбензил)-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-2-(2-метилфенил)хинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-2-(4-метоксифенил)хинолин-4-карбоксамида,
N-(1-фенилциклопентил)-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-2-(4-гидроксифенил)хинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-2-(3,4-метилендиоксифенил)хинолин-4-карбоксамида,
N-(,-диметилбензил)-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(этил)-4-метилбензил]-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-2-(3-пиррил)хинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-2-(3,4-дихлорфенил)хинолин-4-карбоксамида,
(-)-(R)-N-[-(аминометил)бензил]-2-фенилхинолин-4-карбоксамида,
(-)-(S)-N-(-этилбензил)-3-амино-2-фенилхинолин-4-карбоксамида,
(-)-(S)-N-(-этилбензил)-3-хлор-2-фенилхинолин-4-карбоксамида,
(-)-(S)-N-(-этилбензил)-3-бром-2-фенилхинолин-4-карбоксамида,
(R,S)-N-(-изо-пропилбензил)-2-фенилхинолин-4-карбоксамида,
(-)-(S)-N-(-этилбензил)-2-фенилхинолин-4-карбоксамида,
(+)-(R)-N-(-этилбензил)-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-6-фтор-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-2-циклогексилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-2-(3-хлорфенил)хинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-2-(2-хлорфенил)хинолин-4-карбоксамида,
(R,S)-N-[-этилбензил)-3-гидрокси-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-8-ацетилокси-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-8-гидрокси-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-2-(2,4-дихлорфенил)хинолин-4-карбоксамида,
хлоргидрата (-)-(R)-N-[-(метоксикарбонил)-4-гидроксибензил]-2-фенилхинолин-4-карбоксамида,
N-дифенилметил-2-фенилхинолин-4-карбоксамида,
(-)-(S)-N-(-этилбензил)-3-гидрокси-2-фенилхинолин-4-карбоксамида,
(+)-(R)-N-(-этилбензил)-3-гидрокси-2-фенилхинолин-4-карбоксамида,
(-)-(R)-N-[-(метоксикарбонил)бензил]-3-гидрокси-2-фенилхинолин-4-карбоксамида,
(-)-(R)-N-[-(диметиламинометил)бензил]-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(диметиламинокарбонил)бензил]-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(аминокарбонил)бензил]-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(1-пирролидинилкарбонил)бензил]-2-фенилхинолин-4-карбоксамида,
хлоргидрата (-)-(R)-N-[-(карбокси)бензил]-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метоксикарбонил)бензил]-2-(4-хлорфенил)хинолин-4-карбоксамида,
(R)-N-[-(метоксикарбонил)-4-метоксибензил]-2-фенилхинолин-4-карбоксамида,
хлоргидрата (R,S)-N-[-(метоксикарбонил)--(метил)бензил]-N-метил-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метилкарбонил)бензил]-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(2-гидроксиэтил)бензил]-2-фенилхинолин-4-карбоксамида,
хлоргидрата (-)-(S)-N-(-этилбензил)-3-(2-метиламиноэтокси)-2-фенилхинолин-4-карбоксамида,
(-)-(S)-N-(-этилбeнзил)-3-aцeтилaминo-2-фeнилxинoлин-4-кapбoкcaмидa,
хлоргидрата (-)-(S)-N-(-этилбензил)-3-(3-диметиламинопропокси)-2-фенилхинолин-4-карбоксамида,
хлоргидрата (-)-(S)-N-(-этилбензил)-3-[2-(1-фталоил)этокси]-2-фенилхинолин-4-карбоксамида,
хлоргидрата (-)-(S)-N-(-этилбензил)-3-(2-аминоэтокси)-2-фенилхинолин-4-карбоксамида,
хлоргидрата (+)-(S)-N-(-этилбензил)-3-[2-(1-пирролидинил)этокси]-2-фенилхинолин-4-карбоксамида,
(-)-(S)-N-(-этилбензил)-3-(диметиламиноацетиламино)-2-фенилхинолин-4-карбоксамида,
N-(,-диметилбензил)-3-гидрокси-2-фенилхинолин-4-карбоксамида,
N-(,-димeтилбeнзил)-3-aминo-2-фeнилxинoлин-4-кapбoкcaмидa,
(-)-(S)-N-(-этилбензил)-5-метил-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(1-гидроксиэтил)бензил]-3-метил-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(метилкарбонил)бензил]-3-метил-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(этил)-4-пиридилметил]-2-фенилхинолин-4-карбоксамида,
(R,S)-N-[-(этил)-2-тиенилметил]-2-фенилхинолин-4-карбоксамида,
хлоргидрата (+)-(S)-N-(-этилбензил)-3-диметиламинометил-2-фенилхинолин-4-карбоксамида,
(S)-N-(-этилбензил)-3-метил-7-метокси-2-фенилхинолин-4-карбоксамида,
(S)-N-(-этилбензил)-3-амино-5-метил-2-фенилхинолин-4-карбоксамида,
(S)-N-(-этилбензил)-3-метокси-5-метил-2-фенилхинолин-4-карбоксамида.
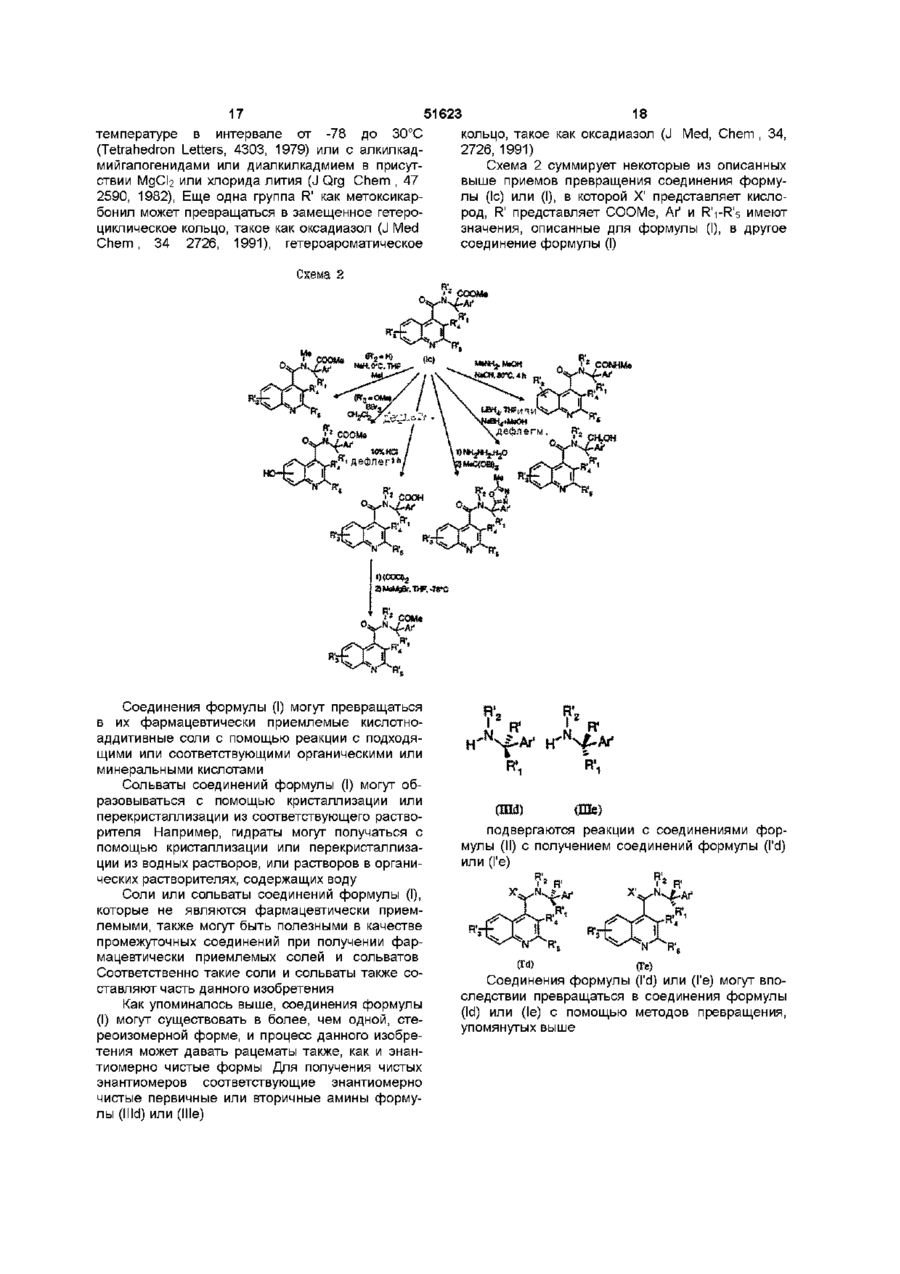
12. Способ получения соединения формулы (I), определенного в любом из пп. 1 - 11, или его сольвата, или соли, который включает реакцию соединения формулы (III):
, (III)
в которой R', R'1, R'2 и Аr' имеют значения R, R1, R2 и Аr, определенные для формулы (I), или представляют группу или атом, превращаемые в R, R1, R2 и Аr, с соединением формулы (II)
, (II)
или его активным производным, в которой R'3, R'4, R'5 и X' имеют значения R3, R4, R5 и X, определенные для формулы (I), или представляют группы, превращаемые в R3, R4, R5 и X, с получением соединения формулы (Ic)
(Іс)
и после этого необязательно осуществляют одну или более из следующих стадий:
(a) когда R', R'1 - R'5, Аr' и X' являются иными, чем R, R1 - R5, Аr и Χ, превращение любого одного из R', R1' - R5', Аr' и X' в R, R1 - R5, Аr и Χ с получением соединения формулы (I),
(b) когда R', R'1 - R'5, Аr' и X' представляют R, R1 - R5, Аr и X, превращение любого одного из R, R1 - R5, Аr и Χ в иной R, R1 - R5, Аr и Χ с получением соединения формулы (I),
(c) образование соли и/или сольвата полученного соединения формулы (Іс).
13. Способ по п. 12, в котором активным соединением формулы (II) является галоидангидрид кислоты.
14. Фармацевтическая композиция, отличающаяся тем, что включает соединения формулы (I), определенные в любом из пп. 1 - 11, или его соли, или сольваты и фармацевтически приемлемый носитель.
15. Соединения формулы (I), определенные в любом из пп. 1 - 11, или их сольваты, или соли для использования в качестве активного терапевтического вещества.
16. Соединения формулы (I), определенные в любом из пп. 1 - 11, или их сольваты, или соли для использования при лечении легочных расстройств (астмы, хронических обструктивных легочных заболеваний -COPD-, гиперреактивности дыхательных путей, кашля), кожных нарушений и зуда или чесотки (например атопического дерматита и кожных волдырей, и красного дермографизма), нейрогенного воспаления и расстройств ЦНС (болезни Паркинсона, нарушений двигательной способности, беспокойства или страха и психоза), конвульсивных расстройств, эпилепсии, почечных расстройств, недержания мочи, глазных воспалений, воспалительных болей, расстройств приема пищи (торможение приема пищи), аллергического ринита, нейродегенеративных расстройств (например болезни Альцгеймера), псориаза, болезни Хантингтона и депрессии.
17. Соединения формулы (I), определенные в любом из пп. 1 - 11, или их сольваты, или соли как непептидные антагонисты рецептора NK3 для использования при лечении конвульсивных расстройств, эпилепсии, почечных расстройств, недержания мочи, глазных воспалений, воспалительных болей, расстройств приема пищи (торможение приема пищи), аллергического ринита, нейродегенеративных расстройств (например болезни Альцгеймера), псориаза, болезни Хантингтона и депрессии.
18. Соединения формулы (I), определенные в любом из пп. 1 - 11, или их сольваты, или соли как непептидные антагонисты NК3 рецептора для использования при лечении вторичных расстройств.
19. Способ лечения и/или профилактики легочных расстройств (астмы, хронических обструктивных легочных заболеваний -COPD-, гиперреактивности дыхательных путей, кашля), кожных нарушений и зуда или чесотки (например атонического дерматита и кожных волдырей, и красного дермографизма), нейрогенного воспаления и расстройств ЦНС (болезни Паркинсона, нарушений двигательной способности, беспокойства или страха и психоза), конвульсивных расстройств, эпилепсии, почечных расстройств, недержания мочи, глазных воспалений, воспалительных болей, расстройств приема пищи (торможение приема пищи), аллергического ринита, нейродегенеративных расстройств (например болезни Альцгеймера), псориаза, болезни Хантингтона и депрессии у млекопитающих, который включает назначение млекопитающему, нуждающемуся в таком лечении и/или профилактике, эффективного количества соединения формулы (I), определенного в п. 1, или его сольвата, или соли.
20. Способ лечения и/или профилактики конвульсивных расстройств, эпилепсии, почечных расстройств, недержания мочи, глазных воспалений, воспалительных болей, расстройств приема пищи (торможение приема пищи), аллергического ринита, нейродегенеративных расстройств (например болезни Альцгеймера), псориаза, болезни Хантингтона и депрессии у млекопитающих, который включает назначение млекопитающему, нуждающемуся в таком лечении и/или профилактике, эффективного количества соединений формулы I по п. 1 как непептидных антагонистов NK3 рецептора.
Текст
1 Производные хинолина формулы (I), его сольваты или соли Ц2 карбонил, карбокси, Сі є алкоксикарбонил, Сі є ал кокси карбон ил Сі є алкил, аминокарбонил, Сі є алкиламинокарбонил, ди Сі є алкиламинокарбонил, галоид Сі є алкил, или представляет группу (CbbV, когда он циклизован с Аг, где р представляет 2 или 3, Ri и F?2, которые могут быть одинаковыми или различными, представляют независимо водород или Сі є линейный, или разветвленный алкил, или вместе образуют группу -(Cbbjn-, в которой п представляет 3, 4 или 5, или Ri вместе с R образует группу -(CbbV, в которой q представляет 2, 3, 4 или 5, R3 и R4, которые могут быть одинаковыми или различными, представляют независимо водород, Сі є линейный или разветвленный алкил, Сі є алкенил, арил, Сі є алкокси, гидрокси, галоген, нитро, циано, карбокси, карбоксамидо, сульфонамидо, Сі є алкоксикарбонил, трифторметил, ацилокси, фталимидо, амино, моно- или ди-Сі є алкиламино, -O(CH2)r-NT2, в которой г представляет 2, 3 или 4, и Т представляет водород или Сі є алкил, или он образует с соседним азотом группу О (I) ГО (О в которой Аг представляет необязательно замещенную фенильную, нафтильную или Cs і циклоалкдиенильную группу или необязательно замещенную одинарную или сконденсированную кольцевую гетероциклическую группу, имеющую ароматический характер, содержащую от 5 до 12 кольцевых атомов и включающую до четырех гетероатомов в кольце или каждом кольце, выбранных из S, О, N, R представляет линейный или разветвленный Ci s алкил, Сз 7 циклоалкил, С4-7 циклоалкилалкил, необязательно замещенный фенил или фенил Сі є алкил, необязательно замещенное пятичленное гетероа ром этическое кольцо, включающее до четырех гетероатомов, выбранных из О и N, гидрокси Сі є алкил, амино Сі є алкил, Сі є алкиламиноалкил, ди Сі є алкиламиноалкил, Сі є ациламиноалкил, Сі є алкоксиалкил, Сі є алкил ю в которой V и Vi представляют независимо водород или кислород, и и представляет 0,1 или 2, O(CH2)S-OW, в которой s представляет 2, 3 или 4, и W представляет водород или Сі є алкил, гидроксиалкил, аминоалкил, моноили диалкиламиноалкил, ациламино, алкилсульфониламино, аминоациламино, моноили диалкиламиноациламино, причем в хинолиновом ядре присутствует до четырех R3 заместителей, или R4 представляет группу -(Cbbjt, когда он циклизован с R5 в виде арила, в которой t представляет 1, 2 или 3, Rs представляет линейный или разветвленный Сі є алкил, Сз 7 циклоалкил, С^і циклоалкилалкил, необязательно замещенный арил или необязательно замещенную одинарную или сконденсированную кольцевую гетероциклическую группу, имеющую ароматический характер, содержащую от 5 до 12 кольцевых атомов и включающую до четырех гетероатомов в кольце или в каждом кольце, выбранных из S, О, N, X представляет О, S или N-C = N 2 Соединение по п 1, в котором Аг представляет фенил, необязательно замещенный Сі є алкилом или галогеном, тиенильную или Сб 7 циклоалкдиенильную группу 3 Соединение по п 1 или 2, в котором R представляет Сі є алкил, Сі є алкоксикарбонил, Сі є алкилкарбонил или гидрокси Сі є алкил 4 Соединение по любому из пп 1 - 3, в котором Ri и R2 каждый представляет водород или Сі є алкил 5 Соединение по любому из пп 1 - 4, в котором R3 представляет водород, гидрокси, галоген, Сі є алкокси или Сі є алкил 6 Соединение по любому из пп 1 - 5, в котором R4 представляет водород, Сі є алкил, Сі є алкокси, гидрокси, амино, галоген, аминоалкокси, моноили ди-алкиламиноалкокси, моно- или диалкиламиноалкил, фталоилалкокси, моно- или диалкиламиноациламино или ациламино 7 Соединение по любому из пп 1 - 6, в котором Rs представляет фенил, тиенил, фурил, пиррил или тиазолил 8 Соединение формулы (I) по п 1 или его соль или сольват, в котором Аг представляет фенил, 2-хлорфенил, 2-тиенил или циклогексадиенил, R представляет метил, этил, н-пропил, -СООМе или -СОМе, Ri и R2 каждый представляет водород или метил, R3 представляет водород, метокси или гидрокси, R4 представляет водород, метил, этил, метокси, гидрокси, амино, хлор, бром, диметиламиноэтокси, 2-(1-фталоил)этокси, аминоэтокси, 2-(1пирролидинил)этокси, диметиламинопропокси, диметиламиноацетиламино, ацетиламино или диметиламинометил, Rs представляет фенил, 2-тиенил, 2-фурил, 2пиррил, 2-тиазолил или 3-тиенил, и X представляет кислород 9 Соединение по любому из пп 1 - 7 или его соль, или сольват, имеющее формулу (la) Д о 1а) в которой R, F?2, R3 и R4 имеют значения, определенные для формулы (I) в любом из пп 1 - 7, и Y и Z, которые могут быть одинаковыми или различными, каждый 51623 представляет Аг, как он определен для формулы (І) в п 1 или 2 10 Соединение по п 9 формулы (Ib) (Ib) N Y в которой R, F?2, R3 и R4, Y и Z имеют значения, определенные в п 9 11Соединение по п 1, выбранное из группы, состоящей из (R,S)-N-( а -метилбензил)-2-фенилхинолин-4карбоксамида, (+)-(S)-N-( а -метилбензил)-2-фенилхинолин-4карбоксамида, (-)-(R)-N-( а -метилбензил)-2-фенилхинолин-4карбоксамида, (R,S)-N-[ а -(метоксикарбонил)бензил]-2фенилхинолин-4-карбоксамида, (+)-(S)-N-[ а -(метоксикарбонил)бензил]-2фенилхинолин-4-карбоксамида, (-)-(R)-N-[ а -(метоксикарбонил)бензил]-2фенилхинолин-4-карбоксамида, (R,S)-N-[ а -(метоксикарбонил)бензил]-7-метокси2-фенилхинолин-4-карбоксамида, (R,S)-N-[ а -(метоксикарбонил)бензил]-7-гидрокси2-фенилхинолин-4-карбоксамида, xnoprnflpaTa(R,S)-N-[ а -(карбокси)бензил]-7метокси-2-фенилхинолин-4-карбоксамида, (R,S)-N-[ а -(метиламинокарбонил)бензил]-2фенилхинолин-4-карбоксамида, (R,S)-N-[ а -(метоксикарбонил)бензил]-2-(2тиенил)хинолин-4-карбоксамида, (R,S)-N-[ а -(метоксикарбонил)бензил]-2-(2фурил)хинолин-4-карбоксамида, (R,S)-N-[ а -(метоксикарбонил)бензил]-2-(4пиридил)хинолин-4-карбоксамида, (R,S)-N-[ а -(метоксикарбонил)-2-тиенилметил]-2фенилхинолин-4-карбоксамида, (R,S)-N-[ а -(метоксикарбонилметил)бензил]-2фенилхинолин-4-карбоксамида, (-)-(R)-N-[ а -(метоксикарбонил)-1,4циклогексадиенилметил]-2-фенилхинолин-4карбоксамида, индивидуального диастереомера (R,S)-N-[ a -(1 гидроксиэтил)бензил]-2-фенилхинолин-4карбоксамида, (R,S)-N-( а -этилбензил)-3-метокси-2фенилхинолин-4-карбоксамида, (R,S)-N-( а -этилбензил)-3-н-бутил-2фенилхинолин-4-карбоксамида, (R,S)-N-[ а -(метоксикарбонил)бензил]бензо-1,3циклогептадиено[1,2-Ь]хинолин-8-карбоксамида, (R,S)-N-( а -этилбензил)-3-гексил-2фенилхинолин-4-карбоксамида, (-)-(S)-N-( а -этилбензил)-3-метил-2фенилхинолин-4-карбоксамида, (+)-(R)-N-( а -этилбензил)-3-метил-2фенилхинолин-4-карбоксамида, 51623 (R,S)-N-[ а -(метоксикарбонил)бензил]-2-(2метоксифенил)хинолин-4-карбоксамида, (R,S)-N-( a -этилбензил)-3-фенил-2фенилхинолин-4-карбоксамида, (R,S)-N-[ a -(метоксикарбонил)бензил]-2-(2фторфенил)хинолин-4-карбоксамида, (R,S)-N-[ a -(этил)-3,4-дихлорбензил]-2фенилхинолин-4-карбоксамида, (R,S)-N-[ a -(гидроксиметил)бензил]-2фенилхинолин-4-карбоксамида, (R,S)-N-( a -этилбензил)-2-фенилхинолин-4карбоксамида, (R,S)-N-[ a -(метоксикарбонил)бензил]-3-метил-2фенилхинолин-4-карбоксамида, (R,S)-N-( a -этилбензил)-3-метил-2-фенилхинолин4-карбоксамида, (R,S)-N-[ a -(метоксикарбонил)бензил]-7-хлор-2фенилхинолин-4-карбоксамида, (R,S)-N-[ a -(метоксикарбонил)бензил]-6-метил-2фенилхинолин-4-карбоксамида, (R,S)-N-[ a -(метоксиметил)бензил]-2фенилхинолин-4-карбоксамида, (R,S)-N-[ a -(метоксикарбонил)бензил]-6-хлор-2фенилхинолин-4-карбоксамида, (R,S)-N-[ a -(метоксикарбонил)бензил]-3-этил-2фенилхинолин-4-карбоксамида, (R,S)-N-( a -н-пропилбензил)-2-фенилхинолин-4карбоксамида, (R,S)-N-( a -этилбензил)-3-этил-2-фенилхинолин4-карбоксамида, (R,S)-N-( a -этилбензил)-3-фталимидо-2фенилхинолин-4-карбоксамида, (R,S)-N-( a -этилбензил)-3-н-пропил-2фенилхинолин-4-карбоксамида, (-)-(S)-N-( a -этилбензил)-6-бром-3-метил-2-(4бромфенил)хинолин-4-карбоксамида, (-)-(S)-N-( a -этилбензил)-6-бром-3-метил-2фенилхинолин-4-карбоксамида, (R,S)-N-[ a -(метоксикарбонил)бензил]-6-метокси2-фенилхинолин-4-карбоксамида, (R,S)-N-[ a -(метоксикарбонил)бензил]-2-(2бензофурил)хинолин-4-карбоксамида, ^,3)-1\1-[(1,2-дифенил)этил]-2-фенилхинолин-4карбоксамида, (R,S)-N-( a -трифторметилбензил)-2фенилхинолин-4-карбоксамида, (-)-(S)-N-( a -этилбензил)-3-метокси-2фенилхинолин-4-карбоксамида, (-)-(S)-N-( a -этилбензил)-3-этил-2-фенилхинолин4-карбоксамида, (R,S)-N-[ a -(этил)-4-хлорбензил]-2-фенилхинолин4-карбоксамида, (R,S)-N-[ a -(метоксикарбонил)бензил]-І\І-метил-2фенилхинолин-4-карбоксамида, (R,S)-N-[ a -(метоксикарбонил)бензил]-2-(3тиенил)хинолин-4-карбоксамида, (R,S)-N-[ a -(метоксикарбонил)бензил]-5,6дигидробензо[а]-акридин-7-карбоксамида, (R,S)-N-[ a -(метоксикарбонил)бензил]-2-(2пиррил)хинолин-4-карбоксамида, (R,S)-N-[ a -(метоксикарбонил)бензил]-2-(2тиазолил)хинолин-4-карбоксамида, карбоксамида, (R,S)-N-( а -н-бутилбензил)-2-фенилхинолин-4карбоксамида, (R,S)-N-[ а -(метоксикарбонил)бензил]-2-(4метилфенил)хинолин-4-карбоксамида, (R,S)-N-( а -гептилбензил)-2-фенилхинолин-4карбоксамида, (R,S)-N-[ а -(метоксикарбонил)бензил]-2-(2метилфенил)хинолин-4-карбоксамида, (R,S)-N-[ а -(метоксикарбонил)бензил]-2-(4метоксифенил)хинолин-4-карбоксамида, N-(1-фенил циклопентил)-2-фенилхинолин-4карбоксамида, (R,S)-N-[ а -(метоксикарбонил)бензил]-2-(4гидроксифенил)хинолин-4-карбоксамида, (R,S)-N-[ а -(метоксикарбонил)бензил]-2-(3,4метилендиоксифенил)хинолин-4-карбоксамида, N-( а а -диметилбензил)-2-фенилхинолин-4карбоксамида, (R,S)-N-[ а -(этил)-4-метилбензил]-2фенилхинолин-4-карбоксамида, (R,S)-N-[ а -(метоксикарбонил)бензил]-2-(3пиррил)хинолин-4-карбоксамида, (R,S)-N-[ а -(метоксикарбонил)бензил]-2-(3,4дихлорфенил)хинолин-4-карбоксамида, (-)-(R)-N-[a-(aMHHOMeTHn)6eH3Hn]-2фенилхинолин-4-карбоксамида, (-)-(S)-N-( а -этилбензил)-3-амино-2фенилхинолин-4-карбоксамида, (-)-(S)-N-( а -этилбензил)-3-хлор-2-фенилхинолин4-карбоксамида, (-)-(S)-N-( а -этилбензил)-3-бром-2-фенилхинолин4-карбоксамида, (R,S)-N-( а -изо-пропилбензил)-2-фенилхинолин-4карбоксамида, (-)-(3)-М-(а-этилбензил)-2-фенилхинолин-4карбоксамида, (+)-(R)-N-( а -этилбензил)-2-фенилхинолин-4карбоксамида, (R,S)-N-[ а -(метоксикарбонил)бензил]-6-фтор-2фенилхинолин-4-карбоксамида, (R,S)-N-[ а -(метоксикарбонил)бензил]-2циклогексилхинолин-4-карбоксамида, (R,S)-N-[ а -(метоксикарбонил)бензил]-2-(3хлорфенил)хинолин-4-карбоксамида, (R,S)-N-[ а -(метоксикарбонил)бензил]-2-(2хлорфенил)хинолин-4-карбоксамида, (R,S)-N-[ а -этилбензил)-3-гидрокси-2фенилхинолин-4-карбоксамида, (R,S)-N-[ а -(метоксикарбонил)бензил]-8ацетилокси-2-фенилхинолин-4-карбоксамида, (R,S)-N-[ а -(метоксикарбонил)бензил]-8-гидрокси2-фенилхинолин-4-карбоксамида, (R,S)-N-[ а -(метоксикарбонил)бензил]-2-(2,4дихлорфенил)хинолин-4-карбоксамида, хлоргидрата (-)-(R)-N-[ (X -(метоксикарбонил)-4гидроксибензил]-2-фенилхинолин-4-карбоксамида, М-дифенилметил-2-фенилхинолин-4карбоксамида, (-)-(S)-N-( а -этилбензил)-3-гидрокси-2фенилхинолин-4-карбоксамида, 51623 (+)-(R)-N-( (X -этилбензил)-3-гидрокси-2фенилхинолин-4-карбоксамида, (-)-^)-|\|-[(Х-(метоксикарбонил)бензил]-3гидрокси-2-фенилхинолин-4-карбоксамида, (-)-^)-|\|-[(Х-(диметиламинометил)бензил]-2фенилхинолин-4-карбоксамида, (R,S)-N-[ (X -(диметиламинокарбонил)бензил]-2фенилхинолин-4-карбоксамида, (R,S)-N-[ (X -(аминокарбонил)бензил]-2фенилхинолин-4-карбоксамида, (R,S)-N-[ (X -(1 -пирролидинилкарбонил)бензил]-2фенилхинолин-4-карбоксамида, хлоргидрата (-)-(R)-N-[ (X -(карбокси)бензил]-2фенилхинолин-4-карбоксамида, (R,S)-N-[ (X -(метоксикарбонил)бензил]-2-(4хлорфенил)хинолин-4-карбоксамида, (R)-N-[ (X -(метоксикарбонил)-4-метоксибензил]-2фенилхинолин-4-карбоксамида, хлоргидрата (R,S)-N-[(X-(MeTOKCHKap6oi-mn)-(X(метил)бензил]-І\І-метил-2-фенилхинолин-4карбоксамида, (R,S)-N-[ (X -(метилкарбонил)бензил]-2фенилхинолин-4-карбоксамида, (R,S)-N-[ а -(2-гидроксиэтил)бензил]-2фенилхинолин-4-карбоксамида, хлоргидрата (-)-(3)-г\1-((Х-этилбензил)-3-(2метиламиноэтокси)-2-фенилхинолин-4карбоксамида, (-)-(3)-г\1-((Х-этилбензил)-3-ацетиламино-2фенилхинолин-4-карбоксамида, хлоргидрата (-)-(3)-г\1-((Х-этилбензил)-3-(3диметиламинопропокси)-2-фенилхинолин-4карбоксамида, хлоргидрата (-)-(3)-1\1-((Х-этилбензил)-3-[2-(1фталоил)этокси]-2-фенилхинолин-4карбоксамида, хлоргидрата (-)-(3)-1\1-((Х-этилбензил)-3-(2аминоэтокси)-2-фенилхинолин-4-карбоксамида, хлоргидрата (+)-(3)-г\1-((Х-этилбензил)-3-[2-(1пирролидинил)этокси]-2-фенилхинолин-4карбоксамида, (-)-(3)-М-(а-этилбензил)-3(диметиламиноацетиламино)-2-фенилхинолин-4карбоксамида, N-( (X, (X -диметилбензил)-3-гидрокси-2фенилхинолин-4-карбоксамида, N-((X (Х-диметилбензил)-3-амино-2фенилхинолин-4-карбоксамида, (-)-(3)-1\1-((Х-этилбензил)-5-метил-2фенилхинолин-4-карбоксамида, (R,S)-N-[ a -(1 -гидроксиэтил)бензил]-3-метил-2фенилхинолин-4-карбоксамида, (R,S)-N-[ a -(метилкарбонил)бензил]-3-метил-2фенилхинолин-4-карбоксамида, ^,3)-1\1-[(Х-(этил)-4-пиридилметил]-2фенилхинолин-4-карбоксамида, (R,S)-N-[a-(3THn)-2-THeHHnMeTHn]-2фенилхинолин-4-карбоксамида, хлоргидрата (+)-(3)-1\1-((Х-этилбензил)-3диметиламинометил-2-фенилхинолин-4карбоксамида, (S)-N-( a -этилбензил)-3-метил-7-метокси-2фенилхинолин-4-карбоксамида, 8 (S)-N-( a -этилбензил)-3-амино-5-метил-2фенилхинолин-4-карбоксамида, (S)-N-( a -этилбензил)-3-метокси-5-метил-2фенилхинолин-4-карбоксамида 12 Способ получения соединения формулы (I), определенного в любом из пп 1 - 11, или его сольвата, или соли, который включает реакцию соединения формулы (III) R'2 -N Н Аг' (III) в которой R', R'i, R'2 и Аг' имеют значения R, Ri, R2 и Аг, определенные для формулы (I), или представляют группу или атом, превращаемые в R, Ri, R2 и Аг, с соединением формулы (II) (II) или его активным производным, в которой R'3, R'4, R'5 и X' имеют значения R3, R4, Rs и X, определенные для формулы (I), или представляют группы, превращаемые в R3, R4, Rs и X, с получением соединения формулы (Ic) (Ic) и после этого необязательно осуществляют одну или более из следующих стадий (a) когда R', R'i - R'5, Аг' и X являются иными, чем R, Ri - R5, Аг и X, превращение любого одного из R', RT - R5', Аг' и X в R, Ri - R5, Аг и X с получением соединения формулы (I), (b) когда R', R'i - R'5, Аг' и X представляют R, Ri R5, Аг и X, превращение любого одного из R, Ri R5, Аг и X в иной R, Ri - R5, Аг и X с получением соединения формулы (I), (c) образование соли и/или сольвата полученного соединения формулы (Ic) 13 Способ по п 12, в котором активным соединением формулы (II) является галоидангидрид кислоты 14 Фармацевтическая композиция, отличающаяся тем, что включает соединения формулы (I), определенные в любом из пп 1 - 11, или его соли, или сольваты и фармацевтически приемлемый носитель 15 Соединения формулы (I), определенные в любом из пп 1 - 11, или их сольваты, или соли для использования в качестве активного терапевтического вещества 16 Соединения формулы (I), определенные в любом из пп 1 - 11, или их сольваты, или соли для использования при лечении легочных расстройств (астмы, хронических обструктивных легочных заболеваний -COPD-, гиперреактивности дыхательных путей, кашля), кожных нарушений и зуда или чесотки (например атопического дерматита и кожных волдырей, и красного дермографизма), нейрогенного воспаления и расстройств ЦНС (болезни Паркинсона, нарушений двигательной способности, беспокойства или страха и психоза), конвульсивных расстройств, эпилепсии, почечных расстройств, недержания мочи, глазных воспалений, воспалительных болей, расстройств приема пищи (торможение приема пищи), аллергического ринита, нейродегенеративных расстройств (например болезни Альцгеймера), псориаза, болезни Хантингтона и депрессии 17 Соединения формулы (I), определенные в любом из пп 1 - 11, или их сольваты, или соли как непептидные антагонисты рецептора ІЧКз для использования при лечении конвульсивных расстройств, эпилепсии, почечных расстройств, недержания мочи, глазных воспалений, воспалительных болей, расстройств приема пищи (торможение приема пищи), аллергического ринита, нейродегенеративных расстройств (например болезни Альцгеймера), псориаза, болезни Хантингтона и депрессии 18 Соединения формулы (I), определенные в любом из пп 1 - 11, или их сольваты, или соли как 51623 10 непептидные антагонисты ІЧКз рецептора для использования при лечении вторичных расстройств 19 Способ лечения и/или профилактики легочных расстройств (астмы, хронических обструктивных легочных заболеваний -COPD-, гиперреактивности дыхательных путей, кашля), кожных нарушений и зуда или чесотки (например атонического дерматита и кожных волдырей, и красного дермографизма), нейрогенного воспаления и расстройств ЦНС (болезни Паркинсона, нарушений двигательной способности, беспокойства или страха и психоза), конвульсивных расстройств, эпилепсии, почечных расстройств, недержания мочи, глазных воспалений, воспалительных болей, расстройств приема пищи (торможение приема пищи), аллергического ринита, нейродегенеративных расстройств (например болезни Альцгеймера), псориаза, болезни Хантингтона и депрессии у млекопитающих, который включает назначение млекопитающему, нуждающемуся в таком лечении и/или профилактике, эффективного количества соединения формулы (I), определенного в п 1, или его сольвата, или соли Настоящее изобретение относится к новым производным хинолина, к способам их получения и их использованию в медицине Пептид млекопитающих Нейрокинин В (NKB) принадлежит к семейству пептида Тахикинина (ТК), которое включает также Вещество Р (SP) и Нейрокинин A (NKA) Фармакологические и молекулярно-биологические свидетельства показали существование трех подтипов ТК рецептора (NK-i, NK2 и Г\1Кз), и NKB связывается предпочтительно с ІЧКз рецептором, хотя он также распознает и другие два рецептора с более низким сродством (Maggi et al, 1993, J Auton Pharmacol , 13, 23 - 93) Известны селективные пептидные антагонисты ІЧКз рецептора (Drapeau, 1990 Regul Pept, 31, 125 - 135) и находки или открытия, связанные с пептидными антагонистами ІЧКз рецептора, предполагают, что NKB путем активирования ІЧКз рецептора играет ключевую роль в модуляции неврального входа в верхние дыхательные пути, кожу, спинной мозг и нигро-стриатальные пути (Myers and Undem, 1993, J Phisiol , 470, 665 - 679, Counture et al , 1993, Regul Peptides, 46, 426 - 429, Mccarson and Krause, 1994, J Neurosci , 14(2), 712 - 720, Arenas et al , 1991, J Neurosci , 1 1 , 2332-8) 20 Способ лечения и/или профилактики конвульсивных расстройств, эпилепсии, почечных расстройств, недержания мочи, глазных воспалений, воспалительных болей, расстройств приема пищи (торможение приема пищи), аллергического ринита, нейродегенеративных расстройств (например болезни Альцгеймера), псориаза, болезни Хантингтона и депрессии у млекопитающих, который включает назначение млекопитающему, нуждающемуся в таком лечении и/или профилактике, эффективного количества соединений формулы I по п 1 как непептидных антагонистов ІЧКз рецептора Однако, пептидно-подобный характер известных антагонистов заставляет их, вероятно, быть слишком лабильными с метаболической точки зрения, чтобы служить в качестве практических терапевтических агентов В настоящее время изобретатели обнаружили новый класс селективных не-пептидных ІЧКз антагонистов, которые являются гораздо более стабильными с метаболической точки зрения, чем известные пептидные антагонисты ІЧКз рецептора, и представляют потенциальную терапевтическую полезность или применимость при лечении легочных расстройств (астмы, хронических обструктивных легочных заболеваний -COPD-, гиперреактивности дыхательных путей, кашля), кожных нарушений и зуда или чесотки (например, атонического дерматита и кожных волдырей и красного дермографизма), нейрогенного воспаления и расстройств ЦНС (болезни Паркинсона, нарушений двигательной способности, беспокойства или страха и психоза) Данные расстройства или нарушения далее здесь называют первичными нарушениями или расстройствами Новые антагонисты МКз настоящего изобретения представляют также потенциальную тера 12 11 51623 певтическую полезность при лечении конвульсивв которой V и Vi представляют независимо ных расстройств (например, эпилепсии), почечных водород или кислород, и и представляет 0, 1 или расстройств, недержания мочи, глазных воспале2, -0(CH2)s-0W, в которой s представляет 2, 3 или ний, воспалительных болей, расстройств приема 4, и W представляет водород или Сі є алкил, гидпищи (торможения приема пищи), аллергического роксиалкил, аминоалкил, моноили диринита, нейродегенеративных расстройств (наалкиламиноалкил, ациламино, алкилсульфонилапример, болезни Альцгеймера), псориаза, болезни мино, аминоациламино, моно или диХантингтона и депрессии (далее называемых алкиламиноациламино, причем в хинолиновом здесь вторичными нарушениями) ядре присутствует до четырех R3 заместителей, или R4 представляет группу -(Cbbjt, когда он цикСогласно настоящему изобретению предослизован с R5 в виде арила, в которой t представтавляются соединения, или их сольваты, или соли ляет 1, 2 или 3, формулы (I) Rs представляет линейный или разветвленный С-і є алкил, Сз 7 циклоалкил, C^i циклоалкилалкил, необязательно замещенный арил или (I) необязательно замещенную одинарную или сконденсированную кольцевую гетероциклическую группу, имеющую ароматический характер, содержащую от 5 до 12 кольцевых атомов и вклюв которой чающую до четырех гетеро-атомов в кольце или в Аг представляет необязательно замещенную каждом кольце, выбранных из S, О, N, фенильную, нафтильную или Cs і циклоалкдиеX представляет О, S или N-C^N нильную группу или необязательно замещенную Примерами Аг являются фенил, необязательодинарную или сконденсированную кольцевую но замещенный гидрокси, галогеном, Сі є алкокси гетероциклическую группу, имеющую ароматичеили Сі є алкилом Примерами галогена являются ский характер, содержащую от 5 до 12 кольцевых хлор и фтор, примером Сі є алкокси является меатомов и включающую до четырех гетеро-атомов токси, и примером Сі є алкила - метил в кольце или в каждом кольце, выбранных из S, О, N, Примерами Аг как гетероциклической группы являются тиенил и пиридил R представляет линейный или разветвленный Примерами Аг как Cs і циклоалкдиенильной Сі в алкил, Сз-7 циклоалкил, С^і циклоалкилалкил, группы является циклогексадиенил необязательно замещенный фенил или фенил Сі Примерами R являются следующие є алкил, необязательно замещенное пятичленное гетероа ром этическое кольцо, включающее до чеСі в алкил метил, этил, n-пропил, изопропил, тырех гетеро-атомов, выбранных из О и N, гидроп-бутил, гептил, кси Сі є алкил, амино Сі є алкил, Сі є алкиламинофенил Сі б алкил бензил, алкил, ди Сі є алкиламиноалкил, Сі є гидрокси Сі б алкил -СН2ОН, -CH2CH2OH, ациламиноалкил, Сі є алкоксиалкил, Сі є алкилСН(Ме)ОН, карбонил, карбокси, Сі є алкоксикарбонил, Сі є амино Сі є алкил -CH2NH2, алкоксикарбонил-Сі є алкил, аминокарбонил, Сі є ди Сі є алкиламиноалкил -СНгЫМег, алкиламинокарбонил, ди С-і є алкиламинокарбоСі є алкоксиалкил -СЬЬОМе, нил, галоид Сі є алкил, или представляет группу Сі є алкилкарбонил СОМе, (Cbbjp-, когда он циклизован с Аг, где р представСі є алкоксикарбонил СООМе, ляет 2 или 3 Сі є алкоксикарбонил Сі є алкил СЬЬСООМе, Сі є алкиламинокарбонил CONHMe, R3 и R2, которые могут быть одинаковыми или ди С-і є алкиламинокарбонил CONMe2, CO(1различными, представляют независимо водород пирролидинил), или Сі є линейный или разветвленный алкил, или вместе образуют группу -(Cbbjn, в которой п предгалоген Сі є алкил трифторметил, ставляет 3, 4 или 5, или Ri вместе с R образует когда циклизован с Аг группу -(Cbbjq, в которой q представляет 2, 3, 4 или 5 R3 и F?4, которые могут быть одинаковыми или различными, представляют независимо водород, С-і є линейный или разветвленный алкил, Сгє алПримером Ri и R2 в виде Сі є алкила является кенил, арил, Сі є алкокси, гидрокси, галоген, нитро, метил, примером Ri вместе с R, образующими циано, карбокси, карбоксамидо, сульфонамидо, группу -(CH 2 ) q , является спироциклопентан Сі є алкоксикарбонил, трифторметил, ацилокси, Примерами R3 и R4 являются метил, этил, пфталимидо, амино, моно- или ди-Сі є алкиламино, пропил, п-бутил, метокси, гидрокси, амино, хлор, -O(CH2)r-NT2, в которой г представляет 2, 3 или 4, фтор, бром, ацетилокси, 2-(диметиламино)этокси, и Т представляет водород или Сі є алкил, или он 2-(1-фталоил)этокси, аминоэтокси, 2-(1образует с соседним азотом группу пирролидинил)этокси, фталоил, диметиламинопропокси, диметиламиноацетиламино, ацетиламино, диметиламинометил и фенил Примерами Rs являются циклогексил, фенил, необязательно замещенный, как это определено выше для Аг, примерами Rs в виде гетероциклической группы являются фурил, тиенил, пиррил, 13 14 мацевтически приемлемой или по существу чистой форме Под фармацевтически приемлемой формой соединений имеются в виду, наряду с другими, соединения фармацевтически приемлемого уровня чистоты, исключая обычные фармацевтические добавки, такие как разбавители и носители, и не включающие вещества, считающиеся токсичными при обычных дозировочных уровнях По существу чистая форма обычно содержит, по крайней мере, 50% (исключая обычные фармацевтические добавки), предпочтительно 75%, более предпочтительно 90% и еще более предпочтительно 95% соединения формулы (I) или его соли или сольвата Одну из предпочтительных фармацевтически приемлемых форм составляет кристаллическая форма, включая такую форму в фармацевтической композиции В случае солей и сольватов дополнительные части ионная и растворителя также должны быть нетоксичными 51623 тиазолил, бензофурил и пиридил Предпочтительной группой соединений формулы (I) являются соединения, в которых Аг представляет фенил, необязательно замещенный Сі є алкилом или галогеном, тиенил или Сб 7 циклоалкдиенильную группу, R представляет Сі є алкил, Сі є алкоксикарбонил, Сі є ал кил карбон ил, гидрокси Сі є алкил, Ri и R2 представляют каждый водород или Сі є алкил, R3 представляет водород, гидрокси, галоген, Сі є алкокси, Сі є алкил, R4 представляет водород, Сі є алкил, Сі є алкокси, гидрокси, амино, галоген, аминоалкокси, моно- или ди-алкиламиноалкокси, моно- или диалкиламиноалкил, фталоилалкокси, моно- или диалкиламиноациламино и ациламино, Rs представляет фенил, тиенил, фурил, пиррил и тиазолил Дополнительную предпочтительную группу соединений формулы (I) составляют соединения, в которых Аг представляет фенил, 2-хлорфенил, 2тиенил или циклогексадиенил, R представляет метил, этил, п-пропил, СООМе, -СОМе, Ri и R2 каждый представляет водород или метил, R3 представляет водород, метокси или гидрокси, R4 представляет водород, метил, этил, метокси, гидрокси, амино, хлор, бром, диметиламиноэтокси, 2-(1-фталоил)этокси, аминоэтокси, 2-(1пирролидинил)этокси, диметиламинопропокси, диметиламиноацетиламино, ацетиламино и диметиламинометил, Rs представляет фенил, 2-тиенил, 2-фурил, 2пиррил, 2-тиазолил и 3-тиенил, и X представляет кислород Предпочтительную подгруппу соединений в объеме формулы (I), представленной выше, составляют соединения формулы (1а) Примеры фармацевтически приемлемых солей соединения формулы (I) включают кислотноаддитивные соли с обычными фармацевтическими кислотами, например, малеиновой, соляной, бромиетоводородной, фосфорной, уксусной, фумаровой, салициловой, лимонной, молочной, миндальной, винной, янтарной, бензойной, аскорбиновой кислотами и метансульфоновой кислотой Примеры фармацевтически приемлемых сольватов соединения формулы (I) включают гидраты Соединения формулы (I) могут иметь, по крайней мере, один асимметрический центр и поэтому могут существовать в более, чем одной, стереоизомерной форме Данное изобретение охватывает все такие формы и их смеси, включая рацематы Данное изобретение предоставляет также способ получения соединений формулы (I), который включает реакцию соединения формулы (III) ^ Ра la) в которой R, R2, R3 и R4 имеют значения, определенные для формулы (I), и Y и Z, которые могут быть одинаковыми или различными, каждый представляет Аг, как он определен для формулы (I) Особенно предпочтительной группой соединений формулы (la) являются соединения формулы (Ib), в которой группа R ориентирована в направлении вниз, и Н - вверх (III) в которой R', R'i, R^ и Аг' представляют R, Ri, R2 и Аг, как они определены для формулы (I), или группу или атом, способные превращаться в R, Ri, R2, и Аг, с соединением формулы (II) (II) или его активным производным, в которой R'a, R'4, R's и X' представляют R3, R4, Rs и X, как они определены для формулы (I), или группу способную превращаться в R3, R4, Rs и X, с получением соединения формулы (Ic) (Ib) ІС) Соединения формулы (I) или их соли или сольваты представлены предпочтительно в фар 16 15 51623 и необязательное выполнение после этого гидрокси-бензотриазоловый эфир, или карбокси одной или более из следующих стадий группа может активироваться с использованием карбодиимида или г\І,г\Г-карбонилдиимидазола (a) когда R', R'i - R'5, Ar' и X' являются иными, чем R, Ri - R5, Аг и X, превращение любого одного Например, согласно стандартным методам, 1 і из R', R-і -R5', Аг и X в R, Ri - R5, Аг и X с получехорошо известным специалистам в данной обласнием соединения формулы (I), ти, соединения формулы (III) могут сочетаться і (b) когда R', R'i - R'5 Ar' и X представляют R, (a) с хлорангидридом кислоты в присутствии Ri - R5, Ar и X, превращение любого одного из R, неорганического или органического основания в Ri - R5, Ar и X в иной R, Ri - R5, Ar и X с получеподходящем апротонном растворителе, таком как нием соединения формулы (I), диметилформамид (DMF или ДМФ), при температуре в интервале от -70 до 50°С (предпочтительно (c) образование соли и/или сольвата полученв интервале от -10 до 20°С), ного соединения формулы (Ic) Подходящими активными производными со(b) с кислотой в присутствии подходящего единений формулы (II) являются галоидангидриды конденсирующего агента, такого как, например, кислот (предпочтительно хлорангидриды), азиды г\І,г\Г-карбонилдиимидазол (GDI) или карбодиимид, кислот или ангидриды кислот Еще одним подхотакой как дициклогексилкарбодиимид (DCC) или дящим производным является смешанный ангидг\1-диметиламинопропил-г\Г-этилкарбодиимид и Nрид, образованный между кислотой и алкилхлоргидроксибензотриазол (НОВТ), для достижения формиатом, еще одним подходящим производным максимальных выходов и для того, чтобы избеявляется активированный сложный эфир, такой жать процессов рацемизации (Synthesis, 453, как цианометиловый, тиофениловый, п1972) в апротонном растворителе, таком как смесь нитрофениловый, n-нитротиофениловый эфиры, ацетонитрила (MeCN) и тетрагидрофурана (TGF 2,4,6-трихлорфениловый эфир, пентахлорфениили ТГФ) в соотношении от 1 9 до 7 3 соответстловый, пентафторфениловый эфиры, N-гидроксивенно, при температуре в интервале от -70 до фталимидо эфир, N-гидроксипиперидиновый 50°С (предпочтительно в интервале от -10 до эфир, N- гидроксисукцинимидный эфир, N25°С) (смотри Схему 1) Схема 1 СООШ (Г > ...рос, новт e (НІ) (с) со смешанным ангидридом, получаемым на месте (инситу) из кислоты и алкил (например, изопропил)хлорформиата в подходящем апротонном растворителе, таком как дихлорметан, при температуре в интервале от -70 до 50°С (предпочтительно в интервале от -20 до 20°С) Очевидно, понятно, что соединение формулы (Ic) может превращаться в соединение формулы (I), или одно соединение формулы (I) может превращаться в другое соединение формулы (I) с помощью взаимопревращений подходящих ваместителей Таким образом, некоторые соединения формулы (I) и (Ic) являются полезными промежуточными соединениями при образовании других соединений настоящего изобретения Например, R^ может представлять водород и превращаться в R2 алкильную группу, например, метильную, с помощью общепринятых процедур амидного алкилирования (Zabicky, The chemistry of amides, Interscience, London, 1970, стр 749) Когда Xі представляет кислород, он может превращаться в X серу с помощью стандартных реагентов образования тиоамидов, таких как P2S5 (Chem Rev, 61, 45, 1961 или Angew Chem, 78, 517, 1966) или реагент Lawesson (Tetrahedron, 41, 5061, 1985) Когда Ar' или R's представляет метокси-замещенный фенил, он может превращаться в иной А'г или R'5 гидрокси-замещенный фенил с помощью стандартных приемов деметилирова 0-20-C ния с использованием кислот Льюиса, таких как трехбромистый бор (Synthesis, 249, 1983), или минеральных кислот, таких как бромистоводородная или иодистоводородная кислота Когда R представляет алкоксикарбонильную группу, например, метоксикарбонильную, он может превращаться в иной R, такой как этоксикарбонил с помощью сложной транеэтерификации соответствующим спиртом при температуре в интервале от 0 до 120°С, карбокси с помощью гидролиза в кислой или основной среде, аминокарбонил, алкиламинокарбонил или диалкиламинокарбонил с помощью трансамидирования аммиаком, первичным амином или вторичным амином в метаноле в качестве растворителя при температуре в интервале от 10 до 120°С, необязательно в присутствии каталитического количества NaCN (J Org Chem, 52, 2033, 1987) или с помощью использования триметилалюминия (Ме3А1) ("Tetrahedron Letters, 48, 4171, 1977), гидроксиметил с помощью селективного восстановления гидридом металла, такого как восстановление боргидридом лития (Tetrahedron, 35, 567, 1979) или восстановление боргидридом натрия в смеси ТГФ + МеОН (Bull Chem See Japan, 57, 1948, 1984 или Syntn Commun , 12, 463, 1982), алкилкарбонил - с помощью образования ацилхлорида и последующей реакции с алкилмагнийгалогенидами в ТГФ в качестве растворителя при 17 51623 18 температуре в интервале от -78 до 30°С кольцо, такое как оксадиазол (J Med, Chem , 34, (Tetrahedron Letters, 4303, 1979) или с алкилкад2726, 1991) мийгалогенидами или диал кил кадмием в присутСхема 2 суммирует некоторые из описанных ствии МдСЬ или хлорида лития (J Qrg Chem , 47 выше приемов превращения соединения форму2590, 1982), Еще одна группа R' как метоксикарлы (Ic) или (І), в которой X' представляет кислобонил может превращаться в замещенное гетерород, R' представляет СООМе, Аг' и R'I-R'S имеют циклическое кольцо, такое как оксадиазол (J Med значения, описанные для формулы (І), в другое Chem , 34 2726, 1991), гетероа ром этическое соединение формулы (I) Схема 2 „ f* C O e OM «%^ІЧ Соединения формулы (І) могут превращаться в их фармацевтически приемлемые кислотноаддитивные соли с помощью реакции с подходящими или соответствующими органическими или минеральными кислотами Сольваты соединений формулы (I) могут образовываться с помощью кристаллизации или перекристаллизации из соответствующего растворителя Например, гидраты могут получаться с помощью кристаллизации или перекристаллизации из водных растворов, или растворов в органических растворителях, содержащих воду Соли или сольваты соединений формулы (I), которые не являются фармацевтически приемлемыми, также могут быть полезными в качестве промежуточных соединений при получении фармацевтически приемлемых солей и сольватов Соответственно такие соли и сольваты также составляют часть данного изобретения Как упоминалось выше, соединения формулы (I) могут существовать в более, чем одной, стереоизомерной форме, и процесс данного изобретения может давать рацематы также, как и энантиомерно чистые формы Для получения чистых энантиомеров соответствующие энантиомерно чистые первичные или вторичные амины формулы (Hid) или (Hie) R. Н' R\ and) подвергаются реакции с соединениями формулы (II) с получением соединений формулы (I'd) или (Ге) В', R', Xі. Соединения формулы (I'd) или (Ге) могут впоследствии превращаться в соединения формулы (Id) или (1е) с помощью методов превращения, упомянутых выше 51623 20 дихлорфенил, п-метоксифенил, описываются в работе Nicolai et al , Eur J Med Chem , 27, 977, 1992, соединения формулы (II), в которой X представляет кислород, R'3 представляет 6-бром, R\ представляет водород и R's представляет фенил или п-фторфенил, описываются в работе Nicolai et al , Eur J Med Chem, 27, 977, 1992, другие соединения формулы (II) описываются в немецкой выложенной заявке DE 3721222 и в европейской (Id) fle) патентной заявке ЕР 384313 Соединения формулы (II) являются известными или могут получаться из известных соединений Соединения формул (III), (Hid) и (Ше) являются с помощью известных способов промышленно доступными соединениями или моНапример, соединение формулы (II), в котогут быть получены из известных соединений с рой X' представляет кислород, R's, R'4 и R's предпомощью известных способов (например, соедиставляют водород, описано в работе Pfitzmger, J нения формулы (III), в которой R' представляет Prakt Chem , 38, 582, 1882 и в работе Pfitzmger, J ал кокси карбон ил, Ri и R'2 представляют водород Prakt Chem , 56, 293, 1897, соединение формулы и Аг' имеет значения, определенные для соедине(II), в которой X' представляет кислород, R's и R\ ний формулы (I), описываются в Liebigs Ann der представляют водород и R's представляет 2Chemie, 523, 199, 1936) пиридил, описано в работе Risahti, Ric Scient, 28, Активность соединений формулы (І) в качест561, 1958, соединения формулы (II), в которой X ве антагонистов ІЧКз рецептора в стандартных представляет кислород, R'3 и R\ представляют испытаниях указывает на то, что они имеют поводород, и R's представляет о-, м- и п-хлорфенил, тенциальную терапевтическую полезность при о-фторфенил и 3,4-дихлорфенил, описаны в раболечении как первичных, так и вторичных расте Brown et al J Am Chem Soo , 68, 2705, 1946, стройств, на которые здесь ранее давалась ссылсоединение формулы (II), в которой X представка Обнаружение того, что антагонисты ІЧКз рецепляет кислород, R'3 и R'4 представляют водород, и тора представляют потенциальную R's представляет, п-метоксифенил, терапевтическую полезность при лечении вторичных расстройств, является новым, и в соответстописано в работе Ciusa и Luzzatto, Gazz Chim вии со следующим аспектом настоящего изобреItal , 44, 64, 1914, соединение формулы (II), в котения предоставляется использование торой X представляет кислород, R'a и R\ предантагонистов ІЧКз рецептора при лечении вторичставляют водород, и R's представляет мных расстройств Предоставляется также испольтрифторметилфенил, описано в работе Shargier и зование антагонистов ІЧКз рецептора при произLalezan, J Chem Eng Data, 8, 276, 1963, соединеводстве медикаментов для лечения любого из ние формулы (II), в которой X представляет кивторичных расстройств слород, R's и R'4 представляют водород, и R's представляет п-фторфенил, описано в работе Ви Настоящее изобретение также предоставляет Hoi et al , Rec Trav Chim , 68, 781, 1949, соединесоединения формулы (I) или их фармацевтически ние формулы (II), в которой X представляет киприемлемые соли или сольваты для использоваслород, R'3 и R'4 представляют водород, и R's ния в качестве активных терапевтических вепредставляет п-метилфенил, описано в работе ществ Prevost et al , Compt Rend, Acad Sci , 258, 954, Настоящее изобретение далее предоставляет 1964, соединение формулы (II), в которой X предфармацевтические композиции, включающие составляет кислород, R'3 и R'4 представляют водоединение формулы (I) или его фармацевтически род, и R's представляет п-бромфенил, описано в приемлемую соль или сольват и фармацевтически работе Nicolai et al , Eur J Med Chem , 27, 977, приемлемый носитель 1992, соединение формулы (II), в которой X предНастоящее изобретение предоставляет также ставляет кислород, R'4 и R's представляют водоиспользование соединений формулы (I) или их род, и R'3 представляет 6-метил, описано в работе фармацевтически приемлемых солей или сольваBuchmann and Howton, J Am Chem Soc, 68, тов в производстве медикаментов для лечения 2718, 1946, соединение формулы (II), в которой X первичных и вторичных расстройств представляет кислород, R\ и R's представляют Такие медикаменты и композиции данного водород, и R'3 представляет 8-нитро, описано в изобретения могут быть получены с помощью работе Buchmann et al, J Am Chem Soc , 69, 380, смешения соединения изобретения с соответст1947, соединение формулы (II), в которой X предвующим носителем Они могут содержать общеставляет кислород, R'4 представляет водород, R's принятые разбавители, связующие, наполнители, представляет 6-хлор, R's представляет пдезинтегрирующие агенты, вкусовые или аромахлорфенил, описано в работе Lutz et al , J Am тизирующие агенты, красящие агенты, смазочные Chem Soc, 68, 1813, 1946, соединение формулы или консервирующие агенты (II), в которой X представляет кислород, R'3 и R\ Данные общепринятые эксципиенты являются представляют водород, и R's представляет 2такими, как те, что могут применяться, например, тиазолил, описано в европейской патентной заявпри получении композиций с известными агентами ке ЕР 112776, соединения формулы (II), в которой для лечения указанных состояний X представляет кислород, R'3 представляет 8трифторметил, R'4 представляет водород и R's Предпочтительно фармацевтическая компопредставляет фенил, о- и п-фторфенил, 3,4зиция изобретения находится в форме единичной дозы и в форме, приемлемой для использования в 22 21 51623 медицинской или ветеринарной областях Наприпредставлены в виде сухого продукта, предназнамер, такие препараты могут быть в упакованной ченного для реконституирования с водой или друформе, сопровождаемой написанными или отпегим подходящим носителем перед использованичатанными инструкциями по использованию в каем Такие жидкие композиции могут содержать честве агента при лечении указанных состояний обычные добавки, такие как суспендирующие агенты, например, сорбит, сироп, метилцеллюлоИнтервал подходящих доз для соединений зу, желатин, гидроксиэтилцеллюлозу, карбоксимеизобретения зависит от применяемого соединения тилцеллюлозу, алюминийстеаратный гель, гидрии от состояния пациента Он зависит также от свярованные съедобные жиры, эмульгирующие зи активности или силы действия и способности к агенты, например, лецитин, сорбитанмоноолеат поглощению и частоты и способа назначения к или камеди акации, водные или неводные носитеприему препарата ли, которые включают съедобные масла, наприСоединение или композиция изобретения момер, миндальное масло, фракционированное гут быть изготовлены в виде препаративной формасло кокосовых орехов, масляные сложные эфимы для назначения любым способом, и предпочры, например, сложные эфиры глицерина или тительно в форме единичной дозы или в форме, пропиленгликоля или этиловый спирт, глицерин, которую человек может сам принять в виде дозы воду или обычный физиологический или солевой на один прием Композиция с успехом может быть раствор, консервирующие агенты, например, мев форме, подходящей для орального, ректальнотил- или пропил-п-гидроксибензоат или аскорбиго, топического или местного, парентерального, новую кислоту, и, при желании, общепринятые внутривенного или внутримышечного приема вкусовые или красящие агенты Препараты могут производиться таким образом, чтобы обеспечивать медленное высвобождение Композиции данного изобретения могут также активного ингредиента назначаться для приема неоральным способом В соответствии с обычными фармацевтическими Композиции могут быть, например, в форме процедурами, композиции могут формироваться таблеток, капсул, саше, флаконов или пробирок, для ректального назначения в виде медицинских порошков, гранул, лепешек, реконструируемых свечей Они могут также формироваться или соили пересоставляемых порошков или жидких преставляться для представления в инъецируемой паратов, например, растворов или суспензий, или форме в водном или неводном растворе, суспенв форме медицинских свечей или суппозиторий зии или эмульсии в фармацевтически приемлемой Композиции, например, те, что являются поджидкости, например, стерильной, свободной от ходящими для орального назначения, могут сопирогенов воде или в парентерально приемлемом держать общепринятые эксципиенты, такие как масле или смеси жидкостей Жидкость может сосвязующие агенты, например, сироп, камедь акадержать антибактериальные агенты, антиоксиданции, желатин, сорбит, трагакант или поливинилти или другие предохраняющие агенты, буферы пиррол идон, наполнители, например, лактозу, или растворенные вещества для придания рассахар, кукурузный крахмал, фосфат кальция, сортвору изотоничности по отношению к крови, загубит или глицин, таблеточные смазочные агенты, щающие агенты, суспендирующие агенты или друнапример, стеарат магния, дезинтегрирующие гие фармацевтически приемлемые добавки Такие агенты, например, крахмал, поливинилформы представляются в форме единичной дозы, пиррол идон, натрийкрахмалгликолят или микротакой как ампулы или разовые изделия для инъкристаллическую целлюлозу, или фармацевтичеекций или в форме многих доз, таких как бутылочски приемлемые агенты для застывания, такие как ка или флакон, из которых может быть взята соотлаурилсульфат натрия ветствующая доза, или твердая форма или Твердые композиции могут получаться с поконцентрат, которые могут использоваться для мощью общепринятых методов смешения, заполприготовления инъецируемых готовых форм нения, таблетирования или аналогичных Повторные операции смешения могут использоваться Соединения данного изобретения могут также для распределения или распространения активноназначаться с помощью ингаляции через нос или го агента в тех композициях, в которых применярот Такой прием лекарства может осуществлятьются огромные количества наполнителей Когда ся с помощью готовой формы в виде спрея, вклюкомпозиция находится в форме таблетки, порошка чающего соединение изобретения и подходящий или лепешки, может использоваться любой носиноситель, необязательно суспендированные, натель, подходящий для образования твердых фарпример, в углеводородном реактивном топливном мацевтических композиций, причем, примерами веществе являются стеарат магния, крахмал, глюкоза, лакПредпочтительные готовые формы в виде тоза, сахароза, рисовая мука и мел Таблетки моспрея включают мельчайшие (микронизировангут покрываться в соответствии со способами, ные) частицы соединения в сочетании с поверхнохорошо известными в обычной фармацевтической стно-активным агентом, растворителем или диспрактике, в частности энтерическим покрытием пергирующим агентом для предотвращения Композиция может быть также в форме проглатыоседания суспендированных частиц Размер часваемой капсулы, например, из желатинтиц соединения составляет предпочтительно присодержащего соединения, при желании, с носитемерно от 2 до 10 микрон лем или другими эксципиентами Дополнительный способ назначения соединеКомпозиции для орального назначения в виде ний изобретения включает трансдермальную досжидкостей могут быть в форме, например, эмультавку с использованием готовой формы препарата сий, сиропов или элекси-ров, или они могут быть в виде накожного пластыря Предпочтительная 24 23 51623 готовая препаративная форма включает соединесоединения Примеров 22, 47, 48 и 85 показывают ние изобретения, диспергированное в чувствиK,S (нМ) соответственно 5 6, 8 8, 1 2 0 и 4 8 (п=3) тельном к давлению адгезиве, который прилипает І\ІКз-антагонистическая активность соединений к коже, позволяя тем самым соединению диффунастоящего изобретения определяется по их спозировать из адгезива через кожу для доставки собности ингибировать вызванное сенктидом сопациенту Для постоянной степени или скорости кращение подвздошной кишки морской свинки абсорбции через кожу могут использоваться чув(Maggi et al, 1990, Br J, Pharmacol, 101, 996 ствительные к давлению адгезивы, известные в 1000) и изолированной сфинктерной мышцы раданной области техники, такие как природный каудужной оболочки кролика (Hall et al , 1991, Eur J чук или силикон Pharmacol , 199, 9 - 14) и опосредуемую ІЧКз++ рецепторами Са мобилизацию (Mochizuki et al , Как упоминалось выше, эффективная доза 1994, J Biol Chern , 269 9651 - 9658) Функциосоединения зависит от конкретно применяемого нальные анализы ин-витро на морских свинках и соединения, от состояния пациента и от частоты и на кроликах дают для каждого испытываемого способа назначения Единичная доза обычно сосоединения среднюю величину Кв от 3 - 8 отдельдержит от 20 до 1000мг, и предпочтительно от 30 ных экспериментов, где Кв представляет концендо 500мг, в частности 50, 100, 150, 200, 250, 300, трацию индивидуального соединения, необходи350, 400, 450 или 500мг Композиция может намую для получения 2-кратного сдвига вправо на значаться для приема один или более раз в сутки, кривой сенктида концентрация-ответная реакция например, 2, 3 или 4 раза в день, и общая дневная Функциональный анализ с рецепторами человека доза для взрослого человека весом 70кг обычно позволяет определить концентрацию индивидусоставляет в интервале от 100 до 3000мг Альтерального соединения, необходимую для уменьшенативно единичная доза содержит от 2 до 20мг ния на 50% (величины IC50) Ca ++ мобилизации, активного ингредиента и принимается многократиндуцируемой антагонистом NKB В данном анано, если необходимо, чтобы дать указанную дневлизе соединения настоящего изобретения ведут ную дозу себя как антагонисты В случае соединений изобретения, когда они принимаются в соответствии с изобретением, не Терапевтический потенциал соединений наожидается никаких неприемлемых токсикологичестоящего изобретения при лечении указанных ских эффектов состояний может быть оценен с использованием моделей заболевания на грызунах Настоящее изобретение также предоставляет способ лечения и/или профилактики первичных и Следующие ниже Описания иллюстрируют вторичных расстройств у млекопитающих, в частполучение промежуточных соединений, тогда как ности людей, который включает назначение млеПримеры иллюстрируют получение соединений копитающему, нуждающемуся в таком лечении настоящего изобретения Соединения приведени/или профилактике, эффективного количества ных примеров представлены в Таблицах 1-6 соединения формулы (I) или его фармацевтически ОПИСАНИЕ 1 приемлемой соли или сольвата Хлорангидрид 2-фенилхинолин-4-карбоновой кислоты 11,7мл (136,3ммоля) оксалилхлорида Изобретение далее предоставляет способ лерастворялось в 150мл метиленхлорида Раствор чения и/или профилактики вторичных расстройств охлаждался при -10°С, и порциями добавлялось у млекопитающих, особенно людей, который 20г (80,2ммоля) промышленно доступной 2включает назначение млекопитающему, нуждаюфенил-хинолин-4-карбоновой кислоты Реакционщемуся в таком лечении и/или профилактике, ная смесь оставлялась на ночь при комнатной эффективного количества антагониста ІЧКз рецептемпературе, а затем выпаривалась досуха, давая тора 22г указанного в заголовке соединения, испольАктивность соединений настоящего изобретезуемого без дальнейшей очистки ния в качестве лигандов ІЧКз определяется по их способности ингибировать связывание радиоакCi 6 Hi 0 CINO тивно меченых лигандов ІЧКз, [1251] - [Ме-Рпе7]М В =267,76 NKB или [3Н]-Сенктида, с ІЧКз рецепторами морОписание 2 ских свинок и человека (Renzetti et al , 1991 Neu7-метокси-2-фенилхинолин-4-карбоновая киropeptide, 18, 104 - 114, Buell et al, 1992 FEBS, слота 5г (28,2ммоля) 6-метоксиизатина, 4мл 299(1), 90-95, Chung etal, 1994, Biochem Biophys (33,8ммоля) ацетофенона и 5,2г (92,6ммоля) гидRes Commun , 198(3), 967-972) Используемые роокиси калия растворялось в 22,9мл абсолютноанализы связывания позволяют определить конго этанола, и суспензия нагревалась при 80°С в центрацию отдельного соединения, требуемую течение 42 часов После охлаждения реакционной для снижения на 50% специфического связывания смеси добавлялось 50мл воды, и раствор экстра[i25l]-[Me-Phe7]-NKB и [3Н]-Сенктида с NK3 рецепгировался 50мл-ми диэтилового эфира Охлажтором в условиях равновесия (ICso) Анализы свяденная льдом водная фаза подкислялась до рН 1с зывания дают для каждого испытанного соединепомощью 37% HCI, и осадок собирался фильтрония среднюю величину ICso от 2 - 5 отдельных ванием и промывался водой Полученное твердое экспериментов, выполненных с двукратным или вещество сушилось в вакууме при 40°С, давая трехкратным повторением Наиболее активные 7,0г указанного в заголовке соединения соединения настоящего изобретения показывают C17H13NO3 величины ICso в интервале 1 - ЮООнМ, в частноТ пл = 226 - 228°С сти, в опыте с корой головного мозга морских свиМ В - 279,30 нок с замещением (вытеснением) [3Н]-Сенктида Элементный анализ 25 51623 26 Вычислено С 7311, Н 4 69, N5 01 Описание 7 Найдено С 72 07, Н 4 59, N 4 90 Хлорангидрид 2-(2-фурил)хинолин-41 карбоновой кислоты ИК(КВг) 3420, 1630см Описание 3 5,2мл (60,4ммоля) оксалилхлорида растворялось в 70мл метиленхлорида Раствор охлаждалХлорангидрид 7-метокси-2-фенилхинолин-4ся при -10°С, и порциями добавлялось 8,5г карбоновой кислоты (35,5ммолей) 2-(2-фурил)хинолин-4-карбоно-вой 2,8мл (32,3ммоля) оксалилхлорида растворякислоты Реакционная смесь оставлялась на ночь лось в 60мл метиленхлорида Раствор охлаждалпри комнатной температуре, а затем выпаривася при -10°С, и порциями добавлялось 6г лась досуха, давая 9,2г указанного в заголовке (19,0ммолей) 7-метокси-2-фенилхинолин-4соединения, используемого без дальнейшей очикарбоновой кислоты Реакционная смесь оставлястки лась на ночь при комнатной температуре , а затем выпаривалась досуха, давая 7г указанного в загоCi4H8CINO2 ловке соединения, используемого без дальнейшей М В = 257,78 очистки Описание 8 Ci 7 Hi 2 CINO 2 M В -297,74 Хлорангидрид 2-(4-пиридил)хинолин-4Описание 4 карбоновой кислоты Гидроиодид 7-гидрокси-2-фенилхинолин-45г (34,0ммоля) изатина, 4,5мл (40,8ммоля) 4карбоновой кислоты ацетил-пиридина и 6,3г (112,2ммоля) гидроокиси калия растворялось в 40мл абсолютного этанола, 1,5г (5,4ммоля) 7-метокси-2-фенилхинолин-4и суспензия нагревалась при 80°С в течение 12 карбоновой кислоты добавлялось порциями к часов После охлаждения реакционной смеси до50мл 57% водного HI Реакционная смесь нагребавлялось 50мл воды, и раствор экстрагировался валась с обратным холодильником и энергично 50мл-ми диэтилового эфира Охлажденная льдом перемешивалась в течение 5 часов, затем она водная фаза подкислялась до рН 1 с помощью выпаривалась в вакууме досуха, давая 2,1 г ука37% HCI, и осадок собирался фильтрованием и занного в заголовке соединения промывался водой C 16 HnNO 3 HI Водный раствор выпаривался в вакууме досуМ В =393,17 ха, остаток растирался с этанолом и отфильтроИК(КВг) 3120, 1650, 1620см 1 вывался Выпаривание растворителя давало 6,0г Описание 5 сырого указанного в заголовке соединения Дан2-(2-тиенил)хинолин-4-карбоновая кислота 5г ный продукт объединялся с полученным ранее (34,0ммоля) изатина, 4,4мл (40,8ммоля) 2-ацетилосадком и перекристаллизовывался из толуола, тиофена и 6,3г (112,2ммоля) гидроокиси калия содержащего следы метанола, давая 4,5г указанрастворялось в 40мл абсолютного этанола, и сусного в заголовке соединения пензия нагревалась при 80°С в течение 16 часов После охлаждения реакционой смеси добавляC15H10N2O2 HCI лось 50мл воды, и раствор экстрагировался 50млТпл -297-301 °С ми диэтилового эфира Охлажденная льдом водМ В = 286,72 ная фаза подкислялась до рН 1 с помощью 37% ИК(КВг) 1705, 1635, 1610см 1 HCI, и осадок собирался фильтрованием и промы300МГц 1Н-НМР (flMCO-d6) 5 8,90 (д , 2Н), вался водой Полученный сырой продукт сушился 8,70 (м , 2Н), 8,50 (с , 2Н), 8,28 (д , 1Н), 7,89 (дт , в вакууме при 40°С и растирался с зтилацетатом, 2Н) давая 4,8г указанного в заголовке соединения ОПИСАНИЕ 9 Ci 4 H 9 NO 2 S Хлоргидрат хлорангидрида 2-(4Тпл = 181 -183°С пиридил)хинолин-4-карбо-новой кислоты М В = 255,29 1,3мл (10,4ммоля) оксалилхлорида растворя1 ИК(КВг) 1620см лось в 60мл метиленхлорида Раствор охлаждал300МГц 1Н-ЯМР (flMCO-d6) 5 8,60 (д , 1Н), ся при -10°С, и порциями добавлялось 3,0г (14,4 8,45 (с, 1Н), 8,10 (м , 2Н), 7,78 (м , 2Н), 7,68 (т , ммоля) хлоргидрата 2-(4-пиридил)хино-лин-41Н), 7,22 (м , 1Н) карбоновой кислоты Реакционная смесь оставлялась на 72 часа при комнатной температуре, а Описание 6 затем выпаривалась досуха, давая 4,Ог указанного 2-(2-фурил)хинолин-4-карбоновая кислота в заголовке соединения, используемого без даль5г (34,0ммоля) изатина, 4мл (40,8ммоля) 2нейшей очистки ацетилфу-рана и 6,3г (112,2ммоля) гидроокиси калия растворялись в 40,9мл абсолютного этаноCi5HgCIN2O HCI ла, и суспензия нагревалась при 80°С в течение М В = 305,22 12 часов После охлаждения реакционной смеси Пример 1 добавлялось 50мл воды, и раствор экстрагиро(Р,3)-І\І-(а-метилбензил)-2-фенилхинолин-4вался 50мл-ми диэтилового эфира Охлажденная карбоксамид 1,2мл (9,4ммоля) (R,S) aльдом водная фаза подкислялась до рН 1 с пометилбензиламина и 1,6мл (11,7ммоля) триэтимощью 37% HCI, и осадок собирался фильтроваламина (TEA) растворялось в атмосфере азота в нием и промывался водой Полученный сырой 50мл 1 1 смеси сухого метиленхлорида и СНзСІЧ продукт сушился в вакууме при 40°С, давая 8,5г К охлажденному льдом раствору аминов добавляуказанного в заголовке соединения лось по каплям 2,0г (7,8ммоля) 2-фенилхинолин-4карбонилхлорида, растворенного в 50мл 1 4 смеси Ci 4 HgNO 3 сухого метиленхлорида и ДМФ, и реакционная М В - 239,23 28 27 51623 смесь хранилась при 0-5°С в течение 1 часа и ос(R,S)-N-[a-(MeTOKCHKap6oHHn)6eH3nn]-2тавлялась на ночь при комнатной температуре фенилхинолин-4-карбоксамид Реакционная смесь выпаривалась в вакууме досу2,0г (8,0ммолей) 2-фенилхинолин-4ха, остаток растворялся в етилацетате и промыкарбоновой кислоты растворялось в атмосфере вался дважды насыщенным раствором бикарбоазота в 130мл сухого ТГФ и 100мл CH3CN Добавната натрия Органический слой отделялся, лялось 2,0г (9,9ммоля) хлоргидрата (D,L) метилсушился над сульфатом натрия, фильтровался и фенилглицианата и 1,5мл (10,7ммоля) TEA, и ревыпаривался в вакууме досуха Остаточное масло акционная смесь охлаждалась при 5°С По каплям кристаллизовалось из этилацетата, давая 1,1 г добавлялось 2,5г (12,1ммоля) дициклогексилкарцелевого соединения в виде белого твердого вебодиимида (DCC), растворенного в 10мл сухого щества метиленхлорида, и раствору давалась возможность достичь комнатной температуры, раствор C24H20N20 перемешивался в течение 5 часов и оставлялся Тпл -156-157°С на ночь Выпавшая в осадок дициклогексилмочеМ В = 352,43 вина отфильтровывалась, и раствор выпаривался Элементный анализ в вакууме досуха Остаток растворялся в метиВычислено С 81,79 Н 5,72 N7,95 ленхлориде, а затем промывался водой ОрганиНайдено С 81,99 Н 5,69 N7,89 ческий слой отделялся, сушился над сульфатом ИК(КВг) 3240, 1645см 1 натрия и выпаривался в вакууме досуха, давая 300 МГц 1Н-ЯМР (ДМСО-de) 5 9,29 (д , 1Н), 6,0г сырого продукта, который растворялся в 20мл 8,32 (д , 2Н), 8,13 (д , 1Н), 8,13 (с , 1Н), 8,06 (д , метиленхлорида и оставлялся на ночь Еще неко1Н), 7,81 (ддд , 1Н), 7,68-7,52 (м , 4Н), 7,47 (д , 2Н), торое количество дициклогексилмочевины выпа7,39 (дд , 2Н), 7,27 (дд , 1Н), 5,30 (дкв , 1Н), 1,52 дало в осадок и отфильтровывалось (Д , ЗН) МС (ЕІ, источник 200°С, 70В, 200мА) 352 (М+,), 337, 232, 204, 77 Пример 2 3-(+)-^(а-метилбензил)-2-фенилхинолин-4карбоксамид Получался, как в примере 1, из 1,2мл (9,4ммоля) 3-(-)-а-метилбензиламина, 1,6мл (11,7ммоля) TEA, 2,0г (7,8ммоля) 2фенилхинолин-4-карбонилхлорида в 100мл смеси метиленхлорида, CH3CN и ДМФ Обработка реакционной смеси осуществлялась таким же образом, как описано в примере 1 Остаточное масло кристаллизовалось из этилацетата, давая 1,1 г целевого соединения C24H20N2O Тпл = 161 -162°С М В - 352,43 [a]D20=+25(0=0,5 ДМФ) ИК (КВг) 3240, 1645см 1 300 МГц ?Н-ЯМР (ДМСО-de) 5 9,29 (д , 1Н), 8,32 (д , 2Н), 8,13 (д , 1Н), 8,13 (с , 1Н), 8,06 (д , 1Н), 7,81 (ддд , 1Н), 7,68-7,52 (м , 4Н), 7,47 (д , 2Н), 7,39 (дд 1Н), 7,27 (дд , 1Н), 5,30 (дкв, 1Н), 1,52 (Д , ЗН) МС спектр был идентичен спектру примера 1 Пример 3 R- (-)-N- (а-метилбензил)-2-фенилхинолин-4карбоксамид Получался, как в примере 1, из 1,2мл (9,4ммоля) Р-(+)-а-метилбензиламина, 1,6мл (11,7ммоля) TEA, 2,0г (7,8ммоля) 2фенилхинолин-4-карбонилхлорида в 100мл смеси метиленхлорида, CH3CN и ДМФ Обработка реакционной смеси осуществлялась таким же образом, как описано в примере 1 Остаточное масло кристаллизовалось из этилацетата, давая 1,1 г целевого соединения C24H20N2O Тпл = 158-160°С М В = 352,43 [a] D 2 0 = -25(0-0,5 ДМФ) ИК (КВг) 3240, 1645см1 Н-ЯМР и МС спектры были идентичными спектрам примеров 1 и 2 Пример 4 Раствор выпаривался в вакууме досуха, и остаток подвергался флешхроматографии на 230 400меш силикагеле, с злюированием смесью гексан/эти л ацетат 3/2, содержащей 0,5% гидроокиси аммония Полученное сырое или неочищенное твердое вещество растиралось с теплым диизопропиловым эфиром, отфильтровывалось, промывалось и сушилось, давая 1,1 г целевого соединения C25H2oN£203 Тпл -170-172°С М В - 396,45 Элементный анализ Вычислено С 75,74 Н 5,09 N 7,07 Найдено С 75,88 Н 5,12 N7,06 ИК (нуйол) 3240, 1750, 1670см 1 300МГц 1Н-ЯМР (ДМСО-de) 5 9,72 (д , 1Н), 8,28 (дд , 2Н), 8,20 (дд , 1Н), 8,13 (дд , 1Н), 8,11 (с , 1Н), 7,83 (ддд , 1Н), 7,66 (ддд , 1Н), 7,60-7,50 (м , 5Н), 7,47-7,37 (м , ЗН), 5,78 (д , 1Н), 3,72 (с , ЗН) МС (EI, источник 200°С, 70 В, 200 мА) 396 (М+ ), 337, 232, 204 Пример 5 (+)-(3)^-[а-(метоксикарбонил)бензил]-2фенилхинолин-4-карбокеамид 2,0г (8,0ммолей) 2-фенилхинолин-4карбоновой кислоты растворялось в атмосфере азота в 70мл сухого ТГФ и 30мл CH3CN Добавлялось 1,7г (8,4ммоля) хлоргидрата (L) метилфенилглицината, 1,1 мл (9,9ммоля) Nметилморфолина и 2,1мл (15,5ммолей) Nгидроксибензотриазола (НОВТ), и реакционная смесь охлаждалась при 0°С По каплям добавлялось 1 85г (9,0ммолей) DCC, растворенного в 10мл метиленхлорида, и раствор хранился при 0 5°С в течение 1 часа, а затем при комнатной температуре в течение 2 часов Выпавшая в осадок дициклогек-силмочевина отфильтровывалась , и раствор выпаривался в вакууме досуха Остаток растворялся в метиленхлориде и промывался водой, насыщенным раствором бикарбоната натрия, 5% лимонной кислотой, насыщенным раствором бикарбоната натрия и насыщенным рас 29 51623 твором хлорида натрия Органический слой отделялся, сушился над сульфатом натрия и выпаривался в вакууме досуха, остаток растворялся в 20мл метиленхлорида и оставлялся на ночь Еще некоторое количество дициклогексил мочевины выпадало в осадок и отфильтровывалось Раствор выпаривался в вакууме досуха, и получалось 2,6г сырого продукта, который растирался с петролейным эфиром, растворялся, промывался диизопропиловым эфиром, а затем перекристаллизовывался из 70мл изопропанола, давая 1,7г целевого соединения C25H20N2O3 Т ПЛ = 180 -181 °С М В - 396,45 1 ИК (нуйол) 3300, 1750, 1640см [a] D = +42 (С-0,5 метанол) Н-ЯМР и МС спектры были идентичными спектрам примера 4 Пример 6 (-)- (R)-N- [а- (метоксикарбонил) бензил]-2фенилхинолин-4-карбоксамид Получался, как в примере 5, из 2,0г (8,0 ммолей) 2-фенилхинолин-4-карбоновой кислоты, 1,7г (8,4ммоля) хлоргидрата (D) метилфенилглицината, 1,1мл (9,9 ммоля) N-метилморфолина, 2,1 г (15,5ммолей) НОВТ и 1,85г (9,0ммолей) DCC в 70мл сухого ТГФ и 30мл CH3CN Обработка реакционной смеси осуществлялась таким же образом, как описано в примере 5 Полученный сырой продукт (3,5г) растирался дважды с теплым диизопропиловым эфиром, фильтровался, промывался, а затем перекристаллизовывался из 80мл изопропанола, давая 2,3г целевого соединения C25H20N2O3 Тпл - 1 8 0 - 1 8 Г С М В - 396,45 ИК (нуйол) 3300, 1750, 1640см 1 [a] D = -42,0 (С=0,5 метанол) Н-ЯМР и МС спектры были идентичными спектрам примеров 4 и 5 Пример 7 (Р,3)-І\І-[а-(метоксикарбонил)бензил]-7метокси-2-фенилхинолин-4-карбоксамид 1,0г (5,0ммолей) хлоргидрата (D,L) метилфенилглицината растворялся в атмосфере азота в 30мл сухого ДМФ Добавлялось 2,5г (18,1ммоля) безводного карбоната калия, и раствор охлаждался до 0°С По каплям добавлялось 0,7г (2,3ммоля) соединения Описания 3, растворенного в 25мл сухого ДМФ, и раствор хранился при 0 - 5°С в течение 1 часа и при комнатной температуре на протяжении ночи Реакционная смесь выпаривалась в вакууме досуха, и остаток растворялся в этилацетате и промывался дважды водой Органический слой отделялся, сушился над сульфатом натрия, фильтровался и выпаривался в вакууме досуха Остаточное масло подвергалось флешхроматографии на 230 - 400 меш силикагеле при элюировании смесью гексана и этилацетата 3 2, содержащей 0,5% гидроокиси аммония, давая 0,1 г сырого продукта, который растирался с диизопропиловым эфиром, давая 0,08г целевого соединения C26H22N2O4 Тпл -187-190°С М В = 426,48 ИК (КВг) 3220, 1750, 1660, 1620 см 1 30 1 300МГц Н-ЯМР (CDCI3) 5 8,13-8,08 (м , ЗН), 7,80 (с , 1Н), 7,55 -7,38 (м , 9Н), 7,21 (дд , 1Н), 7,02 (д широкий, Н), 5,88 (д , 1Н), 3,97 (с , ЗН), 3,80 (с , ЗН) МС (EI, источник 200°С, 70 В, 200 мА) 426 (М+,), 367, 262, 234, 191, 77 Пример 8 (Р,3)-І\І-[а-(метоксикарбонил)бензил]-7гидрокси-2-фенил-хинолин-4-карбоксамид Получался, как в примере 5, из 2,1 г (5,3ммоля) соединения Описания 4, 1,08г (5,3ммоля) хлоргидрата (D,L) метилфенилглицината, 1,5мл (10,7ммоля) TEA, 1,7г (12,5ммолей) НОЕТ и 1,2 г (5,8ммоля) DCC в 70мл сухого ТГФ и 30мл CH3CN Обработка реакционной смеси осуществлялась таким же образом, как описано в примере 5 Полученный сырой продукт растирался с диизопропиловым эфиром, а затем перекристаллизовывался дважды из изопропанола, давая 0,06г целевого соединения C25H20N2O4 Тпл -256-257°С М В =412,45 ИК(ЕВг) 3270, 1750, 1650, 1620 с м 1 300МГц 1Н-ЯМР (ДМСО-de) 5 10,30 (с широкий, 1Н), 9,64 (д , 1Н), 8,22 (д , 2Н), 8,04 (д , 1Н), 7,85 (с , 1Н), 7,60-7,34 (м , 9Н), 7,21 (дд , 1Н), 5,74 (д , 1Н), 3,71 (с, ЗН) МС (EI, источник 200°С, 70 В, 200мА) 412 (М+,), 353, 248, 220, 77 Пример 9 Хлоргидрат (R,S)-N- [а- (карбокси)бензил]-7метокси-2-фенилхинолин-4-карбоксамид 0,18г (0,4ммоля) продукта примера 7 растворялось в 10мл 10% HCI и 5мл диоксана Реакционная смесь нагревалась с обратным холодильником и перемешивалась в течение 3 часов, а затем выпаривалась в вакууме досуха Сырой продукт растирался с теплым этилацетатом (содержащим несколько капель этанола), давая 0,16г целевого соединения C25H2oN204 HCI Т пл = 228 - 230°С М В = 448,91 1 ИК (КВг) 3180, 1735, 1655, 1630см 1 300МГц Н-ЯМР (ДМСО-de) 5 9,6 (д , 1Н), 8,26 (дд , 2Н), 8,14 (д , 1Н), 7,98 (с , 1Н), 7,63-7,52 (м , 6Н), 7,46-7,36 (м , ЗН), 7,33 (дд , 1Н), 5,66 (д , 1Н), 3,98 (с , ЗН) МС (ЕІ, источник 200°С, 70В, 200мА) 412 (М+,), 368, 262, 234, 191, 77 Пример 10 (Р,3)-І\І-[а-(метиламинокарбонил)бензил]-2фенилхинолин-4-карбоксамид 0,45г (1,1 ммоля) продукта примера 4 растворялось в 40мл смеси 33% МеІЧНг/ЕЮН, добавлялось каталитическое количество NaCN, и реакционная смесь нагревалась при 70°С в течение 1 часа в аппарате Парра Внутреннее давление поднималось до 40фунт/кв дюйм (2,812кг/см2) Раствор выпаривался в вакууме досуха, и остаток растирался с водой, фильтровался и перекристаллизовывался из смеси изопропанола (50мл) и этанола (30мл), давая 0,2г целевого соединения C25H21N3O2 Т пл = 261 - 263°С 32 31 51623 М В = 395,47 Пример 13 Элементный анализ (R,S)-N-[a-(MeTOKCHKap6oHHn)6eH3Hn]-2-(4Вычислено С 75,93 Н 5,35 N10,63 пиридил)хинолин-4-карбоксамид Найдено С 75,65 Н 5,34 N10,55 Получался, как в примере 1, из 3,4г 1 ИК (КВг) 3300, 3270, 1660, 1635см (16,7ммолей) хлоргидрата (D,L) метил фен ил гли1 цината, 3,9мл (27,8ммоля) TEA и 3,0г (11,1ммоля) 300МГц Н-ЯМР (ДМСО-de) 5 9,48 (д , 1Н), 2-(4-пиридил)хинолин-4-карбонилхло-рида в 8,33-8,25 (м , ЗН), 8,18-8,10 (м , ЗН), 7,80 (ддд , 100мл смеси метиленхлорида, метил цианида и 1Н), 7,68-7,50 (м , 6Н), 7,40-7,28 (м , ЗН), 5,75 (д , ДМФ Обработка реакционной смеси осуществля1Н), 2,63 (д , ЗН) лась таким же образом, как описано в примере 1 МС (EI, источник 200°С, 70 В, 200 мА) 395 Полученный сырой продукт перекрис(М+,), 337, 232, 204, 77 таллизовывался три раза из этилацетата, давая Пример 11 1,9г целевого соединения (R,S)-N-[a-(MeTOKCHKap6oHHn)6eH3Hn]-2-(2тиенил)хинолин -4-карбоксамид C24H19N3O3 Тпл -172-174°С Получался, как в примере 5, из 2,0г (7,3ммоля) М В = 397,43 2-(2-тиенил)хинолин-4-карбоновой кислоты, 1,7г (8,4ммоля) хлоргидрата Элементный анализ Вычислено С 72,53 Н 4,82 N10,57 (О,І_)метилфенилглицината, 1,1мл (Юммолей) NНайдено С 71,87 Н 4,87 N10,44 метилморфолина, 2,1 г (15,5ммолей) НОВТ и 1,85г ИК (КВг) 3240, 1750, 1670см 1 (9,0ммолей) DCC в 70мл сухого ТГФ, 30мл метилцианида и 10мл метиленхлорида Обработка ре300МГц 1Н-ЯМР (ДМСО-de) 5 9,74 (д , 1Н), акционной смеси осуществлялась таким же обра8,79 (дд , 2Н), 8,27-8,17 (м , 5Н), 7,89 (ддд , 1Н), зом, как описано в примере 5 Полученный сырой 7,74 (ддд , 1Н), 7,54 (дд , 2Н), 7,47-7,38 (м , ЗН), продукт кристаллизовался из этилацетата, а затем 5,8 (д , 1Н), 3,75 (с, ЗН) перекристаллизовывался из абсолютного этанола, МС (EI, источник 200°С, 70 В, 200 мА) 397 давая 0,9г целевого соединения (М+ ), 338, 233, 205, 77 C23H18N2O3S Пример 14 Тпл -178-180°С (Р,3)-^[а-(метоксикарбонил)-2-тиенилметил]М В = 402,47 2-фенилхи-нолин-4-карбоксамид Элементный анализ Получался, как в примере 1, из 1,94г Вычислено С 68,64 Н 4,51 N6,96 (9,4ммолей) хлоргидрата (D,L) метилфенилглициНайдено С 67,50 Н 4,99 N7,43 ната, 2,7мл (19,5ммолей) TEA и 2,0г (7,8ммоля) 2ИК (КВг) 3300, 1745, 1645 см 1 фенилхинолин-4-карбонилхлорида в 100мл смеси метиленхлорида, метилцианида и ДМФ Обработ300МГц 1Н-ЯМР (ДМСО-de) 5 9,70 (д , 1Н), ка реакционной смеси осуществлялась таким же 8,12 (д , 1Н), 8,08 (с , 1Н), 8,04 (д , 1Н) 8,02 (д , 1Н), образом, как описано в примере 1 Полученный 7,19 (т, 1Н), 7,76 (д , 1Н), 7,62 (т , 1Н), 7,53 (д , сырой продукт перекристаллизовывался три раза 2Н), 7,46-7,37 (м , ЗН), 7,3 (дд , 1Н), 5,68 (д , 1Н), из этилацетата, давая 0,66г целевого соединения 3,68 (с , ЗН) МС (EI, источник 200°С, 70 В, 200 мА) 402 C23H18N2O3S (М+), 343, 238, 210, 77 Тпл = 144-145°С Пример 12 М В = 402,47 Элементный анализ (R,S)-N-[a-(MeTOKCHKap6oHHn)6eH3Hn]-2-(2Вычислено С 68,64 Н 4,51 N6,96 фурил)хинолин-4-карбоксамид Найдено С 68,81 Н 4,46 N6,96 Получался, как в примере 1, из 7,2г 1 ИК (КВг) 3295, 1745, 1640см (35,5ммолей) хлоргидрата (D,L) метил фен ил глицината, 12,4мл (88,8ммолей) TEA и 9,1 г 300 МГц 1Н-ЯМР (ДМСО-de) 5 8,25 (дд f 1H), (35,5ммолей) сырого 2-(2-фурил)хинолин-4-карбо8,22 (дд,1Н), 8,17 (дд , 2Н), 7,95 (с 1Н), 7,78 нилхлорида в 350мл смеси метиленхлорида, ме(ддд, 1Н) 7,60 (ддд, 1Н), 7,56-7,45 (м, ЗН), 7,35 тилцианида и ДМФ Обработка реакционной смеси (дд , 1Н), 7,20 (д, 1Н), 7,05 (дд , 1Н), 7,05 (с, широосуществлялась таким же образом, как описано в кий, 1Н), 6,22 (д , 1Н), 3,9 (с, ЗН) примере 1 Полученный сырой продукт растиралМС (EI, источник 200°С, 70 В, 200мА) 402 ся с метанолом, давая 3,3г целевого соединения (М+ ), 343, 232, 204 Пример 15 C23H18N2O4 Тпл -178-180°С ^,3)-^[а-(метоксикарбонилметил)бензил]-2М В = 386,405 фенилхино-лин-4-карбоксамид Элементный анализ Получался, как в примере 5, из 1,39г Вычислено С 71,49 Н 4,70 N7,25 (5,60ммоля) 2-фенилхинолин-4-карбоновой кислоНайдено С 71,67 Н 4,74 N7,17 ты, 1,2г (5,60ммоля) хлоргидрата (R,S) метил-3ИК (КВг) 3300, 1750, 1650см 1 амино-3-фенилпропионата, 0,78мл (-5,60ммоля) TEA, 1,51г (11,2ммоля) НОВТ и 2,31 г (11,2ммоля) 300МГц 1Н-ЯМР (ДМСО-de) 5 9,72 (д , 1Н), DCC в 10мл ТГФ, 4мл CH3CN и 7мл метиленхло8,12 (д , 1Н), 8,06 (д , 1Н), 7,96 (дд , 1Н), 7,92 (с , риде Обработка реакционной смеси осуществля1Н), 7,80 (ддд , 1Н), 7,62 (ддд , 1Н), 7,52 (дд , 2Н), лась таким же образом, как описано в примере 5 7,45-7,35 (м , 4Н), 6,73 (дд , 1Н), 5,77 (д , 1Н), 3,74 Полученный сырой продукт растворялся в мети(с , ЗН) ленхлориде и оставлялся на ночь при 0°С ВыпаМС (EI, источник 200°С, 70 В, 200 мА) 386 дало в осадок еще некоторое количество дицикло(М+,), 327, 222, 194, 77 51623 33 гексил мочевины и отфильтровывалось Раствор выпаривался в вакууме досуха, и получалось 1,4г сырого продукта, который растирался со смесью диизопропилового эфира и ацетона 99 1, давая 1,2г целевого соединения в виде белого твердого вещества C26H22N2O3 Тпл = 156-158°С М В =410,47 Элементный анализ Вычислено С 76,07 Н 5,40 N 6,82 34 Найдено С 75,77 Н 5,38 N6,94 ИК (КВг) 3295, 1755, 1645, 1590, 1530 см 1 300МГц 1Н-ЯМР (ДМСО-de) 5 9,40 (д , 1Н), 8,29 (дд , 2Н), 8,14 (д , 1Н), 8,07 (д , 1Н), 8,04 (с , 1Н), 7,83 (ддд, 1Н), 7,66-7,52 (м , 4Н), 7,50 (д , 2Н), 7,40 (дд, 2Н), 7,31 (ддд , 1Н), 5,60 (дт , 1Н), 3,65 (с , ЗН), 3,40-2,89 (М , 2Н) МС (ЕІ, источник 200°С, 70 В, 200 мА) 410 (М+ ), 337, 233, 205 ТАЬЛИЦА 1 В, В Прим Аг R Щ Me H Me _ к H H H H H H H H H H H H H R2 «3 R4 Rs * Молекулярная формула 1 1 2 Pis . „ p h 3 Ph 4 , Ph COOMe Ph COOMe 6 , Ph COOMe 7 ' Ph COOMe 8 PJi COOMe 9 j Ph 5 t 10 _ s P h 11 Me COOH в "|ph" COOMe Г2 s 13 j Ph 14 і 2 т и е н и п COOMe 15 Ph_ CONHMe^ Ph COOMe COOMe CH?COOMe H H H H H H H H H H и a H H H H H H H H H H Ph „ Ph to'I ' H P _ h H P h H P h 7O G - M H Ph 7O _ m H_ Ph -H 7O e [H Ph -M H H Ph H . ~ 2-тиеииг H H 2-фурил H . . 4-Py Ph и H N Ph ^R,S) Точка гзлавл С2^20^2^ ! (S) *-24^20^2^ * R ) , jC24 H 20 N 2° (R,S) i C25H2QN2O3 (S) 1 C25H20H2&J C t c=0.5,MeOH І 156-157 161-162 , 1 158-160 j 170-172 ' 180-181 25 H 2QN2J. j 180-181 (R.S> ,С2бН22^2О4_ +25° a -25° a *42° * " -42" і 187-190 (R) ^R,S) (R,S) С25ЩоЩ°4„ 1256-257 C25H20N2.O4.HCl 122B-230 (R,S) і С25Н2|ИзО2 ^R,S> 1 C23H18N2O3S І1261-2ЙЗ | 178-180 ! (R,S) C23HHJ5N2O4 (R,Sjl Ї C24HJ9N3O3 (R,S) ' C53HJ8N2O3S (R,S) C9fiH?7N7O-i ', j 178-180 I 172-174 | 144-145 156-138 '""растеоритель Д Ф М Соединения примеров 16-49 общей формулы (I) (приведены в следующей Таблице 2) синтезировались, исходя из соответствующих ацилхлоридов соединений (II) и аминов (III), показанных в таблице, и следуя процедуре синтеза, описанной в Примере 1 Ацилхлориды синтезировались, ис ходя из соответствующей кислоты формулы (II) и следуя Описанию 1 Выходы в результате реакции вычислены на очищенном, но неперекристаллизованном материале Аналитические и спектроскопические данные соединений примеров 16-49 приведены в Таблице 5 Таблица ? Ацилхлорид соединении ( I I ) + ( п і ) (Ш) т Стерео Молекулярная химия Формула T nn i°C) раєте ( перекр ) ) т 120 132
ДивитисяДодаткова інформація
Назва патенту англійськоюDerivatives of quinoline as antagonists of nk3 receptor, method of their preparation, a pharmaceutical composition of their base and method of treatment
Назва патенту російськоюПроизводные хинолина как антагонисты nk3 рецептора, способ их получения, фармацевтическая композиция на их основе и способ лечения заболеваний
МПК / Мітки
МПК: A61P 25/00, C07D 215/22, A61P 17/06, A61P 11/06, A61P 29/00, A61K 31/47, A61P 17/04, A61P 13/12, A61P 13/10, C07D 215/36, A61P 37/08, A61P 11/14, C07D 215/42, C07D 215/50
Мітки: основі, похідні, рецептора, антагоністи, захворювань, хіноліну, одержання, спосіб, фармацевтична, композиція, лікування
Код посилання
<a href="https://ua.patents.su/35-51623-pokhidni-khinolinu-yak-antagonisti-nk3-receptora-sposib-kh-oderzhannya-farmacevtichna-kompoziciya-na-kh-osnovi-ta-sposib-likuvannya-zakhvoryuvan.html" target="_blank" rel="follow" title="База патентів України">Похідні хіноліну як антагоністи nk3 рецептора, спосіб їх одержання, фармацевтична композиція на їх основі та спосіб лікування захворювань</a>
Попередній патент: Лікарський засіб для регулювання мейозу
Випадковий патент: П'ятиступінчаста коробка зміни швидкостей з електромеханічним приводом керування