4-(амінометил)піперидинбензаміди як 5нт4-антагоністи
Номер патенту: 88607
Опубліковано: 10.11.2009
Автори: Гійсен Хенрікус Якобус Марія, Босманс Жан-Поль Рене Марі Андре, Мевеллек Лоренс Анн
Формула / Реферат
1. Сполука формули (І)
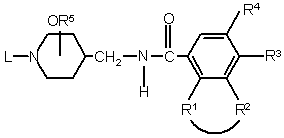 , (I)
, (I)
її стереохімічно ізомерні форми, її N-оксидні форми або її фармацевтично прийнятні кислотно- або основно-адитивні солі,
де
-R1-R2- являє собою двовалентний радикал формули
-О-СН2-О-, (а-1)
-О-СН2-СН2, (а-2)
-О-СН2-СН2-О-, (а-3)
-О-СН2-СН2-СН2-, (а-4)
-О-СН2-СН2-СН2-О-, (а-5)
-О-СН2-СН2-СН2-СН2-, (а-6)
-О-СН2-СН2-СН2-СН2-О-, (а-7)
-О-СН2-СН2-СН2-СН2-СН2-, (а-8)
де в зазначених двовалентних радикалах, при потребі, один або два атоми водню на одному або різних атомах вуглецю можуть бути замінені С1-6-алкілом або гідроксигрупою,
R3 являє собою водень, галоген, С1-4-алкіл;
R4 являє собою С1-6-алкіл, С1-6-алкіл, заміщений ціаногрупою або С1-6-алкілоксигрупою, С1-6-алкілоксигрупу, ціаногрупу, аміногрупу або моно- або ді(С1-6-алкіл)аміногрупу;
R5 являє собою водень або С1-6-алкіл, а радикал -OR5 розташовується в 3 або 4 положенні піперидинової складової;
L являє собою водень, або L являє собою радикал формули
-Alk-R6, (b-1)
-Alk-X-R7, (b-2)
-Alk-Y-C(=O)-R9 (b-3) або
-Alk-Z-C(=O)-NR11R12, (b-4)
де кожен Alk являє собою С1-12-алкандіїл; та
R6 являє собою водень, гідроксигрупу, ціаногрупу, С3-6-циклоалкіл; С1-6-алкілсульфоніламіногрупу, арил або Het;
R7 являє собою С1-6-алкіл, С1-6-алкіл, заміщений гідроксигрупою, C3-6-циклоалкіл, арил або Het;
X являє собою О, S, SO2 або NR8, при цьому зазначений R8 являє собою водень або С1-6-алкіл;
R9 являє собою водень, С1-6-алкіл, С3-6-циклоалкіл, гідроксигрупу або арил;
Y являє собою прямий зв'язок або NR10, де R10 являє собою водень або С1-6-алкіл;
Z являє собою прямий зв'язок, О, S або NR10, де R10 являє собою водень або С1-6-алкіл;
R11 та R12 являють собою, кожен незалежно, водень, С1-6-алкіл, С3-6-циклоалкіл, або
R11 та R12, об'єднані з атомом азоту, до якого R11 та R12 приєднані, можуть утворювати піролідинілове, піперидинілове, піперазинілове або 4-морфолінілове кільце, при цьому обидва, при потребі, можуть бути заміщені С1-6-алкілом;
арил являє собою незаміщений феніл або феніл, заміщений одним, двома або трьома замісниками, кожний з яких незалежно один від одного вибраний з атома галогену, гідроксигрупи, С1-6-алкілу, C1-6-алкілоксигрупи, С1-6-алкілкарбонілу, нітрогрупи, трифторметилу, аміногрупи, амінокарбонілу та аміносульфонілу, та
Het являє собою фураніл, фураніл, заміщений С1-6-алкілом або галогеном, тетрагідрофураніл, тетрагідрофураніл, заміщений С1-6-алкілом, діоксоланіл, діоксоланіл, заміщений С1-6-алкілом, діоксаніл, діоксаніл, заміщений С1-6-алкілом, тетрагідропіраніл, тетрагідропіраніл, заміщений С1-6-алкілом, 2,3-дигідро-2-оксо-1Н-імідазоліл, 2,3-дигідро-2-оксо-1Н-імідазоліл, заміщений одним або двома замісниками, вибраними, кожен незалежно, з галогену або С1-6-алкілу, піролідиніл, піролідиніл, заміщений одним або двома замісниками, вибраними, кожен незалежно, з галогену, гідроксигрупи або С1-6-алкілу, піридиніл, піридиніл, заміщений одним або двома замісниками, вибраними, кожен незалежно, з галогену, гідроксигрупи або С1-6-алкілу, піримідиніл, піримідиніл, заміщений одним або двома замісниками, вибраними, кожен незалежно, з галогену, гідроксигрупи або С1-6-алкілу, піридазиніл, піридазиніл, заміщений одним або двома замісниками, вибраними, кожен незалежно, з гідроксигрупи, С1-6-алкілоксигрупи, С1-6-алкілу або галогену, піразиніл, піразиніл, заміщений одним або двома замісниками, вибраними, кожен незалежно, з гідроксигрупи, С1-6-алкілоксигрупи, С1-6-алкілу або галогену.
2. Сполука за п. 1, яка відрізняється тим, що -R1-R2- являє собою двовалентний радикал формули
-О-СН2-СН2-О-, (а-3)
-О-СН2-СН2-СН2-О-, (а-5)
R3 являє собою водень, галоген, С1-4-aлкіл;
R4 являє собою С1-6-алкіл, С1-6-алкіл, заміщений ціаногрупою або С1-6-алкілоксигрупою, С1-6-алкілоксигрупу, ціаногрупу, аміногрупу або моно- або ді(С1-6-алкіл)аміногрупу;
R5 являє собою водень або С1-6-алкіл, та радикал -OR5 розташовується в положенні 3 або 4 піперидинової групи;
L являє собою водень, або L являє собою радикал формули
-Alk-R6, (b-1)
-Alk-X-R7, (b-2)
-Alk-Y-C(=O)-R9 (b-3) або
-Alk-Z-C(=O)-NR11R12, (b-4)
де кожен Alk являє собою С1-12-алкандіїл; і
R6 являє собою водень, гідроксигрупу, ціаногрупу, С3-6-циклоалкіл, С1-6-алкілсульфоніламіногрупу, арил або Het;
R7 являє собою С1-6-алкіл, С1-6-алкіл, заміщений гідроксигрупою, С3-6-циклоалкіл, арил або Het;
X являє собою О, S, SO2 або NR8, причому зазначений R8 являє собою водень або С1-6-алкіл;
R9 являє собою С1-6-алкіл або гідроксигрупу;
Y являє собою прямий зв'язок;
Z являє собою прямий зв'язок або О;
R11 та R12 являють собою, кожен незалежно, водень або С1-6-алкіл, або R11 та R12, об'єднані з атомом азоту, до якого приєднані R11 та R12, можуть утворювати піролідиніл або піперазиніл, заміщений С1-6-алкілом;
арил представляє незаміщений феніл або феніл, заміщений 1, 2 або 3 замісниками, вибраними, кожен незалежно, з галогену, гідроксигрупи, С1-6-алкілу, С1-6-алкілоксигрупи та аміносульфонілу; та
Het являє собою тетрагідрофураніл, тетрагідрофураніл, заміщений С1-6-алкілом, діоксоланіл, діоксоланіл, заміщений С1-6-алкілом, піридиніл, піридиніл, заміщений одним або двома замісниками, вибраними, кожен незалежно, з галогену, гідроксигрупи, С1-6-алкілу, піримідиніл, піримідиніл, заміщений одним або двома замісниками, вибраними, кожен незалежно, з галогену, гідроксигрупи або С1-6-алкілу, піридазиніл, піридазиніл, заміщений одним або двома замісниками, вибраними, кожен незалежно, з гідроксигрупи, С1-6-алкілоксигрупи, C1-6-алкілу або галогену; піразиніл, піразиніл, заміщений одним або двома замісниками, вибраними, кожен незалежно, з гідроксигрупи, С1-6-алкілоксигрупи, С1-6-алкілу або галогену.
3.Сполука за п. 1 або п. 2, яка відрізняється тим, що радикал -OR5 розташовується в положенні 3 піперидинової групи, що має трансконфігурацію.
4. Сполука за п. 3, яка відрізняється тим, що абсолютною конфігурацією зазначеної піперидинової групи є (35,43)-конфігурація.
5. Сполука за будь-яким з попередніх пунктів, яка відрізняється тим, що -R1-R2- являє собою радикал формули (а-5), R3 являє собою водень, R4 являє собою метил, та R5 являє собою водень.
6. Сполука за п. 5, яка відрізняється тим, що L являє собою радикал формули (b-2), де X являє собою О, Alk являє собою С1-4-алкандіїл, та R7 являє собою С1-6-алкіл.
7. Сполука за п. 1, яка відрізняється тим, що є сполукою (3S-тpaнc)-8-метил-3,4-дигідро-2Н-бензо[b][1,4]діоксипін-6-карбоксильна кислота [3-гідрокси-1-(3-метоксипропіл)-піперидин-4-ілметил]-амідом або її фармацевтично прийнятною кислотно-адитивною сіллю.
8. Фармацевтична композиція, що містить фармацевтично прийнятний носій та терапевтично ефективну кількість сполуки за будь-яким з пп. 1-7.
9. Спосіб одержання фармацевтичної композиції за п. 8, де терапевтично ефективну кількість сполуки за будь-яким з пп. 1-7 ретельно змішують з фармацевтично прийнятним носієм.
10. Сполука за будь-яким з пп. 1-7 для застосування як лікарського засобу.
11. Спосіб одержання сполуки формули (І), при якому проміжну сполуку формули (II) піддають реакції з похідним карбонової кислоти формули (III) або її функціональним похідним, здатним вступати у реакцію;
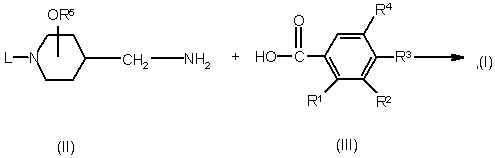 ,
,
де радикали -R1-R2-, R3, R4, R5 та L мають значення, визначені в п. 1;
або сполуки формули (І) перетворюють одну в іншу за допомогою відомих з рівня техніки реакцій перетворення; або,
якщо бажано, сполуку формули (І) перетворюють у фармацевтично прийнятну адитивну сіль, або, навпаки, адитивну сіль кислоти сполуки формули (І) перетворюють лугом у форму вільної основи;
та при цьому, якщо бажано, одержують її стереохімічно ізомерну форму.
12. Спосіб одержання сполуки формули (І), при якому проміжну сполуку формули (V) N-алкілують сполукою формули (I-а), визначеною як сполука формули (І), де L являє собою водень, у розчиннику, інертному для реакції, та, при потребі, у присутності придатної основи, причому в такий спосіб одержують сполуки формули (І-b), визначені як сполуки формули (І), де L інший, ніж водень,
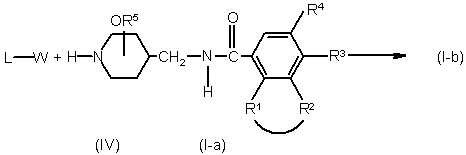 ,
,
де радикали -R1-R2-, R3, R4, R5 та L мають значення, визначені в п. 1, та W являє собою придатну кінцеву групу;
або сполуки формули (І) перетворюють одну в іншу за допомогою відомих з рівня техніки реакцій перетворення; або,
якщо бажано, сполуку формули (І) перетворюють у фармацевтично прийнятну адитивну сіль,
або, навпаки, адитивну сіль кислоти сполуки формули (І) перетворюють лугом у форму вільної основи;
та при цьому, якщо бажано, одержують її стереохімічно ізомерну форму.
13. Спосіб одержання сполуки формули (І), при якому відповідний проміжний кетон або проміжний альдегід формули L'=О (V), причому зазначений L'=O являє собою сполуки формули L-H, де два гем-атоми водню в С1-12-аландіїльній групі замінені =O, піддають реакції зі сполукою формули (I-а), причому в такий спосіб одержують сполуки формули (І-b)
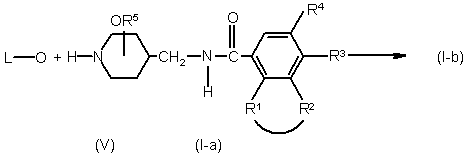 ,
,
де радикали -R1-R2-, R3, R4, R5 та L мають значення, визначені в п. 1;
або сполуки формули (І) перетворюють одну в іншу за допомогою відомих з рівня техніки реакцій перетворення; або,
якщо бажано, сполуку формули (І) перетворюють у фармацевтично прийнятну адитивну сіль, або, навпаки,
адитивну сіль кислоти сполуки формули (І) перетворюють лугом у форму вільної основи;
та при цьому, якщо бажано, одержують її стереохімічно ізомерну форму.
Текст
Приклад А.22 a) Одержання проміжної сполуки (58) 1,1-диметилетил-(транс)-3-гідрокси-4[[(фенилметил)аміно]метил]-1-піперидин карбоксилат [описаний в Міжнародній публікації WO00/37461 як проміжна сполука (1-d)] (2,73моль) відокремлюють та очищують за допомогою хіральної колоночної хроматографії на Chiracel AD (елюент гексан/етанол, 80/20). Потрібні фракції збирають та випарюють розчинник. Додають толуол, здійснюють азеотропний відгін на роторному випарнику та одержують на виході 377г 1,1диметилетил-(3S-транс)-3-гідрокси-4[[(фенилметил)аміно]метил]-1піперидинкарбоксилата (проміжна сполука 58) 37 88607 38 публікації WO-00/37461 як проміжна сполука (1-c)] (0,27моль) у THF (1300мл). Суміш перемішують b) Одержання протягом 30 хвилин. Додають метилйодид (0,54моль) та отриману реакційну суміш перемішують протягом 90 хвилин. Додають невелику кількість води. Розчинник випарюють та залишок проміжної сполуки (59) обробляють водою та DCM. Органічний шар відоСуміш проміжної сполуки (58) (0,028моль) та кремлюють, сушать, фільтрують та випарюють метанолу (100мл) гідрують з палладієм-на-карбоні розчинник, та одержують на виході 1,1(10%, 2г), як каталізатором. Після поглинання воддиметилетил-(транс)-4-[[[(4ню (1 еквівалент) каталізатор відфільтровують та метилфенил)сульфоніл]окси]метил]-3-метокси-1фільтрат упарюють, та одержують на виході 4,7г піперидинкарбоксилат (проміжна сполука 62). 1,1-диметилетил-(3S-транс)-4-(амінометил)-3гідрокси-1-піперидин карбоксилата (проміжна сполука 59; [a]20.D=+4,37° (с=24,03мг/5мл у СН3ОН)). b) Одержання проміжПриклад А.23 а) Одержання проміжної сполуки (60) Суміш 1,1-диметилетил-(3RЇ-транс)-3-гідрокси4-[[(4-метилфенил)сульфоніл]оксиметил]-1піперидинкарбоксилата [описаного в Міжнародній публікації WO-00/37461 як проміжна сполука (1-сІ)] (0,03моль) та бензиламіну (0,1моль) у THF (250мл) перемішують протягом 16 годин при температурі 125°С (автоклав). Реакційну суміш охолоджують та випарюють розчинник. Залишок обробляють DCM та водяним розчином K2СО3. Органічний шар відокремлюють, сушать, фільтрують та випарюють розчинник. Залишок кристалізують із DIPE та одержують на виході 5,3г 1,1диметилетил-(3R-транс)-3-гідрокси-4[[(фенилметил)аміно]метил]-1-піперидин карбоксилату (проміжна сполуки (60) ([a]20.D=-68,65° (с=23,16мг/5мл у СН3ОН); температура плавлення 91°С). b) Одержання проміжної сполуки (61) Суміш проміжної сполуки (60) (0,016моль) та метанолу (150мл) гідрують з палладієм-на-карбоні (10%, 2г), як каталізатором, при температурі 50°С. Після поглинання водню (1 еквівалент) каталізатор відфільтровують та фільтрат упарюють, та одержують на виході 1,1-диметилетил-(3R-транс)-4(амінометил)-3-гідрокси-1-піперидинкарбоксилат (проміжна сполука 61). Приклад А.24 a) Одержання проміжної спо луки (62) Взаємодія відбувається в атмосфері азоту. Гідрид натрію (0,3моль) додають до розчину 1,1диметилетил-(транс)-3-гідрокси-4-[[[(4метилфенил)сульфоніл]окси]метил]-1піперидинкарбоксилата [описаного в Міжнародній ної сполуки (63) Суміш проміжної сполуки (62) (0,065моль) та THF (250мл) обробляють рідким NН3 в автоклаві при температурі 125°С протягом 16 годин. Реакційну суміш фільтрують та фільтрат упарюють. Залишок обробляють 5% водним розчином NaOH та DCM. Органічний шар відокремлюють, сушать, фільтрують та випарюють розчинник, та одержують на виході 16г 1,1-диметилетил-(транс)-4амінометил)-3-метокси-1-піперидинкарбоксилату (проміжна сполука 63). Приклад А.25 a) Одержання проміж ної сполуки (64) Суміш трет-бутил-4-оксо-1піперидинкарбоксилату (0,1моль) та нітрометану (0,1моль) у метанолі (200мл) перемішують при температурі 10°С. При температурі 10°С додають по краплях метанолат натрію (0,11моль). Реакційну суміш перемішують протягом 20 годин при кімнатній температурі. Розчинник випарюють. Залишок розчиняють у воді, потім нейтралізують оцтовою кислотою та потім двічі екстрагують DCM. Органічний шар відокремлюють, промивають водою, сушать, фільтрують та випарюють розчинник. Залишок суспендують в DIPE, відфільтровують, промивають та сушать, та одержують на виході 17,2г проміжної сполуки (64) (температура плавлення 160°С). b) Одержання промі жної сполуки (65) Суміш проміжної сполуки (64) (0,058моль) та оцтової кислоти (12мл) у метанолі (250мл) гідрують при температурі 14°С із палладієм-на-карбоні (10%, 1г), як каталізатором. Після поглинання водню (3 еквіваленти) каталізатор відфільтровують та фільтрат упарюють. Залишок розчиняють у суміші лід/вода, потім підлужують гідроксидом калію та висалюють за допомогою K2СО3. Отриману суміш двічі екстрагують DCM. Органічний шар відокремлюють, сушать, фільтрують та випарюють розчинник. Залишок суспендують в DIPE, відфільтровують, промивають та сушать, та одержують на виході 7,5г проміжної сполуки (65). Приклад А.26 39 88607 40 фільтрат упарюють, та одержують на виході 3,3г проміжної сполуки (69). Приклад А.28 a) Одержання проміжної сполуки (66) Суміш (транс)-4-[[(фенилметил)аміно]метил]3-піперидинола [отриманого в Міжнародній публікації WO-00/37461 як проміжну сполуку (6)] (0,04моль), 3-бром-1-пропанолу (0,04моль) та Na2CO3 (0,08моль) у метилізобутилкетоні (400мл) перемішують та кип'ятять зі зворотним холодильником протягом 18 годин. Розчинник випарюють. Залишок обробляють водою та DCM. Органічний шар відокремлюють, сушать, фільтрують та випарюють розчинник. Залишок обробляють водою та DCM. Органічний шар відокремлюють, сушать, фільтрують та випарюють розчинник. Залишок очищують за допомогою колоночної хроматографії на силікагелі (елюент СН2СІ2/СН3ОН/NН3), 93/7). Потрібні фракції збирають та випарюють розчинник. Додають толуол, розчинник знову випарюють, та одержують на виході 7,2г проміжної сполуки (66). b) Одержання промі жної сполуки (67) Суміш проміжної сполуки (66) (0,026моль) та метанолу (150мл) гідрують з палладієм-на-карбоні (10%, 2г), як каталізатором. Після поглинання водню (1 еквівалент) каталізатор відфільтровують та фільтрат упарюють, та одержують на виході 4,4г проміжної сполуки (67). Приклад А.27 а) Одержання а) Одержання промі жної сполуки (70) Суміш 1,1-диметилетил-(транс)-3-гідрокси-4[[(фенилметил)аміно]метил]-1піперидинкарбоксилату [проміжна сполуки (1-d) в Міжнародній публікації WO-99/02156] (0,426моль), бензальдегіду (0,5моль) та палладій-на-карбоні (10%, 5г) у розчині тіофену (5мл) та метанолі (1000мл) перемішують при температурі 70-80°С протягом ночі. Розчинник випарюють. Залишок обробляють DCM (150мл) та 5% водяним розчином NaOH (150мл). Суміш розділяють на шари. Водний шар екстрагують DCM. Об'єднані органічні шари сушать, фільтрують та випарюють розчинник. Залишок очищують за допомогою колоночної хроматографії на силікагелі (елюент СН2СІ2/(СН3ОН/NН3), 90/10). Чисті фракції збирають та випарюють розчинник. Залишок кристалізують із DIPE із краплею ACN. Речовину, що випала в осад, відфільтровують та сушать, та одержують на виході 2,35г 1,1-диметилетил(транс)-4-[[біс(фенилметил)аміно]метил]-3гідрокси-1-піперидинкарбоксилату (проміжна сполуки 70), температура плавлення 133°С). b) Одержання проміжної проміжної сполуки (68) Суміш (транс)-4-[[(фенилметил)аміно]метил]3-піперидинолу [отриманого в Міжнародній публікації WO-00/37461 як проміжна сполука (6)] (0,04моль), 1-хлор-3-метоксипропану (0,04моль) та Na2CO3 (0,08моль) у метилізобутилкетоні (300мл) перемішують та кип'ятять зі зворотним холодильником протягом 20 годин, потім охолоджують та випарюють розчинник. Залишок розчиняють в DCM, потім розчин промивають водою, сушать, фільтрують та випарюють розчинник. Залишок очищують за допомогою колоночної хроматографії на силікагелі (елюент СН2СІ2/(СН3ОН/NН3), 97/3). Чисті фракції збирають, випарюють розчинник та одержують на виході 5г проміжної сполуки (68). b) Одержання проміж ної сполуки (69) Суміш проміжної сполуки (68) (0,016моль) та метанолу (150мл) гідрують з палладієм-на-карбоні (10%, 1г), як каталізатором. Після поглинання водню (1 еквівалент) каталізатор відфільтровують та сполуки (71) Суміш проміжної сполуки (70) (0,284моль) в 2пропанолі (1000мл) та розчину 6N НСІ в 2пропанолі (250мл) перемішують та кип'ятять зі зворотним холодильником протягом 15 хвилин та потім охолоджують. Розчинник випарюють. Додають 5% водяний розчин NaOH (750мл). Суміш двічі екстрагують DCM. Органічний шар відокремлюють, сушать, фільтрують та випарюють розчинник, та на виході одержують 88,95г (транс)-4[[біс(фенилметил)аміно]метил]-3-піперидинолу (проміжна сполука 71). c) Одержання проміж ної сполуки (72) Суміш проміжної сполуки (71) (0,083моль) та бутилальдегіду (7г) у метанолі (300мл) гідрують з палладієм-на-карбоні (10%, 2г), як каталізатором, у присутності розчину тіофену (3мл). Після погли 41 88607 42 нання водню (1 еквівалент) каталізатор відфільткип'ятять зі зворотним холодильником протягом 30 ровують на целіті та фільтрат упарюють. Залишок хвилин та потім охолоджують. Випарюють розчинрозчиняють в 2N соляній кислоті (500мл). Суміш ник та проводять спільне випарювання з толуопромивають толуолом та потім розділяють на шалом. Залишок сушать, та одержують на виході 12г ри. Водний шар підлужують 50% водяним розчипроміжної сполуки (76). ном NaOH та потім три рази екстрагують толуолом. Об'єднані органічні шари сушать, фільтрують проміжb) Одержання та випарюють розчинник, та одержують на виході 29г (транс)-4-[[біс(фенилметил)аміно]метил]-1бутил-3-піперидинолу (проміжна сполука 72). ної сполуки (77) Суміш 4-бромбутаннітрилу (0,06моль), проміжної сполуки (76) (0,06моль) та Na2CO3 (0,24моль) d) Одержання проміжв ACN (600мл) перемішують та кип'ятять зі зворотним холодильником протягом 20 годин та потім охолоджують, та фільтрують Розчинник випарюної сполуки (73) ють. Залишок очищують за допомогою колоночної Суміш проміжної сполуки (72) (0,079моль) та хроматографії на силікагелі (елюент метанолу (250мл) гідрують з палладієм-на-карбоні СН2СІ2/(СН3ОН/NН3), 85/15). Потрібні фракції зби(10%, 2г), як каталізатором. Після поглинання водрають, випарюють розчинник, та одержують на ню (2 еквіваленти) каталізатор відфільтровують на виході 4,5г проміжної сполуки (77). цілите, фільтрат упарюють, та одержують на виПриклад А.31 ході 13,8г (транс)-4-(амінометил)-1-бутил-3піперидинолу (проміжна сполука 73). Приклад А.29 a) Одержання a) Одержання промі жної сполуки (74) Проміжну сполуку (71) (0,0387моль) розчиняють в 2-метилпропанолі (200мл). Додають тетрагідрофурфурилметансульфонат (0,0 моль) та Na2CO3 (0,0774моль) Реакційну суміш перемішують та кип'ятять зі зворотним холодильником протягом 24 годин та потім охолоджують. Речовину, що випала в осад, відфільтровують. Розчинник випарюють. Залишок очищують за допомогою колоночної хроматографії на силікагелі (елюент СН2СІ2/СН3ОН, 97/3). Потрібні фракції збирають та випарюють розчинник, та одержують на виході 11,1г проміжної сполуки (74). b) Одержання луки (78) Суміш трифтороцтової кислоти (1,15моль) та води (2000мл) перемішують при кімнатній температурі. До суміші додають по краплях 1,2,3,6тетрагідро-1-(фенилметил)піридин (1,15моль) та суміш перемішують при кімнатній температурі протягом 15 хвилин. Додають окремими частинами Nбромсукцинімід (1,4моль) та суміш гріють при температурі 30-35°С протягом 1 години. Реакційну суміш перемішують протягом 30 хвилин. Знову додають окремими частинами N-бромсукцинімід (0,085моль) та суміш нагрівають до температури 35°С. Реакційну суміш перемішують протягом ночі при кімнатній температурі, потім декантують та додають по краплях 20% розчин NaOH (2000мл). Суміш перемішують протягом ночі при кімнатній температурі Продукт реакції екстрагують DCM (3х). Органічний шар відокремлюють, сушать, фільтрують та концентрують, та одержують на виході 193г проміжної сполуки (78). проміжної сполуки (75) Проміжну сполуку (74) (0,0279моль) гідрують у метанолі (150мл) з палладієм-на-карбоні (10%, 2г), як каталізатором. Після поглинання водню (2 еквіваленти) каталізатор відфільтровують на декаліті, випарюють розчинник, та одержують на виході 5,74г проміжної сполуки (75). Приклад А.30 а) Одержання проміжної спо проміжної спо луки (76) 1,1-диметилетил-(транс)-4-(амінометил)-3гідрокси-1-піперидинкарбоксилат [отриманий в Міжнародній публікації WO-00/37461 як проміжну сполуку (1-і)] (0,06моль), 2-пропанол, насичений НСІ (60мл) та 2-пропанол (400мл) перемішують та b) Одержання проміжної сполуки (79) Суміш гідриду літію (0,66моль) та THF (600мл, р.а.) піддають реакції при кімнатній температурі в атмосфері азоту, потім додають по краплях суміш 2-гідрокси-2-метилпропаннітрилу (0,66моль) та THF (150мл), реакційну суміш перемішують протягом 2 годин при кімнатній температурі, та одержують суміш (А). Суміш проміжної сполуки (78) (0,6моль) та THF (250мл) додають по краплях до суміші (А), та по завершенні додавання реакційну суміш перемішують та кип'ятять зі зворотним холодильником протягом 4 годин та потім перемішують протягом ночі при кімнатній температурі. Додають DCM та воду, органічний шар відокремлюють, сушать, фільтрують, випарюють 43 88607 розчинник, та одержують на виході 128г проміжної сполуки (79). 44 b) Одержання с) Одержання промі проміжної сполуки (80) Проміжну сполуку (79) (0,6моль) гідрують при температурі 14°С в CH3OH/NH3 (1,5л) з нікелем Ренея, як каталізатором. Після поглинання водню (2 еквіваленти) каталізатор відфільтровують та випарюють розчинник. Залишок розчиняють в ACN та обробляють етандіовою кислотою (0,6мл) перетворюють у сіль етандіової кислоти (1:1). Розчинник декантують. Залишок суспендують в 2пропанолі. Речовину, що випала в осад, відфільтровують та розчиняють у метанолі, суміш кип'ятять та охолоджують. Речовину, що випала в осад, відфільтровують, промивають та сушать, та одержують на виході 107г проміжної сполуки (80). Приклад А.32 жної сполуки (83) Проміжну сполуку (82) (0,15моль), 6N розчин НСІ/2-пропанол (120мл) та 2-пропанол (1200мл) перемішують та кип'ятять зі зворотним холодильником протягом 2 годин. Реакційну суміш залишають прохолоджуватися до кімнатної температури на ніч. Отриману речовину, що випала в осад, відфільтровують та сушать, та одержують на виході 54,5г проміжної сполуки (83) (температура плавлення 150°С). Подібним чином одержують проміжні сполуки (84) та (85). Одержання проміжної сполуки (81) Суміш 1,1-диметилетилового ефіру метил-[4[(метилсульфоніл)окси]бутил]карбамінової кислоти (0,02моль), проміжної сполуки (76) (0,02моль) та Na2CO3 (0,08моль) в ACN (100мл) перемішують та кип'ятять зі зворотним холодильником протягом 48 годин, охолоджують, фільтрують та фільтрат упарюють. Залишок очищують за допомогою колоночної хроматографії на силікагелі (елюент CH2Cl2/(CH3OH/NH3), 80/20), та одержують на виході 1,4г проміжної сполуки (81). Приклад А.33 a) Одержання Приклад А.34 a) Одержання проміжної сполуки (82) Проміжну сполуку (3) (0,146моль) перемішують в DCM (400мл). Додають триетиламін (0,146моль). Реакційну суміш охолоджують до температури нижче за 10°С. При зазначеній температурі додають по краплях мурашину кислоту (0,146моль) та реакційну суміш перемішують при зазначеній температурі протягом 1 години (=суміш А). Проміжне сполуки (56) (0,146моль) перемішують в DCM (400мл) при кімнатній температурі протягом 1 години та потім додають до суміші (А). Реакційну суміш перемішують протягом 90 хвилин при кімнатній температурі. Додають воду. Органічний шар відокремлюють, сушать, фільтрують, випарюють розчинник та одержують на виході 81г проміжної сполуки (82). проміжної сполуки (86) Суміш проміжної сполуки (7) (0,08моль), DCM (400мл) та триетиламіну (0,1моль) перемішують при температурі 5°С. Додають по краплях мурашину кислоту (0,08моль). Суміш перемішують протягом 30 хвилин при температурі 5°С При температурі 5°С додають проміжну сполуку (80) (0,08моль) та триетиламін (0,25моль) в DCM (400мл). Реакційну суміш нагрівають до кімнатної температури та промивають водою. Органічний шар відокремлюють, сушать, фільтрують, випарюють розчинник, проводять спільне випарювання з толуолом, та одержують на виході 41г проміжної сполуки (86). b) Одержання 45 88607 46 від -5°C до -10°. Відразу додають проміжну сполуку (56) (0,06моль) в DCM (50мл) та триетиламін (8,4мл). Крижану ванну забирають та суміш перемішують при кімнатній температурі протягом 2 годин. Додають DCM (200мл). Суміш промивають у послідовності вода/NaOH (5% водний розчин)/вода/холодна НСІ (5% соляна кислота)/вода. проміжної сполуки (87) Органічний шар відокремлюють, сушать, фільтруПроміжну сполуку (86) (0,08моль) гідрують у ють та випарюють розчинник. Залишок перетираметанолі (250мл) з палладієм-на-карбоні (10%, 2г), ють із сумішшю DIPE/ACN. Речовину, що випала в як каталізатором. Після поглинання водню (1 еквіосад, відфільтровують та сушать, та одержують на валент) каталізатор відфільтровують, випарюють виході 23,2г проміжної сполуки (90). розчинник та одержують на виході 34г проміжної b) Одержання сполуки (87). Подібним чином одержують проміжну сполуку (88). Приклад А.35 Одержання проміжної сполуки (91) Проміжну сполуку (90) (0,0478моль) гідрують у метанолі (250мл) при температурі 50°С із платиною-на-карбоні (5%, 3г), як каталізатором, у присутності розчину тіофену (3мл). Після поглинання водню (3 еквіваленти) каталізатор відфільтровують на декаліті та випарюють розчинник. Залишок перетирають із DIPE. Речовину, що випала в осад, відфільтровують та сушать, та одержують на виході 19,7г проміжної сполуки (91) (температура плавлення 161°С). Подібним чином одержують проміжні сполуки (92), (93) та 94. проміжної сполуки (89) Проміжну сполуку (7) (0,013моль) перемішують із DCM (100мл) Додають триетиламін (0,015моль) та суміш перемішують при температурі 5°С. При температурі 5°С додають по краплях мурашину кислоту (0,013моль), та потім реакційну суміш перемішують при температурі 5°С протягом 30 хвилин. При температурі 5°С додають триетиламін (0,03моль) та проміжну сполуку (67) (0,013моль) в DCM (100мл). Реакційну суміш нагрівають до кімнатної температури та потім промивають водою. Органічний шар відокремлюють, сушать, фільтрують, випарюють розчинник, та одержують на виході 5,3г проміжної сполуки (89). Приклад А.36 a) Одержання проміжної сполуки (90) Проміжне сполуки (9) (0,06моль) додають до DCM (250мл). Додають триетиламін (8,4мл), та суміш охолоджують до температури -5°C. Протягом 5 хвилин додають по краплях мурашину кислоту (0,06моль). Реакційну суміш перемішують протягом 40 хвилин при температурі в інтервалі Приклад А.37 Одержання 47 88607 48 плях етилхлорформиат (0,35моль), та реакційну суміш перемішують протягом 30 хвилин. До отриманої суміші при температурі 5°С додають розчин проміжної сполуки (59) (83г) в DCM (1000мл), потім реакційну суміш залишають до досягнення кімнатної температури та промивають водою. Органічпроміжної сполуки (95) ний шар відокремлюють, сушать, фільтрують, виСуміш проміжної сполуки (17) (0,336моль) та парюють розчинник, та одержують на виході 150г триетиламіна (0,4моль) в DCM (1000мл) переміпроміжної сполуки (95). шують при температурі 5°С, потім додають по краТаблица I-1 Проміжні сполуки (96)-(114) одержують відповідно до тієї ж процедури, що в прикладі А.38 49 88607 Приклад А.38 Одержання проміжної сполуки (115) 4-Метокси-1-бутанол (0,9моль) перемішують в DCM (1500мл) та додають триетиламін (1,35моль), потім додають по краплях метилсульфонілхлорид (1,1моль) (температура піднімається до 40°С), та реакційну суміш перемішують протягом 2 годин при кімнатній температурі. Суміш промивають водою. Органічний шар відокремлюють, сушать, випарюють розчинник, потім проводять спільне випарювання з толуоолом, та одержують на виході 167г проміжної сполуки (115). Приклад А.39 Одержання проміжної сполуки (116) До суміші 3-циклогексилоксипропан-1-олу (0,063моль) та DCM (120мл) додають триетиламін (0,11моль), потім додають по краплях метилсульфонілхлорид (0,07моль), та реакційну суміш перемішують при кімнатній температурі протягом 1 години. Суміш промивають водяним розчином Na2CO3 та водою. Органічний шар відокремлюють, сушать, фільтрують та випарюють розчинник. За 50 лишок очищують за допомогою колоночної хроматографії на силікагелі (елюент СН2СІ2/СН3ОН, 99/1). Фракції, що містять продукт реакції, збирають, випарюють розчинник, потім проводять спільне випарювання з толуолом, та одержують на виході 8,6г проміжної сполуки (116). Приклад А.40 a) Одержання промі жної сполуки (117) Суміш 4-феноксибутилхлориду (0,135моль) та DCM (50мл) перемішують та охолоджують до температури 0°С. Додають по краплях протягом 45 хвилин хлорсульфоновую кислоту (0,149моль). Крижану ванну забирають та реакційну суміш перемішують при кімнатній температурі протягом 2 годин. Потім додають по краплях етандіоїлдихлорид (0,176моль), а потім DMF (2мл). Реакційну суміш перемішують при кімнатній температурі протягом 20 годин. Потім суміш виливають на лід, екстрагують DCM, екстракт сушать, випарюють розчинник, та одержують на виході проміжну сполуку (117). 51 88607 52 кагелі на скляному фільтрі (елюент DCM). Фракції, що містять продукт реакції, збирають, випарюють b) Одержання пророзчинник, та одержують на виході 4г проміжної міжної сполуки (118) сполуки (121) Розчин проміжної сполуки (117) (0,135моль) у Приклад А.42 THF (500мл) перемішують та охолоджують до теа) Одержання мператури 0°С та потім через розчин барботують аміак (газ). Реакційну суміш фільтрують та випарюють розчинник. До залишку додають DCM (600мл) та суміш промивають НСІ (600мл, 1N). Водний шар відокремлюють та екстрагують DCM (2 рази по 300мл). Об'єднані органічні шари пропроміжної сполуки (122) мивають розсолом, сушать та випарюють розчинСуміш проміжної сполуки (87) (0,0154моль), ник. Залишок кристалізують із CH3OH/DIPE, відфіметилового ефіру 4-бромбутанової кислоти льтровують та сушать, та одержують на виході (0,02моль) та триетиламіну (0,02моль) у DMF 18,5г проміжної сполуки (118). (150мл) перемішують протягом ночі при темпераПодібним чином, але використовуючи 4турі 70°С. Реакційну суміш охолоджують та випафеноксипропілхлорид або 4-феноксиетилхлорид, рюють розчинник Залишок розчиняють в DCM та одержують на виході проміжні сполуки (119) та промивають водою. Органічний шар відокремлю(120). ють, сушать, фільтрують та випарюють розчинник, та одержують на виході 8г проміжної сполуки (122). b) Одержання Приклад А.41 Одержання проміжної спо луки (121) 1-Піролидинкарбонілхлорид (0,037моль) розчиняють у тетрахлорметані (12мл). Додають по краплях 3-бром-1-пропанол (0,036моль) та реакційну суміш перемішують при кімнатній температурі протягом 7 діб. Суміш охолоджують на льоді, та додають СН3ОН/(NН3) (2мл). Потім додають DCM (100мл), суміш промивають водою, сушать та випарюють розчинник. Залишок очищують на сілі проміжної сполуки (123) Проміжну сполуку (122) (0,0154моль), 6N розчин НСІ/2-пропанол (0,09моль) та метанол (100мл) перемішують та кип'ятять зі зворотним холодильником протягом 1 години. Реакційну суміш охолоджують. Розчинник випарюють. Залишок розчиняють в DCM та промивають H2O/NH3. Органічний шар відокремлюють, сушать, фільтрують, та випарюють розчинник. Залишок очищують за допомогою колоночної хроматографії на силікагелі (елюент СН2СІ2/(CH3OH/NH3), 97/3). Потрібні фракції збирають, випарюють розчинник, та одержують на виході 1,75г проміжної сполуки (123). Подібним чином одержують проміжні сполуки (124)-(129). 53 Для одержання кінцевих сполук також використовують проміжні сполуки, відомі з рівня техніки, такі як, наприклад, 3-ціанопропілбромід, тетрагідрофураніл-метансульфонат, 3гідроксипропілбромід, 2-метоксиетилбромід, 3метоксипропіл-хлорид, (транс)-4-(амінометил)-1[2-(1,3-діоксолан-2-іл)етил]-3-піперидин [описаний в Міжнародній публікації WO-00/37461 як проміжна сполука 8], 1-хлор-3-(1-метилетокси)пропан, 2-(3хлорпропіл)-2-метил-1,3-діоксолан, 2-(2брометил)-1,3-діоксолан, метил-4-бромбутаноат, 2-хлорацетонітрил, 2-(2-хлоретокси)етанол, N-(2хлоретил)метансульфонамід та N-[3[(метилсульфоніл)окси]пропіл]метансульфонамід. В. Одержання кінцевих сполук Приклад В.1 Суміш проміжної сполуки (95) (0,336моль) в НСІ/2-пропанолі (160мл) та 2-пропанолу (1400мл) перемішують та кип'ятять зі зворотним холодильником протягом 1 години. Розчинник випарюють, та залишок розчиняють у суміші DCM та невеликої кількості метанолу. Суміш промивають водяним розчином аміаку, органічний шар відокремлюють, сушать, фільтрують та упарюють, та одержують на виході 71г сполуки (255). Приклад В.2 а) Одержання 88607 54 проміжної сполуки (20) Суміш проміжної сполуки (85) (0,01моль), проміжної сполуки (115) (0,014моль) та карбонату натрію (0,02моль) в iзобутанолі (100мл) перемішують та кип'ятять зі зворотним холодильником протягом 40 годин, потім охолоджують та фільтрують. З фільтрату випарюють розчинник. Залишок очищують за допомогою колоночної хроматографії на силікагелі (елюент СН2СІ2/(СН3ОН/NН3), 97/3). Потрібні фракції збирають, випарюють розчинник, та одержують на виході 2,6г проміжної сполуки (20). b) Проміжну сполуки (20) (0,006моль) гідрують у метанолі з палладієм-на-карбоні (10%, 1г), як каталізатором, у присутності розчину тіофену (0,5мл). Після поглинання водню (3 еквіваленти) каталізатор відфільтровують, та випарюють розчинник. Залишок очищують на силікагелі на скляному фільтрі (елюент СН2СІ2/(СН3OН/NН3), 96/4). Потрібні фракції збирають, фільтрують, та випарюють розчинник. Залишок розчиняють в 2пропанолі та за допомогою обробки (Е)-2 55 88607 56 бутандиовой кислотою перетворюють у сіль (Е)-2рюють. Залишок очищують за допомогою колонобутандиовой кислоти (1:1). Речовину, що випала в чної хроматографії на силікагелі (елюент осад, відфільтровують, промивають та сушать, та СН2СІ2/(СН3ОН/NН3), 97/3). Фракції, що містять одержують на виході 1,8г сполуки (1) (температура продукт реакції, збирають, випарюють розчинник, плавлення 174°С). та одержують на виході 3,3г проміжні сполуки (20). Приклад В.З b) Суміш проміжної сполуки (44) (0,0067моль), а) Одержання 6N НСІ/2-пропанолу (0,03моль) та 2-пропанолу (80мл) перемішують та кип'ятять зі зворотним холодильником протягом 1 години, потім реакційну суміш охолоджують, та випарюють розчинник Залишок розчиняють в DCM, та розчин промивають 2% водяним розчином NaOH. Органічний шар відокремлюють, сушать, фільтрують, та випарюють розчинник Залишок суспендують в DIPE, суміш проміжної сполуки (43) Проміжну сполуки (26) (0,012моль) розчиняють кип'ятять та охолоджують Отриману речовину, що в DCM (60мл). Додають триетиламін (0,012моль) випала в осад, відфільтровують, промивають та та реакційну суміш охолоджують до температури сушать, та на виході одержують 1,78г сполуки (33) нижче 10°C. Обережно додають мурашину кислоту (температура плавлення 135°С). Приклад В.5 (0,012моль), реакційну суміш перемішують протяСуміш сполуки (255) (0,0125моль), 3гом 45 хвилин при температурі нижче за 10°С, та метоксипропілхлориду (0,025моль) та карбонату одержують суміш (А). Проміжну сполуки (67) калію (0,0375моль) в ACN (50мл) перемішують та (0,011моль) перемішують в DCM (60мл). Додають триетиламін (0,029моль), реакційну суміш перемікип'ятять зі зворотним холодильником протягом 20 шують протягом 45 хвилин при кімнатній темперагодин Реакційну суміш охолоджують виливають у турі, та одержують суміш (В). Суміш (А) додають воду та екстрагують DCM. Органічний шар відодо суміші (В), та отриману реакційну суміш перекремлюють, сушать, фільтрують, та випарюють мішують протягом ночі при кімнатній температурі. розчинник. Залишок очищують за допомогою колоночної хроматографії на силікагелі (елюент Реакційну суміш промивають 5% розчином NaOH СН2СІ2/(СН3ОН/NН3), 93/7/0,5). Чисті фракції збита потім водою. Органічний шар відокремлюють, рають, та випарюють розчинник. Речовину, що сушать, фільтрують, та випарюють розчинник. Залишок очищують за допомогою колоночної хровипала в осад, відфільтровують, перекристалізуматографії на силікагелі (елюент СН2СІ2/СН3ОН, ють із суміші 1-пропанону та DIPE, та одержують 95/5). Фракції, що містять продукт реакції, збирана виході 3г сполуки (200). (температура плавленють, випарюють розчинник, та одержують на вихоня 108°C; [a]20.D=-10,70° (с=10,28мг/2мл у метаноді 3,5г проміжної сполуки (43). лі)). b) Суміш проміжної сполуки (43) (0,007моль), Приклад В.6 6N НСІ/2-пропанолу (7мл) та 2-пропанолу (70мл) Суміш сполуки (8) (0,0094моль), бутаналю перемішують та кип'ятять зі зворотним холодиль(0,0094моль) та ацетату калію (0,015моль) гідруником протягом однієї години Розчинник випарюють у метанолі (100мл) із платиною-на-карбоні ють. Залишок обробляють водою та DCM Додають (5%, 1г), як каталізатором, у присутності розчину карбонат натрію. Органічний шар відокремлюють, тіофену (2мл). Після поглинання водню (1 еквівасушать, фільтрують, та випарюють розчинник. лент) каталізатор відфільтровують на целіті, та Залишок суспендують в DIPE, відфільтровують та фільтрат упарюють. Залишок обробляють 2% восушать (вакуум, 40°С) Залишок розчиняють у воді дяним розчином NaOH (100мл) та DCM (150мл). та 50% розчині NaOH. Отриману суміш екстрагуШари розділяють. Водну фазу знову екстрагують ють DCM. Органічний шар відокремлюють, сушать, DCM (100мл). Об'єднані органічні шари сушать, фільтрують, та випарюють розчинник Залишок фільтрують, та випарюють розчинник. Залишок сушать (вакуум, 40°С), потім кристалізують із очищують за допомогою колоночної хроматографії DIPE/ACN, відфільтровують та сушать, та одерна силікагелі (елюент СН2СІ2/(СН3ОН/NН3), 97/3). жують на виході 1,3г сполуки (2) (температура Фракції, що містять продукт реакції, збирають, та плавлення 150°С). випарюють розчинник. Залишок розчиняють в ACN Приклад В.4 та перетворюють у сіль етандіової кислоти (1:2), a) Одержання потім відфільтровують та сушать, та одержують на виході 1,62г сполуки (11) (температура плавлення >110°С). Подібну процедуру можна використати для одержання сполук, таких як, наприклад, сполуки (64), заміняючи бутиральдегид на 4фторбензальдегид. проміжної сполуки (44) Приклад В.7 Суміш проміжної сполуки (88) (0,0106моль), 1Проміжну сполуки (123) (0,004моль) у воді бром-2-метоксиетану (0,015моль) та карбонату (100мл) перемішують та кип'ятять зі зворотним натрію (0,02моль) в ізобутанолі (100мл) переміхолодильником протягом 6 годин. Реакційну суміш шують та кип'ятять зі зворотним холодильником охолоджують та промивають DCM. Розчинник випротягом 20 годин, потім реакційну суміш охолопарюють. Залишок суспендують в ACN. Речовину, джують, солі відфільтровують, та фільтрат упащо випала в осад, відфільтровують, промивають 57 88607 58 та сушать, та одержують на виході 1,58г сполуки дують в DIPE/ACN (0°С) Речовину, що випала в (16) (температура плавлення 240°С). осад, відфільтровують та сушать, та одержують на Приклад В.8 виході 1,1г сполуки (63) (температура плавлення До суспензії проміжної сполуки (12) (0,01моль) 180°С). в DCM (75мл) додають триетиламін (1,4мл), та Приклад В.11 реакційну суміш охолоджують до температури Суміш проміжної сполуки (130) (0,016моль), 2нижче за 0°С. При температурі нижче за 0°С дохлор-3-метилпиразину (0,016моль) та оксиду дають по краплях мурашину кислоту (0,96мл), та кальцію (0,02моль) в DMA (5мл) перемішують при реакційну суміш перемішують протягом 30 хвилин температурі 120°С протягом 48 годин та потім при температурі нижче за 0°С. Додають суспензію охолоджують. Додають воду, та суміш екстрагують проміжної сполуки (69) (0,01моль) в DCM (25мл) та сумішшю СН2СІ2/СН3ОН. Органічний шар відокретриетиламін (2,4мл), та потім суміш перемішують млюють, сушать, фільтрують, та випарюють розпри кімнатній температурі протягом 3 годин. Дочинник. Залишок очищують за допомогою колонодають DCM (100мл) та воду (150мл), суміш перечної хроматографії на силікагелі (елюент мішують, та шари розділяють. Органічний шар СН2СІ2/(СН3ОН/NН3), 93/7). Потрібні фракції збипромивають 5% водяним розчином NaOH та ворають, та випарюють розчинник. Залишок суспендою, потім сушать, фільтрують, та випарюють роздують в DIPE (0°С). Речовину, що випала в осад, чинник. Залишок очищують за допомогою колоновідфільтровують та сушать, та одержують на вичної хроматографії на силікагелі (елюент ході 1, 45г сполуки (68) (температура плавлення СН2СІ2/(СН3ОН/NН3), 96/4). Фракції, що містять 100°С). продукт реакції, збирають, та випарюють розчинПриклад В.12 ник. Залишок кристалізують із DIPE з невеликою a) Одержання кількістю ACN, отримане Речовину, що випала в осад, відфільтровують та сушать, та одержують на виході 2,2г сполуки (26) (температура плавлення 106-108°С). Приклад В.9 Суміш сполуки (43) (0,0051моль) в 5% соляній проміжної сполуки (131) кислоті (50мл) та THF (50мл) перемішують протяСуміш проміжної сполуки (88) (0,01моль) та гом ночі при кімнатній температурі та потім конце1,1-диметилового ефіру метил-(3нтрують у вакуумі. Концентрат подлужують водяоксопропіл)карбамінової кислоти (±0,015моль) ним розчином аміаку та екстрагують DCM (3х). гідрують у THF (100мл) з палладієм-на-карбоні Органічний шар відокремлюють, сушать, фільтру(10%, 2г), як каталізатором, у присутності розчину ють, та випарюють розчинник. Залишок кристалітіофену (2мл). Після поглинання водню (1 еквівазують із DIPE/ACN. Речовину, що випала в осад, лент) каталізатор відфільтровують, та фільтрат відфільтровують та сушать, та одержують на виупарюють. Залишок очищують хроматографією на ході 1,9г сполуки (44) (температура плавлення коротких колонках на силікагелі. Фракції, що міс130°С). тять продукт реакції, збирають, випарюють розПриклад В.10 чинник, та одержують на виході 2,9г проміжної a) Одержання сполуки (131). b) Суміш проміжної сполуки (131) (0,0048моль), НСІ/2-пропанолу (6N, 5мл) та 2пропанолу (100мл) перемішують та кип'ятять зі зворотним холодильником протягом 1 години, потім реакційну суміш охолоджують, та випарюють розчинник. Залишок розчиняють в DCM та промипроміжної сполуки (130) вають 2% водяним розчином NaOH. Органічний Сполуки (24) (0,026моль) гідрують в шар відокремлюють, сушать, фільтрують, та випаCH3OH/NH3 (250мл) з нікелем Ренея, як каталізарюють розчинник. Залишок очищують за допомотором, у присутності розчину тіофену (1мл). Після гою колоночної хроматографії на силікагелі (елюпоглинання водню (2 еквіваленти) каталізатор ент СН2СІ2/(СН3ОН/NН3), 90/10). Фракції, що відфільтровують, та випарюють розчинник. Залимістять продукт реакції, збирають, та випарюють шок кристалізують із ACN (0°С). Речовину, що вирозчинник. Залишок розчиняють в 2-пропанолі та пала в осад, відфільтровують та сушать, та одерза допомогою обробки фумаровою кислотою (2 жують на виході 8г проміжної сполуки (130). еквіваленти) перетворюють у сіль (Е)-2b) Проміжну сполуку (130) (0,008моль) розчибутандіової кислоти (2:3). Речовину, що випала в няють у хлороформі (100мл). Додають триетилаосад, відфільтровують та сушать, та одержують на мін (0,012моль). Додають по краплях розчин метавиході 1,13г сполуки (81) (температура плавлення нсульфонілхлориду (0,008моль) у хлороформі >130°С). (10мл) при температурі нижче за 5°С. Реакційну Приклад В.13 суміш перемішують протягом 30 хвилин, промиваa) Одержання ють водою, сушать, фільтрують, та випарюють розчинник. Залишок очищують за допомогою колоночної хроматографії на силікагелі (елюент СН2СІ2/(СН3ОН/NН3), 93/7). Потрібні фракції збирають, та випарюють розчинник. Залишок суспен 59 88607 60 та одержують на виході 3,1 г проміжної сполуки (133). b) Суміш проміжної сполуки (133) (0,006моль), НСІ/2-пропанолу (6N, 6мл) та 2-пропанолу (60мл) перемішують та кип'ятять зі зворотним холодильником протягом 1 години. Реакційну суміш залипроміжної сполуки (132) шають на ніч при кімнатній температурі та потім Суміш проміжної сполуки (3) (0,013моль) та концентрують. Залишок обробляють водяним розDCM (60мл) перемішують та охолоджують на кричином аміаку та DCM. Органічний шар відокремжаній лазні. Обережно додають триетиламін люють, сушать, фільтрують та концентрують. Про(0,013моль), суміш перемішують при температурі дукт реакції кристалізують із ACN та DIPE, 10°С, потім додають по краплях мурашину кислоту відфільтровують та сушать, та одержують на ви(0,013моль), та суміш перемішують протягом 45 ході 1,55г сполуки (113) (температура плавлення хвилин. Додають розчин проміжної сполуки (73) 126°С). (0,012моль) в DCM (30мл), та реакційну суміш пеПриклад В.15 ремішують протягом ночі при кімнатній температуa) Одержання рі. Реакційну суміш промивають 5% водяним розчином NaOH та водою. Водний шар відокремлюють та екстрагують DCM. Органічний шар відокремлюють, сушать, фільтрують та концентрують. Залишок очищують за допомогою колоночної хроматографії на силікагелі (елюент СН2СІ2/СН3ОН, 90/10). Чисті фракції збирають, та випарюють розчинник. Залишок концентрують із толуолом, випарюють розчинник, та одержують на виході 2,75г проміжної сполуки (132). b) Суміш проміжної сполуки (132) (0,0069моль) та метанолу (150мл) гідрують з палладієм-накарбоні (10%, 1г), як каталізатором, у присутності розчину тіофену (1мл). Після поглинання водню (3 еквіваленти) каталізатор відфільтровують на декаліті та фільтрат концентрують. Залишок кристалізують із 2-пропанолу та DIPE та перетворюють у сіль етандіової кислоти (2:3). Залишок відфільтровують та сушать, та одержують на виході 2,25г сполуки (107) (температура плавлення >160°С). Приклад В.14 а) Одержання проміжної сполуки (133) Суміш проміжної сполуки (26) (0,016моль) та DCM (60мл) перемішують, додають триетиламін (0,016моль), та реакційну суміш охолоджують на крижаній лазні (температура нижче за 10°С). Потім додають по краплях мурашину кислоту (0,016моль), та реакційну суміш перемішують при температурі нижче за 10°С протягом 45 хвилин (розчин А). Розчин проміжної сполуки (69) (0,013моль) в DCM (60мл) перемішують при кімнатній температурі, додають триетиламін (0,03моль), та реакційну суміш перемішують при кімнатній температурі протягом 45 хвилин. Додають перший розчин (А), та реакційну суміш перемішують протягом ночі при кімнатній температурі. Реакційну суміш промивають водою. Органічний шар відокремлюють, сушать, фільтрують та концентрують. Залишок очищують за допомогою колоночної хроматографії на силікагелі (елюент СН2СІ2/(СН3ОН/NН3, 7N), 95/5). Фракції, що містять продукт реакції, збирають, випарюють розчинник, проміжної сполуки (134) Сполуку (226) (0,013моль) гідрують в CH3OH/NH3 (300мл) з нікелем Ренея (1г), як каталізатором. Після поглинання водню (2 еквіваленти) каталізатор відфільтровують, фільтрат упарюють, та одержують на виході 5,1г проміжної сполуки (134). b) До суміші проміжної сполуки (134) (0,0064моль) та триетиламіну (0,013моль) в DCM (60мл) при кімнатній температурі додають по краплях метансульфонілхлорид (0,54мл). Через 3 години додають метансульфонілхлорид (0,2мл), та суміш перемішують протягом 24 годин. Суміш промивають водою, органічний шар сушать, фільтрують, та випарюють розчинник. Залишок очищують колоночной флеш-хроматографiей на силікагелі (елюент СН2СІ2/(СН3ОН/NН3), 99/1, 98/2, 97/3). Фракції, що містять продукт реакції, збирають, та випарюють розчинник. Залишок кристалізують із DIPE з невеликою кількістю ACN, відфільтровують, промивають та сушать, та одержують на виході 0,7г сполуки (193) (температура плавлення 134°С; [a]20.D=-9,83° (С=23,40мг/5мл у СН3СН)). Приклад В.16 Суміш сполуки (192) (0,006моль), піридину (0,012моль), DCM (50мл) та THF (50мл) перемішують (5°С) в атмосфері аргону. Додають по краплях (5°С) тіонілхлорид (0,006моль). Реакційну суміш перемішують при температурі 5°С протягом 1 години, та барботують через неї аміак (газ) при температурі 5°С протягом 10 хвилин. Після досягнення кімнатної температури суміш перемішують протягом 2 годин, розчиняють в DCM та промивають водою. Органічний шар сушать, фільтрують, та випарюють розчинник. Залишок очищують на скляному фільтрі на силікагелі (елюент СН2СІ2/(СН3ОН/NН3), 93/7). Фракції, що містять продукт реакції, збирають, та випарюють розчинник. Залишок кристалізують із DIPE, відфільтровують, промивають та сушать, та одержують на виході 0,4г сполуки (197) (температура плавлення 136°С; [[a]20.D=-11,52° (с=10,42мг/5мл у СН3ОН)). Приклад В.17
ДивитисяДодаткова інформація
Назва патенту англійською4-(aminomethyl)-piperidine benzamides as 5ht4-antagonists
Автори англійськоюBosmans Jean-Paul Rene Marie Andre, Gijsen Henricus Jacobus Maria, Mevellec Laurence Anne
Назва патенту російською4-(аминометил)пиперидинбензамиды как 5нт4-антагонисты
Автори російськоюБосманс Жан-Поль Рене Мари Андре, Гийсен Хенрикус Якобус Мария, Мевеллек Лоренс Анн
МПК / Мітки
МПК: C07D 405/14, A61K 31/453, C07D 405/12, A61P 1/04
Мітки: 4-(амінометил)піперидинбензаміди, 5нт4-антагоністи
Код посилання
<a href="https://ua.patents.su/70-88607-4-aminometilpiperidinbenzamidi-yak-5nt4-antagonisti.html" target="_blank" rel="follow" title="База патентів України">4-(амінометил)піперидинбензаміди як 5нт4-антагоністи</a>
Попередній патент: Ножова головка кутера, диск ножової головки, система з диска і ножів (варіанти) і спосіб складання ножової головки (варіанти)
Наступний патент: Кухонно-столовий прибор із чохлом тримача
Випадковий патент: Підсилювач постійного струму












