Кристалічні похідні піразолу
Формула / Реферат
1. Кристалічна форма, Форма І, 4-[5-(4-фторфеніл)-3-(трифторметил)-1Н-піразол-1-іл]-бензолсульфонаміду, яка має дифрактограму рентгенівського випромінювання на порошку, що включає піки, виражені в градусах (±0,1 градус) кутів два тета 14,0, 18,9, 21,3, 21,9 та 25,7, одержані з використанням рентгенівських променів ![]() (довжина хвилі =
(довжина хвилі = ![]() ).
).
2. Спосіб перетворення кристалічної форми, Форми II, 4-[5-(4-фторфеніл)-3-(трифторметил)-1Н-піразол-1-іл]-бензолсульфонаміду на кристалічну форму за п. 1, в якому здійснюють:
(a) змішування суспензії Форми II 4-[5-(4-фторфеніл)-3-(трифторметил)-1Н-піразол-1-іл]-бензолсульфонаміду в придатному розчиннику при температурі від приблизно 0 °С до приблизно 60 °С;
(b) перемішування суспензії при температурі від приблизно 0 °С до приблизно 60 °С з витримуванням при цій температурі протягом 24-72 год.; та
(c) збирання кристалів Форми І.
3. Спосіб за п. 2, в якому розчинник вибирають з групи, що складається з води, метанолу, етанолу, ізопропанолу, ацетону, ацетонітрилу, метиленхлориду, толуолу і тетрагідрофурану, а також сумішей цих компонентів.
4. Спосіб перетворення кристалічної форми, Форми II, 4-[5-(4-фторфеніл)-3-(трифторметил)-1Н-піразол-1-іл]-бензолсульфонаміду на кристалічну форму за п. 1, в якому здійснюють:
(a) розчинення вказаної Форми II у розчиннику, що змішується з водою, в якому розчинність Форми II становить більше 2 мг/мл при температурі від приблизно 10 °С до приблизно 60°С;
(b) осадження сполуки додаванням води;
(c) перемішування суспензії із стадії іі) протягом періоду від 2 до 72 год. при температурі від приблизно 15 °С до приблизно 45 °С; та
d) збирання кристалів Форми І.
5. Спосіб за п. 4, в якому розчинник вибирають з групи, що складається з етанолу, ацетону, ацетонітрилу, тетрагідрофурану, діоксану та диметилформаміду.
6. Фармацевтична композиція, яка містить кристалічну форму за п. 1.
7. Композиція за п. 6, яка відрізняється тим, що додатково містить фармацевтично прийнятний носій або ексципієнт.
8. Спосіб профілактики або лікування запального стану у тварини, який включає введення тварині терапевтично ефективної кількості кристалічної форми за п. 1.
9. Спосіб за п. 8, в якому вказана тварина вибрана з групи, що складається з великої рогатої худоби, овець, кіз, коней, свиней, птахів, котів, собак і людей.
10. Застосування композиції за п. 6 для виробництва медикаменту для профілактики або лікування запального стану у тварини.
11. Спосіб одержання кристалічної форми за п. 1, який включає наступні стадії:
(a) змішування 1,0-1,6 моль алкілтрифторацетату на моль 4-фторацетофенону, 1,0-1,5 моль алкоксиду металу на моль 4-фторацетофенону та відомої кількості 4-фторацетофенону для утворення суміші;
(b) поєднання суміші із стадії (а) з комбінацією від 415 до 1245 мл води на моль 4-фторацетофенону, 1,1-2,0 моль концентрованої хлористоводневої кислоти на моль 4-фторацетофенону, 0,8-1,2 моль гідрохлориду 4-сульфонамідофенілгідразину на моль 4-фторацетофенону та придатним розчинником, таким чином, що загальна кількість розчинника в суміші становить від 550 до 1660 мл на моль 4-фторацетофенону;
(c) додавання до суміші затравної кількості кристалів Форми І 4-[5-(4-фторфеніл)-3-(трифторметил)-1Н-піразол-1-іл]-бензолсульфонаміду на базі 4-фторацетофенону;
(d) збирання кристалів Форми І.
12. Спосіб за п. 11, в якому додатково додають до суміші на стадії (а) придатний розчинник в об'ємі до 1380 мл на моль 4-фторацетофенону.
13. Спосіб за п. 12, в якому розчинником є 2-пропанол.
14. Спосіб за п. 11, в якому алкоксид металу вибирають з групи, що складається з метоксиду натрію, етоксиду натрію, ізопропоксиду натрію, трет-бутоксиду натрію, метоксиду літію, етоксиду літію, ізопропоксиду літію, трет-бутоксиду літію, метоксиду калію, етоксиду калію, ізопропоксиду калію, трет-бутоксиду калію та сумішей цих компонентів.
15. Спосіб за п. 14, в якому алкоксидом металу є метоксид натрію.
16. Спосіб за п. 11, який після стадії (а) додатково включає стадію, що полягає в нагріванні суміші до температури в інтервалі від температури, вищої за кімнатну, до температури кипіння із зворотним холодильником до закінчення реакції.
17. Спосіб за п. 16, який після стадії нагрівання додатково включає стадію, яка полягає в охолодженні суміші до температури від -5 °С до 30 °С.
18. Спосіб за п. 11, в якому стадія (b) включає додавання суміші до комбінації води, хлористоводневої кислоти та гідрохлориду 4-сульфонамідофенілгідразину.
19. Спосіб за п. 11, в якому розчинник на стадії (b) є спиртом.
20. Спосіб за п. 19, в якому спиртом є 2-пропанол.
21. Спосіб за п. 11, який після стадії (b) додатково включає стадію, яка полягає в нагріванні суміші при температурі, вище за кімнатну температуру, до температури кипіння із зворотним холодильником до закінчення реакції.
22. Спосіб за п. 21, який після стадії нагрівання додатково включає стадію, яка включає стабілізацію суміші при температурі від кімнатної температури до -71,5 °С.
23. Спосіб за п. 11, в якому затравна кількість становить від 0,0001 % до 50 % (мас).
24. Спосіб за п. 23, в якому затравна кількість становить від 0,001 % до 5 % (мас).
25. Спосіб за п. 23, в якому затравна кількість становить від 0,01 % до 0,5 % (мас).
26. Спосіб за п. 11, який після стадії (с) додатково включає стадію, яка полягає в нагріванні суміші при температурі від 40 °С до менше 71,5 °С, з витримуванням при цій температурі протягом 1-10 год.
27. Спосіб за п. 26, який після стадії нагрівання додатково включає стадію, яка включає охолодження суміші до температури від -5 °С до 30 °С.
28. Спосіб за п. 11, який після стадії (с) додатково включає стадію, яка полягає у фільтруванні суміші і промиванні кристалів Форми І придатним розчинником або водою або сумішшю цих компонентів.
29. Спосіб за п. 28, в якому розчинником є спирт.
30. Спосіб за п. 29, в якому спиртом є 2-пропанол.
31. Спосіб за п. 11, який після стадії (d) додатково включає стадію сушіння кристалів Форми І при температурі від 15 °С до 80 °С.
32. Спосіб одержання кристалічної форми, вказаної в п. 1, який включає наступні стадії:
(а) змішування 1,2-1,45 моль алкілтрифторацетату на моль 4-фторацетофенону, 1,1-1,35 моль алкоксиду металу на моль 4-фторацетофенону та відомої кількості 4-фторацетофенону для утворення суміші;
(b) поєднання суміші із стадії (а) з комбінацією 650-870 мл води на моль 4-фторацетофенону, 1,2-1,7 моль концентрованої хлористоводневої кислоти на моль 4-фторацетофенону, 0,9-1,1 моль гідрохлориду 4-сульфонамідофенілгідразину на моль 4-фторацетофенону і придатним розчинником, таким чином, що загальна кількість розчинника в суміші становить від 600 до 1000 мл на моль 4-фторацетофенону;
(c) додавання до суміші затравної кількості кристалів Форми І 4-[5-(4-фторфеніл)-3-(трифторметил)-1Н-піразол-1-іл]-бензолсульфонаміду по відношенню до 4-фторацетофенону;
(d) збирання кристалів Форми І.
33. Спосіб за п. 32, в якому додатково додають до суміші на стадії (а) об'єм придатного розчинника до 900 мл на моль 4-фторацетофенону.
34. Спосіб за п. 33, в якому розчинником є 2-пропанол.
35. Спосіб за п. 32, в якому алкоксид металу вибирають з групи, що складається з метоксиду натрію, етоксиду натрію, ізопропоксиду натрію, трет-бутоксиду натрію, метоксиду літію, етоксиду літію, ізопропоксиду літію, трет-бутоксиду літію, метоксиду калію, етоксиду калію, ізопропоксиду калію та трет-бутоксиду калію, а також сумішей цих компонентів.
36. Спосіб за п. 35, в якому алкоксидом металу є метоксид натрію.
37. Спосіб за п. 32, який після стадії (а) додатково включає стадію, яка полягає в нагріванні суміші при температурі, вище за кімнатну температуру, до температури кипіння із зворотним холодильником до закінчення реакції.
38. Спосіб за п. 37, який після стадії нагрівання додатково включає стадію, яка включає охолодження суміші до кімнатної температури.
39. Спосіб за п. 32, в якому стадія (b) включає додавання суміші до комбінації води, хлористоводневої кислоти та гідрохлориду 4-сульфонамідофенілгідразину.
40. Спосіб за п. 32, в якому розчинником на стадії (b) є спирт.
41. Спосіб за п. 40, в якому спиртом є 2-пропанол.
42. Спосіб за п. 32, який після стадії (b) додатково включає стадію, яка полягає в нагріванні суміші при температурі, вище за кімнатну температуру, до температури кипіння із зворотним холодильником до закінчення реакції.
43. Спосіб за п. 42, який після стадії нагрівання додатково включає стадію стабілізації суміші при температурі від 40 °С до 65 °С.
44. Спосіб за п. 33, в якому затравна кількість становить від 0,0001 % до 50 % (мас).
45. Спосіб за п. 44, в якому затравна кількість становить від 0,001 % до 5 % (мас).
46. Спосіб за п. 44, в якому затравна кількість становить від 0,01 % до 0,5 % (мас).
47. Спосіб за п. 32, який після стадії (с) додатково включає стадію нагрівання суміші до температури від 50 °С до менше 71,5 °С, витримуючи при цій температурі протягом 3-8 год.
48. Спосіб за п. 47, який після стадії нагрівання додатково включає стадію охолодження суміші до кімнатної температури.
49. Спосіб за п. 32, який після стадії (с) додатково включає стадію фільтрування суміші та промивання кристалів Форми І придатним розчинником або водою або сумішшю цих компонентів.
50. Спосіб за п. 49, в якому розчинником є спирт.
51. Спосіб за п. 50, в якому спиртом є 2-пропанол.
52. Спосіб за п. 32, який після стадії (d) додатково включає стадію сушіння кристалів Форми І при температурі від 30 °С до 65 °С.
Текст
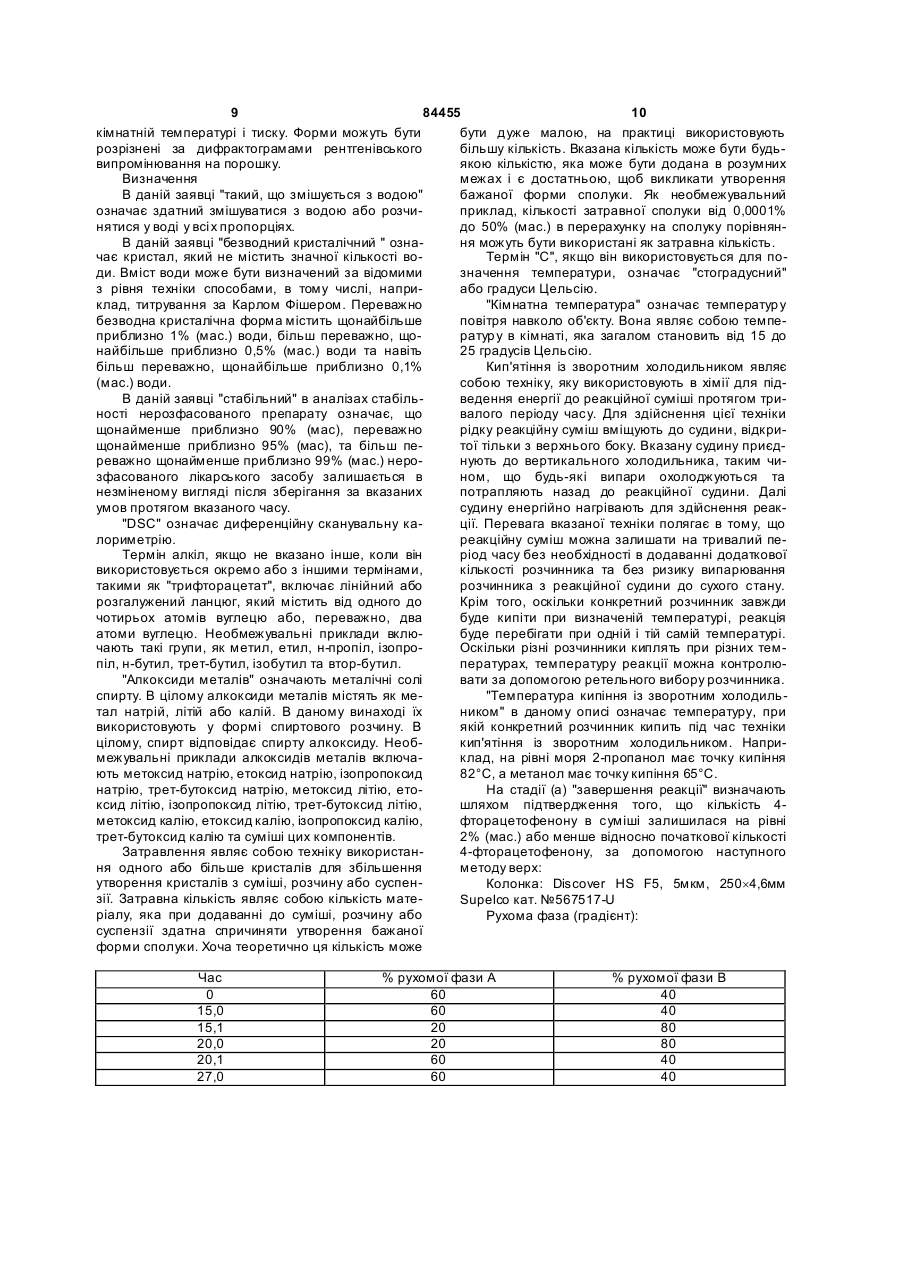
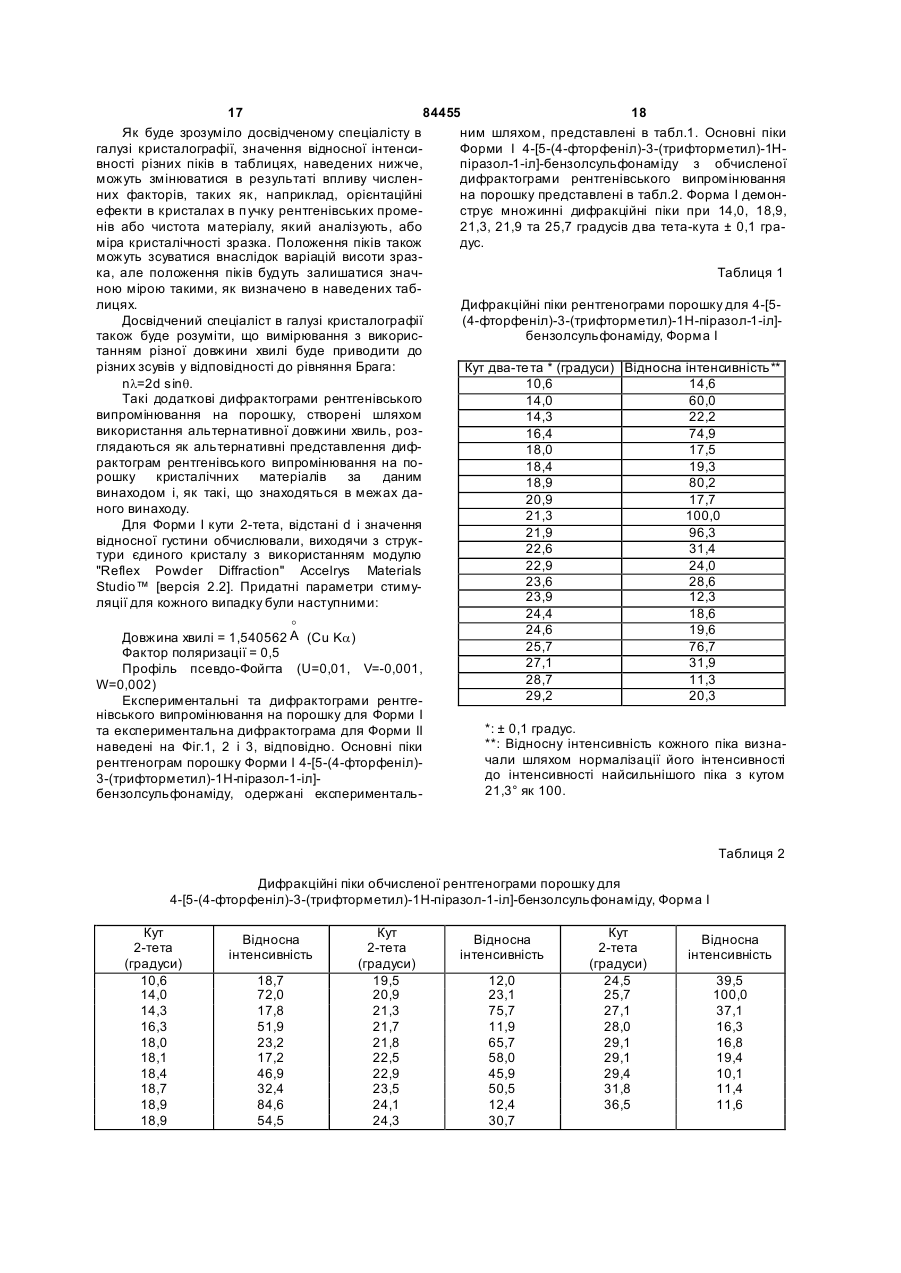
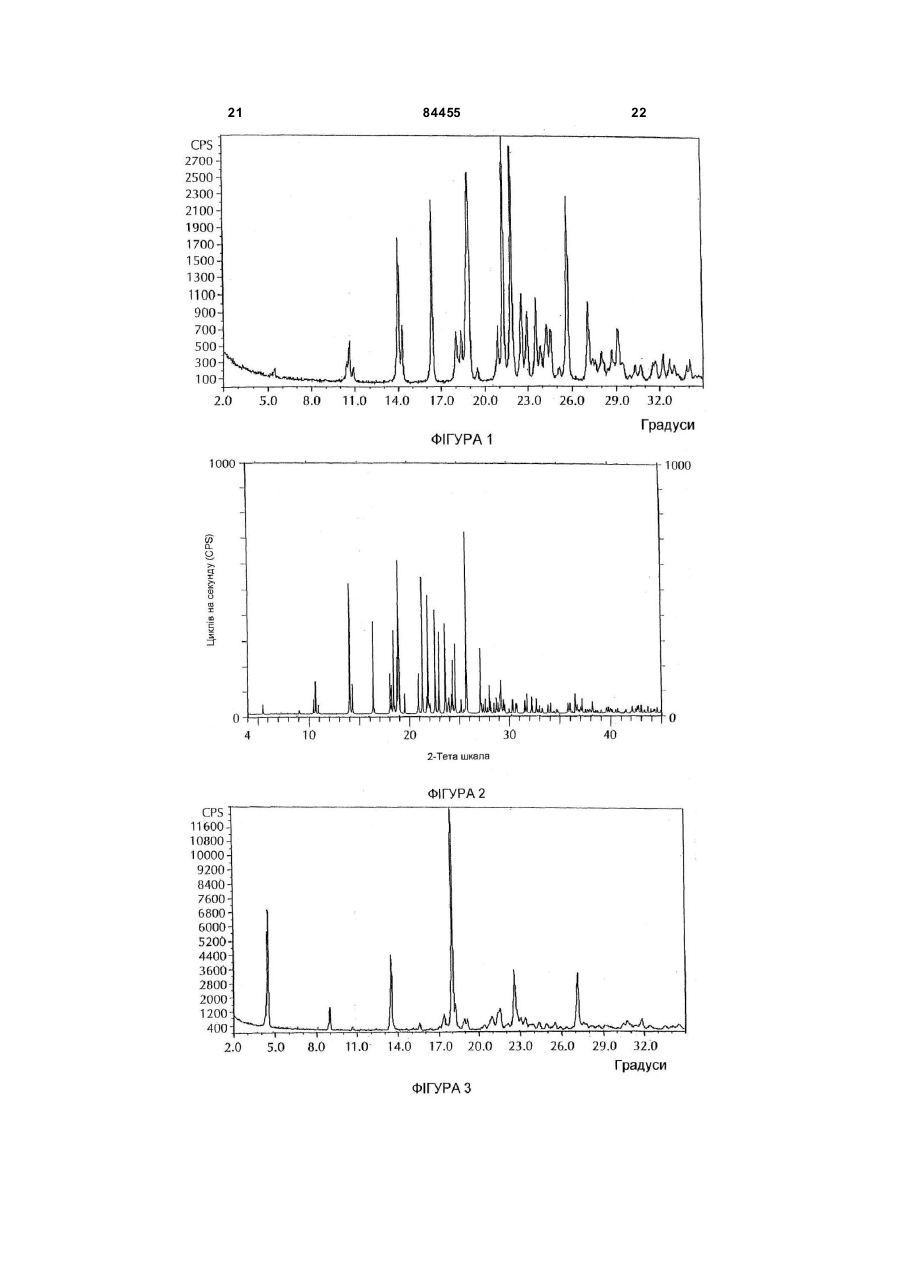
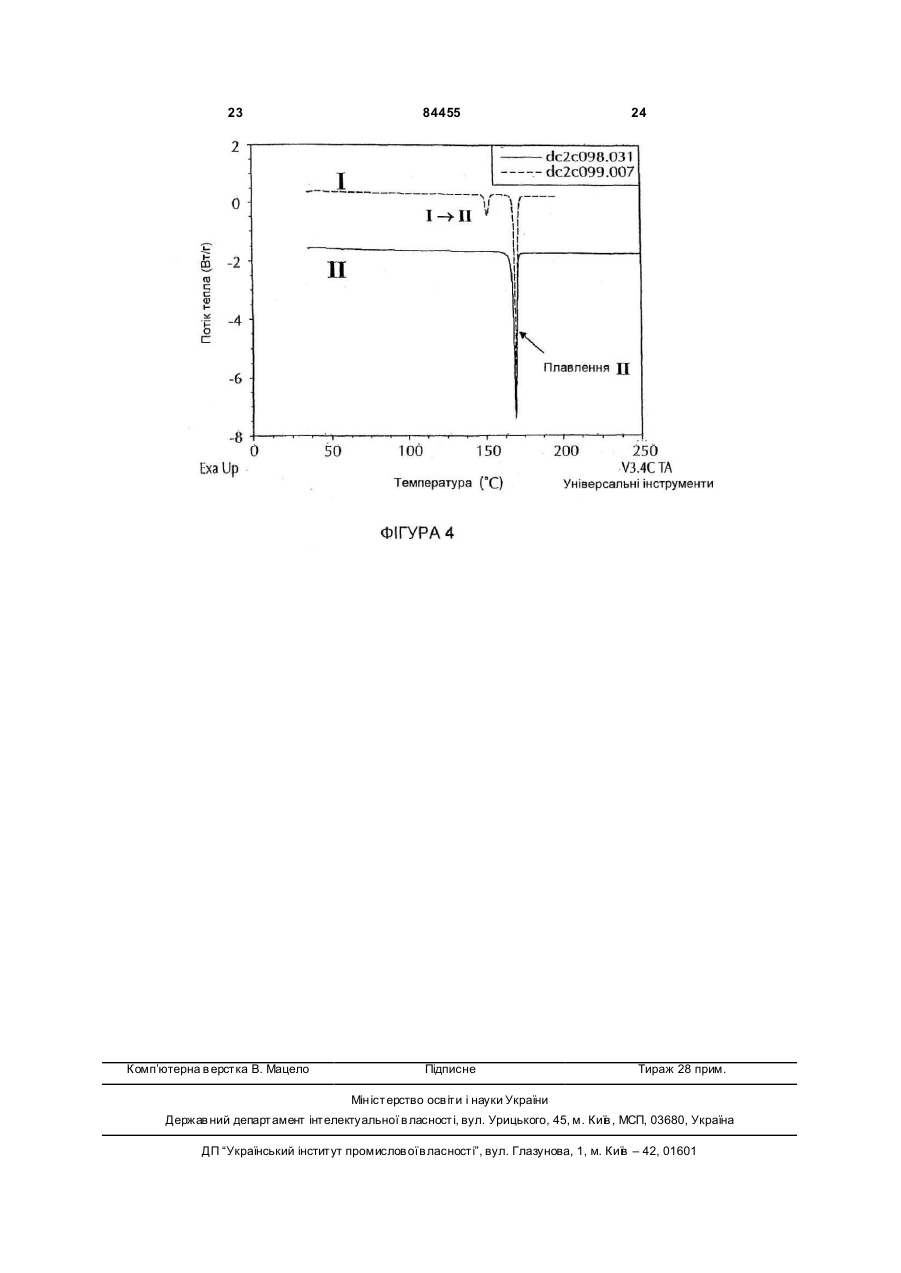
1. Кристалічна форма, Форма І, 4-[5-(4фтор феніл)-3-(трифторметил)-1Н-піразол-1-іл]бензолсульфонаміду, яка має дифрактограму рентгенівського випромінювання на порошку, що включає піки, виражені в градусах (±0,1 градус) кутів два тета 14,0, 18,9, 21,3, 21,9 та 25,7, одержані з використанням рентгенівських C2 2 (19) 1 3 84455 4 (трифторметил)-1Н-піразол-1-іл](а) змішування 1,2-1,45 моль алкілтрифторацетату бензолсульфонаміду на базі 4-фторацетофенону; на моль 4-фторацетофенону, 1,1-1,35 моль алкок(d) збирання кристалів Форми І. сиду металу на моль 4-фторацетофенону та відо12. Спосіб за п. 11, в якому додатково додають до мої кількості 4-фторацетофенону для утворення суміші на стадії (а) придатний розчинник в об'ємі суміші; до 1380 мл на моль 4-фторацетофенону. (b) поєднання суміші із стадії (а) з комбінацією 65013. Спосіб за п. 12, в якому розчинником є 2870 мл води на моль 4-фторацетофенону, 1,2-1,7 пропанол. моль концентрованої хлористоводневої кислоти на 14. Спосіб за п. 11, в якому алкоксид металу вибимоль 4-фторацетофенону, 0,9-1,1 моль гідрохлорають з групи, що складається з метоксиду натрію, риду 4-суль фонамідофенілгідразину на моль 4етоксиду натрію, ізопропоксиду натрію, третфторацетофенону і придатним розчинником, табутоксиду натрію, метоксиду літію, етоксиду літію, ким чином, що загальна кількість розчинника в ізопропоксиду літію, трет-бутоксиду літію, метоксуміші становить від 600 до 1000 мл на моль 4сиду калію, етоксиду калію, ізопропоксиду калію, фторацетофенону; трет-бутоксиду калію та сумішей цих компонентів. (c) додавання до суміші затравної кількості крис15. Спосіб за п. 14, в якому алкоксидом металу є талів Форми І 4-[5-(4-фторфеніл)-3метоксид натрію. (трифторметил)-1Н-піразол-1-іл]16. Спосіб за п. 11, який після стадії (а) додатково бензолсульфонаміду по відношенню до 4включає стадію, що полягає в нагріванні суміші до фторацетофенону; температури в інтервалі від температури, вищої за (d) збирання кристалів Форми І. кімнатну, до температури кипіння із зворотним 33. Спосіб за п. 32, в якому додатково додають до холодильником до закінчення реакції. суміші на стадії (а) об'єм придатного розчинника 17. Спосіб за п. 16, який після стадії нагрівання до 900 мл на моль 4-фторацетофенону. додатково включає стадію, яка полягає в охоло34. Спосіб за п. 33, в якому розчинником є 2дженні суміші до температури від -5 °С до 30 °С. пропанол. 18. Спосіб за п. 11, в якому стадія (b) включає до35. Спосіб за п. 32, в якому алкоксид металу вибидавання суміші до комбінації води, хлористоводрають з групи, що складається з метоксиду натрію, невої кислоти та гідрохлориду 4етоксиду натрію, ізопропоксиду натрію, третсульфонамідофенілгідразину. бутоксиду натрію, метоксиду літію, етоксиду літію, 19. Спосіб за п. 11, в якому розчинник на стадії (b) ізопропоксиду літію, трет-бутоксиду літію, метокє спиртом. сиду калію, етоксиду калію, ізопропоксиду калію та 20. Спосіб за п. 19, в якому спиртом є 2-пропанол. трет-бутоксиду калію, а також сумішей цих компо21. Спосіб за п. 11, який після стадії (b) додатково нентів. включає стадію, яка полягає в нагріванні суміші 36. Спосіб за п. 35, в якому алкоксидом металу є при температурі, ви ще за кімнатну температуру, метоксид натрію. до температури кипіння із зворотним холодильни37. Спосіб за п. 32, який після стадії (а) додатково ком до закінчення реакції. включає стадію, яка полягає в нагріванні суміші 22. Спосіб за п. 21, який після стадії нагрівання при температурі, ви ще за кімнатну температуру, додатково включає стадію, яка включає стабілізадо температури кипіння із зворотним холодильницію суміші при температурі від кімнатної темпераком до закінчення реакції. тури до -71,5 °С. 38. Спосіб за п. 37, який після стадії нагрівання 23. Спосіб за п. 11, в якому затравна кількість стадодатково включає стадію, яка включає охолоновить від 0,0001 % до 50 % (мас). дження суміші до кімнатної температури. 24. Спосіб за п. 23, в якому затравна кількість ста39. Спосіб за п. 32, в якому стадія (b) включає доновить від 0,001 % до 5 % (мас). давання суміші до комбінації води, хлористовод25. Спосіб за п. 23, в якому затравна кількість станевої кислоти та гідрохлориду 4новить від 0,01 % до 0,5 % (мас). сульфонамідофенілгідразину. 26. Спосіб за п. 11, який після стадії (с) додатково 40. Спосіб за п. 32, в якому розчинником на стадії включає стадію, яка полягає в нагріванні суміші (b) є спирт. при температурі від 40 °С до менше 71,5 °С, з ви41. Спосіб за п. 40, в якому спиртом є 2-пропанол. тримуванням при цій температурі протягом 1-10 42. Спосіб за п. 32, який після стадії (b) додатково год. включає стадію, яка полягає в нагріванні суміші 27. Спосіб за п. 26, який після стадії нагрівання при температурі, ви ще за кімнатну температуру, додатково включає стадію, яка включає охолодо температури кипіння із зворотним холодильнидження суміші до температури від -5 °С до 30 °С. ком до закінчення реакції. 28. Спосіб за п. 11, який після стадії (с) додатково 43. Спосіб за п. 42, який після стадії нагрівання включає стадію, яка полягає у фільтруванні суміші додатково включає стадію стабілізації суміші при і промиванні кристалів Форми І придатним розчинтемпературі від 40 °С до 65 °С. ником або водою або сумішшю цих компонентів. 44. Спосіб за п. 33, в якому затравна кількість ста29. Спосіб за п. 28, в якому розчинником є спирт. новить від 0,0001 % до 50 % (мас). 30. Спосіб за п. 29, в якому спиртом є 2-пропанол. 45. Спосіб за п. 44, в якому затравна кількість ста31. Спосіб за п. 11, який після стадії (d) додатково новить від 0,001 % до 5 % (мас). включає стадію сушіння кристалів Форми І при 46. Спосіб за п. 44, в якому затравна кількість статемпературі від 15 °С до 80 °С. новить від 0,01 % до 0,5 % (мас). 32. Спосіб одержання кристалічної форми, вказа47. Спосіб за п. 32, який після стадії (с) додатково ної в п. 1, який включає наступні стадії: включає стадію нагрівання суміші до температури 5 84455 6 від 50 °С до менше 71,5 °С, витримуючи при цій ня кристалів Форми І придатним розчинником або температурі протягом 3-8 год. водою або сумішшю ци х компонентів. 48. Спосіб за п. 47, який після стадії нагрівання 50. Спосіб за п. 49, в якому розчинником є спирт. додатково включає стадію охолодження суміші до 51. Спосіб за п. 50, в якому спиртом є 2-пропанол. кімнатної температури. 52. Спосіб за п. 32, який після стадії (d) додатково 49. Спосіб за п. 32, який після стадії (с) додатково включає стадію сушіння кристалів Форми І при включає стадію фільтрування суміші та промивантемпературі від 30 °С до 65 °С. Даний винахід стосується кристалічних форм 4-[5-(4-фторфеніл)-3-(трифторметил)-1Н-піразол1-іл]бензолсульфонаміду та способів виготовлення, взаємного перетворення і виділення таких кристалів. 5-Фенілпіразоліл-1-бензолсульфонаміди являють собою новий синтетичний клас сполук з потужною ЦОГ-2-інгібуючою активністю, корисних для лікування артриту та інших станів, які є наслідком запалення. 4-[5-(4-Фторфеніл)-3(трифторметил)-1Н-піразол-1-іл]бензолсульфонамід являє собою 5фенілпіразоліл-1-бензолсульфонамід наступної структури: Сполука Формули І розкрита в [Патентах США №№5,466,823 (Tally та ін.) та 5,521,207 (Graneto)]. Вказані патенти включені до даного опису шляхом посилання. Хоча виготовлення сполуки Формули І розкрите, в специфікації не згадується про одержання і природу кристалічних форм агента. Існує потреба ідентифікувати поліморфну поведінку для забезпечення стабільності процесів, уникнення проблем при таблетуванні, руйнування таблеток, росту кристалів в суспензіях і наступного спікання, осадження з суспензій, а також проблем в процесі хімічного виробництва, таких як здатність до відфільтровування та забезпечення відтворюваності аналітичних методик [див. Analysis of Organic Polymorphs, A Review; Threlfall, T.L., Analyst, 120, pp.2435-2459]. В одному з аспектів даний винахід стосується кристалу Форми І 4-[5-(4-фторфеніл)-3(трифторметил)-1Н-піразол-1-іл]бензолсульфонаміду, який має дифрактограму рентгенівського випромінювання на порошку, що включає піки, виражені в градусах (±0,1 градус) кута два тета 14,0, 18,9, 21,3, 21,9 та 25,7, одержані з використанням рентгенівських променів o СuКa 1 (довжина хвилі = 1,5406 A ). В іншому аспекті винаходу передбачається спосіб перетворення кристалічної Форми II 4-[5-(4-фторфеніл)-3(трифторметил)-1Н-піразол-1-іл] бензолсульфонаміду на кристалічну Форму І, який включає і) змішування суспензії Форми II 4-[5-(4фтор феніл)-3-(трифторметил)-1Н-піразол-1-іл]бензолсульфонаміду з придатним розчинником при температурі від приблизно 0°С до приблизно 60°С; іі) перемішування суспензії при температурі від приблизно 0°С до приблизно 60°С з витримуванням при цій температурі протягом періоду від 24 до 72год.; та ііі) збирання кристалів Форми І. В іншому аспекті винаходу розчинник у вказаному способі вибирають з групи, що складається з води, метанолу, етанолу, ізопропанолу, ацетону, ацетонітрилу, метиленхлориду, толуолу і тетрагідрофурану, а також сумішей цих компонентів. Додатковий аспект винаходу являє собою спосіб перетворення кристалічної Форми II 4-[5-(4фтор феніл)-3-(трифторметил)-1Н-піразол-1-іл]бензолсульфонаміду на кристалічну Форму І, який включає (і) розчинення вказаної Форми II у розчиннику, який змішується з водою, в якому розчинність Форми II становить більше 2мг/мл, при температурі від приблизно 10°С до приблизно 60°С; (іі) осадження сполуки додаванням води; (ііі) перемішування суспензії із стадії (іі) протягом періоду від 2 до 72год. при температурі від приблизно 15°С до приблизно 45°С; та (iv) збирання кристалів Форми І. В іншому аспекті винаходу розчинник для вказаного процесу вибраний з групи, що складається з етанолу, ацетону, ацетонітрилу, тетрагідрофурану, діоксану та диметилформаміду. В іншому аспекті винахід стосується фармацевтичної композиції, яка включає кристалічну Форму І сполуки Формули І. В іншому аспекті винаходу фармацевтична композиція додатково містить фармацевтично прийнятний носій або допоміжну речовину. Ще одним об'єктом даного винаходу є спосіб профілактики або лікування запальних станів у тварин шляхом використанням терапевтично ефективної кількості нової композиції за даним винаходом. Іншим об'єктом даного винаходу є застосування нової композиції за даним винаходом для виробництва медикаменту для профілактики або лікування запального стану у тварини. Ще один об'єктом даного винаходу є одержання кристалічної Форми І 4-[5-(4-фторфеніл)-3(трифторметил)-1Н-піразол-1-іл]бензолсульфонаміду наступним шляхом. Стадія (а): змішування 1,0-1,6 моль або, переважно, 1,2-1,45 моль або, більш переважно, 1,251,35 моль алкілтрифторацетату на моль 4фторацетофенону з 1,0-0,5 моль або, переважно, 1,1-1,35 моль або, більш переважно, 1,15-1,25 моль алкоксиду металу на моль 4фторацетофенону та відомої кількості 4 7 84455 8 фторацетофенону для утворення суміші. На цій або, переважно, від 600 до 1060мл або, більш пестадії необов'язково додають до 1380мл або, переважно, від 800 до 860мл на моль 4реважно, до 900мл або, більш переважно, до фторацетофенону, та вода присутня в кількості від 490мл придатного розчинника, переважно 2100 до 700мл або, переважно, від 285 до 545мл пропанолу. С уміш із стадії (а) необов'язково нагріабо, більш переважно, від 385 до 445мл на моль вають до температури в інтервалі від температури 4-фторацетофенону. вище за кімнатну до температури кипіння із звороСтадія (d) Далі кристали Форми І збирають. тним холодильником або, переважно, до темпераКристали Форми І необов'язково сушать при темтури від 40°С до 70°С або, більш переважно, до пературі від 15°С до 80°С або, переважно, при температури від 50°С до 60°С, витримуючи при цій температурі від 30°С до 65°С, більш переважно, температурі протягом 1-24год. або, переважно, при температурі від 50°С до 60°С. протягом 1-10год. або, більш переважно, протягом В іншому аспекті винаходу алкоксид металу із 1-4 год. або, більш переважно, до закінчення реастадії (а) вибраний з групи, що складається з накції. Після такого нагрівання суміш необов'язково трію метоксиду, натрію етоксиду, натрію ізопропоохолоджують до температури від -5 °С до 30°С ксиду, натрію трет-бутоксиду, літію метоксиду, або, більш переважно, до кімнатної температури. літію етоксиду, літію ізопропоксиду, літію тpeтСтадія (b): суміш із стадії (а) поєднують з або, бутоксиду, калію метоксиду, калію етоксиду, калію переважно, додають до комбінації 415-1245мл ізопропоксиду та калію тpeт-бутоксиду, а також або, переважно, 650-870мл або, більш переважно, сумішей цих компонентів або, переважно, натрію 725-795мл води на моль 4-фторацетофенону плюс метоксиду. 1,1-2,0 моль або, переважно, 1,2-1,7 моль або, Вказані та інші об'єкти будуть легко зрозумібільш переважно, 1,3-1,5 моль, концентрованої лими спеціалістам в даній галузі. хлористоводневої кислоти на моль 4Фігура 1. На Фігурі 1 представлено визначену фторацетофенону плюс 0,8-1,2 моль або, переваекспериментально дифрактограму рентгенівського жно, 0,9-1,1 моль або, більш переважно, 0,95-1,05 випромінювання на порошку (PXRD) Форми І 4-[5моль гідрохлориду 4-сульфонамідофенілгідразину (4-фторфеніл)-3-(трифторметил)-1Н-піразол-1-іл]на моль 4-фторацетофенону і придатного розчинбензолсульфонаміду. ника, переважно С 1-С6 спирту або, більш переваФігура 2. На Фігурі 2 представлено обчислену жно, 2-пропанолу, таким чином, що загальна кільдифрактограму рентгенівського випромінювання кість розчинника в суміші становить від 550 до на порошку (PXRD) Форми І 4-[5-(4-фторфеніл)-31660мл або, переважно, від 600 до 1000мл або, (трифторметил)-1Н-піразол-1-іл]більш переважно, від 650 до 750мл на моль 4бензолсульфонаміду. фторацетофенону. Необов'язково суміш із стадії Фігура 3. На Фігурі 3 представлено дифрактог(b) нагрівають до температури в інтервалі від темраму рентгенівського випромінювання на порошку ператури вище за кімнатну до температури кипіння (PXRD) Форми II 4-[5-(4-фтор феніл)-3із зворотним холодильником або, переважно, до (трифторметил)-1Н-піразол-1-іл]температури від 40°С до 70°С або, переважно, до бензолсульфонаміду. температури від 50°С до 70°С протягом 1-24год. Фігура 4. На Фігурі 4 представлено дані дифеабо, переважно, протягом 1-10год. або, більш перенційної сканувальної калориметрії (DSC) для реважно, протягом 1-4год. або, більш переважно, Форм І та II 4-[5-(4-фторфеніл)-3-(трифторметил)до закінчення реакції. Після такого нагрівання су1Н-піразол-1-іл]-бензолсульфонаміду. міш необов'язково стабілізують при температурі в Селективний інгібітор ЦОГ-2 4-[5-(4інтервалі від кімнатної температури до 71,5°С або, фтор феніл)-3-(трифторметил)-1Н-піразол-1-іл]переважно, від 40°С до 65°С або, більш переважбензолсульфонамід (Формула І) но, від 50°С до 60°С. Стадія (с) Далі до суміші додають затравну кількість або, переважно, від 0,0001% до 50% (мас.) або, більш переважно, 0,001% до 5% (мас.) або, більш переважно, 0,01% до 0,5% (мас.) кристалів Форми І 4-[5-(4-фторфеніл)-3-(трифторметил)-1Нпіразол-1-іл]-бензолсульфонаміду відносно 4фторацетофенону. С уміш із стадії (с) необов'язково нагрівають до температури від 40°С до менше 71,5°С або, переважно, до температури від 50°С до менше 71,5°С або, більш переважно, до температури від 50°С до 60°С, витримуючи при цій тем[описаний в Патентах США №№5,466,823 and пературі протягом періоду від 1 до 10год. або, пе5,521,207]. В патенті описано синтез сполуки, але реважно, від 3 до 8год. або, більш переважно, від не згадується про кристалічну форму, яку одержу5 до 7год.. Після такого нагрівання суміш необоють. Як описано в прикладах, здійснення методив'язково охолоджують до температури від -5°С до ки, наведеної у вказаних патентах, приводить до 30°С або, більш переважно, до кімнатної темперакристалів Форми II, що було продемонстровано за тури. Суміш необов'язково фільтрують і промивадопомогою дифрактограм рентгенівського випроють з придатним розчинником, переважно спирмінювання на порошку (PXRD). Винахідниками том, більш переважно, 2-пропанолом або водою було виявлено, що вказана кристалічна форма є або сумішшю цих компонентів. Розчинник необонестабільною відносно іншої форми, Форми І, при в'язково присутній в кількості від 300 до 1500мл 9 84455 10 кімнатній температурі і тиску. Форми можуть бути бути дуже малою, на практиці використовують розрізнені за дифрактограмами рентгенівського більшу кількість. Вказана кількість може бути будьвипромінювання на порошку. якою кількістю, яка може бути додана в розумних Визначення межах і є достатньою, щоб викликати утворення В даній заявці "такий, що змішується з водою" бажаної форми сполуки. Як необмежувальний означає здатний змішуватися з водою або розчиприклад, кількості затравної сполуки від 0,0001% нятися у воді у всі х пропорціях. до 50% (мас.) в перерахунку на сполуку порівнянВ даній заявці "безводний кристалічний " ознаня можуть бути використані як затравна кількість. чає кристал, який не містить значної кількості воТермін "С", якщо він використовується для поди. Вміст води може бути визначений за відомими значення температури, означає "стоградусний" з рівня техніки способами, в тому числі, наприабо градуси Цельсію. клад, титрування за Карлом Фішером. Переважно "Кімнатна температура" означає температур у безводна кристалічна форма містить щонайбільше повітря навколо об'єкту. Вона являє собою темпеприблизно 1% (мас.) води, більш переважно, щоратур у в кімнаті, яка загалом становить від 15 до найбільше приблизно 0,5% (мас.) води та навіть 25 градусів Цельсію. більш переважно, щонайбільше приблизно 0,1% Кип'ятіння із зворотним холодильником являє (мас.) води. собою техніку, яку використовують в хімії для підВ даній заявці "стабільний" в аналізах стабільведення енергії до реакційної суміші протягом триності нерозфасованого препарату означає, що валого періоду часу. Для здійснення цієї техніки щонайменше приблизно 90% (мас), переважно рідку реакційну суміш вміщують до судини, відкрищонайменше приблизно 95% (мас), та більш петої тільки з верхнього боку. Вказану судину приєдреважно щонайменше приблизно 99% (мас.) неронують до вертикального холодильника, таким чизфасованого лікарського засобу залишається в ном, що будь-які випари охолоджуються та незміненому вигляді після зберігання за вказаних потрапляють назад до реакційної судини. Далі умов протягом вказаного часу. судину енергійно нагрівають для здійснення реак"DSC" означає диференційну сканувальну кації. Перевага вказаної техніки полягає в тому, що лориметрію. реакційну суміш можна залишати на тривалий пеТермін алкіл, якщо не вказано інше, коли він ріод часу без необхідності в додаванні додаткової використовується окремо або з іншими термінами, кількості розчинника та без ризику випарювання такими як "трифторацетат", включає лінійний або розчинника з реакційної судини до сухого стану. розгалужений ланцюг, який містить від одного до Крім того, оскільки конкретний розчинник завжди чотирьох атомів вуглецю або, переважно, два буде кипіти при визначеній температурі, реакція атоми вуглецю. Необмежувальні приклади вклюбуде перебігати при одній і тій самій температурі. чають такі групи, як метил, етил, н-пропіл, ізопроОскільки різні розчинники киплять при різних темпіл, н-бутил, тpeт-бутил, ізобутил та втор-бутил. пературах, температуру реакції можна контролю"Алкоксиди металів" означають металічні солі вати за допомогою ретельного вибору розчинника. спирту. В цілому алкоксиди металів містять як ме"Температура кипіння із зворотним холодильтал натрій, літій або калій. В даному винаході їх ником" в даному описі означає температуру, при використовують у формі спиртового розчину. В якій конкретний розчинник кипить під час техніки цілому, спирт відповідає спирту алкоксиду. Необкип'ятіння із зворотним холодильником. Напримежувальні приклади алкоксидів металів включаклад, на рівні моря 2-пропанол має точку кипіння ють метоксид натрію, етоксид натрію, ізопропоксид 82°С, а метанол має точку кипіння 65°С. натрію, тpeт-бутоксид натрію, метоксид літію, етоНа стадії (а) "завершення реакції" визначають ксид літію, ізопропоксид літію, трет-бутоксид літію, шляхом підтвердження того, що кількість 4метоксид калію, етоксид калію, ізопропоксид калію, фторацетофенону в суміші залишилася на рівні тpeт-бутоксид калію та суміші цих компонентів. 2% (мас.) або менше відносно початкової кількості Затравлення являє собою техніку використан4-фторацетофенону, за допомогою наступного ня одного або більше кристалів для збільшення методу верх: утворення кристалів з суміші, розчину або суспенКолонка: Discover HS F5, 5мкм, 250´4,6мм зії. Затравна кількість являє собою кількість матеSupelco кат. №567517-U ріалу, яка при додаванні до суміші, розчину або Рухома фаза (градієнт): суспензії здатна спричиняти утворення бажаної форми сполуки. Хоча теоретично ця кількість може Час 0 15,0 15,1 20,0 20,1 27,0 % рухомої фази А 60 60 20 20 60 60 % рухомої фази В 40 40 80 80 40 40 11 А: 0,05 % (об./об.) ТФО у воді В: 0,05 % (об./об.) ТФО в ацетонітрилі Швидкість потоку: Об'єм ін'єкції: Довжина хвилі детектування: 84455 1мл/хв 20мкл 247нм Колонка: Рухома фаза: Час утримування: Температура колонки: Швидкість потоку: Об'єм ін'єкції: Довжина хвилі визначення: Концентрація зразка: "Терапевтично ефективна кількість" означає таку кількість сполуки, яку вводять, що буде запобігати стану (наприклад, запальному стану) або полегшувати до певної міри один або більше з симптомів розладу, який підлягає лікуванню. Фармацевтичні композиції, придатні до застосування за даним винаходом, включають композиції, в яких активні інгредієнти містяться в кількості, достатній для досягнення передбаченої мети. Визначення терапевтично ефективної кількості знаходиться в межах кваліфікації спеціаліста в даній галузі, особливо у світлі детального розкриття, викладеного в даному описі. Тварини, які є придатними реципієнтами сполук за даним винаходом, включають, не обмежуючись ними, людей або інших ссавців або тварин, наприклад, сільськогосподарських тварин,: в тому числі велику рогату худобу, овець, свиней, коней, кіз та птахів (наприклад, курчат, індиків, качок і гусей та інши х пта хів), а також домашніх тварин, таких як собаки, коти та екзотичні тварини та/або тварини зоопарків. Передбачається лікування гризунів та інши х тварин. На практиці кількість сполуки для введення знаходиться в інтервалі від приблизно 0,001 до 100мг на кг маси тіла тварини, така загальна доза може бути введена в один прийом або розділена на кілька прийомів. Вона може бути введена окремо або в комбінації з одним або більше інших лікарських засобів. Загалом, вона буде вводитися у вигляді препарату в поєднанні з однією або більше фармацевтично прийнятними допоміжними речовинами. Термін "допоміжна речовина" в даному описі використовується для позначення будь-якого інгредієнта окрім сполук(и) за винаходом. Вибір допоміжної речовини буде великою мірою залежати від таких факторів, як конкретний спосіб введення, вплив допоміжної речовини на розчинність і стабільність, а також природа лікарської форми. Фармацевтичні композиції, придатні для введення сполук за даним винаходом, та способи їх виготовлення будуть легко зрозумілі спеціалістам в даній галузі. Такі композиції і способи їх виготовлення можуть бути знайдені, наприклад, в Remington's Pharmaceutical Sciences, 19-е вид. [Mack Publishing Company, 1995]. Для використання в ролі протизапального агента у тварин сполука за винаходом може вводити 12 На стадії (b), "завершення реакції" визначають шляхом підтвердження того, що кількість утвореного 4-[5-(4-фторфеніл)-3-(трифторметил)-1Нпіразол-1-іл]-бензолсульфонаміду становить більше 90%, за допомогою наступного методу ВЕРХ: Zorbax Eclipse XDB Phenil, 3,5мкм, 150´4,6мм 55/45 об./об. метанол/ 25мМ Н3РО4 при pH2,5 (pH коригують за допомогою NaOH) 30хв 35°С 1,0мл/хв 15мкл УФ при 254нм 0,4мг/мл ся перорально або шляхом ін'єкції. Якщо бажаним є вводити сполуку за винаходом у сухій, твердій дозованій лікарській формі, звичайно використовують капсули, пігулки або таблетки, які містять бажану кількість активних сполук. Вказані лікарські форми виготовляють шляхом ретельного однорідного змішування активного інгредієнта з придатними тонко подрібненими розбавниками, такими як крохмаль, лактоза, тальк, стеарат магнію, рослинні камеді і т.п. Такі дозовані лікарські форми можуть широко варіювати з урахуванням їхньої загальної маси і вмісту протизапального агента, в залежності від таких факторів, як тип тварини-хазяїна, яка підлягає лікуванню, сила і вид запалення та маса хазяїна. Рецептура таблеток обговорюється в Н. Lieberman та L. Lachman, Pharmaceutical Dosage Forms: Tablets, том 1, [Marcel Dekker, New York, 1980]. Альтернативно, протизапальні композиції за даним винаходом можуть вводитися тваринам парентерально, наприклад, внутрішньорубцево, внутрішньом'язово або шляхом підшкірної ін'єкції, і в цьому випадку активні інгредієнти розчиняють або диспергують в рідкому розчиннику-носії. Для парентерального введення активні матеріали придатним чином змішують з прийнятним розчинником, переважно з числа різноманітних рослинних олій, таких як арахісова олія, олія насіння бавовни і т.п. Також використовують інші розчинники для парентерального введення, такі як органічні препарати з використанням солкеталю (solketal), пропіленгліколю, гліцеринформалю та водні препарати для парентерального введення, часто в комбінації в різних пропорціях. Активну сполуку або сполуки розчиняють або суспендують в парентеральній композиції для введення; такі рецептури загалом містять від 0,005 до 5% (мас.) активної сполуки. В наступному описі винаходу наведені конкретні варіанти, в яких може бути втілений та описаний винахід. Вказані варіанти описані досить детально, щоб дати можливість спеціалістам в даній галузі втілити винахід. Можуть використовуватися інші варіанти і логічні та інші зміни можуть бути здійснені без виходу за межі винаходу. Наступний детальний опис, таким чином, не повинен бути інтерпретований як обмежуючий, і межі винаходу визначаються тільки формулою винаходу, яка до 13 84455 14 дається, разом з повною множиною еквівалентів, Стадія 2. Одержання 4-[5-(4-фторфеніл)-3які названі у вказаних пунктах формули. (трифторметил)-1Н-піразол-1-іліФорма II являє собою кристалічну форму, бензолсульфонаміду одержану за методикою, [описаною в Патенті США Гідрохлорид 4-сульфонамідофенілгідразину №5,466,823]. Способи одержання кристалічної (982мг, 4,4 ммоль) додають при перемішуванні до Форми І проілюстровані наступним, не обмежуюрозчину 4,4,4-трифтор-1-[4-(фтор)феніл]-бутанчим описом і прикладами. 1,3-діону (0,936г, 4,0 ммоль) в етанолі (50мл). РеаВ одному способі кристалічна Форма II 4-[5-(4кційну суміш нагрівають до кипіння із зворотним фтор феніл-3-(трифторметил)-1Н-піразол-1-іл]холодильником та перемішують протягом 20 год.. бензолсульфонаміду може бути суспендована і Після охолодження до кімнатної температури реазмішана з придатним розчинником, в якому концекційну суміш упарюють під вакуумом. Залишок нтрація лікарського засобу є вищою за точку насипереносять в етилацетат, промивають водою та чення, при температурі від приблизно 0°С до прирозсолом, сушать над магнію сульфатом, фільтблизно 60°С. Придатним розчинником є такий, в рують та упарюють під вакуумом з одержанням якому розчинність лікарського засобу є вищою за твердої речовини коричневого кольору, яку пере1мг/мл і меншою за 800мг/мл. Приклади придатних кристалізовують з етилацетату та ізооктану з одерозчинників включають, не обмежуючись ними, ржанням 0,8г 4-[5-(4-фторфеніл)-3воду, метанол, етанол, ізопропанол, ацетон, аце(трифторметил)-1Н-піразол-1-іл]тонітрил, метиленхлорид, толуол і тетрагідрофубензолсульфонаміду. 1 ран, а також їхні суміші. Суспензію перемішують Н ЯМР (CDCI3): d 7,92, 7,47, 7,22, 7,09, 6,76, при температурі від приблизно 0°С до приблизно 4,92. 60°С протягом періоду від 24 до 72год.. Кристали MC m/e ES-(M-H) 384. Форми І збирають фільтрацією. Тпл 167-171°С. За іншою методикою кристали Форми І можуть Методика 2 бути виготовленні шляхом осадження з розчину 4Одержання Форми І 4-[5-(4-фторфеніл)-3[5-(4-фторфеніл-3-(трифторметил)-1Н-піразол-1(трифторметил)-1Н-піразол-1-іл]іл]-бензолсульфонаміду в придатному розчиннику, бензолсульфонаміду без виділення кристалічної який змішується з водою, в якому розчинність споФорми II. луки вища за 2мг/мл, шляхом додавання води при Наступна методика описує загальний спосіб температурі від приблизно 10°С до приблизно одержання кристалічної Форми І 4-[5-(460°С. Приклади придатних розчинників для вигофтор феніл)-3-(трифторметил)-1Н-піразол-1-іл]товлення Форми І з Форми II включають етанол, бензолсульфонаміду без виділення кристалічної ацетон, ацетонітрил, тетрагідрофуран, діоксан і Форми II. диметилформамід. Після початкового осадження Частина А. 4-Фторацетофенон (1 молярний водою суспензію перемішують протягом періоду еквівалент) поєднують з сумішшю алкілтрифторавід 24 до 72год. при температурі від приблизно цетату (1,0-1,6 молярних еквівалентів), алкоксиду 15°С до приблизно 45°С і кристали Форми І збиметалу (1,0-1,5 молярних еквівалентів) та, необорають фільтрацією. в'язково, придатним розчинником (до 10л на кілоМетодика 1 грам 4-фторацетофенону). Одержана суміш може Одержання 4-[5-(4-фторфеніл)-3бути нагріта до температури кипіння із зворотним (трифторметил)-1Н-піразол-1-іл]холодильником (для завершення реакції). "Придабензолсульфонаміду, Форма II. тний розчинник" для вказаної частини А являє соНаступна методика є істотною мірою подібною бою С1-С6 насичений аліфатичний спирт, в тому до методики, [описаної в Прикладі 1 Патенту США числі нерозгалужені, розгалужені та циклічні спир№ 5,521,207] з некритичною варіацією використи. Необмежувальні приклади придатних розчинтання 4-фторацетофенону як вихідного матеріалу, ників включають такі спирти, як метанол, етанол, замість 4-хлорацетофенону. ізопропанол і т.п. та суміші цих компонентів. Стадія 1. Одержання 4,4,4-трифтор-144Частина В. Суміш з Частини А поєднують з су(фтор)феніл1-бутан-1,3-діону Етилтрифторацетат мішшю гідрохлориду 4(2,35г, 1,66ммоль) вміщують до круглодонної колсульфонамідофенілгідразину (0,8-1,2 молярних би об'ємом 50мл та розчиняють в метил-третеквівалентів відносно кількості 4бутиловому е фірі (7,5мл). При перемішуванні до фторацетофенону) і водної хлористоводневої кисрозчину крізь додаткову лійку додають 25% (мас.) лоти (1,1-2,0 молярних еквівалентів відносно кільнатрію метоксид (4,0мл, 17,7 ммоль) протягом 2хв. кості 4-фторацетофенону) у воді (3-9л на 1кг 4Далі 4'-фторацетофенон (2,1г, 15 ммоль) розчифторацетофенону). При необхідності може доданяють в метил-трет-бутиловому е фірі (2мл), і доватись придатний розчинник, таким чином, що дають до реакційної суміші по краплях протягом загальна кількість розчинника, присутня в Частині 5хв. Після перемішування протягом ночі В, знаходиться в інтервалі 4-12л на 1кг 4(15,75год.) додають 3н НСІ (7,0мл). Органічну фторацетофенону. Реакційна суміш може бути фракцію збирають, промивають розсолом (7.5мл), нагріта до температури кипіння із зворотним холосушать над сульфатом магнію, фільтрують та упадильником (для здійснення завершення реакції). рюють під вакуумом з одержанням 3,2г твердої Після завершення реакції суміш затравлюють криречовини блідо-оранжевого кольору. Тверду речосталами Форми І (0,0001% (мас.) або більше по вину перекристалізують з ізооктану з одержанням відношенню до 4-фторацетофенону) при темпера2,05г дюну. турах нижче 71,5°С. Тверді речовини відокремлюють фільтрацією і їх можна промивати та/або ре 15 84455 16 суспендувати в придатному розчиннику. Продукт Приклад 2 може бути висушений при температурі до 80°С. 380мг Форми II суспендують в 2мл етанолу. "Придатний розчинник" для вказаної частини В Частину сполуки розчиняють та надлишок твердої являє собою C1-С6-насичений аліфатичний спирт, сполуки суспендують в розчині. Одержану суспенв тому числі нерозгалужені, розгалужені та циклічзію перемішують за допомогою магнітної мішалки ні спирти і воду, а також суміші цих компонентів. при температурі від приблизно 20°С до приблизно Наступна методика описує переважний спосіб 30°С, витримуючи при цій температурі протягом 2 одержання кристалічної Форми І 4-[5-(4тижнів. В кінці вказаного періоду тверду речовину фтор феніл)-3-(трифторметил)-1Н-піразол-1-іл]відфільтровують та ідентифікують за допомогою бензолсульфонаміду без виділення кристалічної рентгеноструктурного аналізу порошку як Форму І. Форми II. До першої судини додають 2-пропанол Приклад 3 (70мл) та етилтрифторацетат (27,15г, 0,191 моль), 1,5г Форми II додають до 2мл ацетонітрилу з з наступним промиванням лінії 2-пропанолом одержанням суспензії. Суспензію перемішують за (10мл). Далі до судини додають 25% натрію методопомогою магнітної мішалки при температурі від ксид в метанолі (37,5г, 0,174 моль), з наступним приблизно 20°С до приблизно 30°С, витримуючи промиванням лінії 2-пропанолом (10мл). Далі допри цій температурі протягом 2 тижнів. В кінці вкадають 4-фторацетофенон (20г, 0,145 моль) з назаного періоду тверду речовину відфільтровують ступним промиванням лінії 2-пропанолом (10мл). та ідентифікують за допомогою рентгеноструктурВміст судини нагрівають до 55°С, витримуючи при ного аналізу порошку як Форму І. цій температурі протягом 2 год., після чого охолоПриклад 4 джують до кімнатної температури. Воду (110мл), 0,5г Форми II додають до 2мл суміші метанол концентровану хлористоводневу кислоту (20,0г, + вода (1:1, об./об.) з одержанням суспензії. Су0,203 моль) та гідрохлорид 4спензію перемішують за допомогою магнітної місульфонамідофенілгідразину (32,4г, 0,145 моль) шалки при температурі від приблизно 20°С до додають до другої судини з наступним промиванприблизно 30°С, витримуючи при цій температурі ням лінії водою (10мл). Вміст першої судини допротягом 4 тижнів. В кінці вказаного періоду твердають до другої судини, з наступним промиванням ду речовину відфільтровують та ідентифікують за лінії 2-пропанолом (60мл). Об'єднаний вміст нагрідопомогою рентгеноструктурного аналізу порошку вають до 70°С, витримуючи при цій температурі як Форму І. протягом 2год., потім охолоджують до 55°С і заПриклад 5 травлюють 10мг (0,05% (мас.) відносно кількості 481,5кг 4-[5-(4-фторфеніл)-3-(трифторметил)фторацетофенону) Форми І 4-[5-(4-фтор феніл)-31Н-піразол-1-іл]-бензолсульфонаміду повністю (трифторметил)-1Н-піразол-1-іл]розчиняють в 81,5кг етанолу (6 об'ємів) при 40°С і бензолсульфонаміду. Вміст нагрівають до 55°С, фільтрують в гарячому стані. Додають до розчину витримуючи при цій температурі протягом 6год., 154л води (9 об'ємів) протягом періоду 1год., підпотім охолоджують до кімнатної температури та тримуючи температуру на рівні 40°С, з наступним фільтрують. Продукт промивають 50% водним 2охолодженням до 20°С. Суспензію перемішують пропанолом (120мл) і водою (60мл), потім сушать при 20°С, витримуючи при цій температурі протяпід вакуумом при температурі 55°С з одержанням гом 24год., та фільтрують з одержанням 4-[5-(44-[5-(4-фторфеніл)-3-(трифторметил)-1Н-піразолфтор феніл)-3-(трифторметил)-1Н-піразол-1-іл]1-іл]-бензолсульфонаміду поліморфу бажаної Фобензолсульфонаміду у ви гляді Форми І. рми І (44,8г, 80%). Приклад 6. Рентгеноструктурний аналіз пороВинахід далі описаний більш детально за дошку. помогою наступних необмежувальних прикладів. Рентгеноструктурний аналіз порошку провоПриклади дили з використанням системи Scintag X2 AdПриклад 1 vanced Diffraction System (під контролем Scintag 1Мл деіонізованої води ретельно перемішують DMS/NT 1.30а та програмного забезпечення Miз 1мл ізопропілового спирту в скляному флаконі crosoft Windows NT 4.0). Система використовує об'ємом 20мл. До флакону додають Форму II 4-[5мідне джерело рентгенівських променів (45кВ та (4-фторфеніл)-3-(трифторметил)-1Н-піразол-1-іл]40мА) з одержанням СuКa-, емісії 1,5406 А і твербензолсульфонаміду (258,6мг). Вставляють магнідофазного охолоджуючого детектора Peltier. Щітну мішалку і флакон ретельно закупорюють. Сулину для променів контролювали з використанням спензію перемішують при -200об./хв протягом трубкової дивергенції та щілин проти розсіювання приблизно 30хв. Спостерігається утворення густої 2 і 4мм, а також щілин детектора проти розсіяння і пастоподібної суспензії. Перемішування припинясприймаючих щілин 0,5 та 0,2мм шириною. Дані ють і флакону дозволяють стояти протягом 3 днів. реєстрували в інтервалі від 2° до 35° (два-тета) з Частину суспензії видаляють та сушать на абсорвикористанням покрокового сканування від буючому папері. Дифрактограма рентгенівського 0,037крок з періодом зчитування одна секунда на випромінювання на порошку вказаної твердої рекрок. Для експериментів використовували круглі човини наведена на Фігурі 1. Температура плавалюмінієві тримачі зразків Scintag, які завантажулення деяких виділених кристалів, яке спостерігаються зверху, з діаметром порожнини 12мм. Поли під мікроскопом для високотемпературних рошки пакували в тримач і обережно притискали досліджень, становила 148-152°С. Однак, вказапредметним склом для забезпечення компланарний інтервал може не відтворюватися внаслідок ності між поверхнею зразка і поверхнею тримача переходу Форми І у Форму II в інтервалі від 140 до зразка. 155°С. 17 84455 18 Як буде зрозуміло досвідченому спеціалісту в ним шляхом, представлені в табл.1. Основні піки галузі кристалографії, значення відносної інтенсиФорми І 4-[5-(4-фторфеніл)-3-(трифторметил)-1Нвності різних піків в таблицях, наведених нижче, піразол-1-іл]-бензолсульфонаміду з обчисленої можуть змінюватися в результаті впливу числендифрактограми рентгенівського випромінювання них факторів, таких як, наприклад, орієнтаційні на порошку представлені в табл.2. Форма І демонефекти в кристалах в п учку рентгенівських проместрує множинні дифракційні піки при 14,0, 18,9, нів або чистота матеріалу, який аналізують, або 21,3, 21,9 та 25,7 градусів два тета-кута ± 0,1 граміра кристалічності зразка. Положення піків також дус. можуть зсуватися внаслідок варіацій висоти зразка, але положення піків будуть залишатися значТаблиця 1 ною мірою такими, як визначено в наведених таблицях. Дифракційні піки рентгенограми порошку для 4-[5Досвідчений спеціаліст в галузі кристалографії (4-фторфеніл)-3-(трифторметил)-1Н-піразол-1-іл]також буде розуміти, що вимірювання з викорисбензолсульфонаміду, Форма І танням різної довжини хвилі буде приводити до різних зсувів у відповідності до рівняння Брага: Кут два-те та * (градуси) Відносна інтенсивність** nl=2d sinq. 10,6 14,6 Такі додаткові дифрактограми рентгенівського 14,0 60,0 випромінювання на порошку, створені шляхом 14,3 22,2 використання альтернативної довжини хвиль, роз16,4 74,9 глядаються як альтернативні представлення диф18,0 17,5 рактограм рентгенівського випромінювання на по18,4 19,3 рошку кристалічних матеріалів за даним 18,9 80,2 винаходом і, як такі, що знаходяться в межах да20,9 17,7 ного винаходу. 21,3 100,0 Для Форми І кути 2-тета, відстані d і значення 21,9 96,3 відносної густини обчислювали, виходячи з струк22,6 31,4 тури єдиного кристалу з використанням модулю 22,9 24,0 "Reflex Powder Diffraction" Accelrys Materials 23,6 28,6 Studio™ [версія 2.2]. Придатні параметри стиму23,9 12,3 ляції для кожного випадку були наступними: 24,4 18,6 o 24,6 19,6 A (Сu Κa) Довжина хвилі = 1,540562 25,7 76,7 Фактор поляризації = 0,5 27,1 31,9 Профіль псевдо-Фойгта (U=0,01, V=-0,001, 28,7 11,3 W=0,002) 29,2 20,3 Експериментальні та дифрактограми рентгенівського випромінювання на порошку для Форми І *: ± 0,1 градус. та експериментальна дифрактограма для Форми II **: Відносну інтенсивність кожного піка визнанаведені на Фіг.1, 2 і 3, відповідно. Основні піки чали шляхом нормалізації його інтенсивності рентгенограм порошку Форми І 4-[5-(4-фторфеніл)до інтенсивності найсильнішого піка з кутом 3-(трифторметил)-1Н-піразол-1-іл]21,3° як 100. бензолсульфонаміду, одержані експерименталь Таблиця 2 Дифракційні піки обчисленої рентгенограми порошку для 4-[5-(4-фторфеніл)-3-(трифторметил)-1Н-піразол-1-іл]-бензолсульфонаміду, Форма І Кут 2-тета (градуси) 10,6 14,0 14,3 16,3 18,0 18,1 18,4 18,7 18,9 18,9 Відносна інтенсивність 18,7 72,0 17,8 51,9 23,2 17,2 46,9 32,4 84,6 54,5 Кут 2-тета (градуси) 19,5 20,9 21,3 21,7 21,8 22,5 22,9 23,5 24,1 24,3 Відносна інтенсивність 12,0 23,1 75,7 11,9 65,7 58,0 45,9 50,5 12,4 30,7 Кут 2-тета (градуси) 24,5 25,7 27,1 28,0 29,1 29,1 29,4 31,8 36,5 Відносна інтенсивність 39,5 100,0 37,1 16,3 16,8 19,4 10,1 11,4 11,6 19 84455 20 Приклад 7. Диференційна сканувальна калоратурі додавали надлишок одного поліморфу у риметрія (DSC). вигляді твердої речовини. Щонайменше через Дані диференціальної сканувальної калориме30хв додавали інший поліморф. Суспензію безпетрії (DSC) одержували з використанням калоримерервно перемішували протягом щонайменше тра DSC (ТА Instruments 2920). Порошок (1-5мг) трьох днів. Частину суспензії відбирали і негайно пакували в алюмінієвій формі для DSC. Алюмінієфільтрували. Відфільтровану тверду речовину ву кришечку розташовували на верхній частині аналізували за допомогою рентгеноструктурного форми і запресовували. Запресовану форму вміаналізу порошку для ідентифікації рівноваги тверщували в кювету для зразка разом з порожньою дої речовини при вказаній температурі. Рівноважформою як зразком порівняння. Температуру підний поліморф є термодинамічно більш стабільним вищували від 30°С до 250°С зі швидкістю 10°С/хв, при конкретній температурі. Шляхом повторення якщо не вказано інше. Термічну кювету продували експерименту визначали Тt при різних температусухим азотом при 50мл/хв. ТА Instruments Thermal рах. Solutions™ для NT (версія 1.3L) застосовували для Результати. збирання даних та для аналізу даних застосовуКристалізація суспензії. Результати кристалівали Universal Analysis™ для NT (версія 2.4F). Як зації суспензії продемонстрували, що при темпеможна побачити на Фігурі 4, дані диференціальної ратурі вище 71,5°С суміш Форм І та II завжди песканувальної калориметрії для Форми І демонретворюється на Форму II, але при температурі струють перехід ендотермальної фази з Форми І менше 71,0°С Форма І являє собою рівноважну до Форми II при температурі від 140°С до 155°С. тверду фазу. Таким чином, Форма І є термодинаПриклад 8. Термодинамічний взаємозв'язок мічно більш стабільною при температурах менше між Формами І та II. 71,0°С, тоді як Форма II є більш стабільною при В даному прикладі описано температуру перетемпературах ви ще за 71,5°С. Значення Tt, повиходу між Формами І та II. Форма І та Форма II є нно знаходитися між 71,0 та 71,5°С. енантіотропними, що означає, що один поліморф є Обговорення стабільним при температурах нижче за темпераВажливо визначити Tt для одержання та обротуру переходу, Тt тоді як інший поліморф є стабібки нерозфасованого лікарського засобу. Наприльним при температурах вище за Tt. Дві тверді клад, стадію, яка включає кристалізацію з розчину, фази мають рівні значення вільної енергії при темчасто здійснюють до кінцевого одержання нерозпературі переходу. Знання взаємозв'язку термофасованого лікарського засобу. Якщо Tt, для цідинамічної стабільності є необхідним для вибору льової форми є нижчою за температуру кристаліпридатних умов кристалізації для утворення Форзації, може бути важко кристалізувати лікарський ми І, а також для розробки і комерційного виробзасіб у вигляді чистої фази. Ін шим прикладом є ництва препарату. Для виготовлення і обробки сушка гранул, які містять лікарський засіб, після нерозфасованого лікарського засобу важливо вивологої грануляції. Якщо температура сушки вища значити Tt. за Tt, можуть виникати неконтрольовані поліморфМатеріали та методи. ні зміни лікарського засобу. Зміни, в свою чергу, Матеріали. Зразок Форми І, який використовуможуть впливати на наступну обробку, якість та вали в даному дослідженні, мав чистоту 100% за ефективність кінцевих продуктів. Температура даними ВЕРХ. Форму II готували шляхом нагріпереходу Tt визначена на рівні приблизно 71°С з вання Форми І до 155°С, витримуючи при цій темвикористанням суспензійної кристалізації. Оскільки пературі протягом 3 днів в сухій печі з наступним Форма І є більш стабільною при температурах охолодженням до кімнатної температури. На монижче приблизно 71°С та стає метастабільною мент дослідження за даними ВЕРХ вказаний зравідносно Форми II при температурі вище ~71°С, зок Форми II був вільним від хімічного розкладанкристал Форми І повинен зберігати стабільність ня. твердої фази в нормальному інтервалі температур Методи. Кристалізація суспензії. Взаємозв'язок кристалізації і зберігання, до тих пір, поки темпевідносної стабільності між Формами І та II при конратура нижче 71°С. кретній температурі були визначали шляхом суДаний винахід детально описаний, в тому чисспендування суміші двох поліморфів в толуолі в лі шляхом посилання на різні конкретні і переважні закупореному скляному флаконі, врівноваженому варіанти і техніки. Однак, слід розуміти, що можуть при цільовій температурі. Спочатку до насиченого бути здійснені численні варіації та модифікації без толуолу в скляному флаконі при вибраній темпевиходу за межі даного винаходу. 21 84455 22 23 Комп’ютерна в ерстка В. Мацело 84455 Підписне 24 Тираж 28 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюCrystalline pyrazole derivatives
Автори англійськоюSun Changquan Calvin, O'connor Garry
Назва патенту російськоюКристаллические производные пиразола
Автори російськоюСун Чангкван Келвин, О'Коннор Гарри
МПК / Мітки
МПК: A61P 29/00, C07D 231/12, A61K 31/415
Мітки: піразолу, кристалічні, похідні
Код посилання
<a href="https://ua.patents.su/12-84455-kristalichni-pokhidni-pirazolu.html" target="_blank" rel="follow" title="База патентів України">Кристалічні похідні піразолу</a>
Попередній патент: Спосіб одержання гідрофобних поліолів та поліуретанові системи, що їх містять
Наступний патент: Гербіцидний засіб
Випадковий патент: Пристрій для занурювання будівельних елементів