17a-фторалкілстероїди, що мають андрогенну активність, спосіб їх одержання та фармацевтична композиція, яка містить ці сполуки
Номер патенту: 76125
Опубліковано: 17.07.2006
Автори: Вурва Ральф, Рінг Свен, Кауфманн Гюнтер, ЕЛЬГЕР Вальтер
Формула / Реферат
1. 17![]() -фторалкілстероїди загальної формули І
-фторалкілстероїди загальної формули І
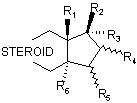 , (І)
, (І)
у якій
R1 являє собою С1-С4алкільну групу,
R2 являє собою гідроксигрупу, групу ОС(О)-R20 або ОR21, де R20 і R21 означають С1-С12алкільну групу, С3-С8циклоалкільну групу, арильну групу або арил-С1-С4алкільну групу,
R3 являє собою залишок формули CnF2n+1, де n означає 1, 2, 3, 4, 5 або 6,
R4 і R5 кожний являє собою атом водню або обидва разом утворюють подвійний зв’язок або метиленовий місток,
R5 і R6 кожний являє собою атом водню або обидва разом утворюють подвійний зв’язок або метиленовий місток,
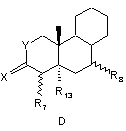
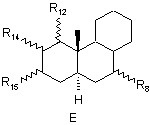
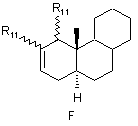
STEROID являє собою стероїдну АВС-циклічну систему субформул А, В, С, D, Е і F
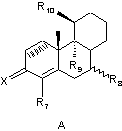 ,
,
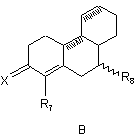 ,
,
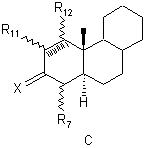 ,
,
 ,
,
 ,
,
 ,
,
при цьому у формулах А і С у положенні 1,2 може знаходитися додатковий подвійний зв'язок, а у формулі В у положенні 8,9 і в положенні 11,12 можуть знаходитися один або два додаткові подвійні зв'язки,
R7 являє собою атом водню, атом галогену, гідроксильну групу або трифторметильну групу,
Х означає атом кисню або два атоми водню,
R8 являє собою атом водню, метильну або етильну групу,
R9 являє собою атом водню або атом галогену або разом з R10 утворює подвійний зв'язок,
R10 являє собою атом водню, гідроксильну групу, метильну або етильну групу або разом з R9 утворює подвійний зв'язок,
R11 являє собою атом водню, С1-С4алкільну групу, нітрильну групу, гідроксиметиленову або формільну групу,
R12 являє собою атом водню, С1-С4алкільну групу або нітрильну групу,
R11 і R12 поряд з вищевказаними значеннями разом утворюють метиленовий місток,
R13 являє собою атом водню або разом з R7 утворює подвійний зв'язок,
R14 і R15 разом утворюють подвійний зв'язок, оксиранове кільце, тіїранове кільце, [2,3с]оксадіазольне кільце, [3,2с]ізоксазольне кільце або [3,2с]піразольне кільце,
Y означає атом кисню або азоту,
при цьому хвилясті лінії біля R7, R8, R11, R12, R13, R14 і R15 означають, що дані замісники можуть знаходитися в ![]() - або
- або ![]() -положенні, за винятком сполук із групи, яка включає
-положенні, за винятком сполук із групи, яка включає
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметиландрост-4-ен-3-он,
-трифторметиландрост-4-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметилестр-4-ен-3-он,
-трифторметилестр-4-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметилестр-4,9-дієн-3-он,
-трифторметилестр-4,9-дієн-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметилестр-4,9,11-триєн-3-он,
-трифторметилестр-4,9,11-триєн-3-он,
13-етил-17![]() -гідрокси-17
-гідрокси-17![]() -трифторметилгон-4-ен-3-он,
-трифторметилгон-4-ен-3-он,
13-етил-17![]() -гідрокси-17
-гідрокси-17![]() -трифторметилгон-4,9-дієн-3-он і
-трифторметилгон-4,9-дієн-3-он і
13-етил-17![]() -гідрокси-17
-гідрокси-17![]() -трифторметилгон-4,9,11-триєн-3-он.
-трифторметилгон-4,9,11-триєн-3-он.
2. 17![]() -фторалкілстероїди за п. 1, при цьому STEROID являє собою стероїдну циклічну систему субформули А.
-фторалкілстероїди за п. 1, при цьому STEROID являє собою стероїдну циклічну систему субформули А.
3. 17![]() -фторалкілстероїди за п. 1, при цьому STEROID являє собою стероїдну циклічну систему субформули В.
-фторалкілстероїди за п. 1, при цьому STEROID являє собою стероїдну циклічну систему субформули В.
4. 17![]() -фторалкілстероїди за п. 1, при цьому STEROID являє собою стероїдну циклічну систему субформули С.
-фторалкілстероїди за п. 1, при цьому STEROID являє собою стероїдну циклічну систему субформули С.
5. 17![]() -фторалкілстероїди за п. 1, при цьому STEROID являє собою стероїдну циклічну систему субформули D.
-фторалкілстероїди за п. 1, при цьому STEROID являє собою стероїдну циклічну систему субформули D.
6. 17![]() -фторалкілстероїди за п. 1, при цьому STEROID являє собою стероїдну циклічну систему субформули Е.
-фторалкілстероїди за п. 1, при цьому STEROID являє собою стероїдну циклічну систему субформули Е.
7. 17![]() -фторалкілстероїди за п. 1, при цьому STEROID являє собою стероїдну циклічну систему субформули F.
-фторалкілстероїди за п. 1, при цьому STEROID являє собою стероїдну циклічну систему субформули F.
8. 17![]() -фторалкілстероїди за будь-яким з пп. 1-7, при цьому R1 являє собою метильну групу.
-фторалкілстероїди за будь-яким з пп. 1-7, при цьому R1 являє собою метильну групу.
9. 17![]() -фторалкілстероїди за будь-яким з пп. 1-8, при цьому R2 являє собою гідроксигрупу, формілоксигрупу, ацетилоксигрупу, пропіонілоксигрупу, бутирилоксигрупу, [(транс-4-бутилциклогексил)карбоніл]оксигрупу, фенілпропіонілоксигрупу, ізобутирилоксигрупу, гептанілоксигрупу або ундеканілоксигрупу.
-фторалкілстероїди за будь-яким з пп. 1-8, при цьому R2 являє собою гідроксигрупу, формілоксигрупу, ацетилоксигрупу, пропіонілоксигрупу, бутирилоксигрупу, [(транс-4-бутилциклогексил)карбоніл]оксигрупу, фенілпропіонілоксигрупу, ізобутирилоксигрупу, гептанілоксигрупу або ундеканілоксигрупу.
10. 17![]() -фторалкілстероїди за будь-яким з пп. 1-9, при цьому R3 являє собою трифторметильну групу або пентафторетильну групу.
-фторалкілстероїди за будь-яким з пп. 1-9, при цьому R3 являє собою трифторметильну групу або пентафторетильну групу.
11. 17![]() -фторалкілстероїди за будь-яким з пп. 1-3 і 8-10, при цьому R8 являє собою метильну групу.
-фторалкілстероїди за будь-яким з пп. 1-3 і 8-10, при цьому R8 являє собою метильну групу.
12. 17![]() -фторалкілстероїди за будь-яким з пп. 1-5 і 8-11, при цьому R7 являє собою атом фтору, хлору або брому або трифторметильну або гідроксигрупу.
-фторалкілстероїди за будь-яким з пп. 1-5 і 8-11, при цьому R7 являє собою атом фтору, хлору або брому або трифторметильну або гідроксигрупу.
13. 17![]() -фторалкілстероїди за будь-яким з пп. 1, 2 і 8-11, при цьому R10 являє собою гідроксигрупу.
-фторалкілстероїди за будь-яким з пп. 1, 2 і 8-11, при цьому R10 являє собою гідроксигрупу.
14. 17![]() -фторалкілстероїди за будь-яким з пп. 1, 2 і 8-12, при цьому R9 являє собою атом фтору.
-фторалкілстероїди за будь-яким з пп. 1, 2 і 8-12, при цьому R9 являє собою атом фтору.
15. 17![]() -фторалкілстероїди за будь-яким з пп. 1, 4, 7 і 12, при цьому R11 являє собою гідроксиметиленову групу або формільну групу.
-фторалкілстероїди за будь-яким з пп. 1, 4, 7 і 12, при цьому R11 являє собою гідроксиметиленову групу або формільну групу.
16. 17![]() -фторалкілстероїди за будь-яким з пп. 1, 5, 11 і 12, при цьому Y означає атом кисню.
-фторалкілстероїди за будь-яким з пп. 1, 5, 11 і 12, при цьому Y означає атом кисню.
17. 17![]() -фторалкілстероїди за п. 1 із групи, яка включає
-фторалкілстероїди за п. 1 із групи, яка включає
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-7
-трифторметил-7![]() -метиландрост-4-ен-3-он,
-метиландрост-4-ен-3-он,
17![]() , 4-дигідрокси-17
, 4-дигідрокси-17![]() -трифторметиландрост-4-ен-3 -он,
-трифторметиландрост-4-ен-3 -он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-4-хлорандрост-4-ен-3-он,
-трифторметил-4-хлорандрост-4-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-4-бромандрост-4-ен-3-он,
-трифторметил-4-бромандрост-4-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() ,4-біс(трифторметил)андрост-4-ен-3-он,
,4-біс(трифторметил)андрост-4-ен-3-он,
17![]() ,11
,11![]() -дигідрокси-17
-дигідрокси-17![]() -трифторметиландрост-4-ен-3-он,
-трифторметиландрост-4-ен-3-он,
17![]() ,11
,11![]() -дигідрокси-17
-дигідрокси-17![]() -трифторметил-9
-трифторметил-9![]() -фторандрост-4-ен-3-он,
-фторандрост-4-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметиландрост-1,4-дієн-3-он,
-трифторметиландрост-1,4-дієн-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-4-хлорандрост-1,4-дієн-3-он,
-трифторметил-4-хлорандрост-1,4-дієн-3-он,
17![]() ,4-дигідрокси-17
,4-дигідрокси-17![]() -трифторметиландрост-1,4-дієн-3-он,
-трифторметиландрост-1,4-дієн-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-7
-трифторметил-7![]() -метиландрост-1,4-дієн-3-он,
-метиландрост-1,4-дієн-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-7
-трифторметил-7![]() -метил-4-хлорандрост-1,4-дієн-3-он,
-метил-4-хлорандрост-1,4-дієн-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетиландрост-4-ен-3-он,
-пентафторетиландрост-4-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-7
-пентафторетил-7![]() -метиландрост-4-ен-3-он,
-метиландрост-4-ен-3-он,
17![]() ,4-дигідрокси-17
,4-дигідрокси-17![]() -пентафторетиландрост-4-ен-3-он,
-пентафторетиландрост-4-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-4-хлорандрост-4-ен-3-он,
-пентафторетил-4-хлорандрост-4-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-4-бромандрост-4-ен-3-он,
-пентафторетил-4-бромандрост-4-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-4-трифторметиландрост-4-ен-3-он,
-пентафторетил-4-трифторметиландрост-4-ен-3-он,
17![]() ,11
,11![]() -дигідрокси-17
-дигідрокси-17![]() -пентафторетиландрост-4-ен-3-он,
-пентафторетиландрост-4-ен-3-он,
17![]() ,11
,11![]() -дигідрокси-17
-дигідрокси-17![]() -пентафторетил-9
-пентафторетил-9![]() -фторандрост-4-ен-3-он,
-фторандрост-4-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетиландрост-1,4-дієн-3-он,
-пентафторетиландрост-1,4-дієн-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-4-хлорандрост-1,4-дієн-3-он,
-пентафторетил-4-хлорандрост-1,4-дієн-3-он,
17![]() ,4-дигідрокси-17
,4-дигідрокси-17![]() -пентафторетиландрост-1,4-дієн-3-он,
-пентафторетиландрост-1,4-дієн-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-4-трифторметиландрост-1,4-дієн-3-он,
-пентафторетил-4-трифторметиландрост-1,4-дієн-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-7
-пентафторетил-7![]() -метиландрост-1,4-дієн-3-он,
-метиландрост-1,4-дієн-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-7
-пентафторетил-7![]() -метил-4-хлорандрост-1,4-дієн-3-он,
-метил-4-хлорандрост-1,4-дієн-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-7
-трифторметил-7![]() -метилестр-4-ен-3-он,
-метилестр-4-ен-3-он,
17![]() ,4-дигідрокси-17
,4-дигідрокси-17![]() -трифторметилестр-4-ен-3-он,
-трифторметилестр-4-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-4-хлорестр-4-ен-3-он,
-трифторметил-4-хлорестр-4-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-4-броместр-4-ен-3-он,
-трифторметил-4-броместр-4-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() , 4-біс(трифторметил)естр-4-ен-3-он,
, 4-біс(трифторметил)естр-4-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-7
-трифторметил-7![]() -метилестр-4,9-дієн-3-он,
-метилестр-4,9-дієн-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-7
-трифторметил-7![]() -метилестр-4,9,11-триєн-3-он,
-метилестр-4,9,11-триєн-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетилестр-4-ен-3-он,
-пентафторетилестр-4-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-7
-пентафторетил-7![]() -метилестр-4-ен-3-он,
-метилестр-4-ен-3-он,
17![]() ,4-дигідрокси-17
,4-дигідрокси-17![]() -пентафторетилестр-4-ен-3-он,
-пентафторетилестр-4-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-4-хлорестр-4-ен-3-он,
-пентафторетил-4-хлорестр-4-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-4-броместр-4-ен-3-он,
-пентафторетил-4-броместр-4-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-4-трифторметилестр-4-ен-3-он,
-пентафторетил-4-трифторметилестр-4-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетилестр-4,9-дієн-3-он,
-пентафторетилестр-4,9-дієн-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетилестр-4,9,11-триєн-3-он,
-пентафторетилестр-4,9,11-триєн-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-7
-пентафторетил-7![]() -метилестр-4,9-дієн-3-он,
-метилестр-4,9-дієн-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-7
-пентафторетил-7![]() -метилестр-4,9,11-триєн-3-он,
-метилестр-4,9,11-триєн-3-он,
13-етил-17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-4-хлоргон-4-ен-3-он,
-трифторметил-4-хлоргон-4-ен-3-он,
13-етил-17![]() ,4-дигідрокси-17
,4-дигідрокси-17![]() -трифторметилгон-4-ен-3-он,
-трифторметилгон-4-ен-3-он,
13-етил-17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-7
-трифторметил-7![]() -метилгон-4-ен-3-он,
-метилгон-4-ен-3-он,
13-етил-17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-7
-трифторметил-7![]() -метилгон-4,9-дієн-3-он,
-метилгон-4,9-дієн-3-он,
13-етил-17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-7
-трифторметил-7![]() -метилгон-4,9,11-триєн-3-он,
-метилгон-4,9,11-триєн-3-он,
13-етил-17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетилгон-4-ен-3-он,
-пентафторетилгон-4-ен-3-он,
13-етил-17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-7
-пентафторетил-7![]() -метилгон-4-ен-3-он,
-метилгон-4-ен-3-он,
13-етил-17![]() ,4-дигідрокси-17
,4-дигідрокси-17![]() -пентафторетилгон-4-ен-3-он,
-пентафторетилгон-4-ен-3-он,
13-етил-17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-4-хлоргон-4-ен-3-он,
-пентафторетил-4-хлоргон-4-ен-3-он,
13-етил-17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-4-бромгон-4-ен-3-он,
-пентафторетил-4-бромгон-4-ен-3-он,
13-етил-17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-4-трифторметилгон-4-ен-3-он,
-пентафторетил-4-трифторметилгон-4-ен-3-он,
13-етил-17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетилгон-4,9-дієн-3-он,
-пентафторетилгон-4,9-дієн-3-он,
13-етил-17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетилгон-4,9,11-триєн-3-он,
-пентафторетилгон-4,9,11-триєн-3-он,
13-етил-17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-7
-пентафторетил-7![]() -метилгон-4,9-дієн-3-он,
-метилгон-4,9-дієн-3-он,
13-етил-17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-7
-пентафторетил-7![]() -метилгон-4,9,11-триєн-3-он,
-метилгон-4,9,11-триєн-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-5
-трифторметил-5![]() -андростан-3-он,
-андростан-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-5
-пентафторетил-5![]() -андростан-3-он,
-андростан-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-7
-трифторметил-7![]() -метил-5
-метил-5![]() -андростан-3-он,
-андростан-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-7
-пентафторетил-7![]() -метил-5
-метил-5![]() -андростан-3-он,
-андростан-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-2-гідроксиметилен-5
-трифторметил-2-гідроксиметилен-5![]() -андростан-3-он,
-андростан-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-2-гідроксиметилен-5
-пентафторетил-2-гідроксиметилен-5![]() -андростан-3-он,
-андростан-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-2
-трифторметил-2![]() -метил-5
-метил-5![]() -андростан-3-он,
-андростан-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-2
-пентафторетил-2![]() -метил-5
-метил-5![]() -андростан-3-он,
-андростан-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-1
-трифторметил-1![]() -метил-5
-метил-5![]() -андростан-3-он,
-андростан-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-1
-пентафторетил-1![]() -метил-5
-метил-5![]() -андростан-3-он,
-андростан-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-5
-трифторметил-5![]() -андрост-2-ен,
-андрост-2-ен,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-5
-пентафторетил-5![]() -андрост-2-ен,
-андрост-2-ен,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-2-метил-5
-трифторметил-2-метил-5![]() -андрост-2-ен,
-андрост-2-ен,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-2-метил-5
-пентафторетил-2-метил-5![]() -андрост-2-ен,
-андрост-2-ен,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-2-ціано-5
-трифторметил-2-ціано-5![]() -андрост-2-ен,
-андрост-2-ен,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-2-ціано-5
-пентафторетил-2-ціано-5![]() -андрост-2-ен,
-андрост-2-ен,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-2-форміл-5
-трифторметил-2-форміл-5![]() -андрост-2-ен,
-андрост-2-ен,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-2-форміл-5
-пентафторетил-2-форміл-5![]() -андрост-2-ен,
-андрост-2-ен,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-[2,3с]оксадіазол-5
-трифторметил-[2,3с]оксадіазол-5![]() -андростан,
-андростан,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-[2,3с]оксадіазол-5
-пентафторетил-[2,3с]оксадіазол-5![]() -андростан,
-андростан,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-[3,2с]ізоксазол-5
-трифторметил-[3,2с]ізоксазол-5![]() -андростан,
-андростан,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-[3,2с]ізоксазол-5
-пентафторетил-[3,2с]ізоксазол-5![]() -андростан,
-андростан,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-[3,2с]піразол-5
-трифторметил-[3,2с]піразол-5![]() -андростан,
-андростан,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-[3,2с]піразол-5
-пентафторетил-[3,2с]піразол-5![]() -андростан,
-андростан,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-2
-трифторметил-2![]() ,3
,3![]() -епітіо-5
-епітіо-5![]() -андростан,
-андростан,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-2
-пентафторетил-2![]() ,3
,3![]() -епітіо-5
-епітіо-5![]() -андростан,
-андростан,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-2
-трифторметил-2![]() ,3
,3![]() -епітіо-5
-епітіо-5![]() -андростан,
-андростан,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-2
-пентафторетил-2![]() ,3
,3![]() -епітіо-5
-епітіо-5![]() -андростан,
-андростан,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-2-окса-5
-трифторметил-2-окса-5![]() -андростан-3-он,
-андростан-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-2-окса-5
-пентафторетил-2-окса-5![]() -андростан-3-он,
-андростан-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-5
-трифторметил-5![]() -андрост-1-ен-3-он,
-андрост-1-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-5
-пентафторетил-5![]() -андрост-1-ен-3-он,
-андрост-1-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-1-метил-5
-трифторметил-1-метил-5![]() -андрост-1-ен-3-он,
-андрост-1-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-1-метил-5
-пентафторетил-1-метил-5![]() -андрост-1-ен-3-он,
-андрост-1-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметил-2-метил-5
-трифторметил-2-метил-5![]() -андрост-1-ен-3-он і
-андрост-1-ен-3-он і
17![]() -гідрокси-17
-гідрокси-17![]() -пентафторетил-2-метил-5
-пентафторетил-2-метил-5![]() -андрост-1-ен-3-он.
-андрост-1-ен-3-он.
18. Спосіб одержання 17![]() -фторалкілстероїдів загальної формули І за п. 1, який відрізняється тим, що сполуки загальної формули II
-фторалкілстероїдів загальної формули І за п. 1, який відрізняється тим, що сполуки загальної формули II
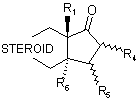 , (ІІ)
, (ІІ)
у якій R1, R4, R5, R6 і STEROID мають значення, вказані в п. 1, у присутності фториду піддають взаємодії з перфторалкілтриалкілсиланами (Alk)3SiCnF2n+1 або з фторалкіллітієм LiCnF2n+1, відповідно з фторалкільними реактивами Гриньяра ZMgCnF2n+1, де n означає 1, 2, 3, 4, 5, або 6, Z означає атом хлору, брому або йоду і Alk означає С1-С4алкіл.
19. Фармацевтична композиція, яка містить у своєму складі принаймні один 17![]() -фторалкілстероїд загальної формули I за будь-яким з пп. 1-17, при необхідності разом з фармацевтично прийнятними допоміжними речовинами і носіями.
-фторалкілстероїд загальної формули I за будь-яким з пп. 1-17, при необхідності разом з фармацевтично прийнятними допоміжними речовинами і носіями.
20. 17![]() -фторалкілстероїди загальної формули I за будь-яким з пп.1-17 для застосування як терапевтично активна речовина.
-фторалкілстероїди загальної формули I за будь-яким з пп.1-17 для застосування як терапевтично активна речовина.
21. Застосування 17![]() -фторалкілстероїдів загальної формули I
-фторалкілстероїдів загальної формули I
 , (І)
, (І)
у якій
R1 являє собою С1-С4алкільну групу,
R2 являє собою гідроксигрупу, групу ОС(О)-R20 або ОR21, де R20 і R21 означають С1-С12алкільну групу, С3-С8циклоалкільну групу, арильну групу або арил-С1-С4алкільну групу,
R3 являє собою залишок формули CnF2n+1, де n означає 1, 2, 3, 4, 5 або 6,
R4 і R5 кожний являє собою атом водню або обидва разом утворюють подвійний зв’язок або метиленовий місток,
R5 і R6 кожний являє собою атом водню або обидва разом утворюють подвійний зв’язок або метиленовий місток,
STEROID являє собою стероїдну АВС-циклічну систему субформул А, В, С, D, Е і F
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
при цьому у формулах А і С у положенні 1, 2 може знаходитися додатковий подвійний зв'язок, а у формулі В у положенні 8, 9 і в положенні 11, 12 можуть знаходитися один або два додаткові подвійні зв'язки,
R7 являє собою атом водню, атом галогену, гідроксильну групу або трифторметильну групу,
Х означає атом кисню або два атоми водню,
R8 являє собою атом водню, метильну або етильну групу,
R9 являє собою атом водню або атом галогену або разом з R10 утворює подвійний зв'язок,
R10 являє собою атом водню, гідроксильну групу, метильну або етильну групу або разом з R9 утворює подвійний зв'язок,
R11 являє собою атом водню, С1-С4алкільну групу, нітрильну групу, гідроксиметиленову або формільну групу,
R12 являє собою атом водню, С1-С4алкільну групу або нітрильну групу,
R11 і R12 поряд з вищевказаними значеннями разом утворюють метиленовий місток,
R13 являє собою атом водню або разом з R7 утворює подвійний зв'язок,
R14 і R15 разом утворюють подвійний зв'язок, оксиранове кільце, тіїранове кільце, [2,3с]оксадіазольне кільце, [3,2с]ізоксазольне кільце або [3,2с]піразольне кільце,
Y означає атом кисню або азоту,
при цьому хвилясті лінії біля R7, R8, R11, R12, R13, R14 і R15 означають, що дані замісники можуть знаходитися в ![]() - або
- або ![]() -положенні, за винятком сполук із групи, яка включає
-положенні, за винятком сполук із групи, яка включає
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметиландрост-4-ен-3-он,
-трифторметиландрост-4-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметилестр-4-ен-3-он,
-трифторметилестр-4-ен-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметилестр-4,9-дієн-3-он,
-трифторметилестр-4,9-дієн-3-он,
17![]() -гідрокси-17
-гідрокси-17![]() -трифторметилестр-4,9,11-триєн-3-он,
-трифторметилестр-4,9,11-триєн-3-он,
13-етил-17![]() -гідрокси-17
-гідрокси-17![]() -трифторметилгон-4-ен-3-он,
-трифторметилгон-4-ен-3-он,
13-етил-17![]() -гідрокси-17
-гідрокси-17![]() -трифторметилгон-4,9-дієн-3-он і
-трифторметилгон-4,9-дієн-3-он і
13-етил-17![]() -гідрокси-17
-гідрокси-17![]() -трифторметилгон-4,9,11-триєн-3-он, для одержання фармацевтичних композицій, призначених для контролю репродуктивної здатності в чоловіків, для гормонзамісної терапії (ГЗТ) у чоловіків і жінок або для лікування зумовлених гормональними факторами захворювань у чоловіків і жінок, таких, наприклад, як ендометріоз, рак молочної залози або гіпогонадизм.
-трифторметилгон-4,9,11-триєн-3-он, для одержання фармацевтичних композицій, призначених для контролю репродуктивної здатності в чоловіків, для гормонзамісної терапії (ГЗТ) у чоловіків і жінок або для лікування зумовлених гормональними факторами захворювань у чоловіків і жінок, таких, наприклад, як ендометріоз, рак молочної залози або гіпогонадизм.
Текст
1. 17 -фторалкілстероїди загальної формули І 2 3 76125 4 R12 являє собою атом водню, С1-С4алкільну групу хлору або брому або трифторметильну або гідроабо нітрильну групу, ксигрупу. R11 і R12 поряд з вищевказаними значеннями ра13. 17 -фторалкілстероїди за будь-яким з пп. 1, 2 зом утворюють метиленовий місток, і 8-11, при цьому R10 являє собою гідроксигрупу. 13 7 R являє собою атом водню або разом з R утво14. 17 -фторалкілстероїди за будь-яким з пп. 1, 2 рює подвійний зв'язок, і 8-12, при цьому R9 являє собою атом фтору. R14 і R15 разом утворюють подвійний зв'язок, ок15. 17 -фторалкілстероїди за будь-яким з пп. 1, сиранове кільце, тіїранове кільце, 4, 7 і 12, при цьому R11 являє собою гідроксиме[2,3с]оксадіазольне кільце, [3,2с]ізоксазольне кітиленову групу або формільну групу. льце або [3,2с]піразольне кільце, 16. 17 -фторалкілстероїди за будь-яким з пп. 1, Y означає атом кисню або азоту, 5, 11 і 12, при цьому Y означає атом кисню. 7 8 11 12 13 при цьому хвилясті лінії біля R , R , R , R , R , 17. 17 -фторалкілстероїди за п. 1 із групи, яка 14 15 R і R означають, що дані замісники можуть знавключає ходитися в - або -положенні, за винятком спо17 -гідрокси-17 -трифторметил-7 лук із групи, яка включає метиландрост-4-ен-3-он, 17 -гідрокси-17 -трифторметиландрост-4-ен-317 , 4-дигідрокси-17 -трифторметиландрост-4он, ен-3 -он, 17 -гідрокси-17 -трифторметилестр-4-ен-3-он, 17 -гідрокси-17 -трифторметил-4-хлорандрост17 -гідрокси-17 -трифторметилестр-4,9-дієн-34-ен-3-он, он, 17 -гідрокси-17 -трифторметил-4-бромандрост17 -гідрокси-17 -трифторметилестр-4,9,114-ен-3-он, триєн-3-он, 17 -гідрокси-17 ,4-біс(трифторметил)андрост-413-етил-17 -гідрокси-17 -трифторметилгон-4-енен-3-он, 3-он, 17 ,11 -дигідрокси-17 -трифторметиландрост13-етил-17 -гідрокси-17 -трифторметилгон-4,94-ен-3-он, дієн-3-он і 17 ,11 -дигідрокси-17 -трифторметил-9 13-етил-17 -гідрокси-17 -трифторметилгонфторандрост-4-ен-3-он, 4,9,11-триєн-3-он. 17 -гідрокси-17 -трифторметиландрост-1,4-дієн2. 17 -фторалкілстероїди за п. 1, при цьому 3-он, STEROID являє собою стероїдну циклічну систему 17 -гідрокси-17 -трифторметил-4-хлорандростсубформули А. 1,4-дієн-3-он, 3. 17 -фторалкілстероїди за п. 1, при цьому 17 ,4-дигідрокси-17 -трифторметиландрост-1,4STEROID являє собою стероїдну циклічну систему дієн-3-он, субформули В. 17 -гідрокси-17 -трифторметил-7 4. 17 -фторалкілстероїди за п. 1, при цьому метиландрост-1,4-дієн-3-он, STEROID являє собою стероїдну циклічну систему 17 -гідрокси-17 -трифторметил-7 -метил-4субформули С. 5. 17 -фторалкілстероїди за п. 1, при цьому хлорандрост-1,4-дієн-3-он, 17 -гідрокси-17 -пентафторетиландрост-4-ен-3STEROID являє собою стероїдну циклічну систему субформули D. он, 6. 17 -фторалкілстероїди за п. 1, при цьому 17 -гідрокси-17 -пентафторетил-7 STEROID являє собою стероїдну циклічну систему метиландрост-4-ен-3-он, субформули Е. 17 ,4-дигідрокси-17 -пентафторетиландрост-47. 17 -фторалкілстероїди за п. 1, при цьому ен-3-он, STEROID являє собою стероїдну циклічну систему 17 -гідрокси-17 -пентафторетил-4-хлорандростсубформули F. 4-ен-3-он, 8. 17 -фторалкілстероїди за будь-яким з пп. 1-7, 17 -гідрокси-17 -пентафторетил-4-бромандрост1 при цьому R являє собою метильну групу. 4-ен-3-он, 9. 17 -фторалкілстероїди за будь-яким з пп. 1-8, 17 -гідрокси-17 -пентафторетил-42 при цьому R являє собою гідроксигрупу, формітрифторметиландрост-4-ен-3-он, локсигрупу, ацетилоксигрупу, пропіонілоксигрупу, 17 ,11 -дигідрокси-17 -пентафторетиландростбутирилоксигрупу, [(транс-44-ен-3-он, бутилциклогексил)карбоніл]оксигрупу, фенілпро17 ,11 -дигідрокси-17 -пентафторетил-9 піонілоксигрупу, ізобутирилоксигрупу, гептанілоксигрупу або ундеканілоксигрупу. фторандрост-4-ен-3-он, 10. 17 -фторалкілстероїди за будь-яким з пп. 1-9, 17 -гідрокси-17 -пентафторетиландрост-1,4при цьому R3 являє собою трифторметильну грудієн-3-он, пу або пентафторетильну групу. 17 -гідрокси-17 -пентафторетил-4-хлорандрост11. 17 -фторалкілстероїди за будь-яким з пп. 1-3 1,4-дієн-3-он, і 8-10, при цьому R8 являє собою метильну групу. 17 ,4-дигідрокси-17 -пентафторетиландрост-1,412. 17 -фторалкілстероїди за будь-яким з пп. 1-5 дієн-3-он, 7 і 8-11, при цьому R являє собою атом фтору, 17 -гідрокси-17 -пентафторетил-4трифторметиландрост-1,4-дієн-3-он, 5 76125 6 17 -гідрокси-17 -пентафторетил-7 13-етил-17 -гідрокси-17 -пентафторетилгон-4,9метиландрост-1,4-дієн-3-он, дієн-3-он, 17 -гідрокси-17 -пентафторетил-7 -метил-413-етил-17 -гідрокси-17 -пентафторетилгонхлорандрост-1,4-дієн-3-он, 4,9,11-триєн-3-он, 17 -гідрокси-17 -трифторметил-7 -метилестр13-етил-17 -гідрокси-17 -пентафторетил-7 4-ен-3-он, метилгон-4,9-дієн-3-он, 17 ,4-дигідрокси-17 -трифторметилестр-4-ен-313-етил-17 -гідрокси-17 -пентафторетил-7 он, метилгон-4,9,11-триєн-3-он, 17 -гідрокси-17 -трифторметил-4-хлорестр-4-ен17 -гідрокси-17 -трифторметил-5 -андростан3-он, 3-он, 17 -гідрокси-17 -трифторметил-4-броместр-417 -гідрокси-17 -пентафторетил-5 -андростанен-3-он, 3-он, 17 -гідрокси-17 , 4-біс(трифторметил)естр-4-ен17 -гідрокси-17 -трифторметил-7 -метил-5 3-он, андростан-3-он, 17 -гідрокси-17 -трифторметил-7 -метилестр17 -гідрокси-17 -пентафторетил-7 -метил-5 4,9-дієн-3-он, андростан-3-он, 17 -гідрокси-17 -трифторметил-7 -метилестр17 -гідрокси-17 -трифторметил-24,9,11-триєн-3-он, гідроксиметилен-5 -андростан-3-он, 17 -гідрокси-17 -пентафторетилестр-4-ен-3-он, 17 -гідрокси-17 -пентафторетил-217 -гідрокси-17 -пентафторетил-7 -метилестргідроксиметилен-5 -андростан-3-он, 4-ен-3-он, 17 -гідрокси-17 -трифторметил-2 -метил-5 17 ,4-дигідрокси-17 -пентафторетилестр-4-ен-3андростан-3-он, он, 17 -гідрокси-17 -пентафторетил-2 -метил-5 17 -гідрокси-17 -пентафторетил-4-хлорестр-4андростан-3-он, ен-3-он, 17 -гідрокси-17 -трифторметил-1 -метил-5 17 -гідрокси-17 -пентафторетил-4-броместр-4андростан-3-он, ен-3-он, 17 -гідрокси-17 -пентафторетил-1 -метил-5 17 -гідрокси-17 -пентафторетил-4андростан-3-он, трифторметилестр-4-ен-3-он, 17 -гідрокси-17 -трифторметил-5 -андрост-217 -гідрокси-17 -пентафторетилестр-4,9-дієн-3ен, он, 17 -гідрокси-17 -пентафторетил-5 -андрост-217 -гідрокси-17 -пентафторетилестр-4,9,11ен, триєн-3-он, 17 -гідрокси-17 -трифторметил-2-метил-5 17 -гідрокси-17 -пентафторетил-7 -метилестрандрост-2-ен, 4,9-дієн-3-он, 17 -гідрокси-17 -пентафторетил-2-метил-5 17 -гідрокси-17 -пентафторетил-7 -метилестрандрост-2-ен, 4,9,11-триєн-3-он, 17 -гідрокси-17 -трифторметил-2-ціано-5 13-етил-17 -гідрокси-17 -трифторметил-4андрост-2-ен, хлоргон-4-ен-3-он, 17 -гідрокси-17 -пентафторетил-2-ціано-5 13-етил-17 ,4-дигідрокси-17 -трифторметилгонандрост-2-ен, 4-ен-3-он, 17 -гідрокси-17 -трифторметил-2-форміл-5 13-етил-17 -гідрокси-17 -трифторметил-7 андрост-2-ен, метилгон-4-ен-3-он, 17 -гідрокси-17 -пентафторетил-2-форміл-5 13-етил-17 -гідрокси-17 -трифторметил-7 андрост-2-ен, метилгон-4,9-дієн-3-он, 17 -гідрокси-17 -трифторметил-[2,3с]оксадіазол13-етил-17 -гідрокси-17 -трифторметил-7 5 -андростан, метилгон-4,9,11-триєн-3-он, 17 -гідрокси-17 -пентафторетил13-етил-17 -гідрокси-17 -пентафторетилгон-4[2,3с]оксадіазол-5 -андростан, ен-3-он, 17 -гідрокси-17 -трифторметил-[3,2с]ізоксазол13-етил-17 -гідрокси-17 -пентафторетил-7 5 -андростан, метилгон-4-ен-3-он, 17 -гідрокси-17 -пентафторетил-[3,2с]ізоксазол13-етил-17 ,4-дигідрокси-17 -пентафторетилгон5 -андростан, 4-ен-3-он, 17 -гідрокси-17 -трифторметил-[3,2с]піразол13-етил-17 -гідрокси-17 -пентафторетил-45 -андростан, хлоргон-4-ен-3-он, 17 -гідрокси-17 -пентафторетил-[3,2с]піразол13-етил-17 -гідрокси-17 -пентафторетил-45 -андростан, бромгон-4-ен-3-он, 17 -гідрокси-17 -трифторметил-2 ,3 -епітіо13-етил-17 -гідрокси-17 -пентафторетил-45 -андростан, трифторметилгон-4-ен-3-он, 7 76125 8 R4 і R5 кожний являє собою атом водню або обид17 -гідрокси-17 -пентафторетил-2 ,3 -епітіова разом утворюють подвійний зв’язок або мети5 -андростан, леновий місток, 17 -гідрокси-17 -трифторметил-2 ,3 -епітіоR5 і R6 кожний являє собою атом водню або обид5 -андростан, ва разом утворюють подвійний зв’язок або мети17 -гідрокси-17 -пентафторетил-2 ,3 -епітіоленовий місток, 5 -андростан, STEROID являє собою стероїдну АВС-циклічну 17 -гідрокси-17 -трифторметил-2-окса-5 систему субформул А, В, С, D, Е і F R андростан-3-он, R R 17 -гідрокси-17 -пентафторетил-2-окса-5 андростан-3-он, R R8 X 17 -гідрокси-17 -трифторметил-5 -андрост-1R X X H R7 R ен-3-он, R B C A 17 -гідрокси-17 -пентафторетил-5 -андрост-1ен-3-он, R R 17 -гідрокси-17 -трифторметил-1-метил-5 Y R R андрост-1-ен-3-он, R8 X 17 -гідрокси-17 -пентафторетил-1-метил-5 R13 R R R7 H H андрост-1-ен-3-он, D F E 17 -гідрокси-17 -трифторметил-2-метил-5 при цьому у формулах А і С у положенні 1, 2 може андрост-1-ен-3-он і знаходитися додатковий подвійний зв'язок, а у 17 -гідрокси-17 -пентафторетил-2-метил-5 формулі В у положенні 8, 9 і в положенні 11, 12 андрост-1-ен-3-он. можуть знаходитися один або два додаткові по18. Спосіб одержання 17 -фторалкілстероїдів двійні зв'язки, R7 являє собою атом водню, атом галогену, гідрозагальної формули І за п. 1, який відрізняється ксильну групу або трифторметильну групу, тим, що сполуки загальної формули II R1 O Х означає атом кисню або два атоми водню, R8 являє собою атом водню, метильну або етильSTEROID ну групу, R4 R9 являє собою атом водню або атом галогену R6 або разом з R10 утворює подвійний зв'язок, R5 , (ІІ) 1 4 5 6 R10 являє собою атом водню, гідроксильну групу, у якій R , R , R , R і STEROID мають значення, метильну або етильну групу або разом з R9 утвовказані в п. 1, у присутності фториду піддають рює подвійний зв'язок, взаємодії з перфторалкілтриалкілсиланами R11 являє собою атом водню, С1-С4алкільну групу, (Alk)3SiCnF2n+1 або з фторалкіллітієм LiCnF2n+1, нітрильну групу, гідроксиметиленову або формівідповідно з фторалкільними реактивами Гриньяльну групу, ра ZMgCnF2n+1, де n означає 1, 2, 3, 4, 5, або 6, Z R12 являє собою атом водню, С1-С4алкільну групу означає атом хлору, брому або йоду і Alk означає або нітрильну групу, С1-С4алкіл. R11 і R12 поряд з вищевказаними значеннями ра19. Фармацевтична композиція, яка містить у свозом утворюють метиленовий місток, єму складі принаймні один 17 -фторалкілстероїд R13 являє собою атом водню або разом з R7 утвозагальної формули I за будь-яким з пп. 1-17, при рює подвійний зв'язок, необхідності разом з фармацевтично прийнятниR14 і R15 разом утворюють подвійний зв'язок, окми допоміжними речовинами і носіями. сиранове кільце, тіїранове кільце, 20. 17 -фторалкілстероїди загальної формули I [2,3с]оксадіазольне кільце, [3,2с]ізоксазольне кіза будь-яким з пп.1-17 для застосування як теральце або [3,2с]піразольне кільце, певтично активна речовина. Y означає атом кисню або азоту, 21. Застосування 17 -фторалкілстероїдів загапри цьому хвилясті лінії біля R7, R8, R11, R12, R13, льної формули I R14 і R15 означають, що дані замісники можуть зна10 12 11 9 8 7 7 11 12 11 14 15 R1 R2 R3 STEROID R4 R6 R5 , (І) у якій R1 являє собою С1-С4алкільну групу, R2 являє собою гідроксигрупу, групу ОС(О)-R20 або ОR21, де R20 і R21 означають С1-С12алкільну групу, С3-С8циклоалкільну групу, арильну групу або арил-С1-С4алкільну групу, R3 являє собою залишок формули CnF2n+1, де n означає 1, 2, 3, 4, 5 або 6, 8 ходитися в - або -положенні, за винятком сполук із групи, яка включає 17 -гідрокси-17 -трифторметиландрост-4-ен-3он, 17 -гідрокси-17 -трифторметилестр-4-ен-3-он, 17 -гідрокси-17 -трифторметилестр-4,9-дієн-3он, 17 -гідрокси-17 -трифторметилестр-4,9,11триєн-3-он, 13-етил-17 -гідрокси-17 -трифторметилгон-4-ен3-он, 13-етил-17 -гідрокси-17 -трифторметилгон-4,9дієн-3-он і 9 76125 10 лікування зумовлених гормональними факторами 13-етил-17 -гідрокси-17 -трифторметилгонзахворювань у чоловіків і жінок, таких, наприклад, 4,9,11-триєн-3-он, для одержання фармацевтичяк ендометріоз, рак молочної залози або гіпогонаних композицій, призначених для контролю репродизм. дуктивної здатності в чоловіків, для гормонзамісної терапії (ГЗТ) у чоловіків і жінок або для ліку Даний винахід стосується 17метиленстероїдів, способу їх одержання і фармацевтичних композицій, які містять ці сполуки. Запропоновані у винаході сполуки мають андрогенну активністю. 17-перфторалкіловані сполуки естранового і 13-етилгонанового ряду відомі. 17-гідрокси-17-трифторметилестр-4-ен-3-он, 17-гідрокси-17-трифторметилестр-4,9-дієн3-он і 17-гідрокси-17-трифторметилестр-4,9,11триєн-3-он, а також 13-етил-17-гідрокси-17-трифторметилгон-4ен-3-он, 13-етил-17-гідрокси-17-трифторметилгон4,9-дієн-3-он і 13-етил-17-гідрокси-17-трифторметилгон4,9,11-триєн-3-он [описані в Sci. China, серія В: Chem. 40(3) (1997), стор.294-301, CN 94-11218, відповідно в Bioorg. Med. Chem. Lett. 5(17) (1995), стор.1899-1902]. Згідно з цими публікаціями вказані сполуки мають гестагенну активність. 17гідрокси-17-трифторметиландрост-4-ен-3-он [описаний у заявці WO 9313122] як проміжний продукт. Що стосується 17пентафторетилалкілованих стероїдів естранового, відповідно андростанового ряду, то дотепер вони не відомі. Згідно із даним винаходом в ньому пропонуються 17-фторалкілстероїди загальної формули І I у якій R1 являє собою С1-C4алкільну групу, R2 являє собою гідроксигрупу, групу OC(O)-R20 або OR21, де R20 і R21 означають С1-C12алкільну групу, С3-С8циклоалкільну групу, арильну групу або арил-С1-C4алкільну групу, R3 являє собою залишок формули CnFmH0, де n означає 1, 2, 3, 4, 5 або 6, m означає число більше 1, а сума m+0 дорівнює 2n+1, R4 і R5 кожний являє собою атом водню або обидва разом утворюють подвійний зв'язок або метиленовий місток, R5 і R6 кожний являє собою атом водню або обидва разом утворюють подвійний зв'язок або метиленовий місток, STEROID являє собою стероїдну ABCциклічну систему субформул А, В, С, D, Ε I F при цьому у формулах А і С у положенні 1,2 може знаходитися додатковий подвійний зв'язок, а у формулі В в положенні 8,9 і в положенні 11,12 можуть знаходитися один або два додаткові подвійні зв'язки, R7 являє собою атом водню, атом галогену, гідроксильну групу або трифторметильну групу, X означає атом кисню, два атоми водню або гідроксііміногрупу, R8 являє собою атом водню, метильну або етильну групу, R9 являє собою атом водню або атом галогену або разом з R10 утворює подвійний зв'язок, R10 являє собою атом водню, гідроксильну групу, метильну або етильну групу або разом з R9 утворює подвійний зв'язок, R11 являє собою атом водню, С1-С4алкільну групу, нітрильну групу, гідроксиметиленову або формільну групу, R12 являє собою атом водню, С1-C4алкільну групу або нітрильну групу, R11 і R12 поряд з вищевказаними значеннями разом утворюють метиленовий місток, R13 являє собою атом водню або разом з R7 утворює подвійний зв'язок, R14 і R15 разом утворюють подвійний зв'язок, оксиранове кільце, тіїранове кільце, [2,3с]оксадіазольне кільце, [3,2с]ізоксазольне кільце або [3,2с]піразольне кільце, Υ означає атом кисню або азоту, при цьому хвилясті лінії біля R7, R8, R11, R12, 13 R , R14 і R15 означають, що дані замісники можуть знаходитися в - або -положенні, за винятком сполук із групи, яка включає 17-гідрокси-17-трифторметиландрост-4-ен3-он, 17-гідрокси-17-трифторметилестр-4-ен-3-он, 17-гідрокси-17-трифторметилестр-4,9-дієн3-он, 17-гідрокси-17-трифторметилестр-4,9,11триєн-3-он, 13-етил-17-гідрокси-17-трифторметилгон-4 11 76125 12 ен-3-он, ють подвійний зв'язок. Якщо STEROID являє собою стероїдну цикліч13-етил-17-гідрокси-17-трифторметилгонну систему субформули D, то R7 переважно озна4,9-дієн-3-он і чає атом водню, атом хлору або гідроксигрупу, R8 13 -етил-17-гідрокси-17-трифторметилгонпереважно означає атом водню або метильну гру4,9,11-триєн-3-он. 13 7 пу, a R і R разом утворюють переважно подвійЗапропоновані у винаході сполуки мають андний зв'язок і Υ переважно означає атом кисню. рогену активність. Якщо STEROID являє собою стероїдну циклічПід поняттям "С1-C4алкільна група" згідно із ну систему субформули Е, то R8 переважно ознаданим винаходом мається на увазі розгалужена чає атом водню або метильну групу, a R14 і R15 або лінійна алкільна група з 1-4 атомами вуглецю. переважно утворюють разом тіїранове кільце або Як приклади можна назвати метил, етил, н-пропіл, [3,2с]піразольне кільце. ізопропіл, н-бутил, ізобутил і трет-бутил. Якщо STEROID являє собою стероїдну циклічПід поняттям "С1-C12алкільна група" згідно із ну систему субформули F, то R11 переважно ознаданим винаходом мається на увазі розгалужена чає С1-C4алкільну групу або нітрильну групу. або лінійна алкільна група з 1-12 атомами вуглеR1 означає переважно метильну групу. цю. Як приклади можна назвати метил, етил, нR2 означає переважно гідроксигрупу, формілопропіл, ізопропіл, н-бутил, ізобутил, mpem-бутил, ксигрупу, ацетилоксигрупу, пропіонілоксигрупу, н-пентил, ізопентил, н-гексил, 2-метиленпентил, 3бутирилоксигрупу, [(транс-4метиленпентил, 2,2-диметилбутил, 2,3бутилциклогексил)карбоніл]оксигрупу, фенілпропідиметилбутил, октил, ноніл, децил і ундецил. онілоксигрупу, ізобутирилоксигрупу, гептанілоксигВищезгадана С3-C8циклоалкільна група являє рупу або ундеканілоксигрупу. собою відповідно до винаходу моно- або бициклічR3 означає переважно трифторметильну групу ну групу, таку, наприклад, як циклопропіл, циклоабо пентафторетильну групу. бутил, циклопентил або циклогексил. До особливо переважних належать наступні Під поняттям "арильна група" згідно із даним 17-фторалкілстероїди: винаходом мається на увазі заміщена або незамі1)17β-гідрокси-17-трифторметил-7ащена арильна група з 6-15 атомами вуглецю, наприклад фенільна група, заміщена фенільна груметиландрост-4-ен-3-он, па, така як галогенфенільна група або 2) 17β ,4-дигідрокси-17нітрофенільна група, або нафтильна група. трифторметиландрост-4-ен-3 -он, Під поняттям "арил-С1-C4алкільна група" згід3) 17β-гідрокси-17-трифторметил-4но із даним винаходом мається на увазі заміщений хлорандрост-4-ен-3-он, арилом алкіл, які містять разом 7-15 атомів вугле4) 17β-гідрокси-17-трифторметил-4цю, при цьому арил може у свою чергу нести інші бромандрост-4-ен-3-он, замісники, такі, наприклад, як атом галогену. Як 5) 17β-гідрокси-17,4приклад можна назвати вільну або ароматично біс(трифторметил)андрост-4-ен-3-он, заміщену бензильну групу, таку як бензильна гру6) 17β,11β-дигідрокси-17па або галогенбензильна група. трифторметиландрост-4-ен-3-он, Під поняттям "атом галогену" у контексті дано7) 17β,11β-дигідрокси-17-трифторметил-9го опису мається на увазі атом фтору, хлору, брофторандрост-4-ен-3-он, му або йоду. 8) 17β-гідрокси-17-трифторметиландрост-1,4Залишок формули CnFmH0, де n означає 1, 2, дієн-3-он, 3, 4, 5 або 6, m означає число більше 1, а сума 9) 17β-гідрокси-17-трифторметил-4m+0 дорівнює 2n+1, може являти собою розгалухлорандрост-1,4-дієн-3-он, жений або лінійний фторалкіл з 1-6 атомами вуг10) 17β,4-дигідрокси-17лецю, при цьому як приклади такого залишку можтрифторметиландрост-1,4-дієн-3-он, на назвати трифторметил, пентафторетил, 11) 17β-гідрокси-17-трифторметил-7гептафтор-н-пропіл і гептафторізопропіл, переваметиландрост-1,4-дієн-3-он, жним з яких відповідно до винаходу є трифторме12) 17β-гідрокси-17-трифторметил-7-метилтил або пентафторетил. 4-хлорандрост-1,4-дієн-3-он, Якщо STEROID являє собою стероїдну цикліч13) 17β-гідрокси-17-пентафторетиландростну систему субформули А, то R7 переважно озна4-ен-3-он, чає атом водню, атом хлору або гідроксигрупу, R10 14) 17β-гідрокси-17-петафторетил-7переважно означає атом водню або гідроксигрупу, метиландрост-4-ен-3-он, a R9 переважно означає атом водню або атом 15) 17β,4-дигідрокси-17фтору. пентафторетиландрост-4-ен-3-он, Якщо STEROID являє собою стероїдну цикліч16) 17β-гідрокси-17-пентафторетил-4ну систему субформули В, то R7 переважно ознахлорандрост-4-ен-3-он, чає атом водню, атом хлору або гідроксигрупу, a 8 R переважно означає атом водню або метильну 17) 17β-гідрокси-17-пентафторетил-4групу. бромандрост-4-ен-3-он, Якщо STEROID являє собою стероїдну цикліч18) 17β-гiдpoкcи-17-пeнтaфтopeтил-4ну систему субформули С, то R7 переважно ознатpифтopмeтилaндpocт-4-eн-3-oн, чає атом водню, атом хлору або гідроксигрупу, a 19) 17β,11β-дигідрокси-17R11 переважно означає гідроксиметиленову групу пентафторетиландрост-4-ен-3-он, або формільну групу або R11 і R12 разом утворю20) 17β,11β-дигiдpoкcи-17-пeнтaфтopeтил 13 76125 14 4-хлоргон-4-ен-3-он, 9-фтopaндpocт-4-eн-3-oн, 53) 13-етил-17β-гідрокси-17-пентафторетил21)17 β-гідрокси-17-пентафторетиландрост4-бромгон-4-ен-3-он, 1,4-дієн-3-он, 54) 13-етил-17β-гідрокси-17-пентафторетил22) 17 β-гідрокси-17-пентафторетил-44-трифторметилгон-4-ен-3-он, хлорандрост-1,4-дієн-3-он, 55) 13-етил-17β-гідрокси-1723) 17β,4-дигідрокси-17пентафторетилгон-4,9-дієн-3-он, пентафторетиландрост-1,4-дієн-3-οн, 56) 13-етил-17β-гідрокси-1724) 17β-гідрокси-17-пентафторетил-4пентафторетилгон-4,9,11-триєн-3-он, трифторметиландрост-1,4-дієн-3-он, 57) 13-етил-17β-гідрокси-17-пентафторетил25) 17β-гідрокси-17-пентафторетил-7метиландрост-1,4-дієн-3-он, 7-метилгон-4,9-дієн-3-он, 26) 17β-гiдρoкcи-17-пeнтaфтopeтил-758) 13-етил-17β-гідрокси-17-пентафторетилмeтил-4-xлopaндpocт-1,4-дiєн-3-oн, 7-метилгон-4,9,11-триєн-3-он, 27) 17β-гідрокси-17-трифторметил-759) 17β-гідрокси-17-трифторметил-5аметилестр-4-ен-3-он, андростан-3-он, 28) 17β,4-дигідрокси-17-трифторметилестр-460) 17β-гідрокси-17-пентафторетил-5ен-3-он, андростан-3-он, 29) 17β-гідрокси-17-трифторметил-461) 17β-гідрокси-17-трифторметил-7-метилхлорестр-4-ен-3-он, 5-андростан-3-он, 30) 17β-гідрокси-17-трифторметил-462) 17β-гідрокси-17-пентафторетил-7броместр-4-ен-3-он, метил-5-андростан-3-он, 31)17β-гідрокси-17,4-біс(трифторметил)естр63) 17β-гідрокси-17-трифторметил-24-ен-3-он, гідроксиметилен-5-андростан-З-он, 32) 17β-гідрокси-17-трифторметил-764) 17β-гідрокси-17-пентафторетил-2метилестр-4,9-дієн-3-он, гідроксиметилен-5-андростан-3-он, 33) 17β-гідрокси-17-трифторметил-765) 17β-гідрокси-17-трифторметил-2-метилметилестр-4,9,11-триєн-3-он, 5-андростан-3-он, 34) 17β-гідрокси-17-пентафторетилестр-4-ен66) 17β-гідрокси-17-пентафторетил-23-он, метил-5-андростан-3-он, 35) 17β-гідрокси-17-пентафторетил-767) 17β-гідрокси-17-трифторметил-1-метилметилестр-4-ен-3-он, 5-андростан-3-он, 36) 17,4-дигідрокси-17-пентафторетилестр68) 17β-гідрокси-17-пентафторетил-14-ен-3-он, метил-5-андростан-3-он, 37) 17β-гідрокси-17-пентафторетил-469) 17β-гідрокси-17-трифторметил-5хлорестр-4-ен-3-он, андрост-2-ен, 38) 17β-гідрокси-17-пентафторетил-470) 17β-гідрокси-17-пентафторетил-5броместр-4-ен-3-он, андрост-2-ен, 39) 17β-гідрокси-17-пентафторетил-471) 17β-гідрокси-17-трифторметил-2-метилтрифторметилестр-4-ен-3-он, 5-андрост-2-ен, 40) 17β-гідрокси-17--пентафторетилестр-4,972) 17β-гідрокси-17-пентафторетил-2-метилдієн-3-он, 5-андрост-2-ен, 41) 17β-гідрокси-17-пентафторетилестр73) 17β-гідрокси-17-трифторметил-2-ціано4,9,11-триєн-3-он, 5-андрост-2-ен, 42) 17β-гідрокси-17-пентафторетил-774) 17β-гідрокси-17-пентафторетил-2-ціанометилестр-4,9-дієн-3-он, 5-андрост-2-ен, 43) 17β-гідрокси-17-пентафторетил-775) 17β-гідрокси-17-трифторметил-2-формілметилестр-4,9,11-триєн-3-он, 5-андрост-2-ен, 44) 13-етил-17β-гідрокси-17-трифторметил-476) 17β-гідрокси-17-пентафторетил-2хлоргон-4-ен-3-он, форміл-5-андрост-2-ен, 45) 13-етил-17β,4-дигідрокси-1777) 17β-гідрокси-17-трифторметилтрифторметилгон-4-ен-3-он, [2,3с]оксадіазол-5-андростан, 46) 13-етил-17β-гідрокси-17-трифторметил78) 17β-гідрокси-17-пентафторетил7-метилгон-4-ен-3-он, [2,3с]оксадіазол-5-андростан, 47) 13-етил-17β-гідрокси-17-трифторметил79) 17β-гідрокси-17-трифторметил7-метилгон-4,9-дієн-3-он, [3,2с]ізоксазол-5-андростан, 48) 13-етил-17β-гідрокси-17-трифторметил80) 17β-гідрокси-17-пентафторетил7-метилгон-4,9,11-триєн-3-он, [3,2с]ізоксазол-5-андростан, 49) 13-етил-17β-гідрокси-17пентафторетилгон-4-ен-3-он, 81) 17β-гідрокси-17-трифторметил50) 13 -етил-17β-гідрокси-17-пентафторетил[3,2с]піразол-5-андростан, 7-метилгон-4-ен-3-он, 82) 17β-гідрокси-17-пентафторетил51) 13-етил-17β,4-дигідрокси-17[3,2с]піразол-5-андростан, пентафторетилгон-4-ен-3-он, 83) 17β-гідрокси-17-трифторметил-2,352) 13-етил-17β-гідрокси-17-пентафторетил 15 76125 16 нортестостерон і 3,3-диметоксіестр-5(10)-17-он епітіо-5-андростан, (DD 79-213049); 84) 17β-гідрокси-17-пентафторетил-2,3для стероїдних циклічних систем С, D і Е: епіепітіо-5-андростан, андростерон; 85) 17β-гідрокси-17-трифторметил-2,3для стероїдної циклічної системи F: 5епітіо-5-андростан, андрост-2-ен-17-он з епіандростерону [US 86) 17β-гідрокси-17-пентафторетил-2,33098851]. епітіо-5-андростан, Функціональні групи, які містяться в субструк87) 17β-гідрокси-17-трифторметил-2-окса-5турах вихідних матеріалів для стероїдних циклічандростан-3-он, них систем A-F, при необхідності можна захищати 88) 17β-гідрокси-17-пентафторетил-2-оксаза методами, відомим фахівцям у даній галузі. 5-андростан-3-он, Так, наприклад, кетогрупи у вихідних матеріалах 89) 17β-гідрокси-17-трифторметил-5субструктур A-F за методами, відомими фахівцю, андрост-1-ен-3-он, можна захищати у вигляді кеталей або тіоацета90) 17β-гідрокси-17-пентафторетил-5лей. андрост-1-ен-3-он, Замісники R7-R15 за відомими фахівцям мето91) 17β-гідрокси-17-трифторметил-1-метилдами можна вводити в субструктури A-F як до, так 5-андрост-1-ен-3-он, і після вбудовування 17-алкільного ланцюга. 92) 17β-гідрокси-17-пентафторетил-1-метилЗапропоновані у винаході сполуки мають анд5-андрост-1-ен-3-он, рогенну активність, що наочно підтверджують 93) 17β-гідрокси-17-трифторметил-2-метилпредставлені нижче результати дослідження афінності до андрогенових рецепторів (АР) 5-андрост-1-ен-3-он і 94) 17β-гідрокси-17-пентафторетил-2-метилАР у 5-андрост-1-ен-3-он. Сполука % Ще одним об'єктом даного винаходу є спосіб тестостерон 35 одержання 17-фторалкілстероїдів загальної фоR 1881 (метилтриєнолон) 100 15 17β,4-дигідрокси-17-трифторметилестр-4-ен-3-он рмули І, який полягає в тому, що сполуки загальної 40 17β-гідрокси-17-трифторметил-7-метилестр-4-ен-3-он формули II II у якій R1, R4, R5, R6 і STEROID мають значення, вказані в п.1 формули винаходу, у присутності фториду піддають взаємодії з перфторалкілтриалкілсиланами (Alk)3SiCnFmH0 або з фторалкіллітієм LiCnFmH0, відповідно з фторалкільними реактивами Гриньяра ZMgCnFmH0, де n означає 1, 2, 3, 4, 5, або 6, m означає число більше 1, а сума m+0 дорівнює 2n, Ζ означає атом хлору, брому або йоду і Alk означає С1-С4алкіл. Фторований 17-алкільний ланцюг можна вводити шляхом приєднання (перфторалкіл)триметилсиланів у присутності фториду [реактив Рупперта і його гомологи, див. Journ. Org. Chem. 56 (1991), стор.984-989] або шляхом приєднання фторалкіллітію, відповідно фторалкільних реактивів Гриньяра до 17-оксогрупи загальної формули II. 17-перфторалкільні ланцюги можна вводити шляхом приєднання перфторалкіллітію до 17-оксогрупи загальної формули II [див. Tetr. Lett. 26 (1985), стор.5243; Journ. Org. Chem. 52 (1987), стор.2481]. Вказані в загальної формули II замісники R4, 5 R і R6 за відомими фахівцям методами доцільно вводити в стероїдний цикл D до введення фторованого 17-алкільного ланцюга. Для одержання сполук загальної формули II субформул A-F можна використовувати відомі стероїдні основні компоненти. Так, наприклад, можна використовувати наступні стероїдні основні компоненти: для стероїдної циклічної системи А: андрост-4ен-3,17-діон і дегідроепіандростерон; для стероїдної циклічної системи В: 19 17β-гідрокси-17-трифторметил-4-хлорестр-4-ен-3-он 17β-гідрокси-17-трифторметиландрост-4-ен-3-он 17β-гідрокси-17-трифторметил-4-хлорандрост-4-ен-3-он 17β,11β-дигідрокси-17-трифторметиландрост-4-ен-3-он 17β-гідрокси-17-трифторметил-7-метиландрост-4-ен-3он 17β-гідрокси-17-пентафторетилестр-4-ен-3-он 17β-гідрокси-17-пентафторетил-7-метилестр-4-ен-3-он 17β,4-дигідрокси-17-пентафторетилестр-4-ен-3-он 17β-гідрокси-17-пентафторетил-4-хлорестр-4-ен-3-он 41 9,4 20 8,6 30 21 34 20 27 Результати дослідження дозволяють зробити висновок про те, що перед запропонованими у винаході сполуками загальної формули І відкриваються широкі можливості їх застосування для контролю фертильності (репродуктивної здатності) у чоловіків, для гормонзамісної терапії (ГЗТ) у чоловіків і жінок або для лікування зумовлених гормональними факторами захворювань у чоловіків і жінок, таких, наприклад, як ендометріоз, рак молочної залози або гіпогонадизм. Об'єктом даного винаходу відповідно до цього є також фармацевтичні композиції, які містять у своєму складі принаймні один 17фторалкілстероїд загальної формули І, при необхідності разом з фармацевтично прийнятними допоміжними речовинами і носіями. Ці фармацевтичні композиції і лікарські засоби можуть призначатися для перорального, ректального, вагінального, підшкірного, черезшкірного, внутрішньовенного або внутрішньом'язового введення. Поряд зі звичайними носіями і/або розріджувачами до їх складу входить принаймні одна сполука загальної формули І. Лікарські засоби за винаходом разом із звичайними твердими або рідкими носіями або розріджувачами і звичайно використовуваними в цих цілях фармацевтично-технологічними допоміжними речовинами залежно від методики введення, 17 76125 18 яка передбачається, виготовляють за відомою порціями по 100мл. Об'єднані органічні екстракти технологією у відповідному дозуванні. Переважні сушать, концентрують і хроматографують на силікомпозиції являють собою лікарські форми, призкагелі. У результаті одержують 12г 3 β-ацетоксиначені для перорального введення. Такими лікар17β-триметилсилілокси-17ськими формами є, наприклад, таблетки, філмтатрифторметиландрост-5-ену. блетки, драже, капсули, пігулки, порошки, розчини 12г 3β-ацетокси-17-триметилсилілокси-17або суспензії або ж форми з ефектом депо. трифторметиландрост-5-ену розчиняють у 100мл Як очевидні можуть розглядатися композиції, ТГФ і змішують при кімнатній температурі з 20мл призначені для парентерального введення, такі як 30%-ною фтористоводневою кислоти. Через 3год. розчини для ін'єкції. Далі можна назвати серед суміш зливають на 200мл 12%-ного розчину аміаінших такі композиції, як супозиторії або засоби ку, тричі екстрагують етиловим ефіром оцтової для вагінального застосування. кислоти порціями по 100мл, органічні екстракти Таблетки можна виготовляти, наприклад, сушать і концентрують. У результаті одержують 9г шляхом змішування активної речовини з відомими 3β-ацетокси-17-гідрокси-17допоміжними речовинами, наприклад з інертними трифторметиландрост-5-ену, який розчиняють у розріджувачами, такими як декстроза, цукор, сор300мл метанолу і змішують з 6г гідроксиду калію. біт, маніт, полівінілпіролідон, з розпушувачами, Після 30-хвилинного перемішування при кімнатній такими як кукурудзяний крохмаль або альгінова температурі нейтралізують 2н. соляною кислотою і кислота, зі зв'язувальними, такими як крохмаль метанол видаляють під вакуумом. Залишок чотири або желатин, зі змащувальними речовинами, тарази екстрагують етиловим ефіром оцтової кислокими як стеарат магнію або тальк, і/або з засобати порціями по 100мл і об'єднані органічні екстракми, які забезпечують ефект депо, такими як карботи сушать і концентрують. У результаті одержують ксиполіметилен, карбоксиметилцелюлоза, 7,5г 3,17р-дигідрокси-17ацетофталат целюлози або полівінілацетат. Табтрифторметиландрост-5-ену, який протягом 3год. летки можуть також складатися з декількох шарів. нагрівають зі зворотним холодильником разом з Відповідним чином можуть виготовлятися і 80мл циклогексанону, 5г триізопропаноляту алюдраже, а саме, нанесенням на отримані аналогічно мінію і 250мл толуолу. Суміші дають охолонути, до таблеток ядра покриття (оболонки) із речовин, після чого змішують її з 200мл 2н. розчину тартраякі звичайно використовуються з такою метою, ту натрію-калію, органічну фазу відокремлюють і наприклад, як полівінілпіролідон, шелак, гуміарадвічі екстрагують етиловим ефіром оцтової кислобік, тальк, оксид титану або цукор. При цьому оботи порціями по 100мл. Об'єднані органічні екстраклонка драже також може складатися з декількох ти концентрують, залишок очищають хроматограшарів, для формування яких можуть використовуфією і кристалізують з метанолу. Таким шляхом ватися такі ж допоміжні речовини, що і вказані виодержують 17-гідрокси-17ще для таблеток. трифторметиландрост-4-ен-3-он. 1 До складу розчинів і суспензій, які містять споН-ЯМР (ДМСО-D6): 0,89 (s, 3Н, Н-18), 1,15 (s, луки загальної формули І за винаходом, додатково 3Н, Н-19), 5,62 (s, 1H, Н-4). 19 можуть входити смакові добавки, такі як сахарин, F-ЯMP: -75,3. цикламат або цукор, а також, наприклад, ванілін Приклад 2 або апельсиновий екстракт. Крім того, вони мо17β-гідрокси-17-трифторметил-7жуть містити також допоміжні суспендувальні реметиландрост-4-ен-3-он човини, такі як натрійкарбоксиметилцелюлоза, або 7г 17-гідрокси-17-трифторметиландрост-4консерванти, такі як n-гідроксибензоат. ен-3-ону протягом 30хв. кип'ятять разом з 8,5г Капсули, які містять сполуки загальної формухлоранілу в 200мл трет-бутаполу зі зворотним ли І, можна виготовляти, наприклад, змішуванням холодильником. Потім суміші дають охолонути ісполуки(-к) загальної формули І з інертним носієм, концентрують її досуха. Залишок хроматографутаким як лактоза або сорбіт, і наступним інкапсують на силікагелі. Для наступного очищення перелюванням у желатинові капсули. кристалізовують із суміші дихлорметану і гексану. Відповідні супозиторії можна виготовляти, наУ результаті одержують 17-гідрокси-17приклад, змішуванням з передбаченими для цих трифторметиландрост-4,6-дієн-3-он. цілей носіями, такими як нейтральні жири або по1 Н-ЯМР: 1,04 (s, 3Н, Н-18), 1,13 (s, 3Н, Н-19), ліетиленгліколь або з їх похідними. 5,69 (s, 1Н, Н-4), 6,11 (m, 2H, Н-6, Н-7). Нижче даний винахід більш докладно поясню19 F-ЯMP: -75,3. ється на прикладах, які не обмежують його обсяг. До розчину метилмагніййодиду (отриманому з Приклад 1 2,5г магнію і 6,4мл метилйодиду в 80мл діетилово17-гідрокси-17-трифторметиландрост-4-енго ефіру) додають 80мл ТГФ і після охолодження 3-он до -5°С додають 1г моногідрату ацетату міді, роз10г 3-ацетоксидегідроепіандростерону розчиненого в 50мл ТГФ. Далі охолоджують до -20°С і чиняють у 300мл ТГФ і змішують з 0,5г фториду потім по краплях додають розчин 5г 17-гідрокситетрабутиламонію. Потім при перемішуванні при 17-трифторметиландрост-4,6-дієн-3-ону в 80мл кімнатній температурі повільно додають по крапТГФ. Через 2год. зливають на суміш льодяної води лях 15мл трифторметилтриметилсилану і переміі 2н. сірчаної кислоти і тричі екстрагують етиловим шують протягом 3год. Після цього додають 200мл ефіром оцтової кислоти порціями по 80мл. Органінапівконцентрованого розчину гідрокарбонату начний екстракт сушать і концентрують. Залишок трію і під вакуумом відганяють ТГФ. Залишок тричі хроматографують на силікагелі. Для наступного екстрагують етиловим ефіром оцтової кислоти 19 76125 20 очищення перекристалізовують з етилового ефіру рафують на силікагелі і перекристалізовують з етилового ефіру оцтової кислоти. оцтової кислоти. Таким шляхом одержують 171 Н-ЯМР: 1,02 (s, 3Н, Н-18), 1,24 (s, 3Н, Н-19), гідрокси-17-трифторметил-7-метиландрост-46,07 (m, 1Н, Н-4), 6,22 (dd, J=1,6, 10Гц, 1Н, H-2), ен-3-он. 1 7,04 (d, J=10Гц, 1H, H-1). Н-ЯМР: 0,77 (d, J=7Гц, 3Н, Н-7-метил), 0,99 (s, 19 F-ЯМР: -75,4. 3Н, Η-18), 1,20 (s, 3Н, Η-19), 5,73 (m, 1H, H-4). 19 Приклад 6 F-ЯMP: -75,3. 17β-гідрокси-17-трифторметил-4Приклад 3 хлорандрост-1,4-дієн-3-он 17-гідрокси-17-трифторметил-4Вказану в заголовку сполуку одержують з 17хлорандрост-4-ен-3-он Стадія 1 гідрокси-17-трифторметил-4-хлорандрост-4-ен-317-гідрокси-17-трифторметил-4,5ону аналогічно до рекомендації з одержання 17епоксіандростан-3-он гідрокси-17-трифторметиландрост-1,4-дієн-3-ону. 1 2г 17-гідрокси-17-трифторметиландрост-4H-ЯМР: 1,02 (s, 3Н, Н-18), 1,31 (s, 3Н, Н-19), ен-3-ону розчиняють у 120мл метанолу, а також у 6,36 (d, J=10Гц, 1H, Н-2), 7,07 (d, J=10Гц, 1Н,Н-1). 19 70мл ТГФ і при 10°С змішують з 20мл розчину пеF-ЯМР: -75,8. роксиду водню (35%-ного). При перемішуванні Приклад 7 додають 5мл 10%-ного розчину гідроксиду натрію і 17-гідрокси-17-трифторметил-7продовжують перемішувати ще протягом 3год. метилестр-4-ен-3-он Реакційний розчин концентрують до об'єму 50мл, Стадія 1 потім змішують з 50мл дихлорметану і 25мл води 7-метилестр-4-ен-3,17-діон й органічну фазу відокремлюють. Далі промивають 10г 17-гідрокси-7-метилестр-4-ен-3-ону напівконцентрованим розчином тіосульфату, су(одержання див. Steroids (1963), стор.317) розчишать і концентрують досуха. Отриманий залишок няють у 200мл ацетону і при -20°С оксидують 15мл являє собою суміш 4,5-, відповідно 4,58н. хромосірчаної кислоти. Після завершення реаепоксидів і без подальшого очищення його викокції додають 10мл метанолу і дають нагрітися до ристовують на наступній стадії. кімнатної температури. Потім під вакуумом видаСтадія 2 ляють розчинники і залишок змішують з 300мл 17-гідрокси-17-трифторметил-4води, при цьому продукт випадає в осад. Його віхлорандрост-4-ен-3-он докремлюють вакуум-фільтрацією, одержуючи в 2г суміші епоксидів (зі стадії 1) розчиняють у результаті 6,5г 7-метилестр-4-ен-3,17-діону. 200мл ацетону і при 5°С змішують з 12мл конценСтадія 2 трованої соляної кислоти. Через 2 год нейтралізу3,3-етилендитіо-7-метилестр-4-ен-17-он ють розчином соди й ацетон видаляють під вакуу5г 7-метилестр-4-ен-3,17-діону розчиняють у мом. Залишок екстрагують дихлорметаном. 50мл метанолу і змішують з 3мл етандитіолу. ПоОрганічні екстракти сушать і концентрують. Після тім додають 1,5мл діетилетерату трифториду бору кристалізації із суміші дихлорметану і гексану одеі перемішують при кімнатній температурі протягом ржують 17-гідрокси-17-трифторметил-42год., при цьому продукт випадає у вигляді крисхлорандрост-4-ен-3-он. талів. Його відокремлюють вакуум-фільтрацією, 1 Н-ЯМР: 0,99 (s, 3Н, Н-18), 1,24 (s, 3Н, Н-19). одержуючи в результаті 6г3,3-етилендитіо-719 F-ЯМР: -75,3. метилестр-4-ен-17-ону. Приклад 4 Стадія 3 17,4-дигідрокси-17-трифторметиландрост-417-гідрокси-17-трифторметил-7ен-3-он метилестр-4-ен-3-он 2г суміші епоксидів (стадія 1, одержання 175г 3,3-етилендитіо-7-метилестр-4-ен-17-ону гідрокси-17-трифторметил-4-хлорандрост-4-ен-3змішують у 150мл ТГФ при кімнатній температурі з ону) розчиняють у 20мл оцтової кислоти, що міс0,25г фториду тетрабутиламонію і потім повільно тить 2об.% концентрованої сірчаної кислоти, і розпо краплях додають 8мл трифторметилтриметилчин протягом 24год. витримують при 10°С. Після силану. Після 3-годинного перемішування додають цього його змішують з 200мл етилового ефіру оц200мл напівконцентрованого розчину гідрокарботової кислоти і нейтралізують розчином соди. Орнату натрію і під вакуумом відганяють ТГФ. Залиганічну фазу сушать і концентрують. Залишок шок тричі екстрагують етиловим ефіром оцтової хроматографують на силікагелі і кристалізують з кислоти порціями по 100мл. Об'єднані органічні етилового ефіру оцтової кислоти/гексану. екстракти сушать, концентрують і хроматографу1 Н-ЯМР: 0,99 (s, 3Н, Н-18), 1,19 (s, 3Н, Н-19), ють на силікагелі. У результаті одержують 3г 176,10 (s, 1H, 4-ОН). триметилсилілокси-17-трифторметил-3,319 F-ЯМР: -75,3. етилендитіо-7-метилестр-4-ену. Приклад 5 3г 17-триметилсилілокси-17-трифторметил17-гідрокси-17-трифторметиландрост-1,43,3-етилендитіо-7-метилестр-4-ену розчиняють у дієн-3-он 40мл ТГФ і при кімнатній температурі змішують з 2г 17-гідрокси-17-трифторметиландрост-45мл 30%-ної фтористоводневої кислоти. Через ен-3-ону протягом 60год. перемішують при 85°С з 3год. суміш зливають на 200мл 12%-ного розчину 1,8г ДДХ (2,3-дихлор-5,6-диціано-1,4-бензохінон). аміаку, тричі екстрагують етиловим ефіром оцтоПотім осад відфільтровують, промивають толуової кислоти порціями по 100мл, органічні екстракти лом і фільтрат концентрують. Залишок хроматогсушать і концентрують. Залишок розчиняють у 21 76125 22 100мл 95%-ного метанолу, змішують з 9мл метил3-он йодиду, а також з 2,5г карбонату кальцію і протяВказану в заголовку сполуку одержують з 17гом 20год. нагрівають зі зворотним холодильнигідрокси-17-трифторметил-4,5-eпoкciecтpaн-3ком. Після охолодження суміш піддають вакуумoнy аналогічно до одержання 17,4-дигідроксифільтрації і фільтрат концентрують до утворення 17-трифторметиландрост-4-ен-3-ону. 1 сухого залишку, який хроматографують потім на Н-ЯМР (CDCl3): 1,00 (s, 3Н, Н-18), 6,1 (s, 1H, силікагелі і кристалізують з дихлорметану/гексану. 4-ОН). 19 У результаті одержують 17β-гідрокси-17F-ЯMP: -75,3. трифторметил-7-метилестр-4-ен-3-он. Приклад 9 1 H-ЯМР (D6-ДМСО): 0,70 (d, J=7,7Гц, 3Н, 717β-гідрокси-17-пентафторетил андрост-4метил), 0,93 (s, 3Н, Η-18), 5,71 (s, 1Н, H-4). ен-3-он 19 F-ЯМР: -75,5. 20г 3,3-етилендитіоандрост-4-ен-17-ону суПриклад 8 спендують у 600мл діетилового ефіру і при пере17-гідрокси-17-трифторметил-4-хлорестр-4мішуванні охолоджують до -78°С. Потім додають ен-3-он і 17,4-дигідрокси-17-трифторметилестр48г пентафторетилйодиду, а після цього повільно 4-ен-3-он по краплях додають 76мл 1,5-молярного розчину Стадія 1 комплексу сполуки метиллітійбромід літію в діети17β-гідрокси-17-трифторметилестр-4-ен-3 -он ловому ефірі. Далі протягом 2год. перемішують 10г 3,3-диметоксіестр-5(10)-ен-17-ону розчипри -78°С, після чого зливають на 2л насиченого няють у 300мл ТГФ і змішують з 0,5г фториду тетрозчину гідрокарбонату натрію. Потім екстрагують рабутиламонію. Далі при перемішуванні при кімнаетиловим ефіром оцтової кислоти, сушать і концетній температурі повільно додають по краплях нтрують. Залишок розчиняють у 500мл 95%-ного 15мл трифторметилтриметилсилану і перемішуметанолу, змішують з 72мл метилйодиду, а також ють протягом 3год. Потім додають 200мл напівкоз 20г карбонату кальцію і протягом 20год. нагріванцентрованого розчину гідрокарбонату натрію і під ють зі зворотним холодильником. Після охоловакуумом відганяють ТГФ. Залишок тричі екстрадження проводять вакуум-фільтрацію і фільтрат гують етиловим ефіром оцтової кислоти порціями концентрують до утворення сухого залишку, який по 100мл. Об'єднані органічні екстракти сушать і потім хроматографують на силікагелі і перекрисконцентрують. Таким шляхом одержують 17βталізовують з етилового ефіру оцтової кислоти. триметилсилілокси-17-трифторметил-3,3Таким шляхом одержують 17-гідрокси-17диметоксіестр-5(10)-ен. пентафторетиландрост-4-ен-3-он. 1 H-ЯМР (CDCl3): 0,99 (s, 3Н, Н-18), 1,19 (s, 3Н, 12г 17β-триметилсилілокси-17Н-19), 5,74 (s, 1H, Н-4). трифторметил-3,3-диметоксіестр-5(10)-ену розчи19 F-ЯМР: -77,3 (3F, CF3), -119 (2F, CF2). няють у 100мл ТГФ і змішують при кімнатній темПриклад 10 пературі з 20мл 30%-ної фтористоводневої кислоти. Через 24год. суміш зливають на 200мл 12%17-гідрокси-17-пентафторетил-4ного розчину аміаку, тричі екстрагують етиловим хлорандрост-4-ен-3-он і 17β,4-дигідрокси-17ефіром оцтової кислоти порціями по 100мл, оргапентафторетиландрост-4-ен-3-он нічні екстракти сушать і концентрують. Залишок Стадія 1 очищають хроматографією на силікагелі й у ре17β-гiдpoкcи-17-пeнтaфтopeтил-4,5зультаті одержують 17β-гідрокси-17αeпoкciaндpocтaн-3-oн трифторметилестр-4-ен-3-он. Вказану в заголовку сполуку одержують ана1 Н-ЯМР (CDCl3): 1,00 (s, 3Н, Н-18), 5,82 (s, 1H, логічно до одержання 17β-гідрокси-17Н-4). трифторметил-4,5-епоксіандростан-3-ону. Утво19 F-ЯМР:-75,1. рений залишок являє собою суміш 4,5-, відповіСтадія 2 дно 4β,5β-епоксидів і без подальшого очищення 17-гідрокси-17-трифторметил-4,5його використовують на наступній стадії. епоксіестран-3-он Стадія 2 Вказану в заголовку сполуку одержують ана17β-гідрокси-17β-пентафторетил-4логічно до одержання 17β-гідрокси-17хлорандрост-4-ен-3-он трифторметил-4,5-епоксіандростан-3-ону. УтвоВказану в заголовку сполуку одержують з 17βрений залишок являє собою суміш 4,5-, відповігідрокси-17β-пентафторетил-4,5дно 4,5-епоксидів і без подальшого очищення eпoкciaндpocтaн-3-oнy аналогічно до одержання його використовують на наступній стадії. 17β-гідрокси-17β-трифторметил-4-хлорандрост-4Стадія 3 ен-3-ону. 1 17-гідрокси-17-трифторметил-4-хлорестр-4H-ЯМР (CDCl3): 0,99 (s, 3Н, Н-18), 1,23 (s, 3Н, ен-3-он Н-19). 19 F-ЯМР: -77,4 (3F, CF3), -119,2 (2F, CF2). Вказану в заголовку сполуку одержують з 17Стадія 3 гідрокси-17-трифторметил-4,5-eпoкciecтpaн-317β,4-дигідрокси-17-пентафторетиландростoнy аналогічно до одержання 17-гідрокси-174-ен-3-он трифторметил-4-хлорандрост-4-ен-3-ону. 1 Вказану в заголовку сполуку одержують з 17βH-ЯМP (CDCl3): 1,00 (s, 3Н, Η-18). 19 гідрокси-17-пентафторетил-4,5F-ЯMP: -75,3. eпoкciaндpocтaн-3-oнy аналогічно до одержання Стадія 4 17,4-дигідрокси-17-трифторметиландрост-4-ен17,4-дигідрокси-17-трифторметилестр-4-ен 23 76125 24 3-ону. Сирий продукт розчиняють у 500мл 95%-ного ме1 H-ЯМР (CDCl3): 0,98 (s, 3Н, Н-18), 1,18 (s, 3Н, танолу, змішують з 72мл метилйодиду, а також з Н-19), 6,09 (s, 1H, 4-ОН). 20г карбонату кальцію і протягом 20год. нагріва19 F-ЯМР: -77,4 (3F, CF3), -119,5 (2F, CF2). ють зі зворотним холодильником. Після охолоПриклад 11 дження проводять вакуум-фільтрацію і фільтрат концентрують до утворення сухого залишку, який 17β-гідрокси-17-пентафторетил-7потім хроматографують на силікагелі і перекрисметиландрост-4-ен-3-он талізовують з етилового ефіру оцтової кислоти. Стадія 1 Таким шляхом одержують 17-гідрокси-1717β-гідрокси-17-пентафторетиландрост-4,6дієн-3-он пентафторетил-7-метилестр-4-ен-3-он. 1 H-ЯМР (CDCl3): 0,77 (d, J=8Гц, 3Н, Н-7Ме), 1г 17β-гідрокси-17-пентафторетиландрост-41,02 (s, 3Н, Н-18), 5,84 (s 1H, Н-4)· ен-3-ону протягом 30хв. кип'ятять разом з 1,2г 19 F-ЯМР: -77,3 (3F, CF3), -119,2 (2F, CF2). хлоранілу в 50мл трет-бутанолу зі зворотним хоПриклад 14 лодильником, потім суміші дають охолонути і концентрують її до утворення сухого залишку, який 17,4-дигідрокси-17-пентафторетилестр-4хроматографують на силікагелі. ен-3-он 1 Н-ЯМP (CDCl3): 1,04 (s, 3Н, Η-18), 1,12 (s, 3Н, Стадія 1 Η-19), 5,68 (s, 1H, H-4), 6,11 (m, 2H, H-6, H-7). 17-гідрокси-17-пентафторетил-4,519 F-ЯМР: -77,4 (3F, CF3), -119,0 (2F, CF2). епоксіестран-3-он До розчину метилмагніййодиду (отриманому з Вказану в заголовку сполуку одержують ана5г магнію і 13мл метилйодиду в 150мл діетилового логічно до одержання 17β-гідрокси-17ефіру) додають 160мл ТГФ, потім охолоджують до тpифтopмeтил-4,5-eкпoкciaндpocтaн-3-oнy. -5°С і додають 2г моногідрату ацетату міді, розчиУтворений в результаті залишок являє собою суненого в 100мл ТГФ. Після охолодження до -20°С міш 4,5-, відповідно 4,5-епоксидів і без подапо краплях додають розчин 10г 17β-гідрокси-17льшого очищення його використовують на наступпентафторетиландрост-4,6-дієн-3-ону в 120мл ній стадії. ТГФ. Через 2год. зливають на льодяну воду/2н. Стадія 2 сірчану кислоту і тричі екстрагують етиловим ефі17,4-дигідрокси-17-пентафторетилестр-4ром оцтової кислоти порціями по 80мл. Органічний ен-3-он екстракт сушать і концентрують. Залишок хромаВказану в заголовку сполуку одержують з 17тографують на силікагелі. Для наступного очигідрокси-17-пентафторетил-4,5-eпoкciecтpaн-3щення його перекристалізовують з етилового ефіoнy аналогічно до одержання 17,4-дигідроксиру оцтової кислоти. 17-трифторметиландрост-4-ен-3-ону. 1 H-ЯМР (CDCl3): 0,78 (d, 1=8Гц, 3Н, Н-7Ме), 1 H-ЯМР (CDCl3): 1,00 (s, 3Н, Н-18), 6,10 (s, 1H, 1,01 (s, 3Н, Н-18), 1,21 (s, 3Н, Н-19), 5,74 (s 1H, Н4-ОН). 4). 19 F-ЯМР: -77,3 (3F, CF3), -119,2 (2F, CF2). 19 F-ЯMP: -77,4 (3F, CF3), -119,3 (2F, CF2). Приклад 15 Приклад 12 17-гідрокси-17-пентафторетил-4-хлорестр17-гідрокси-17-пентафторетилестр-4-ен-34-ен-3-он он Вказану в заголовку сполуку одержують з 1720г 3,3-диметоксіестр-5(10)-ен-17-ону розчигідрокси-17-пентафторетил-4,5-епоксіестран-3няють у 600мл діетилового ефіру і при перемішуοну аналогічно до одержання 17-гідрокси-17ванні охолоджують до -78°С. Потім додають 48г трифторметил-4-хлорандрост-4-ен-3-ону. пентафторетилйодиду, а після цього повільно по 1 Н-ЯМР (CDCl3): 1,01 (s, 3Н, Η-18). краплях додають 76мл 1,5-молярного розчину 19 F-ЯМР: -77,3 (3F, CF3), -119,2 (2F, CF2). комплексу сполуки метиллітій-бромід літію в діеПриклад 16 тиловому ефірі. Далі протягом 2год. перемішують 17β-гідрокси-17-трифторметил-5при -78°С, після чого зливають на 2л насиченого андростан-3-он розчину гідрокарбонату натрію. Потім екстрагують Стадія 1 етиловим ефіром оцтової кислоти, сушать і конце3р-ацетокси-17-триметилсилілокси-17нтрують. Залишок хроматографують на силікагелі і трифторметил-5-андростан перекристалізовують з етилового ефіру оцтової 10г 3-ацетоксіепіандростерону розчиняють у кислоти. Таким шляхом одержують 17-гідрокси300мл ТГФ і змішують з 0,5г фториду тетрабути17-пентафторетилестр-4-ен-3-он. 1 ламонію. Далі при перемішуванні при кімнатній H-ЯМР (CDCl3): 1,02 (s, 3H, H-18), 5,83 (s, 1H, температурі повільно додають по краплях 15мл H-4). 19 трифторметилтриметилсилану і перемішування F-ЯМР: -77,3 (3F, CF3), -119,2 (2F, CF2). продовжують ще протягом 3год. Потім додають Приклад 13 200мл напівконцентрованого розчину гідрокарбо17-гідрокси-17-пентафторетил-7нату натрію і під вакуумом відганяють ТГФ. Залиметилестр-4-ен-3-он шок тричі екстрагують етиловим ефіром оцтової 3,3-етилендитіо-7-метилестр-4-ен-17-он (див. кислоти порціями по 100мл. Об'єднані органічні одержання 17-гідрокси-17-трифторметил-7екстракти сушать, концентрують і хроматографуметилестр-4-ен-3-ону), аналогічно до того, як опиють на силікагелі. У результаті одержують 9г 3сано вище, піддають взаємодії з комплексом споацетокси-17-триметилсилілокси-17луки пентафторетилйодид/метиллітій/бромід літію. 25 76125 26 протягом 1год. для перемішування і потім зливатрифторметил-5-андростану. ють на 1л насиченого розчину гідрокарбонату наСтадія 2 трію, екстрагують етиловим ефіром оцтової кисло3β-аыетокси-17-гідрокси-17-трифторметилти і концентрують. Залишок розчиняють у 100мл 5-андростан ТГФ і змішують з 8г фториду тетрабутиламонію. 9г 3-ацетокси-17-триметилсилілокси-17Через 30хв. додають 200мл насиченого розчину трифторметил-5-андростану розчиняють у 100мл гідрокарбонату натрію і ТГФ видаляють під вакууТГФ і при кімнатній температурі змішують з 20мл мом, при цьому продукт випадає в осад. Його відо30%-ної фтористоводневої кислоти. Через 3год. кремлюють вакуум-фільтрацією і промивають восуміш зливають на 200мл 12%-ного розчину аміадою. У результаті одержують 13г 3,17ку, тричі екстрагують етиловим ефіром оцтової дигідрокси-17-пентафторетил-5-андростану. кислоти порціями по 100мл, органічні екстракти Стадія 3 сушать і концентрують. Таким шляхом одержують 17-гідрокси-17-пентафторетил-57г 3β-ацетокси-17-гідрокси-17-трифторметиландростан-3-он 5-андростану. 10г 3,17-дигідрокси-17-пентафторетил-5Стадія 3 андростану оксидують у 100мл ацетону при 0°С 3, 17-дигідрокси-17-трифторметил-516мл 8н. хромсірчаної кислоти. Потім додають 3мл андростан метанолу, 100мл води й ацетон видаляють під 7г 3-ацетокси-17-гідрокси-17вакуумом, при цьому продукт випадає у вигляді трифторметил-5-андростану розчиняють у 300мл кристалів. Його відокремлюють вакуумметанолу і змішують з 6г гідроксиду калію. Після фільтрацією і промивають водою. Таким шляхом 30-хвилинного перемішування при кімнатній темодержують 17-гідрокси-17-пентафторетил-5пературі нейтралізують 2н. соляною кислотою і андростан-3-он. метанол видаляють під вакуумом. Залишок чотири 1 H-ЯМР (CDCl3): 0,96 (s, 3Н, Η-18), 1,02 (s, 3Н, рази екстрагують етиловим ефіром оцтової кислоΗ-19). ти порціями по 100мл і об'єднані органічні екстрак19 F-ЯMP: -77,3 (3F, CF3), -119,2 (2F, CF2). ти сушать і концентрують. У результаті одержують Приклад 18 4,5г зр,17-дигідрокси-17-трифторметил-517-гідрокси-17-трифторметил-2андростану. гідроксиметилен-5-андростан-3-он Стадія 4 4г 17-гідрокси-17-трифторметил-517-гідрокси-17-трифторметил-5андростан-3-ону змішують у 150мл толуолу з 3,2г андростан-3-он гідриду натрію і 8мл етилового ефіру мурашиної Отриманий на стадії 3 продукт оксидують у кислоти. Через 4год. обережно гідролізують во50мл ацетону при 0°С 9мл 8н. хромсірчаної кислодою. Потім підкисляють 5н. соляною кислотою, ти. Після завершення реакції додають 2мл метаорганічну фазу відокремлюють, сушать і концентнолу і 50мл води, після чого ацетон видаляють під рують. Для очищення її хроматографують на силівакуумом, при цьому продукт випадає в осад. Його кагелі і кристалізують з ацетону/гексану. Таким відокремлюють вакуум-фільтрацією і промивають шляхом одержують 17-гідрокси-17водою. Для очищення продукт хроматографують і трифторметил-2-гідроксиметилен-5-андростан-3кристалізують з етилового ефіру оцтової кислоти. он. Таким шляхом одержують 17-гідрокси-171 H-ЯМР (CDCl3): 0,76 (s, 3H, Η-18), 0,97 (s, 3H, трифторметил-5-андростан-3-он. 1 Η-19), 8,62 (m, 1H, H-2-CHO). H-ЯМР (CDCl3): 0,96 (s, 3Н, Η-18), 1,02 (s, 3Н, 19 F-ЯMP: -75,2. Η-19). 19 Приклад 19 F-ЯМР:-75,4. 17-гідрокси-17-пентафторетил-2Приклад 17 гідроксиметилен-5-андростан-3-он 17-гідрокси-17-пентафторетил-5Вказану в заголовку сполуку одержували анаандростан-3-он логічно до прикладу 17 з 17β-гідрокси-17Стадія 1 пентафторетил-5-андростан-3-ону. 3-триметилсилілокси-5-андростан-17-он 1 Н-ЯМР (CDCl3): 0,77 (s, 3Н, Η-18), 0,96 (s, 3Н, 10г епіандростерону розчиняють у 75мл ДМФ і Η-19), 8,62 (m, 1H, H-2-CHO). 20мл піридину і змішують з 10мл триметилхлорси19 F-ЯМР: -77,3 (3F, CF3), -119,2 (2F, CF2). лану. Через 3год. суміш зливають у 300мл насичеПриклад 20 ного розчину гідрокарбонату натрію, після чого 17-гідрокси-17-трифторметил-[3,2с]піразолвідокремлюють вакуум-фільтрацією, промивають 5-андростан водою й одержують у результаті 15г 31г 17-гідрокси-17-трифторметил-2триметилсилілокси-5-андростан-17-ону. гідроксиметилен-5-андростан-3-ону протягом Стадія 2 30хв. нагрівають зі зворотним холодильником у 3β,17-дигідрокси-17-пентафторетил-550мл етанолу, додаючи при цьому 0,3мл гідрату андростан гідразину. Потім концентрують, осаджують за до15г 3-триметилсилілокси-5-андростан-17помогою води і проводять вакуум-фільтрацію. ону розчиняють у 300мл діетилового ефіру і охоПродукт очищають шляхом кристалізації з третлоджують до -78°С. Потім додають 14г пентафтобутилметилового ефіру/гексану. Таким шляхом ретилйодиду, а після цього по краплях додають одержують 17-гідрокси-17-трифторметил38мл 1,5-молярного розчину комплексу метиллітійбромід літію в діетиловому ефірі. Далі витримують [3,2с]піразол-5-андростан. 27 76125 28 Н-ЯМР (CDCl3): 0,74 (s, 3Н, Η-18), 0,96 (s, 3Н, рують. Для наступного очищення продукт хроматоΗ-19). графують на силікагелі і перекристалізовують з 19 F-ЯМР: -75,3. етилового ефіру оцтової кислоти. Таким шляхом Приклад 21 одержують 17-гідрокси-17-трифторметил-217-гідрокси-17-пентафторетил-[3.2с]піразолокса-5-андростан-3-он. 1 5-андростан Н-ЯМР (CDCl3): 0,94 (s, 3H, Η-18), 1,00 (s, 3Η, Вказану в заголовку сполуку одержують анаΗ-19), 2,22 (dd, J=19,1, 13,1Гц, 1H, Н-4), 2,53 (dd, J=18,7, 5,8Гц, 1Н, H-4), 3,92 (d, J=10Гц, 1Н, H-1), логічно до прикладу 19 з 17β-гідрокси-174,21 (d, J=10Гц, 1Η,Η-1). пентафторетил-2-гідроксиметилен-5-андростан19 F-ЯМР: -75,4. 3-ону. 1 Приклад 25 H-ЯМР (CDCl3): 0,74 (s, 3Н, Н-18), 0,96 (s, 3Н, 17-гідрокси-17-пентафторетил-2-окса-5Н-19). 19 андростан-3-он F-ЯМР: -77,3 (3F, CF3), -119,3 (2F, CF2). Вказану в заголовку сполуку одержують анаПриклад 22 логічно до прикладу 23 з 17β-гідрокси-1717β-гідрокси-17-трифторметил-5-андрост-1ен-3-он пентафторетил-5-андрост-1-ен-3-ону. 1 Н-ЯМР (CDCl3): 0,94 (s, 3Н, Н-18), 1,00 (s, 3Н, 10г 17-гідрокси-17-трифторметил-5Н-19), 2,22 (dd, J=19,1, 13,0Гц, 1H, H-4), 2,53 (dd, андростан-3-ону при перемішуванні в 200мл ТГФ J=19,1, 6,2Гц, 1H, H-4), 3,93 (d, J=10 Гц, 1H, H-1), змішують з гідробромідом піридинійперброміду. 4,22 (d, J=10Гц, 1H, H-1). Через 15хв. додають 250мл насиченого розчину 19 F-ЯMP: -77,3 (3F, CF3), -119,2 (2F, CF2). гідрокарбонату натрію, екстрагують хлороформом, Приклад 26 сушать і концентрують. Залишок разом з 10г карбонату літію і 20г броміду літію в 100мл ТГФ нагрі17-гідрокси-17-трифторметил-5-андрост-2вають протягом 6год. зі зворотним холодильником. ен Потім дають охолонути, розбавляють 500мл толуСтадія 1 олу, промивають водою, сушать і концентрують. 17β-триметилсилілокси-17-трифторметил-5Для наступного очищення продукт хроматографуандрост-2-ен ють на силікагелі і перекристалізовують з етилово10г 5-андрост-2-ен-17-ону (одержання згідно го ефіру оцтової кислоти. Таким шляхом одержуіз US-A 3098851) розчиняють у 300мл ТГФ і зміють 17-гідрокси-17-трифторметил-5-андрост-1шують з 0,5г фториду тетрабутиламонію. Потім ен-3-он. при перемішуванні при кімнатній температурі пові1 H-ЯМР (CDCl3): 0,98 (s, 3Н, Н-18), 1,02 (s, 3Н, льно додають по краплях 15мл трифторметилтриН-19), 5,85 (d, J=10Гц, 1H, Н-2), 7,12 (d, J=10Гц, метилсилану і продовжують перемішувати ще 1Н, H-1). протягом 3год. Після цього додають 200мл напів19 F-ЯMP: -75,3. концентрованого розчину гідрокарбонату натрію і Приклад 23 ТГФ відганяють під вакуумом. Залишок тричі екст17-гідрокси-17-пентафторетил-5-андрострагують етиловим ефіром оцтової кислоти порція1-ен-3-он ми по 100мл. Об'єднані органічні екстракти суВказану в заголовку сполуку одержують анашать, концентрують і хроматографують на логічно до прикладу 21 з 17β-гідрокси-17силікагелі. У результаті одержують 10г 17пентафторетил-5-андростан-3-ону. триметилсилілокси-17-трифторметил-51 Н-ЯМР (CDCl3): 0,98 (s, 3Н, Н-18), 1,02 (s, 3Н, андрост-2-ену. Н-19), 5,85 (d, J=10Гц, 1Н, Н-2), 7,12 (d, J=10Гц, Стадія 2 1H, H-1). 17-гідрокси-17-трифторметил-5-андрост-219 F-ЯMP: -77,3 (3F, CF3), -119,2 (2F, CF2). ен Приклад 24 10г 17-триметилсилілокси-1717β-гідрокси-17-трифторметил-2-окса-5трифторметил-5-андрост-2-ену андростан-3-он розчиняють у 100мл ТГФ і змішують при кімна4г 17-гідрокси-17-трифторметил-5тній температурі з 20мл 30%-ної фтористоводнеандрост-1-ен-3-ону піддають у 200мл 90%-ної оцвої кислоти. Через 3год суміш зливають на 200мл тової кислоти взаємодії з 30г тетраацетату свинцю 12%-ного розчину аміаку, тричі екстрагують етилоі 280мг тетраоксиду осмію. Через 24год. витримки вим ефіром оцтової кислоти порціями по 100мл, при кімнатній температурі розбавляють 500мл органічні екстракти сушать і концентрують. Після води і тричі екстрагують хлороформом. Об'єднані кристалізації з метанолу одержують 17-гідроксиорганічні фази підлуговують 2н. їдким натрієм і 17-трифторметил-5-андрост-2-ен. 1 тричі екстрагують 2н. їдким натрієм порціями по Н-ЯМР (CDCl3): 0,76 (s, 3Н, Н-18), 0,93 (s, 3Н, 200мл. Об'єднані водні фази підкисляють 5н. соН-19), 5,60 (m, 2Н, Н-2, Н-3). 19 ляною кислотою і тричі екстрагують хлороформом. F-ЯМР:-75,1. Об'єднані органічні фази сушать і концентрують. Приклад 27 Залишок розчиняють у 80мл ТГФ і 80мл метанолу. 17-гідрокси-17-пентафторетил-5-андростДалі при перемішуванні послідовно додають роз2-ен чин 1г гідрокарбонату натрію в 75мл води і 4,2г 15г 5-андрост-2-ен-17-ону розчиняють у борогідриду натрію. Через 2год. підкисляють кон300мл діетилового ефіру і охолоджують до -78°С. центрованою соляною кислотою, екстрагують етиДалі додають спочатку 14г пентафторетилйодиду, ловим ефіром оцтової кислоти, сушать і концента потім по краплях додають 38мл 1,5-молярного 1 29 76125 30 розчину комплексу метиллітій-бромід літію. Після ють на силікагелі і таким шляхом одержують 17цього витримують протягом 1год. для перемішугідрокси-17-пентафторетил-5-андрост-2-ен. 1 вання компонентів між собою і потім суміш зливаH-ЯМР (CDCl3): 0,76 (s, 3Н, Н-18), 0,95 (s, 3Н, ють на 1л насиченого розчину гідрокарбонату наН-19), 5,62 (m, 2Н, Н-2, Н-3). 19 трію, екстрагують етиловим ефіром оцтової F-ЯМР: -77,5 (3F, CF3), -119,3 (2F, CF2). кислоти і концентрують. Залишок хроматографу Комп’ютерна верстка Т. Чепелева Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійською170100090000039d00000002001c00000000000500000009020000000005000000020101000000050000000102ffffff00050000002e0118000000050000000b0200000000050000000c02400140011200000026060f001a00ffffffff000010000000c0ffffff0100000000010000410100000b00000026060f000c004d61746854797065000030001c000000fb02e0fe0000000000009001000000020002001053796d626f6c007740000000330a0a60e6c0f477efc0f4770100000000003000040000002d01000008000000320ae00037000100000061790a00000026060f000a00ffffffff0100000000001c000000fb021000070000000000bc02000000cc0102022253797374656d000000000a000000040000000000ffffffff0100000000003000040000002d01010004000000f0010000030000000000 fluoroalkyl steroids having androgenic activity, a method for producing thereof and a pharmaceutical composition containing these compounds
Автори англійськоюRing, Sven, Kaufmann Gunter, Elger Walter
Назва патенту російською170100090000039d00000002001c00000000000500000009020000000005000000020101000000050000000102ffffff00050000002e0118000000050000000b0200000000050000000c02400140011200000026060f001a00ffffffff000010000000c0ffffff0100000000010000410100000b00000026060f000c004d61746854797065000030001c000000fb02e0fe0000000000009001000000020002001053796d626f6c007740000000330a0a60e6c0f477efc0f4770100000000003000040000002d01000008000000320ae00037000100000061790a00000026060f000a00ffffffff0100000000001c000000fb021000070000000000bc02000000cc0102022253797374656d000000000a000000040000000000ffffffff0100000000003000040000002d01010004000000f0010000030000000000-фторалкилстероиды, обладающие андрогенной активностью, способ их получения и фармацевтическая композиция, содержащая эти соединения
Автори російськоюКауфманн Гюнтер, Эльгер Вальтер
МПК / Мітки
МПК: C07J 11/00, A61K 8/63, C07J 1/00, A61P 5/26, C07J 71/00, A61K 31/565, A61P 35/00
Мітки: одержання, фармацевтична, сполуки, 17a-фторалкілстероїди, яка, композиція, андрогенну, містить, мають, спосіб, активність
Код посилання
<a href="https://ua.patents.su/15-76125-17a-ftoralkilsterodi-shho-mayut-androgennu-aktivnist-sposib-kh-oderzhannya-ta-farmacevtichna-kompoziciya-yaka-mistit-ci-spoluki.html" target="_blank" rel="follow" title="База патентів України">17a-фторалкілстероїди, що мають андрогенну активність, спосіб їх одержання та фармацевтична композиція, яка містить ці сполуки</a>
Попередній патент: Планетарний редуктор з прохідним валом
Наступний патент: Спосіб поділу суспензій і фільтрпрес для його здійснення
Випадковий патент: Склопакет



















