Спосіб одержання індазолілсечовин, які пригнічують ванілоїдні рецептори підтипу 1 (vr1)
Номер патенту: 94100
Опубліковано: 11.04.2011
Автори: Лінна Марвін Р., Котекі Брайан Дж., Фернандо Діліні П., Лукін Кірілл А., Чі-Пін Су Маргарет
Формула / Реферат
1. Спосіб одержання сполуки, що має структурну формулу (І)
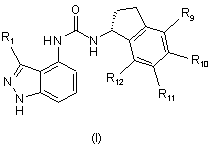 ,
,
де R1 вибраний із групи, яка складається з водню, алкенілу, алкоксигрупи, алкоксіалкоксигрупи, алкоксіалкілу, алкоксикарбонілу, алкоксикарбонілалкілу, алкілу, алкілкарбонілу, алкілкарбонілалкілу, алкілкарбонілокси, алкілтіо, алкінілу, карбокси, карбоксіалкілу, ціано, ціаноалкілу, циклоалкілу, циклоалкілалкілу, формілу, формілалкілу, галоалкокси, галоалкілу, галоалкілтіо, галогену, гідрокси, гідроксіалкілу, меркапто, меркаптоалкілу, нітро, (СF3)2(НО)С-, RB(SO)2RAN-, RAO(SO)2-, RBO(SO)2-, ZAZBN-, (ZAZBN)алкілу, (ZAZBN)карбонілу, (ZAZвN)кapбoнiлaлкiлy і (ZAZвN)сульфонілу;
R9, R10, R11 і R12, кожний незалежно один від одного, вибрані з групи, яка складається з водню, алкенілу, алкоксигрупи, алкоксіалкоксигрупи, алкоксіалкілу, алкоксикарбонілу, алкоксикарбонілалкілу, алкілу, алкілкарбонілу, алкілкарбонілалкілу, алкілкарбонілокси, алкілтіо, алкінілу, арилу, карбокси, карбоксіалкілу, ціано, ціаноалкілу, формілу, формілалкілу, галоалкокси, галоалкілу, галоалкілтіо, галогену, гетероарилу, гетероциклу, гідрокси, гідроксіалкілу, меркапто, меркаптоалкілу, нітро, (CF3)2(HO)C-, RB(SO)2RAN-, RAO(SO)2, RBO(SO)2-, ZAZBN-, (ZAZвN)алкілу, (ZAZBN)карбонілу, (ZAZBN)карбонілалкілу і (ZAZвN)сульфонілу;
RA являє собою водень або алкіл;
RB являє собою алкіл, арил або арилалкіл; і
ZA і ZB, незалежно один від одного, являють собою водень, алкіл, алкілкарбоніл, форміл, арил або арилалкіл,
що включає стадії:
(а) нагрівання суміші сполуки формули (III), основи, вибраної з групи, яка складається з гідроксиду натрію, фосфату калію і карбонату цезію, і композиції, що містить суміш сполуки формули (IIа) і сполуки формули (IIb), де Р вибраний із групи, яка складається з алкоксіалкілу, алкілкарбонілу, алкоксикарбонілу, арилалкілу, арилкарбонілу та арилоксикарбонілу, R1 має значення, зазначені для сполуки формули (І), і Y являє собою хлор або бром, у присутності паладієвого каталізатора і ліганду на основі фосфіну,
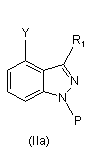 ,
,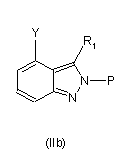 ,
,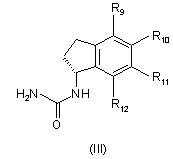 ,
,
з одержанням композиції, що складається з суміші сполуки формули (IVa) і сполуки формули (IVb), в якій R9, R10, R11 і R12 мають значення, зазначені для сполуки формули (І),
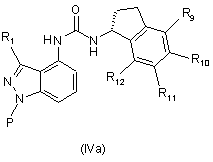 ,
,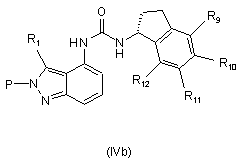 ,
,
(b) подальшої обробки композиції, що складається з суміші сполуки формули (IVa) і сполуки формули (IVb), в умовах, які дають сполуку формули (І).
2. Спосіб за п. 1, де
паладієвий каталізатор стадії (а) складається з ацетату паладію або Pd2(DBA)3.
3. Спосіб за п. 2, де
стадію (а) виконують в інертній атмосфері.
4. Спосіб за п. 3, де
ліганд на основі фосфіну вибраний із групи, яка складається з Xantphos, 2-ди-трет-бутилфосфіно-1-1'-бінафтилу і 5-(ди-трет-бутилфосфаніл)-1',3',5'-трифеніл-1'Н-[1,4']біпіразолілу.
5. Спосіб за п. 4, де
Y являє собою бром;
паладієвий каталізатор являє собою Pd2(DBA)3; і
основа стадії (а) являє собою карбонат цезію.
6. Спосіб за п. 5, де
суміш стадії (а) нагрівають до температури кипіння протягом 2-10 годин у диметиловому ефірі етиленгліколю.
7. Спосіб за п. 6, де
Р являє собою бензил, і
умови стадії (b) додатково включають:
обробку паладієвим каталізатором в присутності донора водню, вибраного з групи, яка складається з газоподібного водню, мурашиної кислоти і циклогексадієну в розчиннику, вибраному з групи, яка складається з спиртового розчинника, тетрагідрофурану або етилацетату, для одержання сполуки формули (І).
8. Спосіб за п. 1, де
Y являє собою бром;
паладієвий каталізатор стадії (а) являє собою Pd2(DBA)3;
стадію (а) виконують в атмосфері азоту;
ліганд на основі фосфіну являє собою Xantphos;
основа стадії (а) являє собою карбонат цезію;
суміш нагрівають до температури кипіння розчинника протягом 5 годин;
суміш охолоджують до приблизно 70 °С, потім фільтрують;
зменшують об'єм фільтратів під зниженим тиском;
до фільтрату додають гептан;
осад, що утворився, фільтрують для одержання композиції, що складається з суміші сполуки формули (IVa) і сполуки формули (IVb); і
обробляють композицію, що складається з суміші сполуки формули (IVa) і сполуки формули (IVb), 20 % гідроксидом паладію і мурашиною кислотою в тетрагідрофурані при температурі приблизно 60 °С протягом приблизно 3 годин, із подальшою фільтрацією і концентруванням під зниженим тиском для одержання сполуки формули (І).
9. Спосіб за п. 4, де
Y являє собою хлор;
паладієвий каталізатор являє собою ацетат паладію; і
основа стадії (а) являє собою фосфат калію.
10. Спосіб за п. 9, де
суміш стадії (а) нагрівають до температури кипіння протягом 5-20 годин у диметиловому ефірі етиленгліколю.
11. Спосіб за п. 10, де
Р являє собою бензил, і
умови стадії (b) включають:
обробку паладієвим каталізатором у присутності донора водню, вибраного з групи, яка складається з газоподібного водню, мурашиної кислоти і циклогексадієну в розчиннику, вибраному з групи, яка складається зі спиртового розчинника, тетрагідрофурану або етилацетату, для одержання сполуки формули (І).
12. Спосіб за п. 1, де
Y являє собою хлор;
паладієвий каталізатор являє собою ацетат паладію;
стадію (а) виконують в атмосфері азоту;
ліганд на основі фосфіну являє собою 2-ди-трет-бутилфосфіно-1-1'-бінафтил;
основа стадії (а) являє собою фосфат калію;
суміш нагрівають до температури кипіння розчинника протягом 5-20 годин;
суміш охолоджують до приблизно 70 °С, потім фільтрують;
зменшують об'єм фільтратів під зниженим тиском;
до фільтратів додають гептан;
осад, що утворився, фільтрують для одержання композиції, що складається з суміші сполуки формули (IVa) і сполуки формули (IVb);
із подальшою обробкою композиції, що містить суміш сполуки формули (IVa) і сполуки формули (IVb), 20 % гідроксидом паладію і мурашиною кислотою в тетрагідрофурані при температурі приблизно 60 °С протягом приблизно 3 годин, із подальшим фільтруванням і концентруванням під зниженим тиском для одержання сполуки формули (І).
13. Спосіб за п. 1, де композицію, що складається з суміші сполуки формули (IIа) і сполуки формули (IIb)
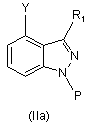 ,
,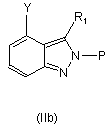 ,
,
одержують способом, що включає стадії:
(a) обробки сполуки формули (V), в якій Y являє собою хлор або бром, літієвим реагентом;
подальшої
(b) обробки суміші сполукою формули R1C(=O)-X, в якій R1 являє собою водень, алкеніл або алкіл, і X являє собою хлор, (СН3)2N-, фенокси або нітрофенокси, для одержання сполуки формули (VI)
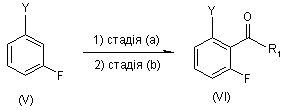 ,
,
подальшої
(с) обробки сполуки формули (VI) гідразином при нагріванні для одержання сполуки формули (VII)
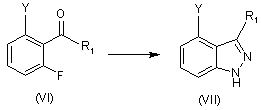 ,
,
подальшої
(d) обробки сполуки формули (VII) сполукою формули P-Z, в якій Р вибраний із групи, яка складається з алкоксіалкілу, алкілкарбонілу, алкоксикарбонілу, арилалкілу, арилкарбонілу та арилоксикарбонілу для одержання композиції, що складається з суміші сполуки формули (IIа) і сполуки формули (IIb),
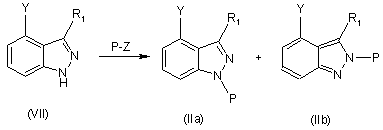 .
.
14. Спосіб за п. 13, де
стадія (а) включає обробку мета-бромфторбензолу діізопропіламідом літію в THF при температурі приблизно від -70 °С до приблизно -75 °С протягом приблизно 1 години.
15. Спосіб за п. 14, де
R1C(O)-X стадії (b) являє собою DMF; і
стадія (b) включає додавання DMF протягом періоду приблизно від 5 хвилин до приблизно 15 хвилин; подальше безперервне перемішування суміші при охолодженні протягом періоду від приблизно 30 хвилин до приблизно 1 години; подальше додавання оцтової кислоти; подальше, що стало можливим, нагрівання суміші до температури навколишнього середовища; подальше розведення розчинником, що містить метил трет-бутиловий простий ефір або етилацетат, подальше екстрагування водною кислотою; подальше концентрування для одержання сполуки формули (VI), де R1 являє собою водень.
16. Спосіб за п. 15, де:
стадія (с) включає додавання гідразину до розчину сполуки формули (VI) у DMSO, при підтриманні внутрішньої температури менше, ніж 35 °С, подальше нагрівання суміші до температури від приблизно 70 °С до приблизно 75 °С протягом приблизно від 18 до 24 годин, після чого внутрішню температуру знижують до приблизно 25 °С, подальше розведення суміші водою, із подальшим додаванням гептанів при підтриманні внутрішньої температури менше, ніж 40 °С; подальше перемішування суміші протягом приблизно 1 години, подальшу фільтрацію для одержання сполуки формули (VII), де R1 являє собою водень.
17. Спосіб за п. 16, де
умови стадії (d) додатково включають нагрівання і перемішування суміші сполуки формули (VII), де R1 являє собою водень, і бензилброміду в N,N-диметилформаміді до температури приблизно від 40 °С до приблизно 120 °С протягом періоду від приблизно 4 годин до приблизно 30 годин для одержання композиції, що складається зі сполуки формули (IIа) і сполуки формули (IIb)
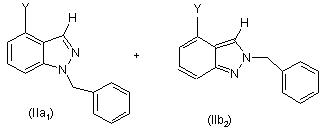 .
.
18. Спосіб за п. 17, де
умови стадії (d) додатково включають нагрівання і перемішування суміші сполуки формули (VII) і бензилброміду в N,N-диметилформаміді до температури приблизно від 105 °С до приблизно 115 °С протягом періоду від приблизно 20 годин до приблизно 24 годин для одержання сполуки формули (IIa1)
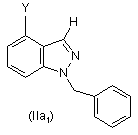 .
.
19. Спосіб за п. 18, де
Y являє собою бром.
20. Спосіб за п. 18, де
Y являє собою хлор.
21. Спосіб за п. 17, де
умови стадії (d) додатково включають нагрівання і перемішування суміші сполуки формули (VI) і бензилброміду в N,N-диметилформаміді до температури приблизно від 50 °С до приблизно 60 °С протягом періоду від приблизно 20 годин до приблизно 24 годин для надання сполуки формули (IIb2)
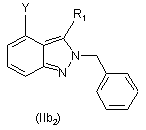 .
.
22. Спосіб за п. 21, де
Y являє собою бром.
23. Спосіб за п. 21, де
Y являє собою хлор.
24. Спосіб за п. 1, де сполуку формули (III)
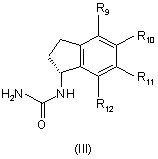 ,
,
де R9, R10, R11 і R12 визначені в п. 1,
одержують способом, що включає:
обробку сполуки формули (VIII) фенілкарбаматом і основою, вибраною з групи, яка складається з триетиламіну, діізопропілетиламіну, N-метилморфоліну, карбонату цезію, карбонату натрію і карбонату калію, в умовах нагрівання для одержання сполуки формули (III)
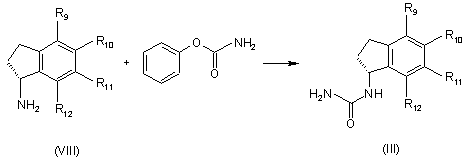 .
.
25. Спосіб за п. 24, де
основа являє собою діізопропілетиламін; суміш нагрівають до температури кипіння розчинника протягом періоду від приблизно 12 годин до приблизно 18 годин, після чого суміш охолоджують до приблизно 25 °С, розводять водою і відфільтровують з одержанням сполуки формули (III).
26. Спосіб одержання сполуки формули (IX)
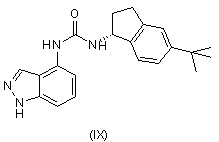 ,
,
що включає стадії:
(а) нагрівання суміші сполуки формули (XI), Pd2(DBA)3, Xantphos, основи, вибраної з групи, яка складається з гідроксиду натрію, фосфату калію і карбонату цезію, і композиції, що складається із сполуки формули (Ха) і сполуки формули (Хb),
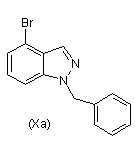 ,
,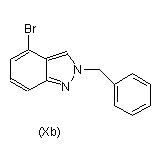 ,
,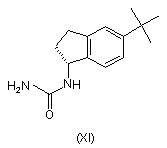 ,
,
для одержання композиції, що складається з суміші сполуки формули (ХIIа) і сполуки формули (ХІІb)
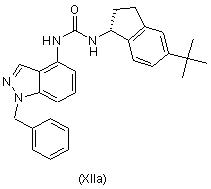 ,
,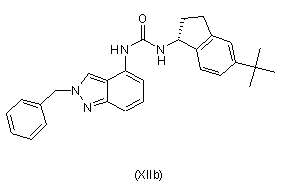 ,
,
подальшої
(b) обробки композиції суміші сполуки формули (ХIIа) і сполуки формули (ХІІb) паладієвим каталізатором, вибраним із групи, яка складається з паладію на вуглеці, гідроксиду паладію і паладію на сульфаті барію, і донором водню, вибраним із групи, яка складається з газоподібного водню, мурашиної кислоти і циклогексадієну, в розчиннику, вибраному з групи, яка складається зі спиртового розчинника, тетрагідрофурану та етилацетату, для одержання сполуки формули (IX).
27. Спосіб за п. 26, де
стадію (а) виконують в атмосфері азоту;
основа стадії (а) являє собою карбонат цезію;
суміш нагрівають до температури кипіння розчинника протягом 5 годин;
суміш охолоджують до приблизно 70 °С, потім фільтрують;
зменшують об'єм фільтратів під зниженим тиском;
до фільтрату додають гептан;
осад, що утворився, фільтрують для одержання суміші сполуки формули (ХIIа) і сполуки формули (ХІІb);
відфільтрований осад обробляють з одержанням суміші сполуки формули (ХIIа) і сполуки формули (ХІІb) 20 % гідроксидом паладію і мурашиною кислотою в тетрагідрофурані при температурі приблизно 60 °С протягом приблизно 3 годин, із подальшою фільтрацією і концентруванням під зниженим тиском з одержанням сполуки формули (IX).
28. Спосіб одержання сполуки формули (IX)
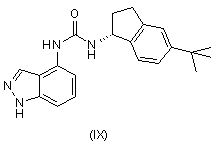 ,
,
що включає стадії:
(а) нагрівання суміші сполуки формули (XI), ацетату паладію, 2-ди-трет-бутилфосфіно-1-1'-бутилнафтилу, основи, вибраної з групи, яка складається з гідроксиду натрію, фосфату калію і карбонату цезію, і композиції, що складається з суміші сполуки формули (Хс) і сполуки формули (Xd),
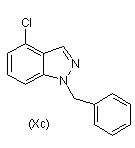 ,
,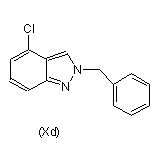 ,
,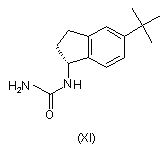 ,
,
для одержання композиції, що складається з суміші сполуки формули (ХІІа) і сполуки формули (ХІІb), подальшої
(b) обробки композиції, що складається з суміші сполуки формули (ХІІа) і сполуки формули (ХІІb), паладієвим каталізатором, вибраним з групи, яка складається з паладію на вуглеці, гідроксиду паладію і паладію на сульфаті барію, і донором водню, вибраним із групи, яка складається з газоподібного водню, мурашиної кислоти і циклогексадієну в розчиннику, вибраному з групи, яка складається зі спиртового розчинника, тетрагідрофурану та етилацетату, для одержання сполуки формули (IX).
29. Спосіб за п. 28, де
стадію (а) виконують в атмосфері азоту;
основа в стадії (а) являє собою фосфат калію;
суміш нагрівають до температури кипіння розчинника протягом 5-20 годин;
суміш охолоджують до приблизно 70 °С, потім фільтрують;
зменшують об'єм фільтратів під зниженим тиском;
до фільтрату додають гептан;
осад, що утворився, фільтрують з одержанням суміші сполуки формули (ХIIс) і сполуки формули (XIId);
суміш сполуки формули (ХIIа) і сполуки формули (ХIIb) обробляють 20 % гідроксидом паладію і мурашиною кислотою в тетрагідрофурані при температурі приблизно 60 °С протягом приблизно 3 годин, із подальшою фільтрацією і концентруванням під зниженим тиском для одержання сполуки формули (IX).
Текст
1. Спосіб одержання сполуки, що має структурну формулу (І) (11) 1 R12 O (III) , з одержанням композиції, що складається з суміші сполуки формули (IVa) і сполуки формули (IVb), в R1 3 якій R9, R10, R11 і R12 мають значення, зазначені для сполуки формули (І), R9 R10 R11 94100 4 суміш охолоджують до приблизно 70 °С, потім фільтрують; O O зменшують об'єм фільтратів під зниженим тиском; R9 R9 до фільтрату додають гептан; R1 осад, що утворився, фільтрують для одержання R1 HN N HN N H композиції, що складається з суміші сполуки форH R10 R10 мули (IVa) і сполуки формули (IVb); і R12 R12 обробляють композицію, що складається з суміші N P N R11 сполуки формули (IVa) і сполуки формули (IVb), 20 R11 N N % гідроксидом паладію і мурашиною кислотою в P тетрагідрофурані при температурі приблизно 60 °С протягом приблизно 3 годин, із подальшою фі(IVa) (IVb) льтрацією і концентруванням під зниженим тиском , для одержання сполуки формули (І). O R9 9. Спосіб за п. 4, де Y являє собою хлор; R1 HN N паладієвий каталізатор являє собою ацетат палаH дію; і R10 основа стадії (а) являє собою фосфат калію. R12 P N 10. Спосіб за п. 9, де R11 N суміш стадії (а) нагрівають до температури кипіння протягом 5-20 годин у диметиловому ефірі етиленгліколю. 11. Спосіб за п. 10, де (IVb) , Р являє собою бензил, і (b) подальшої обробки композиції, що складається умови стадії (b) включають: з суміші сполуки формули (IVa) і сполуки формули обробку паладієвим каталізатором у присутності (IVb), в умовах, які дають сполуку формули (І). донора водню, вибраного з групи, яка складається 2. Спосіб за п. 1, де з газоподібного водню, мурашиної кислоти і циклопаладієвий каталізатор стадії (а) складається з гексадієну в розчиннику, вибраному з групи, яка ацетату паладію або Pd2(DBA)3. складається зі спиртового розчинника, тетрагід3. Спосіб за п. 2, де рофурану або етилацетату, для одержання сполустадію (а) виконують в інертній атмосфері. ки формули (І). 4. Спосіб за п. 3, де 12. Спосіб за п. 1, де ліганд на основі фосфіну вибраний із групи, яка Y являє собою хлор; складається з Xantphos, 2-ди-трет-бутилфосфінопаладієвий каталізатор являє собою ацетат пала1-1'-бінафтилу і 5-(ди-трет-бутилфосфаніл)-1',3',5'дію; трифеніл-1'Н-[1,4']біпіразолілу. стадію (а) виконують в атмосфері азоту; 5. Спосіб за п. 4, де ліганд на основі фосфіну являє собою 2-ди-третY являє собою бром; бутилфосфіно-1-1'-бінафтил; паладієвий каталізатор являє собою Pd2(DBA)3; і основа стадії (а) являє собою фосфат калію; основа стадії (а) являє собою карбонат цезію. суміш нагрівають до температури кипіння розчин6. Спосіб за п. 5, де ника протягом 5-20 годин; суміш стадії (а) нагрівають до температури кипіння суміш охолоджують до приблизно 70 °С, потім протягом 2-10 годин у диметиловому ефірі етиленфільтрують; гліколю. зменшують об'єм фільтратів під зниженим тиском; 7. Спосіб за п. 6, де до фільтратів додають гептан; Р являє собою бензил, і осад, що утворився, фільтрують для одержання умови стадії (b) додатково включають: композиції, що складається з суміші сполуки форобробку паладієвим каталізатором в присутності мули (IVa) і сполуки формули (IVb); донора водню, вибраного з групи, яка складається із подальшою обробкою композиції, що містить з газоподібного водню, мурашиної кислоти і циклосуміш сполуки формули (IVa) і сполуки формули гексадієну в розчиннику, вибраному з групи, яка (IVb), 20 % гідроксидом паладію і мурашиною кисскладається з спиртового розчинника, тетрагідролотою в тетрагідрофурані при температурі прибфурану або етилацетату, для одержання сполуки лизно 60 °С протягом приблизно 3 годин, із подаформули (І). льшим фільтруванням і концентруванням під 8. Спосіб за п. 1, де зниженим тиском для одержання сполуки формуY являє собою бром; ли (І). паладієвий каталізатор стадії (а) являє собою 13. Спосіб за п. 1, де композицію, що складається Pd2(DBA)3; з суміші сполуки формули (IIа) і сполуки формули стадію (а) виконують в атмосфері азоту; (IIb) ліганд на основі фосфіну являє собою Xantphos; основа стадії (а) являє собою карбонат цезію; суміш нагрівають до температури кипіння розчинника протягом 5 годин; 5 Y Y R1 R1 N 94100 Y Y R1 N 6 (с) обробки сполуки формули (VI) гідразином при нагріванні для одержання сполуки формули (VII) R1 Y N P N N N N P (IIa) N N N H F (IIb) (IIb) (VI) , , одержують способом, що включає стадії: (a) обробки сполуки формули (V), в якій Y являє собою хлор або бром, літієвим реагентом; подальшої (b) обробки суміші сполукою формули R1C(=O)-X, в якій R1 являє собою водень, алкеніл або алкіл, і X являє собою хлор, (СН3)2N-, фенокси або нітрофенокси, для одержання сполуки формули (VI) Y Y (VII) , подальшої (d) обробки сполуки формули (VII) сполукою формули P-Z, в якій Р вибраний із групи, яка складається з алкоксіалкілу, алкілкарбонілу, алкоксикарбонілу, арилалкілу, арилкарбонілу та арилоксикарбонілу для одержання композиції, що складається з суміші сполуки формули (IIа) і сполуки формули (IIb), O 1) стадія (а) F R1 R1 P (IIa) Y O P R1 2) стадія (b) F (VI) (V) , подальшої Y Y R1 N Y R1 R1 P-Z N + N N H P N N P (VII) 14. Спосіб за п. 13, де стадія (а) включає обробку метабромфторбензолу діізопропіламідом літію в THF при температурі приблизно від -70 °С до приблизно -75 °С протягом приблизно 1 години. 15. Спосіб за п. 14, де R1C(O)-X стадії (b) являє собою DMF; і стадія (b) включає додавання DMF протягом періоду приблизно від 5 хвилин до приблизно 15 хвилин; подальше безперервне перемішування суміші при охолодженні протягом періоду від приблизно 30 хвилин до приблизно 1 години; подальше додавання оцтової кислоти; подальше, що стало можливим, нагрівання суміші до температури навколишнього середовища; подальше розведення розчинником, що містить метил трет-бутиловий простий ефір або етилацетат, подальше екстрагування водною кислотою; подальше концентрування для одержання сполуки формули (VI), де R1 являє собою водень. 16. Спосіб за п. 15, де: стадія (с) включає додавання гідразину до розчину сполуки формули (VI) у DMSO, при підтриманні внутрішньої температури менше, ніж 35 °С, подальше нагрівання суміші до температури від приблизно 70 °С до приблизно 75 °С протягом приблизно від 18 до 24 годин, після чого внутрішню температуру знижують до приблизно 25 °С, подальше розведення суміші водою, із подальшим додаванням гептанів при підтриманні внутрішньої (IIa) (IIb) . температури менше, ніж 40 °С; подальше перемішування суміші протягом приблизно 1 години, подальшу фільтрацію для одержання сполуки формули (VII), де R1 являє собою водень. 17. Спосіб за п. 16, де умови стадії (d) додатково включають нагрівання і перемішування суміші сполуки формули (VII), де R1 являє собою водень, і бензилброміду в N,Nдиметилформаміді до температури приблизно від 40 °С до приблизно 120 °С протягом періоду від приблизно 4 годин до приблизно 30 годин для одержання композиції, що складається зі сполуки формули (IIа) і сполуки формули (IIb) Y N N (IIa1) Y H H + N N (IIb2) . 18. Спосіб за п. 17, де умови стадії (d) додатково включають нагрівання і перемішування суміші сполуки формули (VII) і бензилброміду в N,N-диметилформаміді до температури приблизно від 105 °С до приблизно 115 °С протягом періоду від приблизно 20 годин до приблизно 24 годин для одержання сполуки формули (IIa1) 7 94100 8 Y являє собою бром. 23. Спосіб за п. 21, де Y являє собою хлор. 24. Спосіб за п. 1, де сполуку формули (III) Y H N R9 N R10 (IIa1) . 19. Спосіб за п. 18, де Y являє собою бром. 20. Спосіб за п. 18, де Y являє собою хлор. 21. Спосіб за п. 17, де умови стадії (d) додатково включають нагрівання і перемішування суміші сполуки формули (VI) і бензилброміду в N,N-диметилформаміді до температури приблизно від 50 °С до приблизно 60 °С протягом періоду від приблизно 20 годин до приблизно 24 годин для надання сполуки формули (IIb2) Y R1 R11 NH H2 N R12 O (III) , де R9, R10, R11 і R12 визначені в п. 1, одержують способом, що включає: обробку сполуки формули (VIII) фенілкарбаматом і основою, вибраною з групи, яка складається з триетиламіну, діізопропілетиламіну, Nметилморфоліну, карбонату цезію, карбонату натрію і карбонату калію, в умовах нагрівання для одержання сполуки формули (III) N N (IIb2) . 22. Спосіб за п. 21, де R9 R9 R10 + O R11 NH2 R10 NH2 O R11 NH H2N R12 R12 O (III) (VIII) 25. Спосіб за п. 24, де основа являє собою діізопропілетиламін; суміш нагрівають до температури кипіння розчинника протягом періоду від приблизно 12 годин до приблизно 18 годин, після чого суміш охолоджують до приблизно 25 °С, розводять водою і відфільтровують з одержанням сполуки формули (III). 26. Спосіб одержання сполуки формули (IX) . складається з гідроксиду натрію, фосфату калію і карбонату цезію, і композиції, що складається із сполуки формули (Ха) і сполуки формули (Хb), Br Br Br Br N N N N N N O HN (Xa) (Xa) NH Br N (Xb) (Xb) , Br N H N (IX)N N , N що включає стадії: (а) нагрівання суміші сполуки формули (XI), (Xa) (Xb) Pd2(DBA)3, Xantphos, основи, вибраної з групи, яка NH H2N O (XI) , N N NH NH H2N H2N O O , (XI) (XI) 9 94100 10 для одержання композиції, що складається з суміші сполуки формули (ХIIа) і сполуки формули (ХІІb) O HN O N H HN N H O HN N N N N (XIIa) , O HN N H N N N H H (IX) , що включає стадії: (а) нагрівання суміші сполуки формули (XI), ацетату паладію, 2-ди-трет-бутилфосфіно-1-1'бутилнафтилу, основи, вибраної з групи, яка складається з гідроксиду натрію, фосфату калію і кар(XIIb) бонату цезію, і композиції, що складається з суміші сполуки формули (Хс) і сполуки формули (Xd), Cl Cl Cl Cl N N N N N N N N N N , (Xd) (Xd) , (XIIb) , Cl подальшої (b) обробки композиції суміші сполуки формули N N (ХIIа) і сполуки формули (ХІІb) паладієвим каталіN затором, вибраним із групи, яка складається з паN ладію на вуглеці, гідроксиду паладію і паладію на сульфаті барію, і донором водню, вибраним із гру(Xc) пи, яка складається з газоподібного водню, мура(Xd) шиної кислоти і циклогексадієну, в розчиннику, вибраному з групи, яка складається зі спиртового розчинника, тетрагідрофурану та етилацетату, для одержання сполуки формули (IX). 27. Спосіб за п. 26, де стадію (а) виконують в атмосфері азоту; основа стадії (а) являє собою карбонат цезію; суміш нагрівають до температури кипіння розчинника протягом 5 годин; суміш охолоджують до приблизно 70 °С, потім фільтрують; зменшують об'єм фільтратів під зниженим тиском; до фільтрату додають гептан; осад, що утворився, фільтрують для одержання суміші сполуки формули (ХIIа) і сполуки формули (ХІІb); відфільтрований осад обробляють з одержанням суміші сполуки формули (ХIIа) і сполуки формули (ХІІb) 20 % гідроксидом паладію і мурашиною кислотою в тетрагідрофурані при температурі приблизно 60 °С протягом приблизно 3 годин, із подальшою фільтрацією і концентруванням під зниженим тиском з одержанням сполуки формули (IX). 28. Спосіб одержання сполуки формули (IX) NH H2N N NH H OO (Xc) (Xc) Cl H2H2N N O (XI) , для одержання композиції, що складається з суміші сполуки формули (ХІІа) і сполуки формули (ХІІb), подальшої (b) обробки композиції, що складається з суміші сполуки формули (ХІІа) і сполуки формули (ХІІb), паладієвим каталізатором, вибраним з групи, яка складається з паладію на вуглеці, гідроксиду паладію і паладію на сульфаті барію, і донором водню, вибраним із групи, яка складається з газоподібного водню, мурашиної кислоти і циклогексадієну в розчиннику, вибраному з групи, яка складається зі спиртового розчинника, тетрагідрофурану та етилацетату, для одержання сполуки формули (IX). 29. Спосіб за п. 28, де стадію (а) виконують в атмосфері азоту; основа в стадії (а) являє собою фосфат калію; суміш нагрівають до температури кипіння розчинника протягом 5-20 годин; суміш охолоджують до приблизно 70 °С, потім фільтрують; зменшують об'єм фільтратів під зниженим тиском; до фільтрату додають гептан; осад, що утворився, фільтрують з одержанням суміші сполуки формули (ХIIс) і сполуки формули (XIId); суміш сполуки формули (ХIIа) і сполуки формули (ХIIb) обробляють 20 % гідроксидом паладію і мурашиною кислотою в тетрагідрофурані при темпе (XI) (XI) 11 94100 12 ратурі приблизно 60 °С протягом приблизно 3 годин, із подальшою фільтрацією і концентруванням під зниженим тиском для одержання сполуки формули (IX). Споріднені заявки Дана заявка заявляє пріоритет попередньої Заявки США № 60/792099, поданої 14 квітня, 2006 р. Галузь техніки, якої стосується винахід Винахід стосується способу одержання індазолілсечовин, які корисні як інгібітори ванілоїдних рецепторів підтипу 1 (VR1). Винахід також стосується проміжних сполук у способі, яким одержують індазопілсечовини та їхнього застосування. Попередній рівень техніки Сполуки загальної формули (І), які с антагоністами ванілоїдних рецепторів підтипу 1 (VR1) були спочатку одержані синтетичним шляхом, описаним в USSN: 10/864068. Синтетичний напрямок у даному винаході ґрунтується на обробці нітритом натрію нітроаналіну з утворенням проміжного нітроіндазолу. Сучасні розробки налають новий високоефективний напрямок синтезу, за допомогою якого одержують менше домішок і являють більш витратний ефективний спосіб для виробництва зазначеної сполуки, що .дорого коштує. Новий напрямок також включає наступні інноваційні хімічні способи: новий спосіб одержання 4галоіндазолів за допомогою конденсації відповідних галогенованих бензальдегідів або деяких бензольних кілець, заміщених галогенованим кетоном із гідразином; спосіб для вибіркового захисту галоіндазолів у N1 і N2 положеннях і спосіб перетворення галоіндазолів в індазоїлсечовини. Сполуки загальної формули (І), які являють собою антагоністів ванілоїдних рецепторів підтипу 1 (VR1), придатні для лікування розладів, пов'язаних із підвищеною активністю ванілоїдних рецепторів підтипу 1, описаних в USSN: 10/864068. Детальний опис винаходу Даний винахід розкриває новий спосіб одержання сполук формули (І), ΖΑΖΒΝ-, (ΖΑΖΒΝ)алкілу, (ZAZBN)карбонілу, (ZAZBN)карбонілалкілу і (ZAZBN)cyльфoнiлy; R9, R10, R11 і R12 незалежно один від одного вибрані з групи, яка складається і водню, алкенілу, алкоксигрупи, алкоксіалкоксигрупи, алкоксіалкілу, алкоксикарбонілу, алкоксикарбонілалкілу, алкілу, алкілкарбонілу, алкілкарбонілалкілу, алкілкарбонілокси, алкілтіо, алкінілу, арилу, карбокси, карбоксіалкілу, ціано, ціаноалкілу, формілу, формілалкілу, галоалкокси, галоалкілу, галоалкілтіо, галогену, гетероарилу, гетероциклу, гідрокси, гідроксіалкілу, меркапто, меркаптоалкілу, нітро, (CF3)2(HO)C-, RB(SO)2RAN-, RAO(SO)2-, RBO(SO)2-, ZAZBN-, (ZAZBN)алкілу, (ZAZBN)карбонілу, (ZAZBN)кapбoнiлaлкiлy і (ZAZBN)сульфонілу; RA являє собою водень або алкіл; RB являє собою алкіл, арил або арилалкіл; і ZA і ZB незалежно один від одного являють собою водень, алкіл, алкілкарбоніл, форміл, арил або арилалкіл, що включає стадії: (а) нагрівання суміші сполуки формули (III), основи, вибраної з групи, яка складається з гідроксиду натрію, фосфату калію і карбонату цезію, і композиції, що містить сполуку формули (ІІа), сполуку формули (IIb) або їхню суміш, де Ρ вибраний із групи, яка складається з алкоксіалкілу, алкілкарбонілу, алкоксикарбонілу, арилалкілу, арилкарбонілу і арилоксикарбонілу, R1 має значення, зазначені для сполук формули (І), і Υ являє собою хлор або бром, у присутності паладієвого каталізатора і ліганду на основі фосфіну з одержанням композиції, що складається зі сполуки формули (IVa), сполуки формули (IVb) або їхньої суміші, в якій R1, R9, R10, R11 i R12 мають значення, зазначені для сполук формули (І), де R1 вибраний із групи, яка складається з водню, алкенілу, алкоксигрупи, алкоксіалкоксигрупи, алкоксіалкілу, алкоксикарбонілу, алкоксикарбонілалкілу, алкілу, алкілкарбонілу, алкілкарбонілалкілу, алкіикарбонілокси, алкілтіо, алкінілу, карбокси, карбоксіалкілу, ціано, ціаноалкілу, циклоалкілу, циклоалкілалкілу, формілу, формілалкілу, галоалкокси, галоалкілу, галоалкілтіо, галогену, гідрокси, гідроксіалкілу, меркапто, меркаптоалкілу, нітро, (СF3)2(HO)С-, RB(SO)2RAN-, RAO(SO)2-, RBO(SO)2-, подальшої (b) обробки композиції, що містить сполуку формули (IVa), сполуку формули (IVb) або їхню суміш, в умовах, які дають сполуку формули (І). Сполуки формули (І) корисні для регулювання бо 13 лю і захворювань сечової системи у ссавців інгібуванням VR1 рецептора. Зрозуміло, що спосіб винаходу може бути здійснений в інертній атмосфері, переважно в азоті. Не виходячи за рамки винаходу, зрозуміло, що паладієві каталізатори, які можуть бути використані на стадії (а), включають, але не обмежені цим, ацетат паладію і Рd2(DВА)3. Зрозуміло, що в обсязі даного винаходу ліганд на основі фосфіну може включати фосфінові ліганди, які використовуються фахівцем у даній галузі в реакціях сполучення цього типу. Найбільш переважні фосфінові ліганди включають, але не обмежені цим, Xantphos, 2-дитрет-бутилфосфіно-1-1’-бінафтил і 5-(ди-третбугилфосфаніл)-1',3',5'-трифеніл-1’Н[1,4']біпіразоліл. Також зрозуміло, що в способі даного винаходу основою стадії (а) може бути фосфат калію, карбонат калію або карбонат цезію, переважно, карбонат цезію. Також зрозуміло, що в способі даного винаходу суміш стадії (а) нагрівають до температури кипіння розчинника протягом 2-20 годин, в органічному розчиннику, що включає, але не обмежуючись перерахованим, THF, толуол, DMF, NMP або диметиловий ефір етиленгліколю, переважно, диметиловий ефір етиленгліколю. У деяких варіантах здійснення, де Υ являє собою бром, суміш стадії (а) звичайно нагрівають протягом від приблизно 2 до приблизно 10 годин у диметиловому ефірі етиленгліколю. У деяких випадках, коли Υ являє собою бром, суміш стадії (а) нагрівають протягом 5 годин. У деяких варіантах здійснення, де Υ являє собою бром, переважні умови включають використання Рd2(DВА)3, Xantphos і карбонату цезію на стадії (а). В інших варіантах здійснення, де Υ являє собою хлор, суміш стадії (а) звичайно нагрівають протягом від, приблизно 5 до, приблизно 20 годин у диметиловому ефірі етиленгліколю. Якщо Υ являє собою хлор, переважним пала дієвим каталізатором є ацетат паладію. У деяких варіантах здійснення даного винаходу, де Υ являє собою хлор, розкрите використання на стадії (а) ацетату паладію, 2-ди-трет-бугилфосфіно-1-1’-бінафтилу і фосфату калію. За зазначеними стадіями, у загальному випадку, йдуть фільтрація і/або осадження для одержання композиції, що складається зі сполуки формули (ІVa) або (IVb) або їхньої суміші. Даний винахід також включає спосіб одержання сполуки формули (ІІа) і сполуки формули (ІІb), описаний на схемі 1. У рамках варіанту здійснення описують спосіб одержання сполуки формули (ІІа) і сполуки формули (lIb) на стадії (а), де обробка мета-хлор- або мета-бромфторбензолу основою, такою як, але без обмеження перерахованим, діізопропіламід літію, дициклогексіамід літію або біс(триметилсиліл)амід літію в розчиннику здійснюють при температурі від приблизно -50°С до приблизно -78°С протягом приблизно від 1 до 3 годин. Спосіб додатково включає обробку охолодженої суміші сполукою формули R1C(=O)-X, де R1 являє собою водень, алкеніл або алкіл, і X являє собою хлор, (СН3)2N-, фенокси-або нітрофенокси, для одержання сполуки формули (V), 94100 14 Спосіб даного винаходу додатково включає обробку сполуки формули (V) гідразином у розчиннику, що включає, без обмеження перерахованим, DMF, DMSO або THF, переважно DMSO, для одержання сполуки формули (VI), Спосіб додатково включає обробку сполуки формули (VI) реагентом P-Z, де Ρ вибраний із групи, яка складається з алкоксіалкілу, алкілкарбонілу, алкоксикарбонілу, арилалкілу, арилкарбонілу і арилоксикарбонілу, такого як, але не обмежуючись перерахованим, ацетилхлорид, оцтовий ангідрид, бензилбромід, бензилхлорформіат і ди-третбутилдикарбонат, з одержанням композиції, що складається зі сполуки формули (ІІа), сполуки формули (ІІb) або суміші сполуки формули (ІІа) і сполуки формули (ІІb), В одному варіанті здійснення винаходу, розкривають спосіб, який додатково включає нагрівання і перемішування суміші сполуки формули (VI) і бензилброміду в органічному розчиннику, наприклад. Ν,N-диметилформаміді, DMA, NMP, переважно DMF, при температурі від приблизно 40°С до приблизно 120°С протягом періоду від приблизно 4 годин до приблизно 30 годин для введення захисної бензильної групи на один з атомів азоту. В іншому переважному варіанті здійснення винаходу, спосіб додатково включає обробку сполуки формули (VI) бензилбромідом у Ν,Νдиметилформаміді при температурі від приблизно 105°С до приблизно 115°С протягом періоду від приблизно 20 годин до приблизно 24 годин для одержання сполуки формули (VIla), В іншому варіанті здійснення, спосіб також розкриває нагрівання і перемішування суміші сполу 15 ки формули (VI) і бензилброміду в Ν,Νдиметилформаміді при температурі від приблизно 50°С до приблизно 60°С протягом періоду від приблизно 20 годин до приблизно 24 годин для одержання сполуки формули (Vllb), 94100 16 бонату цезію, і композиції, що складається зі сполуки формули (Ха), сполуки формули (Хb) або їхньої суміші, де Υ являє собою хлор або бром, у присутності каталізатора, такою як, але не обмежуючись перерахованим, Pd2(DBA)3 і ліганду на основі фосфіну, включаючи, але не обмежуючись перерахованим, Xantphos, 2-ди-третбутилфосфіно-1-1’-бінафтил і 5-(ди-третбутилфосфаніл)-1',3',5'-трифеніл-1'Н[1,4']біпіразоліл, в атмосфері азоту, Спосіб даного винаходу також розкриває обробку сполуки формули (VIII), як описано на схемі 3, для одержання сполуки формули (ІІІ), для одержання композиції, що складається зі сполуки формули (ХІІа), сполуки формули (ХІІb) або їхньої суміші, Спосіб також описує обробку композиції, що складається зі сполуки формули (VIla), сполуки формули (Vllb) або їхньої суміші, де R1 має значення, зазначені для сполуки формули (І), і Υ являє собою хлор або бром, сполукою формули (ІІІ), основою, вибраною з групи, яка складається з карбонату натрію, карбонату калію і карбонату цезію, у присутності паладієвого каталізатора і ліганду на основі фосфіну, для одержання композиції, що складається зі сполук формули (IVa), сполуки формули (IVb) або їхньої суміші, де група Ρ являє собою бензил. Спосіб додатково описує обробку композиції, що складається зі сполуки формули (IVa), сполуки формули (IVb) або їхньої суміші, де група Ρ являє собою бензил, паладієвим каталізатором, що містить паладій на вуглеці, гідроксид паладію або паладій на сульфаті барію, переважно, гідроксид паладію, більш переважно 20% гідроксид паладію і донор водню, що включає атмосферу водню, мурашину кислоту або циклогексадієн, переважно, мурашину кислоту, у розчиннику, що включає спиртові розчинники, тетрагідрофуран або етилацетат; переважно, тетрагідрофуран, для одержання сполуки формули (І). Даний винахід також включає спосіб одержання сполуки формули (IX), що включає стадії: нагрівання, переважно протягом 5-10 годин, суміші сполуки формули (XI), основи, що складається з фосфату калію, карбонату калію або карбонату цезію, переважно, кар подальшої обробки композиції, що складається зі сполуки формули (ХІІа), сполуки формули (ХІІb) або їхньої суміші, паладієвим каталізатором, що включає паладій на вуглеці, гідроксид паладію або паладій на сульфаті барію, переважно, гідроксид паладію, більш переважно 20% гідроксидом паладію і донором водню, що включає атмосферу водню, мурашину кислоту або циклогексадієн, переважно, мурашину кислоту, у розчиннику, включаючи спиртові розчинники, тетрагідрофуран або етилацетат; переважно, тетрагідрофуран, для одержання сполуки формули (IX). Даний винахід включає композицію, що складається зі сполуки формули (IIа), сполуки формули (IIb) або їхньої суміші, де Υ являє собою хлор або бром; і R1 вибраний із групи, яка складається з водню, алкенілу, алкоксигрупи, алкоксіалкоксигрупи, алкоксіалкілу, алкоксикарбонілу, алкоксикарбонілалкілу, алкілу, алкілкарбонілу, алкілкарбонілалкілу, алкілкарбонілокси, алкілтіо, алкінілу, карбокси, карбоксіалкілу, ціано, ціаноалкілу, циклоалкілу. циююалкілалкілу, формілу, формілалкілу, галоалкокси, галоалкілу, галоалкілтіо, галогену, гідрокси, гідроксіалкілу. меркапто, меркаптоалкілу, нітро, (CF3)2(HO)C-, RB(SO)2RAN-, RAO(SO)2-, RBO(SO)2-, ZAZBN-, 17 (ZAZBN)алкілу, (ZAZBN)карбонілу, (ZAZBN)кapбoнiлaлкiлy і (ZAZBN)cyльфoнiлy. Даний винахід також включає сполуку формули (III), де R9, R10, R11 і R12 кожен незалежно вибраний із групи, яка складається з водню, алкенілу, алкоксигрупи, алкоксіалкоксигрупи, алкоксіалкілу, алкоксикарбонілу, алкоксикарбонілалкілу, алкілу, алкілкарбонілу, алкілкарбонілалкілу, алкілкарбонілокси, алкілтіо, алкінілу, карбокси, карбоксіалкілу, ціано, ціаноалкілу, формілу, формілалкілу, галоалкокси, галоалкілу, галоалкілтіо, галогену, гетероарилу, гетероциклу, гідрокси, гідроксіалкілу, меркапто, меркаптоалкілу, нітро, (CF3)2(HO)C-, RB(SO)2RAN-, RAO(SO)2-, RBO(SO)2-, ZAZBN-, (ZAZBN)алкілу, (ZAZBN)карбонілу, (ZAZBN)кapбoнiлaлкiлy і (ZAZBN)cyльфoнiлy. Даний винахід також включає композицію, що містить сполуку формули (Ха), сполуку формули (Хb) або їхню суміш, де Υ являє собою хлор або бром, яку застосовують у способі одержання сполуки формули (IX). Даний винахід також включає сполуку формули (XI), яку застосовують у способі одержання сполуки формули (IX). Зрозуміло, що сполуки формули (IIа), (IIа1), (lIb), (IIb2) і (III) придатні в способі одержання сполуки формули (I), яка є представником сполук даного винаходу і яка є корисною для лікування розладу шляхом пригнічення ванілоїдних рецепторів підтипу 1 у ссавців, що включає введення терапевтично ефективної кількості сполуки формули (І) або її фармацевтично прийнятної солі або проліків. Зрозуміло, що розлад включає біль, запальну гіперальгезію, нетримання сечі і гіперреактивність сечового міхура. Також зрозуміло, що сполуки формули (Ха), (Xb), (Xc), (Xd) і (XI) придатні в способі одержання сполуки формули (IX), яку 94100 18 застосовують для лікування розладу шляхом інгібування ванілоїдних рецепторів підтипу 1 у ссавців, що включає введення терапевтично ефективної кількості сполуки формули (І) або її фармацевтично прийнятної солі або проліків. Зрозуміло, що розлад включає біль, запальну гіперальгезію, нетримання сечі і гіперреактивність сечового міхура. Визначення Використані в даному документі та у формулі винаходу перераховані нижче терміни мають такі значення: Термін "алкеніл", використаний у даному документі, означає вуглеводень із лінійним або розгалуженим ланцюгом, що містить від 2 до 10 атомів вуглецю і що містить, принаймні, один подвійний вуглець-вуглецевий зв'язок, утворений видаленням двох атомів водню. Типові приклади алкенілів включають, але не обмежені перерахованим, етеніл, 2-пропеніл, 2-метил-2-пропеніл, 3бутеніл, 4-пентеніл, 5-гексеніл, 2-гептеніл, 2метил-1-гептеніл і 3-деценіл. Термін "алкокси", використаний у даному документі, означає алкільну групу, як визначено в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою атома кисню. Типові приклади алкокси включають, але не обмежені перерахованим, метокси, етокси, пропокси, 2пропокси, бутокси, трет-бутокси, пентилокси і гексилокси. Термін "алкоксіалкокси", використаний у даному документі, означає алкоксигрупу, як визначено в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою алкоксигрупи, як визначено в даному документі. Типові приклади алкоксіалкокси включають, але не обмежені перерахованим, метоксиметокси, етоксиметокси і 2етоксіетокси. Термін "алкоксіалкіл", використаний у даному документі, означає алкоксигрупу, як визначено в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою алкільної групи, як визначено в даному документі. Типові приклади алкоксіалкілу включають, але не обмежені перерахованим, трет-бутоксиметил, 2-етоксіетил, 2-метоксіетил і метоксиметил. Термін "алкоксикарбоніл", використаний у даному документі, означає алкоксигрупу, як визначено в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою карбонільної групи, як визначено в даному документі. Типові приклади алкоксикарбонілу включають, але не обмежені перерахованим, метоксикарбоніл, етоксикарбоніл і трет-бутоксикарбоніл. Термін "алкоксикарбонілалкіл", використаний у даному документі, означає алкоксикарбонільну групу, як визначено в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою алкільної групи, як визначено в даному документі. Типові приклади алкоксикарбонілалкілу включають, але не обмежені перерахованим, 3метоксикарбонілпропіл, 4-етоксикарбонілбутил і 2трет-бутоксикарбонілетил. Термін "алкіл", використаний у даному документі, означає вуглеводень із лінійним або розга 19 луженим ланцюгом, що містить від 1 до 10 атомів вуглецю. Типові приклади алкілу включають, але не обмежені перерахованим, метил, етил, нпропіл, ізопропіл, н-бутил, втор-бутил, ізобутил, трет-бутил, н-пентил, ізопентил, неопентил, нгексил, 3-метилгексил, 2,2-диметилпентил, 2,3диметилпентил, н-гептил, н-октил, н-ноніл і ндецил. Термін "алкілкарбоніл", використаний у даному документі, означає алкільну групу, як визначено в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою карбонільної групи, як визначено в даному документі. Типові приклади алкілкарбонілу включають, але не обмежені перерахованим, ацетил, 1-оксопропіл, 2,2димеіил-1-оксопропіл, 1-оксобутилі 1-оксопентил. Термін "алкілкарбонілалкіл", використаний у даному документі, означає алкілкарбонільну групу, як визначено в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою алкільної групи, як визначено в даному документі. Типові приклади алкілкарбонілалкілу включають, але не обмежені перерахованим, 2-оксопропіл, 3,3-диметил-1-оксопропіл, 3-оксобутил і 3оксопентил. Термін "алкілкарбонілокси", використаний у даному документі, означає алкілкарбонільну групу, як визначено в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою атома кисню. Типові приклади алкілкарбонілокси включають, але не обмежені перерахованим, ацетилокси, етилкарбонілокси і третбутилкарбонілокси. Термін "алкілсульфоніл", використаний у даному документі, означає алкільну групу, як визначено в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою сульфонільної групи, як визначено в даному документі. Типові приклади алкілсульфонілу включають, але не обмежені перерахованим, метилсульфоніл і етилсульфоніл. Термін "алкілтіо", використаний у даному документі, означає алкільну групу, як визначено в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою атома сірки. Типові приклади алкілтіо включають, але не обмежені перерахованим, метилсульфаніл, етилсульфаніл, трет-бутилсульфаніл і гексилсульфаніл. Термін "алкініл", використаний у даному документі, означає вуглеводень із лінійним або розгалуженим ланцюгом, що містить від 2 до 10 атомів вуглецю, і що містить, принаймні, один потрійний вуглець-вуглецевий зв'язок. Типові приклади алкінілів включають, але не обмежені перерахованим, ацетиленіл, 1-пропініл, 2-пропініл, 3-бутиніл, 2пентиніл і 1-бутиніл. Термін "арил", використаний у даному документі, означає фенільну групу або біциклічну або трициклічну конденсовану систему, де одне або більше конденсованих кілець являють собою фенільну групу. Біциклічні конденсовані системи проілюстровані фенільною групою, конденсованою з циклоалкільною групою, як визначено в даному документі, або іншою фенільною групою. Трициклічні конденсовані системи проілюстровані біцик 94100 20 лічними конденсованими системами з циклоалкільною групою, як визначено в даному документі, або іншою фенільною групою. Типові приклади арилу включають, але не обмежені перерахованим, антраценіл, азуленіл, флюореніл, інденіл, нафтил, феніл і тетрагідронафтил. Арильні групи даного винаходу необов'язково заміщені 1, 2, 3, 4 або 5 замісниками, незалежно один від одного вибраними з алкенілу, алкоксигрупи, алкоксіалкоксигрупи, алкоксіалкілу, алкоксикарбонілу, алкоксикарбонілалкілу, алкілу, алкілкарбонілу, алкілкарбонілалкілу, алкілкарбонілокси, алкілсульфонілу, алкілтіо, алкінілу, карбокси, карбоксіалкілу, ціано, ціаноалкілу, циклоалкілу, циклоалкілалкілу, етилендіокси, формілу, формілалкілу, галоалкокси, галоалкілу, галоалкілтіо, галогену, гідрокси, гідроксіалкілу, метилендіокси, меркапто, меркаптоалкілу, нітро, ZCZDN-, (ZCZDN)алкілу, (ZCZDN)карбонілу, (ZCZDN)кapбoнiлaлкiлy, і (ZCZDN)сульфонілу, NRAS(O)2RB, -S(O)2ORA і -S(O)2RA, де RA і RB визначені в даному документі. Термін "арилалкіл", використаний у даному документі, означає арильну групу, як визначено в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою алкільної групи, як визначено в даному документі. Типові приклади арилалкілу включають, але не обмежені перерахованим, бензил, 2-фенілетил, 3фенілпропіл і 2-нафт-2-илетил. Термін "карбокси", використаний у даному документі, означає -СО2Н групу. Термін "карбоксіалкіл", використаний у даному документі, означає карбоксигрупу, як визначено в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою алкільної групи, як визначено в даному документі. Типові приклади карбоксіалкілу включають, але не обмежені перерахованим, карбоксиметил, 2-карбоксіетил і 3-карбоксипропіл. Термін "ціано", використаний у даному документі, означає -CN групу. Термін "ціаноалкіл", використаний у даному документі, означає ціаногрупу, як визначено в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою алкільної групи, як визначено в даному документі. Типові приклади ціаноалкілу включають, але не обмежені перерахованим, ціанометил, 2-ціаноетил і 3-ціанопропіл. Термін "циклоалкіл", використаний у даному документі, означає систему з насиченим моноциклічним кільцем, що містить від 3 до 8 атомів вуглецю. Приклади циклоалкілу включають циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил і циклооктил. Термін "циклоалкілалкіл", використаний у даному документі, означає циклоалкільну групу, як визначено в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою алкільної групи, як визначено в даному документі. Термін "етилендіокси", використаний у даному документі, означає -О(СН2)2О-групу, в якій атоми кисню етилендіоксигрупи приєднані до початкового молекулярного фрагмента за допомогою одного атома вуглецю, утворюючи п'ятичленне кільце, 21 або атоми кисню етилендіоксигрупи приєднані до початкового молекулярного фрагмента за допомогою двох суміжних атомів вуглецю, утворюючи шестичленне кільце. Термін "форміл", використаний у даному документі, означає -С(О)Н-групу. Термін "формілалкіл", використаний у даному документі, означає формільну групу, як визначено в даному документі, приєднану до вихідною молекулярного фрагмента за допомогою алкільної групи, як визначено в даному документі. Термін "гало" або "галоген", використаний у даному документі, означає -СІ, -Вr, -І або -F. Термін "галоалкокси", використаний у даному документі, означає, принаймні, один галоген, як визначено в даному документі, приєднаний до початкового молекулярного фрагмента за допомогою алкоксигрупи, як визначено в даному документі. Типові приклади галоалкокси включають, але не обмежені перерахованим, хлорметокси, 2фторетокси, трифторметокси, 2-хлор-3фторпентилокси і пентафторетокси. Термін "галоалкіл", використаний у даному документі, означає, принаймні, один галоген, як визначено в даному документі, приєднаний до початкового молекулярного фрагмента за допомогою алкільної групи, як визначено в даному документі. Типові приклади галоалкілу включають, але не обмежені перерахованим, хлорметил, 2-фторетил, трифторметил, пентафторетил і 2-хлор-3фторпентил. Термін "галоалкілтіо", використаний у даному документі, означає, принаймні, один галоген, як визначено в даному документі, приєднаний до початкового молекулярного фрагмента за допомогою алкілтіогрупи, як визначено в даному документі. Типові приклади галоалкілтіо включають, але не обмежені перерахованим, трифторметилтіо. Термін "гетероарил", використаний у даному документі, означає моноциклічний гетероарил або біциклічний гетероарил. Моноциклічний гетероарил являє собою 5- або 6-членне кільце, що містить, принаймні, один гетероатом, незалежно вибраний із групи, яка складається з О, N і S. П’ятичленне кільце містить два подвійних зв'язки, може містити один, два, три або чотири атоми азоту, один атом азоту та один атом кисню, один атом азоту та один атом сірки, або один атом кисню або один атом сірки. Шестичленне кільце містить три подвійних зв'язки, може містити один, два, три або чотири атоми азоту, один атом азоту та один атом кисню, один атом азоту та один атом сірки, один або два атоми кисню або один або два атоми сірки. П'яти- або шестичленний гетероарил з'єднаний із вихідним молекулярним фрагментом за допомогою будь-якого атома вуглецю або будь-якого атома азоту, що входить до складу гетероарилу. Типові приклади моноциклічного гегероарилу включають, але не обмежені перерахованим, фурил, імідазоліл, ізоксазоліл, ізотіазоліл, оксадіазоліл, оксазоліл, піридиніл, піридазиніл, піримідиніл, піразиніл, піразоліл, піроліл, тетразоліл, тіадіазоліл, триазоліл, тієніл, тіазоліл і триазиніл. Біциклічний гетероарил містить моноциклічний гетероарил, конденсований із фенілом, або 94100 22 моноциклічний гетероарил, конденсований із циклоалкілом, або моноциклічний гетероарил, конденсований із циклоалкенілом, або моноциклічний гетероарил, конденсований із моноциклічним гетероарилом. Біциклічний гетероарил приєднаний до вихідного молекулярного фрагмента за допомогою якого-небудь атома вуглецю або якогонебудь атома азоту, що заміщують, який входить до складу біциклічного гетероарилу. Типові приклади біциклічного гетероарилу включають, але не обмежені перерахованим, бензімідазоліл, бензофураніл, бензотієніл, бензоксадіазоліл, цинолініл, дигідрохінолініл, дигідроізохінолініл, фуропіридиніл, індазоліл, індоліл, ізохінолініл, нафтиридиніл, хінолініл, тетрагідрохінолініл і тієнопіридиніл. Гетероарильні групи даного винаходу необов'язково заміщені 1, 2, 3, 4 або 5 замісниками, вибраними незалежно один від одного з алкенілу, алкокси, алкоксіалкокси, алкоксіалкілу, алкоксикарбонілу, алкоксикарбонілалкілу, алкілу, алкілкарбонілу, алкілкарбонілалкілу, алкілкарбонілокси, алкілсульфонілу, алкілтіо, алкінілу, карбокси, карбоксіалкілу, ціано, ціаноалкілу, циклоалкілу,. циклоалкілалкілу, етилендіокси, формілу, формілалкілу, галоалкокси, галоалкілу, галоалкілтіо, галогену, гідрокси, гідроксіалкілу, метилендіокси, меркапто, меркаптоалкілу, нітро, ZCZDN-, (ZCZDN)алкілу, (ZCZDN)карбонілу, (ZCZDN)карбонілалкілу, (ZCZDN)сульфонілу, NRAS(O)2RB, -S(O)2ORA і -S(O)2RA, де RA і RB визначені в даному документі. Термін "гетероцикл", використаний у даному документі, означає трьох, чотирьох, п'яти, шести, семи або восьмичленне кільце, що містить один або два гетероатоми, незалежно один від одного вибрані з групи, яка складається з азоту, кисню і сірки. Тричленне кільце не містить подвійних зв'язків. Чотирьох і п'ятичленне кільце або не містить або містить один подвійний зв'язок. Шестичленне кільце або не містить, або містить один або два подвійних зв'язки. Семичленні і восьмичленні кільця або не містять, або містять один, два або три подвійних зв'язки. Гетероциклічні групи даного винаходу можуть бути приєднані до вихідного молекулярного фрагмента за допомогою атома вуглецю або азоту. Типові приклади гетероциклічних сполук включають, але не обмежені перерахованим, азабіцикло[2.2.1]гептаніл, азабіцикло[2.2.1]октаніл, азетидиніл, гексагідро-1Назепиніл, гексагідроазоцин-(2Н)-іл, індазоліл, морфолініл, октагідроізохінолін, піперазиніл, піперидиніл, піридиніл, піролідиніл і тіоморфолініл. Гетероциклічні сполуку даного винаходу необов'язково заміщені 1, 2, 3 або 4 замісниками, незалежно один від одного вибраними з алкенілу, алкокси, алкоксіалкокси, алкоксіалкілу, алкоксикарбонілу, алкоксисульфонілу, алкілу, алкілкарбонілу, алкілкарбонілокси, алкілсульфонілу, алкінілу, карбокси, ціано, формілу, галоалкокси, галоалкілу, галогену, гідрокси, гідроксіалкілу, меркапто, нітро, піперидинілу та оксо. Термін "гідрокси", використаний у даному документі:, означає -ОН групу. Термін "гідроксіалкіл", використаний у даному документі, означає принаймні одну гідроксигрупу, 23 визначену в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою алкільної групи, визначеної в даному документі. Типові приклади гідроксіалкілу включають, але не обмежені перерахованим, гідроксиметил, 2гідроксіетил, 3-гідроксипропіл, 2,3дигідроксипентил і 2-етил-4-гідроксигептил. Термін "меркапто", використаний у даному документі, означає -SH групу. Термін "меркаптоалкіл". використаний у даному документі, означає меркаптогрупу, визначену в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою алкільної групи, визначеної в даному документі. Рипові приклади меркаптоалкілу включають, але не обмежені перерахованим, 2-меркаптоетил і 3меркаптопропіл. Термін "метилендіокси", використаний у даному документі, означає -ОСН2О-групу, в якій атоми кисню метилендіокси приєднані до вихідного молекулярного фрагмента за допомогою двох суміжних атомів вуглецю. Термін "нітро", використаний у даному документі, означає -NO2 групу. Термін "захисна група азоту", використаний у даному документі, означає групи, призначені для захисту аміногрупи від небажаних реакцій під час процесів синтезу. Переважними захисними групами азоту є ацетил, бензоїл, бензил, бензилоксикарбоніл (Cbz), форміл, фенілсульфоніл, третбутоксикарбоніл (Вос), трет-бутилацетил, трифторацетил і трифенілметил (тритил). Способи, що описують введення або видалення таких груп, описані в Protecting Groups In Organic Synthesis, 3 Ed. TheodoRA W. Greene and Peter G.M. Wuts, John Wiley & Sons, Inc., або відомі фахівцеві в даній галузі. Термін "оксо", використаний у даному документі, означає =О. Термін "P-Z", використаний у даному документі, означає захисну групу азоту, вибрану з групи, яка складається з алкоксіалкілу, алкілкарбонілу, алкоксикарбонілу, арилалкілу, арилкарбонілу та арилоксикарбонілу. Переважні Ρ групи включають, але не обмежені перерахованим, арилкарбоніл, алкоксикарбоніл, арилалкіл і арилоксикарбоніл. Термін "RA", використаний у даному документі, означає замісник, який вибраний із групи, яка складається з водню та алкілу. Термін "RВ", використаний у даному документі, означає замісник, який вибраний із групи, яка складається з алкілу, арилу та арилалкілу. Термін "сульфоніл", використаний у даному документі, означає -S(O)2-групy. Термін "ZAZBN", використаний у даному документі, означає дві групи, ZA і ZB, які приєднані до початкового молекулярного фрагмента за допомогою атома азоту. ΖА і ΖВ кожна незалежно один від одного вибрана з водню, алкілу, алкілкарбонілу, формулу, арилу та арилалкілу. Типові приклади ZAZBN- включають, але не обмежені перерахованим, аміно, метиламіно, ацетиламіно, бензиламіно, феніламіно та ацетилметиламіно. Термін "(ZAZBN)алкіл", використаний у даному документі, означає ZAZBN-групу, визначену в да 94100 24 ному документі, приєднану до вихідного молекулярного фрагмента за допомогою алкільної групи, визначеної в даному документі. Типові приклади (ZAZBN)алкілу включають, але не обмежені перерахованим, амінометил, 2-(метиламіно)етил, 2(диметиламіно)етил і (етилметиламіно)метил. Термін "(ZAZBN)карбоніл", використаний у даному документі, означає ZAZBN-групy, визначену в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою карбонільної групи, визначеної в даному документі. Типові приклади (ZAZBN)карбонілу включають, але не обмежені перерахованим, амінокарбоніл, (метиламіно)карбоніл, (диметиламіно)карбоніл і (етилметиламіно)карбоніл. Термін "(ZAZBN)кapбoнiлaлкiл", використаний у даному документі, означає (ZAZBN)карбонільну групу, визначену в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою алкільної групи, визначеної в даному документі. Типові приклади (ZAZBN)кapбoнiлaлкiлy включають, але не обмежені перерахованим, (амінокарбоніл)метил, 2-((метиламіно)карбоніл)етил і ((диметиламіно)карбоніл)метил. Термін "(ZAZBN)cyльфoнiл", використаний у даному документі, означає ZAZBN-групу, визначену в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою сульфонільної групи, визначеної в даному документі. Типові приклади (ZAZBN)cyльфoнiлy включають, але не обмежені перерахованим, аміносульфоніл, (метиламіно)сульфоніл, (диметиламіно)сульфоніл і (етилметиламіно)сульфоніл. Термін "ZCZDN-", використаний у даному документі, означає дві групи, ZC і ZD, які приєднані до початкового молекулярного фрагмента за допомогою атома азоту. ZC і ZD кожна незалежно один від одного вибрана з водню, алкілу, алкілкарбонілу, формілу, арилу та арилалкілу. Типові приклади ZCZDN- включають, але не обмежені перерахованим, аміно, метиламіно, ацетиламіно, бензиламіно, феніламіно та ацетилметиламіно. Термін "(ZCZDN)aлкiл", використаний у даному документі, означає -ZCZDN-групу, визначену в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою алкільної групи, визначеної в даному документі. Типові приклади (ZCZDN)алкілу включають, але не обмежені перерахованим, амінометил, 2-(метиламіно)етил, 2(диметиламіно)етил і (етилметиламіно)метил. Термін "(ZCZDN)карбоніл", використаний у даному документі, означає ZCZDN-групy, визначену в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою карбонільної групи, визначеної в даному документі. Типові приклади (ZCZDN)карбонілу включають, але не обмежені перерахованим, амінокарбоніл, (метиламіио)карбоніл, (диметиламіно)карбоніл і (етилметиламіно)карбоніл. Термін "(ZCZDN)кapбoнiлaлкiл", використаний у даному документі, означає (ZCZDN)карбонільну групу, визначену в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою алкільної групи, визначеної в даному документі. Типові приклади (ZCZDN)кapбoнiлaлкiлy 25 включають, але не обмежені перерахованим, (амінокарбоніл)метил, 2-((метиламіно)карбоніл)етил і ((диметиламіно)карбоніл)метил. Термін "(ZCZDN)сульфоніл", використаний у даному документі, означає ZCZDN-групy, визначену в даному документі, приєднану до вихідного молекулярного фрагмента за допомогою сульфонільної групи, визначеної в даному документі. Типові приклади (ZCZDN)сульфонілy включають, але не обмежені перерахованим, аміносульфоніл, (метиламіно)сульфоніл, (диметиламіно)сульфоніл і (етилметиламіно)сульфоніл. Сполуки даного винаходу названі згідно з ACD/ChemSketch версією 5,0 (розроблена Advanced Chemistry Development, Inc., Торонто, ON, Канада) або їм дані назви, які, мабуть, відповідають ACD номенклатурі. Схеми Сполуки винаходу можуть бути краще зрозумілими за допомогою нижченаведених схем синтезу і нижченаведених способів, які ілюструють способи, якими сполуки можуть бути одержані. Скорочення, які використані в описі схем і прикладів, являють собою наступне: DME для 1,2диметоксіетану або диметилового ефіру етиленгліколю, DMF для Ν,Ν-диметилформаміду, DMSO для диметилсульфоксиду, LDA для діізопропіламіду літію, який може бути одержаний повільним додаванням 2,5н бутиллітію в гексані до розчину діізопропіламіну в THF від 0°С до -75°С, МТВЕ для метил трет-бутилового ефіру, THF для тетрагідрофурану, "кт" для "кімнатної температури" або температури навколишнього середовища, відповідно в інтервалі від приблизно 20°С до приблизно 30°С. Схема 1 Як показано на схемі 1, галофторбензол, де галоген галофторбензолу, Y, являє собою хлор або бром, при обробці основою, включаючи, але не обмежуючись перерахованим, діізопропіламід літію (LDA), дициклогексиламід літію або подібні речовини, відомі фахівцеві в даній галузі, у розчиннику, такому як, але не обмежуючись перерахованим, тетрагідрофуран, метил трет-бутиловий ефір або діетиловий ефір, при температурі від приблизно -50°С до приблизно -78°С протягом від приблизно 1 до приблизно 3 годин; подальшій обробці сполуками формули R1C(=O)-X, де R1 являє 94100 26 собою водень, алкеніл або алкіл, і X являє собою хлор, (CH3)2N-, фенокси або нітрофенокси, дає сполуку формули 1. У випадку, де X являє собою (СН3)2N-, обробка звичайно супроводжується додаванням кислоти, такої як оцтова кислота або розведена водна неорганічна кислота. Більш переважні умови включають, але не обмежені перерахованим, використання діізопропіламіду літію в тетрагідрофурані при температурі від приблизно 70°С до приблизно -78°С протягом 1 години, із подальшим додаванням R1C(=O)-X, за яким йде додавання кислоти, такої як оцтова або розведена водна неорганічна кислота, що дозволяє суміші досягнути температури навколишнього середовища, після чого йде розділення між водним і органічним розчинником, із подальшим відділенням органічного розчину і концентруванням. Сполуки формули 1 при обробці безводним гідразином або гідратом гідразину при нагріванні дадуть індазоли формули 2. Умови циклізації включають нагрівання до приблизно від 50°С до приблизно 100°С суміші сполуки формули 1 із безводним гідразином або гідратом гідразину в розчиннику, включаючи, але не обмежуючись перерахованим, DMF, DMSO або THF. Як альтернатива, сполуки формули 1, що містять атом водню в R1, можуть бути зв'язані з гідроксиламіном або О-алкілованим гідроксиламіном з утворенням відповідного оксиму. Оксим може стабілізувати формільну групу сполук формули 1. Оксим може бути використаний безпосередньо для утворення індазолу нагріванням у присутності гідразину для одержання сполук формули 2. Сполуки формули 2 при обробці реагентами, які вступають у реакцію з атомами азоту для захисту їх від додаткових реакцій, наприклад P-Z, які включають ацетилхлорид, оцтовий ангідрид, бензилхлорформіат, ди-трет-бутилдикарбонат або 9флюоренілметилхлорформіат, дадуть або сполуку формули (3), сполуку формули (4) або суміш сполук формули (3) і (4), що залежить від використовуваних умов. Часто може бути одержана суміш, що містить у більшій частині одну сполуку в порівнянні з іншим, яка може бути додатково очищена для виділення однієї сполуки або, принаймні, одержана суміш, яка збагачена однією зі сполук. Переважна захисна група для атома азоту сполук формули 2 являє собою бензил або заміщений бензил (F, ОМе і т.д.). Сполуки формули 2 при обробці бензилбромідом за певних умов нагрівання дають високий вихід або сполуки формули 3, або сполуки формули 4, де Ρ являє собою бензил, залежно від умов, що використовуються. Перекристалізація суміші продуктів знизить кількість однієї сполуки для одержання високозбагаченого або чистого зразка або Ν-1 захищеного ізомеру (сполуку формули 4) або Ν-2 захищеного ізомеру (сполуку формули 3), залежно від умов, що використовуються, і необхідної сполуки. У загальному випадку, сполуку формули 4 одержують нагріванням суміші сполуки формули 2 з бензилбромідом до температури від приблизно 105°С до 115°С протягом 20-24 годин, тоді як сполуку формули 3 одержують нагріванням суміші сполуки 2 з бензилбромідом до температури від приблизно 50°С до 60°С протягом 20-24 годин. Реакцію звичайно про 27 водять у розчиннику, такому як, але не обмежуючись зазначеним, DMF. Схема 2 Аналогічним чином, сполуки формули 7 і 8 можуть бути одержані відповідно до схеми 2. Використання Ν,Ν-диметилформаміду як сполуки формули R1C(=O)-X, із подальшою обробкою кислотою, такою як перемішування в присутності оцтової кислоти, призведе до сполуки формули 1, де R1 являє собою форміл. При обробці LDA галофторбензолу, де галоген Υ являє собою хлор або бром, із подальшим додаванням DMF, необов'язковою подальшою обробкою кислотою будуть одержані сполуки формули 5. Сполуки формули 5 при обробці гідратом гідразину при нагріванні дадуть індазоли формули 6. У ролі альтернативи, сполуки формули 5 при обробці гідроксиламіном або О-заміщеним гідроксиламіном дадуть відповідні оксими, які можуть бути потім оброблені гідразином при нагріванні, даючи індазоли формули 6. Сполуки формули 6 при обробці бензилбромідом за певних умов нагрівання, як зазначено на схемі 1, дадуть високий вихід або сполуки формули 7, або сполуки формули 8, залежно від умов, що використовуються. Перекристалізація суміші сполук знизить кількість небажаних ізомерів залежно від умов і необхідного продукту. Схема 3 Як зазначено на схемі 3, сполуку формули 9, де R9, R10, R11 і R12R9, R10, R11 і R12 незалежно один від одного вибрані з групи, яка складається з водню, алкенілу, алкоксигрупи, алкоксіалкоксигрупи, алкоксіалкілу, алкоксикарбонілу, алкоксикарбонілалкілу, алкілу, алкілкарбонілу, алкілкарбонілалкілу, алкілкарбонілокси, алкілтіо, алкінілу, арилу, карбокси, карбоксіалкілу, ціано, ціаноалкілу, формілу, формілалкілу, галоалкокси, галоалкілу, галоалкілтіо, галогену, гетероарилу, гетероциклу, гідрокси, гідроксіалкілу, меркапто, 94100 28 меркаптоалкілу, нітро, (CF3)2(HO)C-, RB(SO)2RAN-, RAO(SO)2-, RBO(SO)2-, ZAZBN-, (ZAZBN)алкілу, (ZAZBN)карбонілу, (ZAZBN)кapбoнiлaлкiлy і (ZAZBN)сульфонілу, які одержані відповідно до способу, попередньо викладеного в Патенті США 2005/0043351Α1, при обробці фенілкарбаматом або подібним реагентом дадуть сполуку формули 10. Переважні умови включають обробку сполук формули 9 фенілкарбаматом у присутності основи, такої як, але не обмежуючись перерахованим, триетиламін, діізопропілетиламін, Nметилморфолін, карбонат натрію або карбонат калію в розчиннику, такому як, але не обмежуючись перерахованим, THF, ацетонітрил або DMF. Більш переважні умови являють собою ті, за яких суміш сполуку формули 9, фенілкарбамату і діізопропілетиламіну нагрівають при температурі кипіння разом у THF протягом від приблизно 2 годин до приблизно 10 годин. Схема 4 Як показано на схемі 4, обробка суміші сполуки формули 10, основи, що складається з фосфату калію, карбонату калію або карбонату цезію, і сполуки формули 3, сполуки формули 4 або їхньої суміші, де Υ являє собою хлор або бром, у присутності каталізатора, одержаного зі сполуки паладію, переважно, ацетату паладію або Pd2(DBA)3 і ліганду на основі фосфіну, включаючи, але нe обмежуючись перерахованим, Xantphos, 2-ди-третбутилфосфіно-1-1’-бінафтил, 5-(ди-третбутилфосфаніл)-1',3',5'-трифеніл-1'Н[1,4']біпіразоліл, дає або сполуку формули 11, сполуку формули 12, або суміш і сполук формули 11 і сполуки формули 12. Реакцію звичайно проводять у розчиннику, такому як, але не обмежуючись зазначеним, диметиловий ефір етиленгліколю. Переважно, реакцію проводять, використовуючи карбонат цезію як основу і нагрівають при температурі кипіння розчинник протягом від приблизно 3 до приблизно 20 годин. Більш переважно, реакційну суміш нагрівають при температурі кипіння розчинника протягом 5-10 годин. Продукти реакції можуть бути відфільтровані для видалення нерозчинних речовин із метою спрощення виділення продукту і часто, із подальшим концентруванням об'єму суміші під зменшеним тиском, продукт може бути виділений подальшим 29 розведенням іншим розчинником, таким як гексан, гептан і т.ін. із подальшою фільтрацією сполук формули 11 і/або 12. Схема 5 Як продемонстровано на схемі 5, або сполуки формули 11, або сполуки формули 12 або їхня суміш, при обробці, що відповідає умовам, відомим для видалення захисних груп азоту, або як зазначено в Protecting Groups in Organic Synthesis, 3fd Ed. TheodoRA W. Greene і Peter G.M. Wuts, John Wiley & Sons, Inc., дають сполуку формули 13, яка є типовим представником сполук формули (I). Наприклад, коли захисна група являє собою бензил, видалення може бути зроблене обробкою паладієвим каталізатором у присутності донора водню, що включає атмосферу водню, мурашину кислоту або циклогексадієн у розчиннику, що включає спиртові розчинники, тетрагідрофуран або етилацетат; для одержання сполуки формули 13. Приклади паладієвого каталізатора включають, але не обмежені перерахованим, 5-20% паладій на вуглеці, гідроксид паладію або паладій на сульфаті барію. Типові розчинники включають метанол, етанол, тетрагідрофуран, етилацетат і т.ін. Часто оцтова кислота може бути використана для збільшення швидкості реакції. Переважно, 20% гідроксид паладію і мурашина кислота в тетрагідрофурані беруть участь у реакції. Більш переважно, нагрівання сполук формули 11 і/або 12 у присутності 20% гідроксиду паладію і мурашиної кислоти в тетрагідрофурані до 60°С протягом приблизно 15 годин дає сполуку формули 13. Приклади Нижченаведені приклади призначені для ілюстрації і не обмежують обсяг винаходу, визначений доданою формулою винаходу. Приклад 1 2-Бром-6-фторбензальдегід 1-Бром-3-фторбензол (17,3 г, 0,1 моль) додавали протягом 5 хвилин до розчину діізопропіламіду літію (одержаного з 11,5 г, 0,1 Μ діізопропіла 94100 30 міну і 40 мл, 2,5 н бутиллітію в гексанах) у THF від -70 до -75°С. Після перемішування протягом 1 години при -75°С, до суміші додавали DMF (8 мл) протягом 10 хвилин. Перемішування в умовах охолоджування продовжували протягом додаткових 40 хвилин, після чого суміш гасили додаванням оцтової кислоти (26 г). Суміші давали нагрітися до температури навколишнього середовища і додавали в суміш в 200 мл МТВН, 200 мл води і 150 мл соляної кислоти (~4н). Органічний шар відділяли і концентрували у вакуумі з одержанням необхідного бромфторбензальдегіду (19,2 г, 95%): 1 Н ЯМР (CDCІ3, , м.д.) 7,14 (т, 1Н, J=7,6 Гц), 7,39 (м, 1Н), 7,48 (д, 1H, J=7,5 Гц), 10,34 (с, 1Н). Приклад 2 4-Броміндазол Пряме одержання До розчину бромфторбензальдегіду (20,3 г, 0,1 моль) у DMSO (20 мл), що перемішували при кімнатній температурі, додавали моногідрат гідразину (100 мл), у той час як внутрішня температура підтримувалася менше, ніж 35°С. Суміш потім нагрівали до 70-75°С протягом 22 годин після чого внутрішню температуру доводили до 25°С. Суміш розводили водою (125 мл), із подальшим розведенням гептанами (25 мл), у той час як внутрішня температура підтримувалася менш ніж 40°С. Суміш перемішували при температурі навколишнього середовища протягом 1 години і суспензію продукту відфільтровували для одержання твердої речовини. Осад, що відфільтровували, промивали водою/МеОН у співвідношенні 4:1 (220 мл), потім сушили при 50°С у вакуумній печі з одержанням 14,7 г (75%) сполуки, зазначеної в заголовку: 1Н ЯМР (DMSO-d6, , м.д.) 7,28 (т, 1Н, J=7,6 Гц), 7,34 (д, 1Н, J=74 Гц), 7,59 (д, 1Н, J=7,5 Гц), 8,05 (с, 1Н), 13,46 (с, 1H,-NH). Одержання через проміжний оксим Гідроксиламін (50% у воді, 7 г, 0,1 моль) додавали до розчину бромфторбензальдегіду (20,3 г, 0,1 моль) у діоксані (50 мл) у той час як внутрішня температура підтримувалася менше, ніж 30°С. Через 30 хвилин, моногідрат гідразину (50 мл) додавали до суміші і суміш нагрівали при температурі кипіння (85°С) протягом 24 годин. Суміш охолоджували до 25°С і концентрували при зниженому тиску до об'єму приблизно 50 мл. Суміш розводили водою (100 мл), у той час як внутрішня температура підтримувалася менш ніж 40°С. Суміш перемішували при температурі навколишнього середовища протягом, принаймні, 1 години. Одержану суспензію відфільтровували з одержанням твердої речовини. Відфільтрований осад промивали водою/МеОН у співвідношенні 4:1 (220 мл), потім сушили при 50°С у вакуумній печі з одержанням 14,9 г (76%) сполуки, зазначеної в заголовку. 31 Приклад 3 4-Хлоріндазол 4-Хлоріндазол одержували відповідно до способу прикладу 2, використовуючи 2-хлор-6фторбензальдегід замість 2-бром-6фторбензальдегіду як вихідну речовину. Вихід продукту 70-74%: 1Н ЯМР (CDCІ3, , м.д.) 7,15 (д, 1Н, J=7,4 Гц), 7,30 (т, 1Н J=7,6 Гц), 7,40 (д, 1H, J=7,5 Гц), 8,16 (с, 1Н), 10,61 (с, 1Н, -NH). Приклад 4 2-N-Бензил-4-броміндазол 4-Броміндазол прикладу 2 (17,4 г, 0,088 моль), бензилбромід (22,7 г, 0,132 моль) і DMF (35 мл) нагрівали до приблизно 50°С протягом 25 годин (ВЕРХ: 15:1 співвідношення 2-N і 1-N ізомерів). Суміш охолоджували до температури навколишнього середовища і розводили етилацетатом (160 мл) і водою (100 мл). Органічний шар відділяли, промивали водним розчином бікарбонату натрію (5%, 100 мл). Органічний шар відділяли і концентрували під зниженим тиском. Залишок розводили ізопропанолом (160 мл) і концентрували під зниженим тиском до об'єму приблизно 120 мл. Суміш нагрівали до 50°С для розчинення твердої речовини і розводили водою (70 мл) для осадження продукту. Суспензію охолоджували до 0°С і осад відфільтровували. Тверду речовину промивали сумішшю ТРА і води (1:1, 50 мл) і сушили при 50°С з одержанням сполуки, зазначеної в заголовку (16,5 г, 77%, яка містить менше, ніж 2% N-ізомеру відповідно до ВЕРХ): 1Н ЯМР (CDCl3, , м.д), 5,56 (с, 2Н), 7,11 (м, 1Н), 7,21 (д, 1Н, J=7,2 Гц), 7,247,39 (м, 5Н), 7,65 (д, 1Η J=8,6 Гц), 7,88 (с, 1H). Приклад 5 2-N-Бензил-4-хлоріндазол 2-N-Бензил-4-хлоріндазол одержували відповідно до способу прикладу 4, замінюючи сполуку прикладу 2 сполукою прикладу 3 (62% вихід продукту). 1Н ЯМР (CDCІ3, , м.д.) 5,69 (с, 2Н), 7,06 (д, J=7,3 Гц 1Н), 7,21 (дд, J=7,2, 8,6 Гц 1H), 7,30-7,40 (м, 5Н), 7,62 (д, J=8,6 Гц 1Н), 7,95 (с, 1Н). 94100 32 Приклад 6 1-N-Бензил-4-броміндазол 4-Броміндазол прикладу 2 (14,8 г, 0,075 моль), бензилбромід (14,8 г, 0,086 моль) і DMF (30 мл) нагрівали до приблизно 110°С протягом 22 годин (ВЕРХ: 19:1 співвідношення 2-N і 1-N ізомерів). Суміш охолоджували до температури навколишнього середовища і розводили етилацетатом (75 мл), гептанами (75 мл) і водою (75 мл). Органічний шар відділяли і промивали водним розчином бікарбонату натрію (5%, 100 мл). Органічний шар відділяли і концентрували під зниженим тиском. Залишок розчиняли в метанолі (100 мл) і продукт осаджували водою (100 мл). Фільтрація і сушіння під зниженим тиском при 50°С давали 1-N ізомер (15,0 г, 70%, менше ніж 5% 2-N ізомеру відповідно до ВЕРХ): 1Н ЯМР (CDCІ3, , м.д.), 5,56 (с, 2Н), 7,10-7,18 (м, 3Н), 7,23-7,32 (м, 5Н), 8,04 (с, 3Н). Приклад 7 1-N-Бензил-4-хлоріндазол 1-N-Бензил-4-хлоріндазол одержували відповідно до способу прикладу 6, замінюючи сполуку прикладу 2 сполукою прикладу 3 (68% вихід продукту). 1Н ЯМР (CDCІ3, , м.д.) 5,58 (с, 2Н), 7,077,14 (м, 1Н) 7,15-7,20 (м, 2Н) 7,20-7,33 (м, 5Н), 8,11 (с, 1Н). Приклад 8 (R)-1-(5-трет-Бутил-2,3-дигідро-1Н-індан-1іл)сечовина трет-Бутилінданіламінтозилат (26,5 г, 0,072 моль) (як попередньо повідомлялося в заявці США 2005/0043351Α1), фенілкарбамат (9,57 г, 0,07 моль) і діізопропілетиламін (9,9 г, 0,076 моль) у THF (70 мл) нагрівали при температурі кипіння протягом 15 годин. Суміш охолоджували до температури навколишнього середовища, розводили водою (140 мл). Одержаний продукт відфільтровували і промивали водою (100 мл). Сушіння під зниженим тиском при 50°С-60°С давало сполуку, зазначену в заголовку (14,7 г, 88%): 1Н ЯМР (DMSO-d6, , м.д.) 1,26 (с, 9Н), 1,66 (м, 1Н), 2,35 (м, 1Н), 2,73 (м, 1Н), 2,86 (м, 1Н), 4,99 (кв, J=7,9 Гц, 33 1Н), 5,41 (с, 2Н), 6,21 (д, J=8,4 Гц, 1Н), 7,13 (д, J=8,0 Гц, 1Н), 7,19-7,23 (м, 2Н). Приклад 9 (R)-1-(2-Бензил-2Н-індазол-4-іл)-3-(5-третбутил-2,3-дигідро-1Н-індан-1-іл)сечовина Розчин 2-N-бензилброміндазол, приклад 4 (5,0 г, 17,4 ммоль) у DME (65 мл) додавали до суміші інданілсечовини (3,6 г, 15,5 ммоль), карбонат цезію (7,5 г), Pb2(DBA)3 (0,23 г) і Xantphos (0,42 г). Суміш вакуумували, продували двічі азотом, і потім дефлегмували протягом 5 годин. Суміш охолоджували до 70°С, і одержаний продукт фільтрували гарячим, тверду речовину промивали нагрітим DMF (50 мл). Об'єднані разом фільтрати концентрували під зниженим тиском до об'єму приблизно 50 мл, і продукт осаджували додаванням гептану (80 мл). Суміш відфільтровували і відфільтрований осад суспендували в етанолі (25 мл). Продукт збирали фільтруванням і сушили під зниженим тиском з одержанням 5,3 г (70%) сполуки, зазначеної в заголовку: 1Н ЯМР (DMSO-d6, , м.д.) 1,27 (с, 9Н), 1,80 (м, 1Н), 2,44 (м, 1Н), 2,80 (м, 1Н), 2,93 (м, 1Н), 5,13 (кв, J=7,9 Гц, 1Н), 5,64 (с, 2Н), 6,53 (д, J=8,4 Гц, 1Н), 7,09-7,15 (м, 2H), 7,23 (с, 2Н), 7,287,37 (м, 5Н), 7,50 (д, J=6,6 Гц, 1Н), 8,23 (с, 1Н), 8,43 (с, 1Н). Приклад 10 Альтернативний спосіб одержання (R)-1-(2бензил-2Н-індазол-4-іл)-3-(5-трет-бутил-2,3дигідро-1Н-індан-1-іл)сечовини, одержаної з 2-Nбензилхлоріндазолу У реакторі високого тиску, ацетат паладію (29 г) і 2-ди-трет-бутилфосфіно-1-1’-бінафтил (120 мг) змішували в дихлорметані (14 мл) при 85°С протягом 30 хвилин в інертній атмосфері. Після видалення розчинника випаровуванням, у реактор завантажували 2-N-бeнзил-4-хлоріндазол, приклад 5 (1,14 г, 4,7 ммоль), фосфат калію (1,36 г, 1,5 ек.), інданілсечовину (1,0 г, 0,9 ек.) і DME (15 мл). Суміш вакуумували і продували азотом, і потім нагрівали при 85°С протягом 18 годин. Суміш охоло 94100 34 джували до 70°С, розводили DMЕ (50 мл) і фільтрували гарячою, твердий осад промили нагрітим DME (50 мл). Об'єднані разом фільтрати концентрували під зниженим тиском до об'єму приблизно 14 мл і продукт осаджували додаванням гептану (22 мл). Продукт, збирали фільтрацією і сушила під зниженим тиском з одержанням 1,6 г (85%) сполуки, зазначеної в заголовку. Приклад 11 (R)-1-(1-Бензил-1Н-індазол-4-іл)-3-(5-третбутил-2,3-дигідро-1Н-індан-1-іл)сечовина Сполуку, зазначену в заголовку, одержували відповідно до способу, описаного в прикладі 9, використовуючи 1-N-бензилброміндазол замість 2N-бензилброміндазолу (вихід продукту 60%). 1 Н ЯМР (CDCІ3, , м.д.) 1,29 (с, 9Н), 1,80 (м, 1Н), 2,63 (м, 1Н), 2,83 (м, 1Н), 2,92 (м, 1Н), 5,25 (д, J=8,3 Гц, 1Н), 5,40 (кв, J=7,9 Гц, 1Н), 5,55 (с, 2Н), 6,80 (с, 1Н), 7,07 (д, J=7,7 Гц, 1Н), 7,15-7,29 (м, 9Н), 8,02 (с, 1Н). Приклад 12 1-((R)-5-трет-Бутил-2,3-дигідро-1Н-інден-1-іл)3-(3а,7а-дигідро-1Н-індазол-4-іл)сечовина Сполуку прикладу 10 (3,0 г), 20% гідроксид паладію на вуглеводі (1,5 г) і мурашину кислоту (10 мл) змішували в TНF (100 мл) при 60°С в атмосфері азоту протягом 3 годин. Суміш охолоджували до температури навколишнього середовища і фільтрували. Фільтрат концентрували під зниженим тиском, і залишок об'єднували з етанолом (50 мл) й активованим вугіллям (0,5 г). Суміш дефлегмували протягом 1 години, потім відфільтровували. Фільтрат концентрували до об'єму 23 мл під зниженим тиском, і одержаний продукт осаджували додаванням води (8,6 мл). Названу сполуку відфільтровували і сушили до 1,91 г (80% вихід). Як альтернативу, названу сполуку, зазначену в заголовку, можна одержати відповідно до способу, описаного в прикладі 12, замінюючи сполуку прикладу 9 сполукою прикладу 11. 35 Комп’ютерна верстка О. Гапоненко 94100 Підписне 36 Тираж 23 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of indazolyl ureas that inhibit vanilloid subtype 1 (vr1) receptors
Автори англійськоюLukin Kirill A., Chi-Ping Hsu Margaret, Fernando Dilinie P., Kotecki Brian J., Leanna Marvin R.
Назва патенту російськоюСпособ получения индазолилмочевин, которые угнетают ванилоидные рецепторы подтипа 1 (vr1)
Автори російськоюЛукин Кирилл А., Чи-Пин Су Маргарет, Фернандо Дилини П., Котеки Брайан Дж., Линна Марвин Р.
МПК / Мітки
МПК: C07D 231/56, A61K 31/416
Мітки: ванілоїдні, індазолілсечовин, рецептори, vr1, пригнічують, спосіб, підтипу, одержання
Код посилання
<a href="https://ua.patents.su/18-94100-sposib-oderzhannya-indazolilsechovin-yaki-prignichuyut-vanilodni-receptori-pidtipu-1-vr1.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання індазолілсечовин, які пригнічують ванілоїдні рецептори підтипу 1 (vr1)</a>
Попередній патент: Пристрій для маніпулювання трубчастим сегментом (варіанти) і спосіб з’єднання трубчастого сегмента з колоною труб (варіанти)
Наступний патент: Спосіб відновлення рослинного покрову на ділянці захоронення відходів
Випадковий патент: Мережа мобільного зв'язку між двома телефонними апаратами












