Інгібітори тирозинкінази та фармацевтична композиція на їх основі
Номер патенту: 74560
Опубліковано: 16.01.2006
Автори: Хартман Джордж Д., Білодо Марк Т., Хоффман Вілльям Ф., Аррінгтон Кеннет Л., Кім Юнтае, Хангейт Рендалл В., Фрелі Марк Е.
Формула / Реферат
1. Сполука формули I
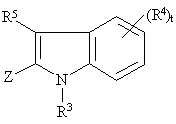 І
І
або її фармацевтично прийнятна сіль або стереоізомер, де
Z представляє формулу
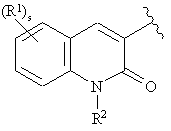 ,
,
а дорівнює 0 або 1;
b дорівнює 0 або 1;
m дорівнює 0, 1 або 2;
s дорівнює 1 або 2;
t дорівнює 1, 2 або 3;
R1 і R5 незалежно вибрані з:
1) Н,
2) (С=O)aObC1-C10алкілу,
3) (С=O)аОbарилу,
4) (С=O)aObC2-C10алкенілу,
5) (С=O)аОbС2-С10алкінілу,
6) CO2Н,
7) галогену,
8) ОН,
9) ОbС1-С6перфторалкілу,
10) (С=O)aNR7R8,
11) CN,
12) (С=О)аОbС3-С8циклоалкілу і
13) (С=O)аОbгетероциклілу,
причому зазначені алкіл, арил, алкеніл, алкініл, циклоалкіл і гетероцикліл необов’язково заміщені одним або декількома замісниками, вибраними з R6;
R2 і R3 незалежно вибрані з:
1) Н,
2) (С=O)ОаС1-С6алкілу,
3) (С=O)Оаарилу,
4) C1-C6алкілу,
5) SО2Ra і
6) арилу;
R4 вибраний з:
1) (С=O)аОbС1-С10алкілу,
2) (С=О)аОbарилу,
3) (С=О)аОbС2-С10алкенілу,
4) (С=O)аОbС2-С10алкінілу,
5) CO2Н,
6) галогену,
7) ОН,
8) ОbС1-С6перфторалкілу,
9) (C=O)aNR7R8,
10) CN,
11) (С=O)аОbС3-С8циклоалкілу і
12) (С=O)аОbгетероциклілу,
причому зазначені алкіл, арил, алкеніл, алкініл, циклоалкіл і гетероцикліл необов’язково заміщені одним або декількома замісниками, вибраними з R6;
R6 представляє:
1) (С=O)аОbС1-С10алкіл,
2) (С=О)аОbарил,
3) С2-С10алкеніл,
4) С2-С10алкініл,
5) (С=O)аОbгетероцикліл,
6) CO2Н,
7) галоген,
8) CN,
9) ОН,
10) ОbС1-С6перфторалкіл,
11) Oa(C=O)bNR7R8,
12) оксо,
13) СНО,
14) (N=O)R7R8 або
15) (С=O)аОbС3-C8циклоалкіл,
причому зазначені алкіл, арил, алкеніл, алкініл, гетероцикліл і циклоалкіл необов’язково заміщені одним або декількома замісниками, вибраними з R6a;
R6а вибраний з:
1) (С=O)rOs(С1-С10)алкілу, де r і s незалежно дорівнюють 0 або 1,
2) Оr(С1-С3)перфторалкілу, де r дорівнює 0 або 1,
3) (С0-С6)алкілен-S(O)mRa, де m дорівнює 0, 1 або 2,
4) оксо,
5) ОН,
6) галогену,
7) CN,
8) (С2-С10)алкенілу,
9) (С2-С10)алкінілу,
10) (С3-С6)циклоалкілу,
11) (C0-С6)алкіленарилу,
12) (С0-С6)алкіленгетероциклілу,
13) (C0-С6)алкілен-N(Rb)2,
14) C(O)Ra,
15) (C0-C6)aлкілeн-CО2Ra,
16) С(O)Н і
17) (C0-С6)алкілен-CO2Н,
причому зазначені алкіл, алкеніл, алкініл, циклоалкіл, арил і гетероцикліл необов’язково заміщені замісниками аж до трьох, вибраними з Rb, ОН, (C1-C6)алкокси, галогену, CO2Н, CN, O(С=O)С1-С6алкілу, оксо і N(Rb)2;
R7 і R8 незалежно вибрані з:
1) Н,
2) (С=О)ОbC1-C10алкілу,
3) (С=O)ОbС3-C8циклоалкілу,
4) (С=О)Obарилу,
5) С(=O)Оbгетероциклілу,
6) С1-С10алкілу,
7) арилу,
8) С2-С10алкенілу,
9) С2-С10алкінілу,
10) гетероциклілу,
11) С3-С8циклоалкілу,
12) SО2Ra і
13) (C=O)NRb2,
причому зазначені алкіл, циклоалкіл, арил, гетероцикліл, алкеніл і алкініл необов’язково заміщені одним або декількома замісниками, вибраними з R6a, або
R7 і R8 можуть бути взяті разом з азотом, до якого вони приєднані, з утворенням моноциклічного або біциклічного гетероциклу з 5-7 членами в кожному кільці, що містить необов’язково крім азоту один або два додаткових гетероатоми, вибраних із N, О і S, причому зазначений моноциклічний або біциклічний гетероцикл, необов’язково, заміщений одним або декількома замісниками, вибраними з R6a;
Ra представляє (C1-C6)алкіл, (С3-С6)циклоалкіл, арил або гетероцикліл і
Rb представляє H, (C1-C6)алкіл, арил, гетероцикліл, (С3-С6)циклоалкіл, (С=O)ОС1-С6алкіл, (С=O)C1-C6алкіл або S(O)2Ra.
2. Сполука за п. 1, де
s дорівнює 1 і
t дорівнює 1 або 2;
R1 і R5 незалежно вибрані з:
1) Н,
2) (C=O)aObC1-C6алкілу,
3) (С=O)аОbарилу,
4) (C=O)аОbС2-C6алкенілу,
5) (С=O)аObC2-C6алкінілу,
6) CO2Н,
7) галогену,
8) OН,
9) ObC1-C3перфторалкілу,
10) (C=O)aNR7R8,
11) CN,
12) (С=O)аОbС3-С8циклоалкілу і
13) (С=O)аОbгетероциклілу,
причому зазначені алкіл, арил, алкеніл, алкініл, циклоалкіл і гетероцикліл необов’язково заміщені одним або декількома замісниками, вибраними з R6;
R4 вибраний з:
1) (C=O)aObC1-C6алкілу,
2) (С=O)аОbарилу,
3) (С=O)аObС2-С6алкенілу,
4) (С=O)аObС2-С6алкінілу,
5) CO2Н,
6) галогену,
7) ОН,
8) ObC1-С3перфторалкілу,
9) (C=O)aNR7R8,
10) CN,
11) (С=O)аОbС3-С6циклоалкілу і
12) (С=O)аОbгетероциклілу,
причому зазначені алкіл, арил, алкеніл, алкініл, циклоалкіл і гетероцикліл необов’язково заміщені одним або декількома замісниками, вибраними з R6;
R6 представляє:
1) (С=О)аОbС1-С6алкіл,
2) (С=О)аОbарил,
3) С2-С6алкеніл,
4) C2-C6алкініл,
5) (С=O)аОbгетероцикліл,
6) CO2Н,
7) галоген,
8) CN,
9) OН,
10) ObC1-C3перфторалкіл,
11) Oa(C=O)bNR7R8,
12) оксо,
13) СНО,
14) (N=O)R7R8 або
15) (С=О)аОbС3-С6циклоалкіл,
причому зазначені алкіл, арил, алкеніл, алкініл, гетероцикліл і циклоалкіл необов’язково заміщені одним або декількома замісниками, вибраними з R6a;
R6а вибраний з:
1) (С=O)rOs(C1-C6)алкілу, де r і s незалежно дорівнюють 0 або 1,
2) Оr(С1-C3)перфторалкілу, де r дорівнює 0 або 1,
3) (C0-C6)алкілен-S(O)mRa, де m дорівнює 0, 1 або 2,
4) оксо,
5) OН,
6) галогену,
7) CN,
8) (C2-C6)алкенілу,
9) (C2-C6)алкінілу,
10) (С3-С6)циклоалкілу,
11) (С0-С6)алкіленарилу,
12) (С0-С6)алкіленгетероциклілу,
13) (C0-С6)алкілен-N(Rb)2,
14) C(O)Ra,
15) (C0-C6)алкілен-CO2Rа,
16) C(O)H і
17) (C0-C6)алкілен-CO2Н,
причому зазначені алкіл, алкеніл, алкініл, циклоалкіл, арил і гетероцикліл необов’язково заміщені замісниками аж до трьох, вибраними з Rb, ОН, (C1-C6)алкокси, галогену, CO2Н, CN, O(С=O)С1-С6алкілу, оксо і N(Rb)2; і
R7 і R8 незалежно вибрані з:
1) Н,
2) (C=O)ObC1-C6алкілу,
3) (С=О)ОbС3-С6циклоалкілу,
4) (С=О)Оbарилу,
5) С(=O)Оbгетероциклілу,
6) C1-C6алкілу,
7) арилу,
8) С2-С6алкенілу,
9) С2-С6алкінілу,
10) гетероциклілу,
11) С3-С6циклоалкілу,
12) SО2Ra і
13) (C=O)NRb2,
причому зазначені алкіл, циклоалкіл, арил, гетероцикліл, алкеніл і алкініл необов’язково заміщений одним або декількома замісниками, вибраними з R6a, або
R7 і R8 можуть бути взяті разом з азотом, до якого вони приєднані, з утворенням моноциклічного або біциклічного гетероциклу з 5-7 членами в кожному кільці, що містить необов’язково крім азоту один або два додаткових гетероатоми, вибраних із N, О і S, причому зазначений моноциклічний або біциклічний гетероцикл, необов’язково заміщений одним або декількома замісниками, вибраними з R6а.
3. Сполука за п. 2, де R2, R3 і R5 представляє Н.
4. Сполука за п. 3, де t дорівнює 1, s дорівнює 1 і R1 представляє Н.
5. Сполука за п. 4, де R4 вибраний з:
1) ОС1-С6алкілен-NR7R8,
2) (С=O)аC0-С6алкілен-Q, де Q представляє Н, OН, CO2Н або OC1-C6алкіл,
3) ОC0-C6алкіленгетероциклілу, необов’язково заміщеного замісниками від одного до трьох, вибраними з R6a,
4) С0-С6алкілен-NR7R8,
5) (C=O)NR7R8 і
6) ОC1-C3алкілен-(С=О)NR7R8.
6. Сполука за п. 1, вибрана з:
3-{5-[3-(4-метилпіперазин-1-іл)пропокси]-1Н-індол-2-іл}-1Н-хінолін-2-ону;
3-(5-{2-[(2-метоксіетил)аміно]етокси}-1H-індол-2-іл)-2(1Н)-хінолінону;
3-[5-(2-{(2-метоксіетил)[(2-метокси-5-піримідиніл)метил]-аміно}етоксі)-1Н-індол-2-іл]-2(1Н)-хінолінону;
3-(5-{[(2S,4R)-4-метоксипіролідиніл]метоксі}-1Н-індол-2-іл)-2(1Н)-хінолінону;
3-[5-({(2S,4R)-4-метокси-1-[(2-метил-5-піримідиніл)метил]-піролідиніл}метоксі)-1Н-індол-2-іл]-2(1Н)-хінолінону;
етилового ефіру 1-(2-{[2-(2-оксо-1,2-дигідро-3-хінолініл)-1Н-індол-5-іл]оксі}етил)-4-піперидинкарбонової кислоти;
1-(2-{[2-(2-оксо-1,2-дигідро-3-хінолініл)-1Н-індол-5-іл]-оксі}етил)-4-піперидинкарбонової кислоти;
3-[(2S,4R)-4-метоксі-2-({[2-(2-оксо-1,2-дигідро-3-хінолініл)-1Н-індол-5-іл]окси}метил)піролідиніл]пропанової кислоти;
3-[5-(4-метансульфонілпіперазин-1-ілметил)-1Н-індол-2-іл]-1Н-хінолін-2-ону;
3-[5-(4-метансульфоніл-1-оксипіперазин-1-ілметил)-1Н-індол-2-іл]-1Н-хінолін-2-ону;
3-[5-(4-ацетилпіперазин-1-ілметил)-1Н-індол-2-іл]-1Н-хінолін-2-ону;
N-циклопропіл-N-[2-(2-оксо-1,2-дигідрохінолін-3-іл)-1Н-індол-5-ілметил]метансульфонаміду;
3-[5-(1-піперазинілкарбоніл)-1Н-індол-2-іл]-2(1Н)-хінолінону;
3-{5-[(4-метил-1-піперазиніл)карбоніл]-1Н-індол-2-іл}-2(1Н)-хінолінону;
трифторацетату 1-{[2-(2-оксо-1,2-дигідро-3-хінолініл)-1Н-індол-5-іл]карбоніл}-4-піперидинамінію;
трифторацетату 1-({[2-(2-оксо-1,2-дигідро-3-хінолініл)-1Н-індол-5-іл]оксі}ацетил)піперазин-4-ію;
3-{5-[2-(1,1-діоксидо-4-тіоморфолініл)-2-оксоетоксі]-1Н-індол-2-іл}-2(1Н)-хінолінону;
N-{[2-(2-оксо-1,2-дигідро-3-хінолініл)-1Н-індол-5-іл]метил}-4-піперидинкарбоксаміду;
3-{5-[1-(4-морфолініл)етил]-1Н-індол-2-іл}-2(1Н)-хінолінону;
3-(5-[1-(1-піролідиніл)етил]-1Н-індол-2-іл}-2(1Н)-хінолінону;
3-{5-[1-(4-ацетил-1-піперазиніл)етил]-1Н-індол-2-іл}-2(1Н)-хінолінону;
3-(5-{1-[4-(метилсульфоніл)-1-піперазиніл]етил}-1Н-індол-2-іл)-2(1Н)-хінолінону;
4-аміно-N-[2-(2-оксо-1,2-дигідро-3-хінолініл)-1Н-індол-5-іл]-1-піперидинкарбоксаміду і
4-аміно-N-{[2-(2-оксо-1,2-дигідро-3-хінолініл)-1Н-індол-5-іл]метил}-1-піперидинкарбоксаміду, або її фармацевтично прийнятної солі або стереоізомера.
7. Сполука за п.1, яка являє собою 3-[5-(4-метансульфонілпіперазин-1-ілметил)-1Н-індол-2-іл]-1Н-хінолін-2-он або її фармацевтично прийнятну сіль.
8. Фармацевтична композиція, яка містить сполуку за п. 1 і фармацевтично прийнятний носій.
9. Композиція за п. 8, яка додатково містить другу сполуку, вибрану з:
1) модулятора рецептора естрогену,
2) модулятора рецептора андрогену,
3) модулятора рецептора ретиноїду,
4) цитотоксичного агента,
5) антипроліферативного агента,
6) інгібітора пренілпротеїнтрансферази,
7) інгібітора HMG-CoA-редуктази,
8) інгібітора ВІЛ-протеази,
9) інгібітора зворотної транскриптази та
10) іншого інгібітора розвитку кровоносних судин.
10. Композиція за п. 9, де другою сполукою є інший інгібітор розвитку кровоносних судин, вибраний з групи, що складається з інгібітора тирозинкінази, інгібітора, отриманого з епідерми фактора росту, інгібітора, отриманого з фібробластів фактора росту, інгібітора, отриманого з тромбоцитів фактора росту, інгібітора ММР (матричної металопротеази), блокатора інтегрину, інтерферону-![]() , інтерлейкіну-12, пентозанполісульфату, інгібітора циклооксигенази, карбоксіамідотриазолу, комбретастатину А-4, скваламіну, 6-О-(хлорацетилкарбоніл)фумагілолу, талідоміду, ангіостатину, тропонілу-1 і антитіл до VEGF.
, інтерлейкіну-12, пентозанполісульфату, інгібітора циклооксигенази, карбоксіамідотриазолу, комбретастатину А-4, скваламіну, 6-О-(хлорацетилкарбоніл)фумагілолу, талідоміду, ангіостатину, тропонілу-1 і антитіл до VEGF.
11. Композиція за п. 9, де другою сполукою є модулятор рецептора естрогену, вибраний з тамоксифену і ралоксифену.
12. Спосіб лікування або профілактики залежного від тирозинкінази захворювання або стану у ссавця, такого як, рак, захворювання, яке включає в себе розвиток кровоносних судин, ретинальне новоутворення кровоносних судин, діабетична ретинопатія, пов’язана з віком дегенерація жовтої плями, запальне захворювання, захворювання, пов’язане з кістковою патологією, який відрізняється тим, що ссавцеві, який потребує такого лікування, вводять терапевтично ефективну кількість сполуки за п. 1.
13. Спосіб за п. 12, який відрізняється тим, що рак вибраний з ракових захворювань головного мозку, сечостатевого тракту, лімфатичної системи, шлунка, гортані і легені.
14. Спосіб за п. 12, який відрізняється тим, що рак вибраний з гістіоцитарної лімфоми, адренокарциноми легень, дрібноклітинних ракових захворювань легень, панкреатичного раку, гіобластом і карциноми молочної залози.
15. Спосіб за п. 12, який відрізняється тим, що захворюванням, яке полягає у розвитку кровоносних судин, є очне захворювання.
16. Спосіб за п. 12, який відрізняється тим, що запальне захворювання вибране з ревматоїдного артриту, псоріазу, контактного дерматиту та алергійних реакцій уповільненого типу.
17. Спосіб за п. 12, який відрізняється тим, що захворювання, пов’язане з кістковою патологією, вибране з остеосаркоми, остеоартриту і рахіту.
18. Спосіб за п. 13, який відрізняється тим, що він додатково включає радіаційну терапію.
19. Спосіб за п. 13, який відрізняється тим, що він додатково включає введення сполуки, вибраної з:
1) модулятора рецептора естрогену,
2) модулятора рецептора андрогену,
3) модулятора рецептора ретиноїду,
4) цитотоксичного агента,
5) антипроліферативного агента,
6) інгібітора пренілпротеїнтрансферази,
7) інгібітора HMG-CoA-редуктази,
8) інгібітора ВІЛ-протеази,
9) інгібітора зворотної транскриптази та
10) іншого інгібітора розвитку кровоносних судин.
20. Спосіб за п. 13, який відрізняється тим, що він додатково включає комбінацію з радіаційною терапією і введення сполуки, вибраної з:
1) модулятора рецептора естрогену,
2) модулятора рецептора андрогену,
3) модулятора рецептора ретиноїду,
4) цитотоксичного агента,
5) антипроліферативного агента,
6) інгібітора пренілпротеїнтрансферази,
7) інгібітора HMG-CoA-редуктази,
8) інгібітора ВІЛ-протеази,
9) інгібітора зворотної транскриптази та
10) іншого інгібітора розвитку кровоносних судин.
21. Спосіб за п. 13, який відрізняється тим, що він включає введення додатково паклітакселу або трастузумабу.
22. Спосіб за п. 13, який відрізняється тим, що він включає додатково введення антагоніста GPIIb/IIIa.
23. Спосіб за п. 22, який відрізняється тим, що антагоністом GPIIb/IIIa є тирофібан.
24. Спосіб зменшення або профілактики ушкодження тканини після церебрального ішемічного нападу, який включає введення терапевтично ефективної кількості сполуки за п. 1.
Текст
1. Сполука формули I C2 2 (19) 1 3 74560 4 одним або декількома замісниками, вибраними з R7 і R8 можуть бути взяті разом з азотом, до якого R6; вони приєднані, з утворенням моноциклічного або R6 представляє: біциклічного гетероциклу з 5-7 членами в кожному 1) (С=O)аОbС1-С10алкіл, кільці, що містить необов’язково крім азоту один 2) (С=О)аОbарил, або два додаткових гетероатоми, вибраних із N, О 3) С2-С10алкеніл, і S, причому зазначений моноциклічний або біцик4) С2-С10алкініл, лічний гетероцикл, необов’язково, заміщений од5) (С=O)аОbгетероцикліл, ним або декількома замісниками, вибраними з R6a; 6) CO2Н, Ra представляє (C1-C6)алкіл, (С3-С6)циклоалкіл, 7) галоген, арил або гетероцикліл і 8) CN, Rb представляє H, (C1-C6)алкіл, арил, гетероцик9) ОН, ліл, (С3-С6)циклоалкіл, (С=O)ОС1-С6алкіл, 10) ОbС1-С6перфторалкіл, (С=O)C1-C6алкіл або S(O)2Ra. 11) Oa(C=O)bNR7R8, 2. Сполука за п. 1, де 12) оксо, s дорівнює 1 і 13) СНО, t дорівнює 1 або 2; 14) (N=O)R7R8 або R1 і R5 незалежно вибрані з: 15) (С=O)аОbС3-C8циклоалкіл, 1) Н, причому зазначені алкіл, арил, алкеніл, алкініл, 2) (C=O)aObC1-C6алкілу, гетероцикліл і циклоалкіл необов’язково заміщені 3) (С=O)аОbарилу, одним або декількома замісниками, вибраними з 4) (C=O)аОbС2-C6алкенілу, R6a; 5) (С=O)аObC2-C6алкінілу, R6а вибраний з: 6) CO2Н, 1) (С=O)rOs(С1-С10)алкілу, де r і s незалежно дорів7) галогену, нюють 0 або 1, 8) OН, 2) Оr(С1-С3)перфторалкілу, де r дорівнює 0 або 1, 9) ObC1-C3перфторалкілу, 3) (С0-С6)алкілен-S(O)mRa, де m дорівнює 0, 1 або 10) (C=O)aNR7R8, 2, 11) CN, 4) оксо, 12) (С=O)аОbС3-С8циклоалкілу і 5) ОН, 13) (С=O)аОbгетероциклілу, 6) галогену, причому зазначені алкіл, арил, алкеніл, алкініл, 7) CN, циклоалкіл і гетероцикліл необов’язково заміщені 8) (С2-С10)алкенілу, одним або декількома замісниками, вибраними з 9) (С2-С10)алкінілу, R6; 10) (С3-С6)циклоалкілу, R4 вибраний з: 11) (C0-С6)алкіленарилу, 1) (C=O)aObC1-C6алкілу, 12) (С0-С6)алкіленгетероциклілу, 2) (С=O)аОbарилу, 13) (C0-С6)алкілен-N(Rb)2, 3) (С=O)аObС2-С6алкенілу, 14) C(O)Ra, 4) (С=O)аObС2-С6алкінілу, 15) (C0-C6)aлкілeн-CО2Ra, 5) CO2Н, 16) С(O)Н і 6) галогену, 17) (C0-С6)алкілен-CO2Н, 7) ОН, причому зазначені алкіл, алкеніл, алкініл, циклоал8) ObC1-С3перфторалкілу, кіл, арил і гетероцикліл необов’язково заміщені 9) (C=O)aNR7R8, замісниками аж до трьох, вибраними з Rb, ОН, (C110) CN, C6)алкокси, галогену, CO2Н, CN, O(С=O)С111) (С=O)аОbС3-С6циклоалкілу і С6алкілу, оксо і N(Rb)2; 12) (С=O)аОbгетероциклілу, R7 і R8 незалежно вибрані з: причому зазначені алкіл, арил, алкеніл, алкініл, 1) Н, циклоалкіл і гетероцикліл необов’язково заміщені 2) (С=О)ОbC1-C10алкілу, одним або декількома замісниками, вибраними з 3) (С=O)ОbС3-C8циклоалкілу, R6; 4) (С=О)Obарилу, R6 представляє: 5) С(=O)Оbгетероциклілу, 1) (С=О)аОbС1-С6алкіл, 6) С1-С10алкілу, 2) (С=О)аОbарил, 7) арилу, 3) С2-С6алкеніл, 8) С2-С10алкенілу, 4) C2-C6алкініл, 9) С2-С10алкінілу, 5) (С=O)аОbгетероцикліл, 10) гетероциклілу, 6) CO2Н, 11) С3-С8циклоалкілу, 7) галоген, a 12) SО2R і 8) CN, 13) (C=O)NRb2, 9) OН, причому зазначені алкіл, циклоалкіл, арил, гетеро10) ObC1-C3перфторалкіл, цикліл, алкеніл і алкініл необов’язково заміщені 11) Oa(C=O)bNR7R8, одним або декількома замісниками, вибраними з 12) оксо, R6a, або 13) СНО, 14) (N=O)R7R8 або 5 74560 6 15) (С=О)аОbС3-С6циклоалкіл, 4) С0-С6алкілен-NR7R8, причому зазначені алкіл, арил, алкеніл, алкініл, 5) (C=O)NR7R8 і гетероцикліл і циклоалкіл необов’язково заміщені 6) ОC1-C3алкілен-(С=О)NR7R8. одним або декількома замісниками, вибраними з 6. Сполука за п. 1, вибрана з: R6a; 3-{5-[3-(4-метилпіперазин-1-іл)пропокси]-1Н-індол6а R вибраний з: 2-іл}-1Н-хінолін-2-ону; 1) (С=O)rOs(C1-C6)алкілу, де r і s незалежно дорів3-(5-{2-[(2-метоксіетил)аміно]етокси}-1H-індол-2нюють 0 або 1, іл)-2(1Н)-хінолінону; 2) Оr(С1-C3)перфторалкілу, де r дорівнює 0 або 1, 3-[5-(2-{(2-метоксіетил)[(2-метокси-53) (C0-C6)алкілен-S(O)mRa, де m дорівнює 0, 1 або піримідиніл)метил]-аміно}етоксі)-1Н-індол-2-іл]2, 2(1Н)-хінолінону; 4) оксо, 3-(5-{[(2S,4R)-4-метоксипіролідиніл]метоксі}-1Н5) OН, індол-2-іл)-2(1Н)-хінолінону; 6) галогену, 3-[5-({(2S,4R)-4-метокси-1-[(2-метил-57) CN, піримідиніл)метил]-піролідиніл}метоксі)-1Н-індол8) (C2-C6)алкенілу, 2-іл]-2(1Н)-хінолінону; 9) (C2-C6)алкінілу, етилового ефіру 1-(2-{[2-(2-оксо-1,2-дигідро-310) (С3-С6)циклоалкілу, хінолініл)-1Н-індол-5-іл]оксі}етил)-411) (С0-С6)алкіленарилу, піперидинкарбонової кислоти; 12) (С0-С6)алкіленгетероциклілу, 1-(2-{[2-(2-оксо-1,2-дигідро-3-хінолініл)-1Н-індол-513) (C0-С6)алкілен-N(Rb)2, іл]-оксі}етил)-4-піперидинкарбонової кислоти; 14) C(O)Ra, 3-[(2S,4R)-4-метоксі-2-({[2-(2-оксо-1,2-дигідро-315) (C0-C6)алкілен-CO2Rа, хінолініл)-1Н-індол-516) C(O)H і іл]окси}метил)піролідиніл]пропанової кислоти; 17) (C0-C6)алкілен-CO2Н, 3-[5-(4-метансульфонілпіперазин-1-ілметил)-1Нпричому зазначені алкіл, алкеніл, алкініл, циклоаліндол-2-іл]-1Н-хінолін-2-ону; кіл, арил і гетероцикліл необов’язково заміщені 3-[5-(4-метансульфоніл-1-оксипіперазин-1замісниками аж до трьох, вибраними з Rb, ОН, (C1ілметил)-1Н-індол-2-іл]-1Н-хінолін-2-ону; C6)алкокси, галогену, CO2Н, CN, O(С=O)С13-[5-(4-ацетилпіперазин-1-ілметил)-1Н-індол-2-іл]С6алкілу, оксо і N(Rb)2; і 1Н-хінолін-2-ону; R7 і R8 незалежно вибрані з: N-циклопропіл-N-[2-(2-оксо-1,2-дигідрохінолін-31) Н, іл)-1Н-індол-5-ілметил]метансульфонаміду; 2) (C=O)ObC1-C6алкілу, 3-[5-(1-піперазинілкарбоніл)-1Н-індол-2-іл]-2(1Н)3) (С=О)ОbС3-С6циклоалкілу, хінолінону; 4) (С=О)Оbарилу, 3-{5-[(4-метил-1-піперазиніл)карбоніл]-1Н-індол-25) С(=O)Оbгетероциклілу, іл}-2(1Н)-хінолінону; 6) C1-C6алкілу, трифторацетату 1-{[2-(2-оксо-1,2-дигідро-37) арилу, хінолініл)-1Н-індол-5-іл]карбоніл}-48) С2-С6алкенілу, піперидинамінію; 9) С2-С6алкінілу, трифторацетату 1-({[2-(2-оксо-1,2-дигідро-310) гетероциклілу, хінолініл)-1Н-індол-5-іл]оксі}ацетил)піперазин-4-ію; 11) С3-С6циклоалкілу, 3-{5-[2-(1,1-діоксидо-4-тіоморфолініл)-212) SО2Ra і оксоетоксі]-1Н-індол-2-іл}-2(1Н)-хінолінону; 13) (C=O)NRb2, N-{[2-(2-оксо-1,2-дигідро-3-хінолініл)-1Н-індол-5причому зазначені алкіл, циклоалкіл, арил, гетероіл]метил}-4-піперидинкарбоксаміду; цикліл, алкеніл і алкініл необов’язково заміщений 3-{5-[1-(4-морфолініл)етил]-1Н-індол-2-іл}-2(1Н)одним або декількома замісниками, вибраними з хінолінону; R6a, або 3-(5-[1-(1-піролідиніл)етил]-1Н-індол-2-іл}-2(1Н)R7 і R8 можуть бути взяті разом з азотом, до якого хінолінону; вони приєднані, з утворенням моноциклічного або 3-{5-[1-(4-ацетил-1-піперазиніл)етил]-1Н-індол-2біциклічного гетероциклу з 5-7 членами в кожному іл}-2(1Н)-хінолінону; кільці, що містить необов’язково крім азоту один 3-(5-{1-[4-(метилсульфоніл)-1-піперазиніл]етил}або два додаткових гетероатоми, вибраних із N, О 1Н-індол-2-іл)-2(1Н)-хінолінону; і S, причому зазначений моноциклічний або біцик4-аміно-N-[2-(2-оксо-1,2-дигідро-3-хінолініл)-1Нлічний гетероцикл, необов’язково заміщений одіндол-5-іл]-1-піперидинкарбоксаміду і ним або декількома замісниками, вибраними з R6а. 4-аміно-N-{[2-(2-оксо-1,2-дигідро-3-хінолініл)-1Н3. Сполука за п. 2, де R2, R3 і R5 представляє Н. індол-5-іл]метил}-1-піперидинкарбоксаміду, або її 4. Сполука за п. 3, де t дорівнює 1, s дорівнює 1 і фармацевтично прийнятної солі або стереоізомеR1 представляє Н. ра. 4 5. Сполука за п. 4, де R вибраний з: 7. Сполука за п.1, яка являє собою 3-[5-(41) ОС1-С6алкілен-NR7R8, метансульфонілпіперазин-1-ілметил)-1Н-індол-22) (С=O)аC0-С6алкілен-Q, де Q представляє Н, OН, іл]-1Н-хінолін-2-он або її фармацевтично прийнятCO2Н або OC1-C6алкіл, ну сіль. 3) ОC0-C6алкіленгетероциклілу, необов’язково за8. Фармацевтична композиція, яка містить сполуку міщеного замісниками від одного до трьох, вибраза п. 1 і фармацевтично прийнятний носій. ними з R6a, 7 74560 8 15. Спосіб за п. 12, який відрізняється тим, що 9. Композиція за п. 8, яка додатково містить другу сполуку, вибрану з: захворюванням, яке полягає у розвитку кровонос1) модулятора рецептора естрогену, них судин, є очне захворювання. 16. Спосіб за п. 12, який відрізняється тим, що 2) модулятора рецептора андрогену, 3) модулятора рецептора ретиноїду, запальне захворювання вибране з ревматоїдного 4) цитотоксичного агента, артриту, псоріазу, контактного дерматиту та алер5) антипроліферативного агента, гійних реакцій уповільненого типу. 17. Спосіб за п. 12, який відрізняється тим, що 6) інгібітора пренілпротеїнтрансферази, 7) інгібітора HMG-CoA-редуктази, захворювання, пов’язане з кістковою патологією, 8) інгібітора ВІЛ-протеази, вибране з остеосаркоми, остеоартриту і рахіту. 18. Спосіб за п. 13, який відрізняється тим, що 9) інгібітора зворотної транскриптази та 10) іншого інгібітора розвитку кровоносних судин. він додатково включає радіаційну терапію. 19. Спосіб за п. 13, який відрізняється тим, що 10. Композиція за п. 9, де другою сполукою є інший інгібітор розвитку кровоносних судин, вибравін додатково включає введення сполуки, вибраний з групи, що складається з інгібітора тирозинкіної з: нази, інгібітора, отриманого з епідерми фактора 1) модулятора рецептора естрогену, росту, інгібітора, отриманого з фібробластів фак2) модулятора рецептора андрогену, тора росту, інгібітора, отриманого з тромбоцитів 3) модулятора рецептора ретиноїду, фактора росту, інгібітора ММР (матричної мета4) цитотоксичного агента, лопротеази), блокатора інтегрину, інтерферону5) антипроліферативного агента, 6) інгібітора пренілпротеїнтрансферази, , інтерлейкіну-12, пентозанполісульфату, інгібі7) інгібітора HMG-CoA-редуктази, тора циклооксигенази, карбоксіамідотриазолу, 8) інгібітора ВІЛ-протеази, комбретастатину А-4, скваламіну, 6-О9) інгібітора зворотної транскриптази та (хлорацетилкарбоніл)фумагілолу, талідоміду, ангі10) іншого інгібітора розвитку кровоносних судин. остатину, тропонілу-1 і антитіл до VEGF. 20. Спосіб за п. 13, який відрізняється тим, що 11. Композиція за п. 9, де другою сполукою є мовін додатково включає комбінацію з радіаційною дулятор рецептора естрогену, вибраний з тамоктерапією і введення сполуки, вибраної з: сифену і ралоксифену. 1) модулятора рецептора естрогену, 12. Спосіб лікування або профілактики залежного 2) модулятора рецептора андрогену, від тирозинкінази захворювання або стану у ссав3) модулятора рецептора ретиноїду, ця, такого як, рак, захворювання, яке включає в 4) цитотоксичного агента, себе розвиток кровоносних судин, ретинальне 5) антипроліферативного агента, новоутворення кровоносних судин, діабетична 6) інгібітора пренілпротеїнтрансферази, ретинопатія, пов’язана з віком дегенерація жовтої 7) інгібітора HMG-CoA-редуктази, плями, запальне захворювання, захворювання, 8) інгібітора ВІЛ-протеази, пов’язане з кістковою патологією, який відрізня9) інгібітора зворотної транскриптази та ється тим, що ссавцеві, який потребує такого ліку10) іншого інгібітора розвитку кровоносних судин. вання, вводять терапевтично ефективну кількість 21. Спосіб за п. 13, який відрізняється тим, що сполуки за п. 1. він включає введення додатково паклітакселу або 13. Спосіб за п. 12, який відрізняється тим, що трастузумабу. рак вибраний з ракових захворювань головного 22. Спосіб за п. 13, який відрізняється тим, що мозку, сечостатевого тракту, лімфатичної системи, він включає додатково введення антагоніста шлунка, гортані і легені. GPIIb/IIIa. 14. Спосіб за п. 12, який відрізняється тим, що 23. Спосіб за п. 22, який відрізняється тим, що рак вибраний з гістіоцитарної лімфоми, адренокаантагоністом GPIIb/IIIa є тирофібан. рциноми легень, дрібноклітинних ракових захво24. Спосіб зменшення або профілактики ушкорювань легень, панкреатичного раку, гіобластом і дження тканини після церебрального ішемічного карциноми молочної залози. нападу, який включає введення терапевтично ефективної кількості сполуки за п. 1. Дана заявка заявляє пріоритет за 35 U.S.C. § 119 (e) із попередньої заявки США 60/160356, зареєстрованої 19 жовтня 1999р. Даний винахід відноситься до сполук, які інгібують, регулюють і/або модулюють трансдукцію сигналу тирозинкінази, композицій, які містять дані сполуки, і способів використання їх для лікування тирозинкіназа-залежних захворювань і станів, таких як розвиток кровоносних судин, рак, ріст пухлини, атеросклероз, пов'язана з віком дегенерація жовтої плями, діабетична ретинопатія, запальні захворювання і тому подібне у ссавців. Тирозинкінази є класом ферментів, які каталізують перенесення кінцевого фосфату аденозинтрифосфату до залишків тирозину в білкових субстратах. Вважається, що тирозинкінази за допомогою фосфорилування субстрату відіграють важливу роль у трансдукції сигналу для ряду клітинних функцій. Хоча точний механізм трансдукції сигналу все ще є неясним, виявлено, що тирозинкінази є важливими факторами, що сприяють проліферації клітин, канцерогенезу і диференціації 9 74560 10 клітин. судин, відповідно. Тирозинкінази можна класифікувати як тироРозвиток кровоносних судин характеризується зинкінази рецепторного типу або нерецепторного надмірною активністю васкулярного ендотеліальтипу. Тирозинкінази рецепторного типу мають поного фактора росту (VEGF). VEGF фактично склазаклітинну, трансмембранну і внутрішньоклітинну дається з родини лігандів (Klagsburn and D'Amore, частину, тоді як тирозинкінази нерецепторного Cytokine and Growth Factor Reviews 7: 259-270, типу є цілком внутрішньоклітинними. 1996). VEGR зв'язується з високою спорідненістю з Тирозинкінази рецепторного типу складаються транс-мембранним рецептором KDR тирозинкіназ великого числа трансмебранних рецепторів із зи і спорідненою fins-подібною тирозинкіназою-1, різною біологічною активністю. Фактично, було відомою також як Flt-1, або рецептором 1 фактора ідентифіковано приблизно двадцять різних підроросту васкулярних ендотеліальних клітин (VEGERдин тирозинкіназ рецепторного типу. Одна підро1). Експерименти з клітинними культурами і "нокадина тирозинкіназ, позначена як підродина HER, ут"-генами показують, що кожен рецептор робить включає EGFR, HER2, HER3 і HER4. Ліганди даної внесок у різні аспекти розвитку кровоносних судин. підродини рецепторів включають епітеліальний KDR опосередковує мітогенну функцію VEGF, тоді як Fit-1, очевидно, модулює немітогенні функції, фактор росту, TGF- , амфірегулін, HB-EGF, бетатакі як функції, пов'язані з клітинною адгезією. Інгіцелулін і герегулін. Іншою підродиною зазначених бування KDR, таким чином, опосередковує рівень тирозинкіназ рецепторного типу є підродина інсумітогенної активності VEGF. Фактично, було виявліну, яка включає INS-R, IGF-IR і IR-R. Підродина лено, що ріст пухлини є чутливим до антиангіогенPDGF включає PDGF- - і- -рецептори, CSFIR, c-kit них дій антагоністів рецептора VEGF (Kim et al, і FLK-II. Крім того, є родина FLK, яка включає реNature 362, pp. 841-844,1993). цептор домену вставки кінази (KDR), кіназу-1 феТверді пухлини, отже, можна лікувати інгібітотальної печінки (FLK-1), кіназу-4 фетальної печінки рами тирозинкінази, оскільки зазначені пухлини (FLK-4) і fins-подібну тирозинкіназу-1 (flt-1). Родини залежать від розвитку кровоносних судин для PDGF і FLK звичайно розглядаються разом внаутворення кровоносних судин, необхідних для заслідок подібності даних двох груп. Для докладного безпечення їхнього росту. Зазначені тверді пухлиобговорення тирозинкіназ рецепторного типу див. ни включають гістіоцитарну лімфому, ракові запублікацію Plowman et al., DN&P 7(6): 334-339, хворювання головного мозку, сечостатевого 1994, яка включається, таким чином, як посиланшляху, лімфатичної системи, шлунка, гортані та ня. легень, включаючи аденокарциному легень і дрібТирозинкінази нерецепторного типу також ноклітинний рак легень. Додаткові приклади вклювключають численні підродини, у тому числі Src, чають ракові захворювання, в яких спостерігається Frk, Btk, Csk, Abi, Zap70, Fes/Fps, Fak, Jak, Ack і надекспресія або активація Raf-активуючих онкоLIMK. Кожна із зазначених підродин далі підроздігенів (наприклад, K-ras, erb-B). Такі ракові захволяється на рецептори, що розрізняються. Наприрювання включають панкреатичну карциному і клад, підродина Src є однією з найбільших і вклюкарциному молочної залози. Відповідно до цього, чає Src, Yes, Fyn, Lyn, Lck, Blk, Hck, Fgr і Yrk. інгібітори зазначених тирозинкіназ є корисними Підродина Src ферментів була пов'язана з онкогедля профілактики і лікування проліферативних незом. Для більш докладного обговорення тирозизахворювань, що залежать від даних ферментів. нкіназ нерецепторного типу див. публікацію Bolen Ангіогенна активність VEGF не обмежується Oncogene, 8: 2025-2031 (1993), яка, таким чином, пухлинами. VEGF є причиною більшої частини включається як посилання. ангіогенної активності, індукованої у сітківці або Тирозинкінази як рецепторного типу, так і небіля сітківки при діабетичній ретинопатії. Такий рецепторного типу беруть участь у клітинних сигваскулярний ріст у сітківці призводить до візуальнальних шляхах, що призводять до різних патоної дегенерації, досягаючи вищої точки при сліпоті. генних станів, у тому числі раку, псоріазу і мРНК і білок очного VEGF збільшуються і3-за тагіперімунних реакцій-відповідей. ких станів, як оклюзія ретинальної вени у приматів Було припущено, що декілька тирозинкіназ реі знижені рівні рО2 у мишей, які призводять до цепторного типу і пов'язані з ними фактори росту утворення нових судин. Внутрішньоочні ін'єкції відіграють роль у розвитку кровоносних судин, моноклональних антитіл проти VEGF або імунозхоча деякі можуть активувати розвиток судин нелиттів рецептора VEGF інгібують утворення нових прямою дією (Mustonen and Alitalo, J. Cell Biol. 129: очних судин на моделях як приматів, так і гризунів. 895-898, 1995). Однією такою тирозинкіназою реНезалежно від причини індукування VEGF у людицепторного типу є кіназа-1 фетальної печінки або ни з діабетичною ретинопатією, інгібування очного FLK-1. Людським аналогом FLK-1 є рецептор KDR, VEGF є корисним при лікуванні такого захворющо містить домен вставки кінази, який відомий вання. також як рецептор 2 фактора росту васкулярних Експресія VEGF також значно підвищується в ендотеліальних клітин або VEGFR-2, оскільки він гіпоксичних зонах пухлин тварин і людини, сусідніх зв'язує VEGF із високою спорідненістю. Нарешті, із ділянкою некрозу. VEGF також позитивно регумишача версія даного рецептора також була налюється експресією онкогенів ras, raf, src і мутантзвана NYK (Oelrichs et al., Oncogene 8(1): 11-15, ного р53 (усі з яких мають відношення до розгля1993). VEGF і KDR є парою ліганд-рецептор, яка нутого раку). Моноклональні антитіла проти VEGF відіграє величезну роль у проліферації васкулярінгібують ріст пухлин людини у голих мишей. Хоча них ендотеліальних клітин і утворенні та прорості ж самі пухлинні клітини продовжують експресутанні кровоносних судин, що називають утворенвати VEGF у культурі, антитіла не зменшують їх ням і розвитком судин і розвитком кровоносних 11 74560 12 мітотичний коефіцієнт. Таким чином, VEGF, що походить із пухлини, не функціонує як аутокринний мітогенний фактор. Отже, VEGF сприяє росту пухлини in vivo стимуляцією розвитку кровоносних судин за допомогою хемотактичної і мітогенної активності його паракринних васкулярних ендотеW1 представляє S, О або N-R; ліальних клітин. Зазначені моноклональні антитіла V1 представляє N або С; інгібують також у типовому випадку ріст ракових W2 представляє N або С; пухлин прямої кишки людини з менш значним V2 представляє S, О або N-R; утворенням кровоносних судин у мишей з атимією а дорівнює 0 або 1; і зменшують число пухлин, що виникають з інокуb дорівнює 0 або 1; льованих клітин. m дорівнює 0, 1 або 2; Вірусна експресія VEGF-зв'язувальної консs дорівнює 1 або 2; трукції Flk-1, Fit-1, гомолога рецептора мишачого t дорівнює 1, 2 або 3; KDR, усіченого для виключення цитоплазматичних X=Y представляє C=N, N=C або С=С; доменів тирозинкінази, але який зберігає мемR представляє Η або С1-С6алкіл; бранний якір, фактично усуває ріст трансплантоR1 і R5, незалежно, вибрані з: ваної гліобластоми у мишей за допомогою доміна1) Н, нтного негативного механізму утворення 2) (С=О)аОbС1-С10алкілу, гетеродимеру трансмембранними рецепторами 3) (С=О)аОbарилу, VEGF ендотеліальних клітин. Ембріональні стов4) (С=O)aObС2-С10алкенілу, бурові клітини, які звичайно ростуть у вигляді тве5) (С=О)аОbС2-С10алкінілу, рдих пухлин у голих мишей, не продукують пухли6) СО2Н, ни, що виявляються, якщо обидва алелі VEGF 7) галогену, руйнуються. Взяті разом, наведені дані показують 8) ОН, роль VEGF у рості солідних пухлин. Інгібування 9) ОbС1-С6перфторалкілу, KDR або Flt-1 залучається до патологічного розви10) (C=O)aNR7R8, тку кровоносних судин, і зазначені рецептори є 11) CN, корисними при лікуванні захворювань, в яких роз12) (С=О)аОbС3-С8циклоалкілу і виток кровоносних судин є частиною загальної 13) (С=О)аОbгетероциклілу, патології, наприклад, запалення, діабетичного причому зазначений алкіл, арил, алкеніл, алкіретинального новоутворення кровоносних судин, а ніл, циклоалкіл і гетероцикліл, необов'язково, затакож різних форм раку, оскільки відомо, що ріст міщений одним або декількома замісниками, вибпухлини залежить від розвитку кровоносних судин раними з R6; (Weidner et al., N. Engl. J. Med., 324, pp. 1-8,1991). R2 і R3, незалежно, вибрані з: Відповідно до цього, ідентифікація невеликих 1) Н, сполук, які специфічно інгібують, регулюють і/або 2) (С=О)ОаС1-С6алкілу, модулюють трансдукцію сигналу тирозинкіназ, є 3) (С=О)Оаарилу, бажаною і є метою даного винаходу. 4) С1-С6алкілу, Даний винахід відноситься до сполук, які здат5) SO2Ra i ні інгібувати, модулювати і/або регулювати транс6) арилу; дукцію сигналу тирозинкіназ як рецепторного типу, R4 вибраний з: так і нерецепторного типу. Одне із втілень даного 1) (С=О)аОbС1-С10алкілу, винаходу ілюструється сполукою формули І і її 2) (С=О)аОbарилу, фармацевтично прийнятними солями і стереоізо3) (С=О)аОbС2-С10алкетлу, мерами: 4) (С=О)аОbС2-С10алкінілу, 5) СО2Н, 6) галогену, 7) ОН, 8) ОbС1-С6перфторалкілу, 9) (C=O)aNR7R8, 10) CN, 11) (С=О)аОbС3-С8циклоалкілу і Сполуки даного винаходу є корисними при ін12) (С=О)аОbгетероциклілу, гібуванні кіназ та ілюструються сполукою формули причому зазначений алкіл, арил, алкеніл, алкіІ: ніл, циклоалкіл і гетероцикліл, необов'язково, заміщений одним або декількома замісниками, вибраними з R6; R6 представляє: 1) (С=О)аОbС1-С10алкіл, 2) (С=О)аОbарил, 3) С2-С10алкеніл, 4) С2-С10алкініл, або її фармацевтично прийнятною сіллю або 5) (С=О)аОbгетероцикліл, стереоізомером, де Ζ представляє 6) СО2Н, 7) галоген, 13 74560 14 8) CN, С6)циклоалкіл, арил або гетероцикліл і 9) ОН, Rb представляє Н, (С1-С6)алкіл, арил, гетеро10) ОbС1-С6перфторалкіл, цикліл, (С3-С6)циклоалкіл, (С=О)ОС1-С6алкіл, 11) Oa(C=O)bNR7R8, (С=О) С1-С6алкіл або S(O)2Ra. 12) оксо, Другим втіленням винаходу є сполука форму13) СНО, ли І, де 14) (N=O)R7R8 або Ζ представляє 15) (С=О)аОbС3-С8циклоалкіл, причому зазначений алкіл, арил, алкеніл, алкініл, гетероцикліл і циклоалкіл, необов'язково, заміщений одним або декількома замісниками, вибраними з R6a; R6a вибраний з: 1) (С=О)rО8(С1-С10)алкілу, де r і s, незалежно, Наступне втілення даного винаходу ілюструдорівнює 0 або 1, ється сполукою формули І, де Ζ має значення, 2) Оr(С1-С3)перфторалкілу, де r дорівнює 0 або вказане безпосередньо вище, де 1, s дорівнює 1 і а 3) (С0-С6)алкілен-8(О)mR , де m дорівнює 0, 1 t дорівнює 1 або 2; або 2, R1 і R5, незалежно, вибрані з: 4) оксо, 1) Н, 5) ОН, 2) (С=О)аОbС1-С6алкілу, 6) галогену, 3) (С=О)аОbарилу, 7) CN, 4) (С=О)аОbС2-С6алкенілу, 8) (С2-С10)алкенілу, 5) (С=О)аОbС2-С6алкінілу, 9) (С2-С10)алкінілу, 6) СО2Н, 10) (С3-С6)циклоалкілу, 7) галогену, 11) (С0-С6)алкіленарилу, 8) ОН, 12) (С0-С6)алкіленгетероциклілу, 9) Оb С1-С3перфторалкілу, b 13) (C0-C6)алкілен-N(R )2, 10) (C=O)aNR7R8, a 14) C(O)R , 11) CN, 15) (С0-С6)алкілен-СO2Rа, 12) (С=О)аОbС3-С8циклоалкілу і 16) С(О)Н і 13) (С=O)аОbгетероциклілу, 17) (С0-С6)алкілен-СО2Н, причому зазначений алкіл, арил, алкеніл, алкіпричому зазначений алкіл, алкеніл, алкініл, ніл, циюіоалкіл і гетероцикліл необов'язково заміциклоалкіл, арил і гетероцикліл, необов'язково, щений одним або декількома замісниками, вибразаміщений замісниками аж до трьох, вибраними з ними з R6; b R , ОН, (С1-С6)алкокси, галогену, СО2Н, CN, R4 вибраний з: О(С=О)С1-С6алкілу, оксо і N(Rb)2; 1) (С=О)аОbС1-С6алкілу, R7 і R8, незалежно, вибрані з: 2) (С=О)аОbарилу, 1)Н, 3) (С=О)аОbС2-С6алкенілу5 2) (С=О)ОbС1-С10алкілу, 4) (С=О)аОbС2-С6алкінілу, 3) (С=О)ОbС3-С8циклоалкілу, 5) СО2Н, 4) (С=О)Оbарилу, 6) галогену, 5) С(=О)Оbгетероциклілу, 7) ОН, 6) С1-С10алкілу, 8) ОbС1-С3перфторалкілу, 7) арилу, 9) (C=O)aNR7R8, 8) С2-С10алкенілу, 10) CN, 9) С2-С10алкінілу, 11) (С=О)аОbС3-С6циклоалкілу і 10) гетероциклілу, 12) (С=О)аОbгетероциклілу, 11) С3-С8циклоалкілу, причому зазначений алкіл, арил, алкеніл, алкі12) SO2Ra і ніл, циклоалкіл і гетероцикліл, необов'язково, заb 13) (C=O)NR 2, міщений одним або декількома замісниками, вибпричому зазначений алкіл, циклоалкіл, арил, раними з R6; гетероцикліл, алкеніл і алкініл, необов'язково, заR6 представляє: міщений одним або декількома замісниками, виб1) (С=О)аОbС1-С6алкіл, раними з R6a, або 2) (С=О)аОbарил, 7 8 R і R можуть бути взяті разом з азотом, до 3) С2-С6алкеніл, якого вони приєднані, з утворенням моноциклічно4) С2-С6алкініл, го або біциклічного гетероциклу з 5-7 членами в 5) (С=О)аОbгетероцикліл, кожному кільці, що містить, необов'язково, крім 6) СО2Н, азоту, один або два додаткових гетероатоми, виб7) галоген, раних із N, О і S, причому зазначений моноцикліч8) CN, ний або біциклічний гетероцикл, необов'язково, 9) ОН, заміщений одним або декількома замісниками, 10) ОbС1-С3перфторалкіл, 6a вибраними з R ; 11) Oa(C=O)bNR7R8, a R представляє (С1-С6)алкіл, (С312) оксо, 15 74560 16 13) СНО, R4 вибраний з: 14) (N=O)R7R8 або 1) OС1-С6алкіленNR7R8, 15) (С=О)аОbС3-С6циклоалкіл, 2) (С=O)аС0-С6алкілен-Q, де Q представляє Н, причому зазначений алкіл, арил, алкеніл, алкіОН, СО2Н або ОС1-С6алкіл, ніл, гетероцикліл і циклоалкіл, необов'язково, за3) ОС0-С6алкіленгетероциклілу, необов'язково міщений одним або декількома замісниками, вибзаміщеного замісниками від одного до трьох, вибраними з R6a; раними з R6a, 6a R вибраний з: 4) C0-C6алкілен-NR7R8 1) (С=О)rОs(С1-С6)алкілу, де r і s, незалежно, 5) (C=O)NR7R8 і дорівнює 0 або 1, 6) OС1-С3алкілен-(C=O)NR7R8. 2) Оr(С1-С3)перфторалкілу, де r дорівнює 0 або Кращим втіленням є сполука, вибрана з 1, 3-{5-[3-(4-метилпіперазин-1-іл)пропокси]-1Н3) (C0-C6)алкілен-S(O)mRas де m дорівнює 0,1 індол-2-іл}-1Н-хінолін-2-ону; або 2, 3-(5-{2-[(2-метоксіетил)аміно]етокси}-1Н-індол4) оксо, 2-іл)-2(1Н)-хінолінону; 5) ОН, 3-[5-(2-{(2-метоксіетил)[(2-метокси-56) галогену, піримідиніл)метил]-аміно}етокси)-1Н-індол-2-іл]7) CN, 2(1Н)-хінолінону; 8) (С2-С6)алкенілу, 3-(5-{[(2S,4R)-4-метоксипіролідиніл]метокси}9) (С2-С6)алкінілу, 1Н-індол-2-іл)-2(1Н)-хінолінону; 10) (С3-С6)циклоалкілу, 3-[5-({(2S,4R)-4-метокси-1-[(2-метил-511) (С0-С6)алкіленарилу, піримідиніл)метил]-піролідиніл}метокси)-1Н-індол12) (С0-С6)алкіленгетероциклілу, 2-іл]-2(1Н)-хінолінону; 13) (С0-С6)алкілен-N(Rb)2, етиловогоефіру1-(2-{[2-(2-оксо-1,2-дигідро-314) C(O)Ra, хінолініл)-1Н-індол-5-іл]окси}етил)-415) (C0-C6)алкілен-CO2Ra, піперидинкарбоновоїкислоти; 16) С(О)Н і 1-(2-{[2-(2-оксо-1,2-дигідро-3-хінолініл)-1Н17) (С0-С6)алкілен-СО2Н, індол-5-іл]-окси}етил)-4причому зазначений алкіл, алкеніл, алкініл, піперидинкарбоновоїкислоти; циклоалкіл, арил і гетероцикліл, необов'язково, 3-[(2S,4R)-4-метокси-2-({[2-(2-оксо-1,2-дигідрозаміщений замісниками аж до трьох, вибраними з 3-хінолініл)-1Н-індол-5Rb, OH, (С1-С6)алкокси, галогену, СО2Н, CN, іл]окси}метил)піролідиніл]пропановоїкислоти; b О(С=О)С1-С6алкілу, оксо і N(R )2; і 3-[5-(4-метансульфонілпіперазин-1-ілметил)R7 і R8, незалежно, вибрані з: 1Н-індол-2-іл]-1Н-хінолін-2-ону; 1) Н, 3-[5-(4-метансульфоніл-1-оксипіперазин-12) (С=О)ОbС1-С6алкілу, ілметил)-1Н-індол-2-іл]-1Н-хінолін-2-ону; 3) (С=О)ОbС3-С6циклоалкілу, 3-[5-(4-ацетилпіперазин-1-ілметил)-1Н-індол-24) (С=О)Оbарилу, іл]-1Н-хінолін-2-ону; 5) С(=О)Оbгетероциклілу, N-циклопропіл-N-[2-(2-оксo-1,2-дигідрохінолін6) С1-С6алкілу, 3-іл)-1Н-індол-5-ілметил]метансульфонаміду; 7) арилу, 3-[5-(1-піперазинілкарбоніл)-1Н-індол-2-іл]8) С2-С6алкенілу, 2(1Н)-хінолінону; 9) С2-Сбалкінілу, 3-{5-[(4-метил-1-піперазиніл)карбоніл]-1Н10) гетероциклілу, індол-2-іл}-2(1Н)-хінолінону; 11) С3-С6циклоалкілу, трифторацетату 1-{[2-(2-оксо-1,2-дигідро-312) SO2Ra i хінолініл)-1Н-індол-5-іл]карбоніл}-413) (C=O)NRb2, піперидинамінію; причому зазначений алкіл, циклоалкіл, арил, трифторацетату 1-({[2-(2-оксо-1,2-дигідро-3гетероцикліл, алкеніл і алісініл, необов'язково, хінолініл)-1Н-індол-5-іл]окси}ацетил)піперазин-4заміщений одним або декількома замісниками, інію; вибраними з R6a, або 3-{5-[2-(1,1-діоксидо-4-тіоморфолініл)-2R7 і R8 можуть бути взяті разом з азотом, до оксоетокси]-1Н-індол-2-іл}-2(1Н)-хінолінону; якого вони приєднані, з утворенням моноциклічноN-{[2-(2-оксо-1,2-дигідро-3-хінолініл)-1Н-індолго або біциклічного гетероциклу з 5-7 членами в 5-іл]метил}-4-піперидинкарбоксаміду; кожному кільці, що містить, необов'язково, крім 3-{5-[1-(4-морфолініл)етил]-1Н-індол-2-іл}азоту, один або два додаткових гетероатоми, виб2(1Н)-хінолінону; раних із Ν, Ο і S, причому зазначений моноцикліч3-(5-[1-(1-гаролідиніл)етил]-1Н-індол-2-іл}ний або біциклічний гетероцикл, необов'язково, 2(1Н)-хінолінону; заміщений одним або декількома замісниками, 3-{5-[1-(4-ацетил-1-піперазиніл)етил]-1Н-індол6a вибраними з R . 2-іл}-2(1Н)-хінолінону; Іншим втіленням є сполука, описана тільки що 3-(5-{1-[4-(метилсульфоніл)-1вище, де R2, R3 і R5 додатково представляють Н. піперазиніл]етил}-1Н-індол-2-іл)-2(1Н)-хінолінону; Є ще одне втілення, де t додатково дорівнює 4-аміно-N-[2-(2-оксо-1,2-дигідро-3-хінолініл)1, s дорівнює 1 і R1 представляє Н. 1Н-індол-5-іл]-1-піперидин-карбоксамідуі Даний винахід включає також сполуку форму4-аміно-N-{[2-(2-оксо-1,2-дигідро-3-хінолініл)ли І, як додатково зазначено тільки що вище, і де 1Н-індол-5-іл]метил}-1-піперидинкарбоксаміду або 17 74560 18 його фармацевтично прийнятної солі або стереоі4) цитотоксичного агента, зомеру. 5) антипроліферативного агента, До обсягу даного винаходу включена також 6) інгібітора пренілпротеїнтрансферази, фармацевтична композиція, яка включає сполуку 7)} інгібітора HMG-CoA-редуктази, формули І, як описано вище, і фармацевтично 8) інгібітора ВІЛ-протеази, прийнятний носій. Даний винахід включає також 9) інгібітора зворотної транскриптази і спосіб лікування або профілактики раку у ссавця, 10) іншого інгібітора розвитку кровоносних сущо потребує такого лікування, який включає введин. дення зазначеному ссавцю терапевтично ефектиКращі інгібітори розвитку кровоносних судин вної кількості сполуки формули І. Переважні ракові вибрані з групи, що складається з інгібітора тирозахворювання для лікування вибрані з ракових зинкінази, інгібітора, отриманого з епідерми факзахворювань молочної залози, сечостатевих шлятора росту, інгібітора, отриманого з фібробластів хів, лімфатичної системи, шлунка, гортані і легень. фактора росту, інгібітора, отриманого з тромбоциІншою групою переважних форм раку є гістіоцитатів фактора росту, інгібітора ММР (матричної мерна лімфома, адренокарцинома легень, дрібнокліталопротеази), блокатора інтегрину, інтерферонутинні ракові захворювання легень, панкреатичний , інтерлейкіну-12, пентозанполісульфату, інгібіторак, гіобластоми і карцинома молочної залози. ра циклооксигенази, карбоксіамідотриазолу, комбВключений також спосіб лікування або профіретастатину А-4, скваламіну, 6-Олактики захворювання, до якого втягується розви(хлорацетилкарбоніл)фумагілолу, талідоміду, ангіток кровоносних судин, який включає введення остатину, тропоніну-1 і антитіл до VEGF. Кращими ссавцю, що потребує такого лікування, терапевтимодуляторами рецептора естрогену є тамоксифен чно ефективної кількості сполуки формули І. Таким і ралоксифен. захворюванням, до якого втягується розвиток кроДо обсягу винаходу включений також спосіб воносних судин, є очні хвороби, такі як ретинальне лікування раку, який включає введення терапевтиновоутворення кровоносних судин, діабетична чно ефективної кількості сполуки формули І у комретинопатія, пов'язана з віком дегенерація жовтої бінації з радіаційною терапією і/або в комбінації зі плями тощо. сполукою, вибраною з: До обсягу даного винаходу включений також 1) модулятора рецептора естрогену, спосіб лікування або профілактики запальних за2) модулятора рецептора андрогену, хворювань, який включає введення ссавцю, що 3) модулятора рецептора ретиноїду, потребує такого лікування, терапевтично ефектив4) цитотоксичного агента, ної кількості сполуки формули І. Прикладами таких 5) антипроліферативного агента, запальних захворювань є ревматоїдний артрит, 6) інгібітора пренілпротеїнтрансферази, псоріаз, контактний дерматит, алергійні реакції 7) інгібітора HMG-CoA-редуктази, уповільненого типу тощо. 8) інгібітора ВІЛ-протеази, Включений також спосіб лікування або профі9) інгібітора зворотної транскриптази і лактики залежного від тирозинкінази захворюван10) іншого інгібітора розвитку кровоносних суня або стану у ссавця, який включає введення дин. пацієнту-ссавцю, що потребує такого лікування, Ще одним втіленням винаходу є спосіб лікутерапевтично ефективної кількості сполуки форвання раку, який включає введення терапевтично мули І. Терапевтична кількість варіюється відповіефективної кількості сполуки формули І у комбінадно до певного захворювання і визначається фахіції з паклітакселом або трастузумабом. вцем у даній галузі без зайвого До обсягу винаходу включений також спосіб експериментування. ослаблення або профілактики ушкодження тканиСпосіб лікування або профілактики ретинальни після церебрального ішемічного нападу, який ного новоутворення кровоносних судин, який включає введення терапевтично ефективної кільвключає введення ссавцю, що потребує такого кості сполуки формули І. лікування, терапевтично ефективної кількості споЦі та інші аспекти винаходу будуть очевидні з луки формули І, також включений до обсягу даного постулатів, що містяться в ньому. винаходу. Способи лікування або профілактики "Залежні від тирозинкінази захворювання або очних хвороб, таких як діабетична ретинопатія і стани" відносяться до патологічних станів, які запов'язана з віком дегенерація жовтої плями, також лежать від активності однієї або декількох тирозиє частиною винаходу. До обсягу даного винаходу нкіназ. Тирозинкінази або безпосередньо, або включений також спосіб лікування або профілактиопосередковано беруть участь у шляхах трансдукки запальних захворювань, таких як ревматоїдний ції сигналу різних клітинних активностей, включаартрит, псоріаз, контактний дерматит і алергійні ючи проліферацію, адгезію та міграцію, і диферереакції уповільненого типу, а також спосіб лікуваннціацію. Захворювання, пов'язані з активностями ня або профілактики захворювань, пов'язаних з тирозинкіназ, включають проліферацію пухлинних кістковою патологією, вибраних із остеосаркоми, клітин, патологічне утворення нових судин, яке остеоартриту і рахіту. забезпечує ріст солідних пухлин, очне утворення Винахід включає також використання заявленових судин (діабетична ретинопатія, пов'язана з них сполук у комбінації з другою сполукою, вибравіком дегенерація жовтої плями тощо), і запалення ною з: (псоріаз, ревматоїдний артрит тощо). 1) модулятора рецептора естрогену, Сполуки даного винаходу можуть мати асиме2) модулятора рецептора андрогену, тричні центри, хіральні осі і хіральні площини (як 3) модулятора рецептора ретиноїду, описано в: E.L. Eliel and S.H. Wilen, Stereochemistry 19 74560 20 of Carbon Compounds, John Wiley and Sons, New ропіл, 2,2-диметилциклобутил, 2York, 1994, pages 1119-1190) і існують у вигляді етилциклопентил, циклогексил і так далі. рацематів, рацемічних сумішей і у вигляді індиві"Алкокси" представляє або циклічну, або нецидуальних діастереомерів, причому до даного виклічну алкільну групу із зазначеним числом атомів находу включені всі можливі ізомери та їхні суміші, вуглецю, приєднану через кисневий місток. "Алковключаючи оптичні ізомери. Крім того, описані в кси", отже, включає визначення вищевказаного ньому сполуки можуть існувати у вигляді таутомеалкілу і циклоалкілу. рів і обох таутомерних форм, і мається на увазі, Якщо число атомів вуглецю не вказується, тещо вони включені до обсягу винаходу, навіть якщо рмін "алкеніл" відноситься до неароматичного вугзображена тільки одна таутомерна структура. Налеводневого радикала, нерозгалуженого, розгалуприклад, мається на увазі, що будь-яка вказівка на женого або циклічного, що містить від 2 до 10 наведену нижче сполуку А включає таутомерну атомів вуглецю і, щонайменше, один вуглецьструктуру В і навпаки, а також їхні суміші. вуглецевий подвійний зв'язок. Переважно, є присутнім один вуглець-вуглецевий подвійний зв'язок, але можуть бути присутні аж до чотирьох неароматичних вуглець-вуглецевих подвійних зв'язків. Таким чином, " С1-С6алкеніл" означає алкенільний радикал, що має від 2 до 6 атомів вуглецю. Алкенільні групи включають етеніл, пропеніл, бутеніл, 2-метилбутеніл і циклогексеніл. Нерозгалужена, розгалужена або циклічна частина алкенільної Коли будь-який радикал, що змінюється, (нагрупи може містити подвійний зв'язок і може бути приклад, R4, R6, R6a і так далі) є присутнім більш заміщеною, якщо вказується заміщена алкенільна ніж один раз у будь-якій складовій частині, її вигрупа. значення в кожному випадку не залежить від кожТермін "алкініл відноситься до вуглеводневого ного іншого випадку. Крім того, комбінації заміснирадикала, нерозгалуженого, розгалуженого або ків і радикалів, що змінюються, є припустимими, циклічного, що містить від 2 до 10 атомів вуглецю тільки якщо такі комбінації призводять до стабільі, щонайменше, один вуглець-вуглецевий потрійних сполук. Лінії, проведені до циклічних систем ний зв'язок. Можуть бути присутніми аж до трьох від замісників, вказують, що наведений зв'язок вуглець-вуглецевих потрійних зв'язків. Таким чиможе бути приєднаний до кожного зі здатних заном, "С2-С6алкініл" означає алкінільний радикал, міщуватися атомів кільця. Якщо циклічна система що має від 2 до 6 атомів вуглецю. Алкінільні групи є поліциклічною, мається на увазі, що зв'язок привключають етиніл, пропініл, бутиніл, 3єднаний до будь-якого з придатних атомів вуглецю метилбутиніл і так далі. Нерозгалужена, розгалутільки на проксимальному кільці. жена або циклічна частина алкінільної групи може Зрозуміло, що замісники і моделі заміщення в містити потрійні зв'язки і може бути заміщеною, сполуках даного винаходу можуть бути обрані фаякщо вказується заміщена алкінільна група. хівцем у даній галузі техніки для одержання споУ деяких випадках замісники можуть бути вилук, які є хімічно стабільними і які можна легко значені в діапазоні вуглеців, які включають нуль, синтезувати способами, відомими в даній галузі, а такі як (С0-С6)алкіленарил. Якщо приймається, що також способами, наведеними нижче, з легко досарил представляє феніл, то дане визначення потупних вихідних матеріалів. Якщо замісник сам винне включати сам феніл, а також-CH2Ph,заміщений більш ніж однією групою, має бути зроCH2CH2Ph, CH(CH3)CH2CH(CH3)Ph і так далі. зумілим, що кілька згаданих груп можуть бути на Мається на увазі, що використовуваний тут тому самому вуглеці або різних вуглецях, поки термін "арил" означає будь-яке стабільне моноциотримується стабільна структура. Фраза "необоклічне або біциклічне вуглецеве кільце, що містить в'язково заміщений одним або декількома замісниаж до 7 атомів у кожному кільці, де, щонайменше, ками" повинна бути використана так, щоб бути одне кільце є ароматичним. Приклади таких ариеквівалентною фразі "необов'язково заміщений, льних елементів включають феніл, нафтил, тетращонайменше, одним замісником", у таких випадках гідронафтил, інданіл, біфеніл, фенантрил, антрил і переважне втілення буде мати від нуля до трьох аценафтил. У випадках, коли арильний замісник є замісників. біциклічним і одне кільце є неароматичним, зрозуМається на увазі, що використовуваний тут міло, що приєднання відбувається через ароматитермін "алкіл" включає насичені аліфатичні вуглечне кільце. водневі групи як із розгалуженим, так і з нерозгаТермін "гетероарил", використовуваний тут, луженим ланцюгом, що мають визначене число представляє стабільне моноциклічне або біциклічатомів вуглецю. Наприклад, встановлено, що С1не кільце з атомами вуглецю в кожному кільці аж С10, як у " С1-С10 алкілі", включає групи, що мають до 7 атомів, де, щонайменше, одне кільце є аро1, 2, 3, 4, 5, 6, 7, 8, 9 або 10 атомів вуглецю в нематичним і містить від 1 до 4 гетероатомів, вибрарозгалуженій або розгалуженій структурі. Наприних із групи, що складається з О, N і S. Гетероариклад, " С1-С10 алкіл" конкретно включає метил, льні групи в обсязі даного визначення включають, етил, н-пропіл, ізопропіл, н-бутил, трет-бутил, ізоале не обмежуються ними: акридиніл, карбазоліл, бутил, пентил, гексил, гептил, октил, ноніл, децил і цинолініл, хіноксалініл, піразоліл, індоліл, бензоттак далі. Термін "циклоалкіл" означає моноциклічриазоліл, фураніл, тієніл, бензотієніл, бензофурану насичену аліфатичну вуглеводневу групу, що ніл, хінолініл, ізохінолініл, оксазоліл, ізоксазоліл, має визначене число атомів вуглецю. Наприклад, індоліл, піразиніл, піридазиніл, піридиніл, піримі"циклоалкіл" включає циклопропіл, метилциклоп 21 74560 22 диніл, піроліл, тетрагідрохінолін. Зрозуміло також, товоднева, бромистоводнева, сірчана, сульфаміщо, як у випадку наведеного нижче визначення нова, фосфорна, азотна тощо, а також солі, отригетероциклу, "гетероарил" включає також Nмані з органічних, кислот, таких як оцтова, пропіооксидне похідне будь-якого азотовмісного гетеронова, бурштинова, гліколева, стеаринова, арилу. У випадках, коли гетероарильний замісник молочна, яблучна, винна, лимонна, аскорбінова, є біциклічним і одне кільце є неароматичним або памоєва, малеїнова, гідроксималеїнова, фенілоцне містить гетероатоми, зрозуміло, що приєднання това, глутамінова, бензойна, саліцилова, сульфавідбувається через ароматичне кільце або через нілова, 2-ацетоксибензойна, фумарова, толуолсукільце, що містить гетероатом, відповідно. льфонова, метансульфонова, етандисульфонова, Мається на увазі, що, як прийнято фахівцями в щавлева, ізетіонова, трифтороцтова тощо. даній галузі, термін "галоген", використовуваний У деяких випадках R7 і R8 мають такі значення, тут, включає хлор, фтор, бром і йод. Мається на що вони можуть бути узяті разом з азотом, до якоувазі, що термін "гетероцикл" або "гетероцикліл", го вони приєднані, з утворенням моноциклічного використовуваний тут, означає 5-10-членний ароабо біциклічного гетероциклу з 5-7 членами в кожматичний або неароматичний гетероцикл, що місному кільці, що містить, необов'язково, крім азоту, тить від 1 до 4 гетероатомів, вибраних із групи, що один або два додаткових гетероатоми, вибраних із складається з О, N і S, і включає біциклічні групи. Ν, Ο і S, причому зазначений гетероцикл, необо"Гетероцикліл", отже, включає вищевказані гетев'язково, заміщений одним або декількома замісроарили, а також їхні дигідро- і тетрагідроаналоги. никами, вибраними з R6a. Приклади гетероциклів, Наступні приклади "гетероциклілу" включають, але які таким чином можуть бути утворені, включають, не обмежуються такими гетероциклілами: бензоіале не обмежуються наступними гетероциклами, мідазоліл, бензофураніл, бензофуразаніл, бензоберучи до уваги, що гетероцикл необов'язково піразоліл, бензотриазоліл, бензотіофеніл, бензокзаміщений одним або декількома замісниками, сазоліл, карбазоліл, карболініл, цинолініл, вибраними з R6a: фураніл, імідазоліл, індолініл, індоліл, індолазиніл, індазоліл, ізобензофураніл, ізоіндоліл, ізохіноліл, ізотіазоліл, ізоксазоліл, нафтпіридиніл, оксадіазоліл, оксазоліл, оксазолін, ізоксазолін, оксетаніл, піраніл, піразиніл, піразоліл, піридазиніл, піридопіридиніл, піридазиніл, піридин, піримідил, піроліл, хіназолініл, хіноліл, хіноксалініл, тетрагідропіраніл, тетразоліл, тетразолопіридил, тіадіазоліл, тіазоліл, тієніл, триазоліл, азетидиніл, 1,4-діоксаніл, гексагідроазепініл, піперазиніл, піперидиніл, піролідиніл, морфолініл, тіоморфолініл, дигідробензоімідазоліл, дигідробензофураніл, дигідробензотіофеніл, дигідробензоксазоліл, дигідрофураніл, дигідроімідазоліл, дигідроіндоліл, дигідроізооксазоліл, дигідроізотіазоліл, дигідрооксадіазоліл, дигідрооксазоліл, дигідропіразиніл, дигідропіразоліл, дигідропіридиніл, дигідропіримідиніл, дигідропіроліл, дигідрохінолініл, дигідротетразоліл, дигідротіадіазоліл, дигідротіазоліл, дигідротієніл, дигідротриазоліл, дигідроазетидиніл, метилендіоксибензоїл, тетрагідрофураніл і тетрагідротієніл і їхні N-оксиди. Приєднання гетероцикПереважно, R1 представляє Η. Переважним є лільного замісника може здійснюватися через також визначення R2 і R3 як Н. Переважно, R5 атом вуглецю або через гетероатом. представляє Н. Переважними гетероциклільними Алкільні, алкенільні, алкінільні, циклоалкільні, замісниками є замісники, показані тільки що, плюс арильні, гетероарильні і гетероциклільні замісники піридин, піримідин, піразин, піридазин, тетраметиможуть бути заміщеними або незаміщеними, якщо ленсульфон, бутиролактон, тетрагідрофуран, фуне зазначено конкретно інше. Наприклад, (С1ран, індол і тіофен. Переважно, t дорівнює 1 і R4 є С6)алкіл може бути заміщений одним, двома або замісником у 5-положенні індолу згідно з такою трьома замісниками, вибраними з ОН, оксо, галосхемою нумерації: гену, алкокси, діалкіламіно або гетероциклілу, такого як морфолініл, піперидиніл і так далі. У цьому випадку, якщо одним замісником є оксо, а іншим є ОН, у визначення включені такі групи:(С=О)СН2СН(ОН)СН3,-(С=О)ОН,-СН(ОН)СН2СН(О) і так далі. Фармацевтично прийнятні солі сполук даного Переважно, R4 представляє ОС1винаходу включають загальноприйняті нетоксичні 7 8 С6алкіленNR R , (С=O)аС0-С6алкілен-Q, де Q солі сполук даного винаходу, утворювані неорганіпредставляє Н, ОН, СО2Н або ОС1-С6алкіл, ОС0чними або органічними кислотами. ЗагальноприйС6алкіленгетероцикліл, необов'язково заміщений няті нетоксичні солі включають, наприклад, солі, замісниками від одного до трьох, вибраних із R6a, отримані з неорганічних кислот, таких як хлорис 23 74560 C0-С6алкіленNR7R8, (C=O)NR7R8 або ОС1С3алкілен(С=О)NR7R8. Найбільш переважно, R4 представляє С1-С3алкіленNR7R8. Переважно, R7 і R8 мають таке значення, що вони повинні бути взяті разом з азотом, до якого вони приєднані, з утворенням моноциклічного 5-7-членного гетероциклу, що містить, необов'язково, крім азоту, один або два додаткових гетероатоми, вибраних із Ν, Ο і S, причому зазначений гетероцикл, необов'язково, заміщений одним або декількома замісниками, вибраними з R6a. Фармацевтично прийнятні солі сполук даного винаходу можна синтезувати зі сполук даного винаходу, які містять основну або кислотну частину, загальноприйнятими хімічними способами. Звичайно солі основних сполук одержують або іонообмінною хроматографією, або взаємодією вільної основи зі стехіометричними кількостями або з надлишком необхідної солетвірної неорганічної або органічної кислоти в підходящому розчиннику або різних комбінаціях розчинників. Аналогічно цьому, солі кислотних сполук одержують взаємодією з підходящою неорганічною або органічною основою. Сполуки даного винаходу можна одержати за допомогою реакцій, показаних на наступних схемах, на додаток до інших стандартних маніпуляцій, які відомі в літературі або зазначені як приклади в експериментальних процедурах. Ці схеми, отже, не обмежуються перерахованими сполуками або будь-якими конкретними замісниками, використовуваними для ілюстративних цілей. Нумерація замісника, як показано на схемах, не обов'язково корелює з нумерацією, використаною у формулі винаходу. Схеми Як показано на схемі А, хіноліновий реагент А2 можна синтезувати відомими методиками, зазначеними в Marsais, F.; Godard, Α.; Queguiner, G.J. Heterocyclic Chem. 1989, 26, 1589-1594). Похідні із заміщенням, що змінюється, можна одержати за допомогою модифікації даної процедури і використання стандартних синтетичних протоколів, відомих у даній галузі. Крім того, на схемі 1 показане одержання індольного проміжного продукту А-6. Схема В ілюструє один можливий протокол для сполучення індольного і хінолонового проміжних продуктів для одержання необхідних сполук. Схема С ілюструє один можливий синтетичний шлях для синтезу сполуки даного винаходу, 3-(5метокси-1Н-піроло[2,3-с]піридин-2-іл)-1Н-хінолін-2ону, С-6. Схема D показує синтез йоднафтиридинів і йодпіридопіридинів. Йодсполуки, що утворилися, можна сполучати з підходящою індолбороновою кислотою, як зазначено в інших схемах, для одержання необхідного продукту. Вихідні хлорсполуки можна одержати за способом, зазначеним DJ. Рокоту and W.W. Paudler в J. Org. Chem. 1972, 37, 3101. 24 25 74560 26 рит і рахіти, відомі також як онкогенна остеомаляція. (Hasegawa et al., Skeletal Radiol., 28, pp. 41-45, 1999; Gerber et al., Nature Medicine, Vol. 5, №6, pp. 623-628, June 1999). І оскільки VEGF безпосередньо стимулює резорбцію остеокластичних кісток за допомогою KDR/Flk-1, експресованих у зрілих остеокластах (FEBS Let. 473: 161-164 (2000); Endocrinology, 141: 1667 (2000), дані сполуки є також корисними при лікуванні і профілактиці станів, що відносяться до резорбції кісток, таких як остеопороз і хвороба Педжета. Заявлені сполуки можна також використовувати для ослаблення або запобігання ушкодження тканини, яке має місце після випадків церебральної ішемії, таких як удар, зниженням церебрального набряку, ушкодження тканини і реперфузійного ушкодження після ішемії (Drug News Perspect 11: 265-270 (1998); J. Clin. Invest. 104: 16131620(1999)). Сполуки даного винаходу можна вводити ссавцям, переважно, людям, або окремо, або, що краще, у комбінації з фармацевтично прийнятними носіями або розріджувачами, необов'язково, з відомими ад'ювантами, такими як галуни, у фармацевтичній композиції у відповідності зі стандартною фармацевтичною практикою. Сполуки можна вводити перорально або парентерально, включаючи внутрішньовенний, внутрішньом'язовий, внутрішньочеревний, підшкірний, ректальний і місцевий шляхи введення. Для перорального використання хіміотерапевтичної сполуки за даним винаходом сполуку можна ввести, наприклад, у формі таблеток або капсул або у вигляді водного розчину або суспензії. У випадку таблеток для перорального використання носії, які звичайно використовують, включають лактозу і кукурудзяний крохмаль, і звичайно додають змащувальні агенти, такі як стеарат магнію. Для перорального введення у формі капсул придатні розріджувачі включають лактозу і висушений кукурудзяний крохмаль. Коли для перорального використання потрібні водні суспензії, активний інгредієнт змішують з емульгуючими і суспендуючими агентами. При бажанні можна додати деякі Дані сполуки можна використовувати як фарпідсолоджуючі агенти і/або коригенти. Для внутрімацевтичні агенти для ссавців, особливо для люшньом'язового, внутрішньочеревного, підшкірного і дей, при лікуванні захворювань, залежних від тивнутрішньовенного використання звичайно одеррозинкіназ. Такі захворювання включають жують стерильні розчини активного інгредієнта, і проліферацію пухлинних клітин, патологічне утвоpH розчинів слід регулювати придатним способом, рення нових судин (або розвиток кровоносних суа розчини потрібно забуферити. Для внутрішньодин), що сприяють росту солідних пухлин, утвовенного введення загальну концентрацію розчинерення нових очних судин (діабетична ретинопатія, них речовин слід регулювати, щоб зробити препапов'язана з віком дегенерація жовтої плями тощо) і рат ізотонічним. запалення (псоріаз, ревматоїдний артрит тощо). Сполуки даного винаходу можна також вводиСполуки даного винаходу можна вводити паціти разом з іншими добре відомими терапевтичниєнтам для використання при лікуванні раку. Дані ми агентами, які вибирають за їхньою конкретною сполуки інгібують розвиток кровоносних судин пупридатністю проти стану, що піддається лікуванхлин, тим самим впливаючи на ріст пухлин (J. Rak ню. Наприклад, у випадку, пов'язаному з кістковим et al. Cancer Research, 55: 4575-4580, 1995). порушенням, комбінації, що будуть придатними, Здатність даних сполук діяти проти розвитку включають комбінації з антирезорбційними бісфокровоносних судин є також придатною при лікусфонатами, такими як алендронат і ризедронат; ванні деяких форм сліпоти, зв'язаних з ретинальблокаторами інтегрину (подальші визначення дані ним новоутворенням кровоносних судин. нижче), такими як v 3-антагоністи; кон'югованими Описані сполуки є також придатними при лікуестрогенами, використовуваними в гормональній ванні деяких захворювань, пов'язаних із кістковою замісній терапії, такими як PREMPRO®, патологією, таких як остеокарцинома, остеоаритPREMARIN® і ENDOMETRION®; селективними 27 74560 28 модуляторами рецептора естрогену (SERMs), тадиметилксантин, зорубіцин, ідарубіцин, бісантрен, кими як ралоксифен, дролоксифен, СР-336156 мітоксантрон, пірарубіцин, пінафід, валрубіцин, (Pfizer) і лазофоксифен; інгібіторами катепсину К амрубіцин, антинеопластон, 3'-деаміно-3'та інгібіторами АТФ-протонних помп. морфоліно-13-деоксо-10-гідроксикарміноміцин, Дані сполуки придатні також у комбінації з віанаміцин, галарубіцин, елінафід, MEN10755 і 4домими протираковими агентами. Такі відомі продеметокси-3-деаміно-3-азиридиніл-4тиракові агенти включають наступні агенти: модуметилсульфоніл-даунорубіцин. лятори рецептора естрогену, модулятори Приклади інгібіторів мікротубуліну включають рецептора андрогену, модулятори рецептора репаклітаксел, віндезинсульфат, 3',4'-дидегідро-4'тиноїдів, цитотоксичні агенти, антипроліферативні деокси-8'-норвінкалеукобластин, доцетаксол, риагенти, інгібітори пренілпротеїнтрансферази, інгізоксин, доластатин, мівобулін ізетіонат, ауристабітори HMG-CoA-редуктази, інгібітори ВІЛтин, цемадотин, RPR109881, BMS184476, вінфлупротеази, інгібітори зворотної транскриптази та нін, криптофіцін, 2,3,4,5,6-пентафтор-R-(3-фтор-4інші інгібітори розвитку кровоносних судин. метоксифеніл)-бензол-сульфонамід, ангідровінб"Модулятори рецептора естрогену" відносятьластин, трет-бутиламід N,N-диметил-L-валіл-Lся до сполук, які перешкоджають зв'язуванню естваліл-R-метил-L-валіл-L-проліл-L-проліну, TDX258 рогену з рецептором або інгібують таке зв'язувані BMS188797. ня, незалежно від механізму. Приклади Деякими прикладами інгібіторів топоізомерази модуляторів рецептора естрогену включають, але є топотекан, гікаптамін, тринотекан, рубітекан, 6не обмежуються ними, тамоксифен, ралоксифен, етоксипропіоніл-3',4'-О-екзоідоксифен, LY353381, LY117081, тореміфен, фубензиліденхартреузин, 9-метокси-N,N-диметил-5львестрант, 4-[7-(2,2-диметил-1-оксопропокси-4нітротразоло[3,4,5-k1]акридин-2(6Н)пропанамін, 1метил-2-[4-[2-(1-піперидиніл)етокси]феніл]-2Н-1аміно-9-етил-5-фтор-2,3-дигідро-9-гідрокси-4бензотран-3-іл]феніл-2,2-диметилпропаноат, 2,4метил-1Н,12Н-бензо[dе]пірано-[3',4':b,7]динітрофенілгідразон 4,4'-дигідроксибензофенону і індолізино[1,2b]хінолін-10,13(9Н,15Н)діон, луртоSH646. текан, 7-[2-(N-ізопропіламіно)-етал]"Модулятори рецептора андрогену" відносять(20S)камптотецин, BNP1350, BNPI1100, BN80915, ся до сполук, які перешкоджають зв'язуванню андBN80942, етопозид-фосфат, теніпозид, собузокрогену з рецептором або інгібують таке зв'язувансан, 2'-диметиламіно-2'-деоксіетопозид, GL331, Nня, незалежно від механізму. Приклади [2-(диметиламіно)етил]-9-гідрокси-5,6-диметил-6Нмодуляторів рецептора андрогену включають фіпіридо[4,3-b]-карбазол-1-карбоксамід, азулакрин, (5а,5аb,8аа,9b)-9-[2-[N-[2-(диметиламiно)етил]-Rнастерид та інші інгібітори 5 -редуктази, нілутамід, метиламіно]етил]-5-[4-гідрокси-3,5флутамід, бікалутамід, ліарозол і абіратеронацедиметоксифеніл]-5,5а,6,8,8а,9-гексагідрофуротат. (3',4':6,7)нафто-(2,3-d)-1,3-діоксол-6-он, 2,3"Модулятори рецептора ретиноїдів" відносять(метилендіокси)-5-метил-7-гідрокси-8ся до сполук, які перешкоджають зв'язуванню реметоксибензо[с]фенантридиній, 6,9-біс-[(2тиноїдів із рецептором або інгібують таке зв'язуаміноетил)-аміно]бензо[g]ізогуїнолін-5,10-діон, 5вання, незалежно від механізму. Приклади таких (3-амінопропіламіно)-7,10-дигідрокси-2-(2модуляторів рецептора ретиноїдів включають бекгідроксіетиламінометил)-6Н-піразоло[4,5,1саротен, третиною, 13-цис-ретиноєву кислоту, 9dе]акридин-6-он, N-[1-[2-(діетиламіно)етиламіно]-7цис-ретиноєву кислоту, -дифторметилорнітин, метокси-9-оксо-9Н-тіоксантен-4-ілметил]формамід, ILX23-7553, транс-N-(4'-гідроксифеніл)-ретинамід, R-(2-(диметиламіно)етил)акридин-4-карбоксамід, N-4-карбоксифенілретинамід. 6-[[2-(диметиламіно)етил]аміно]-3-гідрокси-7Н"Цитотоксичні агенти" відносяться до сполук, індено[2,1-с]хінолін-7-он і димесна. які викликають загибель клітин, головним чином "Антипроліферативні агенти" включають антиперешкодою безпосередньо функціонуванню клісмислові РНR- і ДНR-олігонуклеотиди, такі як тин або інгібують клітинний міоз або перешкоджаG3139, ODN698, RVASKRAS, GEM231 і INX3001, і ють клітинному міозу, включаючи алкілуючі агенти, антиметаболіти, такі як еноцитабін, кармофур, фактори некрозу пухлин, інтеркалатори, інгібітори тегафур, пентостатин, доксифлуридин, триметрекмікротубуліну та інгібітори топоізомерази. сат, флударабін, капецитабін, галоцитабін, цитаПриклади цитотоксичних агентів включають, рабін окфосфат, фостеабін натрій гідрат, ралтитале не обмежуються ними, тирапазимін, сертерексед, палтитрексид, емітефур, тіазофурин, неф, кахектин, іфозфамід, тазонермін, лонідамін, децитабін, нолатрексед, пеметрексед, нелзарабін, карбоплатин, алтретамін, преднімустин, дибром2'-деокси-2'-метиліденцитидин, 2'-фторметилен-2'дульцит, ранімустин, фотемустин, недаплатин, деоксицитидин, R-[5-(2,3-дигідрооксаліплатин, темозоломід, гептаплатин, естрамубензофурил)сульфоніл]-N'-(3,4стин, імпросульфан тозилат, трофосфамід, нимусдихлорфеніл)сечовина, N6-[4-деокси-4-[N2тин, диброспідій хлорид, пумітера, лобаплатин, [2(Е),4(Е)-тетрадекадієноїл]глициламіно]-Lсатраплатин, профіроміцин, цисплатин, ірофульгліцеро- -L-маногептопіранозил]-аденін, аплідин, вен, дексифосфамід, цис-аміндихлор(2ектеїнасцидин, троксацитабін, 4-[2-аміно-4-оксометилпіридин)платина, бензилгуанін, глюфосфа4,6,7,8-тетрагідро-3Н-піримідино[5,4-b][1,4]тіазинмід, GPX100, (транс, транс, транс)-біс-мю-(гексан6-іл-(S)-етил]-2,5-тієноїл-L-глутамінова кислота, 1,6-діамін)-мюаміноптерин, 5-фторурацил, аланозин, 11-ацетил(діамінплатина(ІІ)]біс[діамін(хлор)платина(ІІ)]8-(карбамоїлоксиметил)-4-форміл-6-метокси-14тетрахлорид, діаризидинілспермін, триоксид миокса-1,11-діаза-тетрацикло(7.4.1.0.0)тетрадекаш'яку, 1-(11-додециламіно-10-гідроксіундецил)-3,7 29 74560 30 2,4,6-трієн-9-іловий ефір оцтової кислоти, швайнВ інгібіторах HMG-CoA-редуктази, де може іссонін, лометрексол, дексразоксан, метіоніназа, 2'нувати форма кислоти, утвореної розмиканням кільця, солі та ефіри можна, переважно, одержати ціано-2'-деокси-N4-пальмітоїл-1- -Dз кислоти, утвореної розмиканням кільця, і всі такі арабінофуранозилцитозин і тіосемікарбазон 3форми включені в значення використовуваного тут амінопіридин-2-карбоксальдегіду. "Антипроліфетерміна "інгібітор HMG-CoA-редуктази". Інгібітор ративні агенти" включають також моноклональні HMG-CoA-редуктази, переважно, вибраний з лоантитіла до факторів росту, інші, ніж антипроліфевастатину і симвастатину, кращим є симвастатин. ративні агенти, перераховані як "інгібітори розвитТут термін "фармацевтично прийнятні солі" у відку кровоносних судин", такі як трастузумаб і гениношенні інгібітора HMG-CoA-редуктази буде ознасупресори пухлин, такі як р53, які можна одержати чати нетоксичні солі сполук, використовуваних у за допомогою перенесення опосередкованого реданому винаході, які звичайно одержують взаємокомбінантним вірусом гена (див., наприклад, падією вільної кислоти з підходящою органічною або тент США №6069134). неорганічною основою, особливо основами, утвоІнгібітори "НМО-СоА-редуктази" відносяться реними з таких катіонів, як натрій, калій, алюміній, до інгібіторів 3-гідрокси-3-метилглутарил-СоАкальцій, літій, магній, цинк і тетраметиламоній, а редуктази. Сполуки, які володіють інгібуючою актакож такі солі, утворені з амінів, таких як амоній, тивністю для HMG-CoA-редуктази, можна легко етилендіамін, N-метилглюкамін, лізин, аргінін, орідентифікувати за допомогою використання аналінітин, холін, Ν,Ν'-дибензил-етилендіамін, хлорпрозів, добре відомих у даній галузі. Див., наприклад, каїн, діетаноламін, прокаїн, N-бензиланалізи, описані або цитовані в патенті США фенетиламін, 1-п-хлорбензил-2-піролідин-1'4231938, стовпчик 6, і WO 84/02131 на pp. 30-33. ілметилбензімідазол, діетиламін, піперазин і Терміни "HMG-CoA-редуктази інгібітор" і "інгібітор трис(гідроксиметил)амінометан. Такі приклади HMG-CoA-редуктази" мають однакове значення, солей інгібіторів HMG-CoA-редуктази можуть коли їх використовують тут. включати, але не обмежуються ними, ацетат, бенПриклади інгібіторів HMG-CoA-редуктази, які золсульфонат, бензоат, бікарбонат, бісульфат, можна використовувати, включають, але не обмебітартрат, борат, бромід, кальційедетат, камсилат, жуються ними, ловастатин (MEVACOR®; див. пакарбонат, хлорид, клавуланат, цитрат, дигідрохлотенти США №№4231938; 4294926; 4319039), симрид, едетат, едисилат, естолат, езилат, фумарат, вастатин (ZOCOR®; див. патенти США №4444784; глюцептат, глюконат, глутамат, гліколіларсанілат, 4820850; 4916239), правастатин (PRAVACHOL®; гексилрезорцинат, гідрабамін, гідробромід, гідрохдив. патенти №№4346227; 4537859; 4410629; лорид, гідроксинафтоат, йодид, ізотіонат, лактат, 5030447 і 5180589), флувастатин (LESCOL®; див. лактобіонат, лаурат, малат, малеат, манделат, патенти СІЛА №№5354772, 4911165; 4929437; мезилат, метилсульфат, мукат, напсилат, нітрат, 5189164, 5118853, 5290946; 5356896), аторвастаолеат, оксалат, памоат, пальмітат, пантотенат, тин (LIPITOR®; див. патенти США №№5273995; фосфат/дифосат, полігалактуронат, саліцилат, 4681393; 5489691; 5342952) і церівастатин (відостеарат, субацетат, сукцинат, танат, тартрат, теомий також як рівастатин і BAYCHOL®; див. патент клат, тозилат, триетйодид і валерат. США №5177080). Структурні формули зазначених Складноефірні похідні описаних сполук, що є і додаткових інгібіторів HMG-CoA-редуктази, які інгібіторами HMG-CoA-редуктази, можуть діяти як можна використовувати в даних способах, описані проліки, які при абсорбції у кровотік теплокровної на сторінці 87 публікації М. Yalpani, "Cholesterol тварини можуть розщеплюватися таким чином, Lowering Drags", Chemistry and Industry, pp. 85-89 щоб вивільнити лікарський засіб, що дозволяє лі(5 February 1996) і патентах США №№4782084 і карському засобу підвищити терапевтичну ефек4885314. Термін інгібітор HMG-CoA-редуктази, тивність. використовуваний тут, включає всі фармацевтич"Інгібітор пренілпротеїнтрансферази" відноно прийнятні форми лактонів і відповідних їм кисситься до сполуки, яка інгібує будь-який один або лот, утворених розмиканням кільця (тобто де кільбудь-яку комбінацію ферментів пренілпротеїнтраце лактону розмикається з утворенням вільної нсфераз, включаючи фарнезилпротеїнкислоти), а також форми солей і ефірів сполук, які трансферазу (EРТаза), тип І геранілгеранілпротеїволодіють інгібуючою активністю для HMG-CoAнтрансферази (GGPT-аза-І) і тип II геранілгеранілредуктази, і, отже, використання таких солей, ефіпротеїнтрансферази (GGPTaзa-II, яку називають рів, кислот, утворених розмиканням кільця, і лактакож Rab GGPTaзою). Приклади інгібуючих претонів включається до обсягу даного винаходу. нілпротеїнтрансферазу сполук включають (±)-6Ілюстрація лактонової частини і відповідної їй фо[аміно(4-хлорфеніл)(1-метил-1Н-імідазол-5рми кислоти, утвореної розмиканням кільця, навоіл)метил]-4-(3-хлор-феніл)-1-метил-2(1Н)хінолінон, диться нижче як структури І і II. (-)-6-[аміно(4-хлорфеніл)(1-метил-1Н-імідазол-5іл)метил]-4-(3-хлорфеніл)-1-метил-2(1Н)-хінолінон, (+)-6-[аміно(4-хлорфеніл)(1-метил-1Н-імідазол-5іл)-метил]-4-(3-хлорфеніл)-1-метил-2(1Н)хінолінон, 5(S)-H-бутил-1-(2,3-диметил-феніл)-4-[1(4-ціанобензил)-5-імідазолілметил]-2-піперазинон, (S)-1-(3-хлорфеніл)-4-[1-(4-ціанобензил)-5імідазолілметил]-5-[2-(етансульфоніл)метил]-2піперазинон, 5(S)-н-бутил-1-(2-метил-феніл)-4-[1(4-ціанобензил)-5-імідазоліл-метил]-2-піперазинон, 31 74560 32 1-(3-хлорфеніл)-4-[1-(4-ціанобензил)-2-метил-5включають делавіридин, ефавіренц, GS-840, НВ імідазоліл-метил]-2-піперазинон, 1-(2,2Y097, ламівудин, невірапин, AZT, 3ТС, ddC і DDL дифенілетил)-3-[N-(1-(4-ціанобензил)-1Н-імідазол"Інгібітори розвитку кровоносних судин" відно5-ілетил)карбамоїл]піперидин, 4-{5-[4сяться до сполук, які інгібують утворення нових гідроксиметил-4-(4-хлорпіридин-2-ілметил)кровоносних судин, незалежно від механізму. Припіперидин-1-ілметил]-2-метилімідазол-1клади інгібіторів розвитку кровоносних судин ілметил}бензонітрил, 4-(5-[4-гідрокси-метил-4-(3включають, але не обмежуються ними, інгібітори хлорбензил)-піперидин-1-ілметил]-2тирозинкінази, такі як інгібітори рецепторів Flt-1 метилімідазол-1-ілметил}-бензо-нітрил, 4-{3-[4-(2(VEGFR1) і Flk-1/KDR (VEGFR20) тирозинкінази, оксо-2Н-піридин-1-іл)бензил]-3Н-імідазол-4інгібітори виділених з епідерми, виділених з фібілметил}бензо-нітрил, 4-{3-[4-(5-хлор-2-оксо-2Нробластів або виділених із тромбоцитів факторів [1,2']біпіридин-5'-ілметил]-3Н-імідазол-4росту, інгібітори ММР (матричної металопротеази), ілметил}бензонітрил, 4-{3-[4-(2-оксо-2Нблокатори інтегрину, інтерферон-α, інтерлейкін-12, [1,2']біпіридин-5-iлметил]-3Н-імідазол-4пентозанполісульфат, інгібітори циклооксигенази, ілметил}бензонітрил, 4-[3-(2-оксо-1-феніл-1,2включаючи нестероїдні протизапальні засоби дигідропіридин-4-ілметил)-3Н-імідазол-4(NSAIDs), подібні аспірину та ібупрофену, а також ілметил]бензонітрил, 18,19-дигідро-19-оксо-5Н, селективні інгібітори циклооксигенази-2, подібні 17Н-6,10:12,16-диметено-1Н-імідазо[4,3целекоксибу і рофекоксибу (PNAS, Vol. 89, p. 7384 с][1,11,4]діокса-азациклононадецин-9-карбонітрил, (1992); JNCI, Vol. 69, p. 475 (1982); Arch. Opthalmol, (±)-19,20-дигідро-19-оксо-5Н-18,21-етано-12,14Vol. 108, p.573 (1990); Anat. Rec, Vol. 238, p. 68 етено-6,10-метено-22Н-бензо[h]імідазо[4,3-k](1994); FEBS Letters, Vol. 372, p. 83 (1995); Clin, [1,6,9,12]оксатриазациклооктадецин-9Orthop. Vol. 313, p. 76 (1995); J. Mol. Endocrinol, карбонітрил, 19,20-дигідро-19-оксо-5Н,17Н-18,21Vol. 16, p.107 (1996); Jpn. J. Pharmacol, Vol. 75, p. етано-6,10:12,16-диметено-22Н-імідазо[3,4105 (1997); Cancer Res., Vol. 57, p. 1625 (1997); h][1,8,11,14]оксатриазациклоейкозин-9Cell, Vol. 93, p. 705 (1998); Intl. J. Mol. Med., Vol. 2, карбонітрил і (±)-19,20-дигідро-3-метил-19-оксоp. 715 (1998); J. Biol. Chem., Vol. 274, p. 9116 5Н-18,21-етано-12,14-етено-6,10-метено-22Н(1999)), карбоксіамідотриазол, комбретастатин Абензо[d]імідазо[4,34, скваламін, 6-0-(хлорацетилкарбоніл)фумагілол, k][1,6,9,12]оксатриазациклооктадецин-9талідомід, ангіостатин, тропонін-1, антагоністи карбонітрил. ангіотензину II (див. Fernandez et al, J. Lab. Clin. Інші приклади інгібіторів пренілпротеїнтрансMed. 105: 141-145 (1985)) і антитіла до VEGF (див. ферази можна знайти в таких публікаціях і патенNature Biotechnology, Vol. 17, pp. 963-968 (October тах:[ WO 96/30343, WO 97/13813, WO 97/21701, 1999); Kim et al., Nature, 362, 841-844 (1993)). WO 97/23478, WO 97/38665, WO 98/28980, WO Інші приклади інгібіторів розвитку кровоносних 98/29119, WO 95/32987, патенті США №5420245, судин включають, але не обмежуються ними, енпатенті США №5523430, патенті США №5532359, достатин, україн, ранпірназу, ІМ862, 5-метокси-4патенті США №5510510, патенті США №5589485, [2-метил-3-(3-метил-2-бутеніл)-оксираніл]-1патенті США №5602098, публікації Європейського оксаспіро[2,5]окт-6-іл(хлорацетил)карбамат, ацепатенту 0618221, публікації Європейського патентил-динаналін, 5-аміно-1-[[3,5-дихлор-4-(4ту 0675112, публікації Європейського патенту хлорбензоїл)феніл]метил]-1Н-1,2,3-триазол-40604181, публікації Європейського патенту карбоксамід, СМ101, скваламід, комбретастатин, 0696593, WO 94/19357, WO 95/08542, WO RPI4610, NX31838, сульфатований фосфат мано95/11917, WO 95/12612, WO 95/12572, WO пентаози, 7,7-(карбонілбіс[іміно-N-метил-4,295/10514, патенті США №5,661,152, WO 95/10515, піроло-карбоніліміно[N-метил-4,2WO 95/10516, WO 95/24612, WO 95/34535, WO пірол]карбоніліміно]біс-(1,3-нафталіндисульфонат) 95/25086, WO 96/05529, WO 96/06138, WO і 3-[(2,4-диметилпірол-5-іл)метилен]-2-індолінон 96/06193, WO 96/16443, WO 96/21701, WO (SU5416). 96/21456, WO 96/22278, WO 96/24611, WO Використовувані вище "блокатори інтегрину" 96/24612, WO 96/05168, WO 96/05169, WO відносяться до сполук, які селективно створюють 96/00736, патенті США №5,571,792, WO 96/17861, антагонізм, інгібують або протидіють зв'язуванню WO 96/33159, WO 96/34850, WO 96/34851, WO фізіологічного ліганду з v 3-інтегрином, до сполук, 96/30017, WO 96/30018, WO 96/30362, WO які селективно створюють антагонізм, інгібують 96/30363, WO 96/31111, WO 96/31477, WO або протидіють зв'язуванню фізіологічного ліганду 96/31478, WO 96/31501, WO 97/00252, WO з v 5-інтегрином, до сполук, які створюють анта97/03047, WO 97/03050, WO 97/04785, WO гонізм, інгібують або протидіють зв'язуванню фізі97/02920, WO 97/17070, WO 97/23478, WO ологічного ліганду як з v 3-інтегрином, так і v 597/26246, WO 97/30053, WO 97/44350, WO інтегрином, і до сполук, які створюють антагонізм, 98/02436, і патенті США №5532359. Роль інгібітора інгібують або протидіють активності конкретного пренілпротеїнтрансферази в розвитку кровоносних інтегрину(ів), експресованого на ендотеліальних судин див., наприклад, у European J. of Cancer, клітинах капілярів. Термін відноситься також до Vol. 35, №9, pp. 1394-1401 (1999).]. антагоністів інтегринів v 6, v 8, 1 1, 2 1, 5 1, Приклади інгібіторів ВІЛ-протеази включають 6 1 і 6 4. Термін відноситься також до антагонісампренавір, абакавір, CGP-73547, CGP-61755, тів будь-якої комбінації інтегринів v 3, v 5, v 6, DMP-450, індинавір, нелфінавір, типранавір, ритоv 8, 1 1, 2 1, 5 1, 6 1 і 6 4. навір, сакуїнавір, АВТ-378, AG 1776 і BMS-232632. Деякі визначені приклади інгібіторів тирозинкіПриклади інгібіторів зворотної транскриптази нази включають Ν-(трифторметилфеніл)-5 33 74560 34 метилізоксазол-4-карбоксамід, 3-[(2,4лікарем або іншим клініцистом. диметилпірол-5-іл)метиліденіл)індолін-2-он, 17Термін "лікування раку" або "терапія раку" від(аліламіно)-17-деметоксигелданаміцин, 4-(3-хлорноситься до введення ссавцю, ураженому злоякіс4-фторфеніламіно)-7-метокси-6-[3-(4ним утворенням, і відноситься до дії, яка полегшує морфолініл)пропокси]хіназолін, N-(3-еттилфеніл)злоякісний стан знищенням злоякісних клітин, але 6,7-біс-(2-метоксіетокси)-4-хіназолінамін, також до дії, яка призводить до інгібування росту ВIBX1382, 2,3,9,10,11,12-гексагідро-10і/або метастазів ракового утворення. (гідроксиметил)-10-гідрокси-9-метил-9,12-епоксиДаний винахід включає також фармацевтичну 1Н-дііндоло[1,2,3-fg:3',2',1'-k1]піроло[3,4композицію, придатну при лікуванні раку, що і][1,6]бензодіазоцин-1-он, SH268, геністеїн, STI571, включає терапевтично ефективну кількість сполук СЕР2563, 4-(3-хлорфеніламіно)-5,6-диметил-7Нданого винаходу з фармацевтично прийнятними піроло[2,3-d]піримідин-метан-сульфонат, 4-(3носіями або розріджувачами або без них. Придатні бром-4-гідроксифеніл)аміно-6,7-диметоксикомпозиції даного винаходу включають водні розхіназолін, 4-(4'-гідроксифеніл)аміно-6,7чини, що включають сполуки даного винаходу і диметоксихіназолін, SU6668, STI571A, N-4фармакологічно прийнятні носії, наприклад, фізіохлорфеніл-4-(4-піридилметил)-1-фталазинамін і логічний розчин, при рівні pH, наприклад, 7,4. РозEMD121974. чини можна ввести в кровотік пацієнта місцевою Дані сполуки є також корисними, як такі або в ін'єкцією болюсу. комбінації з антагоністами рецептора фібриногену Коли сполуку за даним винаходом вводять у тромбоцитів (GP ІІЬЯІІа), такими як тирофібан, для організм людини, добова доза буде звичайно виінгібування метастазів злоякісних клітин. Пухлинні значатися прописом лікаря з дозуванням, що звиклітини можуть активувати тромбоцити в значній чайно змінюється відповідно до віку, маси і відпомірі за допомогою генерації тромбіну. Ця активація відної реакції конкретного пацієнта, а також асоційована з вивільненням VEGF. Вивільнення серйозності симптомів пацієнта. VEGF збільшує метастази за допомогою збільВ одному наведеному як приклад застосуванні шення екстравазації у місцях адгезії до васкулярссавцю, що піддається лікуванню внаслідок захвоного ендотелію (Amirkhosravi, Platelets, 10, 285рювання раком, вводять придатну кількість сполу292, 1999). Тому дані сполуки можна використовуки. Введення здійснюють у кількості від приблизно вати, як такі або в комбінації з антагоністами GP 0,1мг/кг маси тіла до приблизно 60мг/кг маси тіла в Ilb/IIIa), для інгібування метастазів. Приклади індень, переважно, від 0,5мг/кг маси тіла до приблиших антагоністів рецептора фібриногену включазно 40мг/кг маси тіла в день. ють абциксимаб, ептифібатид, сибрафібан, ламіАналізи фібан, лотрафібан, кромобіфан і СТ50352. Сполуки даного винаходу, описані в приклаЯкщо такі продукти комбінацій виготовлені у дах, випробовували із застосуванням аналізів, вигляді встановленої дози, у них використовують описаних нижче, і було виявлено, що вони володісполуки даного винаходу в діапазоні доз, описаних ють інгібуючою кіназу активністю. Інші аналізи є нижче, разом з іншим фармацевтично активним відомими в літературі і можуть бути легко провеагентом у межах його схваленого діапазону доз. дені фахівцем у даній галузі (див., наприклад, Сполуки даного винаходу можна в альтернативDhanabal et al.. Cancer Res. 59: 139-197; Xin et al., ному випадку використовувати послідовно з відоJ. Biol. Chem. 274: 9116-9121; Sheu et al., мим фармацевтично прийнятним агентом(ами), Anticancer Res. 18: 4435-4441; Ausprunk et al., Dev. коли готова препаративна форма у вигляді комбіBiol. 38: 237-248; Gimbrone et al., J. Natl. Cancer нації є непридатною. Inst. 52: 413-427; Nicosia et al., In Vitro 18: 533-549). Термін "введення" і його варіанти (наприклад, І. Аналіз рецепторної кінази VEGF "введення" сполуки) у відношенні до сполуки виАктивність рецепторної кінази VEGF вимірюнаходу означає введення сполуки або проліків ють введенням міченого радіоактивним ізотопом сполуки в організм тварини, що потребує такого фосфату до субстрату (поліглутамінова кислота, лікування. Коли сполуку винаходу або її проліки тирозин, 4:1) (pEY). Фосфорилований продукт pEY виготовляють у комбінації з одним або декількома уловлюють на мембранному фільтрі і включення іншими активними агентами (наприклад, цитотокміченого радіоактивним ізотопом фосфату кількіссичним агентом і так далі), зрозуміло, що термін но визначають сцинтиляційним лічильником. "введення" і його варіанти, кожний, включають Рецепторна кіназа VEGF одночасне і послідовне введення сполуки або її Домени внутрішньоклітинної тирозинкінази проліків та інших агентів. людини KDR (Terman, B.I. et al. Oncogene (1991) Мається на увазі, що використовуваний тут vol. 6, pp. 1677-1683) і Flt-1 (Shibuya, M. et al. термін "композиція" містить продукт, що включає Oncogene (1990) vol. 5, pp. 519-524) були клоновапевні інгредієнти у визначених кількостях, а також ні як злиті білки гена глутатіон-3-трансферази будь-який продукт, який є результатом отриманої (GST). Це здійснювали клонуванням цитоплазмабезпосереднім або непрямим способом комбінації тичного домену кінази KDR, як у рамковому злитті певних інгредієнтів у визначених кількостях. біля карбоксильного кінця гена GST. Розчинні реТермін "терапевтично ефективна кількість", комбінантні злиті білки домену GST-кінази були використовуваний тут, означає, що кількість актиекспресовані в клітинах комахи Spodoptera вної сполуки або фармацевтичного агента, який frugiperda (Sf21) (Invitrogen) із використанням веквикликає біологічну або медичну відповідну реактора експресії вакуловірусу (pAcG2T, Pharmingen). цію в тканині, системі, організмі тварини або люІнші використовувані матеріали і їхні суміші дини, встановлюється дослідником, ветеринаром, були такими: 35 74560 36 Буфер для лізису: 50мМ Трис, pH 7,4, 0,5Μ фільтрування. NaCl, 5мМ DTT, 1мМ ЕДТА, 0,5% тритон Х-100, 8. Аспірують і промивають 3 рази розчином 10% гліцерин, 10мг/мл кожного лейпептину, пепсдля промивання. татину та апротиніну, і 1мМ фенілметил9. Додають 30мкл коктейлю для сцинтиляції, сульфонілфторид (всі від Sigma). герметизують планшет і підрахунок проводять у Буфер для промивання: 50мМ Трис, pH 7,4, сцинтиляційному лічильнику Wallac Microbeta. 0,5Μ NaCl, 5мМ DTT, 1мМ ЕДТА, 0,05% тритон ХII. Аналіз мітогенезу ендотеліальних клітин пу100, 10% гліцерин, 10мг/мл кожного лейпептину, пкової вени людини пепстатину та апротиніну, і 1мМ фенілметилЕндотеліальні клітини пупкової вени людини сульфонілфторид. (HUVECs) у культурі проліферують у відповідь на Буфер для діалізу: 50мМ Трис, pH 7,4, 0,5Μ обробку VEGF, і їх можна використовувати як сисNaCl, 5мМ DTT, 1мМ ЕДТА, 0,05% тритон Х-100, тему для аналізу, щоб кількісно визначити впливи 50% гліцерин, 10мг/мл кожного лейпептину, пепскіназних інгібіторів KDR на стимуляцію VEGF. В татину та апротиніну, і 1мМ фенілметилописаному аналізі моношари HUVEC, що знахосульфонілфторид. дяться в спокої, обробляють наповнювачем або Буфер для реакції 10Х: 200мМ Трис, pH 7,4, випробовуваною сполукою за 2 години до дода1,0Μ NaCl, 50мМ МnСl2, 10мМ DTT і 5мг/мл бичавання VEGF або основного фактора росту фібробчого сироваткового альбуміну (Sigma). ластів (bFGF). Мітогенну відповідну реакцію на Буфер для розведення ферменту: 50мМ Трис, VEGF або bFGF визначають вимірюванням вклюpH 7,4, 0,1Μ NaCl, 1мМ DTT, 10% гліцерин, чення [3Н]-тимідину в клітинну ДНК. 100мг/мл BSA. Матеріали Субстрат 10 X: 750мкг/мл полі(глутамінова киHUVECs: HUVECs, заморожені у вигляді ізоляслота, тирозин, 4:1) (Sigma). тів первинних культур, одержували від Clonetics Розчин для зупинки взаємодії: 30% трихлороцCorp. Клітини витримують у середовищі для ендотова кислота, 0,2Μ пірофосфат натрію (обидва від теліального росту (EGM; Clonetics) і використовуFisher). ють для мітогенних аналізів, описаних у наведених Розчин для промивання: 15% трихлороцтова нижче пасажах 3-7. кислота, 0,2Μ пірофосфат натрію. Культуральні планшети: 96-ямкові полістироПланшети для фільтрування: 96-ямковий льні планшети для культур тканин NUNCLON планшет із скляним волокном GF/C (NUNC #167008). Millipore#MAFCNOB. Середовище для аналізу: модифіковане за Спосіб способом Дульбекко середовище Ігла, що містить А. Очищення білка 1 г/мл глюкози (low-glucose DMEM; Mediatech) 1. Клітини Sf21 інфікували рекомбінантним віплюс 10% (об./об.) фетальної бичачої сироватки русом при множинності інфекції 5 вірусних час(Clonetics). ток/клітину і вирощували при 27°С протягом 48 Випробовувані сполуки: Робочі вихідні розчини годин. випробовуваних сполук розводять послідовно в 2. Усі стадії проводили при 4°С. Інфіковані клі100% диметилсульфоксиді (ДМСО) до концентратини збирали центрифугуванням при 1000xg і ліції, яка у 400 разів вище, ніж їхні необхідні кінцеві зували при 4°С протягом 30 хвилин з 1/10 об'ємом концентрації. Кінцеві розведення до концентрації буфера для лізису з наступним центрифугуванням ЇХ проводять безпосередньо в середовищі для при 100000xg протягом 1 години. Супернатант аналізу безпосередньо перед додаванням клітин. потім пропускали через колонці глутатіонової сеФактори росту 10Х: Розчини VEGF165 фарози (Pharmacia), урівноваженої в буфері для (500нг/мл; R&D Systems) і bFGF (10нг/мл; R&D лізису, і промивали 5 об'ємами того ж самого буSystems) людини одержують у середовищі для фера і потім 5 об'ємами буфера для промивання. аналізу. Рекомбінантаий білок GST-KDR елюювали систе10Х [3Н]-тимідин: [Метил-3Н]тимідин мою буфер для промивання/10мМ відновлений (20Ku/ммоль; Dupont-NEN) розводять до глутатіон (Sigma) і діалізували проти буфера для 80мкКu/мл у DMEM з низькою концентрацією глюдіалізу. кози. В. Аналіз рецепторної кінази VEGF Середовище для промивання клітин: збалан1. Додають 5мкл інгібітора або контролю до сований сольовий розчин Ханка (Mediatech), що суміші для аналізу в 50% ДМСО. містить 1мг/мл бичачого сироваткового альбуміну 2. Додають 35мкл реакційної суміші, що міс(Boehringer-Mannheim). тить 5мкл буфера для реакції 10Х, 5мкл 25мМ Розчин для лізису клітин: 1н. NaOH, 2% (мас/ АТФ/10мкКu [33Р]АТФ (Amersham) і 5мкл субстрату об.) Na2CO3. 10Х. Спосіб 3. Починають взаємодію додаванням 10мкл 1. Моношари HUVEC, витримані в EGM, одерKDR (25нм) у буфері для розведення ферменту. жують трипсинізацією і висівають при щільності 4. Проводять змішування та інкубування при 4000 клітин на 100мкл середовища для аналізу в кімнатній температурі протягом 15 хвилин. 96-ямкових планшетах. Ріст клітин затримують 5. Зупиняють взаємодію додаванням 50мкл протягом 24 годин при 37°С у зволоженій атмосрозчину для зупинки взаємодії. фері, що містить 5% СО2. 6. Проводять інкубування протягом 15 хвилин 2. Середовище для затримки росту заміняють при 4°С. на 100мкл середовища для аналізу, що містить 7. Переносять 90мкл аліквоту в планшет для або наповнювач (0,25% [об./об.] ДМСО), або ви 37 74560 38 пробовувану сполуку з необхідною кінцевою конацетонітрилі (300мл) перемішують при 23°С в тецентрацією. Усі визначення проводять у трьох помряві протягом 20 годин. Реакційну суміш конценвторах. Клітини потім інкубують при 37°С з 5% СО2 трують насухо і жовту тверду речовину, що утвопротягом 2 годин, щоб дозволити випробовуваним рилася, розподіляють між насиченим водним сполукам проникнути до клітин. розчином бікарбонату натрію і дихлорметаном. 3. Після 2-годинного періоду попередньої обОрганічний шар промивають водою, потім сушать робки клітини стимулюють додаванням 10мкл/ямку над сульфатом магнію і концентрують, при цьому або середовища для аналізу, розчину VEGF 10X одержуючи 2-хлор-3-йодхінолін у вигляді блідоабо розчину bFGF 10X. Клітини потім інкубують жовтої твердої речовини. 1НЯМР (400МГц, CDCl3) при 37°С і 5% СО2. 8,67 (с, 1Н), 7,99 (шир. д, 1Н, J=8,4Гц), 7,75 (шир. 4. Через 24 години в присутності факторів рост, 1Н, J=7,7Гц), 7,72 (шир. д, 1Н, J=7,8Гц), 7,57 ту додають 10Х [3Н]-тимідин (10мкл/ямку). (шир. т, 1Н, J=7,6Гц). 5. Через три дні після додавання [3Н]-тимідину 5-(трет-Буталдиметилсиланілокси)- 1Н-індол середовище видаляють відсмоктуванням і клітини (1-4) промивають два рази середовищем для промиРозчин 5-гідроксііндолу 1-3 (5,50г, 41,3ммоль, вання клітин (400мкл/ямку, потім 200мкл/ямку). 1еквів.), трет-бутилдиметилсилілхлориду (7,47г, Промиті клітини, що зрослися, потім солюбілізують 49,6ммоль, 1,20еквів.) та імідазолу (7,03г, додаванням розчину для лізису клітин 103ммоль, 2,50еквів.) у Ν,Ν-диметилформаміді (100мкл/ямку) і нагрівають до 37°С протягом 30 (20мл) перемішують при 23°С протягом 20 годин. хвилин. Лізати клітин переносять у 7-мл скляні Реакційну суміш концентрують і залишок розподіпробірки для сцинтиляції, що містять 150мкл води. ляють між етилацетатом і водою. Органічний шар Додають коктейль для сцинтиляційного лічильника промивають водою (3х), потім сушать над сульфа(5мл/пробірку), і пов'язану з клітинами радіоактивтом магнію і концентрують. Залишок очищають ність визначають рідинною сцинтиляційною спектфлеш-колонковою хроматографією (40% дихлорроскопією. метан у гексані, потім 60% дихлорметан у гексані), На підставі вищенаведених аналізів можна при цьому одержуючи 5-(третзробити висновок, що сполуки формули І є інгібібутилдиметилсиланілокси)-1Н-індол у вигляді безторами VEGF і, отже, є придатними для інгібуванбарвного масла, що твердне при стоянні. 1Н ЯМР ня розвитку кровоносних судин, наприклад, при (400МГц, CDCl3) 8,00 (шир. с, 1Н), 7,22 (д, 1Н, лікуванні очної хвороби, наприклад, діабетичної J=8,7Гц), 7,17 (т, 1Н, J=2,8Гц), 7,06 (д, 1Н, ретинопатії, і при лікуванні ракових захворювань, J=2,3Гц), 6,76 (дд, 1Н, J=8,6, 2,3Гц), 6,44 (м, 1Н), наприклад, солідних пухлин. Дані сполуки інгібу1,00 (с, 9Н), 0,19 (с, 6Н). ють VEGF-стимульований мітогенез васкулярних трет-Бутиловий ефір 5-(третендотеліальних клітин людини в культурі з велибутилдиметилсиланілокси)ішюл-1-карбонової кисчинами ІС50 між 0,001 і 5,0мкМ. Дані сполуки виявлоти (1-5) ляють також селективність щодо споріднених тиРозчин 5-(трет-бутилдиметилсиланілокси)-1Нрозинкіназ (наприклад, родини FGFR1 і Src; зв'язок індолу 1-4 (10,2г, 41,3ммоль, 1еквів.), ди-третміж кіназами Src і кіназами VEGFR див. у Еіісеігі et бутилкарбонату (14,4г, 66,0ммоль, 1,60еквів.) і 4al., Molecular Cell, Vol. 4, pp. 915-924, December диметиламінопіридину (1,01г, 3,25ммоль, 1999). 0,200еквів.) у дихлорметані (100мл) перемішують Приклади при 23°С протягом 20 годин. Реакційну суміш конНижченаведені приклади розкривають даний центрують і залишок очищають флеш-колонковою винахід. Використовувані конкретні матеріали, хроматографією (40% дихлорметан у гексанах), типи та умови є ілюстративними для винаходу, при при цьому одержуючи трет-бутиловий ефір 5цьому не обмежуючи його розумний обсяг. (трет-бутилдиметилсиланілокси)індол-1карбонової кислоти (1-5) у вигляді безбарвного масла. 1Н ЯМР (400МГц, CDCl3) 7,96 (шир. д, 1Н, J=7,5Гц), 7,54 (шир. д, 1Н, J=3,1Гц), 6,98 (д, 1Н, J=2,4Гц), 6,83 (дц, 1Н, J=9,0, 2,4Гц), 6,45 (д, 1Н, J=3,7Гц), 1,66 (с, 9Н), 1,00 (с, 9Н), 0,20 (с, 6Н). 1-(трет-Бутоксикарбоніл)-5-{[третбутил(диметил)силіл]окси}-1Н-індол-2-ілборонова кислота (1-6) Розчин трет-бутиллітію в пентані (1,7г, 20,7мл, 35,2ммоль, 1,20еквів.) додають до розчину третбутилового ефіру 5-(трет-бутилдиметилсиланілокси)індол-1-карбонової кислоти (1-5, 10,2г, 29,3ммоль, 1еквів.) у тетрагідрофурані (100мл) при-78°С. Світло-коричневий розчин, що утворився, перемішують при-78°С протягом 30 Схема 1 хвилин, потім додають триметилборат (6,67мл, 2-Хлор-3-йодхінолін (1-2) 58,7ммоль, 2,00 екв.). Суміш, що утворилася, наСуспензію 3-(2-хлор)-хінолінборонової кислоти грівають до 0°С, потім розбавляють насиченим (1-1, 5,05г, 24,3ммоль, 1еквів., отриманий спосоводним розчином хлориду амонію (100мл) і етилобом Marsais, F; Godard, Α.; Queguiner, GJ. вим ефіром (200мл). Водний шар роблять кислотHeterocyclic Chem. 1989, 26, 1589-1594) і Nним водним 10% розчином гідросульфату калію. йодсукциніміду (5,48г, 24,4ммоль, 1,00еквів.) в 39 74560 40 Органічний шар відокремлюють, потім промивають 1,50еквів.) і карбонату цезію (978мг, 3,00ммоль, насиченим розчином солі, сушать над сульфатом 3,00еквів.) у Ν,Ν-диметилформаміді (5мл) нагрімагнію і концентрують. Залишкову жовту тверду вають при 50°С протягом 2 годин. Реакційну суміш речовину розтирають із гексаном, при цьому одеконцентрують і залишок розподіляють між водою ржуючи 1-(трет-бутоксикарбоніл)-5-{[третта етилацетатом. Органічний шар промивають бутил(диметил)силіл]окси}-1Н-індол-2-ілборонову водою, потім насиченим розчином солі, сушать кислоту (1-6) у вигляді не зовсім білої твердої ренад сульфатом магнію і концентрують, при цьому одержуючи блідо-жовту піну. Піну розчиняють у човини. 1Н ЯМР (400МГц, CDCl3) 7,84 (д, 1Н, суміші 1:1 води та оцтової кислоти (60мл) і розчин, J=8,9Гц), 7,37 (с, 1Н), 7,01 (д, 1Н, J=2,4Гц), 6,97 що утворився, нагрівають при 110°С протягом 12 (шир. с, 2Н), 6,88 (дц, 1Н, J=9,0,2,4Гц), 1,73 (с, 9Н), годин. Реакційну суміш концентрують і залишок 1,00 (с, 9Н), 0,20 (с, 6Н). перемішують у водному насиченому розчині бікартрет-Бутил-5-{[третбонату натрію, що дає рудувато-коричневу тверду бутил(диметил)силіл]окси}-2-(2-хлор-3-хінолініл)речовину. Рудувато-коричневу тверду речовину 1Н-індол-1-карбоксилат (1-7) фільтрують, потім суспендують у теплому етанолі Звільнену від кисню суміш 1(трет(2x20мл) і фільтрують, при цьому одержуючи 3-[5бутоксикарбоніл)-5-{[трет(2-піперидин-1-ілетокси)-1Н-індол-2-іл]-1Н-хінолінбутил(диметил)силіл]окси}-1Н-індол-2-боронової 2-он (1-9) у вигляді жовтої твердої речовини. Фількислоти 1-6 (4,10г, 10,5ммоль, 1еквів.), 2-хлор-3трат в етанолі концентрують і залишок очищають йодхіноліну (1-2, 3,64г, 12,6ммоль, 1,20еквів.), фофлеш-колонковою хроматографією (5% етанол, сфату калію (6,67г, 31,4ммоль, 3,00еквів.) і тетранасичений аміаком, в етилацетаті), при цьому кис(трифенілфосфін}паладію (0,605г, 0,524ммоль, одержуючи додаткову кількість 1-9. 0,050еквів.) у діоксані (100мл) нагрівають при 90°С 1 протягом 20 годин. Реакційну суміш охолоджують, Н ЯМР (400MГц, (CD3)2SO) 12,14 (с, 1Н), потім розподіляють між сумішшю води та етилаце11,41 (с, 1Н, 8,50 (с, 1Н), 7,73 (шир. д, 1Н, тату. Органічний шар відокремлюють, промивають J=7,9Гц), 7,51 (шир, т, 1Н, J=7,6Гц), 7,41 (д, 1Н, насиченим розчином солі, сушать над сульфатом J=8,6Гц), 7,37 (шир. д, 1Н, J=3,2Гц), 7,24 (шир. т, магнію і концентрують. Залишок очищають флеш1Н, J=7,7Гц), 7,21 (шир. с, 1Н), 7,06 (шир. с, 1Н), колонковою хроматографією (20% розчин дихлор6,76 (дд, 1Н, J=8,6, 2,2Гц), 4,06 (т, 2Н, J=5,9Гц), метану в гексані, що плавно змінюється до 90% 2,67 (т, 3Н, J=5,5Гц), 2,45 (шир. м, 4Н), 1,51 (шир. дихлорметану в гексані), при цьому одержуючи м, 4Н), 1,39 (шир. м, 2Н). трет-бутил-5-{[трет-бутил(диметил)силіл]окси}-2Сполуки від 1-10 до 1-19, зазначені нижче, і (2-хлор-3-хінолініл)-1Н-індол-1-карбоксилат (1-7) у сполуки від 1-20 до 1-55, наведені нижче в таблиці 1 вигляді піни рудувато-коричневого кольору. Н 1, одержують простими модифікаціями протоколів, описаних вище. Алкілгалогеніди, використовувані ЯМР (400МГц, CDCl3) 8,16 (с, 1Н), 8,15 (д, 1Н, в наступних прикладах, були або комерційно досJ=9,0Гц), 8,07 (д, 1Н, J=8,2Гц), 7,86 (д, 1H, тупними, або отриманими алкілуванням відповідJ=7,8Гц), 7,77 (шир. т, 1Н, J=8,4Гц), 7,60 (шир. т, ного аміну або 1-бром-2-хлоретаном у присутності 1Н, J=8,1Гц), 7,03 (д, 1Н, J=2,4Гц), 6,92 (дц, 1Н, карбонату калію в ацетоні способом Miyahara, Μ.; J=9,0,2,4Гц), 6,55 (с, 1Н), 1,26 (с, 9Н), 1,02 (с, 9Н), Sueyoshi, S.; Kamiya, S. Chem. Pharm. Bull. 1985, 0,23 (с, 6Н). 33, 5557-5561, або 1-бром-3-хлорпропаном у бентрет-Бутил-2-(2-хлор-3-хінолініл)-5-гідроксизолі за способом Adams and Whitmore J. Am. 1H-індол-1-карбоксилат (1-8) Chem. Soc. 1945, 67, 735. У деяких випадках мезиРозчин трет-бутил-5-{[третлати комерційно доступних або легко доступних бутил(диметил)силіл]окси}-2-(2-хлор-3-хінолініл)спиртів одержують (MsCl, Et3N) і використовують 1H-індол-1-карбоксилату 1-7 (2,50г, 4,91ммоль, замість відповідних алкілхлоридів. 1еквів.) і тригідрофториду триетиламіну (3,60мл, 3-[5-(2-Піролідин-1-ілетокси)-1H-індол-2-іл]-1H22,1ммоль, 4,50еквів.) в ацетонітрилі (100мл) пехінолін-2-он (1-10) ремішують при 23°С протягом 20 годин. Реакційну суміш концентрують і залишок розподіляють між насиченим водним розчином бікарбонату натрію та етилацетатом. Органічний шар промивають насиченим розчином солі, сушать над сульфатом магнію і концентрують, при цьому одержуючи третбутил-2-(2-хлор-3-хінолініл)-5-гідрокси-1Н-індол-1карбоксилат (1-8) у вигляді піни рудувато1 коричневого кольору. 1Н ЯМР (400МГц, CDCl3) Н ЯМР (400MГц, (CD3)2SO) 12,14 (с, 1Н), 8,18 (д, 1Н, J=9,0Гц), 8,17 (с, 1Н), 8,07 (д, 1Н, 11,41 (с, 1H), 8,50 (С, 1Н), 7,73 (шир. д, 1Н, J=8,4Гц), 7,86 (д, 1Н, J=8,1Гц), 7,77 (шир. т, 1Н, J=7,7Гц), 7,51 (шир. т, 1Η, J=7,2Гц), 7,41 (д, 1Н, J=8,4Гц), 7,61 (шир. т, 1Н, J=8,1Гц), 7,03 (д, 1Н, J=8,6Гц), 7,37 (шир. д, 1Н, J=8,2Гц), 7,24 (шир. т, J=2,6Гц), 6,93 (дд, 1Н, J=8,8, 2,6Гц), 6,55 (с, 1Н), 1Н, J=7,7Гц), 7,21 (д, 1H, J=1,3Гц), 7,06 (д, 1Н, 1,26 (с, 9Н). J=2,2Гц), 6,76 (дд, 1Н, J=8,6, 2,2Гц), 4,07 (т, 2Η, 3-[5-(2-Піперидин-1-ілетокси)-1Н-індол-2-іл]J=5,9Гц), 2,81 (т, 3Η, J=5,9Гц), 2,55 (шир. м, 4Н), 1Н-хінолін-2-он (1-9) 1,70 (шир. м, 4Н). Суміш трет-бутил-2-(2-хлор-3-хінолініл)-53-[5-(2-Морфолін-4-ілетокси)-1Н-індол-2-іл]гідрокси-1Н-індол-1-карбоксилату 1-8 (395мг, 1Н-хінолін-2-он (1-11) 1,00ммоль, 1еквів.), гідрохлориду 1-(2хлоретил)піперидину (276мг, 1,50ммоль, 41 74560 42 J=8,8Гц), 7,37 (шир. д, 1Н, J=8,2Гц), 7,37 (шир. д, 2Н, J=9,0Гц), 7,32 (шир. т, 2Н, J=7,9Гц), 7,24 (шир. т, 1Н, J=7,9Гц), 7,24 (шир. т, 1Н, J=7,9Гц), 7,20 (д, 1Н, J=2,0Гц), 7,02 (д, 1Н, J=2,2Гц), 6,73 (дд, 1Н, J=8,6, 2,2Гц), 4,05 (т, 2Η, J=6,0Гц), 3,75 (с, 2Н), 3,46 (т, 2Н, J=6,0Гц), 3,23 (с, 3Н), 2,89 (т, 2Η, J=6,2Гц), 2,74 (т, 2Н, J=6,2Гц). 1 Н ЯМР (400MГц, (CD3)2SO) 12,15 (с, 1Η), 3-[5-(2-Діетиламіноетокси)-1Н-індол-2-іл]-1Н11,42 (с, 1Н, 8,51 (с, 1H), 7,73 (шир. д, 1Н, хінолін-2-он (1-15) J=7,9Гц), 7,51 (шир. т, 1Н, J=7,3Гц), 7,41 (д, 1H, J=8,8Гц), 7,37 (шир. д, 1Н, J=8,2Гц), 7,24 (шир. т, 1Н, J=7,6Гц), 7,21 (шир. с, 1Н), 7,07 (д, 1H, J=1,7Гц), 6,76 (дд, 1H, J=8,7, 1,8Гц); 4,09 (т, 2H, J=5,8Гц), 3,59 (шир. т, 4Н, J=4,5Гц), 2,71 (т, 3Н, J=5,7Гц), 2,50 (шир. м, 4Н). 3-[5-(3-Диметиламіно-2-метилпропокси)-1Hіндол-2-іл]-1Н-хінолін-2-он (1-12) 1 Н ЯМР (400MГц, (CD3)2SO) 12,15 (С, 1Н), 11,41 (с, 1H), 8,51 (с, 1Н), 7,73 (шир. д, 1Н, J=7,9Гц), 7,51 (шир. т, 1Н, J=7,9Гц), 7,41 U, 1H, J=8,8Гц), 7,37 (шир. д, 1Н, J=8,1Гц), 7,24 (шир. т, 1Η, J=7,3Гц), 7,21 (шир. с, 1Н), 7,05 (д, 1Н, J=2,2Гц), 6,75 (дд, 1H, J=8,8, 2,4Гц), 4,02 (т, 2Η, J=6,4Гц), 2,79 (т, 2Η, J=6,2Гц), 2,57 (кв., 4Н, J=7,1Гц), 0,99 (т, 6Н, J=7,1Гц). 1 3-{5-[3-(Бензилметиламіно)пропокси]-1Н-індолН ЯМР (400MГц, (CD3)2SO) 12,15 (с, 1Н), 2-іл}-1Н-хінолін-2-он (1-6) 11,41 (с, 1Н), 8,50 (с, 1Н), 7,73 (шир. д, 1Н, J=7,9Гц), 7,51 (шир. т, 1Н, J=8,2Гц), 7,41 (д, 1Н, J=8,8Гц), 7,37 (шир. д, 1Н, J=8,2 Ти), 7,24 (шир. т, 1Η, J=7,9Гц), 7,20 (д, 1Н, J=1,1Гц), 7,03 (д, 1Н, J=2,0Гц), 6,76 (дд, 1Н, J=8,8, 2,4Гц), 3,95 (дд, 1Н, J=9,3, 4,4Гц), 3,77 (дд, 1Н J=9,2, 6,2Гц), 2,31 (м, 1H, 2,15 (с, 6Н), 2,10 (м, 2Н), 1,01 (д, 3Н, J=6,0Гц). 3-[5-(3-Піперидин-1-ілпропокси)-1Н-індол-2-іл]1H-хінолін-2-он (1-13) 1 1 Н ЯМР (400MГц, (CD3)2SO) 12,15 (с, 1Н), 11,41 (с, 1Н), 8,50 (с, 1Н), 7,73 (шир. д, 1Н, J=8,0Гц), 7,51 (шир. т, 1Н, J=7,2Гц), 7,41 (д, 1Н, J=8,8Гц), 7,37 (шир. д, 1Н, J=8,2Гц), 7,24 (шир. т, 1Н, J=7,7Гц), 7,21 (шир. с, 1Н), 7,04 (д, 1H, J=2,1Гц), 6,76 (дд, 1H, J=8,7, 2,3Гц), 3,99 (т, 2Η, J=6,4Гц), 2,41 (Τ/ 2Η, J=7,1Гц), 2,34 (шир. м, 4Н), 1,87 (пентет, 2H, J=7,2Гц), 1,50 (шир. м, 4Н), 1,39 (м, 2H). 3-(5-{2-[Бензил-(2-метоксіетил)-аміно]стокси}1Н-індол-2-іл)-1Н-хінолін-2-он (1-14) 1 Н ЯМР (400МГц, (CD3)2SO) 12,15 (с, 1Н), 11,41 (с, 1Н), 8,50 (с, 1Н), 7,73 (шир. д, 1Н, J=7,7Гц), 7,51 (шир. т, 1Н, J=7,1Гц), 7,40 (д, 1Н, Н ЯМР (400MГц, (CD3)2SO) 12,14 (с, 1Н), 11,42 (с, 1Н), 8,50 (с, 1H), 7,73 (шир. д, 1Н, J=7,7Гц), 7,51 (шир. т, 1Н, J=7,3Гц), 7,41 (д, 1H, J=8,8Гц), 7,37 (шир. д, 1Н, J=8,2Гц), 7,32 (шир. м, 5Н), 7,24 (шир. т, 1Н, J=7,5Гц), 7,22 (шир. с, 1Н), 7,04 (д, 1Н, J=1,7Гц), 6,73 (дд, 1Н, J=8,6, 2,2Гц), 4,03 (шир. м, 2Н), 3,50 (шир. с, 2Н), 2,70 (шир. м, 2Н), 2,16 (шир. с, 3Н), 1,94 (шир. м, 2Н). 1-{2-[2-(2-Оксо-1.2-дигідрохінолін-3-іл)-1Ніндол-5-ілокси]-етил}-піперидин-4-карбонітрил (117) 1 Н ЯМР (400МГц, (CD3)2SO) 12,14 (с, 1Н), 11,41 (с, 1Н), 3,50 (с, 1Н), 7,73 (шир. д, 1Н, J=7,5Гц), 7,51 (шир. т, 1Н, J=7,9Гц), 7,41 (д, 1Н, J=8,6Гц), 7,37 (шир. д, 1Н, J=7,9Гц), 7,24 (шир. т, 1Н, J=7,1Гц), 7,21 (д, 1H, J=1,3Гц), 7,06 (д, 1H, J=2,2Гц), 6,76 (дд, 1H, J=8,6, 2,4Гц), 4,07 (т, 2Η, J=5,7Гц), 2,86 (м, 1H, 2,72 (т, 2Η, J=5,7Гц), 2,67 (м, 2Н), 2,41 (м, 2Н), 1,87 (м, 2Н), 1,72 (м, 2Н). 3-{5-[3-(4-Метилпіперазин-1-іл)пропокси]-1Нінол}-іл}-1H-хінолін-2-он (1-1S) 43 1 Н ЯМР (400MГц, (CD3)2SO) 12,15 (с, 1Н), 11,41 (с, 1Н), 8,49 (с, 1H), 7,72 (шир. д, 1Н, J=7,9Гц), 7,51 (шир. т, 1Н, J=7,7Гц), 7,40 (д, 1Н, J=8,8Гц), 7,37 (шир. д, 1Н, J=8,2Гц), 7,24 (шир. т, 1Н, J=7,5Гц), 7,20 (шир. с, 1Н), 7,03 (щир. с, 1H), 6,75 (дд, 1H, J=8,8, 1,8Гц), 3,99 (т, 2Η, J=6,4Гц), 2,44 (т, 3Η, J=7,1Гц), 2,36 (шир. м, 8Н), 2,15 (с, 3Н), 1,87 (м, 2Н). 3-[5-(3-Морфолін-4-ілпропокси)-1H-індол-2-іл]1Н-хінолін-2-он (1-19) 1 Н ЯМР (400MГц, (CD3)2SO) 12,14 (c, 1H), 11,14 (c, 1H), 8,50 (c, 1H), 7,73 (шир. д, 1Н, J=7,1Гц), 7,51 (шир. т, 1Н, J=7,6Гц), 7,41 (д, 1H, J=8,8Гц), 7,37 (щир. д, 1Н, J=8,2Гц), 7,24 (шир. т, 1Η, J=7,7Гц), 7,21 (д, 1Н, J=1,5Гц), 7,04 (д, 1Н, J=2,2Гц), 6,76 (дд, 1Н, J=8,6, 2,2Гц), 4,01 (т, 2Н, J=6,4Гц), 3,58 (т, 4Н, J=4,6Гц), 2,45 (т, 2Н, J=7,1Гц), 2,38 (шир. м, 4Н), 1,89 (пентет, 2Н, J=7,0Гц). Таблиця 1 74560 44 45 74560 46 індол-2-іл)-2(1Н)-хінолінону, сполука 1-27 (840мг, 1,8ммоль), у ЕtOАс (150мл) і суміш, що утворилася, перемішують під тиском водню з балона протягом 18 годин. Каталізатор видаляють фільтруванням і фільтрат концентрують, одержуючи при цьому жовту тверду речовину, яку очищають хроматографією на колонці з діоксидом кремнію. Елюювання з градієнтом від ЕЮАс до 25% розчину NH3-EtOH/EtOAc дає 3-(5-(2-[(2метоксіетил)аміно]-етокси}-1Н-індол-2-іл)-2(1Н)хінолінон (2-1) у вигляді жовтої твердої речовини. 1 Н ЯМР (300МГц, CDCl3) 11,05 (с, 1Н), 9,65 (шир. с, 1H), 8,32 (с, 1Н), 7,67 (д, 1H, J=8Гц), 7,51 (т, 1Η, J=8Гц), 7,34 (д, 1Н, J=8Гц), 7,29 (т, 1Η, J=8Гц), 7,24 (д, 1Н, J=8Гц), 7,09 {с, 1Н), 6,96 (с, 1Н), 6,90 (дд, 1Н, J=8, 2Гц), 4,15 (т, 2Η, J=5Гц), 3,55 (т, 2H, J=5Гц), 3,38 (с, 3Н), 3,07 (т, 2Η, J=5Гц), 2,91 (т, 2Η, J=5Гц). 3-[5-(2-{(2-Метоксіетил)[(2-метокси-5піримідиніл)метил]-аміно}етокси)-1Н-індол-2-іл]2(1H-хінолінон (2-2) Розчин 3-(5-{2-[(2-метоксіетріл)аміно]етокси}1Н-індол-2-іл)-2(1H)-хінолінону 2-1 (150мг, 0,4ммоль), 2-метокси-піримідин-5карбоксальдегіду (ПОмг, 0,8ммоль) і триацетоксиборогідриду натрію (168мг, 0,8ммоль) у DCE (25мл) перемішують в умовах навколишнього середовища протягом 18 годин. Реакційну суміш концентрують і залишок розподіляють між ЕtOАс і насиченим розчином NaHCO3. Органічний шар промивають насиченим розчином солі, сушать над MgSO4 і концентрують. Залишок суспендують в етиловому ефірі за допомогою обробки ультразвуком, потім фільтрують і сушать на повітрі, при цьому одержуючи 3-[5-(2-{(2-метоксіетил)[(2метокси-5-піримідиніл)-метил]аміно}-етокси)-1Ніндол-2-іл]-2(1Н)-хінолінон (2-2) у вигляді жовтої твердої речовини. 1 Н ЯМР (300МГц, CDCl3) 11,05 (с, 1H, 9,60 (c, 1Н), 8,53 (с, 2Н), 8,33 (с, 1Н), 7,68 (д, 1Н, J=9Гц), 7,52 (т, 1Н, J=8Гц), 7,34 (д, 1Н, J=8Гц), 7,27 (т, 1Н, J=3Гц), 7,22 (д, 1Н, J=8Гц), 7,05 (с, 1Н), 6,96 (с, 1Н), 6,86 (дд, 1H, J=8,2Гц), 4,13 (т, 2Н, J=6Гц), 4,01 (с, 3Н), 3,80 (с, 2Н), 3,53 (т, 2Н, J=6Гц), 3,34 (с, 3Н), 3,01 (т, 2Н, J=6Гц), 2,84 (т, 2Н, J=6Гц). Сполуки від 2-3 до 2-12 у таблиці 2 одержували простими модифікаціями до описаних вище протоколів. Вибрані ЯМР-спектри для 2-3 і 2-4 були такими: 2-3 1Н ЯМР (400МГц, CDCl3) 11,05 (с, 1H), 9,65 (с, 1H), 3,54 (дд, 1H, J=4,1Гц), 8,33 (с, 1H), 7,68 (д, 1H, J=7Гц), 7,52 (т, 1Н, J=8Гц), 7,33 (м, 3Н), 7,28 (т, 1Н, J=7Гц), 7,24 (д, 1Н, J=8Гц), 7,03 (д, 1Н, J=2Гц), 6,96 (д, 1Н, J=2Гц), 6,85 (дд, 1Н, J=8, 2Гц), 4,13 (т, 2Н, J=6Гц), 3,85 (с, 2Н), 3,53 (т, 2Η, J=6Гц), 3,33 (с, 3Н), 3,03 (т, 2Н, J=6Гц), 2,86 (т, 2Н, J=6Гц), 2-4, 1Н ЯМР (400МГц, CDCl3) 11,05 (с, 1Н), 9,40 (шир. с, 1Н), 8,53 (д, 1Н, J=5Гц), 8,32 (с, 1H), 7,68 (д, 1H, J=9Гц), 7,64 (т, 1Н, J=7Гц), 7,56 (д, 1Н, J=8Гц), 7,51 (т, 1Н, J=8Гц), 7,34-7,21 (м, 3Н), 7,14 (т, 1Н, J=7Гц), 7,05 (с, 1Н), 6,95 (с, 1Н), 6,85 (д, 1Н, J=8Гц), 4,14 (т, 2Η, J=6Гц), 3,99 (с, 2Н), 3,55 (т, 2Н, J=6Гц), 3,33 (с, 3Н), 3,09 (т, 2Н, J=6Гц), 2,93 (т, 2Н, 3-(5-{2-[(2-Метоксіетил)аміно]стокси}-1Н-індолJ=6Гц). 2-іл)-2(1H)-хінолінон (2-1) 10% Pd/C (840мг) додають до розчину (150мл) 3-(5-{2-[бензил(2-метоксіетил)аміно]етокси}-1Н 47 74560 48 (2S.4R)-1-[(Бензидокси)карбоніл]-4-метокси-2піролідинкарбонова кислота (3-2) Гідрид натрію (543мг, 22,6ммоль, 2,00еквів.) обережно додають до розчину (23,4К)-1[(бешилокси)карбоніл]^-гідрокси-2піролідинкарбонової кислоти (3-1, 3,00г, 11,3ммоль, 1екв.) у ТГФ (100мл) при 0°С і суміш, що утворилася, перемішують протягом 20 хвилин. Додають йодметан (2,11мл, 33,9ммоль, 3,00еквів.), суміш нагрівають до 23°С і перемішують протягом 20 годин. Реакційну суміш потім розбавляють насиченим розчином бікарбонату натрію, промивають етилацетатом (2x100мл). Водний шар потім підкисляють 1 н. розчином НСl до pH 3 і екстрагують етилацетатом (100мл). Даний органічний шар потім сушать над сульфатом натрію і концентрують, при цьому одержуючи (2S,4R)-1[(бензилокси)-карбоніл]-4-метокси-2піролідинкарбонову кислоту (3-2) у вигляді світложовтого масла. 1 Н ЯМР (400МГц, CDCl3) основнийротамер: 7,40-7,25 (шир. м, 5Н), 5,20 (с, 2Н), 4,52 (т, 1Н, J=7,4Гц), 4,00 (м, 1Н), 3,67 (дд, 1Н, J=11,4, 2,8Гц), 3,57 (дд, 1Н, J=11,4, 4,6Гц), 3,32 (с, 3Н), 2,34 (м, 2Н). Безил-(2S,4R)-2-(гідроксимстил)-4-метокси-1піролідинкарбоксилат (3-3) Розчин комплексу боран-тетрагідрофуран у ТГФ (1г, 53,0мл, 53,0ммоль, 3,50еквів.) додають до розчину (2S,4R)-1-[(бензилокси)карбоніл]-4метокси-2-піролідинкарбонової кислоти (3-2,4,23г, 15,1ммоль, 1еквів.) у ТГФ (200мл) при 0°С. Суміш, 49 74560 50 що утворилася, нагрівають до 23°С і перемішують 8,17 (м, 2Н), 8,08 (д, 1Н, J=8,5Гц), 7,87 (шир. д, 1Н, протягом 1 години. Надлишковий боран обережно J=8,6Гц), 7,78 (т, 1Н, J=8,4Гц), 7,61 (т, 1Η, гасять водою. Суміш потім розподіляють між суміJ=8,4Гц), 7,38-7,22 (шир. м, 5Н), 7,10 (шир. с, 1Н), шшю 1:1 насиченого розчину карбонату натрію і 6,94 (шир. м, 1H), 6,56 (с, 1Н), 5,17 (шир. с, 2Н), насиченого розчину солі (300мл) і етилацетатом 4,35 (шир. м, 2Н), 4,16 (шир. м, 2Н), 3,60 (шир. м, (300мл). Органічний шар сушать над сульфатом 2Н), 3,34 (с, 3Н), 2,88 (с, 3Н), 2,32 (м, 1Н), 2,23 (м, натрію і концентрують. Залишок очищають флеш1Н). колонковою хроматографією (спочатку 100% гектрет-Бутил-2-(2-хлор-3-хінолініл)-5-{[(2S.4R)-4сан, який поступово змінюється до 100% ЕtOАс), метоксипіролідиніл]метокси}-1Η-індол-1при цьому одержуючи бензил-(2S,4R)-2карбоксилат (3-6) (гідроксиметил)-4-метокси-1-піролідинкарбоксилат Суміш трет-бутил-5-({(2S,4R)-1(3-3) у вигляді безбарвного масла. [(бензилокси)карбоніл]-4-метокси1 піролідиніл}метокси)-2-(2-хлор-3-хінолініл)-1НН ЯМР (300МГц, CDCl3) основний ротамер: індол-1-карбоксилату (3-5, 295мг, 0,459ммоль, 7,37-7,25 (шир. м, 5Н), 5,18 (д, 1Н, J=12,4Гц), 5,13 1еквів.) і 10% паладію на вугіллі (200мг, (д, 1Н, J=12,2Гц), 4,51 (дд, 1Н, J=8,3, 2,2Гц), 3,86 0,188ммоль, 0,410еквів.) в етанолі (10мл) перемі(м, 1Н), 3,78 (дд, 1Η, J=11,7, 2,2Гц), 3,72 (шир. д, шують в атмосфері водню з балона протягом 1,5 1Н, J=11,7Гц), 3,61 (ддд, 1Н, J=9,8, 7,4, 2,2Гц), 3,44 години. Каталізатор фільтрують на подушці целіту (дд, 1Н, J=12,2, 4,4Гц), 3,30 (с, 3Н), 2,18 (м, 1Н), і промивають етанолом (20мл). Фільтрат концент1,64 (м, 1Н). рують і залишок очищають рідинною хроматограБензил-(2S,4R)-4-метокси-2фією з оберненою фазою (градієнт суміші ([(метилсульфоніл)окси]метил}-1-піролідинН2О/СН3СК/присутня 0,1% ТФО), при цьому одеркарбоксилат (3-4) жуючи трет-бутил-2-(2-хлор-3-хінолініл)-5Метансульфонілхлорид (0,175мл, 2,26ммоль, {[(2S,4R)-4-метоксипіролідиніл]-метокси}-1Н-індол1,2еквів.) додають до розчину бензил-(2S,4R)-21-карбоксилат(3-6). (гідроксиметил)-4-метокси-11 піролідинкарбоксилату (3-3, 0,500г, 1,83ммоль, Η ЯМР (300МГц, CD3OD) 8,41 (с, 1Н), 8,23 1еквів.) і триетиламіну (0,394мл, 2,83ммоль, (д, 1H, J=9,3Гц), 8,02 (шир. т, 2Н, J=7,1Гц), 7,86 1,50еквів.) у дихлорметані (30мл) при 0°С. Суміш, (шир. т, 1Η, J=7,9Гц), 7,70 (шир. т, 1Н, J=8,1Гц), що утворилася, нагрівають до 23°С і перемішують 7,25 (д, 1H, J=2,4Гц), 7,09 (дд, 1H, J=9,0, 2,7Гц), протягом 1 години. Реакційну суміш розподіляють 6,73 (с, 1H), 4,45 (м, 1H), 4,23 (шир. м, 3Н), 3,51 між насиченим розчином бікарбонату натрію і дих(шир. д, 1Н, J=12,7Гц), 3,41 (дд, 1Н, J=12,7, 3,4Гц), лорметаном (2x40мл). Об'єднані органічні шари 3,40 (с, 3Н), 2,47 (м, 1Η), 2,06 (м, 1H). сушать над сульфатом натрію і концентрують. 3-(5-{[(2S.4R)-4-Метоксипіролідиніл]метокси}Залишок очищають флеш-колонковою хроматог1Н-індол-2-іл)-2(1Н)-хінолінон (3-7) рафією (спочатку 100% гексан, який поступово Розчин трет-бутил-2-(2-хлор-3-хінолініл)-5змінюється до 100% ЕЮ Ас), при цьому одержую{[(2S,4R)-4-метоксипіролідиніл]-метокси}-1Н-індолчи бензил-(2S,4R)-4-метокси-21-карбоксилату (6-6, 29мг, 0,057ммоль) нагрівають {[(метилсульфоніл)окси]метил}-1у суміші 8:1 оцтової кислоти і води (5мл) при 90°С піролідинкарбоксилат (3-4) у вигляді світлопротягом 1,5 години. Реакційну суміш охолоджужовтого масла 1Н ЯМР (400МГц, CDCl3) основний ють і концентрують і залишок очищають рідинною хроматографією з оберненою фазою (градієнт ротамер: 7,37-7,25 (шир. м, 5Н), 5,17 (д, 1Н, суміші Н2О/СН3СN/присутня 0,1% ТФО), при цьому J=11,8Гц), 5,10 (д, 1Н, J=11,8Гц), 4,65 (дд, 1H, одержуючи 3-(5-{[(2S,4R)-4-метоксипіролідиніл]J=8,3, 3,8Гц), 4,24 (шир. м, 2Η), 3,95 (м, 1Η), 3,68 метокси}-1Н-індол-2-іл)-2(1Н)-хінолінон (3-7) у ви(шир. д, 1Н, J=12,0Гц), 3,45 (дд, 1Н, J=12,0, 4,4Гц), гляді жовтої твердої речовини. 3,30 (с, 3Н), 2,88 (с, 3Н), 2,39 (м, 1Н), 2,12 (м, 1Н). 1 трет-Бутил-5-({(2S.4R)-1Н ЯМР (400МГц, CD3OD) 8,45 (С, 1Н), 7,75 [(бензилокси)карбоніл]-4-метоксипіролідинілІ(д, 1Н, J=7,8Гц), 7,53 (шир, т, 1Н, J=7,8Гц), 7,38 (д, метокси)-2-(2-хлор-3-хінолініл)-1H-індол-11Н, J=8,9Гц), 7,38 (я, 1H, J=8,1Гц), 7,29 (шир. т, 1Η, карбоксилат (3-5) J=7,3Гц), 7,19 (с, 1H), 7,17 (д, 1H, J=2,4Гц), 6,89 Суміш 6eH3Hii-(2S,4R)-4-метокси-2(дд, 1H, J=3,8, 2,4Гц), 4,39 (дд, 1Н, J=10,2, 2,8Гц), {[(метилсульфоніл)окси]-метил}-14,25 (м, 1Н), 4,20 (м, 1Н), 4,14 (м, 1Н), 3,49 (дд, 1Н, піролідинкарбоксилату (3-4, 380мг, 1,11ммоль, J=13,9, 6,9Гц), 3,41 {дд, 1Н, J=12,6, 3,6Гц), 3,39 (с, 1еквів.), 2-В (437мг, 1,11ммоль, 1,00еквів.) і карбо3Н), 2,45 (шир. дд, 1Н, J=13,9, 6,5Гц), 2,05 (м, 1Н). нату цезію (433мг, 1,33ммоль, 1,20еквів.) у ДМФ Сполуки від 3-8 до 3-21, наведені нижче, у (5,0мл) нагрівають при 70°С протягом 3 годин. таблиці 3, отримані простими модифікаціями проРеакційну суміш розподіляють між водою та етитоколів, описаних вище. Для прикладів від 3-13 до лацетатом (2x50мл). Об'єднані органічні шари су3-15 (2R,4R)-1-[(бензилокси)карбоніл]-4-гідрокси-2шать над сульфатом натрію і концентрують. Запіролідинкарбонову кислоту використовували як лишок очищають флеш-колонковою вихідний матеріал. Для прикладів від 3-17 до 3-19 хроматографією (спочатку 100% гексан, який посTBSC1 використовували замість йодметану в петупово змінюється до 40% ЕtOАс у гексані), при ршій стадії послідовності, описаної у схемі 3. Для цьому одержуючи трет-бутил-5-({(2S,4R)-1прикладів 3-20 і 3-21 1-(трет-бутоксикарбоніл)-4[(бензилокси)карбонїл]-4-метоксипшеридинкарбонову кислоту і 1-(третпіролідиніл}метокси)-2-(2-хлор-3-хінолініл)-1Hбутоксикарбоніл)-3-піперидинкарбонову кислоту індол-1-карбоксилат (3-5). використовували як вихідний матеріал, відповідно. 1 Вибрані ЯМР-спектри для 3-8 і 3-9 були такими: Н ЯМР (400МГц, CDCl3) основнийротамер: 51 74560 3-8. Н ЯМР (400МГц, СDСІ3) 11,1 (с, 1Н), 9,27 (шир. с, 1Н), 8,62 (с, 2Н), 8,32 (с, 1Н), 7,68 (д, 1Н, J=8Гц), 7,51 (т, 1Н, J=8Гц), 7,34 (д, 1Н, J=8Гц), 7,29 (т, 1Н, J=7Гц), 7,19 (д, 1Н, J=8Гц), 7,07 (д, 1Н, J=2Гц), 6,96 (шир. с, 1Н), 6,87 (дд, 1Н, J=8,2Гц), 4,25 (д, 1Н, J=14Гц), 4,05 (м, 2Н), 3,94 (м, 1Н), 3,58 (д, 1Н, J=14Гц), 3,36-3,22 (м, 2Н), 3,30 (с, 3Н), 2,71 (с, 3Н), 2,38 (м, 1Н), 2,12 (м, 1Н), 1,96 (м, 1Н), 3-9, 1 H ЯМР (400МГц, ДМСО-d6) 12,2 (с, 1Н), 11,4 (с, 1Н), 8,51 (с, 1Н), 8,13 (д, 2Н, J=7Гц), 7,72 (д, 1Н, J=7Гц), 7,51 (т, 1Η, J=3Гц), 7,42-7,32 (м, 4Н), 7,24 (т, 1Η, J=3Гц), 7,20 (с, 1Н), 7,05 (с, 1Н), 6,74 (дд, 1Н, J=8,2Гц), 4,13 (д, 1Н, J=14Гц), 4,04 (м, 1Н), 3,91 (м, 2Н), 3,54 (д, 1Н, J=14Гц), 3,20 (с, 3Н), 3,203,13 (м, 2Н), 2,31 (м, 1Н), 2,01 (м, 1Н), 1,86 (м, 1Н). 52 1 Етиловий ефір 1-(2-{[2-(2-оксо-1.2-дигідро-3хінолініл)-1H-індол-5-іл]-окси}етил)-4піперидинкарбонової кислоти (4-1) Сполуку 4-1 синтезують за методикою, описаною у наведеній вище схемі 1. 1-(2-{[2-(2-Оксо-12-дигідро-3-хінолініл)-1Ніндол-5-іл]окси}етил)-4-піперидинкарбонова кислота (4-2) Етиловий ефір 1-(2-{[2-(2-оксо-1,2-дигідро-3хінолініл)-1Н-індол-5-іл]окси}-етил)-4піперидинкарбонової кислоти (4-1, 138мг, 0,30ммоль, 1еквів.) розчиняють у МеОН (20мл). Додають 1н. NaOH (6мл, 20еквів.) і розчин нагрівають при 50°С протягом 5 годин. Реакційну суміш концентрують і залишок суспендують у 4мл води. Дану суспензію нейтралізують 1н. НСl, при цьому одержуючи 1-(2-{[2-(2-оксо-1,2-дигідро-3-хінолініл)1H-індол-5-іл]окси}етил)-4-піперидинкарбонову кислоту (4-2) у вигляді жовтої твердої речовини. 1 H ЯМР (400МГц, CD3OD) 8,45 (с, 1H), 7,74 (д, 1Н, J=8Гц), 7,53 (т, 1Η, J=8Гц), 7,38 (м, 2Н), 7,28 (т, 1Н, J=8Гц), 7,19 (с, 1Н), 7,16 (с, 1Н), 6,88 (дд, 1Н, J=9, 2Гц), 4,34 (т, 2Н, J=5Гц), 3,53 (м, 2Н), 3,47 (м, 2Н), 3,07 (м, 2Н), 2,42 (м, 1Н), 2,11 (м, 2Н), 1,95 (м, 2Н). Сполуки від 4-3 до 4-16 у наведеній нижче таблиці 4 одержують простою модифікацією описаних вище умов гідролізу. Відповідні складноефірні попередники одержують хімією алкілування, аналогічною хімії алкілування, зазначеній у схемах 1 і 3. Вибрані ЯМР-спектри для 4-3 і 4-4 є такими: 4-3, 1Н ЯМР (400МГц, CD3OD) 8,44 (с, 1Н), 7,74 (д, 1Η, J=8Гц), 7,52 (т, 1H, J=7Гц), 7,34 (д, 1H, J=8Гц), 7,28 (т, 1H, J=7Гц), 7,18 (шир. С, 1Н), 6,92 (д, 1Н, J=8Гц), 4,36 (т, 2Η, J=5Гц), 3,74 (т, 2Н, J=5Гц), 3,62 (т, 2Н, J=5Гц), 3,45 (м, 4Н), 3,36 (с, 3Н), 2,61 (т, 2Н, J=5Гц), 4-4, 1Н ЯМР (400МГц, ДМСО-d6) 12,1 (с, 1Н), 11,5 (с, 1Н), 8,50 (с, 1Н), 53 74560 7,73 (д, 1Н, J=8Гц), 7,51 (т, 1Н, J=8Гц), 7,42 (д, 1Н, J=8Гц), 7,37 (д, 1Н, J=8Гц), 7,25 (т, 1Н, J=8Гц), 7,21 (с, 1Н), 7,05 (С, 1Н), 6,76 (дд, 1Н, J=8, 2Гц), 4,02 (м, 2Н), 3,15-2,75 (м, 4Н), 2,4-1,5 (м, 9Н). 54 (1Н-Індол-5-іл)метанол (5-2) До розчину, що механічно перемішується, 1Ніндол-5-карбонової кислоти (5-1, 20,01г, 124ммоль) у ТГФ (500мл) повільно додають при температурі навколишнього середовища розчин 1Μ LAH у толуолі (186мл, 186ммоль, 1,5еквів.). Реакційну суміш нагрівають при кип'ятінні зі зворотним холодильником протягом 1 години, гасять льодом, розподіляють між етилацетатом і насиченим водним розчином NaHCO3. Органічний шар промивають насиченим розчином солі, відокремлюють, сушать (MgSO4) і концентрують у вакуумі. Сирий 55 74560 56 продукт твердне при стоянні при зниженому тиску. дає необхідну боронову кислоту (5-4) у вигляді Сиру тверду речовину суспендують у гексані білого порошку. 1Н ЯМР (400МГц, CDCl3) 7,96 (д, (200мл) і етилацетаті (10мл), перемішують протя1Н, J=6,8Гц), 7,54 (с, 1Н), 7,47 (с, 1Η), 7,32 (д, 1H, гом ночі, збирають фільтруванням і сушать на поJ=6,3Гц), 7,10 (с, 1Н), 4,82 (с, 2Н), 1,74 (с, 9Н), 0,95 вітрі, при цьому одержуючи необхідний продукт у (с, 9Н), 0,11 (С, 6Н). вигляді світло-коричневої твердої речовини. 3-Йод-1Н-хінолін-2-он (5-5) 1 Н ЯМР Μ00МГц, CDCl3) 8,24 (шир. с, 1Н), 2-Хлор-3-йодхінолін (1-2, 30,0г) зважують у 7,62 (с, 1Н), 7,36 (д, 1Н, J=8,4Гц), 7,23 (d, 1H, 250мл колбу і суспендують у 50% водній оцтовій J=8,4Гц), 7,20 (с, 1Н), 6,54 (с, 1H), 4,75 (с, 2Н), 1,68 кислоті (125мл). Суміш нагрівають до 100°С і під(с, 1Н). дають кип'ятінню зі зворотним холодильником трет-Бутиловий ефір 5-(третпротягом 16 годин до завершення взаємодії за бутилдиметилсиланілоксиметил)-індол-1даними аналізу ТШХ сирої реакційної суміші. Сукарбонової кислоти (5-3) міші дають охолонути до температури навколишРозчин, що перемішується, (1Н-індол-5нього середовища з наступним розведенням іл)метанолу (5-2, 16,5г, 112,1ммоль) у дихлорме200мл води. Суспензію, що утворилася, необхіднотані (300мл) послідовно обробляють при темпераго продукту виділяють вакуумним фільтруванням турі навколишнього середовища діізопропілетилаіз наступним промиванням водою (50мл). Воду і міном (39мл, 224,2ммоль, 2еквів.), трет-бутилсліди оцтової кислоти видаляють у вакуумі протядиметилсилілхлоридом (18,6г, 123,3ммоль, гом 5 годин, при цьому одержуючи необхідний 1,1еквів.) і 4-(N,N-диметиламіно)піридином (1,37г, хінолінон у вигляді рудувато-коричневого порошку 11,2ммоль, 0,1еквів.). Реакційну суміш перемішу(5-5). 1 ють при кімнатній температурі протягом 30 хвилин, Н ЯМР (500МГц, CDCl3) 12,13 (шир. с, 1Н), концентрують у вакуумі, розподіляють між етила3,71 (с, 1Н), 7,65 (д, 1Н, J=7,5Гц), 7,54 (м, 1Н), 7,31 цетатом і 0,5 н. НСl. Органічний шар промивають (д, 1H, J=8,0Гц), 7,20 (м, 1Н). насиченим розчином солі, відокремлюють, сушать трет-Бутиловий ефір 5-гідроксиметил-2-(2(MgSO4), концентрують у вакуумі, при цьому одероксо-1.2-дигідрохінолін-3-іл)індол-1-карбонової жуючи сирий силіловий простий ефір у вигляді кислоти (5-7) світло-коричневої твердої речовини. Сирий проСуміш, що перемішується, йодхінолінону (5-5, дукт і ди-трет-бутилдикарбонат (25,9г, 10г, 36,9ммоль, 1еквів.), боронової кислоти (5-4, 123,3ммоль) розчиняють у дихлорметані (300мл) і 7,5г, 18,45ммоль, 0,5еквів.), тетраперемішують при температурі навколишнього секис(трифенілфосфін)-паладію (1,71г, 1,48ммоль, редовища в присутності 4-(N,N0,04еквів.) і хлориду літію (4,69г, 110,7ммоль, Зекдиметиламіно)тридину (1,37г, 11,2ммоль) протявів.) у суміші діоксан-2 Μ водний Nа2СО3 дегазугом 2 годин. Реакційну суміш концентрують у вакують і нагрівають при 80°С доти, поки боронова умі, розподіляють між етилацетатом і 0,5 н. НСl. кислота не буде виявлятися тонкошаровою хромаОрганічний шар промивають насиченим розчином тографією. До реакційної суміші додають додаткосолі, відокремлюють, сушать (MgSO4) і концентруву боронову кислоту (0,2еквів. за один раз) доти, ють у вакуумі, при цьому одержуючи сире масло. поки не буде витрачений весь йодхінолінон (5-5) Хроматографія (SiO2, 10% етилацетат у гексані) (усього потрібно 1,5 еквівалента боронової кислодає трет-бутиловий ефір 5-(трет-бутиловий-5ти, 5-4). Реакційну суміш розподіляють між етила(трет-бутилдиметилсиланіл-оксиметил)індол-1цетатом і насиченим водним NaHCO3. Органічний карбонової кислоти (5-3) у вигляді білої твердої шар промивають насиченим розчином солі, відоречовини. кремлюють, сушать MgSO4 і концентрують у ваку1 Н ЯМP (400МГц, CDCl3) 7,97 (д, 1Н, умі. Сире масло (5-6) розчиняють у тетрагідрофуJ=8,0Гц), 7,47 (д, 1Н, J=3,2Гц), 7,41 (с, 1Η), 7,15 (д, рані (100мл), переносять у колбу з ПЕГ, 1Η, J=7,7Гц), 6,44 (д, 1H, J=3,6Гц), 4,72 (с, 2Н), обробляють при 0°С комплексом HF-піридин 1,56 (с, 9Н), 0,34 (с, 9Н), 0,00 (с, 6H). (15мл) і перемішують протягом 1 години при тем5-(трет-Бутилдиметилсиланілоксиметил)індолпературі навколишнього середовища. Реакційну 1-трет-бутилокси-карбоніл-індол-2-боронова киссуміш розподіляють між етилацетатом і насиченим лота (5-4) водним NaHCO3. Органічний шар промивають наДо розчину, що перемішується, третсиченим розчином солі, відокремлюють, сушать бутилового ефіру 5-(трет(MgSO4) і концентрують у вакуумі. Сиру тверду бутилдиметилсиланілоксиметил)індол-1речовину розтирають з етилацетатом і гексаном, карбонової кислоти (5-3, 38,6г, 106,7ммоль) у тетзбирають фільтруванням і сушать на повітрі, при рагідрофурані (400мл) повільно додають при-78°С цьому одержуючи необхідний продукт (5-7) у вирозчин діізопропіламіду літію в тетрагідрофурані гляді світло-жовтої твердої речовини. 1Н ЯМР (2М, 80,1мл, 160,1ммоль, 1,5еквів.). Реакційну су(500МГц, ДМСО-d6) 12,1 (с, 1H), 3,07 (с, 1Н), 8,03 міш перемішують при цій же температурі протягом (д, 1H, J=8,5Гц), 7,74 (д, 1Н, J=7,5Гц), 7,55 (с, 1Н), 1 години, обробляють триметилборатом, нагріва7,52 (т, 1Η, J=7,5Гц), 7,35 (д, 1Η, J=3,5Гц), 7,30 (д, ють до температури навколишнього середовища і 1H, J=7,5Гц), 7,22 (т, 1H, J=7,5Гц), 6,77 (с, 1H), 5,21 розподіляють між етилацетатом і 0,5н. НСl. Орга(т, 1H, J=5,5Гц), 4,60 (д, 2Н, J=5,5Гц), 1,35 (с, 9Н). нічний шар промивають насиченим розчином солі, трет-Бутиловий ефір 5-форміл-2-(2-оксо-1.2відокремлюють, сушать (MgSO4) і концентрують у дигідрохінолін-3-іл)-індол-1-карбонової кислоти (5вакуумі, при цьому одержуючи сиру тверду речо8) вину. Розтирання сирого продукту з гексанами з Попередньо активований МnО2 (34,5г, наступним фільтруванням і сушінням на повітрі 15еквів.) і спирт (5-7, 10,32г, 1,0еквів.) зважують у 57 74560 58 колбу на 1л і суспендують у сухому дихлорметані перемішують протягом 1,5 години. Реакційну су(500мл). Реакційну суміш нагрівають до 45°С і взаміш концентрують у вакуумі, розподіляють між ємодію завершують через 1 годину (за даними етилацетатом і насиченим водним NaHCO3. Оргатонкошарової хроматографії). Суміші дають можнічний шар промивають насиченим розчином солі, ливість охолонути до температури навколишнього відокремлюють, сушать (Na2SO4) і концентрують у середовища і оксид(и) марганцю видаляють вакувакуумі. Сиру тверду речовину, що утворилася, умним фільтруванням. Масу оксидів, що утвориочищають рідинною хроматографією з оберненою лася, на фільтрі розтирають із гарячим ТГФ і розфазою (градієнт H2O/CH3CN із присутньою 0,1% чинник фільтрують у вакуумі для видалення будьТФО), при цьому одержуючи сіль трифтороцтової якого продукту з оксидів. Фільтрат, що утворився, кислоти сполуки 5-10. Усі фракції, що містять неконцентрують у вакуумі, при цьому одержуючи обхідний продукт, розподіляють між етилацетатом сирий альдегід у вигляді жовтої твердої речовини. і насиченим водним NaHCO3. Органічний шар Тверду речовину розтирають із метанолом (10мл) і промивають насиченим розчином солі, відокреметилацетатом (15мл) з наступним вакуумним філюють, сушать (Na2SO4) і концентрують у вакуумі, льтруванням для виділення чистого продукту. Свіпри цьому одержуючи 3-[5-(4-метантло-жовтий альдегід сушать у вакуумі (5-8). 1Н сульфонілпіперазин-1-ілметил)-1Н-індол-2-іл]-1Hхінолін-2-он (5-10) у вигляді світло-жовтої твердої ЯМР: (500МГц, ДМСО-d6) 12,15 (с, 1Н), 10,08 (с, 1H), 8,26 (д, 1Н, J=1,5Гц), 8,24 (д, 1H, J=8,5Гц), речовини. 1Н ЯМР (500МГц, ДМСО-d6) 12,07 (с, 8,15 (с, 1Н, 7,90 (дд, 1Н, J=8,5, 1,5Гц), 7,77 (д, 1H, 1Н), 11,54 (с, 1Н), 8,53 (с, 1H), 7,73 (д, 1Н, J=7,5Гц), 7,55 (м, 1Н), 7,37 (д, 1H, J=8,5Гц), 7,24 J=7,5Гц), 7,52 (т, 1Η, J=7,5Гц), 7,47-7,46 (м, 2Н), (м, 1Н), 7,01 (с, 1Н). 7,33 (д, 1Н, J=8,5Гц), 7,29 (шир. с, 1Н), 7,25 (т, 1Н, трет-Бутиловий ефір 5-(4J=7,5Гц), 7,08 (д, 1Н, J=9,0Гц), 3,57 (с, 2Н), 3,11 (м, метансульфонілпіперазин-1-ілметил)-2-(2-оксо4Н), 2,87 (с, 3Н), 2,48 (м, 4Н). 1.2-дигідрохінолін-3-іл)індол-1-карбонової кислоти 3-[5-(4-Метансульфоніл-1-оксипіперазин-1(5-9) ілметил)-1Н-індол-2-іл]-1Н-хінолін-2-он (5-11) До розчину, що перемішується, альдегіду (5-8, Розчин 5-10 (50г, 0,11ммоль, 1еквів.) у СН2Сl2 2,01г, 5,15ммоль, 1еквів.) і солі N(125мл) обробляють при температурі навколишметансульфонілпіперазиноцтової кислоти (4,62г, нього середовища mСРВА (70%, 35мг, 20,60ммоль, 4еквів.) у дихлорметані (400мл) до0,143ммоль). Реакційну суміш перемішують протядають при температурі навколишнього середовигом 1 години, концентрують у вакуумі. Сиру тверду ща оцтову кислоту (1,2мл). Реакційну суміш оброречовину, що утворилася, очищають хроматограбляють триацетоксиборогідридом натрію і фією з оберненою фазою (градієнт H2O/CH3CN із перемішують протягом 3 годин. Взаємодію припиприсутньою 0,1% ТФО), при цьому одержуючи сіль няють при 76% перетворенні і обробляють MgSO4 трифтороцтової кислоти сполуки 5-11. 1 і додатковим 1г гідриду. Після подальшого переΗ ЯМР (500МГц, ДМСО-d6): 12,57 (с, 1Н); мішування протягом 1 години взаємодію завершу12,22 (с, 1Н); 11,86 (с, 1Н); 8,60 (с, 1Н); 7,79 (шир. ють. Реакційну суміш розподіляють між етилацес, 1Н); 7,74 (д, 1Н, J=7,6Гц); 7,64 (д, 1H, J=8,3Гц); татом і насиченим водним NaHCO3. Органічний 7,54 (м, 1H); 7,40 (м, 2H); 7,28 (м, 2Н); 4,97 (с, 2Н); шар знову один раз промивають насиченим вод3,85 (т, 2Η, J=11,7Гц); 3,73 (д, 2Н, J=13,2Гц); 3,61 ним NaHCO3 і потім насиченим розчином солі, ві(д, 2Н, J=12,5Гц); 3,34 (т, 2Н, J=11,9Гц); 3,04 (с, докремлюють, сушать (Na2SO4) і концентрують у 3Н). вакуумі. Сиру тверду речовину розчиняють у диСполуки від 5-12 до 5-65 у наведеній нижче метилформаміді та обробляють активованим вутаблиці 5 (за винятком 5-15, 16, 18, 29, 30 і 31) гіллям. Розчин фільтрату (целіт) концентрують до одержують простою модифікацією методик, описиропу, який швидко розтирають із метанолом саних вище. Вибрані спектри були такими: (100мл). Тверду речовину, що утворилася, збира5-14, 1Н ЯМР (400MГц, ДМСО-d6) 12,18 (с, ють фільтруванням, знову розчиняють у диметил1Н), 11,52 (с, 1Η), 8,52 (с, 1H), 7,73 (д, 1Н, формаміді, концентрують до сиропу, розтирають із J=7,5Гц), 7,52 (дт, 1Н, J=3,5, 1,0Гц), 7,46 (д, 1Н, метанолом (100мл), збирають фільтруванням і J=9,0Гц), 7,45 (с, 1H), 7,38 (д, 1Н, J=8,0Гц), 7,29 (с, сушать у вакуумі, при цьому одержуючи трет1Н), 7,25 (т, 1Η, J=7,5Гц), 7,08 (дд, 1Н, J=3,0, бутиловий ефір 5-(4-метансульфонілпіперазин-11,0Гц), 3,55 (с, 2Н), 3,42 (м, 4Н), 2,38 (м, 2Н), 2,32 ілметил)-2-(2-оксо-1,2-дигідрохінолін-3-іл)індол-1(м, 2Н), 1,97 (с, 3Н); 5-20, , 1Н ЯМР (400MГц, карбонової кислоти (5-9) у вигляді білого порошку. ДМСО-d6) 12,16 (с, 1Н, 11,53 (с, 1H), 8,52 (с, 1Н), 1 Н ЯМР (500МГц, ДМСО-d6) 12,06 (с, 1Н), 7,73 (д, 1Н, J=7,5Гц), 7,52 (дт, 1Н, J=8,5, 1,0Гц), 9,06 (с, 1Н), 8,04 (д, 1H, J=3,5Гц), 7,74 (д, 1H, 7,46 (д, 1H, J=9,0Гц), 7,45 (с, 1Н), 7,38 (д, 1Н, J=8,0Гц), 7,55 (с, 1H), 7,53 (дт, 1Н, J=8,0, 1,5Гц), J=9,0Гц), 7,29 (с, 1Н), 7,25 (т, 1Н, J=7,5Гц), 7,08 7,35 (д, 1Н, J=8,5Гц), 7,30 (дд, 1Н, J=8,5, 1,5Гц), (дц, 1Н, J=8,0, 1,0Гц), 3,61 (с, 2Н), 3,42 (м, 2Н), 7,22 (т, 1Η, J=7,5Гц), 6,76 (с, 1H), 3,62 (с, 2Н), 3,16 2,83 (с, 3Н), 2,54-2,50 (м, 6Н); 5-23, , 1Н ЯМР (м, 4Н), 2,87 (с, 3Н), 2,48 (м, 4Н), 1,35 (с, 9Н). (400MГц, ДМСО-d6) 12,15 (шир. с, 1Н), 11,51 (с, 3-[5-(4-Метансульфонілпіперазин-1-ілметил)1Н), 8,53 (С, 1Н), 7,73 (д, 1Н, J=7,5Гц), 7,52 (дт, 1Н, 1Н-індол-2-іл]-1Н-хінолін-2-он (5-10) J=8,5, 1,0Гц), 7,45 (д, 1Н, J=9,0Гц), 7,44 (с, 1Н, 7,38 Суміш трет-бутилового ефіру 5-(4(д, 1Н, J=8,0Гц), 7,29 (с, 1Н), 7,25 (т, 1Н, J=7,5Гц), метансульфонілпіперазин-1-ілметил)-2-(2-оксо7,08 (дд, 1Н, J=8,0, 1,0Гц), 3,48 (с, 2Н), 2,68 (м, 1,2-дигідрохінолін-3-іл)індол-1-карбонової кислоти 4Н), 2,52 (с, 1Н), 2,30 (м, 4Н); 5-37, 1Н ЯМР (5-9, 1,02г, 1,863ммоль), диметилсульфіду (1,2мл), (500МГц, ДМСО-d6) 12,16 (шир. с, 1Н), 11,53 (с, води (0,6мл) і ТФО (40мл) у дихлорметані (40мл) 1Н), 8,52 (с, 1Н), 7,73 (д, 1Н, J=7,5Гц), 7,52 (дт, 1Н, 59 74560 J=8,5, 1,0Гц), 7,47 (д, 1Н, J=9,0Гц), 7,46 (с, 1Н), 7,38 (д, 1Н, J=8,0Гц), 7,29 (д, 1Н, J=1,0Гц), 7,25 (т, 1Н, J=7,5Гц), 7,08 (дд, 1Н, J=8,0, 1,0Гц), 4,51 (т, 1Н, J=5,5Гц), 4,06 (д, 1Н, J=5,5Гц) 3,55 (с, 2Н), 3,46 (м, 2Н), 3,32 (м, 2H), 2,36 (м, 4Н). Сульфонаміди (5-15 і 16) одержують із відповідних вторинних амінів (обробкою 5-12 і 13, відповідно, метансульфонілхлоридом і діізопропілетиламіном у дихлорметані при температурі навколишнього середовища). Карбонові кислоти (5-18, 29, 30 і 31) синтезують із вихідних складних ефірів (5-17, 26, 27 і 28, відповідно) гідролізом (NaOH/EtOH при 90°С). Вихідний ефір (5-28, 57мг, 124ммоль) розчиняють у ЕtOН (1мл) і 1 н. NaOH (1мл). Суміш нагрівають до 90°С. Моніторинг взаємодії проводять РХ/МС. Вихідний матеріал увесь перетворюється на продукт після перемішування протягом 7 годин. Реакційну суміш конденсують і залишок розчиняють у трифтороцтовій кислоті. Надлишок трифтороцтової кислоти видаляють на роторному випарнику. Залишок розчиняють у воді і матеріал центрифугують. Воду декантують і тверду речовину аналізують ВЕРХ для визначення чистоти. Продукт (5-31) виділяють у вигляді жовтої твердої речовини. 1Н ЯМР: (500МГц, ДМСО-d6): 12,06 (С, 1Н); 11,77 (с, 1Н), 8,58 (с, 1H); 7,74 (д, 1H,); 7,607,52 (м, 3Н); 1,3 (шир. с, 1Н) ; 2,24 (м, 4Η); 2,15 (м, 4Н); 1,12 (шир. с,3Н). 60
ДивитисяДодаткова інформація
Назва патенту англійськоюTyrosine kinase inhibitors and a pharmaceutical composition based thereon
Автори англійськоюBilodeau Mark T.
Назва патенту російськоюИнгибиторы тирозинкиназы и фармацевтическая композиция на их основании
Автори російськоюБилодо Марк Т.
МПК / Мітки
МПК: A61P 17/06, A61P 17/02, A61K 31/541, A61P 19/08, C07D 417/14, A61P 19/02, A61K 31/506, A61K 31/496, A61N 5/10, A61P 27/02, C07D 413/14, A61P 35/00, C07D 405/14, A61K 31/551, C07D 401/14, A61P 43/00, C07D 401/04, A61P 9/10, A61K 31/5377, A61K 31/4709, C07D 409/14, A61P 29/00, A61K 31/495, A61K 45/06, A61K 45/00
Мітки: основі, інгібітори, композиція, тирозинкінази, фармацевтична
Код посилання
<a href="https://ua.patents.su/37-74560-ingibitori-tirozinkinazi-ta-farmacevtichna-kompoziciya-na-kh-osnovi.html" target="_blank" rel="follow" title="База патентів України">Інгібітори тирозинкінази та фармацевтична композиція на їх основі</a>
Попередній патент: Ординарне міцне червоне вино та спосіб його виробництва
Наступний патент: Штемпельна фарба
Випадковий патент: Застосування сполук, що відкривають калієві канали kcnq, для лікування дефіциту уваги/гіперактивності (adhd) або агресії












