Амінотриазоли як інгібітори p13k
Номер патенту: 102828
Опубліковано: 27.08.2013
Автори: Нойбауер Гітте, Міддлмісс Девід, Тейлор Джесс, Рамсден Найджел, Сунозе Міхіро, Белл Кетрін, Кенсфілд Ендрю
Формула / Реферат
1. Сполука формули (І)
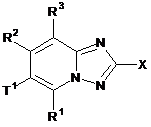 (І)
(І)
або її фармацевтично прийнятні солі, де
X означає NH2;
R1, R2, R3 незалежно вибрані з групи, яку складають Н; галоген; CN; C(O)OR4; OR4; C(O)R4; C(O)N(R4R4a); S(O)2N(R4R4a); S(O)N(R4R4a); S(O)2R4; S(O)R4; N(R4)S(O)2N(R4aR4b); N(R4)S(O)N(R4aR4b); SR4; N(R4R4a); OC(O)R4; N(R4)C(O)R4a; N(R4)S(O)2R4a; N(R4)S(O)R4a; N(R4)C(O)N(R4aR4b); N(R4)C(O)OR4a; OC(O)N(R4R4a) та C1-6алкіл, де C1-6алкіл є необов'язково заміщеним одним або кількома галогенами, які є однаковими або різними;
R4, R4a, R4b незалежно вибрані з групи, яку складають Н та C1-6алкіл, де C1-6алкіл є необов'язково заміщеним одним або кількома галогенами, які є однаковими або різними;
Т1 означає 4-7-членний гетероцикліл; 9-11-членний гетеробіцикліл; феніл; нафтил; інденіл або інданіл; де Т1 є необов'язково заміщеним одним або кількома R5 та/або одним або кількома R6;
R5 означає галоген; CN; C(O)OR7; OR7; оксо (=O), де кільце є щонайменше частково заміщеним; C(O)R7; C(O)N(R7R7a); S(O)2N(R7R7a); S(O)N(R7R7a); S(O)2R7; S(O)R7; N(R7)S(O)2N(R7aR7b); N(R7)S(O)N(R7aR7b); SR7; N(R7R7a); OC(O)R7; N(R7)C(O)R7; N(R7)S(O)2R7a; N(R7)S(O)R7a; N(R7)C(O)N(R7aR7b); N(R7)C(O)OR7a; OC(O)N(R7R7a) або C1-6алкіл, де C1-6алкіл є необов'язково заміщеним одним або кількома R8;
R6 означає Т2; C(O)OR9; OR9; C(O)R9; C(O)N(R9R9a); S(O)2N(R9R9a); S(O)N(R9R9a); S(O)2R9; S(O)R9; N(R9)S(O)2N(R9aR9b); N(R9)S(O)N(R9aR9b); SR9; N(R9R9a); OC(O)R9; N(R9)C(O)R9a; N(R9)S(O)2R9a; N(R9)S(O)R9a; N(R9)C(O)N(R9aR9b); N(R9)C(O)OR9a; OC(O)N(R9R9a) або C1-6алкіл, заміщений одним або кількома Т2 та необов'язково заміщений одним або кількома R8;
R9, R9a, R9b незалежно вибрані з групи, яку складають R9c та R9d, за умови, що принаймні один з R9, R9a, R9b означає R9c;
R9c означає Т2 або C1-6алкіл, де C1-6алкіл є заміщеним одним або кількома Т2 і є необов'язково заміщеним одним або кількома R8;
R7, R7a, R7b, R9d незалежно вибрані з групи, яку складають Н та C1-6алкіл, де C1-6алкіл є необов'язково заміщеним одним або кількома R8;
R8 означає галоген; CN; C(O)OR10; OR10; C(O)R10; C(O)N(R10R10a); S(O)2N(R10R10a); S(O)N(R10R10a); S(O)2R10; S(O)R10; N(R10)S(O)2N(R10aR10b); N(R10)S(O)N(R10aR10b); SR10; N(R10R10a); OC(O)R10; N(R10)C(O)R10a; N(R10)S(O)2R10a; N(R10)S(O)R10a; N(R10)C(O)N(R10aR10b); N(R10)C(O)OR10a; OC(O)N(R10R10a) або C1-6алкіл, де C1-6алкіл є необов'язково заміщеним одним або кількома галогенами, які є однаковими або різними;
R10, R10a, R10b незалежно вибрані з групи, яку складають Н та C1-6алкіл, де C1-6алкіл є необов'язково заміщеним одним або кількома галогенами, які є однаковими або різними;
Т2 означає С3-7циклоалкіл, 4-7-членний гетероцикліл, 9-11-членний гетеробіцикліл; феніл; нафтил; інденіл або інданіл, де Т2 є необов'язково заміщеним одним або кількома R11;
R11 означає галоген; CN; C(O)OR12; OR12; оксо (=O), де кільце є щонайменше частково насиченим; C(O)R12; C(O)N(R12R12a); S(O)2N(R12R12a); S(O)N(R12R12a); S(O)2R12; S(O)R12; N(R12)S(O)2N(R12aR12b); N(R12)S(O)N(R12aR12b); SR12; N(R12R12a); OC(O)R12; N(R12)C(O)R12a; N(R12)S(O)2R12a; N(R12)S(O)R12a; N(R12)C(O)N(R12aR12b); N(R12)C(O)OR12a; OC(O)N(R12R12a) або C1-6алкіл, де C1-6алкіл є необов'язково заміщеним одним або кількома галогенами, які є однаковими або різними;
R12, R12a, R12b незалежно вибрані з групи, яку складають Н та C1-6алкіл, де C1-6алкіл є необов'язково заміщеним одним або кількома галогенами, які є однаковими або різними.
2. Сполука за п. 1, де R1 і R2 незалежно означають Н або СН3.
3. Сполука за будь-яким з пп. 1 або 2, де R3 означає Н, СН3 або галоген.
4. Сполука за будь-яким з пп. 1-3, де Т1 означає незаміщений феніл; заміщений феніл; незаміщений 4-7-членний гетероцикліл; заміщений 4-7-членний гетероцикліл; незаміщений 9-11-членний гетеробіцикліл або заміщений 9-11-членний гетеробіцикліл.
5. Сполука за будь-яким з пп. 1-4, де Т1 є необов'язково заміщений одним R5, двома R5, одним R6, двома R6 або одним R5 та одним R6.
6. Сполука за будь-яким з пп. 1-5, де Т1 означає феніл; піроліл; фурил; тієніл; піразоліл; оксазоліл; тіазоліл; піридил та їх н-оксиди; піримідиніл; індоліл; індолініл; індазоліл; хінолініл; ізохінолініл; бензодіоксоліл; дигідробензофурил; дигідробензоксазиніл; дигідробензодіоксиніл; бензодіоксаніл або діоксид бензотіазолу.
7. Сполука за будь-яким з пп. 1-6, де Т1 означає феніл або піридил.
8. Сполука за будь-яким з пп. 1-7, де R5 означає оксо (=O), причому кільце є щонайменше частково заміщеним; F; Сl; CN; N(R7R7a); OR7; C(O)OR7; C(O)N(R7R7a); N(R7)S(O)2R7a; S(O)2N(R7R7a); S(O)2R7; S(O)R7; N(R7)C(O)R7a або C1-6алкіл, який є необов'язково заміщеним одним або кількома R8.
9. Сполука за будь-яким з пп. 1-8, де R7, R7a є незалежно вибраними з групи, яку складають Н; СН3; СН2СН3; н-бутил; трет-бутил; ізопропіл; н-пентил; ізопентил; неопентил; 2-етилбутил; CF3; СН2СН2ОН; СН2СН2СН2ОН; СН2С(СН3)2СН2ОН; CH2CH2OCH3; CH2CH2NH2; CH2CF3; CH2CH2CF3; CH2CH2CH2CF3; C(CH3)2CF3; CH2CH2NHCH3; CH2CH2N(CH3)2; CH2CH2CH2N(CH3)2; CH2C(O)OH і CH2C(O)N(CH3)2.
10. Сполука за будь-яким з пп. 1-9, де R8 означає F; Сl; Вr; ОН; СН3 або СН2СН3.
11. Сполука за будь-яким з пп. 1-10, де R5 означає оксо (=O), причому кільце є щонайменше частково заміщеним; F; Сl; NH2; NH(CH3); N(CH3)2; NH(CH2)2OH; N((CH2)2OH)2; OH; OCH3; OCF3; OCH(CH3)2; CH2OH; CH2OCH3; CH2Br; CH3; CH2CH3; CH(CH3)2; C(CH3)3; CF3; C(O)OH; C(O)OCH3; C(O)OCH2CH3; C(O)NH2; C(O)NH(CH3); C(O)(CH3)2; C(O)NHCH2CH3; C(O)N(CH3)CH2CH3; C(O)NHCH2CH2OH; C(O)N(CH3)CH2CH2OH; C(O)NHCH2CH2OCH3; C(O)N(CH3)CH2CH2OCH3; C(O)NHCH2CH2NH2; C(O)N(CH3)CH2CH2NH2; C(O)NHCH2CH2NHCH3; C(O)N(CH3)CH2CH2NHCH3; C(O)NHCH2CH2N(CH3)2; C(O)N(CH3)CH2CH2N(CH3)2; HNC(O)H3; S(O)2CH3; S(O)CH3; S(O)2NH2; S(O)2NHC(CH3)3; S(O)2NHCH2CH(CH2CH3)2; S(O)2NH(CH2)2OH; S(O)2NH(CH2)2CF3; S(O)2NH(CH2)3CF3; S(O)2NH(CH2)3OH; S(O)2NHCH2C(CH3)2CH2OH; S(O)2NH(CH2)2OCH3 або NHS(O)2CH3.
12. Сполука за будь-яким з пп. 1-11, де R6 означає S(O)2N(R9R9a); N(R9)S(O)2R9a; S(O)2R9; OR9 або SR9.
13. Сполука за будь-яким з пп. 1-12, де R6 означає S(O)2N(R9cR9d); N(R9d)S(O)2R9c; S(O)2R9c або OR9c.
14. Сполука за будь-яким з пп. 1-13, де R9c означає Т2; СН2-Т2 або С1-4алкіл-Т2.
15. Сполука за будь-яким з пп. 1-14, де R9d означає Н або метил.
16. Сполука за будь-яким з пп. 1-15, де Т2 означає феніл; нафтил; С3-4циклоалкіл або 4-7-членний гетероцикліл, в якому Т2 є необов'язково заміщеним до трьох разів R11.
17. Сполука за будь-яким з пп. 1-16, де Т2 означає азетидиніл; імідазолідиніл; піролідиніл; піперидиніл; піперазиніл; ізоіндолініл; оксазоліл; дигідроізохінолініл; морфолініл; піраніл; азепаніл; азетидиніл; діоксид тіаморфоліну; циклопропіл; циклобутил; циклопентил; циклогексил; циклогептил; феніл або нафтил.
18. Сполука за будь-яким з пп. 1-17, де R11 означає оксо (=O), де кільце є щонайменше частково насиченим; F; Сl; СН3; СН2СН3; СН2СН2СН3; СН(СН3)2; CF3; OH; ОСН3; OCF3; NH2; NHCH3; N(CH3)2.
19. Сполука за п. 1 формули (Ia)
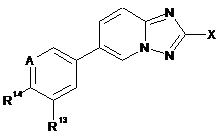 , (Ia)
, (Ia)
в якій
X має значення, вказані в п. 1;
А означає СН або N;
R14 означає Н або R5;
R13 означає Н; R5 або R6.
20. Сполука за п. 19, де R13 означає R5 або R6.
21. Сполука за п. 19 або 20, де R14 означає Н; ОН або ОСН3.
22. Сполука за п. 1, вибрана з групи, яку складають
3-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(2-гідроксіетил)бензолсульфонамід;
6-(5-метансульфонілпіридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-іламін;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)піридин-3-сульфонової кислоти бутиламід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-2-метоксифенол;
1-(6-(3,4-диметоксифеніл)-[1,2,4]триазоло[1,5-а]піридин-2-іл)сечовина;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)піридин-3-сульфонової кислоти трет-бутиламід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)піридин-3-сульфонової кислоти бензиламід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)піридин-3-сульфонової кислоти (2-етилбутил)амід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)піридин-3-сульфонової кислоти (4-хлорфеніл)амід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)піридин-3-сульфонової кислоти (3,5-бістрифторметилфеніл)амід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)піридин-3-сульфонової кислоти (4-фторфеніл)амід;
6-(3-метансульфонілфеніл)-[1,2,4]триазоло[1,5-а]піридин-2-іламін;
6-(3,4-диметоксифеніл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
3-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(2-аміноетил)бензолсульфонамід;
6-(3-ізопропокси-4-метоксифеніл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
4-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-2-метоксифенол;
3-(2-амiно-[1,2,4]триазоло[1,5-а]пiридин-6-iл)-N-бутилбензолсульфонамід;
4,4,4-трифторбутан-1-сульфонової кислоти [5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)піридин-3-іл]амід;
N-[5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)піридин-3-іл]-3-трифторметилбензолсульфонаміду НСl-сіль;
N-[5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)піридин-3-іл]-2-трифторметилбензолсульфонаміду НСl-сіль;
N-[5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)піридин-3-іл]-4-трифторметилбензолсульфонаміду НСl-сіль;
нафталін-2-сульфонової кислоти [5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)піридин-3-іл]аміду НСl-сіль;
N-[5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)піридин-3-іл]-4-ізопропілбензолсульфонаміду НСl-сіль;
нафталін-1-сульфонової кислоти [5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)піридин-3-іл]аміду НСl-сіль;
N-[5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)піридин-3-іл]-4-хлорбензолсульфонаміду НСl-сіль;
6-(3,4-диметоксифеніл)-8-хлор-[1,2,4]триазоло[1,5-а]піридин-2-іламін;
N-[5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)піридин-3-іл]-3-трифторметоксибензолсульфонамід НСl;
N-[5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)піридин-3-іл]-С-(2-трифторметилфеніл)метансульфонамід НСl;
N-[5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)піридин-3-іл]-С-(4-трифторметилфеніл)метансульфонамід НСl;
N-[5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)піридин-3-іл]-С-(4-хлорфеніл)метансульфонамід НСl;
N-[5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)піридин-3-іл]-3,5-бістрифторметилбензолсульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(4-(трифторметил)феніл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(2-(трифторметил)феніл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(3-(трифторметил)феніл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-метил-N-(3-(трифторметил)феніл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(4-(трифторметокси)феніл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-фенілпіридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(3-(трифторметокси)феніл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(3-(1,1,2,2-тетрафторетокси)феніл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(3-(дифторметокси)феніл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(4-(дифторметокси)феніл)піридин-3-сульфонамід;
6-(5-(трифторметил)піридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
6-(4-ізопропокси-3-метоксифеніл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(2-метил-1-(піролідин-1-іл)пропан-2-іл)піридин-3-сульфонамід;
6-(5-(4-фторпіперидин-1-ілсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
6-(5-(4-метилпіперизин-1-ілсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
2-(5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)піридин-3-сульфоамідо)-N,N-диметилацетамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(2-(оксоімідазолідин-1-іл)етил)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(2-(диметиламіно)етил)-метилпіридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(3-(диметиламіно)пропіл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-бутил-N-метилпіридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-ізопентилпіридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(циклопропілметил)піридин-3-сульфонамід;
6-(5-ізоіндолін-2-ілсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
6-(5-піперазин-1-ілсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-бензил-N-метилпiридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-((2,4-диметилоксазол-5-іл)метил)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-бензил-N-бутилпіридин-3-сульфонамід;
6-(5-(3,4-дигідроізохінолін-2(1Н)-ілсульфоніл)піридин-3-іл-[1,2,4]триазоло[1,5-а]піридинамін;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-iл)-N-(2,3-дихлорбензил)-N-метилпіридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-циклопропіл-N-(2-фторбензил)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(2-фенілпропан-2-іл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(2-(4-фторфеніл)пропан-2-іл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(4-фторбензил)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N,N-діетилпіридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(1,1,1-трифтор-2-метилпропан-2-іл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-бутилпіридин-3-сульфонамід;
6-(5-(морфоліносульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(3,3,3-трифторпропіл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N,N-диметилпіридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-неопентилпіридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-циклопентилпіридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(3,4-дихлорбензил)піридин-3-сульфонамід;
3-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(2-(диметиламіно)етил)бензолсульфонамід;
3-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(2-(диметиламіно)етил)-N-метилбензолсульфонамід;
3-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-трет-бутилбензолсульфонамід;
2-(3-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)фенілсульфонамідо)оцтова кислота;
3-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(3-(диметиламіно)пропіл)бензолсульфонамід;
6-(5-хлорпіридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-циклопропілпіридин-3-сульфонамід;
6-(5-(піролідин-1-ілсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-трет-бутил-N-метилпіридин-3-сульфонамід;
6-(5-(піперидин-1-ілсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-ізобутилпіридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-ізопропілпіридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(2,3-дихлорбензил)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-пропілпіридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(2,2,2-трифторетил)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-циклогексилпіридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(тетрагідро-2Н-піран-4-іл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-((тетрагідро-2Н-піран-4-іл)метил)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(4-гідроксициклогексил)піридин-3-сульфонамід;
6-(5-(4,4-дифторпіперидин-1-ілсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
6-(5-(азепан-1-ілсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
6-(5-(азетидин-1-ілсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(циклобутилметил)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-етилпіридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-метилпіридин-3-сульфонамід;
6-(3,4-диметоксифеніл)-8-фтор-[1,2,4]триазоло[1,5-а]піридин-2-амін;
6-(3,4-диметоксифеніл)-8-метил-[1,2,4]триазоло[1,5-а]піридин-2-амін;
6-(5-(бензилсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
6-(5-(трет-бутилсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-етил-N-метилпіридин-3-сульфонамід;
5-(2-аміно-8-фтор-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-трет-бутилпіридин-3-сульфонамід;
6-(5-ізобутоксипіридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
6-(5-(бензилокси)піридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
6-(5-феноксипіридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
6-(5-(неопентилокси)піридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
6-(5-(неопентилсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(циклопентилметил)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(циклогептилметил)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(3-ізопропілфеніл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(2-фторфеніл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(4-ізопропілфеніл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(2-метоксифеніл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(2,4-дифторфеніл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-трет-бутилнікотинамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(4-метоксифеніл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(3-фторфеніл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(3,4-дифторфеніл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(2-ізопропілфеніл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(3,5-дифторфеніл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(3-метоксифеніл)піридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(2,3-дифторфеніл)піридин-3-сульфонамід;
5-(2-амiно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(1-метилциклобутил)пiридин-3-сульфонамід;
5-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(2-аміноетил)піридин-3-сульфонамід;
5-(2-аміно-8-фтор-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-метилпіридин-3-сульфонамід;
5-(2-аміно-8-фтор-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-ізопропілпіридин-3-сульфонамід;
5-(2-аміно-8-фтор-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-пропілпіридин-3-сульфонамід;
6-(5-(азетидин-1-ілсульфоніл)піридин-3-іл)-8-фтор-[1,2,4]триазоло[1,5-а]піридин-2-амін;
5-(2-аміно-8-фтор-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-(2,2,2-трифторетил)піридин-3-сульфонамід;
5-(2-аміно-8-фтор-[1,2,4]триазоло[1,5-а]піридин-6-іл)-N-етил-N-метилпіридин-3-сульфонамід;
8-фтор-6-(3-(метилсульфоніл)феніл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
6-(6-аміно-5-(трифторметил)піридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
5-(3-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)фенілсульфонамідо)пентанова кислота;
4-(3-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)фенілсульфонамідо)бутанова кислота;
6-(5-(бензилтіо)піридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
8-фтор-6-(5-(трифторметил)піридин-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
6-(4-фторфеніл)-[1,2,4]триазоло[1,5-а]піридин-2-аміну гідрохлорид;
6-(3-метоксифеніл)-[1,2,4]триазоло[1,5-а]піридин-2-аміну гідрохлорид;
6-(3,4,5-триметоксифеніл)-[1,2,4]триазоло[1,5-а]піридин-2-аміну гідрохлорид;
6-м-толіл-[1,2,4]триазоло[1,5-а]піридин-2-амін;
3-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)бензонітрил;
6-(3-хлорфеніл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
6-феніл-[1,2,4]триазоло[1,5-а]піридин-2-амін;
6-(2-метоксифеніл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
6-(3-(етиламіно)феніл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
4-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)бензамід;
6-(піримідин-5-іл)-[1,2,4]триазоло[1,5-а]піридин-2-аміну гідрохлорид;
6-(1-метил-1Н-піразол-4-іл)-[1,2,4]триазоло[1,5-а]піридин-2-аміну гідрохлорид;
3-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)фенол;
6-(3-(трифторметил)феніл)-[1,2,4]триазоло[1,5-а]піридин-2-аміну гідрохлорид;
6-(бензо[d][1,3]діоксол-5-іл)-[1,2,4]триазоло[1,5-а]піридин-2-аміну гідрохлорид;
6-(3,4-диметоксифеніл)-7-метил-[1,2,4]триазоло[1,5-а]піридин-2-аміну гідрохлорид;
6-(3,4-дифторфеніл)-[1,2,4]триазоло[1,5-а]піридин-2-аміну гідрохлорид;
6-(3-фторфеніл)-[1,2,4]триазоло[1,5-а]піридин-2-аміну гідрохлорид;
6-(4-метоксифеніл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
N-(3-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)феніл)ацетамід;
6-(2,3-дигідробензо[b][1,4]діоксин-6-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
3-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)бензолсульфонамід;
4-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)бензолсульфонамід;
3-(2-аміно-[1,2,4]триазоло[1,5-а]піридин-6-іл)бензойна кислота;
6-(піридин-4-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
6-(1Н-піразол-3-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін;
6-(тіофен-2-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін та
6-(1Н-піразол-4-іл)-[1,2,4]триазоло[1,5-а]піридин-2-амін.
23. Фармацевтична композиція, яка містить сполуку або її фармацевтично прийнятну сіль за будь-яким з пп. 1-22 разом з фармацевтично прийнятним носієм.
24. Фармацевтична композиція за п. 23 в комбінації з одним або кількома іншими фармацевтичними композиціями.
25. Фармацевтична композиція за п. 23 або 24, яка містить одну або кілька додаткових сполук або їх фармацевтично прийнятних солей, вибраних з групи, яку складають сполуки за будь-яким з пп. 1-22, які відрізняються від першої сполуки; інші РІ3К інгібітори, стероїди, антагоністи лейкотриєну, антигістамінні засоби, циклоспорин або рапаміцин.
26. Сполука або її фармацевтично прийнятна сіль за будь-яким з пп. 1-22 для застосування як лікарського засобу.
27. Сполука або її фармацевтично прийнятна сіль за будь-яким з пп. 1-22 для застосування в способі лікування або запобігання захворюванням та розладам, пов'язаним з РІ3К.
28. Застосування сполуки або її фармацевтично прийнятної солі за будь-яким з пп. 1-22 для виробництва лікарського засобу для лікування або профілактики захворювань та розладів, пов'язаних з РІ3К.
29. Застосування сполуки або її фармацевтично прийнятної солі за будь-яким з пп. 1-22 для виробництва лікарського засобу для лікування або профілактики імунологічних, запальних, аутоімунних або алергійних розладів.
30. Застосування за п. 29 для виробництва лікарського засобу для лікування або профілактики аутоімунних захворювань; відторгнення трансплантованого органа або кісткового мозку; реакції "трансплантат проти хазяїна"; гострого або хронічного запалення; панкреатиту; контактного дерматиту; псоріазу; ревматоїдного артриту; розсіяного склерозу; діабету типу І; запального захворювання кишечнику; хвороби Крона; виразкового коліту; системного червоного вовчака; астми; хронічної обструктивної легеневої хвороби (COPD); гострого респіраторного дистрес-синдрому (ARDS); бронхіту; кон'юнктивіту; дерматиту; алергійного риніту; гострого подагричного запалення; кістозного фіброзу; спадкової середньоземноморської лихоманки; ушкодження тканин після бактеріальної інфекції; синдрому Світа або анафілаксії.
31. Застосування сполуки або її фармацевтично прийнятної солі за будь-яким з пп. 1-22 для виробництва лікарського засобу для лікування або профілактики раку, серцево-судинних розладів, метаболічних захворювань, нейродегенеративних розладів або інфекційних захворювань.
32. Спосіб лікування, контролювання, уповільнення або запобігання у ссавця, що потребує лікування, одному або кільком станам, вибраним з групи, яку складають захворювання та розлади, пов'язані з РІ3К, де спосіб включає введення зазначеному ссавцю терапевтично ефективної кількості сполуки за будь-яким з пп. 1-22 або її фармацевтично прийнятної солі.
33. Спосіб лікування, контролювання, уповільнення або запобігання у ссавця, що потребує лікування, одному або кільком станам, вибраним з групи, яку складають імунологічні; запальні, аутоімунні та алергійні розлади, де спосіб включає введення згаданому ссавцю терапевтично ефективної кількості сполуки за будь-яким з пп. 1-22 або її фармацевтично прийнятна солі.
34. Спосіб за п. 33, в якому один або кілька станів вибрані з групи, яку складають аутоімунні захворювання; відторгнення трансплантованого органа або кісткового мозку; реакція "трансплантат проти хазяїна"; гостре або хронічне запалення; панкреатит; контактний дерматит; псоріаз; ревматоїдний артрит; розсіяний склероз; діабет типу І; запальне захворювання кишечнику; хвороба Крона; виразковий коліт; системний червоний вовчак; астма; хронічна обструктивна легенева хвороба (COPD); гострий респіраторний дистрес-синдром (ARDS); бронхіт; кон'юнктивіт; дерматит; алергійний риніт; гостре подагричне запалення; кістозний фіброз; спадкова середньоземноморська лихоманка; ушкодження тканин після бактеріальної інфекції; синдром Світа або анафілаксія.
35. Спосіб лікування, контролювання, уповільнення або запобігання у ссавця, який потребує лікування, одному або кільком станам, вибраним з групи, яку складають рак, серцево-судинні розлади, метаболічні захворювання, нейродегенеративні розлади, інфекційні захворювання, де спосіб включає введення згаданому ссавцю терапевтично ефективної кількості сполуки за будь-яким з пп. 1-22 або її фармацевтично прийнятна солі.
36. Спосіб одержання сполуки за будь-яким з пп. 1-22, який включає стадію
взаємодії триазолу формули (II)
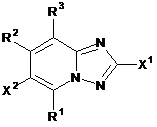 , (II)
, (II)
в якій X2 означає Вr або B(OR)2;
R1, R2, R3 мають значення, вказані в п. 1, і
X1 є таким, як X, що визначений в п. 1,
з бороновою кислотою або естером T1-B(OR)2 або T1-Вr,
де R означає Н або придатний естерний залишок,
в реакції Сузукі з одержанням сполуки формули (І).
37. Спосіб одержання сполуки за будь-яким з пп. 1-22, який включає стадію взаємодії триазолу формули (II)
 , (II)
, (II)
в якій X2 означає Вr або B(OR)2;
R1, R2, R3 мають значення, вказані в п. 1, і
X1 є таким, як X, що визначений в п. 1, в захищеній формі Х-Pro, де Pro означає захисну групу,
з бороновою кислотою або естером T1-B(OR)2 або Т1-Вr,
де R означає Н або придатний естерний залишок,
в реакції Сузукі з одержанням сполуки формули (І) після відщеплення захисної групи.
38. Спосіб за п. 37, в якому захисною групою є ацетил.
Текст
Реферат: Винахід стосується сполук формули (І) R R 3 2 N N T1 R 1 X N , (І) 1 1 3 в якій X, Т і R -R мають значення, зазначені в описі та формулі винаходу. Згадані сполуки є корисними як інгібітори протеїнкіназ, особливо інгібітори РІ3К, для лікування або профілактики імунологічних, запальних, аутоімунних або алергійних розладів. Винахід також стосується фармацевтичних композицій, які включають згадані сполуки, препаратів таких сполук, а також одержання їх та застосування як лікарських засобів. UA 102828 C2 (12) UA 102828 C2 R3 R T 2 N N N 1 R1 X (I) UA 102828 C2 5 10 15 20 25 30 35 40 45 50 55 60 Представлений винахід відноситься до нового класу інгібіторів кінази, включаючи їх фармацевтично прийнятні солі, проліки та метаболіти, які є придатними для модулювання активності протеїнкінази, для модулювання клітинної активності, такої як сигнальна трансдукція, проліферація, диференціація, запрограмована загибель клітин, міграція та секреція цитокінів. Більш конкретно, винахід стосується сполук, що інгібують, регулюють та/або модулюють активність кіназ, зокрема, активність PI3K, та шляхи сигнальної трансдукції, які стосуються клітинної активності, як згадувалося вище. Крім того, даний винахід стосується фармацевтичних композицій, які містять згадані сполуки, наприклад, для лікування захворювань, таких як імунологічні, запальні та алергійні розлади, та способів одержання таких сполук. Протеїн- та ліпідкінази приймають участь в сигнальних реакціях, які контролюють активацію, ріст, диференціацію та виживання клітин у відповідь на екстрацелюлярні медіатори або подразники, такі як фактори росту, цитокіни або хемокіни. Загалом, протеїнкінази діляться на дві групи, протеїнкінази, що переважно фосфорилюють тирозинові залишки, та протеїнкінази, що переважно фосфорилюють серинові та/або треонінові залишки в білкових субстратах. На відміну від цього, ліпідкінази фосфорилюють цілий ряд білкових субстратів. Висока активність протеїн- та ліпідкіназ недоречно залучається в багато захворювань, що включають рак, метаболічні розлади, імунологічні захворювання та запальні захворювання. Це може відбуватися або безпосередньо, або опосередковано як результат розладів контрольних механізмів внаслідок мутації, надекспресії або неадекватної активації ферменту. У всіх цих випадках очікується, що селективне інгібування кінази повинно мати корисний терапевтичний ефект. Фосфоінозитид 3-кінази (також згадувані як фосфатидилінозитол 3-кінази, PI3Ks) є групою ліпідкіназ, що відіграють головну роль у численних внутрішньоклітинних передачах сигналів. Деякі члени родини PI3K також виявляють активність протеїнкіназ. (Cantley, 2002, Science 296(5573):1655-7; Vanhaesebroeck та ін., 2001, Annu. Rev. Biochem. 70:535-602; Bondeva та ін., 1998, Science 282(5387):293-6). PI3Ks належить до суперродини сигнальних ліпідних кіназ, що каталізують фосфорилювання фосфатидилінозитол-4,5-бісфосфату (PtdIns(4,5)P2 або фосфатидилінозитолу (PtdIns) по 3′-OH групі, викликаючи утворення вторинних месенджерів фосфатидилінозитол-3,4,5-трифосфату (PtdIns(3,4,5)P3) або фосфатидилінозитол-3-фосфату (PtdIns(3)P). PtdIns(3,4,5)P3 може бути перетворений на PtdIns(3,4)P2 SH2-вмісною інозитолфосфатазою (SHIP), або може бути дефосфорильований фосфатазою та бензиновим гомологом фосфатази (PTEN) з регенерацією PtdIns(4,5)P2. 3′-Фосфорильовані фосфоінозитиди, PtdIns(3,4,5)P3, PtdIns(3,4)P2 PtdIns(4,5)P2, PtdIns(5)P та PtdIns(3)P, мобілізують та активують різні сигнальні білки (PtdIns-зв'язувальні білки; PtdIns-BPs) шляхом безпосередніх ліпід–протеїнових взаємодій (Fruman та ін., 1998, Annu. Rev. Biochem. 67:481507; Hawkins та ін., 2006, Biochem. Soc. Trans. 34:647-62). Фосфатидилінозитол-3,4,5-трифосфат (PtdIns(3,4,5)P3) грає важливу роль як вторинний месенджер, який працює як стиковочна платформа для ліпід-зв'язувальних доменів, таких як плекстрин-гомологічні (PH) домени різних клітинних білків. Вони включають кінази (такі як 3фосфоінозитид-залежна протеїнкіназа 1 (PDK1) та протеїнкіназа B (PKB)/Akt), що ініціюють даунстрім кіназний каскад, та фактори обміну гуанінових нуклеотидів (такі як Vav та P-Rex), які контролюють активність невеликих GTP-аз (Wymann та ін., 2005, Curr Opin Cell Biol. 17(2):141-9; Wymann та ін., 2003, Trends Pharmacol. Sci. 24(7):366-76). Вважається, що активація PI3-кіназ повинна залучатися в численні провідні шляхи сигнальної трансдукції, включаючи ті, що є суттєвими для проліферації клітин, диференціації клітин, росту клітин, виживання клітин, апоптозу, адгезії, хемотаксису, інвазії, цитоскелетної перебудови, контракції, спрямованої міграції фагосом, інтернаціоналізації рецепторів, секреції, синтезу білків та шляхів метаболізму. Виявляється, що PI3K гамма (γ) та дельта (δ) ізоформи залучаються в ряд аспектів активації лейкоцитів (Rommel та ін., 2007, Nat. Rev. Immunol. 7(3):191-201; Ruckle та ін., 2006, Nat. Rev. Drug Discov. 5(11):903-18). Були ідентифіковані різні типи PI3K, які були згруповані на 3 класи відповідно до їх первинної та вторинної структур, способу регуляції та специфічності субстрату. До теперішнього часу найбільш обширно вивченим був клас I PI3K, який включає гетеродимерні білки, що складаються з каталітичної та регуляторної адаптерних субодиниць, природа яких визначає подальше підрозділення на класи IA та IB PI3K. Клас II PI3K використовує PtdIns як субстрат in vivo, утворюючи фосфатидилінозитол-3-фосфат (PtdIns(3)P). Були представлені певні докази того, що клас II ферментів, подібно до класу I, може бути активований зовнішніми подразниками через рецепторні тирозинкінази (RTKs), рецептори цитокінів та інтегрини, припускаючи роль цих ферментів в розвитку раку, загоюванні ран та інсуліновому сигналізуванні. Напроти, клас III 1 UA 102828 C2 5 10 15 20 25 30 35 40 45 50 55 60 PI3K, представлений єдиним видом (hVps34) у людей, має відносно високу активність навіть в дрімливих клітинах. Клас III представляє найбільш давню форму PI3K, і він використовує виключно PtdIns як субстрат для продукування PtdIns(3)P. Цей клас PI3Ks залучається в транспорт через ендоцитозні мембрани, визрівання фагосом та аутофагію (Falasca та ін., 2007, Biochem. Soc. Trans. 35:211-4; Lindmo та ін., 2006, J. Cell Sci. 119:605-14). Клас IA-PI3Kα, β та δ (PIK3CA, PIK3CB and PIK3CD) – складається з SH2-домен-вмісних регуляторних субодиниць (p85; п'ять окремих лізоформ з яких було ідентифіковано), що утворюють комплекс з однією з трьох каталітичних субодиниць, p110α, p110β або p110δ (Bader та ін., 2005, Nat. Rev. Cancer 5(12):921-9). Генетичний поліморфізм в межах PI3K шляху також пов'язують з підвищеним ризиком діабету 2 типу. Даунстрім рецептора інсуліноподібного фактора росту 1 (IGF1), що передає сигнали через клас I PI3K, контролює ріст та розвиток. Ускладнення структури та точкові мутації гена, що кодує PI3Kα, яка підвищує ферментну активність білка, часто знаходять в різних видах раку людини (Bader та ін., 2005, Nat. Rev. Cancer 5(12):921-9). Активація PI3K та продукування PIP3 є основою для більшості біологічних реакцій, що викликаються інсуліном. Активований рецептор інсуліну (IR) ініціює PI3K активність шляхом зв'язування та фосфорилювання адапторних білків родини субстратів рецепторів інсуліну (IRS). При фосфорилюванні IRS виступає у ролі докінг-сайта для p85 регуляторних субодиниць, що послідовно залучають p110 ферменти (головним чином, α та β ізоформи). В свою чергу, продукування PIP3 активує даунстрім-ефектори, що контролюють різні метаболічні процеси, такі як засвоювання глюкози, утворення тригліцеридів, синтез глікогену, ліполіз та інгібування печінкового глюконеогенезу (Knight та ін., 2006, Cell 125(4): 733-747; Foukas та ін., 2006, Nature, 441(7091):366-70). PI3Kβ залучається в регулювання утворення та стабільності інтегрину α(IIb)β(3), який є необхідним для активації та агрегації тромбоцитів. Були створені ізоформ-селективні PI3K p110β інгібітори, які in vivo усувають оклюзивне утворення тромбів, але не пролонгують час кровотечі. Ці дослідження визначили PI3K p110β як важливу нову мішень для антитромбозної терапії (Jackson та ін., 2005, Nat. Med. 11 (5):507-14). PI3Kδ головним чином експресується в гематопоетичній системі, і миші з дефіцитом PI3Kδ є життєздатними, фертильними, практично здоровими та мають нормальну тривалість життя (Vanhaesebroeck та ін., 2005. Trends in Biochemical Sciences 30, 194-204). PI3Kδ відіграють важливу роль в передачі сигналів T- та B-клітин, алергійних реакціях, опосередкованих тучними клітинами, оксидативному вибуху нейтрофілів та, можливо, крововиливі. Доповідалось, що PI3K інгібітори, селективні для PI3Kδ, блокують активацію нейтрофілів в тваринній моделі активації нейтрофілів, таким чином звертаючи увагу на PI3kδ як мішень для розробки протизапальних лікарських засобів (Sadhu та ін., 2003, Biochem. Biophys. Res. Communications 308, 764-769). PI3Kγ, єдиний член класу IB (PIK3CG), зв'язується з обома з двох регуляторних субодиниць, p101 і p84, що контролюють її активацію та внутрішньоклітинне розташування. Активація PI3Kγ керується безпосередньою асоціацією її каталітичного домену з βγ субодиницями G білків з наступною активацією Gαi-сполучених G-протеїн-сполучених рецепторів (GPCRs), чутливих до токсину коклюшу. Крім того, PI3Kγ можуть бути активовані за допомогою Ras шляхом безпосередньої взаємодії з каталітичною субодиницею. Крім своєї ліпідкіназної активності, PI3Kγ має протеїнкіназну активність. Вона використовує регуляторні субодиниці, а також саму себе як субстрат, і це приводить до підвищення ліпідкіназної активності (Leopoldt та ін., 1998, J. Biol. Chem. 273(12):7024-9). Інші білки, наприклад, фосфодіестерази (PDEs) можуть зв'язуватися з PI3Kγ, виявляючи функцію каркасного білка на додатокдо їх ферментної активності. Було також показано, що PI3Kγ активує MEK кіназу, а також опосередковує чутливе до здвигу ініціювання JNK кіназного шляху в ендотеліальних клітинах (Patrucco та ін., 2004, Cell 118(3):375-87; Voigt та ін., 2006, J. Biol. Chem. 281(15):9977-86). Мишачий PI3Kγ білок кодується Pik3cg локусом. Миші, що втратили функціональну PI3Kγ (PI3Kg-/- миші), були життєздатними, фертильними і виявляли нормальну тривалість життя в стандартних приміщеннях для утримання мишей. Подальші дослідження виявили, що нейтрофіли цих мишей були нездатними продукувати PtdIns (3,4,5) P3 при стимулюванні з використанням GPCR агоністів, таких як формільовані бактеріальні пептиди (N-форміл-Met-LeuPhe, fMLP), комплемент C5a або інтерлейкін 8 (IL-8). Таке спостереження демонструє, що PI3Kγ є єдиною PI3K ізоформою, що сполучається з цими GPCRs в нейтрофілах (Vanhaesebroeck та ін., 2005. Trends in Biochemical Sciences 30, 194-204). Крім того, Ptdlns (3, 4, 5) P3-залежна активація протеїнкінази B (PKB) була також відсутньою в таких нейтрофілах, в той час як PKB могла бути активованою з використанням GM-CSF або 2 UA 102828 C2 5 10 15 20 25 30 IgG/C3b-покритого зимосану. Pi3kcg-/- миші виявили послаблений ріст тимоцитів та збільшення популяцій нейтрофілів, моноцитів та еозинофілів. Крім того, нейтрофіли та макрофаги, виділені з Pi3kcg-/-мишей, виявили сильні дефекти в міграції та оксидативний вибух у реакції на GPCR агоністи та хемотаксичні агенти. Робота з такими мишами також виявила, що PI3Kγ потребує повернення дендритних клітин до лімфатичних вузлів і розвитку та активації T лімфоцитів (разом з PI3Kδ). Разом з IgE-залежною активацією PI3Kδ, PI3Kγ також сприяє активації секреції аденозином тучних клітин. Залучення її в стимулювання аутокринних та паракринних регуляторних петель пуринами також спостерігалось в інших типах клітин. PI3Kγ також сприяє активації агрегації тромбоцитів за допомогою ADP разом з PI3Kβ (Ferguson та ін., 2007, Nat. Cell Biol. 9(1):86-91). Узагальнюючи, вважається, що клас IB фосфоінозитид 3-кіназ PI3Kγ є головним в контролюванні спрямованої міграції лейкоцитів і, відповідно, розвиток ізотип-селективних інгібіторів PI3Kγ повинен бути привабливою стратегією протизапaльної терапії (Rommel та ін., 2007, Nat. Rev. Immunol. 7(3):191-201; Ruckle та ін., 2006, Nat. Rev. Drug Discov. 5(11):903-18). PI3Kγ відіграє вирішальну роль як в судинних клітинах, так і в білих клітинах крові. Вона контролює різноманітні імунні модуляторні та судинні функціях, такі як оксидативний вибух, оновлення клітин, реактивність тучних клітин, агрегація тромбоцитів, активація ендотелію, а також скорочення гладких м'язів. Взаємопов'язана ефективність таких процесів припускає, що блокування функції PI3Kγ може виявитися корисним для захворювань, таких як запалення, алергія, аутоімунне захворювання, тромбоз та основні серцево-судинні розлади, такі як гіпертензія та атеросклероз (Hirsch та ін., 2006, Thromb. Haemost. 95(1):29-35). Крім того, було продемонстровано, що PI3Kγ відіграє роль у мишачій моделі панкреатиту. Смертність від панкреатиту, викликаного дієтою з дефіцитом холіну та добавкою метіоніну, значно зменшувалася у мишей, позбавлених PI3Kγ (Lupia та ін., 2004. Am. J. Pathol. 165(6):2003-2011). Нещодавно повідомлялось про розробку ефективних та селективних PI3Kγ інгібіторів (Pomel та ін., 2006, J. Med. Chem. 49(13):3857-71; Palanki та ін., 2007. J. Med. Chem. 50(18):4279-4294). Таким чином, об'єктом даного винаходу є одержання нового класу сполук як інгібіторів кінази, зокрема PI3K інгібіторів, які можуть бути ефективними в лікуванні або профілактиці імунологічних, запальних, аутоімунних, алергійних розладів або інших захворювань або розладів, пов'язаних з PI3K. Крім того, іншим об'єктом даного винаходу є одержання згаданих сполук, які можуть бути ефективними в лікуванні або профілактиці раку або серцево-судинних розладів, пов'язаних з PI3K. Відповідно, даний винахід стосується сполук формули (I) R3 R 2 T1 35 40 45 50 55 N N N X (I) R1 або їх фармацевтично-прийнятних солей, проліків або метаболітів, де X означає OH; SH; NH2; NHC(O)NH2; або NHC(S)NH2; 1 2 3 4 4 4 R , R , R незалежно вибрані з групи, яку складають H; галоген; CN; C(O)OR ; OR ; C(O)R ; 4 4a 4 4a 4 4a 4 4 4 4a 4b C(O)N(R R ); S(O)2N(R R ); S(O)N(R R ); S(O)2R ; S(O)R ; N(R )S(O)2N(R R ); 4 4a 4b 4 4 4a 4 4 4a 4 4a 4 4a N(R )S(O)N(R R ); SR ; N(R R ); °C(O)R ; N(R )C(O)R ; N(R )S(O)2R ; N(R )S(O)R ; 4 4a 4b 4 4a 4 4a N(R )C(O)N(R R ); N(R )C(O)OR ; °C(O)N(R R ); та C1-6 алкіл, де C1-6 алкіл є необов'язково заміщеним одним або кількома галогенами, які є однаковими або різними; 4 4a 4b R , R , R незалежно вибрані з групи, яку складають H; та C1-6 алкіл, де C1-6 алкіл є необов'язково заміщеним одним або кількома галогенами, які є однаковими або різними; 1 T означає 4-7-членний гетероцикліл; 9-11-членний гетеробiцикліл; феніл; нафтил; інденіл; 1 5 або інданіл; де T є необов'язково заміщеним одним або кількома R та/або одним або кількома 6 R; 5 7 7 R означає галоген; CN; C(O)OR ; OR ; оксо (=O), декільце є щонайменше частково 7 7 7a 7 7a 7 7a 7 7 заміщеним; C(O)R ; C(O)N(R R ); S(O)2N(R R ); S(O)N(R R ); S(O)2R ; S(O)R ; 7 7a 7b 7 7a 7b 7 7 7a 7 7 7 7 7a N(R )S(O)2N(R R ); N(R )S(O)N(R R ); SR ; N(R R ); °C(O)R ; N(R )C(O)R ; N(R )S(O)2R ; 7 7a 7 7a 7b 7 7a 7 7a N(R )S(O)R ; N(R )C(O)N(R R ); N(R )C(O)OR ; °C(O)N(R R ); або C1-6 алкіл, де C1-6 алкіл є 8 необов'язково заміщеним одним або кількома R ; 6 2 9 9 9 9 9a 9 9a 9 9a 9 R означає T ; C(O)OR ; OR ; C(O)R ; C(O)N(R R ); S(O)2N(R R ); S(O)N(R R ); S(O)2R ; 9 9 9a 9b 9 9a 9b 9 9 9a 9 9 9a S(O)R ; N(R )S(O)2N(R R ); N(R )S(O)N(R R ); SR ; N(R R ); °C(O)R ; N(R )C(O)R ; 9 9a 9 9a 9 9a 9b 9 9a 9 9a N(R )S(O)2R ; N(R )S(O)R ; N(R )C(O)N(R R ); N(R )C(O)OR ; °C(O)N(R R ); або C1-6 алкіл, 2 8 заміщений одним або кількома T та необов'язково заміщений одним або кількома R ; 3 UA 102828 C2 9 5 10 15 20 25 30 35 40 45 50 55 60 9a 9b 9c 9d R , R , R незалежно вибрані з групи, яку складають R та R , за умови, що принаймні 9 9a 9b 9c один з R , R , R означає R ; 9c 2 2 R означає T або C1-6 алкіл, де C1-6 алкіл є заміщеним одним або кількома T і є 8 необов'язково заміщеним одним або кількома R ; 7 7a 7b 9d R , R , R , R незалежно вибрані з групи, яку складають H та C 1-6 алкіл, де C1-6 алкіл є 8 необов'язково заміщеним одним або кількома R ; 8 10 10 10 10 10a 10 10a R означає галоген; CN; C(O)OR ; OR ; C(O)R ; C(O)N(R R ); S(O)2N(R R ); 10 10a 10 10 10 10a 10b 10 10a 10b 10 S(O)N(R R ); S(O)2R ; S(O)R ; N(R )S(O)2N(R R ); N(R )S(O)N(R R ); SR ; 10 10a 10 10 10a 10 10a 10 10a 10 10a 10b N(R R ); °C(O)R ; N(R )C(O)R ; N(R )S(O)2R ; N(R )S(O)R ; N(R )C(O)N(R R ); 10 10a 10 10a N(R )C(O)OR ; °C(O)N(R R ) або C1-6 алкіл, де C1-6 алкіл є необов'язково заміщеним одним або кількома галогенами, які є однаковими або різними; 10 10a 10b R , R , R незалежно вибрані з групи, яку складають H та C 1-6 алкіл, де C1-6 алкіл є необов'язково заміщеним одним або кількома галогенами, які є однаковими або різними; 2 T означає C3-7 циклоалкіл, 4-7-членний гетероцикліл, 9-11-членний гетеробiцикліл; феніл; 2 11 нафтил; інденіл або інданіл, де T є необов'язково заміщеним одним або кількома R ; 11 12 12 R означає галоген; CN; C(O)OR ; OR ; оксо (=O), де кільце є щонайменше частково 12 12 12a 12 12a 12 12a 12 12 насиченим; C(O)R ; C(O)N(R R ); S(O)2N(R R ); S(O)N(R R ); S(O)2R ; S(O)R ; 12 12a 12b 12 12a 12b 12 12 12a 12 12 12a N(R )S(O)2N(R R ); N(R )S(O)N(R R ); SR ; N(R R ); °C(O)R ; N(R )C(O)R ; 12 12a 12 12a 12 12a 12b 12 12a 12 12a N(R )S(O)2R ; N(R )S(O)R ; N(R )C(O)N(R R ); N(R )C(O)OR ; °C(O)N(R R ) або C1-6 алкіл, де C1-6 алкіл є необов'язково заміщеним одним або кількома галогенами, які є однаковими або різними; 12 12a 12b R , R , R незалежно вибрані з групи, яку складають H та C 1-6 алкіл, де C1-6 алкіл є необов'язково заміщеним одним або кількома галогенами, які є однаковими або різними. У випадку, якщо перемінний параметр або замісник можуть бути вибрані з групи різних варіантів, і такий перемінний параметр або замісник зустрічається більше, ніж один раз, відповідні варіанти можуть бути однаковими або різними. В контексті даного винаходу використовувані терміни мають наступні значення: "Алкіл" означає вуглеводневий лінійний або розгалужений ланцюг, що може містити подвійні або потрійні зв'язки. Загалом переважним є, коли алкіл не містить подвійні або потрійні зв'язки. Таким чином, термін "алкіл" включає, в контексті даного винаходу, алкільні групи, такі як алкенільні та алкінільні групи. Кожний водень алкільного вуглецю може бути замінений на замісник. "C1-4 Алкіл" означає алкільний ланцюг, що має 1-4 атоми вуглецю, наприклад, якщо він присутній в кінці молекули: метил, етил, -CH=CH2, -CCH, н-пропіл, iзoпропіл, -CH=CH-CH3, CH2-CH=CH2, н-бутил, iзoбутил, -CH=CH-CH2-CH3, -CH=CH-CH=CH2, втор-бутил, трет-бутил, або, наприклад, -CH2-, -CH2-CH2-, -CH=CH-, -CH(CH3)-, -C(CH2)-, -CH2-CH2-CH2-, -CH(C2H5)-, CH(CH3)2-, якщо алкільною групою зв'язані два залишки молекули. Переважно, C 1-4 алкіл включає метил, етил, н-пропіл, iзoпропіл, н-бутил, ізобутил, втор-бутил та трет-бутил. Кожний водень C1-4 алкільного вуглецю може бути замінений на замісник. "C1-6 Алкіл" означає алкільний ланцюг, що має 1-6 атомів вуглецю, наприклад, якщо він присутній в кінці молекули: C1-4 алкіл, метил, етил, -CH=CH2, -CCH, н-пропіл, iзoпропіл, CH=CH-CH3, -CH2-CH=CH2, н-бутил, ізобутил, -CH=CH-CH2-CH3, -CH=CH-CH=CH2, втор-бутил; трет-бутил, н-пентил, н-гексил, або, наприклад, -CH2-, -CH2-CH2-, -CH=CH-, -CH(CH3)-, -C(CH2)-, -CH2-CH2-CH2-, -CH(C2H5)-, -CH(CH3)2-, якщо алкільною групою зв'язані два залишки молекули. Переважно, C1-6 алкіл включає метил, етил, н-пропіл, iзoпропіл, н-бутил, ізобутил, втор-бутил та трет-бутил, н-пентил та н-гексил. Кожний водень C1-6 алкільного вуглецю може бути замінений на замісник. "C3-7 Циклоалкіл" або "C3-7 циклоалкільне кільце" означає циклічний алкільний ланцюг, що має 3-7 атомів вуглецю, наприклад, циклопропіл, циклобутил, циклопентил, циклогексил, циклогексеніл, циклогептил. Кожний водень C1-4 алкільного вуглецю може бути замінений на замісник. "Галоген" означає фтор, хлор, бром або йод. Загалом перевага серед галогенів надається фтору або хлору. "4-7-Членний гетероцикліл" або "4-7-членний гетероцикл" означає кільце з 4, 5, 6 або 7 кільцевими атомами, що може мати до максимальної кількості подвійних зв'язків (ароматичне або неароматичне кільце, яке є повністю або частково насиченим або ненасиченим), в якому щонайменше один кільцевий атом і до 4 кільцевих атомів замінені на гетероатом, вибраний з групи, яку складають сірка (включаючи -S(O)-, -S(O)2-), кисень та азот (включаючи =N(O)-), і де кільце зв'язане із залишком молекули через атом вуглецю або азоту. Прикладами 4-7-членних гетероциклів є азетидин, оксетан, тіетан, фуран, тіофен, пірол, піролін, імідазол, імідазолін, 4 UA 102828 C2 5 10 15 20 25 30 35 40 45 50 55 піразол, піразолін, оксазол, оксазолін, iзоксазол, iзоксазолін, тіазол, тіазолін, iзoтіазол, iзoтіазолін, тіадіазол, тіадіазолін, тетрагідрофуран, тетрагідротіофен, піролідин, імідазолідин, піразолідин, оксазолідин, ізоксазолідин, тіазолідин, ізотіазолідин, тіадіазолідин, сульфолан, піран, дигідропіран, тетрагідропіран, імідазолідин, піридин, піридазин, піразин, піримідин, піперазин, піперидин, морфолін, тетразол, триазол, триазолідин, тетразолідин, діазепан, азепін або гомопіперазин. "9-11-Членний гетеробiцикліл" або "9-11-членний гетеробіцикл" означає гетероциклічну систему з двох кілець з 9-11 кільцевими атомами, де щонайменше один кільцевий атом належить одночасно обом кільцям, і кільця можуть мати до максимальної кількості подвійних зв'язків (ароматичне або неароматичне кільце, яке є повністю або частково насиченим або ненасиченим), де щонайменше один кільцевий атом і до 6 кільцевих атомів замінені на гетероатом, вибраний з групи, яку складають сірка (включаючи -S(O)-, -S(O)2-), кисень та азот (включаючи =N(O)-), і де кільце зв'язане із залишком молекули через атом вуглецю або азоту. Прикладами 9-11-членних гетеробіциклів є індол, індолін, бнзофуран, бензотіофен, бензоксазол, бензізоксазол, бензотіазол, бензiзoтіазол, бензімідазол, бензімідазолін, хінолін, хіназолін, дигідрохіназолін, хінолін, дигідрохінолін, тетрагідрохінолін, декагідрохінолін, iзoхінолін, декагідроiзoхінолін, тетрагідроiзoхінолін, дигідроiзoхінолін, бензазепін, пурин або птеридин. Термін 9-11-членний гетеробіцикл також включає спіро-структури двох кілець, такі як 1,4-діокса-8-азаспіро[4.5]декан або містковані гетероцикли, такі як 8-азабiцикло[3.2.1]октан. Переважними сполуками формули (I) є сполуки, в яких один або кілька залишків, що містяться в них, мають значення, наведені нижче, з усіма комбінаціями переважних визначень замісників, що є предметом даного винаходу. Що стосується усіх переважних сполук формули (I), то даний винахід також включає усі таутомерні та стереоізомерні форми та їх суміші у всіх співвідношеннях, а також їх фармацевтично-прийнятні солі. Те ж саме стосується переважних сполук формули (Ia). В переважних втіленнях даного винаходу замісники, зазначені нижче, незалежно мають наступні значення. Таким чином, один або кілька таких замісників можуть мати переважні або більш переважні значення, подані нижче. Переважно X означає NH2, NC(O)NH2 або NC(S)NH2, більш переважно X означає NH2 або NC(O)NH2; ще більш переважно X означає NH2. 1 2 1 2 Переважно R і R незалежно означають H або CH3. Ще більш переважно R і R означають H. 3 3 Переважно R означає H, галоген або CH3. Ще більш переважно R означає H або F. 1 Переважно T означає незаміщений феніл; заміщений феніл; незаміщений 4-7- членний гетероцикліл; заміщений 4-7-членний гетероцикліл; незаміщений 9-11-членний гетеробiцикліл; або заміщений 9-11-членний гетеробiцикліл. 1 5 5 6 6 Переважно T є незаміщеним або заміщеним одним R , двома R , одним R , двома R , або 5 6 одним R та одним R . 1 Переважно T означає феніл; піроліл; фурил; тієніл; піразоліл; оксазоліл; тіазоліл; піридил та його н-оксид; піримідиніл; індоліл; індолініл; індазоліл; хінолініл; iзoхінолініл; бензодіоксоліл; дигідробензофурил; дигідробензоксазиніл; дигідробензодіоксиніл; бензодіоксаніл; або діоксид 1 бензотіазолу. Більш переважно T означає феніл або піридил. 5 Переважно R означає оксо (=O), де кільце є щонайменше частково заміщеним; F; Cl; CN; 7 7a 7 7 7 7a 7 7a 7 7a 7 7 N(R R ); OR ; C(O)OR ; C(O)N(R R ); N(R )S(O)2R ; S(O)2N(R R ); S(O)2R ; S(O)R ; 7 7a 8 N(R )C(O)R або C1-6 алкіл, який є необов'язково заміщеним одним або кількома R . 7 7a Переважно R , R є незалежно вибраними з групи, яку складають H; CH 3; CH2CH3; н-бутил; трет-бутил; iзo-пропіл; н-пентил; iзoпентил; нeoпентил; 2-етилбутил; CF3; CH2CH2OH; CH2CH2CH2OH; CH2C(CH3)2CH2OH; CH2CH2OCH3; CH2CH2NH2; CH2CF3; CH2CH2CF3; CH2CH2CH2CF3; C(CH3)2CF3; CH2CH2NHCH3; CH2CH2N(CH3)2; CH2CH2CH2N(CH3)2; CH2C(O)OH та CH2C(O)N(CH3)2. 8 Переважно R означає F; Cl; Br; OH; CH3 або CH2CH3. 5 Переважно R означає оксо (=O), де кільце є щонайменше частково заміщеним; F; Cl; NH 2; NH(CH3); N(CH3)2; NH(CH2)2OH; N((CH2)2OH)2; OH; OCH3; OCF3; OCH(CH3)2; CH2OH; CH2OCH3; CH2Br; CH3; CH2CH3; CH(CH3)2; C(CH3)3; CF3; C(O)OH; C(O)OCH3; C(O)OCH2CH3; C(O)NH2; C(O)NH(CH3); C(O)(CH3)2; C(O)NHCH2CH3; C(O)N(CH3)CH2CH3; C(O)NHCH2CH2OH; C(O)N(CH3)CH2CH2OH; C(O)NHCH2CH2OCH3; C(O)N(CH3)CH2CH2OCH3; C(O)NHCH2CH2NH2; C(O)N(CH3)CH2CH2NH2; C(O)NHCH2CH2NHCH3; C(O)N(CH3)CH2CH2NHCH3; C(O)NHCH2CH2N(CH3)2; C(O)N(CH3)CH2CH2N(CH3)2; HNC(O)H3; S(O)2CH3; S(O)CH3; S(O)2NH2; S(O)2NHC(CH3)3; S(O)2NHCH2CH(CH2CH3)2; S(O)2NH(CH2)2OH; S(O)2NH(CH2)2CF3; 5 UA 102828 C2 5 10 15 S(O)2NH(CH2)3CF3; S(O)2NH(CH2)3OH; S(O)2NHCH2C(CH3)2CH2OH; S(O)2NH(CH2)2OCH3 або NHS(O)2CH3. 6 9 9a 9 9a 9 9 9 Переважно R означає S(O)2N(R R ); N(R )S(O)2R ; S(O)2R ; OR або SR . 6 9c 9d 9d 9c 9c 9c Переважно R означає S(O)2N(R R ); N(R )S(O)2R ; S(O)2R або OR . 9c 2 2 2 Переважно R означає T ; CH2-T або C1-4 алкіл-T . 9d Переважно R означає H або метил. 2 Переважно T означає феніл; нафтил; C3-4 циклоалкіл або 4-7-членний гетероцикліл, 2 11 причому T є необов'язково заміщеним до трьох разів R . 2 Переважно T означає азетидиніл; імідазолідиніл; піролідиніл; піперидиніл; піперазиніл; iзoіндолініл; оксазоліл; дигідроiзохінолініл; морфолініл; піраніл; азепаніл; азетидиніл; діоксид тіаморфоліну; циклопропіл; циклобутил; циклопентил; циклогексил; циклогептил; феніл або нафтил. 11 Переважно R означає оксо (=O), де кільце є щонайменше частково насиченим; F; Cl; CH 3; CH2CH3; CH2CH2CH3; CH(CH3)2; CF3; OH; OCH3; OCF3; NH2; NHCH3; N(CH3)2. Сполуками, яким надають перевагу, є сполуки формули (Ia) N (Ia) X N N A R14 20 25 30 35 40 45 50 55 , R 13 в якій X має значення, вказані вище; A означає CH або N; 14 5 R означає H або R ; 13 5 6 R означає H; R або R . 13 5 6 Переважно R означає R або R . 14 Переважно R означає H; OH або OCH3. Сполуки формули (I), в якій деякі або всі з вищезгаданих груп мають переважні значення, є також предметом даного винаходу. Те ж саме відноситься і до сполук формули (Ia). Іншими переважними сполуками даного винаходу є сполуки, що вибрані з групи, яку складають 3-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(2-гідроксиетил)бензолсульфонамід; 6-(5-Метансульфонілпіридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-іламін; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)піридин-3-сульфонової кислоти бутиламід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-2-метоксифенол; 1-(6-(3,4-Диметоксифеніл)-[1,2,4]триазоло[1,5-a]піридин-2-іл)сечовина; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)піридин-3-сульфонової кислоти трет-бутиламід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)піридин-3-сульфонової кислоти бензиламід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)піридин-3-сульфонової кислоти (2-етилбутил)амід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)піридин-3-сульфонової кислоти (4-хлорфеніл)амід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)піридин-3-сульфонової кислоти (3,5-бістрифторметилфеніл)амід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)піридин-3-сульфонової кислоти (4-фторфеніл)амід; 6-(3-Метансульфонілфеніл)-[1,2,4]триазоло[1,5-a]піридин-2-іламін; 6-(3,4-Диметоксифеніл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 3-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(2-аміноетил)бензолсульфонамід; 6-(3-Ізопропокси-4-метоксифеніл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 4-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-2-метоксифенол; 3-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-бутилбензолсульфонамід; 4,4,4-Трифторбутан-1-сульфонової кислоти [5-(2-аміно-[1,2,4]триазоло[1,5-a]піридин-6іл)піридин-3-іл]амід; N-[5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)піридин-3-іл]-3трифторметилбензолсульфонаміду HCl сіль; N-[5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)піридин-3-іл]-2трифторметилбензолсульфонаміду HCl сіль; 6 UA 102828 C2 5 10 15 20 25 30 35 40 45 50 55 60 N-[5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)піридин-3-іл]-4трифторметилбензолсульфонаміду HCl сіль; Нафталін-2-сульфонової кислоти [5-(2-аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)піридин-3іл]аміду HCl сіль; N-[5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)піридин-3-іл]-4-iзoпропілбензолсульфонаміду HCl сіль; Нафталін-1-сульфонової кислоти [5-(2-аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)піридин-3іл]аміду HCl сіль; N-[5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)піридин-3-іл]-4-хлорбензолсульфонаміду HCl сіль; 6-(3,4-Диметоксифеніл)-8-хлор-[1,2,4]триазоло[1,5-a]піридин-2-іламін; N-[5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)піридин-3-іл]-3трифторметоксибензолсульфонамід HCl; N-[5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)піридин-3-іл]-C-(2трифторметилфеніл)метансульфонамід HCl; N-[5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)піридин-3-іл]-C-(4трифторметилфеніл)метансульфонамід HCl; N-[5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)піридин-3-іл]-C-(4хлорфеніл)метансульфонамід HCl; N-[5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)піридин-3-іл]-3,5-бістрифторметилбензолсульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(4-(трифторметил)феніл)піридин-3сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(2-(трифторметил)феніл)піридин-3сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(3-(трифторметил)феніл)піридин-3сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-метил-N-(3-(трифторметил)феніл)піридин-3сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(4-(трифторметокси)феніл)піридин-3сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-фенілпіридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(3-(трифторметокси)феніл)піридин-3сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(3-(1,1,2,2-тетрафторетокси)феніл)піридин3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(3-(дифторметокси)феніл)піридин-3сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(4-(дифторметокси)феніл)піридин-3сульфонамід; 6-(5-(Трифторметил)піридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 6-(4-Ізопропокси-3-метоксифеніл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(2-метил-1-(піролідин-1-іл)пропан-2іл)піридин-3-сульфонамід; 6-(5-(4-Фторпіперидин-1-ілсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 6-(5-(4-Метилпіперизин-1-ілсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 2-(5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)піридин-3-сульфоамідо)-N, Nдиметилацетамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(2-(оксоімідазолідин-1-іл)етил)піридин-3сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(2-(диметиламіно)етил)-N-метилпіридин-3сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(3-(диметиламіно)пропіл)піридин-3сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-бутил-N-метилпіридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-iзoпентилпіридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(циклопропілметил)піридин-3-сульфонамід; 6-(5-Ізоіндолін-2-ілсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 6-(5-Піперазин-1-ілсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-бензил-N-метилпіридин-3-сульфонамід; 7 UA 102828 C2 5 10 15 20 25 30 35 40 45 50 55 60 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-((2,4-диметилоксазол-5-іл)метил)піридин-3сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-бензил-N-бутилпіридин-3-сульфонамід; 6-(5-(3,4-Дигідроізохінолін-2(1H)-ілсульфоніл)піридин-3-іл-[1,2,4]триазоло[1,5-a]піридинамін; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(2,3-дихлорбензил)-N-метилпіридин-3сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-циклопропіл-N-(2-фторбензил)піридин-3сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(2-фенілпропан-2-іл)піридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(2-(4-фторфеніл)пропан-2-іл)піридин-3сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(4-фторбензил)піридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N, N-діетилпіридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(1,1,1-трифтор-2-метилпропан-2-іл)піридин3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)піридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-бутилпіридин-3-сульфонамід; 6-(5-(Морфоліносульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(3,3,3-трифторпропіл)піридин-3сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N, N-диметилпіридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-неопентилпіридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-циклопентилпіридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(3,4-дихлорбензил)піридин-3-сульфонамід; 3-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(2-(диметиламіно)етил)бензолсульфонамід; 3-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(2-(диметиламіно)етил)-Nметилбензолсульфонамід; 3-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-трет-бутилбензолсульфонамід; 2-(3-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)фенілсульфонамідо)оцтова кислота; 3-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(3(диметиламіно)пропіл)бензолсульфонамід; 6-(5-Хлорпіридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-циклопропілпіридин-3-сульфонамід; 6-(5-(Піролідин-1-ілсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-трет-бутил-N-метилпіридин-3-сульфонамід; 6-(5-(Піперидин-1-ілсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-ізобутилпіридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-iзoпропілпіридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(2,3-дихлорбензил)піридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-пропілпіридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(2,2,2-трифторетил)піридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-циклогексилпіридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(тетрагідро-2H-піран-4-іл)піридин-3сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-((тетрагідро-2H-піран-4-іл)метил)піридин-3сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(4-гідроксициклогексил)піридин-3сульфонамід; 6-(5-(4,4-Дифторпіперидин-1-ілсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 6-(5-(Азепан-1-ілсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 6-(5-(Азетидин-1-ілсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(циклобутилметил)піридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-етилпіридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-метилпіридин-3-сульфонамід; 6-(3,4-Диметоксифеніл)-8-фтор-[1,2,4]триазоло[1,5-a]піридин-2-амін; 6-(3,4-Диметоксифеніл)-8-метил-[1,2,4]триазоло[1,5-a]піридин-2-амін; 6-(5-(Бензилсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 6-(5-(трет-Бутилсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-етил-N-метилпіридин-3-сульфонамід; 5-(2-Аміно-8-фтор-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-трет-бутилпіридин-3-сульфонамід; 8 UA 102828 C2 5 10 15 20 25 30 35 40 45 50 55 60 6-(5-Ізобутоксипіридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 6-(5-(Бензилокси)піридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 6-(5-Феноксипіридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 6-(5-(Неoпентилoxy)піридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 6-(5-(Неoпентилсульфоніл)піридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(циклопентилметил)піридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(циклогептилметил)піридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(3-iзoпропілфеніл)піридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(2-фторфеніл)піридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(4-iзoпропілфеніл)піридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(2-метоксифеніл)піридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(2,4-дифторфеніл)піридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-трет-бутилнікотинамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(4-метоксифеніл)піридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(3-фторфеніл)піридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(3,4-дифторфеніл)піридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(2-iзoпропілфеніл)піридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(3,5-дифторфеніл)піридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(3-метоксифеніл)піридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(2,3-дифторфеніл)піридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(1-метилциклобутил)піридин-3-сульфонамід; 5-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(2-аміноетил)піридин-3-сульфонамід; 5-(2-Аміно-8-фтор-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-метилпіридин-3-сульфонамід; 5-(2-Аміно-8-фтор-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-iзoпропілпіридин-3-сульфонамід; 5-(2-Аміно-8-фтор-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-пропілпіридин-3-сульфонамід; 6-(5-(Азетидин-1-ілсульфоніл)піридин-3-іл)-8-фтор-[1,2,4]триазоло[1,5-a]піридин-2-амін; 5-(2-Аміно-8-фтор-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-(2,2,2-трифторетил)піридин-3сульфонамід; 5-(2-Аміно-8-фтор-[1,2,4]триазоло[1,5-a]піридин-6-іл)-N-етил-N-метилпіридин-3-сульфонамід; 8-Фтор-6-(3-(метилсульфоніл)феніл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 6-(6-Аміно-5-(трифторметил)піридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 5-(3-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)фенілсульфонамідо)пентанова кислота; 4-(3-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)фенілсульфонамідо)бутанова кислота; 6-(5-(Бензилтіо)піридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 8-Фтор-6-(5-(трифторметил)піридин-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 6-(4-Фторфеніл)-[1,2,4]триазоло[1,5-a]піридин-2-аміну гідрохлорид; 6-(3-Метоксифеніл)-[1,2,4]триазоло[1,5-a]піридин-2-аміну гідрохлорид; 6-(3,4,5-Триметоксифеніл)-[1,2,4]триазоло[1,5-a]піридин-2-аміну гідрохлорид; 6-м-Толіл-[1,2,4]триазоло[1,5-a]піридин-2-амін; 3-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)бензонітрил; 6-(3-Хлорфеніл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 6-Феніл-[1,2,4]триазоло[1,5-a]піридин-2-амін; 6-(2-Метоксифеніл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 6-(3-(Етиламіно)феніл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 4-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)бензамід; 6-(Піримідин-5-іл)-[1,2,4]триазоло[1,5-a]піридин-2-аміну гідрохлорид; 6-(1-Метил-1H-піразол-4-іл)-[1,2,4]триазоло[1,5-a]піридин-2-аміну гідрохлорид; 3-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)фенол; 6-(3-(Трифторметил)феніл)-[1,2,4]триазоло[1,5-a]піридин-2-аміну гідрохлорид; 6-(Бензо[d][1,3]діоксол-5-іл)-[1,2,4]триазоло[1,5-a]піридин-2-аміну гідрохлорид; 6-(3,4-Диметоксифеніл)-7-метил-[1,2,4]триазоло[1,5-a]піридин-2-аміну гідрохлорид; 6-(3,4-Дифторфеніл)-[1,2,4]триазоло[1,5-a]піридин-2-аміну гідрохлорид; 6-(3-Фторфеніл)-[1,2,4]триазоло[1,5-a]піридин-2-аміну гідрохлорид; 6-(4-Метоксифеніл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; N-(3-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)феніл)ацетамід; 6-(2,3-Дигідробензо[b][1,4]діоксин-6-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 3-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)бензолсульфонамід; 4-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)бензолсульфонамід; 3-(2-Аміно-[1,2,4]триазоло[1,5-a]піридин-6-іл)бензойна кислота; 6-(Піридин-4-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 9 UA 102828 C2 5 10 15 20 25 30 35 40 45 50 55 60 6-(1H-Піразол-3-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; 6-(Тіофен-2-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін; та 6-(1H-Піразол-4-іл)-[1,2,4]триазоло[1,5-a]піридин-2-амін. Проліки сполук даного винаходу також входять в об'єм винаходу. Термін "проліки" означає похідну, яка перетворюється в сполуку згідно з даним винаходом шляхом взаємодії з ферментом, шлунковою кислотою або подібними у фізіологічних умовах живого організму, наприклад, оксидуванням, відновленням, гідролізом або подібними процесами, кожний з яких здійснюється під дією ферментів. Прикладами проліків є сполуки, в яких аміногрупа в сполуці згідно з даним винаходом ацильована, алкілована або фосфорильована з утворенням, наприклад, ейкозаноїламіно, аланіламіно, півалоїлоксиметиламіно, або в яких гідроксильна група ацильована, алкілована, фосфорильована або перетворена на борат, наприклад, ацетилокси, пальмітоїлокси, півалоїлокси, сукцинілокси, фумарилокси, аланілокси, або в яких карбоксильна група є естерифікованою або амідованою. Такі сполуки можуть бути отримані із сполук даного винаходу у відповідності з добре відомими методиками. Метаболіти сполук формули (I) також входять в об'єм даного винаходу. Термін "метаболіти" стосується усіх молекул, що утворюються з будь-якої із сполук згідно з даним винаходом в клітині або організмі, переважно, у ссавця. Переважно термін стосується молекул, що відрізняються від будь-якої молекули, що присутня в будь-якій клітини або організмі у фізіологічних умовах. Структура метаболітів сполук згідно з даним винаходом буде очевидною для будь-якого фахівця в даній галузі з використанням різних придатних методів. У випадку, якщо може спостерігатися таутомерія, така як, наприклад, кето-енольна таутомерія, сполук загальної формули (I), індивідуальні форми, такі як, наприклад, кето- та фенольна форма, існують окремо та разом у вигляді сумішей у будь-якому співвідношенні. Те ж саме відноситься і до стереоізомерів, таких як, наприклад, енантіомери, цис/транс ізомери, конформери та ін. При необхідності ізомери можуть бути розділені способами, добре відомими в галузі, наприклад, рідинною хроматографією. Те ж саме відноситься і до енантіомерів, де використовуються, наприклад, хіральні стаціонарні фази. Крім того, енантіомери можуть бути виділені шляхом перетворення їх на діастереомери, тобто, шляхом сполучення з енантіомерно чистою допоміжною сполукою, з наступним відокремленням одержаних діастереомерів та відщепленням допоміжного залишку. Альтернативно, будь-який енантіомер сполуки формули (I) може бути отриманий стереоселективним синтезом з використанням оптично-чистих вихідних речовин. У випадку, коли сполуки формули (I) містять одну або кілька кислотних або основних груп, винахід також включає їх відповідні фармацевтично або токсикологічно прийнятні солі, зокрема, солі, придатні для фармацевтичного застосування. Таким чином, сполуки формули (I), які містять кислотні групи, можуть використовуватися згідно з винаходом, наприклад, у вигляді солей лужних металів, солей лужноземельних металів або у вигляді амонієвих солей. Більш конкретно, приклади таких солей включають солі натрію, солі кальцію, солі магнію або солі з аміаком або органічними амінами, такими як, наприклад, етиламін, етаноламін, триетаноламін або амінокислоти. Сполуки формули (I), які містять одну або кілька основних груп, тобто, груп, які можуть бути протоновані, можуть бути присутніми та можуть використовуватися згідно з винаходом у формі їх адитивних солей з неорганічними або органічними кислотами. Приклади придатних кислот включають хлорводневу, бромводневу, фосфорну кислоту, сірчану кислоту, азотну кислоту, метансульфонову кислоту, п-толуолсульфонову кислоту, нафталіндисульфонові кислоти, щавлеву кислоту, оцтову кислоту, винну кислоту, молочну кислоту, саліцилову кислоту, бензойну кислоту, мурашину кислоту, пропіонову кислоту, півалінову кислоту, діетилоцтову кислоту, малонову кислоту, бурштинову кислоту, пімелінову кислоту, фумарову кислоту, малеїнову кислоту, яблучну кислоту, сульфамінову кислоту, фенілпропіонову кислоту, глюконову кислоту, аскорбінову кислоту, ізонікотинову кислоту, лимонну кислоту, адипінову кислоту та інші кислоти, відомі фахівцеві в даній галузі. Якщо сполуки формули (I) одночасно містять кислотні та основні групи в молекулі, винахід також охоплює, крім згаданих сольових форм, внутрішні солі або бетаїни (цвіттер-іони). Відповідні солі згідно з формулою (I) можуть бути отримані звичайними способами, відомими фахівцям, такими як, наприклад, взаємодія солей з органічною або неорганічною кислотою або основою в розчиннику або диспергувальному агенті, аніонний обмін або катіонний обмін з іншими солями. Даний винахід також включає всі солі сполук формули (I), які, внаслідок низької фізіологічної сумісності, безпосередньо не є придатними для використання у фармацевтичних засобах, але 10 UA 102828 C2 5 10 15 20 25 30 35 40 45 50 55 60 які можуть використовуватися, наприклад, як проміжні сполуки для хімічних реакцій або для одержання фармацевтично прийнятних солей. Термін "фармацевтично прийнятні" означає схвалені регуляторним органом, таким як EMEA (Europe) (European Medicines Agency – Європейське Агентство лікарських засобів) та/або FDA (US) (Food and Drug Administration – Управління по контролю за продуктами та ліками) та/або будь-яким іншим національним регуляторним органом для застосування у тварин, переважно, людей. Даний винахід, крім того, включає всі сольвати сполук згідно з винаходом. Даний винахід стосується сполук формули (I) як інгібіторів кінази, зокрема, PI3K інгібіторів. Сполуки формули (I) можуть інгібувати одну або обидві з цих кіназ, необов'язково, на додаток до інших кіназ, згаданих вище, без будь-якого обмеження теорією. Відповідно, сполуки даного винаходу є придатними для запобігання або лікування імунологічних розладів (наприклад, імунних або аутоімунних захворювань), запальних захворювань або алергійних захворювань. Таким чином, іншим об'єктом даного винаходу є сполука винаходу або її фармацевтично прийнятна сіль для застосування як лікарський засіб. Іншим об'єктом даного винаходу є сполука або її фармацевтично прийнятна сіль згідно з даним винаходом для застосування в способі лікування та запобігання захворювань та розладів, пов'язаних з PI3K. Ще одним об'єктом даного винаходу є застосування сполуки даного винаходу або її фармацевтично прийнятної солі для виробництва лікарського засобу для лікування або профілактики захворювань та розладів, пов'язаних з PI3K, переважно PI3Kγ. Згідно з даним винаходом "PI3K" або "PI3 кін аза" включає всіх членів родини PI3K, яка включає клас IA (наприклад, PI3K альфа, бета та дельта), клас IB (наприклад, PI3K гамма), клас II (наприклад, PI3KC2 альфа, бета та гамма) та клас III (наприклад, Vps34 гомолог дріжджів). "PI3Kγ“ означає PI3Kγ білок, єдиний член PI3K класу IB (також згадуваний як p110-гамма). Була описана людська к днк, що кодує PI3Kγ білок довжиною 1050 амінокислотних залишків (Stoyanow та ін., 1995, Science 269:690-693). Людський PI3Kγ білок кодується PI3KCG геном, який містить 10 екзонів, та розташовується на хромосомі 7q22 (Kratz та ін., 2002, Blood 99:372374). "PI3Kδ” означає PI3Kδ білок, член PI3K класу IA (також згадуваний як p110-дельта). Була описана людська кДНК, що кодує PI3Kδ білок, який складається з 1044 амінокислот (Vanhaesebroeck та ін., 1997, Proc. Natl. Acad Sci. 94:4330-4335). Людський PI3Kδ білок кодується PI3KCD геном, який локалізується в хромосомі 1p3.2 (Seki та ін., 1997, DNA Research 4:355-358). Ще одним об'єктом даного винаходу є застосування сполуки даного винаходу або її фармацевтично прийнятної солі для виробництва лікарського засобу для лікування або профілактики імунологічних, запальних, аутоімунних або алергійних розладів. Більш конкретно, переважно розладами є аутоімунні захворювання; відторгнення трансплантованого органу або кісткового мозку; реакція "трансплантат проти хазяїна"; гостре або хронічне запалення; пакреатит; контактний дерматит; псоріаз; ревматоїдний артрит; розсіяний склероз; діабет типу I; запальне захворювання кишечника; хвороба Крона; виразковий коліт; системний червоний вовчак; астма; хронічна обструктивна легенева хвороба (COPD); гострий респіраторний дистрес-синдром (ARDS); бронхіт; кон'юнктивіт; дерматит; алергійний риніт; гостре подагричне запалення; кістозний фіброз; сімейна середньоземноморська лихоманка; ушкодження тканин після бактеріальної інфекції; синдром Світа або анафілаксія. Більш переважними є ревматоїдний артрит (RA), запальне захворювання кишечника (IBD), системний червоний вовчак (SLE), псоріаз, розсіяний склероз (MS), астма та хронічна обструктивна легенева хвороба (COPD). Ревматоїдний артрит (RA) є хронічним, прогресуючим, виснажливим запальним захворюванням, яке вражає приблизно 1 % населення світу. RA є симетричним багатосуглобовим артритом, що головним чином уражує невеликі суглоби рук та ніг. Крім запалення в синовіальній оболонці, вистилці, агресивна поверхня тканини, що зветься панусом, уражає та руйнує локальні структури суглобів (Firestein 2003, Nature 423:356-361). Запальне захворювання кишечника (IBD) характеризується хронічним рецидивуючим запаленням кишечника. IBD підрозділяється на хворобу Крона та виразковий коліт. Хвороба Крона найчастіше уражає клубову кишку та товстий кишечник, і є трансмуральною та навперемінною. На відміну від цього, при виразковому коліті запалення є постійним і обмежується слизовими оболонками прямої кишки та товстого кишечника. Приблизно в 10 % випадків, обмежених прямою кишкою та товстим кишечником, остаточна класифікація на 11 UA 102828 C2 5 10 15 20 25 30 35 40 45 50 55 60 хворобу Крона або виразковий коліт не може бути зроблена і використовується термін "недетермінований коліт". Обидва захворювання включають позакишкове запалення шкіри, очей або суглобів. Нейтрофіл-індукованим ушкодженням можна запобігти шляхом застосування інгібіторів міграції нейтрофілів (Asakura та ін., 2007, World J. Gastroenterol. 13(15):2145-9). Системний червоний вовчак (SLE) є хронічним запальним захворюванням, що викликається активацією В-клітин, опосередкованою T-клітинами, яке призводить до гломерулонефриту та ниркової недостатності. Людський SLE характеризується на ранніх стадіях розповсюдженням + тривалих аутореактивних CD4 клітин пам'яті (D'Cruz та ін., 2007, Lancet 369(9561):587-596). Псоріаз є хронічним запальним дерматозом, який вражає приблизно 2 % населення. Він характеризується червоними, лускатими шкірними плямами, які зазвичай розташовані на шкірі голови, ліктях та колінах, і можуть бути пов'язані з важким артритом. Такі плями викликаються аномальною проліферацією кератиноцитів та інфільтрацією запальних клітин в дерму та епідерму (Schön та ін., 2005, New Engl. J. Med. 352:1899-1912). Розсіяний склероз (MS) є запальним та демієлінізуючим неврологічним захворюванням. Вважалось, що він є аутоімунним розладом, опосередкованим 1T хелперними клітинами CD4+ типу, але нещодавні дослідження показали роль інших імунних клітин (Hemmer та ін., 2002, Nat. Rev. Neuroscience 3, 291-301). Астма є комплексним синдромом з багатьма клінічними фенотипами як у дорослих, так і у дітей. Її головними ознаками є різна ступінь обструкції дихальних шляхів, бронхіальна гіперчутливість та запалення дихальних шляхів (Busse and Lemanske, 2001, N. Engl. J. Med. 344:350-362). Хронічна обструктивна легенева хвороба (COPD) характеризується запаленням, обмеженням потоку дихання, що не є повністю зворотним, та поступовою втратою функції легенів. При COPD хронічне вдихання подразників викликає анормальну запальну реакцію, ремоделює дихальні шляхи та звуження потоку повітря в легенях. Подразником, що вдихають, зазвичай є тютюновий дим, але виробничий пил та забруднення навколишнього середовища також маються на увазі (Shapiro 2005, N. Engl. J. Med. 352, 2016-2019). Панкреатит є запаленням підшлункової залози. Гострий панкреатит є станом, який розвивається, коли підшлункова залоза ушкоджується запаленням, що призводить до опухання, а інколи до некрозу частини підшлункової залози (Carroll та ін., 2007. American Family Physiscian 75(1): 1513-1520). При хронічному панкреатиті обширне ушкодження підшлункової залози протягом багатьох років може викликати значне рубцювання та руйнування підшлункової залози. Було показано, що PI3Kγ відіграють значну роль в мишачій моделі панкреатиту. Смертність від панкреатиту, викликаного дієтою з дефіцитом холіну та добавкою метіоніну, значно зменшувалася у мишей, позбавлених PI3Kγ (Lupia та ін., 2004. Am. J. Pathol. 165(6):2003-2011). Гостре подагричне запалення є наслідком відкладення кристалів урату мононатрію в суглобах. Вважається, що нейтрофіли є головним ефектором гострої подагри, які накопичуються в суглобовій рідині, де вони активно захоплюють кристали уратів, агрегати та дегранулят. Гострому подагричному запаленню, а також іншим захворюванням, пов'язаним з відкладенням кристалів, таким як суглобовий хондрокальциноз, силікоз, відкладення кальцію в м'яких тканинах у пацієнтів з хронічною нирковою недостатністю, можна запобігти шляхом інгібування хемотаксису нейтрофілів (Ryckman та ін., 2003, Arthritis & Rheumatism 48 (8): 231020). Кістозний фіброз (CF) є спадковим розладом, що викликається мутаціями регулятора трансмембранної провідності кістозного фіброзу (CFTR), продуктом яких є мембранний протеїн, який, як вважається, діє як канал, що переносить іони хлору. Клінічні прояви летальних випадків без сумніву пов'язані з потовщеною, інфікованою слизовою оболонкою та хронічним запаленням дихальних шляхів, викликаним нейтрофілами. Протизапальний засіб з безпосередньою дією на нейтрофіли може представляти потенційний лікарський засіб для клінічного впливу на CF (McIntosh та ін., 1992, FASEB J 6:2775-82). Сімейна середньоземноморська лихоманка (FMF) є аутосомним рецесивним розладом, що характеризується рецидивними та оборотними нападами лихоманки та серозиту. Випадки запалення характеризуються масивним припливом нейтрофілів в серозні та синовіальні оболонки. Вторинний амілоїдоз, наслідок довготривалого запалення, є найбільш серйозним ускладненням хвороби. Інгібітори активації нейтрофілів можуть сприятливим чином впливати на послаблення захворювання (Molad Y та ін., 2004, J. Investig. Med. 52(1):58-61). Ушкодження тканин після гострої бактеріальної інфекції може бути частково результатом надмірної інфільтрації та активації нейтрофілів в інфікованій тканині. При пієлонефриті бактерія в нирковій паренхімі ініціює сплеск позасудинної міграції нейтрофілів. Експерименти на 12 UA 102828 C2 5 10 15 20 25 30 35 40 45 50 55 60 тваринних моделях показали, що рубцювання нирки після гострого бактеріального пієлонефриту є наслідком ушкодження паренхими нейтрофілами. Ушкодженням тканин після інфікування при пієлонефриті, остеомієліті, ендокардиті, ендотоксичному шоку та гострому респіраторному дистрес-синдромі, можна запобігти шляхом інгібування активації нейтрофілів (Bille та ін., 1982, J. Infect. Dis. 146:220-6). Синдром Світа (має назву - гострий фебрільний нейтрофільний дерматоз) характеризується сукупністю клінічних синдромів, які включають пірексію, підвищену кількість нейтрофілів, хворобливі еритематозні шкіряні плями та дифузний інфільтрат, що складається переважно із зрілих нейтрофілів, зазвичай локалізованих у верхньому шарі дерми. Інгібування активації нейтрофілів може представляти лікування для пацієнта, що страждає на сидром Світа (Cohen та ін., 2007, Orphanet J. Rare Dis. 2:34). Анафілаксія є гострою системною та важкою гіперчутливою алергійною реакцією типу І. Анафілактичний шок є найбільш важким типом анафілаксії. Анафілактичний шок є несподіваною, небезпечною для життя алергійною реакцією, пов'язаною з сильною гіпотензією. Фактор активації тромбоцитів (PAF) залучається в серцево-судинні дисфункції, які спостерігаються при різних синдромах шоку, включаючи анафілаксію. Надлишкове утворення вазодилататора NO викликає збуджувальну гіпотензію і шок. Дослідження показує важливу роль для eNOS ендотеліальної ізоформи синтази оксиду азоту як медіатора анафілаксії та визначає PI3K як нову потенційну мішень для лікування анафілаксії (Cauwels та ін., 2006, J. Clin. Invest. 116(8):2244-51). Захворюванням та розладами, пов'язаними, головним чином, з PI3K, є рак, серцево-судинні розлади, метаболічні захворювання, нейродегенеративні розлади або інфекційні захворювання. Ще одним аспектом даного винаходу є застосування сполуки даного винаходу або її фармацевтично прийнятної солі для виробництва лікарського засобу для лікування або профілактики раку, метаболічних захворювань, нейродегенеративних розладів, інфекційних хвороб або серцево-судинних розладів, більш конкретно, інфаркту міокарда, інсульту, ішемії або атеросклерозу. Рак включає групу захворювань, що характеризується неконтрольованим ростом та розповсюдженням анормальних клітин. Всі типи раку загалом включають певні аномалії в контролюванні росту клітин, ділення та виживання, що призводить до злоякісного росту клітин. Ключовими факторами, що сприяють згаданому злоякісному росту клітин, є незалежність від сигналів росту, нечутливість до сигналів анти-росту, уникання апоптозу, необмежений реплікаційний потенціал, безперервний ангіогенез, проникнення в тканини та метастазування і геномна нестабільність (Hanahan and Weinberg, 2000. The Hallmarks of Cancer. Cell 100, 57-70). Зазвичай, види раку включають гематологічний рак (наприклад, лейкемія та лімфома) та солідний рак, такий як саркома та карцинома (наприклад, рак мозку, молочної залози, легенів, товстого кишечника, шлунку, печінки, підшлункової залози, простати, яєчників). Ожиріння та цукровий діабет типу 2 є фактором ризику, що постійно зростає у всьому світі. Лептин, що секретується жировою тканиною та діє частково через його гіпоталамічний рецептор, об'єднує енергетичний стан периферійних органів та дію центральної нервової системи, інгібуючи споживання їжі та стимулюючи споживання енергії. Пептидний гормон інсулін, що виробляється підшлунковою залозою, проникає до центральної нервової системи (CNS) через гематоенцефалічний бар'єр шляхом рецептор-опосередкованого переносу для регулювання споживання їжі, симпатичної активності та периферійної дії інсуліну через інгібування печінкового глюконеогенезу та репродуктивної ендокринології. На молекулярному рівні деякі дії інсуліну збігаються з механізмом передачі сигналів лептину в місці активації фосфатидилінозитол 3-кінази (PI3K), що приводить до регулювання ATP-залежних калієвих каналів. У відповідності з цією думкою інтрацеребровентрикулярна (icv) ін'єкція PI3K інгібіторів частково знищує здатність як інсуліну,так і лептину інгібувати споживання їжі (Xu та ін., 2005, J. Clin. Inv., 115 (4): 951-8; Niswender та ін., 2003, Diabetes 52:227-231). Крім того, інсулін інгібує нейрональний апоптоз через активацію протеїнкінази B in vitro, та регулює фосфорилювання тау-білка, метаболізм амілоїдного прекурсорного білка та виведення бета-амілоїду з мозку in vivo. Ці дані вказують на те, що нейрональна IR передача сигналів відіграє безпосередню роль в зв'язку між енергетичним гомеостазом, репродукцією та розвитком нейродегенеративних захворювань (Plum та ін., 2005, Trends Endocrinol. Metab. 16(2):59-65). Лептин викликає уповільнений апоптоз зрілих нейтрофілів через сигнальний каскад, залучаючи PI3K (Bruno та ін., 2005, J. Immunol. 174: 8090-96). Інгібітори PI3K можуть виявитися корисними в лікуванні захворювань, в які залучаються процеси, зазначені вище. Нещодавня робота продемонструвала, що шлях передачі сигналів PI3K (фосфоінозитид 3кінази) є важливим для ефективної реплікації вірусу грипу A. Активація PI3K у вірус-інфікованих 13 UA 102828 C2 5 10 15 20 25 30 35 40 45 50 55 60 клітинах опосередковується вірусним NS1 білком, який зв'язується безпосередньо з p85бета регуляторною субодиницею PI3K та викликає PI3K-залежне фосфорилювання Akt (протеїнкінази B). Враховуючи той факт, що рекомбінантний вірус грипу A, який нездатний активувати передачу сигналів PI3K, послаблюється в культурі тканини, PI3K шлях може бути новою ціллю у створенні майбутніх протигрипозних лікарських засобів (Erhardt та ін., 2007, J. Virol. 81 (7): 3058-67; Hale та ін., 2006, PNAS 103, 14194-14199). Іншим об'єктом даного винаходу є спосіб лікування, контролювання, уповільнення або запобігання у ссавця, який потребує лікування, одного або кількох станів, вибраних з групи, яку складають захворювання або розлади, пов'язані з PI3K, який включає введення згаданому пацієнтові терапевтично ефективної кількості сполуки згідно з даним винаходом або її фармацевтично прийнятної солі. Ще одним об'єктом винаходу є спосіб лікування, контролювання, уповільнення або запобігання у ссавця, який потребує лікування, одного або кількох станів, вибраних з групи, яку складають імунологічні; запальні та алергійні розлади, який включає введення згаданому пацієнтові терапевтично ефективної кількості сполуки згідно з даним винаходом або її фармацевтично прийнятної солі. Більш конкретно один або кілька станів є вибраними з групи, яку складають аутоімунні захворювання; відторгнення трансплантату органу або кісткового мозку; реакція "трансплантат проти хазяїна"; гостре або хронічне запалення; панкреатит; контактний дерматит; псоріаз; ревматоїдний артрит; розсіяний склероз; діабет типу I; запальне захворювання кишечника; хвороба Крона; виразковий коліт; системний червоний вовчак; астма; хронічна обструктивна легенева хвороба (COPD); гострий респіраторний дистрес-синдром (ARDS); бронхіт; кон'юнктивіт; дерматит та алергійний риніт; гостре подагричне запалення; кістозний фіброз; сімейна середньоземноморська лихоманка; ушкодження тканин після бактеріальної інфекції; Синдром Світа або анафілаксія. Більш перевага надається ревматоїдному артриту (RA), запальному захворюванню кишечника (IBD), системному червоному вовчаку (SLE), псоріазу, розсіяному склерозу (MS), астмі та хронічній обструктивній легеневій хворобі (COPD). Ще одним іншим об'єктом даного винаходу є спосіб лікування, контролювання, уповільнення або запобігання у ссавця, який потребує лікування, одного або кількох станів, вибраних з групи, яку складають рак; метаболічне захворювання; нейродегенеративні розлади; інфекційні захворювання та серцево-судинні розлади, більш конкретно, інфаркт міокарда, інсульт, ішемія або атеросклероз, де спосіб включає введення зазначеному пацієнтові терапевтично ефективної кількості сполуки згідно з даним винаходом або її фармацевтично прийнятної солі. В даному контексті термін "лікування" або "терапія" стосується всіх процесів, в яких може відбуватися уповільнення, переривання, затримування або зупинка розвитку захворювання, але необов'язково вказує на загальне усунення всіх симптомів. Не обмежуючись теорією механізму дії, сполуки винаходу можуть також модулювати, на додаток або альтернативно, активацію імунних клітин шляхом інгібування PI3K. Особливо важлива роль PI3Kδ та PI3Kγ в передачі сигналів та інших функціях T клітин, B клітин, нейтрофілів, макрофагів і тучних клітин вказує на те, що ці кінази є ефективними терапевтичними мішенями для деяких захворювань, опосередкованих запаленням. Такі захворювання включають ревматоїдний артрит (в який залучаються T клітини, B клітини та нейтрофіли), системний червоний вовчак (в який залучаються нейтрофіли), псоріаз (в який залучаються T клітини, нейтрофіли та макрофаги), розсіяний склероз (в який залучаються T клітини, B клітини та тучні клітини), астма (для якої є важливими T клітини і тучні клітини) та хронічна обструктивна легенева хвороба (яка залучає нейтрофіли, макрофаги і T клітини) (Rommel та ін., 2007, Nat. Rev. Immunology 7:191-201). В деяких випадках зв'язок між PI3Kδ та PI3Kγ як потенційними мішенями лікарських засобів для певних захворювань був експериментально встановлений шляхом тестування мишей, у яких відсутня відповідна PI3K, на тваринних моделях захворювання. Додаткове фармакологічне підтвердження було отримане з використанням низькомолекулярних інгібіторів PI3K на мишах дикого типу, в яких експериментальним шляхом викликали запальні захворювання. Camps та співробітники використали розробку лікарського засобу на основі структури для створення сильнодіючого низькомолекулярного інгібітора PIK3γ, згадуваного як AS-605240 (Camps та ін., 2005. Nat. Med. 11(9):936-43). Спостерігали, що в мишачій моделі лімфоцитнезалежного ревматоїдного артриту (RA), пов'язаного з активацією нейтрофілів, миші, у яких відсутня Pik3cg, були захищеними проти артриту, викликаного колаген II-специфічними антитілам. Ефект пов'язували з послабленим нейтрофільним хемотаксисом. Лікування мишей дикого типу за допомогою орального введення AS-605420 приводило до послаблення клінічних 14 UA 102828 C2 5 10 15 20 25 30 35 40 45 50 55 60 та гістологічних симптомів артриту, індукованого антитілом колагену ІІ, подібно до того, як спостерігалось у мишей, у яких була відсутня Pik3cg. Оральне введення AS-605240 також приводило до зменшення запалення суглобів та ушкодження в іншій мишачій моделі лімфоцитзалежного ревматоїдного артриту, викликаного безпосередньою ін'єкцією колагену ІІ. Автори дійшли висновку, що інгібування PIK3CG впливає як на нейтрофільний, так і на лімфоцитний шлях передачі сигналів хемокінів і, таким чином, може мати лікувальне значення при різних запальних захворюваннях. На MRL-lpr мишачій моделі системного червоного вовчака (SLE) було виявлено, що інтраперитонеальне введення фармакологічного PI3Kγ інгібітора AS-605240 зменшувало кількість CD4+T-клітин, послаблювало гломерулонефрит та подовжувало тривалість життя (Barber та ін., 2005, Nat. Med. 11(9):933-935). Залучення PI3 кіназ в алергійні запальні захворювання, такі як астма, було продемонстровано шляхом фармакологічного інгібування неселективними інгібіторами PI3K, такими як вортманін та LY294002. Однак, такі сполуки були недостатньо селективними для того, щоб провести різницю між різними PI3K ізоформами (Walker та ін., 2006, Drug Discovery Today: Disease Mechanisms, 3(1):63-69). Використовуючи селективні PI3Kδ інгібітори, було продемонстровано, що PI3Kδ відіграє деяку роль в реакціях нейтрофільного запалення. Інгібування PI3Kδ блокувало як fMLP- і TNF1α-індуковане нейтрофілами утворення супероксидів, так і екзоцитоз еластази (Sadhu та ін., 2003, Biochem. Biophys. Res. Commun. 2003 Sep 5;308(4):764-769). Суттєва роль PI3Kδ в алергійних реакціях була продемонстрована шляхом генетичної та фармакологічної інактивації PI3Kδ в тучних клітинах. Таке інгібування приводить до патологічного SCF-опосередкованої in vitro проліферації, адгезії та міграції, та до послабленої алерген-IgE-індукованої де грануляції та вивільнення цитокінів. Крім того, інактивація PI3Kδ захищає мишей від анафілактичних алергійних реакцій. В сполученні ці дослідження пропонують розглядати PI3Kδ як мішень для терапевтичної втручання в алергійних захворюваннях та захворюваннях, пов'язаних з тучними клітинами (Ali та ін., 2004, Nature 431:1007-1011). Нещодавно повідомлялось про вплив генетичної інактивації Pi3kcd гену у мишей на системні реакції цитокінів та хемокінів та алергійне запалення дихальних шляхів. Реакції цитокінів типу 2 (IL-4, IL-5 та IL-13) значно послаблювалися у PI3Kδ мутантів, в той час як реакції цитокінів типу 1 (IFN-γ CXCL10) були стабільними. Наприклад, індукування респіраторної гіперреактивності на вдиханий метахолін, ознаку астми, послаблювалося у мишей, у яких була відсутня PI3Kδ. В підсумку ці результати пропонують PI3Kδ як нову мішень для TH2опосередкованих захворювань дихальних шляхів (Nashed та ін., 2007, Eur. J. Immunol. 37:416424). Таким чином, переважними захворюваннями та розладами є ті, що пов'язані з PI3K дельта та/або PI3K гамма. Особливо переважними є запальні та імунорегуляторні розлади, такі як ревматоїдний артрит, запальне захворювання кишечника, системний червоний вовчак, псоріаз, розсіяний склероз, астма та хронічна обструктивна легенева хвороба. Як згадувалося вище, PI3K відіграє роль в розвитку раку та серцево-судинних захворювань. PI3Kγ був запропонований як можлива мішень для фармакологічної дії при первинному та вторинному запобіганні атеросклеротичних серцево-судинних захворювань людей. Атеросклероз та його наслідки, включаючи інфаркт міокарда та інсульт, є головними причинами смертності та захворюваності в сучасному світі. Доповідалось, що PI3Kγ активується в макрофагах оксидованим LDL (ліпопротеїном низької густини), агоністами, хемокінами та медіаторами запалення, які, як правило, залучаються в ангіогенез. Генетична абляція PI3Kg у гіперхолестеринемічних мишей (apoE-/-) приводить до зменшення атеросклеротичних ушкоджень. Крім уповільнення розвитку бляшок, клінічне значення має можливість того, що інгібування PI3K може впливати на стабільність бляшок (Chang та ін., 2007, PNAS 104 (19):807782). Це може бути засновано на тому, що передача сигналів через PI3Kγ відіграє можливу роль в сенсибілізації лейкоцитів, тромбоцитів та серцево-судинної системи внаслідок стресу. Синхронна збудження лейкоцитів та судин впливає на більшість фізіологічних та патологічних реакцій, що зазвичай приводить до продукування молекул інтрацелюлярних вторинних месенджерів, таких як фосфатидилінозитол(3,4,5)-трифосфат (PIP3), який продукується PI3Kγ, вирішальним сигналом як в клітинах судин, так і в білих клітинах крові. Дослідження мишей, позбавлених PI3Kγ, виявило, що PIP3 шлях передачі сигналу контролює дію імунних клітин та судин, таку як респіраторний імпульс, стимуляція клітин, реактивність тучних клітин, агрегація тромбоцитів, активація ендотелію та скорочуваність клітин гладких м'язів. Специфічність цих дій 15 UA 102828 C2 5 10 15 20 25 30 35 40 45 50 55 60 припускає, що інгібування PI3Kγ може бути корисним для найбільш важливих серцево-судинних розладів, таких як гіпертензія (Hirsch та ін., 2006, Thromb. Haemost. 95(1):29-35). Інфаркт міокарда (MI) є результатом двофазного ішемічного/реперфузійного ушкодження (I/R) серця, ініційованого апоптозом кардіоміоцитів (Crow та ін., 2004, Circ. Res. 95(10):957-970) з наступним переходом до другої хвилі ушкодження внаслідок запалення (Frangogiannis та ін., 2002, Cardiovasc. Res. 53(1):31-47). Нещодавно доповідалось, що низькомолекулярний інгібітор PI3K гамма та дельта забезпечив кардіопротекцію на тваринній моделі інфаркту міокарда. Така сполука, TG100-115, ефективно інгібує набряк та запалення у відповідь на численні медіатори, які, як відомо, відіграють роль в інфаркті міокарда. Важливо, що це було досягнуто, коли введення дози здійснювали після міокардіальної реперфузії (аж до 3 годин після), саме в той період часу, коли пацієнти є найбільш чутливі до терапевтичного втручання (Doukas та ін., 2006, PNAS 103(52):19866-19871; Doukas та ін., 2007, Biochem. Soc. Trans. 35(Pt2):204-206; Palanki та ін., 2007, J. Med. Chem. 50(18)4279-4294). Про перше дослідження для характеризування точкових мутацій PIK3CA гена, який кодує p110α каталітичну субодиницю у випадках колоректального раку, раку мозку, раку шлунку, раку молочної залози та раку легенів, доповідалось в 2004 (Samuels та ін., 2004, Science 304:554). Пізніше деякі додаткові точкові мутації ідентифікували в інших видах раку (розглянуто Bader та ін., 2005, Nat. Rev. Cancer 5(12): 921-929). Було продемонстровано, що PIK3CA мутанти промотують ріст клітин та інвазію клітин людського раку і що лікування неселективним PI3K інгібітором LY294002 знищувало передачу сигналів PIK3A і переважно інгібувало ріст PI3KCA мутантних клітин (Samuels та ін., 2005, Cancer Cell 7(6):561-573), таким чином, пропонуючи PI3K білки як багатообіцяючі мішені лікарських засобів при раковій терапії (Hennessy та ін., 2005, Nat. Rev. Drug Discovery 4(12):988-1004). Нещодавно доповідалось, що надекспресія PI3Kβ (p110β), PI3Kγ (p110γ) або PI3Kδ (p110δ) ізоформ PI3K дикого типу є достатньою для індукування онкогенного фенотипу у вирощуваних клітинах (Kang та ін., 2006, PNAS 103(5): 1289-1294). Такий онкогенний потенціал потребує кіназної активності, припускаючи, що інгібітори такої активності можуть блокувати трансформуючу здатність. Роль PI3K ізоформ не-α класу I у протіканні раку людини не була достатньо досліджена, але є повідомлення про підвищену експресію PI3Kβ та PI3Kδ у різних видах раку людини (Benistant та ін., 2000, Oncogene 19(44):5083-5090; Knobbe and Reifenberger, 2003, Brain Pathol. 13(4):507-518). В іншому дослідженні було продемонстровано, що селективний інгібітор PI3Kδ (p110дельта) інгібує проліферацію та виживаність клітин гострої мієлоїдної лейкемії (AML) та підвищує цитотоксичний ефект інгібітора топоізомерази II, пропонуючи PI3Kδ як потенційну терапевтичну мішень в AML (Billottet та ін., 2006. Oncogene 25(50):6648-6659). Даний винахід охоплює фармацевтичні композиції, які містять сполуку формули (I) або її фармацевтично прийнятну сіль, як активний інгредієнт, разом з фармацевтично прийнятним носієм, необов'язково в комбінації з однією або кількома іншими фармацевтичними композиціями. "Фармацевтична композиція" означає один або кілька активних інгредієнтів та один або кілька інертних інгредієнтів, що складають носій, а також будь-який продукт, який утворюється, безпосередньо або опосередковано, в процесі комбінування, комплексоутворення або агрегації будь-яких двох або більше інгредієнтів, або в процесі дисоціації одного або кількох інгредієнтів, або в процесі реакції або взаємодії одного або кількох інгредієнтів. Таким чином, фармацевтичні композиції згідно з даним винаходом охоплюють будь-яку композицію, утворену шляхом змішування сполуки даного винаходу та фармацевтично прийнятного носія. Термін "носій" стосується розбавника, ад'юванта, ексціпієнта або розчинника, з яким вводиться терапевтичний засіб. Такими фармацевтичними носіями можуть бути стерильні рідини, такі як вода та масла, у тому числі нафтові масла, масла тваринного, рослинного, або синтетичного походження, включаючи, але не обмежуючись ними, арахісову олію, соєву олію, мінеральне масло, кунжутну олію та подібні. Якщо фармацевтична композиція вводиться перорально, переважним носієм є вода. Якщо фармацевтична композиція вводиться внутрішньовенно, носіями переважно є фізіологічний розчин солі та водний розчин декстрози. Фізіологічні розчини та водні розчини декстрози та розчини гліцерину переважно застосовують як рідкі носії розчинів для ін'єкцій. Придатні фармацевтичні ексціпієнти включають крохмаль, глюкозу, лактозу, цукрозу, желатин, солод, рис, муку, крейду, силікагель, стеарат натрію, моностеарат гліцерину, тальк, хлорид натрію, сухе знежирене молоко, гліцерин, пропілeнгліколь, воду, етанол та ін. Композиція при необхідності може також містити невеликі кількості змочувальних агентів або емульгаторів, або pH буферних речовин. Такі композиції можуть бути у формі розчинів, суспензій емульсій, таблеток, пігулок, капсул, порошків, 16 UA 102828 C2 5 10 15 20 25 30 35 40 45 50 55 60 композицій уповільненого вивільнення та ін. Композиція може бути сформована як супозиторій з традиційними зв'язувальними речовинами та носіями, такими як тригліцериди. Композиція для орального прийому може включати стандартні носії, такі як маніт, лактоза, крохмаль, стеарат магнію, сахарин натрію, целюлоза, карбонат магнію і т.п. фармацевтичної категорії. Приклади придатних фармацевтичних носіїв описані в "Remington's Pharmaceutical Sciences" під ред. E.W. Martin. Такі композиції будуть містити терапевтично-ефективну кількість лікарської речовини, переважно в чистій формі, разом з необхідною кількістю носія, для того, щоб забезпечити форму, придатну для введення пацієнту. Композиція повинна відповідати шляху введення. Фармацевтична композиція даного винаходу може містити одну або більше додаткових сполук як активні інгредієнти, подібних до одної або кількох сполук формули (I), які не є основною сполукою в композиції, або PI3K інгібітори. Інші активні інгредієнти для застосування в комбінації з іншим лікуванням імунних, запальних, алергійних розладів можуть включати стероїди, антагоністи лейкотриєну, антигістаміни, циклоспорини або рапаміцин. Фармацевтичні композиції даного винаходу включають композиції, придатні для орального, ректального, місцевого, парентерального (включаючи підшкірне, внутрішньом'язове та внутрішньовенне), очного (офтальмічного), легеневого (назальними або букальними інгаляціями) або назального введення, хоча найбільш придатний шлях в будь-якому випадку буде залежати від характеру та важкості станів, які піддають лікуванню, та природи активного інгредієнта. Вони можуть бути зручним чином представлені у вигляді дозованих лікарських форм та одержані будь-яким способом, відомим в галузі фармації. На практиці сполуки формули (I) може бути скомбінований як активний інгредієнт в однорідній суміші з фармацевтично-прийнятним носієм згідно із стандартною технологією фармацевтичного приготування сумішей. Носій може набувати різноманітних форм в залежності від форми препарату, необхідного для введення, наприклад, для орального або парентерального введення (включаючи внутрішньовенне). В процесі приготування композицій для оральних дозованих форм можуть використовуватися будь-які звичайні фармацевтичні середовища, такі як вода, гліколі, олії, спирти, смакові агенти, консерванти, забарвлювальні агенти та ін. у випадку оральних рідких препаратів, таких як, наприклад, суспензії, еліксири та розчини; або носії, такі як крохмалі, цукри, мікрокристалічна целюлоза, розбавники, гранулювальні агенти, мастильні речовини, зв'язувальні речовини, дезінтегранти та подібні у випадку оральних твердих препаратів, таких як, порошки, тверді та м'які капсули і таблетки, причому перевага надається твердим оральним препаратам, ніж рідким препаратам. З огляду на простоту введення, таблетки та капсули є найбільш переважними дозованими лікарськими формами, у випадку яких застосовують тверді фармацевтичні носії. При необхідності на таблетки можуть бути нанесені покриття з використанням стандартних водних або неводних способів. Такі композиції та препарати повинні містити принаймні 0,1 % активної сполуки. Відсотковий вміст активної сполуки в таких композиціях може, звичайно, змінюватися і може зазвичай коливатися між приблизно 2 % до приблизно 60 % від ваги дозованої одиниці. Кількість активної сполуки в таких терапевтично придатних композиціях є такою, щоб отримати ефективну дозу. Активні сполуки можуть також вводитися інтраназально, наприклад, у вигляді крапель або спреїв. Таблетки, пілюлі, капсули та подібні можуть також містити зв'язувальну речовину, таку як трагакантова камедь, кукурудзяний крохмаль або желатин; ексціпієнти, такі як дикальцій фосфат; дезінтегрант, такий як кукурудзяний крохмаль, картопляний крохмаль, альгінова кислота; мастильну речовину, таку як стеарат магнію; та підсоложувальних агент, такий як цукроза, лактоза або сахарин. Якщо дозованою лікарською формою є капсула, вона може містити, крім речовин вищезгаданого типу, рідкий носій, такий як жирне масло. Можуть бути присутніми різні інші речовини як покриття або для модифікації фізичної форми дозованої одиниці. Наприклад, таблетки можуть бути покриті шелаком, цукром або обома речовинами. Сироп або еліксир може містити, крім активного інгредієнта, цукрозу як підсоложувальний агент, метил- та пропілпарабени як консерванти, барвник та смаковий агент, такий як вишневий або апельсиновий аромат. Сполуки формули (I) можуть також вводитися парентерально. Розчини або суспензії таких активних сполук у воді можуть бути отримані шляхом відповідного змішування з поверхневоактивною речовиною, такою як гідроксипропілцелюлоза. Також можуть бути отримані суспензії в гліцерині, рідких поліетиленгліколях та їх суміші в маслі. У звичайних умовах зберігання та застосування такі препарати містять консерванти для запобігання розмноження мікроорганізмів. Фармацевтичні форми, придатні для ін'єкційного застосування, включають стерильні водні розчини або дисперсії та стерильні порошки, придатні для приготування стерильних ін'єкційних 17 UA 102828 C2 5 10 15 розчинів або дисперсій для негайного прийому. У всіх випадках форма має бути стерильною і повинна бути настільки рідкою, щоб легко вводитися за допомогою шприца. Вона повинна бути стабільною в умовах виробництва та зберігання і повинна бути убезпечена від зараження мікроорганізмами, такими як бактерії та гриби. Носієм може бути розчинник або дисперсійне середовище, яке містить, наприклад, воду, етанол, поліол (наприклад, гліцерин, пропіленгліколь та рідкий поліетиленгліколь), їх придатні суміші та рослинні олії. Для забезпечення ссавця, особливо людини, ефективною дозою сполуки даного винаходу може застосовуватися будь-який придатний шлях введення. Наприклад, оральний, ректальний, місцевий, парентеральний, окулярний, легеневий, назальний та подібні. Дозовані форми включають таблетки, пастилки, дисперсії, суспензії, розчини, капсули, креми, мазі, аерозолі та ін. Сполуки формули (I) переважно вводяться орально. Ефективна доза застосовуваного активного інгредієнта може значною мірою залежати від конкретної використовуваної сполуки, шляху введення, стану, який підлягає лікуванню, та важкості стану, який лікують. Така доза може бути легко встановлена фахівцем в даній галузі. Загальний шлях синтезу сполук формули (I) може починатися з триазолів формули (II), які легко можуть бути отримані стандартними способами одержання гетероциклів цього типу. Такі способи є добре відомими фахівцям в даній галузі. Загальний спосіб одержання сполук згідно даного винаходу включає стадію - взаємодії триазолу формули (II) R3 R2 X2 20 25 30 35 40 45 N N N X1 II R1 , 2 1 2 3 1 в якій X означає Br або B(OR)2; R , R , R мають значення, вказані вище, а X означає X, такий як вказано вище або в захищеній формі X-Pro, де Pro означає захисну групу, 1 1 з бороновою кислотою або естером T -B(OR)2 або T -Br, де R означає H; або придатний естерний залишок, в реакції Сузукі з одержанням сполуки формули (I) після необов'язкового відщеплення захисної групи. Наприклад, такою захисною групою є ацетил. Більш конкретно, загальний та типові шляхи одержання наведено нижче. Загальні способи синтезу Способи синтезу сполук даного винаходу описані, наприклад, в Houben-Weyl, Methoden der Organischen Chemie (Methods of Organic Chemistry), Thieme-Verlag, Stuttgart, або Organic Reactions, John Wiley & Sons, New York. В залежності від обставин конкретного випадку, для того, щоб уникнути побічних реакцій в процесі синтезу сполук формули (I), може бути необхідним або корисним тимчасово блокувати функціональні групи шляхом введення захисних груп та видаляти їх на останній стадії синтезу, або вводити функціональні групи у формі прекурсорних груп, які на останній стадії перетворюються у необхідні функціональні групи. Такі стратегії синтезу та захисні і прекурсорні групи, які є придатними в конкретних випадках, є відомими фахівцям в даній галузі. При необхідності сполуки формули (I) можуть бути очищені звичайними способами очищення, наприклад, перегонкою, перекристалізацією або хроматографією. Вихідні сполуки для одержання сполук формули (I) випускаються серійно або можуть бути отримані згідно із способами, описаними в літературі, або аналогічно їм. Загальний шлях синтезу сполук формули (I) може починатися з триазолів формули (II), які легко можуть бути отримані стандартними способами одержання гетероциклів цього типу. Такі способи є добре відомими фахівцям в даній галузі. 1 Згідно із Схемою 1 триазоли формули (II), в якій X означає X, такий як вказано вище або в 2 1 2 3 захищеній формі, X означає бром, а R , R , R мають значення, вказані вище, під час взаємодії 1 1 з бороновою кислотою T -B(OH)2 або бороновим естером T -B(АБО)2 в умовах конденсування Сузукі (Suzuki та ін., Chem Commun. (1979) 866) можуть утворювати сполуки формули (I). 18 UA 102828 C2 R3 R3 R2 N 1 X N N 2 X R2 T1-B(OH)2 N 1 N N T R1 5 R1 (II) (I) Схема 1 1 1 T -B(OH)2 і T -B(АБО)2 як придатні вихідні речовини для синтезу переважних сполук даного винаходу можуть отримані з комерційно доступних джерел, таких як CombiBlocks, Sigma Aldrich, AlfaAesar або синтезовані фахівцем в даній галузі. В переважному втіленні даного винаходу одержання триазолів формули (II), в якій X означає NH2, може починатися з піридину формули (III), який взаємодіє з етоксикарбонілізотіоціанатом з одержанням, після циклізації в присутності гідроксиламіну, триазолів формули (II), як наведено на Схемі 2. R3 R3 R2 NH2 N X2 R1 10 15 20 25 30 X EtOC(O)NCS R2 N X2 N N NH 2 R1 (III) (II) Схема 2 В загальній процедурі одержання переважних сполук даного винаходу при взаємодії доступного в продажу 2-аміно-5-бромпіридину [1] з етоксикарбонілізотіоціанатом в ДХМ при 20 °C утворюється похідна тіосечовини [2] як проміжний продукт, який піддають процесу . i циклізації, застосовуючи гідроксиламін в протонному розчиннику (NH 2OH HCl, Pr2NEt, EtOH/MeOH, Δ), з одержанням ключової проміжної сполуки 2-аміно-6-бром-[1,2,4]триазоло[1,5a]піридину [3]. Наступне ацилювання піридину з використанням ацетилхлориду в присутності Et3N в CH3CN при 20 °C загалом дає біс-ацильований продукт, який потребує гідролізу до моноацильованого продукту [4] з використанням метанольного розчину аміаку при 20 °C. Взаємодія н-(6-бром-[1,2,4]триазоло[1,5-a]піридин-2-іл)ацетаміду [4] з 4,4,4',4',5,5,5',5'-октаметил-2,2'бi(1,3,2-діоксабороланом) (пінакол-диборон) в ДМФ з основою, такою як карбонат натрію, в присутності Pd(PPh3)2Cl2 як каталізатора, приводить до утворення н-(6-(4,4,5,5-тетраметил1,3,2-діоксаборолан-2-іл)-[1,2,4]триазоло[1,5-a]піридин-2-іл)ацетаміду [5] Схема 3. Схема 3 Переважні сполуки даного винаходу можуть бути синтезовані конденсуванням проміжних триазолів [3], [4] або [5] з відповідними арилборонієвими кислотами/естерами або бромідами в умовах реакції Сузукі з використанням Pd(PPh3)2Cl2 як каталізатора і карбонату натрію як основи в ДМE/H2O/EtOH при 100-150 °C з одержанням бажаних продуктів [7], Схема 4. 19 UA 102828 C2 5 10 Схема 4 Ацетильну захисну групу видаляють шляхом обробки проміжної сполуки [6] кислотою в придатному розчиннику, такому як діоксан. Арилборонієві кислоти/естери або броміди були або вибрані з тих, що випускаються серійно, або синтезовані шляхом модифікації проміжних сполук, що випускаються серійно, з використанням способів, наведених нижче. Аналітичні способи ЯМР спектри отримували на Brucker dpx400. РХMС здійснювали на Agilent 1100, використовуючи колонки ZORBAX SB-C18, 4,6 × 150 мм, 5 мікрон, ZORBAX SB-C18, 4,6 × 75 мм, 3,5 мікрон або Gemini™ C18, 3 × 30 мм, 3 мікрон. Швидкість потоку була 1,0 або 1,2 мл/хвил., а використовуваними розчинниками були вода та ацетoнітрил (0,1 % мурашина кислота) з ін'єкційним об'ємом 3 або 10 мкл. Довжина хвилі була 254 та 210 нм. Спосіб A Колонка: ZORBAX SB-C18, 4,6 × 150 мм, 5 мікрон 15 Час (хвил) 0 11 13 13,01 14,00 Вода 95 5 5 95 Ацетoнітрил 5 95 95 5 СТОП Спосіб B Колонка: ZORBAX SB-C18, 4,6 × 75 мм, 3,5 мікрон Час (хвил) 0 1,5 4,5 4,51 5,00 Вода 70 5 5 70 Ацетoнітрил 30 95 95 30 СТОП 20 Спосіб C Колонка: Gemini C18, 3 × 30 мм, 3 мікрон Швидкість протікання: 1,2 мл/хвил Час (хвил) 0 3 4,5 4,6 5,00 Вода 95 5 5 95 СТОП 20 Ацетoнітрил 5 95 95 5 UA 102828 C2 5 Спосіб D Швидкість протікання через колонку була 1 мл/хвил. І використовуваними розчинниками були вода та ацетoнітрил (0,1 % аміаку). Колонка: Gemini C18, 3 × 30 мм, 3 мікрон. Швидкість протікання: 1,2 мл/хвил Час (хвил) 0 3 4,5 4,6 5,00 Вода 95 5 5 95 Ацетoнітрил 5 95 95 5 СТОП Таблиця 1: Абревіатура ДХМ Et3N CH3CN MeOH EtOH i Pr2NEt . NH2OH HCl Дихлорметан Триетиламін Ацетoнітрил Mетанол Етанол Діізопропілетиламін Гідроксиламіну гідрохлорид Бістрифенілфосфіно-паладію(II) Pd(PPh3)2(Cl)2 хлорид [1,1′біс(дифенілфосфіно)фероцен] Pd(dppf)(Cl)2 дихлор-паладій (II) CsF Фторид цезію ДМФ N, N-Диметилформамід ДМЕ 1,2-Диметоксиетан HOBt 1-Гідроксибензотриазол N-Етил-N′-(3ЕДК диметиламінопропіл)карбодііміду гідрохлорид H2O Вода с Синглет д Дублет дд Дублет дублетів т Триплет септ Септет м Мультиплет ш Широкий мл Мілілітри л літр год. години 10 Для одержання сполук формули (I) використовували наступні способи Спосіб 1 1.1 3-Бром-N, N-біс(2-гідроксиетил)бензолсульфонамід Br O S N O OH OH 21 UA 102828 C2 5 До розчину 3-бромбензолсульфонілхлориду (0,25 мл, 1,73 ммоль) в діоксані (2,0 мл) додавали краплями розчин діетаноламіну (0,547 г, 5,20 ммоль) в діоксані (1,0 мл) протягом 1 хвил. Реакційну суміш перемішували при кімнатній температурі (20 °C) протягом 16 год. Після цього суміш виливали в насичений розчин солі (30 мл) та екстрагували етилацетaтом (25 мл). Органічний розчин концентрували у вакуумі з одержанням вказаної у заголовку сполуки (0,495 г, 88 %). Ні в якому додатковому очищенні не було потреби. Інші сульфонаміди отримували аналогічним чином, використовуючи 3бромбензолсульфонілхлорид або 3-бромпіридинсульфонілхлорид та різні аміни. 1.2 N-(5-Бромпіридин-3-іл)бензолсульфонамід Br N NH O S O 10 15 До розчину 3-аміно-5-бромпіридину (0,500 г, 2,89 ммоль) в піридині (2 мл) додавали краплями бензолсульфонілхлорид (0,404 мл, 3,18 ммоль). Реакційну суміш перемішували при кімнатній температурі (20 °C) протягом 16 годин. Після цього додавали до реакційної суміші воду (5 мл). Отриману кристалічну тверду речовину збирали фільтрацією, промивали водою та сушили у вакуумній шафі з одержанням вказаної у заголовку сполуки (0,898 г, 2,89 ммоль, кількісний вихід). Ні в якому додатковому очищенні не було потреби. Інші сульфонаміди отримували, використовуючи аналогічний спосіб з різними сульфонілхлоридами або при кімнатній температурі, або при 60 °C. 1.3 4-Бром-2-ізопропокси-1-метоксибензол Br O O 20 25 30 35 До розчину 5-бром-2-метоксифенолу (0,200 г, 1 ммоль) в ДМФ (4 мл) додавали карбонат калію (0,209 г, 1,5 ммоль) та ізопропілйодид (120 мкл, 1,2 ммоль), реакційну суміш перемішували при кімнатній температурі (20 ºC) протягом 3 годин. Після цього неочищену реакційну суміш розводили етилацетaтом (100 мл) і промивали водою (2 × 100 мл). Органічний шар сушили над сульфатом магнію, фільтрували та концентрували у вакуумі з одержанням масла жовтого кольору (200 мг, 0,81 ммоль, 82 %). Ні в якому додатковому очищенні не було потреби. 1.4 1-(6-Бром-[1,2,4]триазоло[1,5-a]піридин-2-іл)сечовина N NH N N NH 2 Br O До розчину 6-бром-[1,2,4]триазоло[1,5-a]піридин-2-іламіну (0,500 г, 2,34 ммоль) в суміші ТГФ:піридин (1:1, 15 мл) при 0 °C додавали трифосген (0,348 г, 1,17 ммоль) протягом 5 хвил. Температурі дозволяли підніматися до 5 ºC і додавали10 % аміак (20 мл). Реакційну суміш потім залишали нагріватися до кімнатної температури (25 ºC) і перемішували протягом 16 годин. Після цього розчинник видаляли у вакуумі, і залишок очищали колонковою хроматографією (елюент: етилацетат/гексан → етилацетат/метанол) з одержанням вказаної у заголовку сполуки (0,089 г, 0,351 ммоль, 15 %). Спосіб 2 2.1 1-(5-Бромпіридин-2-іл)-3-карбоетокситіосечовина (2) Br S OEt N 40 N N O H H До розчину 2-аміно-5-бромпіридину (1) (200,0 г, 1,156 моль) в ДХМ (2,0 л), охолодженого до температури 5 ºC, додавали краплями етоксикарбонілізотіоціанат (134,9 мл, 1,156 моль) протягом 15 хвил. Реакційну суміш потім залишали нагріватися до кімнатної температури (20 22 UA 102828 C2 5 10 15 20 25 30 35 40 45 ºC) і перемішували протягом 16 годин. Випарюванням у вакуумі отримували тверду речовину жовтого кольору, яку збирали фільтрацією, ретельно промивали бензином (3 × 500 мл) і сушили на повітрі з одержанням вказаної у заголовку сполуки (351,5 г, кількісний вихід). Ні в якому додатковому очищенні не було потреби. 1 H ЯМР (d6-ДМСО) δ 12,22 (шс, 1H), 11,75 (шс, 1H), 8,66 (шс, 1H), 8,57 (д, 1H), 8,16 (дд, 1H), 4,26 (к, 2H), 1,28 (т, 3H). 2.2 6-Бром-[1,2,4]триазоло[1,5-a]піридин-2-іламін (3) N NH 2 N N Br До суспензії гідрохлориду гідроксиламіну (409,2 г, 5,888 моль) в EtOH/MeOH (1:1, 2,5 л) додавали N, N-дiiзoпропілетиламін (606,1 мл, 3,480 моль), суміш перемішували при кімнатній температурі (20 ºC) протягом 1 години. Потім додавали 1-(6-бромпіридин-2-іл)-3карбоетокситіосечовину (2) (352,8 г, 1,160 моль), і суміш повільно нагрівали до кипіння (Примітка: для гасіння H2S, який виділяється, потрібен вилуговувальний скрубер). Через 2 години кип'ятіння зі зворотним холодильником суміш залишали охолоджуватися і фільтрували для того, щоб зібрати осаджену тверду речовину. Зібрану тверду речовину промивали послідовно водою (1,0 л), EtOH/MeOH (1:1, 1,0 л) та діетиловим етером (500 мл)і потім сушили на повітрі з одержанням вказаної у заголовку сполуки у вигляді білої твердої речовини (169,2 г, 69 %). Ні в якому додатковому очищенні не було потреби. 1 H ЯМР (d6-ДМСО) δ 8,94 (д, 1H), 7,58 (дд, 1H), 7,36 (д, 1H), 6,16 (шс, 2H). + m/z 213/215 (1:1, M+H , 100 %). 2.3 N-(6-бром-[1,2,4]триазоло[1,5-a]піридин-2-іл)ацетамід (4) N NH N N Br O До розчину 6-бром-[1,2,4]триазоло[1,5-a]піридин-2-іламіну (3) (7,10 г, 33,3 ммоль) в сухому ацетoнітрилі (150 мл) при 5 ºC додавали триетиламін (11,6 мл, 83,3 ммоль) з наступним додаванням ацетилхлориду (2,35 мл 83,3 ммоль). Реакційну суміш потім залишали нагріватися до кімнатної температури (20 °C) і перемішували доти, поки не витрачалася уся вихідна речовина (при необхідності додавали додаткову кількість триетиламіну (4,64 мл, 33,3 ммоль) та ацетилхлориду (33,3 ммоль), щоб забезпечити завершення реакції). Після цього розчинник видаляли у вакуумі і до утвореного залишку додавали 7 N (метанольний розчин аміаку (50 мл)). Реакційну суміш перемішували при кімнатній температурі (20 °C) з тим, щоб гідролізувати будьяку біс-ацильовану речовину. Через 16 годин випарювання у вакуумі та розтирання з діетиловим етером (50 мл) отримували казану у заголовку сполуку, яку збирали фільтрацією, промивали водою (2×50 мл), ацетоном (50 мл) та діетиловим етером (50 мл) і потім сушили у вакуумі. 1 H ЯМР (d6-ДМСО) δ 10,87 (с, 1H), 9,29 (д, 1H), 7,78 (дд, 1H), 7,65 (д, 2H), 2,13 (с, 3H). 2.4 N-(6-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)-[1,2,4]триазоло[1,5-a]піридин-2іл)ацетамід (5) N NH N N O B O O До розчину н-(6-бром-[1,2,4]триазоло[1,5-a]піридин-2-іл)ацетаміду (4) (20,0 г, 78,4 ммоль) в толуолі (400 мл) додавали біс(пінаколато)диборон (20,35 г, 86,2 ммоль) та ацетaт калію (15,39 г, 156,8 ммоль). Реакційну суміш піддавали дегазації і додавали однією порцією хлорид [1,1’бісдифенілфосфін)фероцен]паладію(II), 1:1 комплекс з ДХМ (3,2 г, 3,92 ммоль). Суміш піддавали додатковій дегазації і нагрівали до 100 °C протягом 16 годин. Після цього реакційну суміш залишали охолоджуватися до кімнатної температури (20 °C), фільтрували через целіт і промивали етилацетaтом. Фільтрат промивали насиченим розчином солі, сушили над безводним сульфатом натрію, і розчинник видаляли у вакуумі з одержанням вказаної у заголовку сполуки (24,5 г, 78,4 ммоль, кількісний вихід). Сиру речовину використовували без подальшого очищення. Спосіб 3 23 UA 102828 C2 5 10 15 20 25 30 35 40 3.1 Загальний спосіб одержання (6-арил-[1,2,4]триазоло[1,5-a]піридин-2-іламіну) з (6-бром[1,2,4]триазоло[1,5-a]піридин-2-іламіну) Суспензію 6-бром-[1,2,4]триазоло[1,5-a]піридин-2-іламіну (3) (0,3 ммоль, 1 екв.), боронової кислоти (0,36 ммоль, 1,2 екв.), комплексу [1,1′-біс(дифенілфосфіно)фероцен]дихлорпаладію (II) з CH2Cl2 (0,006 ммоль, 0,02 екв.) та карбонату натрію (0,45 ммоль, 1,5 екв.) в ДМЕ: H 2O: EtOH, (7:3:2, 2 мл) нагрівали до 120 ºC протягом 30 хвилин в мікрохвильовій печі. Неочищений продукт реакції або розподіляли між водою та етилацетатом, фази розділяли і органічний шар промивали насиченим розчином солі, сушили над сульфатом магнію, фільтрували і розчинник видаляли у вакуумі, або осаджували додаванням води, осад збирали фільтрацією і промивали етилацетатом та метанолом. Сирі залишки очищали або флеш-хроматографією або препаративною ВЕРХ, якщо необхідно отримати цільовіпродукти. 3.2 Загальний спосіб одержання (6-арил-[1,2,4]триазоло[1,5-a]піридин-2-іламіну) з (N-(6(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)-[1,2,4]триазоло[1,5-a]піридин-2-іл)ацетаміду) Сполуки отримували за методикою, подібною до методики способу 3.1, використовуючи (N(6-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)-[1,2,4]триазоло[1,5-a]піридин-2-іл)ацетамід та відповідний арилбромід, хоча перед очищенням сирий залишок обробляли 4M розчином HCl/діоксан протягом 18 годин при кімнатній температурі. Розчинник видаляли у вакуумі і залишки очищали, як описано вище. Спосіб 4 4.1 Загальний спосіб одержання 3-O-заміщених 5-бромпіридинів Спосіб A: 5-Бромпіридин-3-ол (174 мг, 1,0 ммоль) та карбонат калію (143 мг, 1,03 ммоль) охолоджували до 0 °C в ДМФ (5 мл). Додавали галоїд R'X (1,0 ммоль), і реакційну суміш перемішували при 0 °C протягом 90 хвилин. Після цього додавали етилацетат (50 мл), і органічну фазу промивали гідроксидом натрію (3 × 30 мл, 2M водний розчин). Органічну фазу концентрували у вакуумі з одержанням необхідної проміжної сполуки. Ні в якому додатковому очищенні не було потреби. Спосіб B: Гідрид натрію (42 мг, 1,05 ммоль) при перемішуванні обережно додавали до розчину спирту R'OH (1,0 ммоль) в ДМФ (8 мл). Реакційну суміш перемішували при 0 °C протягом 60 хвилин, після чого додавали 3-бром-5-фторпіридин (176 мг, 1,0 ммоль). Реакційну суміш перемішували при 110 °C протягом ночі. Після охолодження реакційну суміш виливали на насичений розчин солі (25 мл) та екстрагували етилацетaтом (2 × 30 мл). Органічні екстракти об'єднували і концентрували у вакуумі з одержанням необхідної проміжної сполуки. Ні в якому додатковому очищенні не було потреби. 4,2 Загальний спосіб одержання 3-SO2-заміщених 5-бромпіридинів Гідрид натрію (130 мг, 3,24 ммоль) додавали до розчину бензилмеркаптану (0,37 мл, 3,15 ммоль) в ДМФ (9 мл) при 0 °C, і реакційну суміш перемішували протягом 70 хвилин. Додавали краплями 3,5-дибромпіридин (711 мг, 3,0 ммоль) в ДМФ (4 мл), і реакційну суміш перемішували при кімнатній температурі протягом ночі. Після цього реакційну суміш виливали на розбавлений розчин гіпохлориту натрію (
ДивитисяДодаткова інформація
Назва патенту англійськоюAmino triazoles as p13k inhibitors
Автори англійськоюRamsden, Nigel, Bell, Kathryn, Cansfield Andrew, Taylor Jess, Sunose, Mihiro, Middlemiss, David, Neibauer, Gitte
Назва патенту російськоюАминотриазолы как ингибиторы p13k
Автори російськоюРамсден Найджел, Белл Кетрин, Кенсфилд Эндрю, Тейлор Джесс, Сунозе Михиро, Миддлмисс Девид, Нойбауер Гитте
МПК / Мітки
МПК: A61K 31/437, A61P 37/00, A61P 29/00, C07D 471/04
Мітки: амінотриазоли, інгібітори
Код посилання
<a href="https://ua.patents.su/73-102828-aminotriazoli-yak-ingibitori-p13k.html" target="_blank" rel="follow" title="База патентів України">Амінотриазоли як інгібітори p13k</a>
Попередній патент: Спосіб виробництва горілки
Наступний патент: Пристрій і спосіб виштовхування коксового пирога з камери коксової печі
Випадковий патент: Бітумна емульсійна мастика












