Індазольні сполуки як антипроліферативні агенти, фармацевтична композиція (варіанти) та спосіб лікування захворювань або порушень (варіанти), пов’язаних з небажаним ангіогенезом та/або клітинною проліферацією
Номер патенту: 75880
Опубліковано: 15.06.2006
Автори: Ромінес Вільям Генрі III, Райх Зігфрид Хайнц, Блекмен Тед Майкл, Кепхарт С'юзен Елізабет, Воллес Майкл Б.
Формула / Реферат
1. Сполука формули І
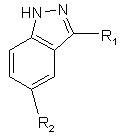 , (І)
, (І)
де R1 є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
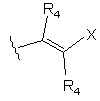 ,
,
де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, та
R2 є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
 ,
,
де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним, алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
фармацевтично прийнятна сіль сполуки формули І або проліки або фармацевтично активний метаболіт сполуки формули І, або фармацевтично прийнятна сіль проліків або їх метаболіту.
2. Сполука, фармацевтично прийнятна сіль, проліки або фармацевтично активний метаболіт за п. 1, який відрізняється тим, що
R1 є
 ,
,
де R4 є воднем, або
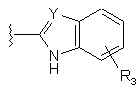 ,
,
де Y є СН або N та R3 є Н або заміщеним або незаміщеним алкілом, арилом, карбоциклічною, гетероарильною або гетероциклічною групою, або
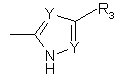 ,
,
де Y є С або N та R3 є Н або заміщеним або незаміщеним алкілом, арилом, гетероарильною, карбоциклічною або гетероциклічною групою.
3. Сполука, вибрана із групи, яка включає
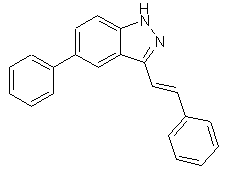 ,
,
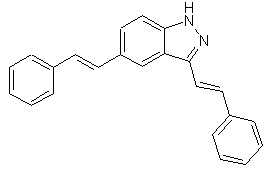 ,
,
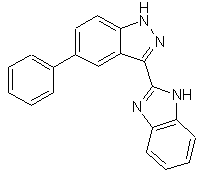 ,
,
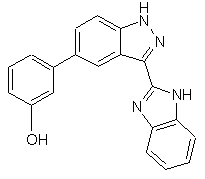 ,
,
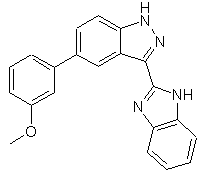 ,
,
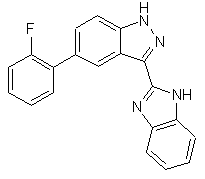 ,
,
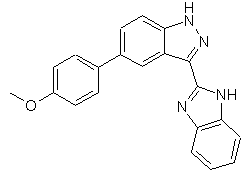 ,
,
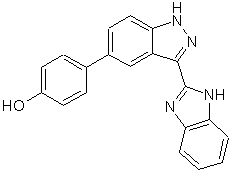 ,
,
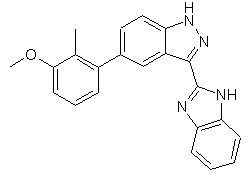 ,
,
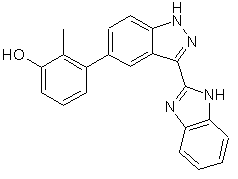 ,
,
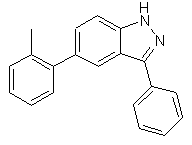 ,
,
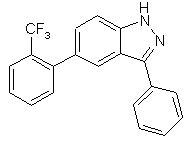 ,
,
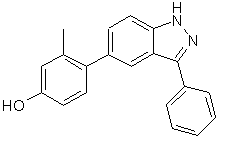 ,
,
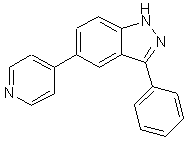 та
та
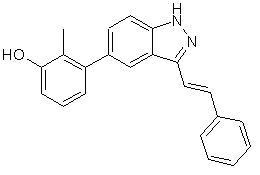 ;
;
або
фармацевтично прийнятна сіль сполуки формули І або проліки або фармацевтично активний метаболіт сполуки формули І або фармацевтично прийнятна сіль проліків або метаболіту.
4. Фармацевтична композиція, яка містить:
кількість агента регулювання клітинного циклу, достатньо ефективну для інгібування протеїнкіназ, причому вказаний агент регулювання контрольного циклу є сполукою формули І:
 , (І)
, (І)
де R1 є воднем або заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
 ,
,
де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, та
R2 є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
 ,
,
де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
фармацевтично прийнятною сіллю сполуки формули І або проліками або фармацевтично активним метаболітом сполуки формули І, або фармацевтично прийнятною сіллю проліків або метаболіту, та фармацевтично прийнятний носій.
5. Спосіб лікування захворювання або порушення, опосередкованого інгібуванням комплексу кіназ, за яким пацієнту у разі необхідності такого лікування призначають агент регулювання клітинного циклу, вибраний із групи, що містить сполуку формули І:
 , (І)
, (І)
де R1 є воднем або заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
 ,
,
де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, та
R2 є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
 ,
,
де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
фармацевтично прийнятну сіль сполуки формули І або проліки або фармацевтично активний метаболіт сполуки формули І, або фармацевтично прийнятну сіль проліків або метаболіту.
6. Фармацевтична композиція, яка містить:
(а) терапевтично ефективну кількість сполуки формули І:
 , (І)
, (І)
де R1 є воднем або заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
 ,
,
де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, та
R2 є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
 ,
,
де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
фармацевтично прийнятну сіль сполуки формули І або проліки або фармацевтично активний метаболіт сполуки формули І, або фармацевтично прийнятну сіль проліків або метаболіту та (б) фармацевтично прийнятний носій, розріджувач, переносник або наповнювач для цього.
7. Спосіб лікування симптомів захворювання у ссавців, причому симптоми опосередковані активністю кіназ, за яким ссавцю у разі необхідності такого лікування призначають терапевтично ефективну кількість сполуки формули І:
 , (І)
, (І)
де R1 є воднем або заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
 ,
,
де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, та
R2 є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
 ,
,
де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним, алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
фармацевтично прийнятної солі сполуки формули І або проліків або фармацевтично активного метаболіту сполуки формули І, або фармацевтично прийнятної солі проліків або метаболіту.
8. Спосіб за п. 7, за яким лікують симптоми захворювання у ссавців, пов'язані із ростом пухлин, клітинною проліферацією або ангіогенезом.
9. Спосіб модулювання або інгібування активності рецептора протеїн-кінази, за яким рецептор з'єднують із ефективною кількістю сполуки формули І:
 , (І)
, (І)
де R1 є воднем або заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
 ,
,
де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, та
R2 є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
 ,
,
де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
фармацевтично прийнятної солі сполуки формули І або проліків або фармацевтично активного метаболіту сполуки формули І, або фармацевтично прийнятної солі проліків або метаболіту.
10. Спосіб за п. 9, в якому як рецептор протеїн-кіназ використовують CDK комплекс, VEGF або СНК1.
11. Фармацевтична композиція, яка містить ефективну для інгібування комплексу кіназ кількість агента регулювання клітинного циклу, наданого сполукою формули І:
 , (І)
, (І)
де R1 є воднем або заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
 ,
,
де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, та
R2 є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
 ,
,
де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
фармацевтично прийнятною сіллю сполуки формули І або проліками або фармацевтично активним метаболітом сполуки формули І, або фармацевтично прийнятною сіллю проліків або метаболіту.
12. Спосіб лікування хворобливих станів або порушень, асоційованих із нерегульованою клітинною проліферацією, за яким пацієнту у разі необхідності такого лікування призначають терапевтично ефективну кількість сполуки формули І:
 , (І)
, (І)
де R1 є воднем або заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
 ,
,
де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, та
R2 є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
 ,
,
де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
фармацевтично прийнятної солі сполуки формули І або проліків або фармацевтично активного метаболіту сполуки формули І, або фармацевтично прийнятної солі проліків або метаболіту.
13. Сполука формули II:
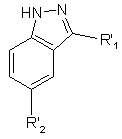 , (II)
, (II)
де R'1 є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
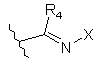 або
або 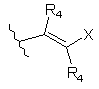 ,
,
де R4 у кожній реалізації незалежно є воднем або нижчим алкілом та Х є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, та
R'2 є заміщеною або незаміщеною аміногрупою, нітрогрупою, алкенілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту,  або
або  групою,
групою,
де R4 групи є незалежно воднем або нижчим алкілом та Х є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
фармацевтично прийнятна сіль сполуки формули II або проліки або фармацевтично активний метаболіт сполуки формули II, або фармацевтично прийнятна сіль проліків або метаболіту.
14. Сполука, фармацевтично прийнятна сіль, проліки або її фармацевтично активний метаболіт за п. 13, яка відрізняється тим, що R'1 є
 ,
, 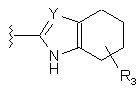 або
або  ,
,
де Y є незалежно СН, СR3 або N та групи R3 незалежно є одним або більше Н, заміщеним або незаміщеним алкілом, алкенілом, арилом, карбоциклом, гетероарилом, гетероциклом, гідроксигрупою, галогеном, алкоксигрупою, арилоксигрупою, гетероарилоксигрупою, тіоарилом, тіогетероарилом, тіоалкілом, тіоацилом або аміногрупою, за умови, що може бути більше однієї групи R3.
15. Сполука за п. 14, яка відрізняється тим, що R'2 є заміщеним або незаміщеним гетероарилом із вмістом азоту, a R'1 є
 .
.
16. Сполука за п. 13, яка відрізняється тим, що R'2 є заміщеним або незаміщеним гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту.
17. Сполука за п. 13, яка відрізняється тим, що R'2 є заміщеною або незаміщеною групою формули
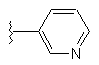 .
.
18. Сполука за п. 13, яка відрізняється тим, що R'2 є заміщеною або незаміщеною групою формули
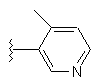 .
.
19. Сполука за п. 13, яка відрізняється тим, що R'2 є заміщеною або незаміщеною групою формули
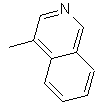 .
.
20. Сполука за п. 14, яка відрізняється тим, що R'2 містить заміщену або незаміщену групу формули
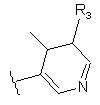 .
.
21. Сполука за п. 13, яка відрізняється тим, що R'2 містить заміщену або незаміщену групу формули
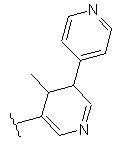 .
.
22. Сполука, вибрана із групи, що містить
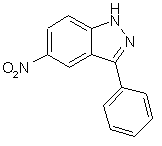 ,
,
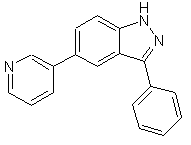 ,
,
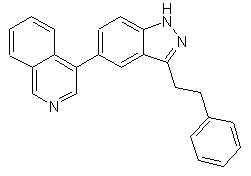 ,
,
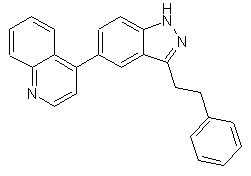 ,
,
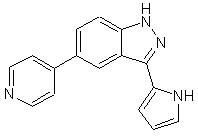 ,
,
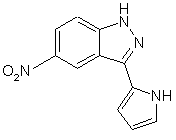 ,
,
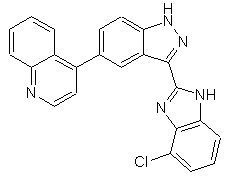 ,
,
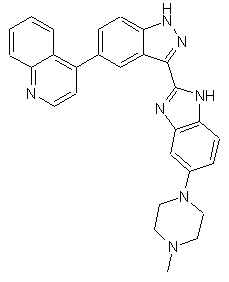 ,
,
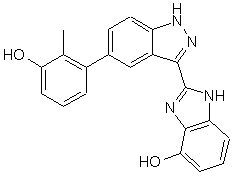 ,
,
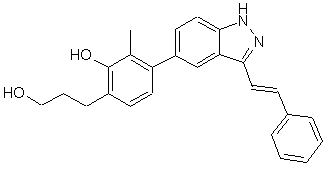 ,
,
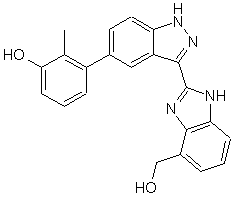 ,
,
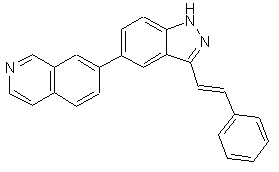 ,
,
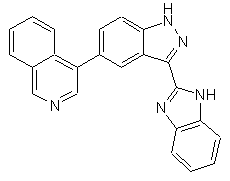 ,
,
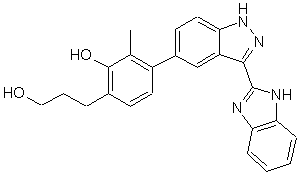 ,
,
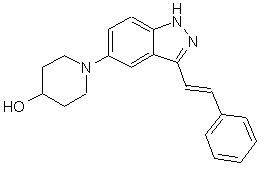 ,
,
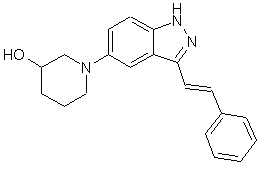 ,
,
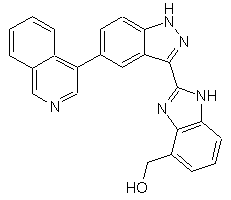 ,
,
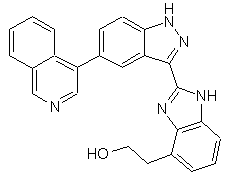 ,
,
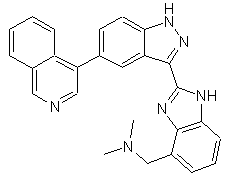 ,
,
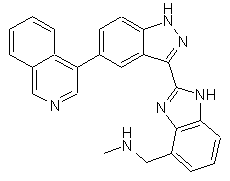 ,
,
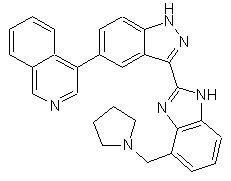 ,
,
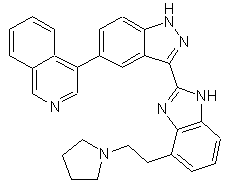 ,
,
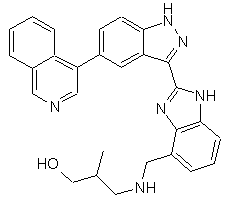 ,
,
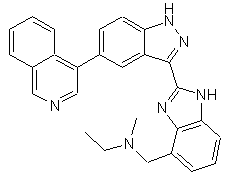 ,
,
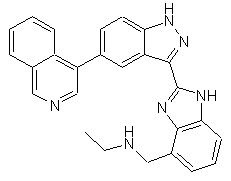 ,
,
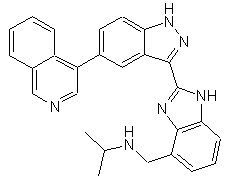 ,
,
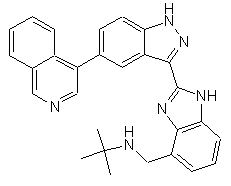 ,
,
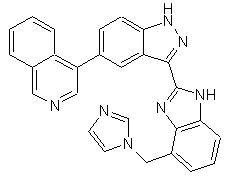 ,
,
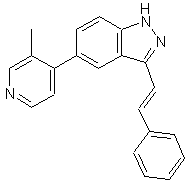 ,
,
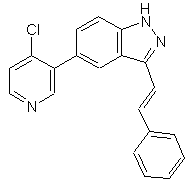 ,
,
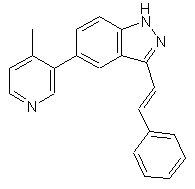 ,
,
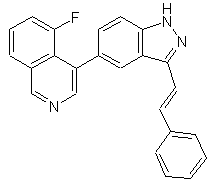 ,
,
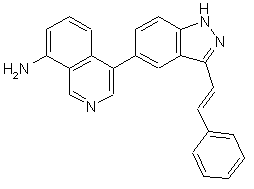 ,
,
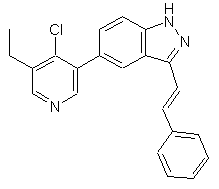 ,
,
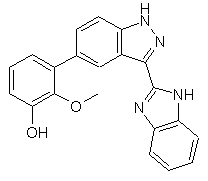 ,
,
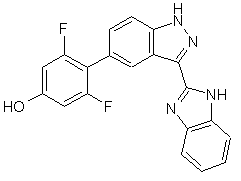 ,
,
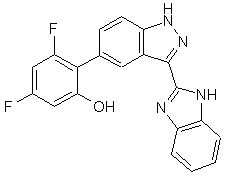 ,
,
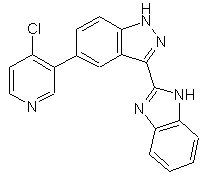 ,
,
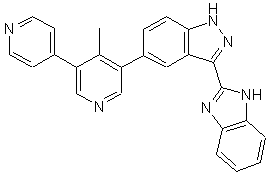 ,
,
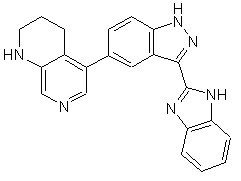 ,
,
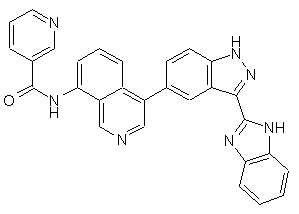 ,
,
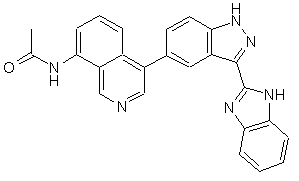 ,
,
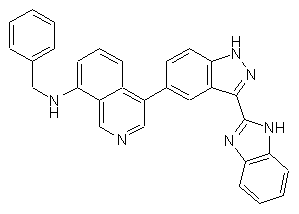 ,
,
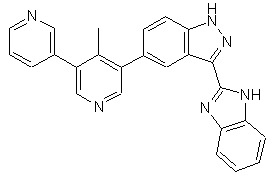 ,
,
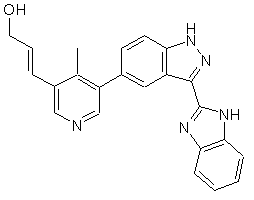 ,
,
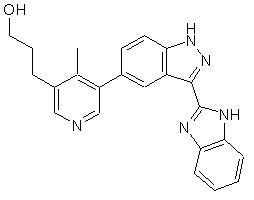 ,
,
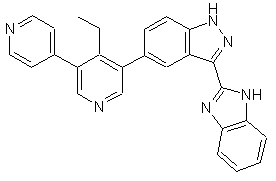 ,
,
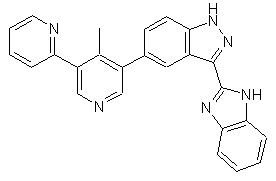 ,
,
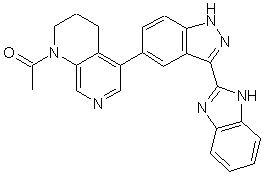 ,
,
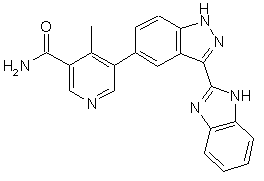 ,
,
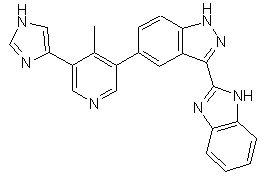 ,
,
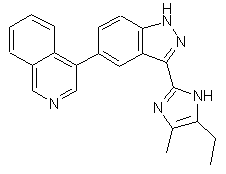 ,
,
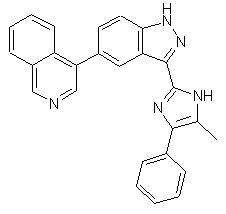 ,
,
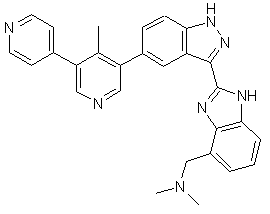 ,
,
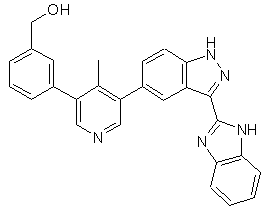 ,
,
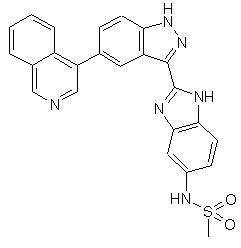 ,
,
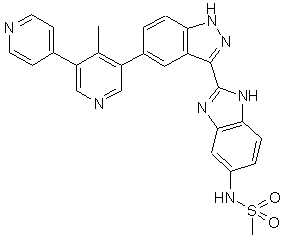 ,
,
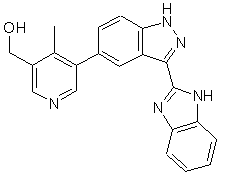 ,
,
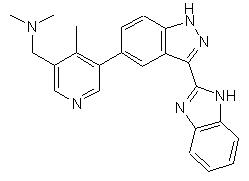 ,
,
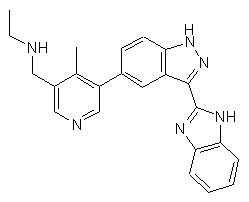 ,
,
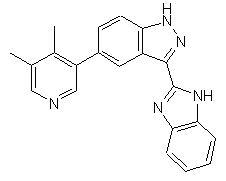 ,
,
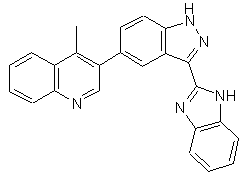 ,
,
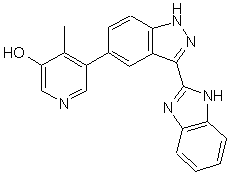 ,
,
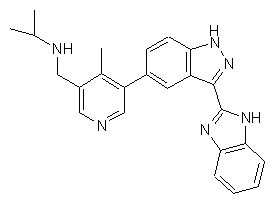 ,
,
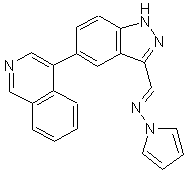 ,
,
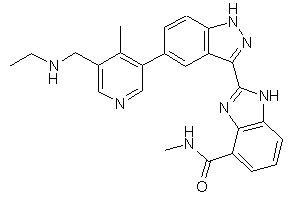 ,
,
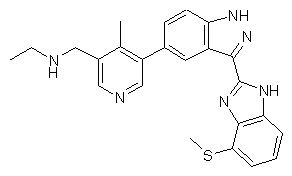 ,
,
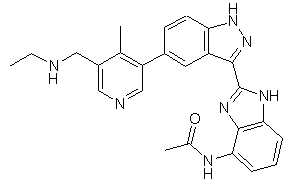 ,
,
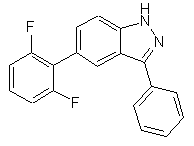 ,
,
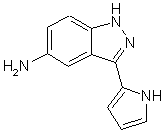
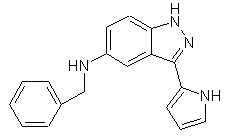 ,
,
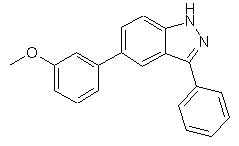 ,
,
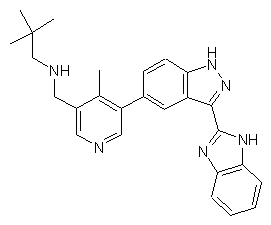 ,
,
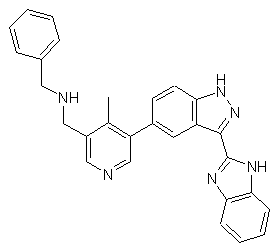 ,
,
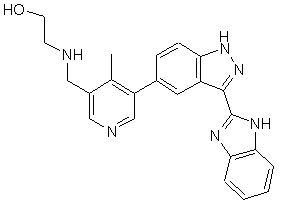 ,
,
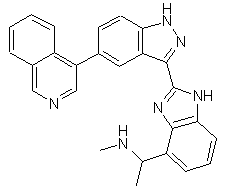 ,
,
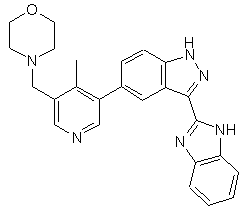 ,
,
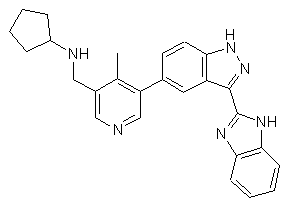 та
та
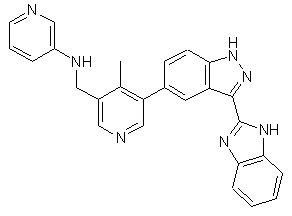 ;
;
або її фармацевтично прийнятна сіль, її проліки або фармацевтично активний метаболіт, або фармацевтично прийнятна сіль проліків або метаболіт.
23. Фармацевтична композиція для лікування симптомів, асоційованих із нерегульованою клітинною проліферацією, містить:
і) сполуку за п. 13 або її фармацевтично прийнятну сіль, проліки або фармацевтично активний метаболіт або фармацевтично прийнятну сіль проліків або метаболіту, та
іі) фармацевтично прийнятний носій.
24. Спосіб лікування хворобливого стану або порушення, асоційованого із нерегульованою клітинною проліферацією, який включає призначення пацієнту в разі необхідності такого лікування терапевтично ефективної кількості сполуки формули II
 (II)
(II)
де R'1 є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
 або
або  ,
,
де R4 у кожній реалізації незалежно є воднем або нижчим алкілом та Χ є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, та
R'2 є заміщеною або незаміщеною аміногрупою, нітрогрупою, алкенілом, алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту,
 або
або  групою,
групою,
де R4 групи є незалежно воднем або нижчим алкілом та Χ є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або
фармацевтично прийнятної солі сполуки формули II або проліків або фармацевтично активного метаболіту сполуки формули II, або фармацевтично прийнятної солі проліків або метаболіту.
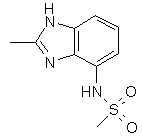
25. Сполука за п. 1, яка відрізняється тим, що R1 є
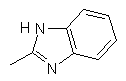 ,
, 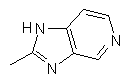 ,
, 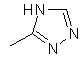 ,
,
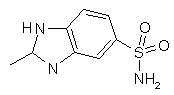 ,
, 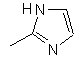 ,
, 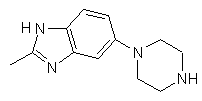 ,
,
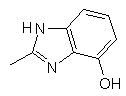 ,
, 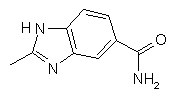 ,
, 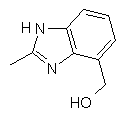 ,
,
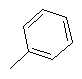 ,
, 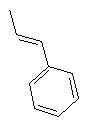 ,
, 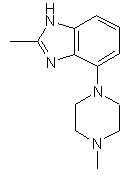 ,
,
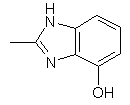 ,
, 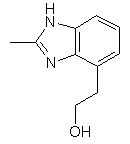 ,
,
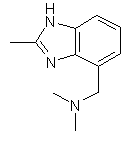 ,
, 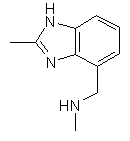 ,
, 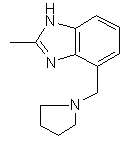 ,
,
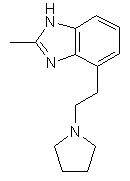 ,
, 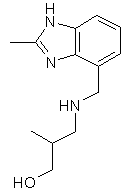 ,
, 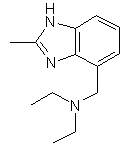 ,
,
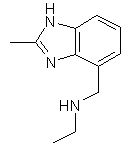 ,
, 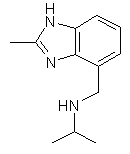 ,
,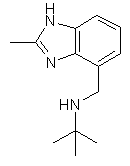 ,
,
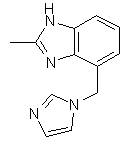 ,
, 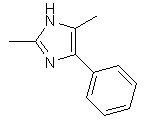 ,
,
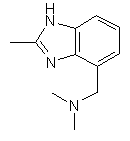 ,
, 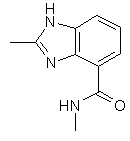 ,
, 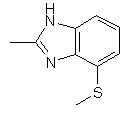 ,
,
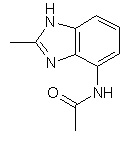 ,
, 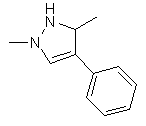 ,
, 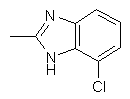 ,
,
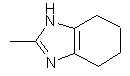 ,
, 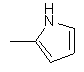 ,
, 
або 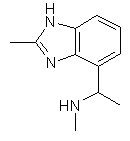 ;
;
та де R2 є
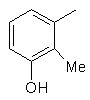 ,
, 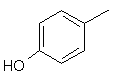 ,
, 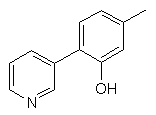 ,
, 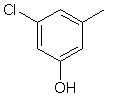 ,
,
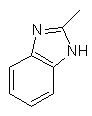 ,
, 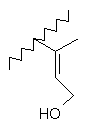 ,
, 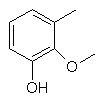 ,
, 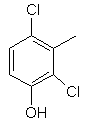 ,
,
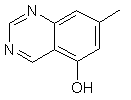 ,
, 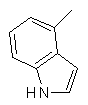 ,
, 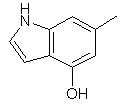 ,
,
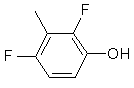 ,
, 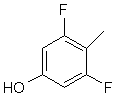 ,
, 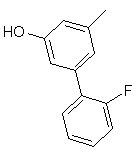 ,
,
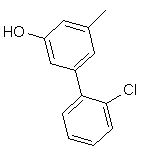 ,
, 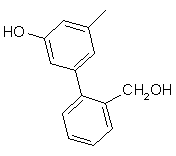 ,
, 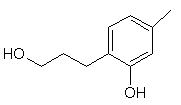 ,
,
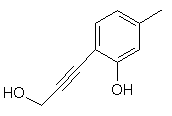 ,
, 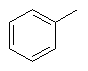 ,
, 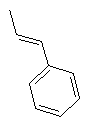 ,
,
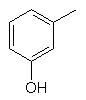 ,
, 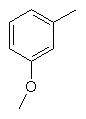 ,
, 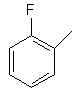 ,
,
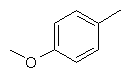 ,
, 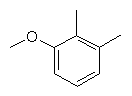 ,
, 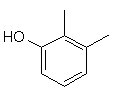 ,
,
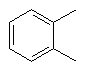 ,
, 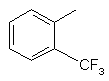 ,
, 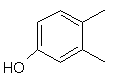 ,
,
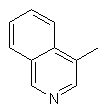 ,
, 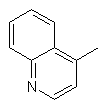 ,
, 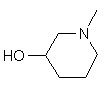 ,
,
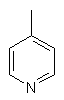 ,
, 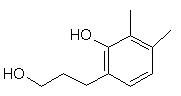 ,
,
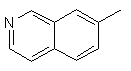 ,
, 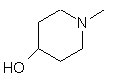 ,
, 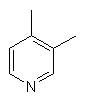 ,
,
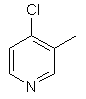 ,
, 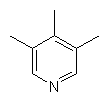 ,
, 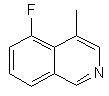 ,
,
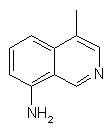 ,
, 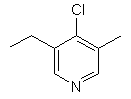 ,
, 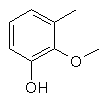 ,
,
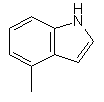 ,
, 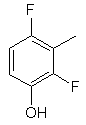 ,
, 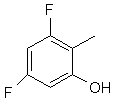 ,
,
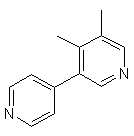 ,
, 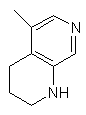 ,
, 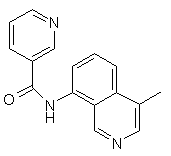 ,
,
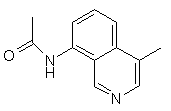 ,
, 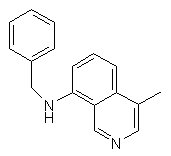 ,
, 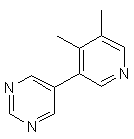 ,
,
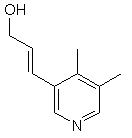 ,
, 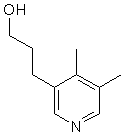 ,
, 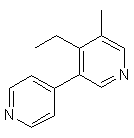 ,
,
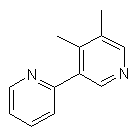 ,
, 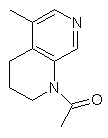 ,
, 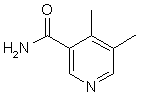 ,
,
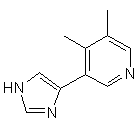 ,
, 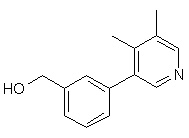 ,
,
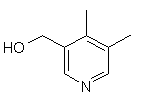 ,
, 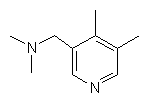 ,
, 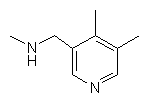 ,
,
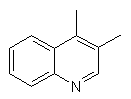 ,
, 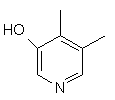 ,
, 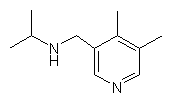 ,
,
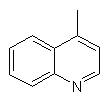 ,
, 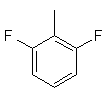 ,
, 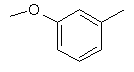 ,
,
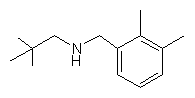 ,
, 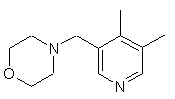 ,
,
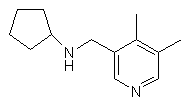 ,
,  ,
,
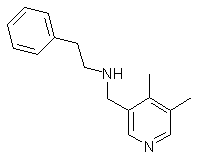 ,
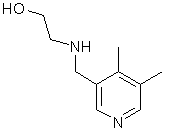
, 
або 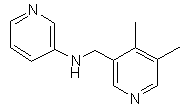 .
.
26. Сполука за п. 13, яка відрізняється тим, що R1 є
 ,
,  ,
,  ,
,
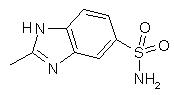 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
, 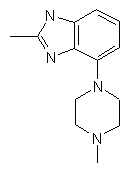 ,
,
 ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
, ,
,
 ,
,  ,
,
 ,
, 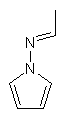 ,
,
 ,
, ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
, 
або  ;
;
та де R’2 є
 ,
,  ,
,  ,
, 
 ,
,  ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
, 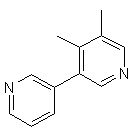 ,
,
 ,
,  ,
,  ,
,
 ,
, 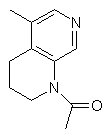 ,
,  ,
,
 ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,
 ,
,  ,
,
 ,
, 
або  .
.
Текст
1. Сполука формули І 2 3 75880 R1 є R4 X R4 , де R4 є воднем, або Y N H R , де Y є СН або N та R3 є Н або заміщеним або незаміщеним алкілом, арилом, карбоциклічною, гетероарильною або гетероциклічною групою, або 3 N HN R1 R3 Y N H 4 або фармацевтично прийнятна сіль сполуки формули І або проліки або фармацевтично активний метаболіт сполуки формули І або фармацевтично прийнятна сіль проліків або метаболіту. 4. Фармацевтична композиція, яка містить: кількість агента регулювання клітинного циклу, достатньо ефективну для інгібування протеїнкіназ, причому вказаний агент регулювання контрольного циклу є сполукою формули І: R2 Y , де Y є С або N та R3 є Н або заміщеним або незаміщеним алкілом, арилом, гетероарильною, карбоциклічною або гетероциклічною групою. 3. Сполука, вибрана із групи, яка включає H N H N , (І) де R1 є воднем або заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або R4 N N X , , H N H N N N NH N NH N OH , , H N N NH N H N F N NH N R4 , де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 13 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, та R2 є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 13 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або R4 O X , H N H N N N O NH N , HO NH N , , H N H N N O N HO NH N N , H N CF3 N , H N N , , H N H N R1 N HO та , H N HO N HN N N NH R4 , де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або фармацевтично прийнятною сіллю сполуки формули І або проліками або фармацевтично активним метаболітом сполуки формули І, або фармацевтично прийнятною сіллю проліків або метаболіту, та фармацевтично прийнятний носій. 5. Спосіб лікування захворювання або порушення, опосередкованого інгібуванням комплексу кіназ, за яким пацієнту у разі необхідності такого лікування призначають агент регулювання клітинного циклу, вибраний із групи, що містить сполуку формули І: N ; R , (І) де R1 є воднем або заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або 2 5 R4 X R4 , де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, та R2 є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 13 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або R4 6 фармацевтично прийнятну сіль сполуки формули І або проліки або фармацевтично активний метаболіт сполуки формули І, або фармацевтично прийнятну сіль проліків або метаболіту та (б) фармацевтично прийнятний носій, розріджувач, переносник або наповнювач для цього. 7. Спосіб лікування симптомів захворювання у ссавців, причому симптоми опосередковані активністю кіназ, за яким ссавцю у разі необхідності такого лікування призначають терапевтично ефективну кількість сполуки формули І: N HN R1 R2 X R , де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або фармацевтично прийнятну сіль сполуки формули І або проліки або фармацевтично активний метаболіт сполуки формули І, або фармацевтично прийнятну сіль проліків або метаболіту. 6. Фармацевтична композиція, яка містить: (а) терапевтично ефективну кількість сполуки формули І: 4 N HN 75880 R1 R2 , (І) де R1 є воднем або заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або R4 X R4 , де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, та R2 є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 13 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або R4 X , (І) де R1 є воднем або заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або R4 X R4 , де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 13 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, та R2 є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або R4 X R4 , де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним, алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 13 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або фармацевтично прийнятної солі сполуки формули І або проліків або фармацевтично активного метаболіту сполуки формули І, або фармацевтично прийнятної солі проліків або метаболіту. 8. Спосіб за п.7, за яким лікують симптоми захворювання у ссавців, пов'язані із ростом пухлин, клітинною проліферацією або ангіогенезом. 9. Спосіб модулювання або інгібування активності рецептора протеїн-кінази, за яким рецептор з'єднують із ефективною кількістю сполуки формули І: HN N R1 R4 , де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або R2 , (І) де R1 є воднем або заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, кар 7 75880 8 боциклом або гетероциклом, що містить 5-10 де R4 є воднем або нижчим алкілом та Х є замікільцевих атомів та 1-3 гетероатоми азоту, або щеним або незаміщеним арилом, гетероарилом, R4 що містить 5-10 кільцевих атомів та 1-3 гетероаX томи азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми R4 , азоту, або де R4 є воднем або нижчим алкілом та Х є заміфармацевтично прийнятною сіллю сполуки форщеним або незаміщеним алкілом, арилом, гетемули І або проліками або фармацевтично активроарилом, що містить 5-10 кільцевих атомів та 1ним метаболітом сполуки формули І, або фарма3 гетероатоми азоту, карбоциклом або гетероцицевтично прийнятною сіллю проліків або клом, що містить 5-10 кільцевих атомів та 1-3 метаболіту. гетероатоми азоту, та 12. Спосіб лікування хворобливих станів або поR2 є заміщеним або незаміщеним алкілом, арирушень, асоційованих із нерегульованою клітинлом, гетероарилом, що містить 5-10 кільцевих ною проліферацією, за яким пацієнту у разі необатомів та 1-3 гетероатоми азоту, карбоциклом хідності такого лікування призначають або гетероциклом, що містить 5-10 кільцевих терапевтично ефективну кількість сполуки форатомів та 1-3 гетероатоми азоту, або мули І: R4 HN X N R1 R4 , де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або фармацевтично прийнятної солі сполуки формули І або проліків або фармацевтично активного метаболіту сполуки формули І, або фармацевтично прийнятної солі проліків або метаболіту. 10. Спосіб за п.9, в якому як рецептор протеїнкіназ використовують CDK комплекс, VEGF або СНК1. 11. Фармацевтична композиція, яка містить ефективну для інгібування комплексу кіназ кількість агента регулювання клітинного циклу, наданого сполукою формули І: N HN R1 R , (І) де R1 є воднем або заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або 2 R4 X R4 , де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 13 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, та R2 є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 13 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або R4 X R4 , R2 , (І) де R1 є воднем або заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або R4 X R4 , де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 13 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, та R2 є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або R4 X R4 , де R4 є воднем або нижчим алкілом та Х є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або фармацевтично прийнятної солі сполуки формули І або проліків або фармацевтично активного метаболіту сполуки формули І, або фармацевтично прийнятної солі проліків або метаболіту. 13. Сполука формули II: HN N R'1 R'2 , (II) де R'1 є заміщеним або незаміщеним арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1 9 3 гетероатоми азоту, або 75880 10 R4 R4 N X X R 4 або , де R4 у кожній реалізації незалежно є воднем або нижчим алкілом та Х є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, та R'2 є заміщеною або незаміщеною аміногрупою, нітрогрупою, алкенілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми N . 19. Сполука за п.13, яка відрізняється тим, що R'2 є заміщеною або незаміщеною групою формули N . 20. Сполука за п.14, яка відрізняється тим, що R'2 містить заміщену або незаміщену групу формули R3 R4 N R4 N X X R 4 азоту, або групою, де R4 групи є незалежно воднем або нижчим алкілом та Х є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або фармацевтично прийнятна сіль сполуки формули II або проліки або фармацевтично активний метаболіт сполуки формули II, або фармацевтично прийнятна сіль проліків або метаболіту. 14. Сполука, фармацевтично прийнятна сіль, проліки або її фармацевтично активний метаболіт за п.13, яка відрізняється тим, що R'1 є Y N H Y R3 N H N . 22. Сполука, вибрана із групи, що містить H N H N N N O2 N N , , H N H N N N Y R , або , де Y є незалежно СН, СR3 або N та групи R3 незалежно є одним або більше Н, заміщеним або незаміщеним алкілом, алкенілом, арилом, карбоциклом, гетероарилом, гетероциклом, гідроксигрупою, галогеном, алкоксигрупою, арилоксигрупою, гетероарилоксигрупою, тіоарилом, тіогетероарилом, тіоалкілом, тіоацилом або аміногрупою, за умови, що може бути більше однієї групи R3. 15. Сполука за п.14, яка відрізняється тим, що R'2 є заміщеним або незаміщеним гетероарилом із вмістом азоту, a R'1 є 3 N R3 Y N H . 21. Сполука за п.13, яка відрізняється тим, що R'2 містить заміщену або незаміщену групу формули N N , , H N H N N N O2 N N NH NH , , H N N N H N NH N N Y N N H NH N N R3 . 16. Сполука за п.13, яка відрізняється тим, що R'2 є заміщеним або незаміщеним гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту. 17. Сполука за п.13, яка відрізняється тим, що R'2 є заміщеною або незаміщеною групою формули N Cl , , H N H N N HO N HO NH N HO HO , , H N N . 18. Сполука за п.13, яка відрізняється тим, що R'2 є заміщеною або незаміщеною групою формули N HO H N N N HO NH N , , 11 75880 H N H N N NH N NH N , N N , , H N H N H N F N N N N HO O , F HO NH N , H N N NH N OH , H N , H N F N N , H N N HO N H2 N HO N H N Cl N N HO N 12 H N H N Cl N N NH N N NH N OH F NH N N N NH HO , HO , H N N N , H N N NH N N N N N N HN NH N , H N H N NH N N NH N H N N , , , H N H N N N , N H N H N N N N NH N N NH N O O N H N N H NH N N NH N N N , , H N , N H N N N H N N N NH N , H N N N N HO N N H NH NH N N NH N N NH , , H N H N , OH , OH N N H N H N N N NH N N H N H N N , NH N H N N NH N , , H N N H N N NH N N , H N N N NH N N H N N N N N , H N N NH N , , N N N N H2 N N , NH N , F N N N NH , , H N H N H N H N H N O N H N , H N O N N NH N H N Cl N N N NH N N N N N N N , , N NH N , N NH , 13 H N 75880 N N 14 H N H N H N N N N O HN N NH N N NH NH N , N , , H N NH H N , N H N NH N N OH N H N N N NH N N NH N NH N , N NH N HN O , H N H N O S NH , N N N N NH N N NH N H N H N OH NH N N H N N , HO , N , O N HN S NH N H N N N O O N , , N H N N N NH N H N NH N N N NH N H N NH N NH та , N NH N N H N NH N , , H N H N N N NH N N N N , N NH N H N NH N N N NH N , ,H N H N N N N H N N NH N N H N N , , O H N NH N N N H N H N N S NH N H , H2 N NH F , N O N N HN N N H N H N F NH ; або її фармацевтично прийнятна сіль, її проліки або фармацевтично активний метаболіт, або фармацевтично прийнятна сіль проліків або метаболіт. 23. Фармацевтична композиція для лікування симптомів, асоційованих із нерегульованою клітинною проліферацією, містить: і) сполуку за п.13 або її фармацевтично прийнятну сіль, проліки або фармацевтично активний метаболіт або фармацевтично прийнятну сіль проліків або метаболіту, та іі) фармацевтично прийнятний носій. 24. Спосіб лікування хворобливого стану або порушення, асоційованого із нерегульованою клітинною проліферацією, який включає призначення пацієнту в разі необхідності такого лікування терапевтично ефективної кількості сполуки формули II NH , H N HO N N NH R'1 , R'2 (II) де R'1 є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або 15 75880 16 H N R4 H N N R4 N X N X R 4 або , де R4 у кожній реалізації незалежно є воднем або нижчим алкілом та Φ є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, та R'2 є заміщеною або незаміщеною аміногрупою, нітрогрупою, алкенілом, алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, N , , H N H N N N N HN HN HN , , H N , H N H N N N N N X N , HN N O S , H N , H N N H Cl , H N H N O HN або O ; Cl NH , Me , OH HO , OH N , OH , N O N NH2 NH HO , , OH , OH N , F , , HO H N F , , HO N Cl , CH2OH , N HN , HO H N N , OH N N OH , F F F N , HO N H N HN , , H N OH OH N N , , H N N , Cl O HO , N OH , Cl H N H N OH , N HN N , N N HN HN N , H N N N N , NH , N N , та де R2 є , O O HN HN S O NH2 N , N N HN S N H N H N HN N , N HN HN , , H N R 4 або групою, де R4 групи є незалежно воднем або нижчим алкілом та Φ є заміщеним або незаміщеним алкілом, арилом, гетероарилом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, карбоциклом або гетероциклом, що містить 5-10 кільцевих атомів та 1-3 гетероатоми азоту, або фармацевтично прийнятної солі сполуки формули II або проліків або фармацевтично активного метаболіту сполуки формули II, або фармацевтично прийнятної солі проліків або метаболіту. 25. Сполука за п.1, яка відрізняється тим, що R1 є N , H N X HN HO N R4 N N HN N R4 N H N , HO , OH , 17 18 N HO OH HO 75880 , , N HO , N , N , N , , F HO N H O OH , , , N O O N , HO , F , CF3 HO , , N H , , , , N N HO , N N H O HO , , O , N N , HO N , N , N N N , , , N , HO Cl N NH NH N N H HO N , N , N , , NH2 N , OH , N , F S O NH2 N F OH , OH F , , N , N N H N , NH , HN O N OH , N O N N NH2 N HO , N H N , N , H N N N N N , H N N , , N N N , , N N , N N N N N , , , N , H N N HN N , N N N , , H N N N N , H N HN H2N N , H N O O , N HN N , H N N N OH OH , H N H N OH N , N OH N H , HN HN N O , HN N , N N , HN O N N N , HN F H N HN HN O , N HN N N N , або . 26. Сполука за п.13, яка відрізняється тим, що R1 є N Cl F NH F N H N , , HO , HN , , 19 75880 H N H N H N N HO H N N 20 N , , H N , H N N , , , , N , HO , NH N H Cl , N , N , , F N N N , N , , H N H N N N O HN O S N H N Cl H N , , N HO , N , Cl , , HO N HO S H N O N O , N HO N N HN H N , , H N N N N CF3 , N N N , N HN HN NH2 O , H N N , OH , , , F F N N N F HN або ; та де R’2 є OH OH F , N , NH , , Cl N Me OH , HO OH N , OH , O O N H Cl N N N H N H N , NH N , OH Cl O HO , OH , OH , , H N N , OH N N N , N N , N , N , N , , N OH HN , OH , O , N HO F N H2N O N F N N , , , F OH F HO , F , , N HN N HO , HO Cl , N H HO N OH , HO , N CH2OH N HO N , , , HO F N H N OH HO , , , OH , N , O , O , , O , , , , N N H F O N , F , O N , 21 75880 22 HO NH N NH N N H N , N N H N , N , Дана заявка використовує пріоритет та в цілому включає попередню заявку США за реєстраційним номером 60/176,484, подану 18 січня 2000 року. Даний винахід спрямовано на отримання індазольних сполук, які опосередковують та/або інгібують клітинну проліферацію, наприклад, інгібуванням активності протеїн-кіназ, таких як VEGF, СНК-1, та циклінозалежних кіназ (CDK), таких як CDK1, CDK2, CDK4 та CDK6. Крім того, цей винахід стосується фармацевтичних композицій, що містять такі сполуки та їх композиції, та способи лікування раку, а також інших станів захворювань, пов'язаних із небажаним ангіогенезом та/або клітинною проліферацією, шляхом введення ефективних доз таких сполук. Нерегульована клітинна проліферація є характерною відзнакою раку. Про клітинну проліферацію, викликану різними побудниками, свідчить розрегульований цикл поділу клітин, процес, за яким клітини розмножуються та поділяються. Пухлинні клітини звичайно пошкоджують гени, які безпосередньо або посередньо регулюють прогресію протягом циклу поділу клітин. Для гіперпроліферативної симптоматики, включаючи рак, характерними є клітини, які інтенсивно звиваються протягом циклу із нерегульованою енергією, наприклад, за рахунок пошкодження генів, які безпосередньо або посередньо регулюють розвиток протягом циклу. Таким чином, агенти, які модулюють клітинний цикл та при цьому гіперпроліферацію, можна використовувати для лікування різних хворобливих станів, асоційованих із нерегульованою або небажаною клітинною проліферацією. Крім агентів хіміотерапії раку, інгібітори клітинного циклу також було запропоновано як антипаразити [дивись, Gray et al., Curr. Med. Chem. 6, 859-875 (1999)] та недавно показали себе як потенційний противірусний засіб [дивись Schang et al., J. Virol. 74, 2107-2120 (2000)]. Більш того, застосовність антипроліферативних агентів можна поширити для лікування серцево-судинних порушень, таких як артеросклероз або рестеноз [дивись Braun-Dullaeus et al., Circulation, 98, 82-89 (1998)] та запалювальних станів, таких як артрит [дивись Taniguchi et al., Nature Med., 5, 760-767 (1999)] або псоріаз. Зараз активно проводяться дослідження механізмів клітинної проліферації на клітинному та молекулярному рівнях. На клітинному рівні розрегульованість напрямків сигналів, втрата контролю клітинного циклу, нестриманого ангіогенезу або стимуляція запального спрямування знаходиться під уважним спостереженням, в той час як на молекулярному рівні ці процеси модулюються різними протеїнами, серед яких протеїн-кінази є або N . найбільш вірогідними. Загальне усування проліферації може також бути викликане програмованою смертю клітин, або апоптозом, який також регулюється багатьма різними шляхами, деякі з яких включають протеолітичні ферментні протеши. Як варіант регуляторних протеїнів протеїн кінази є сімейством ферментів, яке прискорює фосфориляцію гідроксильних груп визначених залишків тирозину, серину або треоніну в протеїнах. Звичайно така фосфориляція в значній мірі порушує функцію протеїну, та при цьому протеїнкінази відіграють керівну роль в регулюванні різноманітних клітинних процесів, включаючи метаболізм, клітинну проліферацію, клітинну диференціацію та виживання клітин. Із багатьох різних функцій клітин, виконання яких потребує, як відомо, активності протеїн-кіназ, деякі процеси є привабливими мішенями для терапевтичного втручання при наявності певних хворобливих станів. Двома прикладами цього є ангіогенез та регуляція клітинного циклу, в яких протеїн-кінази відіграють керівну роль; ці процеси суттєво впливають на розвиток солідних пухлин, а також інших захворювань. CDK складають клас ферментів, які відіграють критичну роль у регуляції переходів одних стадій клітинного циклу в інші, таких як розвиток із стану спокою G1 (проміжок між мітозом та початком реплікації ДНК для нового циклу поділу клітин) у S (період активного синтезу ДНК), або розвиток із G2 у фазу М, в якій наступає активний мітоз та поділ клітин. [Дивись, наприклад, статті, зібрані в Science, том 274 (1996) стор.1643-1677; та Ann. Rev. Cell Dev. Βiol, том 13 (1997), стор.261-291.]. Комплекси CDK утворюються під час з’єднання регуляторної субодиниці цикліну (наприклад, циклін А, В1, В2, Dl, D2, D3, та Е) та субодиниці каталітичної кінази (наприклад, cdc2 (CDK1), CDK2, CDK4, CDK5 та CDK6). Як видно з назви, CDK повністю залежать від субодиниці цикліну для фосфориляції їх субстратів-мішеней та від функції комплексів кіназа/циклін для регуляції прогресії протягом специфічних фаз клітинного циклу. Цикліни D є чуттєвими до сигналів позаклітинного розростання та активуються у відповідь на мітогени протягом фази G1 клітинного циклу. Комплекс CDK4/циклін D відіграє важливу роль у прогресії клітинного циклу за рахунок фосфориляції та при цьому інактивації ретинобластомного протеїну (Rb). Гіперфосфорильований Rb з'єднується із сімейством транскрипційних регуляторів, але після гіперфосфориляції Rb за рахунок CDK4/цикліну D транскрипційні фактори вивільнюються для активації генів, продукт яких відповідає за розвиток фази S. Фосфориляція Rb та 23 75880 24 інактивація CDK4/циклін D дозволяє проходженстрат, так і інгібітор СОK2/цикліну Е, є ненорманя клітин поза обмежувальним пунктом фази G1 в льно низькими при раці груді, ободової кишки та наслідок чого втрачається чутливість до позакліпростати, а рівні експресії р27 навпаки пов’язані тинного розростання або інгібіторного сигналу та із станом захворювання (дивись Loda et al., клітина піддається поділу. Протягом останньої "Increased Proteasome-dependent Degradation of фази G1 Rb також фосфорилюється та інактивуthe CyClin-Dependent Kinase Inhibitor p27 in ється комплексом CDK2/циклін Ε та ця нова відAggressive Colorectal Carcenomas", (Підвищена знака вказує нате, що CDK2/циклін Ε може також протеазомозалежна деградація інгібітора р27 регулювати розвиток у фазу S по паралельному циклінозалежної кінази в агресивних колоректашляху, який не залежить від фосфориляції Rb льних карциномах) [Nature Medicine, том 3 (1997) [дивись Lukas et al., "Cyklin Ε-induced S Phase стор.231-234]). Недавно було виявлено, що Without Activation of the pRb/E2F Pathway" (ІндуCDK4/цикліну D міг зв’язувати р27, як було [опикована цикліном Е фаза S без активації шляху сано у Sherr, et al., Genes Dev., vol.13 (1999), pRb/E2F) Genes and Dev., том 11 (1997)6 p.1501-1502]. Крім того, появляються також простор.1479-1492]. теїни р21 для передачі пухлиннопригнічувального На розвиток із G в фазу S під дією сигналу р53 у CDK; таким чином, мутація р53 у CDK4/цикліну D та CDK2/цикліну Ε впливають приблизно 50% всіх видів раку людини може порізні регулювальні механізми росту, як негативні, середньо викликати розрегулювання активності так і позитивні. Ростовий стимул, такий як мітоCDK. ген, викликає збільшений синтез цикліну D1 і, Вихідні дані підтверджують ефективну застотаким чином, збільшену функціональну CDK4. совність сполук, інгібуючих CDK, та зокрема осоНавпаки розростання клітин може бути "зупинебливо CDK4 та CDK2, як антипроліферативних но" у відповідь на пошкодження ДНК або негатиагентів. З цією метою були запропоновані певні вний стимул росту шляхом стимулювання ендобіомолекули. [Наприклад, в патенті США генних інгібіторних протеїнів. Такі натуральні 5,621,082, Xiong et al.,описано нуклеїнову кислопротеїнові інгібітори включають сімейства ту, яка кодує інгібітори CDK6, та в заявці WO p21WAF1/CIP1 р27KIР1 та р16INК4, причому останнє 99/06540] описано інгібітори CDK. Пептиди та інгібує виключно CDK4 [дивись Harper, "CyClin пептидоподібні інгібітори [описані в ЄвропейсьDependent Kinase Inhibitors" Cancer Surv., том 29 кому патенті №0 666 270 А2, Bandara et al., (1997), стор.91-107]. Відхилення в цій системі Nature Biotechnology, том 15 (1997), стор.896-901 регулювання, зокрема ті, що впливають на функта Chen, et al., Proceedings of the Natuional цію CDK4 та CDK2, включаються в розвиток кліAcademy of Science, США, vol.96 (1999), pp.4325тин до відзнаки злоякісностей високо проліфера4329]. Пептидні аптамери були визначені відботивного стану, таких як спадкоємні мелономи, ром [у Cohen, et al., Proc. Nati. Acad. Sci. U.S.A., стравохідні карциноми та різновиди раків підшлутом 95 (1998), стор.14272-14277]. Декілька дрібнкової залози. (Дивись, наприклад, Hall and них молекул були визначені як CDK інгібітори (із Peters, "Genetic Alterations of CyClins, CyClinостанніх оглядів дивись Webster, "Therapeutic Dependent Kinases, and CDK Inhibitors in Human Potential of Targeting the Cell СуСlе" (ТерапевтичСаnсеr" (Генетичні зміни циклінів, циклінона еффективність виконання мішенів в клітиннозалежних кіназ та інгібіторів циклінозалежних му циклі), [Exp. Opin. Invest. Drugs, том 7 (1998), кіназ при раці людини", [Adv. Cancer Res., том 68 стор.865-887], та Stover, et al., "Recent Advances (1996), стор.67-108; та Kamb et al., "A cell CyCle in Protein Kinase Inhibition: Current Molecular Regulator Potentially Involved in Genesis of Many Scaffolds used for Inhibitor Synthesis" (Нові досягTumor Types", Science, том 264 (1994), стор.436нення в галузі інгібування протеїн-кіназ: Поточні 440]). Надмірна експрессія цикліну D1 з'єднується молекулярні клітинні каркаси у використанні для із карциномами стравоходу, грудної клітки та інгібіторного синтезу), [Current Opinion in Drug плоскоклітинною карциномою, (дивись, наприDiscovery and Development, том 2 (1999), клад, DelSal et al., "Cell CyCle and Cancer: Critical стор.274-285]). Флавопіридол флавону показав Events at the Gl Restriction Point" (Клітинний цикл обмежену селективність для інгібування CDK у та рак: критичні події в межовій ділянці фази G1), порівнянні із іншими кіназами, але виявив еквіпо[Critical Rev. Oncogenesis, том 71 (1996), тенціальне інгібування CDK4, CDK2 та CDK1 із стор.127-142]). Генне кодування CDK4 інгібіторів ІС50 в діапазоні 0,1-0,3мкМ. Флавопіридол зараз сімейства p16 часто мають делеції та мутації у проходить клінічні випробування у фазі II онколоспадкоємних мелономах, гліомах, лейкеміях, саргічний хіміотерапевтичний агент [Sedlacek et al., комах та карциномах підшлункової залози, недрі"Flavopiridol (L86-8275; NSC 649890), A New бноклітинних карциномах легенів та карциномах Kinase inhibitor for Tumor Therapy" (Флавопіридол голови та шиї (дивись Nobori et al., "Deletions of (L86-8275; NSC 649890), новий інгібітор кіназ при the CyClin-Dependent Kinase-4 Inhibitor Gene in лікуванні пухлин), Int. J. Oncol, vol.9 (1996), Multiple Human Cancers" (Делеції гену інгібітору pp.1143-1168]. Аналоги флавопіридолу розглядациклінозалежних кіназ- 4 в різних формах раків лись в інших публікаціях, [наприклад, в патенті людини), [Nature, том 368 (1994), стор.753-756]). США 5,733,920 Masuri et al., (Міжнародна заявка Крім того, в різноманітних твердих пухлинах споWO 97/16447) та в міжнародних заявках WO стерігалися амплифікація та/або надмірна екс97/42949 та WO 98/17662]. Результати досліпрессія цикліну Е, а підвищені рівні цикліну Ε буджень із похідними на основі пурину [описані в ли пов'язані із поганими прогнозами. Більш того, Schow et al.,Biorg. Med. Chem. Lett., vol.7 (1997), клітинні рівні CDK інгібітору р27, який діє як субpp.2697-2702; Grant et al., Proc. Amer. Assoc. 25 75880 26 Cancer Res., vol.39 (1998), Abst.,1207; Legravend (1998); Thompson, Oncogene, 15, 3025-3035 et al., Biorg. Med. Chem. Lett., vol.8 (1998), pp.793(1997)]. Після визначення суттєвої ролі провідно798; Gray et al., Science, том 281 (1998), стор.533го спрямування р53 як пригнічувача пухлин в ро538; Chang, et al., Chemistry & Biology, том 6 звитку раку людини були проведені активні пошу(1999), стор.361-375, WO 99/02162, WO 99/43675 ки способів терапевтичних впливів на рак, та WO 99/43676]. Крім того, наступні публікації викликаний дефектом р53. При появі таких вразописують певні піримідини, які інгібують цикліноливих місць, вони розташовуються в полі дії конзалежні кінази та кінази, опосередковані ростотрольної точки G2 в клітинах раку, викликаного вим фактором: [Міжнародні публікації WO дефектом р53. Ракові клітини через недостатнє 98/33798; Ruetz et al., Proc. Amer. Assoc. Cancer керування контрольних точок G1 особливо вразRes., vol.39 (1998), abstr. 3796; та Meyer et al., ливі при знищенні останнього бар'єру, що залиProc. Amer. Assoc. Cancer Res., том 39 (1998), шився для захисту їх від знищувального ефекту abstr. 3794. Бензолсульфонаміди, які блокують пошкоджувальних ДНК агентів: контрольна точка клітини в G1 досліджуються у Eisai, дивись Owa, G2. Контрольна точка G2 регулюється системою et al., J. Med. Chem. Том 42 (1999), стор. 3789керування, яка збереглася у процесі еволюції від 3799. Оксидольний CDK інгібітор досліджується у дріжджових клітин до клітин людей. Важливою в Glazo-Wellcome, дивись Luzzio, et al., Proc. Amer. цій збереженій системі є кіназа, СНК1, яка трансAssoc. Cancer Res., том (1999), рефю 4102 та дукує сигнали із сенсорного комплексу пошкоWO99/15500. Паулони були винайдені у сполудженої ДНК для інгібування активації кінази цикченні із NCI, Schultz, et al., J. Med. Chem.TOM ліну В/Cdc2, що сприяє входженню клітин у (1999), стор. 2909-2919. Індопіразоли описані в мітотичну стадію. Дивись, [наприклад, Peng et al., WO 99/17769 та у Seitz, et al., 218th ACS Nati. Mtg. Science, 277, 1501-1505 (1997); Sanchez et al., (Aug. 22-26, 1999, New Orleans) Abst. MEDI 316. Science, 277, 1497-1501 (1997)]. Була показана Амінотіазоли використовуються у WO 99/24416 інактивація СНК1 в обох випадках пригнічення G2j та WO 99/21845.] викликаних пошкодженням ДНК, яке відбувається CHК1 є іншою протеїн-кіназою. В процесі ровнаслідок дії антиракових агентів або за рахунок звитку клітинного циклу СНК1 важливу роль відігендогенного пошкодження ДНК, а також у рерає як контрольна точка. Контрольні точки є сисзультаті переважного знищення клітин, в яких темами керування, які координують розвиток спостерігається дефект функції контрольних токлітинного циклу шляхом впливу на утворення, чок. Дивись, [наприклад, Nurse, Cell, 91, 865-867 активацію та наступну інактивацію цикліно(1997); Weinert, Science, 277, 1450-1451 (1997); залежних кіназ. Контрольні точки припиняють Walworth et al., Nature, 363, 368-371 (1993); Alрозвиток клітинного циклу у невідповідні періоди, Khodairy et al., Molec. Biol. Cell. 5, 147-160 (1994)]. підтримують метаболічний баланс клітин при Селективні маніпуляції, спрямовані на регуляцію затримці клітин та у деяких випадках можуть інконтрольних точок ракових клітин, можуть знайти дикувати апоптоз (запрограмовану смерть клішироке застосування у радіотерапії та хіміотератин), якщо вимоги для контрольних точок не були пії раку та, крім того, приведуть до виведення виконані. [Дивись, наприклад, O'Connor, Cancer загальної відзнаки "геномної нестійкості" раку surveys, 29 151-182 (1997); Nurse, Cell, 91, 865людини, що можна буде застосовувати як базу 867 (1997); Hartwell et al., Science, 266, 1821-1828 для руйнування ракових клітин. Ряд факторів (1994); Hartwell et al., Science, 246, 629-634 свідчить про керівну роль СНК1 у регулюванні (1989)]. пошкоджень ДНК контрольними точками. ТрактуОдна послідовність контрольних точок відсвання інгібіторів цієї та функціонально подібних лідковує цілісність геному та при наявності пошкіназ, таких як CDS1/СНК2, кінази, що, як недавно коджень ДНК ці "контрольні точки пошкоджень винайдено, зв'язуються із СНК1 при регулюванні ДНК" блокують розвиток циклу клітин у фазах G1 розвитку S фази [дивись Zeng et al., Nature, 395, та G2 та повільнюють розвиток протягом фази S. 507-510 (1998); Matsuoka, Science, 282, 1893[Дивись O'Connor, Cancer surveys, 29 151-182 1897 (1998)], і може забезпечити нові цінні тера(1997); Hartwell et al., Science, 266, 1821-1828 певтичні заходи для лікування раку. (1994)]. Ця дія дозволяє виконання процесів відІншою групою кіназ є тирозин-кінази. Тирозин новлення ДНК для завершення їх функцій перед - кінази можуть бути рецепторного типу (маючи тим, як розпочнеться реплікація геному та наступозаклітинні, трансмембранні або внутрішньо пне розділення цього генетичного матеріалу на клітинні домени) або нерецепторного типу (якщо нові дочірні клітини. Дуже важливим моментом є вони повністю внутрішньоклітинні). Принаймні те, що ген, який найчастіше мутує при раку у люоднаіз протеїнових кіназ тиразину нерецепторнодини, це ген р53, що пригнічує пухлину, виробляє го типу, а саме, LCK, опосередковує трансдукцію протеїн контрольних точок пошкодження ДНК, в Т-клітинах сигналу із взаємодії протеїну, що який блокує розвиток клітинного циклу в фазі G1 знаходиться на поверхні клітини, (Cd4) із перехта/або індукує апоптоз (запрограмована смерть ресно-зв'язаним анти-Сd4 антитілом. Більш деклітин), який наступає за пошкодженням ДНК. тальний опис нерецепторних тирозин-кіназ нада[Дивись Hartwell et al., Science, 266, 1821-1828 но в Bolen, Oncogene, 8, 2025-2031 (1993), на що (1994)]. Було виявлено, що ген р53 - пригнічувач в описі даного винаходу зроблено посилання. пухлин -підсилює дію "контрольної точки пошкоКрім їх значення при регулюванні клітинного цикдження ДНК" у фазі G2 клітинного циклу. Дивись, лу протеїн-кінази також відіграють ключову роль [наприклад, Bunz et al., Science, 28, 1497-1501 у ангіогенезі, який є механізмом, при якому із іс(1998); Winters et al., Oncogene, 17, 673-684 нуючих судин утворюються нові капіляри. При 27 75880 28 необхідності судинна система здатна утворювати судин. З іншого боку, виявилось, що фактор ангінові капілярні мережі для підтримки належного опоіетин-2 справляє протилежну ангіопоіетину-1 функціонування тканин та органів. Однак, у дородію на ТЕК та перериває ангіогенез. [Дивись слих ангіогенез достатньо обмежений і наступає Maisonpierre et al., Science, 277, 55-60 (1997)]. тільки в процесі загоювання ран та неоваскуляНа основі результатів вищеописаних досліризації ендометрія протягом менструального циджень було запропоновано пригнічувати ангіогеклу. Дивись [Merenmies, J., Parada, L.F., нез шляхом застосування сполук, які інгібують Henkemeyer, M., Cell Growth & Differentiation, 8, 3активність кіназ VEGF - R2, FGF - R та/або ТЕК. 10 (1997)]. З другого боку, небажаний ангіогенез є Наприклад, [в міжнародній публікації WIPO No відзнакою декількох захворювань, таких як ретиWO 97/34876] описано певні похідні сіноліну, які є нопатія, псоріаз, ревматоїдний артрит, вікова інгібіторами VEGF - R2, що можна використовудегенерація рогівки (ВДР) та рак (солідні пухливати для лікування хворобливих станів, пов'язани). Дивись [Folkman, Nature Med.,l, 27-31 (1995)]. них із патологічним ангіогенезом та/або судинною Протеїн-кінази, які, як було виявлено, втягуються проникністю, наприклад, рак, діабет, псоріаз, рев ангіогенний процес, містять три члени сімействматоїдний артрит, саркома Капоші, гемангіома, ва тирозин-кіназ рецепторів фактора росту: VEGF гострі або хронічні нефропатії, атерома, рестиноз - R2 (судинний ендотеліальний рецептор фактоартерій, аутоімунні захворювання, гострі запальні ра росту 2, відомий також як KDR (рецептор ділязахворювання та очні захворювання з проліфенки вставки кінази) та FLK - 1); FGF - R (рецептор рацією судин сітківки. фактора росту фібробластів) та ТЕК (також відоКрім протеїн-кіназ, вказаних вище, можна ромий як Тіе-2). VEGF-R2, який експресується тільзглядати багато інших протеїн-кіназ як терапевки на ендотеліальних клітинах, зв'язує сильний тичні цілі, та багато публікацій описують інгібітори ангіогенний фактор росту VEGF та опосередкоактивності кіназ, як надано в наступних роботах: вує наступну трансдукцію сигналу за рахунок під[McMahon et al., Current Opinion in Drug Discovery вищення активності внутрішньоклітинних кіназ. & Development, 1, 131-146 (1998); Strawn et al., Таким чином, припускається, що безпосереднє Exp. Opin. Invest. Drugs, 7, 553-573 (1998)]. Однак, інгібування активності кіназ рецептора VEGF-R2 досі існує потреба в дрібномолекулярних сполуповинно привести до послаблення ангіогенезу ках, які можуть легко синтезуватись та є ефектинавіть в присутності екзогенного VEGF [дивись вними інгібіторами клітинної проліферації, наприStrawn et al, Cancer Research, 56, 3540-3545 клад, інгібіторами однієї або більше протеїн-кіназ, (1996)], як було показано на мутантних VEGF таких як СНК1, VEGF, CDK або CDK/циклінових R2, які не опосередковували трансдукцію сигнакомплексів. За рахунок того, що CDK4 може слулу. [Дивись Millauer et al., Cancer Research, 56, жити основним активатором поділу більшості 1615-1620 (1996)]. Крім того, VEGF - R2 у доросклітин, а комплекси CDK4/циклін D та лих, як виявилось, не має іншої функції, крім опоCDK2/циклін Ε впливають на ранню фазу G1 клісередковування ангіогенної активності VEGF. тинного циклу, виникає потреба в ефективних Отже, припускається, що вибраний інгібітор актиінгібіторах CDK4 та/або CDK2 для лікування одвності кіназ VEGF - R2 показує незначну токсичного або більше видів ракових пухлин. ність. Отже цей винахід спрямовано на створення Аналогічно FGF - R зв'язує фактори росту сусильних антипроліферативних агентів. Відповідно дин aFGF та bFGF та опосередковує наступну одним об'єктом винаходу є отримання сполук та внутрішньоклітинну сигнальну трансдукцію. Нелікувальних композиції, які інгібують активність давно було висловлено думку, що фактори росту, однієї або більше кіназ, таких як CDK, VEGF та такі як bFGF, можуть грати критичну роль в ініціСНК-1 або їх циклінових комплексів. Крім того, ації ангіогенезу в солідних твердих пухлинах, які об’єктом даного винаходу є створення ефективдосягай певного розміру. [Дивись Yoshiji et al., ного способу лікування симптоматики раку шляCancer Research, 57, 3924-3928 (1997)]. Однак, на хом інгібування VEGF, CHK1, CDK4 або відміну від VEGF - R2, FGF - R проявляється в CDK/комплексів циклінів D типу та/або CDK2 або цілому ряді різних типів клітин у всьому тілі і моCDK2/комплексів циклінів Ε типу. Іншим об’єктом же відігравати важливу роль у інших нормальних є отримання фармацевтичних композицій, які фізіологічних процесах у дорослих. Не дивлячись містять сполуки, ефективні для блокування перена це, як було виявлено, систематичне введення ходу ракових клітин у їх проліферативну фазу. Ці інгібітора активності кінази FGF - R малої молета інші об'єкти та переваги даного винаходу, що кулярної маси блокує індукований bFGF ангіогестануть очевидними із детального опису, навенез у миші, не викликаючи явної токсичності. [Диденого нижче, створюються шляхом використанвись Mohammad et al., EMBO Journal, 17, 5996ня регулювальних агентів даного винаходу, опи5904 (1998)]. ТЕК (також відомий як Тіе-2) є інсаних нижче. За поставленими задачами згідно із шим рецептором тирозин-кінази, виявленим тільцим винаходом створюється сполука формули І: ки у ендотеліальних клітинах, які, як було показано, приймають участь у ангіогенезі. Зв'язування (I) фактора ангіопоіетину-1 викликає аутофосфориляцію домена ТЕК-кіназ та в результаті цього процес сигнальної трансдукції, що, як виявилося, Де: опосередковує взаємодію ендотеліальних клітин із періендотеліальними підтримуючими клітинами, цим полегшуючи утворення нових кров'яних 29 75880 30 R1 є заміщеним або незаміщеним алкілом, (а) агент регулювання клітинного циклу, вибарилом, гетероарилом, карбоциклічною або гетераний із: роциклічною групою або (і) сполуки формули І або II, (іі) фармацевтично прийнятної солі сполуки формули І або II; або (ііі) проліку або фармацевтично активного метаболіту сполуки формули І Де R4 є воднем або нижчим алкілом та X є або II, або фармацевтично прийнятної солі заміщеним або незаміщеним алкілом, арилом, проліку або метаболіту; та гетероарилом, карбоциклічною або гетероцикліч(б) фармацевтично прийнятний носій. ною групою; та Крім того, даний винахід спрямовано на R2 є заміщеним або незаміщеним алкілом, створення способів отримання сполук формули І арилом, гетероарилом, карбоциклічною або гетета II. роциклічною групою або Далі цим винаходом забезпечено створення способу використання сполуки як агенту регулювання клітинного циклу для лікування захворювання або порушення, опосередкованого інгібуванням кінази, за яким призначають пацієнту у Де R4 є воднем або нижчим алкілом та X є разі необхідності сполуку формули І або II, пролізаміщеним або незаміщеним арилом, гетероарики або фармацевтично активний метаболіт сполом, карбоциклічною або гетероциклічною грулуки формули І або II або фармацевтично прийнпою; або ятну сіль метаболіту або проліку. Подальшим фармацевтично прийнятна сіль сполуки об’єктом винаходу є спосіб лікування микозної формули І; або проліки або інфекції, злоякісностей або раку а також інші хвофармацевтично активний метаболіт споробливі стани, пов'язані із небажаними ангіогенелуки формули І; або зом та/або клітинною проліферацією, за яким фармацевтично прийнятна сіль проліку пацієнту у разі необхідності призначають ефектиабо метаболіту. вні кількості сполуки формули І або II або фармаЗа цими задачами також створюється сполуцевтично прийнятної солі сполуки формули І або ка формули II: II; або проліку або фармацевтично активного метаболіту сполуки формули І або II; або фармацевтично прийнятної солі проліку або метаболіту. За цим винаходом також створюється спосіб (II) модулювання та/або інгібування активності кінази, за яким пацієнту у разі необхідності призначають сполуку формули І або II або фармацевтиR`1 є заміщеним або незаміщеним алкілом, чно прийнятну сіль сполуки формули І або II; або арилом, гетероарилом, карбоциклічною або гетепроліки або фармацевтично активний метаболіт сполуки формули І або II; або фармацевтично роциклічною групою прийнятну сіль проліків або метаболіту. Подальшим об'єктом цього винаходу є отримання фармацевтичної композиції, яка містить де R4 у кожній реалізації незалежно є воднем сполуку формули І або II або фармацевтично або нижчим алкілом та X є заміщеним або незаприйнятну сіль сполуки формули І або II; або міщеним алкілом, арилом, гетероарилом, карбопроліки або фармацевтично активний метаболіт циклічною або гетероциклічною групою, та сполуки формули І або II; або фармацевтично R`2 є заміщеною або незаміщеною аміногруприйнятну сіль проліку або метаболіту, а також пою, нітрогрупою, алкенілом, алкілом, арилом, терапевтичне використання композиції для лікугетероарилом, вання захворювань, опосередкованих активністю карбоциклічною або гетероциклічнок кіназ, таких як рак, а також інших хворобливих станів, пов'язаних із небажаними ангіогенезом групою тa/або клітинною проліферацією, таких як діабетична ангіопатія сітківки, неоваскулярна глаукоде R4 у кожній реалізації незалежно є воднем ма, ревматоїдний артрит та псоріаз. або нижчим алкілом та X є заміщеним або незаДля таких об'єктів цього винаходу як фармаміщеним арилом, гетероарилом, карбоциклічною цевтична композиція та спосіб у формулі І та II R1 або гетероциклічною групою, або може бути також воднем. фармацевтично прийнятна сіль сполуки фоАгенти цього винаходу та композиції, що їх рмули II; або проліки або містять, можуть використовуватись у лікування фармацевтично активний метаболіт сполуки різних порушень або хворобливих станів, пов'яформули II; або заних із нерегульованою або небажаною клітинфармацевтично прийнятна сіль проліку або ною проліферацією, таких як рак, аутоімунні пометаболіту. рушення, вірусні та грибкові захворювання, Згідно із цим винаходом фармацевтична нейродегенеративні захворювання та серцевосукомпозиція містить: динні захворювання. Таким чином, винахід також спрямовано на створення способів лікування та 31 75880 32 ких захворювань шляхом введення пацієнту ефективної кількості агенту даного винаходу. Інші аспекти, переваги та відзнаки цього винаходу стануть очевидними із детального опису, поданого нижче. Сполуки та композиції даного винаходу є коДе групи R3 є такими як визначено вище. Крім рисними як антипроліферативні агенти та як інгітого, два R3 разом із суміжним азотом можуть бітори комплексів кіназ у ссавців, комплексів кіназ утворювати гетероарильне або гетероциклічне комах або грибкових кіназ. Наприклад, можуть кільце. бути інгібовані VEGF, СНК-1 та/або CDK. Такі Переважно R2 та R`2 є заміщеним або незасполуки та композиції також є корисними для реміщеним фенілом або гулювання проліферації, диференціації та/або апоптозу. Переважними прикладами R1, R2, R`1 та R`2 в сполуках формул І та II показані нижче: Де R4 є воднем або нижчим алкілом, а X є заміщеною або незаміщеною групою, вибраною із алкілу, арилу, гетероарилу, карбоциклу або гетероциклу. Інші переважні групи R2 та R`2 є заміщеними або незаміщеними гетероарилами, такими як Інші переважні групи R2 та R`2 є Переважно R1 та R`1 є: Де Υ є СН або N або CR3, X є такими, як визначено вище та R3 є Η або одним або більше замісником, розміщеним на кільці, таким як заміщений або незаміщений алкіл, алкеніл, арил, гетероарил, карбоцикл, гетероцикл, гідроксигрупа, галоген, алкоксигрупа, арилоксигрупа, гетероарилоксигрупа, тіоарил, тіоацил, тіогетероарил або аміно; або Де два Υ можуть бути однаковими або різними. В цих варіантах, де R1 або R`1 є може бути один або більше замісників на фенільному кільці. Більш переважно R1 та R`1 заміщені або незаміщені Де R3 є таким, як визначено вище. Особливо переважні замісники фенілу в R2 включають фтор, хлор, гідроксильну або алкоксильну групу, таку як метоксигрупа. Приклади переважних R груп, груп X або Υ надані нижче в ілюстративних сполуках. Υ є переважно азотом X є переважно арилом, гетероарилом, карбоциклом або гетероциклом та найбільш переважно фенілом. R2 та R`2 можуть також бути аміногрупою (NR`R``), де R` тa R`` незалежно є такими, як визначено для R3 вище, та разом із суміжним азотом можуть утворювати кільце. R4 переважно є воднем або може бути нижчим алкілом, який має 1-6 атомів вуглецю та який може бути заміщеним або незаміщеним. Два R4 можуть бути однаковими або різними. Інші переважні групи R1, R2, R`1 та R`2 можна побачити в ілюстративних сполуках, поданих нижче. Можна використовувати будь-яку бажану алкільну груп, наприклад, R1 або R2, R`1 або R`2, R3 або X. Алкільна група може бути групою прямого або розгалуженого ланцюга алкілу, яка має від одного до дванадцяти атомів вуглецю. Ілюстративні групи алкілу містять метил, етил (Et), нпропіл, ізопропіл, бутил, ізобутил, втор-бутил, трет-бутил, пентил, ізопентил, трет-пентил, гексил, ізогексил та подібні. Алкіл може бути заміщеним або незаміщеним. Переважні заміщені алкіли включають фторметил, дифторметил, трифторметил, 2-фторметил, 3-фторпропіл, гід 33 75880 34 роксиметил, 2-гідроксиетил, 3-гідроксипропіл та Такі частки можна також при необхідності заподібні. містити конденсованою кільцевою структурою Будь-які бажані арил, гетегоарил, карбоцикабо містком, наприклад, ОСН2-О. лічна або гетероциклічна група може бути викоЦі замісники можна при необхідності далі заристана, наприклад, як R1 або R2 або R`1 або R`2 містити замісником із інших груп. або R3 або X. Групи можуть бути конденсовані Переважні сполуки показані в прикладах ниабо не конденсовані, моноциклічні або поліцикліжче а також: чні. Переважні арильні та гетероарильні групи включають моноциклічні та поліциклічні ненасичені або ароматичні кільцеві структури, причому "арил" стосується структур, що є карбоциклами, а "гетероарил" стосується структур, що є гетероциклами. Приклади ароматичних кільцевих структур Крім того, даний винахід стосується проміжвключають феніл, нафтил, 1,2,3,4них сполук, корисних при отриманні сполук фортетрагідронафтил, фурил, тієніл, піроліл, піридил, мули І або II. Особливо переважні проміжні спопіридиніл, піразоліл, імідазоліл, піразиніл, піридалуки мають структуру зиніл, 1,2,3-триазиніл, 1,2,4-оксадіазоліл, 1,3,4оксадіазоліл, 1-Η-тетразол-5-іл, індоліл, хінолініл, бензотіофеніл (тіанафтеніл), фураніл, тіофеніл, імідазоліл, оксазоліл, ізоксазоліл, тіазоліл, триазоліл, тетразоліл, ізохінолініл, акридиніл, піриміІнша проміжна сполука має структуру диніл, бензімідазоліл, бензофураніл та подібні. Переважні карбоциклічні групи включають такі групи, які мають від трьох до дванадцяти атомів вуглецю, включаючи біциклічні та трициклічні циклоалкільні структури. Переважні карбоциклічні групи включають циклопропіл, циклобутил, цикІнша проміжна сполука має структуру лопентил, циклогексил, циклогептил та подібні. Переважні гетероциклічні групи включають групи, що мають 4 або 5 атомів вуглецю у кільці, та принаймні один гетероатом, вибраний з азоту, кисню або сірки, та є насиченими. Переважні гетероциклічні групи включають піролідиніл, піперідиніл, тіазиніл та морфолініл. R1, R2, Υ, X та інші групи R можуть бути незаміщені або заміщені Замість SEM, показаних вище у проміжних будь-яким бажаним замісником або замісниками, сполуках, можна використовувати інші відомі заякі не мають зворотного ефекту на бажану активхисні групи, такі як бензилоксікарбоніл (CBZ), ність сполуки. Приклади переважних замісників трет-бутокси карбоніл (ВОС), тетрагідропіраніл можна знайти у складі ілюстративних сполук, що (ТНР) та флуорен-9-метилоксикарбоніл (FMOC). надані нижче, наприклад, галоген (хлоро, йодо, Інші переважні проміжні сполуки включають бромо або фторо), С1-6алкіл, С1-6алкеніл, С1гідроксил, С1-6алкоксил; аміногрупа, 6алкиніл, нітрогрупа, тіол, тіоефір, імін, ціаногрупа, амідогрупа, фосфонатогрупа, фосфін, карбоксил, тіокарбоніл, сульфаніл, сульфонамід, кетон, альдегід, естер, кисень (=O), галоалкіл (наприклад, трифторметил), карбоциклічний циклоалкіл, який може бути моноциклічним або конденсованим або неконденсованим поліциклічним (наприклад, піролідиніл, піперазиніл, морфолініл або тіазиніл), карбоциклічний або гетероциклічний, моноциклічний або конденсований або неконденсований поліциклічний арил (наприклад, феніл, нафтил, піроліл, індоліл, фураніл, тіофеніл, імідазоліл, оксазоліл, ізоксазоліл, тіазоліл, тріазоліл, тетразоліл, піразоліл, піридиніл, хінолініл, ізохінолініл, акридиніл, піразиніл, пирідазиніл, піримідиніл, бензімідазоліл, бензотіофеніл або бензоАбревіатури "SEM" та "РМВ" стосуються фураніл), аміногрупа (первинні, вторинні або (триметилсілил) етоксиметилу та ртретинні), нітрогрупа, тіол, тіоефір, О-нижчий алметоксибензилу відповідно. Переважна проміжна кіл, О-арил, арил, арил-нижчий алкіл, СО2СН3, сполука має структуру: CONH2, OCH2CONH2, NH2, SO2NH2, OCHF2, CF3, Де PG є захисною групою, Τ є реактивною OCF3, та подібні. групою, такою як заміщений або незаміщений бор, галоген, група ΝΟ2 або ΝΗ2, а Τ` є реактив 35 75880 36 ною групою, такою як СНО, СО2Н, CO2R3, більш переважно принаймні 97,5 % (95% е.н. або CONR3R3, де R3 групи були визначені вище. д.е.) та більш переважно принаймні 99% (98% Фармацевтичні композиції згідно з даним вие.н. або д.е.). Крім того, формулами охоплюються находом альтернативно або додатково із сполусольвати, а також нерозчинні форми ідентифікокою формули І або II можуть містити як активний ваних структур. Наприклад, формули І або II місінгредієнт фармацевтично прийнятну сіль сполутять сполуки вказаної структури як в гідратній, так ки формули І або II або проліки або фармацевтиі не в гідратній формах. Інші приклади сольватів чно активний метаболіт такої сполуки або солі включають структури в комбінації із ізопропаноабо сіль проліків або метаболіту. Такі сполуки, лом, етанолом, метанолом, DMSO, етилацетасолі, проліки та метаболіти іноді означають загатом, оцтовою кислотою або етаноламіном. льно названі в цьому описі " агенти регулювання "Фармацевтично прийнятна сіль" означає клітинного циклу". сіль, що зберігає біологічну ефективність вільних Термін "проліки" означає метаболічний попекислот та основ визначеної сполуки та не може редник сполуки формули І або II (або їх солей), бути біологічно або інакше небажаною. Сполука який є фармацевтично прийнятним. Проліки моцього винаходу може мати практично кислотну, жуть бути неактивними, при їх введенні пацієнту, практично основну або обидві функціональні груале перетворюються in vivo в активну сполуку пи та відповідно реагувати з будь-якою з ряду формули І або II. Термін "активний метаболіт" або неорганічних, або органічних основ, або неозначає метаболічний продукт сполуки формули І органічних та органічних кислот для утворення або II, який є фармацевтично прийнятним та фармацевтично прийнятної солі. Ілюстративні ефективним. Проліки та активні метаболіти можфармацевтично прийнятні солі включають солі, на визначити за відомими методиками в цій галуотримані шляхом проведення реакції сполук цьозі. Проліки та активні метаболіти сполуки можна го винаходу із мінеральною або органічною кисідентифікувати за звичайними методиками, відолотою або неорганічною основою, наприклад, мими з рівня техніки. Дивись, [наприклад, солі, що включають сульфати, піросульфати, Bertolini, G et al., J. Med. Chem., 40, 2011-2016 бісульфати, сульфіти, бісульфіти, фосфати, мо(1997); Shan, D. et al., J. Pharm. Set, 86 (7), 765ногідрогенфосфати, дигідрогенфосфати, мета767; Bagshawe K., Drug Dev. Res., 34, 220-230 фосфати, пірофосфати, хлориди, бромиди, йо(1995); Bodor, N., Advances in Drug Res., 13, 224диди, ацетати, пропіонати, деканоати, каприлати, 331 (1984); Bundgaard, Design of Prodrugs акрилати, формати, ізобутирати, капроати, геп(Elsevier Press 1985); та Larsen, Design and таноати, пропіолати, оксалати, малонати, суксіApplication of Prodrugs, Drug Design and нати, суберати, себакати, фумарати, малеати, Development (Krogsgaard-Larsen et al., Harwood бутин-1,4-діоати, гексин-1,6-діоати, бензоати, Academic Publishers, 1991]. хлоробензоати, метилбензоати, динітробензоати, Слід розуміти, що сполука формули І або II гідроксибензоати, метоксибензоати, фталати, може виражати явище таутомерності, та структусульфонати, ксиленсульфонати, фенілацетати, ри формули в межах цього опису показують тільфенілпропіонати, фенілбутирати, цитрати, лактаки одну із можливих таутомерних форм. Отже ти, -гідроксибутирати, гліколяти, тартрати, меслід розуміти, що в межах цього винаходу фортан-сульфонати, пропансульфонати, нафталенмули включені будь-які таутомерні форм, які мо1-сульфонати, нафтален-2-сульфонати та мандулюють та/або інгібують активність кінази та які делати. Якщо сполука, що заявляється, є осноне обмежуються будь-якою однією таутомерною вою, то бажану фармацевтично прийнятну сіль формою, використаною в межах структур форможна отримати за будь-яким відповідним існуюмули. чим способом, наприклад, обробкою вільної осДеякі сполуки цього винаходу можуть існуванови неорганічною кислотою, такою як хлористоти як одиничні стереоізомери (тобто практично воднева, бромистоводнева, сірчана, азотна, вільні від інших стереоізомерів), рацемати та/або фосфорна та подібні, або органічною кислотою, суміші енантіомерів та/або діастереомери. Всі такою як оцтова, малеїнова, бурштинова, мигдатакі одиничні стереоізомери, рацемати та їх сулева, фумарова, малонова, піровиноградна, щаміші входять в обсяг даного винаходу. Переважвлева, гліколева, саліцилова, піраносидильною но оптично активні сполуки, що заявляються, кислотою, такою як, глюциронова або галактуронадаються в оптично чистій формі. нова кислота, альфагідрозиновою кислотою, таЯк буде зрозуміло для фахівця в цій галузі, кою як лимонна або винна, амінокислотою, такою оптично чиста сполука, що має один хіральний як аспарагінова або глутамінова, ароматочною центр (тобто один асиметричний атом вуглецю), кислотою, такою як бензойна або корична, сульмістить, по суті, один з двох можливих енантіофоновою кислотою, такою як пмерів (тобто є енантімерно чистим), а оптично толуолсульфонова або етансульфонова кислота чиста сполука, що містить більше одного хіральта подібні. ного центру, є як діастереомерно, так і енантіоЯкщо сполука, що заявляється, є кислотою, мерно чистою. Переважно сполуки цього винахото бажану фармацевтично прийнятну сіль можна ду використовуються у формі, яка принаймні на отримати будь-яким відповідним способом, на90 відсотків є енантіомерно чистою, тобто форма, приклад, шляхом обробки вільної кислоти органіщо містить принаймні 90 відсотків одиничного чною або неорганічною основою, наприклад, аміізомеру (80% енантіомерного надлишку ("е.н.") ном (первинним, вторинним або третинним), або діастереомерного надлишку ("д.н."), більш гідроксидом лужних або лужноземельних металів переважно принаймні 95% (90% е.н. або д.е.), ще та подібним. Ілюстративні приклади відповідних 37 75880 38 солей включають органічні солі, похідні від амінорювання (включаючи без обмежень хронічну та кислот, такі як гліцин та аргінін, аміак, первинні, апластичну анемії), дегенеративні захворювання вторинні та третинні аміни та циклічні аміни, такі скелетно-м'язової системи (включаючи без обяк піперідин, морфолін та піперазин та органічні межень остеропороз та артрит), риносинусит, з солі, похідні від натрію, кальцію, калію, магнію, реакцією на аспірин, кістозний фіброз, розсіяний марганцю, заліза, міді, цинку, алюмінію та літію. склероз, ниркові захворювання та болі при раках. У випадку агентів у вигляді твердих речовин Активні агенти цього винаходу можна також для фахівців зрозуміло, що сполуки цього виназастосовувати при інгібуванні розвитку інвазивходу та їх солі можуть існувати у різних кристаліних раків, ангіогенезу пухлин та метастаз. Більше чних або поліморфних формах, які входять в обтого, активні інгредієнти за цим винаходом, насяг винаходу та визначених формул. приклад, як CDK інгібітори, можуть модулювати Агенти регулювання клітинного циклу згідно рівень клітинного синтезу РНК та ДНК та отже є із цим винаходом є корисними як фармацевтичні корисними при лікуванні вірусних інфекцій, таких агенти для лікування проліферативних порушень як ВІЧ, вірус папіломи у людей, герпес вірус, віу ссавців, зокрема людей, із характерними небарус Епстайна-Барра, аденовірус, вірус Синдбіс, жаними проліфераціями ендогенних тканин. Спопоксвірус та подібні. луки формули І або II можна використовувати Сполуки та композиції за цим винаходом інгідля пацієнтів, що мають порушення, пов'язані із бують активність кіназ, наприклад, комплекси надмірною клітинною проліферацією, наприклад, CDK/цикліну, такі, що є активними в фазах G0 або раки, псоріаз, імунологічні порушення, включаючи G1 клітинного циклу, наприклад, комплекси CDK2, небажану проліферацію лейкоцитів, та рестеноз CDK4 та/або CDK6. та інші порушення гладкої мускулатури. Крім того, Специфічні дози агенту для регулювання клітакі сполуки можна використовувати для припитинного циклу, призначені для отримання теранення дедиференціації постмітотичних тканин певтичного або інгібіторного ефекту, можна вита/або клітин. Захворювання або порушення, позначити згідно із звичайно прийнятими в'язані із нерегульованою або ненормальною методиками та визначеними умовами стосовно клітинною проліферацією, включають, але без конкретного випадку, включаючи, наприклад, обмежень, наступні: призначений специфічний агент, спосіб введенРізні види раків, включаючи, але без обменя, умов лікування, особистого стану пацієнта. жень, карціному, гематопоіетичні пухлини лімфоНаприклад, денна доза агенту для регулювання вузлів, гематопоіетичні пухлини мієлоїдного поклітинного циклу, який може бути призначений в ходження, пухлини мезенхимного походження, разовій або багаторазових дозах, може містити пухлини центральної та периферійної нервової приблизно від 0,01мг/кг до 50мг/кг ваги тіла. системи та інші пухлини, включаючи меланому, Агенти для регулювання клітинного циклу за семіному та саркому Капоші та подібні. цим винаходом можна вводити за будь-яким відХворобливий процес, для якого характерна повідним способом, наприклад, орально, ректаненормальна клітинна проліферація, наприклад, льно, трансдермально, підшкірно, внутрішньодоброякісна гіперплазія простати, спадкоємний венно, внутрішньом’язовo або інтраносально. аденоматозний поліпоз, нейрофіброматоз, атеАгенти для регулювання клітинного циклу переросклероз, легеневий фіброз, артрит, псоріаз, важно вводять у склад композицій до їх введення гломерулонефрит, рестеноз з наступною хірургіпацієнту відповідно із призначенням. чною операцією ангіопластики або судин, утвоФармацевтичні композиції або препарати згірення гіпертрофічних шрамів, запальні кишкові дно із цим винаходом містять ефективну кількість захворювання, відторгнення трансплантованих агенту для регулювання клітинного циклу, при органів, ендотоксичний шок та грибкові інфекції. необхідності один або більше активних агентів, та Симптоми дефектів, пов'язаних із апоптозом, фармацевтично прийнятний носій, такий як розтакі як раки (включаючи без обмежень згадані ріджувач або наповнювач для агенту; якщо носій вище види), вірусні інфекції (включаючи без обслужить розріджувачем, він може бути твердою межень герпесвірус, поксвірус, вірус Епстайнаречовиною, напівтвердою речовиною або рідиБарра, вірус Сінбіс та аденовірус), припинення ною, які діють як транспортний засіб, наповнювач розвитку СНІДу у ВІЧ-інфікованих пацієнтів, аутоабо середовище для активного (них) інгредієнту імунні захворювання (включаючи без обмежень (тів). Композиції згідно із винаходом можуть бути хронічну червону волчанку, ревматоїдний артрит, отримані шляхом змішування активного (них) псоріаз, гломерулонефрит на засаді автоімунного інгредієнту (тів) із носієм, або розрідження його із порушення, запальне кишечне захворювання, носієм або капсулювання його в носій, та можуть аутоімунний цукровий діабет), нейродегенератибути у формі капсул, маленьких пакетиків, папевні захворювання (включаючи без обмежень хворових коробок тощо. Приклади інгредієнтів, які робу Альцгеймера, аміотрофний латеральний комбінують із одним або більше агентом для ресклероз, пігментоз сітківки, захворювання Паркінгулювання клітинного циклу та із будь-якими інсона, слабоумство на засаді СНІДу, спинальна шими активними інгредієнтами, включають Авіатрофія мускулатури та мозжечкова дегенерацель (мікрокристалічну целюлозу), крохмаль, ція), мієлодиспластичні синдроми, апластична лактозу, дигідрат сульфату кальцію, білу трубчаанемія, ішемічна травма на засаді інфарктів міосту глину, цукрозу, тальк, желатин, агар, пектин, карду, ударів та реперфузійних травм, аритмія, гуміарабік, стеарат магнію, стеаринову кислоту, атеросклероз, захворювання печінки, викликані горіхове масло, оливкове масло, моностеарат токсинами або алкоголем, гематологічні захвогліцерилу, Tween 80 (полісорбат 80), 1,3 39 75880 40 бутандіол, масло какао, бджолиний віск, поліетинаходом можна виготовити у формі водних розленгліколь, пропіленгліколь, моностеарат сорбіту, чинів, переважно у фізіологічно сумісних буфеполісорбат 60, 2-октилдодесанол, бензильний рах, таких як розчин Хенкса, розчин Ринжера або спирт, гліцин, сорбінову кислоту, сорбат калію, фізіологічний розчин. Для трансмукозального дікальцієвий гідрофосфат, хлорид натрію та вовведення проникливі агенти відповідають допусду. тимим нормам, що використовуються у рецептуКомпозиції можна отримати в різних формах рі. Такі проникливі агенти взагалі відомі в цій газгідно із бажаним призначенням. Наприклад, фалузі. рмацевтичні композиції можна виготовити у форДля орального введення сполуки можна мі таблеток, пілюль, порошків, драже, капсул, включити у композицію шляхом комбінування еліксирів, суспензій, емульсій, розчинів, сиропів, активних сполук з фармацевтично прийнятними аерозолів (як твердий препарат або у рідкому носіями, відомими в цій галузі. Такі носії дають середовищі), мастила (наприклад, яке містить можливість виготовити композиції із сполуками агенту для регулювання клітинного циклу до 10% даного винаходу у вигляді таблеток, пілюль, дравід ваги тіла), твердо- або м'якожелатинових капже, капсул, рідин, гелів, сиропів, гідросумішей, сул, супозиторіїв стерильних ін'єкційних розчинів, суспензій та ін. для орального сприйняття пацієнстерильно упакованих порошків та ін. том, який лікується. Фармацевтичні композиції Аналогічно носій або розріджувач можуть для орального призначення можна отримати, включати відомі речовини з витримкою або вивівикористовуючи твердий наповнювач у суміші з льненням у часі, такі як гліцерильний моностеаактивним інгредієнтом (агентом), при необхідносрат або гліцерильний дістеарат у чистому вигляді ті розтираючи результуючу суміш у порошок та або змішані із воском, етилцелюлозу, гідроксипобробляючи суміш гранул після додавання відпоропілметилцелюлозу, метилметакрилат та ін. відних добавок за бажанням для отримання табМожна застосовувати різні фармацевтичні форлеток або ядер драже. Відповідні наповнювачі ми. Таким чином, якщо використовується твердий включають: цукри, що містять лактозу, манітол носій, препарат можна виготовляти у вигляді або сорбіт; кукурудзяний крохмаль, пшеничний таблеток, поміщати у желатинові капсули у формі крохмаль, рисовий крохмаль, картопляний крохпорошку або таблетки. Кількість твердого носія маль, желатин, смолу, метилцелюлозу, гідроксиможна змінювати, але взагалі в межах від прибпропілметилцелюлозу, карбоксиметилцелюлозу лизно 25мг до 1г. При використанні рідкого носія натрію або полівінілпіролідон (ПВП). При бажанні препарат буде у формі сиропу, емульсії, м'яких можна додавати дезінтегрувальні агенти, такі як желатинових капсул, стерильних інжекційних рополівінілпіролідон із перехресними зв'язками, зчинів або суспензій в ампулах або флаконах або агар, або алгінову кислоту або її сіль, наприклад, неводних рідких суспензіях. алгінат натрію. Для отримання стійкої водорозчинної дозоНа ядра драже наносять відповідне покриття. ваної форми фармацевтично прийнятну сіль агеДля цього застосовують концентровані цукрові нта за цим винаходом розчиняли у водному розрозчини, які можуть при необхідності містити гучині органічної або неорганічної кислоти, такій як моарабік, полівінілпіролідон, гель Карбополь, 0,3Μ розчин бурштинової або лимонної кислоти. поліетиленгліколь та/або тітановий діоксид, розЯкщо розчинної сольової форми не існує, агент чини глазурі та відповідні органічні розчинники може бути розчинений у відповідному сорозчинабо їх суміші. До таблеток або драже можна донику або суміші сорозчинників. Приклади відповідавати барвники або пігменти для ідентифікації дних сорозчинників включають, але не обмежуабо розрізняння різних комбінацій активних агенють, спирт, пропіленгліколь, поліетиленгліколь тів. 300, полісосорбат 80, гліцерин, та подібні у конФармацевтичні препарати, які можна застоцентраціях в діапазоні від 0 до 60% від загальносовувати орально, включають капсули для прого об'єму. У проілюстрованому варіанті сполуку ковтування, вироблені із желатину, а також м'які формули І або II розчиняють у ДМСО та розрігерметичні капсули, виготовлені із желатину та джували водою. Композиція може бути також у пластифікатору, такого як гліцерол або сорбіт. формі розчину солі активного інгредієнта у відпоКапсули для проковтування можуть містити активідному водному носію, такому як вода або ізотовні інгредієнти в суміші з наповнювачами, такими нічний сольовий розчин або розчин декстрози. як лактоза, зв'язувальними агентами, такими як Композиції за цим винаходом можна виготовкрохмалі, та/ або із мастилами, такими як тальк ляти за загально відомими способами отримання або стеарат магнію, та при необхідності стабілікомпозицій, наприклад, використовуючи такі призатори. В м'яких капсулах активні агенти можуть йняті технології, як змішування, розчинення, грабути розчинені або суспендовані у відповідних нулювання, виготовлення драже, виготовлення рідинах, таких як жирні олії, зріджений парафін порошків, емульсій, капсулювання, уловлювання або рідкі поліетиленгліколі. Крім того, можна доабо ліофілізування. Фармацевтичні композиції давати стабілізатори. Всі рецептури для оральноможна скласти за звичайним способом, викорисго ведення повинні бути у дозах, відповідних для товуючи фізіологічно прийнятні носії, які можна такого призначення. Для введення в ротову попідібрати із наповнювачів та добавок, які полегрожнину композиції можуть приймати форму табшують переробку активних сполук у препарати, леток або пілюль, виготовлених за звичайними принадні для фармацевтичного застосування. рецептурами. Принадна рецептура залежить від вибраного Для призначення в ніс або шляхом інгаляцій способу введення. Для ін'єкцій агенти за цим висполуки для використання згідно з цим винахо 41 75880 42 дом зручно поступають у формі аерозолю з конклад, сполуки можна скласти у композицію з відтейнерів під тиском або балонів з використанням повідним полімерним або гідрофобним матеріапереносного агенту, наприклад, дихлордифторлом (наприклад, як емульсію у прийнятному масметану, трихлорфторметану, дихлортетрафторелі) або іонообмінними полімерами, або як мало тану, діоксиду вуглецю або іншого відповідного розчинні похідні, наприклад, як малорозчинна газу. У випадку стиснутого аерозолю доза може сіль. бути визначена вмонтованим клапаном для поФармацевтичний носій для гідрофобних сподачі дозованої кількості. Капсули та картриджі лук є сорозчинною системою, що містить бензижелатину для використання у інгаляторі або вдульний спирт, неполярний сурфактант, водозмівному апараті та подібних можна отримати з пошувальний органічний полімер та водну фазу. рошкової суміші сполуки та відповідного порошку Сорозчинна система може бути VPD. VPD - це основи, наприклад, лактози або крохмалю. розчин 3 об'ємно-масових відсотка бензильного Сполуки можна приготувати для парентераспирту, 8об./мас. відсотка неполярного поверхльного введення шляхом ін'єкцій, наприклад, бонево-активного полісорбату 80 та 65об./мас. відлюсним або безперервним влиттям. Рецептури сотка поліетиленгліколя 300, доведеного до ін'єкцій можуть бути надані в одиничній дозі, наоб’єму у абсолютному етанолі. Сорозчинна сисприклад, в ампулах або багаторазових упаковках тема VPD (VPD:5W) містить VPD, розчинений 1:1 з додатковим консервантом. Композиції можуть із 5% декстрозою у водному розчині. Сорозчинна мати такі форми як суспензії, розчини або емульсистема VPD добре розчинює гідрофобні сполуки сії в олії або водних носіях та можуть містити фота сама майже не має токсичності при системармулюючі агенти, наприклад, суспензійні, стабілітичному введенні. Звичайно пропорції сорозчинзатори та/або диспергувальні агенти. ної системи можна міняти в широкому діапазоні, Фармацевтичні рецептури для парентеральне порушуючи її властивостей розчинності та ного введення включають водні розчини активних токсичності. Крім того, ідентичність сорозчинних сполук у водорозчинній формі. Крім того, суспенкомпонентів можна змінювати: наприклад, інші зії активних агентів можна отримати як відповідні низько токсичні неполярні сурфактанти можна масляні інжекційні суспензії. Відповідні ліпофільні використовувати замість полісорбату 80; розмір розчинники або носії включають жирні масла, такі фракції поліетиленгліколю можна змінювати; пояк масло сезаму, або синтетичні естери жирних ліетиленгліколь можна замінювати іншими біосукислот, такі як етилалеати або тригліцериди або місними полімерами, наприклад, полівініловим ліпосоми. Водні ін'єкційні розчини можуть містити пиролідоном; та декстрозу можна замінювати речовини, які збільшують в'язкість суспензії, такі іншими цукрами або полісахаридами. як карбоксиметильна натрієва целюлоза, сорбіт Альтернативно можна застосовувати інші сиабо декстран. При необхідності в суспензії можна стеми постачання для гідрофобних фармацевтитакож ввести відповідні стабілізатори або агенти, чних сполук. Як приклади постачальних носіїв які збільшують розчинність сполук для можливосабо переносних засобів для гідрофобних ліків ті отримання високо концентрованих розчинів. відомо ліпосоми та емульсії. Можна застосовуваДля введення в око активний інгредієнт вводять у ти визначені органічні розчинники, такі як диметакий фармацевтично прийнятний офтальмологітилсульфоксид, хоча вони мають підвищену токчний носій, щоб сполука зберігалася у контакті з сичність. Крім того, сполуки можна вводити, очною поверхнею протягом досить значного часу використовуючи системи підтримання виділення, для можливості проникнення сполуки в рогівкову такі як напівпроникні матриці твердих гідрофобта внутрішню оболонку ока, включаючи, наприних полімерів, що містять терапевтичні агенти. клад, передню камеру ока, задню камеру ока, Були визначені принадними різні відомі в даній склоподібне тіло, водянисту вільготу ока, рогівку, галузі матеріали, що підтримують виділення. Карадужну оболонку, тіло вій, хрусталик ока, судинпсули поступового виділення в залежності від їх ну оболонку /сітчатку та селеру. Фармацевтично хімічного походження можуть виділяти сполуки прийнятний офтальмологічний носій може бути у протягом від декількох тижнів до більше, ніж 100 вигляді мазі, овочевої олії або матеріалу для капднів. В залежності від їх хімічного походження та сул. Сполука цього винаходу може бути також біостійкості терапевтичних реагентів можна завидавлена безпосередньо в склоподібне тіло ока стосовувати додаткові заходи для стійкості прота водянисту вільготу ока. теїнів. Фармацевтичні композиції також можуть Альтернативно активний інгредієнт може бумістити носії або наповнювачі твердої або гелети у вигляді порошку для змішування перед викової фази. Приклади таких носіїв або наповнюваристанням із відповідним носієм, наприклад, із чів включають карбонат кальцію, фосфат кальстерильною водою, вільною від пірогену. Сполуки цію, цукри, крохмалі, похідні целюлози, желатин можна також приготувати у вигляді ректальних та полімери, такі як поліетиленгліколь. Деякі спокомпозицій, таких як свічки або стримувальна луки цього винаходу можна отримати у вигляді клізма, наприклад, що містить звичайну свічкову солей з фармацевтично прийнятними протиіонаоснову, таку як масло какао або гліцериди. ми. Фармацевтично прийнятні солі можна утвоКрім складів, описаних вище, сполуки можна рювати з багатьма кислотами, включаючи хлориотримати як препарат пролонгованої дії. Такі довстоводневу, сірчану, оцтову, молочну, винну, годіючі композиції можна вводити шляхом імяблучну, бурштинову та інші кислоти. Солі мають плантації (наприклад, підшкірно, внутрішньом'ятенденцію розчинюватись краще у водних та інзово або внутрішньо очно) або шляхом ших апротонних розчинниках, ніж існувати у відвнутрішньом'язових ін'єкцій. Таким чином, наприповідних формах вільних основ. 43 75880 44 Фармацевтична композиція згідно з цим витором, наприклад, Pd(PPh3)4, для прискорення находом містить агент регулювання клітинного вибіркової реакції в позиції С-3. Потім шляхом циклу та, при необхідності один або більше інших реакції із другою алкільною або арильною борактивних інгредієнтів, таких як відомий антипроною кислотою або естером та відповідним палаліферативний агент, який узгоджується із агентом дієвим каталізатором отримується бажана 3,5регулювання клітинного циклу та є принадним дизаміщена проміжна сполука Е, яка потім звільдля лікування даної симптоматики. нюється від захисту для отримання кінцевої споСполуки можна використовувати як антиангілуки F. Умови звільнення від захисту узгоджуогенні агенти та агенти для модулювання та/або ються із визначеною захисною групою, для якої інгібування активності протеїн-кіназ, таким чином були застосовані, наприклад, кислотні умови для забезпечуючи лікування раку або інших захворюзняття ТГП захисної групи. R1 та R2 є такими, як вань, пов'язаних із клітинною проліферацією, визначено вище, та можуть бути R`1, R`2. опосередкованою протеїн-кіназами. ТерапевтичВаріант Схеми 1 но ефективні кількості агентів за цим винаходом можна використовувати для лікування захворювань, опосередкованих модуляцією або регулюванням протеїн-кіназ. "Ефективна кількість" означає кількість агента, яка при введенні її ссавцям в разі необхідності, є достатньою для ефективного лікування захворювання, опосередкованого актиВище показаний альтернативний варіант вністю однієї або більше протеїн-кінази. Таким схеми синтезу 1 включає обробку проміжної спочином, наприклад, терапевтично ефективною луки С, де X є СІ, частками алкільного дітину, кількістю сполуки формули І, її солі, активного наприклад, гексаметильний дітин, у супроводі метаболіту або проліку є кількість, достатня для відповідного паладієвого каталізатора для отримодуляції, регулювання або інгібіції активності мання проміжної сполуки G. За реакцією проміжоднієї або більше кіназ таким чином, щоб посланої сполуки G із алкільним або арильним галідом бити або частково зняти хворобливий стан, опота відповідним паладієвим каталізатором отрисередкований цією активністю. мали бажану проміжну сполуку D, яка далі перет"Лікування" означає принаймні послаблення ворюється, як вказано вище. хворобливого стану у ссавця, наприклад, людиСХЕМА 2 ни, яка знаходиться, принаймні частково, під дією активності однієї або більше протеїн-кіназ та включає: запобігання виникнення хворобливого стану у ссавців, зокрема, коли відомо, що ссавець схильний до хворобливого стану, але його наявність не була продіагностована; модуляцію та/або інгібіцію хворобливого стану; та/або послаблення хворобливого стану. Агенти, що заявляються, можна отримати, використовуючи схеми реакцій та схеми синтезу, описані нижче, застосовуючи відомі методики з використанням вихідних речовин, які існують. Ілюстративні загальні схеми 1-6, показані нижче, можна використати для отримання сполук за цим винаходом СХЕМА 1 Галогеновану проміжну сполуку А можна отримати за стандартною діатозацією 5аміноіндазолу та обробкою отриманої солі діазонію відповідною сіллю галіду, наприклад, CuCl або KI. Потім для отримання 3-галоіндазолу В подальша галогенізація досягається обробкою відповідною основою, такою як гідроксид натрію або калію та елементарним галогеном, наприклад, йодом. Проміжна сполука В захищається за допомогою будь-якою із відповідних захисних груп та обробляється (переважно стоіхометрично) алкільною або арильною борною кислотою або естером та відповідним паладієвим каталіза Альтернативно, як показано на схемі 2 вище, 5-нітро індазол можна галогенізувати, як показано вище для проміжної А при отриманні нітросполуки Н, шляхом обробки відповідною основою, такою як гідроксид натрію або калію та елементарним галоген, наприклад, йод, для отримання проміжної сполуки І після проведення стандартного захисту відповідної захисною групою. Обробка проміжної сполуки І видами алкільного дітину, наприклад, гексаметильним дітином, у супроводі відповідного паладієвого каталізатора для отримання проміжної сполуки J. Далі проведенням реакції нітросполуки J із алкільною або арильною борною кислотою або естером та відповідним паладієвим каталізатором отримали 3-заміщений індазол K. Відновленням K відповідним відновлювальним агентом, таким як водень, у супроводі паладієвого каталізатора або SnCl2 отримується амін. Діазотизацією отриманого 5-аміно індазолу та обробкою отриманої солі діазонію відповідною 45 75880 46 сіллю галіду, наприклад, CuCl або KI, отримали ним окислювальним агентом, таким як сірка, для проміжну галосполуку L. Проведенням реакції L із отримання бензімідазолу С``. Перетворення споалкільною або арильною борною кислотою або луки С`` у відповідний борний естер D`` супровоестером та відповідним паладієвим каталізатоджується реакцією із відповідної сполукою дибором отримали проміжну сполуку М, яку звільнили ру, наприклад, дипінаколатодибор або інше від захисту, як вказано вище, для отримання кінелектрофільне джерело бору, та паладієвим кацевої сполуки F. R1 та R2 є такими, як визначено талізатором. Проміжна сполука D`` далі реагує із вище, та можуть бути R`1, R`2. галогенованим арильним або алкільним галідом у СХЕМА 3 супроводі паладієвого каталізатора для отримання 5-заміщеної проміжної індазольної сполуки Е``, яка після відповідного звільнення від захисту приведе до отримання кінцевої сполуки Н``. Альтернативно проводять реакцію вихідної сполуки D` із відповідним видом дибору, таким як біс(пінаколато)дибор або інше електрофільне джерело бору, та відповідним паладієвим каталізатором для отримання борного естеру F``. Перетворенням сполуки F`` у проміжну сполуку D`` виконується, як описано вище для проміжної На схемі 3, показаній вище, 3сполуки D`. карбоксиіндазол активується для отримання ациІнше альтернативне перетворення можна вильованої сполуки, такої як карбонілдиімідазол, конати проведенням реакції проміжного альдегіду яка потім обробляється відповідним алкоксиF`` із заміщеним арильним або алкільним галідом алкільним аміном, таким як Ν,Νдля забезпечення R2 паладієвим каталізатором диметилгідроксиламін, для отримання аміду А`. для отримання G``, яка далі реагує із заміщеним Вибірковою галогенізацією проміжної сполуки А` діаміном В`` та відповідним окислювальним агенелементарним галогеном, таким як бром або йод, том, таким як сірка для отримання бензімідазолу та переважно каталізатором, таким як Е``. Звільненням від захисту, аналогічно описабіс(трифторацетокси)йодозобензол або ному вище, отримали кінцеву сполуку H``. R1 та біс(ацетокси)йодозобензол отримали 5-галоR2 є такими, як визначено вище, та можуть бути індазол В`. Шляхом захисту проміжної В` при R`2, R3 є таким, як визначено вище. стандартних умовах відповідною захисною груЗа іншим способом отримання проміжної пою, такою як ПМБ або ТГП, отримали захисний сполуки Ε`` можна виконати реакцію сполуки, амід С`. Відновленням С` відповідним відновлютакої як С`` безпосередньо із відповідною алкільвальним агентом, таким як гідрид алюмолітію або ною борною кислотою або естером в умовах відподібним гідридним відновлювальним агентом, повідного паладієвого каталізу. отримали проміжний альдегід D`. R3 є таким як Додаткові види електрофільного бору, які описано вище, та є переважно заміщеним або можна використовувати, мають наступну струкнезаміщеним алкілом, переважно нижчим алкітуру: лом. СХЕМА 4 , де R3 є таким як визначено вище, а дві R3 групи можуть утворювати кільце Специфічні приклади включають: Схема 5 В схемі 4, показаній вище, проміжна сполука D` реагує із заміщеним діаміном В`` та відповід В схемі 5 вище спиртова проміжна сполука Х1 може бути активована, наприклад, проведенням реакції із сульфоновим галідом, таким як метансульфоновий хлорид, та відповідною основою, такою як заміщений амін для отримання проміжної сполуки Х2, яка потім звільнюється від захисту у відповідних умовах. R2 є таким, як визначено вище, та може бути R`2. R3 є таким, як визначено вище. СХЕМА 6 47 В схемі 6, показаній вище, структура ядра індазолу формується при утворенні структури 2гало-5-нітрофеніл-арильного кетону Y1 із гідразином для отримання необхідного 3-арил-5нітроіндазолу Y2. Наступним захистом та відновленням отримали амін Y4. Як описано в схемі 2, диазотизацією, обробкою солі діазонію за допомогою KІ та потім з'єднанням йодної проміжної сполуки із арильною борною кислотою отримали захищену 3,5-бісариліндазольну проміжну сполуку Y6. Потім стандартним звільненням від захисту отримали кінцеві продукти. R1 та R2 є такими, як визначено вище, та можуть бути R`1 та R`2. Отримання певних переважних сполук цього винаходу описано детально в наступних прикладах. Фахівцю в цій галузі стане очевидним, що описані хімічні реакції можна легко прилаштували для отримання ряду інших інгібіторів кіназ за цим винаходом. Наприклад, синтез непоказаних сполук згідно із цим винаходом можна успішно виконати в різних модифікаціях, очевидних для фахівця, наприклад, використовуючи інші відповідні реагенти, відомі з рівня техніки, або змінюючи звичайними способами умови реакцій. Альтернативно інші реакції, надані в цьому описі або відомі із рівня техніки можна визнати застосовними для отримання інших сполук цього винаходу. В прикладах, описаних нижче, якщо іншого не обумовлено, всі значення температур подані в градусах за Цельсієм та всі долі та проценти - за масою. Реагенти були поставлені від комерційних постачальників, таких як Aldrich Chemical Company або Lancaster Synthesis Ltd, та були використані без подальшого очищення, якщо іншого не вказано. Тетрагідрофуран (ТГФ) та Ν,Νдиметилформамід (ДМФ) придбали від Aldrich у якісно герметизованих пляшках та використовували в отриманому вигляді. Всі розчинники очищали, використовуючи стандартні методики, відомі фахівцям, якщо іншого не обумовлено. Реакції, подані нижче, проводили під позитивним тиском аргону або азоту або в осушувальній трубці при температурі оточуючого середовища (якщо іншого не обумовлено) у безводних розчинниках, а реакційні колби були оснащені каучуковою перегородкою для введення підкладок та реагентів шприцом. Скляний посуд був осушений у сушильній шафі та/або нагрівальному пристрої. Аналітична тонкошарова хроматографія (ТШХ) була виконана на 60 F 254 тарілках Analtech із силікагелем та скляною підкладкою (0,25мм) та 75880 48 елюйована з відповідними співвідношеннями розчинників (о/о), і позначена, де відповідність дотримується. Реакції були досліджені за допомогою ТШХ та припинені по мірі витрат вихідних матеріалів. Візуалізація верхніх тарілок була зроблена панізальдегідним розпилювальним реагентом або реагентом фосфомолібденової кислоти (Aldrich Chemical 20% за масою в етанолі) та активована нагріванням. Обробка була типово виконана шляхом подвоєння об'єму реакції з реакційним або екстрагувальним розчинником та потім промивкою вказаним водним розчином з використанням 25% за об'ємом відносно об'єму екстракції, якщо іншого не обумовлено. Кінцеві розчини були осушені крізь безводний розчин Na2SO4 до фільтрації та випарювання розчинників під зниженим тиском на обертальному випарювачі та відмічені як розчинники, вилучені під вакуумом. Флеш колоночну хроматографію [Still et. al., J.Org. Chem., 43, 2923 (1978)] виконували чистим тонким шаром силікагелю Бейкерра (47-61 м) та силікагелем: співвідношення сировини 20:1 до 50:1, якщо іншого не обумовлено. Гідрогеноліз було виконано під тиском, вказаним в прикладах, або під атмосферним тиском. 1 H-ЯМР спектри були зареєстровані на інструменті Брукера при частоті 300МГц та 13СЯМР спектри були зареєстровані на інструменті Брукера при частоті 75МГц. ЯМР спектри були отримані як розчини CDCI3 (результати занотовані у частинах на мільйон) з використанням хлороформу як контрольну речовину (7,25 частин на мільйон та 77,00 частин на мільйон) або CD3OD (3,4 та 4,8 частин на мільйон та 49,3 частин на мільйон), або внутрішньо тетраметилсілан (0,00 частин на мільйон) при відповідності. Інші ЯМР розчинники були використані при необхідності. При реєстрації максимальних мультиплетних рівнів використовують наступні абревіатури: s (синглет), d (дуплет), t (триплет), m (мультиплет), br (поширений), dd (дуплет дуплетів), dt (дуплет триплетів). Зв’язувальні константи, при їх наявності, подані в герцах (Hz). Інфрачервоні спектри (IR) записані на спектрометрі Perkin-Elmer FT-IR як кісткове масло, пігулки KВr або розчини CDCL3, та при наявності реєструються у хвильових числах (см-1). Масові спектри були отримані з використанням LSIMS або електропульверізацією. Всі точки плавлення (ТП) не коригуються. Вихідні матеріали, використані в прикладах, комерційно існують та/або можуть бути отримані за відомими технологіями. Приклад 1: 5-феніл-3-стирил-1H-індазол 49 (а) Проміжна сполука 1а - 5-хлоро-3-йодо-1Ніндазол: 5-Аміно-1Н-індазол (15,41г, 116ммоль) суспензували у суміші води (250мл), льоду (250мл) та концентрованої соляної кислоти (100мл). Суміш охолоджували в крижаній соляній ванні до внутрішньої температури -5°С. До цієї суміші додавали нітрит натрію (8,78г, 127ммоль) у воді (75мл), охолодженій до 0°С Результуючий розчин діазонію перемішували протягом 15 хвилин при 5°С. Розчин хлориду міді (І) (14,9г, 151ммоль) у концентрованій соляній кислоті (150мл) охолоджували до 0°С та потім по краплях додавали до розчину діазонію, утворюючи при цьому оранжевий осад. Охолоджувальну ванну знімали та дозволили реакційній суміші нагрітись до кімнатної температури. Виділення газу починається при внутрішній температурі 10°С. Після перемішування при кімнатній температурі протягом 1,5 годин виділення газу припиналося. Потім колбу нагрівали до 60°С протягом 30 хвилин, потім нагрівали до -15°С. При цьому утворювався коричневий осад. Його збирали відсосною фільтрацією та осушували у вакуумному ексикаторі крізь NaOH протягом 16 годин для отримання 5-хлоро1Н-індазол (25,6г) у вигляді жовтуватокоричневого порошку. Цю необроблену проміжну сполуку розчиняли у 1,4-діоксані (400мл). До розчину додавали 3Μ водний NaOH (400мл) та йодні флокени (35,3г, 139ммоль). Після перемішування при кімнатній температурі протягом 2 годин реакційну суміш нейтралізували до рН=6 20% водним розчином лимонної кислоти, викликаючи зміну темного забарвлення на світло зелений. До розчину додавали насичений водний розчин тіосульфату натрію (~400мл), викликаючи зміну зеленого забарвлення на жовтий, та розчин екстрагували етил ацетатом (3 1000мл). Комбіновані органічні екстракти осушували крізь сульфат натрію, збирали відсосною фільтрацією крізь грубу фриту та концентрували до зеленого осаду, який потім розчиняли у етилацетаті (500мл), відфільтрованому крізь шар целіту, концентрували до утворення твердої речовини зеленого кольору. Очищенням хроматографією крізь силікагель (25% етилацетат/гексани) отримали 5-хлоро-3-йодо1Н-індазол 1а (14,18г, 44% із 5-аміно-1Ніндазолу) у вигляді білуватої твердої речовини. ТП=198-199°С; Rf=0,53 (59% етилацетат/гексани); 1 Н ЯМР (DMSO-d6): δ 7,44 (m, 2Η), 7,60 (d, 1Η, J=8,7 Hz), 13,68 (s, 1H). Анал. (C7H4CIIN2) С, Η, Ν. (b) Проміжна сполука 1b - 5-хлоро-3-йодо-1[2-(триметилсиланіл)-етоксиметил]-1Н-індазол: 75880 50 5-хлоро-3-йодо-1Н-індазол 1а (8,86г, 31,8ммоль) розчиняли у ТГФ (100мл) та охолоджували у крижаній соляній ванні до 0°С. Потім додавали твердий т-бутоксид натрію (3,67г, 38,2ммоль) та суміш перемішували при 0°С протягом 1 години. Потім додавали 2(триметилсиліл)етоксиметильний хлорид (7,96г, 38,2ммоль) та продовжували перемішування при 0°С протягом ще 1 години. Розчин розріджували етилацетатом (200мл), промивали водою (100мл) та розсолом (100мл). Органічний шар осушували сульфатом магнію, відфільтровували та концентрували. Очищенням хроматографією крізь силікагель (5-20% етилацетат/гексани) отримали 1b (9,75г, 75%) у вигляді жовтого масла: Rf=0,39 (5% етилацетат/гексани); 1Н ЯМР (CDCl3): δ - 0,06 (s, 9Η), 0,87 (t, 2Η, J=8,1 Hz), 3,55 (t, 2Η, J=8,1 Hz), 5,70 (s, 2H), 7,43 (dd, 1H, J=8,9, 1,7 Hz), 7,49 (m, 2H). Анал. (C13H18CllN2OSi) C, H, N. (c) Проміжна сполука 1c - 5-хлоро-3-стирил-1[2-(триметилсиланіл)-етоксиметил]-1Н-індазол: 5-хлоро-3-йодо-2-8ЕМ-індазол lb (553мг, 1,35ммоль), стирилборну кислоту (300мг, 2,03ммоль) та тетракіс (трифенілфосфін) паладій (78,2мг, 0,068ммоль) розчиняли у толуолі (10мл) та метанолі (1,4мл). Потім додавали насичений водний розчин бікарбонату натрію (1,7мл) та суміш нагрівали у 90 С масляній ванні протягом 3 годин. При цьому спостерігається легке кипіння. Після охолодження до кімнатної температури розчин розчиняли водою (15мл) та екстрагували етилацетатом (4 50мл). Комбіновані органічні екстракти осушували сульфатом магнію, фільтрували та концентрували. Очищенням хроматографією крізь силікагель (толуол) отримали чисту речовину 1с (350,7мг, 67%) у вигляді жовтого масла: Rf=0,20 (толуол); 1Н ЯМР (CDCL3): δ - 0,09 (s, 9Η), 0,86 (t, 2Η, J=8,1 Hz), 3,55 (t, 2Η, J=8,3 Hz), 5,65 (s, 2H), 7,2-7,4 (m, 7H), 7,54 (d, 2H, J=7,6 Hz), 7,93 (d, 1H, J=1,6 Hz). 13C ЯМР (CDC13): δ 1,5, 17,7, 66,5, 77,9, 111,0, 119,2, 120,3, 123,6, 126,5, 127,3, 127,4, 128,0, 128,7, 131,6, 136,9, 139,4, 142,5. Анал. (C21H25CIN2OSi 0,02 CHCI3) С, Η, Ν, СІ. (d) Проміжна сполука 1d - 5-феніл-3-стирил1-[2-(триметилсиланіл)-етоксиметил]-1Н-індазол: До розчину 5-хлоро-3-стирил-2-8ЕМ-індазолу 1с (209,4мг, 0,544ммоль) у сухому 1,4-діоксані (0,5мл) додали феніл борну кислоту (69,6мг, 0,571ммоль), карбонат цезію (213мг, 0,653ммоль) та тріс(дибензилідинацетон)дипаладій (10,0мг, 0,0108ммоль). Потім додали розчин фосфін тритрет-бутилу у 1,4-діоксані (0,1М, 0,217мл) та сумішнагрівали до 80°С протягом 6 годин. Після охолодження до кімнатної температури розчин розрідили етильним естером (20мл) та фільтрували крізь шар целіту для вилучення чорного осаду паладію. Фільтрат осушували сульфатом магнію, фільтрували, концентрували та очищали хроматографією крізь силікагель (толуол) для отримання 1d (77,2мг, 33%) у вигляді безбарвного масла: Rf=0,09 (толуол); 1H ЯМР (CDCl3) δ 0,04 (s, 9Н), 0,93 (t, 2Н, J=8,1 Hz), 3,62 (t, 2H, J=8,1 Hz), 5,76 (s, 2H, J), 7,3-7,7 (m, 14H), (m, 14H), 8,17 (s, 1H). Анал. (C23H30N2OSi 0,2 H2O) С, Н, N. 51 75880 52 (e) Приклад 1 - 5-феніл-3-стирил-1Н-індазол: Rf=0,39 (30% етилацетат/гексани); 1H ЯМР Проміжну сполуку 1d (68,1мг, 0,16ммоль) ро(DMSO-d6) δ 7,41 (d, 1H, J=8,7 Hz), 7,66 (dd, 1H, зчиняли у чистому етанолі (2,0мл) та 3Μ НСl J=8,7, 1,5 Hz), 7,77 (d, 1H, J=0,9 Hz) 13,65 (s, 1H). (2,0мл). Розчин нагрівали до кипіння із зворотним (c) Проміжна сполука 2с - 3,5-Дийодо-1-[2холодильником протягом 20 годин, охолоджували (триметилсиланіл)-етоксиметил]-1Н-індазол: до кімнатної температури та екстрагували етилаЗа способом синтезу, подібним способу синтезу проміжної сполуки 1b, обробкою 3,5цетатом (3 30мл). Комбіновані органічні екстракдийодоіндазолу 2b т-бутоксидом натрію та хлоти осушували сульфатом магнію, відфільтровуридом 2-(триметилсілил)етоксиметилу отримали вали, концентрували, очищали хроматографією 2с (64%) у вигляді жовтого масла: Rf=0,53 (30% крізь силікагель (25-50% етилацетат/гексани) та етилацетат/гексани); 1H ЯМР (CDCL3) δ - 0,05 (s, отримали вказану сполуку (19,2мг, 40%) у вигляді 9Н), 0,86 (t, 2Н, J=8,1 Hz), 3,54 (t, 1H, J=8,1 Hz), білої твердої речовини: Rf=0,14 (25% етилаце5,69 (s, 2H), 7,34 (d, 1H, J=8,7 Hz), 7,69 (dd, 1H, тат/гексани); 1H ЯМР (CDCL3) δ 6,92 (d, 1Н, J=6,3 J=8,7, 1,5 Hz), 7,87 (d, 1H, J=1,5 Hz). Hz), 7,3-7,7 (m, 13H), 8,20 (s, 1H), 10,3 (br s, 1H). (d) Проміжна сполука 2d - 3,5-Дистирил-1-[2HRMS обчислено для C21H17N2 297,1392 (MH+), (триметилсиланіл)-етоксиметил]-1H-індазол: знайдено 297,1398. Анал. (C21H16N2 0,7 H2O) С, Н, Стирилборну кислоту (186мг, 1,26ммоль) доN. дали до розчину 2с (210,0мг, 0,42ммоль) та тетПриклад 2: 3,5-дистирил-1H-індазол: ракіс (трифенілфосфін) паладію (48,5мг, 0,042ммоль) у толуолі (3,5мл) та метанолі (0,5мл). Потім додавали насичений водний розчин бікарбонату натрію (1,05мл) та суміш нагрівали у 90°С масляній ванні (легке кипіння) протягом 4 годин. Після охолодження до кімнатної температури розчин заливали у воду (15мл) та екстрагували етилацетатом (4 50мл). Комбіновані органічні екстракти осушували сульфатом магнію, фільтрували, концентрували та очищали хроматографією крізь силікагель (толуол) отримали 2d (170,9мг, 90%) у вигляді жовтого масла: Rf=0,10 (толуол); 1Н ЯМР (CDCL3) δ 0,01 (s, 9H), 0,98 (t, 2Н, J=8,5 Hz), 3,67 (t, 2H, J=8,5 Hz), 5,73 (s, 2H), 7,17 (d, 1H, J=16 Hz), 7,3-7,7 (m, 15H), (а) Проміжна сполука 2а - 5-йодо-1-1Н8,05 (s, 1H), 13C ЯМР (CDCL3) δ - 1,5, 17,6, 66,4, індазол: 77,7, 110,1, 119,4, 119,8, 123,3, 125,1, 126,3, 5-йодо-1Н-індазол (10,21г, 76,7ммоль) су126,5, 127,8, 128,6, 128,7, 128,9, 131,3, 137,1, спендували у суміші води (100мл), льоду (100мл) 137,3, 140,6, 143,3. Анал. (C29H32N2OSi 0,1 та концентрованої соляної кислоти (35мл). Суміш CHCL3) C, H,N. охолоджували в крижаній соляній ванні до внут(e) Приклад 2 - 3,5-дистирил-1H-індазол: рішньої температури -5°С. До цієї суміші додаваОбробкою 2d за допомогою 3М НСl аналогічли нітрит натрію (5,82г, 84,4ммоль) у воді (30мл), но прикладу 1 отримали приклад 2 3,5-дистирилохолодженій до 0°С Результуючий розчин діазо1Н-індазол (33%) у вигляді яскраво жовтої твернію перемішували протягом 10 хвилин при -5°С, дої речовини: Rf=0,11 (25% етилацетат/гексани); потім повільно по краплях додавали розчин йо1 НЯМР (CDCl3): δ 7,2-7,7 (m, 16Η), 8,076 (s, 1Η), диду калію (15,3г, 92ммоль) у воді (50мл). При 10,05 (br s, 1Η). HRMS обчислено для C23H19N2 додаванні перших крапель розчину KІ починаєть323,1548 (МН+), знайдено 323,1552. Анал. ся значне спінювання, а потім утворюється чорна (C23H18N2 0,5 Н2О) С, Η, Ν. смола. Після закінчення додавання суміш нагріПриклад 3: 3-(1H-бензоімідазол-2-іл)-5-фенілвали до 90°С протягом години. Смолянистий 1Н-індазол: осад розчиняли та при нагріванні виділяється перламутровий пар. Потім реакцію охолоджували до кімнатної температури і при цьому утворюється дрібнозернистий коричневий осад. Цей осад збирали відсосною фільтрацією та осушували у вакуумі для отримання 5-йодоіндазолу 2а (14,12г, 75%) у вигляді коричневого порошку: Rf=0,28 (50% етилацетат/гексани); 1Н ЯМР (DMSO-d6) δ 7,40 (d, 1H, J=9,0 Hz), 7,56 (dd, 1H, J=8,5, 1,5 Hz), 8,01 (s, 1H), 8,16 (s, 1H), 13,23 (s, 1H). Анал. (C7H5IN2) C, H, I, N. (b) Проміжна сполука 2b - 3,5-дийодо-1-1Ніндазол Проміжну сполуку 2b отримали способом синтезу аналогічно синтезу проміжної сполуки 1а. Обробкою проміжної сполуки 2а йодом та гідроксидом натрію отримали 3,5-дийодо-1-1Н-індазол 2b (84%) у вигляді жовтої твердої речовини.: 53 75880 54 (а) Проміжна сполука 3а 1-[2(c) Проміжна сполука 3с - 5-хлоро-1-[2(триметилсиланіл)-етоксиметил]-1H(триметилсиланіл)-етоксиметил]-3бензоімідазол: (триметилстаніл)-1Н-індазол: (Дивись аналогічну процедуру у Whitten et al., Суміш проміжної сполуки 1b (6,25г, J. Org. Chem. 51, 1891 (1986), на що в цьому опи15,3ммоль), гексаметилдитин (10,2г, 30,5ммоль) сі зроблено посилання): Твердий 1Нта біс(трифенілфосфін)паладій(ІІ)дибромид бензоімідазол (30г, 254ммоль) додавали по ма(242мг, 0,306ммоль) у толуолі (50мл) нагрівали лих порціях до суспензії гідриду натрію (10,2г до кипіння із зворотним холодильником протягом 60% дисперсії у мінеральному маслі, 254ммоль) у 15 хвилин, потім охолоджували, фільтрували та ДМФ (350мл) при кімнатній температурі. Суміш концентрували. Очищенням хроматографією перемішували протягом 3 годин та потім охолокрізь силікагель (5-50% етилацетат/гексани) джували до 0°С у крижаній ванні. Потім по крапотримали речовину 3с (6,34мг, 93%) у вигляді лях додавали 2-(триметилсиліл)етоксиметильний світло-жовтого масла: Rf=0,21(5% етилацехлорид (46,57г, 279ммоль) протягом 10 хвилин. тат/гексани), Rf=0,23(толуол); 1Н ЯМР (CDCl3): δ Реакційну суміш перемішували протягом 16 го0,06 (s, 9Η), 0,56 (s, із малими боковими смугами дин, нагріваючи до кімнатної температури по мірі частот 9Н), 0,87 (t, 2Н, J=8,4 Hz), 3,54 (t, 2Н, J=8,4 розтоплювання льоду, потім заливали у воду (1л) Hz), 5,75 (s, 2Н), 7,34 (dd, 1Н, J=8,7, 1,8 Hz), 7,51 та екстрагували етилацетатом. Органічний шар (d, 1H, J=8,7 Hz), 7,66 (d, 1H, J=1,8 Hz). Анал. промивали розсолом, осушували сульфатом на(C13H27CIN2OSiSn) C, H, I, N. трію, фільтрували, концентрували та очищали (d) Проміжна сполука 3d - 5-хлоро-1-[2хроматографією крізь силікагель (50-85% етила(триметилсиланіл)-етоксиметил]-3-{1-[2цетат/гексани) і отримали 3а (56,63мг, 90%) у (триметилстаніл)-етоксиметил]-1H-бензоімідазолвигляді яскраво-жовтого масла: Rf=0,40 (50% 2іл}-1H-індазол: етилацетат/гексани); 1H ЯМР (CDCL3) δ - 0,04 (s, Суміш 3с (4,47г, 10,03ммоль) 3b (4,12г, 9Н), 0,90 (t, 2Н, J=8,1 Hz), 3,50 (t, 2H, J=8,1 Hz), 11,03ммоль), тетракіс (трифенілфосфін) паладій 5,53 (s, 2H), 7,31 (m, 2H), 7,54 (m, 1H), 7,81 (m, (0) (579мг, 0,50ммоль) та йодид міді (І) (190мг, 1,00ммоль) у ТГФ (100мл) нагрівали до кипіння із 1H), 7,96 (s, 1H). Анал. (C13H20N2OSi 0,5 H20) С, Н, зворотним холодильником протягом 1 години. N. Додатково додавали каталізатор (580мг, 0,50 та (b) Проміжна сполука 3b - 2-йодо-1-[2Cul (200мг, 1,05ммоль) та продовжували кип'ятін(триметилсиланіл)-етоксиметил]-1Hня із зворотним холодильником протягом 20 гобензоімідазол: дин. Після охолодження до кімнатної температуРозчин N-SEM-бензімідазол (проміжна спори чорний осад фільтрували, фільтрат лука 3а) (19,19г, 77,25ммоль) у сухому етильному концентрували та залишок очищали хроматограефірі (150мл), охолоджений до -78°С у ванні із фією крізь силікагель (толуол) для отримання суміші сухого льоду та ацетону, додали крізь качистої 3d (2,29г, 43%) у вигляді безбарвного мастетер по краплях до розчину н-бутиллітію (46мл ла, яке кристалізується при відстоюванні ТП=802,5Μ у гексанах, 116ммоль) у сухому етильному 82°С; Rf=0,10 (10% етилацетат/гексани), Rf=0,13 ефірі (150мл), також охолодженому до -78°С у (толуол); 1НЯМР (CDCL3) δ - 0,15 (s, 9H), -0,06 (s, ванні із суміші сухого льоду та ацетону. Додаван9Н), 0,85 (t, 2Н, J=8,1 Hz), 0,91 (t, 2H, J=8,4 Hz), ня розчину бензімідазольного розчину займає 10 3,60 (t, 2H, J=8,4 Hz), 3,61 (t, 2H, J=8,1 Hz), 5,80 хвилин. Перемішування продовжували більше 15 (s, 2H), 6,24 (s, 2H), 7,36 (m, 2H), 7,47 (dd, 1H, хвилин, протягом цього періоду суміш приймає J=9,0, 2,1 Hz), 7,57(d, 1H, J=9,0 Hz), 7,62 (m, 1H), темно-червоне забарвлення. Результуючий роз7,91 (m, 1H), 8,73 (d, 1H, J=2,1 Hz). Анал. чин ариллітію по краплях додавали крізь катетер (C26H37CLN4O2Si2) С, Η, СІ, N. у розчин йодних флокенів (49г, 193ммоль) у су(e) Проміжна сполука 3е - 5-фенілхлоро-1-[2хому ефірі (500мл), охолодженому до -78°С у (триметилсиланіл)-етоксиметил]-3-{1-[2ванні із суміші сухого льоду та ацетону. Після (триметилсиланіл)-етоксиметил]-1Нзакінчення додавання (10 хвилин) охолоджувабензоімідазол-2-іл}-1Н-індазол: льну ванну знімали та реакційній суміші давали Суміш 3d (192,0мг, 0,363ммоль), фенілборної нагрітися протягом 30 хвилин до внутрішньої текислоти (66,4мг, 0,544ммоль), ацетату паладію мператури - 10°С. Потім додавали воду (250мл) (II) (3,3мг, 0,0145ммоль (СуМАР-1 [дивись аналота суміш промивали насиченим водним розчином гічну процедуру у Old et.al., J. Am.Chem. Soc, 120, бісульфату натрію (2 200мл). Органічний шар 9722 (1998)] (5,7мг, 0,0145ммоль) та фторид цеосушували сульфатом натрію, фільтрували, конзію (165мг, 1,09ммоль) у 1,4-діоксані (3,6мл) нацентрували та очищали хроматографією крізь грівали у 100°С масляній ванні протягом 1 годисилікагель для отримання 3-йодо-n-SEM-1Нни. Після охолодження до кімнатної температури бензоімідазоле 3b (22,84мг, 80%) у вигляді жовтої суміш розріджували етилацетатом (20мл) та фітвердої речовини: ТП=60-63°С Rf=0,70 (етилацельтрували для вилучення чорного осаду. Фільттат/гексани); 1H ЯМР (CDCL3) δ - 0,04 (s, 9Н), рат промивали ЇМ водним розчином гідроксиду 0,92 (t, 2Н, J=8,1 Hz), 3,58 (t, 2H, J=8,1 Hz), 5,53 натрію (20мл), осушували сульфатом натрію, (s, 2H), 7,27 (m, 2H), 7,51 (m, 1H), 7,73 (m, 1H). концентрували та очищали хроматографією крізь HRMS обчислено для C13H19IN2OSINa 397,0209 силікагель (0-4% метанолу у дихлорметані) для (MNa+), знайдено 397,0204. Анал. (C13H19IN2OSi) отримання 3е (107,0мг, 52%) у вигляді світлоС, Η, Ι, Ν. жовтого масла: Rf=0,26 (дихлорметан); 1Н ЯМР (CDCL3) δ - 0,15 (s, 9Н), -0,04 (s, 9Н), 0,86 (t, 2Н, 55 75880 56 J=8,1 Hz), 0,95 (t, 2H, J=8,1 Hz), 3,61 (t, 2H, J=8,1 J=8,1 Hz), 3,66 (t, 2H, J=8,1 Hz), 3,91 (s, 3H), 5,85 Hz), 3,66 (t, 2H, J=8,1 Hz), 5,85 (s, 2H), 6,28 (s, (s, 2H), 6,27 (s, 2H), 6,93 (ddd, 1H, J=1,1, 2,5, 8,1 2H), 7,37 (M, 3H), 7,49 (t, 2H, J=7,5 Hz), 7,63-7,80 Hz), 7,27-7,40 (m, 5H), 7,63-7,70 (m, 2Н), 7,77 (dd, (m, 5H), 7,91 (m, 1H), 8,88 (s, 1H). Анал. 1Н, J=1,5, 8,7 Hz), 7,93 (m, 1H), 8,87 (s, 1H). Анал. (C33H44N4O3Si2) С, Н, N. (C32H42N4O2Si2 0,4 H2O) C, H, N. Приклад 4 -3-[3-(1Н-бензоімідазол-2-іл)-1НПриклад 3: 3-(1H-бензоімідазол-2-іл)-5-феніліндазол-5-іл]-феніл: 1H-індазол: Розчин проміжної сполуки 4а (88,3мг, Фторид тетрабутиламонію (1,0Μ у ТГФ, 0,147ммоль) у 1,2-дихлоретані (3,0мл) обробляли 3,16мл) та 1,23-діаміноетан (95мг, 1,58ммоль) комплексом трибромиду бору-сульфіду метилу додавали до проміжної сполуки 3е (90,2мг, (1,0Μ у дихлометані, 0,588мл) та нагрівали до 0,158). Розчин нагрівали у 70°С масляній ванні кип'ятіння із зворотним холодильником протягом (легке кипіння) протягом 20 годин та продовжу1 години. Перемішування продовжували при кімвали кип’ятіння із зворотним холодильником пронатній температурі протягом 16 годин. Потім дотягом ще 24 годин. Після охолодження до кімнатдали воду (5,0мл) та перемішування продовжуної температури розчин розріджували вали ще протягом 30 хвилин при кімнатній етилацетатом (30мл) та промивали насиченим температурі. Суміш розріджували диетильним водним розчином бікарбонату натрію (20мл). Орефіром (30мл), та промивали насиченим водним ганічний шар осушували сульфатом магнію, фірозчином бікарбонату натрію (20мл). Органічний льтрували, концентрували та очищали хроматографією крізь силікагель (25-50% шар промивали 1М NaOH (3 30мл). Комбіновані етилацетат/гексани) отримали 3-(1Hводні шари окислювали соляною кислотою до бензоімідазол-2-іл)-5-феніл-1H-індазол 3 (33,9мг, рН=1 6М НСl та екстрагували поступово ефіром 69%) у вигляді білої твердої речовини: Rf=0,30 (30мл), етилацетатом (30мл) та дихлорметаном (50% етилацетат/гексани); 1H ЯМР (CDCL3) δ 7,21 (2 20мл). Ці органічні екстракти комбінували, (квінтет d, 2Н, J=5,7, 1,5 Hz), 7,39 (t, 1H, J=7,4 осушували сульфатом магнію, фільтрували, конHz), 7,53 (t, 3H, J=7,5 Hz), 7,76 (m, 5H), 8,71 (s, центрували та очищали хроматографією крізь 1H), 13,01 (s, 1H), 13,70 (s, 1H). HRMS обчислено силікагель (50-75% етилацетат/гексани) для для C20H15N4 311,1297 (MH+), знайдено 311,1283. отримання фенолу 4 (11,6мг, 24%) у вигляді білоПриклад 4: 3-[3-(1H-бензоімідазол-2-іл)-1Hго порошку: 1H ЯМР (DMSO-d6) δ 6,78 (dd, 1Н, індазол-5-іл]-фенол: J=1,9, 7,7 Hz), 7,12-7,27 (m, 4H), 7,31 (t, 1H, J=7,7 Hz), 7,52 (dd, 1H, J=2,1, 6,6 Hz), 7,71 (d, 2H, J=1,1 Hz), 7,76 (dd, 1H, J=1,5, 6,8 Hz), 8,67 (s, 1H), 9,57 (s, 1H), 13,00 (s, 1H), 13,68 (s, 1H). HRMS обчислено для C20H15N4O 327,1246 (MH+), знайдено 327,1237. Приклад 5: 3-(1H-бензоімідазол-2-іл)-5-(3метоксифеніл)-1H-індазол: (а) Проміжна сполука 4а 5-(3метоксифеніл)-1-[2-(триметилсиланіл)етоксиметил]-3-{1-[2-(триметилсиланіл)етоксиметил]-1Н-бензоімідазол-2-іл}-1H-індазол: Суміш 3d (371,5мг, 0,702ммоль), 3метоксифенілборної кислоти (160мг, 1,05ммоль), ацетату паладію (II) (7,9мг, 0,0355ммоль) СуМАР1 [дивись аналогічну процедуру у Old et.al., J. Am.Chem. Soc, 120, 9722 (1998)], на яку в цьому описі зроблено посилання, (14мг, 0,0355ммоль) та фторид цезію (320мг, 2,11ммоль) у 1,4-діоксані (7,1мл) нагрівали у 90°С масляній ванні протягом 22 години. Після охолодження до кімнатної температури суміш розріджували етилацетатом (50мл) та фільтрували для вилучення чорного осаду. Фільтрат осушували сульфатом магнію, концентрували та очищали хроматографією крізь силікагель (10% етилацетат/гексани) для отримання 4а (178,3мг, 42%) у вигляді світло-жовтого масла: Rf=0,20 (10% етилацетат/гексани); 1Н ЯМР (CDCL3) δ - 0,14 (s, 9Н), -0,03 (s, 9Н), 0,86 (t, 2Н, J=8,1 Hz), 0,95 (t, 2H, J=8,1 Hz), 3,61 (t, 2H, (а) Приклад 5: 3-(1H-бензоімідазол-2-іл)-5-(3метоксифеніл)-1Н-індазол: Ту ж саму необроблену реакційну суміш, із якої отримали сполуку прикладу 4, також використовують для отримання метоксифенільного аналогу 5 наступним чином: Розчин проміжної сполуки 4а (88,3мг, 0,147ммоль) у 1,2-дихлоретані (3,0мл) обробляли комплексом трибромиду бору-сульфіду метилу. (1,0Μ у дихлорметані, 0,588мл) та нагрівали до кип’ятіння із зворотним холодильником протягом 1 години. Перемішування продовжували при кімнатній температурі протягом 16 годин. Потім добавляли воду (5,0мл) та перемішування продовжували ще протягом 30 хвилин при кімнатній температурі. Суміш розріджували диетильним ефіром (30мл), та промивали насиченим водним розчином бікарбонату натрію (20мл). Органічний шар промивали 1М NaOH (3 30мл). Органічний шар потім осушували, фільтрували, концентрували та очищали хроматографією крізь силікагель (50-75% етилацетат/гексани) для отримання 5 (9,3мг, 19%) у вигляді білого порошку: 1H ЯМР 57 75880 (DMSO-d6) δ 3,86 (s, 3Н), 6,98 (dd, 1H, J=2,1, 7,8 Hz), 7,19-7,23 (m, 3H), 7,30 (d, 1H, J=7,8 Hz), 7,45 (t, 1H, J=7,8 Hz), 7,52 (dd, 1H, J=1,8, 5,7 Hz), 7,75 (m, 3H), 8,70 (s, 1H), 13,00 (s, 1H), 13,70 (s, 1H). HRMS обчислено для C21H16N4ONa 363,1222 + MNa ), знайдено 363,1225. Приклад 6: 3-(1H-бензоімідазол-2-іл)-5-(2фторофеніл)-1H-індазол: (a) Проміжна сполука 6а - 5-(2-фторфеніл)-1[2-(триметилсиланіл)-етоксиметил]-3-{1-[2(триметилсиланіл)-етоксиметил]-1Hбензоімідазол-2-іл}-1H-індазол: Суміш проміжної сполуки 3d (419,0мг, 0,792ммоль), 2-фторфенілборної кислоти (166мг, 1,19ммоль), ацетату паладію (II) (9,9мг, 0,04ммоль), СуМАР-1 (дивись аналогічну процедуру [у Old et.al., J. Am.Chem. Soc, 120, 9722 (1998)], на яку в цьому описі зроблено посилання) (16мг, 0,04ммоль) та фторид цезію (361мг, 2,38ммоль) у 1,4-діоксані (8,0мл) нагрівали у 70°С масляній ванні протягом 1 години. Оскільки спостерігалося тільки часткове перетворення, додавали більше ацетату паладію (II) (12мг, 0,05ммоль) та СуМАР-1(14мг, 0,035ммоль) та продовжували перемішування при температурі 70°С протягом 16 годин. Після охолодження до кімнатної температури суміш розріджували етилацетатом (50мл) та фільтрували для вилучення чорного осаду. Фільтрат осушували сульфатом натрію, концентрували та очищали хроматографією крізь силікагель (10% етилацетат/гексани) для отримання 6а (155,6мг, 43%) у вигляді безбарвного масла: 1Н ЯМР (CDCL3) δ - 0,14 (s, 9Н), -0,03 (s, 9Н), 0,86 (t, 2Н, J=8,1 Hz), 0,95 (t, 2H, J=8,1 Hz), 3,61 (t, 2H, J=8,1 Hz), 3,66 (t, 2H, J=8,1 Hz), 5,86 (s, 2H), 6,27 (s, 2H), 7,15-7,39 (m, 5H), 7,57-7,75 (m, 4H), 7,88 (m, 1H) 8,82 (s, 1H). Анал. (C32H41FN4O2Si2 0,4 H2O) С, Н, N. (b) Приклад 6: 3-(1H-бензоімідазол-2-іл)-5-(2фторофеніл)-1H-індазол: Приклад 6 отримали за способом синтезу, аналогічно прикладу 3. Обробкою проміжної сполуки 6а фторидом тетрабутиламонію отримали 6 (21,2мг, 18%) у вигляді білого порошку: Rf=0,35 (50% етилацетат/гексани); 1Н ЯМР (DMSO-d6) δ 7,20 (m, 2H), 7,33-7,52 (m, 4H), 7,62 (m, 2H), 7,74 (m, 2H), 8,65 (s, 1H), 13,02 (s, 1H), 13,75 (s, 1H). HRMS обчислено для C20H14FN4 329,1202 (MH+), знайдено 329,1212. Анал. (C20H13FH4 1,1 H2O) C, H, N. Приклад 7`: 3-(1Н-бензоімідазол-2-іл)-5-(2фторофеніл)-1Н-індазол: 58 (а) Проміжна сполука 7a` - 5-йодо-3-((Е)стирил)-1-(2-триметилсиланіл-етоксиметил)-1Ніндазол: Проміжну сполуку 7а` отримали із 5нітроіндазолу (Acros organics, A division of Fisher Scientific, Pittsburg, PA) за п'ять етапів за способом який застосовується для отримання 6-йодо3-((Е)-стирил)-1-(2-триметилсиланілетоксиметил)-1Н-індазолу із 6-нітроіндазолу (Дивись Kania, Braganza, et al., заявка на видачу [патенту США №60/142,130, дата подачі 2 липня 1999, "Сполуки та фармацевтичні композиції для інгібування протеїн-кіназ та способи їх використання" (від стор.52, рядок 10 до стор.53, рядок 26; та від стор.59, рядок 16 до стор.60, рядок 4), пріоритетна заявка США Реєстр. №60/142,130, подана 2 липня 1999], на яку в цьому винаході зроблено посилання в цілому): 1Н ЯМР (CDCL3) 5 - 0,06 (s, 9Н), 0,89 (t, 2Н, J=8,4 Hz), 3,57 (t, 2H, J=8,4 Hz), 5,70 (s, 2H), 7,29-7,44 (m, 6H), 7,59 (d, 2H, J=7,0 Hz), 7,67 (dd, 1H, J=8,7, 1,5 Hz), 8,36 (s, 1H). (b) Проміжна сполука 7b` - 5-йодо-1- (2триметилсиланіл-етоксиметил)-1Н-індазол-3карбальдегід: Озон барботують у розчин 5-йодо-3-стирил-2SЕМ-індазол 7а` (4,93г, 10,35ммоль) у дихлорметані (500мл) при -78°С. Через 20 хвилин забарвлення розчину змінюється з оранжевого на темно блакитний. Суміш очищали аргоном протягом 30 хвилин для вилучення озону, потім додавали диметилсульфід (1,29г, 20,7ммоль). Охолоджувальну ванну знімали та перемішування продовжували до досягнення температури 15°С приблизно протягом 2 годин. Розчин промивали водою (2 200мл), осушували сульфатом магнію, фільтрували та концентрували. Очищенням хроматографією крізь силікагель (10% етилацетат/гексани) отримали альдегід 7b` (2,74г, 66%) у вигляді жовтого масла: 'Н ЯМР (CDCL3) δ - 0,05 (s, 9Н), 0,89 (t, 2Н, J=8,4 Hz), 3,56 (t, 2H, J=8,4 Hz), 5,79 (s, 2H), 7,43 (d, 1H, J=8,7 Hz), 7,76 (dd, 1H, J=8,8, 1,5 Hz), 8,71 (s, 1H), 10,22 (s, 1H). (c) Проміжна сполука 7с` 3-(1Нбензоімідазол-2-іл)-5-йодо-1(2триметилсиланіл-етоксиметил)-1Н-індазол: До розчину альдегіду 7b` (2,7'4 г, 6,81ммоль) у ДМФ (130мл) додавали 1,2-фенілендіамін (0,74г, 6,81ммоль) та елементарну сірку (0,26г, 8,2ммоль). Суміш нагрівали у 95°С масляній ванні протягом 14,5 години, охолоджували до кімнатної температури та розріджували етилацетатом (500мл). Розчин промивали сумішшю насиченого 59 75880 60 водного розчину хлориду натрію (100мл) та водою (100мл). Потім органічний шар промивали насиченим водним розчином бікарбонату натрію (100мл), потім водою (100мл), осушували сульфатом магнію, фільтрували, концентрували та очищали хроматографією крізь силікагель (20% Суміш анізолу 7` (44,6мг, 0,131ммоль) та гідетилацетат/гексани) для отримання неоднорідної рохлориду піридину (912мг, 7,9ммоль) нагрівали 7с` у вигляді блідо-жовтої твердої речовини. у 180°С масляній ванні протягом 3 години. Сіль Осаджуванням із суміші хлороформу та гексанів піридину знаходиться у рідкому стані при цій теотримали чисту 7с` (2,15г, 64%) у вигляді білого мпературі. Після охолодження до кіімнатної темпорошку: Rf=0,23 (20% етилацетат/гексани); 1H ператури суміш розділяли між етилацетатом ЯМР (DMSO-d6) δ - 0,12 (s, 9H), 0,82 (t, 2H, J=7,9 (20мл) та насиченим водним розчином бікарбоHz), 3,59 (t, 2H, J=7,9 Hz), 5,87 (s, 2H), 7,23 (m, нату натрію (15мл). Потім водний шар екстрагу2H), 7,52 (d, 1H, J=7,2 Hz), 7,73-7,84 (Μ, 3Н), 8,94 вали етилацетатом ((3 20мл). Ці комбіновані ор(s, 1Н), 13,13 (s, 1H). HRMS обчислено для ганічні екстракти осушували сульфатом натрію, C20H23IN4OSI 491,0159 (MH+), знайдено 491,0738. фільтрували та концентрували. Очищенням хро(d) Проміжна сполука 7d` - 3-(1Hматографією крізь силікагель (50% етилацебензоімідазол-2-іл)-5-(4-метокси-феніл)-1-(2тат/гексани) отримали чисту фенольну сполуку 8` триметилсиланіл-етоксиметил)-1Н-індазол: (29,4мг, 69%) у вигляді світло-жовтої твердої ре2М водний розчин карбонату натрію (6,4мл) човини: Rf=0,23 (60% етилацетат/гексани); 1H додавали до розчину 7с` (2,50г, 5,10ммоль), 4ЯМР (DMSO-d6) δ 6,91 (d, 2Н, J=8,4 Hz), 7,21 (m, метоксифенільної борної кислоти (1,01г, 2H), 7,53 (m, 3H), 7,68 (s, 2H), 7,75 (d, 1H, J=6,9 6,63ммоль) та тетракіс (трифенілфосфін) паладій Hz), 8,61 (s, 1H), 9,53 (s, 1H), 12,98 (s, 1H), 13,63 (0,59г, 0,51ммоль) у 1,4-діоксані (35мл) та мета(s, 1H). HRMS обчислено для C20H14N4O 327,1246 нолі (15мл). Суміш нагрівали до кипіння із зворо(MH+), знайдено 327,1253. Анал. (C20H13N4O 0,8 тним холодильником протягом 5 години. Потім DMSO) С, Η, Ν. охолоджували та розділяли між етилацетатом Приклад 9`: -3-(1Н-бензоімідазол-2-іл)-5-(4(300мл) та сумішшю насиченого водного розчину метокси-2-метил-феніл)-1Н-індазол: хлориду натрію (100мл) та води (100мл). Потім органічний шар осушували сульфатом магнію, фільтрували, концентрували та очищали хроматографією крізь силікагель (20% етилацетат/гексани) для отримання темно-коричневої твердої речовини. Осаджуванням із суміші дихлорметану та гексанів отримали чисту 7d` (948,6мг, 40%) у вигляді білого порошку: Rf=0,13 (20% етилацетат/гексани); 1Н ЯМР (DMSO-d6) δ – 0,10 (s, 9Н), 0,85 (t, 2Н, J=7,9 Hz), 3,63 (t, 2Н, J=7,9 Hz), 3,82 (s, 3Н), 5,91 (s, 2H), 7,10 (d, 2H, J=8,7 Hz), 7,23 (m, 2H), 7,43 (m, 1H), 7,54 (d, 1H, J=6,8 Hz), 7,69 (d, 2H, J=8,7 Hz), 7,80 (m, 1H), 7,92 (d, 1H, J=8,9 Hz), 8,70 (s, 1H), 13,08 (s, 1H). (e) Приклад 7`: -3-(1Н-бензоімідазол-2-іл)-5(4-метоксифеніл)-1H-індазол: Розчин проміжної сполуки 7d` (148,4мг, 0,315ммоль) у етилацетаті (15мл) при -78°С оброблюють трибромидом бору (1,0Μ у дихлорме(a) Проміжна сполука 9а` -3-Метокси-2-метилтані, 4,73мл). Розчин перемішували протягом 17 феніламін: годин, дозволяючи суміші поступово нагрітися до Суспензію 2-метил-3-нітроанізол (Aldrich кімнатної температури. Потім додавали воду Chemicals) (8,87г, 53ммоль) та 10% паладій на (10мл) та суміш залишали для перемішування вуглеці (800мг) у етанолі (400мл) взбовтували протягом 6 днів при кімнатній температурі .Потім при тиску водню 40psi протягом 1 години. Після розчин обробляли 3Μ розчином гідроксиду нафільтрації крізь шар целіту розчин концентрували трію для доведення до рН10, потім екстрагували та очищали хроматографією крізь силікагель етилацетатом (3 20мл). Комбіновані органічні (30% етилацетат/гексани) і отримали анілінову екстракти осушували сульфатом магнію, фільтсполуку 9а` (6,94г, 95%) у вигляді світлорували та концентрували. Очищенням хроматогоранжевого масла: Rf=0,20 (25% етилацерафією крізь силікагель (50% етилацетат/гексани); 1Н ЯМР (DMSO-d6) δ 1,88 (s, 3Н), тат/гексани) отримали 7` (60,5мг, 56%) у вигляді 3,68 (s, 3Н), 4,74 (br s, 2H), 6,17 (d, 1H, J=8,1 Hz), білої твердої речовини: Rf=0,21 (50% етилаце6,26 (d, 1H, J=8,1 Hz), 6,81 (t, 1H, J=8,1 Hz). Анал. 1 тат/гексани); H ЯМР (DMSO-d6) δ 3,82 (s, 3Н), (C8H11NO) C, H, N. 7,08 (d, 2Н, J=8,9 Hz), 7,21 (m, 2H), 7,53-7,78 (m, (b) Проміжна сполука 9b` - 1-йодо-3-Метокси6H), 8,66 (s, 1H), 12,96 (s, 1H), 13,63 (s, 1H). Анал. 2-метил-бензол: (C21H16N4O 0,25 CH2CL2) С, Н, N. 3-Метокси-2-метил-феніламін (5,28г, Приклад 8`: 4-[3-(1H-бензоімідазол-2-іл)-5-(438,5ммоль) діазотизують згідно із способом метоксифеніл)-1H-індазол-5-ил]-фенол:
ДивитисяДодаткова інформація
Назва патенту англійськоюIndazole compounds as antiproliferative agents, a pharmaceutical composition (variants) and a method for treatment of diseases and disorders (variants) associated wiyh unwanted angiogenesis and/or cellular proliferation
Назва патенту російськоюИндазольные соединения как антипролиферативные агенты, фармацевтическая композиция (варианты) и способ лечения заболеваний или нарушений (варианты), связанных с нежелательным ангиогенезом и/или клеточной пролиферацией
МПК / Мітки
МПК: A61K 31/416, A61K 31/4184, C07D 401/04, A61K 31/4439, C07D 403/04, C07D 401/14, A61P 35/00, C07D 231/56
Мітки: лікування, проліферацією, порушень, захворювань, пов'язаних, небажаним, агенти, фармацевтична, антипроліферативні, індазольні, композиція, спосіб, сполуки, клітинною, варіанти, ангіогенезом
Код посилання
<a href="https://ua.patents.su/74-75880-indazolni-spoluki-yak-antiproliferativni-agenti-farmacevtichna-kompoziciya-varianti-ta-sposib-likuvannya-zakhvoryuvan-abo-porushen-varianti-povyazanikh-z-nebazhanim-angiogenezom-ta.html" target="_blank" rel="follow" title="База патентів України">Індазольні сполуки як антипроліферативні агенти, фармацевтична композиція (варіанти) та спосіб лікування захворювань або порушень (варіанти), пов’язаних з небажаним ангіогенезом та/або клітинною проліферацією</a>
Попередній патент: Композиція фульвестранту (варіанти)
Випадковий патент: Пристрій для випробовування матеріалів на фрикційну утомленість












