Кахалалідні сполуки
Номер патенту: 76949
Опубліковано: 16.10.2006
Автори: Альберісіо Фернандо, Хіменес Хосе Карлос, Хіральт Ернест, Ройо Міріам, Мансанарес Ігнасіо, Родрігес Ігнасіо, Лопес Анхель
Формула / Реферат
1. Похідне кахалаліду F, що не є сумішшю ізомерів, відомих як кахалалід F, де похідне має структуру з циклічною частиною і бічним ланцюгом, одержане з формули (І):
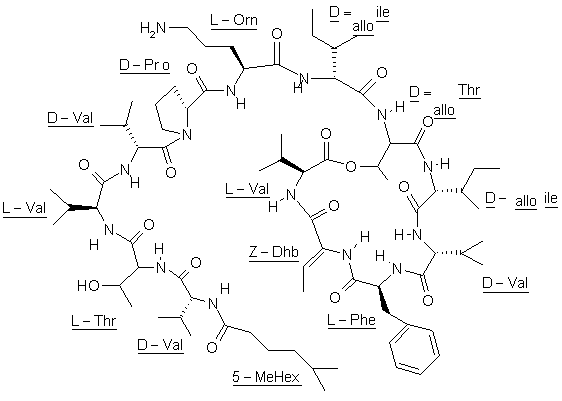
формула (І),
причому похідне відрізняється від формули (І) однією або більше з наступних ознак:
1 - 2 амінокислотами, що не є тими ж самими, що й амінокислоти в структурній формулі (І), або відсутні;
1 - 10 додатковими метиленовими групами вацильній групі бічного ланцюга структурної формули (І);
1 - 5 метиленовими групами, що відсутні в ацильній групі бічного ланцюга структурної формули (І);
1 - 3 замісниками, доданими до ацильної групи бічного ланцюга структурної формули (І);
5-метилзамісником, відсутнім в ацильній групі бічного ланцюга; і
відсутньою ацильною групою бічного ланцюга.
2. Сполука за п. 1, яка відрізняється від формули (І) однією або більше з наступних ознак:
1 амінокислотою, що не є тією ж самою, що й амінокислота в структурній формулі (І);
1 додатковою метиленовою групою в ацильній групі бічного ланцюга структурної формули (І);
1 метиленовою групою, відсутньою в ацильній групі бічного ланцюга структурної формули (І);
1 замісником, доданим до ацильної групи бічного ланцюга структурної формули (І);
5-метилзамісником, відсутнім в ацильній групі бічного ланцюга.
3. Сполука за п. 1 або 2, де 1 або 2 амінокислоти відсутні, і це - пропуск у циклічній частині.
4. Сполука за п. 1 або 2, де 1 або 2 амінокислоти відсутні, і це - пропуск у бічному ланцюзі структури.
5. Сполука за п. 1 або 2, де кожна амінокислота є такою ж, як і у формулі (І).
6. Сполука за будь-яким з пп. 1-5, де бічний ланцюг споріднений з 5-MeHex-D-Val-L-Thr-L-Val-D-Val-D-Pro-L-Orn-D-allo-ile.
7. Сполука за п. 6, де 5-МеНех заміщене кінцевим алкілом, алкенілом, алкінілом, арилом, аралкілом, гетероарилом, гетероалкілом або аліциклічною групою.
8. Сполука за п. 7, з кінцевою алкільною групою.
9. Сполука за п. 8, де кінцева алкільна група містить від 4 до 10 атомів вуглецю.
10. Сполука за п. 9, де кінцева алкільна група містить 1 або більше метильних або етильних груп, розгалужених на віддалені від точки приєднання до іншої частини молекули.
11. Сполука за пп. 8, 9 або 10, де алкільна група містить єдину розгалужену метильну групу.
12. Сполука за будь-яким з пп. 8-10, де алкільна група заміщена галогеном, гідрокси, алкокси, аміно, карбоксилом, карбоксамідо, ціано, нітро, алкілсульфонілом, алкокси, алкоксіалкільною, арилалкіларильною, гетероциклічною, аліциклічною або аралкільною групами.
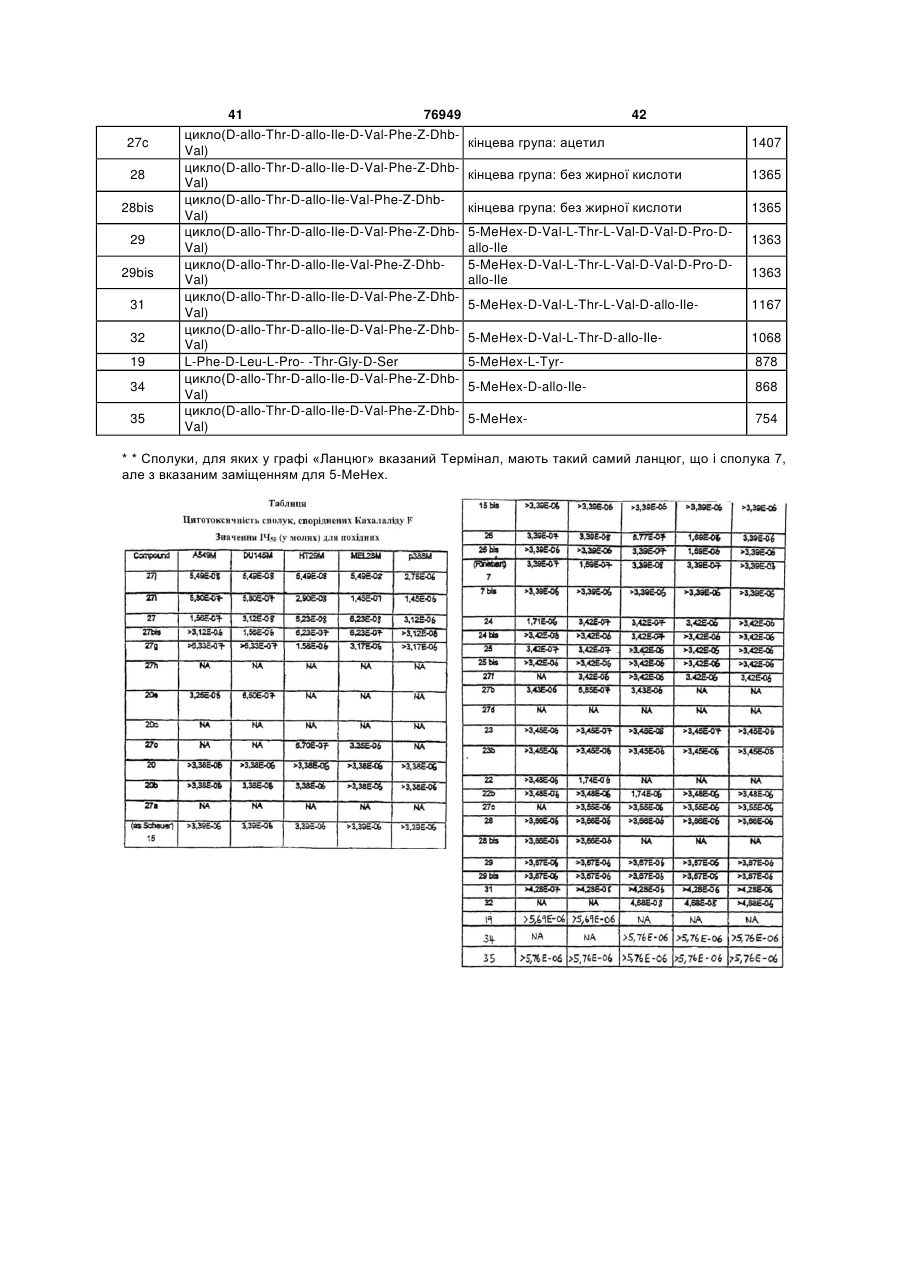
13. Сполука за п. 1, що має формулу
Циклічна частина похідного кахалаліду F
Бічний ланцюг**
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val)
кінцева група: TFA-Lit-
цикло(D-аllо-Тhr-D-аllо-Ilе-D-Val-Phe-Z-Dhb-Val)
кінцева група: літохолоїл(Lit).
цикло(D-allo-Thr-D-allo-Ile-D-Vat-Phe-Z-Dhb-Val)
кінцева група: пальмітоїл Palm
цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb-Val)
кінцева група: пальмітоїл Palm
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val)
кінцева група: 4-{4-ацетоксибутаноїлоксибутирил (AcButBut-)
цикло(D-аllо-Тhr-D-аllо-Іlе-D-Val-Phe-Z-Dhb-Val)
IBut-D-allo-Ile-D-Val-L-Thr-L-Val-D-Val-D-Pro-L-Om-D-allo-Ile-
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-D-Phe-Val)-D-Phe: a,b-дидегідрофенілаланін
5-MeHex-D-Val-L-Thr-L-Val-D-Val-D-Pro-L-Om-D-allo-Ile-
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Thr-Val)
5-MeHex-D-Val-L-Thr-L-Val-D-Val-D-Pro-L-Om-D-allo-Ile-
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val)
кінцева група: 4-ацетоксибутирил (4-AcBut)
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-L-Etg-Val)
5-MeHex-D-Val-L-Thr-L-Val-D-Val-D-Pro-L-Om-D-allo-Ile-
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-D-Etg-Val)
5-MeHex-D-Val-L-Thr-L-Val-D-Val-D-Pro-L-Om-D-allo-Ile-
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val)
кінцева група: N,N-диметил-4-амінобутирил(4-DіМеАВut)
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val)
5-MeHex-D-Val-L-Thr-D-Val-L-Val-D-Pro-L-Om-D-allo-Ile-
цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb-Val)
5-MeHex-D-Val-L-Thr-D-Val-L-Val-D-Pro-L-Om-D-allo-Ile-
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val)
кінцева група: гептаноїл (Нер)
цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb-Val)
кінцева група: гептаноїл (Нер)
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val)
5-MeHex-D-Val-L-Thr-L-Val-D-Val-D-Pro-L-Om-D-allo-Ile-
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val)
кінцева група: 3,3-диметилбутирил (3,3-DiMeBut)
цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb-Val)
кінцева група: 3,3-диметилбутирил (3,3-DiMeBut)
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val)
кінцева група: 4-метилпентаноїл (4-МеРеn)
цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb-Val)
кінцева група: 4-метилпентаноїл (4-МеРеn)
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val)
кінцева група: трифторацетил (TFA)
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val)
кінцева група: 2,4-гексадієноїл (Hedo)
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val)
кінцева група: 4-гідроксибутирил
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val)
кінцева група: 3-метилбутирил (3-MetBut)
цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb-Val)
кінцева група: 3-метилбутирил (3-MetBut)
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val)
кінцева група: бутирил (But)
цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb-Val)
кінцева група: бутирил
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val)
кінцева група: ацетил
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val)
кінцева група: без жирної кислоти
цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb-Val)
кінцева група: без жирної кислоти
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val)
5-MeHex-D-Val-L-Thr-L-Val-D-Val-D-Pro-D-allo-Ile-
цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb-Val)
H-D-Val-L-Thr-L-Val-D-Val-D-Pro-L-Orn-D-allo-Ile
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val)
H-D-Val-L-Thr-L-Val-D-Val-D-Pro-L-Orn-D-allo-Ile
цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val)
5-MeHex-D-Val-L-Thr-D-allo-Ile-
** кінцева група бічного ланцюга (далі бічний ланцюг без змін), що заміняє 5-МеНех.
14. Фармацевтична композиція, з протопухлинною активністю, яка містить сполуку за будь-яким з попередніх пунктів і фармацевтично прийнятний носій або розріджувач.
15. Спосіб одержання сполуки, що має структуру (І):
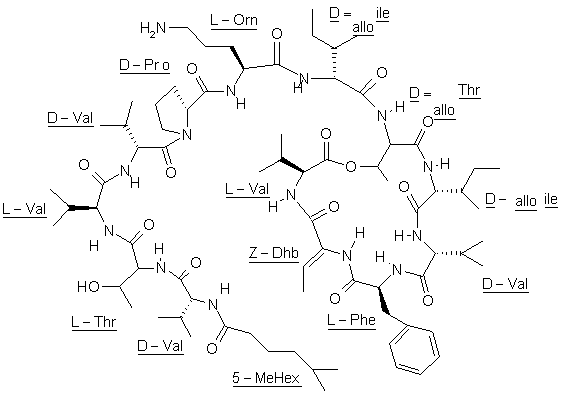 ,
,
або похідного кахалаліду F за будь-яким з пунктів 1-13, при якому проводять реакцію замикання кільця за наступною схемою:
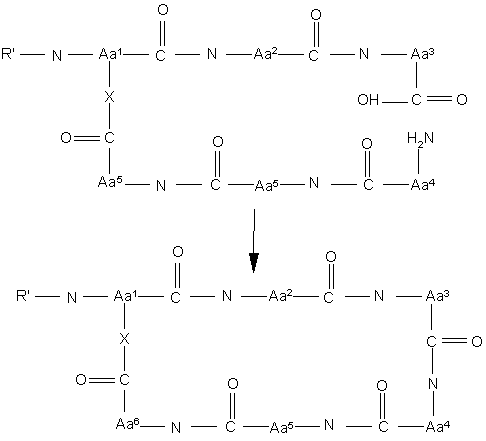 ,
,
де кожний з R', Аа1, Аа2, Аа3, Аа4, Аа5, Аа6 і Х має те ж значення, яке було зазначене для формули (І), за умови що щонайменше один з R', Аа1, Аа2, Аа3, Аа4, Аа5, Аа6 і Х може мати одну з дозволених відмінностей, R' необов'язково може бути попередником, одна або більше з амінокислот Аа1, Аа2, Аа3, Аа4, Аа5, Аа6 необов'язково можуть мати захисні групи, а -СООН у Аа3 і/або -NH2 у Аа4 можуть необов'язково бути захищені, активовані або дериватизовані.
Текст
1. Похідне кахалаліду F, що не є сумішшю ізомерів, відомих як кахалалід F, де похідне має структуру з циклічною частиною і бічним ланцюгом, одержане з формули (І): C2 2 (19) 1 3 76949 4 12. Сполука за будь-яким з пп. 8-10, де алкільна кіларильною, гетероциклічною, аліциклічною або група заміщена галогеном, гідрокси, алкокси, аміаралкільною групами. но, карбоксилом, карбоксамідо, ціано, нітро, алкіл13. Сполука за п. 1, що має формулу сульфонілом, алкокси, алкоксіалкільною, арилалЦиклічна частина похідного кахалаліду F цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) цикло(D-аllо-Тhr-D-аllо-Ilе-D-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-D-Vat-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) цикло(D-аllо-Тhr-D-аllо-Іlе-D-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-D-Phe-Val)-D-Phe: a,b-дидегідрофенілаланін цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Thr-Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-L-Etg-Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-D-Etg-Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) Бічний ланцюг** кінцева група: TFA-Litкінцева група: літохолоїл(Lit). кінцева група: пальмітоїл Palm кінцева група: пальмітоїл Palm кінцева група: 4-{4-ацетоксибутаноїлоксибутирил (AcButBut-) IBut-D-allo-Ile-D-Val-L-Thr-L-Val-D-Val-D-Pro-LOm-D-allo-Ile5-MeHex-D-Val-L-Thr-L-Val-D-Val-D-Pro-L-Om-Dallo-Ile5-MeHex-D-Val-L-Thr-L-Val-D-Val-D-Pro-L-Om-Dallo-Ileкінцева група: 4-ацетоксибутирил (4-AcBut) 5-MeHex-D-Val-L-Thr-L-Val-D-Val-D-Pro-L-Om-Dallo-Ile5-MeHex-D-Val-L-Thr-L-Val-D-Val-D-Pro-L-Om-Dallo-Ileкінцева група: N,N-диметил-4-амінобутирил(4DіМеАВut) 5-MeHex-D-Val-L-Thr-D-Val-L-Val-D-Pro-L-Om-Dallo-Ile5-MeHex-D-Val-L-Thr-D-Val-L-Val-D-Pro-L-Om-Dallo-Ileкінцева група: гептаноїл (Нер) кінцева група: гептаноїл (Нер) 5-MeHex-D-Val-L-Thr-L-Val-D-Val-D-Pro-L-Om-Dallo-Ileкінцева група: 3,3-диметилбутирил (3,3-DiMeBut) кінцева група: 3,3-диметилбутирил (3,3-DiMeBut) кінцева група: 4-метилпентаноїл (4-МеРеn) кінцева група: 4-метилпентаноїл (4-МеРеn) кінцева група: трифторацетил (TFA) кінцева група: 2,4-гексадієноїл (Hedo) кінцева група: 4-гідроксибутирил кінцева група: 3-метилбутирил (3-MetBut) кінцева група: 3-метилбутирил (3-MetBut) кінцева група: бутирил (But) кінцева група: бутирил кінцева група: ацетил кінцева група: без жирної кислоти кінцева група: без жирної кислоти 5-MeHex-D-Val-L-Thr-L-Val-D-Val-D-Pro-D-allo-IleH-D-Val-L-Thr-L-Val-D-Val-D-Pro-L-Orn-D-allo-Ile H-D-Val-L-Thr-L-Val-D-Val-D-Pro-L-Orn-D-allo-Ile 5-MeHex-D-Val-L-Thr-D-allo-Ile ** кінцева група бічного ланцюга (далі бічний ланцюг без змін), що заміняє 5-МеНех. 5 76949 14. Фармацевтична композиція, з протопухлинною активністю, яка містить сполуку за будь-яким з попередніх пунктів і фармацевтично прийнятний носій або розріджувач. 15. Спосіб одержання сполуки, що має структуру (І): L H2N D Pr o D Orn O N H Val D L N H Val H N O N H N H C C H2N C O allo O C N Aa5 N O R' D O Aa4 O N N Aa1 O Aa2 N C C N X N D Aa3 allo ile H N H O L Phe Thr Val O Aa3 O C Thr D NH H Z Dhb N D H O O HO L Val N H N OH N C X Aa5 O O Aa1 N O O H N R' O Aa2 ile O L O allo N O 6 Val O C C O O O N O O Aa6 C N 5 MeHex , або похідного кахалаліду F за будь-яким з пунктів 1-13, при якому проводять реакцію замикання кільця за наступною схемою: Даний винахід відноситься до кахалалідних сполук, конкретніше - до кахалаліду F та споріднених йому сполук, а також до способу синтезу таких сполук. Кахалалід F є біоактивним циклічним депсипептидом, виділеним з молюска Elysia rufescens (sarcoglossan) і його корму, зеленої водорості Bryopsis sp. Кахалалід F був уперше виділений Hamann та Scheuer, див. [Hamann, M.T.; Scheuer, PJ. J. Am. Chem. Soc. 1993, 115, 5825-5826]. У цій публікації не була визначена абсолютна стереохімія індивідуальних валінів (3 D-Val та 2 L-Val) та треонінів (L-Thr та D-allo-Thr). У пізнішій публікації Scheuer et al. [Goetz, G.; Yoshida, W.Y.; Scheuer, PJ. Tetrahedron 1999, 55, 7739-7746] визначили положення у молекулі для 5 Val та 2 Thr. Таким чином, структура Кахалаліду F, за Scheuer et al., виглядала таким чином: Aa5 3 N C Aa4 4 5 6 , де кожний з R', Аа , Аа , Аа , Аа , Аа , Аа і Х має те ж значення, яке було зазначене для формули (І), за умови що щонайменше один з R', Аа1, Аа2, Аа3, Аа4, Аа5, Аа6 і Х може мати одну з дозволених відмінностей, R' необов'язково може бути попередником, одна або більше з амінокислот Аа1, Аа2, Аа3, Аа4, Аа5, Аа6 необов'язково можуть мати захисні групи, а -СООН у Аа3 і/або -NH2 у Аа4 можуть необов'язково бути захищені, активовані або дериватизовані. 1 2 Тим часом професор Reinhart також визначив індивідуальні положення для 5-Val та 2-Thr (K.L. Rinehart, персональне повідомлення). Хоча для 2 Thr та 3 Val, його визначення співпадали з визначеннями проф. Scheuer, для останнього 2 Val спостерігається розходження. Так, відповідно до визначення Rinehart, два послідовних Val у бічному ланцюгу мають відмінний вигляд, й структура має вигляд формули (І): У цей час прийнято - й у даному тексті це знову показано - що правильна формула кахалаліду F відповідає формулі (І). Його будова досить складна, і складається з шести амінокислот у циклічній частині, й екзоцик 7 76949 лічний ланцюжок включає в себе сім амінокислот з кінцевою ацильною групою. Кахалалід F (І) є надзвичайно ефективним та рідкісним протипухлинним агентом морського походження, хоча відсутність його у достатній кількості затримала плани клінічних досліджень. Відомі й інші сполуки кахалалідів, описані, наприклад, [Hamann, M.T., et al., J. Org. Chem., 1996, «Kahalalides: Bioactive Peptides from Marine Mollusk Elysia rufescens and its Algal Diet Bryopsis sp», vol.61, pp.6594-6660. Крім кахалаліду F, в цій статті наведені структури кахалалідів А-Е. Повідомлення про Кахалалід К зустрічається у [J Nat. Prod. 1999, 62, 1169], а про Кахалалід О зустрічається у [J Nat Prod. 2000, 63, 152]. Структури цих інших сполук кахалалідів представлені такими формулами: 8 Циклічні кахалаліди містять кільцеві амінокислоти та бічний ланцюг, який закінчується ацильною групою. Кахалаліди мають різну біологічну активність, особливо протипухлинну та протитуберкульозну активність. У даному винаході запропоновані імітатори природних кахалалідів. Сполуки можуть відрізнятися однією або більшою кількістю амінокислот, і одним або більшою кількістю компонентів ацильного бічного ланцюга. Бажано, щоб імітатори згідно з даним винаходом відрізнялися щонайменше однією з наступних характеристик вихідного від природного кахалаліду: Від 1 до 7, переважно від 1 до 3, більш переважно - 1 або 2, і найбільш переважно - 1 амінокислота відрізняється від вихідної сполуки; Від 1 до 10, переважно від 1 до 6, більш переважно - від 1 до 3, особливо 1 або 2 додатковими метиленовими групами у бічному ацильному ланцюгу вихідної сполуки; Від 1 до 10, переважно від 1 до 6, більш переважно - від 1 до 3, особливо 1 або 2 метиленові групи опущені у бічному ацильному ланцюгу вихідної сполуки; Від 1 до 6, переважно від 1 до 3, більш переважно - 1 або 3 замісники додані або пропущені у бічному ланцюгу ацильної групи вихідної сполуки. Для циклічних кахалалідів додавання та видалення амінокислоти можна здійснити як у циклічному кільці, так і у бічному ланцюгу. Прикладами згідно з винаходом є сполуки, споріднені кахалаліду F, який має таку формулу: 9 76949 10 де Ааа1, Ааа2, Ааа3, Ааа4, Ааа6 та Ааа7 являодержання сполук кахалаліду F та споріднених ють собою незалежно а-амінокислоти L- або Dструктур. конфігурації, (якщо це можна застосувати); де R1, Переважні сполуки є спорідненими кахалаліду R2, R3, R4, R5, R6, R7 незалежно являють собою Η F (І), в яких у формулі (II) Ааа-1 являє собою Dабо органічну групу, вибрану з групи, яка складаallo-Thr (X1=О, R1=CH3), Aaa-2 являє собою D-alloється з алкільної групи, арильної групи, аралкільlle (R3=1-метилпропіл), Ааа-3 являє собою D-Val ної групи та їх похідних, заміщених гідрокси(R4=ізопропіл), Ааа-4 являє собою Phe групою, меркапто-групою, аміно-групою, гуанідино(R5=бензил), Ааа-5 являє собою Z-Dhb групою, галогеном; де X1 незалежно являє собою (Х2=С=СНСН3 з Ζ конфігурацією), Ааа-6 являє соО, S, або N; де R2 незалежно являє собою (якщо бою L-Val (R6=ізопропіл), Ааа-7 являє собою Dприсутній) Η або органічну групу, вибрану з групи, allo-Ile (R7=1-метилпропіл), і R8 містить гексапепяка складається з алкільної групи та аралкільної тидне похідне наступної формули (формула VI): групи; де Aaa5 незалежно являє собою амінокислоту L- або D-конфігурації (якщо це має місце); де Х2 незалежно являє собою органічну групу, вибрану з групи, яка складається з алкенілу, алкільної групи, арильної групи, аралкільної групи та їх похідних, заміщених незалежно гідрокси-групою, меркапто-групою, аміно-групою, гуанідино-групою, галогеном; де R8 незалежно являє собою сполуку, що виражається такими формулами III, IV, або V: де R9, R10 та R11 незалежно являють собою Η або органічну групу, вибрану з групи, яка складається з алкільної групи, арильної групи, аралкільної групи та їх похідних, заміщених гідроксигрупою, меркапто-групою, аміно-групою, гуанідиногрупою, карбоксильною групою, карбоксамідогрупою, галогеном; R9 та R10 можуть становити частину того самого циклу; R9 (якщо присутній) може бути у S або R конфігурації по відношенню до вуглецю, до якого він приєднаний; і n приймає значення від 0 до 6. Визначення амінокислот також можуть варіюватися (мається на увазі пролін та аналогічні амінокислоти, включаючи гідроксипролін). Формули (III), (IV) та (V) можуть бути перемішані, що призводить до утворення бічного ланцюга, який складається із ланок, що повторюються більш ніж в одній з цих формул. При модифікації одна або більша кількість з кільцевих амінокислот Ааа-6 та Ааа-5 гексаамінокислотного циклу відсутня, або амінокислота Ааа-7 додана між Ааа-6 та Ааа-1, внаслідок чого утворюються кільця, що містять чотири, п'ять або сім амінокислот у кільці. Переважними кільцями є ті, що містять шість амінокислот. Далі даний винахід відноситься до способу Інші переважні сполуки є аналогічними спорідненими сполуками інших кахалалідів і містять амінокислоти та бічні ланцюги, загальні з такими сполуками. Є посилання на відомі структури кахалалідів. Переважно, щоб сполуки згідно з винаходом імітували природний кахалалід, з модифікацією, вставкою або виключенням в одній або більше кількості точок у молекулі. Особливо переважні сполуки, які містять ті самі амінокислоти, що і в природних циклічних кахалалідних сполуках, але відрізняються бічним ланцюгом, особливо в ацильній частині. Такі відмінності можуть включати в себе збільшення або зменшення числа метиленових груп, звичайно найбільше - зміна двох метиленових груп, і збільшення або зменшення числа замісників, особливо додавання замісника-галогена, такого як фтор. У використаному тут значенні термін «органічна група» означає вуглеводневу групу, яка класифікується як аліфатична група, циклічна група або комбінація аліфатичних та циклічних груп (наприклад, аралкільні групи). У контексті згідно з винаходом термін «аліфатична група» означає насичений або ненасичений лінійний або розгалужений вуглеводень. Цей термін охоплює, наприклад, алкільні, алкенільні та алкінільні групи. Термін «алкільна група» означає насичену лінійну або розгалужену вуглеводневу групу, включаючи, наприклад, метильну, етильну, ізопропільну, ізобутильну, трет-бутильну, гептильну, додецильну, октадецильну, амільну, 2етилгексильну, 2-метилбутильну, 5метилгексильну, 9-метил-3-децильну та інш., особливо алкільні групи, які містять єдину розгалужену метиленову групу. Відповідними алкільними групами є групи з довгими ланцюгами, які містять 11 76949 12 від 1 до 20 атомів вуглецю, звичайно від 1 до 15 фраза «алкільний фрагмент» обмежена включенабо від 1 до 10 атомів вуглецю, або вони можуть ням тільки чистих насичених вуглеводневих замісбути коротшими, і можуть містити від 1 до 6 або ників з відкритими ланцюгами, таких як метил, від 1 до 3 атомів вуглецю. Зручно, щоб група R11 етил, пропіл, ізобутил та ін. була групою з довгим ланцюгом, а інші групи пеУ найбільш переважному варіанті згідно з виреважно були б короткими. находом запропонована сполука формули (А): Термін «алкенільна група» означає ненасичену лінійну або розгалужену вуглеводневу групу з однією або більшою кількістю вуглець-вуглецевих подвійних зв'язків, такий як вінільна група. Відповідні алкенільні групи містять від 2 до 8 або від 2 до 4 атомів вуглецю. Термін «алкінільна група» означає ненасичену лінійну або розгалужену вуглеводневу групу, з однією або більшою кількістю вуглець-вуглецевих потрійних зв'язків. Відповідні алкінільні групи містять від 2 до 8 або від 2 до 4 атомів вуглецю. де кожний з Аа1-Аа6 з сусідніми -N- та -CO-, віТермін «циклічна група» означає замкнену кідповідно, являє собою - або -амінокислоту, пельцеву вуглеводневу групу, яка класифікується як реважно -амінокислоту, Χ являє собою групу, яка аліциклічна група, ароматична група або гетероцизв'язує Аа1, переважно вибрану з аміно, гідрокси клічна група. Термін «аліциклічна група» означає або тіолу, більш переважно - гідрокси, і R являє циклічну вуглеводневу групу, що зберігає властисобою групу, що необов'язково включає в себе вості аліфатичних груп, і яка є моно- або біциклом, який містить від 4 до 10 атомів вуглецю. Термін одну або більше з або амінокислот, переважно «ароматична група» або «арильна група» означає амінокислоти. Як варіант можуть бути відсутніми моно- або поліциклічну ароматичну вуглеводневу -СО-Aa5-N-, можливо також одночасна відсутність групу, яка представляє моно- або біцикл, і яка міс-CO-Aa5-N-, або - в іншому варіанті -між Аа6 і Аа1 тить від 5 до 10 атомів вуглецю. Термін «гетероциможе бути вставлена група -CO-Aa7-N-. клічна група» означає замкнений кільцевий вуглеАмінокислоти можуть бути у L- або Dводень, в якому один або більше атомів кільця конфігурації. Переважно, щоб конфігурація була являє собою елемент, відмінний від вуглецю (натакою самою, як і конфігурація відповідних аміноприклад, від 1 до 3 з одного або більше з азоту, кислот у кахалалідній сполуці, особливо у кахала1 7 кисню, сірки інш.), відповідно, моно- або біцикл, ліді F. Один або більше з Аа -Аа переважно відякий містить від 4 до 10 атомів у кільці. повідає амінокислоті у тому самому положенні, що Як зрозуміло фахівцям у цій області, великий і у природному кахалаліді або спорідненій йому ступінь заміщення не тільки допустимий, але часто сполуці. У найбільш переважному варіанті кожна з буває бажаним. Заміщення передбачаються у амінокислот відповідає амінокислоті у природному сполук згідно з винаходом. Щоб спростити посикахалаліді F. Так, переважно, щоб Аа1 являв солання та вказівки на деякі терміни, що використобою D-allo-Thr, Аа2 являв собою D-allo-lle, Аа3 яввуються в описі, який розглядається, терміни «груляв собою D-Val, Аа4 являв собою Phe, Аа5 являв па» та «фрагмент» використовують для того, щоб собою Z-Dhb, Аа6 являв собою L-Val. розрізнити види хімічних сполук, які допускають Якщо використовують споріднені сполуки, віднаявність замісників, і ті, які не допускають наявповідні споріднені сполуки містять заміщені аміноності замісників або не заміщені. Так, якщо термін кислоти, в яких заміщення відповідають структурі «група» використовують для опису хімічного замівідповідних амінокислот у природному кахалаліді, сника, хімічний матеріал, що описується, включає такому як Кахалалід F. Замісники для треоніну в себе незаміщену, групу, і наприклад, групу з включають у себе серин та інші гомологи, а також атомами О, N або S, в ланцюгу, а також карбоніцистеїн та гомологи. Замісники ізолейцину вклюльну групу, або інші звичайні замісники. Якщо терчають у себе інші амінокислоти з неполярними мін «фрагмент» використовують для опису хімічної групами, включаючи аланін, валін, лейцин та просполуки або замісника, припускається тільки незалін, а також аналоги та гомологи. У цьому плані міщений хімічний матеріал. Наприклад фраза «алнаявність атомів азоту -N- у формулі (А) не виклюкільна група» повинна включати в себе не тільки чає можливості утворення кільця, такого, яке утвочисті з розкритим ланцюгом насичені алкільні вугрюється з проліном. Замісники валіну включають у леводневі замісники, такі як метил, етил, пропіл, себе ізолейцин та інші амінокислоти з неполярниізобутил та ін., але також і алкільні замісники, що ми групами, включаючи аналоги та гомологи. Замістять інші замісники, відомі фахівцям, такі як місники фенілаланіну включають у себе триптогідрокси, алкокси, аміно, карбоксил, карбоксамідо, фан та тирозин. Замісники Dhb включають у себе атоми галогенів, ціано, нітро, алкілсульфоніл та інші амінокислоти з таким алкеніліденовим замісінш. Так, «алкільна група» включає в себе ефірні ником, включаючи амінокислоти з С3 або з вищими групи, галогеналкіли, спирти, тіоли, карбоксил, бічними ланцюгами, а також аналоги та гомологи. аміни, гідроксіалкіли, сульфоалкіли та інш. ПереПереважно, щоб Аа1 мав вигляд: важними є галогеналкільні групи. З іншого боку, 13 де Raa1 являє собою бічний ланцюг, що містить зв'язок X. Приклади бічних ланцюгів включають у себе алкіл, арил та аралкіл, особливо алкіл, більш типово алкіл, що містить від 1 до 4, наприклад, 2 атоми вуглецю. Переважний розгалужений алкіл. Зв'язувальна група X звичайно являє собою кисень, причому Aa1 переважно одержаний з треоніну, але можуть бути використані сірка, аміно (незаміщений або заміщений алкілом, арилом або аралкілом) та інші зв'язуючі. Відповідною групою X є єдина полярна група в Аа1. Аа1 може бути рацемічним, може мати L- або D-конфігурацію, але переважна D-конфігурація. Переважно, щоб Аа2 мав вигляд де Raa2 являє собою бічний ланцюг, такий як алкіл, арил або аралкіл, особливо алкіл, конкретніше - алкіл, який містить від 1 до 5 атомів вуглецю, наприклад, 3 атоми вуглецю. Переважний розгалужений алкіл, такий як ізолейцин. Бажано, щоб в Аа2 не було полярних замісників. Аа2 може бути рацемічним, може мати L- або D-конфігурацію, але D-конфігурація переважна. Переважно, щоб Аа3 мав вигляд: де Raa3 являє собою бічний ланцюг, такий як алкіл, арил або аралкіл, особливо алкіл, конкретніше - алкіл, який містить від 1 до 5 атомів вуглецю, наприклад, 3 атоми вуглецю. Переважний розгалужений алкіл, такий як валін. Бажано, щоб в Аа3 не було полярних замісників. Аа3 може бути рацемічним, може мати L- або D-конфігурацію, але переважною є D-конфігурація. Переважно, щоб Аа4 мав вигляд: де Raa4 являє собою бічний ланцюг, такий як алкіл, арил або аралкіл, особливо аралкіл, конкретніше - аралкіл, який містить від 7 до 10 атомів вуглецю, наприклад, 7 атоми вуглецю. Переважний бензил, такий як фенілаланін. Бажано, щоб в 76949 14 Аа4 не було полярних замісників. Аа4 може бути рацемічним, може мати L-або D-конфігурацію, але переважною є L-конфігурація. Переважно, щоб Аа5 мав вигляд: де Raa5a та Raa5b кожний вибирають з водню або бічного ланцюга, такого як алкіл, арил або аралкіл, особливо алкіл, конкретніше - алкіл, який містить від 1 до 4 атомів вуглецю, наприклад, 1 атом вуглецю. Переважно, щоб Raa5a являв собою водень, забезпечуючи Ζ конфігурацію, як в переважній а,b-дидегідро-а-аміномасляній кислоті. Бажано, щоб в Аа5 не було полярних замісників. Аа3 може бути рацемічним, може мати L- або Dконфігурацію, але переважною є L-конфігурація. Переважно, щоб Аа6 мав вигляд: де Raa6 являє собою бічний ланцюг, такий як алкіл, арил або аралкіл, особливо алкіл, конкретніше - алкіл, який містить від 1 до 5 атомів вуглецю, наприклад, 3 атоми вуглецю. Переважний розгалужений алкіл, такий як валін. Бажано, щоб в Аа6 не було полярних замісників. Аа6 може бути рацемічним, може мати L- або D-конфігурацію, але переважною є L-конфігурація. Амінокислоти Аа1 до Аа7 можуть бути такими, які визначені для груп Ааа-1 до Ааа-7 формули (II). Переважно, щоб бічний ланцюг R включав в себе 5-MeHex-D-Val-L-Thr-L-Val-D-Val-D-Pro-L-OrnD-allo-Ile або споріднену йому сполуку, включаючи аналоги та гомологи. Приклади споріднених сполук включають в себе сполуки загальної формули (Rt)m-(амінокислота)п-, причому m+n не дорівнює нулю, де R1 являє собою кінцеву групу, переважно алкіл, алкеніл, алкініл, арил, аралкіл, гетероарил, гетероалкіл, аліциклічну, або іншу кінцеву групу, і (амінокислота)n- являє собою довільний ланцюг амінокислот. Кінцева алкільна група переважно містить від 1 до 12 атомів вуглецю, конкретніше - від 4 до 10 атомів вуглецю, вона може бути заміщена і переважно є розгалуженою. Приклади включають в себе бутил, пентил, гексил, гептил, октил та інші алкільні групи, які містять 1 або більше метильних або етильних груп, або довші бічні групи, що переважно містять від 1 до 6 атомів вуглецю, особливо 5-метилгексил та інші алкільні групи з розгалуженнями удалині від точки приєднання до іншої частини молекули. Відповідні замісники включають у себе галогени, гідрокси, алкокси, аміно, карбоксил, карбоксамідо, ціано, нітро, алкілсульфоніл, алкок 15 76949 16 си, алкоксіалкіл, арилалкіларил, гетероциклічні, фармацевтичної композиції, яка її містить. аліциклічні, арильні, аралкільні та інші групи, згаДаний винахід відноситься також до фармацедані вище. Відповідно, такі замісники можуть місвтичних препаратів, які містять як активний інгретити додаткові замісники, як наприклад, толільна дієнт сполуку або сполуки згідно з винаходом, а група. Найбільш переважні галогенові замісники, також до способів їх одержання. особливо 1 або більше, наприклад, від 1 до 3 атоПриклади фармацевтичних композицій вклюмів фтору. Інші кінцеві групи можна вибрати відпочають в себе будь-які тверді композиції (таблетки, відно до вказівок, наведених в описі, і вони вклюпілюлі, капсули, гранули та інш.) або рідкі компочають в себе аліциклічні, аралкільні, арильні, зиції (розчини, суспензії або емульсії) відповідного гетероциклічні або інші групи, які можуть містити 1 складу для перорального, зовнішнього або паренабо більше, зокрема, від 1 до 3, замісників. терального введення, і вони можуть містити або Бічний ланцюг R-CO-N- може містити водень чисту сполуку, або її комбінацію з будь-яким носіабо замісник у азоту, такий як алкільна, арильна єм або іншими фармацевтично прийнятними споабо аралкільна група. луками. Може виявитися необхідним стерилізуваУ бічних ланцюгах відповідних споріднених ти ці композиції, призначені для парентерального сполук використовують заміщені амінокислоти, введення. вибрані відповідно до викладених вище принципів, Введення сполук згідно з винаходом можна альтернативних ізолейцину, валіну та треоніну, здійснити будь-яким зручним способом, таким як причому їх вибирають як для цих амінокислот у внутрішньовенне вливання, у вигляді препаратів циклічній частині молекули, так альтернативні ордля перорального прийому, внутрішньочеревинних нітину, включаючи лізин, гістидин, аргінін; альтерта внутрішньовенних ін'єкцій. Автори рекомендунативні проліну, включаючи аланін та інші неполяють використати тривалість вливань аж до 24 горні амінокислоти, такі як гліцин, ізолейцин та інші, дин, більш переважно - від 2 до 12 годин, і найякі згадувалися вище. Звичайно ланцюг R містить більш переважно - 2-6 годин. Особливо бажані від 0 до 10, більш переважно - від 4 до 8, наприкороткочасні вливання, які дозволяють провести клад, 5, 6 або 7, особливо 7, амінокислотних залікування без необхідності залишатися у лікарні на лишків. Якщо присутні більше семи амінокислот, ніч. Однак при необхідності вливання можуть тритоді переважно, щоб ці додаткові амінокислоти вати від 12 до 24 годин і навіть довше. Вливання були такими, які існують у природі, особливо ті, які можна здійснювати з відповідними інтервалами, були вказані вище. наприклад, від 2 до 4 тижнів. Фармацевтичні комМожуть бути використані L- або Dпозиції, які містять сполуки згідно з винаходом, амінокислоти або їх рацемічні суміші. Переважно, можна постачати в інкапсульованому у ліпосоми якщо амінокислоти є присутніми у бічному ланцюгу вигляді або у вигляді наносфер, у композиціях з R, щоб одна або більша кількість з них була б у уповільненим виділенням активної речовини, або конфігурації, відповідній конфігурації природного за допомогою інших стандартних способів достабічного ланцюга. Вважаючи з циклічного гексапепвки. тиду, амінокислотні залишки знаходяться у конфіТочне дозування сполук буде мінятися в залегурації DLDDLLD. Зручно, щоб кінцева алкільна жності від конкретної лікарської форми, способу група містила від 1 до 12 атомів вуглецю, більш введення та конкретних ділянок введення, від папереважно - від 4 до 10 атомів вуглецю, і може цієнта і пухлини, що підлягає лікуванню. Потрібно бути заміщеною, і переважно розгалуженою. Відвраховувати і інші фактори, такі як вік, вага, стать, повідні замісники включають в себе галоген, гідрохарчовий раціон, швидкість виведення, стан пацієкси, алкокси, аміно, карбоксил, карбоксамідо, ціанта, комбінацію ліків, реакційну чутливість та тяжно, нітро, алкілсульфоніл та інші згадані тут групи. кість захворювання, що підлягає лікуванню. ВвеНайбільш переважні як замісники галогени. дення препарату можна здійснювати безперервно У більш загальній формі бічний ланцюг R-COабо періодично у рамках максимальної переносиN- можна визначити для бічного ланцюга R8-NHмої дози. CHR7-CO-NH- у сполуках формули (II), включаючи Сполуки та композиції згідно з винаходом мосполуки зі сумішами амінокислот, що визначаютьжна використати разом з іншими ліками для зася формулами (III), (IV) та (V). безпечення комбінованої терапії. Інші ліки можуть Хоча переважні характеристики були сформустановити частину тієї самої композиції або мольовані у відношенні кахалаліду F, інші переважні жуть надаватися у вигляді окремої композиції для сполуки згідно з даним винаходом одержані із заодночасного введення або для введення в інший стосуванням тих самих принципів створення імітачас. Склад інших ліків конкретно не обмежений, і торів інших кахалалідів. Так, амінокислоти та бічні відповідні варіанти включають в себе ланцюги можуть бути змінені, переважно при збеa) лікарські засоби, які мають антимітотичну реженні гідрофобно-гідрофільної рівноваги між дію, особливо такі, мішенню яких є цитоскелетні полярними та неполярними угрупуваннями. елементи, включаючи модулятори мікротрубочок, Сполуки згідно з винаходом мають корисну бітакі як таксанові лікарські засоби (такі як таксол, ологічну активність, включаючи протипухлинну паклітаксел, таксотере, доцетаксел), подофілотокактивність. сини або алкалоїди барвінку (вінкристин, вінбласУ даному винаході запропонований спосіб літин); кування будь-якого ссавця, особливо людини, з b) антиметаболічні агенти, такі як 5раковим захворюванням, який включає в себе фторурацил, цитарабін, гемцитабін, пурин та анавведення хворому індивідууму терапевтично ефелоги, такі як пентостатин, метотрексат); ктивної кількості сполуки згідно з винаходом або c) алкілуючі агенти, такі як азотистий іприт (та 17 76949 18 кі як циклофосфамід або іфосфамід); d) лікарські засоби, які діють на ДНК, такі як ліки антрациклінового ряду, адріаміцин, доксорубіцин, фарморубіцин або епірубіцин; e) лікарські засоби, які діють на топоізомерази, такі як етопозид; f) гормони та агоністи гормонів або їх антагоністи, такі як естрогени, антиестрогени (тамоксифен та споріднені сполуки) і андрогени, флутамід, леупрорелін, гозерелін, ципротрон або октреотид; g) лікарські засоби, які діють на сигнальну трансдукцію в пухлинних клітинах, включаючи похідні антитіл, такі як герцептин; h) алкілуючі агенти, такі як лікарські препарати на основі платини (цис-платин, карбонплатин, оксаліплатин, параплатин) або нітрозоуреаза; і) лікарські засоби, що потенційно впливають на метастази пухлин, такі як інгібітори матричної металопротемази; j) агенти генної терапії та антисмислові агенти; k) лікарські засоби на основі антитіл; l) інші біоактивні сполуки морського походження, особливо ектеїнасцидини, такі як ектеїнасцидин 743 або дидемніни, такі як аплідин; m) аналоги стероїдів, зокрема дексаметазон; де R' являє собою групу R-CO-, або її попереn) протизапальні лікарські засоби, особливо дник, і де одна або більше з амінокислот може дексаметазон; та мати захисні групи, і де -СООН в Аа3 і/або -NH2 в о) протиблювотних ліків, зокрема, дексаметаАа4 можуть бути необов'язково захищені, активозон. вані, або можуть бути одержані їх похідні. Такі Даний винахід охоплює також сполуки згідно з процедури з використанням попередників, шляхом винаходом, які використовуються у способі лікуактивації або одержання похідних самі по собі є вання, і застосування сполук для одержання комабсолютно звичайними, і в їх деталізації немає позицій для лікування раку. необхідності при викладі способу згідно з винахоПрипускається також, що сполуки згідно з видом. находом мають протитуберкульозну активність. Спосіб згідно з винаходом можна здійснити, Відповідно до даного винаходу, запропоновавиходячи з вихідних матеріалів енантіо- і стереоний спосіб одержання сполук згідно з винаходом, контрольованим швидким способом, використовувключаючи кахалалід F, який включає у себе заючи переваги способу твердофазного синтезу, при микання кільця між Аа3 та Аа4. Автори виявили, що якому молекула у конструкції зв'язана з нерозчинзамикання кільця у цьому положенні забезпечує ним носієм протягом всього процесу синтезу. Тагарний спосіб. Замикання кільця може відбуватися ким чином, надлишок реагентів та розчинних побіперед іншими модифікаціями у молекулі, або його чних продуктів можна легко видалити шляхом можна здійснити після модифікацій (модифікації промивки молекул-на-смолі відповідними розчинвключають в себе створення або подовження бічниками. Toму можна використати великий надлиного ланцюга у Аа1 і/або видалення захисних груп, шок розчинних реагентів для доведення реакції до і/або модифікацію замісників у амінокислот. завершення за короткий проміжок часу, при цьому Так, спосіб можна проілюструвати наступною уникаючи рацемізації (якщо вона можлива) та інсхемою: ших вторинних реакцій. Переважний варіант способу синтезу згідно з винаходом краще усього представлений на схемі 1, де представлено конструювання сполук формули (II). 19 76949 20 Wang - замість хлортритилу. Переважний спосіб згідно з винаходом проілюстрований на схемі 1. Як там представлено і як зазначається детальніше у наведених далі прикладах, цей спосіб здійснюють таким чином: Fmoc-Aaa3-OH вводять переважно у хлортритил-полістирольну смолу, див. [Barlos, К.; Gatos, В.; Schafer, W. Angew. Chem. Int. Ed. Engl. 1991, 30, 590-593], в присутності DIEA, зберігаючи рівень заміщення приблизно 0,15-0,5ммоль/г. Використання великих кількостей призведе до утворення пептидів з кінцевими групами у кінцевому продукті, див. [Chiva, С; Vilaseca, M.; Giralt, Ε.; Albericio, F. J. Pept. Sci. 1999, 5, 131-140]. Видалення Fmoc групи здійснюють, використовуючи піперидин-ДМФ (2:8, об/об) (1x1хв, 3x5хв, 1x10хв). Реакцію сполучення Fmoc-, Alloc-Aaa-OH та R11-СООН (5еквів.) здійснюють, використовуючи HATU-DIEA, див. [Carpino, L.A.; Е1-Faham, Α.; Minor, C.A.; Albericio, F. J. Chem. Soc, Chem. Як представлено вище на схемі 1, переважний Commun. 1994, 201-203], (5:10) у ДМФ протягом 90 спосіб синтезу кахалаліду F (І) та його похідних й хвилин. Після реакції сполучення проводять нінгіаналогів заснований на твердофазному підході, дриновий тест, і, якщо він виявляється позитивдив., наприклад, [Lloyd-Williams, P., et al., Chemical ним, реакцію сполучення повторюють у тих самих Approaches to the Synthesis of Peptides and умовах, в іншому випадку процес, продовжують. Proteins, CRC Press, Boca Raton (FL), 1997]. Промивки між стадіями видалення захисних груп, Спосіб, представлений на схемі 1, включає в реакції сполучення і знову видалення захисних себе послідовні стадії груп здійснюють у ДМФ (5x0,5хв) та СН2Сl2 (a) включення Fmoc-амінокислоти (Ааа3) на (5x0,5хв), використовуючи кожний раз по 10мл тверду основу (наприклад, полістирол, поліетилен, розчинника на 1г смоли. прищеплений на полістирол, та інш.), яка містить Включення Аllос-Ааа6-ОН (7екв.), якщо Х1=О, супер-кислотний лабільний кінець або лінкер (наздійснюють, використовуючи еквімолярну кількість приклад, хлортритил, поліалкоксибензил та інш.), DIPCDI та 0,7еквів. DMAP протягом 2 годин. Цю який створює складноефірний зв'язок; реакцію сполучення повторюють двічі. (b) подовження пептидного ланцюга трьома Видалення Аllос групи здійснюють, використоамінокислотами (Ааа2, Ааа1, Ааа7) з використанвуючи Pd(PPh3)4 (0,1еквів.) у присутності PhSiH3 ням підходу на основі Fmoc/tBu. Для І, X1=ОН і (10еквів.) в атмосфері Аr, див. [Gomez-Martinez, P.; вводиться без захисних груп. Якщо Х1=NH2, його Thieriet, N.; Albericio, R; Guibe, F. J. Chem. Soc. вводять із захисною групою Аllос; Perkin 11999, 2871-2874]. (c) включення (Ааа6) з використанням підходу Дегідратацію здійснюють у твердій фазі, викона основі Alloc/tBu; ристовуючи EDC (розчинний у воді карбодіімід, (d) подовження пептидного ланцюга іншими 100еквів.) у присутності CuCl (60еквів.) в СН2Сl2амінокислотами і Ru-COOH через Ааа7 з викорисДМФ (10:2) протягом 6 днів. EDC/CuCl був викоританням підходу на основі Fmoc/tBu; станий у дегідратації у розчині залишку Thr у фра(е-1) подовження пептидного ланцюга двома гменті Nisin. [Fukase, К.; Kitazawa, M.; Sano, Α.; амінокислотами [Ааа5 (ΟΗ,Η), Ааа4] через Ааа6 з Shimbo, К.; Horimoto, S.; Fujita, H.; Kubo, Α.; використанням підходу на основі Alloc/tBu. ПриєдWakamiya, Т.; Shibe, A. Bull. Chem. Soc. Jpn. 1992, нана до Ааа5 ОН не захищена; 65, 2227-2240]. (е-2) дегідратації у твердій фазі до одержання Здійснюють реакцію сполучення дипептиду пептиду з Ааа5; Аllос-Ааа4-Ааа5-ОН (5еквів.), одержаного в розчині або з Аllос-Ааа4-ОН і Н-Ааа5 (ОН, H)-OtBu з EDC, з (e'-1) включення дипептиду Аllос-Ааа4-Ааа5подальшою дегідратацією та обробкою TFA, з ОН, який об'єднували та піддавали дегідратації у HATU-DIEA (5:10) протягом 16 годин, і повторне розчині; сполучення протягом 3 годин. Використання інших (f) видалення Аllос групи Ааа4, при цьому пепагентів у реакції сполучення на основі HOBt, таких тид все ще прикріплений до твердого носія; як HBTU або DIPCDI-HOBt, призводить до непов(g) відщеплення пептиду із захищеним бічним ного включення дипептиду. ланцюгом (якщо він захищений) від твердого носія; Відщеплення захищеного дипептиду від смоли (h) циклізації пептиду у розчині; здійснюють, використовуючи TFA- СН2Сl2 (1:99) (і) видалення TFA лабільних захисних груп бі(5x30с). чного ланцюга. Стадію циклізації здійснюють, використовуючи Потрібно враховувати, що конкретний вибір DIPCDI-HOBt (3:3 еквів.) в СН2Сl2-ДМФ протягом 2 захисних груп не є критичним, і є широкі можливогодин. Можна також використати і інші способи, сті для вибору інших варіантів. Наприклад, групи такі як з використанням PyBOP/DlEA (3:6 еквів.) у типу Bzl можна замінити на tBu/Boc; Boc викорисДМФ. тати замість Fmoc; Fmoc - замість Alloc; смолу Остаточне видалення захисних груп здійсню 21 76949 22 ють, використовуючи TFA-H2O (95:5) протягом 1 нти та розчинники використовували у тому вигляді, години. в якому вони були одержані, за винятком ДМФ та Приклади винаходу СН2Сl2, через які пропускали азот для видалення Скорочення летких домішок (ДМФ), і зберігали над активоваСкорочення, використані для амінокислот, і ними молекулярними ситами 4Å (Merck, Darmstadt, позначення пептидів відповідають правилам Germany) (ДМФ) або СаСI2 (СН2Сl2). Реакції у розIUPAC-IUB [Commission of Biochemical чинах здійснювали у круглодонних колбах. ЕкстраNomenclature в J. Biol Chem. 1972, 247, 977-983]. кти органічних розчинників сушили над безводним Використані такі скорочення: 4-AcBut-OH, 4MgSO4, з подальшим видаленням розчинника при ацетоксимасляна кислота; AcButBut-OH, 4-(4зниженому тиску та температурі 70%, за 0,75ммоль, 5еквів.) та DIEA (261мл, 1,5ммоль, даними ВЕРХ (Умова В, tR 25,7хв). ESMS, розра10еквів.) у ДМФ (2,5мл). У всіх випадках, після ховано для С84Н142N14O19, 1651,1. Знайдено: m/z 90хв здійснення реакції сполучення нінгідриновий 1652,3 [М+Н]+. або хлораніловий (після включення D-Val) тести Приклад 7 були негативними. Видалення Fmoc-груп та проКахалалід F (І). мивки здійснюють за способом, розкритим у роздіЗахищений пептид (Приклад 6) (40,0мг, лі «Загальні процедури». Аліквоту пептидил-смоли 24мкмоль) розчиняють у ДМФ (25мл), і додають обробляють TFA-H2O (9:1) протягом 60хв, і за даРуВОР (37,8мг, 73мкмоль, 3еквів.) та DIEA (25мл, ними ВЕРХ (Умова В, tR 17,2хв) для сирого проду145мкмоль, 6еквів.). Суміш перемішують протягом кту, одержаного після випаровування, ступінь чис1 години, потім розчинник видаляють, випаровуютоти становить >82%. ESMS. Розраховано для чи при зниженому тиску. Захищений циклічний С66Н116N12O17, 1348,9 Знайдено: m/z 1350,0 [М+Н]+. пептид розчиняють у TFA-H2O (19:1, 5мл), і суміш Приклад 4 перемішують протягом 1 години. Розчинник вида5-MeHex-D-Val-Thr(tBu)-Val-D-Val-D-Proляють, випаровуючи при зниженому тиску, і потім Orn(Boc)-D-аllо-Ile-D-аllо-Thr(Val-Thr-Phe-Alloc)-Dдодають Н2О (5мл) та ліофілізують. Сирий продукт аllо-Ile-D-Val-O-TrtCl-смола очищають за допомогою хроматографії середньо 25 76949 26 го тиску (Vydac С18 15-20мкм, 300Å, 240x24мм), С75Н124Ν14О16, 1477,9. Знайдено: m/z 1478,7 лінійний градієнт від 20% до 60% ацетонітрил [М+Н]+, 1500,6 [M+Na]+, 1516,5 [М+К]+. Продукт (+0,05% TFA) у воді (+0,05% TFA) протягом 5 госпів-елюють, використовуючи ВЕРХ [Умову D (tR дин (300мл кожного розчинника), 120мл/година, 12,5хв), Ε (tR 17,4хв), та F (tR 12,1хв) з аутентичним реєстрація при 220нм, у результаті одержують зразком кахалаліду F. Спектр 1Н ЯМР (500МГц, d6вказаний у заголовку продукт (5,0мг, 3,4мкмоль, ДМСО) сполуки був ідентичний спектру природновихід 14%). MALDI-TOF-MS, розраховано для го продукту (результати представлені у таблиці І) Таблиця І Залишок (Z)-Dhb D-allo-Ile 1 L-Phe D-allo-Thr D-Val 3 L-Orn D-allo-Ile 2 D-Val 5 L-Thr D-Val 2 L-Val 4 L-Val 1 N-H 9,69 (c) 8,82 (д, J=10,0Гц) 8,79 (д, J=5,5Гц) 8,56 (д, J=8,0Гц) 8,10(д, J=8,5Гц) 7,95 (д, J=8,5Гц) 7,90 (д) 7,88 (д) 7,82 (д, J=8,0Гц) 7,62 (д, J=8,5Гц) 7,57 (д, J=8,5Гц) 6,76 (д, J=9,0Гц) D-Pro 5-MeHex Інші характеристики Η 6,34 (кв., J=7,0Гц) 1,26 (д, J=7,5Гц, -СН3) 1,73 1,31, 1,02, 0,77 ( -СН2, -СН3, -СН3) 2,93 (м) 7,20 (1Η Αr, м) 7,28 (4Н Аr, м) 4,96 (м) 1,07 ( , J=6,5Гц, -СН3) 1,94 0,86 (2 -СН3) 1,48 (2Н) 1,67 ( -СН2), 2,74 (bs, -CH2), 7,69 ( -ΝΗ3+) 1,69 1,30, 1,03, 0,77 ( -СН2, -СН3, -СН3) 1,96 0,84 (2 -СН3) 3,97 (м) 4,88 (д, J=5,0Гц, ОН), 0,98 (д, J=6,5Гц, -СН3) 2,17 0,77 ( -СН3), 0,62 (д, J=7,0Гц, -СН3) 1,98 0,80 (2 -СН3) 1,39 0,62 (д, J=7,0Гц, -СН3), 0,58 (д, J=6,0Гц, -СН3) 2,03, 1,87, 1,79 ( -СН2, -СН2), 3,76 (1Н, м, 5-СН2), 3,53 (1H, м, **4,36 СН2) 2,13 (2Н) 1,47 ( -СН2, -CH), 1,11 ( -СН2), 0,82 (2 -СН3) Н 4,31 4,42 4,53 4,26 4,49 4,37 4,23 4,26 4,46 4,28 3,86 Приклад 7біс 5-MeHex-D-Val-Thr-Val-D-Val-D-Pro-Orn-D-alloIle-цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb-Van. Одержують як побічний продукт під час одержання (у процесі рацемізації на стадії циклізації) прикладу 7. Продукт охарактеризований за допомогою ВЕРХ (tR 17,4хв. Умова В) і ESMS, розраховано для С75Н124N14O16, 1477,9. Знайдено: m/z 1501,3 [M+Na]+, 1517,3 [М+К]+. Кахалалід F (І) Приклад 8 Alloc-Phe-Thr-OtBu H-Thr-OtBu-HCl (3,1г, 15ммоль, 1,3еквів.) розчиняють у СН2Сl2 (30мл) і додають DIEA (2,9мл, 17ммоль, 1,5еквів.), і суміш перемішують протягом 30хв. Потім додають Alloc-Phe-OH (2,8г, 11ммоль, 1еквів.) та EDC (2,8г, 15ммоль, 1,3еквів.) у СН2Сl2 (35мл), і реакційну суміш перемішують протягом 18 годин. Органічну реакційну суміш промивають Н2О (3x25мл), сушать (MgSO4) і концентрують у вакуумі. Одержане масло (4,12г) очищають за допомогою флеш-хроматографії [СНСІ3-МеОН-НОАс (9:1:0,2)], одержуючи вказану у заголовку сполуку (3,25г, 8ммоль, 71% вихід), яку характеризують за допомогою аналітичної ВЕРХ (tR 20,9хв, ступінь чистоти >98%; Умова С); ESMS, розраховано для С21Н30N2О6 406,2. Знайдено: m/z 408,0 [М+Н]+; 1Н ЯМР (200МГц, CDCl3): 7,1-7,3 (5Н, м, Аr); 6,89 (1Н, д, J=8,8Гц, NH); 5,7-5,9 (1Н, м, СН аліл); 5,56 (1Н, д, J=8,0Гц, ОН); 5,2-5,3 (2Н, м, СН2 g-аліл); 4,52 (2Н, д, J=5,4Гц, СН2 а-аліл); 4,45 (1Н, дд, J=8,4Гц, 2,8Гц, а-СН Thr); 4,22 (1Н, дкв., J=6,2Гц, J=3,0Гц, b-CH Thr); 3,0-3,2 (2Η, м, b-CH2 Phe); 1,47 (9H, s, tBu); 1,15 (3H, д, J=6,6Гц, g-CH3 Thr); 13C ЯМР (50МГц, CDCl3): 172,2 (CO), 169,5 (CO); 156,0 (CO); 136,1 (Cq, Ar); 132,5 (СН, аліл); 129,3 (CH, Ar); 128,5 (CH, Ar); 126,9 (CH, Ar); 117,7 (CH2, аліл); 82,7 (Cq, tBu); 68,5 (b-CH Thr); 65,9 (CH2, аліл); 58,0 (a-CH Thr); 56,2 (a-CH Phe); 38,3 (b-CH2 Phe); 28,0 (CH3, tBu); 20,8 (g-CH3 Thr). Приклад 9 Alloc-Phe-Z-Dhb-OtBu Alloc-Phe-Thr-OtBu (3,25г, 8,0ммоль), EDC (9,90г, 52ммоль, 6,5еквів.) і CuCl (2,14г, 22ммоль, 2,7еквів.) розчиняють у суміші СН2Сl2-безводний ДМФ (65мл, 12:1) в атмосфері N2, і суміш перемішують протягом 2 днів в атмосфері N2. Органічний розчинник видаляють у вакуумі, і залишок вміщують у насичений розчин EDTA (100мл), який екстрагують EtOAc (3x50мл). Об'єднані органічні розчини промивають розсолом (3x60мл), сушать (MgSO4) і концентрують у вакуумі, одержуючи тверду речовину блідо-жовтого кольору (2,8г), яку очищають за допомогою флеш-хроматографії [СНСl3-МеОН-НОАс (9:1:0,1)], одержуючи вказану у заголовку сполуку (2,6г, 6,7ммоль, 84% вихід), яку характеризують за допомогою аналітичної ВЕРХ (tR 23,1хв, ступінь чистоти >95%; Умова С); ESMS, розраховано для С21Н28N2О5 388,2. Знайдено: m/z 389,6 [М+Н]+; 1H ЯМР (200МГц, CDCl3): 7,2-7,4 (5 Η, м, Ar); 6,69 (1Н, кв., J=7,4Гц, CH Dhb); 5,8-6,0 (1Η, м, CH аліл); 5,2-5,3 (2H, м, СН2 g-аліл); 4,5-4,6 (2Η, м, а-СН2 аліл); 3,1-3,3 (2Н, м, b-СН2 Phe); 1,67 (3Н, д, J=7,2Гц, СН3 Dhb); 1,47 (9Н, s, tBu); 13C ЯМР (50МГц, CDCl3): 168,9 (CO); 163,1 (CO); 156,0 (CO); 136,0 (Cq, Ar); 132,6, 132,3 (CH, аліл; b-CH Dhb); 129,3 (CH, Ar); 128,7 (CH, Ar); 127,0 (CH, Ar); 117,9 (CH2, аліл); 81,7 (Cq, ffiu); 66,0 (CH2, аліл); 56,3 (a-CH Phe); 38,2 (b-CH2 Phe); 28,0 (CH3, tBu); 14,7 (CH3 Dhb). Приклад 10 Alloc-Phe-Z-Dhb-OH Alloc-Phe-Z-Dhb-OtBu (2,6г, 6,7ммоль) розчиняють у суміші TFA-СН2Сl2-Н2О (90:8:2, 5,5мл), і 27 76949 28 цю суміш перемішують протягом 3 годин. Органічдаляють, використовуючи Pd(PPh3)4 (15,1мг, ну реакційну суміш концентрують у вакуумі, одер0,013ммоль, 0,1еквів.) в присутності PhSiH3 жуючи вказану у заголовку сполуку (2,2г, (161мкл, 1,3ммоль, 10еквів.) в атмосфері Аr. Кін6,6ммоль, 99% вихід), яку характеризують за доцевий вихід, розрахований за допомогою ААА, помогою аналітичної ВЕРХ (tR 17,0хв, ступінь чисстановить 0,16ммоль/г (79% повний вихід). Захитоти >95%; Умова С); ESMS, розраховано для щений пептид відщеплюють від смоли (235мг, С17Н20N2O5 332,1. Знайдено m/z 333,7 [М+Н]+; 37,5ммоль) за допомогою TFA-СН2Сl2 (1:99) 1 НЯМР (200МГц, CD3OD): 7,2-7,3 (5Н, м, Аг); 6,84 (5x30с). Об'єднані фільтрати випаровують досуху (1Н, кв., J=7,2Гц, СН Dhb); 5,8-6,0 (1Н, м, CH аліл); при зниженому тиску та ліофілізують, одержуючи 5,1-5,3 (2Н, м, СН2 g-аліл); 4,4-4,5 (2Н, м, а-СН2 40,5мг (24,5ммоль, 65%) вказаної у заголовку споаліл); 3,2-3,3 (1Н, м, b-CH2 Phe); 1,66 (3Н, д, луки зі ступенем чистоти >80% за даними ВЕРХ J=7,4Гц, СН3 Dhb); 13С ЯМР (50МГц, CD3OD): 173,1 (Умова В, tR 24,3хв). MALDI-TOF-MS, розраховано (CO); 138,5 (Cq, Аr); 136,7, 134,1 (CH, аліл; b-CH для С84Н142N14O19, 1651,1. Знайдено: m/z 1674,8 Dhb); 130,3 (CH, Ar); 129,4 (CH, Ar); 127,7 (CH, Ar); [M+Na]+, 1690,8 [М+К]+. 117,4 (CH2 аліл); 66,6 (CH2 аліл); 57,8 (a-CHPhe); Приклад 14 39,1 (b-CH2 Phe); 14,1 (CH3 Dhb). Кахалалід F (І) Приклад 11 Захищений пептид (Приклад 13) (38,5мг, 5-MeHex-D-Val-Thr(tBu)-Val-D-Pro-Orn(Boc)-D23ммоль) розчиняють у ДМФ (25мл), і додають allo-Ile-D-allo-Thr(Val-Alloc)-D-allо-llе-D-VаI-О-ТrtСlРуВОР (36,4мг, 70мкмоль, 3еквів.) та DIEA (24мл, смола 140мкмоль, 6еквів.). Суміш залишають при переCl-TrtCl-смолу (0,45г, 1,35ммоль/г) вміщують у мішуванні на 1 годину, а потім розчинник видаля10мг поліпропіленовий шприц, обладнаний поліеють, випаровуючи його при зниженому тиску. Затиленовим дисковим фільтром. Пептидил-смолу хищений циклічний пептид розчиняють у TFA-H2O одержують тим самим способом, що і у прикладах (19:1, 5мл) і суміш перемішують протягом 1 годи1-3, крім того, що у реакції сполучення першої аміни. Розчинник видаляють, випаровуючи його при нокислоти (Fmoc-D-Val-OH) зі смолою використозниженому тиску, і потім додають Н2О (5мл) та вують 0,3 еквівалента замість 0,2 еквівалентів. ліофілізують. Сирий продукт очищають за спосоПочатковий вихід при розрахунку за допомогою бом прикладу 7, одержуючи вказану у заголовку ААА становить 0,29ммоль/g. Після здійснення реасполуку (3,6мг, 2,4мкмоль, 10% вихід), яка було кцій сполучення амінокислот, аліквоту пептидилідентична сполуці, одержаній у прикладі 7. смоли обробляють TFA-H2O (9:1) протягом 60хв, і 5-MeHex-D-Val-Thr-D-Val-Val-D-Pro-Orn-D-alloза даними ВЕРХ (Умова В, tR 17,3хв) для сирого Ile-цикло(D-allo-Thr-D-allo-lle-D-Val-Phe-Z-Dhb-Val) продукту, одержаного після випаровування, сту[структура приписана Кахалаліду F Goetz, G., et al. пінь чистоти становить >80%. ESMS, розраховано Tetrahedron, 1999, vol.55, pp.7739-7746] для С66Н116N12О17, 1348,9. Знайдено: m/z 1350,1 Приклад 15 [М+Н]+. 5-MeHex-D-Val-Thr-D-Val-Val-D-Pro-Orn-D-alloПриклад 12 (D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dnb-Val) [в ре5-MeHex-D-Val-Thr(tBu)-Val-D-Val-D-Proзультаті дегідратації у твердій фазі] Orn(Boc)-D-allo-Ile-D-allo-Thr(Val-Z-Dhb-Рhе-Аllос)Експериментальні процедури здійснюють за D-аIIо-ІIе-D-VаI-О-ТrtСl-смола [внаслідок включенспособом, описаним у прикладах 1-7, за єдиним ня дипептиду] винятком в тому, що у прикладі 3 Fmoc-Val-OH Пептидил-смолу обробляють Pd(PPh3)4 включають у D-Pro-пептидил-смолу, а потім після (15,1мг, 0,013ммоль, 0,1еквів.) в присутності видалення Fmoc групи, включають Fmoc-D-ValPhSiH3 (161мкл, 1,3ммоль, 10еквів.) в атмосфері OH. Кінцевий вихід, розрахований за допомогою Аr, для видалення Аllос групи. ААА, становить 0,106ммоль/г (87% повний вихід), Alloc-Phe-Z-Phb-OH (217мг, 0,65ммоль, 5еквів.) вихід відщеплення становить 83%, і одержують та HATU (249мг, 0,65ммоль, 5еквів.) розчиняють у 4,7мг вказаної у заголовку сполуки, яка являє соДМФ (1,25мл) і додають до пептидил-смоли, потім бою 13% повний вихід стадій циклізації, видалення додають DІЕА (228мкл, 1,3ммоль, 10еквів.), і суміш захисних груп та очищення. При обробці за допоперемішують протягом ночі. Після промивок, помогою ВЕРХ цей продукт елюється на 0,8-1,9хв вторюють реакцію сполучення з тією самою кількіпізніше, ніж аутентичний зразок кахалаліду F стю реагентів протягом 3 годин, коли нінгідрино[Умова D (tR 13,3 в порівнянні з 12,5хв), Ε (tR 18,8 в вий тест стає негативним. Після промивок ДМФ та порівнянні з 17,4хв), і F(tR 14,0 в порівнянні з СН2Сl2, аліквоту пептидил-смоли обробляють TFA12,1хв)]. MALDI-TOF-MS, Розраховано для H2O (9:1) протягом 60хв, і за даними ВЕРХ (Умова С75Н124Ν14Ο16 1477,9. Знайдено: m/z 1478,7 [М+Н]+, В, tR 18,3хв) для сирого продукту, одержаного піс1500,7 [M+Na]+, 1516,6 [М+К]+. ля випаровування, ступінь чистоти становить Спектр 1Н ЯМР (500МгГц, d6-ДМСО) сполуки >80%. MALDI-TOF-MS, розраховано для (таблиці II та III) відрізнений від спектра, одержаС79Н130Ν14О19, 1597,0. Знайдено: m/z 1580,3 ного для аутентичного зразка кахалаліду F. Найбі+ + + [М+Н] , 1602,2 [M+Na] , 1618,2 [М+К] . льша відмінність полягає у тому, що одержана Приклад 13 синтетичним шляхом сполука має дві конформації, 5-MeHex-D-Val-Thr(tBu)-Val-D-Val-D-Proзумовлені цис-транс рівновагою між L-Val-D-Pro Orn(Boc)-D-allo-Ile-D-allo-Thr(Val-Z-Dhb-Phe-H)-Dзалишками, не спостерігається ні в природному allo-Ile-D-Val-OH продукті, ні в ізомері, одержаному у прикладі 7. Alloc групу з пептидил-смоли (Приклад 12) ви 29 76949 30 Таблиця II (Основний, транс-ізомер) Залишок (Z)-Dhb D-allo-Ile 1 L-Phe D-allo-Thr L-Val 3 L-Orn N-H 9,67 (c) 8,80 (д) 8,78 (д, J=5,5Гц) 8,58 (д, J=9,0Гц) 7,97 (д, J=8,0Гц) 7,77 (д, J=8,5Гц) Н 4,31 4,43 4,53 4,34 4,47 Η 6,33 (кв.) 1,73 2,93 (м) 4,95 (м) 1,94 1,46 (2Н) Інші характеристики 1,27 (д, J=7,0Гц, -СН3) 1,32, 0,77 ( -СН2, -СН3, -СН3) 7,20 (1Η Аr, м) 7,28 (4Н Аr, м) 1,07 (д, J=6,5Гц, -СН3) 0,84 (2 -СН3) 1,66 ( -СН2), 2,72 (bs, -СН2), 7,66 ( -ΝΗ3+) D-allo-Ile 2 D-Val 5 L-Thr D-Val 2 D-Val 4 L-Val 1 7,87 (д, J=8,5Гц) 7,90 7,90 (д) 7,63 (д, J=8,5Гц) 7,56 (д, J=9,0Гц) 6,75 (д) 4,37 4,22 4,24 4,45 4,34 3,86 D-Pro 4,30 1,68 0,75 ( -СН3 або d-CH3 та -СН3) 1,95 0,85 (2 -СН3) 4,02 4,98 (ОН), 1,02 ( -СН3) 2,18 0,77 ( -СН3), 0,62 ( -СН3) 2,02 0,84 ( -СН3), 0,79 ( -СН3), 1,39 0,62 (2 -СН3) 2,03, 1,81, 1,73 ( -СН2, -СН2), 3,73 (1Н, м, 5-СН2), 3,52 (1H, м, СН2) 5-MeHex 2,08 (1Н) 1,48 (b-СН2, -CH), 1,11 ( -СН2), 0,82 (2 -СН3) 2,15 (1Н) Таблиця III (менший, цис-ізомер) Залишок N-H (Ζ)-Dhb 9,63 (c) D-allo-Ile 1 8,76 (д) L-Phe D-allo-Thr L-Val 3 L-Orn D-allo-Ile 2 D-Val 5 L-Thr D-Val 2 D-Val 4 L-Val 1 D-Pro 8,78 (д, J=5,5Гц) 8,58 (д, J=9,0Гц) 8,06 (д, J=8,5Гц) 8,37 (д, J=9,0Гц) 8,09 (д, J=9,0Гц) 7,90 7,88 (d) 7,63 (д, J=8,5Гц) 7,49(д, J=9,0Гц) 6,72 (d) 5-MeHex Н 4,30 4,43 4,53 4,11 4,62 4,42 4,22 4,23 4,45 4,34 3,84 4,93 2,08 (1H) 2,15 (1H) Η 6,33 (кв.) 1,71 Інші характеристики 1,28 (д, J=6,5Гц, -СН3) 1,33, 0,76 ( -СН2, -СН3, -СН3) 2,93 (м) 7,20 (1Н Аr, м) 7,28 (4Н Аr, м) 4,95 (м) 1,00 ( -СН3) 1,81 0,71 ( -СН3), 0,60 ( -СН3) 1,52 (2Н) 1,64 ( -СН2), 2,78 (bs, -СН2), 7,66 ( -ΝΗ3+) 1,64 0,77 ( -СН3 або d-CH3 та -СН3) 1,95 0,85 (2 -СН3) 3,99 4,93 (ОН), 1,02 ( -СН3) 2,18 0,77 ( -СН3), 0,62 ( -СН3) 1,94 0,79 ( -СН3), 0,73 ( -СН3) 1,38 0,62 (2 -СН3) 2,06, 1,89, 1,75 ( -CH2, -CH2), 3,3 (м, -CH2) 1,48 ( -CH2, -CH), 1,11 ( -СН2), 0,82 (2 -СН3) Приклад 15біс 5-МеНех-D-VаI-Тhr-D-VаI-VаI-D-Рrо-Оrn-D-allоІlе-цикло(D-аIIо-Тhr-D-allо-Ile-D-Val-Phe-Z-Dhb-Val) Одержують як побічний продукт під час одержання (в процесі рацемізації на стадії циклізації) прикладу 15. Продукт охарактеризований за допомогою ВЕРХ (tR 17,6хв, Умова В) та MALDI-TOFMS, Розраховано для С75Н124N14O16, 1477,9. Знайдено: m/z 1479,3 [М+Н]+, 1501,2 [M+Na]+, 1517,2 [М+К]+. Приклад 16 5-MeHex-D-Val-Thr-D-Val-Val-D-Pro-Orn-D-alloIle-(D-aIIo-Thr-D-allo-Ile-D-Val-Phe-Z-Phb-Val) (у результаті включення дипептиду) Експериментальні процедури здійснюють за способом, описаним у прикладах 8-14, за єдиним винятком в тому, що у прикладі 14 Fmoc-Val-OH включають у D-Pro-пептидил-смолу, а потім після видалення Fmoc групи, включають Fmoc-P-Val-ОН. Кінцевий вихід, розрахований за допомогою ААА, становить 0,106ммоль/г (79% повний вихід), вихід відщеплення становить 78%, і одержують 3,4мг вказаної у заголовку сполуки, яка являє собою 10% повний вихід зі стадій циклізації, видалення захисних груп та очищення. Очищений продукт ідентичний продукту, одержаному у прикладі 15. Hamann et al. Кахалалід В [5-MeHex-Tyrцикло(D-Ser-Phe-D-Leu-Pro-Thr-Gly)] Приклад 17 H-ThritBu)-O-TrtCl-CM-смолa Cl-TrtCl-смолу (0,5г, 1,35ммоль/г) вміщують у 10мл поліпропіленовий шприц, забезпечений поліетиленовим фільтром-диском. Потім смолу промивають СН2Сl2 (5x0,5хв), і додають розчин FmocThr(tBu)-OH (54мг, 0,135ммоль, 0,2еквів.) та DIEA (235мл, 1,35ммоль, 2еквів.) у СН2Сl2 (1,25мл), і 31 76949 32 одержану суміш перемішують протягом 1 години. 877,5. Знайдено: m/z 878,7 [М+Н]+, 900,6 [M+Na]+, Реакцію зупиняють, додаючи МеОН (400мл), після 916,5 [М+К]+. ААА: Gly 1,02 (1), Thr 0,95 (1), Phe перемішування протягом 15хв. Рmос-Тhr(tBu)-О0,99 (1), Ser 1,00 (1), Pro 1,20 (1), Leu 1,00 (1), Tyr ТrtСl-смолу піддають наступним промив0,87 (1). кам/обробці: СН2Сl2 (3x0,5хв), ДМФ (3x0,5хв), піпеПриклад 20 ридин-CH2Cl2-DMF (1:9,5:9,5, 1x10хв), піперидин5-МеНех-D-VаI-Тhr-VаI-Р-VаI-D-Рrо-Оrn-D-allоДМФ (1:4, 1x15хв), ДМФ (5x0,5хв), ізопропанол Іlе-цикло(D-аIIo-Тhr-D-аIIо-Ile-D-Val-Phe-Etg-Van (2x1хв), ДМФ (5x0,5хв), МеОН (2x1хв) і сушать у Експериментальні процедури здійснюють за вакуумі. Вихід, розрахований за допомогою ААА, способом, описаним у прикладах 1-4 та 6-7, вихостановить 0,15ммоль/м. дячи з 200мг смоли, за винятком того, що у прикПриклад 18 ладі 4, Fmoc-Thr-ОН замінюють на Fmoc-Etg-OH. 5-MeHex-Tyr-D-Ser(Gly-H)-Phe-D-Leu-Pro-ThrПродукт характеризують за допомогою ВЕРХ (tR OH 16,8хв. Умова В) та MALDI-TOF-MS, Розраховано Fmoc-Pro-OH (178мг, 0,53ммоль, 7еквів.), для С75H126N14O16, 1479,0. Знайдено: m/z 1480,2 Fmoc-D-Leu-OH (187мг, 0,53ммоль, 7еквів.), Fmoc[М+Н]+, 1502,2 [M+Na]+, 1518,0 [М+К]+. Phe-OH (204мг, 0,53ммоль, 7еквів.), Fmoc-D-SerПриклад 20b OH (вільна гідроксильна група) (173мг, 0,53ммоль, 5-МеНех-D-VаI-Тhr-VаI-D-VаI-D-Рrо-Оrn-D-allо7еквів.), Fmoc-Tyr(tBu)-OH (243мг, 0,53ммоль, Іlе-цикло(D-allо-Тhr-D-allо-Ile-D-Val-Phe-D-Etg-Val) 7еквів.), та 5-МеНех-ОН (69мг, 0,53ммоль, 7еквів.) Експериментальні процедури здійснюють за додають послідовно до одержаної вище Нспособом, описаним у прикладах 1-4 та 6-7, вихоТhr(tBu)-О-ТrtСl-смолі, використовуючи DIPCDI дячи з 200мг смоли, за винятком того, що у прик(82мкл, 0,53ммоль, 7еквів.) та HOBt (81мг, ладі 4, Fmoc-Thr-ОН замінюють на Fmoc-P-Etg-OH. 0,53ммоль, 7еквів.) у ДМФ (1,25 л). У всіх випадПродукт характеризують за допомогою ВЕРХ (tR ках, крім D-Ser, після 90 хвилин здійснення реакції 17,0хв. Умова В) та MALDI-TOF-MS, Розраховано сполучення, нінгідриновий тест був негативним. для С75Η126Ν14Ο16 1479,0. Знайдено: m/z 1501,0 Fmoc-D-Ser-OH (173мг, 0,53ммоль, 7еквів.) знову [M+Na]+, 1517,9 [M+К]+. поєднують з HATU (201мг, 0,53ммоль, 7еквів.) у Приклад 20с присутності DIEA (184мкл, 1,06ммоль, 14еквів.) у 5-МеНех-D-VаI-Тhr-VаI-D-VаI-D-Рrо-Оrn-D-allоДМФ протягом 90хв. Видалення Fmoc групи та Іlе-цикло(D-аIIо-Тhr-D-allо-Ile-D-Val-Phe-D-Thr-Val) промивки здійснюють за способом, розкритим у Експериментальні процедури здійснюють за розділі загальні процедури. Здійснюють реакцію способом, описаним у прикладах 1-4 та 6-7, вихосполучення Boc-Gly-OH (119мг, 0,68ммоль, дячи з 200мг смоли, за винятком того, що у прик9еквів.) з DIPCDI (105мкл, 0,68ммоль, 9еквів.) у ладі 4, Fmoc-Thr(tBu)-OH замінюють на Fmoc-Dприсутності DMAP (8,3мг, 68мкмоль, 0,9еквів.) Thr(tBu)-OH. Продукт характеризують за допомопротягом 2,5 години. Реакцію сполучення повтогою ВЕРХ (tR 19,9хв. Умова В) та MALDI-TOF-MS, рюють зі свіжими реагентами протягом 1,5 години. Розраховано для С75H126N14O17, 1494,9. Знайдено: Кінцевий вихід становить 0,10ммоль/г, і відповідає 1517,4 [M+Na]+, 1533,4 [M+К]+. 77% виходу синтезу. Незахищений пептид відщеПриклад 20d плюють від смоли (525мг, 54ммоль) використову5-МеНех-D-VаI-Тhr-VаI-D-VаI-D-Рro-Оrn-D-аIIоючи TFA-H2O (92:8) протягом 2 годин. Об'єднані ІIе-цикло(D-аIIо-Тhr-D-allо-Ile-D-Val-Phe-D-allo-Thrфільтрати випаровують досуху при зниженому Val) тиску, додають Н2О (5мл) і розчин ліофілізують, Експериментальні процедури здійснюють за одержуючи 43,0мг (48,0мкмоль, 89% вихід) вказаспособом, описаним у прикладах 1-4 та 6-7, вихоної у заголовку сполуки зі ступенем чистоти >85% дячи з 200мг смоли, за винятком того, що у прикза даними ВЕРХ (Умова A, tR 18,5хв). ESMS, розладі 4, Fmoc-Thr(tBu)-OH замінюють на Fmoc-Pраховано для С45Н65N7О12 895,5. Знайдено: m/z allo-Thr-OH. Продукт характеризують за допомо896,6 [М+Н]+. гою ВЕРХ (tR 18,0хв. Умова В) та MALDI-TOF-MS, Приклад 19 Розраховано для С15H126N14O17, 1494,9. Знайдено: Кахалалід В [5-MeHex-Tyr-цикло(D-Ser-Phe-D1496.6 [М+Н]+, 1518,6 [M+Na]+, 1534,6 [М+К]+. Leu-Pro-Thr-Glv] Приклад 20е Незахищений пептид (приклад 18) (40,5мг, 5-МеНех-D-VаI-Тhr-VаI-D-VаI-D-Рrо-Оrn-D-allо45мкмоль) розчиняють у ДМФ (48мл), і додають Іlе-цикло(D-allо-Тhr-D-аIIо-Ile-D-Val-Phe-D-Dhe-Val) РуВОР (70мг, 0,135ммоль, 3еквів.) та DIEA (47мл, Експериментальні процедури здійснюють за 0,271ммоль, 6еквів.). Суміш перемішують протяспособом, описаним у прикладах 1-7, виходячи з гом 2 годин, і потім розчинник видаляють, випаро200мг смоли, за винятком того, що у прикладі 4, вуючи при зниженому тиску, додають Н2О (5мл), і Fmoc-Thr-OH замінюють на Fmoc-D/L-(b-OH)Pheрозчин ліофілізують. Сирий продукт очищають за OH. Продукт характеризують за допомогою ВЕРХ допомогою хроматографії середнього тиску (Vydac (tR 22,2хв. Умова В) та MALBI-TOF-MS. РозраховаС18 15-20мкм, 300А, 240x24мм), лінійний градієнт но для С80Н126N14O16, 1533,95. Знайдено: 1540,3 + + + від 20% до 60% ацетонітрилу (+0,05% TFA) у воді [М+Н] , 1562,4 [M+Na] , 1578,3 [М+К] . (+0,05% TFA) протягом 5 годин (300мл кожного Приклад 21 розчинника), 120мл/година, детектування на 5-МеНех-D-VаI-Тhr-VаI-D-VаI-D-Рrо-Оrn-D-allо220нм, одержуючи вказану у заголовку сполуку Іlе-цикло-(D-Dра-Р-аIIо-ІIе-D-Val-Phe-Z-Dhb-Val) (8,7мг, 9,9мкмоль, 22% вихід). Продукт характериЕкспериментальні процедури здійснюють за зують за допомогою ВЕРХ (Умова A, tR 21,6хв) та способом, описаним у прикладах 1-7, виходячи з MALDI-TOF-MS, розраховано для С45Н63N7О11, 200мг смоли, за винятком того, що у прикладі 2, 33 76949 34 Fmoc-D-aIIo-Thr-ОН замінюють на Fmoc-DTOF-MS. Розраховано для С74Н122N14O16, 1463,9. Dpa(Alloc)-OH і перед включенням Alloc-Val-OH, Знайдено: m/z 1487,3 [M+Na]+, 1503,3 [М+К]+. який включають як інші захищені амінокислоти, Приклад 25 АIIoс групу з Dра видаляють як указано вище. 4-МеРеn-D-VаI-Тhr-VаI-D-VаI-D-Рrо-Оrn-D-аIIоПродукт характеризують за допомогою ВЕРХ та ІIе-цикло(D-allо-Тhr-D-allо-Ile-D-Val-Phe-Z-Phb-Van ESMS. Розраховано для С74Н123N15О15, 1461,9. Експериментальні процедури здійснюють за Знайдено: m/z 1463,3 [М+Н]+. способом, описаним у прикладах 1-7, виходячи з Приклад 22 200мг смоли, за винятком того, що у прикладі 3, 5Вut-D-VаI-Тhr-VаI-D-VаI-D-Рrо-Оrn-D-allо-ІlеМеНех, замінюють на 4-МеРеn-ОН. Продукт харацикло(B-аIIо-Тhr-D-allо-Іlе-D-Val-Phe-Z-Dhb-Val). ктеризують за допомогою ВЕРХ, (tR 16,5хв. Умова Експериментальні процедури здійснюють за В) та MALDI-TOF-MS. Розраховано для способом, описаним у прикладах 1-7, виходячи з С74Н122N14О1б, 1463,9. Знайдено: m/z 1487,7 200мг смоли, за винятком того, що у прикладі 3, 5[M+Na]+, 1503,6 [M+К]+. МеНех, замінюють на But-OH. Продукт характериПриклад 25біс зують за допомогою ВЕРХ, (tR 14,7хв. Умова В) та 4-МеРеn-D-VаI-Тhr-VаI-D-VаI-D-Рrо-Оrn-D-allоMALDI-TOF-MS. Розраховано для С72Н118N14O16, Іlе-цикло(D-allо-Тhr-D-allо-Ile-Val-Phe-Z-Dhb-Val) 1435,9. Знайдено: 1459,6 [M+Na]+, 1475,6 [М+К]+. Одержують як побічний продукт під час одерПриклад 22біс жання (під час рацемізації на стадії циклізації) But-D-Val-Thr-Val-D-Val-D-Pro-Orn-D-allo-Ileпродукту прикладу 25. Продукт характеризують за цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb-Val) допомогою ВЕРХ, (tR 17,8хв. Умова В) та MALDIОдержують як побічний продукт під час одерTOF-MS. Розраховано С74Н122N14О16, 1463,9. жання (під час рацемізації на стадії циклізації) Знайдено: m/z 1487,8 [M+Na]+, 1503,6 [М+К]+. продукту прикладу 22. Продукт характеризують за Приклад 26 допомогою ВЕРХ, (tR 16,0хв. Умова В) та MALDIHep-D-Val-Thr-Val-D-Val-D-Pro-Orn-D-allo-IleTOF-MS. Розраховано для С72Н118N14O16, 1435,9. цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-VаI) Знайдено: 1459,5 [M+Na]+, 1475,5 [М+К]+. Експериментальні процедури здійснюють за Приклад 23 способом, описаним у прикладах 1-7, виходячи з 3-MeBut-D-Val-Thr-Val-D-Val-D-Pro-Orn-D-allo200мг смоли, за винятком того, що у прикладі 3, 5Ile-цикло (D-aIIo-Thr-D-aIIo-Ile-D-Val-Phe-Z-Dhb-Val) МеНех, замінюють на Нер-ОН. Продукт характериЕкспериментальні процедури здійснюють за зують за допомогою ВЕРХ, (tR 17,5хв. Умова В) та способом, описаним у прикладах 1-7, виходячи з MALDI-TOF-MS. Розраховано для С75Н124N14O16, 200мг смоли, за винятком того, що у прикладі 3, 51477,9. Знайдено: m/z 1501,4 [M+Na]+, 1517,5 + МеНех, замінюють на 3-MeBut-OH. Продукт харак[М+К] . теризують за допомогою ВЕРХ, (tR 15,9хв. Умова Приклад 26біс В) та MALDI-TOF-MS. Розраховано для Нер-D-VаI-Тhr-VаI-D-VаI-D-Рrо-Оrn-D-allо-ІlеС73Н120N14O16, 1449,9. Знайдено: 1473,2 [M+Na]+, цикло(D-allо-Тhr-D-allо-Іlе-D-Val-Phe-Z-Dhb-Val) 1489,2 [М+К]+. Одержують як побічний продукт під час одерПриклад 23 біс жання (під час рацемізації на стадії циклізації) 3-MeBut-D-Val-Thr-Val-D-Val-D-Pro-Orn-D-alloпродукту прикладу 26. Продукт характеризують за Ile-цикло-(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb-Val) допомогою ВЕРХ, (tR 18,9хв. Умова В) та MALDIОдержують як побічний продукт під час одерTOF-MS. Розраховано для С75H124N14О1б, 1477,9. жання (під час рацемізації на стадії циклізації) Знайдено: m/z 1501,6 [M+Na]+, 1517,7 [М+К]+. продукту прикладу 23. Продукт характеризують за Приклад 27 допомогою ВЕРХ, (tR 17,0хв. Умова В) та ESMS і РаI-D-VаI-Тhr-VаI-D-VаI-D-Рrо-Оrn-D-allо-Іlерозраховано для С73Н120N14О16, 1449,9. Знайдено: цикло(D-allо-Тhr-D-allо-Іlе-D-Val-Phe-Z-Dhb-Val) 1473,3 [M+Na]+, 1489,4 [M+К]+. Експериментальні процедури здійснюють за Приклад 24 способом, описаним у прикладах 1-7, виходячи з 3,3-DіМеВut-D-VаI-Тhr-VаI-D-VаI-D-Рrо-Оrn-D200мг смоли, за винятком того, що у прикладі 3, 5аIIо-ІIе-цикло-(D-аIIо-Тhr-D-aIIo-Ile-D-Val-Phe-ZМеНех, замінюють на Pal-ОН. Продукт характериDhb-Val) зують за допомогою ВЕРХ, (tR 22,1хв. Умова В) та Експериментальні процедури здійснюють за MALDI-TOF-MS. Розраховано для С84Н142N14O16, способом, описаним у прикладах 1-7, виходячи з 1603,1. Знайдено: m/z 1626,9 [M+Na]+, 1642,9 200мг смоли, за винятком того, що у прикладі 3, 5[М+К]+. МеНех, замінюють на 3,3-DіМеВut-OH. Продукт Приклад 27біс характеризують за допомогою ВЕРХ, (tR 16,3хв. Pal-D-Val-Thr-Val-P-Val-D-Pro-Orn-D-allo-IleУмова В) та MALDI-TOF-MS. Розраховано для циклo(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-VаI) С74Н122N14O16, 1463,9. Знайдено: m/z 1487,4 Одержують як побічний продукт під час одер[M+Na]+, 1503,6 [М+К]+. жання (під час рацемізації на стадії циклізації) Приклад 24біс продукту прикладу 27. Продукт характеризують за 3,3-DіМеВut-D-Vаl-Тhr-VаI-D-VаI-D-Рrо-Оrn-Dдопомогою ВЕРХ, (tR 23,2хв. Умова В) та MALDIallо-Іlе-цикло(D-allо-Тhr-D-allo-Ile-D-Val-Phe-Z-DhbTOF-MS. Розраховано для С84Н142N14O16, 1603,1. Val) Знайдено: m/z 1626,8 [M+NaJ+, 1642,8 [М+К]+. Одержують як побічний продукт під час одерПриклад 27а жання (під час рацемізації на стадії циклізації) 4-DіМеВut-D-Val-Thr-Val-D-Val-D-Pro-Orn-Dпродукту прикладу 24. Продукт характеризують за allo-Ile-цикло(D-allo-Thr-D-allo-Ile-D-Val-Dhe-Z-Dhbдопомогою ВЕРХ, (tR 17,6хв. Умова В) та MALDIVal) 35 76949 36 Експериментальні процедури здійснюють за способом, описаним у прикладах 1-7, виходячи з способом, описаним у прикладах 1-7, виходячи з 200мг смоли, за винятком того, що у прикладі 3, 5200мг смоли, за винятком того, що у прикладі 3, 5МеНех, замінюють на AcButBut-OB. Продукт хараМеНех, замінюють на 4-DiMeABut-OH. Продукт ктеризують за допомогою ВЕРХ, (tR 14,1хв Умова характеризують за допомогою ВЕРХ, (tR 12,0хв. В) та MALDI-TOF-MS. Розраховано для Умова В) та MALDI-TOF-MS. Розраховано для С78Η126Ν14Ο20, 1578,9. Знайдено: m/z 1581,2 С74Н123Ν15О16, 1477,9. Знайдено: m/z 1478,6 [М+Н]+, 1602,2 [M+Na]+, 1618,2 [М+К]+. + + + [М+Н] , 1500,6 [M+Na] , 1516,6 [М+К] . Приклад 27h Приклад 27b IBut-D-allo-Ile-D-Val-Thr-Val-D-Val-D-Pro-Orn-D2-Неао-D-VаI-Тhr-VаI-D-VаI-D-Рrо-Оrn-D-allоallo-Ile-цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-DhbІlе-цикло(D-аIIо-Тhr-D-аIIо-ІIе-D-Val-Dhe-Z-Dhb-Val) Val) Експериментальні процедури здійснюють за Експериментальні процедури здійснюють за способом, описаним у прикладах 1-7, виходячи з способом, описаним у прикладах 1-7, виходячи з 200мг смоли, за винятком того, що у прикладі 3, 5200мг смоли, за винятком того, що у прикладі 3, 5МеНех, замінюють на 2-Hedo-OH. Продукт харакМеНех, замінюють на Fmoc-D-allo-Ile-OH. Продукт теризують за допомогою ВЕРХ, (tR 15,8хв Умова В) характеризують за допомогою ВЕРХ, (tR 15,3хв та MALDI-TOF-MS. Розраховано для Умова В) та MALDI-TOF-MS. Розраховано для С74H118N14O16, 1458,9. Знайдено: m/z 1460,0 С78Н129N15O17, 1548,0. Знайдено: m/z 1548,8 [М+Н]+, 1482,0 [M+Na]+, 1497,9[M+К]+. [М+Н]+, 1570,8 [M+Na]+, 1586,8 [М+К]+. Приклад 27с Приклад 27і 4-АсВut-D-VаI-Тhr-VаI-D-VаI-D-Рrо-Оrn-D-allоLit-D-Val-Thr-Val-D-Val-D-Pro-Orn-D-allo-IleІlе-цикло(D-аIIо-Тhr-D-allо-Ile-D-Val-Phe-Z-Dhb-Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-VаI) Експериментальні процедури здійснюють за Експериментальні процедури здійснюють за способом, описаним у прикладах 1-7, виходячи з способом, описаним у прикладах 1-7, виходячи з 200мг смоли, за винятком того, що у прикладі 3, 5200мг смоли, за винятком того, що у прикладі 3, 5МеНех, замінюють на 4-AcBut-OH. Продукт харакМеНех, замінюють на Lit-OH. Продукт характеритеризують за допомогою ВЕРХ, (tR 18,2хв Умова В) зують за допомогою ВЕРХ, (tR 13,1хв Умова Н) та та MALDI-TOF-MS. Розраховано для MALDI-TOF-MS. Розраховано для С92Н150N14O17, С74Н120N14О18, 1492,9. Знайдено: m/z 1493,7 1,7231. Знайдено: m/z 1724,6 [М+Н]+, 1746,6 [М+Н]+, 1515,8 [M+Na]+, 1531,7 [М+К]+. [M+Na]+, 1761,5 [М+К]+. Приклад 27d Приклад 27і 4-НОВut-D-VаI-Тhr-VаI-D-VаI-D-Рrо-Оrn-D-аllоTFA-Lit-D-Val-Thr-Val-D-Val-D-Pro-Orn-D-aIIoІlе-цикло(D-allо-Тhr-D-аIIо-Ile-D-Val-Dhe-Z-Dhb-Val) Ile-цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) Експериментальні процедури здійснюють за Одержують як побічний продукт · під час одеспособом, описаним у прикладах 1-7, виходячи з ржання (у час трифторацетилування на стадії цик200мг смоли, за винятком того, що у прикладі 3, 5лізації) продукту прикладу 27і. Продукт характериМеНех, замінюють на 4-HOBut-OH. Продукт харакзують за допомогою ВЕРХ (tR 17,1хв. Умова Н) та теризують за допомогою ВЕРХ, (tR 16,6хв Умова В) MALDI-TOF-MS. Розраховано для С94Н159F3N14O18, та MALDI-TOF-MS. Розраховано для 1819,1. Знайдено: m/z 1820,6 [М+Н]+, 1842,6 С72Н118Ν14Ο17, 1450,9. Знайдено: m/z 1451,6 [M+Na]+, 1858,6 [М+К]+. + + + [М+Н] , 1473,6 [M+Na] , 1489,6 [М+К] . Приклад 27k Приклад 27е TIco-D-Val-Thr-Val-D-Val-D-Pro-Orn-D-allo-IleAc-D-Val-Thr-Val-D-Val-D-Pro-Orn-D-allo-Ileциклo(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-VаI) циклo(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-VаI) Експериментальні процедури здійснюють за Експериментальні процедури здійснюють за способом, описаним у прикладах 1-7, виходячи з способом, описаним у прикладах 1-7, виходячи з 200мг смоли, за винятком того, що у прикладі 3, 5200мг смоли, за винятком того, що у прикладі 3, 5МеНех, замінюють на ТІсо-ОН. Продукт характеМеНех, замінюють на НОАс. Продукт характериризують за допомогою ВЕРХ, (tR 16,8хв Умова Н) зують за допомогою ВЕРХ, (tR 17,0хв Умова В) та та ES-MS. Розраховано для С92Н158N14O16, 1715,2. MALDI-TOF-MS. Розраховано для С70Н114Ν14Ο16, Знайдено: m/z 858,2 [М+Н]72, 1171,8 [М+Н]+. + 1406,9. Знайдено: m/z 1407,8 [М+Н] , 1429,8 Приклад 28 [M+Na]+. H-D-Val-Thr-Val-D-Val-D-Pro-Orn-D-allo-IleПриклад 27f циклo(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) TFA-D-Val-Thr-Val-D-Val-D-Pro-Orn-D-allo-IleЕкспериментальні процедури здійснюють за цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) способом, описаним у прикладах 1-7, виходячи з Одержують як побічний продукт під час одер200мг смоли, за винятком того, що у прикладі 3 5жання (у час трифторацетилування на стадії цикМеНех не включений. Продукт характеризують за лізації) продукту прикладу 27е. Продукт характедопомогою ВЕРХ, (tR 11,6хв. Умова В) та MALDTризують за допомогою ВЕРХ, (tR 14,7хв. Умова В) TOF-MS. Розраховано для С68Н112N14O15, 1364,8. + + та MALDI-TOF-MS. Розраховано для Знайдено: m/z 1388,3 [M+Na] , 1404,3 [М+К] . С70Н111F3N14O16, 1460,8. Знайдено: m/z 1462,0 Приклад 28біс [М+Н]+, 1484,1 [M+Na]+, 1500,0[M+К]+. Н-D-VаI-Тhr-VаI-D-VаI-D-Рrо-Оrn-D-allо-llеПриклад 27g цикло(D-allо-Тhr-D-allо-llе-VаI-Phe-Z-Dhb-Val) AcButBut-D-Val-Thr-Val-D-Val-D-Pro-Orn-D-alloОдержують як побічний продукт під час одерIle-цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) жання (у процесі рацемізації на стадії циклізації) Експериментальні процедури здійснюють за продукту прикладу 28. Продукт характеризують за 37 76949 38 допомогою ВЕРХ (tR 12,9хв. Умова В) та MALDIС60Н98N10O13, 1166,7. Знайдено: m/z 1190,9 TOF-MS. Розраховано для С68Н112N14O15, 1364,8. [M+Na]+, 1206,9 [М+К]+. + + Знайдено: m/z 1388,4 [M+Na] , 1404,4 [М+К] . Приклад 32 Приклад 29 5-MeHex-D-Val-Thr-D-aIIo-Ile-цикло(D-allo-Thr5-МеНех-D-VаI-Тhr-VаI-D-VаI-D-Рrо-D-аIIо-ІIеD-allo-Ile-D-Val-Phe-Z-Dhb-Val) цикло(D-аIIо-Тhr-D-аIIо-ІIе-D-Val-Phe-Z-Dhb-Val) Експериментальні процедури здійснюють за Експериментальні процедури практично відпоспособом, описаним у прикладах 1-7, але відповівідно до прикладів 1-7, але відповідно до схеми 2. дно до схеми 2. Синтез починають, виходячи з 200мг смоли, і Fmoc-Orn(Boc)-OH, Fmoc-D-Pro-OH, Fmoc-D-ValOH, і Fmoc-Val-OH не включають. Продукт характеризують за допомогою ВЕРХ, (tR 24,6хв Умова А) та MALDI-TOF-MS. Розраховано для C55H89N9O12, 1067,7. Знайдено: m/z 1068,7 [М+Н]+, 1090,6 [M+Na]+, 1106,5 [М+К]+. Приклад 33 5-MeHex-D-Val-D-aIIo-Ile-цикло(D-aIIo-Thr-Dallo-Ile-D-Val-Phe-Z-Dhb-Val) Експериментальні процедури здійснюють за способом, описаним у прикладах 1-7, але відповідно до схеми 2. Синтез починають, виходячи з 200мг смоли, і Fmoc-Orn(Boc)-OH, Fmoc-D-Pro-OH, Fmoc-D-Val-OH Fmoc-Val-OH та Fmoc-Thr(tBu)-OH не включають. Продукт характеризують за допомогою ВЕРХ, (tR 19,8хв, Умова В) та MALDI-TOFMS. Розраховано для C51H82N8O10, 966,6. Найдено: m/z 990,7 [M+Na]+, 1007,2 [М+К]+. Приклад 34 5-МеНех-D-allо-Іlе-цикло(D-аIIо-Тhr-D-аIIо-ІIеD-VаI-Рhе-Z-Dhb-VаI) Синтез починають, виходячи з 200 мг смоли, і Експериментальні процедури здійснюють за Fmoc-Orn(Boc)-OH не включають. Продукт харакспособом, описаним у прикладах 1-7, але відповітеризують за допомогою ВЕРХ (tR 23,9хв. Умова В) дно до схеми 2. Синтез починають, виходячи з та MALDI-TOF-MS. Розраховано для 200мг смоли, і Fmoc-Orn(Boc)-OH, Fmoc-D-Pro-OH, С70Н114N12О15, 1362,9. Знайдено: m/z 1386,4 Fmoc-D-Val-OH, Fmoc-Val-OH, Fmoc-Thr(tBu)-OH, і [M+Na]+, 1402,4 [М+К]+. Fmoc-D-Val-OH не включають. Продукт характериПриклад 29біс зують за допомогою ВЕРХ, (tR 22,0хв, Умова В) та 5-МеНех-D-VаI-Тhr-VаI-D-VаI-D-Рrо-D-аIIо-ІIеMALDI-TOF-MS. Розраховано для C46H73N7O9, цикло(D-аIIо-Тhr-D-аIIо-ІIе-Val-Phe-Z-Dhb-Val) 867,6. Знайдено: m/z 890,6 [M+Na]+, 906,6 [М+К]+. Одержують як побічний продукт під час одерПриклад 35 жання (у процесі рацемізації на стадії циклізації) 5-MeHex-цикло(D-allo-Thr-D-aIIo-Ile-D-Val-Pheпродукту прикладу 29. Продукт характеризують за Z-Dhb-Val) допомогою ВЕРХ та MALDI-TOF-MS. Експериментальні процедури здійснюють за Приклад 30 способом, описаним у прикладах 1-7, але відпові5-МеНех-D-VаI-Тhr-VаI-D-VаI-D-аIIо-ІIедно до схеми 2. Синтез починають, виходячи з цикло(D-аIIо-Тhr-D-аIIо-ІIе-D-VаI-Dhe-Z-Dhb-Val) 200мг смоли, і Fmoc-D-aIIo-Ile-OH, Fmoc-Orn(Boc)Експериментальні процедури здійснюють за OH, Fmoc-D-Pro-OH, Fmoc-D-Val-OH, Fmoc-Valспособом, описаним у прикладах 1-7, але відповіOH, Fmoc-Thr(tBu)-OH, і Fmoc-D-Val-OH не вклюдно до схеми 2. Синтез починають, виходячи з чають. Продукт характеризують за допомогою 200мг смоли, і Fmoc-Orn(Boc)-OH та Fmoc-P-ProВЕРХ, (tR 17,1хв Умова В) та ESMS. Розраховано OH не включають. Продукт характеризують за додля С40Н62N6О8, 754,5. Знайдено: m/z 755,7 [М+Н]+, помогою ВЕРХ, (tR 20,3хв Умова В) та MALDI-TOF777,7[M+Na]+, 793,7[M+К]+. MS. Розраховано для С65H107N11О14, 1265,8. ЗнайБіоактивність дено: m/z 1288,5 [M+Na]+, 1304,5 [М+К]+. Біоактивність сполук згідно з винаходом проПриклад 31 демонстрована на результатах наступних таб5-MeHex-D-Val-Thr-Val-D-allo-Ile-цикло(D-alloлиць, причому результати ці одержані за способом Thr-D-allo-Ile-D-Val-Phe-Z-Dhb-Val) [Berjeron et al., Biochem and Bioph Res. Comm., Експериментальні процедури здійснюють 1984, 121, 3, 848-854]. Клітинні лінії: Р388, мишача практично за способом, описаним у прикладах 1-7, лімфома; А549, карцинома легень людини; НТ-29, але відповідно до схеми 2. Синтез починають, викарцинома ободової кишки людини; MEL-28, меходячи з 200мг смоли, і Fmoc-Orn(Boc)-OH і Fmocланома людини; PU-145, карцинома простати люP-Pro-OH і Fmoc-P-Val-OH не включають. Продукт дини. характеризують за допомогою ВЕРХ, (t 20,0хв, R Умова В) та MALDI-TOF-MS. Розраховано для 39 76949 40 Таблиця Сполуки, споріднені кахалаліду F Сполука Цикл цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb27j Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb27і Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb27 Val) цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb27bis Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb27g Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb27h Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-D-Phe20е Val)-D-Phe: a, b-didehydro-phenylalanine цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Thr20с Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb27с Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-L-Etg20 Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-D-Etg20b Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb27а Val) (as Scheuer) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb15 Val) цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb15bis Val) цикло(D-allo-Thr-D-allo-Ile-Val-D-Phe-Z-Dhb26 Val) цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb26bis Val) (Rinehart) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb7 Val) цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb7bis Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb24 Val) цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb24bis Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb25 Val) цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb25bis Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb27f Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb27b Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb27d Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb23 Val) цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb23b Val) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-Dhb22 Val) цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-Dhb22b Val) Ланцюг MB кінцева група: TFA-Lit 1820 кінцева група: літохіліл (Lit) 1724 кінцева група: пальмітоїл Palm 1604 кінцева група: пальмітоїл Palm 1604 кінцева група: 4-(4-ацетоксибутаноїлоксибутирил (AcButBut-) IBut-D-allo-Ile-D-Val-L-Thr-L-Val-D-Val-DPro-L-Orn-D-allo-Ile 5-MeHex-D-Val-L-Thr-L-Val-D-Val-Pro-L-OrnD-allo-Ile 5-MeHex-D-Val-L-Thr-L-Val-D-Val-D-Pro-LOrn-D-allo-Ile 1579 1548 1539 1495 кінцева група: 4-ацетоксибутирил (4-AcBut) 1493 5-MeHex-D-Val-L-Thr-L-Val-D-Val-D-Pro-LOrn-D-allo-Ile 5-MeHex-D-Val-L-Thr-L-Val-D-Val-D-Pro-LOrn-D-allo-Ile кінцева група: Ν,Ν-диметил-4-амінобутирил (4-DiMeABut) 5-MeHex-D-Val-L-Thr-D-Val-L-Val-D-Pro-LOrn-D-allo-Ile 5-MeHex-D-Val-L-Thr-D-Val-L-Val-D-Pro-LOrn-D-allo-Ile 1479 1479 1478 1477 1477 кінцева група: гептаноїл (Hep) 1477 кінцева група: гептаноїл (Hep) 1477 5-MeHex-D-Val-L-Thr-L-Val-D-Val-D-Pro-LOrn-D-allo-Ile 5-MeHex-D-Val-L-Thr-L-Val-D-Val-D-Pro-LOrn-D-allo-Ile кінцева група: 3,3-диметилбутирил (3,3DiMeBut) кінцева група: 3,3-диметилбутирил (3,3DiMeBut) 1477 1477 1463 1463 кінцева група: 3-метилпентаноїл (4-МеРеn) 1463 кінцева група: 3-метилпентаноїл (4-МеРеn) 1463 кінцева група: трифторацетил (TFA) 1461 кінцева група: 2,4-гексадієноїл (Hedo) 1459 кінцева група: 4-гідроксибутирил 1451 кінцева група: 3-метилбутирил (3-MeBut) 1451 кінцева група: 3-метилбутирил (3-MeBut) 1451 кінцева група: бутирил (But) 1435 кінцева група: бутирил 1435 27c 28 28bis 29 29bis 31 32 19 34 35 41 76949 цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-DhbVal) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-DhbVal) цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-DhbVal) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-DhbVal) цикло(D-allo-Thr-D-allo-Ile-Val-Phe-Z-DhbVal) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-DhbVal) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-DhbVal) L-Phe-D-Leu-L-Pro- -Thr-Gly-D-Ser цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-DhbVal) цикло(D-allo-Thr-D-allo-Ile-D-Val-Phe-Z-DhbVal) 42 кінцева група: ацетил 1407 кінцева група: без жирної кислоти 1365 кінцева група: без жирної кислоти 1365 5-MeHex-D-Val-L-Thr-L-Val-D-Val-D-Pro-Dallo-Ile 5-MeHex-D-Val-L-Thr-L-Val-D-Val-D-Pro-Dallo-Ile 1363 1363 5-MeHex-D-Val-L-Thr-L-Val-D-allo-Ile 1167 5-MeHex-D-Val-L-Thr-D-allo-Ile 1068 5-MeHex-L-Tyr 878 5-MeHex-D-allo-Ile 868 5-MeHex 754 * * Сполуки, для яких у графі «Ланцюг» вказаний Термінал, мають такий самий ланцюг, що і сполука 7, але з вказаним заміщенням для 5-МеНех. 43 76949 Посилання 1. Hamann, M.T.; Scheuer, PJ. J. Am. Chew, Soc, 1993. «Kahalalide F: a Bioactive Depsipeptide from the Sacoglossan Mollusk Elysia refescens and the Green Alga Bryopsis sp.», vol.115, pp.5825-5826. 2. Hamann, M.T., et al. J. Org. Chem., 1996. «Kahalalides: Bioactive Peptides from Marine Mollusk Elysia rufescens and its Algal Diet Bryopsis sp.» vol.61, pp.6594-6660, 3. Garcia-Rocha, M., et al. Cancer Lett., 1996. «The Antitumoral Compound Kahalalide F Acts on Cell Lysosomes», vol.99, pp.43-50. 4. Hamann, M.T., et al. J. Org. Chem., 1998. «Kahalalides: Bioactive Peptides from Marine Mollusk Elysia rufescens and its Algal Diet Bryopsis sp.» Комп’ютерна верстка О. Гапоненко 44 vol.63, p.485 (Correction of J. Org. Chem., 1996, vol.61, pp.6594-6660). 5. Lloyd-Williams, P., et al. Chemical Approaches to the Synthesis of Peptides and Proteins. CRC Press, Boca Raton (FL), 1997. 6. Goetz, G., et al. J. Nat Prod., 1997. «Two Acyclic Kahalalides from the Sacoglossan Mollusk Elysia rufescens», vol.60, pp.562-567. 7. Goetz, G., et al. Tetrahedron, 1999. The Absolute Stereochemistry of Kahalalide F, vol.55, pp.77397746. 8. Kan, Y., et al. J. Nat Prod., 1999, vol.62, pp.11691172. 9. Horgen, F.D. et al. J. Nat Prod., 2000, vol.63, pp.152-154. Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюKahalalide compounds
Назва патенту російськоюКахалалидные соединения
МПК / Мітки
МПК: A61K 38/00, C07K 11/00, C07K 7/08, A61P 35/00, C07K 7/06
Мітки: сполуки, кахалалідні
Код посилання
<a href="https://ua.patents.su/22-76949-kakhalalidni-spoluki.html" target="_blank" rel="follow" title="База патентів України">Кахалалідні сполуки</a>
Попередній патент: Дротяна підставка для нагрівання, придатна для складання в стос
Наступний патент: Електромагнітостатичний рушій (варіанти)
Випадковий патент: Спосіб визначення технічного ресурсу екранних поверхонь нагріву з труб