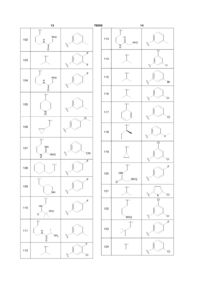
Сполуки, що застосовуються при лікуванні сибірки і інгібують летальний фактор
Номер патенту: 76059
Опубліковано: 15.06.2006
Автори: Петчетт Артур А., Ксіонг Юшенг, Сінгх Суреш, Чепман Кевін, Гуо Дзіан
Формула / Реферат
1. Сполука формули І
 (І)
(І)
або її фармацевтично прийнятна сіль, енантіомер, діастереомер або складний ефір, що гідролізується in vivo, або їх суміш, де R1 являє собою С6-10арил, С5-10гетероарил або С5-10гетероцикліл, причому вказаний арил, гетероарил і гетероцикліл необов'язково заміщений 1-3 групами Ra;
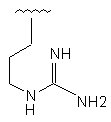
Ra являє собою С1-6алкіл, галоген, ОН, арил(С1-6)алкіл, (С1-6)алкокси, (С1-6)алкоксі(С1-6)алкіл, галоген(С1-6)алкіл, нітро, аміно, моно- або ді-N-(С1-6)алкіламіно, ациламіно, ацилокси, карбокси, солі карбонових кислот, складні ефіри карбонових кислот, карбамоїл, моно- і ді-N-(С1-6)алкілкарбамоїл, (С1-6)алкоксикарбоніл, арилоксикарбоніл, уреїдо, гуанідино, сульфоніламіно, аміносульфоніл, (С1-6)алкілтіо, (С1-6)алкілсульфініл, (С1-6)алкілсульфоніл, гетероцикліл, гетероцикліл(С1-6)алкіл; і
R являє собою С1-8алкіл, С3-10циклоалкіл, С3-10гетероциклоалкіл, С5-10гетероарил або С5-11гетероцикліл, причому гетероарил і гетероцикліл необов'язково заміщені 1-3 групами Ra, і вказаний алкіл необов'язково заміщений 1-3 групами, вибраними з групи, що складається з арилу, гетероциклілу, (С1-6)алкілтіо, ціано, гетероарилу, гуанідино, ((1-аміноетил)карбоніл)аміно, ((амінометил)карбоніл)аміно, ((2-амінопроп-2-іл)карбоніл)аміно, ацетамідо, 4-(амінометил)фенілу, тіо, трет-бутилсульфонілу, (С2-6)алкенілтіо, (С2-6)алкінілтіо, аміно, моно- або ді-(С1-6)алкіламіно, арилтіо, гетероциклілтіо, (С1-6)алкокси, арил(С1-6)алкокси, арил(С1-6)алкілтіо, циклоалкілу, циклоалкенілу, карбокси і складних ефірів карбонових кислот, гідрокси і галогену.
2. Сполука за п. 1, де R являє собою гетероциклоалкіл, а всі інші змінні є такими, як вони описані вище.
3. Сполука за п. 1, де R являє собою гетероарил, а всі інші змінні є такими, як вони описані вище.
4. Сполука за п. 1, де R1 являє собою фенільну групу, необов'язково заміщену 1-3 групами Ra, і R являє собою гетероциклоалкільну або гетероарильну групу.
5. Сполука за п. 1, де R1 являє собою фенільну групу, необов'язково заміщену 1-3 групами, вибраними з метокси, галогену, метилу, етилу, пропілу, бутилу, нафтилу, 5-(2-піридил)тіофен-2-ілу або їх суміші, і R являє собою гетероциклоалкіл або гетероарил.
6. Сполука за п. 1, вибрана з групи, що складається з:
N-трет-бутоксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-3-метилбутираміду;
N-гідроксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-3-метилбутираміду;
N-трет-бутоксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-2-(4'-тетрагідропіраніл)ацетаміду;
N-гідроксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-2-(4'-тетрагідропіраніл)ацетаміду;
N-гідроксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-3-(S)-циклопропілбутираміду;
і із сполук, представлених нижче в таблицях 1 і 2,
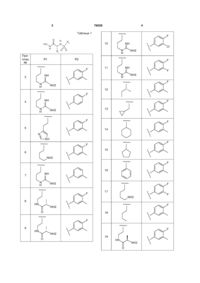
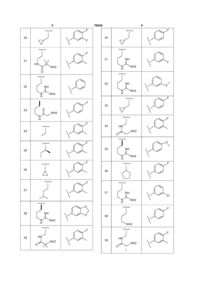
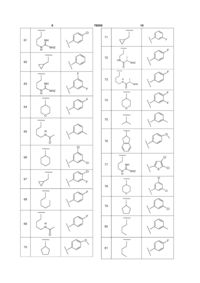
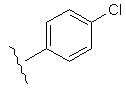
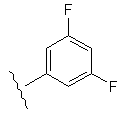
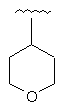
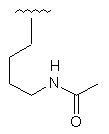
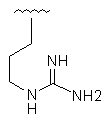
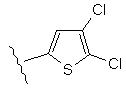
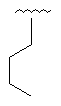
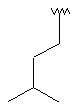
Таблиця 1
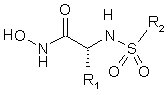
Приклад №
R1
R2
3

4

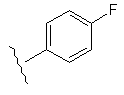
5
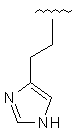

6
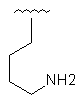

7

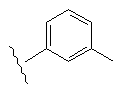
8
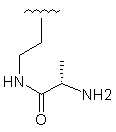

9
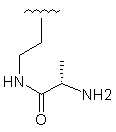

10
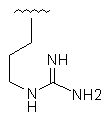
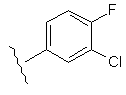
11

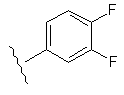
12
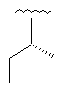

13
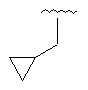

14
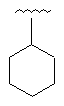

15
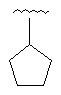

16
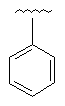

17


18
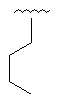

19

20


21
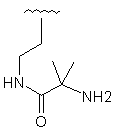

22
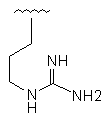
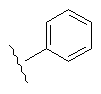
23
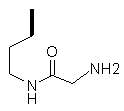
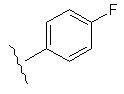
24
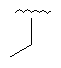

25
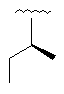

26
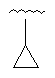

27
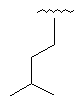

28
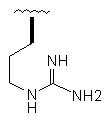
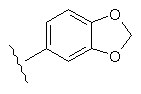
29
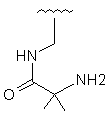

30


31

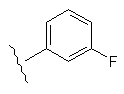
32

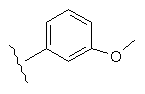
33


34
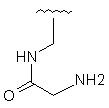

35
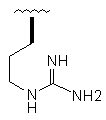
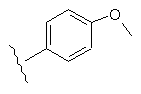
36


37

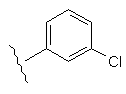
38


39
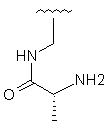

40

41
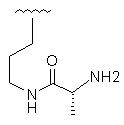

42


43

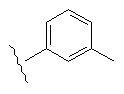
44


45

46

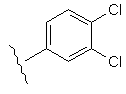
47
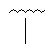

48


49

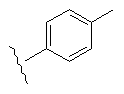
50

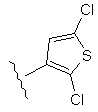
51


52


53
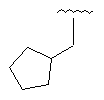

54
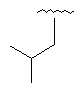

55
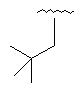

56


57


58
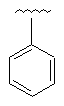

59


60
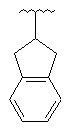

61

62


63

64

65

66


67

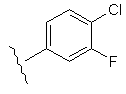
68
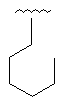

69


70


71


72
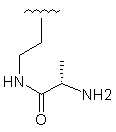

73


74


75
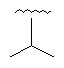

76


77
78


79


80

81


82
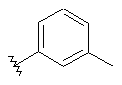
83

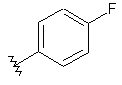
84
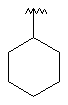
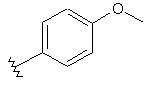
85
![]()
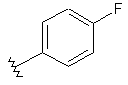
86
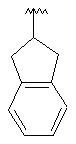
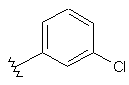
87
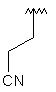
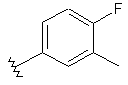
88
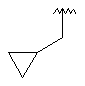
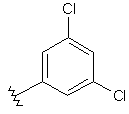
89
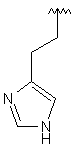

90
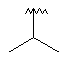

91
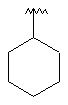

92
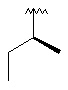

93
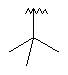

94


95
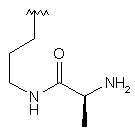
96

97

98
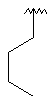

99
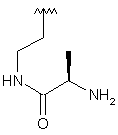

100
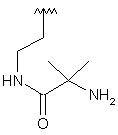

101
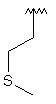

102
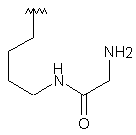

103

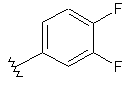
104


105
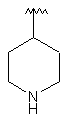

106


107
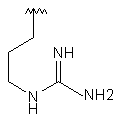
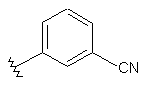
108
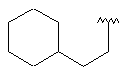

109
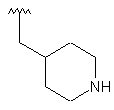

110
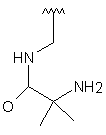

111


112

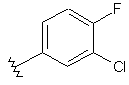
113
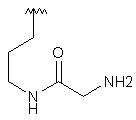

114

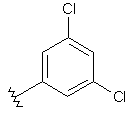
115

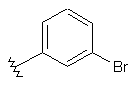
116


117
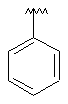

118

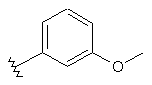
119
![]()

120
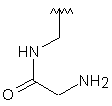

121

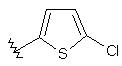
122
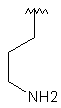

123
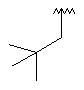

124
![]()

125
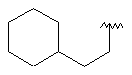
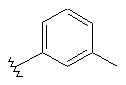
126
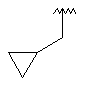
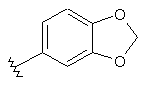
127
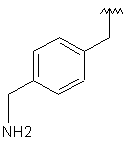

128
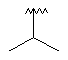
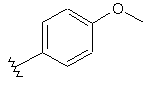
129
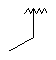
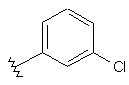
130
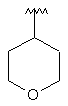
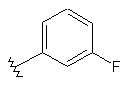
131

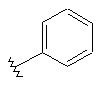
132
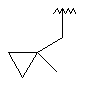

133
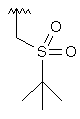

134
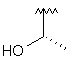

135
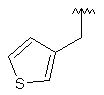
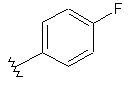
136
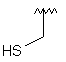

137
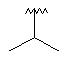
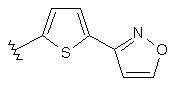
138
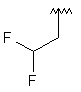

139

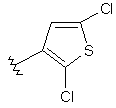
140
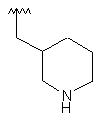

141
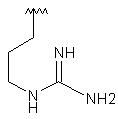
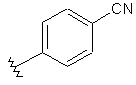
142
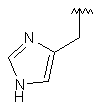

143
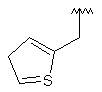
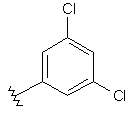
144
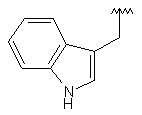

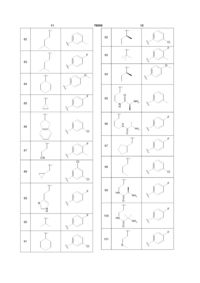
Таблиця 2
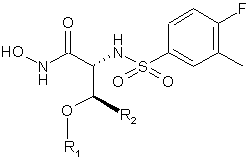
Приклад №
R1
R2
146
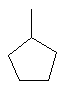
Me
147
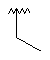
Me
148
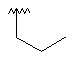
Me
149
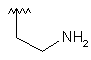
H
150
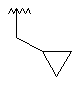
Me
151
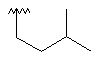
Me
152
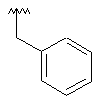
Me
153
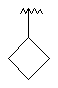
Me
і їх фармацевтично прийнятних солей, енантіомерів, діастереомерів або складних ефірів, що гідролізуються in vivo, або їх сумішей.
7. Сполука за п. 6, вибрана з групи, що складається з:
N-трет-бутоксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-3-метилбутираміду;
N-гідроксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-3-метилбутираміду;
N-трет-бутоксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-2-(4'-тетрагідропіраніл)ацетаміду;
N-гідроксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-2-(4'-тетрагідропіраніл)ацетаміду;
N-гідроксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-3-(S)-циклопропілбутираміду
і їх фармацевтично прийнятних солей, енантіомерів, діастереомерів або складних ефірів, що гідролізуються in vivo, або їх сумішей.
8. Сполука за п. 7, яка являє собою:
N-гідроксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-3-метилбутирамід або
N-гідроксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-2-(4'-тетрагідропіраніл)ацетамід, або їх фармацевтично прийнятні солі, енантіомери, діастереомери або складні ефіри, що гідролізуються in vivo, або їх суміші.
9. Композиція, що містить сполуку формули І за п.1 і фармацевтично прийнятний носій.
10. Спосіб інгібування активності летального фактора (ЛФ) (LF), що виділяється бактерією у ссавця, який включає введення хворому, у разі необхідності, терапевтично ефективної кількості сполуки структурної формули І
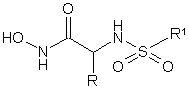 (І)
(І)
або її фармацевтично прийнятної солі, енантіомеру, діастереомеру або складного ефіру, що гідролізується in vivo, або їх суміші, де R1 являє собою С6-10арил, С5-10гетероарил або С5-10гетероцикліл, причому вказаний арил, гетероарил і гетероцикліл необов'язково заміщений 1-3 групами Rа;
Rа являє собою С1-6алкіл, галоген, ОН, арил(С1-6)алкіл, (С1-6)алкокси, (С1-6)алкоксі(С1-6)алкіл, галоген(С1-6)алкіл, нітро, аміно, моно- або ді-N-(С1-6)алкіламіно, ациламіно, ацилокси, карбокси, солі карбонових кислот, складні ефіри карбонових кислот, карбамоїл, моно- і ді-N-(С1-6)алкілкарбамоїл, (С1-6)алкоксикарбоніл, арилоксикарбоніл, уреїдо, гуанідино, сульфоніламіно, аміносульфоніл, (С1-6)алкілтіо, (С1-6)алкілсульфініл, (С1-6)алкілсульфоніл, гетероцикліл, гетероцикліл(С1-6)алкіл; і
R являє собою С1-8алкіл, С3-10циклоалкіл, С3-10гетероциклоалкіл, C5-10гетероарил або С5-10гетероцикліл, причому гетероарил і гетероцикліл необов'язково заміщені 1-3 групами Rа, і вказаний алкіл необов'язково заміщений 1-3 групами, вибраними з групи, що складається з арилу, гетероциклілу, (С1-6)алкілтіо, ціано, гетероарилу, гуанідино, ((1-аміноетил)карбоніл)аміно, ((амінометил)карбоніл)аміно, ((2-амінопроп-2-іл)карбоніл)аміно, ацетамідо, 4-(амінометил)фенілу, тіо, трет-бутилсульфонілу, (С2-6)алкенілтіо, (С2-6)алкінілтіо, аміно, моно- або ді-(С1-6)алкіламіно, арилтіо, гетероциклілтіо, (С1-6)алкокси, арил(С1-6)алкокси, арил(С1-6)алкілтіо, циклоалкілу, циклоалкенілу, карбокси і складних ефірів карбонових кислот, гідрокси і галогену.
11. Спосіб за п.10, в якому сполука вибрана з групи, що складається з:
N-трет-бутоксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-3-метилбутираміду;
N-гідроксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-3-метилбутираміду;
N-трет-бутоксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-2-(4'-тетрагідропіраніл)ацетаміду;
N-гідроксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-2-(4'-тетрагідропіраніл)ацетаміду;
N-гідроксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-3-(S)-циклопропілбутираміду;
і із сполук, представлених нижче в таблицях 1 і 2,
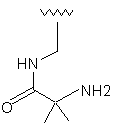
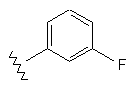
Таблиця 1
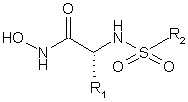
Приклад №
R1
R2
3


4


5


6


7


8
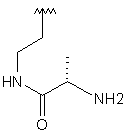

9
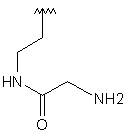

10
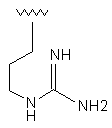
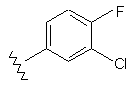
11

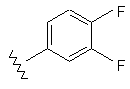
12
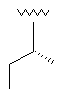
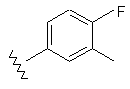
13
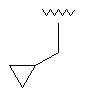

14
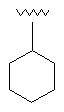

15
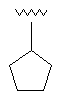

16
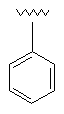

17
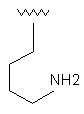

18
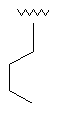

19
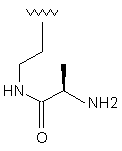

20


21
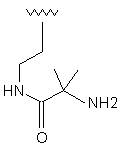

22

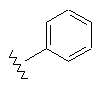
23
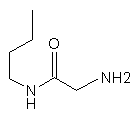

24
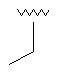

25
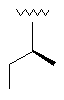

26
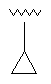

27
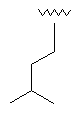

28

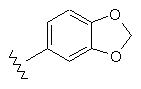
29

30


31

32

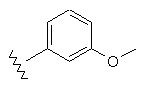
33


34
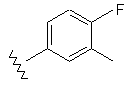
35

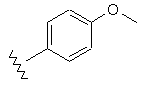
36


37

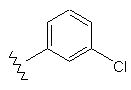
38
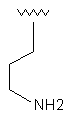

39
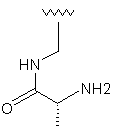

40

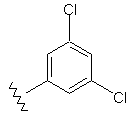
41
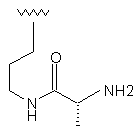

42
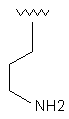

43

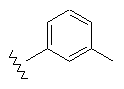
44
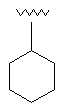
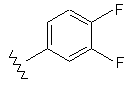
45

46

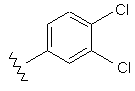
47
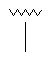

48
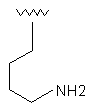

49

50

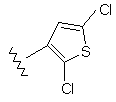
51


52


53
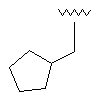

54
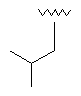

55
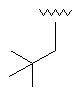

56


57


58


59
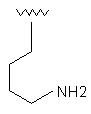

60
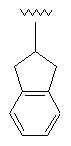

61

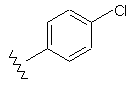
62


63

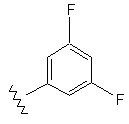
64
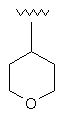

65
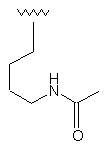

66


67

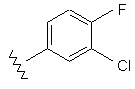
68
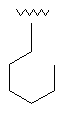

69


70


71


72
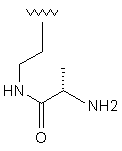

73
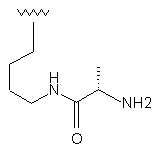

74


75
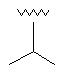

76


77

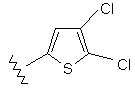
78


79


80


81


82


83


84


85


86


87
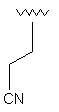

88


89
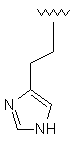

90


91


92
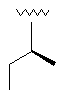

93
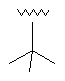

94


95
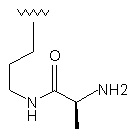

96


97


98
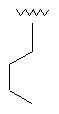

99
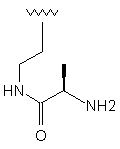

100
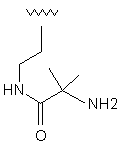

101
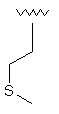

102
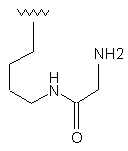

103


104


105
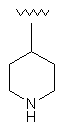

106


107

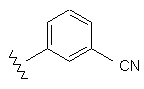
108
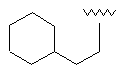

109
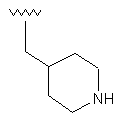

110


111


112
113
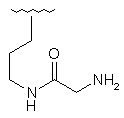
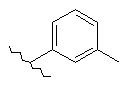
114

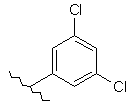
115

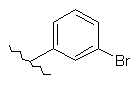
116

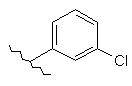
117
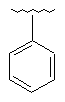

118
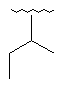
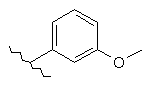
119
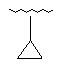

120
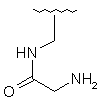
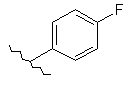
121

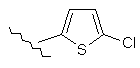
122
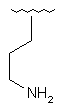

123
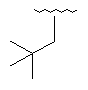

124
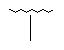

125
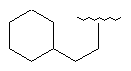
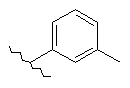
126
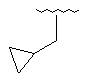
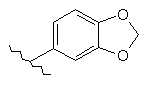
127
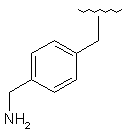

128

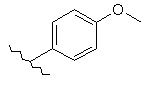
129
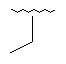

130
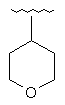
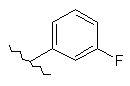
131

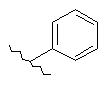
132
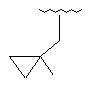
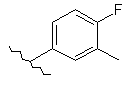
133
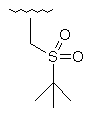

134
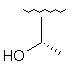

135
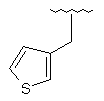

136
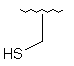

137

138
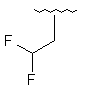

139

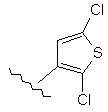
140
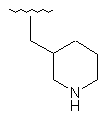

141
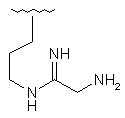
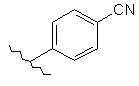
142
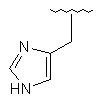

143
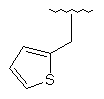

144
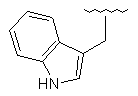
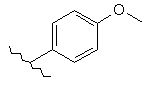
Таблиця 2
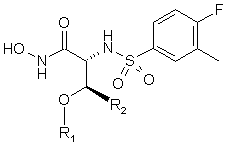
Приклад №
R1
R2
146
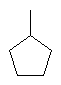
Me
147
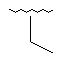
Me
148
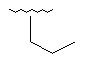
Me
149
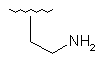
H
150
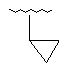
Me
151
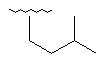
Me
152
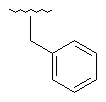
Me
153
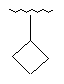
Me
і їх фармацевтично прийнятних солей, енантіомерів, діастереомерів або складних ефірів, що гідролізуються in vivo, або їх сумішей.
12. Спосіб за п. 11, в якому сполука являє собою:
N-трет-бутоксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-3-метилбутирамід;
N-гідроксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-3-метилбутирамід;
N-трет-бутоксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-2-(4'-тетрагідропіраніл)ацетамід;
N-гідроксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-2-(4'-тетрагідропіраніл)ацетамід;
N-гідроксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-3-(S)-циклопропілбутирамід
і їх фармацевтично прийнятні солі, енантіомери, діастереомери або складні ефіри, що гідролізуються in vivo, або їх суміші.
13. Спосіб за п. 12, в якому сполука являє собою:
N-гідроксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-3-метилбутирамід або
N-гідроксі-2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-2-(4'-тетрагідропіраніл)ацетамід, або їх фармацевтично прийнятні солі, енантіомери, діастереомери або складні ефіри, що гідролізуються in vivo, або їх суміші.
14. Спосіб за п. 10, в якому сполука формули І об'єднана з одним або декількома відомими лікарськими засобами, вибраними з бета-лактамів, аміноглікозидів, інгібіторів бета-лактамази, блокаторів ниркових канальців і інгібіторів метаболічних ферментів, N-ацильованих амінокислот.
15. Спосіб за п. 14, в якому відомі лікарські засоби вибрані з групи, що складається з іміпенему, меропенему, ванкоміцину, циластатину, цефокситину, пеніциліну, клавуланової кислоти, пробенециду, тетрацикліну, ципрофлоксацину, норфлоксацину або їх суміші, при тому, коли як лікарський засіб використовується іміпенем, його використовують в комбінації з циластатином у вигляді PRIMAXIN®.
Текст
1. Сполука формули І 2 (19) 1 3 76059 4 Таблиця 1 O HO Приклад № N H H N R1 O R1 R2 F 10 NH Cl S O N H R2 F F 11 NH F N H NH 3 NH2 NH2 F N H NH2 12 F NH 4 N H F 13 NH2 F 5 F 14 N NH F F 15 6 NH2 F 16 NH 7 N H NH2 F F 17 NH2 F 8 HN F NH2 O 18 F 9 F HN NH2 O 19 HN NH2 O 5 76059 6 F F 30 20 F F 31 21 NH F HN N H NH2 NH2 O 32 22 NH O NH N H N H NH2 NH2 F F 33 O 23 NH2 N H F F 34 HN NH2 24 O O F 35 25 NH N H NH2 F 26 F 36 F 27 37 NH N H Cl NH2 O 28 NH N H O F 38 NH2 NH2 F F HN 29 NH2 O HN 39 NH2 O 7 76059 8 Cl 40 Cl 50 NH N H Cl NH2 S NH N H NH2 Cl F 51 O 41 NH2 N H F Cl 52 42 NH2 Cl F 53 43 F F 54 44 F F 55 F HN 45 NH2 O 56 NH2 Cl 46 NH Cl N H F 57 F NH2 F F 58 47 O 59 48 Cl NH2 NH2 F 60 49 NH2 9 76059 10 Cl 71 61 F NH N H NH2 F 72 HN 62 NH2 O F F 73 63 NH N H H N NH2 O F NH2 F F 74 F 64 O O 75 65 H N O 76 O Cl Cl 66 Cl 77 NH N H Cl NH2 S Cl Cl 67 F 78 Cl F O 68 79 Cl F 69 H N 80 O O 70 F 81 11 76059 12 92 82 Cl F F 93 83 O 94 O 84 F O 95 85 NH2 N H F H N 96 86 Cl NH2 O F F 97 87 CN Cl 98 Cl 88 Cl F F 99 HN 89 NH2 O N N H F F 100 HN NH2 90 O F 101 91 Cl S 13 NH2 H N 102 76059 14 O 113 NH2 N H O Cl F 114 103 F Cl F H N 104 115 NH2 Br O 116 Cl 105 N H 117 Cl O 106 118 O Cl NH 107 NH2 N H CN 119 Cl F F 108 HN 120 F O NH 2 109 121 NH S Cl F 110 Cl HN 122 NH2 O NH2 Cl F 111 123 H N NH2 O F 112 124 Cl Cl 15 76059 16 F 125 136 HS O N 126 O 138 127 O S 137 F F F Cl NH2 O S 139 128 Cl 140 129 Cl N H CN 130 F NH 141 O N H NH2 F 131 N 142 F N H 132 Cl 143 O S 133 S O Cl O 144 134 HO Cl F 135 S N H 17 76059 Таблиця 2 F O HO H N N H S O O O R2 R1 Приклад № R1 R2 146 Me 147 Me 18 і їх фармацевтично прийнятних солей, енантіомерів, діастереомерів або складних ефірів, що гідролізуються in vivo, або їх сумішей. 8. Сполука за п. 7, яка являє собою: N-гідроксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-3-метилбутирамід або N-гідроксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-2-(4'тетрагідропіраніл)ацетамід, або їх фармацевтично прийнятні солі, енантіомери, діастереомери або складні ефіри, що гідролізуються in vivo, або їх суміші. 9. Композиція, що містить сполуку формули І за п.1 і фармацевтично прийнятний носій. 10. Спосіб інгібування активності летального фактора (ЛФ) (LF), що виділяється бактерією у ссавця, який включає введення хворому, у разі необхідності, терапевтично ефективної кількості сполуки структурної формули І O 148 HO Me H N N H R 149 NH2 H 150 Me 151 Me 152 Me 153 Me і їх фармацевтично прийнятних солей, енантіомерів, діастереомерів або складних ефірів, що гідролізуються in vivo, або їх сумішей. 7. Сполука за п. 6, вибрана з групи, що складається з: N-трет-бутоксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-3-метилбутираміду; N-гідроксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-3-метилбутираміду; N-трет-бутоксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-2-(4'тетрагідропіраніл)ацетаміду; N-гідроксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-2-(4'тетрагідропіраніл)ацетаміду; N-гідроксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-3-(S)циклопропілбутираміду O R1 S O (І) або її фармацевтично прийнятної солі, енантіомеру, діастереомеру або складного ефіру, що гідролізується in vivo, або їх суміші, де R1 являє собою С6-10арил, С5-10гетероарил або С5-10гетероцикліл, причому вказаний арил, гетероарил і гетероцикліл необов'язково заміщений 1-3 групами Rа; Rа являє собою С1-6алкіл, галоген, ОН, арил(С16)алкіл, (С1-6)алкокси, (С1-6)алкоксі(С1-6)алкіл, галоген(С1-6)алкіл, нітро, аміно, моно- або ді-N-(С16)алкіламіно, ациламіно, ацилокси, карбокси, солі карбонових кислот, складні ефіри карбонових кислот, карбамоїл, моно- і ді-N-(С1-6)алкілкарбамоїл, (С1-6)алкоксикарбоніл, арилоксикарбоніл, уреїдо, гуанідино, сульфоніламіно, аміносульфоніл, (С1(С1-6)алкілсульфініл, (С16)алкілтіо, 6)алкілсульфоніл, гетероцикліл, гетероцикліл(С16)алкіл; і R являє собою С1-8алкіл, С3-10циклоалкіл, С3C5-10гетероарил або С510гетероциклоалкіл, 10гетероцикліл, причому гетероарил і гетероцикліл необов'язково заміщені 1-3 групами Rа, і вказаний алкіл необов'язково заміщений 1-3 групами, вибраними з групи, що складається з арилу, гетероциклілу, (С1-6)алкілтіо, ціано, гетероарилу, гуанідино, ((1-аміноетил)карбоніл)аміно, ((амінометил)карбоніл)аміно, ((2-амінопроп-2іл)карбоніл)аміно, ацетамідо, 4(амінометил)фенілу, тіо, трет-бутилсульфонілу, (С2-6)алкенілтіо, (С2-6)алкінілтіо, аміно, моно- або ді-(С1-6)алкіламіно, арилтіо, гетероциклілтіо, (С1арил(С1-6)алкокси, арил(С1-6)алкілтіо, 6)алкокси, циклоалкілу, циклоалкенілу, карбокси і складних ефірів карбонових кислот, гідрокси і галогену. 11. Спосіб за п.10, в якому сполука вибрана з групи, що складається з: N-трет-бутоксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-3-метилбутираміду; N-гідроксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-3-метилбутираміду; 19 76059 N-трет-бутоксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-2-(4'тетрагідропіраніл)ацетаміду; N-гідроксі-2(R)-[(4-фтор-39 метилфенілсульфоніл)]аміно-2-(4'тетрагідропіраніл)ацетаміду; N-гідроксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-3-(S)циклопропілбутираміду; і із сполук, представлених нижче в таблицях 1 і 2, Таблиця 1 F HN NH2 O F NH 10 Cl O HO 20 H N N H O S N H R2 NH2 O R1 ПрикR1 лад № F R2 11 F F N H NH 3 NH NH2 F N H NH2 12 F NH 4 F N H NH2 13 F 5 F N 14 N H F F 6 15 NH2 F NH 7 16 N H NH2 F 8 F 17 HN NH2 O NH2 F 21 76059 22 F 18 F 27 O F NH 28 19 HN O N H NH2 NH2 O F F HN 29 20 NH2 F O F F 30 21 HN NH2 O NH 31 F NH 22 N H N H NH2 F O 23 N H NH2 NH 32 O N H NH2 NH2 F F 33 24 F F 34 HN 25 NH2 O F 26 O NH 35 N H NH2 23 76059 24 F F 36 HN 45 NH2 O NH 37 Cl Cl N H NH2 NH 46 Cl N H F NH2 F 38 47 NH2 F HN 39 48 NH2 Cl NH2 O Cl 49 NH 40 NH2 N H Cl NH2 Cl F O 41 N H NH 50 N H NH2 S NH2 Cl 51 Cl 42 F NH2 Cl 52 43 F 53 F F 44 F 54 25 76059 26 F 55 65 H N O Cl 56 66 NH2 Cl F 57 F F 67 Cl F 58 F 68 O 59 F 69 H N NH2 O F 60 O 70 Cl 71 NH 61 N H F NH2 F 72 62 HN NH2 O F F NH 63 73 N H NH2 H N F NH2 O F 64 F 74 F O O 27 76059 28 F 75 85 O 76 86 Cl Cl F NH 77 Cl S N H 87 NH2 CN Cl Cl 78 88 O Cl Cl 79 F Cl 89 N NH 80 F 90 F 81 91 Cl 82 92 Cl F F 83 93 O 84 O 94 29 76059 30 F 103 O F 95 NH2 N H F NH2 104 H N O F H N 96 NH2 105 O N H F O 97 106 98 Cl NH 107 CN N H NH2 F F 108 99 HN NH2 F O 109 F NH 100 HN F NH2 HN 110 O NH2 O F 101 S 111 H N NH2 O NH2 102 H N F 112 Cl O 31 76059 32 O 126 O 113 N H O NH2 Cl 127 114 NH2 Cl O 128 115 Br 129 Cl 116 Cl 130 117 F O Cl 131 118 O F 132 Cl 119 O Cl S 133 O F HN 120 NH2 O 134 Cl HO 121 F Cl S 135 Cl S F 122 NH2 136 Cl HS F N 137 123 138 124 S F F Cl Cl 125 S 139 Cl O 33 76059 34 151 140 Me 152 Me 153 Me N H CN NH 141 NH2 N H F 142 N HN 143 Cl S O 144 HN Таблиця 2 O HO N H O F H N S O O R2 R1 Приклад № R1 R2 146 Me 147 Me 148 Me 149 150 NH2 H Me Цитовані в даній заявці посилання не треба розглядати як попередній рівень для заявленого винаходу. і їх фармацевтично прийнятних солей, енантіомерів, діастереомерів або складних ефірів, що гідролізуються in vivo, або їх сумішей. 12. Спосіб за п. 11, в якому сполука являє собою: N-трет-бутоксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-3-метилбутирамід; N-гідроксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-3-метилбутирамід; N-трет-бутоксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-2-(4'тетрагідропіраніл)ацетамід; N-гідроксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-2-(4'тетрагідропіраніл)ацетамід; N-гідроксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-3-(S)циклопропілбутирамід і їх фармацевтично прийнятні солі, енантіомери, діастереомери або складні ефіри, що гідролізуються in vivo, або їх суміші. 13. Спосіб за п. 12, в якому сполука являє собою: N-гідроксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-3-метилбутирамід або N-гідроксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-2-(4'тетрагідропіраніл)ацетамід, або їх фармацевтично прийнятні солі, енантіомери, діастереомери або складні ефіри, що гідролізуються in vivo, або їх суміші. 14. Спосіб за п. 10, в якому сполука формули І об'єднана з одним або декількома відомими лікарськими засобами, вибраними з бета-лактамів, аміноглікозидів, інгібіторів бета-лактамази, блокаторів ниркових канальців і інгібіторів метаболічних ферментів, N-ацильованих амінокислот. 15. Спосіб за п. 14, в якому відомі лікарські засоби вибрані з групи, що складається з іміпенему, меропенему, ванкоміцину, циластатину, цефокситину, пеніциліну, клавуланової кислоти, пробенециду, тетрацикліну, ципрофлоксацину, норфлоксацину або їх суміші, при тому, коли як лікарський засіб використовується іміпенем, його використовують в комбінації з циластатином у вигляді PRIMAXIN®. Сибірка являє собою бактерійну інфекцію, що продукується Bacillus anthracis. Ендоспори Bacillus anthracis можуть потрапити в організм через садно 35 76059 36 на шкірі, шляхом дихання або ковтання. Bacillus поріз або дряпину на шкірі. [Дивись: Synder, J.W., anthracis продукує сибірковий токсин, який часто є Shapiro, D.S., Gilchrist, M.J.R., et al., «Basic летальним [Dixon et al., (1999) N. Engl. J. Med. 341, Diagnostic Testing Protocols for Level A Laboratories 815-26]. (For The Presumptive Identification of Bacillus Сибірковий токсин складається з трьох білків: Anthracis)» на: www.ban.asm.la.cp. 102401f, Oct.24, компонента, зв'язуючого рецептор, позначеного як 2001, pgs. 1-20 і Dixon et al., NEJM 341:815-826 захисний антиген, і двох ферментативних компоSept 9, 1999 Number 11]. Симптоми шкірної інфекнентів, названих набряклий фактор і летальний ції звичайно включають нарости або шишку, схожу фактор («ЛФ»). [Mock et al., (2001) Annu. Rev. на укус комахи, яка викликає свербіж. Протягом Microbiol. 55, 647-71]. Летальний фактор являє від одного до двох днів нарости або шишка розвисобою цинкозалежну металопротеазу, яка спричиваються в наповнений рідиною пухирець, який няє виникнення токсичних ефектів за рахунок ророзривається з утворенням безболісної виразки з зщеплення мітогенактивованих кіназ протеїнкінази характерною чорною некротичною (омертвілою) (МКК) [Vitale et al., (1998) Biochem. Biophys. Res. ділянкою в середині. Якщо не провести лікування, Commun. 248, 706-11, Vitale et al., (2000) Biochem. може наступити смерть, однак, якщо провести J. 352 Pt 3, 739-45, Duesbery et al., (1998) Science антибіотикотерапію, смертельні випадки не часті. 280, 734-7, Duesbery et al., опублікована міжнароШлунково-кишкова форма сибірки звичайно дна заявка №WO 99/50439, опубл. 7 жовтня виникає внаслідок споживання забрудненого бак1999p.]. теріями м'яса, що приводить до гострого запаленДля ідентифікації сайта в різних МКК, які розня кишкового тракту. Такі симптоми як нудота, щеплюються летальним фактором, Vitale і співровтрата апетиту, блювання, жар, разом з болем в бітники використали мікросеквенування [дивись ділянці черевної порожнини, блюванням з кров'ю і таблицю 1, Vitale et al., (2000) Biochem. J. 352 Pt 3, сильною діареєю є показниками шлунково739-45]. Розщеплення летальним фактором різних кишкової виразки. Летальність внаслідок даної МКК відбувалося в N-кінцевій ділянці, що передує форми сибірки у людей становить 25-60%. домену кінази. Вирівнювання послідовностей, Легенева форма сибірки найбільш ймовірно є фланкуючих сайт розщеплення, виявило деякі результатом навмисного аерозольного застосумотиви узгодженості: гідрофобний залишок в повання Bacillus anthracis, наприклад, в результаті ложенні Р2 і Ρ1' і, щонайменше, один залишок між біотероризму. Дана форма людської сибіркової Р4 і Р7. [Vitale et al., (2000) Biochem. J. 352 Pt 3, інфекції звичайно має інкубаційний період від од739-45]. ного до шести днів, при цьому первинними ознаБуло показано, що летальний фактор розщепками є жар, нездужання, непродуктивний кашель лює синтетичні пептиди in vitro [Hammond et al., і/або іноді невеликий дискомфорт в ділянці грудної (1998) Infect. Immun. 66, 2374-8]. Розщеплення in клітки. Після вказаних первинних симптомів часто vitro інгібувалося 1,10-фенантроліном або 10мМ йде короткий період поліпшення, після якого виниEDTA, обидва з яких утворюють хелатну сполуку з кає раптовий розвиток важкого респіраторного цинком. дистрес-синдрому з ускладненим диханням, потоBacillus anthracis являє собою спороутворювавиділенням і посинінням шкіри. Незважаючи на льну грампозитивну бацилу, яка є етіологічним інтенсивне лікування, через 24-36 годин після виагентом сибірки виразки. Сибірка являє собою никнення респіраторного дистрес-синдрому звизахворювання, яке може бути повсюдно знайдене чайно наступає смерть. в зонах з помірним кліматом (наприклад в ПівденБільшість штамів Bacillus anthracis сприйнятній і Центральній Америці, в Південній і Східній ливі до широкого діапазону антибіотиків. Лікарські Європі, Азії, Африці, на Середньому Сході і Казасоби, що найчастіше використовуються в цей рибських островах) і передається людям через час, включають ципрофлоксацин, пеніцилін або контакти або споживання забруднених продуктів доксициклін. Однак профілі ефективності і побічтваринного походження (наприклад, через вжиних дій даних лікарських засобів не є ідеальними. вання недостатньо прожареного м'яса інфікованих Хоч антибіотики можуть вбивати бактерії, які тварин). Дикі ссавці, такі як олень, гну, слони і довикликають сибірку, сибірковий токсин, що складамашні тварини, такі як кози, вівці, велика рогата ється з трьох частин, продовжує вражати організм худоба, коні і свині, представляють велику небезнавіть коли самі бактерії гинуть. Тому все ще існує пеку для зараження. Зараження звичайно виникає потреба в нових і ефективних лікарських препарапри утримуванні худоби на зараженому пасовищі, тах з поліпшеною ефективністю, що надають непри вживанні забрудненої їжі або вживанні води із значну побічну дію або не мають такої, які інгібузабруднених свердловин. Спори Bacillus anthracis ють «ножицеподібну» здатність летального можуть залишатися життєздатними в ґрунті протяфактора відрізати значущі молекули хазяїна. гом багатьох років. [Дивись: Helgason et al., Applied Даний винахід відноситься до нових сполук and Environmental Microbiology 2000 66(6) pgs. формули І 2627-2630; Wiber et al., Antimicrob Agents and Chemotherapy 1988 32 (5):642-645; і Doganay et al., I Scand. J. Inf. Dis. 1991 23:333-335 для додаткового обговорення Bacillus anthracis]. або до фармацевтично прийнятної солі, енанУ людей можуть зустрічатися три форми сибітіомеру, діастереоізомеру або складного ефіру, ркової інфекції: шкірна, шлунково-кишкова і легещо гідролізується in vivo, або їх суміші, де нева. При шкірній формі інфікування відбувається R1 являє собою С6-10арил, С5-10гетероарил або в тому випадку, коли бактерія або спора попадає в 37 76059 38 С5-10гетероцикліл, причому вказаний арил, гетеровуглецю. Він може містити від 1 до 4-х кілець, які є арил і гетероцикліл необов'язково заміщений 1-3 конденсованими. Прикладами циклоалкільних груп групами Ra; є циклопропіл, циклобутил, циклопентил, циклогеRa являє собою С1-6алкіл, галоген, ОН, ксил і циклогептил. арил(С1-6)алкіл, (С1-6)алкокси, (С1-6)алкоксі(С1Гетероциклоалкіл означає циклоалкільні циклічні групи, що складаються з атомів вуглецю і 6)алкіл, галоген(С1-6)алкіл, нітро, аміно, моно- або ді-N-(С1-6)алкіламіно, ациламіно, ацилокси, карбоодного-чотирьох гетероатомів, вибраних з групи, кси, солі карбонових кислот, складні ефіри карбощо складається з Ν, Ο і S, і включає біициклічні нових кислот, карбамоїл, моно- і ді-N-(С1-6) алкілгрупи. Вказаний гетероциклоалкіл може бути некарбамоїл, (С1-6)алкоксикарбоніл, обов'язково заміщений представленими в даному арилоксикарбоніл, уреїдо, гуанідино, сульфонілаописі 1-3 групами Ra. Прикладами гетероциклоалміно, аміносульфоніл, (С1-6)алкілтіо, (С1кілів є океан, метилоксан, діоксан, піран, тіолан, піперидин, піролідин, азиридин, азетидин і т.д. 6)алкілсульфініл, (С1-6)алкілсульфоніл, гетероцикліл, гетероцикліл(С1-6) алкіл; і Алкокси відноситься до С1-6алкіл-О-, при цьоR являє собою С1-8алкіл, С3-10циклоалкіл, С3му алкільна група необов'язково заміщена як укаС5-10гетероарил або С5зано вище. Прикладами алкоксигруп є метокси, 10гетероциклоалкіл, етокси, пропокси, бутокси і їх ізомерні групи. 11гетероцикліл, причому гетероарил і гетероцикліл необов'язково заміщені 1-3 групами Ra і вказаний «Гало» є скороченою назвою галогену і відноалкіл необов'язково заміщений 1-3 групами, вибситься до хлориду, фториду, броміду і йодиду. раними з групи, що складається з арилу, гетероциВикористаний в даному описі термін «арил» клілу, (С1-6)алкілтіо, ціано, гетероарилу, гуанідино, означає будь-яке стійке моноциклічне або біциклі(1-аміноетилкарбоніл)аміно, (амінометилкарбочне вуглецеве кільце, що містить до 7 членів в ніл)аміно, ((2-амінопроп-2-іл)карбоніл)аміно, ацекожному кільці, причому щонайменше одне кільце тамідо, 4-(амінометил)фенілу, тіо, третє ароматичним. Приклади таких арильних фрагбутилсульфонілу, (С2-6)алкенілтіо, (С2-6)алкінілтіо, ментів включають феніл, нафтил, тетрагідронафаміно, моно- або ді-(С1-6)алкіламіно, арилтіо, гететил, інданіл, біфеніл, фенантрил, антрил або ацероциклілтіо, (С1-6)алкокси, арил(С1-6)алкокси, нафтил. арил(С1-6)алкілтіо, циклоалкілу, циклоалкенілу, Використаний в даному описі термін «гетерокарбокси і складних ефірів карбонових кислот, цикліл» або «гетероциклічний» являє собою стійке гідрокси і галогену. 5-7-членне моноциклічне або стійке 8-11-членне Даний винахід відноситься також до застосубіциклічне гетероциклічне кільце, яке є насиченим вання сполук формули І при лікуванні сибірки і або ненасиченим і яке складається з атомів вуглеінших станів, які пов'язані з сибірковою інфекцією. цю і одного-чотирьох гетероатомів, вибраних з Вказані і інші аспекти винаходу стануть більш групи, що складається з Ν, Ο і S, і включає будьясними при уважному розгляді винаходу загалом. яку біциклічну групу, в якій будь-яке з визначених Даний винахід відноситься до сполук формули вище гетероциклічних кілець конденсоване з бенІ і способу лікування сибірки або до інгібування зольним кільцем. Гетероциклічне кільце може бути летального фактора шляхом введення композиції, приєднане до будь-якого гетероатому або атому що містить сполуку формули І і фармацевтично вуглецю, що приводить до створення стійкої струкприйнятний носій, переважно внутрішньовенно тури. Конденсована гетероциклічна кільцева сисабо внутрішньом'язово. тема може включати карбоциклічні кільця і за неВинахід описаний детально з використанням обхідності може включати тільки одне визначених нижче термінів, якщо не вказане інше. гетероциклічне кільце. Термін «гетероцикл» або Коли будь-яка змінна (наприклад, арил, гете«гетероциклічний» включає гетероарильні групи. роцикл, R1, R і т.д.) зустрічається в будь-якій склаПриклади таких гетероциклічних фрагментів вклюдовій більше одного разу, її визначення в кожному чають, але без обмеження, азепініл, бензімідазомісці є незалежним від визначення в кожному інліл, бензізоксазоліл, бензофуразаніл, бензопірашому місці. Крім того, комбінації замісників/або ніл, бензотіопіраніл, бензофурил, бензотіазоліл, змінних допустимі тільки в тому випадку, якщо такі бензотієніл, бензоксазоліл, хроманіл, цинолініл, комбінації приводять до отримання стійких сполук. дигідробензофурил, дигідробензотієніл, дигідроТермін «алкіл» відноситься до радикала, бензотіопіраніл, дигідробезотіопіранілсульфон, зробленого з одновалентного алкану (вуглевод1,3-діоксоланіл, фурил, імідазолідиніл, імідазоліню), що містить від 1 до 10 атомів вуглецю, якщо ніл, імідазоліл, індолініл, індоліл, ізохроманіл, ізоіне визначено інше. Він може бути прямим, розгандолініл, ізохінолініл, ізотіазоліл, ізотіазолідиніл, луженим або циклічним. Переважні алкільні групи морфолініл, нафтиридиніл, оксадіазоліл, 2включають метил, етил, пропіл, ізопропіл, бутил, оксоазепініл, оксазоліл, 2-оксопіперазиніл, 2трет-бутил, циклопентил і циклогексил. Коли говооксопіперидиніл, 2-оксопіролідиніл, піперидил, риться, що алкільна група заміщена алкільною піперазиніл, піридил, піразиніл, піразолідиніл, пігрупою, це означає, що її використовують взаєморазоліл, піридазиніл, піримідиніл, піролідиніл, пізамінно з «розгалуженою алкільною групою». роліл, хіназолініл, хінолініл, хіноксалініл, тетрагідАлкеніл переважно являє собою С2-6алкеніл. рофурил, тетрагідроізохінолініл, Алкініл переважно являє собою С2-6алкініл. тетрагідрохінолініл, тіаморфолініл, тіаморфолінілЦиклоалкіл є різновидом алкілу, що містить від сульфоксид, тіазоліл, тіазолініл, тієнофурил, тієно3 до 15 атомів вуглецю, якщо не вказане інше, при тієніл і тієніл. Варіант прикладів таких гетероцикліцьому він не має резонансних подвійних зв'язків, чних фрагментів включає, але без обмеження, або подвійних зв'язків, що чергуються між атомами азепініл, бензімідазоліл, бензізоксазоліл, бензо 39 76059 40 фуразаніл, бензопіраніл, бензотіопіраніл, бензособою гетероциклоалкіл, а всі інші змінні є такими, фурил, бензотіазоліл, бензотієніл, бензоксазоліл, як вони описані вище. хроманіл, цинолініл, дигідробензофурил, дигідроВ іншому варіанті даного винаходу, що віднобензотієніл, дигідробензотіопіраніл, дигідробензоситься до сполук формули la, R являє собою гететіопіранілсульфон, фурил, імідазолідиніл, імідазороарил, а всі інші змінні є такими, як вони описані лініл, імідазоліл, індолініл, індоліл, ізохроманіл, вище. ізоіндолініл, ізохінолініл, ізотіазоліл, ізотіазолідиВ іншому варіанті даного винаходу, що відноніл, морфолініл, нафтиридиніл, оксадіазоліл, 2ситься до сполук формули la, R являє собою С1оксазепініл, оксазоліл, 2-оксопіперазиніл, 24алкіл, а всі інші змінні є такими, як вони описані оксопіперидиніл, 2-оксопіролідиніл, піперидил, вище. піперазиніл, піридил, 2-піридиноніл, піразиніл, піУ ще одному іншому варіанті даного винаходу, разолідиніл, піразоліл, піридазиніл, піримідиніл, що відноситься до сполук формули la, R1 являє піролідиніл, піроліл, хіназолініл, хінолініл, хіноксасобою фенільну групу, необов'язково заміщену 1-3 лініл, тетрагідрофурил, тетрагідроізохінолініл, тетгрупами Ra, і R являє собою алкільну, гетероцикрагідрохінолініл, тіаморфолініл, тіаморфолінілсулоалкільну або гетероарильну групу. льфоксид, тіазоліл, тіазолініл, тієнофурил, У ще одному іншому варіанті даного винаходу, тієнотієніл, тієніл і триазоліл. що відноситься до сполук формули la, R1 являє Гетероцикл переважно вибраний з 2собою фенільну групу, заміщену 1-3 групами, вибазепінонілу, бензімідазолілу, 2-діазапінонілу, іміраними з метокси, галогену, метилу, етилу, пропідазолілу, 2-імідазолідинонілу, індолілу, ізохінолінілу, бутилу, нафтилу, 5-(2-піридил)тіофен-2-ілу або лу, морфолінілу, піперидилу, піперазинілу, піридиїх суміші, і R являє собою алкіл, гетероциклоалкіл лу, піролідинілу, 2-піперидинонілу, 2або гетероарил. піримідинонілу, 2-піролідинонілу, хінолінілу, тетраІнший варіант даного винаходу відноситься до гідрофурилу, тетрагідроізохінолінілу і тієнілу. фармацевтичної композиції, що містить сполуку Використаний в даному описі термін «гетероаформули І і фармацевтично прийнятний носій. рил» означає будь-яке стійке моноциклічне і біциІнший варіант даного винаходу включає застоклічне вуглецеве кільце, що містить до 7 членів в сування сполуки формули І для отримання лікаркожному кільці, де щонайменше одне кільце є ського препарата, призначеного для лікування або ароматичним і де від одного до чотирьох атомів профілактики сибірки і пов'язаних з нею станів. Ще вуглецю заміщене гетероатомами, вибраними з один інший варіант винаходу включає застосувангрупи, що складається з N, О і S. Приклади таких ня сполуки формули І для отримання лікарського гетероциклічних фрагментів включають, але без препарата, призначеного для інгібування летальобмеження, бензімідазоліл, бензізоксазоліл, бенного фактора. зофуразаніл, бензопіраніл, бензотіопіраніл, бенСполуки формули І можуть бути об'єднані з зофурил, бензотіазоліл, бензотієніл, бензоксазоодним або декількома відомими лікарськими засоліл, хроманіл, цинолініл, дигідробензофурил, бами, вибраними з клінічно застосовних антибакдигідробензофураніл, дигідробензотієніл, дигідротерійних засобів (наприклад, інших бета-лактамів бензотіопіраніл, дигідробензотіопіранілсульфон, або аміноглікозидів), інгібіторів бета-лактамази, фурил, імідазоліл, індолініл, індоліл, ізохроманіл, блокаторів ниркових канальців (наприклад пробеізоіндолініл, ізохінолініл, ізотіазоліл, нафтиридиніл, нециду) і інгібіторів метаболічних ферментів (наоксадіазоліл, піридил, піразиніл, піразоліл, піридаприклад, інгібіторів дегідропептидаз, наприклад Zзиніл, піримідиніл, піроліл, хіназолініл, хінолініл, 2-ациламіно-3-заміщених пропеноатів, таких як хіноксалініл, тетрагідроізохінолініл, тетрагідрохіциластатин) і N-ацильованих амінокислот [дивись, нолініл, тіазоліл, тієнофурил, тієнотієніл, тієніл і наприклад, ЕР-А-178911], які зменшують небажану триазоліл. дію на нирки. Прикладами лікарських засобів, які В одному варіанті даного винаходу, що відноможуть бути об'єднані із сполуками формули І, є ситься до сполук формули І, R являє собою гетеіміпенем, меропенем, ванкоміцин, циластатин, роциклоалкіл, а всі інші змінні є такими, як вони цефокситин, пеніцилін, клавуланова кислота, проописані вище. бенецид, тетрациклін, ципрофлоксацин, норфлокВ іншому варіанті даного винаходу, що відносацин або їх суміш. Коли як лікарський засіб викоситься до сполук формули І, R являє собою гетеристовується іміпенем, його переважно роарил, а всі інші змінні є такими, як вони описані використовувати в комбінації з циластатином (давище. на комбінація представлена на ринку під торговою У ще одному іншому варіанті даного винаходу, маркою PRIMAXIN®). що відноситься до сполук формули І, R1 являє Відповідні фармацевтично прийнятні солі способою фенільну групу, необов'язково заміщену 1-3 лук, використаних в даному винаході, включають групами Ra, і R являє собою гетероциклоалкільну адитивні кислотні солі, такі як гідрохлорид, гідробабо гетероарильну групу. ромід, цитрат, малеат, і солі, утворені фосфорною У ще іншому варіанті даного винаходу, що віді сірчаною кислотами. Відповідно до іншого аспекноситься до сполук формули І, R являє собою фету відповідні солі являють собою основні солі, такі нільну групу, заміщену 1-3 групами, вибраними з як сіль лужного металу, наприклад натрію або каметокси, галогену, метилу, етилу, пропілу, бутилу, лію, сіль лужноземельного металу, наприклад, нафтилу, 5-(2-піридил)тіофен-2-ілу або їх суміші, і кальцію або магнію, органічну сіль аміну, наприR являє собою гетероциклоалкіл або гетероарил. клад триетиламіну, морфоліну, NУ ще одному іншому варіанті даного винаходу, метилпіперидину, N-етилпіперидину, прокаїну, що відноситься до сполук формули la, R являє дибензиламіну, Ν,Ν-дибензил етил аміну, або амі 41 76059 42 нокислот, наприклад лізину. Переважними фармають собою: цевтично прийнятними солями є солі натрію і каN-трет-бутоксі-2(R)-[(4-фтор-3лію. метилфенілсульфоніл)]аміно-3-метилбутирамід; Складні ефіри, що гідролізуються in vivo, явN-гідрокси-2(N)-[(4-фтор-3ляють собою такі фармацевтично прийнятні скламетилфенілсульфоніл)]аміно-3-метилбутирамід; дні ефіри, які гідролізуються в організмі людини з N-трет-бутоксі-2(R)-[(4-фтор-3продукуванням вихідної сполуки. Такий складний метилфенілсульфоніл)]аміно-2-(4'ефір може бути ідентифікований введенням піддотетрагідропіраніл)ацетамід; слідній тварині, наприклад внутрішньовенно, виN-гідроксі-2(R)-[(4-фтор-3пробуваної сполуки і подальшим дослідженням метилфенілсульфоніл)]аміно-2-(4'рідин організму піддослідної тварини. Відповідні тетрагідропіраніл)ацетамід; складні ефіри карбонових кислот, що гідролізуN-гідроксі-2(R)-[(4-фтор-3ються in vivo, включають С1-6алкоксиметилові ефіметилфенілсульфоніл)]аміно-3-(S)ри, наприклад метоксиметиловий, С1циклопропілбутирамід; і їх фармацевтично прийнятні солі, енантіоме6алканоїлоксиметилові ефіри, наприклад півалоїлоксиметиловий, фталидиловий ефіри і додаткові ри, діастереомери або складні ефіри, що гідроліскладні ефіри, розкриті [в патенті США №5478820], зуються in vivo, або їх суміші. включеному в даний опис у всій своїй повноті як Додаткові сполуки даного винаходу розкриті в посилання. таблиці 1: Використані в даному винаході сполуки являТаблиця 1 43 76059 44 Продовження таблиці 1 45 76059 46 Продовження таблиці 1 47 76059 48 Продовження таблиці 1 49 76059 50 Продовження таблиці 1 51 76059 52 Продовження таблиці 1 і їх фармацевтично прийнятні солі, енантіомери, діастереомери або складні ефіри, що гідролізуються in vivo, або їх суміші. Інші додаткові сполуки даного винаходу розкриті в таблиці 2: Таблиця 2 53 і їх фармацевтично прийнятні солі, енантіомери, діастереомери або складні ефіри, що гідролізуються in vivo, або їх суміші. Використані в даному описі переважні сполуки являють собою: N-трет-бутоксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-3-метилбутирамід; N-гідроксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-3-метилбутирамід; N-трет-бутоксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-2-(4'тетрагідропіраніл) ацетамід; N-гідроксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-2-(4'тетрагідропіраніл)ацетамід; N-гідроксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-3-(S)циклопропілбутирамід; і їх фармацевтично прийнятні солі, енантіомери, діастереомери або складні ефіри, що гідролізуються in vivo, або їх суміші. Для застосування сполуки формули І або її фармацевтично прийнятної солі, енантіомеру, діастереомеру або складного ефіру, що гідролізується in vivo, або їх суміші для терапевтичного лікування ссавців, включаючи людину, особливо для лікування сибірки або інгібування летального фактора, її звичайно приготовляють відповідно до стандартної фармацевтичної практики у вигляді фармацевтичної композиції. Використані в даному винаході сполуки можуть бути введені в терапевтично ефективній кількості внутрішньовенно, підшкірно, внутрішньом'язово або будь-яким іншим шляхом, відомим фахівцям в даній галузі (наприклад, ректально, перорально, парентерально). Відповідна фармацевтична композиція, використана в даному винаході, є такою, яка приготована як стерильний ін'єкційний розчин, що містить від 1 до 50мас./мас.% сполук, використаних в даному винаході. Відповідні суб'єкти для введення препарата даного винаходу включають приматів, людей і інших тварин, особливо людей і домашніх тваринах, таких як кішки, кролики і собаки. Наступні необмежувальні приклади, дані з метою ілюстрації, наочно показують, що сполуки, використані в даному винаході, застосовні для лікування сибірки і інгібування летального фактора. Визначення термінів: НОВТ - гідроксибензотриазол DMF - диметилформамід DIEA - діізопропілетиламін TMSONH2 - О-триметилсилілгідроксиламін РуВОР бензотриазол-1-ілокси-триспіролідинофосфонійгексафторфосфат TFA - трифтороцтова кислота HPLC - високоефективна рідинна хроматографія DCM - дихлорметан EDC 1-(3-диметиламінопропіл)-3етилкарбодіімід THF - тетрагідрофуран DIC - Ν,Ν'-діізопропілкарбодіімід DMAP - 4-диметиламінопіридин NMP - 1-метил-2-піролідинон 76059 54 EDTA - етилендіамінтетраоцтова кислота. N-трет-бутоксі-2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-3-метилбутирамід (1,8г, 4,99ммоль) розчиняли при 0°С в 75мл безводного дихлоретану, що містить етанол (0,30мл, 5ммоль). Протягом 30 хвилин через суміш барботували газоподібний хлористий водень. Колбу закривали мембраною і реакційна суміш перемішувалася протягом 2-х днів. Після видалення розчинника в роторному випарнику залишок розчиняли в метанолі (1-2мл) і розбавляли DCM (20мл). Збирали кристали, що утворилися, і промивали додатковою кількістю DCM з отриманням після вакуумного сушіння N-гідроксі-2(R)-[(4-фтор3-метилфенілсульфоніл)]аміно-3метилбутираміду. ЯМР (500МГц, CD3OD) δ: 0,86 (д, 3Н), 0,91 (д, 3Н), 1,86 (м, 1H), 2,30 (д, 3Н), 3,30 (д, 1Н), 7,16 (т, 1Н), 7,67 (м, 1H), 7,72 (м, 1Н). Вихідні продукти для прикладу 1 отримували таким чином: D-Валін (1,39г, 11,9ммоль) розчиняли в 80мл суміші діоксан/вода (1:1), що містить K2СО3 (3,3г, 24ммоль). При ретельному перемішуванні додавали по краплях розчин 4-фтор-3метилфенілсульфонілхлориду (10ммоль) в діоксані (4мл). Реакційну суміш перемішували при кімнатній температурі протягом 30 хвилин. Додавали етилацетат (80мл), 1н НСl (50мл). Органічний шар два рази промивали 1н НСl і екстрагували 5% K2СО3 (3 25мл). Об'єднані основні екстракти підкисляли і екстрагували етилацетатом (80мл). Органічний шар промивали насиченим розчином солі (2 рази), сушили над Na2SO4. У роторному випарнику видаляли розчинник і залишок розтирали в гексані. Тверду речовину, що утворилася, сушили з отриманням 2(R)-[(4-фтор-3метилфенілсульфоніл)]аміно-3-метилмасляної кислоти. 2(R)-[(4-Фтор-3-метилфенілсульфоніл)]аміно3-метилмасляну кислоту (2,64г, 9,12ммоль) розчиняли в DCM (30мл) і потім додавали DIEA (3,18мл, 2екв.) і гідрохлорид О-трет-бутилгідроксиламіну (2,3г, 2екв.). Потім порціями додавали EDC.HCl (2,1г, 1,2екв.) у вигляді твердої речовини. Через 40 хвилин додавали додаткову кількість EDC (0,6г, 0,5екв.) і реакційну суміш перемішували протягом ще 30 хвилин. У роторному випарнику при кімнатній температурі видаляли розчинник і залишок розподіляли між етилацетатом (80мл) і 1н НСl (50мл). Органічний шар промивали 1н НСl, насиченим розчином солі і сушили над Na2SO4. Неочищений продукт очищали флешхроматографією на колонках при елююванні розчинником з градієнтом, яким був 5-12% етилацетат в DCM, з отриманням продукту N-трет-бутоксі2(R)-[(4-фтор-3-метилфенілсульфоніл)]аміно-3метилбутираміду у вигляді білої піни. ТШХ (TLC) (етилацетат:DСМ 1:10) Rf 0,16. ЯМР (500 МГц, CD3OD) δ: 0,89 (д, 3Н), 0,90 (д, 3Н), 1,08 (с, 9Н), 1,86 (м, 1Н), 2,30 (д, 3Н), 3,44 (д, 1Н), 7,18 (т, 1H), 55 7,70 (м, 1H), 7,77 (м, 1Н). 76059 56 гом 2-х годин. Смолу три рази промивали DMF і три рази - DCM. До смоли додавали розчин DIEA (73мкл, 0,42ммоль, 4екв.) в суміші THF-DCM (0,5мл, 1:1), що містить DMAP (~2мг), потім додавали розчин 3-хлорфенілсульфонілхлориду (66мг, 3екв.) в суміші THF-DCM (0,5мл). Через 3 години смолу три рази промивали DMF, три рази - DCM і У прикладі 2, відповідно до методики прикладу двічі розщеплювали сумішшю 5% TFA/DCM 1, з D-4'-тетрагідропіранілгліцину отримували N(0,5мл) протягом 30 хвилин. Випаровували отригідроксі-2(R)-[(4-фтор-3маний при розщепленні об'єднаний розчин і залиметилфенілсульфоніл)]аміно-2-(4'шок розчиняли в суміші CH3CN:H2O і очищали тетрагідропіраніл)ацетамід. ЯМР (500МГц, CD3OD) ВЕРХ із оберненою фазою з отриманням сполуки δ: 1,19 (м, 1Н), 1,34 (м, 1Н), 1,40 (м, 1Н), 1,74 (м, прикладу 25, якою є амід N-гідроксі-2(R)-(31Н), 1,80 (м, 1Н), 2,32 (д, 3Н), 3,31 (м, 2Н), 3,37 (д, хлорфенілсульфоніл)аміно-3(S)1Н), 3,90 (м, 2Н), 7,18 (т, 1Н), 7,65 (м, 1Н), 7,72 (м, метилвалеріанової кислоти. ЯМР (500МГц, 1Н). CD3OD) δ: 0,82 (д,д, 6Н), 1,04 (м, 1H), 1,35 (м, 1Н), Приклади 3-144 1,64 (м, 1H), 3,52 (д, 1Н), 7,50 (т, 1H), 7,60 (д, 1H), Приклади 3-144, представлені в таблиці 1, 7,76 (д, 1H), 7,84 (м, 1Н). здійснювали в твердій фазі таким чином. У таблиці 1 перераховані структури сполук Стадія 1. Структурування смоли прикладів 3-144. Фахівцям в даній галузі зрозуміло, що, відповідно до методики отримання сполуки прикладу 3, з деякими змінами можуть бути отримані сполуки прикладів 4-144. Для деяких сполук після відщеплення смоли необхідна стадія видаРозчин N-гідроксифталіміду (2,8г, 17ммоль), лення захисної групи (обробка сумішшю 50% DIEA (3,0мл, 17ммоль) в дихлорметані (30мл) і TFA/DCM). DMF (15мл) швидко додавали до 4,39г 2Приклад 145 хлортритилової смоли (завантаження 1,1ммоль/г) в забезпеченому фритою картриджі. Суспензію смоли переривисто струшували і залишали на столі на ніч. Смолу п'ятикратно промивали DMF і потім обробляли 40мл розчину гідразину (0,5Μ в 2(R)-[(4-фтор-3-метилфеніл)сульфоніл]аміноTHF) протягом 2-х годин. Навколо смоли утворю3-(S)-циклопропілмасляну кислоту (10мг, валася велика кількість білої твердої речовини. її 31мкмоль) розчиняли в DMF (0,3мл) в присутності два рази промивали сумішшю DMF-вода (1:1) і НОВТ (4,5мг, 0,031ммоль), DIEA (11мкл, чотири рази - DMF. Обробку гідразином повторю0,062ммоль), О-триметилсилілгідроксиламіну вали більше одного разу протягом ще 3-х годин. (20мкл, 0,16ммоль). Додавали розчин РуВОР Смолу два рази промивали сумішшю DMF-вода (20мг, 0,038ммоль) в DMF (0,3мл). Через 30 хви(1:1), чотири рази - DMF, п'ять разів - DCM, сушили лин реакційну суміш гасили сумішшю CH3CN:H2O у вакуумі всю ніч з отриманням 4,53г смоли 1. (1:1, 5% TFA) і обробляли ВЕРХ із оберненою фаПриріст становив приблизно 1,0ммоль/г зміни мазою з отриманням після ліофілізації N-гідроксі-2си. (R)-[(4-фтор-3-метилфеніл)сульфоніл]аміно-3-(S)Стадія 2. Завантаження амінокислоти циклопропілбутираміду. ЯМР (500МГц, CD3OD) δ: 0,04 (м, 1H), 0,20 (м, 1Н), 0,35 (м, 1H), 0,41 (м, 1Н), 0,54 (м, 1H), 0,90 (д, 3Н), 1,08 (м, 1H), 2,32 (д, 3Н), 3,60 (д, 1H), 7,17 (т, 1Н), 7,68 (м, 1Н), 7,75 (м, 1H). МС: 331,1 (М+Н+). 500мг (завантаження ~1,0ммоль/г) О-зв'язаної Вихідні продукти для прикладу 145 отримувагідроксиламінової смоли і піддавали набуханню в ли таким чином: DCM в картриджі, забезпеченому фритою, і дренуМетилгліколят (10,4г, 114ммоль), кротиловий вали. Додавали розчин Fmoc-D-алоізолейцину спирт (100мл, надлишок) кип'ятили із зворотним (530мг, 1,5ммоль, 3екв.), DIC (0,120мл, 0,75ммоль, холодильником в присутності K2СО3 (0,8г) протя1,5екв.) в 3мл DMF. Недовго струшували картридж гом 1 години, при цьому протягом вказаного часу і залишали на столі протягом 1 години. Додавали через пастку Діна-Старка було видалено приблизще одну порцію DIG (0,04мл, 0,25ммоль, 0,5екв.). но 10мл конденсату. Після розбавлення гексаном Через годину смолу чотири рази промивали DMF, (100мл) тверду речовину фільтрували через корочотири рази - DCM і всю ніч сушили у вакуумі з тку колонку з силікагелем (50г), промивали сумішотриманням смоли 2. Приблизний приріст станошю етилацетат:гексан (250мл) при співвідношенні вив 0,70ммоль/г приросту маси. компонентів в суміші 1:5. Об'єднаний фільтрат і Стадія 3 промивки концентрували до 100мл і знову розбавляли гексаном (100мл), пропускали через колонку з силікагелем і промивали. Розчин концентрували з отриманням ~12,5г масла, яке переганяли у вакуумі з отриманням кротилгліколяту: 9,3г (97°С/20ммHg) у вигляді суміші цис-:транс-ізомерів 150мг смоли 2, завантаження ~0,7ммоль/г, об(1:10). ЯМР (500МГц, CDCl3) δ: 1,3 (м, 3Н), 4,15 (с, робляли 2 мл суміші піперидин/DMF (25%) протя 57 76059 58 2Н), 4,62 (д, 2Н), 5,6 (м, 1Н), 5,84 (м, 1H), інші піки розчинника одержували 5,3г трифлату у вигляді перекриваються транс-ізомером. масла. Його перемішували протягом 15год. з NaN3 Вищевказаний отриманий кротилгліколят (2,4г, 36ммоль) у DMF (80мл). Реакційну суміш (9,3м, 71ммоль) у THF (10мл) повільно додавали розбавляли етилацетатом (400мл), промивали три при -78°С до розчину LiN(TMS)2 (200мл, 1,0М) у рази розведеною НСl, два рази - насиченим розTHF (200мл). Через 40 хвилин при зазначеній темчином соли і сушили над Na2SO4. Після випарюпературі додавали триметилсилілхлорид (25,5мл, вання розчинника залишалося 2,96г масла. У ре200ммоль). Видаляли охолоджувальну ванну ізультаті здійснення флеш-хроматографії в колонку реакційна суміш перемішувалася всю ніч. Реакційіз силікагелем з використанням як елюенту 5% ну суміш концентрували до ~150мл і розбавляли простого ефіру в гексані одержували метил-2етилацетатом (500мл). Її двічі промивали 2н НСl. азидо-3-циклопропілбутират у вигляді безбарвного Промивання реекстрагували додатковою кількістю масла. Необхідний діастереоізомер 1 [(2R,3S) і етилацетату. Об'єднаний органічний шар тричі (2S,3R)] може бути виділений препаративною екстрагували 5% K2СО3. Об'єднаний лужний розВЕРХ із оберненою фазою при елююванні розчинчин підкисляли холодною концентрованою НСl, ником із градієнтом, яким була суміш CH3CN:H2O. екстрагували етилацетатом. ЯМР (500МГц, CDCl3) для діастереомера 1 Етилацетатний розчин промивали насиченим [(2R,3S) і (2S,3R) ] δ:0,04 (м, 1H), 0,18 (м, 1Н), 0,48 NaCl, сушили над Na2SO4. У результаті випарю(м, 2Н), 0,74 (м, 1H), 1,09 (д, 3Н), 1,35 (м, 1H), 3,80 вання розчинника і вакуумного сушіння одержува(с, 3Н), 3,92 (д, 1H). ли 2-гідрокси-3-метилпропен-4-енову кислоту у Вищевказаний виділений діастереоізомер виді суміші діастереоізомерів. ЯМР (500Мгц, [(2R,3S) і (2S,3R)]азиду (400мг, 2,2ммоль) розчиCD3OD) для діастереомера 1 [(2R,3S) і (2S,3R)] няли в МеОН (10мл), охолодженому на водяній 6:1,02 (д, 3Н), 2,60 (м, 1H), 4,05 (д, 1H), 5,02 (м, бані при 20°С. Додавали хлорид олова (II) (860мг, 1Н), 5,09 (м, 1Н), 5,87 (м, 1Н); діастереомер 2 4,4ммоль). Суміш перемішувалася протягом 15 [(2R,3R) і (2S,3S)] 5:1,11 (д, 3Н), 2,6 (м, 1Н), 4,03 годин. До реакційної суміші додавали діоксан (д, 1Н), 5,0 (м, 1H), 5,09 (м, 1Н), 5,80 (м, 1Н). (10мл), суміш K2СО3 (1,5г, 10,1ммоль)/Н2О (10мл). Відношення діастереоізомерів, визначене Відфільтровували тверду речовину і промивали ЯМР, складало приблизно 7:1, при цьому основдіоксаном (5мл). До об'єднаних фільтрату і проминим був діастереоізомер 1. вкам додавали розчин 4-фтор-3Вищевказану отриману кислоту (8,5г, метилфенілсульфонілхлориду (560мг, 2,4ммоль) у 65ммоль) розчиняли в сухому DMF (100мл) і DIEA діоксані (5мл). Через 30 хвилин реакційну суміш (16мл, 91ммоль). Додавали метилйодид (11,7мл, підкисляли НСl до рН3 і розбавляли сумішшю 85ммоль). Отримана суміш перемішувалася проCH3CN:H2O. У результаті препаративної ВЕРХ із тягом 15 годин і її розбавляли етилацетатом оберненою фазою (повторні інжекції) виділяли (500мл), промивали три рази 0,1н НСl, два рази продукт, яким був метил-2-(4-фтор-3насиченим розчином соли і сушили над Na2SO4. метилфенілсульфонамідо)-3-циклопропілбутират. Після випарювання розчинника залишався складПісля додаткового розділення через колонку ний метил-2-гідрокси-3-метилпентен-4-еновий Chiralpk AD при елююванні 7%. EtOH у гептані ефір. ЯМР (500МГц, CD3OD) для діастереомера 1 одержували два енантіомери, причому необхідний [(2R,3S) і (2S,3R)] 6:1,02 (д, 3Н), 2,55 (м, 1Н), 3,70 ізомер 1 (2R,3S) екстрагувався першим. ЯМР (с, 3Н), 4,04 (д, 1H), 5,02 (м, 1Н), 5,06 (м, 1H), 5,81 (500МГц, CD3OD) δ:0,01 (м, 2Η), 0,39 (м, 2Η), 0,62 (м, 1H); діастереомер 2 [(2R,3R) і (2S,3S)] 5:1,08 (м, 1H), 1,01 (д, 3Н), 1,19 (м, 1Н), 2,312 (д, 3Н), (д, 3Н), 2,58 (м, 1H), 3,70 (с, 3Н), 4,07 (д, 1Н), 5,00 3,23 (с, 3Н), 3,90 (д, 1H), 7,18 (т, 1Н), 7,68 (м, 1Н), (м, 1Н), 5,06 (м, 1Н), 5,80 (м, 1H). 7,73 (м, 1H). Вищевказаний отриманий складний метилоСкладний метиловий ефір 2(R)-[(4-фтор-3вий ефір (2,9г, 20ммоль) розчиняли в сухому DCM метилфеніл)сульфоніл]аміно-3-(S)(100мл) у присутності дійодметану (8,1мл, циклопропілмасляної кислоти (20мг, 0,061ммоль) 100ммоль) і охолоджували до 0°С. Додавали розрозчиняли в МеОН (0,2мл), потім додавали суміш чин діетилцинку (100мл, 1,0М в гексані). Видаляли LiOH (8мг, надлишок)/Н2О (0,15мл). Через 2 годиохолоджувальну ванну і суміш перемішувалася під ни реакційну суміш підкисляли 1,5мл суміші азотом протягом 3-х днів. Для гасіння реакції доCH3CN:H2O (1:1, 5% TFA) і піддавали ВЕРХ із обедавали розчин NH4Cl. Органічний шар два рази рненою фазою з одержанням 2(RІ)-(4-фтор-3промивали НСl, два рази - насиченим розчином метилфенілсульфонамідо)-3-(S)соли і сушили над Na2SO4. Після випарювання циклопропілмасляної кислоти. ЯМР (500МГц, розчинника залишалося масло, що містить 70% CD3OD) δ: -0,01 (м, 1H), 0,15 (м, 1H), 0,40 (м, 2Η), продукту, яким був метил-2-гідрокси-30,65 (м, 1Η), 1,02 (д, 3Н), 1,22 (м, 1H), 2,31 (д, 3Н), циклопропілбутират, і 30% вихідного продукту. 4,83 (д, 1Н), 7,16 (т, 1Н), 7,69 (м, 1H), 7,75 (м, 1Н). Його використовували без подальшого очищення. Розчин вищевказаного отриманого складного ефіру (3г, 20ммоль), піридину (2,0мл, 24ммоль) у сухому DCM (10мл) при 0°С повільно додавали до розчину, що перемішується, Tf2O (4мл, 24ммоль) у DCM (100мл). Для гасіння реакції через 1 годину при 0°С додавали воду. Потім суміш промивали 2(R)-[(4-Фтор-3-метилфеніл)сульфоніл]амінорозведеною НСl (0,1н), насиченим розчином соли і 3(R)-циклопентоксилмасляну кислоту (11мг, сушили над Na2SO4. У результаті випарювання 59 76059 60 0,03ммоль) розчиняли в DMF (200мкл) у присутно1,28 (д, 3Н), 1,4-1,7 (м, 8Н), 3,92 (м, 1H), 4,06 (д, сті DIEA (12мкл, 0,12ммоль), НОВТ (8мг, 1Н), 4,14 (д кв,1H), 5,26 (д, J=12Гц, 1Н), 5,31 (д, 0,06ммоль) і TMSONH2 (10мкл, 0,08ммоль). ДодаJ=12Гц, 1Н), 7,38 (м, 3Н), 7,43 (м, 2Н). вали розчин РуВОР (31мг, 0,06ммоль) у DMF Трифторацетат бензил-2(R)-аміно-3(R)(100мкл). Через 20 хвилин реакцію гасили сумішциклопентоксилбутирату (63мг, 0,16ммоль), DIEA шю 5% TFA/H2O і в результаті ВЕРХ із оберненою (174мкл, 1,0моль), DMAP (1мг) розчиняли в діокфазою після ліофілізації виділяли продукт, яким сані (2мл), після чого повільно додавали розчин 4був N-гідроксі-2(R)-[(4-фтор-3фтор-3-метилфенілсульфонілхлориду метилфеніл)сульфоніл]аміно-3(R)(~0,33ммоль) в діоксані (1мл). Через 15 хвилин циклопентоксилбутирамід. ЯМР (500МГц, CD3OD) реакцію гасили сумішшю 5% TFA/H2O і очищали δ:0,97 (д, 3Н), 1,44-1,68 (м, 8Н), 2,32 (д, JH-F, 3Н), ВЕРХ із оберненою фазою з отриманням бензил3,61 (д, 1H), 3,72 (м, 1H), 3,67 (м, 1Н), 7,18 (м, 1Н), 2(R)-[(4-фтор-3-метилфеніл)сульфоніл]аміно-3(R)7,70 (м, 1Н), 7,76 (м, 1H). циклопентоксилбутирату. Захисну групу для склаВихідні продукти для приклада 146 одержувадного бензилового ефіру видаляли гідруванням в ли в такий спосіб: суміші МеОН:ЕА (1мл) з використанням 10% Pd/C N-Тритил-В-треонінбензиловий ефір (2,5г, (2мг) протягом ночі з отриманням при цьому 2(R)5,5ммоль), TEA (2,8мл, 20ммоль) розчиняли при [(4-фтор-3-метилфеніл)сульфоніл]аміно-3(R)50°С в 100мл сухого толуолу. Протягом 15 хвилин циклопентоксилмасляної кислоти. додавали розчин сульфурилхлориду (800мкл, Відповідно до методики прикладу 146, з вико8ммоль) в толуолі (20мл). Реакційній суміші даваристанням модифікацій, відомих фахівцям в даній ли можливість нагріватися до к.т. Додавали етигалузі, отримували сполуки прикладів 147-153, лацетат (100мл) і суміш промивали насиченим представлених в таблиці 2. розчином NaCl і сушили над Na2SO4. Продукт криАналіз для виявлення інгібування летального сталізували в МеОН (10мл) з одержанням бензилфактора N-тритил-3(S)-метилазиридин-2(R)-карбоксилату. Наведений нижче аналіз розкритий [в: ЯМР (500МГц, CDCl3) δ: 1,37 (д, 3Н), 1,64 (м, 1Н), Cummings et al., PNAS, May 14, 2002, vol.99, №10, 1,95 (д, 1Н), 5,15 (д, J=12Гц, 1H), 5,28 (д, J=12Гц, page 6603-6606 і в заявці США 03/05552 від 1H), 7,19-7,28 (м, 12 Η), 7,33-7,36 (м, 1H), 7,36-7,39 2/21/2003, поданої відповідно до договору РСТ (м, 3Н), 7,51-7,54 (м, 4Н). (заявка на патент США №60/359707, подана Бензил-N-тритил-3(S)-метилазиридин-2(R)2/25/2002)], включеної в даний опис як посилання карбоксилат (2,13г, 4,92ммоль) при 0°С розчиняли у всій своїй повноті. Термін «інгібування летальнов 20мл суміші MeOH:DCM (1:1), потім додавали го фактора» означає, що летальний фактор провTFA (20мл). Після перемішування при кімнатній заємодіяв із сполукою і вважається, що така спотемпературі протягом 1 години в роторному випалука є інгібітором летального фактора. рнику видаляли надлишок реагенту і розчинник Сполуки, що інгібують летальний фактор, мо(Т
ДивитисяДодаткова інформація
Назва патенту англійськоюCompounds used for treating anthrax or inhibiting lethal factor
Назва патенту російськоюСоединения, используемые для лечения сибирской язвы и ингибирования летального фактора
МПК / Мітки
МПК: A61K 31/00, A61K 35/00
Мітки: сполуки, інгібують, сибірки, лікуванні, летальний, застосовуються, фактор
Код посилання
<a href="https://ua.patents.su/31-76059-spoluki-shho-zastosovuyutsya-pri-likuvanni-sibirki-i-ingibuyut-letalnijj-faktor.html" target="_blank" rel="follow" title="База патентів України">Сполуки, що застосовуються при лікуванні сибірки і інгібують летальний фактор</a>
Попередній патент: Опорна система доменної печі
Наступний патент: Металокерамічний фрикційний матеріал на основі дибориду титану
Випадковий патент: Ядерна енергетична установка та спосіб її будівництва