Похідні 3-оксопіридазину як антагоністи брадикініну b1
Номер патенту: 108373
Опубліковано: 27.04.2015
Автори: Чечі Анджело, Вальтер Райнер, Конетцкі Інго, Мак Йюрген, Пріпке Хеннінг, Віденмайєр Дітер, Доодс Хенрі, ХАУЕЛЬ Норберт, Шулер-Метц Аннетте
Формула / Реферат
1. Сполука загальної формули І
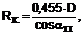 , (І)
, (І)
в якій
R1 означає групу
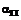 ,
,
R2 означає Η або СН3,
R3 і R4 спільно з атомом вуглецю, до якого вони приєднані, утворюють С3-С6циклоалкіленову групу, в якій одна -СН2-група може бути замінена на атом кисню,
R5 означає Η або СН3,
R6 означає H, F, Сl або метил,
R7 означає Н, F, Сl, Br, -CN, С1-С4алкіл, CF3 або CHF2,
R8 означає H,
R9 означає F, Сl, Br, С1-С4-алкіл, -О-С1-С4-алкіл або -S-С1-С4-алкіл,
R10 означає H,
R11 означає F, Сl, Br, -CN, С1-С4алкіл, CF3 або CHF2, і
X означає СН або N,
або її енантіомер, її діастереомер, їх суміш або її сіль.
2. Сполука за п. 1, в якій R2 означає Н, або її енантіомер, її діастереомер, їх суміш або її сіль.
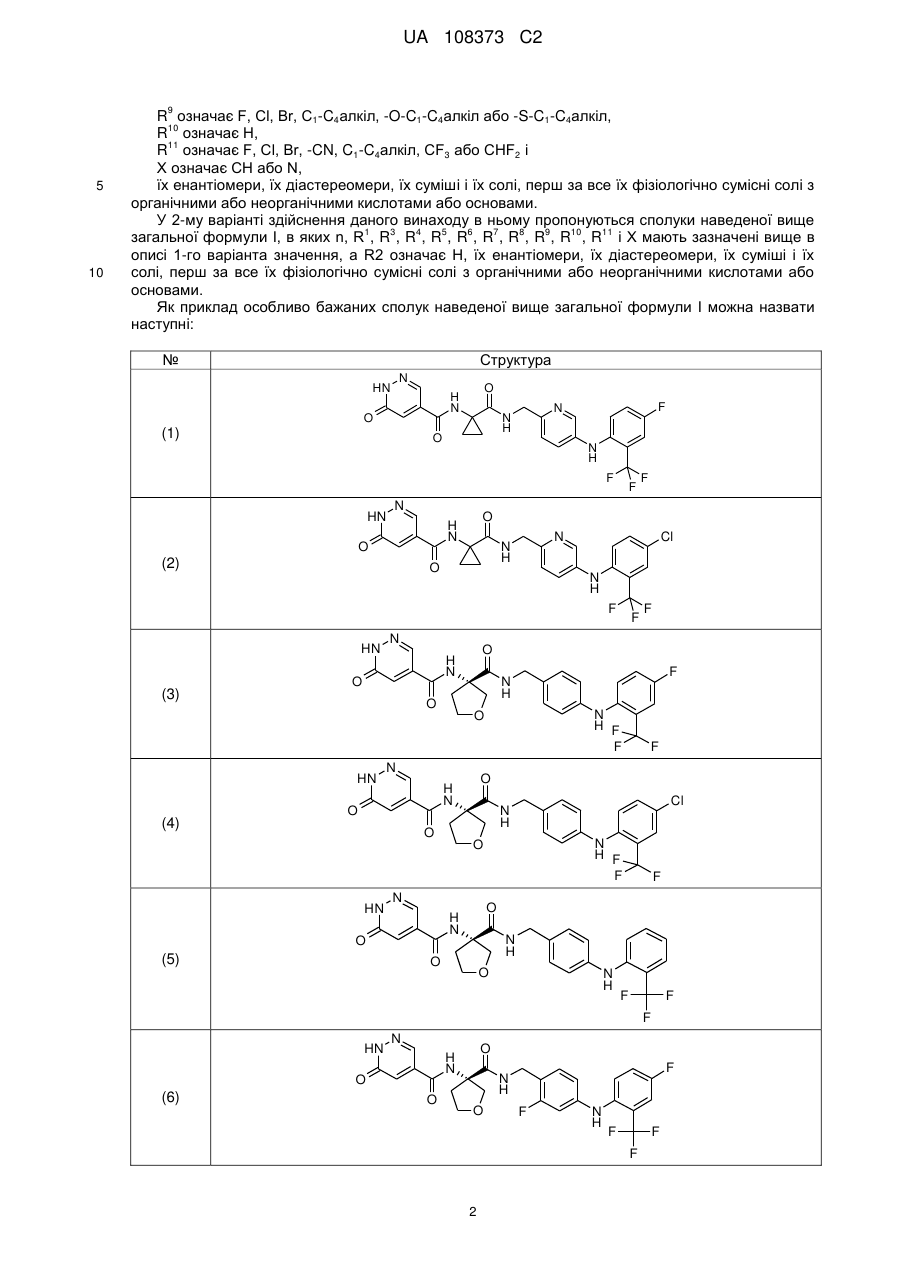
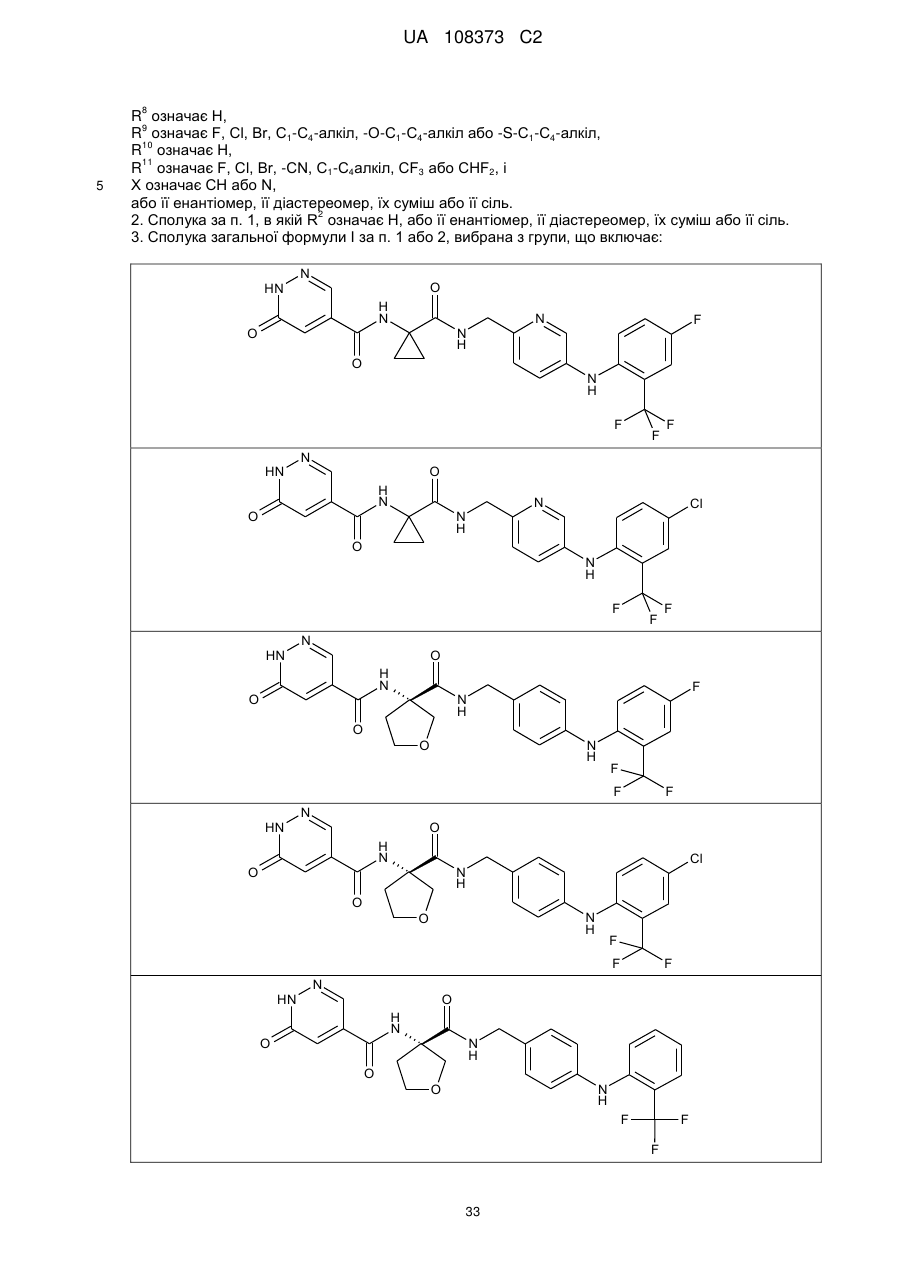
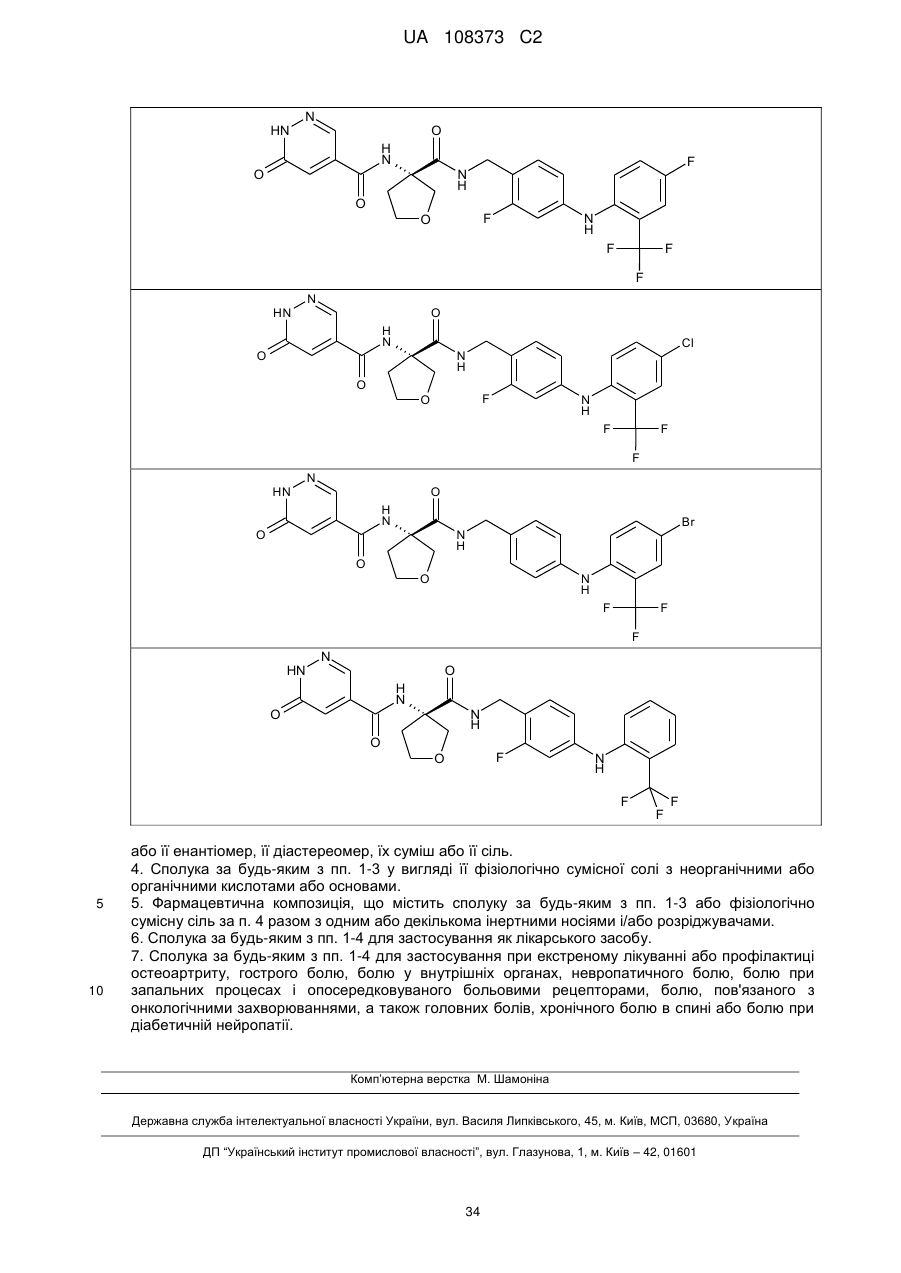
3. Сполука загальної формули І за п. 1 або 2, вибрана з групи, що включає:

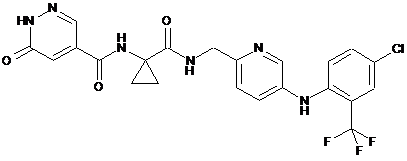






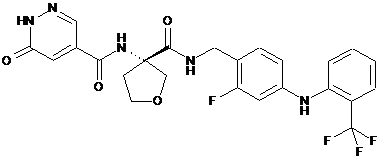
або її енантіомер, її діастереомер, їх суміш або її сіль.
4. Сполука за будь-яким з пп. 1-3 у вигляді її фізіологічно сумісної солі з неорганічними або органічними кислотами або основами.
5. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-3 або фізіологічно сумісну сіль за п. 4 разом з одним або декількома інертними носіями і/або розріджувачами.
6. Сполука за будь-яким з пп. 1-4 для застосування як лікарського засобу.
7. Сполука за будь-яким з пп. 1-4 для застосування при екстреному лікуванні або профілактиці остеоартриту, гострого болю, болю у внутрішніх органах, невропатичного болю, болю при запальних процесах і опосередковуваного больовими рецепторами, болю, пов'язаного з онкологічними захворюваннями, а також головних болів, хронічного болю в спині або болю при діабетичній нейропатії.
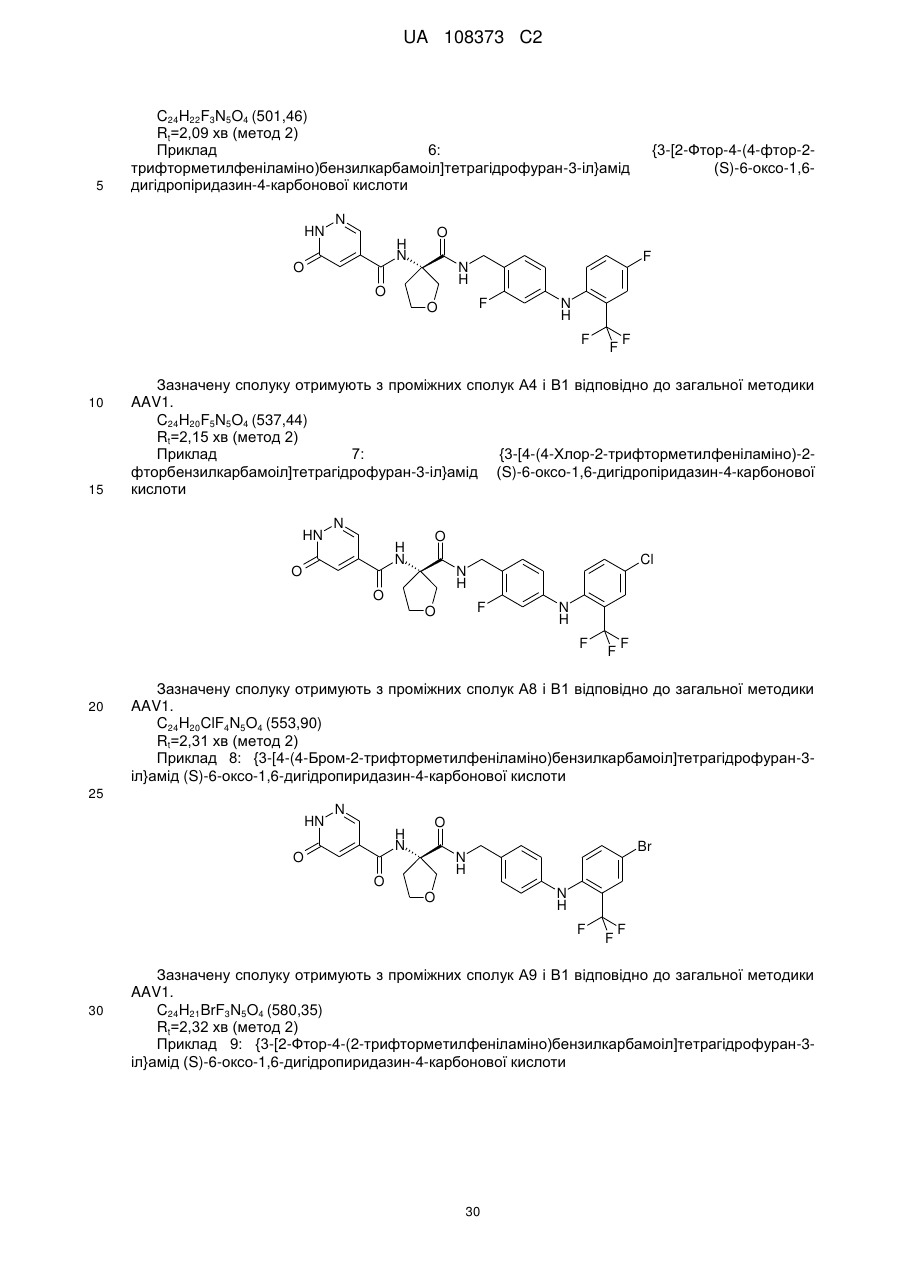
Текст
Реферат: У заявці описані сполуки загальної формули (І) UA 108373 C2 ДЕРЖАВНА СЛУЖБА ІНТЕЛЕКТУАЛЬНОЇ ВЛАСНОСТІ УКРАЇНИ UA 108373 C2 R R 1 2 O N O R 5 X N R 3 R 4 R R R 8 7 R 9 2 R 6 N R R 2 R 11 10 , (І) 1 2 3 4 5 6 7 8 9 10 11 в якій n, R , R , R , R , R , R , R , R , R , R , R і X мають зазначені в описі винаходу значення, їх енантіомери, їх діастереомери, їх суміші та їх солі, перш за все їх фізіологічно сумісні солі з органічними або неорганічними кислотами або основами, які мають цінні властивості, спосіб їх отримання, лікарські засоби, що містять такі фармакологічно активні сполуки, спосіб їх приготування та їх застосування. UA 108373 C2 Даний винахід належить до таких, що мають цінні властивості сполук загальної формули I R R 1 2 O N O R R 5 R X N 3 R 4 R R 7 10 15 20 25 1 2 3 4 5 6 N (I), R 6 N 7 8 9 10 R 10 11 11 N N N H N HO * * O O Від відомих з рівня техніки сполук запропоновані у винаході нові сполуки відрізняються тим, що вони проявляють високу дію блокаторів рецептора B1 і одночасно з цим мають кращу метаболічну стабільність. Докладний опис винаходу У 1-му варіанті здійснення винаходу в ньому пропонуються сполуки наведеної вище загальної формули I, у якій HN 1 40 2 R H O 35 9 в якій n, R , R , R , R , R , R , R , R , R , R , R і X мають зазначені в подальшому описі значення, їх енантіомерів, їх діастереомерів, їх сумішей і їх солей, перш за все їх фізіологічно сумісних солей з органічними або неорганічними кислотами або основами, до способу їх отримання, до лікарських засобів, які містять такі фармакологічно активні сполуки, до способу їх приготування і до їх застосування. Передумови створення винаходу Галузь техніки, до якої належить винахід Об'єктами даного винаходу е 3-оксопіридазинові сполуки та їх застосування в якості антагоністів рецептора B1, фармацевтичні композиції, що містять ці сполуки, а також способи їх застосування для попередження або лікування гострих болів, болів у внутрішніх органах, невропатичних болів, супроводжуючих запальні процеси і опосередковуваних больовими рецепторами болів, болів, пов'язаних з онкологічними захворюваннями, а також головних болів. Рівень техніки У заявці PCT/EP2010/052232, відповідно до такої, що полягаю в її основі пріоритетній заявці вже описані сполуки, що мають дію антагоністів брадікінінового рецептору B1. В основу даного винаходу була покладена задача запропонувати нові сполуки, які були б придатні для застосування насамперед у якості фармакологічних діючих речовин у лікарських засобах, які можна використовувати для лікування захворювань, щонайменше частково опосередковуваних рецептором B1. Важливою відмінною рисою структури пропонованих у винаході нових сполук е 6-оксо-1,6дігідропірідазін-4-карбоксамідна група, яка знаходиться в таутомерній рівновазі з 6 гідроксіпірідазін-4-карбоксамідною групою: HN 30 R 2 R 5 8 O N * R означає групу , 2 R означає H або CH3, 3 4 R і R спільно з атомом вуглецю, до якого вони приєднані, утворюють C 3-C6 циклоалкіленову групу, в якій одна -CH2-група може бути замінена на атом кисню, 5 R означає H або CH3, 6 R означає H, F, Cl або метил, 7 R означає H, F, Cl, Br, -CN, C1-C4алкіл, CF3 або CHF2, 8 R означає H, 1 UA 108373 C2 9 5 10 R означає F, Cl, Br, C1-C4алкіл, -O-C1-C4алкіл або -S-C1-C4алкіл, 10 R означає H, 11 R означає F, Cl, Br, -CN, C1-C4алкіл, CF3 або CHF2 і X означає CH або N, їх енантіомери, їх діастереомери, їх суміші і їх солі, перш за все їх фізіологічно сумісні солі з органічними або неорганічними кислотами або основами. У 2-му варіанті здійснення даного винаходу в ньому пропонуються сполуки наведеної вище 1 3 4 5 6 7 8 9 10 11 загальної формули I, в яких n, R , R , R , R , R , R , R , R , R , R і X мають зазначені вище в описі 1-го варіанта значення, а R2 означає H, їх енантіомери, їх діастереомери, їх суміші і їх солі, перш за все їх фізіологічно сумісні солі з органічними або неорганічними кислотами або основами. Як приклад особливо бажаних сполук наведеної вище загальної формули I можна назвати наступні: № Структура N HN O H N O (1) O F N N H N H F HN N (2) Cl N N H O N H F HN (3) HN F Cl N H N H F F O N F O H N O N H F F O H N (5) F O O F N H N O F O H N O HN (4) N O F O H N O F N H O O N H F F F HN N O (6) O H N O F N H O F N H F F F 2 UA 108373 C2 № Структура HN N O H N O (7) Cl N H O O F N H F F F HN N O H N O (8) Br N H O O N H F F F HN N O (9) O H N N H O O F N H F 5 10 15 20 25 30 35 F F їх енантіомери, їх діастереомери, їх суміші і їх солі, перш за все їх фізіологічно сумісні солі з органічними або неорганічними кислотами або основами. Використовувані терміни і поняття Якщо не вказано інше, то всі замісники не залежать один від одного. За наявності у одній групи, наприклад, декількох C1-C4алкільних груп в якості замісників у разі трьох замісників вони можуть мати незалежні один від одного значення, тобто один з C1-C4алкільних замісників може бути метил, другий – н-пропіл, а третій – трет-бутил. У даному описі і в формулі винаходу при вказівці значень можливих замісників вони можуть бути також представлені у вигляді структурної формули. При цьому зірочка (*) при її наявності в структурній формулі замісника означає місце або положення, в якому такий замісник приєднаний до іншої частини молекули. Рівним чином в обсяг даного винаходу включені також ті запропоновані в ньому сполуки, в тому числі і їх солі, в яких один або кілька атомів водню, наприклад, один, два, три, чотири або п'ять атомів водню, заміщені на дейтерій. Під терміном "C1-C4алкіл" (в тому числі і коли він е фрагментом інших залишків) маються на увазі алкільні групи з 1-4 атомами вуглецю. Як приклад таких груп можна назвати метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, втор-бутил і трет-бутил. Для позначення подібних груп в деяких випадках використовуються також відповідні їм скорочені назви Me, Et, н-Pr, ізо-Pr, н-Bu, ізо-Bu, трет-Bu або tBu і т.д. Якщо не вказано інше, то в поняття "пропіл" і "бутил" включені також всі можливі ізомерні форми кожного з таких залишків. Так, наприклад, в поняття "пропіл" включені н-пропіл і ізопропіл, а в поняття "бутил" включені ізобутіл, втор-бутил і трет-бутил. Крім цього в зазначені вище поняття включені також ті залишки, в яких кожна метиленова група може бути заміщена 1 або 2, а кожна метильна група може бути заміщена 1-3 атомами фтору. Під терміном "C3-C6циклоалкіл" (в тому числі і коли він е фрагментом інших залишків) маються на увазі циклічні алкільні групи з 3-6 атомами вуглецю. Як приклад подібних залишків можна назвати циклопропіл, циклобутил, циклопентил або циклогексил. Сполуки загальної формули I при наявності у них прийнятних оснóвних функціональних груп, наприклад, аміногруп, можна перш за все для фармацевтичного застосування переводити в їх фізіологічно сумісні солі з неорганічними або органічними кислотами. В якості прикладу придатних для застосування в цих цілях неорганічних кислот можна назвати бромистоводневу кислоту, фосфорну кислоту, азотну кислоту, соляну кислоту, сірчану кислоту, метансульфонову кислоту, етансульфонову кислоту, бензолсульфонову кислоту або паратолуолсульфонову кислоту, а в якості прикладу органічних кислот можна назвати яблучну кислоту, бурштинову кислоту, оцтову кислоту, фумарову кислоту, малеїнову кислоту, мигдалеву кислоту, молочну кислоту, винну кислоту або лимонну кислоту. 3 UA 108373 C2 5 10 15 20 Крім цього сполуки загальної формули I при наявності у них прийнятних функціональних карбоксигруп можна насамперед для фармацевтичного застосування переводити в їх фізіологічно сумісні солі з неорганічними або органічними основами. В якості прикладу придатних для застосування в цих цілях неорганічних основ можна назвати гідроксиди лужних або лужноземельних металів, наприклад, гідроксид натрію або гідроксид калію, карбонати, аміак, гідроксиди цинку або амонію, а в якості прикладу органічних амінів можна назвати діетиламін, триетиламін, етаноламін, діетаноламін, триетаноламін, циклогексиламін або дициклогексиламін. Запропоновані у винаході сполуки за наявності в їх молекулі тільки одного елемента хіральності можуть бути представлені у вигляді рацематів, однак їх можна отримувати і у вигляді чистих енантіомерів, тобто в (R) - або (S)-формі. Разом з тим в обсяг даного винаходу включені і окремі діастереомерні пари антиподів або їх суміші, що існують при наявності у сполуках загальної формули I більше одного елемента хіральності, а також індивідуальні оптично активні енантіомери, з яких складаються згадані вище рацемати. Сполуки з одним подвійним вуглець-вуглецевим зв'язком можуть існувати і в E-, і в Z-формі. У тому випадку, коли сполука може існувати в різних таутомерних формах, під конкретно представленим або розглянутим з'єднанням мається на увазі не одна його таутомерна формах, а всі його таутомерні форми. Сказане в першу чергу відноситься також до азотовмісних гетероарилів: N N * 25 OH N H N * * O * Способи отримання пропонованих у винаході сполук Згідно винаходу сполуки загальної формули I отримують способами, які в принципі відомі, наприклад, розглянутими нижче способами. (A) Амідне сполучення 5 8 R 2 R 1 R O N OH 3 O R + R X HN 2 R X R 10 (R6)n 2 R (I) R N 4 R 9 7 R 11 R (III) (II) 30 35 40 45 Проілюстроване на наведеній вище схемі поєднання карбонових кислот загальної формули II, в якій всі залишки мають зазначені вище значення, з амінами загальної формули III, у якій всі залишки мають зазначені вище значення, з утворенням карбоксамід загальної формули I, у якій всі залишки мають зазначені вище значення, можна проводити звичайними методами утворення амідів. Вказану реакцію поєднання бажано проводити з використанням відомих з хімії пептидів методів (див., наприклад, Houben Weyl, Methoden der Organischen Chemie, т. 15/2), застосовуючи, наприклад, карбодііміди, такі як діціклогексілкарбодіімід (ДЦК), діізопропілкарбодіімід (ДІК) або етил-(3-диметиламінопропіл)карбодімід, гексафторфосфат або тетрафторборат O-(1H-бензотриазол-1-іл)-N, N,N',N'-тетраметилуронія (ГБТУ, відповідно ТБТУ) або гексафторфосфат 1H-бензотриазол-1-ілокси-трис-(диметиламіно)фосфонію (БОФ). Підвищити швидкість реакції можна додаванням 1 гідроксібензотріазола (ГОБТ) або 3 гідрокси 4-оксо-3,4-дигідро-1,2,3-бензотріазіна (ГООБТ). Реакції сполучення зазвичай проводять з використанням еквімолярних кількостей що піддаються поеднанню компонентів, а також агента поєднання в розчинниках, таких як дихлорметан, тетрагідрофуран (ТГФ), ацетонітрил, диметилформамід (ДМФ), диметилацетаміді (ДМА), N метілпірролідон (N-МП) або їх суміші. При 4 UA 108373 C2 необхідності додатково використовують діізопропілетіламін (ДІПЕА, основа Хюніга). (Б) Амідне сполучення 2 R 5 O HN R 4 R R R 11 2 R R R X (R6)n (V) R 8 7 R 35 5 8 R 9 X HN R N R R 2 R R 10 11 2 X (R6)n 9 7 R R 10 R N 2 R 11 R (III) (VI) 30 O R N OH Інший метод одержання сполук загальної формули I полягаю в поєднанні карбонових кислот загальної формули V, в якій всі залишки мають зазначені вище значення, з амінами загальної формули IV, в якій всі залишки мають зазначені вище значення. Сполуки загальної формули V або е у продажу, або їх можна одержувати відомими з літератури методами. Крім цього існує можливість переводити карбонові кислоти загальної формули V в їх хлорангідриди з подальшим їх взаемодіею з амінами загальної формули IV. Хлорангідриди карбонових кислот синтезують відомими з літератури методами (див., наприклад, Houben Weyl, Methoden der Organischen Chemie, т. E5 / 1). (В) Відновлення нітрильної групи X 25 як (I) 10 (IV) N 20 1 R + X 5 15 наприклад, 9 7 X (R6)n 10 таку, R 2 R основу, 8 R N 3 допоміжну Відновлення нітрилу загальної формули VI до аміну загальної формули III, у якій залишок R2 у амінного атома азоту означає водень, а інші залишки мають зазначені вище значення, можна проводити в стандартних умовах каталітичного гідрогенолизом в присутності каталізатора, такого, наприклад, як нікель Ренея, у розчиннику, такому як аміачний розчин метанолу або етанолу, або в присутності відновника, такого як алюмогідрід літію або борогідрід натрію, в розчиннику, такому як тетрагідрофуран, при необхідності в присутності кислоти Льюїса, такої як хлорид алюмінію. Сполуки ж загальної формули III, у якій залишок R2 у амінного атома азоту означає не водень, а, наприклад, алкільний залишок, також можна отримувати з сполук загальної формули VI. Так, наприклад, в результаті взаємодії нітрилу загальної формули VI з алкілзаміщенним реактивом Грин'яра отримують кетони, які шляхом гідро амінування можна перевести в сполуки загальної формули III. Гідроамінування проводять відомими способами, наприклад, з використанням відновника, такого як тріацетоксіборогідрід натрію, борогідрід натрію або ціаноборогідрід натрію, переважно в розчиннику, такому як тетрагідрофуран або дихлорметан, при необхідності з додаванням оцтової кислоти. В іншому варіанті отримані кетони можна також переводити в оксими. В результаті подальшого відновлення оксимів в цьому випадку одержують сполуки загальної формули III. (Г) Нуклеофільне ароматичне заміщення або каталізоване перехідним металом сполучення 5 UA 108373 C2 8 8 R N X R Hal (R6)n (VII) 10 15 20 25 30 2 R X 10 R HN (R6)n 11 R (VIII) 9 7 R R 10 R N R 2 11 R (VI) Реакцію аніліну загальної формули VIII, в якій всі залишки мають зазначені вище значення, з нітрилом загальної формули VII, в якій X, R6 і n мають зазначені вище значення, а Hal означає атом фтору, хлору або брому, проводять за відомим методам, наприклад, в розчиннику, такому як тетрагідрофуран, диметилформамід або диметилсульфоксид, переважно у присутності підстави, такого як триетиламін, розчин їдкого натру або карбонат калію, при температурі в межах від 20 до 160 °C. У тому випадку, коли анілін загальної формули VIII являє собою рідину, реакцію можна також проводити у відсутність розчинника і додаткової основи. Інший метод одержання сполук загальної формули VI полягаю в каталізованій паладієм взаємодії нітрилу загальної формули VII, в якій Hal означає бром або хлор, з аніліном загальної формули VIII. Умови такого хімічного перетворення, відомого також як реакція БухвальдХартвіг, відомі з літератури. Опис методики за визначенню зв'язування з cynoBK1-рецептором Клітини яєчника китайського хом'ячка (CHO клітини), експресуються B1-рецептор мавпи Cynomolgus, культивують у середовищі Хема F12. Від злиплих клітин видаляють середовище, клітини промивають забуференим фосфатом фізіологічним розчином (ЗФР), зішкрібають або відокремлюють за допомогою версена і виділяють шляхом центрифугування. Потім клітини гомогенізують в суспензії, гомогенат центрифугують і ресуспендують. Після визначення вмісту білка 200 мкл гомогенату (50-250 мкг білка з розрахунку на один аналіз) протягом 60-180 хв інкубують при кімнатній температурі в присутності калідину (DesArg10, Leu9), [3,4-пролив-3, 43H (N) ] в 0,5-5,0-наномолярной концентрації і в присутності тестованої речовини в зростаючих концентраціях в загальному обсязі 250 мкл. Інкубацію припиняють шляхом швидкої фільтрації через скловолокнисті фільтри GF/B, попередньо оброблені поліетиленімін (0,3 %-ним). Пов'язану з білком радіоактивність вимірюють за допомогою лічильника TopCount NXT. За міру неспецифічного зв'язування беруть пов'язану радіоактивність в присутності 1,0-мікромолярних калідину (DesArg10). Криві концентрація-зв'язування аналізують шляхом комп'ютерного нелінійного узгодження кривих для визначення таким шляхом відповідних значень Ki для конкретного тестованої речовини. Результати дослідів за визначенню зв'язування з cynoBK1-рецептором Приклад № (1) (2) (3) (4) (5) (6) (7) (8) (9) 35 X R + X 5 9 7 R N Ki [нМ] 3,5 5,1 12 27 11 3,2 30 37 6,6 Важливою відмінною рисою структури запропонованих у винаході нових сполук е 6-оксо-1,6дігідропірідазін-4-карбоксамідна група, яка присутня у всіх пропонованих у винаході сполуках і яка знаходиться в таутомерній рівновазі з 6 гідроксіпірідазін-4-карбоксамідною групою: 6 UA 108373 C2 HN N N H N O 10 H N HO * * O O 5 N Від відомих з рівня техніки сполук запропоновані у винаході нові сполуки відрізняються тим, що вони проявляють високу дію блокаторів рецептора B1 і одночасно з цим мають значно кращою метаболічну стабільність. Метаболічну стабільність можна оцінювати, визначаючи розкладання в гепатоцитах людини і обчислюючи на підставі швидкості розкладання кліренс, який в свою чергу виражають у відсотках кровотоку через печінку людини (% Qh). Речовина з високим метаболічним кліренсом (наприклад, більше 70 % Qh) приблизно буде проявляти в організмі людини дію, яка за своєю тривалістю коротше тривалості дії речовини, яка метаболічно стабільніше і яка тим самим проявляє менший кліренс (наприклад, менше 30 % Qh). Тому для досягнення необхідної тривалої дії наявність високої метаболічної стабільності (низький кліренс) у діючої речовини е значною перевагою. Запропоновані у винаході нові сполуки несподівано виявляють низький кліренс в гепатоцитах людини, як це випливає з наведеної нижче таблиці: 15 Приклад № (1) (3) (5) (6) 20 25 30 Ki [нМ] 3,5 12 11 3,2 Кліренс [% Qh] 1 7 22 6 Методика визначення метаболічного кліренсу в гепатоцитах людини Метаболічний розпад тестованої речовини визначають у суспензії гепатоцитів. Кріоконсервовані первинні гепатоцити людини інкубують в прийнятному інкубаційному середовищі (наприклад, в модифікованому за способом Дульбекко середовищі Ігла, DMEM), що містить сироватку людини в кількості 5 %. Після 30-хвилинної попередньої інкубації в інкубаторі (37 °C, 10 % діоксиду вуглецю) до 395 мкл суспензії гепатоцитів (концентрація клітин у межах від 0,25 до 1 млн клітин на мл, зазвичай 1 млн клітин на мл; кінцева концентрація тестованої речовини 1мкм) додають 5 мкл тестованої речовини (80-мікромолярного, отриманого з 2міллімолярного концентрованого розчину в диметилсульфоксиді і розведеного інкубаційним середовищем в пропорції 1:25). Клітини протягом 6 год. інкубують в інкубаторі з орбітальним шейкером. У моменти часу 0, 0,5, 1, 2, 4 і 6 год. відбирають за 25 мкл середовища. Відібрані порції середовища змішують з надлишком ацетонітрилу і центрифугують протягом 5 хв. Надосадову рідину відбирають, концентрують досуха в атмосфері азоту і розводять в суміші з 25 % метанолу і 0,1 %-ної мурашиної кислоти. Зменшення концентрації тестованої речовини в інкубаційному середовищі визначають шляхом рідинної хроматографії у поєднанні з масспектроскопіею з іонізаціею електроспреем. Для обчислень використовують лінійну фазу зменшення концентрації тестованої речовини в середовищі. Власний кліренс обчислюють за наступною формулою: 35 CLвласн. = доза/AUC = (C0/CD)/(AUD+cкінц./k)•1000/60, 40 де C0 означає вихідну концентрацію в інкубаційному середовищі [мкМ], CD означає концентрацію живих клітин [106 клітин / мл], AUD означає площа під кривою [мкМ•ч], cкінц. означає концентрацію в останній експериментальній точці [мкМ], а k означає нахил прямої регресії для зменшення концентрації тестованої речовини [h-1]. Далі обчислений таким шляхом власний кліренс in vitro перераховують у власний кліренс in vivo за наступною формулою: 6 45 CLвласн. in vivo [мл/хв/кг] = (CLвласн. [мл/хв/10 клітин] • 6 • гепатоцелюлярність [10 клітин/г печінки] • • печінковий коефіцієнт [г/кг маси тіла])/1000 і, використовуючи "well-stirred"-модель, обчислюють оцінний метаболічний кліренс в організмі людини: 50 7 UA 108373 C2 CL [мл/хв/кг] = CLвласн. in vivo [мл/хв/кг] • • кровотік через печінку [мл/хв/кг]/(CLвласн. in vivo [мл/хв/кг] + + кровотік через печінку [мл/хв/кг]). 5 10 15 20 25 30 35 40 45 50 55 60 Для обчислень використовують наступні параметри: гепатоцелюлярний, організм людини: 6 120•10 клітин/г печінки, печінковий коефіцієнт, організм людини: 25,7 г печінки на кг маси тіла; кровотік через печінку, організм людини: 21 мл / (хв•кг). Показання до застосування запропонованих у винаході сполук Завдяки своїм фармакологічним властивостям запропоновані у винаході нові сполуки і їх фізіологічно сумісні солі придатні для лікування захворювань і симптомів, які щонайменше частково обумовлені стимуляцією брадікінінових рецепторів B1 або при яких антагонізація брадікінінових рецепторів B1 дозволяє добитися поліпшення симптомів. Ще одним об'єктом даного винаходу е пропоновані в ньому сполуки наведеної на початку опису загальної формули I для застосування в якості лікарських засобів. Запропоновані у винаході сполуки з урахуванням їх фармакологічної дії придатні для знеболюючого лікування (а) при гострих болях, таких, наприклад, як зубні болі, пери-і післяопераційні болі, травматичні болі, м'язові болі, опікові болю, болю при сонячній еритемі, невралгія трійчастого нерва, коліки, а також болі при спазмах органів шлунково-кишкового тракту або матки; (б) при болях у внутрішніх органах, таких, наприклад, як хронічні болі в області таза, болі в жіночих статевих органах, болю до менструації і під час менструації, болю при панкреатиті, болі при пептичних виразках, болі при інтерстиціальному циститі, ниркова колька, біль при холециститі, болі при простатиті, болі при стенокардії, болі при синдромі подразненої товстої кишки, болі при невиразковій диспепсії, болю при гастриті, некардіального болю в грудній клітині і болю при ішемії міокарда і інфаркті міокарда; (в) при невропатичних болях, таких, наприклад, як хворобливі поліневропатії, болі при діабетичній невропатії, пов'язані зі СНІДом невропатичні болі, не пов'язана з герпесом невралгія, невралгія після оперізувального лишаю, болі при ушкодженнях нервів, болю при черепно-мозкових травмах, болі при ушкодженнях нервів внаслідок впливу токсинів або внаслідок хіміотерапії, фантомні болі, болі при множинному склерозі, болі при відриві нервових корінців і хворобливі ушкодження окремих нервів унаслідок травми, а також центральна біль, наприклад, біль після апоплексичного удару, біль при пошкодженнях спинного мозку або біль при пухлинах; (г) при супроводжуючих запальні процеси / опосередковуваних больовими рецепторами болях, пов'язаних з такими захворюваннями, як, наприклад, остеоартрит, ревматоїдний артрит, ревматична лихоманка, тендосиновіт, бурсит, тендиніт, подагра і подагричний артрит, посттравматичні артрити, вульводініі, пошкодження і захворювання м'язів і фасцій (травми м'язів, фіброміалгія), ювенільний артрит, спондиліт, псоріатичний артрит, міозити, захворювання зубів, вірусний грип і інші вірусні інфекції, такі як простудні захворювання, системний червоний вовчак або опікові болі; (д) при болях, пов'язаних з онкологічними захворюваннями, такими, наприклад, як лімфоабо міелолейкоз, хвороба Ходжкіна, неходжкінські лімфоми, лімфогранулематоз, лімфосаркоми, злоякісні солідні пухлини і обширні метастази; (е) при головних болях, викликаних різними причинами, таких, наприклад, як кластерні головні болі, мігрені (супроводжуються або не супроводжуються аурою) i головні болі вазомоторного характеру; (ж) при больових станах змішаної етіології, таких, наприклад, як хронічні болі в спині або хребті, включаючи люмбаго, або фіброміалгія. Запропоновані у винаході сполуки придатні далі (з) для лікування запальних захворювань або запальних проявів при сонячній еритемі і опіках, гінгівітів, запальних проявів при набряках після опікових травм, при набряках головного мозку і судинних набряках, при захворюваннях кишечника, включаючи хворобу Крона і виразковий коліт, при синдромі подразненого кишечника, при панкреатиті, при нефриті, при циститі (інтерстиціальному циститі) i при увеїті, запальних захворювань шкіри (таких, наприклад, як псоріаз і екземи), судинних колагенозів, розтягнень і переломів, а також захворювань м'язово-скелетної системи із запальними проявами, таких як гостра ревматична лихоманка, ревматична поліміалгія, реактивні артрити, ревматоїдний артрит, спондилоартрити і остеоартрит, а також запальні колагенози іншого генезу і колагенози будь-якого генезу, такі як системний червоний вовчак, склеродермія, поліміозит, дерматоміозит, синдром Сьегрена, хвороба Стілла або синдром Фелті; 8 UA 108373 C2 5 10 15 20 25 30 35 40 45 50 55 60 (і) для лікування запальних змін, пов'язаних із захворюваннями дихальних шляхів, такими як бронхіальна астма, включаючи алергічну астму (атопічну і неатопіческім), а також бронхоспазми при напрузі, професійна астма, вірусні або бактеріальні загострення існуючого астматичного захворювання і інші астматичні захворювання не алергічного характеру; (к) для лікування хронічного бронхіту, а також хронічного обструктивного захворювання легень (ХОЗЛ), включаючи емфізему легенів, вірусних або бактеріальних загострень хронічного бронхіту, гострого респіраторного дистрес-сіндромома у дорослих (РДСД), бронхіту, запалення легенів, алергічного риніту (сезонного і цілорічного), вазомоторного риніту і пневмоконіози, таких як алюміноз, антракоз, азбестоз, халькоз, сідероз, силікоз, табакоз і біссіноз, екзогенного алергічного альвеоліту, фіброзу легень, бронхоектазів, захворювань легенів при дефіциті α1 антитрипсину і кашлю; (л) для лікування цукрового діабету і пов'язаних з ним ускладнень (таких, наприклад, як діабетична васкулопатія, діабетична нейропатія, діабетична ретинопатія) i діабетичних симптомів при інсуліті (наприклад, гіперглікемії, порушень діурезу, протеїнурії і підвищеного виділення нітритів і калікреінів нирками); (м) для лікування сепсису і септичного шоку після бактеріальних інфекцій або після травми; (н) для лікування викликаних сверблячкою (шкірною сверблячкою) синдромів і алергічних шкірних реакцій; (о) для лікування пошкоджень центральної нервової системи; (п) для лікування ран і пошкоджень тканин; (р) для лікування доброякісної гіперплазії простати і гіперактивності сечового міхура; (с) для лікування судинних захворювань, таких як вузликовий панартериит, вузликовий поліартрит, вузловий періартеріїт, скроневий артеріїт, гранулематоз Вегенера, гігантоклітинний артеріїт, артеріосклероз, вузлувата еритема; (т) для лікування порушень рухливості або моторики або спазмів респіраторних, сечостатевих, шлунково-кишкових, включаючи жовчних, або васкулярних структур і органів; (у) для лікування післяопераційної гарячки;(ф) для лікування і профілактики серцевосудинних захворювань, таких, наприклад, як артеріальна гіпертонія і родинні захворювання;(х) для лікування і профілактики раку і споріднених захворювань;(ц) для лікування і профілактики психіатричних захворювань, таких, наприклад, як депресії;(ч) для лікування і профілактики нетримання сечі і споріднених захворювань;(ш) для лікування і профілактики хворобливого надмірної ваги і споріднених захворювань; (щ) для лікування і профілактики артеріосклерозу і споріднених захворювань; (ї) для лікування і профілактики епілепсії. Запропоновані у винаході сполуки придатні для етіотропної терапії, під якою мається на увазі уповільнення або зупинка розвитку хронічно прогресуючих захворювань, перш за все остеоартриту, ревматоїдного артриту і спондилоартрити. Ще одним об'єктом даного винаходу е застосування запропонованих у винаході сполук наведеної на початку опису загальної формули I для приготування лікарського засобу, призначеного для терапевтичного застосування при вказаних вище показаннях. Запропоновані у винаході сполуки загальної формули I переважно застосовувати для лікування остеоартриту, ревматоїдного артриту або ХОЗЛ. Під терміном "лікування" або "терапія" мається на увазі терапевтичне лікування пацієнтів з проявленим, гострим або хронічним патологічним станом, при цьому зазначений термін охоплює, з одного боку, симптоматичне (паліативне) лікування для послаблення симптомів хвороби, а з іншого боку, етіотропне лікування патологічного стану, мета якого лікування в залежності від типу або тяжкості патологічного стану полягаю в його припинення, в зниженні мірі його тяжкості або в уповільненні його прогресування. Ще одним об'єктом даного винаходу е застосування сполуки загальної формули I для приготування лікарського засобу, призначеного для екстреного лікування і профілактики гострих болів, болів у внутрішніх органах, невропатичних болів, супроводжуючих запальні процеси / опосередковуваних больовими рецепторами болів, болів при пухлинах, головних болів і больових станів змішаної етіології, а також інших, зазначених вище захворювань. При цьому таке застосування відрізняється тим, що воно полягаю у введенні сполуки загальної формули I або його фізіологічно сумісною солі в ефективному кількості в організм пацієнта, що потребує в подібному лікуванні або в подібній профілактиці. Під терміном "пацієнт" переважно мається на увазі людина. Запропоновані у винаході сполуки поряд із застосуванням в якості лікарських засобів в медицині придатні також для застосування у ветеринарії для лікування домашніх тварин, екзотичних тварин і корисних тварин. 9 UA 108373 C2 5 10 15 20 25 30 35 40 45 50 55 60 Комбінації Для знеболюючого лікування може виявитися кращим або доцільне застосовувати запропоновані у винаході сполуки в комбінації зі стимулюючими речовинами, такими як кофеїн, або іншими болезаспокійливими діючими речовинами. При наявності діючих речовин, придатних для етіотропного лікування, спрямованого на усунення причини болю, їх також можна використовувати в комбінації з пропонованими у винаході сполуками. В якості прикладу сполук, які можна використовувати для комбінованого лікування у поєднанні з пропонованими у винаході сполуками, можна назвати наступні: – нестероїдні антиревматичні засоби (НСАРС), такі як похідні пропіонової кислоти, які можуть бути обрані з групи, що включає алмінопрофен, буклоксінову кислоту, карпрофен, фенопрофен, ібупрофен, кетопрофен, напроксен, оксапрозін, пірпрофен, пранопрофен і тіапрофеновую кислоту, похідні оцтової кислоти, які можуть бути обрані з групи, що включає індометацин, ацеметацін, аклофенак, ізоксепак, суліндак і толметін, похідні фенаміновой кислоти, які можуть бути обрані з групи, що включає меклофенамінова кислоту, мефенамінову кислоту і толфенаміновую кислоту, похідні біфенілкарбонової кислоти, оксиками, які можуть бути обрані з групи, що включає мелоксикам, піроксикам і теноксикам, похідні саліцилової кислоти, які можуть бути обрані з групи, що включає ацетилсаліцилову кислоту і сульфасалазин, піразолону, які можуть бути обрані з групи, що включає апазоне і фепразон, і коксиби, які можуть бути обрані з групи, що включає целекоксиб і еторикоксиб; – агоністи опіатних рецепторів, які, наприклад, можуть бути обрані з групи, що включає морфін, дарвон, трамадол і бупренорфін; – агоністи канабіноїдних рецепторів, такі, наприклад, як GW-1000; – блокатори натрієвих каналів, які, наприклад, можуть бути обрані з групи, що включає карбамазепін, мексилетин, прегабалін, тектін і ралфінамід; – блокатори кальцієвих каналів N-типу, такі, наприклад, як зіконотід; – серотонергічні і норадренергічні модулятори, які, наприклад, можуть бути обрані з групи, що включає дулоксетин і амітріптілін; – кортикостероїди, які, наприклад, можуть бути обрані з групи, що включає бетаметазон, будесонід, кортизон, дексаметазон, гідрокортизон, метилпреднізолон, преднізолон, преднізон і триамцинолон; – антагоністи гістамінових H1-рецепторів, які, наприклад, можуть бути обрані з групи, що включае бромфенірамін, хлорфенірамін, дексхлорфенірамін, трипролідин, клемастин, дифенгидрамін, діфенілпіралін, тріпеленнамін, гідроксизин, прометазин, трімепразін, азатадін, ципрогептадину, антазолін, феніраміну, піріламін, лоратадин, цетиризин, дезлоратадин, фексофенадин і левоцетиризин; – антагоністи лейкотріенів і інгібітори 5-ліпоксигенази, які, наприклад, можуть бути обрані з групи, що включае зафірлукаст, монтелукаст, пранлукаст і зілеутон (зілейтон); – місцеві анестетики, які, наприклад, можуть бути обрані з групи, що включае амброксол і лідокаїн; – антагоністи TRPV1, які, наприклад, можуть бути обрані з групи, що включае AZD-1386, JTS-653 і PHE-377; – агоністи нікотинових рецепторів, такі, наприклад, як A-366833; – антагоністи P2X3-рецепторів, такі, наприклад, як A-317491; – антитіла до фактору росту нервів (NGF) i його антагоністи, які, наприклад, можуть бути обрані з групи, що включае JNJ-42160443 і PPH 207; – антагоністи NK1 і NK2, такі, наприклад, як CP-728663; – антагоністи NMDA, які, наприклад, можуть бути обрані з групи, що включае CNS-5161, AZ756 і V-3381; – модулятори каліевих каналів, такі, наприклад, як CL-888; – модулятори ГАМК, такі, наприклад, як баклофен; – терапевтичні засоби проти мігрені, які, наприклад, можуть бути обрані з групи, що включае суматриптан, золмітриптан, наратріптан і елетриптан. Для лікування одного або декількох з числа зазначених вище захворювань дихальних шляхів може виявитися кращим використовувати пропоновані у винаході сполуки загальної формули I в поєднанні з іншими діючими речовинами, призначеними для лікування захворювань дихальних шляхів. При наявності діючих речовин, придатних для етіотропного лікування захворювань дихальних шляхів, такі діючі речовини можна використовувати в комбінації з пропонованими у винаході сполуками. При необхідності сполуки загальної формули I можна також використовувати в комбінації з фармакологічно активними діючими речовинами інших класів. Переважно при цьому 10 UA 108373 C2 5 10 15 20 25 30 35 40 45 50 55 60 використовувати діючі речовини, вибрані, наприклад, з групи, що включае бетаміметікі, антихолінергічні засоби, кортикостероїди, інші інгібітори PDE4, антагоністи рецептора LTD4 (CysLT1, CysLT2, CysLT3), інгібітори MAP-кіназ, таких, наприклад, як p38, ERK1, ERK2, JNK1, JNK2, JNK3 або SAP, антагоністи рецептора LTB4 (BLT1, BLT2), інгібітори EGFR, антагоністи Н1-рецептора, протигістамінні засоби, антагоністи Н4-рецептора, антагоністи фактора активації тромбоцитів (PAF), інгібітори PI3-кінази, антагоністи рецептора CXCR1 і / або рецептора CXCR2 і протикашльові речовини. Сполуки загальної формули I можна також використовувати у вигляді двох-або трьохкомпонентих комбінацій із зазначеними вище діючими речовинами, таких, наприклад, як комбінації з сполук формули I з одним або двома сполуками з групи, що включае – бетаміметікі, кортикостероїди, інгібітори PDE4, інгібітори EGFR і антагоністи LTD4, – антихолінергічні засоби, бетаміметікі, кортикостероїди, інгібітори PDE4, інгібітори EGFR і антагоністи LTD4, – інгібітори PDE4, кортикостероїди, інгібітори EGFR і антагоністи LTD4, – інгібітори EGFR, інгібітори PDE4 і антагоністи LTD4, – інгібітори EGFR і антагоністи LTD4, – інгібітори CCR3, інгібітори iNOS (інгібітори індуцибельної синтази оксиду азоту), (6R)-Lеритро-5,6,7,8-тетрагідробіоптеріна (нижче званий "BH4") i його похідні, описані в WO 2006/120176, і інгібітори SYK (інгібітори селезінкової тирозинкінази), – антихолінергічні засоби, бетаміметики, кортикостероїди, інгібітори PDE4 і інгібіторів MRP4. В обсяг винаходу включені також комбінації трьох діючих речовин, за одному з кожного зазначеного вище класу сполук. В якості бетаміметиків в комбінації з пропонованими у винаході сполуками переважно використовувати сполуки, вибрані з групи, що включає арформотерол, кармотерол, формотерол, індакатерол, салметерол, Албутерол, бамбутерол, бітолтерол, броксатерол, карбутерол, кленбутерол, фенотерол, гексопреналін, ібутерол, ізоетарін, ізопреналін, левосалбутамол, мабутерол, мелуадрін, метапротеренол, мілветерол, оркіпреналін, пірбутерол, прокатерол, репротерол, рімітерол, ритодрин, салмефамол, сотеренол, сульфонтерол, тербуталін, тіарамід, толубутерол, зінтерол, 6-гідрокси-8-{1-гідрокси-2-[2-(4метоксифеніл)-1,1-диметилетиламіно]етил}-4H-бензо[1,4]оксазин-3-он, 8-{2-[2-(2,4дифторфеніл)-1,1-диметилетиламіно]-1-гідроксиетил}-6-гідрокси-4H-бензо[1,4]оксазин-3-он, 8{2-[2-(3,5-дифторфеніл)-1,1-диметилетиламіно]-1-гідроксиетил}-6-гідрокси-4H-бензо[1,4]оксазин3-он, 8-{2-[2-(4-етоксифеніл)-1,1-диметилетиламіно]-1-гідроксиетил}-6-гідрокси4H-бензо[1,4]оксазин-3-он, 8-{2-[2-(4-фторфеніл)-1,1-диметилетиламіно]-1-гідроксиетил}-6гідрокси-4H-бензо[1,4]оксазин-3-он, N-(5-{2-[3-(4,4-диетил-2-оксо-4H-бензо[d][1,3]оксазин-1-іл)1,1-диметилпропіламіно]-1-гідроксиетил}-2-гідроксифеніл)метансульфонамід, N-(5-{2-[3-(4,4диетил-6-фтор-2-оксо-4H-бензо[d][1,3]оксазин-1-іл)-1,1-диметилпропіламіно]-1-гідроксиетил}-2гідроксифеніл)метансульфонамід, N-(5-{2-[3-(4,4-діетил-6-метокси-2-оксо-4Hбензо[d][1,3]оксазин-1-іл)-1,1-диметилпропіламіно]-1-гідроксиетил}-2гідроксифеніл)метансульфонамід, N-(5-{2-[1,1-диметил-3-(2-оксо-4,4-дипропіл-4Hбензо[d][1,3]оксазин-1-іл)пропіламіно]-1-гідроксиетил}-2-гідроксифеніл)метансульфонамід, 8-{2[1,1-диметил-3-(2-оксо-2,3-дигідробензоимидазол-1-іл)пропіламіно]-1-гідроксиетил}-6-гідрокси4H-бензо[1,4]оксазин-3-он, 8-{2-[1,1-диметил-3-(6-метил-2-оксо-2,3-дигідробензоімідазол-1іл)пропіламіно]-1-гідроксиетил}-6-гідрокси-4H-бензо[1,4]оксазин-3-он, 8-{2-[1,1-диметил-3-(2оксо-5-трифторметил-2,3-дигідробензоимидазол-1-іл)пропіламіно]-1-гідроксиетил}-6-гідрокси4H-бензо[1,4]оксазин-3-он, 8-{2-[1,1-диметил-3-(3-метил-2-оксо-2,3-дигідробензоимидазол-1іл)пропіламіно]-1-гідроксиетил}-6-гідрокси-4H-бензо[1,4]оксазин-3-он, N-[2-гідрокси-5-((1R)-1гідрокси-2-{2-[4-(2-гідрокси-2-фенілетиламіно)феніл]етиламіно}етил)феніл]формамід (Milveterol),, 8-гідрокси-5-((1R)-1-гідрокси-2-{2-[4-(6-метоксидифеніл-3іламіно)феніл]етиламіно}етил)-1H-хінолін-2-он, 8-гідрокси-5-[(1R)-1-гідрокси-2-(6фенетиламіногексиламіно)етил]-1H-хінолін-2-он, 5-[(1R)-2-(2-{4-[4-(2-аміно-2метилпропокси)феніламіно]феніл}етиламіно)-1-гідроксиетил]-8-гідрокси-1H-хінолин-2-он, [3-(4{6-[(2R)-2-гідрокси-2-(4-гідрокси-3-гідроксиметилфеніл)етиламіно]гексилокси}бутил)-5метилфеніл]сечовину, 4-((1R)-2-{6-[2-(2,6-дихлорбензилокси)етокси]гексиламіно}-1гідроксиетил)-2-гідроксиметилфенол, 3-(4-{6-[(2R)-2-гідрокси-2-(4-гідрокси-3гідроксиметилфеніл)етиламіно]гексилокси}бутил)бензолсульфонамід, 3-(3-{7-[(2R)-2-гідрокси-2(4-гідрокси-3-гідроксиметилфеніл)етиламіно]гептилокси}пропіл)бензолсульфонамід, 4-((1R)-2{6-[4-(3-циклопентансульфонилфеніл)бутокси]гексиламіно}-1-гідроксиетил)-2гідроксиметилфенол, N-1-адамантаніл-2-{3-[(2R)-2-({(2R)-2-гідрокси-2-[4-гідрокси-3(гідроксиметил)феніл]етил}аміно)пропіл]феніл}ацетамід, (1R)-5-{2-[6-(2,2-дифтор-2 11 UA 108373 C2 5 10 15 20 25 30 35 40 45 50 55 60 фенілетокси)гексиламіно]-1-гідроксиетил}-8-гідрокси-1H-хінолін-2-он, , (R, S)-4-(2-{[6-(2,2дифтор-4-фенілбутокси)гексил]аміно}-1-гідроксиетил)-2-(гідроксиметил)фенол, (R, S)-4-(2-{[6(2,2-дифтор-2-фенілетокси)гексил]аміно}-1-гідроксиетил)-2-(гідроксиметил)фенол, (R, S)-4-(2{[4,4-дифтор-6-(4-фенілбутокси)гексил]аміно}-1-гідроксиетил)-2-(гідроксиметил)фенол, (R, S)-4(2-{[6-(4,4-дифтор-4-фенілбутокси)гексил]аміно}-1-гідроксиетил)-2-(гідроксиметил)фенол, (R, S)5-(2-{[6-(2,2-дифтор-2-фенілетокси)гексил]аміно}-1-гідроксиетил)-8-гідроксихінолін-2(1H)-он, (R, S)-[2-({6-[2,2-дифтор-2-(3-метилфеніл)етокси]гексил}аміно)-1гідроксиетил]2-(гідроксиметил)фенол, 4-(1R)-2-{[6-(2,2-дифтор-2-фенілетокси)гексил]аміно}-1-гідроксиетил)-2(гідроксиметил)фенол, (R, S)-2-(гідроксиметил)-4-(1-гідрокси-2-{[4,4,5,5-тетрафтор-6-(3фенілпропокси)гексил]аміно}етил)фенол, (R, S)-[5-(2-{[6-(2,2-дифтор-2фенілетокси)гексил]аміно}-1-гідроксиетил)-2-гідроксифеніл]формамід, (R, S)-4-[2-({6-[2-(3бромфеніл)-2,2-дифторетокси]гексил}аміно)-1-гідроксиетил]-2-(гідроксиметил)фенол, (R, S)-N[3-(1,1-дифтор-2-{[6-({2-гідрокси-2-[4-гідрокси-3(гідроксиметил)феніл]етил}аміно)гексил]окси}етил)феніл]сечовину, 3-[3-(1,1-дифтор-2-{[6-({2гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гексил]окси}етил)феніл]імідазолідин2,4-діон, (R, S)-4-[2-({6-[2,2-дифтор-2-(3-метоксифеніл)етокси]гексил}аміно)-1-гідроксиетил]2-(гідроксиметил)фенол, 5-((1R)-2-{[6-(2,2-дифтор-2-фенілетокси)гексил]аміно}-1-гідроксиетил)8-гідроксихинолин-2(1H)-он, 4-((1R)-2-{[4,4-дифтор-6-(4-фенілбутокси)гексил]аміно}-1гідроксиетил)-2-(гідроксиметил)фенол, (R, S)-4-(2-{[6-(3,3-дифтор-3фенілпропокси)гексил]аміно}-1-гідроксиетил)-2-(гідроксиметил)фенол, (R, S)-(2-{[6-(2,2-дифтор2-фенілетокси)-4,4-дифторгексил]аміно}-1-гідроксиетил)-2-(гідроксиметил)фенол, (R, S)-4-(2-{[6(2,2-дифтор-3-фенілпропокси)гексил]аміно}-1-гідроксиетил)-2-(гідроксиметил)фенол, 3-[2-(3хлорфеніл)етокси]-N-(2-диетиламіноетил)-N-{2-[2-(4-гідрокси-2-оксо-2,3-дигідробензотиазол-7іл)етиламіно]етил}пропіонамід, N-(2-диетиламіноетил)-N-{2-[2-(4-гідрокси-2-оксо-2,3дигідробензотиазол-7-іл)етиламіно]етил}-3-(2-нафталин-1-ілетокси)пропіонамід і 7-[2-(2-{3-[2-(2хлорфеніл)етиламіно]пропілсульфаніл}етиламіно)-1-гідроксиетил]-4-гідрокси-3H-бензотиазол-2он, необов'язково у вигляді їх рацематів, енантіомеров, діастереомерів і необов'язково у вигляді їх фармакологічно прийнятних кислотно-адитивних солей, сольвати або гідратів. До переважних згідно винаходу кислотно-адитивних солей бетаміметіків належать солі, вибрані з групи, що включає гідрохлорид, гідробромід, гідроіодід, гідросульфат, гідрофосфат, гідрометансульфонат, гідронітрат, гідромалеат, гідроацетат, гідроцітрат, гідрофумарат, гідротартрат, гідрооксалат, гідросукцінат, гідробензоат і гідропаратолуолсульфонат. В якості антихолінергічних засобів у комбінації з пропонованими у винаході сполуками переважно використовувати сполуки, вибрані з групи, що включає солі тіотропію, переважно його бромід, солі оксітропія, переважно його бромід, солі флутропія, переважно його бромід, солі іпратропію, переважно його бромід, солі аклідінія, переважно його бромід, солі глікопірронія, переважно його бромід, солі троспія, переважно його хлорид, толтеродин і солі (3R)-1-фенетил-3-(9H-ксантен-9-карбонілокси)-1-азоніабіцикло[2.2.2]октану. У зазначених вище солях фармакологічно активними компонентами є катіони. У якості ж аніонів X-вищезазначені солі в кращому варіанті можуть містити хлорид, бромід, йодид, сульфат, фосфат, метансульфонат, нітрат, малеат, ацетат, цитрат, фумарат, тартрат, оксалат, сукцинат, бензоат або паратолуолсульфонат, серед яких як протиіонів переважні хлорид, бромід, йодид, сульфат, метансульфонат і паратолуолсульфонат. З числа всіх зазначених солей особливо переважні хлориди, броміди, йодиди і метансульфонати. В якості прикладу інших антихолінергічних засобів можна назвати сполуки, вибрані з групи, що включає метобромід тропенолового ефіру 2,2-діфенілпропіонової кислоти, метобромід скопінового ефіру 2,2-діфенілпропіонової кислоти, метобромід скопінового ефіру 2-фтор-2,2діфенілоцтової кислоти, метобромід тропенолового ефіру 2-фтор-2,2-діфенілоцтової кислоти, метобромід тропенолового ефіру 3,3', 4,4'-тетрафторбензілової кислоти, метобромід скопінового ефіру 3,3', 4,4'-тетрафторбензілової кислоти, метобромід тропенолового ефіру 4,4'діфторбензілової кислоти ¬, метобромід скопінового ефіру 4,4'-діфторбензілової кислоти, метобромід тропенолового ефіру 3,3'-діфторбензілової кислоти, метобромід скопінового ефіру 3,3'-діфторбензілової кислоти, метобромід тропенолового ефіру 9-гідроксіфлуорен-9-карбонової кислоти, метобромід тропенолового ефіру 9-фторфлуорен-9-карбонової кислоти, метобромід скопінового ефіру 9-гідроксифлуорен-9-карбонової кислоти, метобромід скопінового ефіру 9фторфлуорен-9-карбонової кислоти, метобромід тропенолового ефіру 9-метилфлуорен-9карбонової кислоти, метобромід скопінового ефіру 9-метилфлуорен-9-карбонової кислоти, метобромід циклопропілтропінового ефіру бензилової кислоти, метобромід циклопропілтропінового ефіру 2,2-дифенілпропіонової кислоти, метобромід циклопропілтропінового ефіру 9-гідроксиксантен-9-карбонової кислоти, метобромід 12 UA 108373 C2 5 10 15 20 25 30 35 40 45 50 55 60 циклопропілтропінового ефіру 9-метилфлуорен-9-карбонової кислоти, метобромід циклопропілтропінового ефіру 9-метилксантен-9-карбонової кислоти, метобромід циклопропілтропінового ефіру 9-гідроксифлуорен-9-карбонової кислоти, метобромід циклопропілтропінового ефіру і метилового ефіру 4,4'-дифторбензилової кислоти, метобромід тропенолового ефіру 9-гідроксиксантен-9-карбонової кислоти, метобромід скопінового ефіру 9гідроксиксантен-9-карбонової кислоти, метобромід тропенолового ефіру 9-метилксантен-9карбонової кислоти, метобромід скопінового ефіру 9-метилксантен-9-карбонової кислоти, метобромід тропенолового ефіру 9-етилксантен-9-карбонової кислоти, метобромід тропенолового ефіру 9-дифторметилксантен-9-карбонової кислоти і метобромід скопінового ефіру 9-гідроксиметилксантен-9-карбонової кислоти. Зазначені вище сполуки згідно з цим винаходом можна також використовувати у вигляді солей, які являють собою не метоброміди, а солі мето-X, де X може мати зазначені вище для X-значення. В якості кортикостероїдів в комбінації з пропонованими у винаході сполуками переважно використовувати сполуки, вибрані з групи, що включає беклометазон, бетаметазон, будесонід, бутіксокорт, ціклесонід, дефлазакорт, дексаметазон, етіпреднол, флунісоліда, флутиказон, лотепреднол, мометазон, преднізолон, преднізон, рофлепонід, триамцинолон, тіпредан, прегна1,4-дієн-3,20-діон, 6-фтор-11-гідрокси-16,17-[(1-метилетиліден)-біс-(окси)]-21-[[4[(нітроокси)метил]бензоіл]окси]-(6α,11β,16α)-(9CI) (NCX-1024), 16,17-бутилідендиокси-6,9дифтор-11-гідрокси-17-(метилтіо)андрост-4-ен-3-он (RPR-106541), (S)-фторметиловий ефір 6,9дифтор-17-[(2-фуранілкарбоніл)окси]-11-гідрокси-16-метил-3-оксоандроста-1,4-дієн-17карботіонової кислоти, (S)-(2-оксотетрагідрофуран-3S-іловий) ефір 6,9-дифтор-11-гідрокси-16метил-3-оксо-17-пропионілоксиандроста-1,4-дієн-17-карботіонової кислоти і цианометиловий ефір 6α,9α-дифтор-11β-гідрокси-16α-метил-3-оксо-17α-(2,2,3,3тетраметилциклопропілкарбоніл)оксиандроста-1,4-дієн-17β-карбонової кислоти, необов'язково у вигляді їх рацематів, енантіомерів або діастереомерів і необов'язково у вигляді їх солей і похідних, їх сольвати та / або гідратів. При будь-якому згадуванні у цьому описі стероїдів маються на увазі також їх можливо існуючі солі або похідні, гідрати або сольвати. В якості прикладів можливих солей і похідних стероїдів можна назвати солі з лужними металами, такі, наприклад, як натрієві або калієві солі, сульфобензоати, фосфати, ізонікотінати, ацетати, діхлорацетати, пропіонат, дігідрофосфати, пальмітат, півалату або ж фуроат. В якості інгібіторів PDE4 в комбінації з пропонованими у винаході сполуками переважно використовувати сполуки, вибрані з групи, що включає енпрофіллін, теофілін, рофлуміласт, аріфло (ціломіласт), тофіміласт, пумафентрін, ліріміласт, апреміласт, арофіллін, атізорам, оглеміласт, тетоміласт, 5-[(N-(2,5-дихлор-3-піридиніл)карбоксамід]-8-метоксихінолін (D-4418), 5[N-(3,5-дихлор-1-оксидо-4-піридиніл)карбоксамід]-8-метокси-2-(трифторметил)хінолін (D-4396 (Sch-351591)), амід N-(3,5-дихлорпірид-4-іл)-[1-(4-фторбензил)-5-гідроксиіндол-3-іл]гліоксилової кислоти (AWD12-281 (GW-842470)), 9-[(2-фторфеніл)метил]-N-метил-2-(трифторметил)-9H-пурин-6-амін (NCS-613), 4-[(2R)-2-[3(циклопентилокси)-4-метоксифеніл]-2-фенілетил]піридин (CDP-840), N-[(3R)-3,4,6,7-тетрагідро9-метил-4-оксо-1-фенілпіроло[3,2,1-jk][1,4]бензодіазепін-3-іл]-4-піридинкарбоксамід (PD-168787), 4-[6,7-діетокси-2,3-біс-(гідроксиметил)-1-нафталініл]-1-(2-метоксиетил)-2(1H)-піридинон (T-440), 2-[4-[6,7-діетокси-2,3-біс-(гідроксиметил)-1-нафталініл]-2-піридиніл]-4-(3-піридиніл)-1(2H)фталазинон (T-2585), (3-(3-циклофенілокси-4-метоксибензил)-6-етиламіно-8-ізопропіл-3H-пурин (V-11294A), β-[3-(циклопентилокси)-4-метоксифеніл]-1,3-дигідро-1,3-діоксо-2H-ізоіндол2-пропанамід (CDC-801), 9-етил-2-метокси-7-метил-5-пропілімідазо[1,5-a]піридо[3,2-e]піразин6(5H)-он (D-22888),, (3S, 5S)-2-піперидинон-5-[3-(циклопентилокси)-4-метоксифеніл]-3-[(3метилфеніл)метил] (HT-0712), 4-[1-[3,4-біс-(дифторметокси)феніл]-2-(3-метил-1-оксидо-4піридиніл)етил]-α,α-біс-(трифторметил)бензолметанол (L-826141), N-(3,5-дихлор-1-оксопіридин4-іл)-4-дифторметокси-3-циклопропілметоксибензамід, (–)п-[(4aR*,10bS*)-9-етокси-1,2,3,4,4a, 10b-гексагідро-8-метокси-2-метилбензо[s][1,6]нафтиридин-6-іл]-N, N-діізопропілбензамід, (R)(+)-1-(4-бромбензил)-4-[(3-циклопентилокси)-4-метоксифеніл]-2-піролідон, 3-(циклопентилокси4-метоксифеніл)-1-(4-N'-[N-2-ціано-S-метилізотиоуреідо]бензил)-2-піролідон, цис-[4-циано-4-(3циклопентилокси-4-метоксифеніл)циклогексан-1-карбонову кислоту], 2-карбометокси-4-циано-4(3-циклопропілметокси-4-дифторметоксифеніл)циклогексан-1-он, цис-[4-циано-4-(3циклопропілметокси-4-дифторметоксифеніл)циклогексан-1-ол], (R)-(+)-етил[4-(3циклопентилокси-4-метоксифеніл)піролідин-2-іліден]ацетат, (S)-(–)-етил[4-(3-циклопентилокси4-метоксифеніл)піролідин-2-іліден]ацетат, 9-циклопентил-5,6-дигідро-7-етил-3-(2-тіеніл)-9Hпіразоло[3,4-c]-1,2,4-триазоло[4,3-a]піридин і 9-циклопентил-5,6-дигідро-7-етил-3-(трет-бутил)9H-піразоло[3,4-c]-1,2,4-триазоло[4,3-a]піридин, необов'язково у вигляді їх рацематів, 13 UA 108373 C2 5 10 15 20 25 30 35 40 45 50 55 60 енантіомерів, діастереомерів і необов'язково у вигляді їх фармакологічно прийнятних кислотноадитивних солей, сольвати або гідратів. До переважним згідно винаходу кислотно-адитивним солям відносяться солі, вибрані з групи, що включає гідрохлорид, гідробромід, гідроіодід, гідросульфат, гідрофосфат, гідрометансульфонат, гідронітрат, гідромалеат, гідроацетат, гідроцітрат, гідрофумарат, гідротартрат, гідрооксалат, гідросукцінат, гідробензоат і гідропаратолуолсульфонат. В якості інгібіторів EGFR в комбінації з пропонованими у винаході сполуками переважно використовувати сполуки, вибрані з групи, що включає цетуксимаб, трастузумаб, панітумумаб (ABX-EGF), Mab ICR-62, гефітинібу, канертініб, ерлотініб, 4-[(3-хлор-4-фторфеніл)аміно]-6-{[4(морфолін-4-іл)-1-оксо-2-бутен-1-іл]аміно}-7-циклопропілметоксихіназолін, 4-[(3-хлор-4фторфеніл)аміно]-6-{[4-(N, N-діетиламіно)-1-оксо-2-бутен-1-іл]аміно}7-циклопропілметоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-{[4-(N, N-диметиламіно)-1-оксо2-бутен-1-іл]аміно}-7-циклопропілметоксихіназолін, 4-[(R)-(1-фенілетил)аміно]-6-{[4-(морфолін-4іл)-1-оксо-2-бутен-1-іл]аміно}-7-циклопентилоксихіназолін, 4-[(3-хлор-4-фтор-феніл)аміно]-6-{[4((R)-6-метил-2-оксоморфолін-4-іл)-1-оксо-2-бутен-1-іл]аміно}-7-циклопропілметоксихіназолін, 4[(3-хлор-4-фторфеніл)аміно]-6-{[4-((R)-6-метил-2-оксоморфолін-4-іл)-1-оксо-2-бутен-1-іл]аміно}7-[(S)-(тетрагідрофуран-3-іл)окси]хіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-{[4-((R)-2метоксиметил-6-оксоморфолін-4-іл)-1-оксо-2-бутен-1-іл]аміно}-7-циклопропілметоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-[2-((S)-6-метил-2-оксоморфолін-4-іл)етокси]-7-метоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-({4-[N-(2-метоксиетил)-N-метиламіно]-1-оксо-2-бутен-1іл}аміно)-7-циклопропілметоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-{[4-(N, Nдиметиламіно)-1-оксо-2-бутен-1-іл]аміно}-7-циклопентилоксихіназолін, 4-[(R)-(1фенілетил)аміно]-6-{[4-(N, N-бис-(2-метоксиетил)аміно)-1-оксо-2-бутен-1-іл]аміно}-7циклопропілметоксихіназолін, 4-[(R)-(1-фенілетил)аміно]-6-({4-[N-(2-метоксиетил)-N-етиламіно]1-оксо-2-бутен-1-іл}аміно)-7-циклопропілметоксихіназолін, 4-[(R)-(1-фенілетил)аміно]-6-({4-[N-(2метоксиетил)-N-метиламіно]-1-оксо-2-бутен-1-іл}аміно)-7-циклопропілметоксихіназолін, 4-[(R)(1-фенілетил)аміно]-6-({4-[N-(тетрагідропіран-4-іл)-N-метиламіно]-1-оксо-2-бутен-1-іл}аміно)-7циклопропілметоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-{[4-(N, N-диметиламіно)-1-оксо-2бутен-1-іл]аміно}-7-((R)-тетрагідрофуран-3-ілокси)хіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-{[4(N, N-диметиламіно)-1-оксо-2-бутен-1-іл]аміно}-7-((S)-тетрагідрофуран-3-ілокси)хіназолін, 4-[(3хлор-4-фторфеніл)аміно]-6-({4-[N-(2-метоксиетил)-N-метиламіно]-1-оксо-2-бутен-1-іл}аміно)-7циклопентилоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-{[4-(N-циклопропіл-N-метиламіно)-1оксо-2-бутен-1-іл]аміно}-7-циклопентилоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-{[4-(N, Nдиметиламіно)-1-оксо-2-бутен-1-іл]аміно}-7-[(R)-(тетрагідрофуран-2-іл)метокси]хіназолін, 4-[(3хлор-4-фторфеніл)аміно]-6-{[4-(N, N-диметиламіно)-1-оксо-2-бутен-1-іл]аміно}-7-[(S)(тетрагідрофуран-2-іл)метокси]хіназолін, 4-[(3-етинілфеніл)аміно]-6,7-бис-(2метоксиетокси)хіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-7-[3-(морфолін-4-іл)пропілокси]-6[(вінілкарбоніл)аміно]хіназолін, 4-[(R)-(1-фенілетил)аміно]-6-(4-гідроксифеніл)-7H-піроло[2,3d]піримідин, 3-циано-4-[(3-хлор-4-фторфеніл)аміно]-6-{[4-(N, N-диметиламіно)-1-оксо-2-бутен-1іл]аміно}-7-етоксихинолин, 4-{[3-хлор-4-(3-фторбензилокси)феніл]аміно}-6-(5-{[(2метансульфонилетил)аміно]метил}фуран-2-іл)хіназолін, 4-[(R)-(1-фенілетил)аміно]-6-{[4-((R)-6метил-2-оксоморфолін-4-іл)-1-оксо-2-бутен-1-іл]аміно}-7-метоксихіназолін, 4-[(3-хлор-4фторфеніл)аміно]-6-{[4-(морфолін-4-іл)-1-оксо-2-бутен-1-іл]аміно}-7-[(тетрагідрофуран-2іл)метокси]хіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-({4-[N, N-бис-(2-метоксиетил)аміно]-1оксо-2-бутен-1-іл}аміно)-7-[(тетрагідрофуран-2-іл)метокси]хіназолін, 4-[(3-етинилфеніл)аміно]-6{[4-(5,5-диметил-2-оксоморфолін-4-іл)-1-оксо-2-бутен-1-іл]аміно}хіназолін, 4-[(3-хлор-4фторфеніл)аміно]-6-[2-(2,2-диметил-6-оксоморфолін-4-іл)етокси]-7-метоксихіназолін, 4-[(3-хлор4-фторфеніл)аміно]-6-[2-(2,2-диметил-6-оксоморфолін-4-іл)етокси]-7-[(R)-(тетрагідрофуран-2іл)метокси]хіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-7-[2-(2,2-диметил-6-оксоморфолін-4іл)етокси]-6-[(S)-(тетрагідрофуран-2-іл)метокси]хіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-{2-[4(2-оксоморфолін-4-іл)піперидин-1-іл]етокси}-7-метоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]6-[1-(трет-бутилоксикарбоніл)піперидин-4-ілокси]-7-метоксихіназолін, 4-[(3-хлор-4фторфеніл)аміно]-6-(транс-4-аміноциклогексан-1-ілокси)-7-метоксихіназолін, 4-[(3-хлор-4фторфеніл)аміно]-6-(транс-4-метансульфониламіноциклогексан-1-ілокси)-7-метоксихіназолін, 4[(3-хлор-4-фторфеніл)аміно]-6-(тетрагідропіран-3-ілокси)-7-метоксихіназолін, 4-[(3-хлор-4фторфеніл)аміно]-6-(1-метилпіперидин-4-ілокси)-7-метоксихіназолін, 4-[(3-хлор-4фторфеніл)аміно]-6-{1-[(морфолін-4-іл)карбоніл]піперидин-4-ілокси}-7-метоксихіназолін, 4-[(3хлор-4-фторфеніл)аміно]-6-{1-[(метоксиметил)карбоніл]піперидин-4-ілокси}-7-метоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-(піперидин-3-ілокси)-7-метоксихіназолін, 4-[(3-хлор-4фторфеніл)аміно]-6-[1-(2-ацетиламіноетил)піперидин-4-ілокси]-7-метоксихіназолін, 4-[(3-хлор-4 14 UA 108373 C2 5 10 15 20 25 30 35 40 45 50 55 60 фторфеніл)аміно]-6-(тетрагідропіран-4-ілокси)-7-етоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]6-((S)-тетрагідрофуран-3-ілокси)-7-гідроксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6(тетрагідропіран-4-ілокси)-7-(2-метоксиетокси)хіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-{транс4-[(диметиламіно)сульфониламіно]циклогексан-1-ілокси}-7-метоксихіназолін, 4-[(3-хлор-4фторфеніл)аміно]-6-{транс-4-[(морфолін-4-іл)карбоніламіно]циклогексан-1-ілокси}-7метоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-{транс-4-[(морфолін-4іл)сульфоніламіно]циклогексан-1-ілокси}-7-метоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6(тетрагідропіран-4-ілокси)-7-(2-ацетиламіноетокси)хіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6(тетрагідропіран-4-ілокси)-7-(2-метансульфоніламіноетокси)хіназолін, 4-[(3-хлор-4фторфеніл)аміно]-6-{1-[(піперидин-1-іл)карбоніл]піперидин-4-ілокси}-7-метоксихіназолін, 4-[(3хлор-4-фторфеніл)аміно]-6-(1-амінокарбонілметилпіперидин-4-ілокси)-7-метоксихіназолін, 4-[(3хлор-4-фторфеніл)аміно]-6-(цис-4-{N-[(тетрагідропіран-4-іл)карбоніл]-Nметиламіно}циклогексан-1-ілокси)-7-метоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-(цис-4{N-[(морфолін-4-іл)карбоніл]-N-метиламіно}циклогексан-1-ілокси)-7-метоксихіназолін, 4-[(3-хлор4-фторфеніл)аміно]-6-(цис-4-{N-[(морфолін-4-іл)сульфоніл]-N-метиламіно}циклогексан-1-ілокси)7-метоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-(транс-4-етансульфоніламіноциклогексан1-ілокси)-7-метоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-(1-метансульфонилпіперидин-4ілокси)-7-етоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-(1-метансульфонілпіперидин-4ілокси)-7-(2-метоксиетокси)хіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-[1-(2метоксиацетил)піперидин-4-ілокси]-7-(2-метоксиетокси)хіназолін, 4-[(3-хлор-4-фторфеніл)аміно]6-(цис-4-ацетиламіноциклогексан-1-ілокси)-7-метоксихіназолін, 4-[(3-етинілфеніл)аміно]-6-[1(трет-бутилоксикарбоніл)піперидин-4-ілокси]-7-метоксихіназолін, 4-[(3-етинілфеніл)аміно]-6(тетрагідропіран-4-ілокси]-7-метоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-(цис-4-{N[(піперидин-1-іл)карбоніл]-N-метиламіно}циклогексан-1-ілокси)-7-метоксихіназолін, 4-[(3-хлор-4фторфеніл)аміно]-6-(цис-4-{N-[(4-метилпіперазин-1-іл)карбоніл]-N-метиламіно}циклогексан-1ілокси)-7-метоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-{цис-4-[(морфолін-4іл)карбоніламіно]циклогексан-1-ілокси}-7-метоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-{1[2-(2-оксопіролидин-1-іл)етил]піперидин-4-ілокси}-7-метоксихіназолін, 4-[(3-хлор-4фторфеніл)аміно]-6-{1-[(морфолін-4-іл)карбоніл]піперидин-4-ілокси}-7-(2метоксиетокси)хіназолін, 4-[(3-етинилфеніл)аміно]-6-(1-ацетилпіперидин-4-ілокси)-7метоксихіназолін, 4-[(3-етинилфеніл)аміно]-6-(1-метилпіперидин-4-ілокси)-7-метоксихіназолін, 4[(3-етинилфеніл)аміно]-6-(1-метансульфонилпіперидин-4-ілокси)-7-метоксихіназолін, 4-[(3-хлор4-фторфеніл)аміно]-6-(1-метилпіперидин-4-ілокси)-7-(2-метоксиетокси)хіназолін, 4-[(3-хлор-4фторфеніл)аміно]-6-(1-изопропілоксикарбонілпіперидин-4-ілокси)-7-метоксихіназолін, 4-[(3-хлор4-фторфеніл)аміно]-6-(цис-4-метиламіноциклогексан-1-ілокси)-7-метоксихіназолін, 4-[(3-хлор-4фторфеніл)аміно]-6-{цис-4-[N-(2-метоксиацетил)-N-метиламіно]циклогексан-1-ілокси}-7метоксихіназолін, 4-[(3-етинилфеніл)аміно]-6-(піперидин-4-ілокси)-7-метоксихіназолін, 4-[(3етинілфеніл)аміно]-6-[1-(2-метоксиацетил)піперидин-4-ілокси]-7-метоксихіназолін, 4-[(3етинилфеніл)аміно]-6-{1-[(морфолін-4-іл)карбоніл]піперидин-4-ілокси}-7-метоксихіназолін, 4-[(3хлор-4-фторфеніл)аміно]-6-{1-[(цис-2,6-диметилморфолін-4-іл)карбоніл]піперидин-4-ілокси}-7метоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-{1-[(2-метилморфолін-4іл)карбоніл]піперидин-4-ілокси}-7-метоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-{1-[(S, S)(2-окса-5-азабицикло[2.2.1]гепт-5-іл)карбоніл]піперидин-4-ілокси}-7-метоксихіназолін, 4-[(3-хлор4-фторфеніл)аміно]-6-{1-[(N-метил-N-2-метоксиетиламіно)карбоніл]піперидин-4-ілокси}-7метоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-(1-етилпіперидин-4-ілокси)-7метоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-{1-[(2-метоксиетил)карбоніл]піперидин-4ілокси}-7-метоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-{1-[(3метоксипропіламіно)карбоніл]піперидин-4-ілокси}-7-метоксихіназолін, 4-[(3-хлор-4фторфеніл)аміно]-6-[цис-4-(N-метансульфоніл-N-метиламіно)циклогексан-1-ілокси]-7метоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-[цис-4-(N-ацетил-N-метиламіно)циклогексан1-ілокси]-7-метоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-(транс-4-метиламіноциклогексан1-ілокси)-7-метоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-[транс-4-(N-метансульфонил-Nметиламіно)циклогексан-1-ілокси]-7-метоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-(транс-4диметиламіноциклогексан-1-ілокси)-7-метоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-(транс4-{N-[(морфолін-4-іл)карбоніл]-N-метиламіно}циклогексан-1-ілокси)-7-метоксихіназолін, 4-[(3хлор-4-фторфеніл)аміно]-6-[2-(2,2-диметил-6-оксоморфолін-4-іл)етокси]-7-[(S)(тетрагідрофуран-2-іл)метокси]хіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-(1метансульфонилпіперидин-4-ілокси)-7-метоксихіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-6-(1цианопіперидин-4-ілокси)-7-метоксихіназолін, 3-циано-4-[(3-хлор-4-фторфеніл)аміно]-6-{[4-(N, Nдиметиламіно)-1-оксо-2-бутен-1-іл]аміно}-7-етоксихінолін, [4-[(3-хлор-4-фторфеніл)аміно]-6-{[4 15 UA 108373 C2 5 10 15 20 25 30 35 40 45 50 55 60 (гомоморфолін-4-іл)-1-оксо-2-бутен-1-іл]аміно}-7-[(S)-(тетрагідрофуран-3-іл)окси]хіназолін, 4-[(3хлор-4-фторфеніл)аміно]-7-(2-{4-[(S)-(2-оксотетрагідрофуран-5-іл)карбоніл]-піперазин-1іл}етокси)-6-[(вінілкарбоніл)аміно]хіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-7-[2-((S)-6-метил2-оксоморфолін-4-іл)етокси]-6-[(вінілкарбоніл)аміно]хіназолін, 4-[(3-хлор-4-фторфеніл)аміно]-7[4-((R)-6-метил-2-оксоморфолін-4-іл)бутилокси]-6-[(вінілкарбоніл)аміно]хіназолін, 4-[(3-хлор-4фторфеніл)аміно]-7-[4-((S)-6-метил-2-оксоморфолін-4-іл)бутилокси]-6[(вінілкарбоніл)аміно]хіназолін і 4-[(3-хлор-4-фторфеніл)аміно]-6-[(4-{N-[2-(етоксикарбоніл)-етил]N-[(етоксикарбоніл)метил]аміно}-1-оксо-2-бутен-1-іл)аміно]-7-циклопропілметоксихіназолін, необов'язково у вигляді їх рацематів, енантіомерів або діастереомерів і необов'язково у вигляді їх фармакологічно прийнятних кислотно-адитивних солей, їх сольвати та / або гідратів. До переважним згідно винаходу кислотно-адитивним солям відносяться солі, вибрані з групи, що включає гідрохлорид, гідробромід, гідроіодід, гідросульфат, гідрофосфат, гідрометансульфонат, гідронітрат, гідромалеат, гідроацетат, гідроцітрат, гідрофумарат, гідротартрат, гідрооксалат, гідросукцінат, гідробензоат і гідропаратолуолсульфонат. В якості антагоністів рецептора LTD4 в комбінації з пропонованими у винаході сполуками переважно використовувати сполуки, вибрані з групи, що включає монтелукаст, пранлукаст, зафірлукаст, (E)-8-[2-[4-[4-(4-фторфеніл)бутокси]феніл]етеніл]-2-(1H-тетразол-5-іл)-4H-1-бензопіран-4-он (MEN-91507), 4-[6-ацетил-3-[3-(4-ацетил-3-гідрокси-2-пропілфенілтио)пропокси]-2пропілфенокси]масляну кислоту (MN-001), 1-(((R)-(3-(2-(6,7-дифтор-2-хінолініл)етеніл)феніл)-3(2-(2-гідрокси-2-пропіл)феніл)тио)метилциклопропаноцтову кислоту, 1-(((1(R)-3-(3-(2-(2,3дихлортіено[3,2-b]піридин-5-іл)-(E)-етеніл)феніл)-3-(2-(1-гідрокси-1метилетил)феніл)пропіл)тио)метил)циклопропаноцтову кислоту і [2-[[2-(4-трет-бутил-2тиазоліл)-5-бензофураніл]оксиметил]феніл]оцтову кислоту, необов'язково у вигляді їх рацематів, енантіомерів, діастереомерів і необов'язково у вигляді їх фармакологічно прийнятних кислотно-адитивних солей, сольватів або гідратів. До переважним згідно винаходу кислотно-адитивним солям відносяться солі, вибрані з групи, що включає гідрохлорид, гідробромід, гідроіодід, гідросульфат, гідрофосфат, гідрометансульфонат, гідронітрат, гідромалеат, гідроацетат, гідроцітрат, гідрофумарат, гідротартрат, гідрооксалат, гідросукцінат, гідробензоат і гідропаратолуолсульфонат. Під солями або похідними, які в деяких випадках здатні утворювати антагоністи рецептора LTD4, маються на увазі, наприклад, солі з лужними металами, такі, наприклад, як натрієві або калієві солі, солі з лужноземельними металами, сульфобензоати, фосфати, ізонікотінати, ацетати, пропіонати, дігідрофосфати, пальмітати, півалати або ж фуроати. В якості антагоністів гістамінового H1-рецептора в комбінації з пропонованими у винаході сполуками переважно використовувати сполуки, вибрані з групи, що включає епінастін, цетиризин, азеластин, фексофенадин, левокабастин, лоратадин, мізоластин, кетотифен, емедастін, диметинден, клемастин, баміпін, цексхлорфенірамін, фенірамін, доксіламін, хлорфеноксамін, діменгідрінат, діфенгідрамін, прометазин, ебастін, олопатадину, деслоратідін і меклозин, необов'язково у вигляді їх рацематів, енантіомерів, діастереомерів і необов'язково у вигляді їх фармакологічно прийнятних кислотно-адитивних солей, сольвати або гідратів. До переважних згідно винаходу кислотно-адитивних солей відносяться солі, вибрані з групи, що включає гідрохлорид, гідробромід, гідроіодід, гідросульфат, гідрофосфат, гідрометансульфонат, гідронітрат, гідромалеат, гідроацетат, гідроцітрат, гідрофумарат, гідротартрат, гідрооксалат, гідросукцінат, гідробензоат і гідропаратолуолсульфонат. В якості антагоністів гістамінового H4-рецептора в комбінації з пропонованими у винаході сполуками переважно використовувати такі сполуки, як, наприклад, (5-хлор-1H-індол-2-іл) - (4метил-1-піперазініл) метанон (JNJ-7777120), необов'язково у вигляді їх рацематів, енантіомерів, діастереомерів і необов'язково у вигляді їх фармакологічно прийнятних кислотно-адитивних солей, сольвати або гідратів. До переважних згідно винаходу кислотно-адитивних солей відносяться солі, вибрані з групи, що включає гідрохлорид, гідробромід, гідроіодід, гідросульфат, гідрофосфат, гідрометансульфонат, гідронітрат, гідромалеат, гідроацетат, гідроцітрат, гідрофумарат, гідротартрат, гідрооксалат, гідросукцінат, гідробензоат і гідропаратолуолсульфонат. В якості інгібіторів MAP-кіназ в комбінації з пропонованими у винаході сполуками переважно використовувати сполуки, вибрані з групи, що включає бентамапімод (AS-602801), дорамапімод (BIRB-796), 5 карбамоіліндол (SD-169), 6-[(амінокарбоніл)(2,6-дифторфеніл)аміно]-2-(2,4дифторфеніл)-3-піридинкарбоксамід (VX-702), α-[2-[[2-(3-піридиніл)етил]аміно]-4-піримідиніл]-2бензотиазолацетонітрил (AS-601245), 9,12-епокси-1H-дііндоло[1,2,3-fg:3',2',1'-kl]піроло[3,4i][1,6]бензодіазоцин-10-карбонову кислоту (CEP-1347) і 4-[3-(4-хлорфеніл)-5-(1-метил-4 16 UA 108373 C2 5 10 15 20 25 30 35 40 45 піперидиніл)-1H-піразол-4-іл]піримідин (SC-409), необов'язково у вигляді їх рацематів, енантіомерів, діастереомерів і необов'язково у вигляді їх фармакологічно прийнятних кислотноадитивних солей, проліків, сольватів або гідратів. В якості антагоністів нейрокінін (NK1 або NK2) в комбінації з пропонованими у винаході сполуками переважно використовувати сполуки, вибрані з групи, що включає саредутант, непадутант і фігопітант, необов'язково у вигляді їх рацематів, енантіомерів, діастереомерів і необов'язково у вигляді їх фармакологічно прийнятних кислотно-адитивних солей, проліків, сольватів або гідратів. В якості протикашльових засобів в комбінації з пропонованими у винаході сполуками переважно використовувати сполуки, вибрані з групи, що включає гідрокодон, караміфен, карбетапентан і декстраметорфан, необов'язково у вигляді їх рацематів, енантіомерів, діастереомерів і необов'язково у вигляді їх фармакологічно прийнятних кислотно-адитивних солей, проліків, сольвати або гідратів. В якості антагоністів CXCR1 або CXCR2 в комбінації з пропонованими у винаході сполуками переважно використовувати такі сполуки, як, наприклад, (SCH-527123), необов'язково у вигляді його рацематів, енантіомерів, діастереомерів і необов'язково у вигляді його фармакологічно прийнятних кислотно-адитивних солей, проліків, сольвати або гідратів. Для досягнення відповідної болезаспокійливої дії пропоновані у винаході сполуки доцільно вводити в організм від одного до трьох разів на день у дозі, яка при внутрішньовенному введенні становить від 0,01 до 3 мг / кг ваги тіла, переважно від 0,1 до 1 мг / кг ваги тіла, а при пероральному введенні становить від 0,1 до 8 мг / кг ваги тіла, переважно від 0,5 до 3 мг / кг ваги тіла. Пропоновані у винаході сполуки можна застосовувати внутрішньовенно, підшкірно, внутрішньом'язово, інтраректального,інтраназально, шляхом інгаляції, трансдермально або перорально, при цьому для інгаляції придатні насамперед препарати для аерозольній інгаляції. Пропоновані у винаході сполуки, при необхідності спільно з одним або декількома звичайними інертними носіями і / або розчинниками, наприклад, з кукурудзяним крохмалем, лактозою, тростинним цукром, мікрокристалічною целюлозою, стеаратом магнію, полівінілпіролідоном, лимонною кислотою, винною кислотою, водою, водою / етанолу, водою / гліцерином, водою / сорбітом, водою / поліетиленгліколь, пропіленгліколем, цетілстеаріловим спиртом, карбоксиметилцелюлозою або жировмісними речовинами, такими як отвердний жир, або їх відповідними сумішами, можна переробляти в звичайні лікарські форми, такі як таблетки, драже, капсули, порошки, суспензії, розчини, дозовані аерозолі або супозиторії. Експериментальна частина Для отриманих в розглянутих нижче прикладах сполук звичайно є дані про їх мас-спектрах і / або 1H ЯМР-спектрах. Зазначені в прикладах для систем розчинників (елюентів) співвідношення між їх компонентами відносяться до одиниць обсягу відповідної розчинника. Зазначені в прикладах для аміаку одиниці об'єму відносяться до концентрованого розчину аміаку у воді. Використовувані при переробці реакційних розчинів розчини кислот, основ і солей являють собою, якщо не вказано інше, водні системи зазначених концентрацій. В якості силікагелю для хроматографічної очистки використовували силікагель, що випускається фірмою Millipore (MATREXTM, 35-70 мкм), або оксид алюмінію (алокс) (фірма E. Merck, Дармштадт, оксид алюмінію 90 стандартизований, 63-200 мкм, артикул № 1.01097.9050). У подальшій експериментальний частині опису використовуються наступні скорочення: ТШХ тонкошарова хроматографія ДМСО диметилсульфоксид ОФ обернена фаза Rt час утримання трет третинний ТБТУ тетрафторборат 2-(1H-бензотриазол-1-іл)-1,1,3,3-тетраметилуронія ТГФ тетрагідрофуран При отриманні сполук у описаних нижче прикладах використовували такі методи аналітичної рідинної хроматографії високого тиску (РХВД). 17 UA 108373 C2 5 Метод 1 Колонка: Interchim Strategy C18, 5 мкм, 4,650 мм. Виявлення: 220-320 нм. Розчинник А: вода/0,1 % оцтової кислоти. Розчинник Б: ацетонітрил. Градієнт: Час в хв 0,0 0,3 2,0 2,4 2,45 2,8 10 % розчинника А 95,0 95,0 2,0 2,0 95,0 95,0 % розчинника Б 5,0 5,0 98,0 98,0 5,0 5,0 Швидкість потоку в мл/хв 3,0 3,0 3,0 3,0 3,0 3,0 Метод 2 Колонка: Merck Cromolith Flash RP18e, 4,625 мм. Розчинник А: вода/0,1 % мурашиної кислоти. Розчинник Б: ацетонітрил/0,1 % мурашиної кислоти. Градієнт: Час в хв 0,0 2,7 3,0 3,3 % розчинника А 90,0 10,0 10,0 90,0 % розчинника Б 10,0 90,0 90,0 10,0 Швидкість потоку в мл/хв 1,6 1,6 1,6 1,6 15 20 Метод 3 Колонка: YMC-Pack ODS-AQ, 3 мкм, 4,675 мм. Розчинник А: вода/0,15 % мурашиної кислоти. Розчинник Б: ацетонітрил. Градієнт: Час в хв 0,0 2,0 5,0 5,5 25 % розчинника А 95,0 10,0 10,0 90,0 % розчинника Б 5,0 90,0 90,0 10,0 Швидкість потоку в мл/хв 1,6 1,6 1,6 1,6 Метод 4 Колонка: Zorbax Stable Bond C18, 1,8 мкм, 330 мм. Розчинник А: вода/0,15 % мурашиної кислоти. Розчинник Б: ацетонітрил. Градієнт: Час в хв 0,0 1,0 2,5 2,75 % розчинника А 95,0 10,0 10,0 95,0 % розчинника Б 5,0 90,0 90,0 5,0 30 18 Швидкість потоку в мл/хв 1,6 1,6 1,6 1,6 UA 108373 C2 5 Метод 5 Колонка: Sunfire C18, 3,5 мкм, 4,650 мм. Виявлення: 180-820 нм. Розчинник А: вода/0,1 % трифтороцтової кислоти. Розчинник Б: ацетонітрил/0,1 % трифтороцтової кислоти. Температура: 40 °C. Градієнт: Час в хв 0,0 2,0 2,5 2,6 10 15 % розчинника Б 5,0 100,0 100,0 5,0 Швидкість потоку в мл/хв 1,5 1,5 1,5 1,5 Метод 6 Колонка: Sunfire C18, 3,5 мкм, 4,650 мм. Виявлення: 180-820 нм. Розчинник А: вода/0,1 % трифтороцтової кислоти. Розчинник Б: ацетонітрил/0,1 % трифтороцтової кислоти. Температура: 40 °C. Градієнт: Час в хв 0,0 2,0 3,0 3,4 20 % розчинника А 95,0 0,0 0,0 95,0 % розчинника А 95,0 0,0 0,0 95,0 % розчинника Б 5,0 100,0 100,0 5,0 Швидкість потоку в мл/хв 1,5 1,5 1,5 1,5 Метод 7 Колонка: YMC-Pack ODS-AQ, 3 мкм, 4,675 мм. Розчинник А: вода/0,15 % мурашиної кислоти. Розчинник Б: ацетонітрил. Градієнт: Час в хв 0,0 4,5 5,0 5,50 % розчинника А 95,0 10,0 10,0 90,0 % розчинника Б 5,0 90,0 90,0 10,0 Швидкість потоку в мл/хв 1,6 1,6 1,6 1,6 25 30 Метод 8 Колонка: Zorbax Stable Bond C18, 1,8 мкм, 330 мм. Розчинник А: вода/0,15 % мурашиної кислоти. Розчинник Б: ацетонітрил. Градієнт: Час в хв 0,0 2,00 2,25 2,50 2,75 % розчинника А 95,0 50,0 10,0 10,0 95,0 % розчинника Б 5,0 50,0 90,0 90,0 5,0 19 Швидкість потоку в мл/хв 1,6 1,6 1,6 1,6 1,6 UA 108373 C2 5 Метод 9 Колонка: Zorbax Stable Bond C18, 1,8 мкм, 330 мм. Розчинник А: вода/0,15 % мурашиної кислоти. Розчинник Б: ацетонітрил. Градієнт: Час в хв 0,0 2,25 2,50 2,75 10 20 Швидкість потоку в мл/хв 1,6 1,6 1,6 1,6 % розчинника А 95,0 10,0 10,0 90,0 % розчинника Б 5,0 90,0 90,0 10,0 Швидкість потоку в мл/хв 1,6 1,6 1,6 1,6 Метод 11 Колонка: X Terra C18, 3,5 мкм, 4,650 мм. Виявлення: 180-820 нм. Розчинник А: вода/0,1 % трифтороцтової кислоти. Розчинник Б: ацетонітрил/0,1 % трифтороцтової кислоти. Температура: 40 °C. Градієнт: Час в хв 0,0 2,0 3,0 3,4 25 % розчинника Б 5,0 90,0 90,0 5,0 Метод 10 Колонка: Zorbax Stable Bond C18, 3,5 мкм, 4,675 мм. Розчинник А: вода/0,15 % мурашиної кислоти. Розчинник Б: ацетонітрил. Градієнт: Час в хв 0,0 4,5 5,0 5,50 15 % розчинника А 95,0 10,0 10,0 95,0 % розчинника А 95,0 0,0 0,0 95,0 % розчинника Б 5,0 100,0 100,0 5,0 Швидкість потоку в мл/хв 1,5 1,5 1,5 1,5 Метод 12 Колонка: Merck Cromolith Flash RP18e, 4,625 мм. Розчинник А: вода/0,1 % мурашиної кислоти. Розчинник Б: ацетонітрил/0,1 % мурашиної кислоти. Градієнт: Час в хв 0,0 2,7 3,0 3,3 % розчинника А 90,0 10,0 10,0 95,0 % розчинника Б 10,0 90,0 90,0 5,0 30 20 Швидкість потоку в мл/хв 1,6 1,6 1,6 1,6 UA 108373 C2 5 Метод 13 Колонка: Merck Cromolith SpeedROD RP-18e, 4,650 мм. Розчинник А: вода/0,1 % мурашиної кислоти. Розчинник Б: ацетонітрил/0,1 % мурашиної кислоти. Градієнт: Час в хв 0,0 4,5 5,0 5,5 10 20 Швидкість потоку в мл/хв 1,5 1,5 1,5 1,5 % розчинника А 95,0 10,0 10,0 90,0 % розчинника Б 5,0 90,0 90,0 10,0 Швидкість потоку в мл/хв 1,6 1,6 1,6 1,6 При отриманні сполук у описаних нижче прикладах використовували такі методи препаративної хроматографії з оберненою фазою. Метод 1 Колонка: Atlantis C18, 5 мкм, 10030 мм. Виявлення: 210-500 нм. Розчинник А: вода/0,1 % трифтороцтової кислоти. Розчинник Б: ацетонітрил. Градієнт: Час в хв 0,0 0,5 8,0 9,0 9,5 10,0 10,1 25 % розчинника Б 10,0 90,0 90,0 5,0 Метод 14 Колонка: Zorbax Stable Bond C18, 3,5 мкм, 4,675 мм. Розчинник А: вода/0,15 % мурашиної кислоти. Розчинник Б: ацетонітрил. Градієнт: Час в хв 0,0 2,0 5,0 5,5 15 % розчинника А 90,0 10,0 10,0 95,0 % розчинника А 95,0 95,0 5,0 5,0 95,0 95,0 95,0 % розчинника Б 5,0 5,0 95,0 95,0 5,0 5,0 5,0 Швидкість потоку в мл/хв 5 50 50 50 50 50 5 Метод 2 Колонка: Varian Pursuit, 5 мкм, 50200 мм. Розчинник А: вода/0,1 % трифтороцтової кислоти. Розчинник Б: ацетонітрил/0,1 % трифтороцтової кислоти. Градієнт: 30 Час в хв 0,0 1,15 12,4 14,0 15,3 15,3 % розчинника А 95,0 95,0 2,0 2,0 95,0 95,0 % розчинника Б 5,0 5,0 98,0 98,0 5,0 5,5 21 Швидкість потоку в мл/хв 180 180 180 180 180 180 UA 108373 C2 Метод 3 Колонка: YMC-Pack ODS-AQ, 5 мкм, 30100 мм. Розчинник А: вода/0,15 % мурашиної кислоти. Розчинник Б: ацетонітрил. Градієнт: 5 Час в хв 0,0 2,0 6,0 12,0 13 % розчинника А 95,0 95,0 10,0 10,0 90,0 % розчинника Б 5,0 5,0 90,0 90,0 10,0 Швидкість потоку в мл/хв 50 50 50 50 50 Отримання вихідних сполук Сполуки загальної формули I можна отримувати з наступних проміжних сполук A, B і C: 10 R R 1 2 O R N O R 5 R 3 R 4 R 2 7 R N X N 8 R R X (R6)n R 2 R 9 10 11 B A C R R AAV1 + AAV2 1 2 O N O R NH 3 R 4 R 2 B R 2 O R HN AAV1 + AAV3 5 R 3 R 4 R 2 R R R X (R6) 7 N X N R 8 n R 2 R 9 10 11 C R R 1 2 O HN OH + R O R 5 R X N 3 R 4 R 2 R X 8 R 7 R N (R6)n R R 2 R 9 R 1 2 O R N O R 10 5 R X N 3 R 4 R 2 R X 7 R N (R6)n 11 8 R R 2 R 9 10 11 C R R 1 R 2 O R R O N NH 3 5 R B 4 R 2 + X HN R 2 R X 8 7 R N (R6)n R R 2 R R 9 10 R 1 2 O N O R R 5 R 3 R 4 R 2 X (R6) 11 A 22 n R N X N 8 7 R R R 2 R 11 9 10 UA 108373 C2 5 10 15 20 AAV1: Амідне сполучення Розчин карбоновокислотного компонента (1 молярний еквівалент), тріетіламіна (2,5 молярних еквівалента) i ТБТУ (1,1 молярних еквівалента) в ТГФ перемішують протягом 30 хв при кімнатній температурі. Потім додають аміновий компонент (1,1 молярних еквівалента у вигляді гідрохлоріда) i залишають перемішуватися на ніч. Після цього суміш упарюють, змішують з водою, підлужують розведеним розчином карбонату калію і екстрагують етілацетатом. Продукт виділяють і очищають колоночною хроматографією (або хроматографією на силікагелі, або хроматографією з оберненою фазою). AAV2: Гідроліз складних ефірів До розчину складного ефіру (1 молярний еквівалент) в метанолі додають 2н. розчин їдкого натру (2 молярних еквівалента) i суміш перемішують протягом 1-5 год. при кімнатній температурі. Після цього підкислюють оцтової кислотою і суміш насухо упарюють у вакуумі. Отриманий таким шляхом сирий продукт зазвичай очищають колонковою хроматографією на силікагелі. AAV3: Відщіплення трет-бутилоксикарбонільної захисної групи Розчин трет-бутоксикарбоніламіносполуки (1 молярний еквівалент) в дихлорметані змішують з трифтороцтовою кислотою (3-10 молярних еквівалентів) і перемішують при кімнатній температурі до повного відщеплення захисної групи. Після цього реакційну суміш упарюють насухо і отриманий таким шляхом сирий продукт очищають хроматографією. AAV4: Отримання проміжних сполук A R N R X 8 7 R 9 + H2N F (R6)n X (R6) n R N H R X (R6)n R 10 (R6)n R R 9 HO N H 10 (R6)n 11 R 30 R N H X R R R 9 10 11 8 7 N H 10 8 R R (R6)n 25 R 9 11 7 Alkyl H2N R R X N 8 7 Alkyl R R X H2N 8 7 N H 9 11 R R H H R R 10 11 8 7 Alkyl O R R N R R R R 9 10 11 AAV2: Гідроліз складних ефірів До розчину складного ефіру (1 молярний еквівалент) в метанолі додають 2н. розчин їдкого натру (2 молярних еквівалента) i суміш перемішують протягом 1-5 год. при кімнатній температурі. Після цього підкислюють оцтової кислотою і суміш насухо упарюють у вакуумі. Отриманий таким шляхом сирий продукт зазвичай очищають колонковою хроматографією на силікагелі. AAV3: Відщеплення трет-бутілоксікарбонільної захисної групи 23 UA 108373 C2 5 10 15 20 25 30 Розчин трет-бутоксикарбоніламіносполуки (1 молярний еквівалент) в дихлорметані змішують з тріфтороцтовою кислотою (3-10 молярних еквівалента) i перемішують при кімнатній температурі до повного відщеплення захисної групи. Після цього реакційну суміш упарюють насухо і отриманий таким шляхом сирий продукт очищають хроматографією. AAV4: Отримання проміжних сполук A Розчин анілінового компонента (1 молярний еквівалент) i сильної основи, такої, наприклад, як трет-бутилат калію (1 молярний еквівалент), в ДМСО перемішують протягом години при кімнатній температурі, після чого змішують з 4-фторбензонітрільним компонентом (1 молярний еквівалент) і залишають перемішуватися на ніч при температурі близько 80 °C. Для переробки суміш фільтрують через алокс і насухо упарюють у вакуумі. Нітрільну групу отриманого таким шляхом дифеніламінового проміжного продукту потім відновлюють з додаванням нікелю Ренея при температурі 55 °C і при надлишковому тиску водню 3 бари до амінометільной групи і отриманий продукт очищають хроматографією. Для отримання проміжних сполук A з α-алкілбензільною групою (наприклад, проміжних сполук A1, A4, A5) нітрильне похідне (1 молярний еквівалент) розчиняють в діетіловому ефірі і при температурі 0-5 °C і при перемішуванні за краплях додають до розчину алкілмагнійброміда (4 молярних еквівалента) в діетіловому ефірі, після чого перемішують ще протягом приблизно 30 хв. Далі реакційну суміш при 5 °C домішують до 1-молярної соляної кислоти і отриманий таким шляхом алкілкетон звичайним чином виділяють і очищають хроматографією. Розчин отриманого таким шляхом кетону (1 молярний еквівалент) в ацетонітрилі змішують з тріетіламіном (2 молярних еквівалента) i гідрохлоридом гідроксіламіну (1,3 молярних еквівалента) i протягом 4 год. кип'ятять із зворотним холодильником. Після цього додають воду і екстрагують дихлорметаном. З органічної фази звичайним методом виділяють і очищають утворився оксим. Розчин цього оксиму (1 молярний еквівалент) в метанолі змішують з метанольною соляною кислотою (6,6 молярних еквівалента). Після додавання пилоподібного цинку (1,4 молярних еквівалента) суміш протягом 3 год. при перемішуванні кип'ятять із зворотним холодильником. Після охолодження суміш змішують з водою і екстрагують дихлорметаном. Отриманий таким шляхом амін при необхідності очищають хроматографією. Інша можливість відновлення оксиму до відповідного аміну полягає в каталітичному гідруванні. Для цього оксим в метанольного розчині аміаку гідрують після додавання нікелю Ренея при температурі 50 °C і при надлишковому тиску водню 50 фунтів / кв.дюйм до повного поглинання водню. Отриманий таким шляхом амін при необхідності очищають хроматографією. Отримання проміжних сполук A 35 5 8 R R HN 2 R 9 X (R6)n 7 R N X R R 10 2 11 R R Відповідно до загальної методики AAV4 отримують наступні проміжні сполуки A1-A9. Проміжна сполука A1: (6-Амінометилпіридин-3-іл)-(4-хлор-2-трифторметилфеніл)амін 40 H2N N Cl N H F 45 F F РХВД: Rt=1,74 хв (метод 13) + Мас-спектр (ESI): [M+H] = 302 Проміжна сполука A2: (4-Амінометилфеніл)-(4-фтор-2-трифторметилфеніл)амін 24 UA 108373 C2 F H2N N H F F F + 5 Мас-спектр (ESI): [M+H] = 285 Тонкошарова хроматографія (силікагель, CH2Cl2/етанол в співвідношенні 19:1): Rf=0,16 Проміжна сполука A3: (6-Амінометилпіридин-3-іл)-(4-фтор-2-трифторметилфеніл)амін N H2N F N H F 10 F F РХВД: Rt=2,06 хв (метод 3) + Мас-спектр (ESI): [M+H] = 286; [M-H] = 284 Проміжна сполука A4: (4-Амінометил-3-фторфеніл)-(4-фтор-2-трифторметилфеніл)амін F H2N F N H F 15 F F + Мас-спектр (ESI): [M+H] = 303 Тонкошарова хроматографія (силікагель, CH2Cl2/етанол в співвідношенні 19:1): Rf=0,08 Проміжна сполука A5: (4-Амінометил-3-фторфеніл)-(2-трифторметилфеніл)амін H2N F N H F 20 F F Мас-спектр (ESI): [M-H] = 283 Тонкошарова хроматографія (силікагель, CH2Cl2/етанол в співвідношенні 19:1): Rf=0,09 Проміжна сполука A6: (4-Амінометилфеніл)-(2-трифторметилфеніл)амін H2N N H F 25 F F РХВД: Rt=1,36 хв (метод 1) + Мас-спектр (ESI): [M+H-NH3] = 250 Проміжна сполука A7: (4-Амінометилфеніл)-(4-хлор-2-трифторметилфеніл)амін 30 25 UA 108373 C2 Cl H2N N H F F F + Мас-спектр (ESI): [M+H-NH3] = 284/286 Проміжна сполука A8: (4-Амінометил-3-фторфеніл)-(4-хлор-2-трифторметилфеніл)амін 5 Cl H2N F N H F F F РХВД: Rt=1,83 хв (метод 2) Проміжна сполука A9: (4-Амінометилфеніл)-(4-бром-2-трифторметилфеніл)амін 10 Br H2N N H F F F РХВД: Rt=1,81 хв (метод 2) Отримання проміжних сполук B 15 2 R 1 R N OH 3 O R 20 O 4 R Наступну проміжну сполуку B1 отримують шляхом амідного поєднання відповідно до Загальної методики AAV1 і шляхом подальшого омилення складного ефіру відповідно до Загальної методики AAV2. Проміжна сполука B1: (S)-3-[(6-Оксо-1,6-дигідропіридазин-4карбоніл)амінo]тетрагідрофуран-3-карбонова кислота HN N H N O O OH O O 25 30 РХВД: Rt=0,33 хв (метод 2) + Мас-спектр (ESI): [M+H] = 254 Аналогічним шляхом можна одержати наступну проміжну сполуку B2. Проміжна сполука B2: 1-[(6-Оксо-1,6-дигідропіридазин-4карбоніл)амінo]циклопропанкарбонова кислота HN N H N O O 26 O OH UA 108373 C2 Отримання проміжних сполук C R 2 O R HN 5 R R 4 R 2 X (R6)n 5 7 R N X N 3 R 8 R R R 2 R 9 10 11 Наступні проміжні сполуки C1-C6 отримують шляхом амідного поєднання відповідно до Загальної методики AAV1 і шляхом подальшого відщеплення трет-бутілоксі карбонільно захисної групи відповідно до Загальної методики AAV3. Проміжна сполука C1: [5-(4-Хлор-2-трифторметилфеніламінo)піридин-2-ілметил]амід 1аміноциклопропанкарбонової кислоти 10 O H2N N N H Cl N H F 15 F F РХВД: Rt=1,55 хв (метод 13) Мас-спектр (ESI): [M-H] = 383 Проміжна сполука C2: [5-(4-Фтор-2-трифторметилфеніламінo)піридин-2-ілметил]амід 1аміноциклопропанкарбонової кислоти O H2N N N H F N H F 20 F F РХВД: Rt=2,33 хв (метод 7) + Мас-спектр (ESI): [M+H] = 369; [M-H] = 367 Проміжна сполука C3: 2-Фтор-4-(4-фтор-2-трифторметилфеніламінo)бензиламід амінотетрагідрофуран-3-карбонової кислоти (S)-3 O H2N F N H O F N H F 25 F F + Мас-спектр (ESI): [M+H] = 416 Проміжна сполука C4: 4-(4-Фтор-2-трифторметилфеніламінo)бензиламід амінотетрагідрофуран-3-карбонової кислоти 30 27 (S)-3 UA 108373 C2 O H2N F N H N H O F 5 F F РХВД: Rt=1,99 хв (метод 2) + Мас-спектр (ESI): [M+H] = 398 Проміжна сполука C5: 4-(4-Хлор-2-трифторметилфеніламінo)бензиламід амінотетрагідрофуран-3-карбонової кислоти (S)-3 O H2N Cl N H N H O F 10 F F РХВД: Rt=2,41 хв (метод 2) Проміжна сполука C6: 2-Фтор-4-(2-трифторметилфеніламінo)бензиламід амінотетрагідрофуран-3-карбонової кислоти (S)-3 O H2 N N H O F N H F 15 F F + Мас-спектр (ESI): [M+H] = 398 Отримання кінцевих сполук Приклад 1: (1-{[5-(4-Фтор-2-трифторметилфеніламінo)піридин-2ілметил]карбамоіл}циклопропіл)амід 6-оксо-1,6-дигідропіридазин-4-карбонової кислоти HN N H N O O O N H N F N H F 20 25 F F Зазначену сполуку отримують з проміжного сполуки C2 і 6-оксо-1,6-дігідропірідазін-4карбонової кислоти відповідно до загальної методики AAV1. C22H18F4N6O3 (490,42) Rt=2,80 хв (метод 7) Приклад 2: (1-{[5-(4-Хлор-2-трифторметилфеніламінo)піридин-2ілметил]карбамоіл}циклопропіл)амід 6-оксо-1,6-дигідропіридазин-4-карбонової кислоти 28
ДивитисяДодаткова інформація
Автори англійськоюHauel, Norbert, Ceci, Angelo, Doods, Henri, Konetzki, Ingo, Mack, Juergen, Priepke, Henning, Schuler-Metz, Annette, Walter, Rainer, Wiedenmayer, Dieter
Автори російськоюХауэль Норберт, Чечи Анджело, Доодс Хенри, Конетцки Инго, Мак Йюрген, Припке Хеннинг, Шулер-Метц Аннетте, Вальтер Райнер, Видэнмайер Дитер
МПК / Мітки
МПК: C07D 271/10, C07D 239/557, C07D 261/18, C07D 233/90, A61K 31/506, C07D 405/12, C07D 213/80, A61K 31/165, C07D 401/12, C07D 211/62, C07D 207/277, A61K 31/44, A61K 31/505, C07D 239/28, C07C 237/24
Мітки: антагоністи, брадикініну, похідні, 3-оксопіридазину
Код посилання
<a href="https://ua.patents.su/36-108373-pokhidni-3-oksopiridazinu-yak-antagonisti-bradikininu-b1.html" target="_blank" rel="follow" title="База патентів України">Похідні 3-оксопіридазину як антагоністи брадикініну b1</a>