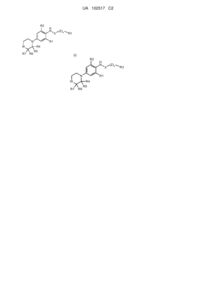
Заміщені похідні морфоліну та тіоморфоліну, фармацевтична композиція на їх основі та їх застосування для виробництва лікарського засобу для лікування розладу або захворювання центральної нервової системи
Номер патенту: 102517
Опубліковано: 25.07.2013
Автори: Рітсен Андреас, Венсель Торньое Крістіан, Ватсон Вільям Патрик, Роттлондер Маріо, Ханжин Ніколай
Формула / Реферат
1. Заміщені похідні морфоліну або тіоморфоліну загальної формули І
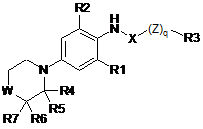 , (І)
, (І)
де q дорівнює 0 або 1;
W являє собою О або S;
Х являє собою CO;
Z являє собою О;
R1 вибраний з групи, що складається з галогену, ціано, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, галоген-С1-6-алк(ен/ін)ілу, галоген-С3-8-циклоалк(ен)ілу, галоген-С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, С1-6-алк(ен/ін)ілокси, С3-8-циклоалк(ен)ілокси і С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілокси;
R2 вибраний з групи, що складається з галогену, ціано, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, галоген-С1-6-алк(ен/ін)ілу, галоген-С3-8-циклоалк(ен)ілу, галоген-С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, С1-6-алк(ен/ін)ілокси, С3-8-циклоалк(ен)ілокси, С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілокси, необов'язково заміщеного фенілу і необов'язково заміщеного піридилу; де феніл і піридил необов'язково заміщені одним або більше замісниками, що незалежно являють собою галоген, С1-6-алк(ен/ін)іл, С3-8-циклоалк(ен)іл або С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)іл;
R3 являє собою С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)іл;
кожний з R4, R5, R6 і R7 незалежно вибраний з групи, що складається з водню і Аr;
Аr вибраний з групи, що складається з необов'язково заміщеного фенілу, необов'язково заміщеного нафтилу, необов'язково заміщеного піридину, необов'язково заміщеного тіофену, необов'язково заміщеного фурану, необов'язково заміщеного тіазолу, необов'язково заміщеного хіноліну, необов'язково заміщеного індолу, необов'язково заміщеного 2,3-дигідробензофурану, необов'язково заміщеного піримідину, необов'язково заміщеного піролу і необов'язково заміщеного оксазолу, де замісники є незалежно вибраними з галогену, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, галоген-С1-6-алк(ен/ін)ілу, С1-6-алк(ен/ін)ілокси або С3-8-алк(ен/ін)ілокси;
у вигляді вільної основи або їх солі.
2. Сполука за п. 1, де Аr вибраний з групи, що складається з необов'язково заміщеного фенілу, необов'язково заміщеного нафтилу, необов'язково заміщеного піридину, необов'язково заміщеного 2,3-дигідробензофурану і необов'язково заміщеного тіофену.
3. Сполука за будь-яким з пп. 1, 2, де будь-який Ar може бути заміщений одним або більше замісниками, які незалежно являють собою галоген, С1-6-алк(ен/ін)іл, галоген-С1-6-алк(ен/ін)іл або С1-6-алк(ен/ін)ілокси.
4. Сполука за будь-яким з пп. 1-3, де q дорівнює 0.
5. Сполука за будь-яким з пп. 1-3, де q дорівнює 1.
6. Сполука за будь-яким з пп. 1-5, де W являє собою атом кисню.
7. Сполука за будь-яким з пп. 1-5, де W являє собою атом сірки.
8. Сполука за будь-яким з пп. 1-7, де R1 вибраний з групи, що складається з галогену, ціано, С1-6-алк(ен/ін)ілу, галоген-С1-6-алк(ен/ін)ілу і С1-6-алк(ен/ін)ілокси.
9. Сполука за п. 8, де R1 являє собою С1-6-алк(ен/ін)іл.
10. Сполука за будь-яким з пп. 1-6, де R2 вибраний з групи, що складається з галогену, ціано, С1-6-алк(ен/ін)ілу, галоген-С1-6-алк(ен/ін)ілу, С1-6-алк(ен/ін)ілокси, необов'язково заміщеного фенілу і необов'язково заміщеного піридилу.
11. Сполука за п. 10, де R2 являє собою С1-6-алк(ен/ін)іл.
12. Сполука за п. 10, де необов'язково заміщений феніл і необов'язково заміщений піридил може бути заміщений одним або більше замісниками, які незалежно являють собою галоген або С1-6-алк(ен/ін)іл.
13. Сполука за будь-яким з пп. 1-12, де R4 не містить Ar.
14. Сполука за будь-яким з пп. 1-13, де R5 не містить Ar.
15. Сполука за будь-яким з пп. 1-14, де R6 не містить Ar.
16. Сполука за будь-яким з пп. 1-15, де R7 не містить Ar.
17. Заміщене похідне морфоліну за п. 1, де q дорівнює 0 або 1;
W являє собою О або S;
Х являє собою CO;
Z являє собою О;
R1 і R2 незалежно вибрані з групи, що складається з галогену, галоген-С1-6-алк(ен/ін)ілу, С1-6-алк(ен/ін)ілу і ціано;
R3 являє собою С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)іл; і
R4, R5, R6 і R7 незалежно вибрані з групи, що складається з водню і Ar;
або його солі.
18. Сполука за будь-яким з пп. 1-17, де згадана сполука вибрана з групи, що складається з:
2-циклопентил-N-(2-бром-6-трифторметил-4-морфолін-4-ілфеніл)ацетаміду;
N-(2-бром-4-морфолін-4-іл-6-трифторметилфеніл)-3-циклопентилпропіонаміду;
N-(2-хлор-6-ціано-4-морфолін-4-ілфеніл)-3-циклогексилпропіонаміду;
2-циклопентил-N-(2,6-диметил-4-тіоморфолін-4-ілфеніл)ацетаміду;
2-циклопентил-N-[2,6-диметил-4-(2-фенілморфолін-4-іл)феніл] ацетаміду;
2-циклопентил-N-[2,6-диметил-4-(2-фенілтіоморфолін-4-іл)феніл]ацетаміду;
2-циклопентил-N-[2,6-диметил-4-(3-піридин-3-іл-тіоморфолін-4-іл)феніл]ацетаміду;
2-циклопентил-N-{2,6-диметил-4-[2-(4-трифторметилфеніл)тіоморфолін-4-іл]феніл}ацетаміду;
N-{4-[2-(2-хлорфеніл)тіоморфолін-4-іл]-2,6-диметилфеніл}-2-циклопентилацетаміду;
2-біцикло[2.2.1]гепт-2-ил-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетаміду;
2-циклогексил-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетаміду;
2-циклопентил-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетаміду;
3-циклогексил-N-(2,6-диметил-4-морфолін-4-ілфеніл)пропіонаміду;
3-циклопентил-N-(2,6-диметил-4-морфолін-4-ілфеніл)пропіонаміду;
2-циклогептил-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетаміду;
N-(2-бром-4-морфолін-4-іл-6-трифторметилфеніл)-3-циклогексилпропіонаміду;
N-(2-xлop-4-мopфoлiн-4-iл-6-трифторметилфеніл)-2-циклопентилацетаміду;
2-циклопентил-N-{2,6-диметил-4-[2-(4-трифторметилфеніл)морфолін-4-іл]феніл}ацетаміду;
N-{4-[2-(2-хлорфеніл)морфолін-4-іл]-2,6-диметилфеніл}-2-циклопентилацетаміду;
2-циклопентил-N-{4-[2-(4-фторфеніл)морфолін-4-іл]-2,6-диметилфеніл}ацетаміду;
2-циклопент-2-еніл-N-(2,6-диметил-4-морфолін-4-ілфеніл) ацетаміду;
2-циклопентил-N-(4-морфолін-4-іл-2-піридин-3-іл-6-трифторметилфеніл)ацетаміду;
2-циклопентил-N-(5-морфолін-4-іл-3-трифторметилбіфеніл-2-іл)ацетаміду;
2-циклопентил-N-(4'-фтop-5-мopфoлiн-4-iл-3-трифтopмeтилбiфeнiл-2-іл)ацетаміду;
2-циклопентил-N-(4'-метил-5-мopфoлiн-4-iл-3-трифтopмeтилбiфeнiл-2-іл)ацетаміду;
2-циклопентил-N-(3’-метил-5-мopфoлiн-4-iл-3-трифтopмeтилбiфeнiл-2-іл)ацетаміду;
2-циклопентил-N-(3',4'-дифтop-5-мopфoлiн-4-iл-3-тpифтopмeтилбiфeнiл-2-іл)ацетаміду;
2-циклопентил-N-(2,6-діетил-4-морфолін-4-ілфеніл)ацетаміду;
2-циклопентил-N-(2,6-діізопропіл-4-морфолін-4-ілфеніл)ацетаміду;
2-циклопентил-N-(2,6-дифтор-4-морфолін-4-ілфеніл)ацетаміду;
2-циклопент-2-еніл-N-(2,6-дифтор-4-морфолін-4-ілфеніл)ацетаміду;
2-біцикло[2.2.1]гепт-2-ил-N-(2,6-дифтор-4-морфолін-4-ілфеніл)ацетаміду;
2-біцикло[2.2.1]гепт-2-ил-N-(2-метил-4-морфолін-4-іл-6-трифторметилфеніл)ацетаміду;
2-циклопент-2-еніл-N-(2-метил-4-морфолін-4-іл-6-трифторметилфеніл)ацетаміду;
2-циклопентил-N-(2-метил-4-морфолін-4-іл-6-трифторметилфеніл)ацетаміду;
2-циклопентил-N-(2-метокси-6-метил-4-морфолін-4-ілфеніл)ацетаміду;
2-циклопент-2-еніл-N-(2-метокси-6-метил-4-морфолін-4-ілфеніл)ацетаміду;
2-біцикло[2.2.1]гепт-2-ил-N-(2-метокси-6-метил-4-морфолін-4-ілфеніл)ацетаміду і N-(2-xлop-6-мeтил-4-мopфoлiн-4-iлфeнiл)-2-циклoпeнтилaцeтaмiдy.
19. Сполука за будь-яким одним з пп. 1-18 для застосування як медикаменту.
20. Фармацевтична композиція, яка містить один або більше фармацевтично прийнятних носіїв або розріджувачів і одну або більше сполук у відповідності з будь-яким з пп. 1-19.
21. Застосування сполуки у відповідності з будь-яким з пп. 1-19 для виробництва фармацевтичної композиції для лікування розладу або захворювання, сприйнятливого до посиленого потоку іонів в калієвих каналах, що переважно є розладом або захворюванням центральної нервової системи.
22. Застосування за п. 21, де розлад або захворювання, що слід лікувати, вибрані з групи, що складається з судомних нападів, тривожних розладів, розладів невропатичного болю і розладів мігреневого болю і нейродегенеративних розладів.
23. Застосування за п. 22, де судомні напади вибрані з групи, що складається з гострих судомних нападів, конвульсій, епілептичного статусу, епілепсії, такої як епілептичні синдроми і епілептичні напади.
24. Застосування за п. 22, де тривожні розлади вибрані з групи, що складається з тривоги і розладів і захворювань, пов'язаних з панічною атакою, агорафобії, панічних розладів з агорафобією, панічних розладів без агорафобії, агорафобії без історії панічного розладу, специфічної фобії, соціальної фобії та інших специфічних фобій, обсесивно-компульсивного розладу, посттравматичного стресового розладу, гострих стресових розладів, генералізованого тривожного розладу, тривожного розладу, пов'язаного із загальним станом здоров'я, тривожного розладу, що викликається речовинами, тривожного розладу, пов'язаного з розлукою, розладів адаптації, страху діяльності, іпохондричних розладів, тривожного розладу, пов'язаного із загальним станом здоров'я, і тривожного розладу, що викликається речовинами, і тривожних розладів, які конкретно не визначені.
25. Застосування за п. 22, де розлади невропатичного болю і розлади мігреневого болю вибрані з групи, що складається з алодинії, гіпералгічного болю, фантомного болю, невропатичного болю, пов'язаного з діабетичною невропатією, невропатичного болю, пов'язаного з тригемінальною невралгією, і невропатичного болю, пов'язаного з мігренню.
26. Застосування за п. 22, де нейродегенеративні розлади вибрані з групи, що складається з хвороби Альцгеймера, хореї Гентінгтона, розсіяного склерозу, бічного аміотрофічного склерозу, хвороби Крейтцфельда-Якоба, хвороби Паркінсона, індукованих СНІДом енцефалопатій або енцефалопатій, викликаних вірусами коревої краснухи, герпесвірусами, бореліями або невідомими патогенами, викликаних травмою нейродегенерацій, станів нейронального гіперзбудження, таких як при синдромі відміни ліків або при інтоксикації, і нейродегенеративних захворювань периферичної нервової системи, таких як поліневропатії і поліневрити.
27. Застосування за п. 21, де згаданий розлад або захворювання є біполярним розладом.
28. Заміщені похідні морфоліну або тіоморфоліну загальної формули І
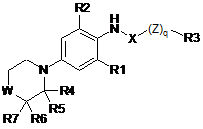 , (І)
, (І)
де q дорівнює 0 або 1;
W являє собою О або S;
Х являє собою CO;
Z являє собою О;
R1 вибраний з групи, що складається з галогену, ціано, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, галоген-С1-6-алк(ен/ін)ілу, галоген-С3-8-циклоалк(ен)ілу, галоген-С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу,С1-6-алк(ен/ін)ілокси, С3-8-циклоалк(ен)ілокси і С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілокси;
R2 вибраний з групи, що складається з галогену, ціано, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, галоген-С1-6-алк(ен/ін)ілу, галоген-С3-8-циклоалк(ен)ілу, галоген-С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, С1-6-алк(ен/ін)ілокси С3-8-циклоалк(ен)ілокси,С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілокси, необов'язково заміщеного фенілу і необов'язково заміщеного піридилу; де феніл і піридил необов'язково заміщені одним або більше замісниками, що незалежно являють собою галоген, С1-6-алк(ен/ін)іл, С3-8-циклоалк(ен)іл або С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)іл;
R3 являє собою С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)іл;
кожний з R4, R5, R6 і R7 незалежно вибраний з групи, що складається з водню і Аr;
Аr вибраний з групи, що складається з необов'язково заміщеного фенілу, необов'язково заміщеного нафтилу, необов'язково заміщеного піридилу, необов'язково заміщеного тієнілу, необов'язково заміщеного фурилу, необов'язково заміщеного тіазолілу, необов'язково заміщеного хінолілу, необов'язково заміщеного індолілу, необов'язково заміщеного 2,3-дигідробензофурилу, необов'язково заміщеного піримідинілу,необов'язково заміщеного піролілу і необов'язково заміщеного оксазолілу, де замісники є незалежно вибраними з галогену, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, галоген-С1-6-алк(ен/ін)ілу, С1-6-алк(ен/ін)ілокси або С3-8-алк(ен/ін)ілокси;
або їх солі;
для лікування біполярного розладу.
Текст
Реферат: Цей винахід стосується похідних морфоліну і тіоморфоліну загальної формули І або до їх фармацевтично прийнятних солей і до їх застосування. UA 102517 C2 (12) UA 102517 C2 R2 R7 R6 X (Z)q R3 R1 N W H N R4 R5 (I) R2 R1 N W R7 R6 H N R4 R5 X (Z)q R3 UA 102517 C2 5 10 15 20 25 30 35 40 45 50 55 60 Цей винахід стосується нових заміщених похідних морфоліну і тіоморфоліну, які відкривають іонні калієві канали сімейства KCNQ. Дані сполуки використовуються для лікування розладів і захворювань, сприйнятливих до відкриття іонних калієвих каналів сімейства KCNQ, одним з таких захворювань є епілепсія. Іонні канали є клітинними білками, які регулюють потік іонів, включаючи іони калію, кальцію, хлору і натрію, в клітини і з них. Такі канали присутні у всіх клітинах тварин і людини, та вони беруть участь в різних процесах, включаючи нейрональну передачу, скорочення м'язів і клітинну секрецію. У людей є більше 70 генів, що кодують субодиниці калієвих каналів (Jentsch Nature Reviews Neuroscience 2000, 1, 21-30), причому вони відрізняються великою різноманітністю відносно як їх будови, так і функцій. Нейрональні калієві канали, які знаходяться в мозку, відповідальні, головним чином, за підтримку негативного мембранного потенціалу спокою, а також контролюють реполяризацію мембран після потенціалу дії. Однією підгрупою генів калієвих каналів є сімейство KCNQ. Мутації в чотирьох з п'яти генів KCNQ, як було показано, лежать в основі захворювань, включаючи серцеві аритмії, глухоту і епілепсію (Jentsch Nature Reviews Neuroscience 2000, 1, 21-30). Вважають, що ген KCNQ4 кодує молекулярну кореляцію калієвих каналів, що знаходяться в зовнішніх волосних клітинах завитка вуха і у волосних клітинах типу І вестибулярного апарата, мутації в якому можуть привести до форми спадкової глухоти. KCNQ1 (KvLQTl) пов'язаний з продуктом гена KCNE1 (мінімальний К(+)-білок каналу) в серці для створення в серці К(+) струму, подібного до сповільненого випрямляча. Мутації в цьому каналі можуть викликати одну з форм спадкового синдрому подовженого QT типа 1 (LQT1), також вони пов'язані з формою глухоти (Robbins Pharmacol Ther 2001, 90, 1-19). Гени KCNQ2 і KCNQ3 були відкриті в 1988 p. і, як з'ясувалося, мали мутації при спадковій формі епілепсії, відомої як легка форма спадкових неонатальних судом (Rogawski Trends in Neurosciences 2000, 23, 393-398). Білки, кодовані генами KCNQ2 і KCNQ3, локалізовані в пірамідальних нейронах кори головного мозку і гіпокампа людини, в ділянках мозку, пов'язаних з виникненням і розвитком судомних нападів (Cooper et al. Proceedings National Academy of Science USA 2000, 97, 4914-4919). KCNQ2 і KCNQ3 є двома субодиницями калієвих каналів, які формують "М-струми" при експресії in vitro. М-струм є не-інактивуючим калієвим струмом, виявленим в багатьох типах нейронів. У кожному типі клітин він є домінантним в регулюванні мембранної збудливості, оскільки є єдиним постійним струмом в інтервалі ініціації потенціалу дії (Marrion Annual Review Physiology 1997, 59, 483-504). Модуляція М-струму значно впливає на нейрональну збудливість, наприклад, активація струму знижує нейрональну збудливість. Відкривачі вказаних каналів KCNQ або активатори М-струму, знижують надмірну нейрональну активність і можуть бути, таким чином, використані для лікування судомних нападів і інших захворювань і розладів, що характеризуються надмірною нейрональною активністю, таких як нейрональна гіперзбудливість, включаючи конвульсивні розлади, епілепсію і невропатичний біль. Ретигабін (D-23129; етиловий естер N-(2-аміно-4-(4-фторбензиламіно)феніл)-карбамінової кислоти) і його аналоги розкриті в ЕР554543. Ретигабін є антиконвульсивною сполукою з широким спектром дії та з сильними антиконвульсивними властивостями як в умовах in vitro, так і in vivo. Він є активним при пероральному і внутрішньочеревинному введенні щурам і мишам у ряді антиконвульсивних тестів, включаючи електрично індуковані судомні напади, судомні напади, хімічно індуковані пентилентетразолом, пікротоксином і N-метил-D-аспартатом (NMDA), і в генетичній моделі на тваринах, мишах DBA/2 (Rostock et al. Epilepsy Research 1996, 23, 211223). Крім того, ретигабін є активним на моделі збудження мигдалини мозочка складних парціальних нападів, що додатково вказує на те, що вказана сполука має потенційну можливість для застосування в антиконвульсивній терапії. У нещодавно проведених клінічних випробуваннях було показано, що ретигабін виявляє ефективність в зниженні частоти судомних нападів у пацієнтів з епілепсією (Bialer et al. Epilepsy Research 2002,51,31-71). Було показано, що ретигабін активує К(+)-струм в нейрональних клітинах, і фармакологія індукованого таким чином струму узгоджується з опублікованими даними по фармакології для М-каналу, які недавно були скорельовані з гетеромультимером К(+)-каналів KCNQ2/3. Це дає можливість припустити, що активація каналів KCNQ2/3 може бути відповідальна за деяку антиконвульсивну активність вказаного агента (Wickenden et al. Molecular Pharmacology 2000, 58, 591-600) і що інші агенти, які діють за таким же механізмом, можуть знайти аналогічні застосування. Повідомлялося також, що канали KCNQ 2 і 3 стимулюються на моделях невропатичного болю (Wickenden et al. Society for Neuroscience Abstracts 2002,454, 7), і була висловлена 1 UA 102517 C2 5 10 15 20 25 30 35 40 45 50 55 гіпотеза про те, що модулятори калієвих каналів є активними як при невропатичному болю, так і при епілепсії (Schroder et al. Neuropharmacology 2001, 40, 888-898). Було також показано, що ретигабін надає сприятливу дію при невропатичному болю в моделях на тваринах (Blackbum-Munro and Jensen European Journal of Pharmacology 2003, 460, 109-116), і тому передбачається, що відкривачі каналів KCNQ можуть знайти застосування при лікуванні больових розладів, включаючи невропатичний біль. Повідомляється, що локалізація мРНК каналів KCNQ в мозку та інших відділах центральної нервової системи пов'язана з болем (Goldstein et al. Society for Neuroscience Abstracts 2003, 53.8). На додаток до ролі в невропатичному болю, експресія мРНК для KCNQ 2-5 в гангліях тригемінального і дорсального коренів і в тригемінальному хвостатому ядрі дає можливість припустити, що відкривачі вказаних каналів можуть також впливати на сенсорний процесинг мігреневого болю (Goldstein et al. Society for Neuroscience Abstracts 2003, 53.8). Недавні повідомлення демонструють, що мРНК для KCNQ 3 і 5, в доповнення до мРНК для KCNQ2, експресуютьтся в астроцитах і гліальних клітинах. Таким чином, канали KCNQ 2, 3 і 5 можуть допомогти модулювати синаптичну активність в ЦНС і внести свій внесок до нейропротекторних функцій відкривачів каналів KCNQ (Noda et al., Society for Neuroscience Abstracts 2003, 53.9). Ретигабін і інші модулятори KCNQ можуть таким чином демонструвати захист проти нейродегенеративних аспектів епілепсії, оскільки було показано, що ретигабін запобігає лімбічній нейродегенерації і експресії маркерів апоптозу після індукованого каїновою кислотою епілептичного статусу у щурів (Ebert et al, Epilepsia 2002, 43 Suppi 5, 86-95). Це може мати значення в запобіганні розвитку епілепсії у пацієнтів, тобто бути анти-епілептогенним чинником. Було також показано, що ретигабін затримує розвиток збудження гіпокампа у щурів, що є додатковою моделлю розвитку епілепсії (Tober et al., European Journal of Pharmacology 1996, 303, 163-169). Таким чином, передбачається, що вказані властивості ретигабіну і інших модуляторів KCNQ можуть запобігти нейрональним пошкодженням, що викликаються надмірною нейрональною активацією, і такі сполуки можуть бути використані для лікування нейродегенеративних захворювань, і можуть модифікувати захворювання (або бути антиепілептогенними) у пацієнтів, страждаючих епілепсією. Беручи до уваги, що протисудомні сполуки, такі як бензодіазепіни і хлорметіазол, використовують в клініках для лікування синдрому припинення вживання етанолу, і що інші протисудомні сполуки, наприклад, габапентин, виявляються надзвичайно ефективними при вказаному синдромі в моделях на тваринах (Watson et al., Newopharmacology 1997, 36,13691375), автори чекають, що інші протисудомні сполуки, такі як відкривачі KCNQ, будуть також ефективними при даному стані. мРНК субодиниць KCNQ 2 і 3 виявлені в ділянках мозку, пов'язаних з тривогою і емоційною поведінкою, такою як біполярний розлад, наприклад, в гіпокампі та мигдалині мозочка (Saganich et al… Journal ofNeuroscience 2001, 21, 4609-4624), і повідомляється, що ретигабін є активним в деяких моделях на тваринах зі схожою на тривогу поведінкою (Hartz et al… Journal ofPsychopharmacology 2003, 17 suppl. 3, А28, В16), та інші клінічно використовувані протисудомні сполуки використовуються для лікування біполярного розладу. Отже, відкривачі KCNQ можуть бути корисними для лікування тривожних розладів і біполярного розладу. WO 200196540 розкриває використання модуляторів М-струму, утвореного експресією генів KCNQ2 і KCNQ3 при інсомнії, тоді як у WO 2001092526 повідомляється, що модулятори KCNQ5 можуть бути використані для лікування розладів сну. WO 01/022953 розкриває використання ретигабіну для профілактики та лікування невропатичного болю, такого як алодинія, гіпералгічний біль, фантомний біль, невропатичний біль, пов'язаний з діабетичною невропатією, і невропатичний біль, пов'язаний з мігренню. WO 02/049628 розкриває використання ретигабіну для лікування тривожних розладів, таких як тривога, генералізований тривожний розлад, панічна тривога, обсесивно-компульсивний розлад, соціальна фобія, страх діяльності, посттравматичний стресовий розлад, гостра стресова реакція, розлад адаптації, іпохондричні розлади, страх розлуки, агорафобія та специфічні фобії. У заявці WO 97/15300 розкрито використання ретигабіну для лікування нейродегенеративних розладів, таких як хвороба Альцгеймера; хорея Гентінгтона; склерозів, таких як розсіяний склероз і бічний аміотрофічний склероз; хвороби Крейтцфельда-Якоба (кортико-стриоспінальної дегенерації); хвороби Паркінсона; 2 UA 102517 C2 5 10 15 20 25 індукованої СНІДом енцефалопатії та інших пов'язаних з інфекціями енцефалопатій, викликаних вірусами коревої краснухи (rubella вірусами), герпесвірусами, бореліями і невідомими патогенами, викликаних травмою нейродегенерацій; станів нейронального гіперзбудження, таких як ті, що виникають при синдромі медикаментозного скасування або при інтоксикації, та нейродегенеративних розладів периферичної нервової системи, таких як поліневропатії і поліневрити. Отже, існує величезна потреба в нових сполуках, які є ефективними відкривачами калієвих каналів сімейства KCNQ. Необхідні також нові сполуки з поліпшеними властивостями в порівнянні з властивостями відомих сполук, які є відкривачами калієвих каналів сімейства KCNQ, такі як ретигабін. Бажано поліпшення одного або більше з наступних параметрів: періоду напіввиведення, кліренсу, селективності, взаємодії з іншими лікарськими препаратами, біодоступності, ефективності, здатності змішуватися, хімічної стабільності, метаболічної стабільності, проникності через мембрани, розчинності та терапевтичного індексу. Поліпшення вказаних параметрів може призвести до таких поліпшень, як - поліпшений режим дозування за рахунок зниження числа необхідних доз на день, - простота введення пацієнтам при прийомі багатьох ліків, - зменшення побічних ефектів, - підвищення терапевтичного індексу, - поліпшення переносності або - поліпшення сприйняття. Суть винаходу Однією з цілей цього винаходу є забезпечення новими сполуками, які є ефективними відкривачами калієвих каналів сімейства KCNQ. Сполуками цього винаходу є заміщені похідні морфоліну і тіоморфоліну загальної формули І або їх солі R2 R7 30 35 40 45 50 R6 X (Z)q R3 R1 N W H N R4 R5 , (I) де q, W, X, Z, R1, R2, R3, R4, R5, R6 і R7 є такими, як визначено нижче. У цьому винаході запропоновано сполуки формули І для застосування як лікарський засіб. Зокрема сполуки формули І запропоновані для лікування біполярного розладу. Цей винахід далі стосується фармацевтичної композиції, яка містить сполуку формули І, а також до її застосування. У цьому винаході запропонована фармацевтична композиція, що містить сполуку формули І і фармацевтично прийнятний носій або розріджувач. Цей винахід далі належить до застосування сполуки формули І для виробництва фармацевтичної композиції для лікування розладу або захворювання, сприйнятливого до посиленого потоку іонів в калієвих каналах, що переважно є розладом або захворюванням центральної нервової системи, зокрема згаданий розлад або захворювання є біполярним розладом. У цьому винаході запропоновано застосування сполуки формули І для отримання лікарського засобу для лікування судомних нападів, тривожних розладів, невропатичного болю і мігреневого болю або нейродегенеративних розладів. Цей винахід, крім того, належить до застосування сполуки формули І в способі лікування судомних нападів, тривожних розладів, невропатичного болю і мігреневого болю або нейродегенеративних розладів. Докладний опис цього винаходу Цей винахід належить до заміщених похідних морфоліну і тіоморфоліну, які є ефективними відкривачами калієвих каналів KCNQ. Відповідно, цей винахід належить до заміщених похідних морфоліну і тіоморфоліну загальної формули І 3 UA 102517 C2 R2 R7 5 10 15 20 25 30 35 40 45 50 R6 X (Z)q R3 R1 N W H N R4 R5 , (I) де q дорівнює 0 або 1; W являє собою О або S; Х являє собою CO; Z являє собою О; R1 вибраний з групи, що складається з галогену, ціано, С 1-6-алк(ен/ін)ілу, С3-8циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, галоген-С1-6-алк(ен/ін)ілу, галоген-С3-8циклоалк(ен)ілу, галоген-С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, С1-6-алк(ен/ін)ілокси, С3-8циклоалк(ен)ілокси і С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілокси; R2 вибраний з групи, що складається з галогену, ціано, С 1-6-алк(ен/ін)ілу, С3-8циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, галоген-С1-6-алк(ен/ін)ілу, галоген-С3-8циклоалк(ен)ілу, галоген-С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, С1-6-алк(ен/ін)ілокси, С3-8циклоалк(ен)ілокси, С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілокси, необов'язково заміщеного фенілу і необов'язково заміщеного піридилу; де феніл і піридил необов'язково заміщені одним або більше замісниками, які незалежно являють собою галоген, С 1-6-алк(ен/ін)іл, С3-8-циклоалк(ен)іл або С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)іл; R3 вибраний з групи, що складається з С1-10-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, С3-8циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, Аr-С1-6-алк(ен/ін)ілу, Аr-С3-8-wиклоалк(ен)ілу, Аr-С3-8циклоалк(ен)іл-С1-6-алк(ен/ін)ілу і Аr; і кожний з R4, R5, R6 і R7 незалежно вибраний з групи, що складається з водню і Аr; у вигляді вільної основи або їх солей. У одному з варіантів здійснення сполуки формули І, q дорівнює 0; у іншому варіанті здійснення сполуки формули І q дорівнює 1. У наступному варіанті здійснення сполуки формули І, W являє собою атом кисню; у іншому варіанті здійснення, W являє собою атом сірки. У наступному варіанті здійснення сполуки формули І, R1 вибраний з групи, що складається з С3-8-циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, галоген-С3-8-циклоалк(ен)ілу, галогенС3-8-пиклоалк(ен)іл-С1-6-алк(ен/ін)Ілу, С3-8-пиклоалк(ен)ілокси і С3-8-циклоалк(ен)іл-С1-6алк(ен/ін)ілокси; у іншому варіанті здійснення, R1 вибраний з групи, що складається з галогену, галоген-С1-6алк(ен/ін)ілу, С1-6-алк(ен/ін)ілу і ціано. Звичайно R1 вибраний з групи, що складається з галогену, ціано, С 1-6-алк(ен/ін)ілу, галогенС1-6-алк(ен/ін)ілу і С1-6-алк(ен/ін)ілокси. Для подальшої ілюстрації винаходу, але без його обмеження, одним з варіантів здійснення R1 є галоген; інший варіант здійснення R1 являє собою ціано; інший варіант здійснення R1 являє собою С 1-6-алк(ен/ін)іл; інший варіант здійснення R1 являє собою галоген-С1-6-алк(ен/ін)іл; інший варіант здійснення R1 являє собою С 1-6-алк(ен/ін)ілокси. У наступному варіанті здійснення сполуки формули І, R2 вибраний з групи, що складається з С3-8-циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, галоген-С3-8-циклоалк(ен)ілу, галогенС3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілокси і С3-8-циклоалк(ен)іл-С1-6алк(ен/ін)ілокси; у іншому варіанті здійснення, R2 вибраний з групи, що складається з галогену, галоген-С1-6алк(ен/ін)ілу, С1-6-алк(ен/ін)ілу і ціано. Звичайно R2 вибраний з групи, що складається з галогену, ціано, С 1-6-алк(ен/ін)ілу, галоген-С1-6-алк(ен/ін)ілу, С1-6-алк(ен/ін)ілокси, необов'язково заміщеного фенілу і необов'язково заміщеного піридилу. Для подальшої ілюстрації, але без обмежень цього винаходу, один з варіантів здійснення R2 являє собою галоген; інший варіант здійснення R2 являє собою ціано; інший варіант здійснення R2 являє собою С 1-6-алк(ен/ін)іл; інший варіант здійснення R2 являє собою галоген-С1-6-алк(ен/ін)іл; 4 UA 102517 C2 5 10 15 20 25 30 35 40 45 50 55 60 інший варіант здійснення R2 являє собою С 1-6-алк(ен/ін)ілокси; інший варіант здійснення R2 являє собою необов'язково заміщений феніл; інший варіант здійснення R2 являє собою необов'язково заміщений піридил. У наступному варіанті здійснення R2, необов'язково заміщений феніл і необов'язково заміщений піридил можуть бути заміщені одним або більше замісниками, які незалежно вибрані з групи, що складається з галогену або С1-6-алк(ен/ін)ілу; у іншому варіанті здійснення R2, феніл і піридил не заміщені; у ще одному варіанті здійснення R2, необов'язково заміщений феніл і необов'язково заміщений піридил заміщені одним замісником; у ще одному варіанті здійснення R2, необов'язково заміщений феніл і необов'язково заміщений піридил заміщені двома замісниками; у ще одному варіанті здійснення R2, необов'язково заміщений феніл і необов'язково заміщений піридил заміщені трьома замісниками. У наступному варіанті здійснення сполуки формули І, R3 вибраний з групи, що складається з С3-8-циклоалк(ен)ілу, Аr-С3-8-циклоалк(ен)ілу і Аr-С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілу. Звичайно R3 вибраний з групи, що складається з С 1-10-алк(ен/ін)ілу, С3-8-циклоалк(ен)іл-С1-6алк(ен/ін)ілу, Аr-С1-6-алк(ен/ін)ілу і Аr. Для подальшої ілюстрації, але без обмеження цього винаходу, одним з варіантів здійснення R3 є С1-10-алк(ен/ін)іл; інший варіант здійснення R3 являє собою С 3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)іл; інший варіант здійснення R3 являє собою Аr-С1-6-алк(ен/ін)іл; інший варіант здійснення R3 являє собою Аr. У наступному варіанті здійснення сполуки формули І, Аr вибраний з групи, що складається з необов'язково заміщеного фурану, необов'язково заміщеного тіазолу, необов'язково заміщеного хіноліну, необов'язково заміщеного індолу, необов'язково заміщеного піримідину, необов'язково заміщеного піролу і необов'язково заміщеного оксазолу; у іншому варіанті здійснення Аr вибраний з групи, що складається з необов'язково заміщеного фенілу, необов'язково заміщеного тіофену і необов'язково заміщеного нафтилу; у іншому варіанті здійснення Аr вибраний з групи, що складається з необов'язково заміщеного фенілу, необов'язково заміщеного тіофену, необов'язково заміщеного нафтилу і необов'язково заміщеного 2,3-дигідробензофурану; у іншому варіанті здійснення Аr вибраний з групи, що складається з необов'язково заміщеного фенілу і необов'язково заміщеного піридину. У одному з варіантів здійснення цього винаходу Аr являє собою необов'язково заміщений феніл, необов'язково заміщений нафтил, необов'язково заміщений тіофен або необов'язково заміщений 2,3-дигідробензофуран. Звичайно Аr вибраний з групи, що складається з необов'язково заміщеного фенілу, необов'язково заміщеного нафтилу, необов'язково заміщеного піридину, необов'язково заміщеного 2,3-дигідробензофурану і необов'язково заміщеного тіофену. Для подальшої ілюстрації, але без обмеження цього винаходу, одним з варіантів здійснення Аr є необов'язково заміщений феніл; інший варіант здійснення Аr являє собою необов'язково заміщений нафтил; інший варіант здійснення Аr являє собою необов'язково заміщений піридин; інший варіант здійснення Аr являє собою необов'язково заміщений 2,3-дигідробензофуран; інший варіант здійснення Аr являє собою необов'язково заміщений тіофен. У наступному варіанті здійснення сполуки формули І, Аr належить до необов'язково заміщених ароматичних систем, що складаються з 5-10 атомів вуглецю. Звичайно такі необов'язково заміщені ароматичні системи, що складаються з 5-10 атомів вуглецю, вибрані з необов'язково заміщеного фенілу і необов'язково заміщеного нафтилу. У наступному варіанті здійснення сполуки формули І, Аr належить до необов'язково заміщених ароматичних систем, що складаються з 5-10 атомів вуглецю, де 1, 2, 3 або 4 атоми вуглецю замінені гетероатомами, незалежно вибраними з N, S або О. У наступному варіанті здійснення сполуки формули І, така необов'язково заміщена ароматична система, що складається з 5-10 атомів вуглецю, де 1, 2, 3 або 4 атоми вуглецю замінені гетероатомами, вибрана з групи, що складається з необов'язково заміщеного піридину, необов'язково заміщеного тіофену, необов'язково заміщеного фурану, необов'язково заміщеного тіазолу, необов'язково заміщеного хіноліну, необов'язково заміщеного індолу, необов'язково заміщеного 2,3-дигідробензофурану, необов'язково заміщеного піримідину, необов'язково заміщеного піролу і необов'язково заміщеного оксазолу. Звичайно така необов'язково заміщена ароматична система, що складається з 5-10 атомів вуглецю, де 1, 2, 3 або 4 атоми вуглецю замінені 5 UA 102517 C2 5 10 15 20 25 30 35 40 45 50 55 60 гетероатомами, вибрана з групи, що складається з необов'язково заміщеного піридину, необов'язково заміщеного 2,3-дигідробензофурану і необов'язково заміщеного тіофену. У наступному варіанті здійснення сполуки формули І, Аr необов'язково заміщений одним або більше замісниками, незалежно вибраними з гідрокси, ацилу, нітро або ціано, -СО-НН-С1-6алк(ен/ін)ілу, -СО-Н(С1-6-алк(ен/ін)іл)2, -NH2, -NН-С1-6-алк(ен/ін)ілу, -N(C1-6-алк(ен/ін)іл)2, -S-С1-6алк(ен/ін)ілу, -SO2-С1-6-алк(ен/ін)ілу, -SO2Н(С1-6-алк(ен/ін)іл)2 та -SO2NH-C1-6-алк(eн/iн)iлу, або два суміжні замісники можуть разом з ароматичною групою, до якої вони приєднані, утворювати 4-8-членне кільце, яке необов'язково містить один, два або три гетероатоми; у іншому варіанті здійснення Аr необов'язково заміщений одним або більше замісниками, незалежно вибраними з галогену, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, С3-8-циклоалк(ен)іл-С16-алк(ен/ін)ілу, галоген-С1-6-алк(ен/ін)ілу, С1-6-алк(ен/ін)ілокси або С3-8-алк(ен/ін)ілокси; у іншому варіанті здійснення Аr необов'язково заміщений одним або більше замісниками, незалежно вибраними з галогену або галоген-С1-6-алк(ен/ін)ілу. У наступному варіанті здійснення цього винаходу. Аr заміщений одним або більше замісниками, незалежно вибраними з галогену, С1-6-алк(ен/ін)ілу, галоген-С1-6-алк(ен/ін)ілу, С1-6алк(ен/ін)ілокси. Для подальшої ілюстрації, але без обмеження цього винаходу, можна вказати, що у одному з варіантів здійснення Аr заміщений галогеном; у іншому варіанті здійснення Аr заміщений С1-6-алк(ен/ін)ілом; у іншому варіанті здійснення Аr заміщений галоген-С1-6-алк(ен/ін)ілом; у іншому варіанті здійснення Аr заміщений С1-6-алк(ен/ін)ілокси; у іншому варіанті здійснення Аr є незаміщеним; у іншому варіанті здійснення Аr заміщений 1 замісником; у іншому варіанті здійснення Аr заміщений 2 замісниками; у іншому варіанті здійснення Аr заміщений 3 замісниками. Один з варіантів здійснення належить до сполук загальної формули І, де принаймні один з R4 і R5 не являє собою Аr. Інший варіант здійснення належить до сполук загальної формули І, де принаймні один з R6 і R7 не являє собою Аr. Ще один варіант здійснення належить до сполук загальної формули І, де принаймні три з R4, R5, R6 і R7 не являють собою Аr. Ще один варіант здійснення належить до сполук загальної формули І, де не більше ніж один з R3, R4, R5, R6 і R7 включає Аr; ще один варіант здійснення належить до сполук загальної формули І, де не більше ніж два з R3, R4, R5, R6 і R7 включають Аr; ще один варіант здійснення належить до сполук загальної формули І, де не більше ніж три з R3, R4, R5, R6 і R7 включають Аr; ще один варіант здійснення належить до сполук загальної формули І, де R3 не включає Аr; ще один варіант здійснення належить до сполук загальної формули І, де R4 не включає Аr; ще один варіант здійснення належить до сполук загальної формули І, де R5 не включає Аr; ще один варіант здійснення належить до сполук загальної формули І, де R6 не включає Аr; ще один варіант здійснення належить до сполук загальної формули І, де R7 не включає Аr. Один з варіантів здійснення належить до сполук загальної формули І, де стереоконфігурація стосовно атома вуглецю, до якого приєднані R4 і R5, є S-конфігурацією. Інший варіант здійснення належить до сполук загальної формули І, де стереоконфігурація стосовно атома вуглецю, до якого приєднані R4 і R5, є R-конфігурацією. Ще один варіант здійснення належить до сполук загальної формули І, де стереоконфігурація стосовно атома вуглецю, до якого приєднані R6 і R7, є S-конфігурацією. Ще один варіант здійснення належить до сполук загальної формули І, де стереоконфігурація стосовно атома вуглецю, до якого приєднані R6 і R7, є R-конфігурацією. Ще один варіант здійснення належить до сполук загальної формули І, де стереоконфігурація стосовно атома вуглецю, до якого приєднані R4 і R5, ідентична стереоконфігурації стосовно атома вуглецю, до якого приєднані R6 і R7. Ще один варіант здійснення належить до сполук загальної формули І, де стереоконфігурація стосовно атома вуглецю, до якого приєднані R4 і R5, відрізняється від стереоконфігурації стосовно атома вуглецю, до якого приєднані R6 і R7. Сполуки, представлені в наступному переліку, та їх солі ілюструють цей винахід, причому цей перелік жодним чином не слід розглядати як обмежувальний: N-(2-бром-4-морфолін-4-іл-6-трифторметилфеніл)-2-(4-фторфеніл)ацетамід; 2-циклопентил-N-(2-бром-6-трифторметил-4-морфолін-4-ілфеніл)ацетамід; 6 UA 102517 C2 5 10 15 20 25 30 35 40 45 50 55 60 N-(2-бром-4-морфолін-4-іл-6-трифторметилфеніл)-3-циклопентилпропіонамід; N-(2-xлop-6-цiaнo-4-мopфoлін-4-iлфeнiл)-3-циклoгeкcилпропioнaмiд; 2-циклопентил-N-(2,6-диметил-4-тіоморфолін-4-ілфеніл)ацетамід; 2-циклопентил-N-[2,6-диметил-4-(2-фенілморфолін-4-іл)феніл]ацетамід; 2-циклопентил-N-[2,6-диметил-4-(2-фенілтіоморфолін-4-іл)феніл]ацетамід; 2-циклопентил-N-[2,6-диметил-4-(3-тридин-3-ілтіоморфолін-4-іл)феніл]ацетамід; 2-циклопенттил-N-[2,6-диметил-4-[2-(4-трифторметилфеніл)тіоморфолін-4іл]феніл}ацетамід; N-{4-[2-(2-xлopфeнiл)тioмopфoлін-4-iл]-2,6-димeтилфeнiл}-2-циклoпeнтилaцeтaмiд; 2-біцикло[2.2.1]гепт-2-ил-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід; 2-циклогексил-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід; 3-(3,4-дифторфеніл)-N-(2,6-диметил-4-морфолін-4-ілфеніл)пропіонамід; 2-циклопентил-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід; бутиловий естер (2,6-диметил-4-морфолін-4-ілфеніл)карбамінової кислоти; 2-(4-хлорфеніл)-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід; (2,6-диметил-4-морфолін-4-ілфеніл)амід 2,3-дигідробензофуран-2-карбонової кислоти; 3-циклогексил-N-(2,6-диметил-4-морфолін-4-ілфеніл)пропіонамід; 3-циклопентил-N-(2,6-диметил-4-морфолін-4-ілфеніл)пропіонамід; N-(2,6-диметил-4-мopфoлін-4-iлфeнiл)-2-(4-фтopфeнiл)aцeтaмiд; N-(2,6-диметил-4-морфолін-4-ілфеніл)-2-тіофен-2-ілацетамід; N-(2,6-диметил-4-морфолін-4-ілфеніл)-3,3-диметилбутирамід; (2,б-диметил-4-морфолін-4-ілфеніл)амід гексанової кислоти; 2-циклогептил-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід; бензиловий естер (2,6-диметил-4-морфолін-4-ілфеніл)карбамінової кислоти; 2-хлорбензиловий естер (2,6-диметил-4-морфолін-4-ілфеніл)карбамінової кислоти; (2,6-диметил-4-морфолін-4-ілфеніл)амід 3,5,5-триметилгексанової кислоти; (2,6-диметил-4-морфолін-4-ілфеніл)амід октанової кислоти; (2,6-диметил-4-морфолін-4-ілфеніл)амід гептанової кислоти; N-(2,6-диметил-4-морфолін-4-ілфеніл)-2-фенілацетамід; 2-(3,4-дихлорфеніл)-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід; 2-(4-алілокси-3-хлорфеніл)-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід; N-(2,6-диметил-4-морфолін-4-ілфеніл)-2-(3-трифторметилфеніл)ацетамід; N-(2,6-диметил-4-морфолін-4-ілфеніл)-2-нафтален-2-ілацетамід; 3-(3-хлорфеніл)-N-(2,6-диметил-4-морфолін-4-ілфеніл)пропіонамід; N-(2,6-диметил-4-морфолін-4-ілфеніл)-2-(3,4-диметилфеніл)ацетамід; 2-(3-бромфеніл)-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід; 2-(3-хлорфеніл)-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід; N-(2,6-диметил-4-морфолін-4-ілфеніл)-2-n-толілацетамід; N-(2,6-диметил-4-морфолін-4-ілфеніл)-2-м-толілацетамід; 2-(3,4-дифторфеніл)-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід; N-(2,6-диметил-4-морфолін-4-ілфеніл)-2-(3-фторфеніл)ацетамід; N-(2-бром-4-морфолін-4-іл-6-трифторметилфеніл)-3-циклогексилпропіонамід; N-(2-бром-4-морфолм-4-іл-6-трифторметилфеніл)-2-(3-фторфеніл)ацетамід; N-(2-бром-4-морфолін-4-іл-6-трифторметилфеніл)пропіонамід; N-(2-бром-4-морфолін-4-іл-6-трифторметилфеніл)бутирамід; N-(2-хлор-4-морфолін-4-іл-6-трифторметилфеніл)-2-(3-фторфеніл)ацетамід; N-(2-хлор-4-морфолін-4-іл-6-трифторметилфеніл)-2-циклопентилацетамід; 2-циклопентил-N-{2,6-диметил-4-[2-(4-трифторметилфеніл)морфолін-4-іл]феніл}ацетамід; N-{4-[2-(2-хлорфеніл)морфолм-4-іл]-2,6-диметилфеніл}-2-циклопентилацетамід; 2-циклопентил-N-{4-[2-(4-фторфеніл)морфолін-4-іл]-2,6-диметилфеніл}ацетамід; 2-(2-хлорфеніл)-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід; (2,6-диметил-4-морфолін-4-ілфеніл)амід пептонової кислоти; (2,6-диметил-4-морфолін-4-ілфеніл)амід 4-метилпентанової кислоти; 2-циклопент-2-еніл-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід; (2,6-диметил-4-морфолін-4-ілфеніл)амід 5-метилгексанової кислоти; (2,6-диметил-4-морфолін-4-ілфеніл)амід 3-метилпентанової кислоти; (2,6-диметил-4-морфолін-4-ілфеніл)амід гекс-5-енової кислоти; (2,6-диметил-4-морфолін-4-ілфеніл)амід 3-етилпентанової кислоти; 2-циклопентил-N-(4-морфолін-4-іл-2-піридин-3-іл-6-трифторметилфеніл)ацетамід; 2-циклопентил-N-(5-морфолін-4-іл-3-трифторметилбіфеніл-2-іл)ацетамід; 7 UA 102517 C2 5 10 15 20 25 30 35 40 45 50 55 60 2-циклопентил-N-(4'-фтор-5-морфолін-4-іл-3-трифторметилбіфеніл-2-іл)ацетамід; 2-циклопентил-N-(4'-метил-5-морфолін-4-іл-3-трифторметилбіфеніл-2-іл)ацетамід; 2-циклопентил-N-(3'-метил-5-морфолін-4-іл-3-трифторметилбіфеніл-2-іл)ацетамід; 2-циклопентил-N-(3',4'-дифтор-5-морфолін-4-іл-3-трифторметилбіфеніл-2-іл)ацетамід; 2-(4-фторфеніл)-N-(4-морфолін-4-іл-2-піридин-3-іл-6-трифторметилфеніл)ацетамід; 2-циклопентил-N-(2,6-діетил-4-морфолін-4-ілфетл)ацетамід; 2-циклопентил-N-(2,6-дизопропіл-4-морфолін-4-ілфеніл)ацетамід; 2-циклопентил-N-(2,6-дифтор-4-морфолін-4-ілфеніл)ацетамід; 2,6-дифтор-4-морфолін-4-ілфеніл)амід гексанової кислоти; N-(2,6-дифтор-4-морфолін-4-ілфеніл)-3,3-диметилбутирамід; N-(2,6-дифтор-4-морфолін-4-ілфеніл)-2-(3-фторфеніл)ацетамід; 2-циклопент-2-еніл-N-(2,6-дифтор-4-морфолін-4-ілфеніл)ацетамід; 2-біцикло[2.2.1]гепт-2-ил-N-(2,6-дифтор-4-морфолін-4-ілфеніл)ацетамід; 2-біцикло[2.2.1]гепт-2-ил-N-(2-метил-4-морфолін-4-іл-6-трифторметилфеніл)ацетамід; (2-метил-4-морфолін-4-іл-6-трифторметилфеніл)амід 5-метилпентанової кислоти; (2-метил-4-морфолін-4-іл-6-трифторметилфеніл)амід 5-метилгексанової кислоти; 2-циклопент-2-еніл-N-(2-метил-4-морфолін-4-іл-6-трифторметилфеніл)ацетамід; 2-циклопентил-N-(2-метил-4-морфолін-4-іл-6-трифторметилфеніл)ацетамід; (2-метил-4-морфолін-4-іл-6-трифторметилфеніл)амід гексанової кислоти; 3,3-диметил-N-(2-метил-4-морфолін-4-іл-6-трифторметилфеніл)бутирамід; 2-(3,4-дифторфеніл)-N-(2-метил-4-морфолін-4-іл-6-трифторметилфеніл)ацетамід; (2-метокси-6-метил-4-морфолін-4-ілфеніл)амід гексанової кислоти; 2-циклопентил-N-(2-метокси-6-метил-4-морфолін-4-ілфеніл)ацетамід; N-(2-метокси-6-метил-4-морфолін-4-ілфеніл)-3,3-диметилбутирамід; 2-(3,4-дифторфеніл)-N-(2-метокси-6-метил-4-морфолін-4-ілфеніл)ацетамід; 2-циклопент-2-еніл-N-(2-метокси-6-метил-4-морфолін-4-ілфеніл)ацетамід; 2-(3-фторфеніл)-N-(2-метокси-6-метил-4-морфолін-4-ілфеніл)ацетамід; 2-біцикло[2.2.1]гепт-2-ил-N-(2-метокси-6-метил-4-морфолін-4-ілфеніл)ацетамід; (2-метокси-6-метил-4-морфолін-4-ілфеніл)амід 4-метилпентанової кислоти; (2-метокси-6-метил-4-морфолін-4-ілфеніл)амід 5-метилгексанової кислоти; N-(2-хлор-6-метил-4-морфолін-4-ілфеніл)-2-(3-фторфеніл)ацетамід; і N-(2-хлор-6-метил-4-морфолін-4-ілфеніл)-2-циклопентилацетамід; у вигляді вільної основи або їх солей. Переважними є наступні сполуки: 2-циклопентил-N-(2-бром-6-трифторметил-4-морфолін-4-ілфеніл)ацетамід; N-(2-бром-4-морфолін-4-іл-6-трифторметилфеніл)-3-циклопентилпропіонамід; N-(2-хлор-6-ціано-4-морфолін-4-ілфеніл)-3-циклогексилпропіонамід; 2-циклопентил-N-(2,6-диметил-4-тіоморфолін-4-ілфеніл)ацетамід; 2-циклопентил-N-[2,6-диметил-4-(2-фенілморфолін-4-іл)феніл]ацетамід; 2-циклопентил-N-[2,6-диметил-4-(2-фенілтіоморфолін-4-іл)феніл]ацетамід; 2-циклопентил-N-[2,6-диметил-4-(3-тридин-3-іл-тіоморфолін-4-іл)феніл]ацетамід; 2-циклопентил-N-[2,6-диметил-4-[2-(4-трифторметилфеніл)тіоморфолін-4-іл]феніл}ацетамід; N-{4-[2-(2-хлорфеніл)тіоморфолін-4-іл]-2,6-диметилфеніл}-2-циклопентилацетамід; 2-біцикло[2.2.1]гепт-2-ил-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід; 2-циклогексил-N-(2,6-диметил-4-морфолін-4-ілфеніл}ацетамід; 2-циклопентил-N-(2,6-диметил~4-морфолін-4-ілфеніл)ацетамід; 3-циклогексил-N-(2,6-диметил-4-морфолін-4-ілфеніл)пропіонамід; 3-циклопентил-N-(2,6-диметил-4-морфолін-4-ілфеніл)пропіонамід; 2-циклогексил-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід; N-(2-бром-4-морфолін-4-іл-6-трифторметилфеніл)-3-циклогексилпропіонамід; N-(2-хлор-4-морфолін-4-іл-6-трифторметилфеніл)-2-циклопентилацетамід; 2-циклопентил-N-{2,6-диметил-4-[2-(4-трифторметіілфеніл)морфолін-4-іл]феніл}ацетамід; N-{4-[2-(2-хлорфетл)морфолін-4-іл]-2,6-диметилфеніл}-2-циклопентилацетамід; 2-циклопентил-N-{4-[2-(4-фторфеніл)морфолін-4-іл]-2,6-диметшфеніл}ацетамід; 2-циклопент-2-еніл-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетаміду; 2-циклопентил-N-(4-морфолін-4-іл-2-піридин-3-іл-6-трифторметилфеніл)ацетаміду; 2-циклопентил-N-(5-морфолін-4-іл-3-трифторметилбіфеніл-2-іл)ацетаміду; 2-циклопентил-N-(4'-фтор-5-морфолін-4-іл-3-трифторметилбіфеніл-2-іл)ацетамід; 2-циклопентил-N-(4'-метил-5-морфолін-4-іл-3-трифторметилбіфеніл-2-іл)ацетамід; 2-циклопентш-N-(3'-метил-5-морфолін-4-іл-3-трифторметилбіфеніл-2-іл)ацетамід; 8 UA 102517 C2 5 10 15 20 25 30 35 40 45 50 55 2-циклопентил-N-(3', 4'-дифтор-5-морфолін-4-іл-3-трифторметилбіфеніл-2-іл)ацетамід; 2-циклопентил-N-(2,6-діетил-4-морфолін-4-ілфеніл)ацетамід; 2-циклопенил-N-(2,6-діізопроіл-4-морфолін-4-ілфеніл)ацетамід; 2-циклопентил-N-(2,6-дифтор-4-морфолін-4-ілфеніл)ацетамід; 2-циклопент-2-еніл-N-(2,6-дифтор-4-морфолін-4-ілфеніл)ацетамід; 2-біцикло[2.2.1]гепт-2-ил-N-(2,6-дифтор-4-морфолін-4-ілфеніл)ацетамід; 2-біцикло[2.2.1]гепт-2-ил-N-(2-метил-4-морфолін-4-іл-6-трифторметилфеніл)-ацетамід; 2-циклопент-2-еніл-N-(2-метил-4-морфолін-4-іл-6-трифторметилфеніл)ацетамід; 2-циклопентил-N-(2-метил-4-морфолін-4-іл-6-трифторметилфеніл)ацетамід; 2-циклопентил-N-(2-метокси-6-метил-4-морфолін-4-ілфеніл)ацетамід; 2-циклопент-2-еніл-N-(2-метокси-6-метил-4-морфолін-4-ілфеніл)ацетамід; 2-біцикло[2.2.1]гепт-2-ил-N-(2-метокси-6-метил-4-морфолін-4-ілфениі)ацетамід і N-(2-хлор-6-метил-4-морфолін-4-ілфеніл)-2-циклопентилацетамід у вигляді вільної основи або їх солей. Кожна з вищевказаних сполук розглядається як конкретний варіант здійснення, і може бути змістом окремих пунктів формули винаходу. Цей винахід включає також солі сполук цього винаходу, звичайно фармацевтично прийнятні солі. Солі цього винаходу включають кислотно-адитивні солі, солі металів, солі амонію і солі алкілованого амонію. Солі цього винаходу є переважно кислотно-адитивними солями. Кислотно-адитивні солі цього винаходу переважно є фармацевтично прийнятними солями сполук цього винаходу, утвореними з нетоксичними кислотами. Кислотно-адитивні солі включають солі як неорганічних, так і органічних кислот. Приклади відповідних неорганічних кислот включають хлористоводневу, бромистоводневу, йодистоводневу, фосфорну, сірчану, сульфамінову, азотну кислоти і тому подібні. Приклади відповідних органічних кислот включають мурашину, оцтову, трихлороцтову, трифтороцтову, пропіонову, бензойну, коричну, лимонну, фумарову, гліколеву, ітаконову, молочну, метансульфонову, малеїнову, яблучну, малонову, мигдалеву, щавлеву, пікринову, піровиноградну, саліцилову, бурштинову, метансульфонову, етансульфонову, винну, аскорбінову, памову, бісметиленсаліцилову, етандисульфонову, глюконову, цитраконову, аспарагінову, стеаринову, пальмітинову, EDTA, гліколеву, п-амінобензойну, глутамінову, бензолсульфонову, п-толуолсульфонову кислоти, теофілін-оцтові кислоти, а також 8галогентеофіліни, наприклад, 8-бромтеофілін і тому подібні. Додаткові приклади фармацевтично прийнятних неорганічних або органічних кислотно-адитивних солей включають фармацевтично прийнятні солі, перелічені в J. Pharm. Sci. 1977, 66, 2, яку включено в даний опис шляхом посилання. Гідрати, які здатні утворювати сполуки цього винаходу, також розглядаються як кислотноадитивні солі. Приклади солей металів включають солі літію, натрію, калію, магнію і тому подібні. Приклади солей амонію і солей алкілованого амонію включають солі амонію, метил-, диметил-, триметил-, етил-, гідроксіетил-, діетил-, н-бутил-, втор-бутил-, трет-бутил-, тетраметиламонію і тому подібні. Далі, сполуки цього винаходу можуть існувати в несольватованій формі або у формі сольватів з фармацевтично прийнятними розчинниками, такими як вода, етанол і тому подібні. Зазвичай для цілей цього винаходу сольватовані форми розглядають як еквіваленти несольватованих форм. Сполуки цього винаходу можуть мати один або декілька асиметричних центрів і передбачається, що будь-які оптичні ізомери (тобто енантіомери або діастереомери), як виділені, чисті або частково очищені оптичні ізомери і будь-які їх суміші, включаючи рацемічні суміші, тобто суміші стереоізомерів, включені в обсяг цього винаходу. Рацемічні форми можна розділити на оптичні антиподи за відомими способами, наприклад, використовуючи розділення їх діастереомерних солей за допомогою оптично активних кислот і виділяючи оптично активні амінні сполуки шляхом обробки основою. Інший спосіб розділення рацематів на оптичні антиподи заснований на використанні хроматографії на оптично активних матрицях. Рацемічні сполуки цього винаходу можна також розділити на їх оптичні антиподи, наприклад, фракційною кристалізацією. Сполуки цього винаходу можна також розділити, використовуючи утворення діастереомерних похідних. Можна використовувати додаткові способи розділення оптичних ізомерів, відомі фахівцям в даній галузі. Такі способи включають ті, що описані у J. Jaques, A. Collet and S. Wilen в "Enantiomers, Racemates, and Resolutions", John Wiley і Sons, New York (1981). Оптично активні сполуки можна також отримати з оптично активних початкових матеріалів або використовуючи стереоселективний синтез. 9 UA 102517 C2 5 10 15 20 25 30 35 40 45 50 55 60 Крім того, коли в молекулі присутній подвійний зв'язок або повністю або частково насичена кільцева система, можуть бути утворені геометричні ізомери. Передбачається, що будь-які геометричні ізомери у вигляді розділених, чистих або частково очищених геометричних ізомерів або їх сумішей включені в обсяг винаходу. Аналогічно, молекули, що мають зв'язок з обмеженим обертанням, можуть утворювати геометричні ізомери. Вони також призначені до включення в обсяг цього винаходу. Крім того, деякі сполуки за цим винаходом можуть знаходитися в різних таутомерних формах, і мається на увазі, що будь-які таутомерні форми, які здатні утворити сполуки, включені в обсяг цього винаходу. Цей винахід також охоплює проліки цих сполук, які після введення зазнають хімічного перетворення в процесах метаболізму до того, як стануть фармакологічно активними речовинами. В основному, такими проліками можуть бути функціональні похідні сполук загальної формули І, які легко перетворюються in vivo в потрібні сполуки формули І. Звичайні способи відбору і отримання відповідних похідних проліків розкриті, наприклад, в "Design ofProdrugs", ed. H, Bundgaard, Elsevier, 1985. Цей винахід також охоплює активні метаболіти сполук цього винаходу. У одному з аспектів цього винаходу запропоновано сполуку формули І або її сіль для застосування як лікарський засіб. У одному з варіантів здійснення цей винахід належить до застосування однієї або більше сполук цього винаходу в способі лікування. Розлад або захворювання, яке слід лікувати, є сприйнятливим до посиленого потоку іонів в калієвих каналах, таких як канали калієвих іонів сімейства KCNQ. Такий розлад або захворювання є переважно розладом або захворюванням центральної нервової системи. У ще одному варіанті здійснення цього винаходу запропоновані фармацевтична композиція, яка містить один або більше фармацевтично прийнятних носіїв або розріджувачів і одну або більше сполук формули І або їх солей. Наступний варіант цього винаходу належить до застосування сполуки формули І або її солі для отримання фармацевтичної композиції для лікування захворювання або розладу, при якому корисні відкривачі калієвих каналів KCNQ, такі як відкривач калієвих каналів KCNQ2. Звичайний такий розлад або захворювання вибрані з групи, що складається з судомних нападів, тривожних розладів, невропатичного болю і мігреневого болю або нейродегенеративних розладів. У одному з варіантів здійснення сполуки цього винаходу можна вводити як тільки одну терапевтично ефективну сполуку. У іншому варіанті здійснення сполуки цього винаходу можна вводити як частину комбінованої терапії, тобто сполуки цього винаходу можна вводити в комбінації з іншими терапевтично ефективними сполуками, що мають, наприклад, антиконвульсивні властивості. Ефекти таких інших сполук, що мають антиконвульсивні властивості, можуть включати, але не обмежуватися цим, активність у відношенні: - іонних каналів, таких як натрієвий, калієвий або кальцієвий канали; - збудливих амінокислотних систем, наприклад, блокади або модуляції NMDA-рецепторів; - інгібіторних систем нейромедіаторів, наприклад, при посиленні вивільнення ГАМК або блокаді поглинання ГАМК або - ефектів стабілізації мембрани. Антиконвульсивні препарати, що існують в даний час, включають, але не обмежуються тільки ними, тіагабін, карбамазепін, вальпроат натрію, ламотригін, габапентин, прегабалін, етосуксимід, леветирацетам, фенітоїн, топірамат, зонісамід, а також члени класів бензодіазепінів і барбітуратів. Вважають, що сполуки цього винаходу можна використовувати для посилення потоку іонів в потенціалозалежних калієвих каналах у ссавців, таких як людина. Тому вважають, що сполуки цього винаходу можна використовувати для лікування розладів або захворювань, сприйнятливих до посиленого потоку іонів в потенціалозалежних калієвих каналах, таких як канали калієвих іонів сімейства KCNQ. Такий розлад або захворювання є переважно розладом або захворюванням центральної нервової системи. У одному з варіантів здійснення розлад або захворювання вибрані з групи, що складається з судомних нападів; таких як гострі судомні напади, конвульсії, епілептичний статус і епілепсії, таких як епілептичні синдроми і епілептичні напади; зокрема судоми, епілепсія і епілептичний статус. У іншому варіанті здійснення розлад або захворювання вибрані з групи, що складається з невропатичного болю і мігреневого болю; такого як алодинія, гіпералгічний біль, фантомний біль, невропатичний біль, пов'язаний з діабетичною невропатією, невропатичний біль, 10 UA 102517 C2 5 10 15 20 25 30 35 40 45 50 55 пов'язаний з тригемінальною невралгією, і невропатичний біль, пов'язаний з мігренню; зокрема, алодинії, гіпералгічного болю, фантомного болю, невропатичного болю, пов'язаного з діабетичною невропатією, і невропатичного болю, пов'язаного з мігренню. У ще одному варіанті здійснення розлад або захворювання вибрані з групи, що складається з тривожних розладів; таких як тривога та розлади і захворювання, пов'язані з панічною атакою, агорафобії, панічних розладів з агорафобією, панічних розладів без агорафобії, агорафобії без історії панічного розладу, специфічної фобії, соціальної фобії та інших специфічних фобій, обсесивно-компульсивного розладу, посттравматичного стресового розладу, гострих стресових розладів, генералізованого тривожного розладу, тривожного розладу, пов'язаного із загальним станом здоров'я, тривожного розладу, що викликається речовинами, тривожного розладу, пов'язаного з розлукою, розладів адаптації, страху діяльності, іпохондричних розладів, тривожного розладу, пов'язаного із загальним станом здоров'я, і тривожного розладу, що викликаються речовинами, і тривожних розладів, які конкретно не визначені; зокрема тривоги, генералізованого тривожного розладу, панічної атаки, обсесивно-компульсивного розладу, соціальних фобій, страху діяльності, посттравматичного стресового розладу, гострого стресового розладу, розладів адаптації, іпохондричних розладів, тривожного розладу, пов'язаного з розлукою, агорафобії, специфічних фобій, тривожного розладу, пов'язаного із загальним станом здоров'я, і тривожного розладу, що викликається речовинами. У ще одному варіанті здійснення розлад або захворювання вибрані з групи, що складається з нейродегенеративних розладів; таких як хвороба Альцгеймера, хорея Ґентінґтона; розсіяний склероз; бічний аміотрофічний склероз, хвороби Крейтцфельда-Якоба, хвороби Паркінсона, енцефалопатій, що індукуються СНІДом або інфікуванням вірусом коревої краснухи, герпесвірусом, бореліями і невідомими патогенами, викликаних травмою нейродегенерацій, станів нейронального гіперзбудження, таких як ті, що виникають при синдромі медикаментозного скасування або при інтоксикації, та нейродегенеративних захворювань периферичної нервової системи, таких як поліневропатії і поліневрити; зокрема хвороби Альцгеймера, хореї Ґентінґтона, розсіяного склерозу, бічного аміотрофічного склерозу, енцефалопатії, що індукуються СНІДом, або інших енцефалопатій, викликаних інфекцією вірусом коревої краснухи, герпесвірусом, бореліями і невідомими патогенами, хвороби Крейтцфельда-Якоба, хвороби Паркінсона, викликаних травмою нейродегенерацій. У ще одному варіанті здійснення розлад або захворювання вибрані з групи, що складається із станів нейронального гіперзбудження, таких як ті, що виникають при синдромі медикаментозного скасування або при інтоксикації. У ще одному варіанті здійснення розлад або захворювання вибрані з групи, що складається з біполярних розладів. У ще одному варіанті здійснення розлад або захворювання вибрані з групи, що складається з порушень сну, таких як безсоння. Термін "лікування", використаний у зв'язку із захворюваннями або розладами, включає також профілактику, інгібування і полегшення, залежно від обставин. У одному з варіантів здійснення було виявлено, що сполуки цього винаходу мають вплив на калієві канали сімейства KCNQ, зокрема підгрупи KCNQ2. У цьому винаході запропоновані сполуки, що демонструють позитивний результат в одному або більше з наступних тестів: - "відносний витік через канал KCNQ2", який є показником активності сполуки відносно каналу-мішені; - "максимальний електрошок", який є показником судомних нападів, індукованих неспецифічною стимуляцією ЦНС електричними засобами; - "індуковані пілокарпіном судомні напади", індуковані пілокарпіном судомні напади часто важко лікувати багатьма наявними протисудомними препаратами і, таким чином, вони є моделлю "несприйнятливих до препаратів судомних нападів"; - "Тести визначення електричного порогу судомних нападів" і "Тести визначення хімічного порогу судомних нападів", за допомогою цих моделей визначають порогові значення, при яких починаються судомні напади, тому вони є моделями, які визначають, чи можуть випробовувані сполуки відстрочити початок судомного нападу; - "Збудження мигдалини мозочка", який використовують як спосіб оцінки розвитку захворювання, оскільки у здорових тварин судоми в цій моделі стають більш суворими при додатковій стимуляції тварин; 11 UA 102517 C2 5 10 15 20 25 30 - "Електрофізіологічна петч-кламп реєстрація в СНО клітинах" і "електрофізіологічна реєстрація каналів KCNQ2, KCNQ2/KCNQ3 або KCNQ5 в ооцитах"; у цих тестах реєструються ті струми, що активуються напругою KCNQ2, KCNQ2/KCNQ3 або KCNQ5. У одному з варіантів здійснення сполуки є KCNQ2 активними при значенні ЕС50 менше ніж 15000 нМ, наприклад, менше ніж 10000 нМ за результатами тесту "Відносний витік через канали KCNQ2". У іншому варіанті здійснення сполуки є KCNQ2 активними при значенні ЕС 50 менше ніж 2000 нМ, наприклад, менше ніж 1500 нМ за результатами тесту "Відносний витік через канали KCNQ2". У ще одному варіанті здійснення сполуки є KCNQ2 активними при значенні ЕС50 менше ніж 200 нМ, наприклад, менше ніж 150 нМ за результатами тесту "Відносний витік через канали KCNQ2". Тест "Відносний витік через канали KCNQ2" описаний далі. У одному з варіантів здійснення сполуки демонструють ED50 менше ніж 15 мг/кг в тесті "Максимальний електрошок". У іншому варіанті здійснення сполуки демонструють ED 50 менше ніж 5 мг/кг в тесті "Максимальний електрошок". Тест "Максимальний електрошок" описаний далі. У одному з варіантів здійснення сполуки демонструють ED 50 менше ніж 5 мг/кг в тестах "Визначення електричного порогу судом" і "Визначення хімічного порогу судом", які розкриті далі. Деякі сполуки мають незначні або клінічно малозначимі побічні ефекти. Таким чином, деякі сполуки протестовані на моделях стосовно небажаної седативної, гіпотермічної і атаксичної дії цих сполук. Деякі сполуки мають високий терапевтичний індекс між протисудомною дією і побічними ефектами, такими як порушення рухової активності або атаксичні ефекти, що визначають постановкою "тесту на стрижні, що обертається". Такі сполуки, як очікується, добре переноситимуться пацієнтами, дозволяючи використовувати високі дози, перш ніж виявляться побічні ефекти. При цьому сприйняття лікування буде гарним, і можна буде вводити високі дози, що дозволить зробити лікування ефективнішим для пацієнтів, введення яким інших ліків викликало б побічні ефекти. Необмежувальний аспект цього винаходу належить до сполук відповідно до наданих далі варіантів здійснення 1-10: 1. Заміщені похідні морфоліну або тіоморфоліну загальної формули І R2 R7 35 40 45 50 R6 X (Z)q R3 R1 N W H N R4 R5 , (I) де q дорівнює 0 або 1; W являє собою О або S; Х являє собою CO; Z являє собою О; R1 і R2 незалежно вибрані з групи, що складається з галогену, галоген-С1-6-алк(ен/ін)ілу, С16-алк(ен/ін)ілу і ціано; R3 вибраний з групи, що складається з С 1-10-алк(ен/ін)ілу, С3-8-циклоалк(ен)іл-С1-6алк(ен/ін)ілу, Аr-С1-6-алк(ен/ін)ілу і Аr; і R4, R5, R6 і R7 незалежно вибрані з групи, що складається з водню і Аr; у вигляді вільної основи або їх солей. 2. Сполука відповідно до варіанту здійснення 1, яка вибрана з групи, що складається з: N-(2-бpoм-4-мopфoлін-4-iл-6-трифтopмeтилфeнiл)-2-(4-фтopфeнiл)aцeтaмiдy; 2-циклопентил-N-(2-бром-6-трифторметил-4-морфолін-4-ілфеніл)ацетаміду; N-(2-бром-4-морфолін-4-іл-6-трифторметилфеніл)-3-циклопентилпропіонаміду; N-(2-хлор-6-ціано-4-морфолін-4-ілфеніл)-3-циклогексилпропіонаміду; 2-циклопентил-N-(2,6-диметил-4-тіоморфолін-4-ілфеніл)ацетаміду; 2-циклопентил-N-[2,6-диметил-4-(2-фенілморфолін-4-іл)феніл}ацетаміду; 2-циклопентил-N-[2,6-диметил-4-(2-фенілтіоморфолін-4-іл)феніл]ацетаміду; 2-циклопентил-N-[2,6-диметил-4-(3-піридин-3-ілтіоморфолін-4-іл)феніл]ацетаміду; 2-циклопентил-N-{2,6-диметил-4-[2-(4-трифторметилфеніл)тіоморфолін-4іл]феніл}ацетаміду; N-{4-[2-(2-хлорфеніл)тіоморфолін-4-іл]-2,6-диметилфеніл}-2-циклопентилацетаміду; 12 UA 102517 C2 5 10 15 20 25 30 35 40 45 50 55 2-біцикло[2.2.1]гепт-2-іл-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетаміду; 2-циклогексил-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетаміду; 3-(3,4-дифторфеіл)-N-(2,6-диметил-4-морфолін-4-ілфеніл)пропіонаміду; 2-циклопентил-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетаміду; бутилового естеру (2,6-диметил-4-морфолін-4-ілфеніл)карбамінової кислоти; 2-(4-хлорфеніл)-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетаміду; (2,6-диметил-4-морфолін-4-ілфеніл)аміду 2,3-дигідробензофуран-2'-карбонової кислоти; 3-циклогексил-N-(2,6-диметил-4-морфолін-4-ілфеніл)пропіонаміду; 3-циклопентил-N-(2,6-диметил-4-морфолін-4-ілфеніл)пропіонаміду; N-(2,6-диметил-4-морфолін-4-ілфеніл)-2-(4-фторфеніл)ацетаміду; N-(2,6-диметил-4-морфолін-4-ілфеніл)-2-тіофен-2-ілацетаміду; N-(2,6-диметил-4-морфолін-4-ілфеніл)-3,3-диметилбутираміду; (2,б-диметил-4-морфолін-4-ілфеніл)аміду гексанової кислоти; 2-циклогептил-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетаміду; бензилового естеру (2,6-диметил-4-морфолін-4-ілфеніл)карбамтової кислоти; 2-хлорбензилового естеру (2,6-диметил-4-морфолін-4-ілфеніл)карбамінової кислоти; (2,6-диметил-4-морфолін-4-ілфеніл)аміду 3,5,5-триметилгексанової кислоти; (2,6-диметил-4-морфолін-4-ілфеніл)аміду октанової кислоти; (2,6-диметил-4-морфолін-4-ілфеніл)аміду гептанової кислоти; N-(2,6-диметил-4-морфолін-4-ілфеніл)-2-фенілацетаміду; 2-(3,4-дихлорфеніл)-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетаміду; 2-(4-алілокси-3-хлорфеніл)-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетаміду; N-(2,6-дuмeтил-4-мopфoлiн-4-iлфeнiл)-2-(3-тpифтopмeтилфeнiл)aцeтaмiдy; N-(2,6-дuмeтил-4-мopфoлiн-4-iлфeнiл)-2-нaфтaлeн-2-iлaцeтaмiдy; 3-(3-хлорфеніл)-N-(2,6-диметил-4-морфолін-4-ілфеніл)пропіонаміду; N-(2,6-диметил-4-морфолін-4-ілфеніл)-2-(3,4-диметилфеніл)ацетаміду; 2-(3-бромфеніл)-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетаміду; 2-(3-хлорфеніл)-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетаміду; N-(2,6-диметил-4-морфолін-4-ілфеніл)-2-n-толілацетаміду; N-(2,6-диметил-4-морфолін-4-ілфеніл)-2-м-толілацетаміду; 2-(3,4-дифторфеніл)-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетаміду; і N-(2,6-диметил-4-морфолін-4-ілфеніл)-2-(3-фторфеніл)ацетаміду. 3. Фармацевтична композиція, яка містить один або більше фармацевтично прийнятних носіїв або розріджувачів і одну або більше сполук відповідно до будь-якого з варіантів здійснення 1 і 2. 4. Застосування фармацевтичної композиції відповідно до варіанту здійснення 3 для посилення потоку іонів в потенціалозалежних калієвих каналах ссавців, таких як людина. 5. Застосування відповідно до варіанту здійснення 4 для лікування розладу або захворювання, сприйнятливого до посиленого потоку іонів в потенціалозалежних калієвих каналах, причому такий розлад або захворювання є переважно розладом або захворюванням центральної нервової системи. 6. Застосування відповідно до варіанту здійснення 5, яке відрізняється тим, що розлад або захворювання вибрані з групи, що складається з судомних нападів, таких як судоми, епілепсія і епілептичний статус. 7. Застосування відповідно до варіанту здійснення 5, яке відрізняється тим, що розлад або захворювання вибрані з групи, що складається з невропатичного і мігреневого болю, такого як алодинія, гіпералгічний біль, фантомний біль, невропатичний біль, пов'язаний з діабетичною невропатією, і невропатичний біль, пов'язаний з мігренню. 8. Застосування відповідно до варіанту здійснення 5, яке відрізняється тим, що розлад або захворювання вибрані з групи, що складається з тривожних розладів, таких як тривога, генералізований тривожний розлад, панічна атака, обсесивно-компульсивний розлад, соціальна фобія, страх діяльності, посттравматичний стресовий розлад, гострий стресовий розлад, розлади адаптації, іпохондричні розлади, тривожний розлад, пов'язаний з розлукою, агорафобія, специфічні фобії, тривожні розлади, пов'язані із загальним станом здоров'я, і тривожні розлади, що викликаються речовинами. 9. Застосування відповідно до варіанту здійснення 5, яке відрізняється тим, що розлад або захворювання вибрані з групи, що складається з нейродегенеративних розладів, таких як хвороба Альцгеймера, хорея Гентінгтона, розсіяний склероз, бічний аміотрофічний склероз, індукована СНІДом енцефалопатія та інші енцефалопатії, пов'язані з інфекцією, викликаною 13 UA 102517 C2 5 10 15 20 25 30 35 40 45 50 55 60 вірусом коревої краснухи, герпесвірусом, бореліями і невідомими патогенами, хвороба Крейтцфельда-Якоба, хвороба Паркінсона, викликані травмою нейродегенерації. 10. Застосування відповідно до варіанту здійснення 5, яке відрізняється тим, що розлад або захворювання вибрані з групи, що складається із станів нейронального гіперзбудження, таких як при синдромі відміни ліків або при інтоксикації. Визначення Термін "гетероатом" належить до атомів азоту, кисню або сірки, Термін "галоген" означає фтор, хлор, бром або йод. Вираз "С1-6-алк(ен/ін)іл" означає С1-6-алкільну, С2-6-алкенільну або С2-6-алкінільну групу. Термін "С1-6-алкіл" належить до розгалуженої або нерозгалуженої алкільної групи, що містить від одного до шести атомів вуглецю включно, включаючи, але не обмежуючись тільки ними, метил, етил, 1-пропіл, 2-пропіл, і-бутил, 2-бутил, 2-метил-2-пропіл і 2-метил-1-пропіл. Аналогічним чином, "С2-6-алкеніл" і "С2-6-алкініл", відповідно, означають такі групи, що містять від двох до шести атомів вуглецю, включаючи один подвійний зв'язок і один потрійний зв'язок, відповідно, включаючи, але не обмежуючись тільки ними, етеніл, пропеніл, бутеніл, етиніл, пропініл і бутиніл. Вираз "С1-10-алк(ен/ін)іл" означає С1-10-алкільну, С2-10-алкенільну або С2-10-алкінільну групу. Термін "С1-10-алкіл" стосується розгалуженої або нерозгалуженої алкільної групи, що містить від одного до шести атомів вуглецю включно, включаючи, але ними не обмежуючись тільки ними, метил, етил, 1-пропіл, 2-пропіл, 1-бутил, 2-бутил, 1-пентил, 1-гексил, 1-гептил, 1-октил, 1-ноніл, 1-децил, 2-метил-2-пропіл і 2-метил-1-пропіл. Аналогічним чином, "С2-10-алкеніл" і "С2-10-алкініл", відповідно, означають такі групи, що містять від двох до шести атомів вуглецю, включаючи один подвійний зв'язок і один потрійний зв'язок, відповідно, включаючи, але ними не обмежуючись тільки ними, етеніл, пропеніл, бутеніл, пентеніл, гексеніл, гептеніл, октеніл, ноненіл, деценіл, етиніл, пропініл, бутиніл, пентиніл, гексиніл, гептиніл, октиніл, нонініл і дециніл. Вираз "С3-8-циклоалк(ен)іл" означає С3-8-циклоалкільну або циклоалкенільну групу. Термін "С3-8-пиклоалкіл" означає моноциклічний або біциклический карбоцикл, що містить від трьох до восьми атомів вуглецю, включаючи, але ними не обмежуючись тільки ними, циклопропіл, циклопентил, циклогексил, циклогептил, циклооктил, [1.1.1]біциклопентил, біцикло[2.2.1]гептил, [2.2.2]біциклооктил і [3.3.0]біциклооктил тощо. Термін "С3-8-циклоалкеніл" означає моноциклічний або біциклический карбоцикл, що містить від трьох до восьми атомів вуглецю і включає один подвійний зв'язок. Термін "галоген-С1-6-алк(ен/ін)іл" означає С1-6-алк(ен/ін)іл, заміщений одним або більше атомами галогенів, включаючи, але не обмежуючись тільки ними, трифторметил. Аналогічним чином, термін "галоген-С3-8-циклоалк(ен)іл" означає С3-8-циклоалк(ен)іл, заміщений одним або більше атомами галогену. У виразі "галоген-С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)іл" терміни "С1-6-алк(ен/ін)іл" і "галоген-С38-диклоалк(ен)іл" є такими, як визначено вище. Якщо два суміжні замісники разом з ароматичною групою, до якої вони приєднані, утворюють 4-8-членне кільце, яке необов'язково містить один, два або три гетероатоми, тоді кільцева система утворюється 4-8 атомами, вибраними з 4-8 атомів вуглецю 10-3 гетероатомів, вибраних з N, S або О. Такі два суміжні замісники можуть разом утворити: -(СН2)а-СН2-, -СН=СН-(СН2)b-, -СН2-СН=СН-(СН2)с, -СН-СН-СН=СН-, -(СН2)а-О-, -O-(CH2)b-O-, -СН2-O-(СН2)с-O-, -СН2-O-СН2-O-СН2-. -(CH2)a-S-, -S-(CH2)b-S-, -CH2-S-(CH2)c-S-, -CH2-S-CH2-SCH2-, -(СH2)а-NН-, -NH-(CH2)b-NH-, -CH2-NH-(CH2)c-NH-. -CH=CH-NH-, -O-(CH2)b-NH-, -CH2-O(CH2)c-NH- або -O-(CH2)c-NH-CH2-, -S-(CH2)b-NH-, -N-CH-NH-, -N-CH-O- або -N=CH-S- або -N=NNH-, де b дорівнює 1, 2 або 3, а дорівнює 2, 3 або 4 і с дорівнює 1 або 2. Термін "Аr" стосується необов'язково заміщених ароматичних систем, що складаються з 510 атомів вуглецю, де 0, 1,2, 3 або 4 атоми вуглецю можуть бути замінені гетероатомами, незалежно вибраними з N, S або О. Прикладами таких Аr-груп є необов'язково заміщений феніл, необов'язково заміщений нафтил, необов'язково заміщений піридин, необов'язково заміщений тіофен, необов'язково заміщений фуран, необов'язково заміщений тіазол, необов'язково заміщений хінолін, необов'язково заміщений індол, необов'язково заміщений 2,3дигідробензофуран, необов'язково заміщений піримідин, необов'язково заміщений пірол і необов'язково заміщений оксазол. Аr може бути заміщений одним або більше замісниками, незалежно вибраними з гідрокси, галогену, С1-6-алк(ен/ін)ілу, С3-8-циклоалк(ен)ілу, С3-8циклоалк(ен)іл-С1-6-алк(ен/ін)ілу, галоген-С1-6-алк(ен/ін)ілу, С1-6-алк(ен/ін)ілокси, С3-8алк(ен/ін)ілокси, ацилу, нітро або ціано, -СО-NН-С1-6-алк(ен/ін)ілу, -СО-N(С1-6-алк(ен/ін)іл)2, -NH2, -NН-С1-6-алк(ен/ін)ілу, -N(С1-6-алк(ен/ін)іл)2, -S-С1-6-алк(ен/ін)ілу, -SO2-С1-6-алк(ен/ін)ілу, -SO2N(С16-алк(ен/ін)іл)2 і -SO2NH-C1-6-алк(eн/iн)ілу; або два суміжні замісники можуть разом з 14 UA 102517 C2 5 10 15 20 25 30 35 40 45 50 55 60 ароматичною групою, до якої вони приєднані, утворювати 4-8-членне кільце, яке необов'язково містить один, два або три гетероатоми. Якщо Аr заміщений СО-NН-С1-6-алк(ен/ін)ілом або СО'N(С1-6-алк(ен/ін)іл)2, тоді атом вуглецю CO групи приєднаний до Аr. Якщо Аr заміщений NH 2, NН-С1-6-алк(ен/ін)ілом або N(С1-6-алк(ен/ін)іл)2, тоді атом азоту приєднаний до Аr. Якщо Аr заміщений -5-С1-6-алк(ен/ін)ілом, -SO2-С1-6-алк(ен/ін)ілом, -SO2N(C1-6-алк(ен/ін)іл)2 або -SO2NН-С1-6-алк(ен/ін)ілом, тоді атом сірки приєднаний до Аr. Термін "ацил" стосується формільної, С1-6-алк(ен/ін)ілкарбонільної, С3-8циклоалк(ен)ілкарбонільної, Аr-карбонільної, Аr-С1-6-алк(ен/ін)ілкарбонільної або С3-8циклоалк(ен)іл-С1-6-алк(ен/ін)ілкарбонільної групи, де С1-6-алк(ен/ін)іл, С3-8-циклоалк(ен)іл і Аr є такими, як визначено вище. Терміни "С3-8-циклоалк(ен)іл-С1-б-алк(ен/ін)іл", "Аr-С1-6-алк(ен/ін)іл", "С1-6-алк(ен/ін)ілокси" і "С3-8-циклоалк(ен)ілокси" означають такі групи, в яких С1-6-алк(ен/ін)іл, С3-8-циклоалк(ен)іл і Аr є такими, як визначено вище. Аналогічним чином, термін "С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)ілокси" означає такі групи, в яких С3-8-циклоалк(ен)іл і С1-6-алк(ен/ін)ілокси є такими, як визначено вище. Вирази "Аr-С3-8-циклоалк(ен)іл" і "Аr-С3-8-циклоалк(ен)іл-С1-6-алк(ен/ін)іл" означають такі групи, в яких С1-6-алк(ен/ін)іл, С3-8-циклоалк(ен)іл і Аr є такими, як визначено вище. Фармацевтичні композиції Цей винахід належить також до фармацевтичної композиції. Сполуки цього винаходу або їх солі можна вводити окремо або в комбінації з фармацевтично прийнятними носіями або розріджувачами, у вигляді разової або багатократної дози. Фармацевтичні композиції відповідно до цього винаходу можуть бути приготовані з фармацевтично прийнятними носіями або розріджувачами, а також з іншими відомими ад'ювантами і ексципієнтами відповідно до звичайних методик, таких як ті, що описані в Remington: The Science and Practice of Pharmacy, 19 Edition, Gennaro, Ed., Mack Publishing Co., Easton, PA, 1995. Фармацевтичні композиції можуть бути спеціально створені для введення будь-яким відповідним шляхом, таким як пероральний, ректальний, назальний, легеневий, місцевий (включаючи букальний і сублінгвальний), трансдермальний, інтрацистернальний, внутрішньочеревинний, вагінальний і парентеральний (включаючи підшкірний, внутрішньом'язовий, інтратекальний, внутрішньовенний та інтрадермальний) шлях, причому переважним є пероральний шлях введення. Слід розуміти, що переважний шлях залежатиме від загального стану і віку суб'єкта, який піддається лікуванню, природи розладу або захворювання, що лікується, і вибраного активного інгредієнта. Фармацевтичні композиції, утворені змішуванням сполуки цього винаходу і фармацевтично прийнятних носіїв, потім легко вводять в різних дозованих формах, придатних для описаних шляхів введення. Композиції зручно представляти у вигляді одиничних дозованих форм за способами, відомими фахівцям-фармацевтам. Сполуки цього винаходу звичайно використовують у вигляді вільних речовин або у вигляді їх фармацевтично прийнятних солей. Одним з прикладів є кислотно-адитивна сіль сполуки, яка знаходить застосування у вигляді вільної основи. Якщо сполуки цього винаходу являють собою вільну основу, такі солі отримують за звичайним способом, обробляючи розчин або суспензію вільної основи цього винаходу хімічним еквівалентом фармацевтично прийнятної кислоти. Репрезентативні приклади наведені вище. Фармацевтичні композиції для перорального введення можуть бути твердими або рідкими. Тверді дозовані форми для перорального введення включають, наприклад, капсули, пігулки, драже, пілюлі, пастили, порошки, гранули і маленькі пігулки, наприклад, поміщені в тверді желатинові капсули у формі порошків або гранул, або, наприклад, у формі коржиків або пастилок. У відповідному випадку фармацевтичні композиції для перорального введення можуть бути виготовлені з покриттями, такими як ентеросолюбільне покриття, або вони можуть бути виготовлені так, щоб забезпечити регульоване вивільнення активного інгредієнта, таке як сповільнене або пролонговане вивільнення, за способами, добре відомими в даній галузі. Рідкі дозовані форми для перорального введення включають, наприклад, розчини, емульсії, суспензії, сиропи і еліксири. Композиції цього винаходу, придатні для перорального введення, можуть бути у вигляді дискретних одиниць, таких як капсули або пігулки, кожна з яких містить певну кількість активного інгредієнта, і які можуть містити відповідний ексципієнт. Крім того, композиції для перорального введення можуть бути у формі порошків або гранул, розчинів або суспензій у водній або неводній рідині, або у вигляді емульсій типу олія-уводі або вода-в-олії. Відповідні фармацевтичні носії включають інертні тверді розріджувачі або наповнювачі, стерильні водні розчини та різні органічні розчинники. Прикладами твердих носіїв є лактоза, біла глина, сахароза, циклодекстрин, тальк, желатин, агар, пектин, аравійська камедь, стеарат 15 UA 102517 C2 5 10 15 20 25 30 35 40 45 50 магнію, стеаринова кислота, нижчі алкілові естери целюлози, кукурудзяний крохмаль, картопляний крохмаль, камеді тощо. Прикладами рідких носіїв є сиропи, арахісова олія, оливкова олія, фосфоліпіди, жирні кислоти, аміни жирних кислот, поліоксіетилен і вода. Носій або розріджувач може включати будь-які відомі фахівцям матеріали із сповільненим вивільненням, такі як гліцерилмоностеарат або гліцерилдистеарат, окремо або в суміші з воском. Можна використовувати будь-які ад'юванти та добавки, зазвичай використовувані для таких цілей, такі як барвники, ароматизатори, консерванти і т.д., за умови, що вони сумісні з активними інгредієнтами. Кількість твердого носія може мінятися, але зазвичай складає від біля 25 мг до біля 1 г. Якщо використовують рідкий носій, препарати можуть бути у формі сиропів, емульсій, м'яких желатинових капсул і стерильних рідин для ін'єкцій, таких як водні або неводні рідкі суспензії або розчини. Пігулки можна отримати, змішуючи активний інгредієнт із звичайними ад'ювантами або розріджувачами, і потім пресуючи отриману суміш в звичайній таблетувальній машині. Фармацевтичні композиції для парентерального введення включають стерильні водні розчини і неводні розчини для ін'єкцій, дисперсії, суспензії або емульсії, а також стерильні порошки, які необхідно перед використанням знову перетворити на стерильні розчини або дисперсії для ін'єкцій. Передбачаються придатні для ін'єкцій препарати типу депо, які входять до обсягу цього винаходу. Для парентерального введення можна використовувати розчини сполук цього винаходу в стерильному водному розчині, водному розчині пропіленгліколю, водному розчині вітаміну Е або в кунжутній або арахісовій олії. Такі водні розчини повинні бути відповідним чином забуферені, якщо це необхідно, та рідкому розріджувачу спочатку потрібно надати ізотонічності достатньою кількістю сольового розчину або глюкози. Водні розчини є особливо відповідними для внутрішньовенного, внутрішньом'язового, підшкірного і внутрішньочеревинного введення. Вживане стерильне водне середовище є цілком легко доступним для застосування за стандартними способами, відомими фахівцям в даній галузі. Розчини для ін'єкцій можуть бути одержані розчиненням активного інгредієнта і можливих добавок в частині розчинника для ін'єкції, переважно стерильній воді, доведенням розчину до бажаного об'єму, стерилізацією розчина і наповненням ним відповідних ампул або пляшечок. Може бути додана будь-яка добавка, звичайно використовувана в даній галузі, наприклад, агенти ізотонічності, консерванти, антиоксиданти тощо. Інші відповідні форми введення включають супозиторії, спреї, мазі, креми, гелі, засоби для інгаляції, нашкірні пластири, імплантати і т.д. Типове дозування при пероральному введенні знаходиться в інтервалі від біля 0,001 до біля 100 мг/кг маси тіла на добу, переважно від біля 0,01 до біля 50 мг/кг маси тіла на добу, а більш переважно від біля 0,05 до біля 10 мг/кг маси тіла на добу, що вводиться у вигляді однієї або більше доз, наприклад 1-3 дози. Точне дозування буде залежати від частоти і способу введення, статі, віку, маси і загального стану суб'єкта, що піддається лікуванню, і природи і тяжкості розладу або захворювання, що піддається лікуванню, і будь-яких супутніх захворювань, що піддаються лікуванню, та інших факторів, очевидних для фахівців в даній галузі. Препарати можуть бути придатним чином представлені в стандартній дозованій лікарській формі за способами, відомими фахівцям в даній галузі. Стандартна дозована лікарська форма для перорального введення один або кілька разів на день, наприклад 1 -З рази на день, може містити від 0,01 до біля 1000 мг, наприклад, від біля 0,01 до 100 мг, переважно від біля 0,05 до біля 500 мг, і більш переважно від біля 0,5 мг до біля 200 мг. Для парентеральних способів введення, таких як внутрішньовенний, інтратекальний, внутрішньом'язовий і аналогічні способи введення, типові дози складають порядку приблизно половини дози, вживаної для перорального введення. Типовими прикладами прописів для лікарської форми даного винаходу є: 1) Пігулки, що містять 5,0 мг сполуки цього винаходу, в розрахунку на вільну основу: Сполука формули І 5,0 мг Лактоза 60 мг Кукурудзяний крохмаль 30 мг Гідроксипропілцелюлоза 2,4 мг Мікрокристалічна целюлоза 19,2 мг Натрію кроскармелоза типу А 2,4 мг 16 UA 102517 C2 5 10 Магнію стеарат 0,84 мг 2) Пігулки, що містять 0,5 мг сполуки цього винаходу, в розрахунку на вільну основу: Сполука формули І 0,5 мг Лактоза 46,9 мг Кукурудзяний крохмаль 23,5 мг Повідон 1,8 мг Мікрокристалічна целюлоза 14,4 мг Натрію кроскармелоза типу А 1,8 мг Магнію стеарат 0,63 мг 3) Сироп, що містить на мілілітр: Сполука формули І 25 мг Сорбіт 500 мг Гідроксипропілцелюлоза 15 мг Гліцерин 50 мг Метилпарабен 1 мг Пропілпарабен 0,1 мг Етанол 0,005 мл Смаковий і ароматичний 0,05 мг коригент Натрієва сіль сахарину 0,5 мг Вода до 1 мл 4) Розчин для ін'єкцій, що містить на мілілітр: Сполука формули І 0,5 мг Сорбіт 5,1 мг Оцтова кислота 0,05 мг Натрієва сіль сахарину 0,5 мг Вода до 1 мл. Під виразом "сполуки цього винаходу" мається на увазі будь-який з варіантів здійснення формули І, як описано у цьому описі винаходу. У наступному аспекті цей винахід стосується способу одержання сполуки цього винаходу, як описано далі. Одержання сполук цього винаходу Сполуки цього винаходу загальної формули І, де q, W, X, Z, R1, R2, R3, R4, R5, R6 і R7 є такими, як визначено вище, можна одержати за способами, представленими на схемах, і так, як описано далі: Схема 1 R2 R2 O2N R1 O2N H2N R1 III II R2 NH2 NH2 NH2 NH2 R1 R1 N W IV R7 R6 R4 R5 R2 H N R7 R6 Схема 2 R4 R5 R2 NH2 Br R1 VI Br H N X (Z)q R3 H N R1 N W R1 R7 VII 17 R6 (Z)q R3 I R2 R2 X R1 N W V R4 R5 I X (Z)q R3 UA 102517 C2 Схема 3 R2 R2 R2 NH2 Br H N NH2 R1 VI R7 R4 R5 R6 W V R7 R6 (Z)q R3 R1 N R1 N W X R4 R5 I Схема 4 R2 R2 Br R2 R2 NH2 NO2 R1 R1 N W VIII R7 R6 R4 R5 H N NH2 IX R7 R6 R4 R5 W V R7 R6 (Z)q R3 R1 N R1 N W X R4 R5 I Схема 5 Br R7 R6 X (Z)q R4 R5 H N R3 X W (I: R2 = Br) R7 R6 X (Z)q R3 R1 N R1 N W R2 H N R4 R5 I 5 Схема 6 R2 R2 R2 NO R1 F H N O O R1 R2 R2 NH2 R1 N R7 R6 H N S O O R1 O2N XII XI W S R4 R5 R7 R6 R2 H N S O O R1 N W V XIII R4 R5 H2N H N S O O R1 XIV XV Схема 7 R2 R2 NH2 R1 XI 10 15 NH2 Br R1 VI У сполуках загальних формул I-XV, q, W, X, Z, Rl, R2, R3, R4, R5, R6 і R7 є такими, як визначено для формули І. Сполуки загальних формул II, III, VI, VIII і XI або одержують з комерційних джерел, або одержують за стандартними способами, відомими фахівцям в даній галузі. У іншому варіанті сполуки загальної формули III, де R2 являє собою галоген, такий як СІ, Вr або І (схема 1), одержують, використовуючи регіоселективне електрофільне ароматичне заміщення, добре відоме фахівцям в даній галузі, використовуючи відповідні електрофільні сполуки, такі як N-хлорсукцинімід, N-бромсукцинімід, бром, йод або хлорид йоду, у відповідному розчиннику, такому як оцтова кислота, як описано в "Electrophilic Halogenations" by P.B.D. de la Mare, Cambridge University Press, Cambridge, 1976. 18 UA 102517 C2 5 10 15 20 25 30 35 40 45 50 55 60 Нітрогрупу в сполуках загальних формул III, IX і XIII (схеми 1, 4 і 6) можна відновити, використовуючи відповідні відновлювальні агенти, такі як порошок цинку або заліза у присутності кислоти, такої як оцтова кислота або водна хлористоводнева кислота, або використовуючи газоподібний водень або форміат амонію у присутності відповідного каталізатора гідрування, такого як паладій на активованому вуглеці, у відповідних розчинниках, таких як метанол, етанол або тетрагідрофуран, при відповідних температурах або під дією ультразвука, до одержання анілінів загальних формул IV, V і XIV, відповідно. У іншому варіанті хлорид олова(П) або дитіоніт натрію можна використовувати як відновлювальні агенти в умовах, добре відомих фахівцям в даній галузі. Сполуки загальних формул І і VII (схеми 1, 2, 3 і 4) можна одержати, здійснюючи взаємодію сполук загальних формул V і VI, відповідно, з відповідними електрофільними реагентами, такими як, але не обмежуючись тільки ними), відповідним чином заміщені хлорангідриди, бромангідриди, йодангідриди, ангідриди карбонових кислот, активовані естери, хлорформіати, з додаванням або без додавання основ, таких як піридин, триалкіламіни, карбонат калію, оксид магнію або алкоголят літію, натрію або калію, у відповідному розчиннику, такому як етилацетат, діоксан, тетрагідрофуран, ацетонітрил або діетиловий етер, при відповідній температурі, такій як кімнатна температура або температура утворення флегми. У іншому варіанті сполуки загальних формул І і V (схеми 2 і 3) можна одержати, використовуючи реакцію утворення зв'язку C-N з використанням паладієвого каталізатора для відповідним чином заміщених сполук загальних формул VII і VI і відповідним чином заміщених морфолінів або тіоморфолінів, як описано у S.L. Buchwald et al. (M.C. Harris, X. Hang і S.L. Buchwald, Organic Letters, 2002,4, 2885). Сполуки загальних формул V і XV (схеми 1 і 6) можна одержати, здійснюючи взаємодію сполук загальних формул IV і XIV з відповідним чином заміщеними біс-(2-галогенетил)етерами та з додаванням або без додавання основ, таких як триалкіламіни, карбонат калію або алкоголят літію, натрію або калію, у відповідному розчиннику, такому як диметилсульфоксид або N, N-диметилформамід, при відповідній температурі, такій як кімнатна температура або температура утворення флегми. У іншому варіанті сполуки загальної формули V (схема 3) можна одержати, здійснюючи взаємодію сполук загальної формули VI з відповідним чином заміщеними похідними морфоліну або тіоморфоліну у присутності паладієвого каталізатора, такого як біс(дибензиліденацетон)паладій з додаванням відповідного фосфінового ліганду, такого як (±)2,2'-біс(дифенілфосфіно)-1,1'-бінафтил, у присутності основи, такої як карбонат калію або алкоголят літію, натрію або калію, у відповідному розчиннику, такому як толуол або тетрагідрофуран, при відповідній температурі, такій як кімнатна температура або температура утворення флегми. Сполуки загальної формули IX (схема 4) можна одержати, здійснюючи взаємодію сполук загальної формули VIII з відповідним чином заміщеними морфолінами або тіоморфолінами і з додаванням або без додавання основ, таких як карбонат калію, у відповідному розчиннику, такому як диметилсульфоксид або N, N-диметилформамід, при відповідній температурі, такій як кімнатна температура або температура утворення флегми. Сполуки загальної формули І, де R2 являє собою Аr або Het (схема 5), можна одержати із сполук загальної формули X, використовуючи реакції крос-сполучання, відомі фахівцям в даній галузі, такі як сполучання за Сузукі, сполучання за Стілле або інші реакції крос-сполучання, що каталізуються перехідними металами (D.W. Knight, "Coupling reactions between sp2 carbon centers" в Comprehensive Organic Synthesis, v. 3, pp. 481-520, Pergamon Press, 1991). Сполуки загальної формули VI (схема 7) можна одержати із сполук загальної формули XI, використовуючи електрофільне ароматичне заміщення, добре відоме фахівцям в даній галузі, використовуючи відповідні електрофільні сполуки, такі як N-бромсукцинімід або бром, у відповідному розчиннику, такому як оцтова кислота, як описано у P.B.D. de la Мате and J.H. Ridd, "Preparative methods of aromatic halogenation" в Aromatic substitutions, pp. 105-115, Butterworths Scientific Publications, London, 1959. Сполуки загальної формули XII (схема 6) можна одержати, здійснюючи взаємодію сполук загальної формули XI з n-толуолсульфонілхлоридом з додаванням або без додавання основ, таких як піридин, триалкіламіни, карбонат калію, бікарбонат натрію, оксид магнію або алкоголят літію, натрію або калію, у відповідному розчиннику, такому як піридин, етилацетат, діоксан, тетрагідрофуран, ацетонітрил або діетиловий етер, при відповідній температурі, такій як кімнатна температура або температура утворення флегми. Сполуки загальної формули XIII (схема б) можна одержати із сполук загальної формули XII, використовуючи реакції нітрування, відомі фахівцям в даній галузі, такі як реакція з 19 UA 102517 C2 5 10 15 20 25 30 35 40 45 50 55 60 концентрованою азотною кислотою, нітритом натрію або нітратом натрію, у відповідному розчиннику, такому як льодяна оцтова кислота, оцтовий ангідрид, трифтороцтова кислота, концентрована сірчана кислота або їх суміші, при відповідних температурах, наприклад так, як описано P.B.D. de la Мате and J.H. Ridd, "Preparative Methods of Nitration" в Aromatic substitutions, pp. 48-56, Butterworths Scientific Publications, London, 1959. Сполуки загальної формули V (схема 6) можна одержати, обробляючи сполуки загальної формули XV в сильно кислотних умовах, таких як водний розчин сірчаної кислоти або водна хлористоводнева кислота, при відповідній температурі, такій як кімнатна температура або температура утворення флегми. Приклади Дані аналітичної РХ-МС (LC-MS) одержували на устаткованні РЕ Sciex API 150EX, обладнаному системою фотоіонізації при атмосферному тиску і РХ-системою Shimadzu LC8A/SLC-10A. Колонка: колонка Waters Symmetry C18, 30 × 4,6 мм з розміром частинок 3,5 мкм; Система розчинників: А = вода/трифтороцтова кислота (100:0,05) і В = вода/ацетонітрил/трифтороцтова кислота (5:95:0,03); Метод: елюювання з лінійним градієнтом від 90 % А до 100 % В протягом 4 хвилин і з витратою 2 мл/хв. Чистоту визначали інтеграцією УФ- (254 нм) і ELSD сліду. Час утримування (tp) виражено в хвилинах. Препаративне РХ-МС-очищення здійснюють на тому ж самому устаткованні, використовуючи хімічну іонізацію при атмосферному тиску. Колонка: YMC ODS-A 50 20 мм з розміром частинок 5 мкм; Метод: елюювання з лінійним градієнтом від 80 % А до 100 % В протягом 7 хвилин і з витратою 22,7 мл/хв. Збір фракцій проводили при МС-детектуванні з розгалуженим потоком. Дані аналітичної LC-MS-TOF (TOF = час прольоту) отримують, використовуючи прилад мікромас LCT 4-ways MUX, забезпечений детекторною системою Waters 2488/Sedex 754. Колонка: колонка Waters Symmetry C18, 30 4,6 мм з розміром частинок 3,5 мкм; Система розчинників: А = вода/трифтороцтова кислота (100:0,05) і В = вода/ацетонітрил/трифтороцтова кислота (5:95:0,03); Метод: елюювання з лінійним градієнтом від 90 % А до 100 % В протягом 4 хвилин і з витратою 2 мл/хв. Чистоту визначали інтеграцією УФ - (254 нм) і ELSD сліду. Час утримування (tp) виражено в хвилинах. Результати GC-MS отримують, використовуючи газовий хроматограф Varian CP 3800, укомплектований колонкою Phenomenex (Zebron ZB-5, довжина: 15 метрів, внутрішній діаметр: 0,25 мм), сполучений з мас-спектрометром Varian Saturn 2000 iontrap. Метод: тривалість 15 хвилин, потік в колонці 1,4 мл/хв. (газ-носій - гелій), градієнт температури: 0-1 хвилина, 60 °C; 113 хвилин, 60-300 °C; 13-15 хвилин, 300 °C. 1 Спектри Н ЯМР реєстрували при 500,13 МГц на приладі Bruker Avance DRX500. Дейтерований хлороформ (99,8 % D) або диметилсульфоксид (99,8 % D) використовували як розчинник. ТМС (TMS) використовували як внутрішній стандарт. Значення хімічних зсувів 1 виражали в млн.- (ррm). Для різноманітних ЯМР-сигналів застосовували наступні скорочення: с - синглет, д = дублет, т = триплет, к. = квартет, кві. = квінтет, г = гептет, дд = дублет дублетів, ддд = дублет дублету дублетів, дт = дублет триплетів, дк = дублет квартетів, тт = триплет триплетів, м = мультиплет і шир.с = широкий синглет. Мікрохвильові експерименти здійснювали в запаяних ампулах або реакторах, використовуючи синтезатор Emrys Synthesizer або оптимізатор Emrys Optimizer EXP від Personal Chemistry, або прилад Milestone Microsynth від Milestone. Якщо реакційну суміш нагрівають в мікрохвильовому приладі, тоді перед наступною стадією процесу її охолоджують до 25 °C. Отримання проміжних сполук 2,6-Диметил-4-морфолін-4-ілфеніламін Біс(дибензиліденацетон)паладій (2,88 г) і (±)-2,2'-біс(дифенілфосфіно)-1,1'-бінафтил (4,69 г) додають до сухого толуолу (175 мл, очищений аргоном) і перемішують протягом 15 хвилин в атмосфері аргону. Послідовно додають wpew-бутоксид калію (7,06 г), морфолін (8,7 мл) і 4бром-2,6-диметиланілін (10,03 г). Реакційну суміш нагрівають до температури кипіння із зворотним холодильником протягом 1 б годин в атмосфері аргону, охолоджують і фільтрують через діоксид кремнію (200 г). Додають сольовий розчин (250 мл) і отриману суміш екстрагують етилацетатом (3 × 200 мл). Об'єднані органічні фази сушать над сульфатом магнію і концентрують у вакуумі. Сирий продукт розчиняють в діетиловому етері (250 мл), фільтрують через діоксид кремнію (200 г) і концентрують у вакуумі, отримуючи 8,5 г (41 % вихід) вказаної в заголовку сполуки у вигляді темної оливи. Продукт використовують без подальшого очищення. GC-MS (m/z) 206 (М"1"); 1 tR=6,90. Н ЯМР (500 МГц, СDСl3):2,18 (с, 6Н). 3,02 (м, 4Н), 3,85 (м, 4Н), 6,62 (шир.с, 2Н). 20 UA 102517 C2 5 10 15 20 25 30 35 40 45 50 55 60 N-(4-Бром-2,б-диметилфеніл)-2-циклопентилацетамід 4-Бром-2,6-диметиланілін (5,92 г) і циклопентилацетилхлорид (4,87 мл) розчиняють в ацетонітрилі (26 мл) і нагрівають до 150 °C протягом 10 хвилин в запаяній ампулі для мікрохвильової обробки. Реакційну суміш охолоджують до 0 °C, продукт фільтрують і промивають холодним ацетонітрилом (50 мл), отримуючи 8,43 г (92 % вихід) вказаної в заголовку сполуки у вигляді твердої речовини коричневого кольору. Сирий продукт + використовують без подальшого очищення. РХ-МС (m/z) 312 (MН4 ); tR=3,10, (UV (УФ), ELSD) 1 89 %, 99 %. Н ЯМР (500 МГц, CDCl3):1,22 (м, 2Н), 1,52 (м, 2Н), 1,63 (м, 2Н), 1,77 (м, 2Н), 2,06 (с, 6Н), 2,31 (м, 1Н), 2.64 (д, 2Н), 7,15 (с, 2Н), 9,98 (шир.с, 1Н). 2-Бром-4-нітро-б-трифторметилфеніламін Бром (0,60 мл), розчинений в оцтовій кислоті (11 мл), додають по краплях до розчину 4нітро-2-трифторметилфеніламіну (2,4 г) в оцтовій кислоті (12 мл). Реакційну суміш нагрівають до 120 °C протягом 2,5 годин, виливають у воду (400 мл) і фільтрують. Зібрану тверду речовину промивають водою (200 мл) і сушать у вакуумі, отримуючи 3,03 г 1 (91 % вихід) вказаної в заголовку сполуки у вигляді твердої речовини жовтого кольору. Н ЯМР (500 МГц, ДМСО-d6):7,08 (с, 2Н), 8,23 (д, 1Н), 8,51 (д, 1Н). 2-Бром-6-трифторметилбензол-1,4-діамін Водну хлористоводневу кислоту (2М, 45 мл) поволі додають до суміші цинкового порошку (8,6 г) і 2-бром-4-нітро-6-трифторметилфеніламіну (2,5 г) в тетрагідрофурані (50 мл). Реакційну суміш перемішують протягом 1 години, фільтрують і нейтралізують, використовуючи насичений водний розчин бікарбонату натрію (100 мл). Додають воду (100 мл) і отриману суміш екстрагують етилацетатом (2 × 100 мл). Об'єднані органічні фази промивають водою (2 × 200 мл) і сольовим розчином (200 мл), сушать над сульфатом натрію і концентрують у вакуумі, отримуючи 2,22 г (98 % вихід) вказаної в заголовку сполуки у вигляді твердої речовини 1 червоного кольору. Н ЯМР (500 МГц, ДМСО-d6): 4,55 (с, 2Н), 4,91 (с, 2Н), 6.76 (д, 1Н), 7,01 (д, 1Н). 2-Бром-4-морфолін-4-іл-6-трифторметилфеніламін 2-Бром-6-трифторметилбензол-1,4-діамін (2,21 г), біс-(2-брометил)етер (1,30 мл) і N, Nдіізопропілетиламін (4,64 мл) перемішують в N, N-диметилформаміді (19 мл) і нагрівають до 180 °C протягом 30 хвилин в запаяній ампулі для мікрохвильової обробки. Додають насичений водний розчин бікарбонату (100 мл) і сиру суміш екстрагують етилацетатом (100 мл). Органічну фазу промивають водою (100 мл) і сольовим розчином (100 мл), сушать над сульфатом натрію і концентрують у вакуумі. Сирий продукт очищають, використовуючи флеш-хроматографію, отримуючи 1,78 г (63 %) вказаної в заголовку сполуки у вигляді твердої речовини жовтого + 1 кольору. РХ-МС (m/z) 326 (МН ); tR=2,54, (UV, ELSD) 83 %, 75 %. H ЯМР (500 МГц, ДМСОd6):2,99 (м, 4Н), 3,70 (м, 4Н), 5,00 (с, 2Н). 7,00 (д, 1Н), 7,38 (д, 1Н). 2,5-Діаміно-3-хлорбензонітрил Водну хлористоводневу кислоту (12 М, 5,3 мл) поволі додають до суміші цинкового порошку (2,01 г) і 2-аміно-3-хлор-5-нітробензонітрилу (0,50 г) в тетрагідрофурані (40 мл). Реакційну суміш перемішують протягом 2 годин, нейтралізують, використовуючи насичений водний розчин карбонату натрію (50 мл), і екстрагують етилацетатом (3 × 50 мл). Об'єднані органічні фази сушать над сульфатом натрію і концентрують у вакуумі, отримуючи 0,42 г (99 % вихід) вказаної в заголовку сполуки у вигляді твердої речовини червоного кольору. 'Н ЯМР (500 МГц, ДМСОd6):4,89 (с, 2Н), 5,13 (с, 2Н), 6,64 (д. 1Н), 6,89 (д, 1Н). 2-Аммо-3-хлор-5-морфолін-4-ілбензонітрил 2,5-Діаміно-З-хлорбензонітрил (387 мг), біс-(2брометил)етер (0,35 мл) і N, N-діізопропілетиламін (1,25 мл) перемішують в N, Nдиметилформаміді (4 мл) і нагрівають до 180 °C протягом 30 хвилин в запаяній ампулі для мікрохвильової обробки. Додають, насичений водний розчин бікарбонату (20 мл) і сиру суміш екстрагують етилацетатом (20 мл). Органічну фазу промивають водою (20 мл) і сольовим розчином (20 мл), сушать над сульфатом натрію і концентрують у вакуумі, отримуючи 0,50 г (91 %) вказаної в заголовку сполуки у вигляді твердої речовини коричневого кольору. РХ-МС + (m/z) 238 (МH ); 1 tR=2,31, (UV, ELSD) 85 %, 95 %. H ЯМР (500 МГц. ДМСО-d6):2,97 (м, 4Н), 3,69 (м, 4Н), 5,59 (с, 2Н), 7,04 (д, 1Н), 7,29 (д, 1Н). трет-Бутиловий естер [2-(4-фторфеніл)-2-гідроксіетил]карбамінової кислоти До перемішуваного розчину wpew-бутилового естеру карбамінової кислоти (0,22 г) в ацетонітрилі (6 мл) додають послідовно при 0 °C: гідроксид натрію (52 мг) у воді (5 мл); через 2 хвилини wpew-бутилгіпохлорит (139 мкл); через 10 хвилин дигідрат осмату(УІ) калію (9 мг) у воді (1 мл); через 1 хвилину гідрохінін (антрахінон-1,4-дііл)діетер (26 мг) в ацетонітрилі (4 мл); через 3 хвилини ацетонітрил (6,7 мл) і фосфатний буфер (3,3 мл, 0,5 М, рН 7,65); через 5 21 UA 102517 C2 5 10 15 20 25 30 35 40 45 50 55 60 хвилин достатню кількість моногідрату біфосфату натрію, щоб довести до рН 7,65; і, нарешті, 4фторстирол. Реакцію гасять після перемішування протягом 3 годин при 25 °C, використовуючи сульфіт натрію (0,20 г) у воді (2 мл), при 0 °C. Фази розділяють і водний шар екстрагують етилацетатом (3 × 20 мл). Об'єднані органічні фази промивають водою (1 × 50 мл), сушать над сульфатом натрію, концентрують у вакуумі та очищають, використовуючи флешхроматографію, отримуючи 90 мг (57 %) вказаної в заголовку сполуки у вигляді безбарвної 1 оливи. Н ЯМР (500 МГц, CDCla):1,45 (с, 9Н), 3,18 (м, 1Н), 3,23 (м, 1Н), 3,44 (м, 1Н), 4,83 (м, 1Н), 4,92 (шир.с, 1Н), 7,04 (т, 2Н). 7,34 (м, 2Н). Наступні сполуки отримують аналогічним чином: трет-Бутиловий естер [2-гідрокси-2-(4-трифторметилфеніл)етил]карбамінової кислоти 1 Вихід: 82 %. Н ЯМР (500 МГц, СDСl3):1,44 (с. 9Н). 3,26 (м, 1Н), 3,52 (м, 2Н), 4,40 (шир.с, 1Н), 4,92 (шир.с, 1Н), 7,49 (д, 2Н), 7,61 (д, 2Н). трет-Бутиловий естер [2-(2-хлорфеніл)-2-гідроксіетил]карбамінової кислоти 1 Вихід: 61 %. Н ЯМР (500 МГц, СDСl3):1,44 (с, 9Н), 3,32 (м, 1Н), 3,51 (м, 1Н), 4,23 (м, 1Н), 5,08 (шир.с, 1Н), 5,19 (шир.с, 1Н), 7,20 (м, 1Н). 7,28 (м, 1Н), 7.59 (м. 1Н). 2-(4-Фторфеніл)морфолін Розчин трет-бутилового естеру [2-(4-фторфеніл)-2-гідроксіетил]карбамінової кислоти (90 мг) в дихлорметані (1 мл) і трифтороцтову кислоту (1 мл) перемішують при 25 °C протягом 1 години і потім концентрують у вакуумі. Залишок розділяють між етилацетатом (5 мл) і насиченим водним розчином карбонату калію (5 мл). Органічну фазу сушать над сульфатом натрію, концентрують у вакуумі і знову розчиняють в сухому тетрагідрофурані (3 мл) і триетиламіні (54 мкл). Хлорацетилхлорид (31 мкл) в сухому тетрагідрофурані (1 мл) додають по краплях при 0 °C. Через 30 хвилин реакційну суміш розбавляють етилацетатом (10 мл) і промивають сумішшю вода/сольовий розчин (1:1, 3 10 мл). Органічну фазу сушать над сульфатом натрію, концентрують у вакуумі і знову розчиняють в трет-бута.їіол.і (5 мл). Додають трет-бутоксид калію (79 мг) і реакційну суміш перемішують при 25 °C протягом 1,5 години. Реакцію гасять насиченим водним розчином амонію хлориду (30 мл) і екстрагують етилацетатом (2 30 мл). Об'єднані органічні фази сушать над сульфатом натрію, концентрують у вакуумі і випаровують разом з толуолом (2 5 мл). Залишок розчиняють в сухому толуолі (5 мл) в атмосфері аргону і обробляють біс(2-метоксіетокси)алюмогідридом натрію (70 % в толуолі, 205 мкл) по краплях і перемішують при 25 °C протягом 5 годин. Реакцію гасять при 0 °C, використовуючи 10 % водний розчин гідроксиду натрію (5 мл), і отриману суміш екстрагують діетиловим етером (2 15 мл). Об'єднані органічні фази сушать над сульфатом натрію і концентрують у вакуумі, отримуючи 60 мг (94 %) вказаної в заголовку сполуки у вигляді безбарвної оливи. + РХ-МС (m/z) 182 (МН ); tR=1,06, (UV, ELSD) 78 %, 98 %. Наступні сполуки отримують аналогічним чином: 2- (4- Трифторфеніл)морфоліл + Вихід: 85 %. РХ-МС (m/z) 232 (МН ); tR=l, 59, (UV, ELSD) 79 %, 99 %. 2-(2-Хлорфеніл)морфолін + Вихід: 86 %. РХ-МС (m/z) 198 (МН ); tR=1,21, (UV, ELSD) 66 %, 99 %. 4-Бром-2-метокси-6-метилфеніламін До 2-метокси-б-метилфеніламіну (10,0 г), розчиненого в ацетонітрилі (200 мл), додають TVбромсукцинімід (14,3 г) і реакційну суміш нагрівають до 145 °C протягом 15 хвилин в запаяній ампулі для мікрохвильової обробки. Сиру суміш фільтрують через Celite, розбавляють діетиловим етером (200 мл), промивають гідроксидом натрію (2М, 2 100 мл) і сольовим розчином (1 100 мл). Органічну фазу сушать над сульфатом магнію, концентрують у вакуумі і очищають, використовуючи флеш-хроматографію, отримуючи 3,4 г (26 %) вказаної в заголовку сполуки у вигляді твердої речовини чорного кольору. Н ЯМР (500 МГц, ДМСО-d6):2,06 (с, 3Н), 3,77 (с, ЗН), 4,55 (с, 2Н), 6,78 (д, 1Н), 6,82 (д, 1Н). Наступну сполуку отримують аналогічним чином: 4-Бром-2-метил-б-трифторметилфеніламін + Вихід: 80 %. GC-MS (m/z) 254 (М ); tR=3,73. 2-Метокси-6-метил-4-морфолін-4-ілфеніламін Біс(дибензиліденацетон)паладій (0,63 г) і (2'-дициклогексилфосфанілбіфеніл-2-іл)диметиламін (0,68 г) додають до сухого толуолу (100 мл, очищений аргоном) і перемішують протягом 15 хвилин в атмосфері аргону. Послідовно додають трет-бутоксид калію (3,70 г), морфолін (4,0 мл) і 4-бром-2-метокси-6-метилфеніламін (3,40 г). Реакційну суміш нагрівають при кипінні із зворотним холодильником протягом 16 годин в атмосфері аргону, охолоджують і фільтрують через діоксид кремнію (50 г). Додають гідроксид натрію (2 М, 200 мл) і суміш екстрагують етилацетатом (3 200 мл). Об'єднані органічні фази промивають сольовим 22 UA 102517 C2 5 10 15 20 25 30 35 40 45 50 55 розчином (1 200 мл), сушать над сульфатом магнію і концентрують у вакуумі. Сирий продукт очищають, використовуючи флеш-хроматографію, отримуючи 1,0 г (29 % вихід) вказаної в 1 заголовку сполуки у вигляді оливи чорного кольору. H ЯМР (500 МГц, ДМСО-d6):2,05 (с, 3Н), 2,91 (т, 4Н), 3,69 (т, 4Н), 3,74 (с, 3Н), 3,95 (с, 2Н), 6,23 (д, 1Н), 6,39 (д, 1Н). Наступну сполуку отримують аналогічним чином: 2-Метил-4-морфолін-4-іл-б-трифторметилфеніламін 1 Вихід: 28 %. H ЯМР (500 МГц. ДМСО-d6):2,13 (с, 3Н), 2,93 (т, 4Н), 3,70 (т, 4Н), 4.67 (с, 2Н), 6,75 (д, 1Н), 6,99 (д, 1Н). 4-(3,5-Дифтор-4-нітрофеніл)морфолін 2,4,6-трифторнітробензол (4,95 г) і карбонат калію (4,63 г) змішують в сухому диметилсульфоксиді (40 мл) і охолоджують до 10 °C в атмосфері аргону. Додають морфолін (2,56 мл), реакційну суміш залишають нагріватися до 25 °C і перемішують в атмосфері аргону протягом 16 годин. Реакційну суміш концентрують у вакуумі. Додають сольовий розчин (50 мл) і продукт екстрагують етилацетатом (3 × 50 мл). Об'єднані органічні фази сушать над сульфатом магнію і концентрують у вакуумі. Сирий матеріал очищають, використовуючи флешхроматографію, отримуючи 2,49 г (37 % вихід) вказаної в заголовку сполуки у вигляді твердої 1 речовини жовтого кольору. Н ЯМР (500 МГц, ДМСО-d6):3,43 (т, 4Н), 3,69 (т, 4Н), 6,87 (д, 2Н). 2,6-Дифтор-4-морфолін-4-ілфеніламін Концентровану хлористоводневу кислоту (4,2 мл) поволі додають до суміші цинкового порошку (3,3 г) і 4-(3,5-дифтор-4-нітрофеніл)морфоліну (2,49 г) в тетрагідрофурані (40 мл), охолодженому до 0 °C. Потім реакційну суміш перемішують протягом 1 години при 0 °C і протягом 2 годин при 25 °C. Реакційну суміш фільтрують через Celite (10 г), концентрують у вакуумі і очищають, використовуючи флеш-хроматографію, отримуючи 1,96 г (90 % вихід) + вказаної в заголовку сполуки у вигляді твердої речовини білого кольору. GC-MS (m/z) 214 (М ); 1 tR=5,83. H ЯМР (500 МГц, ДМСО-d6); 2,94 (т, 4Н), 3.69 (т, 4Н), 4,53 (с, 2Н), 6,57 (м, 2Н). 2-Хлор-4-нітро-6-трифторметилфеніламін 4-Нітро-2-трифторметилфеніламін (5,6 г) і N-хлорсукцинімід (4,0 г) суспендують в ацетонітрилі (15 мл) і нагрівають до 150 °C протягом 10 хвилин в запаяній ампулі для мікрохвильової обробки. Додають етилацетат (80 мл) і органічну фазу промивають 5 % водним розчином NAOH (2 50 мл), водою (2 50 мл) і сольовим розчином (2 50 мл). Органічну фазу сушать над сульфатом магнію і концентрують у вакуумі. Сирий продукт очищають, використовуючи флеш-хроматографію, отримуючи 4,9 г (75 % вихід) вказаної в заголовку 1 сполуки у вигляді твердої речовини жовтого кольору. Н ЯМР (500 МГц, СDСl3):5,35 (шир.с. 2Н). 8,35 (шир.с, 1Н), 8,37 (шир.с, 1Н). Наступну сполуку отримують аналогічним чином: 2-Хлор-6-метил-4-нітрофеніламін 1 Вихід: 95 %. Н ЯМР (500 МГц, ДМСО-d6):2,22 (с, 3Н), 6,56 (шир.с, 2Н), 7,89 (д, 1Н), 8,00 (д, 1Н). N-(2-Xлop-6-мeтил-4-нiтpoфeнiл)-2-циклопентилацетамід 2-хлор-6-метил-4-нітрофеніламін (6,0 г) і циклопентилацетилхлорид (5,1 г) розчиняють в ацетонітрилі (45 мл) і нагрівають до 150 °C протягом 20 хвилин в запаяній ампулі для мікрохвильової обробки. Реакційну суміш охолоджують до 0 °C, продукт, що випав в осад, збирають фільтруванням і промивають холодним ацетонітрилом, отримуючи 5,5 г (58 %) 1 вказаної в заголовку сполуки у вигляді твердої речовини жовтого кольору. Н ЯМР (500 МГц, ДМСО-d6):1,24 (м, 2Н), 1,58 (м, 4Н). 1,78 (м, 2Н), 2,27 (м, 1Н), 2,30 (с, 3Н), 2,38 (д, 2Н), 8,15 (д, 1Н), 8,18 (д, 1Н), 9,83 (с, 1Н). Наступну сполуку отримують аналогічним чином: N-(2-Xлop-6-метил-4-нiтpoфeнiл)-2-(3-фтopфeніл)aцeтaмiд 1 Вихід: 72 %. Н ЯМР (500 МГц, ДМСО-d6):2,24 (с, 3Н), 3,77 (с. 2Н), 7,10 (дт, 1Н), 7,21 (м, 2Н), 7,39 (м, 1Н), 8,14 (д, 1Н), 8,19 (д. 1Н), 10,15 (с, 1Н). 2-Хлор-6-трифторметилбензол-1,4-діамін Оцтову кислоту (13 мл) поволі додають до суміші цинкового порошку (12,4 г) і 2-хлор-4нітро-б-трифторметилфеніламіну (4 г) в тетрагідрофурані (40 мл). Реакційну суміш перемішують протягом 1 години, фільтрують через діоксид кремнію і концентрують у вакуумі. Сирий продукт очищають, використовуючи флеш-хроматографію, отримуючи 2,9 г (83 %) вказаної в заголовку 1 сполуки у вигляді твердої речовини чорного кольору. Н ЯМР (500 МГц, CDCI3):3,44 (шир.с, 2Н), 4.16 (шир.с, 2Н), 6.77 (д, 1Н), 6,86 (д, 1Н). Наступні сполуки отримують аналогічним чином: N-(4-Аміно-2-хлор-6-метилфеніл)-2-циклопентилацетамід 23 UA 102517 C2 1 5 10 15 20 25 30 35 40 45 50 55 60 Вихід: 69 %. Н ЯМР (500 МГц, ДМСО-d6):1,21 (м, 2Н), 1,57 (м, 4Н), 1,76 (м, 2Н), 2,00 (с, 3Н), 2,23 (д, 2Н), 2,26 (м, 1Н), 5,23 (с, 2Н), 6,36 (д, 1Н), 6,48 (д, 1Н), 8,98 (с, 1Н). N-(4-Амто-2-хлор-б-метилфеніл)-2-(3-фторфеніл)ацетамід 1 Вихід: 88 %. Н ЯМР (500 МГц, ДМСО-d6):1,90 (с, ЗН), 3,62 (с, 2Н), 5,26 (с, 2Н), 6,35 (д, 1Н), 6.49 (д, 1Н), 7,07 (дт, 1Н), 7,20 (м, 2Н), 7,37 (м, 1Н), 9,34 (с, 1Н). 2-Хлор-4-морфолін-4-іл-6-трифторметилфеніламін 2-Хлор-6-трифторметилбензол-1,4-діамін (2,9 г), біс-(2-хлоретил)етер (1,7 мл) і йодид натрію (516 мг) змішують в ацетонітрилі (45 мл) і нагрівають до 165 °C протягом 1 години в запаяній ампулі для мікрохвильової обробки. Сиру суміш концентрують у вакуумі, знову розчиняють в етилацетаті (100 мл), промивають водою (2 100 мл) і сольовим розчином (1 100 мл). Органічну фазу сушать над сульфатом магнію і концентрують у вакуумі. Сирий продукт очищають, використовуючи флеш-хроматографію, отримуючи 940 мг (24 %) вказаної в заголовку сполуки у вигляді оливи чорного кольору. 1 Н ЯМР (500 МГц. СDСl3):3,02 (м, 4Н), 3,84 (м, 4Н), 4,30 (шир.с, 2Н), 6,97 (д, 1Н), 7,06 (д, 1Н). N-(2,6-Діізопропіл-4-нітрофеніл)-4-метилбензолсульфонамід 2,6-діізопропілфеніламін (1,80 мл) і пара-толуолсульфонілхлорид (2,00 г) розчиняють в піридині (4 мл) і нагрівають до 160 °C протягом 10 хвилин в запаяній ампулі для мікрохвильової обробки. Отриману суспензію розбавляють етилацетатом (10 мл) і промивають хлористоводневою кислотою (2М, 10 мл) і сольовим розчином (10 мл). Органічну фазу сушать над сульфатом натрію, концентрують у вакуумі і суспендують в 65 % азотній кислоті (15 мл) і воді (60 мл). Послідовно додають оцтову кислоту (60 мл) і нітрит натрію (0,99 г) і реакційну суміш нагрівають до 100 °C протягом 12 годин. Отриману суміш охолоджують до 25 °C, виливають в крижану воду (200 мл) і фільтрують, отримуючи 2,07 г (58 %) вказаної в заголовку сполуки у вигляді твердої речовини жовтого кольору, 'Н ЯМР (500 МГц, СDСl 3):1,06 (д, 12Н), 2.43 (с, 3Н), 3,19 (м, 2Н), 6,29 (с, 1Н), 7,28 (д, 2Н), 7,59 (д, 2Н), 7,97 (с, 2Н). N-(4-Аміно-2,6-діізопропілфеніл}-4-метилбензолсульфонамід До суспензії N-(2,6-діізопропіл-4-нітрофеніл)-4-метилбензолсульфонаміду (3,72 г) у етанолі (50 мл) додають дигідрат хлориду олова (ІІ) (11,2 г) і отриману суміш нагрівають до 80 °C протягом 1,5 години. Потім її виливають на лід (300 мл), сильно підлужують, використовуючи твердий гідроксид натрію (20 г), і розбавляють етилацетатом (100 мл). Суспензію фільтрують і екстрагують етилацетатом (3 100 мл). Об'єднані органічні фази сушать над сульфатом натрію і концентрують у вакуумі. Сирий продукт очищають, використовуючи флеш-хроматографію, отримуючи 2,60 г (76 %) вказаної в заголовку 1 сполуки у вигляді твердої речовини не зовсім білого кольору. Н ЯМР (500 МГц, CDCh): 0,95 (д, 12Н), 2,40 (с, ЗН), 3,02 (м, 2Н), 3.68 (шир.с, 2Н), 5,74 (с, 1Н), 6,39 (с, 2Н). 7,23 (д, 2Н),7,60(д, 2Н). 2,6-Діізопропіл-4-морфолін-4-ілфеніламін Суміш N-(4-аміно-2,6-діізопропілфеніл)-4-метилбензолсульфонаміду (346 мг), біс-(2брометил)етеру (151 мкл), N, N-діізопропілетиламіну (0,53 мл) і N-метилпіролідину (1,0 мл) нагрівають до 180 °C протягом 20 хвилин в запаяній ампулі для мікрохвильової обробки. Отриману суміш розбавляють етилацетатом (20 мл), промивають сольовим розчином (30 мл) і насиченим водним розчином карбонату калію (30 мл) і сушать над сульфатом натрію. Органічну фазу концентрують у вакуумі і знову розчиняють в суміші сірчаної кислоти (1,9 мл) і води (0,1 мл) і перемішують при 40 °C протягом 3 годин. Додають лід (30 мл) і воду (30 мл) і отриману суміш підлужують, використовуючи твердий карбонат калію. Отриману суміш екстрагують етилацетатом (3 20 мл), об'єднані органічні фази сушать над сульфатом натрію і концентрують у вакуумі, отримуючи 260 мг (99 %) вказаної в заголовку сполуки у вигляді твердої 1 речовини білого кольору. H ЯМР (500 МГц, СDСl3):1,26 (д, 12Н), 2,95 (м, 2Н), 3,06 (м, 4Н), 3,49 (шир.с, 2Н), 3,87 (м, 4Н), 6,69 (с, 2Н). N-(2,6-Діетил-4-нітрофеніл)-4-метилбензолсульфонамід 2,6-Діетилфеніламін (1,57 мл) і пара-толуолсульфонілхлорид (2,00 г) розчиняють в піридині (4 мл) і нагрівають до 160 °C протягом 10 хвилин в запаяній ампулі для мікрохвильової обробки. Отриману суспензію розбавляють етилацетатом (10 мл), промивають хлористоводневою кислотою (2 М, 10 мл) і сольовим розчином (10 мл). Органічну фазу сушать над сульфатом натрію, концентрують у вакуумі і суспендують в 65 % азотній кислоті (15 мл) і воді (60 мл). Послідовно додають оцтову кислоту (60 мл) і нітрит натрію (0,99 г) і реакційну суміш нагрівають при 100 °C протягом 12 годин. Отриману суміш охолоджують до 25 °C і виливають в крижану воду (200 мл), підлужують, використовуючи твердий гідроксид натрію, і екстрагують етилацетатом (3 50 мл). Об'єднані органічні фази промивають сольовим розчином (1 100 мл), сушать над сульфатом натрію і концентрують у вакуумі, отримуючи 0,31 г (9 %) вказаної в 24 UA 102517 C2 5 10 15 20 25 30 35 40 45 50 55 60 заголовку сполуки у вигляді сиропу жовтого кольору. 'Н ЯМР (500 МГц, ДМСО-(іб):0,98 (т, 6Н), 2,34 (с, 3Н), 3,30 (м, 4Н), 7,25 (д, 2Н), 7,52 (д, 2Н), 7,80 (с, 2Н). N-(4-Аміно-2,6-діетилфеніл)-4-метилбензолсульфонамід Розчин дитіоніту натрію (772 мг) у воді (6 мл) додають до розчину N-(2,6-діетил-4нітрофеніл)-4-метилбензолсульфонаміду (309 мг) у тетрагідрофурані (6 мл) і отриману суміш перемішують при 50 °C протягом 20 годин. Після охолоджування воду насичують карбонатом калію і екстрагують етилацетатом (2 10 мл). Об'єднані органічні фази сушать над сульфатом натрію, концентрують у вакуумі і очищають, використовуючи флеш-хроматографію, отримуючи 70 мг (25 %) вказаної в заголовку сполуки у вигляді твердої речовини не зовсім білого кольору. Продукт використовують безпосередньо в наступній реакції без отримання спектральних характеристик. N-(2,6-Діетил-4-морфолін-4-ілфеніл)-4-метилбензолсульфонамід Суміш N-(4-аміно-2,6-діетилфеніл)-4-метилбензолсульфонаміду (70 мг), біс-(2брометил)етеру (33 мкл), N, N-діізопропілетиламіну (115 мкл) і N-метилпіролідину (0,3 мл) нагрівають до 180 °C протягом 20 хвилин в запаяній ампулі для мікрохвильової обробки. Отриману суміш розбавляють етилацетатом (20 мл), промивають сольовим розчином (30 мл), насиченим водним розчином карбонату калію (30 мл) і сушать над сульфатом натрію. Органічну фазу концентрують у вакуумі, отримуючи 78 мг (91 %) вказаної в заголовку сполуки. РХ-МС + (m/z) 389 (MН ); tR=2.77, (UV, ELSD) 57 %, 98 %. Сирий продукт використовують без подальшого очищення. (3,4-Дифторфеніл)ацетилхлорид До (3,4-дифторфеніл)оцтової кислоти (2,0 г), розчиненої в 1,2-дихлоретані (5 мл), додають тіонілхлорид (5 мл) і отриману суміш кип'ятять із зворотним холодильником протягом 16 годин в атмосфері аргону. Сиру суміш концентрують у вакуумі, отримуючи 2,2 г (100 %) вказаної в 1 заголовку сполуки у вигляді оливи жовтого кольору. Н ЯМР (500 МГц, СDСl3):4,10 (с, 2Н), 7,00 (м, 1Н), 7,11 (м, 1Н), 7,17 (м, 1Н). Наступну сполуку отримують аналогічним чином: (3-Фторфеніл) ацетилхлорид 1 Вихід: 99 %. Н ЯМР (500 МГц, СDСl3):4,13 (с, 2Н). 6,92 (м, 1Н), 7,01 (м, 2Н), 7,34 (м, 1Н). Сполуки цього винаходу Кислотно-адитивні солі сполук цього винаходу можна легко отримати, використовуючи способи, відомі фахівцям в даній галузі. Приклад 1 1a. N-(2-Бром-4-морфолін-4-іл-6-трифторметилфеніл)-2-(4-фторфеніл)ацетамід 2-бром-4морфолін-4-іл-6-трифторметилфеніламін (0,236 г) і 4-фторфенілацетилхлорид (0,105 мл) розчиняють в ацетонітрилі (5 мл) і нагрівають до 150 °C протягом 10 хвилин в запаяній ампулі для мікрохвильової обробки. Додають воду (25 мл) і продукт екстрагують етилацетатом (3 25 мл). Органічні фази промивають сольовим розчином (50 мл), сушать над сульфатом магнію і концентрують у вакуумі. Сирий продукт очищають, використовуючи флеш-хроматографію, отримуючи 0,027 г (9 %) вказаної в заголовку сполуки у вигляді твердої речовини не зовсім + білого кольору. РХ-МС (m/z) 462 (МH ); 1 tR=2,84, (UV, ELSD) 96 %, 100 %. Н ЯМР (500 МГц, ДМСО-d6):3,23 (м, 4Н), 3,62 (с, 2Н). 3,72 (м, 4Н), 7,14 (дд, 2Н), 7,19 (д, 1Н). 7,35 (дд, 2Н), 7,46 (д, 1Н), 9,78 (с, 1Н). Наступні сполуки отримують аналогічним чином: 1b. 2-Циклопентил-N-(2-бром-6-трифторметил-4-морфолін-4--ілфеніл)ацетамід Вихід: 22 %. + 1 PX-MCS (m/z) 436 (МН ); tR=2,95, (UV, ELSD) 97 %, 98 %. Н ЯМР (500 МГц, ДМСО-d6):1,20 (м, 2Н), 1,50 (м, 2Н), 1,60 (м, 2Н), 1,77 (м, 2Н), 2,24 (м, 1Н), 2,26 (д, 2Н), 3,23 (м, 4Н), 3,72 (м, 4Н), 7,19 (д. 1Н), 7,46 (д, 1Н), 9,46 (с, 1Н). 1с. N-(2-Бром-4-морфолін-4-іл-6-трифторметилфеніл)-3-циклопентилпропіонамід Вихід: + 1 20 %. РХ-МС (m/z) 450 (МН ); tR=3,20, (UV, ELSD) 99 %. 98 %. Н ЯМР (500 МГц, ДМСО-d6):1,09 (м, 2Н), 1.49 (м, 2Н), 1,59 (м, 4Н), 1.76 (м, 2Н), 1,80 (м, 1Н). 2,27 (т, 2Н), 3,22 (м, 4Н), 3,72 (м, 4Н), 7,18 (д, 1Н), 7,46 (д, 1Н), 9,48 (с, 1Н). 1d. N-(2-Хлор-6-ціано-4-морфолін-4-ілфеніл)-3-циклогексилпропіонамід Вихід: 24 %. РХ-МС + 1 (m/z) 376 (МН ); tR=3,10, (UV, ELSD) 98 %, 100 %. Н ЯМР (500 МГц, ДМСО-d6):0,90 (м, 2Н), 1,23 (м, 4Н). 1,51 (м, 2Н), 1.64 (м, 1Н), 1,70 (м, 4Н), 2,33 (т, 2Н), 3,22 (м, 4Н), 3,71 (м, 4Н), 7,37 (с, 2Н), 9,79 (с, 1Н). 1е. N-(2-Бром-4-морфолін-4-іл-6-трифторметилфеніл)-3-циклогексилпропіонамід Вихід: + 1 19 %. РХ-МС (m/z) 464 (MH ); tR=3,38, (UV, ELSD) 97 %, 99 %. H ЯМР (500 МГц, ДМСО-d6):0,86 (дк, 2Н), 1,16 (м, ЗН), 1,27 (м. 1Н), 1,48 (к, 2Н). 1,61 (м, 1Н), 1,70 (м, 4Н), 2,27 (т, 2Н), 3,23 (м, 4Н), 3,72 (м, 4Н), 7,18 (д, 1Н), 7,46 (д, 1Н), 9,47 (с, 1Н). 25 UA 102517 C2 5 10 15 20 25 30 35 40 45 50 55 60 1f. N-(2-Бром-4-морфолін-4-іл-6-трифторметилфеніл)-2-(3-фторфеніл)ацетамід Вихід: 44 %. + РХ-МС (m/z) 462 (МН ); tR=2,85, (UV, ELSD) 98 %, 99 %. 1Н ЯМР (500 МГц, ДМСО-d6):3,23 (м, 4Н), 3,67 (с, 2Н), 3,72 (м, 4Н), 7,10 (м, 2Н). 7,18 (м, 2Н), 7,36 (м, 1Н), 7,46 (м, 1Н), 9,82 (с, 1Н). 1g. N-(2-Бром-4-морфолін-4-іл-6-трифторметилфеніл)пропіонамід Вихід: 41 %. РХ-МС (m/z) + 1 382 (МН ); tR=2,16, (UV, ELSD) 99 %, 99 %. Н ЯМР (500 МГц, ДМСО-d6):1,09 (т, 3Н), 2,27 (к. 2Н), 3,23 (м, 4Н), 3,72 (м, 4Н), 7,19 (д, 1Н), 7,47 (д, 1Н),9,46(с, 1Н). 1h. N-(2-Бром-4-морфолін-4-іл-6-трифторметилфеніл)бутирамід Вихід: 76 %. РХ-МС (m/z) + 6 396 (NН ); tR-2,43, (UV, ELSD) 99 %, 96 %. 1Н ЯМР (500 МГц, ДМСО-d ):0,93 (т, 3Н), 1.60 (м, 2Н), 2,24 (т, 2Н), 3,23 (м, 4Н), 3,72 (м, 4Н). 7,18 (д, 1Н),7,46(д, 1Н),9,45(с, 1Н). 1h. N-(2-Хлор-4-морфолін-4-іл-6-трифторметилфеніл)-2-(3-фторфеніл)ацетамід + 1 Вихід: 21 %. РХ-МС (m/z) 417 (MH ); tR=2,84, (UV, ELSD) 97 %. 99 %. H ЯМР (500 МГц, ДМСО-d6):3,23 (м, 4Н), 3,67 (с, 2Н), 3,72 (м, 4Н), 7,07 (дт, 1Н), 7,15 (м, 3Н), 7,32 (д, 1Н), 7,36 (м, 1Н), 9,76 (с, 1Н). 1i. N-(2-Хлор-4-морфолін-4-іл-6-трифторметилфеніл)-2-циклопентилацетамід Вихід: 76 %. + 1 РХ-МС (m/z) 391 (МН ); tR=2,97, (UV, ELSD) 99 %, 99 %. H ЯМР (500 МГц, ДМСО-d6):1,19 (м, 2Н), 1,50 (м, 2Н), 1,60 (м, 2Н), 1,76 (м, 2Н), 2,23 (м, 1Н), 2,26 (д, 2Н), 3,23 (м, 4Н), 3,72 (м, 4Н), 7,15 (д, 1Н), 7,32 (д, 1Н), 9,40 (с, 1Н). Приклад 2 2а. 2-Циклопентил-Н-(2,6-диметил-4-тіоморфолін-4-ілфеніл)ацетамід Біс(дибензиліденацетон)паладій (37 мг) і (2'-дициклогексилфосфанілбіфеніл-2-іл)диметиламін (38 мг) змішують в сухому дегазованому толуолі (2 мл) в атмосфері аргону протягом 5 хвилин. До цієї суміші додають N-(4-бром-2,6-диметилфеніл)-2-циклопентилацетамід (200 мг), третбугоксид, калію (90 мг) і тіоморфолін (80 мг) і реакційну суміш нагрівають до 90 °C в запаяній 4 мл ампулі в атмосфері аргону протягом 16 годин, охолоджують і фільтрують через діоксид кремнію (2 г). Додають суміш вода/сольовий розчин (1:1, 4 мл усього) і отриману суміш екстрагують етилацетатом (32 мл). Об'єднані органічні фази сушать над сульфатом магнію і концентрують у вакуумі. Сирий продукт очищають, використовуючи препаративну РХ-МС, + отримуючи 5,6 мг (3 % вихід) вказаної в заголовку сполуки. LC-MS-TOF (m/z) 333 (МН ); tR=2,03, (UV, ELSD) 98 %, 100 %. Наступні сполуки отримують аналогічним чином: 2b. 2-Циклопентил-N-[2,6-диметгиі-4-(2-фенілморфолін-4-іл) феніл] ацетамід Вихід: 3 %. LC+ MS-TOF (m/z) 393 (МН ); tR=3,l 1, (UV, ELSD) 96 %, 98 %. 2 с. 2-Циклопентил-N-[2,6-диметил-4(2-фенілтіоморфолін-4-іл)феніл]ацетамід + Вихід: 4 %. LC-MS-TOF (m/z) 409 (МН ); tR=3,30, (UV, ELSD) 99 %, 98 %. 2d. 2-Циклопентил-N-[2,6-диметил-4-(3-піридин-3-іл-тіоморфолін-4-іл)феніл] ацетамід Вихід: 12 %. LC-MS-TOF (m/z) 410 (МЇҐ); tR=2,00, (UV, ELSD) 99 %, 100 %. 2е. 2-Циклопентил-N-{2,6-диметил-4-[2-(4-трифторметилфеніл)тіоморфолін-4іл]феніл}ацетамід + Вихід: 6 %. РХ-МС (m/z) 477 (МН ); tR=3,64, (UV, ELSD) 95 %, 100 %. 2f. N-{4-[2-(2-Хлорфеніл)тіоморфолін-4-іл]-2,6-диметилфеніл}-2-циклопентилацетамід + Вихід: 20 %. LC-MS-TOF (m/z) 444 (МН ); tR=3,59, (UV, ELSD) 89 %, 100 %. 2g. 2-Циклопентил-N-{2,6-диметил-4-[2-(4-трифторметилфеніл)морфолін-4-іл]феніл} ацетамід + Вихід: 26 %. РХ-МС (m/z) 461 (MH ); tR=3,55, (UV, ELSD) 90 %, 95 %. 2h. N-{4-[2-(2-Хлорфеніл)морфолін-4-іл]-2,6-диметилфеніл}-2-циклопентилацетамід + Вихід: 35 %. РХ-МС (m/z) 427 (MH ); tR=3,44, (UV, ELSD) 77 %, 95 %. 2i. 2-Циклопентил-N-{4-[2-(4-фторфеніл)морфолін-4-іл]-2,6-диметилфеніл}ацетамід Вихід: 17 %. РХ-МС (m/z) 411 (МІҐ); tR=3,17, (UV, ELSD) 98 %, 99 %. Приклад 3 3а. 2-Біцикло[2.2.1]гепт-2-ил-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід Біцикло[2.2.1]гепт-2-илоцтову кислоту (0,41 г) нагрівають до 50 °C протягом 2 годин в атмосфері аргону в суміші 1:1 тіонілхлориду і 1,2-дихлоретану (10 мл усього). Розчинники видаляють у вакуумі і отриманий хлорангідрид знову розчиняють в ацетонітрилі (5 мл) і додають 2,6диметил-4-морфолін-4-ілфеніламін (0,50 г). Реакційну суміш нагрівають до 150 °C протягом 10 хвилин в запаяній ампулі для мікрохвильової обробки. Додають воду (25 мл) і продукт екстрагують етилацетатом (3 25 мл). Об'єднані органічні фази промивають сольовим розчином (50 мл), сушать над сульфатом магнію і концентрують у вакуумі. Сирий продукт очищають, використовуючи флеш-хроматографію, отримуючи 0,074 г (9 %) вказаної в заголовку + сполуки у вигляді твердої речовини не зовсім білого кольору. LC-MS-TOF (m/z) 343 (МН ); 1 tR=2,21, (UV, ELSD) 98 %, 100 %. H ЯМР (500 МГц, ДМСО-d6):1,14 (м, 4Н), 1,41 (м, 4Н), 1,90 (м, 26 UA 102517 C2 5 10 15 20 25 30 35 40 45 50 55 60 1Н), 2,02 (м, 1Н), 2,06 (с, 6Н), 2,10 (м, 1Н), 2,20 (м, 2H), 3,05 (м, 4Н), 3,71 (м, 4Н), 6,62 (с, 2Н), 8,92 (с, 1Н). Наступні сполуки отримують аналогічним чином: 3b. 2-Циклогексил-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід + 1 Вихід: 19 %. LC-MS-TOF (m/z) 331 (МН ); tR=2,21, (UV, ELSD) 97 %, 100 %. H ЯМР (500 МГц, ДМСО-d6):0,98 (м, 2H), 1,22 (м, 4Н), 1,68 (м, 6Н), 2,07 (с, 6Н), 2,15 (д, 2H), 3,05 (м, 4Н), 3,71 (м, 4Н), 6,63 (с, 2H), 8.93 (с, 1Н). 3с. 3(3,4-Дифторфеніл)-N-(2,6-диметил-4-морфолін-4-ілфеніл)пропіонамід Вихід: 40 %. LC1 MS-TOF (m/z) 375 (MH^); tR=2,39, (UV, ELSD) 97 %, 100 %. H ЯМР (500 МГц, ДМСО-сІб):1,95 (с, 6Н), 2,60 (т, 2H), 2,91 (т, 2H), 3,04 (м, 4Н), 3,71 (м, 4Н), 6,60 (с, 2H), 7,10 (м, 1Н), 7,34 (м, 2H), 8,97 (с, 1Н). Приклад 4 4а. 2-Циклопентил-Н-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід 2,6-диметил-4-морфолін4-ілфеніламін (0,50 г) і циклопентилацетилхлорид (0,53 мл) розчиняють в ацетонітрилі (5 мл) і нагрівають до 150 °C протягом 10 хвилин в запаяній ампулі для мікрохвильової обробки. Додають воду (25 мл) і продукт екстрагують етилацетатом (3 25 мл). Органічні фази промивають сольовим розчином (50 мл), сушать над сульфатом магнію і концентрують у вакуумі. Сирий продукт очищають, використовуючи флеш-хроматографію, отримуючи 0,1 38 г (20 %) вказаної в заголовку сполуки у вигляді твердої речовини не зовсім білого кольору. LCMS-TOF (m/z) 317 (МН4); tR=l, 93, (UV, ELSD) 95 %, 100 %. ^ ЯМР (500 МГц, ДМСО-сіб):1,21 (м, 2Н), 1,52 (м, 2Н), 1,61 (м, 2Н), 1,76 (м, 2Н), 2,07 (с, 6Н), 2,11 (м, 1Н), 2,25 (д, 2Н), 3,05 (дд, 4Н), 3,71 (дд, 4Н), 6,63 (с, 2Н), 8,94 (с, 1Н). Наступні сполуки отримують аналогічним чином: 4b. Бутиловий естер (2,6-диметил-4-морфолін-4-ілфеніл)карбамінової кислоти Вихід: 2 %. + LC-MS-TOF (m/z) 307 (МН ); tR=2,25, (UV/ELSD) 99 %, 100 %. 4с. 2-(4-Хлорфеніл)-М-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід Вихід: 8 %. LC-MS-TOF + (m/z) 359 (MH ); tR=2,16, (UV, ELSD) 98 %, 100 %. ^ ЯМР (500 МГц, ДМСО-сІб):2,01 (с, 6Н), 3,04 (дд, 4Н), 3,60 (с, 2Н), 3,71 (дд, 4Н), 6,62 (с, 2Н), 7,39 (м, 4Н), 9,24 (с, 1Н). 4d. (2,6-Диметил-4-морфолін-4-ілфеніл)амід 2,3-дигідробензофуран-2-карбонової кислоти + 1 Вихід: 13 %. LC-MS-TOF (m/z) 353 (МН4 ); tR-2,11, (UV, ELSD) 97 %, 100 %. H ЯМР (500 МГц, ДМСО-dб):2,01 (с, 6Н), 3,05 (дд, 4Н), 3,30 (м, 1Н), 3,55 (дд, 1Н), 3,71 (дд, 4Н), 5,31 (дд, 1Н), 6,64 (с, 2Н), 6,88 (т, 2Н), 7,15 (т, 1Н), 7,25 (д, 1Н), 9,33 (с, 1Н). 4е. 3-Циклогексил-Н-(2,6-диметил4-морфолін-4-ілфеніл)пропіонамід Вихід: 8 %. LC-MS-TOF {m/z) 345 (МЇҐ); tR=2,64, (UV, ELSD) 1 97 %, 98 %. H ЯМР (500 МГц, ДМСО-d6):0,88 (м, 2Н), 1,16 (м, 2Н), 1,25 (м, 2Н), 1,49 (к, 2Н), 1,63 (м, 1Н), 1,69 (м, 4Н), 2,06 (с, 6Н), 2,27 (т, 2Н), 3,05 (дд, 4Н), 3,71 (дд, 4Н), 6,63 (с, 2Н), 8,95 (с, 1Н). 4f. 3-Циклопентил-N-(2,6-диметил-4-морфолін-4-ілфеніл)пропіонамід Вихід: 34 %. РХ-МС + 1 (m/z) 331 (MH ); tR=2,33, (UV, ELSD) 97 %, 100 %. H ЯМР (500 МГц, ДМСО-d6):1,11 (м, 2Н), 1,49 (м, 2Н), 1,60 (м, 4Н), 1,77 (м, 2Н), 2,07 (с, 6Н), 2,28 (т, 2Н), 3,11 (дд, 4Н), 3,73 (дд, 4Н), 6,74 (с, 2Н), 9,01 (с, 1Н). 4g. N-(2,6-Диметил-4-морфолін-4-ілфеніл)-2-(4-фторфеніл)ацетамід + 1 Вихід: 13 %. LC-MS-TOF (m/z) 343 (MH ); tR=2,05, (UV, ELSD) 98 %, 100 %. H ЯМР (500 МГц, ДМСО-d6):2,01 (с, 6Н), 3,05 (м, 4Н), 3,59 (с, 2Н), 3,70 (м, 4Н), 6,61 (с, 2Н), 7,16 (дд, 2Н), 7,38 (дд, 2Н), 9,22 (с, 1Н). 4h. N-(2,6-Диметил-4-морфолін-4-ілфеніл)-2-тіофен-2-ілацетамід + Вихід: 3 %. LC-MS-TOF (m/z) 331 (МH ), tR=l, 94, (UV, ELSD) 97 %, 100 %. 4i. N-(2,6-Диметил-4-морфолін-4-ілфеніл)-3,3-диметилбутирамід + 1 Вихід: 43 %. LC-MS-TOF (m/z) 305 (МH ); tR=2,14, (UV, ELSD) 99 %, 100 %. H ЯМР (500 МГц, ДМСО-d6):1,05 (с, 9Н), 2,09 (с, 6Н), 2,17 (с, 2Н), 3,05 (м, 4Н), 3,72 (м, 4Н), 6,63 (с, 2Н), 8,89 (с, 1Н). 4j. (2,6-Диметил-4-морфолін-4-ілфеніл)амід гексанової кислоти Вихід: 14 %. РХ-МС (m/z) 305 + 1 (МН ); tR=1,99, (UV, ELSD) 95 %, 97 %. H ЯМР (500 МГц, ДМСО-d6):0,88 (т, 3Н), 1,31 (м, 4Н), 1,60 (м, 2Н), 2,06 (с, 6Н), 2,26 (т, 2Н), 3,05 (м, 4Н), 3,71 (м, 4Н), 6,63 (с, 2Н), 8,94 (с, 1Н). Приклад 5 5а. 2-Циклогептил-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід Циклогептилоцтову кислоту (0,45 г) і одну краплю N, N-диметилформаміду перемішують при 25 °C протягом 2 годин в атмосфері аргону в суміші 1:1 оксалілхлориду (2 М в дихлорметані) і 1,2-дихлоретану (12 мл усього). Розчинники видаляють у вакуумі і отриманий хлорангідрид знову розчиняють в ацетонітрилі (8 мл), додають 2,6-диметил-4-морфолін-4-ілфеніламін (0,50 г) і оксид магнію (0,20 г). Реакційну суміш перемішують при 25 °C протягом 16 годин в атмосфері 27 UA 102517 C2 5 10 15 20 25 30 35 40 45 50 55 60 аргону і потім фільтрують через Celite (10 г). Органічну фазу концентрують у вакуумі і сирий продукт очищають, використовуючи флеш-хроматографію, отримуючи 0,133 г (16 %) вказаної в + заголовку сполуки у вигляді твердої речовини не зовсім білого кольору. РХ-МС (m/z) 345 (МН ); 1 tR=2,36, (UV, ELSD) 97 %, 100 %. H ЯМР (500 МГц, ДМСО-d6):1,23 (м, 2Н), 1,44 (м, 4Н), 1,60 (м, 4Н), 1,73 (м, 2Н), 1,99 (м, 1Н), 2,07 (с, 6Н), 2,18 (д, 2Н), 3,05 (м, 4Н), 3,71 (м, 4Н), 6,63 (с, 2Н), 8,94 (с, 1Н). Приклад 6 6а. Бензиловий естер (2,6-диметил-4-морфолін-4-ілфеніл)карбамінової кислоти Бензилхлорформіат (32 мг) додають до розчину 0,15 М 2,6-диметил-4-морфолін-4-ілфеніламіну і 0,30 М N, N-діізопропілетиламіну в 1,2-дихлоретані (1 мл). Ампулу струшують протягом 16 годин і вміст концентрують у вакуумі. Додають водний розчин гідроксиду натрію (1 М, 2 мл) і сиру суміш екстрагують сумішшю ізопропілацетат/тетрагідрофуран (4:1, 2,5 мл). Органічну фазу концентрують у вакуумі і знову розчиняють в диметилсульфоксиді (0,5 мл), 0,2 мл якого обробляють, використовуючи препаративне очищення РХ-МС, отримуючи 9,5 мг (47 % вихід) + вказаної в заголовку сполуки у вигляді оливи. РХ-МС (m/z) 341 (MH ); tR=2,28, (UV, ELSD) 100 %, 100 %. Наступні сполуки отримують аналогічним чином: 6b. 2-Хлорбензиловий естер (2,6-диметил-4-морфолін-4-ілфеніл)карбамінової кислоти Вихід: 33 %. РХ-МС (m/z) 375 (МЇҐ), tp-2,53, (UV, ELSD) 99 %, 100 %. 6с. (2,6-Диметил-4-морфолін-4-ілфеніл)амід 3,5,5-триметилгексанової кислоти Вихід: 36 %. + РХ-МС (m/z) 347 (МH ); tR=2,53, (UV, ELSD) 99 %, 100 %. 6d. (2,6-Диметил-4-морфолін-4-ілфеніл)амід октанової кислоти Вихід: 47 %. РХ-МС (m/z) 333 + (МH ); tR=2,47, (UV, ELSD) 99 %, 100 %. 6е. (2,6-Диметил-4-морфолін-4-ілфеніл)амід гептанової кислоти Вихід: 40 %. РХ-МС (m/z) + 319 (МH ), tR=2,20, (UV, ELSD) 91 %, 99 %. 6f. N-(2,6-Диметил-4-морфолін-4-ілфеніл)-2-фенілацетамід Вихід: 35 %. РХ-МС (m/z) 325 + (МН ); tR=1,80, (UV, ELSD) 99 %, 100 % Приклад 7 7а. 2-(3,4-Дихлорфешл)-N-(2,6-диметил'4-морфолін-4-ілфеніл)ацетамід 3,4-Дихлорфенілоцтову кислоту (39 мг) перемішують при 25 °C протягом 2 годин в атмосфері аргону в суміші 1:1 оксалілхлориду (2 М в дихлорметані) і 1,2-дихлоретану (1 мл усього). Розчинники видаляють у вакуумі і до отриманого хлорангідриду додають розчин 0,15 М 2,6-диметил-4-морфолін-4-ілфеніламіну і 0,3 ОМ N, N-діізопропілетиламіну в 1,2-дихлоретані (1 мл). Ампулу струшують протягом 16 годин і вміст концентрують у вакуумі. Додають водний розчин гідроксиду натрію (1 М, 2 мл) і сиру суміш екстрагують сумішшю ізопропілацетат/тетрагідрофуран (4:1, 2,5 мл). Органічну фазу концентрують у вакуумі і знову розчиняють в диметилсульфоксиді (0,5 мл), 0,2 мл розчину обробляють, використовуючи препаративне очищення РХ-МС, отримуючи 2,7 мг (11 % вихід) вказаної в заголовку сполуки у + вигляді оливи. РХ-МС (m/z) 394 (МH ), tR=2,40, (UV, ELSD) 80 %, 100 %. Наступні сполуки отримують аналогічним чином: 7b. 2-(4-Алілокси-3-хлорфеніл)-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід + Вихід: 14 %. РХ-МС (m/z) 415 (МH ); tR=2,40, (UV, ELSD) 91 %, 100 %. 7с. N-(2,6-Диметил-4-морфолін-4-ілфеніл)-2-(3-трифторметилфеніл)ацетамід + Вихід: 18 %. РХ-МС (m/z) 393 (МH ); tR=2,31, (UV, ELSD) 97 %, 100 %. 7d. N-(2,6-Диметил-4-морфолін-4-ілфеніл)-2-нафтален-2-ілацетамід + Вихід: 16 %. РХ-МС (m/z) 375 (МH ); tR=2,27, (UV, ELSD) 83 %, 100 %. 7e. 3-(3-Хлорфеніл)-N-(2,6-диметил-4-морфолін-4-ілфеніл)пропіонамід + Вихід: 10 %. РХ-МС (m/z) 373 (МH ), tR=2,23, (UV, ELSD) 71 %, 94 %. 7f. N-(2,6-Диметил-4-морфолін-4-ілфеніл)-2-(3,4-диметилфеніл)ацетамід + Вихід: 44 %. РХ-МС (m/z) 353 (МН ; tR=2,21, (UV, ELSD) 80 %, 100 %. 7g. 2-(3-Бромфеніл)-Н-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід + Вихід: 22 %. РХ-МС (m/z) 404 (МH ); tR=2,19, (UV, ELSD) 95 %, 100 %. 7h. 2-(3-Хлорфеніл)-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід + Вихід: 25 %. РХ-МС (m/z) 359 (МH ); tR=2,13, (UV, ELSD) 95 %, 100 %. 7i. N-(2,6-Диметил-4-морфолін-4-ілфеніл)-2-п-толілацетамід + Вихід: 26 %. РХ-МС (m/z) 339 (МH ); tR=2,04, (UV, ELSD) 99 %, 100 %. 7j. N-(2,6-Диметил-4-морфолін-4-ілфеніл)-2-м-толілацетамід + Вихід: 24 %. РХ-МС (m/z) 339 (МH ); tR=2,03, (UV, ELSD) 88 %, 100 %. 7k. 2-(3,4-Дифторфеніл)-N-(2,6-диметил-4-морфолін-4-ілфеніл)ацетамід + Вихід: 24 %. РХ-МС (m/z) 361 (MH ); tR=2,03, (UV, ELSD) 99 %, 100 %. 28
ДивитисяДодаткова інформація
Назва патенту англійськоюSubstituted morpholine and thiomorpholine derivatives, pharmaceutical composition based thereon and use thereof for the preparation of medicament for the treatment of a disorder or disease of the central nervous system
Автори англійськоюWenzel Tornoe Christian, Rottlaender Mario, Khanzhin, Nikolay, Ritzen, Andreas, Watson William Patrick
Назва патенту російськоюЗамещенные производные морфолина и тиоморфолина, фармацевтическая композиция на их основе и их применение для производства лекарственного средства для лечения расстройства или заболевания центральной нервной системы
Автори російськоюВенсель Торньое Кристиан, Роттлондер Марио, Ханжин Николай, Ритсен Андреас, Ватсон Вильям Патрик
МПК / Мітки
МПК: A61K 31/5355, C07D 279/12, A61K 31/541, C07D 265/06, A61K 31/4406, C07D 417/04, C07D 295/12, A61P 25/22
Мітки: похідні, застосування, заміщені, тіоморфоліну, системі, основі, лікування, нервової, морфоліну, лікарського, розладу, композиція, фармацевтична, центральної, виробництва, захворювання, засобу
Код посилання
<a href="https://ua.patents.su/41-102517-zamishheni-pokhidni-morfolinu-ta-tiomorfolinu-farmacevtichna-kompoziciya-na-kh-osnovi-ta-kh-zastosuvannya-dlya-virobnictva-likarskogo-zasobu-dlya-likuvannya-rozladu-abo-zakhvoryuva.html" target="_blank" rel="follow" title="База патентів України">Заміщені похідні морфоліну та тіоморфоліну, фармацевтична композиція на їх основі та їх застосування для виробництва лікарського засобу для лікування розладу або захворювання центральної нервової системи</a>
Попередній патент: Інгібітори mcl-1 на основі 7-заміщених індолів
Наступний патент: Спосіб синтезу івабрадину і його адитивних солей з фармацевтично прийнятною кислотою
Випадковий патент: Безалкогольний низькокалорійний напій "чорничка"