Акриламідопохідні, застосовні як інгібітори переходу мітохондріальної проникності
Номер патенту: 105018
Опубліковано: 10.04.2014
Автори: Вілла Мануела, Паін Джиллес, Каренці Джакомо, Мінуччі Саверіо, Пліт Сімон, Каппа Анна, Варазі Маріо, Балларіні Марко, Фанчеллі Даніеле
Формула / Реферат
1. Сполука загальної формули (І)
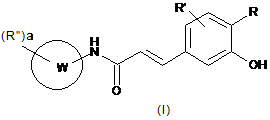 ,
,
де:
W є арилом або гетероарилом;
а дорівнює 0, 1, 2 або 3;
R і R' є однаковими або різними і незалежно один від одного вибрані з: водню; галогену; (С1-С3)алкокси; (С1-С2)галоалкокси; (С1-С2)галоалкілу; NR1R2; CN; SO2NH2 або факультативно заміщеного (С1-С6)алкілу, арилу або гетероарилу;
R" є незалежно вибраним з: галогену; (С1-С3)алкілу; (С1-С3)алкокси; (С1-С3)алкоксіалкілу; (С1-С2)галоалкокси; (С1-С2)галоалкілу; NR3R4 або (CH2)n-X-(CH2)m-Q, де:
n, m незалежно дорівнюють 0, 1 або 2;
X є прямим зв'язком; О; S; NH; N(С1-С3)алкілом;
Q є факультативно заміщеним арилом, гетероарилом, гетероциклоалкілом або циклоалкілом;
R1, R2, R3 і R4 є однаковими або різними і незалежно один від одного є атомом водню; (С1-С3)алкілом, або, коли взяті разом з атомом азоту, до якого вони приєднані, R1-N-R2 і R3-N-R4 можуть утворювати гетероциклічне кільце формули:
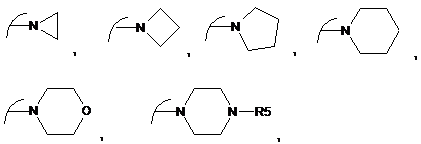 ,
,
де:
R5 є атомом водню або (С1-С3)алкільною групою; за умови, що: (E)-3-(3-гідроксифеніл)-N-[4-[[4-[[(E)-3-(3-гідроксифеніл)проп-2-еноїл]аміно]феніл]метил]феніл]-акриламід виключено і, коли W є фенілом, а не дорівнює 0;
коли W є фенілом і R є воднем, R" не є хлором, метилом, ізопропілом, CF3 або NH2;
коли W є індазол-5-ілом або пірид-2-илом, R не є воднем, (С1-С3)алкокси;
або ізомери, таутомери, рацемічні форми, енантіомери, діастереомери, епімери, поліморфи, їх суміші, проліки та їх фармацевтично прийнятні солі.
2. Сполука за п. 1, де:
W є фенільним кільцем, заміщеним 1 або 2 групами R";
R є галогеном; (С1-С3)алкокси; (С1-С3)алкілом;
R' є воднем;
R" є незалежно вибраним з:
галогену; (С1-С3)алкоксіалкілу; (С1-С2)галоалкілу або (СН2)n-Х-(CH2)m-Q,
де:
n дорівнює 0 або 1;
m дорівнює 0 або 1;
X є О; S; NH; N(С1-С3)алкілом;
Q є арилом або гетероарилом;
або її ізомери, таутомери, рацемічні форми, енантіомери, діастереомери, епімери, поліморфи, їх суміші, проліки та їх фармацевтично прийнятні солі.
3. Сполука за будь-яким з пп. 1, 2, де:
R є фтором; метокси; метилом;
R" є галогеном або (CH2)n-X-(CH2)m-Q, де:
n і m вибрані таким чином, що їх сума (n+m) дорівнює 1;
Х є О; і
Q є арилом або гетероарилом;
або її ізомери, таутомери, рацемічні форми, енантіомери, діастереомери, епімери, поліморфи, їх суміші, проліки та їх фармацевтично прийнятні солі.
4. Сполука за п. 1, де:
W є біциклічним арильним або біциклічним гетероарильним кільцем, факультативно заміщеним 1 або 2 групами R";
R є галогеном; (С1-С3)алкокси; (С1-С3)алкілом;
R' є воднем;
R" є незалежно вибраним з:
галогену; (С1-С2)галоалкілу; 4-(С1-С3)алкілпіперазин-1-ілу або (CH2)n-X-(CH2)m-Q, де:
n дорівнює 0 або 1;
m дорівнює 0 або 1;
X є О; S; NH; N(С1-С3)алкілом;
Q є арилом або гетероарилом;
або її ізомери, таутомери, рацемічні форми, енантіомери, діастереомери, епімери, поліморфи, їх суміші, проліки та їх фармацевтично прийнятні солі.
5. Сполука за будь-яким з пп. 1, 4, де:
W є біциклічним арильним або біциклічним гетероарильним кільцем, незаміщеним або заміщеним однією групою (CH2)n-X-(CH2)m-Q, де:
n і m вибрані таким чином, що їх сума (n+m) дорівнює 1;
Х є О; і
Q є арилом або гетероарилом;
і факультативно заміщеним другою групою R", вибраною з хлору; брому; (С1-С2)галоалкілу; 4-(С1-С3)алкілпіперазин-1-ілу;
R є фтором; метокси; метилом;
або її таутомери, рацемічні форми, енантіомери, діастереомери, епімери, поліморфи, їх суміші, проліки та їх фармацевтично прийнятні солі.
6. Сполука формули (І) за пп. 1-5, факультативно у формі своєї фармацевтично прийнятної солі, вибрана з групи, що включає:
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-нафталін-1-ілакриламід;
(Е)-N-(2-бензилоксифеніл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[3-(4-метилпіперазин-1-іл)-феніл]-акриламід;
(Е)-N-(2-хлорпіридин-4-іл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-N-(3-хлор-2-метоксифеніл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-N-(3,4-дихлорфеніл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-N-(3-хлор-4-метоксифеніл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-N-(2,3-дихлорфеніл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-N-(3-бензиламінофеніл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-N-[3-(бензилметиламіно)-феніл]-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-N-[2-хлор-3-(піридин-4-ілметокси)-феніл]-3-(3-гідрокси-4-метоксифеніл)-акриламіду гідрохлорид;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-{3-[(піридин-4-ілметил)-аміно]-феніл}-акриламід;
(Е)-N-(3-бензилокси-2-хлорфеніл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-N-(2-бензилокси-3-хлорфеніл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(E)-N-(l-бензил-1Н-індол-4-іл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-N-[3-хлор-2-(піридин-4-ілметокси)-феніл]-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-N-[4-хлор-3-(піридин-4-ілметокси)-феніл]-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-(1-метил-1Н-індол-4-іл)-акриламід;
(E)-N-(l-бензил-1Н-індол-7-іл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[3-(3-метил-3Н-імідазол-4-ілметокси)-феніл]-акриламід;
(Е)-3-(4-фтор-3-гідроксифеніл)-N-(2-феноксиметилфеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[3-(1Н-імідазол-4-ілметокси)-феніл]-акриламіду гідрохлорид;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[3-(піридин-4-ілоксиметил)-феніл]-акриламіду гідрохлорид;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-(3-оксазол-5-ілфеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-індан-1-ілакриламід;
(Е)-N-(2-бензилсульфанілфеніл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-(1-метил-1Н-бензімідазол-2-іл)-акриламіду гідрохлорид;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-(2-феноксиметилфеніл)-акриламід;
(Е)-N-бензоксазол-4-іл-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(E)-N-(1-бензил-1Н-бензімідазол-4-іл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-(1-метил-1Н-бензімідазол-4-іл)-акриламіду гідрохлорид;
(Е)-N-(1-бензил-1Н-індазол-7-іл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-(1-метил-1Н-бензотриазол-4-іл)-акриламід;
(E)-N-(1-бензил-1Н-індазол-4-іл)-3-(3-гідрокси-4-метоксифеніл)-акриламіду гідрохлорид;
(Е)-N-(2-бензил-2Н-індазол-7-іл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-(2-метил-2Н-індазол-7-іл)-акриламід;
(Е)-N-[3-(2,5-диметил-2Н-піразол-3-ілметокси)-феніл]-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[3-(1-метил-1Н-імідазол-2-ілметокси)-феніл]-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[2-(3-метоксифеноксиметил)-феніл]-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[2-(2-метоксифеноксиметил)-феніл]-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[2-(4-метоксифеноксиметил)-феніл]-акриламід;
(Е)-N-(2-циклобутоксиметилфеніл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[2-(піридин-4-ілоксиметил)-феніл]-акриламіду гідрохлорид;
(Е)-N-[2-(4-фторфеноксиметил)-феніл]-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[2-(4-імідазол-1-ілфеноксиметил)-феніл]-акриламід;
(Е)-N-[2-(2-фторфеноксиметил)-феніл]-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-(2-метоксиметилфеніл)-акриламід;
(E)-N-[2-(3-фторфеноксиметил)-феніл]-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-N-(3-бромфеніл)-3-(4-фтор-3-гідроксифеніл)-акриламід;
(Е)-N-(2-бензилоксифеніл)-3-(4-фтор-3-гідроксифеніл)-акриламід;
(Е)-N-(2,3-дихлорфеніл)-3-(4-фтор-3-гідроксифеніл)-акриламід;
(E)-N-(l-бензил-1Н-індол-7-іл)-3-(4-фтор-3-гідроксифеніл)-акриламід;
(Е)-N-(3-фторфеніл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-N-(3-хлорфеніл)-3-(3-гідроксифеніл)-акриламід;
(Е)-N-(3-хлорфеніл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-N-(2-хлорфеніл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-N-(4-хлорфеніл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-(3-йодфеніл)-акриламід;
(Е)-N-(3-бромфеніл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-(3-ізопропоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-(3-феноксифеніл)-акриламід;
(Е)-N-(3-бензилоксифеніл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-(3-метоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-(3-трифторметилфеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[3-(піридин-4-ілметокси)-феніл]-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[3-(1-метилпіперидин-3-ілметокси)-феніл]-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[3-(піридин-4-ілокси)-феніл]-акриламід;
(Е)-N-(3,5-дихлорфеніл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[3-(1-метилпіперидин-4-ілокси)-феніл]-акриламід;
(Е)-N-(4-бензилоксифеніл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-N-(3-хлорфеніл)-3-(3-гідрокси-4-метилфеніл)-акриламід;
(Е)-3-(4-фтор-3-гідроксифеніл)-N-нафталін-1-ілакриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-(4-метоксипіримідин-2-іл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[3-(1Н-тетразол-5-ілметокси)-феніл]-акриламід;
(Е)-N-(3-хлорфеніл)-3-(4-фтор-3-гідроксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-(2-фенетилоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[2-(піридин-4-ілметокси)-феніл]-акриламіду гідрохлорид;
(Е)-3-(4-фтор-3-гідроксифеніл)-N-[3-(піридин-4-ілметокси)-феніл]-акриламіду гідрохлорид;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[3-(піридин-4-ілметилсульфаніл)-феніл]-акриламіду гідрохлорид;
(Е)-N-1,3-бензодіоксол-5-іл-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-(1-метил-1Н-індазол-7-іл)-акриламід;
(E)-N-(4-етокси-1-метил-1Н-індазол-7-іл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-(1-метил-1Н-індазол-4-іл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[3-(5-метилфуран-2-ілметокси)-феніл]-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[3-(піридин-3-ілметокси)-феніл]-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-(3-фенетилоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[3-(піридин-2-ілметокси)-феніл]-акриламід;
(Е)-N-(5-хлор-2-феноксиметилфеніл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[4-(4-метилпіперазин-1-іл)-2-феноксиметилфеніл]-акриламіду гідрохлорид;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[2-(3-трифторметилфеноксиметил)-феніл]-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[2-(3-хлорфеноксиметил)-феніл]-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[2-(4-морфолін-4-ілметилфеноксиметил)-феніл]-акриламіду гідрохлорид;
(Е)-3-(4-фтор-3-гідроксифеніл)-N-{2-[4-(1-метилпіперидин-4-ілокси)-феноксиметил]-феніл}-акриламіду трифторацетат;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[2-(2-трифторметилфеноксиметил)-феніл]-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-{2-[3-(піперидин-4-ілокси)-феноксиметил]-феніл}-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-{2-[4-(піперидин-4-ілокси)-феноксиметил]-феніл}-акриламіду гідрохлорид;
(Е)-3-(4-хлор-3-гідроксифеніл)-N-{2-[3-(піперидин-4-ілокси)-феноксиметил]-феніл}-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-{2-[4-(1-метилпіперидин-4-іл)-феноксиметил]-феніл}-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-{2-[2-(4-метилпіперазин-1-іл)-феноксиметил]-феніл}-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-{2-[3-(1-метилпіперидин-4-ілокси)-феноксиметил]-феніл}-акриламіду гідрохлорид;
(Е)-3-(4-хлор-3-гідроксифеніл)-N-(3-хлорфеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-{2-[3-(4-метилімідазол-1-іл)-феноксиметил]-феніл}-акриламід;
(Е)-3-(2-хлор-3-гідрокси-4-метоксифеніл)-N-(3-хлорфеніл)-акриламід;
(Е)-3-(4-фтор-3-гідроксифеніл)-N-[3-(піридин-4-ілметилсульфаніл)-феніл]-акриламід;
(Е)-N-(1-бензил-1Н-індазол-7-іл)-3-(4-фтор-3-гідроксифеніл)-акриламід;
(E)-3-(3-гiдpoкcи-4-мeтoкcифeнiл)-N-{2-[4-(l-мeтилпiпepидин-4-iлoкcи)-феноксиметил]-феніл}-акриламіду гідрохлорид;
(Е)-N-(3-бензил-3Н-бензоімідазол-4-іл)-3-(4-фтор-3-гідроксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[2-(4-трифторметилфеноксиметил)-феніл]-акриламід;
(Е)-N-[2-(2-хлорфеноксиметил)-феніл]-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[1-(4-імідазол-1-ілбензил)-1Н-індол-7-іл]-акриламід;
(Е)-3-(4-фтор-3-гідроксифеніл)-N-[1-(4-імідазол-1-ілбензил)-1Н-індол-7-іл]-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-{2-[4-(1-метилпіперидин-4-ілметил)-феноксиметил]-феніл}-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-{2-[3-(4-метилпіперазин-1-іл)-феноксиметил]-феніл}-акриламіду гідрохлорид;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-{2-[4-(4-метилімідазол-1-іл)-феноксиметил]-феніл}-акриламіду гідрохлорид;
(Е)-N-(1-бензил-2-оксо-2,3-дигідро-1Н-індол-7-іл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-N-(3-хлорнафталін-1-іл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[2-(2-метил-2Н-піразол-3-ілоксиметил)-феніл]-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[2-(3-піперазин-1-ілфеноксиметил)-феніл]-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[1-(1-метил-1Н-імідазол-4-ілметил)-1Н-індол-7-іл]-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[1-(1-метил-1Н-піразол-3-ілметил)-1Н-індол-7-іл]-акриламід;
(Е)-3-(3-гідроксифеніл)-N-(2-феноксиметилфеніл)-акриламід;
(Е)-N-(3-хлорфеніл)-3-(2,4-дифтор-3-гідроксифеніл)-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[2-(4-піролідин-1-ілметилфеноксиметил)-феніл]-акриламіду гідрохлорид;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-{2-[4-(4-метилпіперазин-1-ілметил)-феноксиметил]-феніл}-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[2-(4-піперидин-1-ілметилфеноксиметил)-феніл]-акриламіду трифторацетат;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-{1-[3-(1-метилпіперидин-4-ілокси)-бензил]-1Н-індол-7-іл}-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-{2-[2-(1-метилпіперидин-4-ілокси)-феноксиметил]-феніл}-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-{2-[3-(1-метилпіперидин-4-іл)-феноксиметил]-феніл}-акриламід;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-{2-[4-(4-метилпіперазин-1-іл)-феноксиметил]-феніл}-акриламіду трифторацетат;
(Е)-3-(4-фтор-3-гідроксифеніл)-N-[2-(4-імідазол-1-ілфеноксиметил)-феніл]-акриламід;
(Е)-3-(2,4-дифтор-3-гідроксифеніл)-N-{2-[3-(1-метилпіперидин-4-ілокси)-феноксиметил]-феніл}-акриламід;
(Е)-3-(2-хлор-3-гідрокси-4-метоксифеніл)-N-{2-[3-(1-метилпіперидин-4-ілокси)-феноксиметил]-феніл}-акриламід;
(E)-N-(3-хлорфеніл)-3-(4-ціано-3-гідроксифеніл)-акриламід;
(Е)-3-(4-ціано-3-гідроксифеніл)-N-{2-[3-(1-метилпіперидин-4-ілокси)-феноксиметил]-феніл}-акриламід;
(Е)-3-(2,4-дифтор-3-гідроксифеніл)-N-{2-[3-(піперидин-4-ілокси)-феноксиметил]-феніл}-акриламід;
(Е)-3-(2,4-дифтор-3-гідроксифеніл)-N-{2-[4-(1-метилпіперидин-4-ілокси)-феноксиметил]-феніл}-акриламід;
(Е)-3-(2,4-дифтор-3-гідроксифеніл)-N-{2-[4-(піперидин-4-ілокси)-феноксиметил]-феніл}-акриламід;
(Е)-3-(2-хлор-3-гідрокси-4-метоксифеніл)-N-{2-[3-(піперидин-4-ілокси)-феноксиметил]-феніл}-акриламід;
(Е)-3-(4-ціано-3-гідроксифеніл)-N-{2-[3-(піперидин-4-ілокси)-феноксиметил]-феніл}-акриламід;
(Е)-3-(4-ціано-3-гідроксифеніл)-N-{2-[4-(1-метилпіперидин-4-ілокси)-феноксиметил]-феніл}-акриламід;
(Е)-N-(3-бензил-3Н-бензоімідазол-4-іл)-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-N-[2-(4-хлорфеноксиметил)-феніл]-3-(3-гідрокси-4-метоксифеніл)-акриламід;
(Е)-N-(3-хлорфеніл)-3-(3-гідрокси-4-сульфамоїлфеніл)-акриламід;
натрію (Е)-5-(3-(3-хлорфеніламіно)-3-оксопроп-1-еніл)-2-метоксифенілфосфат;
(Е)-3-(3-гідрокси-4-метоксифеніл)-N-[1-(3-метил-3Н-імідазол-4-ілметил)-1Н-індол-7-іл]-акриламід;
(Е)-N-(3-хлорфеніл)-3-(4-аміно-3-гідроксифеніл)-акриламід
або їх ізомери, таутомери, рацемічні форми, енантіомери, діастереомери, поліморфи, суміші і проліки.
7. Спосіб одержання сполуки загальної формули (І) за будь-яким одним з попередніх пунктів, при якому:
(а) вводять у реакцію гідроксикоричну кислоту формули (II), де R і R' є такими, як визначено в п. 1, із захисним засобом гідроксилу з одержанням відповідної захищеної сполуки формули (III)
 ,
,
де R і R' є такими, як визначено вище, і PG є зазначеною захисною групою;
(b) активують карбоксильну частину сполуки формули (III), як визначено вище, для амідування, щоб одержати сполуку формули (V)
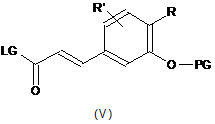 ,
,
де R, R' і PG є такими, як визначено вище, і LG є будь-якою придатною активаційною групою карбоксильної частини;
(с) ацилюють аміносполуку формули (IV), де W, R" і а є такими, як визначено в п. 1, зі сполукою формули (V), як визначено вище, з одержанням сполуки формули (VI), де R, R', R", W, а і PG є такими, як визначено вище,
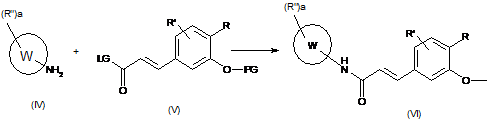 ,
,
(d) видаляють захисну групу PG зі сполуки формули (VI), як визначено вище, з одержанням сполуки формули (І) і, за потреби, перетворюють сполуку формули (І) на іншу сполуку формули (І) або перетворюють сполуку формули (І) на фармацевтично прийнятну сіль, або перетворюють її сіль на вільну сполуку формули (І).
8. Спосіб одержання сполуки загальної формули (І) за будь-яким одним з пп. 1-6, при якому:
(а) активують карбоксильну частину сполуки формули (II), як визначено в п. 7, для амідування, щоб одержати сполуку формули (Va)
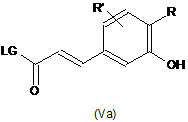 ,
,
де R і R' є такими, як визначено в п. 1, і LG є такою, як визначено в п. 7;
(b) ацилюють аміносполуку формули (IV), як визначено в п. 7, зі сполукою формули (Va), як визначено вище, з одержанням сполуки формули (І), де R, R', R", W і а є такими, як визначено в п. 1,
 ,
,
і, за потреби, перетворюють сполуку формули (І) на іншу сполуку формули (І) або перетворюють сполуку формули (І) на фармацевтично прийнятну сіль, або перетворюють її сіль на вільну сполуку формули (І).
9. Спосіб одержання сполуки загальної формули (І) за будь-яким одним з пп. 1-6, при якому:
(а) ацилюють аміносполуку формули (VII), де W, R" є такими, як визначено в п. 1, а дорівнює 0, 1 або 2, і X є О або S, зі сполукою формули (V), як визначено в п. 7, з одержанням сполуки формули (VIII), де R, R', R", W, а, X і PG є такими, як визначено вище,
 ,
,
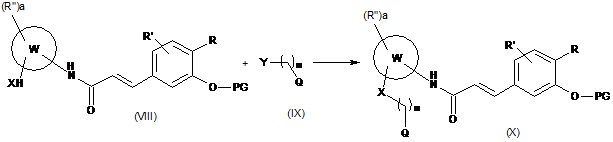
(b) алкілують сполуку формули (VIII), як визначено вище, зі сполукою формули (IX), де Υ є будь-якою придатною відхідною групою або гідроксигрупою, m і Q є такими, як визначено в п. 1, з одержанням сполуки формули (X), де R, R', R", W, a, m, X, Q і PG є такими, як визначено вище,
 ,
,
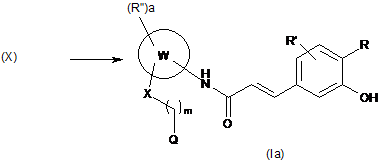
(с) видаляють захисну групу зі сполуки формули (X), як визначено вище, з одержанням сполуки формули (Іа), де R, R', R", W, а, m, X і Q є такими, як визначено вище, і, за потреби, перетворюють сполуку формули (Іа) в іншу сполуку формули (Іа) або перетворюють сполуку формули (Іа) у фармацевтично прийнятну сіль, або перетворюють її сіль у вільну сполуку формули (Іа)
 .
.
10. Сполука загальної формули (І) за будь-яким одним з пп. 1-6 або її ізомери, рацемічні форми, таутомери, енантіомери, діастереомери, епімери, поліморфи, їх суміші, проліки і їх фармацевтично прийнятні солі для застосування в терапії.
11. Сполука за п. 10 для одержання лікарського препарату для попередження та/або лікування хвороб і станів, пов'язаних з активністю пори переходу мітохондріальної проникності (МРТР).
12. Сполука за п. 11 для одержання лікарського препарату для попередження та/або лікування хвороб, що виникають внаслідок ушкодження ішемією/реперфузією або окисного ушкодження, хвороб, пов'язаних з віком, дегенеративних і нейродегенеративних хвороб.
13. Сполука за п. 12 для одержання лікарського препарату для попередження та/або лікування гострого інфаркту міокарда, серцевої недостатності, ішемії органа, ішемічного і травматичного ушкодження мозку, м'язової дистрофії Дюшенна, уродженої м'язової дистрофії Ульріха, міопатії Бентама, бічного аміотрофічного склерозу, хвороби Хантігтона, хвороби Альцгеймера, хвороби Паркінсона, діабетів І типу і II типу, ускладнень діабету, гіперглікемічного ушкодження тканини, гіпоглікемічного ушкодження тканини, холестазу, ушкодження, викликаного алкоголем.
14. Застосування сполуки загальної формули (І) за будь-яким одним з пп. 1-6 або її ізомерів, рацемічних форм, таутомерів, енантіомерів, діастереомерів, епімерів, поліморфів, їх сумішей, проліків і їх фармацевтично прийнятних солей для одержання лікарського препарату для попередження та/або лікування хвороб і станів, пов'язаних з активністю пори переходу мітохондріальної проникності (МРТР).
15. Фармацевтична композиція, що містить одну або більше сполук загальної формули (І) за будь-яким одним з пп. 1-6 або проліків, або їх фармацевтично прийнятну сіль і щонайменше один фармацевтично прийнятний наповнювач.
Текст
Реферат: У даному винаході описані акриламідопохідні, застосовні як терапевтичні засоби, особливо для попередження та/або лікування хвороб і станів, пов'язаних з активністю пори переходу мітохондріальної проникності (МРТР), таких як хвороби, що характеризуються ішемією/реперфузією, окисним або дегенеративним ушкодженням тканини. Ці сполуки належать до структурної формули (І), де R, R', R", W і а є такими, як визначено в описі. Даний винахід також стосується одержання цих сполук, а також фармацевтичних композицій, що містять їх. UA 105018 C2 5 10 15 20 25 30 35 40 45 50 55 60 Галузь винаходу Даний винахід стосується акриламідо-похідних та їх застосування як терапевтичних засобів, зокрема, для попередження та/або лікування хвороб і станів, пов'язаних з активністю пори переходу мітохондріальної проникності (MPTP), таких як хвороби, що характеризуються ішемією/реперфузією, окисним або дегенеративним ушкодженням тканини. Даний винахід також стосується одержання цих сполук, а також фармацевтичних композицій, що містять їх. Передумови винаходу Перехід мітохондріальної проникності (MPT) стосується переходу в стан проникності внутрішньої мітохондріальної мембрани для розчинів з молекулярною масою нижче приблизно 2+ 1500 Да. Вважається, що MPT є опосередкованим оборотним відкриттям потенціал- і Ca залежного з високою провідністю білкового каналу у внутрішній мітохондріальній мембрані, MPT пори (MPTP). Наслідки відкриття MPTP є двоїстими: по-перше, роз'єднання окисного фосфорилування, та, як наслідок, F1F0-АТФаза обертається для випробування та підтримання мембранного потенціалу (ΔΨm), що призводить до зниження рівнів АТФ в клітині та втрати метаболічного гомеостазу. По-друге, MPTP дозволяє розчинам вільно входити в матрикс мітохондрії, що призводить до набухання і можливого розриву зовнішньої мітохондріальної мембрани з наступним вивільненням накопиченого кальцію та проапоптотичних факторів. Вивільнення накопиченого кальцію може викликати перевантаження кальцієм, утворення активних форм кисню (ROS) і MPT у сусідній мітохондрії, призводячи до "ланцюгової реакції" у всій клітині. Залежно від енергетичного стану клітини пізніше виникає апоптоз або некроз, призводячи до необоротного ушкодження тканини і органа (Grimm S., Brdiczka D. The permeability transition pore in cell death Apoptosis, 2007, 12, 841-847). Точний молекулярний склад MPTP усе ще не відомий. Циклофілін D був представлений як фармакологічно (із застосуванням інгібітору, циклоспорин A), так і генетично в якості основного регулятора MPTP. Провели багато досліджень, що демонструють роль MPTP при хворобі, застосовуючи циклофілін D-нульових мишей (Ppif-/-) або циклоспорин A. MPTP можна 2+ регулювати за допомогою декількох факторів, включаючи високу концентрацію [Ca ], окисне ушкодження (ROS), хімічні засоби, що поперечно зшивають, передачу стресового сигналу і PI3кіназний шлях передачі сигналу, умови, які часто присутні в клітинах з уражених хворобою тканин (Rasola, A., Bernardi, P., The mitochondrial permeability transition pore and its involvement in cell death and in disease pathogenesis. Apoptosis, 2007, 12, 815-833). Добре встановлена роль опосередкованого мітохондрією апоптозу і некрозу в етіології багатьох хвороб, і підвищений ступінь апоптозу/некрозу, типовий для умов патологічного стресу, таких як ті, що спостерігаються під час інфаркту міокарда, ниркової ішемії або нейродегенеративних хвороб, співвідноситься з MPT і втратою мітохондріальної цілісності. Отже, MPTP залучена в етіологію і розвиток декількох хвороб, включаючи: - гострий інфаркт міокарда (летальне реперфузійне ушкодження); - напад і неврологічні хвороби; - спадкові дистрофії; - гепатит; - діабет і діабетична ретинопатія. Гострий інфаркт міокарда (летальне реперфузійне ушкодження) При ішемічній хворобі серця виникають послідовні події ішемії-реперфузії, що призводять до загибелі клітин міокарда шляхом некрозу та/або апоптозу. Летальне реперфузійне ушкодження (загибель кардіоміоцитів як прямий наслідок реперфузії тканини), як вважається, становить до 50% кінцевого розміру інфаркту міокарда, і, як показано, залежить від шляху RISK (кіназа збереження при реперфузійному ушкодженні) і відкриття MPTP (Yellon, D.M., Hausenloy, D.J., Myocardial Reperfusion Injury. N. Engl. J. Med., 2008, 357, 1121-1135.). При ішемії присутнє 2+ виснаження ATФ, зменшення клітинного pH і внутрішньоклітинне завантаження Ca . При 2+ реперфузії підвищена концентрація внутрішньоклітинного [Ca ] призводить до перевантаження 2+ Ca у мітохондрії, що разом з великим вибухом ROS і поверненням до фізіологічного pH викликає, парадоксально, відкриття MPT і загибель клітин кардіоміоцитів через некроз та/або апоптоз. Таким чином, очікується, що інгібування MPTP зменшує загибель кардіоміоцитів і знижує розмір інфаркту після ушкодження ішемією/реперфузією. Дійсно, Debio-025, аналог циклоспорину A, що має MPT-інгібіторну активність, знижував розмір інфаркту і поліпшував функціональне відновлення і знижував смертність у мишачій моделі інфаркту міокарда і реперфузійного ушкодження (Gomez, L., Thibault. H., Gharib, A., Dumont, J-M., Vuagniaux, G., Scalfaro, P., Derumeaux, G., Ovize, M. Inhibition of mitochondrial permeability transition improves functional recovery and reduces mortality following acute myocardial infarction in mice. Am. J. Physiol. Heart Circ. Physiol., 2007, 293, 1654-1661). 1 UA 105018 C2 5 10 15 20 25 30 35 40 45 50 55 60 Напад і неврологічні хвороби. Церебральна ішемія з подальшою реперфузією активує кілька шляхів, включаючи шлях, який викликає вивільнення великих кількостей збуджувальної амінокислоти глутамату в синапси. Активація рецепторів N-метил-D-аспартату викликає збільшення поглинання кальцію і утворення ROS, призводячи до відкриття MPTP і мітохондріальної дисфункції. Отже, відкриття MPTP залучене до загибелі клітин нейронів і клінічних симптомів, пов'язаних з нападом. Крім того, NIM811, аналог циклоспорину A, інгібітор MPT, що забезпечує 40% захист на щурячій моделі транзиторної фокальної церебральної ішемії, характеризується зниженням вивільнення цитохрому C і утворення ROS (Korde, A.S., Pettigrew, L.C., Craddock, S.D., Pocernich, C.B., Waldmeier, P.C., Margolis., W.F. Protective effects of NIM81 1 in transient focal cerebral ischemia suggests involvement of the mitochondrial permability transition. J. Neurotrauma, 2007, 24 (5), 895908). Гостра викликана інсуліном гіпоглікемія призводить до ушкодження нейронів певних областей мозку, включаючи зовнішні шари кори головного мозку і зубчасту звивину. На щурячій моделі викликаної інсуліном гіпоглікемічної коми циклоспорин A, імунодепресивний лікарський засіб з MPTP-інгібіторною активністю, але не FK506 (імунодепресивний засіб, подібний до CSA, але без MPTP-активності), показав сильне зниження ультраструктурного ушкодження мозку при введенні за 30 хвилин до гіпоглікемічного інсульту (Friberg, H., Ferrand-Drake, M., Bengtsson, F., Halestrap, A.P., Wieloch, T. Cyclosporin A, but not FK 506, protects mitochondria and neurons against hypoglycaemic damage and implicates the mitochondrial permeability transition in cell death. J. Neurosci., 1998, 18, 5151,5159). 2+ Мітохондріальна дисфункція, порушена передача сигналів Ca і окисний стрес є характеристиками бічного аміотрофічного склерозу, хвороб Альцгеймера, Паркінсона і Хантігтона, і відкриття MPTP було причинно зв'язане з усіма чотирма хворобами вибірковим застосуванням циклоспорину A (Norenberg, M.D., Rama Rao, K.V. The mitochondrial permeability transition in neurologic disease. Neurochem. Int., 2007, 50, 983-997). MPTP і мітохондріальне набухання були також залучені до ушкодження мозку, що відбувається в результаті гіперглікемічного інсульту, експериментальної травми і епілепсії (Li, P.A., Uchino, H., Elmer, E., Siesjö, B.K. Amelioration by cyclosporin A of brain damage following 5 or 10 min of ischemia in rats subjected to preischemic hyperglycaemia. Brain Res., 1997, 753, 133-140; Scheff, S.W., Sullivan P.G. Cyclosporin A significantly ameliorates cortical damage following experimental traumatic brain injury in rodents. J. Neurotrauma, 1999, 16, 783-792; Kudin, A. P., Debska-Vielhaber, G., Vielhaber, S., Elger, C.E., Kunz, W.S. The mechanism of neuroprotection by topiramate in an animal model of epilepsy. Epilepsia, 2004, 45, 1478-1487). Спадкові дистрофії 2+ Багато з патологічних ознак, що призводять до відкриття MPTP (перевантаження Ca і накопичення ROS), присутні при м'язових дистрофіях, і мітохондрії, виділені з скелетного м'яза -/від Scgd мишей (модель із важкою дистрофією), набухали послідовно з відкриттям MPTP. -/Scgd , -/Ppif миші (без циклофіліну D) не мали набухлих мітохондрій і не проявляли важкої м'язової дегенерації у віці 8 тижнів. Окрім того, лікування mdx (модель м'язової дистрофії Дюшена) і -/Scgd мишей Debio-025 знижує мітохондріальне набухання і некротичну хворобу (Millay, D.P., Sargent, M.A., Osinska, H., Baines, C.P., Barton, E.R., Vuagniaux, G., Sweeney, H.L. Robbins, J., Molkentin, J.D. genetic and pharmacologic inhibition of mitochondrial-dependent necrosis attenuates muscular dystrophy. Nature Medicine, 2008, 14, 442-447). Уроджена м'язова дистрофія Ульріха і міопатія Бетлема є двома спадковими дистрофіями, які характеризуються мутаціями в гені колагену VI. Мишачі моделі хвороб висунули на перший план приховану мітохондріальну дисфункцію, яка характеризується підвищеною чутливістю до відкриття MPTP і дегенерацією м'язових волокон. Міобласти у пацієнтів з уродженою м'язовою дистрофією Ульріха показують мітохондріальну дисфункцію і раннє відкриття MPTP, що призводить до підвищеного апоптозу. Пацієнти з коллаген VI-міопатіями, яких лікували MPTPінгібітором циклоспорином A протягом одного місяця, показали поліпшення мітохондріальної функції та мали ознаки м'язової регенерації (Merlini, L., Angelin, A., Tiepolo, T., Braghetta, P., Sabatelli, P., Zamparelli, A., Ferlini, A., Maraldi, M., Bonaldo, P., Bernardi, P. Cyclosporin A corrects mitochondrial dysfunction and muscle apoptosis in patients with collagen VI myopathies. P.N.A.S., 2008, 105 (13), 5225-5229). Гепатит Печінка може бути ушкоджена різними засобами, такими як хімічні отрути, запальні фактори або віруси. У всіх випадках гепатоцити зазнають масового апоптозу, до якого призводить MPTP. Крім того, повідомили, що інгібування відкриття MPTP лікуванням циклоспорином A сильно 2 UA 105018 C2 5 10 15 20 25 30 35 40 45 50 55 60 знижує ураження печінки на щурячій моделі Tnf-α-залежного гострого запального гепатиту (Soriano, M.E., Nicolosi, L. Desensitization of the permeability transition pore by cyclosporine A prevents activation of the mitochondrial apoptotic pathway and liver damage by tumour necrosis factor-alpha. J. Biol. Chem., 2004, 279, 36803-36808). Діабет Діабет викликає ушкодження і відмирання клітин кількома механізмами. Діабетична ретинопатія (DR) є одним з периферичних мікросудинних ускладнень, що сильно збільшують відсоток смертності від діабетичних судинних хвороб. DR починається на ранньому препроліферативному етапі (фонова ретинопатія), який характеризується втратою капілярних перицитів, прогресуючим закриттям капілярів, мікро-аневризмами і набряком сітківки. Подальша ретинальна ішемія (або гіпоксія) через непрохідність судин викликає патологічний ріст судин сітківки. Нео-судини простягаються уздовж внутрішньої поверхні сітківки та/або в порожнину склоподібного тіла і можуть призвести до відшарування сітківки і крововиливу. Цей етап відомий як проліферативна діабетична ретинопатія (PDR). Гіперглікемічний стрес розглядають як ключовий фактор в PDR, оскільки він індукує підвищене утворення фактора росту ендотелію судин (VEGF) клітинами сітківки, приводячи до неоваскуляризації, і викликає окисне ушкодження клітин, що впливає на мітохондрії. ROS, які утворюються в більш високих кількостях при діабеті, можуть ініціювати більшість патологічних внутрішньоклітинних шляхів, включених в PDR, і показано, що ROS утворюються в сітківці при реперфузії після ішемії, викликаної діабетом. До того ж окисний стрес також порівнювали з рівнем і розвитком ретролентальної фіброплазії (ROP). Незріла сітківка містить відносно низькі рівні антиоксидантів, таких як гемоксигеназа-1 і каталаза. Під час гіпероксигенації утворюються ROS і, крім цього, вона сприяє утворенню біологічно активних ізопростанів, що сприяють ішемії і, отже, патогенезу ROP. MPTP ініціюється ROS, і її відкриття може призвести до додаткового утворення ROS, і тому мітохондріальна дисфункція може бути основою для ускладнень діабету. Дотепер, інгібування MPTP, головним чином, було обмежено фармакологічною модуляцією компонента циклофіліну D MPTP із застосуванням сильного імунодепресивного лікарського засобу циклоспорину A або його аналогів NIM811 і Debio-025 (які позбавлені імунодепресивної активності). Це великі, складні молекули на основі пептидної структури циклоспорину A. До того ж інгібіторна ефективність цих молекул обмежена межами регулюючої ролі циклофіліну D у функціонуванні MPTP і його рівнем експресії. Інші відомі сполуки, які часто показують ряд біологічних активностей і фармакологічних профілів, як повідомили, також мають кілька додаткових неспецифічних взаємодій з MPTP. Наприклад, було показано, що засіб N-[(3,5-ди-tert-бутил-4-гідрокси-1-тіофеніл)]-3-пропіл-N'(2,3,4-триметоксибензил)піперазин (S-15176) взаємодіє з кількома мішенями на мітохондріальних мембранах печінки пацюків і проявляє деякі антиішемічні властивості, коли дозується in vitro при низькій концентрації. Навпаки, при більш високих дозах він викликає деполяризацію мітохондріальної мембрани і роз'єднання дихання, що типово пов'язане із сильною цитотоксичністю. (Morin D. et al. Effect of the mitochondrial transition pore inhibitor, S15176, on rat liver mitochondria: ATP synthase modulation and mitochondrial uncoupling induction. Biochemical Pharmacology, Pergamon, Oxford, GB, 72, 7, 911-91). Отже, існує потреба ідентифікувати більш сильні і ефективні невеликі молекули інгібіторів MPTP, що мають іншу і більш ефективну мішень в MPTP, які застосовні для попередження або лікування хвороб і станів, пов'язаних з активністю MPTP. Акриламідо-сполуки даного винаходу є невеликими молекулами, що мають сильну MPTP-інгібіторну активність, які застосовні при лікуванні ряду хвороб, таких як ті, що виникають у результаті ушкодження ішемією/реперфузією або окисного ушкодження, хвороб, пов'язаних з віком, дегенеративних і нейродегенеративних хвороб. Певні акриламідо-сполуки відомі в даному рівні техніки як терапевтичні засоби. Наприклад, арильні і гетероарильні пропенаміди розкриті як антипроліферативні, радіозахисні і цитозахисні засоби в патентній заявці WO 04/037751. Ліганд акриламідо-сполук ванілоїдного рецептора розкритий у патентній заявці WO 03/049702 як анальгетик для лікування болю різного походження і етіології. N-гетероцикліламідні сполуки, серотонінергічні антагоністи, розкриті в патентній заявці WO 01/068585 для лікування або попередження розладів центральної нервової системи. До того ж певні аніліди кавової кислоти також відомі в даному рівні техніки як засоби проти агрегації тромбоцитів і антиокислювальні засоби, як повідомили в Bioorganic & Medicinal Chemistry 2005, 13(5), 1791-7. Короткий опис даного винаходу Даний винахід спрямований на сполуки, які мають MPT-інгібуючу активність і застосовуються в терапії як засоби проти MPTP-зв'язаних захворювань у пацієнта. 3 UA 105018 C2 Виявили, що акриламідо-сполуки загальної формули (I) і їх похідні мають MPT-інгібуючу активність. Даний винахід забезпечує сполуку формули (I) 5 10 15 20 25 30 , де: W є арилом або гетероарилом; a дорівнює 0, 1, 2 або 3; R і R' є однаковими або різними і незалежно один від одного вибрані з: водню; галогену; (C1C3)алкокси; (C1-C2)галоалкокси; (C1-C2)галоалкілу; NR1R2; CN; SO2NH2; або факультативно заміщеного (C1-C6)алкілу, арилу або гетероарилу; R" є незалежно вибраним з: галогену; (C1-C3)алкілу; (C1-C3)алкокси; (C1-C3)алкоксіалкілу; (C1-C2)галоалкокси; (C1-C2)галоалкілу; NR3R4 або (CH2)n-X-(CH2)m-Q, де: n, m незалежно дорівнюють 0, 1 або 2; X є прямим зв'язком; O; S; NH; N(C1-C3)алкілом; Q є факультативно заміщеним арилом, гетероарилом, гетероциклоалкілом або циклоалкілом; R1, R2, R3 і R4 є однаковими або різними і незалежно один від одного є атомом водню; (C1C3)алкілом або, коли взяті разом з атомом азоту, до якого вони приєднані, R1-N-R2 і R3-N-R4 можуть утворювати гетероциклічне кільце формули: , де: R5 є атомом водню або (C1-C3)алкільною групою; за умови, що: коли W є фенілом, a не дорівнює 0; коли W є фенілом, і R є воднем, R" не є хлором, метилом, ізопропілом, CF3 або NH2; коли W є індазол-5-ілом або пірид-2-ілом, R не є воднем, (C1-C3)алкокси; а також її ізомери, таутомери, рацемічні форми, енантіомери, діастереомери, епімери, поліморфи, їх суміші, проліки та їх фармацевтично прийнятні солі. Даний винахід також стосується способів синтезу акриламідо-сполук загальної формули (I), їх проліків і фармацевтично прийнятних солей. Даний винахід забезпечує спосіб одержання сполуки загальної формули (I), при якому: (a) приводять у реакцію гідроксикоричну кислоту формули (II), де R і R' є такими, як визначено вище, із захисним засобом гідроксилу для одержання відповідної захищеної сполуки формули (III) 4 UA 105018 C2 , де R і R' є такими, як визначено вище, і PG є зазначеною захисною групою; (b) активують карбоксильну частину сполуки формули (III), як визначено вище, для амідування, щоб одержати сполуку формули (V) 5 10 15 , де R, R' і PG є такими, як визначено вище, і LG є будь-якою придатною активаційною групою карбоксильної частини; (c) ацилюють аміносполуку формули (IV), де W, R" і a є такими, як визначено вище, зі сполукою формули (V), як визначено вище, для одержання сполуки формули (VI), де R, R', R", W, a і PG є такими, як визначено вище , (d) видаляють захисну групу PG зі сполуки формули (VI), як визначено вище, для одержання сполуки формули (I) і, за потреби, перетворюють сполуку формули (I) на іншу сполуку формули (I), або перетворюють сполуку формули (I) на фармацевтично прийнятну сіль, або перетворюють її сіль на вільну сполуку формули (I). В іншому варіанті здійснення даний винахід забезпечує спосіб одержання сполуки загальної формули (I), при якому: (a) активують карбоксильну частину сполуки формули (II), як визначено вище, для амідування, щоб одержати сполуку формули (Va) 20 (Va) 25 де R, R' і LG є такими, як визначено вище; (b) ацилюють аміносполуку формули (IV), як визначено вище, зі сполукою формули (Va), як визначено вище, для одержання сполуки формули (I), де R, R', R", W і a є такими, як визначено 5 UA 105018 C2 вище 10 , і, за потреби, перетворюють сполуку формули (I) на іншу сполуку формули (I), або перетворюють сполуку формули (I) на фармацевтично прийнятну сіль, або перетворюють її сіль на вільну сполуку формули (I). В іншому варіанті здійснення даний винахід забезпечує спосіб одержання сполуки загальної формули (I), при якому: (a) ацилюють аміносполуку формули (VII), де W, R" є такими, як визначено вище, a дорівнює 0, 1 або 2, і X являє собою O або S, зі сполукою формули (V), як визначено вище, для одержання сполуки формули (VIII), де R, R', R", W, a, X і PG є такими, як визначено вище, 15 , (b) алкілують сполуку формули (VIII), як визначено вище, зі сполукою формули (IX), де Y є будь-якою придатною групою, що відходить, або гідроксигрупою, m і Q є такими, як визначено вище, для одержання сполуки формули (X), де R, R', R", W, a, m, X, Q і PG є такими, як визначено вище, 5 20 25 , (с) видаляють захисну групу зі сполуки формули (X), як визначено вище, для одержання сполуки формули (Ia), де R, R', R", W, a, m, X і Q є такими, як визначено вище, і, за потреби, перетворюють сполуку формули (Ia) на іншу сполуку формули (Ia), або перетворюють сполуку формули (Ia) на фармацевтично прийнятну сіль, або перетворюють її сіль на вільну сполуку формули (Ia) . В іншому варіанті здійснення даний винахід забезпечує сполуки загальної формули (I), як визначено вище, а також їх ізомери, рацемічні форми, таутомери, енантіомери, діастереомери, епімери, поліморфи, їх суміші, проліки і їх фармацевтично прийнятні солі для застосування в терапії. Даний винахід також стосується застосування сполук загальної формули (I), як визначено вище, а також їх ізомерів, рацемічних форм, таутомерів, енантіомерів, діастереомерів, епімерів, 6 UA 105018 C2 5 10 15 20 25 30 35 40 45 50 55 60 поліморфів, їх сумішей, проліків і їх фармацевтично прийнятних солей для виготовлення лікарського препарату для попередження та/або лікування хвороб і станів, пов'язаних з активністю MPTP. Даний винахід також стосується фармацевтичних композицій, що містять одну або більше сполук загальної формули (I), як визначено вище, та/або проліки, та/або їх фармацевтично прийнятну сіль, і, щонайменше, один фармацевтично прийнятний наповнювач. Детальний опис винаходу Усі вирази, як використовується в даній заявці, якщо не зазначено інше, слід розуміти в їх звичайному значенні, як відомо в даному рівні техніки. Інші більш конкретні визначення для певних виразів, як використано в даній заявці, наведені нижче і призначені для застосування однаково у всьому описі і формулі винаходу, якщо спеціально зазначене інше визначення не забезпечує більш широке визначення. Вираз "арил" стосується будь-якої ароматичної карбоциклічної кільцевої системи з 1 або 2 кільцевих частин, або злитих, або зв'язаних один з одним через одинарний зв'язок. Придатні арильні групи включають, але без обмеження, феніл α- або β-нафтил, біфеніл, інданіл, інденіл і подібне. Вираз "гетероарил" стосується моноциклічних або поліциклічних ароматичних кілець, що містять атоми вуглецю і один або більше гетероатомів, переважно, 1-3 гетероатоми, незалежно вибраних з азоту, кисню і сірки. Як добре відомо фахівцям у даній галузі техніки, гетероарильні кільця мають менші ароматичні властивості, ніж їх аналоги, що повністю складаються з вуглецю. Таким чином, для цілей даного винаходу гетероарильна група повинна мати ароматичні властивості лише до певної міри. Ілюстративні приклади гетероарильних груп включають, але без обмеження, фурил, бензoфураніл, бензодіоксоліл, тієніл, піридил, піридилN-оксид, піримідил, піримідиніл, піридазиніл, піразил, піразиніл, піразоліл, оксазоліл, тіазоліл, ізоксазоліл, хіноліл, (1,2,3,)- і (1,2,4)-триазоліл, тетразоліл, триазиніл, піридазиніл, піроліл, імідазоліл, імідазо[1,2-a]піридин-3-іл, індазоліл, ізотіазоліл, індоліл, бензoімідазоліл, бензoтриазоліл, бензоксазоліл, оксадіазоліл і подібне. Вираз "гетероциклоалкіл" стосується неароматичного моноциклічного або поліциклічного кільця, що містить атоми вуглецю і водню, і, щонайменше, один гетероатом, переважно, 1-4 гетероатоми, вибрані з азоту, кисню і сірки. Гетероциклоалкільна група може мати один або більше подвійних зв'язків вуглець-вуглець або подвійних зв'язків вуглець-гетероатоми в кільці, при умові, що їх присутність не перетворює кільце на ароматичне. Приклади гетероциклоалкільних груп включають, але без обмеження, азиридиніл, морфолініл, тіоморфолініл, піперидиніл, піперазиніл, тіазолідиніл, оксазолідиніл, тетрагідротієніл, дигідрофураніл, тетрагідрофураніл, тетрагідротіофураніл, тетрагідропіраніл, піразолідиніл, 1,3діоксоланіл, піролідиніл, піраніл, дигідропіраніл, ізоксазолідиніл, імідазолідиніл і подібне. Гетероциклоалкільна група може бути незаміщеною або заміщеною одним або двома замісниками. Вираз "циклоалкіл" стосується будь-якої неароматичної карбоциклічної кільцевої системи з 1 або 2 кільцевих частин. Циклоалкільна група може мати один або більше подвійних зв'язків вуглець-вуглець у кільці, при умові, що їх присутність не перетворює кільце на ароматичне. Приклади циклоалкільних груп включають, але без обмеження, (C3-C7)циклоалкільні групи, такі як циклопропіл, циклобутил, циклопентил, циклогексил і циклогептил, та насичені циклічні і біциклічні терпени, і (C3-C7)циклоалкенільні групи, такі як циклопропеніл, циклобутеніл, циклопентеніл, циклогексеніл і циклогептеніл, та ненасичені циклічні і біциклічні терпени. Вираз "(C1-C3)алкіл" або "(C1-C3)алкокси" стосуються будь-якої групи, такої як метил, етил, n-пропіл, ізопропіл, метокси, етокси, n-пропокси та ізопропокси. Вираз "(C1-C2)галоалкокси" стосується (C1-C2)алкокси-групи, заміщеної на атомах вуглецю одним або більше атомами галогену. Такі групи включають, але без обмеження, трифторметокси, дифторметокси, 2,2-дифторетокси, 2,2,2-трифторетокси, 2-хлоретокси, 1фтор-2,2-дихлоретокси і подібне. Вираз "(C1-C2)галоалкіл" стосується C1-C2 галоалкільної групи, зокрема, CF3. Вираз "галоген" стосується атома фтору, хлору, брому або йоду. Вирази "алкіл", "(C1-C6)алкіл" або "алкокси" стосуються, якщо не забезпечено інше, будьякої прямої або розгалуженої C1-C6 алкільної або алкокси групи, отже, охоплює вищезгадані "(C1-C3)алкільні" або "(C1-C3)алкокси" групи, а також включає n-бутил, ізо-бутил, sec-бутил, tertбутил, n-пентил, n-гексил, n-бутокси, ізо-бутокси, sec-бутокси, tert-бутокси, n-пентилокси, nгексилокси і подібне. Кожна з вищеописаних (C1-C6)алкільних, арильних, гетероарильних, гетероциклоалкільних або циклоалкільних груп може бути факультативно додатково заміщена в кожному з їх вільних 7 UA 105018 C2 5 10 15 20 25 30 35 40 45 50 55 60 положень однією або більше групами, наприклад, 1-6 групами, вибраними з: галогену, карбокси, ціано, алкілу, поліфторованого алкілу, алкенілу, алкінілу, циклоалкілу, арилу, гетероарилу, алкіл-гетероарилу, гетероарил-алкілу, аміно-алкілу, аміногруп і їх похідних, таких як, наприклад, алкіламіно, діалкіламіно, ариламіно, діариламіно, уреїдо, алкілуреїдо або арилуреїдо; карбоніламіно групи і їх похідні, такі як, наприклад, форміламіно, алкілкарбоніламіно, алкенілкарбоніламіно, арилкарбоніламіно, алкоксикарбоніламіно; гідроксигруп і їх похідних, таких як, наприклад, алкокси, поліфторований алкокси, арилокси, гетероарилокси, алкілкарбонілокси, арилкарбонілокси або циклоалкілокси, гетероциклоалкілокси, арил-алкокси, гетероарил-алкокси; карбонільних груп і їх похідних, таких як, наприклад, алкілкарбоніл, арилкарбоніл, алкоксикарбоніл, арилоксикарбоніл, циклоалкілоксикарбоніл, амінокарбоніл, алкіламінокарбоніл, діалкіламінокарбоніл; похідних, що містять сірку, таких як, наприклад, алкілтіо, арилтіо, алкілсульфоніл, арилсульфоніл, алкілсульфініл, арилсульфініл, арилсульфонілокси, аміносульфоніл, алкіламіносульфоніл або діалкіламіносульфоніл. У свою чергу, якщо бажано, кожний з вищеописаних замісників може додатково заміщуватися однією або більше з вищезгаданих груп. Вираз "алкеніл" або "алкініл" стосуються, якщо не зазначено інше, будь-якої ненасиченої прямої або розгалуженої C2-C6 алкенільної або алкінільної групи, такої як, наприклад, вініл, аліл, 1-пропеніл, ізопропеніл, 1-, 2- або 3-бутеніл, пентеніл, гексеніл, етиніл, 1- або 2-пропініл, бутиніл, пентиніл, гексиніл і подібне. Вираз "поліфторований алкіл" або "поліфторований алкокси" стосується будь-якої прямої або розгалуженої C1-C6 алкільної або алкокси групи, як визначено вище, де більш ніж один атом водню заміщений атомами фтору, такої як, наприклад, трифторметил, трифторметокси, 2,2,2-трифторетил, 2,2,2-трифторетокси, 1,2-дифторетил, 1,1,1,3,3,3-гексафторпропіл-2-іл і подібне. Із усього вищеописаного фахівцям даної галузі зрозуміло, що будь-яка група, назва якої визначена як складена назва, така як, наприклад, циклоалкілалкіл, арилалкіл, гетероарилалкіл, алкілгетероарил, (C1-C3)алкоксіалкіл, алкілтіо, арилтіо, аміно-алкіл, алкіламіно, діалкіламіно, ариламіно, діариламіно, алкілуреїдо, арилуреїдо, алкілкарбоніламіно, алкенілкарбоніламіно, арилкарбоніламіно, арилокси, арилалкілокси, алкілкарбонілокси, алкоксикарбоніламіно; гетероарилокси, арилкарбонілокси, алкіліденамінокси; алкілкарбоніл, арилкарбоніл, алкоксикарбоніл, арилоксикарбоніл, циклоалкілоксикарбоніл, амінокарбоніл, алкіламінокарбоніл, діалкіламінокарбоніл, алкілсульфоніл, арилсульфоніл, алкілсульфініл, арилсульфініл, арилсульфонілокси, аміносульфоніл, алкіламіносульфоніл або діалкіламіносульфоніл і подібне, передбачається як умовно складена з частин, від яких вони походять. Дотепер, наприклад, вираз циклоалкілалкіл означає пряму або розгалужену алкільну групу, заміщену циклоалкільною групою, де алкіл і циклоалкіл є такими, як визначено вище. Аналогічно, вираз алкоксикарбоніл означає радикал, що містить алкокси-радикал, як визначено вище, приєднаний через атом кисню до карбонільного радикала. Вираз "приблизно" охоплює діапазон експериментальної помилки, яка може типово зустрічатися при вимірюванні. Вираз "група, що відходить", як використовується в даному документі, має те ж значення для фахівця даної галузі (Advanced Organic Chemistry: reactions, mechanisms and structure - Third Edition by Jerry March, John Wiley and Sons Ed.; 1985, page 179) і представляє групу, яка є частиною та приєднана до субстратної молекули; у реакції, де субстратна молекула зазнає реакції заміщення (наприклад, нуклеофілом), група, що відходить, потім заміщується. Переважними групами, що відходять, є галоген, сульфонові складні ефіри, такі як pтолуолсульфонат, p-бромбензолсульфонат, p-нітробензолсульфонат, метансульфонат, трифторметансульфонат,.... Вираз "фармацевтично прийнятні солі" стосується відносно нетоксичних мінеральних і органічних кислотно-адитивних солей і основно-адитивних солей сполук даного винаходу. Ці солі можна одержати in situ під час остаточного виділення і очищення сполук. Зокрема, кислотно-адитивні солі можна одержати окремою реакцією очищеної сполуки в її очищеній формі з органічною або мінеральною кислотою і виділенням утвореної в такий спосіб солі. Одержаними солями є, наприклад, гідрохлориди, гідроброміди, сульфати, гідросульфати, дигідрофосфати, цитрати, малеати, фумарати, трифторацетати, 2-нафталінсульфонати, паратолуолсульфонати. Даний винахід також стосується фармацевтично прийнятних солей з органічними або неорганічними основами. Зокрема, основно-адитивні солі можна одержати окремою реакцією очищеної сполуки в її очищеній формі з органічною або неорганічною основою і виділенням утвореної в такий спосіб солі. Одержаними солями є, наприклад, солі металу, зокрема, солі 8 UA 105018 C2 5 10 15 20 25 30 35 40 45 лужного металу, солі лужноземельного металу і солі перехідного металу (такого як натрій, калій, кальцій, магній, алюміній), або солі, одержані з основами, такими як аміак, або вторинні, або третинні аміни (такі як діетиламін, триетиламін, піперидин, піперазин, морфолін), або з основними амінокислотами, або з озамінами (такими як меглумін), або з аміноспиртами (такими як 3-амінобутанол і 2-аміноетанол). Даний винахід також стосується всіх ізомерів і їх домішок, таутомерних форм, рацемічних форм, енантіомерів, діастереоізомерів, епімерів, а також їх кристалічних форм, включаючи їх поліморфні форми, і їх сумішей. У випадках, коли сполуки можуть існувати в таутомерних формах, кожна форма розглядається як включена в даний винахід, або існуюча в рівновазі, або переважно в одній формі. Даний винахід спрямований не тільки на рацемічні суміші цих сполук, але також на окремі їх стереоізомери та/або діастереоізомери, а також і на їх суміші у всіх співвідношеннях. Аналогічно, метаболіти і фармацевтично прийнятні біопопередники (інакше названі як проліки) сполук формули (I) включені в обсяг і підходять для застосування в даному винаході. Так звані "проліки" сполук формули (I) також перебувають в обсязі даного винаходу. "Пролікарський засіб" є сполукою, яка метаболічно перетворюється на терапевтично активну сполуку після введення. Вираз "пролікарський засіб" має тлумачитися в даному документі так широко, як його звичайно розуміють в даному рівні техніки. Без намірів обмежити обсяг даного винаходу, перетворення може відбуватися за допомогою гідролізу біологічно лабільних груп in vivo. Наприклад, сполуку, що містить гідроксигрупу, можна вводити у вигляді складного ефіру, який перетворюється гідролізом in vivo на гідроксисполуку. Таким чином, певні похідні сполук формули (I), які самі можуть мати невелику або не мати фармакологічної активності, при введенні в організм можуть перетворюватися на сполуки формули (I), що мають бажану активність, наприклад, за допомогою гідролітичного розщеплення. Проліки відповідно до даного винаходу можуть, наприклад, бути одержані заміщенням відповідних функціональних груп, що присутні у сполуках формули (I), певними частинами, відомими фахівцям даної галузі техніки як прокомпоненти, як описано, наприклад, в Design of Prodrugs by H. Bundgaard (Elsevier, 1985) або в Prodrugs: design and clinical applications by Jarkko Rautio et al. (Nature reviews drug discovery, volume 7, March 2008, 255-270). Необмежувальні приклади проліків включають: i) складний ефір карбонової кислоти фенольної частини сполук формули (I); ii) складний ефір фосфату фенольної частини сполук формули (I); iii) фосфонооксиметиловий ефір фенольної частини сполук формули (I); iv) карбаматну похідну фенольної частини сполук формули (I). Переважними проліками є складний ефір карбонової кислоти або фосфату фенольної частини сполук формули (I). Не призначаючись для обмеження, складним ефіром може бути алкільний складний ефір, арильний складний ефір, гетероарильний складний ефір або неорганічний складний ефір. Акриламідо-похідні за даним винаходом мають наступну формулу (I): , де R, R', R", a і W є такими, як визначено вище. У переважному варіанті здійснення даний винахід забезпечує акриламідо-похідні формули (I), де: W є фенільним кільцем, заміщеним 1 або 2 групами R"; R є галогеном; (C1-C3)алкокси; (C1-C3)алкілом; R' є воднем; R" є незалежно вибраним з: галогену; (C1-C3)алкоксіалкілу; (C1-C2)галоалкілу або (CH2)n-x(CH2)m-Q, де: 9 UA 105018 C2 5 10 15 20 25 30 35 40 45 50 55 60 n дорівнює 0 або 1; m дорівнює 0 або 1; X є O; S; NH; N(C1-C3)алкілом; Q є арилом або гетероарилом. Навіть більш переважно, R є фтором; метокси; метилом; R" є галогеном або (CH2)n-X-(CH2)m-Q, де: n і m вибрані таким чином, що їх сума (n+m) дорівнює 1; X є O; і Q є арилом або гетероарилом; а також його ізомери, таутомери, рацемічні форми, енантіомери, діастереомери, епімери, поліморфи, їх суміші, проліки та їх фармацевтично прийнятні солі. В іншому переважному варіанті здійснення даний винахід забезпечує акриламідо-похідні формули (I), де: W є біциклічним арильним або біциклічним гетероарильним кільцем, факультативно заміщеним 1 або 2 групами R"; R є галогеном; (C1-C3)алкокси; (C1-C3)алкілом; R' є воднем; R" є незалежно вибраним з: галогену; (C1-C2)галоалкілу; 4-(C1-C3)алкілпіперазин-1-ілу або (CH2)n-X-(CH2)m-Q, де: n дорівнює 0 або 1; m дорівнює 0 або 1; X є O; S; NH; N(C1-C3)алкілом; Q є арилом або гетероарилом. Навіть більш переважно, W є біциклічним арильним або біциклічним гетероарильним кільцем, незаміщеним або заміщеним однієї групою (CH2)n-X-(CH2)m-Q, де: n і m вибрані таким чином, що їх сума (n+m) дорівнює 1; X є O; Q є арилом або гетероарилом; і факультативно заміщений другою групою R", вибраною з хлору; брому; (C1-C2)галоалкілу; 4-(C1-C3)алкілпіперазин-1-ілу; R є фтором; метокси; метилом; а також його ізомери, таутомери, рацемічні форми, енантіомери, діастереомери, епімери, поліморфи, їх суміші, проліки та їх фармацевтично прийнятні солі. Для посилання на будь-які специфічні сполуки формули (I) даного винаходу, факультативно, у формі фармацевтично прийнятної солі, дивись наступний експериментальний розділ. Специфічні необмежувальні приклади сполук формули (I) показані в наступному переліку: (E)-3-(3-Гідрокси-4-метокси-феніл)-N-нафталін-1-іл-акриламід; (E)-N-(2-Бензилокси-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[3-(4-метил-піперазин-1-іл)-феніл]-акриламід; (E)-N-(2-Хлор-піридин-4-іл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-N-(3-Хлор-2-метокси-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-N-(3,4-Дихлор-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-N-(3-Хлор-4-метокси-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-N-(2,3-Дихлор-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-N-(3-Бензиламіно-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-N-[3-(Бензил-метил-аміно)-феніл]-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-N-[2-Хлор-3-(піридин-4-ілметокси)-феніл]-3-(3-гідрокси-4-метокси-феніл)-акриламіду гідрохлорид; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-{3-[(піридин-4-ілметил)-аміно]-феніл}-акриламід; (E)-N-(3-Бензилокси-2-хлор-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-N-(2-Бензилокси-3-хлор-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-N-(1-Бензил-1H-індол-4-іл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-N-[3-Хлор-2-(піридин-4-ілметокси)-феніл]-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-N-[4-Хлор-3-(піридин-4-ілметокси)-феніл]-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-(1-метил-1H-індол-4-іл)-акриламід; (E)-N-(1-Бензил-1H-індол-7-іл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[3-(3-метил-3H-імідазол-4-ілметокси)-феніл]-акриламід; (E)-3-(4-Фтор-3-гідрокси-феніл)-N-(2-феноксиметил-феніл)-акриламід; 10 UA 105018 C2 5 10 15 20 25 30 35 40 45 50 55 60 (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[3-(1H-імідазол-4-ілметокси)-феніл]-акриламіду гідрохлорид; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[3-(піридин-4-ілоксиметил)-феніл]-акриламіду гідрохлорид; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-(3-оксазол-5-іл-феніл)-акриламід ; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-індан-1-іл-акриламід; (E)-N-(2-Бензилсульфаніл-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-(1-метил-1H-бензімідазол-2-іл)-акриламіду гідрохлорид; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-(2-феноксиметил-феніл)-акриламід; (E)-N-Бензоксазол-4-іл-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-N-(1-Бензил-1H-бензімідазол-4-іл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-(1-метил-1H-бензімідазол-4-іл)-акриламіду гідрохлорид; (E)-N-(1-Бензил-1H-індазол-7-іл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-(1-метил-1H-бензoтриазол-4-іл)-акриламід; (E)-N-(1-Бензил-1H-індазол-4-іл)-3-(3-гідрокси-4-метокси-феніл)-акриламіду гідрохлорид; (E)-N-(2-Бензил-2H-індазол-7-іл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-(2-метил-2H-індазол-7-іл)-акриламід; (E)-N-[3-(2,5-Диметил-2H-піразол-3-ілметокси)-феніл]-3-(3-гідрокси-4-метокси-феніл)акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[3-(1-метил-1H-імідазол-2-ілметокси)-феніл]-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[2-(3-метокси-феноксиметил)-феніл]-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[2-(2-метокси-феноксиметил)-феніл]-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[2-(4-метокси-феноксиметил)-феніл]-акриламід; (E)-N-(2-Циклобутоксиметил-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[2-(піридин-4-ілоксиметил)-феніл]-акриламіду гідрохлорид; (E)-N-[2-(4-Фтор-феноксиметил)-феніл]-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[2-(4-імідазол-1-іл-феноксиметил)-феніл]-акриламід; (E)-N-[2-(2-Фтор-феноксиметил)-феніл]-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-(2-метоксиметил-феніл)-акриламід; (E)-N-[2-(3-Фтор-феноксиметил)-феніл]-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-N-(3-Бром-феніл)-3-(4-фтор-3-гідрокси-феніл)-акриламід; (E)-N-(2-Бензилокси-феніл)-3-(4-фтор-3-гідрокси-феніл)-акриламід; (E)-N-(2,3-Дихлор-феніл)-3-(4-фтор-3-гідрокси-феніл)-акриламід; (E)-N-(1-Бензил-1H-індол-7-іл)-3-(4-фтор-3-гідрокси-феніл)-акриламід; (E)-N-(3-Фтор-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-N-(3-Хлор-феніл)-3-(3-гідрокси-феніл)-акриламід; (E)-N-(3-Хлор-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-N-(2-Хлор-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-N-(4-Хлор-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-(3-йод-феніл)-акриламід; (E)-N-(3-Бром-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-(3-ізопропокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-(3-фенокси-феніл)-акриламід; (E)-N-(3-Бензилокси-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-(3-метокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-(3-трифторметил-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[3-(піридин-4-ілметокси)-феніл]-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[3-(1-метил-піперидин-3-ілметокси)-феніл]-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[3-(піридин-4-ілокси)-феніл]-акриламід; (E)-N-(3,5-Дихлор-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[3-(1-метил-піперидин-4-ілокси)-феніл]-акриламід; (E)-N-(4-Бензилокси-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-N-(3-Хлор-феніл)-3-(3-гідрокси-4-метил-феніл)-акриламід; (E)-3-(4-Фтор-3-гідрокси-феніл)-N-нафталін-1-іл-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-(4-метокси-піримідин-2-іл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[3-(1H-тетразол-5-ілметокси)-феніл]-акриламід; (E)-N-(3-Хлор-феніл)-3-(4-фтор-3-гідрокси-феніл)-акриламід; 11 UA 105018 C2 5 10 15 20 25 30 35 40 45 50 55 60 (E)-3-(3-Гідрокси-4-метокси-феніл)-N-(2-фенетилокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[2-(піридин-4-ілметокси)-феніл]-акриламіду гідрохлорид; (E)-3-(4-Фтор-3-гідрокси-феніл)-N-[3-(піридин-4-ілметокси)-феніл]-акриламіду гідрохлорид; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[3-(піридин-4-ілметилсульфаніл)-феніл]-акриламіду гідрохлорид; (E)-N-1,3-Бензодіоксол-5-іл-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-(1-метил-1H-індазол-7-іл)-акриламід; (E)-N-(4-Етокси-1-метил-1H-індазол-7-іл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-(1-метил-1H-індазол-4-іл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[3-(5-метил-фуран-2-ілметокси)-феніл]-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[3-(піридин-3-ілметокси)-феніл]-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-(3-фенетилокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[3-(піридин-2-ілметокси)-феніл]-акриламід; (E)-N-(5-Хлор-2-феноксиметил-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[4-(4-метил-піперазин-1-іл)-2-феноксиметил-феніл]акриламіду гідрохлорид; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[2-(3-трифторметил-феноксиметил)-феніл]-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[2-(3-хлор-феноксиметил)-феніл]-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[2-(4-морфолін-4-ілметил-феноксиметил)-феніл]акриламіду гідрохлорид; (E)-3-(4-Фтор-3-гідрокси-феніл)-N-{2-[4-(1-метил-піперидин-4-ілокси)-феноксиметил]-феніл}акриламіду трифторацетат; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[2-(2-трифторметил-феноксиметил)-феніл]-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-{2-[3-(піперидин-4-ілокси)-феноксиметил]-феніл}акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-{2-[4-(піперидин-4-ілокси)-феноксиметил]-феніл}акриламіду гідрохлорид; (E)-3-(4-Хлор-3-гідрокси-феніл)-N-{2-[3-(піперидин-4-ілокси)-феноксиметил]-феніл}акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-{2-[4-(1-метил-піперидин-4-іл)-феноксиметил]-феніл}акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-{2-[2-(4-метил-піперазин-1-іл)-феноксиметил]-феніл}акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-{2-[3-(1-метил-піперидин-4-ілокси)-феноксиметил]феніл}-акриламіду гідрохлорид; (E)-3-(4-Хлор-3-гідрокси-феніл)-N-(3-хлор-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-{2-[3-(4-метил-імідазол-1-іл)-феноксиметил]-феніл}акриламід; (E)-3-(2-Хлор-3-гідрокси-4-метокси-феніл)-N-(3-хлор-феніл)-акриламід; (E)-3-(4-Фтор-3-гідрокси-феніл)-N-[3-(піридин-4-ілметилсульфаніл)-феніл]-акриламід; (E)-N-(1-Бензил-1H-індазол-7-іл)-3-(4-фтор-3-гідрокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-{2-[4-(1-метил-піперидин-4-ілокси)-феноксиметил]феніл}-акриламіду гідрохлорид; (E)-N-(3-Бензил-3H-бензoімідазол-4-іл)-3-(4-фтор-3-гідрокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[2-(4-трифторметил-феноксиметил)-феніл]-акриламід; (E)-N-[2-(2-Хлор-феноксиметил)-феніл]-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[1-(4-імідазол-1-іл-бензил)-1H-індол-7-іл]-акриламід; (E)-3-(4-Фтор-3-гідрокси-феніл)-N-[1-(4-імідазол-1-іл-бензил)-1H-індол-7-іл]-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-{2-[4-(1-метил-піперидин-4-ілметил)-феноксиметил]феніл}-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-{2-[3-(4-метил-піперазин-1-іл)-феноксиметил]-феніл}акриламіду гідрохлорид; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-{2-[4-(4-метил-імідазол-1-іл)-феноксиметил]-феніл}акриламіду гідрохлорид; (E)-N-(1-Бензил-2-оксо-2,3-дигідро-1H-індол-7-іл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-N-(3-Хлор-нафталін-1-іл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[2-(2-метил-2H-піразол-3-ілоксиметил)-феніл]акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[2-(3-піперазин-1-іл-феноксиметил)-феніл]-акриламід; 12 UA 105018 C2 5 10 15 20 25 30 35 40 45 50 55 60 (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[1-(1-метил-1H-імідазол-4-ілметил)-1H-індол-7-іл]акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[1-(1-метил-1H-піразол-3-ілметил)-1H-індол-7-іл]акриламід; (E)-3-(3-Гідрокси-феніл)-N-(2-феноксиметил-феніл)-акриламід; (E)-N-(3-Хлор-феніл)-3-(2,4-дифтор-3-гідрокси-феніл)-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[2-(4-піролідин-1-ілметил-феноксиметил)-феніл]акриламіду гідрохлорид; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-{2-[4-(4-метил-піперазин-1-ілметил)-феноксиметил]феніл}-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[2-(4-піперидин-1-ілметил-феноксиметил)-феніл]акриламіду трифторацетат; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-{1-[3-(1-метил-піперидин-4-ілокси)-бензил]-1H-індол-7іл}-акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-{2-[2-(1-метил-піперидин-4-ілокси)-феноксиметил]феніл}-акриламід (E)-3-(3-Гідрокси-4-метокси-феніл)-N-{2-[3-(1-метил-піперидин-4-іл)-феноксиметил]-феніл}акриламід; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-{2-[4-(4-метил-піперазин-1-іл)-феноксиметил]-феніл}акриламіду трифторацетат; (E)-3-(4-Фтор-3-гідрокси-феніл)-N-[2-(4-імідазол-1-іл-феноксиметил)-феніл]-акриламід; (E)-3-(2,4-Дифтор-3-гідрокси-феніл)-N-{2-[3-(1-метил-піперидин-4-ілокси)-феноксиметил]феніл}-акриламід; (E)-3-(2-Хлор-3-гідрокси-4-метокси-феніл)-N-{2-[3-(1-метил-піперидин-4-ілокси)феноксиметил]-феніл}-акриламід; (E)-N-(3-Хлор-феніл)-3-(4-ціано-3-гідрокси-феніл)-акриламід; (E)-3-(4-Ціано-3-гідрокси-феніл)-N-{2-[3-(1-метил-піперидин-4-ілокси)-феноксиметил]-феніл}акриламід; (E)-3-(2,4-Дифтор-3-гідрокси-феніл)-N-{2-[3-(піперидин-4-ілокси)-феноксиметил]-феніл}акриламід; (E)-3-(2,4-Дифтор-3-гідрокси-феніл)-N-{2-[4-(1-метил-піперидин-4-ілокси)-феноксиметил]феніл}-акриламід; (E)-3-(2,4-Дифтор-3-гідрокси-феніл)-N-{2-[4-(піперидин-4-ілокси)-феноксиметил]-феніл}акриламід; (E)-3-(2-Хлор-3-гідрокси-4-метокси-феніл)-N-{2-[3-(піперидин-4-ілокси)-феноксиметил]феніл}-акриламід; (E)-3-(4-Ціано-3-гідрокси-феніл)-N-{2-[3-(піперидин-4-ілокси)-феноксиметил]-феніл}акриламід; (E)-3-(4-Ціано-3-гідрокси-феніл)-N-{2-[4-(1-метил-піперидин-4-ілокси)-феноксиметил]-феніл}акриламід; (E)-N-(3-Бензил-3H-бензoімідазол-4-іл)-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-N-[2-(4-Хлор-феноксиметил)-феніл]-3-(3-гідрокси-4-метокси-феніл)-акриламід; (E)-N-(3-Хлор-феніл)-3-(3-гідрокси-4-сульфамоїл-феніл)-акриламід; Натрію (E)-5-(3-(3-хлорфеніламіно)-3-оксопроп-1-еніл)-2-метоксифеніл фосфат; (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[1-(3-метил-3H-імідазол-4-ілметил)-1H-індол-7-іл]акриламід; (E)-N-(3-Хлор-феніл)-3-(4-аміно-3-гідрокси-феніл)-акриламід. А також ізомери, таутомери, рацемічні форми, енантіомери, діастереомери, поліморфи, суміші, проліки та їх фармацевтично прийнятні солі. Даний винахід також стосується способів одержання сполук загальної формули (I), як визначено вище, наступними способами (Спосіб A і Спосіб B), які можна за способами, добре відомими фахівцю у даній галузі техніки. Наступні способи представлені для ілюстративних цілей. Залежно від природи сполук формули (I), які належить одержати, представлена методика може бути адаптована фахівцем у даній галузі техніки шляхом вибору придатних вихідних матеріалів, у яких природа замісників R, R', R" і W може бути модифікованою. Додаткова мета даного винаходу представлена способом одержання сполук формули (I), проліків і їх фармацевтично прийнятних солей (Спосіб A), при якому: (a) приводять у реакцію гідроксикоричну кислоту формули (II), де R і R' є такими, як визначено вище у формулі (I), із захисним засобом гідроксилу для одержання відповідної захищеної сполуки формули (III) 13 UA 105018 C2 , де R і R' є такими, як визначено вище, і PG є зазначеною захисною групою; (b) активують карбоксильну частину сполуки формули (III) для амідування, щоб одержати сполуку формули (V) 5 10 15 20 25 30 , де LG є будь-якою придатною активаційною групою карбоксильної частини, і R, R' і PG є такими, як визначено вище у формулі (III); (с) ацилюють аміносполуку формули (IV), де W, R" і a є такими, як визначено вище у формулі (I), зі сполукою формули (V) для одержання сполуки формули (VI), де R, R', R", W, a і PG є такими, як визначено вище; , (d) видаляють захисну групу PG зі сполуки формули (VI) для одержання сполуки формули (I) і, за потреби, перетворюють сполуку формули (I) на іншу сполуку формули (I), або перетворюють сполуку формули (I) на фармацевтично прийнятну сіль, або перетворюють її сіль на вільну сполуку формули (I). Згідно з етапом (a) способу захист фенольного гідроксилу сполуки формули (II) можна виконати різними способами, добре відомими фахівцю в даній галузі техніки (Theodora W. Greene, Peter G. M. Wuts, Protective Groups in Organic Synthesis, Wiley- Interscience). Наприклад, сполуку формули (II) можна обробити ацилхлоридом або ангідридом карбонової кислоти в присутності основи для одержання відповідного фенольного складного ефіру. Реакцію проводять у придатному розчиннику, такому як полярні апротонні розчинники, наприклад, дихлорметан, тетрагідрофуран, 1,4-діоксан, N,N'-диметилформамід, у присутності основи, такої як гідрид натрію або калію, або tert-бутилат калію, при температурі в діапазоні від кімнатної температури до температури дефлегмації розчинника протягом часу від приблизно 30 хвилин до 18 годин. Переважно, етап (a) здійснюють шляхом реакції сполуки формули (II) з оцтовим ангідридом у присутності гідриду металу, такого як гідрид натрію або калію, у тетрагідрофурані або 1,4діоксані при температурі в діапазоні від кімнатної температури до температури дефлегмації. Згідно з етапом (b) способу одержане в такий спосіб фенол-захищену похідну карбонової кислоти формули (III) приводять у взаємодію з аніліном формули (IV) за допомогою дій згідно зі способами, добре відомими фахівцю у даній галузі техніки, для одержання карбоксамідопохідних. Наприклад, карбонова кислота (III) проміжним етапом перетворюється на придатний 14 UA 105018 C2 5 10 15 20 25 30 35 ацилюючий засіб (V), такий як ацилхлорид, який потім застосовують у реакції амідування. Типово, у сполуках формули (V) R" представляє атом галогену та, навіть більш переважно, атом хлору. Реакцію з'єднання проводять у придатному розчиннику, такому як полярні апротонні розчинники, наприклад, тетрагідрофуран, 1,4-діоксан, диметилформамід, дихлорметан або їх суміші, при температурі в діапазоні від приблизно 0 °C до дефлегмації і за час від приблизно 30 хвилин до 96 годин, якщо потрібно, у присутності придатного поглинача протонів, такого як триетиламін, N,N-діізопропілетиламін або піридин. Згідно з етапом (d) способу фенольну захисну групу сполуки формули (VI) вибірково видаляють для одержання відповідного фенолу формули (I). Залежно від природи захисної групи її видалення можна проводити при різних умовах, таких як, наприклад, кислотний або лужний гідроліз, гідрогеноліз або обробка фторидними солями. Переважно, у сполуках формули (VI) PG представляє фенольний складний ефір, який відповідним чином гідролізується або при кислотних, або при основних умовах. Типово, кислотний гідроліз можна провести обробкою соляною, метансульфоновою, трифтороцтовою кислотою та подібним у придатному розчинника, такого як полярні апротонні розчинники, наприклад, дихлорметан, або полярні протонні розчинники, наприклад, метанол або етанол, при температурі в діапазоні від приблизно 0 °C до кімнатної температури за час від приблизно 15 хвилин до 24 годин. Альтернативно, зі сполуки формули (VI) знімають захист при основних умовах, і діючи згідно із традиційними методиками, наприклад, обробкою водним гідроксидом натрію або калію в присутності придатного співрозчинника, такого як полярні протонні розчинники, наприклад, метанол, етанол, або полярні апротонні розчинники, наприклад, диметилформамід, 1,4-діоксан, або обробкою третинним аміном, таким як триетиламін або N,N-діізопропілетиламін, і застосовуючи спирт, такий як метанол або етанол, у якості розчинника. Зняття захисту може проходити при температурі в діапазоні від приблизно 0 °C до температури дефлегмації розчинника за час від приблизно 30 хвилин до 72 годин. Як зазначено вище, фахівцю даної галузі зрозуміло, що залежно від хімічної реакційної здатності похідних формул (II) і (IV) вищевказаних етапів захисту/зняття захисту, етап (a) і етап (d), фенольної частини в деяких випадках можна зручно уникнути, у такий спосіб дозволяючи пряму з’єднання карбонової кислоти (II) з аніліном (IV) при умовах, описаних вище для етапу (b), для безпосереднього утворення відповідної похідної формули (I). Так, згідно з додатковим варіантом здійснення даного винаходу спосіб одержання сполук формули (I), проліків і їх фармацевтично прийнятних солей містить етапи, на яких: (a) активують карбоксильну частину сполуки формули (II), як визначено вище, для амідування, щоб одержати сполуки формули (Va) , де R, R' і LG є такими, як визначено вище; (b) ацилюють аміносполуки формули (IV), як визначено вище, зі сполукою формули (Va) для одержання сполуки формули (I), як визначено вище, 40 , і, за потреби, перетворюють сполуку формули (I) на іншу сполуку формули (I), або перетворюють сполуку формули (I) на фармацевтично прийнятну сіль, або перетворюють її сіль на вільну сполуку формули (I). 15 UA 105018 C2 5 Згідно з додатковим варіантом здійснення даного винаходу забезпечують альтернативний спосіб одержання сполуки формули (I), проліків і їх фармацевтично прийнятних солей (Спосіб B), що містить етапи, на яких: (a) ацилюють аміносполуки формули (VII), де W, R" є такими, як визначено вище у формулі (I), a дорівнює 0, 1 або 2, і X є O або S, зі сполукою формули (V), як визначено вище, для одержання сполуки формули (VIII), де R, R', R", W, a, X і PG є такими, як визначено вище; 10 , (b) алкілують сполуку формули (VIII) зі сполукою формули (IX), де Y є будь-якою прийнятною групою, що відходить, або гідроксигрупою, m і Q є такими, як визначено вище у формулі (I), для одержання сполуки формули (X), де R, R', R", W, a, m, X, Q і PG є такими, як визначено вище; 15 , (с) видаляють захисну групу зі сполуки формули (X) для одержання сполуки формули (Ia), де R, R', R", W, a, m, X і Q є такими, як визначено вище, і, за потреби, перетворюють сполуку формули (Ia) на іншу сполуку формули (Ia), або перетворюють сполуку формули (Ia) на фармацевтично прийнятну сіль, або перетворюють її сіль на вільну сполуку формули (Ia) 20 25 30 35 . Згідно з етапом (a) способу з’єднання карбонової кислоти формули (V) з аніліном формули (VII) можна здійснити, як описано вище для Способу A, етап (c). Згідно з етапом (b) способу алкілування фенольної або тіофенольної частини сполуки формули (VIII) можна здійснити, наприклад, за допомогою реакції з придатною похідною галогеніду (IX) у присутності основи, або, альтернативно, реакцією з придатною гідрокси-похідною (IX) при умовах Міцунобу, як описано в Organic Syntheses, Coll. Vol. 7, p.501 (1990); Vol. 62, p.48 (1984) і Organic Syntheses, Coll. Vol. 10, p.482 (2004); Vol. 79, p.186 (2002). Типово, сполуки формули (VIII) обробляють придатною галогенідною похідною (IX) у присутності основи, такої як, наприклад, гідриди літію, натрію або калію, гідроксиди або карбонати, у придатному розчиннику, такому як полярні апротонні розчинники, наприклад, N,N'-диметилформамід, тетрагідрофуран або 1,4-діоксан, при температурі в діапазоні від приблизно 0 °C до температури дефлегмації розчинника за час від приблизно 30 хвилин до 48 годин. Альтернативно, етап (b) можна завершити з’єднанням фенольної або тіофенольної сполуки формули (VIII) з прийнятним активованим спиртом (IX) при стандартних умовах реакції Міцунобу, наприклад, за допомогою реакції з трифенілфосфіном і діетилазодикарбоксилатом при температурі в діапазоні від приблизно 0 °C до 80 °C у придатному розчиннику, такому як полярні апротонні або неполярні розчинники, наприклад, тетрагідрофуран або толуол, за час від приблизно 30 хвилин до 48 годин. Згідно з етапом (c) способу фенольну захисну групу сполуки формули (X) можна вибірково видалити для одержання відповідного фенолу формули (Ia), як описано вище для Способу A, 16 UA 105018 C2 5 10 15 20 25 етап (d). За потреби утворення солі сполуки формули (I) або перетворення її відповідної солі на вільну сполуку (I) згідно з етапом (d) способу можна легко здійснювати згідно з добре відомими фахівцю в даній галузі техніки способами. Фахівцю в даному рівні техніки зрозуміло, що якщо сполука формули (I), виготовлена згідно з вищеописаними способами (Спосіб A або Спосіб B), одержана у вигляді суміші ізомерів, їх розділення на окремі ізомери формули (I), що здійснюється допомогою традиційних методик, залишається в межах обсягу даного винаходу. Як буде оцінено фахівцем у даному рівні техніки, коли під час синтезу сполук формули (I) певні функціональні групи можуть викликати небажані побічні реакції, ці групи повинні бути належним чином захищені згідно з загальноприйнятими методиками. Аналогічно, перетворення цих сполук у відповідні незахищені сполуки можна проводити згідно з процедурами, добре відомими фахівцю у даному рівні техніки. Усі зі сполук формули (II), (III), (IV), (VII), (IX) відомі, або комерційно доступні, або можуть бути одержані з відомих сполук згідно зі стандартними процедурами. Наприклад, вихідні матеріали формули (IV), де W є фенілом, можна легко одержати, як викладено в Схемі 1 (A-D) нижче, починаючи з придатних комерційно доступних структурних елементів. Схема 1: Приклад синтезу вихідних матеріалів формули (IV), де W є фенілом Коли потрібно, проміжні похідні в Схемі 1 можуть додатково оброблятися, застосовуючи стандартні процедури синтезу. Як додатковий приклад, коли (гетеро)арилом-OH у Схемі 1 є резорцин, відповідні проміжні сполуки можна додатково обробити спиртом Rx-OH, де Rx є алкільною, циклоалкільною, гетероциклоалкільною, арил-алкільною або гетероарил-алкільною групою при стандартних умовах Міцунобу, для одержання вихідних матеріалів формули (IV), наведених у Схемі 2. Схема 2: Приклад синтезу вихідних матеріалів формули (IV), де W є фенілом, заміщеною похідною резорцину 17 UA 105018 C2 5 У якості додаткового прикладу вихідні матеріали формули (II) можна легко одержати, як викладено в схемі 3 нижче, шляхом з’єднання комерційно доступних або відомих бензальдегідів з малоновою кислотою при основних умовах. Схема 3: Приклад синтезу вихідних матеріалів формули (II) 10 У якості додаткового прикладу фосфатні складні ефіри проліків сполук формули (I) можна одержати, дотримуючись відомої процедури синтезу (J.Medchem. 2000, 43, 2731-2737), представленої в схемі 4. Схема 4: Приклад синтезу фосфатного складного ефіру сполук формули (I) Сполуки формули (I), як визначено вище, застосовуються в терапії як засоби проти MPTPзв'язаних хвороб у пацієнта. Більш конкретно, сполуки згідно з даним винаходом застосовні для одержання лікарського 18 UA 105018 C2 5 10 15 20 25 30 35 40 45 50 55 60 препарату для лікування ряду хвороб, таких як ті, що виникають у результаті ішемії та реперфузійного ушкодження або окисного ушкодження, хвороб, пов'язаних з віком, дегенеративних і нейродегенеративних хвороб, включаючи, але без обмеження: хворобу серця (гострий інфаркт міокарда, серцева недостатність), трансплантаційну хірургію (ішемія органа), ішемічне (напад) і травматичне ушкодження мозку, м'язову дистрофію Дюшена, уроджену м'язову дистрофію Ульріха, міопатію Бентама, бічний аміотрофічний склероз, хворобу Хантігтона, хворобу Альцгеймера, хворобу Паркінсона, діабети I типу і II типу, ускладнення діабету (діабетична ретинопатія, нефропатія), гіперглікемічне ушкодження тканини, гіпоглікемічне ушкодження тканини, холестаз, ушкодження, викликане алкоголем. Даний винахід також стосується способів інгібування MPTP і забезпечує спосіб для лікування хвороб і станів, пов'язаних з активністю пор переходу мітохондріальної проникності (MPTP). Такий спосіб включає введення ссавцю, що потребує цього, ефективної кількості сполуки формули (I). Вищеописаний спосіб дозволяє лікування розладів, що характеризуються ішемією/реперфузією, окисним або дегенеративним ушкодженням тканини, хвороб, пов'язаних з віком, дегенеративних і нейродегенеративних хвороб. У переважному варіанті здійснення способу, описаного вище, розладами є гострий інфаркт міокарда та діабетична ретинопатія. Інгібуюча активність і ефективність вибраних сполук визначені шляхом in vitro аналізу, який оцінює здатність сполук даного винаходу перешкоджати MPT у виділеній мітохондрії. Мітохондріальний in vitro аналіз: спосіб і результати Мітохондріальний in vitro аналіз заснований на вивченні фізіологічних процесів у виділених і функціональних мітохондріальних органелах. Можливо досліджувати багато мітохондріальних процесів, включаючи утримання кальцію і дихання, у суспензіях виділених мітохондрій, отриманих з різних тканин. Здатність виділеної мітохондрії поглинати кальцій ззовні є прямою мірою мітохондріальної цілісності і функції. Перевантаження кальцієм викликає MPT, який потім порушує мітохондріальну цілісність, погіршує здатність мітохондрії накачувати кальцій і викликає вивільнення накопиченого кальцію з мітохондріального матриксу. Аналіз використовує цей феномен поглинання кальцію, перевантаження і вивільнення у виділеній мітохондрії для оцінки здатності сполук даного винаходу інгібувати MPTP і попереджати MPT. Одержання мітохондрій мишачої печінки Мітохондрії одержували з печінок самців 129 або C57/B6 мишей вагою 20-25 г. Тварин умертвляли вивихом шиї. Виділяли печінку і розміщали на крижане середовище виділення (0,25 М сахарози, 10 мМ Tris-HCl, 0,1 мМ етилен-bis(оксоетиленнітрило)тетраоцтової кислоти (EGTA), pH 7,4). Печінки промивали три-чотири рази крижаним середовищем, різали ножицями і пропускали через ручний гомогенізатор Поттера, який тримали в крижаній бані. Гомогенат розбавили до 50 мл на печінку, а незруйновані клітини і ядра осадили за допомогою центрифугування при 900 x g в охолодженій центрифузі Beckman Avantitm J-25, яку тримали при 4 °C, протягом 10 хвилин. Супернатант обережно декантували і центрифугували при 7000 x g у тій же центрифузі протягом 10 хв. Супернатант видалили, осад мітохондрій обережно ресуспендували в крижаному середовищі виділення і центрифугували, як зазначено вище. Отриманий осад мітохондрій ресуспендували в невеликій кількості крижаного середовища виділення і зберігали на льоду. Вміст білка мітохондрії визначали за допомогою біуретового аналізу. Здатність утримувати кальцій (CRC) Здатність утримувати кальцій (CRC) мітохондрій є мірою чутливості схильності мітохондрій до відкриття MPTP після поглинання кальцію. У присутності позамітохондріального кальцію виділені мітохондрії поглинають кальцій у матрикс за допомогою уніпортера кальцію. Тривале додавання позамітохондріального кальцію і наступне поглинання призводить до викликаного кальцієм відкриття MPTP, втрати мітохондріальної цілісності і вивільнення накопиченого кальцію. Концентрація кальцію, який може утримуватися до викликаного кальцієм відкриття MPTP, виражається в здатності утримувати кальцій і виражена в нмоль кальцію на мг мітохондрій. CRC мітохондріальних препаратів (200 мкл суспензії 0,5 мг/мл) вимірювали 2+ флуориметрично в присутності флуоресцентного індикатору Ca (0,3 мкМ Calcium Green-5N), застосовуючи планшетний зчитувач Tecan Infinite F200 (збудження: 505 нм; емісія: 535 нм) (Ichas, F.; Jouaville, L.S.; Mazat, J.P. Mitochondria are excitable organelles capable of generating and conveying electrical and calcium signal. Cell. 1997, 89, 1145-1153). Calcium Green-5N є флуорометричним зондом, який не проникає через мембрани і при додаванні до 19 UA 105018 C2 2+ 5 10 15 20 25 30 35 40 45 50 55 60 мітохондріальної суспензії здатний виявляти присутність Ca у середовищі поза мітохондрією. Мітохондрії навантажували послідовними 10 мкМ імпульсами кальцію (1 мкл 2 мМ CaCl 2 в 200 мкл мітохондріальної суспензії) при інтервалах 1 хв., змішували і сигнал позамітохондріального кальцію вимірювали приблизно через 1 хв. після кожного додавання для полегшення мітохондріального поглинання (виконували на автоматизованій робочій станції Tecan Freedom 2+ Evo 200). При цих умовах мітохондрії активно поглинали і утримували Ca до точки, у якій 2+ мітохондрії піддавалися швидкому процесу вивільнення Ca , обумовленого відкриттям MPTP. Кінцевою концентрацією кальцію, необхідного для відкриття MPTP і вивільнення накопиченого 2+ кальцію, є мітохондріальна CRC. Цей протокол завантаження Ca , таким чином, забезпечує придатний і чутливий аналіз для вимірювання відкриття MPTP і застосовується для оцінки здатності сполук даного винаходу інгібувати відкриття MPTP. Сполуки (кінцева концентрація 1 мкМ) додавали безпосередньо в мітохондріальний розчин за 1 хв. до початку імпульсів кальцію і визначали кількість імпульсів кальцію, необхідних для відкриття PTP. Співвідношення між кількістю кальцію, необхідного для початку MPT у присутності сполуки (CRC i), відносно необхідного для того, щоб викликати MPT при відсутності сполуки (CRC о), є мірою інгібіторного ефекту сполуки на MPTP. Це значення назвали ефективністю CRC, і результати, одержані від кількох сполук даного винаходу, повідомили в біологічному прикладі 1. Ефективності сполук оцінили шляхом порівняння інгібіторної активності при 1 мкМ. Додатковий об'єкт даного винаходу представлений застосуванням сполуки загальної формули (I), як визначено вище, а також її ізомерів, рацемічних форм, таутомерів, енантіомерів, діастереомерів, епімерів, поліморфів, їх сумішей, проліків і їх фармацевтично прийнятних солей для одержання лікарського препарату для попередження та/або лікування хвороб і станів, пов'язаних з активністю MPT-пори. Забезпечений спосіб застосування сполуки згідно з даним винаходом для виготовлення лікарського препарату для застосування при лікуванні хворобливого стану, який, як відомо, опосередкований MPTP або яке, як відомо, лікується інгібіторами MPTP. Додатковим об'єктом даного винаходу є фармацевтична композиція, що містить у якості активного інгредієнта одну або більше сполук формули (I), як визначено вище, та/або проліки, та/або їх фармацевтично прийнятну сіль у комбінації з одним або кількома фармацевтично прийнятними наповнювачами. Фахівцю в даній галузі техніки відомий цілий ряд таких наповнювачів, що придатні для складання фармацевтичної композиції. Придатні фармацевтично прийнятні наповнювачі добре відомі фахівцям даної галузі техніки. Наповнювачі включають, у якості ілюстрації та без обмеження, розріджувачі, заповнювачі, аглютинуючі речовини, засоби, що поліпшують розпадання, інгібітори розпадання, прискорювачі абсорбції, допоміжна речовина, сполучні, носії, суспендуючі/диспергуючі засоби, плівкоутворювачі/покриття, адгезиви, антиадгезиви, засоби, що зволожують, змащувальні засоби, гліданти, консерванти, сорбенти, поверхнево-активні засоби, речовини, додані для маскування або нейтралізації неприємного смаку або запаху, ароматизатори, барвники, віддушки, ароматизуючі засоби, підсолоджувачі і речовини, додані для поліпшення зовнішнього вигляду композиції. Вибір наповнювача буде у великій мірі залежати від факторів, таких як конкретний спосіб введення, вплив наповнювача на розчинність і стабільність та природи лікарської форми. Фармацевтичні композиції даного винаходу можна вводити різними шляхами, включаючи пероральний, парентеральний, внутрішньовенний, підшкірний, внутрішньом'язовий, трансмукозальний (включаючи букальний, сублінгвальний, трансуретральний і ректальний), місцевий, трансдермальний, інгаляційний, через слизову оболонку або через шкіру, або застосовуючи будь-який інший шлях введення. Таким чином, вони будуть присутні у формі розчинів або суспензій для ін'єкції або багатодозових флаконів, у формі простих або покритих таблеток, таблеток, покритих цукром або плівкою, облаткових капсул, гелевих капсул, пігулок, крохмальних капсул, саше, порошків, гранул, болюсу, електуарію, пасти, супозиторіїв або ректальних капсул, сиропів, емульсій, розчинів або суспензій, для черезшкірного застосування в полярному розчиннику, або для застосування через слизову оболонку. Наприклад, тверді пероральні форми можуть містити разом з активною сполукою, розріджувачі, наприклад, карбонати лужноземельного металу, магнію фосфат, лактозу, декстрозу, тростинний цукор, сахарозу, целюлозу, похідні мікрокристалічної целюлози, крохмалі, кукурудзяний крохмаль або картопляний крохмаль, модифіковані крохмалі і подібне; змащувальні засоби, наприклад, діоксид кремнію, тальк, стеаринова кислота, магнію або кальцію стеарат та/або поліетиленгліколі; сполучні засоби, наприклад, крохмалі, аравійська камедь, желатинова метилцелюлоза, карбоксиметилцелюлоза або полівінілпіролідон; засоби, 20 UA 105018 C2 5 10 15 20 25 30 35 40 45 50 55 60 що поліпшують розпадання, наприклад, крохмаль, альгінова кислота, альгінати або гліколят натрієвого крохмалю; суміші, що виділяють бульбашки газу; барвники; підсолоджувачі; зволожувальні засоби, такі як лецитин, полісорбати, лаурилсульфати і, в основному, нетоксичні і фармакологічно неактивні речовини, що застосовуються у фармацевтичних складах. Ці фармацевтичні препарати можна виготовити відомим способом, наприклад, за допомогою процесів змішування, гранулювання, таблетування, покриття цукром або покриття плівкою. Рідкими дисперсіями для перорального введення можуть бути, наприклад, сиропи, емульсії і суспензії. Наприклад, сиропи можуть містити в якості носія сахарозу, або сахарозу із гліцерином та/або манітом, і сорбіт. Суспензії і емульсії можуть містити як приклади носіїв натуральну камедь, агар, альгінат натрію, пектин, метилцелюлозу, карбоксиметилцелюлозу або полівініловий спирт. Суспензія або розчини для внутрішньом'язових ін'єкцій можуть містити разом з активною сполукою фармацевтично прийнятний носій, наприклад, стерильну воду, маслинове масло, етилолеат, гліколі, наприклад, пропіленгліколь і, за потреби, придатну кількість лідокаїну гідрохлориду. Розчини для внутрішньовенних ін'єкцій або інфузій можуть містити в якості носія стерильну воду, або переважно вони можуть бути у формі стерильних водних ізотонічних сольових розчинів, або вони можуть містити пропіленгліколь у якості носія. Супозиторії можуть містити разом з активною сполукою фармацевтично прийнятний носій, наприклад, какао-масло, поліетиленгліколь, поверхнево-активну речовину поліоксиетиленового складного ефіру сорбітану і жирної кислоти або лецитин. Вищеописані компоненти для фармацевтичної композиції, що вводиться, є лише типовими представниками. Додаткові матеріали, а також методики обробки і подібне викладені частково в th 5 частині Remington's Pharmaceutical Sciences, 20 Edition, 2000, Merck Publishing Company, Easton, Pennsylvania, яка включена в даний документ за допомогою посилання. Сполука даного винаходу формули (I) може також вводитися у формах тривалого вивільнення або з систем доставки лікарського засобу тривалого вивільнення. Опис типових матеріалів тривалого вивільнення можна також знайти у включених матеріалах в Remington's Pharmaceutical Sciences. Фармацевтичні композиції, що містять сполуки даного винаходу, звичайно одержують, дотримуючись загальноприйнятих способів, і вводять у придатній фармацевтичній формі. Тверді композиції для перорального введення можна одержати звичайним змішуванням, наповненням або пресуванням. Можна повторювати операції змішування, щоб диспергувати активний засіб у композиціях, що містять високі кількості наповнювачів. Ці співвідношення є загальноприйнятими. Рідкі пероральні препарати можна скласти, наприклад, як водні або масляні суспензії або розчини, емульсії, сиропи або еліксир, або можна представити як ліофілізований продукт, який відновлюють додаванням води або придатного носія перед застосуванням. Зазначені рідкі препарати можуть містити стандартні добавки, такі як суспендуючі засоби, наприклад сорбіт, сироп, метилцелюлозу, желатин, гідроксиетилцелюлозу, карбоксиметилцелюлозу, гель стеарату алюмінію або гідрогенізовані харчові жири, емульгуючі засоби, наприклад, лецитин, сорбітан моноолеат або гуміарабік; неводні носії (які можуть включати харчові масла), наприклад, мигдальне масло, фракціоноване кокосове масло, масляні складні ефіри, такі як гліцеринові складні ефіри, пропіленгліколь або етиловий спирт; консерванти, наприклад, метилабо пропіл-p-гідроксибензоат або сорбінова кислота, і, за потреби, загальноприйняті речовини для надання смаку і барвники. Для парентерального введення можна одержати рідкі одиниці дозування, що містять сполуку і стерильний носій. Сполуку залежно від вибраного носія і концентрації можна суспендувати або розчинити. Парентеральні розчини звичайно готують шляхом розчинення сполуки в носії, стерилізації фільтрацією, заповнення в придатні посудини і запаювання. Переважно, також можна розчинити в носії придатні допоміжні речовини, такі як місцеві анестетики, консерванти і буферні засоби. Для підвищення стабільності композицію можна заморозити після заповнення посудини і видалити воду під вакуумом. Парентеральні суспензії готують, в основному, тим же способом, з тією відмінністю, що сполуку можна скоріше суспендувати, ніж розчинити в носії, і їх можна стерилізувати обробкою етиленоксидом перед суспендуванням у стерильному носії. Переважно, у композицію можна включити поверхневоактивну речовину або зволожуючий засіб з метою полегшення рівномірного розподілу сполуки даного винаходу. Сполуки даного винаходу також можна вводити місцево. Місцеві склади можуть містити, наприклад, мазь, крем, гель, лосьйон, розчин, пасту або подібне, та/або можуть бути одержані так, щоб містити ліпосоми, міцели та/або мікросфери. Мазі, як добре відомо в галузі техніки 21 UA 105018 C2 5 10 15 20 25 30 35 40 45 50 55 60 фармацевтичних складів, є напіврідкими препаратами, які типово основані на вазеліні або інших нафтових похідних. Приклади мазей включають маслянисті основи мазей, наприклад, рослинні олії, жири, одержані із тварин, і напіврідкі вуглеводні, одержані з нафти, емульговані основи мазей, наприклад, гідроксистеарину сульфат, безводний ланолін і гідрофільний вазелін, емульсійні основи мазей, наприклад, цетиловий спирт, гліцерилмоностеарат, ланолін та стеаринова кислота, і водорозчинні основи мазей, одержані з поліетиленгліколів різної молекулярної ваги. Креми, як також добре відомо фахівцям даної галузі техніки, є в’язкими рідинами або напіврідкими емульсіями і містять масляну фазу, емульгатор і водну фазу. Масляна фаза звичайно містить вазелін і жирний спирт, такий як цетиловий або стеариловий спирт. Водна фаза звичайно містить зволожувач. Емульгатор у складі крему вибраний з неіонних, аніонних, катіонних або амфотерних поверхнево-активних речовин. Однофазні гелі містять органічні макромолекули, розподілені, в основному, однорідно по всьому рідкому носію, який типово є водним, але також, переважно, містить спирт і, факультативно, масло. Переважними гелеутворюючими засобами є поперечно-зшиті акриловокислотні полімери (такі як "карбомерні" полімери, наприклад, карбоксиполіалкілени, які можуть бути одержані комерційно під торгівельною назвою Carbopol). Також переважними є гідрофільні полімери, такі як поліетиленоксиди, співполімери поліоксиетилену та поліоксипропілену і полівініловий спирт; целюлозні полімери, такі як гідроксипропілцелюлоза, гідроксиетилцелюлоза, гідроксипропілметилцелюлоза, гідроксипропілметилцелюлози фталат і метилцелюлоза; камеді, такі як трагакантова і ксантанова камедь; альгінат натрію і желатин. Для одержання однорідних гелів, можна додати диспергуючі засоби, такі як спирт або гліцерин, або гелеутворюючий засіб можна диспергувати перетиранням на порошок, механічним змішуванням та/або перемішуванням. Сполуки даного винаходу можна також вводити шляхом трансдермального вивільнення. Типові трансдермальні склади включають традиційні водні і неводні переносники, такі як креми, масла, лосьйони або пасти, або можуть бути забезпечені у вигляді мембран або медикаментозних пластирів. У варіанті здійснення сполука даного винаходу диспергована в чутливому до тиску пластирі, приклеєному до шкіри. Цей склад дозволяє сполуці проникати з пластиру пацієнту через шкіру. Для одержання лікарського засобу тривалого вивільнення через шкіру, може використовуватися натуральний каучук і силікон в якості клейких речовин, чутливих до тиску. Сполуки формули (I) даного винаходу, що придатні для введення ссавцю, наприклад, людям, можна вводити звичайними шляхами, і рівень дозування залежить від ряду факторів, включаючи активність конкретної застосовуваної сполуки; вік, вагу тіла, загальний стан здоров'я, стать і харчування пацієнта, що одержує лікування; час і шлях введення; швидкість екскреції; інші лікарські засоби, які раніше були введені; і тяжкість конкретного захворювання, що підлягає терапії, як добре зрозуміло фахівцям у даному рівні техніки. Наприклад, придатне дозування затверджене для перорального введення сполуки формули (I), може знаходитися в діапазоні від приблизно 30 до 500 мг на дозу від 1 до 5 разів щодня. В основному будуть вводитися більш низькі дози, коли застосовують парентеральний шлях. Таким чином, наприклад, для внутрішньовенного введення буде звичайно застосовуватися доза в діапазоні, наприклад, від 0,5 мг до 30 мг на кг ваги тіла. Сполуки даного винаходу можна вводити в ряді лікарських формах, наприклад, перорально у формі таблеток, таблеток, покритих цукром або плівкою, капсул, крохмальних капсул, як порошок або гранули; як сиропи, емульсії, розчин або суспензія у водній або неводній рідині, як емульсія масло-у-воді або емульсія вода-у-маслі, як болюс, електуарій або паста; ректально у формі супозиторіїв; парентерально, наприклад, внутрішньом'язово або шляхом внутрішньовенної ін'єкції або інфузії. З метою кращої ілюстрації даний винахід, без будь-якого його обмеження, представлені наступні приклади. Приклади Способи Якщо не зазначено інше, було встановлено, що всі вихідні реагенти є комерційно доступними або легко одержуються наступними стандартними описаними методиками, і застосовуються без будь-якого попереднього очищення. Спектри ¹H-NMR (ядерно-магнітний резонанс) одержували з Bruker 400 Мгц. Хімічні зсуви виражали в частинах на мільйон (ppm, δ одиниці). Константи з’єднання виражені в герцах (Гц), і патерни розщеплення описані як s (синглет), bs (широкий синглет), d (дуплет), t (триплет), q (квартет), quint (квінтет), m (мультиплет). LC-MS (рідинна хроматографія-мас-спектрометрія) експерименти виконали згідно з 22 UA 105018 C2 5 10 15 20 25 30 35 40 45 наступними способами. Спосіб_A - 220: Waters Acquity UPLC, Waters SQD Single Quadrupole. Колонка Acquity UPLCBEH C18 50 x 2,1 мм x 1,7 мкм. Швидкість потоку: 0,6 мл/хв. Рухлива фаза: A фаза=вода/CH 3CN 95/5 + 0,07% TFA; B фаза=CH3CN + 0,05% TFA. Градієнт: 0 хв. (A: 98%, B: 2%), 3 хв. (A: 0%, B: 100%), 3,5 хв. (A: 0%, B: 100%). Довжина хвилі УФ визначення: 220 нм. Об'єм введення: 0,5 мкл. Спосіб_N - 254: Waters Acquity UPLC, Micromass ZQ 2000 Single Quadrupole (Waters). Колонка Acquity UPLC-BEH C18 50 x 2,1 мм x 1,7 мкм. Швидкість потоку: 0,6 мл/хв. співвідношення розщеплення MS: відходи/1:4. Рухлива фаза: A фаза=вода/CH3CN 95/5 + 0,1% TFA; B фаза=вода/CH3CN 5/95 + 0,1% TFA. Градієнт: 0-0,25 хв. (A: 95%, B: 5%), 0,25-3,30 хв. (A: 0%, B: 100%), 3,30-4,00 хв. (A: 0%, B: 100%). Довжина хвилі УФ визначення: 254 нм. Об'єм введення: 2 мкл. Спосіб_N1: Waters Acquity UPLC, Micromass ZQ 2000 Single Quadrupole (Waters). Колонка Acquity UPLC-BEH C18 50 x 2,1 мм x 1,7 мкм. Швидкість потоку: 0,6 мл/хв. співвідношення розщеплення MS: відходи/1:4. Рухлива фаза: A фаза=вода/MeOH 95/5 + 0,1% мурашина кислота; B фаза=вода/CH3CN 5/95 + 0,1% мурашина кислота. Градієнт: 0-0,25 хв. (A: 95%, B: 5%), 0,25-3,30 хв. (A: 0%, B: 100%), 3,30-4,00 хв. (A: 0%, B: 100%). Довжина хвилі УФ визначення: 254 нм. Об'єм введення: 2 мкл. Спосіб_N2: Waters 1525 ВЕРХ насос, з'єднаний з PDA (996 Waters) детектором і Single Quadrupole ZQ (Waters). Довжина хвилі УФ визначення 254 нм або BPI; ESI+ визначення 3,2KV, 25V, 350 °C. Швидкість потоку: 2,0 мл/хв. Колонка Xbridge C8 3,5мкм 50 x 4,6 мм. Рухлива фаза: A фаза=вода + 0,1% TFA; B фаза=CH3CN + 0,1% TFA. Градієнт: 0-1 хв. (A: 95%, B: 5%), 1-7,5 хв. (A: 0%, B: 100%), 7,5-8,5 хв. (A: 0%, B: 100%). Довжина хвилі УФ визначення: 254 нм. Об'єм введення: 2 мкл. Спосіб_N3: Waters Acquity UPLC, Micromass ZQ 2000 Single Quadrupole (Waters). Колонка Acquity UPLC-BEH C18 50 x 2,1 мм x 1,7 мкм. Швидкість потоку: 0,6 мл/хв. Рухлива фаза: A фаза=вода/CH3CN 95/5 + 0,1% TFA; B фаза=вода/CH3CN 5/95 + 0,1% TFA. Градієнт: 0-0,50 хв. (A: 95%, B: 5%), 0,50-6,00 хв. (A: 0%, B: 100%), 6,00-7,00 хв. (A: 0%, B: 100%). Об'єм введення: 2 мкл. Довжина хвилі УФ визначення 254 нм або BPI; ESI+ визначення 3,2KV, 25V, 350ºC. Спосіб_N4: Waters Acquity UPLC, Micromass ZQ 2000 Single Quadrupole (Waters). Колонка Acquity UPLC-BEH C18 50 x 2,1 мм x 1,7 мкм. Швидкість потоку: 0,6 мл/хв. співвідношення розщеплення MS: відходи/1:4. Рухлива фаза: A фаза=вода/MeOH 95/5 + 0,1% мурашина кислота; B фаза=вода/CH3CN 5/95 + 0,1% мурашина кислота. Градієнт: 0-0,5 хв. (A: 95%, B: 5%), 0,5-6,0 хв. (A: 0%, B: 100%), 6,0-7,0 хв. (A: 0%, B: 100%). Довжина хвилі УФ визначення: 254 нм. Об'єм введення: 2 мкл. Спосіб_N5: Waters 1525 ВЕРХ насос, з'єднаний з PDA (996 Waters) детектором і Single Quadrupole ZQ (Waters). Довжина хвилі УФ визначення 254 нм або BPI; ESI+ визначення 3,2KV, 25V, 350ºC. Швидкість потоку: 0,4 мл/хв. Колонка Synergy 2,5 мкм 20 x 2,0 мм. Рухлива фаза: A фаза=вода/CH3CN 95/5 + 0,1% TFA; B фаза=вода/CH3CN 5/95 + 0,1% TFA. Градієнт: 0-0,2 хв. (A: 95%, B: 5%), 0,2-5 хв. (A: 0%, B: 100%), 5-6 хв. (A: 0%, B: 100%). Довжина хвилі УФ визначення: 254 нм. Об'єм введення: 2 мкл. Наступні абревіатури стосуються відповідно до визначень нижче: AcOEt (етилацетат); DIPEA (діізопропілетиламін); DCM (дихлорметан); DMF (диметилформамід); год. (година); год. (години); EDC (1-етил-3-(3диметиламінопропіл)карбодіімід); EtOH (етанол); HOBT (гідроксибензoтриазол); MeOH (метанол); хв. (хвилини); RT (кімнатна температура); rt (час утримання); SCX (сильний катіонообмінник); TEA (триетиламін); ТГФ (тетрагідрофуран). Приклад 1 Одержання заміщених (E)-3-(3-гідрокси-феніл)-акрилових анілідів із відповідних (E)-3-(3ацетокси-феніл)-похідних лужним гідролізом 50 (1) (E)-3-(3-Гідрокси-4-метокси-феніл)-N-нафталін-1-іл-акриламід 23 UA 105018 C2 5 10 15 20 25 30 35 Суспензію (E)-3-(3-ацетокси-4-метокси-феніл)-N-нафталін-1-іл-акриламіду (254 мг, 0,70 ммоль) в суміші MeOH (4,5 мл) та 50% вага/вага водного NaOH (74 мкл) нагрівали при перемішуванні протягом 40 хв. При температурі дефлегмації. Суміш потім концентрували при зниженому тиску для одержання світло-жовтого масла, яке поглинули і перетерли на порошок з 4 мл водної 0,5 н HCl. Після фільтрування та сушіння 213 мг названого (E)-3-(3-гідрокси-4метокси-феніл)-N-нафталін-1-іл-акриламіду одержали у вигляді білого порошку. 1 H NМР R(DMSO-d6) δ (ppm): 10,04 (s, 1H), 9,24 (s, 1H), 8,16 (d, J=8,4 Гц, 1H), 7,96-7,94 (m, 1H), 7,90 (d, J=7,2 Гц, 1H), 7,76 (d, J=8,4 Гц, 1H), 7,60-7,47 (m, 4H), 7,10-7,06 (m, 2H), 6,99 (d, J=8,0 Гц, 1H), 6,93 (d, J=15,6 Гц, 1H), 3,83 (s, 3H). LC-MS: Спосіб_A - 220, rt=1,68 (ES+) [2M+Na]+: 661 Аналогічно гідролізом відповідних (E)-3-(3-ацетокси-феніл)-акрилових анілідів одержали наступні сполуки: (2) (E)-N-(2-Бензилокси-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід (очищення колонковою хроматографією на силікагелі, елюант n-гексан/AcOEt 65:35) 1 H NМR (DMSO-d6) δ (ppm): 9,25 (s, 1H), 9,17 (s, 1H), 8,06 (d, J=7,2 Гц, 1H), 7,52-7,50 (m, 2H), 7,43-7,36 (m, 3H), 7,32-7,28 (m, 1H), 7,09-7,00 (m, 4H), 6,98-6,89 (m, 3H), 5,25 (s, 2H), 3,81 (s, 3H). LC-MS: Спосіб_A - 220, rt=2,08 (ES+) [2M+Na]+: 773 (3) (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[3-(4-метил-піперазин-1-іл)-феніл]-акриламід (з наступною нейтралізацією гідрохлориду) 1 H NMR (DMSO-d6) δ (ppm): 9,97 (s, 1H), 9,23 (s, 1H), 7,40 (d, J=15,6 Гц, 1H), 7,36 (s, 1H), 7,16-7,12 (m, 1H), 7,10 (d, J=8,0 Гц, 1H), 7,02 (d, J=8,4 Гц, 2H), 6,97 (d, J=8,0 Гц, 1H), 6,66 (d, J=8,0 Гц, 1H), 6,59 (d, J=15,6 Гц, 1H), 3,81 (s, 3H), 3,15 (bs, 4H), 2,59 (bs, 4H), 2,32 (bs, 3H). LC-MS: Спосіб_A - 220, rt=0,98 (ES+) [M+H]+: 368. (4) (E)-N-(2-Хлор-піридин-4-іл)-3-(3-гідрокси-4-метокси-феніл)-акриламід (з наступною нейтралізацією гідрохлориду) 1 H NMR (DMSO-d6) δ (ppm): 10,70 (s, 1H), 9,30 (s, 1H), 8,27 (d, J=5,6 Гц, 1H), 7,85 (d, J=1,6 Гц, 1H), 7,55-7,51 (m, 2H), 7,09-7,07 (m, 2H), 6,98(d, J=8,0 Гц, 1H), 6,56 (d, J=15,6 Гц, 1H), 3,81 (s, 3H). LC-MS: Спосіб_A - 220, rt=1,44 (ES+) [M+H]+: 305. (5) (E)-N-(3-Хлор-2-метокси-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід 24 UA 105018 C2 1 5 H NMR (DMSO-d6) δ (ppm): 9,56 (s, 1H), 9,20 (s, 1H), 8,21-8,19 (m, 1H), 7,45 (d, J=15,6 Гц, 1H), 7,20 (dd, J=8,4 Гц, J=2,0 Гц, 1H), 7,13 (t, J=8,4 Гц, 1H), 7,08-6,97 (m, 4H), 3,82 (s, 3H), 3,80 (s, 3H). LC-MS: Спосіб_A - 220, rt=1,83 (ES+) [2M+Na]+: 689. (6) (E)-N-(3,4-Дихлор-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід 1 10 15 20 H NMR (DMSO-d6) δ (ppm): 10,39 (s, 1H), 9,26 (s, 1H), 8,10 (d, J=2,0 Гц, 1H), 7,60-7,54 (m, 2H), 7,47 (d, J=15,6 Гц, 1H), 7,06-7,04 (m, 2H), 6,98 (d, J=8,8 Гц, 1H), 6,54 (d, J=15,6 Гц, 1H), 3,81 (s, 3H). LC-MS: Спосіб_A - 220, rt=1,83 (ES+) [2M+Na]+: 699. (7) (E)-N-(3-Хлор-4-метокси-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід 1 H NMR (DMSO-d6) δ (ppm): 10,11 (s, 1H), 9,24 (s, 1H), 7,89 (d, J=2,4 Гц, 1H), 7,50 (dd, J=8,8 Гц, J=2,4 Гц, 1H), 7,42 (d, J=15,6 Гц, 1H), 7,13 (d, J=9,2 Гц, 1H), 7,04-7,02 (m, 2H), 6,97 (d, J=8,8 Гц, 1H), 6,53 (d, J=15,6 Гц, 1H), 3,82 (s, 3H), 3,81 (s, 3H). LC-MS: Спосіб_A - 220, rt=1,72 (ES+) [2M+Na]+: 689. (8) (E)-N-(2,3-Дихлор-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід 1 25 H NMR (DMSO-d6) δ (ppm): 7,88 (dd, J=8,4 Гц, J=1,6 Гц, 1H), 7,45-7,41 (m, 2H), 7,35 (t, J=8,4 Гц, 1H), 7,02 (s, 1H), 6,86 (s, 2H), 6,80 (d, J=15,6 Гц, 1H), 3,77 (s, 3H). LC-MS: Спосіб_A - 220, rt=2,01 (ES+) [M+H]+: 338. (9) (E)-N-(3-Бензиламіно-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід 1 30 35 40 H NMR (DMSO-d6) δ (ppm): 9,78 (s, 1H), 9,20 (s, 1H), 7,40-7,30 (m, 5H), 7,23-7,20 (m, 1H), 7,02-7,00 (m, 3H), 6,97-6,93 (m, 2H), 6,86 (d, J=8,0 Гц, 1H), 6,58 (d, J=15,6 Гц, 1H), 6,30-6,27 (m, 2H), 4,25 (d, J=6,0 Гц, 2H), 3,80 (s, 3H). LC-MS: Спосіб A - 220, rt=1,89 (ES+) [M+H]+: 375 (10) (E)-N-[3-(Бензил-метил-аміно)-феніл]-3-(3-гідрокси-4-метокси-феніл)-акриламід 1 H NMR (DMSO-d6) δ (ppm): 9,87 (s, 1H), 9,21 (s, 1H), 7,39 (d, J=15,2 Гц, 1H), 7,34-7,30 (m, 2H), 7,24-7,21 (m, 3H), 7,15 (s, 1H), 7,07 (t, J=8,0 Гц, 1H), 7,02-6,99 (m, 3H), 6,96 (d, J=8,8 Гц, 1H), 6,57 (d, J=15,6 Гц, 1H), 6,44 (dd, J=8,0 Гц, J=2,0 Гц, 1H), 4,55 (s, 2H), 3,80 (s, 3H), 2,99 (s, 3H). LC-MS: Спосіб_A - 220, rt=2,07 (ES+) [M+H]+: 389. Приклад 2 Одержання заміщених (E)-3-(3-гідрокси-феніл)-акрилових анілідів із відповідних (E)-3-(3ацетоки-феніл)-похідних кислотним гідролізом 25 UA 105018 C2 (11) (E)-N-[2-Хлор-3-(піридин-4-ілметокси)-феніл]-3-(3-гідрокси-4-метокси-феніл)-акриламіду гідрохлорид 5 10 15 20 3 н метанольний розчин соляної кислоти (10 мл, 30 ммоль) додали до розчину (E)-N-[2-хлор3-(піридин-4-ілметокси)-феніл]-3-(3-ацетокси-4-метокси-феніл)-акриламіду гідрохлориду (240 мг, 0,53 ммоль) в ТГФ (5 мл). Отриману в результаті суміш перемішували при RT протягом 16 годин, концентрували при зниженому тиску, поглинули з розчинником та повторно випарили (3 рази з MeOH і один раз з ацетоном) для одержання світло-жовтого залишку, який перетерли на порошок з етиловим ефіром. Після фільтрації та сушіння одержали 232 мг названої сполуки (E)N-[2-хлор-3-(піридин-4-ілметокси)-феніл]-3-(3-гідрокси-4-метокси-феніл)-акриламіду гідрохлориду у вигляді світло-жовтого порошку. 1 H NMR (DMSO-d6) δ (ppm): 9,57 (s, 1H), 9,25 (bs, NH+), 8,88 (d, J=4,4 Гц, 2H), 7,97 (d, bs, 2H), 7,64 (d, J=8 Гц, 1H), 7,47 (d, J=15,6 Гц, 1H), 7,32 (t, J=8 Гц, 1H), 7,09-6,98 (m, 4H), 6,92 (d, J=15,6 Гц, 1H), 5,55 (s, 2H), 3,83 (s, 3H). LC-MS: Спосіб_A - 220, rt=1,17 (ES+) [M+H]+: 411. Аналогічно гідролізуючи відповідні (E)-3-(3-ацетокси-феніл)-акрилові аніліди, одержали наступні сполуки: (12) (E)-3-(3-Гідрокси-4-метокси-феніл)-N-{3-[(піридин-4-ілметил)-аміно]-феніл}-акриламід 1 25 H NMR (DMSO-d6) δ (ppm): 9,80 (s, 1H), 9,20 (s, 1H), 8,51-8,49 (m, 2H), 7,39-7,35 (m, 3H), 7,01-6,95 (m, 5H), 6,86 (d, J=8,4 Гц, 1H), 6,57 (d, J=15,6 Гц, 1H), 6,47-6,44 (m, 1H), 6,25-6,23 (m, 1H), 4,30 (bs, 2H), 3,80 (s, 3H). LC-MS: Спосіб_A - 220, rt=1,01. (ES+) [M+H]+: 376. (13) (E)-N-(3-Бензилокси-2-хлор-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід 1 30 35 H NMR (DMSO-d6) δ (ppm): 9,50 (s, 1H), 9,21 (s, 1H), 7,60-6,97 (m, 12H), 6,90 (d, J=15,6 Гц, 1H), 5,23 (s, 2H), 3,82 (s, 3H). LC-MS: Спосіб_A - 220, rt=2,08 (ES+) [M+H]+: 410. (14) (E)-N-(2-Бензилокси-3-хлор-феніл)-3-(3-гідрокси-4-метокси-феніл)-акриламід (очищення колонковою хроматографією на силікагелі, елюант n-гексан/AcOEt 70:30) 1 H NMR (DMSO-d6) δ (ppm): 9,46 (s, 1H), 9,23 (s, 1H), 8,04 (m, 1H), 7,55-6,98 (m, 11H), 6,83 (d, J=16 Гц, 1H), 5,01 (s, 2H), 3,83 (s, 3H). LC-MS: Спосіб_A - 220, rt=2,21 26 UA 105018 C2 (ES+) [M+H]+: 410. (15) (E)-N-(1-Бензил-1H-індол-4-іл)-3-(3-гідрокси-4-метокси-феніл)-акриламід 1 5 10 15 H NMR (DMSO-d6) δ (ppm): 9,70 (s, 1H), 9,22 (s, 1H), 7,85 (m, 1H), 7,55-6,85 (m, 14H), 5,42 (s, 2H), 3,83 (s, 3H). LC-MS: Спосіб_A - 220, rt=1,96 (ES+) [M+H]+: 399. (16) (E)-N-[3-Хлор-2-(піридин-4-ілметокси)-феніл]-3-(3-гідрокси-4-метокси-феніл)-акриламід (очищення колонковою хроматографією на силікагелі, елюант DCM/MeOH/водний гідроксид амонію 98:2:0,2) 1 H NMR (DMSO-d6) δ (ppm): 9,58 (s, 1H), 9,22 (s, 1H), 8,59 (d, J=5,4Гц, 2H), 8,08 (m, 1H), 7,56 (d, J=5,4 Гц, 2H), 7,44 (d, J=15,4 Гц, 1H), 7,28 (m, 1H), 7,19 (t, J=8,2 Гц, 1H), 7,06-6,97 (m, 3H), 6,85 (d, J=15,4 Гц, 1H), 5,05 (s, 2H), 3,82 (s, 3H). LC-MS: Спосіб_A - 220, rt=1,33 (ES+) [M+H]+: 411. (17) (E)-N-[4-Хлор-3-(піридин-4-ілметокси)-феніл]-3-(3-гідрокси-4-метокси-феніл)-акриламід 1 20 25 30 35 H NMR (DMSO-d6) δ (ppm): 9,58 (s, 1H), 9,22 (s, 1H), 8,59 (d, J=5,4 Гц, 2H), 8,08 (m, 1H), 7,56 (d, J=5,4 Гц, 2H), 7,44 (d, J=15,4 Гц, 1H), 7,28 (m, 1H), 7,19 (t, J=8,2 Гц, 1H), 7,06-6,97 (m, 3H), 6,85 (d, J=15,4 Гц, 1H), 5,05 (s, 2H), 3,82 (s, 3H). LC-MS: Спосіб_A - 220, rt=1,30 (ES+) [M+H]+: 411. (18) (E)-3-(3-Гідрокси-4-метокси-феніл)-N-(1-метил-1Н-індол-4-іл)-акриламід (очищення колонковою хроматографією на силікагелі, елюант DCM/MeOH 100:1) 1 H NMR (DMSO-d6) δ (ppm): 9,69 (s, 1H), 9,22 (s, 1H), 7,88 (m, 1H), 7,46 (d, J=15,6 Гц, 1H), 7,30 (m, 1H), 7,20-6,92 (m, 6H), 6,78 (m, 1H), 3,83 (s, 3H), 3,79 (s, 3H). LC-MS: Спосіб_A - 220, rt=1,56 (ES+) [M+H]+: 323. (19) (E)-N-(1-Бензил-1H-індол-7-іл)-3-(3-гідрокси-4-метокси-феніл)-акриламід (очищення колонковою хроматографією на силікагелі, елюант DCM/MeOH 100:1) 1 H NMR (DMSO-d6) δ (ppm): 9,76 (s, 1H), 9,22 (s, 1H), 7,49-6,92 (m, 13H), 6,57 (m, 2H), 5,46 (s, 2H), 3,82 (s, 3H). LC-MS: Спосіб_A - 220, rt=1,83 (ES+) [M+H]+: 399. 27 UA 105018 C2 (20) акриламід 5 10 15 20 25 (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[3-(3-метил-3H-імідазол-4-ілметокси)-феніл] (очищення колонковою хроматографією на силікагелі, елюант DCM/MeOH/водний гідроксид амонію 90:10:1) 1 H NMR (DMSO-d6) δ (ppm): 10,09 (s, 1H), 9,24 (s, 1H), 7,65 (s, 1H), 7,51 (m, 1H), 7,44 (d, J=15,6 Гц, 1H), 7,26-7,2 (m, 2H), 7,05-6,97 (m, 4H), 6,77-6,74 (m, 1H), 6,59 (d, J=15,6 Гц, 1H), 5,08 (s, 2H), 3,82 (s, 3H), 3,66 (s, 3H). LC-MS: Спосіб_A - 220, rt=1,01 (ES+) [M+H]+: 380. (21) (E)-3-(4-Фтор-3-гідрокси-феніл)-N-(2-феноксиметил-феніл)-акриламід (очищення колонковою хроматографією на силікагелі, елюант DCM/MeOH/AcOEt 97:3) 1 H NMR (DMSO-d6) δ (ppm): 10,1 (s, 1H), 9,71 (s, 1H), 7,62-7,47 (m, 3H), 7,37-7,18 (m, 6H), 7,08-6,92 (m, 4H), 6,77 (d, J=15,2 Гц, 1H), 5,14 (s, 2H). LC-MS: Спосіб_A - 220, rt=1,95 (ES+) [M+H]+: 364. (22) (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[3-(1H-імідазол-4-ілметокси)-феніл]-акриламіду гідрохлорид 1 H NMR (DMSO-d6) δ (ppm): 10,1 (s, 1H), 9,71 (s, 1H), 7,62-7,47 (m, 3H), 7,37-7,18 (m, 6H), 7,08-6,92 (m, 4H), 6,77 (d, J=15,2 Гц, 1H), 5,14 (s, 2H). LC-MS: Спосіб_A - 220, rt=1,00 (ES+) [M+H]+: 366. (23) (E)-3-(3-Гідрокси-4-метокси-феніл)-N-[3-(піридин-4-ілоксиметил)-феніл]-акриламіду гідрохлорид 1 30 35 H NMR (DMSO-d6) δ (ppm): 10,32 (s, 1H), 8,75-8,73 (m, 2H), 7,74 (s, 1H), 7,63 (d, J=8,0 Гц, 1H), 7,45-7,36 (m, 4H), 7,07 (d, J=8,0 Гц, 1H), 7,04-7,02 (m, 2H), 6,97 (d, J=8,0 Гц, 1H), 6,61 (d, J=15,6 Гц, 1H), 5,61 (s, 2H), 3,81 (s, 3H). LC-MS: Спосіб_A - 220, rt=1,05 (ES+) [2M+H]+: 753. (24) (E)-3-(3-Гідрокси-4-метокси-феніл)-N-(3-оксазол-5-іл-феніл)-акриламід 1 H NMR (DMSO-d6) δ (ppm): 10,33 (s, 1H), 8,47 (s, 1H), 8,13 (s, 1H), 7,66-7,64 (m, 2H), 7,487,41 (m, 3H), 7,06-7,04 (m, 2H), 6,98 (d, J=8,4 Гц, 1H), 6,63 (d, J=15,6 Гц, 1H), 3,81 (s, 3H). LC-MS: Спосіб_A - 220, rt=1,44 (ES+) [2M+Na]+: 695. (25) (E)-3-(3-Гідрокси-4-метокси-феніл)-N-індан-1-іл-акриламід 28
ДивитисяДодаткова інформація
Назва патенту англійськоюAcrylamido derivatives useful as inhibitors of the mitochondrial permeability transition
Автори англійськоюFancelli, Daniele, Varasi, Mario, Plyte, Simon, Ballarini, Marco, Cappa, Anna, Carenzi, Giacomo, Minucci, Saverio, Pain, Gilles, Villa, Manuela
Автори російськоюВарази Марио
МПК / Мітки
МПК: C07D 213/30, C07D 213/68, C07C 235/38, C07D 209/08, C07C 323/41, C07D 213/38, C07D 211/22, C07D 295/135, C07D 231/12, C07D 211/46, C07D 213/32, C07D 233/60, C07D 231/56, C07C 235/36
Мітки: застосовні, мітохондріальної, акриламідопохідні, переходу, інгібітори, проникності
Код посилання
<a href="https://ua.patents.su/101-105018-akrilamidopokhidni-zastosovni-yak-ingibitori-perekhodu-mitokhondrialno-proniknosti.html" target="_blank" rel="follow" title="База патентів України">Акриламідопохідні, застосовні як інгібітори переходу мітохондріальної проникності</a>
Попередній патент: Чутливі до сульфонілсечовини репресорні білки
Наступний патент: Дисперсія, що містить інгібітори гідроксифенілпіруват-діоксигенази
Випадковий патент: М'ясо-овочевий продукт












