Спосіб одержання оксазолідинзахищених амінодіолів корисних як проміжні сполуки для одержання флорфеніколу
Формула / Реферат
1. Спосіб одержання сполуки Формули XI:
 , Формула ХІ
, Формула ХІ
в якій:
R1 є водень, метилтіо, метилсульфокси, метилсульфоніл, фторметилтіо, фторметилсульфокси, фторметилсульфоніл, нітро, фтор, бром, хлор, ацетил, бензил, феніл, заміщений галогеном феніл, С1-6алкіл, С1-6галоалкіл, С3-8циклоалкіл, С2-6алкеніл, С2-6алкініл, С1-6алкокси, С1-6аралкіл, С2-6аралкеніл або С2-6гетероциклічна група; і
R7 є водень, С1-6алкіл, С1-6галоалкіл, С1-6дигалоалкіл, С1-6тригалоалкіл, С3-8циклоалкіл, С3-8 циклогалоалкіл, С3-8циклодигалоалкіл, С3-8циклотригалоалкіл, С2-6алкеніл, С2-6алкініл, С1-6алкокси, С1-6аралкіл, С2-6аралкеніл, С2-6гетероцикліл, бензил, феніл або фенілалкіл, де фенільне кільце може бути заміщене одним або двома галогенами, С1-6алкілами або С1-6алкокси,
в якому здійснюють:
а) взаємодію сполуки Формули VI
 , Формула VI
, Формула VI
в якій:
R1 є таким, як визначено вище;
R5 є водень, C1-6алкіл, С3-8циклоалкіл, бензил, феніл або С1-6алкілфеніл,
у реакторі з відновлювальним агентом в спиртовому розчиннику з утворенням амінодіолу Формули VII
 , Формула VII
, Формула VII
де R1 є таким, як визначено вище;
b) взаємодію амінодіолу Формули VII in situ з оксазолідинформуючим реагентом з утворенням сполуки Формули VIII
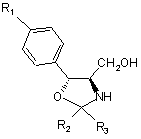 , Формула VIII
, Формула VIII
в якій:
R1 є таким, як визначено вище;
R2 є водень, C1-6алкіл, C1-6галоалкіл, С3-8циклоалкіл, С2-6алкеніл, С2-6алкініл, C1-6алкокси, C1-6аралкіл, С2-6аралкеніл, арил або С2-6гетероциклічна група; і
R3 є водень, C1-6алкіл, C1-6галоалкіл, С3-8циклоалкіл, С2-6алкеніл, С2-6алкініл, C1-6алкокси, C1-6аралкіл, С2-6аралкеніл, арил або С2-6 гетероциклічна група;
с) взаємодію сполуки Формули VIII in situ з третім N-ацилюючим агентом з утворенням оксазолідинзахищеного амінодіолу Формули XII
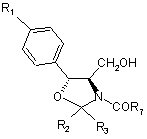 , Формула XII
, Формула XII
в якій:
R1, R2, R3 і R7 є такими, як визначено вище;
d) фторування сполуки Формули XII фторувальним агентом в присутності органічного розчинника з утворенням сполуки Формули XIII
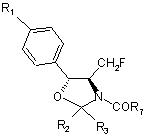 , Формула XIII
, Формула XIII
в якій:
R1, R2, R3 і R7 є такими, як визначено вище; і
е) селективний гідроліз сполуки Формули XIII, використовуючи кислотний або основний каталізатор, з утворенням сполуки Формули XI.
2. Спосіб за пунктом 1, де R1 є метилтіо, метилсульфокси або метилсульфоніл, переважно метилсульфоніл.
3. Спосіб за пунктом 1, де R2 і R3 є водень, метил, етил або пропіл, переважно метил.
4. Спосіб за пунктом 1, де R5 є метил, етил, н-пропіл, ізопропіл, бутил, т-бутил або пентил.
5. Спосіб за пунктом 1, де сполуку Формули VI вибирають з групи, що містить
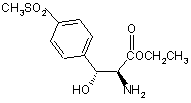 і
і 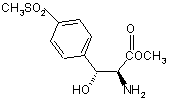 .
.
6. Спосіб за пунктом 1, де відновлювальний агент вибирають з групи, що містить NaBH4, KBH4, Са(ВН4)2 і LiBH4 і їх суміші, переважно відновлювальним агентом є KВН4.
7. Спосіб за пунктом 6, де молярне співвідношення KВН4 і сполуки Формули VI становить приблизно від 1:1 до 2:1, переважно згадане співвідношення становить приблизно 1,5:1.
8. Спосіб за пунктом 6, де відновлення проводять при температурі нижче 60 °С.
9. Спосіб за пунктом 8, де відновлення завершується за 6 годин.
10. Спосіб за пунктом 1, де спиртовий розчинник вибирають з групи, що містить метанол, етанол, пропанол, ізопропанол, бутанол, пентанол, етиленгліколь, гліцерин і їх суміші, переважно розчинником є метанол або етанол, більш переважно метанол.
11. Спосіб за пунктом 1, де сполукою Формули VII є
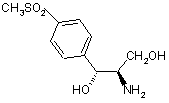 .
.
12. Спосіб за пунктом 1, де оксазолідинформуючий розчинник вибирають з толуолу, ксилену, гексанів або їх суміші, переважно оксазолідинформуючим розчинником є толуол.
13. Спосіб за пунктом 12, де співвідношення толуолу і метанолу становить від 0,5:1 до 3:1, переважно згадане співвідношення становить приблизно 1:1.
14. Спосіб за пунктом 1, де оксазолідинформуючий реагент вибирають з групи, що містить формальдегід, ацетон, 2-метоксипропен, 2,2-диметоксипропан, 2,2-діетоксипропан і їх суміші, переважно оксазолідинформуючим реагентом є ацетон.
15. Спосіб за пунктом 14, де співвідношення ацетону і толуолу становить приблизно від 0,5:1 до 3:1, переважно згадане співвідношення становить приблизно 1:1.
16. Спосіб за пунктом 1, де оксазолідинпромотуючу основу вибирають з групи, що містить карбонат калію, карбонат натрію, триметиламін і триетиламін, переважно оксазолідинпромотуючою основою є карбонат калію або триетиламін.
17. Спосіб за пунктом 1, де сполуку Формули VIII вибирають з групи, що містить
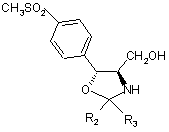 і
і 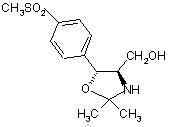 .
.
18. Спосіб за пунктом 1, де третім N-ацилюючим агентом є сполука формули:
R6COR7,
в якій:
R6 є гало або С1-6алкокси; і
R7 є водень, С1-6алкіл, С1-6галоалкіл, С1-6дигалоалкіл, С1-6тригалоалкіл, С3-8циклоалкіл, С3-8циклогалоалкіл, С3-8циклодигалоалкіл, С3-8циклотригалоалкіл, С2-6алкеніл, С2-6алкініл, С1-6алкокси, С1-6аралкіл, С2-6аралкеніл, С2-6гетероцикліл, бензил, феніл або фенілалкіл, де фенільне кільце може бути заміщене одним або двома галогенами, С1-6алкілами або С1-6алкокси.
19. Спосіб за пунктом 18, де R6 є Сl, Вr, метокси або етокси, переважно Сl.
20. Спосіб за пунктом 18, де R7 є СН2Сl, СНСl2, ССl3, CH2Br, CHBr2, CBr3, CH2F, CHF2 або CF3, переважно СНСl2.
21. Спосіб за пунктом 18, де третій N-ацилюючий агент вибирають з групи, що містить метилдихлорацетат, етилдихлорацетат, дихлорацетилхлорид, метилхлорацетат, етилхлорацетат, хлорацетилхлорид, метилтрихлорацетат, етилтрихлорацетат, трихлорацетилхлорид, метилдифторацетат, етилдифторацетат, дифторацетилхлорид, метилфторацетат, етилфторацетат, фторацетилхлорид, метилтрифторацетат, етилтрифторацетат, трифторацетилхлорид, дихлорацетилбромід, дифторацетилбромід, ацетилхлорид і ацетилбромід і їх суміші, переважно третім N-ацилюючим агентом є метилдихлорацетат або дихлорацетилхлорид, більш переважно дихлорацетилхлорид.
22. Спосіб за пунктом 1, де третю основу N-ацилювання вибирають з групи, що містить карбонат калію, карбонат натрію, триметиламін і триетиламін, переважно третьою основою N-ацилювання є карбонат калію або триетиламін.
23. Спосіб за пунктом 22, де співвідношення молярних еквівалентів третьої основи N-ацилювання і сполуки Формули VIII становить від 1:1 до 3:1, переважно згадане співвідношення становить приблизно 1,1:1.
24. Спосіб за пунктом 23, де молярне співвідношення дихлорацетилхлориду і сполуки Формули VIII становить приблизно від 1:1 до 3:1, переважно згадане співвідношення становить приблизно 1,1-1.
25. Спосіб за пунктом 21, де третю стадію N-ацилювання проводять при температурі 20-30 °С.
26. Спосіб за пунктом 25, де третя реакція N-ацилювання завершується за 2-4 години.
27. Спосіб за пунктом 1, де R7 є СН2Сl, СНСl2, ССl3, СН2Вr, СНВr2, СВr3, CH2F, CHF2 або CF3, переважно СНСl2 або CHF2, більш переважно СНСl2.
28. Спосіб за пунктом 1, де сполуку Формули XII вибирають з групи, що містить
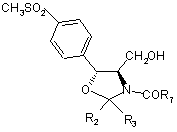 ,
, 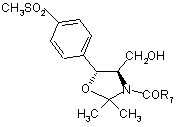 ,
,
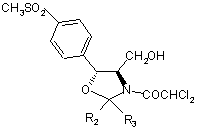 і
і 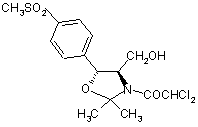 .
.
29. Спосіб за пунктом 1, де фторувальний агент вибирають з групи, що містить N-(2-хлор-1,1,2-трифторетил)діетиламін, N-(2-хлор-1,1,2-трифторетил)диметиламін, N-(2-хлор-1,1,2-трифторетил)дипропіламін, N-(2-хлор-1,1,2-трифторетил)піролідин, N-(2-хлор-1,1,2-трифторетил)-2-метилпіролідин, N-(2-хлор-1,1,2-трифторетил)-4-метилпіперазин, N-(2-хлор-1,1,2-трифторетил)морфолін, N-(2-хлор-1,1,2-трифторетил)піперидин, 1,1,2,2-тетрафторетил-N,N-диметиламін, (діетиламіно)трифторид сірки, біс-(2-метоксіетил)амінотрифторид сірки, N,N-діетил-1,1,2,3,3,3-гексафтор-1-пропанамін (реагент Ішикава) і їх суміші, переважно N,N-діетил-1,1,2,3,3,3-гексафтор-1-пропанамін.
30. Спосіб за пунктом 29, де молярне співвідношення N,N-діетил-1,1,2,3,3,3-гексафтор-1-пропанаміну і сполуки Формули XII становить приблизно від 1:1 до 2:1, переважно згадане співвідношення становить приблизно 1,5:1.
31. Спосіб за пунктом 30, де стадію фторування проводять при температурі від приблизно 80 °С до приблизно 110 °С і при тиску приблизно 60 псі.
32. Спосіб за пунктом 1, де органічний розчинник вибирають з групи, що містить 1,2-дихлоретан, метиленхлорид, хлороформ, хлорбензол, хлоровані вуглеводні і їх суміші, переважно органічним розчинником є метиленхлорид.
33. Спосіб за пунктом 1, де сполуку Формули XIII вибирають з групи, що містить
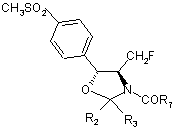 ,
, 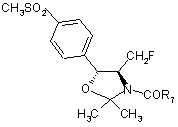 ,
,
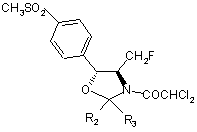 ,
, 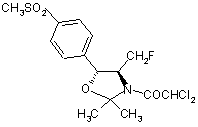 і
і
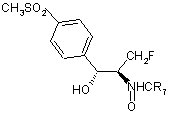 .
.
34. Спосіб за пунктом 33, де сполукою є Флорфенікол
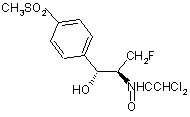 Формула І.
Формула І.
35. Спосіб за пунктом 1, де кислотним каталізатором є розведена водна хлороводнева кислота, сірчана кислота або фосфорна кислота, метансульфонова кислота або п-толуолсульфонова кислота, переважно кислотним каталізатором є п-толуолсульфонова кислота.
36. Спосіб за пунктом 1, де основним каталізатором є LiOH, NaOH, KOH, Li2CO3, Na2CO3, K2CO3, метоксид натрію, етоксид натрію, метоксид калію і етоксид калію, переважно основним каталізатором є K2СО3.
37. Спосіб за пунктом 1, де температура селективного гідролізу становить менше 80 °С.
38. Спосіб за пунктом 1, де метиленхлорид є органічним розчинником для селективного гідролізу.
39. Спосіб за пунктом 1, де сполуку Формули XI очищують сумішшю С1-10 моно-, ди- або триалканолу і води з утворенням чистої форми сполуки Формули XI, переважно очищення проводять в суміші метанолу, етанолу, пропанолу, ізопропанолу, бутанолу, втор-бутанолу, т-бутанолу, пентанолу, етиленгліколю, пропіленгліколю, бутиленгліколю або гліцерину і води, більш переважно очищення проводять в суміші метанолу, етанолу, пропанолу, ізопропанолу, бутанолу, втор-бутанолу, т-бутанолу або пентанолу і води.
40. Спосіб за пунктом 39, де очищення проводять в суміші ізопропанолу і води.
41. Спосіб за пунктом 40, де співвідношення ізопропанолу і води становить від 1:5 до 5:1, переважно згадане співвідношення становить 1:1.
42. Спосіб за пунктом 41, де температурою розчинення для очищення є температура кипіння 1:1 ізопропанолу і води.
43. Спосіб за пунктом 39, де реакцію очищення охолоджують до 10-30 °С для кристалізації бажаного продукту, переважно реакцію очищення охолоджують до приблизно 20-25 °С для кристалізації бажаного продукту.
Текст
1. Спосіб одержання сполуки Формули XI: R1 2 3 93212 C1-6аралкіл, С2-6аралкеніл, арил або С2-6 гетероциклічна група; с) взаємодію сполуки Формули VIII in situ з третім N-ацилюючим агентом з утворенням оксазолідинзахищеного амінодіолу Формули XII R1 CH2OH O N R2 COR7 R3 , Формула XII в якій: R1, R2, R3 і R7 є такими, як визначено вище; d) фторування сполуки Формули XII фторувальним агентом в присутності органічного розчинника з утворенням сполуки Формули XIII R1 4 7. Спосіб за пунктом 6, де молярне співвідношення KВН4 і сполуки Формули VI становить приблизно від 1:1 до 2:1, переважно згадане співвідношення становить приблизно 1,5:1. 8. Спосіб за пунктом 6, де відновлення проводять при температурі нижче 60 °С. 9. Спосіб за пунктом 8, де відновлення завершується за 6 годин. 10. Спосіб за пунктом 1, де спиртовий розчинник вибирають з групи, що містить метанол, етанол, пропанол, ізопропанол, бутанол, пентанол, етиленгліколь, гліцерин і їх суміші, переважно розчинником є метанол або етанол, більш переважно метанол. 11. Спосіб за пунктом 1, де сполукою Формули VII є CH3SO 2 CH2OH HO CH2F O N R2 COR7 R3 , Формула XIII в якій: R1, R2, R3 і R7 є такими, як визначено вище; і е) селективний гідроліз сполуки Формули XIII, використовуючи кислотний або основний каталізатор, з утворенням сполуки Формули XI. 2. Спосіб за пунктом 1, де R1 є метилтіо, метилсульфокси або метилсульфоніл, переважно метилсульфоніл. 3. Спосіб за пунктом 1, де R2 і R3 є водень, метил, етил або пропіл, переважно метил. 4. Спосіб за пунктом 1, де R5 є метил, етил, нпропіл, ізопропіл, бутил, т-бутил або пентил. 5. Спосіб за пунктом 1, де сполуку Формули VI вибирають з групи, що містить CH3SO 2 O COCH2 CH3 HO NH2 і CH3SO 2 O COCH3 HO NH2 . 6. Спосіб за пунктом 1, де відновлювальний агент вибирають з групи, що містить NaBH4, KBH4, Са(ВН4)2 і LiBH4 і їх суміші, переважно відновлювальним агентом є KВН4. NH2 . 12. Спосіб за пунктом 1, де оксазолідинформуючий розчинник вибирають з толуолу, ксилену, гексанів або їх суміші, переважно оксазолідинформуючим розчинником є толуол. 13. Спосіб за пунктом 12, де співвідношення толуолу і метанолу становить від 0,5:1 до 3:1, переважно згадане співвідношення становить приблизно 1:1. 14. Спосіб за пунктом 1, де оксазолідинформуючий реагент вибирають з групи, що містить формальдегід, ацетон, 2-метоксипропен, 2,2диметоксипропан, 2,2-діетоксипропан і їх суміші, переважно оксазолідинформуючим реагентом є ацетон. 15. Спосіб за пунктом 14, де співвідношення ацетону і толуолу становить приблизно від 0,5:1 до 3:1, переважно згадане співвідношення становить приблизно 1:1. 16. Спосіб за пунктом 1, де оксазолідинпромотуючу основу вибирають з групи, що містить карбонат калію, карбонат натрію, триметиламін і триетиламін, переважно оксазолідинпромотуючою основою є карбонат калію або триетиламін. 17. Спосіб за пунктом 1, де сполуку Формули VIII вибирають з групи, що містить 5 93212 CH3SO2 CH2OH O R2 NH R3 і CH3SO 2 6 згадане співвідношення становить приблизно 1,11. 25. Спосіб за пунктом 21, де третю стадію Nацилювання проводять при температурі 20-30 °С. 26. Спосіб за пунктом 25, де третя реакція Nацилювання завершується за 2-4 години. 27. Спосіб за пунктом 1, де R7 є СН2Сl, СНСl2, ССl3, СН2Вr, СНВr2, СВr3, CH2F, CHF2 або CF3, переважно СНСl2 або CHF2, більш переважно СНСl2. 28. Спосіб за пунктом 1, де сполуку Формули XII вибирають з групи, що містить CH3SO2 CH2OH O H3C CH2OH NH CH3 . 18. Спосіб за пунктом 1, де третім N-ацилюючим агентом є сполука формули: R6COR7, в якій: R6 є гало або С1-6алкокси; і R7 є водень, С1-6алкіл, С1-6галоалкіл, С16дигалоалкіл, С1-6тригалоалкіл, С3-8циклоалкіл, С3С3-8циклодигалоалкіл, С38циклогалоалкіл, 8циклотригалоалкіл, С2-6алкеніл, С2-6алкініл, С1С1-6аралкіл, С2-6аралкеніл, С26алкокси, 6гетероцикліл, бензил, феніл або фенілалкіл, де фенільне кільце може бути заміщене одним або двома галогенами, С1-6алкілами або С1-6алкокси. 19. Спосіб за пунктом 18, де R6 є Сl, Вr, метокси або етокси, переважно Сl. 20. Спосіб за пунктом 18, де R7 є СН2Сl, СНСl2, ССl3, CH2Br, CHBr2, CBr3, CH2F, CHF2 або CF3, переважно СНСl2. 21. Спосіб за пунктом 18, де третій N-ацилюючий агент вибирають з групи, що містить метилдихлорацетат, етилдихлорацетат, дихлорацетилхлорид, метилхлорацетат, етилхлорацетат, хлорацетилхлорид, метилтрихлорацетат, етилтрихлорацетат, трихлорацетилхлорид, метилдифторацетат, етилдифторацетат, дифторацетилхлорид, метилфторацетат, етилфторацетат, фторацетилхлорид, метилтрифторацетат, етилтрифторацетат, трифторацетилхлорид, дихлорацетилбромід, дифторацетилбромід, ацетилхлорид і ацетилбромід і їх суміші, переважно третім N-ацилюючим агентом є метилдихлорацетат або дихлорацетилхлорид, більш переважно дихлорацетилхлорид. 22. Спосіб за пунктом 1, де третю основу Nацилювання вибирають з групи, що містить карбонат калію, карбонат натрію, триметиламін і триетиламін, переважно третьою основою Nацилювання є карбонат калію або триетиламін. 23. Спосіб за пунктом 22, де співвідношення молярних еквівалентів третьої основи N-ацилювання і сполуки Формули VIII становить від 1:1 до 3:1, переважно згадане співвідношення становить приблизно 1,1:1. 24. Спосіб за пунктом 23, де молярне співвідношення дихлорацетилхлориду і сполуки Формули VIII становить приблизно від 1:1 до 3:1, переважно O R2 N COR 7 R3 , CH3SO 2 CH2OH O N COR 7 H3 C CH3 , CH3SO2 CH2OH O R2 N COCHCl 2 R3 і CH3SO 2 CH2OH O N COCHCl 2 H3C CH3 . 29. Спосіб за пунктом 1, де фторувальний агент вибирають з групи, що містить N-(2-хлор-1,1,2трифторетил)діетиламін, N-(2-хлор-1,1,2трифторетил)диметиламін, N-(2-хлор-1,1,2трифторетил)дипропіламін, N-(2-хлор-1,1,2трифторетил)піролідин, N-(2-хлор-1,1,2трифторетил)-2-метилпіролідин, N-(2-хлор-1,1,2трифторетил)-4-метилпіперазин, N-(2-хлор-1,1,2трифторетил)морфолін, N-(2-хлор-1,1,2трифторетил)піперидин, 1,1,2,2-тетрафторетилN,N-диметиламін, (діетиламіно)трифторид сірки, біс-(2-метоксіетил)амінотрифторид сірки, N,Nдіетил-1,1,2,3,3,3-гексафтор-1-пропанамін (реагент Ішикава) і їх суміші, переважно N,N-діетил1,1,2,3,3,3-гексафтор-1-пропанамін. 7 93212 30. Спосіб за пунктом 29, де молярне співвідношення N,N-діетил-1,1,2,3,3,3-гексафтор-1пропанаміну і сполуки Формули XII становить приблизно від 1:1 до 2:1, переважно згадане співвідношення становить приблизно 1,5:1. 31. Спосіб за пунктом 30, де стадію фторування проводять при температурі від приблизно 80 °С до приблизно 110 °С і при тиску приблизно 60 псі. 32. Спосіб за пунктом 1, де органічний розчинник вибирають з групи, що містить 1,2-дихлоретан, метиленхлорид, хлороформ, хлорбензол, хлоровані вуглеводні і їх суміші, переважно органічним розчинником є метиленхлорид. 33. Спосіб за пунктом 1, де сполуку Формули XIII вибирають з групи, що містить CH3SO 2 8 CH3SO2 CH2F HO . 34. Спосіб за пунктом 33, де сполукою є Флорфенікол CH3SO 2 CH2F HO R2 N COR7 R3 , CH3SO 2 CH2F O N COR 7 H3 C CH3 , CH3SO2 CH2F O R2 NHCCHCl2 O CH2F O NHCR7 O N COCHCl 2 R3 , CH3SO 2 CH2F O N COCHCl 2 H3C CH3 і Представлений винахід загалом стосується нового способу одержання оксазолідинзахищених Формула І. 35. Спосіб за пунктом 1, де кислотним каталізатором є розведена водна хлороводнева кислота, сірчана кислота або фосфорна кислота, метансульфонова кислота або п-толуолсульфонова кислота, переважно кислотним каталізатором є птолуолсульфонова кислота. 36. Спосіб за пунктом 1, де основним каталізатором є LiOH, NaOH, KOH, Li2CO3, Na2CO3, K2CO3, метоксид натрію, етоксид натрію, метоксид калію і етоксид калію, переважно основним каталізатором є K2СО3. 37. Спосіб за пунктом 1, де температура селективного гідролізу становить менше 80 °С. 38. Спосіб за пунктом 1, де метиленхлорид є органічним розчинником для селективного гідролізу. 39. Спосіб за пунктом 1, де сполуку Формули XI очищують сумішшю С1-10 моно-, ди- або триалканолу і води з утворенням чистої форми сполуки Формули XI, переважно очищення проводять в суміші метанолу, етанолу, пропанолу, ізопропанолу, бутанолу, втор-бутанолу, т-бутанолу, пентанолу, етиленгліколю, пропіленгліколю, бутиленгліколю або гліцерину і води, більш переважно очищення проводять в суміші метанолу, етанолу, пропанолу, ізопропанолу, бутанолу, вторбутанолу, т-бутанолу або пентанолу і води. 40. Спосіб за пунктом 39, де очищення проводять в суміші ізопропанолу і води. 41. Спосіб за пунктом 40, де співвідношення ізопропанолу і води становить від 1:5 до 5:1, переважно згадане співвідношення становить 1:1. 42. Спосіб за пунктом 41, де температурою розчинення для очищення є температура кипіння 1:1 ізопропанолу і води. 43. Спосіб за пунктом 39, де реакцію очищення охолоджують до 10-30 °С для кристалізації бажаного продукту, переважно реакцію очищення охолоджують до приблизно 20-25 °С для кристалізації бажаного продукту. амінодіолів. Ці сполуки є корисними як проміжні сполуки в способі одержання Флорфеніколу. 9 Передумови створення винаходу Флорфенікол є антибіотиком широкого спектру дії Формули І . Він знайшов широке застосування у ветеринарії для лікування як Грам-позитивних, так і Грамнегативних бактерій, також як і риккетсиозних інфекцій. Флорфенікол також відомий як [R-(R*,8*)]2,2-Дихлор-N-[1-(фторметил)-2-гідрокси-2-[4(метилсульфоніл)-феніл]етил]ацетамід. Патент US 5,663,361, права на який передані звичайним чином, опис якого включений сюди як посилання, описує синтез проміжних сполук для Флорфеніколу і їх застосування в способі одержання Флорфеніколу. Основною перевагою, що тут обговорюється, є те, що спосіб запропонований в документі рівня техніки виключає необхідність виділення амінодіолсульфону (ADS) з реактору перед проведенням синтезу Флорфеніколу. Зовсім нещодавно, в заявці US 2005/0075506 А1 описаний спосіб одержання сполуки Формули II, що є корисною як проміжна сполука в синтезі Флорфеніколу. . Спосіб передбачає взаємодію гідрохлоридної солі необов'язково чистої амінодіольної сполуки Формули III з ацетоном і потім з ацетилхлоридом з утворенням сполуки Формули II. Сполука Формули II надалі взаємодіє забезпечуючи Флорфенікол Формули І. Основним недоліком способу описаного в 2005/0075506 А1 є застосування амінодіолу Формули III, як вихідної сполуки. Амінодіольна сполука Формули III є дорогою. Її також складно виділити і маніпулювати з нею внаслідок її амфотерної природи. 93212 10 Іншим основним недоліком способу описаного в 2005/0075506 А1 є необхідність гідролізу оксазолідину і N-ацетильної групи сполуки Формули ІХа; з утворенням сполуки Формули Ха; з наступним ацилюванням, використовуючи другий N-ацилюючий агент з утворенням сполуки Формули І. Представлений винахід спрямований на усунення цих недоліків і покликаний забезпечити альтернативні способи одержання корисних проміжних сполук включених в синтез Флорфеніколу. В одному з втілень, представлений винахід включає спосіб одержання оксазолідинзахищеного амінодіолу Формули V: в якій: R1 є водень, метилтіо, метилсульфокси, метилсульфоніл, фторметилтіо, фторметилсульфокси, фторметилсульфоніл, нітро, фтор, бром, хлор, ацетил, бензил, феніл, заміщений галогеном феніл, С1-6 алкіл, С1-6 галоалкіл, С3-8 циклоалкіл, С2-6 алкеніл, С2-6 алкініл, С1-6 алкокси, С1-6 аралкіл, С2-6 аралкеніл або С2-6 гетероциклічна група; R2 є водень, С1-6 алкіл, С1-6 галоалкіл, С3-8 циклоалкіл, С2-6 алкеніл, С2-6 алкініл, С1-6 алкокси, С1-6 аралкіл, С2-6 аралкеніл, арил або С2-6 гетероциклічна група; R3 є водень, С1-6 алкіл, С1-6 галоалкіл, С3-8 циклоалкіл, С2-6 алкеніл, С2-6 алкініл, С1-6 алкокси, С1-6 аралкіл, С2-6 аралкеніл, арил або С2-6 гетероциклічна група; і R4 є водень, ОН, С1-6 алкіл, С1-6 галоалкіл, С3-8 циклоалкіл, бензил, феніл або С1-6 фенілалкільна група, де фенільне кільце може бути заміщене одним або двома галогенами, С1-6 алкілами або С1-6 алкокси. 11 93212 12 В іншому переважному втіленні, представлений винахід включає спосіб одержання оксазолідинзахищеного амінодіолу Формули XII: в якій: R1, R2 і R3 є такими як визначено вище; і R7 є водень, С1-6 алкіл, С1-6 галоалкіл, С1-6 дигалоалкіл, С1-6 тригалоалкіл, С3-8 циклоалкіл, С3-8 циклогалоалкіл, С3-8 циклодигалоалкіл, С3-8 циклотригалоалкіл, С2-6 алкеніл, С2-6 алкініл, С1-6 алкокси, С1-6 аралкіл, С2-6 аралкеніл, С2-6 гетероцикліл, бензил, феніл або фенілалкіл, де фенільне кільце може бути заміщене одним або двома галогенами, С1-6 алкілами або С1-6 алкокси. Переважно, R7 є СН2СІ, СНСІ2, ССІ3, СН2Вr, CHBr2, CBr3, CH2F, CHF2 або CF3. В одному з втілень, Спосіб включає стадії: а) взаємодію сполуки Формули VI: де R1, R2 і R3 є такими як визначено вище; і с) взаємодію сполуки Формули VIII у реакторі без виділення (тобто, in situ) з першим Nацилюючим агентом з утворенням оксазолідинзахищеного амінодіолу Формули V. В іншому переважному втіленні, спосіб включає стадії: a) взаємодію сполуки Формули VI у реакторі з відновлювальним агентом в спиртовому розчиннику з утворенням амінодіолу Формули VII; b) взаємодію амінодіолу Формули VII у реакторі без виділення (тобто, in situ) з оксазолідинформуючим агентом з утворенням сполуки Формули VIII; c) взаємодію сполуки Формули VIII у реакторі без виділення (тобто, in situ) з N-ацилюючим агентом з утворенням оксазолідинзахищеного амінодіолу Формули XII; d) фторування сполука Формули XII фторувальним агентом в присутності органічного розчинника з утворенням сполуки Формули XIII: в якій: R1 є таким як визначено вище і R5 є водень, С1-6 алкіл, С3-8 циклоалкіл, бензил, феніл або С1-6 фенілалкіл, у реакторі з відновлювальним агентом в спиртовому розчиннику з утворенням амінодіолу Формули VII: де R1, R2, R3 і R7 є такими як визначено вище; є) селективний гідроліз сполуки Формули XIII використовуючи кислотний або основний каталізатор з утворенням сполуки Формули XI: в якій: R1 є таким як визначено вище; b) взаємодію амінодіолу Формули VII у реакторі без виділення (тобто, in situ) з оксазолідинформуючим реагентом з утворенням сполуки Формули VIII: де R1 і R7 є такими як визначено вище; і f) якщо необхідно, очищення сполуки формули XI використовуючи суміш С1-10 моно, ди або триалканолу і води з утворенням чистої сполуки Формули XI. Винахідниками неочікувано було знайдені значні переваги для способу при формуванні оксазолідинзахищених амінодіолів Формули V і Формули 13 XII. Одержуються сполуки Формули V, або особливо Формули II, коли як вихідні матеріали використовують естерний попередник вільної основи амінодіолу Формули III. Такі естери загалом відповідають Формулі VI і естер Формули IV є одним з особливо переважних естерів: . Використання естерів Формул IV і VI забезпечує дорогу вільну основу вихідного матеріалу Формули III in situ, таким чином, виключаючи необхідність виділення цієї сполуки, що має певні складності. Для вільної основи вихідного матеріалу Формули III внаслідок виділення зменшується вихід і таке виключення призводить до збільшення виходу і зменшення вартості оксазолідинзахищеного амінодіолу Формули V, або особливо сполуки Формули II, або в більш переважному втіленні оксазолідинзахищеного амінодіолу Формули XII. Винахідниками також було знайдено шляхи використання сполуки Формули IV з більшою ефективністю і способів заощадження коштів. Таким чином, представлений винахід має переваги, якими є ефективність і економічність способу одержання Флорфеніколу, його аналогів і його оксазолідинових проміжних сполук. Детальний опис втілень Коли використовується в представленому описі і пунктах формули, що додаються, терміни приведені тут нижче, якщо не вказано інше, мають наступні визначення: Термін "спиртовий розчинник" включає С1-10 спирти, такі як метанол і етанол і їх суміші, С2-10 диспирти, такі як етиленгліколь і С1-10 триспирти, такі як гліцерин. Альтернативно, спиртовий розчинник може бути змішаний з будь-яким придатним співрозчинником. Такими спив розчинниками є інші розчинники, які змішуються із спиртовим розчинником, таким як С4-10 алкани, ароматичні розчинники, такі як бензол, толуол, ксилени, галобензоли, такі як хлорбензол, і етери, такі як діетиловий етер, трет-бутилметиловий етер, ізопропіловий етер і тетрагідрофуран, або суміші будь-яких згаданих вище розчинників або співрозчинників. Термін "алкіл" означає нерозгалужений або розгалужений алкіл, такий як метил, етил, пропіл або втор-бутил. Альтернативно, кількість вуглеців в алкілі може бути певною. Наприклад, " С1-6 алкіл" означає "алкіл", як описано вище, що містить 1-6 атомів вуглецю. "Галоалкіл" означає "алкіл", як описано вище, де один або більше воднів замінені галогеном. Термін "арил" означає феніл або феніл заміщений С1-6 алкілом або галогеном. "Заміщений бензил" означає бензил заміщений С1-6 алкілом або галогеном. Термін "гало" означає фтор, хлор, бром або йод. 93212 14 Термін "галоарил" означає феніл заміщений галогеном. В одному з аспектів винаходу, забезпечується спосіб одержання оксазолідинзахищеного амінодіолу Формули V: в якій: R1 є водень, метилтіо, метилсульфокси, метилсульфоніл, фторметилтіо, фторметилсульфокси, фторметилсульфоніл, нітро, фтор, бром, хлор, ацетил, бензил, феніл, заміщений галогеном феніл, С1-6 алкіл, С1-6 галоалкіл, С3-8 циклоалкіл, С2-6 алкеніл, С2-6 алкініл, С1-6 алкокси, С1-6 аралкіл, С2-6 аралкеніл або С2-6 гетероциклічна група; R2 є водень, С1-6 алкіл, С1-6 галоалкіл, С3-8 циклоалкіл, С2-6 алкеніл, С2-6 алкініл, С1-6 алкокси, С1-6 аралкіл, С2-6 аралкеніл, арил або С2-6 гетероциклічна група; R3 є водень, С1-6 алкіл, С1-6 галоалкіл, С3-8 циклоалкіл, С2-6алкеніл, С2-6 алкініл, С1-6 алкокси, С1-6 аралкіл, С2-6 аралкеніл, арил або С2-6 гетероциклічна група; і R4 є водень, ОН, С1-6 алкіл, С1-6 галоалкіл, С3-8 циклоалкіл, бензил, феніл або С1-6 фенілалкільна група, де фенільне кільце може бути заміщене одним або двома галогенами, С1-6 алкілами або С1-6 алкокси. Сполуки приведені тут є корисними як проміжні сполуки при одержанні Флорфеніколу і подібних сполук. Один з переважних способів винаходу включає наступні стадії: а) взаємодію сполуки Формули VI: в якій: R1 є таким як визначено вище і R5 є водень, С1-6 алкіл, С3-8 циклоалкіл, бензил, феніл або С1-6 алкілфеніл, у реакторі з відновлювальним агентом в спиртовому розчиннику з утворенням амінодіолу Формули VII: 15 93212 16 де R1 є таким як визначено вище; b) взаємодію амінодіолу Формули VII у реакторі без виділення (тобто, in situ) з оксазолідинформуючим реагентом з утворенням сполуки Формули VIII: В ще одному іншому аспекті, естери відповідають: де R1, R2, R3 і R4 є такими як визначено вище; і с) взаємодію сполуки Формули VIII у реакторі без виділення (тобто, in situ) з першим Nацилюючим агентом з утворенням оксазолідинзахищеного амінодіолу Формули V: де R1, R2, R3 і R4 є такими як визначено вище. В межах загального способу описаного вище, існують певні переважні аспекти винаходу: R1 є метилтіо, метилсульфокси або метилсульфоніл. Більш переважно, R1 є метилсульфоніл; R2 і R3 є водень, метил, етил або пропіл. Більш переважно, R2 і R3 є метилами; R4 є метил, етил, пропіл або ізопропіл. Більш переважно, R4 є метил; і R5 є метил, етил, н-пропіл, ізопропіл, бутил, тбутил, або пентил. Сполука Формули IV є комерційно доступною. Альтернативні сполуки, що відповідають Формулі VI можна одержати використовуючи стандартні методики органічного синтезу без надзвичайних експериментів. Одним з переважних естерів, що відповідає Формулі VI є В іншому аспекті винаходу, естером Формули VI є де R5 є таким як визначено вище. В більш переважному втіленні, коли Флорфенікол є бажаним кінцевим продуктом, сполукою, що відповідає Формулі VI, є сполука Формули IV. Як згадано вище, перша частина способу включає взаємодію сполуки Формули VI в реакторі з відновлювальним агентом. Для цілей представленого винаходу, під терміном "реактор" слід розуміти контейнер відомий середньому спеціалісту в цій галузі, який здатний утримувати реактанти і забезпечує протікання стадії реакції до завершення. Звичайно, розмір і тип реактора будуть залежати від розміру завантаження і вибраних певних реактантів. Може бути використаний широкий перелік придатних відновлювальних агентів при проведенні способу винаходу. Необмежуючим переліком придатних відновлювальних агентів є NaBH4, KBH4, Са(ВН4)2 і LiBH4 і їх суміші, коли використовується спиртовий розчинник. Спиртовим розчинником також може бути один із багатьох загальноприйнятих розчинників, але деякими переважними розчинниками є метанол, етанол, пропанол, ізопропанол, бутанол і пентанол і їх суміші. Одним з переважних відновлювальних агентів є KВН4. Молярне співвідношення відновлювального агента, такого як KВН4, до сполуки Формули IV становить від приблизно 1:1 до приблизно 2:1. Переважно, коли відновлювальним агентом є KВН4, молярне співвідношення KВН4 до сполуки Формули IV становить приблизно 1,5:1 і переважним розчинником є метанол. Це відновлення можна проводити при температурі приблизно від 30°С до приблизно 80°С приблизно 8 годин. Переважно, при температурі нижче 60°С і час необхідний для повного завершення реакції становить 6 годин. В альтернативному аспекті винаходу, фахівець може використати відновлювальні агенти, такі як LiAIH4 або NaAIH4, коли бажаними є безводні умови. В таких ситуаціях, можуть бути використані розчинники подібні ефіру або тетрагідрофурану. Утворюється амінодіольна сполука, що відповідає Формулі VII, вона взаємодіє, переважно в тому ж самому реакторі (тобто, in situ), з оксазолідинформуючим реагентом таким як формальдегід, 17 ацетон, 2-метоксипропен, 2,2-диметоксипропан, 2,2-діетоксипропан і їх суміші, за умов таких як ті, що приведені в прикладах одержання сполуки Формули VIII. Однією з переважних амінодіольних сполук, що відповідає Формулі VII, є В переважному втіленні, коли Флорфенікол є бажаним кінцевим продуктом, сполукою, що відповідає Формулі VIII є сполука: В переважному втіленні, метанол видаляють перегонкою і замінюють іншим розчинником визначеним тут, як оксазолідинформуюючий розчинник, такий як толуол, ксилен, гексан або їх суміш. Переважним оксазолідинформуючим розчинником є толуол. Співвідношення оксазолідинформуючого розчинника до метанолу становить приблизно 0,5:1-3:1 з переважним співвідношенням приблизно 1:1. Потім додають оксазолідинформуючий реагент, такий як формальдегід, ацетон, 2метоксипропен, 2,2-диметоксипропан, 2,2діетоксипропан і їх суміші. Одним з переважних оксазолідинформуючим реагентів є ацетон, який додають у співвідношенні до толуолу приблизно 0,5:1-3:1 з переважним співвідношенням приблизно 1:1. Реакція завершується утворенням оксазолідинової сполуки Формули VIII через приблизно 12-18 годин в присутності основи визначеної тут, як оксазолідинпромотуюча основа, така як карбонат калію, карбонат натрію, триметиламін або триетиламін. Переважною основою є карбонат калію або триетиламін. Оксазолідинформуючу реакцію можна проводити при температурі приблизно 6585°С. Переважно сполука Формули VIII залишається в тому ж самому реакторі після завершення стадії реакції, коли додається перший N-ацилюючий агент. Номенклатура "перший", "другий" і "третій" використовується для опису (1) N-ацилюючих (перші) агентів для того щоб відрізняти агенти, які використовуються для одержання оксазолідинзахищених амінодіолів Формули V від (2) Nацилюючих (другі) агентів, які використовуються при одержанні сполуки Формули XI після формування проміжної сполуки Формули X, і від (3) Nацилюючих (треті) агентів, які використовуються під час способу одержання оксазолідинзахищених 93212 18 амінодіолів Формули XII. Таким чином, деякими переважними першими N-ацилюючими сполуками є сполуки формули R6COR4 в якій: R4 є водень, ОН, С1-6 алкіл, С1-6 галоалкіл, С3-8 циклоалкіл, бензил, феніл або С1-6 фенілалкільна група, де фенільне кільце може бути заміщене одним або двома галогенами, С1-6 алкілами або С1-6 алкокси; і R6 є гало або С1-6 алкокси. Деякими більш переважними першими ацилюючими агентами э ацетилхлорид, ацетилбромід, пропіонілхлорид, пропіонілбромід, бутилхлорид, метилхлорформіат, етилхлорформіат, пропілхлорформіат і їх суміші. В переважному втіленні, коли Флорфенікол є бажаним кінцевим продуктом, сполукою, що відповідає Формулі V є сполука: . В переважному втіленні, додають основу, таку як карбонат калію, карбонат натрію, триметиламін або триетиламін у співвідношенні молярних еквівалентів до сполуки Формули VII приблизно 1:11:3. Переважним основою є карбонат калію або триетиламін і переважним співвідношенням молярних еквівалентів є приблизно 1,1-1. Переважно перший N-ацилюючий агент, ацетилхлорид, додають у молярному співвідношенні до сполуки Формули VII приблизно 1:1-3:1 з переважним співвідношенням 1,1:1. Температура реакції становить приблизно 20-30°С і реакція завершується за приблизно 2-4 години. Після одержання оксазолідинзахищеного амінодіолу Формули V, він може бути використаний в синтезі Флорфеніколу і подібних сполук. Таким чином, в наступному аспекті винаходу, спосіб винаходу продовжується фторуванням сполуки Формули V: де R1, R2, R3 і R4 є такими як визначено вище, фторувальним агентом в присутності органічного розчинника з одержанням сполуки Формули IX: 19 де R1, R2, R3 і R4 є такими як визначено вище. В одному з переважних аспектів цього втілення, коли Флорфенікол є бажаним кінцевим продуктом, сполукою, що відповідає Формулі IX є особливо: . Придатними фторувальними агентами є, без обмеження, N-(2-хлор-1,1,2трифторетил)діетиламін, N-(2-хлор-1,1,2трифторетил)диметиламін, N-(2-хлор-1,1,2трифторетил)дипропіламін, N-(2-хлор-1,1,2трифторетил)піролідин, N-(2-хлор-1,1,2трифторетил)-2-метилпіролідин, N-(2-хлор-1,1,2трифторетил)-4-метилпіперазин, N-(2-хлор-1,1,2трифторетил)-морфолін, N-(2-хлор-1,1,2трифторетил)піперидин, 1,1,2,2-тетрафторетилN,N-диметиламін, (діетиламіно)трифторидсірки, біс-(2-метоксиетил)амінотрифторидсірки, N,Nдіетил-1,1,2,3,3,3-гексафтор-1-пропанамін (реагент Ішикава) і їх суміші. Одним з переважних фторуючих агентів є N,N-діетил-1,1,2,3,3,3-гексафтор-1пропанамін. Молярне співвідношення фторувального агента, такого як N,N-діетил-1,1,2,3,3,3-гексафтор-1пропанамін до сполуки згідно з Формулою V становить приблизно від 1:1 до приблизно 2:1. Переважно, молярне співвідношення N,N-діетил1,1,2,3,3,3-гексафтор-1-пропанаміну до сполуки Формули V становить приблизно 1,5:1. Стадію фторування можна проводити при температурі приблизно від 80°С до приблизно 110°С і при тиску приблизно 60псі. Органічним розчинником використовуваним під час стадії фторування є переважно 1,2дихлоретан, метиленхлорид, хлороформ, хлорбензол, хлоровані вуглеводні або їх суміші. Більш переважним органічним розчинником є метиленхлорид. Після одержання сполуки Формули IX, її гідролізують кислотою з утворенням сполуки Формули X: 93212 20 де R1 є таким як визначено вище. Переважно, R1 є CH3SO2. Кислотою використовуваною в цій частині способу може бути неорганічна кислота, така як водна хлорводнева кислота, сірчана кислота або фосфорна кислота або органічна кислота, така як метансульфонова кислота. Стадію гідролізу переважно проводять шляхом нагрівання сполуки Формули IX з 6N водною хлорводневою кислотою при температурі приблизно від 90°С до приблизно 105°С протягом приблизно 60 хвилин. Інші придатні стадії гідролізу будуть очевидні середньому фахівцю в цій галузі. В одному з переважних аспектів цього втілення, коли Флорфенікол є бажаним кінцевим продуктом, сполукою, що відповідає Формулі X є: . Після завершення гідролізу, сполука Формули X взаємодіє без виділення (тобто, in situ) з другим N-ацилюючим агентом з утворенням сполук Формули XI: де R1 є такими як визначено вище, переважно CH3SO2; і R7 є водень, С1-6 алкіл, С1-6 галоалкіл, С1-6 дигалоалкіл, С1-6 тригалоалкіл, С3-8 циклоалкіл, С3-8 циклогалоалкіл, С3-8 циклодигалоалкіл, С3-8 циклотригалоалкіл, С2-6 алкеніл, С2-6 алкініл, С1-6 алкокси, С1-6 аралкіл, С2-6 аралкеніл, С2-6 гетероциклічний бензил, феніл або фенілалкіл, де фенільне кільце може бути заміщене одним або двома галогенами, С1-6 алкілами або С1-6 алкокси. Переважно, R7 є СН2СІ, СНСІ2, ССІ3, СН2Вr, CHBr2, CBr3, CH2F, CHF2 або CF3. Таким чином, однією з переважних сполук Формули XI є: 21 де R7 є таким як визначено вище. В одному з переважних аспектів цього втілення, коли Флорфенікол є бажаним кінцевим продуктом, сполукою, що відповідає Формулі XI є сполука Формули І: . Придатними другими N-ацилюючими сполуками є сполуки формули R8COR7, де R7 є таким же самим як описано вище і R8 є ОН, гало або С1-6 алкокси. Деякими більш переважними другими Nацилюючими агентами є дихлороцтова кислота або її реактивне похідне. Необмежуючий перелік включає реагенти, такі як метилдихлорацетат, етилдихлорацетат або дихлорацетилхлорид. Стадію другого N-ацилювання переважно проводять шляхом взаємодії сполуки Формули X в метанолі з метилдихлорацетатом при температурі приблизно від 20°С до приблизно 30°С протягом приблизно 12 години. Після одержання сполуки Формули XI і, якщо необхідно, сполуку Формули XI можна, необов'язково, очистити шляхом нагрівання в суміші моно-, ди- або три-алканолів і води. Спиртами в цій частині способу можуть бути С1-10 моноалканоли, С1-10 диалканоли і С1-10 триалканоли і їх суміші. Необмежуючий перелік С1-10 моноалканолів включає метанол, етанол, пропанол, ізопропанол, бутанол, втор-бутанол, т-бутанол і пентанол. Одним з переважних С1-10 моноалканолів є ізопропанол. Необмежуючий перелік С1-10 диалканолів включає етиленгліколь, пропіленгліколь і бутиленгліколь, серед яких пропіленгліколь є переважним. Гліцерин є переважним С1-10 триалканолом. С1-10 моноалканол є переважним для очищення. Одним з найбільш переважних С1-10 моноалканолів є ізопропанол. Співвідношення спирту, такого як ізопропанол, до води становить від 1:5 до 5:1. Переважно, коли спиртом є ізопропанол, співвідношення ізопропанолу до води становить 1:1. Сполуку Формули XI розчиняють в 1:1 суміші ізопропанолу і води і нагрівають до температури кипіння суміші. Розчин очищають фільтруванням з активованим вугіллям і потім охолоджують до приблизно 10-30°С і очищена сполука Формули XI кристалізується з розчину. Переважно, розчин охолоджують до приблизно 20 93212 22 25°С і очищена сполука Формули XI кристалізується з розчину. В переважному втіленні, коли Флорфенікол є бажаним кінцевим продуктом, очищена сполука, що відповідає Формулі XI, є сполукою Формули І. В іншому переважному втіленні, спосіб винаходу включає стадії: a) взаємодію сполуки Формули VI у реакторі з відновлювальним агентом в спиртовому розчиннику з утворенням амінодіолу Формули VII; b) взаємодію амінодіолу Формули VII у реакторі без виділення (тобто, in situ) з оксазолідинформуючим агентом з утворенням сполуки Формули VIII: c) взаємодію сполуки Формули VIII у реакторі без виділення (тобто, in situ) з третім Nацилюючим агентом з утворенням оксазолідинзахищеного амінодіолу Формули XII: ; в якій: R1, R2, R3 і R7 є такими як визначено вище. Переважно, R7 є СН2СІ, СНСІ2, ССІ3, СН2Вr, СНВr2, СВr3, CH2F, CHF2 або CF3; d) фторування сполуки Формули XII фторувальним агентом в присутності органічного розчинника з утворенням сполуки Формули XIII: де R1, R2, R3 і R7 є такими як визначено вище; є) селективний гідроліз сполуки Формули XIII використовуючи кислотний або основний каталізатор з утворенням сполуки Формули XI; і f) якщо необхідно, очищення сполуки Формули XI використовуючи суміш С1-10 моно, ди або триалканолу і води з утворенням чистої сполуки Формули XI. В переважному втіленні описаному вище, існують деякі переважні аспекти винаходу. Одним з переважних аспектів є такий, що після одержання сполуки Формули VIII вона взаємодіє переважно в тому ж самому реакторі (тобто, in situ) з придатною третьою N-ацилюючою сполукою. Деякими переважними третіми N-ацилюючими сполуками є сполуки формули R6COR7, де R6 і R7 є такими як визначено вище. В переважному втіленні, R6 є СІ і R7 23 є СН2СІ, СНСІ2, ССІ3, CH2Br, CHBr2, CBr3, CH2F, CHF2 або CF3. Деякими переважними третіми N-ацилюючими агентами є похідні алкілгалооцтової кислоти. Необмежуючий перелік включає реагенти, такі як метилдихлорацетат, етилдихлорацетат, дихлорацетилхлорид, метилхлорацетат, етилхлорацетат, хлорацетилхлорид, метилтрихлорацетат, етилтрихлорацетат, трихлорацетилхлорид, метилдифторацетат, етилдифторацетат, дифторацетилхлорид, метилфторацетат, етилфторацетат, фторацетилхлорид, метилтрифторацетат, етилтрифторацетат, трифторацетилхлорид, дихлорацетилбромід, дифторацетилбромід, ацетилхлорид і ацетилбромід. В переважному втіленні, коли Флорфенікол є бажаним кінцевим продуктом, сполукою, що відповідає Формулі XII є сполука Формули ХІІа: . В переважному втіленні, основу, таку як карбонат калію, карбонат натрію, триметиламін або триетиламін, додають у співвідношенні молярних еквівалентів до сполуки Формули VIlla приблизно 1:1-1:3. Переважною основою є карбонат калію або триетиламін і переважним співвідношенням молярних еквівалентів є приблизно 1,1-1. Переважний N-ацилюючий агент, дихлорацетилхлорид, додають у молярному співвідношенні до сполуки Формули VIlla приблизно 1:1-3:1, з переважним співвідношенням 1,1:1. Температура реакції становить приблизно 20-30°С і реакція завершується за приблизно 2-4 години. Після одержання оксазолідинзахищеного амінодіолу Формули XII, він може бути використаний в синтезі Флорфеніколу і подібних сполук. Таким чином, в наступному аспекті винаходу, винайдений спосіб продовжується фторуванням сполуки Формули XII: де R1, R2, R3 і R7 є такими як визначено вище, використовуючи фторувальний агент, як визначено раніше, в присутності органічного розчинника, як визначено раніше, з утворенням сполуки Формули XIII: 93212 24 де R1, R2, R3 і R7 є такими як визначено вище. В одному з переважних аспектів цього втілення, коли Флорфенікол є бажаним кінцевим продуктом, сполукою, що відповідає Формулі XIII, є особливо сполука Формули Xllla: Після одержання сполуки Формули XIII, її селективно гідролізують використовуючи кислотний або основний каталізатор з утворенням сполуки Формули XI. Широкий перелік кислотних каталізаторів може бути використаний при здійсненні способу винаходу. Необмежуючий перелік придатних кислотних каталізаторів включає неорганічні кислоти, такі як водна хлорводнева кислота, сірчана кислота або фосфорна кислота, або органічні кислоти, такі як метансульфонова кислота або птолуолсульфонова кислота. Одним з переважних кислотних каталізаторів є п-толуолсульфонова кислота. Аналогічно, широкий перелік основних каталізаторів може бути використаний при здійсненні способу винаходу. Необмежуючий перелік придатних основних каталізаторів включає неорганічні основи, такі як LiOH, NaOH, KОН, Lі2СО3, Na2CO3, K2CO3 або органічні основи, такі як метоксид натрію, етоксид натрію, метоксид калію і етоксид калію. Одним з переважних основних каталізаторів є K2СО3. Стадію селективного гідролізу переважно проводять при нагріванні сполуки Формули XIII з п-толуолсульфоновою кислотою в суміші органічного розчинника і води при температурі нижче 80°С. Одним з переважних органічних розчинників є метиленхлорид. Інші придатні стадії селективного гідролізу будуть очевидні середньому фахівцю в цій галузі. В одному з переважних аспектів цього втілення, коли Флорфенікол є бажаним кінцевим продуктом, сполукою, що відповідає Формулі XI є сполука Формули І: 25 . Після одержання сполуки Формули XI і якщо необхідно, її можна необов'язково очистити за способом, як описано вище. В переважному втіленні, коли Флорфенікол є бажаним кінцевим продуктом, очищена сполука, що відповідає Формулі XI, є сполукою Формули І. ПРИКЛАДИ Наступні препаративні приклади переважних нових похідних слугують лише засобом для розуміння винаходу і не призначені для якого б то не було обмеження рамок винаходу. Приклад 1 Одержання (4R,5R)-3-ацетил-2,2-диметил-4гідроксиметил-5-[4-(метилсульфоніл)феніл]-1,3оксазолідину (Сполука II) (2S,3R)-Етил-2-аміно-3-[4-(метилсульфоніл) феніл]-3-гідрокси-пропаноат (Сполука IV) (100г, 0,3480моль) в 500мл метанолу реагує з боргідридом калію (28,2г, 0,5220моль) протягом 4-8 годин при 50-60°С з кількісним утворенням (1R,2R)-2аміно-1-[4-(метилсульфоніл)феніл]-1,3пропандіолу (Сполука VII: R1 є метилсульфоніл) (85,36г, 0,3480моль) в розчині. Толуолом (500мл) і ацетоном (500мл) замінюють метанол, який відганяють. Додавання карбонату калію (6.9г, 0,0696моль) з нагріванням при 75-85°С протягом 12-18 годин дає (4R,5R)-2,2-диметил-4гідроксиметил-5-[4-(метилсульфоніл)феніл]-1,3оксазолідин (Сполука VIII: R1 є метилсульфоніл і R2 і R3 є метилами). Додавання карбонату калію (19,0г, 0,1914моль) і ацетилхлориду (30,0г, 0,3828моль) при 20-25°С протягом 2-4 годин і наступне додавання води (500мл) осаджує неочищений продукт. Фільтрування, промивання водою (250мл) і наступне висушування дає (4R,5R)-3ацетил-2,2-диметил-4-гідроксиметил-5-[4(метилсульфоніл)феніл]-1,3-оксазолідин (Сполука II). Приклад 2 Одержання (4R,5R)-3-ацетил-2,2-диметил-4гідроксиметил-5-[4-(метилсульфоніл)феніл]-1,3оксазолідину (Сполука II) (2S,3R)-Етил-2-аміно-3-[4-(метилсульфоніл) феніл]-3-гідрокси-пропаноат (Сполука IV) (100г, 0,3480моль) в метанолі (450мл) реагує з боргідридом калію (28,2г, 0,5220моль) протягом 4-8 години при 50-60°С з кількісним утворенням (1R,2R)-2аміно-1-[4-(метилсульфоніл)феніл]-1,3пропандіолу (Сполука VII: R1 є метилсульфоніл) (85,4г, 0,3480моль) в розчині. Толуолом (450мл) і ацетоном (450мл) замінюють метанол, який відганяють. Додавання триетиламіну (8,8г, 0,0870моль) з нагріванням при 70-80°С протягом 12-18 годин дає (4R,5R)-2,2-диметил-4-гідроксиметил-5-[4(метилсульфоніл)феніл]-1,3-оксазолідин (Сполука 93212 26 VIII: R1 є метилсульфоніл і R2 і R3 є метилами). Додавання триетиламіну (44,5г, 0,4402моль) і ацетилхлориду (30,0г, 0,3828моль) при 20-25°С протягом 2-4 годин і наступне додавання води (500мл) осаджує неочищений продукт. Фільтрування, промивання водою (200мл) і наступне висушування дає (4R,5R)-3-aцeтил-2,2-димeтил-4гiдpoкcимeтил-5-[4-(мeтилcyльфoнiл)фeнiл]-1,3оксазолідин (Сполука II). Приклад 3 Одержання (4R,5R)-3-ацетил-2,2-диметил-4гідроксиметил-5-[4-(метилсульфоніл)феніл]-1,3оксазолідину (Сполука II) (2S,3R)-Етил-2-аміно-3-[4-(метилсульфоніл) феніл]-3-гідрокси-пропаноат (Сполука IV) (100г, 0,3480моль) в тетрагідрофурані (500мл) реагує з алюмогідридом літію (16,0г, 0,4224моль) протягом 4-8 годин при 60-70°С з кількісним утворенням (1R,2R)-2-аміно-1-[4-(метилсульфоніл)феніл]-1,3пропандіолу (Сполука VII: R1 є метилсульфоніл) (85,36г, 0,3480моль). Додають етилацетат (75мл), що руйнує будь-який надлишок алюмогідриду літію. Додавання ксилену (600мл), 2метоксипропену (37,6г, 0,5220моль) і моногідрату п-толуолсульфонової кислоти (6,6г, 0,0348моль) при перемішуванні при 20-30°С протягом 10-16 годин дає (4R,5R)-2,2-диметил-4-гідроксиметил-5[4-(метилсульфоніл)феніл]-1,3-оксазолідин (Сполука VIII: R1 є метилсульфоніл і R2 і R3 є метилами). Додавання триетиламіну (81,3г, 0,8039моль) і ацетилхлориду (30,0г, 0,3828моль) при 20-25°С протягом 2-4 годин і наступне додавання води (650мл) осаджує неочищений продукт. Фільтрування, промивання водою (300мл) і наступне висушування дає (4R,5R)-3-aцeтил-2,2-димeтил-4гiдpoкcимeтил-5-[4-(мeтилcyльфoнiл)фeнiл]-1,3оксазолідин (Сполука II). Приклад 4 Одержання (4R,5R)-3-пpoпioнiл-2,2-димeтил-4гілдpoкcимeтил-5-[4-(метилсульфоніл)феніл]-1,3оксазолідину (Сполука V: R1 є метилсульфоніл, R2 і R3 є метилами і R4 є етил) (2S,3R)-Метил-2-аміно-3-[4(метилсульфоніл)феніл]-3-гідрокси-пропаноат (Сполука VI: R1 є метилсульфоніл і R5 є метил) (75г, 0,2744моль) в 350мл метанолу реагує з боргідридом натрію (16,6г, 0,4390моль) протягом 4-8 годин при 50-60°С з кількісним утворенням (1R,2R)-2-аміно-1-[4-(метилсульфоніл)феніл]-1,3пропандіолу (Сполука VII: R1 є метилсульфоніл) (67,31г, 0,2744моль) в розчині. Додавання 20% хлорводневої кислоти і 2,2-диметоксипропану (35,7г, 0,3430моль) при перемішуванні при 25-35°С протягом 3-5 години і наступне додавання ксилену (650мл) і нагрівання при 75-85°С протягом ще 1216 годин дає (4R,5R)-2,2-диметил-4-гідроксиметил5-[4-(метилсульфоніл)феніл]-1,3-оксазолідин (Сполука VIII: R1 є метилсульфоніл і R2 і R3 є метилами). Додавання триетиламіну (52,1г, 0,5145моль) і пропіонілхлориду (31,7г, 0,3430моль) при 20-25°С протягом 2-4 години і наступне додавання води (625мл) осаджує неочищений продукт. Фільтрування, промивання водою (300мл) наступне висушування дає (4R,5R)-3-пропіоніл-2,2диметил-4-гідроксиметил-5-[4-(метилсульфоніл) 27 феніл]-1,3-оксазолідин (Сполука V: R1 є метилсульфоніл, R2 і R3 є метилами і R4 є етил). Приклад 5 Одержання (4S,5R)-3-ацетил-2,2-диметил-4фторметил-5-[4-(метилсульфоніл)феніл]-1,3оксазолідину (Сполука IX: R1 є метилсульфоніл; R2, R3 і R4 є метилами) (4R,5R)-3-aцeтил-2,2-димeтил-4гiдpoкcимeтил-5-[4-(мeтилcyльфoнiл)фeнiл]-1,3оксазолідин (Сполука II) (75г, 0,2291моль) в метиленхлориді (525мл) реагує з N,N-діетил-1,1,2,3,3,3гексафтор-1-пропанаміном (реагент Ішикава) (76,7г, 0,3437моль) при 95-105°С протягом приблизно 4 годин. Охолодження до 20-25°С, додавання до гідроксиду натрію (6г) у воді (2500мл), відокремлення метиленхлоридного шару, перегонка і замінення метиленхлориду ізопропанолом (750мл), забезпечує осадження бажаного продукту. Фільтрування, промивання водою (100мл) і ізопропанолом (75мл), наступне висушування дає (4S,5R)-3-ацетил-2,2-диметил-4-фторметил-5-[4(метилсульфоніл)феніл]-1,3-оксазолідин (Сполука IX: R1 є метилсульфоніл; R2, R3 і R4 є метилами). Приклад 6 Одержання (4S,5R)-3-пропіоніл-2,2-диметил-4фторметил-5-[4-(метил-сульфоніл)феніл]-1,3оксазолідину (Сполука IX: R1 є метилсульфоніл, R2 і R3 є метилами і R4 є етил) (4R,5R)-3-пpoпioнiл-2,2-димeтил-4гiдpoкcимeтил-5-[4-(мeтилcyльфoнiл)фeнiл]-1,3оксазолідин (Сполука V: R1 є метилсульфоніл, R2 і R3 є метилами і R4 є етил) (70г, 0,2050моль) в метиленхлориді (450мл) реагує з N,N-діетил1,1,2,3,3,3-гексафтор-1-пропанаміном (реагент Ішикава) (73,2г, 0,328моль) при 95-105°С протягом 2-4 годин. Охолодження до 20-25°С, гасіння 25% водним гідроксидом натрію і водою (2000мл) і відокремлення метиленхлоридного шару дає розчин (4S,5R)-3-пропіоніл-2,2-диметил-4-фторметил-5-[4(метилсульфоніл)феніл]-1,3-оксазолідину (Сполука IX: R1 є метилсульфоніл, R2 і R3 є метилами і R4 є етил) для використання на наступній стадії. Приклад 7 Одержання (1R,2S)-2-дихлорацетамідо-3фтор-1-[4-(метилсульфоніл)феніл]-1-пропанолу (Флорфенікол) (4S,5R)-3-ацетил-2,2-диметил-4-фторметил-5[4-(метилсульфоніл)феніл]-1,3-оксазолідин (Сполука IX: R1 є метилсульфоніл; R2, R3 і R4 є метилами) (50,0г, 0,1518моль) гідролізує у воді (300мл), що містить 20% хлорводневу кислоту при 90100°С протягом приблизно 1 години. Доводять рН до значення більше ніж 12 шляхом додавання гідроксиду натрію і екстрагують метиленхлоридом (500мл) одержуючи (1R,2S)-1-[4(метилсульфоніл)феніл]-2-аміно-3-фтор-1пропанол (Сполука Ха) в розчині. Метанолом (100мл) замінюють метиленхлорид, який відганяють. Додавання метилдихлорацетату (65,1г, 0,4554моль) і триетиламіну (16,1г, 0,1594моль) при перемішування протягом 12-16 годин при 20-25°С, наступне додавання води (175мл) і толуолу (100мл) осаджує продукт. Фільтрування, промивання водою (100мл) і толуолом (175мл) і наступне висушування дає (1R,2S)-2-дихлорацетамідо-3 93212 28 фтор-1-[4-(метилсульфоніл)феніл]-1-пропанол (Флорфенікол). Приклад 8 Одержання (1R,2S)-2-дихлорацетамідо-3фтор-1-[4-(метилсульфоніл)феніл]-1-пропанолу (Флорфенікол) (4S,5R)-3-ацетил-2,2-диметил-4-фторметил-5[4-(метилсульфоніл)феніл]-1,3-оксазолідин (Сполука IX: R1 є метилсульфоніл; R2, R3 і R4 є метилами) (50,0г, 0,1518моль) гідролізує у воді (300мл), що містить 20% хлорводневу кислоту при 90100°С протягом приблизно 1 години. Доводять рН до значення більше ніж 12 шляхом додавання гідроксиду натрію і екстрагують метиленхлоридом (500мл) одержуючи (1R,2S)-1-[4(метилсульфоніл)феніл]-2-аміно-3-фтор-1пропанол (Сполука Ха) в розчині. Додавання триетиламіну (16,9г, 0,1670моль) і дихлорацетилхлориду (24,6г, 0,1670моль) при 20-30°С протягом 4-6 годин і наступне видалення метиленхлориду перегонкою і заміна толуолом (350мл) і водою (100мл) осаджує продукт. Фільтрування, промивання водою (150мл) і толуолом (150мл) і наступне висушування дає (1R,2S)-2-дихлорацетамідо-3-фтор-1[4-(метилсульфоніл)феніл]-1-пропанол (Флорфенікол). Приклад 9 Очищення (1R,2S)-2-дихлорацетамідо-3-фтор1-[4-(метилсульфоніл)феніл]-1-пропанолу (Флорфенікол) (1R,2S)-2-дихлорацетамідо-3-фтор-1-[4(метилсульфоніл)феніл]-1-пропанол (Флорфенікол) (45г, 0,1256моль) розчиняють у воді (115мл) і ізопропанолі (115мл) при кип'ятінні. Охолодження до 20-25°С, фільтрування твердих речовин, промивання 1:1 вода/ізопропанол (50мл) і наступне висушування дає чистий (1R,2S)-2дихлорацетамідо-3-фтор-1-[4(метилсульфоніл)феніл]-1-пропанол (Флорфенікол). Приклад 10 Одержання і очищення (1R,2S)-2дихлорацетамідо-3-фтор-1-[4-(метилсульфоніл) феніл]-1-пропанолу (Флорфенікол) (4S,5R)-3-ацетил-2,2-диметил-4-фторметил-5[4-(метилсульфоніл)феніл]-1,3-оксазолідин (Сполука IX: R1 є метилсульфоніл; R2, R3 і R4 є метилами) (50,0г, 0,1518моль) гідролізує у воді (300мл), що містить 20% хлорводневу кислоту при 90100°С протягом приблизно 1 години. Промивають метиленхлоридом (200мл), доводять рН до значення більше ніж 12 шляхом додавання гідроксиду натрію і екстрагують метиленхлоридом (300мл) одержуючи (1R,2S)-1-[4-(метилсульфоніл)феніл]2-аміно-3-фтор-1-пропанол (Сполука Ха) в розчині. Метанолом (100мл) замінюють метиленхлорид, який відганяють. Додавання метилдихлорацетату (65,1г, 0,4554моль) і триетиламіну (16,1г, 0,1594моль) при перемішування протягом 12-16 години при 20-25°С і наступне додавання води (175мл) і толуолу (100мл) осаджує неочищений продукт. Фільтрування, промивання водою (100мл) і толуолом (174мл) і наступне розчинення у воді (115мл) і ізопропанолі (115мл) при кип'ятінні, охолодження до 20-25°С, фільтрування твердих ре 29 93212 човин, промивання 1:1 вода/ізопропанол (50мл) і наступне висушування дає чистий (1R,2S)-2дихлорацетамідо-3-фтор-1-[4(метилсульфоніл)феніл]-1-пропанол (Флорфенікол). Приклад 11 Одержання і очищення (1R,2S)-2дихлорацетамідо-3-фтор-1-[4-(метилсульфоніл) феніл]-1-пропанолу (Флорфенікол) Метиленхлорид (450мл) відганяють з розчину (4S,5R)-3-пропіоніл-2,2-диметил-4-фторметил-5-[4(метилсульфоніл)феніл]-1,3-оксазолідину (Сполука IX: R1 є метилсульфоніл, R2 і R3 є метилами і R4 є етил) (50,0г, 0,1456моль) і потім додають воду (300мл), що містить 20% хлорводневу кислоту, і нагрівають до 90-100°С протягом 2-4 годин. Доводять рН до значення більше ніж 12 шляхом додавання гідроксиду натрію і екстрагують метиленхлоридом (350мл) одержуючи розчин (1R,2S)-1-[4(метилсульфоніл)феніл]-2-аміно-3-фтор-1пропанолу (Сполука Ха). Метанолом (150мл) замінюють метиленхлорид, який відганяють. Додавання метилдихлорацетату (52,0г, 0,3640моль) і триетиламіну (11,0г, 0,1092моль) при перемішування протягом 12-16 години при 20-25°С і наступне додавання води (150мл) і толуолу (100мл) осаджує неочищений продукт. Фільтрування, промивання водою (75мл) і толуолом (125мл) і наступне розчинення у воді (50мл) і ізопропанолі (100мл) при кип'ятінні, охолодження до 20-25°С, фільтрування твердих речовин, промивання 1:1 вода/ізопропанол (50мл) і наступне висушування дає чистий (1R,2S)-2-дихлорацетамідо-3-фтор-1-[4(метилсульфоніл)феніл]-1-пропанол (Флорфенікол). Приклад 12 Одержання (4R,5R)-3-дихлорацетил-2,2диметил-4-гідроксиметил-5-[4(метилсульфоніл)феніл]-1,3-оксазолідину (Сполука ХІІа) (2S,3R)-Етил-2-аміно-3-[4(метилсульфоніл)феніл]-3-гідрокси-пропаноат (Сполука IV) (100г, 0,3480моль) в 500мл метанолу реагує з боргідридом калію (28,2г, 0,5220моль) протягом 4-8 годин при 50-60°С з кількісним утворенням (1R,2R)-2-аміно-1-[4(метилсульфоніл)феніл]-1,3-пропандіолу (Сполука VII: R1 є метилсульфоніл) (85,36г, 0,3480моль) в розчині. Толуолом (500мл) і ацетоном (500мл) за Комп’ютерна верстка М. Ломалова 30 мінюють метанол, який відганяють. Додавання карбонату калію (6.9г, 0,0696моль) і нагрівання при 75-85°С протягом 12-18 годин дає (4R,5R)-2,2димeтил-4-гiдpoкcимeтил-5-[4(метилсульфоніл)феніл]-1,3-оксазолідин (Сполука VIII: R1 є метилсульфоніл і R2 і R3 є метилами). Додавання карбонату калію (19,0г, 0,1914моль) і дихлорацетилхлориду (56,4г, 0,3828моль) при 2025°С протягом 2-4 години і наступне додавання води (500мл) осаджує неочищений продукт. Фільтрування, промивання водою (250мл) наступне висушування дає (4R,5R)-3-дихлорацетил-2,2диметил-4-гідроксиметил-5-[4(метилсульфоніл)феніл]-1,3-оксазолідин (Сполука ХІІа). Приклад 13 Одержання (4S,5R)-3-дихлорацетил-2,2диметил-4-фторметил-5-[4-(метил-сульфоніл)феніл]-1,3-оксазолідину (Сполука ХІІІа) (4R,5R)-3-дихлорацетил-2,2-диметил-4гідроксиметил-5-[4-(метилсульфоніл)феніл]-1,3оксазолідин (Сполука ХІІа) (81г, 0,2050моль) в метиленхлориді (450мл) реагує з N,N-діетил1,1,2,3,3,3-гексафтор-1-пропанаміном (реагент Ішикава) (73,2г, 0,328моль) при 95-105°С протягом 2-4 годин. Охолодження до 20-25°С, гасіння 25% водним гідроксидом натрію і водою (2000мл) і відокремлення метиленхлоридного шару дає розчин (4S,5R)-3-дихлорацетил-2,2-диметил-4фторметил-5-[4-(метилсульфоніл)феніл]-1,3оксазолідину (Сполука ХІІІа) для застосування як проміжного продукту на наступній стадії способу. Приклад 14 Одержання (1R,2S)-2-дихлорацетамідо-3фтор-1-[4-(метилсульфоніл)феніл]-1-пропанолу (Флорфенікол) (4S,5R)-3-дихлорацетил-2,2-диметил-4фторметил-5-[4-(метилсульфоніл)феніл]-1,3оксазолідин (Сполука ХІІІа) (60,5г, 0,1519моль) селективно гідролізує в метиленхлориді (300мл) і воді (100мл), що містить п-толуолсульфонову кислоту, при 60°С протягом декількох годин. Видалення метиленхлориду перегонкою і охолодження до 20-25°С осаджує продукт. Фільтрування, промивання водою (100мл) і толуолом (100мл) і наступне висушування дає (1R,2S)-2дихлорацетамідо-3-фтор-1-[4(метилсульфоніл)феніл]-1-пропанол (Флорфенікол). Підписне Тираж 23 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюA process for preparing oxazolidine protected aminodiol compounds useful as intermediates to florfenicol
Автори англійськоюTowson James C.
Назва патенту російськоюСпособ получения оксазолидинзащищенных аминодиолов полезных kak промежуточные соединения для получения флорфеникола
Автори російськоюТаусон Джеймс K.
МПК / Мітки
МПК: C07D 263/06, C07C 315/00
Мітки: проміжні, спосіб, амінодіолів, флорфеніколу, корисних, сполуки, оксазолідинзахищених, одержання
Код посилання
<a href="https://ua.patents.su/15-93212-sposib-oderzhannya-oksazolidinzakhishhenikh-aminodioliv-korisnikh-yak-promizhni-spoluki-dlya-oderzhannya-florfenikolu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання оксазолідинзахищених амінодіолів корисних як проміжні сполуки для одержання флорфеніколу</a>
Попередній патент: Ложе магазинної гвинтівки та ствольна коробка магазинної гвинтівки для такого ложа
Наступний патент: Піримідинамідні сполуки як інгібітори pgds
Випадковий патент: Спосіб витягування чистого бензола з вуглеводневих сумішей












