Спосіб одержання сполук на основі імідазолу
Формула / Реферат
1. Спосіб одержання сполуки формули І:
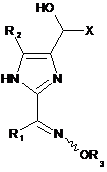 , (I)
, (I)
де X являє собою необов’язково заміщений алкіл; R1 являє собою необов’язково заміщений алкіл; R2 являє собою водень, галоген, нітрил або необов’язково заміщений алкіл, арил, алкіларил, арилалкіл, гетероалкіл, гетероцикл, алкілгетероцикл або гетероциклоалкіл, і R3 являє собою водень або необов’язково заміщений алкіл, арил, алкіларил, арилалкіл, гетероалкіл, гетероцикл, алкілгетероцикл або гетероциклоалкіл; в якому здійснюють
взаємодію сполуки формули II:
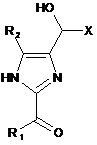 , (II)
, (II)
зі сполукою формули III:
H2N-OR3, (III)
за умов, достатніх для утворення суміші Е- і Z-ізомерів сполуки формули І; і взаємодію суміші ізомерів Е і Z із сильною кислотою.
2. Спосіб за п. 1, в якому X являє собою алкіл, необов’язково заміщений одним або декількома гідроксильними, ацетатними або галогеновими залишками.
3. Спосіб за п. 1, в якому R2 являє собою водень.
4. Спосіб за п. 1, в якому R3 являє собою водень.
5. Спосіб за п. 1, в якому сполука формули І являє собою сполуку формули I(a)
 , (I(a))
, (I(a))
де
R4 являє собою OR4A, OC(O)R4A, N(R4B)2, NHC(O)R4B, водень або галоген;
R5 являє собою OR5A, OC(O)R5A, N(R5B)2, NHC(O)R5B, водень або галоген;
R6 являє собою OR6A, OC(O)R6A, N(R6B)2, NHC(O)R6B, водень або галоген;
R7 являє собою алкіл, CH2OR7A, CH2OC(O)R7A, CH2N(R7B)2, CH2NHC(O)R7B, водень або галоген, і
кожен із R4A, R5A, R6А, R7A, R4B, R5B, R6B і R7B незалежно являє собою водень або необов’язково заміщений алкіл, арил, алкіларил, арилалкіл, гетероалкіл, гетероцикл, алкілгетероцикл або гетероциклоалкіл.
6. Спосіб за п. 5, в якому сполука формули І(а) являє собою стереомерно чисту сполуку формули І(b):
 (I(b)).
(I(b)).
7. Спосіб за п. 5, в якому один або декілька з R4, R5 і R6 являють собою гідрокси або галоген.
8. Спосіб за п. 5, в якому всі R4, R5 і R6 являють собою гідроксил або ацетат.
9. Спосіб за п. 1, в якому сильна кислота являє собою йодистоводневу, бромистоводневу, хлористоводневу, сірчану, азотну, фосфорну, алкансульфонову або аренсульфонову кислоту.
10. Спосіб збільшення відношення головний ізомер:другорядний ізомер у суміші сполук формули І:
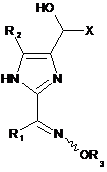 , (I)
, (I)
в якому здійснюють
взаємодію розчину, що містить першу суміш сполук формули І, із сильною кислотою за умов, достатніх для одержання другої суміші сполук формули І, де
відношення головний ізомер:другорядний ізомер першої суміші є меншим, ніж відношення головний ізомер:другорядний ізомер другої суміші;
X являє собою необов’язково заміщений алкіл;
R1 являє собою необов’язково заміщений алкіл;
R2 являє собою водень, галоген, нітрил або необов’язково заміщений алкіл, арил, алкіларил, арилалкіл, гетероалкіл, гетероцикл, алкілгетероцикл або гетероциклоалкіл, і
R3 являє собою водень або необов’язково заміщений алкіл, арил, алкіларил, арилалкіл, гетероалкіл, гетероцикл, алкілгетероцикл або гетероциклоалкіл.
11. Спосіб за п. 10, в якому сполуки формули І одержують шляхом взаємодії сполуки формули II:
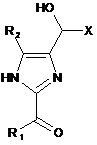 , (II)
, (II)
зі сполукою формули III:
H2N-OR3, III
за умов, достатніх для утворення сполуки формули І.
12. Спосіб за п. 10, в якому X являє собою алкіл, необов’язково заміщений одним або декількома гідроксильними, ацетатними або галогеновими залишками.
13. Спосіб за п. 10, в якому R2 являє собою водень.
14. Спосіб за п. 10, в якому R3 являє собою водень.
15. Спосіб за п. 10, в якому сполука формули І являє собою сполуку формули І(а):
 , (I(a))
, (I(a))
де
R4 являє собою OR4A, OC(O)R4A, N(R4B)2, NHC(O)R4B, водень або галоген;
R5 являє собою OR5A, OC(O)R5A, N(R5B)2, NHC(O)R5B, водень або галоген;
R6 являє собою OR6A, OC(O)R6A, N(R6B)2, NHC(O)R6B, водень або галоген;
R7 являє собою алкіл, CH2OR7A, CH2OC(O)R7A, CH2N(R7B)2, CH2NHC(O)R7B, водень або галоген, і
кожен із R4A, R5A, R6А, R7A, R4B, R5B, R6B і R7B незалежно являє собою водень або необов’язково заміщений алкіл, арил, алкіларил, арилалкіл, гетероалкіл, гетероцикл, алкілгетероцикл або гетероциклоалкіл.
16. Спосіб за п. 15, в якому сполука формули І(а) являє собою стереохімічно чисту сполуку формули І(b):
 (I(b)).
(I(b)).
17. Спосіб за п. 15, в якому один або декілька з R4, R5, R6 являє собою гідрокси або галоген.
18. Спосіб за п. 15, в якому всі R4, R5, R6 являють собою гідроксил або ацетат.
19. Спосіб за п. 10, в якому розчин містить спирт.
20. Спосіб за п. 19, в якому спирт являє собою метанол, етанол, пропанол або ізопропанол.
21. Спосіб за п. 10, в якому сильна кислота являє собою йодистоводневу, бромистоводневу, хлористоводневу, сірчану, азотну, фосфорну, алкансульфонову або аренсульфонову кислоту.
22. Спосіб за п. 10, який додатково включає нагрівання розчину до температури більше ніж приблизно 30 °С (наприклад, більше ніж приблизно 40, 50 або 60 °С).
23. Спосіб за п. 10, в якому відношення головний ізомер:другорядний ізомер збільшується від менше ніж приблизно 5:1 до більше ніж приблизно 8:1.
24. Спосіб за п. 23, в якому відношення головний ізомер:другорядний ізомер збільшується від менше ніж приблизно 4:1 до більше ніж приблизно 10:1.
25. Спосіб за п. 24, в якому відношення головний ізомер:другорядний ізомер збільшується від приблизно 3:1 до більше ніж приблизно 13:1.
26. Спосіб за п. 10, який додатково включає збільшення рН розчину, що містить другу суміш.
27. Спосіб за п. 26, в якому рН збільшують до більше ніж приблизно 6,0 (наприклад, більше ніж приблизно 7,0 або 8,0).
28. Спосіб збільшення відношення E:Z ізомерів у суміші (Е)-1-(4-((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1Н-імідазол-2-іл)етаноноксиму і (Z)-1-(4-((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1H-імідазол-2-іл)етаноноксиму, який включає
контактування розчину, що містить першу суміш (E)-1-(4-((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1Н-імідазол-2-іл)етаноноксиму і (Z)-1-(4-((1R,2S,3R)-1,2,3,4-тeтpaгiдpoкcибyтил)-1H-iмiдaзoл-2-iл)eтaнoнoкcимy, із сильною кислотою за умов, достатніх для одержання другої суміші (Е)-1-(4-((1R,2S,3R)-1,2,3,4-тeтpaгiдpoкcибyтил)-1H-iмiдaзoл-2-iл)eтaнoнoкcимy і (Е)-1-(4-((1R,2S,3R)-1,2,3,4-тeтpaгiдpoкcибyтил)-1H-iмiдaзoл-2-iл)eтaнoнoкcимy;
де відношення E:Z ізомерів першої суміші є меншим, ніж відношення ізомерів E:Z другої суміші.
29. Спосіб за п. 28, в якому першу суміш одержують шляхом взаємодії 1-(4-((1R,2S,3R)-1,2,3,4-тeтpaгiдpoкcибyтил)-1H-iмiдaзoл-2-iл)eтaнoнy з гідроксиламіном за умов, достатніх для утворення 1-(4-((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1Н-імідазол-2-іл)етаноноксиму.
30. Спосіб за п. 29, в якому 1-(4-((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1Н-імідазол-2-іл)етанон одержують шляхом взаємодії 1-аміно-1-дезокси-D-фруктози з 2-етоксіакрилонітрилом за умов, достатніх для утворення 1-(4-((1R,2S,3R)-1,2,3,4-тeтpaгiдpoкcибyтил)-1H-iмiдaзoл-2-iл)eтaнoнy.
31. Спосіб за п. 28, в якому розчин містить спирт.
32. Спосіб за п. 31, в якому спирт являє собою метанол, етанол, пропанол або ізопропанол.
33. Спосіб за п. 28, в якому сильна кислота являє собою йодистоводневу, бромистоводневу, хлористоводневу, сірчану, азотну, фосфорну, алкансульфонову або аренсульфонову кислоту.
34. Спосіб за п. 28, який додатково включає нагрівання розчину при температурі більше ніж приблизно 30 °С (наприклад, більше ніж приблизно 40, 50 або 60 °С).
35. Спосіб за п. 28, в якому відношення E:Z ізомерів збільшують від менше ніж приблизно 5:1 до більше ніж приблизно 8:1.
36. Спосіб за п. 35, в якому відношення E:Z ізомерів збільшують від менше ніж приблизно 4:1 до більше ніж приблизно 10:1.
37. Спосіб за п. 36, в якому відношення E:Z ізомерів збільшують від приблизно 3:1 до більше ніж приблизно 13:1.
38. Спосіб за п. 28, який додатково включає збільшення рН розчину, що містить другу суміш.
39. Спосіб за п. 38, в якому рН збільшують до більше ніж приблизно 6,0 (наприклад, більше ніж приблизно 7,0 або 8,0).
40. Спосіб одержання 1-(4-((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1Н-імідазол-2-іл)етанону, в якому здійснюють
додавання першої частини метоксиду натрію до розчину, що містить 2-етоксіакрилонітрил, з одержанням першої суміші;
взаємодію першої суміші з 1-аміно-1-дезокси-D-фруктозою з одержанням другої суміші;
додавання другої частини метоксиду натрію до другої суміші з одержанням третьої суміші;
додавання оцтової кислоти до третьої суміші з одержанням четвертої суміші, і
змішування четвертої суміші протягом часу і при температурі, достатніх для утворення 1-(4-((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1Н-імідазол-2-іл)етанону;
де другу суміш підтримують при температурі більше ніж приблизно 5 °С (наприклад, більше ніж приблизно 10, 15 або 20 °С).
41. Спосіб за п. 40, в якому першу суміш підтримують при температурі більше ніж приблизно 5 °С (наприклад, більше ніж приблизно 10, 15 або 20 °С).
42. Спосіб за п. 40, в якому першу частину метоксиду натрію додають у вигляді розчину метоксиду натрію в метанолі в кількості більше ніж приблизно 15 % мас. (наприклад, більше ніж приблизно 20 або 25 % мас.).
43. Спосіб за п. 40, в якому другу частину метоксиду натрію додають у вигляді розчину метоксиду натрію в метанолі в кількості більше ніж приблизно 15 % мас. (наприклад, більше ніж приблизно 20 або 25 % мас.).
44. Спосіб за п. 40, в якому 1-аміно-1-дезокси-D-фруктозу одержують у суспензії, що додатково містить її сіль з оцтовою кислотою.
45. Спосіб за п. 40, в якому третю суміш розводять водою перед додаванням до неї оцтової кислоти.
46. Спосіб за п. 40, в якому четверту суміш нагрівають до температури більше ніж приблизно 30 °С (наприклад, більше ніж приблизно 35, 40, 45, 50, 55 або 60 °С).
47. Спосіб за п. 45, в якому четверту суміш нагрівають протягом менше ніж приблизно 5 годин (наприклад, менше ніж приблизно 4, 3 або 2 годин).
48. Спосіб за п. 40, в якому 1-(4-((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1H-імідазол-2-іл)етанон виділяють із виходом більше ніж приблизно 50 % (наприклад, більше ніж приблизно 55, 60, 65, 70, 75 або 80 %).
Текст
Реферат: Описуються способи одержання сполуки на основі імідазолу. Конкретні сполуки являють собою сполуку формули (І) HO R2 HN R1 X N N OR 3 . UA 97664 C2 (12) UA 97664 C2 UA 97664 C2 5 10 15 20 25 30 35 40 45 50 Даний винахід стосується способів синтезу сполук на основі імідазолу. Сполука 1-(4-((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1Н-імідазол-2-іл)етанон (ТНІ) являє собою другорядний компонент Carmel Color III, і як повідомляють, знижує кількість відліків лімфоцитів, циркулюючих у крові в щурів. Способи одержання ТНІ відомі. Див., наприклад, Kröplien, U. and Rosdorfer, J. J. Org. Chem. 50: 1131-1133 (1985); патент США 4567194, Kröplien et al.; Cliff, M.D. and Pyne, S.G., Tet. Lett. 36(33): 5969-5972 (1995); Cliff, M.D. and Pyne, S.G., J. Org. Chem. 62: 1023-1032 (1997). Конкретний спосіб, як повідомляють, дає ТНІ із загальним виходом 46%. Див. Halweg, K.M. and Büchi, G.J. Org. Chem. 50:1134-1136. 1135(1985). Останнім часом повідомляють, що певні сполуки на основі імідазолу являють собою сильнодіючі інгібітори імунної реакції і можуть бути придатними для лікування таких захворювань, як ревматоїдний артрит і діабет І типу. Див. заявку на патент США 11/698253, Augeri et al., зареєстровану 25 січня 2007 року. Для полегшення їхнього дослідження і використання є бажаними додаткові способи їхнього синтезу. Даний винахід охоплює способи одержання сполук формули І: де X являє собою необов'язково заміщений алкіл; R1 являє собою необов'язково заміщений алкіл; R2 являє собою водень, галоген, нітрил або необов'язково заміщений алкіл, арил, алкіларил, арилалкіл, гетероалкіл, гетероцикл, алкілгетероцикл або гетероциклоалкіл і R3 являє собою водень або необов'язково заміщений алкіл, арил, алкіларил, арилалкіл, гетероалкіл, гетероцикл, алкілгетероцикл або гетероциклоалкіл. Даний винахід також охоплює способи збільшення відношення головного ізомеру до другорядного (головний ізомер:другорядний ізомер) у сумішей сполук формули І. Даний винахід також охоплює способи одержання 1-(4-((1R,2S,3R)-1,2,3,4тетрагідроксибутил)-1H-імідазол-2-іл)етанону. Короткий опис фігур Аспекти даного винаходу можуть бути зрозумілими з посиланням на фіг. 1, яка показує 1 спектр Н ЯМР суміші (E)-1-(4-((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1Н-імідазол-2іл)етаноноксиму і (Z)-1-(4-((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1H-імідазол-2іл)етаноноксиму. Детальний опис Даний винахід частково ґрунтується на виявленні нових способів одержання сполук формули І. Конкретні способи є добре пристосованими для одержання сполук у великому масштабі (наприклад, у масштабі кілограмів). Даний винахід також ґрунтується на виявленні нових способів одержання 1-(4-((1R,2S,3R)1,2,3,4-тeтpaгiдpoкcибyтил)-1H-iмiдaзoл-2-iл)eтaнoнy. Конкретні способи дають сполуки з високим виходом. Якщо не зазначено інше, термін "алкеніл" означає вуглеводень із прямим ланцюгом, розгалужений і/або циклічний, що має від 2 до 20 (наприклад, 2-10 або 2-6) атомів вуглеводу і що містить, принаймні, один подвійний зв'язок вуглець-вуглець. Репрезентативні алкенільні залишки включають вініл, аліл, 1-бутеніл, 2-бутеніл, ізобутиленіл, 1-пентеніл, 2-пентеніл, 3метил-1-бутеніл, 2-метил-2-бутеніл, 2,3-диметил-2-бутеніл, 1-гексеніл, 2-гексеніл, 3-гексеніл, 1гептеніл, 2-гептеніл, 3-гептеніл, 1-октеніл, 2-октеніл, 3-октеніл, 1-ноненіл, 2-ноненіл, 3-ноненіл, 1-деценіл, 2-деценіл і 3-деценіл. Якщо не зазначено інше, термін "алкокси" означає -О-алкільну групу. Приклади алкоксигруп включають, але без обмеження, -ОСН3, -ОСН2СН3, -О(СН2)2СН3, -О(СН2)3СН3, -О(СН2)4СН3 і О(СН2)5СН3. Термін "нижчий алкокси" стосується -О-(нижчого алкілу). Якщо не зазначено інше, термін "алкіл" означає вуглеводень із прямим ланцюгом, розгалужений і/або циклічний ("циклоалкіл"), що має від 1 до 20 (наприклад, 1-10 або 1-4) атомів вуглецю. Алкільні залишки, що мають від 1 до 4 атомів вуглецю, згадуються як "нижчий алкіл". 1 UA 97664 C2 5 10 15 20 25 30 35 40 45 50 55 60 Приклади алкільних груп включають метил, етил, пропіл, ізопропіл, н-бутил, трет-бутил, ізобутил, пентил, гексил, ізогексил, гептил, 4,4-диметилпентил, октил, 2,2,4-триметилпентил, ноніл, децил, ундецил і додецил. Циклоалкільні залишки можуть бути моноциклічними або мультициклічними та їхні приклади включають циклопропіл, циклобутил, циклопентил, циклогексил і адамантил. Додаткові приклади алкільних залишків мають лінійні, розгалужені і/або циклічні частини (наприклад, 1-етил-4-метилциклогексил). Термін "алкіл" включає насичені вуглеводні, а також алкенільні та алкінільні залишки. Якщо не зазначено інше, термін "алкіларил" або "алкіл-арил" означає алкільний залишок, зв'язаний з арильним залишком. Якщо не зазначено інше, термін "алкілгетероарил" або "алкіл-гетероарил" означає алкільний залишок, зв'язаний із гетероарильним залишком. Якщо не зазначено інше, термін "алкілгетероцикл"або "алкіл-гетероцикл" означає алкільний залишок, зв'язаний із гетероциклічним залишком. Якщо не зазначено інше, термін "алкініл" означає вуглеводень із прямим ланцюгом, розгалужений або циклічний, що має від 2 до 20 (наприклад, 2-20 або 2-6) атомів вуглецю і що містить, принаймні, один потрійний зв'язок вуглець-вуглець. Репрезентативні алкінільні залишки включають ацетиленіл, пропініл, 1-бутиніл, 2-бутиніл, 1-пентиніл, 2-пентиніл, З-метил-1-бутиніл, 4-пентиніл, 1-гексиніл, 2-гексиніл, 5-гексиніл, 1-гептиніл, 2-гептиніл, 6-гептиніл, 1-октиніл, 2октиніл, 7-октиніл, 1-нониніл, 2-нониніл, 8-нониніл, 1-дециніл, 2-дециніл і 9-дециніл. Якщо не зазначено інше, термін "арил" означає ароматичне кільце або ароматичну або частково ароматичну кільцеву систему, що складається з атомів вуглецю і водню. Арильний залишок може містити безліч кілець, зв'язаних або конденсованих разом. Приклади арильних залишків включають антраценіл, азуленіл, біфеніл, флуореніл, індан, інденіл, нафтил, фенантреніл, феніл, 1,2,3,4-тетрагідронафталін і толіл. Якщо не зазначено інше, термін "арилалкіл" або "арил-алкіл" означає арильний залишок, зв'язаний з алкільним залишком. Якщо не зазначено інше, термін "відношення ізомерів E:Z", коли він стосується суміші Εізомеру сполуки і відповідного його Z-ізомеру, означає відношення цих ізомерів. Такі відношення можуть визначатися за допомогою різних способів, відомих у даній галузі, включаючи хроматографічні (наприклад, ВЕРХ) і спектроскопічні способи (наприклад, ЯМР, Рамановське розсіювання та інфрачервоне поглинання). Якщо не зазначено інше, термін "галоген" охоплює фтор, хлор, бром і йод. Якщо не зазначено інше, термін "гетероалкіл" стосується алкільного залишку (наприклад, лінійного, розгалуженого або циклічного), в якому, принаймні, один із його атомів вуглецю замінюється гетероатомом (наприклад, Ν, Ο або S). Якщо не зазначено інше, термін "гетероарил" означає арильний залишок, де, принаймні, один із його атомів вуглецю замінюється гетероатомом (наприклад, Ν, Ο або S). Приклади включають акридиніл, бензімідазоліл, бензофураніл, бензоізотіазоліл, бензоізоксазоліл, бензохіназолініл, бензотіазоліл, бензоксазоліл, фурил, імідазоліл, індоліл, ізотіазоліл, ізоксазоліл, оксадіазоліл, оксазоліл, фталазиніл, піразиніл, піразоліл, піридазиніл, піридил, піримідиніл, піримідил, піроліл, хіназолиніл, хінолініл, тетразоліл, тіазоліл і триазиніл. Якщо не зазначено інше, термін "гетероарилалкіл" або "гетероарил-алкіл" означає гетероарильний залишок, зв'язаний з алкільним залишком. Якщо не зазначено інше, термін "гетероцикл" стосується ароматичного, частково ароматичного або неароматичного моноциклічного або поліциклічного кільця або кільцевої системи, що складається з вуглецю, водню і, принаймні, одного гетероатома (наприклад, Ν, Ο або S). Гетероцикл може містити безліч (тобто два або більше) кілець, конденсованих або зв'язаних разом. Гетероцикли включають гетероарили. Приклади включають бензо[1,3]діоксоліл, 2,3-дигідробензо[1,4]діоксиніл, цинолініл, фураніл, гідантоїніл, морфолініл, оксетаніл, оксираніл, піперазиніл, піперидиніл, піролідиноніл, піролідиніл, тетрагідрофураніл, тетрагідропіраніл, тетрагідропіридиніл, тетрагідропіримідиніл, тетрагідротіофеніл, тетрагідротіопіраніл і валеролактаміл. Якщо не зазначено інше, термін "гетероциклоалкіл" або "гетероцикл-алкіл" стосується гетероциклічного залишку, пов'язаного з алкільним залишком. Якщо не зазначено інше, термін "гетероциклоалкіл" стосується неароматичного гетероциклу. Якщо не зазначено інше, термін "гетероциклоалкілалкіл" або "гетероциклоалкіл-алкіл" стосується гетероциклоалкільного залишку, зв'язаного з алкільним залишком. Якщо не зазначено інше, термін "відношення головний ізомер:другорядний ізомер", коли стосується суміші двох ізомерів сполуки - головного ізомеру (тобто ізомеру, присутнього в 2 UA 97664 C2 5 10 15 20 25 30 35 40 45 50 55 більше ніж 50% мас.) і відповідного йому другорядного ізомеру (тобто ізомеру, присутнього в менше ніж 50% мас.) - означає відношення цих ізомерів. Такі відношення можуть визначатися за допомогою різних способів, відомих у даній галузі, включаючи хроматографічні (наприклад, ВЕРХ) і спектроскопічні способи (наприклад, ЯМР, Рамановське розсіювання та інфрачервоне поглинання). Коли вони використовуються для згадки сполуки, що містить залишок оксиму, термін "відношення головний ізомер:другорядний ізомер" стосується геометрії оксиму. Таким чином, якщо сполука, що містить залишок оксиму, має додаткові стереоцентри, термін стосується відношення діастереомерів, що містять оксим в одній конфігурації, до діастереомерів, що містять оксим в іншій. Якщо не зазначено інше, термін "стереомерно збагачена композиція" сполуки стосується суміші названої сполуки і його стереоізомера(ів), яка містить більше сполуки, ніж її стереоізомера(ів). Наприклад, стереоізомерно збагачена композиція (S)-бутан-2-олу охоплює суміші (S)-бутан-2-олу і (R)-бутан-2-олу у відношеннях, наприклад, приблизно 60/40, 70/30, 80/20, 90/10, 95/5 і 98/2. Якщо не зазначено інше, термін "стереоізомерна суміш" охоплює рацемічні суміші, а також стереомерно збагачені суміші (наприклад, R/S=30/70, 35/65, 40/60, 45/55, 55/45, 60/40, 65/35 і 70/30). Якщо не зазначено інше, термін "стереомерно чиста" означає композицію, яка містить один стереоізомер сполуки і по суті не містить інших стереоізомерів цієї сполуки. Наприклад, стереомерно чиста композиція сполуки, що має один стереоцентр, по суті не буде містити протилежного стереоізомера сполуки. Стереомерно чиста композиція сполуки, що має два стереоцентри, не буде по суті містити інших діастереомерів сполуки. Стереомерно чиста композиція сполуки, яка має безліч стереоцентрів, але яка зображується або іменується таким чином, що визначена стереохімія не всіх її стереоцентрів, по суті не містить ізомерів сполуки, які мають іншу стереохімію стереоцентрів, для яких визначена стереохімія. Наприклад, "стереомерно чистий ((1R)-1,2-дихлорпропіл)бензол" стосується ((1R)-1,2дихлорпропіл)бензолу, який по суті не містить ((1S)-1,2-дихлорпропіл)бензолу. Типова стереомерно чиста сполука містить більше ніж приблизно 80% мас. однієї стереоізомерної сполуки і менше ніж приблизно 20% мас. іншої стереоізомерної сполуки, більше ніж приблизно 90% мас. однієї стереоізомерної сполуки і менше ніж приблизно 10% мас. іншої стереоізомерної сполуки, більше ніж приблизно 95% мас. однієї стереоізомерної сполуки і менше ніж приблизно 5% мас. іншої стереоізомерної сполуки, більше ніж приблизно 97% мас. однієї стереоізомерної сполуки і менше ніж приблизно 3% мас. іншої стереоізомерної сполуки або більше ніж приблизно 99% мас. однієї стереоізомерної сполуки і менше ніж приблизно 1% мас. іншої стереоізомерної сполуки. Якщо не зазначено інше, термін "заміщений", коли використовується для опису хімічної структури або залишку, стосується похідного цієї структури або залишку, де один або декілька з його атомів водню заміщуються атомом, хімічним залишком або функціональною групою, такою як, але без обмеження, спирт, альдегід, алкокси, алканоїлокси, алкоксикарбоніл, алкеніл, алкіл (наприклад, метил, етил, пропіл, трет-бутил), алкініл, алкілкарбонілокси (-ОС(О)алкіл), амід (С(О)NH-алкіл- або -алкілNНС(О)алкіл), амідиніл (-С(NH)NН-алкіл- або -C(NR)NH2), амін (первинний, повторний і третинний, такий як алкіламіно, ариламіно, арилалкіламіно), ароїл, арил, арилокси, азо, карбамоїл (-NНС(О)О-алкіл- або -ОС(О)NН-алкіл), карбаміл (наприклад, CONH2, а також CONH-алкіл, CONH-арил і CONH-арилалкіл), карбоніл, карбоксил, карбонова кислота, ангідрид карбонової кислоти, хлорангідрид карбонової кислоти, ціано, складний ефір, епоксид, простий ефір (наприклад, метокси, етокси), гуанідино, галоген, галогеналкіл (наприклад, -ССІ3, -CF3, -С(СF3)3), гетероалкіл, хеміацеталь, імін (первинний і повторний), ізоціанат, ізотіоціанат, кетон, нітрил, нітро, кисень (тобто для одержання оксогрупи), складний фосфодіефір, сульфід, сульфонамідо (наприклад, SO2NH2), сульфон, сульфоніл (включаючи алкілсульфоніл, арилсульфоніл і арилалкілсульфоніл), сульфоксид, тіол (наприклад, сульфгідрил, простий тіоефір) і сечовина (-NHCONH-алкіл-). Якщо не зазначено інше, "терапевтично ефективна кількість" сполуки являє собою кількість, достатню для забезпечення терапевтичного виграшу при лікуванні або в тактиці лікування захворювання або стану, або для сповільнення або зведення до мінімуму одного або декількох симптомів, пов'язаних із захворюванням або станом. Терапевтично ефективна кількість сполуки являє собою кількість терапевтичного агента, самого по собі або в поєднанні з іншими терапевтичними агентами, яка забезпечує терапевтичний виграш при лікуванні або в тактиці лікування захворювання або стану. Термін "терапевтично ефективна кількість" може охоплювати кількість, яка поліпшує загальний терапевтичний стан, зменшує або усуває 3 UA 97664 C2 5 10 15 20 25 30 35 40 45 симптоми або причини виникнення захворювання або стану або поліпшує терапевтичну ефективність іншого терапевтичного агента. Якщо не зазначено інше, терміни "лікування", "лікований" і "лікувати" передбачають дію, яка відбувається тоді, коли пацієнт страждає від конкретного захворювання або розладу, і яка знижує тяжкість захворювання або розладу або один або декілька з його симптомів, або затримує або сповільнює розвиток захворювання або розладу. Якщо не зазначено інше, фраза "більше ніж X", де X являє собою число, має таке саме значення, як "X або більше ніж X". Подібно до цього, фраза "більше ніж приблизно X", де X являє собою число, має таке саме значення, як "приблизно X або більше ніж приблизно X". Якщо не зазначено інше, фраза "менше ніж X", де X являє собою число, має таке саме значення, як "X або менше ніж X". Подібно до цього, фраза "менше ніж приблизно X", де X являє собою число, має таке саме значення, як "приблизно X або менше ніж приблизно X". Якщо не зазначено інше, термін "включають" має таке саме значення, як "включає", і термін "включає" має таке саме значення, як "включає, але без обмеження". Подібно до цього, термін "такі як" має таке саме значення, як термін "такі як, але без обмеження". Якщо не зазначено інше, один або декілька прикметників, які безпосередньо передують ряду іменників, повинні розглядатися як такі, що застосовуються до кожного з іменників. Наприклад, фраза "необов'язково заміщений алкіл, арил або гетероарил" має таке саме значення, як "необов'язково заміщений алкіл, необов'язково заміщений арил або необов'язково заміщений гетероарил". Необхідно зазначити, що хімічний залишок, який формує частину більшої сполуки, може бути описаний тут із використанням найменування, що звичайно охоплює його, коли він існує як окрема молекула, або найменування, що звичайно охоплює його радикал. Наприклад, терміни "піридин" і "піридил" відповідають одному і тому самому значенню, коли використовуються для опису залишку, зв'язаного з іншими хімічними залишками. Таким чином, дві фрази "ΧΟΗ, де X являє собою піридил" і "ΧΟΗ, де X являє собою піридин", відповідають одному і тому самому значенню та охоплюють сполуки піридин-2-ол, піридин-3-ол і піридин-4-ол. Необхідно також зазначити, що якщо стереохімія структури або частини структури не зазначається, наприклад, за допомогою товстої або пунктирної лінії, структура або частина структури повинна інтерпретуватися як та, що охоплює всі її стереоізомери. Подібно до цього, найменування сполук, що мають один або декілька хіральних центрів, які не описують стереохімію цих центрів, охоплюють чисті стереоізомери та їхні суміші. Крім того, будь-який атом, показаний на зображенні з ненасиченою валентністю, як передбачається, повинен бути зв'язаний із достатньою кількістю атомів водню, щоб наситити валентності. У доповнення до цього, хімічні зв'язки, зображені однією суцільною лінією, паралельною до однієї пунктирної лінії, охоплюють як одинарні, так і подвійні (наприклад, ароматичні) зв'язки, якщо дозволяє валентність. Способи синтезу Даний винахід охоплює спосіб одержання сполуки формули І: де X являє собою необов'язково заміщений алкіл; R1 являє собою необов'язково заміщений алкіл; R2 являє собою водень, галоген, нітрил або необов'язково заміщений алкіл, арил, алкіларил, арилалкіл, гетероалкіл, гетероцикл, алкілгетероцикл або гетероциклоалкіл і R3 являє собою водень або необов'язково заміщений алкіл, арил, алкіларил, арилалкіл, гетероалкіл, гетероцикл, алкілгетероцикл або гетероциклоалкіл; який включає контактування сполуки формули II: 4 UA 97664 C2 5 10 15 20 25 30 35 зі сполукою формули III: H2N-OR3 III за умов, достатніх для утворення суміші Е- і Z-ізомерів сполуки формули І; і контактування суміші Е- і Z-ізомерів із сильною кислотою. Інший варіант здійснення охоплює спосіб збільшення відношення головний ізомер:другорядний ізомер у суміші сполук формули І: який включає контактування розчину, що містить першу суміш сполук формули І, із сильною кислотою за умов, достатніх для одержання другої суміші сполук формули І, де відношення головний ізомер:другорядний ізомер для першої суміші є меншим, ніж відношення головний ізомер:другорядний ізомер для другої суміші; X являє собою необов'язково заміщений алкіл; R1 являє собою необов'язково заміщений алкіл; R2 являє собою водень, галоген, нітрил, або необов'язково заміщений алкіл, арил, алкіларил, арилалкіл, гетероалкіл, гетероцикл, алкілгетероцикл або гетероциклоалкіл і R3 являє собою водень або необов'язково заміщений алкіл, арил, алкіларил, арилалкіл, гетероалкіл, гетероцикл, алкілгетероцикл або гетероциклоалкіл. У різних способах і варіантах здійснення, описаних тут, сполуки (наприклад, сполуки формули І, II і/або III) можуть існувати або бути одержані як сольвати і/або солі. У конкретному варіанті здійснення розчин містить спирт (наприклад, метанол, етанол, пропанол або ізопропанол). В іншому варіанті здійснення розчин нагрівають до температури більше ніж приблизно 30°С (наприклад, більше ніж приблизно 40, 50 або 60°С). В іншому варіанті здійснення відношення головний ізомер:другорядний ізомер збільшується від менше ніж приблизно 5:1 до більше ніж приблизно 8:1. В іншому варіанті здійснення відношення головний ізомер:другорядний ізомер збільшується від менше ніж приблизно 4:1 до більше ніж приблизно 10:1. В іншому варіанті здійснення відношення головний: другорядний ізомер збільшується від приблизно 3:1 до більше ніж приблизно 13:1. В іншому варіанті здійснення рН розчину, що містить другу суміш, підвищують. У конкретних способах, рН підвищують до більше ніж приблизно 6,0 (наприклад, до більше ніж приблизно 7,0 або 8,0). Із посиланнями на різні способи, описані тут, по можливості, конкретні варіанти здійснення є такими, що X являє собою алкіл, необов'язково заміщений одним або декількома гідроксильними, ацетатними або галогеновими залишками. В інших варіантах здійснення R2 являє собою водень. В інших варіантах здійснення R3 являє собою водень. В інших варіантах здійснення сполука формули І являє собою сполуку формули І(а): 5 UA 97664 C2 5 10 15 20 25 де R4 являє собою OR4A, OC(O)R4A, N(R4B)2, NHC(O)R4B, водень або галоген; R5 являє собою OR5A, OC(O)R5A, N(R5B)2, NHC(O)R5B, водень або галоген; R6 являє собою OR6A, OC(O)R6A, N(R6B)2, NHC(O)R6B, водень або галоген; R7 являє собою алкіл, CH2OR7A, CH2OC(O)R7A, CH2N(R7B)2, CH2NHC(O)R7B, водень або галоген і кожен із R4A, R5A, R6A, R7A, R4B, R5B, R6B, і R7B незалежно являє собою водень або необов'язково заміщений алкіл, арил, алкіларил, арилалкіл, гетероалкіл, гетероцикл, алкілгетероцикл або гетероциклоалкіл. В інших варіантах здійснення сполука формули І(а) являє собою стереомерно чисту сполуку формули І(b): Звертаючись до структур І(а) і (b), тут конкретні варіанти здійснення даного винаходу являють собою такі, в яких один або декілька з R4, R5 і R6 являють собою гідрокси або галоген. В інших, всі R4, R5 і R6 являють собою гідроксил або ацетат. Приклади сильних кислот включають йодистоводневу, бромистоводневу, хлористоводневу, сірчану, азотну, фосфорну, алкансульфонову і аренсульфонову кислоту. Конкретний варіант здійснення даного винаходу представлений нижче, на схемі 1: У цьому способі збільшується відношення ізомерів E:Z у суміші (Е)-1-(4-((1R,2S,3R)-1,2,3,4тетрагідроксибутил)-1Н-імідазол-2-іл)етаноноксиму і (Z)-1 -(4-((1R,2S,3R)-1,2,3,4тeтpaгiдpoкcибyтил)-1H-iмiдaзoл-2-iл)eтaнoнoкcимy. Спосіб включає контактування розчину, що містить першу суміш (Е)-1-(4-((1R,2S,3R)-1,2,3,4тетрагідроксибутил)-1Н-імідазол-2-іл)етаноноксиму і (Z)-1 -(4-((1R,2S,3R)-1,2,3,4тeтpaгiдpoкcибyтил)-lH-iмiдaзoл-2-iл)eтaнoнoкcимy, із сильною кислотою, за умов, достатніх для одержання другої суміші (Е)-1-(4-((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)- 1H-імідазол-2іл)етаноноксиму і (Z)-1 -(4-((1R,2S,3R)-1,2,3,4-тeтpaгiдpoкcибyтил)-1H-iмiдaзoл-2iл)eтaнoнoкcимy; де відношення ізомерів E:Z для першої суміші є меншим, ніж відношення ізомерів E:Z для другої суміші. 6 UA 97664 C2 5 10 15 20 25 30 35 40 45 50 У конкретному варіанті здійснення першу суміш одержують шляхом контактування 1-(4((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1H-імідазол-2-іл)етанону з гідроксиламіном за умов, достатніх для утворення 1-(4-((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1Н-імідазол-2іл)етаноноксиму. 1-(4-((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1Н-імідазол-2-іл)етанон може бути одержаний шляхом контактування 1-аміно-і-дезокси-D-фруктози з 2-етоксіакрилонітрилом за умов, достатніх для утворення 1(4-((1R,2S,3R)-1,2,3,4-тетрагідроксилбутил)-1H-імідазол-2іл)етанону, як показано нижче на схемі 2: Як перевага, даний винахід передбачає нові способи одержання 1-(4-((1R,2S,3R)-1,2,3,4тетрагідроксибутил)-1Н-імідазол-2-іл)етанону. Один із варіантів здійснення охоплює спосіб одержання 1-(4-((1R,2S,3R)-1,2,3,4тетрагідроксибутил)-1Н-імідазол-2-іл)етанону, який включає додавання першої частини метоксиду натрію до розчину, що містить 2-етоксіакрилонітрил, для одержання першої суміші; контактування першої суміші з 1-аміно-1-дезокси-D-фруктозою для одержання другої суміші; додавання другої частини метоксиду натрію до другої суміші для одержання третьої суміші; додавання оцтової кислоти до третьої суміші для одержання четвертої суміші і змішування четвертої суміші протягом часу і при температурі, достатніх для утворення 1-(4-((1R,2S,3R)1,2,3,4-тетрагідроксибутил)-1Н-імідазол-2-іл)етанону. У конкретному способі другу суміш підтримують при температурі більше ніж приблизно 5°С (наприклад, більше ніж приблизно 10, 15 або 20°С). В іншому варіанті здійснення першу суміш підтримують при температурі більше ніж приблизно 5°С (наприклад, більше ніж приблизно 10, 15 або 20°С). В іншому варіанті здійснення першу частину метоксиду натрію додають у вигляді розчину метоксиду натрію в метанолі в кількості більше ніж приблизно 15% мас. (наприклад, більше ніж приблизно 20 або 25% мас). В іншому варіанті здійснення другу частину метоксиду натрію додають у вигляді розчину метоксиду натрію в метанолі в кількості більше ніж приблизно 15% мас. (наприклад, більше ніж приблизно 20 або 25% мас). В іншому варіанті здійснення 1-аміно-1-дезокси-0-фруктозу одержують у суспензії, що додатково містить її сіль з оцтовою кислотою. В іншому варіанті здійснення третю суміш розводять водою перед додаванням до неї оцтової кислоти. В іншому варіанті здійснення четверту суміш нагрівають до температури більше ніж приблизно 30°С (наприклад, більше ніж приблизно 35, 40, 45, 50, 55 або 60°С). В іншому варіанті здійснення четверту суміш нагрівають протягом менше ніж приблизно 5 годин (наприклад, менше ніж приблизно 4, 3 або 2 години). В іншому варіанті здійснення 1-(4-((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1Н-імідазол-2іл)етанон виділяють із виходом більше ніж приблизно 50% (наприклад, більше ніж приблизно 55, 60, 65, 70, 75 або 80%). Приклади Аспекти даного винаходу можуть бути зрозумілими з наведених далі прикладів, які не обмежують його рамок. Приклад 1 Одержання етоксіакрилонітрилу У 250-мл оснащену кожухом 3-горлу круглодонну колбу з бруском магнітної мішалки, каучуковою перегородкою з датчиком температур, пластиковою пробкою та урівноваженою за тиском наповнювальною лійкою з пристроєм для барботування завантажують бромацетальдегід діетилацеталь (35,33 г/179,28 ммоль) і хлорид олова(II) (167,1 мг/0,88 ммоль/0,5% моль). Суспензію охолоджують до 3°С. Потім додають триметилсилілціанід (17,69 г/178,31 ммоль) протягом 11 хвилин при температурі нижче за 15°С. 7 UA 97664 C2 5 10 15 20 25 30 35 40 45 50 55 60 Суміш підтримують приблизно при 10°С протягом 35 хвилин, а потім приблизно при 20°С протягом, принаймні, 1,75 години або доти, поки GC (газохроматографічний) аналіз не покаже витрату бромацетальдегіду діетилацеталю. Зазначений вище ясно-жовтий розчин розводять 85 мл МТВЕ. Діетиламін (19,61 г, 268,11 ммоль/1,50 екв.) додають протягом 6 хвилин при температурі нижче за 35°С. Одержану густу суспензію розводять за допомогою додаткових 25 мл МТВЕ. Реакційну суміш перемішують при приблизно 25°С протягом, принаймні, 1,75 години або доти, поки реакція не завершиться, згідно з GC аналізом. Суміш фільтрують і зібраний твердий продукт промивають МТВЕ (2x30 мл). Об'єднаний фільтрат концентрують у вакуумі (кінцевий вакуум: приблизно 95 Торр). Одержаний сирий етоксіакрилонітрил (17,46 г) піддають тонкому фільтруванню і вакуумній відгонці з одержанням прозорої рідини (11,2 г, 67% вихід). Т.пл.: 46-49°С/31 мм Hg. 1 Н ЯМР (CDCl3) δ 4,85 (д, J=3,54 Гц, 1Н), 4,75 (д, J=3,28 Гц, 1H), 3,73 (кв, J=6,99 Гц, 2H), 1,24 (т, J=6,95 Гц, 3Н). 13 С ЯМР (CDCl3) δ 136,58, 115,23, 101,11,65,54, 14,40. Приклад 2 Одержання 1-(4-((1R,2S,3R))-1,2,3,4-тетрагідроксибутил)-1H-імідазол-2-іл)етанону У 3-горлу 12-л круглодонну колбу, оснащену механічною мішалкою, контролером температури, додають етоксіакрилонітрил (100,0 г, 1,03 моль) і метанол (якість для ВЕРХ, 1,0 л, 10х). До зазначеного вище розчину, що перемішується, протягом 15 хвилин додають метоксид натрію в метанолі (25% мас, 140,6 мл, 0,60 екв.). Суміш перемішують при 20°С протягом, 1 принаймні, 3 годин або доти, поки Н ЯМР не покаже, принаймні, 95% перетворення етоксіакрилонітрилу у відповідний імідат). Зазначений вище розчин переносять протягом 15 хв у суспензію солі фруктозаміну та оцтової кислоти (246,9 г, 1,0 екв., одержують відповідно до Hodge, J.E.; Fisher, B.E., Methods in Carbohydrate Chemistry 11: 99-103 (1963)) у метанолі (1,0 л, 10х), і суміш перемішують при 20°С протягом 6 годин. Іншу частину метоксиду натрію в метанолі (25% мас, 117,3 мл, 0,50 екв.) додають до суміші протягом 10 хвилин і суміш перемішують при 20°С протягом додаткових 16 годин. Потім суміш розводять водою (2,0 л, 20х) та обробляють оцтовою кислотою (118 мл, 2,0 екв.). Після перемішування при 60°С протягом 1 години розчин концентрують (50°С, 200 мбар 70 мбар) до одержання загального об'єму 1,2 л. Суміш у вигляді суспензії охолоджують до 0°С і перемішують протягом 1 години, потім фільтрують і тверді речовини промивають водою (100 мл, х2). Тверді речовини збирають і сушать у вакуумі при 50°С з одержанням 196,8 г сирого продукту у вигляді блідо-жовтої твердої речовини, який потім обробляють водою (980 мл, 5х), та одержану суспензію нагрівають до кипіння протягом 15 хв, потім повторно охолоджують до 0°С і перемішують протягом додаткової 1 години. Суміш знову фільтрують, і тверді речовини промивають водою (100 мл, х2) і сушать до постійної маси у вакуумній печі при 50°С з одержанням 194,8 г (82%) зазначеного в заголовку продукту (ТНІ) у вигляді блідо-жовтої твердої речовини (KF=0,4%). 1 Н ЯМР (вода D2О/крапля DCl у D2O) 7,48 (д, J=2,0 Гц, 0,9Η), 7,19 (д, J=2,0 Гц, 0,1 Η), 5,09 (с, 0,9 Η), 4,98 (с, 0,1 Η), 3,40-3,70 (м, 4Н), 2,53 (д, J=2,4 Гц, 3Н); 13 С ЯМР (вода D2О/крапля DCl у D2O) 185,0, 139,4, 138,0, 119,5, 73,0, 70,9, 65,0, 63,2, 26,7; + МН =231,2. Приклад 3 Одержання дигідрату (Е)-1-(4-((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1Н-імідазол-2іл)етаноноксиму У 3-горлу 3-л круглодонну колбу, оснащену механічною мішалкою, контролером температури і холодильником, завантажують 1-(4-((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1Hімідазол-2-іл)етанон (100,0 г, 434,4 ммоль), сіль гідроксиламіну і хлористоводневої кислоти (45,2 г, 1,5 екв.), ацетат натрію (53,4 г, 1,5 екв.) і метанол (якість для ВЕРХ, 1,0 л, 10х). Зазначений вище розчин нагрівають при 65°С при перемішуванні протягом 2 годин.) Потім до суміші додають протягом 15 хв розчин НСl в ізопропанолі (щойно приготований за допомогою повільного додавання 92,7 мл ацетилхлориду до 200 мл ізопропанолу при 0°С, 3,0 екв.) та одержану суміш перемішують при 65°С протягом 3 годин. Суміш розводять МеОН (1,0 л, 10х) та охолоджують до кімнатної температури, і осаджений хлорид натрію видаляють за допомогою фільтрування. Тверді речовини промивають МеОН (100 мл, 1х) і розчин концентрують при 40°С у вакуумі доти, поки не почнуть утворюватися тверді речовини (приблизно 200 мл). Потім додають воду (1,0 л, 10х), і залишки органічних розчинників видаляють при 40°С у вакуумі. Здійснюють тонке фільтрування з одержанням прозорого жовтого розчину. До цього розчину повільно додають 50% водний розчин NaOH при кімнатній температурі таким чином, щоб температура суміші не перевищувала 40°С, доти, поки не буде 8 UA 97664 C2 5 10 15 20 25 30 досягнутий рН 7,2 (7,0-7,5). Потім одержаний розчин нагрівають до 65°С із утворенням гомогенного розчину і концентрують у вакуумі при 65°С (60-70°С) доти, поки розчин не досягне загального об'єму приблизно 500 мл (5х). Потім суміш повільно охолоджують до кімнатної температури, додатково охолоджують до 0°С і перемішують при 0°С протягом 1 години. Тверді продукти збирають за допомогою фільтрування і промивають водою (0°С, 100 мл, 1х, х2) з одержанням білої кристалічної твердої речовини. До одержаної вище вологої твердої речовини додають воду (400 мл) і одержану суміш нагрівають до 70-80°С до повного розчинення. Розчин охолоджують до кімнатної температури, а потім перемішують при 0°С протягом 1 години. Тверді речовини збирають за допомогою фільтрування і промивають водою (0°С, 100 мл, 1х, х2), а потім сушіння у вакуумі при 30°С протягом ночі з одержанням 99,4 г зазначеної в заголовку сполуки. Аналіз ЯМР показує, що матеріал містить приблизно 3% Z-ізомеру.) Приклад 4 Одержання безводного (Е)-1-(4-((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1Н-імідазол-2іл)етанону оксиму Тверду речовину з прикладу 3 суспендують за допомогою EtOH (800 мл, 8х) і нагрівають при 75°С протягом 1 години. Одержану суміш охолоджують до 0°С і перемішують при 0°С протягом 1 години. Білу тверду речовину збирають за допомогою фільтрування і промивають ЕtOН (0°С, 100 мл, 1х, х2) і сушать при 50°С у вакуумі до постійної маси, з одержанням зазначеної в заголовку сполуки. Аналіз ЯМР показує приблизно 2% Z-ізомеру. 1 Н ЯМР (D2O) 7,05 (с, 1H), 4,83 (д, J=3,6 Гц, 1H), 3,60-3,80 (м, 3Н), 3,50 (дд, J=11,6, 6,8 Гц, 1H), 2,11 (д, J=4,0 Гц, 3Н); 1 Н ЯМР (вода D2О/крапля DCl у D2O) 7,30 (с, 1Н), 5,04 (с, 1H), 3,45-3,75 (м, 4Н),2,13(с, 3Н); 13 С ЯМР (вода D2О/крапля DCl у D2O) 143,8, 140,9, 135,0, 116,9, 72,5, 70,6, 64,4,62,7, + 10,5;МН =246,1. Приклад 5 Визначення відношень ізомерів E:Ζ Відносні кількості ізомерів Ε і Ζ сполук формули І можуть визначатися за допомогою різних методик, відомих у даній галузі. Наприклад, відносні кількості (Е)- 1-(4-((1R,2S,3R)-1,2,3,4тетрагідроксибутил)-1Н-імідазол-2-іл)етаноноксиму і (2)1-(4-((1R,2S,3R)-1,2,3,4тетрагідроксибутил)-1Н-імідазол-2-іл)етаноноксиму в суміші їх обох можуть швидко визначатися за допомогою ЯМР, як показано на фіг. 1. Всі цитовані публікації, патенти і заявки на патенти включені в даний опис за допомогою посилань у всій повноті. 35 ФОРМУЛА ВИНАХОДУ 1. Спосіб одержання сполуки формули І: HO R2 HN R1 X N N OR 40 45 3 , (I) де X являє собою необов’язково заміщений алкіл; R1 являє собою необов’язково заміщений алкіл; R2 являє собою водень, галоген, нітрил або необов’язково заміщений алкіл, арил, алкіларил, арилалкіл, гетероалкіл, гетероцикл, алкілгетероцикл або гетероциклоалкіл, і R3 являє собою водень або необов’язково заміщений алкіл, арил, алкіларил, арилалкіл, гетероалкіл, гетероцикл, алкілгетероцикл або гетероциклоалкіл; в якому здійснюють взаємодію сполуки формули II: 9 UA 97664 C2 HO R2 HN R1 5 10 X N O , (II) зі сполукою формули III: H2N-OR3, (III) за умов, достатніх для утворення суміші Е- і Z-ізомерів сполуки формули І; і взаємодію суміші ізомерів Е і Z із сильною кислотою. 2. Спосіб за п. 1, в якому X являє собою алкіл, необов’язково заміщений одним або декількома гідроксильними, ацетатними або галогеновими залишками. 3. Спосіб за п. 1, в якому R2 являє собою водень. 4. Спосіб за п. 1, в якому R3 являє собою водень. 5. Спосіб за п. 1, в якому сполука формули І являє собою сполуку формули I(a) R5 R6 HO R7 R4 HN R1 N N OR 15 20 3 , (I(a)) де R4 являє собою OR4A, OC(O)R4A, N(R4B)2, NHC(O)R4B, водень або галоген; R5 являє собою OR5A, OC(O)R5A, N(R5B)2, NHC(O)R5B, водень або галоген; R6 являє собою OR6A, OC(O)R6A, N(R6B)2, NHC(O)R6B, водень або галоген; R7 являє собою алкіл, CH2OR7A, CH2OC(O)R7A, CH2N(R7B)2, CH2NHC(O)R7B, водень або галоген, і кожен із R4A, R5A, R6А, R7A, R4B, R5B, R6B і R7B незалежно являє собою водень або необов’язково заміщений алкіл, арил, алкіларил, арилалкіл, гетероалкіл, гетероцикл, алкілгетероцикл або гетероциклоалкіл. 6. Спосіб за п. 5, в якому сполука формули І(а) являє собою стереомерно чисту сполуку формули І(b): R5 R6 HO R4 HN R1 N N OR 25 3 (I(b)). 7. Спосіб за п. 5, в якому один або декілька з R4, R5 і R6 являють собою гідрокси або галоген. 8. Спосіб за п. 5, в якому всі R4, R5 і R6 являють собою гідроксил або ацетат. 9. Спосіб за п. 1, в якому сильна кислота являє собою йодистоводневу, бромистоводневу, хлористоводневу, сірчану, азотну, фосфорну, алкансульфонову або аренсульфонову кислоту. 10. Спосіб збільшення відношення головний ізомер:другорядний ізомер у суміші сполук формули І: 10 UA 97664 C2 HO R2 X HN N R1 N OR 5 10 3 , (I) в якому здійснюють взаємодію розчину, що містить першу суміш сполук формули І, із сильною кислотою за умов, достатніх для одержання другої суміші сполук формули І, де відношення головний ізомер:другорядний ізомер першої суміші є меншим, ніж відношення головний ізомер:другорядний ізомер другої суміші; X являє собою необов’язково заміщений алкіл; R1 являє собою необов’язково заміщений алкіл; R2 являє собою водень, галоген, нітрил або необов’язково заміщений алкіл, арил, алкіларил, арилалкіл, гетероалкіл, гетероцикл, алкілгетероцикл або гетероциклоалкіл, і R3 являє собою водень або необов’язково заміщений алкіл, арил, алкіларил, арилалкіл, гетероалкіл, гетероцикл, алкілгетероцикл або гетероциклоалкіл. 11. Спосіб за п. 10, в якому сполуки формули І одержують шляхом взаємодії сполуки формули II: HO R2 HN 15 20 R1 X N O , (II) зі сполукою формули III: H2N-OR3, III за умов, достатніх для утворення сполуки формули І. 12. Спосіб за п. 10, в якому X являє собою алкіл, необов’язково заміщений одним або декількома гідроксильними, ацетатними або галогеновими залишками. 13. Спосіб за п. 10, в якому R2 являє собою водень. 14. Спосіб за п. 10, в якому R3 являє собою водень. 15. Спосіб за п. 10, в якому сполука формули І являє собою сполуку формули І(а): R5 R6 HO R7 R4 HN R1 N N OR 25 3 , (I(a)) де R4 являє собою OR4A, OC(O)R4A, N(R4B)2, NHC(O)R4B, водень або галоген; R5 являє собою OR5A, OC(O)R5A, N(R5B)2, NHC(O)R5B, водень або галоген; R6 являє собою OR6A, OC(O)R6A, N(R6B)2, NHC(O)R6B, водень або галоген; R7 являє собою алкіл, CH2OR7A, CH2OC(O)R7A, CH2N(R7B)2, CH2NHC(O)R7B, водень або галоген, і 11 UA 97664 C2 5 кожен із R4A, R5A, R6А, R7A, R4B, R5B, R6B і R7B незалежно являє собою водень або необов’язково заміщений алкіл, арил, алкіларил, арилалкіл, гетероалкіл, гетероцикл, алкілгетероцикл або гетероциклоалкіл. 16. Спосіб за п. 15, в якому сполука формули І(а) являє собою стереохімічно чисту сполуку формули І(b): R5 R6 HO R4 HN R1 N N OR 10 15 20 25 30 35 40 45 3 (I(b)). 17. Спосіб за п. 15, в якому один або декілька з R4, R5, R6 являє собою гідрокси або галоген. 18. Спосіб за п. 15, в якому всі R4, R5, R6 являють собою гідроксил або ацетат. 19. Спосіб за п. 10, в якому розчин містить спирт. 20. Спосіб за п. 19, в якому спирт являє собою метанол, етанол, пропанол або ізопропанол. 21. Спосіб за п. 10, в якому сильна кислота являє собою йодистоводневу, бромистоводневу, хлористоводневу, сірчану, азотну, фосфорну, алкансульфонову або аренсульфонову кислоту. 22. Спосіб за п. 10, який додатково включає нагрівання розчину до температури більше ніж приблизно 30 °С (наприклад, більше ніж приблизно 40, 50 або 60 °С). 23. Спосіб за п. 10, в якому відношення головний ізомер:другорядний ізомер збільшується від менше ніж приблизно 5:1 до більше ніж приблизно 8:1. 24. Спосіб за п. 23, в якому відношення головний ізомер:другорядний ізомер збільшується від менше ніж приблизно 4:1 до більше ніж приблизно 10:1. 25. Спосіб за п. 24, в якому відношення головний ізомер:другорядний ізомер збільшується від приблизно 3:1 до більше ніж приблизно 13:1. 26. Спосіб за п. 10, який додатково включає збільшення рН розчину, що містить другу суміш. 27. Спосіб за п. 26, в якому рН збільшують до більше ніж приблизно 6,0 (наприклад, більше ніж приблизно 7,0 або 8,0). 28. Спосіб збільшення відношення E:Z ізомерів у суміші (Е)-1-(4-((1R,2S,3R)-1,2,3,4тетрагідроксибутил)-1Н-імідазол-2-іл)етаноноксиму і (Z)-1-(4-((1R,2S,3R)-1,2,3,4тетрагідроксибутил)-1H-імідазол-2-іл)етаноноксиму, який включає контактування розчину, що містить першу суміш (E)-1-(4-((1R,2S,3R)-1,2,3,4тетрагідроксибутил)-1Н-імідазол-2-іл)етаноноксиму і (Z)-1-(4-((1R,2S,3R)-1,2,3,4тeтpaгiдpoкcибyтил)-1H-iмiдaзoл-2-iл)eтaнoнoкcимy, із сильною кислотою за умов, достатніх для одержання другої суміші (Е)-1-(4-((1R,2S,3R)-1,2,3,4-тeтpaгiдpoкcибyтил)-1H-iмiдaзoл-2iл)eтaнoнoкcимy і (Е)-1-(4-((1R,2S,3R)-1,2,3,4-тeтpaгiдpoкcибyтил)-1H-iмiдaзoл-2iл)eтaнoнoкcимy; де відношення E:Z ізомерів першої суміші є меншим, ніж відношення ізомерів E:Z другої суміші. 29. Спосіб за п. 28, в якому першу суміш одержують шляхом взаємодії 1-(4-((1R,2S,3R)-1,2,3,4тeтpaгiдpoкcибyтил)-1H-iмiдaзoл-2-iл)eтaнoнy з гідроксиламіном за умов, достатніх для утворення 1-(4-((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1Н-імідазол-2-іл)етаноноксиму. 30. Спосіб за п. 29, в якому 1-(4-((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1Н-імідазол-2-іл)етанон одержують шляхом взаємодії 1-аміно-1-дезокси-D-фруктози з 2-етоксіакрилонітрилом за умов, достатніх для утворення 1-(4-((1R,2S,3R)-1,2,3,4-тeтpaгiдpoкcибyтил)-1H-iмiдaзoл-2-iл)eтaнoнy. 31. Спосіб за п. 28, в якому розчин містить спирт. 32. Спосіб за п. 31, в якому спирт являє собою метанол, етанол, пропанол або ізопропанол. 33. Спосіб за п. 28, в якому сильна кислота являє собою йодистоводневу, бромистоводневу, хлористоводневу, сірчану, азотну, фосфорну, алкансульфонову або аренсульфонову кислоту. 34. Спосіб за п. 28, який додатково включає нагрівання розчину при температурі більше ніж приблизно 30 °С (наприклад, більше ніж приблизно 40, 50 або 60 °С). 35. Спосіб за п. 28, в якому відношення E:Z ізомерів збільшують від менше ніж приблизно 5:1 до більше ніж приблизно 8:1. 36. Спосіб за п. 35, в якому відношення E:Z ізомерів збільшують від менше ніж приблизно 4:1 до більше ніж приблизно 10:1. 12 UA 97664 C2 5 10 15 20 25 30 35 37. Спосіб за п. 36, в якому відношення E:Z ізомерів збільшують від приблизно 3:1 до більше ніж приблизно 13:1. 38. Спосіб за п. 28, який додатково включає збільшення рН розчину, що містить другу суміш. 39. Спосіб за п. 38, в якому рН збільшують до більше ніж приблизно 6,0 (наприклад, більше ніж приблизно 7,0 або 8,0). 40. Спосіб одержання 1-(4-((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1Н-імідазол-2-іл)етанону, в якому здійснюють додавання першої частини метоксиду натрію до розчину, що містить 2-етоксіакрилонітрил, з одержанням першої суміші; взаємодію першої суміші з 1-аміно-1-дезокси-D-фруктозою з одержанням другої суміші; додавання другої частини метоксиду натрію до другої суміші з одержанням третьої суміші; додавання оцтової кислоти до третьої суміші з одержанням четвертої суміші, і змішування четвертої суміші протягом часу і при температурі, достатніх для утворення 1-(4((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1Н-імідазол-2-іл)етанону; де другу суміш підтримують при температурі більше ніж приблизно 5 °С (наприклад, більше ніж приблизно 10, 15 або 20 °С). 41. Спосіб за п. 40, в якому першу суміш підтримують при температурі більше ніж приблизно 5 °С (наприклад, більше ніж приблизно 10, 15 або 20 °С). 42. Спосіб за п. 40, в якому першу частину метоксиду натрію додають у вигляді розчину метоксиду натрію в метанолі в кількості більше ніж приблизно 15 % мас. (наприклад, більше ніж приблизно 20 або 25 % мас.). 43. Спосіб за п. 40, в якому другу частину метоксиду натрію додають у вигляді розчину метоксиду натрію в метанолі в кількості більше ніж приблизно 15 % мас. (наприклад, більше ніж приблизно 20 або 25 % мас.). 44. Спосіб за п. 40, в якому 1-аміно-1-дезокси-D-фруктозу одержують у суспензії, що додатково містить її сіль з оцтовою кислотою. 45. Спосіб за п. 40, в якому третю суміш розводять водою перед додаванням до неї оцтової кислоти. 46. Спосіб за п. 40, в якому четверту суміш нагрівають до температури більше ніж приблизно 30 °С (наприклад, більше ніж приблизно 35, 40, 45, 50, 55 або 60 °С). 47. Спосіб за п. 45, в якому четверту суміш нагрівають протягом менше ніж приблизно 5 годин (наприклад, менше ніж приблизно 4, 3 або 2 годин). 48. Спосіб за п. 40, в якому 1-(4-((1R,2S,3R)-1,2,3,4-тетрагідроксибутил)-1H-імідазол-2-іл)етанон виділяють із виходом більше ніж приблизно 50 % (наприклад, більше ніж приблизно 55, 60, 65, 70, 75 або 80 %). Комп’ютерна верстка І. Скворцова Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 13
ДивитисяДодаткова інформація
Назва патенту англійськоюMethods of preparing imidazole-based compounds
Автори англійськоюWu, Wenxue, Yan, Jie, Zhang, Haiming
Назва патенту російськоюСпособ получения соединений на основе имидазола
Автори російськоюУ Веньсюе, Янь Цзе, Чжан Хаймин
МПК / Мітки
МПК: C07D 233/64
Мітки: основі, сполук, одержання, спосіб, імідазолу
Код посилання
<a href="https://ua.patents.su/15-97664-sposib-oderzhannya-spoluk-na-osnovi-imidazolu.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання сполук на основі імідазолу</a>
Попередній патент: Застосування bifidobacterium lactis cncm i-3446 для покращення кишкової мікробіоти у дітей, народжених шляхом кесарева розтину
Наступний патент: Розширений мікропотужний режим енергозбереження для зв’язку
Випадковий патент: Дротоцвяховий автомат












