Гідроізоіндолінові антагоністи рецептора тахікініну
Номер патенту: 84192
Опубліковано: 25.09.2008
Автори: Девіта Роберт Дж., Міллз Сандер Г., Цзян Цзіньлун, Бунда Джайме Лінн
Формула / Реферат
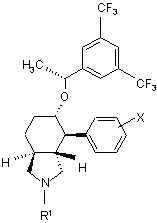
1. Сполука формули І:
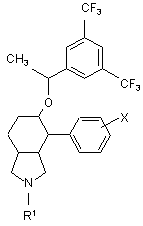 , І
, І
де:
R1 вибраний з групи, яка складається з:
(1) водню,
(2) С1-6алкілу, який не заміщений або заміщений галогеном, гідроксилом або фенілом,
(3) циклопентенону, який не заміщений або заміщений гідроксилом або метилом,
(4) -(СО)-С1-6алкілу,
(5) -(CO)-NH2,
(6) -(СО)-NHC1-6алкілу, і
(7) -(СО)-N(С1-6алкіл)(С1-6алкілу);
X незалежно вибраний з групи, яка складається з:
(1) водню,
(2) фтору і
(3) метилу;
і її фармацевтично прийнятні солі і індивідуальні енантіомери і діастереоізомери.
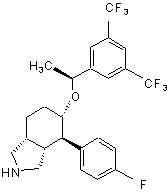
2. Сполука за п. 1 формули Іа:
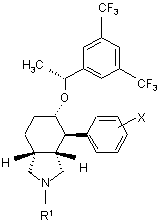 Ia
Ia
і її фармацевтично прийнятні солі, індивідуальні енантіомери і діастереоізомери.
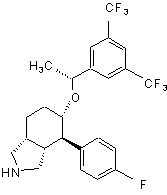
3. Сполука за п. 1 формули Іb:
 Іb
Іb
і її фармацевтично прийнятні солі, індивідуальні енантіомери і діастереоізомери.
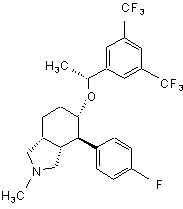
4. Сполука за п. 1, в якій R1 вибраний з групи, яка складається з:
(1) водню,
(2) метилу,
(3) 2-фенілетилу,
(4) 2-гідроксіетилу,
(5) циклопент-2-ен-1-ону,
(6) 5-гідроксициклопент-2-ен-1-ону,
(7) 4-гідроксициклопент-2-ен-1-ону,
(8) 2-метилциклопент-2-ен-1-ону,
(9) ацетилу,
(10) -(CO)-NH2,
(11) CH3NH-(CO)- і
(12) (CH3)2N-(CO)- .
5. Сполука за п. 1, де X являє собою водень.
6. Сполука за п. 1, де X являє собою фтор.
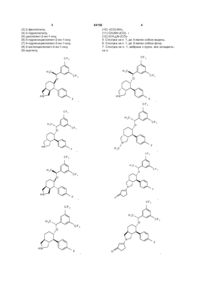
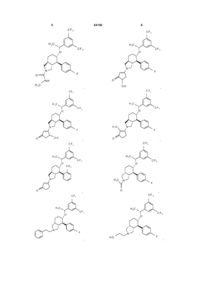
7. Сполука за п. 1, вибрана з групи, яка складається з:
 ,
,  ,
,
 ,
,  ,
,
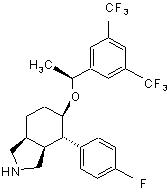 ,
, 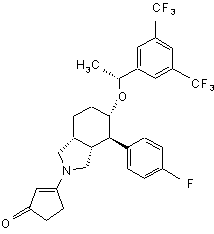 ,
,
 ,
,
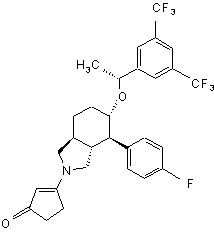 ,
,
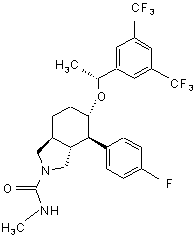 ,
, 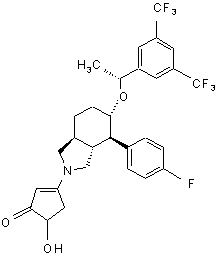 ,
,
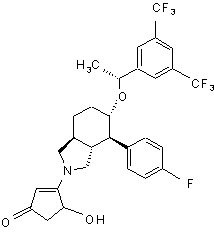 ,
, 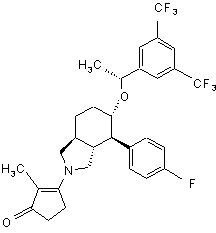 ,
,
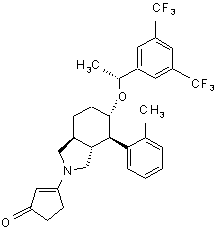 ,
, 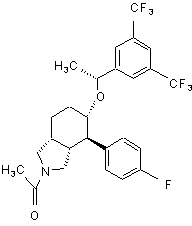 ,
,
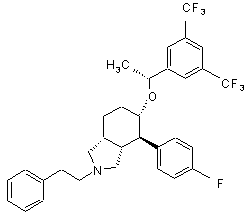 ,
, 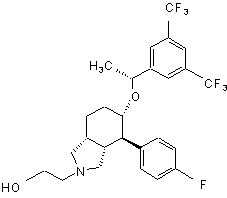 ,
,
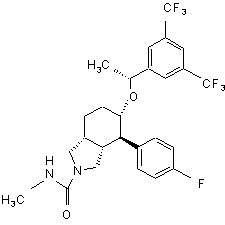 ,
, 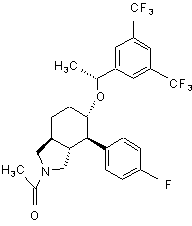 ,
,
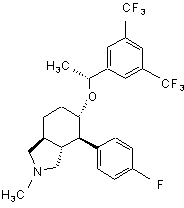 ,
,  ,
,
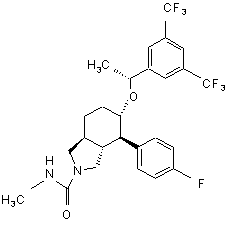 ,
, 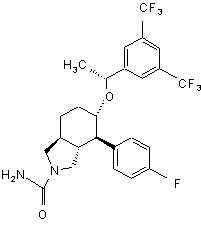
і її фармацевтично прийнятні солі.
8. Фармацевтична композиція, яка містить інертний носій і сполуку за п. 1 або її фармацевтично прийнятну сіль.
9. Спосіб отримання лікарського засобу для протидії впливу речовини Ρ на її клітинний рецептор або для блокади рецепторів нейрокініну-1 у ссавця, що передбачає об'єднання сполуки відповідно до п. 1 даного винаходу або її фармацевтично прийнятної солі з фармацевтичним носієм або розріджувачем.
10. Спосіб за п. 9, де лікарський засіб призначений для лікування фізіологічного порушення, пов'язаного з надлишком тахікінінів у ссавця.
Текст
1. Сполука формули І: 3 (3) 2-фенілетилу, (4) 2-гідроксіетилу, (5) циклопент-2-ен-1-ону, (6) 5-гідроксициклопент-2-ен-1-ону, (7) 4-гідроксициклопент-2-ен-1-ону, (8) 2-метилциклопент-2-ен-1-ону, (9) ацетилу, 84192 4 (10) -(CO)-NH 2, (11) CH 3NH-(CO)- і (12) (CH 3)2N-(CO)- . 5. Сполука за п. 1, де X являє собою водень. 6. Сполука за п. 1, де X являє собою фтор. 7. Сполука за п. 1, вибрана з групи, яка складається з: CF 3 C F3 H 3C H 3C CF 3 O HN C F3 O HN F F , , C F3 C F3 H 3C H 3C CF 3 O CF 3 O N HN F F H 3C , , CF3 CF3 H 3C H3C CF3 O C F3 O N HN F F O , , CF 3 CF3 H 3C H 3C O O CF3 N HN CF 3 F , O F , 5 84192 6 CF3 CF3 H 3C H 3C CF3 O CF3 O N N F F O O NH H 3C OH , , C F3 CF 3 H 3C H 3C C F3 O H 3C N N F F OH O C F3 O O , , C F3 C F3 H 3C H 3C O CF3 CH3 N H 3C O C F3 O N F O , , CF 3 CF 3 H 3C O N H 3C CF 3 O F N , HO C F3 F , 7 84192 8 C F3 C F3 H 3C O H N H 3C H 3C CF3 CF 3 O N H 3C F O N F O , , CF 3 C F3 H 3C CF 3 O H 3C CF3 O N N F H 3C O , , CF3 CF3 H 3C O H N H 3C H 3C C F3 O N O N H 2N F , CF3 F O і її фармацевтично прийнятні солі. 8. Фармацевтична композиція, яка містить інертний носій і сполуку за п. 1 або її фармацевтично прийнятну сіль. 9. Спосіб отримання лікарського засобу для протидії впливу речовини Ρ на її клітинний рецептор або для блокади рецепторів нейрокініну-1 у ссав ця, що передбачає об'єднання сполуки відповідно до п. 1 даного винаходу або її фармацевтично прийнятної солі з фармацевтичним носієм або розріджувачем. 10. Спосіб за п. 9, де лікарський засіб призначений для лікування фізіологічного порушення, пов'язаного з надлишком тахікінінів у ссавця. Речовина P являє собою ундекапептид, який зустрічається в природі, що належить до сімейства пептидів тахікінінів, останні називаються так в результаті швидкої скорочувальної дії на екстраваскулярні гладком'язові тканини. Тахікініни відрізняються консервативною карбокси-кінцевою послідовністю. У доповнення до речовини P відомі тахікініни ссавців включають нейрокінін А і нейрокінін В. Дана номенклатура означає рецептори до речовини P, нейрокініну А і нейрокініну В як нейро кінін-1 (NK-1), нейрокінін-2 (NK-2) і нейрокінін-3 (NK-3), відповідно. Антагоністи тахікініну і, зокрема, речовини P корисні в лікуванні клінічних станів, які характеризуються наявністю надлишку активності тахікініну, зокрема, речовини P, включаючи розлади центральної нервової системи, ноцицепцію і біль, шлунково-кишкові розлади, порушення функції сечового міхура і респіраторні захворювання. 9 84192 Даний винахід направлений на певні гідроізоіндолінові сполуки, які є корисними як антагоністи рецептора нейрокініну-1 (NK-1) і на інгібітори тахікініну і, зокрема, речовину P. Винахід також відноситься до фармацевтичних препаратів, що містять дані сполуки як активні інгредієнти і до застосування сполук і їх препаратів для лікування певних порушень, включаючи блювання, нетримання сечі, депресію і тривогу. Даний винахід відноситься до сполук формули І: де: R1 вибраний з групи, яка складається з: (1) водню, (2) С1-6алкілу, який не заміщений або заміщений галогеном, гідроксилом або фенілом, (3) циклопентенону, який не заміщений або заміщений гідроксилом або метилом, (4) -(СО)-С1-6алкілу, (5) -(CO)-NH 2, (6) -(CO)-NHC 1-6алкілу, і (7) -(СО)-N(С1-6алкіл)(С1-6алкілу); X незалежно вибраний з групи, яка складається з: (1) водню, (2) фтор у і (3) метилу; їх фармацевтично прийнятних солей і індивідуальних енантіомерів і діастереоізомерів. Один з варіантів здійснення даного винаходу включає сполуки формули Ia: де R1 і X визначені в даній заявці; і їх фармацевтично прийнятні солі і їх індивідуальні енантіомери і діастереоізомери. Ще один варіант здійснення даного винаходу включає сполуки формули Ib: 10 де R1 і X визначені в даній заявці; і їх фармацевтично прийнятні солі і їх індивідуальні енантіомери і діастереоізомери. Інший варіант здійснення даного винаходу включає сполуки, в яких R1 вибраний з групи, яка складається з: (1) водню, (2) С1-3алкілу, який не заміщений або заміщений гідроксилом або фенілом, (3) циклопент-2-ен-1-ону, який не заміщений або заміщений гідроксилом або метилом, (4) -(CO)-С1-3алкілу, (5) -(CO)-NH 2, (6) -(СО)-NНС1-3алкілу і (7) -(СО)-N(С1-3алкіл)(С1-3алкілу). Згідно з даним варіантом здійснення даного винаходу запропоновані сполуки, в яких R1 вибраний з групи, яка складається з: (1) водню, (2) метилу, (3) 2-фенілетилу, (4) 2-гідроксіетилу, (5) циклопент-2-ен-1-ону, (6) 5-гідроксициклопент-2-ен-1-ону, (7) 4-гідроксициклопент-2-ен-1-ону, (8) 2-метилциклопент-2-ен-1-ону, (9) ацетилу, (10) ацетамідо, (11) метилацетамідо і (12) диметилацетамідо. Додатково в даному варіанті здійснення даний винахід відноситься до сполук, в яких R1 являє собою водень. Також додатково в даному варіанті здійснення даний винахід відноситься до сполук, в яких R1 являє собою метил, 2-фенілетил або 2гідроксіетил. Також додатково в даному варіанті здійснення даного винаходу запропоновані сполуки, в яких R1 являє собою: який не заміщений або заміщений гідроксилом або метилом. Крім того, додатково в даному варіанті здійснення, даний винахід направлений на сполуки, в яких R1 являє собою ацетил, ацетамідо, метилацетамідо або диметилацетамідо. 11 84192 12 Ще один варіант здійснення даного винаходу включає сполуки, в яких X являє собою водень. Інший варіант здійснення даного винаходу включає сполуки, в яких X являє собою фтор. Ще один варіант здійснення даного винаходу включає сполуки, в яких X являє собою метил. Конкретні варіанти здійснення даного винаходу включають сполуку, яка вибрана з групи, яка складається із сполук, що є предметом прикладів Наприклад, наведену вище сполуку можна нав даній заявці і їх фармацевтично прийнятних созивати "(3aR,4R,5S,7aR)трет-бутил-5-гідрокси-4лей і їх індивідуальних енантіомерів і діастереоіфенілоктагідро-2Н-ізоіндол-2-сарбоксилат" або зомерів. "трет-бутил-(3аR,4R,5S,7аR)-5-гідрокси-4Сполуки згідно з даним винаходом можуть місфенілоктагідро-2Н-ізоіндол-2-карбоксилат". Загатити один або більше центрів асиметрії і можуть, лом, центральна структура може називатися як таким чином, виникати у вигляді рацематів і рацеоктагідроізоіндольні, гексагідроізоіндолінові, пергімічних сумішей, окремих енантіомерів, діастереоідроізоіндолінові, гідроізоіндолінові, або гідроізоінзомерних сумішей і індивідуальних діастереоізодольні сполуки. мерів. Можуть бути присутніми додаткові центри Як відомо фахівцям в даній галузі, передбачаасиметрії в залежності від природи різних замісниється, що галоген в контексті даної заявки включає ків в молекулі. Кожний такий центр асиметрії незафтор, хлор, бром і йод. Аналогічно С1-6, як в С1лежно виробляє два оптичних ізомери, і мається 6алкілі, за визначенням ідентифікує гр упу, яка місна увазі, що всі можливі оптичні ізомери і діастетить 1, 2, 3, 4, 5 або 6 вуглеців в лінійній або розреоізомери в сумішах і у вигляді чистих або частгалуженій структурі таким чином, що С1-8алкіл, ково очищених сполук включені в межі даного визокрема, включає метил, етил, н-пропіл, ізо-пропіл, находу. Мається на увазі, що даний винахід н-бутил, ізо-бутил, трет-бутил, пентил і гексил. охоплює всі такі ізомерні форми цих сполук. На Група, визначена як незалежно заміщена замісниформулі І показана структура класу сполук без ками, може бути незалежно заміщена безліччю переважної стереохімії. Незалежні способи синтетаких замісників. зу цих діастереоізомерів або їх хроматографічного Термін "фармацевтично прийнятні солі" ознарозділення, як відомо з рівня техніки, можуть бути чає солі, приготовані з фармацевтично прийнятних досягнуті шля хом відповідної зміни методології, нетоксичних основ або кислот, включаючи неоргарозкритої в даній заявці. Їх абсолютна стереохімія нічні або органічні основи і неорганічні або органіможе бути визначена шляхом рентгенокристалогчні кислоти. Солі, отримані з неорганічних основ рафії кристалічних продуктів або кристалічних інвключають солі алюмінію, амонію, кальцію, міді, термедіатів, отриманих у разі необхідності шляхом тривалентного заліза, двовалентного заліза, літію, обробки реактивом, що містить центр асиметрії з магнію, марганцовисті солі, марганцоватисті, кавідомою абсолютною конфігурацією. Якщо потріблію, натрію, цинку і т. п. Особливо переважними є но, рацемовані суміші сполук можуть бути роздісолі амонію, кальцію, магнію, калію і натрію. Солі в лені таким чином, щоб були виділені індивідуальні твердій формі можуть існувати в більш ніж одній енантіомери. Розділення може бути виконане спокристалічній структурі, і можуть також бути в формі собами, відомими в рівні техніки такими, як зв'язугідратів. Солі, отримані з фармацевтично прийнятвання рацемічної суміші сполук з енантіомерно них органічних нетоксичних основ включають солі чистою сполукою для утворення діастереоізомерпервинних, вторинних і третинних амінів, заміщеної суміші з подальшим розділенням індивідуальних амінів, включаючи циклічні аміни, заміщені них діастереоізомерів стандартними методами аміни, що зустрічаються в природі, і основні іонотакими, як дробова кристалізація або хроматограобмінні смоли такі, як аргінін, бетаїн, кофеїн, холін, фія. Реакція зв'язування часто являє собою форN,N'-дибензилетилендіамін, діетиламін, 2мування солей із застосуванням енантіомерно діетиламіноетанол, 2-диметиламіноетанол, етаночистої кислоти або основи. Потім діастереоізомерламін, етилендіамін, N-етилморфолін, Nні похідні можуть бути перетворені в чисті енантіетилпіперидин, глюкамін, глюкозамін, гістидин, омери шляхом відщеплення доданого хірального гідрабамін, ізопропіламін, лізин, метилглюкамін, залишку. Рацемічна суміш сполук може також бути морфолін, піперазин, піперидин, поліамінні смоли, розділена безпосередньо за допомогою хроматогпрокаїн, пурини, теобромін, триетиламін, триметирафічних способів, що використовують хіральні ламін, трипропіламін, трометамін, і т. п. Коли спостаціонарні фази, такі способи відомі з рівня технілука відповідно до даного винаходу є основною, ки. Альтернативно, будь-який енантіомер сполуки солі можуть бути приготовані з фармацевтично може бути отриманий за допомогою стереоселекприйнятних нетоксичних кислот, включаючи неортивного синтезу із застосуванням оптично чистих ганічні і органічні кислоти. Такі кислоти включають вихідних матеріалів або реагентів відомої конфігуоцтову, бензолсульфонову, бензойну, камфорсурації способами, відомими з рівня техніки. льфонову, лимонну, етансульфонову, фумарову, Існує декілька прийнятних способів присвоєнглюконову, глутамінову, бромистоводневу, хлориня назв сполукам, що обговорюються в даній застоводневу, ізетіонову, молочну, малеїнову, яблуявці. чну, мигдалеву, метансульфонову, муцинову, азотну, памову, пантотенову, фосфорну, янтарну, сірчану, винну, п-толуолсульфонову кислоту і т. п. Особливо переважними є лимонна, бромистовод 13 84192 14 нева, хлористоводнева, малеїнова, фосфорна, зуючі захворювання такі, як MS і ALS і інші нейросірчана, фумарова і винна кислоти. Потрібно ропатологічні розлади такі, як периферична неврозуміти, що, як передбачається, в значенні, яке випатія, наприклад діабетична і індукована користовується в даній заявці, звернення до спохіміотерапією невропатія, і постгерпетична невралук відповідно до даного винаходу також лгія, невралгія трійчастого нерва, сегментальна включають фармацевтично прийнятні солі. або міжреберна невралгія і інші невралгії; і розлаЗастосування сполук, розкрите в прикладах і в ди судин головного мозку внаслідок гострого або даному розділі, пояснює винахід. Конкретні сполухронічного цереброваскулярного пошкодження ки в даному винаході включають сполуку, вибрану такого, як інфаркт головного мозку, субарахноїдаз групи, яка складається із сполук, розкритих в льна кровотеча або набряк головного мозку. наступних прикладах і їх фармацевтично прийнятАктивність тахікініну і, зокрема, речовини P, них солей і їх індивідуальних діастереоізомерів. також бере участь в ноцицепції і болю. У зв'язку Сполуки згідно з даним винаходом корисні в цим, сполуки згідно з даним винаходом корисні в профілактиці і лікуванні широкої різноманітності профілактиці або лікуванні захворювань і станів, в клінічних станів, що характеризується наявністю яких переважає біль, включаючи пошкодження надлишку активності тахікініну, зокрема, речовини м'якої тканини і периферичне пошкодження таке, P. Таким чином, наприклад, надлишок активності як гостра травма, остеоартрит, ревматоїдний арттахікініну, зокрема, речовини P, спричиняє різнорит, скелетно-м'язовий біль, зокрема, після травманітні розлади центральної нервової системи. ми, спинальний біль, синдроми міофасціального Такі розлади включають порушення настрою такі, болю, головний біль, біль внаслідок епізіотомії і як депресія або, зокрема, депресивні, наприклад, опіки; глибокий і вісцеральний біль такий, як серодиничні епізодичні або рекурентні глибокі депрецевий біль, м'язовий біль, очний біль, ротолицевий сивні розлади і дистимічні розладу, або біполярні біль, наприклад, одонталгія, біль в животі, гінекорозлади, наприклад, біполярний розлад І, біполялогічний біль, наприклад, дисменорея і родові перний розлад II і циклотимічний розлад; тривожні рейми; біль, пов'язаний з пошкодженням нерва і розлади такі, як панічний розлад з агорафобією корінця такий, як біль, пов'язаний з порушеннями або без неї, агорафобія без історії панічного розпериферичного нерва, наприклад, затиснення неладу, специфічні фобії, наприклад, специфічні рва і розриви плечового сплетення, ампутація, фобії до тварин, соціальні фобії, обсесивнопериферичні невропатії, тригемінальна невралгія, компульсивний розлад, стресові розлади, включаатиповий лицьовий біль, пошкодження нервового ючи посттравматичний стресовий розлад і гострий корінця і арахноїдит; біль пов'язаний з раком, часстресовий розлад і генералізовані тривожні розлато званий раковим болем; біль, що виникає в ди; шизофренія і інші психотичні розлади, наприцентральній нервовій системі, такий, як болі внаклад, шизофреніформні розлади, шизоафективні слідок пошкодження спинного мозку або стовбура розлади, маревні розлади, короткі психотичні розголовного мозку; біль в області попереку; ішіалгія; лади, індуковані психотичні розлади і психотичні анкілозуючий спондиліт, подагра і біль шрамів. розлади з маренням або галюцинаціями; делірій, Антагоністи тахікініну і, зокрема, речовини P, деменція і амнестичний і інші когнітивні або нейможуть також бути корисні в лікуванні респіраторродегенеративні розлади такі, як хвороба Альцних захворювань, зокрема, пов'язаних з надмірною геймера, сенільна деменція, деменція типу Альцсекрецією слизу таких, як хронічна непрохідність геймера, судинна деменція і інші деменції, дихальних шляхів, бронхопневмонія, хронічний наприклад, внаслідок ВІЛ захворювання, травми бронхіт, муковісцидоз і астма, респіраторний дисголови, хвороби Паркінсона, хвороби Хантінгтона, трес-синдром дорослих, і бронхоспазм; запальні хвороби Піка, хвороби Крейтцфельдта-Якоба, або захворювання, такі, як запальне захворювання внаслідок множинної етіології; хвороба Паркінсона кишок, псоріаз, фіброзит, остеоартрит, ревматоїді інші екстра-пірамідальні розлади руху такі, як ний артрит, свербіж і сонячний опік; алергії такі, як індуковані лікарським препаратом розлади руху, екзема і риніт; розлади, пов'язані з гіперчутливіснаприклад, індукований нейролептичним засобом тю, такі, як від сумаху отр утоносного; очні захвопаркінсонізм, злоякісний нейролептичний синдром, рювання такі, як кон'юнктивіт, весняний кон'юнктиіндукована нейролептичним засобом гостра дисвіт і т. п.; очні стани, пов'язані з проліферацією тонія, індукована нейролептичним засобом гостра клітин, такі, як проліферативна вітреоретинопатія; акатизія, індукована нейролептичним засобом пізшкірні захворювання, такі, як контактний дерматит, ня дискінезія і індукований лікарським препаратом алергічний дерматит, кропивниця і інший екземапостуральний тремор; пов'язані з речовиною розтоїдний дерматит. Антагоністи та хікініну і, зокрема, лади, що є результатом вживання алкоголю, амречовини P, можуть також бути корисні в лікуванні фетамінів (або подібних до амфетаміну речовин), пухлин, включаючи пухлини молочної залози, нейкофеїну, конопель, кокаїну, галюциногенів, летюрогангліобластому і дрібноклітинні карциноми такі, чих препаратів і аерозольних стислих газів, нікотияк дрібноклітинний рак легень. ну, опіоїдів, похідних фенілгліцидину, седативних Антагоністи тахікініну і, зокрема, речовини P, засобів, снотворних засобів і анксіолітиків, де зв'яможуть також бути корисні в лікуванні шлунковозані з речовиною розлади включають залежність і кишкових (ШК) порушень, включаючи запальні зловживання, інтоксикацію, абстиненцію, марення порушення і захворювання ШК тракту такі, як гастпри інтоксикації, марення при абстиненції, персисрит, гастродуоденальні виразки, шлункові карцитуючу деменцію, психотичні розлади, розлади наноми, шлункові лімфоми, порушення, пов'язані з строю, розлади неспокою, статеву дисфункцію і нейронним контролем внутрішніх органів, несперозлади сну; епілепсію; синдром Дауна; демієлініцифічний виразковий коліт, хвороба Крона, синд 15 84192 16 ром подразненої кишки і блювота, включаючи госпохідні подофілотоксину; і ци тотоксичні антибіотитру, відстрочену або передчасну блювання таку, ки. Конкретні приклади хіміотерапевтичних агентів як блювота, індукована хіміотерапією, радіацією, описані, наприклад, у [д. J. Stewart в Nausea and токсинами, вірусними або бактерійними інфекціяVomiting: Recent Research and Clinical Advances, ми, вагітністю, вестибулярні розлади, наприклад, Eds. J. Kucharczyk et al, CRC Press Inc., Boca морська хвороба, вертиго, запаморочення і хвороRaton, Florida, USA (1991) стор.177-203, особливо, ба Меньєра, хірургія, мігрень, зміни внутрішньочестор.188]. Хіміотерапевтичні агенти, що звичайно репного тиску, гастроезофагеальна рефлюксна використовуються, включають цисплатин, дакархвороба, порушення травлення з підвищеною кисбазин (DTIC), дактиноміцин, мехлоретамін, стреплотністю, надмірне вживання їжі або рідин, підвитозоцин, циклофосфамід, кармустин (BCNU), лощена кислотність шлунка, кисла відрижка або ремустин (CCNU), доксорубіцин (адріаміцин), гургі тація, печія, наприклад, епізодична, нічна або даунорубіцин, прокарбазин, мітоміцин, цитарабін, індукована їжею печія, і диспепсія. етопозид, метотрексат, 5-фторурацил, вінбластин, Антагоністи тахікініну і, зокрема, речовини P, вінкристин, блеоміцин і хлорамбуцил [R. J. Gralla і можуть також бути корисні в лікуванні інших різних інш. в Cancer Treatment Reports (1984) 68(1), 163умов, включаючи пов'язані зі стресом соматичні 172]. Додатковий аспект даного винаходу містить порушення; симпатичну рефлекторну дистрофію застосування сполуки згідно з даним винаходом таку, як синдром плече-рука; несприятливі імунодля досягнення хронобіологічного (зміщення фази логічні реакції такі, як відторгнення трансплантоциркадного ритму) ефекту і полегшення порушень ваних тканин і розлади, пов'язані з імунною актициркадного ритму у ссавців. Даний винахід додатвацією або супресією такі, як системний червоний ково направлений на застосування сполуки згідно вовчак; виливання плазми, внаслідок цитокінової з даним винаходом для блокування ефектів зміхіміотерапії, розлади функції сечового міхура такі, щення фази світла у ссавця. як цистит, гіперрефлексія детрузора сечового міДаний винахід додатково направлений на захура, часте сечовипускання і нетримання сечі, стосування сполуки згідно з даним винаходом або включаючи профілактику або лікування надактивїї фармацевтично прийнятної солі для посилення ного сечового міхура з симптомами невідкладного або поліпшення якості сну, а також запобігання і нетримання сечі, невідкладності і частот позиву; лікування розладів сну і порушень сну у ссавців. фіброзні і колагенові захворювання такі, як склеЗокрема, даний винахід забезпечує спосіб посиродермія і еозинофільний фасціольоз; розлади лення або поліпшення якості сну шляхом збількровотоку, викликані захворюваннями з розширеншення ефективності сну і посилення збереження ням і звуженням судин такі, як стенокардія, судинсну. Крім того, даний винахід забезпечує спосіб ний головний біль, мігрень і хвороба Рейнода і запобігання і лікування розладів сну і порушень біль або ноцицепцію, що відноситься до або пов'ясну у ссавця, який містить введення сполуки згідно зану з будь-яким з попередніх станів, особливо з даним винаходом або її фармацевтично прийняпередачу болю при мігрені. Сполуки згідно з даним тної солі. Даний винахід корисний для лікування винаходом мають також значення в лікуванні порозладів сну, включаючи розлади ініціювання і єднання наведених вище умов, особливо в лікузбереження сну (безсоння) ("DIMS"), які можуть ванні поєднання післяопераційного болю і післявиникнути за психофізіологічними причинами, як операційної нудоти і блювоти. наслідок психіатричних порушень (зокрема пов'яСполуки згідно з даним винаходом, зокрема, заних з тривогою), внаслідок вживання і зловжикорисні при профілактиці або лікуванні блювоти, вання наркотичними засобами і алкоголем (зокревключаючи гостру, відстрочену або передчасну ма в ході стадій абстиненції), дитячі розвинені блювання таку, як блювота, індукована хіміотераDIMS, нічний міоклонус, фіброміалгія, м'язовий пією, радіацією, токсинами, вагітністю, вестибулябіль, апное у сні і стомлені ноги і неспецифічні рними порушеннями, рухом, хірургією, мігренню і порушення швидкого сну, що відмічаються при змінами внутрішньочерепного тиску. Наприклад, старінні. сполуки згідно з даним винаходом можуть бути Особливо переважними варіантами здійсненкорисні необов'язково в поєднанні з іншими протиня даного винаходу є лікування блювоти, нетриблювотними агентами для профілактики гострої і мання сечі, депресії або тривог шляхом введення відстроченої нудоти і блювоти, пов'язаної з початсполук відповідно до даного винаходу індивідууму ковими і повторними курсами помірної або сильної (людині або тварині), якому потрібне таке лікуваннудотної хіміотерапії раку, включаючи високу дозу ня. цисплатину. Особливо сполуки згідно з даним виВідповідно до даного винаходу запропонованаходом корисні в лікуванні блювоти, індукованої ний спосіб отримання лікарського засобу для пропротипухлинними (цитотоксичними) агентами, тидії ефекту речовини P на клітинний рецептор включаючи звичайно ті, що використовуються в або для блокади рецепторів нейрокініну-1 у ссавхіміотерапії раку, і блювоти, індукованої іншими ця, що містить поєднання сполуки згідно з даним фармакологічними агентами, наприклад, роліправинаходом з фармацевтичним носієм або розрімом. Приклади таких хіміотерапевтичних агентів джувачем. Крім того, даний винахід відноситься до включають алкілуючі агенти, наприклад, етиленіспособу отримання лікарського засобу для лікумінові сполуки, алкілсульфонати і інші сполуки з вання фізіологічного порушення, пов'язаного з алкілуючою дією такі, як нітрозосеовини, циспланадлишком тахікінінів у ссавця, що містить поєдтин і дакарбазин; антиметаболіти, наприклад, аннання сполуки згідно з даним винаходом з фарматагоністи фолієвої кислоти, пурину або піримідину; цевтичним носієм або розріджувачем. інгібітори мітозу, наприклад, алкалоїди барвінку і 17 84192 18 Даний винахід також відноситься до способу сованого в клітинах COS або CHO, заснований на лікування або профілактики фізіологічних порувикористанні як радіоактивно міченого ліганду І25Ішень, пов'язаних з надлишком тахікінінів, особлиречовини P (125I-SP від DU PONT, Boston, MA), яка во речовини P, даний спосіб передбачає введення конкурує з неміченою речовиною P або будь-яким пацієнту, якому це потрібно, сполуки згідно з даіншим лігандом за зв'язування з NK1R людини. ним винаходом, що зменшує кількість тахікініну, Одношарові клітинні культури COS або CHO були або композиції, що містить сполуку згідно з даним дисоційовані неферментативним розчином винаходом. У значенні, що використовується в (SPECIALTY MEDIA, Lavallette, NJ) і ресуспендоданій заявці, термін "лікування" або "лікувати" вані у відповідному об'ємі зв'язувального буфера означає введення сполук згідно з даним винахо(50мМ Tris рН 7,5, 5мМ MnCl2, 150мМ NaCl, дом, для зменшення, поліпшення, або усунення 0,04мг/мл бацитрацину, 0,004мг/мл лейпептину, симптомів або основної причини відмічених хво0,2мг/мл BSA, 0,01мМ фосфорамідону) так, що робливих станів у індивідуума (людини або твари200мкл суспензії клітини дало б початок приблизни), який страждає на цей стан або має його клініно 10000імп./хв. специфічного зв'язування 125I-SP чні ознаки. Термін "профілактика" або "запобігати" (приблизно 50000-200000 клітин). В аналізі на зв'яозначає введення сполук даного винаходу для зування, 200мкл клітин було додано в пробірку, що зменшення, поліпшення, або усунення ризику або містить 20мкл 1,5-2,5нМ 125I-SP і 20мкл неміченої імовірності виникнення відмічених хворобливих речовини P або будь-якої іншої сполуки, що тестустанів у індивідуума (людини або тварини) сприйється. Пробірки були інкубовані при 4°С або при нятливого або схильного до даного стану. кімнатній температурі протягом 1 години зі слабСполуки згідно з даним винаходом корисні для ким струшуванням. Зв'язана радіоактивна речовипротидії тахікінінам, зокрема речовині P, при лікуна була відділена від незв'язаної радіоактивної ванні шлунково-кишкових розладів, розладів речовини за допомогою фільтра GF/C (BRANDEL, центральної нервової системи, запальних захвоGaithersburg, MD), який був заздалегідь змочений рювань, болю або мігрені і астми у ссавця, якому 0,1% поліетиленіміном. Фільтр був три рази пропотрібне таке лікування. Дана активність може митий 3мл буфера для промивання (50мМ Tris рН бути продемонстрована наступними аналізами. 7,5, 5мМ MnCl2, 150мМ NaCl), і його радіоактивЕкспресія рецептора в COS: Для швидкої ексність була визначена за допомогою гаммапресії клонованого рецептора нейрокініну-1 лічильника. Також активація фосфоліпази C за (NK1R) людини в COS, кДНК NK1R людини клонурахунок NK1R в клітинах CHO, що експресують вали у вектор експресії pCDM9, який був отримаNK1R людини, може бути виміряна шляхом визнаний з pCDM8 (INVITROGEN) шляхом інсерції гена чення накопичення інозитолмонофосфату, який є резистентності до ампіциліну (нуклеотиди 1973продуктом деградації IP3. Клітини CHO висівають в 2964 з BLUESCRIPT SK+) в сайт SacII. Трансфек12-ямкову плашку при 250000 клітин на ямку. Пісція 20мкг плазмідної ДНК в 10 мільйонів клітин ля інкубування в середовищах CHO протягом 4 COS була досягнута шляхом електропорації в днів, клітини завантажують 0,025мкКі/мл 3Н800мкл буфера трансфекції (135мМ NaCl, 1,2мМ міоінозитолу шляхом інкубування протягом ночі. CaCl2, 1,2мМ MgCl2, 2,4мМ K2HPO 4, 0,6мМ Позаклітинну радіоактивну речовину видаляють KH2PO4, 10мМ глюкози, 10мМ HEPES pH 7,4) при шляхом промивання фосфатно-буферним сольо260В і 950мкФ із застосуванням IBI GENEZAPPER вим розчином. У ямку додають LiCl при кінцевій (IBI, New Haven, CT). Клітини інкубували в 10% концентрації 0,1мМ із сполукою, що тестується, фетальній телячій сироватці, 2мМ глутаміну, або без неї і продовжують інкубування при 37°С 100од./мл пеніцілин-стептоміцину, і 90% середопротягом 15хв. У ямку додають речовину P при вища DMEM (GIBCO, Grand Island, NY) при 5% кінцевій концентрації 0,3нМ для активації NK1R CO2 при 37°С протягом трьох днів перед аналізом. людини. Після закінчення 30 хвилин інкубування Стійка Експресія в CHO: Для забезпечення при 37°С, середовища видаляють і додають 0,1н стійкої лінії клітин, що експресують клонований HCl. Кожну ямку обробляють ультразвуком при NK1R людини, кДНК субклонували у вектор 4°С і екстрагують СНСІ3/метанолом (1:1). Водну pRcCMV (INVITROGEN). Трансфекція 20мкг плазфазу вносять в 1мл іонообмінну колонку Dowex мідної ДНК в клітини CHO була досягн ута електAG 1X8. Колонку промивають 0,1н мурашиною ропорацією в 800мкл буфера трансфекції з добавкислотою, потім 0,025M форміатом амонію-0,1н кою 0,625мг/мл ДНК сім'яної рідини оселедця при мурашиною кислотою. Інозитолмонофосфат елю300В і 950мкФ із застосуванням IBI GENEZAPPER юють 0,2M форміатом амонію-0,1н мурашиною (IBI). Клітини, що трансфікуються, інкубували в кислотою і піддають кількісному аналізу за допосередовищах CHO [10% фетальної телячої сиромогою бета-лічильника частинок. За допомогою ватки, 100од./мл пеніцилін-стептоміцину, 2мМ глуданих аналізів, зокрема, може бути продемонсттаміну, 1/500 гіпоксантин-тимідину (ATCC), 90% рована власна активність антагоніста тахікініновосередовища IMDM (JRH BIOSCIENCES, Lenexa, го рецептора сполук відповідно до даного винахоKS), 0,7мг/мл G418 (GIBCO)] при 5% CO2 при 37°С, ду. Сполуки відповідно до наступних прикладів поки колонії не ставали видимими. Кожна колонія мають активність у вказаних вище аналізах в діабула відділена і розмножена. Був вибраний клон пазоні від 0,05нМ до 10мкМ. Активність даних споклітин з найбільшою кількістю NK1R людини для лук може також бути продемонстрована за допоподальших застосувань таких, як відбір лікарськомогою аналізу, розкритого [Lei, et al., British J. го засобу. Pharmacol., 105, 261-262 (1992)]. Протокол аналізу з використанням COS або Відповідно до додаткового або альтернативCHO: аналіз на зв'язування NK1R людини, експреного аспекту, даний винахід забезпечує сполуку 19 84192 20 згідно з даним винаходом для застосування як сул, в яких активний інгредієнт змішаний з інерткомпозиції, яка може бути введена індивідууму, ним твердим розріджувачем, наприклад, карбонаякому потрібне зниження кількості тахікініну або том кальцію, фосфатом кальцію або каоліном, або речовини P в організмі. у вигляді м'яких желатинових капсул, в яких активПередбачається, що термін "композиція" в ний інгредієнт змішаний з водним або масляним значенні, що використовується в даній заявці, охосередовищем, наприклад, арахідним маслом, ваплює продукт, що містить певні інгредієнти в зазеліновим маслом або оливковим маслом. Водні здалегідь визначених кількостях або співвідносуспензії містять активні речовини в суміші з інершеннях, а також будь-який продукт, який виходить, тними наповнювачами, що підходять для виробпрямо або непрямо, з поєднання вказаних інгредіництва водних суспензій. Масляні суспензії можуть єнтів у вказаних кількостях. Передбачається, що бути приготовані шляхом суспендування активного даний термін відносно фармацевтичних композиінгредієнта у відповідному маслі. Також можуть цій, охоплює продукт, що містить один або більше використовува тися емульсії типу "масло у воді". активних інгредієнтів, і необов'язковий носій, що Порошки і гранули, що диспергуються, які підхомістить інертні інгредієнти, а також будь-який продять для приготування водної суспензії шляхом дукт, який виходить, прямо або непрямо, з поєддодавання води забезпечують активний інгредієнт нання, комплексоутворення або агрегації будьв суміші з диспергуючим або змочувальним агеняких дво х або більше з інгредієнтів, або з дисоціатом, суспендуючим агентом і одним або більше ції одного або більше з інгредієнтів, або з інших консервантами. типів реакцій або взаємодій одного або більше Фармацевтичні композиції даних сполук моінгредієнтів. Загалом, фармацевтичні композиції жуть бути в формі стерильної водної або масляної готують шляхом рівномірного і безпосереднього суспензії для ін'єкції. Сполуки згідно з даним виназлиття активного інгредієнта з рідким носієм або ходом можна також вводити в формі свічок для дрібно роздробленим твердим носієм або з обома ректального введення. Для місцевого застосувані, у разі необхідності, з подальшим формуванням ня, можна використовувати креми, мазі, гелі, розпродукту в необхідний препарат. У фармацевтиччини або суспензії і т.д., що містять сполуки згідно ній композиції цільова активна сполука включена в з даним винаходом. Сполуки згідно з даним винакількості, достатній для створення необхідної дії ходом також можуть бути приготовані для введенна перебіг або стан захворювань. Відповідно, фаня за допомогою інгаляції. Сполуки згідно з даним рмацевтичні композиції відповідно до даного винавинаходом можна також вводити за допомогою ходу охоплюють будь-яку композицію, отриману трансдермального пластиру способами, відомими шляхом змішування сполуки згідно з даним виназ рівня техніки. ходом і фармацевтично прийнятного носія. Під Композиції, що містять сполуки згідно з даним "фармацевтично прийнятним" мається на увазі винаходом, можуть бути представлені у вигляді носій, розріджувач або інертний наповнювач, який одиничної дозованої форми і можуть бути пригоповинен бути сумісним з іншими інгредієнтами товані будь-яким з способів, відомих з рівня техніпрепарату і не бути шкідливим для його реципієнки фармакології. Термін "одинична дозована форта. ма" використовується для позначення одиничної Фармацевтичні композиції, призначені для педози, в якій всі активні і неактивні інгредієнти об'рорального застосування можуть бути приготовані єднані у відповідній системі, такій, що пацієнт або відповідно до будь-якого способу, відомого з рівня людина, що вводить лікарський засіб пацієнту, техніки для виробництва фармацевтичних компоможе відкрити одну ємність або упаковку з повною зицій, і такі композиції можуть містити один або дозою, що міститься там, без необхідності змішубільше агентів, вибраних з групи, яка складається вання будь-яких компонентів з двох або більше з підсолоджувачів, ароматизаторів, барвників і ємностей або пакетів. Типовими прикладами одиконсервантів з метою забезпечення фармацевтиничної дозованої форми є таблетки або капсули чно привабливих і їстівних препаратів. Таблетки для перорального прийому, флакони однократної містять активний інгредієнт в суміші з нетоксичнидози для ін'єкції або свічки для ректального ввеми фармацевтично прийнятними формоутворювадення. Передбачається, що даний список одиничльними, що підходять для виробництва таблеток. них дозованих форм не є таким, що обмежує в Дані формоутворювальні, наприклад, можуть явбудь-якому випадку, але представляє типові приляти собою інертні розріджувачі такі, як карбонат клади одиничних дозованих форм в рівні техніки кальцію, карбонат натрію, лактоза, фосфат кальфармакології. Композиції, що містять сполуки згідцію або фосфат натрію; гранулюючі і дезінтегруючі но з даним винаходом, можуть також бути предагенти, наприклад, кукурудзяний крохмаль або ставлені у вигляді набору, за допомогою якого два альгінову кислоту; зв'язувальні агенти, наприклад, або більше компонентів, які можуть являти собою крохмаль, желатин або гуміарабік і мастильні агеактивні або неактивні інгредієнти, носії, розріджунти, наприклад, стеарат магнію, стеаринову кисловачі і т. п., надані з інструкціями для приготування ту або тальк. Таблетки можуть бути непокритими, фактичної форми дозування пацієнтом або людиабо вони можуть бути покриті за допомогою відоною, що вводить лікарський засіб пацієнту. Такі мих методик для сповільнення дезінтеграції і набори можуть бути надані з всіма необхідними всмоктування в шлунково-кишковому тракті і, таматеріалами, що містяться в них, і інгредієнтами, ким чином, забезпечення уповільненої дії протяабо вони можуть містити інструкції для застосугом більш тривалого періоду часу. Композиції для вання або приготування матеріалів або компоненперорального застосування також можуть бути тів, які повинні бути незалежно отримані пацієнтом представлені у вигляді тверди х желатинових кап 21 84192 22 або людиною, що вводить лікарський засіб пацієняк агоніст опіатів, інгібітор ліпоксигенази такий, як ту. інгібітор 5-ліпоксигенази, інгібітор циклооксигенази Під "фармацевтично прийнятним" потрібно ротакий, як інгібітор циклооксигенази-2, інгібітор інзуміти носій, розріджувач або формоутворювальні, терлейкіну такий, як інгібітор інтерлейкіну-1, антаякі повинні бути сумісними з іншими інгредієнтами гоніст NMDA, інгібітор оксиду азоту або інгібітор препарату і не бути шкідливими для їх реципієнта. синтезу оксиду азоту, нестероїдний протизапальТерміни "введення" або "що вводить" сполуку ний засіб, або цитокін-супресуючий протизапальпотрібно розуміти в значенні забезпечення сполуний засіб. ки згідно з винаходом індивідууму, якому потрібне Враховується, що при використанні будь-якого лікування, в формі, яка може бути введена в оргапоєднання, описаного в даній заявці, як сполуки нізм даного індивідуума в терапевтично придатній згідно з даним винаходом, так і іншу активну речоформі і терапевтично ефективній кількості, вклювину (речовини) вводять пацієнту протягом доцічаючи, без обмежень: пероральні лікарські форми льного проміжку часу. Сполуки можуть бути в одтакі, як таблетки, капсули, сиропи, суспензії і т. п.; ному і тому ж фармацевтично прийнятному носії і лікарські форми для ін'єкцій такі, як внутрішньотому можуть бути введені одночасно. Вони можуть венні, внутрішньом'язові або інтраперитонеальні і бути в роздільних фармацевтичних носіях, наприт. п.; трансдермальні лікарські форми, включаючи клад, звичайних пероральних лікарських формах, креми, гелі, порошки або пластири; щічні лікарські які приймають одночасно. Термін "поєднання" таформи; порошки для інгаляції, спреї, суспензії і т. кож означає випадок, в якому сполуки надані в п.; і ректальні свічки. Термін "терапевтично ефекроздільних лікарських формах і їх вводять послітивну кількість" означає достатню кількість сполук довно. У зв'язку з цим, як приклад, одна активна відповідно до даного винаходу у відповідній комскладова може бути введена у вигляді таблетки і позиції і у відповідній лікарській формі для лікупотім, в межах доцільного проміжку часу, друга вання або запобігання відміченим хворобливим активна складова може бути введена у вигляді станам. пероральної лікарської форми такої, як таблетки Сполуки згідно з даним винаходом можна ввоабо швидкорозчинна пероральна лікарська фордити в поєднанні з іншою речовиною, яка має дома. Під "швидкорозчинним пероральним препараповнюючий ефект до інгібіторів тахікініну і речовитом" мається на увазі пероральна форма доставни P відповідно до даного винаходу. Відповідно, в ки, яка при попаданні на язик пацієнта, профілактиці або лікуванні блювоти, сполука згідрозчиняється в межах приблизно 10 секунд. Під но з даним винаходом може бути використана ра"доцільним проміжком часу" мається на увазі інзом з іншими протиблювотними агентами, особлитервал часу, який не перевищує приблизно 1 гово з антагоністами рецептора 5HT3 такими, як дини. Таким чином, наприклад, якщо перша активондансетрон, гранісетрон, тропісетрон, паленосена складова представлена у вигляді таблетки, то трон і затисетрон, кортикостероїдом таким, як декдруга активна складова повинна бути введена саметазон, або агоністами рецептора GABAB тапротягом однієї години, або в тому ж типі лікарськими, як баклофен. Аналогічно, для профілактики кої форми, або в іншій лікарській формі, яка забезабо лікування мігрені сполука згідно з даним винапечує ефективн у доставку медикаменту. ходом може бути використана разом з іншими заСполуки згідно з даним винаходом можуть бусобами проти мігрені такими, як агоністи ерготаміти введені пацієнтам (тваринам і людям), яким нів або 5HT1, особливо суматриптан, наратриптан, потрібне таке лікування, в дозуванні, яке забезпезолматриптан або ризатриптан. чує оптимальну фармацевтичну ефективність. Враховується, що для лікування депресії або Враховується, що доза, необхідна для введення в тривоги, сполука згідно з даним винаходом може будь-якому конкретному застосуванні змінюється використовува тися разом з іншими засобами провід пацієнта до пацієнта і визначається не тільки ти депресії або тривоги, як інгібітори зворотного конкретно вибраною сполукою або композицією, захоплення норепінефрину, селективні інгібітори але також і шляхом введення, природою стану від зворотного захоплення серотоніну (SSRIs), інгібіякого лікують, віком і станом пацієнта, спільним тори моноаміноксидази (MAOIs), інгібітори монолікуванням або спеціальними дієтами, яких потім аміноксидази (RIMAs), що діють зворотно, інгібітодотримується пацієнт і іншими чинниками, відомири зворотного захоплення серотоніну і ми фахівцям в даній галузі, при цьому, в кінцевому результаті, відповідне дозування приймають за норадреналіну (SNRIs), антагоністи aадренорецептора, атипові антидепресанти, бензорозсудом лікаря, що обслуговує. У лікуванні станів, пов'язаних з надлишком тадіазепіни, агоністи або антагоністи 5-НТ1А, особлихікінінів, відповідний рівень дозування сполук відво, часткові агоністи 5-НТ1А, антагоністи релізингповідно до даного винаходу, або їх фармацевтичфактора кортикотропіну (CRF) і їх фармацевтично но прийнятних солей, становить приблизно 0,001прийнятні солі. Для лікування або профілактики розладів харчової поведінки, включаючи ожиріння, 50мг/кг на добу, зокрема, від приблизно 0,01 до приблизно 25мг/кг, наприклад, від приблизно 0,05 нейрогенну булімію і компульсивні розлади харчодо приблизно 10мг/кг на добу. Загалом, діапазон вої поведінки, сполука згідно з даним винаходом дозування становить приблизно 0,5-1000мг кожможе бути використана разом з іншими анорексиному пацієнту на добу, яка може бути введена в генними засобами. Враховується, що для лікування або профілактики болю або ноцицепції або заодиничній або багаторазових дозах. Переважно, діапазон дозування становить приблизно 0,5мгпальних захворювань, сполука згідно з даним 500мг кожному пацієнту на добу; більш переважно, винаходом може бути використана разом з протиприблизно 0,5мг-200мг кожному пацієнту на добу; і запальним або болезаспокійливим засобом таким, 23 84192 24 ще більш переважно, приблизно 5мг-50мг кожному А) в ~150мл сухого ефір у. Реакційну суміш перепацієнту на добу. Конкретне дозування сполук мішували при 0°C протягом 0,5 години, потім повівідповідно до даного винаходу або їх фармацевльно наливали в суміш льоду/2н водн. HCl. Суміш, тично прийнятних солей для введення включає що виходила, розбавляли ефіром і сольовим роз1мг, 5мг, 10мг, 30мг, 100мг і 500мг. Фармацевтичні чином, переносили в ділильну лійку і відділяли композиції відповідно до даного винаходу можуть органічний шар. Органічний шар промивали собути забезпечені в препараті, що містить приблизльовим розчином, сушили над осушувачем, фільтно 0,5мг-1000мг активного інгредієнта; більш перували і випарювали розчинник у вакуумі для реважно, що містить приблизно 0,5мг-500мг актиотримання 14,2г необробленої сполуки відповідно вного інгредієнта; або 0,5мг-250мг активного до заголовка, яку використовували без додатковоінгредієнта; або 1мг-100мг активного інгредієнта. го очищення. 1H ЯМР (CDCl3): d: 7,19 (2H, м), 7,02 Конкретні фармацевтичні композиції для лікування (2H, т, J=9,5Гц), 6,42 (1H, дд, J=14,2Гц, J2=11Гц), або профілактики надлишку тахікінінів містять 6,34 (1H, д, J=14,2Гц), 5,86 (1H, д, J=11Гц), 3,87 приблизно 1мг, 5мг, 10мг, 30мг, 100мг і 500мг ак(2H, с). тивного інгредієнта. Етап C: 1E і 1Z трет-бутил{[1-(4Декілька способів приготування сполуки згідно фторбензиліден)проп-2-ен-1-іл]окси]диметилсилан з даним винаходом проілюстровані в наступних У розчин 104мл (104,0ммоль, 1,2еквів.) 1,0M прикладах. Вихідні матеріали і необхідні інтермерозчину трет-бутоксиду калію в ТГФ і 100мл сухого діати в деяких випадках комерційно доступні, або ТГФ в атмосфері азоту при -78°С додавали розчин можуть бути приготовані відповідно до процедур, 14,2г (86,6ммоль, 1еквів.) 1-(4-фторфеніл)бут-3відомих з літератури або як проілюстровано в даен-2-ону (етап В) і 13,0г (86,6ммоль) трет1 ній заявці. Всі спектри H ЯМР були отримані на бутилхлордиметилсилану в 100мл сухого ТГФ. вимірювальній апаратурі при напруженості поля Реакційну суміш перемішували при -78°С протягом 400 або 500МГц. 6 годин і при кімнатній температурі протягом 6 Приклад 1 годин, потім гасили шляхом додавання 50мл води. Суміш, що ви ходила, нагрівали до кімнатної температури, розбавляли 150мл гексану, переносили в ділильну лійку і відділяли органічний шар. Органічний шар промивали 50мл сольового розчину, сушили над безводним сульфатом магнію, фільтрували і випарювали розчинник у вакуумі для отримання 20,5г необроблених сполук відповідно до заголовка, які використовували без додаткового очищення. 1H ЯМР (CDCl3): d: 7,52 (2H, м), 6,98 (2H, м), 6,33 (1H, дд, J1=13,2Гц, J2=8,5Гц), 5,97 (1H, с), 5,52 (1H, д, J=13,2Гц), 5,17 (1H, д, J=8,5Гц). (3aR,4R,5S,7aR)-5-{1(S)-[3,5Етап D: (3аS,4R,7аR-2-бензил-5-{[третбіс(трифторметил)феніл]етокси}-4-(4бутил(диметил)силіл]окси}-4-(4-фторфеніл)(фтор феніл)октагідро-1Н-ізоіндол і 3а,4,7,7а-тетрагідро-1Н-ізоіндол-1,3(2Н)-діон і (3aS,4S,5R,7aS)-5-{1(S)-[3,5(3aR,4S,7aS)-2-бензил-5-{[третбіс(трифторметил)феніл]етокси}-4-(4-фторфеніл)бутил(диметил)силіл]окси)-4-(4-фторфеніл)октагідро-1Н-ізоіндол 3а,4,7,7а-тетрагідро-1Н-ізоіндол-1,3(2Н)-діон Етап А: 2-(4-Фторфеніл)-N-метокси-NРозчин 15г (54,0ммоль, 1еквів.) 1E і 1Z третметилацетамід бутил{[1-(4-фторбензиліден)проп-2-ен-1У розчин 16,7г (108,4ммоль) (4іл]окси}диметилсилану (етап C) і 12,1г (64,6ммоль) фтор феніл)оцтової кислоти в сухому метиленхлоN-бензилмалеїміду в 150мл сухого толуолу в атриді в атмосфері азоту додавали 13,8г мосфері азоту нагрівали із зворотним холодильни(141,5ммоль) N,O-диметилгідроксиламіну, 20мл ком протягом 16 годин, потім охолоджували до триетиламіну, 14,2г (119,3ммоль) 4кімнатної температури. Випарювали розчинник у диметиламінопіридину (DMAP) і 27г (140,6ммоль) вакуумі для отримання 31г необроблених сполук EDC. Реакційну суміш перемішували при кімнатній відповідно до заголовка, які містили Nтемпературі протягом 2 годин, потім переносили в бензилмалеїмід, що не прореагував, і використоділильну лійку. Суміш промивали послідовно 2н вували без додаткового очищення. 1H ЯМР водн. HCl, сольовим розчином, насиченим водн. (CDCl3): d: 7,37-7,26 (3H, м), 7,22 (2H, м), 7,00 (2H, NaHCO3 і сольовим розчином. Органічний шар м), 6,78 (2H, т, J=8,5Гц), 5,07 (1H, т, J =2,3Гц), 4,22 сушили над осушувачем, фільтрували і випарюва(1H, д, J=16Гц), 4,15 (1H, д, J=16Гц), 3,66 (1H, д, ли розчинник у вакуумі для отримання 21г необроJ=6,5Гц), 3,52 (1H, т, J=7,0Гц), 3,14 (1H, м), 2,87 бленої сполуки відповідно до заголовка, яку вико(1H, м), 2,68 (1H, м), 0,92 (1H, м), 0,78 (9H, с), 0,11 1 ристовували без додаткового очищення. H ЯМР (3H, с), -0,1 (3H, с). (CDCl3): d: 7,26 (2H, м), 7,02 (2H, м), 3,77 (2H, с), Етап E: (3аS,4S,7аS)-2-бензил-5-([трет3,65 (3H, с), 3,21 (3H, с). бутил(диметил)силіл]окси}-4-(4-фторфеніл)Етап В: 1-(4-Фторфеніл)бут-3-ен-2-он 2,3,3а,4,7,7а-гексагідро-1Н-ізоіндол i (3aR,4R,7aR)У розчин 220мл (1,0м, 220ммоль) вінілмагній2-бензил-5-([трет-бутил(диметил)силіл]окси)-4-(4броміду в 100мл ТГФ, додавали по краплях в атфтор феніл)-2,3,3а,4,7,7а-гексагідро-1Н-ізоіндол мосфері азоту при 0°C розчин 21г (106,6ммоль) 2У колбу з круглим дном додавали 7,3г (4-фторфеніл)-N-метокси-N-метилацетаміду (етап (192,0ммоль, надлишок) алюмогідриду літію в су 25 84192 26 хому ефірі в атмосфері азоту при 0°C. До суміші, Інтермедіат етапу G піддавали гідрогенізації що виходила, додавали по краплях розчин 31г при 50фунт/кв. дюйм водню з більше за 10% по необробленого інтермедіату етапу D в 100мл суховазі 10% Pd-C в етанолі протягом 16 годин при го метиленхлориду в атмосфері азоту. Суміш, що кімнатній температурі. Каталізатор фільтрували і виходила, перемішували при кімнатній температурозчинник з фільтрату випарювали у вакуумі для рі протягом 1 години, потім акуратно гасили при отримання необроблених сполук відповідно до 0°C шляхом додавання 12мл води по краплях, заголовка, які використовували без додаткового потім 10мл 5,0н водн. NaOH. Суспензію, що вихоочищення. дила, перемішували при кімнатній температурі Етап І: трет-Бутил-(3аS,4S,5R,7аS)-4-(4протягом 0,5 години і відфільтровували тверді фтор феніл)-5-гідроксіоктагідро-2Н-ізоіндол-2речовини. Розчинник з фільтрату випарювали у карбоксилат і трет-бутил-(3aR,4R,5S,7аR)-4-(4вакуумі для отримання необроблених сполук відфтор феніл)-5-гідроксі-октагідро-2Н-ізоіндол-2повідно до заголовка, які використовували без карбоксилат. додаткового очищення. У розчин 7,5г (31,9ммоль) інтермедіату етап у Етап F: (3аS,4S,7аS)-2-бензил-4-(4H в сухому метиленхлориді в атмосфері азоту при фтор феніл)октагідро-5Н-ізоіндол-5-он і кімнатній температурі додавали 9,0г (41,5ммоль) (3аR,4R,7аR)-2-бензил-4-(4-фторфеніл)октагідробікарбонату дитрет-бутилу. С уміш, що ви ходила, 5Н-ізоіндол-5-он перемішували при кімнатній температурі протягом У розчин інтермедіату етапу E в 60мл сухого 16год., потім випарювали розчинник у вакуумі. ацетонітрилу в атмосфері азоту при кімнатній темСуміш, що ви ходила, розчиняли в метанолі і додапературі додавали 100мл (250ммоль) 2,5М розчивали 5,0н водн. NaOH. Суміш, що виходила, перену HF в ацетонітрилі. Суміш, що ви ходила, перемішували протягом 2 годин, і видаляли метанол у мішували при кімнатній температурі протягом 16 вакуумі. Водний залишок розбавляли EtOAc, пегодин, потім гасили при 0°C шляхом додавання по реносили в ділильну лійку і відділяли органічний краплях 120мл 5,0н водн. NaOH. Ацетонітрил вишар. Водний шар екстрагували додатковою частпарювали у вакуумі, і водн у суміш, що ви ходила, кою EtOAc. Об'єднані органічні шари промивали розбавляли ефіром і водою. Суміш, що виходила, 50мл сольового розчину, сушили над сульфатом переносили в ділильну лійку і відділяли органічний магнію, фільтрували і випарювали розчинник у шар. Водний шар екстрагували додатковою частвакуумі. Залишок очищали з допомогою колонкокою ефіру. Об'єднані органічні шари промивали 50 вої флеш-хроматографії на силікагелі з елюцією мл сольового розчину, сушили над осушувачем, EtOАс/гексанами (1/4) для отримання 2,8г рацеміфільтрували і випарювали розчинник у вакуумі. чних сполук відповідно до заголовка. 1H ЯМР Залишок очищали з допомогою колонкової флеш(CDCl3): d: 7,22 (2H, м), 7,07 (2H, м), 3,73 (1H, м), хроматографії на силікагелі з елюцією 3,48-3,33 (2H, м), 3,21-3,10 (2H, м), 2,51 (1H, м), EtOАс/гексанами (1/1) для отримання 9,0г рацемі2,18 (1H, т, J=10,7Гц), 2,25 (1H, м), 1,98 (1H, м), чних сполук відповідно до заголовка. 1H ЯМР 1,97-1,85 (1H, м), 1,63 (1H, м), 1,51-1,40 (1H, м), (CDCl3): d: 7,27-7,23 (3H, м), 7,12-7,03 (2H, м), 3,75 1,49, 1,43 (9H, два синглети). Також виділили не(1H, д, J=12,9Гц), 3,61 (2H, д, J=4,8Гц), 3,61 (1H, значну кількість суміші цис-спирту (менш поляркв, J=14,5Гц), 2,93 (1H, т, J=8,5Гц), 2,68-2,52 (3H, ний): трет-бутил-(3аR,4R,5R,7аR)-4-(4-фторфеніл)м), 2,43-2,33 (2H, м), 2,25 (1H, м), 2,05 (2H, м). 5-гідроксіоктагідро-2Н-ізоіндол-2-карбоксилат і Етап G: (3аS,4S,5R,7аS)-2-бензил-4-(4трет-бутил-(3aS,4S,5S,7aS)-4-(4-фторфеніл)-51 фтор феніл)октагідро-1Н-ізоіндол-5-ол і гідроксіоктагідро-2Н-ізоіндол-2-карбоксилат. H (3аR,4R,5S,7аR)-2-бензил-4-(4ЯМР (CDCl3): d: 7,25 (2Н, м), 7,05 (2H, м), 3,95 (1H, фтор феніл)октагідро-1Н-ізоіндол-5-ол м), 3,50-3,20 (3H, м), 3,08, 2,95 (1H, два дублети, У розчин інтермедіату (9,0г) етапу F в атмосJ=14,3Гц), 2,77 (1H, м), 2,65-2,55 (2H, м), 2,15 (1H, фері азоту в сухому е фірі при -78°C додавали м), 1,82 (2H, м), 1,58 (1H, м), 1,45, 1,40 (9H, два 1,0M розчин алюмогідриду літію (38,3мл) в ефірі. синглети). Суміш, що виходила, перемішували при -78°C Етап J: трет-Бутил-(3аS,4S,5R,7аS)-5-{[3,5протягом 0,5 години, потім акуратно гасили шлябіс(трифторметил)бензоїл]окси}-4-(4-фторфеніл)хом додавання по краплях води, потім 5,0н водн. октагідро-2Н-ізоіндол-2-карбоксилат і трет-бутилNaOH. Суспензію, що виходила, перемішували при (3аR,4R,5S,7аR)-5-{[3,5-біс(трикімнатній температурі протягом 0,5 години і відфіфторметил)бензоїл]окси}-4-(4льтровували тверді речовини. Розчинник з фільтфтор феніл)октагідро-2Н-ізоіндол-2-карбоксилат рату випарювали у вакуумі для отримання необУ розчин 0,09г (0,26ммоль) інтермедіату етапу роблених сполук відповідно до заголовка як І в сухому метиленхлориді в атмосфері азоту при основних сполук, які використовували без додаткімнатній температурі додавали 0,089г кового очищення. 1Н-ЯМР (CDCl3): d: 7,38-7,20 (7H, (0,32ммоль) 3,5-біс(трифторметил)-бензоїлхлорид, м), 7,05 (2H, т, J=8,5Гц), 3,75 (2H, с), 3,75 (1H, м), 0,07мл TEA і каталітичну кількість DMAP. Суміш, 2,8-2,65 (4H, м), 2,60 (1H, м), 2,50 (1H, м), 2,38 (1H, що ви ходила, перемішували при кімнатній темпед, J=8,1Гц), 2,21 (1H, м), 1,95 (1H, м), 1,81 (2H, м), ратурі протягом 2 годин, потім переносили в діли1,73-1,62 (2H, м). MS: (MH)+ 261,9. льну лійку, промивали насиченим водн. NaHCO3, Етап H: (3аS,4S,5R,7аS)-4-(4водн. KHSO4 і сольовим розчином. Об'єднані оргафтор феніл)октагідро-1Н-ізоіндол-5-ол і нічні шари сушили над сульфа том магнію, фільт(3аR,4R,5S,7аR)-4-(4-фторфеніл)октагідро-1Нрували і випарювали розчинник у вакуумі для ізоіндол-5-ол отримання 0,15г необробленої сполуки відповідно до заголовка, яку використовували без додатково 27 84192 28 Етап M: (3aR,4R,5S,7aR)-5-{1(S)-[3,5го очищення. 1Н-ЯМР (CDCl3): d: 8,63 (1H, с), 8,19 біс(трифторметил)феніл]етокси}-4-(4-фторфеніл)(2H, с), 7,25 (2H, м), 7,00 (2H, м), 5,22 (1H, м), 3,593,43 (2Н, м), 3,30-3,20 (2H, м), 2,83 (1H, т, J - 12,7 октагідро-1Н-ізоіндол і (3aS,4S,5R,7aS)-5-{1(R)[3,5-біс(трифторметил)феніл]етокси)-4-(4Гц), 2,62 (1H, м), 2,43 (1H, м), 2,20 (1H, м), 2,02 фтор феніл)октагідро-1Н-ізоіндол (1H, м), 1,90-1,70 (2H, м), 1,55, 1,47 (9H, два сингМенш полярний головний діастереоізомер лети). проміжного Етапу L розчиняли в сухому метиленЕтап K: трет-Бутил-(3aS,4S,7aS)-5-({1-[3,5біс(трифторметил)феніл]вініл}окси)-4-(4хлориді і обробляли анізолом і ТФК при кімнатній температурі протягом 2 годин. Розчинник випарюфтор феніл)октагідро-2Н-ізоіндол-2-карбоксилат і вали у вакуумі, і залишок поглинали з допомогою трет-бутил-(3aR,4R,5S,7aR)-5-({1-[3,5EtOAc. Розчин промивали водн. NaOH, потім собіс(трифторметил)феніл] вініл} окси)-4-(4льовим розчином, сушили над осушувачем і фільфтор феніл)октагі дро-2Н-ізоіндол-2-карбоксилат У розчин 0,15г (0,26ммоль) інтермедіату етапу трували. Розчинник випарювали у вакуумі для отримання необроблених сполук відповідно до J в сухому ТГФ в атмосфері азоту при 0°C додавали 2мл 0,5M розчину реактиву Tebbe в толуолі. заголовка. 1H ЯМР (CDCl3): d: 7,77 (1H, с), 7,60 Суміш, що ви ходила, перемішували при 0°C про(2H, с), 7,28 (2H, м), 7,12 (2H, т, J=8,2Гц), 4,07 (1H, тягом 0,5 години, потім акуратно гасили шляхом м), 3,35 (1H, м), 3,22-3,10 (2H, м), 3,00 (1H, м), 2,85 додавання по краплях 0,5мл води, потім 0,5мл 5,0 (1H, д, J=11,3Гц), 2,65 (1H, т, J=11,3Гц), 2,50 (1H, н водн. NaOH. Суспензію, що виходила, розбавлям), 2,40 (1H, м), 1,87-1,68 (2H, м), 1,53 (1H, м), 1,30 ли етилацетатом, перемішували при кімнатній те(1H, м), 0,95 (3H, д, J=6,0Гц). мпературі протягом 0,5 години і відфільтровували Приклад 2 тверді речовини. Фільтрат, що ви ходив, перемішували з 0,5мл 5,0н водн. NaOH протягом 16 годин і тверді речовини відфільтровували через прокладку допоміжного фільтрувального матеріалу. Розчинник випарювали у вакуумі для отримання необроблених сполук відповідно до заголовка, які використовували без додаткового очищення. 1НЯМР (CDCl3): d: 7,73 (1H, с), 7,55 (2H, зс), 7,30-7,18 (2H, м), 7,03 (2H, м), 4,67 (1H, с), 4,37 (1H, с), 4,25 (1H, м), 3,55-3,30 (3H, м), 3,27-3,15 (2H, м), 2,81 (1H, т, J=12,7Гц), 2,60 (1H, м), 2,40-30 (2H, м), 1,98 (3аR,4R,5S,7аR)-5-{(1R)-1-[3,5(1H, м), 1,83 (1H, м), 1,55, 1,47 (9H, два синглети). біс(трифторметил)феніл]етокси}-4-(4Етап L: трет-Бутил-(3aS,4S,5R,7aS)-5-{1R-[3,5фтор феніл)октагідро-1Н-ізоіндол біс(трифторметил)феніл]-етокси}-4-(4Етап А: (3аS,4S,5R,7аS)-2-Бензил-4-(4фтор феніл)октагідро-2Н-ізоіндол-2-карбоксилат і фтор феніл)октагідро-1Н-ізоіндол-5-ол і трет-бутил-(3aR,4R,5S,7aR)-5-{1S-[3,5(3аR,4R,5S,7аR)-2-бензил-4-(4бic(тpифтopмeтил)феніл]eтoкcи)-4-(4фтор феніл)октагідро-1Н-ізоіндол-5-ол фтор феніл)октагідро-2Н-ізоіндол-2-карбоксилат і Починаючи з 3,5г рацемічної суміші трет-Бутил-(3aS,4S,5R,7aS)-5-{1S-[3,5(3aS,4S,5R,7aS)-2-бензил-4-(4біс(трифторметил)феніл]етокси}-4-(4фтор феніл)октагідро-1Н-ізоіндол-5-олу і фтор феніл)октагідро-2Н-ізоіндол-2-карбоксилат, (3aR,4R,5S,7aR)-2-бензил-4-(4трет-бутил-(3аR,4R,5S,-7аR)-5-{1R-[3,5фтор феніл)октагідро-1Н-ізоіндол-5-олу (інтермедібіс(трифторметил)феніл]-етокси}-4-(4ат Прикладу 1, етапу G), вони були розділені з фтор феніл)октагідро-2Н-ізоіндол-2-карбоксилат допомогою хіральної ВЕРХ із застосуванням колоІнтермедіат етапу G піддавали гідрогенізації нки CHIRACEL AD з елюцією гексанами/EtOH (9/1) при 50 фунт/кв. дюйм водню з більше за 10% по для отримання першого елюйованого ізомеру вазі 10% Pd-C в етанолі протягом 16 годин при (3аS,4S,5R,7аS)-2-бензил-4-(4кімнатній температурі. Каталізатор фільтрували, і фтор феніл)октагідро-1Н-ізоіндол-5-олу і другого розчинник з фільтрату випарювали у вакуумі для елюйованого ізомеру (3aR,4R,5S,4aR)-2-бензил-4отримання необроблених сполук відповідно до (4-фторфеніл)октагідро-1IH-ізоіндол-5-олу. заголовка, які очищали з допомогою препаративЕтап В: трет-Бутил-(3аR,4R,5S,7аR)-4-(4ної TШX з елюцією EtOАс/гексанами (1/3) для фтор феніл)-5-гідроксіоктагідро-2Н-ізоіндол-2отримання двох діастереоізомерів. Менш поляркарбоксилат ний (основний) ізомер, 1H ЯМР (CDCI3): d: 7,73 (1H, У розчин 5,36г (15,8ммоль) другого ізомеру с), 7,58 (2H, с), 7,25 (2H, м), 7,10 (2H, м), 4,05 (1H, (3aR,4R,5S,7aR)-2-бензил-4-(4м), 3,23-3,30 (3H, м), 3,20-3,07 (2H, м), 2,55 (1H, т, фтор феніл)октагідро-1Н-ізоіндол-5-олу, що елююJ=10,3Гц), 2,45 (1H, м), 2,33 (1H, м), 2,20-1,55 (3H, ється, (інтермедіату етапу А), в 80мл EtOH додам), 1,50, 1,43 (9H, два синглети), 0,95 (3H, д, вали 4,31г (19,7ммоль) бікарбонату дитрет-бутилу 1 J=6,9Гц), 1,0-0,82 (1H, м). Не основний ізомер, H і 0,5г 10% Pd-C. Суміш, що ви ходила, піддавали ЯМР (CDCl3): d 7,70 (1H, с), 7,20 (2H, с), 6,95 (2H, гідрогенізації при 50фунт/кв. дюйм водню протягом м), 6,87 (2H, м), 4,45 (1H, м), 3,40 (1H, м), 3,27 (1H, 16 годин при кімнатній температурі. Каталізатор м), 3,15-3,05 (2H, м), 2,47 (2H, т, J=I 1,2 Гц), 2,15 фільтрували і додавали 5мл 5,0н водн. NaOH. (2H, м), 1,93 (1H, м), 1,75 (1H, м), 1,62 (1H, м), 1,50 Розчинник випарювали у вакуумі. Водний залишок (1H, м), 1,50, 1,45 (9H, с), 1,30 (3H, два дублети, розбавляли EtOAc, переносили в ділильну лійку, J=6,0Гц). 29 84192 30 промивали сольовим розчином, сушили над осу50фунт/кв. дюйм водню з більше ~1г 10% Pd-C в шувачем, фільтрували і випарювали розчинник у етанолі протягом 3 годин при кімнатній температувакуумі. Залишок очищали з допомогою колонкорі. Каталізатор фільтрували, і розчинник з фільтвої флеш-хроматографії на силікагелі з елюцією з рату випарювали у вакуумі для отримання необEtOАс/гексанами (1/4) для отримання сполуки відроблених сполук відповідно до заголовка, які очищали з допомогою колонкової хроматографії з повідно до заголовка. 1H ЯМР (CDCl3): d: 7,22 (2H, елюцією EtOАс/гексанами (2/3) для отримання 8,9г м), 7,07 (2H, м), 3,73 (1H, м), 3,48-3,33 (2H, м), 3,21-3,10 (2H, м), 2,51 (1H, м), 2,18 (1H, т, (15,5моль) двох діастереоізомерів з основним (S) діастереоізомером. Дану суміш поглинали ~150мл J=10,7Гц), 2,25 (1H, м), 1,98 (1H, м), 1,97-1,85 (1H, сухого ТГФ в атмосфері азоту і обробляли 80мл м), 1,63 (1H, м), 1,51-1,40 (1H, м), 1,49, 1,43 (9H, (80ммоль) 1,0м розчину трет-бутоксиду калію в два синглети). ТГФ. Суміш, що виходила, нагрівали при 40°C проЕтап С: трет-Бутил-(3аR,4R,5S,7аR)-5-{[3,5біс(трифторметил)бензоїл]окси}-4-(4тягом 1 години, охолоджували до кімнатної температури і гасили шляхом додавання води. Суміш фтор феніл)октагідро-2Н-ізоіндол-2-карбоксилат розбавляли EtOAc, переносили в ділильну лійку, У розчин 4,75г (14,0ммоль) інтермедіату етапу промивали сольовим розчином, сушили над осуВ в сухому метиленхлориді в атмосфері азоту при шувачем, фільтрували і випарювали розчинник у кімнатній температурі додавали 4,71г (17,0ммоль) 3,5-біс(трифторметил)-бензоїлхлориду, 2,4мл вакуумі. Залишок очищали з допомогою колонкової флеш-хроматографії на силікагелі з елюцією з (17,3ммоль) TEA і каталітичну кількість DMAP. EtOAc/гексанами (1/3) для отримання менш поляСуміш, що ви ходила, перемішували при кімнатній рного трет-бутил-(3aR,4R,5S,7aR)-5-{(1S)-1-[3,5температурі протягом 2 годин, потім переносили в біс(трифторметил)феніл]етокси}-4-(4ділильну лійку, промивали насиченим водн. NaHCO3 і сольовим розчином. Об'єднані органічні фтор феніл)октагідро-2Н-ізоіндол-2-карбоксилату і більш полярного трет-бутил-(3aR,4R,5S,7aR)-5шари сушили над сульфатом магнію, фільтрували {(1R)-1-[3,5-біс(трифторметил)феніл]етокси}-4-(4і випарювали розчинник у вакуумі для отримання фтор феніл)октагідро-2Н-ізоіндол-2-карбоксилату. необробленої сполуки відповідно до заголовка, яку 1 використовували без додаткового очищення. 1H Н-ЯМР (CDCl3): d: менш полярного ізомеру: d: 7,73 (1H, с), 7,58 (2H, с), 7,25 (2H, м), 7,10 (2H, м), ЯМР (CDCl3): d: 8,63 (1H, с), 8,19 (2H, с), 7,25 (2H, 4,05 (1H, м), 3,23-3,30 (3H, м), 3,20-3,07 (2H, м), м), 7,00 (2H, м), 5,22 (1H, м), 3,59-3,33 (2H, м), 2,55 (1H, т, J=10,3Гц), 2,45 (1H, м), 2,33 (1H, м), 3,30-3,20 (2H, м), 2,83 (1H, т, J=12,7Гц), 2,62 (1H, 2,20-1,55 (3H, м), 1,50, 1,43 (9H, два синглети), м), 2,43 (1H, м), 2,20 (1H, м), 2,02 (1H, м), 1,90-1,70 0,95 (3H, д, J=6,9Гц), 1,0-0,82 (1H, м). 1H ЯМР (2H, м), 1,55, 1,47 (9H, два синглети). (CDCl3) більш полярного ізомеру: 7,71 (1H, с), 7,20 Етап D: трет-Бутил-(3aR,4R,5S,7aR)-5-({1-[3,5(2H, с), 6,97 (2H, м), 6,85 (2H, м), 4,47 (1H, м), 3,43біс(трифторметил)феніл]-вініл}окси)-4-(43,03 (4H, м), 2,47 (2H, м), 2,15 (2H, м), 1,92 (1H, т, фтор феніл)октагідро-2Н-ізоіндол-2-карбоксилат J=10,5Гц), 1,80-1,57 (3H, м), 1,50, 1,43 (9H, два У розчин 9,5г (14,0ммоль) необробленого інсинглети), 1,30 (3H, д, J=6,9Гц). термедіату етапу C в сухому ТГФ в атмосфері азоЕтап F: хлористоводнева сіль ту при 0°C додавали 66мл (33ммоль) 0,5M розчину (3aR,4R,5S,7aR)-5-{(1R)-1-[3,5реактиву Tebbe в толуолі. Суміш, що ви ходила, біс(трифторметил)феніл]етокси|-4-(4перемішували при 0°C протягом 2 годин, потім фтор феніл)октагідро-1Н-ізоіндолу акуратно гасили шляхом додавання по краплях Більш полярний діастереоізомер проміжного 7,5мл води, потім 7,5мл 5,0н водн. NaOH. СуспенЕтапу E (1,5 г, 2,6ммоль) розчиняли в ~20мл 4н HCl зію, що виходила, перемішували при кімнатній в діоксані і перемішували при кімнатній температемпературі протягом 0,5 години і відфільтровуватурі протягом 2 годин. Розчинник випарювали у ли тверді речовини. Фільтрат, що виходив, перевакуумі, і залишок поглинали EtOAc. Розчин промішували з 5мл 5,0н водн. NaOH протягом 16 гомивали водн. NaOH, потім сольовим розчином, дин і тверді речовини відфільтровували через сушили над осушувачем і фільтрували. Розчинник допоміжний фільтрувальний матеріал. Розчинник випарювали у вакуумі для отримання необроблевипарювали у вакуумі і залишок очищали з допоної сполуки відповідно до заголовка. Обробка з могою колонкової хроматографії з елюцією EtOАс/гексанами (1/3) для отримання сполуки відHCl в діоксані дала сіль HCl 1H ЯМР (CDCl3): d: 1 7,75 (1H, с), 7,37 (2H, с), 7,13 (2H, м), 6,87 (2H, т, повідно до заголовка. Н-ЯМР (CDCl3): d: 7,73 (1H, J=8,5 Гц), 4,63 (1H, кв, 6,5Гц), 3,45 (1H, тд, J1=4Гц, с), 7,55 (2H, с), 7,30-7,18 (2H, м), 7,03 (2H, м), 4,67 J2=11,9Гц), 3,17 (1H, м), 3,10 (1H, дд, J1=6,5Гц, (1H, с), 4,37 (1H, с), 4,25 (1H, м), 3,55-3,30 (3H, м), J2=9,5Гц), 2,90 (1H, J=12,7Гц), 2,57 (2H, м), 2,47 3,27-3,15 (2H, м), 2,81 (1H, т, J=12,7Гц), 2,60 (1H, (1H, т, J=9,5Гц), 2,25 (1H, м), 1,98 (2H, м), 1,68 (1H, м), 2,40-30 (2H, м), 1,98 (1H, м), 1,83 (1H, м), 1,55, 1,47 (9H, два синглети). м), 1,10 (3H, д, 6,5Гц). MS: (MH)+ 475,9. Приклад 3 Етап E: трет-бутил-(3аR,4R,5S,7аR)-5-{(1S)-1[3,5-біс(трифторметил)феніл]-етокси}-4-(4фтор феніл)октагідро-2Н-ізоіндол-2-карбоксилат і трет-бутил-(3аR,4R,5S,7аR)-5-((1R)-1-[3,5біс(трифторметил)феніл]етокси}-4-(4фтор феніл)октагідро-2Н-ізоіндол-2-карбоксилат Розчин 10,2г необробленого інтермедіату етапу D в етанолі піддавали гідрогенізації при 31 84192 (3аR,4R,5S,7аR)-5-{(1R)-1-[3,5біс(трифторметил)феніл]етокси}-4-(4-фторфеніл)2-метил-октагідро-1Н-ізоіндол Етап А: (3аR,4R,5S,7аR)-5-{(1R)-1-[3,5біс(трифторметил)феніл]етокси}-4-(4-фторфеніл)2-метилоктагідро-1Н-ізоіндол У розчин 30мг (0,063ммоль) (3aR,4R,5S,7aR)5-{(1R)-1-[3,5-біс(трифторметил)феніл]етокси}-4(4-фторфеніл)октагідро-1Н-ізоіндолу (Приклад 2) в ~2мл метанолу додавали ~20мг (надлишок) водн. формальдегіду і 40мг ацетату натрію. Суміш, що виходила, перемішували при кімнатній температурі протягом 10 хвилин, потім додавали 20мг NaBH4. Суміш, що ви ходила, перемішували при кімнатній температурі протягом 1 години, потім додавали воду. Метанол випарювали у вакуумі і залишок екстрагували ефіром (2´25мл). Об'єднані екстракти сушили над осушувачем, фільтрували і випарювали розчинник у вакуумі. Залишок очищали з допомогою препаративної ТШХ з елюцією EtOAc/MeOH (9/1) для отримання сполуки відповідно до заголовка. 1H ЯМР (CDCl3): d: ч/млн 7,68 (1H, с), 7,23 (2H, с), 7,02 (2H, м), 6,87 (2Н, м), 4,45 (1H, м), 3,27 (1 H,), 2,78-2,65 (2H, м), 2,57 (2H, м), 2,45-2,30 (3H, м), 2,23-2,12 (2H, м), 1,98 (1H, м), 1,83-1,68 (2H, м), 1,30 (3H, 6,2) MS: (MH)+ 489,9. Приклад 4 (3аS,4S,5R,7аS)-5-{(1S)-1-[3,5біс(трифторметил)феніл]етокси}-4-(4-фторфеніл)октагідро-1Н-ізоіндол Етап А: трет-Бутил-(3аS,4S,5R,7аS)-4-(4фтор феніл)-5-гідроксіоктагідро-2Н-ізоіндол-2карбоксилат Сполуку відповідно до заголовка готували з (3aS,4S,5R,7aS)-2-бензил-4-(4фтор феніл)октагідро-1Н-ізоіндол-5-олу (перший елюйований ізомер Прикладу 2, етапу А) відповідно до процедури Прикладу 2, етапу В). 1H ЯМР (CDCl3): d: 7,22 (2H, м), 7,07 (2H, м), 3,73 (1H, м), 3,48-3,33 (2H, м), 3,21-3,10 (2H, м), 2,51 (1H, м), 2,18 (1H, т, J=10,7Гц), 2,25 (1H, м), 1,98 (1H, м), 1,97-1,85 (1H, м), 1,63 (1H, м), 1,51-1,40 (1H, м), 1,49, 1,43 (9H, два синглети). 32 Етап В; трет-Бутил-(3аS,4S,5R,7аS)-5-{[3,5біс(трифторметил)бензоїл]окси}-4-(4фтор феніл)октагідро-2Н-ізоіндол-2-карбоксилат Сполуку відповідно до заголовка готували з інтермедіату етапу А відповідно до процедури Прикладу 2, етапу C. 1Н-ЯМР (CDCl3): d: 8,63 (1H, с), 8,19 (2H, с), 7,25 (2H, м), 7,00 (2H, м), 5,22 (1H, м), 3,59-3,433 (2H, м), 30-3,20 (2H, м), 2,83 (1H, т, J=12,7Гц), 2,62 (1H, м), 2,43 (1H, м), 2,20 (1H, м), 2,02 (1H, м), 1,90-1,70 (2H, м), 1,55, 1,47 (9H, два синглети). Етап C: трет-Бутил-(3аS,4S,5R,7аS)-5-({1-[3,5біс(трифторметил)феніл]вініл}окси)-4-(4фтор феніл)октагідро-2Н-ізоіндол-2-карбоксилат Сполуку відповідно до заголовка готували з інтермедіату етапу В відповідно до процедури Прикладу 2, етапу D. 1H ЯМР (CDCl3): d: 7,73 (1H, с), 7,55 (2H, с), 7,30-7,18 (2H, м), 7,03 (2H, м), 4,67 (1H, с), 4,37 (1H, с), 4,25 (1H, м), 3,55-3,30 (3H, м), 3,27-3,15 (2H, м), 2,81 (1H, т, J=12,7Гц), 2,60 (1H, м), 2,40-2,30 (2H, м), 1,98 (1H, м), 1,83 (1H, м), 1,55, 1,47 (9H, два синглети). Етап D: трет-Бутил-(3aS,4S,5R,7aS)-5-{(1S)-1[3,5-біс(трифторметил)феніл]етокси}-4-(4фтор феніл)октагідро-2Н-ізоіндол-2-карбоксилат і трет-бутил-(3aS,4S,5R,7aS)-5-{(1R)-1-[3,5біс(трифторметил)феніл]етокси)-4-(4фтор феніл)октагідро-2Н-ізоіндол-2-карбоксилат. Сполуку відповідно до заголовка готували з інтермедіату етапу C відповідно до процедури Прикладу 2, етапу E. 1H ЯМР (CDCl3): d: менш полярного ізомеру, d: 7,73 (1H, с), 7,58 (2H, с), 7,25 (2H, м), 7,10 (2H, м), 4,05 (1H, м), 3,23-3,30 (3H, м), 3,20-3,07 (2H, м), 2,55 (1H, т, J=10,3Гц), 2,45 (1H, м), 2,33 (1H, м), 2,20-1,55 (3H, м), 1,50, 1,43 (9H, два синглети), 0,95 (3H, д, J=6,9Гц), 1,0-0,82 (1H, м). 1H ЯМР (CDCl3) більш полярного ізомеру: 7,71 (1H, с), 7,20 (2H, с), 6,97 (2H, м), 6,85 (2H, м), 4,47 (1H, м), 3,43-3,03 (4H, м), 2,47 (2H, м), 2,15 (2H, м), 1,92 (1H, т, J=10,5Гц), 1,80-1,57 (3H, м), 1,50, 1,43 (9H, два синглети), 1,30 (3H, д, J=6,9Гц). Етап Е:(3аS,4S,5R,7аS)-5-{(1S)-1-[3,5біс(трифторметил)феніл]етокси}-4-(4фтор феніл)октагідро-1Н-ізоіндол Сполуку відповідно до заголовка готували з трет-бутил-(3aS,4S,5R,7aS)-5-{(1S)-1-[3,5біс(трифторметил)феніл]етокси}-4-(4фтор феніл)октагідро-2Н-ізоіндол-2-карбоксилату (етап D) відповідно до процедури Прикладу 2, етапу F. Більш полярний ізомер, 1Н-ЯМР (CDCl3): d: 7,68 (1H, с), 7,20 (2H, с), 7,05 (2H, м), 6,87 (2H, т, J=8,2Гц), 4,27 (1H, м), 3,28 (1H, м), 3,20-3,05 (2H, м), 2,88 (1H, м), 2,72 (1H, д, J=11,7Гц), 2,58 (1H, т, J=11,9Гц), 2,40 (1H, м), 2,20 (1H, м), 2,10 (1H, м), 1,92 (1H, м), 1,83 (1H, м), 1,60 (1H, м), 1,30 (3H, д, J=6,0Гц). MS: (MH)+ 475,9. Приклад 5 33 84192 34 тонітрилі. Суміш, що виходила, перемішували при кімнатній температурі протягом 24 годин. Реакційну суміш додавали в суміш 125мл 5,0н водн. NaOH і 100г льоду, потім перемішували при кімнатній температурі протягом 5хв. С уміш, що ви ходила, розбавляли 300мл ефіру. Суміш, що ви ходила, переносили в ділильну лійку і відділяли органічний шар. Водний шар насичували NaCl, потім екстрагували додатковою часткою ефіру. Об'єднаний органічний шар промивали сольовим розчином, сушили над осушувачем, фільтрували і випарюва3-[(3аR,4R,5S,7аR)-5-{(1R)-1-[3,5ли розчинник у вакуумі для отримання 40,8г сполук біс(трифторметил)феніл]етокси}-4-(4-фторфеніл)відповідно до заголовка. 1Н-ЯМР (CDCl3): d: 7,10 октагідро-2Н-ізоіндол-2-іл]циклопент-2-ен-1-он (2H, м), 7,05 (2H, м), 4,23-4,15 (2H, м), 3,90-3,80 У розчин 12,3мг (0,26ммоль) (3aR,4R,5S,7aR)(3H, м), 3,32 (1H, тд, J1=13,0Гц, J2=4,0Гц), 3,21 (1H, 5-{(1R)-1-[3,5-біс(трифторметил)феніл]етокси}-4т, J=12,9Гц), 2,68 (2H, м), 2,55 (1H, м), 2,07 (1H, м), (4-фторфеніл)октагідро-1Н-ізоіндолу (Приклад 2) в 1,30 (3H, т, J=7,2Гц), 0,85 (3H, т, J=7,2Гц). ~2мл сухого толуолу додавали 2,7мг (0,028ммоль) Етап C: Рацемічний діетил-(1S,2S,3R,4S)-3-(4циклопентан-1,3-діону і каталітичну кількість фтор феніл)-4-гідроксициклогексан-1,2(~0,5мг) PTSA. Суміш, що виходила, нагрівали із дикарбоксилат і діетил-(1R,2R,3S,4R)-3-(4зворотним холодильником протягом 16 годин. фтор феніл)-4-гідроксициклогексан-1,2Розчинник видаляли у вакуумі і залишок очищали дикарбоксилат з допомогою препаративної ТШХ з елюцією У розчин 40,2г (119,3ммоль) інтермедіату етаEtOAc/МеОН (95/5) для отримання сполуки відпопу В в 150мл етанолу в атмосфері азоту при -78°С 1 відно до заголовка. H ЯМР (CDCl3): d: 7,73 (1H, с), додавали 4,1г (108,5ммоль) порошки NaBH4. Су7,20 (2H, с), 7,03-6,90 (2H, м), 4,98, 4,80 (1H, с), міш, що ви ходила, перемішували при -78°C протя4,50 (1H, м), 3,62-3,18 (2H, м), 3,30-3,18 (3H, м), гом 0,5 години, потім при кімнатній температурі 3,15, 2,97 (1H, д, J=11,2Гц), 2,68 (2H, м), 2,55-2,40 протягом 2 годин. Реакційну суміш акуратно гаси(4H, м), 2,17 (1H, м), 2,20 (1H, м), 2,00 (1H, м), 1,85 ли шляхом додавання 30мл води і акуратно підки(1H, м), 1,62 (1H, м), 1,33 (3H, д, J=6,2Гц). MS: сляли 2н водн. HCl. Розчинник випарювали у ваку+ (MH) 556,0. умі. Залишок розчиняли в ефірі, переносили в Приклад 6 ділильну лійку, промивали з насич. водн. NaHCO3 і сольовим розчином, сушили над осушувачем, фільтрували і випарювали розчинник у вакуумі для отримання необроблених сполук відповідно до заголовка, які очищали на наступному етапі. 1H ЯМР (CDCl3): d: 7,25 (2H, м), 7,05 (2H, т, J=8,2Гц), 4,20-4,05 (2H, м), 3,85-3,72 (3H, м), 2,85 (2H, м), 2,70 (1H, т, J=7,8Гц), 2,25 (2H, м), 1,70 (1H, м), 1,60 (1H, м), 1,25 (3H, т, J=7,2Гц), 0,85 (3H, т, J=7,2Гц). Етап D: Діетил-(1S,2S,3R,4S)-3-(4фтор феніл>4-гідроксициклогексан-1,2(3aR,4R,5S,7aR)-5-{(1R)-1-[3,5дикарбоксилат біс(трифторметил)феніл]етокси}-4-(4-фторфеніл)Починаючи з 21г рацемічної суміші діетилоктагідро-1Н-ізоіндол (1S,2S,3R,4S)-3-(4-фторфеніл)-4Етап A: Діетил-4-{[третгідроксициклогексан-1,2-дикарбоксилату і діетилбутил(диметил)силіл]окси}-3-(4(1R,2R,3S,4R)-3-(4-фторфеніл)-4фтор феніл)циклогекс-4-ен-1,2-дикарбоксилат гідроксициклогексан-1,2-дикарбоксилату (етап C), У розчин 37г (чистий на ~80%, 133,1ммоль, їх розділяли з допомогою препаративної хіральної 1еквів.) 1E і 1Z-трет-бутил-{[1-(4ВЕРХ із застосуванням колонки CHIRACEL AD з фторбензиліден)проп-2-ен-1елюцією гептанами/i-PrOH (9/1) для отримання іл]окси}диметилсилану (Приклад 1, етап C) і 17мл 9,09г необхідного першого елюйованого ізомеру (18г, 104,6ммоль) діетил (2Е)-бут-2-ендіоату в діетил-(1S,2S,3R,4S)-3-(4-фторфеніл)-4200мл ксилолів в атмосфері азоту нагрівали при гідроксициклогексан-1,2-дикарбоксилату. 160°C протягом 5год., потім охолоджували до кімЕтап E: (1S)-1-[3,5натної температури. Розчинник випарювали у вабіс(трифторметил)феніл]етил-2,2,2куумі для отримання маслянистої рідини, яку витрихлоретанімідоат користовували без додаткового очищення. Розчин 25,82г (100ммоль) (1S)-1-[3,5Етап В: Рацемічний діетил-(1S,2S,3R)-3-(4біс(трифторметил)феніл]етанолу в 200мл сухого фтор феніл)-4-оксоциклогексан-1,2-дикарбоксилат і діетилового ефіру в атмосфері азоту о холоджувадіетил-(1R,2R,3S)-3-(4-фторфеніл)-4ли у льоду/водяній бані. У реакційну колбу додаоксоциклогексан-12-дикарбоксилат вали 3мл (20ммоль, 0,2еквів.) чистого DBU, потім У розчин наведеного вище інтермедіату в суміш перемішували при 0°C протягом десяти хв. 30мл ацетонітрилу ватмосфері азоту при кімнатПовільно додавали по краплях 15мл (150ммоль, ній температурі в пластиковій реакційній колбі до1,5еквів.) трихлорацетонітрилу протягом більше давали 200мл (500ммоль) 2,5M розчину HF в аце15хв. Реакцію перемішували при 0°C протягом 2 35 84192 36 годин, за цей час вона стала насиченого жовтого Етап Н: [(1S,2R,3R,4S)-4-{(1R)-1-[3,5кольору. Летючі речовини видаляли у вакуумі із біс(трифторметил)феніл]етокси}-3-(4застосуванням холодної ванни (
ДивитисяДодаткова інформація
Назва патенту англійськоюHydroisoindoline tachykinin receptor antagonists
Автори англійськоюBunda Jaime Lynn, Devita Robert J., Jiang Jinlong, Mills Sander G.
Назва патенту російськоюГидроизоиндолиновые антагонисты рецептора тахикинина
Автори російськоюБунда Джайме Линн, Девита Роберт Дж., Цзян Цзиньлун, Миллз Сандер Г.
МПК / Мітки
МПК: A61P 25/00, A61K 31/4035, C07D 209/44
Мітки: тахікініну, рецептора, антагоністи, гідроізоіндолінові
Код посилання
<a href="https://ua.patents.su/22-84192-gidroizoindolinovi-antagonisti-receptora-takhikininu.html" target="_blank" rel="follow" title="База патентів України">Гідроізоіндолінові антагоністи рецептора тахікініну</a>
Попередній патент: Засіб з ноотропною та антихолінестеразною дією
Наступний патент: Спосіб виробництва оцтової кислоти
Випадковий патент: Блоковані поліізоціанати для тепло- та термостійких матеріалів