Похідні фенетаноламіну для лікування респіраторних хвороб, спосіб їх одержання (варіанти), проміжні сполуки, фармацевтична композиція, комбінація та спосіб профілактики чи лікування стану, для якого показано се
Номер патенту: 76443
Опубліковано: 15.08.2006
Автори: Мур Ребекка Джейн, Лукер Брайан Едґар, Едні Дін Дейвід, Монтіт Майкл Джон, Коу Дайан Мері, антріп Стівен Баррі, Голтон Абіґейл, Біґґадайк Кіт, Пател Раджнікант, Прокопіу Панайотіс Александру
Формула / Реферат
1. Сполука формули (І)
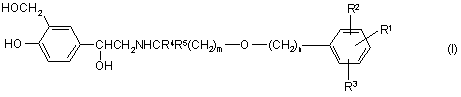
або її сіль або сольват, в яких
m є цілим числом від 2 до 8;
n є цілим числом від 3 до 11;
за умови, що m + n є від 5 до 19;
R1 є -ХSО2NR6R7,
де Х є -(СН2)Р- або С2-6 алкенілен;
R6 та R7, кожний незалежно, вибрано з групи, що складається з гідрогену, С1-6 алкілу, С3-7циклоалкілу, С(О)NR8R9, фенілу та феніл(С1-4алкіл)-,
або R6 та R7, разом з атомом нітрогену, до якого вони приєднані, утворюють 5-, 6- або 7-членне нітрогеновмісне кільце,
та R6 та R7, кожний, як варіант, заміщений одним або двома замісниками, вибраними з групи, що складається з атома галогену, С1-6алкілу, С1-6галогеналкілу, С1-6алкоксилу, гідроксизаміщеного С1-6алкоксилу, -СО2R8, -SО2NR8R9, -СОNR8R9, -NR8С(О)R9 або 5-, 6- або 7-членного гетероциклічного кільця;
R8 та R9 незалежно вибрано з групи, що складається з атома гідрогену, С1-6алкілу, С3-6циклоалкілу, фенілу та феніл(С1-4алкіл)-; та
р є цілим числом від 0 до 6;
R2 та R3 незалежно вибрано з групи, що складається з атома гідрогену, С1-6алкілу, С1-6алкоксилу, атома галогену, фенілу та С1-6галогеналкілу; та
R4 та R5 незалежно вибрано з групи, що складається з атома гідрогену та С1-4алкілу, за умови, що загальне число атомів карбону у R4 та R5 не перевищує 4.
2. Сполука формули (І) за п. 1 або її сіль або сольват, в яких групу R1 приєднано до мета-позиції відносно зв'язку –O-(CH2)n.
3. Сполука формули (І) за п. 1 або 2 або її сіль або сольват, в яких група R1 є -SО2NR6R7, де R6 та R7 незалежно вибрано з групи, що складається з гідрогену та С1-6алкілу.
4. Сполука формули (І) за будь-яким з пп. 1-3 або її сіль або сольват, в яких R1 є -SО2NН2.
5. Сполука формули (І) за будь-яким з пп. 1-4 або її сіль або сольват, в яких обидва R4 та R5 є гідроген.
6. Сполука формули (І) за будь-яким з пп. 1-5 або її сіль або сольват, в яких m є 5 або 6, а n є 3 або 4 за умови, що m + n є 8, 9 або 10.
7. Сполука формули (Іа):
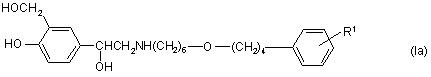
або її сіль або сольват, в яких
R1 визначено у п. 1 для формули (І).
8. Сполука формули (Іа) за п. 7 або її сіль або сольват, в яких R1 є -SО2NR6R7, де R6 та R7 незалежно вибрано з групи, що складається з гідрогену та С1-6алкілу.
9. Сполука формули (Іа) за п. 7 або 8 або її сіль або сольват, в яких R1 є SО2NН2.
10. Сполука формули (Іа) за будь-яким з пп. 7-9 або її сіль або сольват, в яких R1 приєднано до мета-позиції відносно зв'язку –O-(CH2)4.
11. Сполука формули (Іb):
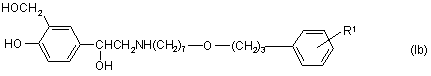
або її сіль або сольват, в яких R1 визначено у п. 1 для формули (І).
12. Сполука формули (Іb) за п. 11 або її сіль або сольват, в яких R1 є -SО2NR6R7, де R6 та R7 незалежно вибрано з групи, що складається з гідрогену та С1-6алкілу.
13. Сполука формули (Іb) за п. 11 або 12 або її сіль або сольват, в яких R1 є SО2NН2.
14. Сполука формули (Іb) за будь-яким з пп. 11-13 або її сіль або сольват, в яких R1 приєднано до мета-позиції відносно зв'язку –O-(CH2)3.
15. Сполука формули (І) або (Іа) за п. 1 або 7, якою є 3-(4-{[6-({(2R)2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гексил]окси}бутил)бензолсульфонамід, або її сіль або сольват.
16. Сполука формули (І) або (Іа) за п. 1 або 7, якою є 3-(4-{[6-({(2S)2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гексил]окси}бутил)бензолсульфонамід, або її сіль або сольват.
17. Сполука формули (І) або (Іа) за п. 1 або 7, якою є 3-(4-{[6-({(2R/S)2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гексил]окси}бутил)бензолсульфонамід, або її сіль або сольват.
18. Сполука формули (І) або (Іb) за п. 1 або 11, якою є 3-(3-{[7-({(2R)-2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гептил]окси}пропіл)бензолсульфонамід, або її сіль або сольват.
19. Сполука формули (І) або (Іb) за п. 1 або 11, якою є 3-(3-{[7-({(2S)-2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гептил]окси}пропіл)бензолсульфонамід, або її сіль або сольват.
20. Сполука формули (І) або (Іb) за п. 1 або 11, якою є 3-(3-{[7-({(2R/S)-2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гептил]окси}пропіл)бензолсульфонамід, або її сіль або сольват.
21. Сполука за будь-яким з пп. 1-20, сіль або сольват якої є фармацевтично прийнятними.
22. Сполука за будь-яким з пп. 1-21, яка має форму солі, утвореної з фармацевтично прийнятної кислоти, вибраної з групи, що складається з цинамової, заміщеної цинамової, трифенілоцтової, сульфамової, сульфанілової, нафталінакрилової, бензойної, 4-метоксибензойної, 2- або 4-гідроксибензойної, 4-хлорбензойної та 4-фенілбензойної кислот.
23. Сполука за п. 15, якою є цинамат 3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гексил]окси}бутил)бензолсульфонаміду.
24. Сполука за п. 15, якою є 1-гідроксинафтоат 3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гексил]окси}бутил)бензолсульфонаміду.
25. Сполука за п. 15, якою є 4-фенілбензоат 3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гексил]окси}бутил)бензолсульфонаміду.
26. Сполука за п. 15, якою є трифенілацетат 3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гексил]окси}бутил)бензолсульфонаміду.
27. Сполука за п. 15, якою є 4-метилцинамат 3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гексил]окси}бутил)бензолсульфонаміду.
28. Сполука за п. 15, якою є 4-метоксицинамат 3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гексил]окси}бутил)бензолсульфонаміду.
29. Сполука за п. 15, якою є 3-(2-нафталініл)-2-пропаноатова сіль 3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гексил]окси}бутил)бензолсульфонаміду.
30. Сполука за п. 18, якою є (Е)-3-(нафталін-2-іл)-2-пропеноат 3-(3-{[7-({(2R)-2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гептил]окси}пропіл)бензолсульфонаміду.
31. Сполука за п. 18, якою є 4-фенілбензоат 3-(3-{[7-({(2R)-2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гептил]окси}пропіл)бензолсульфонаміду.
32. Сполука за п. 18, якою є трифенілацетат 3-(3-{[7-({(2R)-2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гептил]окси}пропіл)бензолсульфонаміду.
33. Сполука за п. 18, якою є 4-фенілціанамат 3-(3-{[7-({(2R)-2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гептил]окси}пропіл)бензолсульфонаміду.
34. Сполука за п. 18, якою є сульфамат 3-(3-{[7-({(2R)-2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гептил]окси}пропіл)бензолсульфонаміду.
35. Сполука за п. 18, якою є сульфанілат 3-(3-{[7-({(2R)-2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гептил]окси}пропіл)бензолсульфонаміду.
36. Спосіб профілактики чи лікування клінічного стану у ссавця, наприклад людини, для якого показано селективний агоніст ![]() -адренорецептора, при якому застосовують терапевтично ефективну кількість сполуки формули (І), (Іа) або (Іb) за будь-яким з пп. 1–35, або її фармацевтично прийнятної солі або сольвату.
-адренорецептора, при якому застосовують терапевтично ефективну кількість сполуки формули (І), (Іа) або (Іb) за будь-яким з пп. 1–35, або її фармацевтично прийнятної солі або сольвату.
37. Сполука формули (І), (Іа) або (Іb) за будь-яким з пп. 1–35 або її фармацевтично прийнятна сіль або сольват для застосування у медичній терапії.
38. Фармацевтична композиція, що містить сполуку формули (І), (Іа) або (Іb) за будь-яким з пп. 1–35 або її фармацевтично прийнятну сіль або сольват та фармацевтично прийнятний носій або ексципієнт.
39. Комбінація, що містить сполуку формули (І), (Іа) або (Іb) за будь-яким з пп. 1–35 або її фармацевтично прийнятну сіль або сольват та один або більше інших терапевтичних інгредієнтів.
40. Комбінація за п. 39, де іншим терапевтичним інгредієнтом є інгібітор РDЕ4, або антихолінергічний засіб, або кортикостероїд.
41. Комбінація за п. 39, що містить сполуку формули (І), (Іа) або (Іb) за будь-яким з пп. 1–35 або її фармацевтично прийнятну сіль або сольват та S-флуорметиловий естер ![]() ,
, ![]() -дифлуор-
-дифлуор-![]() -[(2-фуранілкарбоніл)окси]-
-[(2-фуранілкарбоніл)окси]-![]() -гідрокси-
-гідрокси-![]() -метил-3-оксоандроста-1,4-дієн-
-метил-3-оксоандроста-1,4-дієн-![]() -карботіонової кислоти.
-карботіонової кислоти.
42. Комбінація за п. 41, в якій сполукою формули (І) є 3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гексил]окси}бутил)бензолсульфонамід або її сіль або сольват.
43. Комбінація за п. 41, в якій сполукою формули (І) є 3-(3-{[7-({(2R)-2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гептил]окси}пропіл)бензолсульфонамід або її сіль або сольват.
44. Комбінація за п. 39, що містить сполуку формули (І), (Іа) або (Іb) за будь-яким з пп. 1–35 або її фармацевтично прийнятну сіль або сольват та S-флуорметиловий естер ![]() ,
, ![]() -дифлуор-
-дифлуор-![]() -гідрокси-
-гідрокси-![]() -метил
-метил ![]() -[(4-метил-1,3-тіазол-5-карбоніл)окси]-3-оксоандроста-1,4-дієн-
-[(4-метил-1,3-тіазол-5-карбоніл)окси]-3-оксоандроста-1,4-дієн-![]() -карботіонової кислоти.
-карботіонової кислоти.
45. Комбінація за п. 44, в якій сполукою формули (І) є 3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гексил]окси}бутил)бензолсульфонамід або її сіль або сольват.
46. Комбінація за п. 44, в якій сполукою формули (І) є 3-(3-{[7-({(2R)-2-гідрокси-2-[4-гідрокси-3-(гідроксиметил)феніл]етил}аміно)гептил]окси}пропіл)бензолсульфонамід або її сіль або сольват.
47. Сполука формули (І), (Іа) або (Іb) за будь-яким з пп. 1–35 або її фармацевтично прийнятна сіль або сольват, яку призначено для виробництва медикаменту для профілактики чи лікування клінічного стану, для якого показано селективний агоніст ![]() -адренорецептора.
-адренорецептора.
48. Спосіб отримання сполуки формули (І), (Іа) або (Іb) за будь-яким з пп. 1–35 або її солі або сольвату, який полягає в тому, що
(а) знімають захист із захищеного інтермедіату, наприклад формули (ІІ)
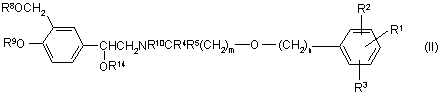 ,
,
або його солі або сольвату, де R1, R2, R3, R4, R5, m та n визначено для сполуки формули (І), (Іа) або (Іb), а групи R8, R9 та R10 кожна окремо є атомом гідрогену або захисною групою, за умови, що щонайменше одна з груп R8, R9 та R10 є захисною групою, а R14 є атомом гідрогену або захисною групою;
(б) після чого у будь-якому порядку
(і) довільно видаляють будь-яку захисну групу,
(іі) із суміші енантіомерів довільно відділяють будь-який енантіомер,
(ііі) продукт довільно перетворюють у його відповідну сіль або сольват.
49. Спосіб отримання сполуки формули (І), (Іа) або (Іb) за будь-яким з пп. 1–35 або її солі або сольвату, який полягає в тому, що
(а) алкілують амін формули (ХІІ)
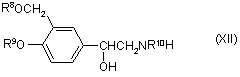 ,
,
де групи R8 та R9 та R10 кожна окремо є атомом гідрогену або захисною групою,
сполукою формули (ХІІІ)
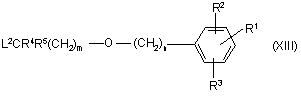 ,
,
де R1, R2, R3, R4, R5, m та n визначено для сполуки формули (І) або (Іа), а L2 є відхідною групою;
(б) після чого у будь-якому порядку
(і) довільно видаляють будь-яку захисну групу,
(іі) із суміші енантіомерів довільно відділяють будь-який енантіомер,
(ііі) продукт довільно перетворюють у його відповідну сіль або сольват.
50. Спосіб отримання сполуки формули (І), (Іа) або (Іb) за будь-яким з пп. 1–35 або її фармацевтично прийнятної солі або сольвату, який полягає в тому, що
(а) сполуку формули (ХVІІ):
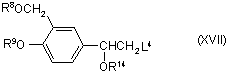 ,
,
де R8, R9 та R14 визначено у п. 48, а L4 є відхідною групою,
уводять у реакцію з аміном формули (ХVІІІ):
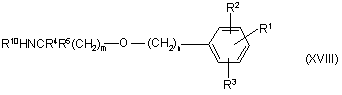 ,
,
де R1 - R5, R10, m та n визначено у п. 48,
(б) після чого у будь-якому порядку
(і) довільно видаляють будь-яку захисну групу,
(іі) із суміші енантіомерів довільно відділяють будь-який енантіомер,
(ііі) продукт довільно перетворюють у його відповідну сіль або сольват.
51. Спосіб отримання сполуки формули (І), (Іа) або (Іb) за будь-яким з пп. 1–35 або її солі або сольвату, який полягає в тому, що
(а) видаляють хіральний допоміжник зі сполуки формули (ІІа):
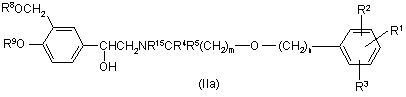 ,
,
де R1 - R5, R8, R9, m та n визначено вище, а R15 є хіральним допоміжником;
(б) після чого у будь-якому порядку
(і) довільно видаляють будь-яку захисну групу,
(іі) із суміші енантіомерів довільно відділяють будь-який енантіомер,
(ііі) продукт довільно перетворюють у його відповідну сіль або сольват.
52. Проміжні сполуки, вибрані з сполук формул (ІІ), (ІІІ) та (IV):
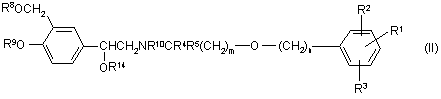 ,
,
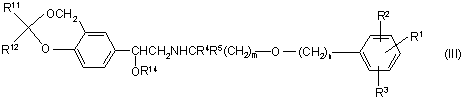 ,
,
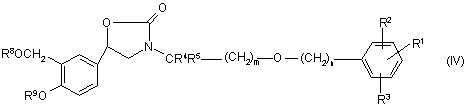 ,
,
де R1, R2, R3, R4, R5, R8, R9, R10 та R14, m та n визначено у п. 47, а R11 та R12 незалежно вибрано з групи, що складається з гідрогену, С1-6алкілу або арилу.
Текст
1. Сполука формули (І) C2 2 (19) 1 3 76443 4 заміщеної цинамової, трифенілоцтової, сульфамоR1 вої, сульфанілової, нафталінакрилової, бензойної, 4HO CHCH2NH(CH2)6 O (CH2)4 (Ia) метоксибензойної, 2- або 4-гідроксибензойної, 4OH хлорбензойної та 4-фенілбензойної кислот. 23. Сполука за п. 15, якою є цинамат 3-(4-{[6або її сіль або сольват, в яких ({(2R)-2-гідрокси-2-[4-гідрокси-31 R визначено у п. 1 для формули (І). (гідроксиме8. Сполука формули (Іа) за п. 7 або її сіль або сольтил)феніл]етил}аміно)гексил]окси}бутил)бензолсул 1 6 7 6 7 ват, в яких R є -SО2NR R , де R та R незалежно ьфонаміду. вибрано з групи, що складається з гідрогену та С124. Сполука за п. 15, якою є 1-гідроксинафтоат 36алкілу. (4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-39. Сполука формули (Іа) за п. 7 або 8 або її сіль або (гідроксимесольват, в яких R1 є SО2NН2. тил)феніл]етил}аміно)гексил]окси}бутил)бензолсул 10. Сполука формули (Іа) за будь-яким з пп. 7-9 або ьфонаміду. її сіль або сольват, в яких R1 приєднано до мета25. Сполука за п. 15, якою є 4-фенілбензоат 3-(4позиції відносно зв'язку –O-(CH2)4. {[6-({(2R)-2-гідрокси-2-[4-гідрокси-311. Сполука формули (Іb): (гідроксимеHOCH2 тил)феніл]етил}аміно)гексил]окси}бутил)бензолсул 1 R ьфонаміду. HO CHCH2NH(CH2)7 O (CH2)3 (Ib) 26. Сполука за п. 15, якою є трифенілацетат 3-(4OH {[6-({(2R)-2-гідрокси-2-[4-гідрокси-3або її сіль або сольват, в яких R1 визначено у п. 1 (гідроксимедля формули (І). тил)феніл]етил}аміно)гексил]окси}бутил)бензолсул 12. Сполука формули (Іb) за п. 11 або її сіль або соьфонаміду. льват, в яких R1 є -SО2NR6R7, де R6 та R7 незалеж27. Сполука за п. 15, якою є 4-метилцинамат 3-(4но вибрано з групи, що складається з гідрогену та {[6-({(2R)-2-гідрокси-2-[4-гідрокси-3С1-6алкілу. (гідроксиме13. Сполука формули (Іb) за п. 11 або 12 або її сіль тил)феніл]етил}аміно)гексил]окси}бутил)бензолсул або сольват, в яких R1 є SО2NН2. ьфонаміду. 14. Сполука формули (Іb) за будь-яким з пп. 11-13 28. Сполука за п. 15, якою є 4-метоксицинамат 3або її сіль або сольват, в яких R1 приєднано до мета(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3позиції відносно зв'язку –O-(CH2)3. (гідроксиме15. Сполука формули (І) або (Іа) за п. 1 або 7, якою тил)феніл]етил}аміно)гексил]окси}бутил)бензолсул є 3-(4-{[6-({(2R)2-гідрокси-2-[4-гідрокси-3ьфонаміду. (гідроксиме29. Сполука за п. 15, якою є 3-(2-нафталініл)-2тил)феніл]етил}аміно)гексил]окси}бутил)бензолсул пропаноатова сіль 3-(4-{[6-({(2R)-2-гідрокси-2-[4ьфонамід, або її сіль або сольват. гідрокси-316. Сполука формули (І) або (Іа) за п. 1 або 7, якою (гідроксимеє 3-(4-{[6-({(2S)2-гідрокси-2-[4-гідрокси-3тил)феніл]етил}аміно)гексил]окси}бутил)бензолсул (гідроксимеьфонаміду. тил)феніл]етил}аміно)гексил]окси}бутил)бензолсул 30. Сполука за п. 18, якою є (Е)-3-(нафталін-2-іл)ьфонамід, або її сіль або сольват. 2-пропеноат 3-(3-{7-({(2R)-2-гідрокси-2-4-гідрокси17. Сполука формули (І) або (Іа) за п. 1 або 7, якою 3є 3-(4-{[6-({(2R/S)2-гідрокси-2-[4-гідрокси-3(гідроксиме(гідроксиметил)фенілетил}аміно)гептилокси}пропіл)бензолсу тил)феніл]етил}аміно)гексил]окси}бутил)бензолсул льфонаміду. ьфонамід, або її сіль або сольват. 31. Сполука за п. 18, якою є 4-фенілбензоат 3-(318. Сполука формули (І) або (Іb) за п. 1 або 11, якою є 3-(3-{[7-({(2R)-2-гідрокси-2-[4-гідрокси-3{7-({(2R)-2-гідрокси-2-4-гідрокси-3(гідроксиме(гідроксиметил)феніл]етил}аміно)гептил]окси}пропіл)бензолсу тил)фенілетил}аміно)гептилокси}пропіл)бензолсу льфонамід, або її сіль або сольват. льфонаміду. 19. Сполука формули (І) або (Іb) за п. 1 або 11, 32. Сполука за п. 18, якою є трифенілацетат 3-(3якою є 3-(3-{[7-({(2S)-2-гідрокси-2-[4-гідрокси-3{7-({(2R)-2-гідрокси-2-4-гідрокси-3(гідроксиме(гідроксиметил)феніл]етил}аміно)гептил]окси}пропіл)бензолсу тил)фенілетил}аміно)гептилокси}пропіл)бензолсу льфонамід, або її сіль або сольват. льфонаміду. 20. Сполука формули (І) або (Іb) за п. 1 або 11, 33. Сполука за п. 18, якою є 4-фенілціанамат 3-(3якою є 3-(3-{[7-({(2R/S)-2-гідрокси-2-[4-гідрокси-3{7-({(2R)-2-гідрокси-2-4-гідрокси-3(гідроксиме(гідроксиметил)феніл]етил}аміно)гептил]окси}пропіл)бензолсу тил)фенілетил}аміно)гептилокси}пропіл)бензолсу льфонамід, або її сіль або сольват. льфонаміду. 21. Сполука за будь-яким з пп. 1-20, сіль або сольват 34. Сполука за п. 18, якою є сульфамат 3-(3-{7якої є фармацевтично прийнятними. ({(2R)-2-гідрокси-2-4-гідрокси-322. Сполука за будь-яким з пп. 1-21, яка має форму (гідроксимесолі, утвореної з фармацевтично прийнятної кислоти, вибраної з групи, що складається з цинамової, HOCH2 5 76443 6 47. Сполука формули (І), (Іа) або (Іb) за будь-яким тил)фенілетил}аміно)гептилокси}пропіл)бензолсу з пп. 1–35 або її фармацевтично прийнятна сіль льфонаміду. або сольват, яку призначено для виробництва 35. Сполука за п. 18, якою є сульфанілат 3-(3-{7медикаменту для профілактики чи лікування кліні({(2R)-2-гідрокси-2-4-гідрокси-3чного стану, для якого показано селективний аго(гідроксименіст 2 -адренорецептора. тил)фенілетил}аміно)гептилокси}пропіл)бензолсу льфонаміду. 48. Спосіб отримання сполуки формули (І), (Іа) 36. Спосіб профілактики чи лікування клінічного або (Іb) за будь-яким з пп. 1–35 або її солі або стану у ссавця, наприклад людини, для якого покасольвату, який полягає в тому, що зано селективний агоніст 2 -адренорецептора, при (а) знімають захист із захищеного інтермедіату, наприклад формули (ІІ) якому застосовують терапевтично ефективну кільR8OCH2 R2 кість сполуки формули (І), (Іа) або (Іb) за будьR1 яким з пп. 1–35, або її фармацевтично прийнятної R9 O (CH2)n CHCH2NR10CR4R5(CH2)m O (II) солі або сольвату. OR14 37. Сполука формули (І), (Іа) або (Іb) за будь-яким R3 , з пп. 1–35 або її фармацевтично прийнятна сіль або сольват для застосування у медичній терапії. або його солі або сольвату, де R1, R2, R3, R4, R5, m та n 38. Фармацевтична композиція, що містить сповизначено для сполуки формули (І), (Іа) або (Іb), а луку формули (І), (Іа) або (Іb) за будь-яким з групи R8, R9 та R10 кожна окремо є атомом гідрогену пп. 1–35 або її фармацевтично прийнятну сіль або або захисною групою, за умови, що щонайменше одна сольват та фармацевтично прийнятний носій або з груп R8, R9 та R10 є захисною групою, а R14 є атомом ексципієнт. гідрогену або захисною групою; 39. Комбінація, що містить сполуку формули (І), (б) після чого у будь-якому порядку (Іа) або (Іb) за будь-яким з пп. 1–35 або її фарма(і) довільно видаляють будь-яку захисну групу, цевтично прийнятну сіль або сольват та один або (іі) із суміші енантіомерів довільно відділяють більше інших терапевтичних інгредієнтів. будь-який енантіомер, 40. Комбінація за п. 39, де іншим терапевтичним (ііі) продукт довільно перетворюють у його відпоінгредієнтом є інгібітор РDЕ4, або антихолінергічвідну сіль або сольват. ний засіб, або кортикостероїд. 49. Спосіб отримання сполуки формули (І), (Іа) 41. Комбінація за п. 39, що містить сполуку форабо (Іb) за будь-яким з пп. 1–35 або її солі або мули (І), (Іа) або (Іb) за будь-яким з пп. 1–35 або її сольвату, який полягає в тому, що фармацевтично прийнятну сіль або сольват та S(а) алкілують амін формули (ХІІ) флуорметиловий естер 6 , 9 -дифлуор- 17 R8OCH2 [(2-фуранілкарбоніл)окси]- 11 -гідрокси- 16 (XII) метил-3-оксоандроста-1,4-дієн- 17 R9 O CHCH2NR10H карботіонової кислоти. OH , 42. Комбінація за п. 41, в якій сполукою формули де групи R8 та R9 та R10 кожна окремо є атомом гідро(І) є 3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3гену або захисною групою, (гідроксимесполукою формули (ХІІІ) тил)феніл]етил}аміно)гексил]окси}бутил)бензолсул R2 ьфонамід або її сіль або сольват. R1 43. Комбінація за п. 41, в якій сполукою формули O (CH2)n L2CR4R5(CH2)m (XIII) (І) є 3-(3-{7-({(2R)-2-гідрокси-2-4-гідрокси-3(гідроксиметил)фенілетил}аміно)гептилокси}пропіл)бензолсу R3 , льфонамід або її сіль або сольват. 1 2 3 4 5 де R , R , R , R , R , m та n визначено для сполуки 44. Комбінація за п. 39, що містить сполуку форформули (І) або (Іа), а L2 є відхідною групою; мули (І), (Іа) або (Іb) за будь-яким з пп. 1–35 або її (б) після чого у будь-якому порядку фармацевтично прийнятну сіль або сольват та S(і) довільно видаляють будь-яку захисну групу, флуорметиловий естер 6 , 9 -дифлуор- 11 (іі) із суміші енантіомерів довільно відділяють гідрокси- 16 -метил 17 -[(4-метил-1,3-тіазол-5будь-який енантіомер, карбоніл)окси]-3-оксоандроста-1,4-дієн- 17 (ііі) продукт довільно перетворюють у його відповідну сіль або сольват. карботіонової кислоти. 50. Спосіб отримання сполуки формули (І), (Іа) 45. Комбінація за п. 44, в якій сполукою формули або (Іb) за будь-яким з пп. 1–35 або її фармацев(І) є 3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3тично прийнятної солі або сольвату, який полягає (гідроксимев тому, що тил)феніл]етил}аміно)гексил]окси}бутил)бензолсул (а) сполуку формули (ХVІІ): ьфонамід або її сіль або сольват. R8OCH2 46. Комбінація за п. 44, в якій сполукою формули (І) є 3-(3-{7-({(2R)-2-гідрокси-2-4-гідрокси-3(XVII) R9 O (гідроксимеCHCH2 L4 тил)фенілетил}аміно)гептилокси}пропіл)бензолсу OR14 , льфонамід або її сіль або сольват. 7 76443 8 де R8, R9 та R14 визначено у п. 48, а L4 є відхідною (б) після чого у будь-якому порядку групою, (і) довільно видаляють будь-яку захисну групу, уводять у реакцію з аміном формули (ХVІІІ): (іі) із суміші енантіомерів довільно відділяють R2 будь-який енантіомер, R1 (ііі) продукт довільно перетворюють у його відпо(CH2)n R10HNCR4R5(CH2)m O відну сіль або сольват. (XVIII) 52. Проміжні сполуки, вибрані з сполук формул (ІІ), (ІІІ) та (IV): R8OCH2 R3 R2 , 1 5 10 R1 де R - R , R , m та n визначено у п. 48, R9 O (CH2)n CHCH2NR10CR4R5(CH2)m O (II) (б) після чого у будь-якому порядку OR14 (і) довільно видаляють будь-яку захисну групу, R3 , (іі) із суміші енантіомерів довільно відділяють R OCH R будь-який енантіомер, R (ііі) продукт довільно перетворюють у його відпоO R CHCH NHCR R (CH ) O (CH ) (III) відну сіль або сольват. OR R 51. Спосіб отримання сполуки формули (І), (Іа) , O або (Іb) за будь-яким з пп. 1–35 або її солі або O R сольвату, який полягає в тому, що R N R OCH (CH ) (а) видаляють хіральний допоміжник зі сполуки O (CH ) CR R (IV) формули (ІІа): R O R OCH R R , R де R1, R2, R3, R4, R5, R8, R9, R10 та R14, m та n визначеR O O (CH ) CHCH NR CR R (CH ) но у п. 47, а R11 та R12 незалежно вибрано з групи, що OH (IIa) складається з гідрогену, С1-6алкілу або арилу. R , 11 2 2 1 12 4 2 5 2 m 2 n 14 3 2 1 8 8 9 2 2 2 4 5 2 m 2 n 3 1 9 2 15 4 5 2 m 2 n 3 1 5 8 9 де R - R , R , R , m та n визначено вище, а R15 є хіральним допоміжником; Представлений винахід стосується похідних фенетаноламіну, способу їх отримання, композицій, що їх містять та їх застосування у медицині, зокрема при профілактиці та лікуванні респіраторних хвороб. Деякі фенетаноламінові сполуки відомі у рівні техніки як такі, що мають селективну стимулювальну дію на 2-адренорецептори, а тому використовувані при лікуванні бронхіальної астми та споріднених розладів. Так, GB 2140800 описує фенетаноламінові сполуки, що включають 4гідрокси-1-[[[6-(4фенілбутокси)гексил]аміно]метил]-1,3бензолдиметанол 1-гідрокси-2нафталінкарбоксилат (салметерол-ксинафоат), який зараз застосовують клінічно при лікуванні таких медичних станів. Хоч салметерол та інші комерційно доступні агоністи 2-адренорецептору є ефективними бронхорозширювачами, максимум протяжності дії є 12 годин, відтак часто потрібна подвійна добова доза. Тому існує клінічна необхідність у сполуках, що мають потужну та селективну стимулювальну дію на 2-адренорецептори і мають корисний профіль дії. Згідно з представленим винаходом, запропоновано сполуку формули (І) або її сіль, сольват, або фізіологічно функціо нальне похідне, де: m представляє ціле число від 2 до 8; n представляє ціле число від 3 до 11, переважно від 3 до 7; за умови, що m+n дорівнює від 5 до 19, переважно від 5 до 12; R1 представляє -XSO2NR6R7 де X представляє -(СН2)Р- або С2-6алкенілен; R6 та R7 незалежно вибрані з групи: атом гідрогену, С1-6алкіл, С3-7циклоалкіл, C(O)NR8R9, феніл, та феніл(С1-4алкіл)-, або R6 та R7, разом з атомом нітрогену, до якого вони приєднані, утворюють 5-, 6-, або 7членне нітрогено-вмісне кільце, та R6 та R7, кожний, як варіант, заміщені одним або двома замісниками, вибраними з групи, атом галогену, С1-6алкіл, С1-6галогеналкіл, С1-6алкоксил, гідрокси-заміщений С1-6алкоксил, -CO2R8, 8 9 8 9 8 9 SO2NR R , -CONR R , -NR C(O)R , або 5-, 6- або 7-членне гетероциклічне кільце; R8 та R9 незалежно вибрані з групи: атом гідрогену, С1-6алкіл, С3-6циклоалкіл, феніл, та феніл(С1-4алкіл)-; а р представляє ціле число від 0 до 6, переважно від 0 до 4; R2 та R3 незалежно вибрані з групи: атом гідрогену, С1-6алкіл, С1-6алкоксил, атом галогену, феніл, та С1-6галогеналкіл; а R4 та R5 незалежно вибрані з групи: атом гідрогену та С1-4алкіл за умови, що загальне число атомів карбону у R4 та R5 не перевищує 4. У сполуках формули (І) групу R1 переважно приєднано до мета-позиції відносно -О-через (СН2)n-. 9 76443 10 R1 переважно представляє групу -SO2NR6R7 аміно)гексил]окси}бутил)-Nде R6 та R7 незалежно вибрані з групи: атом гідроізопропілбензолсульфонамід; гену та С1-6алкіл, більш переважно R1 представляє N-(трет-бутил)-3-(4-{[6-({(2R)-2-гідрокси-2-[4групу -SO2NH2. гідрокси-3-(гідроксиметил)феніл]R4 та R5 переважно незалежно вибрані з групи етил}аміно)гексил]окси}бутил)бензолсульфонамід; 4 5 атом гідрогену та метил, більш переважно R Ta R 2-(гідроксиметил)-4-{(1R)-1-гідрокси-2-[(6-{4-[3обидва представляють атом гідрогену. (піперидин-1-ілсульфоніл)феніл]m придатно дорівнює 4, 5, або 6, а n придатно бутокси}гексил)аміно]етил}фенол; дорівнює 3, 4, 5 або 6. Переважно m дорівнює 5 1-[3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3або 6, а n дорівнює 3 або 4, так щоб m+n дорівню(гідроксиметил)феніл]етил}аміно)вало 8, 9 або 10, переважно 9. гексил]окси}бутил)феніл]метансульфонамід; Згідно з переважним аспектом винаходу, за3-(5-{[5-({(2R)-2-гідрокси-2-[4-гідрокси-3пропоновано сполуку формули (Іа) (гідроксиметил)феніл]етил}аміно)пентил]окси}пентил)бензолсульфонамід; 3-(3-{[7-({(2R)-2-гідрокси-2-[4-гідрокси-3(гідроксиметил)феніл]етил}аміно)гептил]окси}пропіл)бензолсульфонамід; 3-{6-[4-({(2R)-2-гідрокси-2-[4-гідрокси-3(гідроксиметил)феніл]етил}або її сіль, сольват, або фізіологічно функціоаміно)бутокси]гексил}бензолсульфонамід; нальне похідне, де R1 визначено вище для фор4-[3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3мули (І). (гідроксиметил)феніл]етил}Згідно з наступним переважним аспектом виаміно)гексил]окси}бутил)феніл]бутан-1находу, запропоновано сполуку формули (Іb) сульфонамід; 3-(5-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3(гідроксиметил)феніл]етил}аміно)гексил]окси}пентил)бензолсульфонамід; 3-(6-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3(гідроксиметил)феніл]етил}аміно)гексил]окси}гексил)бензолсульфонамід; або її сіль, сольват, або фізіологічно функціо3-(3-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3нальне похідне, де (гідроксиметил)феніл]етил}1 R визначено вище для формули (І). аміно)гексил]окси}пропіл)бензолсульфонамід; У сполуках формул (Іа) та (Іb), групу R1 пере3-(4-{[5-({(2R)-2-гідрокси-2-[4-гідрокси-3важно приєднано у мета-позиції відносно зв'язку (гідроксиметил)феніл]етил}аміно)пентил]О-(СН2)n-, -О-(СН2)4- або -О-(СН2)3-, відповідно. окси}бутил)бензолсульфонамід; У сполуках формул (Іа) та (Ib), R1 переважно 1-[2-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-36 7 6 7 представляє -SO2NR R де-R та R незалежно (гідроксимевибрані з групи: атом гідрогену та С1-6алкіл, більш тил)феніл]етил}аміно)гексил]окси}бутил)феніл]мет переважно R1 представляє -SO2NH2. ансульфонамід; Слід розуміти, що представлений винахід охо1-[4-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3плює усі комбінації певних та переважних груп, (гідроксиметил)феніл]етил}аміно)гексил]описаних вище. окси}бутил)феніл]метансульфонамід; Кращі сполуки винаходу включають: N-[3-(aмiнocyльфoнiл)фeнiл]-3-(4-{[6-({(2R)-23-(4-{[6-({(2R)-гідрокси-2-[4-гідрокси-3гiдpoкcи-2-[4-гiдpoкcи-3(гідроксиметил)феніл]етил} (гідроксимеаміно)гексил]окси}бутил)бензолсульфонамід; тил)феніл]етил}аміно)гексил]окси}бутил)бензолсул 4-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3ьфонамід; (гідроксиметил)феніл]етил}N-бензил-3-(4-{[6-({(2R)-2-гідрокси-2-[4аміно)гексил]окси}бутил)бензолсульфонамід; гідрокси-3-(гідроксиметил)феніл]етил}2-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3аміно)гексил]окси}бутил)бензолсульфонамід; (гідроксиметил)феніл]етил}4-{(1R)-2-[(6-{4-[3аміно)гексил]окси}бутил)бензолсульфонамід; ({[(етиламі3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3но)карбоніл]аміно}сульфоніл)феніл]бутокси}гексил (гідроксиметил)феніл]етил})аміно]-1-гідроксіетил}-1-гідрокси-2аміно)гексил]окси}бутил)-N(гідроксиметил)бензол; метилбензолсульфонамід; 3-(4-{[6-({2-гідрокси-2-[4-гідрокси-32-(гідроксиметил)-4-{(1R)-1-гідрокси-2-[(6-{4-[3(гідроксиметил)феніл]етил}аміно)гексил]окси}(морфолін-4-ілсульфоніл)бутил)бензолсульфонамід; феніл]бутокси}гексил)аміно]етил}фенол; 3-(4-{[6-({(2S)-2-гідрокси-2-[4-гідрокси-33-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3(гідроксиметил)феніл]етил}аміно)гексил](гідроксиметил)феніл]етил}окси}бутил)бензолсульфонамід; аміно)гексил]окси}бутил)-N,МN-[4-({[3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3диметилбензолсульфонамід; (гідроксиметил)феніл]етил}3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3амі(гідроксиметил)феніл]етил}но)гексил]окси}бутил)феніл]сульфоніл}аміно)фені 11 76443 12 л]ацетамід нальні похідні. N-циклобутил-3-(4-{[6-({(2R)2-гідрокси-2-[4Зокрема кращі сполуки винаходу включають: гідрокси-3-(гідроксиметил)феніл]3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3етил}аміно)гексил]окси}бутил)бензолсульфонамід; (гідроксиметил)феніл]етил}N-циклогексил-3-(4-{[6-({(2R)-2-гідрокси-2-[4аміно)гексил]окси}бутил)бензолсульфонамід; гідрокси-3-(гідроксиметил)феніл]етил}3-(4-{[6-({(2S)-2-гідрокси-2-[4-гідрокси-3аміно)гексил]окси}бутил)бензолсульфонамід; (гідроксиметил)феніл]етил}3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3аміно)гексил]окси}бутил)бензолсульфонамід; (гідроксиметил)феніл]етил}3-(4-{[6-({(2R/S)-2-гідрокси-2-[4-гідрокси-3аміно)гексил]окси}бутил)-N-(2-морфолін-4(гідроксиметил)феніл]етил}ілетил)бензолсульфонамід; аміно)гексил]окси}бутил)бензолсульфонамід; N-[2-(2-гідроксіетокси)етил]-3-(4-{[6-({(2R)-23-(3-{[7-({(2R)-2-гідрокси-2-[4-гідрокси-3гідрокси-2-[4-гідрокси-3(гідроксиметил)феніл]етил}(гідроксимеаміно)гептил]окси}пропіл)бензолсульфонамід; тил)феніл]етил}аміно)гексил]окси}бутил)бензолсул 3-(3-{[7-({(2S)-2-гідрокси-2-[4-гідрокси-3ьфонамід; (гідроксиметил)феніл]етил}N-(4-флуорфеніл)-3-(4-{[6-({(2R)-2-гідрокси-2аміно)гептил]окси}пропіл)бензолсульфонамід; [4-гідрокси-33-(3-{[7-({(2R/S)-2-гідрокси-2-[4-гідрокси-3(гідроксиме(гідроксиметил)феніл]етил}тил)феніл]етил}аміно)гексил]окси}бутил)бензолсул аміно)гептил]окси}пропіл)бензолсульфонамід; ьфонамід; та їх солі, сольвати, або фізіологічно функціоN-[4-(аміносульфоніл)феніл]-3-(4-{[6-({(2R)-2нальні похідні. гідрокси-2-[4-гідрокси-3З цих сполук 3-(4-{[6-({(2R)-2-гідрокси-2-[4(гідроксимегідрокси-3-(гідроксиметил)тил)феніл]етил}аміно)гексил]окси}бутил)бензолсул феьфонамід; ніл]етил}аміно)гексил]окси}бутил)бензолсульфона 2-(гідроксиметил)-4-{(1R)-1-гідрокси-2-[(6-(4-[3мід та 3-(3-{[7-({(2R)-2-гідрокси-2-[4-гідрокси-3(піперазин-1гідроксиметил)феніл]етил}ілсульфоаміно)гептил]окси}пропіл)бензолсульфонамід є ніл)феніл]бутокси}гексил)аміно]етил}фенол; особливо переважними. 3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3У дефініції R1, де R6 та R7 разом з атомом ніт(гідроксиметил)феніл]етил}рогену, до якого вони приєднані, утворюють 5-, 6-, аміно)гексил]окси}бутил)-N-((1-бметил-1або 7-членне нітрогено-вмісне кільце, термін "5-, 6фенілетил)бензолсульфонамід; , або 7-членне нітрогено-вмісне кільце" означає 5-, 5-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-36-, або 7-членне насичене або ненасичене кільце, (гідроксиметил)феніл]-етил}аміно)гексил]як включає сульфонамідний атом нітрогену та, як окси}бутил)-2-метоксибензолсульфонамід; варіант, 1 або 2 інші гетероатоми незалежно виб3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3рані з атомів оксигену, нітрогену та сульфуру. (гідроксиметил)феніл]етил}аміно)гексил]Придатні приклади такого кільця включають піпеокси}бутил)-5-пентилбензолсульфонамід; ридиніл, морфолініл, та піперазиніл. (Е)-2-[3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3У дефініції R1 конкретно довільні замісники на (гідроксиметил)феніл]етил}R6 та R7, термін "5-, 6-, або 7-членне гетероциклічаміно)гексил]окси}бутил)феніл]-Nне кільце" означає 5-, 6-, або 7-членне повністю метилетенсульфонамід; або частково насичене або ненасичене кільце, яке 2-[3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3включає 1, 2, 3 або 4 гетероатоми, незалежно ви(гідроксиметил)феніл]етил}аміно)гексил]брані з атомів оксигену, нітрогену та сульфуру. окси}бутил)феніл]етансульфонамід; Придатні приклади такого кільця включають піро5-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3ліл, фурил, тієніл, піридиніл, піразиніл, піридази(гідроксиметил)феніл]етил}аміно)гексил]ніл, імідазоліл, тетразоліл, тетрагідрофураніл, окси}бутил)[1,1'дифеніл]-3-сульфонамід; охазоліл, тіазоліл, тіадіазоліл, піперидиніл, мор3-флуор-5-(4-{[6-({(2R)-2-гідрокси-2-[4-гідроксифолініл та піперазиніл. 3-(гідроксиметил)феніл]етил}аміно)У дефініції X, термін "алкенілен" включає обигексил]окси}бутил)бензолсульфонамід; дві цис та транс структури. Придатні приклади ал5-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3кеніленгруп включають -СН=СН-. (гідроксиметил)феніл]етил}аміно)гексил]Сполуки формул (І), (Іа) та (Іb) включають окси}бутил)-3-трифлуорметилбензолсульфонамід; асиметричний центр, а саме атом карбону групи 3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3СН(ОН)-. Представлений винахід охоплює обидва (гідроксиметил)феніл]етил}аміно)гексил](S) та (R) енантіомери у по суті чистій формі або у окси}бутил)-5-метилбензолсульфонаміду ацетат; суміші у будь-яких пропорціях. 4 5 N-{[3-(4-{[6-({(2/J)-2-гідрокси-2-[4-гідрокси-3Подібно, там, де R та R є різними групами, (гідроксиметил)феніл]етил}аміно)гексил]атом карбону, до якого вони приєднані, є асиметокси}бутил)феніл]сульфоніл}гліцин; ричним центром та представлений винахід охопN2-{[3-(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3лює обидва (S) та (R) енантіомери по цьому (гідроксиметил)феніл]етил}аміно)гексил]центру у по суті чистій формі або у суміші у будьокси}бутил)феніл]сульфоніл}гліцинамід; яких пропорціях. та їх солі, сольвати, або фізіологічно функціоОтже сполуки формул (І), (Іа) та (Іb) включа 13 76443 14 ють усі енантіомери та діастереоізомери, а також солі включають цинамат, 4-метоксицинамат, 4їх суміші у будь-яких пропорціях. метилцинамат, нафталінпропеноат та 4Солі та сольвати сполук формул (І), (Іа) та (Іb), фенілцинамат. які є придатними для застосування у медицині є Фармацевтично прийнятні естери сполук фортакими, де протиіон або асоційований розчинник є мул (І), (Іа) та (Іb) можуть мати гідроксильну групу, фармацевтично прийнятними. Однак, солі та соперетворену у С1-6алкільний, арильний, арилС1львати, що мають фармацевтично неприйнятні 6алкільний, або амінокислотний естер. протиіони або асоційовані розчинники знаходяться Як згадано вище, сполуки формул (І), (Іа) та в рамках представленого винаходу, наприклад, (Іb) є селективними агоністами 2для застосування як інтермедіатів при отриманні адренорецептору, як продемонстровано, викорисінших сполук формул (І), (Іа) та (Іb) та їх фармацетовуючи зчитування функціональних або репортевтично прийнятних солей, сольватів, та фізіологічрних генів з ліній клітин, трансфектованих бетано функціональних похідних. адренорецепторами людини, як описано нижче. Термін "фізіологічно функціональні похідні" Сполуки згідно з представленим винаходом також означає хімічні похідні сполуки формули (І), (Іа) мають потенційну можливість поєднання довгої або (Іb), що мають такі ж фізіологічні функції, як протяжності дії зі швидким початком дії. Далі, деякі вихідна сполука формули (І), (Іа) -або (Іb), наприсполуки показали збільшений терапевтичний інклад, можливим перетворенням у тілі. декс у тваринних моделях відносно наявних довЗгідно з представленим винаходом, приклади годіючих бронхорозширювальних 2-агоністів. Як фізіологічно функціональних похідних включають такі, сполуки винаходу можуть бути придатними естери. для застосування раз на добу. Придатні солі згідно з винаходом включають Сполуки формул (І), (Іа) та (Іb) та їх фармацесолі, утворені органічними та неорганічними кисвтично прийнятні солі, сольвати та фізіологічно лотами або основами. Фармацевтично прийнятні функціональні похідні мають застосування при кислотно-адитивні солі включають солі, утворені з профілактиці та лікуванні клінічних станів, для яких гідрохлоридною, гідробромідною, сульфатною, показаний селективний агонія 2лимонною, винною, фосфатною, молочною, піроадренорецептору. Такі стани включають хвороби, виноградною, оцтовою, трифлуороцтовою, трифеасоційовані з оборотною обструкцією дихальних нілоцтовою, сульфамовою, сульфаніловою, янташляхів, як-то астма, хронічні обструктивні хвороби рною, щавлевою, фумаровою, малеїновою, легенів (COPD) (наприклад, хронічний та астматияблучною, глутаміновою, аспарагіновою, оксалоочний бронхіт, емфізема), інфекція респіраторного цтовою, метансульфоновою, етансульфоновою, тракту та хвороба вищого респіраторного тракту арилсульфоновою (наприклад п(наприклад, риніт, що включає сезонний та алергітолуолсульфоновою, бензолсульфоновою, нафчний риніт). талінсульфоновою або нафталіндисульфоновою), Інші стани, як можна лікувати, включають песаліциловою, глутаровою, глюконовою, трикарбаредчасні пологи, депресію, застійну серцеву неліловою, цинамовою, заміщеної цинамовою (настачу, хвороби шкіри (наприклад, запальні, алергіприклад, заміщеною фенілом, метилом, метоксичні, псоріазні та проліферативні хвороби шкіри), лом або галогеном цинамовою, що включають 4стани, де бажане зниження кислотності у шлунку метил та 4-метоксицинамову кислоту), аскорбіно(наприклад, укривання виразками шлунку та кишевою, олеїновою, нафтойною, гідроксинафтойною чнику) та м'язову слабкість. (наприклад 1- або 3-гідрокси-2-нафтойною), нафВідповідно, представлений винахід стосується талінакриловою (наприклад нафталін-2способу профілактики чи лікування клінічного стаакриловою), бензойною, 4-метоксибензойною, 2ну у ссавця, як-то людини, для якого показаний або 4-гідроксибензойною, 4-хлорбензойною, 4селективний агоніст 2-адренорецептору, спосіб фенілбензойною, бензолакриловою (наприклад включає застосування терапевтично ефективної 1,4-бензолдіакриловою) та ізетіоновою кислотами. кількості сполуки формули (І), (Іа) або (Іb), або її Фармацевтично прийнятні солі основ включають фармацевтично прийнятної солі, сольвату або солі амонію, такі солі лужних металів, як солі нафізіологічно функціонального похідного. Зокрема, трію та калію, такі солі лужноземельних металів, представлений винахід стосується таких профілаяк солі кальцію та магнію, та солі з такими органічктики чи лікування хвороби, асоційованої з обороними основами, як дициклогексиламін та N-метилтною обструкцією дихальних шляхів, як-то астма, D-глюкамін. хронічна обструктивна хвороба легенів (COPD), Переважно, такі кращі сполуки винаходу, як 3інфекція респіраторного тракту або хвороба вищо(4-{[6-({(2R)-2-гідрокси-2-[4-гідрокси-3го респіраторного тракту. Згідно з наступним аспе(гідроксиметил)ктом представлений винахід стосується такого феспособу профілактики чи лікування клінічного станіл]етил}аміно)гексил]окси}бутил)бензолсульфона ну, вибраного з передчасні пологи, депресію, замід та 3-(3-{[7-({(2R)-2-гідрокси-2-[4-гідрокси-3стійну серцеву нестачу, хвороби шкіри (наприклад, гідроксиметил)феніл]етил}-аміно)гептил]запальні, алергічні, псоріазні та проліферативні окси}пропіл)-бензолсульфонамід запропоновані у хвороби шкіри), стани, де бажане зниження кислоформі кристалічної солі, наприклад вибрані з сотності у шлунку (наприклад, укривання виразками лей, представлених нижче в експериментальному шлунку та кишечнику) або м'язової слабкості. розділі. Вказані кристалічні солі мають сприятливі Альтернативно, запропоновано також сполуку фізичні властивості так як низьку гігроскопічність формули (І), (Іа) або (Іb) або її фармацевтично та/або збільшену стабільність. Зокрема переважні прийнятну сіль, сольват, або фізіологічно функціо 15 76443 16 нальне похідне для застосування у терапії, зокретично прийнятну сіль, сольват, або фізіологічно ма, для застосування при профілактиці чи лікуванфункціональне похідне та фармацевтично прийняні клінічного стану у ссавця, як-то людини, для тний носій або ексципієнт, та, як варіант, один або більше інших терапевтичних інгредієнтів. якого показаний селективний агоніст 2Надалі, термін "активний інгредієнт" означаадренорецептору. Зокрема, запропоновано сполутиме сполуку формули (І), (Іа) або (Іb), або її фарку формули (І), (Іа) або (Іb) або її фармацевтично мацевтично прийнятну сіль, сольват, або фізіолоприйнятну сіль, сольват, або фізіологічно функціогічно функціональне похідне. нальне похідне для профілактики чи лікування Композиції включають композиції, придатні хвороби, асоційованої з оборотною обструкцією для перорального, парентерального (включаючи дихальних шляхів, як-то астма, хронічна обструкпідшкірне, інтрадермальне, внутрішньом'язове, тивна хвороба легенів (COPD), інфекція респіравнутрішньовенне та внутрішньосуглобове), інгаляторного тракту або хвороба вищого респіраторноцію (включаючи високодисперсні порошки або, які го тракту. Згідно з наступним аспектом можна отримувати засобами різних типів дозовазапропоновано сполуку формули (І), (Іа) або (Іb) них аерозолів від тиском, розпилювачів або вдуабо її фармацевтично прийнятну сіль, сольват, вачів), ректального та локального (включаючи деабо фізіологічно функціональне похідне для прормальне, букальне, сублінгвальне та філактики чи лікування клінічного стану, вибраного інтраокулярне) застосування, хоч найпридатніший з передчасних пологів, депресії, застійної серцевої шлях може залежати, наприклад, від стану та рознестачі, хвороб шкіри (наприклад, запальних, алеладу реципієнта. Композиції можна зручно предргічних, псоріазних та проліферативних хвороб ставляти у формі одиничної дози та можна отришкіри), станів, де бажане зниження кислотності у мувати будь-якими способами, добре відомими у шлунку (наприклад, укривання виразками шлунку рівні техніки фармакопеї. Усі способи включають та кишечнику) або м'язової слабкості. етап поєднання активного інгредієнту з носієм, Представлений винахід стосується також заякий складається з одного або більше допоміжних стосування сполуки формули (І), (Іа) або (Іb), або її інгредієнтів. Загалом, композиції отримують однофармацевтично прийнятної солі, сольвату або рідним та ретельним змішуванням активного інгфізіологічно функціонального похідного у виробредієнту з рідкими носіями або високодисперсниництві медикаменту для профілактики чи лікуванми твердими носіями або обома, а далі, якщо ня клінічного стану, для якого показаний селективнеобхідно, формування продукту у потрібну комний агоніст 2-адренорецептору, наприклад позицію. хвороб, асоційованих з оборотною обструкцією Композиції представленого винаходу, придатні дихальних шляхів, як-то астма, хронічна обструкдля перорального застосування, можна представтивна хвороба легенів (COPD), інфекція респіраляти як дискретні одиниці, як-то капсули, облатки торного тракту або хвороба вищого респіраторноабо таблетки, кожна з яких містить попередньо го тракту. Згідно з наступним аспектом визначену кількість активного інгредієнту; як позапропоновано сполуку формули (І), (Іа) або (Іb), рошок або гранули; як розчин або суспензію у воабо її фармацевтично прийнятну сіль, сольват, дній або неводній рідині; або як рідку емульсію або фізіологічно функціональне похідне у виробмасло-у-воді або вода-у-маслі. Активний інгредієнт ництві медикаменту для профілактики чи лікуванможна також представляти як болюс, електуарій ня клінічного стану, вибраного з передчасних поабо пасту. логів, депресії, застійної серцевої нестачі, хвороб Таблетку можна виробляти пресуванням або шкіри (наприклад, запальних, алергічних, псоріазвідливкою, як варіант, з одним або більше допоміних та проліферативних хвороб шкіри), станів, де жними інгредієнтами. Пресовані таблетки можна бажане зниження кислотності у шлунку (наприотримувати пресуванням у придатному агрегаті клад, укривання виразками шлунку та кишечнику) активного інгредієнт у вільно сипучій формі, як-то та м'язової слабкості. порошок або гранули, як варіант, змішані зі зв'язуКількість сполуки формули (І), (Іа) або (Іb), або вальним засобом, змащувачем, інертним розріїї фармацевтично прийнятної солі, сольвату або джувачем, поверхнево-активним або диспергувафізіологічно функціонального похідного, що потрільним засобом. Відлиті таблетки можна виробляти бна для досягнення терапевтичної дії безумовно відливкою у придатному агрегаті суміші порошку залежатиме від певної сполуки, шляху застосусполуки з інертним рідким розріджувачем. Таблетвання, лікуємого суб'єкту, та певного лікуємого ки можуть, як варіант, бути покритими або надрірозладу або хвороби. Сполуки винаходу можна заними і їх можна формувати для забезпечення застосовувати інгаляцією у дозі від 0,0005мг до повільного або контрольованого вивільнення з них 10мг, переважно від 0,005мг до 0,5мг. Межі доз активного інгредієнту. для дорослої людини є загалом від 0,0005мг до Композиції для парентерального застосування 100мг на добу, а переважно від 0,01мг до 1мг на включають водні та неводні стерильні розчини для добу. ін'єкцій, як можуть містити анти-оксиданти, буфеПри тому, що можливо сполуку формули (І), ри, бактеріостатики та розчинні добавки, як роб(Іа) або (Іb), або її фармацевтично прийнятну сіль, лять композицію ізотонічною з кров'ю реципієнта; сольват, або фізіологічно функціональне похідне та водні та неводні стерильні суспензії, які можуть можна застосовувати поодинці, краще представвключати суспендувальні засоби та згущувачі. ляти її як фармацевтичну композицію. Композиції можна представляти у одиничноВідповідно, представлений винахід стосується дозових або багато-дозових контейнерах, наприкрім того фармацевтичної композиції, що містить клад герметизованих ампулах та склянках, та мосполуку формули (І), (Іа) або (Іb) або її фармацев 17 76443 18 жуть зберігатися у висушеному сублімацією (ліопелент. Аерозольні композиції можуть бути вільфілізованому) стані, що потребує тільки додаванними від ексципієнту або можуть, як варіант, місня стерильного рідкого носія, наприклад сольового тити додаткові композиційні ексципієнти, добре розчину або води для ін'єкцій, негайно перед завідомі у рівні техніки, як-то сурфактанти, напристосуванням. Незаплановані розчини та суспензії клад, олеїнову кислоту або лецитин та співрозчиндля ін'єкцій можна отримувати з раніше описаних ники, наприклад, етанол. Композиції під тиском стерильних порошків, гранул та таблеток. загалом зберігають у каністрі (наприклад, алюмініСухі композиції порошку для локальної достаєвій каністрі), закритій клапаном (наприклад, дозувки у легені інгаляцією можна, наприклад, предвальним клапаном) з активатором у мундштуку. ставляти у капсулах та патронах, наприклад, з Медикаменти для застосування інгаляцією желатину, або блістерах, наприклад, з ламінованої бажано мають контрольований розмір . частинок. алюмінієвої фольги, для застосування у інгаляторі Оптимум розміру частинок для інгаляції у бронхіаабо вдувачі. Композиції загалом містять змішаний льну систему є звичайно 1-10мкм, переважно 2порошок для інгаляції зі сполуки винаходу та при5мкм. Частинки, що мають розмір вище 20мкм є датної порошкової основи (речовини носія), як-то загалом надто великими для досягнення невелилактоза або крохмаль. Застосування лактози є ких дихальних шляхів. Для досягнення цього розпереважним. Кожна капсула або патрон можуть міру частинок частинки активного інгредієнту, які загалом містити 20-10мг сполуки формули (І), як продукують, можна зменшувати у розмірі звичайваріант, у комбінації з іншим терапевтично активними засобами, наприклад, мікронізацією. Потрібним інгредієнтом. Альтернативно, сполуку винахону фракцію можна відділити струмом повітря або ду можна представляти без ексципієнтів. Упаковапросіюванням. Переважно, частинки повинні бути ні композиції можуть бути придатними для кристалічними. Коли застосовують ексципієнт, якодинично-дозової або багато-дозової доставки. У то лактозу, загалом, розмір частинок ексципієнту випадку багато-дозової доставки композиція може повинен бути набагато більше, ніж медикаменту в бути попередньо дозованою (наприклад, як у рамках представленого винаходу. Коли ексципієнDiskus, дивися GB 2242134 або Diskhaler, дивися том є лактоза, вона звичайно повинна бути змелеGB 2178965,2129691 та 2169265) або дозованою ною лактозою, де не більше, ніж 85% частинок при застосуванні (наприклад, як у Turbuhaler, дилактози мають MMD 60-90мкм та не менше, ніж вися ЕР 69715). Прикладом однодозового при15% мають MMD менше, ніж 15мкм. строю є Rotahaler (дивися GB 2064336). Пристрій Інтраназальні спреї можна формувати з воддля інгаляції Diskus містить подовжену стрічку, ними або неводними носіями додаванням таких створену з основного листа, що має множинність засобів, як згущувачі, буферні солі або кислоту чи переривчастих порожнин вздовж її довжини та луг для підгонки рН, засоби ізотонічності або антипокриваючого герметично але з можливістю відоксиданти. шаровування герметизованого листа, створюючи Розчини для інгаляції розпиленням можна фомножинність контейнерів, кожний контейнер має рмувати з водним носієм додаванням таких засокомпозицію для інгаляції, що містить сполуку форбів, як кислота або луг, буферні солі, засоби ізотомули (І) переважно з лактозою. Переважно, стрічка нічності або антимікробні засоби. Вони можуть є достатньо гнучкою, щоб бути скрученою у рулон. бути стерилізованими фільтруванням або нагріПокриваючий лист та основний лист переважно ванням в автоклаві, або представленими як немають ведучі кінцеві частини, які не герметизовані стерильний продукт. одна стосовно іншої та щонайменше одна з ведуКомпозиції для ректального застосування мочих кінцевих частин є створеною так, щоб бути жна представляти як супозиторій зі звичайними приєднаною до засобів намотки. Також, переважно носіями, як-то масло какао або поліетиленгліколь. герметична склейка між основним та покриваючим Композиції для локального застосування у ролистами простягається на повну ширину. Покриті, наприклад букально або сублінгвально, вклюваючий лист може переважно бути відірваним від чають коржі, що містять активний інгредієнт у смаосновного листа у напрямі від першого кінця вкаковій основі, як-то сахароза та камедь акації або заного основного листа. трагаканту, та пастилки, що містять активний інгСпрей-композиції для локальної доставки у лередієнт у основі, як-то желатин та гліцерин або гені інгаляцією можна, наприклад, формувати як сахароза та камедь акації. водні розчини або суспензії або як аерозолі, досКращі композиції одиничної дози є тими, що тавлені з упаковок під тиском, як-то дозувальний містять ефективну дозу активного інгредієнту, яку інгалятор, з застосуванням придатного зріджувавизначено вище, або прийнятну його фракцію. ного пропеленту. Аерозольні композиції, придатні Слід розуміти, що на додаток до інгредієнтів, для інгаляції, можуть бути суспензією або розчизокрема, згаданих вище, композиції цього винахоном та містити загалом сполуку формули (І), як ду можуть включати інші звичайні у рівні техніки варіант, у комбінації з іншим терапевтично активзасоби з огляду на тип розглянутої композиції, ним інгредієнтом та придатним пропелентом, як-то наприклад композиції, придатні для перорального флуорокарбон або гідрогено-вмісний хлорфлуорозастосування, можуть включати смакові засоби. карбон або їх суміші, зокрема гідрофлуоралкани, Сполуки та фармацевтичні композиції згідно з наприклад, дихлордифлуорметан, трихлорфлуорвинаходом можна застосовувати у комбінації з метан, дихлортетрафлуоретан, особливо 1,1,1,2одним або більше іншими терапевтичними засотетрафлуоретан, 1,1,1,2,3,3,3-гептафлуор-нбами або включати їх, наприклад, засобами, вибпропан або їх суміш. Діоксид карбону або інший раними з анти-запальних, антихолінергічних (зокпридатний газ можна також застосовувати як прорема антагоністу рецепторів М1, М2, М1/М2 або М3), 19 76443 20 триєну, інгібітори синтезу лейкотриєну, інгібітори інших агоністів 2-адренорецептору, антиінфекційiNOS, інгібітори триптази та еластази, антагоністи них засобів (наприклад, антибіотиків, антивірусних інтегрину бета-2 та агоністи або антагоністи адезасобів), або антигістамінних засобів. Винахід стонозину рецептору (наприклад, агоністи аденозину сується тому згідно з наступним аспектом комбі2а), антагоністи цитокіну (наприклад, антагоністи нації, що містить сполуку формули (І) або її фархемокіну) або інгібітори синтезу цитокіну. Придатні мацевтично прийнятну сіль, сольват або інші агоністи 2-адренорецептору включають салфізіологічно функціональне похідне разом з одним або більше іншими терапевтично активними засометерол (наприклад, як ксинафоат), салбутамол бами, наприклад вибраними з анти-запального (наприклад, як сульфат або вільну основу), форзасобу (наприклад кортикостероїду або NSAID), мотерол (наприклад, як фумарат), фенотерол або тербуталін та їх солі. антихолінергічного засобу, інших агоністів 2Окремий інтерес представляє застосування адренорецептору, антиінфекційного засобу (насполуки формули (І) у комбінації з інгібітором фоприклад, антибіотику або антивірусного засобу), сфодіестерази 4 (PDE4) або змішаним інгібітором або антигістамінного засобу. Кращими є комбінаPDE3/PDE4. PDE4-специфічний інгібітор, корисний ції, що містять сполуку формули (І) або її фармау цьому аспекті винаходу, може бути будь-якою цевтично прийнятну сіль, сольват або фізіологічно сполукою, здатною інгібувати фермент PDE4 або функціональне похідне разом з кортикостероїдом, діючою як інгібітор PDE4, які є тільки інгібіторами антихолінергічним засобом та/або інгібітором PDEPDE4, а не сполуками, які інгібують інші члени ро4. Кращі комбінації є такими, що містять один чи дини PDE, а також PDE4. Загалом краще застосодва інші терапевтичні засоби. вувати інгібітор PDE4, який має співвідношення Фахівцям зрозуміло, що прийнятні інші тераІК50 приблизно 0,1 або більше, яке стосується ІК50 певтичні інгредієнти можна застосовувати у формі для каталітичної форми PDE4, яка зв'язує роліпсолей, (наприклад, солей лужних металів або сорам з високою афінністю, поділеною на ІК50 для лей амінів чи як кислотно-адитивних солей), або форми, яка зв'язує роліпрам з низькою афінністю. проліків, або естерів (наприклад, нижчих алкілДля розкриття цього, каталітичну ділянку сАМР, естерів), або як сольвати (наприклад, гідрати) для яка зв'язує R- та S-роліпрам з низькою афінністю оптимізації активності, стабільності та/або фізичназивають ділянкою зв'язування "з низькою афінних характеристик (наприклад, розчинності) тераністю" (LPDE4), а іншу форму цієї каталітичної певтичного інгредієнту. Фахівцям також ясно, що ділянки, яка зв'язує роліпрам з високою афінністю прийнятні терапевтичні інгредієнти можна застоназивають ділянкою зв'язування "з високою афінсовувати у оптично чистій формі. ністю" (HPDE 4). Цей термін "HPDE4" не слід плуПридатні анти-запальні засоби включають тати з терміном "hPDE4", який застосовують для кортикостероїди та NSAID. Придатні кортикостеропозначення РОЕ4людини. їди, як можна застосовувати у комбінації зі сполуПочаткові експерименти можна проводити для ками винаходу, є тими пероральними та інгаляційвстановлення та підтвердження аналіз зв'язування ними кортикостероїдами та їх проліками, як мають [3Н]-роліпраму. Деталі цього надано у аналізах анти-запальну активність. Приклади включають зв'язування, детально описаних нижче. метил-преднізолон, преднізолон, дексаметазон, Аналізи зв'язування фосфодіестерази та роліфлукатизон-пропіонат, 6,9-дифлуор-17-[(2праму фуранілкарбоніл)окси]-11-гідрокси-16-метил-3Спосіб аналізу 1А оксо-андроста-1,4-дієн-17-карботіонової кислоти Виділений людини моноцит PDE4 та hrPDE S-флуорметиловий естер, 6,9-дифлуор-11(рекомбінантний PDE4 людини) визначали як пергідрокси-16-метил-3-оксо-17-пропіонілоксивинно наявний у формі з низькою афінністю. Тому, андроста-1,4-дієн-17-карботіонової кислоти S-(2активність тест-сполук проти форми PDE4 з низьоксо-тетрагідро-фуран-3S-іл)-естер, естери беккою афінністю можна визначити з використанням лометазону (наприклад, 17-пропіонатний естер стандартних аналізів каталітичної активності або 17,21-дипропіонатний естер), естери будезоPDE4, застосовуючи 1мкМ [3Н]сАМР як субстрат ніду, флунізоліду, мометазону (наприклад, фуроа[Torphy et al., J. of Biol. Chem., Vol. 267, No. 3 тні естери), триамцинолон-ацетонід, рофлепонід, pp.1798-1804, 1992]. Високошвидкісні надосадкові циклезонід, бутиксокорт-пропіонат, RPR-106541 та шари мозку щурів застосовували як джерело білку ST-126. Кращі кортикостероїди включають флуката обидва енантіомери [3Н]-роліпраму отримували тизон-пропіонат, 6,9-дифлуор-17-[(2зі специфічною активністю 25,6Кі/ммоль. Стандарфуранілкарбоніл)окси]-11-гідрокси-16-метил-3тні умови аналізу модифікували з опублікованої оксо-андроста-1,4-дієн-17-карботіонової кислоти методики до умов аналізу PDE, за винятком S-флуорметиловий естер, 6,9-дифлуор-11останнього сАМР: 50мМ Трис НСІ (рН 7,5), 5мМ гідрокси-16-метил-3-оксо-17-пропіонілоксиМgСІ2, 50мкМ 5'-АМР та 1нМ [3Н]-роліпраму андроста-1,4-дієн-17-карботіонової кислоти S[Torphy et al.. J. Biol. Chem., Vol. 267, No. 3 флуорметиловий естер, більш переважно 6,9рр.1798-1804, 1992]. Аналіз здійснювали протягом дифлуор-17-[(2-фуранілкарбоніл)окси]-111 години при 30°С. Реакцію зупиняли та зв'язаний ліганд відділяли від вільного ліганду, використогідрокси-16-метил-3-оксо-андроста-1,4-дієн-17вуючи збирач клітин Brandel. Конкуренцію для викарботіонової кислоти S-флуорметиловий естер. соко-афінної ділянки зв'язування оцінювали в умоПридатні NSAID включають натрію кромоглівах, що були ідентичними до застосовуваних для кат, недокроміл-натрій, інгібітори фосфодіестерази вимірювання активності PDE з низькою афінністю, (PDE) (наприклад, теофілин, інгібітори PDE4 або за винятком того, що не був присутнім [3Н]-сАМР. змішані інгібітори PDE3/PDE4), антагоністи лейко 21 76443 22 Спосіб аналізу IB (R)-(+)-1-(4-бромбензил)-4-[(3Вимір активності Фосфодіестерази циклопентилокси)-4-метоксифеніл]-2-піролідон; Активність PDE аналізували з використанням (R)-(+)-1-(4-бромбензил)-4-[(3[3Н]сАМР SPA або [3H]cGMP SPA-ферментним циклопентилокси)-4-метоксифеніл]-2-піролідон; аналізом, як описано постачальником (Amersham 3-(циклопентилокси-4-метоксифеніл)-1-(4-N'2 Life Sciences). Реакції проводили у 96-коміркових [N -ціано-S-метил-ізотіоуреїдо]бензил)-2планшетах при кімнатній температурі, у 0,1мл реапіролідон; кційного буферу, що містить (кінцеві концентрації): цис-4-ціано-4-(3-циклопентилокси-450мМ Трис-НСІ, рН 7,5, 8,3мМ МgСІ2, 1,7мМ метоксифеніл)циклогексан-1-карбонова кислота]; EGTA, [3Н]сАМР або [3Н] cGMP (приблизно цис-[4-ціано-4-(3-циклопропілметокси-42000dpm/пмоль), фермент та різні концентрації дифлуорметоксифеніл)циклогексан-1-ол]; інгібіторів. Аналіз проводили протягом 1 години та (R)-(+)-етил [4-(3-циклопентилокси-4зупиняли додаванням 50мкл SPA-ітрий-силікатних метоксифеніл)піролідин-2-іліден]ацетат; та кульок у присутності сульфату цинку. Планшети (S)-(-)-етил [4-(3-циклопентилокси-4струшували та давали їм стояти при кімнатній теметоксифеніл)піролідин-2-іліден]ацетат. мпературі протягом 20 хвилин. Утворення радіоміНайкращими є ті інгібітори PDE4, які мають ченого продукту оцінювали сцинтиляційною спектспіввідношення ІК50 більше 0,5, а зокрема сполуки, рометрією. що мають співвідношення більше 1,0. Кращими Аналіз зв'язування [3H]R-роліпраму сполуками є цис-4-ціано-4-(3-циклопентилокси-4Аналіз зв'язування [3Н]Р-роліпраму проводили метоксифеніл)циклогексан-1-карбонова кислота, модифікацією способу Schneider et al., дивися 2-карбометокси-4-ціано-4-(3-циклопропілметокси[Nicholson, et al., Trends Pharmacol. Sci., Vol. 12, 4-дифлуорметоксифеніл)циклогексан-1-он та цисpp.19-27 (1991) та McHale et al., МоI. Pharmacol., [4-ціано-4-(3-циклопропілметокси-4Vol. 39, 109-113 (1991)]. R-Роліпрам зв'язується з дифлуорметоксифеніл)циклогексан-1-ол]; вони є каталітичною ділянкою PDE4 дивися [Torphy et al., прикладами сполук, які зв'язуються преференційМоI. Pharmacol., Vol. 39, pp.376-384 (1991)]. Далі, но з ділянкою зв'язування з низькою афінністю та конкуренція стосовно зв'язування [3Н]Рч-роліпраму мають співвідношення ІК50 0,1 або більше. забезпечує незалежне підтвердження РОЕ4Інші переважні сполуки включають: інгібіторної потужності немічених конкурентів. Сполуки, представлені у патенті США 5552438 Аналіз проводили при 30°С протягом 1 години у від 03 вересня, 1996; цей патент та сполуки, що 0,5мкл буферу, що містить (кінцеві концентрації): він розкриває, представлено як посилання. Особ50мМ Трис-НСІ, рН 7,5, 5мМ МgдСІ2, 0,05% альливо переважною сполукою, яку розкрито у патенті 3 буміну бичачої сироватки, 2нМ [ Н]R-роліпрам США 5552438, є цис-4-ціано-4-[3(циклопентилокси)-4-метоксифеніл]циклогексан-1(5,7104dpm/пмоль) та різні концентрації радіонекарбонова кислота (також відома як циломаласт) мічених інгібіторів. Реакцію зупиняли додаванням та її солі, естери, проліки або фізичні форми; 2,5мл льодяного реакційного буферу (без [3Н]RAWD-12-281 від Asta Medica (Hofgen, N. et al. роліпрам) та швидким вакуумним фільтруванням 15th EFMC Int Symp Med Chem (Sept 6-10, (збирач клітин Brandel) через фільтри Whatman Edinburgh) 1998, Abst P,98; CAS-посилання No. GF/B, просочені у 0,3% поліетиленіміном. Фільтри 247584020-9); похідне 9-бензиладеніну, номіновапромивали додатково 7,5мл холодного буферу, не NCS-613 (INSERM); D-4418 від Chiroscience та сушили, та обраховували рідинною сцинтиляційSchering-Plough; бензодіазепіновий інгібітор PDE4, ною спектрометрією. Кращі інгібітори PDE4, викоідентифікований як CI-1018 (PD-168787) та припиристовувані у цьому винаході, бути сполуками, як суваний Pfizer; похідне бензодіоксолу, розкрите мають корисне терапевтичне співвідношення, тобKyowa Hakko у WO99/16766; К-34 від Kyowa Hakko; то, сполуки, як преференційно інгібують каталітичV-l 1294A від Napp (Landells, LJ. et al. Eur Resp J ну активність сАМР, де фермент є у формі, що Annu Cong Eur Resp Soc (Sept 19-23, Geneva) зв'язує роліпрам з низькою афінністю, тим змен1998] 1998,12 (Suppl. 28): Abst P2393); рофлумішуючи побічну дію, яка ймовірно зв'язана з інгібуласт (CAS-посилання No 162401-32-3) та фталавальною формою, яка зв'язує роліпрам з високою зинон (WO99/47505, розкриття якого представлено афінністю. Іншим шляхом досягнення цього є те, як посилання) від Byk-Gulden; пумафентрин, (-)-pщо кращі сполуки повинні мати співвідношення [(4aR*, 106S*)-9-етокси-1,2,3,4,4а,10b-гексагідро-8ІК50 приблизно 0,1 або більше, яке стосується ІК50 метокси-2-метилбензо[с][І,6]нафтаридин-6-іл]-N,Nдля PDE4 каталітичної форми, яка зв'язує роліпдіізопропілбензамід, який є змішаним інгібітором рам з високою афінністю, поділеної ІК50 для форPDE3/PDE4, як отримано та описано Byk-GuIden, ми, яка зв'язує роліпрам з низькою афінністю. зараз Altana; арофілин, розроблений AlmirallНаступне удосконалення цього стандарту є те, Prodesfarma; VM554/UM565 від Vemalis; або Т-440 що інгібітор PDE4 повинен мати співвідношення (Tanabe Seiyaku; Fuji, К. et al. J Pharmacol Exp ІК50 приблизно 0,1 або більше; вказане співвідноTher,1998, 284(1): 162), та Т2585. шення є співвідношення м величини ІК50 для кон3 Інші можливі інгібітори PDE-4 та змішані інгібікуренції зі зв'язуванням 1нМ [ Н]R-роліпраму з тори PDE3/PDE4 включають представлені у формою PDE4, яка зв'язує роліпрам з високою WO01/13953, розкриття якого представлено як афінністю, відносно величини ІК50 для інгібувальпосилання. ної каталітичної активності форми PDE4, яка зв'яПридатні антихолінергічні засоби є тими спозує роліпрам з низькою афінністю з використанням луками, що діють як антагоністи на мускариновому 1мкМ [3Н]-сАМР як субстрату. рецепторі, зокрема сполуки, які є антагоністами Прикладами корисних інгібіторів PDE4 є: 23 76443 24 рецепторів M1 та М2. тин фумарат, дифенілгідрамін-гідрохлорид, та Приклади сполук включають алкалоїди беладименгідринат. дони, які ілюстровано атропіном, скополаміном, Етилендіаміни: піриламін-малеат, трипеленагоматропіном, гіосціаміном; ці сполуки звичайно мін НСІ, та трипеленамін цитрат. застосовують як сіль третинного аміну. Ці ліки, Алкіламіни: хлрофенірамін та його солі, як-то зокрема сольові форми, легко доступні від ряду малеат, та акривастин. комерційних джерел або їх можна виробляти або Піперазини: гідроксизин НСІ, гідроксизин паотримати за літературними даними: моат, циклізин НСІ, циклізин лактат, мекліизин Атропін - CAS-51-55-8 або CAS-51-48-1 (безНСІ, та цетризин НСІ. водна форма), атропінсульфат - CAS-5908-99-6; Піперидини: астемозол, левокабастин НСІ, атропін-оксид - CAS-4438-22-6 або його сіль лоратидин або його дезкарбоетоксильний аналог, НСІ - CAS-4574-60-1 та метилатропіннітрат - CASта терфенадин та фексофенадин-гідрохлорид або 52-88-0. інші фармацевтично прийнятні солі. Гоматропін- CAS-87-00-3, гідробромід - CASАзеластин-гідрохлорид є ще іншим антагоніс51-56-9, метилбромід-сіль - CAS-80-49-9. том Hi-рецептору, який можна застосовувати у Гіосціамін (d, f) - CAS-101-31-5, гідробромід комбінації з інгібітором PDE4. CAS-306-03-6 та сульфат - CAS-6835-16-1. Приклади кращих анти-гістаміннів включають Скополамін - CAS-51-34-3, гідробромід - CASметапірилен та лоратидин. 6533-68-2, метилбромід- CAS-155-41-9. Винахід стосується тому, згідно з наступним Кращі антихолінергічні засоби включають іпрааспектом, комбінації, що містить сполуку формули топіум (наприклад, як бромід), під назвою атро(І), її фармацевтично прийнятні сіль, сольват або вент, окситропіум (наприклад, як бромід) та тіотфізіологічно функціональне похідне разом з інгібіропіум (наприклад, як бромід) (CAS-139404-48-1). тором PDE4. Також корисними є: метантелін (CAS-53-46-3), Винахід стосується тому, згідно з наступним пропантелін-бромід (CAS-50-34-9), анізотропінаспектом, комбінації, що містить сполуку формули метилбромід або валпін 50 (CAS-80-50-2), клідині(І), її фармацевтично прийнятні сіль, сольват або ум-бромід (Quarzan, CAS-3485-62-9), копіролат фізіологічно функціональне похідне разом з корти(Robinul), ізопропамід-йодид (CAS-71-81-8), мепекостероїдом. нзолат-бромід (патент США 2,918,408), тридигекВинахід стосується тому, згідно з наступним сетилхлорид (Pathilone, CAS-4310-35-4) та метиласпектом, комбінації, що містить сполуку формули сульфат гексоцикліуму (Tral, CAS-115-63-9). (І), її фармацевтично прийнятні сіль, сольват або Дивися також гідрохлорид циклопентолату (CASфізіологічно функціональне похідне разом з анти5870-29-1), тропікамід (CAS-1508-75-4), тригексихолінергічним засобом. фенідил-гідрохлорид (CAS-144-11-6), пірензепін Винахід стосується тому, згідно з наступним (CAS-29868-97-1), телензепін (CAS-80880-90-9), аспектом, комбінації, що містить сполуку формули AF-DX 116, або меоктрамін, та сполуки, розкриті у (І), її фармацевтично прийнятні сіль, сольват або WO 01/04118, розкриття якого представлено як фізіологічно функціональне похідне разом з антипосилання. гістамінним засобом. Придатні антигістамінні засоби (також познаВинахід стосується тому, згідно з наступним чені як антагоністи Н1-рецептору) включають будьаспектом, комбінації, що містить сполуку формули який один або більше з ряду відомих антагоністів, (І), її фармацевтично прийнятні сіль, сольват або які інгібують Н1-рецептори, та є безпечними для фізіологічно функціональне похідне разом з інгібівикористання людиною. Усі є оборотними, конкутором PDE4 та кортикостероїдом. рентними інгібіторами взаємодії гістаміну з Н1Винахід стосується тому, згідно з наступним рецепторами. Більшість цих інгібіторів, головним аспектом, комбінації, що містить сполуку формули чином антагоністів першої генерації, мають серце(І), її фармацевтично прийнятні сіль, сольват або винну структуру, яка може бути представленою фізіологічно функціональне похідне разом з антинаступною формулою: холінергічним засобом та інгібітором PDE-4. Вищенаведені комбінації можна зручно представляти для застосування у формі фармацевтичної композиції, а відтак фармацевтичні композиції, що містять комбінацію, яку визначено вище, разом з фізіологічно прийнятним розріджувачем або носієм, представляють наступний аспект винаходу. Певні сполуки таких комбінацій можна застоЦя узагальнена структура представляє три тисовувати послідовно або одночасно, окремо або у пи антигістамінних, загалом доступних засобів: фармацевтичних композиціях. Прийнятні дози віетаноламіни, етилендіаміни, та алкіламіни. На домих терапевтичних засобів фахівцям зрозумілі. додаток, інші антигістамінні засоби першої генераЗгідно з наступним аспектом винаходу, запроції включають засоби, які можна охарактеризувати поновано спосіб отримання сполуки формули (І), як основані на піперизині та фенотіазинах. Антаго(Іа) або (Іb) або її солі, сольвату, або фізіологічно ністи другої генерації, які є неседативними, мають функціонального похідного, спосіб включає етапи подібну спорідненість структура-активність, зали(а) (b) (с) або (d), які визначено нижче, у будьшаючи серцевинну етиленову групу (алкіламіни) якому порядку: або мімічну третинну аміногрупу з піперизином або (і) довільне видалення будь-яких захисних піперидином. Прикладами антагоністів є такі: груп; Етаноламіни: карбіноксамін-малеат, клемас 25 76443 26 (іі) довільне виділення енантіомеру з суміші енантіомерів; (iiі) довільне перетворення продукту у відповідні її сіль, сольват або фізіологічно функціональне похідне. На загальному етапі (а), сполука формули (І), або її солі або сольвату, де R1, R2, R3, R4, R5, 14 (Іа) або (Іb) може бути отриманою зняттям захисту R , m та n визначені для сполук формули (І), (Іа) захищеного інтермедіату, наприклад формули (II): або (Ib), R11 та R12 незалежно вибрані з групи: або його солі або сольвату, де R1, R2, R3, R4, R , m та n визначені для сполук формули (І), (Іа) або (Ib), R8, R9, та R10, кожний незалежно, представляють атом гідрогену або захисну групу за умови, що щонайменше одна з R8, R9, та R10 є захисною групою, та R14 представляє атом гідрогену або захисну групу. Придатні захисні групи можуть бути будь-якою звичайною захисною групою, як-то групою, описаною у ["Protective Groups in Organic Synthesis" Theodora W Greene та Peter G Μ Wuts, 3rd edition (John Wiley & Sons, 1999)]. Приклади придатних захисних груп гідроксилу представлених R8 та R9, є естери, як-то ацетатний, аралкіли, як-то бензил, дифенілметил, або трифенілметил, та тетрагідропіраніл. Приклади придатних захисних груп аміногрупи представлених R10, включають бензил, метилбензил, дифенілметил, трифенілметил, бензилоксикарбоніл, трет-бутоксикарбоніл, та ацилгрупи, як-то трихлорацетил або трифлуорацетил. Як треба розуміти фахівцями, застосування таких захисних груп може включати ортогональний захист груп у сполуках формули (II) для полегшення селективного видалення одної групи у присутності іншої, отже даючи змогу селективної функціоналізації одиничної аміно- або гідроксифункціональної групи. Наприклад, група -СН(ОН) може бути ортогонально захищеною групою CHOR14 з використанням, наприклад, триалкілсилілу, як-то триетилсиліл. Фахівцям також відомі інші стратегії ортогонального захисту, доступні звичайними засобами, які описано Theodora W Greene (дивися вище). Зняття захисту з отриманням сполук формули (І), (Іа) або (Іb) можна здійснити використанням звичайних способів. Отже, наприклад, коли R8, R9, та/або R10 представляє аралкіл, його можна відщепити гідруванням у присутності металевого каталізатору (наприклад, паладію на вугіллі). Коли R8 та/або R9 представляє тетрагідропіраніл, його можна відщепити гідролізом у кислотних умовах. Ацилгрупи, представлені R10, можна видалити гідролізом, наприклад основою, як-то гідроксид натрію, або групу, як-то трихлоретоксикарбоніл, можна видалити відновленням, наприклад, цинком та оцтовою кислотою. Інші зняття способи захисту можна знайти у Theodora W Greene (дивися вище). В окремому втіленні етапу (a) R8 та R9 можуть разом представляти захисну групу, як у сполуці формули (III). s атом гідрогену, С1-6алкіл, або арил. У кращому аспекті обидва R11 та R12 представляють метил. Сполука формули (III) може бути перетвореною у сполуку формули (І), (Іа) або (Іb) гідролізом розбавленою водною кислотою, наприклад оцтовою кислотою або гідрохлоридною кислотою у придатному розчиннику або транкеталізацією у спирті, наприклад етанолі, у присутності каталізатору, як-то кислоти (наприклад, толуолсульфонової кислоти) або солі (такої, як тозилат піридинію) при нормальній або підвищеній температурі. Треба розуміти, що захисні групи R8, R9, R10 та 14 R (включаючи циклізовані захисні групи, утворені R8 та R9, які визначені у формулі (III), можна видалити одним етапом або послідовно. Точний порядок, в якому видаляють захисні групи, частково залежатиме від природи вказаних груп та буде зрозумілим фахівцям. Переважно, коли R8 та R9 разом формують захисну групу, як у формулі (III), цю захисну групу видаляють разом з будь-якою захисною групою на частці СН(ОН), з наступним видаленням R10. Сполуки формул (II) та (III), де R10 представляє атом гідрогену можна отримувати з відповідної сполуки формули (IV): або її солі або сольвату, де R1, R2, R3, R4, R5, R , R9 m та n визначені для сполук формули (II) або (III). Перетворення сполуки формули (IV) у сполуку формули (II) або (III) можна здійснити обробкою основою, наприклад неводною основою, як-то триметилсиланоатом калію, або водною основою, як-то водний гідроксид натрію, у придатному розчиннику, як-то тетрагідрофуран. Сполуки формули (IV) можна отримувати з відповідної сполуки формули (V): 8 або її солі або сольвату, де R4, R5, R8, R9, m та n визначені для сполуки формули (IV); сполученням зі сполукою формули (VI): 27 де R1, R2, та R3 визначені для сполуки формули (IV), a L представляє відщеплювану групу, як-то галогеногрупа (звичайно, бром або йод) або сульфонатний естер, як-то галогеналкілсульфонат (звичайно, трифлуорметансульфонат), з наступним відновленням. Сполучення сполуки формули (V) зі сполукою формули (VI) зручно здійснювати у присутності каталізаторнної системи, як-то дихлориду біс(трифенілфосфін)паладію з органічною основою, як-то триалкіламін, наприклад, триетиламін, у придатному розчиннику, наприклад ацетонітрил або диметилформамід. Утворений алкін можна далі відновлювати з виділенням або без нього для формування сполуки формули (IV). Відновлення можна здійснити будь-яким придатним способом, як-то гідрування у присутності каталізатору, наприклад, паладію/на вугіллі або оксиду платини. Альтернативно, у сполуках формули (VI) R1, 2 R , та R3 можуть представляти групи, перетворювані у R1, R2 та R3, наприклад галогеногрупи. Це, зокрема, корисно, коли одна з груп R1, R2, та R3 може бути порушена будь-якою з наступних трансформацій. Отже, наприклад, коли R1 містить алкеніленову частину, її переважно уводять після відновлення алкіну, утвореного реакцією сполук (V), а (VI). Сполуки формули (VI) комерційно доступні або їх можна отримувати способами, добре відомими фахівцям. Сполуки формули (V) можна отримувати сполученням сполук формули (VII): або її солі або сольвату, де R8 та R9 визначені для сполуки формули (V), зі сполукою формули (VIII): (VIII) L1CR4R5(CH2)m-O-(CH2)n-2 -ССН де R4, R5, m та n визначені для сполуки формули (V), a L1 представляє відщеплювану групу, наприклад галогеногрупу (звичайно бром або йод) або сульфонат, як-то алкілсульфонат (звичайно, метансульфонат), арилсульфонат (звичайно, толуол сульфонат), або галогеналкілсульфонат (звичайно, трифлуорметансульфонат). Сполучення сполуки формули (VII) зі сполукою формули (VIII) можна здійснити у присутності основи, як-то гідрид металу, наприклад гідрид натрію, або неорганічної основи, як-то карбонат цезію, у апротонному розчиннику, наприклад диметилформаміді. Сполуки формули (VIII) можна отримувати з відповідного дигалогеналкану та гідроксіалкіну звичайними способами, звичайно у присутності неорганічної основи, як-то водний гідроксид на 76443 28 трію, в умовах фазопереносу у присутності солі, як-то броміду тетраалкіламонію. Сполуки формули (VII) можна отримувати замкненням кільця сполуки формули (IX): де R8 та R9 визначені для сполуки формули (VII), a R13 представляє С1-6алкіл, наприклад третбутил, або арил, наприклад, феніл. Замкнення кільця можна здійснити обробкою основою, як-то гідрид металу, наприклад гідрид натрію, у присутності апротонного розчиннику, наприклад, диметилформаміду. Сполуки формули (IX) можна отримувати з відповідного кетону формули (X): де R8 та R9 та R13 визначені для сполуки формули (IX), відновленням будь-яким придатним способом, наприклад обробкою бораном, у присутності хірального каталізатору, як-то CBSоксазаборолідин, у придатному розчиннику, як-то тетрагідрофуран. Сполуку формули (X) можна отримувати з відповідного галогеніду формули (XI) де R8 та R9 визначені для сполуки формули (X), a Y представляє атом галогену, придатно бром. Перетворення сполуки формули (XI) у сполуку формули (X) можна здійснити реакцією з захищеним аміном HN(COOR13)2 де R13 визначено для сполуки формули (X), у присутності неорганічної основи, як-то карбонат цезію, з наступним селективним видаленням одної з груп COOR13, наприклад обробкою кислотою, як-то трифлуороцтова кислота. Сполуки формули (XI) можна отримувати з відповідної сполуки, що має вільні гідроксиметильні та гідроксильні замісники (самі які можна отримувати з 2-бром-1-(4-гідрокси)-3-гідроксиметилфенетил)етанону, отримання якого описано у GB2140800, обробкою 2-метоксипропаном у ацетоні у присутності кислоти, наприклад, п-толуолсульфонової кислоти в атмосфері азоту або іншими стандартними способами) утворенням захищеної групи R8OCH2- та R9O- де R8 та R9 визначені для сполуки формули (XI). Такі способи описані у DE 3513885 (Glaxo). 29 76443 30 Сполуки формули (II) або (III), де R10 предстазвичайними перетвореннями, коли наявний попевляє захисну групу, можна отримувати як описано редник. у способі (b) нижче, або способами, аналогічними Алкін формули (XIV) можна також отримувати способу (с) нижче. реакцією сполуки формули (XV): У наступному етапі (b), сполуку формули (І), L2CR4R5(CH2)mL3 (XV) (Іа) або (Іb) можна отримати алкілуванням аміну зі сполукою формули (XVI): формули (XII): де R8, R9, R10 та R14, кожний незалежно, представляють атом гідрогену або захисну групу. Придатні захисні групи обговорені у дефініції сполук формули (II); зі сполукою формули (XIII): де R1, R2, R3, R4, R5, m та n визначені для сполуки формули (І), (Іа) або (Ib), a L2 представляє відщеплювану групу, як-то атом галогену (звичайно бром); з наступним видаленням будь-якої наявної захисної групи звичайними способами, які описано вище для зняття захисту у сполуці формули (II). Реакцію сполук формул (XII) та (XIII), як варіант, проводять у присутності органічної основи, якто триалкіламін, наприклад, діізопропілетиламін, та у придатному розчиннику наприклад диметилформаміді. Сполуки формули (XII) відомі у рівні техніки (наприклад ЕР-А 0947498) або можуть бути легко отримані фахівцями. Сполуки формули (XIII) можна отримувати сполученням сполук формули (VI), яку визначено вище, або її попереднику (де один або більше замісників R1, R2 або R3 представляє групу, як здатна перетворитися у потрібну групу R1, R2, або R3) зі сполукою формули (VIII), яку показано вище, де R4, R5, m та n визначені для сполуки формули (XIII), a L1 представляє відщеплювану групу, яку визначено вище. Сполучення сполуки формули (VIII) зі сполукою (VI) можна здійснити способами, аналогічними описаним вище для сполучення сполуки формули (V) зі сполукою формули (VI), з наступним відновленням утвореного алкіну формули (XIV): також як описано вище. Якщо необхідно, замісники R1, R2, та/або R3 можуть бути утвореними з використанням звичайних способів, наприклад, як описано для отримання сполуки (VIII), Сполуки формули (XVI) можна отримувати реакцією гідроксиалкіну зі сполукою формули (VI) з використанням способів, аналогічних описаним вище для сполучення сполуки (V) зі сполукою (VI). У наступному етапі (с) сполуку формули (І), (Іа) або (Іb) можна отримувати реакцією сполуки формули (XVII): де R8, R9 та R14 визначені вище, a L4 представляє відщеплювану групу, реагує з аміном формули (XVIII): з наступним видаленням будь-якої наявної захисної групи звичайними способами, які описано вище для зняття захисту у сполуці формули (II). Реакцію можна здійснити з використанням звичайних умов для таких реакцій заміщення. Сполуки формули (XVII) можна отримувати способами, відомими у рівні техніки. Сполуки формули (XVIII) можна отримувати реакцією сполуки формули (XIII) з аміном R10NH2. У наступному етапі (d) сполуку формули (І), (Іа) або (Іb) можна отримувати видаленням хірального допоміжнику зі сполуки формули (llа): 31 76443 32 де R1 - R5, R8, R9, m та n визначені вище, a R15 представляє хіральний допоміжник. "Хіральний допоміжник" є часткою, яку уводять у молекулу для впливу на стереобудову утвореного продукту, та видаляють цілком чи частково пізніше. Хіральний допоміжник може одночасно функціонувати як захисна група. Переважно у сполуках формул (llа) та (XIX) Багато хіральних допоміжників є комерційно захисні групи R8 та R9 разом утворюють групу доступними, та фахівці вибиратимуть їх на основі CR11R12- як у сполуках формули (III). потрібних властивостей, тобто потрібної абсолютВідновлення алкіну формули (XIX) можна здійної стереобудови та сумісності із застосовуваними снити способами, добре відомими у рівні техніки, способами. Хіральні допоміжники, придатні для наприклад каталітичним гідруванням, з викорисзастосування за цим способом включають, але без танням паладію на вугіллі або більш переважно обмеження S-ізомер та/або R-ізомер фенілгліцигідроксиду паладію (каталізатор Перельмана). нолу та його заміщені похідні. Хіральний допоміжник може також бути видаленим Хіральний допоміжник переважно представляє у відновних умовах. Переважно, відновлення алкігрупу формули: ну та видалення хірального допоміжнику можна здійснити одною реакцією. Алкін формули (XIX) можна отримувати реакцією сполуки формули (XX) або її одиничний енантіомер, де R16 представляє С1-6алкіл, як варіант, заміщений феніл або бензил де, як варіант, замісник є одним або більше незалежно вибраним з атому галогену, гідроксилу, С1-6алкоксилу або нітрогрупу, наприклад, пара-гідроксифеніл. Більш переважно хіральний допоміжник представляє частку: зі сполукою формули (VI) в умовах, описаних вище для сполучення сполук (V) та (VI). Сполуку формули (XX) можна отримувати реакцією сполуки формули (ХІІа): де R16 визначено вище. Альтернативно він може бути часткою формули: з альдегідом формули (XXI): де R16 визначено вище. Переважно R16 представляє феніл, як варіант, заміщений як описано вище. Найпереважніше R16 представляє незаміщений феніл. Хіральний допоміжник за цим способом можна звичайно видалити гідруванням з використанням каталізатору, наприклад паладію на вугіллі, або переважно використанням гідроксиду паладію (каталізатор Перельмана). Переважно, коли застосовують каталізатор Перельмана, видалення хірального допоміжнику є найефективнішим. Цей спосіб видалення є особливо придатним, коли R1 представляє феніл або заміщений феніл. Альтернативно, атом нітрогену, до якого приєднано допоміжник, можна дериватизувати в окиснювальних умовах для формування N-оксиду перед видаленням нагріванням з утворенням вторинного аміну. Сполуку формули (llа) можна отримувати відновленням відповідного алкіну формули (XIX): з використанням відомих способів відновного амінування, наприклад, триацетоксиборогідридом натрію у розчиннику, як-то хлороформ. Альдегід формули (XXI) можна отримувати з відповідного галогеніду формули (VIII) з використанням стандартних способів, як-то обробка гідрокарбонатом натрію у розчиннику, як-то ДМСО при підвищеній температурі, переважно в межах 130160°С. Сполуку формули (ХІІа) можна отримувати зі сполуки формули (XXII): де R8, R9 та R15 визначені вище, обробкою відновним засобом, як-то джерелом гідриду, напри 33 76443 34 клад, борогідридом натрію. Переважно це відбу(1R)-1-(2,2-Диметил-4Н-1,3-бензодіоксин-6-іл)вається у присутності інертної солі металу, як-то 2-[(6-{4-[3-(морфолін-4хлориду кальцію, придатно при неекстремальній ілсульфоніл)феніл]бутокси}гексил)аміно]етанол; температурі, наприклад, нижче зовнішньої, як-то 3-{4-[(6-{[(2R)-2-(2,2-Диметил-4Н-1,30°С. Це дає потрібну стереобудову з гарним енанбензодіоксин-6-іл)-2тіомерним надлишком на ранньому етапі синтезу, гідроксіетил]аміно}гексил)окси]бутил}-N,Nз використанням недорогих та відносно безпечних диметилбензолсульфонамід; реагентів. Далі, енантіомерний надлишок можна 3-{4-[(6-{[(2R)-2-(2,2-Диметил-4Н-1,3збільшити перекристалізацією продукту. бензодіоксин-6-іл)-2Сполуку формули (XXII) можна отримувати зі гідроксіетил]аміно}гексил)окси]бутил}-Nсполуки формули (XI), яку визначено вище, реакізопропілбензолсульфонамід; цією з прийнятним хіральним аміном, наприклад, 3-[4-({6-[(5R)-5-(2,2-Диметил-4Н-1,3(S)-фенілгліцинолом, у присутності ненуклеофільбензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3ної основи у інертному розчиннику при неекстреіл]гексил}окси)бутил]бензолсульфонамід; мальній температурі. N-[4-(Аміносульфоніл)феніл]-3-[4-({6-[(5R)-5Детальний опис способу, аналогічному етапу (2,2-диметил-4Н-1,3-бензодіоксин-6-іл)-2-оксо-1,3(d) можна знайти в опублікованій міжнародній паоксазолідин-3тентній заявці № WO/0196278. іл]гексил}окси)бутил]бензолсульфонамід; На вищенаведеному етапі (d) краще, щоб за3-[4-({6-[(5R)-5-(2,2-диметил-4Н-1,3хисні групи R8 та R9 разом утворювали захисну бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3групу, як наведено у формулі (III). іл]гексил}окси)бутил]-N-(4Треба розуміти, що у будь-якому з описаних флуорфеніл)бензолсульфонамід; вище шляхів (а)-(d), точний порядок етапів синтезу 3-[4-({6-[(5R)-5-(2,2-Диметил-4Н-1,3в залежності від уведення різних груп та часток у бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3молекулу може варіювати. Це гарантуватиме фаіл]гексил}окси)бутил]-N-(2-морфолін-4хівцям, що групи або частки, уведені на одному ілетил)бензолсульфонамід; етапі способу не порушуватимуться наступними N-циклогексил-3-[4-({6-[(5R)-5-(2,2-диметилтрансформаціями та реакціями при вибраному 4Н-1,3-бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3порядку етапів синтезу відповідно. іл]гексил}окси)бутил]бензолсульфонамід; Енантіомерні сполуки винаходу можна отри4-[4-({6-[(5R)-5-(2,2-Диметил-4Н-1,3мати (і) розділенням компонентів відповідної рабензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3цемічної суміші, наприклад, засобами хіральної іл]гексил}окси)бутил]бензолсульфонамід; хроматографії на колонці, ферментними способа2-[4-({6-[(5R)-5-(2,2-Диметил-4Н-1,3ми розділення, або утворенням та розділенням бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3придатних діастереоізомерів, або (іі) прямим синіл]гексил}окси)бутил]бензолсульфонамід; тезом з прийнятних хіральних інтермедіатів спосо(5R)-5-(2,2-Диметил-4Н-1,3-бензодіоксин-6-іл)бами, описаними вище. 3-(6-{4-[3-(піперазин-1Довільні перетворення сполук формули (І), (Іа) ілсульфоніл)феніл]бутокси}гексил)-1,3або (Іb) у відповідну сіль можна зручно здійснити оксазолідин-2-он; реакцією з прийнятною кислотою або основою. 3-[4-({6-[(5R)-5-(2,2-Диметил-4Н-1,3Довільне перетворення сполуки формули (І), (Іа) бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3або (Іb) у відповідний сольват або фізіологічно 1л]гексил}окси)бутил]-N-((1-бметил-1функціональне похідне можна здійснити способафентетил)бензолсульфонамід; ми, відомими фахівцям. 3-[4-({6-[(5R)-5-(2,2-Диметил-4Н-1,3Згідно з наступним аспектом, представлений бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3винахід стосується нових інтермедіатів для отриіл]гексил}окси)бутил]-N-метилбензолсульфонамід; мання сполук формули (І), (Іа) або (Іb), наприклад: (5R)-5-(2,2-Диметил-4Н-1,3-бензодіоксин-6-іл)сполуки формул (II) та (III), які визначено ви3-(6-{4-[3-(морфолін-4ще, або їх оптичний ізомер, сіль, або захищене ілсульфоніл)феніл]бутокси}гексил)-1,3похідне; зокрема, сполука вибрана з групи: оксазолідин-2-он; 3-{4-[(6-{[(2R)-2-(2,2-Диметил-4Н-1,33-[4-({6-[(5R)-5-(2,2-Диметил-1Н-1,3бензодіоксин-6-іл)-2бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3гідроксіеiл]гексил}окси)бутил]-N,Nтил]аміно}гексил)окси]бутил}бензолсульфонамід; диметилбензолсульфонамід; 4-{4-[(6-{[(2R)-2-(2,2-Диметил-4Н-1,33-[4-({6-[(5R)-5-(2,2-Диметил-4Н-1,3бензодіоксин-6-іл)-2бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3гідроксіеіл]гексил}окси)бутил]-Nтил]аміно}гексил)окси]бутил}бензолсульфонамід; ізопропілбензолсульфонамід; 2-{4-[(6-{[(2R)2-(2,2-Диметил-4Н-1,3N-(трет-бутил)-3-[4-({6-[(5R)-5-(2,2-диметилбензодіоксин-6-іл)-24Н-1,3-бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3гідроксіеіл]гексил}окси)бутил]бензолсульфонамід; тил]аміно}гексил)окси]бутил}бензолсульфонамід; (5R)-5-(2,2-Диметил-4Н-1,3-бензодіоксин-6-іл)3-{4-[(6-{[(2R)2-(2,2-Диметил-4Н-1,33-(6-{4-[3-(піперидин-1бензодіоксин-6-іл)-2ілсульфоніл)феніл]бутокси}гексил)-1,3гідроксіетил]аміно}гексил)окси]бутил}-Nоксазолідин-2-он; метилбензолсульфонамід; 3-[4-({6-[(5R)-5-(2,2-Диметил-4Н-1,3 35 76443 36 бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-31,1'-дифеніл; іл]гексил}окси)бутил]фенілметансульфонамід; трет-бутилу {3-[4-({6-[(5R)-5-(2,2-диметил-4Н3-[5-({5-[(5R)-5-(2,2-Диметил-4Н-1,31,3-бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3іл]гексил}окси)бутил]-5-пентилфеніл}сульфоніл{[2іл]пентил}окси)пентил]бензолсульфонамід; (триметилсиліл)етокси]метил}карбамат; 5-[4-{6-[(5R)-5-(2,2-Диметил-4Н-1,31-{4-[4-({6-[(5R)-5-(2,2-Диметил-4Н-1,3бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3іл]гексил}окси)бутил]-2іл]гексил}окси)бутил]феніл}метансульфонамід; та метоксибензолсульфонамід; 1-{2-[4-({6-[(5R)-5-(2,2-Диметил-4Н-1,33-[3-({7-[(5R)-5-(2,2-Диметил-4Н-1,3бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3іл]гексил}окси)бутил]феніл}метансульфонамід. іл]гептил}окси)пропіл]бензолсульфонамід; Для кращого розуміння винаходу для ілюстра3-(6-{4-[(5R)-5-(2,2-Диметил-4Н-1,3ції надано наступні приклади. бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3Приклади синтезу іл]бутокси}гексил)бензолсульфонамід; У прикладах, застосовують наступні скорочен4-{3-[4-({6-[(5R)-5-{2,2-Диметил-4Н-1,3ня: бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3РХ: рідинна хроматографія іл]гексил}окси)бутил]феніл}бутан-1-сульфонамід; РХМС: рідинна хроматографія/мас3-[5-({6-[(5R)-5-(2,2-Диметил-4Н-1,3спектрометрія. бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3ЧУ: час утримання іл]гексил}окси)пентил]бензолсульфонамід; ТГФ: тетрагідрофуран 3-[6-({6-[(5R)-5-(2,2-Диметил-4Н-1,3ДМФ: Ν,Ν-диметилформамід бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3РДМП: рентгенодифрактометрія порошку іл]гексил}окси)гексил]бензолсульфонамід; Силікагель стосується силікагелю Merck силі3-[3-({6-[(5R)-5-(2,2-Диметил-4Н-1,3кагель 60 Art №7734. бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3Флеш-силікагель стосується силікагелю Merck іл]гексил}окси)пропіл]бензолсульфонамід; 60 Art №9385. 3-[4-({5-[(5R)-5-(2,2-Диметил-4Н-1,3Biotage стосується попередньо упакованого бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3силікагелевого патрону, що містить KP-Sil для іл]пентил}окси)бутил]бензолсульфонамід; флеш-хроматографічного модуля 12і N-[3-(Аміносульфоніл)феніл]-3-[4-({6-[(5R)-5Bond But стосується попередньо упакованого (2,2-диметил-4Н-1,3-бензодіоксин-6-іл)-2-оксо-1,3патрону, застосовуваного у паралельній очистці, оксазолідин-3звичайно під вакуумом, і є комерційно доступним іл]гексил}окси)бутил]бензолсульфонамід; від Varian. N-бензил-3-[4-({6-[(5R)-5-(2,2-диметил-4Н-1,3РХ проводили на колонці Luna С18(2) (5см бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-32,0мм ID), елюючи 0,05%(за об'ємом) трифлуороіл]гексил}окси)бутил]бензолсульфонамід; цтовою кислотою у воді (розчинник А) та 0,05%(за 3-[4-({6-[(5R)-5-(2,2-Диметил-4Н-1,3об'ємом) трифлуороцтовою кислотою в ацетонітбензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3рилі (розчинник В) з використанням градієнту елюіл]гексил}окси)бутил]-Nвання 0,00-8,00 хвилин 0%В, 8,00-8,01 хвилин [(етиламіно)карбоніл]бензолсульфонамід; 95%В, 8,01-10,00 хвилин 0%В при швидкості пото3-[4-({6-[5-(2,2-Диметил-4Н-1,3-бензодіоксин-6ку 1,0мл/хвилин з температурою колонки 40°С. іл)-2-оксо-1,3-оксазолідин-3ЯМР-експерименти при 400МГц (якщо не виіл]гексил}окси)бутил]бензолсульфонамід; значено інше). N-{4-[({3-[4-({6-[(5R)-5-(2,2-Диметил-4Н-1,3РХМС проводили на колонці Supelcosil бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3LCABZ+PLUS (3,3см 4,6мм ID), елюючи 0,1% іл]гексил}окси)бутил]феніл}сульфоніл)аміно]феніл} НСО2Н та 0,01Μ ацетату амонію у воді (розчинник ацетамід; А), та 0,05% НСО2Н 5% води у ацетонітрилі (розN-циклобутил-3-[4-({6-[(5R)-5-(2,2-диметил-4Нчинник В), з використанням градієнту елювання 01,3-бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-30,7 хвилин 0%В, 0,7-4,2 хвилин 100%В, 4,2-5,3 іл]гексил}окси)бутил]бензолсульфонамід; хвилин 0%В, 5,3-5,5 хвилин 0%В при швидкості 3-[4-({6-[(5R)-5-(2,2-Диметил-4Н-1,3потоку 3мл/хвилин. Мас-спектри реєстрували на бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3спектрометрі Fiзons VG Platform з використанням іл]гексил}окси)бутил]-N-[2-(2режимів позитивного та негативного електророзгідроксіетокси)етил]бензолсульфонамід; пилення (ES+ve та ES-ve). (Е)-2-{3-[4-({6-[(5R)-5-(2,2-Диметил-4Н-1,3РДМП-аналіз, показаний у фігурах, проводили бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3на порошковому дифрактометрі Phillips X'pert Pro, іл]гексил}окси)бутил]феніл}-NМодель PW3040/60, серійний номер DY1379. Спометилетенсульфонамід; сіб проводили від 2 до 45 градусів 2Тета з розмі(Е)-2-{3-[4-({6-[(5R)-5-(2,2-Диметил-4Н-1,3ром кроку 0,02 градусів 2Тета та 2с часу витримки бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3на кожному кроку. іл]гексил}окси)бутил]феніл}етенсульфонамід; Приклад 1: 3-(4-((6-(((2R-2-гідрокси-2-(43-[((трет-бутоксикарбоніл){[2гідрокси-3-(гідроксиметил)феніл)-етил)-аміно)(триметилсиліл)етокси]метил}аміно)сульфоніл]-5гексил)оксибутил)бензолсульфонаміду ацетат [4-({6-[(5R)-5-(2,2-диметил-4Н-1,3-бензодіоксин-6і) Ди(трет-бутил) 2-(2,2-диметил-4Н-1,3іл)-2-оксо-1,3-оксазолідин-3-іл]гексил}окси)бутил]бензодіоксин-6-іл)-2-оксоетилімідодикарбонат це 37 76443 38 шуваної суспензії гідриду натрію (60% дисперсія у Карбонат цезію (70,4г) додавали до перемішумаслі, 11,9г) у ДМФ (160мл) при охолодженні так, ваної суспензії 2-бром-1-(2,2-диметил-4Н-1,3щоб внутрішня температура залишалася при 0°С бензодіоксин-6-іл)етанону, (Glaxo, DE 3513885, під азотом. Суміш перемішували при 21°С протя1985) (61,8г) та ди-т-бутилу імінодикарбоксилату гом 2 годин. Суміш знов охолоджували до 0°С та (47,15г) в ацетонітрилі (600мл) під азотом. Після додавали 2М НСІ (134мл). Суміш розбавляли воінтенсивного перемішування при 21°С протягом 24 дою та продукт двічі екстрагували етилацетатом. годин суміш розбавляли водою (приблизно 800мл) Розчин двічі промивали розсолом, сушили та продукт екстрагували діетиловим етером (1л, (MgSO4) та випарювали з утворенням потрібної далі 200мл). Поєднані органічні шари промивали сполуки (63,55г) РХМС ЧУ = 2,66 хвилин. розсолом, сушили (MgSO4) та концентрували до ν) 6-Бромгексил-бут-3-иніловий етер приблизно 400мл. Білі кристали збирали фільтру3-бутин-1-ол (42,4мл) перемішували інтенсивванням, промивали діетиловим етером та сушили но з 1,6-дибромгексаном (260мл) та гідросульфатом тетрабутиламонію (2,4г) у 50% водному розз утворенням потрібної сполуки (24,4г) (CDCI3) чині гідроксиду натрію (200мл) під азотом 7,78 (1Η, dd, J 8,2Гц), 7,65 (1H, brs), 6,87 (1Η, d, J протягом 3 діб. Воду (приблизно 700мл) додавали 8Гц), 4,97 (2H, s), 4,88 (2H, s), 1,56 (6H, s) та 1,48 та органічний шар відділяли. Водний шар екстра(18H, s). Наступна концентрація маточнику дала додатковий продукт (13,8г). Третю партію (7,1г) гували двічі дихлорметаном (2100мл) та поєднані отримували хроматографією маточнику на силікаорганічні шари промивали водою, сушили (MgSO4) гелі, випарюючи прийнятний елюат та розтираючи та концентрували. Залишок у петролейному ефірі з діетиловим етером. (темп. кипіння 40-60°) завантажували на колонку з іі) трет-бутилу 2-(2,2-диметил-4Н-1,3силікагелем (1,5кг) та колонку елювали петролейбензодіоксин-6-іл)-2-оксоетилкарбамат ним ефіром (темп. кипіння 40-60°), далі 10% діетиТрифлуороцтову кислоту (92мл) додавали до ловим етером у петролейному ефірі (темп. кипіння перемішуваного розчину ди(трет-бутилу) 2-(2,240-60°) з утворенням потрібної сполуки (103,3г), диметил-4Н-1,3-бензодіоксин-6-іл)-2(CDCI3) 3,56 (2Н, t, J 7Гц), 3,47 (2Н, t, J 7Гц), 3,42 оксоетилімідодикарбонату цезію, (352,55г) у дих(2Н, t, J 7Гц), 2,45 (2Н, m), 1,99 (1 Η, t, J 2Гц), 1,87 лорметані (3,6л) при 21°С та реакційну суміш пе(2H, m), 1,60 (2H, m) та 1,50-1,33 (4H, m). ремішували протягом 1,5 годин. Водний розчин yi) (5R)-3-(6-(Бут-3-инілокси)гексил)-5-(2,2NaOH (1,75л) додавали та після 10 хвилин фази диметил-4Н-1,3-бензодіоксин-6-іл)-1,3розділяли. Органічний шар промивали водою, суоксазолідин-2-он шили (MgSO4) та випарювали протягом ночі. Це (5R)-5-(2,2-диметил-4Н-1,3-бензодіоксин-6-іл)зберігали під високим вакуумом протягом ночі та 1,3-оксазолідин-2-он (10г) у ДМФ (100мл) додавадалі розтирали з сумішшю гексан:етер (3:1) з ли краплями 1 до перемішуваної суспензії гідриду утворенням сирого продукту (226,61г). Це очищали натрію (60% дисперсія у маслі, 2,33г) у ДМФ перекристалізацією з діетилового етеру з утворен(50мл) з перемішуванням під азотом та підтримням потрібної сполуки (122,78г). Наступний прокою внутрішньої температури при 0°. Перемішудукт (61,5г) отримували з маточнику випарюванвання продовжували при 0-5°С протягом 1 годин. ням та хроматографією на Biotage з Суміш знов охолоджували до 0°С та розчин 6використанням 15% етилацетату у гексані. РХМС бромгексил-бут-3-инілового етеру (14,7г) у ДМФ ЧУ = 3,37 хвилин. (50мл) додавали протягом 1 хвилини. Суміш далі ііі) трет-бутилу (2R)-2-(2,2-диметил-4Н-1,3перемішували при 20-30°С протягом 2 годин. 2М бензодіоксин-6-іл)-2-гідроксіетил-карбамат НСІ (9мл) додавали та суміш розподіляли між во2М розчин боран-диметилсульфіду у ТГФ дою та діетиловим етером. Водний шар екстрагу(28мл) додавали повільно до 1Μ розчину (R)вали ще діетиловим етером та поєднані органічні тетрагідро-1-метил-3,3-дифеніл-1Н,3Н-піроло(1,2шари промивали двічі розсолом. Після сушки с)(1,3,2)оксазаборолу у толуолі (56мл) при 0°С під (MgSO4) розчин концентрували та завантажували азотом. Розчин трет-бутилу 2-(2,2-диметил-4Н-1,3на колонку з силікагелем (600г) у суміші діетилов бензодіоксин-6-іл)-2-оксоетилкарбамат, (108,2г) у етер:петролейний ефір (темп.кипіння 40-60°) (1:2). ТГФ (1,3л) додавали повільно, тримаючи темпераКолонку елювали послідовно цією сумішшю, далі туру нижче 5°С, а потім 2М розчин боран(1:1) та далі діетиловим етером з утворенням потдиметилсульфіду у ТГФ (252мл) протягом 50 хвирібної, сполуки (13,88г) РХМС ЧУ = 3,45 хвилин. лин. Після 1 години 2М НСІ (170мл) додавали при vii) 3-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3охолодженні та суміш розподіляли між етилацетабензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-З-іл)том та водою. Органічний шар промивали насичегексил)окси)бут-1-иніл)бензолсульфонамід ним розчином NaHCO3 та розсолом та сушили (5R)-3-(6-(Бут-3-инілокси)гексил)-5-(2,2(MgSO4). Розчин концентрували та продукт очидиметил-4Н-1,3-бензодіоксин-6-іл)-1,3щали хроматографією на флеш-силікагелі (800г), оксазолідин-2-он (1,79г) перемішували з 3елюючи послідовно сумішшю гексан:етилацетат йодбензолсульфонамідом (1,4г) у суміші ацетоніт(4:1 далі 3:1) з утворенням потрібної сполуки рилтриетиламін (1:1, 42мл) під азотом протягом 10 (93,3г), РХМС ЧУ = 3,31 хвилин. хвилин. Йодид купруму (0,083г) та дихлорiv) (5R)-5-(2,2-Диметил-4Н-1,3-бензодіоксин-6біс(трифенілфосфін)паладій (0,192г) додавали та іл)-1,3-оксазолідин-2-он суміш перемішували протягом 17 годин під азотом Трет-бутилу (2R)-2-(2,2-диметил-4Н-1,3при 21°С. Суміш випарювали досуха та залишок бензодіоксин-6-іл)-2-гідроксіетилкарбамат3 (86,37г) хроматографували на силікагелі (250г) у суміші у ДМФ (600мл) додавали краплями 1 до перемі30% етилацетату:петролейний ефір (темп.кипіння зію 39 76443 40 40-60°), далі 50%, далі 75% та під кінець етилацегексил)окси)бутил)бензолсульфонамід отримували тат з утворенням потрібної сполуки (2,35%), РХМС з використанням способів, подібних описаним у ЧУ = 3,44 хвилин. прикладі 1 іх. РХМС ЧУ = 2,65 хвилин. viii) 3-F4-((6-((5RV5-(2,2-Диметил-4Н-1,3iv) 4-(4-((6-(((2R)-2-Гідрокси-2-(4-гідрокси-3бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3(гідроксиметил)феніл)етил)аміно)іл)гексил)окси)burul)бензолсульФонамід гексил)окси)бутил)бензолсульфонаміду ацетат 3-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3отримували з використанням способів, подібних бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3описаним у прикладі 1 х. РХМС ЧУ = 2,38 хвилин. іл)гексил)окси)бут-1-иніл)бензолсульфонамід ЕР +ve 495 (МН)+. (2,35г) перемішували з оксид платини (0,3г) у ТГФ Приклад 3: 2-(4-((6-(((2R)-2-Гідрокси-2-(4(30мл) під воднем протягом 2 годин. Каталізатор гідрокси-3-(гідроксиметил)фенілетил)видаляли фільтруванням з використанням фільтаміно)гексил)окси)бутил)бензолсульфонаміду ацерувального допоміжнику та шар на фільтрі промитат вали етилацетатом. Поєднані фільтрати пропусі) 2-(4-((6-((5Р)-5-(2,2-Диметил-4Н-1,3кали через силікагель (200г) у етилацетаті та бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3елюат випарювали з утворенням потрібної сполуілгексил)окси)бут-1-иніл)бензолсульфонамід ки (232%), РХМС ЧУ = 3,49 хвилин. отримували з використанням способів, подібіх) 3-(4-((6-(((2R)-2-(2,2-Диметил-4Н-1,3них описаним у прикладі 1 vii. РХМС ЧУ = 3,58 бензодіоксин-6-іл)-2-гідроксіетил)-аміно)хвилин. гексил)окси)бути)бензолсульфонамід іі) 2-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,33-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3іл)гексил)окси)бутил)бензолсульфонамід іл)гексил)окси)бутил)бензолсульфонамід (0,43г) отримували з використанням способів, подібперемішували у ТГФ (10мл) з продувкою інтенсивних описаним у прикладі 1 viii. РХМС ЧУ= 3,61 ним струмом азоту протягом 5 хвилин. Калію трихвилин. метилсиланоат (0,43г) додавали та суміш переміііі) 2-(4-((6-(((2R)-2-(2,2-Диметил-4Н-1,3шували при 70°С під азотом протягом 2,5 годин. бензодіоксин-6-іл)-2-гідроксіетил)аміно)Суміш розподіляли між дихлорметаном та фосфагексил)окси)бутил)бензолсульфонамід отримували тним буфером з рН 6,4 та водний шар екстрагуваз використанням способів, подібних описаним у ли ще дихлорметаном. Поєднані органічні шари прикладі 1 іх. РХМС ЧУ = 2,80 хвилин. промивали водою, сушили (MgSO4) та концентруiv) 2-(4-((6-(((2R)-2-Гідрокси-2-(4-гідрокси-3вали. Залишок очищали на силікагелі (60г), елюю(гідроксиметил)фенілетил)аміно)гексил)чи послідовно сумішшю етилацетат:петролейний окси)бутил)бензолсульфонаміду ацетат отримуефір (темп.кипіння 40-60°) (1:1), етилацетатом, вали з використанням способів, подібних описа10% далі 20% метанолом у етилацетаті з утворенним у прикладі 1 х. РХМС ЧУ = 2,43 хвилин, ЕР ням потрібної сполуки (0,286г), РХМС ЧУ = 2,56 +ve 495 (МН)+. хвилин. Приклад 4: 3-(4-((6-(((2R)-2-Гідрокси-2-(4х) 3-(4-((6-(((2R)-2-Гідрокси-2-(4-гідрокси-3гідрокси-3-(гідроксиметил)фенілетил)аміно)(гідроксиметил)феніл)етил)аміно)гексил)окси)бутил)-N-метилбензолсульфонаміду гексил)окси)бутил)бензолсульфонаміду ацетат ацетат 3-(4-((6-(((2R)-2-(2,2-диметил-4Н-1,3і) 3-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3бензодіоксин-6-іл)-2-гідроксіетил)аміно)гексил)бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3окси)бутил)бензолсульфонамід (0,283г) перемішуіл)гексил)-окси)бут-1-иніл)-Nвали з оцтовою кислотоою (8мл) та водою (4мл) метилбензолсульфонамід при 70°С протягом 35 хвилин перед випарюванням отримували з використанням способів, подібдосуха. Залишок знов випарювали двічі з толуоних описаним у прикладі 1 vii. EP+ve571(MH)+. лом з утворенням потрібної сполуки (0,318г) РХМС іі) 3-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3ЧУ = 2,34 хвилин. ЕР +ve 495 (МН)+. бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3Приклад 2: 4-(4-((6-(((2R)-2-Гідрокси-2-(4іл)гексил)окси)бутил)-N-метилбензолсульфонамід гідрокси-3-(гідроксиметил)феніл)етил)отримували з використанням способів, подібаміно)гексил)окси)бутил)бензолсульфонаміду ацених описаним у прикладі 1 viii. EP+ve 575 (МН)+. тат ііі) 3-(4-((6-(((2R)-2-(2,2-Диметил-4Н-1,3і) 4-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3бензодіоксин-6-іл)-2-гідроксіетил)аміно)бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3гексил)окси)бутил)-N-метилбензолсульфонамід іл)гексил)окси)бут-1-иніл)бензолсульфонамід отримували з використанням способів, подібних отримували з використанням способів, подібописаним у прикладі 1 іх. EP+ve 549 (МН)+. них описаним у прикладі 1 vii. РХМС ЧУ = 3,47 iv) 3-(4-((6-(((2R)-2-Гідрокси-2-(4-гідрокси-3хвилин. (гідроксиметил)феніл)етил)-аміно)гексил)іі) 4-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3окси)бутил)-N-метилбензолсульфонаміду ацетат бензодіоксин-6-іл)-2-оксо-1,3З-оксазолідин-3отримували з використанням способів, подібних іл)гексил)окси)бутил)бензолсульфонамід описаним у прикладі 1 х. РХМС ЧУ = 2,45 хвилин отримували з використанням способів, подібEP+ve 509 (МН)+. них описаним у прикладі 1 viii. РХМС ЧУ = 3,47 Приклад 5: 2-(Гідроксиметил)-4((R)-1-гідроксихвилин. 2-((6-4-(3-(морфолін-4-ілсульфоніл)ііі) 4-(4-((6-(((2R)-2-(2,2-Диметил-4Н-1,3феніл)бутокси)гексил)аміно)етил)фенолу ацетат бензодіоксин-6-іл)-2-гідроксіетил)аміно)і) (5R)-5-(2,2-Диметил-4Н-1,3-бензодіоксин-6 41 76443 42 іл)-3-(6-(М-(3-(морфолін-4-ілсульфоніл)-феніл)бутсил)окси|бутин-N-iзопроптбензолсульфонамiду 3-иніл)окси)гексил-1,3-оксазолідин-2-он ацетат отримували з використанням способів, подібi) 3-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3них описаним у прикладі 1 vii. EP+ve 627 (МН)+. бензодіоксин-6-iл)-2-оксо-1,3-оксазолідин-3іі) (5R)-5-(2,2-Диметил-4Н-1,3-бензодіоксин-6іл)гексил)окси)бут-1-иніл)-Nіл)-3-(6-(4-(3-(морфолін-4-ілсульфоніл)ізопропілбензолсульфонамід феніл)бутоксил)ексил)-1,3-оксазолідин-2-он отримували з використанням способів, подіботримували з використанням способів, подібних описаним у прикладі 6 і. ЕР +ve 599 (МН)+. них описаним у прикладі 1 viii. EP+ve 631 (МН)+. ii) 3-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3ііі) (1R)-1-(2,2-Диметил-4Н-1,3-бензодіоксин-6бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3іл)-2-((6-(4-(3-(морфолін-4-ілсульфоніл)іл)гексил)окси)бутил)-Nфеніл)бутокси)гексил)аміно)етанол ізопропілбензолсульфонамід отримували з використанням способів, подіботримували з використанням способів, подібних описаним у прикладі 1 іх. EP+ve 605 (МН)+. них описаним у прикладі 1 viii. EP+ve 603 (MH)+. iv) 2-(Гідроксиметил)-4((R)-1-гідрокси-2-((6-14ііi) 3-(4-((6-(((2R)-2-(2,2-Диметил-4Н-1,3(3-(морфолін-4-ілсульфоніл)феніл)бензодіоксин-6-іл)-2-гідроксіетил)аміно)гексил)бутокси)гексил)аміно)етил)фенолу ацетат окси)бутил)-N-ізопропілбензолсульфонамід отримували з використанням способів, подіботримували з використанням способів, подібних описаним у прикладі Iх. РХМС ЧУ = 2,54 хвиних описаним у прикладі 1 іх. EP+ve 577 (МН)+. лин EP+ve 565 (МН)+. iv) 3-(4-((6-(((2R)-2-гідрокси-2-(4-гідрокси-3Приклад 6: 3-(4-((6-(((2R)-2-Гідрокси-2-(4(гідроксиметил)феніл)етил)-аміно)гексил)гідрокси-3-(гідроксиметил)феніл)етил)окси)бутил)-N-ізопропілбензолсульфонаміду ацеаміно)гексил)окси)бутил)-N,Nтат отримували з використанням способів, подібдиметилбензолсульфонаміду ацетат них описаним у прикладі 1 х. РХМС ЧУ = 2,56 хвиі) 3-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3лин EP+ve 537 (МН)+. бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3-іл)Приклад 8: N-(трет-бутил-3-(4-((6-(((2R)-2гексил)окси)бут-1-иніл)-N,Nгідрокси-2-(4-гідрокси-3-(гідроксиметил)диметилбензолсульфонамід феСуміш (5R)-3-(6-(бут-3-инілокси)гексил)-5-(2,2ніл)етил)аміно)гексил)окси)бутил)бензолсульфона диметил-4Н-1,3-бензодіоксин-6-іл)-1,3міду ацетат оксазолідин-2-ону (0,256г) та 3-бром-N,Nі) N-(трет-бутил-3-(4-((6-((5R)-5-(2,2-диметилдиметилбензолсульфонаміду (0,208г) у піролідині 4Н-1,3-бензодіоксин-6-iл)-2-оксо-1,3-оксазолідин-3(4мл) дегазували з використанням циклу вакуіл)гексил)-окси)бут-1-иніл)бензолсульфонамід ум/азот. Йодид купруму (0,005г) та дихлоротримували з використанням способів, подіббіс(трифенілфосфін)паладій (0,037г) додавали та них описаним у прикладі 6і. EP+ve 613 (MH)+. суміш перемішували при 80°С протягом 45 хвилин ii) N-(трет-бутин-3-(4-((6-((5R)-5-(2,2-диметилпід азотом. Суміш розбавляли EtOAc та промива4Н-1,3-бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3ли водою. Водну фазу екстрагували EtOAc та поіл)гексил)окси)бутил)бензолсульфонамід єднані органічні фази промивали розсолом, сушиотримували з використанням способів, подібли (Na2SO4) та випарювали досуха. Залишок них описаним у прикладі 1 viii. EP+ve 617 (MH)+. розчиняли у СН2СІ2 та обробляли патроном з діокііі) N-(трет-бутил)-3-(4-((6-(((2R)-2-(2,2сидом силіцію Bond Elut (10г). Патрон елювали диметил-4Н-1,3-бензодіоксин-6-іл)-2СН2СІ2, циклогексан/Еt2О, Et2O та EtOAc. Випарюгідроксіевання етерних фракцій дало масло, яке знов очитил)аміно)гексил)окси)бутил)бензолсульфонамід щали діоксидом силіцію Bond Elut з утворенням отримували з використанням способів, подібпотрібної сполуки (0,23г),EP+ve 585 (МН)+. них описаним у прикладі 1 іх. EP+ve 591 (МН)+. іі) 3-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3iv) N-(трет-бутин-3-(4-((6-(((2R)-2-гідрокси-2-(4бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3гідрокси-3-(гідроксиметил)феніл)іл)гексил)окси)бутил)-N,Nетил)аміно)гексил)окси)бутил)бензолсульфонамід диметилбензолсульфонамід у ацетат отримували з використанням способів, подіботримували з використанням способів, подібних описаним у прикладі 1 viii. EP+ve 587 (МН)+. них описаним у прикладі Iх. РХМС ЧУ = 2,63 хвиііі) 3-(4-((6-(((2R)-2-(2,2-Диметил-4Н-1,3лин EP+ve 551 (МН)+. бензодіоксин-6-іл)-2-гідроксіетил)аміно)гексил)Приклад 9: 2-(Гідроксиметил)-4-((1R)-1окси)бутил)-N,N-диметилбензолсульфонамід гідрокси-2-((6-(4-(3-(піперидин-1отримували з використанням способів, подібілсульфоних описаним у прикладі 1 іх. EP+ve 563 (МН)+. ніл)феніл)бутокси)гексил)аміно)етил)фенолу ацеiv) 3-(4-((6-(((2R)-2-гідрокси-2-(4-гідрокси-3тат (гідроксиметил)феніл)етил)і) (5R)-5-(2,2-Диметил-4Н-1,3-бензодіоксин-6аміно)гексил)окси)бутил)-N,Nіл)-3-(6-((4-(3-(піперидин-1-ілсульфоніл)феніл)бутдиметилбензолсульфонаміду ацетат отримували з 3-иніл)окси)гексил)-1,3-оксазолідин-2-он використанням способів, подібних описаним у приотримували з використанням способів, подібкладі 1 х. РХМС ЧУ = 2,52 хвилин EP+ve 523 них описаним у прикладі 6 і. EP+ve 625 (МН)+. (MH)+. іі) (5R)-5-(2,2-Диметил-4Н-1,3-бензодіоксин-6Приклад 7: 3-(4-((6-(((2R)-2-Гідрокси-2-(4іл)-3-(6-(4-(3-(піперидин-1гідрокси-3-(гідроксиметил)феніл)етил)-амiно) гекілсульфоніл)феніл)бутокси)гексил-1,3-оксазолідин 43 76443 44 2-он і) 5-((5-Бромпентил)окси)пент-1-ин отримували з використанням способів, подіботримували з використанням способів, подібних описаним у прикладі 1 viii. EP+ve 629 (МН)+. них описаним у прикладі 1 ν. РХМС ЧУ=3,62 хвиііі) (1R)-1-(2,2-Диметил-4Н-1,3-бензодіоксин-6лин. іл)-2-((6-(4-(3-(піперидин-1іі) (5R)-5-(2,2-Диметил-4Н-1,3-бензодіоксин-6ілсульфоніл)феніл)бутокси)гексил)аміно)етанол іл)-3-(5-(пент-4-инілокси)пентил)-1,3-оксазолідинотримували з використанням способів, подіб2-он них описаним у прикладі 1 іх. EP+ve 603 (МН)+. отримували з використанням способів, подібiv) 2-(гідроксиметил)-4-1(1R)-1-гідрокси-2-((6них описаним у прикладі 1 vi. РХМС ЧУ=3,50 хви(4-(3-(піперидин-1-ілсульфоніл)лин. феніл)бутокси)гексил)аміноіетил)фенолу ацетат ііі) 3-(5-((5-((5R)-5-(2,2-Диметил-4Н-1,3отримували з використанням способів, подіббензодіоксин-6-іл-2-оксо-1,3-оксазолідин-3них описаним у прикладі 1 х. РХМС ЧУ = 2,72 хвиіл)пентил)оксилпент-1-иніл)бензолсульфонамід лин EP+ve 563 (МН)+. отримували з використанням способів, подібПриклад 10: 1-(3-(4-((6-(((2R)-2-Гідрокси-2-(4них описаним у прикладі 1 vii. РХМС ЧУ=3,42 хвигідрокси-3-(гідроксиметил)феніл)-етил)аміно)лин. гексил)окси)-бути)феніл)метансульфонамід iv) 3-(5-((5-((5R)-5-(2,2-Диметил-4Н-1,3і) Натрію (3-йодфеніл)метансульфонат бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3Розчин 3-йодбензилброміду (3г) та сульфіту іл)пентил)окси)пентил)бензолсульфонамід натрію (1,26г) в ацетоні (15мл) та воді (30мл) гріли отримували з використанням способів, подібпри 70°С протягом 3 годин. Розчинник видаляли них описаним у прикладі 1 viii. РХМС ЧУ=3,58 хвипід зниженим тиском та залишок розтирали у ефірі лин. з утворенням потрібної сполуки (3,8г). РХМС v) 3-(5-((5-(((2R)-2-(2,2-Диметил-4Н-1,3ЧУ=3,66 хвилин. бензодіоксин-6-іл)-2-гідроксіетил)аміно)іі) (3-Йодфенілметансульфонілхлорид пентил)окси)пентил)бензолсульфонамід Перемішувану суміш (3отримували з використанням способів, подібйодфеніл)метансульфонату натрію (3,6г) і фосфоних описаним у прикладі 1 іх. РХМС ЧУ=2,75 хвирилхлориду (10мл ) у сульфолані (20мл) та ацетолин. нітрилі (30мл) гріли при 70°С протягом 2 годин. vi) 3-(5-((5-(((2R)-2-Гідрокси-2-(4-гідрокси-3Суміш виливали на подрібнений лід (200мл) та (гідроксиметил)феніліетил)аміно)осаджений продукт збирали та сушили з утворенпентил)окси)пентил)бензолсульфонаміду ацетат ням потрібного продукту (2,8г) РХМС ЧУ= 3,47 отримували з використанням способів, подібхвилин. них описаним у прикладі 1 х. РХМС ЧУ=2,46 хвиііі) (3-Йодфеніл )метансульфонамід лин, EP+ve 495 (МН)+. Перемішуваний розчин (3Приклад 12: 3-(3-((7-(((2R)-2-Гідрокси-2-(4йодфеніл)метансульфонілхлориду (1г) у ТГФ гідрокси-3-(гідроксиметил)феніл)етил)(20мл) обробляли 0,88 аміаку (25мл) при кімнатній аміно)гептил)окси)пропіл)бензолсульфонаміду температурі протягом 30 хвилин. Розчинник видаацетат ляли під зниженим тиском та залишок розтирали у і) 3-((7-Бромгептил)окси)проп-1-ін ефірі з утворенням потрібної сполуки (0,35г). отримували з використанням способів, подібРХМС ЧУ=2,71 хвилин. них описаним у прикладі 1 ν. РХМС ЧУ=0,63 хвиiv) (3-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3лин. бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3іі) (5R)-5-(2,2-Диметил-4Н-1,3-бензодіоксин-6іл)гексил)окси)бут-1-иніл)феніл)метансульфонамід іл)-3-(7-(проп-2-инілокси)гептил-1,3-оксазолідин-2отримували з використанням способів, подібон них описаним у прикладі 1 vii. EP+ve 571 (МН)+ отримували з використанням способів, подібν) 3-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3них описаним у прикладі 1 vi. РХМС ЧУ=3,57 хвибензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3лин. іл)гексил)окси)бутил)фенілметансульфонамід ііі) 3-(3-((7-((5R)-5-(2,2-Диметил-4Н-1,3отримували з використанням способів, подіббензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3них описаним у прикладі 1 viii. EP+ve 575(MH)+ іл)гептил)окси)проп-1-ініл)бензолсульфонамід vi) (3-[4-((6-(((2R)-2-(2,2-Диметил-4-Н-1,3отримували з використанням способів, подіббензодіоксин-6-іл)-2-гідроксіетил)аміно)них описаним у прикладі 1 vii. РХМС ЧУ=3,51 хвигексил)окси)бутил)феніл)метансульфонамід лин. отримували з використанням способів, подібiv) 3-(3-((7-((5R)-5-(2,2-Диметил-4Н-1,3них описаним у прикладі 1 іх. EP+ve 549(MH)+ бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3vіі) (3-(4-((6-(((2R)-2-Гідрокси-2-(4-гідрокси-3іл)гептил)окси)пропіл)бензолсульфонамід (гідроксиметил)-феніл)-етил)аміно)отримували з використанням способів, подібгексил)оксилбутил)феніл)метансульфонамід них описаним у прикладі 1 viii. РХМС ЧУ=3,58 хвиотримували з використанням способів, подіблин. них описаним у прикладі 1 х. РХМС ЧУ=2,22 хвиv) 3-(3-((7-(((2R)-2-(2,2-Диметил-4Н-1,3лин EP+ve 509 (ΜΗ )+ бензодіоксин-6-іл)-2-гідроксіетил)аміно)Приклад 11: 3-(5-((5-(((2R)-2-Гідрокси-2-(4гептил)окси)пропіл)бензолсульфонамід гідрокси-3-(гідроксиметил)феніл)отримували з використанням способів, подібетил)аміно)пентил)оксилпентил)бензолсульфонам них описаним у прикладі 1 іх. РХМС ЧУ=2,75 хвиіду ацетат лин. 45 76443 46 vi) 3-(3-((7-(((2R)-2-Гідрокси-2-(4-гідрокси-3випарювали протягом ночі. Це розчиняли у етано(гідроксиметил)феніл)етил)аміно)-гептил)лі (10мл) та воді (5мл) і суміш кип'ятили під звороокси)пропіл)бензолсульфонаміду ацетат тним холодильником на паровій бані протягом 12 отримували з використанням способів, подібгодин з сульфітом натрію (0,138г). Суміш охолоних описаним у прикладі 1 х. РХМС ЧУ=2,46 хвиджували та твердий продукт збирали фільтруван+ лин, EP+ve 495 (МН) . ням, промивали водою та сушили. Цей залишок Приклад 13: 3-(6-(4-(((2R)-2-Гідрокси-2-(4кип'ятили під зворотним холодильником з оксихгідрокси-3-(гідроксиметил)феніл)етил)аміно)лоридом фосфору (4мл) під азотом протягом 4 бутокси)гексил)бензолсульфонаміду ацетат годин та далі видували сухим струмом азоту. 0,880 і) 6-(4-Бромбутокси)гекс-1-ин розчин аміаку (5мл) додавали та суміш кип'ятили отримували з використанням способів, подібпід зворотним холодильником протягом 2 годин. них описаним у прикладі 1 ν. РХМС ЧУ=3,49 хвиЩе розчин аміаку (5мл) додавали та кип'ятіння під лин. зворотним холодильником продовжували протяіі) (5R)-5-(2,2-Диметил-4Н-1,3-бензодіоксин-6гом 45 хвилин. Суміш охолоджували та твердий іл)-3-(4-(гекс-5-инілокси)бутил)-1,3-оксазолідин-2продукт збирали фільтруванням, промивали воон дою та сушили з утворенням потрібної сполуки отримували з використанням способів, подіб(0,2г). РХМС ЧУ=3,15 хвилин. них описаним у прикладі 1 vi. РХМС ЧУ=3,48 хвиііі) 4-(3-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3лин.' бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3iii) 3-(6-(4-((5R)-5-(2,2-Диметил-4Н-1,3іл)гексил)окси)бут-1-иніл)феніл)бутан-1бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3сульфонамід іл)бутокси)-гекс-1-иніл)бензолсульфонамід отримували з використанням способів, подіботримували з використанням способів, подібних описаним у прикладі 1 vii. РХМС ЧУ=3,62 хвиних описаним у прикладі 1 vii. РХМС ЧУ=3,42 хвилин. лин. іv) 4-(3-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3iv) 3-(6-(4-((5R)-3-(2,2-Диметил-4Н-1,3бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3іл)гексил)окси)бутил)феніл)бутан-1-сульфонамід іл)бутокси)гексил)бензолсульфонамід отримували з використанням способів, подіботримували з використанням способів, подібних описаним у прикладі 1 viii. РХМС ЧУ=3,71 хвиних описаним у прикладі 1 viii. РХМС ЧУ=3,58 хвилин. лин. v) 4-(3-(4-((6-(((2R)-2-Гідрокси-2-(4-гідрокси-3ν) 3-(6-(4-(((2R)-2-(2,2-Диметил-4Н-1,3(гідроксиметил)феніл)етил)аміно)бензодіоксин-6-іл)-2-гідроксіетил)аміно)гексил)окси)бутил)феніл)бутан-1-сульфонамід бутокси)гексил)бензолсульфонамід 4-(3-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3отримували з використанням способів, подіббензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3них описаним у прикладі 1 іх. РХМС ЧУ=2,66 хвиіл)гексил)окси)бутил)феніл)бутан-1-сульфонамід лин. (0,097г) перемішували та кип'ятили під зворотним vi) 3-(6-(4-(((2R)-2-Гідрокси-2-(4-гідрокси-3холодильником з триметилсиланоатом калію (0,1г) (гідроксиметил)феніл)етил)аміно)бутокси)під азотом протягом 2 годин. Суміш випарювали гексил)бензолсульфонаміду ацетат досуха та знов випарювали з метанолом. Залишок отримували з використанням способів, подібпереносили у метанол та завантажували у патрон них описаним у прикладі 1 х. РХМС ЧУ=2,47 хвиBond Elut SCX2 (10г), який попередньо обробили лин, EP+ve 495 (ΜΗ) 4. метанолом. Патрон залишали на 30 хвилин та Приклад 14: 4-(3-(4-((6-(((2R)-2-Гідрокси-2-(4далі елювали послідовно метанолом та далі 1% гідрокси-3-(гідроксиметил)феніл)етил)0,880 розчином водного аміаку у метанолі. Це дааміно)гексил)окси)бутил)феніл)бутан-1ло потрібну сполуку (0,064г), РХМС ЧУ=2,72 хвисульфонамід лин, EP+ve 551 (МН)+. і) 4-(3-Йодфенілбутилу метансульфонат Приклад 15: 3-(5-((6-(((2R)-2-Гідрокси-2-(44-(3-Йодфеніл)бутан-1-ол (1,7г) перемішували гідрокси-3з діізопропіламіном (1,74мл) та метансульфонілхгідроксимелоридом (0,66мл) у дихлорметані (50мл) при 21°С тил)феніл)етил)аміно)гексил)окси)пентил)бензолс протягом 2 годин. Розчин промивали послідовно ульфонамід розчином гідрокарбонату натрію, водою, водою, і) 5-((6-бромгексил)окси)пент-1-ин підкисленою кількома краплями 2М НСІ та водою, отримували з використанням способів, подібкожного разу знов екстрагуючи дихлорметаном. них описаним у прикладі 1 ν. 45 GCMS ЧУ = 5,6 Поєднані органічні шари сушили (MgSO4) та випахвилин рювали з утворенням потрібної сполуки (2,23г), ii) (5R)-5-(2,2-Диметил-4Н-1,3-бензодіоксин-6ТШХ Rf =0,28 (1:3 етилацетат у циклогексані) іл)-3-(6-(пент-4-инілокси)гексил-1,3-оксазолідин-2іі) 4-(3-йодфеніл)бутан-1-сульфонамід он 4-(3-Йодфеніл)бутилу метансульфонат отримували з використанням способів, подіб(0,354г) перемішували з йодидом натрію (0,75г) в них описаним у прикладі 1 iv. РХМС ЧУ=3,65 хвиацетоні (5мл) під азотом протягом 3 годин та при лин 35°С протягом 30 хвилин, руміш розподіляли між iii) 3-(5-((6-((5R)-5-(2,2-Диметил-4Н-1,3дихлорметаном та водою. Водний шар екстрагубензодіоксин-6-іл)-2-оксо-),3-оксазолідин-3вали ще дихлорметаном та поєднані органічні шаіл)гексил)окси)пент-1-иніл)бензолсульфонамід ри промивали водою. Після сушки (MgSO4) розчин отримували з використанням способів, подіб 47 76443 48 них описаним у прикладі 1 vii. РХМС ЧУ=3,76 хвиотримували з використанням способів, подіблин них описаним у прикладі 1 vii. РХМС ЧУ=3,52 хвиіv) 3-(6-((6-((5R)-5-(2,2-Диметил)-4Н-1,3лин бензодіоксин-3-іл)-2-оксо-1,3-оксазолідин-3iv) 3-(3-((6-((5R)-5-(2,2-Диметил-4Н-1,3іл)гексил)окси)пентил)бензолсульфонамід бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3отримували з використанням способів, подібіл)гексил )окси)пропіл)бензолсульфонамід них описаним у прикладі 1 viii. РХМС ЧУ=3,57 хвиотримували з використанням способів, подіблин них описаним у прикладі 1 viii. РХМС ЧУ=3,48 хвиv) 3-(5-((6-(((2R)-2-Гідрокси-2-(4-гідрокси-3лин (гідроксиметил)феніл)етил)аміно)ν) 3-(3-((6-(((2R)-2-(2,2-Диметил-4Н-1,3ексил)окси)пентил)бензолсульфонамід бензодіоксин-6-іл)-2-гідроксіетил)аміно)гексил )окотримували з використанням способів, подібси)пропіл)бензолсульфонамід них описаним у прикладі 14 ν. РХМС R=2,47 хвиотримували з використанням способів, подіблин, EP+ve 509 (МН)+. них описаним у прикладі 1 іх. РХМС ЧУ=2,81 хвиПриклад 16: 3-(6-((6-(((R)-2-Гідрокси-2-(4лин гідрокси-3vi) 3-(3-((6-(((2R)-2-Гідрокси-2-(4-гідрокси-3(гідроксиме(гідроксиметил)феніл)етил)аміно)гексил)тил)феніл)етил)аміно)гексил)окси)гексил)бензолсу окси)пропіл)бензолсульфонаміду ацетат льфонамід отримували з використанням способів, подібi) 6-((6-Бромгексил)окси)гекс-1-ин них описаним у прикладі 1 х. РХМС ЧУ=2,48 хвиотримували з використанням способів, подіблин, EP+ve 481 (MH)+. них описаним у прикладі 1 ν. GCMS ЧУ=5,99 хвиПриклад 18: 3-(4-((5-(((2R)-2-Гідрокси-2-(4лин гідрокси-3-(гідроксиметил)фенілетил)аміно)ii) (5R)-5-(2,2-Диметил-4Н-1,3-бензодіоксин-6пентил)окси)бутил)бензолсульфонаміду ацетат іл)-3-(6-(гекс-5-инілокси)гексил)-1,3-оксазолідин-2і) 4-((5-Бромпентил)окси)бут-1-ин он отримували з використанням способів, подіботримували з використанням способів, подібних описаним у прикладі 1 ν. них описаним у прикладі 1 iv. РХМС ЧУ=3,73 хви (MeOD) 3,43 (2Н, t, J ТГц), 3,41-3,32 (4H, m), лин 2,32 (2Н, dt, J 2,7Гц), 2,15 (1H, t, J 2Гц), 1,81-1,73 iii) 3-(6-((6-((5R)-5-(2,2-Диметил-4Н-1,3(2H, m), 1,54-1,38 (4Н, m). бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3ii) (5R)-3-(5-(Бут-3-инілокси)пентил)-5-(2,2іл)гексил)окси)гекс-1-иніл)бензолсульфонамід диметил-4Н-1,3-бензодіоксин-6-іл)-1,3отримували з використанням способів, подібоксазолідин-2-он них описаним у прикладі 1 vii. РХМС ЧУ=3,74 хвиотримували з використанням способів, подіблин них описаним у прикладі 1 vi. РХМС ЧУ=3,87 хвиiv) 3-(6-((6-((5R)-5-(2,2-Диметил-4Н-1,3лин бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3ііі) 3-(4-((5-((5R)-5-(2,2-Диметил-4Н-1,3іл)гексил)окси)гексил)бензолсульфонамід бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3отримували з використанням способів, подібіл)пентил)окси)бут-1-иніл)бензолсульфонамід них описаним у прикладі 1 viii. РХМС ЧУ=3,69 хвиотримували з використанням способів, подіблин них описаним у прикладі 1 vii. РХМС ЧУ=3,47 хвиv) 3-(6-((6-(((2R)-2-гідрокси-2-(4-гідрокси-3лин (гідроксиметил)феніл)етил)-аміно)гексил)окси)iv) 3-(4-((5-((5R)-5-(2,2-Диметил-4Н-1,3гексил)бензолсульфонамід бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3отримували з використанням способів, подібіл)пентил)окси)бутил)бензолсульфонамід них описаним у прикладі 14 ν. РХМС ЧУ=2,57 хвиотримували з використанням способів, подіблин, EP+ve 523 (МН)+. них описаним у прикладі 1 viii. РХМС ЧУ=3,37 хвиПриклад 17: 3-(3-((6-(((2R)-2-Гідрокси-2-(4лин гідрокси-3-(гідроксиметил)фенілетил)v) 3-(4-((5-(((2R)-2-(2,2-Диметил-4Н-1,3аміно)гексил)оксилпропіл)бензолсульфонаміду бензодіоксин-6-іл)-2-гідроксіетил)аміно)ацетат пентил)окси)бутил)бензолсульфонамід і) 3-((6-Бромгексил)окси)проп-1-ін отримували з використанням способів, подіботримували з використанням способів, подібних описаним у прикладі 1 іх. РХМС ЧУ=2,81 хвиних описаним у прикладі 1 ν. лин (CDCI3) 4,13 (2Н, s), 3,52 (2Н, t, J 7Гц), 3,41 vi) 3-(4-((5-(((2R)-2-Гідрокси-2-(4-гідрокси-3(2H, t, J 7Гц), 2,42 (1H, t, J 2Гц), 1,91-1,82 (2H, m), (гідроксиметил)фенілетил)аміно)пентил)1,66-1,58 (2Н, m) та 1,51-1,35 (4Н, m). окси)бутил)бензолсульфонаміду ацетат іі) (5R)-5-(2,2-Диметил-4Н-1,3-бензодіоксин-6отримували з використанням способів, подібіл)-3-(6-(проп-2-инілокси)гексил)-1,3-оксазолідин-2них описаним у прикладі 1 х. РХМС ЧУ=2,41 хви+ он лин, EP+ve481 (MH) . отримували з використанням способів, подібПриклад 19: N-(3-(Аміносульфоніл)феніл)-3них описаним у прикладі 1 vi. РХМС ЧУ=3,45 хви((4-((6-(((2R)-2-гідрокси-2-(4-гідрокси-3лин (гідроксимеііі) 3-(3-((6-((5R)-5-(2,2-Диметил-4Н-1,3тил)феніл)етил)аміно)гексил)окси)бутил)бензолсу бензодіоксин-6-іл)-оксо-1,3-оксазолідин-3льфонаміду ацетат іл)гексил)окси)проп-1-ініл)бензолсульфонамід N-(3-(Аміносульфоніл)феніл)-3-(4-((6-((5R)-5 49 76443 50 (2,2-диметил-4Н-1,3-бензодіоксин-6-іл)-2-оксо-1,3RP=0,63. оксазолідин-3-іл)гексил)окси)бут-1іі) 1-(2-Йодфеніл)метансульфонамід иніл)бензолсульфонамід отримували з використанням способів, подіботримували з використанням способів, подібних описаним у прикладі 10 ііі. РХМС ЧУ=2,44 хвиних описаним у прикладі 1 vii. РХМС ЧУ=3,72 хвилин лин. iii) 1-(2-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3і) N-(3-(Аміносульфоніл)феніл)-3-(4-((6-((5R)-5бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3(2,2-диметил-4Н-1,3-бензодіоксин-6-іл)-2-оксо-1,3іл)гексил)окси)бут-1-иніл)феніл метансульфонамід оксазолідин-3отримували з використанням способів, подібіл)гексил)окси)бутил)бензолсульфонамід них описаним у прикладі 1 vii. РХМС ЧУ=3,46 хвиотримували з використанням способів, подіблин них описаним у прикладі 1 viii. РХМСЧУ=3,61 хвиiv) 1-(2-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3лин. бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3іі) N-(3-(Аміносульфоніл)феніл)-3-(4-((6-(((2R)іл)гексил)окси)бутил)феніл)метансульфонамід 2(2,2-диметил)-4Н-1,3-бензодіоксин-6-іл)отримували з використанням способів, подібгідроксіених описаним у прикладі 1 viii. РХМС ЧУ=3,50 хвитил)аміно)гексил)окси)бутил)бензолсульфонамід лин отримували з використанням способів, подібv) 1-(2-(4-((6-(((2R)-2-Гідрокси-2-(4-гідрокси-3них описаним у прикладі 1 іх. РХМС ЧУ=2,88 хви(гідроксиметил)феніл)етил)аміно)лин. гексил)окси)бутил)феніл)метансульфонамід ііі) N-(3-(Амiносульфонiл)феніл)-3-(4-((6-(((2R)отримували з використанням способів, подіб2-Гідрокси-2-(4-Гідрокси-3них описаним у прикладі 14 ν. РХМС ЧУ = 2,40, (гідроксимеEP+ve 509 (МН)+. тил)феніл)етил)аміно)гексил)окси)бутил)бензолсу Приклад 22: N-бензил-3-(4-((6-(((2R)-2льфонаміду ацетат гідрокси-2-(4-гідрокси-3отримували з використанням способів, подіб(гідроксимених описаним у прикладі 1 х. РХМС ЧУ=2,95 хвитил)фенілетил)аміно)гексил)окси)бутил)бензолсул лин, EP+ve 650 (МН)+. ьфонаміду ацетат Приклад 20: 1-(4-(4-((6-(((2R)-2-Гідрокси-2-(4і) N-бензил-3-(4-((6-((5R)-5-(2,2-диметил-4Нгідрокси-3-(гідроксиметил)феніл))1,3-бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3етил)аміно)гексил)окси)бутил)фенілметансульфон іл)гексил)-окси)бут-1-иніл)бензолсульфонамід амід отримували з використанням способів, подіб+ і) Натрію (4-йодфеніл)метансульфонат них описаним у прикладі 6 і. EP+ve 647 (МН) отримували з використанням способів, подібіі) N-бензил-3-(4-((6-((5R)-5-(2,2-диметил-4Нних описаним у прикладі 10 і. ТШХ (SiO2, 1:1 1,3-бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3ЕtOАс/Циклогексан/1% АсОН) Rf=0,57). іл)гексил)окси)бутил)бензолсульфонамід іі) 1-(4-Йодфеніл)метансульфонамід отримували з використанням способів, подіботримували з використанням способів, подібних описаним у прикладі 1 viii. EP+ve 651 (МН)+ них описаним у прикладі 10 ііі. РХМС ЧУ=2,63 хвиііі) N-бензил-3-(4-((6-(((2R)-2-(2,2-диметил-4Нлин 1,3-бензодіоксин-6-іл)-2ііі) 1-(4-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3гідроксіебензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3тил)аміно)гексил)окси)бутил)бензолсульфонамід іл)гексил)-окси)бут-1отримували з використанням способів, подібиніл)феніл)метансульфонамід них описаним у прикладі 1 іх. EP+ve 625 (МН)+ отримували з використанням способів, подібiv) N-бензил-3-(4-((6-(((2R)-2-гідрокси-2-(4них описаним у прикладі 1 vii. РХМС ЧУ=3,43 хвигідрокси-3-отримували з використанням способів, лин подібних описаним у прикладі 1 х. РХМС ЧУ=2,72 iv) 1-(4-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3хвилин. EP+ve 585 (МН)+ бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3Приклад 23: 4-((1R)-2-((6-(4-(3іл)гексил)окси)бутил)феніл)метансульфонамід ((((Етиламіно)карбоніл)аміно)сульфоніл)отримували з використанням способів, подібфенілбутокси)гексил)аміно)-1-гідроксіетил)-1них описаним у прикладі 1 viii. РХМС ЧУ=3,50 хвигідрокси-2-(гідроксиметил)бензолу ацетат лин і) 3-(4-((6-((5R)-5-(2,2-Диметил-4Н-(3ν) 1-(4-(4-((6-(((2R)-2-Гідрокси-2-(4-гідрокси-3бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3(гідроксиметил)феніл)етил)аміно)іл)гексил)окси)бутил)-Nгексил)окси)бутил)феніл)метансульфонамід ((етиламіно)карбоніл)бензолсульфонамід отримували з використанням способів, подібЕтилізоціанат (0,015г) додавали до перемішуних описаним у прикладі 14 ν. РХМС ЧУ=2,35, ЕР ваної суміші 3-(4-((6-((5R)-5-(2,2-диметил-4Н-1,3+ve 509 (МН)+. бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3Приклад 21: 1-(2-(4-((6-(((2R)-2-Гідрокси-2-(4іл)гексил)окси)бутил)бензол-сульфонаміду (0,11г) гідрокси-3-(гідроксиметил)феніл)етил)та К2СО3 (0,055г) в ацетоні (2мл). Суміш гріли при аміно)гексил)окси)бутил)феніл)метансульфонамід кип'ятінні під зворотним холодильником протягом і) Натрію (2-йодфенілметансульфонат) 2 годин, далі додавали етилізоціанат (0,005г). Пісотримували з використанням способів, подібля 0,5 годин реакціїйну суміш охолоджували та них описаним у прикладі 10 і. гасили водою (1мл). Суміш розподіляли між ЕtOАс tic (SiO2, 1:1 ЕtOАс/Циклогексан/1% АсОН) (20мл) та Н2О (20мл). Водну фазу екстрагували 51 76443 52 ЕtOАс (20мл). Поєднані етилацетатні фази проми(гідроксиметил)фенілетил)аміно)гексил)вали розсолом (10мл) далі сушили (Na2SO4) та окси)бутил)бензолсульфонаміду ацетат концентрували. Залишок очищали SPE (діоксид отримували з використанням способів, подібних описаним у прикладі 1 х. РХМС ЧУ=2,44 хвисиліцію 5г) з СН2СІ2 (215мл), Et2O (215мл) та лин, EP+ve 495 (МН)+ ЕtOАс (215мл), випарювання фракцій з ЕtOАс + Приклад 26: N-(4-(((3-(4-((6-(((2R)-2-Гідрокси-2дало потрібну сполуку (0,067г). EP+ve 632 (МН) (4-гідрокси-3іі) 4-((1R)-2-((6-(4-(3(гідроксиме((((Етиламітил)феніл)етил)аміно)гексил)окси)бутил)феніл)сул но)карбоніл)аміно)сульфоніл)фенілбутокси)ьфоніл)аміно)феніл)ацетаміду ацетат гексил)аміно)-1-гідроксіетил)-1-гідрокси-2і) N-(4-(((3-(4-((6-((5R)-5-(2,2-Димeтил-4H-1,3(гідроксиметил)бензолу ацетат бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3отримували з використанням способів, подібіл)гексил)окси)бут-1них описаним у прикладі 1 х. РХМС ЧУ=2,86 хвииніл)феніл)сульфоніл)аміно)феніл)ацетамід лин, EP+ve 606 (МН)+ отримували з використанням способів, подібПриклад 24: 3-(4-((6-((2-Гідрокси-2-(4-гідроксиних описаним у прикладі 1 vii. EP-ve 688 (М-Н) 3ii) N-(4-(((3-(4-((6-((5R)-3-(2,2-Диметил-4Н-1,3(гідроксимебензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3тил)феніл)етил)аміно)гексил)окси)бутил)бензолсу іл)гексил)окси)бутил)феніл)сульфоніл)аміно)феніл льфонаміду ацетат )ацетамід і) трет-бутил 2-(2,2-диметил-4Н-1,3отримували з використанням способів, подіббензодіоксин-6-іл)-2-гідроксіетилкарбамат них описаним у прикладі 1 viii. EP-ve 692 (М-Н)~ Перекристалізація партії 3:1 (R:S) Прикладу 1 ііі) N-(4-(((3-(4-((6-(((2R)-2-(2,2-Диметил-4Н-1,3ііі (78,94г) дала потрібну сполуку (27,6г). РХМС бензодіоксин-6-іл)-2-гідроксіетил)аміно)ЧУ=3,31 хвилин гексил)окси)бутил)феніл)сульфоніл)аміно)іі) 5-(2,2-Диметил-4Н-1,3-бензодіоксин-6-іл)феніл)ацетамід 1,3-оксазолідин-2-он отримували з використанням способів, подіботримували з використанням способів, подібних описаним у прикладі 1 іх. EP+ve 668 (МН)+ них описаним у прикладі 1 iv. EP+ve 250 (МН)+ iv) N-(4-(((3-(4-((6-(((2R)-2-Гідрокси-2-(4ііі) 3-(6-(Бут-3-инілокси)гексил)-5-(2,2-диметилгідрокси-34Н-1,3-бензодіоксин-6-іл)-1,3-оксазолідин-2-он (гідроксимеотримували з використанням способів, подібтил)феніл)етил)аміно)гексил)окси)бутил)феніл)сул них описаним у прикладі 1 vi. EP+ve 402 (МН)+ ьфоніл)аміно)феніл)ацетаміду ацетат GW671337A iv) 3-(4-((6-(5-(2,2-Диметил-4Н-1,3R5965/48/11 бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3отримували з використанням способів, подібіл)гексил)окси)бут-1-иніл)бензспесульфонамід них описаним у прикладі 1 х. РХМС ЧУ = 2,59 хвиотримували з використанням способів, подіблин, EP+ve 628 (ΜΗ)* них описаним у прикладі 1 vii. EP+ve 557 (МН)+ Приклад 27: N-Циклобутил-3-(4-((6-(((2R)-2ν) 3-(4-((6-(5-(2,2-Диметил-4Н-1,3Гідрокси-2-(4-Гідрокси-3бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3(гідроксимеіл)гексил)окси)бутил)бензолсульфонамід тил)феніл'|етил)аміно)гексил)окси)бутил)бензолсу отримували з використанням способів, подібльфонамід ацетат них описаним у прикладі 1 viii. EP+ve 561 (МН)+ i) N-Циклобутил-3-(4-((6-((5R)-5-(2,2-диметилvi) 3-(4-((6-((2-(2,2-Диметил-4Н-1,34Н-1,3-бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3бензодіоксин-6-іл)-2-гідроксіетил)аміноігексил)іл)гексил)окси)бут-1-иніл)бензолсульфонамід окси)бутил)бензолсульфонамід отримували з використанням способів, подіботримували з використанням способів, подібних описаним у прикладі 1 vii. EP+ve 611(МН)+ них описаним у прикладі 1 іх. EP+ve 535 (МН)+ іі) N-Циклобутил-3-(4-((6-((5R)-5-(2,2-диметилvi) 3-(4-((6-((2-Гідрокси-2-(4-гідрокси-34Н-1,3-бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3(гідроксиметил)фенілетил)аміно)гексил)іл)гексил)окси)бутил)бензолсульфонамід окси)бутил)бензолсульфонаміду ацетат отримували з використанням способів, подіботримували з використанням способів, подібних описаним у прикладі 1 viii. EP+ve615(MH)+ них описаним у прикладі 1 х. РХМС ЧУ=2,90 хвиііі) N-Циклобутил-3-(4-((6-(((2R)-2-(2,2лин, EP+ve 495 (МН)+ диметил-4Н-1,3-бензодіоксин-6-іл)-2Приклад 25: 3-(4-((6-(((2S)-2-Гідрокси-2-(4гідроксіегідрокси-3тил)аміно)гексил)окси)бутил)бензолсульфонамід (гідроксиметил)феніл)етил)аміно)гексил)оксил отримували з використанням способів, подіббутил)бензолсульфонаміду ацетат них описаним у прикладі 1 іх. EP+ve 589 (МН)+ і) 3-(4-((6-(((2S)-2-(2,2-Диметил-4Н-1,3іv) N-Циклобутил-3-(4-((6-(((2R)-2-гідрокси-2-(4бензодіоксин-6-1л)-2-гідроксiетил)амiно)гідрокси-3-(гідроксиметил)феніл)гексил)окси)бутил)бензолсульфонамід етил)аміно)гексил)окси)бутил)бензолсульфонамід Розділення 3-(4-((6-((2-(2,2-диметил-4Н-1,3у ацетат бензодіоксин-6-іл)-2-гідроксіетил)аміно)отримували з використанням способів, подібгексил)окси)бутил)бензолсульфонаміду (0,403г) на них описаним у прикладі 1 х. РХМС ЧУ = 2,72 хвиколонці ВЕРХ Chiralcel OJ з використанням суміші лин, EP+ve 549 (МН)+ 40% етанол/гептан дало потрібну сполуку (0,096г). Приклад 28: N-Циклогексил-3-(4-((6-(((2R)-2іі) 3-(4-((6-(((2S)-2-Гідрокси-2-(4-гідрокси-3 53 76443 54 Гідрокси-2-(4-Гідрокси-3-(гідроксиметил)отримували з використанням способів, подібфених описаним у прикладі 6 і. EP+ve 645 (МН)+ ніл)етил)аміно)гексил)окси)бутил)бензолсульфона іі) 3-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3міду ацетат бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3і) N-Циклогексил-3-(4-((6-((5R)-5-(2,2-диметиліл)гексил)окси)бутил)-N-(2-(24Н-1,3-бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3гідроксіетокси)етил)бензолсульфонамід ілгексил)окси)бут-1-иніл)бензолсульфонамід отримували з використанням способів, подіботримували з використанням способів, подібних описаним у прикладі 1 viii. EP+ve 647 (МН)+ них описаним у прикладі 1 vii. EP+ve 639 (МН)+ iii) N-(2-(2-Гідроксiетокси)етил)-3-(4-((6-(((2R)іі) N-Циклогексил-3-(4-((6-((5R)-5-(2,2-диметил2-Гідрокси-2-(4-Гідрокси-3-(Гідроксиметил)4Н-1,3-бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3феіл)гексил)-окси)бутил)бензолсульфонамід ніл)етил)аміно)гексил)окси)бутил)бензолсульфона отримували з використанням способів, подібмід них описаним у прикладі 1 viii. EP+ve 643 (МН)+ отримували з використанням способів, подібііі) N-Циклогексил-3-(4-((6-(((2R)-2-(2,2них описаним у прикладі 14 ν. РХМС ЧУ = 2,62 диметил-4Н-1,3-бензодіоксин-6-іл)-2хвилин, EP+ve 583 (МН)+ гідроксіеПриклад 31: N-(4-Флуорфеніл)-3-(4-((6-(((2R)тил)аміно)гексил)окси)бутил)бензолсульфонамід 2-гідрокси-2-(4-гідрокси-3отримували з використанням способів, подіб(гідроксимених описаним у прикладі 1 іх. EP+ve 617 (МН)+ тил)феніл)етил)аміно)гексил)окси)бутил)бензолсу іv) N-Циклогексил-3-(4-((6-(((2R)-2-гідрокси-2льфонаміду ацетат (4-гідрокси-3-(гідроксиметил)фенілетил)і) 3-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3аміно)гексил)окси)бутил)бензолсульфонаміду ацебензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3тат іл)гексил)окси)бут-1-иніл)-N-(4отримували з використанням способів, подібфлуорфеніл)бензолсульфонамід них описаним у прикладі 1 х. РХМС ЧУ=2,85 хвиотримували з використанням способів, подіблин, EP+ve577 (МН)+ них описаним у прикладі 1 vii. EP+ve 651 (МН)+ Приклад 29: 3-(4-((6-(((2R)-2-Гідрокси-2-(4іі) 3-(4-((6-((5R)-5-(2,2-диметил-4Н-1,3гідрокси-3бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3(гідроксимеіл)гексил)окси)бутил)-N-(4тил)феніл)етил)аміно)гексил)окси)бутил)-N-(2флуорфенілбензолсульфонамід) морфолін-4-ілетил)-бензолсульфонаміду ацетат отримували з використанням способів, подіб+ і) 3-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3них описаним у прикладі 1 viii. EP+ve 655 (МН) бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3iii) 3-(4-((6-(((2R)-2-(2,2-Диметил-4Н-1,3іл)гексил)окси)бут-1-иніл-N-(2-морфолін-4бензодіоксин-6-іл)-2ілетил)бензолсульфонамід гідроксіетил)аміноігексил)окси)бутил)-N-(4отримували з використанням способів, подібфлуорфеніл)бензолсульфонамід них описаним у прикладі 1 vii. EP+ve 670 (МН)+ отримували з використанням способів, подібіі) 3-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3них описаним у прикладі 1 іх. EP+ve 629 (MH)+ бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3iv) N-(4-Флуорфеніл)-3-(4-((6-(((2R)-2-гідроксиіл)гексил)окси)бутил)-N-(2-морфолін-42-(4-гідрокси-3ілетил)бензолсульфонамід (гідроксимеотримували з використанням способів, подібтил)феніл)етил)аміно)гексил)окси)бутил)бензолсу них описаним у прикладі 1 viii. EP+ve 674 (Mtff льфонаміду ацетат ііі) 3-(4-((6-(((2R)-2-(2,2-Диметил-4Н-1,3отримували з використанням способів, подіббензодіоксин-6-іл)-2-гідроксіетил)-аміно)них описаним у прикладі 1 х. РХМС ЧУ=2,81 хвигексил)окси)бутил)-N-(2-морфолін-4лин, EP+ve 589 (МН)+ ілетил)бензолсульфонамід Приклад 32; N-(4-(Аміносульфоніл)феніл)-3-(4отримували з використанням способів, подіб((6-(((2R)-2-гідрокси-2-(4-гідрокси-3них описаним у прикладі 1 іх. EP+ve 648 (МН)+ (гідроксимеiv) 3-(4-((6-(((2R)-2-Гідрокси-2-(4-гідрокси-3тил)феніл)етил)аміно)гексил)окси)бутил)бензолсу (гідроксиметил)феніл)етил)аміно)льфонаміду ацетат гексил)окси)бутин-N-(2-морфолін-4і) N-(4-(Аміносульфоніл)феніл)-3-(4-((6-((5R)-5ілетил)бензолсульфонаміду ацетат (2,2-диметил-4Н-1,3-бензодіоксин-6-іл)-2-оксо-1,3отримували з використанням способів, подібоксазолідин-3-іл)гексил)окси)бут-1них описаним у прикладі 1 х. РХМС ЧУ=2,22 хвииніл)бензолсульфонамід лин, EP+ve 608 (МН)+ отримували з використанням способів, подібПриклад 30: N-(2-(2-Гідроксіетокси)етил)-3-(4них описаним у прикладі 1 vii. EP+ve 712 (МН)+ ((6-(((2R)-2-гідрокси-2-(4-гідрокси-3іі) N-(4-(Аміносульфоніл)феніл)-3-(4-((6-((5R)(гідроксиме5-(2,2-диметил!-4Н-1,3-бензодіоксин-6-іл)-2-оксотил)феніл)етил)аміно)гексил)окси)бутил)бензолсу 1,3-оксазолідин-3льфонамід іл)гексил)окси)бутил)бензолсульфонамід і) 3-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3отримували з використанням способів, подіббензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3них описаним у прикладі 1 viii. EP+ve 716 (МН)+ іл)гексил)окси)бут-1-иніл)-N-(2-(2ііі) N-(4-(Аміносульфоніл)феніл)-3-(4-((6-(((2R)гідроксіетокси)етил)бензолсульфонамід 2-(2,2-диметил-4Н-1,3-бензодіоксин-6-іл)-2 55 76443 56 гідроксіетил)аміно)гексил)оксил буних описаним у прикладі 1 х. РХМС ЧУ = 2,90 хвитил)бензолсульфонамід лин, EP+ve 613 (МН)+ отримували з використанням способів, подібПриклад 35: 5-(4-((6-(((2R)-2-гідрокси-2-(4них описаним у прикладі 1 іх. EP+ve 690 (МН)+ гідрокси-3-(гідроксиметил)-фенілетил)аміно)iv) N-(4-(Аміносульфоніл)феніл)-3-(4-((6-(((2R)гексил)окси)бутил)-2-метоксибензолсульФонаміду 2-гідрокси-2-(4-гідрокси-3ацетат (гідроксимеі) 5-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3тил)феніл)етил)аміно)гексил)окси)бутил)бензолсу бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3льфонаміду ацетат іл)гексил)окси)бут-1-иніл)-2-метоксибензолсул отримували з використанням способів, подібьфонамід них описаним у прикладі 1 х. РХМС ЧУ = 2,61 хвиотримували з використанням способів, подіблин, EP+ve 650 (МН)+ них описаним у прикладі 1 vii. EP+ve 587 (МН)+ Приклад 33: 2-(Гідроксиметил-4-(1R)-1іі) 5-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3гідрокси-2-((6-(4-(3-(піперазин-1бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3ілсульфоіл)гексил)окси)бутил)-2ніл)феніл)бутокси)гексил)аміно)етил)фенолу ацеметоксибензолсульфонамід тат отримували з використанням способів, подібі) (5R)-5-(2,2-Диметил-4Н-1,3-бензодіоксин-6них описаним у прикладі 1 viii. EP+ve 591 (МН)+ іл)-3-(6-((4-(3-(піперазин-1-ілсульфоніл)фенілбут-3iii) 5-(4-((6-(((2R)-2-(2,2-Диметил-4Н-1,3иніл)окси)гексил)-1,3-оксазолідин-2-он бензодіоксин-6-іл)-2-гідроксіетил)аміно)отримували з використанням способів, подібгексил)окси)бутил)-2-метоксибензолсульфонамід них описаним у прикладі 1 vii. EP+ve 626 (МН)+ отримували з використанням способів, подібii) (5R)-8-(2,2-Диметил-4Н-1,3-бензодіоксин-6них описаним у прикладі 1 іх. EP+ve 565 (МН)+ іл)-3-(6-(4-(3-(піперазин-1iv) 5-(4-((6-(((2R)-2-Гідрокси-2-(4-гідрокси-3ілсульфоніл)фенілбутокси|гексил)-1,3-оксазолідин(гідроксиметил)феніл)етил)2-он аміно)гексил)окси)бутил)-2отримували з використанням способів, подібметоксибензолсульфонаміду ацетат них описаним у прикладі 1 viii. EP+ve 630 (ΜΗ)"1" отримували з використанням способів, подібiii) (1R)-1-(2,2-Диметил-4Н-1,3-бензодіоксин-6них описаним у прикладі 1 х. РХМС ЧУ = 2,41 хвиіл)-2-((6-(4-(3-піперазин-1лин, EP+ve 525 (МН)+ ілсульфоніл)феніл)бутокси)гексил)аміно)етанол Приклад 36: (Е)-2-(3-(4-((6-(((2R)-2-Гідрокси-2отримували з використанням способів, подіб(4-гідрокси-3-(гідроксиметил)фенілетил)+ них описаним у прикладі 1 іх. EP+ve 604 (МН) аміно)гексил)окси)бутил)феніл)-Niv) 2-(Гідроксиметил-4-1(1R)-1-гідрокси-2-((6метилетенсульфонамід (4-(3-(піперазин-1-ілсульфоніл)феніл)і) 4-О-Бромфеніл)бут-3-ил)-1-ол бутокси)гексил)аміно)етил)фенолу ацетат Перемішуваний охолоджений розчин 1-бромотримували з використанням способів, подіб3-йодбензолу (31г) та 3-бутин-олу (7мл) в ацетоніних описаним у прикладі 1 х. РХМС ЧУ = 2,23 хвитрилі (100мл) та триетиламіні (100мл) продували лин, EP+ve 564 (МН)+ азотом протягом 20 хвилин під азотом. ДихлорПриклад 34: 3-(4-((6-(((2R)-2-Гідрокси-2-(4біс(трифенілфосфін)паладій (500мг) та йодид купгідрокси-3-(гідроксиметил)феніл)етил)руму (800мг) додавали. Суміш перемішували проаміно)гексил)окси)бутил)-N-((-метил-1тягом 18 годин та далі розчинник видаляли у фенілетил)бензолсульфонаміду ацетат вакуумі. Остаточне масло розтирали з етилацетаі) 3-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3том (200мл) та фільтрували. Фільтрат випарювали бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3досуха та залишок очищали хроматографією на іл)гексил)окси)бут-1-иніл)-N-(1-метил-1Biotage (90г), елюючи світлим керосином 40-60°С фенілетил)бензолсульфонамід діетиловим етером (3:2) з утворенням потрібної отримували з використанням способів, подібсполуки (21г). РХМС ЧУ = 3,26 хвилин. них описаним у прикладі 1 vii. EP-ve 673 (М-Н)~ ii) 4-(3-Бромфеніл)бутан-1-ол іі) 3-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3Розчин 4-(3-бромфеніл)бут-3-ин-1-олу (21г) у бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3етанолі (1000мл) гідрували над оксидом платини іл)гексил)окси)бутил)-N-((-метил-1(500мг) протягом 4 годин. Каталізатор видаляли фенілетил)бензолсульфонамід фільтруванням та фільтрат випарювали з утвоотримували з використанням способів, подібренням потрібної сполуки (18г) ТШХ (SiO2) діетиних описаним у прикладі 1 viii. EP-ve 677 (М-Н) ловий етер Rf=0,38. ііі) 3-(4-((6-(((2R)-2-(2,2-Диметил-4Н-1,3ііі) 1-Бром-3-(4-((6бензодіоксин-6-іл)-2-гідроксіетил)-аміно)бромгексил)окси)бутил)бензол гексил)окси)бутил)-N-(1-метил-1Перемішувану суміш 4-(3-бромфеніл)бутан-1фенілетил)бензолсульфонамід олу (18г) та 1,6 дибромгексану (48мл) у 50% водотримували з використанням способів, подібному гідроксиді натрію (500мл) з бромідом тетраних описаним у прикладі 1 іх. EP+ve 653 (МН)+ бутиламонію (1,5г) перемішували протягом 2 годин iv) 3-(4-((6-(((2R)-2-Гідрокси-2-(4-гідрокси-3при 20°. Суміш виливали у воду (1000мл) та екст(Гідроксиметил)феніл)етилВ-аміно)гексил)рагували етилацетатом (3500мл). Поєднані екстокси)бутил)-N-(1-метил-1ракти промивали водою (1000мл), сушили сульфенілетил)бензолсульфонаміду ацетат фатом натрію. Розчинник видаляли у вакуумі та отримували з використанням способів, подібостаточне масло очищали флеш-хроматографією 57 76443 58 (500г) з використанням дихлорметану як елюенту, метилетансульфонамід, сполука з (2Е)-бут-2замінюючи на суміш світлий керосин (40-60°)ендюновою кислотою (1:1) діетиловий етер (9:1) з утворенням потрібної споРозчин (Е)-2-(3-(4-((6-(((2R)-2-гідрокси-2-(4луки (18г). РХМС ЧУ = 4,34 хвилин. гідрокси-3-(пдроксиметил)феніл)етил)iv) (5R)-3-(6-(4-(3-Бромфенілбутокси)гексил)-5аміно)гексил)окси)бутил)феніл)-N(2,2-диметил-4Н-1,3-бензодіоксин-6-іл)-1,3метилетенсульфонаміду (60мг) та фумарової кисоксазолідин-2-он лоти (6,5мг) у етанолі випарювали досуха з утвоГідрид натрію (60% дисперсія у маслi, 690мг) ренням потрібної сполуки (66мг) РХМС ЧУ = 2,65 додавали до перемішуваного розчину 5R-(2,2хвилин, EP+ve 537 (МН)+ диметил-4Н-1,3-бензодіоксин-6-іл)-1,3Приклад 37: 2-(3-(4-((6-(((2R)-2-Гідрокси-2-(4оксазолідин-2-ону (3,0г) у сухому ДМФ (35мл) при гідрокси-3-(гідроксиметил)феніл)етил)5°С під азотом. Після 20 хвилин додавали розчин аміно)гексил)окси)бутил)феніл)етансульфонамід 1-бром-3-(4-((6-бромгексил)окси)бутил)бензолу і) трет-бутил вінілсульфонілкарбамат (5,64г) у сухому ДМФ (15мл). Суміш перемішували Ди-трет-бутилдикарбонат цезію (8,62г) додапри · зовнішній температурі протягом 4 годин. Сували до перемішуваного охолодженого на льодяміш виливали у розчин хлориду амонію (300мл) та ній бані розчину етенсульфонаміду (S Hirooka, Bull. Chem. Soc. Jpn. 1991, 64, 1431) (3,4г), 4екстрагували етилацетатом (3100мл). Поєднані (диметиламіно)піридину (410мг) та триетиламіну екстракти промивали водою (200мл), сушили су(7мл) у дихлорметані (40мл) під азотом. Розчин льфатом натрію та випарювали. Остаточне масло перемішували протягом 30 хвилин, промивали 2М очищали хроматографією на Biotage (90г), елюючи гідрохлоридною кислотою (30мл), водою (50мл) та сумішшю діетиловий етер-світлий керосин сушили (Na2SO4) з утворенням потрібної сполуки (темп.кипіння 40-60°С) (4:1) з утворенням потріб(5,0г) ТШХ (SiO2, 1:1 діетиловий етер-циклогексан) ної сполуки (5,2г). РХМС ЧУ=4,13 хвилин. Rf=0,4. ν) (Е)-2-(3-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3іі) (Е)-2-(3-(4-((6-((5R)-5-(2,2-Диметил-4Н-1,3бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3бензодюксин-6-іл)-2-оксо-1,3-оксазолідин-3іл)гексил)окси)бутил)феніл)-Nіл)гексил)окси)бутил)феніл)етенсульфонамід метилетенсульфонамід Отримували з використанням способів, подібПеремішувану суміш (5R)-3-(6-(4-(3них описаним у прикладі 36 ν. РХМС ЧУ = 3,6 хвибромфеніл)бутокси)гексил)-5-(2,2-диметил-4Н-1,3лин бензодюксин-6-іл)-1,3-оксазолідин-2-ону (1,0г), Nііі) (Е)-2-(3-(4-((6-(((2R)-2-(22-Диметил-4Н-1,3метилетенсульфонаміду (WO 95/09166), (462мг) бензодіоксин-6-іл)-2-гідроксіетил)три-о-толілфосфіну (200мг), ацетату паладію аміно)гексил)окси)бутил)феніл)етенсульфонамід (165мг) та триетиламіну (5мл) у сухому ДМФ Отримували з використанням способів, подіб(15мл) гріли при 90°С протягом 18 годин. Суміш них описаним у прикладі 1 іх. РХМС ЧУ=2,87 хвиохолоджували та фільтрували. Фільтрат виливали лин у воду (200мл) та екстрагували етилацетатом iv) (Е)-2-(3-(4-((6-(((2R)-2-Гідрокси-2-(4(350мл). Поєднані екстракти промивали водою гідрокси-3-(гідроксиметил)феніл)етил)(100мл) та (Na2SO4) та випарювали у вакуумі. Осаміно)гексил)окси)-бутил)феніл)етенсульфонамід таточне масло очищали хроматографією на Отримували з використанням способів, подібBiotage (40г) елюючи сумішшю діетиловий етерних описаним у прикладі 1 х. РХМС ЧУ = 2,55 хвиетилацетат (9:1) з утворенням потрібної сполуки лин (220мг) РХМС ЧУ = 3,70 хвилин. v) 2-(3-(4-((6-(((2R)-2-Гідрокси-2-(4-гідрокси-3vі) (Е)-2-(3-(4-((6-(((2R)-2-(2,2-Диметил-4Н-1,3(гідроксиметил)феніл)етил)аміно)-гексил)окси)бензодюксин-6-іл)-2-гідроксіетил)бутил)феніл)етансульфонамід аміно)гексил)окси)бутил)феніл)-NОтримували з використанням способів, подібметилетенсульфонамід них описаним у прикладі 1 viii. РХМС ЧУ = 2,73 Отримували з використанням способів, подібхвилин, EP+ve 523 (МН)+ них описаним у прикладі Ііх. РХМС ЧУ = 2 96 хвиПриклад 38: 5-(4-((6-(((2R)-2-Гідрокси-2-(4лин гідрокси-3vіі) (Е)-2-(3-(4-((6-(((2R)-2-Гідрокси-2-(4(гідроксимегідрокси-3-(гідроксиметил)феніл)етил)тил)фенілетил)аміно)гексил)окси)бутил)(1,1'аміно)гексил)окси)бутил)феніл)-Nдифеніл)-3-сульфонаміду ацетат метилетенсульфонамід і) трет-бутил (3,5Розчин (Е)-2-(3-(4-((6-(((2R)-2-(2,2-диметил-4Ндійодфеніл)сульфонілкарбамат 1,3-бензодюксин-6-іл)-2Ди-трет-бутилдикарбонат цезію(І.I 1г) додавагідроксіетил)аміно)гексил)окси)бутил)феніл)-Nли до перемішуваного розчину 3,5 ди-йодметилетенсульфонаміду (100мг) у метанолі (15мл) бензолсульфонаміду (Tsatsas, Chem. Chron. 1974, завантажували у патрон Bond Elut SCX2 (10г), який 3, 143) (1,6г), 4-(диметиламіно)піридину (50мг) та попередньо промивали метанолом. Патрон елютриетиламіну (0,8мл) у дихлорметані (30мл) при вали метанолом (225мл), а потім сумішшю 15% 5°С. Розчин перемішували при зовнішній темпераводний. аміаку-метанол (220мл). Випарювання турі протягом 1 години, промивали 1М гідрохлориостанніх фракцій дало потрібну сполуку (70мг) + дною кислотою (30мл), водою (50мл) та сушили РХМС ЧУ = 2,59 хвилин, EP+ve 535 (МН) сульфатом натрію . Розчинник випарювали з утвоviiі) (Е)-2-(3-(4-((6-(((2R)-2-гідрокси-2-(4ренням потрібної сполуки (1,6г). РХМС ЧУ = 4,24 гідрокси-3-(гідроксиметил)феніл)етил)хвилин. аміно)гексил)окси)бутил)феніл)-N 59 76443 60 іі) трет-бутил (3.5-дийодфеніл)сульфоніл((2Отримували з використанням способів, подіб(триметилсиліл)етокси)метил)карбамат них описаним у прикладі 1 iх. РХМС ЧУ = 2,86 хвиГідрид натрію (60% дисперсія у масл, 157мг) лин. додавали до перемішуваного розчину трет-бутилу vii) 5-(4-((6-(((2R)-2-Гідрокси-2-(4-гідрокси-3(3,5-дийодфеніл)сульфонілкарбамату (1,6г) у ДМФ (гідроксиме(10мл) при 5°С під азотом. Після 10 хвилин додатил)феніл)етил)аміно)гексил)окси)бутил)(1,1'вали 2-(триметилсиліл)етоксиметилхлорид дифеніл)-3-сульфонаміду ацетат (0,61мл). Суміш перемішували протягом 30 хвиОтримували з використанням способів, подіблин. Реакційну суміш виливали у водний хлорид них описаним у прикладі 1 х. РХМС ЧУ=2,76 хвиамонію (100мл) та екстрагували діетиловим етелин, EP+ve571(MH)+. Приклад 39: 3-(4-((6-(((2R)-2-Гідрокси-2-(4ром (340мл). Органічні екстракти промивали вогідрокси-3-(гідроксиметил)феніл)етил)дою (30мл), сушили (Na2SO4) та випарювали з аміно)гексил)окси)бутил)-5утворенням потрібної сполуки (1,95г). РХМС ЧУ = пентилбензолсульФонаміду ацетат 4,47 хвилин. і) трет-бутилу (3-(4-((6-((5R)-5-(2,2-диметилііі) трет-бутил (3-(4-((6-((5R)-5-(2,2-диметил4Н-1,3-бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-34Н-1,3-бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3іл)гексил)окси)бут-1-иніл)-5-пент-1іл)гексил)окси)бут-1-иніл)-5инілфеніл)сульфоніл((2-(триметилсиліл)йодфеніл)сульфоніл((2-(триметилсиліл)етокси)етоксилметил)карбамат метил)карбамат Отримували з використанням способів, подібРозчин (5R) 3-(6-(бут-3-инілокси)гексил)-5-(2,2них описаним у прикладі 1 vii. РХМС ЧУ = 4,77 диметил-4Н-1,3-бензодіоксин-б-іл)-1,3хвилин. оксазолідин-2-ону (233мг) та трет-бутилу (3,5ii) трет-бутилу (3-(4-((6-((5R)-5-(2,2-диметилдийодфеніл)сульфоніл((24Н-1,3-бензодіоксин-6-іл)-2-оксо-1,3-оксазолідин-3(триметилсиліл)етокси)метил)карбамату (410мг) у iл)гексил)-окси)бутил)-5сухому ацетонітрилі (3мл) та триетиламіні (3мл) пентилфеніл)сульфоніл((2продували азотом протягом 30 хвилин. Йодид куп(триметилсиліл)етокси)-метил)карбамат руму (50мг) та дихлорбіс(трифенілфосфін)паладій Отримували з використанням способів, подіб(50мг) додавали далі. Суміш перемішували протяних описаним у прикладі 1 viii. РХМС ЧУ = 4,7 хвигом 18 годин при зовнішній температурі та далі лин. випарювали досуха. Остаточне масло очищали ііі) 3-(4-((6-(((2R)-2-(2,2-Диметил-4Н-1,3хроматографією на Biotage (8г), елюючи сумішшю бензодіоксин-6-іл)-2-гідроксіетил)аміно)діетиловий етер:петролейний ефір (темп. кипіння гексил)окси)бутил)-5-пентилбензолсульфонамід 40-60°), прийнятні фракції випарювали з утворенОтримували з використанням способів, подібням потрібної сполуки (190мг). РХМС ЧУ = 4,54 них описаним у прикладі 1 іх. РХМС ЧУ = 3,21 хвихвилин. лин. iv) 3-(((трет-бутоксикарбоніл)((2iv) 3-(4-((6-(((2R)-2-Гідрокси-2-(4-гідрокси-3(триметилсиліл)етокси)метил)аміно)сульфоніл)-5(гідроксиметил)феніл)етил)(4-((6-((5R)-5-(2,2-диметил-4Н-1,3-бензодіоксин-6аміно)гексил)окси)бутил)-5іл)-2-оксо-1,3-оксазолідин-3-іл)гексил)окси)бут-1пентилбензолсульфонаміду ацетат иніл-1,1'-дифеніл Отримували з використанням способів, подібПеремішувану суміш трет-бутилу (3-(4-((6них описаним у прикладі 1 x. РХМС ЧУ = 2,93 хви((5R)-5-(2,2-диметил-4Н-1,3-бензодіоксин-6-іл)-2лин, EP+ve 565 (МН)+ оксо-1,3-оксазолідин-3-іл)гексил)окси)бут-1-иніл)Приклад 40: 3-(4-((6-(((2R)-2Гідрокси-2-(45-йодфеніл)сульфоніл((2гідрокси-3(триметилсиліл)етокси)метил)карбамату (190мг), (гідроксимебензолборонової кислоти (62мг) у диметоксіетані тил)феніл)етил)аміногексил)окси)бутил)бензолсул (4мл) та 1М карбонату натрію (2мл) з тетраьфонамід кіс(трифенілфосфін)паладієм(0) (25мг) гріли при і) 6-(Бут-3-инілокси)гексаналь 80°С протягом 1 години. Суміш виливали у воду 6-Бромгексилбут-3-иніловий етер (20мл) та екстрагували етилацетатом (330мл). (DE3513885A1) (525мг) у ДМСО (2мл) додавали до Органічні екстракти сушили (Na2SO4) та випарюсуміші гідрокарбонату натрію (1г) у ДМСО (8мл) вали. Остаточне масло очищали хроматографією при 150°С з інтенсивним перемішуванням та прона Biotage (8г), елюючи сумішшю циклогексанпусканням азоту через розчин. Суміш перемішудіетиловий етер (4:1) з утворенням потрібної сповали протягом 20 хвилин при 150°С та далі давали луки (140мг). РХМС ЧУ = 4,54 хвилин. охолонути до кімнатної температури, розбавляли ν) 3-(((трет-бутоксикарбоніл)((2діетиловим етером та промивали водою. Водний (триметилсиліл)етокси)метил)аміно)-сульФоніл)-5шар екстрагували діетиловим етером та поєднані (4-((6-((5R)-5-(2,2-диметил-4Н-1,3-бензодіоксин-6етерні шари промивали розбавленою гідрохлориіл)-2-оксо-1,3-оксазолідин-3-іл)гексил)-окси)бутил)дною кислотою, розсолом, сушили сульфатом ма1,1'-дифеніл гнію та випарювали досуха з утворенням потрібної отримували з використанням способів, подібсполуки (325мг): ІЧ 1726см-1 МС (TSP+ve) m/z 186 них описаним у прикладі 1 viii. РХМС ЧУ = 4,55 (M+MH4]+. хвилин. (іі) (1R)-2-((6-(Бут-3-инілокси)гексил)][(S)-2vi) 5-(4-((6-(((2R)-2-(2,2-Диметил-4Н-1,3гідрокси-1-фенілетил)аміно)-1-(2,2-диметил-4Нбензодіоксин-6-іл)-2-гідроксіетил)аміно)1,3-бензодіоксин-6-іл)етанол гексил)окси)бутил)(1,1'-дифеніл)-3-сульфонамід
ДивитисяДодаткова інформація
Назва патенту англійськоюPhenetanolamine derivatives for the treatment of respiratory diseases, a method for producing thereof (variants), intermediary compounds, pharmaceutical composition, combination and a method for prophylaxis or treatment of state to which selective agonist of ?2- adrenoreceptor is prescribed
Назва патенту російськоюПроизводные фенетаноламина для лечения респираторных болезней, способ их получения (варианты), промежуточные соединения, фармацевтическая композиция, комбинация и способ профилактики или лечения состояния, для которого показан селективный агонист ?2-адренорецептора
МПК / Мітки
МПК: C07C 311/29, A61K 31/18, C07C 311/58, C07D 295/26, A61P 11/06, C07C 311/27, C07D 295/12
Мітки: хвороб, одержання, проміжні, варіанти, похідні, спосіб, сполуки, якого, респіраторних, фенетаноламіну, композиція, комбінація, показано, профілактики, лікування, фармацевтична, стану
Код посилання
<a href="https://ua.patents.su/39-76443-pokhidni-fenetanolaminu-dlya-likuvannya-respiratornikh-khvorob-sposib-kh-oderzhannya-varianti-promizhni-spoluki-farmacevtichna-kompoziciya-kombinaciya-ta-sposib-profilaktiki-chi-li.html" target="_blank" rel="follow" title="База патентів України">Похідні фенетаноламіну для лікування респіраторних хвороб, спосіб їх одержання (варіанти), проміжні сполуки, фармацевтична композиція, комбінація та спосіб профілактики чи лікування стану, для якого показано се</a>
Попередній патент: Спосіб перемішування сталі у ковші
Наступний патент: Спосіб виготовлення вістряного автоемітера з локалізованою емісією
Випадковий патент: Спосіб отримання похідних імідазола або його фармацевтично прийнятих солей