Похідні піперидину, спосіб їх отримання, фармацевтична композиція на їх основі та спосіб лікування опосередкованої хемокіном хвороби
Номер патенту: 80268
Опубліковано: 10.09.2007
Автори: ФЕРБЕР Марк, СПРІНҐТОРП Браян, ПЕРДІ Марк, АЛЬКАРАЗ Ліліан
Формула / Реферат
1. Сполука формули (І):
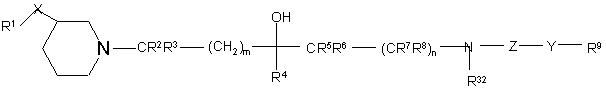 ,
,
де:
X представляє CH2, O, S(O)2 або NR10;
Y представляє зв'язок, CH2, NR35, CH2NH, CH2NHC(O), CH(OH), CH(NHC(O)R33), CH(NHS(O)2R34), CH2O або CH2S;
Z представляє С(O) або, коли Y представляє зв'язок, Z може також представляти S(O)2;
R1 представляє заміщений, як варіант, арил, заміщений, як варіант, гетероцикліл або С4-6циклоалкіл, конденсований з бензольним кільцем;
R4 представляє гідроген, С1-6алкіл (як варіант, заміщений С3-6циклоалкілом) або С3-6циклоалкіл;
R2, R3, R5, R6, R7 та R8 представляють, незалежно, гідроген, С1-6алкіл або С3-6циклоалкіл;
m та n дорівнюють, незалежно, 0 або 1;
R9 представляє заміщений, як варіант, арил або заміщений, як варіант, гетероцикліл;
R10, R32 та R35 представляють, незалежно, гідроген, С1-6алкіл або С3-6циклоалкіл;
R33 та R34 представляють С1-6алкіл або С3-6циклоалкіл;
де вищезазначені арил та гетероцикліл, де можливо, як варіант, заміщені замісником, вибраним з групи: галоген, ціано, нітро, гідрокси, оксо, S(O)kR12, OC(O)NR13R14, NR15R16, NR17C(O)R18, NR19C(O)NR20R21, S(O)2NR22R23, NR24S(O)2R25, C(O)NR26R27, C(O)R28, CO2R29, NR30CO2R31, С1-6алкіл (сам, як варіант, монозаміщений NНС(О)фенілом), С1-6галогеналкіл, С1-6алкоксі(С1-6)алкіл, С1-6алкокси, С1-6галогеналкокси, С1-6алкоксі(С1-6)алкокси, С1-6алкілтіогрупа, С2-6алкеніл, С2-6алкініл, С3-10циклоалкіл, метилендіокси, дифлуорметилендіокси, феніл, феніл(С1-4)алкіл, фенокси, фенілтіогрупа, феніл(С1-4)алкокси, морфолініл, гетероарил, гетероарил(С1-4)алкіл, гетероарилокси або гетероарил(С1-4)алкокси, де будь-який з вищезазначених фенілу та гетероарилу, як варіант, заміщено таким замісником: галоген, гідрокси, нітро, S(O)r(С1-4алкіл), S(O)2NH2, S(O)2NН(С1-4алкіл), S(O)2N(C1-4алкіл)2, ціано, С1-4алкіл, С1-4алкокси, C(O)NH2, С(O)NН(С1-4алкіл), СO2Н, СO2(С1-4алкіл), NHC(O)(C1-4aлкіл), NНS(O)2(С1-4алкіл), С(O)(С1-4алкіл), СF3 або ОСF3;
k та r дорівнюють, незалежно, 0, 1 або 2;
R13, R14, R15, R16, R17, R18, R19, R20, R21, R22, R23, R24, R26, R27, R29 та R30, незалежно, представляють гідроген, С1-6алкіл (як варіант, заміщений галогеном, гідрокси або С3-10циклоалкілом), СН2(С2-6алкеніл), С3-6циклоалкіл, феніл (сам, як варіант, заміщений галогеном, гідрокси, нітро, NH2, NH(С1-4алкілом), NН(С1-4алкілом)2, S(O)2(С1-4алкілом), S(O)2NH2, S(O)2NН(С1-4алкілом), S(O)2N(С1-4алкілом)2, ціано, С1-4алкілом, С1-4алкокси, C(O)NH2, С(O)NН(С1-4алкілом), С(O)N(С1-4алкілом)2, СO2Н, СO2(С1-4алкілом), NНС(O)(С1-4алкілом), NНS(O)2(С1-4алкілом), С(O)(С1-4алкілом), СF3 або ОСF3) або гетероцикліл (сам, як варіант, заміщений галогеном, гідрокси, нітро, NH2, NН(С1-4алкілом), N(С1-4алкілом)2, S(O)2(С1-4алкілом), S(O)2NH2, S(O)2NH(С1-4алкілом), S(O)2N(С1-4алкілом)2, ціано, С1-4алкілом, С1-4алкокси, C(O)NH2, С(O)NН(С1-4алкілом), С(O)N(С1-4алкілом)2, СO2Н, СO2(С1-4алкілом), NНС(O)(С1-4алкілом), NНS(O)2(С1-4алкілом), С(O)( С1-4алкілом), СF3 або ОСF3);
альтернативно NR13R14, NR15R16, NR20R21, NR22R23, NR26R27 можуть, незалежно, утворювати 4-7-членне гетероциклічне кільце, вибране з групи: азетидин (сам, як варіант, заміщений гідрокси або С1-4алкілом), піролідин, піперидин, азепін, 1,4-морфолін або 1,4-піперазин, останній, як варіант, заміщений С1-4алкілом на дистальному атомі нітрогену;
R12, R25, R28 та R31 представляють, незалежно, С1-6алкіл (як варіант, заміщений галогеном, гідрокси або С3-10циклоалкілом), СН2(С2-6алкеніл), феніл (сам, як варіант, заміщений галогеном, гідрокси, нітро, NH2, NН(С1-4алкілом), N(С1-4алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 вище), S(O)2(С1-4алкілом), S(O)2NН2, S(O)2NН(С1-4алкілом), S(O)2N(С1-4алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 вище), ціано, С1-4алкілом, С1-4алкокси, С(O)NН2, С(O)NН(С1-4алкілом), С(O)N(С1-4алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 вище), СO2Н, СO2(С1-4алкілом), NНС(O)( С1-4алкілом), NНS(O)2(С1-4алкілом), С(O)( С1-4алкілом), СF3 або ОСF3) або гетероцикліл (сам, як варіант, заміщений галогеном, гідрокси, нітро, NH2, NН(С1-4алкілом), N(С1-4алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 вище), S(O)2(С1-4алкілом), S(O)2NH2, S(O)2NН(С1-4алкілом), S(O)2N(С1-4алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 вище), ціано, С1-4алкілом, С1-4алкокси, С(O)NН2, С(O)NН(С1-4алкілом), С(O)N(С1-4алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 вище), СO2Н, СO2(С1-4алкілом), NНС(O)( С1-4алкілом), NНS(O)2(С1-4алкілом), С(O)(С1-4алкілом), СF3 або ОСF3); за умови, що коли Х представляє CN2, a m та n дорівнюють 0, тоді Y не представляє NR35; або її N-оксид; або її фармацевтичнo прийнятна сіль, сольват або сольват солі.
2. Сполука за п. 1, де: Х представляє О; Y представляє зв'язок, СН2, NR35, CH2NH, СН(ОН), CH(NHC(O)R33), CH(NHS(O)2R34) або СН2O; Z представляє С(O) або, коли Y представляє зв'язок, Z може також представляти S(O)2; R1 представляє заміщений, як варіант, феніл;
R4 представляє гідроген або С1-6алкіл; R2, R3, R5, R6, R7 та R8, усі, при наявності, представляють гідроген; m та n дорівнюють, незалежно, 0 або 1; R9 представляє заміщений, як варіант, арил або заміщений, як варіант, гетероцикліл; R32 та R35 представляють, незалежно, гідроген або С1-6алкіл; R33 та R34 представляють С1-6алкіл; де вищезазначені феніл, арил та гетероцикліл, де можливо, як варіант, заміщено таким замісником: галоген, ціано, гідрокси, оксо, S(O)2R12, NR15R16, NR17C(O)R18, S(O)2NR22R23, NR24S(O)2R25, C(O)NR26R27, CO2R29, С1-6алкіл (сам, як варіант, монозаміщений NНС(О)фенілом), СF3, феніл або гетероарил; де будь-який з вищезазначених фенілу та гетероарилу, як варіант, заміщено таким замісником: галоген, С1-4алкіл, С1-4алкокси або CF3;
R15, R16, R17, R18, R22, R23, R24, R26, R27 тa R29 представляють, незалежно, гідроген, С1-6алкіл (як варіант, заміщений гідрокси) або С3-6циклоалкіл; альтернативно NR22R23 може утворювати азетидинове кільце (саме, як варіант, заміщене гідрокси або С1-4алкілом);
R12 та R25 представляють, незалежно, С1-6алкіл або феніл; або її фармацевтично прийнятна сіль.
3. Сполука за пп. 1 або 2, де R1 представляє феніл, як варіант, заміщений галогеном, ціано, С1-4алкілом, С1-4алкокси, S(O)2(С1-4алкілом), S(O)2NH2, S(O)2NН(С1-4алкілом), S(O)2NН(С3-6циклоалкілом), С(O)2(С1-4алкілом), С(O)NH(С1-4алкілом) або С(O)NН2.
4. Сполука за п. 1 або 3, де Х представляє О.
5. Сполука за пп. 1, 2, 3 або 4, де Y представляє зв'язок.
6. Сполука за пп. 1, 2 ,3, 4 або 5, де Z представляє С(O).
7. Сполука за будь-яким з попередніх пунктів, де обидва m та n дорівнюють 0.
8. Сполука за будь-яким з попередніх пунктів, де R2, R3, R4, R5, R6, R7 та R8, усі, при наявності, представляють гідроген.
9. Сполука за будь-яким з попередніх пунктів, де R9 представляє заміщений, як варіант, гетероцикліл; де гетероциклілом є: тієніл, піроліл, тіазоліл, піразоліл, оксазоліл, ізоксазоліл, імідазоліл, 1,2,5-оксадіазоліл, піридиніл, 1,6-дигідропіридиніл, піримідиніл, індоліл, індазоліл, 2,3-дигідро-1Н-індазоліл, імідазопіридиніл, 2,1,3-бензотіадіазоліл, хіноксалініл, хінолініл, 1,2-дигідрохінолініл, 1,4-дигідрохінолін, ізохінолініл, 1,2-дигідроізохінолініл, цинолініл, 3,4-дигідрофталазиніл, 2,3-дигідро-4Н-1,4-бензоксазиніл, 3,4-дигідро-2Н-1,4-бензоксазиніл, 1,3-дигідро-2Н-ізоіндоліл, піразолотриазиніл, піразолопіримідиніл, імідазобензотіазоліл, імідазопіримідиніл, або 2,1,3-бензоксадіазоліл, 1,3-бензотіазол, 2,3-дигідро-1,3-бензотіазол, 4,5,6,7-тетрагідроіндазол або 2,3-дигідро-1Н-бензімідазол; де гетероцикліл незаміщено або заміщено одним або більше замісниками: оксо (де можливо), галоген, С1-4алкіл, СF3, С1-4алкокси, S(O)2(С1-4алкіл), S(O)2NH2, S(O)2NH(С1-4алкіл), S(O)2N(С1-4алкіл)2 або ОСF3.
10. Спосіб отримання сполуки за п. 1, в якому проводять реакцію сполуки формули (II):
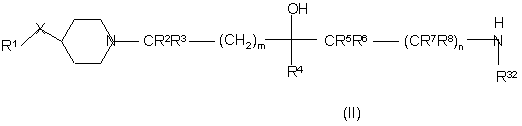 ,
,
де X, R1, R2, R3, R4, R5 R6, R7, R8, R32, m та n визначено вище, таким чином:
(і) коли Y представляє зв'язок, СH2, NR35, CH2NH, CH2NHC(O), CH(OH), CH(NHCOR33),
CH(NHSO2R34), CH2O або CH2S, Z представляє С(O), R35 не представляє гідроген, а R33 та R34 визначено вище, зі сполукою формули (IIIа):
L1–CO–Y–R9, (IIIa)
де R9 визначено вище, a L1 представляє відщеплювану групу, при наявності основи, як варіант, при наявності засобу сполучення;
(іі) коли Y представляє NH, a Z представляє С(O), зі сполукою формули (ІІІb):
![]() ,
,
де R9 визначено вище; або
(ііі) коли Y представляє зв'язок, а Z представляє S(O)2, зі сполукою формули (IIIс):
![]() ,
,
де R9 визначено вище, а L1 представляє відщеплювану групу, при наявності основи.
11. Фармацевтична композиція, що містить сполуку формули (І) або її фармацевтичнo прийнятну сіль, сольват або сольват солі за п. 1 та фармацевтичнo прийнятний ад'ювант, розріджувач або носій.
12. Сполука формули (І) або її фармацевтичнo прийнятна сіль, сольват або сольват солі за п. 1, для застосування у терапії.
13. Сполука формули (І) або її фармацевтичнo прийнятна сіль, сольват або сольват солі за п. 1 у виробництві медикаменту для застосування у терапії.
14. Спосіб лікування опосередкованої хемокіном хвороби у ссавця, що страждає від вказаної хвороби або має ризик захворіти нею, який включає введення ссавцю, що потребує такого лікування, терапевтичнo ефективної кількості сполуки формули (I) або її фармацевтичнo прийнятної солі, сольвату або сольвату солі за п. 1.
Текст
1. Сполука формули (І): OH R1 N CR2R3 (CH2 )m CR5R6 (CR7R8)n R4 де: X представляє CH2, O, S(O)2 або NR10; Y представляє зв'язок, CH2, NR35, CH2NH, CH2NHC(O), CH(OH), CH(NHC(O)R 33), 34 CH(NHS(O)2R ), CH 2O або CH2S; Z представляє С(O) або, коли Y представляє зв'язок, Z може також представляти S(O)2; R1 представляє заміщений, як варіант, арил, заміщений, як варіант, гетероцикліл або С 46циклоалкіл, конденсований з бензольним кільцем; R4 представляє гідроген, С1-6алкіл (як варіант, заміщений С3-6циклоалкілом) або С3-6циклоалкіл; R2, R3, R5, R6, R7 та R8 представляють, незалежно, гідроген, С1-6алкіл або С 3-6циклоалкіл; m та n дорівнюють, незалежно, 0 або 1; R9 представляє заміщений, як варіант, арил або заміщений, як варіант, гетероцикліл; R10, R32 та R35 представляють, незалежно, гідроген, С1-6алкіл або С3-6циклоалкіл; R33 та R34 представляють С 1-6алкіл або С 36циклоалкіл; де вищезазначені арил та гетероцикліл, де можливо, як варіант, заміщені замісником, вибраним з групи: галоген, ціано, нітро, гідрокси, оксо, S(O)kR12, OC(O)NR 13R14, NR15R16 , NR17C(O)R 18, NR19C(O)NR20R21, S(O)2NR22R 23, NR24S(O)2R 25, C(O)NR26R27, C(O)R28 , CO2R29 , NR30CO2R31, С1(сам, як варіант, монозаміщений 6алкіл NНС(О)фенілом), С1-6галогеналкіл, С1-6алкоксі(С 1С1-6алкокси, С1-6галогеналкокси, С16)алкіл, С1-6алкілтіогрупа, С26алкоксі(С 1-6)алкокси, 6алкеніл, С 2-6алкініл, С 3-10циклоалкіл, метилендіокси, дифлуорметилендіокси, феніл, феніл(С 1фенокси, фенілтіогрупа, феніл(С14)алкіл, 4)алкокси, морфолініл, гетероарил, гетероарил(С 1гетероарилокси або гетероарил(С14)алкіл, 4)алкокси, де будь-який з вищезазначених фенілу та гетероарилу, як варіант, заміщено таким замісником: галоген, гідрокси, нітро, S(O)r(С1-4алкіл), S(O)2NH2, S(O) 2NН(С1-4алкіл), S(O)2N(C1-4алкіл)2, ціано, С1-4алкіл, С1-4алкокси, C(O)NH2, С(O)NН(С14алкіл), СO2Н, СO2(С 1-4алкіл), NHC(O)(C 1-4aлкіл), NНS(O)2(С1-4алкіл), С(O)(С1-4алкіл), СF3 або ОСF3 ; k та r дорівнюють, незалежно, 0, 1 або 2; R13, R14 , R15, R16, R17, R18, R19 , R20, R21, R22 , R23, R24, R 26, R27 , R29 та R30 , незалежно, представляють гідроген, С1-6алкіл (як варіант, заміщений галогеном, гідрокси або С3-10циклоалкілом), СН2(С26алкеніл), С 3-6циклоалкіл, феніл (сам, як варіант, заміщений галогеном, гідрокси, нітро, NH2, NH(С1 N R32 4алкілом), Z Y R9 , NН(С1-4алкілом)2, S(O)2(С1-4алкілом), S(O)2NH2, S(O) 2NН(С1-4алкілом), S(O)2N(С1ціано, С1-4алкілом, С1-4алкокси, 4алкілом)2, C(O)NH2, С(O)NН(С1-4алкілом), С(O)N(С14алкілом)2, СO2Н, СO2(С 1-4алкілом), NНС(O)(С 14алкілом), NНS(O)2(С 1-4алкілом), С(O)(С 1-4алкілом), СF3 або ОСF3) або гетероцикліл (сам, як варіант, заміщений галогеном, гідрокси, нітро, NH2, NН(С1N(С1-4алкілом)2, S(O)2(С1-4алкілом), 4алкілом), S(O)2NH2, S(O) 2NH(С1-4алкілом), S(O)2N(С1ціано, С1-4алкілом, С1-4алкокси, 4алкілом)2, C(O)NH2, С(O)NН(С1-4алкілом), С(O)N(С14алкілом)2, СO2Н, СO2(С 1-4алкілом), NНС(O)(С 1NНS(O)2(С1-4алкілом), С(O)( С14алкілом), 4алкілом), СF3 або ОСF3); альтернативно NR13R14, NR15R16 , NR20R21 , NR22R23, NR26R27 можуть, незалежно, утворювати 4-7членне гетероциклічне кільце, вибране з групи: азетидин (сам, як варіант, заміщений гідрокси або С1-4алкілом), піролідин, піперидин, азепін, 1,4морфолін або 1,4-піперазин, останній, як варіант, заміщений С 1-4алкілом на дистальному атомі нітрогену; R12, R25, R28 та R31 представляють, незалежно, С16алкіл (як варіант, заміщений галогеном, гідрокси або С3-10циклоалкілом), СН2(С2-6алкеніл), феніл (сам, як варіант, заміщений галогеном, гідрокси, нітро, NH2, NН(С1-4алкілом), N(С1-4алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 вище), S(O) 2(С1S(O)2NН2, S(O) 2NН(С1-4алкілом), 4алкілом), S(O)2N(С1-4алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 ви ще), ціано, С1-4алкілом, С1-4алкокси, С(O)NН2, С(O)NН(С1-4алкілом), С(O)N(С1-4алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 ви ще), СO 2Н, СO 2(С1NНС(O)( С1-4алкілом), NНS(O)2(С14алкілом), 4алкілом), С(O)( С 1-4алкілом), СF3 або ОСF3) або гетероцикліл (сам, як варіант, заміщений галогеном, гідрокси, нітро, NH2, NН(С1-4алкілом), N(С14алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 вище), S(O)2(С1-4алкілом), S(O)2NH2, S(O)2NН(С14алкілом), S(O)2N(С 1-4алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 вище), ціано, С1-4алкілом, С1-4алкокси, С(O)NН2, С(O)NН(С1-4алкілом), С(O)N(С1-4алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 ви ще), СO 2Н, СO 2(С1 5 80268 4алкілом), NНС(O)( С1-4алкілом), NНS(O)2(С1С(O)(С1-4алкілом), СF3 або ОСF3); за умови, що коли Х представляє CN2, a m та n дорівнюють 0, тоді Y не представляє NR35; або її Nоксид; або її фармацевтичнo прийнятна сіль, сольват або сольват солі. 2. Сполука за п. 1, де: Х представляє О; Y представляє зв'язок, СН2, NR35, CH2NH, СН(ОН), CH(NHC(O)R33), CH(NHS(O)2R34) або СН2O; Z представляє С(O) або, коли Y представляє зв'язок, Z може також представляти S(O)2; R1 представляє заміщений, як варіант, феніл; R4 представляє гідроген або С 1-6алкіл; R2, R3, R5, R6, R7 та R8, усі, при наявності, представляють гідроген; m та n дорівнюють, незалежно, 0 або 1; R9 представляє заміщений, як варіант, арил або заміщений, як варіант, гетероцикліл; R32 та R35 представляють, незалежно, гідроген або С1-6алкіл; R33 та R34 представляють С 1-6алкіл; де вищезазначені феніл, арил та гетероцикліл, де можливо, як варіант, заміщено таким замісником: галоген, ціано, гідрокси, оксо, S(O)2R12, NR15R16 , NR17C(O)R18, S(O)2NR22R23, NR24S(O) 2R25 , C(O)NR26R27, CO2R 29, С1-6алкіл (сам, як варіант, монозаміщений NНС(О)фенілом), СF3, феніл або гетероарил; де будь-який з вищезазначених фенілу та гетероарилу, як варіант, заміщено таким замісником: галоген, С1-4алкіл, С1-4алкокси або CF3; R15, R16 , R17, R18, R22 , R23, R24, R26, R27 тa R29 представляють, незалежно, гідроген, С1-6алкіл (як варіант, заміщений гідрокси) або С3-6циклоалкіл; альтернативно NR22R23 може утворювати азетидинове кільце (саме, як варіант, заміщене гідрокси або С1-4алкілом); R12 та R25 представляють, незалежно, С1-6алкіл або феніл; або її фармацевтично прийнятна сіль. 3. Сполука за пп. 1 або 2, де R 1 представляє феніл, як варіант, заміщений галогеном, ціано, С14алкілом), 6 4алкілом, С1-4алкокси, S(O)2(С1-4алкілом), S(O)2NH2, S(O)2NН(С1-4алкілом), S(O)2NН(С3С(O)2(С1-4алкілом), С(O)NH(С16циклоалкілом), 4алкілом) або С(O)NН 2. 4. Сполука за п. 1 або 3, де Х представляє О. 5. Сполука за пп. 1, 2, 3 або 4, де Y представляє зв'язок. 6. Сполука за пп. 1, 2 ,3, 4 або 5, де Z представляє С(O). 7. Сполука за будь-яким з попередніх пунктів, де обидва m та n дорівнюють 0. 8. Сполука за будь-яким з попередніх пунктів, де R2, R3, R4, R5, R6 , R7 та R8, усі, при наявності, представляють гідроген. 9. Сполука за будь-яким з попередніх пунктів, де R9 представляє заміщений, як варіант, гетероцикліл; де гетероциклілом є: тієніл, піроліл, тіазоліл, піразоліл, оксазоліл, ізоксазоліл, імідазоліл, 1,2,5оксадіазоліл, піридиніл, 1,6-дигідропіридиніл, піримідиніл, індоліл, індазоліл, 2,3-дигідро-1Ніндазоліл, імідазопіридиніл, 2,1,3-бензотіадіазоліл, хіноксалініл, хінолініл, 1,2-дигідрохінолініл, 1,4дигідрохінолін, ізохінолініл, 1,2-дигідроізохінолініл, цинолініл, 3,4-дигідрофталазиніл, 2,3-дигідро-4Н1,4-бензоксазиніл, 3,4-дигідро-2Н-1,4бензоксазиніл, 1,3-дигідро-2Н-ізоіндоліл, піразолотриазиніл, піразолопіримідиніл, імідазобензотіазоліл, імідазопіримідиніл, або 2,1,3-бензоксадіазоліл, 1,3-бензотіазол, 2,3-дигідро-1,3-бензотіазол, 4,5,6,7-тетрагідроіндазол або 2,3-дигідро-1Нбензімідазол; де гетероцикліл незаміщено або заміщено одним або більше замісниками: оксо (де можливо), галоген, С1-4алкіл, СF3, С1-4алкокси, S(O)2(С1-4алкіл), S(O)2NH2, S(O)2NH(С1-4алкіл), S(O)2N(С1-4алкіл)2 або ОСF3. 10. Спосіб отримання сполуки за п. 1, в якому проводять реакцію сполуки формули (II): OH X N R1 CR 2R 3 (CH2 )m CR 5R 6 R4 (CR 7R 8)n H N R 32 (II) де X, R1, R2, R3 , R4, R5 R6, R7, R8 , R32, m та n визначено вище, таким чином: (і) коли Y представляє зв'язок, СH2, NR35, CH2NH, CH2NHC(O), CH(OH), CH(NHCOR33), CH(NHSO2R34), CH2O або CH2S, Z представляє С(O), R 35 не представляє гідроген, а R33 та R34 визначено вище, зі сполукою формули (IIIа): L1–CO–Y–R9, (IIIa) де R9 визначено вище, a L1 представляє відщеплювану гр упу, при наявності основи, як варіант, при наявності засобу сполучення; (іі) коли Y представляє NH, a Z представляє С(O), зі сполукою формули (ІІІb): O N R9 де R9 визначено вище; або (IIIb) , (ііі) коли Y представляє зв'язок, а Z представляє S(O)2, зі сполукою формули (IIIс): L1 S(O)2 R9 (IIIc) , 9 де R визначено вище, а L1 представляє відщеплювану гр уп у, при наявності основи. 11. Фармацевтична композиція, що містить сполуку формули (І) або її фармацевтичнo прийнятну сіль, сольват або сольват солі за п. 1 та фармацевтичнo прийнятний ад'ювант, розріджувач або носій. 12. Сполука формули (І) або її фармацевтичнo прийнятна сіль, сольват або сольват солі за п. 1, для застосування у терапії. 13. Сполука формули (І) або її фармацевтичнo прийнятна сіль, сольват або сольват солі за п. 1 у 7 80268 8 виробництві медикаменту для застосування у терапії. 14. Спосіб лікування опосередкованої хемокіном хвороби у ссавця, що страждає від вказаної хвороби або має ризик захворіти нею, який включає введення ссавцю, що потребує такого лікування, терапевтичнo ефективної кількості сполуки формули (I) або її фармацевтичнo прийнятної солі, сольвату або сольвату солі за п. 1. Представлений винахід стосується похідних піперидину, що мають фармацевтичну активність, способів отримання таких похідних, фармацевтичних композицій, що містить такі похідні та застосування таких похідних, як активних терапевтичних засобів. Винахід також забезпечує спосіб отримання 4-(3,4-дихлорфенокси)піперидину, який є корисним як інтермедіат для отримання деяких сполук винаходу. Фармацевтично активні похідні піперидину розкрито [у WO 01/62728, WO 01/62729 та WO 01/62757]. Хемокіни є хемотактичними цитокінами, що вивільняються багатьма клітинами до притягнення макрофагів, Т-клітин, еозинофілів, базофілів та нейтрофілів до ділянок запалення, а також грають роль у визріванні клітин імунної системи. Хемокіни грають важливу рол в імунних та запальних реакціях у різних хворобах та розладах, включаючи астму та алергічні хвороби, а також автоімунні патології, як-то ревматоїдний артрит та атеросклероз. Ці невеликі секретовані молекули є зростаючою надродиною білків 8-14кДа, що характеризуються чотирма збереженими цистеїновими функціональними послідовностями. Хемокінову надродину можна поділити на дві головні групи, що виявляють характеристичні структурні функціональні послідовності, родини Cys-X-Cys (C-X-C, або α) та Cys-Cys (C-C, або β). Ці виявлено на основі одиничної амінокислотної вставки між NHпроксимальною парою цистеїнових залишків та подібністю послідовностей. С-Х-С хемокіни залучають кілька потужних хемоатрактантів та активаторів нейтрофілів, як-то інтерлейкін-8 (IL-8) та активуючий нейтрофіли пептид 2 (ΝΑΡ-2). С-С хемокіни залучають потужні хемоатракганти моноцитів та лімфоцитів, але не нейтрофілів, як-то моноцитні хемотакгичні білки 1-3 людини (МСР-1, МСР-2 та МСР-3), RANTES (Регульовані на Активації, Нормально Т-Експресовані та Секретовані), еотаксини та запальні білки макрофагів 1а та 1β (МІР-1α та ΜΙΡ-1β). Дослідженнями продемонстровано, що дія хемокінів є опосередкованою підродинами сполучених з G-білком рецепторів, серед, яких є рецептори, позначені CCR1, CCR2, CCR2A, CCR2B, CCR3, CCR4, CCR5, CCR6, CCR7, CCR8, CCR9, CCR10, CXCR1, CXCR2, CXCR3 та C XCR4. Ці рецептори репрезентують гарні цілі для розробки ліків, оскільки агенти, які модулюють ці рецептори, могли б бути корисними у лікуванні вищезазначенених розладів та хвороб. Гістамін є основним аміном, 2(4-імідазоліл)-етиламіном, та утворюється з гістидину гістидин-декарбоксилазою. Його знайдено у більшості тканин організму, але у високій концентрації у легенях, шкірі та у шлунково-кишковому тракті. На клітинному рівні запальні клітини, як-то тучні клітини та базофіли зберігають великі кількості гістаміну. Виявлено, що дегрануляція тучних клітин та базофілів та наступне вивільнення гістаміну є фундаментальним механізмом, відповідним за клінічне виявлення алергічного процесу. Гістамін діє впливом на специфічні сполучені з Gбілком рецептори гістаміну трьох головних типів, H1, Н2 та Н3. Антагоністи гістаміну Н1 містять найбільший клас лікарняних засобів, застосовуваних у лікуванні пацієнтів з алергічними розладами, особливо ринітом та кропивницею. Антагоністи Н1 є корисними у контролюванні алергічної реакції, наприклад блокуванням дії гістаміну на гладенькі м'язи пост-капілярних вен, що призводить до зменшеної судинної проникності, ексудації та набряку. Антагоністи також блокують дію гістаміну на рецептори Н1 на ноцицептивних нервових волокнах стипу, що призводить до зменшеного свербежу та чхання. Вірусні інфекції, як відомо, викликають запалення легенів. Показано експериментально, що звичайна застуда збільшує виробку слизовою еотаксину у ди хальних шляха х. Інстиляція еотаксину у ніс може імітувати деякі ознаки та симптоми звичайної застуди. [Дивись, Greiff L et al. Allergy (1999) 54(11) 1204-8 Experimental common cold increase mu-cosal output of eotaxin in atopic individuals (Експериментальна звичайна застуда збільшує продукцію еотаксину слизовою у атопічних осіб) та Kawaguchi Μ et al. hit Arch. Allergy Tmmunol. (2000) 122 SI 44 Expression of eotaxin by normal airway epithelial cells after virus A infection (Експресія еотаксину нормальними епітеліальними клітинами дихальних шля хів після вірусної А інфекції).] Представлений винахід стосується сполуки формули (І): (I) 9 80268 Де: X представляє СН 2, О, S(O)2 або NR10; Υ представляє зв'язок, СН2> NR35, CH2NH, CH2NHC(O), CH(OH), CH(NHC(O)R33), 34 CH(NHS(O)2R ), CH 2O або CH2S; Ζ представляє С(О), або коли Υ представляє зв'язок, Ζ може також бути S(O)2; R1 представляє заміщений, як варіант, арил, заміщений, як варіант, гетероцикліл або С 46циклоалкіл, конденсований з бензольним кільцем; R4 представляє гідроген, С1-6алкіл (як варіант, заміщений С3-6циклоалкілом) або С3-6циклоалкіл; R2, R3, R 5, R6 , R7 та R8 представляють, незалежно, гідроген, С1-6алкіл або С3-6циклоалкіл; m та n дорівнюють, незалежно, 0 або 1; R9 представляє заміщений, як варіант, арил або, заміщений, як варіант, гетероцикліл; R10, R32 та R 35 представляють, незалежно, гідроген, С1-6алкіл або С 3-6циклоалкіл; R33 та R34 представляє С 1-6алкіл або С 36циклоалкіл; де вищезазначені арил та гетероцикліл, де можливо, як варіант, заміщені групою: галоген, ціано, нітро, гідрокси, оксо, S(O)kR12, 13 14 15 16 17 OC(O)NR R , NR R , NR C(O)R 18, 19 20 21 22 23 NR C(O)NR R , S(O)2NR R , NR24S(O)2R 25, C(O)NR26R27, C(O)R28 , CO2R29 , NR30CO2R31, С1(сам, як варіант, монозаміщений 6алкіл ΝNΟ(Ο)фенілом), С1-6галогеналкіл, С1-6алкокси(С 1С1-6алкокси, С1-6галогеналкокси, С16)алкіл, С1-6алкілтіогрупа, С26алкокси(С 1-6)алкокси, 6алкеніл, С 2-6алкініл, С 3-10циклоалкіл, метилендіокси, дифлуорметилендіокси, феніл, феніл(С 1фенокси, фенілтіогрупа, феніл(С14)алкіл, 4)алкокси, морфолініл, гетероарил, гетероарил(С 1гетероарилокси або гетероарил(С14)алкіл, 4)алкоксил; де будь-який з вищезазначених фенілу та гетероарилу, як варіант, заміщено таким замісником: галоген, гідрокси, нітро, S(О)r(С1-4алкіл), S(O)2NH2, S(О) 2NН(С1-4алкіл), S(O)2N(C1-4алкіл)2, ціано, С1-4алкіл, С1-4алкокси, C(O)NH2, C(O)NH(С14алкіл), СО2Н, СО2(С 1-4алкіл), NHC(O)(C 1-4алкіл), NHS(O)2(С1-4алкіл), С(О)(C1-4алкіл), CF3; k та r дорівнюють, незалежно, 0, 1 або 2; R13, R14, R15 , R16, R17, R18 , R19, R20 , R21, R 22, R23 , 24 R , R 26, R27 , R29 та R30 представляють, незалежно, гідроген, C1-6алкіл (як варіант, заміщений галогеном, гідрокси або С3-10циклоалкілом), СН2(С26алкеніл), С 3-6циклоалкіл, феніл (сам, як варіант, заміщений галогеном, гідрокси, нітро, NH2, NH(C1NH(C1-4aлкiлoм)2, S(О)2(С1-4алкілом), 4aлкiлoм), S(O)2NH2, S(O) 2NH(C1-4aлкiлoм), S(O)2N(C1ціано, С1-4алкілом, С1-4алкокси, 4aлкiлoм)2, C(O)NH2, C(O)NH(С1-4алкілом), С(О)N(С14алкілом)2, СО2Н, СО2(С 1-4алкілом), NHC(O)(С 14алкілом), NHS(O)2(C 1-4алкілом), С(О)(С 1-4алкілом), CF3 або OCF3) або гетероцикліл (сам, як варіант, заміщений галогеном, гідрокси, нітро, NH2, NН(С14алкілом), N(C 1-4алкілом)2, S(O)2(C 1-4C алкілом), S(O)2NH2, S(О) 2NН(С1-4алкілом), S(O)2N(C1ціано, С1-4алкілом, С1-4алкокси, 4aлкiлoм)2, C(O)NH2, С(O)NН(С1-4алкілом), С(O)N(С14алкілом)2, СО2Н, СО(С 1-4алкілом), NHC(O)(С 14алкілом), NHS(O)2(С 1-4алкілом), С(О)(С 1-4алкілом), CF3 або OCF3); 10 альтернативно NR13R14, NR15R16, NR20R21 , NR R23, NR26R27, можуть, незалежно, утворювати 4-7-членне гетероциклічне кільце, вибране з групи: азетидин (сам, як варіант, заміщений гідрокси або С1-4алкілом), піролідин, піперидин, азепін, 1,4морфолін або 1,4-піперазин, останній, як варіант, заміщений С 1-4алкілом на дистальному атомі нітрогену; R12, R25 , R28 та R31 представляють, незалежно, С1-6алкіл (як варіант, заміщений галогеном, гідрокси або С 3-10циклоалкілом), СН2(С2-6алкеніл), феніл (сам, як варіант, заміщений галогеном, гідрокси, нітро, NH2, NH(С1-4алкілом), N(С1-4алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 вище), S(О) 2(С1S(O)2NH2, S(O) 2NH(C1-4aлкiлoм), 4алкілом), S(O)2N(С1-4алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 ви ще), ціано, С1-4алкілом, С1-4алкокси, C(O)NH2, C(O)NH(С1-4алкілом), C(O)N(C1-4алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 ви ще), СО 2Н, СО 2(С1NНС(O)(С1-4алкілом), NHS(O)2(С14алкілом), 4алкілом), C(O)( С 1-4алкілом), CF3 або OCF3) або гетероцикліл (сам, як варіант, заміщений галогеном, гідрокси, нітро, NH2, NH(C1-4алкілом), N(C14aлкiлoм)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 вище), S(O)2(С1-4алкілом), S(O)2NH2, S(О)2NH(С14алкілом), S(O)2N(С 1-4алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 ви ще), ціано, С1-4алкілом, С1-4алкокси з утворенням кільця, як описано для R13 та R14 вище), ціано, С1-4алкілом, С1-4алкокси, C(O)NH2, С(О)NН(С1-4алкілом), С(O)N(С1-4алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 вище), СО2Н, СО2(С1NHC(O)(C1-4алкілом), NНS(О)2(С14алкілом), 4алкілом), С(O)(С 1-4алкілом), CF3 або OCF3); за умови, що коли X представляє СН2, a m та n дорівнюють 0, тоді Υ не представляє NR35; або її N-оксид; або її фармацевтично прийнятну сіль, сольват або сольват солі. Деякі сполуки представленого винаходу можуть існувати у відмінних ізомерних формах (як-то енантіомери, діастереомери, геометричні ізомери або таутомери). Представлений винахід стосується усі х таких ізомерів та їх сумішей в усі х пропорціях. Придатні солі залучають кислотно-адитивні солі, як-то гідрохлорид, дигідрохлорид, гідробромід, фосфат, сульфат, ацетат, діацетат, фумарат, малеат, тартрат, цитрат, оксалат, метансульфонат або п-толуолсульфонат. Сполуки винаходу можуть існувати , як сольвати (як-то гідрати) та представлений винахід стосується усіх таких сольватів. Галоген включає флуор, хлор, бром та йод. Алкіли представлені лінійним або розгалуженим ланцюгом як, наприклад, метил, етил, нпропіл, ізо-пропіл або трет-бутил. Алкіли переважно містять 1-6 атомів карбону. Алкенілом є, наприклад, вініл або аліл. Алкеніли переважно містять 2-6 атомів карбону. 22 11 80268 Алкінілом є, наприклад, пропаргіл. Алкініли переважно містять 2-6 атомів карбону. Циклоалкіл є моноциклічним як, наприклад, циклопропіл, циклопентил або циклогексил. Циклоалкіл и переважно містять 3-6 атомів карбону. Циклоалкілом, конденсованим з бензольним кільцем є, наприклад, дицикло[4,2,0]окта-1,3,5триєніл. Арилом є переважно феніл або нафтил. Гетероцикліл є ароматичним або неароматичним 5 або 6-членним кільцем, як варіант, конденсованим з одним або більше іншими кільцями, що міститьпринаймні один гетероатом вибраний з групи, в яку залучено нітроген, оксиген та сульфур; або його N-оксид, S-оксид або S-діоксид. Гетероциклілом є, наприклад, фурил, тієніл (також відомий як тіофеніл), піроліл, 2,5-дигідропіроліл, тіазоліл, піразоліл, оксазоліл, ізоксазоліл, імідазоліл, піперидиніл, морфолініл, піридиніл, 1,6дигідропіридиніл (наприклад у 6-оксо-1,6дигідропіридинілі), піримідиніл, індоліл, 2,3дигідроіндоліл, бензо[b]фурил (також відомий як бензфурил), бенз[b]тієніл (також відомий як бензтієніл або бензтіофеніл), 2,3-дигідробенз[b]тієніл (наприклад у 1,1-діоксо-2,3-дигідробенз[b]тієнілі), індазоліл, бензімідазоліл, бензтриазоліл, бензоксазоліл, бензтіазоліл, 1,2-дигідробензтіазоліл (наприклад у 1Н-бензтіазол-2-онілі), 2,3дигідробензтіазоліл (наприклад у 2,3дигідробензтіазол-2-онілі), 1,2,3-бензотіадіазоліл, імідазопіридиніл (як-то імідазо[1,2-а]піридиніл), тієно[3,2-b]піридин-6-іл, 1,2,3-бензоксадіазоліл (також відомий як бензо[1,2,3]тіадіазоліл), 2,1,3бензотіадіазоліл, бензофуразан (також відомий як 2,1,3-бензоксадіазоліл), хіноксалініл, 3,4-дигідро1Н-2,1-бензотіазиніл (наприклад у 2-діоксо-3,4дигідро-1Н-2,1-бензотіазинілі), піразолопіридин (наприклад 1Н-піразоло[3,4-b]піридиніл), апурин, 3,7-дигідро-пуриніл (наприклад у 3,7-дигідропурин-2,6-діон-8-ілі), хінолініл, ізохінолініл, 1,2дигідроізохінолініл (наприклад у 2Н-ізохінолін-1онілі (альтернативно під назвою 1-оксо-1,2дигідроізохінолініл або 1,2-дигідроізохінолініл-1он)), нафтиридиніл (наприклад [1,6]нафтиридиніл або [1,8]нафтиридиніл), 1,4дигідро[1,8]нафтиридиніл (наприклад у 1Н[1,8]нафтиридин-4-онілі), або бензотіазиніл, 4Нбензо[1,4]тіазоліл (наприклад у 4Нбензо[1,4]тіазин-3-онілі); або його N-оксид (як-то піридин N-оксид), або його S-оксид або S-діоксид. 1,2-дигідропіридиніл (альтернативна нумерація у 1,6-дигідропіридинілі) може також бути наявним у 2-оксо-1,2-дигідропіридинілі; а 2,3-дигідро-1Ніндазоліл може також бути наявним у 3-оксо-2,3дигідро-1Н-індазолілі. Гетероцикліл також включає цинолініл, фталазиніл, 3,4-дигідрофталазиніл (наприклад у 4-оксо3,4-дигідрофталазинілі), бензоксазиніл, 2,3дигідро-4Н-1,4-бензоксазиніл (наприклад у 3-оксо2,3-дигідро-4Н-1,4-бензоксазинілі), 3,4-дигідро-2Н1,4-бензоксазиніл (наприклад у 3-оксо-3,4-дигідро2Н-1,4-бензоксазинілі), ізоіндоліл, 1,3-дигідро-2Нізоіндоліл (наприклад у 1,3-діоксо-1,3-дигідро-2Нізоіндолілі), піразолотриазиніл (наприклад піразоло[5,1-с][1,2,4]триазиніл), піразиніл, піридазиніл, 9Н-пуриніл, піразолопіримідиніл (наприклад піра 12 золо[1,5-а]піримідиніл), імідазобензотіазоліл (наприклад імідазо[2,1-b][1,3]бензотіазоліл), 1,2,5оксадіазоліл, імідазопіримідиніл (наприклад імідазо[1,2-а]піримідиніл), хінолініл, 1,2-дигідрохінолініл (наприклад у 2-оксо-1,2-дигідрохінолінілі) або 2,1,3-бензоксадіазоліл (наприклад, як 1-оксид); або може додатково бути його N-оксидом, Sоксидом або S-діоксидом. Наступні приклади гетероцикпілу представляють 1,3-бензотіазол, 2,3дигідро-1,3-бензотіазол (наприклад у 2-оксо-2,3дигідро-1,3-бензотіазолі), 4,5,6,7тетрагідроіндазол; 2,3-дигідро-1Н-бензімідазол (наприклад у 2-оксо-2,3-дигідро-1Н-бензімідазолі) та 1,4-дигідрохінолін (наприклад у 4-оксо-і ,4дигідрохіноліні). N-оксидом сполуки формули (І) або (Іа) є, наприклад, 1-окси-піперидинільна сполука. Гетероарил є ароматичним гетероциклілом. Ним є, наприклад фурил, тієніл, піроліл, тіазоліл, піразоліл, оксазоліл, ізоксазоліл, імідазоліл, піридиніл, піримідиніл, індоліл, бензо[b]фурил, бенз[b]тієніл, індазоліл, бензімідазоліл, бензтриазоліл, бензоксазоліл, бензтіазоліл, 1,2,3бензотіадіазоліл, імідазопіридиніл, тієно[3,2b]піридин-6-іл 1,2,3-бензоксадіазоліл, 2,1,3бензотіадіазоліл, бензофуразан, хіноксалініл, піразолопіридин, пурин, хінолініл, ізохінолініл, нафтиридиніл, бензотіазиніл, цинолініл, фталазиніл, бензоксазиніл, ізоіндоліл, піразолотриазиніл, піразиніл, піридазиніл, піразолопіримідиніл, імідазобензотіазоліл, імідазопіримідиніл, хінолініл або 2,1,3бензоксадіазоліл; або його N-оксидом (як-то піридин N-оксид), S-оксидом або S-діоксидом. Галогеналкіл є алкілом, що несе один або більше (як-то 1-6) атомів галогену та представляє, наприклад, CF3. Алкоксіалкіл представляє, наприклад, СН3ОСН2, СН3СН2ОСН2 або СН3СН2О(СН2)2. Галогеналкілокси представляє алкоксигрупу, що несе один або більше (як-то 1-6) атомів галогену та представляє, наприклад, OCF3. Алкоксіалкокси представляє, наприклад, СН3ОСН2О, СН3СН2ОСН2О або СН3СН2О(СН2)2О. Фенілалкіл представляє, наприклад, бензил, фенілет-1-ил або фенілет-2-ил. Фенілалкокси представляє, наприклад бе-нзилоксил. Гетероарилалкіл представляє, наприклад, піридинілметил або піримідинілметил. Гетероарилокси представляє, наприклад, піридинілокси або піримідинілоксил.Гетероарилалкокси представляє, наприклад, піридинілметокси або піримідинілметокси. Згідно з одним аспектом представленого винаходу запропоновано сполуку формули (І) де: X представляє СН 2, О, S(O) 2 або NR10; Υ представляє зв'язок, СН2, NR35, CH2NH, CH2NHC(O), СН(ОН), CH(NHC(O)R33), CH(NHS(O)2R34), СН2О або CH2S; Ζ представляє С(О), або коли Υ представляє зв'язок, Ζ може також бути S(O)2; R1 представляє заміщений, як варіант, арил, заміщений, як варіант, гетероцикліл або С4-6циклоалкіл, конденсований з бензольним кільцем; R4 представляє гідроген, С1-6алкіл (як варіант, заміщений С 32 3 5 6 6циклоалкілом) або С 3-6циклоалкіл; R , R , R , R , 7 8 R та R представляють, незалежно, гідроген, С16алкіл або С 3-6циклоалкіл; m та n дорівнюють, незалежно, 0 або 1; R9 представляє заміщений, як 13 80268 варіант, арил або, заміщений, як варіант, гетероцикліл; R10, R32, R33 та R35 представляють, незалежно, гідроген або С1-6алкіл; R34 представляє С 16алкіл; де вищезазначені арил та гетероцикліл, де можливо, як варіант, заміщені групою: галоген, ціано, нітро, гідрокси, оксо, S(O)kR12, 13 14 1S 16 17 OC(O)NR R , NR R , NR C(O)R 18, 19 20 21 22 23 NR C(O)NR R , S(O) 2NR R , R24S(O)2R 25, C(O)NR26R27, C(O)R28 , CO2R29 , NR30CO2R31, С16алкіл, С 1-6галогеналкіл, С 1-6алкокси(С 1-6)алкіл, С 1С1-6галогеналкокси, С1-6алкокси(С 16алкокси, С1-6алкілтіогрупа, С2-6алкеніл, С26)алкокси, 6алкініл, С 3-10циклоалкіл, метилендіокси, дифлуорметилендіокси, феніл, феніл(С1-4)алкіл, фенокси, фенілтіогрупа, феніл(С1-4)алкокси, гетероарил, гетероарил(С1-4)алкіл, гетероарилокси або гетероарил(С 1-4)алкоксил; де будь-який з вищезазначених фенілу та гетероарилу, як варіант, заміщено таким замісником: галоген, гідрокси, нітро, S(О)r(С1-4алкіл), S(O)2NH2, ціано, С1-4алкіл, С1C(O)NH2, С(О)NН(С1-4алкіл), СО2Н, 4алкокси, СО2(С1-4алкіл), NHC(O)(С1-4алкіл), NHS(O)2(C14aлкiл), С(О)(С 1-4алкіл), CF3 або OCF3; k та r дорівнюють, незалежно, 0, 1 або 2; R13, R14, R15 , R16, R17, R18, R19, R20, R21, R22 , R23, R24 , R26, R27 , R29, R30 та R31 представляють, незалежно, гідроген, С16алкіл (як варіант, заміщений галогеном, гідрокси або С3-10циклоалкілом), СН2(С2-6алкеніл), феніл (сам, як варіант, заміщений галогеном, гідрокси, нітро, NH2, NH(С1-4алкілом), NH(С1-4алкілом)2, S(О)2(С1-4алкілом), S(O)2NH2, S(O)2NH(С14алкілом), S(O)2N(С 1-4алкілом)2, ціано, С 1-4алкілом, С1--4алкокси, C(O)NH2, Ο(Ο)ΝN(С1-4алкілом), C(O)N(C1-4aлкiлoм)2, СО2Н, CO2(С1-4алкілом), NHC(O)(C1-4aлкiлoм), NHS(O)2(С1-4алкілом), С(О)(С1-4алкілом), CF3 або OCF3) або гетероцикліл (сам, як варіант, заміщений галогеном, гідрокси, нітро, NH2, NH(C1-4алкілом), N(C 1-4aлкiлoм)2, S(O)2(С1-4алкілом), S(O)2NH2, S(O)2NH(С14алкілом), S(O)2N(С 1-4алкілом)2, ціано, С 1-4алкілом, С1-4алкокси, C(O)NH2, С(О)NН(С1-4алкілом), C(O)N(С1-4алкілом)2, CO2H, СО2(С1-4алкілом), 14 NHC(O)(С1-4алкілом), NНs(О)2(С1---4алкілом), С(О)(С1-4алкілом), CF3 або OCF3); альтернативно NR13R14, NR15R16 , NR20R21 , NR22R23, NR26R27, можуть, незалежно, утворювати 4-7-членне гетероциклічне кільце, азетидин, піролідин, піперидин, азепін, 1,4-морфолін або 1,4-піперазин, останній, як варіант, заміщений С1-4алкілом на дистальному атомі нітрогену; R12, R25 та R28 представляють, незалежно, С1-6алкіл (як варіант, заміщений галогеном, гідрокси або С 3-10циклоалкілом), СН2(С26алкеніл), феніл (сам, як варіант, заміщений галогеном, гідрокси, нітро, NH2, NH(С1-4алкілом), N(С14алкіломом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 вище), S(О) 2(С1-4алкілом), S(O)2NH2, S(O)2NH(C14алкілом), S(O)2N(C 1-4алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 вище), ціано, С1-4алкілом, С1-4алкокси, C(O)NH2, C(O)NH(С1-4алкілом), С(О)N(С1-4алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 ви ще), СО 2Н, СО 2(С1NНС(O)(С1-4алкілом), NHS(O)2(С14алкілом), 4алкілом), С(О)(С 1-4алкілом), CF3 або OCF3) або гетероцикліл (сам, як варіант, заміщений галогеном, гідрокси, нітро, NH2, NH(C1-4алкілом), N(С14алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 вище), S(O)2(С1-4алкілом), S(O)2NH2, S(О)2NН(С14алкілом), S(O)2N(C 1-4aлкiлoм)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 вище), ціано, С1-4алкілом, С1-4алкокси, C(O)NH2, C(O)NH(С1-4алкілом), С(О)N(С1-4алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 ви ще), СО 2Н, СО 2(С1NHC(O)(С1-4алкілом), NHS(O)2(С14алкілом), 4aлкiлoм), С(О)(С 1-4алкілом), CF3 або OCF3); за умови, що коли X представляє СН2, a m та n дорівнюють 0, тоді Υ не представляє NR35; або її Nоксид; або її фармацевтично прийнятну сіль, сольват або сольват солі. Згідно з іншим аспектом представленого винаходу запропоновано сполуку формули (lа): (Ia) де: X представляє СН 2, О, S(O)2 або NR10; R1 представляє заміщений, як варіант, арил або, заміщений, як варіант, гетероцикліл; R4 представляє гідроген, С1-6алкіл (як варіант, заміщений С32 3 5 6 6циклоалкілом) або С 3-6циклоалкіл; R , R , R , R , 7 8 R та R представляють, незалежно, гідроген, С14алкіл або С 3-6циклоалкіл; m та n дорівнюють, незалежно, 0 або 1; R9 представляє заміщений, як варіант, арил або, заміщений, як варіант, гетероцикліл; R10 представляє гідроген або С 1-4алкіл; де вищезазначені арил та гетероцикліл, де можливо, як варіант, заміщені групою: галоген, ціано, нітро, гідрокси, оксо, S(O)kR12, OC(O)NR 13R14 , NR15R16, NR17C(O)R18 , NR19C(O)NR20R21 , S(O)2NR22R23, NR24S(O) 2R25 , C(O)NR26R27 , 28 29 30 31 C(O)R , CO 2R , NR CO2R , С1-6алкіл, С16галогеналкіл, С 1-6алкокси(С 1-6)алкіл, С 1-6алкокси, С1-6галогеналкокси, С1-6алкокси(С 1-6)алкокси, С1С2-6алкеніл, С2-6алкініл, С36алкілтіогрупа, 10циклоалкіл, метилендіокси, дифлуорметилендіокси, феніл, феніл(С 1-4)алкіл, фенокси, фенілтіогрупа, феніл(С1-4)алкокси, гетероарил, гетеро арил(С 1-4)алкіл, гетероарилокси або гетероарил(С 1-4)алкоксил; де будь-який з вищезазначених фенілу та гетероарилу, як варіант, заміщено таким будь-який з вищезазначених фенілу та гетероарилу, як варіант, заміщено таким замісником: галоген, гідрокси, нітро, S(O)r(С1-4алкіл), S(O)2NH2, ціано, С1-4алкіл, С1-4алкокси, C(O)NH2, С(О)NH(С1-4алкіл), СО2Н, СО2(С1-4алкіл), NHC(O)(C1-4алкіл), NHS(O)2(С1-4алкіл), C(O)(С14алкіл), CF3 або OCF3; k та r дорівнюють, незалежно, 0,1 або 2; R13, R14,R15, R 16, R17, R18 , R19 , R20 , R21, R22 , R23, R24, R28 , R27, R29, R30 та R31 предста 15 вляють, незалежно, гідроген, С1-4алкіл (як варіант, заміщений галогеном, гідрокси або С 310циклоалкілом), СН 2(С 2-6алкеніл), феніл (сам, як варіант, заміщений галогеном, гідрокси, нітро, NH2, NH(C1-4алкілом), NH(С1-4алкілом)2, S(O)2(С1S(O)2NH2, ціано, С1-4алкілом, С14алкілом), 4алкокси, C(O)NH 2, C(O)NH(С 1-4алкілом), СО2Н, СО2(С1-4алкілом), NНС(О)(С1-4алкiлом), NHS(O)2(С1-4алкілом), С(О)(С1-4алкілом), CF3 або OCF3) або гетероцикліл (сам, як варіант, заміщений галогеном, гідрокси, нітро; NH2, NH(C1N(С1-4алкілом)2, S(O)2(С1-4алкілом), 4алкілом), S(O)2NH2, S(O)2NH(С1-4алкілом), S(O)2N(С1ціано, С1-4алкілом, С1-4алкокси, 4алкілом)2, C(O)NH2, C(O)NH(C1-4aлкiлoм), C(O)N(C14алкілом)2, CO2H, СО2(С 1-4алкілом), NHC(O)(С 1NHS(O)2(С1-4алкілом), С(О)(С14алкілом), CF3 або OCF3); альтернативно 4алкілом), NR13R14, NR15R16 , NR20R21, NR22R23, NR26R27 , можуть, незалежно, утворювати 4-7-членне гетероциклічне кільце, азетидин, піролідин, піперидин, азепін, 1,4-морфолін або 1,4-піперазин, останній, як варіант, заміщений С1-4алкілом на дистальному атомі нітрогену; R12 , R25 та R28 представляють, незалежно, С1-6алкіл (як варіант, заміщений галогеном, гідрокси або С3-10циклоалкілом), СН2(С26алкеніл), феніл (сам, як варіант, заміщений галогеном, гідрокси, нітро, NH2, NH(С1-4алкілом), N(С14алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 ви ще), S(О)2(С1-4алкілом), S(O)2NH2, S(O)2NH(C14алкілом), S(O)2N(C 1-4алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 вище), ціано, C1-4алкілом, С1C(O)NH2, С(О)NН(С1-4алкілом), 4алкокси, С(О)N(С1-4алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R 13 та R14 вище), СО 2Н, СО2(C1-4алкілом), NHC(O)(C1NНS(О)2(C1-4алкілом), С(О)(С14алкілом), 4алкілом), CF3 або OCF3) або гетероцикліл (сам, як варіант, заміщений галогеном, гідрокси, нітро, NH2, NH(C1-4алкілом), N(C1-4алкілом) (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 ви ще), S(O) 2(C1-4алкілом), S(O)2NH2, S(O)2NH(C1-4алкілом), S(O)2N(C14алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 ви ще), ціано, C1-4алкілом, С1-4алкокси, C(O)NH2, C(O)NH(C1-4алкілом), C(O)N(C1-4алкілом)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 вище), СО2Н, СО2(C1NHC(O)(C1-4алкілом), NHS(O)2(C14алкілом), 4алкілом), С(О)(C 1-4алкілом), CF3 або OCF3); або її N-оксид; або її фармацевтично прийнятну Згідно з наступним аспектом представленого винаходу запропоновано сполуку формули (І) де: X представляє О; Υ представляє зв'язок, СН2, NR35, CH2NH, CH(OH), CH(NHC(O)R 33), 34 CHCNHS(O)2R ) або СН2О; Ζ представляє С(О), або коли Υ представляє зв'язок, Ζ може також бути S(O)2; R1 представляє заміщений, як варіант, феніл; R4 представляє гідроген або С1-6алкіл; R2, R3, R5 , R6, R7 та R8, при наявності, усі представляють гідроген; m та n дорівнюють, незалежно, 0 або 1; R9 представляє заміщений, як варі 80268 16 ант, арил або, заміщений, як варіант, гетероцикліл; R32 та R35 представляють, незалежно, гідроген або С1-6алкіл; R33 та R34 представляють С 1-6алкіл; де будь-який з вищезазначених фенілу та гетероарилу, коли можливо, як варіант, заміщено таким замісником: галоген, ціано, гідрокси, оксо, S(O)2R12, NR15R16, NR17C(O)R18 , S(O)2NR22R23, KR24S(O)2R25, C(O)NR26R27 , CО2R29 , C1-6алкіл (сам, як варіант, монозаміщений ΝNC(Ο)фенілом), CF3, OCF 3, феніл або гетероарил; де будь-який з вищезазначених фенілу та гетероарилу, як варіант, заміщено таким замісником: галоген, С1-4алкіл, С1-4алкокси або CF3; R15, R16, R17 , R18, R22, R23 , R24, R26, R27 тa R29 представляють, незалежно, гідроген, С1-4алкіл (як варіант, заміщений гідрокси) або С3-6циклоалкіл; альтернативно NR22R23 може утворювати азетидинове кільце (саме, як варіант, заміщене гідрокси або С 1-4алкілом); R12 та R25 представляють, незалежно, С1-6алкіл або феніл; або її фармацевтично прийнятну сіль. Згідно з подальшим аспектом R1 представляє феніл, як варіант, заміщений (наприклад одним, двома або трьома) галогенами (особливо флуором або хлором), ціано, С1-4алкілом (особливо метилом), С1-4алкокси (особливо метокси), S(O)2(С1-4алкілом), S(O)2NH2, S(O)2NH(С14алкілом), S(О)2NН(С 3-6циклоалкілом), С(О)2(С 14алкілом), C(O)NH(С 1-4алкілом) або C(O)NH 2. Згідно з іншим аспектом R1 представляє феніл, як варіант, заміщений (наприклад одним, двома або трьома) галогенами (особливо флуором або хлором), ціано, С1-4алкілом (особливо метилом) або С 1-4алкокси (особливо метокси). Згідно з наступним аспектом R1 представляє феніл, заміщений одним, двома або трьома флуорами, хлорами, метилами або ціано. Згідно з іншим аспектом R1 є феніл заміщений одним, двома або трьома флуорами, хлорами, метилами. Відтак, R1 представляє, наприклад, 2-метил4-хлорфеніл, 3-метил-2,4-дихлорфеніл, 3,4дифлуорфеніл, 3-флуор-4-хлорфеніл або 4хлорфеніл. Згідно з подальшим аспектом R1 представляє 3,4-дихлорфеніл. Згідно з іншим аспектом X представляє О. Згідно з ще одним аспектом Υ представляє зв'язок. Згідно з іншим аспектом Ζ представляє С(О). Згідно з наступним аспектом m дорівнює 0. Згідно з подальшим аспектом n дорівнює 0. Згідно з іншим аспектом обидва m та n дорівнюють 0. Згідно з іншим аспектом R4 представляє гідроген або С1-4алкіл (як-то метил). Згідно з ще одним аспектом R4 представляє гідроген. Згідно з ще одним аспектом R2, R3, R5, R6, R7 та R8 усі представляють гідроген; а згідно з наступним аспектом n дорівнює 0, a R2, R3, R5 та R6 усі представляють гідроген. Згідно з наступним аспектом R2, R3, R4, R5, 6 R , R7 та R8 усі, при наявності, представляють гідроген. Згідно з подальшим аспектом R9 представляє моно- або дизаміщений феніл, незамі-щений ге 17 тероцикліл або моно- або дизаміщений гетероцикліл, замісники вибрано з описаних вище. Згідно з іншим аспектом R9 є, заміщений, як варіант, гетероцикліл де гетероцикліл представляє: тієніл, піроліл, тіазоліл, піразоліл, оксазоліл, ізоксазоліл, імідазоліл, 1,2,5-оксадіазоліл, піридиніл, 1,6-дигідропіридиніл (наприклад у 6-оксо1,6-дигідропіридинілі або 2-оксо-1,2дигідропіридинілі), піримідиніл, індоліл, індазоліл, 2,3-дигідро-1Н-індазоліл (наприклад у 3-оксо-2,3дигідро-1Н-індазолілі), імідазопіридиніл (як-то імідазо[1,2-а]піридиніл), 2,1,3-бензотіадіазоліл, хіноксалініл, хінолініл, 1,2-дигідрохінолініл (наприклад у 2-оксо-1,2-дигідрохінолінілі), 1,4дигідрохінолін (наприклад у 4-оксо-1,4дигідрохіноліні), ізохінолініл, 1,2дигідроізохінолініл (наприклад у 2Н-ізохінолін-1онілі (альтернативно під назвою 1-оксо-1,2дигідроізохінолініл або 1,2-дигідроізохінолініл-1он)), цинолініл, 3,4-дигідрофталазиніл (наприклад у 4-оксо-3,4-дигідрофталазинілі), 2,3-дигідро-4Н1,4-бензоксазиніл (наприклад у 3-оксо-2,3дигідро-4Н-1,4-бензоксазинілі), 3,4-дигідро-2Н1,4-бензоксазиніл (наприклад у 3-оксо-3,4дигідро-2Н-1,4-бензоксазинілі), 1,3-дигідро-2Нізоіндоліл (наприклад у 1,3-діоксо-1,3-дигідро-2Нізоіндолілі), піразолотриазиніл (наприклад піразоло[5,1-с][1,2,4]триазиніл), піразолопіримідиніл (наприклад піразоло[1,5-а]піримідиніл), імідазобензотіазоліл (наприклад імідазо[2,1b][1,3]бензотіазоліл), імідазо-піримідиніл (наприклад імідазо[1,2-а]піримідиніл), або 2,1,3бензоксадіазоліл (наприклад, як 1-оксид), 1,3бензотіазол, 2,3-дигідро-1,3-бензотіазол (наприклад у 2-оксо-2,3-дигідро-1,3-бензотіазолі), 4,5,6,7-тетрагідроіндазол або 2,3-дигідро-1Нбензімідазол (наприклад у 2-оксо-2.,3-дигідро-1Нбензімідазоліл). У ще одному аспекті арил (як-то феніл) або гетероцикліл R9 незаміщено або заміщено одним або більше з: оксо (де можливо), галогену, С1CF3, С 1-4алкокси, S(О)2(С1-4алкілу), 4алкілу, S(O)2NH2, S(O)2NH(С1-4алкілу), S(O) 2N(С1-4алкілу)2 або OCF3. Згідно з наступним аспектом, коли R9 є гетероциклілом, він представляє заміщений, як варіант, тієніл, хінолініл, 1,2-дигідрохінолініл, 1,3бензтіазоліл, 2,3-дигідро-1,3-бензотіазоліл, імідазо[1,2-а]піридиніл, ізохінолініл або 1,2дигідроізохінолініл; або 1,2-дигідропіридон, 1,6дигідропіридон, піразоліл, піроліл або індоліл. У ще одному аспекті R9 представляє феніл або гетероцикліл (як визначено будь-де вище), кожний з яких, як варіант, заміщений галогеном, гідрокси, нітро, ціано, оксо, аміногрупою, С14алкілом (самим, як варіант, заміщеним S(О)2(С 1або S(О)2фенілом), С1-4алкокси, 4алкілом) S(O)kR12 {де k дорівнює 0, 1 або 2 (переважно 2); a R12 представляє С 1-4алкіл, С1-4гідроксіалкіл, С37циклоалкіл(С 1-4алкіл) (як-то циклопропілметил) або феніл}, C(O)NH 2, NHS(O)2(С1-4алкіл), S(O)2NH2, S(O)2NH(С1-4алкіл) або S(O)2N(С14алкіл)2 (ці алкіли можуть поєднуватися з утворенням кільця, як описано для R13 та R14 ви ще). 80268 18 Згідно з іншим аспектом R32 представляє гідроген. Згідно з наступним аспектом R13, R14, R15 , R16, R17, R18, R19, R20, R21, R22 , R23 , R24 , R23 , R27 , R29 , R30 та R31 представляють, незалежно, гідроген, С1-4алкіл (як варіант, заміщений галогеном, гідрокси або С3-10циклоалкілом), СН2(С2-6алкеніл), феніл (сам, як варіант, заміщений галогеном або С 14алкілом) або гетероцикліл (сам, як варіант, заміщений галогеном або С1-4алкілом); a R12, R25 та R28 представляють, незалежно, С1-4алкіл (як варіант, заміщений галогеном, гідрокси, нітро, NH2, NН(С1-4алкілом), N(C1-4алкілом)2, S(O)2(C1-4C алкілом), S(O)2NH2, S(О)2NН(С1-4алкілом), S(O)2N(C1-4aлкiлoм)2, ціано, С1-4алкілом, С1C(O)NH2, С(O)NН(С1-4алкілом), 4алкокси, С(O)N(С1-4алкілом)2, СО2Н, СО(С1-4алкілом), NHC(O)(С1-4алкілом), NHS(O)2(С1-4алкілом), С(О)(С1-4алкілом); a R12, R25 та R28 представляють, незалежно, С1-4алкіл (як варіант, заміщений галогеном, гідрокси або С3-10циклоалкілом), СН2(С2-6алкеніл), феніл (сам, як варіант, заміщений галогеном або С 1-4алкілом) або гетероцикліл (сам, як варіант, заміщений галогеном або С 14алкілом). Згідно з подальшим аспектом R13, R14 , R15, 16 R , R17, R18, R19, R20, R21 , R22 , R23 , R24 , R26 , R27 , R29 та R30 представляють, незалежно, гідроген, С1-4алкіл (як варіант, заміщений галогеном, гідрокси або С3-10циклоалкілом), СН2(С2-6алкеніл), феніл (сам, як варіант, заміщений галогеном або С 14алкілом) або гетероцикліл (сам, як варіант, заміщений галогеном або С 1-4алкілом); a R12, R25, R28 та R 31 представляють, незалежно, С1-4алкіл (як варіант, заміщений галогеном, гідрокси або С3-10циклоалкілом), СН2(С2-6алкеніл), феніл (сам, як варіант, заміщений галогеном або С 1-4алкілом) або гетероцикліл (сам, як варіант, заміщений галогеном або С1-4алкілом). У ще одному аспекті R13, R14, R15, R16, R17, 18 R , R19, R20, R21, R22, R23, R24, R26, R27, R29 та R30 представляють, незалежно, гідроген або С112 25 28 та R31 представляють, неза4алкіл; a R , R , R лежно, С1-6алкіл (як варіант, заміщений гідрокси) або феніл. Згідно з наступним аспектом R10 представляє гідроген. Згідно з іншим аспектом R35 представляє гідроген або С 1-6алкіл (як-то метил); (наприклад R35 представляє гідроген). У ще одному аспекті R33 представляє С 16алкіл (як-то метил). Згідно з наступним аспектом R34 представляє С1-6алкіл (як-то метил). Згідно з подальшим аспектом представлений винахід забезпечує сполуку формули (І) або (Іа) де: R1 представляє феніл, як варіант, заміщений 2 галогенами (як-то хлор); X представляє О; m дорівнює 0; n дорівнює 0 або 1; R2 R3, R4, R5, R6 , R7 та R8 усі представляють гідроген; a R9 представляє феніл, тієніл, хінолініл, 1,3-бензтіазоліл, 2,3-дигідро-1,3-бензотіазоліл5 імідазо[1,2а]піридиніл або 1,2-дигідроізохінолініл, як варіант, заміщений S(О)2(С1-4алкілом) (наприклад S(O)2CH3), галогеном (наприклад хлор або флу 19 ор), ΝN2, С1-4алкокси (як-то ОСН 3), ціано або, де можливо, оксо. Згідно з іншим аспектом представленого винаходу запропоновано сполуку формули (І) або (Іа) де: R1 представляє феніл, як варіант, заміщений 1 або 2 галогенами (як-то хлор), або 1 або 2 галогенами (як-то хлор) та С1-4алкіл. (як-то метил); X представляє О; m дорівнює 0; n дорівнює 0 або 1; R2, R3, R4, R5 та R6, а при наявності, R7 та R8 усі представляють гідроген; a R9 представляє феніл, тієніл, хінолініл, 1,3-бензтіазоліл, 2,3дигідро-1,3-бензотіазоліл, імідазо[1,2-а]піридиніл, 1,2-дигідроізохінолініл, 1,2-дигідропіридиніл, 1,6дигідропіридиніл або піразоліл, усі які заміщені, як варіант, S(О)2(С1-4алкілом) (наприклад S(O)2CH3), S(O)2NH2, S(O)2NH(С1-4алкілом), S(О)2N(С1-4алкілом)2 (де два алкіли можуть поєднуватися разом з утворенням азетидинового кільця), галогеном (наприклад хлор або флуор), NH2, С1-4алкілом (як-то СН 3), С1-4алкокси (як-то ОСН3), CF3 , ціано або, де можливо, оксо. Згідно з іншим аспектом представленого винаходу запропоновано сполуку формули (І) або (Іа). де: R1 представляє феніл, як варіант, заміщений 1 або 2 галогенами (як-то хлор) та, як варіант, заміщений 0 або 1 С1-6алкілом (як-то метил); X представляє О; m дорівнює 0; n дорівнює 0 або 1; R2, R3, R4, R5 та R6 та, при наявності, R7 та R8, усі представляють гідроген; a R9 представляє феніл, тієніл, хінолініл, 1,3-бензтіазоліл, 2,3дигідро-1,3-бензотіазоліл, імідазо[1,2-а]піридиніл, 1,2-дигідроізохінолініл, 1,2-дигідропіридиніл, 1,6дигідропіридиніл, піразоліл, піроліл або індоліл, усі які, як варіант, заміщені 8(О)2(С1^)алкілом) (наприклад S(O)2CH3), S(O)2NH2 , S(O) 2NH(C14алкілом), S(O)2N(C 1-4aлкiлoм)2, галогеном (наприклад хлор або флуор), NH2, С1-4алкокси (як-то ОСН3), С1-4алкілом (як-то метил), CF3, OCF3, ціано або, де можливо, оксо. Згідно з ще одним аспектом представленого винаходу запропоновано сполуку формули (І) або (Іа) де: R1 представляє феніл, як варіант, заміщений 1 або 2 галогенами (як-то хлор) та, як варіант, заміщений 0 або 1 С1-4алкілом (як-то метил); X представляє О; m дорівнює 0; n дорівнює 0 або 1; R2, R3 , R4, R5, R6, R7 та R8 усі представляють гідроген; a R9 представляє феніл, тієніл, хінолініл, 1,3-бензтіазоліл, 2,3-дигідро-1,3бензотіазоліл, імідазо[1,2-а]піридиніл або 1,2дигідроізохінолініл, усі які, як варіант, заміщені S(О)2(С1-4алкілом) (наприклад S(O)2CH3), галогеном (наприклад хлор або флуор), NH2, С14алкокси (як-то ОСН 3), С 1-4алкілом (як-то метил), CF3, OCF 3, ціано або, де можливо, оксо. Згідно з іншим аспектом представленого винаходу запропоновано сполуку формули (І) або (Іа) де R9 представляє ізохінолініл, 1-оксо-1,2дигідроізохінолініл, хінолініл, 2-оксо-1,2дигідрохінолініл, 2чжсо-1,2-дигідропіридиніл, 6оксо-1,6-дигідропіридиніл або піразоліл; кожний, як варіант, заміщений галогеном (як-то флуор), С1-4алкілом (як-то метил або етил), CF3, С14алкокси (як-то метокси), S(О)2(С 1-4алкілом) (наприклад S(O)2CH3), S(O)2NH2, S(O)2NH(C1-4алкіл), S(O)2N(C1-4алкілом)2 або OCF3. 80268 20 Згідно з іншим аспектом представленого винаходу запропоновано сполуку формули (І) або (Іа) де R9 представляє ізохінолініл, 1-оксо-1,2дигідроізохінолініл, хінолініл або 2-оксо-1,2дигідрохінолініл; кожний, як варіант, заміщений галогеном (як-то флуор), С1-4алкілом (як-то метил або етил), CF3, С1-4алкокси (як-то метокси), S(О)2(С1-4алкілом) (наприклад S(O)2CH3) або OCF3. Згідно з подальшим аспектом R9 представляє 1-оксо-1,2-дигідроізохінолініл, як варіант, заміщений галогеном (як-то флуор), С1-4алкілом (як-то метил або етил), CF3, С1-4алкокси (як-то метокси), S(O)2(С1-4алкілом) (наприклад S(O)2CH3) або OCF3. Альтернативно, R9 представляє 2-оксо-1,2дигідрохінолініл, як варіант, заміщений галогеном (як-то флуор), С1-4алкілом (як-то метил або етил), CF3, С1-4алкокси (як-то метокси), S(О)2(С14алкілом) (наприклад S(O)2CH 3) або OCF3. Згідно з іншим аспектом R9 представляє оксо-заміщений дигідропіридиніл (як-то 6-оксо-1,6дигідропіридин-3-іл, 2-оксо-1,2-дигідропіридин-5іл або 2-оксо-1,2-дигідропіридин-4-іл, оксозаміщений дигідроізохінолініл (як-то 1-оксо-1,2дигідроізохінолін-4-іл), оксо-заміщений дигідрофталазиніл (як-то 4-оксо-3,4-дигідрофталазин-1-іл), піразиніл (як-то піразин-4-іл), піроліл (як-то пірол3-іл) або індоліл (як-то індол-3-іл), кожний з яких не заміщено далі або заміщено галогеном (як-то хлор або флуор), С1-4алкілом (як-то метил), CF3 або С3-5циклоалкілом (як-то циклопропіл). Згідно з наступним аспектом R9 представляє оксо-заміщений дигідропіридиніл (як-то 6-оксо1,6-дигідропіридин-3-іл, 2-оксо-1,2дигідропіридин-5-іл або 2-оксо-1,2дигідропіридин-4-іл)) оксо-заміщений дигідроізохінолініл (як-то 1-оксо-1,2-дигідроізохінолініл-4-іл) або піразиніл (як-то піразин-4-іл), кожний з яких не заміщено далі або заміщено галогеном (як-то хлор або флуор), С1-4алкілом (як-то метил) чи CF3. Прикладом сполуки формули (І) або (Іа) є: Ν-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-2(метилсульфоніл)бензамід; N-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-4(метилсульфоніл)бензамід; 2-хлор-N-{(2R)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2-гідроксипропіл}4-(метилсульфоніл)бензамід; 4-аміно-N-{(2R)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2-гідроксипропіл)3-метоксибензамід; N-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-3(метилсульфоніл)бензамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-5-(метилсульфоніл)тіофен-2карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}xiнoлiн-6-карбоксамід; N-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-2-оксо-2,3-дигідро-1,3бензотіазол-6-карбоксамід ацетат; 21 N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-6-флуорімідазо[1,2а]піридин-2-карбоксамід; N-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-1-оксо-1,2-дигідроізохінолін4-карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-1,3-бeнзoтiaзoл-6карбоксамід; 3-ціано-N-{(2R)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2гідроксипропіл}бензамід; N-{4-[4-(3,4-дихлорфенокси)піперидин-1-іл]-3гідроксибутил}-2-(метилсульфоніл)бензамід; N-{4-[4-(3,4-дихлорфенокси)піперидин-1-іл]-3гідроксибутил}-2-оксо-2,3-дигідро-1,3бензотіазол-6-карбоксамід; 4-аміно-N-{4-[4-(3,4дихлорфенокси)піперидин-1-іл]-3-гідроксибутил}3-метоксибензамід; N-{4-[4-(3,4-дихлорфенокси)піперидин-1-іл]-2гідроксибутил}-2-(метилсульфоніл)бензамід; N-{(2R)-3-[4-(2,4-дихлор-3метилфенокси)піперидин-1-іл]-2-гідроксипропіл}2-(метилсульфоніл)бензамід; N-{(2R)-3-[4-(2,4-дихлор-3метилфенокси)піперидин-1-іл]-2-гідроксипропіл}1-оксо-1,2-дигідроізохінолін-4-карбоксамід; N-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-2(метилсульфоніл)бензамід; N-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-3[(метиламіно)сульфоніл]бензамід; 3,5-біс(ацетиламіно)-N-{(2R)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2гідроксипропіл}бензамід; 3-(Ацетиламіно)-N-{(2R)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2гідроксипропіл}бензамід; N-{(2R)-3-[4-(3)4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-1H-пipaзoл-4-карбоксамід; 2-(Aцeтилaмiнo)-5-бpoм-N-{(2R)-3-[4-(3,4диxлopфeнoкcи)пiпepидин-1-iл]-2гідроксипропіл}бензамід; Ν-{(2S)-3-[4-(3,4-диxлopфeнoкcи)niпepидин-1ілі-2-гідроксипропіл}-2-οκοο-1,2-дигідропіридин-3карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)niпepидин-1ілі-2-гідроксипропіл}-1-оксо-1,2-дигідроізохінолін5-карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-1H-xiнoлiнiн-4-карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-1H-iндoл-4-карбоксамід; 2-(Aцeтилaмiнo)-N-{(2R)-3-[4-(3,4дихлopфeнoкcи)пiпepидин-1-iл]-2гідроксипропіл}бензамід; 2-(Aцeтилaмiнo)-5-xлop-N-{(2R)-3-[4-(3)4диxлopфeнoкcи)пiпepидин-1-iл]-2гідроксипропіл}бензамід; 2-(Aцeтилaмiнo)-4-хлop-N-{(2R)-3-[4-(3,4диxлopфeнoкcи)пiпepидин-1-iл]-2гідроксипропіл}бензамід; 80268 22 5-xлop-N-{(2R)-3-[4-(3,4дихлopфeнoкcи)пiпepидин-1-iл]-2-гiдpoкcипpoпiл}2-[(метилсульфоніл)аміно]бензамід; 4-xлop-N-{(2R)-3-[4-(3,4диxлopфeнoкcи)пiпepидин-1-iл]-2-гiдpoкcипpoпiл}2-[(метилсульфоніл)аміно]бензамід; 2-Aмiнo-4-xлop-N-{(2R)-3-[4-(3,4диxлopфeнoкcи)пίпepидин-1-iл]-2гідроксипропіл}бензамід; 5-хлор-N-{(2R)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-6-оксо-1,6дигідропіридин-3-карбоксамід; 2-(Аміносульфоніл)-1-хлор-N-{(2R)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2гідроксипропіл]бензамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-1H-iндaзoл-3-карбоксамід; 1-трет-бутил-Ν-{(2R)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2-гідроксипропіл}3-метил-1Н-піразол-5-карбоксамід; Ν-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-4,5,6,7-тетрагідро-2Ніндазол-3-карбоксамід; N-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-3-(трифлуорметил)-1Нпіразол-4-карбоксамід; N-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-2-метилімідазо [1,2а]піридин-3-карбоксамід; N-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-4-(1Н-піразол-3-іл)бензамід; N-{(2R)-3-[4-(3,4-дихлopфeнoкcи)пiпepидин4iл]-2-гiдpoкcипpoпiл}цинoлiн-4-карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-rιдpoкcипpoпiл}-2-гiдpoкcиxiнoлiн-4карбоксамід; Ν-{3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1-iл]-2rιдpoкcипpoпiл}-2-оксо-2,3-дигідро-1Нбензімідазол-1-карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-4-oкco-3,4-дигідрофталазин1-карбоксамід; Ν-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гідpoкcипpoпiл}-1Н-індол-3-карбоксамід; N-{(2R)-3-[4-(4-Xлopфeнoкcи)пiпepидин-1-iл]2-гiдpoкcипpoпiл}-2-(метилсульфоніл)бензамід; N-{(2R)-3-[4-(4-xлopфeнoкcи)пiпepидин-1-іл]2-гідроксипропіл}-1-оксо-1,2-дигідроізохінолін-4карбоксамід; N-{(2R)-3-[4-(4-Xлop-3флyopфeнoкcи)пiпepидин-1-іл]-2-гідроксипропіл}1-оксо-1,2-дигідроізохінолін-4-карбоксамід; N-{(2R)-3-[4-(3,4-дифлyopфeнoкcи)пiпepидин1-iл]-2-гiдpoкcипpoпiл}-1-oкco-1,2дигідроізохінолін-4-карбоксамід; Ν-{(2S)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-N-мeтил-1-оксо-1,2дигідроізохінолін-4-карбоксамід; N-{(2S)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-N-мeтил-1H-iндaзoл-3карбоксамід; N-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-N-метил-4-оксо-[3,4дигідрофталазин-1-карбоксамід; 23 Бензойної кислоти 3-[[2-[[(2R)-3-[4-(3,4дихлорфенокси)-1-піперидиніл]-2гідроксипропіл]аміно]-2-оксоетил]аміно]-, метиловий естер; Пропанамід, N-[2-[[2-[[(2R)-3-[4-(3,4дихлорфенокси)-1-піперидиніл]-2гідроксипропіл]аміно]-2-оксоетил]аміно]феніл]-; Пропанамід, N-[2-[[2-[[(2R)-3-[4-(3,4дихлорфенокси)-1-піперидиніл]-2гідроксипропіл]аміно]-2-оксоетил]аміно]феніл]-; (2S)-N-{(2R)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2-гідроксипропіл}2-гідрокси-2-фенілетанамід; 2-[2-({(2R)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2гідроксипропіл}аміно)-2-оксоетокси]бензамід; Ν-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-2-(3-оксо-2,3-дигідро-4Н-1,4бензоксазин-4-іл]ацетамід; N-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-2-метоксибензамід; Ν-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-2-(метиламіно)бензамід; Ν-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}нікотинамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}iзoнiкoтинaмiд; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)п iпepидин-1iл]-2-гiдpoкcипpoпiл}-3-(диметиламіно)бензамід; Ν-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-2-(1,3-діоксо-1,3-дигідро-2Нізоіндол-2-іл)ацетамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-6-гідроксинікотинамід; Ν-{(2R)-3-[4-(3,4--дихлорфенокси)піперидин1-іл]-2-гідроксипропіл}-2-(1H-індол-3-іл)ацетамід; N-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}дицикло[4,2,0]окта-1,3,5триєн-7-карбоксамід; N-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-4,7-диметилпіразоло[5,1с][1,2,4]триазин-3-карбоксамід; Ν-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}піразин-2-карбоксамід; N-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-9Н-пурин-6-карбоксамід; N-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}хінолін-6-карбоксамід; Ν-{(2R)-3-[4-дихлорфенокси)піперидин-1-іл]2-гідроксипропіл}-2,7-диметилпіразоло[1,5а]піримідин-6-карбоксамід; Ν-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-2-(піримідин-2ілтіо)ацетамід; N-{(2R)-3-[4-(3,4-дихлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-5-флyop-1H-iндoл-2карбоксамід; Ν-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1ілі-2-гідроксипропіл}1,3-бензотіазол-6карбоксамід; Ν-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-5-феніл-1,3-оксазол-4карбоксамід; 80268 24 N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-6-гiдpoкcипipидин-2карбоксамід; Ν-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-3-оксо-3,4-дигідро-2Н-1,4бензоксазин-7-карбоксамід; N-{(2R)-3-[4-(3,4-дихлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-3-гiдpoкcипipидин-2карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-1H-бeнзiмiдзoл-5карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-1H-iндoл-5-кapбo-ксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-1-мeтил-1H-індол-2карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пίпepидин-1iл]-2-гiдpoкcипpoпiл}-1H-iмiдaзoл-4-карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-1H-iндoл-6-карбоксамід; Ν-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-1-метил-1Н-індол-3карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-1H-iндoл-7-карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-riдpoкcипpoпiл}-3[(метиламіно)сульфоніл]бензамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-3,4біс(метилсульфоніл)бензамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcиnpoпiл}-2-пipидин-3-ілацетамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-5-гiдpoкcи-1H-індол-2карбоксамід; N-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-1,5-диметил-1Н-піразол-3карбоксамід; N-{(2R)-3-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-5-(метилсульфоніл)-1Ніндол-2-карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-xiнoкcaлiн-6-карбоксамід; N-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-1,8-нафтиридин-2карбоксамід; N-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-1Н-імідазо[2,1][1,3]бензотіазол-2-карбоксамід; N-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-2,6-диметилімідазо[1,2а]піридин-3-карбоксамід; Ν-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-3-оксо-2,3-дигідро-1Ніндазол-4-карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-3-гiдpoкcи-1H-індазол-6карбоксамід; Ν-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-3-(трифлуорметил)-1Нпіразол-4-карбоксамід; 25 2-(1Н-бензімідазол-1-іл)-N-{(2R)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2-гідроксипропіл} ацетамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-1-eтил-3-мeтил-1 Н-піразол5-карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-5-мeтил-1H-піразол-3карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гιдpoкcипpoпiл}-4-мeтил-1,2,5-оксадіазол-3карбоксамід; 6-xлop-N-{(2R)-3-[4-(3,4диxлopфeнoкcи)пiпepидин-1-iл]-2гідроксипропіл}імідазо[1,2-а]піридин-2карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-2-метилімідазо[1,2а]піридин-3-карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-riдpoкcипponiл}iмiдaзo[1,2-а[піримідин-2карбоксамід; N-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-2-[(4-метилпіримідин-2іл)тіо]ацетамід; N-{(2R)-3-[4-(3,4-дихлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-4-гiдpoкcиxiнoлiн-2карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-riдpoкcипpoпiл}xiнoлiн-8-кapбoкcaмiд; Ν-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-5-метилімідазо[1,2а]піридин-2-карбоксамід; Ν-{(2Κ)-3-[4-(3,4--дихлорфенокси)піперидин1-іл]-2-гідроксипропіл}-імідазо[1,2-а]піридин-2карбоксамід; Ν-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-1,6-нафтиридин-2карбоксамід; N-{(2R)-3-[4-(3,4-дихлopфeнoкcи)пiпepидин-1іл]-2-гідроксипропіл}-2,1,3-бензоксадіазол-5карбоксамід 1-оксид; Ν-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-6-оксо-1,6-дигідропіридин-3карбоксамід; 4-Хлор-Ν-{(2R)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2-гідроксипропіл}1N-піразол-3-карбоксамід; Ν-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-5-феніл-1,3-оксазол-4карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-riдpoкcипpoпiл}-3,5-димeтил-1H-піразол-4карбоксамід; (2R)-2-(Aцeтилaмiнo)-N-{(2R)-3-[4-(3,4диxлopфeнoкcи)пiпepидин-1-iл]-2-гiдpoкcипpoпiл}2-фенілетанамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гідроксипpoпiл}-2-(2-гідроксифеніл)ацетамід; (2R)-N-{(2R)-3-[4-(3,4диxлopфeнoкcи)пiпepидин-1-iл]-2-гідpoкcипpoпіл}2-[(метилсульфоніл)аміно]-2-фенілетанамід; (2S}-2-(Ацетиламіно)-N-{(2R)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2-гідроксипропіл}2-фенілетанамід; 80268 26 (2S)-N-{(2R)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2-гідроксипропіл}2-[(метилсульфоніл)аміно]-2-фенілетанамід; 1-{2R-4.(3,4-диxлopфeнoкcи)пiпepидин-1-iл]2-гiдpoкcипpoпiл}-3-o-тoлiл-ceчoвинa; 1-{(R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-3-п-тoлiл-ceчoвинa; 1-{(R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідрокси-2-метилпропіл}-1-оксо-1,2дигідроізохінолін-4-карбоксамід; N-{(2S)-3-[4-(3,4-диxлopфeнoкcи)п iпepидин-1іл]-2-гідрокси-2-метилпропіл}-1-оксо-1,2дигідроізохінолін-4-карбоксамід; N-{(2S)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcи-2-мeтилпpoпiл}-2-oкco-1,2дигідрохінолін-4-карбоксамід; N-{(2S)-3-[4-(3,4-диxлopфeнoкcи)п iпepидин-1iл]-2-гiдpoкcи-2-мeтилпpoпiл}-4-oкco-3,4дигідрофталазин-1-карбоксамід; (2S)-N-{(2S)-3-[4-(3,4диxлopфeнoкcи)пiпepидин-1-iл]-2-гiдpoкcи-2мeтилпpoпiл}-2-гідрокси-2-фенетанамід; Ν-{(2R)-3-[4-(4-хлор-2метилфенокси)піперидин-1-іл]-2-гідроксипропіл}1-оксо-1,2-дигідроізохінолін-4-карбоксамід; Ν-((2R)-3-{4-[2-(Амінокарбоніл)-3,4дихлорфенокси]піперидин-1-іл}-2-гідроксипропіл)1-оксо-1,2-дигідроізохінолін-4-карбоксамід; 3-ціано-N-{(2S)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2гідроксипропіл}бензолсульфонамід; 5-[({(2S)-3-[4-(3,4-дихлорфенокси)піперидин1-іл]-2-гідроксипропіл}аміно)-сульфоніл]-2метоксибензамід; Ν-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}1-оксо-1,2-дигідроізохінолін4-сульфонамід ацетат; N-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-2,4дифлуорбензолсульфонамід; N-{(2S)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-riдpoкcипpoпiл}мeтaнcyльфoнaмiд; N-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}бензолсульфонамід; N-{(2S)-3-[4-(3,4-дихлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-1-фенілметансульфонамід; N-{(2S)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoп iл}-4метоксибензолсульфонамід; N-({5-[({(2S)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2гідроксипропіл}аміно)сульфоніл]-2тієніл}метил)бензамід; 4-ціано-Ν-{(2S)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2гідроксипропіл}бензолсульфонамід; N-{5-[({(2S)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2гідроксипропіл}аміно)сульфоніл]-4-метил-1,3тіазол-2-іл}ацетамід; N-{(2S)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}тioфeн-2-сульфонамід; 4-[({(2S)-3-[4-(3,4-дихлорфенокси)піперидин1-іл]-2-гідроксипропіл) аміно)сульфоніл]бензойна кислота; 27 N-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-2,5диметоксибензолсульфонамід; N-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-4-(фенілсульфоніл)тіофен-2сульфонамід; Ν-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-5-(1,3-оксазол-5-іл)тіофен-2сульфонамід; N-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-5-[1-метил-5(трифлуорметил)-1Н-піразол-3-іл]тіофен-2сульфонамід; N-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-5-піридин-2-ілтіофен-2сульфонамід; 5-хлор-N-{(2S)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2-гідроксипропіл}1,3-диметил-1Н-піразол-4-сульфонамід; N-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-3,5-диметилізоксазол-4сульфонамід; N-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-2,1,3-бензотіадіазол-4сульфонамід; N-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-1-метил-1Н-імідазол-4сульфонамід; N-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-2,1,3-бензоксадіазол-4сульфонамід; N-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-лдроксипропіл}-5-ізоксазол-3-ілтіофен-2сульфонамід; метил 3-[({(2S)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2гідроксипропіл}аміно)сульфоніл]тіофен-2карбоксилат; 2,6-дихлop-N-{(2S)-3-[4-(3,4дихлopфeнoкcи)пiпepидин-1-iл]-2гідроксипропіл}бензолсульфонамід; Ν-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-3-метилбензолсульфонамід; 3-хлор-N-{(2S)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2гідроксипропіл}бензолсульфонамід; N-{(2S)-3-[4-(3,4-дихлopфeнoкcи)пiпepидин-1iл]-2-гідpoкcипpoпiл}пpoпaн-2-сульфонамід; N-{(2S)-3-[4-(3,4-дихлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}пpoпaн-1-cyльфoнaмiд; N-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-5-метил-1-феніл-1Н-піразол4-сульфонамід; 3-хлор-N-{(2S)-3-[4-{3,4дихлорфенокси)піперидин-1-іл]-2-гідроксипропіл}2-метилбензолсульфонамід; метил 5-[({(2S)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2гідроксипропіл}аміно)сульфоніл]-2-метил-3фуроат; метил 5-[({(2S)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2гідроксипропіл}аміно)сульфоніл]-1-метил-1Нпірол-2-карбоксилат; 80268 28 N-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-3,4диметоксибензолсульфонамід; 5-xлop-N-{(2S)-3-[4-(3,4дихлopфeнoкcи)пiпepидин-1-iл]-2гiдpoкcипpoпiл}тioфeн-2-сульфонамід; Ν-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-6-морфолін-4-ілпіридин-3сульфонамід; N-{2-хлор-4-[({(2S)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2гідроксипропіл}аміно)сульфоніл]феніл}ацетамід; Ν-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-2,3-дигідроксихіноксалін-6сульфонамід; Ν-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-2,4диметоксибензолсульфонамід; 5-[({(2S)-3-[4-(3,4-дихлорфенокси)піперидин1-іл]-2-гідроксипропіл}аміно)сульфоніл]-2метоксибензамід; N-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-2-метилбензолсульфонамід; Ν-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-2,4-диметил-1,3-тіазол-5сульфонамід; Ν-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-2-гідроксихіноксалін-6сульфонамід; Ν-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-4-метил-3,4-дигідро-2Н-1,4бензоксазин-7-сульфонамід; N-{(2S)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}пipидин-3-сульфонамід; 4-ціано-N-{(2S)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2гідроксипропіл}біфеніл-2-сульфонамід; N-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-1,2-диметил-1Н-імідазол-4сульфонамід; 4-ацетил-N-{(2S)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2гідроксипропіл}бензолсульфонамід; Ν-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-4(метилсульфоніл)бензолсульфонамід; 2-хлор-4-ціано-Ν-{(2S)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2гідроксипропіл}бензолсульфонамід; Ν-{(2S)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-1,3,5-триметил-1Н-піразол-4сульфонамід; Ν-[(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл]-1,4-піразол-4-оксо-3хінолінкарбоксамід; Ν-{(2S)-3-[4-(4-Хлор-2метилфенокси)піперидин-1-іл]-2-гідроксипропіл}1-оксо-1,2-дигідроізохінолін-4-карбоксамід ацетат; N-{(2S)-3-{4-(3,4-дихлopфeнoкcи)пiпepидин-1іл]-2-гідроксипропіл}-1-оксо-1,2-дигідроізохінолін4-карбоксамід; Ν-{(218)-3-{4-(3,4-дихлорфенокси)піперидин1-іл]-2-гідроксипропіл}-1-оксо-1,2дигідроізохінолін-4-карбоксамід; 29 Ν-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-7-[(метиламіно)сульфоніл]-1оксо-1,2-дигідроізохінолін-4-карбоксамід; Ν-{(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідроксипропіл}-7-{[(2гідроксіетил)аміно]сульфоніл}-1-оксо-2дигідроізохінолін-4-карбоксамід ацетат; 7-[(Циілопропіламіно)сульфоніл]-N-{(2R)-3-[4(3,4-дихлорфенокси)піперидин-1-іл]-2гідроксипропіл}-1-оксо-1,2-дигідроізохінолін-4карбоксамід; 7-(Азетидин-1-ілсульфоніл)-N-{(2R)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2-гідроксипропіл}1-оксо-1,2-дигідроізохінолін-4-карбоксамід ацетат; 7-(Аміносульфоніл)-N-{(2R)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2-гідроксипропіл}1-оксо-1,2-дигідроізохінолін-4-карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-7[(диметиламіно)сульфоніл]-1-оксо-1,2дигідроізохінолін-4-карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-7-[(3-гідрокси-3метилазетидин-1-іл)сульфоніл]-1-оксо-1,2дигідроізохінолін-4-карбоксамід ацетат; N-[(2R)-3-(4-{3,4-дихлор-2[(циклопропіламіно)карбоніл]фенікси}піперидин1-іл)-2-гідроксипропіл]-1-оксо-1,2дигідроізохінолін-4-карбоксамід ацетат; N-{(2R)-3-[4-(3-xлop-4цiaнoфeнoкcи)пiпepидин-1-iл]-2-гiдpoкcипpoпiл}-1оксо-1,2-дигідроізохінолін-4-карбоксамід; N-((2R)-2-Гiдpoкcи-3-{4-[4(мeтилcyльфoнiл)фeнoкcи]пiпepидин-1-іл}пропіл)1-оксо-1,2-дигідроізохінолін-4-карбоксамід; N-{(2R)-3-[4-(4-цiaнoфeнoкcи)пiпepидин-1-іл]2-гідроксипропіл}-1-оксо-1,2-дигідроізохінолін-4карбоксамід; N-((2R)-3-{4-[2-(Aмiнoкapбoнiл)-4xлopфeнoкcи]пiпepидин-1-iл}-2-гiдpoкcипpoпiл)-1oкco-1,2-дигідроізохінолін-4-карбоксамід; N-[(2R)-3-(4-{4-Хлор-2[(метиламіно)карбоніл]фенікси}піперидин-1-іл)-2гідроксипропіл]-1-оксо-1,2-дигідроізохінолін-4карбоксамід; Метил 5-хлор-2-{[1-((2R)-2-гідрокси-3-{[(1оксо-1,2-дигідроізохінолін-4іл)карбоніл]аміно}пропіл)піперидин-4іл]окси}бензоат ацетат; N-((2R)-3-{4-[2-(Aмiнocyльфoнiл-{3,4дихлopфeнoкcи}пiпepидин-1-iл)-2-гідроксипропіл]1-оксо-1,2-дигідроізохінолін-4-карбоксамід трифлуорацетат; N-[(2R)-3-(4-{3,4-дихлop-2[(мeтилaмiнo)cyльфoнiл]фeнoкcи}пiпepидин-1-iл)2-гідроксипропіл]-1-оксо-1,2-дигідроізохінолін-4карбоксамід ацетат; N-[(2R)-3-(4-{3,4-диxлop-2[(циклoпpoпiлaмiнo)cyльфoнiл]фeнoкcи}пiпepидин -1-iл)-2-гідроксипропіл]-1-оксо-1,2дигідроізохінолін-4-карбоксамід ацетат; N-{(2R)-3-[4-(3-xлop-4цiaнoфeнoкcи)пiпepидин-1-iл]-2-гiдpoкcипpoпiл}-7 80268 30 (метилсульфоніл)-1-оксо-1,2-дигідроізохінолін-4карбоксамід; N-{(2R)-3-{4-(4-хлор-2метилфенокси)піперидин-1-іл]-2-гідрокси-2метилпропіл}-6-(метилсульфоніл)-ІН-індол-3карбоксамід; N-{(2R)-3-{4-(3,4-диxлopфeнoкcи)пinepидин-1iл]-2-гідроксипpoпiл}-6-(мeтилcyльфoнiл)-1Hіндол-3-карбоксамід; Ν-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гідроксипропіл}-7-флуор-1-оксо-1,2дигідроізохінолін-4-карбоксамід; N-{(2R)-3-[4-(4-Xлop-2мeтилфeнoкcи)пiпepидин-1-iл]-2-гiдpoкcипpoпiл}7-флyop-1-oкco-1,2-дигідроізохінолін-4карбоксамід; Ν-{(2R)-3-[4-(4-Xлop-2мeтилфeнoкcи)пiпepидин-1-iл]-2-гiдpoкcипpoпiл}6-(метилсульфоніл)-1-оксо-1,2-дигідроізохінолін4-карбоксамід; Ν-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-riдpoкcипpoпiл}-6-(метилсульфоніл)-1-оксо1,2-дигідроізохінолін-4-карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-riдpoкcипpoпiл}-7-(мeтилcyльфoнiл)-1-оксо1,2-дигідроізохінолін-4-карбоксамід ацетат; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-riдpoкcипpoпiл}-7-(мeтилcyльфoнiл)-1-оксо1,2-дигідроізохінолін-4-карбоксамід ацетат; Ν-{(2R)-3-[4-(2,4-дихлор-3метилфенокси)піперидин-1-іл]-2-гідроксипропіл}7-(метилсульфоніл)-1-оксо-1,2-дигідроізохінолін4-карбоксамід ацетат; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-riдpoкcипpoпiл}-6-(мeтилcyльфoнiл)-1-оксо1,2-дигідроізохінолін-4-карбоксамід; Ν-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-riдpoкcипpoпiл}-6-флуор-1-оксо-1,2дигідроізохінолін-4-карбоксамід; N-{(2R)-3-[4-(4-xлop-2мeтилфeнoкcи)пiпepидин-1-iл]-2-гiдpoкcипpoпiл}6-флyop-1-oкco-1,2-дигідроізохінолін-4карбоксамід; N-((2R)-3-{4-[3,4-диxлop-2(мeтилcyльфoнiл)фeнoкcи]пiпepидин-1-iл}-2гідроксипропіл)-1-оксо-1,2-дигідроізохінолін-4карбоксамід ацетат; Ν-{(2R)-3-[4-(3,4-(3,4диxлopфeнoкcи)пiпepидин-1-iл]-2-riдpoкcипpoпiл}6-οксο-4-(трифлуорметил)-1,6-дигідропіридин-3карбоксамід ацетат; Ν-{(2R)-3-[4-(4-xлop-2мeтилфeнoкcи)пiпepидин-1-iл]-2-гідроксипропіл}6-оксо-4-(трифлуорметил)-1,6-дигідропіридин-3карбоксамід ацетат; N-{(2R)-3-[4-(2,4-диxлop-3мeтилфeнoкcи)пiпepидин-1-iл]-2-гiдpoкcипpoпiл}6-oкco-4-(трифлуорметил)-1,6-дигідропіридине-3карбоксамід; N-{(2S)-3-[4-(3,4-диxлopфeнoкcи)п iпepидин-1iл]-2-гiдpoкcипpoпiл}-2-(2-oкcoxiнoкcaлiн-1-(2Н)іл)ацетамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-3-oкco-3,4-дигідрохіноксалін1-(2Н)-карбоксамід; 31 80268 N-{(2R)-3-[4-(4-хлop-2мeтилфeнoкcи)пiпepидин-1-iл]-2-гідpoкcипpoпiл}3-(трифлуорметил)-1Н-піразол-4-карбоксамід; N-{(2R)-3-[4-(2,4-дихлор-3метилфенокси)піперидин-1-іл]-2-гідроксипропіл}3-(трифлуорметил)-1Н-піразол-4-карбоксамід; N-{(2R)-3-{4-(3,4-дихлорфенокси)піперидин-1іл}-2-гідроксипропіл}-1-оксо-1,2-дигідро-2метилізохінолін-4-карбоксамід; 32 N-{(2R)-3-{4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-2-oкco-1,2-дигiдpo-1метилхінолін-4-карбоксамід; N-{(2R)-3-[4-(3,4-диxлopфeнoкcи)пiпepидин-1iл]-2-гiдpoкcипpoпiл}-8-флуор-1-оксо-1,2дигідроізохінолін-4-карбоксамід; або N-{(2R)-3-[4-(4-хлор-2метилфенокси)піперидин-1-іл]-гідроксипропіл}-8флуор-1-оксо-1,2-дигідроізохінолін-4-карбоксамід. Сполуку формули (І) або (Іа) можна отримувати реакцією сполуки формули (II): (II) де X, R1, R 2 R33 R4 , R53 R6 , R7, R8 3 R32, m та п визначено вище, таким чином: (і) коли Υ представляє зв’язок, СН2, NR35, CH2NH, CH2NHC(O), CH(OH), CH(NHCOR33), CH(NHSO2R34), СН2О або CH2S, тоді Ζ представляє С(О), R35 не є гідрогеном, a R33 тa R34 визначеновише. зі сполукою формули (ІІІа): (IIIа) де R9 визначено вище, a L1 представляє відщеплювану гр упу (наприклад гідроксильну або хлоридну відщеплювану гр упу) при наявності основи (наприклад діізопропілетиламіну), як варіант, при наявності засобу сполучення (наприклад бром-трис-піролідинофосфоній гексафлуорфосфату, РуВrOР або О-(7-азабензотриазол-1-іл)Ν,Ν,Ν',Ν'-тетраметилуроній гексафлуорфосфату); (іі) коли Υ представляє ΝN, а Ζ представляє С(О), зі сполукою формули (Illb): (IIIb) де R9 визначено вище. (ііі) коли Υ представляє зв'язок, a Z представляє S(O)2, зі сполукою формули (ІІІс): (IIIc) де R визначено вище, а L представляє відщеплювану гр упу (наприклад гідроксильну або хлоридну відщеплювану гр упу) при наявності основи (наприклад піридину). Сполуку формули (II) можна отримувати, [як описано у WO 00/58305 або WO 01/77101], або реакцією сполуки формули (IV): (IV) де X та R1 визначено вище, таким чином: (i), коли m та n дорівнюють 0, R2, R3, R5 та R6 представляє гідроген, a R4 та R32 визначено для формули (І), зі сполукою формули (V): (V) в якій L2 представляє відщеплювану групу (наприклад хлор або нозилокси{3-NО2-C6H4S(O)2O-}), а потім реакцією з аміаком, аміном R32 NH2 або з натрій азидом та наступним відновленням, наприклад, трифенілфосфіном; (іі) коли m та n дорівнюють 0, R 2 та R3 представляють гідроген, a R4, R5, R6 та R32 визначено для формули (І), зі сполукою формули (VI): (VI) в якій Р1 та Р2 представляють, поодинці або разом, придатні захисні групи (наприклад разом вони утворюють фталамід), або будь-який з Р1 або Р2 представляє R32, а потім зняттям захисту, використовуючи, наприклад, коли Р1 та Р 2 утворюють фталамід, гідразин; (ііі) коли m дорівнює 0, n дорівнює 1, R2 та R3 представляють гідроген, a R4, R5, R6, R7, R8 та R32 визначено для формули (І), зі сполукою формули (VII): (VII) в якій Р1 та Р2 представляють, поодинці або разом, придатні захисні групи (наприклад разом вони утворюють фталамід), або будь-який з Р1 або Р2 є R32, а потім зняттям захисту, використовуючи, наприклад, коли Р1 та Р2 утворюють фталамід, гідразин; (iv) коли m та n дорівнюють 1, R2 та R3 представляють гідроген, a R4, R5, R6, R7, R 8 та R32 визначено для формули (І), зі сполукою формули (VIII): (VIII) в якій L2 визначено для формули (V), а Р 1 та Р2 представляють, поодинці або разом, придатні захисні групи (наприклад разом вони утворюють фталамід), або будь-який з Р1 або Р2 представляє R32, а потім зняттям захисту, використовуючи, наприклад, коли Р1 та Р2 утворюють фталамід, гідразин; 33 80268 (ν) коли m дорівнює 1, a n дорівнює 0, R2 та R представляють гідроген, R5 та R6 представляють, незалежно, гідроген, С1-6алкіл або С 34 32 визначено для формули 6циклоалкіл, a R та R (І), зі сполукою формули (IX): 3 (IX) в якій L2 визначено для формули (V) та Р1 та Р представляють, поодинці або разом, придатні захисні групи (наприклад разом вони утворюють фталамід), або будь-який з Р1 або Р2 представляє R32, а потім зняття захисту, використовуючи, наприклад, коли Р1 та Р2 утворюють фталамід, гідразин; (vi) коли m дорівнює 1, а n дорівнює 0, R2, R3, 5 R та R6 представляють гідроген, a R4 та R32визначено для формули (І), зі сполукою формули (X): 2 (X) в якій L2 представляє відщеплювану групу (наприклад бром), а потім реакцією з аміаком, аміном R32-NH2 або натрій азидом та наступним відновленням, наприклад, трифеніл-фосфіном; (vii) коли m дорівнює 1, а n дорівнює 0, R2, R3, 5 R та R6 представляють, незалежно, гідроген, С11 4 32 визна6алкіл або С 3-6циклоалкіл, a R , R та R чено для формули (І), зі сполукою формули (XI): (XI) в якій Р1 та Р2 представляють, поодинці або разом, придатні захисні групи (наприклад разом вони утворюють фталамід), або будь-який з Р1 або Р2 представляє R32, а потім відновленням гідридом (наприклад натрій борогідридом), або додаванням прийнятного металоорганічного засобу (наприклад R4MgX, де X представляє галогенід); або, (viii) коли m дорівнює 1, а n дорівнює 1, R2, 3 R , R5, R6, R7 та R8 представляють, незалежно, гідроген, С1-6алкіл або С3-6циклоалкіл, a R1, R4 та R32 визначено для формули (І), зі сполукою формули (XII): (XII) в якій Ρ1 та Ρ2 представляють, поодинці або разом, придатні захисні групи (наприклад разом вони утворюють фталамід), або будь-який з Р1 або Р2 представляє R32, а потім відновленням гідридом (наприклад натрій борогідридом), або додаванням прийнятногс металоорганічного засобу (наприклад R4MgW, де W є галогенідом). Коли m дорівнює 0, а n дорівнює 0, R2, R3, R5 та R6 представляють, незалежно, гідро ген, С16алкіл або С 3-6циклоалкіл, сполуки формули (II) 34 можна отримувати реакцією сполуки формули (XIII): (XIII) де X та R1 визначено для формули (І), а L3 представляє гідроген або відщеплювану груп у (наприклад етоксил, Ν,Ο-диметилгідроксиламін), зі сполукою формули (XIV): (XIV) в якій Μ репрезентує метал (наприклад Li або Na), a L4 представляє аміногрупу (на приклад амоній), а потім перегрупуванням (наприклад з фенілйодоній діацетатом Tetrahedron Letters, 2001,42,1449.) та прийнятним відновленням (наприклад натрій борогідридом), або додаванням прийнятного металорганічного засобу (наприклад R4MgW де W представляє галогенід). Коли m дорівнює 0, n дорівнює 1, a R2, R3, R5, 6 R , R7 та R8 представляють, незалежно, гідроген, алкіл або С3-6циклоалкіл, сполуки формули (II) можна отримувати реакцією сполуки формули (XX): (XX) де X, R1 та R4 описано у формулі (І) вище, a Z представляє альдегід, захисну груп; (наприклад ціаногідрин або дитіан), зі сполукою формули (XXI): (XXI) в якій R5, R6, R7 та R8 описано вище, a L5 представляє алкокси або аміногрупу (напри клад етокси або амоній) при наявності основи (наприклад LDA або н-бутиллітію), а потім гідролітичним видаленням групи L5, перегрупуванням (наприклад з фенілйодоній діацетатом) та прийнятним відновленням (наприклад натрій борогідридом), або додаванням прийнятного металорганічного засобу (наприклад R4MgW, де W представляє галогенід). Сполуку формули (V) можна отримувати реакцією сполуки формули (XXII): (XIII) з перкислотою (наприклад метахлорпербензойною кислотою), або використовуючи умови асиметричного епоксидування [Sharpless, J. Am. Chem. Soc. 1980,102, 59745976], а потім активацією спирту, як відщеплюваної групи (наприклад, як нозилокси). Сполуку формули (VI) можна отримувати: (a) коли R5 та R6 представляють гідроген, реакцією сполуки формули (XXIII): (XXIII) з перкислотою (наприклад метахлорпербензойною кислотою) або, використовуючи умови асиметричного епоксидування (Sharpless), а потім, наприклад, реакцією Міцуно 35 80268 бу, використовуючи фталімід, 1,1(азодикарбоніл)дипіперидин та трибутилфосфін [Tetrahedron Lett. 1993, 34,1639]. (b) коли R5 та R6 представляють, незалежно, гідроген, С1-4алкіл або C3-6циклоалкіл, реакцією сполуки формули (XXIV): (XXIV) в якій Р1 та Р2 представляють, поодинці або разом, придатні захисні групи (наприклад разом вони утворюють фталамід), або будь-який з Р1 або Р2 представляє R32, з сульфурілідом [наприклад триметилсульфоній метилід, J. Am. Chem. Soc. 1965, 87, 1353-1364]; або фосфоній ілід (наприклад трифенілфосфоній метилід), а потім епоксидуванням утвореного алкен, використовуючи перкислоту (наприклад метахлорпербензойну кислоту). Сполуку формули (VII) можна отримувати реакцією сполуки формули (XXV): (XXV) в якій Р1 та Р2 представляють, поодинці або разом, придатні захисні групи (наприклад разом вони утворюють фталамід.), або будь-який з Р1 або Р2 представляє R32, з сульфур ілідом (наприклад триметилсульфоній метилідом), або фосфоній ілідом (наприклад трифенілфосфоній метилідом), а потім епоксидуванням утвореного алкену, використовуючи перкислоту (наприклад мета-хлорпербензойну кислоту). Сполуку формули (VIII) можна отримувати реакцією сполуки формули (XXV) з аніоном етилацетату (який можна отримувати дією літій діізопропіламіду на етилацетат), а потім відновленням утвореного естеру, або, наприклад, вінілмагнієм та наступним гідроборуванням (наприклад катехолбораном)/окисненням (наприклад гідроген пероксид) алкену. Сполуку формули (IX) можна отримувати зі сполуки формули (XXIV) подібним шляхом, як для сполуки (VIII). Сполуку формули (X) можна отримувати реакцією сполуки формули (XXVI): (XXVI) з перкислотою (наприклад метахлорпербензойною кислотою), а потім селективною активацією первинного спирту, як відщеплюваної групи (наприклад нозилокси). Далі, сполуки формул (І) та (Іа) можна отримувати звичайною адаптацією шляхів, що описано вище, способів, що описано у рівні техніки, або прикладів, описаних нижче. Визначені вище інтермедіати комерційно доступні або їх можна отримувати використанням або адаптацією способів, що описано у рівні техніки. Згідно з наступним аспектом винаходу запропоновано спосіб отримання 4-(3,4дихлорфенокси)піперидину, що залучає етапи: 36 a. реагування 4-гідроксипіперидину з придатною основою у придатному розчиннику при кімнатній температурі; та, b. нагрівання утвореної так суміші разом з 1,2-дихлор-4-флуорбензолом при температурі у межах 50-90°С, або при кипінні під зворотним холодильником застосовуваного розчиннику. Згідно з наступним аспектом представленого винаходу запропоновано спосіб отримання 4-(3,4дихлорфенокси)піперидину, що залучає реагування 4-гідроксипіперидину з придатною основою {як-то С 1-10алкоксид лужного металу (переважно натрію або калію) [як-то С4-10третинний алкоксид (наприклад С 4-6третинний алкоксид)], наприклад калій трет-бутоксид або калій 3,7-диметил-3октаноксид} у придатному розчиннику {як-то: етер [наприклад тетрагідрофуран або метил-третбутиловий естер], ароматичний розчинник [як-то толуол] або суміш цих розчинників) при кімнатній температурі (10-30°С); нагрівання утвореної так суміші разом з 1,2-дихлор-4-флуорбензолом при температурі у межах 50-90°С, або при кипінні під зворотним холодильником застосовуваного розчиннику, Згідно з ще одним аспектом представленого винаходу запропоновано спосіб отримання 4-(3,4дихлорфенокси)піперидину, що залучає реагування 4-гідроксипіперидину з придатною основою {як-то С 1-10алкоксид лужного металу (переважно натрію або калію) (як-то С4-10третинний алкоксид), наприклад, С1-6алкоксид (як-то С 46третинний алкоксид), наприклад, калій третбутоксид} у придатному розчиннику {як-то: етер [наприклад, тетрагідрофуран або метил-третбутиловий естер], ароматичний розчинник [як-то толуол] або суміш цих розчинників} при кімнатній температурі (10-30°С) та нагрівання утвореної так суміші до температури у межах 50-90°С, або при кипінні під зворотним холодильником застосовуваного розчиннику, та додавання 1,2-дихлор-4флуорбензолу. Приклади третинних алкоксидів представляють калій трет-бутоксид та калій 3,7-диметил-3октаноксид. Згідно з іншим аспектом представленого винаходу запропоновано способи отримання сполук формул (І) та (Іа). Інтермедіати формули (VI), (VII) та (VIII), що визначено тут є новими та ці інтермедіати та способи їх отримання, запропоновано як наступні особливості винаходу. Сполуки винаходу мають активність, як фармацевтичні, зокрема, як модулятори активності рецепторів хемокінів (особливо CCR3), та можуть бути застосовуваними у лікуванні автоімунних, запальних, проліферативних або гіперпроліферативних хвороб, або імунологічноопосередкованих хвороб (включаючи відторгнення трансплантованих органів або тканин та синдром набутого Імунодефіциту (СНІД)). Згідно з одним аспектом прикладами цих станів є: (1) (респіраторний тракт) обструктивні хвороби дихальних шляхів, включаючи: хронічну обструктивн у хворобу легенів (COPD) (як-то незво 37 ротний COPD); астму {як-то бронхіальна, алергічна, екзогенна, ендогенна або пилова астма, особливо хронічна або застаріла астма (наприклад, пізня астма або гіперчутливість дихальних шляхів)}; бронхіт {як-то еозинофільний бронхіт); гострий, алергічний, атрофічний риніт або хронічний риніт, включаючи хронічний риніт з утворенням казеозних мас, гіпертрофічний риніт, гнійний риніт, сухий риніт або медикаментозний риніт; мембранний риніт, включаючи крупозний, фіброзний або псевдомембранний риніт або золотушний риніт; сезонний риніт, включаючи риніт нервоза (сінна лихоманка) або вазомоторний риніт; саркоїдоз; легені фермера та споріднені хвороби; назальний поліпоз; фіброїдні легені, ідіопатичну внутрішньотканинну пневмонію, активність проти кашлю, лікування хронічного кашлю, асоційованого із запальними станами дихальних шляхів, або ятрогенного індукованого кашлю; (2) (кістки та суглоби) артрити, включаючи ревматичний, інфекційний, автоімунний, серонегативні спондилоартропатії (як-то анкілозивний спондиліт, псоріатичний артрит або хвороба Рейтера, хвороба Бекхета, синдром Сьоргена або системний склероз; (3) (шкіра та очі) псоріаз, атопічний дерматит, контактний дерматит або інші екзематозні дермітиди, себорейний дерматит, пемфіигоїдний плоский лишай, пемфігус, булезний пемфігус, булезний епідермоліз, кропивниця, ангіодерміти, васкулітидні еритеми, еозинофіли шкіри, увеїт, осередкова алопеція або весняний кон'юнктивіт; (4) (шлунково-кишковий тракт) черевнопорожнинна хвороба, проктит, еозинофільний гастроентерит, мастоцитоз, хвороба Крона, виразковий коліт, хвороба подразненого кишечнику або споріднені з їжею алергії, які мають вплив на відстані від травного каналу (наприклад мігрень, риніт або екзема); (5) (Відторгнення алотрансплантату) гостре та хронічне після, наприклад, трансплантації нирок, серця, печінки, легенів, кісткового мозку, шкіри або роговиці; або хронічна хвороба трансплантат проти хазяїна; та/або (6) (інші тканини або хвороби) хвороба Альцгеймера, розсіяний склероз, атеросклероз, синдром набутого імунодефіциту (СНІД), вовчакові розлади (як-то червоний вовчак або системний вовчак), еритематоз, тиреоїдит Хашимото, злоякісна міастенія, діабет типу І діабет, нефротичний синдром, еозинофілійний фасцит, синдром гіпер ІgЕ, лепра (як-то лепроматозна лепра), пародонтоз, синдром Сезарі, ідіопатична тромбоцитопенійна пурпура або розлади менструального циклу. Сполуки винаходу є також антагоністами Н1 та можуть бути застосовуваними у лікуванні алергічних розладів. Сполуки винаходу можуть також бути застосовуваними для контролю ознак та/або симптому того, що звичайно позначено, як застуда (наприклад ознак та/або симптомів звичайної застуди або грипу чи інших асоційованих респіраторних вірусних ін фекцій). 80268 38 Згідно з наступною особливістю винаходу запропоновано сполуку формули (І) або (Іа), або її фармацевтично прийнятну сіль або сольват, для застосування у способі лікування теплокровних тварин (як-то людини) терапією (включаючи профілактику). Згідно з наступною особливістю представленого винаходу запропоновано спосіб модулювання активності рецептору хемокіну (особливо активності рецептору CCR3), або антагонізування Н1, у теплокровних тварин, як-то людини, при необхідності такого лікування, спосіб полягає у застосуванні до вказаної тварини ефективної кількості сполуки формули (І) або (Іа), або її фармацевтично прийнятної солі або сольвату. Винахід також забезпечує сполуку формули (І) або (Іа), або її фармацевтично прийнятну сіль або сольват, для застосування як медикаменту. Згідно з одним аспектом представленого винаходу запропоновано застосування сполуки формули (І) або (Іа), або її фармацевтично прийнятної солі або сольвату, у виробництві медикаменту для застосування у терапії (наприклад модулювання активності рецептору хемокіну (особливо активності рецептору CCR3), або антагонізування Н1, у теплокровних тварин, як-то людини). Винахід крім того забезпечує застосування сполуки формули (І) або (Іа), або її фармацевтично прийнятної солі, у виробництві медикаменту для застосування у лікуванні: (1) (респіраторний тракт) обструктивні хвороби дихальних шляхів, включаючи: хронічну обструктивн у хворобу легенів (COPD) (як-то незворотну COPD); астму {як-то бронхіальна, алергічна, екзогенна, ендогенна або пилова астма, особливо хронічна або застаріла астма (наприклад, пізня астма або гіперчутливість дихальних шляхів)}; бронхіт {як-то еозинофільний бронхіт); гострий, алергічний, атрофічний риніт або хронічний риніт, включаючи хронічний риніт з утворенням казеозних мас, гіпертрофічний риніт, гнійний риніт, сухий риніт або медикаментозний риніт; мембранний риніт, включаючи крупозний, фіброзний або псев-домембранний риніт або золотушний риніт; сезонний риніт, включаючи риніт нервоза (сінна лихоманка) або вазомоторний риніт; саркоїдоз; легені фермера та споріднені хвороби; назальний поліпоз; фіброїдні легені, ідіопатичну внутрішньотканинну пневмонію, активність проти кашлю, лікування хронічного кашлю, асоційованого із запальними станами дихальних шляхів або ятрогенного індукованого кашлю; (2) (кістки та суглоби) артрити, включаючи ревматичний, інфекційний, автоімунний, серонегативні спондилоартропатії (як-то анкілозивний спондиліт, псоріатичний артрит або хвороба Рейтера), хвороба Бекхета, синдром Сьоргена або системний склероз; (3) (шкіра та очі) псоріаз, атопічний дерматит, контактний дерматит або інші екзематозні дермітиди, себорейний дерматит, пемфіигоїдний плоский лишай, пемфігус, булезний пемфігус, булезний епідермоліз, кропивниця, ангіодерміти, 39 васкулітидні еритеми, еозинофілії шкіри, увеїт, осередкова алопеція або весняний кон'юнктивіт; (4) (шлунково-кишковий тракт) черевнопорожнинна хвороба, проктит, еозинофільний гастроентерит, мастоцитоз, хвороба Крона, виразковий коліт, хвороба подразненого кишечнику або споріднені з їжею алергії, як мають вплив на відстані від травного каналу (наприклад мігрень, риніт або екзема); (Відторгнення алотрансплантату) гостре та хронічне після, наприклад, трансплантації нирок, серця, печінки, легенів, кісткового мозку, шкіри або роговиці; або хронічна хвороба трансплантат проти хазяїна; та/або (6) (інші тканини або хвороби) хвороба Альцгеймера, розсіяний склероз, атеросклероз, синдром набутого імунодефіциту (СНІД), вовчакові розлади (як-то червоний вовчак або системний вовчак), еритематоз, тиреоїдит Хашимото, злоякісна міастенія, діабет типу І діабет, нефротичнийсиндром, еозинофільний фасцит, синдром гіпер ІgЕ, лепра (як-то лепроматозна лепра), пародонтоз, синдром Сезарі, ідіопатична тромбоцитопенійна пурпура або розлади менструального циклу; у теплокровних тварин, як-то людини. Згідно з наступним аспектом сполука формули (І) або (Іа), або її фармацевтично прийнятна сіль, є корисною у лікуванні астми {як-то бронхіальна, алергічна, екзогенна, ендогенна або пилова астма, особливо хронічна або застаріла астма (наприклад, пізня астма або гіперчутливість дихальних шля хів)}; або риніт (включаючи хронічний риніт з утворенням казеозних мас, гіпертрофічний риніт, гнійний риніт, сухий риніт або медикаментозний риніт; мембранний риніт, включаючи крупозний, фіброзний чи псевдомембранний риніт або золотушний риніт; сезонний риніт, включаючи риніт нервоза (сінна лихоманка) або вазомоторний риніт}. Згідно з ще одним аспектом сполука формули (І) або (Іа), або її фармацевтично прийнятна сіль, є корисною у лікуванні астми. Представлений винахід також забезпечує застосування сполуки формули (І) або (Іа), або її фармацевтично прийнятної солі, у виробництві медикаменту для застосування у лікуванні астми або риніту. Представлений винахід крім того забезпечує спосіб лікування опосередкованої хемокіном хвороби (особливо опосередкованої CCR3 хвороби, особливо астми) у теплокровних тварин, як-то людини, спосіб полягає у застосуванні до вказаного ссавця, що потребує такого лікування, ефективної кількості сполуки формули (І) або (!а), або її фармацевтично прийнятної солі або сольвату. Для застосування сполуки винаходу, або її фармацевтично прийнятної солі або сольвату для терапевтичного лікування теплокровних тварин, як-то людини, зокрема модулювання активності рецептору хемокіну (особливо активності рецептору CCR3 або антагонізування Н1, вказаний інгредієнт звичайно формують згідно зі стандартною фармацевтичною практикою, як фармацевтичну композицію. 80268 40 Тому згідно з іншим аспектом представленого винаходу запропоновано фармацевтичну композицію, яка містить сполуку формули (І) або (Іа), або її фармацевтично прийнятну сіль або сольват (активний інгредієнт) та фармацевтично прийнятний ад'ювант, розріджувач або носій. Згідно з наступним аспектом представленого винаходу запропоновано спосіб отримання вказаної композиції, спосіб полягає у змішуванні активного інгредієнту з фармацевтично прийнятним ад'ювантом, розріджувачем або носієм. Залежно від режиму застосування, фармацевтична композиція переважно вміщуватиме від 0,05 до 99% (масова частка), більш переважно від 0,05 до 80%, ще більш переважно від 0,10 до 70% та навіть більш переважно від 0,10 до 50%, активного інгредієнту, усі проценти показують масову частку у загальній композиції. Фармацевтичні композиції цього винаходу можна застосовувати стандартним чином для хвороби, яку потрібно лікувати, наприклад місцевим (як-то до легенів та/або дихальних шляхів або до шкіри), пероральним, ректальним або парентеральним застосуванням. Для цього сполуки цього винаходу можна формувати засобами, відомими у рівні техніки у форму, наприклад, аерозолів, сухих композицій порошку, таблеток, капсул, сиропів, порошків, гранул, водних чи масляних розчинів або суспензій, (ліпідів) емульсій, дисперсивних порошків, супозиторіїв, мазей, кремів, крапель та стерильних водних або масляних розчинів або суспензії для ін'єкцій. Придатна фармацевтична композиція цього винаходу є композицією, придатною для перорального застосування в одиничній дозованій формі, наприклад таблетки або капсули, яка містить між 0,1мг та 1г активного інгредієнту Згідно з іншим аспектом фармацевтична композиція цього винаходу є композицією, придатною для внутрішньовенних, підшкірних або внутрішньом'язових ін'єкцій. Кожний пацієнт може отримувати, наприклад, внутрішньовенну, підшкірну або внутрішньом'язову дозу від 0,01мг/кг до 100мг/кг сполуки цього винаходу, переважно у межах від 0,1мг/кг до 20мг/кг, композицію застосовують 1-4 рази на добу. Внутрішньовенну, підшкірну або внутрішньом'язову дозу можна уводити засобами болюсної ін'єкції. Альтернативно внутрішньовенну дозу можна уводити постійною інфузією протягом часу. Альтернативно кожний пацієнт отримуватиме добову пероральну дозу як є приблизно еквівалентною добовій парентеральній дозі, композицію застосовують 1-4 рази на добу. Винахід далі ілюстровано наступними необмежувальними прикладами в яких, якщо не визначено інше: (і) дані 1Н ЯМР представлено у формі величин дельта для головних діагностичних протонів, у частинах на мільйон (млн-1) відносно тетраметилсилану (TMS), як внутрішнього стандарту, визначених при 300МГц або 400МГц, використовуючи попередньо дейтерований ДMCO-D6 41 (CD3SOCD3), метанол-D4 (CD3OD) або CDCI3, як розчинник якщо не визначено інше; (іі) мас-спектри (МС) отримували з енергією електронів 70еВ у режимі хімічної іонізації (XI), використовуючи безпосереднє піддавання зразків іонізації електронним ударом (ЕУ) або бомбардуванням швидкими атомам (БША) або електророзпиленням (ІЕР); де величини для m/z надано, загалом, тільки вихідної для іона, а якщо не визначено інше, маса іона є масою позитивного іона - (М+Н)+; (ііі) потрібні сполуки прикладів та способи названо, використовуючи програму ACD/lndex version 4,55 від Advanced Chemistry Development, Inc; (iv) якщо не визначено інше, оберненофазову ВЕРХ провадили, використовуючи обернено-фазову колонку Symmetry NovaPak або Xterra на діоксиді силіцію; та (ν) застосовано такі скорочення: ХІАТ ДМФ ВЕРХ МТВЕ ДМСО ТГФ ДХМ XI при атмосферному тиску N, N-диметил формамід Високоефективна рідинна хроматографія Метил-трет-бутиловий етер диметилсульфоксид тетрагідрофуран дихлорметан Препарат 1 (2R)-1-аміно-3-[4-(3,4дихлорфенокси)піперидин-1-іл]пропан-2-ол Етап 1: 2-{(2S)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2-гідроксипропіл}1Н-ізоіндол-1,3(2Н)-діон (R)-2-(Оксиранілметил)-1Н-ізоіндол-1,3(2Н)діон (Tetrahedron Asymmetry, 1996, 7,1641, 5г) у суміші 50мл етанолу та 15мл диметилформаміду обробляють 4-(3,4-дихлорфенокси)-піперидином (6г). Суміш перемішують протягом ночі при кімнатній температурі. Розчин концентрують у вакуумі та залишок двічі переганяють з толуолом. Сирий матеріал очищають хроматографією (етилацетат), отримуючи потрібну сполуку як жовте масло. МС (ХІАТ) 449/451 (М+Н)+ 1 Н ЯМР δ (CDCI3) 7,92-7,81(2Н, m), 7,77-7,70 (2Н, m), 7,30 (1Н, d), 6,98 (1Н, t), 6,74 (1Н, dt), 4,34420 (1Н, m), 4,09-3,97 (1Н, m), 3,83 (1Н, dd), 3,73 (1Н, dd), 2,93-2,79 (1Н, m), 2,73-2,60 (1Н, m), 2,59-2,37 (3Н, m), 2,31 (1Н, t), 2,02-1,86 (2Н, m), 1,86-1,67(2Н, m). Етап 2: (2R)-1-аміно-3-[4-(3,4дихлорфенокси)піперидин-1-іл]пропан-2-ол (S)-2-[3-[4-(3,4-дихлорфенокси)-1піперидинілі-2-гідроксипропілі-1Н-ізоіндол1,3(2Н)-діон (4г) в етанолі (100мл) обробляють 80268 42 20мл гідразин моногідрату та нагрівають суміш при кипінні під зворотним холодильником протягом 3 годин. Реакційну суміш о холоджують та фільтрують. Фільтрат випарюють та продукт хроматографують (етилацетат), отримуючи потрібну сполуку як жовте масло, яке отвережується при стоянні (2,5г). МС(ХІАТ) 319/321 (М+Н)+ 1 Н ЯМР δ (CDCI3) 7,31 (1Н, d), 7,00 (1Н, d), 6,75 (1Н, dd), 4,00 (1Н, sept), 3,74-3,62 (1Н, m), 2,94-2,84 (1Н, m), 2,82 (1Н, d), 2,72-2,61 (1Н, m), 2,65 (1Н, d); 2,60-2,49 (1Н, m), 2,46-2,21 (3Н, m), 2,06-1,91 (2Н, m), 1,90-1,72 (2Н, m). Препарат 2 4-аміно-1-[4-(3,4-дихлорфенокси)піперидин-1іл]бутан-2-ол Етап 1: 2-{4-[4-(3,4дихлорфенокси)піперидин-1-іл]-3-гідроксибутил}1Н-ізоіндол-11,3(2Н)-діон Суміш 4-(3,4-дихлорфенокси)піперидину [WO 0058305, WO 0177101] (4,40г) та 2-(2-оксиран-2ілетил)-1Н-ізоіндол-1,3(2Н)-діону (J. Med. Chem. 1979, 22(6), 631-9. 5,00г) в етанолі (50мл) перемішують при 60°С протягом 12 годин. Суміш охолоджують та залишають на ніч. Утворені кристали збирають фільтруванням, промивають холодним етанолом та суша ть у вакуумі, отримуючи потрібну сполуку як білий твердий продукт (30г). МС (ХІАТ) 463/465 (М+Н)+ 1 Н ЯМР δ (ДМСО) 7,90-7,80 (4Н, m), 7,49 (1Н, d), 7,25 (1Н, d), 6,97 (1Н, dd), 4,53-4,33 (2Н, m), 3,80-3,69 (1Н, m), 3,69-3,58 (2Н, m), 2,77-2,60 (2Н, m), 2,38-2,17 (4Н, m), 1,94-1,84 (2Н, m), 1,85-1,75 (1Н,m), 1,65-1,50 (3Н, m). Етап 2:4-аміно-1-[4-(3,4дихлорфенокси]піперидин-1-іл]бутан-2-ол Розчин суміші 2-{4-[4-(3,4дихлорфенокси)піперидин-1-іл]-3-гідроксибутил}1Н-ізоіндол-1,3(2Н)-діону (3,00г) у суміші етанолу (75мл) та 35% водного гідразину (15мл) нагрівають при кипінні під зворотним холодильником 4 години. Суміш охолоджують та розчинники видаляють у вакуумі. Залишок розтирають з гарячим дихлорметаном. Білий твердий продукт видаляють фільтруванням та фільтрат сушать натрій сульфатом. Суміш фільтрують та розчинник випарюють, отримуючи потрібну сполуку як жовте масло (2,10г), яке застосовують без наступної очистки на наступному етапі. МС (ХІАТ) 333/335 (М+Н)+ 1 Н ЯМР δ (CDCI3) 7,29 (1Н, d), 6,96 (1Н, d), 6,76 (1Н, dd), 4,40-4,25 (1Н, m), 3,95-3,85 (1Н, m), 3,20-3,00 (2Н, m), 2,96-2,79 (1Н, m), 2,78-2,63 (1Н, 43 m), 2,60-2,45 (1Н, m), 2,41-2,23 (3Н, m), 2,10-1,88 (2Н, m), 1,88-1,70 (3Н, m), 1,70-1,58 (1Н, m). Препарат 3 1-аміно-4-[4-(3,4-дихлорфенокси)піперидин-1іл]бутан-2-ол Етап 1: 4-(3,4-дихлорфенокси)-1-(2-оксиран2-ілетил)піперидин Суміш [4-(3,4-дихлорфенокси)піперидину [WO 0058305, WO 0177101] (2,00г), 2-(2брометил)оксирану (J. Am. Chem. Soc. 1981,103, 7520-8) (1,36г) та калій карбонату (2,2г) в ацетоні (20мл) перемішують при 50°С протягом 12 годин. Розчинник видаляють у вакуумі. Залишок розподіляють між водою та етилацетатом. Органічний шар промивають водою, розсолом та сушать магній сульфатом. Суміш фільтр ують та розчинник випарюють, отримуючи потрібну сполуку як жовте масло (2,50г), яке застосовують без наступної очистки на наступному етапі. МС (ХІАТ) 316/318 (М+Н)+ 1 Н ЯМР δ (CDCI3) 7,31 (1Н, d), 7,00 (1Н, d), 6,75 (1Н, dd), 4,27 (1Н, dквінтет), 3,02-2,95 (1Н, m), 2,78 (1Н, t), 2,77-2,68 (2Н, m), 2,57-2,49 (3Н, m), 2,39-2,24 (2Н, m), 2,03-1,94 (2Н, m), 1,87-1,75 (2Н, m), 1,77-1,72 (1Н, m), 1,73-1,61 (1Н, m). Етап 2:1-аміно-4-[4-(3,4дихлорфенокси)піперидин-1-іл]бутан-2-ол У герметизованій металевій тубі нагрівають при 70°С розчин 4-(3,4-дихлорфенокси)-1-(2оксиран-2-ілетил)піперидину (1,00г) у 7Η аміаку у метанолі (25мл) протягом 12 годин. Розчинник видаляють у вакуумі та залишок очищають на силікагелі (0-10% 7Η аміаку у метанолі/дихлорметані), отримуючи потрібну сполуку як жовте масло (0,55г). МС (ХІАТ) 333/335 (М+Н)+ 1 Н ЯМР δ (CDCI3) 7,31 (1Н, d), 6,99 (1Н, d), 6,75 (1Н, dd), 4,36-4,27 (1Н, m), 5 3,79-3,70 (1Н, у), 2,93-2,78 (1Н, m), 2,76-2,59 (5Н, m), 2,61-2,50 (1Н, m), 2,37-2,27 (1Н, m), 2,03-1,90 (2Н, m), 1,891,76 (2Н, m), 1,74-1,61 (1Н, m), 1,54-1,46 (1Н, m). Препарат 4 (2R)-1-аміно-3-[4-(4-хлорфенокси)піперидин1-іл]пропан-2-ол Отримано, як описано при отриманні 1. 1 Н ЯМР δ (CD3OD) 7,13 (2Н, d), 6,80 (2Н, d), 4,26 (1Н, септет), 3)68-3,59 (1Н, m), 2,77-2,65 (2Н, m), 2,62 (1Н, dd), 2,46 (1Н, dd), 2,38-2,24 (4Н, m), 1,95-1,85 (2Н, m), 1,73-1,61 (2Н, m). Препарат 5 (2R)-1-аміно-3-[4-(4-хлор-3Флуорфенокси)піперидин-1-іліпропан-2-ол 80268 44 Отримано, як описано при отриманні 1. МС (ІЕР) 303/305 (М+Н)+ 1 Н ЯМР δ (CD3OD) 7,32 (1Н, t), 6,86 (1Н, dd), 6,77 (1Н, ddd), 4,40 (1Н, квінтет), 3,74 (1Н, ddd), 2,87-2,75 (2Н, m), 2,72 (1Н, dd), 2,56 (1Н, dd), 2,50-2,37 (4Н, m), 2,08-1,95 (2Н, m), 1,85-1,72 (2Н,т). Препарат 6 (2R)-1-аміно-3-[4-(3,4дифлуорфенокси)піперидин-1-іліпропан-2-ол Отримано, як описано при отриманні 1. МС (ІЕР) 287 (М+Н)+ 1 Н ЯМР δ (CD3OD) 7,14 (1Н, dt), 6,87 (1Н, ddd), 6,75-6,69 (1Н, m), 4,35 (1Н, септет), 3,803,71 (1Н, m), 2,88-2,75 (2Н, m), 2,75 (1Н, dd), 2,58 (1Н, dd), 2,51-2,34 (4Н, m), 2,07-1,94 (2Н,т), 1,851,71 (2Н, m). Препарат 7 (2R)-1-аміно-3-[4-(3,4дихлорфенокси)піперидин-1-іл]пропан-2-ол. Етап 1: 4-(3,4-дихлорфенокси)піперидин 4-Гідроксипіперидин (50г, 494ммоль) додають порціями до перемішуваної суспензії калію третбутоксиду (110,9г, 990ммоль) у тетрагідрофурані (900мл) при кімнатній температурі та під азотом. Суміш нагрівають при кипінні під зворотним холодильником та додають краплями 1,2-дихлор-4флуорбензол (98г, 594ммоль) протягом 30 хвилин. Суміш перемішують при кипінні під зворотним холодильником протягом ще 1 години, тоді охолоджують до кімнатної температури, розбавляють етилацетатом (500мл) та промивають водою (500мл). Органічну фазу ще розбавляють етилацетатом (500мл) та екстрагують 1Μ гідрохлоридною кислотою (200мл), Водний екстракт доводять до рН>10 додаванням розчину натрій гідроксиду та екстрагують двічі третбутилметилетер (750мл). Органічні екстракти сушать магній сульфатом, фільтрують та концентрують у вакуумі, отримуючи потрібну сполук у як темне масло, яке застосовують по суті на наступному етапі. МС (ІЕР) 246/248 (М+Н)* 1 Н ЯМР δ (CDCI3) 7,31 (1Н, d), 7,00 (1Н, d), 6,78 (1Н, dd), 4,29-4,37 (1Н, m), 3,15 (2Н, dt), 2,75 (2Н, td), 1,97-2,03 (2Н, m), 1,60-1,70 (2Н, m). Альтернативний Етап 1: 4-(3.4дихлорфенокси)піперидин Тонку кашку 4-гідроксипіперидину (50г, 494ммоль) у тетрагідрофурані (200мл) додають до перемішуваної суспензії калію трет-бутоксиду (110,9г, 990ммоль) у тетрагідрофурані (650мл) при кімнатній температурі та промивають ТГФ (50мл). Утворену суміш перемішують під азотом протягом 20 хвилин. 1,2-дихлор-4-флуорбензол (98г, 594ммоль) додають та утворену суміш нагрівають при кипінні під зворотним холодильником протягом 90 хвилин. Реакційну суміш охоло 45 джують до кімнатної температури та додають воду (500мл). Шари розділяють та розчинник відділяють від органічної фракції. Матеріал тоді розподіляють між МТВЕ та 10% водним розчином лимонної кислоти. Шари розділяють та водний шар ще промивають МТВЕ (2´250мл). Водну фазу підлужують до рН>10 додаванням 10Н розчину NaOH та продукт екстрагують ізопропілацетатом (2´300мл). Органічні продукти промивають розсолом (300мл), сушать магній сульфатом, фільтрують та концентрують у вакуумі, отримуючи потрібну сполуку як темне масло, яке застосовують по суті на наступному етапі (109,1г, 90%). Етап 2: (2S)-1-азидо-3-[4-(3,4дихлорфенокси)піперидин-1-іл]пропан-2-ол (2R)-Оксиран-2--ілметил 3нітробензолсульфонат (21,1г, 81,3ммоль) у диметилфо-рмаміді (300мл) обробляють триетиламіном (22,6мл, 163,0ммоль), а потім 4-(3,4дихлорфенокси)-піперидином (20г, 81,3ммоль). Суміш перемішують протягом ночі при 60°С. Натрій азид (16г, 243,9ммоль) додають у суміш та реакційну суміш перемішують ще 72 години. Розчин обережно концентрують у вакуумі та залишок розбавляють водою (600мл), екстрагують етилацетатом (1500мл). Органічний шар промивають двічі водою (500мл), тоді розсолом (200мл) та концентрують у вакуумі, отримуючи масло. Етап 3: (2R)-1-аміно-3-[4-(3,4дихлорфенокси)піперидин-1-іл]пропан-2-ол Утворене масло з етапу 2 розчиняють у вологому тетрагідрофурані (225мл) та обробляють трифенілфосфіном (53,3г, 203ммоль). Реакційну суміш нагрівають при 60°С та перемішують протягом 4 годин. Розчинник видаляють у вакуумі, залишок знов розчиняють у 2Η гідрохлоридній кислоті (1000мл) та водний шар екстрагують етилацетатом (3 рази 700мл). Водну фазу підлужують з 2Η розчин натрій гідроксиду та екстрагують дихлорметаном (3 рази 1000мл). Комбіновані органічні шари промивають розсолом, сушать натрій сульфатом, фільтрують та концентрують у вакуумі. Сирий матеріал очищають хроматографією (8% 7Η аміак у метанолі/ДХМ), отримуючи потрібну сполуку як жовте масло (17г). МС (ХІАТ) 319/321 (М+Н)+ 1 Н ЯМР δ (CDCI3) 7,31 (1Н, d), 7,00 (1Н, d), 6,75 (1Н, dd), 4,0 (1Н, sept), 3,74-3,62 (1Н, m), 2,94-2,84 (1Н, m), 2,82 (1Н, d), 2,72-2,61 (1Н, m), 2,65 (1Н, d), 2,60-2,49 (1Н, m), 2,46-2,21 (3Н, m), 2,06-1,91 (2Н, m), 1,90-1,72 (2Н, m). Препарат 8 (2R)-1-аміно-3-[4-(3,4дихлорфенокси)піперидин-1-іл]пропан-2-ол Етап 1: (2-S)-1-Хлор-3-[4-(3,4дихлорфенокси)піперидин-1-іл]пропан-2-ол (S)-(4)-Епіхлоргідрин (3,50мл, 44,7ммоль) додають до перемішуваного розчину 4-(3,4 80268 46 дихлорфенокси)піперидину (10,0г, 40,6ммоль) в етанолі (50мл). Через 20г додають воду (50мл). Суміш перемішують протягом ще 2 години, тоді твердий осад збирають фільтруванням, промивають водою та сушать у вакуумі при 50°С протягом 2 годин, отримуючи потрібну сполуку. МС (ІЕР) 338/340/342/344 (М+Н)+ 1 Н ЯМР δ (CDCI3) 7,31 (1Н, d), 7,00 (1Н, d), 6,75 (1Н, dd), 4,28-4,33 (1Н, m), 3,89-3,96 (1Н, m), 3,54-3,62 (3Н, m), 2,84-2,92 (1Н, m), 2,65-2,72 (1Н, m), 2,45-2,59 (3Н, m), 2,32-2,36 (1Н, m), 1,90-2,01 (2Н, m), 1,77-1,87 (2Н, m). Етап 2: (2R)-1-аміно-3-[4-(3,4дихлорфенокси)піперидин-1-іл]пропан-2-ол Розчин натрій гідроксиду (1,62г, 40,6ммоль)у метанолі. (200мл) додають до продукту з попереднього етапу та суміш перемішують протягом 1 години, коли розчинився твердий продукт. Водний розчин аміаку (28%, 80мл) додають та перемішування продовжують при зовнішній температурі протягом 3 діб. Розчин концентрують у вакуумі до об'єму 100мл тоді розчиняють у гідрохлоридній кислоті (0,5М, 800мл) та екстрагують діетиловим етером (2´200мл). Водний екстракт фільтрують для видалення нерозчинного забруднення, тоді підлужують додаванням натрій гідроксиду та екстрагують дихлорметаном (4´200мл) з фільтруванням двофазної суміші для видалення нерозчинного забруднення. Органічні екстракти сушать безводним магній сульфатом, фільтрують та випарюють під зниженим тиском, отримуючи потрібну сполуку як масло (10,6г). МС(ХІАТ) 319/321 (М+Н)+ 1 Н ЯМР δ (CDCI3) 7,31 (1Н, d), 7,00 (1Н, d), 6,75 (1Н, dd), 4,0 (1Н, септ.), 3,74-3,62 (1Н, m), 2,94-2,84 (1Н, m), 2,82 (1Н, d), 2,72-2,61 (1Н, m), 2,65 (1Н, d), 2,60-2,49 (1Н, m), 2,46-2,21 (3Н, m), 2,06-1,91 (2Н, m), 1,90-1,72 (2Н, m). Препарат 9 (2S)-аміно-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2-метилпропан-2ол Отримано, як описано при отриманні 7 (Етапи 2 та 3), використовуючи [(2R)-2-метилоксиран-2іл]метил-3-нітробензолсульфонат. МС (ХІАТ) 333/335 (М+Н)+ 1 Н ЯМР δ (CDCI3) 7,30 (1Н, d), 6,99 (1Н, d), 6,75 (1Н, dd), 4,38-4,30 (1Н, m), 3,48 (2Н, s), 2,962,78 (2Н, m), 2,62-2,30 (4Н, m), 2,00-1,90 (2Н, m), 1,85-1,72 (2Н, m), 1,25 (3Н, s). Препарат 10 (2R)-1-аміно-3-[4-(4-хлор-2-метилфенокси)піперидин-1-іл]пропан-2-ол 47 80268 48 Етап. 2: ілокси)бензамід Отримано, як описано при отриманні 7 (Етапи 2 та 3) з 4-(4-хлор-2-метилфенокси)-піперидину. МС (ЕР) 299/301 (М+Н)+1. 1 Н ЯМР δ (CD3OD) 7,12-7,05 (2Н, m), 6,87 (1Н, d), 4,39 (1Н, септет), 3,77-3,70 (1Н, m), 2,84-2,72 (2Н, m), 2,71 (1Н, dd), 2,55 (1Н, dd), 2,50-2,39 (2Н, m), 2,40 (1Н, d), 2,39 (1Н, d), 2,18 (3Н, s), 2,041,95 (2Н, m), 1,86-1,75 (2Н, m). Препарат 11 6-С-(1-(2R)-3-амінo-2гідроксипропіл]піперидин-4-іл}окси)-2,3дихпорбензамід Етап 1: Трет-бутил 4-[2-(амінокарбоніл)-3,4дихлорфенокси]піперидин-1-карбоксилат До перемішуваного розчину трет-бутил 4[3,4-дихлорфенокси]піперидин-1-карбоксилату (7,0г, 20,3ммоль) у сухому тетрагідрофурані (250мл) при-70°С в атмосфері азоту додають краплями втор-бутиллітій (18мл, 1,3Μ у циклогексані). Розчин перемішують ще 30 хвилин, при цій температурі і обробляють гранулами твердого карбон діоксиду (надлишок). Охолоджувальну баню видаляють та суміш перемішують інтенсивно, поки відбувається нагрівання до кімнатної температури протягом 1 години. Після ще 1 години розчин концентрують до об'єму приблизно 50мл тоді розподіляють між водним розчином натрій гідрокарбонату та діетилетером. Водну фазу тоді промивають діетиловим етером (3´), тоді підкислюють до рН4 та екстрагують дихлорметаном (3´). Комбіновані екстракти сушать (магній сульфат) та концентрують. Обробка сирої карбонової кислоти (2,5г, 6,4ммоль) карбоніл-1,1діімідазолідом (1,25г, 7,7ммоль) у дихлорметані (50мл) при кімнатній температурі протягом 72 годин дає сирий імідазолід, який концентрують у вакуумі, знов розчиняють в етанолі (20мл) та обробляють 35% водним аміаком (20мл) в автоклаві при 100°С протягом 2 годин. Суміш повільно охолоджують до кімнатної температури для кристалізації потрібної сполуки. Кристалічний продукт фільтрують та промивають водою. Перекристалізація з етанолу/води дає потрібну сполуку (1,90г). МС (ХІАТ) 289/291 (М+Н-ВОС)+ 1 Н ЯМР δ (CDCI3) 7,40 (1Н, d), 6,83 (1Н, d), 5,91 (1Н, s), 5,73 (m, s), 4,52 (m, m), 3,59 (2H, m), 3,41 (2H, m), 1,86 (4H, m), 1,43 (9H, s). 2,3-дихлор-6-(піперидин-4 До перемішуваного розчину трет-бутил 4-[-[2(амінокарбоніл)-3,4-дихлорфенокси]піперидин-1карбоксилату (1,8г, 4,6ммоль) у дихлорметані (10мл) додають трифлуороцтову кислоту (10мл). Після 30 хвилин при кімнатній температурі розчин концентрують у вакуумі та розподіляють між насиченим водним натрій гідрокарбонатом та дихлорметаном. Водний шар реекстрагують ще 3 рази дихлорметаном та 3 рази етилацетатом. Комбіновані органічні екстракти сушать (безводний калій карбонат) та концентрують, отримуючи потрібну сполуку як білий твердий продукт (1,15г). МС (ХІАТ) 289/291 (М+Н)+ 1 Н ЯМР δ (CD3OD) 7,49 (1Н, d), 7,09 (1Н, d), 4,65 (1Н, Μ), 3,15 (2Н, m), 2,84 (2Н, m), 2,02 (2Н, m), 1,82 (2Н, m). Етап 3: 6-({1-[(2R)-3-аміно-2гідроксипропіл]піперидин-4-іл)окси)-2,3дихлорбензамід Етап а: До перемішуваного розчину 2,3дихлор-6-(піперидин-4-ілокси)бензаміду (1,1г, 3,8ммоль) у диметилформаміді (10мл) додають триетиламін (1,06мл, 7,6ммоль) та (2R)-гліцидил3-нітробензолсульфонат (1,0г, 3,8ммоль) і суміш нагрівають при 60°С протягом 3 годин. Натрій азид (1,0г, 15,2ммоль) додають та температуру підтримують ще 48 годин. Суміш концентрують у вакуумі майже досуха та продукт розподіляють між дихлорметаном та водним розчином натрій гідрокарбонату. Водний шар реекстрагують дихлорметаном, тоді етилацетатом. Комбіновані органічні екстракти сушать (безводний калій карбонат) та концентрують у вакуумі. Етап b: Продукт знов розчиняють у тетрагідрофурані (50мл) та обробляють водою (5мл) та трифенілфосфіном (2,4г). Суміш нагрівають при 60°С протягом 4 годин, тоді концентрують у вакуумі. Продукт розподіляють між етилацетатом та 1Η водною гідрохлоридною кислотою. Водні екстракти ще промивають етилацетатом, тоді підлужують 48% розчином натрій гідроксиду до рН11. Водний шар екстрагують дихлорметаном (3´) та комбіновані органічні екстракти сушать (безводний калій карбонат) та концентрують у вакуумі, отримуючи сирий амін, який застосовують без будь-якої очистки на наступному етапі (Дивись Приклад 132). Препарат 12 (R)-1-[4-(3,4-дихлор-фенокси)-піперидин-1-іл]3-метиламіно-пропан-2-ол Розчин 4-(3,4-дихлорфенокси)-1-[(2R)оксиран-2-ілметил]піперидину (1г, 3,31ммоль) та метиламіну (2,56мл 40% у воді, 33,1ммоль) в 49 етанолі (15мл) нагрівають при 60°С у герметизованій посудині протягом 16 годин. Розчинник випарюють під зменшеним тиском та залишок очищають флеш-хроматографією на колонці, елюючи 8% 7М аміаку у метанолі у дихлорметані, отримуючи потрібну сполуку (875мг). МС (ХІАТ) 333/335 (М+Н)+ 1 Н ЯМР δ (CDOH3) 7,31 (1Н, d), 6,99 (1Н, d), 6,75 (1Н, dd), 4,32-4,26 (1Н, m), 3,86-3,80 (1Н, m), 2,91-2,86 (1Н, m), 2,71-2,65 (2Н, m), 2,65 (1Н, dd), 2,56-2,51 (2Н, m), 2,54 (1Н, dd), 2,48-2,42 (2Н, m), 2,46 (3Н, s), 2,38-2,27 (3Н, m). Препарат 13 (2R)-1-аміно-3-[4-(2,4-дихлор-3метилфенокси)піперидин-1-іл]пропан-2-ол Отримано, як описано при отриманні 10, використовуючи 4-(2,4-дихлор-3-метилфенокси)піперидин. МС (ХІАТ) 333/335 (М+Н)+ 1 Н ЯМР δ (CD3OD) 7,25 (2Н, d), 6,94 (2Н, d), 4,54-4,37 (1Н, m), 3,88-3,71 (1Н, m), 3,35-3,24 (2Н, m), 2,93-2,72 (4Н, m), 2,72-2,57 (1Н, m), 2,08-1,90 (2Н, m), 1,92-1,75(2H, m). Препарат 14 (2S)-аміно-3-[4-(3,4дихлорфенокси)піперидин-1-іл]пропан-2-ол Отримано, як описано при отриманні 7, використовуючи (2S)-оксиран-2-ілметил-3нітробензолсульфонат. МС(ІЕР)319/321 (М+Н)+ 1 Н ЯМР δ (CDCI3) 7,30 (1Н, d), 6,99 (1Н, d), 6,75 (1Н, dd), 4,36-4,24 (1Н, m), 3,75-3,65 (1Н, m), 2,94-2,78 (2Н, m), 2,70-2,60 (2Н, m), 2,59-2,51 (1Н, m), 2,41-2,25 (3Н, m), 2,03-1,93 (2Н, m), 1,87-1,77 (2H,m). Препарат 15 (2R)-1-Аміно-2-метил-3-[4-(3,4дихлорфенокси)піперидин-1-іл]пропан-2-ол. Етап 1: 2-[[(2R)-2-метилоксираніл]метил]-1 Нізоіндол-1,3(2Н)-діон. До розчину (2S)-(2-метилоксиран-2-іл)метил 3-нітробензолсульфонату (1,913г, 7ммоль) у сухому диметилформаміді (15мл), додають калій фталімід (1,304г, 7ммоль). Суміш перемішують при 50°С протягом 5 годин та тоді охолоджують до кімнатної температури. Утворену суміш розподіляють між етилацетатом та водою. Водну фазу промивають етилацетатом (2´100мл) та комбіновані органічні екстракти промивають водою (3´100мл), насиченим розсолом, сушать натрій сульфатом та концентрують у вакуумі до сирого оранжевого воску. Очищають хроматог 80268 50 рафією (діоксид силіцію, 20% етилацетат у ізогексані), отримуючи потрібну сполуку як білий твердий продукт (0,864г). МС(ІЕР)189(М-СО)+ 1 Н ЯМР δ (CDCI3) 7,90-7,85 (2Н, m), 7,78-7,71 (2Н, m), 4,02 (1Н, d), 3,71 (1Н, d), 2,82 (1Н, d), 2,62 (1H,d), 1,39 (3H,s). Етап 2: 2-[(2R)-3-[4-(3,4-дихлорфенокси)піперидин-1іл]-2-гідрокси-2-метилпропіл]-1Н-ізоіндол-1,3(2Н)діон. Розчин 4-(3,4-дихлорфенокси)піперидину (0,985г, 4ммоль), 2-[[(2R)-2метилоксираніл]метил]-1Н-ізоіндол-1,3(2Н)-діону (0,869г, 4ммоль) та триетиламіну (0,809г, 1,12мл, 8ммоль) в етанолі (20мл) перемішують при 50°С протягом 5 годин. Утворений розчин охолоджують до кімнатної температури та концентрують у вакуумі до сирої жовтої смоли. Флешхроматографія (діоксид силіцію, 2% 7Η метанольного аміаку у ди хлорметані, як елюенті) дає потрібну сполуку як жовте масло (1,24г). МС (АРС1) 463/465/467 (М+Н)+ 1 Н ЯМР δ (CDCI3) 7,89-7,85 (2Н, m), 7,76-7,72 (2Н, m), 7,30 (1Н, d), 6,98 (1Н, d), 6,78 (1Н, dd), 4,27-4,21 (1Н, m), 3,88 (1Н, d), 3,70 (1Н, d), 3,43 (1Н, bd s), 2,96-2,81 (2Н, m), 2,60-2,42 (4Н, m), 1,95-1,89 (2Н, m), 1,80-1,70 (2Н, m), 1,15 (3Н, s). Етап 3: (2R)-1-аміно-2-метил-3-[4-(3,4дихлорфенокси)піперидин-1-іл]пропан-2-ол. До розчину 2-[(2S)-3-[4-(3,4дихлорфенокси)піперидин-1-іл]-2-гідрокси-2метилпропіл]-1Н-ізоіндол-1,3(2Н)-діону (278мг, 0,6ммоль) в етанолі (5мл) додають водний метиламін (40% розчин у воді, 6мл). Суміш перемішують при кімнатній температурі протягом 24 годин та тоді концентрують у вакуумі до сирого жовтого скла. Це скло розчиняють у метанолі (2мл), додають до флеш-патрону SC X (2г), промивають метанолом (25мл) та 7Η аміаком у метанолі (25мл). Метанольний аміак концентрують у вакуумі, отримуючи потрібну сполуку як жовте скло (165мг). МС (ІЕР) 333/335/337 (М+Н)+ 1 Н ЯМР δ (CDCI3) 7,31 (1Н, d), 6,99 (1Н, d), 6,75 (1Н, dd), 4,29-4,21 (1Н, m), 2,96-2,80 (2Н, m), 2,60-2,30 (4Н, m), 2,00-1,90 (3Н, m), 1,85-1,75 (3Н, m), 1,13 (3Н, s). Препарат 16 7-(Хлорсульфоніл)-1-оксо-1,2дигідроізохінолін-4-карбонова кислота 51 1-оксо-7-сульфо-1,2-дигідроізохінолін-4карбонову кислоту (5г) додають до хлорсульфонової кислоти (25мл). Суміш нагрівають при 100°С протягом 84 годин та тоді повільно крапають на лід, перемішуючи. Суміш фільтрують та залишок промивають водою та етером та сушать, отримуючи 7-(хлорсульфоніл)-1-оксо-1,2дигідроізохінолін-4-карбонову кислоту, як темножовтий твердий продукт (7,5г). МС (АРСТ) 286 (М-Н)1 Н ЯМР δ (ДМСО) 11,81 (1Н, d), 8,79 (1 Η, d), 8,48 (1 Η, d), 8,03 (1 Η, d), 7,96 (1 Η, dd). Препарат 17 7-[(Метиламіно)сульфонал]-1-оксо-1,2дигідроізохінолін-4-карбонова кислота МС (ХІАТ) 283 (М+Н)+ 1 Н ЯМР δ (ДМСО) 12,93 (1Н, s), 12,13 (1Н, d), 9,03 (1Н, d), 8,61 (1Н, d), 8,16 (1Н, d), 8,12 (1H,dd), 7,65 (1H,q), 2,43 (3Н, d). Препарат 18 1,2-дигідро-7-[[(2гідроксіетил)аміно]сульфоніл]-1-оксо-4ізохінолінкарбонова кислота 7-(Хлорсульфоніл)-1-оксо-1,2дигідроізохінолін-4-карбонову кислоту (1г) додають до водного метиламіну (60мл) та суміш перемішують протягом 18 годин. Концентровану гідрохлоридну кислоту додають для підкислення суміші яку фільтрують 7-(Хлорсульфоніл)-1-оксо-1,2дигідроізохінолін-4-карбонову кислоту (1г) додають до етаноламіну (3мл) у тетрагідрофурані (3мл) та суміш перемішують протягом 18 годин. Гідрохлоридну кислоту додають для підкислення суміші, яку фільтрують, отримуючи 1,2-дигідро-7[[(2-гідроксіетил)аміно]сульфоніл]-1-оксо-4ізохінолінкарбонову кислоту як білий твердий продукт. МС(ХІАТ)313(М+Н)+. 1 Н ЯМР δ (ДМСО) 12,92 (5Н, s), 12,12 (5Н, s), 9,01 (6Н, d), 8,62 (6Н, s), 8,16 (13Н, d), 8,13 (13Н, dd), 7,81 (6Н, t), 4,67 (5Н, s), 3,39-3,25 (84Н, m), 2,81 (13Н, q). Препарат 19 7-[(Цикпопропіламіно)сульфоніл]-1,2-дигідро1-оксо-4-ізохінолінкарбонова кислота 80268 52 7-(Хлорсульфоніл)-1-оксо-1,2дигідроізохінолін-4-карбонову кислоту (1г) додають до циклопропіламіну (3мл) у тетрагідрофурані (20мл) та суміш перемішують протягом 18 годин. Гідрохлоридну кислоту додають для підкислення суміші, яку фільтрують, отримуючи 7-[(циклопропіламідо)сульфоніл]-1,2-дигідро-1оксо-4-ізохінолінкарбонову кислоту як білий твердий продукт. 55 МС (APCT) 307 (М-Н)1 Н ЯМР δ (ДМСО) 12,93 (1Н, s), 12,13 (1Н, d), 9,03 (1Н, d), 8,65 (1Н, d), 8,16 (1Н, d), 8,14 (1Н, dd), 8,08 (1Н, d), 2,13 (1Н, dceкстет), 0,48 (2Н, td), 0,39-0,34 (2Н, m). Препарат 20 7-(Азетидин-1-ілсульфоніл)-1-оксо-1,2дигідроізохінолін-4-карбонова кислота 7-(Хлорсульфоніл)-1-оксо-1,2дигідроізохінолін-4-карбонову кислоту (1г) додають до азетидину (0,7мл) та діізопропілетиламіну (0,4мл) у тетрагідрофурані (5мл) та ацето-нітрилі (5мл) і суміш перемішують протягом 72 годин, тоді випарюють. Твердий продукт кристалізують з метанолу і гідрохлоридну кислоту додають для підкислення суміші, яку фільтрують, отримуючи 7-(азетидин-1-ілсульфоніл)-1-оксо-1,2дигідроізохінолін-4-карбонову кислоту як білий твердий продукт. МС (ХІАТ) 309 (М+Н)+ 1 Н ЯМР δ (ДМСО) 12,99 (1Н, s), 12,21 (1Н, d), 9,12 (1Н, d), 8,54 (1Н, d), 8,20 (1Н, d), 8,16 (1Н, dd), 3,70 (4Н, t), 1,99 (2Н, квінтет). Препарат 21 7-(Аміносульфоніл)-1-оксо-1,2дигідроізохінолін-4-карбонова кислота 7-(Хлорсульфоніл)-1-оксо-1,2дигідроізохінолін-4-карбонову кислоту (1г) додають до 0,880 аміаку (60мл) та суміш перемішують протягом 18 годин. Додають концентровану гідрохлоридну кислоту для підкислення суміші, яку фільтрують, о тримуючи 7-(аміносульфоніл)-іоксо-1,2-дигідроізохінолін-4-карбонову кислоту як білий твердий продукт. MC (XIAT) 269 (М+Н)+ 53 1 Н ЯМР δ (ДМСО) 12,91 (1Н, s), 12,08 (1Н, d), 8,99 (1Н, d), 8,68 (1Н, d), 8,16 (1Н, dd), 8,14 (1H,d), 7,53 (2H,s). Препарат 22 7-[(Диметиламіно)сульфоніл]-1-оксо-1,2дигідроізохінолін-4-карбонова кислота 7-(Хлорсульфоніл)-1-оксо-1,2дигідроізохінолін-4-карбонову кислоту (0,8г) додають, до диметиламіну (15мл) та суміш перемішують протягом 18 годин. Суміш підкислюють концентрованою гідрохлоридною кислотою та тоді фільтрують, отримуючи 7[(диметиламіно)сульфоніл]-1-оксо-1,2-дигідроізодигідроізохінолін-4-карбонову кислоту як білий твердий продукт. MC (XIAT) 295 (М-Н)1 Н ЯМР δ (ДМСО) 12,96 (1Н, s), 12,19 (1Н, d), 9,07 (1Н, d), 8,50 (1Н, d), 8,18 (1Н, d), 8,11 (1H,dd),2,65(6H,s). Препарат 23 7-[(3-Гідрокси-3-метилазетидин-1іл)сульфоніл]-1-оксо-1,2-дигідроізохінолін-4карбонова кислота 7-(Хлорсульфоніл)-1-оксо-1,2-дигідроізодигідроізохінолін-4-карбонову кислоту (1г), діізопропілетиламін (3мл) та 3-метилазетидин-3-ол гідрохлорид (0,8г) у тетрагідрофурані (8мл) нагрівають при 55°С протягом 3 діб. Суміш підкислюють гідрохлоридною кислотою та тоді фільтрують, отримуючи 7-[(3-гідрокси-3-метилазетидин1-іл)сульфоніл]-1-оксо-1,2-дигідроізохінолін-4карбонову кислоту як блідо-рожевий твердий продукт. МС (ІЕР) 337 (М-Н)1 H ЯМР δ (ДМСО) 12,99 (1Н, s), 12,22 (1Н, d), 9,11 (1Н, d), 8,53 (1Н, s), 8,21 (1Н, d), 8,16 (1Н, dd), 3,61 (2Н, d), 3,46 (2Н, d), 1,25 (3Н, t). Препарат 24 Етап 1: трет-бутил 4-(3-хлор-4ціанофенокси)піперидин-1-карбоксилат 80268 54 4-({1-[(2R)-3-аміно-2гідроксипропіл]піперидин-4-іл}окси)-2хлорбензонітрил Калій трет-бутоксид (5,57г, 49,68ммоль) додають до розчину трет-бутил 4гідроксипіперидин-1-карбоксилату (5,00г, 24,84ммоль) у глімі (100мл) та суміш перемішують протягом 30 хвилин перед додаванням 2хлор-4-флуор-бензонітрилу (7,73г, 49,68ммоль). Реакційну суміш перемішують при кімнатній температурі протягом ночі та тоді розподіляють між етилацетатом (250мл) та водою (200мл). Органічний шар відділяють, сушать магній сульфатом та розчинник випарюють. Залишок очищають флеш-хроматографією, елюючи сумішшю етилацетат:ізогексан (4:1), отримуючи потрібну сполуку як безбарвний твердий продукт (3,45г). МС (ІЕР) 337 (М+Н)+ 1 Н ЯМР δ (CDCI3) 1,47 (9Н, s), 1,72-1,80 (2Н, m), 1,90-1,97 (2Н, m), 3,37 (2Н, ddd), 3,68 (2Н, ddd), 4,54 (1Н, dквінтет), 6,86 (1Н, dd), 7,01 (1Н, d), 7,57 (1Н, d). Етап 2: 4-({1-[(2R)-3-аміно-2гідроксипропіл]піперидин-4-іл}окси)-2хлорбензонітрил До розчину трет-бутил 4-(3-хлор-4ціанофенокси)піперидин-1-карбоксилату (2,75г, 9,09ммоль) у дихлорметані (20мл) додають трифлуороцтову кислоту (20мл) та суміш перемішують протягом 90 хвилин.. Розчинники випарюють та залишок переганяють з толуолом (2´20мл) перед розчиненням у воді (30мл) та додаванням натрій гідроксиду для доведення розчину до рН11. Вільну основу екстрагують ди хлорметаном (5´100мл). Органічні продукти комбінують, сушать натрій сульфатом та розчинник видаляють під зниженим тиском, отримуючи густе масло, як розчиняють у диметилформаміді (30мл) перед додаванням (2R)-оксиран-2-ілметил-3нітробензолсульфонату (2,35г, 9,09ммоль) та триетиламіну (2,54мл, 18,18ммоль). Суміш нагрівають при 60°С протягом 4 годин перед додаванням натрій азиду (1,36г, 27,27ммоль). Нагрівання подовжують при 60°С ще 72 години. Реакційну суміші охолоджують та розподіляють між водою (50мл) та етилацетатом (100мл). Органічний шар відділяють та розчинник видаляють під зниженим тиском. Залишок розчиняють у тетрагідрофурані (20мл) та воді (2мл) та додають трифенілфосфін (5,90г, 22,72ммоль). Суміш нагрівають при 60°С протягом 16 годин перед розбавленням етилацетатом (100мл). Розчин промивають 1Η НСІ (50мл) та водний шар відділяють та доводять до рН11 натрій гідроксидом. Продукт екстрагують дихлорметаном (4´100мл). Органічні продукти комбінують та сушать натрій сульфатом та розчинник видаляють під зниженим тиском. Залишок очищають флеш-хроматографією, отримуючи потрібну сполуку як блідо-жовтий твердий продукт (1,10г). МС (ІЕР) 310 (М+Н)+ 1 Н ЯМР δ (CDCI3) 7,56 (1Н, d), 7,00 (1Н, d), 6,85 (1Н, dd), 4,42 (1Н, септет), 3,73-3,67 (1Н, m), 2,93-2,86 (1Н, m), 2,86-2,78 (1Н, m), 2,71-2,62 (2Н, 55 80268 56 m), 2,61-2,55 (1Н, m), 2,45-2,30 (3Н, m), 2,06-1,96 (2Н, m), 1,91-1,79 (2Н, m). Препарат 25 (2R)-1-аміно-3-{4-[4(метилсульфоніл)фенокси]піперидин-1-іл}пропан2-ол Отримано, як описано при отриманні 24, починаючи з 1-флуор-4-(метилсульфоніл) бензолу. Етап 1: трет-бутил 4-[4(метилсульфоніл)фенокси]піперидин-1карбоксилат 1 Н ЯМР δ (CDCI3) 1,48 (9Н, s), 1,74-1,82 (2Н, m), 1,91-1,99 (2Н, m), 3,04 (3Н, s), 3,38 (2Н, ddd), 3,69 (2Н, ddd), 4,57-4,62 (1Н, m), 7,02 (2Н, d), 7,86 (2Н, d). Етап 2: (2R)-1-аміно-3-{4-[4(метилсульфоніл)фенокси]піперидин-1-іл}пропан2-ол МС (ІЕР) 329 (М4Н)+ 1 Н ЯМР δ (CDCI3) 7,85 (2Н, d), 7,01 (2Н, d), 4,47 (1Н, септет), 3,73-3,67 (1Н, m), 3,03 (3Н, s), 2,95-2,88 (1Н, m), 2,86-2,78 (1Н, m), 2,72-2,62 (2Н, m), 2,61-2,55 (1Н, m), 2,45-2,30 (3Н, m), 2,08-1,98 (2Н, m), 1,92-1,81 (2Н, m). Препарат 26 4-({1-[(2R)-3-аміно-2гідроксипропіл1піперидин-4-іл}окси)бензонітрил Отримано, як описано при отриманні 24, починаючи з 4-флуорбензонітрилу. Етап 1: трет-бутил 4-(4ціанофенокси)піперидин-1-карбоксилат МС (ІЕР) 303 (М+Н)+. 1 Н ЯМР δ (CDCI3) 7,58 (2Н, d), 6,95 (2Н, d), 4,55 (1Н, m), 3,69 (2Н, ddd), 3,37 (2Н, ddd), 1,971,90 (2Н, m), 1,80-1,72 (2Н, m), 1,47 (9Н, s). Етап 2: 4-({1-[(2R)-3-Аміно-2гідроксипропіл1піперидин-4-іл)окси)бензонітрил МС (ІЕР) 276 (М+Н)+ 1 Н ЯМР δ (CDCI3) 7,57 (2Н, d), 6,94 (2Н, d), 4,46-4,41 (1Н, m), 3,74-3,68 (1Н, m), 2,94-2,88 (1Н, m), 2,83 (1Н, dd), 2,73-2,66 (1Н, m), 2,64 (1Н, dd), 2,61-2,55 (1Н, m), 2,46-2,30 (3Н, m), 2,07-1,97 (2Н, m), 1,91-1,80 (2Н, m). Препарат 27 трет-бутил 4-[4-хлор-2(метоксикарбоніл)фенокси]піперидин-1карбоксилат Діізопропілазодикарбоксилат (5,2мл, 26,8ммоль) додають краплями до розчину 5хлор-2-гідроксиметилбензоату (5,0г, 26,8ммоль), трет-бутил 4-гідроксипіперидин-1-карбоксилату (5,4г, 26,8ммоль) та трифенілфосфіну (7,02г, 26,8ммоль) у тетрагідрофу-рані (200мл) при 0°С. Реакційну суміші нагрівають до зовнішньої температури протягом ночі. Розчинник видаляють під зниженим тиском та залишок розтирають з діетиловим етером (200мл). Трифенілфосфіноксид відфільтровують та діетилетер видаляють під зниженим тиском. Залишок очищають флешхроматографією на колонці, елюючи сумішшю етилацетат:ізогексан (1:9), отримуючи потрібну сполуку як коричневе масло (8,1г). МС (ІЕР) 370 (М+Н)+ 1 Н ЯМР δ (ДМСО) 1,47 (9Н, в), 1,79-1,92 (4Н, гл), 3,45-3,54 (2Н, m), 3,56-3,62 (2Н, m), 3,89 (3Н, s), 4,5Ф4,59 (1Н, m), 6,92 (1Н, d), 7,38 (1Н, dd), 7,77 (1Н, d). Препарат 28 2-{[1-(трет-бутоксикарбоніл)піперидин-4іл]окси)-5-хпорбензойна кислота Водний розчин 2Η натрій гідроксиду (20мл) додають до розчину трет-бутил 4-[4-хлор-2(метоксикарбоніл)фенокси]піперидин-1карбоксилату (8,1г, 22,0ммоль) у тетрагідрофурані (70мл) при 45°С. Суміш перемішують інтенсивно протягом 3 годин тоді доводять до рН2 2Η гідрохлоридною кислотою. Продукт екстрагують етилацетатом та органічний шар промивають повторно водою до рН промивок 6. Органічний шар сушать магній сульфатом та випарюють. Залишок переганяють з толуолом, отримуючи потрібну сполуку як безбарвний твердий продукт (7,5г). МС (ІЕР) 356 (М+Н)+ 1 Н ЯМР δ (ДМСО) 1,47 (9Н, s), 1,79-1,88 (2Н, m), 2,03-2,11 (2Н, m), 3,30 (2Н, ddd), 3,77-3,85 (2Н, m), 4,72 (1Н, m), 7,02 (1Н, d), 7,49 (1Н, dd), 8,12 (1Н, d), 10,91 (1 Η, s). Препарат 29 4-(4-хлор-2-метилкарбамоїл-фенокси)піперидин-1-карбонової кислоти трет-бутиловий естер 57 Бром-трис-піролідинофосфоній гексафлуорфосфа т (1,57г, 3,37ммоль) додають до інтенсивно перемішуваної суміші 2-{[1-(третбутоксикарбоніл)піперидин-4-іл]окси}-5хлорбензойної кислоти (1,00г, 2,81ммоль) та 40% водного, метиламіну (2мл) у ДХМ (10мл), перемішування подовжують протягом 30 хвилин, перед розподілом між 1Η гідрохлоридною кислотою (10мл) та дихлорметаном (10мл). Органічний шар відділяють та промивають насиченим розчином натрій гідрокарбонату (20мл) та водою (20мл), тоді суша ть натрій сульфатом та розчинник видаляють під зниженим тиском. Залишок очищають флеш-хроматографією на колонці, елюючи сумішшю етилацетат:ізогексан (1:1), отримуючи потрібну сполуку як безбарвний твердий продукт (0,84г). МС (ІЕР) 369 (М+Н)+ 1 Н ЯМР δ (CDCI3) 8,17 (1Н, d), 7,75 (1Н, s), 7,35 (1Н, dd), 6,91 (1Н, d), 4,58 (1Н, tt), 3,81-3,71 (2Н, m), 3,29 (2Н, ddd), 3,00 (3Н, d), 2,08-1,98 (2Н, m), 1,82-1,71 (2Н, m), 1,48 (9Н, s). Препарат 30 трет-бутил 4-[2-(амінокарбоніл)-4хлорфенокси]піперидин-1-карбоксилат Отримано, як описано при отриманні 29, використовуючи водний аміак. МС (ІЕР) 355 (М+Н)+ 1 Н ЯМР δ (CDCI3) 8,18 (1Н, d), 7,67-7,61 (1Н, m), 7,40 (1Н, dd)3 6,94 (1Н, d), 5,83-5,76 (1Н, m), 4,61 (1Н, m), 3,84-3,76 (2Н, m), 3,26 (2Н, ddd), 2,09-2,01 (2Н, m), 1,82-1,73 (2Н, m), 1,47 (9H,s). Препарат 31 Метил 2-({1-[(2R)-3-аміно-2гідроксипропіл]піперидин-4-іл}окси)-5хлорбензоат Отримано, як описано при отриманні 24, етап 2 з трет-бутил 4-[4-хлор-2(метоксикарбоніл)фенокси]піперидин-1карбоксилату. МС (ІЕР) 343 (М+Н)* 1 Н ЯМР δ (CDCI3) 7,75 (1Н, d), 7,37 (1Н, dd), 6,92 (1Н, d), 4,46-4,39 (1Н, m), 3,89 (3Н, s), 3,723,66 (1Н, m), 2,93-2,87 (1Н, m), 2,81 (1Н, dd), 2,692,55 (2Н, m), 2,63 (1Н, dd), 2,43-2,31 (3Н, m), 2,001,84 (2Н, m), 1,67-1,46 (2Н, m). Препарат 32 2-({1-[(2R)-3-аміно-2гідроксипропіл]піперидин-4-іл}окси)-5-хлор-Nметилбензамід 80268 58 Отримано, як описано при отриманні 24, етап 2 з 4-(4-хлор-2-метилкарбамоїл-фенокси)піперидин-1-карбонової кислоти трет-бутилового естеру. МС (ІЕР) 342 (М+Н)+ 1 Н ЯМР δ (CDCI3) 8,18 (1Н, d), 7,88 (1Н, s), 7,34 (1Н, dd), 6,91 (1Н, d), 4,54^,48 (1Н, m), 3,733,67 (1Н, m), 3,01 (3Н, d), 2,89-2,83 (1Н, m), 2,83 (1Н, dd), 2,68-2,56 (2Н, m), 2,63 (1Н, dd), 2,44 (1Н, dd), 2,39-2,33 (1Н, m), 2,34 (1Н, dd), 2,13-2,03 (2Н, m), 1,94-1,83 (2Н, m). Препарат 33 2-({1-((2R)-3-аміно-2гідроксипропіл]піперидин-4-іл}окси)-5хлорбензамід Отримано, як описано при отриманні 24, етап 2 з трет-бутил 4-[2-(амінокарбоніл)-4хлорфенокси]піперидин-1-карбоксилату. МС (ІЕР) 328 (М+Н)+ 1 Н ЯМР δ (CDCI3) 8,19 (1Н, d), 7,75 (1Н, s), 7,39 (1Н, dd), 6,93 (1Н, d), 5,85 (1Н, s), 4,56-4,48 (1Н, m), 3,73-3,67 (1Н, m), 2,93-2,86 (1Н, m), 2,83 (1Н, dd), 2,73-2,66 (1Н, m), 2,63 (1Н, dd), 2,61-2,54 (1Н, m), 2,44 (1Н, dd), 2,37-2,30 (1Н, m), 2,35 (1Н, dd), 2,15-2,05 (2Н, m), 1,90 (2Н, dtd). Препарат 34 трет-бутил 4-{3,4-дихлор-2[(циклопропіламіно)карбоніп]фенокси}піперидин1-карбоксилат Розчин трет-бутил 4-[3,4-дихлор-2-(1Німідазол-1-ілкарбоніл)фенокси]піперидин-1карбоксилату (описано при отриманні 11 етап 1) (2,0г, 4,5ммоль) у циклопропіламіні (12мл) нагрівають при 50°С протягом 14 годин. Розчин концентрують у вакуумі, тоді розподіляють між етилацетатом та 1Η водною гідрохлоридною кислотою. Органічні продукти сушать магній сульфатом та концентрують у вакуумі. Кристалізація з суміші дихлорметан:ізогексан, дає потрібну сполуку як білий твердий продукт (0,64г). МС (ІЕР) 429/431 (М+Н)+ 1 Н ЯМР δ (ДМСО) 8(46 (1Н, d), 7,56 (1Н, d), 7,17 (1Н, d), 4,68 (1Н, m), 3,42-3,27 (4Н, m), 2,74 (1Н, m), 1,78 (2Н, m), 1,55 (2Н, m), 0,68 (2Н, m), 0,44 (2Н, m). Препарат 35 59 6-{[1-(3-Аміно-2-гідроксипропіл)піперидин-4іл]окси}-2,3-дихлор-N-циклопропілбензамід Отримано, як описано при отриманні 24, етап 2 з препарату 34. МС (ІЕР) 402 (М+Н)+ 1 Н ЯМР δ (CDCI3) 7,35 (1Н, d), 6,78 (1Н, d), 5,82 (1Н, s), 4,40-4,33 (1Н, m), 3,68 (1Н, tt), 2,922,85 (2Н, m), 2,85-2,77 (2Н, m), 2,81 (1Н, dd), 2,62 (1Н, dd), 2,42-2,29 (3Н, m), 2,00-1,89 (2Н, m), 1,881,79 (2Н, m), 0,89 (2Н, td), 0,66-0,62 (2Н, m). Препарат 36 трет-бутил4-[3,4-дихлор-2(хлорсуль фоніл)фенокси]піперидин-1карбоксилат До перемішуваного розчину трет-бутил 4[3,4-дихлорфенокси]піперидин-1-карбоксилату (10,0г, 28,9ммоль) у сухому тетрагідрофурані (400мл) при-70°С в атмосфері азоту додають краплями втор-бутиллітій (26,7мл, 1,3М у циклогексані). Розчин перемішують ще 15 хвилин, при цій температурі та тоді сульфурдіоксид продувають через суміш протягом 10 хвилин. Охолоджувальну баню видаляють та суміш нагрівають до кімнатної температури протягом 1 години. Nхлорсукцинімід (4,63г, 35ммоль) додають та суміш перемішують при кімнатній температурі протягом 72 годин. Розчин концентрують у вакуумі та розподіляють між етилацетатом та 1Η водною гідрохлоридною кислотою. Органічні екстракти сушать (магній сульфат) та концентрують. Хроматографія на діоксид силіцію (етилацетат: ізогексан/1:3), дає потрібну сполуку як (2,40г) МС (ІЕР) 445 (М+Н)+ 1 Н ЯМР δ (ДМСО) 7,45 (1Н, d), 7,03 (1Н, d), 4,65 (1Н, m), 3,59 (2Н, m), 3,33 (3Н, s), 1,66 (4Н, m), 1,40 (9H, s). Препарат 37 2,3-дихлор-6-(піперидин-4ілокси)бензолсульфонаміду Трет-бутил-4-[3,4-дихлор-2(хлорсуль фоніл)фенокси]піперидин-1карбоксилат (0,80г, 1,8ммоль) розчиняють у 7Η аміаку у метанолі та перемішують при кімнатній температурі протягом 20 хвилин. Розчин концентрують у вакуумі та тоді одноразово переганяють з толуолом. Залишок знов розчиняють у суміші дихлорметан:трифлуороцтова кислота 71:1 (20мл) та перемішують при кімнатній температурі 80268 60 протягом 15 хвилин. Розчин концентрують у вакуумі, тоді розподіляють між етилацетатом та насиченим водним розчином натрій гідрокарбонату. Водну фазу реекстрагують етилацетатом (4 рази) та комбіновані органічні продукти сушать безводним калій карбонатом. Концентрація у вакуумі дала потрібну сполуку як білий порошок (0,54г). МС (ІЕР) 325/327 (М+Н)+ 1 Н ЯМР δ (ДМСО) 7,74 (1Н, d), 7,34 (1Н, d), 4,66 (1Н, m), 2,96 (2Н, m), 2,55 (2Н, m), 1,91 (2Н, m), 1,63 (2Н, m). Препарат 38 2,3-дихлор-N-метил-6-(піперидин-4ілокси)бензолсульфонамід Трет-бутил 4-[3,4-дихлор-2(хлорсуль фоніл)фенокси]піперидин-1карбоксилат (0,70г, 1,8ммоль) розчиняють у 40% водному метиламіні у воді (10мл) та метанолі (10мл) та перемішують при кімнатній температурі протягом 30 хвилин. Розчин концентрують у вакуумі та тоді переганяють з толуолом (4 рази). Залишок знов розчиняють у суміші дихлорметан:трифлуороцтова кислота (1:1) (20мл) та перемішують при кімнатній температурі протягом 15 хвилин. Розчин концентрують у вакуумі, тоді розподіляють між етилацетатом та насиченим водним розчином натрій гідрокарбонату. Водн у фазу реекстрагують етилацетатом (4 рази) та комбіновані органічні продукти суша ть безводним калій карбонатом. Концентрація у вакуумі дає потрібну сполуку як білий порошок (0,69г). МС (ІЕР) 339/341 (М+Н)+ 1 Н ЯМР δ (ДМСО) 7,76 (1Н, d), 7,35 (1Н, d), 4,64 (1Н, m), 2,96 (2Н, m), 2,54 (3Н, s), 2,54 (2Н, m), 1,90 (2Н, m), 1,61 (2Н, m). Препарат 39 2,3-дихлор-N-циклопропіл-6-(піперидин-4ілокси)бензолсульфонамід Трет-бутил 4-[3,4-дихлор-2(хлорсуль фоніл)фенокси]піперидин-1карбоксилат (0,70г, 1,8ммоль) розчиняють у циклопропіламіні (8мл) та перемішують при кімнатній температурі протягом 30 хвилин. Розчин концентрують у вакуумі та тоді переганяють з толуолом(4 рази). Залишок знов розчиняють у суміші дихлорметані/трифлуороцтова кислота 1:1 (20мл) та перемішують при кімнатній температурі протягом 15 хвилин. Розчин концентрують у вакуумі, тоді розподіляють між етилацетатом та насиченим водним розчином натрій гідрокарбо
ДивитисяДодаткова інформація
Назва патенту англійськоюPiperidine derivatives, process for the preparation thereof, pharmaceutical composition based thereon and method for treatment chemokine mediated disease
Автори англійськоюAlcaraz Lilian, Furber Mark, Purdie Mark, Springthorpe Brian
Назва патенту російськоюПроизводные пиперидина, способ их получения, фармацевтическая композиция на их основе и способ лечения опосредованной хемокином болезни
Автори російськоюАлькараз Лилиан, Фербер Марк, Перди Марк, Спринґторп Браян
МПК / Мітки
МПК: A61P 29/00, A61P 1/02, A61P 15/00, C07D 211/14, C07D 413/14, C07D 417/12, C07D 487/04, A61P 19/02, A61K 31/53, A61P 11/00, C07D 409/12, C07D 211/44, C07D 413/12, A61K 31/506, C07D 471/04, A61P 17/00, A61K 31/4709, A61K 31/4535, A61P 35/00, A61K 31/502, C07D 405/12, A61P 21/04, A61K 31/519, A61P 37/06, A61K 31/4725, A61P 9/10, A61P 31/08, A61P 7/00, A61P 37/08, A61P 43/00, A61P 3/10, C07D 401/12, A61P 27/16, C07D 211/46, C07D 407/12, A61P 17/14, A61K 31/498, A61P 1/04, A61P 25/04, A61P 31/00, A61P 11/06, A61K 31/453, C07D 401/14, C07D 409/14, A61K 31/4545, A61K 31/445, A61P 13/12, A61K 31/454, A61P 37/04, A61P 17/06, A61P 25/28, A61P 5/16, A61P 37/00, C07D 211/52
Мітки: отримання, опосередкованої, композиція, хемокіном, хвороби, лікування, похідні, основі, спосіб, фармацевтична, піперидину
Код посилання
<a href="https://ua.patents.su/60-80268-pokhidni-piperidinu-sposib-kh-otrimannya-farmacevtichna-kompoziciya-na-kh-osnovi-ta-sposib-likuvannya-oposeredkovano-khemokinom-khvorobi.html" target="_blank" rel="follow" title="База патентів України">Похідні піперидину, спосіб їх отримання, фармацевтична композиція на їх основі та спосіб лікування опосередкованої хемокіном хвороби</a>
Попередній патент: Пристрій для оцінки біоелектричної активності точок акупунктури
Наступний патент: Пасивація металу в установці теплообмінного риформінгу
Випадковий патент: Сплав на основі міді