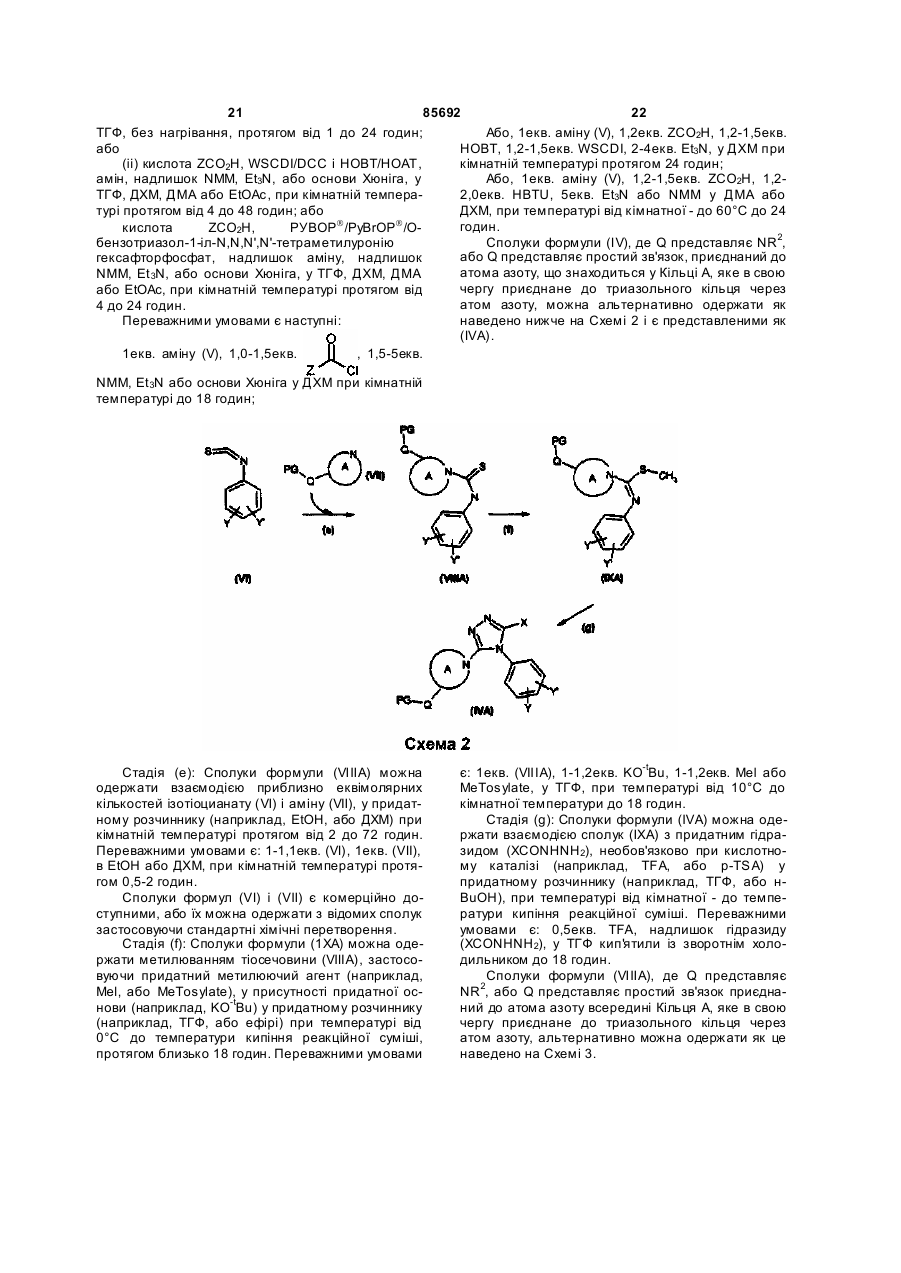
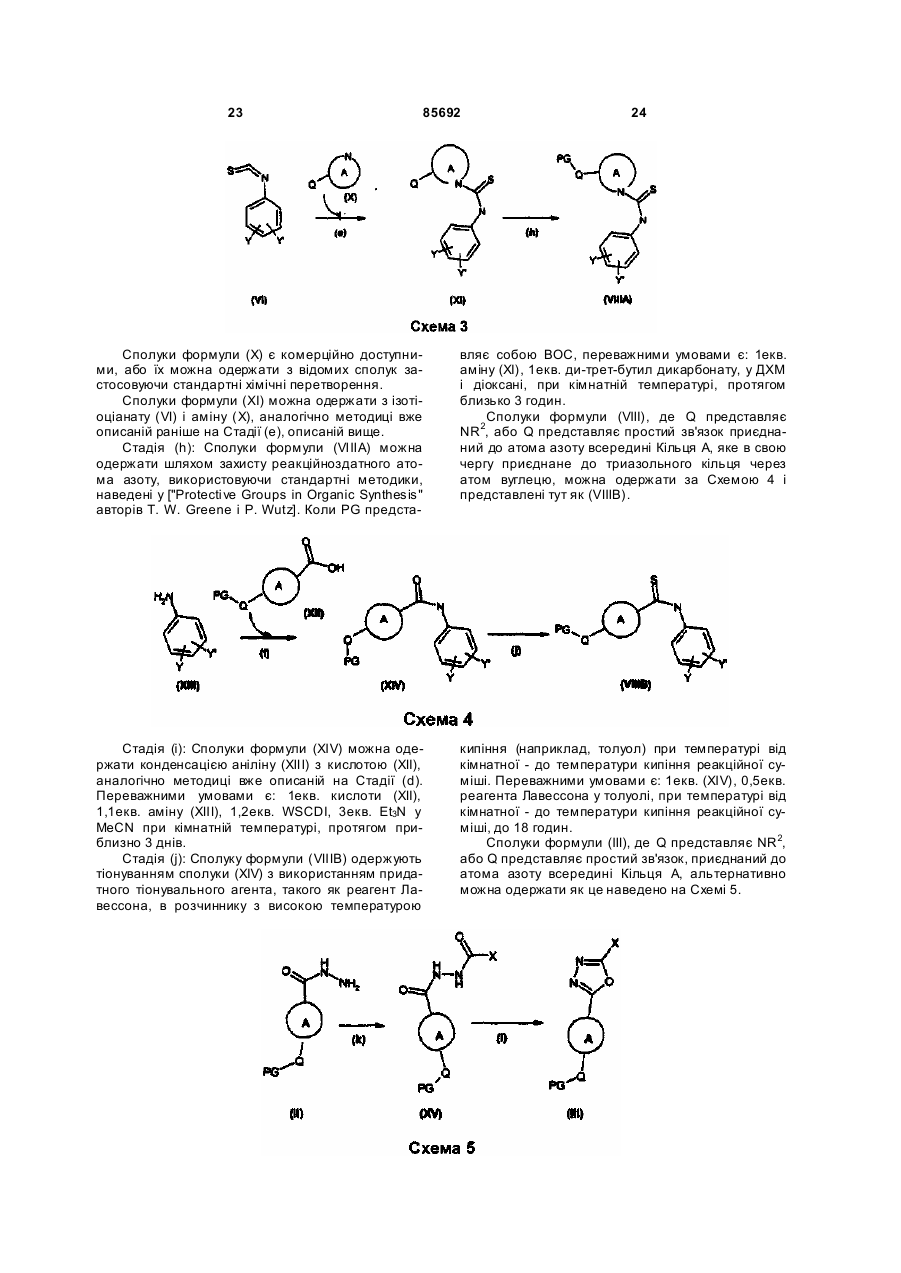
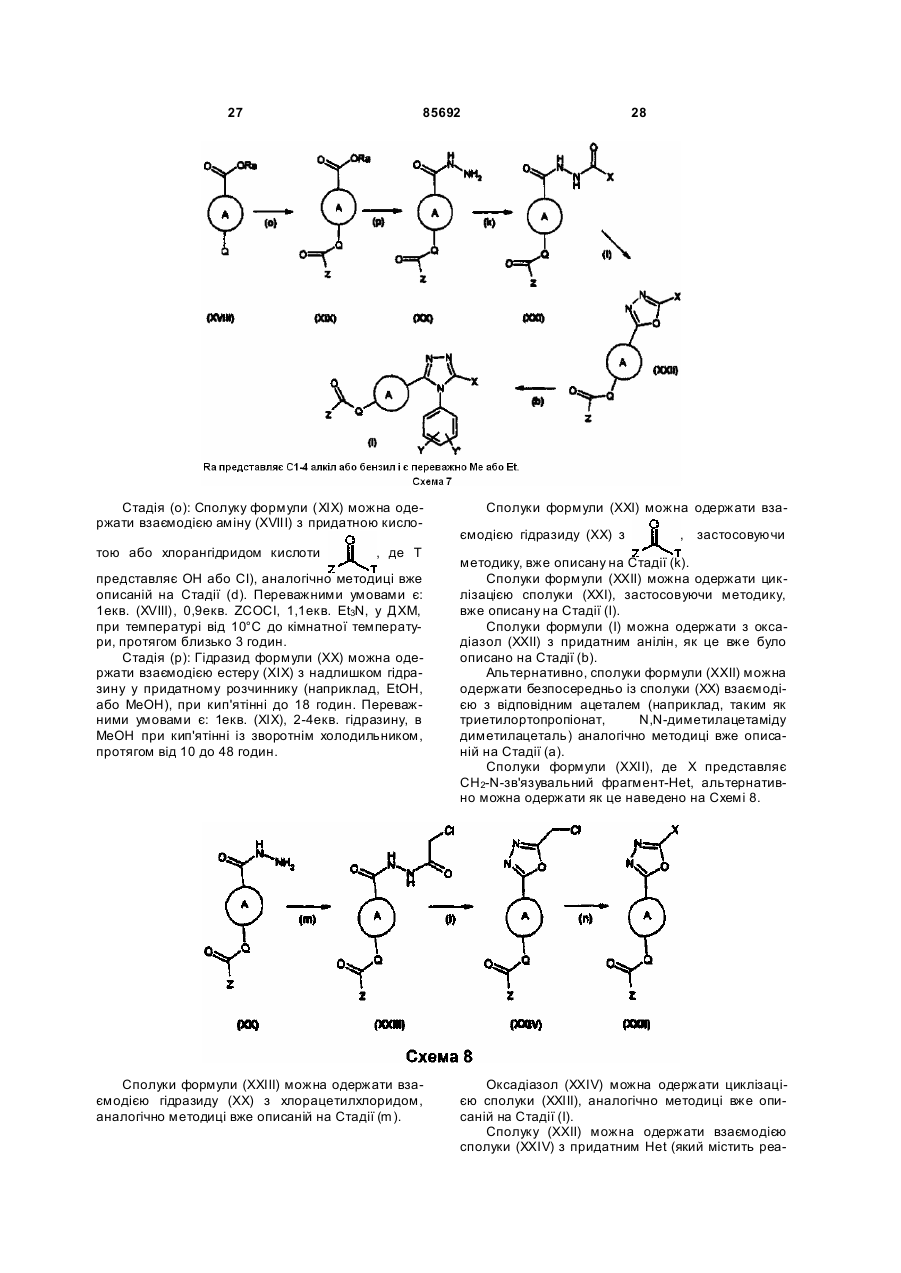
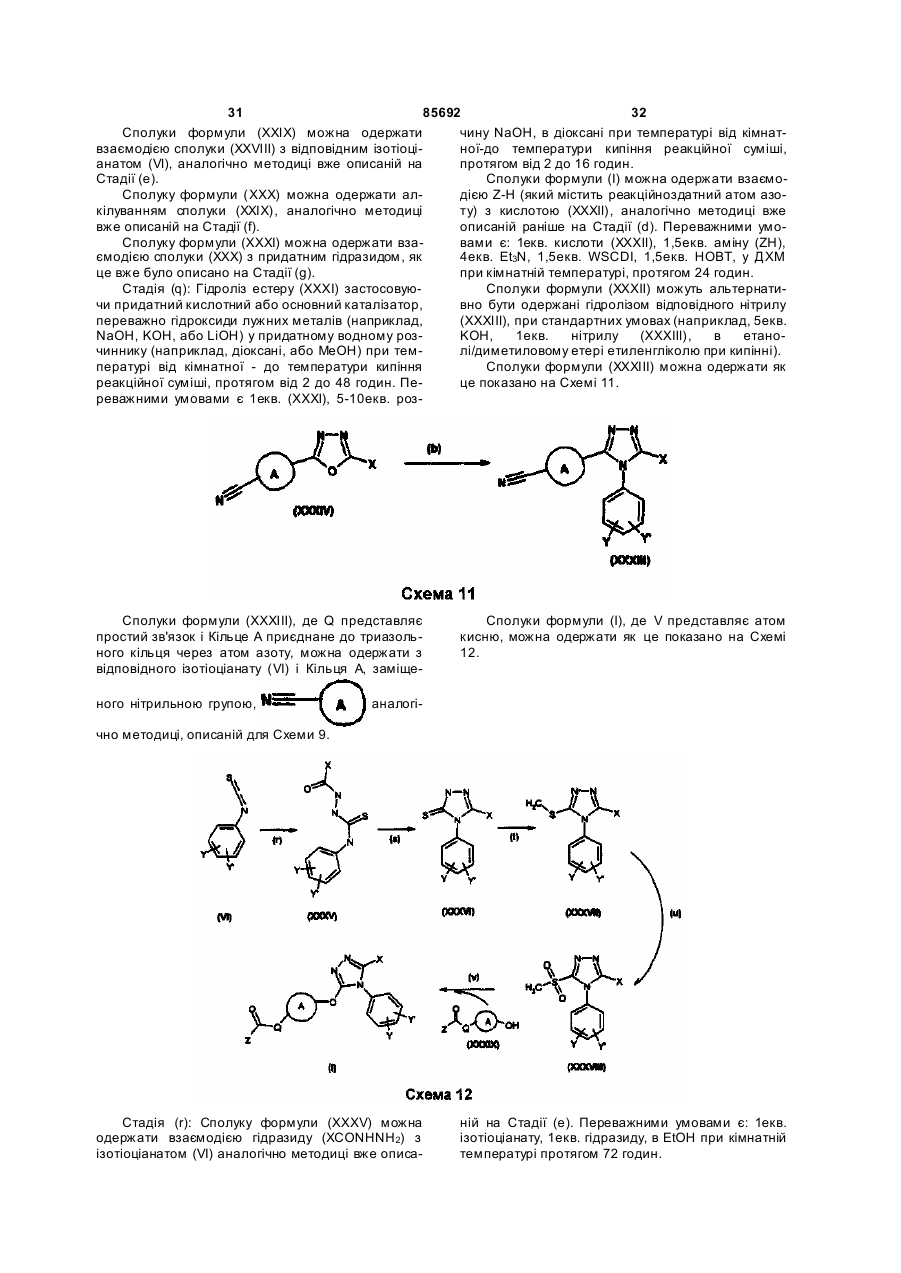
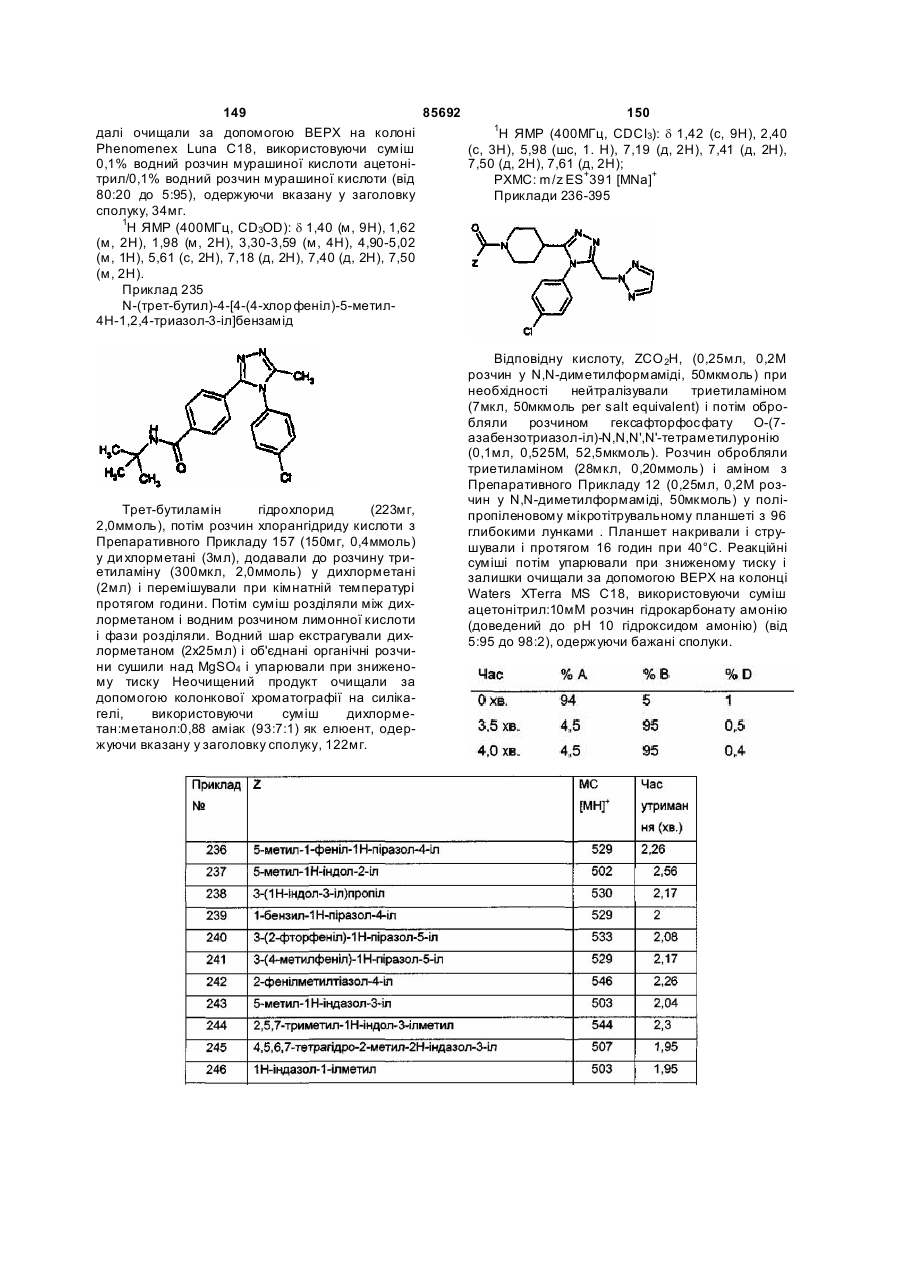
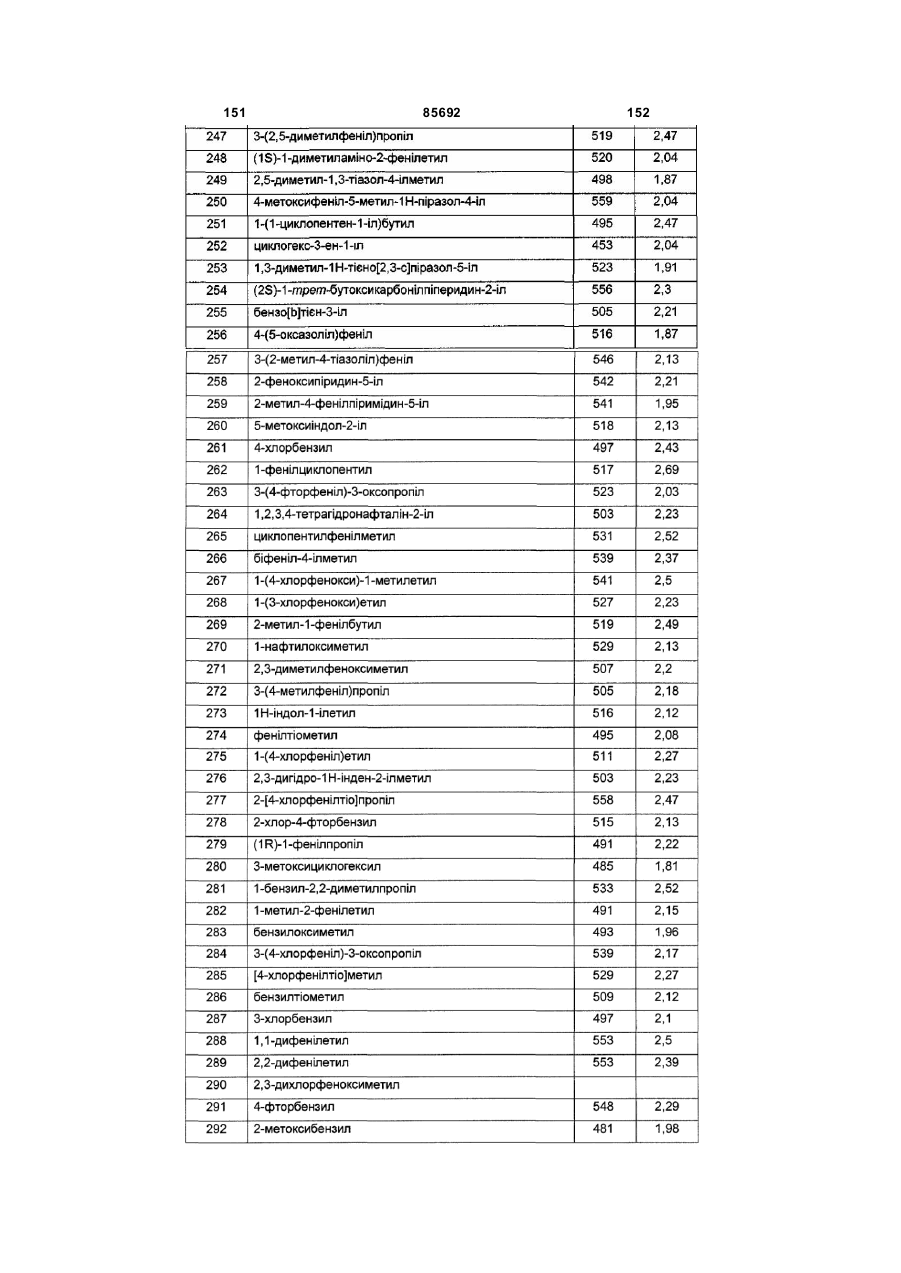
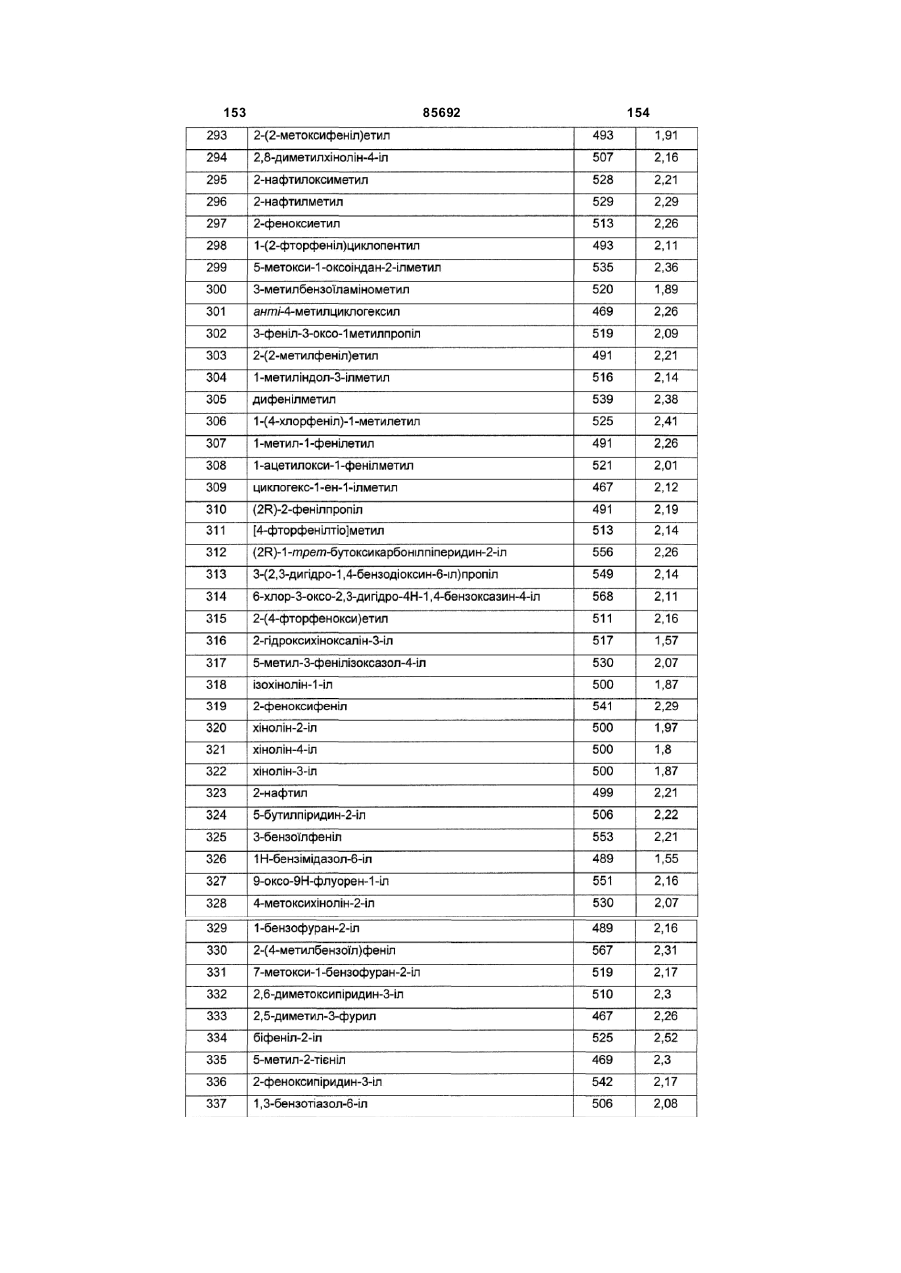
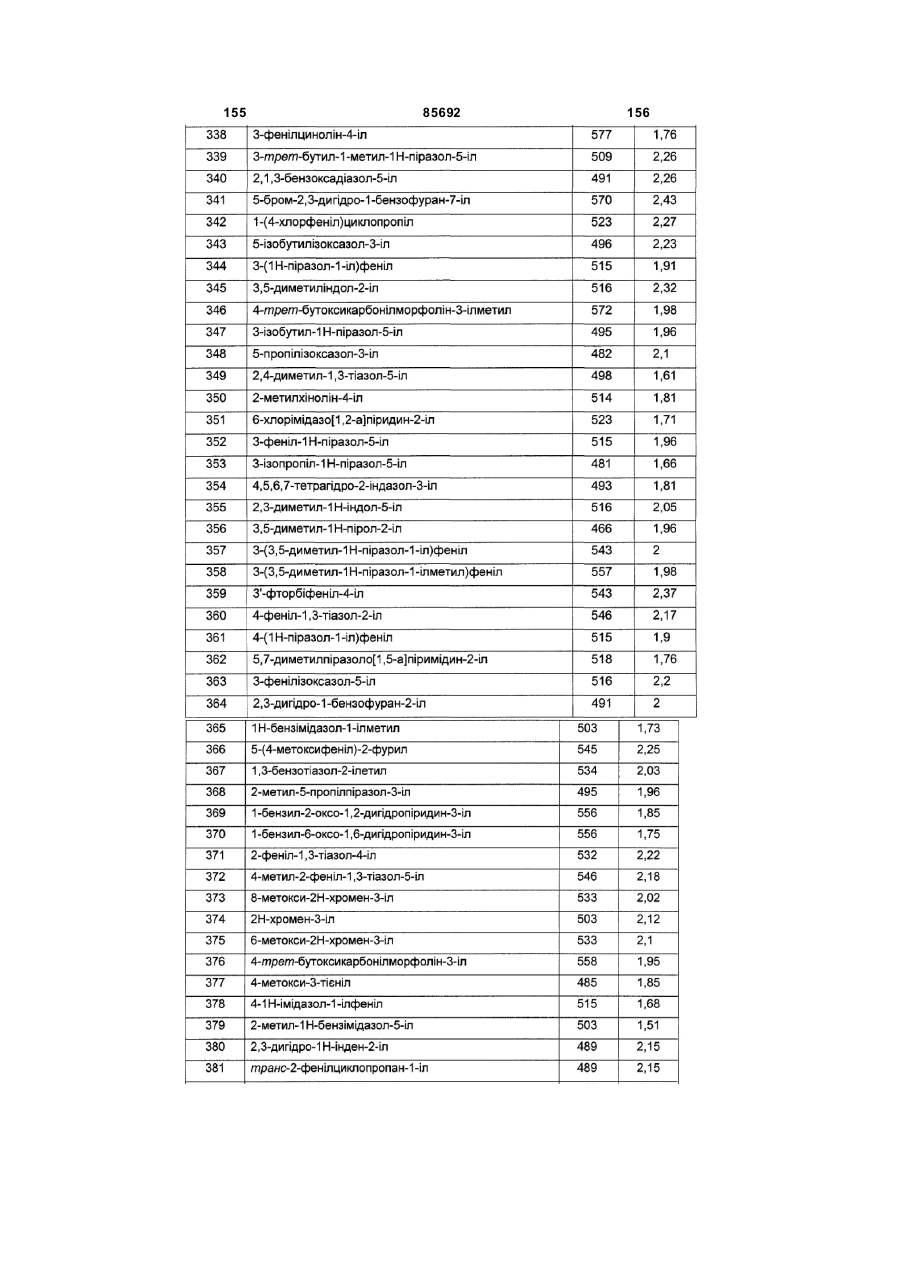
Похідні триазолу як антагоністи вазопресину
Номер патенту: 85692
Опубліковано: 25.02.2009
Автори: Рікманс Томас, Робертс Лі Річард, Джонсон Патрік Стівен, Браянс Джастін Стівен
Формула / Реферат
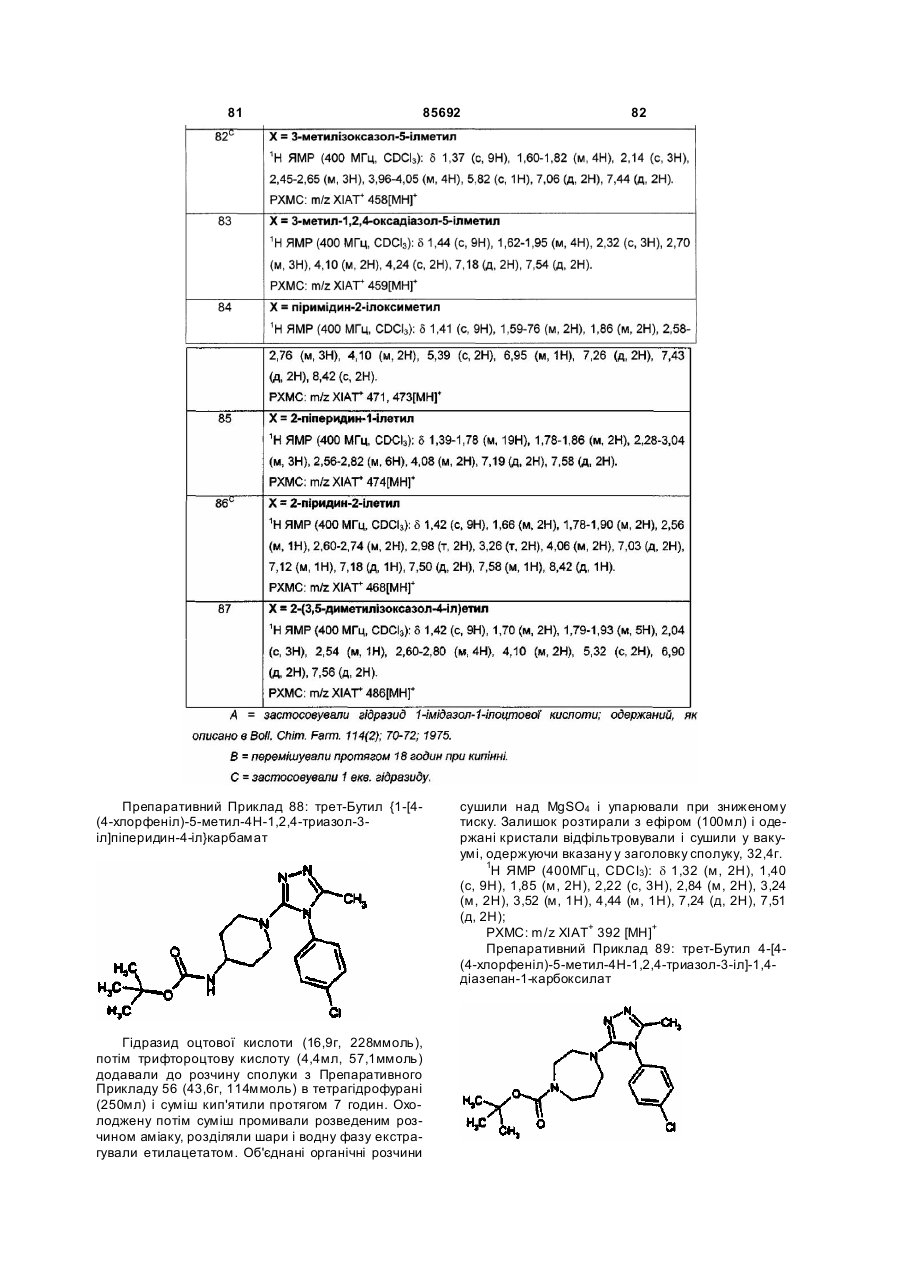
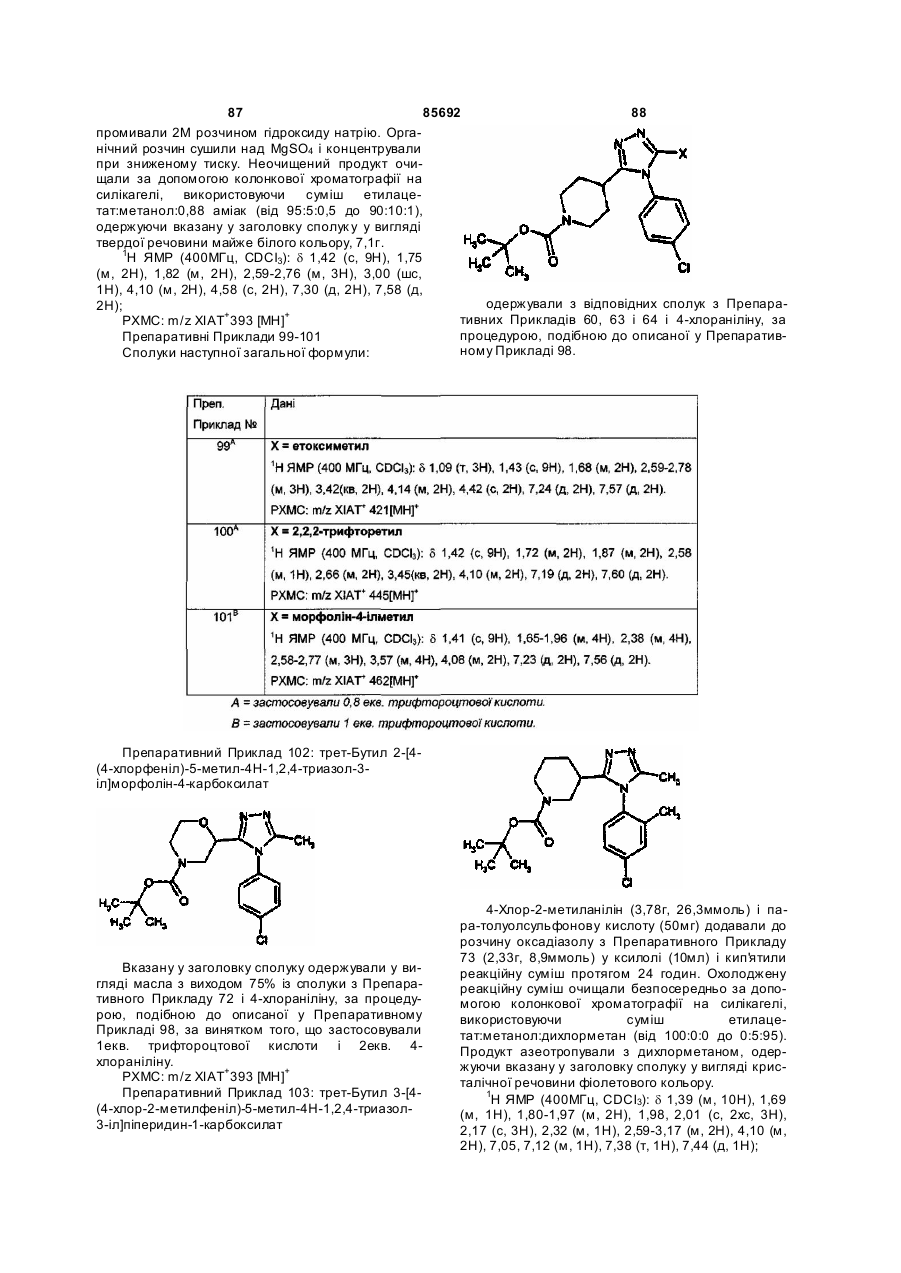
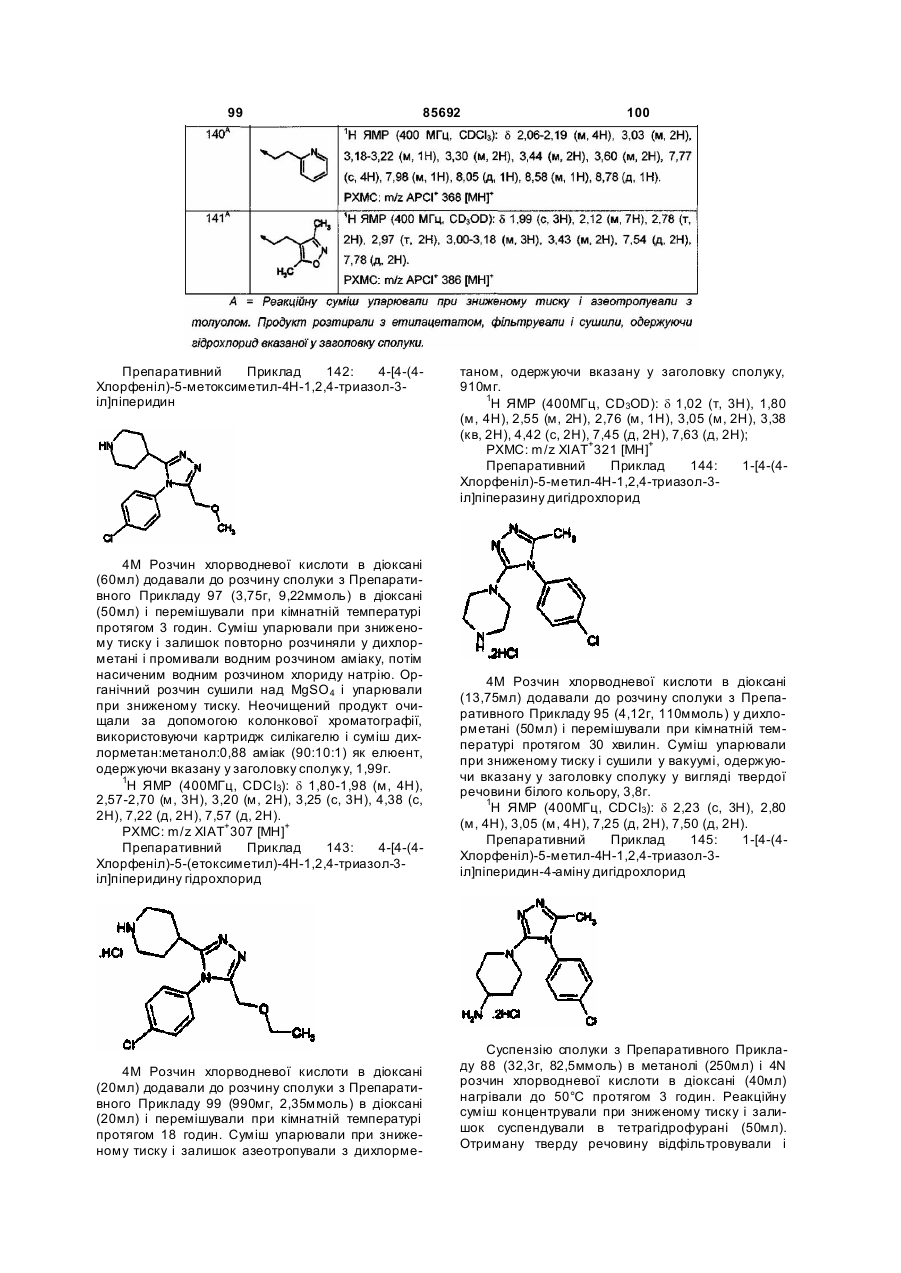
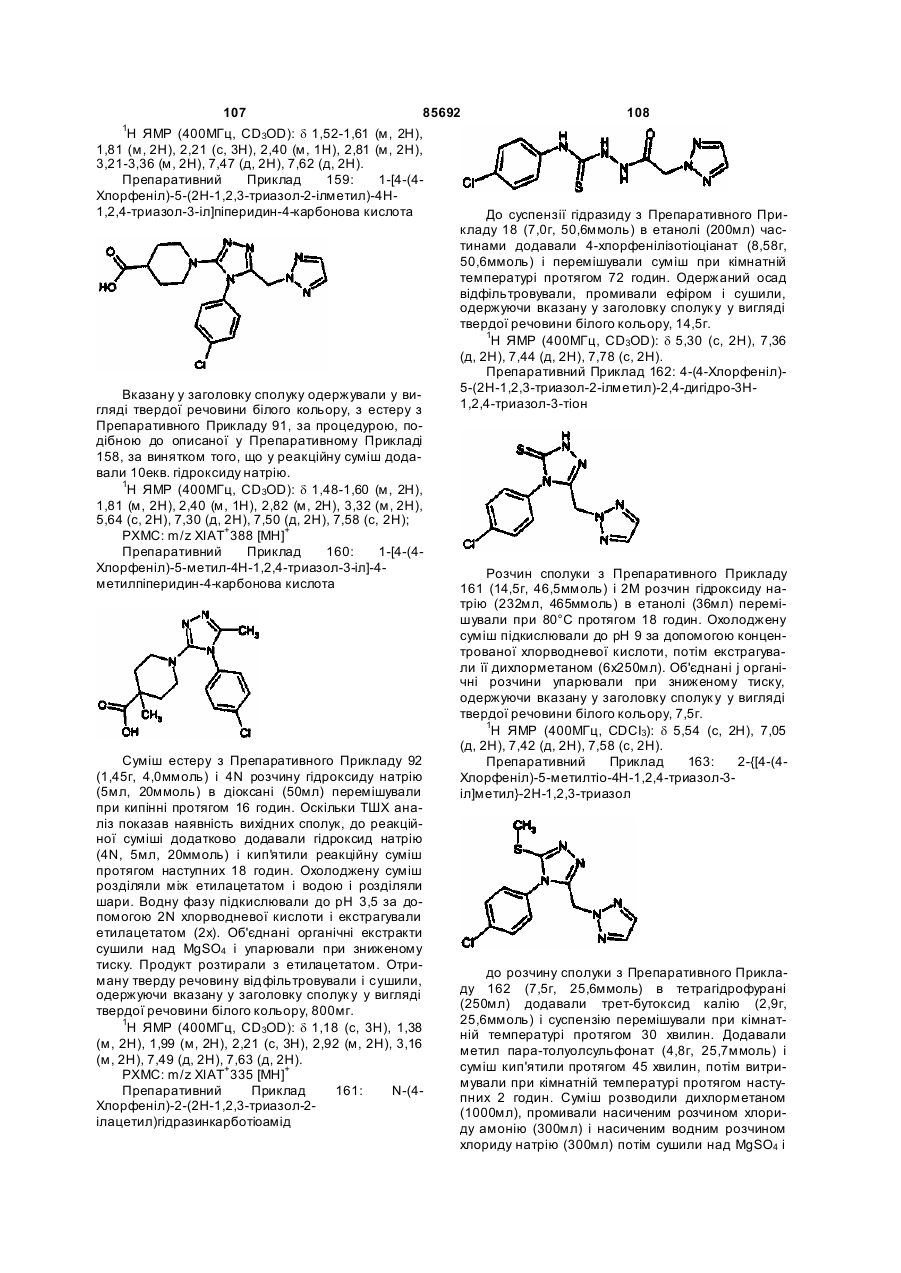
1. Сполука формули (І)
 (I)
(I)
або її фармацевтично прийнятне похідне, де:
Х представляє -[СН2]а-R або -[СН2]а-О-[СH2]b-R;
а представляє число від 0 до 6;
b представляє число від 0 до 6;
R представляє Н, СF3 або Het;
Het представляє 5- або 6-членне насичене, частково насичене або ароматичне гетероциклічне кільце, що має або (а) від 1 до 4 атомів азоту, (b) 1 атом кисню або 1 атом сірки, або (с) 1 атом кисню або 1 атом сірки і 1 або 2 атоми азоту, необов'язково заміщене одним або більшою кількістю незалежно вибраних замісників W;
Y або Y' незалежно представляють один або більшу кількість замісників, незалежно вибраних з групи, що містить -[O]c-[CH2]d-R1, які можуть бути однаковими або різними у кожному випадку;
с у кожному випадку незалежно представляє число, що дорівнює 0 або 1;
d у кожному випадку незалежно представляє число від 0 до 6;
R1 у кожному випадку незалежно представляє Н, галоген, СF3, CN або Het1;
Het1 у кожному випадку незалежно представляє 5- або 6-членне ненасичене гетероциклічне кільце, що має або (а) від 1 до 4 атомів азоту, (b) 1 атом кисню або 1 атом сірки, або (с) 1 атом кисню або 1 атом сірки і 1 або 2 атоми азоту;
V представляє простий зв'язок або -O-;
Кільце А представляє 5-7-членне насичене гетероциклічне кільце, що має або (а) від 1 до 4 атомів азоту, (b) 1 атом кисню або 1 атом сірки, або (с) 1 атом кисню або 1 атом сірки і 1 або 2 атоми азоту, або представляє собою феніленову групу;
Кільце А є необов'язково заміщеним одним або більшою кількістю замісників, вибраних з групи, що містить С1-6алкіл, феніл або гідрокси;
Q представляє простий зв'язок або -N(R2)-;
R2 представляє водень або С1-6алкіл;
Z представляє -[O]e-[CH2]f-R3, фенільне кільце (необов'язково приконденсоване до бензольного кільця або Het2 і одержана група є необов'язково заміщеною одним або більшою кількістю незалежно вибраних замісників W) або Het3 (необов'язково приконденсоване до бензольного кільця або Het4 і одержана група є необов'язково заміщеною одним або більшою кількістю незалежно вибраних замісників W);
R3 представляє С1-6алкіл (необов'язково заміщений одним або більшою кількістю незалежно вибраних замісників W), С3-6циклоалкіл, С3-6циклоалкеніл, феніл (необов'язково заміщений одним або більшою кількістю незалежно вибраних замісників W), Het5 або NR4R5;
е представляє число, що дорівнює 0 або 1;
f представляє число від 0 до 6;
Het2 і Het5 незалежно представляють 5- або 6-членне насичене, частково насичене або ароматичне гетероциклічне кільце, що має або (а) від 1 до 4 атомів азоту, (b) 1 атом кисню або 1 атом сірки, або (с) 1 атом кисню або 1 атом сірки і 1 або 2 атоми азоту, необов'язково заміщених одним або більшою кількістю замісників W;
Het3 представляє 4-6-членне насичене, частково насичене або ароматичне гетероциклічне кільце, що має або (а) від 1 до 4 атомів азоту, (b) 1 атом кисню або 1 атом сірки, або (с) 1 атом кисню або 1 атом сірки і 1 або 2 атоми азоту, необов'язково заміщених одним або більшою кількістю замісників W;
Het4 представляє 6-членне ароматичне гетероциклічне кільце, що має або (а) від 1 до 4 атомів азоту, (b) 1 атом кисню або 1 атом сірки, або (с) 1 атом кисню або 1 атом сірки і 1 або 2 атоми азоту, необов'язково заміщених одним або більшою кількістю замісників W;
R4 і R5 незалежно представляють водень, С1-6алкіл, С1-6алкілокси, С3-8циклоалкіл (необов'язково приконденсований до С3-8циклоалкілу) або Het6;
R4 і R5 є необов'язково заміщеними одним або більшою кількістю замісників, вибраних незалежно з групи, що містить С1-6алкіл, С1-6алкілокси, С3-8циклоалкіл (необов'язково приконденсований до С3-8циклоалкілу) або феніл;
Het6 представляє 5- або 6-членне насичене, частково насичене або ароматичне гетероциклічне кільце, що має або (а) від 1 до 4 атомів азоту, (b) 1 атом кисню або 1 атом сірки, або (с) 1 атом кисню або 1 атом сірки і 1 або 2 атоми азоту, необов'язково заміщених одним або більшою кількістю замісників W;
W незалежно у кожному випадку представляє галоген, [O]gR6, SO2R6, SR6, SO2NR6R7, [O]h[CH2]iCF3, [O]jCHF2, феніл (необов'язково заміщений галогеном, С1-6алкілом або С1-6алкілокси), CN, фенокси (необов'язково заміщений галогеном), ОН, бензил, NR6R7, NCOR6, бензилокси, оксо, CONHR6, NSO2R6R7, COR6, С1-6алкілен-NCOR7, Het7;
R6 представляє водень, С1-6алкіл, С3-6циклоалкіл, С3-6циклоалкеніл або С1-6алкілен-O-С1-6алкіл;
R7 представляє водень або С1-6алкіл;
і представляє число від 0 до 6;
h представляє число, що дорівнює 0 або 1;
g представляє число, що дорівнює 0 або 1;
j представляє число, що дорівнює 0 або 1;
Het7 представляє 5- або 6-членне насичене, частково насичене або ароматичне гетероциклічне кільце, що має або (а) від 1 до 4 атомів азоту, (b) 1 атом кисню або 1 атом сірки, або (с) 1 атом кисню або 1 атом сірки і 1 або 2 атоми азоту, необов'язково заміщене R6 і/або R7, і/або оксогрупою.
2. Сполука згідно з пунктом 1, де Х представляє -[СН2]а-R.
3. Сполука згідно з пунктом 2, де R представляє Het.
4. Сполука згідно з пунктом 1, де Y представляє галоген.
5. Сполука згідно з пунктом 1, де V представляє простий зв'язок.
6. Сполука згідно з пунктом 1, де Q представляє простий зв'язок.
7. Сполука згідно з пунктом 1, де Кільце А представляє шестичленне кільце.
8. Сполука згідно з пунктом 1, де Z представляє феніл.
9. Сполука згідно з пунктом 1, де Z є заміщеним галогеном.
10. Сполука згідно з пунктом 1, вибрана з наступних:
(3-хлорфеніл)-{4-[4-(4-хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}-метанон;
(4-хлорфеніл)-{4-[4-(4-хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}-метанон;
(5-хлор-2-фторфеніл)-{4-[4-(4-хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}-метанон;
{4-[4-(4-хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}-(3,5-дифторфеніл)-метанон;
{4-[4-(4-хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}-(3-фторфеніл)-метанон;
{4-[4-(4-хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}-(2,3-дифторфеніл)-метанон;
(3-хлор-2-фторфеніл)-{4-[4-(4-хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}-метанон;
(3-хлор-4-фторфеніл)-{4-[4-(4-хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}-метанон;
{4-[4-(4-хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}-(4-трифторметилфеніл)-метанон;
{4-[4-(4-хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}-(3-трифторметилфеніл)-метанон;
{4-[4-(4-хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}-(2-трифторметилфеніл)-метанон;
(3-хлор-5-фторфеніл)-{4-[4-(4-хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}-метанон;
{4-[4-(4-хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}-(4-дифторметилфеніл)-метанон;
{4-[4-(4-хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}-(1Н-індазол-3-іл)-метанон;
і їх фармацевтично прийнятні похідні.
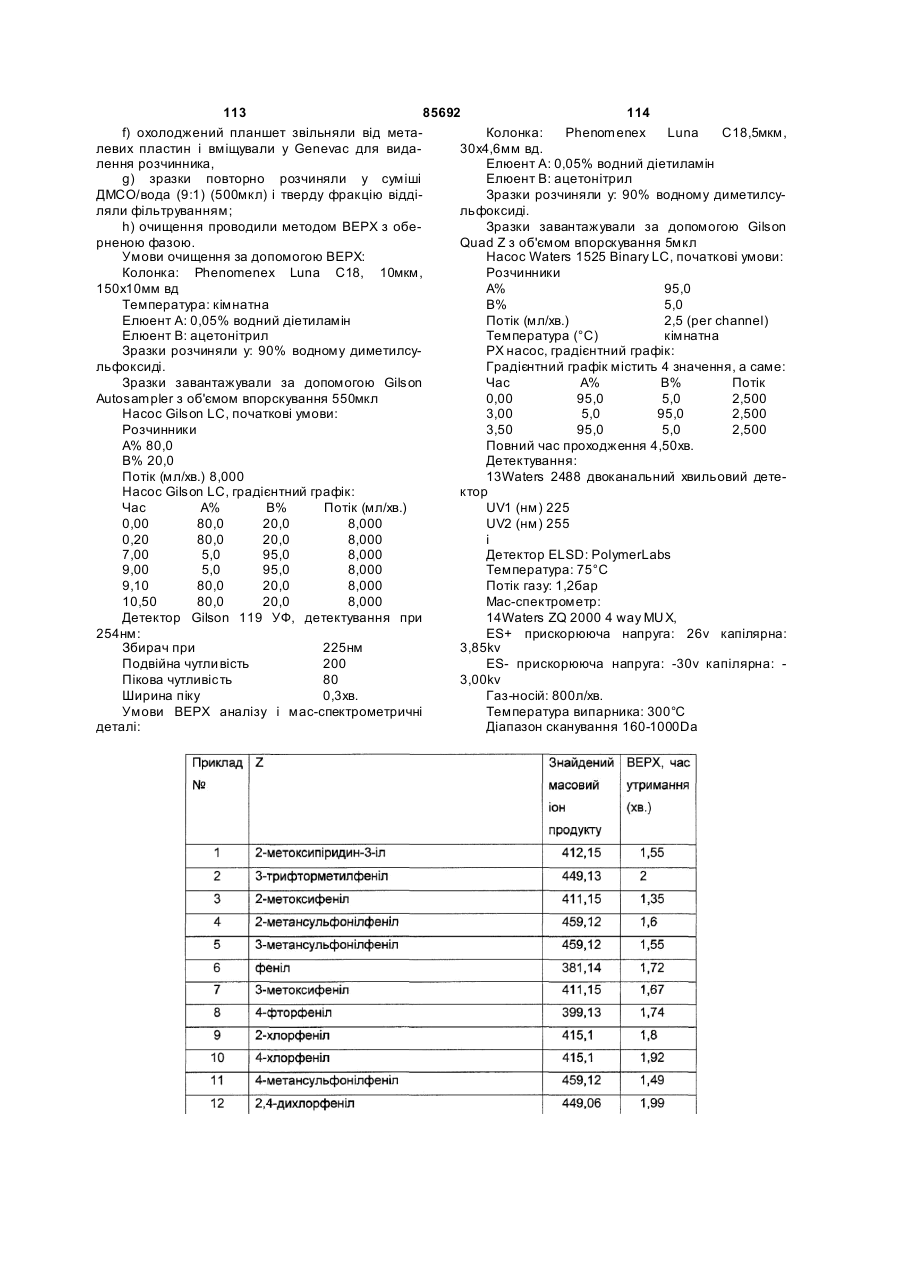
11. Сполука згідно з пунктом 1, що має формулу (I’)
 , (I’)
, (I’)
або її фармацевтично прийнятне похідне, де:
Х представляє -[СH2]а-R або -[СН2]а-O-[СН2]b-R;
а представляє число від 0 до 6;
b представляє число від 0 до6;
R представляє Н, СF3 або Het;
Het представляє а 5- або 6-членне гетероциклічне кільце, що має або (а) від 1 до 4 атомів азоту, (b) 1 атом кисню або 1 атом сірки, або (с) 1 атом кисню або 1 атом сірки і 1 або 2 атоми азоту;
Y представляє -[O]c-[CH2]d-R1;
Y' представляє -[O]c-[CH2]d’-R1;
с і с' незалежно представляють число, що дорівнює 0 або 1;
d і d' незалежно представляють число від 0 до 6;
R1 і R1' незалежно представляють Н, галоген, СF3 або Het1;
Het1 представляє 5- або 6-членне ненасичене гетероциклічне кільце, що має або (а) від 1 до 4 атомів азоту, (b) 1 атом кисню або 1 атом сірки, або (с) 1 атом кисню або 1 атом сірки і 1 або 2 атоми азоту;
Кільце А представляє 5- або 6-членне насичене гетероциклічне кільце, що містить щонайменше один атом азоту;
Z представляє -[O]e-[CH2]f-R2, фенільне кільце (необов'язково приконденсоване до фенільного кільця або 5- чи 6-членного насиченого, частково ненасиченого або ароматичного гетероциклічного кільця, і/або необов'язково заміщене одним або більшою кількістю незалежно вибраних замісників W) або 6-членне ароматичне гетероциклічне кільце (необов'язково приконденсоване до фенільного кільця або 6-членного ароматичного гетероциклічного кільця, і/або необов'язково заміщене одним або більшою кількістю незалежно вибраних замісників W);
R2 представляє С1-6алкіл або С3-6циклоалкіл;
е представляє число, що дорівнює 0 або 1;
f представляє число від 0 до 6;
W представляє галоген, [O]gR3, SO2R3, SR3, SO2NR3R4, [О]h[СH2]iСF3, OCHF2, феніл, CN, фенокси (необов'язково заміщений галогеном), ОН, бензил, NCOR3, бензилокси, окси, CONHR3, NSO2R3R4, COR3, С1-6алкілен-NCOR3, Het2;
R3 представляє водень, С1-6алкіл, С3-6циклоалкіл або С1-6алкілен-О-С1-6алкіл;
R4 представляє водень або С1-6алкіл;
і представляє число від 0 до 6;
h представляє число, що дорівнює 0 або 1;
g представляє число, що дорівнює 0 або 1;
Het2 представляє а 5- або 6-членну насичену, частково ненасичену або ароматичну гетероциклічну групу, що має або (а) від 1 до 4 атомів азоту, (b) 1 атом кисню або 1 атом сірки, або (с) 1 атом кисню або 1 атом сірки і 1 або 2 атоми азоту, причому гетероциклічна група є необов'язково заміщеною R3 і/або R4, і/або оксигрупою.
12. Застосування сполуки згідно з будь-яким з пунктів 1-11 як медикаменту.
13. Спосіб лікування захворювання у ссавця, включаючи людину, при якому призначають антагоніст V1a і який включає введення терапевтичнo ефективної кількості сполуки, згідно з будь-яким з пунктів 1-11.
14. Спосіб лікування тривоги, серцево-судинного захворювання (включаючи стенокардію, атеросклероз, гіпертонію, серцеву недостатність, набряк, гіпернатріємію), дисменореї (первинної і вторинної), ендометріозу, блювання (включаючи закачування), затримки внутрішньоутробного розвитку, запалення (включаючи ревматоїдний артрит), міжменструального болю, передеклампсії, передчасної еякуляції, передчасних пологів (недоношеної вагітності) і хвороби Рейно у ссавця, включаючи людину, який включає введення згаданому суб'єкту, що страждає від такого захворювання, терапевтичнo ефективної кількості сполуки згідно з будь-яким з пунктів 1-11.
15. Спосіб лікування згідно з пунктом 13 або 14, де захворюванням є первинна або вторинна дисменорея.
16. Застосування сполуки згідно з будь-яким з пунктів 1-11 для виготовлення медикаменту для лікування захворювання, при якому призначають антагоніст V1a рецептора.
17. Застосування сполуки згідно з будь-яким з пунктів 1-11 для виготовлення медикаменту для лікування тривоги, серцево-судинного захворювання (включаючи стенокардію, атеросклероз, гіпертонію, серцеву недостатність, набряк, гіпернатріємію), дисменореї (первинної і вторинної), ендометріозу, блювання (включаючи закачування), затримки внутрішньоутробного розвитку, запалення (включаючи ревматоїдний артрит), міжменструального болю, передеклампсії, передчасної еякуляції, передчасних пологів (недоношеної вагітності) і хвороби Рейно.
18. Застосування згідно з пунктом 16 або 17, де захворюванням є первинна або вторинна дисменорея.
19. Фармацевтична рецептура, що містить сполуку згідно з будь-яким з пунктів 1-11 і фармацевтично прийнятний наповнювач, розріджувач або носій.
20. Комбінація (А) сполуки згідно з будь-яким з пунктів 1-11 і (В) іншого фармакологічно активного інгредієнта.
21. Комбінація згідно з пунктом 20, де (В) представляє оральний контрацептив, інгібітор PDEV, інгібітор СОХ, NО-донор або L-аргінін.
22. Застосування комбінації згідно з пунктом 20 або 21 для виготовлення медикаменту для комбінованої терапії шляхом одночасного, окремого або послідовного застосування при лікуванні дисменореї.
23. Спосіб лікування дисменореї, який включає введення суб'єкту, що потребує такого лікування, комбінації певних кількостей (А) і (В), згідно з пунктом 20 або 21, які взяті разом є ефективними.
24. Фармацевтичний продукт, що містить комбінацію (А) і (В), згідно з пунктом 20 або 21 у вигляді комбінованого препарату для одночасного, окремого або послідовного застосування при лікуванні дисменореї (первинної або вторинної).
Текст
1. Сполука формули (І) 2 3 85692 4 атом кисню або 1 атом сірки і 1 або 2 атоми азоту, R6 представляє водень, С1-6алкіл, С3-6циклоалкіл, або представляє собою феніленову гр уп у; С3-6циклоалкеніл або С1-6алкілен-O-С1-6алкіл; Кільце А є необов'язково заміщеним одним або R7 представляє водень або С1-6алкіл; більшою кількістю замісників, вибраних з групи, що і представляє число від 0 до 6; містить С1-6алкіл, феніл або гідрокси; h представляє число, що дорівнює 0 або 1; Q представляє простий зв'язок або -N(R2)-; g представляє число, що дорівнює 0 або 1; R2 представляє водень або С1-6алкіл; j представляє число, що дорівнює 0 або 1; Z представляє -[O]e-[CH2]f-R3, фенільне кільце (неHet7 представляє 5- або 6-членне насичене, частобов'язково приконденсоване до бензольного кіково насичене або ароматичне гетероциклічне льця або Het2 і одержана група є необов'язково кільце, що має або (а) від 1 до 4 атомів азоту, (b) 1 заміщеною одним або більшою кількістю незалежатом кисню або 1 атом сірки, або (с) 1 атом кисню но вибраних замісників W) або Het3 (необов'язково або 1 атом сірки і 1 або 2 атоми азоту, необов'язприконденсоване до бензольного кільця або Het4 і ково заміщене R6 і/або R7, і/або оксогрупою. одержана група є необов'язково заміщеною одним 2. Сполука згідно з пунктом 1, де Х представляє або більшою кількістю незалежно вибраних заміс[СН2]а-R. ників W); 3. Сполука згідно з пунктом 2, де R представляє R3 представляє С 1-6алкіл (необов'язково заміщеHet. ний одним або більшою кількістю незалежно виб4. Сполука згідно з пунктом 1, де Y представляє раних замісників W), С3-6циклоалкіл, С3галоген. 5. Сполука згідно з пунктом 1, де V представляє 6циклоалкеніл, феніл (необов'язково заміщений одним або більшою кількістю незалежно вибраних простий зв'язок. замісників W), Het5 або NR4R5; 6. Сполука згідно з пунктом 1, де Q представляє е представляє число, що дорівнює 0 або 1; простий зв'язок. f представляє число від 0 до 6; 7. Сполука згідно з пунктом 1, де Кільце А предHet2 і Het5 незалежно представляють 5- або 6ставляє шестичленне кільце. членне насичене, частково насичене або арома8. Сполука згідно з пунктом 1, де Z представляє тичне гетероциклічне кільце, що має або (а) від 1 феніл. до 4 атомів азоту, (b) 1 атом кисню або 1 атом сір9. Сполука згідно з пунктом 1, де Z є заміщеним ки, або (с) 1 атом кисню або 1 атом сірки і 1 або 2 галогеном. атоми азоту, необов'язково заміщених одним або 10. Сполука згідно з пунктом 1, вибрана з наступбільшою кількістю замісників W; них: Het3 представляє 4-6-членне насичене, частково (3-хлорфеніл)-{4-[4-(4-хлорфеніл)-5-[1,2,3]триазолнасичене або ароматичне гетероциклічне кільце, 2-ілметил-4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}що має або (а) від 1 до 4 атомів азоту, (b) 1 атом метанон; кисню або 1 атом сірки, або (с) 1 атом кисню або 1 (4-хлорфеніл)-{4-[4-(4-хлорфеніл)-5-[1,2,3]триазолатом сірки і 1 або 2 атоми азоту, необов'язково 2-ілметил-4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}заміщених одним або більшою кількістю замісників метанон; W; (5-хлор-2-фторфеніл)-{4-[4-(4-хлорфеніл)-5Het4 представляє 6-членне ароматичне гетероцик[1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]лічне кільце, що має або (а) від 1 до 4 атомів азопіперидин-1-іл}-метанон; ту, (b) 1 атом кисню або 1 атом сірки, або (с) 1 {4-[4-(4-хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4Натом кисню або 1 атом сірки і 1 або 2 атоми азоту, [1,2,4]триазол-3-іл]-піперидин-1-іл}-(3,5необов'язково заміщених одним або більшою кільдифторфеніл)-метанон; кістю замісників W; {4-[4-(4-хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4НR4 і R5 незалежно представляють водень, С1[1,2,4]триазол-3-іл]-піперидин-1-іл}-(3-фторфеніл)метанон; 6алкіл, С 1-6алкілокси, С 3-8циклоалкіл (необов'язково приконденсований до С3-8циклоалкілу) або Het6; {4-[4-(4-хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4НR4 і R5 є необов'язково заміщеними одним або [1,2,4]триазол-3-іл]-піперидин-1-іл}-(2,3більшою кількістю замісників, вибраних незалежно дифторфеніл)-метанон; з групи, що містить С1-6алкіл, С1-6алкілокси, С3(3-хлор-2-фторфеніл)-{4-[4-(4-хлорфеніл)-5[1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]8циклоалкіл (необов'язково приконденсований до С3-8циклоалкілу) або феніл; піперидин-1-іл}-метанон; Het6 представляє 5- або 6-членне насичене, част(3-хлор-4-фторфеніл)-{4-[4-(4-хлорфеніл)-5ково насичене або ароматичне гетероциклічне [1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]кільце, що має або (а) від 1 до 4 атомів азоту, (b) 1 піперидин-1-іл}-метанон; атом кисню або 1 атом сірки, або (с) 1 атом кисню {4-[4-(4-хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4Набо 1 атом сірки і 1 або 2 атоми азоту, необов'яз[1,2,4]триазол-3-іл]-піперидин-1-іл}-(4ково заміщених одним або більшою кількістю замітрифторметилфеніл)-метанон; сників W; {4-[4-(4-хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4НW незалежно у кожному випадку представляє га[1,2,4]триазол-3-іл]-піперидин-1-іл}-(3логен, [O]g R6, SO2R6, SR6, SO 2NR6R7, [O]h [CH2]iCF3, трифторметилфеніл)-метанон; [O]jCHF2, феніл (необов'язково заміщений галоге{4-[4-(4-хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4Нном, С1-6алкілом або С1-6алкілокси), CN, фенокси [1,2,4]триазол-3-іл]-піперидин-1-іл}-(2(необов'язково заміщений галогеном), ОН, бензил, трифторметилфеніл)-метанон; NR6R7, NCOR 6, бензилокси, оксо, CONHR 6, NSO2R6R7, COR 6, С1-6алкілен-NCOR7, Het7; 5 85692 6 (3-хлор-5-фторфеніл)-{4-[4-(4-хлорфеніл)-5R3 представляє водень, С1-6алкіл, С3-6циклоалкіл [1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]або С1-6алкілен-О-С 1-6алкіл; піперидин-1-іл}-метанон; R4 представляє водень або С1-6алкіл; {4-[4-(4-хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4Ні представляє число від 0 до 6; [1,2,4]триазол-3-іл]-піперидин-1-іл}-(4h представляє число, що дорівнює 0 або 1; дифторметилфеніл)-метанон; g представляє число, що дорівнює 0 або 1; {4-[4-(4-хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4НHet2 представляє а 5- або 6-членну насичену, час[1,2,4]триазол-3-іл]-піперидин-1-іл}-(1Н-індазол-3тково ненасичену або ароматичну гетероциклічну іл)-метанон; груп у, що має або (а) від 1 до 4 атомів азоту, (b) 1 і їх фармацевтично прийнятні похідні. атом кисню або 1 атом сірки, або (с) 1 атом кисню 11. Сполука згідно з пунктом 1, що має формулу або 1 атом сірки і 1 або 2 атоми азоту, причому (I’) гетероциклічна група є необов'язково заміщеною R3 і/або R4, і/або оксигрупою. N N 12. Застосування сполуки згідно з будь-яким з пунX ктів 1-11 як медикаменту. N 13. Спосіб лікування захворювання у ссавця, A (I’) включаючи людину, при якому призначають антаN гоніст V1a і який включає введення терапевтичнo Z ефективної кількості сполуки, згідно з будь-яким з Y' O пунктів 1-11. Y , 14. Спосіб лікування тривоги, серцево-судинного або її фармацевтично прийнятне похідне, де: захворювання (включаючи стенокардію, атероХ представляє -[СH2] а-R або -[СН2]а-O-[СН2]b-R; склероз, гіпертонію, серцеву недостатність, наа представляє число від 0 до 6; бряк, гіпернатріємію), дисменореї (первинної і втоb представляє число від 0 до 6; ринної), ендометріозу, блювання (включаючи R представляє Н, СF3 або Het; закачування), затримки внутрішньоутробного розHet представляє а 5- або 6-членне гетероциклічне витку, запалення (включаючи ревматоїдний арткільце, що має або (а) від 1 до 4 атомів азоту, (b) 1 рит), міжменструального болю, передеклампсії, атом кисню або 1 атом сірки, або (с) 1 атом кисню передчасної еякуляції, передчасних пологів (недоабо 1 атом сірки і 1 або 2 атоми азоту; ношеної вагітності) і хвороби Рейно у ссавця, 1 Y представляє -[O]c-[CH2] d-R ; включаючи людину, який включає введення згадаY' представляє -[O]c-[CH2] d’-R1; ному суб'єкту, що страждає від такого захворюс і с' незалежно представляють число, що доріввання, терапевтичнo ефективної кількості сполуки нює 0 або 1; згідно з будь-яким з пунктів 1-11. d і d' незалежно представляють число від 0 до 6; 15. Спосіб лікування згідно з пунктом 13 або 14, де 1 1 R і R ' незалежно представляють Н, галоген, СF3 захворюванням є первинна або вторинна дисмеабо Het1; норея. 1 Het представляє 5- або 6-членне ненасичене ге16. Застосування сполуки згідно з будь-яким з пунтероциклічне кільце, що має або (а) від 1 до 4 ктів 1-11 для виготовлення медикаменту для лікуатомів азоту, (b) 1 атом кисню або 1 атом сірки, вання захворювання, при якому призначають анабо (с) 1 атом кисню або 1 атом сірки і 1 або 2 тагоніст V1a рецептора. атоми азоту; 17. Застосування сполуки згідно з будь-яким з пунКільце А представляє 5- або 6-членне насичене ктів 1-11 для виготовлення медикаменту для лікугетероциклічне кільце, що містить щонайменше вання тривоги, серцево-судинного захворювання один атом азоту; (включаючи стенокардію, атеросклероз, гіпертоZ представляє -[O]e-[CH2]f-R2, фенільне кільце (ненію, серцеву недостатність, набряк, гіпернатрієобов'язково приконденсоване до фенільного кільмію), дисменореї (первинної і вторинної), ендомеця або 5- чи 6-членного насиченого, частково нетріозу, блювання (включаючи закачування), насиченого або ароматичного гетероциклічного затримки внутрішньоутробного розвитку, запаленкільця, і/або необов'язково заміщене одним або ня (включаючи ревматоїдний артрит), міжменструбільшою кількістю незалежно вибраних замісників ального болю, передеклампсії, передчасної еякуW) або 6-членне ароматичне гетероциклічне кільляції, передчасних пологів (недоношеної це (необов'язково приконденсоване до фенільного вагітності) і хвороби Рейно. кільця або 6-членного ароматичного гетероцикліч18. Застосування згідно з пунктом 16 або 17, де ного кільця, і/або необов'язково заміщене одним захворюванням є первинна або вторинна дисмеабо більшою кількістю незалежно вибраних заміснорея. ників W); 19. Фармацевтична рецептура, що містить сполуку 2 R представляє С 1-6алкіл або С3-6циклоалкіл; згідно з будь-яким з пунктів 1-11 і фармацевтично е представляє число, що дорівнює 0 або 1; прийнятний наповнювач, розріджувач або носій. f представляє число від 0 до 6; 20. Комбінація (А) сполуки згідно з будь-яким з W представляє галоген, [O]g R3, SO2R3, SR3, пунктів 1-11 і (В) іншого фармакологічно активного 3 4 SO2NR R , [О] h[СH2]iСF3 , OCHF2, феніл, CN, феноінгредієнта. кси (необов'язково заміщений галогеном), ОН, 21. Комбінація згідно з пунктом 20, де (В) предста3 3 бензил, NCOR , бензилокси, окси, CONHR , вляє оральний контрацептив, інгібітор PDEV, інгі3 4 3 3 2 NSO2R R , COR , С1-6алкілен-NCOR , Het ; бітор СОХ, NО-донор або L-аргінін. 7 85692 8 22. Застосування комбінації згідно з пунктом 20 комбінації певних кількостей (А) і (В), згідно з пункабо 21 для виготовлення медикаменту для комбітом 20 або 21, які взяті разом є ефективними. нованої терапії шляхом одночасного, окремого або 24. Фармацевтичний продукт, що містить комбінапослідовного застосування при лікуванні дисменоцію (А) і (В), згідно з пунктом 20 або 21 у вигляді реї. комбінованого препарату для одночасного, окре23. Спосіб лікування дисменореї, який включає мого або послідовного застосування при лікуванні введення суб'єкту, що потребує такого лікування, дисменореї (первинної або вторинної). Даний винахід стосується похідних триазолу та способів їх одержання, проміжних сполук, що застосовуються при їх одержанні, композицій, що містять такі похідні та їх застосування. Похідні триазолу, відповідно до даного винаходу, є антагоністами вазопресину. Зокрема, вони є антагоністами V1a рецептора і мають деяке терапевтичне застосування, особливо при лікуванні дисменореї (первинної та вторинної). Існує висока незадоволена потреба в області менструальних розладів і, за оцінками спеціалістів, до 90% всіх жінок, що мають менструацію, в деякій мірі страждають від цих розладів. До 42% жінок пропускають роботу або інші види діяльності через менструальний біль, в США в результаті цього втрачається приблизно 600 мільйонів робочих годин на рік [Coco, A. S. (1999). Primary Dysmenorrhoea. [Review] [30 refs]. American Family Physician, 60, 489-96]. Менструальний біль у нижній частині черевної порожнини викликається міометріальною гіперфункцією і зниженим матковим кровотоком. Ці патофізіологічні зміни призводять до болю в животі, що поширюється на спину і ноги. Це може призводити до відчуття нудоти у жінок, головного болю і безсоння. Цей стан називають дисменореєю, і він може бути класифікований або як первинна, або як вторинна дисменорея. Первинну дисменорею діагностують, коли не можна ідентифікувати ніякого відхилення, що викликає такий стан. Від цього страждає до 50 % населення жіночої статі [Coco, A. S. (1999). Primary Dysmenorrhoea. [Review] [30 refs]. American Family Physician, 60, 489-96; Schroeder, B. & Sanfilippo, J. S. (1999). Dysmenorrhoea and pelvic pain in adolescents. [Review] [78 refs]. Pediatric Clinics of North America, 46, 555-71]. Коли присутній основний гінекологічний розлад, такий як ендометріоз, тазове запальне захворювання (PID), фіброзні пухлини або ракові утворення, діагностують вторинну дисменорею. Вторинна дисменорея діагностується тільки приблизно у 25% жінок, що страждають від дисменореї. Дисменорея може проходити сумісно з менорагією, що пояснює приблизно до 12% звернень до гінекологічних амбулаторних закладів. В даний час, жінок, що страждають від первинної дисменореї лікують, використовуючи нестероїдні протизапальні засоби (NSAID) або оральні контрацептивні пігулки. У випадках вторинної дисменореї можуть бути вжиті хірургічні заходи для усунення основного гінекологічного розладу. Жінки, що страждають від дисменореї, мають циркуляторні рівні вазопресину більші за ті, що спостерігалися у здорових жінок у той же самий час менструального циклу. Запобігати дисменореї можна інгібуванням фармакологічної дії вазопресину в матковому рецепторі вазопресину. Сполуки представленого винаходу є потенціально корисними для лікування широкого спектра захворювань, зокрема агресії, хвороби Альцгеймера, нервово-психічної анорексії, тривоги, тривожного розладу, астми, атеросклерозу, аутизму, серцевосудинного захворювання (включаючи стенокардію, атеросклероз, гіпертонію, серцеву недостатність, набряк, гіпернатремію), катаракти, захворювання центральної нервової системи, цереброваскулярної ішемії, цирозу, когнітивного розладу, хвороби Кушинга, депресії, цукрового діабету, дисменореї (первинної та вторинної), блювоти (включаючи закачування), ендометріозу, шлунково-кишкового захворювання, глаукоми, гінекологічного захворювання, серцевого захворювання, затримки внутрішньоутробного розвитку, запалення (включаючи ревматоїдний артрит), ішемії, ішемічного захворювання серця, пухлини легень, розладу сечовипускання, міжменструального болю, новоутворення, ниркової токсичності, не-інсулінзалежного діабету, ожиріння, обсесивно/компульсивного розладу, окулярної гіпертонії, передеклампсії, передчасної еякуляції, передчасних пологів (недоношеної вагітності), легеневих захворювань, хвороби Рейно, захворювання нирок, ниркової недостатності, чоловічої або жіночої статевої дисфункції, септичного шоку, розладу сну, ушкодження спинного мозку, тромбозу, інфекції сечостатевого тракту або сечокаменевого захворювання. Особливо представляють інтерес наступні захворювання або розлади: тривога, серцево-судинне захворювання (включаючи стенокардію, атеросклероз, гіпертонію, серцеву недостатність, набряк, гіпернатремію), дисменорея (первинна і вторинна), ендометріоз, блювота (включаючи закачування), затримка внутрішньоутробного розвитку, запалення (включаючи ревматоїдний артрит), міжменструальний біль, передеклампсія, передчасна еякуляція, передчасні пологи (недоношена вагітність) і хвороба Рейно. Сполуки відповідно до винаходу і їх фармацевтично прийнятні солі і сольвати мають перевагу, оскільки вони є селективними інгібіторами V1a рецептора (і тому, ймовірно, мають незначну побічну дію), можуть мати більш короткий початок дії, більш сильну дію, довшу тривалість дії, більшу біодоступність або можуть мати інші, більш бажані 9 85692 10 властивості порівняно до сполук попереднього вибраних замісників W), С3-6циклоалкіл, С3рівня техніки. 6циклоалкеніл, феніл (необов'язково заміщений Представлений винахід забезпечує сполуку одним або більшою кількістю незалежно вибраних формули (І), замісників W), Het5 або NR4R5; e представляє число, що дорівнює 0 або 1; f представляє число від 0 до 6; Het2 і Het5 незалежно представляють 5- або 6членне насичене, частково насичене або ароматичне гетероциклічне кільце, що має або (а) від 1 до 4 атомів азоту, (b) 1 атом кисню або 1 атом сірки, або (с) 1 атом кисню або 1 атом сірки і 1 або 2 атоми азоту, необов'язково заміщених одним або більшою кількістю замісників W; Het3 представляє 4-6-членне насичене, частково насичене або ароматичне гетероциклічне кільце, що має або (а) від 1 до 4 атомів азоту, (b) 1 атом кисню або 1 атом сірки, або (с) 1 атом кисню або її фармацевтично прийнятне похідне, де: X представляє -[CH2]a-R або -[CH2]a-O-[CH 2] bабо 1 атом сірки і 1 або 2 атоми азоту, необов'язково заміщених одним або більшою кількістю заміR; сників W; а представляє число від 0 до 6; Het4 представляє 6-членне ароматичне гетеb представляє число від 0 до 6; роциклічне кільце, що має або (а) від 1 до 4 атомів R представляє Н, CF3 або Het; Het представляє 5- або 6-членне насичене, азоту, (b) 1 атом кисню або 1 атом сірки, або (с) 1 атом кисню або 1 атом сірки і 1 або 2 атоми азоту, частково насичене або ароматичне гетероциклічне необов'язково заміщених одним або більшою кількільце, що має або (а) від 1 до 4 атомів азоту, (b) 1 кістю замісників W; атом кисню або 1 атом сірки, або (с) 1 атом кисню R4 і R5 незалежно представляють водень, С1-6 або 1 атом сірки і 1 або 2 атоми азоту, необов'язково заміщене одним або більшою кількістю незаалкіл, С1-6 алкілокси, С3-8 циклоалкіл (необов'язково приконденсований до С3-8 циклоалкілу) або лежно вибраних замісників W; Het6; Υ представляє один або більшу кількість заміR4 і R5 є необов'язково заміщеним одним або сників, незалежно вибраних з групи, що містить 1 більшою кількістю замісників, вибраних незалежно [O]c-[CH2] d-R , які можуть бути однаковими, або різними у кожному випадку; з групи, що містить С1-6 алкіл, С1-6 алкілокси, С3-8 циклоалкіл (необов'язково приконденсований до с у кожному випадку незалежно представляє С3-8 циклоалкілу), або феніл; число, що дорівнює 0 або 1; Het6 представляє 5- або 6-членне насичене, d у кожному випадку незалежно представляє частково насичене або ароматичне гетероциклічне число від 0 до 6; R1 у кожному випадку незалежно представляє кільце, що має або (а) від 1 до 4 атомів азоту, (b) 1 атом кисню або 1 атом сірки, або (с) 1 атом кисню Н, галоген, CF3, CN або Het1; або 1 атом сірки і 1 або 2 атоми азоту, необов'язHet1 у кожному випадку незалежно представково заміщених одним або більшою кількістю заміляє 5- або 6-членне ненасичене гетероциклічне сників W; кільце, що має або (а) від 1 до 4 атомів азоту, (b) 1 атом кисню або 1 атом сірки, або (с) 1 атом кисню W незалежно у кожному випадку представляє галоген, [O]g R6, SO2R 6, SR6 , SO2NR6R7, або 1 атом сірки і 1 або 2 атоми азоту; [O]h [CH2]iCF3, [O]jCHF2 , феніл (необов'язково заміV представляє простий зв'язок або -О-; щений галогеном, С1-6 алкілом або С1-6 алкілокси), Кільце А представляє 5-7-членне насичене геCN, фенокси (необов'язково заміщений галогетероциклічне кільце, що має або (а) від 1 до 4 атомів азоту, (b) 1 атом кисню або 1 атом сірки, ном), ОН, бензил, NR6R7, NCOR 6, бензилокси, оксо, CONHR6, NSO2R6R7, COR6, С1-6алкілен-NCOR7, або (с) 1 атом кисню або 1 атом сірки і 1 або 2 Het7; атоми азоту, або представляє собою феніленову R6 представляє водень, С1-6алкіл, С3груп у; Кільце А є необов'язково заміщеним одним або більшою кількістю замісників, вибраних з гру6циклоалкіл, С 3-6 циклоалкеніл або С 1-6алкілен-Опи, що містить С 1-6 алкіл, феніл або гідрокси; С1-6алкіл; R7 представляє водень або С1-6алкіл; Q представляє простий зв'язок або -N(R2)-; 2 і представляє число від 0 до 6 R представляє водень або С1-6 алкіл; h представляє число, що дорівнює 0 або 1; Ζ представляє -[O]e-[CH2]f-R3 , фенільне кільце g представляє число, що дорівнює 0 або 1; (необов'язково приконденсоване до бензольного кільця або Het2 і одержана група є необов'язково j представляє число, що дорівнює 0 або 1; Het7 представляє 5- або 6-членне насичене, заміщеною одним або більшою кількістю незалеж3 частково насичене або ароматичне гетероциклічне но вибраних замісників W), або Het (необов'язкокільце, що має або (а) від 1 до 4 атомів азоту, (b) 1 во приконденсоване до бензольного кільця або атом кисню або 1 атом сірки, або (с) 1 атом кисню Het4 і одержана група є необов'язково заміщеною одним або більшою кількістю незалежно вибраних або 1 атом сірки і 1 або 2 атоми азоту, необов'язково заміщене R6 і/або R7 і/або оксогрупою. замісників W); 3 Альтернативне втілення даного винаходу заR представляє С 1-6алкіл (необов'язково замібезпечує сполуку формули (I'): щений одним або більшою кількістю незалежно 11 85692 або її фармацевтично прийнятне похідне, де: X представляє -[CH2]a-R або -[CH2]a-O-[CH 2] bR; а представляє число від 0 до 6; b представляє число від 0 до 6; R представляє Н, CF3 або Het; Het представляє а 5- або 6-членне гетероциклічне кільце, що має або (а) від 1 до 4 атомів азоту, (b) 1 атом кисню або 1 атом сірки, або (с) 1 атом кисню або 1 атом сірки і 1 або 2 атоми азоту; Υ представляє -[O]c-[CH2] d-R1; Υ' представляє -[O]c-[CH2] d-R1; с і с' незалежно представляють число, що дорівнює 0 або 1; d і d' незалежно представляють число від 0 до 6; R1 і R1 незалежно представляють Н, галоген, CF3 або Het1; Het1 представляє 5- або 6-членне ненасичене гетероциклічне кільце, що має або (а) від 1 до 4 атомів азоту, (b) 1 атом кисню або 1 атом сірки, або (с) 1 атом кисню або 1 атом сірки і 1 або 2 атоми азоту; Кільце А представляє 5- або 6-членне насичене гетероциклічне кільце, що містить щонайменше один атом азоту; Ζ представляє -[O]e-[CH2]f-R2 , фенільне кільце (необов'язково приконденсоване до фенільного кільця або 5- чи 6-членного насиченого, частково ненасиченого або ароматичного гетероциклічного кільця, і/або необов'язково заміщене одним або більшою кількістю незалежно вибраних замісників W), або 6-членне ароматичне гетероциклічне кільце (необов'язково приконденсоване до фенільного кільця або 6-членного ароматичного гетероциклічного кільця, і/або необов'язково заміщене одним або більшою кількістю незалежно вибраних замісників W); R2 представляє С 1-6 алкіл або С 3-6 циклоалкіл; e представляє число, що дорівнює 0 або 1; f представляє число від 0 до 6; W представляє галоген, [O]g R3, SO2R3 , SR3 , SO2NR3R4, [O] h[CH2]iCF3 , OCHF2, феніл, CN, фенокси (необов'язково заміщений галогеном), ОН, бензил, NCOR 3, бензилокси, окси, CONHR 3, NSO2R3R4, COR 3, С1-6алкілен-NCOR3, Het2; R3 представляє водень, С1-6алкіл, С36циклоалкіл або С 1-6алкілен-О-С 16алкіл; R4 представляє водень або С1-6алкіл; і представляє число від 0 до 6 h представляє число, що дорівнює 0 або 1; g представляє число, що дорівнює 0 або 1; 12 Het2 представляє а 5- або 6-членну насичену, частково ненасичену або ароматичну гетероциклічну гр упу, що має або (а) від 1 до 4 атомів азоту, (b) 1 атом кисню або 1 атом сірки, або (с) 1 атом кисню або 1 атом сірки і 1 або 2 атоми азоту, причому гетероциклічна група є необов'язково заміщеною R3 і/або R4 і/або оксигрупою. У преставлених визначеннях, галоген означає фтор, хлор, бром або йод. Алкільні, алкіленові та алкілоксигрупи, що містять необхідну кількість атомів вуглецю, можуть бути нерозгалуженими або розгалуженими, прикладами алкілу є метил, етил, н-пропіл, ізо-пропіл, н-бутил, ізо-бутил, вторбутил та трет-бутил. Прикладами алкілокси є метокси, етокси, н-пропокси, ізо-пропокси, н-бутокси, ізо-бутокси, втор-бутокси і трет-бутокси. Приклади алкілену включають метилен, 1,1-етилен, 1,2етилен, 1,1-пропілен, 1,2-пропілен, 1,3-пропілен і 2,2-пропілен. Het представляє гетероциклічну групу, приклади якої включають тетрагідрофураніл, тетрагідротіофеніл, піролідиніл, тетрагідропіраніл, тетрагідротіопіраніл, піперидиніл, 1,4-діоксаніл, 1,4-оксатіаніл, морфолініл, 1,4-дітіаніл, піперазиніл, 1,4-азатіаніл, 3,4-дигідро-2Н-піраніл, 5,6дигідро-2Н-піраніл, 2Н-піраніл, 1,2,3,4тетрагідропіридиніл, 1,2,5,6-тетрагідропіридиніл, піроліл, фураніл, тіофеніл, піразоліл, імідазоліл, ізоксазоліл, оксазоліл, ізотіазоліл, тіазоліл, 1,2,3триазоліл, 1,3,4-триазоліл, 1-окса-2,3-діазоліл, 1окса-2,4-діазоліл, 1-окса-2,5-діазоліл, 1-окса-3,4діазоліл, 1-тіа-2,3-діазоліл, 1-тіа-2,4-діазоліл, 1-тіа2,5-діазоліл, 1-тіа-3,4-діазоліл, тетразоліл, піридиніл, піридазиніл, піримідиніл і піразиніл. Переважною є сполука, де X представляє СН2ОСН3. Більш переважною є сполука, в якій X представляє -[CH2]aR. Переважною є сполука, де а представляє число від 0 до 5. Більш переважною є сполука, в якій а представляє число від 0 до 4. Ще більш переважною є сполука, в якій а представляє число від 0 до 3. Ще більш переважною є сполука, в якій а представляє число від 0 до 2. Більш переважною є сполука, в якій а представляє число 1. Переважною є сполука, де R представляє Н. Більш переважною є сполука, в якій R представляє Het. Ще більш переважною є сполука, в якій R представляє триазоліл. Переважною є сполука, де Υ представляє один або два замісники. Більш переважною є сполука, в якій Υ представляє єдиний замісник. Переважною є сполука, де Υ представляє галоген. Більш переважною є сполука, в якій Υ представляє хлор і/або фтор. Переважною є сполука, де V представляє простий зв'язок. Переважною є сполука, де Q представляє простий зв'язок. Більш переважною є сполука, в якій обидва замісники V і Q представляють простий зв'язок. Переважною є сполука, де Кільце А містить 2 атоми азоту. Більш переважною є сполука, в якій Кільце А містить 1 атом азоту. Переважною є сполука, де Кільце А представляє 5-членне кільце. Більш переважною є сполука, в якій Кільце А представляє 6-членне кільце. Ще більш переважною є сполука, де Кільце А представляє піперидинілен. 13 85692 14 Переважною є сполука, де Кільце А приєднане {4-[4-(4-Хлорфеніл)-5-[1,2,3]триазол-2-ілметилдо V через атом азоту. Більш переважною є спо4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}-(1Н-індазоллука, в якій Кільце А приєднане до Q через атом 3-іл)-метанон; азоту. і їх фармацевтично прийнятні похідні. Переважною є сполука, де Кільце А приєднане Фармацевтично прийнятні похідні сполук фордо обох замісників Q і V через атом азоту. мули (І) відповідно до винаходу включають солі, Переважною є сполука, де Ζ представляє Het3. сольвати, комплекси, поліморфи, проліки, стереоHet3 може представляти необов'язково заміщену ізомери, геометричні ізомери, таутомерні форми і груп у, що містить індазоліл, індоліл, інденіл, пірасполуки формули (І), мічені ізотопами. Переважно, золіл, піперидиніл, піридиніл, піримідиніл, піроліл, фармацевтично прийнятні похідні сполук формули тіазоліл, бензотієніл, бензотіазоліл, хіноліл, бензо(І) включають солі, сольвати, естери і аміди сполук ксазиніл, ізоксазоліл, імідазоліл, фурил, бензофуформули (І). Більш переважно, фармацевтично рил, циноліл, морфоліл, хроменіл, або їх похідні. прийнятними похідними сполук формули (І) є солі і Більш переважною є сполука, в якій Ζ представляє сольвати. феніл. Фармацевтично прийнятні солі сполук формуПереважною є сполука, де Ζ є моно- або дили (І) включають кислотноадитивні і основні солі. заміщеним. Більш переважною є сполука, в якій Ζ Придатні кислотноадитивні солі утворюються з є монозаміщеним. кислот, які утворюють нетоксичні солі. Прикладами Переважною є сполука, де Ζ заміщений триє ацетат, аспартат, бензоат, безилат, бікарбофторметилом. Більш переважною є сполука, в якій нат/карбонат, бісульфат, борат, камсилат, цитрат, Ζ заміщено галогеном. Більш переважною є споедизилат, езилат, форміат, фумарат, глуцептат, лука, в якій Ζ заміщений хлором і/або фтором. глюконат, глюкуронат, гексафторфосфат, гібензат, Особливо переважними сполуками винаходу є гідрохлорид/хлорид, гідробромід/бромід, гідройосполуки, наведені нижче у Прикладах і їх фармадид/йодид, ізетіонат, D- і L-лактат, малат, малеат, цевтично прийнятні солі, зокрема: малонат, мезилат, метилсульфат, на фтилат, 2(3-Хлорфеніл)-{4-[4-(4-хлорфеніл)-5напсилат, нікотинат, нітрат, оротат, оксалат, паль[1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]мітат, пальмоат, фосфат, гідрофосфат, дигідропіперидин-1-іл}-метанон; фосфа т, са харат, стеарат, сукцинат, сульфат, D- і (4-Хлорфеніл)-{4-[4-(4-хлорфеніл)-5L-тартрат, тозилат і трифторацетат. Особливо [1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]придатною сіллю є безплатне похідне сполук, відпіперидин-1-іл}-метанон; повідно до даного винаходу. (5-Хлор-2-фторфеніл)-[4-[4-{4-хлорфеніл)-5Придатні основні солі одержують з викорис[1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]танням основ, які утворюють нетоксичні солі. Припіперидин-1-іл}-метанон; кладами є солі алюмінію, аргініну, бензатину, {4-[4-(4-Хлорфеніл)-5-[1,2,3]триазол-2-ілметилкальцію, холіну, діетиламіну, діоламіну, гліцину, 4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}-(3,5лізину, магнію, меглуміну, оламіну, калію, натрію, дифторфеніл)-метанон; трометаміну і цинку. {4-[4-(4-Хлорфеніл)-5-[1,2,3]триазол-2-ілметилДля ознайомлення з придатними солями, ди4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}-(3віться ["Handbook of Pharmaceutical Salts: фтор феніл)-метанон; Properties, Selection, and Use" авторів Stahl і {4-[4-(4-Хлорфеніл)-5-[1,2,3]триазол-2-ілметилWermuth, Wiley-VCH, Weinheim, Germany, 2002)]. 4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}-(2,3Фармацевтично прийнятну сіль сполуки фордифторфеніл)-метанон; мули (І) можна легко одержати змішуванням разом (3-Хлор-2-фторфеніл)-{4-[4-(4-хлорфеніл)-5розчинів сполуки формули (І) і бажаної кислоти [1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]або солі, як це необхідно. Сіль можна осадити з піперидин-1-іл}-метанон, розчину і зібрати фільтруванням або можна одер(3-Хлор-4-фторфеніл)-{4-[4-(4-хлорфеніл)-5жати випарюванням розчинника. Ступінь іонізації в [1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]солі може змінюватись від повністю іонізованої до піперидин-1-іл}-метанон; майже неіонізованої. {4-[4-(4-Хлорфеніл)-5-[1,2,3]триазол-2-ілметилСполуки винаходу можуть існувати як в несо4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}-(4льватованій, так і в сольватованій формах. Термін трифторметилфеніл)-метанон; "сольват" використовується тут для опису молеку{4-[4-(4-Хлорфеніл)-5-[1,2,3]триазол-2-ілметиллярного комплексу, що містить сполуку винаходу і 4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}-(3одну або більшу кількість фармацевтично прийнятрифторметилфеніл)-метанон; тних молекул розчинника, наприклад, етанолу. {4-[4-(4-Хлорфеніл)-5-[1,2,3]триазол-2-ілметилТермін "гідрат" використовується, коли згаданим 4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}-(2розчинником є вода. трифторметилфеніл)-метанон; Включеними в межі винаходу є комплекси, такі (3-Хлор-5-фторфеніл)-{4-[4-(4-хлорфеніл)-5як клатрати, комплекси включення лікарський за[1,2,3]триазол-2-ілметил-4Н-[1,2,4]триазол-3-іл]сіб-хазяїн, в яких, на відміну від згаданих вище піперидин-1-іл}-метанон; сольватів, лікарський засіб і хазяїн присутні в сте{4-[4-(4-Хлорфеніл)-5-[1,2,3]триазол-2-ілметилхіометричній або нестехіометричній кількості. Та4Н-[1,2,4]триазол-3-іл]-піперидин-1-іл}-(4кож включеними є комплекси лікарського засобу, дифторметилфеніл)-метанон; що містять два або більше органічних і/або неорганічних компонентів, які можуть бути в сте хіометричній або нестехіометричній кількостях. Одержані 15 85692 16 комплекси можуть бути іонізованими, частково на ізомерія ("таутомерія"). Звідси випливає, що іонізованими або неіонізованими. Для ознайомодна сполука може проявляти більш ніж один тип лення з такими комплексами, дивіться [J Pharm ізомерії. Sci, 64 (8), 1269-1288, Haleblian (August 1975)]. Всі стереоізомери, геометричні ізомери і тауТут далі всі посилання на сполуки формули (І) томерні форми сполук формули (І), включаючи і їх фармацевтично прийнятні похідні включають сполуки, що проявляють більш ніж один тип ізомепосилання на їх солі, сольвати і комплекси і на рії, і суміші однієї або більшої кількості таких спосольвати і комплекси їх солей. лук є включеними в рамки представленого винаСполуками винаходу є сполуки формули (І), як ходу. Також включеними є кислотноадитивні або було визначено раніше, їх поліморфи, пролікарські основні солі, де протиіоном є оптичноактивна резасоби і ізомери (включаючи оптичні, геометричні i човина, наприклад, D-лактат або L-лізин, або ратаутомерні ізомери), як тут визначено далі і сполуцемічна суміш, наприклад, DL-тартрат або DLки формули (І) мічені ізотопами. аргінін. Як вказано, винахід включає всі поліморфи Цис/транс ізомери можна розділити за допосполук формули (І), як тут визначено раніше. могою звичайних методик добре відомих спеціаліТакож в межі рамок винаходу попадають так сту в цій галузі, таких, як наприклад, дробна крисзвані "проліки" сполук формули (І). Таким чином, талізація і хроматографія. деякі похідні сполук формули (І), які самі по собі Звичайними методами одержання/виділення мають малу або не мають зовсім фармакологічної окремих енантіомерів є хіральний синтез з придаактивності, при введенні всередину або нанесенні тних оптично чистих ви хідних сполук або роздіна тіло можуть перетворюватись у сполуки форлення рацемату (або рацемічної солі, або похідномули (І), що мають бажану активність, наприклад, го рацемату) використовуючи, наприклад, хіральну під дією гідролітичного розщеплення. Такі похідні високоефективну рідинну хроматографію (ВЕРХ). відносяться до "проліків". Додаткову інформацію Альтернативно, рацемат (або рацемічний попо використанню проліків можна знайти в ["Proпередник) може вступати в реакцію з придатною drugs as Novel Delivery Systems, Vol. 14, ACS оптичноактивною сполукою, наприклад, спиртом, Symposium Series (T Higuchi i W Stella) і або, у випадку, коли сполука формули (І) містить "Bioreversible Носійв in Drug Design", Pergamon кислотний або основний замісник, кислотою або Press, 1987 (ed. Ε Β Roche, American основою, такою як винна кислота або 1Pharmaceutical Association)]. фенілетиламін. Одержану діастереомерну суміш Проліки у відповідності з винаходом можуть, можна розділити хроматографічно і/або дробною наприклад, бути одержані шляхом заміни відповікристалізацією і перетворити один або обидва дних функціональних груп присутніх в сполуках діастереомери у відповідний чистий енантіомер(и) формули (І) деякими замісниками відомими спецівикористовуючи засоби добре відомі спеціалісту в алістам в цій галузі як "прозамісники" як описано, цій галузі. наприклад, у ["Design of Prodrugs", H Bundgaard Хіральні сполуки винаходу (і їх хіральні попе(Elsevier, 1985)]. редники) можна одержати в енантіомерно збагаДеякими прикладами пролікарських засобів у ченій формі використовуючи хроматографію, тивідповідності з винаходом є: пово ВЕРХ, на асиметричній смолі з рухомою (і) естер, коли сполука формули (І) містить кафазою, що представляє собою вуглеводень, типорбоксильну груп у (-СООН), наприклад, заміна во, гептан або гексан, який містить від 0 до 50% атому водню С1-8алкілом; ізопропанолу, типово від 2 до 20% і від 0 до 5% (іі) етер, коли сполука формули (І) містить алкіламіну, типово 0,1% діетиламіну. Контцентруспиртову гр упу (-ОН), наприклад, заміна атому ванням елюату одержують збагачену суміш. водню С 1-6алканоїлоксиметилом; і Стереоізомерні конгломерати можна розділити (ііі) амід, коли сполука формули (І) містить пеза допомогою звичайних методик відомих спеціарвинну або вторинну аміногрупу (-NH2 або -NHR, лісту в цій галузі - дивіться, наприклад, ["Stereochemistry of Organic Compounds" автора Е. де R¹H), наприклад, заміна одного або обох водL. Eliel (Wiley, New York, 1994)]. нів С 1-10алканоїлом. Представлений винахід включає всі фармацеІнші приклади груп у відповідності з наведенивтично прийнятні мічені ізотопами сполуки формуми прикладами і прикладами інших типів проліків ли (І), де один або більша кількість атомів замінеможна знайти у згаданих ви ще посиланнях. На кінець, деякі сполуки формули (І) самі по на атомами, що мають той самий атомний номер, але атомну масу або масове число, що відрізнясобі можуть виступати як проліки інших сполук ється від атомної маси або масового числа, яке формули (І). зазвичай зустрічається у природі. Також в межі рамок винаходу потрапляють Прикладами ізотопів придатних для включенметаболіти сполук формули (І), що утворюються in vi vo. ня в сполуки винаходу є ізотопи водню, такі як 2Н і 3 Н, вуглецю, такі як 11С, 13С і 14С, азоту, такі як 13N і Сполуки формули (І), що містять один або бі15 N, кисню, такі як 15O, 17O і 18 O, фосфору, такий як льшу кількість асиметричних атомів вуглецю мо32 Р і сірки, такий як 35S, фтору, такий як 18F, йоду, жуть існувати як два або більше стереоізомерів. такі як 123І і 125І і хлору, такий як 36СІ. Коли сполука формули (І) містить алкенільну або алкеніленову гр упу, можливе утворення геометріДеякі мічені ізотопами сполуки формули (І), наприклад, ті що включають радіоактивний ізотоп, чних цис/транс (або Z/E) ізомерів. Коли сполука є корисними для дослідження розподілення лікармістить, наприклад, кето або оксимну групу або ського засобу і/або субстрату в тканинах. Радіоакароматичний замісник, може мати місце таутомер 17 85692 18 тивні ізотопи тритію, тобто 3Н і вуглецю-14, тобто V1a і полягає у введенні ссавцю терапевтично 14 С, є особливо корисними для цих цілей з огляду ефективної кількості сполуки формули (І), або її на легкість їх включення і легкість детектування. фармацевтично прийнятної солі або сольвату. Заміщення більш важкими ізотопами, такими Зокрема, сполуки формули (І) є корисними при як дейтерій, тобто 2Н, може забезпечувати деякі лікуванні тривоги, серцево-судинної хвороби терапевтичні переваги обумовлені збільшенням (включаючи стенокардію, атеросклероз, гіпертенметаболітичної стабільності, наприклад, збільзію, серцеву недостатність, набряки, гіпернатрешенням часу напіврозкладу in vivo або зменшенмію), дисменорею (первинну і вторинну), ендометням необхідної дози і тому може бути переважним ріоз, блювання (включаючи закачування), в деяких випадках. затримку внутрішньоутробного розвитку, запаленЗаміщення позитронно-активними ізотопами, ня (включаючи ревматоїдний артрит), міжменструтакими як 11С, 18F, 15 O і 13N, може бути корисним в альний біль, передеклампсію, передчасну еякулядослідженнях позитронноемісійної топографії цію, передчасні пологи (недоношену вагітність), (ПЕТ) для визначення зв'язування субстрату з реабо хворобу Рейно. Навіть більш особливо, вони є цептором. корисними при лікуванні дисменореї (первинної Мічені ізотопами сполуки формули (І) загалом або вторинної). одержують використовуючи звичайні методики, Ще одним аспектом даного винаходу є застовідомі спеціалістам в цій галузі або використовуюсування сполуки формули (І), або її фармацевтиччи процеси аналогічні тим, що описані в супровідно прийнятної солі або сольвату у виго товленні них Прикладах і Препаративних Прикладах викомедикаменту для лікування розладів, при яких ристовуючи прийнятні мічені ізотопами реагенти призначають антагоніст V1 а рецептора. замість не мічених реагентів, які використовували Всі сполуки формули (І) можна одержати вираніше. користовуючи методики, наведені у загальних споФармацевтично прийнятними сольватами у собах, наведених нижче, або за допомогою конквідповідності з винаходом є сполуки, в яких крисретних методик описаних у розділах Приклади і талізаційний розчинник може бути ізотопзаміщеПрепаративні Приклади, або використовуючи їх ним, наприклад, D2O, d6-ацетон, d6-ДМСО. загальновідомі модифікації. Даний винахід також Сполуки відповідно до винаходу є корисними у включає будь-яку з цих методик, а саме одну чи терапії. Отже, ще одним аспектом даного винахобільшу їх кількість для одержання сполук формули ду є застосування сполуки формули (І), або її фа(І), а також будь-які нові проміжні сполуки, що замацевтичної солі, або сольвату як медикаменту. стосовуються в цих процесах. Сполуки відповідно до винаходу проявляють Якщо не вказано інше, то в даному тексті вжиактивність як антагоністи V1a. Зокрема вони є ковані наступні позначення: рисними при лікуванні хворобливих станів, до яких WSCDI означає 1-(3-диметиламінопропіл)-3входять агресивність, хвороба Альцгеймера, неретилкарбодііміду гідрохлорид, DCC означає Ν,Ν'вово-психічна анорексія, тривожний стан, тривождициклогексилкарбодіімід, НОАТ означає 1ний розлад, астма, атеросклероз, аутизм, серцевогідрокси-7-азабензотриазол і НОВТ означає 1судинна хвороба (включаючи стенокардію, атерогідроксибензотриазолгідрат; склероз, гіпертензію, серцеву недостатність, наРуВОРÒ означає гексафторфосфат бензотрибряки, гіпернатремію), катаракта, захворювання азол-1-ілокситріс-піролідинфосфонію, РуВrОРÒ центральної нервової системи, цереброваскулярозначає гексафторфосфат бром-трісна ішемія, цироз, когнітивний розлад, хвороба Купіролідинфосфонію і HBTU означає гексафторфошинга, депресія, цукровий діабет, дисменорея сфат О-бензотриазол-1-іл-N,N,N',N'(первинна і вторинна), блювання (включаючи затетраметилуронію; качування), ендометріоз, захворювання шлунковоmCPBA означає мета-хлорпербензойну кислокишкового тракту, гла укома, гінекологічне захвоту, АсОН означає оцтову кислоту, НСІ означає рювання, серцеве захворювання, затримка внутхлорводневу кислоту, TFA означає трифтороцтову рішньоутробного розвитку, запалення (включаючи кислоту і p-TSA означає пара-толуолсульфонову ревматоїдний артрит), ішемія, ішемічне захворюкислоту; вання серця, пухлина легень, розлад сечовипусEt3N означає триетиламін і NMM означає Nкання, міжменструальний біль, новоутворення, метилморфолін; ниркова токсичність, не-інсулінзалежний діабет, K2СО3 означає карбонат калію і KОt-Вu ознаожиріння, обсесивно/компульсивний розлад, окучають калію трет-бутоксид; лярна гіпертонія, передеклампсія, передчасна еяNaOH, KОН і LiOH означають відповідно гідрокуляція, передчасні пологи (недоношена вагітксид натрію, калію і літію; ність), легеневі захворювання, хвороба Рейно, Вос означає трет-бутоксикарбоніл і CBz озназахворювання нирок, ниркова недостатність, чочає бензилоксикарбоніл; ловіча або жіноча статева дисфункція, септичний PTFE означає політетрафторетан; шок, розлад сну, ушкодження спинного мозку, МeІ означає метилйодид; тромбоз, інфекція сечостатевого тракту або сечоMeTosylate означає метил паракаменева хвороба. Предметом особливого зацікатолуолсульфонат; влення є дисменорея (первинна або вторинна), МеОН означає метанол, EtOH означає етанол більш особливо, первинна дисменорея. і н-BuOH означає н-бутиловий спирт; Отже, ще одним аспектом даного винаходу є EtOAc означає етилацетат, MeCN означає спосіб лікування розладу у ссавця, включаючи ацетонітрил, ТГФ означає тетрагідрофуран, ДМСО людину, який потребує призначення антагоніста означає диметилсульфоксид, ДХМ означає дихло 19 85692 20 рметан, ДМФА означає Ν,Ν-диметилформамід, замісники V, X, Q, Ζ, Υ, Υ', Het, Het1, та Het2 є таNMP означає N-метил-2-піролідон і ДМА означає кими, як визначено вище для сполук формули (І). диметилацетамід; Коли Q представляє NR2, або Q представляє проMe означає метил, Et означає етил, СІ означає стий зв'язок, приєднаний до атома азоту всередині хлор і ОН означає гідрокси; Кільця А, тоді сполуки формули (І) можуть бути cat означає каталізатор або каталітичний. одержані як це представлено на Схемі 1. У наведених далі загальних способах, якщо не вказане інше, замісники R, R1, R2, R3, кільце А, Сполуки формули (II) можна одержати за методикою, наведеною у [WO 9703986 А1 19970206], або взаємодією відповідного нижчого алкілового естеру (наприклад, метилового або етилового) з гідразином у стандартних умовах, як це проілюстровано у Препаративних Прикладах, наведених нижче. Стадія (а): Сполуки формули (III) можна одержати взаємодією гідразину (II) з придатним ацеталем (наприклад, диметилацеталем Ν,Νдиметилацетаміду) у придатному розчиннику, такому як ТГФ, або ДМФА, при температурі від кімнатної - до приблизно 60°С, протягом до 18 годин. Одержаний проміжний продукт піддавали обробці за наявності кислотного каталізу (наприклад, у присутності p-TSA, або TFA) в розчиннику з високою температурою кипіння (наприклад, толуолі, або ксилолі) протягом близько 18 годин, з одержанням сполуки формули (IIІ). Переважними умовами є: 1,5-2,0екв. ацеталю (наприклад, Ν,Ν-диметилацетаміду диметилацеталю, триетилортопропіонату), у ТГФ або ДМФА при температурі від кімнатної - до 60°С, протягом близько 18 годин, потім додавали p-TSA, або TFA (cat), кип'ятили у толуолі із зворотнім холодильником протягом 18 годин. Стадія (b): Утворення триазолу (IV) досягають взаємодією сполуки (III) з придатним аніліном, у присутності придатного кислотного каталізатора, такого як TFA або p-TSA, у придатномв розчиннику з високою температурою кипіння (наприклад, толуолі, або ксилолі), при підвищеній температурі. Переважними умовами є: 0,5-1,0екв. TFA, 1,02,0екв. аніліну у толуолі при температурі близької до температури кипіння реакційної суміші до 18 годин. Стадія (с): Відщеплення захисної групи сполуки (IV) відбувається ії застосуванням стандартних методик, описаних у ["Protecting Groups in Organic Synthesis" авторів Т. W. Greene і P. Wutz]. Коли PG представляє собою BOC, переважними умовами є: 4М НСІ в діоксані в МеОН, діоксані або ДХМ при температурі від кімнатної - до приблизно 50°С, до 18 годин; Або, 2,2М НСІ в МеОН до 18 годин при кімнатній температурі; Або, TFA у ДХМ при кімнатній температурі протягом приблизно 1 години. Альтернативно, Коли PG представляє собою ВОС, сполуку (V) можна одержати безпосередньо із сполуки (III) взаємодією з надлишком TFA, (типово 1,1-1,5екв.) і відповідним аніліном у толуолі, при кип'я тінні до 4 діб. Стадія (d): Сполуки формули (І) можна одержати взаємодією аміну (V) з придатною кислотою або хлорангідридом кислоти ( , де Τ пред ставляє ОН або СІ). Конденсація може відбуватися із застосуванням комбінації: (і) ацилхлорид, +амін (V), при надлиш ку основи у придатному розчиннику; або (іі) кислота ZCO2H з типовим конденсувальним агентом+амін (V) необов'язково у присутності каталізатора, при надлишку основи у придатному розчиннику. Типово умови реакції є наступними: (і) хлорангідрид кислоти , амін (V) (не обов'язково при надлишку третинного аміну, такого як Et3N, основа Хюніга або NMM) у ДХМ або 21 85692 22 ТГФ, без нагрівання, протягом від 1 до 24 годин; Або, 1екв. аміну (V), 1,2екв. ZCO2H, 1,2-1,5екв. або НОВТ, 1,2-1,5екв. WSCDI, 2-4екв. Et3N, у ДХМ при (іі) кислота ZCO2H, WSCDI/DCC і НОВТ/НОАТ, кімнатній температурі протягом 24 годин; амін, надлишок NMM, Et3N, або основи Хюніга, у Або, 1екв. аміну (V), 1,2-1,5екв. ZCO2H, 1,2ТГФ, ДХМ, ДМА або EtOAc, при кімнатній темпера2,0екв. HBTU, 5екв. Et3N або NMM у ДМА або турі протягом від 4 до 48 годин; або ДХМ, при температурі від кімнатної - до 60°С до 24 годин. кислота ZCO2H, РУВОРÒ /РуВrOРÒ /Oбензотриазол-1-іл-N,N,N',N'-тетраметилуронію Сполуки формули (IV), де Q представляє NR2, або Q представляє простий зв'язок, приєднаний до гексафторфосфат, надлишок аміну, надлишок атома азоту, що знаходиться у Кільці А, яке в свою NMM, Et 3N, або основи Хюніга, у ТГФ, ДХМ, ДМА чергу приєднане до триазольного кільця через або EtOAc, при кімнатній температурі протягом від атом азоту, можна альтернативно одержати як 4 до 24 годин. Переважними умовами є наступні: наведено нижче на Схемі 2 і є представленими як (IVА). 1екв. аміну (V), 1,0-1,5екв. , 1,5-5екв. NMM, Et 3N або основи Хюніга у ДХМ при кімнатній температурі до 18 годин; Стадія (e): Сполуки формули (VIIIA) можна одержати взаємодією приблизно еквімолярних кількостей ізотіоцианату (VI) і аміну (VII), у придатному розчиннику (наприклад, EtOH, або ДХМ) при кімнатній температурі протягом від 2 до 72 годин. Переважними умовами є: 1-1,1екв. (VI), 1екв. (VII), в EtOH або ДХМ, при кімнатній температурі протягом 0,5-2 годин. Сполуки формул (VI) і (VII) є комерційно доступними, або їх можна одержати з відомих сполук застосовуючи стандартні хімічні перетворення. Стадія (f): Сполуки формули (1ХА) можна одержати метилюванням тіосечовини (VIIIА), застосовуючи придатний метилюючий агент (наприклад, Mel, або MeTosylate), у присутності придатної основи (наприклад, KО-tВu) у придатному розчиннику (наприклад, ТГФ, або ефірі) при температурі від 0°С до температури кипіння реакційної суміші, протягом близько 18 годин. Переважними умовами є: 1екв. (VIIIA), 1-1,2екв. KО-tВu, 1-1,2екв. Mel або MeTosylate, у ТГФ, при температурі від 10°С до кімнатної температури до 18 годин. Стадія (g): Сполуки формули (IVA) можна одержати взаємодією сполук (ІХА) з придатним гідразидом (XCONHNH2), необов'язково при кислотному каталізі (наприклад, TFA, або p-TSA) у придатному розчиннику (наприклад, ТГФ, або нBuOH), при температурі від кімнатної - до температури кипіння реакційної суміші. Переважними умовами є: 0,5екв. TFA, надлишок гідразиду (XCONHNH2), у ТГФ кип'я тили із зворотнім холодильником до 18 годин. Сполуки формули (VIIIA), де Q представляє NR2, або Q представляє простий зв'язок приєднаний до атома азоту всередині Кільця А, яке в свою чергу приєднане до триазольного кільця через атом азоту, альтернативно можна одержати як це наведено на Схемі 3. 23 85692 24 Сполуки формули (X) є комерційно доступними, або їх можна одержати з відомих сполук застосовуючи стандартні хімічні перетворення. Сполуки формули (XI) можна одержати з ізотіоціанату (VI) і аміну (X), аналогічно методиці вже описаній раніше на Стадії (e), описаній вище. Стадія (h): Сполуки формули (VIIIA) можна одержати шляхом захисту реакційноздатного атома азоту, використовуючи стандартні методики, наведені у ["Protecti ve Groups in Organic Synthesis" авторів Т. W. Greene і P. Wutz]. Коли PG предста вляє собою ВОС, переважними умовами є: 1екв. аміну (XI), 1екв. ди-трет-бутил дикарбонату, у ДХМ і діоксані, при кімнатній температурі, протягом близько 3 годин. Сполуки формули (VIII), де Q представляє NR2, або Q представляє простий зв'язок приєднаний до атома азоту всередині Кільця А, яке в свою чергу приєднане до триазольного кільця через атом вуглецю, можна одержати за Схемою 4 і представлені тут як (VIIIB). Стадія (і): Сполуки формули (XIV) можна одержати конденсацією аніліну (XIII) з кислотою (XII), аналогічно методиці вже описаній на Стадії (d). Переважними умовами є: 1екв. кислоти (XII), 1,1екв. аміну (XIII), 1,2екв. WSCDI, 3екв. Et3N у MeCN при кімнатній температурі, протягом приблизно 3 днів. Стадія (j): Сполуку формули (VIIIВ) одержують тіонуванням сполуки (XIV) з використанням придатного тіонувального агента, такого як реагент Лавессона, в розчиннику з високою температурою кипіння (наприклад, толуол) при температурі від кімнатної - до температури кипіння реакційної суміші. Переважними умовами є: 1екв. (XIV), 0,5екв. реагента Лавессона у толуолі, при температурі від кімнатної - до температури кипіння реакційної суміші, до 18 годин. Сполуки формули (III), де Q представляє NR 2, або Q представляє простий зв'язок, приєднаний до атома азоту всередині Кільця А, альтернативно можна одержати як це наведено на Схемі 5. 25 85692 Стадія (k): Діацилгідразиди (XV) можна одержати конденсацією гідразидів (II) з кислотою або хлорангідридом кислоти , де Τ представляє СІ або ОН), аналогічно методиці вже описаній на Стадії (d). Переважними умовами є: 1екв. гідразиду (II), 1,1екв. ХСО 2Н, 1,1екв. WSCDI, 1,1екв. НОВТ, 1,2екв. Et3N, в ДМФА при кімнатній температурі протягом 18 годин. Стадія (І): Оксадіазол (III) можна одержати циклізацією сполуки (XV), типово при кислотному каталізі (наприклад, поліфосфорною кислотою, РОСІ3, ангідридом трифторметансульфонової кислоти у піридині, або 1-метилімідазолом), необов'язково у придатному розчиннику (наприклад, ДХМ), при температурі від 0°С і до температури Сmадія (m): Сполуки формули (XVI) можна одержати взаємодією гідразиду (II) з хлорацетилхлоридом, у присутності придатного третинного аміну як основи (наприклад, Et3N, або NMM) у придатному розчиннику (наприклад, EtOAc, або ДХМ) при температурі від 0°С до кімнатної температури, протягом близько 18 годин. Переважними умовами є: 1екв. (II), 1екв. ацетилхлориду, 1,1екв. NMM; у ДХМ, при температурі від 10°С до кімнатної температури, до 18 годин. Сполуки формули (XVII) можна одержати циклізацією сполуки (XVI), аналогічно методиці вже описаній на Стадії (І) вище. 26 кипіння реакційної суміші. Переважними умовами є: 1екв. (XV), надлишок піридину або 1метилімідазолу, 1,5-2екв. ангідриду трифторметансульфонової кислоти, у ДХМ, при температурі від 0°С до кімнатної температури до 3 годин. Сполуки формули (XV) можуть альтернативно бути одержані конденсацією кислоти (XII) з придатним гідразидом (XCONHNH2), аналогічно методиці вже описаній на Стадії (d). Переважними умовами є: 1екв. кислоти (XII), 1екв. гідразиду, 1,02екв. WSDCI, у ДХМ при температурі від 0°С до кімнатної температури. Сполуки формули (llІ), де X представляє СН2N-зв'язувальний фрагмент-Het, альтернативно можна одержати як це наведено на Схемі 6. Стадія (n): Сполуки формули (III) можна одержати взаємодією сполуки (XVII) з придатним Het (який містить реакційноздатний атом азоту), у присутності придатної основи (наприклад, Et3N, або K2СО3), у придатному розчиннику (наприклад, ДМФА, або MeCN), при температурі від кімнатної до температури кипіння реакційної суміші, протягом близько 18 годин. Переважними умовами є: 1екв. (XVII), 1,4екв. K2СО3, 2екв. Het, в ДМФА при кімнатній температурі, протягом 18 годин. Сполуки формули (І), де Q представляє NR 2, або Q представляє простий зв'язок, приєднаний до атома азоту всередині Кільця А, альтернативно можна одержати як це наведено на Схемі 7. 27 85692 Стадія (о): Сполуку формули (XIX) можна одержати взаємодією аміну (XVIII) з придатною кислотою або хлорангідридом кислоти , де Τ представляє ОН або СІ), аналогічно методиці вже описаній на Стадії (d). Переважними умовами є: 1екв. (XVIII), 0,9екв. ZCOCI, 1,1екв. Et3N, у ДХМ, при температурі від 10°С до кімнатної температури, протягом близько 3 годин. Стадія (р): Гідразид формули (XX) можна одержати взаємодією естеру (XIX) з надлишком гідразину у придатному розчиннику (наприклад, EtOH, або МеОН), при кип'ятінні до 18 годин. Переважними умовами є: 1екв. (XIX), 2-4екв. гідразину, в МеОН при кип'ятінні із зворотнім холодильником, протягом від 10 до 48 годин. Сполуки формули (XXIII) можна одержати взаємодією гідразиду (XX) з хлорацетилхлоридом, аналогічно методиці вже описаній на Стадії (m). 28 Сполуки формули (XXI) можна одержати взаємодією гідразиду (XX) з , застосовуючи методику, вже описану на Стадії (k). Сполуки формули (XXII) можна одержати циклізацією сполуки (XXI), застосовуючи методику, вже описану на Стадії (І). Сполуки формули (І) можна одержати з оксадіазол (XXII) з придатним анілін, як це вже було описано на Стадії (b). Альтернативно, сполуки формули (XXII) можна одержати безпосередньо із сполуки (XX) взаємодією з відповідним ацеталем (наприклад, таким як триетилортопропіонат, Ν,Ν-диметилацетаміду диметилацеталь) аналогічно методиці вже описаній на Стадії (а). Сполуки формули (XXII), де X представляє СН2-N-зв'язувальний фрагмент-Het, альтернативно можна одержати як це наведено на Схемі 8. Оксадіазол (XXIV) можна одержати циклізацією сполуки (XXIII), аналогічно методиці вже описаній на Стадії (І). Сполуку (XXII) можна одержати взаємодією сполуки (XXIV) з придатним Het (який містить реа 29 85692 30 кційноздатний атом азоту), як це вже було описано нативно можна одержати як це наведено на Схемі на Стадії (n). 9. Сполуки формули (І), де Кільце А приєднане до триазольного кільця через атом азоту, альтер Сполуки формули (XXV) є або наявними у продажу, або їх можна одержати з комерційно доступних сполук, застосовуючи стандартні хімічні перетворення. Сполуки формули (XXVI) можна одержати взаємодією сполуки (XXV) з відповідним ізотіоціанатом (VI), аналогічно методиці вже описаній на Стадії (e). Сполуку формули (XXVII) можна одержати алкілуванням сполуки (XXVI), аналогічно методиці вже описаній на Стадії (f). Сполуку формули (І) можна одержати взаємодією сполуки (XXVII) з придатним гідразидом, як це вже було описано на Стадії (g). Сполуки формули (І), де Q представляє простий зв'язок, приєднаний до атома вуглецю у Кільці А, яке в свою чергу приєднане до триазольного кільця через атом азоту у Кільці А і Ζ представляє NR4R5, можна одержати як це показано на Схемі 10. Сполуки формули (XXVIII) є або наявними у продажу, або їх можна одержати з комерційно до ступних сполук, застосовуючи стандартні хімічні перетворення. 31 85692 32 Сполуки формули (XXIX) можна одержати чину NaOH, в діоксані при температурі від кімнатвзаємодією сполуки (XXVIII) з відповідним ізотіоціної-до температури кипіння реакційної суміші, анатом (VI), аналогічно методиці вже описаній на протягом від 2 до 16 годин. Стадії (e). Сполуки формули (І) можна одержати взаємоСполуку формули (XXX) можна одержати алдією Z-H (який містить реакційноздатний атом азокілуванням сполуки (XXIX), аналогічно методиці ту) з кислотою (XXXII), аналогічно методиці вже вже описаній на Стадії (f). описаній раніше на Стадії (d). Переважними умоСполуку формули (XXXI) можна одержати взавами є: 1екв. кислоти (XXXII), 1,5екв. аміну (ZH), ємодією сполуки (XXX) з придатним гідразидом, як 4екв. Et3N, 1,5екв. WSCDI, 1,5екв. НОВТ, у ДХМ це вже було описано на Стадії (g). при кімнатній температурі, протягом 24 годин. Стадія (q): Гідроліз естеру (XXXI) застосовуюСполуки формули (XXXII) можуть альтернатичи придатний кислотний або основний каталізатор, вно бути одержані гідролізом відповідного нітрилу переважно гідроксиди лужних металів (наприклад, (XXXIII), при стандартних умовах (наприклад, 5екв. NaOH, KOH, або LiOH) у придатному водному розKOH, 1екв. нітрилу (XXXIII), в етаночиннику (наприклад, діоксані, або МеОН) при темлі/диметиловому етері етиленгліколю при кипінні). пературі від кімнатної - до температури кипіння Сполуки формули (XXXIII) можна одержати як реакційної суміші, протягом від 2 до 48 годин. Пеце показано на Схемі 11. реважними умовами є 1екв. (XXXI), 5-10екв. роз Сполуки формули (XXXIII), де Q представляє простий зв'язок і Кільце А приєднане до триазольного кільця через атом азоту, можна одержати з відповідного ізотіоціанату (VI) і Кільця А, заміщеного нітрильною групою, Сполуки формули (І), де V представляє атом кисню, можна одержати як це показано на Схемі 12. аналогі чно методиці, описаній для Схеми 9. Стадія (r): Сполуку формули (XXXV) можна одержати взаємодією гідразиду (XCONHNH2) з ізотіоціанатом (VI) аналогічно методиці вже описа ній на Стадії (e). Переважними умовами є: 1екв. ізотіоціанату, 1екв. гідразиду, в EtOH при кімнатній температурі протягом 72 годин. 33 85692 34 Стадія (s): Сполуки формули (XXXVI) можна Ще одним аспектом даного винаходу є фародержати циклізацією сполуки (XXXV) у кислотних мацевтична композиція, яка містить сполуку форабо основних умовах, переважно при кислотному мули (І), або її фармацевтично прийнятну сіль або каталізі (наприклад, гідроксидами лужних металів) сольват, а також фармацевтично прийнятний нау водному розчиннику (наприклад, вода/EtOH), при повнювач, розріджувач або носій. Наступноме втіпідвищеній температурі, протягом близько 24 голення забезпечує фармацевтичну композицію для дин. Переважними умовами є: 1екв. (XXXV), 10екв. профілактичного призначення або при виникненні NaOH (aq) в EtOH при 80°С протягом 18 годин. болю. Стадія (t): Алкілування сполуки (XXXVI) з одеФармацевтичні композиції придатні для вивіржанням сполуки (XXXVII) проводили взаємодією з льнення сполук представленого винаходу і спосопридатним алкілайпд agent (наприклад, Mel, або би їх одержання очевидні для спеціаліста в цій Me-Tosylate), аналогічно методиці вже описаній на галузі. Такі композиції і способи їх одержання моСтадії (f). Переважними умовами є: 1екв. (XXXVI), жна знайти в, наприклад, [Remington's 1екв. KО-tВu, 1екв. Me-Tosylate, у ТГФ при темпеPharmaceutical Sciences. 19th Edition (Mack ратурі від кімнатної - до температури кипіння реаPublishing Company, 1995)]. кційної суміші протягом 3 годин. Сполуки винаходу можна вводити перорально. Стадія (u): Сполуки формули (XXXVIII) можна Пероральне введення може включати заковтуванодержати окисненням сполуки (XXXVII) придатним ня, так що сполука попадає в гастроінтестинальокиснюючим агентом (наприклад, mCPBA, або ний тракт, або може бути використане букальне перокисом водню) у придатному розчиннику (наабо сублінгвальне введення і в цьому випадку приклад, ДХМ) при кімнатній температурі протягом сполука попадає в кров безпосередньо з рота. близько 18 годин. Переважними умовами є: 1екв. Рецептурами придатними для перорального (XXXVII), 4екв. mСРВА, у ДХМ при кімнатній темвведення є тверді рецептури, такі як таблетки, пературі протягом 18 годин. капсули, що містять частинки, рідини або порошки, Стадія (ν): Сполуки формули (І) можна одерпастилки (включаючи наповнені рідиною), гумки, жати взаємодією сульфоксиду (XXXVIII) при надмульти- і нано-частинки, гелі, тверді розчини, ліполишку спирту (XXXIX) у присутності придатної оссоми, плівки, овули, спреї і рідкі рецептури. нови (наприклад, NaH, або KО-tВu), у придатному Рідкими рецептурами є суспензії, розчини, сирозчиннику (наприклад, ТГФ, або ефірі) при темропи і еліксири. Такі рецептури можна використопературі від 0° до кімнатної температури до 18 вувати як наповнювачі м'яких і твердих капсул і годин. Переважними умовами є. 1екв. (XXXVIII), типово містять носій, наприклад, воду, етанол, 2екв. NaH, 2екв. спирту (XXXIX), у ТГФ протягом поліетиленгліколь, пропіленгліколь, метилцелюло18 годин при кімнатній температурі. за або придатна олія і один або декілька емульСполуки формули (XXXIX) є або наявними у сифікаторів і/або суспендувальних агентів. Рідкі продажу, або їх можна одержати з комерційно дорецептури також можна одержати шляхом відновступних сполук, застосовуючи стандартні хімічні лення твердої речовини, наприклад, з саше. перетворення. Сполуки винаходу також можна використати у Деякі сполуки формул (І) (III), (IV), (V), (XXII) і швидкорозчинних, швидкодезінтегруємих дозова(XXXI) можуть бути піддані взаємоперетворенню них формах, таких як ті що описані в [Expert функціональних груп (наприклад, алкілуванню, або Opinion in Therapeutic Patents, Ц (6), 981-986 by гідролізу) з одержанням альтернативних сполук Liang and Chen (2001)]. формул (І) (III), (IV), (V), (XXII), або (XXXI), відповіВ таблетках, в залежності від дози, лікарський дно. засіб може складати від 1ваг.% до 80ваг.% дозоСполуки винаходу призначені для фармацевваної форми, більш типово від 5ваг.% до 60ваг.% тичного використання можна вводити як кристалідозованої форми. На додаток до лікарського засочний або аморфний продукт. Їх можна одержати, бу, таблетки зазвичай містять дезінтегрант. Принаприклад, як тверді пластинки, порошки або плівкладами дезінтегрантів є натрій крохмальгілколят, ки за методами, такими як осадження, кристалізанатрій карбоксиметилцелюлоза, кальцій карбокція, висушування виморожуванням, висушування симетилцелюлоза, натрій кроскармелоза, кроспорозпиленням або висушування упарюванням. Для відон, полівінілпіролідон, метилцелюлоза, мікроцих цілей може бути використане висушування під кристалічна целюлоза, нижчий алкіл-заміщена дією мікрохвильового або радіовипромінювання. гідроксипропілцелюлоза, крохмаль, прежелатиніВони можуть бути введенні окремо або в комзований крохмаль і алгінат натрію. Загалом, дезінбінації з одним або більшою кількістю інших сполук тегрант складає від 1ваг.% до 25ваг.%, переважно винаходу або в комбінації з одним або декількома від 5ваг.% до 20ваг.% дозованої форми. іншими лікарськими засобами (або як будь-яка їх Зв'язувальні агенти зазвичай використовуютькомбінація). Загалом, вони можуть бути введенні ся для зв'язування компонентів таблетки разом. як рецептура у поєднанні з одним або декількома Придатними зв'язувальними агентами є мікрокрисфармацевтично прийнятними екціпієнтами Термін талічна целюлоза, желатин, цукри, поліетиленглі"екціпієнт" використовується тут для опису будьколь, природні і синтетичні смоли, полівінілпіроліякого інгредієнту іншого ніж сполука(и) винаходу. дон, прежелатинізований крохмаль, Вибір екціпієнту буде у великій мірі залежати від гідроксипропілцелюлоза і гідроксипропілметилцефакторів, таких як особливості шляху введення, люлоза. Таблетки також можуть містити розріджувплив екціпієнту на розчинність і стабільність і вачи, такі як лактоза (моногідрат, моногідрат виприрода дозованої форми. сушений розпиленням, безводну і їм подібні), маніт, ксиліт, декстроза, цукроза, сорбіт, мікрокри 35 85692 36 сталічна целюлоза, крохмаль і дигідрат дигідросмаку, консерванти, агенти, що стимулюють слифосфа ту кальцію. новиділення, охолоджувальні агенти, співрозчинТаблетки також можуть містити поверхневоники (включаючи масла), пом'я кшувачі, наповнюактивні агенти, такі як лаурилсульфат натрію і повачі, протипінні агенти, поверхнево-активні лісорбат 80 і агенти, що покращують ковзкість, такі речовини і агенти, що маскують смак. як діоксид креміню і тальк. Коли присутні, поверхПлівки у відповідності з винаходом типово нево-активні агенти можуть складати від 0,2ваг.% одержують шляхом сушіння випарюванням тонких до 5ваг.% таблетки і агенти, що покращують ковзводних плівок на носії з якого вона легко відшарокість, складають від 0,2ваг.% до 1ваг.% таблетки. вується або папері. Це можна здійснити у сушильТаблетки також зазвичай містять змащувальні ній шафі або тунелі, типово поєднують висушувач агенти, такі як стеарат магнію, стеарат кальцію, покриттів або шляхом сушіння виморожуванням стеарат цинку, стеарилфумарат натрію і суміші або вакуумуванням. стеарату магнію з стеарилфумаратом натрію. Тверді рецептури для перорального введення Змащувальні агенти зазвичай складають від можна сформувати для негайного і/або модифіко0,25ваг.% до 10ваг.%, переважно від 0,5ваг.% до ваного вивільнення. Рецептурами модифікованого 3ваг.% таблетки. вивільнення є рецептури з затриманим-, триваІншими можливими інгредієнтами є антиоксилим-, пульсуючим-, контрольованим-, цільовим- і данти, барвники, ароматизатори, консерванти і програмованим-вивільненням. агенти, що маскують смак. Придатні рецептури з модифікованим вивільТипові таблетки містять до приблизно 80% ліненням для цілей цього винаходу описуються в карського засобу, від приблизно 10ваг.% до при[патенті US 6,106,864]. Деталі інших придатних близно 90ваг.% зв'язувального агенту, від приблитехнологій вивільнення, такі як високоенергійні зно 0ваг.% до приблизно 85ваг.% розріджувача, дисперсії і осмотичні частинки і частинки з покритвід приблизно 2ваг.% до приблизно 10ваг.% дезінтям описані в [Verma et al, Pharmaceutical тегратора і від приблизно 0,25ваг.% до приблизно Technology On-line. 25(2), 1-14 (2001)]. Викорис10ваг.% змащувального агенту. тання жувальних гумок для досягнення контрольоТаблеткові суміші можуть бути спресовані ваного вивільнення описується в [WO 00/35298]. безпосередньо або використовуючи валки для Сполуки винаходу можна вводити безпосереформування таблеток. Таблеткові суміші або часдньо в кров, в м'язи, або у внутрішні органи. Притини сумішей можуть бути піддані перед таблетудатними шляхами для парентерального введення ванням вологому-, сухому-гранулюванню або грає внутрішньовенне, внутрішньоартеріальне, інтранулюванню розплаву, отвердженню розплаву або перітонеальне, інтратекальне, інтравентрикулярекструдуванню. Кінцева рецептура може включати не, інтрауретарльне, інтрастернальне, інтракраніодин або більшу кількість шарів і може мати поальне, внутрішньом'язове і підшкірне. Придатними криття або не мати такого; вона може навіть бути пристроями для парентерального введення є голінкапсульована. кові (включаючи мікроголкові) інжектори, безголкоРецептури таблеток розглядаються в ві інжектори і засоби для вливання. х"Pharmaceutical Dosage Forms : Tablets". Vol. 1, by Парентеральними рецептурами є типово водні Η. Lieberman and L. Lachman (Marcel Dekker, New розчини, які можуть містити екціпієнти, такі як солі, York, 1980)ї. вуглеводи і буферуючі агенти (переважно до рН Використовуваними плавкими пероральними від 3 до 9), але, для деяких застосувань, вони моплівками для людей або ветеринарії є пластичні жуть бути сформовані більш придатно як стерильводорозчинні або водонабухаючі тонкоплівкові ний неводний розчин або як суха форма для викодозовані форми, які можуть швидко розчинятись ристання у поєднанні з придатним розчинником, або поглинатись слизовою оболонкою і типово таким як стерильна пірогенвільна вода. містять сполуку формули (1), плівкоутворюючий Одержання парентеральних рецептур за степолімер, зв'язувальний агент, розчинник, вологорильних умов, наприклад, шляхом ліофілізації, поглинач, пластифікатор, стабілізатор або емульможна легко здійснити використовуючи стандартні сифікатор, агент, що модифікує в'язкість і розчинфармацевтичні методики добре відомі спеціалісту ник. Деякі компоненти рецептури можуть в цій галузі. виконувати більше ніж одну функцію. Розчинність сполук формули (І), що викорисСполуки формули (1) можуть бути водорозтовується при одержанні парентеральних розчичинними або нерозчинними. Водорозчина сполука нів, можна збільшити через використання прийнятипово містить від 1ваг.% до 80ваг.%, більш типотних методик формулювання, такі як включення во від 20ваг.% до 50ваг %, розчиненої речовини. агентів, що збільшують розчинність. Менш розчинні сполуки можуть складати більшу Рецептури для парентерального введення частину композиції, типово до 88ваг.% розчиненої можна сформувати у форми для негайного і/або речовини. Альтернативно, сполука формули (1) модифікованого вивільнення. Рецептури з модифіможе бути у формі мілких часточок. кованим вивільненням мають затримане-, триваПлікоутворюючий полімер може бути вибрале-, пульсуюче-, контрольоване-, цільове- і проний з природних полісахаридів, протеїнів або синграмоване вивільнення. Таким чином, сполуки тетичних гідроколоїдів і типово присутній в інтервинаходу можуть бути сформовані як тверда, навалі від 0,01 до 99ваг.%, більш типово в інтервалі півтверда або тиксотропна рідина для введення як від 30 до 80ваг.%. імплантуєме депо, що забезпечує модифіковане Іншими можливими інгредієнтами є антиоксививільнення активної сполуки. Прикладами таких данти, барвники, ароматизатори і підсилювачі рецептур є покриті лікарським засобом стенти і 37 85692 38 мікросфери полі-DL-молочної-співгліколевої кисторі можна сформувати так що вони містять поролоти (PGLA). шкоподібну суміш сполуки винаходу, придатною Сполуки винаходу також можуть бути нанесені основою для порошків є лактоза або крохмаль і на шкіру або слизову оболонку, тобто, можуть бути модифікаторами характеристик є І-лейцин, маніт використані дермально або трансдермально. Тиабо стеарат магнію. Лактоза може бути безводною повими рецептурами для цих цілей є гелі, гідрогеабо у формі моногідрату, переважно, остання. Інлі, лосьйони, розчини, креми, мазі, порошки для шими придатними екціпієнтами є декстран, глюкоприсипання, пов'язки, піни, плівки, пластири, пласза, мальтоза, сорбіт, ксиліт, фруктоза, цукроза і тини, імплантати, тампони, волокна, бандажі і міктрегалоза. роемульсії. Також можуть бути використані ліпоПридатна рецептура розчину, для використансоми. Типовими носіями є спирт, вода, мінеральна ня в розпилювачі, що використовує електродинаолія, рідкий парафін, білий парафін, гліцерин, помічне розпилення для одержання доброго туману, ліетиленгліколь і пропіленгліколь. Сюди можна може містити від 1мкг до 20мг сполуки винаходу включити агенти, що підвищують проникність, дина один пуск і об'єм пуску може змінюватись від віться, наприклад, [J Pharm Sci, 88 (10), 955-958 1мкл до 100мкл. Типова рецептура може містити автори Finnin і Morgan (October 1999)]. сполуку формули (І), пропіленгліколь, стерильну Іншими засобами місцевого введення є вивіводу, е танол і хлорид натрію. Альтернативними льнення за допомогою електропорація, іонтофорозчинниками, які можуть бути використані замість рез, фонофорез, сонофорез і мікроголкове або пропіленгліколю є гліцерин і поліетиленгліколь. Придатні ароматизатори, такі як ментол і лебезтолкове (наприклад, PowderjectÔ , BiojectÔ і воментол, або підсолоджувачи, такі як сахарин т.і.) ін'єктування. або сахарин натрію, можуть бути додані до цих Рецептури для місцевого введення можуть бути зформовані для негайного і/або модифікованорецептур винаходу призначених для інгаляційного/інтраназального введення. го вивільнення. Рецептури модифікованого вивіРецептури для інгаляційного/інтраназального льнення мають затримане-, тривале-, пульсуюче-, введення можна сформувати для негайного і/або контрольоване-, цільове- і програмоване вивільмодифікованого вивільнення використовуючи, нанення. Сполуки винаходу також можна вводити інтраприклад, PGLA Рецептури модифікованого вивільнення мають затримане-, тривале-, пульсуюче-, назально або за допомогою інгаляції, типово у контрольоване-, цільове- і програмоване вивільформі сухого порошку (або окремо, або як суміш, нення. наприклад, суха суміш з лактозою, або як суміш У випадку інгаляторів і аерозолів для сухого часточок компонентів, наприклад, суміш з фосфоліпідами, такими як фосфатидилхолін) з інгалятопорошку, одиниця дозування визначається за допомогою клапану, який вивільнює виміряну кільру для сухого порошку або як аерозольний спрей з кість. Загальна добова доза буде типово знаходиконтейнеру під тиском, насосу, спрею, розпилюватись в інтервалі від 0,01мкг до 15мг, які можна ча (переважно використовують електродинамічний вводити в одиничній дозі або, більш звичайно, як розпилювач для одержання доброго туману), або розпорошувача, з або без використання придатнорозподілені дози протягом дня. Сполуки винаходу можна вводити ректально го пропеланту, такого як 1,1,1,2-тетрафторетан або вагінально, наприклад, у формі супозиторію, або 1,1,1,2,3,3,3-гептафторпропан. Для інтраназапесарію або клізми. Масло какао є традиційною льного застосування, порошок може містити біоадосновою супозиторію, але якщо прийнятно можуть гезивний компоненти, наприклад, хітозан або циклодекстрин. бути використані різні альтернативи. Рецептури ректального/інтравагінального ввеКонтейнер під тиском, насос, спрей, розпилюдення можуть бути сформовані для негайного вач або розпорошувач містить розчин або суспені/або модифікованого вивільнення. Рецептури мозію сполук(и) винаходу, що включає, наприклад, дифікованого вивільнення мають затримане-, триетанол, водний етанол або придатний альтернативний агент для диспергування, солюбілізації або вале-, пульсуюче-, контрольоване-, цільове- і програмоване вивільнення. розтягнення вивільнення активного агенту, пропеСполуки винаходу також можуть бути введенні ланту(ів), як розчинника, і, необов'язково, поверхбезпосередньо у око або вухо, типово у формі нево-активну речовину, таку як триолеат сорбіту, крапель мікронізованої суспензії або розчину в олеїнову кислоту або олігомолочну кислоту. Перед застосуванням в рецептурі сухого поізотонічному, рН-коригованому, стерильному саліні. Іншими рецептурами придатними для окуляррошку або суспензії, лікарський засіб мікронізують ного і аурального введення є мазі, біодеградуємі до розміру придатного для вивільнення за допомо(наприклад, губки з абсорбуючого гелю, колагену) і гою інгаляції (типово менше ніж 5 мікрон). Це можнебіодеградуємі (наприклад, сиілкон) імплантати, на здійснити за допомогою будь-якого прийнятного методу подрібнення, такого як змелення в спіраоблатки, лінзи i частинкові або везикулярні системи, такі як ніосоми або ліпосоми. Може бути вклюльно-кулачковому млині, змелення в млині з псевчений полімер, такий як поперечнозв'язана поліакдозрідженим шаром, одержання наночасток за рилова кислота, полівініловий спирт, гіалуронова допомогою оброки надкритичною рідиною, гомогекислота, целюлозний полімер, наприклад, гідронізація при високому тиску або висушування розпиленням. ксипропілметилцелюлоза, гідроксиетилцелюлоза або метилцелюлоза, або гетерополісахаридний Капсули (виготовлені, наприклад, з желатину полімер, наприклад, геланова смола, разом з конабо гідроксипропілметилцелюлози), блістери і карсервантом, таким як хлорид бензалконію. Такі ретриджі для використання в інгаляторі або інсуфля 39 85692 40 цептури також можна вивільнювати за допомогою Для усунення сумнівів, приведене тут посиіонтофорезу. лання на "лікування" включає зцілююче, пом'якРецептури окулярного/аурального введення шуюче і профілактичне лікування. можуть бути сформовані для негайного і/або моСполуки представленого винаходу можуть будифікованого вивільнення. Рецептури модифікоти перевірені в наборі аналізів, викладених нижче: ваного вивільнення мають затримане-, тривале-, 1.0 Фільтрувальний аналіз зв'язування V1A пульсуюче-, контрольоване-, цільове- і програмо1.1 Одержання мембрани ване вивільнення. Дослідження зв'язування рецептора виконуваСполуки винаходу можуть бути об'єднані з ли на клітинних мембранах, одержаних з клітин розчинними макромолекулами, такими як циклолінії СНО, що стабільно експресують V1A рецептор декстрин і його придатними похідними або полілюдини, (СНО-hV1A). Лінія клітин CHO-hV1A згідно з етиленгліколь-вмісними полімерами, для того щоб умовами ліцензійного договору була люб'язно напокращити їх розчинність, швидкість розчинення, дана Marc Thibonnier, Департамент Медицини, замаскувати смак, біодоступність і/або стабільCase Western Reserve University School of ність для використання в будь-якому із згадних Medicine, Клівленд, штат Огайо. CHO-h V1A клітини вище методів введення. звичайно утримували при 37°С у зволоженій атмоКомплекси лікарський засіб-циклодекстрин, сфері з 5% вмістом СО2 у живильному середовищі наприклад, знайшли широке застосування в більDMEM/Hams F12, доповненій 10% фетальною бишості дозованих форм і шляхів введення. Можуть чачою сироваткою, 2мМ L-глутаміну, 15мМ HEPES бути використані комплекси включення і не вклюі 400мкг/мл G418. Для одержання в великих кільчення. Як альтернатива безпосередньому комплекостях клітинних осадів, зв'язані CHO-hV1A клітини ксоутворенню з лікарським засобом, циклодекствиростали до зрілості 90-100% у 850см 2 циліндририн може бути використаний як доповнювач, тобто чних пляшках, що містять середовище як носій, розріджувач або солюбілізатор. Найбільш DMEM/Hams F12 живильного середовища, доповчасто для цих цілей використовують альфа-, бетаненого 10% фетальною бичачою сироваткою, 2мМ і гама-циклодекстрини, приклади яких можна знайL-глутаміну і 15мм HEPES. Конфлюентні клітини ти в [Міжнародних заявках № WO 91/11172, WO CHO-hV1A промивали фосфатно забуферованим 94/02518 і WO 98/55148]. сольовим розчином (PBS), збирали в охолоджеОскільки може бути бажаним введення комбіному льодом PBS і центрифуговали при нації активних сполук, наприклад, з ціллю лікуван1000об./хвилину До використання осади клітин ня окремих станів або захворювань, в межі предзберігали при -80°С. Осади клітин розморожували ставленого винаходу також попадають комбінації, на льоді і гомогенізували в буфері для одержання що складаються з двох або декількох фармацевмембран, що містить Tris-HCI 50мм, рН 7,4, 5мМ тичних композицій, де, принаймні, одна з яких місМgСІ2 і додавали суміш інгібіторів протеаз (від тить сполуку згідно з винаходом, у формі набору Roche). Клітинний гомогенат центрифугували при придатного для спільного введення композицій. 1000 об./хвилину протягом 10 хвилин при 4°С і Таким чином, набір винаходу містить дві або супернатант видаляли і зберігали на льоду. Осад, декілька окремих фармацевтичних композицій, що залишився, гомогенізували і ще раз центрифупринаймні, одна з яких містить сполуку формули гували. Супернатанти об'єднували і центрифугу(І) у відповідності з винаходом і засоби для окревали при 25000об./хвилину протягом 30 хвилин мого зберігання згаданих композицій, такі як конпри 4°С. Осад ресуспендували у заморожувальтейнер, окрема пляшечка, або окремий пакет з ному буфері, що складається з Tris-HCI 50мМ, рН фольги Прикладом такого набору є звичайна бліс7,4, 5мМ МgСІ 2 і 20 % гліцерину і зберігали до витерна упаковка, що використовується для пакукористання маленькими аліквотами при -80°С. вання таблеток, капсул і їм подібного. Концентрацію білку визначали за Бредфордом, Набір винаходу є особливо придатним для використовуючи БС А як стандарт. введення рідних дозованих форм, наприклад, пе1.2 V1A Фільтрувальне зв'язування рорально і парентерально, для введення окремих Дослідження лінійності білку і наступне за ним композицій з різним інтервалом дозування або для дослідження насичення зв'язування виконували титрування окремих композицій одна проти іншої. для кожної нової порції мембран. Концентрацію Для допомоги, набір типово містить інструкції по мембран вибирали таким чином, щоб вона забезвведенню і може бути забезпечений так званою печувала специфічне зв'язування на лінійній часпам'яткою. тині кривої. Дослідження насичення зв'язування Для введення людям, загальна добова доза проводили, використовуючи різні концентрації [3Н]сполук винаходу типово знаходиться в інтервалі арпнінвазопресину, [ 3H]-AVP (0,05нМ-100нМ) і вивід 0,01мг до 15мг, звичайно, в залежності від значали Kd і Вmах. шляху введення. Загальна добова доза може бути Сполуки перевіряли на їх вплив на зв'язування введена за один раз або може бути розділена на [3H]-AVP з CHO-h V1A мембранами, (3H-AVP; спедекілька доз і, за рішенням лікаря, не співпадати з цифічна активність 65,5Сі/ммол; NEN Life наведеним тут типовим інтервалом. Sciences). Сполуки розчиняли у диметилсульфокЦі дози орієнтовані на середню людину, що сиді (ДМСО) і розводили буфером для аналізу, що має вагу приблизно від 60 до 70кг. Лікар легко вимістить Tris-HCI 50мМ рН 7,4, 5мМ МgСІ 2 і 0,05% значить дози для суб'єктів, чия вага випадає з цьоBSA до 10% робочої концентрації у ДМСО. 25мкл го інтервалу, таких як діти і люди похилого віку. сполуки і 25мкл [3H]-AVP, (кінцева концентрація дорівнює або нижча за Kd, визначеного для партії мембран, типово - 0,5нМ-0,6нМ) додавали до 96 41 85692 42 лункового поліпропіленового планшету і з круглим сольовий розчин Дюльбекко (DPBS), 2,5мМ продном Реакцію зв'язування ініціалізували додаванбенециду і барвник, який складається з культураням 200мкл мембран і обережно струшували льного клітинного середовища, що містить 4мкМ планшети протягом 60 хвилин при кімнатній темFluo-3-AM (розчиненого у ДМСО і плюронієвій киспературі. Реакцію завершували шля хом швидкого лоті), (від Molecular Probes) і 2,5мМ пробенециду, фільтрування, використовуючи Filtermate Cell був одержаний у день проведення досліджень. Harvester (від Packard Instruments) через 96Сполуки солюбілізували у ДМСО і розводили в лунковий фільтрувальний планшет GF/B UniFilter буфері для аналізу, що складається з DPBS, що Plate, який для попередження склеювання пептимістить 1% ДМСО, 0,1% BSA і 2,5мМ пробенециду. дів попередньо замочували в 0,5% поліетиленіміні. Клітини інкубували з 100мкл введеного у кожну Фільтри промивали три рази, використовуючи 1мл лунку барвника протягом 1 години при 37°С у звоохолодженого льодом промивного буферу, що ложеній атмосфері з 5% вмістом СО2. Після ввемістить 50мМ Tris-HCI, рН 7,4 і 5мМ МgСІ2 . Пландення барвника клітини три рази промивали шети висушували і до кожної лунки додавали 100мкл промивочного буферу, використовуючи 50мкл Microscint-0 (Packard Instuments). Планшети пристрій Denley для промивання для планшетів. В герметизували і вимірювали на сцинтиляційному кожній лунці залишили 100мкл промивочного булічильнику TopCount Microplate (від Packard феру. Вн утрішньоклітинну флуоресценцію виміInstruments). Неспецифічне зв'язування (NSB) вирювали, використовуючи FLIPR. Флуоресцентні значали, використовуючи 1мкМ неміченого зчитування отримували через кожні 2 секунди і через 30 секунд додавали 50мкл досліджуваної d(CH2)5Tyr(Me)AVP ([b-меркапто-b,bсполуки. Для виявлення агоністичної активності циклопентаметиленпропіонілб 0-Ме-Tyr 2, Аrg8]сполуки додатково проводили 155 вимірювань вазопресину) (bMCPVP), (від Sigma). Дані радіолічерез 2 секундні інтервали. Потім додавали 50мкл гандного зв'язування аналізували, використовуючи аргінінвазопресину (AVP) таким чином, щоб кінцелогістичне рівняння з чотирма параметрами з мівий об'єм досліджуваного розчину складав німумом, що наближається до 0%. Нахил був до200мкл. Подальші флуоресцентні зчитування збивільно встановлений і падав при значеннях в діарали через 1 секундні інтервали протягом 120 сепазоні між -0,75 і -1,25 для наявних кривих. кунд. Відповіді вимірювали як піки флуоресцентної Специфічне зв'язування розраховували відніманінтенсивності (FI). Для фармакологічної характеням середньої кількості NSB імпульсів у хвилину ристики від кожної флуоресцентної відповіді віднівід загальної кількості імпульсів у хвилину. Для мали базальний FI. Для кривих залежності відподосліджуваних сполук ступінь зв'язування ліганда віді від дози AVP, кожне значення відповіді було з рецептором була виражена наступним чином: виражене як % відповіді на максимальну концентзв'язування,%=(кількість імпульсів у хвилину зразрацію AVP у цьому ряді. Для визначення ІС50, кожку, тобто кількість імпульсів NSB за хвилину/ кільне значення відповіді було виражене як % відповікість імпульсів специфічного зв'язування за хвилиді на AVP. Значення ІС50 були переведені у ну)x100. Залежність % зв'язування від модифіковану величину Kb , використовуючи рівконцентрації досліджуваної сполуки представляє няння Ченга-Прусова, в яке входять агоністична собою сигмоїдну криву. Константу дисоціації інгіконцентрація, [А], агоніст ЕС50 і нахил: бування (Ki) розраховували, використовуючи рівKb=ІС50 /(2+[А]/А50 ]n) 1/n-1, де [А] є концентрацією няння Ченга-Прусова: Ki=IC50/(1+[L]/K d), де [L] є AVP, А50 означає ЕС 50 AVP, визначену з кривої концентрацією ліганда в лунці і Kd означає констазалежності відповіді від і дози і n=нахил кривої нту дисоціації радіоліганда, отриманого з залежності відповіді від дози AVP. Scatchard графічного аналізу. Сполуки відповідно до винаходу можуть при2.0 V1-A Функціональний аналіз, Інгібування значатися поодинці або в комбінації з одним або AVP/V1-A-R опосередковане мобілізацією Са2+ за більшою кількістю інших лікарських засобів (або у допомогою FLIPR (зчитувача Флуоресцентного вигляді будь-якої їх комбінації). Сполуки представзображення планшетів) (від Molecular devices) леного винаходу можуть призначатися в комбінації Внутрішньоклітинне вивільнення кальцію виміз оральним контрацептивним засобом. Отже, нарювали у клітинах лінії CHO-hV1A, використовуючи ступним аспектом даного винаходу є забезпечення FLIPR, що забезпечує швидке виявлення кальцію фармацевтичного продукту, що містить антагоніст після активації рецептора. CHO-hV1A клітинна лінія V1a і оральний контрацептив, у вигляді комбіновалюб'язно забезпечувалася згідно з умовами ліценного препарату для одночасного, окремого або зійного договору Marc Thibonnier, Департамент послідовного застосування при лікуванні дисменоМедицини, Case Western Reserve University School реї. of Medicine, Кливленда, Штату Огайо. CHO-hV1A Сполуки даного винаходу можуть призначатиклітини звичайно утримували при 37°С у зволожеся в комбінації з інгібітором PDE5. Отже, наступній атмосфері з 5% вмістом СО2 у живильній суміним аспектом даного винаходу є забезпечення ші DMEM/Hams F12, доповненій 10% фетальною фармацевтичного продукту, що містить антагоніст бичачою сироваткою, 2мМ L-глутаміну, 15мМ V1a і інгібітор PDEV у вигляді комбінованого преHEPES і 400мкг/мл G418. Опівдні перед досліпарату для одночасного, окремого або послідовнодженням клітини висаджували у планшет з щільніго застосування при лікуванні дисменореї. стю 20000 клітин на лунку в чорні стерильні 96Інгібітори PDEV, корисні для поєднання з анталункові планшети з прозорим дном, для забезпегоністами V1a включають наступні сполуки, але не чення можливості огляду клітин і вимірювань флуобмежуються ними: оресценції з дна кожної лунки. Свіжий промивочний буфер, що містить фосфа тно забуферений 43 85692 44 (і) Інгібітори PDE5, описані в наступних публіWO99/54333]; (+)-3-етил-5-[5-(4-етилпіперазин-1каціях [міжнародних патентних заявок: ілсульфоніл)-2-(2-метокси-1(R)WO03/000691; WO02/64590; WO02/28865; метилетокси)піридин-3-іл]-2-метил-2,6-дигідро-7НWO02/28859; WO02/38563; WO02/36593; піразоло[4,3-d]піримідин-7-он, також відомий як 3WO02/28858; WO02/00657; WO02/00656; етил-5-{5-[4-етилпіперазин-1-ілсульфоніл]-2-([(1R)WO02/10166; WO02/00658; WO01/94347; 2-метокси-1-метилетил]окси)піридин-3-іл}-2-метилWO01/94345; WO00/15639 і WO00/15228]; 2,6-дигідро-7Н-піразоло[4,3-d]піримідин-7-он [див. (іі) Інгібітори PDE5, описані в [U.S. Pat. Nos. WO99/54333]; 5-[2-етокси-5-(4-етилпіперазин-16,143,746; 6,143,747 і 6,043,252]; ілсульфоніл)піридин-3-іл]-3-етил-2-[2(ііі) Піразоло[4,3-d]піримідин-7-они розкриті у метоксиетил]-2,6-дигідро-7Н-піразоло[4,3[ЕР-А-0463756]; піразоло[4,3-d]піримідин-7-они d]піримідин-7-он, також відомий як 1-{6-етокси-5розкриті у [ЕР-А-0526004]; піразоло[4,3[3-етил-6,7-дигідро-2-(2-метоксиетил)-7-оксо-2Нd]піримідин-7-они розкриті в опублікованій [міжнапіразоло[4,3-d]піримідин-5-іл]-3родній патентній заявці WO 93/06104]; ізомерні піридилсульфоніл}-4-етилпіперазин [див. WO піразоло[3,4-d]піримідин-4-они розкриті у опубліко01/27113, Приклад 8]; 5-[2-ізо-бутокси-5-(4ваній [міжнародній патентній заявці WO 93/07149]; етилпіперазин-1-ілсульфоніл)піридин-3-іл]-3-етилі хіназолін-4-они розкриті у опублікованій [міжна2-(1-метилпіперидин-4-іл)-2,6-дигідро-7Нродній патентній заявці WO 93/12095]; піридо[3,2піразоло[4,3-d]піримідин-7-он [див. WO 01/27113, d]піримідин-4-они розкриті у опублікованій [міжнаПриклад 15]; 5-[2-етокси-5-(4-етилпіперазин-1родній патентній заявці WO 94/05661]; пурин-6-они ілсульфоніл)піридин-3-іл]-3-етил-2-феніл-2,6розкриті у оп ублікованій [міжнародній патентній дигідро-7Н-піразоло[4,3-d]піримідин-7-он [див. WO заявці WO 94/00453]; піразоло[4,3-d]піримідин-701/27113, Приклад 66]; 5-(5-ацетил-2-пропокси-3они розкриті у опублікованій [міжнародній патентпіридиніл)-3-етил-2-(1-ізопропіл-3-азетидиніл)-2,6ній заявці WO 98/49166]; піразоло[4,3-d]піримідиндигідро-7Н-піразоло[4,3-d]піримідин-7-он [див. WO 7-они розкриті у опублікованій [міжнародній патен01/27112, Приклад 124]; 5-(5-ацетил-2-бутокси-3тній заявці WO 99/54333]; піразоло[4,3-d]піримідинпіридиніл)-3-етил-2-(1-етил-3-азетидиніл)-2,64-они розкриті у [ЕР-А-0995751]; піразоло[4,3дигідро-7Н-піразоло[4,3-d]піримідин-7-он [див. WO d]піримідин-7-они розкриті у опублікованій [міжна01/27112, Приклад 132]; (6R, 12aR)-2,3,6,7,12,12ародній патентній заявці WO 00/24745]; піразогексагідро-2-метил-6-(3,4ло[4,3-d]піримідин-4-они розкриті у [ЕР-А-0995750]; метилендіоксифеніл)піразино[2', 1':6,1]піридо[3,4гексагідропіразино[2',1':6,1]піридо[3,4-b]індол-1,4b]індол-1,4-діон (тадалафіл, ІС-351, CialisÒ ), тобто діони розкриті в публікації [міжнародної заявки сполука Прикладів 78 і 95 опублікованої [міжнароWO95/19978]; піразоло[4,3-d]піримідин-4-они роздної заявки WO95/19978], так само, як і сполука криті у [WO00/27848]; імідазо[5,1Прикладів 1, 3, 7 і 8; 2-[2-етокси-5-(4-етилf][1,2,4]триазинони розкриті у [ЕР-А-1092719 і в піперазин-1-іл-1-сульфоніл)феніл]-5-метил-7публікації міжнародної заявки WO 99/24433], а пропіл-3H-імідазо[5,1-f][1,2,4]триазин-4-он (вардетакож біциклічні сполуки розкриті в публікації [міжнафіл, LEVITRAÒ ) також відомий як 1-[[3-(3,4народної заявки WO 93/07124]; піразоло[4,3дигідро-5-метил-4-оксо-7-пропілімідазо[5,1-f]-asd]піримідин-7-они розкриті в публікації [міжнародтриазин-2-іл)-4-етоксифеніл]сульфоніл]-4ної заявки WO 01/27112]; піразоло[4,3-d]піримідинетилпіперазин, тобто сполука Прикладів 20, 19, 7-они розкриті в публікації [міжнародної заявки WO 337 і 336 опублікованої [міжнародної заявки 01/27113]; сполуки розкриті у [ЕР-А-1092718] і споWO99/24433; сполука Прикладу 11 опублікованої луки розкриті у [ЕР-А-1092719]; трициклічні сполуміжнародної заявки WO93/07124 (EISAI); сполуки 3 ки розкриті у [ЕР-А-1241170]; алкілсульфонові і 14 з Rotella D Ρ, J. Med. Chem., 2000, 43, 1257]; 4сполуки розкриті в публікації [міжнародної заявки (4-хлорбензил)аміно-6,7,8-триметоксихіназолін; NWO 02/074774]; сполуки розкриті в публікації [між[[3-(4,7-дигідро-1-метил-7-оксо-3-пропіл-1Ннародної заявки WO 02/072586]; сполуки розкриті піразоло[4,3-d]-піримідин-5-іл)-4в публікації [міжнародної заявки WO 02/079203] і пропоксифеніл]сульфоніл]-1-метил-2сполуки розкриті у [WO 02/074312]. піролідинпропанамід ["DA-8159" (Приклад 68 з (iv) Переважно 5-[2-етокси-5-(4-метил-1WO00/27848)]; і 7,8-дигідро-8-оксо-6-[2піперазинілсульфоніл)феніл]-1-метил-3-н-пропілпропоксифеніл]-1Н-імідазо[4,5-g]хіназолін і 1-[3-[11,6-дигідро-7Н-піразоло[4,3-d]піримідин-7-он (сил[(4-фтор феніл)метил]-7,8-дигідро-8-оксо-1Нденафіл, доступний, наприклад, під торговою марімідазо[4,5-g]хіназолін-6-іл]-4кою ViagraÒ ) також відомий як 1-[[3-(6,7-дигідро-1пропоксифеніл]карбоксамід. метил-7-оксо-3-пропіл-1Н-піразоло[4,3(ν) 4-Бром-5-(піридилметиламіно)-6-[3-(4d]піримідин-5-іл)-4-етоксифеніл]сульфоніл]-4хлорфеніл)-пропокси]-3-(2Н)піридазинон; 1-[4-[(1,3метилпіперазин [див. ЕР-А-0463756]; 5-(2-етоксибензодіоксол-5-ілметил)аміно]-6-хлор-2-хіназоліл]5-морфоліноацетилфеніл]-1-метил-3-н-пропіл-1,64-піперидинкарбонової кислоти мононатрієва сіль; дигідро-7Н-піразоло[4,3-d]піримідин-7-он [див. ЕР(+)-цис-5,6а,7,9,9,9а-гексагідро-2-[4А-0526004]; 3-етил-5-[5-(4-етилпіперазин-1(трифторметил)-фенілметил-5-метилілсульфоніл)-2-н-пропоксифеніл]-2-(піридин-2циклопент[4,5]імідазо[2,1-b]пурин-4(3H)он; фуразіл)метил-2,6-дигідро-7Н-піразоло[4,3-d]піримідинлоцилін; цис-2-гексил-5-метил-3,4,5,6a,7,8,9,9a7-он [див. WO98/49166]; 3-етил-5-[5-(4октагідроциклопент[4,5]-імідазо[2,1-b]пурин-4-он; етилпіперазин-1-ілсульфоніл)-2-(23-ацетил-1-(2-хлорбензил)-2-пропіліндол-6метоксиетокси)піридин-3-іл]-2-(піридин-2-іл)метилкарбоксилат; 3-ацетил-1-(2-хлорбензил)-22,6-дигідро-7Н-піразоло[4,3-d]піримідин-7-он [див. пропіліндол-6-карбоксилат; 4-бром-5-(3 45 85692 46 піридилметиламіно)-6-(3-(4-хлорфеніл)пропокси)фенін, оксифенбутазон, фенілбутазон, проглуме3-(2Н)піридазинон; 1-метил-5-(5тацин, ацеметацин, фентіазак, кліданак, оксипінак, морфоліноацетил-2-н-пропоксифеніл)-3-н-пропілмефенамінова кислота, меклофенамінова кисло1,6-дигідро-7Н-піразоло[4,3-d]піримідин-7-он; 1-[4та, флуфенамінова кислота, ніфлумінова кислота, [(1,3-бензодіоксол-5-ілметил)аміно]-6-хлор-2флуфенісал, судоксикам, етодолак, піпрофен, сахіназолініл]-4-піперидинкарбонова кислота, моноліцилова кислота, трисаліцилат магнію холіну, натрієва сіль; Pharmaprojects No. 4516 (Glaxo саліцилат, бенорилат, фентіазак, клопінак, фепраWellcome); Pharmaprojects No. 5051 (Bayer); зон, ізоксикам і 2-фтор-a-метил[1,1'-біфеніл]-4Pharmaprojects No. 5064 (Kyowa Hakko; див WO оцтова кислота, 4-нітроксибутиловий естер [Див. 96/26940); Pharmaprojects No. 5069 (Schering Wenk, et al., Europ. J. Pharmacol. 453 : 319-324 Plough); GF-196960 (Glaxo Wellcome); E-8010 і E(2002)]; 4010 (Eisai); Bay-38-3045 & 38-9456 (Bayer); (ii) мелоксикам, [реєстраційний номер CAS FR229934 і FR226807 (Fujisawa); і Sch-51866. 71125-38-7; описаний в патенті США 4,233,299], Зміст опублікованих патентних заявок і журнаабо його фармацевтично прийнятна сіль чи пролільних статей і, зокрема, загальні формули терапеки; втично активних сполук, включених в формулу цих (ііі) Заміщені похідні бензопірану, описані в заявок і, також, сполук, наведених у Прикладах, [патенті США 6,271,253]. Також похідні бензопіравключені сюди як посилання в усій своїй повноті. ну описані в [патенті США 6,034,256 і 6,077,850 Переважно інгібітор PDEV обирають з групи, поряд з міжнародними публікаціями WO 98/47890 і до якої входять силденафіл, тадалафіл, варденаWO 00/23433]; філ, D A-8159 і 5-[2-етокси-5-(4-етилпіперазин-1(iv) Хромен СОХ2 селективні інгібітори, описаілсульфоніл)піридин-3-іл]-3-етил-2-[2ні в [патенті США 6,077,850 і патенті США метоксиетил]-2,6-дигідро-7Н-піразоло[4,36,034,256]; d]піримідин-7-он. (ν) Сполуки, описані в публікаціях [міжнародНайбільш переважно інгібітором PDE5 є силних патентних заявок WO 95/30656, WO 95/30652, денафіл і його фармацевтично прийнятні солі. WO 96/38418 і WO 96/38442] і сполуки, описані в Цитрат силденафілу є переважною сіллю. публікації [європейської патентної заявки 799823], Сполуки даного винаходу можуть призначатита їх фармацевтично прийнятні похідні; ся в комбінації з донором NO. Отже, наступним (vi) целекоксиб [патент США 5,466,823], валаспектом даного винаходу є забезпечення фармадекоксиб [патент США 5,633,272], деракоксиб [пацевтичного продукту, що містить антагоніст V1a і тент США 5,521,207], рофекоксиб [патент США донор NO у вигляді комбінованого препарату для 5,474,995], еторікоксиб [публікація міжнародної одночасного, окремого або послідовного застосупатентної заявки WO 98/03484], JTE-522 [публікавання при лікуванні дисменореї. ція японської патентної заявки 9052882], або їх Сполуки даного винаходу можуть призначатифармацевтично прийнятна сіль чи проліки; ся в комбінації з L-аргініном, або у вигляді аргіна(vii) Парекоксиб [описаний в патенті США ту. Отже, наступним аспектом даного винаходу є 5,932,598], який є терапевтично ативними пролізабезпечення фармацевтичного продукту, що місками трициклічного Сох-2 селективного інгібітора тить антагоніст V1а і L-аргінін у вигляді комбіновавалдекоксиба [описаного в патенті США ного препарату для одночасного, окремого або 5,633,272], зокрема натрію парекоксиб; послідовного застосування при лікуванні дисмено(viii) АВТ-963 [описаний в публікації міжнародреї. ної патентної заявки WO 00/24719] Сполуки даного винаходу можуть призначати(їх) Німесулід [описаний в патенті США ся в комбінації з Інгібітором СОХ. Отже, наступним 3,840,597], флосулід [обговорюється у J. Carter, аспектом даного винаходу є забезпечення фармаExp. Opin. Ther. Patents, 8(1), 21-29 (1997)], NS-398 цевтичного продукту, що містить антагоніст V1a і [розкрито у патенті США 4,885,367], SD 8381 [опиінгібітор СОХ у вигляді комбінованого препарату саний в патенті США 6,034,256], BMS-347070 [опидля одночасного, окремого або послідовного засаний в патенті США 6,180,651], S-2474 [описаний стосування при лікуванні дисменореї. в публікації європейського патенту 595546] і МКІнгібітори СОХ, корисні для поєднання з спо966 [описаний в патенті США 5,968,974]; луками даного винаходу включають наступні спо(x) Сполуки і фармацевтично прийнятні похідлуки, але не обмежуються ними: ні, описані в [патентах США 6,395,724, 6,077,868, (і) ібупрофен, напроксен, беноксапрофен, 5,994,381, 6,362,209, 6,080,876, 6,133,292, флурбіпрофен, фенопрофен, фенбуфен, кетоп6,369,275, 6,127,545, 6,130,334, 6,204,387, рофен, індопрофен, пірпрофен, карпрофен, окса6,071,936, 6,001,843, 6,040,450, публікації міжнапрозин, прапопрофен, міропрофен, тіоксапрофен, родної патентної заявки WO 96/03392, публікації супрофен, алмінопрофен, тіапрофенова кислота, міжнародної патентної заявки WO 96/24585, патефлупрофен, 4-(4-циклогексил-3-хлорфеніл-4нтах США 6,340,694, 6,376,519, 6,153,787, окомасляна кислота, індометацин, суліндак, тол6,046,217, 6,329,421, 6,239,137, 6,136,831, метін, зомепірак, діклофенак, фенклофенек, алк6,297,282, 6,239,173, 6,303,628, 6,310,079, лофенак, ібуфенак, ізоксепак, фурофенак, тіопі6,300,363, 6,077,869, 6,140,515, 5,994,379, нак, зідометацин, ацетилсаліцилова кислота, 6,028,202, 6,040,320, 6,083,969, 6,306,890, індометацин, піроксикам, теноксикам, набуметон, 6,307,047, 6,004,948, 6,169,188, 6,020,343, кетопролак, азапропазон, мефенамінова кислота, 5,981,576, 6,222,048, 6,057,319, 6,046,236, толфенамінова кислота, дифлунізал, похідні по6,002,014, 5,945,539, 6,359,182, публікації міжнадофілотоксину, ацеметацин, дроксикам, флоктародної патентної заявки WO97/13755, публікацї 47 85692 48 міжнародної патентної заявки WO 96/25928, публікації міжнародної патентної заявки WO 96/374679, До розчину 9,0г трет-бутилового естеру 4публікації міжнародної патентної заявки WO гідразинкарбонілпіперидин-1-карбонової кислоти 95/15316, публікації міжнародної патентної заявки [див. посилання WO 9703986 А1 19970206] WO 95/15315, публікації міжнародної патентної (37ммоль, 1екв.) в 40мл ТГФ, додавали 8,1мл дизаявки WO 96/03385, міжнародній патентній заявці метилацеталю диметилформаміду (55,4ммоль, WO 95/00501, міжнародній патентній заявці WO 1,5екв.). Реакційну перемішували суміш при 50°С 94/15932, публікації міжнародної патентної заявки протягом 4 годин в атмосфері азоту. Розчинник WO 95/00501, публікації міжнародної патентної видаляли при пониженому тиску, залишок розчизаявки WO 94/27980, публікації міжнародної патеняли в 40мл толуолу і додавали 400мг парантної заявки WO 96/25405, публікації міжнародної толуолсульфонової кислоти. Потім суміш нагрівапатентної заявки WO 96/03388, публікації міжнали при 100°С в атмосфері азоту протягом 18 городної патентної заявки WO 96/03387, патенті дин, леткі компоненти видаляли при пониженому США 5,344,991, публікації міжнародної патентної тиску і залишок розділяли між метиленхлоридом і заявки WO 95/00501, публікації міжнародної патеводним розчином бікарбонату натрію. Органічний нтної заявки WO 96/16934, публікації міжнародної шар сушили над сульфатом магнію і фільтрували. патентної заявки WO 96/03392, публікації міжнаЛеткі компоненти видаляли при пониженому тиску родної патентної заявки WO 96/09304, публікації і залишок очищали за допомогою колонкової хроміжнародної патентної заявки WO 98/47890 і пубматографії на силікагелі, використовуючи метилікації міжнародної патентної заявки WO ленхлорид/метанол як елюент (від 98:2 об/об до 00/24719]. 95:5 об/об), одержуючи 8,07г вказаної в заголовку Зміст будь-яких патентних заявок і, зокрема, сполуки у вигляді твердої речовини білого кольору загальні формули терапевтично активних сполук, (81%). 1 включених в формулу цих заявок і, також, сполук, Н ЯМР (400МГц, CD3OD): d 1,42 (с, 9Н), 1,70 наведених у Прикладах, включені сюди як поси(м, 2Н), 2,05 (м, 2Н), 2,50 (с, 3H), 3,00 (м, 2Н), 3,15 лання в усій своїй повноті. (м, 1Н), 4,05 (м, 2Н); Наступні Препаративні Приклади і Приклади РХМС: m/z ХІАT+, 268 [МН]+; ілюструють одержання сполук формули (І). Знайдено : С, 58,26%; Н, 7,96%; N, 15,78%; Спектри 1Н-ядерного магнітного резонансу Розраховано для С 13Н21N3О 3 С, 58,41%, Н, (ЯМР) в усі х випадках підтверджували запропоно7,92%, N, 15,72% вані структури. Хімічні зсуви (d) наведені у мільПрепаративний Приклад 2а: 4-[4-(4йонних долях відносносно тетраметилсилану із Хлорфеніл)-5-метил-4Н-[1,2,4]триазол-3-іл]застосуванням звичайних скорочень для познапіперидин: чення основних піків: наприклад, с - синглет; д дублет; т - триплет; кв - квартет; м - м ултиплет; ш широкий. Мас-спектри (m/z) записували, застосовуючи або електроспрей іонізацію (ЕСІ) або хімічну іонізацію при атмосферному тиску (ХІАТ). Для типових розчинників застосовували наступні скорочення: CDCI3 - дейтерохлороформ; D6-ДMCO дейтеродиметилсульфоксид; CD3OD - дейтерометанол; ТГФ -тетрагідрофуран. Термін "аміак" означає концентрований розчин аміаку у воді, який має питому вагу, що дорівнює 4,0г сполуки з Препаративного Прикладу 1 0,88. Там, де застосовували тонкошарову хрома(15ммоль, 1екв.) розчиняли в 100мл толуолу. Дотографію (ТШХ) мається на увазі ТШХ на силікагедавали 2,1г пара-хлораніліну (16,5ммоль, 1,1екв.), лі, з використанням пластин 60 F254, Rf дорівнює після чого додавали 2мл TFA. Розчин нагрівали відстані, яку пройшла сполука, поділеній на відпри 110°С протягом 16 годин, додавали 2мл of стань, яку пройшов фронт розчинника на пластині TFA і розчин нагрівали при 110°С протягом настудля ТШХ. Як джерело мікрохвильового випроміпних 48 годин. Реакційну суміш о холоджували, нення застосовували дві мікрохвильові печі: Emrys додавали водний розчин бікарбонату натрію і деCreator і Emrys Liberator, обидві від Personal кантували органічну фазу. Водну фазу підлуговуChemistry Ltd. Потужність складала 15-300Вт при вали карбонатом калію і екстрагували 4 рази ме2,45ГГц. Фактичну напругу, що подавали під час тиленхлоридом (50мл). Розчин метиленхлориду проходження реакції, варіювали для того, щоб сушили над сульфатом магнію і видаляли розчинпідтримувати постійну температуру. ник у вакуумі, одержуючи 2,90г вказаної в заголовПрепаративний Приклад 1: 4-(5-Метилку сполуки у вигляді твердої речовини білого ко[1,3,4]оксадіазол-2-іл)-піперидин-1-карбонової кисльору. 1 лоти трет-бутиловий естер Н ЯМР (400МГц, CDCI3): d 1,60-2,00 (м), 2,20 (с, 3H), 2,40-2,80 (м, 5Н), 3,10 (м, 2Н), 7,10 (д,2Н), 7,55 (д, 2Н); РХМС: m/z ХІАT+, 277 [МН]+ Препаративний Приклад 2b: 4-[4-(4Хлорфеніл)-5-метил-4Н-1,2,4-триазол-3іл]піперидину гідрохлорид 49 85692 Розчин хлорводневої кислоти в діоксані (4М, 10мл) додавали до охолодженого (5°С) розчину сполуки з Препаративного Прикладу 1 (1,32г, 4,76ммоль) в метанолі (30мл) і розчин залишали нагріватися до кімнатної температури при перемішуванні протягом і наступних 90 хвилин. Оскільки ТШХ аналіз показав наявність вихідних сполук, до реакційної суміші додатково додавали Розчин хлорводневої кислоти в діоксані (4М, 10мл) і перемішували протягом наступних 4 годин. Реакційну суміш концентрували при зниженому тиску і залишок азеотропували з толуолом (3х), одержуючи вказану у заголовку сполуку, 1,4г. 1 Н ЯМР (400МГц, ДMCO-d6): d 1,86 (м, 4Н), 2,25 (м, 3H), 2,80-2,97 (м, 3H), 3,22 І (м, 2Н), 7,64 (м, 2Н), 7,77 (д, 2Н). Препаративний Приклад 3: 1-(3-Хлорбензоїл)піперидин-4-карбонової кислоти етиловий естер Розчин етилізоніпекотату (27,6 , 175ммоль) у дихлорметані (50мл) додавали краплями протягом 10 хвилин до розчину 3-хлорбензоїлхлориду (20мл, 160ммоль) і триетиламіну (28мл, 200ммоль) у ди хлорметані (500мл), охолодженому до температури від 10 до 15°С. Реакційну перемішували суміш при кімнатній температурі протягом 3 годин і концентрували при зниженому тиску. Залишок розводили ефіром, розчин промивали 1Ν хлорводневою кислотою, розчином карбонату натрію (x3) і насиченим водним розчином хлориду натрію. Потім сушили над MgSO4 і упарювали при зниженому тиску, одержуючи вказану в заголовку сполуку у вигляді твердої речовини, 44,4г. 1 Н ЯМР (400МГц, CDCI3): d 1,24 (т, 3H), 1,622,10 (м, 4Η), 2,58 (м, 1Н), 2,98-3,16 (м, 2Н), 3,70 (м, 1Н), 4,15 (кв, 2Н), 4,49 (м, 1Н), 7,24 (м, 1Н), 7,317,40 (м, 3H). РХМС: m/z (ХІАT+) 296 [МН]+ Препаративний Приклад 4: 1-(3-Хлорбензоїл)піперидин-4-карбонової кислоти гідразид 50 Суміш естеру з Препаративного Прикладу 3 (44,4г, 0,15моль) і гідразин гідрату (30мл, 0,58моль) в метанолі (120мл) кип'ятили протягом 10 годин і залишали охолоджуватись до кімнатної температури. Реакційну суміш концентрували при зниженому тиску і продукт перекристалізовували з етилацетату/етер у, одержуючи вказану у заголовку сполуку у вигляді твердої речовини, 32,5г. 1 Н ЯМР (400МГц, CDCI3): d 1,62-1,98 (м, 4Н), 2,36 (м, 1Н), 2,78-3,09 (м, 2Н), 3,64-4,00 (м, 2Н), 4,65 (м, 1Н), 7,04 (м, 1Н), 7,26 (м, 1Н), 7,36 (м, 3H). РХМС: m/z (ХІАT+) 282 [МН]+ Препаративний Приклад 5: 1-(3-Хлорбензоїл)піперидин-4-карбонова кислота N'-(2-хлор-ацетил)гідразид Ацетилхлорид (4,3мл, 53ммоль) додавали краплями, протягом 30 хвилин, до охолодженого льодом розчину гідразиду з Препаративного Прикладу 4 (10г, 35,5ммоль) і N-метилморфоліну (5,4г, 53ммоль) у дихлорметані (200мл), підтримуючи температуру реакційної суміші нижчою за 10°С. Реакційну суміш залишали охолоджуватись до кімнатної температури і перемішували протягом наступних 18 годин. Реакційну суміш розводили етилацетатом, промивали насиченим розчином бікарбонату натрію, потім насиченим водним розчином хлориду натрію. Розчин сушили над MgSO4, концентрували при зниженому тиску i залишок розтирали з ефіром, одержуючи вказану у заголовку сполуку у вигляді твердої речовини білого кольору, 10,2г. 1 Н ЯМР (400МГц, CD3OD): d 1,66-1,84 (м, 3H), 1,98 (м, 1Н), 2,61 (м, 1Н), 2,99 (м, 1Н), 3,19 (м, 1Н), 3,74 (м, 1Н), 4,14 (с, 2Н), 4,60 (м, 1Н), 7,35 (дд, 1Н), 7,46 (м, 3H). PXMC: m/z (ES+) 358 [MH]+ Препаративний Приклад 6: [4-(5-Хлорметил[1,3,4]оксадіазол-2-іл)-піперидин-1-іл]-(3хлорфеніл)-метанон Трифтороцтовий ангідрид (9,45мл, 57ммоль) додавали краплями протягом 30 хвилин до охолодженого розчину (0-5°С) сполуки з Препаративного Прикладу 5 (10,2г, 28,5ммоль) і піридину (11,5мл, 142,5ммоль) у дихлорметані (300мл). Після завершення додавання, одержану суспензію рожевого кольору перемішували протягом наступних 90 хвилин при 10°С. Реакційну суміш обережно виливали у насичений розчин бікарбонату натрію (600мл) і розділяли шари. Органічну фазу проми 51 85692 52 вали насиченим розчином бікарбонату натрію (x2), Препаративний Приклад 8: 4-(5-Хлорметилсушили над MgSO4 і обробляли активованим ву[1,3,4]оксадіазол-2-іл)-піперидин-1-карбонової кисгіллям. Суміш фільтрували і фільтрат упарювали лоти трет-бутиловий естер при зниженому тиску, одержуючи вказану у заголовку сполуку, 13г. 1 Н ЯМР (400МГц, CD3OD): d 1,80-1,97 (м, 2Н), 2,08 (м, 1Н), 2,22 (м, 1Н), 3,15-3,40 (м, 3H), 3,76 (м, 1Н), 4,56 (м, 1Н), 4,84 (с, 2Н), 7,37 (м, 1Н), 7,48 (м, 3H). PXMC: m/z (ХІАT+) 340 [МН]+ Препаративний Приклад 7: 4-[N'-(2Гідразид з Препаративного Прикладу 7 (5,0г, Хлорацетил)-гідразинокарбоніл]-піперидин-115,6ммоль) суспендували у ди хлорметані (200мл), карбонової кислоти трет-бутиловий естер додавали піридин (6,4мл, 78ммоль) і охолоджували суміш до 10°С. Трифтороцтовий ангідрид (6,6мл, 39ммоль) додавали краплями протягом 15 хвилин і перемішували при кімнатній температурі протягом 3 годин. Реакційну суміш розділяли з водою (50мл), органічний шар сушили над сульфатом магнію, фільтрували і фільтрат упарювали при зниженому тиску. Залишок очищали за допоТрет-бутиловий естер 4-гідразинокарбонілмогою колонкової хроматографії на силікагелі, піперидин-1-карбонової кислоти [див. посилання використовуючи метанол у дихлорметані як елюWO 2000039125, Преп. Приклад 27] (25г, ент (2:98), одержуючи вказану у заголовку сполуку 103ммоль) розчиняли в дихлорметані (300мл) і у вигляді твердої речовини білого кольору (2,95г). 1 потім додавали 4-метилморфолін (12,5мл, Н ЯМР (400МГц, CD3OD): d 1,45 (с, 9Н), 1,74 113ммоль). Суміш охолоджували на крижаній бані (м, 2Н), 2,19 (м, 2Н), 3,04 (м, 2Н), 3,24 (м, 1Н), 4,09 і краплями додавали хлорацетилхлорид (8,2мл, (м, 2Н), 4,85 (с, 2Н) 103ммоль). Реакційну суміш залишали охолоджуПрепаративний Приклад 9а: 4-(5ватись до кімнатної температури і перемішували [1,2,3]Триазол-2-ілметил-[1,3,4]оксадіазол-2-іл)протягом 4 годин. Реакційну суміш розділяли з піперидин-1-карбонової кислоти трет-бутиловий водним розчином гідрокарбонату натрію, сушили естер і І над сульфатом магнію, фільтрували і фільтрат 4-(5-[1,2,3]Триазол-1-ілметилупарювали, одержуючи вказану у заголовку сполу[1,3,4]оксадіазол-2-іл)-піперидин-1-карбонової киску у вигляді твердої речовини майже білого кольолоти трет-бутиловий естер ру (29,6г). PXMC: m/z XIAT 318 [M-H] Суміш сполуки з Препаративного Прикладу 8 (8г, 26,5ммоль), триазолу (3,7г, 53ммоль) і карбонату калію (5,2г, 38ммоль) в Ν,Νдиметилформаміді (60мл) перемішували при кімнатній температурі протягом 18 годин. Суміш фільтрували і фільтрат концентрували при зниженому тиску. Залишок розділяли між етилацетатом і насиченим водним розчином хлориду натрію, розділяли шари і органічний розчин сушили над MgSO4 і концентрували при зниженому тиску, одержуючи вказані у заголовку сполуки у вигляді ізомерів. 1 Н ЯМР (400МГц, CD3 OD): d 1,43 (с, 9Н), 1,621,78 (м, 2Н), 2,02 (м, 2Н), 3,00 (м, 2Н), 3,19 (м, 1Н), 4,03 (м, 2Н), 5,95, 5,99 (2хс, 2Н), [7,77 (с), 7,80 (д), 8,18 (с) всього 2Н]. Препаративний Приклад 9b: 4-(5[1,2,3]Триазол-2-ілметил-[1,3,4]оксадіазол-2-іл)піперидин-1-карбонової кислоти трет-бутиловий естер До суспензії гідразиду з Препаративного Прикладу 170 (132,3г, 375ммоль) в 1-метилімідазолі (120мл) додавали дихлорметан (500мл) і одержаний розчин охолоджували на бані з льодом і ацетоном. Ангідрид трифторметансульфонової кислоти (92мл, 561ммоль) додавали краплями протягом 2,5 годин, підтримуючи температуру реакції нижче 0°С. Після завершення додавання перемішували суміш протягом наступних 20 хвилин. Реакцію зупиняли додаванням 2М хлорводневої кислоти (350мл). Фази розділяли і водний шар екстрагували дихлорметаном (200мл). Об'єднані органічні розчини промивали насиченим водним розчином хлориду натрію, сушили над MgSO4 i упарювали при зниженому тиску. Залишок очищали за допомогою колонкової хроматографії на силікагелі, використовуючи ди хлорметан як елюент, одержуючи вказану у заголовку сполуку у ви гляді в'язкого масла. 53 85692 54 1 Препаративний Приклад 10: (3-Хлорфеніл)-[4Н ЯМР (400МГц, CD3 OD): d 1,42 (с, 9Н), 1,68(5-[1,2,3]триазол-2-ілметил-[1,3,4]оксадіазол-2-іл)1,82 (м, 4Н), 2,62-2,78 (м, 3H), 4,08 (м, 2Н), 5,70 (с, піперидин-1-іл]-метанон 2Н), 7,24 (д, 2Н), 7,56 (д, 2Н), 7,59 (с, 2Н); РХМС: m/z (ХІАT+) 444 [МН]+ Препаративний Приклад 11b: 4-[4-(4хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4Н[1,2,4]триазол-3-іл]-піперидин-1-карбонової кислоти трет-бутиловий естер N-Метилімідазол (4,66г, 56,75ммоль) і дихлорметан (20мл) додавали до біс-ацилгідразиду з Препаративного Прикладу 170 (5,00г, 14,19ммоль) і одержаний розчин охолоджували до -20°С. ДодаСуміш сполуки з Препаративного Прикладу 6 вали ангідрид трифторметансульфонової кислоти (2г, 5,9ммоль), триазолу (810мг, 11,75ммоль) і ка(6,00г, 21,28ммоль), підтримуючи температуру рбонату калію (1,2г, 8,85ммоль) в ацетонітрилі нижче 0°С. Після завершення додавання, реакцію (20мл) перемішували при кімнатній температурі нагрівали до температури оточуючого середовища протягом 30 хвилин і далі ще протягом години при і перемішували протягом 15 годин. Реакцію зупи50°С. Реакційну суміш фільтрували, промивали няли додаванням Н 2О (10мл), фази розділяли і етилацетатом і фільтрат концентрували при зниводний шар екстрагували дихлорметаном (10мл). женому тиску. Одержане коричневе масло роздіОб'єднані органічні фази сушили над сульфатом ляли між етилацетатом і водою, розділяли шари і магнію, фільтрували, дихлорметан відганяли у органічну фазу додатково промивали водою, потім вакуумі і замінювали толуолом, одержуючи розчин насиченим водним розчином хлориду натрію. Розпроміжного оксадіазолу в толуолі (~20мл за об'чин сушили над MgSO4 і упарювали при зниженоємом). До розчину в толуолі додавали 4-хлоранілін му тиску. Неочищений продукт очищали за допо(1,90г, 14,90ммоль) після чого додавали трифтомогою колонкової хроматографії на силікагелі, роцтову кислоту (0,81г, 7,09ммоль) і перемішували використовуючи суміш ди хлорметан:метанол (від при 85°С протягом 5,5 годин. Суміш охолоджували 100:0 до 95:5), одержуючи вказану у заголовку до температури оточуючого середовища i перемісполуку (202мг). шували з 1,8Ν водним розчином аміаку (14мл) 1 Н ЯМР (400МГц, CD3OD): d 1,76-1,90 (м, 2Н), протягом 5 хвилин. Фази розділяли, органічну фа2,02 (м, 1Н), 2,18 (м, 1Н), 3,12-3,38 (м, 3H), 3,72 (м, зу розводили трет-бутилметиловим етером (20мл) 1Н), 4,50 (м, 1Н), 5,97 (с, 2Н), 7,37 (дд, 1Н), 7,41і потім перемішували протягом 15 годин. Одержа7,51 (м, 3H), 7,78 (с, 2Н). ний твердий осад збирали фільтруванням, проми+ + РХМС: m/z (ES ) 373, 375 [МН] вали трет-бутилметиловим етером (2x5мл), одерПрепаративний Приклад 11а: 4-[4-(4жуючи вказану у заголовку сполуку у вигляді Хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4Нтвердої речовини бежевого кольору (2,72г). [1,2,4]триазол-3-іл]-піперидин-1-карбонової кисло1 Н ЯМР (400МГц, CDCI3): d 1,43 (с, 9Н), 1,72 ти трет-бутиловий естер (д, 2Н), 1,85 (шм, 2Н), 2,56 (м, 1Н), 2,66 (шм, 2Н), 4,09 (шд, 2Н), 5,64 (с, 2Н), 7,01 (д, 2Н), 7,43 (д, 2Н), 7,50 (с, 2Н). Препаративний Приклад 12а: 4-[4-(4Хлорфеніл)-5-[1,2,3]триазол-2-ілметил-4Н[1,2,4]триазол-3-іл]-піперидин До розчину сполуки з Препаративного Прикладу 9а (8,8г, 26,5ммоль) додавали трифтороцтову кислоту (1мл, 13,2ммоль) і 4-хлоранілін (5г, 39,75ммоль) у толуолі (200мл) і реакційну перемішували суміш кип'ятили із зворотнім холодильником протягом 5 годин. Охолоджену суміш розводили дихлорметаном, потім промивали 1N розчином гідроксиду натрію і насиченим водним розчином хлориду натрію і упарювали при зниженому тиску. Одержане коричневе масло очищали за допомогою колонкової хроматографії на силікагелі, використовуючи градієнтне елюювання сумішшю ди хлорметан: метанол: 0,88 аміак (від 100:0:0 до 90:10:1) і потім повторно пропускали через колонку, використовуючи суміш етилацетат:метанол:0,88 аміак (від 100:0:0 до 90:10:1), одержуючи вказану у заголовку сполук у (2,3г). 4М Розчин хлорводневої кислоти в діоксані (10мл) додавали до розчину сполуки з Препаративного Прикладу 11а (2,3г, 5,2ммоль) в метанолі (30мл) і перемішували при кімнатній температурі протягом 2 годин. Розчин концентрували при зниженому тиску, залишок розводили дихлорметаном, підлуговували 1Ν розчином гідроксиду натрію до рН 10 і розділяли шари. Водну фазу реекстрагували дихлорметаном, об'єднані органічні розчини сушили над MgSO4 i концентрували при зниженому тиску, одержуючи вказану у заголовку сполуку у ви гляді піни, (1,65г). 55 85692 56 азеотропували з толуолом, одержуючи вказану у Н ЯМР (400МГц, CD3OD): d 1,79 (м, 4Н), 2,48 заголовку сполуку. (м, 2Н), 2,65 (м, 1Н), 3,02 (м, 2Н), 5,70 (с, 2Н), 7,22 1 (д, 2Н), 7,55 (д, 2Н), 7,59 (с, 2Н); Н ЯМР (400МГц, CDCI3): d 2,30 (с, 3H), 4,32 (с, РХМС: m/z (ХІАT+) 344 [МН]+ 2Н), 6,18 (с, 1Н). Препаративний Приклад 12b: 4-[4-(4Препаративний Приклад 15: Етил 2-метил-1НХлорфеніл)-5-[1,2,3]триазол-2-ілметил-4Німідазол-1-ілацетат [1,2,4]триазол-3-іл]-піперидину бiс-паратолуолсульфонат 1 До суміші сполуки з Препаративного Прикладу 11b (6,5г, 14,6ммоль) додавали етилацетат (30мл) і моногідрат пара-толуолсульфонової кислоти (8,4 г, 44,2ммоль) і перемішували при кімнатній температурі протягом 17 годин. Твердий осад збирали фільтруванням, промивали етилацетатом (20мл), одержуючи вказану у заголовку сполук у у вигляді твердої речовини білого кольору (9,32г). 1 Н ЯМР (400МГц, ДMCO-d6): d 1,85 (м, 4Н), 2,26 (с, 6Н), 2,83 (м, 3H), 3,24 (м, 2Н), 5,68 (с, 2Н), 7,10 (д, 4Н), 7,32 (д, 2Н), 7,47 (д, 4Н), 7,54 (д, 2Н), 7,65 (с, 2Н), 8,29 (м, 1Н), 8,49 (м,1Н). PXMC: m/z (ХІАT+) 344 [МН]+ Препаративний Приклад 13: Метил 1Нтетразол-1-ілацетат Карбонат калію (8,42г, 61ммоль) додавали до розчину 2-метилімідазолу (5г, 61ммоль) в тетрагідрофурані (100мл) і перемішували суспензію протягом 30 хвилин. Додавали етил бромацетат (6,75мл, 61ммоль) і перемішували протягом наступних 30 хвилин при кімнатній температурі. Суміш фільтрували, промивали сумішшю дихлорметан:метанол (90:10). Фільтрат упарювали при зниженому тиску і очищали неочищений продукт за допомогою колонкової хроматографії на силікагелі, використовуючи суміш дихлорметан:метанол:0,88 аміак (93:7:0,5) як елюент, одержуючи вказану у заголовку сполуку у вигляді масла, 5,28г. 1 Н ЯМР (400МГц, CDCI3): d 1,26 (т, 3H), 2,35 (с, 3H), 4,22 (кв, 2Н), 4,58 (с, 2Н), 6,81 (с, 1Н),6,94(с, 1Н). PXMC: m/z ХІАT+ 69 [МН]+ Препаративний Приклад 16: 2-(1Н-Тетразол-1іл)ацилгідразид Суміш тетразол-1-ілоцтової кислоти (5г, 39ммоль) і 4М хлорводневої кислоти в діоксані (100мкл) в метанолі (50мл) кип'ятили протягом 18 годин. Охолоджену суміш упарювали при зниженому тиску, одержуючи вказану у заголовку сполуку. 1 Н ЯМР (400МГц, ДMCO-d6): d 3,74 (с, 3H), 5,58 (с, 2Н), 9,39 (с, 1Η); PXMC: m/z ХІАT+ 43 [MH]+ Препаративний Приклад 14: 3-Метилізоксазол-5-ілацетилхлорид Гідразин гідрат (3,2г, 63ммоль) додавали до розчину естеру з Препаративного Прикладу 13 (3г, 21,1ммоль) в метанолі (18мл) і суміш кип'ятили протягом 18 годин. Охолоджену реакційну суміш концентрували при зниженому тиску і залишок азеотропували з толуолом, одержуючи вказану у заголовку сполуку. 1 Н ЯМР (400МГц, ДMCO-d6): d 5,18 (с, 2Н), 9,38 (с, 1Н). РХМС: m/z APCI+ 143 [MH]+ Препаративний Приклад 17: Етиловий естер [1,2,3]триазол-1-іл-оцтової кислоти і етиловий естер [1,2,3]триазол-2-іл-оцтової кислоти Ν,Ν-Диметилформамід (декілька крапель), потім оксалілхлорид (9,5мл, 106ммоль) додавали краплями до охолодженого (10°С) розчину 3метил-ізоксазол-5-ілоцтової кислоти (5г, 35,4ммоль) у дихлорметані (50мл) і розчин залишали нагріватися до кімнатної температури. Перемішували протягом наступних 3 годин, потім концентрували при зниженому тиску. Залишок До суспензії карбонату калію (42,15кг, 305моль) в етанолі (80л) протягом 30 хвилин додавали 1,2,3-триазол (19,00кг, 275моль) і змивали етанолом (2л). Повільно додавали розчин етил бромацетату (45,8кг, 274моль) в етанолі (30л) і змивали етанолом (2л). Весь час температуру реакції підтримували нижче 20°С. Реакційну суміш нагрівали до кімнатної температури і перемішува 57 85692 58 ли протягом ночі. Суспензію фільтрували; залишок промивали етанолом (25л і 17л) і потім фільтрат Вказану у заголовку сполуку одержували з меконцентрували при зниженому тиску. Концентрат тилового естеру 3-метил-1,2,4-оксадіазол-5-ілрозчиняли в етилацетаті (120л) і розчин промиваоцтової кислоти (NL 7807076) і гідразину за процели 1N хлорводневою кислотою (1x40л, 7x20л, дурою, подібною до описаної у Препаративному 4x15л). Промивні води об'єднували і екстрагували Прикладі 16, за винятком того, що використовуваетилацетатом (3x21л). Органічні фази об'єднували 8 еквівалентів гідразину і як розчинник для проли, сушили над сульфатом магнію, фільтрували і ведення реакції використовували ізопропанол. 1 концентрували досуха, одержуючи суміш вказаних Н ЯМР (400МГц, CDCI3): d 2,42 (с, 3H), 3,86 (с, у заголовку сполук (25кг). Аналіз 1Н ЯМР спектрів 2Н), 6,89 (шс, 1Н), 8,18 (шс, 1Н). виявив, що продукт представляє собою суміш (6:5) Препаративний Приклад 21: 2-(Піримідин-2Ν-2/Ν-1 ізомерів. ілокси)ацилгідразид 1 Н ЯМР (400МГц, CDCI3): d 1,25 (м, 3H), 4,13 (кв, 2Н, Ν-1 ізомер), 4,25 (кв, 2Н, N-2 ізомер), 5,20 (с, 2Н, Ν-1 ізомер), 5,22 (с, 2Н, Ν-2 ізомер), 7,70 (с, 2Н, Ν-2 ізомер), 7,77 (с, 2Н, Ν-1 ізомер). Препаративний Приклад 18: Гідразид [1,2,3]триазол-2-іл-оцтової кислоти Суміш етил 2-піримідинілоксиацетату (GB2373186, стадія і, Приклад 368) (4,4г, 24,15ммоль) і гідразин гідрат (5мл, 160ммоль) в ізопропанолі (30мл) кип'ятили протягом 1 години. Потім суміш охолоджували, концентрували при зниженому тиску і залишок очищали за допомогою колонкової хроматографії на силікагелі, викорисГідразин гідрат (8,65кг, 270моль) додавали до товуючи суміш дихлорметан:метанол:0,88 аміак охолодженого (
ДивитисяДодаткова інформація
Назва патенту англійськоюTriazole derivatives as vasopressin antagonists
Автори англійськоюBryans Justin Stephen, Johnson Patrick Stephen, Roberts Lee Richard, Ryckmans Thomas
Назва патенту російськоюПроизводные триазола как антагонисты вазопрессина
Автори російськоюБраянс Джастин Стивен, Джонсон Патрик Стивен, Робертс Ли Ричард, Рикманс Томас
МПК / Мітки
МПК: C07D 405/14, C07D 471/04, C07D 401/14, C07D 401/04, A61K 31/454, C07D 413/14, A61P 25/00
Мітки: вазопресину, триазолу, похідні, антагоністи
Код посилання
<a href="https://ua.patents.su/81-85692-pokhidni-triazolu-yak-antagonisti-vazopresinu.html" target="_blank" rel="follow" title="База патентів України">Похідні триазолу як антагоністи вазопресину</a>
Попередній патент: Тверда ветеринарно-медична композиція, що містить ароматизатор та/або смакову речовину
Наступний патент: Тверда фармацевтична композиція для перорального застосування, спосіб її виробництва та її застосування
Випадковий патент: Спосіб оздоровлення господарств з неспецифічними пара алергічними реакціями на туберкулін у великої рогатої худоби