Інгібування il17 і ifn-гамма для лікування аутоімунного запалення
Номер патенту: 110048
Опубліковано: 10.11.2015
Автори: Лебан Йоханн, Таслер Штефан, Зеб Вель, Шевр'є Карін
Формула / Реферат
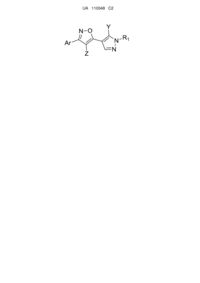
1. Сполука загальної формули (І)
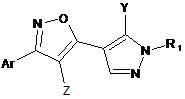 формула (І)
формула (І)
і її фармацевтично прийнятні солі або сольвати,
дe
R1 означає арил, гетероарил, циклоалкіл, гетероцикліл або алкіл, який може бути заміщений одним або декількома замісниками R';
Аr означає арил, циклоалкіл, гетероцикліл або гетероарил, який може бути заміщений одним або декількома замісниками R';
Z означає арил, гетероарил, циклоалкіл або гетероцикліл, який може бути заміщений одним або декількома замісниками R';
Y означає Н, галоген, галогеналкіл, алкіл або складний алкіловий ефір, який може бути заміщений одним або декількома замісниками R';
R' незалежно означає Н, -CO2R", -CONHR", -CR''O, -SO2N(R")2, -SO2NHR", -NR''-CO-галогеналкіл, -NO2, -NR"-SО2-галогеналкіл, -NR"-SО2-алкіл, -SО2-алкіл, -NR''-CO-алкіл, -CN, алкіл, циклоалкіл, аміноалкіл, алкіламіно, алкокси, -ОН, -SH, алкілтіо, гідроксіалкіл, гідроксіалкіламіно, галоген, галогеналкіл, галогеналкокси, аміно, гетероцикліл, арил, галогенарил, галогенарилалкіл, арилалкіл або гетероарил;
R" незалежно означає Н, галогеналкіл, гідроксіалкіл, аміно, алкокси, -N=C(R')2, -NR'-CO-R', -CR'O, -CO2R', алкіл, циклоалкіл, арил, галогенарил, галогенарилалкіл, гетероарил, гетероцикліл, арилалкіл або аміноалкіл, які необов'язково заміщені одним або декількома замісниками R'.
2. Сполука за пунктом 1, де
Аr означає арил або гетероарил, який може бути заміщений одним або декількома замісниками R';
R1, Z, Y, R' і R" приймають значення, визначені у пункті 1.
3. Сполука за пунктом 1, де
R1 означає арил або гетероарил, який може бути заміщений одним або декількома замісниками R';
Аr означає арил або гетероарил, який може бути заміщений одним або декількома замісниками R';
Z, Y, R' і R" приймають значення, визначені у пункті 1.
4. Сполука за пунктом 1, де
R1 означає арил або гетероарил, який може бути заміщений одним або декількома замісниками R';
Аr означає арил або гетероарил, який може бути заміщений одним або декількома замісниками R';
Z означає арил, циклоалкіл, гетероцикліл або гетероарил, який може бути заміщений одним або декількома замісниками R';
Y означає Н, галоген, галогеналкіл або алкіл, який може бути заміщений одним або декількома замісниками R';
R' незалежно означає Н, -CO2R", -CONHR", -CR''O, -SO2N(R")2, -SO2NHR", -CN, алкіл, циклоалкіл, аміноалкіл, алкокси, -ОН, гідроксіалкіл, галоген, галогеналкіл, галогеналкокси, аміно, гетероцикліл, арил, галогенарил, галогенарилалкіл, арилалкіл або гетероарил;
R" незалежно означає Н, галогеналкіл, гідроксіалкіл, аміно, алкокси, -N=C(R')2, -NR'-CO-R', -CR'O, -CO2R', алкіл, циклоалкіл, арил, галогенарил, галогенарилалкіл, гетероарил, гетероцикліл, арилалкіл або аміноалкіл, які необов'язково заміщені одним або декількома замісниками R'.
5. Сполука за пунктом 1, де
R1 означає арил або гетероарил, який може бути заміщений одним або декількома замісниками R';
Аr означає арил або гетероарил, який може бути заміщений одним або декількома замісниками R';
Z означає арил, циклоалкіл, гетероцикліл або гетероарил, який може бути заміщений одним або декількома замісниками R';
Y означає Н, галоген, галогеналкіл або алкіл, який може бути заміщений одним або декількома замісниками R';
R' незалежно означає Н, -CO2R", -SO2N(R")2, -SO2NHR", -CN, алкіл, алкокси, -ОН, гідроксіалкіл, галоген, галогеналкіл, галогеналкокси, гетероцикліл, арил, галогенарил, галогенарилалкіл, арилалкіл або гетероарил;
R" незалежно означає Н, галогеналкіл, гідроксіалкіл, аміно, алкокси, -N=C(R')2, -NR'-CO-R', -CR'O, -CO2R', алкіл, циклоалкіл, арил, галогенарил, галогенарилалкіл, гетероарил, гетероцикліл, арилалкіл або аміноалкіл, які необов'язково заміщені одним або декількома замісниками R'.
6. Сполука за пунктом 1, де
R1 означає арил або гетероарил, який може бути заміщений одним або декількома замісниками R';
Аr означає арил або гетероарил, який може бути заміщений одним або декількома замісниками R';
Z означає арил, циклоалкіл, гетероцикліл або гетероарил, який може бути заміщений одним або декількома замісниками R';
Y означає Н, галоген, галогеналкіл або алкіл, який може бути заміщений одним або декількома замісниками R';
R' незалежно означає Н, -CO2R", -CONHR", -CR''O, -SO2N(R")2, -SO2NHR", -CN, алкіл, алкокси, -ОН, галоген, галогеналкіл або галогеналкокси;
R" незалежно означає Н, галогеналкіл, гідроксіалкіл, аміно, алкокси, -N=C(R')2, -NR'-CO-R', -CR'O, -CO2R', алкіл, циклоалкіл, арил, галогенарил, галогенарилалкіл, гетероарил, гетероцикліл, арилалкіл або аміноалкіл, які необов'язково заміщені одним або декількома замісниками R'.
7. Сполука за будь-яким із пунктів 1-6, де
R1 вибирають із групи, що включає феніл, який необов'язково заміщений одним або декількома замісниками, окремо вибраними з трифторметилу, фтору, хлору, брому, нітро, NH2, -CN, -NHCO-C1-4-алкілу, метокси, С1-4-алкілу, -SO2NH2 або -SО2NH-С1-4-алкілу; піридил, який необов'язково заміщений одним або декількома вищезазначеними замісниками для фенілу; піримідил, який необов'язково заміщений одним або декількома вищезазначеними замісниками для фенілу; тієніл, який необов'язково заміщений одним замісником -СОО-С1-4алкілом; 1,1-діоксотетрагідротієніл, 2,2,2-трифторетил, ізопропіл, ізобутил, 2-метоксіетил, тетрагідропіран-4-ілметил, 2-морфоліноетил, піридин-2-ілметил і тетрагідрофуран-2-ілметил;
Аr вибирають із групи, що включає феніл і піридил, які можуть бути заміщені одним або декількома замісниками, незалежно вибраними з фтору, метокси або хлору;
Z вибирають із групи, що включає феніл або гетероарил, який може бути заміщений одним або декількома замісниками, вибраними з групи, що включає С1-4алкіл, С1-4галогеналкіл, водень, гідроксил, С1-4алкокси і С1-4алкоксикарбоніл;
Y вибирають із групи, що включає Н, трифторметил і метоксикарбоніл.
8. Сполука за будь-яким із пунктів 1-6, де
R1 вибирають із групи, що включає феніл, який необов'язково заміщений одним або декількома замісниками, окремо вибраними з фтору, хлору, брому, нітро, NH2, -CN, -NHCO-C1-4-алкілу, метокси, т-бутилу, -SO2NH2 або -SО2NН-ізопропілу; піридил; піримідил, який необов'язково заміщений одним або декількома замісниками, вибраними з метилу або трифторметилу; тієніл, який необов'язково заміщений одним замісником -СОО-метилом, 1,1-діоксотетрагідротієніл, 2,2,2-трифторетил, ізопропіл, ізобутил, 2-метоксіетил, тетрагідропіран-4-ілметил, 2-морфоліноетил, піридин-2-ілметил і тетрагідрофуран-2-ілметил;
Аr вибирають із групи, що включає феніл, 2,6-дифторфеніл, 2-хлор-6-фторфеніл, 2-хлор-6-метоксифеніл, 2-фторфеніл, 2-хлорфеніл, 2,6-дихлорфеніл, 2,4-дихлорфеніл, 3-фторпіридин-4-іл, 3,5-дихлорпіридин-4-іл і 3,5-дифторпіридин-4-іл;
Z вибирають із групи, що включає феніл, тетразоліл, тіазоліл, 1,3,4-оксадіазоліл, оксазоліл, 1,3,4-тіадіазоліл, фураніл і тіофеніл, які можуть бути заміщені одним або декількома замісниками, вибраними з групи, що включає метил, трифторметил, водень, гідроксил, метокси, метоксикарбоніл і етоксіоксикарбоніл;
Y вибирають із групи, що включає Н, трифторметил і метоксикарбоніл.
9. Сполука за будь-яким із пунктів 1-6, де
R1 вибирають із групи, що включає феніл, 2-фторфеніл, 2-метоксифеніл, 2-хлорфеніл, 2-бромфеніл, 2-нітрофеніл, 2-амінофеніл, 4-фторфеніл, 4-трет-бутилфеніл, 3-фторфеніл, 3-хлорфеніл, 3-ціанофеніл, 3-ацетамідофеніл, 2-ацетамідофеніл, 3-аміносульфонілфеніл, 3-(ізопропіламіно)сульфонілфеніл, 3-нітрофеніл, 3-амінофеніл, 2,4-дифторфеніл, 3,5-дифторфеніл, 3,5-дихлорфеніл, 2,3,5,6-тетрафторфеніл, 2-піридил; 3-піридил; 4-піридил; 4-трифторметилпіримід-2-ил, 2,6-диметилпіримід-4-ил, 2-метоксикарбонілтієн-3-іл, 1,1-діоксотетрагідротієніл, 2,2,2-трифторетил, ізопропіл, ізобутил, 2-метоксіетил, тетрагідропіран-4-ілметил, 2-(морфолін-4-іл)етил і тетрагідрофуран-2-ілметил;
Аr вибирають із групи, що включає феніл, 2-хлор-6-фторфеніл, 2-фторфеніл, 2-хлорфеніл, 2,6-дихлорфеніл, 2,4-дихлорфеніл, 3-фторпіридин-4-іл і 3,5-дифторпіридин-4-іл;
Z вибирають із групи, що включає 1Н-тетразол-5-іл, 4-метилтіазол-2-іл, тіазол-2-іл, 5-(трифторметил)-1,3,4-оксадіазол-2-іл, 5-метил-1,3,4-оксадіазол-2-іл, 1,3,4-оксадіазол-2-іл, оксазол-5-іл, 4-гідрокситіазол-2-іл, 4-метокситіазол-2-іл, 5-метил-1,3,4-тіадіазол-2-іл, 1,3,4-тіадіазол-2-іл, фуран-3-іл, фуран-2-іл, тіофен-3-іл, феніл, 4-метоксикарбонілтіазол-2-іл і 4-етоксикарбонілтіазол-2-іл;
Y вибирають із групи, що включає Н, трифторметил і метоксикарбоніл.
10. Сполука за будь-яким із пунктів 1-9, де сполуку вибирають із групи, що включає сполуки прикладів даного винаходу:
3-(2-хлор-6-фторфеніл)-5-(1-(3-хлорфеніл)-5-(трифторметил)-1Н-піразол-4-іл)-4-(4-метилтіазол-2-іл)ізоксазол,
3-(2-хлор-6-фторфеніл)-5-(1-(3-хлорфеніл)-5-(трифторметил)-1Н-піразол-4-іл)-4-(тіазол-2-іл)ізоксазол,
2-(3-(2-хлор-6-фторфеніл)-5-(1-(3-фторфеніл)-5-(трифторметил)-1Н-піразол-4-іл)ізоксазол-4-іл)-5-(трифторметил)-1,3,4-оксадіазол,
2-(3-(2-хлор-6-фторфеніл)-5-(1-(3-фторфеніл)-5-(трифторметил)-1Н-піразол-4-іл)ізоксазол-4-іл)-1,3,4-оксадіазол,
3-(2-хлор-6-фторфеніл)-5-(1-(3-хлорфеніл)-5-(трифторметил)-1Н-піразол-4-іл)-4-(оксазол-5-іл)ізоксазол,
3-(2-хлор-6-фторфеніл)-5-(1-(3-фторфеніл)-5-(трифторметил)-1Н-піразол-4-іл)-4-(4-метокситіазол-2-іл)ізоксазол,
2-(3-(2-хлор-6-фторфеніл)-5-(1-(2-фторфеніл)-5-(трифторметил)-1Н-піразол-4-іл)ізоксазол-4-іл)-5-метил-1,3,4-оксадіазол,
3-(2-хлор-6-фторфеніл)-5-(1-(2-фторфеніл)-5-(трифторметил)-1Н-піразол-4-іл)-4-(5-метил-1,3,4-тіадіазол-2-іл)ізоксазол,
3-(2-хлор-6-фторфеніл)-5-(1-(3-фторфеніл)-5-(трифторметил)-1Н-піразол-4-іл)-4-фенілізоксазол,
3-(2-хлор-6-фторфеніл)-5-(1-(3-фторфеніл)-5-(трифторметил)-1Н-піразол-4-іл)-4-(тіофен-3-іл)ізоксазол,
3-(2-хлор-6-фторфеніл)-5-(1-(3-фторфеніл)-5-(трифторметил)-1Н-піразол-4-іл)-4-(фуран-2-іл)ізоксазол,
метил-2-(3-(2-хлор-6-фторфеніл)-5-(1-(3-фторфеніл)-5-(трифторметил)-1Н-піразол-4-іл)ізоксазол-4-іл)тіазол-4-карбоксилат,
3-(2-хлор-6-фторфеніл)-5-(1-(3-хлорфеніл)-5-(трифторметил)-1Н-піразол-4-іл)-4-(5-метил-1,3,4-тіадіазол-2-іл)ізоксазол,
2-(3-(2-хлор-6-фторфеніл)-5-(1-(3-хлорфеніл)-5-(трифторметил)-1Н-піразол-4-іл)ізоксазол-4-іл)-5-метил-1,3,4-оксадіазол,
2-(3-(2-хлор-6-фторфеніл)-5-(1-(3-хлорфеніл)-5-(трифторметил)-1Н-піразол-4-іл)ізоксазол-4-іл)-1,3,4-оксадіазол,
3-(2-хлор-6-фторфеніл)-5-(1-(3-хлорфеніл)-5-(трифторметил)-1Н-піразол-4-іл)-4-(фуран-2-іл)ізоксазол,
3-(2-хлор-6-фторфеніл)-5-(1-(3-хлорфеніл)-5-(трифторметил)-1Н-піразол-4-іл)-4-(фуран-3-іл)ізоксазол,
3-(2-хлор-6-фторфеніл)-5-(1-(3-хлорфеніл)-5-(трифторметил)-1Н-піразол-4-іл)-4-(1,3,4-тіадіазол-2-іл)ізоксазол,
3-(2-хлор-6-фторфеніл)-5-(1-(2-фторфеніл)-5-(трифторметил)-1Н-піразол-4-іл)-4-(фуран-3-іл)ізоксазол,
2-(3-(2-хлор-6-фторфеніл)-5-(1-(піридин-3-іл)-5-(трифторметил)-1Н-піразол-4-іл)ізоксазол-4-іл)-5-метил-1,3,4-оксадіазол,
3-(2-хлор-6-фторфеніл)-4-(5-метил-1,3,4-тіадіазол-2-іл)-5-(1-(піридин-3-іл)-5-(трифторметил)-1Н-піразол-4-іл)ізоксазол,
3-(2-хлор-6-фторфеніл)-4-(5-метил-1,3,4-тіадіазол-2-іл)-5-(1-(піридин-4-іл)-5-(трифторметил)-1Н-піразол-4-іл)ізоксазол,
3-(2-хлор-6-фторфеніл)-4-(фуран-3-іл)-5-(1-(піридин-4-іл)-5-(трифторметил)-1Н-піразол-4-іл)ізоксазол,
2-(3-(2-хлор-6-фторфеніл)-5-(1-(піридин-2-іл)-5-(трифторметил)-1Н-піразол-4-іл)ізоксазол-4-іл)-1,3,4-оксадіазол,
2-(3-(2-хлор-6-фторфеніл)-5-(1-(піридин-2-іл)-5-(трифторметил)-1Н-піразол-4-іл)ізоксазол-4-іл)-5-метил-1,3,4-оксадіазол,
3-(2-хлор-6-фторфеніл)-4-(5-метил-1,3,4-тіадіазол-2-іл)-5-(1-(піридин-2-іл)-5-(трифторметил)-1Н-піразол-4-іл)ізоксазол та
3-(2-хлор-6-фторфеніл)-5-(1-(2-фторфеніл)-5-(трифторметил)-1Н-піразол-4-іл)-4-(тіазол-2-іл)ізоксазол.
11. Сполука за будь-яким із пунктів 1-10 для застосування як лікарського засобу.
12. Сполука за будь-яким із пунктів 1-10 для застосування при лікуванні захворювання або показання, вибраного з групи, що складається з псоріазу, псоріатичного артриту, аутоімунного тиреоїдиту, базедової хвороби, ревматоїдного артриту, вітиліго, хвороби Крона, неспецифічного виразкового коліту, запальної хвороби кишечнику, анкілозуючого спондиліту, діабету типу 1, розсіяного склерозу, глютенової хвороби, системного червоного вовчака, увеїту, хвороби Бехчета, атопічного дерматиту, червоного плоского лишаю, синдрому Шегрена, грижі міжхребцевих дисків, акне, реакції трансплантат проти хазяїна, реакції хазяїн проти трансплантата і остеоартриту.
13. Застосування сполук формули (І) за будь-яким з пунктів 1-10 і їх фармакологічно переносимих солей для приготування лікарського засобу для застосування при лікуванні захворювання або терапевтичного показання, при якому є сприятливим інгібування інтерлейкіну-17 (IL-17) і/або інтерферону-g (INF-g).
14. Застосування за пунктом 12, де захворювання або показання вибирають з групи, що складається з псоріазу, псоріатичного артриту, аутоімунного тиреоїдиту, базедової хвороби, ревматоїдного артриту, вітиліго, хвороби Крона, неспецифічного виразкового коліту, запальної хвороби кишечнику, анкілозуючого спондиліту, діабету типу 1, розсіяного склерозу, глютенової хвороби, системного червоного вовчака, увеїту, хвороби Бехчета, атопічного дерматиту, червоного плоского лишаю, синдрому Шегрена, грижі міжхребцевих дисків, акне, реакції трансплантат проти хазяїна, реакції хазяїн проти трансплантата і остеоартриту.
Текст
Реферат: Даний винахід стосується сполук загальної формули (І) і їх фармацевтично прийнятних солей або сольватів як протизапальних і імуномодулюючих засобів. формула (I) UA 110048 C2 (12) UA 110048 C2 UA 110048 C2 5 10 15 20 25 30 35 40 45 50 IL-17 родина цитокінів була пов’язана з патогенезом аутоімунних захворювань й, як правило, на неї покладають провину за патогенні симптоми аутоімунного запалення. Надекспресія IL-17 є відмінною рисою аутоімунних захворювань, таких як ревматоїдний артрит, системний червоний вовчак, запальна хвороба кишечнику, розсіяний склероз і псоріаз (Yao Z і ін., J Immunol, 155(12), 1995, 5483-6. Chang S H, і ін., Cytokine, 46, 2009, 7-11; Hisakata Yamada і ін., Journal of Inflamm. Res., 3, 2010, 33-44)). IL-17 родина цитокінів включає шість членів, із яких найкраще охарактеризовані IL-17A і IL-17F. IL-17A і IL-17F існують у вигляді гомо-, а також у вигляді гетеродимерів (IL-17AA, IL-17AF, IL-17FF). IL-17A і IL-17F чітко пов’язують із запаленням (Gaffen S H, Cytokine, 43, 2008, 402-407; Torchinsky M B і ін., Cell. Mol. Life Sci., 67, 2010, 1407-1421). Секреція IL-17 переважно викликається особливим підтипом Т-хелперних клітин, називаним TH-17 клітини. Було показано, що IL-23, TGFβ і IL-6 є важливими факторами, що приводять до перетворення наївних CD4+ T-клітин на TH17 клітини. Також було повідомлено, що TGFβ і IL-6 в синергізмі сильно індукують TH17 диференціацію. Важливими чинниками транскрипції для секреції IL-17 із TH17 клітин, є RORγt і STAT3 (Ivanov, I і ін. Cell 126, 2006, 1121-1133). IL-17 індукує прозапальні цитокіни (IL-6, TNF-α і IL-1b) і хемокіни (CXCL1, GCP-2, CXCL8 або IL-8, CINC, MCP-1). Це збільшує вироблення оксиду азоту, простагландину E2 і матричних металопротеїназ. Внаслідок цих подій виникає інфільтрація нейтрофілів, пошкодження тканин і хронічне запалення (PECK A і ін., Clin Immunol., 132(3), 2009, 295-304). До усвідомлення важливості IL-17 в аутоімунному запаленні, IFN-гамма, одержаний з TH1 клітин, вважали важливим цитокіном, який управляє аутоімунними порушеннями (Takayanagi H і ін. Nature, 408, 2000, 600-605. Huang W. і ін. Arthritis Res. Ther., 5, 2002, R49-R59). Секреція IFN-гамма є основною рисою лінії TH1 ефекторних клітин, причому секреція регулюється факторами транскрипції T-bet і STAT4 (Bluestone JA і ін. Nat Rev Immunol, 11, 2009, 811-6). Інфільтрація активованих T-клітин і підвищення M-CSF, IL-10 і TNF підтверджують цю думку (Yamanda H і ін. Ann. Rheu. Dis., 67, 2008, 1299-1304; Kotake S і ін. Eur. J. Immunol, 35, 2005, 3353-3363). Останнім часом, була запропонована більш складна картина, де гібридні TH17/TH1 клітини, індуковані IL-23 і IL-6 узгоджено з IL-1 секретують IL-17 і IFN-гамма. Ці клітини знаходяться під контролем факторів транскрипції RORγt і T-bet, підтверджуючи думку, що вони є істинними гібридами TH1 і TH17 клітин. Також було показано, що ці подвійні продукуючі клітини є патогенними видами в IBD і EAE (Buonocore S і ін. Nature, 464, 2010, 1371-5; Ghoreshi K. і ін. Nature, 467, 2010, 967-971). Сполуки, які націлені на IL-17 і IFN-гамма і пригнічують їх, потенційно придатні для лікування аутоімунних порушень. Ефективність блокування IL-17 передачі сигналів як терапевтичного лікування аутоімунних захворювань вже була доведена в клінічних дослідженнях з, наприклад, моноклональними антитілами проти IL-17A (AIN457, секукінумаб; Ly2439821, іксекізумаб; RG4934) і/або IL-17 рецептором IL-17RA (AMG827, бродалумаб). Про позитивні результати повідомляли у випадку лікування ревматоїдного артриту, псоріазу і увеїту (Hueber W і ін., Sci. Transl. Med., 2, 2010, 52ra72, DOI: 10.1126/scitranslmed.3001107; van den Berg W B і ін., Nat. Rev. Rheumatol., 5, 2009, 549-553), анкілозуючого спондиліту і спондилоартриту (Song I-H і ін., Curr. Opin. Rheumatol., 23, 2011, 346-351). Секукінумаб на даний час вивчається на стадії клінічних досліджень для лікування псоріатичного артриту, хвороби Бехчета, увеїту, запальної хвороби кишечнику, хвороби Крона, розсіяного склерозу (Kopf M і ін., Nat. Rev. Drug Disc., 9, 2010, 703-718; Song I-H і ін., Curr. Opin. Rheumatol., 23, 2011, 346-351). Бродалумаб, іксекізумаб і RG4934 на даний час знаходяться на стадії клінічних досліджень для лікування ревматоїдного артриту, псоріазу і/або псоріатичного артриту (Kopf M і ін., Nat. Rev. Drug Disc., 9, 2010, 703-718; clinicaltrials.gov; Medicines in development for skin diseases, 2011, опубл. PhRMA, www.phrma.com). Що стосується блокування IFN-гамма передачі сигналів як терапевтичного лікування аутоімунних захворювань, на стадії клінічних досліджень для лікування системного червоного вовчака на даний час знаходиться IFN-гамма специфічне моноклональне антитіло AMG811 (Kopf M і ін., Nat. Rev. Drug Disc., 9, 2010, 703-718). Даний винахід відноситься до сполуки формули (I) 1 UA 110048 C2 формула (I) 5 10 15 20 і до її фармацевтично прийнятної солі або сольвату, де 1 R означає арил, гетероарил, циклоалкіл, гетероцикліл або алкіл, який може бути заміщений одним або декількома замісниками R’ Ar означає арил, циклоалкіл, гетероцикліл або гетероарил, який може бути заміщений одним або декількома замісниками R’; Z означає арил, гетероарил, циклоалкіл або гетероцикліл, який може бути заміщений одним або декількома замісниками R’; Y означає H, галоген, галогеналкіл, алкіл або складний алкіловий ефір, який може бути заміщений одним або декількома замісниками R’; R’ незалежно означає H, -CO2R’’, -CONHR’’, -CR’’O, -SO2N(R’’)2, -SO2NHR’’, -NR’’-CO-галогеналкіл, -NO2, -NR’’-SO2-галогеналкіл, -NR’’-SO2-алкіл, -SO2-алкіл, -NR’’-CO-алкіл, -CN, алкіл, циклоалкіл, аміноалкіл, алкіламіно, алкокси, -OH, -SH, алкілтіо, гідроксіалкіл, гідроксіалкіламіно, галоген, галогеналкіл, галогеналкокси, аміно, гетероцикліл, арил, галогенарил, галогенарилалкіл, арилалкіл або гетероарил; R’’ незалежно означає H, галогеналкіл, гідроксіалкіл, аміно, алкокси, -N=C(R’)2, -NR’-CO-R’, CR’O, -CO2R’, алкіл, циклоалкіл, арил, галогенарил, галогенарилалкіл, гетероарил, гетероцикліл, арилалкіл або аміноалкіл, які необов’язково заміщені одним або декількома замісниками R’. Даний винахід додатково відноситься до сполуки формули (I) формула (I) 25 30 35 40 і до її фармацевтично прийнятної солі або сольвату, де 1 R означає арил, гетероарил, циклоалкіл, гетероцикліл або алкіл, який може бути заміщений одним або декількома замісниками R’ Ar означає арил, циклоалкіл, гетероцикліл або гетероарил, який може бути заміщений одним або декількома замісниками R’; Z означає арил, гетероарил, циклоалкіл або гетероцикліл, який може бути заміщений одним або декількома замісниками R’; Y означає H, галоген, галогеналкіл або алкіл, який може бути заміщений одним або декількома замісниками R’; R’ незалежно означає H, -CO2R’’, -CONHR’’, -CR’’O, -SO2N(R’’)2, -SO2NHR’’, -NR’’-CO-галогеналкіл, -NO2, -NR’’-SO2-галогеналкіл, -NR’’-SO2-алкіл, -SO2-алкіл, -NR’’-CO-алкіл, -CN, алкіл, циклоалкіл, аміноалкіл, алкіламіно, алкокси, -OH, -SH, алкілтіо, гідроксіалкіл, гідроксіалкіламіно, галоген, галогеналкіл, галогеналкокси, аміно, гетероцикліл, арил, галогенарил, галогенарилалкіл, арилалкіл або гетероарил; R’’ незалежно означає H, галогеналкіл, гідроксіалкіл, аміно, алкокси, -N=C(R’)2, -NR’-CO-R’, CR’O, -CO2R’, алкіл, циклоалкіл, арил, галогенарил, галогенарилалкіл, гетероарил, гетероцикліл, арилалкіл або аміноалкіл, які необов’язково заміщені одним або декількома замісниками R’. У кращому варіанті здійснення, даний винахід відноситься до сполуки формули (I) і її фармацевтично прийнятної солі або сольвату, де 2 UA 110048 C2 1 5 10 15 20 25 30 35 40 45 50 55 60 R означає арил, який може бути заміщений одним або декількома замісниками R’. У більш кращому варіанті здійснення, даний винахід відноситься до сполуки формули (I) і її фармацевтично прийнятної солі або сольвату, де 1 R означає гетероарил, який може бути заміщений одним або декількома замісниками R’. У більш кращому варіанті здійснення, даний винахід відноситься до сполуки формули (I) і її фармацевтично прийнятної солі або сольвату, де Ar означає арил, який може бути заміщений одним або декількома замісниками R’. У більш кращому варіанті здійснення, даний винахід відноситься до сполуки формули (I) і її фармацевтично прийнятної солі або сольвату, де Ar означає гетероарил, який може бути заміщений одним або декількома замісниками R’. У більш кращому варіанті здійснення, даний винахід відноситься до сполуки формули (I) і її фармацевтично прийнятної солі або сольвату, де Z означає арил, який може бути заміщений одним або декількома замісниками R’. У більш кращому варіанті здійснення, даний винахід відноситься до сполуки формули (I) і її фармацевтично прийнятної солі або сольвату, де Z означає гетероарил, який може бути заміщений одним або декількома замісниками R’. У більш кращому варіанті здійснення, даний винахід відноситься до сполуки формули (I) і її фармацевтично прийнятної солі або сольвату, де Z означає гетероцикліл, який може бути заміщений одним або декількома замісниками R’. У більш кращому варіанті здійснення, даний винахід відноситься до сполуки формули (I) і її фармацевтично прийнятної солі або сольвату, де Z означає циклоалкіл, який може бути заміщений одним або декількома замісниками R’. У більш кращому варіанті здійснення, даний винахід відноситься до сполуки формули (I) і її фармацевтично прийнятної солі або сольвату, де Y означає галоген, який може бути заміщений одним або декількома замісниками R’. У більш кращому варіанті здійснення, даний винахід відноситься до сполуки формули (I) і її фармацевтично прийнятної солі або сольвату, де Y означає галогеналкіл, який може бути заміщений одним або декількома замісниками R’. У більш кращому варіанті здійснення, даний винахід відноситься до сполуки формули (I) і її фармацевтично прийнятної солі або сольвату, де Y означає алкіл, який може бути заміщений одним або декількома замісниками R’. В іншому кращому варіанті здійснення, даний винахід відноситься до сполуки формули (I) і її фармацевтично прийнятної солі або сольвату, де 1 R означає арил, гетероарил, циклоалкіл, гетероцикліл або алкіл, який може бути заміщений одним або декількома замісниками R’; Ar означає арил або гетероарил, який може бути заміщений одним або декількома замісниками R’; Z означає арил, гетероарил, циклоалкіл або гетероцикліл, який може бути заміщений одним або декількома замісниками R’; Y означає H, галоген, галогеналкіл або алкіл, який може бути заміщений одним або декількома замісниками R’; R’ незалежно означає H, -CO2R’’, -CONHR’’, -CR’’O, -SO2N(R’’)2, -SO2NHR’’, -NR’’-CO-галогеналкіл, -NO2, -NR’’-SO2-галогеналкіл, -NR’’-SO2-алкіл, -SO2-алкіл, -NR’’-CO-алкіл, -CN, алкіл, циклоалкіл, аміноалкіл, алкіламіно, алкокси, -OH, -SH, алкілтіо, гідроксіалкіл, гідроксіалкіламіно, галоген, галогеналкіл, галогеналкокси, аміно, гетероцикліл, арил, галогенарил, галогенарилалкіл, арилалкіл або гетероарил; R’’ незалежно означає H, галогеналкіл, гідроксіалкіл, аміно, алкокси, -N=C(R’)2, -NR’-CO-R’, CR’O, -CO2R’, алкіл, циклоалкіл, арил, галогенарил, галогенарилалкіл, гетероарил, гетероцикліл, арилалкіл або аміноалкіл, які необов’язково заміщені одним або декількома замісниками R’. 3 UA 110048 C2 5 10 15 20 25 30 35 40 45 50 55 60 В іншому кращому варіанті здійснення, даний винахід відноситься до сполуки формули (I) і її фармацевтично прийнятної солі або сольвату, де 1 R означає арил або гетероарил, який може бути заміщений одним або декількома замісниками R’; Ar означає арил або гетероарил, який може бути заміщений одним або декількома замісниками R’; Z означає арил, циклоалкіл, гетероцикліл або гетероарил, який може бути заміщений одним або декількома замісниками R’; Y означає H, галоген, галогеналкіл або алкіл, який може бути заміщений одним або декількома замісниками R’; R’ незалежно означає H, -CO2R’’, -CONHR’’, -CR’’O, -SO2N(R’’)2, -SO2NHR’’, -NR’’-CO-галогеналкіл, -NO2, -NR’’-SO2-галогеналкіл, -NR’’-SO2-алкіл, -SO2-алкіл, -NR’’-CO-алкіл, -CN, алкіл, циклоалкіл, аміноалкіл, алкіламіно, алкокси, -OH, -SH, алкілтіо, гідроксіалкіл, гідроксіалкіламіно, галоген, галогеналкіл, галогеналкокси, аміно, гетероцикліл, арил, галогенарил, галогенарилалкіл, арилалкіл або гетероарил; R’’ незалежно означає H, галогеналкіл, гідроксіалкіл, аміно, алкокси, -N=C(R’)2, -NR’-CO-R’, CR’O, -CO2R’, алкіл, циклоалкіл, арил, галогенарил, галогенарилалкіл, гетероарил, гетероцикліл, арилалкіл або аміноалкіл, які необов’язково заміщені одним або декількома замісниками R’. В іншому кращому варіанті здійснення, даний винахід відноситься до сполуки формули (I) і її фармацевтично прийнятної солі або сольвату, де 1 R означає арил, який може бути заміщений одним або декількома замісниками R’; Ar означає арил або гетероарил, який може бути заміщений одним або декількома замісниками R’; Z означає арил, циклоалкіл, гетероцикліл або гетероарил, який може бути заміщений одним або декількома замісниками R’; Y означає H, галоген, галогеналкіл або алкіл, який може бути заміщений одним або декількома замісниками R’; R’ незалежно означає H, -CO2R’’, -CONHR’’, -CR’’O, -SO2N(R’’)2, -SO2NHR’’, -NR’’-CO-галогеналкіл, -NO2, -NR’’-SO2-галогеналкіл, -NR’’-SO2-алкіл, -SO2-алкіл, -NR’’-CO-алкіл, -CN, алкіл, циклоалкіл, аміноалкіл, алкіламіно, алкокси, -OH, -SH, алкілтіо, гідроксіалкіл, гідроксіалкіламіно, галоген, галогеналкіл, галогеналкокси, аміно, гетероцикліл, арил, галогенарил, галогенарилалкіл, арилалкіл або гетероарил; R’’ незалежно означає H, галогеналкіл, гідроксіалкіл, аміно, алкокси, -N=C(R’)2, -NR’-CO-R’, CR’O, -CO2R’, алкіл, циклоалкіл, арил, галогенарил, галогенарилалкіл, гетероарил, гетероцикліл, арилалкіл або аміноалкіл, які необов’язково заміщені одним або декількома замісниками R’. В іншому кращому варіанті здійснення, даний винахід відноситься до сполуки формули (I) і її фармацевтично прийнятної солі або сольвату, де 1 R означає гетероарил, який може бути заміщений одним або декількома замісниками R’; Ar означає арил або гетероарил, який може бути заміщений одним або декількома замісниками R’; Z означає арил, циклоалкіл, гетероцикліл або гетероарил, який може бути заміщений одним або декількома замісниками R’; Y означає H, галоген, галогеналкіл або алкіл, який може бути заміщений одним або декількома замісниками R’; R’ незалежно означає H, -CO2R’’, -CONHR’’, -CR’’O, -SO2N(R’’)2, -SO2NHR’’, -NR’’-COгалогеналкіл, -NO2, -NR’’-SO2-галогеналкіл, -NR’’-SO2-алкіл, -SO2-алкіл, -NR’’-CO-алкіл, -CN, алкіл, циклоалкіл, аміноалкіл, алкіламіно, алкокси, -OH, -SH, алкілтіо, гідроксіалкіл, гідроксіалкіламіно, галоген, галогеналкіл, галогеналкокси, аміно, гетероцикліл, арил, галогенарил, галогенарилалкіл, арилалкіл або гетероарил; R’’ незалежно означає H, галогеналкіл, гідроксіалкіл, аміно, алкокси, -N=C(R’)2, -NR’-CO-R’, CR’O, -CO2R’, алкіл, циклоалкіл, арил, галогенарил, галогенарилалкіл, гетероарил, гетероцикліл, арилалкіл або аміноалкіл, які необов’язково заміщені одним або декількома замісниками R’. В іншому кращому варіанті здійснення, даний винахід відноситься до сполуки формули (I) і її фармацевтично прийнятної солі або сольвату, де 1 R означає арил або гетероарил, який може бути заміщений одним або декількома замісниками R’; Ar означає арил або гетероарил, який може бути заміщений одним або декількома замісниками R’; Z означає арил, циклоалкіл, гетероцикліл або гетероарил, який може бути заміщений одним або декількома замісниками R’; 4 UA 110048 C2 5 10 15 20 25 30 35 40 45 50 55 60 Y означає H, галоген, галогеналкіл або алкіл, який може бути заміщений одним або декількома замісниками R’; R’ незалежно означає H, -CO2R’’, -CONHR’’, -CR’’O, -SO2N(R’’)2, -SO2NHR’’, -CN, алкіл, циклоалкіл, аміноалкіл, алкокси, -OH, гідроксіалкіл, галоген, галогеналкіл, галогеналкокси, аміно, гетероцикліл, арил, галогенарил, галогенарилалкіл, арилалкіл або гетероарил; R’’ незалежно означає H, галогеналкіл, гідроксіалкіл, аміно, алкокси, -N=C(R’)2, -NR’-CO-R’, CR’O, -CO2R’, алкіл, циклоалкіл, арил, галогенарил, галогенарилалкіл, гетероарил, гетероцикліл, арилалкіл або аміноалкіл, які необов’язково заміщені одним або декількома замісниками R’. В іншому кращому варіанті здійснення, даний винахід відноситься до сполуки формули (I) і її фармацевтично прийнятної солі або сольвату, де 1 R означає арил або гетероарил, який може бути заміщений одним або декількома замісниками R’; Ar означає арил або гетероарил, який може бути заміщений одним або декількома замісниками R’; Z означає арил, циклоалкіл, гетероцикліл або гетероарил, який може бути заміщений одним або декількома замісниками R’; Y означає H, галоген, галогеналкіл або алкіл, який може бути заміщений одним або декількома замісниками R’; R’ незалежно означає H, -CO2R’’, -SO2N(R’’)2, -SO2NHR’’, -CN, алкіл, алкокси, -OH, гідроксіалкіл, галоген, галогеналкіл, галогеналкокси, гетероцикліл, арил, галогенарил, галогенарилалкіл, арилалкіл або гетероарил; R’’ незалежно означає H, галогеналкіл, гідроксіалкіл, аміно, алкокси, -N=C(R’)2, -NR’-CO-R’, CR’O, -CO2R’, алкіл, циклоалкіл, арил, галогенарил, галогенарилалкіл, гетероарил, гетероцикліл, арилалкіл або аміноалкіл, які необов’язково заміщені одним або декількома замісниками R’. В іншому кращому варіанті здійснення, даний винахід відноситься до сполуки формули (I) і її фармацевтично прийнятної солі або сольвату, де 1 R означає арил або гетероарил, який може бути заміщений одним або декількома замісниками R’; Ar означає арил або гетероарил, який може бути заміщений одним або декількома замісниками R’; Z означає арил, циклоалкіл, гетероцикліл або гетероарил, який може бути заміщений одним або декількома замісниками R’; Y означає H, галоген, галогеналкіл або алкіл, який може бути заміщений одним або декількома замісниками R’; R’ незалежно означає H, -CO2R’’, -CONHR’’, -CR’’O, -SO2N(R’’)2, -SO2NHR’’, -CN, алкіл, алкокси, -OH, галоген, галогеналкіл або галогеналкокси; R’’ незалежно означає H, галогеналкіл, гідроксіалкіл, аміно, алкокси, -N=C(R’)2, -NR’-CO-R’, CR’O, -CO2R’, алкіл, циклоалкіл, арил, галогенарил, галогенарилалкіл, гетероарил, гетероцикліл, арилалкіл або аміноалкіл, які необов’язково заміщені одним або декількома замісниками R’. В іншому кращому варіанті здійснення, даний винахід відноситься до сполуки формули (I) і її фармацевтично прийнятної солі або сольвату, де 1 R означає арил, або гетероарил, який може бути заміщений одним або декількома замісниками R’; Ar означає арил або гетероарил, який може бути заміщений одним або декількома замісниками R’; Z означає арил, циклоалкіл, гетероцикліл або гетероарил, який може бути заміщений одним або декількома замісниками R’; Y означає H, галоген, галогеналкіл або алкіл, який може бути заміщений одним або декількома замісниками R’; R’ незалежно означає H, -CO2R’’, -CONHR’’, -CR’’O, -SO2N(R’’)2, -SO2NHR’’, -CN, алкіл, алкокси, -OH, галоген, галогеналкіл або галогеналкокси; R’’ незалежно означає H, галогеналкіл або алкіл, який може бути заміщений одним або декількома замісниками R’. В іншому кращому варіанті здійснення, даний винахід відноситься до сполуки формули (I) і її фармацевтично прийнятної солі або сольвату, де 5 UA 110048 C2 1 R означає арил, який може бути заміщений одним або декількома замісниками R’; Ar означає арил, який може бути заміщений одним або декількома замісниками R’; Z означає арил, циклоалкіл, гетероцикліл або гетероарил, який може бути заміщений одним або декількома замісниками R’; 5 10 15 20 25 30 35 40 45 50 55 60 Y означає H, галоген, галогеналкіл або алкіл, який може бути заміщений одним або декількома замісниками R’; R’ незалежно означає H, -CO2R’’, -CONHR’’, -CR’’O, -CN, алкіл, алкокси, -OH, галоген, галогеналкіл або галогеналкокси; R’’ незалежно означає H, галогеналкіл або алкіл, який може бути заміщений одним або декількома замісниками R’; де арильна група означає ароматичну групу, що містить від п’яти до п’ятнадцяти атомів вуглецю, яка може бути заміщена одним або декількома замісниками R’, і може бути конденсована з іншим ароматичним кільцем; арильна група переважно є фенільною групою, -о-C6H4-R’, -м-C6H4-R’, -пC6H4-R’, 1-нафтилом, 2-нафтилом, 1-антраценілом або 2-антраценілом; гетероарильна група означає 5- або 6-членну гетероциклічну групу, яка містить принаймні один гетероатом, подібний O, N, S. Ця гетероциклічна група може бути конденсована з іншим ароматичним кільцем. Наприклад, ця група може бути вибрана із тіадіазольної, тіазол-2-ільної, тіазол-4-ільної, тіазол-5-ільної, ізотіазол-3-ільної, ізотіазол-4-ільної, ізотіазол-5-ільної, оксазол-2ільної, оксазол-4-ільної, оксазол-5-ільної, ізоксазол-3-ільної, ізоксазол-4-ільної, ізоксазол-5-ільної, 1,2,4-оксадіазол-3-ільної, 1,2,4-оксадіазол-5-ільної, 1,2,5-оксадіазол-3-ільної, бензоксазол-2-ільної, бензоксазол-4-ільної, бензоксазол-5-ільної, бензоізоксазол-3-ільної, бензоізоксазол-4-ільної, бензоізоксазол-5-ільної, 1,2,5-оксадіазол-4-ільної, 1,3,4-оксадіазол-2-ільної, 1,2,4-тіадіазол-3-ільної, 1,2,4-тіадіазол-5-ільної, 1,3,4-тіадіазол-2-ільної, ізотіазол-3-ільної, ізотіазол-4-ільної, ізотіазол-5ільної, бензоізотіазол-3-ільної, бензоізотіазол-4-ільної, бензоізотіазол-5-ільної, 1,2,5-тіадіазол-3ільної, 1-імідазолільної, 2-імідазолільної, 1,2,5-тіадіазол-4-ільної, 4-імідазолільної, бензімідазол-4ільної, 1-піролільної, 2-піролільної, 3-піролільної, 2-фуранільної, 3-фуранільної, 2-тієнільної, 3тієнільної, 2-піридильної, 3-піридильної, 4-піридильної, 2-піранільної, 3-піранільної, 4-піранільної, 2піримідинільної, 4-піримідинільної, 5-піримідинільної, пірид-2-ильної, пірид-3-ильної, пірид-4-ильної, пірид-5-ильної, пірид-6-ильної, 3-піридазинільної, 4-піридазинільної, 2-піразинільної, 1піразолільної, 3-піразолільної, 4-піразолільної, 1,2,3-триазол-4-ільної, 1,2,3-триазол-5-ільної, 1,2,4триазол-3-ільної, 1,2,4-триазол-5-ільної, 1H-тетразол-2-ільної, 1H-тетразол-3-ільної, тетразолільної, акридильної, феназинільної, карбазолільної, феноксазинільної, індолізинової, 2індолільної, 3-індолільної, 4-індолільної, 5-індолільної, 6-індолільної, 7-індолільної, 1-ізоіндолільної, 3-ізоіндолільної, 4-ізоіндолільної, 5-ізоіндолільної, 6-ізоіндолільної, 7-ізоіндолільної, 2-індолінільної, 3-індолінільної, 4-індолінільної, 5-індолінільної, 6-індолінільної, 7-індолінільної, бензо[b]фуранільної, бензофуразанової, бензотіофуразанової, бензотриазол-1-ільної, бензотриазол-4-ільної, бензотриазол-5-ільної, бензотриазол-6-ільної, бензотриазол-7-ільної, бензотриазинової, бензо[b]тіофенільної, бензімідазолільної, бензотіазолільної, хіназолінільної, хіноксазолінільної, цінолінової, хінолінільної, тетрагідрохінолінільної, ізохінолінільної, або тетрагідроізохінолінільної, пуринової, фталазинової, птеридинової, тіатетраазаінденової, тіатриазаінденової, ізотіазолопіразинової, 6-піримідинільної, 2,4-диметокси-6-піримідинільної, бензімідазол-2-ільної, 1H-бензімідазолільної, бензімідазол-4-ільної, бензімідазол-5-ільної, бензімідазол-6-ильної, бензімідазол-7-ільної, тетразольної, тетрагідро-тієно[3,4-d]імідазол-2-онової, піразоло[5,1-c][1,2,4]триазинової, ізотіазолопіримідинової, піразолотриазинової, піразолопіримідинової, імідазопіридазинової, імідазопіримідинової, імідазопіридинової, імідазолотриазинової, триазолотриазинової, триазолопіридинової, триазолопіразинової, триазолопіримідинової або триазолопіридазинової групи. Ця гетероциклічна група може бути заміщеною одним або декількома замісниками R’, де R’ приймає визначені вище значення; гетероциклільна група означає 3 - 8-членну гетероциклічну неароматичну групу, яка містить принаймні один гетероатом, вибраний із O, N, і S, де гетероциклільна група може бути конденсована з іншим неароматичним кільцем і група може бути заміщена одним або декількома замісниками R’, де R’ приймає визначені вище значення; C3-C8-гетероциклільний залишок може бути вибраний із групи, що складається з морфолін-4-ілу, піперазинілу, ізоксазолідин-2-ілу, 1алкілпіперазин-4-ілу, піролідинілу, піролідино, піперидинілу, піперидино, піперазинілу, піперазино, морфолінілу, морфоліно, тіоморфолінілу, тіоморфоліно, тетрагідрофуранілу, тетрагідротіофуранілу, тетрагідропіранілу і піранілу. З метою дотримання максимальної стислості визначень, в наступних абзацах “алкіл” слід розуміти як такий, що охоплює алкіл, алкеніл і алкініл. 6 UA 110048 C2 5 10 15 20 25 30 35 40 45 50 55 60 Стосовно даного винаходу, алкільна група, якщо не вказано інше, означає лінійний або розгалужений C1-C6-алкіл, краще лінійний або розгалужений ланцюг з одного - п'яти атомів вуглецю; алкенільна група, якщо не вказано інше, означає лінійний або розгалужений C2-C6алкеніл; і алкінільна група, якщо не вказано інше, означає лінійний або розгалужений C2-C6-алкініл, кожен з яких може бути заміщений одним або декількома замісниками R’. Залишок C1-C6-алкіл, C2-C6-алкеніл і C2-C6-алкініл може бути вибраний з групи, що складається з -CH3, -C2H5, -CH=CH2, -C≡CH, -C3H7, -CH(CH3)2, -CH2-CH=CH2, -C(CH3)=CH2, -CH=CH-CH3, -C≡CCH3, -CH2-C≡CH, -C4H9, -CH2-CH(CH3)2, -CH(CH3)-C2H5, -C(CH3)3, -C5H11, -C6H13, -C(R’)3, -C2(R’)5, CH2-C(R’)3, -C3(R’)7, -C2H4-C(R’)3, -C2H4-CH=CH2, -CH=CH-C2H5, -CH=C(CH3)2, -CH2-CH=CH-CH3, -CH=CH-CH=CH2, -C2H4-C≡CH, -C≡C-C2H5, -CH2-C≡C-CH3, -C≡C-CH=CH2, -CH=CH-C≡CH, -C≡C-C≡CH, -C2H4-CH(CH3)2, -CH(CH3)-C3H7, -CH2-CH(CH3)-C2H5, -CH(CH3)CH(CH3)2, -C(CH3)2-C2H5, -CH2-C(CH3)3, -C3H6-CH=CH2, -CH=CH-C3H7, -C2H4-CH=CH-CH3, -CH2-CH=CH-C2H5, -CH2-CH=CH-CH=CH2, -CH=CH-CH=CH-CH3, -CH=CH-CH2-CH=CH2, -C(CH3)=CH-CH=CH2, -CH=C(CH3)-CH=CH2, -CH=CH-C(CH3)=CH2, -CH2-CH=C(CH3)2, C(CH3)=C(CH3)2, -C3H6-C≡CH, C≡C-C3H7, -C2H4-C≡C-CH3, -CH2-C≡C-C2H5, -CH2-C≡C-CH=CH2, -CH2-CH=CH-C≡CH, -CH2-C≡CC≡CH, -C≡C-CH=CH-CH3, -CH=CH-C≡C-CH3, -C≡C-C≡C-CH3, -C≡C-CH2-CH=CH2, -CH=CH-CH2-C≡CH, -C≡C-CH2-C≡CH, -C(CH3)=CH-CH=CH2, -CH=C(CH3)-CH=CH2, -CH=CH-C(CH3)=CH2, -C(CH3)=CH-C≡CH, CH=C(CH3)-C≡CH, -C≡C-C(CH3)=CH2, -C3H6-CH(CH3)2, -C2H4-CH(CH3)-C2H5, -CH(CH3)-C4H9, -CH2CH(CH3)-C3H7, -CH(CH3)-CH2-CH(CH3)2, -CH(CH3)-CH(CH3)-C2H5, -CH2-CH(CH3)-CH(CH3)2, -CH2C(CH3)2-C2H5, -C(CH3)2-C3H7, -C(CH3)2-CH(CH3)2, -C2H4-C(CH3)3, -CH(CH3)-C(CH3)3, -C4H8-CH=CH2, CH=CH-C4H9, -C3H6-CH=CH-CH3, -CH2-CH=CH-C3H7, -C2H4-CH=CH-C2H5, -CH2-C(CH3)=C(CH3)2, C2H4-CH=C(CH3)2, -C4H8-C≡CH, -C≡C-C4H9, -C3H6-C≡C-CH3, -CH2-C≡C-C3H7, і -C2H4-C≡C-C2H5; арилалкільна група означає лінійний або розгалужений C1-C6-алкіл, заміщений принаймні однією арильною групою, визначеною у даному документі. Ілюстративні арилалкільні групи включають бензил, фенілетил, 4-гідроксибензил, 3-фторбензил, 2-фторфенілетил, і т.п. Ця арилалкільна група може бути заміщена одним або декількома замісниками R’, де R’ приймає визначені вище значення; циклоалкільна група означає неароматичну кільцеву систему, що містить від трьох до восьми атомів вуглецю, краще від чотирьох до восьми атомів вуглецю, де один або декілька атомів вуглецю в кільці можуть бути замінені групою E, E означає O, S, SO, SO2, N, або NR’’, R’’ приймає визначені вище значення; C3-C8-циклоалкільний залишок може бути вибраний із групи, що складається з -цикло-C3H5, -цикло-C4H7, -цикло-C5H9, -цикло-C6H11, -цикло-C7H13, -цикло-C8H15, морфолін-4-ілу, піперазинілу, і 1-алкілпіперазин-4-ілу. Ця циклоалкільна група може бути заміщеною одним або декількома замісниками R’, де R’ приймає визначені вище значення; якщо він використовується, термін “карбоциклоалкіл” визначає неароматичну кільцеву систему, що містить від трьох до восьми атомів вуглецю, краще від чотирьох до восьми атомів вуглецю, більш краще від п’яти до семи атомів вуглецю, і найкраще шість атомів вуглецю, тобто циклогексильне кільце. Карбоциклоалкільна група не містить гетероатоми в кільці. Ця карбоциклоалкільна група може бути заміщеною одним або декількома замісниками R’, де R’ приймає визначені вище значення; якщо він використовується, термін “гетероциклоалкіл” визначає циклоалкільну групу відповідно до вищенаведеного визначення, де один або декілька атомів вуглецю в кільці замінені на O, S, SO, SO2, N, або NR’’, R’’ приймає визначені вище значення. Кращим гетероциклоалкілом або гетероциклілом є морфолін-4-іл, піперазиніл і 1-алкілпіперазин-4іл; алкокси група означає O-алкільну групу, алкільна група приймає визначені вище значення; алкокси група краще означає метокси, етокси, ізопропокси, т-бутокси або пентокси групу; алкілтіо група означає S-алкільну групу, алкільна група приймає визначені вище значення; галогеналкільна група означає алкільну групу відповідно до вищенаведеного визначення, заміщену одним або декількома атомами галогену, краще заміщену одним - п'ятьма атомами 10 10 10’ 10 10’ 10’’ 10 галогену, галогеналкільна група краще означає -C(R )3, -CR (R )2, -CR (R )R , -C2(R )5, -CH210 10’ 10’ 10 10’ 10 10’ 10’’ 10 10 10 C(R )3, -C(R )2-CH(R )2, -CH2-CR (R )2, -CH2-CR (R )R , -C3(R )7, або -C2H4-C(R )3, де R , 10’ 10’’ R , R означають F, Cl, Br або I, краще F; більш переважно, галогеналкіл означає CF3; галогенарильна група означає арильну групу відповідно до вищенаведеного визначення, заміщену одним або декількома атомами галогену, краще заміщену одним - п’ятьма атомами галогену; галогенарилалкільна група означає лінійний або розгалужений C1-C6-алкіл, заміщений 7 UA 110048 C2 5 10 15 20 25 30 35 40 45 50 55 принаймні однією галогенарильною групою, визначеною у даному документі; гідроксіалкільна група означає HO-алкільну групу, алкільна група приймає визначені вище значення; галогеналкокси група означає алкокси групу відповідно до вищенаведеного визначення, заміщену одним або декількома атомами галогену, краще заміщену одним - п’ятьма атомами 10 галогену, галогеналкокси група краще означає -OC(R )3, 10 10’ 10 10’ 10’’ 10 10 10 10’ 10 10’ 10’’ -OCR (R )2, -OCR (R )R , -OC2(R )5, -OCH2-C(R )3, -OCH2-CR (R )2, -OCH2-CR (R )R , 10 10 10 10’ 10’’ OC3(R )7 або -OC2H4-C(R )3, де R , R , R означають F, Cl, Br або I, краще F; гідроксіалкіламіно група означає (HO-алкіл)2-N- групу або HO-алкіл-NH- групу, алкільна група приймає визначені вище значення; алкіламіно група означає HN-алкільну або N-діалкільну групу, алкільна група приймає визначені вище значення; галоген або галогенова група означає фтор, хлор, бром, або йод; краще хлор або фтор. Сполуки, що мають нескінченні ланцюги, що складаються, наприклад, із повторюваних ланок R’ і R’’ і подібних, не охоплюються даним винаходом. Таким чином, найдовший ланцюг, що 1 допускається для кожного бічного ланцюга R , Ar, Z і Y сполук відповідно до винаходу, являє собою три з’єднаних замісника R’ і/або R’’, наприклад R’, який заміщений за допомогою R’’, додатково заміщеного R’ або т.п. Відповідно, слід розуміти, що олігомерні або полімерні бічні ланцюги, що містять число повторюваних одиниць R’ і/або R’’ більше, ніж вказано вище, не входять до обсягу даного винаходу. Структурні складові, які необов’язково заміщені, як зазначено в даному описі, можуть бути заміщені, якщо не вказано інше, в будь-якому хімічно можливому положенні. У варіантах здійснення даного винаходу, Ar краще не означає , який може бути необов’язково заміщеним, і де X означає N або C, і де q і r незалежно можуть приймати значення 0 або 1; крім того, у варіантах здійснення даного винаходу Ar переважно є іншим, ніж необов’язково заміщений карбоциклоалкіл, більш краще іншим, ніж необов’язково заміщений циклобутил. Таким чином, переважно, вищезгадані групи виключаються за допомогою дисклеймера із визначення Ar. У варіантах здійснення даного винаходу, R’ переважно не означає CONHR’’ і/або R’’ переважно не означає гетероарил. Таким чином, переважно, вищезгадані групи виключаються за допомогою дисклеймера із визначення Ar. В кращих варіантах здійснення даного винаходу, Z вибирають із групи, що включає арил і гетероарил, який може бути заміщений одним або декількома замісниками R’; більш краще Z означає феніл або гетероарил, який може бути заміщений одним або декількома замісниками R’; ще більш краще Z вибирають із групи, що включає феніл, тетразоліл, тіазоліл, 1,3,4оксадіазоліл, оксазоліл, 1,3,4-тіадіазоліл, фураніл і тіофеніл, які можуть бути заміщені одним або декількома замісниками R’; ще більш краще Z вибирають із групи, що включає феніл, тетразоліл, тіазоліл, 1,3,4оксадіазоліл, оксазоліл, 1,3,4-тіадіазоліл, фураніл і тіофеніл, які можуть бути заміщені одним або декількома замісниками R’; де у вищезазначених кращих варіантах, що стосуються групи Z, R’ переважно вибирають із групи, що включає C1-4алкіл, C1-4галогеналкіл, водень, гідроксил, C1-4алкокси, і C1-4алкоксикарбоніл, більш краще метил, трифторметил, водень, гідроксил, метокси, і метоксикарбоніл і етоксіоксикарбоніл; ще більш краще Z вибирають із групи, що включає 1H-тетразол-5-іл, 4-метилтіазол-2-іл, тіазол2-іл, 5-(трифторметил)-1,3,4-оксадіазол-2-іл, 5-метил-1,3,4-оксадіазол-2-іл, 1,3,4-оксадіазол-2-іл, оксазол-5-іл, 4-гідрокси-тіазол-2-іл, 4-метокси-тіазол-2-іл, 5-метил-1,3,4-тіадіазол-2-іл, 1,3,4тіадіазол-2-іл, фуран-3-іл, фуран-2-іл, тіофен-3-іл, феніл, 4-метоксикарбоніл-тіазол-2-іл і 4етоксикарбоніл-тіазол-2-іл; найкраще Z вибирають із групи, що включає 4-метилтіазол-2-іл, тіазол-2-іл, 5-(трифторметил)1,3,4-оксадіазол-1-іл, 5-метил-1,3,4-оксадіазол-1-іл, 1,3,4-оксадіазол-1-іл, оксазол-5-іл, 4-метокситіазол-2-іл, 5-метил-1,3,4-тіадіазол-2-іл, 1,3,4-тіадіазол-2-іл, фуран-3-іл, фуран-2-іл, тіофен-3-іл, 8 UA 110048 C2 5 10 15 20 25 30 35 40 45 50 55 60 феніл, і 4-метоксикарбоніл-тіазол-2-іл. 1 В кращих варіантах здійснення даного винаходу, R вибирають із групи, що включає арил, який необов’язково заміщений одним або декількома замісниками R’, гетероарил, який необов’язково заміщений одним або декількома замісниками R’, циклоалкіл, який необов’язково заміщений одним або декількома замісниками R’, і C1-4алкіл, який необов’язково заміщений групою, вибраною з групи, що включає трифторметил, гідроксил, метокси, тетрагідропіраніл, морфолініл, піридил, піридиніл, фторфеніл і тетрагідрофураніл; 1 в інших кращих варіантах здійснення даного винаходу, R вибирають із групи, що включає арил, який необов’язково заміщений одним або декількома замісниками R’, гетероарил, який необов’язково заміщений одним або декількома замісниками R’, циклоалкіл, який необов’язково заміщений одним або декількома замісниками R’, і C1-4алкіл, який необов’язково заміщений групою, вибраною з групи, що включає трифторметил, метокси, тетрагідропіраніл, морфолініл, піридил і тетрагідрофураніл; 1 більш краще R вибирають із групи, що включає феніл, який необов’язково заміщений одним або декількома замісниками R’, піридил, який необов’язково заміщений одним або декількома замісниками R’, піримідил, який необов’язково заміщений одним або декількома замісниками R’, тієніл, який необов’язково заміщений одним або декількома замісниками R’, тіазоліл, який необов’язково заміщений одним або декількома замісниками R’, 1,1-діоксо-тетрагідротієніл, 2,2,2трифторетил, ізопропіл, ізобутил, 2-піперидин-4-ілетил, 2-гідроксіетил, 2-метоксіетил, тетрагідропіран-4-ілметил, 2-морфоліноетил, піридин-2-ілметил, 2-фторфенілметил, 6етоксипіримідин-4-ілметил і тетрагідрофуран-2-ілметил; 1 більш краще R вибирають із групи, що включає феніл, який необов’язково заміщений одним або декількома замісниками R’, піридил, який необов’язково заміщений одним або декількома замісниками R’, піримідил, який необов’язково заміщений одним або декількома замісниками R’, тієніл, який необов’язково заміщений одним або декількома замісниками R’, 1,1-діоксотетрагідротієніл, 2,2,2-трифторетил, ізопропіл, ізобутил, 2-метоксіетил, тетрагідропіран-4-ілметил, 2-морфоліноетил, піридин-2-ілметил і тетрагідрофуран-2-ілметил; 1 ще більш краще R вибирають із групи, що включає феніл, який необов’язково заміщений одним або декількома замісниками, окремо вибраними з трифторметилу, фтору, хлору, брому, йоду, нітро, NH2, -CN, -NHCO-C1-4-алкілу, метокси, C1-4-алкілу, -SO2NH2, або -SO2NH-C1-4-алкілу; піридил, який необов’язково заміщений одним або декількома вищезазначеними замісниками для фенілу; піримідил, який необов’язково заміщений одним або декількома вищезазначеними замісниками для фенілу; тієніл, який необов’язково заміщений одним замісником –COO-C1-4алкілом; тіазоліл, який необов’язково заміщений одним замісником, вибраним з –COO-C1-4алкілу або фторфенілу; 1,1-діоксо-тетрагідротієніл, 2,2,2-трифторетил, ізопропіл, ізобутил, 2-піперидин-4-ілетил, 2-гідроксіетил, 2-метоксіетил, тетрагідропіран-4-ілметил, 2-морфоліноетил, піридин-2-ілметил, 2-фторфенілметил, 6-етоксипіримідин-4-ілметил і тетрагідрофуран-2-ілметил; 1 ще більш краще R вибирають із групи, що включає феніл, який необов’язково заміщений одним або декількома замісниками, окремо вибраними з трифторметилу, фтору, хлору, брому, нітро, NH2, -CN, -NHCO-C1-4-алкілу, метокси, C1-4-алкілу, -SO2NH2, або -SO2NH-C1-4-алкілу; піридил, який необов’язково заміщений одним або декількома вищезазначеними замісниками для фенілу; піримідил, який необов’язково заміщений одним або декількома вищезазначеними замісниками для фенілу; тієніл, який необов’язково заміщений одним замісником –COO-C1-4алкілом; 1,1-діоксо-тетрагідротієніл, 2,2,2-трифторетил, ізопропіл, ізобутил, 2-метоксіетил, тетрагідропіран-4-ілметил, 2-морфоліноетил, піридин-2-ілметил і тетрагідрофуран2-ілметил; 1 ще більш краще R вибирають із групи, що включає феніл, який необов’язково заміщений одним або декількома замісниками, окремо вибраними з трифторметилу, фтору, хлору, брому, йоду, нітро, NH2, -CN, -NHCO-C1-4-алкілу, метокси, C1-4-алкілу, -SO2NH2, або -SO2NH-C1-4-алкілу; піримідил, який необов’язково заміщений одним або декількома заміснікамі, вибраними з метилу, метокси або трифторметилу; тієніл, заміщений одним замісником –COO-метилом, тіазоліл, який необов’язково заміщений одним замісником, вибраним з –COOетилу або 4-фторфенілу, 1,1-діоксо-тетрагідротієнілу, 2,2,2-трифторетилу, ізопропілу, ізобутилу, 2піперидин-4-ілетилу, 2-гідроксіетилу, 2-метоксіетилу, тетрагідропіран-4-ілметилу, 2морфоліноетилу, піридин-2-ілметилу, 2-фторфенілметилу, 6-етоксипіримідин-4-ілметилу і тетрагідрофуран-2-ілметилу; 1,1-діоксо-тетрагідротієніл, 2,2,2-трифторетил, ізопропіл, ізобутил, 2метоксіетил, тетрагідропіран-4-ілметил, 2-морфоліноетил, піридин-2-ілметил і тетрагідрофуран-2ілметил; 1 ще більш краще R вибирають із групи, що включає феніл, який необов’язково заміщений 9 UA 110048 C2 5 10 15 20 25 30 35 40 45 50 55 60 одним або декількома замісниками, окремо вибраними з фтору, хлору, брому, нітро, NH2, -CN, NHCO-C1-4-алкілу, метокси, т-бутилу, -SO2NH2, або -SO2NH-ізопропілу; піридил; піримідил, який необов’язково заміщений одним або декількома замісниками, вибраними з метилу або трифторметилу; тієніл, який необов’язково заміщений одним замісником –COO-метилом, 1,1діоксо-тетрагідротієніл, 2,2,2-трифторетил, ізопропіл, ізобутил, 2-метоксіетил, тетрагідропіран-4ілметил, 2-морфоліноетил, піридин-2-ілметил і тетрагідрофуран-2-ілметил; 1 ще більш краще R вибирають із групи, що включає феніл, 2-фторфеніл, 2-метоксифеніл, 2хлорфеніл, 2-бромфеніл, 2-йодфеніл, 2-нітрофеніл, 2-ціанофеніл, 2-амінофеніл, 4трифторметоксифеніл, 4-метилсульфонілфеніл, 4-хлорфеніл, 4-фторфеніл, 4-трет-бутилфеніл, 4нітрофеніл, 4-ціанофеніл, 3-трифторметилфеніл, 3-фторфеніл, 3-хлорфеніл, 3-ціанофеніл, 4ацетамідо-феніл, 3-ацетамідо-феніл, 2-ацетамідо-феніл, 3-аміносульфоніл-феніл, 3(ізопропіламіно)сульфоніл-феніл, 3-нітрофеніл, 3-амінофеніл, 2,4-дифторфеніл, 2,4-дихлорфеніл, 2,6-дихлорфеніл, 2,3-дихлорфеніл, 3-хлор-5-трифторметилфеніл, 3,5-дифторфеніл, 3,5дихлорфеніл, 2,3,5,6-тетрафторфеніл, 2-піридил; 3-піридил; 4-піридил; 4-трифторметил-піримід-2ил, 6-етоксил-піримід-4-ил, 2,6-диметил-піримід-4-ил, 2-метоксикарбоніл-тієн-3-іл, 4етоксикарбоніл-тіазол-2-іл, 4-(4-фторфеніл)тіазол-2-іл, 1,1-діоксо-тетрагідротієніл, 2,2,2трифторетил, ізопропіл, ізобутил, 2-піперидин-4-ілетил, 2-гідроксіетил, 2-метоксіетил, тетрагідропіран-4-ілметил, 2-морфоліноетил, піридин-2-ілметил, 2-фторфенілметил, 6етоксипіримідин-4-ілметил і тетрагідрофуран-2-ілметил; 1,1-діоксо-тетрагідротієніл, 2,2,2трифторетил, ізопропіл, ізобутил, 2-метоксіетил, тетрагідропіран-4-ілметил, 2-морфоліноетил, піридин-2-ілметил і тетрагідрофуран-2-ілметил; 1 ще більш краще R вибирають із групи, що включає феніл, 2-фторфеніл, 2-метоксифеніл, 2хлорфеніл, 2-бромфеніл, 2-нітрофеніл, 2-амінофеніл, 4-фторфеніл, 4-трет-бутилфеніл, 3фторфеніл, 3-хлорфеніл, 3-ціанофеніл, 3-ацетамідо-феніл, 2-ацетамідо-феніл, 3-аміносульфонілфеніл, 3-(ізопропіламіно)сульфоніл-феніл, 3-нітрофеніл, 3-амінофеніл, 2,4-дифторфеніл, 3,5дифторфеніл, 3,5-дихлорфеніл, 2,3,5,6-тетрафторфеніл, 2-піридил; 3-піридил; 4-піридил; 4трифторметил-піримід-2-ил, 2,6-диметил-піримід-4-ил, 2-метоксикарбоніл-тієн-3-іл, 1,1-діоксотетрагідротієніл, 2,2,2-трифторетил, ізопропіл, ізобутил, 2-метоксіетил, тетрагідропіран-4-іл-метил, 2-(морфолін-4-іл)-етил і тетрагідрофуран-2-іл-метил; 1 ще більш краще R вибирають із групи, що включає феніл, 2-фторфеніл, 2-хлорфеніл, 2метоксифеніл, 2-нітрофеніл, 2-амінофеніл, 4-фторфеніл, 3-фторфеніл, 3-хлорфеніл, 3-ціанофеніл, 3-ацетамідо-феніл, 3-нітрофеніл, 3-амінофеніл, 3,5-дифторфеніл, 3,5-дихлорфеніл, 2-піридил; 3піридил; 4-піридил; 2-метоксикарбоніл-тієн-3-іл, 2,2,2-трифторетил, ізобутил, і тетрагідрофуран-2іл-метил; 1 ще більш краще R вибирають із групи, що включає феніл, 2-фторфеніл, 2-хлорфеніл, 3фторфеніл, 3-хлорфеніл, 2-піридил; 3-піридил і 4-піридил. В кращих варіантах здійснення даного винаходу, Ar вибирають із групи, що включає феніл і піридил, які можуть бути заміщені одним або декількома замісниками R’; більш краще Ar вибирають із групи, що включає феніл і піридил, які можуть бути заміщені одним або декількома замісниками, незалежно вибраними із фтору, метокси або хлору; також більш краще Ar вибирають із групи, що включає феніл, 2,6-дифторфеніл, 2-хлор-6фторфеніл, 2-хлор-6-метоксифеніл, 2-фторфеніл, 3-фторфеніл, 2-хлорфеніл, 4-хлорфеніл, 4метоксифеніл, 2,6-дихлорфеніл, 3,4-дихлорфеніл, 2,4-дихлорфеніл, 3-фторпіридин-4-іл, 3,5дихлорпіридин-4-іл і 3-хлор-5-фторпіридин-4-іл; ще більш краще Ar вибирають із групи, що включає феніл, 2-хлор-6-фторфеніл, 2-фторфеніл, 2-хлорфеніл, 2,6-дихлорфеніл, 2,4-дихлорфеніл, 3-фторпіридин-4-іл, 3,5-дихлорпіридин-4-іл і 3хлор-5-фторпіридин-4-іл. ще більш краще Ar вибирають із групи, що включає 2-хлор-6-фторфеніл, і 2-хлор-6метоксифеніл. В кращих варіантах здійснення даного винаходу, Y вибирають із групи, що включає H, галогеналкіл, і складний алкіловий ефір, який може бути заміщений одним або декількома замісниками R’; більш краще Y вибирають із групи, що включає H, і галогеналкіл, який може бути заміщений одним або декількома замісниками R’; більш краще Y вибирають із групи, що включає H, пентафторетил, трифторметил і метоксикарбоніл; ще більш краще Y вибирають із групи, що включає H, трифторметил і метоксикарбоніл; ще більш краще Y означає трифторметил. В кращих варіантах здійснення даного винаходу, R’ незалежно вибирають із групи, що включає H, метил, етил, пропіл, бутил, ізопропіл, трет-бутил, морфолініл, піперазиніл, циклогексил, 10 UA 110048 C2 5 10 15 20 25 30 35 40 45 50 55 60 піролідиніл, CF3, F, Cl, Br, метокси, тетрагідропіраніл, ізоксазолідиніл, нітро, -NH2, ацетамідо, SO2NH2, -SO2NHiPr і -COO-метил; більш краще R’ незалежно вибирають із групи, що включає H, метил, етил, пропіл, бутил, ізопропіл, трет-бутил, CF3, F, Cl, метокси, тетрагідропіраніл, ізоксазолідиніл, нітро, -NH2, і -COOметил. В кращих варіантах здійснення даного винаходу, R’’ незалежно вибирають із групи, що включає H, трифторметил, метокси, NH2, і метил. Особливо кращими сполуками даного винаходу є сполуки зазначених нижче прикладів даного винаходу, більш краще сполуки зазначених нижче прикладів 4, 5, 6, 7, 8, 10, 11, 12, 14, 16, 17, B-2, B-3, B-4, B-5, B-6, B-7, B-8, B-9, B-10, B-21, B-22, B-24, B-25, B-26, B-27, і B-30, найкраще сполуки зазначених нижче прикладів 4, 5, 7, 8, 16, 17, B-3, B-4, B-5, B-6, B-7, і B-8. 1 Очевидно, що вищезгадані кращі варіанти здійснення, що стосуються залишків X, Y, Ar, R , R’ і R’’, можуть бути поєднані з одержанням додаткових більш кращих варіантів здійснення. Деякими прикладами таких комбінацій є, без обмеження винаходу цими окремими комбінаціями: Сполука відповідно до даного винаходу, де 1 R вибирають із групи, що включає феніл, який необов’язково заміщений одним або декількома замісниками, окремо вибраними з трифторметилу, фтору, хлору, брому, нітро, NH2, -CN, -NHCO-C1-4-алкілу, метокси, C1-4-алкілу, -SO2NH2, або -SO2NH-C1-4-алкілу; піридил, який необов’язково заміщений одним або декількома вищезазначеними замісниками для фенілу; піримідил, який необов’язково заміщений одним або декількома вищезазначеними замісниками для фенілу; тієніл, який необов’язково заміщений одним замісником –COO-C1-4алкілом; 1,1-діоксотетрагідротієніл, 2,2,2-трифторетил, ізопропіл, ізобутил, 2-метоксіетил, тетрагідропіран-4-ілметил, 2-морфоліноетил, піридин-2-ілметил і тетрагідрофуран-2-ілметил; Ar вибирають із групи, що включає феніл і піридил, які можуть бути заміщені одним або декількома замісниками, незалежно вибраними з фтору, метокси або хлору; Y вибирають із групи, що включає H, трифторметил і метоксикарбоніл. Сполука відповідно до даного винаходу, де 1 R вибирають із групи, що включає феніл, який необов’язково заміщений одним або декількома замісниками, окремо вибраними з фтору, хлору, брому, нітро, NH2, -CN, -NHCO-C1-4-алкілу, метокси, т-бутилу, -SO2NH2, або -SO2NH-ізопропілу; піридил; піримідил, який необов’язково заміщений одним або декількома замісниками, вибраними з метилу або трифторметилу; тієніл, який необов’язково заміщений одним замісником –COO-метилом, 1,1-діоксо-тетрагідротієніл, 2,2,2трифторетил, ізопропіл, ізобутил, 2-метоксіетил, тетрагідропіран-4-ілметил, 2-морфоліноетил, піридин-2-ілметил і тетрагідрофуран-2-ілметил; Ar вибирають із групи, що включає феніл, 2,6-дифторфеніл, 2-хлор-6-фторфеніл, 2-хлор-6метоксифеніл, 2-фторфеніл, 2-хлорфеніл, 2,6-дихлорфеніл, 2,4-дихлорфеніл, 3-фторпіридин-4-іл, 3,5-дихлорпіридин-4-іл і 3,5-дифторпіридин-4-іл; Z вибирають із групи, що включає феніл, тетразоліл, тіазоліл, 1,3,4-оксадіазоліл, оксазоліл, 1,3,4-тіадіазоліл, фураніл і тіофеніл, які можуть бути заміщені одним або декількома замісниками, вибраними з групи, що включає метил, трифторметил, водень, гідроксил, метокси, і метоксикарбоніл і етоксіоксикарбоніл; Y вибирають із групи, що включає H, трифторметил і метоксикарбоніл. Сполука відповідно до даного винаходу, де 1 R вибирають із групи, що включає феніл, 2-фторфеніл, 2-метоксифеніл, 2-хлорфеніл, 2бромфеніл, 2-нітрофеніл, 2-амінофеніл, 4-фторфеніл, 4-трет-бутилфеніл, 3-фторфеніл, 3хлорфеніл, 3-ціанофеніл, 3-ацетамідо-феніл, 2-ацетамідо-феніл, 3-аміносульфоніл-феніл, 3(ізопропіламіно)сульфоніл-феніл, 3-нітрофеніл, 3-амінофеніл, 2,4-дифторфеніл, 3,5-дифторфеніл, 3,5-дихлорфеніл, 2,3,5,6-тетрафторфеніл, 2-піридил; 3-піридил; 4-піридил; 4- трифторметилпіримід-2-ил, 2,6-диметил-піримід-4-ил, 2-метоксикарбоніл-тієн-3-іл, 1,1-діоксо-тетрагідротієніл, 2,2,2-трифторетил, ізопропіл, ізобутил, 2-метоксіетил, тетрагідропіран-4-іл-метил, 2-(морфолін-4іл)-етил і тетрагідрофуран-2-іл-метил; Ar вибирають із групи, що включає феніл, 2-хлор-6-фторфеніл, 2-фторфеніл, 2-хлорфеніл, 2,6дихлорфеніл, 2,4-дихлорфеніл, 3-фторпіридин-4-іл, 3,5-дихлорпіридин-4-іл і 3,5-дифторпіридин-4іл; Z вибирають із групи, що включає 1H-тетразол-5-іл, 4-метилтіазол-2-іл, тіазол-2-іл, 5(трифторметил)-1,3,4-оксадіазол-2-іл, 5-метил-1,3,4-оксадіазол-2-іл, 1,3,4-оксадіазол-2-іл, оксазол5-іл, 4-гідрокси-тіазол-2-іл, 4-метокси-тіазол-2-іл, 5-метил-1,3,4-тіадіазол-2-іл, 1,3,4-тіадіазол-2-іл, фуран-3-іл, фуран-2-іл, тіофен-3-іл, феніл, 4-метоксикарбоніл-тіазол-2-іл і 4-етоксикарбоніл-тіазол2-іл; Y вибирають із групи, що включає H, трифторметил і метоксикарбоніл. 11 UA 110048 C2 5 10 15 20 25 30 35 40 45 50 55 60 Відповідно до спеціальних знань, сполуки винаходу, а також їх солі можуть містити, наприклад, при виділенні в кристалічній формі, різні кількості розчинників. Внаслідок цього, до обсягу даного винаходу включені всі сольвати і, зокрема, всі гідрати сполук формули (I), а також всі сольвати і, зокрема, всі гідрати солей сполук формули (I). У даному контексті, терміни захворювання, показання і медичний стан вживатися як синоніми. Даний винахід далі стосується способу лікування захворювання або терапевтичного показання, при якому є сприятливим інгібування інтерлейкіну-17 (IL-17) і/або інтерферону-γ (INF-γ), або захворювання або показання, вибраного з групи, що складається з псоріазу, псоріатичного артриту, аутоімунного тиреоїдиту, базедової хвороби, ревматоїдного артриту, вітиліго, хвороби Крона, неспецифічного виразкового коліту, запальної хвороби кишечнику, анкілозуючого спондиліту, діабету типу 1, розсіяного склерозу, глютенової хвороби, системного червоного вовчака, увеїту, хвороби Бехчета, атопічного дерматиту, червоного плоского лишаю, синдрому Шегрена, грижі міжхребцевих дисків, акне, реакції трансплантат проти хазяїна, реакції хазяїн проти трансплантата і остеоартриту, де спосіб включає введення суб’єкту, що потребує цього, ефективної кількості сполуки формули (I). Аналогічно, далі даний винахід відноситься до способів, таких, як описаний вище, які охоплюють додаткові варіанти, описані в даному описі, зокрема, кращі сполуки, медичні застосування і сполуки для застосування в медичних методах лікування, як описано в даному описі. Даний винахід далі відноситься до фармацевтичних композицій, наборів і наборів частин, що містять сполуки відповідно до даного винаходу. Даний винахід далі відноситься до застосування сполук відповідно до даного винаходу для одержання фармацевтичних композицій, які використовуються для лікування і/або профілактики захворювань, порушень, розладів і/або станів, як зазначено в даному описі. Даний винахід далі відноситься до способів і медичних застосувань, описаних в даному описі, що охоплюють фармацевтичні композиції, як описано в даному описі. Фармацевтичні композиції, як описано в даному описі, містять одну або декілька сполук відповідно до даного винаходу, і фармацевтично прийнятний носій або розріджувач. Крім того, винахід відноситься до готового виробу, який містить пакувальний матеріал і фармацевтичний засіб, що міститься всередині зазначеного пакувального матеріалу, де фармацевтичний засіб є терапевтично ефективним по відношенню до медичних станів, як описано в даному описі, і де пакувальний матеріал містить етикетку або листівку-вкладиш, яка вказує, що фармацевтичний засіб є корисним для запобігання або лікування вищевказаних медичних станів, і де вищевказаний фармацевтичний засіб містить одну або декілька сполук формули (I) відповідно до винаходу. Пакувальний матеріал, етикетка і листівка-вкладиш є або аналогічними, або схожими з відомими стандартними пакувальними матеріалами, етикетками і листівками-вкладишами для фармацевтичних продуктів, що мають схожу корисність. Фармацевтичні композиції відповідно до даного винаходу одержують способами, які відомі per se і добре знайомі спеціалісту в даній галузі техніки. Як фармацевтичні композиції, сполуки винаходу (= активні сполуки) або використовують як такі, або краще в комбінації з придатними фармацевтичними допоміжними речовинами і/або наповнювачами, наприклад у вигляді таблеток, покритих таблеток, капсул, каплет, супозиторіїв, пластирів (наприклад, у вигляді TTS), емульсій, суспензій, гелів або розчинів, причому вміст активної сполуки переважно знаходиться між 0.1 і 95%, при цьому, шляхом відповідного вибору допоміжних речовин і/або наповнювачів, може бути досягнута фармацевтична форма введення (наприклад, форма з відстроченим вивільненням або кишковорозчинна форма), що точно підходить активній сполуці і/або бажаному початку дії. Спеціаліст в даній галузі техніки знайомий з допоміжними речовинами, середовищами для лікарських засобів, наповнювачами, розріджувачами, носіями або допоміжними речовинами, які придатні для цільових фармацевтичних складів, препаратів або композицій на підставі його спеціальних знань. На додаток до розчинників, загусників, мазевих основ і інших активних сполук, можуть використовуватися наповнювачі, наприклад антиокисники, диспергатори, емульгатори, консерванти, солюбілізатори, барвники, комплексоутворювачі або промотори проникності. Залежно від конкретного захворювання, що підлягає лікуванню або попередженню, спільно зі сполуками відповідно до даного винаходу необов’язково можуть бути введені додаткові терапевтично активні засоби, які звичайно вводять для лікування або попередження такого захворювання. У даному контексті, додаткові терапевтичні засоби, які звичайно вводять для лікування або попередження конкретного захворювання, відомі як придатні для лікування такого захворювання. У наступному аспекті даного винаходу, сполуки відповідно до даного винаходу або солі зазначених сполук формули (I), можуть бути поєднані зі стандартними терапевтичними засобами, які звичайно застосовуються для лікування медичних станів, як описано в даному описі. 12 UA 110048 C2 5 10 15 20 25 30 35 40 45 50 55 60 Спеціалісту в даній галузі техніки на підставі його спеціальних знань відома загальна добова доза(-и) і форма(-и) введення додаткового терапевтичного засобу(-ів), що вводиться спільно. Зазначена загальна добова доза(-и) може змінюватись в широкому діапазоні. При практичному здійсненні даного винаходу і залежно від деталей, особливостей або цілей їх застосувань, згаданих вище, сполуки відповідно до даного винаходу можуть вводитися в комбінованій терапії роздільно, послідовно, разом або хронологічно розподіленими у часі (наприклад, як лікарські форми з об’єднаними одиницями доз, як лікарські форми з окремими одиницями, або лікарські форми з розташованими поруч окремими одиницями, як фіксовані або нефіксовані комбінації, як набір частин або як домішки) з одним або декількома стандартними терапевтичними засобами, зокрема відомими в даній галузі хіміотерапевтичними або цільовими специфічними протираковими засобами, такими як згадані вище. Таким чином, наступним аспектом даного винаходу є комбінація або фармацевтична композиція, що містить перший активний компонент, який являє собою сполуку відповідно до даного винаходу або її сіль, другий активний компонент, який являє собою відомий в даній галузі стандартний терапевтичний засіб для медичних станів, як описано в даному описі, і необов’язково фармакологічно прийнятний носій, розріджувач і/або наповнювач для послідовного, роздільного, одночасного або хронологічно розподіленого у часі застосування в терапії в будь-якому порядку, наприклад для лікування, попередження або зменшення інтенсивності у пацієнта медичних станів, як описано в даному описі. У цьому контексті, даний винахід далі відноситься до комбинації, що містить перший активний компонент, який являє собою принаймні одну сполуку відповідно до даного винаходу, і другий активний компонент, який являє собою принаймні один відомий в даній галузі стандартний терапевтичний засіб для медичних станів, як описано в даному описі, для роздільного, послідовного, одночасного або хронологічно розподіленого у часі застосування в терапії, такого як, наприклад, застосування в терапії захворювань, згаданих у даному описі. Термін “комбінація” відповідно до даного винаходу може бути присутнім для позначення фіксованої комбінації, нефіксованої комбінації або набору частин. “Фіксовану комбінацію” визначають як комбінацію, в якій зазначений перший активний компонент і зазначений другий активний компонент присутні разом в одній одиничній дозі або в єдиному цілому. Одним із прикладів “фіксованої комбінації” є фармацевтична композиція, в якій зазначений перший активний компонент і зазначений другий активний компонент присутні в суміші для одночасного введення, наприклад, в складі. Іншим прикладом “фіксованої комбінації” є фармацевтична комбінація, в якій зазначений перший активний компонент і зазначений другий активний компонент присутні в одній одиниці без змішування один з одним. "Набір частин” визначають як комбінацію, де зазначений перший активний компонент і зазначений другий активний компонент присутні у більш ніж одній одиниці. Одним із прикладів “набору частин” є комбінація, де зазначений перший активний компонент і зазначений другий активний компонент присутні окремо. Компоненти набору частин можуть вводитися окремо, послідовно, разом або хронологічно розподіленими у часі. Перший і другий активний компонент комбінації або набору частин відповідно до даного винаходу можуть бути забезпечені у вигляді окремих складів (тобто, незалежно один від одного), які потім об’єднують разом для одночасного, послідовного, роздільного або хронологічно розподіленого у часі застосування в комбінованій терапії; або упаковані і представлені разом у вигляді окремих компонентів упаковки комбінації для одночасного, послідовного, роздільного або хронологічно розподіленого у часі застосування в комбінованій терапії. Тип фармацевтичного складу першого і другого активного компонента комбінації або набору частин відповідно до даного винаходу може бути однаковим, тобто обидва компонента можуть бути складені в окремі таблетки або капсули, або може бути різним, тобто придатним для різних форм введення, як, наприклад, один активний компонент може бути складений у вигляді таблетки або капсули, а інший активний компонент може бути складений для, наприклад, внутрішньовенного введення. Кількості першого і другого активних компонентів комбінацій, композицій або наборів відповідно до даного винаходу, можуть разом містити терапевтично ефективну кількість для лікування, профілактики або зменшення інтенсивності симптомів медичного стану, як описано в даному описі. Наступним аспектом даного винаходу є спосіб співтерапевтичного лікування медичних станів, як описано в даному описі, у пацієнта, який потребує такого лікування, що включає роздільне, послідовне, спільне введення фіксованої або нефіксованої фармакологічно активної і терапевтично ефективної і переносимої кількості однієї або декількох сполук відповідно до даного винаходу і фармакологічно активної і терапевтично ефективної і переносимої кількості одного або декількох відомих в даній галузі терапевтичних засобів для медичних станів, як описано в даному 13 UA 110048 C2 5 10 15 20 25 30 35 40 описі, зазначеному пацієнту. Для одержання фармацевтичних композицій, сполуки винаходу (= активні сполуки) переважно змішують з придатними фармацевтичними допоміжними речовинами, і далі обробляють з одержанням придатних фармацевтичних складів. Придатними фармацевтичними складами є, наприклад, порошки, емульсії, суспензії, аерозолі, масла, мазі, маслянисті мазі, креми, пасти, гелі або розчини. Фармацевтичні композиції відповідно до винаходу одержують способами, відомими per se. Дозування активних сполук здійснюють у величинах звичайного порядку. Таким чином, форми для місцевого нанесення (такі як мазі) містять активні сполуки в концентрації, наприклад, 0.1-99%. Звичайна доза у випадку системної терапії (п/о) звичайно становить від 0.3 до 30 мг/кг на добу, у разі системної терапії (в/в) звичайно становить від 0.3 до 30 мг/кг/год. Вибір оптимальної схеми прийому і тривалості медикаментозного лікування, особливо оптимальної дози і шляху введення активних сполук, необхідних у кожному випадку, може бути виконаний спеціалістом в даній галузі техніки на підставі його спеціальних знань. Метод синтезу сполук формули (I) включає стадію реакції нітрилоксиду з ацетоацетатом, галогеналкеном або метилкротонатом з одержанням метил-ізоксазольної похідної (Hanson JC і ін. J Chem Soc 1965, 5976-5979, Lasri J і ін. J Heterocyclic Chem, 45,2008, 1385-1389). Нітрилоксиди одержують із альдегідів за реакцією з гідроксиламіном з одержанням оксимів (II) (Cheng FK і ін. Bioorg Med Chem Lett 2006, 16, 3376). Оксими піддають реакції з н-хлорсукцинімідом з одержанням відповідного хлороксиму (III) (Balachandran S і ін. Bioorg Med Chen Lett. 19, 2009, 4773-4776). Схема (1) Хлороксим (III) використовують in situ для утворення нітрилоксиду (IV), а циклоприєднання до придатного диполярофілу дає придатний 3-феніл-5-метилізоксазол (VI). Схема (2) Ізоксазольний продукт (VI) може бути перетворений за допомогою реагенту Бредерека (VIII) в толуолі при нагріванні із зворотним холодильником на придатний єнамін (IXa) (Bredereck H і ін. Chem Ber 101, 1968, 41-50). Цю єнамінову сполуку (IXa) обробляють ангідридом кислоти або відповідною активованою кислотою (X) з одержанням ключової проміжної сполуки фенілдиметиламіно-трифтороксобутеніл-ізоксазолу (XIa). Цю проміжну сполуку нагрівають з заміщеним гідразином (XII) з одержанням піразолу (XX). Омилення складного ефіру (XX) (метил або етил) дає відповідну свободну кислоту (XXI), яку перетворюють на амід (XXII) по реакції сполучення з гідрохлоридом амонію, HBTU (гексафторфосфат 2-(1H-бензотриазол-1-іл)-1,1,3,3-тетраметилуронію) і основою (DIEPA) в DMA як розчиннику (Fields C.G. і ін. Peptide Research, т. 4, 1991, 95-101). Амід перетворюють на тіоамід за допомогою реагенту Лоусона в діоксані як розчиннику (Thomsen, I.; Clausen, K.; Scheibye, S.; Lawesson, S.-O., Org. Synth., Coll. т. 7, 1990, 372). Тіоамід (XIX) перетворюють на тіазол (сполука 5) за допомогою 1,2-дихлор-1-етоксіетану відповідно до Boedeker, J., Pries, H., Roesch, D., Malewski, G., Journal fuer Praktische Chemie (Leipzig), т. 317, вид. 6, 1975, 953-8. Схема (3) 14 UA 110048 C2 5 10 15 20 25 30 35 Клас сполук даного винаходу є корисним для розробки імуномодулюючих і протизапальних лікарських засобів або, загалом, для лікування захворювань, при яких є сприятливим інгібування інтерлейкіну-17 (IL-17) і/або інтерферону-γ (INF-γ). Сполуки даного винаходу також є корисними для лікування захворювань, які залежні від або опосередковані запальними цитокінами, таких як псоріаз, псоріатичний артрит, аутоімунний тиреоїдит, базедова хвороба, ревматоїдний артрит, вітиліго, хвороба Крона, неспецифічний виразковий коліт, запальна хвороба кишечнику, анкілозуючий спондиліт, діабет типу 1, розсіяний склероз, глютенова хвороба, системний червоний вовчак, увеїт, хвороба Бехчета, атопічний дерматит, червоний плоский лишай, синдром Шегрена, грижа міжхребцевих дисків, акне, реакція трансплантат проти хазяїна, реакція хазяїн проти трансплантата і остеоартрит. Приклади Були придбані наступні сполуки: 1. трет-бутокси-біс(диметиламіно)метан (Apollo Scientific Ltd, Сполучене Королівство) 2. Метил 3-(2-хлор-6-фторфеніл)-5-метилізоксазол-4-карбоксилат (Apollo Scientific Ltd, Сполучене Королівство) 3. 3-(2-Хлор-6-фторфеніл)-5-метилізоксазол-4-карбонітрил (Fisher Scientific GmbH, Сполучене Королівство) 4. Гідрохлорид метиламіну (Sigma Aldrich Chemie GmbH, Німеччина) 5. Оксим 2-хлор-6-фторбензальдегіду (Fisher Scientific GmbH, Сполучене Королівство) 6. N-Хлорсукцинімід, NCS (Acros Organics BVBA, Бельгія) 7. Етилацетоацетат, метилацетоацетат (Sigma Aldrich Chemie GmbH, Німеччина) 8. Трифтороцтовий ангідрид (Sigma Aldrich Chemie GmbH, Німеччина) 9. Гексафторфосфат 2-(1H-бензотриазол-1-іл)-1,1,3,3-тетраметилуронію, HBTU (Iris Biotech GmbH, Німеччина) 10. Гідроксибензотриазол, HOBT (Sigma Aldrich Chemie GmbH, Німеччина) 11. Метил 3-(2-хлор-6-фторфеніл)-5-[2-(диметиламіно)-1-(2-етокси-2-оксоацетил)вініл]-4ізоксазолкарбоксилат (Key Organics Ltd, Сполучене Королівство) 12. Гідрохлорид 1-(3-диметиламінопропіл)-3-етилкарбодііміду, EDC (Sigma Aldrich Chemie GmbH, Німеччина) 13. Гідразини (ABCR GmbH & Co. KG, Німеччина) 14. Розчинники, звичайно (Sigma Aldrich Chemie GmbH, Німеччина) 15. N,N-Діізопропілетиламін, DIPEA (ACROS Organics, Бельгія) 16. Хлорид амонію ч.д.а. (Sigma Aldrich Chemie GmbH, Німеччина) 17. 2,4-Дисульфід 2,4-біс(4-метоксифеніл)-1,3,2,4-дитіадифосфетану, реагент Лоусона (Sigma 15 UA 110048 C2 5 Aldrich Chemie GmbH, Німеччина) 18. 1,2-Дихлоретил-етиловий простий ефір (ABCR GmbH & Co. KG, Німеччина) 19. Азид натрію (ACROS Organics, Бельгія) 20. N,O-Диметилгідроксиламін (ChemPur GmbH, Німеччина) 21. Алюмогідрид літію (Sigma Aldrich Chemie GmbH, Німеччина) 22. Тозилметил ізоціанід, TosMIC (ACROS Organics, Бельгія) Синтез сполук формули (I) Загальна методика одержання 5-метилізоксазол-4-карбоксилату, що як приклад показана для етил 3-(2-хлор-6-фторфеніл)-5-метилізоксазол-4-карбоксилату 10 15 20 25 30 35 40 До перемішуваної суміші альдегіду A (5 г, 31,5 ммоль), етанолу (10 мл), льоду і води (30 мл) і гідрохлориду гідроксиламіну (2.8 г, 40.3 ммоль) додавали водний розчин NaOH (3.6 г, 90 ммоль в 5 мл води). Суміш перемішували впродовж години і екстрагували за допомогою 40 мл ефіру для видалення забруднень. Водний шар нейтралізували за допомогою HCl і екстрагували ефіром (2x50 мл). Екстракти сушили над Na2SO4 і упарювали з одержанням 5.19 г оксиму B (вихід 93%). До розчину альдоксиму B (2 г, 11.5 ммоль) в 10 мл ДМФА, при кімнатній температурі додавали 0.23 г (1.72 ммоль) N-хлорсукциніміду (NCS). Сухий хлороводень барботували в ДМФА розчин до тих пір, поки температура реакції не піднялася до 35°C. Потім додавали частинами 1.31 г (9.8 ммоль) NCS, температуру витримували на рівні 35-45°C. Реакційну суміш охолоджували до кімнатної температури і виливали в 30 мл льоду і екстрагували за допомогою ефіру. Об’єднані екстракти сушили і упарювали з одержанням 2.5 г гідроксамоїлхлориду C у вигляді жовтого масла. Розчин етилнатрійацетоацетату [з натрію (0.3 г, 13 ммоль), сухого етанолу (10 мл) і етилацетоацетату (1.7 г, 13 ммоль)] повільно додавали до перемішуваного розчину гідроксамоїлхлориду C (2.5 г, 12 ммоль) в 20 мл ефіру при 0-3°C. Суміші давали нагрітися до кімнатної температури впродовж ночі, і розчинник упарювали в вакуумі. Залишок вносили в воду і ефір, ефірний екстракт упарювали і продукт очищали за допомогою колонкової хроматографії (гексан) з одержанням 2.2 г ізоксазольної похідної D у вигляді безбарвного масла. Етил 3-(2-хлор-6-фторфеніл)-5-метилізоксазол-4-карбоксилат, масло, вихід 67% + Результат РХ/МС [M+H] : 283.95 1 H ЯМР (ДМСО-D6, CCl4): 1.06 (3H, t, CH3), 2.78 (3H, s, CH3), 4.09 (2H, q, CH2), 7.26 (1H, t, CHаром.), 7.39 (1H d, CH-аром.), 7.55 (1H, m, CH-аром.). Алогічним чином одержаний: Етил 3-(2,4-дихлорфеніл)-5-метилізоксазол-4-карбоксилат, масло, вихід 82% 1 H ЯМР (ДМСО-D6, CCl4): 1.10 (3H, t, CH3), 2.74 (3H, s, CH3), 4.10 (2H, q, CH2), 7.42 (1H, d, CHаром.), 7.47 (1H dd, CH-аром.), 7.59 (1H, d, CH- аром.). Метил 3-(4-метоксифеніл)-5-метилізоксазол-4-карбоксилат, вихід 65% 1 H ЯМР (DCCl3): 2.71 (3H, s, CH3), 3.79 (3H, s, OCH3), 3.85 (3H, s, OCH3), 6.97 (2H, AB-сист., CHаром.), 7.60 (2H AB-сист., CH-аром.). Метил 3-ізопропіл-5-метилізоксазол-4-карбоксилат, масло, вихід 64% 1 H ЯМР (ДМСО-D6, CCl4): 1.26 (3H, s, CH3), 1.27 (3H, s, CH3), 2.62 (3H, s, CH3), 3.37 (1H, m, CH-і 16 UA 110048 C2 Pr.), 3.81 (1H s, OCH3). Синтез метил 3-(2-хлор-6-фторфеніл)-5-(2-(диметиламіно)вініл)ізоксазол-4-карбоксилату 5 10 15 20 25 30 35 До розчину 0.1 г (0.3708 ммоль) метил 3-(2-хлор-6-фторфеніл)-5-метилізоксазол-4карбоксилату в 10 мл сухого толуолу, додавали 0.15 мл (0.7417 ммоль) трет-бутоксибіс(диметиламіно)метану (реагент Бредерека). Реакційну суміш нагрівали зі зворотним холодильником впродовж 6 год. Суміш концентрували в вакуумі і сушили у високому вакуумі. До маслянистого залишку додавали петролейний ефір, в результаті чого формувався кристалічний продукт. Продукт збирали шляхом фільтрування, і одержували 0.070 г (вихід від теорії: 58%) вінілізоксазольної похідної. + 1 Результат РХ/МС [M+H] : 325.0; H ЯМР (ДМСО-d6; CCl4): 3.02 (6H, s, N-CH3), 3.53 (3H, s, CH3), 5.54-5.58 (1H, d, CH), 7.72-7.76 (1H, d, CH), 7.32-7.38 (1H, dd, CH-аром.), 7.44-7.47 (1H, d, CH-аром.), 7.56-7.58 (1H, d, CH-аром.) Синтез метил 3-(2-хлор-6-фторфеніл)-5-(1-(диметиламіно)-4,4,4-трифтор-3-оксобут-1-ен-2іл)ізоксазол-4-карбоксилату До розчину 0.5 г (1.5397 ммоль) метил 3-(2-хлор-6-фторфеніл)-5-[2-(диметиламіно) вініл]ізоксазол-4-карбоксилату в 20 мл сухого дихлорметану при охолодженні на льодяній бані додавали по краплях 0.32 мл (2.309 ммоль) трифтороцтового ангідриду. Реакційну суміш перемішували впродовж 3 год. при кімнатній температурі. Пізніше суміш концентрували в вакуумі і сушили у високому вакуумі. Маслянистий залишок кристалізували з петролейного ефіру, і продукт збирали шляхом фільтрування з одержанням 0.604 г (вихід від теорії: 94%) 5-(1-(диметиламіно)-4,4,4-трифтор-3-оксобут-1-ен-2-іл)ізоксазольної + 1 похідної. Результат РХ/МС [M+H] : 420.9; H ЯМР (ДМСО-d6; CCl4): 2.63 (3H, s, N-CH3), 3.40 (3H, s, N-CH3), 3,59 (3H, s, CH3), 7.40-7.46 (1H, dd, CH-аром.), 7.51-7.55 (1H, d, CH-аром.), 7.64-7.66 (1H, d, CH-аром.), 8.12 (1H, s, CH). Синтез метил 3-(2-хлор-6-фторфеніл)-5-(1-(3-хлорфеніл)-5-(трифторметил)-1H-піразол-4іл)ізоксазол-4-карбоксилату До розчину 0.5047 г (1.1994 ммоль) метил 3-(2-хлор-6-фторфеніл)-5-(1-(диметиламіно)-4,4,4трифтор-3-оксобут-1-ен-2-іл)ізоксазол-4-карбоксилату в сухому етанолі додавали 0.1790 г (0.9995 ммоль) 3-хлорфенілгідразину і 0.17 мл (0.9995 ммоль) N,N-діізопропілетиламіну (DIPEA). Реакційну суміш нагрівали зі зворотним холодильником впродовж 2 год. Продукт виділяли з застосуванням колонкової хроматографії (петролейний ефір:діетиловий ефір 80:20), і одержували 0.305 г (вихід + 1 від теорії: 61%) піразоліл-ізоксазольної похідної. Результат РХ/МС [M+H] : 499.9; H ЯМР (ДМСОd6; CCl4): 3.66 (3H, s, CH3), 7.45-7.50 (1H, dd, CH-аром.), 7.55-7.58 (1H, d, CH-аром.), 7.65-7.77 (1H, d, CH-аром.), 7.65-7.77 (1H, dd, CH-аром. фенілгідразин), 7.65-7.77 (1H, d, CH-аром. фенілгідразин), 7.85 (1H, s, CH-аром. фенілгідразин), 8,56 (1H, s, 1-піразол). Синтез (E)-3-(2-хлор-6-фторфеніл)-5-(2-(диметиламіно)вініл)ізоксазол-4-карбонітрилу 17 UA 110048 C2 5 10 15 20 25 30 До розчину 1.5 г (6,3389 ммоль) 3-(2-хлор-6-фторфеніл)-5-метилізоксазол-4-карбонітрилу в 100 мл сухого толуолу, додавали 2.10 г (12.6779 ммоль) трет-бутокси-біс(диметиламіно)метану (реагент Бредерека). Реакційну суміш нагрівали зі зворотним холодильником впродовж 12 год. Суміш концентрували в вакуумі і сушили у високому вакуумі. До сирої речовини додавали петролейний ефір для ініціювання кристалізації продукту. Продукт збирали шляхом фільтрування, і + одержували 1.791 г (вихід від теорії: 95.9%) вінілізоксазольної похідної. Результат РХ/МС MH : 1 292.0; H ЯМР (ДМСО- d6; CCl4): 2.93 (3H, s, N-CH3), 3.17 (3H, s, N-CH3), 5.15-5.20 (1H, d, C2H2), 7.74-7.78 (1H, d , C2H2), 7.45-7.52 (1H, dd, CH-аром.), 7.57-7.59 (1H, d, CH-аром.), 7.65-7.71 (1H, d, CH-аром.) Синтез (Z)-3-(2-хлор-6-фторфеніл)-5-(1-(диметиламіно)-4,4,4-трифтор-3-оксобут-1-ен-2іл)ізоксазол-4-карбонітрилу До розчину 0.5 г (1.714 ммоль) (E)-3-(2-хлор-6-фторфеніл)-5-(2-(диметиламіно)вініл)ізоксазол-4карбонітрилу в 20 мл сухого дихлорметану при охолодженні на льодяній бані додавали по краплях 0.36 мл (2.571 ммоль) трифтороцтового ангідриду. Реакційну суміш перемішували впродовж 2 год. при к.т. Пізніше суміш концентрували в вакуумі і сушили у високому вакуумі. До сирої речовини додавали петролейний ефір для ініціювання кристалізації продукту, який збирали шляхом фільтрування з одержанням 0.625 г (вихід від теорії: 94%) 5-(1-(диметиламіно)-4,4,4-трифтор-3+ 1 оксобут-1-ен-2-іл)ізоксазольної похідної. Результат РХ/МС MH : 388.0; H ЯМР (ДМСО-d6; CCl4): 2,75 (3H, s, N-CH3), 3.46 (3H, s, N-CH3), 7.53-7.59 (1H, dd, CH-аром.), 7-64-7.67 (1H, d, CH-аром.), 7.73-7.81 (1H, d, CH-аром.), 8.23 (1H, s, CH) Синтез 3-(2-хлор-6-фторфеніл)-5-(1-(3-хлорфеніл)-5-(трифторметил)-1H-піразол-4-іл)ізоксазол4-карбонітрилу До розчину 0.1 г (0.2579 ммоль) (Z)-3-(2-хлор-6-фторфеніл)-5-(1-(диметиламіно)-4,4,4-трифтор3-оксобут-1-ен-2-іл)ізоксазол-4-карбонітрилу в сухому етанолі додавали 0.0462 г (0.2579 ммоль) 3хлорфенілгідразину і 0.78 мл (0.2579 ммоль) DIPEA. Реакційну суміш нагрівали зі зворотним холодильником впродовж 3 год. Суміш концентрували в вакуумі і сушили у високому вакуумі. Очищення досягали з застосуванням пТШХ, і одержували 0.0037 г (вихід від теорії: 3.0%) піразоліл+ 1 ізоксазольної похідної. Результат РХ/МС MH : 466.9; H ЯМР (ДМСО-d6; CCl4): 7.73-7.97 (6H, m, CHаром.), 8.04 (1H, s, CH-аром.), 8.81 (1H, s, CH-піраз.) Синтез 3-(2-хлор-6-фторфеніл)-5-(1-(3-хлорфеніл)-5-(трифторметил)-1H-піразол-4-іл)-4-(1Hтетразол-5-іл)ізоксазолу (приклад 3) 18 UA 110048 C2 5 10 15 20 25 30 35 40 До розчину 0.115 г (0.246 ммоль) ціаноізоксазолу в 10 мл сухого ДМФА додавали 0.080 г (1.231 ммоль) азиду натрію і 0,065 г (1.231 ммоль) хлориду амонію. Суміш перемішували впродовж 4 год. при 90°C. Суміш фільтрували, і осад на фільтрі промивали ацетонітрилом. Фільтрат упарювали в вакуумі. Коричневий, маслянистий залишок очищали за допомогою пТШХ (петролейний ефір:етилацетат 80:20 + 5 % оцтової кислоти) і сушили в вакуумі з одержанням 49 мг (61%) 1 прикладу 3. Результат РХ/МС MH+: 509,71; H ЯМР (ДМСО-d6; CCl4): 7.42-7.48 (1H, t, CH-аром.), 7.51-7.534 (1H, d, CH-аром.), 7.63-7.55 (4H, m, CH-аром.), 7.81 (1H, s, CH-аром.), 8.58 (1H, s CHпіраз.) Приклади 1 і 2 синтезували аналогічно. Синтез 3-(2-хлор-6-фторфеніл)-5-(1-(3-хлорфеніл)-5-(трифторметил)-1H-піразол-4-іл)-4-(тіазол2-іл)ізоксазолу (приклад 5) 7.13 г (13.86 ммоль) складного етилового ефіру розчиняли в 150 мл етанолу, і додавали 10 мл NaOH (2.0 ммоль). Суміш нагрівали зі зворотним холодильником впродовж 1 години. Етанол упарювали в вакуумі і значення pH основного розчину встановлювали на 2 шляхом додавання соляної кислоти (10% водн.). Кислий розчин екстрагували за допомогою етилацетату. Органічний шар сушили над безводним сульфатом магнію. Розчинник видаляли в вакуумі і залишок сушили в вакуумі з одержанням 6.0 г (89%) відповідної карбонової кислоти. До розчину 6.0 г (12.34 ммоль) карбонової кислоти і 1.98 г (37.021 ммоль) хлориду амонію в 20 мл сухого DMA додавали 9.36 г (24.681 ммоль) HBTU і 6.45 мл (37.021 ммоль) DIPEA. Суміш перемішували впродовж 3 годин при к.т. До реакційної суміші додавали етилацетат, і суміш двічі промивали гідрокарбонатом натрію (5%, водн.) і лимонною кислотою (5%, водн.). Органічний шар сушили над безводним сульфатом магнію, і розчинник видаляли при зниженому тиску. Маслянистий залишок ставав твердим при висушуванні в вакуумі. Тверду речовину промивали петролейним ефіром, відфільтровували і сушили в вакуумі з одержанням 5.37 г (90%) відповідного карбоксаміду. До розчину 5.355 г (11.036 ммоль) карбоксаміду в 20 мл сухого діоксану додавали 4.463 г (11.036 ммоль) реагенту Лоусона. Суміш перемішували впродовж 4 год. із зворотним холодильником. Потім розчинник видаляли в вакуумі. Маслянистий залишок очищали за допомогою колонкової хроматографії (петролейний ефір:етилацетат 80:20) з одержанням 1.716 г (31%) відповідного карботіоаміду. До розчину 1.022 г (2.039 ммоль) карботіоаміду в 20 мл сухого ДМФА додавали 0.5 мл (4.077 ммоль) 1,2-дихлоретил-етилового простого ефіру. Суміш перемішували 2 години при 90°C і потім 2 години при 130°C. Розчинник видаляли в вакуумі, і маслянистий залишок очищали за допомогою колонкової хроматографії (петролейний ефір:етилацетат 80:20) з одержанням 180 мг (17%) + 1 прикладу 5. Результат РХ/МС MH : 524,9; H ЯМР (ДМСО-d6; CCl4): δ 7.47-7.53 (1H, t, CH-аром.), 7.58-7.60 (1H, d CH-аром.),7.65-7.66 (1H, d, CH-аром.) 7.65-7.67 (1H, d, CH-аром.), 7.71-7.73 (1H, t, CH-аром.), 7.74-7.75 (1H, d CH-аром.), 7.74-7.75 (1H, s, CH-тіаз.), 7.83 (1H, s, CH-аром.), 7.84-7.85 (1H, s,CH-тіаз.), 7.59 (1H, s, CH-піраз.) Альтернативний шлях був реалізований для прикладів 29 і 30, і як приклад показаний для 29: 19 UA 110048 C2 5 10 15 20 25 30 3-(2-хлор-6-фторфеніл)-5-(1-(2-хлорфеніл)-5-(трифторметил)-1H-піразол-4-іл)ізоксазол-4карбонову кислоту (100 мг, 0.21 ммоль), хлорид амонію (10 мг, 0.21 ммоль), HOBt ( 27.8 мг, 0.21 ммоль) і EDCI (38.3 мг, 0.25 ммоль) розчиняли в 2 мл сухого ДМФА. Додавали N-метилморфолін (104.2 мкл, 2.1 ммоль), і реакційну суміш перемішували при кімнатній температурі впродовж 72 год. ДМФА видаляли шляхом упарювання. Додавали водний розчин водної 5% лимонної кислоти. Осад відфільтровували і сушили. Суміш очищали за допомогою пТШХ (CH2Cl2/MeOH 95/5) з одержанням 50 мг (вихід 50 %) відповідного карбоксаміду. Стадію з реагентом Лоусона виконували, як описано у межах прикладу синтезу 5. До розчину 3-(2-хлор-6-фторфеніл)-5-(1-(2-хлорфеніл)-5-(трифторметил)-1H-піразол-4іл)ізоксазол-4-карботіоаміду (15 мг, 0.03 ммоль) в 0.5 мл етанолу додавали 2-хлорацетальдегід (0.046 мл, 0.4 ммоль). Суміш перемішували впродовж 48 год. при 85°C. Суміш концентрували, розбавляли дихлорметаном і промивали водою (3 x), сушили над сульфатом натрію, фільтрували і концентрували при зниженому тиску. Одержуване масло очищали за допомогою пТШХ (ДХМ : MeOH 100:5) з одержанням 10.4 мг прикладу 29 у вигляді жовтого масла (вихід 66%). Результат + 1 РХ/МС MH : 524,57; H ЯМР (CDCl3): δ 7,11 (m, 1H), 7,28 (m, 1H), 7,33-7,42 (m, 6H), 7,52 (m , 1H), 8,37 (s, 1H) Синтез метил 3-(2-хлор-6-фторфеніл)-5-(1-(2,4-дифторфеніл)-5-(трифторметил)-1H-піразол-4іл)ізоксазол-4-карбоксилату (приклад 4) 3-(2-хлор-6-фторфеніл)-5-(1-(3-хлорфеніл)-5-(трифторметил)-1H-піразол-4-іл) ізоксазол-4карботіоамід (50.0 мг, 0.100 ммоль) і хлорацетон (0.04 мл 0.5 ммоль) розчиняли в 10 мл сухого етанолу. Суміш перемішували при к.т. впродовж 4 год. Очищення продукту досягали за допомогою пТШХ (петролейний ефір:етилацетат 80:20). Висушування у високому вакуумі давало 20 мг (37%) прикладу 4 у вигляді безбарвного масла. Результат РХ/МС MH+: 538,76 1 H ЯМР (ДМСО-d6; CCl4): 2.32 (s, 1H, CH3), 6.72 (s, 1H, CH-тіаз.), 7.04-7.52 (m, 7H, аром.), 8.33 (s, 1H, CH-піраз.) Синтез 4-бром-3-(2-хлор-6-фторфеніл)-5-(1-(3-фторфеніл)-5-(трифторметил)-1H-піразол-4іл)ізоксазолу 0.32 г (0.70 ммоль) карбонової кислоти розчиняли у водн. розчині NaOH (20 мл води + 0.115 г NaOH). До цього розчину при перемішуванні і охолодженні (0-5°C) повільно і по краплях додавали 20 UA 110048 C2 5 10 15 20 25 30 35 бром (0.34 г, 2.1 ммоль). Перемішування продовжували впродовж 2 годин при 0-5°C і впродовж 2 днів при к.т. Осад відфільтровували і суспендували в 5% водн. розчині NaOH (10 мл). Після 2 годин перемішування тверді речовини відфільтровували, промивали водою і сушили в вакуумі з одержанням 0.15 г (0.30 ммоль, 42%) бромованого ізоксазолу у вигляді білих кристалів. Результат 1 РХ/МС MH+: 505.7; H ЯМР (ДМСО-d6; CCl4): 7.35 - 7.48 (m, 4 H) 7.52 (d, J=8.28 Гц, 1 H) 7.61 - 7.74 (m, 2 H) 8.4 (s, 1 H) Синтез метил 3-(2-хлор-6-фторфеніл)-5-(1-(3-фторфеніл)-5-(трифторметил)-1H-піразол-4іл)ізотіазол-4-карбоксилату (приклад 7) Розчин 102 мг (0.217 ммоль) карбонової кислоти в 8 мл SOCl2 нагрівали зі зворотним холодильником впродовж 3 год. Леткі компоненти повністю упарювали в вакуумі. Залишок розчиняли в 8 мл абсолютного діоксану і додавали по краплях до перемішуваної суміші 825 мг N2H4*H2O і 6 мл абсолютного діоксану. Леткі компоненти упарювали, і для осадження маслянистої рожевої твердої речовини додавали небагато води. Воду видаляли, залишок промивали водою, потім обробляли 5 мл води з 10 краплями AcOH, і на закінчення промивали водою. Продукт частково екстрагували киплячим гептаном (38 мг) і частково екстрагували ефіром з наступною обробкою ефірного розчину гептаном (39 мг). Гідразид одержували із загальним виходом 77 мг (73%). Розчин гідразиду (125 мг, 0.258 ммоль) в 2.0 мл метилового ортоефіру нагрівали до температури кипіння і негайно охолоджували до к.т. Потім додавали додаткові 2 мл метилового ортоефиру, і розчин нагрівали зі зворотним холодильником впродовж 1.5 днів. Надлишок ортоефіру упарювали, залишок обробляли киплячим гептаном і упарювали. Залишок очищали за допомогою колонкової хроматографії на силікагелі (елюент EtOAc/гептан 1/3 - 1/1), фракції з чистим продуктом об’єднували і упарювали з одержанням 47 мг (37%) прикладу 7. Результат 1 РХ/МС MH+: 494.8; H ЯМР (ДМСО-d6; CCl4): 7.20 (td, J=8.53, 0.75 Гц, 1 H) 7.24 - 7.44 (m, 5 H) 7.47 7.59 (m, 2 H) 8.35 (s, 1 H) 8.40 (s, 1 H). Синтез 3-(2-хлор-6-фторфеніл)-5-(1-(3-хлорфеніл)-5-(трифторметил)-1H-піразол-4-іл)-4(оксазол-5-іл)ізоксазолу (приклад 8) До розчину 10.8 г (22.2 ммоль) карбонової кислоти, 2.17 г (1 екв.) N,O-диметилгідроксиламіну і 8.42 г (1 екв.) HBTU в ДМФА додавали 3.68 мл DIPEA. Суміш перемішували впродовж ночі при к.т. Розчинник видаляли в вакуумі. Залишок розчиняли в етилацетаті і екстрагували за допомогою гідрокарбонату натрію (5%, водн.) і лимонної кислоти (5%, водн.). Органічний шар сушили над безводним сульфатом магнію і розчинник видаляли в вакуумі. Продукт виділяли за допомогою 21 UA 110048 C2 5 10 15 колонкової хроматографії (6:4 петролейний ефір:етилацетат). Одержуваний продукт - амід Вайнреба сушили в вакуумі з виходом 2.28 г (19%). До охолодженого льодом розчину 1.0 г (1.8895 ммоль) аміду Вайнреба в сухому ТГФ 0.95 мл (0.5 екв. = 2 екв. H) додавали алюмогідрід літію. Після перемішування впродовж 30 хв., ТШХ (4:1 петролейний ефір:етилацетат) більше не показувала едукту. Для гасіння залишкового алюмогідриду літію, до суміші обережно додавали лід. Для додаткового очищення, розчин розбавляли етилацетатом і три рази екстрагували гідрокарбонатом натрію (5%, водн.) і лимонною кислотою (5%, водн.). Органічний шар сушили над безводним сульфатом магнію і розчинник видаляли в вакуумі. Одержуваний альдегід сушили в вакуумі з виходом 520 мг (58%). До розчину 0.5 г (1.0634 ммоль) альдегіду в сухому метанолі (10 мл) під аргоном обережно додавали 5 мл метанолату натрію (із 83 мг натрію в 5 мл сухого метанолу). Після перемішування впродовж 5 хв. при к.т., поетапно додавали 0.25 г (1.2 екв.) TosMIC. Суміш перемішували із зворотним холодильником впродовж 2 годин. Продукт прикладу 8 виділяли за допомогою препаративної ВЕРХ/МС з виходом 128 мг (24%). Результат РХ/МС MH+: 508.78 1 H ЯМР (ДМСО-d6; CCl4): 6.92 (1H, s, CH-оксазол), 7.49-7.78 (6H, m, CH-аром.), 7.87 (1H, s, CHаром.), 8.41 (1H, s, CH-оксазол), 8.50 (1H, s, CH-піраз.) Альтернативний шлях був реалізований для прикладів 28, 32 і 33, і як приклад показаний для 28: 20 25 30 3-(2-хлор-6-фторфеніл)-5-(1-(2-фторфеніл)-5-(трифторметил)-1H-піразол-4-іл)ізоксазол-4карбонову кислоту (0.3 г, 0.64 ммоль), N,O-диметилгідроксиламін (0.062 г, 0.64 ммоль), HOBt (0.082 г, 0.064 ммоль) і EDCI (0.118 г, 0.76 ммоль) розчиняли в 3 мл сухого ДМФА. Додавали Nметилморфолін (104 мкл, 6.4 ммоль), і реакційну суміш перемішували при кімнатній температурі впродовж ночі. ДМФА видаляли шляхом упарювання. Додавали водний розчин 5% лимонної кислоти. Осад відфільтровували і сушили. Продукт очищали за допомогою пТШХ (PE/EE 7/3) з одержанням аміду Вайнреба у вигляді оранжевої твердої речовини (149 мг, вихід 45%). Наступні стадії виконували, як описано для прикладу синтезу 8. В межах останньої стадії цього шляху синтезу, в подібних перетвореннях в деяких випадках спостерігалося утворення побічних продуктів в результаті заміни ароматичного замісника - фтора на метанолат, що приводить до прикладів 31 і 34. Синтез 2-(3-(2-хлор-6-фторфеніл)-5-(1-(3-фторфеніл)-5-(трифторметил)-1H-піразол-4іл)ізоксазол-4-іл)тіазол-4-олу (приклад 9) 22 UA 110048 C2 5 10 15 20 25 30 Суміш 0.145 г (0.03 ммоль) вищезазначеного тіоаміду, 0.60 г (0.42 ммоль) бромоцтової кислоти і 5 мл толуолу нагрівали зі зворотним холодильником впродовж 2 год. Потім реакційну суміш упарювали в вакуумі. В’язке масло промивали водою і очищали за допомогою колонкової хроматографії на силікагелі, використовуючи CCl4, потім CHCl3/CCl4 (1:1, об./об.) як елюенти. Вихід 1 склоподібної речовини прикладу 9 складав 0.063 г (40%). Результат РХ/МС MH+: 525.01; H ЯМР (ДМСО-d6; CCl4): 7.60-7.94 (7H, m, CH-аром.), 8.62 (1H, s, CH-піраз.), 8.84 (1H, s, CH-тіазол), 10.81 (1H, s, OH) Синтез 3-(2-хлор-6-фторфеніл)-5-(1-(3-фторфеніл)-5-(трифторметил)-1H-піразол-4-іл)-4-(4метокситіазол-2-іл)ізоксазолу (приклад 10) До перемішуваного розчину 52 мг (0.1 ммоль) гідроксилтіазолу (приклад 9) в 5 мл діоксану додавали по черзі невеликими порціями 0.140 г (1.0 ммоль) CH3I і розчин 40 мг (1.0 ммоль) NaOH в 1 мл води. pH необхідно було підтримувати на значенні 8-9, а температуру - на позначках 40-50ºC. Потім реакційну суміш перемішували впродовж 1 години при 40-50 ºC, розбавляли за допомогою 15 мл води, нейтралізували за допомогою HCl до pH 6-7. В’язке масло екстрагували за допомогою CCl4, сушили MgSO4 і очищали за допомогою колонкової хроматографії на силікагелі, використовуючи CCl4, потім CHCl3 / CCl4 (1:1, об./об.) як елюенти. Вихід склоподібної речовини 1 прикладу 10 складав 20 мг (37%). Результат РХ/МС MH+: 539.03; H ЯМР (ДМСО-d6; CCl4): 3.73 (3H, s, CH3), 6.59 (1H, s, CH-тіазол), 7.52-7.78 (7H, m, CH-аром.), 8.62 (1H, s, CH-піраз.) Синтез 2-(3-(2-хлор-6-фторфеніл)-5-(1-(2-фторфеніл)-5-(трифторметил)-1H-піразол-4іл)ізоксазол-4-іл)-5-метил-1,3,4-оксадіазолу (приклад 11) Розчин 3-(2-хлор-6-фторфеніл)-5-[1-(2-фторфеніл)-5-(трифторметил)-1H-піразол-4-іл]ізоксазол4-карбогідразиду (66 мг, 0.137 ммоль) в оцтовому ангідриді (3.5 г) витримували в запаяної трубці o при 140 C впродовж 18 годин. Розчинник видаляли в вакуумі. Залишок повторно упарювали з етанолом, і обробляли киплячим гептаном. Концентрування і охолодження гептанового екстракту давало тверду речовину. Колонкова хроматографія на силікагелі (елюент EtOH/гептан, 1/1) давала 40 мг (58%) безбарвного порошку прикладу 11. Результат РХ/МС MH+: 508.05 1 H ЯМР (400 MГц, МЕТАНОЛ-d4) м.д. 2.44 (s, 3 H) 7.28 - 7.35 (m, 1 H) 7.41 - 7.49 (m, 3 H) 7.69 (s, 3 H) 8.48 (d, J=0.50 Гц, 1 H) Альтернативно, реакція може бути виконана при мікрохвильовому опроміненні, як реалізовано для прикладів 4, 10, 18, 19 і 26, і як приклад показано для 4. 23 UA 110048 C2 5 Подібну суміш, утворену у межах прикладу синтезу 11, що складається з гідразиду в оцтовому ангідриді, нагрівали при мікрохвильовому опроміненні при 140°C впродовж 6 год. Суміш розбавляли дихлорметаном і промивали водою, сушили над сульфатом натрію, фільтрували і концентрували при зниженому тиску. Продукт очищали за допомогою пТШХ (EE/PE 1:1). Синтез N-(3-(4-(3-(2-хлор-6-фторфеніл)-4-(5-метил-1,3,4-оксадіазол-2-іл)ізоксазол-5-іл)-5(трифторметил)-1H-піразол-1-іл)феніл)ацетаміду (приклад 11) 10 15 20 25 30 35 5-(1-(3-ацетамідофеніл)-5-(трифторметил)-1H-піразол-4-іл)-3-(2-хлор-6-фторфеніл) ізоксазол-4карбонову кислоту (100 мг, 0.196 ммоль), ацетгідразид (16.0 мг, 0.216 ммоль) і HATU (97.1 мг, 0.255 ммоль) розчиняли в ТГФ (2.00 мл). Додавали DIPEA (268 мкл, 0.589 ммоль) і одержувану суміш перемішували при к.т. впродовж 3.5 год. Додавали додатковий ацетгідразид (160 мг) і HATU (100 мг), і перемішування продовжували при к.т. впродовж 19 год. Реакційну суміш розбавляли за допомогою CH2Cl2 (40 мл) і промивали 1 н. водн. HCl (1 x 20 мл) і водою (2 x 20 мл). Об’єднані водні шари повторно екстрагували за допомогою CH2Cl2 (20 мл) і об’єднані органічні шари сушили над Na2SO4 і концентрували в вакуумі. Залишок очищали за допомогою пТШХ (EtOAc/MeOH = 9:1) з одержанням 34 мг проміжної сполуки у вигляді коричневого масла (вихід 31 %). Проміжну сполуку N-(3-(4-(4-(2-ацетилгідразинкарбоніл)-3-(2-хлор-6-фторфеніл)ізоксазол-5-іл)5-(трифторметил)-1H-піразол-1-іл)феніл)ацетамід (25.0 мг, 0.044 ммоль) розчиняли в оцтовій кислоті (1.50 мл). Додавали оцтовий ангідрид (104 мкл, 1.1 ммоль), і реакційну суміш нагрівали в мікрохвильовій печі до 140 °C впродовж 8 год. Реакційну суміш розбавляли водою (40 мл) і екстрагували за допомогою CH2Cl2 (3 x 20 мл). Об’єднані органічні шари промивали водою (10 мл), сушили над Na2SO4 і концентрували в вакуумі. Залишок очищали за допомогою пТШХ (CH2Cl2/MeOH = 9:1) з одержанням 2.6 мг прикладу 11 у + 1 вигляді жовтої твердої речовини (вихід 8%). Результат РХ/МС MH : 546,87; H ЯМР (MeOD): δ м.д.: 2,05 (s, 3H), 2,33 (s, 3H), 7,20 (m, 2H), 7,33-7,61 (m, 4H), 7,93 (s, 1H), 8,39 (s, 1H) Синтез 3-(2-хлор-6-фторфеніл)-4-(5-метил-1,3,4-тіадіазол-2-іл)-5-(1-(піридин-4-іл)-5(трифторметил)-1H-піразол-4-іл)ізоксазолу (приклад 22) До розчину 3-(2-хлор-6-фторфеніл)-5-(1-(піридин-4-іл)-5-(трифторметил)-1H-піразол-4іл)ізоксазол-4-карбогідразиду (0.03 г, 0.06 ммоль) в оцтовій кислоті (0.03 мл) додавали оцтовий ангідрид (0.01 мл, 0.06 ммоль). Суміш перемішували при к.т. впродовж 2 год. Суміш розбавляли дихлорметаном і промивали водою, сушили над сульфатом натрію, фільтрували і концентрували при зниженому тиску з одержанням 29 мг проміжної сполуки у вигляді коричневого масла. До розчину N'-ацетил-3-(2-хлор-6-фторфеніл)-5-(1-(піридин-4-іл)-5-(трифторметил)-1H-піразол4-іл)ізоксазол-4-карбогідразиду (0.029 мг, 0.01 ммоль) в діоксані (1.5 мл) додавали реагент Лоусона (23.1 мг, 0.01 ммоль). Суміш перемішували при нагріванні із зворотним холодильником впродовж 24 UA 110048 C2 5 10 15 20 25 30 35 40 30 хв. Суміш потім розбавляли дихлорметаном і промивали водою (3 x), сушили над сульфатом натрію, фільтрували і концентрували при зниженому тиску. Продукт очищали за допомогою пТШХ (CH2Cl2:MeOH 100:5) з одержанням 7.7 мг прикладу 22 у + 1 вигляді масла (вихід 26%). Результат РХ/МС MH : 506,69; H ЯМР (CDCl3): δ м.д.: 2,27 (s, 3H), 7,18 (m, 1H), 7,30 (d, 1H), 7,36 (m, 2H), 7,57 (m, 1H), 8,00 (s, 1H), 8,41 (d, 1H), 8,58 (d, 1H) Приклади 20, 21, 23, 27 і 3 синтезували аналогічно прикладу 22. Синтез N-(3-(4-(3-(2-хлор-6-фторфеніл)-4-(5-метил-1,3,4-тіадіазол-2-іл)ізоксазол-5-іл)-5(трифторметил)-1H-піразол-1-іл)феніл)ацетаміду (приклад 12) Обробка N-(3-(4-(4-(2-ацетилгідразинкарбоніл)-3-(2-хлор-6-фторфеніл)ізоксазол-5-іл)-5(трифторметил)-1H-піразол-1-іл)феніл)ацетаміду реагентом Лоусона відповідно до методики, що описана для прикладу 22, привела до утворення тіадіазолу, але одночасно і до утворення тіоаміду в арильному заміснику на піразольному кільці. Для регенерації ацетиламіно замісника, N-(3-(4-(3(2-хлор-6-фторфеніл)-4-(5-метил-1,3,4-тіадіазол-2-іл)ізоксазол-5-іл)-5-(трифторметил)-1H-піразол1-іл)феніл)етантіоамід (19.0 мг, 0.032 ммоль) розчиняли в CH2Cl2 (2.0 мл). Додавали 3хлорпероксибензойну кислоту (70%, 16.2 мг, 0.065 ммоль), і одержувану суміш перемішували при к.т. впродовж 1 год. Реакційну суміш розбавляли насич. Na2SO3 (10 мл) і енергійно перемішували впродовж 10 хв. Потім додавали насич. NaHCO3 (10 мл), і суміш екстрагували за допомогою CH2Cl2 (3 x 15 мл). Об’єднані органічні шари промивали насиченим NaHCO3 (10 мл), сушили над Na2SO4 і концентрували в вакуумі. Залишок очищали за допомогою пТШХ (CH2Cl2/MeOH = 95:5) з одержанням 10.2 мг жовтої + 1 твердої речовини (вихід 37 %). Результат РХ/МС MH : 562,75; H ЯМР (CDCl3): δ м.д.: 2,10 (s, 3H), 2,62 (s, 3H), 7,11 (t, 1H), 7,33 (d, 1H), 7,35-7,48 (m, 2H), 7,65 (m, 3H), 8,21 (s, 1H) Синтез 3-(2-хлор-6-фторфеніл)-5-(1-(2-фторфеніл)-5-(трифторметил)-1H-піразол-4-іл)-4-(5метил-1,3,4-тіадіазол-2-іл)ізоксазолу (приклад 12) 3.44 г (7.3 ммоль) 3-(2-хлор-6-фторфеніл)-5-(1-(2-фторфеніл)-5-(трифторметил)-1H-піразол-4іл)ізоксазол-4-карбонової кислоти розчиняли в 19 мл ДМФА. При к.т. додавали 2.92 г (7.7 ммоль) HBTU і 6.06 мл (36.65 ммоль) DIPEA. Після 20 хв. перемішування при к.т. додавали 1.63 г (22 ммоль) гідразиду оцтової кислоти і суміш перемішували при к.т. впродовж ночі. Суміш розбавляли етилацетатом (60 мл) і промивали 60 мл води. Водний шар повторно екстрагували за допомогою EE і об’єднані органічні шари сушили над MgSO4, фільтрували, і розчинник видаляли при зниженому тиску. Залишок очищали за допомогою пТШХ (CH2Cl2/MeOH 95/5) з одержанням 1.3 г проміжної сполуки у вигляді оранжевої твердої речовини (вихід 34%). Утворення тіадіазолу із проміжної сполуки досягалося з використанням реагенту Лоусона відповідно до методики, що описана для прикладу 22. Синтез 3-(2-хлор-6-фторфеніл)-5-(1-(3-хлорфеніл)-5-(трифторметил)-1H-піразол-4-іл)-4-(1,3,4тіадіазол-2-іл)ізоксазолу (приклад 8) 3-(2-хлор-6-фторфеніл)-5-(1-(3-хлорфеніл)-5-(трифторметил)-1H-піразол-4-іл)ізоксазол-4карбогідразид (85 мг, 0.2 ммоль) обробляли мурашиною кислотою (6.4 мкл, 0.2 ммоль). Суміш перемішували при к.т. впродовж 72 год. До реакційної суміші додавали воду, одержуваний осад збирали, промивали водою і сушили в вакуумі з одержанням 61 мг проміжної сполуки у вигляді 25 UA 110048 C2 5 10 15 20 25 безбарвної твердої речовини. До розчину проміжної сполуки - 3-(2-хлор-6-фторфеніл)-5-(1-(3хлорфеніл)-5-(трифторметил)-1H-піразол-4-іл)-N'-формілізоксазол-4-карбогідразиду (20 мг, 0.038 ммоль) в діоксані (2 мл) додавали реагент Лоусона (0.033 мл, 0.1 ммоль). Суміш перемішували при нагріванні із зворотним холодильником впродовж 3 год. Суміш розбавляли дихлорметаном і промивали водою (3 x), сушили над сульфатом натрію, фільтрували і концентрували при зниженому тиску. Продукт очищали за допомогою пТШХ (EE/PE 1:1) з одержанням 6 мг прикладу 8 + 1 у вигляді безбарвної твердої речовини (вихід 31 %). Результат РХ/МС MH : 525,72; H ЯМР (MeOD): δ 7,35 (t, 1H), 7,49 (d, 1H), 7,59-7,71 (m, 5H), 8,37 (s, 1H), 9,38 (s, 1H) Синтез 3-(2-хлор-6-фторфеніл)-5-(1-(3-фторфеніл)-5-(трифторметил)-1H-піразол-4-іл)-4(фуран-3-іл)ізоксазолу (приклад 13) У пробірку завантажували 4-бром-3-(2-хлор-6-фторфеніл)-5-(1-(3-фторфеніл)-5(трифторметил)-1H-піразол-4-іл)ізоксазол (30 мг, 0.06 ммоль), тетракіс(трифенілфосфін)паладій(0) (0.010 г), 1.5 мл 1,2-диметоксіетану і продували аргоном. Потім додавали фуран-3-ілборонову кислоту (0.012 г, 0.1 ммоль) і водний розчин карбонату цезію (0.05 г в 0.2 мл). Реакційну суміш нагрівали при мікрохвильовому опроміненні до 100°C впродовж 2 год. Розчинник упарювали, і продукт виділяли за допомогою колонкової хроматографії (гексан: етилацетат 25 : 1) з одержанням 5 мг (17%) жовтуватого твердої речовини прикладу 13. Як головну побічну реакцію, спостерігали гідродебромування. 1 Результат РХ/МС MH+: 492.05; H ЯМР (CDCl3; CCl4): 6.18 (1H, m, CH-фурил), 7.12-7.53 (9H, m, CH-аром.+ CH-фурил), 7.91 (1H, s, CH-піраз.) Приклад 17 одержували за аналогією з прикладом 13. Подібну методику застосовували для синтезу прикладів 14, 6, 7, 9 і 24, замінюючи тільки тетракіс(трифенілфосфін)паладій(0) на дихлорбіс(трифенілфосфін)паладій (для прикладу 14), і, для прикладів 6, 7, 9 і 24, також замінюючи водний розчин карбонату цезію водним розчином карбонату натрію. Синтез 3-(2-хлор-6-фторфеніл)-5-(1-(3-фторфеніл)-5-(трифторметил)-1H-піразол-4-іл)-4(тіофен-3-іл)ізоксазолу (приклад 16) 30 35 40 У пробірку для мікрохвильової печі завантажували 4-бромізоксазол (0.03 г, 0.06 ммоль), Pd(PPh3)Cl2 (0.003 г), DME (1.5 мл), і продували аргоном. Потім додавали 3-тієнілборонову кислоту (0.014 г, 0.1 ммоль) і водний розчин Cs2CO3 (0.05 г в 0.2 мл). Реакційну суміш нагрівали при мікрохвильовому опроміненні до 100°C впродовж 1.5 год. Розчинник упарювали, і одержувану суміш розділяли за допомогою колонкової хроматографії (гексан, гексан:EtOAc 50:1, гексан:EtOAc 1 25:1) з одержанням 0.010 г цільового продукту (вихід 33%).; H ЯМР (CDCl3): 6,85 (1H, m, CH-тієніл), 7,04 (1H, m, CH-тієніл), 7,11 (1H, m, CH-аром.), 7,24-,54 (7H, m, CH-аром.+CH-тієніл), 7,80 (1H, s, CH-піраз.). Синтез 2-(3-(2-хлор-6-фторфеніл)-5-(1-(2-фторфеніл)-5-(трифторметил)-1H-піразол-4іл)ізоксазол-4-іл)-1,3,4-оксадіазолу (приклад 15) Розчин 3-(2-хлор-6-фторфеніл)-5-(1-(2-фторфеніл)-5-(трифторметил)-1H-піразол-4-іл)ізоксазол 26 UA 110048 C2 5 10 15 20 25 30 4-карбогідразиду (0.076 г, 0.157 ммоль) в 4 г триметилортоформіату витримували в запаяної трубці при 125°C впродовж 3 днів. Розчин упарювали насухо і залишок кристалізували з гептану з одержанням 36 мг (46%) жовтуватого твердої речовини прикладу 15. Результат РХ/МС MH+: 1 493.75; H ЯМР (метанол-d4; 400 МГц) м.д.: 7.30-7.35 (1H, m, CH-аром.), 7.42-7.48 (3H, m, CHаром.), 7.60-7.70 (3H, m, CH-аром.), 8.51 (1H, s, CH-оксадіазол), 8.93 (1H, s, CH-піраз.) Варіант цієї методики застосовували для синтезу прикладів 5, 13, 14, 15, 16, 17 і 25, і як приклад показаний для 5: Вищезгадану суміш гідразиду і триметилортоформіату (порівн. синтез прикладу 15) нагрівали при мікрохвильовому опроміненні до 125°C впродовж 8 год. Суміш розбавляли дихлорметаном і промивали водою (3 x), сушили над сульфатом натрію, фільтрували і концентрували при зниженому тиску. Продукт очищали за допомогою пТШХ EE/PE 1:1 з одержанням 6 мг прикладу 5 у вигляді білої твердої речовини (вихід 24 %). Синтез метил і етил 2-{3-(2-хлор-6-фторфеніл)-5-[1-(3-фторфеніл)-5-(трифторметил)-1Hпіразол-4-іл]ізоксазол-4-іл}-1,3-тіазол-4-карбоксилату (приклади 1 і 2) Суміш карботіоаміду (0.242 г, 0.5 ммоль) і етилбромпірувату (0.118 г, 0.6 ммоль) нагрівали зі зворотним холодильником впродовж 3 год. в 2 мл сухого діоксану. Реакційну суміш охолоджували до кімнатної температури і розбавляли 20 мл води. Одержуване масло відокремлювали шляхом декантування, розчиняли в CCl4, сушили MgSO4. Сполуку очищали за допомогою колонкової хроматографії із застосуванням силікагелю і CCl4, і потім CHCl3 як елюентів з одержанням 0.17 г прикладу 1 у вигляді масла (вихід 59%). 1 H ЯМР (ДМСО-d6, 400 МГц): δ 8.76 (1H, s, Hтіазол), 8.50 (1H, s, Hпіразол), 7.80…7.53 (7H, m, Hаром.), 4.28 (2H, q, J=7.3 Гц, CH2), 1.27 (3H, t, J=7.3 Гц, Me). Переетерифікація сполуки прикладу 1 в сполуку прикладу 2 досягалася наступним чином: До киплячого розчину 0.118 г (0.2 ммоль) складного етилового ефіру в 5 мл етанолу додавали розчин 0.08 г (2 ммоль) NaOH в 0.5 мл води. Реакційну суміш нагрівали зі зворотним холодильником впродовж 10 хв., потім охолоджували до кімнатної температури, розбавляли водою, підкисляли до pH 3-4 і концентрували до об’єму 1 мл. Кислоту екстрагували за допомогою 10 мл CH2Cl2 і сушили над MgSO4. До розчину додавали 0.1 мл (1.4 ммоль) SOCl2, і суміш нагрівали зі зворотним холодильником впродовж 1 год. Суміш упарювали в вакуумі. Залишок вносили в 2 мл сухого метанолу і нагрівали зі зворотним холодильником впродовж 20 хв. Потім 27 UA 110048 C2 5 10 15 20 25 30 35 40 суміш концентрували в вакуумі і розбавляли 10 мл води. Продукт екстрагували за допомогою 10 мл CH2Cl2 і сушили над MgSO4. Розчин упарювали в вакуумі з одержанням прикладу 2 у вигляді 1 склоподібної твердої речовини (0.063 г, 56 %). H ЯМР (ДМСО-d6, 400 МГц): δ 8.72 (1H, s, Hтіазол), 8.52 (1H, s, Hпіразол), 7.82-7.53 (7H, m, Hаром), 3.82 (3H, s, OMe). Синтез 2-{3-(2-хлор-6-фторфеніл)-5-[1-(3-фторфеніл)-3-(трифторметил)-1H-піразол-4іл]ізоксазол-4-іл}-5-(трифторметил)-1,3,4-оксадіазолу (приклад 6) Розчин 3-(2-хлор-6-фторфеніл)-5-[1-(3-фторфеніл)-3-(трифторметил)-1H-піразол-4-іл]ізоксазол4-карбогідразиду (158 мг, 0.327 ммоль) і ангідриду трифтороцтової кислоти (342 мг, 1.628 ммоль) в 9 г абсолютного діоксану нагрівали зі зворотним холодильником. ТШХ показувала проміжний продукт, який поступово перетворювався на цільовий 1,3,4-оксадіазол. Після нагрівання впродовж 3 днів, суміш упарювали насухо. Маслянистий залишок екстрагували за допомогою киплячого гептану, гептанові екстракти об’єднували і упарювали насухо. Маслянистий залишок очищали за допомогою колонкової хроматографії на силікагелі, елюент EtOAc/гептан, 1/2 з одержанням 18 мг 1 чистого прикладу 6 у вигляді в’язкого масла (вихід 10%). H ЯМР (CDCl3; CCl4): δ 7,24 (t, 1H), 7,32 (m, 2H), 7,41 (m 2H), 7,55 ( m, 2H), 8,38 (s, 1H) Синтез сполук ілюстративних прикладів описується нижче: 1. Синтез сполук формули (I) Сполуки формули (I) одержували шляхом синтезу, описаним у схемі (1). Метил 3-(2-хлор-6фторфеніл)-5-метилізоксазол-4-карбоксилат був придбаний в Apollo Scientific Ltd, Whitefield Rd, Bredbury, Stockport, Cheshire, SK6 2QR. Реагент Бредерека (трет-бутокси-біс(диметиламіно)метан) був придбаний в Apollo Scientific Ltd, Whitefield Rd, Bredbury, Stockport, Cheshire, SK6 2QR. Трифтороцтовий ангідрид був придбаний в Acros Organics BVBA, Janssen Pharmaceuticalaan 3a, 2440 Geel, Бельгія. Гідрохлорид 3-хлорфенілгідразину був придбаний в Alfa Aesar, 26 Parkridge Road, Ward Hill, MA 01835, США. Синтез бензальдоксимних похідних, як приклад показаний для оксиму 2-хлор-6фторбензальдегіду До перемішуваної суміші 2-хлор-6-фторбензальдегіду (5 г, 31.5 ммоль), етанолу (10 мл), льоду і води (30 мл) і гідрохлориду гідроксиламіну (2.8 г, 40.3 ммоль) додавали водний розчин NaOH (3.6 г, 90 ммоль в 5 мл води). Суміш перемішували впродовж години і екстрагували за допомогою 40 мл ефіру для видалення забруднень. Водний шар нейтралізували за допомогою HCl і екстрагували ефіром (2x50 мл). Екстракти сушили над Na2SO4 і упарювали з одержанням 5.19 г альдоксиму (вихід 93%). Синтез етил 3-(2-хлор-6-фторфеніл)-5-метилізоксазол-4-карбоксилату До розчину (E)-2-хлор-6-фторбензальдегідоксиму (2 г) в 10 мл диметилформаміду (ДМФА) при кімнатній температурі додавали 0.23 г N-хлорсукциніміду (NCS). В ДМФА розчин барботували сухий хлороводень до тих пір, поки температура реакції не піднялася до 35°C. Потім порціями додавали 1.21 г N-хлор-сукциніміду, і температуру витримували на рівні 35 - 45°C. Реакційну суміш охолоджували до кімнатної температури і виливали в 30 мл льоду і екстрагували за допомогою ефіру. Об’єднані екстракти сушили і упарювали з одержанням 2.5 г 2-хлор-6-фтор-N 28
ДивитисяДодаткова інформація
Назва патенту англійськоюNormal;heading 1;heading 2;heading 3;il17 and ifn-gamma inhibition for the treatment of autoimmune inflammation
Автори англійськоюLeban, Johann, Tasler, Stefan, Saeb, Wael, Shevrier, Carine
Назва патенту російськоюИнгибирование il17 и ifn-гамма для лечения аутоиммунного воспаления
Автори російськоюЛебан Йоханн, Таслер Штефан, Зеб Вель, Шаврье Карин
МПК / Мітки
МПК: C07D 413/14, A61K 31/4155, A61P 29/00, A61P 19/00, C07D 413/04, C07D 417/14
Мітки: ifn-гамма, аутоімунного, лікування, запалення, інгібування
Код посилання
<a href="https://ua.patents.su/91-110048-ingibuvannya-il17-i-ifn-gamma-dlya-likuvannya-autoimunnogo-zapalennya.html" target="_blank" rel="follow" title="База патентів України">Інгібування il17 і ifn-гамма для лікування аутоімунного запалення</a>
Попередній патент: Спосіб оцінки біомаси риб-бентофагів в континентальних водоймах
Наступний патент: Лікування остеоартриту імуноглобуліновим зв’язувальним білком з подвійним варіабельним доменом, що зв’язує il-1a і il-1b
Випадковий патент: Тороїдальний балон