Похідні бензімідазолону як інгібітори бромодомену
Номер патенту: 111315
Опубліковано: 11.04.2016
Автори: Сперандіо Дейвід, Актоудіанакіс Еванджелос, Ян Хай, Заблоккі Джефф, Шевік Софі, Елбель Крістіна, Кобаясі Тецуя, Цзян Роберт Х., Цзінь Грегорі, Міш Майкл, Корки Бріттон Кеннет, Метобо Семюель І., Мартінес Рубен, Ду Цзіньфа
Формула / Реферат
1. Сполука формули (І)
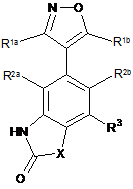 , (І)
, (І)
де
R1а та R1b кожен незалежно являє собою С1-С6алкіл, С1-С6алкокси, С1-С6галогеналкіл, С1-С6галогеналкокси, С1-С6гідроксіалкіл, С3-С6циклоалкіл або СH2-С3-С6циклоалкіл;
R2a та R2b кожен незалежно являє собою Н або галоген;
R3 являє собою
С5-С10арил, С5-С10гетероарил або C5-С10гетероарилалкіл, кожен з яких необов'язково заміщений від 1 до 5 R20-групами; або
-S(O)2NHR4,
де R4 являє собою C1-C6алкіл або С3-С7циклоалкіл, кожен з яких необов'язково заміщений від 1 до 5 R20-групами; або фрагмент формули
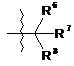 ,
,
де
R6 являє собою Н, ОН або галоген; та R7 та R8 кожен незалежно являє собою С1-С6алкіл, С2-С6алкеніл, С2-С6алкініл, С3-С6циклоалкіл, С1-С6гетероалкіл, С5-С12арил, С5-С12гетероарил або С5-С12гетероарилалкіл, кожен з яких необов'язково заміщений від 1 до 5 R20-групами; або
R6 являє собою Н, С1-С6алкіл, С2-С6алкеніл, С2-С6алкініл, С3-С6циклоалкіл, феніл, нафтил або С3-С12гетероарил; та R7 та R8 разом утворюють С1-С6алкіліденову групу, що має подвійний зв'язок з вуглецем, до якого приєднаний кожен з R6, R7 та R8, де кожна з С1-С6алкільної, С2-С6алкенільної, С2-С6алкінільної, -С3-С6циклоалкільної, фенільної, нафтильної або С3-С12гетероарильної груп необов'язково заміщена від 1 до 5 R20-групами;
X являє собою N-Q або О;
Q являє собою Н, С1-С3алкіл, С1-С3галогеналкіл, бензил або заміщений бензил;
кожен R20 незалежно являє собою С1-С6алкіл, С3-С6циклоалкіл, С1-С6гетероалкіл, С3-С6гетероцикл, С5-С12арил, С5-С12гетероарил, галоген, оксо, -ORa, -C(O)Ra, -C(O)ORa, -C(O)NRaRb, -OC(O)NRaRb, -NRaRb, -NRaC(O)Rb, -NRaC(O)ORb, -S(O)0-2Ra, -S(O)2NRaRb, -NRaS(O)2Rb, -N3, -CN або -NO2, де кожен С1-С6алкіл, С3-С6циклоалкіл, С1-С6гетероалкіл, С3-С6гетероцикл, С5-С12арил, С5-С12гетероарил необов'язково заміщений від одного до п'яти галогенами, оксо, -ORa, -C(O)Ra, -C(O)ORa, -C(O)NRaRb, -OC(O)NRaRb, -NRaRb, -NRaC(O)Rb, -NRaC(O)ORb, -S(O)0-2Ra, -S(O)2NRaRb, -NRaS(O)2Rb, -N3, -CN або -NO2;
кожен Ra та Rb незалежно являє собою Н; або С1-С6алкіл, С3-С6циклоалкіл, С1-С6гетероалкіл, С3-С6гетероцикл, С5-С12арил, С5-С12гетероарил, кожен з яких необов'язково заміщений від одного до п'яти R21;
або Ra та Rb разом з атомами, до яких вони приєднані, утворюють гетероцикл, та
кожен R21 незалежно являє собою С1-С6алкіл, С3-С6циклоалкіл, С1-С6гетероалкіл, С3-С6гетероцикл, С5-С12арил, С5-С12гетероарил або галоген;
або її фармацевтично прийнятна сіль.
2. Сполука за п. 1, що має формулу (Іа)
 , (Ia)
, (Ia)
де
R3 являє собою
С5-С10арил, С5-С10гетероарил або С5-С10гетероарилалкіл, кожен з яких необов'язково заміщений від 1 до 5 R20-групами; або
-S(O)2NHR4,
де R4 являє собою С1-С6алкіл або С3-С7циклоалкіл, кожен з яких необов'язково заміщений від 1 до 5 R20-групами; або
фрагмент формули
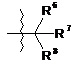 ,
,
де
R6 являє собою Н, ОН або галоген; та R7 та R8 кожен незалежно являє собою С1-С6алкіл, С2-С6алкеніл, С2-С6алкініл, С3-С6циклоалкіл, С1-С6гетероалкіл, С5-С12арил, С5-С12гетероарил або С5-С12гетероарилалкіл, кожен з яких необов'язково заміщений від 1 до 5 R20-групами; або
R6 являє собою Н, С1-С6алкіл, С2-С6алкеніл, С2-С6алкініл, С3-С6циклоалкіл, феніл, нафтил або С3-С12гетероарил; та R7 та R8 разом утворюють C1-C6алкіліденову групу, що має подвійний зв'язок з вуглецем, до якого приєднаний кожен з R6, R7 та R8, де кожна з С1-С6алкільної, С2-С6алкенільної, С2-С6алкінільної, -С3-С6циклоалкільної, фенільної, нафтильної або С3-С12гетероарильної груп необов'язково заміщена від 1 до 5 R20-групами;
Q являє собою Н, С1-С3алкіл, С1-С3галогеналкіл, бензил або заміщений бензил;
кожен R20 незалежно являє собою С1-С6алкіл, С3-С6циклоалкіл, С1-С6гетероалкіл, С3-С6гетероцикл, С5-С12арил, С5-С12гетероарил, галоген, оксо, -ORa, -C(O)Ra, -C(O)ORa, -C(O)NRaRb, -OC(O)NRaRb, -NRaRb, -NRaC(O)Rb, -NRaC(O)ORb, -S(O)0-2Ra, -S(O)2NRaRb, -NRaS(O)2Rb, -N3, -CN або -NO2, де кожен С1-С6алкіл, С3-С6циклоалкіл, С1-С6гетероалкіл, С3-С6гетероцикл, С5-С12арил, С5-С12гетероарил необов'язково заміщений від одного до п'яти галогенами, оксо, -ORa, -C(O)Ra, -C(O)ORa, -C(O)NRaRb, -OC(O)NRaRb, -NRaRb, -NRaC(O)Rb, -NRaC(O)ORb, -S(O)0-2Ra, -S(O)2NRaRb, -NRaS(O)2Rb, -N3, -CN або -NO2;
кожен Ra та Rb незалежно являє собою Н; або С1-С6алкіл, С3-С6циклоалкіл, С1-C6гетероалкіл, С3-С6гетероцикл, С5-С12арил, С5-С12гетероарил, кожен з яких необов'язково заміщений від одного до п'яти R21;
або Ra та Rb разом з атомами, до яких вони приєднані, утворюють гетероцикл, та
кожен R21 незалежно являє собою С1-С6алкіл, С3-С6циклоалкіл, С1-С6гетероалкіл, С3-С6гетероцикл, С5-С12арил, С5-С12гетероарил або галоген;
або її фармацевтично прийнятна сіль.
3. Сполука за п. 1, що має формулу (Іb)
 , (Іb)
, (Іb)
де
R3 являє собою
С5-С10арил, С5-С10гетероарил або C5-C10гетероарилалкіл, кожен з яких необов'язково заміщений від 1 до 5 R20-групами; або -S(O)2NHR4,
де R4 являє собою С1-С6алкіл або С3-С7циклоалкіл, кожен з яких необов'язково заміщений від 1 до 5 R20-групами; або фрагмент формули
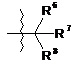 ,
,
де
R6 являє собою Н, ОН або галоген; та R7 та R8 кожен незалежно являє собою С1-С6алкіл, С2-С6алкеніл, С2-С6алкініл, С3-С6циклоалкіл, С1-С6гетероалкіл, С5-С12арил, С5-С12гетероарил або С5-С12гетероарилалкіл, кожен з яких необов'язково заміщений від 1 до 5 R20-групами; або
R6 являє собою Н, С1-С6алкіл, С2-С6алкеніл, С2-С6алкініл, С3-С6циклоалкіл, феніл, нафтил або С3-С12гетероарил; та R7 та R8 разом утворюють С1-С6алкіліденову групу, що має подвійний зв'язок з вуглецем, до якого приєднаний кожен з R6, R7 та R8, де кожна з С1-С6алкільної, С2-С6алкенільної, С2-С6алкінільної, -С3-С6циклоалкільної, фенільної, нафтильної або С3-С12гетероарильної груп необов'язково заміщена від 1 до 5 R20-групами;
кожен R20 незалежно являє собою С1-С6алкіл, С3-С6циклоалкіл, С1-С6гетероалкіл, С3-С6гетероцикл, С5-С12арил, С5-С12гетероарил, галоген, оксо, -ORa, -C(O)Ra, -C(O)ORa, -C(O)NRaRb, -OC(O)NRaRb, -NRaRb, -NRaC(O)Rb, -NRaC(O)ORb, -S(O)0-2Ra, -S(O)2NRaRb, -NRaS(O)2Rb, -N3, -CN або -NO2, де кожен С1-С6алкіл, С3-С6циклоалкіл, С1-С6гетероалкіл, С3-С6гетероцикл, С5-С12арил, С5-С12гетероарил необов'язково заміщений від одного до п'яти галогенами, оксо, -ORa, -C(O)Ra, -C(O)ORa, -C(O)NRaRb, -OC(O)NRaRb, -NRaRb, -NRaC(O)Rb, -NRaC(O)ORb, -S(O)0-2Ra, -S(O)2NRaRb, -NRaS(O)2Rb, -N3, -CN або -NO2;
кожен Ra та Rb незалежно являє собою Н; або С1-С6алкіл, С3-С6циклоалкіл, С1-С6гетероалкіл, С3-С6гетероцикл, C5-C12арил, С5-С12гетероарил, кожен з яких необов'язково заміщений від одного до п'яти R21;
або Ra та Rb разом з атомами, до яких вони приєднані, утворюють гетероцикл, та
кожен R21 незалежно являє собою С1-С6алкіл, С3-С6циклоалкіл, С1-С6гетероалкіл, С3-С6гетероцикл, С5-С12арил, С5-С12гетероарил або галоген;
або її фармацевтично прийнятна сіль.
4. Сполука за будь-яким з пп. 1-3, де R3 являє собою С5-С10арил, C5-C10гетероарил або С5-С10гетероарилалкіл, кожен з яких необов'язково заміщений від 1 до 5 R20-групами.
5. Сполука за будь-яким з пп. 1-3, де R3 являє собою фрагмент формули
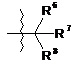 ,
,
де R6 являє собою Н, ОН або галоген; та
R7 та R8 кожен незалежно являє собою С1-С6алкіл, С2-С6алкеніл, С2-С6алкініл, С3-С6циклоалкіл, С1-С6гетероалкіл, С5-С12арил, С5-С12гетероарил або С5-С12гетероарилалкіл, кожен з яких необов'язково заміщений від 1 до 5 R20-групами.
6. Сполука за п. 5, де R6 являє собою ОН.
7. Сполука за п. 5, де R7 та R8 кожен незалежно являє собою С1-С6алкіл, С3-С6циклоалкіл, С1-С6гетероалкіл, С5-С12арил, С5-С12гетероарил або С5-С12гетероарилалкіл, кожен з яких необов'язково заміщений від 1 до 5 R20-групами.
8. Сполука за п. 5, де R7 та R8 кожен незалежно являє собою С1-С6алкіл, С6арил або С6гетероарил, кожен з яких необов'язково заміщений від 1 до 5 R20-групами.
9. Сполука за п. 5, де R7 та R8 кожен незалежно являє собою С6арил або С6гетероарил, кожен з яких необов'язково заміщений від 1 до 5 R20-групами.
10. Сполука за п. 5, де R7 та R8 кожен незалежно являє собою С1-С6алкіл, кожен з яких необов'язково заміщений від 1 до 5 R20-групами.
11. Сполука, вибрана з наступного переліку:
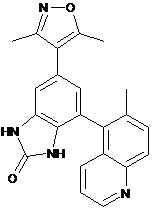 ,
,  ,
,  ,
,  ,
,
 ,
, 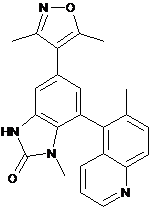 ,
,  ,
,  ,
,
 ,
, 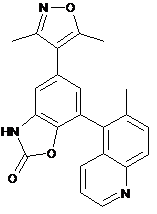 ,
,  ,
, 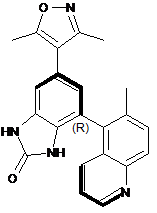 ,
,
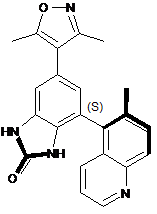 та
та  .
.
12. Сполука, вибрана з наступного переліку:
 ,
, 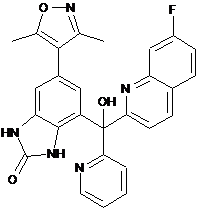 ,
,  ,
,
 ,
, 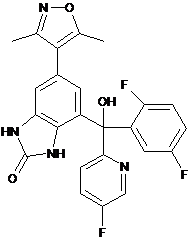 ,
,
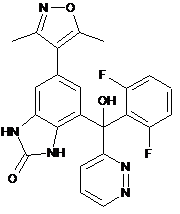 ,
,
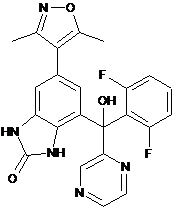 ,
, 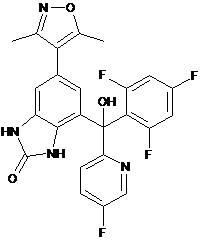 ,
,
 ,
, 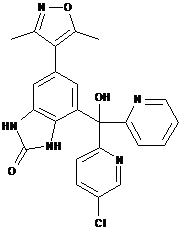 ,
,  ,
,
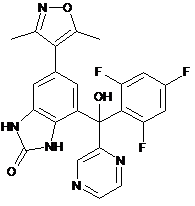 ,
,  ,
,  ,
,  ,
,
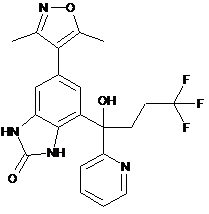 ,
, 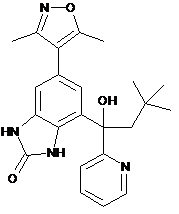 ,
, 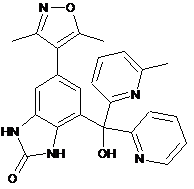 ,
,
 ,
,  та
та  .
.
13. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-12 або її фармацевтично прийнятну сіль та фармацевтично прийнятний носій.
14. Застосування сполуки за будь-яким з пп. 1-12 для лікування людини, яка має захворювання або стан, чутливий до інгібування бромодоменвмісного білка.
15. Застосування сполуки за будь-яким з пп. 1-12 для одержання лікарського засобу для лікування людини, яка має захворювання або стан, чутливий до інгібування бромодоменвмісного білка.
16. Застосування за будь-яким з пп. 14 або 15, яке відрізняється тим, що бромодоменвмісний білок являє собою BRD4.
17. Застосування за будь-яким з пп. 14 або 15, яке відрізняється тим, що захворювання або стан являє собою солідну пухлину товстої кишки, прямої кишки, передміхурової залози, легенів, підшлункової залози, печінки, нирок, шийки матки, шлунка, яєчників, молочної залози, шкіри, головного мозку, мозкових оболонок або центральної нервової системи.
18. Застосування за будь-яким з пп. 14 або 15, яке відрізняється тим, що захворювання або стан являє собою множинну мієлому.
19. Застосування за будь-яким з пп. 14 або 15, яке відрізняється тим, що захворювання або стан являє собою В-клітинну лімфому.
20. Застосування за будь-яким з пп. 14 або 15, яке відрізняється тим, що захворювання або стан являє собою дифузну великоклітинну В-клітинну лімфому або лімфому Беркітта.
Текст
Реферат: Дана заявка стосується хімічних сполук, які можуть діяти як інгібітори або які можуть іншим чином модулювати активність бромодоменвмісного білка, включаючи бромодоменвмісний білок 4 (BRD4), та композицій та складів, що містять такі сполуки, та способів застосування та одержання таких сполук. Сполуки включають сполуки формули (І) UA 111315 C2 (12) UA 111315 C2 N O R1a R1b R2a R2b R HN 3 X O , (І) 1a 1b 2a 2b 3 де R , R , R , R , R та X описані у даній заявці. UA 111315 C2 5 10 15 20 25 30 35 40 45 50 Дана заявка заявляє пріоритет на основі попередньої заявки на патент США № 61/805995, поданої 28 березня 2013 р., та попередньої заявки на патент США № 61/860230, поданої 30 липня 2013 р., зміст яких повністю включено у дану заявку шляхом посилання. ГАЛУЗЬ ТЕХНІКИ Дана заявка відноситься до хімічних сполук, які можуть інгібувати або іншим способом модулювати активність бромодомен-вмісного білку, включаючи бромодомен-вмісний білок 4 (BRD4), та до композицій та складів, що містять такі сполуки, та способів застосування та одержання таких сполук. РІВЕНЬ ТЕХНІКИ Сімейство бромодомен-вмісних та екстратермінальних (BET) білків (BET-білків) являє собою сімейство зчитувачів епігенетичного коду, які зв'язують ацетильовані фрагменти залишків лізину у гістонах для зміни структури хроматину та експресії генів. Сімейство BET включає BRD2, BRD3, BRD4 та BRDT, кожен з яких широко експресується у різноманітних тканинах, за винятком BRDT, експресія якого відбувається у сім’яниках. Див. Wu, S.Y. & Chiang, C.M., J. Biol. Chem., 282: 13141-13145 (2007). Кожний член сімейства BET містить тандемні бромодомени у N-термінальних ділянках, які специфічно зв'язують ацетильовані залишки лізину у гістонах Н3 та Н4. Після зв'язування з гістонами Bet-білки збирають білкові комплекси, які модулюють транскрипцію гену або безпосередньо, наприклад, як активатори або репресори транскрипції, або побічно, наприклад, як комплекси ремоделювання хроматину. BRD4 є найбільш добре вивченим членом сімейства BET та, як відомо, переважно розпізнає тетра-ацетильовані епігенетичні мітки гістонів Н4. Див. Filippakopoulos, P., et al., Cell, 149: 214-231 (2012). BRD4 збирають p-TEFb комплекс у нуклеосомах, які у свою чергу фосфорилюють C- термінальний кінець РНК-полімерази II та збільшують елонгацію транскрипції сусідніх генів. Див. Yang, Z., et al., Mol. Cell Biol., 28: 967-976 (2008); Urano, E., et al., FEBS Lett., 582: 4053-4058 (2008). Епігенетичний код, у тому числі ацетилування гістонів, сильно порушується при багатьох патологічних хворобливих станах, що приводить до аберантної експресії генів, які контролюють результат клітин, диференціювання клітин, виживаність клітин та запальні процеси. Див., наприклад, Cohen, I., et al., Genes Cancer, 2: 631-647 (2011); Brooks, W.H., et al., J. Autoimmun., 34: J207-219 (2010); Wierda, R.J., et al., J. Cell Mol. Med., 14: 1225-1240 (2010); Shirodkar, A.V. & Marsden, P.A., Curr. Opin. Cardiol., 26: 209-215 (2011); Villeneuve, L.M., et al., Clin. Exp. Pharmacol. Physiol., 38: 401-409 (2011). Виявлено, що BET білки, включаючи BRD4, є важливими медіаторами профілів експресії змінених генів, знайдених при багатьох захворюваннях, включаючи рак, діабет, ожиріння, атеросклероз, серцево-судинні та ниркові розлади та вірусні інфекції. Див. Muller, S., et al., Expert Rev. Mol. Med., 13: e29 (2011); Zhou, M., et al., J. Virol., 83: 1036-1044 (2009); Chung, C.W., et al., J. Med. Chem., 54: 3827-3838 (2011). Наприклад, MYC був виявлений при багатьох злоякісних пухлинах людини, та BET білки були ідентифіковані як регулюючі фактори с-Myc; було показано, що інгібування BET, у тому числі BRD4, пригнічує транскрипцію MYC. Див. Delmore, J.E., et al. Cell, 146, 904-17 (2011); Lovén, J. et al., Cell, 153, 320-34 (2013). Таким чином, необхідні інгібітори та модулятори BET-білків, включаючи BRD4. КОРОТКИЙ ОПИС ВИНАХОДУ У одному аспекті запропонована сполука формули (I) (I), де 1a 1b R та R кожен незалежно являє собою C 1-C6 алкіл, C1-C6 алкокси, C1-C6 галоалкіл, C1-C6 галоалкокси, C1-C6 гідроксиалкіл, C3-C6 циклоалкіл або CH2-C3-C6 циклоалкіл; 2a 2b R та R кожен незалежно являє собою H або галоген; 3 R являє собою C5-C10 арил, C5-C10 гетероарил або C5-C10 гетероарилалкіл, кожен з яких необов’язково 20 заміщений від 1 до 5 R групами; або 4 -S(O)2NHR , 1 UA 111315 C2 4 де R являє собою C1-C6 алкіл або C3-C7 циклоалкіл, кожен з яких необов’язково заміщений 20 від 1 до 5 R групами; або фрагмент формули 5 10 15 20 25 30 35 40 45 50 55 , де 6 7 8 R являє собою H, OH або галоген; та R та R кожен незалежно являє собою C1-C6 алкіл, C2-C6 алкеніл, C2-C6 алкініл, C3-C6 циклоалкіл, C1-C6 гетероалкіл, C5-C12 арил, C5-C12 гетероарил 20 або C5-C12 гетероарилалкіл, кожен з яких необов’язково заміщений від 1 до 5 R групами; або 6 R являє собою H, C1-C6 алкіл, C2-C6 алкеніл, C2-C6 алкініл, C3-C6 циклоалкіл, феніл, нафтил 7 8 або C3-C12 гетероарил; та R та R разом утворюють C1-C6 алкіліденову групу, що має подвійний 6 7 8 зв’язок з вуглецем, до якого приєднаний кожен з R , R , та R , де кожна з C1-C6 алкільної, C2-C6 алкенільної, C2-C6 алкінільної, -C3-C6 циклоалкільної, фенільної, нафтильної або C3-C12 20 гетероарильної груп необов’язково заміщена від 1 до 5 R групами; X являє собою N-Q або O; Q являє собою H, C1-C3 алкіл, C1-C3 галоалкіл, бензил або заміщений бензил; 20 кожен R незалежно являє собою C1-C6 алкіл, C3-C6 циклоалкіл, C1-C6 гетероалкіл, C3-C6 a a a a b гетероцикл, C5-C12 арил, C5-C12 гетероарил, галоген, оксо, -OR , -C(O)R , -C(O)OR , -C(O)NR R , a b a b a b a b a a b a b -OC(O)NR R , -NR R , -NR C(O)R , -NR C(O)OR , -S(O)0-2R , -S(O)2NR R , -NR S(O)2R , -N3, -CN або -NO2, де кожен C1-C6 алкіл, C3-C6 циклоалкіл, C1-C6 гетероалкіл, C3-C6 гетероцикл, C5-C12 a арил, C5-C12 гетероарил необов’язково заміщений від одного до п’яти галогенами, оксо, -OR , a a a b a b a b a b a b a C(O)R , -C(O)OR , -C(O)NR R , -OC(O)NR R , -NR R , -NR C(O)R , -NR C(O)OR , -S(O)0-2R , a b a b S(O)2NR R , -NR S(O)2R , -N3, -CN або -NO2; a b кожен R та R незалежно являє собою H; або C1-C6 алкіл, C3-C6 циклоалкіл, C1-C6 гетероалкіл, C3-C6 гетероцикл, C5-C12 арил, C5-C12 гетероарил, кожен з яких необов’язково 21 a b заміщений від одного до п’яти R ; або R та R разом з атомами, до яких вони приєднані, утворюють гетероцикл, та 21 кожен R незалежно являє собою C1-C6 алкіл, C3-C6 циклоалкіл, C1-C6 гетероалкіл, C3-C6 гетероцикл, C5-C12 арил, C5-C12 гетероарил або галоген; або її фармацевтично прийнятна сіль. У іншому аспекті запропонована сполука, вибрана з групи, що складається зі сполук, зазначених у заголовках, перерахованих у прикладах від 1 до 201. У іншому аспекті запропонована фармацевтична композиція, що містить сполуку формули (I) або її фармацевтично прийнятну сіль та фармацевтично прийнятний носій. У іншому аспекті запропоноване застосування сполуки формули (I) або її фармацевтично прийнятної солі у терапії. Такі аспекти включають застосування сполуки формули (I) або її фармацевтично прийнятної солі для лікування суб'єкта, що має захворювання або стан, чутливий до інгібування бромодомен-вмісного білку; та застосування сполуки формули (I) або її фармацевтично прийнятної солі для одержання лікарського засобу для лікування людини, що має захворювання або стан, чутливий до інгібування бромодомен-вмісного білку. У іншому аспекті запропонований спосіб лікування суб'єкта, що має захворювання або стан, чутливий до інгібування бромодомен-вмісного білку, що включає введення терапевтично ефективної кількості сполуки формули (I) або її фармацевтично прийнятної солі. У деяких аспектах бромодомен-вмісний білок являє собою BRD4. У деяких аспектах захворювання або стан являє собою аутоімунне захворювання, запальне захворювання, нейродегенеративне захворювання, рак, серцево-судинний розлад, нирковий розлад, вірусну інфекцію або ожиріння. У конкретних варіантах реалізації захворювання або стан вибраний з ревматоїдного артриту, остеоартриту, атеросклерозу, псоріазу, системного червоного вовчаку, розсіяного склерозу, запального захворювання кишечнику, астми, хронічної обструкції дихальних шляхів, пневмонії, дерматиту, алопеції, нефриту, васкуліту, атеросклерозу, хвороби Альцгеймера, гепатиту, первинного біліарного цирозу, склерозуючого холангіту, діабету (у тому числі діабету типу I), гострого відторгнення трансплантованих органів, лімфом, множинних мієлом, лейкемії, новоутворень та солідних пухлин. У деяких аспектах захворювання або стан являє собою солідну пухлину товстої кишки, прямої кишки, простати, легенів, підшлункової залози, печінки, нирок, шейки матки, шлунку, яєчників, молочної залози, шкіри, головного мозку, мозкових оболонок або центральної нервової системи (у тому числі нейробластому або гліобластому). У деяких аспектах захворювання або стан являє собою лімфому. У деяких аспектах захворювання або 2 UA 111315 C2 5 10 15 20 25 30 35 40 45 стан являє собою B-клітинну лімфому. У деяких аспектах захворювання або стан являє собою лімфому Беркітта. У деяких аспектах захворювання або стан являє собою дифузійну великоклітинну В-клітинну лімфому. У деяких аспектах захворювання або стан являє собою множинну мієлому. У деяких аспектах захворювання або стан являє собою карциному. У деяких аспектах захворювання або стан являє собою серединну карциному NUT. У деяких аспектах суб'єкт являє собою людину. У іншому аспекті запропонований спосіб пригнічення або зниження транскрипції MYC у суб'єкта, що включає введення суб'єктові сполуки формули (I). У іншому аспекті запропонований спосіб лікування захворювання або стану у суб'єкта, у який залучена активація MYC, що включає введення суб'єктові сполуки формули (I). У деяких аспектах сполуку вводять внутрішньовенно, внутрішньом’язово, парентерально, назально або перорально. У одному аспекті сполуку вводять перорально. Також запропонований спосіб інгібування бромодомену у суб'єкта, що включає забезпечення суб'єктові терапевтично ефективної кількості сполуки формули (I) або її фармацевтично прийнятної солі. Також запропонований спосіб інгібування бромодомену у клітині, що включає введення у клітину сполуки формули (I). Слід розуміти, що введення у клітину може бути здійснене за допомогою введення сполуки суб'єктові. Також запропонований спосіб інгібування бромодомену, що включає приведення бромодомену у контакт зі сполукою формули (I) або її фармацевтично прийнятною сіллю. Також запропоноване застосування сполуки формули (I) або її фармацевтично прийнятної солі для одержання лікарського засобу для лікування захворювання або стану, чутливого до інгібування бромодомену. Також запропоновані набори, які включають сполуку формули (I) або її фармацевтично прийнятну сіль. У одному аспекті набір додатково включає інструкцію щодо застосування. У одному аспекті набір включає сполуку формули (I) або її фармацевтично прийнятну сіль та інструкції щодо застосування сполук для лікування захворювань або станів, описаних вище. Також запропоновані вироби, які включають сполуку формули (I) або її фармацевтично прийнятну сіль. У одному варіанті реалізації ємність може являти собою віалу, банку, ампулу, попередньо наповнений шприц або внутрішньовенний пакет. ДЕТАЛЬНИЙ ОПИС ВИНАХОДУ У даному документі описані сполуки формули (I), які включають сполуки формул (Ia) та (Ib), композиції та склади, які містять такі сполуки, та способи застосування та одержання таких сполук. Один аспект даного опису відноситься до сполук формули (I) (I) де 1a 1b R та R кожен незалежно являє собою C 1-C6 алкіл, C1-C6 алкокси, C1-C6 галоалкіл, C1-C6 галоалкокси, C1-C6 гідроксиалкіл, C3-C6 циклоалкіл або CH2-C3-C6 циклоалкіл; 2a 2b R та R кожен незалежно являє собою H або галоген; 3 R являє собою C5-C10 арил, C5-C10 гетероарил або C5-C10 гетероарилалкіл, кожен з яких необов’язково 20 заміщений від 1 до 5 R групами; або 4 -S(O)2NHR , 4 де R являє собою C1-C6 алкіл або C3-C7 циклоалкіл, кожен з яких необов’язково заміщений 20 від 1 до 5 R групами; або фрагмент формули 3 UA 111315 C2 5 10 15 20 25 30 35 40 45 де 6 7 8 R являє собою H, OH або галоген; та R та R кожен незалежно являє собою C1-C6 алкіл, C2-C6 алкеніл, C2-C6 алкініл, C3-C6 циклоалкіл, C1-C6 гетероалкіл, C5-C12 арил, C5-C12 гетероарил 20 або C5-C12 гетероарилалкіл, кожен з яких необов’язково заміщений від 1 до 5 R групами; або 6 R являє собою H, C1-C6 алкіл, C2-C6 алкеніл, C2-C6 алкініл, C3-C6 циклоалкіл, феніл, нафтил 7 8 або C3-C12 гетероарил; та R та R разом утворюють C1-C6 алкіліденову групу, що має подвійний 6 7 8 зв’язок з вуглецем, до якого приєднаний кожен з R , R , та R , де кожна з C1-C6 алкільної, C2-C6 алкенільної, C2-C6 алкінільної, -C3-C6 циклоалкільної, фенільної, нафтильної або C3-C12 20 гетероарильної груп необов’язково заміщена від 1 до 5 R групами; X являє собою N-Q або O; Q являє собою H, C1-C3 алкіл, C1-C3 галоалкіл, бензил або заміщений бензил; 20 кожен R незалежно являє собою C1-C6 алкіл, C3-C6 циклоалкіл, C1-C6 гетероалкіл, C3-C6 a a a a b гетероцикл, C5-C12 арил, C5-C12 гетероарил, галоген, оксо, -OR , -C(O)R , -C(O)OR , -C(O)NR R , a b a b a b a b a a b a b -OC(O)NR R , -NR R , -NR C(O)R , -NR C(O)OR , -S(O)0-2R , -S(O)2NR R , -NR S(O)2R , -N3, -CN або -NO2, де кожен C1-C6 алкіл, C3-C6 циклоалкіл, C1-C6 гетероалкіл, C3-C6 гетероцикл, C5-C12 a арил, C5-C12 гетероарил необов’язково заміщений від одного до п’яти галогенами, оксо, -OR , a a a b a b a b a b a b a C(O)R , -C(O)OR , -C(O)NR R , -OC(O)NR R , -NR R , -NR C(O)R , -NR C(O)OR , -S(O)0-2R , a b a b S(O)2NR R , -NR S(O)2R , -N3, -CN або -NO2; a b кожен R та R незалежно являє собою H; або C1-C6 алкіл, C3-C6 циклоалкіл, C1-C6 гетероалкіл, C3-C6 гетероцикл, C5-C12 арил, C5-C12 гетероарил, кожен з яких необов’язково 21 a b заміщений від одного до п’яти R ; або R та R разом з атомами, до яких вони приєднані, утворюють гетероцикл, та 21 кожен R незалежно являє собою C1-C6 алкіл, C3-C6 циклоалкіл, C1-C6 гетероалкіл, C3-C6 гетероцикл, C5-C12 арил, C5-C12 гетероарил або галоген; або її фармацевтично прийнятної солі. Одна підгрупа сполук формули (I) відноситься до сполук формули (Ia) (Ia) де 3 R являє собою C5-C10 арил, C5-C10 гетероарил або C5-C10 гетероарилалкіл, кожен з яких необов’язково 20 заміщений від 1 до 5 R групами; або 4 -S(O)2NHR , 4 де R являє собою C1-C6 алкіл або C3-C7 циклоалкіл, кожен з яких необов’язково заміщений 20 від 1 до 5 R групами; або фрагмент формули де 6 7 8 R являє собою H, OH або галоген; та R та R кожен незалежно являє собою C1-C6 алкіл, C2-C6 алкеніл, C2-C6 алкініл, C3-C6 циклоалкіл, C1-C6 гетероалкіл, C5-C12 арил, C5-C12 гетероарил 20 або C5-C12 гетероарилалкіл, кожен з яких необов’язково заміщений від 1 до 5 R групами; або 6 R являє собою H, C1-C6 алкіл, C2-C6 алкеніл, C2-C6 алкініл, C3-C6 циклоалкіл, феніл, нафтил 7 8 або C3-C12 гетероарил; та R та R разом утворюють C1-C6 алкіліденову групу, що має подвійний 6 7 8 зв’язок з вуглецем, до якого приєднаний кожен з R , R , та R , де кожна з C1-C6 алкільної, C2-C6 алкенільної, C2-C6 алкінільної, -C3-C6 циклоалкільної, фенільної, нафтильної або C3-C12 20 гетероарильної груп необов’язково заміщена від 1 до 5 R групами; Q являє собою H, C1-C3 алкіл, C1-C3 галоалкіл, бензил або заміщений бензил; 4 UA 111315 C2 20 5 10 15 20 25 30 35 40 45 кожен R незалежно являє собою C1-C6 алкіл, C3-C6 циклоалкіл, C1-C6 гетероалкіл, C3-C6 a a a a b гетероцикл, C5-C12 арил, C5-C12 гетероарил, галоген, оксо, -OR , -C(O)R , -C(O)OR , -C(O)NR R , a b a b a b a b a a b a b -OC(O)NR R , -NR R , -NR C(O)R , -NR C(O)OR , -S(O)0-2R , -S(O)2NR R , -NR S(O)2R , -N3, -CN або -NO2, де кожен C1-C6 алкіл, C3-C6 циклоалкіл, C1-C6 гетероалкіл, C3-C6 гетероцикл, C5-C12 a арил, C5-C12 гетероарил необов’язково заміщений від одного до п’яти галогенами, оксо, -OR , a a a b a b a b a b a b a C(O)R , -C(O)OR , -C(O)NR R , -OC(O)NR R , -NR R , -NR C(O)R , -NR C(O)OR , -S(O)0-2R , a b a b S(O)2NR R , -NR S(O)2R , -N3, -CN або -NO2; a b кожен R та R незалежно являє собою H; або C1-C6 алкіл, C3-C6 циклоалкіл, C1-C6 гетероалкіл, C3-C6 гетероцикл, C5-C12 арил, C5-C12 гетероарил, кожен з яких необов’язково 21 a b заміщений від одного до п’яти R ; або R та R разом з атомами, до яких вони приєднані, утворюють гетероцикл, та 21 кожен R незалежно являє собою C1-C6 алкіл, C3-C6 циклоалкіл, C1-C6 гетероалкіл, C3-C6 гетероцикл, C5-C12 арил, C5-C12 гетероарил або галоген; або до їх фармацевтично прийнятних солей. Інша підгрупа сполук формули (I) відноситься до сполук формули (Ib) (Ib) де 3 R являє собою C5-C10 арил, C5-C10 гетероарил або C5-C10 гетероарилалкіл, кожен з яких необов’язково 20 заміщений від 1 до 5 R групами; або 4 -S(O)2NHR , 4 де R являє собою C1-C6 алкіл або C3-C7 циклоалкіл, кожен з яких необов’язково заміщений 20 від 1 до 5 R групами; або фрагмент формули де 6 7 8 R являє собою H, OH або галоген; та R та R кожен незалежно являє собою C1-C6 алкіл, C2-C6 алкеніл, C2-C6 алкініл, C3-C6 циклоалкіл, C1-C6 гетероалкіл, C5-C12 арил, C5-C12 гетероарил 20 або C5-C12 гетероарилалкіл, кожен з яких необов’язково заміщений від 1 до 5 R групами; або 6 R являє собою H, C1-C6 алкіл, C2-C6 алкеніл, C2-C6 алкініл, C3-C6 циклоалкіл, феніл, нафтил 7 8 або C3-C12 гетероарил; та R та R разом утворюють C1-C6 алкіліденову групу, що має подвійний 6 7 8 зв’язок з вуглецем, до якого приєднаний кожен з R , R , та R , де кожна з C1-C6 алкільної, C2-C6 алкенільної, C2-C6 алкінільної, -C3-C6 циклоалкільної, фенільної, нафтильної або C3-C12 20 гетероарильної груп необов’язково заміщена від 1 до 5 R групами; 20 кожен R незалежно являє собою C1-C6 алкіл, C3-C6 циклоалкіл, C1-C6 гетероалкіл, C3-C6 a a a a b гетероцикл, C5-C12 арил, C5-C12 гетероарил, галоген, оксо, -OR , -C(O)R , -C(O)OR , -C(O)NR R , a b a b a b a b a a b a b -OC(O)NR R , -NR R , -NR C(O)R , -NR C(O)OR , -S(O)0-2R , -S(O)2NR R , -NR S(O)2R , -N3, -CN або -NO2, де кожен C1-C6 алкіл, C3-C6 циклоалкіл, C1-C6 гетероалкіл, C3-C6 гетероцикл, C5-C12 a арил, C5-C12 гетероарил необов’язково заміщений від одного до п’яти галогенами, оксо, -OR , a a a b a b a b a b a b a C(O)R , -C(O)OR , -C(O)NR R , -OC(O)NR R , -NR R , -NR C(O)R , -NR C(O)OR , -S(O)0-2R , a b a b S(O)2NR R , -NR S(O)2R , -N3, -CN або -NO2; a b кожен R та R незалежно являє собою H; або C1-C6 алкіл, C3-C6 циклоалкіл, C1-C6 гетероалкіл, C3-C6 гетероцикл, C5-C12 арил, C5-C12 гетероарил, кожен з яких необов’язково 21 a b заміщений від одного до п’яти R ; або R та R разом з атомами, до яких вони приєднані, утворюють гетероцикл, та 21 кожен R незалежно являє собою C1-C6 алкіл, C3-C6 циклоалкіл, C1-C6 гетероалкіл, C3-C6 гетероцикл, C5-C12 арил, C5-C12 гетероарил або галоген; 5 UA 111315 C2 5 10 15 20 25 30 35 або до їх фармацевтично прийнятних солей. 1a 1b У деяких сполуках формули (I) R та R кожен незалежно являє собою C1-C6 алкіл. У 1a 1b деяких сполуках формули (I) R та R кожен незалежно являє собою метил, етил або пропіл. У 1a 1b 1a 1b деяких сполуках формули (I) R та R є різними. У деяких сполуках формули (I) R та R є 1a 1b однаковими. У деяких сполуках формули (I) R та R обидва являють собою метил. 2a 2b У деяких сполуках формули (I) R та R обидва являють собою H. У деяких сполуках 2a 2b 2a формули (I) R та R обидва являють собою гало. У деяких сполуках формули (I) один з R та 2b R являє собою H та інший являє собою гало. У деяких сполуках формули (I) гало являє собою -F або -Cl. У деяких сполуках формули (I) X являє собою N-Q. У деяких сполуках формули (I) або (Ia) Q являє собою H, C 1-C3 алкіл або C1-C3 галоалкіл. 3 У деяких сполуках формули (I), (Ia) або (Ib) R являє собою C5-C10 арил, C5-C10 гетероарил 20 або C5-C10 гетероарилалкіл, кожен з яких необов’язково заміщений від 1 до 5 R групами. 3 У деяких сполуках формули (I), (Ia) або (Ib) R являє собою феніл, оксетаніл, тетрагідрофураніл, фураніл, тетрагідротіофеніл, тіофеніл, піроліл, піролініл, піролідиніл, діоксоланіл (dioxolanayl), оксазоліл, тіазоліл, імідазоліл, імідазолініл, імідазолідиніл, піразоліл, піразолініл, піразолідиніл, ізоксазоліл, ізотіазоліл, оксадіазоліл, триазоліл, тіадіазоліл, піраніл, піридиніл, піперидиніл, діоксаніл, морфолініл, тіоморфолініл, піридазиніл, піримідиніл, піразиніл, піперазиніл, триазиніл, індолізиніл, індоліл, ізоіндоліл, індолініл, хроменіл, бензофураніл, бензотіофеніл, дигідробензотіофеніл, індазоліл, бензімідазоліл, бензотіазоліл, бензоксазоліл, імідазо[1,2-a]піридиніл, пуриніл, хінолініл, хінолізиніл, ізохінолініл, циннолініл, фталазиніл, хіназолініл, хіноксалініл, інденіл, нафталеніл або азуленіл, кожен з яких необов’язково 20 заміщений від 1 до 5 R групами. 3 У деяких сполуках формули (I), (Ia) або (Ib) R являє собою фрагмент формули 6 7 8 де R являє собою H, OH або галоген; та R та R кожен незалежно являє собою C1-C6 алкіл, C2-C6 алкеніл, C2-C6 алкініл, C3-C6 циклоалкіл, C1-C6 гетероалкіл, C5-C12 арил, C5-C12 гетероарил 20 або C5-C12 гетероарилалкіл, кожен з яких необов’язково заміщений від 1 до 5 R групами. У 6 7 8 деяких сполуках R являє собою OH. У деяких сполуках R та R кожен незалежно являє собою C1-C6 алкіл, C3-C6 циклоалкіл, C1-C6 гетероалкіл, C5-C12 арил, C5-C12 гетероарил або C5-C12 20 гетероарилалкіл, кожен з яких необов’язково заміщений від 1 до 5 R групами. У деяких 7 8 сполуках формули (I), (Ia) або (Ib) R та R кожен незалежно являє собою C 1-C6 алкіл, C6 арил 20 або C6 гетероарил, кожен з яких необов’язково заміщений від 1 до 5 R групами. У деяких 7 8 сполуках R та R кожен незалежно являє собою C6 арил або C6 гетероарил (наприклад, 20 піридил), кожен з яких необов’язково заміщений від 1 до 5 R групами. У деяких сполуках 7 8 формули (I), (Ia) або (Ib) R та R кожен незалежно являє собою C1-C6 алкіл, кожен з яких 20 необов’язково заміщений від 1 до 5 R групами. 3 Інші необмежуючі приклади R включають наступні: 40 6 UA 111315 C2 5 10 7 UA 111315 C2 3 Додаткові необмежуючі приклади R включають наступні: 5 10 8 UA 111315 C2 5 У іншому аспекті сполука формули (I) може являти собою будь-яку з наступних сполук: , , , , , , , , , , 9 , , UA 111315 C2 та . У іншому аспекті сполука формули (I) може являти собою будь-яку з наступних сполук: , , , 5 , , , , , , 10 , , , , , UA 111315 C2 , , 5 10 15 20 25 30 , , , , , , , та . Якщо не зазначене інше, усі технічні та наукові терміни, використовувані у даному документі, мають таке ж значення, як і ті, що звичайно розуміються фахівцем зі звичайною кваліфікацією у даній галузі. Слід зазначити, що у даному документі та у прикладеній формулі винаходу форми однини включають посилання на множину, якщо з контексту явно не випливає інше. Таким чином, наприклад, посилання на «сполуку» включає безліч таких сполук, та посилання на «аналіз» включає посилання на один або кілька аналізів та їх еквівалентів, відомих фахівцям у даній галузі, і так далі. Тире на початку або наприкінці хімічної групи є питанням зручності; хімічні групи можуть бути зображені такими, що мають або що не мають одного або більше тире, не втрачаючи своє звичайне значення. Хвиляста лінія, проведена через лінію у структурі, вказує на точку приєднання групи. Пунктирна лінія вказує на необов'язковий зв'язок. Якщо це не потрібно хімічно або структурно, спрямованість не зазначена або не мається на увазі порядком, у якому написана хімічна група. Наприклад, група «-SO2CH2-» еквівалентна «-CH2SO2-», та обидві можуть бути з'єднані у будь-якому напрямку. Префікс «Cu-v» вказує, що наступна група має від u до v атомів вуглецю, один або більше із яких у конкретних групах (наприклад, гетероалкілі, гетероарилі, гетероарилалкілі і т.д.), можуть бути заміщені одним або більше гетероатомами або гетероатомними групами. Наприклад, «C1-6 алкіл» означає, що алкільна група має від 1 до 6 атомів вуглецю. Крім того, можуть бути використані або не використані конкретні альтернативні хімічні назви, які звичайно застосовують. Наприклад, двовалентна група, така як двовалентна «алкільна» група, двовалентна «арильна» група і т.д., також можуть згадуватися як «алкіленова» група або «алкіленільна» група, «ариленова» група або «ариленільна» група, відповідно. «Алкіл» відноситься до будь-якої групи, отриманої з лінійного або розгалуженого насиченого вуглеводню. Алкільні групи включають, але не обмежуються ними, метил, етил, пропіли, такі як пропан-1-іл, пропан-2-іл (ізо-пропіл), бутили, такі як бутан-1-іл, бутан-2-іл (втор-бутил), 2-метилпропан-1-іл (ізо-бутил), 2-метил-пропан-2-іл (t-бутил), пентили, гексили, октили, децили та їм подібні. Якщо не зазначене інше, алкільна група має від 1 до приблизно 10 атомів вуглецю, наприклад, від 1 до 10 атомів вуглецю, наприклад, від 1 до 6 атомів вуглецю, наприклад, від 1 до 4 атомів вуглецю. «Алкеніл» відноситься до будь-якої групи, отриманої з прямого або розгалуженого 11 UA 111315 C2 5 10 15 20 25 30 35 40 45 50 55 60 вуглеводню, який має щонайменше один подвійний зв’язок вуглець-вуглець. Алкенільні групи включають, але не обмежуються ними, етеніл (вініл), пропеніл (аліл), 1-бутеніл, 1,3-бутадієніл та їм подібні. Якщо не зазначене інше, алкенільна група має від 2 до приблизно 10 атомів вуглецю, наприклад, від 2 до 10 атомів вуглецю, наприклад, від 2 до 6 атомів вуглецю, наприклад, від 2 до 4 атомів вуглецю. «Алкініл» відноситься до будь-якої групи, отриманої з прямого або розгалуженого вуглеводню, який має щонайменше один потрійний зв’язок вуглець-вуглець, та включає такі групи, які мають один потрійний зв’язок та один подвійний зв’язок. Приклади алкінільних груп включають, але не обмежуються ними, етиніл (-CCH), пропаргіл (-CH2CCH), (E)-пент-3-ен-1ініл та їм подібні. Якщо не зазначене інше, алкінільна група має від 2 до приблизно 10 атомів вуглецю, наприклад, від 2 до 10 атомів вуглецю, наприклад, від 2 до 6 атомів вуглецю, наприклад, від 2 до 4 атомів вуглецю. «Арил» відноситься до будь-якої групи, отриманої з одного або більше ароматичних кілець, яка являє собою одиничне ароматичне кільце, біциклічну або поліциклічну кільцеву систему. Арильні групи включають, але не обмежуються ними, групи, отримані з аценафтилену, антрацену, азулену, бензолу, хризену, циклопентадієнільного аніону, нафталену, флуорантену, флуорену, індану, перилену, феналену, фенантрену, пірену та подібних. «Арилалкіл» (також «аралкіл») відноситься до будь-якої комбінації однієї або більше арильних груп та однієї або більше алкільних груп. Арилалкільні групи включають, але не обмежуються ними, групи, отримані з бензилу, толілу, диметилфенілу, 2-фенілетан-1-ілу, 2нафтилметилу, фенілметилбензилу, 1,2,3,4-тетрагідронафтилу та їм подібних. Арилалкільна група містить від 6 до приблизно 30 атомів вуглецю, наприклад, алкільна група може містити від 1 до приблизно 10 атомів вуглецю, та арильна група може містити від 5 до приблизно 20 атомів вуглецю. «Циклоалкіл» відноситься до циклічної алкільної групи. Циклоалкільна група може містити одне або більше циклічних кілець та включать конденсовані та місткові групи. Приклади включають, але не обмежуються ними, циклопропіл, циклобутил, циклопентил, циклогексил, адамантил, метилциклопропіл (циклопропілметил), етилциклопропіл та їм подібні. «Гало» та «галоген» відноситься до радикалів фтору, хлору, брому та йоду. «Галоалкіл» відноситься до алкілу, у якому один або більше атомів водню кожен заміщений галогеном. Приклади включають, але не обмежуються ними, -CH2Cl, -CH2F, -CH2Br, -CFClBr, CH2CH2Cl, -CH2CH2F, -CF3, -CH2CF3, -CH2CCl3 та їм подібні, а також алкільні групи, такі як перфторалкіл, у яких усі атоми водню заміщені атомами фтору. «Гетероалкіл» відноситься до алкілу, у якому один або більше атомів вуглецю (та будь-які зв’язані атоми водню) кожен незалежно заміщені однаковими або різними гетероатомами або гетероатомними групами. Гетероатоми включають, але не обмежуються ними, N, P, O, S тощо. Гетероатомні групи включають, але не обмежуються ними, -NR-, -O-, -S-, -PH-, -P(O)2-, -S(O)-, S(O)2- та їм подібні, де R являє собою H, алкіл, арил, циклоалкіл, гетероалкіл, гетероарил або циклогетероалкіл. Термін «гетероалкіл» включає гетероциклоалкіл (циклічну гетероалкільну групу), алкіл-гетероциклоалкіл (лінійну або розгалужену C1-C6 алкільну групу, приєднану до циклічної гетероалкільної групи) та їм подібні. Гетероалкільні групи включають, але не обмежуються ними, -OCH3, -CH2OCH3, -SCH3, -CH2SCH3, -NRCH3, -CH2NRCH3 та їм подібні, де R являє собою водень, алкіл, арил, арилалкіл, гетероалкіл або гетероарил, кожен з яких необов’язково може бути заміщений. Гетероалкільна група містить від 1 до приблизно 10 вуглецевих та гетероатомів, наприклад, від 1 до 6 вуглецевих та гетероатомів. «Гетероарил» відноситься до арильної групи, у якій один або більше атомів вуглецю (та будь-які зв’язані атоми водню) кожен незалежно заміщені однаковими або різними гетероатомами або гетероатомними групами, як визначено вище. Гетероарильні групи включають, але не обмежуються ними, групи, отримані з акридину, бензімідазолу, бензтіофену, бензофурану, бензоксазолу, бензотіазолу, карбазолу, карболіну, циноліну, фурану, імідазолу, імідазопіридину, індазолу, індолу, індоліну, індолізину, ізобензофурану, ізохромену, ізоіндолу, ізоіндоліну, ізохіноліну, ізотіазолу, ізоксазолу, нафтиридину, оксадіазолу, оксазолу, перимідину, фенантридину, фенантроліну, феназину, фталазину, птеридину, пурину, пірану, піразину, піразолу, піридазину, піридину, піримідину, піролу, піролізину, хіназоліну, хіноліну, хінолізину, хіноксаліну, тетразолу, тіадіазолу, тіазолу, тіофену, триазолу, ксантену та їм подібних. «Гетероарилалкіл» відноситься до арилалкільної групи, у якій один або більше атомів вуглецю (та будь-які зв’язані атоми водню) незалежно заміщені однаковими або різними гетероатомами або гетероатомними групами, як визначено вище. Гетероарилалкільні групи включають, але не обмежуються ними, групи, отримані з гетероарильних груп з алкільними замісниками (наприклад, метилпіридинів, етилтіофенів, метилтіазолів, диметилізоксазолів 12 UA 111315 C2 5 10 15 20 25 30 35 40 45 50 55 60 тощо), гідрогенізованих гетероарильних груп (дигідрохінолінів, наприклад, 3,4-дигідрохіноліну, дигідроізохінолінів, наприклад, 1,2-дигідроізохіноліну, дигідроімідазолу, тетрагідроімідазолу тощо), індоліну, ізоіндоліну, ізоіндолонів (наприклад, ізоіндолін-1-ону), ізатину, дигідрофталазину, хінолінону, спіро[циклопропан-1,1'-ізоіндолін]-3'-ону та їм подібних. «Гетероцикл», «гетероциклічний» та «гетероцикліл» відноситься до одиничного насиченого або частково ненасиченого неароматичного кільця або неароматичної багатокільцевої системи, що має щонайменше один гетероатом або гетероатомну групу, як визначено вище. Гетероцикли включають, але не обмежуються ними, групи, отримані з азетидину, азиридину, імідазолідину, морфоліну, оксирану (епоксиду), оксетану, піперазину, піперидину, піразолідину, піперидину, піролідину, піролідинону, тетрагідрофурану, тетрагідротіофену, дигідропіридину, тетрагідропіридину, хінуклідину, N-бромпіролідину, N-хлорпіперидину та їм подібних. Термін «фармацевтично прийнятний» по відношенню до речовини відноситься до такої речовини, яку в цілому вважають безпечною та підходящою для застосування, яка не має надмірної токсичності, не викликає подразнення, алергійної реакції та їм подібних, порівнянних з виправданим співвідношенням користь/ризик. «Фармацевтично прийнятна сіль» відноситься до солі сполуки, яка є фармацевтично прийнятною та яка має (або може бути перетворена у форму, яка має) необхідну фармацевтичну активність вихідної сполуки. Такі солі включають солі приєднання кислоти, утворені неорганічними кислотами, такими як хлористоводнева кислота, бромистоводнева кислота, сірчана кислота, азотна кислота, фосфорна кислота та їм подібні; або утворені органічними кислотами, такими як оцтова кислота, бензолсульфонова кислота, бензойна кислота, камфорсульфонова кислота, лимонна кислота, етансульфонова кислота, фумарова кислота, глюкогептонова кислота, глюконова кислота, молочна кислота, малеїнова кислота, малонова кислота, мигдальна кислота, метансульфонова кислота, 2-нафталенсульфонова кислота, олеїнова кислота, пальмітинова кислота, пропіонова кислота, стеаринова кислота, бурштинова кислота, винна кислота, п-толуолсульфонова кислота, триметилоцтова кислота та їм подібні, та солі, утворені, коли кислотний протон, наявний у вихідній сполуці, заміщається або іоном металу, наприклад, іоном лужного металу, іоном лужноземельного металу або іоном алюмінію; або утворює координаційний зв'язок з органічною основою, такою як діетаноламін, триетаноламін, N-метилглюкамін та подібні. Також у даний опис включені солі амонію та заміщені або четвертинні солі амонію. Зразкові необмежуючі переліки фармацевтично прийнятних солей можна знайти у S.M. Berge et al., J. Pharma Sci., 66(1), 1-19 (1977), та Remington: The Science and Practice of Pharmacy, R. Hendrickson, ed., 21st edition, Lippincott, Williams & Wilkins, Philadelphia, PA, (2005), at p. 732, Table 38-5, які включені у дану заявку за допомогою посилання. «Суб'єкт» та «суб'єкти» відносяться до людини, свійських тварина (наприклад, собак та кішок), сільськогосподарських тварин (наприклад, великої рогатої худоби, коней, овець, кіз та свиней), лабораторних тварин (наприклад, мишей, щурів, хом'яків, морських свинок, свиням, кроликів, собак та мавп) та їм подібних. «Обробка» та «лікування» захворювання включає наступне: (1) запобігання або зниження ризику розвитку захворювання, тобто забезпечення відсутності розвитку клінічних симптомів захворювання у суб'єкта, який може зазнати або схильний до захворювання, але ще не відчуває або не проявляє симптомів захворювання, (2) інгібування захворювання, тобто припинення або зниження розвитку захворювання або його клінічних симптомів, або (3) ослаблення захворювання, тобто забезпечення регресії захворювання або його клінічних симптомів. «Ефективна кількість» відноситься до кількості, яка може бути ефективною для досягнення необхідної біологічної, клінічної або медичної відповіді, включаючи кількість сполуки, яка, при введенні суб'єктові для лікування захворювання, є достатньою для здійснення такого лікування. Ефективна кількість буде варіюватися залежно від сполуки, захворювання та його важкості та віку, маси та т.д. суб'єкта, що підлягає лікуванню. Ефективна кількість може включати діапазон кількостей. Слід розуміти, що можна застосовувати комбінації хімічних груп, та вони будуть розпізнані фахівцями у даній галузі. Наприклад, група «гідроксиалкіл» буде відноситися до гідроксильної групи, прикріпленої до алкільної групи. Може бути легко передбачена велика кількість таких комбінацій. Також запропоновані сполуки, у яких від 1 до n атомів водню, приєднані до атому вуглецю, можуть бути заміщені атомом дейтерію або D, у яких n являє собою кількість атомів водню у молекулі. Як відомо у даній галузі, атом дейтерію являє собою нерадіоактивний ізотоп атому 13 UA 111315 C2 5 10 15 20 25 30 35 40 45 50 55 60 водню. Такі сполуки можуть проявляти підвищену стійкість до метаболізму та, отже, можуть підходити для збільшення періоду напіврозпаду сполук при введенні ссавцеві. Див., наприклад, Foster, “Deuterium Isotope Effects in Studies of Drug Metabolism,” Trends Pharmacol. Sci., 5(12):524-527 (1984). Такі сполуки синтезують за способами, добре відомими у даній галузі, наприклад, із застосуванням вихідних матеріалів, у яких один або кілька атомів водню були замінені дейтерієм. Сполуки даної формули, описаної у даному документі, охоплюють розкриту сполуку та всі її фармацевтично прийнятні солі, стереоізомери, таутомери, сольвати та їх дейтеровані форми, якщо не зазначене інше. Фармацевтичні композиції сполук формули (I) (включаючи сполуки формул (Ia) та (Ib)) можна вводити або однією або декількома дозами будь-яким із прийнятних способів введення агентів, що мають подібні властивості, наприклад, як описано у патентах та патентних заявках, включених за допомогою посилання, включаючи ректальний, буккальний, інтраназальний та трансдермальний шляхи, за допомогою внутрішньоартеріальної ін'єкції, внутрішньовенно, внутрішньочеревинно, парентерально, внутрішньом’язово, підшкірно, перорально, місцево, у вигляді інгаляцій або через просочені або покриті пристрої, такі як стент, наприклад, або циліндричний полімер, що поміщають у артерію. У одному аспекті сполуки, описані у даному документі, можна вводити перорально. Пероральне введення можна здійснювати, наприклад, за допомогою капсул або таблеток, покритих кишковорозчинною оболонкою. При приготуванні фармацевтичних композицій, які містять, щонайменше одну сполуку формули (I) або її фармацевтично прийнятну сіль, складний ефір, проліки або сольват, активний інгредієнт звичайно розбавляють допоміжною речовиною та/або поміщають у носій, який може бути у формі капсули, саше, паперу або іншої ємності. У випадку, коли допоміжна речовина слугує розріджувачем, вона може бути у формі твердого, напівтвердого або рідкого матеріалу (як описано вище), який діє як наповнювач, носій або середовище для активного інгредієнту. Таким чином, композиції можуть бути у формі таблеток, пігулок, порошків, пастилок, саше, крохмальних капсул, еліксирів, суспензій, емульсій, розчинів, сиропів, аерозолів (у формі твердої речовини або у рідкому середовищі), мазей, що містять, наприклад, не більше 10% по масі активної сполуки, м'яких та твердих желатинових капсул, стерильних розчинів для ін'єкцій та стерильно упакованих порошків. Деякі приклади підходящих допоміжних речовин включають лактозу, декстрозу, сахарозу, сорбіт, маніт, крохмалі, аравійську камедь, фосфат кальцію, альгінати, трагакант, желатин, силікат кальцію, мікрокристалічну целюлозу, полівінілпіролідон, целюлозу, стерильну воду, сироп та метилцелюлозу. Склади можуть додатково включати: змащувальні агенти, такі як тальк, стеарат магнію та мінеральне масло; змочувальні агенти; емульгуючі та суспендуючі агенти; консервуючі агенти, такі як метил- та пропілгідроксибензоати; підсолоджувачі; та ароматизатори. Композиції, які включають щонайменше одну сполуку формули (I) або її фармацевтично прийнятну сіль, складний ефір, проліки або сольват, можуть бути приготовлені таким чином, щоб забезпечити швидке, уповільнене або відстрочене вивільнення активного інгредієнта після введення суб'єктові із застосуванням процедур, відомих у даній галузі. Системи доставки лікарських засобів з контрольованим вивільненням для перорального введення включають системи осмотичних насосів та системи розчинення, що містять резервуари з полімерним покриттям або склади з полімерною матрицею, що містить лікарський засіб. Приклади систем з контрольованим вивільненням наведені у патентах США № 3845770; 4326525; 4902514 та 5616345. У іншому складі для застосування у способах згідно із даним винаходом застосовують пристрої трансдермальної доставки («пластири»). Такі трансдермальні пластири можна застосовувати для безперервної або періодичної інфузії сполук згідно із даним винаходом у контрольованих кількостях. Конструкція та застосування трансдермальних пластирів для доставки фармацевтичних агентів добре відомі у даній галузі. Див., наприклад, патенти США № 5023252, 4992445 та 5001139. Такі пластири можуть бути виконані для безперервної, періодичної доставки фармацевтичних агентів або доставки при необхідності. У деяких варіантах реалізації композиції можуть бути приготовлені у вигляді одиничної лікарської форми. Термін «одиничні лікарські форми» відноситься до фізично дискретних одиниць, які підходять у якості разових доз для суб'єктів людини та інших ссавців, причому кожна одиниця містить задану кількість активного матеріалу, розраховану на одержання необхідного терапевтичного ефекту, у комбінації з підходящою фармацевтичною допоміжною речовиною (наприклад, таблетки, капсули, ампули). Сполуки в цілому вводять у фармацевтично ефективній кількості. У деяких варіантах реалізації для перорального введення кожна одинична лікарська форма містить від приблизно 10 мг до приблизно 1000 мг сполуки, описаної у даному 14 UA 111315 C2 5 10 15 20 25 30 35 40 45 50 55 60 документі, наприклад, від приблизно 50 мг до приблизно 500 мг, наприклад, приблизно 50 мг, приблизно 75 мг, приблизно 100 мг, приблизно 150 мг, приблизно 200 мг, приблизно 250 мг або приблизно 300 мг. У інших варіантах реалізації для парентерального введення кожна лікарська форма містить від 0,1 до 700 мг сполуки, описаної у даному документі. Слід розуміти, однак, що кількість сполуки, що фактично вводиться, звичайно визначає лікар у світлі відповідних обставин, включаючи стан, що підлягає лікуванню, обраний шлях введення, конкретну сполуку, що вводиться, та її відносну активність, вік, масу та реакцію конкретного суб'єкта та важкість симптомів суб'єкта. У конкретних варіантах реалізації рівні дозувань можуть становити від 0,1 мг до 100 мг на кілограм маси тіла на день, наприклад, від приблизно 1 мг до приблизно 50 мг на кілограм, наприклад, від приблизно 5 мг до приблизно 30 мг на кілограм. Такі рівні дозувань у деяких випадках можуть підходити для лікування вищевказаних станів. У інших варіантах реалізації рівні дозувань можуть становити від приблизно 10 мг до приблизно 2000 мг для суб'єкта на день. Кількість активного інгредієнта, яку можна комбінувати з наповнювачем для одержання одиничної лікарської форми, буде варіюватися залежно від хазяїна та конкретного способу введення. Одиничні лікарські форми можуть містити від 1 мг до 500 мг активного інгредієнту. Частота дозування також може змінюватися залежно від використовуваної сполуки та конкретного захворювання або стану, що підлягає лікуванню. У деяких варіантах реалізації, наприклад, для лікування аутоімунного та/або запального захворювання, застосовують режим дозування 4 рази на день або менше. У деяких варіантах реалізації застосовують режим дозування 1 або 2 рази на день. Проте слід розуміти, що конкретний рівень дози для будь-якого конкретного суб'єкта буде залежати від безлічі факторів, включаючи активність конкретної використовуваної сполуки, вік, масу тіла, загальний стан здоров'я, стать, раціон харчування, час введення, спосіб введення та швидкість виведення комбінації лікарських засобів та важкість конкретного захворювання у суб'єкта, що зазнає лікування. Для одержання твердих композицій, таких як таблетки, основний активний інгредієнт може бути змішаний з фармацевтичною допоміжною речовиною з одержанням твердої композиції для надання їй лікарської форми, що містить гомогенну суміш сполуки формули (I) або її фармацевтично прийнятної солі, складного ефіру, проліків або сольвату. У випадках, коли, посилаючись на дані композиції до надання їм лікарської форми, як на гомогенні, активний інгредієнт може бути рівномірно диспергований по всій композиції, тоді композицію можна легко розділити на рівні ефективні одиничні лікарські форми, такі як таблетки, пігулки та капсули. Таблетки або пігулки, що містять сполуки, описані у даному документі, можуть бути покриті або приготовлені за іншим способом, щоб одержати лікарську форму, яка забезпечує перевагу пролонгованої дії, або для захисту від кислих умов у шлунку. Наприклад, таблетка або пігулка може містити внутрішній дозований та зовнішній дозований компонент, причому останній міститься у вигляді оболонки над першим. Два компоненти можуть бути розділені ентеросолюбільним шаром, який слугує для розпаду у шлунку та дозволяє внутрішньому компоненту попадати у дванадцятипалу кишку неушкодженим або бути відстроченим для вивільнення. Для таких ентеросолюбільних шарів або покриттів можна застосовувати різноманітні матеріали, включаючи ряд полімерних кислот та суміші полімерних кислот з такими матеріалами, як шелак, цетиловий спирт та ацетат целюлози. Запропоновані набори, які містять сполуку формули (I) або її фармацевтично прийнятну сіль та підходяще упакування. У одному варіанті реалізації набір додатково містить інструкції щодо застосування. У одному аспекті набір містить сполуку формули (I) або її фармацевтично прийнятну сіль та інструкції щодо застосування сполук для лікування захворювань або станів, описаних у даному документі. Запропоновані вироби, які включають сполуку формули (I) або її фармацевтично прийнятну сіль у підходящій ємності. Ємність може являти собою віалу, банку, ампулу, попередньо наповнений шприц або внутрішньовенний пакет. Сполуки формули (I) можуть бути об'єднані з одним або більш додатковими протираковими або протизапальними агентами, включаючи один з наступних. Для лікування різних видів раку застосовують та розробляють різні інгібітори кінази. Наприклад, при раку людини спостерігають активацію фосфатидилінозитол 3-кіназного (PI3K) шляху, та агенти, що інгібують PI3K, досліджують або розробляють як потенційні протиракові лікарські засоби та для застосування у протираковій терапії. Додаткові інгібітори кінази включають інгібітори тирозинкінази селезінки (Syk) та Янус-кінази (JAK). Інші агенти, що інгібують споріднені шляхи, також становлять інтерес у якості протиракових або протизапальних агентів, включаючи агенти, що інгібують Ras/Raf/MEK/ERK шляхи та PI3K/PTEН/Оkt/mTOR шляхи. Як описано у даному документі, такі інгібітори включають агенти, які інгібують усі цільові підкласи (наприклад, PI3K альфа, бета, 15 UA 111315 C2 5 10 дельта та гама), агенти, які інгібують у першу чергу один підклас та агенти, які інгібують підмножину всіх підкласів. Сполуки формули (I) також можуть бути об'єднані з одним або більше додатковими протираковими або протизапальними агентами, включаючи інгібітори або антагоністи лізилоксидази 2 (LOXL2) та інгібітори або антагоністи рецептору аденозину A2B. У різних аспектах сполуки формули (I) можуть бути об'єднані з одним або більше інгібіторами кінази. Приклади інгібіторів кінази включають інгібітори PI3K, інгібітори Syk та інгібітори JAK. Приклади інгібіторів PI3K включають сполуку A, сполуку B та сполуку C: (Сполука A) (Сполука B) 15 (Сполука C). Додаткові приклади інгібіторів PI3K включають XL147, BKM120, GDC-0941, BAY80-6946, PX866, CH5132799, XL756, BEZ235 та GDC-0980. Інгібітори mTOR включають OSI-027, AZD2014 та CC-223. Інгібітори AKT включають MK-2206, GDC-0068 та GSK795. Приклади інгібіторів Syk включають сполуку D: 16 UA 111315 C2 (Сполука D). Додаткові інгібітори Syk включають R788 (фостаматиніб), R-406 (таматиніб) та PRT062607. Приклади інгібіторів JAK включають сполуку E: 5 10 15 20 25 30 35 40 (Сполука E). Додаткові інгібітори JAK включають руксолітиніб, тофацитиніб, барицитиніб, CYT387, лестауртиніб, пакритиніб та TG101348. У інших аспектах сполуки формули (I) можуть бути об’єднані з одним або більше інгібіторами або модуляторами (наприклад, антагоністами) LOXL2, рецептора аденозину A2B, MMP-9, ASK1, BTK, mTOR, HDAC та MEK. У інших аспектах сполука формули (I) може бути об’єднана з одним або більше компонентами CHOP-терапії (циклофосфамід, адріаміцин, вінкристин, преднізолон). У інших аспектах сполука формули (I) може бути об’єднана з одним або більше з рибавірину та інтерферону. У інших аспектах сполука формули (I) може бути об’єднана з одним або більше агентами, які активують або реактивують прихований вірус імунодефіциту людини (HIV). Наприклад, сполуки формули (I) можуть бути об’єднані з інгібітором гістондеацетилази (HDAC) (перерахованими вище) або активатором протеїнкінази C (PKC). Наприклад, сполуки формули (I) можуть бути об’єднані з ромідепсином або панобіностатом. ПРИКЛАДИ Загальні способи. Синтез конкретних сполук та проміжних сполук, які застосовували для одержання сполук, докладно описаний у наступних розділах. Номера сполук зазначені для зручності. Усі операції із застосуванням матеріалів, чутливих до вологи та/або кисню, проводили у атмосфері сухого азоту у попередньо висушеному скляному посуді. Якщо не зазначене інше, матеріали одержували з комерційно доступних джерел та використовували без додаткового очищення. Флеш-хроматографію проводили на Isco Combiflash Companion із застосуванням RediSep Rf силікагелевих картриджів від Teledyne Isco. Тонкошарову хроматографію проводили із застосуванням попередньо покритих пластин, придбаних у E. Merck (силікагель 60 PF254, 0,25 мм), та плями візуалізували із застосуванням довгохвильового ультрафіолетового світла після відповідного забарвлюючого реагенту. Спектри ядерного магнітного резонансу («ЯМР») записували на резонансному спектрометрі 1 Varian 400 МГц. H ЯМР хімічні зсуви наведені у частинах на мільйон (δ) убік слабкого поля тетраметилсилану («TMS»), із застосуванням сигналу TMS або залишкового розчиннику (CНСl3 1 = δ 7,24, ДМСО = δ 2,50) як внутрішнього стандарту. H ЯМР інформація наведена у наступному форматі: мультиплетність (s, синглет; d, дублет; t, триплет; q, квартет; m, мультиплет), коефіцієнт зв'язку(ів) (J) у Герцах, число протонів. Приставку app іноді застосовували у випадках, коли мультиплетність дійсного сигналу була не розділена, та br указує на розширення досліджуваного сигналу. Сполуки називали із застосуванням ChemBioDraw Ultra Version 12.0. Аналіз рідинною хроматомас-спектрометрією (LCMS) проводили із застосуванням 17 UA 111315 C2 5 10 15 20 25 30 35 40 спектрометру PE SCIEX API 2000 зі колонкою Phenomenex Luna 5 мікрон C18. Препаративну ВЕРХ проводили на рідинному хроматографі Gilson HPLC 215 з колонкою Phenomenex (Gemini 10 µ, C18, 110A) та детектором UV/VIS 156. Коли одержання вихідних матеріалів конкретно не описане, сполуки є відомими або можуть бути отримані аналогічно способам, відомим у даній галузі або як описано у прикладах. Фахівцеві у даній галузі буде зрозуміло, що методики синтезу, описані у даному документі, наведені тільки як зразкові способи одержання сполук, описаних у даному документі, та що можна застосовувати інші відомі способи та варіанти способів, описаних у даному документі. Способи або ознаки, описані у різних прикладах, можна поєднувати або адаптувати різним чином, щоб забезпечити додаткові шляхи одержання сполук, описаних у даному документі. Способи одержання нових сполук, описані у даному документі, будуть очевидні фахівцям у даній галузі з методик, описаних, наприклад, у схемах реакцій та прикладах нижче та у посиланнях, наведених у даному документі. ПРИКЛАДИ Способи одержання нових сполук, описаних у даному документі, будуть очевидні спеціалістам у даній галузі з описаних підходящих методик, наприклад, у схемах реакцій та прикладах нижче та у посиланнях, приведених у даному документі. Схема 1 Сполука формули (1-a) може бути отримана шляхом реакції сполучення Сузукі для комерційно доступної сполуки формули (a) з комерційно доступним ізоксазоловим складним ефіром боронової кислоти, представленим вище, у присутності основи. Замісники X у сполуці (a) можуть являти собою будь-яку підходящу відхідну групу (наприклад, Cl, Br, I, OTf). Підходящі каталізатори можуть включати паладієві каталізатори, такі як (1,3-біс(2,6діізопропілфеніл)імідазоліден)(3-хлорпіридил)паладію(II) дихлорид (Peppsi-iPr). Підходящі основи можуть включати, наприклад, карбонат цезію або 1,8-діазобіциклоундец-7-ен. Підходящі розчинники можуть включати комбінацію органічних розчинників та води, включаючи, наприклад, 1,4-діоксан, ТГФ, диметоксиетан або диметилформамід та воду. Реакцію проводили у підходящому розчиннику у атмосфері азоту при підвищеній температурі від приблизно 70 °C до 150 °C впродовж від приблизно 30 секунд до 5 годин. Коли реакція по суті була закінчена, реакційну суміш залишали остигати до кімнатної температури. Реакційну суміш можна розділити на водну фазу та органічну фазу. Водну фазу відкидали, та органічну фазу концентрували при зниженому тиску, та залишок очищали шляхом обернено-фазної високоефективної рідинної хроматографії, проводячи елюювання сумішшю підходящого розчиннику, такого як ацетонітрил, та води, щоб виділити сполуки формули (A). Інші прикладові способи одержання сполук формули (B) представлені на реакційній схемі №. 2. Схема 2 Стадія 1 - Одержання сполук формули (B-1) Сполука формули (B-1) може бути отримана шляхом реакції сполучення Сузукі для комерційно доступної хлор-бром заміщеної ароматичної гетероциклічної сполуки, яка може нести додаткове гетероарильне кільце, як показано вище, у двох можливих точках приєднання з 18 UA 111315 C2 5 10 15 20 25 30 35 40 45 50 комерційно доступним ізоксазоловим складним ефіром боронової кислоти, показаним вище, у присутності основи. Підходящі каталізатори можуть включати паладієві каталізатори, такі як [1,1'-біс(дифенілфосфіно)фероцен]дихлорпаладій(II). Підходящі основи можуть включати, наприклад, карбонат цезію або 1,8-діазобіциклоундец-7-ен. Підходящі розчинники можуть включати комбінацію органічних розчинників та води, включаючи, наприклад, 1,4-діоксан, ТГФ, диметоксиетан або диметилформамід та воду. Реакцію проводили у підходящому розчиннику у атмосфері азоту при підвищеній температурі від приблизно 70 °C до 150 °C впродовж від приблизно 30 секунд до 5 годин. Коли реакція по суті була закінчена, реакційну суміш залишали остигати до кімнатної температури. Реакційну суміш можна розділити на водну фазу та органічну фазу. Водну фазу відкидали, та органічну фазу концентрували при зниженому тиску, та залишок очищали шляхом обернено-фазної високоефективної рідинної хроматографії, проводячи елюювання сумішшю підходящого розчиннику, такого як ацетонітрил, та води, щоб ізолювати сполуки формули (B-1). Сполука формули (B-1) також може бути очищена іншими традиційними способами, такими як хроматографія на силікагелі. Стадія 2 - Одержання сполук формули (B-2) Сполука формули (B-2) може бути отримана шляхом реакції сполучення Сузукі для сполуки 3 формули (B-1) з комерційно доступними похідними боронової кислоти, що несуть замісник R , визначений у описі для сполук формули (I). Підходящі каталізатори можуть включати паладієві каталізатори, такі як (1,3-біс(2,6-діізопропілфеніл)імідазоліден)(3-хлорпіридил)паладію (II) дихлорид (Peppsi-iPr). Підходящі основи можуть включати, наприклад, карбонат цезію або 1,8діазобіциклоундец-7-ен. Підходящі розчинники можуть включати комбінацію органічних розчинників та води, включаючи, наприклад, 1,4-діоксан, ТГФ, диметоксиетан або диметилформамід та воду. Реакцію проводили у підходящому розчиннику у атмосфері азоту при підвищеній температурі від приблизно 70 °C до 150 °C впродовж від приблизно 30 секунд до 5 годин. Коли реакція по суті була закінчена, реакційну суміш залишали остигати до кімнатної температури. Реакційну суміш можна розділити на водну фазу та органічну фазу. Водну фазу відкидали, та органічну фазу концентрували при зниженому тиску, та залишок очищали шляхом обернено-фазної високоефективної рідинної хроматографії, проводячи елюювання сумішшю підходящого розчиннику, такого як ацетонітрил, та води, щоб виділити сполуки формули (B-2). Інші прикладові способи одержання сполук формули (C-2) представлені на реакційній схемі №. 3. Схема 3 Стадія 1 - Одержання сполук формули (C-1) Підходящий реагент, що доставляє карбоніл, приводили у взаємодію зі сполукою формули (C-1) (із замісником Q, що являє собою або H або метил) у підходящому розчиннику, та залишали для здійснення взаємодії впродовж періоду часу, такого як 1-5 годин при підвищеній температурі 80-150 °C. Підходящі розчинники включають органічні розчинники, такі як тетрагідрофуран. Коли реакція по суті була закінчена, сполуку (C-1) виділяли шляхом видалення розчиннику під вакуумом та очищення традиційними способами, такими як перекристалізація або розтирання у суміші підходящих розчинників, таких як гексан та етилацетат. Стадія 2 - Одержання сполук формули (C-2) Сполука формули (C-2) може бути отримана шляхом реакції сполучення Сузукі для сполуки формули (C-1) з бороновою кислотою, представленою вище, у присутності основи. Як показано вище, боронова кислота заміщена зв’язаною через вуглець фенільною, нафтильною або 3 гетероарильною R групою, визначеною у описі для сполук формули (I). Слід розуміти, що боронатні складні ефіри або інші підходящі комплекси бору (тобто -BF3K солі тощо) також можна застосовувати замість боронової кислоти. Підходящі каталізатори можуть включати паладієві каталізатори, такі як (1,3-біс(2,6-діізопропілфеніл)імідазоліден)(3 19 UA 111315 C2 5 10 15 20 25 30 хлорпіридил)паладію(II) дихлорид (Peppsi-iPr). Підходящі основи можуть включати, наприклад, карбонат цезію або 1,8-діазобіциклоундец-7-ен. Підходящі розчинники можуть включати комбінацію органічних розчинників та води, включаючи, наприклад, 1,4-діоксан, ТГФ, диметоксиетан або диметилформамід та воду. Реакцію проводили у підходящому розчиннику у атмосфері азоту при підвищеній температурі від приблизно 70 °C до 150 °C впродовж від приблизно 30 секунд до 5 годин. Коли реакція по суті була закінчена, реакційну суміш залишали остигати до кімнатної температури. Реакційну суміш можна розділити на водну фазу та органічну фазу. Водну фазу відкидали, та органічну фазу концентрували при зниженому тиску, та залишок очищали шляхом оберненофазної високоефективної рідинної хроматографії, проводячи елюювання сумішшю підходящого розчиннику, такого як ацетонітрил, та води, щоб виділити сполуки формули (C-2). Крім того, сполука формули (C-2) може бути очищена іншими традиційними способами, такими як хроматографія на силікагелі або перекристалізація. Коли реакції, описані у даному документі, по суті закінчені, реакційну суміш можна залишати остигати до кімнатної температури. Реакційна суміш може бути концентрована або очищена будь-яким підходящим способом, включаючи, наприклад, хроматографію на силікагелі або препаративну ВЕРХ з одержанням сполук формули (I), (Ia) та (Ib), включаючи кожну зі сполук у прикладах, приведених нижче. Стадія 3: Одержання сполук формули (C1-C5) Сполука формули (C-4, C-5 та C-6) може бути отримана наступним чином: (C-1) приводили у взаємодію з підходящим джерелом карбонілу, як описано раніше, з одержанням (C-2). (C-2) потім приводили у взаємодію з метильованим алкільним або арильним реагентами (наприклад, але не обмежуючись ними, Li або Mg) з одержанням симетричних карбінолів (C-4) або конвертували у амід Weinreb (C-3), після чого приводили у взаємодію з метильованим алкільним або арильним реагентами з одержанням кетону (C-5). Кетон (C-5) потім знову можна приводить у взаємодію з метильованим алкільним або арильним реагентами з одержанням асиметричного карбінолу (C-6). Крім того, зазначені вище сполуки можуть бути отримані шляхом конвертування (C-1) у відповідний 2-алкокси-бензімідазол (C-7), який потім конвертували у (C-4), включаючи (C-6), із застосуванням зазначених вище способів. 20 UA 111315 C2 Схема 3 5 10 15 20 25 Наступні приклади включені для демонстрації конкретних кращих варіантів реалізації. Спеціалістам у даній галузі слід розуміти, що методики, розкриті у наступних прикладах, являють собою методики, розроблені винахідником для нормального функціонування у практичній реалізації даного винаходу, і, таким чином, можна вважати, що вони складають конкретні кращі способи його практичної реалізації. Однак, спеціалістам у даній галузі техніки у світлі даного опису слід розуміти, що у конкретних розкритих варіантах реалізації може бути зроблена множина змін, та при цьому отримані подібні або аналогічні результати, не відходячи від суті та обсягу даного винаходу. Наступні абревіатури використані у прикладах нижче: DME 1,2-диметоксиетан ДМФА диметилформамід EtOAc етилацетат Hepes 4-(2-гідроксиетил)-1-піперазинетансульфонова кислота mCPBA метахлорпербензойна кислота MeCN ацетонітрил NBS N-бромсукцинімід TM Peppsi-iPr (або PEPPSI iPr або PEPPSI -iPr) (1,3-біс(2,6-діізопропілфеніл)імідазоліден)(3-хлорпіридил)паладію(II) дихлорид PdCl2dppf [1,1-біс(дифенілфосфіно)фероцен]дихлорпаладій (II) POCl3 фосфорил хлорид rf фактор утримання TEA триетиламін TFA трифтороцтова кислота 21 UA 111315 C2 ТГФ тетрагідрофуран Приклад 1 N-циклопентил-6-(3,5-диметилізоксазол-4-іл)-2-оксо-2,3-дигідро-1H-бензо[d]імідазол-4сульфонамід 5 10 15 20 25 30 2,3-діаміно-N-циклопентил-5-(3,5-диметилізоксазол-4-іл)бензолсульфонамід (58 мг, 0,17 ммоль) розчиняли у ДМФА (2 мл). До розчину додавали CDI (360 мг, 4 ммоль) та TEA (1 мл). Реакційну суміш потім нагрівали до 150 °C у мікрохвильовій печі впродовж 10 год. Розчинник випарювали, та залишок очищали шляхом препаративної ВЕРХ (0-100% CH3CN/H2O) з одержанням N-циклопентил-6-(3,5-диметилізоксазол-4-іл)-2-оксо-2,3-дигідро-1Hбензо[d]імідазол-4-сульфонаміду. 1 C17H20N4O4S. 377,0 (M+1). H ЯМР (400МГц, CD3OD) δ 7,34 (s, 1H), 7,18 (s, 1H), 3,63-3,58 (m, 1H), 2,41 (s, 3H), 2,25 (s, 3H), 1,70-1,60 (m, 4 H), 1,49-1,31 (m, 4H). Приклад 2 6-(3,5-диметилізоксазол-4-іл)-4-(6-метилхінолін-5-іл)-1H-бензо[d]імідазол-2(3H)-он 6-(3,5-Диметилізоксазол-4-іл)-4-йод-1H-бензо[d]імідазол-2(3H)-он (38,9 мг, 0,11 ммоль) обробляли 6-метилхінолін-5-ілбороновою кислотою (30,9 мг, 0,165 ммоль, 1,5 екв.), 2M-Na2CO3 (водн.) (1 мл) у присутності PEPPSI iPr (3,7 мг, 0,0055 ммоль, 0,05 екв.) у 1,4-діоксані (3 мл) при 150 °C впродовж 20 хвил. у мікрохвильовому реакторі (Biotage, Optimizer). До реакційної суміші додавали воду (30 мл) та EtOAc (70 мл). Розчин повністю фільтрували через целіт (3 г), та потім органічний шар відділяли від фільтрату. Органічний шар промивали сольовим розчином (30 мл) та сушили над Na2SO4. Розчинник видаляли при зниженому тиску з одержанням неочищеного продукту. Неочищений продукт очищали шляхом препаративної ВЕРХ (5-95% ацетонітрил: вода з 0,05% трифтороцтової кислоти, на колонці Phenomenex Luna C18) та хроматографії на силікагелі (MeOH:CH2Cl2 = 3:97~10:90) з одержанням 6-(3,5-диметилізоксазол-4-іл)-4-(6метилхінолін-5-іл)-1H-бензо[d]імідазол-2(3H)-ону. 6-(3,5-диметилізоксазол-4-іл)-4-(6-метилхінолін-5-іл)-1H-бензо[d]імідазол-2(3H)-он: 1 C22H18N4O2. MS. m/z 371,1 (M+1). H ЯМР (MeOH-d4) δ 9,15 (d, J = 5,3 Гц, 1H), 8,58 (t, J = 8,7 Гц, 1H), 8,58 (d, J = 9,0 Гц, 1H), 8,22 (d, J = 9,0 Гц, 1H), 7,95 (dd, J = 8,7, 5,3 Гц, 1H), 7,20 (d, J = 1,5 Гц, 1H), 6,95 (d, J = 1,5 Гц, 1H), 2,46 (s, 3H), 2,45 (s, 3H), 2,30 (s, 3H). Приклад 3 22 UA 111315 C2 4,6-біс(3,5-диметилізоксазол-4-іл)-1H-бензо[d]імідазол-2(3H)-он 5 10 15 20 25 30 4,6-біс(3,5-диметилізоксазол-4-іл)-1H-бензо[d]імідазол-2(3H)-он синтезували із застосуванням 3,5-диметил-4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)ізоксазолу та Cs2CO3 за аналогічним способом, як 6-(3,5-диметилізоксазол-4-іл)-4-(6-метилхінолін-5-іл)-1Hбензо[d]імідазол-2(3H)-он (Приклад 2). 1 C17H16N4O3. MS. 325,1 (M+1). H ЯМР (MeOH-d4) δ 7,04 (d, J = 1,5 Гц, 1H), 6,87 (dd, J = 1,5 Гц, 1H), 2,43 (s, 3H), 2,35 (s, 3H), 2,27 (s, 3H), 2,20 (s, 3H). Приклад 4 6-(3,5-диметилізоксазол-4-іл)-4-(2-фенілпіридин-3-іл)-1H-бензо[d]імідазол-2(3H)-он 6-(3,5-диметилізоксазол-4-іл)-4-(2-фенілпіридин-3-іл)-1H-бензо[d]імідазол-2(3H)-он синтезували із застосуванням 2-фенілпіридин-3-ілборонової кислоти та Cs2CO3 аналогічним способом, як 6-(3,5-диметилізоксазол-4-іл)-4-(6-метилхінолін-5-іл)-1H-бензо[d]імідазол-2(3H)-он (Приклад 2). 1 C23H18N4O2. MS. 383,1 (M+1). H ЯМР (MeOH-d4) δ 8,89 (dd, J = 5,7, 1,5 Гц, 1H), 8,60 (dd, J = 7,9, 1,5 Гц, 1H), 8,04 (dd, J = 7,9, 5,7 Гц, 1H), 7,51 - 7,39 (m, 5H), 6,98 (d, J = 1,5 Гц, 1H), 6,75 (d, J = 1,5 Гц, 1H), 2,19 (s, 3H), 2,03 (s, 3H). Приклад 5 4-(3,5-диметил-1H-піразол-4-іл)-6-(3,5-диметилізоксазол-4-іл)-1H-бензо[d]імідазол-2(3H)-он 4-(1,4-диметил-1H-піразол-5-іл)-6-(3,5-диметилізоксазол-4-іл)-1H-бензо[d]імідазол-2(3H)-он синтезували із застосуванням 3,5-диметил-4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)-1Hпіразолу та Cs2CO3 за аналогічним способом, як 6-(3,5-диметилізоксазол-4-іл)-4-(6метилхінолін-5-іл)-1H-бензо[d]імідазол-2(3H)-он (Приклад 2). 1 C17H17N5O2. MS. 324,1 (M+1). H ЯМР (MeOH-d4) δ 7,51 (s, 1H), 7,11 (d, J = 1,5 Гц, 1H), 6,92 (d, J = 1,5 Гц, 1H), 3,74 (s, 3H), 2,43 (s, 3H), 2,28 (s, 3H), 2,00 (s, 3H). Приклад 6 5-(6-(3,5-диметилізоксазол-4-іл)-2-оксо-2,3-дигідро-1H-бензо[d]імідазол-4-іл)-1-метил-3,4дигідрохінолін-2(1H)-он Стадія 1: Одержання 1-метил-5-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)-3,4дигідрохінолін-2(1H)-ону 23 UA 111315 C2 5 10 5-бром-1-метил-3,4-дигідрохінолін-2(1H)-он (171,4 мг, 0,714 ммоль) обробляли 4,4,4',4',5,5,5',5'-октаметил-2,2'-би(1,3,2-діоксабороланом) (272,0 мг, 1,071 ммоль, 1,5 екв.), KOAc (210,2 мг, 2,142 ммоль, 3,0 екв.) у присутності PdCl2dppf (26,1 мг, 0,0357 ммоль, 0,05 екв.) у ДМСО (4 мл) при 100 °C впродовж 20 хвил. у мікрохвильовому реакторі. До реакційної суміші додавали воду (30 мл) та EtOAc (70 мл). Суміш фільтрували через целіт (3 г), та потім органічний шар відділяли від фільтрату. Органічний шар промивали сольовим розчином (30 мл) та сушили над Na2SO4. Розчинник видаляли при зниженому тиску з одержанням неочищеного продукту. Неочищений продукт очищали шляхом препаративної ВЕРХ (5-95% ацетонітрил: вода з 0,05% трифтороцтової кислоти, на колонці Phenomenex Luna C18) та хроматографії на силікагелі (MeOH:CH2Cl2 = 3:97~10:90) з одержанням 1-метил-5-(4,4,5,5-тетраметил-1,3,2діоксаборолан-2-іл)-3,4-дигідрохінолін-2(1H)-ону (117,2 мг). C16H22BNO3. MS. m/z 389,1 (M+1). Стадія 2: Одержання 5-(6-(3,5-диметилізоксазол-4-іл)-2-оксо-2,3-дигідро-1Hбензо[d]імідазол-4-іл)-1-метил-3,4-дигідрохінолін-2(1H)-ону 15 20 25 30 5-(6-(3,5-диметилізоксазол-4-іл)-2-оксо-2,3-дигідро-1H-бензо[d]імідазол-4-іл)-1-метил-3,4дигідрохінолін-2(1H)-он синтезували із застосуванням 1-метил-5-(4,4,5,5-тетраметил-1,3,2діоксаборолан-2-іл)-3,4-дигідрохінолін-2(1H)-ону та Cs2CO3 за аналогічним способом, як 6-(3,5диметилізоксазол-4-іл)-4-(6-метилхінолін-5-іл)-1H-бензо[d]імідазол-2(3H)-он (Приклад 2). 5-(6-(3,5-диметилізоксазол-4-іл)-2-оксо-2,3-дигідро-1H-бензо[d]імідазол-4-іл)-1-метил-3,41 дигідрохінолін-2(1H)-он: C22H20N4O3. MS. m/z 389,1 (M+1). H ЯМР (MeOH-d4) δ 7,41 (t, J = 8,0 Гц, 1H), 7,24 (dd, J = 8,0, 1,1 Гц, 1H), 7,11 (dd, J = 8,0, 1,1 Гц, 1H), 7,02 (d, J = 1,5 Гц, 1H), 6,84 (d, J = 1,5 Гц, 1H), 3,42 (s, 3H), 2,88 – 2,64 (m, 2H), 2,64 – 2,46 (m, 2H), 2,42 (s, 3H), 2,27 (s, 3H). Приклад 7 5-(3,5-диметилізоксазол-4-іл)-1-метил-7-(6-метилхінолін-5-іл)-1H-бензо[d]імідазол-2(3H)-он Стадія 1: Одержання 4-(3,5-диметилізоксазол-4-іл)-2-йод-N-метил-6-нітроаніліну У колбу, що містить 4-(3,5-диметилізоксазол-4-іл)-2-йод-6-нітроанілін (1000 мг, 2,78 ммоль, 1 екв.), додавали ДМФА (15 мл, 0,2 M) перед додаванням карбонату цезію (1,4 г, 4,17 ммоль, 1,5 екв.) та йодметану (260 мкл, 4,17 ммоль, 1,5 екв.). Через годину реакцію гасили водою, та реакційну суміш розділяли між водою та етилацетатом. Органічний шар промивали сольовим розчином та сушили над сульфатом натрію. Очищення проводили шляхом колонкової флешхроматографії з одержанням 4-(3,5-диметилізоксазол-4-іл)-2-йод-N-метил-6-нітроаніліну (615 мг, 60 %). 24 UA 111315 C2 1 LCMS (m/z +1) 373,85. H ЯМР (400 МГц, СDCl3) δ 7,81 (t, J = 3,0 Гц, 1H), 7,70 (d, J = 2,1 Гц, 1H), 2,97 (s, 3H), 2,40 (d, J = 16,8 Гц, 3 H), 2,26 (d, J = 14,2 Гц, 3H). Стадія 2: Одержання 4-(3,5-диметилізоксазол-4-іл)-6-йод-N1-метилбензол-1,2-діаміну 5 10 15 20 25 30 У колбу для мікрохвильової печі, яка містить 4-(3,5-диметилізоксазол-4-іл)-2-йод-N-метил-6нітроанілін (610 мг, 1,64 ммоль, 1 екв.), додавали EtOH (12 мл, 0,25M) та хлорид олова (II) (622 мг, 3,28 ммоль, 2 екв.). Реакційну суміш нагрівали впродовж 30 хвил. при 110 °C. Реакційну суміш потім перемішували у 2 н. розчині NaOH впродовж 20 хвилин перед розділенням між водою та етилацетатом. Органічний шар промивали сольовим розчином та сушили над сульфатом натрію. Очищення проводили шляхом колонкової флеш-хроматографії з одержанням 4-(3,5-диметилізоксазол-4-іл)-6-йод-N1-метилбензол-1,2-діаміну. LCMS (m/z +1) 344,02. Стадія 3: Одержання 5-(3,5-диметилізоксазол-4-іл)-7-йод-1-метил-1H-бензо[d]імідазол-2(3H)ону У колбу, яка містить 4-(3,5-диметилізоксазол-4-іл)-6-йод-N1-метилбензол-1,2-діамін (299 мг, 0,87 ммоль, 1 екв.), додавали ТГФ (8 мл, 0,1 M) та CDI (282 мг, 1,74 ммоль, 2 екв.). Реакційну суміш нагрівали впродовж 2 год. при 120 °C. Реакційну суміш потім концентрували під вакуумом, та тверду речовину розтирали з діетиловим ефіром перед висушуванням на повітрі зодержанням 5-(3,5-диметилізоксазол-4-іл)-7-йод-1-метил-1H-бензо[d]імідазол-2(3H)-ону у формі світло-жовтої твердої речовини. LCMS (m/z +1) 370,00. Стадія 4: Одержання 5-(3,5-диметилізоксазол-4-іл)-1-метил-7-(6-метилхінолін-5-іл)-1Hбензо[d]імідазол-2(3H)-ону У колбу для мікрохвильової печі, яка містить 5-(3,5-диметилізоксазол-4-іл)-7-йод-1-метил1H-бензо[d]імідазол-2(3H)-он (40 мг, 0,11 ммоль, 1 екв.), додавали 3,5-6-метилхінолін-5ілборонову кислоту (51 мг, 0,27 ммоль, 2,5 екв.), Cs 2CO3 (141 мг, 0,43 ммоль, 4 екв.) та ™ каталізатор PEPPSI -IPr (8 мг, 0,02 ммоль, 0,1 екв.), та розчиняли у DME-H2O (20 мл, 0,2 M, 2/1, об./об.). Суміш нагрівали до 140 °C. Через 2 години реакція була закінчена. Після охолодження реакційну суміш екстрагували EtOAc та промивали водою та насиченим NH 4Cl. Після висушування шляхом MgSO4, її фільтрували та концентрували досуха. Очищення проводили шляхом обернено-фазної ВЕРХ з одержанням 5-(3,5-диметилізоксазол-4-іл)-1-метил-7-(6метилхінолін-5-іл)-1H-бензо[d]імідазол-2(3H)-ону. 25 UA 111315 C2 1 5 10 15 20 25 30 35 LCMS (m/z +1) 385,23. H ЯМР (400 МГц, CD3OD) δ 8,82 (d, J = 4,3 Гц, 1H), 8,09 (d, J = 8,7 Гц, 1H), 7,82 (t, J = 7,1 Гц, 2H), 7,47 (dd, J = 8,5, 4,3 Гц, 1H), 7,17 (d, J = 1,6 Гц, 1H), 6,82 (d, J = 1,6 Гц, 1H), 2,53 (s, 3H), 2,42 (s, 3H), 2,33 (s, 3H), 2,27 (s, 3H). Приклад 8 7-(1,4-диметил-1H-піразол-5-іл)-5-(3,5-диметилізоксазол-4-іл)-1-метил-1H-бензо[d]імідазол2(3H)-он У колбу для мікрохвильової печі, яка містить 5-(3,5-диметилізоксазол-4-іл)-7-йод-1-метил1H-бензо[d]імідазол-2(3H)-он (40 мг, 0,11 ммоль, 1 екв.), додавали 1,4-диметил-1H-піразол-5ілборонову кислоту (72 мг, 0,32 ммоль, 3 екв.), Cs 2CO3 (141 мг, 0,43 ммоль, 4 екв.) та ™ каталізатор PEPPSI -IPr (8 мг, 0,02 ммоль, 0,1 екв.), та розчиняли у DME-H2O (20 мл, 0,2 M, 2/1, об./об.). Суміш нагрівали до 140 °C. Через 1 год. реакція була закінчена. Після охолодження реакційну суміш екстрагували EtOAc та промивали водою та насиченим NH 4Cl. Після висушування шляхом MgSO4, її фільтрували та концентрували досуха. Очищення проводили шляхом обернено-фазної ВЕРХ з одержанням 7-(1,4-диметил-1H-піразол-5-іл)-5-(3,5диметилізоксазол-4-іл)-1-метил-1H-бензо[d]імідазол-2(3H)-ону. 1 LCMS (m/z +1) 338,19. H ЯМР (400 МГц, CD3OD) δ 7,44 (s, 1H), 7,15 (d, J = 1,6 Гц, 1H), 6,88 (d, J = 1,6 Гц, 1H), 3,65 (s, 3H),.90 (s, 3H), 2,42 (s, 3H), 2,27 (s, 7H), 1,95 (s, 3H). Приклад 9 7-(1,4-диметил-1H-піразол-5-іл)-5-(3,5-диметилізоксазол-4-іл)-1-метил-1H-бензо[d]імідазол2(3H)-он У колбу для мікрохвильової печі, яка містить 5-(3,5-диметилізоксазол-4-іл)-7-йод-1-метил1H-бензо[d]імідазол-2(3H)-он (40 мг, 0,11 ммоль, 1 екв.), додавали пінаколовий складний ефір 3,5-диметилізоксазол-4-боронової кислоти (72 мг, 0,32 ммоль, 3 екв.), Cs 2CO3 (141 мг, 0,43 ™ ммоль, 4 екв.) та каталізатор PEPPSI -IPr (8 мг, 0,02 ммоль, 0,1 екв.), та розчиняли у DME-H2O (20 мл, 0,2 M, 2/1, об./об.). Суміш нагрівали до 140 °C. Через 1 год. реакція була закінчена. Після охолодження реакційну суміш екстрагували EtOAc та промивали водою та насиченим NH4Cl. Після висушування шляхом MgSO4, її фільтрували та концентрували досуха. Очищення проводили шляхом обернено-фазної ВЕРХ з одержанням 7-(1,4-диметил-1H-піразол-5-іл)-5(3,5-диметилізоксазол-4-іл)-1-метил-1H-бензо[d]імідазол-2(3H)-ону. 1 LCMS (m/z +1) 339,15. H ЯМР (400 МГц, CD3OD) δ 7,09 (d, J = 1,6 Гц, 1H), 6,81 (d, J = 1,6 Гц, 1H) 3,11 (d, J = 14,5 Гц, 3H), 2,41 (s, 3H), 2,35 – 2,23 (m, 6H), 2,15 (s, 3H). Приклад 10 5,7-біс(3,5-диметилізоксазол-4-іл)бензо[d]оксазол-2(3H)-он 26 UA 111315 C2 5 10 15 20 25 30 5,7-Дибромбензо[d]оксазол-2(3H)-он (100,0 мг, 0,341 ммоль) обробляли 3,5-диметил-4(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)ізоксазолом (304,7 мг, 1,366 ммоль, 4,0 екв.), 2M Na2CO3 (водн.) (1 мл) у присутності PEPPSI-IPr (11,6 мг, 0,017 ммоль, 0,05 екв.) у 1,4-діоксані (3 мл) при 150 °C впродовж 10 хвил. у мікрохвильовому реакторі. До реакційної суміші додавали воду (30 мл) та EtOAc (70 мл). Суміш фільтрували через целіт (3 г), та потім органічний шар відділяли від фільтрату. Органічний шар промивали сольовим розчином (30 мл) та сушили над Na2SO4. Розчинник видаляли при зниженому тиску з одержанням неочищеного продукту. Неочищений продукт очищали шляхом препаративної ВЕРХ (5-95% ацетонітрил: вода з 0,05% трифтороцтової кислоти, на колонці Phenomenex Luna C18) та колонкової хроматографії на силікагелі (MeOH:CH2Cl2 = 3:97~10:90) з одержанням 5,7-біс(3,5-диметилізоксазол-4іл)бензо[d]оксазол-2(3H)-ону. 1 C17H15N3O4. MS. m/z 326,0 (M+1). H ЯМР (MeOH-d4) δ 7,08 (s, 1H), 7,01 (s, 1H), 2,433 (s, 3H), 2,430 (s, 3H), 2,28 (s, 3H), 2,27 (s, 3H). Приклад 11 5-(3,5-диметилізоксазол-4-іл)-7-(6-метилхінолін-5-іл)бензо[d]оксазол-2(3H)-он Стадія 1: 5-Бром-7-хлорбензо[d]оксазол-2(3H)-он (100,0 мг, 0,4025 ммоль) обробляли 3,5-диметил-4(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)ізоксазолом (89,8 мг, 0,4025 ммоль, 1,0 екв.), DBU (183,8 мг, 1,2075 ммоль, 3,0 екв.) у присутності PdCl2dppf (14,7 мг, 0,02015 ммоль, 0,05 екв.) у ДМСО (3 мл) та воді (1 мл) при 120 °C впродовж 1 год. на масляній бані. До реакційної суміші додавали воду (30 мл) та EtOAc (70 мл). Суміш фільтрували через целіт (3 г), та потім органічний шар відділяли від фільтрату. Органічний шар промивали сольовим розчином (30 мл) та сушили над Na2SO4. Розчинник видаляли при зниженому тиску з одержанням неочищеного продукту. Неочищений продукт очищали шляхом препаративної ВЕРХ (5-95% ацетонітрил: вода з 0,05% трифтороцтової кислоти, на колонці Phenomenex Luna C18) та колонкової хроматографії на силікагелі (гексан:EtOAc = 1:1) з одержанням 7-хлор-5-(3,5-диметилізоксазол4-іл)бензо[d]оксазол-2(3H)-ону. C12H9ClN2O3. MS. m/z 265,0 (M-1), 267,0 (M+1). 27 UA 111315 C2 Стадія 2: 5 10 15 20 25 30 7-Хлор-5-(3,5-диметилізоксазол-4-іл)бензо[d]оксазол-2(3H)-он (20,8 мг, 0,0786 ммоль) обробляли 6-метилхінолін-5-ілбороновою кислотою (44,1 мг, 0,2358 ммоль, 3,0 екв.), Cs 2CO3 (153,7 мг, 0,4716 ммоль, 6,0 екв.) у присутності PEPPSI iPr (2,9 мг, 0,00393 ммоль, 0,05 екв.) у 1,4-діоксані (3 мл) та води (1 мл) при 150 °C впродовж 1 год. у мікрохвильовому реакторі. До реакційної суміші додавали воду (30 мл) та EtOAc (70 мл). Суміш фільтрували через целіт (3 г), та потім органічний шар відділяли від фільтрату. Органічний шар промивали сольовим розчином (30 мл) та сушили над Na2SO4. Розчинник видаляли при зниженому тиску з одержанням неочищеного продукту. Неочищений продукт очищали шляхом препаративної ВЕРХ (5-95% ацетонітрил: вода з 0,05% трифтороцтової кислоти, на колонці Phenomenex Luna C18) з одержанням 5-(3,5-диметилізоксазол-4-іл)-7-(6-метилхінолін-5-іл)бензо[d]оксазол-2(3H)ону. 1 C22H17N3O3. MS. m/z 372,1 (M+1). H ЯМР (MeOH-d4) δ 9,16 (d, J = 5,3 Гц, 1H), 8,69 (d, J = 8,7 Гц, 1H), 8,28 (d, J = 8,9 Гц, 1H), 8,21 (d, J = 8,9 Гц, 1H), 7,97 (dd, J = 8,7, 5,3 Гц, 1H), 7,27 (d, J = 1,6 Гц, 1H), 7,07 (d, J = 1,6 Гц, 1H), 2,49 (s, 3H), 2,45 (s, 3H), 2,30 (s, 3H). Приклад 12 5-(3,5-диметилізоксазол-4-іл)-7-(2-фенілпіридин-3-іл)бензо[d]оксазол-2(3H)-он Зазначену у заголовку сполуку синтезували із застосуванням 2-фенілпіридин-3-ілборонової кислоти за способом, аналогічним способу одержання 5-(3,5-диметилізоксазол-4-іл)-7-(6метилхінолін-5-іл)бензо[d]оксазол-2(3H)-ону (Приклад 11). 1 C23H17N3O3. MS. 384,1 (M+1). H ЯМР (MeOH-d4) δ 8,02 (dd, J = 5,4, 1,5 Гц, 1H), 7,68 (dd, J = 8,0, 1,5 Гц, 1H), 7,10 (dd, J = 8,0, 5,4 Гц, 1H), 6,67 - 6,55 (m, 5H), 6,21 (d, J = 1,6 Гц, 1H), 5,97 (d, J = 1,6 Гц, 1H), 1,35 (s, 3H), 1,19 (s, 3H). Приклад 13та Приклад 14 (R)-6-(3,5-диметилізоксазол-4-іл)-4-(6-метилхінолін-5-іл)-1H-бензо[d]імідазол-2(3H)-он та (S)-6-(3,5-диметилізоксазол-4-іл)-4-(6-метилхінолін-5-іл)-1H-бензо[d]імідазол-2(3H)-он (R)-6-(3,5-Диметилізоксазол-4-іл)-4-(6-метилхінолін-5-іл)-1H-бензо[d]імідазол-2(3H)-он та (S)6-(3,5-диметилізоксазол-4-іл)-4-(6-метилхінолін-5-іл)-1H-бензо[d]імідазол-2(3H)-он отримували 28
ДивитисяДодаткова інформація
Назва патенту англійськоюBenzimidazole derivatives as bromodomain inhibitors
Автори англійськоюAktoudianakis, Evangelos, Chin, Gregory, Corkey, Britton Kenneth, Du, Jinfa, Elbel, Kristyna, Jiang, Robert H., Kobayashi, Tetsuya, Martinez, Ruben, Metobo, Samuel E., Mish, Michael, Shevick, Sophie, Sperandio, David, Yang, Hai, Zablocki, Jeff
Назва патенту російськоюПроизводные бензимидазолона как ингибиторы бромодомена
Автори російськоюАктоудианакис Эванджелос, Цзинь Грэгори, Корки Бриттон Кеннет, Ду Цзиньфа, Элбель Кристина, Цзян Роберт Х., Кобаяси Тецуя, Мартинес Рубен, Метобо Сэмюель И., Миш Майкл, Шэвик Софи, Сперандио Дэйвид, Ян Хай, Заблокки Джэфф
МПК / Мітки
МПК: C07D 413/04, A61K 31/42, A61P 35/00, C07D 417/14, C07D 413/14
Мітки: інгібітори, бромодомену, похідні, бензимідазолону
Код посилання
<a href="https://ua.patents.su/129-111315-pokhidni-benzimidazolonu-yak-ingibitori-bromodomenu.html" target="_blank" rel="follow" title="База патентів України">Похідні бензімідазолону як інгібітори бромодомену</a>
Попередній патент: Спосіб обрізання крайньої плоті
Наступний патент: Сировинна суміш для виготовлення безвипалювальних водостійких глиношлакових виробів
Випадковий патент: Роторно-лопатевий двигун