Ненасичений 1-аміно-алкілциклогексан nmda, 5нт3 і антагоністи нікотинового рецептора
Номер патенту: 75478
Опубліковано: 17.04.2006
Автори: Хенріх Маркус, Парсонс Крістофер Грахам Рафаель, Йіргенсонс Айгарс, Калвіньш Іварс, Даниш Войцех, Каусс Валерьянс, Гольд Маркус
Формула / Реферат
1. Сполука формули I:
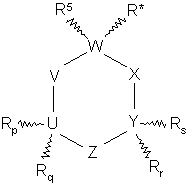 ,
,
де
- R* означає -(A)n-(CR1R2)m-NR3R4;
- n+m=0, 1 або 2;
- А вибраний з групи, що містить лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6);
- R1 і R2 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6);
- R3 і R4 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або разом утворюють алкілен(С2-С10) або алкенілен(С2-С10), або разом з N утворюють необов'язково (С1-С6)алкіл- і/або (С2-С6)алкенілзаміщений 3-7-членний азациклоалкан або азациклоалкен;
- R5 незалежно вибраний з групи, що містить лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або R5 об'єднується з вуглецем, до якого він приєднаний, і сусіднім вуглецем, утворюючи подвійний зв'язок;
- Rp, Rq, Rr і Rs незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або Rp, Rq, Rr і Rs незалежно можуть об'єднуватись з вуглецем, до якого вони приєднані, і сусіднім вуглецем, утворюючи подвійний зв'язок, або Rp, Rq, Rr і Rs незалежно можуть утворювати подвійний зв'язок з U або Y, до якого вони приєднані;
за умови, що U-V-W-X-Y-Z вибраний з
циклогексану,
циклогекс-2-ену,
циклогекс-3-ену,
циклогекса-1,4-дієну,
циклогекса-1,5-дієну,
циклогекса-2,4-дієну і
циклогекса-2,5-дієну,
і за умови, що щонайменше один з Rp і Rq не є воднем і щонайменше один з Rr і Rs не є воднем,
і за умови, що U-Z являє собою циклогексан, якщо щонайменше один з -(A)n(CR1R2)m-, R3, R4, R5, Rp, Rq, Rr і Rs являє собою лінійний або розгалужений нижчий алкеніл(С2-С6) або лінійний або розгалужений нижчий алкініл(С2-С6);
і її оптичні ізомери і фармацевтично прийнятні адитивні солі кислот або основ.
2. Сполука за п. 1, вибрана з групи, що включає:
1-етеніл-3,3,5,5-тетраметилциклогексиламін,
2-(3,3,5,5-тетраметилциклогексиліден)етанамін,
1-аміно-3,3,5-триметил-2-циклогексен,
1,3,5,5-тетраметил-2-циклогексен-1-амін,
1-аліл-3,3,5,5-тетраметилциклогексанамін,
1-(3,3,5,5-тетраметилциклогексиліден)-2-пропанамін,
1-(3,3-діетил-5,5-диметилциклогексиліден)-2-пропанамін, цис-3-вініл-1,3,транс-5-триметилциклогексиламін,
2-метил-1-(3,3,5,5-тетраметил-1-циклогексен-1-іл)-2-пропанамін,
1-(1-аліл-3,3,5,5-тетраметилциклогексил)піперидин,
2-(1-вініл-3,3,5,5-тетраметилциклогексил-1)етиламін,
1-[3,3,5,5-тетраметил-1-(3-метил-2-бутеніл)циклогексил]піперидин,
1-[3,3,5,5-тетраметил-1-(2-пропініл)циклогексил]піперидин,
2-(1,3,3,5,5-пентаметилциклогексил)-4-пентениламін,
3-(3,3,5,5-тетраметилциклогексиліден)пропанамін,
2-метил-1-(3,3,5,5-тетраметилциклогексиліден)-2-пропанамін,
2-(3,3,5,5-тетраметилциклогексиліден)пропанамін,
N-метил-1-етеніл-3,3,5,5-тетраметилциклогексиламін,
N-аліл-1,3,3,5,5-пентаметилциклогексанамін
і їх оптичні ізомери і фармацевтично прийнятні адитивні солі кислот або основ.
3. Фармацевтична композиція, що містить сполуку за п. 1 або п. 2 в комбінації з одним або більше фармацевтично прийнятними розріджувачами, наповнювачами і/або носіями.
4. Спосіб лікування у тварин стану, що виліковується антагоністом NMDA, який включає стадію введення тварині деякої кількості сполуки формули I:
 ,
,
де:
- R* означає -(A)n(CR1R2)m-NR3R4;
- n+m=0, 1 або 2;
- А вибраний з групи, що містить лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6);
- R1 і R2 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6);
- R3 і R4 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або разом утворюють алкілен(С2-С10) або алкенілен(С2-С10), або разом з N утворюють необов'язково (С1-С6)алкіл- і/або (С2-С6)алкенілзаміщений 3-7-членний азациклоалкан або азациклоалкен;
- R5, Rp, Rq, Rr і Rs незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або R5, Rp, Rq, Rr і Rs незалежно можуть об'єднуватись з вуглецем, до якого вони приєднані, і сусіднім вуглецем, утворюючи подвійний зв'язок, або Rp, Rq, Rr і Rs незалежно можуть утворювати подвійний зв'язок з U або Y, до якого вони приєднані;
за умови, що U-V-W-X-Y-Z вибраний з
циклогексану,
циклогекс-1-ену,
циклогекс-2-ену,
циклогекс-3-ену,
циклогекса-1,3-дієну,
циклогекса-1,4-дієну,
циклогекса-1,5-дієну,
циклогекса-2,4-дієну і
циклогекса-2,5-дієну,
і за умови, що U-Z являє собою циклогексан, якщо щонайменше один з -(A)n-(CR1R2)m-, R3, R4, R5, Rp, Rq, Rr являє собою лінійний або розгалужений нижчий алкеніл(С2-С6) або лінійний або розгалужений нижчий алкініл(С2-С6);
її оптичних ізомерів і фармацевтично прийнятних адитивних солей кислот або основ, які ефективні для полегшення вказаного стану.
5. Спосіб лікування у тварин стану, де сполука вибрана за її імуномодуляторною, антималярійною ефективністю, ефективністю проти вірусу Borna або проти вірусу гепатиту С, антитрипаносомальною ефективністю і проти вірусу герпеса, який включає стадію введення тварині деякої кількості сполуки формули I:
 ,
,
де
- R* означає -(A)n-(CR1R2)m-NR3R4;
- n+m=0, 1 або 2;
- А вибраний з групи, що містить лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6);
- R1 і R2 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6);
- R3 і R4 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або разом утворюють алкілен(С2-С10) або алкенілен(С2-С10), або разом з N утворюють необов'язково (С1-С6)алкіл- і/або (С2-С6)алкенілзаміщений 3-7-членний азациклоалкан або азациклоалкен;
- R5, Rp, Rq, Rr і Rs незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або R5, Rp, Rq, Rr і Rs незалежно можуть об'єднуватись з вуглецем, до якого вони приєднані, і сусіднім вуглецем, утворюючи подвійний зв'язок, або Rp, Rq, Rr і Rs незалежно можуть утворювати подвійний зв'язок з U або Y, до якого вони приєднані;
за умови, що U-V-W-X-Y-Z вибраний з
циклогексану,
циклогекс-1-ену,
циклогекс-2-ену,
циклогекс-3-ену,
циклогекса-1,3-дієну,
циклогекса-1,4-дієну,
циклогекса-1,5-дієну,
циклогекса-2,4-дієну і
циклогекса-2,5-дієну,
і за умови, що U-Z являє собою циклогексан, якщо щонайменше один з -(A)n-(CR1R2)m-, R3, R4, R5, Rp, Rq, Rr являє собою лінійний або розгалужений нижчий алкеніл(С2-С6) або лінійний або розгалужений нижчий алкініл(С2-С6);
її оптичних ізомерів і фармацевтично прийнятних адитивних солей кислот або основ, які ефективні для полегшення вказаного стану.
6. Спосіб лікування у тварин стану, що виліковується антагоністом NMDA, вибраного з групи, що включає ексцитотоксичність, вибрану з ішемії при ударі, травми, гіпоксії, гіпоглікемії, глаукоми і печінкової енцефалопатії, хронічні нейродегенеративні захворювання, вибрані з хвороби Альцгеймера, судинної деменції, хвороби Паркінсона, хвороби Хантінгтона, множинного склерозу, бічного аміотрофічного склерозу, СНІД-нейродегенерації, оливопонтоцеребелярної атрофії, синдрому Туретта, рухового нейронного захворювання, мітохондріальної дисфункції, синдрому Корсакова і хвороби Крейтцфельдта-Якоба,
інші порушення, що належать до тривалих пластичних змін в центральній нервовій системі, вибрані з хронічного болю, лікарської переносимості, залежності і адикції (наприклад, опіоїдної, кокаїнової, бензодіазепінової, нікотинової і алкогольної), і
епілепсію, пізню дискінезію, L-DOPA-індуковану дискінезію, шизофренію, стан тривоги, депресію, гострий біль, спастичність і відчуття шуму у вухах,
який включає стадію введення тварині деякої кількості сполуки формули I:
 ,
,
де
- R* означає -(A)n-(CR1R2)m-NR3R4;
- n+m=0, 1 або 2;
- А вибраний з групи, що містить лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6);
- R1 і R2 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6);
- R3 і R4 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або разом утворюють алкілен(С2-С10) або алкенілен(С2-С10), або разом з N утворюють необов'язково (С1-С6)алкіл- і/або (С2-С6)алкенілзаміщений 3-7-членний азациклоалкан або азациклоалкен;
- R5, Rp, Rq, Rr і Rs незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або R5, Rp, Rq, Rr і Rs незалежно можуть об'єднуватись з вуглецем, до якого вони приєднані, і сусіднім вуглецем, утворюючи подвійний зв'язок, або Rp, Rq, Rr і Rs незалежно можуть утворювати подвійний зв'язок з U або Y, до якого вони приєднані;
за умови, що U-V-W-X-Y-Z вибраний з
циклогексану,
циклогекс-1-ену,
циклогекс-2-ену,
циклогекс-3-ену,
циклогекса-1,3-дієну,
циклогекса-1,4-дієну,
циклогекса-1,5-дієну,
циклогекса-2,4-дієну і
циклогекса-2,5-дієну,
і за умови, що U-Z являє собою циклогексан, якщо щонайменше один з -(A)n-(CR1R2)m-, R3, R4, R5, Rp, Rq, Rr являє собою лінійний або розгалужений нижчий алкеніл(С2-С6) або лінійний або розгалужений нижчий алкініл(С2-С6);
її оптичних ізомерів і фармацевтично прийнятних адитивних солей кислот або основ, які ефективні для полегшення вказаного стану.
7. Спосіб лікування у тварин стану, що виліковується антагоністом рецептора 5-НТ3, який включає стадію введення тварині деякої кількості сполуки формули І:
 ,
,
де:
- R* означає -(A)n-(CR1R2)m-NR3R4;
- n+m=0, 1 або 2;
- А вибраний з групи, що містить лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6);
- R1 і R2 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6);
- R3 і R4 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або разом утворюють алкілен(С2-С10) або алкенілен(С2-С10), або разом з N утворюють необов'язково (С1-С6)алкіл- і/або (С2-С6)алкенілзаміщений 3-7-членний азациклоалкан або азациклоалкен;
- R5, Rp, Rq, Rr і Rs незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або R5, Rp, Rq, Rr і Rs незалежно можуть об'єднуватись з вуглецем, до якого вони приєднані, і сусіднім вуглецем, утворюючи подвійний зв'язок, або Rp, Rq, Rr і Rs незалежно можуть утворювати подвійний зв'язок з U або Y, до якого вони приєднані;
за умови, що U-V-W-X-Y-Z вибраний з
циклогексану,
циклогекс-1-ену,
циклогекс-2-ену,
циклогекс-3-ену,
циклогекса-1,3-дієну,
циклогекса-1,4-дієну,
циклогекса-1,5-дієну,
циклогекса-2,4-дієну і
циклогекса-2,5-дієну,
і за умови, що U-Z являє собою циклогексан, якщо щонайменше один з -(A)n-(CR1R2)m-, R3, R4, R5, Rp, Rq, Rr являє собою лінійний або розгалужений нижчий алкеніл(С2-С6) або лінійний або розгалужений нижчий алкініл(С2-С6);
її оптичних ізомерів і фармацевтично прийнятних адитивних солей кислот або основ, які ефективні для полегшення вказаного стану.
8. Спосіб лікування у тварин стану, що виліковується антагоністом нейронних нікотинових рецепторів, який включає стадію введення тварині деякої кількості сполуки формули I:
 ,
,
де
- R* означає -(A)n-(CR1R2)m-NR3R4;
- n+m=0, 1 або 2;
- А вибраний з групи, що містить лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6);
- R1 і R2 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6);
- R3 і R4 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або разом утворюють алкілен(С2-С10) або алкенілен(С2-С10), або разом з N утворюють необов'язково (С1-С6)алкіл- і/або (С2-С6)алкенілзаміщений 3-7-членний азациклоалкан або азациклоалкен;
- R5, Rp, Rq, Rr і Rs незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або R5, Rp, Rq, Rr і Rs незалежно можуть об'єднуватись з вуглецем, до якого вони приєднані, і сусіднім вуглецем, утворюючи подвійний зв'язок, або Rp, Rq, Rr і Rs незалежно можуть утворювати подвійний зв'язок з U або Y, до якого вони приєднані;
за умови, що U-V-W-X-Y-Z вибраний з
циклогексану,
циклогекс-1-ену,
циклогекс-2-ену,
циклогекс-3-ену,
циклогекса-1,3-дієну,
циклогекса-1,4-дієну,
циклогекса-1,5-дієну,
циклогекса-2,4-дієну і
циклогекса-2,5-дієну,
і за умови, що U-Z являє собою циклогексан, якщо щонайменше один з -(A)n-(CR1R2)m-, R3, R4, R5, Rp, Rq, Rr являє собою лінійний або розгалужений нижчий алкеніл(С2-С6) або лінійний або розгалужений нижчий алкініл(С2-С6);
її оптичних ізомерів і фармацевтично прийнятних адитивних солей кислот або основ, які ефективні для полегшення вказаного стану.
9. Спосіб лікування у тварин стану, що виліковується антагоністом 5-НТ3, вибраного з групи, що включає порушення, пов'язані зі станом тривоги, депресивні порушення, шизофренію, і лікування пов'язаних з цим психозів, порушень, пов'язаних зі зловживанням ліками і алкоголем, когнітивних порушень, хвороби Альцгеймера, хвороби Паркінсона, мозочкового тремору, мігрені, порушень апетиту, слизового коліту (IBS) і блювання, який включає стадію введення тварині деякої кількості сполуки формули I:
 ,
,
де
- R* означає -(A)n-(CR1R2)m-NR3R4;
- n+m=0, 1 або 2;
- А вибраний з групи, що містить лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6);
- R1 і R2 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6);
- R3 і R4 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або разом утворюють алкілен(С2-С10) або алкенілен(С2-С10), або разом з N утворюють необов'язково (С1-С6)алкіл- і/або (С2-С6)алкенілзаміщений 3-7-членний азациклоалкан або азациклоалкен;
- R5, Rp, Rq, Rr і Rs незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або R5, Rp, Rq, Rr і Rs незалежно можуть об'єднуватись з вуглецем, до якого вони приєднані, і сусіднім вуглецем, утворюючи подвійний зв'язок, або Rp, Rq, Rr і Rs незалежно можуть утворювати подвійний зв'язок з U або Y, до якого вони приєднані;
за умови, що U-V-W-X-Y-Z вибраний з
циклогексану,
циклогекс-1-ену,
циклогекс-2-ену,
циклогекс-3-ену,
циклогекса-1,3-дієну,
циклогекса-1,4-дієну,
циклогекса-1,5-дієну,
циклогекса-2,4-дієну і
циклогекса-2,5-дієну,
і за умови, що U-Z являє собою циклогексан, якщо щонайменше один з -(A)n-(CR1R2)m-, R3, R4, R5, Rp, Rq, Rr являє собою лінійний або розгалужений нижчий алкеніл(С2-С6) або лінійний або розгалужений нижчий алкініл(С2-С6);
її оптичних ізомерів і фармацевтично прийнятних адитивних солей кислот або основ, які ефективні для полегшення вказаного стану.
10. Спосіб лікування у тварин стану, що виліковується антагоністом нейронних нікотинових рецепторів, вибраного з групи, що включає синдром Туретта, порушення, пов'язані зі станом тривоги, шизофренію, зловживання ліками, зловживання нікотином, зловживання кокаїном, дискінезію (Morbus Huntington, L-DOPA-індуковану), порушення, пов'язані з гіперактивністю при дефіциті уваги (ADHD), хворобу Альцгеймера, хворобу Паркінсона і біль, який включає стадію введення тварині деякої кількості сполуки формули І:
 ,
,
де
- R* означає -(A)n-(CR1R2)m-NR3R4;
- n+m=0, 1 або 2;
- А вибраний з групи, що містить лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6);
- R1 і R2 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6);
- R3 і R4 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або разом утворюють алкілен(С2-С10) або алкенілен(С2-С10), або разом з N утворюють необов'язково (С1-С6)алкіл- і/або (С2-С6)алкенілзаміщений 3-7-членний азациклоалкан або азациклоалкен;
- R5, Rp, Rq, Rr і Rs незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або R5, Rp, Rq, Rr і Rg незалежно можуть об'єднуватись з вуглецем, до якого вони приєднані, і сусіднім вуглецем, утворюючи подвійний зв'язок, або Rp, Rq, Rr і Rs незалежно можуть утворювати подвійний зв'язок з U або Y, до якого вони приєднані;
за умови, що U-V-W-X-Y-Z вибраний з
циклогексану,
циклогекс-1-ену,
циклогекс-2-ену,
циклогекс-3-ену,
циклогекса-1,3-дієну,
циклогекса-1,4-дієну,
циклогекса-1,5-дієну,
циклогекса-2,4-дієну і
циклогекса-2,5-дієну,
і за умови, що U-Z являє собою циклогексан, якщо щонайменше один з -(A)n-(CR1R2)m-, R3, R4, R5, Rp, Rq, Rr являє собою лінійний або розгалужений нижчий алкеніл(С2-С6) або лінійний або розгалужений нижчий алкініл(С2-С6);
її оптичних ізомерів і фармацевтично прийнятних адитивних солей кислот або основ, які ефективні для полегшення вказаного стану.
11. Застосування сполуки формули I за будь-яким з пп. 4-10 і її оптичних ізомерів і фармацевтично прийнятних адитивних солей кислот або основ у виробництві лікарського засобу для використання у способі за будь-яким з пп. 4-10.
Текст
УКРАЇНА (19) UA (11) 75478 (13) C2 (51) МПК (2006) C07C 211/40 (2006.01) C07C 211/35 (2006.01) C07D 211/06 (2006.01) A61P 25/28 (2006.01) A61K 31/13 МІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ ДЕРЖАВНИЙ ДЕПАРТАМЕНТ ІНТЕЛЕКТУАЛЬНОЇ ВЛАСНОСТІ ОПИС ДО ПАТЕНТУ НА ВИНАХІД (54) НЕНАСИЧЕНИЙ 1-АМІНО-АЛКІЛЦИКЛОГЕКСАН NMDA, 5НТ3 І АНТАГОНІСТИ НІКОТИНОВОГО РЕЦЕПТОРА W X V Rp Y U Z Rq Rs Rr , де - R* означає -(A)n-(CR1R2)m-NR3R4; - n+m=0, 1 або 2; - А вибраний з групи, що містить лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R1 і R2 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R3 і R4 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий ал C2 (13) 75478 R* (11) R5 кеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або разом утворюють алкілен(С2С10) або алкенілен(С2-С10), або разом з N утворюють необов'язково (С1-С6)алкіл- і/або (С2С6)алкенілзаміщений 3-7-членний азациклоалкан або азациклоалкен; - R5 незалежно вибраний з групи, що містить лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або R5 об'єднується з вуглецем, до якого він приєднаний, і сусіднім вуглецем, утворюючи подвійний зв'язок; - Rp, Rq, Rr і Rs незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або Rp, Rq, Rr і Rs незалежно можуть об'єднуватись з вуглецем, до якого вони приєднані, і сусіднім вуглецем, утворюючи подвійний зв'язок, або Rp, Rq, Rr і Rs незалежно можуть утворювати подвійний зв'язок з U або Y, до якого вони приєднані; за умови, що U-V-W-X-Y-Z вибраний з циклогексану, циклогекс-2-ену, циклогекс-3-ену, циклогекса-1,4-дієну, циклогекса-1,5-дієну, циклогекса-2,4-дієну і циклогекса-2,5-дієну, і за умови, що щонайменше один з Rp і Rq не є воднем і щонайменше один з Rr і Rs не є воднем, і за умови, що U-Z являє собою циклогексан, якщо щонайменше один з -(A)n(CR1R2)m-, R3, R4, R5, Rp, Rq, Rr і Rs являє собою лінійний або розгалужений нижчий алкеніл(С2-С6) або лінійний або розгалужений нижчий алкініл(С2-С6); і її оптичні ізомери і фармацевтично прийнятні адитивні солі кислот або основ. 2. Сполука за п.1, вибрана з групи, що включає: 1-етеніл-3,3,5,5-тетраметилциклогексиламін, UA (21) 20040604348 (22) 07.11.2002 (24) 17.04.2006 (86) PCT/GB02/05038, 07.11.2002 (31) 60/350,974 (32) 07.11.2001 (33) US (31) 60/337,858 (32) 08.11.2001 (33) US (46) 17.04.2006, Бюл. № 4, 2006 р. (72) Парсонс Крістофер Грахам, DE, Хенріх Маркус , DE, Даниш Войцех , DE, Калвіньш Іварс , LV, Каусс Валер'янс , LV, Йіргенсонс Айгарс , LV, Гольд Маркус , DE (73) МЕРЦ ФАРМА ГМБХ УНД КО. КГАА, DE (56) US 6 071 966 A 06.06.2000 US 6 034 134 A 07.03.2000 (57) 1. Сполука формули I: 2 (19) 1 3 75478 4 2-(3,3,5,5-тетраметилциклогексиліден)етанамін, - R5, Rp, Rq, Rr і Rs незалежно вибрані з групи, що 1-аміно-3,3,5-триметил-2-циклогексен, містить водень, лінійний або розгалужений нижчий 1,3,5,5-тетраметил-2-циклогексен-1-амін, алкіл(С1-С6), лінійний або розгалужений нижчий 1-аліл-3,3,5,5-тетраметилциклогексанамін, алкеніл(С2-С6) і лінійний або розгалужений нижчий 1-(3,3,5,5-тетраметилциклогексиліден)-2алкініл(С2-С6), або R5, Rp, Rq, Rr і Rs незалежно пропанамін, можуть об'єднуватись з вуглецем, до якого вони 1-(3,3-діетил-5,5-диметилциклогексиліден)-2приєднані, і сусіднім вуглецем, утворюючи подвійпропанамін, цис-3-вініл-1,3,транс-5ний зв'язок, або Rp, Rq, Rr і Rs незалежно можуть триметилциклогексиламін, утворювати подвійний зв'язок з U або Y, до якого 2-метил-1-(3,3,5,5-тетраметил-1-циклогексен-1-іл)вони приєднані; 2-пропанамін, за умови, що U-V-W-X-Y-Z вибраний з 1-(1-аліл-3,3,5,5циклогексану, тетраметилциклогексил)піперидин, циклогекс-1-ену, 2-(1-вініл-3,3,5,5-тетраметилциклогексилциклогекс-2-ену, 1)етиламін, циклогекс-3-ену, 1-[3,3,5,5-тетраметил-1-(3-метил-2циклогекса-1,3-дієну, бутеніл)циклогексил]піперидин, циклогекса-1,4-дієну, 1-[3,3,5,5-тетраметил-1-(2циклогекса-1,5-дієну, пропініл)циклогексил]піперидин, циклогекса-2,4-дієну і 2-(1,3,3,5,5-пентаметилциклогексил)-4циклогекса-2,5-дієну, пентениламін, і за умови, що U-Z являє собою циклогексан, якщо 3-(3,3,5,5-тетраметилциклогексиліден)пропанамін, щонайменше один з -(A)n-(CR1R2)m-, R3, R4, R5, Rp, 2-метил-1-(3,3,5,5-тетраметилциклогексиліден)-2Rq, Rr являє собою лінійний або розгалужений нипропанамін, жчий алкеніл(С2-С6) або лінійний або розгалуже2-(3,3,5,5-тетраметилциклогексиліден)пропанамін, ний нижчий алкініл(С2-С6); N-метил-1-етеніл-3,3,5,5її оптичних ізомерів і фармацевтично прийнятних тетраметилциклогексиламін, адитивних солей кислот або основ, які ефективні N-аліл-1,3,3,5,5-пентаметилциклогексанамін для полегшення вказаного стану. і їх оптичні ізомери і фармацевтично прийнятні 5. Спосіб лікування у тварин стану, де сполука адитивні солі кислот або основ. вибрана за її імуномодуляторною, антималярійною 3. Фармацевтична композиція, що містить сполуку ефективністю, ефективністю проти вірусу Borna за п.1 або п.2 в комбінації з одним або більше фаабо проти вірусу гепатиту С, антитрипаносомальрмацевтично прийнятними розріджувачами, напоною ефективністю і проти вірусу герпеса, який внювачами і/або носіями. включає стадію введення тварині деякої кількості 4. Спосіб лікування у тварин стану, що виліковусполуки формули I: R5 R* ється антагоністом NMDA, який включає стадію введення тварині деякої кількості сполуки формуW ли I: X V R5 R* Rp W Z Rq Rp Y U Z Rq Y U X V Rs Rr , де: - R* означає -(A)n(CR1R2)m-NR3R4; - n+m=0, 1 або 2; - А вибраний з групи, що містить лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R1 і R2 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R3 і R4 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або разом утворюють алкілен(С2С10) або алкенілен(С2-С10), або разом з N утворюють необов'язково (С1-С6)алкіл- і/або (С2С6)алкенілзаміщений 3-7-членний азациклоалкан або азациклоалкен; Rs Rr , де - R* означає -(A)n-(CR1R2)m-NR3R4; - n+m=0, 1 або 2; - А вибраний з групи, що містить лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R1 і R2 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R3 і R4 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або разом утворюють алкілен(С2С10) або алкенілен(С2-С10), або разом з N утворюють необов'язково (С1-С6)алкіл- і/або (С2С6)алкенілзаміщений 3-7-членний азациклоалкан або азациклоалкен; - R5, Rp, Rq, Rr і Rs незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий 5 75478 6 алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); алкініл(С2-С6), або R5, Rp, Rq, Rr і Rs незалежно - R3 і R4 незалежно вибрані з групи, що містить можуть об'єднуватись з вуглецем, до якого вони водень, лінійний або розгалужений нижчий алприєднані, і сусіднім вуглецем, утворюючи подвійкіл(С1-С6), лінійний або розгалужений нижчий алний зв'язок, або Rp, Rq, Rr і Rs незалежно можуть кеніл(С2-С6) і лінійний або розгалужений нижчий утворювати подвійний зв'язок з U або Y, до якого алкініл(С2-С6), або разом утворюють алкілен(С2вони приєднані; С10) або алкенілен(С2-С10), або разом з N утворюза умови, що U-V-W-X-Y-Z вибраний з ють необов'язково (С1-С6)алкіл- і/або (С2циклогексану, С6)алкенілзаміщений 3-7-членний азациклоалкан циклогекс-1-ену, або азациклоалкен; циклогекс-2-ену, - R5, Rp, Rq, Rr і Rs незалежно вибрані з групи, що циклогекс-3-ену, містить водень, лінійний або розгалужений нижчий циклогекса-1,3-дієну, алкіл(С1-С6), лінійний або розгалужений нижчий циклогекса-1,4-дієну, алкеніл(С2-С6) і лінійний або розгалужений нижчий циклогекса-1,5-дієну, алкініл(С2-С6), або R5, Rp, Rq, Rr і Rs незалежно циклогекса-2,4-дієну і можуть об'єднуватись з вуглецем, до якого вони циклогекса-2,5-дієну, приєднані, і сусіднім вуглецем, утворюючи подвійі за умови, що U-Z являє собою циклогексан, якщо ний зв'язок, або Rp, Rq, Rr і Rs незалежно можуть щонайменше один з -(A)n-(CR1R2)m-, R3, R4, R5, Rp, утворювати подвійний зв'язок з U або Y, до якого Rq, Rr являє собою лінійний або розгалужений нивони приєднані; жчий алкеніл(С2-С6) або лінійний або розгалужеза умови, що U-V-W-X-Y-Z вибраний з ний нижчий алкініл(С2-С6); циклогексану, її оптичних ізомерів і фармацевтично прийнятних циклогекс-1-ену, адитивних солей кислот або основ, які ефективні циклогекс-2-ену, для полегшення вказаного стану. циклогекс-3-ену, 6. Спосіб лікування у тварин стану, що виліковуциклогекса-1,3-дієну, ється антагоністом NMDA, вибраного з групи, що циклогекса-1,4-дієну, включає ексцитотоксичність, вибрану з ішемії при циклогекса-1,5-дієну, ударі, травми, гіпоксії, гіпоглікемії, глаукоми і печіциклогекса-2,4-дієну і нкової енцефалопатії, хронічні нейродегенеративні циклогекса-2,5-дієну, захворювання, вибрані з хвороби Альцгеймера, і за умови, що U-Z являє собою циклогексан, якщо судинної деменції, хвороби Паркінсона, хвороби щонайменше один з -(A)n-(CR1R2)m-, R3, R4, R5, Rp, Хантінгтона, множинного склерозу, бічного аміотRq, Rr являє собою лінійний або розгалужений нирофічного склерозу, СНІД-нейродегенерації, олижчий алкеніл(С2-С6) або лінійний або розгалужевопонтоцеребелярної атрофії, синдрому Туретта, ний нижчий алкініл(С2-С6); рухового нейронного захворювання, мітохондріаїї оптичних ізомерів і фармацевтично прийнятних льної дисфункції, синдрому Корсакова і хвороби адитивних солей кислот або основ, які ефективні Крейтцфельдта-Якоба, для полегшення вказаного стану. інші порушення, що належать до тривалих пласти7. Спосіб лікування у тварин стану, що виліковучних змін в центральній нервовій системі, вибрані ється антагоністом рецептора 5-НТ3, який включає з хронічного болю, лікарської переносимості, застадію введення тварині деякої кількості сполуки лежності і адикції (наприклад, опіоїдної, кокаїнової, формули І: R5 R* бензодіазепінової, нікотинової і алкогольної), і епілепсію, пізню дискінезію, L-DOPA-індуковану W дискінезію, шизофренію, стан тривоги, депресію, X V гострий біль, спастичність і відчуття шуму у вухах, Y який включає стадію введення тварині деякої кільRp U Rs кості сполуки формули I: Z Rr R5 Rq R* , W де: X - R* означає -(A)n-(CR1R2)m-NR3R4; V - n+m=0, 1 або 2; Y Rp U Rs - А вибраний з групи, що містить лінійний або розZ галужений нижчий алкіл(С1-С6), лінійний або розRr Rq , галужений нижчий алкеніл(С2-С6) і лінійний або де розгалужений нижчий алкініл(С2-С6); 1 2 3 4 - R* означає -(A)n-(CR R )m-NR R ; - R1 і R2 незалежно вибрані з групи, що містить - n+m=0, 1 або 2; водень, лінійний або розгалужений нижчий ал- А вибраний з групи, що містить лінійний або розкіл(С1-С6), лінійний або розгалужений нижчий алгалужений нижчий алкіл(С1-С6), лінійний або розкеніл(С2-С6) і лінійний або розгалужений нижчий галужений нижчий алкеніл(С2-С6) і лінійний або алкініл(С2-С6); розгалужений нижчий алкініл(С2-С6); - R3 і R4 незалежно вибрані з групи, що містить - R1 і R2 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алводень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий кеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або разом утворюють алкілен(С2 7 75478 8 С10) або алкенілен(С2-С10), або разом з N утворюалкіл(С1-С6), лінійний або розгалужений нижчий ють необов'язково (С1-С6)алкіл- і/або (С2алкеніл(С2-С6) і лінійний або розгалужений нижчий С6)алкенілзаміщений 3-7-членний азациклоалкан алкініл(С2-С6), або R5, Rp, Rq, Rr і Rs незалежно або азациклоалкен; можуть об'єднуватись з вуглецем, до якого вони - R5, Rp, Rq, Rr і Rs незалежно вибрані з групи, що приєднані, і сусіднім вуглецем, утворюючи подвіймістить водень, лінійний або розгалужений нижчий ний зв'язок, або Rp, Rq, Rr і Rs незалежно можуть алкіл(С1-С6), лінійний або розгалужений нижчий утворювати подвійний зв'язок з U або Y, до якого алкеніл(С2-С6) і лінійний або розгалужений нижчий вони приєднані; алкініл(С2-С6), або R5, Rp, Rq, Rr і Rs незалежно за умови, що U-V-W-X-Y-Z вибраний з можуть об'єднуватись з вуглецем, до якого вони циклогексану, приєднані, і сусіднім вуглецем, утворюючи подвійциклогекс-1-ену, ний зв'язок, або Rp, Rq, Rr і Rs незалежно можуть циклогекс-2-ену, утворювати подвійний зв'язок з U або Y, до якого циклогекс-3-ену, вони приєднані; циклогекса-1,3-дієну, за умови, що U-V-W-X-Y-Z вибраний з циклогекса-1,4-дієну, циклогексану, циклогекса-1,5-дієну, циклогекс-1-ену, циклогекса-2,4-дієну і циклогекс-2-ену, циклогекса-2,5-дієну, циклогекс-3-ену, і за умови, що U-Z являє собою циклогексан, якщо циклогекса-1,3-дієну, щонайменше один з -(A)n-(CR1R2)m-, R3, R4, R5, Rp, циклогекса-1,4-дієну, Rq, Rr являє собою лінійний або розгалужений нициклогекса-1,5-дієну, жчий алкеніл(С2-С6) або лінійний або розгалужециклогекса-2,4-дієну і ний нижчий алкініл(С2-С6); циклогекса-2,5-дієну, її оптичних ізомерів і фармацевтично прийнятних і за умови, що U-Z являє собою циклогексан, якщо адитивних солей кислот або основ, які ефективні щонайменше один з -(A)n-(CR1R2)m-, R3, R4, R5, Rp, для полегшення вказаного стану. Rq, Rr являє собою лінійний або розгалужений ни9. Спосіб лікування у тварин стану, що виліковужчий алкеніл(С2-С6) або лінійний або розгалужеється антагоністом 5-НТ3, вибраного з групи, що ний нижчий алкініл(С2-С6); включає порушення, пов'язані зі станом тривоги, її оптичних ізомерів і фармацевтично прийнятних депресивні порушення, шизофренію, і лікування адитивних солей кислот або основ, які ефективні пов'язаних з цим психозів, порушень, пов'язаних зі для полегшення вказаного стану. зловживанням ліками і алкоголем, когнітивних по8. Спосіб лікування у тварин стану, що виліковурушень, хвороби Альцгеймера, хвороби Паркінсоється антагоністом нейронних нікотинових рецепна, мозочкового тремору, мігрені, порушень апетиторів, який включає стадію введення тварині дету, слизового коліту (IBS) і блювання, який якої кількості сполуки формули I: включає стадію введення тварині деякої кількості R5 R* сполуки формули I: R5 W V X U Y R* W X V Rp Z Rq Rs Rr Rp де - R* означає -(A)n-(CR1R2)m-NR3R4; - n+m=0, 1 або 2; - А вибраний з групи, що містить лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R1 і R2 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R3 і R4 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або разом утворюють алкілен(С2С10) або алкенілен(С2-С10), або разом з N утворюють необов'язково (С1-С6)алкіл- і/або (С2С6)алкенілзаміщений 3-7-членний азациклоалкан або азациклоалкен; - R5, Rp, Rq, Rr і Rs незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий Y U , Z Rq Rs Rr , де - R* означає -(A)n-(CR1R2)m-NR3R4; - n+m=0, 1 або 2; - А вибраний з групи, що містить лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R1 і R2 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R3 і R4 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або разом утворюють алкілен(С2С10) або алкенілен(С2-С10), або разом з N утворюють необов'язково (С1-С6)алкіл- і/або (С2С6)алкенілзаміщений 3-7-членний азациклоалкан або азациклоалкен; - R5, Rp, Rq, Rr і Rs незалежно вибрані з групи, що 9 75478 10 містить водень, лінійний або розгалужений нижчий галужений нижчий алкеніл(С2-С6) і лінійний або алкіл(С1-С6), лінійний або розгалужений нижчий розгалужений нижчий алкініл(С2-С6); алкеніл(С2-С6) і лінійний або розгалужений нижчий - R1 і R2 незалежно вибрані з групи, що містить 5 алкініл(С2-С6), або R , Rp, Rq, Rr і Rs незалежно водень, лінійний або розгалужений нижчий алможуть об'єднуватись з вуглецем, до якого вони кіл(С1-С6), лінійний або розгалужений нижчий алприєднані, і сусіднім вуглецем, утворюючи подвійкеніл(С2-С6) і лінійний або розгалужений нижчий ний зв'язок, або Rp, Rq, Rr і Rs незалежно можуть алкініл(С2-С6); утворювати подвійний зв'язок з U або Y, до якого - R3 і R4 незалежно вибрані з групи, що містить вони приєднані; водень, лінійний або розгалужений нижчий алза умови, що U-V-W-X-Y-Z вибраний з кіл(С1-С6), лінійний або розгалужений нижчий алциклогексану, кеніл(С2-С6) і лінійний або розгалужений нижчий циклогекс-1-ену, алкініл(С2-С6), або разом утворюють алкілен(С2циклогекс-2-ену, С10) або алкенілен(С2-С10), або разом з N утворюциклогекс-3-ену, ють необов'язково (С1-С6)алкіл- і/або (С2циклогекса-1,3-дієну, С6)алкенілзаміщений 3-7-членний азациклоалкан циклогекса-1,4-дієну, або азациклоалкен; циклогекса-1,5-дієну, - R5, Rp, Rq, Rr і Rs незалежно вибрані з групи, що циклогекса-2,4-дієну і містить водень, лінійний або розгалужений нижчий циклогекса-2,5-дієну, алкіл(С1-С6), лінійний або розгалужений нижчий і за умови, що U-Z являє собою циклогексан, якщо алкеніл(С2-С6) і лінійний або розгалужений нижчий щонайменше один з -(A)n-(CR1R2)m-, R3, R4, R5, Rp, алкініл(С2-С6), або R5, Rp, Rq, Rr і Rg незалежно Rq, Rr являє собою лінійний або розгалужений ниможуть об'єднуватись з вуглецем, до якого вони жчий алкеніл(С2-С6) або лінійний або розгалужеприєднані, і сусіднім вуглецем, утворюючи подвійний нижчий алкініл(С2-С6); ний зв'язок, або Rp, Rq, Rr і Rs незалежно можуть її оптичних ізомерів і фармацевтично прийнятних утворювати подвійний зв'язок з U або Y, до якого адитивних солей кислот або основ, які ефективні вони приєднані; для полегшення вказаного стану. за умови, що U-V-W-X-Y-Z вибраний з 10. Спосіб лікування у тварин стану, що виліковуциклогексану, ється антагоністом нейронних нікотинових рецепциклогекс-1-ену, торів, вибраного з групи, що включає синдром Туциклогекс-2-ену, ретта, порушення, пов'язані зі станом тривоги, циклогекс-3-ену, шизофренію, зловживання ліками, зловживання циклогекса-1,3-дієну, нікотином, зловживання кокаїном, дискінезію циклогекса-1,4-дієну, (Morbus Huntington, L-DOPA-індуковану), порушенциклогекса-1,5-дієну, ня, пов'язані з гіперактивністю при дефіциті уваги циклогекса-2,4-дієну і (ADHD), хворобу Альцгеймера, хворобу Паркінсоциклогекса-2,5-дієну, на і біль, який включає стадію введення тварині і за умови, що U-Z являє собою циклогексан, якщо деякої кількості сполуки формули І: щонайменше один з -(A)n-(CR1R2)m-, R3, R4, R5, Rp, R5 R* Rq, Rr являє собою лінійний або розгалужений нижчий алкеніл(С2-С6) або лінійний або розгалужеW ний нижчий алкініл(С2-С6); X V її оптичних ізомерів і фармацевтично прийнятних Y Rp U Rs адитивних солей кислот або основ, які ефективні Z для полегшення вказаного стану. Rr Rq , 11. Застосування сполуки формули I за будь-яким де з пп.4-10 і її оптичних ізомерів і фармацевтично - R* означає -(A)n-(CR1R2)m-NR3R4; прийнятних адитивних солей кислот або основ у - n+m=0, 1 або 2; виробництві лікарського засобу для використання - А вибраний з групи, що містить лінійний або розу способі за будь-яким з пп.4-10. галужений нижчий алкіл(С1-С6), лінійний або роз Ненасичені 1-аміноалкілциклогексанові сполуки, які є системно активними як антагоністи NMDA, 5-НТ3 і нікотинових рецепторів, включаючи їх фармацевтичні композиції, спосіб їх одержання і спосіб лікування за їх допомогою порушень ЦНС, які включають розлади глутаматергічної, серотонінергічної і нікотинової передачі, для лікування імуномодуляторних порушень і для лікування інфекційних захворювань. Антагоністи NMDA Антагонізм глутаматних рецепторів типу N метил-D-аспартату (NMDA) потенційно має широкий діапазон терапевтичних застосувань [19]. Функціонального інгібування NMDA-рецепторів можна досягнути шляхом впливу на різні сайти рестрикції, такі як первинний медіаторний сайт, стрихніннечутливий гліциновий сайт (гліцинв), поліамінний сайт і фенциклідиновий сайт, розташований всередині катіонного каналу. Блокатори каналів NMDAрецепторів діють неконкурентним чином, що "залежить від застосування"; це має на увазі, що вони звичайно тільки блокують канал у відкритому ста 11 75478 12 ні. Як багато-хто інтерпретує, ця залежність від гіпокампу і мигдалеподібного тіла лімбічної систезастосування означає, що більш сильна активація ми, передбачають, що 5-НТ3-селективні антагонісрецептора повинна приводити до більшої міри ти можуть надавати психотропні дії [Greenshaw & антагонізму. Крім того, вважають, що такий спосіб Silverstone, 1997]. дії має на увазі, що даний клас антагоніста може Дійсно, ранні дослідження на тваринах передбути особливо корисний, коли очікується надмірна бачають, що антагоністи рецепторів 5-НТ3, крім їх активація NMDA-рецепторів, як при епілепсії, ішешироко визнаного протиблювотного застосування, мії і травмі. Однак попередня клінічна практика із можуть бути клінічно корисні в ряді областей. Дані застосуванням селективного, такого, що має висообласті включають хворобливий стан тривоги, ку спорідненість, сильно залежить від застосуваншизофренію, зловживання ліками і алкоголем, ня неконкурентного агоніста NMDA-рецепторів (+)депресивні порушення, когнітивні порушення, хво5-метил-10,11-дигідро-5Н-дибензоциклогептенробу Альцгеймера, мозочковий тремор, психоз, 5,10-імінмалеату ((+)-МК-801) є невтішною. А саме, пов'язаний з лікуванням хвороби Паркінсона, біль терапевтична ефективність при епілепсії низька, (мігрень і слизовий коліт) і порушення апетиту. тоді як при терапевтичних дозах виявляють деякі Антагоністи нейронних нікотинових рецепторів психотропні побічні ефекти. Дані спостереження У цей час відомо десять альфа-підодиниць разом з тим фактом, що ті, хто зловживає фенцик(альфа 1-10) і чотири бета-підодиниці (бета 1-4) лідином, відчувають аналогічні психотропні симпдля нікотинових рецепторів. Рецептори α4β2, ймотоми, приводять до висновку, що неконкурентний вірно, є найбільш загальними в ЦНС, особливо в антагонізм NMDA-рецепторів не може бути багагіпокампі і смугастому тілі. Вони утворюють несетообіцяючим терапевтичним підходом. лективні катіонні канали з повільно не повністю Однак застосування більш складних електродесенсибілізуючими струмами (тип II). Гомомерні фізіологічних методів показує, що не існує рівності рецептори α7 є перед- і постсинаптичними і виявміж різними неконкурентними антагоністами, оскілені в гіпокампі, руховій області головного мозку і льки такі фактори, як швидкість блокади рецептолімбічній системі, а також в периферичній автонора (кінетики включення-виключення) і залежність мній нервовій системі. Дані рецептори характеривід напруження даного ефекту, можуть визначати зуються своєю високою Са2+-проникністю і швидфармакодинамічні відмітні ознаки in vivo, поряд, кими сильно десенсибілізуючими реакціями (тип наприклад, з терапевтичною безпекою. ПарадокlА). Зміни в нікотинових рецепторах причетні до сально, що придатними можуть бути швидше агеряду захворювань. Дані захворювання включають нти зі спорідненістю від низького до помірного, ніж хворобу Альцгеймера, хворобу Паркінсона, синдагенти з високою спорідненістю. Такі відкриття ром Туретта, шизофренію, зловживання ліками, ініціювали перегляд концепції неконкурентного зловживання нікотином і біль. антагонізму NMDA-рецепторів при розробці лікарНа основі спостереження, що нікотиновий агоських засобів [19, 22]. Неконкурентні антагоністи ніст нікотин, мабуть, сам по собі надає корисні дії, NMDA-рецепторів, такі як амантадин і мемантин, розробка лікарського засобу досі мала на увазі які задовольняють вказаним вище критеріям, завідкриття селективних нікотинових агоністів. стосовуються клінічно протягом декількох років З іншого боку, неясно, чи зумовлені ефекти ніпри лікуванні хвороби Паркінсона і слабоумства, котинових агоністів, наприклад, при синдромі Тувідповідно, і насправді рідко дають побічні ефекти ретта і шизофренії, активацією або дезактиваціпри терапевтичних дозах, що використовуються єю/десенсибілізацію нейронних нікотинових при їх відповідних показаннях. рецепторів. З точки зору згаданого вище обґрунтування Ефекти агоністів на нейронні нікотинові рецепзаявники розробили серії нових неконкурентних тори сильно залежать від періоду впливу. Швидка антагоністів NMDA-рецепторів на основі ненасиоборотна десенсибілізація відбувається за мілісеченої 1-аміноалкілциклогексанової структури. Дане кунди, зменшення відбувається за секунди, безподослідження розроблене для порівняння антагоніворотна дезактивація рецепторів, що містять α4β2 стичних властивостей NMDA-рецепторів даних і α7, відбувається за години, і їх позитивна регуляненасичених 1-аміноалкілциклогексанових похідція відбувається за дні. них в дослідженнях зі зв'язування рецепторів, елеІншими словами: ефекти нікотинових "агонісктрофізіологічних експериментах, на одній конвутів" насправді можуть бути зумовлені частковим льсійній моделі і двох моделях рухової агонізмом, дезактивацією і/або десенсибілізацією недостатності. Заміщення для даних ненасичених нейронних нікотинових рецепторів. У свою чергу 1-аміноалкілциклогексанів детально вказані в табпомірні концентрації блокаторів каналів нейронних лиці 6. нікотинових рецепторів можуть виробляти такі ж Антагоністи рецепторів 5-НТ3 ефекти, як ефекти, що повідомляються для нікоРецептори 5-НТ3 являють собою закриті лігантинових агоністів в згаданих вище показаннях. дами іонотропні рецептори, проникні для катіонів. У цей час виявлено, що ряд ненасичених 1Рецептори 5-НТ3 людини мають найвищу щільаміноалкілциклогексанів володіє різко вираженою і ність на ентерохромафінних клітинах в шлунковонесподіваною антагоністичною активністю відноскишковій слизовій оболонці, які подразнюються но NMDA, 5-НТ3 і нікотинових рецепторів. Завдяки вагусними аферентами, і area postrema стовбура вказаній вище властивості, дані речовини підхоголовного мозку, яка утворює хеморецепторну дять для лікування широкого діапазону порушень тригерну зону. ЦНС, які включають розлади глутаматергічної, Оскільки рецептори 5-НТ3 мають високу щільсеротонінергічної і нікотинової передачі, володіють ність не тільки в area postrema, але також в ділянці імуномодуляторним ефектом і властивостями про 13 75478 14 ти інфекційних захворювань. Дані сполуки переалкеніл(С2-С6) і лінійний або розгалужений нижчий важно знаходяться у вигляді фармацевтичних алкініл(С2-С6), або Rp, Rq, Rr і Rs незалежно можуть композицій, в яких вони присутні разом з одним об'єднуватись з вуглецем, до якого вони приєднаабо більшою кількістю фармацевтично прийнятних ні, і сусіднім вуглецем, утворюючи подвійний зв'ярозріджувачів, носіїв або наповнювачів. зок, або Rp, Rq, Rr і Rs незалежно можуть утворюМетою даного винаходу є нові фармацевтичні вати подвійний зв'язок з U або Y, до якого вони сполуки, які являють собою ненасичені 1приєднані; аміноалкілциклогексанові антагоністи NMDA, 5-НТ3 за умови, що U-V-W-X-Y-Z вибраний з і нікотинових рецепторів, і їх фармацевтичні комциклогексану, позиції. Крім того, предметом даного винаходу є циклогекс-2-ену, новий спосіб лікування, припинення, полегшення, циклогекс-3-ену, ослаблення або зменшення інтенсивності небажациклогекса-1,4-дієну, них порушень ЦНС, які включають розлади глутациклогекса-1,5-дієну, матергічної, серотонінергічної, нікотинової перециклогекса-2,4-дієну і дачі, лікування імуномодуляторних порушень і циклогекса-2,5-дієну, лікування інфекційних захворювань за допомогою і за умови, що, щонайменше, один з Rp і Rq не застосування сполуки даного винаходу або фарє воднем і, щонайменше, один з Rr і Rs не є водмацевтичної композиції, яка її містить. Додатковим нем, предметом даного винаходу є спосіб одержання і за умови, що U-Z являє собою циклогексан, ненасичених 1-аміноалкілциклогексанових активякщо, щонайменше, один з -(A)n-(CR1R2)m-, R3, R4, них елементів. Додаткові цілі винаходу будуть ясні R5, Rp, Rq, Rr i Rs являє собою лінійний або розгадалі, і ще інші цілі будуть ясні фахівцеві в даній лужений нижчий алкеніл(С2-С6) або лінійний або області. розгалужений нижчий алкініл(С2-С6); Таким чином, як вважають автори, зміст даноі її оптичні ізомери і фармацевтично прийнятні го винаходу можна підсумувати серед іншого наадитивні солі кислот або основ; ступними словами: спосіб лікування існуючих тварин з метою посполука, вибрана зі сполук формули І: легшення стану, що виліковується антагоністом NMDA, який включає стадію введення тварині деякої кількості сполуки, вибраної зі сполук формули І: де - R* означає -(A)n-(CR1R2)m-NR3R4; - n+m=0, 1 або 2; - А вибраний з групи, що містить лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R1 і R2 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R3 і R4 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або разом утворюють алкілен(С2С10) або алкенілен(С2-С10), або разом з N утворюють необов'язково (С1-С6)алкіл- і/або (С2С6)алкенілзаміщений 3-7-членний азациклоалкан або азациклоалкен; - R5 незалежно вибраний з групи, що містить лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або R5 об'єднується з вуглецем, до якого він приєднаний, і сусіднім вуглецем, утворюючи подвійний зв'язок; - Rp, Rq, Rr і Rs незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий де: - R* означає -(A)n-(CR1R2)m-NR3R4; - n+m=0, 1 або 2; - А вибраний з групи, що містить лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R1 і R2 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R3 і R4 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або разом утворюють алкілен(С2С10) або алкенілен(С2-С10), або разом з N утворюють необов'язково (С1-С6)алкіл- і/або (С2С6)алкенілзаміщений 3-7-членний азациклоалкан або азациклоалкен; 5 - R , Rp, Rq, Rr і Rs незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл (С2-С6), або R5, Rp, Rq, Rr і Rs незалежно можуть об'єднуватись з вуглецем, до якого вони приєднані, і сусіднім вуглецем, утворюючи 15 75478 16 подвійний зв'язок, або Rp, Rq, Rr і Rs незалежно якого вони приєднані; можуть утворювати подвійний зв'язок з U або Y, до за умови, що U-V-W-X-Y-Z вибраний з якого вони приєднані; циклогексану, за умови, що U-V-W-X-Y-Z вибраний з циклогекс-1-ену, циклогексану, циклогекс-2-ену, циклогекс-1-ену, циклогекс-3-ену, циклогекс-2-ену, циклогекса-1,3-дієну, циклогекс-3-eну, циклогекса-1,4-дієну, циклогекса-1,3-дієну, циклогекса-1,5-дієну, циклогекса-1,4-дієну, циклогекса-2,4-дієну і циклогекса-1,5-дієну, циклогекса-2,5-дієну, циклогекса-2,4-дієну і і за умови, що U-Z являє собою циклогексан, циклогекса-2,5-дієну, якщо, щонайменше, один з -(А)п-(СR1R2)m-, R3, R4, і за умови, що U-Z являє собою циклогексан, R5, Rp, Rq, Rr являє собою лінійний або розгалуже1 2 3 4 якщо, щонайменше, один з -(A)n-(CR R )m-, R , R , ний нижчий алкеніл(С2-С6) або лінійний або розгаR5, Rp, Rq, Rr являє собою лінійний або розгалужелужений нижчий алкініл(С2-С6); ний нижчий алкеніл(С2-С6) або лінійний або розгаїї оптичних ізомерів і фармацевтично прийнятлужений нижчий алкініл(С2-С6); них адитивних солей кислот або основ, які ефекїї оптичних ізомерів і фармацевтично прийняттивні для полегшення вказаного стану; них адитивних солей кислот або основ, які ефекспосіб лікування існуючих тварин з метою потивні для полегшення вказаного стану; легшення стану, що виліковується антагоністом спосіб лікування існуючих тварин з метою поNMDA, вибраного з групи, що включає ексцитотоклегшення стану, де сполука вибрана внаслідок її сичність, вибрану з ішемії при ударі, травмі, гіпокімуномодуляторної, антималярійної ефективності, сії, гіпоглікемії, глаукоми і печінкової енцефалопаефективності проти вірусу Воrnа або проти вірусу тії, гепатиту С, антитрипаносомальної ефективності і хронічні нейродегенеративні захворювання, проти вірусу герпеса, що включає стадію введення вибрані з хвороби Альцгеймера, судинної дементварині деякої кількості сполуки, вибраної зі сполук ції, хвороби Паркінсона, хвороби Хантінгтона, формули І: множинного склерозу, бічного, аміотрофічного склерозу, СНІД-нейродегенерації, олівопонтоцеребелярної атрофії, синдрому Туретта, рухового нейронного захворювання, мітохондріальної дисфункції, синдрому Корсакова і хвороби Крейтцфельдта-Якоба, інші порушення, що відносяться до тривалих пластичних змін в центральній нервовій системі, вибрані з хронічного болю, лікарської переносимоде: сті, залежності і адикції (наприклад, опіоїдної, кока- R* означає -(A)n-(CR1R2)m-NR3R4; їнової, бензодіазепінової, нікотинової і алкоголь- n+m=0, 1 або 2; ної), і - А вибраний з групи, що містить лінійний або епілепсію, пізню дискінезію, L-DOPAрозгалужений нижчий алкіл(С1-С6), лінійний або індуковану дискінезію, шизофренію, стан тривоги, розгалужений нижчий алкеніл(С2-С6) і лінійний або депресію, гострий біль, еластичність і відчуття розгалужений нижчий алкініл (С2-С6); 1 2 шуму у вухах, - R і R незалежно вибрані з групи, що містить який включає стадію введення тварині деякої водень, лінійний або розгалужений нижчий алкількості сполуки, вибраної зі сполук формули І: кіл(С -С ), лінійний або розгалужений нижчий ал1 6 кеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R3 і R4 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або разом утворюють алкілен(С2С10) або алкенілен(С2-С10), або разом з N утворюють необов'язково (С1-С6)алкіл- і/або (С2С6)алкенілзаміщений 3-7-членний азациклоалкан або азациклоалкен; - R5, Rp, Rq, Rr і Rs незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або R5, Rp, Rq, Rr і Rs незалежно можуть об'єднуватись з вуглецем, до якого вони приєднані, і сусіднім вуглецем, утворюючи подвійний зв'язок, або Rp, Rq, Rr і Rs незалежно можуть утворювати подвійний зв'язок з U або Y, до де: - R* означає -(A)n-(CR1R2)m-NR3R4; - n+m=0, 1 або 2; - А вибраний з групи, що містить лінійний або розгалужений нижчий алкіл (С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R1 і R2 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); 17 75478 18 - R3 і R4 незалежно вибрані з групи, що містить алкініл(С2-С6), або разом утворюють алкілен(С2водень, лінійний або розгалужений нижчий алС10) або алкенілен(С2-С10), або разом з N утворюкіл(С1-С6), лінійний або розгалужений нижчий алють необов'язково (С1-С6)алкіл- і/або (С2кеніл(С2-С6) і лінійний або розгалужений нижчий С6)алкенілзаміщений 3-7-членний азациклоалкан алкініл(С2-С6), або разом утворюють алкілен(С2або азациклоалкен; 5 С10) або алкенілен(С2-С10), або разом з N утворю- R , Rp, Rq, Rr і Rs незалежно вибрані з групи, ють необов'язково (С1-С6)алкіл- і/або (С2що містить водень, лінійний або розгалужений С6)алкенілзаміщений 3-7-членний азациклоалкан нижчий алкіл(С1-С6), лінійний або розгалужений або азациклоалкен; нижчий алкеніл(С2-С6) і лінійний або розгалужений - R5, Rp, Rq, Rr і Rs незалежно вибрані з групи, нижчий алкініл(С2-С6), або R5, Rp, Rq, Rr і Rs незащо містить водень, лінійний або розгалужений лежно можуть об'єднуватись з вуглецем, до якого нижчий алкіл(С1-С6), лінійний або розгалужений вони приєднані, і сусіднім вуглецем, утворюючи нижчий алкеніл(С2-С10) і лінійний або розгалужеподвійний зв'язок, або Rp, Rq, Rr і Rg незалежно ний нижчий алкініл(С2-С6), або R5, Rp, Rq,Rr і Rs можуть утворювати подвійний зв'язок з U або Y, до незалежно можуть об'єднуватись з вуглецем, до якого вони приєднані; якого вони приєднані, і сусіднім вуглецем, утвоза умови, що U-V-W-X-Y-Z вибраний з рюючи подвійний зв'язок, або Rp, Rq, Rr і Rs незациклогексану, лежно можуть утворювати подвійний зв'язок з U циклогекс-1-ену, або Y, до якого вони приєднані; за умови, що U-Vциклогекс-2-ену, W-X-Y-Z вибраний з циклогекс-3-ену, циклогексану, циклогекса-1,3-дієну, циклогекс-1-ену, циклогекса-1,4-дієну, циклогекс-2-ену, циклогекса-1,5-дієну, цикл огекс-3-eну, циклогекса-2,4-дієну і циклогекса-1,3-дієну, циклогекса-2,5-дієну, циклогекса-1,4-дієну, і за умови, що U-Z являє собою циклогексан, циклогекса-1,5-дієну, якщо, щонайменше, один з -(A)n-(CR1R2)m-, R3, R4, циклогекса-2,4-дієну і R5, Rp, Rq, Rr являє собою лінійний або розгалужециклогекса-2,5-дієну, ний нижчий алкеніл(С2-С6) або лінійний або розгаі за умови, що U-Z являє собою циклогексан, лужений нижчий алкініл(С2-С6); якщо, щонайменше, один з -(А)n-(CR1R2)m-, R3, R4, її оптичних ізомерів і фармацевтично прийнятR5, Rp, Rq, Rr являє собою лінійний або розгалужених адитивних солей кислот або основ, які ефекний нижчий алкеніл(С2-С6) або лінійний або розгативні для полегшення вказаного стану; лужений нижчий алкініл(С2-С6); спосіб лікування існуючих тварин з метою її оптичних ізомерів і фармацевтично прийнятполегшення стану, що виліковується антагоністом них адитивних солей кислот або основ, які ефекнейронних нікотинових рецепторів, який включає тивні для полегшення вказаного стану; стадію введення тварині деякої кількості сполуки, спосіб лікування існуючих тварин з метою повибраної зі сполук формули І: легшення стану, що виліковується антагоністом рецептора 5-НТ3, який включає стадію введення тварині деякої кількості сполуки, вибраної зі сполук формули І: де: - R* означає -(A)n-(CR1R2)m-NR3R4; - n+m=0, 1 або 2; - А вибраний з групи, що містить лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R1 і R2 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R3 і R4 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкені л(С2-С6) і лінійний або розгалужений нижчий де: - R* означає -(A)n-(CR1R2)m-NR3R4; - n+m=0, 1 або 2; - А вибраний з групи, що містить лінійний або розгалужений нижчий алкіл (С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R1 і R незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R3 і R4 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або разом утворюють алкілен(С2С10) або алкенілен(С2-С10), або разом з N утворюють необов'язково (С1-С6)алкіл- і/або (С2С6)алкенілзаміщений 3-7-членний азациклоалкан 19 75478 20 або азациклоалкен; С10) або алкенілен(С2-С10), або разом з N утворю- R5, Rp, Rq, Rr і Rs незалежно вибрані з групи, ють необов'язково (С1-С6)алкіл- і/або (С2що містить водень, лінійний або розгалужений С6)алкенілзаміщений 3-7-членний азациклоалкан нижчий алкіл(С1-С6), лінійний або розгалужений або азациклоалкен; нижчий алкеніл(С2-С6) і лінійний або розгалужений - R5, Rp, Rq, Rr і Rs незалежно вибрані з групи, 5 нижчий алкініл(С2-С6), або R , Rp, Rq, Rr і Rs незащо містить водень, лінійний або розгалужений лежно можуть об'єднуватись з вуглецем, до якого нижчий алкіл(С1-С6), лінійний або розгалужений вони приєднані, і сусіднім вуглецем, утворюючи нижчий алкеніл(С2-С6) і лінійний або розгалужений подвійний зв'язок, або Rp, Rq, Rr і Rs незалежно нижчий алкініл(С2-С6), або R5, Rp, Rq, Rr і Rs незаможуть утворювати подвійний зв'язок з U або Y, до лежно можуть об'єднуватись з вуглецем, до якого якого вони приєднані; вони приєднані, і сусіднім вуглецем, утворюючи за умови, що U-V-W-X-Y-Z вибраний з подвійний зв'язок, або Rp, Rq, Rr і Rs незалежно циклогексану, можуть утворювати подвійний зв'язок з U або Y, до циклогекс-1-eну, якого вони приєднані; циклогекс-2-ену, за умови, що U-V-W-X-Y-Z вибраний з циклогекс-3-eну, циклогексану, циклогекса-1,3-дієну, циклогекс-1-ену, циклогекса-1,4-дієну, циклогекс-2-ену, циклогекса-1,5-дієну, циклогекс-3-ену, циклогекса-2,4-дієну і циклогекса-1,3-дієну, циклогекса-2,5-дієну, циклогекса-1,4-дієну, і за умови, що U-Z являє собою циклогексан, циклогекса-1,5-дієну, якщо, щонайменше, один з -(A)n-(CR1R2)m-, R3, R4, циклогекса-2,4-дієну і R5, Rp, Rq, Rr являє собою лінійний або розгалужециклогекса-2,5-дієну, ний нижчий алкеніл(С2-С6) або лінійний або розгаі за умови, що U-Z являє собою циклогексан, лужений нижчий алкініл(С2-С6); якщо, щонайменше, один з -(A)n-(CR1R2)m-, R3, R4, її оптичних ізомерів і фармацевтично прийнятR5, Rp, Rq, Rr являє собою лінійний або розгалужених адитивних солей кислот або основ, які ефекний нижчий алкеніл(С2-С6) або лінійний або розгативні для полегшення вказаного стану; лужений нижчий алкініл(С2-С6); спосіб лікування існуючих тварин з метою поїї оптичних ізомерів і фармацевтично прийнятлегшення стану, що виліковується антагоністом 5них адитивних солей кислот або основ, які ефекНТ3, вибраного з групи, що включає порушення, тивні для полегшення вказаного стану; пов'язані зі станом тривоги, депресивні порушенспосіб лікування існуючих тварин з метою поня, шизофренію, і лікування пов'язаних з цим псилегшення стану, що виліковується антагоністом хозів, порушень, пов'язаних зі зловживанням ліканейронних нікотинових рецепторів, вибраного з ми і алкоголем, когнітивних порушень, хвороби групи, що включає синдром Туретта, порушення, Альцгеймера, хвороби Паркінсона, мозочкового пов'язані зі станом тривоги, шизофренію, зловжитремору, мігрені, порушень апетиту, слизового вання ліками, зловживання нікотином, зловживанколіту (IBS) і блювоти, який включає стадію ввеня кокаїном, дискінезію (Morbus Huntington, Lдення тварині деякої кількості сполуки, вибраної зі DOPA-індуковану), порушення, пов'язані з гіпераксполук формули І: тивністю при дефіциті уваги (ADHD), хворобу Альцгеймера, хворобу Паркінсона і біль, який включає стадію введення тварині деякої кількості сполуки, вибраної зі сполук формули І: де: - R* означає -(A)n-(CR'R2)m-NR3R4; - n+m=0, 1 або 2; - А вибраний з групи, що містить лінійний або розгалужений нижчий алкіл (С1-С6), лінійний або розгалужений нижчий алкеніл (С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R1 і R2 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R3 і R4 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6), або разом утворюють алкілен(С2 де: - R* означає -(A)n-(CR1R2)m-NR3R4; - n+m=0, 1 або 2; - А вибраний з групи, що містить лінійний або розгалужений нижчий алкіл (С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R1 і R2 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R3 і R4 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий ал 21 75478 22 кіл(С1-С6), лінійний або розгалужений нижчий алніл(С2-С6) і лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий кініл(С2-С6), або разом утворюють алкілен(С2-С10) алкініл(С2-С6), або разом утворюють алкілен(С2або алкенілен(С2-С10), або разом з N утворюють С10) або алкенілен(С2-С10), або разом з N утворюнеобов'язково (С1-С6)алкілі/або (С2ють необов'язково (С1-С6)алкіл- і/або (С2С6)алкенілзаміщений 3-7-членний азациклоалкан С6)алкенілзаміщений 3-7-членний азациклоалкан або азациклоалкен; або азациклоалкен; - R5 незалежно вибраний з групи, що містить 5 - R , Rp, Rq, Rr і Rs незалежно вибрані з групи, лінійний або розгалужений нижчий алкіл(С1-С6), що містить водень, лінійний або розгалужений лінійний або розгалужений нижчий алкеніл(С2-С6) і нижчий алкіл(С1-С6), лінійний або розгалужений лінійний або розгалужений нижчий алкініл(С2-С6), нижчий алкеніл(С2-С6) і лінійний або розгалужений або R5 об'єднується з вуглецем, до якого він приє5 нижчий алкініл(С2-С6), або R , Rp, Rq, Rr і Rs незаднаний, і сусіднім вуглецем, утворюючи подвійний лежно можуть об'єднуватись з вуглецем, до якого зв'язок; вони приєднані, і сусіднім вуглецем, утворюючи - Rp, Rq, Rr і Rs незалежно вибрані з групи, що подвійний зв'язок, або Rp, Rq, Rr і Rs незалежно містить водень, лінійний або розгалужений нижчий можуть утворювати подвійний зв'язок з U або Y, до алкіл(С1-С6), лінійний або розгалужений нижчий якого вони приєднані; алкеніл(С2-С6) і лінійний або розгалужений нижчий за умови, що U-V-W-X-Y-Z вибраний з алкініл(С2-С6), або Rp, Rq, Rr і Rs незалежно можуть циклогексану, об'єднуватись з вуглецем, до якого вони приєднацикл ore кс-1-eну, ні, і сусіднім вуглецем, утворюючи подвійний зв'яциклогекс-2-ену, зок, або Rp, Rq, Rr і Rs незалежно можуть утворюцикл огекс-3-eну, вати подвійний зв'язок з U або Y, до якого вони циклогекса-1,3-дієну, приєднані; циклогекса-1,4-дієну, за умови, що U-V-W-X-Y-Z вибраний з циклогекса-1,5-дієну, циклогексану, циклогекса-2,4-дієну і циклогекс-1-ену, циклогекса-2,5-дієну, циклогекс-2-ену, і за умови, що U-Z являє собою циклогексан, циклогекс-3-ену, якщо, щонайменше, один з -(A)n-(CR1R2)m-, R3, R4, циклогекса-1,3 - дієну, R5, Rp, Rq, Rr являє собою лінійний або розгалужециклогекса-1,4-дієну, ний нижчий алкеніл(С2-С6) або лінійний або розгациклогекса-1,5-дієну, лужений нижчий алкініл(С2-С6); циклогекса-2,4-дієну і її оптичних ізомерів і фармацевтично прийнятциклогекса-2,5-дієну, них адитивних солей кислот або основ, які ефекі за умови, що, щонайменше, один з Rp і Rq не тивні для полегшення вказаного стану; є воднем, і, щонайменше, один з Rr і Rs не є водзастосування сполуки формули І, яке винем, значене в зв'язку з попередніми способами, і її за умови, що U-Z являє собою циклогексан, оптичних ізомерів і фармацевтично прийнятних якщо, щонайменше, один з -(А)n-(CR1R2)m-, Rp, Rq, адитивних солей кислот або основ у виробництві Rr i Rs являє собою лінійний або розгалужений лікарського засобу для використання в будь-якому нижчий алкеніл(С2-С6) або лінійний або розгалутакому способі; і жений нижчий алкініл(С2-С6); фармацевтична композиція, що містить сполуі її оптичні ізомери і фармацевтично прийнятні ку, вибрану зі сполук формули І: адитивні солі кислот або основ, в комбінації з одним або більшою кількістю фармацевтично прийнятних розріджувачів, наповнювачів і/або носіїв. ДОКЛАДНИЙ ОПИС ВИНАХОДУ Подальші деталі і докладні приклади наведені тільки для ілюстрації і не є обмежувальними. Схема: приклади 1 і 2 де: 1 2 3 4 - R* означає -(A)n-(CR R )m-NR R ; - n+m=0, 1 або 2; - А вибраний з групи, що містить лінійний або розгалужений нижчий алкіл (С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R1 і R2 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл(С1-С6), лінійний або розгалужений нижчий алкеніл(С2-С6) і лінійний або розгалужений нижчий алкініл(С2-С6); - R3 і R4 незалежно вибрані з групи, що містить водень, лінійний або розгалужений нижчий алкіл (С1-С6), лінійний або розгалужений нижчий алкеПриклад 1 23 75478 24 Гідрохлорид 3,3,5,5-тетраметил-111Гц, -HC=) i 6,7 (1H, шир.c, NH). вінілциклогексанаміну (5) d) Гідрохлорид 3,3,5,5-тетраметил-1a) Етил 2-(3,3,5,5вінілциклогексанаміну (5) тетраметилциклогексиліден)ацетат (2) Суміш аміду 4 (0,32г, 1ммоль) з порошком До розчину, що перемішується, триетилфосNaOH (0,4г, 10ммоль) в ДМСО (3мл) перемішують фоноацетату (49,32г, 222ммоль) в безводному протягом 7 днів при кімнатній температурі. РеакТГФ (180мл) в атмосфері аргону додають NaH ційну суміш розбавляють Н2О (20мл) і перемішу(8,8г, 222ммоль, 60% суспензія в мінеральному ють протягом ночі при кімнатній температурі. Промаслі) невеликими порціями при охолоджуванні дукт екстрагують гексаном (3 10мл). Об'єднані крижаною водою. Перемішування продовжують екстракти промивають насиченим розчином солі протягом 1год. при кімнатній температурі, потім (20мл), сушать над NaOH і фільтрують через шар додають розчин 3,3,5,5-тетраметилциклогексанону целіту. До одержаного розчину додають 4Μ НСl в (30,85г, 200ммоль) протягом 10хв. і одержану субезводному діетиловому ефірі (0,5мл) і розчинник міш кип'ятять із зворотним холодильником протявипаровують. Залишок обробляють ацетонітрилом гом 22год. Потім її виливають на лід (400г) і про(10мл), а осад відфільтровують і сушать над Р2О5 дукт екстрагують діетиловим ефіром (4 150мл), у вакуумі, одержуючи 5 (0,12г, 53%) у вигляді безекстракти сушать над MgSO4. Після випаровуванбарвної твердої речовини. 1Н-ЯМР (CDCl3, TMS), ня розчинника у вакуумі маслянистий залишок м.ч.: 0,98 і 1,01 (всього 12Н, обидва с, 3,5-СН3); переганяють при 145°С (11мм рт.ст.), одержуючи 1,19 і 1,29 (всього 2Н, обидва д, 14Гц, 4-СН2); 1,62 36,8г (86%) 2 у вигляді олії. 1Н-ЯМР (CDCl3, TMS), (2Н, д, 13,5Гц, 2,6-СН2); 1,72 (2Н, шир.с, Н2О); 2,16 м.ч.: 0,96 і 0,98 (всього 12Н, обидва с, 3,5-СН3); (2Н, д, 13,5Гц, 2,6-СН2); 5,46 і 5,73 (2Н, обидва д, 1,27 (3Н, т, СН3-етил); 1,33 (2Н, м, 4-СН2); 1,95 і 18 і 11Гц, =СН2); 6,16 (1Н, дд, 18 і 11Гц, =СН) і 8,24 2,65 (всього 4Н, обидва с, 2,6-СН2); 4,14 (2Н, кв, (3Н, шир.с, NH3+). СН2-етил) і 5, 69 (1H, с, =Н). Приклад 2 b) 2-(3,3,5,5Гідрохлорид Н3,3,5,5-пентаметил-1тетраметилциклогексиліден)етанол (3) вінілциклогексиламіну (7) До розчину, що перемішується, LiAlH4 (1,7г, а) Метил 3,3,5,5-тетраметил-145ммоль) в безводному ефірі (60мл) додають кравінілциклогексилкарбамат (6) Суміш гідрохлориду плями розчин ацетату 2 (3,2г, 15ммоль) в ефірі аміну 5 (0,25г, 1,2ммоль) і Na2CO3 (0,73г, (20мл) при охолоджуванні крижаною водою. Пе6,9ммоль) в ТГФ (6мл) перемішують при кімнатній ремішування продовжують протягом 1год. і LiAlH4, температурі 1год. Додають метилхлорформіат що залишився, розкладають водою. Водний шар (0,27г, 3,45ммоль) і реакційну суміш перемішують відділяють і двічі екстрагують ефіром (30мл). при кімнатній температурі протягом 15 год. Суміш Об'єднані екстракти промивають насиченим розрозбавляють діетиловим ефіром (20мл), фільтручином солі (50мл) і сушать над MgSO4. Після конють і випаровують досуха. Неочищений продукт центрування у вакуумі маслянистий залишок очиочищають методом флеш-хроматографії на силіщають перегонкою в апараті Kugelrohr з короткою кагелі (легкий петролейний ефір-етилацетат, 10:1), насадкою (150-170°С, 11мм рт.ст.), одержуючи 3 одержуючи 6 (0,24г, 87%) у вигляді безбарвної (2,3г, 89%) у вигляді олії. 1H-ЯМР (CDCl3, TMS), твердої речовини з т.пл. 61-63°С. 1Н-ЯМР (CDCl3, м.ч.: 0,92 (6Н, с, 3, 5-СН3); 1,10 (1Н, шир.с, ОН); TMS), м.ч.: 0,92 і 1,15 (всього 12Н, обидва с, 3,51,28 (2Н, с, 4-СН2); 1,87 і 1,94 (всього 4Н, обидва с, СН3); 1,00-1,40 (4Н, м, 4-СН2 і 2,6-СН); 2,00 (2Н, д, 2,6-СН2); 4,16 (2Н, д, 7Гц, СН2О) і 5,50 (1H, т, 7Гц, 14Гц, 2,6-СН); 3,62 (3Н, с, CH3N); 4,72 (1H, шир.с, =С-Н). NH); 5,00 і 5,06 (всього 2Н, обидва д, 10,5 і 17Гц, с) 2,2,2-трихлор-N-(3,3,5,5-тетраметил-1=СН2) і 5,83 (1Н, дд, 10,5 і 17Гц, =СН). вінілциклогексил)ацетамід(4) b) ГідрохлоридК,3,3,5,5-пентаметил-1До розчину спирту 3 (0,8г, 4,7ммоль) в діетивінілциклогексиламіну (7) ловому ефірі (5мл) додають NaH (0,22г 55% дисСуміш LiAlH4 (0,28г, 7,4ммоль) і карбамату 6 персії в мінеральному маслі (0,22ммоль)). Реак(0,22г, 0,92ммоль) в ТГФ (22мл) кип'ятять із звороційну суміш охолоджують до -10°С і додають тним холодильником протягом 12год. Потім її охокраплями розчин трихлорацетонітрилу (0,68г, лоджують на бані з льодом і додають краплями 4,7ммоль) в діетиловому ефірі (3мл). Розчину даводу (20мл). Одержану суспензію екстрагують гекють нагрітись до кімнатної температури і випаросаном (3 20мл) і об'єднані екстракти промивають вують розчинник. Додають до залишку пентан насиченим розчином солі (20мл). Екстракт сушать (8мл), що містить метанол (0,018мл). Одержану над NaOH, фільтрують і обробляють 2,4Μ розчисуміш фільтрують через шар целіту і випаровують. ном НСl в діетиловому ефірі (1мл). Одержану суМасло, що залишилось, розчиняють в ксилолі спензію випаровують досуха. Залишок обробля(10мл) і кип'ятять із зворотним холодильником ють діетиловим ефіром (10мл) і ацетонітрилом протягом 10год. Основну кількість ксилолу відга(1мл). Осад відфільтровують і сушать у вакуумі няють при зниженому тиску (11мм рт.ст.) і залишок над Р2О5, одержуючи 7 (0,11г, 52%) у вигляді без1 очищають методом флеш-хроматографії на силібарвної твердої речовини. Н-ЯМР (CDCl3, TMS), кагелі (гексан, гексан-етилацетат, 10:1), одержуюм.ч.: 1,00 і 1,02 (всього 12Н, обидва с, 3,5-СН3); чи 4 (0,98г, 66%) у вигляді олії. 1Н-ЯМР (CDCl3, 1,23 і 1,32 (всього 2Н, обидва д, 15Гц, 4-СН2); 1,72 TMS), м.ч.: 0,95 (6Н, с, 3,5-СН3); 1,18 (6Н, с, 3,5(2Н, д, 13Гц, 2,6-СН); 2,15 (2Н, д, 13Гц, 2,6-СН); СН3); 1,1-1,5 (2Н, м, 4-СН2); 1,32 (2Н, д, 15Гц, 2,62,45 (3Н, т, 5Гц, CH3N); 5,64 і 5,69 (всього 2Н, обиСН2); 2,15 (2Н, д, 15Гц, 2,6-СН2); 5,08 (1H, д, 11Гц, два д, 11 і 17Гц, =СН2); 5,98 (1Н, дд, 11 і 17Гц, =СН2); 5,13 (1Н, д, 18Гц, =СН2); 5,85 (1Н, дд, 18 і =СН) і 9,30 (2Н, шир.с, NH3+). 25 Схема: приклади 3 і 4 75478 26 (гексан)) дає 0,425 г (20,3%) азиду 10 у вигляді безбарвної олії. 1H-ЯМР (CDCl3, TMS), м.ч.: 0,91 (6Н, с), 0,94 (3Н, с) і 0,96 (3Н, с, 3',5'-СН3); 1,23 (3Н, д, 6,5Гц, 1-СН3); 1,26 (2Н, с, 4'-СН2); 1,89 (2Н, с) і 1,96 (2H, с, 2',6'-СН2); 4,31 (1Н, дкв, 6,5 і 9,5Гц, 1СН) і 5,21 (1H, дм, 9,5Гц, =СН). с) Гідрохлорид 1-аліл-3,3,5,5тетраметилциклогексанаміну (11) Розчин азиду 9 (0,221г, 1,0ммоль) в безводному ефірі (4мл) додають краплями до суспензії, що перемішується, літійалюмінійгідриду (0,152г, 4ммоль) в ефірі (10мл) за 10хв. Суміш перемішують протягом 4год., потім обробляють 20% водним NaOH (8мл). Водний шар відділяють і екстрагують діетиловим ефіром (2 15мл). Об'єднані органічні екстракти промивають насиченим розчином солі і сушать над NaOH. Профільтрований розчин обробляють безводним розчином НСl в діетиловому ефірі і випаровують. До твердого залишку додають безПриклад 3 водний діетиловий ефір, відфільтровують і промиГідрохлорид 1-аліл-3,3,5,5вають безводним ефіром, одержуючи 11 (0,105г, тетраметилциклогексанаміну (11) 47%) у вигляді безбарвної твердої речовини. 1Ha) 1-аліл-3,3,5,5-тетраметилциклогексанол (8) ЯМР (CDCl3, TMS), м.ч.: 1,03 (6Н, с, 3,5-CH3eq); До 1Μ ефірного розчину, що перемішується, 1,06 (6Н, с, 3,5-СН3ах); 1,29 (2Н, с, 4-СН2); 1,63 (2Н, алілмагнійброміду (60мл, 60ммоль) додають крапд, 13Гц, 2,6-СНах); 1,80 (2Н, д, 13Гц, 2,6-CHeq), 2,71 лями розчин 3,3,5,5-тетраметилциклогексанону (2Н, д, 7Гц, СН2О); 5,10-5,40 (2Н, м, =СН2); 5,75(3,86г, 25ммоль) в безводному ефірі (20мл). Суміш 6,25 (1Н, м, =СН) і 8,25 (3Н, шир.с, NH3+). перемішують 1год. при температурі навколишньоПриклад 4 го середовища і кип'ятять із зворотним холодильГідрохлорид 1-(3,3,5,5ником протягом 10хв. Потім її охолоджують крижатетраметилциклогексиліден)-2-пропанаміну (24) ною водою і обережно розтирають в насиченому Розчин 1-метил-2-(3,3,5,5водному NH4Cl (40мл). Органічний шар відділяють тетраметилциклогексиліден)етилазиду (10) (0,33г, і промивають водою і насиченим розчином солі. 1,5ммоль) в безводному діетиловому ефірі (4мл) Після сушіння над безводним MgSO4 розчин кондодають краплями до суспензії, що перемішуєтьцентрують у вакуумі. Виконують фракційну переся, літійалюмінійгідриду (0,152г, 4ммоль) в ефірі гонку залишку при зниженому тиску, одержуючи (15мл) за 10хв. Дану суміш перемішують протягом 1 3,5г (72%) 8 з т. кип.98-100°С/12мм рт. ст. H-ЯМР 4год., потім обробляють її 20% водним NaOH (CDCl3, TMS), м.ч.: 0,88 (6Н, с, 3,5-CH3eq); 1,20 (6Н, (8мл). Водний шар екстрагують ефіром (2 15мл). с, 3, 5-СН3ах); 0,95-1,60 (6Н, м, 2,4,6-СН2); 2,15 (2Н, Органічні екстракти об'єднують, промивають насид, 7,5Гц, СН2С=); 4,95-5,30 (2Н, м, =СН2) і 5,65-6,20 ченим розчином солі і сушать над NaOH. Профіль(1Н, м, =СН). трований розчин обробляють безводним розчином b) 1-аліл-1-азидо-3,3,5,5НСl в ефірі і випаровують у вакуумі. Додають безтетраметилциклогексан (9) і 1-метил-2-(3,3,5,5водний ефір до твердого залишку, відфільтровутетраметилциклогексиліден)етилазид (10) ють і промивають безводним ефіром, одержуючи До розчину циклогексанолу 8 (1,96г, 10ммоль) 24 (0,18г, 54%) у вигляді безбарвної твердої речов безводному бензолі (20мл) в атмосфері аргону вини. 1H-ЯМР (CDCl3, TMS), м.ч.: 0,89 (6Н, с), 0,92 додають азидотриметилсилан (12ммоль). До да(3Н, с) і 0,98 (3Н, с, 3', 5'-СН3); 1,27 (2Н, с, 4'-СН2); ного охолодженого (5°С) розчину повільно дода1,47 (3Н, д, 6,5Гц, 3-СН3); 1,84 (1H, д, 13,5Гц, 2'ють BF3*OEt2 (12ммоль) за допомогою шприца за СН); 1,87 (2Н, с, 6'-СН2), 2,06 (1Н, д, 13,5Гц, 2'-СН); 20хв. Суміш перемішують протягом 6год., потім 4,17 (1Н, дкв, 6,5 і 9,5Гц, 2-СН); 5,35 (1Н, д, 9,5Гц, повільно додають воду. Органічний шар відділя=СН) і 8,25 (3Н, шир.с, NH3+). ють і промивають насиченим водним NaHCO3 і Схема: приклади 5, 6 і 7 насиченим розчином солі і сушать над MgSO4. Фільтрація і випаровування розчинника при підтриманні температури нижче 25°С дають олію, яку виділяють методом колонкової хроматографії на силікагелі (легкий петролейний ефір). Фракцію з Rf 0,85 (гексан) збирають. Випаровування розчинника дає 9 у вигляді безбарвної олії (0,26г, 11,7%). 1НЯМР (CDCl3, TMS), м.ч.: 0,89 (6Н, с, 3,5-CH3eq); 0,90 (1H, д, 14Гц, 4-СНах); 1,05 (2Н, д, 14Гц, 2,6СНах); 1,18 (6Н, с, 3,5-СН3ах); 1,37 (1Н, д, 14Гц, 4CHeq); 1,60 (2Н, д, 14Гц, 2,6-CHeq), 2,29 (2Н, д, 7Гц, Приклад 5 СН2С=); 4,95-5,25 (2Н, м, =СН2) і 5,65-6,15 (1Н, м, Гідрохлорид 1-(1-аліл-3,3,5,5=СН). тетраметилциклогексил)піперидину (13) Випаровування додаткової фракції (Rf 0,65 a) 1-(3,3,5,5-тетраметил-1-циклогексеніл 27 75478 28 1)піперидин (12) СН2СС); 2,85-3,10 (2Н, м, піперидин 2,6-СН); 3,69 Одержують конденсацією піперидину (1,2 екві(2Н, д, 10,2Гц, піперидин 2,6-СН) і 11,12 (1Н, валенти) і 3,3,5,5-тетраметилциклогексанону при шир.с, NH). нагріванні в бензолі з азеотропним видаленням Схема: приклади 8 і 9 води. Неочищений продукт одержують видаленням вихідних речовин в умовах вакуумної перегонки (100°С/10мм рт.ст.). Янтарна олія. 1Н-ЯМР (CDCI3, TMS), м.ч.: 0,94 (6Н, с) і 0,97 (6Н, с, 3', 5'СН3); 1,25 (2Н, с, 4'-СН2); 1,40-1,70 (6Н, м, піперидин 3,4,5-СН2); 1,76 (2Н, с, 6'-СН2); 2,60-2,85 (4Н, м, піперидин 2,6-СН2) і 4,40 (1Н, с, =СН). b) Гідрохлорид 1-(1-аліл-3,3,5,5тетраметилциклогексил)піперидину (13) До розчину енаміну 12 (2,1г, 9ммоль) в ТГФ (20мл) додають оцтову кислоту (0,675г, 11,25ммоль). Суміш перемішують протягом 5 хв. і додають цинковий порошок (0,74г, 11,25мгА). Потім додають краплями розчин алілброміду (1,63г, Приклад 8 13,5ммоль) в ТГФ (5мл) і суміш перемішують при Гідрохлорид 2-(3,3,5,5-тетраметил-1температурі навколишнього середовища протягом вінілциклогексил)етанаміну (19) 6 год. Додають водний Na2CO3 і одержану суміш a) Етил 2-(3,3,5,5-тетраметил-1екстрагують ефіром. Екстракт промивають насивінілциклогексил)ацетат (16) ченим розчином солі, сушать над безводним Суміш триетилортоацетату (18,6мл, MgSO4 і концентрують у вакуумі. Залишок виділя102ммоль), 2-(3,3,5,5ють методом колонкової хроматографії на силікатетраметилциклогексиліден)етанолу (3) (4,63г, гелі (гексан, 5% ЕtOАс в гексані). Фракцію з Rf 0,85 25,4ммоль) і пропіонової кислоти (0,19мл, (гексан-ЕtOАс, 13:2) збирають, випаровують і об2,5ммоль) нагрівають при 145°С протягом 10год. В робляють безводним розчином НСl в ефірі. Осад ході реакції з суміші відганяють етанол. Реакційну відфільтровують і промивають сумішшю гексансуміш охолоджують і виливають у воду (100мл). ЕtOАс, одержуючи 13 (0,79г, 29%) у вигляді безбаВодну фазу екстрагують гексаном (2 50мл) і об'єрвної твердої речовини. 1Н-ЯМР (CDCl3, TMS), днані органічні фази промивають 5% водним м.ч.: 1,07 (6H, с, 3',5'-CH3eq), 1,10 (6H, с, 3', 5'KHSO4 (50мл) і насиченим розчином солі (50мл). СН3ах); 1,34 (1H, д, 12,2Гц) і 1,45 (1H, д, 12,2Гц, 4'Екстракт сушать над MgSO4, фільтрують і випароСН2); 1,70-1,95 (6Н, м, 2',6'-СНах і піперидин 3,5вують. Залишок очищають методом флешСН, 4-СН2-); 2,37 (2Н, д, 13,4Гц, 2', 6'-CHeq); 2,40хроматографії на силікагелі (легкий петролейний 2,70 (2Н, м, піперидин 3,5-СН); 2,76 (2Н, д, 7,2Гц, ефір і легкий петролейний ефір-етилацетат, СН2С=); 2,75-3,00 (2Н, м, піперидин 2,6-СН); 3,64 100:2), одержуючи 16 (4,64г, 73%) у вигляді олії. 1 (2Н, д, 11,6Гц, піперидин 2,6-СН); 5,13 (1Н, д, H-ЯМР (CDCl3, TMS), м.ч.: 0,91 (6Н, с, 3,5-СН3); 9,6Гц) і 5,24 (1H, д, 17,8Гц, =СН2); 5,85-6,15 (1Н, м, 1,01 (6Н, с, 3,5-СН3); 1,23 (3Н, т, 7Гц, етил СН3) =СН) і 10,72 (1Н, шир.с, NH). 1,00-1,30 (4Н, м, 4-СН2 і 2,6-СН); 1,86 (2Н, д, 13Гц, Приіслад 6 2,6-СН); 2,22 (2Н, с, СН2С=О); 4,08 (2Н, кв, 7Гц, Гідрохлорид 1-[3,3,5,5-тетраметил-1-(3-метилетил СН2); 5,06 і 5,07 (всього 2Н, обидва д, 11 і 2-бутеніл)циклогексил]-піперидину (14) 17,5Гц, =СН2) і 5,95 (1Н, дд, 11 і 17,5Гц, -СН=). Одержують з піперидину 12 згідно з методиb) 2-(3,3,5,5-тетраметил-1кою для сполуки 13 (приклад 5, b), використовуючи вінілциклогексил)оцтова кислота (17) 4-бром-2-метил-2-бутен замість алілброміду. ВиРозчин NaOH (1,03г, 25,8ммоль) і ацетату 16 хід: 20%. 1H-ЯМР (CDCl3, TMS), м.ч.: 1,07 і 1,08 (1,3г, 5,15ммоль) в метанолі (26мл) кип'ятять із (всього 12Н, обидва с, 3',5'-СН3), 1,32 і 1,44 (2Н, зворотним холодильником протягом 3год. Суміш обидва д, 14,2Гц, 4'-СН2); 1,69 і 1,76 (6Н, обидва с, охолоджують до кімнатної температури і вилива=С(СН3)2); 1,68-1 96 (4Н, м, 3,5-СН і 4-СН2.); 1,84 ють у воду (100мл). Водну фазу підкисляють кон(2Н, д, 13,4Гц, 2', 6'-СНах); 2,31 (2Н, д, 13,4Гц, Т, 6'центрованою водною НСl і екстрагують гексаном CHeq); 2,40-2,80 (4Н, м, N(CH)2, 3,5-СН); 2,60 (2H, д, (3 30мл). Об'єднані органічні фази промивають 7,2Гц, СН2С=); 3,63 (2Н, д, 10,4Гц, N(CH)2); 5,31 насиченим розчином солі, сушать над СаСl2, філь(1Н, т, 6,8Гц, =СН) і 10,55 (1H, шир.с, NH). трують і випаровують. Залишок очищають метоПриклад 7 дом флеш-хроматографії на силікагелі (легкий Гідрохлорид 1-[3,3,5,5-тетраметил-1-(2петролейний ефір-етилацетат, 10:1), одержуючи пропініл)циклогексил]піперидину (15) 17 (0,7г, 71%) у вигляді безбарвної твердої речоОдержують з піперидину 12 згідно з методивини з т.пл. 92-94°С. 1H-ЯМР (CDCI3, TMS), м.ч.: кою для сполуки 13 (приклад 5, b), використовуючи 0,92 (6Н, с, 3,5-СН3); 1,02 (6Н, с, 3,5-СН3); 1,001 3-бромпропін замість алілброміду. Вихід: 6%. H1,30 (4Н, м, 4-СН2 і 2,6-СН); 1,90 (2Н, д, 14Гц, 2,6ЯМР (CDCl3, TMS), м.ч.: 1,07 (6Н, с, 3', 5'-CH3eq), СН); 2,27 (2Н, с, СН2С=О); 5,11 і 5,13 (всього 2Н, 1,11 (6Н, с, 3', 5'-СН3ах); 1,23 і 1,44 (всього 2Н, обиобидва д, 11 і 18Гц, =СН2); 5,99 (1Н, дд, 18 і 11Гц, два д, 14,3Гц, 4'-СН2); 1,75-2,00 (4Н, м, піперидин =СН) і 10,80 (1Н, шир.с, СООН). 3,5-СН, 4-СН2'); 1,91 (2Н, д, 13,2Гц, 2', 6'-СНах); c) 2-(3,3,5,5-тетраметил-12,28 (1H, с, НСС); 2,34 (2Н, д, 13,2Гц, 2', 6'-CHeq); вінілциклогексил)ацетамід (18) 2,40-2,70 (2Н, м, піперидин 3,5-СН); 2,81 (2Н, с, N-гідроксисукцинімід (0,25г, 2,2ммоль) і N, N' 29 75478 30 дициклогексилкарбодіімід (0,45г, 2,2ммоль) доданої твердої речовини. 1H-ЯМР (CDCl3, TMS), м.ч.: ють до розчину циклогексилоцтової кислоти 17 0,90 і 0,92 (всього 12Н, обидва с, циклогексан-3,5(0,45г, 2ммоль) в ТГФ (5мл). Суміш перемішують СН3); 1,23 (2Н, с, циклогексан-4-СН2); 1,86 і 1,92 протягом 18год. при кімнатній температурі і охоло(всього 4Н, обидва с, циклогексан-2,6-СН2); 2,49 джують на бані з льодом. Додають однією порцією (2Н, кв, 7Гц, пропанамін-2-СН2); 2,98 (2Н, т, 7Гц, 25% водний NH4OH (2мл) і суміш перемішують при пропанамін-1-СН2); 5,15 (1H, т, 7Гц, =СН-) і 8,30 кімнатній температурі протягом 2год. Осадок від(3Н, шир. с, NH3+). фільтровують і промивають діетиловим ефіром Схема: приклади 10 і 11 (30мл). Органічну фазу фільтрату відділяють і промивають 5% водної KHSO4 (10мл) і насиченим розчином солі. Екстракт сушать над MgSO4, фільтрують і випаровують. Залишок очищають методом флеш-хроматографії на силікагелі (легкий петролейний ефір-етилацетат, від 4:1 до 1:1), одержуючи 18 (0,34г, 76%) у вигляді безбарвної твердої речовини з т.пл. 44-46°С. 1H-ЯМР (CDCl3, TMS), м.ч.: 0,91 (6Н, с, 3,5-СН3); 1,02 (6Н, с, 3,5СН3); 1,00-1,30 (4Н, м, 4-СН2 і 2,6-СН); 1,85 (2Н, д, Приклад 10 14Гц, 2,6-СН); 2,13 (2Н, с, СН2С=О); 5,18 і 5,19 Гідрохлорид 2-(3,3,5,5(всього 2Н, обидва д, 18 і 11Гц, =СН2); 5,40 і 5,60 тетраметилциклогексиліден)етанаміну (22) (всього 2Н, обидва шир.с, NH2) і 6,03 (1Н, дд, 18 і a) 3,3,5,511Гц, =СН). тетраметилциклогексиліденацетонітрил (20) d) Гідрохлорид 2-(3,3,5,5-тетраметил-160% дисперсію NaH в мінеральному маслі вінілциклогексил)етанаміну (19) (0,96г, 24ммоль) додають до розчину діетилціаноСуміш LiAlH4 (0,41г, 11ммоль) і аміду 18 (0,30г, метилфосфонату (4,25г, 24ммоль) в ТГФ (30мл) 1,4ммоль) в ТГФ (18мл) кип'ятять із зворотним при охолоджуванні водою з льодом. Суміш перехолодильником протягом 17год. Потім її охоломішують 30хв. і додають краплями розчин 3,3,5,5джують на бані з льодом і додають краплями воду тетраметилциклогексанону (3,08г, 20ммоль) в ТГФ (30мл). Одержану суспензію екстрагують гексаном (10мл). Охолоджуючу баню прибирають і перемі(3 30мл) і об'єднані органічні фази промивають шують суміш при кімнатній температурі протягом насиченим розчином солі. Екстракт сушать над 72год. Виливають її в крижану воду (100мл) і екстNaOH, фільтрують і концентрують до об'єму -10 рагують діетиловим ефіром (3 50мл). Об'єднані мл. Додають 4,8Μ розчин НСl в діетиловому ефірі органічні фази промивають насиченим розчином (1мл) і одержану суспензію випаровують досуха. солі, сушать над MgSO4, фільтрують і випаровуЗалишок обробляють ацетонітрилом (5мл), осад ють. Неочищений продукт очищають методом відфільтровують і сушать у вакуумі над NaOH, флеш-хроматографії на силікагелі (легкий петроодержуючи 19 (0,16г, 50%) у вигляді безбарвної лейний ефір-етилацетат, 10:1), одержуючи 20 твердої речовини. 1H-ЯМР (CDCl3, TMS), м.ч.: 0,89 (2,38г, 71%) у вигляді безбарвної олії. 1Н-ЯМР (6Н, с, 3,5-СН3); 1,02 (6Н, с, 3,5-СН3); 0,90-1,80 (8Н, (CDCl3, TMS), м.ч.: 0,97 і 1,01 (всього 12Н, обидва м, кільцеві протони і етанамін-2-СН2); 2,92 (2Н, с, 3',5'-СН3); 1,36 (2Н, с, 4'-СН2); 2,01 (2Н, с, 2'шир.с, CH2N); 5,05 і 5,15 (2Н, обидва д, 18 і 11Гц, СН2); 2,26 (2Н, с, 6'-СН2) і 5,14 (1H, с, =СН). =СН2); 5,77 (1H, дд, 18 і 11Гц, =СН) і 8,10 (3Н, b) Гідрохлорид 2-(3,3,5,5шир.с, NH3+). тетраметилциклогексиліден)етанаміну (22) Приклад 9 Суспензію LiAlH4 (0,68г, 18ммоль) в діетилоГідрохлорид 3-(3,3,5,5вому ефірі (30мл) охолоджують на бані з льодом і тетраметилциклогексиліден)пропанаміну (32) додають 1Μ розчин ZnCl2 в діетиловому ефірі Триетиламін (0,25мл, 1,76ммоль) і дифеніл(9мл, 9ммоль). Одержану суміш перемішують профосфорилазид (0,38мл, 1,76ммоль) додають до тягом 15хв. і додають краплями розчин нітрилу 20 розчину кислоти 17 (0,36г, 1,6ммоль) в бензолі (1г, 6ммоль) в діетиловому ефірі (30мл), підтри(6мл). Суміш кип'ятять із зворотним холодильнимуючи температуру 0-5°С. Потім баню з льодом ком протягом 2год., охолоджують до кімнатної теприбирають і суміш перемішують при кімнатній мператури і випаровують досуха. Додають до затемпературі протягом 24год. Додають воду (30мл) лишку холодну (~5°С) концентровану водну НСl і 20% водний NaOH (20мл) при охолоджуванні на (3мл). Одержану суміш перемішують при кімнатній бані з льодом. Водну фазу екстрагують діетилотемпературі протягом 18год. і роблять сильнолужвим ефіром (4 50мл). Об'єднані органічні фази ною, додаючи 10% водний NaOH. До суміші додапромивають насиченим розчином солі (50мл), сують гексан (20мл) і обидві фази фільтрують. Осад шать над NaOH, фільтрують і випаровують. Залипромивають гексаном (2 5мл) і водою (2 5мл). шок очищають перегонкою в апараті Kugelrohr з Органічну фазу фільтрату відділяють. Водну фазу короткою насадкою при 160°С/20мм рт.ст. Дистипромивають гексаном (2 10мл). Об'єднані органічлят розбавляють діетиловим ефіром і додають ні фази промивають насиченим розчином солі 4,8Μ розчин НСl в діетиловому ефірі (3мл). Одер(10мл), сушать над NaOH і фільтрують. Додають жаний осад відфільтровують, промивають діети4,8Μ розчин НСl в діетиловому ефірі (1мл) і одерловим ефіром (3 5мл) і сушать у вакуумі над жану суспензію випаровують. Залишок перекрисNaOH, одержуючи 22 у вигляді безбарвної твердої талізовують з ацетонітрилу і сушать у вакуумі над речовини. 1H-ЯМР (CDCl3,TMS), м.ч.: 0,91 і 0,92 Р2О5, одержуючи 32 (0,1г, 43%) у вигляді безбарв 31 75478 32 (всього 12Н, обидва с, 3', 5'-СН3); 1,28 (2Н, с, 4'b) (E,Z)-1-метил-2-(3,3-діетил-5,5СН2); 1,89 і 1,93 (всього 4Н, обидва с, 2',6'-СН2); диметилциклогексиліден)етилазид (27) Одержу3,62 (2Н, д, 7Гц, CH2N); 5,41 (1H, т, 7Гц, -С=СН) і ють з циклогексанолу 26 згідно з методикою для 8,3 (ЗН, шир.с, ΝΗ3+). сполук 9 і 10 Приклад 11 (приклад З, Ь). Азид 27 одержують у вигляді Гідрохлорид 2-(3,3,5,5безбарвної олії з виходом 15%. Ή-ЯМР (CDC13, тетраметилциклогексиліден)пропанаміну (23) TMS), м.ч.: 0,73 і 0,74 (всього 6Н, обидва т, 7Гц, a) 2(3,3,5,52СН3 етил); 0,91, 0,94 і 0,97 (всього 6Н, всі с, 5і, 5'тетраметилциклогексиліден)пропіонітрил (21) СН3); 1,10-1,45 (4Н, м, 2СН2 етил); 1,22 (ЗН, д, Одержують згідно з методикою для сполуки 20 6,5Гц, 1-СН3); 1,26 (2Н, с, 4'-СН2); 1,89 (2Н, с) і 1,97 (приклад 10, а), використовуючи діетил(1(2Н, м, 2і, 6'-СН2); 4,08-4,48 (Ш, м, 1-СН) і 5,18 (Ш, ціаноетил)фосфонат. Нітрил 21 одержують у видм, 9,5Гц, =СН). гляді безбарвної олії з виходом 41%. 1Н-ЯМР c) Гідрохлорид (Е,2)-1-(3,3-діетил-5,5(CDCl3, TMS), м.ч.: 0,96 і 1,00 (всього 12Н, обидва диметилциклогексиліден)-2-пропанаміну (28) с, циклогексан-3,5-СН3); 1,34 (12Н, с, циклогексанОдержують з азиду 27 згідно з методикою для 4-СН2); 1,91 (3Н, с, пропіонітрил-3-СН3); 2,04 і 2,28 сполуки 24 (приклад 4). Гідрохлорид аміну 28 оде(всього 4Н, обидва с, циклогексан-2,6-СН2). ржують у вигляді безбарвної твердої речовини з b) Гідрохлорид 2-(3,3,5,5виходом 16%. 1Н-ЯМР (CDCl3, TMS), м.ч.: 0,72 (6Н, тетраметилциклогексиліден)пропанаміну (23) шир.т, 7Гц, 2СН3 етил), 0,90, 0,92 і 0,98 (всього 6Н, Одержують з нітрилу 21 згідно з методикою всі с, 5', 5'-СН3); 1,25 (6Н, м, 4'-СН2 і 2СН2 етил); для сполуки 22 (приклад 10, b). 1,47 (3Н, д, 6,5Гц, 2-СН3); 1,70-2,25 (2Н, шир. АВ Гідрохлорид аміну 23 одержують у вигляді кв, 13Гц, 2'-СН2); 1,87 (2Н, с, 6'-СН2), 4,18 (1H, м, 2безбарвної твердої речовини. 1Н-ЯМР (CDCl3, СН); 5,34 (1H, шир.д, 9,5Гц, =СН) і 8,38 (3Н, шир.с, TMS), м.ч.: 0,92 і 0,93 (всього 12Н, обидва с, цикNH3+). логексан-3,5-СН3); 1,27 (2Н, с, циклогексан-4-СН2); Схема: приклад 13 1,89 (3Н, с, пропанамін-3-СН3); 1,99 і 2,01 (всього 4Н, обидва с, циклогексан-2,6-СН2); 3,64 (2Н, шир.с, пропанамін-1-СН2) і 8,40 (ЗН, шир.с, NH3+). Схема: приклад 12 Приклад 12 Гідрохлорид (Ε,Ζ)1-(3,3-діетил-5,5диметилциклогексиліден)-2-пропанаміну (28) а) 1-аліл-3,3-діетил-5,5-диметилциклогексанол (26) До 1Μ ефірного розчину, що перемішується, алілмагнійброміду (20мл, 20ммоль) додають краплями розчин 3,3-діетил-5,5диметилциклогексанону (25) (1,47г, 8,06ммоль) в безводному ефірі (5мл). Дану суміш перемішують протягом 1год. при температурі навколишнього середовища і кип'ятять із зворотним холодильником 10хв. Потім її охолоджують крижаною водою і обробляють насиченим водним NH4Cl (40мл). Органічний шар відділяють і промивають водою і насиченим розчином солі. Після сушіння над безводним MgSO4, розчин концентрують у вакуумі. Залишок очищають методом колонкової хроматографії на силікагелі (легкий петролейний ефір). Фракцію з Rf 0,7 (гексан:ЕtOАс, 13:2) збирають. Випаровування розчинника дає 26 (1,35г, 74%) у вигляді безбарвної олії. 1H-ЯМР (CDCl3, TMS), м.ч.: 0,74 (6Н, т, 7Гц, 2СН3 етил); 0,88 (3Н, с, 5CH3eq); 1,19 (3Н, с, 5-СН3ах); 0,80-2,05 (10Н, м, 2,4,6-СН2 і 2СН2 етил); 2,14 (2Н, д, 7Гц, СН2О); 4,95-5,30 (2Н, м, =СН2) і 5,65-6,20 (1H, м, =СН). Приклад 13 Гідрохлорид 2-метил-1-(3,3,5,5тетраметилциклогексиліден)-2-пропанаміну (31) a) 2-метил-1-(3,3,5,5тетраметилциклогексиліден)-2-пропанол (29) Розчин ацетату 2 (2,14г, 10ммоль) в діетиловому ефірі (20мл) додають до 1,6Μ розчину MeLi в діетиловому ефірі (26мл, 40ммоль) при охолоджуванні на бані з льодом. Реакційну суміш перемішують при кімнатній температурі протягом 1год. Потім її охолоджують на бані з льодом і додають краплями насичений водний NH4Cl (20мл). Водну фазу екстрагують діетиловим ефіром (2 30мл). Об'єднані органічні фази промивають насиченим розчином солі (30мл), сушать над MgSO4, фільтрують і випаровують. Залишок очищають перегонкою в апараті Kugelrohr з короткою насадкою (100°С/4мм рт.ст.), одержуючи 29 (1,86г, 86%) у вигляді безбарвної олії. 1H-ЯМР (CDCl3, TMS), м.ч.: 0,91 і 0,96 (всього 12Н, обидва с, циклогексан-3,5-СН3), 1,25 (2Н, с, циклогексан-4-СН2); 1,38 (6Н, с, -С(СН3)2О); 1,79 і 2,23 (обидва 2Н, обидва с, циклогексан-2,6-СН2) і 5,39 (1Н, с, =СН-). b) 2-азидо-2-метил1-(3,3,5,5тетраметилциклогексиліден)пропан (30) BF3Et2O (0,3мл, 2,4ммоль) додають до розчину спирту 29 (0,42г, 2ммоль) і TMSN3 (0,31мл, 2,4ммоль) в бензолі (4,5мл) протягом 3хв. при охолоджуванні на бані з льодом. Реакційну суміш перемішують при 5-10°С протягом 1год. і фільтрують через коротку колонку з силікагелем. Розчин випаровують і залишок очищають методом флешхроматографії на силікагелі (легкий петролейний 33 75478 34 ефір), одержуючи 30 (0,30г, 64%) у вигляді безбациклогексадієну (37) і 1,5,5-триметил-3-метилен-1рвної олії. 1Н-ЯМР (CDCl3, TMS), м.ч.: 0,92 і 0,98 циклогексену (38) (всього 12Н, обидва с, циклогексан-3,5-СН3); 1,27 До 2Μ ефірного розчину, що перемішується, (2Н, с, циклогексан-4-СН2); 1,40 (6Н, с, -C(CH3)2N3); метилмагніййодиду (15мл, 30ммоль) додають кра1,85 і 2,23 (обидва 2Н, обидва с, циклогексан-2,6плями розчин 3,5,5-триметил-2-циклогексен-1-ону СН2) і 5,27 (1Н, с, =СН-). (36) (1,38г, 10ммоль) в безводному ефірі (15мл). c) Гідрохлорид 2-метил-1-(3,3,5,5Суміш перемішують протягом 1год., охолоджують тетраметилциклогексиліден)-2-пропанаміну (31) крижаною водою і обережно обробляють 15% воОдержують з азиду 30 за такою ж методикою, дної СН3СООН (15мл). Суміш перемішують ще як для аміну 24 (приклад 4). Гідрохлорид аміну 31 одну годину. Органічний шар відділяють і промиодержують у вигляді безбарвної твердої речовини вають водою і насиченим водним NaHCO3. Після з виходом 69%. 1H-ЯМР (CDCl3, TMS), м.ч.: 0,91 і сушіння над MgSO4, розчин концентрують у вакуу0,98 (всього 12Н, обидва с, циклогексан-3,5-СН3); мі. Залишок очищають методом флеш1,26 (2Н, с, циклогексан-4-СН2); 1,68 (6Н, с, хроматографії (легкий петролейний ефір, Rf 0,95 C(CH3)2N); 1,84 і 2,10 (обидва 2Н, обидва с, цикло(гексан), одержуючи суміш 37 і 38 (0,955г, 70%) гексан-2, 6-СН2); 5,15 (1Н, с, =СН-) і 8,5 (ЗН, шир.с, (7:10, на основі ГХ) у вигляді олії. 1Н-ЯМР (CDCl3, + NH3 ). TMS), м.ч.: 0,89, 0,98 і 1,03 (всього 10,2 Н, всі с, Схема: приклади 14 і 15 5,5-СН3); 1,55-2,20 (всього 12,6 Н, м, СН2С= і СН3С=); 4,69 (2Н, дм5 4Гц, =СН2); 5,06 (0,7Н, м, =СН); 5,50 (0,7Н, септет, 1,5Гц, =СН) і 5,92 (1Н, м, =СН). b) 3-азидо-1,5,5,5-тетраметил-1-циклогексен (39) Одержують з суміші 37 і 38 згідно з методикою для сполуки 34 (приклад 14, а). Азид 39 одержують у вигляді безбарвної олії з виходом 43%. 1НЯМР (CDCl3, TMS), м.ч.: 0,93 і 0,99 (всього 6Н, обидва с, 5,5-СН3); 1,31 (3Н; с, 1-СН3); 1,36 і 1,62 (всього 2Н, обидва д, 13Гц, 4-СН2); 1,72 (5Н, с, 1СН3, 6-СН2); 5,32 (1Н, с, С=СН). Приклад 14 c) Гідрохлорид 1,3,5,5-тетраметил-2Гідрохлорид 3,5,5-триметил-2-циклогексен-1циклогексен-1-аміну (40) аміну (35) Одержують з азиду 39 згідно з методикою для a) 3-азидо-1,5,5-триметил-1-циклогексен (34) сполуки 11 (приклад 3, с). До охолодженої (0°С) суспензії азиду натрію Гідрохлорид аміну 40 одержують у вигляді (0,81г, 12,5ммоль) в СН2Сl2 (5мл) додають крапбезбарвної твердої речовини з виходом 60%. 1Нлями 53% водну H2SO4 (8мл). Суміш перемішують ЯМР (CDCl3, TMS), м.ч.: 0,96 і 1,07 (всього 6Н, протягом 10хв., потім додають розчин 3,5,5обидва с, 5,5-СН3); 1,56 (3Н, с, 1-СН3); 1,73 (3Н, с, триметил-2-циклогексанолу (33) (0,70г, 5ммоль) в 3-СН3); 1,60-2,05 (4Н, м, 4,6-СН2); 5,49 (1H, с, СН2Сl2 (8мл). Суміш перемішують протягом 20год., С=СН) і 8,27 (3Н, шир.с, NH3+). виливають в крижану воду, нейтралізують водним Схема: приклад 16 NH4OH і екстрагують СН2Сl2. Екстракт промивають насиченим розчином солі і сушать над MgSO4. Фільтрація і випаровування розчинника при підтримці температури нижче 25°С дають олію, яку виділяють методом колонкової хроматографії на силікагелі (легкий петролейний ефір). Фракцію з Rf 0,8 (гексан) збирають. Випаровування розчинника дає 34 у вигляді безбарвної олії (0,365г, 44%). 1НЯМР (CDCl3, TMS), м.ч.: 0,89 і 1,01 (всього 6Н, Приклад 16 обидва с, 5,5-СН3); 1,34 (1H, м, цикло-4-СН); 1,55Гідрохлорид 1,3-транс-5-триметил-цис-31,95 (3Н, м, 4-СН, 6-СН2); 1,71 (3Н, с, 1-СН3); 3,90 вінілциклогексанаміну (45) (1Н, м, 3-СН) і 5,39 (1Н, с, С=СН). a) 3,5-диметил-З-вінілциклогексанон (42) b) Гідрохлорид 3,5,5-триметил-2-циклогексен1Μ розчин вінілмагнійброміду в ТГФ (90мл, 1-аміну (35) 90ммоль) охолоджують на бані безводний лідОдержують з азиду 34 згідно з методикою для ацетон до -20°С в інертній атмосфері і додають сполуки 11 (приклад 3, с). Гідрохлорид аміну 35 CuCl (4,45г, 45ммоль) однією порцією. Суміш пеодержують у вигляді безбарвної твердої речовини ремішують протягом 30хв. і додають краплями 1 з виходом 57%. Н-ЯМР (CDCl3, TMS), м.ч.: 0,89 і розчин 3,5-диметил-2-циклогексен-1-ону (41) 1,03 (всього 6Н, обидва с, 5,5-СН3); 1,25-2,15 (4Н, (3,73г, 30ммоль) в ТГФ (40мл), підтримуючи темм, 4,6-СН2); 1,72 (3Н, с, 3-СН3); 3,88 (1H, м, 1-СН); пературу реакції при -20°С. Охолоджувальну баню 5,41 (1H, с, С=СН) і 8,40 (3Н, шир.с, NH3+). прибирають і дають температурі реакційної суміші Приклад 15 піднятись до кімнатної протягом 2год. Додають Гідрохлорид 1,3,5,5-тетраметил-2повністю насичений водний NH4Cl (50мл) при охоциклогексен-1-аміну (40) лоджуванні на бані з льодом. Потім додають гекa) Суміш 1,3,5,5-тетраметил-1,3сан (150мл) і водний шар відділяють і екстрагують 35 75478 36 охолодженого (-10°С) в атмосфері аргону 1Μ мегексаном (2 100мл). Об'єднані органічні екстракти тилмагніййодиду в етиловому ефірі (15мл, промивають 20% водною оцтовою кислотою 15ммоль) і перемішують протягом 5хв. Потім до(100мл) і насиченим водним NaHCO3 (3 200мл). дають краплями розчин ацетату 46 (2,5г, 10ммоль) Екстракт сушать над MgSO4, фільтрують і випаров ТГФ (25мл) за 20хв., підтримуючи температуру вують. Неочищений продукт очищають методом нижче 0°С. Суміш перемішують протягом 1год., флеш-хроматографії на силікагелі (легкий петрогасять насиченим водним NH4Cl і екстрагують діелейний ефір-етилацетат, 20:1), одержуючи 42 тиловим ефіром. Екстракт промивають насиченим (2,4г, 52%) у вигляді безбарвної олії. 1Н-ЯМР розчином солі, сушать над безводним MgSO4, фі(CDCl3, TMS), м.ч.: 0,99 (3Н, д, 6Гц, 5-СН3); 1,11 льтрують і випаровують. Залишок очищають ме(3Н, с, 3-СН3); 1,2-2,6 (7Н, м, кільцеві протони); тодом флеш-хроматографії на силікагелі (легкий 4,94 і 5,01 (всього 2Н, обидва д, 17 і 10,5Гц, СН2=) петролейний ефір-етилацетат, 20:1), одержуючи і 5,64 (1Н, дд, 17 і 11Гц, =СН). 47 (1,5г, 56,5%) у вигляді безбарвної олії. 1Н-ЯМР b) 1,3-транс-5-триметил-цис-3(CDCl3, TMS), м.ч.: 1,01, 1,07 і 1,09 (всього 12Н, с, вінілциклогексанол (43) 3',5'-СН3); 1,00-1,85 (6Н, м, кільце СН); 1,30 (3Н, с, Розчин кетону 42 (1г, 6,6ммоль) в діетиловому 1'-СН3); 1,33 (3Н, т, 7Гц, СН3-етил); 3,44 (1H, с, 2ефірі (10мл) додають до 1,6Μ розчину метиллітію СН) і 4,27 (2Н, кв, 7Гц, ОСН2). в діетиловому ефірі (12мл, 19,6ммоль) при охолоb) Етил 2-ціано-2-(1,3,3,5,5джуванні на бані з льодом. Одержану суміш перепентаметилциклогексил)-4-пентеноат (48) мішують протягом 1год. при 0-5°С і додають повніДо розчину ціаноацетату 47 (1,25г, 4,71ммоль) стю насичений водний NH4Cl (10мл). Водний шар в безводному ДМСО (10мл) додають гідрид натрію відділяють і екстрагують діетиловим ефіром (0,284г, 7,09ммоль; 60% дисперсія в мінеральній (2 15мл). Об'єднані органічні фази промивають олії). Суміш перемішують протягом 30хв. при 50°С насиченим розчином солі (20мл) і сушать над і охолоджують до 20°С. До даної суміші додають MgSO4. Екстракт фільтрують і випаровують. Неалілбромід (0,86г, 7,1ммоль) і суміш перемішують очищений продукт очищають методом флешпротягом 3год. при кімнатній температурі, потім хроматографії на силікагелі (3% етилацетат в лег30хв. при 50°С. Суміш охолоджують, обробляють кому петролейному ефірі). Циклогексанол 43 водою і екстрагують діетиловим ефіром. Екстракт (0,82г, 74%) одержують у вигляді безбарвної олії, промивають водою і насиченим розчином солі, яку використовують на наступній стадії без хараксушать над безводним MgSO4, фільтрують і випатеризації. ровують. Залишок очищають методом флешc) 1-азидо-1,3-транс-5-триметил-цис-3хроматографії на силікагелі (легкий петролейний вінілциклогексан (44) ефір-етилацетат, 20:1), одержуючи 48 (0,92г, Одержують з циклогексанолу 43 згідно з мето63,7%) у вигляді безбарвної олії. 1Н-ЯМР (CDCl3, дикою для сполуки 9 (приклад 3, b). Азид 44 одерTMS), м.ч.: 0,98 (6Н, с, 3',5'-CH3eq); 1,11 (6Н, с, 3',5'жують у вигляді безбарвної олії з виходом 17%. 1 СН3ах); 1,00-1,85 (6Н, м, кільце СН); 1,31 (3Н, т, Н-ЯМР (CDCl3, TMS), м.ч.: 0,94 (3Н, д, 6,5Гц, 57Гц, СН3-етил); 1,33 (3Н, с, 1'-СН3); 2,42 і 2,86 СН3); 0,97 (3Н, с, 3-СН3); 1,27 (3Н, с, 1-СН3); 0,7-2,0 (всього 2Н, обидва дд, 13 і 7Гц, 3-СН2); 4,02 (2Н, (7Н, м, кільцеві протони); 4,95 і 4,97 (всього 2Н, кв, 7Гц, ОСН2); 5,05-5,37 (2Н, м, =СН2) і 5,55-6,05 обидва д, 18 і 11Гц, =СН2) і 5,77 (1H, дд, 18 і 11Гц,(1Н, м, =СН). СН). c) Гідрохлорид 2-(1,3,3,5,5d) Гідрохлорид 1,3-транс-5-триметил-цис-3пентаметилциклогексил)-4-пентеніламіну (49) вінілциклогексанаміну (45) До розчину складного ефіру 48 (0,9г, Одержують з азиду 44 згідно з методикою для 2,95ммоль) в ДМСО (10мл) додають воду (0,53мл, сполуки 11 (приклад 3, с). Гідрохлорид аміну 45 2,95ммоль) і хлорид літію (0,25г, 5,9ммоль). Суміш одержують у вигляді безбарвної твердої речовини перемішують протягом 3год. при 175-180°С, потім з виходом 32%. 1H-ЯМР (CDCl3, TMS), м.ч.: 0,92 охолоджують і додають воду (30мл). Суміш екст(3Н, д, 6,5Гц, 5-СН3); 0,96 (3Н, с, 3-СН3); 1,45 (3Н, рагують діетиловим ефіром. Екстракт промивають с, 1-СН3); 0,8-2,1 (9Н, м, 2,4,6-СН2, 5-СН і Н2О); водою і насиченим розчином солі, сушать над. 4,94 і 4,97 (2Н, обидва д, 18 і 11Гц, =СН2); 5,76 безводним MgSO4, фільтрують і концентрують до (1H, дд, 18 і 11Гц, =СН) і 8,26 (3Н, шир.с, NH3+). об'єму 10мл. Одержаний розчин додають крапляСхема: приклад 17 ми до суспензії літійалюмінійгідриду (0,25г, 6,6ммоль) в діетиловому ефірі (15мл) і кип'ятять із зворотним холодильником протягом 3год. Суміш охолоджують, обробляють 20% водним NaOH і екстрагують діетиловим ефіром. Екстракт промивають насиченим розчином солі, сушать над NaOH, фільтрують і обробляють безводним розчином НСl в діетиловому ефірі. Після випаровування розчинника залишок очищають методом Приклад 17 хроматографії на силікагелі (хлороформ-метанол, Гідрохлорид 2-(1,3,3,5,520:1), одержуючи 49 (0,245г, 31%) у вигляді безбапентаметилциклогексил)-4-пентениламіну (49) рвної твердої речовини. 1H-ЯМР (ДМСО-D6, TMS), а) Етил 2-ціано-2-(1,3,3,5,5м.ч.: 0,92, 0,96 і 1,04 (всього 15Н, всі с, 3',5'-СН3 і пентаметилциклогексил)ацетат (47) 1'-СН3), 1,00-1,65 (всього 6Н, м, кільце-СН2); 1,85Хлорид міді(1) (0,05г, 0,5ммоль) додають до 2,40 (3Н, м, 3-СН2, 4-СН); 2,60-3,10 (2Н, м, CH2N); 37 75478 38 4,90-5,25 (2Н, м, =СН2); 5,62-6,10 (1Н, м, =СН) і ведені далі. 7,92 (3Н, шир.с, NH3+). (a) Таблетки, відповідні для перорального ФАРМАЦЕВТИЧНІ КОМПОЗИЦІЇ введення, які містять активний інгредієнт, можна Активні інгредієнти даного винаходу разом з одержати звичайними методиками таблетування. одним або більшою кількістю звичайних ад'юван(b) Для супозиторіїв можна використати будьтів, носіїв або розріджувачів можна приготувати у яку звичайну основу супозиторіїв для включення в вигляді фармацевтичних композицій і їх одиничних неї активного інгредієнта за звичайною методидозованих форм, і в такому вигляді можна застокою, таку як поліетиленгліколь, який є твердим при совувати їх як тверді композиції, такі як таблетки з нормальній кімнатній температурі, але плавиться покриттям або без покриття або заповнені капсупри температурі тіла або близько неї. ли, або рідини, такі як розчини, суспензії, емульсії, (c) Для розчинів для парентерального (вклюеліксири або капсули, заповнені ними, всі для печаючи внутрішньовенне і підшкірне) введення зарорального застосування; у вигляді супозиторіїв стосовують активний інгредієнт разом зі звичайабо капсул для ректального застосування або у ними інгредієнтами у звичайних кількостях, такими вигляді стерильних розчинів для ін'єкцій для пареяк, наприклад, хлорид натрію і двічі дистильована нтерального (включаючи внутрішньовенне або вода, скільки потрібно, згідно із звичайною метопідшкірне) застосування. Такі фармацевтичні комдикою, такою як фільтрування, асептичне заповпозиції і їх одиничні дозовані форми можуть містинення ампул або пляшок для внутрішньовенних ти загальновідомі або нові інгредієнти у звичайних крапельниць, і обробка в автоклаві для стерильабо спеціальних пропорціях, з додатковими активності. ними сполуками або без таких, і такі одиничні доІнші відповідні фармацевтичні композиції бузовані форми можуть містити будь-яку відповідну дуть безпосередньо ясні для фахівців в даній обефективну кількість активного інгредієнта, відповіласті. дну передбачуваному для прийому діапазону денНаступні приклади також дані тільки для ілюсних доз. Таким чином, відповідними типовими трації і не є обмежувальними. одиничними дозованими формами є таблетки, що ПРИКЛАД 18 містять від двадцяти (20) до ста (100) міліграмів Препарат для таблеток активного інгредієнта, або, більш широко, від деВідповідним препаратом для таблетки, що місяти (10) до двохсот п'ятдесяти (250) міліграмів в стить 10мг активного інгредієнта, є наступний: таблетці. мг СПОСІБ ЛІКУВАННЯ Активний інгредієнт 10 Завдяки високій мірі своєї активності і низькій Лактоза 63 токсичності, що представляють разом найбільш Мікрокристалічна целюлоза 21 сприятливий терапевтичний показник, активні реТальк 4 човини даного винаходу можна вводити суб'єкту, Стеарат магнію 1 наприклад, в організм потребуючої цього тварини Колоїдний діоксид кремнію 1 (включаючи людину) для лікування, полегшення ПРИКЛАД 19 або зниження інтенсивності, тимчасового полегПрепарат для таблеток шення або ліквідації показання або стану, сприйІншим відповідним препаратом для таблетки, нятливого до них, або типового показання або що містить 100мг активного інгредієнта, є наступстану, вказаного де-небудь далі в даній заявці, ний: переважно конкурентно, одночасно або разом з мг одним або більшою кількістю фармацевтично приАктивний інгредієнт 100 йнятних наповнювачів, носіїв або розріджувачів, Картопляний крохмаль 20 особливо і переважно у вигляді їх фармацевтичної Полівінілпіролідон 10 композиції перорально, ректально або парентераПокрита плівкою і забарвлена льно (включаючи внутрішньовенний і підшкірний Матеріал покриваючої плівки складається з: способи), або в деяких випадках навіть місцево Лактоза 100 при ефективній кількості. Відповідні діапазони доз Мікрокристалічна целюлоза 80 становлять 1-1000мг в день, переважно 10-500мг в Желатин 10 день, і особливо 50-500 мг в день в залежності, як Полівінілпіролідон зшитий 10 правило, від точного способу введення, форми Тальк 10 введення, показання, на яке направлено введенСтеарат магнію 2 ня, суб'єкта, що бере участь, масу тіла суб'єкта, Колоїдний діоксид кремнію 3 що бере участь, і переваг і досвіду лікуючого лікаКольорові пігменти 5 ря або ветеринара. ПРИКЛАД 20 ПРИКЛАДИ ТИПОВИХ ФАРМАЦЕВТИЧНИХ Препарат для капсул КОМПОЗИЦІЙ Відповідним препаратом для капсули, що місЗа допомогою розчинників, що звичайно викотить 50мг активного інгредієнта, є наступний: ристовуються, допоміжних агентів і носіїв продукти мг реакцій можна переробити в таблетки, таблетки з Активний інгредієнт 50 покриттям, капсули, розчини для крапельниць, Кукурудзяний крохмаль 20 супозиторії, препарати для ін'єкцій і вливань і поДвохосновний фосфат кальцію 50 дібне, і можна застосовувати терапевтично пероТальк 2 ральним, ректальним, парентеральним та іншими Колоїдний діоксид кремнію 2 способами. Типові фармацевтичні композиції наЗаповнюють желатинову капсулу. 39 75478 40 ПРИКЛАД 21 Диметилсульфоксид 5,0 Розчин для ін'єкцій Гідроксіетилцелюлоза 0,4 Відповідним препаратом для розчину для ін'єОчищена вода 19,6 кцій, що містить один процент активного інгредієн1,8мл даного розчину вміщують на тканину, та, є наступний: покриту липкою підкладкою з фольги. Систему Активний інгредієнт, мг 12 закривають захисною прокладкою, яку видаляють Хлорид натрію, мг 8 перед застосуванням. Стерильна вода до 1мл ПРИКЛАД 27 ПРИКЛАД 22 Препарат у вигляді наночастинок 10г полібуРідкий препарат для перорального прийому тилціаноакрилатних наночастинок містять: Відповідним препаратом для 1л рідкої суміші, г що містить 2мг активного інгредієнта в одному мл Активний інгредієнт 1,00 суміші, є наступний: Полоксамер 0,10 г Бутилціаноакрилат 8,75 Активний інгредієнт 2 Маніт 0,10 Сахароза 250 Хлорид натрію 0,05 Глюкоза 300 Полібутилціаноакрилатні наночастинки одерСорбіт 150 жують полімеризацією емульсії в суміші вода/0,1н. Апельсиновий ароматизатор 10 НСІ/етанол як полімеризацйному середовищі. На Барвник Sunset yellow закінчення наночастинки в суспензії ліофілізують у Очищена вода до загального об'єму 1000мл вакуумі. ПРИКЛАД 23 ФАРМАКОЛОГІЯ - КОРОТКИЙ ВИКЛАД Рідкий препарат для перорального прийому Активні речовини даного винаходу, їх фармаІншим відповідним препаратом для 1л рідкої цевтичні композиції і способи лікування з їх допосуміші, що містить 20мг активного інгредієнта в могою відрізняються унікальними перевагами і одному мл суміші, є наступний: неочевидними властивостями, роблячи заявлений г в даному описі матеріал, "що розглядається загаАктивний інгредієнт 20,00 лом", неочевидним. Дані сполуки і їх фармацевтиТрагакант 7,00 чні композиції демонструють в стандартних загаГліцерин 50,00 льноприйнятих методиках дослідження, які Сахароза 400,00 заслуговують на довіру, наступні властивості і хаМетилпарабен 0,50 рактеристики, що оцінюються: Пропілпарабен 0,05 Вони є системноактивними, неконкурентними Чорносмородиновий ароматизатор 10,00 антагоністами рецепторів NMDA з швидкими кінеРозчинний червоний барвник 0,02 тиками блокування/розблокування і сильною заОчищена вода до загального об'єму 1000мл лежністю від напруження і, отже, застосовні при ПРИКЛАД 24 лікуванні, припиненні, полегшенні, ослабленні або Рідкий препарат для перорального прийому зменшенні інтенсивності сприйнятливих станів Іншим відповідним препаратом для 1л рідкої шляхом застосування або введення тваринісуміші, що містить 2мг активного інгредієнта в односієві з метою лікування широкого діапазону поному мл суміші, є наступний: рушень ЦНС, які включають розлади глутаматергіг чної передачі. Активний інгредієнт 2 Дані сполуки також є системноактивними, неСахароза 400 конкурентними антагоністами рецепторів 5-НТ3 і Настій шкірки гіркого апельсина 20 нейронних нікотинових рецепторів і, отже, застоНастій шкірки солодкого апельсина 15 совні при лікуванні, припиненні, полегшенні, ослаОчищена вода до загального об'єму 1000мл бленні або зменшенні інтенсивності сприйнятлиПРИКЛАД 25 вих станів шляхом нанесення або введення Аерозольний препарат 180г аерозольного ротварині-носієві з метою лікування широкого діапазчину містить: зону порушень ЦНС, які включають розлади серог тонінергічної або нікотинової передачі. Активний інгредієнт 10 Методи Олеїнова кислота 5 Дослідження зв'язування рецепторів Етанол 81 Самців щурів Sprague-Dawlew (200-250г) обезОчищена вода 9 головлюють і швидко видаляють мозок. Кору висіТетрафторетан 75 кають і гомогенізують в 20 об'ємах охолодженої на Алюмінієві балончики для аерозолю заповнюльоду 0,32Μ сахарози, використовуючи скляноють 15мл даного розчину, закривають дозувальтефлоновий гомогенізатор. Гомогенат центрифуним клапаном, створюють тиск 3,0бар. гують при 1000xg протягом 10хв. Осад відкидають ПРИКЛАД 26 і супернатант центрифугують при 20000xg протяTDS-препарат гом 20хв. Одержаний осад повторно суспендують 100г розчину містять: в 20 об'ємах дистильованої води і центрифугують г протягом 20хв. при 8000xg. Потім супернатант і Активний інгредієнт 10,0 лейкоцитну плівку центрифугують при 48000xg Етанол 57,5 протягом 20хв. в присутності 50мМ Трис-НСІ, Пропіленгліколь 7,5 рН8,0. Потім осад повторно суспендують і 41 75478 42 центрифугують два-три рази при 48000xg протя500), протягом 2-6 днів після ін'єкції. Електроди гом 20хв. в присутності 50мМ Трис-НСІ, рН8,0. Всі мають опір між 0,2 і 0,4МОм і заповнені 3Μ KСl. стадії центрифугування проводять при 4°С. Після Реєстрацію виготовляють у виготовленій на замоповторного суспендування в 5 об'ємах 50мМ Трисвлення камері з 2-3-секундними часами обміну. НСІ, рН8,0, мембранну суспензію швидко замороРозчин для бані готують без Са2+, уникаючи Са2+жують при -80°С. індукованих СІ -струмів (100мМ NaCl, 2мМ KСl, У день дослідження мембрани розморожують і 5мМ HEPES, 2мМ ВаСl2, рН7,35). Рецептори промивають чотири рази при повторному суспенNMDA активують вручну, застосовуючи спільно дуванні в 50мМ Трис-НСІ, рН8,0, і центрифугуванні 1мМ глутамат і 10мкМ гліцин протягом 30-40сек. при 48000xg протягом 20хв. і остаточно знов сукожні 2-3хв. в овоцити, блоковані при -70мВ. Нейспендують в 50мМ Трис-НСІ, рН7,4. Визначають ронні нікотинові рецептори активують, застосовукількість білка в кінцевому мембранному препараті ючи 100мкМ ацетилхолін протягом 20-30сек. кожні (250-500мкг/мл) згідно зі способом Лоурі та інш. 2-3хв. на овоцитах, блокованих при -70мВ. Після (1951). Інкубацію починають при додаванні [3Н]-(+)одержання стабільних контрольних відгуків одерМK-801 (23,9кюрі/ммоль, 5нМ, Dupont NEN) в прожують повні криві концентрацію-відгук з антагонісбірки з гліцином (10мкМ), глутаматом (10мкМ) і тами шляхом попередньої інкубації 6-7 різних кон125-250мкг білка (загальний об'єм 0,5мл) і різними центрацій з інтервалами log 3. концентраціями агентів, що досліджуються (10 Тільки результати від стабільних клітин прийнконцентрацій, кожна дубльована). Інкубацію проятні для включення у фінальне дослідження, а водять при кімнатній температурі протягом 120хв. саме, що показують, щонайменше, 50% віднов(досягають рівноваги при умовах, що використолення реакцій на NMDA після видалення антагонівуються). Неспецифічне зв'язування визначають ста, що досліджується. Незважаючи на це, відновшляхом додавання неміченого (+)-МK-801 лення від дії ліків не завжди становить 100% через (10мкМ). Інкубацію завершують, застосовуючи незначне загасання або розгін в деяких клітинах. фільтрувальну систему Millipore. Зразки двічі опоДаний ефект, якщо такий присутній, завжди комліскують 4мл дослідницького буфера, охолоджепенсують, закладаючи у вихідний % антагонізму ного на льоду, на фільтрах зі скловолокна при кожній концентрації для контролю і відновлен(Schleicher & Schuell) в постійному вакуумі. Після ня і допускаючи лінійний часовий перебіг для давідділення і споліскування фільтри вміщують в ного загасання. Всі антагоністи оцінюють в стійкосцинтиляційну рідину (5мл, Ultima Gold) і визначаму стані блокади при 6-7 концентраціях, ють радіоактивність, затриману на фільтрах, за щонайменше, на 4 клітинах. Рівноважної блокади допомогою звичайного рідинного сцинтиляційного досягають в межах застосування 1-3 агоністів в лічильника (Hewlett Packard, Liquid Scintillation залежності від концентрації антагоністів. Analyser). Kd [3Н]-(+)-МK-801 для 4,6нМ визначаКінетичні експерименти проводять, застосоють аналізом за Скретчардом і використовують вуючи різні концентрації ненасичених аміноалкілзгідно із співвідношенням Чена-Прусова для розциклогексанів (звичайно 5 концентрацій по схемі рахунку спорідненості замінюючих речовин як ведозування log 3) протягом 10-20сек. при постійній личини Kd. Більшість антагоністів тестують в 3-7 присутності глутамату (100мкМ) і гліцину (10мкМ) окремих експериментах. протягом 90-180сек. в овоцитах Xenopus, експреЕкспресія підтипу рецепторів NMDA і нейронсуючих рецептори NR1a/2A. Перфузійна система, них нікотинових рецепторів в овоцитах Xenopus що застосовується для даних експериментів, явЗрілим жіночим особням Xenopus laevis проляє собою модифіковану овоцитну карусельну водять анестезію в 0,2% трикаїні на льоду протясистему, яка дозволяє швидке вливання і вимигом 15хв. до оперативного втручання. Овоцити вання агоніста і антагоніста з періодами заміни видаляють та інкубують в 2мг/мл колагеназі (тип II) менше однієї секунди. Експонентні залежності в овоцитному розчині Рінгера, що не містить Са2+ одержують, використовуючи програму TIDA для (82,5мМ, NaCl, 2мМ KСl, 2мМ MgCl2, 5мМ HEPES, Windows, і більшість відгуків добре описуються рН7,5), протягом 30хв. при кімнатній температурі і простою експонентною залежністю. Таку ж систеретельно промивають OR-2 (100мМ NaCl, 2мМ му застосовують для одержання залежності блоKСl, 1мМ MgCl2, 2мМ СаСl2, 5мМ HEPES, рН7,5). кади від напруження, але розчин в бані містить Шар фолікулярних клітин, що залишився, видаляфлуфенамову кислоту (100мкМ) для блокування ють вручну за допомогою загостреного пінцета і ендогенних активованих напруженням і Са2+зберігають овоцити в OR-2. РНК розчиняють в активованих Сl--струмів. Також Ва2+ (2мМ) заміDEPC-обробленій стерильній дистильованій воді. нюють низькими концентраціями Са2+ (0,2мМ). РНК для підодиниці NMDA NRla змішують у співПісля рівноважної блокади при високих концентвідношенні 1:1 з РНК для підодиниці NMDA NR2A. раціях антагоніста (звичайно 10-кратних величиАналогічно РНК нейронного нікотинового α4 змінах ІС50) одержую п'ять нахилів від -70мВ до шують у співвідношенні 1:1 з РНК для підодиниці +30мВ за дві сек. Аналогічні нахили одержують β2. Від п'ятдесяти до ста нанолітрів кожної суміші для розчинів в бані і для глутамату без антагонісРНК вводять в цитоплазму овоцитів, застосовуючи та, до застосування антагоніста і після відновленнанолітровий інжектор (World Precision ня відгуків. Витоки за відсутності глутамату відніInstruments). Овоцити інкубують при 19°С в OR-2 мають з кривих для глутамату і глутамату плюс протягом наступних 3-6 днів. антагоніст. Потім визначають залежність від наОдержують електрофізіологічні відгуки, застопруження, порівнюючи криві для глутамату і глусовуючи стандартний двохелектродний метод натамату плюс антагоніст. пруження-блокування (підсилювач GeneClamp 43 75478 44 Блокування рецепторів для NMDA і нікотину лювача ЕРС-7 (List). Складові частини внутрішньоГіпокампи одержують з ембріонів щурів (Е20 і клітинного розчину наступні (мМ): CsCl (130), Е21) і переносять в розчин солі з буфером Хенка, HEPES (10), EGTA (10), MgCl2 (2), СаСl2 (2), К-АТФ що не містить кальцію і магнію (Gibco), на льоду. (2), Трис-ГТФ (0,2), D-глюкоза (10); рН доводять до Клітини роз'єднують механічно в суміші 0,05% 7,3 за допомогою CsOH або НСl. Позаклітинні розДНКаза/0,3% овомукоїд (Sigma) після 8-хвилинної чини мають наступний основний склад (мМ): NaCl попередньої інкубації з сумішшю 0,66% трип(124), KСl (2,8), HEPES (10), рН7,3 регулюють за син/0,1% ДНКаза (Sigma). Потім роз'єднані клітини допомогою NaOH або НСl. центрифугують при 18xg протягом 10хв., повторно Після встановлення конфігурації цілої клітини суспендують в мінімальному підтримуючому серезбирають клітини зі скляної підкладки і вносять довищі (Gibco) і висівають з щільністю серотонін (10мкМ), мемантин і ненасичені аміноа150000клітин•см-2 в пластикові чашки Петрі лкілциклогексанові похідні з різними концентраці(Falcon) із заздалегідь нанесеним полі-L-лізином ями, застосовуючи пристрій для швидкої суперфу(Sigma). Клітини забезпечують мінімальним підтзії. Для впливу на зібрані клітини розчином, що не римуючим середовищем з буфером містить або містить серотонін, застосовують кероNaHCO3/HEPES з додаванням 5% плідної телячої вану п'єзоперетворювачем двоциліндрову піпетку. сироватки і 5% кінської сироватки (Gibco) та інкуДвосекундний імпульс серотоніну надходить кожні бують при 37°С, 5% СО2 і 95% вологості. Середо60сек. Передбачувані антагоністи розчиняють в вище повністю змінюють після інгібування гліальдвічі дистильованій воді і розбавляють розчином з ного мітозу, що продовжується, за допомогою бані до необхідної концентрації. Тільки результати цитозин-D-арабінофуранозиду (20Μ Sigma) прибвід стабільних клітин прийнятні для включення у лизно через 7 днів in vitro. Після цього середовище фінальне дослідження, а саме, що демонструють, замінюють частково двічі на тиждень. щонайменше, 50% відновлення відгуків на серотоРеєстрацію блокування рецепторів проводять нін після видалення сполук. Незважаючи на це, від даних нейронів за допомогою полірованих відновлення від дії інших ліків не завжди становить скляних електродів (4-6МОм) за способом моделі 100% через загасання в деяких клітинах (
ДивитисяДодаткова інформація
Назва патенту англійськоюUnsaturated 1-amino-alkylcyclohexane nmda, 5нт3 and antagonists of nicotinic receptor
Автори англійськоюParsons Christopher Graham Raphael, Henrich Markus, Danysz Wojciech, Kalvinsh, Ivars, Jirgensons Aigars
Назва патенту російськоюНенасыщенный 1-амино-алкилциклогексан nmda, 5нт3 и антагонисты никотинового рецептора
Автори російськоюПарсонс Кристофер Грахам Рафаэль, Хенрих Маркус, Даниш Войцех, Калвиньш Иварс, Йиргенсонс Айгарс
МПК / Мітки
МПК: A61P 31/18, A61P 31/22, A61P 1/04, A61P 25/14, C07D 295/033, A61P 25/02, A61P 25/24, A61P 25/16, A61P 1/08, A61P 1/16, A61P 25/22, A61P 25/30, A61P 9/10, A61P 29/00, C07C 211/25, A61P 25/08, C07C 211/40, A61P 21/04, A61P 9/00, C07D 295/02, A61P 31/12, A61P 25/28, A61P 37/04, A61P 33/06, A61P 25/06, A61P 27/06, A61P 25/32, A61P 25/36, A61P 43/00, A61P 33/02, A61P 3/10, A61P 25/34, A61P 25/00, A61K 31/415, A61K 31/13, A61P 37/02
Мітки: ненасичений, 5нт3, рецептора, nmda, 1-аміно-алкілциклогексан, антагоністи, нікотинового
Код посилання
<a href="https://ua.patents.su/26-75478-nenasichenijj-1-amino-alkilciklogeksan-nmda-5nt3-i-antagonisti-nikotinovogo-receptora.html" target="_blank" rel="follow" title="База патентів України">Ненасичений 1-аміно-алкілциклогексан nmda, 5нт3 і антагоністи нікотинового рецептора</a>
Попередній патент: Спосіб виготовлення поверхневого покриття (варіанти) та поверхневе покриття (варіанти)
Наступний патент: Пристрій для гальмування електромеханічного приводу візка вантажопідйомного крана
Випадковий патент: Засіб пожежогасіння












