Спосіб одержання карбапенемових антибіотиків
Формула / Реферат
1. Спосіб одержання сполуки формули
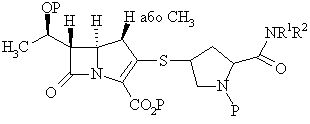 І
І
або її фармацевтично прийнятної солі, або складного ефіру, де кожний Р незалежно позначає Н або захисну групу для карбоксилу або гідроксилу і R1 і R2 - незалежно один від одного позначають Н, С1-6-алкіл, арил або гетероарил або С1-10-алкіл, арил або гетероарил, заміщений 1-3 групами, обраними з групи, що складається з галогену, гідрокси, ціано, ацилу, ациламіно, аралкокси, алкілсульфонілу, арилсульфонілу, алкілсульфоніламіно, арилсульфоніламіно, алкіламінокарбонілу, алкілу, алкокси, арилу, арилокси, аралкокси, аміно, алкіламіно, діалкіламіно, карбокси і сульфоніламіно, що включає взаємодію сполуки
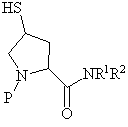 ІІ
ІІ
або її фармацевтично прийнятної солі, або складного ефіру і сполуки
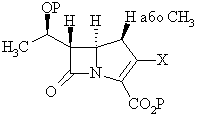 ІІІ
ІІІ
або її фармацевтично прийнятної солі, або складного ефіру, де Х позначає ОР(О)(OR)2 або ОSО2R, де R позначає С1-6-алкіл, С1-6-алкарил, арил або перфтор-С1-6-алкіл, в присутності аміну, обраного з групи, що складається з діізопропіламіну (ДІПА), дициклогексиламіну (ДЦГА), 2,2,6,6-тетраметилпіперидину (ТМП), 1,1,3,3-тетраметилгуанідину (ТМГ), 1,8-діазабіцикло-[4.3.0]ундец-7-ену (ДБУ) і 1,5-діазабіцикло[4.3.0]нон-5-ену (ДБН)
з одержанням сполуки формули І.
2. Спосіб одержання сполуки формули Iа
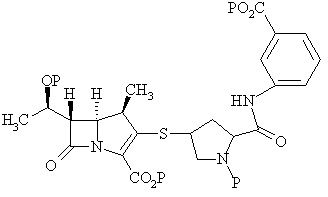 Ia
Ia
або її фармацевтично прийнятної солі, або складного ефіру,
де кожний Р незалежно позначає Н або захисну групу для карбоксилу або гідроксилу, що включає взаємодію сполуки
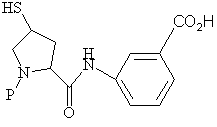 IIa
IIa
або її фармацевтично прийнятної солі, або складного ефіру і сполуки
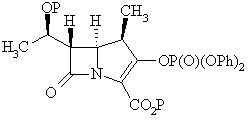 IIIa,
IIIa,
або її фармацевтично прийнятної солі, або складного ефіру, де Ph позначає феніл, в присутності аміну, обраного з групи, що складається з діізопропіламіну (ДІПА), дициклогексиламіну (ДЦГА), 2,2,6,6-тетраметилпіперидину (ТМП), 1,1,3,3-тетраметилгуанідину (ТМГ), 1,8-діазабіцикло[4.3.0]ундец-7-ену (ДБУ) і 1,5-діазабіцикло[4.3.0]нон-5-ену (ДБН),
з одержанням сполуки формули Іа.
3. Спосіб за п. 1, який відрізняється тим, що вторинний амін обирають з групи, що складається з діізопропіламіну (ДІПА) і дициклогексиламіну (ДЦГА).
4. Спосіб за п. 3, який відрізняється тим, що синтез здійснюють в полярному апротонному розчиннику.
5. Спосіб за п. 4, який відрізняється тим, що полярний апротонний розчинник обирають з групи, що складається з диметилформаміду, N-етилпіролідинону і ацетонітрилу.
Текст
1 Спосіб одержання сполуки формули О Р Н Н Н або СП, NR*R2 О або її фармацевтично прийнятної солі, або складного ефіру, де кожний Р незалежно позначає Н або захисну групу для карбоксилу або гідроксилу і R1 і R2 - незалежно один від одного позначають Н, Сі 6-алкіл, арил або гетероарил або Сі ю-алкіл, арил або гетероарил, заміщений 1-3 групами, обраними з групи, що складається з галогену, гідрокси, ціано, ацилу, ациламшо, аралкокси, алкілсульфонілу, арилсульфонілу, алкілсульфоніламіно, арилсульфоніламіно, алкіламшокарбонілу, алкілу, алкокси, арилу, арилокси, аралкокси, аміно, алкіламіно, діалкіламіно, карбокси і сульфоніламшо, що включає взаємодію сполуки або її фармацевтично прийнятної солі, або складного ефіру і сполуки Н Н або СН, О або її фармацевтично прийнятної солі, або складного ефіру, де X позначає OP(O)(OR)2 або OSO2R, де R позначає Сі є-алкіл, Сі є-алкарил, арил або перфтор-Сі є-алкіл, в присутності аміну, обраного з групи, що складається з дмзопропіламіну (ДІПА), дициклогексиламіну (ДЦГА), 2,2,6,6тетраметилпіперидину (ТМП), 1,1,3,3тетраметил гуанідину (ТМГ), 1,8-діазабіцикло[4 3 0]ундец-7-ену (ДБУ) і 1,5 О діазабіцикло[4 3 0]нон-5-ену (ДБН) з одержанням сполуки формули І 2 Спосіб одержання сполуки формули Іа РО„С ОР н,с о ССХР або и фармацевтично прийнятної солі, або складного ефіру, де кожний Р незалежно позначає Н або захисну групу для карбоксилу або гідроксилу, що включає взаємодію сполуки ю 54444 CO2H lla або її фармацевтично прийнятної солі, або складного ефіру і сполуки O P с н . OP(O)(OPhY Ilia, або її фармацевтично прийнятної солі, або складного ефіру, де Рп позначає феніл, в присутності аміну, обраного з групи, що складається з дизоп Дани і винахід стосується синтезу карбапенемових антибіотиків Було виявлено, що включення вторинного аміну в реакції сполучення, що описуються в даній заявці приводить до несподіваного і значного збільшення швидкості реакції, що дозволяє здійснити відносно повне перетворення, за більш короткий час реакції і при порівняно більш низьких температурах, ніж при використанні в цій реакції третинних амінів, Є данні про використання в цих реакціях триетил- і дмзопропілетиламінів, однак, з комерційної точки зору в цьому випадку непридатні час реакції і умови и проведення Так наприклад, Міжнародна публікація WO 93 15078 від 5 серпня 1993 року стосується аналогічних реакцій, що здійснюються в присутності третинного аміну, такого як дизопропілетиламш, або неорганічної основи, такої як карбонат лужного металу, наприклад, карбонат калію Вказані реакції проводяться при температурах від -25°С до температури оточуючого середовища В одному аспекті даний винахід стосується взаємодії між молекулою карбапенемової основи і 2-им положенням бічного ланцюга, так щоб вона стала достатньо швидкою і ефективною з точки зору мінімізації утворення побічних продуктів і з тим, щоб уникнути високих і низьких температур, а також інших ВІДПОВІДНИХ умов реакції В іншому своєму аспекті винахід ставить своєю метою уникнути використання каталізаторів і інших компонентів реакції, які можуть вимагати введення окремої стадії для їх видалення, якщо їх сліди будуть виявлятися в кінцевому продукті Ці І ІНШІ аспекти даного винаходу стануть очевидними з наведеного опису Запропоновано спосіб одержання сполуки формули І ропіламшу (ДІПА), дициклогексиламшу (ДЦГА), 2,2,6,6-тетраметилпіперидину (ТМП), 1,1,3,3тетраметилгуанідину (ТМГ), 1,8діазабіцикло[4 3 0]ундец-7-ену (ДБУ) і 1,5діазабіцикло[4 3 0]нон-5-ену (ДБН), з одержанням сполуки формули Іа 3 Спосіб за п 1, який відрізняється тим, що вторинний амін обирають з групи, що складається з дизопропіламшу (ДІПА) і дициклогексиламшу (ДЦГА) 4 Спосіб за п 3, який відрізняється тим, що синтез здійснюють в полярному апротонному розчиннику 5 Спосіб за п 4, який відрізняється тим, що полярний апротонний розчинник обирають з групи, що складається з диметилформаміду, Nетилпіролідинону і ацетонітрилу Н Н J н,с о абоСНз ~сп або и фармацевтично придатної солі або складного ефіру, де кожний Р незалежно позначає Н або захисну групу і R1 і R2 незалежно один від одного позначають Н, Сі ю алкіл, арил або гетероарил або заміщений Сі ю алкіл, арил або гетероарил, який включає взаємодію сполук HS або- и фармацевтично прийнятної солі або складного ефіру і або його фармацевтично прийнятної солі або складного ефіру, де X позначає OP(O)(OR)2 або OSO2R, де R позначає Сі є алкіл, Сі є алкарил, арил або перфтор Сі є алкіл, в присутності аміну, обраного з групи, що складається з дмзопропіламіну (ДІПА), дициклогексиламшу (ДЦГА), 2,2,6,6-тетраметилпіперидину (ТМП), 54444 1,1,3,3-тетраметилгуанідину (ТМГ), 1,6діазабіцикло[4,3,0]ундец-7-ену (ДБУ) і 1,5діазабіцикло[4,3,0]нон-5-ену (ДБН) з одержанням сполуки формули І Було виявлено, що наведені в даному описі аміни сприяють реакції між сполуками формул І, і III Що стосується сполук формул II і III, то вони можуть бути одержані за методиками, що описані, наприклад, в патентах США № 5 034 384 від 23 липня 1991 р , і № 4 994 568, від 19 лютого 1991, які внесені в даний опис в якості посилань Сполуки, такі як сполуки формул II і ІІІа, можуть бути також одержані за методом з патенту США № 5 478 820, від 26 грудня 1995 р , який також внесений в даний опис в якості посилання Наведені в даному описі реакції проводять в полярному апротонному розчиннику Кращі приклади полярних апротонних розчинників включають диметилформамід, N-етилпіролідинон і ацетон ітр и л Кращий варіант винаходу включає спосіб одержання сполуки формули Іа рад и9с ООгР Іа або и фармацевтичне прийнятної солі або складного ефіру, де кожний Р незалежно позначає Н або захисну групу, який включає взаємодію сполуки lla або її фармацевтичне прийнятної солі або складного ефіру і ОР OP(O){OPh)2 ша або фармацевтичне прийнятної солі або складного ефіру, де Рп позначає феніл, в присутності аміну, обраного з групи, що складається з дмзопропіламіну (ДІПА), дициклогексиламшу (ДЦГА), 2,2,6,6-тетраметилпіперидину (ТМП), 1,1,3,3-тетраметилгуанідину (ТМГ), 1,8діазабіцикло[4,3,0]ундец-7-ену (ДБУ) і 1,5діазабіцикло[4,3,0]нон-5-ену (ДБН) з одержанням сполуки формули Іа Докладний опис даного винаходу містить використання термінів, значення яких, якщо не вказано особо, наведено нижче Термін «алкіл» стосується радикалу, похідного від одновалентного алкану (вуглеводню), що містить від 1 до 15 атомів вуглецю, якщо не вказано інше Він може бути прямим або розгалуженим, і при умові достатньої довжини, наприклад, як Сз 15, бути циклічним Кращі прямі або розгалужені алкільні групи включають метил, етил, пропіл, ізопропіл, бутил і т-бутил Кращі циклоалкільні групи включають циклопропіл, циклопентил і циклогексил Алкіл також включає алкильну групу, що заміщена циклоалкільною групою, таку як циклопропіл метил Алкіл також включає пряму або розгалужену алкильну групу, яка містить або переривається циклоалкіленовим фрагментом Приклади їх включають такі Г де х' і у' приймають значення від 0 до 10, і w і z приймають значення від 0 до 9 Алкіленовий і одновалентний алкильний фрагмент^) алкильної групи можуть бути приєднані в будь-якій доступній для такого приєднання точці до циклоалкіленової частини У випадку, якщо є заміщений алкіл, він стосується певної визначеної вище прямої розгалуженої або циклічної алкільної групи, що заміщена 1-3 групами, визначеними відносно кожної перемінної Термін «гетероалкіл» стосується алкільної групи, що містить 2-15 атомів вуглецю, яка переривається 1-4 гетероатомами, обраними з О, S і N Термін «алкеніл» стосується вуглеводневого радикалу, прямого, розгалуженого або циклічного, що містить від 2 до 15 атомів вуглецю і, принаймні один, подвійний вуглець-вуглецевий зв'язок Краще, є один вуглець-вуглецевий подвійний зв'язок і може бути до чотирьох неароматичних (що не резонують) подвійних вуглець-вуглецевих зв'язків Кращі алкенільні групи включають етеніл, пропеніл, бутеніл і циклогексеніл Аналогічно тому, що було відмічено по відношенню алкілу, пряма, розгалужена або циклічна частина алкенільної групи може містити ПОДВІЙНІ зв'язки і може бути заміщена, утворюючи заміщену алкенільну групу Термін «алкініл» стосується до вуглеводневого радикалу, прямого, розгалуженого або циклічного, що містить від 2 до 15 атомів вуглецю і, принаймні, один потрійний вуглець-вуглецевий зв'язок Може бути до трьох потрійних вуглецьвуглецевих зв'язків Кращі алкінільні групи включають етиніл, пропініл і бутиніл Аналогічно тому, що було відмічені по відношенню алкілу, пряма, розгалужена або циклічна частина алкінільної групи може містити потрійні зв'язки і може бути заміщена, утворюючи заміщену алкінільну групу Термін «арил» позначає ароматичні кільця, наприклад, фенільну, заміщену фенільну і подібні групи, а також конденсовані кільця, наприклад, нафтил і ін Арил, таким чином, має, принаймні, одне кільце, що має, принаймні 6 атомів, при цьому може бути до двух таких кілець, що мають до 10 атомів, з наявністю (резонуючих) подвійних зв'язків, ЯКІ резонують, між суміжними атомами вуглецю Кращими арильними групами є феніл і 54444 нафтил Арильні групи можуть бути також замішені, як було визначено вище Кращі заміщені арильні групи включають феніл і нафтил, заміщені однією-трьома групами, обраними, наприклад, з галогену, алкілу і трифторметилу Термін «гетероарил» стосується моноциклічноі вуглецевої групи, що включає 5 або 6 атомів, або біциклічної ароматичної групи, що включає від 8 до 10 атомів, які мають, принаймі один, гетероатом О, S або N, і в яких точкою прикріплення є атом вуглецю або азоту, а один додатковий атом вуглецю не обов'язково може бути заміщений гетероатомом, обраним з О або S, і в яких також від 1 до 3 додаткових атомів вуглецю можуть бути не обов'язково заміщені гетероатомами азоту Гетероарильна група не обов'язково може в якості замісників містити до трьох груп Гетероарил включає ароматичні і частково ароматичні групи, які можуть мати один або більше гетероатомів Приклади груп першого типу включають тюфен, пурин, імідазопіридин, піридин, оксазол, тіазол, оксазин, піразол, тетразол, імідазол, піридин, піримідин, піразин і тріазин Прикладами частково заміщених ароматичних груп являються тетрапдроімідазо[4,5-с]піридин, фталідил і сахариніл, як визначено вище Заміщені алкил, арил і гетероарил, а також заміщені частини аралкілу, аралкокси, гетероарилкілу, гетероаралкокси і інших груп заміщуються 1-3 групами, обраними з групи, що складається з галогену, гідрокси, ціано, ацилу, ациламшо, аралкокси, алкилсульфонілу, арилсульфонілу, алкилсульфоніламіно, арилсульфоніламіно, алкіламшокарбонілу, алкілу, алкокси, арилу, арилокси, аралкокси, аміно, алкіламшо, діалкіламіно, карбокси і сульфоніламшо Терміни «гетероциклоалкіл» і «гетероцикліл» стосуються циклоалкільної групи (неароматично і), в якій один з атомів вуглецю в КІЛЬЦІ заміщується гетероатомом, обраним з О, S(O)y або N, і в якій до трьох додаткових атомів вуглецю можуть бути заміщені вказаними гетероатомами Коли в гетероциклі є три гетероатоми, вони не зв'язані разом Прикладами гетероциклілів є піперидиніл, морфолініл, азетидиніл, піролІДИНІЛ, тетрапдрофураніл, імідазолініл, піперазиніл, піролідин-2-он, піперидин-2-он і ш Використаний в контексті цього опису ацил стосується -С(О)Сі є алкілу і -С(О)-арилу Ациламшо стосується групи -NHC(O)Ci є алкіл і -І\ІНС(О)арил Аралкокси стосується групи -ОСі є алкіларил Алкарил стосується групи Сі є алкіларилАлкілсульфоніл стосується групи -SO2C1 є алкіл Алкілсульфоніламшо стосується групи NHSO2Ci є алкіл Арилсульфоніламіно стосується групи -NHSO2 арил Алкіламшокарбоніл стосується групи C(O)NHCi є алкіл Арилокси стосується групи -О-арил Сульфоніламшо стосується групи -NHSO3H Галоген означає СІ, F, Вг і І, які обираються незалежно один від одного Сполуки за цим винаходом використовуються 8 у виді різних фармацевтичне прийнятних солей Термін «фармацевтичне прийнятна сіль» відноситься до тих сольових форм, вибір яких очевидний для будь-якого хіміка-фармацевта, тобто це солі, які по суті є нетоксичні і мають потрібні фармакокшетичні властивості, приємний смак, певні параметри абсорбції, розподілу, метаболізму і виведення Іншими факторами, більш практичними по своїй природі, які також відіграють важливу роль при виборі, є ціна сировинних матеріалів, легкість кристалізації, вихід, стабільність, гігроскопічність і плинність одержаної маси лікарського засобу Для зручності використання фармацевтичні композиції можуть бути одержані при сполучені активних інгредієнтів з фармацевтично прийнятними носіями Фармацевтично прийнятні солі сполук формули І включають традиційні нетоксичні солі і четвертинні амонієві солі утворених сполук формули І, наприклад, в сполученні з неорганічною або органічною катіонною групами Ці солі можуть включати, наприклад, навантаження з компенсуючих катіонів, що присутні при необхідності в сполученні з сполукою для надання їй в цілому нейтральних властивостей нейтральності В типовому випадку такі навантаження можуть відноситися до типу фармацевтично прийнятного солеутворюючого юну, такого як натрій, калій, магній і ін Коли протиюн відноситься до типу біс катіону, наприклад, Са+2, він в типовому випадку є присутнім у ВІДПОВІДНІЙ КІЛЬКОС і відносно групування карбапенему для цілей підтримки загальної нейтральності заряду Так, половина молярного еквіваленту Са +2 може бути включена для цілей підтримки загальної нейтральності заряду Всі вказані варіанти включені в рамки цього винаходу В роботі Berge, S М , et al J Pharm Sci 66(1) 1-16(1977), яка вказана в якості посилання, наведені різні солеутворюючі іони Кращий тип солеутворюючих ІОНІВ вибирають з групи, що складається з натрію, калію, кальцію і магнію Найкраще, катіон позначає представника групи, що складається з Na+, Ca +2 1 К+ Фармацевтично прийнятні солі за цим винаходом можуть бути синтезовані за допомогою традиційних ХІМІЧНИХ методів В основному, солі одержують в ході реакції вільних основи або кислоти з стехіометричними кількостями або з надлишком бажаних солеутворюючих неорганічних або органічних кислоти або основи, в підхожому розчиннику або в сполученні розчинників Одна краща для використання за цим винаходом група амінів включає дизопропіламш і дициклогексиламш Ці аміни утворюють кристалічні солі з дифенілфосфорною кислотою, яка кристалізується з суміші в реакції сполучення, що дає можливість видаляти фосфорну кислоту як побічний продукт реакції При використанні вказаних вище амінів швидкість реакції несподівано збільшується Одержаний за цим винаходом сполуки мають асиметричні центри і можуть мати вид як рацематів, рацемичних сумішей, так і індивідуальних діастереомерів Способи синтезу всіх таких ізомерів, включаючи оптичні ізомери, також включені в цей 54444 винахід Карбоксильна група в 3-ому положенні і гідроксильна група у 8-ому положенні карбапенему, азот піролідинилу і, якщо є, м-карбофенільне групування можуть залишатися в блокованому стані до одержання готового продукту Вказані блокуючі групи легко видаляються, наприклад, вони можуть бути видалені, якщо бажано, з застосуванням процедур, які не викликають розщеплення або інших порушень залишених частин молекули Такі процедури включають ХІМІЧНИЙ і ензиматичний гідроліз, обробку в м'яких умовах ХІМІЧНИМИ відновниками або окислювачами, обробку іонами фтору, обробку каталізатором перехідного металу і нуклеофілом і каталітичну гідрогенізацію Приклади підхожих захищаючих груп для гідроксилу включають т-бутилметоксифенілсиліл, тбутоксидифенілсиліл, триметилсиліл, триетилсиліл, о-нітробензилоксікарбоніл, пнітробензилоксікарбоніл, бензилоксикарбоніл, тбутилоксікарбоніл, 2,2,2-трихлоретилоксікарбоніл і алілоксікарбоніл Кращими захищаючими гідроксил групами є триметилсиліл і триетилсиліл Прикладами підхожих захищаючих груп для карбоксилу є бензил гід рил, о-нітробензвил, пнітробензил, 2-нафти л метил, аліл, 2-хлораліл, бензил, 2,2,2-трихлорітил, триметилсиліл, тбутилдіметилсиліл, т-бутилдифенілсиліл, 2(триметілсиліл)етил, фенацил, п-метоксибензил, ацетоніл, п-метоксифеніл, 4-піридилметил і тбутил Кращою захищаючою карбоксил групою є пнітробензил В техніці відомо багато інших груп, підхожих для захисту гідроксилу і карбоксилу (Див , І априклад, T W Greene, Protective Groups in Organic Synthesis, John Wiley & Sons, Inc , 1981 (Chapters 2 and 5) Цей винахід ілюструється такими не обмежуючими його прикладами Препаративний приклад (23,43)-1-(п-нітробензилоксикарбоніл)-2-(3карбоксифенілкарбамоіл)-піролідин-4-ілтюл Сідекаштюл(В) 10 20 - 25°С) В колбу об'ємом 1л вносять 540мл екстракту 6,6г м-амінобензойної кислоти і 1,0мл трибутилфосфіну Суміш дегазують і концентрують до 200мл перегонкою під атмосферним тиском В ході перегонки додають толуол і продовжують и доти, поки температура дистиляту не досягне 110°С Потім додають оцтову кислоту (200мл) і 1пропанол (200мл), охолоджують одержану суміш до 15 - 20°С і витримують при цій температурі 18 годин Продукт ВІДДІЛЯЮТЬ фільтруванням, здійснюючи промивання 1-пропанолом і висушування під вакуумом при 80°С з одержанням 15,4г сідекаїнтюлу HS, DMF PN2 гп-ипробенакпвфбаиат PNB зи-щтробемэип PNZ Приклад 1 З'єднують сполуку А (594мг, 1,0ммоль) і сполуку В (454мг, 1,02ммоль) і додають ДМФ (2,0мл) Дегазують суміш Одержаний розчин охолоджують до температури від -50°С до -30°С Додають дмзопропіламін (204мг, 0,28мл) Через 2 - З години реакція завершується з рівнем конверсії > 98% Порівняльний приклад Здійснюють процедуру Прикладу 1, за винятком того, що в даній реакції дмзопропіламін заміняють рівною молярною КІЛЬКІСТЮ дизопропілетиламіну Через 18 годин реакція завершується (ступінь конверсії 98%) І. DIPEA Н»С' HQ COjPNB ПНЗ Г дроксипропін h .В. 131,13 ПНЗ пдроксипролін (15г) перемішують в суміші ТГФ (225мл) і толуолу (75мл) і суміш охолоджують до - 10°С Додають дмзопропілетиламін (13,4г) і потім розчин 12,1г хлориду дифенілфосфинової кислоти в 15мл толуолу Суміш витримують 2 години при - 10°С і додають 4,1г піридину в 4мл толуолу і потім 6,29г метансульфонілхлориду в 4мл толуолу Через 4 години додають розчин три гідрату сульфіду натрію (7,0г) в 75мл води і суміш нагрівають до 20°С і витримують протягом 14 годин Розділяють шари і органічний шар екстрагують НС1 (150мл, 1,0 N) бікарбонатом натрію (280мл 5%, 40 - 45°С) і водяним NaCI (150мл, насичений, ДМФ -20°С Приклад 2 Використовуючи в основному процедуру, описану в Прикладі 1, заміняють дизопропіламш, що взятий в якості основи, дизопропілетиламіном (ДІПЕА) Швидкість реакції між А и В', яка приводить до одержання С, значно вище у випадку ДІПА і інших наведених в описі амінів, ніж при використанні ДІПЕА 11 54444 12 Таблиця ДБУ (DBU) ДІПА (DIPA) TMr(TMG) ТМП (ТМР) ДІПЕА (DIPEA) Час, необхідний для 98% конверсії 4 год3 Вихід В % Ступінь чистоти, % 98 98 92 Ь 97,3 98,0 В реакціях використовують еквімолярні КІЛЬКОСТІ А І В' при 0,1 ви при -20°С а приблизно 90% конверсія за 4 години, b вихід за 4 години Підписано до друку 03 04 2003 р концентрації і наявності 1,1 еквів осно Тираж 39 прим ТОВ "Міжнародний науковий комітет" вул Артема, 77, м Київ, 04050, Україна (044)236-47-24
ДивитисяДодаткова інформація
Назва патенту англійськоюA process for preparing carbapenem antibiotics
Назва патенту російськоюСпособ получения карбапенемовых антибиотиков
МПК / Мітки
МПК: C07D 477/00
Мітки: одержання, спосіб, карбапенемових, антибіотиків
Код посилання
<a href="https://ua.patents.su/6-54444-sposib-oderzhannya-karbapenemovikh-antibiotikiv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання карбапенемових антибіотиків</a>
Попередній патент: Буровий амортизатор
Наступний патент: Спосіб одержання кишковорозчинних таблеток ацетилсаліцилової кислоти
Випадковий патент: Дисковий кристалізатор










