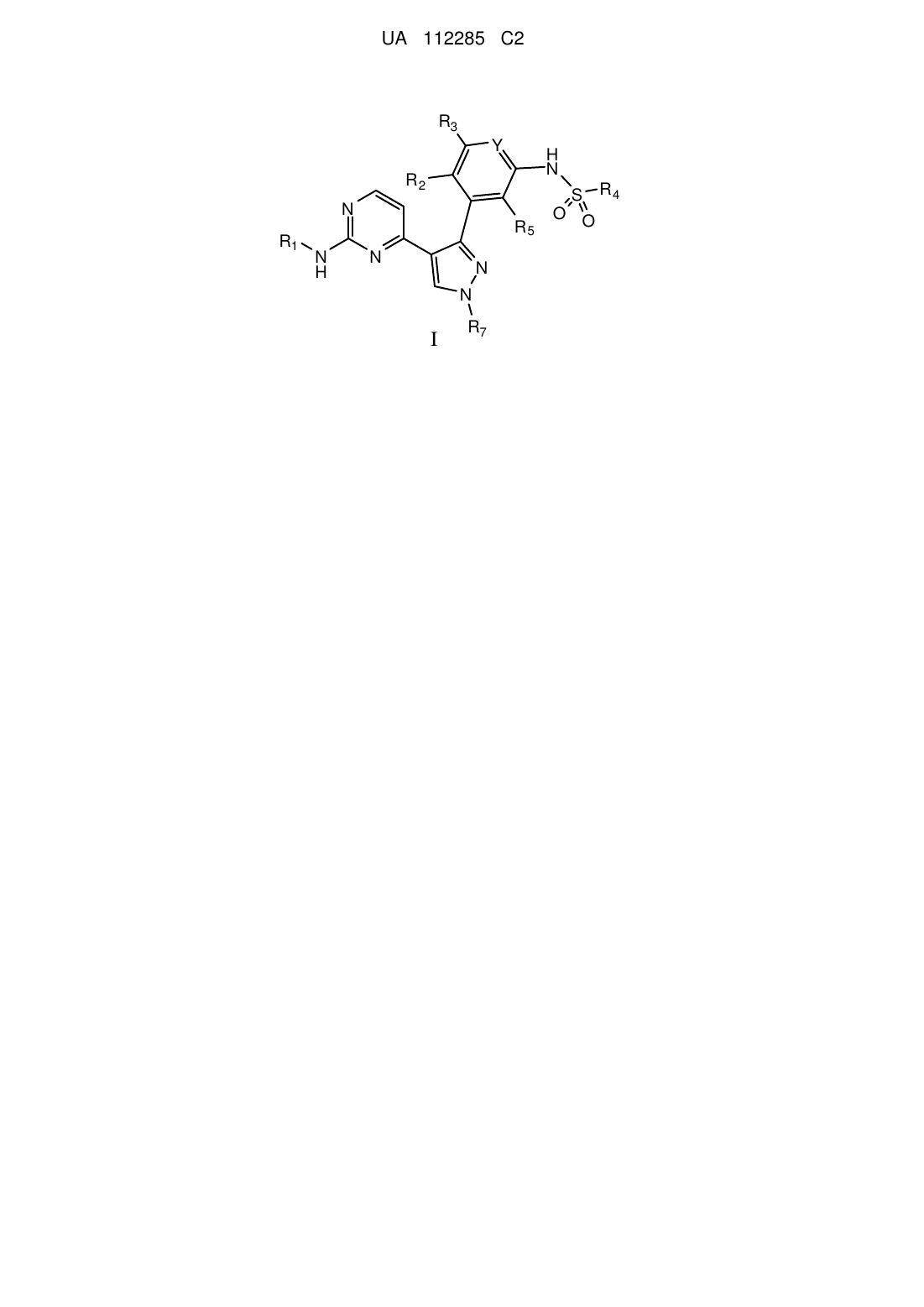
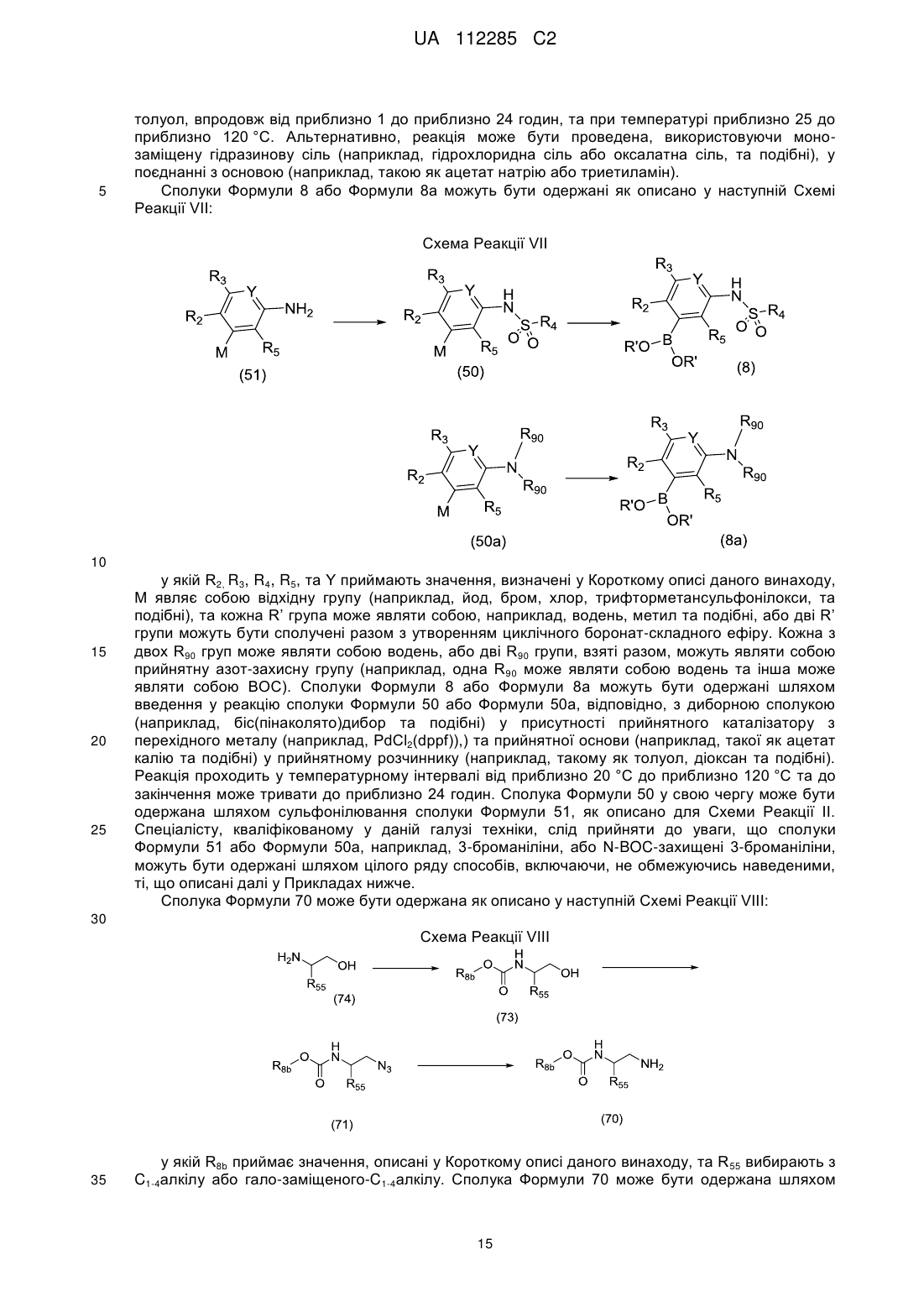
Сполуки та композиція як інгібітори протеїнкінази
Номер патенту: 112285
Опубліковано: 25.08.2016
Автори: Ксіе Йонгпінг, Хуанг Шенлін, Теллью Джон І., Джін Ксіанмінг, Ванг Ксінг, Ліу Зуошенг, Пун Деніел, Ван Йонгцін
Формула / Реферат
1. Сполука Формули Іа:
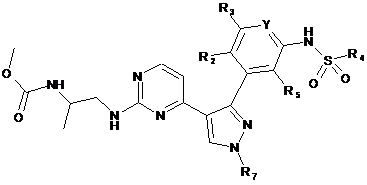 , Ia
, Ia
у якій:
Y вибраний з N та CR6;
R2, R3, R5 та R6 незалежно вибрані з таких як: водень, галоген, ціаногрупа, С1-4алкіл, галогензаміщений С1-4алкіл, С1-4алкоксигрупа та галогензаміщена С1-4алкоксигрупа; за умови, що, коли R5 являє собою фтор, тоді R3 та R6 не обидва являють собою водень;
R4 вибраний з -R9 та -NR10R11; де R9 вибраний з С1-6алкілу, С3-8циклоалкілу, С3-8гетероциклоалкілу, арилу та гетероарилу; де зазначений алкіл, циклоалкіл, гетероциклоалкіл, арил або гетероарил радикала R9 є необов'язково заміщеним за допомогою 1-3 радикалів, що незалежно вибирають з таких як: галоген, ціаногрупа, С1-4алкіл, галогензаміщений С1-4алкіл, С1-4алкоксигрупа та галогензаміщена С1-4алкоксигрупа; та R10 та R11 незалежно вибрані з водню та R9;
R7 вибраний з таких як: водень, С1-4алкіл, С3-5циклоалкіл та С3-5гетероциклоалкіл; де зазначений алкіл, циклоалкіл або гетероциклоалкіл радикала R7 є необов'язково заміщеним за допомогою 1-3 радикалів, що незалежно вибирають з таких як: галоген, ціаногрупа, гідроксил, С1-4алкіл, галогензаміщений С1-4алкіл, С1-4алкоксигрупа та галогензаміщена С1-4алкоксигрупа; або її таутомери, стереоізомери або фармацевтично прийнятні солі.
2. Сполука за п. 1, у якій R4 являє собою -R9; де R9 вибраний з С1-3алкілу та С3-8циклоалкілу; де зазначений алкіл або циклоалкіл радикала R9 є необов'язково заміщеним за допомогою 1-3 радикалів, що незалежно вибирають з таких як: галоген та галогензаміщений С1-4алкіл.
3. Сполука за п. 2, у якій:
R2 вибраний з водню та фтору;
R3 вибраний з хлору, фтору та метилу;
R5 вибраний з таких як: водень, хлор та фтор;
Y вибраний з N та CR6; та
R6 вибраний з водню та фтору.
4. Сполука за п. 1, вибрана з групи, яка включає:
метил-N-[(2S)-1-({4-[3-(3-хлор-5-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)-пропан-2-іл]карбамат;
метил-N-[(2S)-1-[(4-{3-[3-хлор-5-(пропан-1-сульфонамідо)феніл]-1-(пропан-2-іл)-1Н-піразол-4-іл}піримідин-2-іл)аміно]пропан-2-іл]карбамат;
метил-N-[(2S)-1-({4-[3-(3-хлор-2-метансульфонамідопіридин-4-іл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат;
метил-N-[(2S)-l-({4-[3-(3-фтор-2-метансульфонамідопіридин-4-іл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат;
метил-N-[(2S)-1-({4-[3-(2-хлор-3-етансульфонамідо-4,5-дифторфеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат;
метил-N-[(2S)-1-({4-[3-(2,4-дифтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат;
метил-N-[(2S)-1-({4-[1-(пропан-2-іл)-3-(2,4,5-трифтор-3-метансульфонамідофеніл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат;
метил-N-[(2S)-1-({4-[3-(3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат;
метил-N-[(2S)-1-({4-[3-(3-етансульфонамідо-2,4-дифторфеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат;
метил-N-[(2S)-2-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропіл]карбамат;
метил-N-[(2S)-l-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(оксан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат;
метил-N-[(2S)-1-[(4-{3-[2,4-дифтор-3-(пропан-1-сульфонамідо)феніл]-1-(пропан-2-іл)-1Н-піразол-4-іл}піримідин-2-іл)аміно]пропан-2-іл]карбамат;
метил-N-[(2S)-1-({4-[3-(3-циклопропансульфонамідо-2,5-дифторфеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат;
метил-N-[(2S)-1-({4-[3-(5-хлор-3-циклопропансульфонамідо-2-фторфеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат;
метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат та
метил-N-[(2S)-1-[(4-{3-[5-хлор-2-фтор-3-(пропан-1-сульфонамідо)феніл]-1-(пропан-2-іл)-1Н-піразол-4-іл}піримідин-2-іл)аміно]пропан-2-іл]карбамат.
5. Сполука за п. 1, що має Формулу Іb:
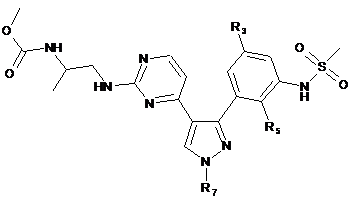 , Ib
, Ib
у якій:
R3 вибраний з хлору, фтору та метилу;
R5 вибраний з фтору та хлору; та
R7 вибраний з етилу та ізопропілу.
6. Сполука за п. 5, вибрана з групи, яка включає:
метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат;
метил-N-[(2S)-1-({4-[3-(2,5-дифтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат;
метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-етил-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат;
метил-N-[(2S)-1-({4-[3-(2-фтор-3-метансульфонамідо-5-метилфеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат;
метил-N-[(2S)-1-({4-[3-(2-хлор-3-метансульфонамідо-5-метилфеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}-аміно)пропан-2-іл]карбамат;
метил-N-[(2S)-1-({4-[3-(2-хлор-5-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат;
метил-N-[(2R)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат та
метил-N-[(2S)-1-({4-[3-(2,5-дихлор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат.
7. Сполука, вибрана з групи, яка включає:
метил-N-[(2S)-1-[(4-{3-[2-фтор-3-(пропан-1-сульфонамідо)феніл]-1-(пропан-2-іл)-1Н-піразол-4-іл}піримідин-2-іл)аміно]пропан-2-іл]карбамат;
метил-N-[(2S)-1-({4-[3-(2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат;
метил-N-[(2S)-1-({4-[3-(2,6-дифтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат;
метил-N-[(2S)-1-[(4-{3-[2,6-дифтор-3-(пропан-1-сульфонамідо)феніл]-1-(пропан-2-іл)-1Н-піразол-4-іл}піримідин-2-іл)аміно]пропан-2-іл]карбамат та
метил-N-[(2S)-1-{[4-(3-{2-фтор-3-[(3,3,3-трифторпропан)сульфонамідо]феніл}-1-(пропан-2-іл)-1Н-піразол-4-іл)піримідин-2-іл]аміно}пропан-2-іл]карбамат.
8. Сполука, вибрана з групи, яка включає:
3-бром-5-хлор-2-фторанілін;
ціано-(2-метилтіопіримідин-4-іл)-оцтової кислоти трет-бутиловий складний ефір;
1-ізопропіл-4-(2-(метилтіо)піримідин-4-іл)-1Н-піразол-3-амін;
2-((2-бензиліден-1-етилгідразиніл)метилен)малононітрил;
1-(3-аміно-1-ізопропіл-1Н-піразол-4-іл)етанон;
1-(3-йод-1-ізопропіл-1Н-піразол-4-іл)етанон;
1-(3-йод-1-етил-1Н-піразол-4-іл)етанон;
1-(3-йод-1-метил-1Н-піразол-4-іл)етанон;
3-(диметиламіно)-1-(3-йод-1-ізопропіл-1Н-піразол-4-іл)проп-2-ен-1-он;
3-(диметиламіно)-1-(3-йод-1-етил-1Н-піразол-4-іл)проп-2-ен-1-он;
3-(диметиламіно)-1-(3-йод-1-метил-1Н-піразол-4-іл)проп-2-ен-1-он;
4-(3-йод-1-ізопропіл-1Н-піразол-4-іл)піримідин-2-амін;
4-(3-йод-1-етил-1Н-піразол-4-іл)піримідин-2-амін;
4-(3-йод-1-метил-1Н-піразол-4-іл)піримідин-2-амін;
4-(3-йод-1-ізопропіл-1Н-піразол-4-іл)піримідин-2-ол;
2-хлор-4-(3-йод-1-ізопропіл-1Н-піразол-4-іл)піримідин;
(S)-метил-1-(4-(3-йод-1-ізопропіл-1Н-піразол-4-іл)піримідин-2-іламіно)пропан-2-ілкарбамат;
(R)-метил-1-(4-(3-йод-1-ізопропіл-1Н-піразол-4-іл)піримідин-2-іламіно)пропан-2-ілкарбамат;
(S)-трет-бутил-1-(4-(3-йод-1-ізопропіл-1Н-піразол-4-іл)піримідин-2-іламіно)пропан-2-ілкарбамат;
3-(4-(3-йод-1-ізопропіл-1Н-піразол-4-іл)піримідин-2-іламіно)пропаннітрил;
4-(3-йод-1-ізопропіл-1Н-піразол-4-іл)-N-метилпіримідин-2-амін;
N1-(4-(3-йод-1-ізопропіл-1Н-піразол-4-іл)піримідин-2-іл)-N2,N2-диметилетан-1,2-діамін;
N-(3-бром-2,4-дифторфеніл)пропан-1-сульфонамід;
3-фтор-4-йодпіридин-2-амін;
3-бром-2,5,6-трифторанілін;
2,4-дибром-3,6-дихлоранілін;
3-бром-2-хлор-5-метиланілін;
3-бром-2,5-дифторанілін;
3-бром-5-хлор-2-фторбензойну кислоту;
трет-бутил-3-бром-5-хлор-2-фторфенілкарбамат;
трет-бутил-3-бром-2-фтор-5-метилфенілкарбамат;
трет-бутил-5-хлор-2-фтор-3-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)фенілкарбамат;
трет-бутил-2,6-дифтор-3-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)фенілкарбамат;
N-(2,4-дифтop-3-(4,4,5,5-тeтpaмeтил-1,3,2-дioкcaбopoлaн-2-iл)фeнiл)пpoпaн-1-сульфонамід;
2,5-дифтор-3-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)анілін;
2-хлор-5-фтор-3-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)анілін;
2,5-дихлор-3-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)анілін;
2-хлор-5-метил-3-(4,4,5,5-тетраметил-1,3,2-дiоксаборолан-2-іл)анілін;
трет-бутил-2-фтор-5-метил-3-(4,4,5,5-тетраметил-1,3,2-дiоксаборолан-2-іл)фенілкарбамат;
3-фтор-4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)піридин-2-амін;
2,3,6-трифтор-5-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)анілін;
3-хлор-4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)піридин-2-амін;
3-хлор-5-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)анілін та
3-метокси-2-метил-5-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)анілін.
9. Фармацевтична композиція, що включає сполуку за будь-яким з пп. 1-7 у суміші з щонайменше одним фармацевтично прийнятним наповнювачем.
10. Фармацевтична композиція за п. 9, у якій наповнювач вибраний з групи, що включає такі як: кукурудзяний крохмаль, картопляний крохмаль, маніоковий крохмаль, крохмальна паста, прежелатинізований крохмаль, цукри, желатин, природні камеді, синтетичні камеді, альгінат натрію, альгінова кислота, трагакантова камедь, гуарова камедь, целюлоза, етилцелюлоза, ацетат целюлози, карбоксиметилцелюлоза кальцію, карбоксиметилцелюлоза натрію, метилцелюлоза, гідроксипропілметилцелюлоза, мікрокристалічна целюлоза, алюмосилікат магнію, полівінілпіролідон, тальк, карбонат кальцію, порошкоподібна целюлоза, декстрати, каолін, маніт, кремнієва кислота, сорбіт, агар-агар, карбонат натрію, кроскармелоза натрію, кросповідон, полакрилін калію, натрію крохмалю гліколят, глини, стеарат натрію, стеарат кальцію, стеарат магнію, стеаринова кислота, мінеральне масло, легке мінеральне масло, гліцерин, поліетиленгліколь, інші гліколі, лаурилсульфат натрію, гідрогенізована рослинна олія, арахісова олія, бавовняна олія, соняшникова олія, кунжутна олія, оливкова олія, кукурудзяна олія, соєва олія, стеарат цинку, олеат натрію, етилолеат, етиллаурат, кремнезем та їх комбінації.
11. Фармацевтична композиція за п. 9, яка додатково включає додатковий терапевтичний агент.
12. Фармацевтична композиція за п. 11, у якій додатковий терапевтичний агент вибраний з таких як: протиракова сполука, знеболюючий засіб, протиблювотний засіб, антидепресант або протизапальний агент.
13. Сполука за будь-яким з пп. 1-7 для лікування раку.
14. Сполука за п. 13, де рак, який необхідно лікувати, вибирають з групи, що включає такі як: карцинома легені, рак підшлункової залози, карцинома сечового міхура, карцинома товстої кишки, мієлоїдні розлади, рак передміхурової залози, рак щитовидної залози, меланома, аденоми та карциноми яєчника, ока, печінки, жовчних проток та нервової системи.
15. Спосіб лікування раку, що включає введення суб'єкту, який потребує такого лікування, ефективної кількості сполуки за будь-яким з пп. 1-7 або фармацевтичної композиції за будь-яким з пп. 9-12.
16. Спосіб за п. 15, де рак вибирають з групи, що включає такі як: карцинома легені, рак підшлункової залози, карцинома сечового міхура, карцинома товстої кишки, мієлоїдні розлади, рак передміхурової залози, рак щитовидної залози, меланома, аденоми та карциноми яєчника, ока, печінки, жовчних проток та нервової системи.
17. Спосіб за п. 15 або 16, який додатково включає введення суб'єкту додаткового терапевтичного агента.
18. Спосіб за п. 17, у якому додатковий терапевтичний агент включає протиракову сполуку, знеболюючий засіб, протиблювотний засіб, антидепресант або протизапальний агент.
19. Спосіб за п. 18, у якому додатковий терапевтичний агент являє собою інший інгібітор Raf-кінази або інгібітор МЕK, mTOR, HSP90, АKТ, РІ3K, CDK9, РАK, протеїнкіназу С, МАР-кіназу, МАРК кіназу або ERK.
20. Спосіб за п. 19, у якому МЕK-інгібітор вибирають з таких як: AS703026; MSC1936369B; GSK1120212; AZD6244; PD-0325901; ARRY-438162; RDEA119; GDC0941; GDC0973; ТАК-733; RO5126766 та XL-518.
21. Спосіб за п. 20, у якому додатковий терапевтичний агент вводять суб'єкту одночасно зі сполукою.
22. Спосіб лікування стану, опосередкованого Raf-кіназою, що включає введення суб'єкту, який потребує такого лікування, ефективної кількості сполуки за будь-яким з пп. 1-7 або фармацевтичної композиції за будь-яким з пп. 9-12.
23. Спосіб за п. 22, у якому Raf-кіназа являє собою мутантну b-Raf-кіназу.
24. Спосіб за п. 23, у якому мутантна b-Raf-кіназа являє собою b-Raf(V600E).
25. Сполука, що має формулу:
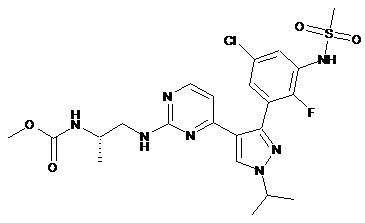
метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат,
або її фармацевтично прийнятна сіль.
26. Сполука за п. 25, яка являє собою метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат.
27. Фармацевтична композиція, що містить сполуку

метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат
або її фармацевтично прийнятну сіль та один або кілька фармацевтично прийнятних наповнювачів.
28. Фармацевтична композиція за п. 27, що містить:

метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1H-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат.
29. Фармацевтична композиція за п. 28, яка сформульована для перорального введення.
30. Фармацевтична композиція за п. 29, у якій один або кілька фармацевтично прийнятних наповнювачів незалежно вибрані з групи, яка складається з: одного або кількох розріджувачів, одного або кількох лубрикантів, однієї або кількох зв'язуючих речовин, одного або кількох дезінтегрантів, одного або кількох абсорбентів, одного або кількох барвників, одного або кількох ароматизаторів та одного або кількох підсолоджувачів.
31. Фармацевтична композиція за п. 30, у якій кожен з одного або кількох фармацевтично прийнятних наповнювачів незалежно вибраний з групи, яка складається з: лактози, декстрози, сахарози, маніту, сорбіту, целюлози, гліцину, кремнезему, тальку, стеаринової кислоти, її магнієвої або кальцієвої солі, поліетиленгліколю, алюмосилікату магнію, крохмальної пасти, желатину, трагаканту, метилцелюлози, карбоксиметилцелюлози натрію, полівінілпіролідону, крохмалів, агар-агару, альгінової кислота або її натрієвої солі, шипучих сумішей, абсорбентів, барвника, ароматизатора та підсолоджувача.
32. Фармацевтична композиція за п. 29, яка сформульована у вигляді таблетки.
33. Фармацевтична композиція за п. 28, де зазначена композиція містить від приблизно 1 мг до приблизно 500 мг метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамату.
34. Фармацевтична композиція за п. 27, яка додатково містить додатковий терапевтичний агент.
35. Фармацевтична композиція за п. 34, у якій додатковий терапевтичний агент являє собою протиракову сполуку.
36. Фармацевтична композиція за п. 35, у якій протиракова сполука являє собою інгібітор МЕK.
37. Фармацевтична композиція за п. 36, у якій МЕK-інгібітор вибраний з таких як: AS703026; MSC1936369B; GSK1120212; AZD6244; PD-0325901; ARRY-438162; RDEA119; GDC0941; GDC0973; ТАК-733; RO5126766 та XL-518.
38. Фармацевтична композиція за п. 37, у якій МЕK-інгібітор являє собою ARRY-438162.
39. Фармацевтична композиція за п. 38, яка містить метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат.
40. Фармацевтична комбінація, яка містить:
і) сполуку, що має формулу:

метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1H-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат
або її фармацевтично прийнятну сіль, та
іі) один або кілька співагентів.
41. Фармацевтична комбінація за п. 40, у якій принаймні один з одного або кількох співагентів являє собою протиракову сполуку.
42. Фармацевтична комбінація за п. 41, у якій протиракова сполука являє собою інгібітор МЕK.
43. Фармацевтична комбінація за п. 42, у якій МЕK-інгібітор вибраний з таких як: AS703026; MSC1936369B; GSK1120212; AZD6244; PD-0325901; ARRY-438162; RDEA119; GDC0941; GDC0973; ТАК-733; RO5126766 та XL-518.
44. Фармацевтична комбінація за п. 43, у якій МЕK-інгібітор являє собою ARRY-438162.
45. Фармацевтична комбінація за п. 44, яка містить:

метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат.
46. Фармацевтична комбінація за п. 45, яка являє собою нефіксовану комбінацію.
47. Фармацевтична комбінація за п. 45, яка являє собою фіксовану комбінацію.
48. Фармацевтична комбінація за п. 45, де зазначена комбінація містить від приблизно 1 мг до приблизно 500 мг зазначеного метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамату.
49. Фармацевтична комбінація за п. 40, де зазначена комбінація являє собою набір.
50. Фармацевтична комбінація за п. 49, де зазначений набір додатково містить інструкції для застосування.
51. Фармацевтична композиція за п. 27, яка містить фармацевтично прийнятну сіль метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамату.
52. Спосіб лікування раку, що включає введення суб'єкту, який потребує такого лікування, ефективної кількості метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамату або його фармацевтично прийнятної солі.
53. Спосіб за п. 52, у якому рак являє собою рак, опосередкований b-Raf-протеїнкіназою.
54. Спосіб за п. 52 або 53, у якому рак вибирають з групи, що включає такі як: карцинома легені, карцинома підшлункової залози, карцинома сечового міхура, карцинома товстої кишки, мієлоїдні розлади, рак передміхурової залози, рак щитовидної залози, меланома, аденоми та карциноми яєчника, ока, печінки, жовчних проток та нервової системи.
55. Спосіб за п. 54, у якому рак являє собою меланому.
56. Спосіб за п. 55, у якому рак являє собою метастатичну меланому.
57. Спосіб за п. 53, у якому рак являє собою меланому з V600E-мутацією в b-Raf-протеїнкіназі.
58. Спосіб за п. 52 або 53, у якому рак являє собою карциному товстої кишки.
59. Спосіб за п. 52 або 53, який додатково включає введення суб'єкту додаткового терапевтичного агента.
60. Спосіб за п. 59, у якому додатковий терапевтичний агент являє собою протиракову сполуку.
61. Спосіб за п. 60, у якому додатковий терапевтичний агент являє собою інший інгібітор Raf-кінази або інгібітор МЕK, mTOR, HSP90, АKТ, РІ3K, CDK9, РАK, протеїнкіназу С, МАР-кіназу, МАРК кіназу або ERK.
62. Спосіб за п. 61, у якому додатковий терапевтичний агент являє собою інгібітор МЕK.
63. Спосіб за п. 62, у якому МЕK-інгібітор вибраний з таких як: AS703026; MSC1936369B; GSK1120212; AZD6244; PD-0325901; ARRY-438162; RDEA119; GDC0941; GDC0973; ТАК-733; RO5126766 та XL-518.
64. Спосіб за п. 63, у якому МЕK-інгібітор являє собою ARRY-438162.
65. Спосіб за п. 64, у якому зазначений метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат або його фармацевтично прийнятна сіль та зазначений ARRY-438162 вводять у вигляді фіксованої комбінації.
66. Спосіб за п. 64, у якому зазначений метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат або його фармацевтично прийнятну сіль та зазначений ARRY-438162 вводять у вигляді нефіксованої комбінації.
67. Спосіб за п. 66, у якому зазначений метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат або його фармацевтично прийнятну сіль та зазначений ARRY-438162 вводять послідовно.
68. Спосіб за п. 66, у якому зазначений метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат або його фармацевтично прийнятну сіль та зазначений ARRY-438162 вводять одночасно.
69. Спосіб за п. 64, у якому рак являє собою меланому.
70. Спосіб за п. 69, у якому рак являє собою метастатичну меланому.
71. Спосіб за п. 69, у якому рак являє собою меланому з V600E-мутацією в b-Raf-кіназі.
72. Спосіб за п. 71, у якому зазначений метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат або його фармацевтично прийнятну сіль та зазначений ARRY-438162 вводять у вигляді нефіксованої комбінації.
73. Спосіб за п. 72, у якому зазначений метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат або його фармацевтично прийнятну сіль та зазначений ARRY-438162 вводять послідовно.
74. Спосіб за п. 71, у якому зазначений метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1H-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат або його фармацевтично прийнятну сіль та зазначений ARRY-438162 вводять у вигляді фіксованої комбінації.
75. Спосіб за п. 64, у якому рак являє собою карциному товстої кишки.
76. Спосіб за п. 75, у якому зазначений метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат або його фармацевтично прийнятну сіль та зазначений ARRY-438162 вводять у вигляді нефіксованої комбінації.
77. Спосіб за п. 76, у якому зазначений метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат або його фармацевтично прийнятну сіль та зазначений ARRY-438162 вводять послідовно.
78. Спосіб за п. 75, у якому зазначений метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат або його фармацевтично прийнятну сіль та зазначений ARRY-438162 вводять у вигляді фіксованої комбінації.
79. Спосіб зменшення розміру однієї або кількох пухлин, що мають мутацію в b-Raf-протеїнкіназі, де спосіб включає приведення в контакт однієї або кількох пухлин з метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбаматом або його фармацевтично прийнятною сіллю, у якому пухлину вибирають з групи, що включає такі як: карцинома легені, рак підшлункової залози, карцинома сечового міхура, карцинома товстої кишки, мієлоїдні розлади, рак передміхурової залози, рак щитовидної залози, меланома, аденоми та карциноми яєчника, ока, печінки, жовчних проток та нервової системи.
80. Спосіб за п. 79, у якому принаймні одна з однієї або кількох пухлин являє собою меланому.
81. Спосіб за п. 80, у якому меланома являє собою метастатичну меланому.
82. Спосіб за п. 80, у якому меланома являє собою меланому з V600E-мутацією в b-Raf-протеїнкіназі.
83. Спосіб за п. 79, у якому принаймні одна з однієї або кількох пухлин являє собою карциному товстої кишки.
84. Спосіб за п. 79, який додатково включає приведення в контакт однієї або кількох пухлин з додатковим терапевтичним агентом.
85. Спосіб викликання стазу та/або смерті однієї або кількох ракових клітин, що мають мутацію в b-Raf-протеїнкіназі, де спосіб включає приведення в контакт однієї або кількох клітин з метил-N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1Н-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбаматом або його фармацевтично прийнятною сіллю, у якому рак вибираний з групи, що включає такі як: карцинома легені, рак підшлункової залози, карцинома сечового міхура, карцинома товстої кишки, мієлоїдні розлади, рак передміхурової залози, рак щитовидної залози, меланома, аденоми та карциноми яєчника, ока, печінки, жовчних проток та нервової системи.
86. Спосіб за п. 85, у якому рак являє собою меланому.
87. Спосіб за п. 86, у якому рак являє собою метастатичну меланому.
88. Спосіб за п. 86, у якому рак являє собою меланому з V600E-мутацією в b-Raf-протеїнкіназі.
89. Спосіб за п. 85, у якому рак являє собою карциному товстої кишки.
90. Спосіб за п. 85, який додатково включає приведення в контакт однієї або кількох ракових клітин з додатковим терапевтичним агентом.
91. Спосіб за будь-яким з пп. 22-24, де сполука має формулу:
 ,
,
або її фармацевтично прийнятна сіль.
92. Спосіб за будь-яким з пп. 22-24 та 91, який додатково включає введення суб'єкту додаткового терапевтичного агента.
93. Спосіб за п. 22, 79 або 85, який здійснюють in vitro.
94. Спосіб за п. 22, 79 або 85, який здійснюють in vivo.
95. Спосіб за п. 84, 90 або 92, у якому додатковий терапевтичний агент являє собою протиракову сполуку.
96. Спосіб за п. 95, у якому додатковий терапевтичний агент являє собою інший інгібітор Raf-кінази або інгібітор МЕK, mTOR, HSP90, АKТ, РІ3K, CDK9, РАK, протеїнкіназу С, МАР-кіназу, МАРК кіназу або ERK.
97. Спосіб за п. 96, у якому додатковий терапевтичний агент являє собою інгібітор МЕK.
98. Спосіб за п. 97, у якому МЕK-інгібітор вибраний з таких як: AS703026; MSC1936369B; GSK1120212; AZD6244; PD-0325901; ARRY-438162; RDEA119; GDC0941; GDC0973; ТАК-733; RO5126766 та XL-518.
99. Спосіб за п. 98, у якому МЕK-інгібітор являє собою ARRY-438162.
Текст
Реферат: Даний винахід забезпечує новий клас сполук, фармацевтичні композиції, що містять такі сполуки, та використання таких сполук для лікування або профілактики хвороб або розладів, пов'язаних з аномальною або дерегульованою активністю кінази, зокрема хвороб або розладів, які залучають аномальну активацію В-Raf. UA 112285 C2 (12) UA 112285 C2 R3 Y H N R2 S R4 N R1 R5 N H N N N I R7 O O UA 112285 C2 5 10 15 20 Дана заявка заявляє пріоритет до Попередніх Патентних Заявок США Номер 61/238,073, поданої 28 серпня 2009 року, та 61/313,039, поданої 11 березня 2010 року. Повні розкриття цих заявок включені у даний опис як посилання у їх повноті та для всіх цілей. ПЕРЕДУМОВИ СТВОРЕННЯ ВИНАХОДУ Галузь винаходу Даний винахід забезпечує новий клас сполук, фармацевтичні композиції, що включають такі сполуки, та способи застосування таких сполук для лікування або профілактики хвороб або розладів, пов’язаних з аномальною або дерегульованою активністю кінази, зокрема хвороб або розладів, які залучають аномальну активацію B-Raf. Попередній рівень техніки Протеїнкінази являють собою велике сімейство білків, які грають головну роль у регулюванні широкого ряду клітинних процесів та підтриманні контролю над клітинною функцією. Частковий, не обмежуючий перелік цих кіназ включає: рецепторні тирозин-кінази, такі як кіназа рецептору тромбоцитарного фактору росту (PDGF-R), рецептор фактору росту нервів, trkB, Met, та рецептор фактору росту фібробластів, FGFR3; нерецепторні тирозин-кінази, такі як Abl та кіназа злиття BCR-Abl, Lck, Csk, Fes, Bmx та c-src; та серин/треонін кінази, такі як B-Raf, sgk, MAP кінази (наприклад, MKK4, MKK6, тощо) та SAPK2α, SAPK2β та SAPK3. Аберантна активність кінази спостерігається при багатьох хворобливих станах, включаючи доброякісні та злоякісні проліферативні розлади, а також хвороби, що є результатом неприйнятної активації імунної та нервової систем. Нові сполуки даного винаходу інгібують активність B-Raf або її мутантних форм (наприклад, V600E) та, тому, як сподіваються, вони будуть корисними у лікуванні пов’язаних з B-Raf хвороб. КОРОТКИЙ ОПИС ВИНАХОДУ У одному аспекті, даний винахід забезпечує сполуки Формули I: 25 R3 Y H N R2 S R4 N R1 R5 N H N O O N N R7 I 30 35 40 45 50 у якій: Y вибирають з N та CR6; R1 вибирають з таких як: водень, –X1R8a, –X1OX2R8a, –X1C(O)NR8aR8b, –X1NR8aX2R8b, – X1NR8aC(O)X2OR8b, –X1NR8aC(O)X2NR8aR8b, –X1NR8aS(O)0-2R8b; де кожен X1 незалежно являє собою C1-4алкілен; та X1 необов’язково має 1-3 атоми водню, замінені групою, що вибирають з таких як: гідрокси-група, гало-група, ціано-група, C1-4алкіл, гало-заміщений-C1-4алкіл, C14алкокси-група та гало-заміщена-C1-4алкокси-група; X2 вибирають зі зв’язку та C1-4алкілену; де R8a та R8b незалежно вибирають з таких як: водень, C1-6алкіл, гало-заміщений-C1-6алкіл, C38циклоалкіл, гетероарил та C 3-8гетероциклоалкіл; де циклоалкіл, гетероциклоалкіл або гетероарил радикалів R8a або R8b необов’язково заміщений за допомогою 1 - 3 радикалів, що незалежно вибирають з таких як: аміно-група, ціано-група, C1-4алкіл, C1-4алкокси-група, галозаміщений-C1-4алкіл та гало-заміщена-C1-4алкокси-група; за умови, що R8b не являє собою водень, коли R1 вибирають з –X1NHC(O)OR8b та –X1NR8aS(O)0-2R8b; R2, R3, R5 та R6 незалежно вибирають з таких як: водень, гало-група, ціано-група, C1-4алкіл, гало-заміщений-C1-4алкіл, C1-4алкокси-група та гало-заміщена-C1-4алкокси-група; за умови, що коли R5 являє собою фтор та R1 вибирають з таких як: водень, –X1R8a, –X1OX2R8a, – X1C(O)NR8aR8b, –X1NR8aX2R8b, –X1NR8aC(O)X2OR8b та –X1NR8aS(O)0-2R8b, R3 та R6 обидва не являють собою водень; R4 вибирають з –R9 та –NR10R11; де R9 вибирають з таких як: C1-6алкіл, C3-8циклоалкіл, C3гетероциклоалкіл, арил та гетероарил; де зазначений алкіл, циклоалкіл, гетероциклоалкіл, 8 арил або гетероарил радикалу R9 необов’язково заміщений за допомогою 1 - 3 радикалів, що незалежно вибирають з таких як: гало-група, ціано-група, C1-4алкіл, гало-заміщений-C1-4алкіл, C1-4алкокси-група та гало-заміщена-C1-4алкокси-група; та R10 та R11 незалежно вибирають з 1 UA 112285 C2 5 10 15 20 25 30 35 40 45 50 55 60 водню та R9; R7 вибирають з таких як: водень, C1-4алкіл, C3-5циклоалкіл та C3-5гетероциклоалкіл; де зазначений алкіл, циклоалкіл або гетероциклоалкіл радикалу R 7 необов’язково заміщений за допомогою 1 - 3 радикалів, що незалежно вибирають з таких як: гало-група, ціано-група, гідроксил, C1-4алкіл, гало-заміщений-C1-4алкіл, C1-4алкокси-група та гало-заміщена-C1-4алкоксигрупа; та їх N-оксидні похідні, пролікарські похідні, захищені похідні, таутомери, окремі ізомери та суміш ізомерів; та фармацевтично прийнятні солі та сольвати (наприклад, гідрати) таких сполук. У другому аспекті, даний винахід забезпечує фармацевтичну композицію, яка містить сполуку Формули I або її N-оксидну похідну, окремі ізомери та суміш ізомерів; або її фармацевтично прийнятну сіль, у суміші з одним або більшою кількістю прийнятних наповнювачів. У третьому аспекті, даний винахід забезпечує спосіб лікування хвороби у тварини, у якому інгібування активності кінази, зокрема активності B-Raf , може запобігати, інгібувати або полегшувати патологію та/або симптомологію хвороб, де спосіб включає введення тварині терапевтично ефективної кількості сполуки Формули I або її N-оксидної похідної, її окремих ізомерів та суміші ізомерів, або її фармацевтично прийнятної солі. У четвертому аспекті, даний винахід забезпечує застосування сполуки Формули I у виробництві лікарського засобу для лікування хвороби у тварини, де активність кінази, зокрема активність B-Raf, особливо мутантної B-raf (наприклад, V600E), вносить свій вклад у патологію та/або симптомологію хвороби. У п’ятому аспекті, даний винахід забезпечує спосіб одержання сполук Формули I та їх Nоксидних похідних, пролікарських похідних, захищених похідних, їх окремих ізомерів та суміші ізомерів, та їх фармацевтично прийнятних солей. КОРОТКИЙ ОПИС МАЛЮНКІВ Фігура 1: На Фігурі 1 показано, що додавання MEK низькомолекулярного інгібітору може обернути викликане ERK сигналювання, клітинний ріст та трансформацію, викликану Raf низькомолекулярним інгібітором. ДЕТАЛЬНИЙ ОПИС ВИНАХОДУ Визначення "Алкіл", як група та як структурний елемент інших груп, наприклад, гало-заміщений-алкіл та алкокси група, може бути або лінійно-ланцюговим або розгалуженим. C1-4-алкокси група включає метокси групу, етокси групу та подібні. Гало-заміщений-C1-4алкіл означає і алкільну групу (розгалужену або нерозгалужену), у якій будь-який з атомів водню може бути заміщений атомом галогену. Наприклад, гало-заміщений-C1-4алкіл може являти собою трифторметил, дифторетил, пентафторетил, та подібні. Аналогічно, гідрокси-заміщений-C1-6алкіл означає і алкільну групу (розгалужену або нерозгалужену), у якій будь-який з атомів водню може бути заміщений гідроксилом. Наприклад, гідрокси-заміщений-C1-6алкіл включає 2-гідроксиетил, та подібні. Аналогічно, ціано-заміщений-C1-6алкіл означає і алкільну групу (розгалужену або нерозгалужену), у якій будь-який з атомів водню може бути заміщений ціано-групою. "Арил" являє собою моноциклічне або сконденсоване біциклічне ароматичне кільце, що містить від шести до десяти кільцевих атомів вуглецю. Наприклад, арил може являти собою феніл або нафтил, переважно феніл. "Арилен" являє собою двовалентний радикал, одержаний з арильної групи. "Циклоалкіл" являє собою насичену або частково ненасичену, моноциклічну, сконденсовану біциклічну або місткову поліциклічну кільцеву систему, що містить зазначену кількість кільцевих атомів. Наприклад, C3-10циклоалкіл включає циклопропіл, циклобутил, циклопентил, циклогексил, тощо. "Гетероарил" приймає значення, визначені вище для арилу, де один або більша кількість кільцевих членів являють собою гетероатом. Наприклад, гетероарил включає піридил, індоліл, індазоліл, хіноксалініл, хінолініл, бензофураніл, бензопіраніл, бензотіопіраніл, бензо[1,3]діоксол, імідазоліл, бензо-імідазоліл, піримідиніл, фураніл, оксазоліл, ізоксазоліл, триазоліл, тетразоліл, піразоліл, тієніл, тощо. "Гетероциклоалкіл" означає циклоалкіл, визначений у даній заявці, за умови, що один або більша кількість показаних кільцевих атомів вуглецю, замінені на залишок, вибраний з таких як: -O-, -N=, -NR-, -C(O)-, -S-, -S(O) - або -S(O)2-, де R являє собою водень, C1-4алкіл або азотзахисну групу. Наприклад, C3-8гетероциклоалкіл, як використано у даній заявці для опису сполук даного винаходу, включає 2H-піран, 4H-піран, піперидин, 1,4-діоксан, морфолін, 1,4-дитіан, тіоморфоліно, імідазолідин-2-он, тетрагідрофуран, піперазин, 1,3,5-тритіан, піролідин, піролідиніл-2-он, піперидин, піперидинон, 1,4-діокса-8-аза-спіро[4,5]дец-8-ил, тощо. 2 UA 112285 C2 5 10 15 "Галоген" (або гало) являє собою хлор, фтор, бром або йод. "pMEK" означає фосфорильований Mek. "pERK" означає фосфорильований ERK. "Лікують", "що лікують" та "лікування" відноситься до способу полегшення симптомів або зменшення хвороби та/або її супровідних симптомів. Сполуки даного винаходу названі, використовуючи Chemdraw Ultra (версія 10,0) та/або ChemAxon Name Generator (JChem Version 5.3.1.0). Опис кращих варіантів втілення Даний винахід забезпечує сполуки, композиції та способи лікування пов’язаної з кіназою хвороби, особливо пов’язаних з B-Raf кіназою хвороб; наприклад, таких як метастатичні меланоми, солідні пухлини, пухлини мозку, такі як Мультиформна гліобластома (GBM), гострий мієлобластний лейкоз (AML), рак передміхурової залози, рак шлунку, папілярна карцинома щитовидної залози, карцинома яєчнику низького рівня злоякісності, та колоректальний рак. У одному варіанті втілення, що стосується сполук Формули I, R 1 вибирають з –X1R8a та – X1NHC(O)OR8b; де кожен X1 являє собою незалежно C1-4алкілен; та X1 необов’язково має 1 - 3 атоми водню, замінені групою, що вибирають з таких як: гідрокси-група, гало-група, ціано-група, C1-4алкіл та гало-заміщений-C1-4алкіл; де R8a та R8b незалежно вибирають з водню та C1-6алкілу; за умови, що R8b не являє собою водень, коли R1 являє собою –X1NHC(O)OR8b. У іншому варіанті втілення представлені сполуки Формули Ia: 20 R3 Y R2 O N NH O H N R5 N H N S R4 O O N N R7 Ia 25 30 35 40 45 у якій: Y вибирають з N та CR6; R2, R3, R5 та R6 незалежно вибирають з таких як: водень, гало-група, ціано-група, C1-4алкіл, гало-заміщений-C1-4алкіл, C1-4алкокси-група та гало-заміщенаC1-4алкокси-група; за умови, що коли R5 являє собою фтор та R1 вибирають з таких як: водень, – X1R8a, –X1OX2R8a, –X1C(O)NR8aR8b, –X1NR8aX2R8b, –X1NR8aC(O)X2OR8b та –X1NR8aS(O)0-2R8b, R3 та R6 обидва не являють собою водень; R4 вибирають з –R9 та –NR10R11; де R9 вибирають з таких як: C1-6алкіл, C3-8циклоалкіл, C3-8гетероциклоалкіл, арил та гетероарил; де зазначений алкіл, циклоалкіл, гетероциклоалкіл, арил або гетероарил радикалу R 9 необов’язково заміщений за допомогою 1 - 3 радикалів, що незалежно вибирають з таких як: гало-група, ціано-група, C14алкіл, гало-заміщений-C1-4алкіл, C1-4алкокси-група та гало-заміщена-C1-4алкокси-група; та R10 та R11 незалежно вибирають з водню та R9; та R7 вибирають з таких як: водень, C1-4алкіл, C35циклоалкіл та C3-5гетероциклоалкіл; де зазначений алкіл, циклоалкіл або гетероциклоалкіл радикалу R7 необов’язково заміщений за допомогою 1 - 3 радикалів, що незалежно вибирають з таких як: гало-група, ціано-група, гідроксил, C1-4алкіл, гало-заміщений-C1-4алкіл, C1-4алкоксигрупа та гало-заміщена-C1-4алкокси-група. У додатковому варіанті втілення, R4 являє собою –R9; де R9 вибирають з C1-3алкілу та C38циклоалкілу; де зазначений алкіл або циклоалкіл радикалу R 9 є необов’язково заміщеним за допомогою 1 - 3 радикалів, що незалежно вибирають з таких як: гало-група та гало-заміщенийC1-4алкіл. У додатковому варіанті втілення, R2 вибирають з водню та фтору; R3 вибирають з хлору, фтору та метилу; R5 вибирають з водню, з хлору та фтору; Y вибирають з N та CR 6; та R6 вибирають з водню та фтору. У додатковому варіанті втілення сполуки вибирають з таких як: метил N-[(2S)-1-({4-[3-(3хлор-5-метансульфонамідофеніл)-1-(пропан-2-іл)-1H-піразол-4-іл]піримідин-2-іл}аміно)пропан-2іл]карбамат; метил N-[(2S)-1-[(4-{3-[2-фтор-3-(пропан-1-сульфонамідо)феніл]-1-(пропан-2-іл)-1Hпіразол-4-іл}піримідин-2-іл)аміно]пропан-2-іл]карбамат; метил N-[(2S)-1-({4-[3-(2-фтор-3метансульфонамідофеніл)-1-(пропан-2-іл)-1H-піразол-4-іл]піримідин-2-іл}аміно)пропан-2іл]карбамат; метил N-[(2S)-1-[(4-{3-[3-хлор-5-(пропан-1-сульфонамідо)феніл]-1-(пропан-2-іл)-1H 3 UA 112285 C2 5 10 15 20 25 піразол-4-іл}-піримідин-2-іл)аміно]пропан-2-іл]карбамат; метил N-[(2S)-1-({4-[3-(2,6-дифтор-3метансульфонамідофеніл)-1-(пропан-2-іл)-1H-піразол-4-іл]піримідин-2-іл}аміно)-пропан-2іл]карбамат; метил N-[(2S)-1-[(4-{3-[2,6-дифтор-3-(пропан-1-сульфонамідо)феніл]-1-(пропан-2іл)-1H-піразол-4-іл}піримідин-2-іл)аміно]пропан-2-іл]карбамат; метил N-[(2S)-1-{[4-(3-{2-фтор-3[(3,3,3-трифторпропан)-сульфонамідо]феніл}-1-(пропан-2-іл)-1H-піразол-4-іл)піримідин-2іл]аміно}пропан-2-іл]карбамат; метил N-[(2S)-1-({4-[3-(3-хлор-2-метансульфонамідопіридин-4-іл)1-(пропан-2-іл)-1H-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат; метил N-[(2S)-1-({4-[3(3-фтор-2-метансульфонамідопіридин-4-іл)-1-(пропан-2-іл)-1H-піразол-4-іл]піримідин-2іл}аміно)пропан-2-іл]карбамат; метил N-[(2S)-1-({4-[3-(2-хлор-3-етансульфонамідо-4,5дифторфеніл)-1-(пропан-2-іл)-1H-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат; метил N-[(2S)-1-({4-[3-(2,4-дифтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1H-піразол-4іл]піримідин-2-іл}аміно)-пропан-2-іл]карбамат; метил N-[(2S)-1-({4-[1-(пропан-2-іл)-3-(2,4,5трифтор-3-метансульфонамідофеніл)-1H-піразол-4-іл]піримідин-2-іл}аміно)пропан-2іл]карбамат; метил N-[(2S)-1-({4-[3-(3-метансульфонамідофеніл)-1-(пропан-2-іл)-1H-піразол-4іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат; метил N-[(2S)-1-({4-[3-(3-етансульфонамідо-2,4дифторфеніл)-1-(пропан-2-іл)-1H-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат; метил N-[(2S)-2-({4-[3-(5-хлор-2-фтор-3-метан-сульфонамідофеніл)-1-(пропан-2-іл)-1H-піразол-4іл]піримідин-2-іл}аміно)-пропіл]карбамат; метил N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3метансульфонамідофеніл)-1-(оксан-2-іл)-1H-піразол-4-іл]піримідин-2-іл}аміно)-пропан-2іл]карбамат; метил N-[(2S)-1-[(4-{3-[2,4-дифтор-3-(пропан-1-сульфонамідо)феніл]-1-(пропан-2іл)-1H-піразол-4-іл}піримідин-2-іл)аміно]пропан-2-іл]карбамат; метил N-[(2S)-1-({4-[3-(3циклопропансульфонамідо-2,5-дифторфеніл)-1-(пропан-2-іл)-1H-піразол-4-іл]піримідин-2іл}аміно)пропан-2-іл]карбамат; метил N-[(2S)-1-({4-[3-(5-хлор-3-циклопропансульфонамідо-2фторфеніл)-1-(пропан-2-іл)-1H-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат; та метил N-[(2S)-1-[(4-{3-[5-хлор-2-фтор-3-(пропан-1-сульфонамідо)феніл]-1-(пропан-2-іл)-1H-піразол-4іл}піримідин-2-іл)аміно]пропан-2-іл]карбамат. У іншому варіанті втілення представлені сполуки Формули Ib: O R3 NH N O N O N H S HN N O R5 N R7 Ib 30 35 40 45 у якій: R3 вибирають з хлору, фтору та метилу; R5 вибирають з фтору та хлору; та R7 вибирають з етилу та ізопропілу. У додатковому варіанті втілення представлені сполуки, які вибирають з таких як: метил N[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1H-піразол-4іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат; метил N-[(2S)-1-({4-[3-(2,5-дифтор-3метансульфонамідофеніл)-1-(пропан-2-іл)-1H-піразол-4-іл]піримідин-2-іл}аміно)пропан-2іл]карбамат; метил N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3-метансульфонамідофеніл)-1-етил-1Hпіразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат; метил N-[(2S)-1-({4-[3-(2-фтор-3метансульфонамідо-5-метилфеніл)-1-(пропан-2-іл)-1H-піразол-4-іл]піримідин-2-іл}аміно)пропан2-іл]карбамат; метил N-[(2S)-1-({4-[3-(2-хлор-3-метансульфонамідо-5-метилфеніл)-1-(пропан-2іл)-1H-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат; метил N-[(2S)-1-({4-[3-(2-хлор-5фтор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1H-піразол-4-іл]піримідин-2-іл}аміно)пропан2-іл]карбамат; метил N-[(2R)-1-({4-[3-(5-хлор-2-фтор-3-метан-сульфонамідофеніл)-1-(пропан-2іл)-1H-піразол-4-іл]піримідин-2-іл}аміно)-пропан-2-іл]карбамат; метил N-[(2S)-1-({4-[3-(2,5дихлор-3-метансульфонамідофеніл)-1-(пропан-2-іл)-1H-піразол-4-іл]піримідин-2іл}аміно)пропан-2-іл]карбамат; та метил N-[(2S)-1-({4-[3-(5-хлор-2-фтор-3метансульфонамідофеніл)-1H-піразол-4-іл]піримідин-2-іл}аміно)пропан-2-іл]карбамат. 4 UA 112285 C2 5 10 15 20 25 30 35 40 45 50 55 60 У іншому варіанті втілення представлені сполуки, які вибирають з таких як: N-[5-хлор-3-(4-{2[(2-ціаноетил)аміно]піримідин-4-іл}-1-(пропан-2-іл)-1H-піразол-3-іл)-2фторфеніл]метансульфонамід; N-{5-хлор-3-[4-(2-{[2-(диметиламіно)етил]аміно}-піримідин-4-іл)1-(пропан-2-іл)-1H-піразол-3-іл]-2-фторфеніл}метансульфонамід; N-(5-хлор-2-фтор-3-{4-[2(метиламіно)піримідин-4-іл]-1-(пропан-2-іл)-1H-піразол-3-іл}феніл)метансульфонамід; та N-{3-[4(2-амінопіримідин-4-іл)-1-(пропан-2-іл)-1H-піразол-3-іл]-5-хлор-2-фторфеніл}метансульфонамід. У додатковому варіанті втілення представлені сполуки, які вибирають з Прикладів та Таблиць, показаних нижче. У додатковому варіанті втілення представлені проміжні сполуки, які вибирають з таких як: 3Бром-5-хлор-2-фторанілін; ціано-(2-метилтіо-піримідин-4-іл)-оцтової кислоти трет-бутиловий складний ефір; 1-Ізопропіл-4-(2-(метилтіо)піримідин-4-іл)-1H-піразол-3-амін; 2-((2-Бензиліден-1етилгідразиніл)метилен)-малононітрил; 1-(3-Аміно-1-ізопропіл-1H-піразол-4-іл)етанон; 1-(3-Йод1-ізопропіл-1H-піразол-4-іл)етанон; 1-(3-Йод-1-етил-1H-піразол-4-іл)етанон; 1-(3-Йод-1-метил1H-піразол-4-іл)етанон; 3-(Диметиламіно)-1-(3-йод-1-ізопропіл-1H-піразол-4-іл)проп-2-ен-1-он; 3(диметиламіно)-1-(3-йод-1-етил-1H-піразол-4-іл)проп-2-ен-1-он; 3-(Диметиламіно)-1-(3-йод-1метил-1H-піразол-4-іл)проп-2-ен-1-он; 4-(3-Йод-1-ізопропіл-1H-піразол-4-іл)піримідин-2-амін; 4(3-Йод-1-етил-1H-піразол-4-іл)піримідин-2-амін; 4-(3-Йод-1-метил-1H-піразол-4-іл)піримідин-2амін; 4-(3-Йод-1-ізопропіл-1H-піразол-4-іл)піримідин-2-ол; 2-Хлор-4-(3-йод-1-ізопропіл-1Hпіразол-4-іл)піримідин; (S)-Метил 1-(4-(3-йод-1-ізопропіл-1H-піразол-4-іл)піримідин-2іламіно)пропан-2-ілкарбамат; (R)-Метил 1-(4-(3-йод-1-ізопропіл-1H-піразол-4-іл)піримідин-2іламіно)пропан-2-ілкарбамат; (S)-трет-бутил 1-(4-(3-йод-1-ізопропіл-1H-піразол-4-іл)піримідин-2іламіно)пропан-2-ілкарбамат; 3-(4-(3-йод-1-ізопропіл-1H-піразол-4-іл)піримідин-21 іламіно)пропаннітрил; 4-(3-йод-1-ізопропіл-1H-піразол-4-іл)-N-метилпіримідин-2-амін; N -(4-(32 2 йод-1-ізопропіл-1H-піразол-4-іл)піримідин-2-іл)-N ,N -диметилетан-1,2-діамін; N-(3-бром-2,4дифторфеніл)пропан-1-сульфонамід; 3-Фтор-4-йодпіридин-2-амін; 3-хлор-4-йодпіридин-2-амін; 3-Бром-2,5,6-трифторанілін; 2,4-Дибром-3,6-дихлоранілін; 3-бром-2-хлор-5-метиланілін; 3-бром2,5-дифторанілін; 3-Бром-5-хлор-2-фторбензойна кислота; трет-бутил 3-бром-5-хлор-2фторфенілкарбамат; трет-бутил 3-бром-2-фтор-5-метилфенілкарбамат; трет-бутил 5-хлор-2фтор-3-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)фенілкарбамат; трет-бутил 2,6-дифтор-3(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)фенілкарбамат; N-(2,4-дифтор-3-(4,4,5,5тетраметил-1,3,2-діоксаборолан-2-іл)феніл)пропан-1-сульфонамід; 2-(2-фтор-3-нітрофеніл)4,4,5,5-тетраметил-1,3,2-діоксаборолан; 2,5-дифтор-3-(4,4,5,5-тетраметил-1,3,2-діоксаборолан2-іл)анілін; 2-хлор-5-фтор-3-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)анілін; 2,5-дихлор-3(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)анілін; 2-хлор-5-метил-3-(4,4,5,5-тетраметил-1,3,2діоксаборолан-2-іл)анілін; трет-бутил 2-фтор-5-метил-3-(4,4,5,5-тетраметил-1,3,2діоксаборолан-2-іл)фенілкарбамат; 3-фтор-4-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2іл)піридин-2-амін; 2,3,6-трифтор-5-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)анілін; 3-хлор-4(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)піридин-2-амін; 3-хлор-5-(4,4,5,5-тетраметил-1,3,2діоксаборолан-2-іл)анілін; та 3-метокси-2-метил-5-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2іл)анілін. Даний винахід також включає всі придатні ізотопні варіанти сполук даного винаходу, або їх фармацевтично прийнятні солі. Ізотопний варіант сполуки даного винаходу або її фармацевтично прийнятної солі визначений як варіант, у якому щонайменше один атом замінений атомом, що має такий же атомний номер, але атомну масу, що відрізняється від атомної маси, яка звичайно виявляється у природі. Приклади ізотопів, які можуть бути включені у сполуки даного винаходу та їх фармацевтично прийнятні солі, включають, не обмежуючись 2 3 11 13 14 15 17 18 наведеними, ізотопи водню, вуглецю, азоту та кисню, такі як H, H, C, C, C, N, O, O, 35 18 36 123 S, F, Cl та I. Певні ізотопні варіанти сполук даного винаходу та їх фармацевтично 3 14 прийнятних солей, наприклад, ті, у які включений радіоактивний ізотоп, такий як H або C, є корисними у дослідженнях лікарських засобів та/або розподілення субстрату у тканині. У певних 3 14 прикладах, H та C ізотопи можуть бути використані для легкості їх одержання та визначення. 2 У інших прикладах, заміна на ізотопи, такі як H, може дозволити певні терапевтичні переваги, що походять з більшої метаболічної стабільності, такі як збільшений in vivo період напіввиведення або знижені вимоги до дози. Ізотопні варіанти сполук даного винаходу або їх фармацевтично прийнятних солей загалом можуть бути одержані за звичайно використовуваними процедурами, використовуючи відповідні ізотопні варіанти підходящих реагентів. Деякі Raf інгібітори, окрім збільшення MEK та ERK сигналювання у B-Raf клітинах дикого типу, також викликають ріст клітин у ракових клітинних лініях та спричиняють перетворення та ріст у фібробластах. Індукція сигналювання у прямому напрямку раніше приписувалась 5 UA 112285 C2 5 10 15 20 25 30 35 40 45 50 55 60 опублікованим контурам зворотного зв’язку Raf шляху. Однак, індукція pMEK та pERK може відбуватися у межах хвилин обробки Raf інгібітору, навіть перед тим, як описані випадки зворотного фосфорилювання були побачені на B-Raf та C-Raf. Як індукція сигналювання, так і ріст клітин відбуваються у біфазній моделі, при цьому низькі концентрації сполуки (0,01-0,1 мкM) викликають максимальну індукцію, та високі концентрації сполуки (1-10 мкM) викликають менш сильну індукцію. Така двофазна модель також спостерігається у біохімічних дослідженнях з очищеними B-Raf або C-Raf дикого типу та передбачає механізм, що включає взаємодію двох сигнальних субодиниць. Крім того, Raf димеризація може ап-регулювати pMEK, не через трансфосфорилювання Raf молекул, але можливо шляхом конформаційної активації кінази. У відповідності з цією моделлю, Raf інгібіторна обробка викликає утворення димеру B-Raf/C-Raf у клітинах. Крім того, нокдаун A- або B-Raf за допомогою кіРНК (короткі інтерферуючі РНК) не анулює Raf інгібіторну індукцію pMEK та pERK, та нокдаун C-Raf тільки злегка знижує цю індукцію. Особливо, нокдаун K-Ras у K-Ras мутантних клітинах також тільки злегка знижує цю індукцію, що означає, що цей ефект, головним чином, не опосередковується Ras. У підсумку, ці дані пропонують модель, у якій зв’язування інгібітору з однією Raf молекулою викликає димеризацію та конформаційну активацію Raf молекули-партнеру у димері. Це може пояснити, чому дикого типу Raf та мутантні Ras пухлини є нечутливими до селективних Raf кіназних інгібіторів та могли б також мати важливі впливи на токсичність, так як індукція сильного мітогенного сигналювання могло б привести до гіпер проліферації нормальних тканин. Розуміння механізму індукції Raf інгібітору може привести до створення покращених інгібіторів. Додавання MEK інгібітору у комбінації з Raf інгібітором веде до значного інгібування ERK сигналювання та, отже, зниження у клітинній проліферації та трансформації. Так як обробки MEK інгібітором окремо призвели до одержання обмежуючої дозу токсичності у клінічних випробуваннях, комбінація Raf плюс MEK інгібітор може являти собою кращу лікувальну стратегію. Даний винахід також включає комбінації BRaf інгібіторів, розкритих у даному винаході, з іншими агентами. Зокрема, даний винахід забезпечує комбінації з MEK1/2 інгібіторами. На Фігурі 1 показано, що додавання MEK низькомолекулярного інгібітору може обернути викликане ERK сигналювання, ріст клітин та трансформацію, викликану Raf низькомолекулярним інгібітором. Наприклад, сполука Формули I (сполука 9 даного винаходу, а саме: ((S)-метил 1-(4-(3-(5-хлор-2фтор-3-(метилсульфонамідо)феніл)-1-ізопропіл-1H-піразол-4-іл)піримідин-2-іламіно)пропан-2ілкарбамат) може привести до індукції у клітинній проліферації, що розглядається як негативне інгібування у Фігурі 1 Cell Titer Glo дослідження, використовуючи SW620 клітини. Y-вісь показує негативне та позитивне інгібування. Кожен з експериментів показують у вигляді серій з 9 серійних розведень від 10 до 0,002 мкM. Сполука A1 (N-(4-метил-3-(1-(6-(4-метилпіперазин-1іламіно)піримідин-4-іл)-1H-імідазол-2-іламіно)феніл)-3-(трифторметил)бензамід) являє собою контроль, A3 являє собою MEK інгібітор (PD0325901). Сполуку 9 досліджують за відсутності та у присутності 1 мкM, 0,1 мкM та 0,01 мкM MEK інгібітору A3. Фармакологія та застосування Сполуки даного винаходу модулюють активність кіназ та, як такі, є корисними для лікування хвороб або розладів, у яких кінази вносять свій вклад у патологію та/або симптомологію хвороби. Приклади кіназ, які інгібуються сполуками та композиціями, розкритими у цьому описі, та проти яких корисними є способи, розкриті у цьому описі, включають, не обмежуючись наведеними, B-Raf, включаючи мутантні форми B-Raf. Мітоген-активований протеїнкіназний (MAPK) шлях опосередковує активність декількох ефекторних молекул, які координуються для контролю клітинної проліферації, виживання, диференціації та міграції. Стимулювання клітин, наприклад, факторами росту, цитокінами або гормонами приводить до того, що пов’язана з плазматичною мембраною Ras стає ГТФзв’язаною і, таким чином, активованою для захоплення Raf. Ця взаємодія викликає кіназну активність Raf, що веде до прямого фосфорилювання MAPK/ERK (MEK), що у свою чергу фосфорилює пов’язану з позаклітинним сигналом кіназу (ERK). Активована ERK потім фосфорилює широкий ряд ефекторних молекул, наприклад, кіназ, фосфатаз, транскрипційних факторів та білків цитоскелету. Тому, Ras-Raf-MEK-ERK сигнальний шлях передає сигнали від рецепторів клітинної поверхні до ядра та є важливим, наприклад, у клітинній проліферації та виживанні. Регулювання цього сигнального каскаду додатково збагачується множинними ізоформами Ras (включаючи K-Ras, N-Ras та H-Ras), Raf (A-Raf, B-Raf, C-Raf/Raf-1), MEK (MEK1 та MEK-2) та ERK (ERK-1 та ERK-2). Так як 10-20% раків людини залучає онкогенні Ras мутації та багато раків людини мають активовані рецептори факторів росту, цей шлях є ідеальною ціллю для впливу. Важлива роль та положення Raf у багатьох сигнальних шляхах показані у дослідженнях, 6 UA 112285 C2 5 10 15 20 25 30 35 40 45 50 55 60 використовуючи дерегульовані та домінантні інгібіторні Raf мутанти у клітинах ссавця, а також у дослідженнях, використовуючи біохімічні та генетичні технології до модельних організмів. В минулому, увага на Raf як на протипухлинну ціль лікарського засобу концентрувалася на її функції як нижчого ефектору Ras. Однак, останні отримані дані показали, що Raf може мати важливу роль в утворенні певних пухлин без необхідної присутності онкогенного Ras алелю. Зокрема, активування алелів B-Raf та N-Ras ідентифіковане у ~70% меланом, 40% папілярних карцином щитовидної залози, 30% карцином яєчнику низького рівня злоякісності, та 10% колоректальних раків. Мутації у K-Ras відбуваються у приблизно 90% раків підшлункової залози. Більшість B-Raf мутацій знайдена у кіназному домені, з одним заміщенням (V600E), що становить щонайменше 80%. Мутовані B-Raf білки активують Raf-MEK-ERK шлях або через підвищену кіназну активність по відношенню до MEK або через активування C-Raf. Тому, розробка кіназного інгібітору для B-Raf забезпечує нову терапевтичну можливість для лікування багатьох типів раку людини, особливо для таких як: метастатичні меланоми, солідні пухлини, пухлини мозку, такі як мультиформна гліобластома (GBM), гострий мієлобластний лейкоз (AML), рак легені; папілярна карцинома щитовидної залози, карцинома яєчнику низького рівня злоякісності, та колоректальний рак. Деякі інгібітори Raf кінази описані як такі, що показують ефективність у інгібуванні проліферації пухлинних клітин у in vitro та/або in vivo дослідженнях (дивись, наприклад, Патенти США №№ 6,391,636, 6,358,932, 6,037,136, 5,717,100, 6,458,813, 6,204,467, та 6,268,391). Інші патенти та патентні заявки описують застосування інгібіторів Raf кінази для лікування лейкемії (дивись, наприклад, Патенти США №№ 6,268,391, 6,204,467, 6,756,410, та 6,281,193; та припинені Патентні Заявки США №№ 20020137774 та 20010006975), або для лікування раку молочної залози (дивись, наприклад, Патенти США №№ 6,358,932, 5,717,100, 6,458,813, 6,268,391, 6,204,467 та 6,911,446). Дані показують, що інгібітори Raf кінази можуть значно інгібувати сигналювання через MAPK шлях, що веде до значного зменшення у B-Raf (V600E) пухлинах. Сполуки даного винаходу інгібують клітинні процеси, що залучають B-Raf кіназу шляхом блокування сигнального каскаду у цих ракових клітинах та зрештою викликаючи стаз та/або смерть клітин. Відповідно до описаного вище, даний винахід додатково забезпечує спосіб профілактики або лікування карциноми легені, раку передміхурової залози, раку шлунку, карциноми підшлункової залози, карциноми сечового міхура, карциноми кишечнику, мієлоїдних розладів, раку передміхурової залози, раку щитовидної залози, меланоми, аденом та карцином яєчнику, ока, печінки, жовчних проток, та нервової системи. Далі, даний винахід додатково забезпечує спосіб профілактики або лікування будь-якої з хвороб або розладів, описаних вище, у суб’єкта, якому необхідне таке лікування, де зазначений спосіб включає введення зазначеному суб’єкту терапевтично ефективної кількості (Дивись, "Введення та фармацевтичні композиції", описане нижче) сполуки Формули I або її фармацевтично прийнятної солі. Для будь-якого з описаних вище застосувань, необхідна доза буде змінюватися в залежності від шляху введення, певного стану, що лікують, та бажаного ефекту. Введення та фармацевтичні композиції Загалом, сполуки даного винаходу будуть вводитися у терапевтично ефективних кількостях через будь-який із звичайних та прийнятних способів, відомих у даній галузі техніки, або окремо або у комбінації з одним або більшою кількістю терапевтичних агентів. Терапевтично ефективна кількість може змінюватися у широких межах в залежності від серйозності хвороби, віку та відносного стану здоров’я суб’єкта, ефективності використовуваної сполуки та інших факторів. Загалом, показано, що задовільні результати отримують систематично при щоденних дозах від приблизно 0,03 до 30 мг/кг маси тіла. Показана щоденна доза у великого ссавця, наприклад, людей, знаходиться у інтервалі від приблизно 0,5 мг до приблизно 2000 мг, при зручному введенні, наприклад, у розділених дозах до чотирьох разів на день або у формі уповільненого вивільнення. Прийнятні одиничні лікарські форми для перорального введення включають від приблизно 1 до 500 мг активного інгредієнта. Сполуки даного винаходу можуть бути введені як фармацевтичні композиції будь-яким зручним шляхом, зокрема ентерально, наприклад, перорально, наприклад, у формі таблеток або капсул, або парентерально, наприклад, у формі ін’єкційних розчинів або суспензій, місцево, наприклад, у формі лосьйонів, гелів, мазей або кремів, або у назальній формі або у формі супозиторію. Фармацевтичні композиції, що включають сполуку даного винаходу у вільній формі або у формі фармацевтично прийнятної солі у поєднанні з щонайменше одним фармацевтично прийнятним носієм або розріджувачем, можуть бути вироблені звичайним способом шляхом змішування, гранулювання або нанесення покриття. Наприклад, пероральні композиції можуть являти собою таблетки або желатинові капсули, що включають активний інгредієнт разом з 7 UA 112285 C2 5 10 15 20 25 30 35 40 45 50 55 60 такими як: a) розріджувачі, наприклад, лактоза, декстроза, сахароза, маніт, сорбіт, целюлоза та/або гліцин; b) любриканти, наприклад, кремнезем, тальк, стеаринова кислота, її магнієва або кальцієва сіль та/або поліетиленгліколь; для таблеток також c) зв’язуючі речовини, наприклад, алюмосилікат магнію, крохмальна паста, желатин, трагакант, метилцелюлоза, карбоксиметилцелюлоза натрію та/або полівінілпіролідон; при бажанні, d) дезінтегранти, наприклад, крохмалі, агар-агар, альгінова кислота або її натрієва сіль, або шипучі суміші; та/або e) абсорбенти, барвники, ароматизатори та підсолоджувачі. Ін’єкційні композиції можуть являти собою водні ізотонічні розчини або суспензії, та супозиторії можуть бути одержані з жирних емульсій або суспензій. Композиції можуть бути стерилізовані та/або можуть містити допоміжні речовини, такі як консерванти, стабілізатори, зволожуючі або емульгуючі агенти, промотори розчинення, солі для регулювання осмотичного тиску та/або буфери. Крім того, вони також можуть містити інші терапевтично цінні речовини. Наприклад, сполуки даного винаходу можуть формулюватися у мікроемульсійний первинний концентрат (MEPC). Сполуки Формули I можуть бути приготовлені при концентрації 40 мг/мл у суміші 56% PEG400, 29% кремофору EL та 15% олеїнової кислоти. Цю суміш, без сполуки Формули I, спочатку готують шляхом вихрового перемішування/струшування. Сполуку даного винаходу додають та обробку ультразвуком використовують для диспергування порошку у носії. Цю суміш нагрівають до 80 °C у водяній бані впродовж приблизно години, перемішуючи, з обробкою ультразвуком, кожні 15 хвилин. Ця суміш є фізично та хімічно стабільною при кімнатній температурі впродовж приблизно одного тижня. Прийнятні композиції для крізьшкірного застосування включають ефективну кількість сполуки даного винаходу з носієм. Носій може включати фармакологічно прийнятні розчинники, що можуть бути абсорбовані, для сприяння проходженню через шкіру хазяїна. Наприклад, крізьшкірні засоби знаходяться у формі перев’язочного матеріалу, що включає основу, резервуар, що містить сполуку необов’язково з носіями, необов’язково бар’єр, що контролює швидкість, для доставки сполуки до шкіри хазяїна при контрольованій та завчасно визначеній швидкості впродовж тривалого періоду часу, та засіб для утримання пристрою на шкірі. Також можуть бути використані матриксні крізьшкірні композиції. Прийнятні композиції для місцевого застосування, наприклад, до шкіри та очей, переважно являють собою водні розчини, мазі, креми або гелі, добре відомі у даній галузі техніки. Вони можуть містити солюбілізатори, стабілізатори, агенти, що посилюють тонічність, буфери та консерванти. Сполуки даного винаходу можуть бути введені у терапевтично ефективних кількостях у комбінації з одним або більшою кількістю терапевтичних агентів (фармацевтичні комбінації). Наприклад, синергетичні ефекти можуть зустрічатися з іншими протипухлинними або антипроліферативними агентами, наприклад, такими як: мітотичні інгібітори, алкілуючі агенти, анти-метаболіти, інтеркалюючі антибіотики, інгібітори факторів росту, інгібітори клітинного циклу, ферменти, інгібітори топоізомерази, модифікатори біологічної відповіді, антитіла, цитотоксичні агенти, анти-гормони, анти-андрогени, агент анти-ангіогенезу, інгібітор кінази, інгібітор пан кінази або інгібітор фактору росту. Сполуки даного винаходу можуть бути введені у терапевтично ефективних кількостях у комбінації з одним або більшою кількістю прийнятних наповнювачів, що вибирають з таких як: кукурудзяний крохмаль, картопляний крохмаль, маніоковий крохмаль, крохмальна паста, прежелатинований крохмаль, цукри, желатин, природні камеді, синтетичні камеді, альгінат натрію, альгінова кислота, трагакантова камедь, гуарова камедь, целюлоза, етилцелюлоза, ацетат целюлози, карбоксиметил-целюлоза кальцію, карбоксиметилцелюлоза натрію, метилцелюлоза, гідроксипропіл-метилцелюлоза, мікрокристалічна целюлоза, алюмосилікат магнію, полівінілпіролідон, тальк, карбонат кальцію, порошкоподібна целюлоза, декстрати, каолін, маніт, кремнієва кислота, сорбіт, агар-агар, карбонат натрію, кроскармелоза натрію, кросповідон, полакрилін калію, натрію крохмаль гліколят, глини, стеарат натрію, стеарат кальцію, стеарат магнію, стеаринова кислота, мінеральне масло, легке мінеральне масло, гліцерин, сорбіт, маніт, поліетиленгліколь, інші гліколі, лаурил-сульфат натрію, гідрогеноване рослинне масло, арахісове масло, бавовняне масло, соняшникове масло, кунжутне масло, оливкове масло, кукурудзяне масло, соєве масло, стеарат цинку, олеат натрію, етилолеат, етиллаурат, кремнезем та їх комбінації. Варіант втілення даного винаходу являє собою спосіб за п. 12 або 13, який додатково включає введення суб’єкту додаткового терапевтичного агенту. Додатковий терапевтичний агент включає протираковий лікарський засіб, знеболюючий засіб, протиблювотний засіб, антидепресант або протизапальний агент. Далі, додатковий терапевтичний агент являє собою інший інгібітор Raf кінази або інгібітор MEK, mTOR, HSP90, AKT, PI3K, CDK9, PAK, Протеїнкіназу C, MAP кіназу, MAPK Кіназу, або ERK та вводиться суб’єкту одночасно зі сполукою даного 8 UA 112285 C2 5 10 15 20 25 30 35 40 винаходу. Наприклад, додавання інгібітору MEK у комбінації з інгібітором Raf приводить до значного інгібування ERK сигналювання та, отже, зменшення у клітинній проліферації та трансформації. Так як лікування тільки MEK інгібітором привели до дозових граничних токсичностей у клінічних випробуваннях, комбінація Raf плюс інгібітор MEK являє собою найкращу лікувальну стратегію. Приклади інгібіторів MEK включають AS703026 (EMD Serono); MSC1936369B (EMD Serono); GSK1120212 (GlaxoSmithKline); AZD6244 (Memorial Sloan-Kettering Cancer Center); PD-0325901 (Pfizer); ARRY-438162 (Array BioPharma); RDEA119 (Ardea Biosciences, Inc.); GDC0941 (Genentech); GDC0973 (Genentech); TAK-733 (Millennium Pharmaceuticals, Inc.); RO5126766 (Hoffmann-La Roche); та XL-518 (Exelixis). У іншому варіанті втілення даного винаходу представлені комбінації та способи лікування раку, що включають терапевтично ефективну кількість сполуки Короткого опису даного винаходу (інгібітор Raf) та щонайменше один інгібітор MEK протеїнкінази. Коли сполуки даного винаходу вводять у поєднанні з іншими терапіями, дози сполук, які спів-вводять, звичайно будуть змінюватися в залежності від типу використовуваного співлікарського засобу, від використовуваного специфічного лікарського засобу, від стану, що лікують, тощо. Даний винахід також забезпечує фармацевтичні комбінації, наприклад, набір, що включає a) перший агент, який являє собою сполуку даного винаходу, як розкрито у цьому описі, у вільній формі або у формі фармацевтично прийнятної солі, та b) щонайменше один спів-агент. Зазначений набір може включати інструкції для його застосування. Вважають, що терміни "спів-введення" або "комбіноване введення" або подібні, як використано у цьому описі, включають введення вибраних терапевтичних агентів одному пацієнту, та, як передбачають, включають лікувальні режими, у яких агенти не обов’язково вводять тим же самим шляхом введення або у той самий час. Термін "фармацевтична комбінація", як використано у цьому описі, означає продукт, який одержують після змішування або об’єднання більше ніж одного активного інгредієнту та включає як фіксовані, так і нефіксовані комбінації активних інгредієнтів. Термін "фіксована комбінація" означає, що активні інгредієнти, наприклад, сполуку Формули I та спів-агент, обидва вводять пацієнту одночасно у формі однієї одиниці або дози. Термін "нефіксована комбінація" означає, що активні інгредієнти, наприклад, сполуку Формули I та спів-агент, обидва вводять пацієнту як окремі одиниці або одночасно, паралельно або послідовно без специфічних обмежень часу, де таке введення забезпечує терапевтично ефективні рівні 2 сполук у організмі пацієнта. Останню також застосовують для лікування сумішами, наприклад, введення 3 або більшої кількості активних інгредієнтів. Способи одержання сполук даного винаходу Даний винахід також включає способи одержання сполук даного винаходу. У описаних реакціях, може бути необхідно захистити реакційно-здатні функціональні групи, наприклад, гідрокси групу, аміно групу, іміно групу, тіо групу або карбокси групу, де для кінцевого продукту бажано захистити його від небажаної участі у зазначених реакціях. Звичайні захисні групи можуть бути використані відповідно до стандартної практики, наприклад, дивись T.W. Greene та P. G. M. Wuts у "Protective Groups in Organic Chemistry", John Wiley and Sons, 1991. Сполуки Формули I можуть бути одержані, слідуючи наступній Схемі Реакції I: 9 UA 112285 C2 Схема Реакції I R3 P R3 P Y Y N R1 R5 N H N N R2 N R2 R7M (4) S R4 O O S R4 O O N R5 R1 N H N N N N NH R7 (2) (3) R3 Y -P H N R2 N R1 R5 N H N S R4 O O N N I 5 10 15 20 R7 у якій R1, R2, R3, R4, R5, R7 та Y приймають значення, визначені у Короткому описі даного винаходу, P являє собою придатну захисну групу (наприклад, MEM, MOM, SEM, R 4SO2, та подібні), та M являє собою відхідну групу (наприклад, хлор, бром, йод, метансульфонілокси, птолуолсульфонілокси, та подібні). Сполука Формули I може бути синтезована шляхом видалення захисної групи P зі сполуки Формули 2 (наприклад, шляхом обробки сильною кислотою, такою як соляна кислота у присутності протонного розчиннику, такого як метанол або вода, коли P являє собою MEM, MOM, або SEM; або шляхом обробки водним або метанольним розчином карбонату натрію або калію, необов’язково у присутності співрозчиннику, такого як толуол, коли P являє собою другу сульфонільну групу R 4SO2). Сполуки Формули 2 можуть бути одержані шляхом введення у реакцію сполуки Формули 3 з алкілуючим агентом Формули 4 у присутності прийнятного розчиннику (наприклад, ДМФА, ДМСО, та подібних) та підходящої основи (наприклад, такої як карбонат калію, гідрид натрію, та подібні). Реакція проходить у температурному інтервалі від приблизно 0 °C до приблизно 150 °C та до закінчення може тривати до приблизно 24 годин. Реакційну суміш необов’язково додатково вводять у реакцію для видалення будь-яких захисних груп. Сполуки Формули I також можуть бути одержані, слідуючи наступній Схемі Реакції II: Схема Реакції II R3 R3 Y R4SO2Cl Y NH 2 R2 N (6) N R1 R1 R5 N H N 30 N S R4 O O N N N 25 R5 N H N (5) H N R2 I R7 R7 у якій R1, R2, R3, R4, R5, та Y приймають значення, визначені у Короткому описі даного винаходу. Сполука Формули I може бути синтезована шляхом введення у реакцію сполуки Формули 5 з сульфонілюючим реагентом Формули 6 у присутності прийнятної основи (наприклад, такої як піридин, триетиламін, 4-(N,N-диметиламіно)піридин, та подібні) та прийнятного розчиннику (такого як піридин, дихлорметан, 2-метилТГФ, та подібні). Реакція проходить у температурному інтервалі від приблизно 0 °C до приблизно 100 °C та до закінчення 10 UA 112285 C2 5 10 може тривати до приблизно 24 годин. Реакційну суміш необов’язково додатково вводять у реакцію для видалення будь-яких захисних груп. У деяких випадках, сульфонілюючий реагент може бути введений у реакцію двічі для створення біс-сульфонільної похідної. У цьому випадку, біс-сульфонільна сполука може бути перетворена у сполуку Формули шляхом обробки підходящою основою (наприклад, гідроксидом натрію або калію, або карбонатом натрію або калію) у присутності протонного розчиннику, такого як метанол або вода, необов’язково у присутності спів розчиннику, такого як толуол або 2-метилТГФ. Реакція відбувається у температурному інтервалі від приблизно 20 °C до приблизно 100 °C та до закінчення може тривати до приблизно 24 годин. Сполуки Формули I також можуть бути одержані, слідуючи наступній Схемі Реакції III: Схема Реакції III R3 Y H N R2 N R1 R'O R50 R5 B S R4 O O R3 Y OR' H N R2 N H N N (8) N R1 N (7) R7 N N N R 90 R3 I Y R7 N R2 R'O R5 N H S R4 O O R 90 R5 B OR' (8a) R 90 R3 Y N R2 N R1 R 90 R5 N H N N N (9) R7 15 20 25 30 у якій R1, R2, R3, R4, R5, та Y приймають значення, визначені у Короткому описі даного винаходу, R50 являє собою відхідну групу (наприклад, йод, бром, хлор, трифторметансульфонілокси, та подібні), кожен R’ може являти собою, наприклад, водень, метил, та подібні, або дві R’ групи можуть бути сполучені разом з утворенням циклічного боронат-складного ефіру. Кожна з двох R90 груп може являти собою водень, або дві R90 групи, взяті разом, можуть являти собою прийнятну азот-захисну групу (наприклад, одна R90 група може являти собою водень та друга може являти собою BOC). Сполука Формули Ia може бути синтезована шляхом введення у реакцію сполуки Формули 7 зі сполукою Формули 8 у присутності підходящого каталізатору з перехідного металу (наприклад, тетракіс(трифенілфосфінпаладій)(0) або PdCl2(dppf), прийнятного розчиннику (наприклад, ДМЕ, діоксан, толуол, етанол, та подібні) та прийнятної основи (наприклад, безводний карбонат калію або водний розчин карбонату натрію, та подібні). Реакція проходить у температурному інтервалі від приблизно 20 °C до приблизно 120 °C та до закінчення може тривати до приблизно 24 годин. Реакційну суміш необов’язково додатково вводять у реакцію для видалення будь-яких захисних груп. Сполука Формули 1 також може бути одержана за допомогою протоколу, подібного описаному для реакції Сузукі, де сполуку Формули 7 вводять у реакцію зі сполукою Формули 8a для одержання сполуки Формули 9. Після зняття захисту R 90 групи, реакція сульфонілювання, як описано для Схеми Реакції II, приводить до одержання сполуки Формули Ia. 11 UA 112285 C2 5 Спеціалісту, кваліфікованому у даній галузі техніки, слід прийняти до уваги, що інші органометалічні реакції сполучення, наприклад, використовуючи реагенти олова (сполучення Стіла) або реагенти цинку (сполучення Негіши), також можуть бути використані замість реакції сполучення Сузукі, використовуючи реагенти бору, описані у Схемі Реакції III. Сполуки Формули 7 можуть бути одержані, слідуючи наступній Схемі Реакції IV: Схема Реакції IV 10 15 20 У цьому випадку, M являє собою відхідну групу (наприклад, хлор, бром, йод, метансульфоніл, та подібні), R50 являє собою відхідну групу (наприклад, йод, бром, хлор, трифторметансульфонілокси, та подібні), та R7 приймає значення, описані у Короткому описі даного винаходу. Сполука Формули 7 може бути одержана шляхом введення у реакцію амінної сполуки Формули 10 зі сполукою Формули 11. Реакцію проводять у присутності прийнятної основи (наприклад, триетиламін, карбонат калію, та подібні) у розчиннику, такому як ізопропанол, ДМСО, NMP, або діоксан при температурі від приблизно 25 до приблизно 120 °C. У деяких випадках подальші перетворення тільки що введеної R 1 групи далі можуть бути проведені для досягнення кінцевої заданої R1 групи. Сполуки Формули 11a, які являють собою підгрупу сполук Формули 11, у яких M являє собою метансульфоніл, можуть бути одержані слідуючи наступній Схемі Реакції V: Схема Реакції V 25 30 у якій R7 та R50 приймають значення, визначені у Короткому описі даного винаходу. Сполука Формули 11a може бути одержана шляхом введення у реакцію сполуки Формули 12 з прийнятною окислюючою системою (наприклад, м-хлорпербензойна кислота у розчиннику дихлорметані, або Oxone ™ у водному метанолі, та подібні), при температурі від приблизно 78 °C до приблизно 50 °C. До закінчення реакція триває до приблизно 24 годин. Сполука Формули 12, у якій R50 являє собою хлор, бром або йод, у свою чергу може бути одержана шляхом введення у реакцію амінної сполуки Формули 13 з прийнятною системою реагентів діазотування (наприклад, азотиста кислота у поєднанні з галогенідною сіллю міді (I), ізоаміл-нітрит у поєднанні з йодидом/метилен-йодидом міді (I), ізоаміл-нітрит у поєднанні з трифторидом бору, йодом та йодидом калію у ацетонітрилі та подібні). Реакція відбувається при 12 UA 112285 C2 5 10 15 20 25 30 температурі приблизно 0 до приблизно 80 °C, та до закінчення займає від приблизно 1 до приблизно 6 годин. Сполука Формули 13 може бути одержана шляхом введення у реакцію сполуки Формули 14 зі сполукою Формули 3, як описано для Схеми Реакції I. Сполука Формули 14 може бути одержана шляхом циклізації енамінонітрильної сполуки Формули 15 з гідразином або гідразиновою сіллю у прийнятному розчиннику (наприклад, такому як етанол та подібні). Реакція відбувається при температурі приблизно 25 до приблизно 100 °C, та може тривати до закінчення від приблизно 1 години до приблизно 24 годин. Альтернативно, сполука Формули 13 може бути одержана зі сполуки Формули 15 за одностадійну процедуру шляхом введення у реакцію сполуки Формули 15 з монозаміщеним гідразином R7NH-NH2. Реакція відбувається при температурі від приблизно 25 до приблизно 100 °C, та може тривати до закінчення від приблизно 1 години до приблизно 24 годин. Сполука Формули 15 у свою чергу може бути одержана за реакцією сполуки Формули 16 з ДМФА ДМА або реагентом Бредеріка, необов’язково у присутності спів-розчиннику, такого як ДМФА, при температурі приблизно 50 до приблизно 150 °C. Реакція триває до закінчення від приблизно 1 до приблизно 24 годин. Сполука Формули 16 може бути одержана шляхом обробки сполуки Формули 17 з прийнятною кислотою (наприклад, п-толуолсульфоновою кислотою, та подібними) у прийнятному інертному розчиннику (наприклад, такому як толуол та подібні). Реакція відбувається при температурі приблизно 50 до приблизно 120 °C, та триває до закінчення від приблизно 1 до приблизно 24 годин. Нарешті, сполука Формули 17 може бути одержана шляхом введення у реакцію 4-хлор-2(метилтіо)піримідину з трет-бутил-ціаноацетатом у присутності прийнятної основи (наприклад, такої як гідрид натрію та подібні) та прийнятного розчиннику (наприклад, такого як ДМСО та подібні), при температурі приблизно 25 до приблизно 80 °C. Реакція триває до закінчення від приблизно 1 до приблизно 24 годин. Сполуки Формули 11b, які являють собою підгрупу сполук Формули 11, у якій M являє собою галоген, можуть бути одержані слідуючи наступній Схемі Реакції VI: Схема Реакції VI 13 UA 112285 C2 5 10 15 20 25 30 35 40 45 50 55 60 у якій R7 та R50 приймають значення, визначені у Короткому описі даного винаходу. Сполука Формули 11b, у якій M являє собою галоген, може бути одержана шляхом введення у реакцію сполуки Формули 20 з прийнятною системою реагентів діазотування (наприклад, азотиста кислота у поєднанні з галогенідною сіллю міді (I), нітрит натрію у поєднанні з птолуолсульфоновою кислотою та йодидом калію. Реакція відбувається при температурі приблизно 0 до приблизно 80 °C, та до закінчення займає від приблизно 1 до приблизно 6 годин. Альтернативно, обробка сполуки Формули 20 реагентом діазотування (наприклад, таким як нітрит натрію та подібні) у присутності карбонової кислоти (наприклад, трифтороцтової кислоти та подібних) при 0 - 40 °C протягом періоду від приблизно 0,5 до приблизно 6 годин, що супроводжують обробкою основним водним розчином (наприклад, таким як водний розчин карбонату калію та подібні), приводить до одержання сполуки Формули 21 (така сполука може існувати у таутомерних формах). Подальша обробка сполуки Формули 21 хлоруючим реагентом (наприклад, оксихлорид фосфору та подібні), необов’язково у присутності основи, такої як N,Nдиметиланілін або DIPEA, та необов’язково у присутності інертного розчиннику, такого як ацетонітрил або толуол, та добавки, такої як ДМФА, при температурі від приблизно 50 до приблизно 110 °C, та впродовж часу від приблизно 1 до приблизно 72 годин, забезпечує одержання сполуки Формули 11b, у якій M являє собою хлор. Сполука Формули 20 у свою чергу може бути одержана за реакцією сполуки Формули 22 з гуанідином або гуанідиновою сіллю (наприклад, гідрохлорид гуанідиніну або карбонат гуанідину), необов’язково у присутності основи (наприклад, такої як гідроксид літію та подібні) у прийнятному розчиннику (наприклад, такому як втор-бутанол, NMP та подібні), при температурі від приблизно 50 до приблизно 180 °C, та впродовж часу від приблизно 2 до приблизно 48 годин. Сполука Формули 22 може бути одержана шляхом введення у реакцію сполуки Формули 23 з ДМФА ДМА або реагентом Бредеріка, необов’язково у присутності спів розчиннику, такого як ДМФА, при температурі від приблизно 50 до приблизно 150 °C. Реакція до закінчення триває від приблизно 1 до приблизно 24 годин. Сполука Формули 23, у якій R50 являє собою хлор, бром або йод, може бути одержана шляхом введення у реакцію амінної сполуки Формули 24 з прийнятною системою реагентів діазотування (наприклад, азотиста кислота у поєднанні з міді (I) галогенідною сіллю та йодидом калію, або ізоамілнітрит у поєднанні з бору трифторидом-ТГФ, йодом, йодидом калію та ацетонітрилом). Реакція відбувається при температурі приблизно 0 до приблизно 80 °C, та до закінчення займає від приблизно 1 до приблизно 6 годин. Сполука Формули 24 у свою чергу може бути одержана шляхом введення у реакцію сполуки Формули 25 з органометалічним реагентом, таким як метиллітій, комплекс метиллітій-бромід літію, або метилмагнієвий галогенідний реагент, у інертному розчиннику, такому як ТГФ, ефір або циклопропіл-метиловий ефір, при температурі від приблизно 0 до приблизно 100 °C, що супроводжують обробкою водним розчином, що гасить. Реакція до закінчення займає від приблизно 2 до приблизно 48 годин. Сполука Формули 25 може бути одержана шляхом введення у реакцію сполуки Формули 26 зі сполукою Формули 3, як описано для Схеми Реакції I. Альтернативно, сполука Формули 25 може бути одержана зі сполуки Формули 27, у якій дві R" групи взяті разом утворюють кислотонестійку захисну групу (наприклад, імін, такий як бензиліден або карбамат, такий як третбутилкарбамат). Реакцію проводять шляхом обробки сполуки Формули 27 водним кислотним реагентом (наприклад, таким як концентрована соляна кислота та подібні) у розчиннику, такому як етанол, при температурі приблизно 25 до приблизно 100 °C. Переважно дві R" групи, взяті разом, утворюють імін, такий як бензилідин. Сполука Формули 27 у свою чергу може бути одержана шляхом введення у реакцію сполуки Формули 28 зі сполукою Формули 29, у якій дві R" групи взяті разом утворюють кислото-нестійку захисну групу (наприклад, імін, такий як бензиліден або карбамат, такий як третбутилкарбамат). Реакцію проводять у розчиннику (наприклад, такому як толуол, метанол або етанол) при температурі від приблизно 25 до приблизно 120 °C, необов’язково у присутності каталізатору, такого як ДМАП, та триває до закінчення від приблизно 1 до приблизно 24 годин. Необов’язково, реакцію проводять у інертному розчиннику (наприклад, ТГФ та подібні) у присутності основи (наприклад, такої як н-бутиллітій та подібні) при температурі приблизно -80 до приблизно 25 °C, впродовж часу від приблизно 0,5 до приблизно 12 годин. Сполука Формули 29 може бути одержана за способами, відомими спеціалістам, кваліфікованим у даній галузі техніки. Наприклад, сполука Формули 29, у якій дві R" групи взяті разом утворюють бензиліденову групу, може бути одержана шляхом введення у реакцію бензальдегіду з моно-заміщеним гідразином R7NHNH2, у розчиннику, такому як етанол або 14 UA 112285 C2 5 толуол, впродовж від приблизно 1 до приблизно 24 годин, та при температурі приблизно 25 до приблизно 120 °C. Альтернативно, реакція може бути проведена, використовуючи монозаміщену гідразинову сіль (наприклад, гідрохлоридна сіль або оксалатна сіль, та подібні), у поєднанні з основою (наприклад, такою як ацетат натрію або триетиламін). Сполуки Формули 8 або Формули 8a можуть бути одержані як описано у наступній Схемі Реакції VII: Схема Реакції VII 10 15 20 25 у якій R2, R3, R4, R5, та Y приймають значення, визначені у Короткому описі даного винаходу, M являє собою відхідну групу (наприклад, йод, бром, хлор, трифторметансульфонілокси, та подібні), та кожна R’ група може являти собою, наприклад, водень, метил та подібні, або дві R’ групи можуть бути сполучені разом з утворенням циклічного боронат-складного ефіру. Кожна з двох R90 груп може являти собою водень, або дві R90 групи, взяті разом, можуть являти собою прийнятну азот-захисну групу (наприклад, одна R90 може являти собою водень та інша може являти собою BOC). Сполуки Формули 8 або Формули 8a можуть бути одержані шляхом введення у реакцію сполуки Формули 50 або Формули 50a, відповідно, з диборною сполукою (наприклад, біс(пінаколято)дибор та подібні) у присутності прийнятного каталізатору з перехідного металу (наприклад, PdCl2(dppf)),) та прийнятної основи (наприклад, такої як ацетат калію та подібні) у прийнятному розчиннику (наприклад, такому як толуол, діоксан та подібні). Реакція проходить у температурному інтервалі від приблизно 20 °C до приблизно 120 °C та до закінчення може тривати до приблизно 24 годин. Сполука Формули 50 у свою чергу може бути одержана шляхом сульфонілювання сполуки Формули 51, як описано для Схеми Реакції II. Спеціалісту, кваліфікованому у даній галузі техніки, слід прийняти до уваги, що сполуки Формули 51 або Формули 50a, наприклад, 3-броманіліни, або N-BOC-захищені 3-броманіліни, можуть бути одержані шляхом цілого ряду способів, включаючи, не обмежуючись наведеними, ті, що описані далі у Прикладах нижче. Сполука Формули 70 може бути одержана як описано у наступній Схемі Реакції VIII: 30 Схема Реакції VIII 35 у якій R8b приймає значення, описані у Короткому описі даного винаходу, та R 55 вибирають з C1-4алкілу або гало-заміщеного-C1-4алкілу. Сполука Формули 70 може бути одержана шляхом 15 UA 112285 C2 5 10 15 20 25 обробки сполуки Формули 71 підходящою відновлюючою системою (наприклад, гідрогенування над паладієвим каталізатором, та подібні) у прийнятному розчиннику (наприклад, такому як етанол або етилацетат) при температурі від приблизно 25 до приблизно 75 °C, впродовж періоду від приблизно 0,5 до приблизно 12 годин. Сполука Формули 71 у свою чергу може бути одержана за допомогою двостадійного процесу, що складається з перетворення гідрокси групи сполуки Формули 73 у прийнятну відхідну групу, що супроводжують заміною на азидний аніон. Для першої стадії, прийнятні реагенти включають трибромід фосфору, або метансульфоніл-хлорид у комбінації з прийнятною основою, такою як триетиламін. Ці реакції проводять у прийнятному розчиннику (наприклад, дихлорметан, та подібні), при температурі від приблизно 0 до приблизно 50 °C. Для другої стадії, заміну проводять азидним регентом (наприклад, азид натрію та подібні) у прийнятному розчиннику (наприклад, ДМФА або ДМСО) при температурі від приблизно 25 до приблизно 150 °C. Реакція триває до закінчення від приблизно 1 до приблизно 24 годин. Альтернативно, перетворення може бути виконане у одну стадію шляхом обробки сполуки Формули 73 фосфіновим реагентом (наприклад, трифенілфосфін та подібні) та азодикарбоксилатним реагентом (наприклад, діетилазодикарбоксилат та подібні) у присутності азотисто-водневої кислоти (утвореної in situ з азидної солі, такої як азид натрію, та кислоти). Реакція відбувається при температурі приблизно -80 °C до приблизно 75 °C, та триває до закінчення від приблизно 1 до приблизно 24 годин. Сполука Формули 73 може бути одержана шляхом обробки сполуки Формули 74 хлорформіатом (наприклад, метил-хлорформіат та подібні) або альтернативним реагентом алкоксикарбонілювання, таким як ди-трет-бутилдикарбоксилат. Реакція відбувається у інертному розчиннику (наприклад, такому як дихлорметан та подібні) при температурі приблизно -80 до приблизно 25 °C, та до закінчення займає від приблизно 1 до приблизно 12 годин, необов’язково може бути використана основа, така як триетиламін. Ця реакція також може проводитися у двофазній системі, що складається з розчиннику, такого як ТГФ або діоксан, та водного основного розчину, такого як водний розчин бікарбонату натрію, при температурі приблизно 25 °C, протягом періоду від приблизно 2 до приблизно 16 годин. Сполука Формули 70 також може бути одержана як описано у наступній Схемі Реакції IX: 30 Схема Реакції IX 35 40 45 50 у якій R8b приймає значення, описані у Короткому описі даного винаходу, R55 вибирають з C1або гало-заміщеного-C1-4алкілу, та R56 являє собою придатну захисну групу, наприклад, бензилоксикарбоніл (CBz). Сполука Формули 70 може бути одержана шляхом зняття захисту зі сполуки Формули 75. Наприклад, сполука Формули 70 може бути одержана шляхом обробки сполуки Формули 75, у якій R56 являє собою Cbz, з прийнятною відновлюючою системою (наприклад, гідрогенування над паладієвим каталізатором, та подібні) у прийнятному розчиннику (наприклад, такому як етанол, метанол, MTBE або етилацетат) при температурі приблизно 25 до приблизно 75 °C, необов’язково у присутності кислоти, такої як соляна кислота, протягом періоду від приблизно 0,5 до приблизно 12 годин. Альтернативно, зняття захисту можу бути проведене за умов трансферного гідрогенування, використовуючи прийнятний донор водню, такий як мурашина кислота, форміат амонію, або 1,4-циклогексадієн. Сполука Формули 75 у свою чергу може бути одержана за реакцією сполуки Формули 76 з хлорформіатом (наприклад, таким як метилхлорформіат та подібні) або альтернативним реагентом алкоксикарбонілювання, таким як ди-трет-бутилдикарбоксилат. Реакція відбувається у інертному розчиннику (наприклад, дихлорметані та подібних) при температурі приблизно -80 до приблизно 25 °C, та триває до закінчення від приблизно 1 до приблизно 24 годин. Необов’язково може бути використана основа, така як триетиламін. Ця реакція також може проводитися у двофазній системі, що складається з розчиннику, такого як ТГФ або діоксан, та 4алкілу 16 UA 112285 C2 5 10 15 20 25 30 35 40 45 50 55 60 водного основного розчину, такого як водний розчин бікарбонату натрію, при температурі приблизно 25 °C, протягом періоду від приблизно 2 до приблизно 16 годин. Сполука Формули 76 може бути одержана шляхом зняття захисту зі сполуки Формули 77. Умови зняття захисту можуть бути вибрані такими, щоб забезпечити переважно або по суті один ізомер Формули 76. Альтернативно можуть бути вибрані умови, у яких не віддається ніякої, навіть невеликої переваги, утворенню одного ізомеру Формули 77, але у яких сполука Формули 76 тим не менше може бути виділена з достатньою чистотою для подальшого застосування. Засоби отримання такої чистоти можуть включати кристалізацію або вільної основи або солі. Сполука Формули 76, у якій R56 являє собою Cbz, може бути одержана шляхом обробки сполуки Формули 77 бензил-хлорформіатом. Реакція відбувається у інертному розчиннику (наприклад, дихлорметані та подібному) при температурі приблизно -80 до приблизно 25 °C, та триває до закінчення від приблизно 1 до приблизно 24 годин. Основа, така як триетиламін, необов’язково може бути використана. Реакція також може проводитися у двофазній системі, що складається з розчиннику, такого як ТГФ або діоксан, та водного основного розчину, такого як водний розчин бікарбонату натрію, при температурі приблизно 25 °C, впродовж періоду від приблизно 2 до приблизно 24 годин. Сіль сполуки Формули 77 може бути використана у поєднанні з основою, такою як триетиламін або карбонат натрію, як добавка замість вільної основи. Спеціалісту, кваліфікованому у даній галузі техніки, слід прийняти до уваги, що сполука Формули 70 може бути або одним енантіомером або сумішшю енантіомерів, та що один енантіомер сполуки Формули 70 може бути отриманий, виходячи з відповідного одного енантіомеру сполуку Формули 74 або Формули 77. Детальні приклади синтезу сполуки Формули Ia можуть бути знайдені у Прикладах, представлених нижче. Додаткові способи одержання сполук даного винаходу Сполука даного винаходу може бути одержана у вигляді солі приєднання кислоти шляхом введення у реакцію вільної основної форми сполуки з фармацевтично прийнятною неорганічною або органічною кислотою. Альтернативно, сіль приєднання фармацевтично прийнятної основи сполуки даного винаходу може бути одержана у реакції вільної кислотної форми сполуки з фармацевтично прийнятною неорганічною або органічною основою. Альтернативно, сольові форми сполук даного винаходу можуть бути одержані, використовуючи солі вихідних матеріалів або проміжних сполук. Вільні кислотні або вільні основні форми сполук даного винаходу можуть бути одержані з відповідної солі приєднання основи або солі приєднання кислоти, відповідно. Наприклад, сполука даного винаходу у формі солі приєднання кислоти може бути перетворена у відповідну вільну основу шляхом обробки прийнятною основою (наприклад, такою як розчин гідроксиду амонію, гідроксид натрію та подібні). Сполука даного винаходу у формі солі приєднання основи може бути перетворена у відповідну вільну кислоту шляхом обробки прийнятною кислотою (наприклад, соляна кислота, тощо). Сполуки даного винаходу у неокисленій формі можуть бути одержані з N-оксидів сполук даного винаходу шляхом обробки відновлюючим агентом (наприклад, таким як сірка, діоксид сірки, трифеніл-фосфін, боргідрид літію, боргідрид натрію, фосфору трихлорид, трибромід, або подібні) у прийнятному інертному органічному розчиннику (наприклад, ацетонітрил, етанол, водний діоксан, або подібні) при 0-80 °C. Похідні проліків сполук даного винаходу можуть бути одержані за способами, відомими спеціалістам, кваліфікованим у даній галузі техніки (наприклад, для більш детального опису дивись Saulnier et al., (1994), Bioorganic and Medicinal Chemistry Letters, том 4, стор. 1985). Наприклад, відповідні пролікарські засоби можуть бути одержані шляхом введення у реакцію недериватизованої сполуки даного винаходу з прийнятним карбамілізуючим агентом (наприклад, 1,1-ацилоксиалкіл-карбано-хлоридат, пара-нітрофеніл карбонат, або подібні). Захищені похідні сполук даного винаходу можуть бути одержані за допомогою засобів, відомих спеціалістам, кваліфікованим у даній галузі техніки. Детальний опис технологій, застосовних для створення захисних груп та їх видалення, може бути знайдений у T. W. Greene, тє "Protecting Groups in Organic Chemistry", 3 видання, John Wiley and Sons, Inc., 1999. Сполуки даного винаходу можуть бути одержані зручним способом, або утворені за способом даного винаходу, як сольвати (наприклад, гідрати). Гідрати сполук даного винаходу можуть бути одержані зручним способом шляхом перекристалізації з суміші водний/органічний розчинник, використовуючи органічні розчинники, такі як діоксин, тетрагідрофуран або метанол. Сполуки даного винаходу можуть бути одержані у вигляді їх окремих стереоізомерів шляхом введення у реакцію рацемічної суміші сполуки з оптично активним розділюючим агентом з 17 UA 112285 C2 5 10 15 20 25 30 35 40 45 утворенням пари діастереоізомерних сполук, розділення діастереоізомерів та відновлення оптично чистих енантіомерів. Хоча розділення енантіомерів може бути виконане, використовуючи ковалентні діастереомерні похідні сполук даного винаходу, кращими є комплекси, що дисоціюються (наприклад, кристалічні діастереомерні солі). Діастереомери мають відмінні фізичні властивості (наприклад, точки плавлення, точки кипіння, розчинності, реакційну здатність, тощо) та можуть бути легко розділені, приймаючи до уваги перевагу цих відмінностей. Діастереомери можуть бути розділені за допомогою хроматографії, або переважно, за допомогою розділення/відділення технологій, основаних на різницях у розчинності. Оптично чистий енантіомер потім відновлюють, з відновлюючим агентом, шляхом будь-яких практичних засобів, які не будуть приводити до рацемізації. Більш детальний опис технологій, застосовний для розділення стереоізомерів сполук з їх рацемічної суміші, може бути знайдений у Jean Jacques, Andre Collet, Samuel H. Wilen, "Enantiomers, Racemates and Resolutions", John Wiley and Sons, Inc., 1981. Коротко, сполуки Формули I можуть бути одержані за способом, який включає: (a) спосіб Схем Реакцій I-IX, та (b) необов’язково перетворення сполуки даного винаходу у фармацевтично прийнятну сіль; (c) необов’язково перетворення сольової форми сполуки даного винаходу у не-сольову форму; (d) необов’язково перетворення неокисленої форми сполуки даного винаходу у фармацевтично прийнятний N-оксид; (e) необов’язково перетворення N-оксидної форми сполуки даного винаходу у її неокислену форму; (f) необов’язково відділення окремого ізомеру, наприклад, стереоізомеру, сполуки даного винаходу від суміші ізомерів; (g) необов’язково перетворення недериватизованої сполуки даного винаходу у фармацевтично прийнятну пролікарську похідну; та (h) необов’язково перетворення пролікарської похідної сполуки даного винаходу у її недериватизовану форму. Оскільки вироблення вихідних матеріалів особливо не описане, сполуки є відомими або можуть бути одержані аналогічно до способів, відомих у даній галузі техніки або як розкрито у Прикладах, представлених нижче. Спеціаліст, кваліфікований у даній галузі техніки, зрозуміє, що описані вище перетворення є тільки типовими прикладами способів для одержання сполук даного винаходу, та що інші добре відомі способи можуть бути використані аналогічно. Приклади Даний винахід додатково проілюстрований на наступних проміжних сполуках та прикладах, але не обмежується ними, які показують одержання сполук Формули I відповідно до даного винаходу. Використовують наступні абревіатури: бензилоксикарбоніл (Cbz); третбутоксикарбоніл (BOC); Клітинна проліферація (CP); дихлорметан (ДХМ); N,N-диізопропілетиламін (DIPEA); [1,1'-Біс(дифенілфосфіно)фероцен]дихлорпаладій(II) (PdCl2(dppf)); 1,2-диметоксиетан (ДМЕ); N,N-диметил-ацетамід (ДМА); N,N-диметиламінопіридин (ДМАП); N,N-диметил-формамід (ДМФА); N,N-диметил-формамід-диметилацеталь (ДМФА ДМА); диметилсульфоксид (ДМСО); етилацетат (EtOAc); високо ефективна рідинна хроматографія (ВЕРХ); ізопропіл-ацетат (iPrOAc); метансульфоніл (Ms); 2-метилтетрагідрофуран (2метилТГФ); N-метилпіролідинон (NMP); тетрагідрофуран (ТГФ); тонкошарова хроматографія (ТШХ); та пара-толуолсульфонова кислота (pTsOH). Проміжна сполука. Ціано-(2-метилтіо-піримідин-4-іл)-оцтової кислоти трет-бутиловий складний ефір 50 55 До суспензії гідриду натрію (7,15 г, 179 ммоль, 60% у маслі) у ДМСО (100 мл) додають третбутил-ціаноацетат (24,8 г, 170 ммоль) при 23 °C. Після закінчення виділення водню, додають 4хлор-2-метилтіопіримідин (13,7 г, 85 ммоль). Реакційну суміш нагрівають при 80 °C впродовж 16 годин. Реакційну суміш потім охолоджують до кімнатної температури та гасять охолодженим льодом насиченим розчином хлориду амонію (300 мл). Тверду речовину фільтрують та 18 UA 112285 C2 5 10 15 промивають водою (2×200 мл). 300 мл гексану додають до цієї твердої речовини та суспензію нагрівають при 60 °C впродовж 1 години та потім охолоджують до кімнатної температури. Тверду речовину фільтрують та промивають гексаном, що забезпечує одержання заголовної 1 сполуки; H ЯМР 400 MГц (CDCl3) δ 7,82 (d, 1H), 6,74 (d, 1H), 2,63 (s, 3H), 2,61 (s, 1H), 1,52 (s, 9H); MS m/z: 266,0 (M + 1). Проміжна сполука. (2-Метилтіо-піримідин-4-іл)-ацетонітрил До розчину Проміжної сполуки ціано-(2-метилтіо-піримідин-4-іл)-оцтової кислоти третбутилового складного ефіру (5,3 г, 20 ммоль) у безводному толуолі (100 мл) додають птолуолсульфонову кислоту (800 мг). Цю суміш нагрівають до зрошення впродовж 8 годин, охолоджують до кімнатної температури та екстрагують етилацетатом. Органічний шар промивають 1N водним розчином гідроксиду натрію та сольовим розчином, сушать над сульфатом натрію, фільтрують та концентрують. Неочищений продукт очищують шляхом силікагелевої хроматографії (елюент 3:1 гексани/етилацетат), що забезпечує одержання 1 заголовної сполуки: H ЯМР 400 MГц (CDCl3) δ 8,56 (d, 1H), 7,12 (d, 1H), 3,84 (s, 2H), 2,57 (s, 3H); MS m/z: 166,0 (M + 1). Проміжна сполука. 4-(2-(Метилтіо)піримідин-4-іл)-1H-піразол-3-амін 20 25 30 35 40 45 Стадія 1. 3-(Диметиламіно)-2-(2-(метилтіо)піримідин-4-іл)акрилонітрил. N,NДиметилформамід-диметил-ацеталь (30 мл) додають до Проміжної сполуки (2-метилтіопіримідин-4-іл)-ацетонітрилу (2,62 г, 15,7 ммоль) та цю суміш нагрівають при 100 °C впродовж 16 годин. Охолоджуючу реакційну суміш концентрують, та залишок використовують без додаткового очищення. Стадія 2. 4-(2-(Метилтіо)піримідин-4-іл)-1H-піразол-3-амін. Суміш неочищеного 3(диметиламіно)-2-(2-(метилтіо)піримідин-4-іл)акрилонітрилу з попередньої стадії (повна кількість) та гідразину моногідрату (2,36 мл, 47 ммоль) у безводному етанолі (75 мл) нагрівають при 80 °C впродовж 16 годин. Реакційну суміш охолоджують до кімнатної температури та концентрують. Реакційну суміш розподіляють між етилацетатом та сольовим розчином. Органічний шар відділяють та промивають сольовим розчином, сушать над сульфатом натрію, фільтрують та концентрують. Неочищений продукт очищують шляхом силікагелевої хроматографії (елюент 2-5% метанолу у дихлорметані), що забезпечує одержання 4-(21 (метилтіо)піримідин-4-іл)-1H-піразол-3-аміну: H ЯМР 400 MГц (ДМСО-d6) δ 11,9 (s, 1H), 8,3 (s, 1H), 7,87 (s, 1H), 7,23 (s, br 1H), 6,43 (s, 1H), 5,74 (s, 1H), 2,53 (s, 3H); MS m/z: 208,0 (M + 1). Проміжна сполука. 1-Ізопропіл-4-(2-(метилтіо)піримідин-4-іл)-1H-піразол-3-амін: Проміжну сполуку 4-(2-(метилтіо)піримідин-4-іл)-1H-піразол-3-амін (10,0 г, 40 ммоль) розчиняють у ТГФ (200 мл), що супроводжують додаванням 2-йодпропану (6,3 мл, 63 ммоль) та метоксиду натрію (25% мас. розчин у метанолі, 14,3 мл, 63 ммоль). Цю суміш нагрівають при 50 °C при перемішуванні у атмосфері азоту впродовж 3 днів, потім концентрують у вакуумі. Залишок переносять у етилацетат (200 мл) та промивають водним розчином карбонату калію та сольовим розчином, потім сушать над сульфатом натрію, фільтрують, та концентрують, що забезпечує одержання коричневого залишку. Залишок хроматографують на силікагелі (елюент гексан/етилацетат), що забезпечує одержання 1-ізопропіл-4-(2-(метилтіо)піримідин-4-іл)-1H1 піразол-3-аміну у вигляді твердої речовини; H ЯМР 400 MГц (CDCl3) δ 8,23 (d, J=5,6 Гц, 1H), 7,60 (s, 1H), 6,83 (d, J=5,6 Гц, 1H), 5,23 (d, J=2,8 Гц, 2H), 4,21-4,25 (m, 1H), 2,50 (s, 3H), 1,37 (d, 19 UA 112285 C2 J=6,8 Гц, 6H); MS m/z: 250,1 (M + 1). Аналогічно отримують: 1-Етил-4-(2-(метилтіо)піримідин-4-іл)-1H-піразол-3-амін та 1-Метил4-(2-(метилтіо)піримідин-4-іл)-1H-піразол-3-амін. Проміжна сполука. 4-(3-Йод-1-ізопропіл-1H-піразол-4-іл)-2-(метилтіо)піримідин: 5 10 15 Суміш Проміжної сполуки 1-ізопропіл-4-(2-(метилтіо)піримідин-4-іл)-1H-піразол-3-аміну (4,0 г, 16,0 ммоль), ізопентилнітриту (13,2 г, 112 ммоль), та метилен-йодиду (30 мл) нагрівають при 100 °C впродовж 3 годин. Видалення летких речовин у вакуумі забезпечує одержання темного залишку, який очищують шляхом силікагелевої хроматографії (елюент 2:1 гексан/етилацетат), що забезпечує одержання заголовної сполуки у вигляді твердої речовини; MS m/z: 361,1 (M + 1). Аналогічно одержують: 4-(3-Йод-1-етил-1H-піразол-4-іл)-2-(метилтіо)піримідин; 4-(3-Йод-1метил-1H-піразол-4-іл)-2-(метилтіо)піримідин; та 4-(3-йод-1H-піразол-4-іл)-2(метилтіо)піримідин. Проміжна сполука. 4-(3-Йод-1-(тетрагідро-2H-піран-2-іл)-1H-піразол-4-іл)-2(метилтіо)піримідин. 20 25 Розчин 4-(3-йод-1H-піразол-4-іл)-2-(метилтіо)піримідину (270 мг, 0,85 ммоль) та п-моногідрат толуолсульфонової кислоти (32 мг, 0,17 ммоль) у 3,4-дигідро-2H-пірані (1 мл) нагрівають при 60 °C впродовж 5 годин. Охолоджену суміш розбавляють етилацетатом, та цю суміш промивають водою та сольовим розчином, та потім сушать над сульфатом натрію, фільтрують, та концентрують. Залишок хроматографують на силікагелі (елюент 10% етилацетату у гексанах), що забезпечує одержання заголовної сполуки. MS (m/z): 402,7 (M+1). Проміжна сполука. 4-(3-Йод-1-ізопропіл-1H-піразол-4-іл)-2-(метилсульфоніл)-піримідин: 30 35 До розчину Проміжної сполуки 4-(3-йод-1-ізопропіл-1H-піразол-4-іл)-2-(метилтіо)піримідину (4,51 г, 12,5 ммоль) у дихлорметані (60 мл) при 0 °C додають м-хлорпербензойну кислоту (3,65 г, 77% чистоти, 16,3 ммоль). Цю суміш перемішують при 0 °C у атмосфері азоту впродовж 3 годин, потім розбавляють етилацетатом та промивають водним розчином карбонату калію та сольовим розчином. Органічний шар сушать над сульфатом магнію, фільтрують, та концентрують, що забезпечує одержання 4-(3-йод-1-ізопропіл-1H-піразол-4-іл)-2(метилсульфоніл)піримідину у вигляді твердої речовини. MS m/z: 393,0 (M + 1). Аналогічно одержують: 4-(3-Йод-1-етил-1H-піразол-4-іл)-2-(метилсульфоніл)-піримідин; та 4(3-Йод-1-метил-1H-піразол-4-іл)-2-(метилсульфоніл)піримідин. 40 20 UA 112285 C2 5 10 15 20 25 30 Проміжна сполука. 1-Бензиліден-2-ізопропілгідразин До круглодонної колби, що містить безводний ацетат натрію (8,2 г, 0,1 моль) у 125 мл 50% етанолу, додають ізопропілгідразин-HCl сіль (11,1 г, 0,1 моль) та бензальдегід (10,6 г, 0,1 моль). Цю суміш перемішують при кімнатній температурі впродовж 20 годин. Реакційну суміш екстрагують ефіром (3×250 мл). Органічні шари об’єднують та промивають водним розчином бікарбонату натрію та сольовим розчином та сушать над сульфатом натрію. Фільтрування, концентрування, та спів-випарювання з толуолом (3x) забезпечує одержання заголовної сполуки у вигляді масла. MS m/z 163,3 (M + 1). Аналогічно одержують: 1-Бензиліден-2-етилгідразин, виходячи з оксалату етилгідразину, використовуючи метанол та триетиламін замість етанолу та ацетату натрію, відповідно; та 1Бензиліден-2-метилгідразин, виходячи з метилгідразину, використовуючи метанол як розчинник, без додавання основи. Проміжна сполука. 2-((2-Бензиліден-1-ізопропілгідразиніл)метилен)-малононітрил: Розчин Проміжної сполуки 1-бензиліден-2-ізопропілгідразину (12,9 г, 0,079 моль) у 200 мл безводного ТГФ охолоджують у бані сухий лід/ацетон у атмосфері аргону. До цього розчину додають н-бутиллітій (1,6 M у гексанах, 66 мл, 0,106 моль) через шприц. Після завершення додавання, цю суміш перемішують при температурі сухого льоду впродовж ще 5 хвилин. Додають розчин (2-(етоксиметилен)малононітрилу (13,6 г, 0,11 моль) у ТГФ (30 мл). Цю суміш перемішують при температурі сухого льоду впродовж 0,5 години, та потім гасять насиченим водним розчином бікарбонату натрію. Загашену реакційну суміш залишають нагрітися до кімнатної температури та екстрагують етилацетатом. Органічні шари об’єднують, сушать над сульфатом натрію, фільтрують, та концентрують. Залишок суспендують у етанолі при обробці ультразвуком. Отриманий осад збирають за допомогою фільтрування та промивають невеликою кількістю холодного етанолу, що приводить до одержання 2-((2-бензиліден-1ізопропілгідразиніл)метилен)малононітрилу у вигляді жовтої твердої речовини. Маточну рідину концентрують та залишок очищують за допомогою силікагелевої колонкової хроматографії (елюент 1:1 гексани/етилацетат), що забезпечує одержання додаткової кількості 2-((2бензиліден-1-ізопропілгідразиніл)-метилен)малононітрилу. MS m/z 239,2 (M + 1). Проміжна сполука. 2-((2-Бензиліден-1-етилгідразиніл)метилен)-малононітрил: 35 40 45 До розчину 2-(етоксиметилен)малононітрилу (15,2 г, 0,124 моль) у 100 мл толуолу додають Проміжну сполуку 1-бензиліден-2-етилгідразин (18,4 г, 0,124 моль). Цю суміш залишають стояти при кімнатній температурі, та утворюється осад. Реакційну суміш перемішують впродовж ще 16 годин. Осад збирають на фільтр та промивають невеликою кількістю холодного етанолу, що приводить до одержання 2-((2-бензиліден-1-етилгідразиніл)метилен)малононітрилу у вигляді твердої речовини. Аналогічно одержують 2-((2-Бензиліден-1-метилгідразиніл)-метилен)малононітрил. Проміжна сполука. 3-Аміно-1-ізопропіл-1H-піразол-4-карбонітрил Суміш Проміжної сполуки 2-((2-бензиліден-1-ізопропілгідразиніл)-метилен)-малононітрилу 21 UA 112285 C2 5 10 (9,42 г, 40 ммоль), концентрованої соляної кислоти (5 мл), та етанолу (50 мл) нагрівають при зрошенні впродовж 20 хвилин. Реакційну суміш концентрують та додають ефір (50 мл). Цю суміш обробляють ультразвуком, потім верхній ефірний шар відкидають. До залишку додають 20 мл 5N водного розчину гідроксиду натрію та цю суміш екстрагують дихлорметаном (3x). Органічні шари об’єднують, сушать над сульфатом натрію, фільтрують та концентрують. Залишок очищують за допомогою силікагелевої колонкової хроматографії (елюент 1:1 гексани/етилацетат), що забезпечує одержання 3-аміно-1-ізопропіл-1H-піразол-4-карбонітрилу у 1 вигляді коричневої твердої речовини. H ЯМР (400 MГц, ДМСО-d6) δ 8,09 (s, 1H), 5,51 (s, 2H), 4,22 (m, 1H), 1,31 (d, J=7 Гц, 6H); MS m/z 151,2 (M + 1). Аналогічно одержують: 3-аміно-1-етил-1H-піразол-4-карбонітрил; та 3-аміно-1-метил-1Hпіразол-4-карбонітрил. Проміжна сполука. 1-(3-Аміно-1-ізопропіл-1H-піразол-4-іл)етанон 15 20 25 До розчину Проміжної сполуки 3-аміно-1-ізопропіл-1H-піразол-4-карбонітрилу (5,29 г, 36,5 ммоль) у 200 мл безводного ТГФ при 0 °C додають розчин броміду метилмагнію (3 M у ефірі, 56,5 мл, 0,17 моль). Реакційну суміш нагрівають при зрошенні впродовж 4 годин. Цю суміш охолоджують до 0 °C та потім гасять 10% водним розчином соляної кислоти до нейтрального pH. Цю реакційну суміш екстрагують великою кількістю суміші 9:1 дихлорметан/ізопропанол. Органічні шари об’єднують та сушать над сульфатом натрію, фільтрують та концентрують. Неочищений продукт очищують за допомогою силікагелевої колонкової хроматографії (елюент від 1:1 етилацетат/гексани до 9:1 етилацетат/метанол), що забезпечує одержання заголовної 1 сполуки у вигляді світло-коричневої твердої речовини. H ЯМР (400 MГц, ДМСО-d6) δ 8,18 (s, 1H), 5,62 (s, 2H), 4,23 (m, 1H), 2,20 (s, 3H), 1,37 (d, J=7 Гц, 6H); MS m/z 168,2 (M + 1). Аналогічно одержують:1-(3-Аміно-1-етил-1H-піразол-4-іл)етанон; та 1-(3-Аміно-1-метил-1Hпіразол-4-іл)етанон. Проміжна сполука. 1-(3-Йод-1-ізопропіл-1H-піразол-4-іл)етанон 30 35 40 45 До розчину Проміжної сполуки 1-(3-аміно-1-ізопропіл-1H-піразол-4-іл)етанону (3,97 г, 24 ммоль) та п-TsOH.H2O (9,07 г, 48 ммоль, 2 екв.) у 150 мл ацетонітрилу при 0 °C додають краплинним способом розчин нітриту натрію (2,97 г, 43 ммоль, 1,8 екв.) та йодид калію (8,0 г, 48 ммоль, 2,0 екв.) у 20 мл води. Цю суміш перемішують при цій температурі впродовж 10 хвилин та потім залишають нагрітися до кімнатної температури та перемішують впродовж 3 годин. Цю суміш концентрують та потім розбавляють водою та нейтралізують водним розчином карбонату натрію до pH 9-10. Цю суміш екстрагують етилацетатом (3x). Об’єднані органічні шари промивають розчином тіосульфату натрію, сушать над сульфатом натрію, фільтрують та концентрують. Залишок очищують за допомогою силікагелевої колонкової хроматографії (елюент 1:1 гексани/етилацетат), що забезпечує одержання заголовної сполуки у вигляді світло1 коричневої твердої речовини. H ЯМР (400 MГц, ДМСО-d6) δ 8,51 (s, 1H), 4,53 (m, 1H), 2,37 (s, 3H), 1,41 (d, J=7 Гц, 6H); MS m/z 279,1 (M + 1). Аналогічно одержують: 1-(3-Йод-1-етил-1H-піразол-4-іл)етанон; та 1-(3-Йод-1-метил-1Hпіразол-4-іл)етанон. Проміжна сполука. 3-(Диметиламіно)-1-(3-йод-1-ізопропіл-1H-піразол-4-іл)проп-2-ен-1-он: 22 UA 112285 C2 5 Суміш Проміжної сполуки 1-(3-йод-1-ізопропіл-1H-піразол-4-іл)етанону (5,0 г, 18,0 ммоль) та N,N-диметилформамід-диметил-ацеталю (50 мл) нагрівають при 155 °C впродовж 20 годин. Цю суміш концентрують у вакуумі, що забезпечує одержання неочищеної заголовної сполуки. MS m/z 334,0 (M + 1). Аналогічно одержують: 3-(Диметиламіно)-1-(3-йод-1-етил-1H-піразол-4-іл)проп-2-ен-1-он; та 3-(Диметиламіно)-1-(3-йод-1-метил-1H-піразол-4-іл)проп-2-ен-1-он. Проміжна сполука. 4-(3-Йод-1-ізопропіл-1H-піразол-4-іл)піримідин-2-амін 10 15 20 Суміш неочищеної Проміжної сполуки 3-(диметиламіно)-1-(3-йод-1-ізопропіл-1H-піразол-4іл)проп-2-ен-1-ону (4,0 г, 12,0 ммоль), гуанідину гідрохлориду (2,63 г, 27,6 ммоль), гідроксиду літію (635 мг, 27,6 ммоль), та втор-бутанолу (50 мл) нагрівають при перемішуванні у запаюваній реакційній колбі при 110 °C впродовж 20 годин. Охолоджуючу реакційну суміш концентрують, потім додають воду та цю суміш екстрагують етилацетатом. Об’єднані екстракти сушать над сульфатом натрію, фільтрують та концентрують. Етилацетат додають до цього залишку твердої речовини, та цю суміш обробляють ультразвуком. Твердий продукт збирають на фільтрі, промивають етилацетатом та сушать, що приводить до одержання заголовної сполуки у вигляді жовто-коричневої твердої речовини. MS m/z 330,0 (M + 1). Аналогічно одержують: 4-(3-Йод-1-етил-1H-піразол-4-іл)піримідин-2-амін; та 4-(3-Йод-1метил-1H-піразол-4-іл)піримідин-2-амін. Проміжна сполука. 4-(3-Йод-1-ізопропіл-1H-піразол-4-іл)піримідин-2-ол 25 30 35 Нітрит натрію (314 мг, 4,55 ммоль) додають частинами до перемішуваної суміші Проміжної сполуки 4-(3-йод-1-ізопропіл-1H-піразол-4-іл)піримідин-2-аміну (500 мг, 1,52 ммоль) та трифтороцтової кислоти (15 мл) при 0 °C. Цю суміш залишають нагрітися до кімнатної температури та перемішують впродовж 1 години, потім розчинник видаляють у вакуумі. Неочищену суміш розбавляють етилацетатом та промивають насиченим водним розчином карбонату калію та сольовим розчином, що забезпечує одержання заголовної сполуки у вигляді твердої речовини. MS m/z 331,0 (M + 1). Аналогічно одержують: 4-(3-Йод-1-етил-1H-піразол-4-іл)піримідин-2-ол; та 4-(3-Йод-1-метил1H-піразол-4-іл)піримідин-2-ол. Проміжна сполука. 2-Хлор-4-(3-йод-1-ізопропіл-1H-піразол-4-іл)піримідин 23 UA 112285 C2 5 10 15 20 25 30 35 40 45 Розчин Проміжної сполуки 4-(3-йод-1-ізопропіл-1H-піразол-4-іл)піримідин-2-олу (438 мг, 1,33 ммоль) у оксихлориді фосфору (10 мл) нагрівають при 110 °C впродовж 16 годин. Цю суміш концентрують у вакуумі, потім водний розчин бікарбонату натрію обережно додають та цю суміш екстрагують етилацетатом. Об’єднані органічні екстракти сушать над сульфатом натрію, фільтрують та концентрують, що забезпечує одержання заголовної сполуки у вигляді жовтої твердої речовини. MS m/z 349,0 (M + 1). Аналогічно одержують: 2-Хлор-4-(3-йод-1-етил-1H-піразол-4-іл)піримідин; та 2-Хлор-4-(3йод-1-метил-1H-піразол-4-іл)піримідин. Проміжна сполука. (S)-Метил 1-гідроксипропан-2-ілкарбамат До розчину (S)-аланінолу (10 г, 130 ммоль) та бікарбонату натрію (32,8 г, 390 ммоль) у ТГФH2O (1:1, 650 мл) при 0 °C додають краплинним способом метил-хлорформіат (11,4 мл, 143 ммоль). Цю суміш перемішують та залишають нагрітися до кімнатної температури впродовж 4 годин, та потім екстрагують етилацетатом. Органічний шар промивають 1N водним розчином гідроксиду натрію та сольовим розчином, та потім сушать над сульфатом натрію, фільтрують та концентрують, що приводить до одержання неочищеної заголовної сполуки, яку використовують без додаткового очищення. MS m/z 134,1(M + 1). Аналогічно одержують: (R)-метил 1-гідроксипропан-2-ілкарбамат, використовуючи (R)алінол замість (S)-аланінолу; та (S)-1,1-Диметилетил 1-гідроксипропан-2-ілкарбамат використовуючи ди-трет-бутил-дикарбонат замість метил-хлорформіату. Проміжна сполука. (S)-Метил 1-азидопропан-2-ілкарбамат: До розчину Проміжної сполуки (S)-метил 1-гідроксипропан-2-ілкарбамату (2,65 г, 20 ммоль) та триетиламіну (7,0 мл, 50 ммоль) у безводному дихлорметані (100 мл) додають метансульфоніл-хлорид (1,91 мл, 23,9 ммоль). Цю суміш перемішують при кімнатній температурі впродовж 3 годин та потім екстрагують етилацетатом. Органічний шар промивають 1N розчином гідроксиду натрію та сольовим розчином, та потім сушать над сульфатом натрію, фільтрують та концентрують. Неочищений мезилатний продукт потім розчиняють у сухому ДМФА (70 мл) та додають азид натрію (5,2 г, 80 ммоль). Цю суміш нагрівають при перемішуванні при 80 °C впродовж 2 годин. Охолоджуючу реакційну суміш концентрують та залишок розподіляють між етилацетатом та сольовим розчином. Органічний шар відділяють та промивають сольовим розчином, сушать над сульфатом натрію, фільтрують та концентрують. Залишок очищують шляхом силікагелевої хроматографії (елюент 8:1 гексан/етилацетат), що забезпечує одержання (S)-метил 1-азидопропан-2-ілкарбамату. MS m/z 159,1 (M + 1). Аналогічно одержують: (R)-Метил 1-азидопропан-2-ілкарбамат; та (S)-1,1-диметилетил 1азидопропан-2-ілкарбамат. Проміжна сполука. (S)-Метил 1-амінопропан-2-ілкарбамат До розчину Проміжної сполуки (S)-метил 1-азидопропан-2-ілкарбамату (2,86 г, 18,2 ммоль) у етилацетаті (200 мл) додають 10% паладій на вугіллі (вологий, 286 мг). Колбу дегазують та 24 UA 112285 C2 5 10 15 20 25 знову заповнюють газоподібним воднем (балон, 1 атмосфера), та цю суміш перемішують при кімнатній температурі впродовж 16 годин. Реакційну суміш фільтрують через фільтр з целіту та промивають етилацетатом. Фільтрат концентрують, що приводить до одержання неочищеного 1 (S)-метил 1-амінопропан-2-ілкарбамату, який використовують без додаткового очищення. H ЯМР 400 MГц (CDCl3) δ 4,79 (s, 1H), 3,71-3,65 (m, 1H), 3,66 (s, 3H), 2,75 (dd, 1H), 2,65 (dd, 1H), 1,14 (d, 3H); MS m/z 133,1 (M + 1). Аналогічно одержують: (R)-Метил 1-амінопропан-2-ілкарбамат; та (S)-1,1-диметилетил 1амінопропан-2-ілкарбамат. Проміжна сполука. (S)-Метил 1-(4-(3-йод-1-ізопропіл-1H-піразол-4-іл)піримідин-2іламіно)пропан-2-ілкарбамат: Розчин Проміжної сполуки 2-хлор-4-(3-йод-1-ізопропіл-1H-піразол-4-іл)піримідину (1,4 г, 4,01 ммоль), (S)-метил 1-амінопропан-2-ілкарбамату (0,8 г, 6 ммоль) та триетиламіну (2,8 мл, 20 ммоль) у ізопропанолі (30 мл) та діоксані (20 мл) нагрівають у запаяній колбі при125 °C впродовж 48 годин. Охолоджену суміш концентрують у вакуумі, та водний розчин бікарбонату натрію додають до залишку. Цю суміш екстрагують етилацетатом, та об’єднані екстракти сушать над сульфатом натрію, фільтрують та концентрують. Неочищений залишок очищують за допомогою силікагелевої колонкової хроматографії (елюент 1:2 гексани/етилацетат), що забезпечує одержання заголовної сполуки у вигляді білої твердої речовини. MS m/z 445,0 (M + 1). Аналогічно одержують: (R)-Метил 1-(4-(3-йод-1-ізопропіл-1H-піразол-4-іл)піримідин-2іламіно)пропан-2-ілкарбамат; (S)-трет-бутил 1-(4-(3-йод-1-ізопропіл-1H-піразол-4-іл)піримідин-2іламіно)пропан-2-ілкарбамат; 3-(4-(3-йод-1-ізопропіл-1H-піразол-4-іл)піримідин-21 іламіно)пропаннітрил; 4-(3-йод-1-ізопропіл-1H-піразол-4-іл)-N-метилпіримідин-2-амін; та N -(42 2 (3-йод-1-ізопропіл-1H-піразол-4-іл)піримідин-2-іл)-N ,N -диметилетан-1,2-діамін. Проміжна сполука. N-(3-бром-2,4-дифторфеніл)пропан-1-сульфонамід 30 35 Розчин 3-бром-2,4-дифтораніліну (4,16 г, 20 ммоль, EP184384), н-пропансульфоніл-хлориду (4,6 мл, 40 ммоль), піридин (8 мл), ДМАП (97 мг), та ДХМ (100 мл) перемішують при кімнатній температурі впродовж 16 годин. Додають водний розчин бікарбонату натрію та цю суміш екстрагують етилацетатом. Органічний шар промивають водним розчином бікарбонату натрію та сольовим розчином. Неочищений продукт очищують шляхом силікагелевої хроматографії (елюент від 8:1 до 3:1 гексани/етилацетат), що приводить до одержання заголовної сполуки. MS m/z 313,9 (M + 1). Проміжна сполука. 3-Фтор-4-йодпіридин-2-амін 40 45 Розчин 2-аміно-3-фторпіридину (1,0 г, 8,9 ммоль) у безводному ТГФ (40 мл) обробляють краплинним способом при -78 °C н-бутиллітієм (1,6 M у гексанах, 13,9 мл, 22,3 ммоль). Після додавання, цю суміш перемішують при -78 °C впродовж 1 години, потім додають розчин йоду (10,2 г, 40,1 ммоль) у ТГФ (20 мл). Цю суміш екстрагують етилацетатом, та органічні екстракти промивають тіосульфатом натрію, бікарбонатом натрію та сольовим розчином. Органічну фазу сушать над сульфатом натрію та концентрують. Неочищений продукт очищують шляхом 25 UA 112285 C2 силікагелевої хроматографії (елюент від 8:1 до 2:1 гексани/етилацетат), що забезпечує одержання заголовної сполуки. MS m/z 238,9 (M + 1). Аналогічно одержують: 3-хлор-4-йодпіридин-2-амін. Проміжна сполука. 3-Бром-2,5,6-трифторанілін 5 10 15 20 До колби для мікрохвильової печі додають 1-бром-2,3,4,5-тетрафторбензол (1,0 г) та 28% водний розчин гідроксиду амонію (5 мл). Цю суміш нагрівають при мікрохвильовому опромінюванні при 150 °C впродовж 2 годин, потім цю суміш виливають у воду та екстрагують гексаном. Органічний шар відділяють, сушать за допомогою MgSO4, потім концентрують. Залишок очищують за допомогою силікагелевої флеш хроматографії (елюент 9:1 гексани/етилацетат), що забезпечує одержання заголовної сполуки у вигляді безбарвної рідини. 1 + H ЯМР (400 MГц, CDCl3) δ 6,75 (m, 1H), 3,95 (br s, 2H) ppm; MS m/z: 226, 228 (M+H) . Проміжна сполука. 2,4-Дибром-3,6-дихлоранілін Суміш 2,5-дихлораніліну (0,2 г), N-бромсукциніміду (0,48 г) та ТГФ (20 мл) перемішують при кімнатній температурі впродовж 2 годин. Розчинник видаляють, та залишок очищують за допомогою силікагелевої флеш хроматографії (елюент 8:2 гексани/етилацетат), що забезпечує + одержання заголовної сполуки. MS m/z: 318 (M+H) . Проміжна сполука. 1,3-Дибром-2,5-дихлорбензол 25 30 35 40 Перемішувану суміш 2,4-дибром-3,6-дихлораніліну (5,0 г), трет-бутил-нітриту (3,3 г) та EtOH (50 мл) нагрівають у запаяній колбі при 50 °C впродовж 2 годин. Цю суміш концентрують та залишок очищують за допомогою силікагелевої флеш хроматографії (елюент-гексани), що + забезпечує одержання заголовної сполуки. MS m/z: 303 (M+H) . Проміжна сполука. 3-Бром-2-хлор-5-фторанілін Стадія 1. 3-бром-2-хлор-N-(дифенілметилен)-5-фторанілін. Суміш 2,6-дибром-4-фтор-1хлорбензолу (865 мг, 3 ммоль), бензофенон-іміну (0,61 мл, 3,6 ммоль), Pd2(dba)3 (137 мг, 0,15 ммоль), трет-бутоксиду натрію (432 мг, 4,5 ммоль), (S)-BINAP (280 мг, 0,45 ммоль), та толуолу (30 мл) нагрівають при 80 °C впродовж 16 годин. Цю суміш екстрагують етилацетатом та об’єднану органічну фазу промивають сольовим розчином. Органічну фазу сушать над сульфатом натрію та концентрують. Неочищений продукт очищують за допомогою силікагелевої флеш хроматографії (елюент - від 40:1 до 20:1 гексани/етилацетат), що забезпечує одержання заголовної сполуки у вигляді порошку. MS m/z 388,9 (M + 1). 26 UA 112285 C2 5 Стадія 2. 3-Бром-2-хлор-5-фторанілін. Розчин 3-бром-2-хлор-N-(дифенілметилен)-5фтораніліну (1,16 г) у ТГФ (20 мл) обробляють за допомогою 2N соляної кислоти (1,5 мл, 1 еквів.) та цю суміш перемішують при кімнатній температурі впродовж 2 годин. Цю суміш екстрагують етилацетатом та об’єднану органічну фазу промивають сольовим розчином. Органічну фазу сушать над сульфатом натрію та концентрують. Неочищений залишок хроматографують на силікагелі (елюент від 40:1 до 15:1 гексани/етилацетат), що забезпечує одержання заголовної сполуки, забрудненої бензофеноном. MS m/z 223,9 (M + 1). Аналогічно одержують: 3-бром-2,5-дихлоранілін; 3-бром-2-хлор-5-метиланілін; та 3-бром2,5-дифторанілін. 10 Проміжна сполука. 3-Бром-5-хлор-2-фторбензойна кислота 15 20 25 30 Розчин 2-бром-4-хлор-1-фторбензолу (4,31 г, 20 ммоль) додають краплинним способом до 78 °C розчину LDA у ТГФ (отриманого з діізопропіламіну (3,38 мл, 24 ммоль) та n-BuLi (1,6 M, 13,1 мл, 21 ммоль)). Цю суміш перемішують при -78 °C впродовж 1 години, та потім повільно (~ 30-60 хв) переносять через канюлі у перемішувану при -78 °C суміш сухого льоду та ТГФ (40 мл). Цю суміш перемішують при -78 °C впродовж 1 години, та потім залишають нагрітися до кімнатної температури (виділення газу). Цю суміш концентрують, та потім обробляють за допомогою 50 мл 1 н. розчину гідроксиду натрію. Цю суміш екстрагують етилацетатом (відкидають). Водний шар підкислюють за допомогою 1 н. соляної кислоти, та потім екстрагують хлороформом (3×400 мл). Хлороформовий екстракт сушать над сульфатом натрію, фільтрують та концентрують, що забезпечує одержання неочищеної заголовної сполуки. Цей продукт забруднений невеликою кількістю ізомерного продукту - 2-бром-6-хлор-3-фторбензойної 1 кислоти. H ЯМР для заголовної сполуки - 3-Бром-5-хлор-2-фторбензойна кислота: (400 MГц, CDCl3) δ 7,93 (dd, 1H, J = 2,8, 5,6 Гц), 7,79 (dd, 1H, J = 2,8, 5,6 Гц) ppm. Аналогічно одержують: 3-бром-2,6-дифторбензойну кислоту; та 3-бром-2-фтор-5метилбензойну кислоту. Проміжна сполука. Трет-бутил 3-бром-5-хлор-2-фторфенілкарбамат 35 40 45 Розчин неочищеної Проміжної сполуки 3-бром-5-хлор-2-фторбензойної кислоти (2,03 г, 8 ммоль), дифенілфосфорил-азиду (2,07 мл, 9,6 ммоль, 1,2 екв.), та DIPEA (1,67 мл, 9,6 ммоль, 1,2 екв.) у 1:1 суміші трет-бутанол/толуол (25 мл) нагрівають при 110 °C впродовж 36 годин. Цю суміш концентрують, потім розподіляють між етилацетатом та водою. Органічний шар промивають сольовим розчином, та потім сушать над сульфатом натрію, фільтрують та концентрують. Неочищений продукт очищують шляхом силікагелевої хроматографії (елюент – від 30:1 до 10:1 гексани/етилацетат), що забезпечує одержання заголовної сполуки. MS m/z: + t 267,8 (M+H) . (M- Bu). Аналогічно одержують: трет-бутил 3-бром-2,6-дифторфенілкарбамат; та трет-бутил 3-бром2-фтор-5-метилфенілкарбамат. Проміжна сполука. 3-Бром-5-хлор-2-фторанілін 27 UA 112285 C2 Cl Br NH 2 F 5 10 Розчин трет-бутил 3-бром-5-хлор-2-фторфенілкарбамату (900 мг, 2,78 ммоль) у ДХМ/ТФОК (1:1, 20 мл) перемішують при кімнатній температурі впродовж 1 год. Реакційну суміш концентрують, потім залишок переносять у етилацетат та промивають водним розчином бікарбонату натрію та сольовим розчином. Органічний шар сушать над сульфатом натрію, фільтрують та концентрують, що забезпечує одержання неочищеної заголовної сполуки (736 мг). MS m/z 223,9 (M+1). Проміжна сполука. 5-бром-3-метокси-2-метиланілін: O Br H 2N 15 20 Гетерогенну реакційну суміш 4-бром-2-метокси-6-нітротолуолу (500 мг, 2,032 ммоль), оцтової кислоти (20 мл), та заліза (1135 мг, 20,32 ммоль) перемішують при кімнатній температурі впродовж 24 годин. Додають етилацетат, потім цю суміш фільтрують через целіт та фільтрат концентрують. Залишок розподіляють між етилацетатом та насиченим водним розчином бікарбонату натрію. Водний шар екстрагують додатковою кількістю етилацетату. Об’єднані органічні фази промивають водою та сольовим розчином, потім сушать над сульфатом натрію, фільтрують та концентрують, що забезпечує одержання заголовної сполуки. + MS m/z: 218,0 (M+H) . Проміжна сполука. Трет-бутил 5-хлор-2-фтор-3-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2іл)фенілкарбамат: 25 30 35 40 Суміш Проміжної сполуки трет-бутил 3-бром-5-хлор-2-фторфенілкарбамату (1,45 г, 4,46 ммоль), біс(пінаколято)дифору (1,7 г, 6,69 ммоль), ацетату калію (1,53 г, 15,6 ммоль), PdCl2(dppf)-CH2Cl2 (163 мг, 0,22ммоль), та діоксану (100 мл) нагрівають у запаяній колбі при 100 °C впродовж 16 годин. Неочищену реакційну суміш переносять у етилацетат та промивають водним розчином бікарбонату натрію та сольовим розчином. Органічний шар сушать над сульфатом натрію, фільтрують та концентрують. Неочищену сполуку розбавляють гарячим гексаном (600 мл), нагрівають до 65 °C впродовж 30 хвилин, потім охолоджують до кімнатної температури. Коричневу суміш фільтрують через Целіт та осад на фільтрі промивають гексанами. Об’єднані фільтрати концентрують, що забезпечує одержання неочищеної заголовної сполуки у вигляді жовтого масла. MS m/z 233 (M-пінакол-tBu). Аналогічно одержують: 5-хлор-2-фтор-3-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)анілін; трет-бутил 2,6-дифтор-3-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)фенілкарбамат; N-(2,4дифтор-3-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)феніл)пропан-1-сульфонамід; 2-(2-фтор3-нітрофеніл)-4,4,5,5-тетраметил-1,3,2-діоксаборолан; 2,5-дифтор-3-(4,4,5,5-тетраметил-1,3,2діоксаборолан-2-іл)анілін; 2-хлор-5-фтор-3-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)анілін; 2,5-дихлор-3-(4,4,5,5-тетраметил-1,3,2-діоксаборолан-2-іл)анілін; 2-хлор-5-метил-3-(4,4,5,5тетраметил-1,3,2-діоксаборолан-2-іл)анілін; трет-бутил 2-фтор-5-метил-3-(4,4,5,5-тетраметил 28
ДивитисяДодаткова інформація
Назва патенту англійськоюCompounds and compositions as protein kinase inhibitors
Автори англійськоюHuang, Shenlin, Jin, Xianming, Liu, Zuosheng, Poon, Daniel, Tellew, John, Wan, Yongqin, Wang, Xing, Xie, Yongping
Автори російськоюХуанг Шенлин, Джин Ксианминг, Лиу Зуошенг, Пун Дениэл, Теллью Джон И., Ван Йонгцин, Ванг Ксинг, Ксие Йонгпинг
МПК / Мітки
МПК: A61K 31/506, C07D 403/04, A61P 35/00, C07D 401/14
Мітки: протеїнкінази, сполуки, композиція, інгібітори
Код посилання
<a href="https://ua.patents.su/66-112285-spoluki-ta-kompoziciya-yak-ingibitori-protenkinazi.html" target="_blank" rel="follow" title="База патентів України">Сполуки та композиція як інгібітори протеїнкінази</a>
Попередній патент: Похідні 5-фторпіримідинону
Наступний патент: Модифікований інсектицидний білок cry1са та спосіб боротьби з лускокрилими комахами з його використанням
Випадковий патент: Стенд для досліджень режимів роботи висівних апаратів