Спіроциклічні піперидини як антагоністи mch1 та їх застосування
Номер патенту: 77814
Опубліковано: 15.01.2007
Автори: Ветзель Джон, Андерсен Кім, Чен Чіен-Ан, Джианг Ю, Марзабаді Мохамед, Делеон Джон, Лу Кай
Формула / Реферат
1. Сполуки, що мають структуру:
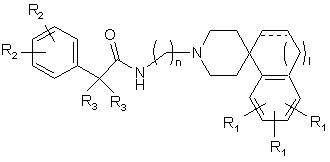 ,
,
де ------- являє собою СН2, О, -СО-, -СО2-, -СН2-СН2- або -СНСН-;
де t являє собою 0 або 1, та де циклічне кільце, що містить t, складається з 5 або 6 членів;
де n являє собою ціле число від 1 до 6 включно;
де кожний R1 та R2 являє собою незалежно -Н, -F, -Сl, -Вr, -І; С1-C7 алкіл, монофторалкіл або поліфторалкіл з прямим або розгалуженим ланцюгом, арил або гетероарил;
де кожний R3 являє собою незалежно -Н; С1-С6 алкіл з прямим або розгалуженим ланцюгом; арил або гетероарил, де арил або гетероарил необов'язково заміщений одним або більше -F, -Сl, -Br, -I, -R2, С1-C7 алкілом з прямим або розгалуженим ланцюгом, арилом, фенокси або гетероарилом; та
де дві складові R3, узяті разом, можуть утворювати С3-С6 циклоалкіл;
або їх фармацевтичнo прийнятні солі.
2. Сполука за п. 1, яка має структуру:
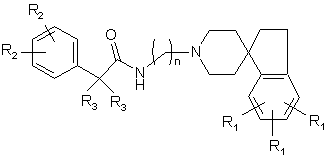 ,
,
де n, R1, R2 та R3 є такими, як визначено у п. 1.
3. Сполука за п. 2, яка має структуру:
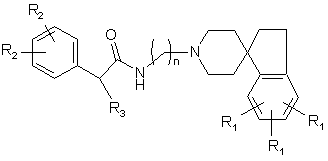 ,
,
де R3 являє собою С1-С6 алкіл з прямим або розгалуженим ланцюгом або арил, де арил необов'язково заміщений одним або більше -F, -Сl, -Br, -I, -R2, С1-С7 алкілом з прямим або розгалуженим ланцюгом, арилом, фенокси або гетероарилом; та
де n, R1 та R2 є такими, як визначено у п. 1.
4. Сполука за п. 3, яка має структуру:
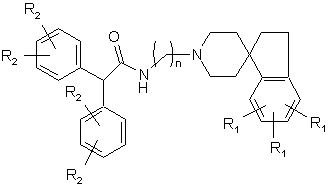 ,
,
де n, R1 та R2 є такими, як визначено у п. 1.
5. Сполука за п. 4, яка має структуру:
 ,
,
де кожний R1 та R2 являє собою незалежно -Н, -F, -Сl, -Вr, -І; С1-С7 алкіл з прямим або розгалуженим ланцюгом, арил або гетероарил; та
де n є таким, як визначено у п. 1.
6. Сполука за п. 5, яка має структуру:
 ,
,
де R1 та R2 є такими, як визначено у п. 1.
7. Сполука за п. 6, яка має структуру
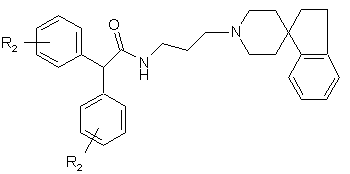 ,
,
де кожний R2 є таким, як визначено у п. 1.
8. Сполука за п. 7, яка має структуру:
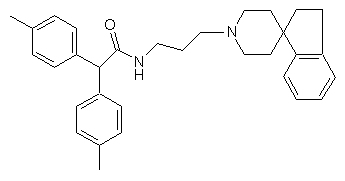 .
.
9. Сполука за п. 7, яка має структуру:
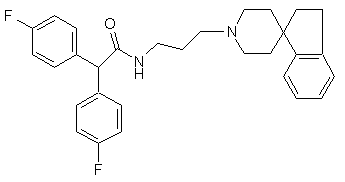 .
.
10. Сполука за п. 7, яка має структуру:
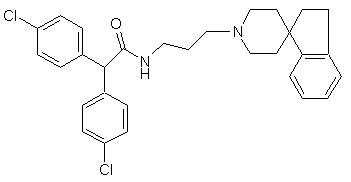 .
.
11. Сполука за п. 2, яка має структуру:
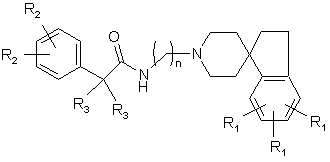 ,
,
де кожний R3 являє собою незалежно Н або С1-С6 алкіл з прямим або розгалуженим ланцюгом; та
де n, R1 та R2 є такими, як визначено у п. 1.
12. Сполука за п. 11, яка має структуру:
 ,
,
де кожний R3 являє собою С1-С6 алкіл з прямим або розгалуженим ланцюгом; та
де R1 та R2 є такими, як визначено у п. 1.
13. Сполука за п. 12, яка має структуру:
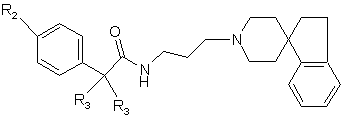 ,
,
де кожний R1 являє собою F, Сl, Вr або С1-С3 алкіл;
де кожний R3 являє собою незалежно Н або С1-С7 алкіл з прямим або розгалуженим ланцюгом; та
де R2 є таким, як визначено у п. 1.
14. Сполука за п. 13, яка має структуру:
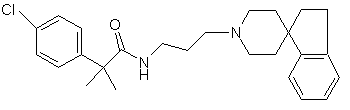 .
.
15. Сполука за п. 2, яка має структуру:
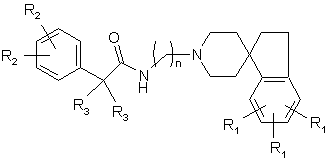 ,
,
де дві складові R3, узяті разом, утворюють С3-С6 циклоалкіл; та
де n, R1 та R2 є такими, як визначено у п. 1.
16. Сполука за п. 15, яка має структуру:
 ,
,
де дві складові R3, узяті разом, утворюють С4-С6 циклоалкіл;
де кожний R1 та R2 являє собою незалежно -Н, -F, -Сl, -Вr, -І; або С1-С7 алкіл з прямим або розгалуженим ланцюгом; та
де n є таким, як визначено у п. 1.
17. Сполука за п. 16, яка має структуру:
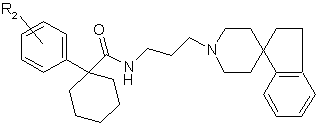 ,
,
де R2 являє собою -Н, -F, -Сl, -Вr, -І.
18. Сполука за п. 17, яка має структуру:
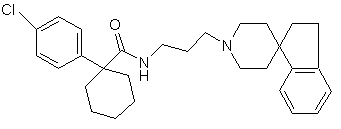 .
.
19. Сполука за п. 1, яка має структуру:
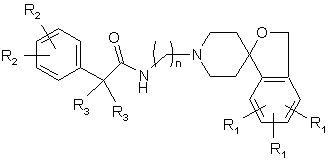 ,
,
де n, R1, R2 та R3 є такими, як визначено у п. 1.
20. Сполука за п. 19, яка має структуру:
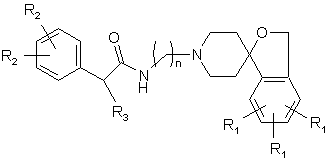 ,
,
де R3 являє собою С1-С6 алкіл з прямим або розгалуженим ланцюгом або арил, де арил необов'язково заміщений одним або більше -F, -Сl, -Br, -I, -R2, С1-С7 алкілом з прямим або розгалуженим ланцюгом, арилом, фенокси або гетероарилом; та
де n, R1 та R2 є такими, як визначено у п. 1.
21. Сполука за п. 20, яка має структуру:
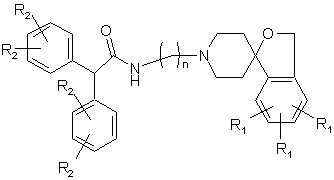 ,
,
де n, R1 та R2 є такими, як визначено у п. 1.
22. Сполука за п. 21, яка має структуру:
 ,
,
де n, R1 та R2 є такими, як визначено у п. 1.
23. Сполука за п. 22, яка має структуру:
 ,
,
де кожний R1 та R2 являють собою незалежно -Н, -F, -Сl, -Br, -І; С1-С7 алкіл з прямим або розгалуженим ланцюгом.
24. Сполука за п. 23, яка має структуру:
 ,
,
де кожний R1 являє собою незалежно -F, -Сl, -Вr, -І або С1-C7 алкіл.
25. Сполука за п. 24, яка має структуру:
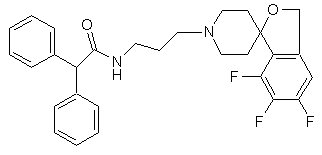 .
.
26. Сполука за п. 23, яка має структуру:
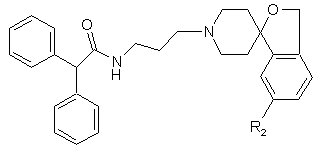 ,
,
де кожний R1 являє собою F, Сl, Вr, І або С1-С7 алкіл.
27. Сполука за п. 26, яка має структуру:
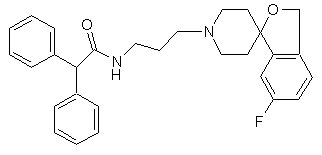 .
.
28. Сполука за п. 26, яка має структуру:
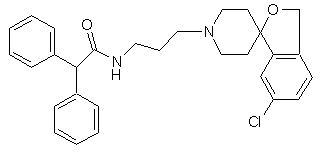 .
.
29. Сполуки, що мають структуру:
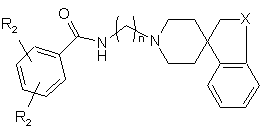 ,
,
де кожний R2 являє собою незалежно Н, F, Сl, Вr, CN або С1-С7 алкіл з прямим або розгалуженим ланцюгом;
де Х являє собою СН2 або О; та
де n являє собою ціле число від 1 до 6 включно.
30. Сполука за п. 29, яка має структуру:
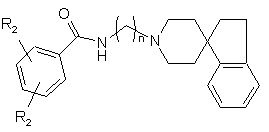 ,
,
де кожний R2 являє собою незалежно Н, F, Сl або Вr; та
де n являє собою ціле число від 1 до 6 включно.
31. Сполука за п. 30, яка має структуру:
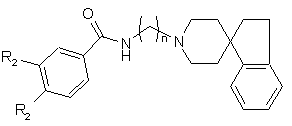 ,
,
де кожний R2 являє собою незалежно Н, F, Сl або Вr; та
де n являє собою ціле число від 3 до 6 включно.
32. Сполука за п. 31, яка має структуру:
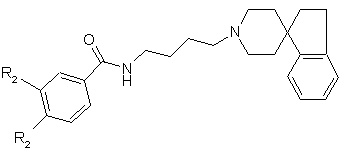 ,
,
де кожний R2 являє собою незалежно F, Сl або Вr.
33. Сполука за п. 31, яка має структуру:
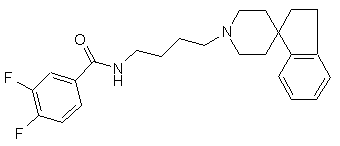 .
.
34. Фармацевтична композиція, яка містить терапевтично ефективну кількість сполуки за п. 1 та фармацевтично прийнятний носій.
35. Фармацевтична композиція, виготовлена шляхом змішування сполуки за п. 1 та фармацевтично прийнятного носія.
36. Спосіб виготовлення фармацевтичної композиції, який включає змішування сполуки за п.1 з фармацевтично прийнятним носієм.
37. Спосіб лікування суб'єкта, що страждає на розлад, опосередкований рецептором МСН1, який включає введення суб'єктові терапевтично ефективної кількості сполуки за п. 1.
38. Спосіб за п. 37, де терапевтично ефективна кількість становить від приблизно 0,03 до приблизно 300 мг.
39. Спосіб за п. 37, де розлад являє собою депресію.
40. Спосіб за п. 37, де розлад являє собою тривожний стан.
41. Спосіб за п. 37, де розлад являє собою ожиріння.
42. Спосіб за п. 37, де розлад являє собою нетримання сечі.
43. Спосіб лікування суб'єкта, що страждає на депресію, тривожний стан, нетримання сечі або ожиріння, який включає введення суб'єктові терапевтично ефективної кількості сполуки за п. 1.
44. Спосіб за п. 43, де терапевтично ефективна кількість становить від приблизно 0,03 до приблизно 300 мг.
45. Спосіб за п. 43, де суб'єкт страждає на депресію.
46. Спосіб за п. 43, де суб'єкт страждає на тривожний стан.
47. Спосіб за п. 43, де суб'єкт страждає на ожиріння.
48. Спосіб за п. 43, де суб'єкт страждає на нетримання сечі.
Текст
1. Сполуки, що мають структур у: 2 3 77814 4 -Сl, -Вr, -І; С1-С7 алкіл з прямим або розгалуженим де кожний R1 являє собою F, Сl, Вr або С 1-С3 алланцюгом, арил або гетероарил; та кіл; де n є таким, як визначено у п.1. де кожний R3 являє собою незалежно Н або С1-С7 6. Сполука за п.5, яка має структур у: алкіл з прямим або розгалуженим ланцюгом; та де R2 є таким, як визначено у п.1. O N R 14. Сполука за п.13, яка має структуру: N 2 Cl H R1 O R1 N R1 N H R , де R1 та R2 є такими, як визначено у п.1. 7. Сполука за п.6, яка має структур у 2 O R2 O R2 N R2 . 15. Сполука за п.2, яка має структур у: N H N H R3 N n R3 R1 R1 R1 , де кожний R2 є таким, як визначено у п.1. 8. Сполука за п.7, яка має структур у: R2 O , де дві складові R3, узяті разом, утворюють С3-С6 циклоалкіл; та де n, R1 та R2 є такими, як визначено у п.1. 16. Сполука за п.15, яка має структуру: N R2 N H O R2 N H R3 . 9. Сполука за п.7, яка має структур у: F O N N H F . 10. Сполука за п.7, яка має структур у: Cl n N R3 R1 R1 R1 , де дві складові R3, узяті разом, утворюють С4-С6 циклоалкіл; де кожний R1 та R2 являє собою незалежно -Н, -F, -Сl, -Вr, -І; або С 1-С7 алкіл з прямим або розгалуженим ланцюгом; та де n є таким, як визначено у п.1. 17. Сполука за п.16, яка має структуру: R2 O O N N N H N H Cl . 11. Сполука за п.2, яка має структур у: , де R2 являє собою -Н, -F, -Сl, -Вr, -І. 18. Сполука за п.17, яка має структуру: Cl O R2 N N H O R2 N H R3 n N R3 . 19. Сполука за п.1, яка має структур у: R1 R1 R2 R1 , де кожний R3 являє собою незалежно Н або С1-С6 алкіл з прямим або розгалуженим ланцюгом; та де n, R1 та R2 є такими, як визначено у п.1. 12. Сполука за п.11, яка має структуру: R2 O N R2 R3 , де кожний R3 являє собою С 1-С6 алкіл з прямим або розгалуженим ланцюгом; та де R1 та R2 є такими, як визначено у п.1. 13. Сполука за п.12, яка має структуру: R2 N N H R3 R3 R1 R1 , де n, R1, R2 та R3 є такими, як визначено у п.1. 20. Сполука за п.19, яка має структуру: O O R1 R1 R1 R3 N R2 R3 O N H n R1 N H R3 O O R2 , R2 N H R3 n N R1 R1 R1 , де R3 являє собою С1-С6 алкіл з прямим або розгалуженим ланцюгом або арил, де арил необов'язково заміщений одним або більше -F, -Сl, -Br, -I, R2, С1-С7 алкілом з прямим або розгалуженим ланцюгом, арилом, фенокси або гетероарилом; та 5 де n, R1 та R2 є такими, як визначено у п.1. 21. Сполука за п.20, яка має структуру: 77814 6 29. Сполуки, що мають структур у: R2 O R2 X O N R2 R1 R1 R1 , де n, R1 та R2 є такими, як визначено у п.1. 22. Сполука за п.21, яка має структуру: R2 O O R2 n N H N n N H R2 O R2 n N N H , де кожний R2 являє собою незалежно Н, F, Сl, Вr, CN або С1-С7 алкіл з прямим або розгалуженим ланцюгом; де Х являє собою СН 2 або О; та де n являє собою ціле число від 1 до 6 включно. 30. Сполука за п.29, яка має структуру: O R2 n N H R1 R1 N R1 R2 , де n, R1 та R2 є такими, як визначено у п.1. 23. Сполука за п.22, яка має структуру: O O N R2 R , де кожний R2 являє собою незалежно Н, F, Сl або Вr; та де n являє собою ціле число від 1 до 6 включно. 31. Сполука за п.30, яка має структуру: 2 O N H R1 R2 , де кожний R1 та R2 являють собою незалежно -Н, F, -Сl, -Br, -І; С1-С7 алкіл з прямим або розгалуженим ланцюгом. 24. Сполука за п.23, яка має структуру: N R2 , де кожний R2 являє собою незалежно Н, F, Сl або Вr; та де n являє собою ціле число від 3 до 6 включно. 32. Сполука за п.31, яка має структуру: O N O N N H n R1 R1 O N H R2 N H R2 R1 R2 R1 R1 , де кожний R1 являє собою незалежно -F, -Сl, -Вr, -І або С1-C7 алкіл. 25. Сполука за п.24, яка має структуру: O O F F F . 26. Сполука за п.23, яка має структуру: O O N N H R2 , де кожний R1 являє собою F, Сl, Вr, І або С1-С7 алкіл. 27. Сполука за п.26, яка має структуру: O O N N H F . 28. Сполука за п.26, яка має структуру: O O N N H Cl . N O F N N H , де кожний R2 являє собою незалежно F, Сl або Вr. 33. Сполука за п.31, яка має структуру: N H F . 34. Фармацевтична композиція, яка містить терапевтично ефективну кількість сполуки за п.1 та фармацевтично прийнятний носій. 35. Фармацевтична композиція, виготовлена шляхом змішування сполуки за п.1 та фармацевтично прийнятного носія. 36. Спосіб виготовлення фармацевтичної композиції, який включає змішування сполуки за п.1 з фармацевтично прийнятним носієм. 37. Спосіб лікування суб'єкта, що страждає на розлад, опосередкований рецептором МСН1, який включає введення суб'єктові терапевтично ефективної кількості сполуки за п.1. 38. Спосіб за п.37, де терапевтично ефективна кількість становить від приблизно 0,03 до приблизно 300 мг. 39. Спосіб за п.37, де розлад являє собою депресію. 40. Спосіб за п.37, де розлад являє собою тривожний стан. 41. Спосіб за п.37, де розлад являє собою ожиріння. 42. Спосіб за п.37, де розлад являє собою нетримання сечі. 7 77814 8 43. Спосіб лікування суб'єкта, що страждає на депресію. пресію, тривожний стан, нетримання сечі або ожи46. Спосіб за п.43, де суб'єкт страждає на тривожріння, який включає введення суб'єктові терапевний стан. тично ефективної кількості сполуки за п.1. 47. Спосіб за п.43, де суб'єкт страждає на ожи44. Спосіб за п.43, де терапевтично ефективна ріння. кількість становить від приблизно 0,03 до прибли48. Спосіб за п.43, де суб'єкт страждає на нетризно 300мг. мання сечі. 45. Спосіб за п.43, де суб'єкт страждає на де Представлений винахід стосується нових сполук, способів їх отримання, фармацевтичних композицій, що їх містять, та їх застосування у терапії. Хемокіни грають важливу роль в імунних та запальних реакціях у різноманітних хворобах та розладах, залучаючи астму та алергічні хвороби, а також аутоімунні патології, як-то ревматоїдний артрит та атеросклероз. Ці малі секретовані молекули є збільшуваною надродиною білків розміром 8-14кДа, охарактеризованою збереженою чотирьох-цистеїновою функціональною послідовністю. Надродину хемокінів можна поділити на дві головні групи, що виявляють характеристичні структурні функціональні послідовності, родини Cys-X-Cys (C-X-C) та C ys-Cys (C-C). Це виявлено на базі одиничних амінокислотних вставок між NHпроксимальною парою цистеїнових залишків та подібності послідовностей. Хемокіни С-Х-С залучають кілька потужних хемоатрактантів та активаторів нейтрофілів, як-то інтерлейкін-8 (IL-8) та нейтрофіл-активувальний пептид 2 (NAP-2). Хемокіни С-С залучають потужні хемоатрактанти моноцитів та лімфоцитів, але не нейтрофілів, як-то хемотактичні білки 1-3 моноцитів людини (МСР-1, МСР-2 та МСР-3), RANTES (регульовані на активування, нормальне Т-експресування та секретування), еотаксин та запальні білки макрофагів 1a та 1b (ΜΙΡ-1a та ΜΙΡ-1b). Дослідження продемонстрували, що дія хемокінів опосередкована підродинами сполучених з білком G рецепторів, серед яких є рецептори CCR1, CCR2, CCR2A, CCR2B, CCR3, CCR4, CCR5, CCR6, CCR7, CCR8, CCR9, CCR10, CXCR1, CXCR2, CXCR3 та C XCR4. Ці рецептори представляють гарні цілі для розробки ліків, оскільки засоби, які модулюють ці рецептори, могли б бути корисними у лікуванні розладів та хвороб, як-то вищезгаданих. Згідно з представленим винаходом запропоновано сполуку формули (I) де m дорівнює 0, 1, 2, 3 або 4; кожне R1 незалежно представляє галоген, ціано, гідроксил, С1-С6алкіл, С1-С6галогеналкіл, С1С6алкокси або сульфонамідо (-SO2NH2); X представляє зв’язок, -СН2-, -О- чи -С(О)-, a Y представляє зв’язок, -СН2-, -О- чи -С(О)-, або X та Υ разом представляють групу -СН= С(СН 3)- або С(СН3)= СН-, a Z представляє зв’язок, -О-, -ΝΗ або -СН2-, за умови, що тільки одне з Χ, Υ та Ζ може представляти зв’язок одночасно, та за умови, що X та Υ не представляють одночасно -О-або -С(О)-; n дорівнює 0, 1 або 2; кожне R2 незалежно представляє галоген або С1-С6алкіл; q дорівнює 0 або 1 ; R3 представляє -NHC(O)R 10, -C(O)NR11R12 або -COOR 12a ; R4, R5, R6, R7 та R8, кожне незалежно, представляють атом гідрогену або С1-С6алкіл; t дорівнює 0, 1 або 2; кожне R9 незалежно представляє галоген, ціано, гідроксил, карбоксил, С1-С6алкокси, С1С6алкоксикарбоніл, С1-С6галогеналкіл, або С1С6алкіл, як варіант, заміщений принаймні одним замісником, вибраним з карбоксилу та С 1С6алкоксикарбонілу; R10 представляє С 1-С6алкіл, С2-С6алкеніл, С3С6циклоалкіл, адамантил, С3-С6ци-клоалкеніл, феніл або насичену або ненасичену 5-10-членну гетероциклічну кільцеву систему, що містить принаймні один кільцевий гетероатом, вибраний з нітрогену, оксигену та сульфур у, кожне з них може бути, як варіант, заміщене одним або більше замісниками, що незалежно вибрано з групи: нітро, гідроксил, оксо, галоген, карбоксил, С1-С6алкіл, С1С6алкокси, С1-С6алкілтіо, С1-С6алкілкарбоніл, С1С6алкоксикарбоніл, феніл та -NНС(О)-R13, або R10 представляє -NR14R15aбo -O-R16; R11 та R 12, кожне незалежно, представляють (і) атом гідрогену, (іі) 3-6-членне насичене або ненасичене кільце, що містить, як варіант, принаймні один кільцевий гетероатом, вибраний з нітрогену, оксигену та сульфур у та, як варіант, крім того містить місткову груп у, кільце, як варіант, заміщене принаймні одним замісником, вибраним з групи: галоген, гідроксил, С1-С6алкіл, С1-С6гідроксіалкіл та С 1С6галогеналкіл, (ііі) С1-С6алкіл, як варіант, заміщений принаймні одним замісником, вибраним з групи: галоген, аміно (-NН2), гідроксил, С1-С6галогеналкіл, карбоксил, С1-С6алкокси, С1-С6алкоксикарбоніл, С1С6алкілкарбоніламіно та 3-6-членне насичене або ненасичене кільце, що містить, як варіант, принаймні один кільцевий гетероатом, вибраний з нітрогену, оксигену та сульфур у та, як варіант, крім того містить місткову групу, кільце, як варіант, заміщене принаймні одним замісником, вибраним з групи: галоген, гідроксил, оксо (=О), С1-С6алкіл, С1-С6гідроксіалкіл та С1-С6галогеналкіл, або (iv) С1-С6алкілсульфоніл, або R11 та R12 разом з атомом нітрогену, до якого 9 77814 10 вони приєднані, утворюють 4-7-членне насичене лічні або ароматичні властивості. гетероциклічне кільце, що, як варіант, крім того Подібно, у визначенні R11 або R12 3-6-членне містить кільцевий атом нітрогену, оксигену або насичене або ненасичене кільце, що містить, як сульфур у, та яке є, як варіант, конденсованим з варіант, принаймні один кільцевий гетероатом бензольним кільцем з утворенням 8-11-членної може мати аліциклічні або ароматичні властивості. кільцевої системи, гетероциклічне кільце або кільНенасичена кільцева система буде частково або цеву систему, як варіант, заміщено принаймні одповністю ненасиченою. ним замісником, вибраним з групи: галоген, гідроУ втіленні винаходу, m дорівнює 0 або 1. ксил, амідо(-CONH2), С1-С6алкіл, С1Кожне R1 незалежно представляє галоген (наС6гідроксіалкіл, С1-С6алкокси, С1приклад, хлор, флуор, бром або йод), ціано, гідроС6алкоксикарбоніл, С1-С6галогеналкіл, С1ксил, С1-С6, переважно С1-С4алкіл (наприклад, С6алкіламіно, діС1-С6алкіламіно, С1метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, С6алкілкарбоніл, С1-С6алкілкарбоніламіно, С1трет-бутил, н-пентил або н-гексил), С1-С6, переваС6алкіламінокарбоніл, ді- С1-С6алкіламінокарбоніл, жно С1-С4галогеналкіл (наприклад, трифлуормефеніл, галогенфеніл, фенілкарбоніл, фенілкарботил), С1-С6; переважно С1-С4алкокси (наприклад, нілокси та гідроксидифенілметил; метокси, етокси, н-пропокси або н-бутокси) або R12a представляє атом гідрогену або С 1сульфонамідо. С6алкіл; У втіленні винаходу, кожне R1 незалежно 13 R представляє С 1-С6алкіл, аміно (-NH2) або представляє галоген, С1-С6, переважно С1-С4алкіл феніл; або С1-С6, переважно С1-С4галогеналкіл. R14 та R15, кожне незалежно, представляють В іншому втіленні кожне R1 незалежно предатом гідрогену, або С1-С6алкіл, С1ставляє флуор, хлор, метил або трифлуорметил. С6алкілсульфоніл, феніл або насичену або ненаКомбінації X та Y, що представляють особлисичену 5-10-членну гетероциклічну кільцеву сисвий інтерес, залучають будь-що одне або більше з тему, що містить принаймні один кільцевий гетенаступного: роатом, вибраний з нітрогену, оксигену та X Y сульфур у, кожна група, як варіант, заміщена, як зв ’язок О визначено вище для R10, або 14 15 О зв ’язок R та R разом з атомом нітрогену, до якого СН 2 зв ’язок вони приєднані, утворюють 4-7-членне насичене зв ’язок СН 2 гетероциклічне кільце, що, як варіант, крім того СН 2 О О СН 2 містить кільцевий атом нітрогену, оксигену або С(О) 0 сульфур у, ге тероциклічне кільце, як варіант, заміО С(О) щене принаймні одним гідроксилом; та СН 2 СН 2 R16 представляє атом гідрогену, або С1-СН=С(СН 3)С6алкіл, феніл або насичену або ненасичену 5-10членну гетероциклічну кільцеву систему, що місУ втіленні винаходу, X та Υ мають значення, тить принаймні один кільцевий гетероатом, вибрапоказані нижче: ний з нітрогену, оксигену та сульфур у, кожна група, як варіант, заміщена, як визначено вище для X Υ зв ’язок 0 R10; О зв ’язок або її фармацевтично прийнятну сіль або соСН 2 О льват. О СН 2 У контексті представленого опису, якщо не С(O) O О С(О) вказано інше, алкільний або алкенільний замісник СН 2 СН 2 або алкіл у заміснику можуть бути лінійними або -СН=С(СН 3)розгалуженими. Алкіли у ді-алкіламіно або діалкіламінокарбонільному заміснику можуть бути У втіленні винаходу Ζ представляє зв’язок, -Ооднаковими або різними. Галогеналкільний або або -СН2-. галогенфенільний замісник містять принаймні Комбінації Χ, Υ та Ζ, що представляють осободин атом галогену, наприклад, один, два, три або ливий інтерес, залучають будь-що одне або більчотири атоми галогену. Гідроксіалкільний замісник ше з наступного: може містити одну або більше гідроксигруп, але переважно містить одну або дві гідроксигрупи. X Υ Ζ У кільці, заміщеному R2, R2 може бути приєдзв ’язок 0 СН 2 наним до будь-якого придатного кільцевого атому О зв ’язок СН 2 СН 2 зв ’язок О карбону, залучаючи атом карбону з (CH2)q , коли зв ’язок СН 2 О R11 та R12 або R14 та R15 представляють 4-7СН 2 О зв ’язок членний насичений гетероцикл, слід розуміти, що С(О) О зв ’язок гетероцикл містить не більше двох кільцевих гетеО С(О) зв ’язок роатомів: кільцевий атом нітрогену, до якого приСН 2 СН 2 зв ’язок 11 12 14 15 О зв ’язок О єднано R та R або R та R , та як варіант, кізв ’язок 0 О льцевий атом нітрогену, оксигену або сульфуру. У СН 2 СН 2 О визначенні R10 (або R14’ R1S або R16), слід зауважиO СН 2 СН 2 ти, що насичена або ненасичена 5-10-членна ге-СН=С(СН 3)зв ’язок тероциклічна кільцева система може мати аліцик 11 77814 12 У втіленні винаходу, Χ, Υ та Ζ мають значення, варіант, заміщене принаймні одним замісником показані нижче: (наприклад, одним, двома або трьома замісниками) незалежно вибраним з карбгідроксилу та С 1X Υ Z C6, переважно С1-С4алкоксикарбоніл (наприклад, зв ’язок O СH 2 метоксикарбоніл, етоксикарбоніл, нO зв ’язок СH 2 пропоксикарбоніл або н-бутоксикарбоніл). СН 2 О зв ’язок У втіленні винаходу, кожне R9 незалежно О СН 2 зв ’язок С(О) 0 зв ’язок представляє галоген, ціано, гідроксил, карбоксил, O С(О) зв ’язок С1-С6, переважно С1-С4алкокси, С1-С6, переважно СН 2 СН 2 зв ’язок С1-С4алкоксикарбоніл, С1-С6, переважно С 1зв ’язок O O С4галогеналкіл або С1-С6, переважно С1-С4алкіл. O зв ’язок O В іншому втіленні винаходу кожне R9 незалеж-СН=С(СН 3)зв ’язок но представляє галоген, гідроксил, карбоксил, метил, метокси, метоксикарбоніл або трифлуормеВ іншому втіленні винаходу, Χ, Y та Ζ мають тил. значення, показані нижче: R переважно зв’язано з атомом карбону, розX Υ Ζ ташованим у пара-позиції відносно атому карбону, зв ’язок О СН 2 з яким зв’язано атом оксигену або R3, як позначеО зв ’язок СН 2 но зірочками у частковій структурі, показаній нижСН 2 зв ’язок О че: зв ’язок СН 2 О СН 2 О зв ’язок у ще одному втіленні винаходу, Χ, Υ та Ζ мають такі значення: X зв ’язок О СН 2 Υ О зв ’язок О Ζ СН 2 СН 2 зв ’язок Кожне R2 незалежно представляє галоген (наприклад, хлор, флуор, бром або йод) або С1-С6, переважно С1-С4алкіл (наприклад, метил, етил, нпропіл, ізопропіл, н-бутил, ізобутил, трет-бутил, нпентил або н-гексил). У втіленні винаходу, η дорівнює 1 та R2 представляє галоген, особливо флуор. У втіленні винаходу, R3 представляє NHC(O)R10. В іншому втіленні винаходу, R представляє C(O)NR11R12. R4, R5, R6, R7 та R8, кожне незалежно, представляють атом гідрогену або С 1-С6, переважно С1-С4алкіл (наприклад, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, трет-бутил, н-пентил або н-гексил). У втіленні винаходу, R4, R5, R6, R7 та R8, кожне незалежно, представляють атом гідрогену або метил. В іншому втіленні винаходу, R4, R 5, R6 та R7 , кожне, представляють атом гідрогену, a R8 представляє метил. У втіленні винаходу, R4, R5, R6, R7 та R8, кожне, представляють атом гідрогену. У втіленні винаходу, t дорівнює 0, 1 або 2. Кожне R9 незалежно представляє галоген (наприклад, хлор, флуор, бром або йод), ціано, гідроксил, карбоксил, С1-С6, переважно С1-С4алкокси (наприклад, метокси, етокси, н-пропокси або нбутокси), С1-С6, переважно С1-С4алкоксикарбоніл (наприклад, метоксикарбоніл, етоксикарбоніл, нпропоксикарбоніл або н-бутоксикарбоніл), С1-С6, переважно С1-С4галогеналкіл (наприклад, трифлуорметил), або С1-С6, переважно С1-С4алкіл (наприклад, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, трет-бутил, н-пентил або н-гексил), та, як R10 може представляти С 1-С6, переважно С1С4алкіл (наприклад, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, трет-бутил, н-пентил або нгексил), С2-С6, переважно С2-С4алкеніл, С1С6циклоалкіл (циклопропіл, циклобутил, циклопентил або циклогексил), адамантил, С3С6циклоалкеніл, феніл або насичену або ненасичену 5-10-членну гетероциклічну кільцеву систему, що містить принаймні один кільцевий гетероатом (наприклад, один, два, три або чотири кільцеві гетероатоми, незалежно), вибрані з нітрогену, оксигену та сульфур у, кожний з яких (тобто кожний з визначених гр уп та кільцевих систем) може бути, як варіант, заміщеним одним або більше (наприклад, один, два, три або чотири) замісники незалежно вибрано з нітро, гідроксил, оксо, галоген (наприклад, флуор, хлор, бром або йод), карбоксил, С1-С6, переважно С1-С4алкіл (наприклад, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, трет-бутил, н-пентил або н-гексил), С1-С6, переважно С1-С4алкокси (наприклад, метокси, етокси, нпропокси або н-бутокси), С1-С6, переважно С 1С4алкілтіо (наприклад, метилтіо або етилтіо), С1С6, переважно С1-С4алкілкарбоніл (наприклад, метилкарбоніл, етилкарбоніл, н-пропілкарбоніл, ізопропілкарбоніл, н-бутил карбоніл, н-пентил карбоніл або н-гексил карбоніл), С1-С6, переважно С1С4алкоксикарбоніл (наприклад, метоксикарбоніл або етоксикарбоніл), феніл та -NHC(O)-R13. Насичена або ненасичена 5-10-членна гетероциклічна кільцева система у R10 може бути моноциклічною або поліциклічною (наприклад, дициклічною), приклади залучають піролідиніл, піперидиніл, піразоліл, тіазолідиніл, тієніл, ізоксазоліл, тіадіазоліл, піроліл, фураніл, тіазоліл, індоліл, хінолініл, бензимідазоліл, триазоліл, тетразоліл, піридиніл та комбінації будь-яких двох або більше їх. У втіленні винаходу, R10 представляє С 1С6алкіл, С3-С6циклоалкіл, феніл або насичену або ненасичену 5-10-членну гетероциклічну кільцеву систему, що містить принаймні один кільцевий 13 77814 14 гетероатом (наприклад, один або два кільцеві геклад, дициклічною), приклади залучають піролідитероатоми, незалежно), вибрані з нітрогену, оксиніл, піперидиніл, піразоліл, тіазолідиніл, тієніл, гену та сульфур у, кожний з яких (тобто кожний з ізоксазоліл, тіадіазоліл, піроліл, фураніл, тіазоліл, визначених гр уп та кільцевих систем) може бути, індоліл, хінолініл, бензимідазоліл, триазоліл, тетяк варіант, заміщеним одним, двома, трьома або разоліл, піридиніл та комбінації будь-яких дво х або чотирма замісниками, незалежно вибраними з більше їх. групи: нітро, гідроксил, оксо, галоген, карбоксил, У втіленні винаходу, R14 та R15 , кожне незалеС1-С6, переважно С1-С4алкіл, С1-С6, переважно С1жно, представляють атом гідрогену або С 1-С6алкіл С4алкокси, С1-С6, переважно С 1-С4алкілтіо, С1-С6, чи С1-С6алкілсульфоніл, кожна група, як варіант, переважно С1-С4алкілкарбоніл, С1-С6, переважно заміщена, як визначено вище для R10, або R14 та 13 С1-С4алкоксикарбоніл, феніл та -NHC(O)-R . R15 разом з атомом нітрогену, до якого вони при10 В іншому втіленні винаходу, R представляє єднані, утворюють 5-6-членне насичене гетероциС1-С6алкіл, С3-С6циклоалкіл або феніл, кожний з клічне кільце, що, як варіант, крім того містить кіяких може бути, як варіант, заміщеним одним або льцевий атом нітрогену, оксигену або сульфур у, двома замісниками, незалежно вибраними з групи: гетероциклічне кільце, як варіант, заміщене пригалоген, С1-С6, переважно С1-С4алкіл та С1-С6, наймні одним гідроксилом. переважно С1-С4алкокси. У наступному втіленні R14 та R15, кожне незаУ ще одному втіленні винаходу, R10 представлежно, представляють атом гідрогену або С 1ляє С 1-С6алкіл, циклопентил або феніл. С6алкілсульфоніл, або R14 та R15 разом з атомом Альтернативно, R10 може представляти групу нітрогену, до якого вони приєднані, утворюють 5-6NR14R15 або -O-R 16. членне насичене гетероциклічне кільце, що, як R14 та R15, кожне незалежно, представляють варіант, заміщено принаймні одним гідроксилом. атом гідрогену, або С1-С6, переважно С1-С4алкіл У ще одному втіленні R14 та R15, кожне неза(наприклад, метил, етил, н-пропіл, ізопропіл, нлежно, представляють атом гідрогену або метилбутил, ізобутил, трет-бутил, н-пентил або нсульфоніл, або R14 та R15 разом з атомом нітрогегексил), С1-С6, переважно С 1-С4алкілсульфоніл ну, до якого вони приєднані, утворюють (наприклад, метилсульфо-ніл, етилсульфоніл, нпіролдинільне або піперидинільне кільце, що як пропілсульфоніл, ізопропілсульфоніл, нваріант, заміщено одним гідроксилом. бутилсульфоніл, ізобутилсульфоніл, третR16 представляє атом гідрогену, або С1-С6, пебутилсульфоніл, н-пентилсульфоніл або нреважно С1-С4алкіл (наприклад, метил, етил, нгексилсульфоніл), феніл або насичену або ненапропіл, ізопропіл, н-бутил, ізобутил, трет-бутил, нсичену 5-10-членну гетероциклічну кільцеву сиспентил або н-гексил), феніл або насичену або нетему, що містить принаймні один кільцевий гетенасичену 5-10-членну гетероциклічну кільцеву сироатом (наприклад, один, два, три або чотири стему, що містить принаймні один кільцевий гетекільцеві гетероатоми, незалежно), вибрані з нітророатом (наприклад, один, два, три або чотири гену, оксигену та сульфур у, кожну гр упу (кожну з кільцеві гетероатоми, незалежно), вибрані з нітровизначених гр уп, залучаючи кільцеві системи), як гену, оксигену та сульфур у, кожну гр упу (кожну з варіант, заміщено, як визначено вище для R 10 (що, визначених гр уп, залучаючи кільцеві системи), як як варіант, заміщено одним або більше (наприваріант, заміщено, як визначено вище для R 10 (що, клад, одним, двома, трьома або чотирма) заміснияк варіант, заміщено одним або більше (наприками, незалежно вибраними з групи: нітро, гідроклад, одним, двома, трьома або чотирма) замісниксил, оксо, галоген (наприклад, флуор, хлор, бром ками, незалежно вибраними з групи: нітро, гідроабо йод), карбоксил, С1-С6, переважно С1-С4алкіл ксил, оксо, галоген (наприклад, флуор, хлор, бром (наприклад, метил, етил, н-пропіл, ізопропіл, набо йод), карбоксил, С1-С6, переважно С1-С4алкіл бутил, ізобутил, трет-бутил, н-пентил або н(наприклад, метил, етил, н-пропіл, ізопропіл, нгексил), С1-С6, переважно С1-С4алкокси (наприбутил, ізобутил, трет-бутил, н-пентил чи н-гексил), клад, метокси, етокси, н-пропокси або н-бутокси), С1-С6, переважно С1-С4алкокси (наприклад, метокС1-С1-6, переважно С1-С4алкілтіо (наприклад, меси, етокси, н-пропокси або н-бутокси), С1-С6, перетилтіо або етилтіо), С1-С6, переважно С 1важно С1-С4алкілтіо (наприклад, метилтіо або етиС4алкілкарбоніл (наприклад, метилкарбоніл, етиллтіо), С1-С6, переважно С1-С4алкілкарбоніл карбоніл, н-пропіл карбоніл, ізопропілкарбоніл, н(наприклад, метилкарбоніл, етилкарбоніл, нбутил карбоніл, н-пентилкарбоніл або н-гексил пропілкарбоніл, ізопропілкарбоніл, нкарбоніл), С1-С6, переважно С1-С4алкоксикарбоніл бутилкарбоніл, н-пентилкарбоніл або н(наприклад, метоксикарбоніл або етоксикарбоніл), гексилкарбоніл), С1-С6, переважно С1феніл та -NHC(O)-R13), або R14 та R15 разом з атоС4алкоксикарбоніл (наприклад, метоксикарбоніл мом нітрогену, до якого вони приєднані, утворюабо етоксикарбоніл), феніл та -NHC(O)-R13). ють 4-7-членне насичене гетероциклічне кільце, У R16 насичена або ненасичена 5-10-членна що, як варіант, крім того містить кільцевий атом гетероциклічна кільцева система може бути мононітрогену, оксигену або сульфур у (наприклад, піциклічною чи поліциклічною (наприклад, дициклічролідиніл, піперидиніл, морфоліно, піперазиніл ною), приклади залучають піролдиніл, піперидиніл, або тіоморфолініл), гетероциклічне кільце, як варіпіразоліл, тіазолідиніл, тієніл, ізоксазоліл, тіадіаант, заміщене принаймні одним гідроксилом (назоліл, піроліл, фураніл, тіазоліл, індоліл, хінолініл, приклад, одним або двома гідроксилами). бензимідазоліл, триазоліл, тетразоліл, піриди-ніл У R14 та R15 насичена або ненасичена 5-10та комбінації будь-яких дво х або більше їх. членна гетероциклічна кільцева система може R11 та R 12, кожне незалежно, представляють бути моноциклічною або поліциклічною (напри(і) атом гідрогену, 15 77814 16 (іі) 3-6-членне насичене або ненасичене кіль(наприклад, дигідроізохінолініл або дигідроізоіндоце, що містить, як варіант, принаймні один кільцеліл), гетероциклічне кільце або кільцеву систему, вий гетероатом (наприклад, один, два, три або як варіант, заміщено принаймні одним замісником чотири кільцеві гетероатоми, незалежно), вибрані (наприклад, одним, двома, трьома або чотирма з нітрогену, оксигену та сульфур у та, як варіант, замісниками, незалежно), вибраними з групи: галокрім того містить місткову гр упу (приклади залучаген (наприклад, флуор, хлор, бром або йод), гідроють циклопропіл, циклобутил, циклопентил, циклоксил, амідо (-CONH2), C1-C6, переважно С 1-С4алкіл гексил, ди-цикло[2,2,1]гептил, феніл, піроліл, імі(наприклад, метил, етил, н-пропіл, ізопропіл, ндазоліл, піридиніл, піразиніл, піридазиніл, бутил, ізобутил, трет-бутил, н-пентил або нтетразоліл, піримідиніл, тієніл, фураніл, тетрагідгексил), С1-С6, переважно С1-С4гідроксіалкіл (нарофураніл та комбінації будь-яких двох або більше приклад, -СН2ОН, -СН2СН2ОН, -СН2СН2СН2ОН або їх), кільце, як варіант, заміщене принаймні одним -СН(ОН)СН3), С1-С6, переважно С1-С4алкокси (назамісником (наприклад, одним, двома або трьома приклад, метокси, етокси, н-пропокси або нзамісниками, незалежно), вибраними з групи: галобутокси), С1-С6, переважно С1-С4алкоксикарбоніл ген (наприклад, флуор, хлор, бром або йод), гідро(наприклад, метоксикарбоніл або етоксикарбоніл), ксил, С1-С6, переважно С1-С4алкіл (наприклад, С1-С6, переважно С1-С4галогеналкіл (наприклад, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, трифлуорметил), С1-С6, переважно С1трет-бутил, н-пентил, 1,1-диметилпропіл або нС4алкіламіно (наприклад, метиламіно або етилагексил), С1-С1, переважно С1-С4гідроксіалкіл (наміно), ді-С1-С6, переважно С1-С4алкіламіно (наприприклад, -СН2ОН, -СН2СН2ОН, -СН2СН2СН2ОН або клад, диметиламіно), С1-С6, переважно С1-СН(ОН)СН3) та С1-С6, переважно С 1С4алкілкарбоніл (наприклад, метилкарбоніл або С6галогеналкіл (наприклад, трифлуорметил), етилкарбоніл), С1-С6, переважно С1(ііі) С1-С6алкіл, як варіант, заміщений принайС4алкілкарбоніламіно (наприклад, метилкарбонімні одним замісником (наприклад, од-ним, двома, ламіно або етилкарбоніламіно), С1-С6, переважно трьома або чотирма замісниками), вибраними з С1-С4алкіламінокарбоніл (наприклад, метиламіногрупи: галоген (наприклад, флуор, хлор, бром або карбоніл або етиламінока-рбоніл), ді-С1-С6, перейод), аміно (-NH2), гідроксил, С1-С6, переважно С1важно С1-С4алкіламінокарбоніл (наприклад, димеС4галогеналкіл (наприклад, трифлуорметил), картиламінокарбоніл), феніл, галогенфеніл боксил, С1-С6, переважно С1-С4алкокси (напри(наприклад, флуор феніл або хлорфеніл), фенілкаклад, метокси, етокси, н-пропокси або н-бутокси), рбоніл, фенілкарбонілокси та гідроксидифенілмеС1-С6, переважно С1-С4алкоксикарбоніл (напритил. клад, метоксикарбоніл або етоксикарбоніл), С1-С6, У втіленні винаходу R11 та/або R12 представпереважно С1-С4алкілкарбоніламіно (наприклад, ляють 3-6-членне насичене або ненасичене кільметилкарбоніламіно або етилкарбоніламіно) та 3це, що містить, як варіант, принаймні один кільце6-членне насичене або ненасичене кільце, що місвий гетероатом (наприклад, один, два, три або тить, як варіант, принаймні один кільцевий гетерочотири кільцеві гетероатоми, незалежно), вибрані атом (наприклад, один, два, три або чотири кільз нітрогену, оксигену та сульфур у та, як варіант, цеві гетероатоми, незалежно), вибрані з нітрогену, крім того містить місткову групу, кільце, як варіант, оксигену та сульфур у та, як варіант, крім того місзаміщено принаймні одним замісником (напритить місткову груп у (приклади залучають циклопклад, одним, двома або трьома замісниками, неропіл, циклобутил, циклопентил, циклогексил, дизалежно), вибраними з групи: гідроксил, С1-С6, цикло[2,2,1]гептил, феніл, піроліл, імідазоліл, переважно С1-С4алкіл (наприклад, метил, етил, нпіридиніл, піразиніл, піридазиніл, тетразоліл, пірипропіл, ізопропіл, н-бутил, ізобутил, трет-бутил, нмідиніл, тієніл, фураніл, тетрагідрофураніл та компентил, 1,1-диметилпропіл чи н-гексил) та С 1-С6, бінації будь-яких двох або більше їх), кільце, як переважно С1-С4гідроксіалкіл (наприклад, -СН2ОН, варіант, заміщене принаймні одним замісником -СН2СН2ОН, -СН2СН2СН2ОН або -СН(ОН)СН3). (наприклад, одним, двома або трьома замісникаУ наступному втіленні винаходу R11 та/або R12 ми, незалежно), вибраними з групи: галоген (напредставляють 3-6-членне насичене або ненасиприклад, флуор, хлор, бром або йод), гідроксил, чене кільце, що містить, як варіант, принаймні оксо (=О), С1-С6, переважно С1-С4алкіл (наприодин кільцевий атом нітрогену та, як варіант, крім клад, метил, етил, н-пропіл, ізопропіл, н-бутил, того містить місткову гр уп у (зокрема, циклопропіл, ізобутил, трет-бутил, н-пентил або н-гексил), С1циклопентил, циклогексил, дицикло(2,2,1]гептил, С6, переважно С1-С4гідроксіалкіл (наприклад, феніл, піролідиніл та тетразоліл), кільце, як варіСН2ОН, -СН2СН2ОН, -СН2СН2СН2ОН або ант, заміщене принаймні одним замісником (наСН(ОН)СН3) та С1-С6, переважно С 1приклад, одним, двома або трьома замісниками, С4галогеналкіл (наприклад, трифлуорметил), або незалежно), вибраними з групи: гідроксил, С1(iv) С1-С6, переважно С1-С4алкілсульфоніл С5алкіл та С 1-С2гідроксіалкіл. (наприклад, метилсульфоніл або ети-лсульфоніл), У втіленні винаходу R11 та/або R12 представабо R11 та R12разом з атомом нітрогену, до якого ляють С 1-С6алкіл, як варіант, заміщений принаймні вони приєднані, утворюють 4-7-членне насичене одним замісником (наприклад, одним, двома, гетероциклічне кільце, що, як варіант, крім того трьома або чотирма замісниками), вибраними з містить кільцевий атом нітрогену, оксигену або групи: аміно, гідроксил, С1-С6, переважно С1сульфур у (наприклад, піролідиніл, піперидиніл, С4алкокси (наприклад, метокси, етокси, н-пропокси піперазиніл, морфолініл або тіоморфолініл), та яке або н-бутокси), С1-С6, переважно С 1є, як варіант, конденсованим з бензольним кільС4алкоксикарбоніл (наприклад, метоксикарбоніл цем з утворенням 8-11-членної кільцевої системи або етоксикарбоніл), С1-С6, переважно С 1 17 77814 18 С4алкілкарбоніламіно (наприклад, метилкарбоніта гідроксидифенілметил. ламіно або етилкарбоніламіно) та 3-6-членне наУ втіленні винаходу R11 та R12 разом з атомом сичене або ненасичене кільце, що містить, як ванітрогену, до якого вони приєднані, утворюють 5-6ріант, принаймні один кільцевий гетероатом членне насичене гетероциклічне кільце, що, як (наприклад, один, два, три або чотири кільцеві варіант, крім того містить кільцевий атом нітрогегетероатоми, незалежно), вибрані з нітрогену та ну, оксигену або сульфур у, та яке є, як варіант, оксигену та, як варіант, крім того містить місткову конденсованим з бензольним кільцем з утворенгруп у, кільце, як варіант, заміщене принаймні одням 9-10-членної кільцевої системи, гетероциклічним замісником (наприклад, одним, двома або не кільце або кільцеву систему, як варіант, замітрьома замісниками, незалежно), вибраними з щено одним або двома замісниками, незалежно групи: галоген (наприклад, флуор, хлор, бром або вибраними з групи: флуор, гідроксил, амідо, С1йод), гідроксил, оксо, С1-С6, переважно С1-С4алкіл С2алкіл, С1-С2гідроксіалкіл, С1-С2алкокси, С1(наприклад, метил, етил, н-пропіл, ізопропіл, нС2алкоксикарбоніл, С1-С2галогеналкіл, ді- С1бутил, ізобутил, трет-бутил, н-пентил або нС2алкіламіно, С1-С2алкілкарбоніламіно, ді-С1гексил), С1-С6, переважно С1-С4гідроксіалкіл (наС2алкіламінокарбоніл, феніл, хлорфеніл, фенілкаприклад, -СН2ОН, -СН2СН2ОН, -СН2СН2СН2ОН або рбоніло-кси та гідроксидифенілметил. -СН(ОН)СН3) та С1-С1, переважно С 1В іншому втіленні винаходу R11 та R12 разом з С4галогеналкіл (наприклад, трифлуорметил). атомом нітрогену, до якого вони приєднані, утвоВ іншому втіленні винаходу R11 та/або R12 рюють гетероциклічне кільце або кільцеву систепредставляють С 1-6алкіл, як варіант, заміщений му, вибрану з гр упи: пі-ролідиніл, піперидиніл, піпринаймні одним замісником (наприклад, одним, перазиніл, морфолініл, тіоморфолініл, двома, трьома або чотирма замісниками), вибрадигідроізохінолініл та дигідроізоіндоліл, гетероциними з групи: аміно, гідроксил, С1-С4алкокси, С1клічне кільце або кільцеву систему, як варіант, С2алкоксикарбоніл, С1-С2алкілкарбоніламіно та 3заміщено одним або двома замісниками, незалеж6-членне насичене або ненасичене кільце, що місно вибраними з групи: флуор, гідроксил, амідо, тить, як варіант, один або два кільцеві гетероатометил, гідроксиметил, 2-гідроксіетил, метокси, меми, вибрані з нітрогену та оксигену, та, як варіант, токсикарбоніл, трифлуорметил, диметиламіно, крім того містить місткову груп у (зокрема, циклопметилкарбоніламіно, диметиламінокарбоніл, феропіл, дицикло[2,2,1]гептил, феніл або тетрагідроніл, хлорфеніл, фенілкарбонілокси та гідроксидифураніл), кільце, як варіант, заміщене принаймні фенілметил. одним замісником (наприклад, одним, двома або R12a представляє атом гідрогену або С 1-С6, трьома замісниками, незалежно), вибраними з переважно С1-С4алкіл (наприклад, метил, етил, ноксо (наприклад з утворенням 2,5пропіл, ізопропіл, н-бутил, ізобутил, трет-бутил, ндіоксоімідазолідинільного кільця) та С1-С2 алкілу. пентил або н-гексил). У втіленні винаходу R11 та R12 разом з атомом У втіленні винаходу R12a представляє атом гінітрогену, до якого вони приєднані, утворюють 4-7дрогену або метил. членне насичене гетероциклічне кільце, що, як R13 представляє С 1-С6, переважно С1-С4алкіл варіант, крім того містить кільцевий атом нітроге(наприклад, метил, етил, н-пропіл, ізопропіл, нну, оксигену або сульфур у (наприклад, піролідиніл, бутил, ізобутил, трет-бутил, н-пентил або нпіперидиніл, піперазиніл, морфолініл або тіоморгексил), аміно або феніл. фолініл), та яке є, як варіант, конденсованим з У втіленні винаходу: бензольним кільцем з утворенням 8-11-членної кожне R1 незалежно представляє галоген або кільцевої системи (наприклад, дигідроізохі-нолініл С1-С6алкіл; або дигідроізоіндоліл), гетероциклічне кільце або одне з X та Υ представляє зв’язок, а інше з X кільцеву систему, як варіант, заміщено принаймні та Υ представляє атом оксигену, а Ζ представляє одним замісником (наприклад, одним, двома, СН2-, або X представляє -СН2-, Υ представляє трьома або чотирма замісниками, незалежно), атом оксигену, a Z представляє зв’язок; вибраними з групи: галоген (наприклад, флуор, R4, R5, R6 та R7, кожне представляють атом гіхлор, бром або йод), гідроксил, амідо, С1-С6, передрогену та R8 представляє атом гідрогену або С 1важно С1-С4алкіл (наприклад, метил, етил, нС6алкіл; пропіл, ізопропіл, н-бутил, ізобутил, трет-бутил, нt дорівнює 1 або 2; та пентил або н-гексил), С1-С6, переважно С1кожне R9 незалежно представляє гідроксил С4гідроксіалкіл (наприклад, -СН2ОН, -СН2СН2ОН, (наприклад, у пара-позиції відносно R) або галоген СН2СН2СН2ОН або -СН(ОН)СН3), С1-С6, переваж(наприклад, у пара-позиції відносно R або у парано С1-С4алкокси (наприклад, метокси, етокси, нпозиції відносно -О-). пропокси або н-бутокси), С1-С6, переважно С 1У втіленні винаходу: С4алкоксикарбоніл (наприклад, метоксикарбоніл m дорівнює 0 або 1; або етоксикарбоніл), С1-С6, переважно С 1кожне R1 незалежно представляє флуор, хлор, С4галогеналкіл (наприклад, трифлуорметил), діметил або трифлуорметил; С1-С6, переважно С1-С4алкіламіно (наприклад, X представляє зв’язок, -СН2-, -О- або -С(О)-, a диметиламіно), С1-С6, переважно С1Y представляє зв’язок, -СН2-, -О- або -С(О)-, або X С4алкілкарбоніламіно (наприклад, метилкарбоніта Υ разом представляють групу -СН= С(СН3)-; a Z ламіно або етилкарбоніламіно), ді- С1-С6, перевапредставляє зв’язок, -О-, або -СН2-, за умови, що жно С1-С4алкіламінокарбоніл (наприклад, диметитільки одне з Χ, Υ та Ζ може представляти зв’язок ламінокарбоніл), феніл, галогенфеніл (наприклад, одночасно, та за умови, що X та Υ не представляфлуорфеніл або хлор феніл), фенілкарбонілокси ють одночасно -О- або -С(О)-; 19 77814 20 n дорівнює 0 або 1; q дорівнює 0 або 1; R2 представляє флуор; R3 представляє -NHC(O)R 10, -C(O)NR11R12 або q дорівнює 0 або 1 ; -COOR 12a ; R3 представляє -NHC(O)R 10, -C(O)NR11R12 або R4, R5, R6, R7 та R8, кожне незалежно, пред12a -COOR ; ставляють атом гідрогену або метил; R4, R5, R6, R7 та R8, кожне незалежно, предt дорівнює 0 або 1; ставляють атом гідрогену або метил; R9 представляє галоген, гідроксил, метокси t дорівнює 0, 1 або 2; або трифлуорметил; кожне R9 незалежно представляє галоген, гідR10 представляє метил; роксил, карбоксил, метил, метокси, метоксикарбоR11 та R12, кожне незалежно, представляють ніл або трифлуорметил; гідроген, метил, циклопропіл, гідроксіетил або аміR10 представляє метил, циклопентил, феніл ноетил, або R11 та R12 разом з атомом нітрогену, або груп -NR R; до якого вони приєднані, утворюють морфолініл, R11 та R 12, кожне незалежно, представляють або утворюють піперидиніл, що заміщено гідро(і) атом гідрогену, ксилом; а (іі) 3-6-членне насичене або ненасичене кільR12a представляє атом гідрогену. це, що містить, як варіант принаймні один кільцеПриклади сполук винаходу залучають: вий атом нітрогену та, як варіант, крім того містить N-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1місткову гр упу, кільце, як варіант, заміщене прибензофуран-2,4’-піперидин]-1’-іл)-2наймні одним замісником, вибраним з групи: гідрогідроксипропіл]окси}-феніл)ацетамід, ксил, С1-С5алкіл та С 1-С2гідроксіалкіл, N-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1(ііі) С1-С6алкіл, як варіант, заміщений принайбензофуран-2,4’-піперидин]-1’-іл)-2мні одним замісником, вибраним з групи: аміно, гідроксипропіл]окси}-4-флуорфеніл)ацетамід, гідроксил, С1-6алкокси, С1-С4алкоксикарбоніл, С1N-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1С2алкілкарбоніламіно та 3-6-членне насичене або бензофуран-2,4’-піперидин]-1’-іл)-2ненасичене кільце, що містить, як варіант, один гідроксипропіл]окси}-4-метоксифеніл)ацетамід, або два кільцеві гетероатоми, вибрані з нітрогену N-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1та оксигену, та, як варіант, крім того містить містбензофуран-2,4’-піперидин]-1’-іл)-2кову гр упу, кільце, як варіант, заміщене принаймні гідроксипропіл]окси}-4-гідроксифеніл)ацетамід, одним замісником, вибраним з групи: оксо та С1N-[2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1С2алкіл, або бензофуран-2,4’-піперидин]-1’-іл)-2(iv) метилсульфоніл, або R11 та R12 разом з гідроксипропіл]окси}-5атомом нітрогену, до якого вони приєднані, утво(трифлуорметил)феніл]ацетамід) рюють 5-6-членне насичене гетероциклічне кільце, 2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуранщо, як варіант, крім того містить кільцевий атом 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси]-Nнітрогену, оксигену або сульфур у, та яке є, як вациклопропілбензамід, ріант, конденсованим з бензольним кільцем з 2-{[(2S)-3-(5-ooiop-1’Н,3Н-спіро[1-бензофуранутворенням 9-10-членної кільцевої системи, гете2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси]-Nроциклічне кільце або кільцеву систему, як варіциклопропiл-4-флуорбензамід, ант, заміщено одним або двома замісниками, не2-{[(2S)-3-{5-хлор-1’Н,3Н-спіро[1-бензофуранзалежно вибраними з групи: флуор, гідроксил, 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-Nамідо, С1-С2алкіл, С1-С2гiдроксіалкіл, С1циклопропіл-4-метоксибензамід, С2алкокси, С1-С2алкоксикарбоніл, С1Ν-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1С2галогеналкіл, ді-С1-С2алкіламіно, С1бензофуран-2,4’-піперидин]-1’-іл)-2-гідрокси-2С2алкілкарбоніламіно, ді- С1-С2алкіламінокарбоніл, метилпропіл]окси}-4-гідроксифеніл)ацетамід, трифеніл, хлор феніл, фенілкарбонілокси та гідроксифлуорацетат, дифенілметил; N-(5-хлор-2-{[(2S)-3-(6-хлор-1’Н,3Н-спіро[2R12a представляє атом гідрогену або метил; а бензофуран-1,4’-піперидин]-1’-іл)-2R14 та R15, кожне незалежно, представляють гідроксипропіл]окси}феніл)ацетамід, атом гідрогену або С 1-С6алкілсульфоніл груп, або N-(2-{[(2S)-3-(6-хлор-1’Н,3Н-спіро[2R14 та R15 разом з атомом нітрогену, до якого вони бензофуран-1,4’-піперидин]-1’-іл)-2приєднані, утворюють 5-6-членне насичене гетегідроксипропіл]окси}-4-флуорфеніл)ацетамід, роциклічне кільце, що, як варіант, заміщено приN-(2-{[(2S)-3-(6-хлор-1’Н,3Н-спіро[2наймні одним гідроксилом. бензофуран-1,4’-піперидин]-1’-іл)-2У втіленні винаходу: гідроксипропіл]окси}феніл)ацетамід, m дорівнює 0 або 1; N-(2-{[(2S)-3-(6-хлор-1’Н,3Н-спіро[2R1 представляє галоген; бензофуран-1,4’-піперидин]-1’-іл)-2X представляє зв’язок, -СН2-, -О- або -С(О)-, а гідроксипропіл]окси}-4-метоксифеніл)ацетамід, Υ представляє зв’язок, -СН2-, -О-або -С(О)-, або X 2-{[(2S)-3-(6-хлор-1’Н,3Н-спіро[2-бензофуранта Υ разом представляють групу -СН= С(СН 3)-, та 1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4Ζ представляє зв’язок, цикпопропіл-4-флуорбензамід, -О- або -СН2-, за умови, що тільки одне з Χ, Υ N-(2-{[(2S)-3-(5-Флуор-1’Н,3Нта Ζ може представляти зв’язок одночасно, та за спіро[бензофуран-1,4’-піперидин]-1’-іл)-2умови, що X та Υ не представляють одночасно -Огідроксипропіл]феніл)ацетамід, або -С(О)-; N-(4-хлор-2-{[(2S)-2-гідрокси-3-(3-оксо-1’Н,3Нn дорівнює 0; спіро[2-бензофуран-1,4’-піперидин]-1’ 21 77814 22 іл)пропіл]окси}феніл)ацетамід, 1,4’-піперидин]-1’-іл)-2-гідрокси-2N-Циклопропт-2-{[(2S)-2-гідрокси-3-(1’Н,3Нметоксипропіл]окси}-N-циклопропіл-4спіро[2-бензофуран-1,4’-піперидин]-1’гідроксибензамід, іл)пропіл]окси}бензамід, 2-{[(2S)-3-(5-хлор-1’Н,3Н-спiро[бензофуран-NN-(4-xлop-2-{[(2S)-2-гідрокси-3-(1’Н,3Н-спіро[2піперидин]-1’-іл)-2-гідроксипропіл]окси}-4-гідроксибензофуран-1,4’-піперидин]-1’N-(2-гідроксіетл)бензамід, іл)пропіл]окси}феніл)ацетамід, N-(2-Аміноетил)-2-{](2S)-3-(5-хлор-1’Н,3НN-(5-xлop-2{[(2S)-2-гідрокси-3-(1’Н,3Н-спіро[[2спіро[1-бензофуран-2,4’-піперидин]-1’-іл)-2бензофуран-1,4’-піперидин]-1’гідроксипропіл]окси}-4-гідроксибензамід, іл)пропіл]окси}феніл)ацетамід, 2-{[(2S)-3-(5-Флуор-1’Н,3Н-спіро[1Ν-(2-{[(2S)-2-гідрокси-2-метил-3-(1’Н,3Ηбензофуран-2,4’-піперидин]-1’-іл)-2спіро[2-бензофуран-1,4’-піперидин]-1’гідроксипропіл]окси}-4-гідрокси-N-метилбензамід, іл)пропіл]окси}-4-метоксифеніл)ацетамід, N-(2-{[(2S)-3-{5-Флуор-1’Н,3Н-спіро[1N-[2-{[(2S)-2-гідрокси-3-(1’Н,3Н-спіро[2бензофуран-2,4’-піперидин]-1’-іл)-2бензофуран-1,4’-піперидин]-1’-іл)пропіл]окси}-5гідроксипропіл]окси}-4-гідроксифеніл)ацетаіиід, (трифлуорметил)феніл]ацетамід, N-(2-{[(2S)-3-(5-Флуор-1’H,3Н-спіро[1N-[2-{[(2S)-2-гідрокси-3-(2-метил-1’Нбензофуран-2,4’-піперидин]-1’-іл)-2спіро[інден-1,4’-піперидин]-1’гідроксипропіл]окси)феніл)ацетамід, іл)пропіл]окси}феніл)ацетамід, N-(2-{[(2S)-3[(2S)-5-хлор-1’Н,3Н-спіро[1N-(2-{[(2S)-3-{2,3-Дигідро-1’Н-спіро[інден-1,4’бензофуран-2,3’-піролідин]-1’-іл]-2піперидин]-1’-іл)-2гідроксипропіл}окси)феніл]ацетамід, гідроксипропіл]окси}феніл)ацетамід, N-(2-({(2S)-3[(2R)-5-xлop-1’Н,3Н-спіро[1N-(2-{[(2S)-2-Гідрокси-3-(2-оксо-1’Н-спіро[1бензофуран-2,3’-піролідин]-1’-іл]-2бензофуран-3,4’-піперидин]-1’гідроксипропіл}окси)феніл]ацетамід, іл)пропіл]окси}феніл)ацетамід, N-[2-({(2S)-3-[(2S)-5-xлop-1’Н,3Н-спіро[12-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуранбензофуран-2,3’-піролідин]-1’-іл]-22,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-Nгідроксипропіл)окси]-4-метоксифеніл]ацетамід, циклопропіл-4-гідроксибензамід, N-(2-{[(2S)-3-[(2R)-5-xлop-1’Н,3Н-спіро[12-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуранбензофуран-2,3’-піролідин]-1’-іл]-22,4’-піперидин]-1’-іл)-2-гідрокси-2гідроксипропіл}окси)-4-метоксифеніл]ацетамід, метилпропіл]окси}-N-циклопропіл-42-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофурангідроксибензамід, 2,3’-піролідин]-1’-іл)-2-гідроксипропіл]окси}-4N-(4-гідрокси-2-{[(2S)-2-гідрокси-3-(1’Н,4Нгідрокси-N-метилбензамід, спіро[хромен-3,4’-піперидин]-1’2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофураніл)пропіл]окси}феніл)ацетамід, 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-42-{[(2S)-3-{5-хлор-1’Н,3Н-спіро[1-бензофурангідроксибензойна кислота (трифлуорацетат), 2,4’-піперидин]-1’-іл)-2-гідрокси-23(S)-1-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1метилпропіл]окси}-4-гідрокси-N-метилбензамід бензофуран-2,41-піперидин]-1’-іл)-2(трифлуорацетат), гідроксипропіл]окси}-4-гідроксибензоїл)піролідин-32-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуранол, 2,4’-піперидин]-1’-іл)-2-гідрокси]окси}-4-гідрокси-N3(S)-1-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1метилбензамід, бензофуран-2,4’-піперидин]-1’-іл)-2N-(2-{[(2S)-3-(5-хлор-1’Н-спіро[1,3гідроксипропіл]окси}-4-гідроксибензоїл)піролідин-3бензодіоксол-2,4’-піперидин]-1’-іл)-2ол, гідроксипропіл]окси)-4-гідроксифеніл)ацетамід, 3-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофурантрифлуорацетат, 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4N-(2-{[(2S)-3-(5-хлор-1’Н-спіро[1,3(морфолін-4-ілкарбоніл)фенол, бензодіоксол-2,4’-піперидин]-1’-іл)-2-гідрокси-22-{[(2S)-3-(5-xлop-1’,Н-спіро 1,3-бензодіоксолметилпропіл]окси}-4-гідроксифеніл)ацетамід, три2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-Nфлуорацетат, метилбензамід, трифлуорацетат, N-(4-Гідрокси-2-{[(2S)-2-гідрокси-3-(1’НN-(2-{[(2S)-3-(6-хлор-3,4-дигідро-1’Нспіро[1,3-бензодіоксол-2,4’-піперидин]-1’спіро[хромен-2,4’-піперидин]-1’-іл)-2іл)пропіл]окси}феніл)ацетамід, трифлуорацетат, гідроксипропіл]окси}феніл)ацетамід, трифлуораN-(4-Гідрокси-2-{[(2S)-2-гідрокси-2-метил-3цетат, (1’Н-спіро[1,3-бензодюксол-2,4’-піперидин]-1’N-(2-{[(2S)-3-(6-хлор-3,4-дигідро-1’Ніл)пропіл]окси}феніл)ацетамід, трифлуорацетат, спіро[хромен-2,4’-піперидин]-1’-іл)-2N-(2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[2гідроксипропіл]окси}-4-флуорфеніл)ацетамід, трибензофуран-1,4’-піперидин]-1’-іл)-2флуорацетат, гідроксипропіл]окси}-4-гідроксифеніл)ацетамід, 2-{[(2S)-3-(6-хлор-3,4-дигідро-1’НN-(2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[2спіро[хромен-2,4’-піперидин}-1’-іл)-2бензофуран-1,4’-піперидин]-1’-іл)-2гідроксипропіл]окси}-N-метилбензамід, трифлуогідроксипропіл]окси}феніл)ацетамід, рацетат, 2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[2-бензофуранN-{2-{[(2S)-3-(6-xлop-3,4-дигідро-1’H1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4cпipo[xpoмен-2,4’-піперидин]-1’-іл)-2гідрокси-N-метилбензамід, гідроксипропіл]окси}-4-гідроксифеніл)ацетамід, 2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[2-бензофурантрифлуорацетат, 23 77814 24 2-{[(2S)-3-(6-xлop-3,4-дигідро-1’Нол, спіро[хромен-2,4’-піперидин]-1’-іл)-2-гідрокси-22-{[(2S)-3-(5-Флуор-1’Н,3Н-спіро[1метилпропіл]окси}-4-гідроксифеніл)ацетамід, трибензофуран-2,4’-піперидин]-1’-іл)-2флуорацетат, гідроксипропіл]окси}-4-бензойна кислота, гідроN-[2-({(2S)-3-[(2R)-5-хлор-1’Н,3Н-спіро[1хлорид, бензофуран-2,3’-піролідин]-1’-іл]-2(2S)-1-(5-хлор-1’Н,3Н-спіро[1-бензофуран-2,4’гідроксипропіл}окси)-4-гідроксифеніл]ацетамід, піперидин]-1’-іл)-3-(2-{[2-(гідроксиметил)морфолінN-[2-({(25)-3-[(2S)-5-хлор-1’Н,3Н-спіро[14-іл]карбоніл}-5-метилфенокси)пропан-2-ол, бензофуран-2,3’-піролідин]-1’-іл]-2(3S)-1-(2-{[(2S)-3-(5-Флуор-1’Н,3Н-спіро[1гідроксипропіл}окси)-4-гідроксифеніл]ацетамід, бензофуран-2,4’-піперидин]-1’-іл)-23-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофурангідроксипропіл]окси}-4-метилбензоїл)піролідин-32,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4ол, (піролідин-1-ілкарбоніл)фенол, 2-{[(25)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуран1-{2-{[(23)-3-(5-хлор-1’Н,3Н-спіро[12,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-Nбензофуран-2,4’-піперидин]-1’-іл)-2{[(4R)-2,5-діоксоімідазолідин-4-іл]метил}-4гідроксипропіл]окси}-4-гідроксибензоїл)піперидингідроксибензамід, 4-ол, 1-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1(3S)-1-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1бензофуран-2,4’-піперидин]-1’-іл)-2бензофуран-2,4’-піперидин]-1’-іл)-2гідроксипропіл]окси}-4-гідроксибензоїл)-3гідроксипропіл]окси}бензоїл)піролідин-3-ол, (трифлуорметил)піролідин-3-ол, 3-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуран3-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуран2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-42,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4-{[3(піперидин-1-ілкарбоніл)фенол, (трифлуорметил)піролідин-1-іл)карбоніл}фенол, (3S)-1-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[2N-[2-(Ацетиламіно)етил]-2-{[(2S)-3-(5-хлорбензофуран-1,4’-піперидин]-1’-іл)-21’Н,3Н-спіро[1-бензофуран-2,4’-піперидин]-1’-іл)-2гідроксипропіл]окси}-4-гідроксибензоїл)піролідин-3гідроксипропіл]окси}-4-гідроксибензамід, ол, N-(5-хлор-2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[11-(2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[2бензофуран-2,4’-піперидин]-1’-іл)-2бензофуран-1,4’-піперидин]-1’-іл)-2гідроксипропіл]окси)-4-метоксифеніл)ацетамід, гідроксипропіл]окси}-4-гідроксибензоїл)піперидин(3S)-N-(5-хлор-2-{[(2S-3-(5-хлор-1’Н,3Н-спіро[14-ол, бензофуран-2,4’-піперидин}-1’-іл)-2N-[4-Гідрокси-2-({(2S)-2-гідрокси-3-[5гідроксипропіл]окси]феніл)-3-гідроксипіролідин-1(трифлуорметил)-1’Н,3Н-спіро[1-бензофуран-2,4’карбоксамід, піперидин]-1’-іл]пропіл}окси)феніл]ацетамід, (3S)-N-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1(3S)-1-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1бензофуран-2,4’-піперидин]-1’-іл)-2бензофуран-2,4’-піперидин]-1’-іл)-2гідроксипропіл]окси)феніл)-3-гідроксипіролідин-1гідроксипропіл]окси}-4-гідроксибензоїл)піролідин-3карбоксамід, ілбензоат, N-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1(3S)-1-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1бензофуран-2,4’-піперидин]-1’-іл)-2бензофуран-2,4’-піперидин]-1’-іл)-2гідроксипропіл]окси}феніл)-4-гідроксипіперидин-1гідроксипропіл]окси}-4-флуорбензоїл)піролідин-3карбоксамід, ол, N-(2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[1(3S)-1-[4-Гідрокси-2-({(2S)-2-гідрокси-3-[5бензофуран-2,4’-піперидин]-1’-іл)-2(трифлуорметил)-1’Н,3Н-спіро[1-бензофуран-2,4’гідроксипропіл]окси}феніл)сечовина, трифлуорапіперидин]-1’-іл]пропіл}окси)бензоїл]піролідин-3цетат, ол) N-(2-{[(2S)-3-(5-хлop-1’Н,3Н-спіро[1(3S)-1-(4-Флуор-2-{[(2S)-2-гідрокси-3-(1’Н,3Нбензофуран-2,4’-піперидин]-1’-іл)-2спіро[1-бензофуран-2,4’-піперидин]-1’гідроксипропіл]окси}-4-гідроксифеніл)сечовина, іл)пропіл]окси}бензоїл)піролідин-3-ол, трифлуорацетат, 4-Флуор-2-{[(2S)-3-(5-флуор-1’Н,3Н-спіро[1N-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1бензофуран-2,4’-піперидин]-1-іл)-2бензофуран-2,4’-піперидин]-1’-іл)-2гідроксипропіл]окси}бензойна кислота (гідрохлогідроксипропіл]окси}-4-флуорфеніл)сечовина, рид), трифлуорацетат, (3S)-1-(4-Флуор-2-{[(2S)-3-(5-флуор-1’Н,3НN-{[(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1спіро[1-бензофуран-2,4’-піперидин]-1’-іл)-2бензофуран-2,4’-піперидин]-1’-іл)-2гідроксипропіл]окси}бензоїл)піролідин-3-ол, гідроксипропіл]окси}-4N-((3S)-1-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1гідроксифеніл)аміно]карбоніл}метансульфонамід, бензофуран-2,4’-піперидин]-1’-іл)-2трифлуорацетат, гідроксипропіл]окси}-4-гідроксибензоїл)піролідин-3(4S)-2-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1іл]ацетамід, бензофуран-2,4’-піперидин]-1’-іл)-22-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофурангідроксипропіл]окси}-42,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4гідроксибензоїл)ізоксазолідин-4-ол, трифлуорацебензойна кислота, гідрохлорид, тат, (3S)-1-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1(4R)-2-(2-{[(2S)-3-(5-xлop-1’H,3H-cпipo[1бензофуран-2,4’-піперидин]-1’-іл)-2бензофуран-2,4’-піперидин]-1’-іл)-2гідроксипропіл]окси]}-4-метилбензоїл)піролідин-3гідроксипропіл]окси]-4 25 77814 26 гідроксибензоїл)ізоксазолідин-4-ол, трифлуорацегідроксипропіл]окси}-4-гідроксифеніл)-3тат, гідроксипіролідин-1-карбоксамід, трифлуорацетат, (4S)-2-(2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[1(3S)-1-(4-гідрокси-2-{[(2S)-2-гідрокси-3-{1’Н,3Нбензофуран-2,4’-піперидин]-1’-іл)-2спіро[1-бензофуран-2,4’-піперидин]-1’гідроксипропіл]окси}-4-гідроксибензоїл)-4іл)пропіл]окси) бензоїл)піролідин-3-ол, трифлуометилізоксазолідин-4-ол, трифлуорацетат, рацетат, (4R)-2-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[12-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуранбензофуран-2,4’-піперидин]-1’-іл)-22,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-5гідроксипропіл]окси}-4-гідроксибензоїл)-4бензойна кислота, гідрохлорид, метилізоксазолідин-4-ол, трифлуорацетат, 2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуран2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуран2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-42,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-Nметоксибензойна кислота, гідрохлорид, (метилсульфоніл)бензамід, трифлуорацетат, (3S)-1-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[12-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуранбензофуран-2,4’-піперидин]-1’-іл)-22,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-N-1Нгідроксипропіл]окси}-5-метилбензоїл)піролідин-3тетразол-5-ілбензамідбіс(трифлуорацетат), ол, трифлуорацетат, 3-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуран(3S)-1-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[12,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4бензофуран-2,4’-піперидин]-1’-іл)-2{[(3R)-3-{диметиламіно)піролідин-1гідроксипропіл]окси}-4-метоксибензоїл)піролідин-3іл]карбоніл}фенол біс(трифлуорацетат), ол, трифлуорацетат, 3-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуран5-хлор-2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[12,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4бензофуран-2,4’-піперидин]-1’-іл)-2{[(3S)-3-(диметиламіно)піролідин-1гідроксипропіл]окси}бензойна кислота, гідрохлоіл]карбоніл}фенол біс(трифлуорацетат), рид, (3S)-1-(5-хлор-2-{[(2S)-3-(5-хлор-1’Н,3Н(3S)-1-(5-хлор-2-{[(2S)-3-(5-хлор-1’Н,3Нспіро[1-бензофуран-2,4’-піперидин]-1’-іл)-2спіро[1-бензофуран-2,41-піперидин]-1’-іл)-2гідроксипропіл]окси}-4-гідроксибензоїл)піролідин-3гідроксипропіл]окси}бензоїл)піролідин-3-ол, трифол, трифлуорацетат, луорацетат, 3-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуран2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуран2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-42,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-5{[(3S)-3-метоксипіролідин-1-іл]карбоніл}фенол, флуорбензойна кислота, гідрохлорид, трифлуорацетат, (3S)-1-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[13-{[(2S)-3-{5-хлор-1’Н,3Н-спіро[1-бензофуранбензофуран-2,41-піперидин]-1’-іл)-22,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4гідроксипропіл]окси}-5-флуорбензоїл)піролідин-3{[(2S)-2-(гідроксиметил)піролідин-1ол, трифлуорацетат, іл]карбоніл}фенол, трифлуорацетат, N-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[13-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуранбензофуран-2,4’-піперидин]-1’-іл)-22,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4гідроксипропіл]окси}феніл)піролідин-1{[(2S)-2-(гідроксиметил)піролідин-1карбоксамід, трифлуорацетат, іл]карбоніл}фенол, трифлуорацетат, Метил 4-(ацетиламіно)-3-{[(2S)-3-(5-хлор3-{[(2S)-3-(5-хлор-1’Η,3Н-спіро[1-бензофуран1’Н,3Н-спіро[1-бензофуран-2,4’-піперидин]-1’-іл)-22,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4-{[3гідроксипропіл]окси}бензоат, трифлуорацетат, (гідроксиметил)піролідин-1-іл]карбоніл}фенол, 4-(ацетиламіно)-3-{[(2S)-3-(5-хлор-1’Н,3Нтрифлуорацетат, спіро[1-бензофуран-2,4’-піперидин]-1’-іл)-21-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1гідроксипропіл]окси}бензойна кислота, трифлуобензофуран-2,4’-піперидин]-1’-іл)-2рацетат, гідроксипропіл]окси}-4-гідроксибензоїл)-DN-(2-{[(2S)-3-(5-хлор-3’-флуор-1’Н,3Н-спіро[1пролінамід, трифлуорацетат, бензофуран-2,4’-піперидин]-1’-іл)-2N-(4-гідрокси2-{[(2S)-2-гідрокси-3-(1’Н,3Нгідроксипропіл]окси}-4-гідроксифеніл)ацетамід, спіро[1-бензофуран-2,4’-піперидин]-1’2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[1-бензофураніл)пропіл]окси}феніл)ацетамід, трифлуорацетат, 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4N-(4-гідрокси-2-{[(2S)-2-гідрокси-3-(5-метилгідрокси-N-(2-гідроксипропіл)бензамід, 1’Н,3Н-спіро[1-бензофуран-2,4’-піперидин]-1’2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофураніл)пропіл]окси}феніл)ацетамід, трифлуорацетат, 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4N-(5-xлop-2-{[(2S)-2-гідрокси-3-(1’Н,3Н-спіро[1гідрокси-N-(2-гідрокси-1,1-диметилетил)бензамід, бензофуран-2,4’-піперидин]-1’-іл)пропіл]окси}-42-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуранметоксифеніл)ацетамід, трифлуорацетат, 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-NN-(5-хлор-4-гідрокси-2-{[(2S)-2-гідрокси-3циклопентил-4-гідроксибензамід, (1’Н,3Н-спіро[1-бензофуран-2,4’-піперидин]-1’2-{[(2S)-3-(5-xлop-1’H,3H-cnipo[1-бензофураніл)пропіл]окси}феніл)ацетамід, трифлуорацетат, 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4(3S)-N-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1гідрокси-N-(2-метоксіетил)бензамід, бензофуран-2,4’-піперидин]-1’-іл)-22-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[1-бензофурангідроксипропіл]окси}-4-метоксифеніл)-32,4’-піперидин]-1’-іл)-2-гідроксипропіл]океи}-4гідроксипіролідин-1-карбоксамід, трифлуорацетат, гідрокси-N-гідроксифеніл)бензамід, (3S)-N-{2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1N-(трет-бутил)-2-{[(2S)-3-(5-xлop-1’Н,3Нбензофуран-2,4’-піперидин]-1’-іл)-2спіро[1-бензофуран-2,4’-піперидин]-1'-іл)-2 27 77814 28 гідроксипропіл]окси}-4-гідроксибензамід, 1-(2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[12-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуранбензофуран-2,4’-піперидин]-1’-іл)-22,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4гідроксипропіл]окси}-4-гідроксибензоїл)-4гідрокси-N-(2-гідрокси-1-метилетил)бензамід, фенілпіперидин-4-ол, 2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуран3-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[1-бензофуран2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-42,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4-(3,4гідрокси-N-ізобутилбензамід, дигідроізохінолін-2(1Н)-ілкарбоніл)фенол, 2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуран3-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[1-бензофуран2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-42,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4-{[2гідрокси-N-(4-гідроксициклогексил)бензамід, (гідроксиметил)піперидин-1-іл]карбоніл}фенол, 2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуран1-(2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[12,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-N-(2,3бензофуран-2,4’-піперидин]-1’-іл)-2дигідроксипропіл)-4-гідроксибензамід, гідроксипропіл]окси}-4-гідроксибензоїл)-N,N2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофурандиметилпролінамід, 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4Метил (4R)-1-{2-{[(2S)-3-(5-хлор-1’Н,3Нгідрокси-N-(2-гідроксіетил)-N-метилбензамід, спіро[1-бензофуран-2,4’-піперидин]-1’-іл)-2Метил N-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1гідроксипропіл]окси}-4-гідроксибензоїл)-4бензофуран-2,4’-піперидин]-1’-іл)-2гідроксипролінат, гідроксипропіл]окси}-4-гідроксибензоїл)серинат, (3R)-1-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[12-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуранбензофуран-2,4’-піперидин]-1’-іл)-22,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-N-(1гідроксипропіл]окси}-4-гідроксибензоїл)піперидинетилпропіл)-4-гідроксибензамід, 3-ол, 2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[1-бензофуран2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуран2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-42)4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4гідрокси-N-{тетрагідрофуран-2-ілметил)бензамід, гідрокси-N-(2-гідроксициклогексил)бензамід, 2-{[(2S)-3-{5-хлор-1’Н,3Н-спіро[1-бензофуран3-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[1-бензофуран2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси)-42,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4-[(4гідрокси-N-[1-(гідроксиметил)-2,2фенілпіперидин-1-іл)карбоніл]фенол, диметилпропіл]бензамід, 3-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуран2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[1-бензофуран2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-42,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-N(тіоморфолін-4-ілкарбоніл)фенол, {[(1S,2R,5S)-6,6-диметилдицикло[3,1,1]гепт-21-(2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[1ил]метил}-4-гідроксибензамід, бензофуран-2,4’-піперидин]-1’-іл)-22-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофурангідроксипропіл]окси}-4-гідроксибензоїл)піперидин2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси]-43-ол, гідрокси-N-[1-(гідроксиметил)-22-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуранметилпропіл]бензамід, 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-N3-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуран(цикпопропілметил)-4-гідрокси-N-пропілбензамід, 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4-{[42-{[(2S)-3-{5-xлop-1’Н,3Н-спіро[1-бензофуран(2-гідроксіетил)піперазин-1-іл]карбоніл}фенол, 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-43-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофурангідрокси-N,N-діізобутилбензамід, 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси)-4-{[33-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуран(гідроксиметил)піперидин-1-іл]карбоніл}фенол, 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4-(1,32-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофурандигідро-2Н-ізоіндол-2-ілкарбоніл)фенол, 2,4'-піперидин]-1’-іл)-2-гідроксипропіл]окси}-N-[5N-(2-трет-бутоксіетил)-2-{[(2S)-3-(5-хлор(1,1-диметилпропіл)-2-гідроксифеніл]-41’Н,3Н-спіро[1-бензофуран-2,4’-піперидин]-1’-іл)-2гідроксибензамід, гідроксипропіл]окси}-4-гідрокси-N2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуранізобутилбензамід, 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-43-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[1-бензофурангідрокси-N-[3-(1-гідроксіетил)феніл]бензамід, 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4-[(42-{[(2S)-3-(5-xлop-1’H,3H-cпipo[1-бензофуранфлуорпіперидин-1-іл)карбоніл]фенол, 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-N3-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[1-бензофуран(циклопропілметил)-4-гідроксибензамід, 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4-((4,42-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофурандифлуорпіперидин-1-іл)карбоніл]фенол, 2,4І-піперидин]-1’-іл)-2-гідроксипропіліоксиН2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[1-бензофурангідрокси-N-піролідин-і-ілбензамід, 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-NN-[(1R,4S)-дицикпо[3,1,1]гепт-2-ил]-2-{[(2S)-3фенілбензамід, (5-хлор-1’Н,3Н-спіро[1-бензофуран-2,4’-піперидин]3-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[2-бензофуран1’-іл)-2-гідроксипропіл]окси}-4-гідроксибензамід, 1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-44-(4-хлорфеніл)-1-(2-{[(2S)-3-(5-хлор-1’Н,3Н({(2R)-2-[гідрокси(дифеніл)метил]піролідин-1спіро[1-бензофуран-2,4’-піперидин]-1’-іл)-2іл}карбоніл)фенол, гідроксипропіл]окси}-4-гідроксибензоїл)піперидин2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[2-бензофуран4-ол, 1,4’-піперидин]-1’-іл)-2-гідроксипропiл]окси}-42-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофурангідрокси-N-(2-гідрокаетил)-N-метилбензамід, 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-43-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[2-бензофурангідрокси-N-(2-гідрокси-1-фенілетил)бензамід, 1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4 29 77814 30 (піролідин-1-ілкарбоніл)фенол, флуорпіперидин-1-іл)карбоніл]фенол, 3-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[2-бензофуран3-{[(2S)-3-{5-хлор-1’Н,3Н-спіро[бензофуран1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4-{[41,4’-піперидин]-1’-іл-2-гідроксипропіл]окси}-4-[(4,4(2-гідроксіетил)піперазин-1-іл]карбоніл) фенол, дифлуорпіперидин-1-іл)карбоніл]фенол, 3-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[2-бензофуран2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[2-бензофуран1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4-{[31,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4(гідроксиметил)піперидин-1-іл]карбоніл}фенол, гідрокси-N-(2-гідроксипропіл)бензамід, 4-(4-хлорфеніл)-1-(2-{[(2S)-3-(5-хлор-1’Н,3Н2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[2-бензофуранспіро[піро[2-бензофуран-1,4’-піперидин]-1’-іл)-21,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4гідроксипропіл]окси}-4-гідроксибензоїл)піперидингідрокси-N-(2-гідрокси-1,1-диметилетил)бензамід, 4-ол, 2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[2-бензофуран3-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[2-бензофуран1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-N1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4-{[4циклопентил-4-гідроксибензамід, (гідроксиметил)піперидин-1-іл]карбоніл}фенол, 2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[2-бензофуран1-(2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[21,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4бензофуран-1,4’-піперидин]-1’-іл)-2гідрокси-N-(2-метоксіетил)бензамід, гідроксипропіл]окси}-4-гідроксибензоїл)-42-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[2-бензофуранфенілпіперидин-4-ол, 1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-43-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[2-бензофурангідрокси-N-(2-гідроксифеніл)бензамід, 1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4-(3,42-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[2-бензофурандигідроізохінолін-2(1Н)-ілкарбоніл)фенол, 1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-43-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[2-бензофурангідрокси-N-(2-гідрокси-1-метилетил)бензамід, 1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси)-4-{[22-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[2-бензофуран(гідроксиметил)піперидин-1-іл]карбоніл}фенол, 1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси)-43-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[2-бензофурангідрокси-N-ізобутилбензамід, 1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4-{[32-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[2-бензофуран(диметиламіно)піролідин-1-іл]карбоніл}фенол, 1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-41-2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[2гідрокси-N-(2-гідроксіетил)бензамід, бензофуран-1,4’-піперидин]-1’-іл)-22-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[2-бензофурангідроксипропіл]окси}-4-гідроксибензоїл)-N,N1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4диметилпролінамід, гідрокси^-(4-гідроксициклогексил)бензамід, 2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[2-бензофуран2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[2-бензофуран1,4’-піперидин]-1’-іл)-2-гідроксипропiл]окси}-N1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-N-(2,3циклогексил-4-гідрокси-N-(2-гідрокаетил)бензамід, дигідроксипропіл)-4-гідроксибензамід, Метил (4R)-1-(2-{[(2S)-3-(5-хлор-1’Н,3НМетил N-(2-{[(2S)-3-(5-хлор-1’H,3Н-спіро[2спіро[2-бензофуран-1,4’-піперидин]-1’-іл)-2бензофуран-N’-піперидин]-1’-іл)-2гідроксипропіл]окси}-4-гідроксибензоїл)-4гідроксипропіл]окси}-4-гідроксибензоїл)серинат, гідроксипролінат, 2-{[(21S}-3-(5-xлop-1’Н,3Н-спіро[2-бензофуран3-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[2-бензофуран1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-N-(11,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4етилпропіл)-4-гідроксибензамід, гідроксибензоїл)піперидин-3-ол, 2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[2-бензофуран3-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[2-бензофуран1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-41,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4-[(4гідрокси-N-(тетрагідрофуран-2-ілметил)бензамід, фенілпіперидин-1-іл)карбоніл]фенол, 2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[2-бензофуран3-{[(2S}-3-(5-хлор-1’Н,3Н-спіро[2-бензофуран1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-41,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4гідрокси-N-[1-(гідроксиметил)-2,2(тіоморфолін-4-ілкарбоніл)фенол, диметилпропіл]бензамід, 1-(2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[22-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[2-бензофуранбензофуран-1,4’-піперидин]-1-іл)-21,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4гідроксипропіл]окси}-4-гідроксибензоїл)піперидингідрокси-N-[1-(гідроксиметил)-23-ол, метилпропіл]бензамід, 2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[2-бензофуран2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[2-бензофуран1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-N1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4(циклопропілметил)-4-гідрокси-N-пропілбензамід, гідрокси-N-[3-(1-гідроксіетил)феніл]бензамід, 2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[2-бензофуран2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[2-бензофуран1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-41,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-Nгідрокси-N,N-діізобутилбензамід) (циклопропілметил)-4-гідроксибензамід, 3-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[2-бензофуран2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[2-бензофуран1,4’-піперидин}-1’-іл)-2-гідроксипропіл]окси}-4-(1,31,4’-піперидин]-1’-іл)-2-гідроксипропіліокси^дигідро-2Н-ізоіндол-2-ілкарбоніл)фенол, гідрокси-N-піролідин-і-ілбензамід, N-(2-трет-бутоксіетил)-2-{[(2S)-3-(5-хлорN-[(1R,4S)-дицикло[2,2,1]гепт-2-ил]-2-{[(2S)-31’Н,3Н-спіро[бензофуран-1,4’-піперидин]-1’-іл)-2{5-хлор-1’Н,3Н-спіро[бензофуран-1,4’-піперидин]гідроксипропіл]окси}-4-гідрокси-N1’-іл)-2-гідроксипропіл]окси}-4-гідроксибензамід, ізобутилбензамід, 2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[2-бензофуран3-{[(2S)-3-{5-хлор-1’Н,3Н-спіро[2-бензофуран1,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси)-41,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси)-4-[(4гідрокси-N-(2-гідрокси-1-фенілетил)бензамід, 31 77814 32 2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[2-бензофуранбензофуран-2,4’-піперидин]-1’-іл)-21,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-4гідроксипропіл]окси}-4-гідроксифеніл)бензамід, гідрокси-N-(2-гідроксициклогексил)бензамід, трифлуорацетат, 1-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1N-(5-хлор-2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1бензофуран-2,4’-піперидин]-1’-іл)-2бензофуран-2,4’-піперидин]-1’-іл)-2гідроксипропіл]окси}-4-гідроксибензоїл)піролідин-3гідроксипропіл]окси}-4-гідроксифеніл)сечовина, карбоксамід, трифлуорацетат, трифлуорацетат, 1-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1N-(5-хлор-2-{[(2S)-3-(5-флуор-1’Н,3Н-спіро[1бензофуран-2,4’-піперидин]-1’-іл)-2бензофуран-2,4’-піперидин]-1’-іл)-2гідроксипропіл]окси}-4-гідроксибензоїл)-Lгідроксипропіл]окси)-4-гідроксифеніл)сечовина, пролінамід, трифлуорацетат, трифлуорацетат, 2-хлор-5-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1N-(5-хлор-2-{[(2S)-3-(5-флуор-1’Н,3Н-спіро[1бензофуран-2,4’-піперидин]-1’-іл)-2бензофуран-2,4’-піперидин]-1’-іл)-2гідроксипропіл]окси}-4-{[(3R)-3гідроксипропіл]окси}феніл)сечовина, (диметиламіно)піролідин-1-іл]карбоніл}фенол, N-(5-хлор-2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1біс(трифлуорацетат), бензофуран-2,4’-піперидин]-1’-іл)-22-xлop-5-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[1гідроксипропіл]окси}феніл)сечовина, бензофуран-2,4’-піперидин]-1’-іл)-2N-(2-{[(2S)-3-(5-флуор-1’Н,3Н-спіро[1гідроксипропіл]окси}-4-{[(3R)-3бензофуран-2,4’-піперидин]-1’-іл)-2(гідроксиметил)піролідин-1-іл]карбоніл}фенол, гідроксипропіл]окси}феніл)сечовина, трифлуорацетат, N-(2-{[(2S)-2-гідрокси-3-(1’Н,3Н-спіро[12-xлop-5-{[(2S)-3-(5-xлop-1’H,3H-cпipo[1бензофуран-2,4’-піперидин]-1’бензофуран-2,4’-піперидин]-1’-іл)-2іл)пропіл]окси}феніл)сечовина, гідроксипропіл]окси}-4-{[(3S)-3N-(4-флуор-2-{[(2S)-3-(5-флуор-1’Н,3Н-спіро[1(гідроксиметил)піролідин-1-іл]карбоніл}фенол, бензофуран-2,4’-піперидин]-1’-іл)-2трифлуора-цетат, гідроксипропіл]окси)феніл)сечовин, 2-хлор-5-{[(2S)-3-(5-Флуор-1’Н,3Н-спіро[1N-(4-флуор-2-{[(2S)-2-гідрокси-3-(1’Н,3Нбензофуран-2,4’-піперидин]-1’-іл)-2спіро[1-бензофуран-2,4’-піперидин]-1’гідроксипропіл]окси}-4-(піролідин-1іл)пропіл]окси}феніл)сечовина, та ілкарбоніл)фенол, трифлуорацетат, фармацевтично прийнятні солі та сольвати N-(2-{[(2R)-3-(5-флуор-1’Н,3Н-спіро[1будь-якої з них. бензофуран-2,4’-піперидин]-1’-іл)-2Представлений винахід крім того стосується гідроксипропіл]окси}-4-метоксифеніл)ацетамід, способів отриманні сполуки формули (І) або її фаМетил 2-{[(2S)-3-(5-флуор-1’Н,3Н-спіро[1рмацевтично прийнятної солі або сольвату, які бензофуран-2,4’-піперидин]-1’-іл)-2визначено вище, які залучають, гідроксипропіл]окси}бензоат, (a) реакцію сполуки формули 2-{[(2S)-3-(5-Флуор-1’Н,3Н-спіро[1бензофуран-2,4’-піперидин]-1’-іл)-2(II) гідроксипропіл]окси}бензойна кислота (гідрохлорид), (3S)-1-(2-{[(2S)-3-(5-Флуор-1’Н,3Н-спіро[1де m, R1, n, R 2, q, Χ, Υ та Ζ визначено у форбензофуран-2,4’-піперидин]-1’-іл)-2мулі (І), зі сполукою формули гідроксипропіл]окси}бензоїл)піролідин-3-ол, 3-{[(2S)-3-(5-Флуор-1’Н,3Н-спіро[1(III) бензофуран-2,4’-піперидин]-1’-іл)-2гідроксипропіл]окси}-4-(піролідин-1де R3, R4, R5, R6, R7, R 8, t та R8 визначено у ілкарбоніл)фенол, формулі (І); або N-(4-флуор-2-{[(2S)-3-(5-флуор-1’Н,3Н-спіро[1(b) реакцію сполуки формули бензофуран-2,4’-піперидин]-1’-іл)-2гідроксипропіл]окси}феніл)ацетамід, N-{5-хлор-2-[3-(5-хлор-1’Н,3Н-спіро[1(IV) бензофуран-2,4’-піперидин]-1’-іл)-2гідроксипропокси]-4гідроксифеніл}циклопентанкарбоксамід, де m, R1, n, R 2, q, Χ, Υ, Ζ, R4, R5, R6, R7 та R8 N-{5-хлор-2-(3-(5-флуор-1’Н,3Н-спіро[1визначено у формулі (І), зі сполукою формули бензофуран-2,4’-піперидин]-1’-іл)-4гідроксипропокси]-4(V) гідроксифеніл}цикпопентанкарбоксамід, N-{5-хлор-4-гідрокси-2-[2-гідрокси-3-(1’Н,3Нспіро[1-бензофуран-2,4’-піперидин]-1’де R3, t та R9 визначено у формулі (І), у присуіл)пропокси]феніл}циклопентанкарбоксамід, тності придатної основи; або (с), коли N-(5-хлор-2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1R3представляє -NHC(O)R 10, реакцію сполук форбензофуран-2,4’-піперидин]-1’-іл)-2мули гідроксипропіл]окси}-4-гідроксифеніл)бензамід, трифлуорацетат, N-(5-хлор-2-{[(2S)-3-(5-флуор-1’Н,3Н-спіро[1 33 77814 (VI) де m, R1, n, R 2, q, Χ, Υ, Ζ, R4, R5, R6, R7, R8, t та R9 визначено у формулі (І), зі сполукою формули (VII) де L1 представляє відщеплювану груп у (наприклад, гідроксигрупу або атом галогену, як-то хлор), a R 10 визначено у формулі (І); або (d), коли R3 представляє -C(O)NR11R12, реакцію сполуки формули (VIII) де L2 представляє відщеплювану груп у (наприклад, гідроксигрупу або атом галогену так як хлор), a m, R1, n, R2, q, Χ, Υ, Ζ, R4 , R5, R6 , R7, R 8, t та R9 визначено у формулі (І), зі сполукою формули (IX) NHR 11R12 де R11 та R 12 визначено у формулі (І); або (e), коли R3 представляє -NHC(O)R 10, R10 представляє -NR14R15, a R14Ta R15 представляють гідроген, реакцію сполуки формули (VI), яки визначено у (с) вище з калій ціанатом; та, як варіант, після (a), (b), (c), (d) або (e), утворення фармацевтично прийнятної солі або сольвату. Способи винаходу можна зручно проводити у розчиннику, наприклад, органічному розчиннику, як-то спирт (наприклад, метанол або етанол), вуглеводень (наприклад, толуол) або тетрагідрофуран, диметилформамід, N-метилпіролідинон або ацетонітрил при температурі, наприклад, 0°С або вище, як-то у межах від 0, 5, 10, 15 чи 20°С до 100, 110 чи 120°С. Деякі сполуки формули (II) є новими. Отже, представлений винахід крім того стосується інтермедіату формули (IIА) (IIA) де R1a вибрано з групи: флуор, хлор, метил та трифлуорметил; s дорівнює 1 або 2; q дорівнює 0 або 1; w дорівнює 0 або 1; a R 2a представляє флуор. Конкретні приклади сполук формули (IIА) залучають: 5-флуор-3Н-спіро[1-бензофуран-2,4’піперидин] ; 5-метил-3Н-спіро[1-бензофуран-2,4’піперидин] ; 5-(трифлуорметил)-3Н-спіро[1-бензофуран2,4’-піперидин] ; 5-хлор-3’-флуор-3Н-спіро[1-бензофуран-2,4’піперидин] 34 ; 5-хлор-3Н-спіро[1-бензофуран-2,3’-піролідин] Та 6-хлор-3,4-дигідроспіро[хромен-2,4’-піперидин] Інші сполуки формули (II) та сполуки формул (III), (IV), (V), (VI), (VII), (VIII) та (IX) є комерційно доступними, відомими з літератури, або їх можна отримати, застосовуючи відомі способи. Наприклад, сполуки формули (II), в яких m дорівнює 1, R1 є хлор або флуор, n дорівнює 0, q дорівнює І, одне з X та Υ представляє зв’язок, а інше з X та Υ представляє атом оксигену, а Ζ представляє СН 2, можна отримати згідно зі схемами реакцій, в яких ДМФ означає диметилформамід, ЕtOН означає етанол, ДМЕ означає 1,2диметоксіетан, і-Рr означає ізопропіл, ТГФ означає тетрагідрофуран, KOtBu означає калій третбутоксид, а НОАс означає оцтову кислоту: 35 77814 36 Шляхи способу (С), (D) та (Н) вище є новими. Отже, представлений винахід крім того стосується способу отримання сполук формули (ПА), які визначено вище, в яких s дорівнює 1, який залучає реакцію сполуки формули Сполуки формули (II), в яких m дорівнює 1, R 1хлор, n дорівнює 0, q дорівнює І, X представляє СН2, Υ представляє атом оксигену, a Z представляє зв’язок, можна отримати згідно зі схемами реакцій, в яких ТГФ означає тетрагідрофуран: (XX) де L1 представляє придатну відщеплювану груп у (наприклад, електроно-акцепторну груп у, якто 2 атом галогену) або алкокси, особливо метокси, груп, L2 представляє придатну відщеплювану груп у, як-то атом галогену, a R1a визначено у формулі (IIА), зі сполукою формули (XXII) де R20 представляє захисну груп у, як-то бензил або група -C(O)-O-R21, в якій R21 представляє алкіл (наприклад, С1-С6алкіл, особливо третбутил) або арил (наприклад, Феніл), a q, w та R2a визначено у формулі (IIА), з утворенням сполуки формули (XXIV) Сполуки формули (II), в як m дорівнює 1, R1хлор, n дорівнює 0, q дорівнює 0, одне з X та Υ представляє зв’язок та інше з X та Υ представляє атом оксигену та Ζ представляє СН 2, можна отримати згідно зі схемою реакцій, в якій ДМФ означає димети-лформамід та EtOH означає етанол: (G) Сполуки формули (II), в як m дорівнює 1, R1метил, n дорівнює 0, q дорівнює 1, одне з X та Υ представляє зв’язок та інше з X та Υ представляє атом оксигену та Ζ представляє СН 2, можна отримати згідно зі схемою реакцій, в як ДМСО означає диметилсульфоксид: потім реакцію циклізації, а потім видалення захисної групи R20. Фахівцям зрозуміло, що у способах представленого винаходу деякі функціональні групи, як-то гідроксил або аміногрупа у реактивах, можуть потребувати захисту захисними групами. Отже, отримання сполук формули (І) може залучати, на прийнятному етапі, видалення одної або більше захисних гр уп. Захист та зняття захисту з функціональних груп [описано у ‘Protective Group in Organic Chemistry’, J.W.F. McOmie, Plenum Press (1973) та ‘Protective Group in Organic Synthesis’, T.W. Greene та P.G.M. Wuts, Wiley-lnterscience (1999)]. Сполуки формули (І) можна перетворити у їх фармацевтично прийнятні солі або сольвати, переважно кислотно-адитивні солі, як-то гідрохлорид, гідробромід, фосфат, ацетат, фумарат, малеат, тартрат, цитрат, оксалат, метансульфонат або п-толуолсуль фонат. Сполуки формули (І) можуть існувати у стереоізомерних формах. Зрозуміло, що винахід залучає застосування усіх геометричних та оптичних ізомерів (залучаючи атропізомери) сполук формули (І) та їх суміші, залучаючи рацемати. Застосування таутомерів та їх сумішей також утворюють аспект представленого винаходу. Енантіомерно чисті форми є особливо потрібними. Сполуки формули (І) мають активність як фа 37 77814 38 рмацевтичні, зокрема, як активність модуляторів прийнятних солей або сольватів, які визначено рецептору хемокіну (особливо рецептору хемокіну вище, для застосування у терапії. Згідно з наступним аспектом, представлений МІР-1a), та їх можна використовувати у лікуванні винахід стосується застосування сполук формули аутоімунних, запальних, проліферативних та гі(І), або прийнятних солей або сольватів, які визнаперпроліферативних хвороб та імунологічночено вище, у виробництві медикаменту для застоопосередкованих хвороб, залучаючи хворобу відсування у терапії. торгнення трансплантованих органів або тканин та синдром набутого імунодефіциту (СНІД). У контексті представленого опису, термін "терапія" також залучає "профілактику" якщо не виПрикладами цих станів є: значено інше. Терміни "терапевтичний" та "тера(1) (респіраторний тракт) хвороби дихальних певтично" визначено відповідно. шляхів, залучаючи хронічну обструктивну хворобу Винахід також стосується способу лікування легенів (ХОХЛ), як-то необоротну ХОХЛ; астму, якто бронхіальну, алергічну, притаманну, набуту та запальних хвороб, який залучає застосування до пацієнта, що цього потребує, терапевтично ефекпилову астму, особливо хронічну або застарілу тивної кількості сполуки формули (І), або її фарастму (наприклад, пізня астма та гіперреактивність мацевтично прийнятної солі або сольвату, які видихальних шляхів); бронхіт; гострий, алергічний, значено вище. атрофічний риніт та хронічний риніт, залучаючи хронічний риніт з утворенням казеозних мас, гіперВинахід крім того стосується способу лікування хвороби дихальних шляхів, як залучає застосутрофічний риніт, риніт гнійний, сухий риніт та мевання до пацієнта, що цього потребує, терапевтидикаментозний риніт; мембранний риніт, залучаючно ефективної кількості сполуки формули (І), або чи крупозний, фібринозний та псевдомембранний її фармацевтично прийнятної солі або сольвату, риніт та золотушний риніт; сезонний риніт, залучаючи анафілактичний риніт (сінна лихоманка) та які визначено вище. Для вищезгаданих терапевтичних застосувань вазомоторний риніт; саркоїдоз, легені фермера та дозування безумовно варіюватиме із застосоваспоріднені хвороби, фіброїдні легені та ідіопатичну ною сполукою, способом застосування, потрібним інтерсти-ціальну пневмонію; лікуванням та визначеним розладом. На добу до(2) (кістки та суглоби) ревматоїдний артрит, серонегативні спондилоартропатії (залучаючи анзування сполуки формули (І) може бути у межах від 0,001мг/кг до 30мг/кг. кілозний спондиліт, псоріатичний артрит та хвороСполуки формули (І) та їх фармацевтично ба Рейтера), хвороба Бекхета, сухий синдром, прийнятні солі та сольвати можна використовуваксеродерматоз та системний склероз; ти як такі, але звичайно їх застосовуватимуть у (3) (шкіра) псоріаз, атопічний дерматит, контактний дерматит та інші екзематозні дермітиди, формі фармацевтичної композиції, в якій сполука/сіль/сольват формули (І) (активний інгредієнт) є себорейний дерматит, пемфігоїдний плоский лив асоціації з фармацевтично прийнятним шай, пухирчатка, булезна пухирчатка, булезний ад’ювантом, розріджувачем та/або носієм. Залежепідермоліз, кропивниця, ангіодерміт, васкуліт, но від режиму застосування, фармацевтична комеритема, шкірні еозинофілії, увеїти, плішивість та весняний кон’юнктивіт; позиція переважно міститиме від 0,05 до 99мас.%, більше переважно від 0,05 до 80мас.%, краще від (шлунково-кишковий тракт) черевно0,10 до 70мас.%, та найкраще від 0,10 до порожнинна хвороба, проктит, еозинофільний гас50мас.%, активного інгредієнту. тро-ентерит, мастоцитоз, хвороба Крона, виразкоПредставлений винахід також стосується фавий коліт, споріднені з їжею алергії, на які впливає харчовий тракт, наприклад, мігрень, риніт та екрмацевтичної композиції, що містить сполуку формули (І), або її фармацевтично прийнятну сіль зема; або сольват їх, які визначено вище, в асоціації з (5) (інші тканини та системні хвороб) розсіяний фармацевтично прийнятним ад’ювантом, розрісклероз, атеросклероз, синдром набутого імуноджувачем та/або носієм. дефіциту (СНІД), червоний вовчак, системний вовчак, еритематоз, тіроїдит Хашимото, важка міастеВинахід крім того стосується способів отриманні фармацевтичної композиції винаходу, який нія, діабет типу І, невротичний синдром, залучає змішування сполуки формули (І), або її еозинофільний фасцит, синдром гіпер ІgЕ, лепра, фармацевтично прийнятної солі чи сольват, які ретикулярна еритродермія та ідіопатична тромбовизначено вище, з фармацевтично прийнятним цитопенічна пурпура; (6) (відторгнення алотрансплантату) гостре та ад’ювантом, розріджувачем та/або носієм. Фармацевтичні композиції можна застосовувахронічне після, наприклад, трансплантації нирок, ти місцево (наприклад, до шкіри або до легенів серця, печінки, легенів, кісткового мозку, шкіри та та/або дихальних шляхів) у формі, наприклад, роговиці; та хронічна хвороба трансплантат проти кремів, розчинів, суспензій, гептафлуоралканових хазяїна; (7) рак, особливо рак немалих клітин легенів аерозолів та сухи х порошкових композицій; або системно, наприклад, пероральним застосуванням (РНМКЛ) та сквамозна саркома; у формі таблеток, капсул, сиропів, порошків або (8) хвороби, в яких ангіогенез асоційований зі гранул; або парентеральним застосуванням у фозбільшеними рівнями хемокіну; та рмі розчинів або суспензій; або підшкірним засто(9) кістозний фіброз, інсульт, реперфузійні ушкодження серця, мозку, периферійних кінцівок суванням; або ректальним застосуванням у формі супозиторіїв; або трансдермально. та сепсис. Винахід ілюстровано наступними необмежуОтже, представлений винахід стосується сповальними прикладами, в яких спектри 1Н ЯМР лук формули (І), або їх фармацевтично 39 77814 40 отримують на Varian Unity Inova 400. Центральний натрій гідрокарбонату (250мл), комбінують, сушать пік розчиннику хлороформ-d3 (δн 7,27млн -1), ацебезводним магній сульфатом, фільтрують та витон-d6 (δн 2,05млн-1), ДМСО-d6 (δΗ 2,50млн-1), або парюють під зменшеним тиском. Залишкове масло метанол- d4 (δн 4,87млн-1) використовують як внутспіввипарюють з толуолом (100мл) з утворенням рішній стандарт. Мас-спектри низького розділення названої сполуки (43,25 г, 81 %), як твердого прота з точним визначенням мас отримують на сисдукту. 1Н-ЯМР (400МГц, CDCI3): δ 1,46 (9Н, s), темі Hewlett-Packard 1100 РХ-МС з іонізаційними 1,43-1,48 (2Н, m), 1,75-1,84 (2Н, m), 2,69 (2Н, s), камерами APCI/ESI. Усі розчинники та покупні реа3,38-3,47 (2Н, m), 3,70-3,75 (2Н, m). ктиви мають лабораторний ґатунок та їх викорис(іі) 5-хлорспіро[1-бензофуран-2,4’-піперидин]товують, як звичайно. Назви сполук створено за 1’-карбонова кислота, 1,1-диметиловий естер ACD/IUPAC Name Pro. Скорочення або терміни у Розчин ізо-пропілмагній хлориду у тетрагідроприкладах мають такі значення: фурані (2М, 106,6мл) додають краплями протягом BuLi бутиллітій 15 хвилин при перемішуванні до розчину 2-бром-4ДХМ ди хлорметан хлор-1-флуорбензолу (42,5g) у безводному тетраDEAD діетилазодикарбоксилат гідрофурані (250мл) при 0°С під азотом. Ще через ДМАП 4-диметиламінопіридин 15 хвилин розчин 1-окса-6-азаспіро[2,5]октан-6ДМЕ 1,2-диметоксіетан карбонової кислоти, 1,1-диметилетиловий естер ДМФ Ν,Ν-диметилформамід (43,2г) додають у безводний тетрагідрофуран ДМСО диметилсульфоксид (50мл) а потім комплекс купрум(І) броEtgO діетиловий етер мід/диметилсульфід (0,4г). Суміш перемішують ЕtOАс етилацетат при 40°С протягом 18 годин, охолоджують до ЕtOН етанол 20°С, розводять водою (300мл) та екстрагують НОАс оцтова кислота трет-бутилметиловим етером (2´300мл). Органічні KotBu калій трет-бутоксид екстракти сушать безводним магній сульфатом, MeCN ацетонітрил фільтрують та випарюють під зменшеним тиском. МеОН метанол Залишкове масло розчиняють у 1,2ΝΜΠ 1-метил-2-піролідинон диметоксипропан (200мл). Калій трет-бутоксид TEA триетиламін (22,8г) додають та суміш перемішують при 40°С ТФОК трифлуороцтова кислота протягом 16 годин тоді при 50°С протягом 24 гоТГФ тетрагідрофуран дин. Ще додають калій трет-бутоксид (5,7г) та пеTMSCl хлортриметилсилан ремішування продовжують при 50°С протягом 2 SELECTFLUOR™ флуор увальний реагент (Alгодин, тоді при 55°С протягом 4 годин. Додають drich) воду (500мл) та суміш екстрагують третХімічна назва: [1-(хлорметил)-4-флуор-1,4бутилметиловим етером (2´300мл). Органічні ексдіазонійдицикло[2,2,2]октан біс(тетрафлуорборат)] тракти сушать безводним магній сульфатом, фільPS-Карбодіімід: прищеплений на смолу засіб трують та випарюють під зменшеним тиском з сполучення утворенням названої сполуки (47,45г, 67%), як Хімічна назва: N-циклогексилкарбодіімід-N’масла. 1Н-ЯМР (400МГц, CDCI3): δ 3,47 (9Н, s), пропілоксиметил полістирол 1,67 (2Н, td), 1,85-1,93 (2Н, m), 2,94 (2Н, s), 3,39 Приклади (2Н, td), 3,65-3,80 (2Н, m), 6,67 (1Н, d), 7,06 (1Н, d), Інтермедіат; 5-хлор-3Н-спіро[1-бензофуран7,10 (1H,s). 2,4’-піперидин] ііі) 5-хлорспіро[1-бензофуран-2,4’-піперидин] Спосіб А: Цю сполуку отримують, [як описано Концентровану гідрохлоридну кислоту (23мл) Effland, R. С; Gardner, В. A; Strupczewski, J., J. Hetдодають до розчину 5-хлорспіро[1-бензофуранerocyclic Chem., 1981,18,811-814]. 2,4’-піперидин]-1’-карбонової кислоти, 1,1диметилового естеру (46,43г) у тетрагідрофурані (230мл). Суміш перемішують при 50°С протягом 6 годин, охолоджують до 20°С, розводять водою (230мл) та екстрагують трет-бутилметиловим етером (2´230мл). Водну фазу підганяють до рН>10 додаванням 50% розчину натрій гідроксиду та екстрагують трет-бутилметиловим етером (3´300мл). Органічні екстракти сушать безводним магній суі) 1-окса-6-азаспіро[2,5]оістан-6-карбонова кильфатом, фільтрують та випарюють під зменшеслота, 1,1-диметилетиловий естер ним тиском. Залишкове масло розчиняють у тетраКалій трет-бутоксид (31г) додають при перегідрофурані (240мл), додають концентровану мішуванні до суспензії три мети л сул ь-фоксоній гідрохлоридну кислоту (12мл) та суміш перемішуйодиду (60,8г) у 1,2-диметоксіетані (250мл) при ють при 20°С протягом 16 годин. Осаджений твер20°С. Через 1 годину суміш додають порціями дий продукт фільтрують та розчиняють у воді протягом 30 хвилин при перемішуванні до розчину (100мл). Розчин підганяють до рН>10 додаванням 4-оксо-1-піперидинкарбонової кислоти, 1,150% розчину натрій гідроксиду та екстрагують диметилетилового естеру, (50г) у 1,2трет-бутилметиловим етером (3´100мл) з утводиметоксіетані (50мл) при 0°С. Ще через 2 години ренням названої сполуки (13,3г, 45%), як твердого додають воду (500мл) та суміш екстрагують третпродукту. 1 бутилметиловим етером (2´500мл). Органічні ексН-ЯМР (400МГц, CDCI3): δ 1,69-1,76 (2Н, m), тракти промивають окремо насиченим розчином 1,83-1,87 (2Н, m), 2,78-2,84 (2Н, m), 2,98-3,03 (4Н, 41 77814 42 m), 6,65 (1Н, d), 7,04 (1Н, d), 7,13 (1Н, s). ХІАТ-МС: (800мг, КОН у 0,8мл Н2О) та реакційну суміш пеm/z 224/6 [М+Н]+ ремішують при температурі кипіння під зворотним Інтермедіат: 5-Флуор-3Н-спіро[1-бензофуранхолодильником протягом ночі, охолоджують до 2,4’-піперидин] кімнатної температури, етанол видаляють у вакуСпосіб А: умі. Водний шар екстрагують Еt2О, комбінований і) 1’-Бензил-5-флуор-3Н-спіро[1-бензофуранетерний шар промивають 3Η водною НСІ. Комбі2,4’-піперидин] нований водний шар доводять до рН10 додаванПри перемішуванні до суспензії ошурків магням водного NaOH. Основний розчин екстрагують нію (763мг) у діетиловому етері (7мл) додають етилацетатом. Комбінований органічний шар прокристал йоду а потім (0,4мл 2-(бромметил)-1,4мивають водою, сушать натрій сульфатом, фільтдифлуорбензолу під азотом. Реакційну суміш грірують та концентрують. Залишок очищають за ють потужним феном, повільно додають 2допомогою ВЕРХ (10-55% CH3CN у воді, 0,1% (бромметил)-1,4-дифлуорбензол 5,0г, 24,25ммоль) амоній гідроксиду), отримуючи названу сполуку у діетиловому етері (7мл), підтримуючи слабке (49мг). 1 кипіння під зворотним холодильником. Після завеН-ЯМР (CD3OD, 400МГц): δ 6,92-6,87 (m, 1H); ршення додавання реакційну суміш перемішують 6,81-6,75 (m, 1H); 6,64 (dd, J=4,2, 8,7Гц, 1H); 3,08при кипінні під зворотним холодильником протягом 2,98 (m, 4H); 2,89-2,81 (m, 2H); 1,91-1,83 (m, 2H); 100 хвилин, охолоджують до кімнатної температу1,78-1,71 (m, 2H). XIAT-MC: m/z 208 (MH +). ри. До цієї реакційної суміші додають краплями з інтенсивним перемішуванням розчин 1бензилпіперидин-4-он (4,57г, 24,25ммоль) у діетиловому етері (12мл). Після завершення додавання реакційну суміш залишають при кімнатній температурі протягом ночі. Водний розчин хлориду амонію додають та перемішують при кімнатній темпе(і) 4-{(5-Флуор-2-метоксифеніл)метил)-4ратурі до завершення гідролізу та екстрагують гідрокси-1-піперидинскарбонова кислота, 1,1діетиловим етером. Органічний шар промивають диметилетиловий естер. водою, сушать натрій сульфатом) фільтрують та Розчин ізо-пропілмагній хлориду у тетрагідроконцентрують у вакуумі. Залишок очищають фурані (2М, 130мл) додають краплями протягом флеш-хроматографією на силікагелі (0-1% мета30 хвилин при перемішуванні до розчину 2-бром-4нолу у ди хлорметані, 0,2% амоній гідроксиду) з флуоранізолу (34,2мл) у безводному тетрагідроутворенням інтермедіату 1-бензил-4-{2,5фурані (400мл) при 30°С під азотом. Ще через 16 дифлуорбензил)піперидин-4-ол (2,74г), що містить годин при 30°С, комплекс купрум(І) бровелику кількість невідомих забруднень. У суспенмід/диметилсульфід (0,4г) додають а потім розчин зію NaH (55% 1,12г, 26,0ммоль) у толуолі (10мл) 1-окса-6-азаспіро[2,5]октан-6-карбонової кислоти, повільно додають розчин 1-бензил-4-(2,51,1-диметилетилового естеру (56,2г) у безводному дифлуорбензил)піперидин-4-олу у толуолі (15мл). тетрагідрофурані (110мл). Ще через 3 годин при Після завершення додавання реакційну суміш пе30°С розчин охолоджують до 20°С, розводять воремішують при 110°С (у попередньо нагрітій масдою (600мл) та екстрагують трет-бутилметиловим ляній бані), після 5 хвилин додають ДМФ (9мл) та етером (600мл) тоді етилацетатом (600мл). Комбіперемішування продовжують при кипінні під звоновані органічні екстракти сушать безводним магротним холодильником температур протягом 2 ній сульфатом, фільтрують та випарюють під змегодин. Реакційну суміш охолоджують до кімнатної ншеним тиском з утворенням сирої названої температури, Воду (20мл) додають та екстрагують сполуки (86г), як твердого продукту. ХІАТ-МС: m/z етилацетатом. Органічний шар сушать натрій су240 [М+Н-(СН3)2ССН2СО2]+ льфатом, фільтрують та концентрують. Залишок (іі) 5-Флуорспіро[1-бензофуран-2,4’-піперидин] очищають флеш-хроматографією на силікагелі (0гідрохлорид 1,5% метанолу у ди хлорметані, 0,2% амоній гідроГідробромідну кислоту (48%, 60мл) додають ксиду), отримуючи названу сполуку (190мг). 1 до розчину сирої 4-{(5-Флуор-2Н-ЯМР (CDCI3, 400МГц): δ 7,39-7,26 (m, 5H); метоксифеніл)метил]-4-гідрокси-16,88-6,76 (m, 2H); 6,67 (dd, J=4,2, 8,7Гц, 1H); 3,59 піперидинкарбоноеої кислоти, 1,1(s, 2H); 2,99 (s, 2H); 2,68-2,47 (m, 4H); 2,03-1,94 (m, диметилетилового естеру в оцтовій кислоті 2H); 1,86-1,76 (m, 2H). XIAT-MC: m/z 298 (MH +). (300мл). Суміш гріють при кипінні під зворотним (ii) 5-Флуор-3Н-спіро[1-бензофуран-2,4’холодильником протягом 5 годин. Ще додають піперидин] гідробромідну кислоту (48%, 60мл) та кипіння під Етилхлорформіат (65,6мг, 0,604ммоль) додазворотним холодильником продовжують протягом ють до розчину 1’-бензил-5-флуор-3Н-спіро[124 годин. Суміш охолоджують до кімнатної темпебензофуран-2,4’-піперидину] (150мг, 0,504ммоль) ратури, додають до води (2л) та екстрагують трету толуолі (2мл) та реакційну суміш кип’ятять під бутилметиловим етером (2´500мл). Водну фазу зворотним холодильником протягом ночі. Реакційпідганяють до рН>10 додаванням 50% розчину ну суміш о холоджують до кімнатної температури, натрій гідроксиду та екстрагують третрозводять додаванням толуолу, промивають побутилметиловим етером (2л+1л). Органічні екстслідовно водним натрій гідрокарбонатом та водою. ракти сушать безводним магній сульфатом, фільтОрганічний шар сушать натрій сульфатом, фільтрують та випарюють під зменшеним тиском. Зарують та концентрують у вакуумі. Залишок розчилишкове масло розчиняють у ι тетрагідрофурані няють в етанолі (3,5мл), додають водний КОН 43 77814 44 (200мл), додають концентровану гідрохлоридну водн. NaOH. Суміш екстрагують етилацетатом (2 χ кислоту (13мл) та розчин випарюють під зменше25мл) та комбіновані органічні екстракти сушать ним тиском. Залишковий твердий продукт кристанатрій сульфатом. Випарювання розчиннику дає лізують з суміші тет-рагідрофуран/треткоричнювате масло. ХІАТ-МС: m/z 314 [M+H]+ бутилметиловий етер (4:1, 500мл), отримуючи (ііі) 1’-бензил-5-метил-3Н-спіро[1-бензофуранназвану сполуку (20,0г, ви хід від загального 31%). 2,4’-піперидин] 1 Н-ЯМР (CD3OD, 400МГц): δ 1,86-1,98 (2Н, m), У суспензію NaH (55% у мінеральному маслі, 2,03-2,07 (2Н, m), 3,05 (2Н, s), 3,16-3,27 (4Н, m), 200мг, 5ммоль) у толуолі (10мл) повільно додають 6,61 (1 Η, dd), 6,74 (1 Η, dt), 6,81 (1 Η, dd). XIATрозчин сирого 1-бензил-4-(2-флуор-5MC: m/z 208 [М+Н]+ метилбензил)піперидин-4-олу у толуолі (15мл). Інтермедіат: 3Н-спіро[1-бензофуран-2,4’Після завершення додавання реакційну суміш гріпіперидин] ють до 110°С та перемішують протягом 5 хвилин. Цю сполуку отримують, [як описано Effland, ДМФ (9мл) додають та перемішування продовжуR.С; Gardner, В. A; Strupczewski, L, J. Heterocyclic ють при температурі кипіння під зворотним холоChem., 1981,18, 811-814]. дильником протягом 10 годин. Реакційну суміш Інтермедіат: 5-Метил-3Н-спіро[1-бензофуранохолоджують до кімнатної температури, вилива2,4’-піперидин] ють у воду (50мл) та екстрагують етилацетатом (і) 6-бензил-1-окса-6-азаспіро[2,5]октан (2´25мл). Органічний шар сушать натрій сульфатом, фільтрують та концентрують. Залишок очищають флеш-хроматографією на силікагелі (етилацетат/н-гептан), отримуючи названу сполуку (240мг, 41%). 1Н-ЯМР (CDCI3, 400МГц): δ 7,2-7,4 (m, 5H); 6,8-6,9 (m, 2H); 6,64 (d, J=10,8Гц, 1Η), 3,54 (s, 2H); 2,91 (s, 2H); 2,4-2,7 (m, 4H); 2,24 (s, ЗН); 1,92 (m, 2H); 1,78 (m, 2H). XIAT-MC: m/z 294 [M+H]+ (iv) 5-метил-3Н-спіро[1-бензофуран-2,4’піперидин] Натрій гідрид (55% суспензію у мінеральному До розчину 1’-бензил-5-метил-3Н-спіро[1маслі, 1,57г, 35ммоль) промивають гептаном, субензофуран-2,4’-піперидину] (0,12г, 0,41мол) у шать струмом азоту та суспендують у сухому дихлорметані (3мл) додають 1ДМСО (10мл). Розчин триметилсульфоксоній йохлоретилхлорформіат (87мг, 0,61ммоль). Розчин диду (4,8г, 22ммоль) у ДМСО (45мл) додають краперемішують при кімнатній температурі протягом плями під азотом. Піcля перемішування протягом ночі. Розчинник видаляють у вакуумі. Залишок 20 хвилин додають краплями розчин 1розчиняють у метанолі (3мл) та розчин гріють при бензилпіперидин-4-ону (3,78г, 20ммоль). Суміш 70°С протягом 2 годин. Розчинник випарюють та перемішують протягом ночі при кімнатній темперазалишок обробляють діетиловим етером. Утворетурі, тоді виливають поверх льоду (200г), та екстний осад збирають фільтруванням, промивають рагують дихлорметаном (2´200мл). Комбіновані діетиловим етером та розчиняють у метанолі екстракти промивають водою (3´100мл) та сушать (1мл). Воду (25мл) додають та рН підганяють до натрій сульфатом. Розчинник видаляють у вакуумі. 10 додаванням 2Μ водн. NaOH. Суміш екстрагуЗалишок розчиняють у діетиловому етері, та неють дихлорметаном (2´25мл) та комбіновані оргарозчинний матеріал видаляють фільтруванням. нічні екстракти сушать натрій сульфатом. ВипарюВипарювання розчиннику дає блідо-жовте масло вання розчиннику дає коричнювате масло (64мг, (2,95г, 73%). 1Н-ЯМР (CDCl3) 400МГц): δ 7,2-7,4 (m, 77%). 5H); 3,57 (s, 2H); 2,5-2,7 (m, 4H); 1,85 (m, 2H); 1,55 1 Н-ЯМР(СОСІ3 , 400МГц) δ 6,95 (s, m); 6,90 (d, (m, 2H). J=8Гц, 1Η); 6,64 (d, J=8Гц, 1Н); 3,11 (m, 2H); 2,95 (ii) 1-бензил-4-(2-флуор-5(s, 2H); 2,85 (m, 2H); 2,26 (s ; 3H); 1,88 (m, 2H); 1,72 метилбензил)піперидин-4-ол (m, 2H). XIAT-МC: m/z 204 [M+H]+ До розчину 2-бром-1-флуор-4-метилбензолу Інтермедіат: 5-(трифлуорметил]-3Н-спіро[1(0,76г, 4ммоль) у ТГФ (15мл) при -70°С під аргоном бензофуран-2,4’-піперидин] розчин н-BuLi (1,6Μ у гексан, 2,5мл, 4ммоль) до(і) 1-бензил-4-{2-флуор-5дають краплями. Реакційну суміш перемішують {трифлуорметил)бензил]піперидин-4-ол при -70°С протягом 1 годин, тоді BF3 Et2O (0,5мл, При перемішуванні до суспензії ошурків маг4ммоль) додають. Після перемішування протягом нію (308мг) у Еt 2О (5мл) додають кристал йоду а 20 хвилин при -70°С додають краплями розчин 6потім 0,3мл 2-(бромметил)-1-флуор-4бензил-1-окса-6-азаспіро[2,5]октану (0,41г, (трифлуорметил)бензолу під аргоном. Реакційну 2ммоль) у сухому ТГФ (5мл). Перемішування просуміш гріють потужним феном, тоді повільно додовжують протягом 2 годин при -70°С, тоді реакдають 2-(бромметил)-1-флуор-4ційну суміш гасять насиченим водним амоній хло(трифлуорметил)бензол (2,5г, 9,73ммоль) у Et2O ридом (20мл), шари відокремлюють, водний шар (5мл) (підтримуючи кипіння під зворотним холодиекстрагують ТГФ. Комбіновані органічні шари сульником). Після завершення додавання реакційну шать натрій сульфатом. Розчинник видаляють у суміш кип’ятять під зворотним холодильником вакуумі. Діетиловий етер (50мл) додають до залипротягом 50 хвилин, охолоджують до кімнатної шку, а потім 2Μ НСІ у Et2O (5мл). Осад збирають, температури. Розчин 1-бензилпіперидин-4-ону промивають Et2O та розчиняють у мінімальному (1,84г, 9,73ммоль) у Et2O (10мл) додають повільно об’ємі метанолу (приблизно. 5мл). Воду (50мл) з інтенсивним перемішуванням. Після завершення додають та рН доводять до 10 додаванням 2Μ 45 77814 46 додавання реакційну суміш залишають при кімнатній температурі протягом 50 хвилин, додають насичений водний розчин хлориду амонію та перемішують при кімнатній температурі до закінчення гідролізу, екстрагують етилацетатом. Комбінований органічний шар промивають водою, сушать натрій сульфатом, фільтрують та концентрують. Залишок очищають флеш-хроматографією на силікагелі (0-1% метанолу у ди хлорметані, 0,2% амоній гідроксиду), отримуючи названу сполуку (і) трет-бутил 4-((триметилсиліл)окси]-3,6(720мг). ХІАТ-МС: m/z 368 (МН+). дигідропіридин-1 (2Н)-карбоксилат (іі) 1’-бензил-5-(трифлуорметил)-3Н-спіро[1До розчину трет-бутил 4-оксопіперидин-1бензофуран-2,4’-піперидин] карбоксилату (10,13г, 50,84ммоль) у ДМФ під арУ суспензію NaH (55%) (127мг, 2,91ммоль) у гоном додають TMSCI (7,74мл, 61,27ммоль), а толуолі (4мл) повільно додають розчин 1-бензилпотім Et3N (17мл). Суміш перемішують при 80°С 4-[2-флуор-5-(трифлуорметил)бензил]піперидинупротягом ночі. Розчин охолоджують до температу4 (715мг, 1,94ммоль) у толуолі (5мл) при кімнатній ри довкілля, а потім розводять гептаном, промитемпературі. Після завершення додавання реаквають концентрованим водним натрій гідрокарбоційну суміш перемішують при 110°С протягом 5 натом та водою. Органічний шар тоді сушать хвилин, тоді додають ДМФ (3мл) та реакційну сунатрій сульфатом, фільтрують та концентрують. міш перемішують при температурі кипіння під звоХроматографічна очистка на силікагелі ротним холодильником протягом 40 хвилин, охо(EtOAc/петролейний ефір 40-60 1:9) дає 9,6г (69%) лоджують до кімнатної температури, додають Н 2О масла, яке отверджується при стоянні. 1 (3мл), екстрагують етилацетатом. Органічний шар Н-ЯМР (CDCI3, 300МГц): δ 4,79 (m, 1H); 3,87 сушать натрій сульфатом, фільтрують та концент(m, 2H); 3,52 (t, J=5,8Гц, 2Н); 2,11 (m, 2H); 1,47 (s, рують. Залишок очищають флеш-хроматографією 9H); 0,19 (s, 9H). XIAT-MC: m/z 272 (M+H)+. на силікагелі (0-1% метанолу у дихлорметані, 0,2% (ii) трет-бутил 3-флуор-4-оксопіперидин-1амоній гідроксиду), отримуючи названу сполуку карбоксилат 1 (380 мг). Н-ЯМР (CDCI3, 400МГц): δ 7,45-7,23 (m, До розчину трет-бутил 46H); 6,82 (d, J=9,0Гц, 1H); 3,60 (s, 2H); 3,02 (s, 2H); [(триметилсиліл)окси]-3,6-дигідропіридин-1(2Н)2,70-2,45 (m, 4H); 2,00 (m, 2H); 1,85 (m, 2H). XIATкарбоксилату (9,52г, 35,07ммоль) у CH3CN під арMC: m/z 348 (MH +). гоном додають флуорувальний реагент (13,7г, (iii) 5-(Трифлуорметил)-3Н-спіро[138,6ммоль) та перемішують при кімнатній темпебензофуран-2,4’-піперидин] ратурі протягом 2 годин. Реакційну суміш розвоДо розчину 1’-бензил-5-(трифлуорметил)-3Ндять ЕtOАс (1000мл), промивають розведеним спіро[1-бензофуран-2,4’-піперидину] (280мг, розсолом, водою, сушать натрій сульфатом, філь0,806ммоль) у толуолі (3мл) додають етилхлортрують та концентрують у вакуумі. Хроматографіформіат (0,093мл, 0,967ммоль) та реакційну суміш чна очистка на силікагелі (МеОН:ЕtOАс, від 0:1 до перемішують при температурі кипіння під зворот2:98) дає 5,35г (70%) масла, яке стверджується ним холодильником протягом ночі, охолоджують при стоянні. 1 до кімнатної температури, розбавляють додаванН-ЯМР (CDCl3, 300МГц): δ 4,73-4,94 (m, 1H), ням толуолу та промивають водним натрій гідро4,14-4,23 (m, 2H), 3,30-3,20 (m, 2H) 2,49-2,66 (m, карбонатом та водою послідовно. Органічний шар 2H), 1,50 (s, 9H) XIAT-MC: m/z 218 (M+H)+ сушать натрій сульфатом, фільтрують та концент(iii) трет-бутил 4-(5-хлор-2-флуорбензил)-3рують. Залишок розчиняють в етанолі ((4мл), дофлуор-4-гідроксипіперидин-1-карбоксилат дають водний КОН (1,14г КОН у 1,2мл води) та До ошурків магнію, покритих етером додають реакційну суміш кип’ятять під зворотним холодиневелику кількість розчину 2-(бромметил)-4-хлорльником протягом ночі, охолоджують до кімнатної 1-флуорбензолу у діетиловому етері та реакційну температури, етанол видаляють у вакуумі. Водний суміш гріють потужним феном. До суміші при кишар екстрагують етером, комбінований етерний пінні під зворотним холодильником додають крапшар промивають 3Η водною НСІ. Комбінований лями залишковий розчин (150мл), підтримуючи кислотний шар доводять до рН10 додаванням вокипіння під зворотним холодильником. Після додного NaOH. Основний розчин екстрагують етиладавання усього розчину суміш перемішують до цетатом. Комбінований органічний шар промиваприпинення кипіння під зворотним холодильником. ють водою, суша ть натрій сульфатом, фільтр ують Розчин трет-бутил 3-флуор-4-оксопіперидин-1та концентрують. Залишок очищають флешкарбоксилату у діетилетері (50мл) додають повіхроматографією на силікагелі (0-2% метанолу у льно. Утворену суміш перемішують протягом ще 4 дихлорметані, 0,2% амоній гідроксиду), отримуючи с при кімнатній температурі., тоді гасять повільним 1 названу сполуку (156мг). Н-ЯМР (CD3OD, додаванням насиченого водного амоній хлориду 400МГц): δ 7,29 (s, 1H); 7,39 (d, J=8,4Гц, 1H); 6,82 (125т), екстрагують ЕtOАс (2´150мл), промивають (d, J=8,4Гц, 1Η); 3,10-3,00 (m, 4H); 2,89-2,81 (m, розсолом, водою, сушать натрій сульфатом, філь2H); 1,94-1,86 (m, 2H); 1,82-1,74 (m, 2H). XIAT-MC: трують та концентрують. Утворений залишок очиm/z 258 (MH +). щають на силікагелі (гептан-ефір 4:1-3:1) з утвоІнтермедіат: 5-хлор-3’-флуор-3Н-спіро[1ренням 1,61г (18%) названої сполуки. 1Н-ЯМР бензофуран-2,4’-піперидин] (CDCI3, 300МГц): δ 6,74 (s, 1H), 7,15 (s, 1H), 7,107,14 (m, 1H), 4,85-5,02 (m, 1H), 3,78-3,88 (m, 2H), 47 77814 48 3,50 (m, 2H) 2,74 (s, 2H), 1,63 -1,67 (m, 2H), 1,44 (s, на льоду, гасять сумішшю вода/натрій гідроксид 9H) XIAT-MC: m/z 362 (M+H)+ (10%) та перемішують при кімнатній температурі (iv) трет-бутил 5-хлор-3’-флуор-1’Н,3Н-спіро[1протягом 1 годин. Тверду речовину відфільтровубензофуран-2,4’-піперидин]-1’-карбоксилат ють та органічний шар сушать натрій сульфатом, У суспензію NaH (60% у мінеральному маслі, фільтрують та концентрують. Сирий матеріал 1,38г, 4,35ммоль) у бензолі (30мл) додають розчин очищають на оксиді силіцію (дихлорметан/етанол) трет-бутил 4-(5-хлор-2-флуорбензил)-3-флуор-4з утворенням 1,0г (61%) названої сполуки. ХІАТгідроксипіперидин-1-карбоксилату у бензолі (50m МС: m/z 314 [МН+] мл) та суміш гріють до кипіння під зворотним хо(ііі) 1’-Бензил-4Н-спіро[хромен-3,4’-піперидин] лодильником, додають ДМФ20 (мл) та кип’ятіння Натрій гідрид (350мг, 7,0ммоль, 50% дисперсія під зворотним холодильником продовжують протяу маслі) промивають три рази гептаном в атмосгом 6 годин. Суміш охолоджують до кімнатної темфері азоту, а потім розчиняють у тетрагідрофурані ператури та виливають у воду і екстрагують ЕТО(50мл). Розчин [1-бензил-4-(2Ас. Ор ганічний шар сушать натрій сульфатом, флуорбензил)піперидин-4-іл]метанолу (1г, фільтрують та концентрують. Залишок очищають 3,2ммоль) у тетрагідрофурані (30мл) додають та хроматографією на SiO2 (етилацетат: н-гептан) з утворену суміш кип’ятять під зворотним холодильутворенням продукту (10мг, 26%). ХІАТ-МС m/z ником протягом 3 годин. Охолоджений розчин 342 [М+Н]+ розподіляють між водою та етилацетатом та орга(ν) 5-хлор-3’-флуор-3Н-спіро[1-бензофураннічний шар сушать магній сульфатом та концент2,4’-піперидин] рують. Сирий продукт очищають на оксиді силіцію Розчин трет-бутил 5-хлор-3’-флуор-1’Н,3Н(дихлорметан/ метанол) з утворенням 0,83г (89%) спіро[1-бензофуран-2,4’-піперидин]-1’названої сполуки. ХІАТ-МС: m/z 294 [ΜΗ4 ] карбоксилату у ДХМ/ТФОК (20мл, 5:2) перемішу(іv) 4Н-Спіро[хромен-3,4’-піперидин] ють при кімнатній температурі протягом 2 годин. 1’-бензил-4Н-спіро[хромен-3,4’-піперидин] Розчинник видаляють у вакуумі, залишок розво(800мг, 2,7ммоль) розчиняють у метанолі (100мл). дять ЕtOАс та промивають насиченим водним наОцтову кислоту (5мл) та паладій на активованому трій гідрокарбонатом та водою. Органічний шар вугіллі (каталітична кількість, 10%) додають. Реаксушать натрій сульфатом, фільтрують та концентція в апараті Парра при 35фунт/кв.дюйм протягом рують, отримуючи названу сполуку (60мг). ХІАТ18 годин, а потім фільтрування, випарювання та МС m/z 242 [М+Н]+ очистка ВЕРХ на С18 (ацетонітрил/вода) дає Інтермедіат: 4Н-спіро[хромен-3,4’-піперидин] 500мг (92%) названої сполуки. 1 Н-ЯМР (400МГц, ДМСО-d6) δ: 8,86 (1Н, bs); 7,10-7,05 (2Н, m); 6,85 (1Н, dt); 6,76 (1Н, d); 3,93 (2Н, s); 3,15-3,01 (4Н, m); 2,71 (2Н, s); 1,66-1,51 (4Н, m) ХІАТ-МС: m/z 204 [МН+] Інтермедіат: 6-хлор-3,4-дигідроспіро[хромен2,4’-піперидин] (і) Етил 1-бензил-4-(2-флуорбензил)піперидин4-карбоксилат Етил 1-бензилпіперидин-4-карбоксилат (2,47г, 10ммоль) розчиняють у тетрагідрофурані (20мл) та охолоджують до -78°С. Літій біс(триметилсиліл)амід (11мл, 1,0Μ у те трагідро(і) r-Бензил-6-хлорспіро[хромен-2,4’фурані) додають повільно та перемішують протяпіперидин]-4(3Н)-он гом 30 хвилин. 2-флуор-бензилбромід (1,34мл, Розчин 1-(5-хлор-2-гідроксифеніл)етанону 11ммоль) у 5мл тетрагідрофурану додають пові(1,7г, 10ммоль), 1-бензилпіперидин-4-ону (2,08г, льно. Утвореному розчину дають досягти кімнатної 11ммоль) та піролідину (1,07г, 15ммоль) у метанотемператури та перемішують протягом ночі. Реаклі (2мл) гріють при 70°С протягом 3 годин. Після ційну суміш гасять амоній хлоридом (водн., насиохолодження до кімнатної температури реакційну чен.) та розподіляють між водою та етилацетатом. суміш виливають у воду (20мл) та екстрагують Органічний шар промивають розсолом та сушать етилацетатом (50мл). Органічний шар промивають магній сульфатом, фільтрують та концентрують. 1Η водн. НСІ (2´50мл), 2Η водн. NaOH (50мл) та Сирий матеріал очищають на оксиді силіцію (гепводою. Сушка натрій сульфатом та випарювання тан/етилацетат) з утворенням 2,7г (77%) названої розчиннику дає названу сполуку, як оранжеве масполуки, як безбарвне масло. ХІАТ-МС: m/z 356 + сло (2,61г, 77%). ХІАТ-МС: m/z 34 [M+H]+ [МН ] (іі) 1’-Бензил-6-хлор-3,4-дигідроспіро[хромен(іі) [1-бензил-4-(2-флуорбензил)піперидин-42,4’-піперидин] іл]метанол При перемішуванні до суспензії АІСІ3 (3,04г, При перемішуванні розчин етил 1-бензил-4-(222,8ммоль) у дихлорметані (75мл) додають при флуорбензил)піперидин-4-карбоксилату (1,85г, 0°С трет-бутиламін-боран (1:1) (3,98г, 45,8ммоль) 5,2ммоль) у діетиловому етері охолоджують суміта перемішування продовжують протягом 15 хвишшю лід/натрій хлорид. Літій-алюміній гідрид лин при цій температурі до отримання прозорого (5,8мл, 1,0Μ у діетиловому етері) додають крапрозчину. Розчин 1’-бензил-6-хлорспіро[хроменлями. Після перемішування при кімнатній темпе2,4’-піперидин]-4(3Н)-он (2,61г, 7,6ммоль) у ди хлоратурі протягом 2 годин суміш знов охолоджують 49 77814 50 рметані (15мл) додають краплями. Перемішування 1,4’-піперидин] продовжують протягом 2 годин при 0°С та протяДо розчину 1’-бензил-6-хлор-3Н-спіро[2гом 3 годин при кімнатній температурі. Реакційну бензофуран-1,4’-піперидин]-3-ону (1,1г, суміш гасять додаванням краплями 0,1Η водн. 3,35ммоль) у ТГФ (15мл) повільно додають 1Μ НСІ. Після припинення виділення газу шари відорозчин комплексу борану у ТГФ [Магхег, А; Rodriкремлюють. Органічний шар промивають 0,1Η НСІ guez, Η. R; McKenna, J. Μ; Tsai, Η. M..J Org. Chem., 1975, 40, 1427-1430] (7мл, 7,0ммоль) при 0°С. Піс(2´50мл) та розсолом (50мл) і сушать натрій сульфатом. Розчинник видаляють у вакуумі, отриля завершення додавання реакційну суміш тримають при кімнатній температурі протягом 30 хвимуючи названу сполуку, як безбарвного твердого лин, тоді кип’ятять під зворотним холодильником продукту (1,63г, 65%). ХІАТ-МС; m/z 328 [М+Н]+ протягом ночі, охолоджують до 0°С повільно до(ііі) 6-хлор-3,4-дигідроспіро[хромен-2,4’дають та 6Μ водну гідрохлоридну кислоту (НСІ) піперидин] гідрохлорид Розчин 1’-бензил-6-хлор-3,4(3,5мл). Реакційну суміш кип’ятять під зворотним холодильником протягом 5 годин, охолоджують до дигідроспіро[хромен-2,4’-піперидину] (1,63г, 0°С, рН реакційної суміші підганяють до 10 дода5,0ммоль) та 1-хлоретилхлорформіат (1,07г, ванням водного 6Μ NaOH та екстрагують етилаце7,5ммоль) у толуолі (5мл) гріють при кипінні під татом. зворотним холодильником протягом ночі. Розчинник видаляють у вакуумі, маслянистий залишок Органічний шар промивають водою, сушать натрій сульфатом, фільтрують та концентрують у розчиняють у метанолі (10мл) та гріють при кипінні вакуумі. Залишок очищають флешпід зворотним холодильником протягом ночі. Розхроматографією на силікагелі (0-30% етилацетату чинник видаляють у вакуумі та залишок обробляу петролейному ефірі) з утворенням названої споють діетиловим етером (50мл). Білий осад збирають фільтруванням, промивають діетиловим луки (900мг). 1 Н-ЯМР (CDCI3, 400МГц): δ 7,44-7,22 (m, 6H); етером та сушать з утворенням названої сполуки, 7,18 (m, 2H); 5,03 (s, 2H); 3,60 (s, 2H)2,87 (br.d, як білого порошку (0,58г, 49%). 1 J=10,5Гц, 2H); 2,45 (br.t, J=11,2Гц, 2H); 2,00 (br.s, Н-ЯМР (CDCI3, 400МГц): δ 7,07 (d, J=10,0Гц, 2H); 1,79 (d, J=11,2Гц, 2Н). 2Н); 7,63 (d, J=8,4Гц, 1Н); 3,2-3,5 (m, 4H); 2,77 (t, J=6,6Гц, 2H); 1,9-2,2 (m, 4H); 1,88 (t, J=6,6Гц, 2Н). XIAT-MC: m/z 314(MH +). + (iii) 6-хлор-3Н-спіро[2-бензофуран-1,4’ХІАТ-МС: m/z 238 [М+Н] піперидин] Інтермедіат: 6-хлор-3Н-спіро[2-бензофуранДо розчину 1’-бензил-6-хлор-3Н-спіро[21,4’-піперидин] бензофуран-1,4’-піперидину] (850мг, 2,7ммоль) у (і) 1’-Бензил-6-хлор-3Н-спіро[2-бензофуран1,4’-піперидин]-3-он дихлорметані (8мл)повільно додають хлоретилхлорформіат [Yang, В. V; o’Rourke, D; Li,]., Synlett, До розчину 2-бром-4-хлорбензойної кислоти 1993, 195-196] (772мг, 5,4ммоль) при 0°С. Після (2,35г, 10,0ммоль) у тетрагідрофурані (15мл) повізавершення додавання реакційну суміш перемільно додають 1,6Μ розчин у гексані н-бутиллітію шують при 0°С протягом 30 хвилин. Летючі проду[Parham, W.t; Egberg, D. С; Sayed, Υ. A; Thraikill, R. W; Keyser, G. E; William, M. N; Montgomery, M. C; кти видаляють у вакуумі, залишок розчиняють у метанолі (10мл)та кип’ятять під зворотним холоJones, L D., J. Org. Chem., 1976, 41, 2628-2633] дильником протягом 40 хвилин. Летючі продукти (20мл, 32,0ммоль) при -78°С під азотом. Після видаляють у вакуумі та залишок очищають флешзавершення додавання реакційну суміш переміхроматографією на силікагелі (0-6% метанолу у шують при -78°С протягом 3 годин. Тоді розчин 1бензилпіперидин-4-ону (3,78г, 20,0ммоль) у ТГФ дихлорметані, 0,2% амоній гідроксиду) з утворенням названої сполуки (170мг) та 1’-бензил-6-хлор(10мл) повільно додають до реакційної суміші при 3Н-спіро[2-бензофуран-1,4’-піперидин] виділяють -78°С. Після завершення додавання температуру (200мг). реакції підвищують до кімнатної температури та 1 Н-ЯМР (CD3OD, 400МГц): δ 7,29-7,21 (m, 3Н); реакційну суміш перемішують при кімнатній температурі протягом ночі. Реакційну суміш вилива5,00 (s, 2H); 2,99 (m, 4H); 1,90-181 (m, 2H); 1,70 (m, 2H). XIAT-MC: m/z 224(MH +). ють у суміш води (Н2О) (60мл) та діетилового етеІнтермедіат: 5-Флуор-3Н-спіро[2-бензофуранру (60мл), шари відокремлюють. Водний шар 1|4’-піперидин] екстрагують діетиловим етером (2´20мл). Водний (iv) 1’-бензил-5-флуор-3Н-спіро[2-бензофураншар підкислюють водною 6Μ HCI до рН2 та 1,4’-піперидин]-3-он кип’ятять протягом 1 години, охолоджують до 0°С, Цю реакцію здійснюють, як описано для (І) рН підганяють до 10 додаванням водного натрій вище, застосовуючи 2-бром-5-флуорбензойну кисгідроксиду (NaOH) (6Μ) та швидко екстрагують лоту (2,19г, 10,0ммоль), 1-бензилпіперидин-4-он трихлорметаном (СНСІ3). Органічний шар проми(3,78г, 20,0ммоль), н-бутил літій (H-BuLi) (20мл)та вають водою, сушать натрій сульфатом, фільтруТГФ (20мл) з утворенням названої сполуки. ють та концентрують у вакуумі з утворенням на1 Н-ЯМР (CDCI3, 400МГц): δ 7,58-7,23 (m, 8H); званої сполуки (1,22г), що є достатньо чистою для 3,68 (s, 2Η); 2,98 (m, 2H); 2,59 (m, 2H); 2,28 (m, 2H); наступного етапу. 1 1,74 (m, 2H). XIAT-MC: m/z 312 (MH +). Н-ЯМР (CDCI3, 400МГц): δ 7,84 (d, J=8,2Гц, (v) 1’-Бензил-5-флуор-3Н-спіро[2-бензофуран1Н); 7,51 (dd, J=1,7, 8,2Гц, 1Н); 7,45-7,25 (m, 6H); 1,4’-піперидин] 3,67 (s, 2H); 3,00 (br.d; J=9,4Гц, 2H); 2,61 (br.t, Цю реакцію здійснюють, як описано для (іі) J=11,2Гц, 2H); 2,32 (br, s, 2H); 1,74 (d, J=12,2Гц, вище, застосовуючи 1’-бензил-5-флуор-3Н-спіро[22Н). XIAT-MC: m/z 328 (MH +). бензофуран-1,4’-піперидин]-3-он (200мг, (ii) r-Бензил-6-хлор-3Н-спіро[2-бензофуран 51 77814 52 0,642ммоль), 1М розчин комплексу боран-ТГФ бензофуран-2,4’-піперидин]-1’-іл)-2(1,34мл, 1,34ммоль) та ТГФ (3мл) з утворенням гідроксипропіл]окси}-4-флуорфеніл)ацетамід названої сполуки (148мг). 1Н-ЯМР (CDCI3, Етап І: 400МГц): δ 7,41-7,27 (m, 5H); 7,08 (dd, J=4,8, 8,3Гц, N-(4-Флуор-2-гідроксифеніл)ацетамід 1H); 6,97 (m, 1H); 6,89 (m, 1H); 5,08 (s, 2H); 3,60 (s, Суміш 5-флуор-2-нітрофенолу (5г, 31,8ммоль), 2H); 2,87 (m, 2H); 2,46 (m, 2H); 1,97 (m, 2H); 1,88 оцтового ангідриду (4,86г, 47,7ммоль) та платин на (m, 2H). XIAT-MC: m/z 298 (MH +). вугіллі (5%, 200мг) у метанолі гідрують при тиску (vi) 5-Флуор-3Н-спіро[2-бензофуран-1,4’35 фунт/кв.дюйм протягом 3 годин. Каталізатор піперидин] відфільтровують та залишок очищають флешЦю реакцію здійснюють, як описано для (ііі) хроматографією на силікагелі з утворенням назвавище, застосовуючи 1’-бензил-5-флуор-3Н-спіро[2ної сполуки (4,7г). 1 бензофуран-1,4’-піперидин] (145мг, 0,487ммоль), Н-ЯМР (CD3OD, 300МГц): δ 7,56-7,51 (m, 1H), хлоретилхлорформіат (0,07мл)з утворенням на6,61-6,50 (m, 2H); 2,15 (s, 3Н). XIAT-MC: m/z 170 званої сполуки. (MH+). 1 Н-ЯМР(СD3OD, 400MГц):57,1S (dd, J=4,9, Етап II: 8,1Гц, 1Н); 7,03-6,96 (m, 2H); 5,01 (s, 2H); 3,09-2,93 N-{4-Флуор-2-[(2S)-оксиран-2(m, 4Н); 1,91 -1,81 (m, 2Н); 1,73-1,66 (m, 2Н). XIATілметокси]феніл}ацетамід MC: m/z 208 (MH +). Суміш N-(4-флуор-2-гідроксифеніл)ацетаміду Інтермедіат: [(2S)-2-метилоксиран-2-іл]метил (1,69г, 10,0ммоль), (2S)-оксиран-2-ілметил-33-нітробензолсульфонат нітробензолсульфонату (2,59г, 10,0ммоль) та Отримано, [як описано Eriksson, Т.; Klingstedt, Cs 2CO3 (4,87г, 15,0ммоль) у ДМФ Т.; Mussie, Т., Опублікована Міжнародна патентне (15мл)перемішують при кімнатній температурі заявка No. WO 01/98273]. протягом 2 годин. Реакційну суміш розподіляють Приклад 1 між етилацетатом та водою. Органічний шар суN-{2-{(2S)-3-(5-хлор-1’Н,3Н-спіро[1шать натрій сульфатом, Фільтрують та концентрубензофуран-1,4’-піперидин]-1’-іл)-2ють.Залишок очищають флеш-хроматографією на гідроксипропіл]окси}феніл)ацетамід силікагелі з утворенням названої сполуки (1,35 г). 1 Етап І: Н-ЯМР (CDCI3, 400МГц): δ 8,33-8,29 (m, 1H); N-{2-{(2S)-Оксиран-27,71 (br. s, 1H), 6,74-6,66 (m, 2H); 4,39-4,36 (m, 1H); ілметокси]феніл}ацетамід 3,95-3,90 (m, 1H); 3,41-3,39 (m, 1H); 2,99-2,97 (m, Суміш N-(2-гідроксифеніл)ацетаміду (1,51г, 1H); 2,80-2,79 (m, 1H). XIAT-MC: m/z 226 (MH +). 10ммоль), (2S)-оксиран-2-ілметил-3Етап III: нітробензолсульфонату (2,59г, 10ммоль) та цезій N-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1карбонату (3,9г, 12ммоль) у диметилформаміді бензофуран-2,4’-піперидин]-1’-іл)-2(ДМФ) (30мл)перемішують при кімнатній темперагідроксипропіл]окси}-4-флуорфеніл)ацетамід турі протягом ночі. Реакційну суміш розподіляють Суміш 5-хлор-3Н-спіро[1-бензофуран-2,4’між етилацетатом та водою. Органічний шар супіперидину] (45мг, 0,201ммоль) та N-{4-флуор-2шать натрій сульфатом, фільтрують, концентру[(2S)-оксиран-2-ілметокси]феніл}ацетаміду (45,3мг, ють та залишок очищають флеш-хроматографією 0,201ммоль) в етанолі (3мл)перемішують при 80°С на силікагелі з утворенням названої сполуки протягом ночі. Летючі продукти видаляють у ваку(1,34г). умі та залишок очищають флеш-хроматографією 1 Н-ЯМР (CDCI3, 400МГц): δ 8,40 (m, 1H); 7,90 на силікагелі (0-3% метанолу у дихлорметані, 0,2% (br.s, 1H); 7,05 (m, 2H); 6,92 (m, 1H); 4,37 (dd, J=2,5, амоній гідроксиду) з утворенням названої сполуки 11,3Гц, 1Η); 3,98 (dd, J=5,9, 11,3Гц, 1Η); 3,40 (m, (33мг), 1Н-ЯМР (CDCI3, 400МГц): δ 8,52 (s, 1H); 1Η); 2,97 (t, J=4,8Гц, 1Η); 2,81 (dd, J=2,7,4,8Гц, 1H); 8,20 (dd, J=64, 8,9Гц, 1H); 7,18 (s, 1H); 7,13 (dd, 2,20 (s, 3Н). J=2,0, 8,5Гц, 1Н); 6,74 (dd, J=2,6, 8,6Гц, 1Н); 6,69 Етап II: (d, J=8,6Гц, 1Н); 6,59 (dd, J=2,6, 9,8Гц, 1Н); 4,48 (m, N-{2-{(2S)-3-(5-хлор-1’Н,3Н-спіро[11H); 4,17 (dd, J=3,7, 9,8Гц, 1Н); 4,00 (dd, J=2,2, бензофуран-2,4’-піперидин]-1’-іл)9,8Гц, 1Н); 3,79 (m, 2Н); 3,59 (br.d, J=11,7Гц, 1Н); гідроксипропіл]окси}феніл)ацетамід 3,38 (m, 1Н); 3,27 (m, 1Н); 3,12 (s, 2Н); 3,05 (m, 1Н); Суміш 5-хлор-3Н-спіро[1-бензофуран-2,4’2,48 (m, 1Н); 2,37 (m, 1Н); 2,24 (s, 3Н); 2,17 (m, 2Н). піперидину] (36мг, 0,16ммоль) та N-{2-[(2S)XIAT-MC: m/z 451 (МН+). оксиран-2-ілметокси]феніл}ацетаміду (33мг, Приклад 3 0,16ммоль) в етанолі (3мл)перемішують при 80°С N-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1протягом ночі. Летючі продукти видаляють у вакубензофуран-2,4’-піперидин]-1’-іл)-2умі та залишок очищають флеш-хроматографією гідроксипропіл]окси}-4-метоксифеніл)ацетамід на силікагелі (0-3% метанолу у дихлорметані, що Етап І: містить 0,2% амоній гідроксиду) з утворенням наN-(2-Гідрокси-4 метоксифеніл)ацетамід званої сполуки (25мг). 1Н-ЯМР (CDCI3, 400МГц): δ 2-Нітро-5-метоксифенол (отримано з 37,82 (d, J=4,8Гц, 1H); 7,22 (m, 1H); 7,13 (m, 2H); метоксифенолу, [R.J.Maleski, Synthetic Communi7,05 (d, J=7,5Гц, 1H); 6,98 (m, 1H); 6,74 (d, J=8,6Гц, cations, 1993, 23, 343-348]) (48,5г, 0,287мол) роз1H); 4,49 (m, 1H); 4,08 (d, J=4,8Гц, 2H); 3,70 (m, чиняють у ТГФ (1,5л) і гідрують при температурі 2H); 3,43 (m, 4H); 3,12 (s, 2H); " 2,20 (m, 7H). XIATдовкілля протягом ночі з 10% паладію на вугіллі MC: m/z 433 (MH +). (10г) доки не поглинається 20,3л водню. Після фіПриклад 2 льтрування та випарювання залишок суспендують N-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1у дегазованій воді (1,7л) та додають оцтовий ангі 53 77814 54 дрид (42,5мл). Суміш гріють до 60°С протягом 1 хвилин. Реакційну суміш охолоджують до 0°С та години, а потім охолоджують до кімнатної темпеповільно додають метанол (2мл)з перемішування ратури, летючі продукти видаляють у вакуумі та протягом 10 хвилин. Летючі продукти видаляють у твердий продукт промивають водою та сушать у вакуумі. Залишок розчиняють у великому об’ємі вакуумі з утворенням червоних кристалів (41,7г, етилацетату, промивають послідовно водним на80%). трій гідрокарбонатом та водою. Органічний шар 1 Н-ЯМР (400МГц, CDCI3): δ 8,98 (s, 1H); 7,34 сушать натрій сульфатом, фільтрують, концент(br.s, 1H); 6,81 (d, 1H); 6,58 (d, 1H); 6,44 (dd, 1H); рують та залишок очищають флеш3,78 (s, 3Н); 2,26 (s, 3Н) хроматографією на силікагелі (0-3% метанолу у Етап II: дихлорметані, 0,2% амоній гідроксиду) з утворенN-{4-Метокси-2[(2S)-оксиран-2ням названої сполуки (155мг). 1Н-ЯМР (CD3OD, ілметокси]феніл}ацетамід 400МГц): δ 7,57 (d, J=8,7Гц, 1H); 7,14 (m, 1H); 7,04 N-(2-Гідрокси-4-метоксифеніл)ацетамід (dd, J=2,3, 8,5Гц, 1Н); 6,66 (d, J=8,5Гц, 1Н); 6,48 (d, (18,12г, 0,1мол) та (2S)-оксиран-2-ілметил-3J=2,5Гц, 1H); 6,32 (dd, J=2,5, 8,6Гц, 1H); 4,17 (m, нітробензолсульфонат (25,92г, 0,1мол) розчиня1H); 4,06 (dd, J=3,4, 9,8Гц, 1Н); 3,93 (dd, J=6,2, ють у сухому ДМФ (75мл)та перемішують під азо9,8Гц, 1H); 3,03 (s, 2H); 2,70 (m, 4H); 2,59 (m, 2H); том (N2) на льодяній бані. Цезій карбонат (35,8г, 2,13 (s, 3Н); 1,95 (m, 2H); 1,84 (m, 2H). XIAT-MC: 0,11мол) додають та перемішування під азотом m/z 447(MH+). продовжують при температурі довкілля протягом Приклад 5 ночі. Суміш виливають в етилацетат (1л) та воду N-[2-{[(2S)-3-{5-хлор-1’Н,3Н-спіро[[1(250мл). Органічну фазу промивають водою бензофуран-2,4’-піперидин]-1’-іл)-2гідроксипропіл]окси}-5(3´250мл), сушать натрій сульфатом, фільтрують та концентрують у вакуумі з утворенням оранже(трифлуорметил)феніл]ацетамід Етап І: вого твердого сирого продукту (29г), який перекриN-{2-{[(2S)-2-Метилоксиран-2-іл]метокси}-5сталізовують з етанолу (100мл)та промивають (трифлуорметил)среніл}ацетаміц етером з утворенням білих кристалів. Більше білих Суміш 2-нітро-4-(трифлуорметил)фенолу кристалів отримують з маточнику, після випарювання та перекристалізації з 2-пропанолу Загаль(310мг, 1,5ммоль), паладію на вугіллі (10%, 125мг) та оцтового ангідриду (306,3мг, 3,0ммоль) у метаний вихід 15г (63%). 1 нолі гідрують протягом 2 годин при атмосферному Н-ЯМР (CDCI3): δ 8,22 (d, 1H); 7,64 (bs, 1H); тиску. Каталізатор відфільтровують, фільтрат кон6,53 (dd, 1H); 6,50 (d, 1H); 4,34 (dd, 1H); 3,92 (dd, центрують у вакуумі з утворенням сирого N-{21Н); 3,79 (s, 3Н); 3,38 (m, 1Н); 2,96 (t, 1Н); 2,78 (dd, 1Н); 2,20 (s, 3Н) гідрокси-5-(трифлуорметил)феніл]ацетаміду (331мг). Частину (219,16мг, 1,0ммоль) N-[2Етап III: гідрокси-5-(трифлуорметил)феніл]ацетаміду оброN-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1бляють [(2S)-2-метилоксиран-2-іл]метил 3бензофуран-2,4’-піперидин]-1’-іл)-2нітробензолсульфонатом (273,27мг, 1,0ммоль) у гідроксипропіл]окси}-4-метоксифеніл)ацетамід Суміш 5-хлор-3Н-спіро[1-бензофуран-2,4’присутності цезій карбонату (406,25мг, 1,25ммоль) у ДМФ (5мл)при кімнатній температурі протягом 5 піперидину] (200мг, 0,894ммоль) та N-{4-метоксигодин. Реакційну суміш розподіляють між етилаце2[(2S)-оксиран-2-ілметокси]феніл}ацетаміду татом та водою. Органічний шар сушать натрій (212мг, 0,894ммоль) в етанолі (5мл) перемішують сульфатом, фільтрують, концентрують. Залишок при 80°С протягом ночі. Летючі продукти видаляють у вакуумі та залишок очищають флешочищають флеш-хроматографією на силікагелі (040% етилацетат у петролейному ефірі) з утворенхроматографією на силікагелі (0-2% метанолу у ням названої сполуки (230мг). дихлорметані, 0,2% амоній гідроксиду) з утворен1 Н-ЯМР (CDCI3, 400МГц): δ 8,86 (s, 1H); 8,00 ням названої сполуки (400мг). 1Н-ЯМР (CD3OD, (br.s, 1H); 7,29 (m, 1H); 6,97 (d, J=8,5Гц, 1Η); 4,23 400МГц): δ 7,74 (d, J=8,9Γц, 1H);7,13(m, 1H); 7,04 (dd, J=2,3, 8,5Гц, 1H); 6,65(d, J=8,5Гц, 1Η); 6,61 (d, (d, J=11,0Гц, 1Η); 4,04 (d, J=11,03Гц, 1Η) 2,93 (m, 1Η); 2,81 (d, J=4,6Гц, 1Η); 2,22 (s, 31Η); 1,42 (s, J=2,7Гц, 1H); 6,51 (dd, J=2,7, 8,8Гц, 1H); 4,17 (m, 3Н). 1H); 4,08 (dd, J=3,4, 10,0Гц, 1Н); 3,98 (dd, J=6,3, Етап II: 9,9Гц, 1H); 3,79 (s, 3Н); 3,03 (s, 2H); 2,72 (m, 4H); N-[2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[12,62 (m, 2H); 2,15 (s, 3Н); 1,95 (m,2H); 1,84 (m,2H). XIAT-MC; m/z 461 (MH +). бензофуран-2,4’-піперидин]-1’-іл)-2гідроксипропіл]окси}-5Приклад 4 (трифлуорметил)феніл]ацетамід N-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1Суміш 5-хлор-3Н-спіро[1-бензофуран-2,4’бензофуран-2,4’-піперидин]-1’-іл)-2піперидину] (35мг, 0,155ммоль) та Ν-[2-{[(2S)-2гідроксипропіл]окси}-4-гідроксифеніл)ацетамід До холодного (0°С) розчину N-(2-{[(2S)-3-(5метилоксиран-2-іл]метокси}-5(трифлуорметил)феніл] ацетамід (45мг, хлор-1’Н,3Н-спіро[1-бензофуран-2,4’-піперидин]-1’0,155ммоль) в етанолі (2мл)перемішують при 80°С іл)-2-гідроксипропіл]окси}-4протягом ночі. Летючі продукти видаляють у вакуметоксифеніл)ацетаміду (380мг, 0,82ммоль) у диумі та залишок очищають флеш-хроматографією хлорметані (8мл)повільно додають 1Μ розчин бор триброміду (ВВr3) у ди хлорметані (2,47мл, на силікагелі (0-1,5% метанолу у дихлорметані, 0,2% амоній гідроксиду) з утворенням названої 2,47ммоль). Після завершення додавання льодяну сполуки (28мг). 1Н-ЯМР (CD3OD, 400МГц): δ 8,40 баню видаляють та реакційну суміш перемішують (d, J=1,8Гц, 1Н); 7,40 (dd, J=1,4, 8,7Гц, 1Н); 7,18 (d, при кімнатній температурі протягом 2 годин 30 55 77814 56 J=8,6Гц, 1H); 7,13 (m, 1H); 7,03 (dd, J=2,2, 8,5Гц, Суспензію метил 4-флуор-2-гідроксибензоату 1Н); 6,63 (d, J=8,5Гц, 1Н); 4,13 (d, J=9,3Гц, 1H); (510мг, 3,0ммоль) у циклопропіламіні 3,98 (d, J=9,3Гц, 1H); 2,99 (s, 2H); 2,78 (m, 1H); 2,68 (5мл)перемішують при кімнатній температурі про(m, 3Н); 2,58 (m, 1H); 2,22 (s, 3Н); 1,88 (m, 2H); 1,78 тягом ночі, коли розчин стає прозорим. Летючі (m, 2H); 1,32 (s, 3Н). XIAT-MC: m/z 513 (MH +). продукти видаляють у вакуумі та залишок очищаПриклад 6 ють флеш-хроматографією на силікагелі (0-30% 2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуранетилацетат у петролейному ефірі) з утворенням 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-Nназваної сполуки (493мг). 1 циклопропілбензамід Н-ЯМР (CD3OD, 400МГц): δ 12,65 (s, 1H); 7,28 Етап І: (m, 1H); 6,69 (dd, J=2,6, 10,4Гц, 1H); 6,56 (ddd, N-Циклопропіл-2-гідроксибензамід J=2,6, 8,0, 10,4Гц, 1H); 6,30 (br. s, 1H); 2,88 (m, 1H); Суміш метилсаліцилату (4,36г, 28,69ммоль) та 0,98 (m, 2H); 0,66 (m, 2H). XIAT-MC: m/z 196 (MH +). циклопропіламіну (1,64г) гріють у запечатаній тубі Етап II: при 80-100°С протягом 3 годин. Ще додають 0,5г N-Циклопропіл-4-флуор-2-(оксиран-2циклопропіламіну та гріють при 70°С протягом ноілметокси)бензамід чі. Летючі продукти видаляють у вакуумі та залиСуміш N-циклопропіл-4-флуор-2шок очищають флеш-хроматографією на силікагегідроксибензаміду (195мг, 1,0ммоль), (2S)лі з утворенням названої сполуки (2,71г). 1Н-ЯМР оксиран-2-ілметил 3-нітробензолсульфонату (CDCI3, 400МГц): δ 12,40 (s, 1H); 7,40 (m, 1H); 7,38 (259мг, 1,0ммоль) та цезій карбонату (390мг, (m, 1H); 7,01 (m, 1H); 6,81 (m, 1H); 6,48 (br.s, 1H); 1,2ммоль) у ДМФ (5мл)перемішують при кімнатній 2,85 (m, 1H); 0,98 (m, 2H); 0,82 (m, 2H). температурі протягом ночі. Реакційну суміш розЕтап II: поділяють між етилацетатом та водою. Органічний N-Циклопропіл-2-[(2S)-оксиран-2шар сушать натрій сульфатом, фільтрують та конілметокси]бензамід центрують. Залишок очищають флешСуміш N-циклопропіл-2-гідроксибензаміду хроматографією на силікагелі (0-30% етилацетат у (270мг, 1,52ммоль), (2S)-оксиран-2-ілметил-3петролейному ефірі) з утворенням названої сполунітробензолсульфонат (378мг, 1,68ммоль) та цезій ки (150мг). 1 карбонату (645мг, 1,98ммоль) у ДМФ Н-ЯМР (CDCI3, 400МГц): δ 8,24 (dd, J=7,0, (4мл)перемішують при кімнатній температурі про8,8Гц, 1Н); 7,80 (br. s, 1H); 6,82 (ddd, J=2,3, 7,6, тягом ночі. Реакційну суміш розподіляють між ети10,2Гц, 1Н); 6,66 (dd, J=2,3, 10,2Гц, 1Н); 4,45 (dd, лацетатом та водою. Органічний шар сушать наJ=2,4, 10,7Гц, 1Н); 4,05 (dd, J=5,1, 10,7Гц, 1Н); 3,40 трій сульфатом, фільтрують та концентрують. (m, 1H); 3,00 (m, 2H); 2,84 (dd, J=2,6,4,8Гц, 1Н); Залишок очищають флеш-хроматографією на си0,86 (m, 2H); 0,65 (m, 2Н). XIAT-MC: m/z 252 (MH +). лікагелі (40% гептан в етилацетаті) з утворенням Етап III: названої сполуки (354мг), 1Н-ЯМР (CDCI3, 2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[піро{1400МГц): δ 8,22 (dd, J=1,8, 7,8Гц, 1H); 7,95 (br.s, бензофуран-2,4’-піперидин]-1’-іл)-21H); 7,42 (m, 1H); 7,10 (m, 1H); 6,93 (d, J=8,3Гц, гідроксипропіл]окси}-N-циклопропіл-41H); 4,44 (dd, J=2,5, 10,7Гц, 1H); 4,08 (dd, J=5,1, флуорбензамід 10,8Гц, 1H); 3,40 (m, 1H); 3,04-2,95 (m, 2H); 2,83 Суміш 5-хлор-3Н-спіро[1-бензофуран-2,4’(dd, J=2,7,4,5Гц, 1H); 0,86 (m, 2H); 0,65 (m, 2H). піперидину] (30мг, 0,134ммоль) та N-циклопропілЕтап III: 4-флуор-2-(оксиран-2-ілметокси)бензаміду (33,6мг, 2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуран0,134ммоль) в етанолі (2мл)перемішують при 80°С 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси]-Nпротягом ночі. Летючі продукти видаляють у вакуциклопропілбензамід умі та залишок очищають флеш-хроматографією Суміш 5-хлор-3Н-спіро[1-бензофуран-2,4’на силікагелі (0-2% метанолу у дихлорметані, 0,2% піперидину] (9мг, 0,04ммоль) та N-циклопропіл-2амоній гідроксиду) з утворенням названої сполуки [(2S)-оксиран-2-ілметокси]бензаміду (9,4мг, (36мг). 1Н-ЯМР (CD3OD, 400МГц): δ 7,97 (dd, J=6,9, 0,4ммоль) в етанолі (1,5мл)перемішують при 80°С 8,7Гц, 1H); 7,14 (m, 1H); 7,05 (dd, J=2,3, 8,5Гц, 1Н); протягом ночі. Летючі продукти видаляють у ваку6,96 (dd, J=2,4, 10,4Гц, 1Н); 6,82 (ddd, J=2,4, 8,0, умі та залишок очищають флеш-хроматографією 10,4Гц, 1Н); 6,66 (d, J=8,5Гц, 1Н); 4,24 (dd, J=3,0, на силікагелі (0-1,5% метанолу у дихлорметані, 9,4Гц, 1H); 4,17 (m, 1H); 4,10 (dd, J=5,5, 9,4Гц, 1H); 0,2% амоній гідроксиду) з утворенням названої 3,05 (s, 2H); 2,82 (m, 1H); 2,71 (br. s, 4H); 2,60 (d, сполуки (7мг). J=6,3Гц, 2H); 1,99 (m, 2H); 1,88 (m, 2H); 0,83 (m, 1 Н-ЯМР (CD3OD, 400МГц): δ 7,92 (m, 1H); 7,47 2H); 0,58 (m, 2H). XIAT-MC: m/z 252 (MH +). (m, 1H); 7,13 (m, 2H); 7,05 (m, 2H); 6,65 (d, J=8,5Гц, Приклад 8 1H); 4,23 (dd, J=3,0, 9,4Гц, 1H); 4,16 (m, 1H); 4,09 2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуран(dd, J=5,5, 9,4Гц, 1Н); 3,03 (s, 2H); 2,93 (m, 1H); 2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-N2,70 (br. s, 4H); 2,60 (d, J=6,3Гц, 1H); 1,96 (m, 2H); циклопропіл-4-метоксибензамід 1,85 (m, 2H); 0,81 (m, 2H); 0,69 (m, 2H). XIAT-MC: Етап І: m/z 457 (MH +). N-Циклопропіл-2-гідрокси-4-метоксибензамід Приклад 7 Суспензію метил 2-гідрокси-42-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуранметоксибензоату (5,1г, 28,0ммоль) у циклопропі2,4’-піперидин]-1’-іл)-2-гідроксипропіл]окси}-Nламініі 24мл, перемішують при кімнатній темперациклопропіл-4-флуорбензамід турі протягом 5 діб. Летючі продукти видаляють у Етап І: вакуумі та залишок очищають флешN-Циклопропіл-4-флуор-2-гідроксибензамід хроматографією на силікагелі (0-60% етилацетат у 57 77814 58 петролейному ефірі) з утворенням названої сполуконцентрують у вакуумі. Залишок розчиняють у ки (1,8г). суміші ацетонітрилу (150мл) та диметилацетаміду 1 Н-ЯМР (CD3OD, 400МГц): δ 7,61 (d, J=8,8Гц, (25мл). Розчин охолоджують-до 5°С, фосфор ок1H); 6,42 (m, 2H); 3,80 (s, 3Н); 2,80 (m, 1H); 0,80 (m, сихлорид (20,4г, 12,2мл, 133ммоль) додають крап2H); 0,62 (m, 2H). XIAT-MC: m/z 208 (MH +) лями, даючи температурі перевищити 10°С. Після Етап II: завершення додавання реакційну суміш переміN-Циклопропіл-2-метокси-2-((2S)-оксиран-2шують при кімнатній температурі протягом 1 годиілметокси]бензамід ни, а потім повільно виливають у суміш натрій каСуміш N-циклопропіл-2-гідрокси-4рбонату (55г) та льоду (приблизно 800г). Після метоксибензамщу (700мг, 3,38ммоль), (2S)плавлення льоду утворену кашку фільтр ують та оксиран-2-ілметил-3-нітробензолсульфонату зібраний твердий продукт промивають водою (876мг, 3,38ммоль) та цезій карбонату (1,31г, (2´150мл). Продукт сушать у вакуумі, отримуючи 4,05ммоль) у ДМФ (12мл)перемішують при кімнатжовтий порошок (14,4г, 97ммоль, 76%). 1 ній температурі протягом ночі. Реакційну суміш Н-ЯМР (400МГц, ДМСО-d6): δ 9,68 (br. s, 1Н), розподіляють між етилацетатом та водою. Органі7,38 (d, J=8,5Гц, 1Н), 6,94 (d, J=2,2Гц, 1H), 6,74 (dd, чний шар сушать натрій сульфатом, фільтрують та J=8,5,2,2Гц, 1Н), 2,50 (s, 3Н). концентрують. Залишок очищають флешЕтап II: хроматографією на силікагелі (0-80% етилацетат у 2-Метил-1,3-бензоксазол-6-іл бензоат петролейному ефірі) з утворенням названої сполуПри перемішуванні до суспензії 2-метил-1,3ки (1,0г). бензоксазол-6-олу (2,99г, 20ммоль) у ди хлормета1 Н-ЯМР (CDCI3, 400МГц): δ 8,20 (d, J=8,8Гц, ні (50мл)додають триетиламін (4,05г, 5,58мл, 1H); 7,85 (br.s, 1H). 6,63 (dd, J=2,3, 8,8Гц, 1Н); 6,45 40ммоль). Розчин бензо-їлхлориду (3,09г, 2,56мл, (d, J=2,3Гц, 1Н); 4,42 (dd, J=2,5, 10,8Гц, 1Н); 4,05 22ммоль) у дихлорметані (20мл) додають крапля(dd, J=5,2, 10,8Гц, 1Н); 3,82 (s, 3Н); 3,40 (m, 1Н); ми протягом приблизно 10 хвилин. Реакційну су3,00 (m, 2Н); 2,83 (dd, J=2,6, 4,8Гц, 1Н); 0,88 (m, міш перемішують при кімнатній температурі протя2Н); 0,68 (m, 2Н). XIAT-MC: m/z 264 (МН+). гом 2,5 годин, тоді промивають водою (2´50мл) та Етап III: сушать натрій сульфатом, фільтрують та концент2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[1-бензофуранрують у вакуумі з утворенням названої сполуки, як 2,4’-піперидин]-1’-іл)-2-гідроксипропіл)окси}-Nбезбарвного твердого продукту (5,05г, 20ммоль). 1 циклопропіл-4-метоксибензамід Н-ЯМР (400МГц, CDCI3): δ 8,22 (m, 2H), 7,66 Суміш 5-хлор-3Н-спіро[1-бензофуран-2,4’(m, 2H), 7,53 (m, 2H), 7,40 (d, 1H), 7.l6(dd, 1H), 2,65 піперидину] (100мг, 0,447ммоль) та N-циклопропіл(s, 3H). XIAT-MC: m/z 254 [MH +]. 4-метокси-2-[(2S)-оксиран-2-ілметокси]бензаміду Етап III: (117,7мг, 0,447ммоль) в етанолі (3мл)перемішують 4-(Ацетиламіно)-3-гідроксифеніл бензоат при 80°С протягом ночі. Летючі продукти видаляДо розчину 2-метил-1,3-бензоксазол-6-іл бенють у вакуумі та залишок очищають флешзоату (5,05г, 20ммоль) у ТГФ (100мл) додають сухроматографією на силікагелі (0-1,5% метанолу у міш трифлуороцтова кислота/вода (4мл/10мл). дихлорметані, 0,2% амоній гідроксиду) з утворенРеакційну суміш перемішують при кімнатній тем1 ням названої сполуки (145мг). Н-ЯМР (CDCI3, пературі протягом 16 годин, тоді додають насиче400МГц); δ 8,18 (m, 2H); 7,12 (m, 1H); 7,09 (dd, ний водний натрій гідрокарбонат (150мл). Суміш J=2,3, 8,5Гц, 1H); 6,70 (d, J=8,5Гц, 1Н); 6,63 (dd, екстрагують етилацетатом (150мл), сушать натрій J=2,3, 8,8Гц, 1Н); 6,44 (d, J=2,3Гц, 1Н); 4,19 (dd, сульфатом, фільтр ують та концентрують у вакуумі J=3,3, 9,4Гц, 1Н); 4,13 (m, 1H); 3,97 (dd, J=5,0, з утворенням названої сполуки. 1 9,4Гц, 1H); 3,88 (s, 3Н); 3,02 (m, 3Н); 2,92 (m, 1H); Н-ЯМР (400МГц, ацетон-d6): δ 9,76 (br.s, 1H), 2,81 (m, 1H); 2,63 (m, 3Н); 2,53 (dd, J=3,6, 12,4Гц, 9,32 (br.s, 1H), 8,15 (m, 2H), 7,71 (m, 1Н), 7,60 (гл, 1H); 2,04 (m, 2H); 1,88 (m, 2H); 0,85 (m, 2H); 0,06 2Н), 7,47 (d, 1Н), 6,85 (m, 1Н), 6,75 (m, 1Н), 2,20 (s, (m, 2H). XIAT-MC: m/z 487 (MH +)3Н). XIAT-MC: m/z 272 [MH +]. Приклад 9 Етап IV: N-(2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[14-(Ацетиламіно)-3-{[(2S)-2-метилоксиран-2бензофуран-2,4’-піперидин]-1’-іл)-2-гідрокси-2іл]метокси}феніл бензоат метилпропіл]окси}-4-гідроксифеніл)ацетамід, триЦю сполуку отримують з 4-(ацетиламіно)-3флуорацетат гідроксифеніл бензоату (2,71г, 10ммоль) та [(2S)-2Етап І: метилоксиран-2-іл]метил 32-Метил-1,3-бензоксазол-6-ол нітробензолсульфонату, застосовуючи стандартПри перемішуванні до розчину 1-(2,4ний спосіб та 1-метилпіролідин-2-он, як розчинник. дигідроксифеніл)етанону (20г, 131ммоль) у піриФлеш-хроматографія на силікагелі (етилацетат/ндині (80мл)додають протягом 15 хвилин невелигептан) дає названу сполуку, як безбарвний тверкими порціями при кімнатній температурі гідроксидий продукт (1,31г, 3,9ммоль, 39%). 1 ламіну гідрохлорид (9,1г, 131ммоль). Реакційну Н-ЯМР (400МГц, CDCI3): δ 8,41 (d, 1H), 8,18 суміш перемішують протягом 20 годин, а потім (m, 2H), 7,91 (br.s, 1H), 7,63 (m, 1H), 7,50. (m, 2H), розводять водою (600мл)та екстрагують етилаце6,83 (m, 1H),4,15 (d, J=10,8Гц, 1Н), 4,03 (d, татом (2´250мл). Комбіновані органічні екстракти J=10,8Гц, 1Н), 3,99 (d, J=10,8Гц, 1H), 2,92 (d, промивають водою (2´250мл) та 5% водною НСІ J=4,6Гц, 1H), 2,78 (d, J=4,6Гц, 1H), 2,22 (s, 3Н), (250мл). Розчинник видаляють у вакуумі. Воду 1,48 (s, 3Н). (200мл) додають до залишку, а потім концентруXIAT-MC: m/z 342 [MH +]. ють у вакуумі, тоді додають толуол (200мл) та 59 77814 60 Етап V: піперидину] (26мг, 0,116ммоль) та N-{5-хлор-2N-(2-{[(2S)-3-(5-xлop-1’Н,3Н-спіро[1[(2S)-оксиран-2-ілметокси]феніл}ацетаміду (28мг, бензофуран-2,4’-піперидин]-1’-іл)-2-гідрокси-20,116ммоль) в етанолі (3мл) перемішують при метилпропіл]окси}-4-гідроксифеніл)ацетамід, три80°С протягом ночі. Летючі продукти видаляють у флуорацетат вакуумі та залишок очищають флешРозчин 5-хлор-3Н-спіро[1-бензофуран-2,4’хроматографією на силікагелі (0-2% метанолу у піперидину] (20,0мг, 0,09ммоль) та 4дихлорметані, 0,2% амоній гідроксиду) з утворен(ацетиламіно)-3-{[(2S)-2-метилоксиран-2ням названої сполуки (28мг). 1 іл]метокси}феніл бензоату (30,5мг, 0,09ммоль) у Н-ЯМР (CD3OD, 400МГц): δ 8,18 (d, J=2,4Гц, метанолі (2мл) кип’ятять під зворотним холодиль1H); 7,30-7,20 (m, 3Н); 7,10-7,00 (m, 2H); 5,02 (s, ником протягом 3 годин. Реакційну суміш охоло2H); 4,23 (m, 1H); 4,14 (dd, J=3,1, 9,9Гц, 1H); 3,99 джують до кімнатної температури та додають 1 (dd, J=6,5, 9,9Гц, 1Н); 2,93 (m, 2H); 2,63 (d, J=6,3Гц, краплю 20% NaOH в етанолі. Суміш перемішують 2H); 2,55 (m, 2H); 2,21 (s, 3Н); 2,00 (m, 2H); 1,73 (m, при кімнатній температурі протягом 3 годин. Роз2H). XIAT-MC: m/z 467 (MH +). чинник відганяють під зменшеним тиском. ЗалиПриклад 11 шок очищають за допомогою ВЕРХ (колонка "KroN-(2-{[(2S)-3-(6-хлор-1’Н,3Н-спіро[2masil"; елюент: [ацетонітрил +0,1% бензофуран-1,4’-піперидин]-1’-іл)-2трифлуороцтова кислота (ТФОК)/вода +0,1% гідроксипропіл]окси}-4-флуорфеніл)ацетамід ТФОК]), отримуючи безбарвний твердий продукт Суміш 6-хлор-3Н-спіро[2-бензофуран-1,4’(41мг, 0,07ммоль, 79%). піперидину] (30мг, 0,134ммоль)та N-{4-флуор-21 Н-ЯМР (400МГц, ацетон-d6): δ 8,67 (br. s, 1H), [(2S)-оксиран-2-ілметокси]феніл}ацетаміду (30мг, 7,71 (d, J=7,0Гц, 1H), 7,22 (s, 1H), 7,12 (dd, J=2,3, 0,134ммоль) в етанолі (3мл) перемішують при 8,5Гц, 1Н), 6,75 (d, J=8,5Гц, 1Н), 6,59 (d, J=2,6Гц, 80°С протягом ночі. Летючі продукти видаляють у 1Н), 6,42 (dd, J=2,6, 8,6Гц, 1H), 4,03 (d, 1H), 3,97 (d, вакуумі та залишок очищають флешJ=9,7Гц, 1H), 3,92 (br.s, 1H), 3,82 (br. s, 1H), 3,70 (d, хроматографією на силікагелі (0-1% метанолу у J=13,6Гц, 1H), 3,52 (m, 3H), 2,1-2,5 (m, 4H), 2,10 (s, дихлорметані, 0,2% амоній гідроксиду) з утворен3H), 1,51 (s, 3H). XIAT-MC: m/z 461 [MH +], ням названої сполуки (40мг). 1Н-ЯМР (CD3OD, Приклад 10 400МГц): δ 7,90 (dd, J=6,2, 8,9Гц, 1H); 7,29-7,20 (m, N-(2-{[(2S)-3-(5-хлор-1’Н,3Н-спіро[13Н); 6,89 (dd, J=2,7, 10,5Гц, 1H); 6,67 (m, 1H); 5,02 бензофуран-2,4’-піперидин]-1’-іл)-2-гідрокси-2(s, 2H); 4,23 (m, 1H); 4,13 (dd, J=3,1, 9,9Гц, 1H); метилпропіл]окси}феніл)ацетамід 4,01 (dd, J=6,3, 9,9Гц, 1H); 2,93 (m, 2H); 2,69-2,50 Етап І: (m, 4H); 2,20 (s, 3Н); 2,00 (m, 2H); 1,73 (br.d, N-(5-хлор-2-гідроксифеніл)ацетамід J=13,5Гц, 2Н). XIAT-MC: m/z 451 (MH +). У суспензію 2-аміно-4-хлорфенолу (1,43г, Приклад 12 10,0ммоль) у метанолі додають оцтовий ангідрид N-(2-{[(28)-3-(6-хлор-1’Н,3Н-спіро[2(0,945мл, 10,0ммоль) та реакційну суміш перемібензофуран-1,4’-піперидин]-1’-іл)-2шують при кімнатній температурі протягом 2 гогідроксипропіл]окси}феніл)ацетамід дин. Летючі продукти видаляють у вакуумі з утвоСуміш 6-хлор-3Н-спіро[2-бензофуран-1,4’ренням названої сполуки (1,5г). піперидину] (25мг, 0,1 13ммоль) та N-{2-[(2S)1 Н-ЯМР (ДMCO-d6 , 400МГц): δ 10,20 (br.s, 1Н); оксиран-2-ілметокси]феніл}ацетаміду (23мг, 9,21 (s, 1Н); 8,00 (d, J=2,6Гц, 1Н); 6,94 (dd, J=2,6, 0,111ммоль) в етанолі (2мл) перемішують при 8,7Гц, 1H); 6,84 (d, J=8,7Гц, 1H); 2,02 (s, 3Н). 80°С протягом ночі. Летючі продукти видаляють у Етап II: вакуумі та залишок очищають флешN-{5-хлор-2-[(2S)-оксиран-2хроматографіею на силікагелі (0-1% метанолу у ілметокси]феніл}ацетамід дихлорметані, 0,2% амоній гідроксиду) з утворенСуміш N-(5-хлор-2-гідроксифеніл)ацетаміду ням названої сполуки (20мг). 1 (500мг, 2,69ммоль), (2S)-оксиран-2-ілметил 3Н-ЯМР (CD3OD, 400МГц): δ 8,00 (dd, J=1,3, нітробензолсульфонату (697мг, 2,69ммоль) та 5,0Гц, 1Н); 7,30-7,20 (m, 3Н); 7,12-7,05 (m, 2H); цезій карбонату (1,04г, 3,22ммоль) у ДМФ (10мл) 6,93 (m, 1H); 5,01 (s, 2H); 4,22 (m, 1H); 4,14 (dd, перемішують при кімнатній температурі протягом J=3,3, 9,9Гц, 1Н); 4,00 (dd, J=6,4, 9,9Гц, 1H); 2,94 ночі. Реакційну суміш розподіляють між етилаце(m, 2H); 2,69-2,52 (m, 4H); 2,20 (s, 3Н); 2,01 (m, 2H); татом та водою. Органічний шар сушать натрій 1,74 (br.d, J=13,5Гц, 2H). XIAT-MC: m/z 433 (MH +). сульфатом, фільтрують та концентрують. Залишок Приклад 13 очищають флеш-хроматографією на силікагелі (0N-(2-{[(2S)-3-(6-хлор-1Н’,3Н-спіро[250% етилацетат у петролейному ефірі) з утворенбензофуран-1,4’-піперидин]-1’-іл)-2ням названої сполуки (600мг). 1Н-ЯМР (CDCI3, гідроксипропіл]окси}-4-метоксифеніл)ацетамід 400МГц): δ 8,47 (d, J=2,3Гц, 1H); 7,93 (br.s, 1Н); Суміш 6-хлор-3Н-спіро[2-бензофуран-1,4’6,98 (dd, 7-2,3, 8,7Гц, 1Н); 6,83 (d, J=8,7Гц, 1Н); піперидину] (46мг, 0,205ммоль) та N-{4-метокси4,36 (dd, J=2,4, 11,3Гц, 1Н); 3,94 (dd, J=6,1, 11,3Гц, 2[(2S)-оксиран-2-ілметокси]феніл}ацетаміду 1Н); 3,39 (m, 1H); 2,98 (m, 1Н); 2,81 (dd, J=2,7, (48,6мг, 0,205ммоль) в етанолі (2мл) перемішують 4,8Гц, 1Н); 2,22-{s, 3Н). XIAT -МС: m/z 242 (МН+). при 80°С протягом ночі. Летючі продукти видаляЕтап III: ють у вакуумі та залишок очищають флешN-(5-хлор-2-{[(2S)-3-(6-хлор-1’Н,3Н-спіро[2хроматографією на силікагелі (0-1,5% метанолу у бензофуран-1,4’-піперидин]-1’-іл)-2дихлорметані, 0,2% амоній гідроксиду) з утворенгідроксипропіл]окси}феніл)ацетамід ням названої сполуки (80мг). 1Н-ЯМР (CD3OD, Суміш 6-хлор-3Н-спіро[2-бензофуран-1,4’400МГц): δ 7,75 (d, J=8,9Гц, 1Н); 7,29-7,20 (m, 3Н);
ДивитисяДодаткова інформація
Назва патенту англійськоюSpirocyclic piperidines as antagonists of mch1 and use thereof
Автори англійськоюJIANG YU, LU KAI, CHEN CHIEN AN, ANDERSEN KIM
Назва патенту російськоюСпироциклические пиперидины как антагонисты mch1 и их применение
Автори російськоюДжианг Ю, Лу Кай, Чен Чиен-Ан, Андерсен Ким
МПК / Мітки
МПК: C07D 413/12, C07D 405/12, C07D 409/12, C07D 401/06, C07D 491/10, C07D 401/12, C07D 221/20
Мітки: піперидини, застосування, спіроциклічні, антагоністи
Код посилання
<a href="https://ua.patents.su/79-77814-spirociklichni-piperidini-yak-antagonisti-mch1-ta-kh-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Спіроциклічні піперидини як антагоністи mch1 та їх застосування</a>
Попередній патент: Спосіб діагностики тромбованої аневризми лівого шлуночка методом електрокардіографії
Наступний патент: Апарат для створення високого тиску і температури
Випадковий патент: Монтажно-випробувальний корпус ракети