Протимікобактеріальні сполуки, спосіб їх одержання, фармацевтична композиція на їх основі
Номер патенту: 81640
Опубліковано: 25.01.2008
Автори: Упадхайайа Рам Шанкар, Сінха Ракеш Кумар, Сінха Нееліма, Арора Судершан Кумар, Джаін Санджай, Аджай Шанкар, Джана Гурхарі
Формула / Реферат
1. Сполука формули (І), її таутомери, енантіомери, діастереомери, N-оксиди, поліморфи і їх фармацевтично прийнятні солі
 , (І)
, (І)
де
R1 - С1-С4 алкіл, С1-С4 алкокси, С1-С4 тіоалкокси, трифторалкіл, трифторалкокси або гідроксіалкіл;
R2 вибраний із групи, яка включає
і) феніл, незаміщений чи заміщений одним або двома замісниками, кожний з яких незалежно вибраний із групи, що включає галоген, С1-С4 алкіл, С1-С4 алкокси, С1-С4 тіоалкокси, нітро, галоалкіл, галоалкокси, незаміщений чи заміщений піперазин, морфолін, тіоморфолін, піролідин і піперидин, або
іі) гідроксіалкіл, або
ііі) тіазол, або
iv) тіадіазол, або
v) піридин, або
vi) нафталін, або
vii) NHCOR6, де R6 - арил, гетероарил;
R3 - феніл або заміщений феніл, арил,
якщо один з R4 і R5 - Н, тоді іншій є -(СH2)n-R7, де n = 1-3 і R7 вибраний із групи
 ,
,
де
R8 - феніл, незаміщений чи заміщений 1-2 замісниками, кожний з яких незалежно вибраний із групи, що включає галоген, С1-С4 алкіл, С1-С4 алкокси, С1-С4 тіоалкокси, нітро, аміно, галоалкіл, галоалкокси; бензил або бензил, заміщений 3,4-метилендіокси; гетероарил; гетероароїл; дифенілметил,
m = 0-2, і
Х є -NCH3, СН2, S, SO або SO2;
так, що коли R2 такий, як зазначено в (і) або (v) вище, a R4 являє собою Н, R7 являє собою
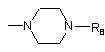 ,
,
R8 - феніл, незаміщений або заміщений 1-2 замісниками, кожний з яких незалежно вибраний із групи, що включає галоген, С1-С4 алкокси, С1-С4 тіоалкокси, нітро, аміно галоалкіл, галоалкокси; бензил або бензил, заміщений 3,4-метилендіокси; гетероарил; гетероароїл; дифенілметил.
2. Сполука, її таутомери, енантіомери, діастереомери, N-оксиди, поліморфи і їх фармацевтично прийнятні солі за п. 1, де сполука формули І вибрана з групи, що включає
1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3-іл]метил}-4-(4-фторфеніл)піперазин,
1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3-іл]метил}-4-(2-метоксифеніл)піперазин,
1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3-іл]метил}-4-(3-трифторметилфеніл)піперазин,
1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3-іл]метил}-4-(2піридил)піперазин,
1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3-іл]метил}-4-(2-піримідил)піперазин,
1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3-іл]піримідил}-4-(дифенілметил)піперазин,
4-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3-іл]піримідил}піперазиніл-2-фурилкетон,
5-[(4-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3-іл]метил}піперазиніл)метил]-2Н-бензо[d]1,3-діоксолен,
1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3-іл]метил}-4-(2-метил-5-хлорфеніл)піперазин,
N-(3-{[4-(4-фторфеніл)піперазиніл]метил}-2-метил-5-фенілпіроліл)-4-піридилкарбоксамід,
N-(3-{[4-(3-фторфеніл)піперазиніл]метил}-2-метил-5-фенілпіроліл)-4-піридилкарбоксамід,
N-(3-{[4-(2-метоксифеніл)піперазиніл]метил}-2-метил-5-фенілпіроліл)-4-піридилкарбоксамід,
N-(3-{[4-(2-піридил)піперазиніл]метил}-2-метил-5-фенілпіроліл)-4-піридилкарбоксамід,
N-(2-метил-5-феніл-3-{[4-бензилпіперазиніл]метил}піроліл)-4-піридилкарбоксамід,
N-{2-метил-3-[(4-метилпіперазиніл]метил}-5-фенілпіроліл)-4-піридилкарбоксамід,
N-(3-{[4-(2H-бензо[d]1,3-діоксолен-5-ілметил)піперазиніл]метил}-2-метил-5-фенілпіроліл)-4-піридилкарбоксамід,
N-(2-метил-5-феніл-3-(піперидилметил)піроліл)-4-піридилкарбоксамід,
N-(2-метил-5-феніл-3-(піролідинілметил)піроліл)-4-піридилкарбоксамід,
N-[2-метил-3-(морфолін-4-ілметил)-5-фенілпіроліл)-4-піридилкарбоксамід,
N-(2-метил-5-феніл-3-(1,4-тіазапергідроїн-4-ілметил)піроліл)-4-піридилкарбоксамід,
N-(3-{[4-(4-фторфеніл)піперазиніл]метил}-5-метил-2-фенілпіроліл)-4-піридилкарбоксамід,
N-(3-{[4-(3-трифторметилфеніл)піперазиніл]метил}-5-метил-2-фенілпіроліл)-4-піридилкарбоксамід,
N-(3-{[4-(2Н-бензо[3,4-d]1,3-діоксолен-5-ілметил)піперазиніл]метил}-5-метил-2-фенілпіроліл)-4-піридилкарбоксамід,
N-(3-{[4-(4-фторфеніл)піперазиніл]метил}-2-метил-5-фенілпіроліл)піразин-2-ілкарбоксамід,
N-(3-{[4-(2-метоксифеніл)піперазиніл]метил}-2-метил-5-фенілпіроліл)піразин-2-ілкарбоксамід,
N-(3-{[4-(3-трифторметилфеніл)піперазиніл]метил}-2-метил-5-фенілпіроліл)піразин-2-ілкарбоксамід,
N-(3-{[4-(2-піpидил)пiпepaзинiл]мeтил}-2-мeтил-5-фeнiлпipoлiл)піpaзин-2-iлкарбоксамід,
N-(3-{[4-(2Н-бензо[d]1,3-діоксолен-5-ілметил)піперазиніл]метил}-2-метил-5-фенілпіроліл)піразин-2-ілкарбоксамід,
N-(3-{[4-(дифенілметил)піперазиніл]метил}-2-метил-5-фенілпіроліл)піразин-2-ілкарбоксамід,
N-(3-{[4-(4-фторфеніл)піперазиніл]метил}-5-метил-2-фенілпіроліл)піразин-2-ілкарбоксамід,
N-(3-{[4-(2-метоксифеніл)піперазиніл]метил}-5-метил-2-фенілпіроліл)піразин-2-ілкарбоксамід,
N-(3-{[4-(3-трифторметилфеніл)піперазиніл]метил}-5-метил-2-фенілпіроліл)піразин-2-ілкарбоксамід,
N-(3-{[4-(2-піридил)піперазиніл]метил}-5-метил-2-фенілпіроліл)піразин-2-ілкарбоксамід,
N-(3-{[4-(2Н-бензо[3,4-d]1,3-діоксолан-5-ілметил)піперазиніл]метил}-5-метил-2-фенілпіроліл)піразин-2-ілкарбоксамід,
N-(3-{[4-(дифенілметил)піперазиніл]метил}-5-метил-2-фенілпіроліл)піразин-2-ілкарбоксамід,
N-(5-(4-хлорфеніл)-3-{[4-(4-фторфеніл)піперазиніл]метил}-2-метил-5-феніліпіроліл)піразин-2-ілкарбоксамід,
N-(5-(4-хлорфеніл)-3-{[4-(2-метоксифеніл)піперазиніл]метил}-2-метил-5-фенілпіроліл)піразин-2-ілкарбоксамід,
N-(5-(4-хлорфеніл)-3-{[4-(3-трифторметилфеніл)піперазиніл]метил}-2-метил-5-фенілпіроліл)піразин-2-ілкарбоксамід,
N-(5-(4-хлорфеніл)-3-{[4-(2-піридил)піперазиніл]метил}-2-метил-5-фенілтроліл)піразин-2-ілкарбоксамід,
N-(2-(4-хлорфеніл)-3-{[4-(4-фторфеніл)піперазиніл]метил}-5-метилпіроліл)піразин-2-ілкарбоксамід,
N-(2-(4-хлорфеніл)-3-{[4-(2-метоксифеніл)піперазиніл]метил}-5-метиліпіроліл)піразин-2-ілкарбоксамід,
N-(2-(4-хлорфеніл)-3-{[4-(3-трифторметилфеніл)піперазиніл]метил}-5-метилпіроліл)піразин-2-ілкарбоксамід,
1-{[1-(2,4-дифторфеніл)-5-(4-хлорфеніл)-2-метилпірол-3-іл]метил}-4-(4-фторфеніл)піперазин,
1-{[1-(2,4-дифторфеніл)-5-(4-хлорфеніл)-2-метилпірол-3-іл]метил}-4-(2-метоксифеніл)піперазин,
1-{[1-(2,4-дифторфеніл)-5-(4-хлорфеніл)-2-метилпірол-3-іл]метил}-4-(3-трифторметилфеніл)піперазин,
1-{[1-(2,4-дифторфеніл)-5-(4-хлорфеніл)-2-метилпірол-3-іл]метил}-4-(2-піридил)піперазин,
1-{[1-(2,4-дифторфеніл)-5-(4-хлорфеніл)-2-метиліпірол-3-іл]метил}-4-(4-дифенілметил)піперазин,
1-{[1-(2,4-дифторфеніл)-2-(4-хлорфеніл)-5-метилпірол-3-іл]метил}-4-(дифенілметил)піперазин,
5-[(4-{[1-(2,4-дифторфеніл)-5-(4-хлорфеніл)-2-метилпірол-3-іл]метил}піперазиніл)метил]-2Н-бензо[d]1,3-діоксолен,
1-{[1-(2,4-дифторфеніл)-2-метил-5-фенілпірол-3-іл]метил}-4-(4-фторфеніл)піперазин,
1-{[1-(2,4-дифторфеніл)-2-метил-5-фенілпірол-3-іл]метил}-4-(2-метоксифеніл)піперазин,
1-{[1-(2,4-дифторфеніл)-2-метил-5-фенілпірол-3-іл]метил}-4-(3-трифторметилфеніл)піперазин,
1-{[1-(2,4-дифторфеніл)-2-метил-5-фенілпірол-3-іл]метил}-4-(2-піридил)піперазин,
1-{[1-(2,4-дифторфеніл)-5-метил-2-фенілпірол-3-іл]метил}-4-(4-фторфеніл)піперазин,
1-{[1-(2,4-дифторфеніл)-5-метил-2-фенілпірол-3-іл]метил}-4-(2-метоксифеніл)піперазин,
1-{[1-(2,4-дифторфеніл)-5-метил-2-фенілпірол-3-іл]метил}-4-(3-трифторметилфеніл)піперазин,
1-{[1-(2,4-дифторфеніл)-5-метил-2-фенілпірол-3-іл]метил}-4-(2-піридил)піперазин,
1-{[5-(4-хлорфеніл)-2-метил-1-нафтилпірол-3-іл]метил}-4-(4-фторфеніл)піперазин,
1-{[5-(4-хлорфеніл)-2-метил-1-нафтилпірол-3-іл]метил}-4-(2-метоксифеніл)піперазин,
1-{[5-(4-хлорфеніл)-2-метил-1-нафтилпірол-3-іл]метил}-4-(3-трифторметилфеніл)піперазин,
5-[(4-{[5-(4-хлорфеніл)-2-метил-1-нафтилпірол-3-іл]метил}піперазиніл)метил]-2Н-бензо[d]1,3-діоксолен,
1-{[2-(4-хлорфеніл)-5-метил-1-нафтилпірол-3-іл]метил}-4-(2-метоксифеніл)піперазин,
1-{[2-(4-хлорфеніл)-5-метил-1-нафтилпірол-3-іл]метил}-4-(3-трифторметилфеніл)піперазин,
1-{[2-(4-хлорфеніл)-5-метил-1-нафтилпірол-3-іл]метил}-4-(2-піридил)піперазин,
N-(5-(4-xлopфeнiл)-3-{[4-(4-фтopфeнiл)піпepaзинiл]мeтил}-2-мeтилпіpoлiл)-4-піридилкарбоксамід,
N-(5-(4-хлорфеніл)-3-{[4-(2-метоксифеніл)піперазиніл]метил}-2-метилпіроліл)-4-піридилкарбоксамід,
N-(5-(4-хлорфеніл)-3-{[4-(3-трифторметилфеніл)піперазиніл]метил}-2-метилпіроліл)-4-піридилкарбоксамід,
N-(5-(4-хлорфеніл)-3-{[4-(2-піридил)піперазиніл]метил}-2-метилпіроліл)-4-піридилкарбоксамід,
N-(3-{[4-(2H-бензо[d]1,3-діоксолен-5-ілметил)піперазиніл]метил}-5-(4-хлорфеніл)-2-метилпіроліл)-4-піридилкарбоксамід,
N-(2-(4-хлорфеніл)-3-{[4-(4-фторфеніл)піперазиніл]метил}-5-метилпіроліл)-4-піридилкарбоксамід,
N-(2-(4-хлорфеніл)-3-{[4-(2-метоксифеніл)піперазиніл]метил}-5-метилпіроліл)-4-піридилкарбоксамід,
N-(2-(4-хлорфеніл)-3-{[4-(3-трифторметилфеніл)піперазиніл]метил}-5-метилпіроліл)-4-піридилкарбоксамід,
N-(2-(4-хлорфеніл)-3-{[4-(2-піридил)піперазиніл]метил}-5-метилпіроліл)-4-піридилкарбоксамід,
N-(3-{[4-(2Н-бензо[3,4-d]1,3-діоксолан-5-ілметил)піперазиніл]метил}-2-(4-хлофеніл)-5-метилпіроліл)-4-піридилкарбоксамід,
4-(4-фторфеніл)-1-[(2-метил-5-феніл-1-(2-піридил)пірол-3-іл)метил]піперазин,
4-(2-метоксифеніл)-1-[(2-метил-5-феніл-1-(2-піридил)пірол-3-іл)метил]піперазин,
4-(3-трифторметилфеніл)-1-[(2-метил-5-феніл-1-(2-піридил)пірол-3-іл)метил]піперазин,
4-(2-піридил)-1-[(2-метил-5-феніл-1-(2-піридил)пірол-3-іл)метил]піперазин,
1-[(2-метил-5-феніл-1-(2-піридил)пірол-3-іл)метил]-4-(2-піридил)піперазин,
5-({4-[(2-метил-5-феніл-1-(2-піридил)пірол-3-іл)метил]піперазиніл}метил)-2Н-бензо[d]1,3-діоксолан,
4-(4-фторфеніл)-1-[(5-метил-2-феніл-1-(2-піридил)пірол-3-іл)метил]піперазин,
4-(2-метоксифеніл)-1-[(5-метил-2-феніл-1-(2-піридил)пірол-3-іл)метил]піперазин,
4-(3-трифторметилфеніл)-1-[(5-метил-2-феніл-1-(2-піридил)пірол-3-іл)метил]піперазин,
1-[(5-метил-2-феніл-1-(2-піридил)пірол-3-іл)метил]-4-(2-піридил)піперазин,
5-({4-[(5-метил-2-феніл-1-(2-піридил)пірол-3-іл)метил]піперазиніл}метил)-2Н-бензо[d]1,3-діоксолан,
1-{[1,5-біс(4-хлорфеніл)-2-етилпірол-3-іл]метил}-4-(3-трифторметилфеніл)піперазин,
N-[5-(4-хлорфеніл)-2-метил-3-(1,4-тіазапергідроїн-4-ілметил)піроліл]-4-піридилкарбоксамід,
2-[3-(гідроксиметил)-5-метил-2-феніл-4-(1,4-тіазапергідроїн-4-ілметил)піроліл]бутан-1-ол і
2-[2-метил-5-феніл-3-(1,4-тіазапергідроїн-4-ілметил)піроліл]бутан-1-ол.
3. Фармацевтична композиція, що містить: а) щонайменше одну або декілька сполук за п. 1 або 2, їх таутомери, енантіомери, діастереомери, N-оксиди, поліморфи і фармацевтично прийнятні солі; b) їх фармацевтично прийнятні носії.
4. Фармацевтична композиція за п. 3, яка є твердим або рідким препаратом.
5. Фармацевтична композиція за п. 3, що призначена для орального або парентерального введення.
6. Спосіб інгібування росту клітини мікроорганізму, при якому виконують контактування/вплив на клітину мікроорганізму щонайменше однією сполукою формули (І), її таутомерами, енантіомерами, діастереомерами, N-оксидами, поліморфами і їх фармацевтично прийнятними солями, з їх фармацевтичними носіями або без них.
7. Спосіб за п. 6, у якому клітиною мікроорганізму є Mycobacterium tuberculosis, резистентна до лікарських препаратів М.tuberculosis, M.Avium - внутрішньоклітинний комплекс, М.Fortuitum і М.kansasii.
8. Спосіб лікування мікобактеріальних інфекцій у ссавців, що включає введення ефективної протимікобактеріальної кількості щонайменше однієї сполуки формули І, її таутомерів, енантіомерів, діастереомерів, N-оксидів, поліморфів і їх фармацевтично прийнятних солей, з їх фармацевтичними носіями або без них.
9. Спосіб за п. 8 лікування туберкульозу у ссавців, що включає введення ефективної протимікобактеріальної кількості щонайменше однієї сполуки формули І, її таутомерів, енантіомерів, діастереомерів, N-оксидів, поліморфів і їх фармацевтично прийнятних солей, з їх фармацевтичними носіями або без них.
10. Спосіб одержання сполуки формули (І)
 , (І)
, (І)
при якому дану сполуку одержують реакцією сполуки формули (V)
 , (V)
, (V)
де
R1 - С1-С4 алкіл, С1-С4 алкокси, С1-С4 тіоалкокси, трифторалкіл, трифторалкокси або гідроксіалкіл;
R2 вибраний із групи, що включає
і) феніл, незаміщений чи заміщений одним або двома замісниками, кожний з яких незалежно вибраний із групи, що включає галоген, С1-С4 алкіл, С1-С4 алкокси, С1-С4 тіоалкокси, нітро, галоалкіл, галоалкокси, незаміщений чи заміщений піперазин, морфолін, тіоморфолін, піролідин і піперидин, або
іі) гідроксіалкіл, або
ііі) тіазол, або
iv) тіадіазол, або
v) піридин, або
vi) нафталін, або
vii) NHCOR6, де R6 - арил, гетероарил, гетероцикліл;
R3 - феніл або заміщений феніл, арил, гетероарил, а один з R4 та R5 являє собою Н, а другий являє собою -(CH2)n-R7, де n = 1-3,
з формальдегідом та аміном формули R7H, де R7 вибраний із групи
 ,
,
де R8 - феніл, незаміщений чи заміщений одним або двома замісниками, кожний з яких незалежно вибраний із групи, що включає галоген, С1-С4 алкіл, С1-С4 алкокси, С1-С4 тіоалкокси, нітро, аміно, галоалкіл, галоалкокси; бензил або бензил, заміщений 3,4-метилендіокси; гетероарил; гетероароїл; дифенілметил;
m - 0-2, і
Х є -NCH3, CH2, S, SO або SO2,
якщо в сполуці формули І один з R4 і R5 є Н, іншій є -(СН2)n-R7,
де n = 1-3 і R7 вибраний із групи
 ,
,
і так, що коли R2 зазначений в (і) або (у) вище, R7 являє собою
 ,
,
де R8 - феніл, незаміщений чи заміщений одним або двома замісниками, кожний з яких незалежно вибраний із групи, що включає галоген, С1-С4 алкіл, С1-С4 алкокси, С1-С4 тіоалкокси, нітро, аміно, галоалкіл, галоалкокси; бензил або бензил, заміщений 3,4-метилендіокси; гетероарил; гетероароїл; дифенілметил;
m = 0-2, і
Х являється -NСН3, СН2, S, SO або SO2;
11. Спосіб за п. 10, у якому сполуку формули (V) одержують реакцією сполуки формули (IV)
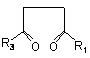 , (IV)
, (IV)
де R1 - С1-С4 алкіл, С1-С4 алкокси, С1-С4 тіоалкокси, трифторалкіл, трифторалкокси або гідроксіалкіл;
R3 - феніл або заміщений феніл, арил, гетероарил,
з аміном формули R2-NH2, де R2 вибраний із групи, що включає
і) феніл, незаміщений чи заміщений одним або двома замісниками, кожний з яких незалежно вибраний із групи, що включає галоген, С1-С4 алкіл, С1-С4 алкокси, С1-С4 тіоалкокси, нітро, галоалкіл, галоалкокси, незаміщений чи заміщений піперазин, морфолін, тіоморфолін, піролідин і піперидин, або
іі) гідроксіалкіл, або
ііі) тіазол, або
iv) тіадіазол, або
v) піридин, чи
vi) нафталін, або
vii) NHCOR6, де R6 - арил, гетероарил, гетероцикліл.
12. Спосіб за п. 11, у якому сполуку формули (IV) одержують реакцією сполуки формули (II)
R3-Н, (ІІ)
де R3 - феніл або заміщений феніл, арил, гетероарил,
із сполукою формули (III)
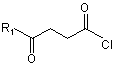 , (III)
, (III)
де R1 - С1-С4 алкіл, С1-С4 алкокси, С1-С4 тіоалкокси, трифторалкіл, трифторалкокси або гідроксіалкіл.
13. Спосіб за п. 12, у якому сполуку формули (IV) одержують реакцією сполуки формули (VI)
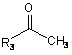 , (VІ)
, (VІ)
де R3 - феніл або заміщений феніл, арил, гетероарил,
із сполукою формули (VII)
 , (VII)
, (VII)
де R1 – С1-С4 алкіл, С1-С4 алкокси, С1-С4 тіоалкокси, трифторалкіл, трифторалкокси або гідроксіалкіл.
Текст
1. Сполука формули (І), її та утомери, енантіомери, діастереомери, N-оксиди, поліморфи і їх фармацевтично прийнятні солі UA (21) a200503537 (22) 20.09.2002 (24) 25.01.2008 (86) PCT/IN2002/000189, 20.09.2002 (72) АРОРА СУДЕРШАН КУМАР, СІНХА НЕЕЛІМА, ДЖАІН САНДЖАЙ, УПАДХАЙ АЙА РАМ ШАНКАР, ДЖАН А ГУРХАРІ, АДЖАЙ ШАНКАР, СІНХА РАКЕШ КУ МАР (73) ЛЮПІН ЛІМІТЕД (56) DE 1938904 A, 05.02.1970 US 2986564 A, 30.05.1961 US 3168531 A, 02.02.1965 US 3168532 A, 02.02.1965 US 3246010 A, 12.04.1966 BIAVA M ET AL: "New Pyrrole Derivatives as Antimycobacterial Agents Analogs of BM212" BIOORGANIC & MEDICIN AL CHEMISTRY LETTERS, OXFORD, GB, vol. 9, no. 20, 18 October 1999 (1999-10-18), pages 2983-2988, XP004180522 ISSN: 0960-894X CERRETO F ET AL: "Studies on anti-Candida agents with a pyrrole moiety. Synthesis and microbiological activity of some 3-(aminomethyl)-1,5-diaryl-2methylpyrrole derivatives" EUROPEAN JOURNAL OF MEDICIN AL CHEMISTR Y, EDITIONS SCIENTIFIQUE ELSEVIER, PARIS, FR, vol. 27, 1992, pages 701-708, XP002230620 ISSN: 02235234 PORRETTA G C ET AL: "RESEARCH ON ANTIBACTERIAL AND ANTIFUNGAL AGENTS. XIISYNTHESIS AND ANTIMICROBIAL ACTIVITY OF SOME MANNICH BASES OF DIAR YLPYRROLES" FAR MACO, SOCIETA CHIMICA ITALIAN A, PAVIA, IT, vol. 50, no. 9, September 1995 (1995-09), pages 2 (19) 1 3 R4 81640 R5 N R3 R1 R2 , (І) де R1 - С1-С4 алкіл, С1-С4 алкокси, С1-С4 тіоалкокси, трифторалкіл, трифторалкокси або гідроксіалкіл; R2 вибраний із групи, яка включає і) феніл, незаміщений чи заміщений одним або двома замісниками, кожний з яких незалежно вибраний із групи, що включає галоген, С1-С4 алкіл, С1-С4 алкокси, С1-С4 тіоалкокси, нітро, галоалкіл, галоалкокси, незаміщений чи заміщений піперазин, морфолін, тіоморфолін, піролідин і піперидин, або іі) гідроксіалкіл, або ііі) тіазол, або iv) тіадіазол, або v) піридин, або vi) нафталін, або vii) NHCOR6, де R6 - арил, гетероарил; R3 - феніл або заміщений феніл, арил, якщо один з R4 і R5 - Н, тоді іншій є -(СH2)n-R7, де n = 1-3 і R7 вибраний із групи ( )m N N R8 і N X , де R8 - феніл, незаміщений чи заміщений 1-2 замісниками, кожний з яких незалежно вибраний із групи, що включає галоген, С1-С4 алкіл, С1-С4 алкокси, С1-С4 тіоалкокси, нітро, аміно, галоалкіл, галоалкокси; бензил або бензил, заміщений 3,4метилендіокси; гетероарил; гетероароїл; дифенілметил, m = 0-2, і Х є -NCH3, СН2, S, SO або SO2; так, що коли R2 такий, як зазначено в (і) або (v) вище, a R4 являє собою Н, R7 являє собою N N R8 , R8 - феніл, незаміщений або заміщений 1-2 замісниками, кожний з яких незалежно вибраний із групи, що включає галоген, С1-С4 алкокси, С1-С4 тіоалкокси, нітро, аміно галоалкіл, галоалкокси; бензил або бензил, заміщений 3,4-метилендіокси; гетероарил; гетероароїл; дифенілметил. 2. Сполука, її та утомери, енантіомери, діастереомери, N-оксиди, поліморфи і їх фармацевтично прийнятні солі за п. 1, де сполука формули І вибрана з групи, що включає 1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3-іл]метил}4-(4-фторфеніл)піперазин, 1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3-іл]метил}4-(2-метоксифеніл)піперазин, 1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3-іл]метил}4-(3-трифторметилфеніл)піперазин, 1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3-іл]метил} 4 4-(2піридил)піперазин, 1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3-іл]метил}4-(2-піримідил)піперазин, 1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3іл]піримідил}-4-(дифенілметил)піперазин, 4-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3іл]піримідил}піперазиніл-2-фурилкетон, 5-[(4-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3іл]метил}піперазиніл)метил]-2Н-бензо[d]1,3діоксолен, 1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3-іл]метил}4-(2-метил-5-хлорфеніл)піперазин, N-(3-{[4-(4-фторфеніл)піперазиніл]метил}-2-метил5-фенілпіроліл)-4-піридилкарбоксамід, N-(3-{[4-(3-фторфеніл)піперазиніл]метил}-2-метил5-фенілпіроліл)-4-піридилкарбоксамід, N-(3-{[4-(2-метоксифеніл)піперазиніл]метил}-2метил-5-фенілпіроліл)-4-піридилкарбоксамід, N-(3-{[4-(2-піридил)піперазиніл]метил}-2-метил-5фенілпіроліл)-4-піридилкарбоксамід, N-(2-метил-5-феніл-3-{[4бензилпіперазиніл]метил}піроліл)-4піридилкарбоксамід, N-{2-метил-3-[(4-метилпіперазиніл]метил}-5фенілпіроліл)-4-піридилкарбоксамід, N-(3-{[4-(2H-бензо[d]1,3-діоксолен-5ілметил)піперазиніл]метил}-2-метил-5фенілпіроліл)-4-піридилкарбоксамід, N-(2-метил-5-феніл-3-(піперидилметил)піроліл)-4піридилкарбоксамід, N-(2-метил-5-феніл-3-(піролідинілметил)піроліл)-4піридилкарбоксамід, N-[2-метил-3-(морфолін-4-ілметил)-5фенілпіроліл)-4-піридилкарбоксамід, N-(2-метил-5-феніл-3-(1,4-тіазапергідроїн-4ілметил)піроліл)-4-піридилкарбоксамід, N-(3-{[4-(4-фторфеніл)піперазиніл]метил}-5-метил2-фенілпіроліл)-4-піридилкарбоксамід, N-(3-{[4-(3трифторметилфеніл)піперазиніл]метил}-5-метил2-фенілпіроліл)-4-піридилкарбоксамід, N-(3-{[4-(2Н-бензо[3,4-d]1,3-діоксолен-5ілметил)піперазиніл]метил}-5-метил-2фенілпіроліл)-4-піридилкарбоксамід, N-(3-{[4-(4-фторфеніл)піперазиніл]метил}-2-метил5-фенілпіроліл)піразин-2-ілкарбоксамід, N-(3-{[4-(2-метоксифеніл)піперазиніл]метил}-2метил-5-фенілпіроліл)піразин-2-ілкарбоксамід, N-(3-{[4-(3трифторметилфеніл)піперазиніл]метил}-2-метил5-фенілпіроліл)піразин-2-ілкарбоксамід, N-(3-{[4-(2-піpидил)пiпepaзинiл]мeтил}-2-мeтил-5фeнiлпipoлiл)піpaзин-2-iлкарбоксамід, N-(3-{[4-(2Н-бензо[d]1,3-діоксолен-5ілметил)піперазиніл]метил}-2-метил-5фенілпіроліл)піразин-2-ілкарбоксамід, N-(3-{[4-(дифенілметил)піперазиніл]метил}-2метил-5-фенілпіроліл)піразин-2-ілкарбоксамід, N-(3-{[4-(4-фторфеніл)піперазиніл]метил}-5-метил2-фенілпіроліл)піразин-2-ілкарбоксамід, N-(3-{[4-(2-метоксифеніл)піперазиніл]метил}-5метил-2-фенілпіроліл)піразин-2-ілкарбоксамід, N-(3-{[4-(3трифторметилфеніл)піперазиніл]метил}-5-метил2-фенілпіроліл)піразин-2-ілкарбоксамід, 5 N-(3-{[4-(2-піридил)піперазиніл]метил}-5-метил-2фенілпіроліл)піразин-2-ілкарбоксамід, N-(3-{[4-(2Н-бензо[3,4-d]1,3-діоксолан-5ілметил)піперазиніл]метил}-5-метил-2фенілпіроліл)піразин-2-ілкарбоксамід, N-(3-{[4-(дифенілметил)піперазиніл]метил}-5метил-2-фенілпіроліл)піразин-2-ілкарбоксамід, N-(5-(4-хлорфеніл)-3-{[4-(4фтор феніл)піперазиніл]метил}-2-метил-5феніліпіроліл)піразин-2-ілкарбоксамід, N-(5-(4-хлорфеніл)-3-{[4-(2метоксифеніл)піперазиніл]метил}-2-метил-5фенілпіроліл)піразин-2-ілкарбоксамід, N-(5-(4-хлорфеніл)-3-{[4-(3трифторметилфеніл)піперазиніл]метил}-2-метил5-фенілпіроліл)піразин-2-ілкарбоксамід, N-(5-(4-хлорфеніл)-3-{[4-(2піридил)піперазиніл]метил}-2-метил-5фенілтроліл)піразин-2-ілкарбоксамід, N-(2-(4-хлорфеніл)-3-{[4-(4фтор феніл)піперазиніл]метил}-5метилпіроліл)піразин-2-ілкарбоксамід, N-(2-(4-хлорфеніл)-3-{[4-(2метоксифеніл)піперазиніл]метил}-5метиліпіроліл)піразин-2-ілкарбоксамід, N-(2-(4-хлорфеніл)-3-{[4-(3трифторметилфеніл)піперазиніл]метил}-5метилпіроліл)піразин-2-ілкарбоксамід, 1-{[1-(2,4-дифторфеніл)-5-(4-хлорфеніл)-2метилпірол-3-іл]метил}-4-(4-фторфеніл)піперазин, 1-{[1-(2,4-дифторфеніл)-5-(4-хлорфеніл)-2метилпірол-3-іл]метил}-4-(2метоксифеніл)піперазин, 1-{[1-(2,4-дифторфеніл)-5-(4-хлорфеніл)-2метилпірол-3-іл]метил}-4-(3трифторметилфеніл)піперазин, 1-{[1-(2,4-дифторфеніл)-5-(4-хлорфеніл)-2метилпірол-3-іл]метил}-4-(2-піридил)піперазин, 1-{[1-(2,4-дифторфеніл)-5-(4-хлорфеніл)-2метиліпірол-3-іл]метил}-4-(4дифенілметил)піперазин, 1-{[1-(2,4-дифторфеніл)-2-(4-хлорфеніл)-5метилпірол-3-іл]метил}-4(дифенілметил)піперазин, 5-[(4-{[1-(2,4-дифторфеніл)-5-(4-хлорфеніл)-2метилпірол-3-іл]метил}піперазиніл)метил]-2Нбензо[d]1,3-діоксолен, 1-{[1-(2,4-дифторфеніл)-2-метил-5-фенілпірол-3іл]метил}-4-(4-фторфеніл)піперазин, 1-{[1-(2,4-дифторфеніл)-2-метил-5-фенілпірол-3іл]метил}-4-(2-метоксифеніл)піперазин, 1-{[1-(2,4-дифторфеніл)-2-метил-5-фенілпірол-3іл]метил}-4-(3-трифторметилфеніл)піперазин, 1-{[1-(2,4-дифторфеніл)-2-метил-5-фенілпірол-3іл]метил}-4-(2-піридил)піперазин, 1-{[1-(2,4-дифторфеніл)-5-метил-2-фенілпірол-3іл]метил}-4-(4-фторфеніл)піперазин, 1-{[1-(2,4-дифторфеніл)-5-метил-2-фенілпірол-3іл]метил}-4-(2-метоксифеніл)піперазин, 1-{[1-(2,4-дифторфеніл)-5-метил-2-фенілпірол-3іл]метил}-4-(3-трифторметилфеніл)піперазин, 1-{[1-(2,4-дифторфеніл)-5-метил-2-фенілпірол-3іл]метил}-4-(2-піридил)піперазин, 1-{[5-(4-хлорфеніл)-2-метил-1-нафтилпірол-3іл]метил}-4-(4-фторфеніл)піперазин, 81640 6 1-{[5-(4-хлорфеніл)-2-метил-1-нафтилпірол-3іл]метил}-4-(2-метоксифеніл)піперазин, 1-{[5-(4-хлорфеніл)-2-метил-1-нафтилпірол-3іл]метил}-4-(3-трифторметилфеніл)піперазин, 5-[(4-{[5-(4-хлорфеніл)-2-метил-1-нафтилпірол-3іл]метил}піперазиніл)метил]-2Н-бензо[d]1,3діоксолен, 1-{[2-(4-хлорфеніл)-5-метил-1-нафтилпірол-3іл]метил}-4-(2-метоксифеніл)піперазин, 1-{[2-(4-хлорфеніл)-5-метил-1-нафтилпірол-3іл]метил}-4-(3-трифторметилфеніл)піперазин, 1-{[2-(4-хлорфеніл)-5-метил-1-нафтилпірол-3іл]метил}-4-(2-піридил)піперазин, N-(5-(4-xлopфeнiл)-3-{[4-(4фтop фeнiл)піпepaзинiл]мeтил}-2-мeтилпіpoлiл)-4піридилкарбоксамід, N-(5-(4-хлорфеніл)-3-{[4-(2метоксифеніл)піперазиніл]метил}-2-метилпіроліл)4-піридилкарбоксамід, N-(5-(4-хлорфеніл)-3-{[4-(3трифторметилфеніл)піперазиніл]метил}-2метилпіроліл)-4-піридилкарбоксамід, N-(5-(4-хлорфеніл)-3-{[4-(2піридил)піперазиніл]метил}-2-метилпіроліл)-4піридилкарбоксамід, N-(3-{[4-(2H-бензо[d]1,3-діоксолен-5ілметил)піперазиніл]метил}-5-(4-хлорфеніл)-2метилпіроліл)-4-піридилкарбоксамід, N-(2-(4-хлорфеніл)-3-{[4-(4фтор феніл)піперазиніл]метил}-5-метилпіроліл)-4піридилкарбоксамід, N-(2-(4-хлорфеніл)-3-{[4-(2метоксифеніл)піперазиніл]метил}-5-метилпіроліл)4-піридилкарбоксамід, N-(2-(4-хлорфеніл)-3-{[4-(3трифторметилфеніл)піперазиніл]метил}-5метилпіроліл)-4-піридилкарбоксамід, N-(2-(4-хлорфеніл)-3-{[4-(2піридил)піперазиніл]метил}-5-метилпіроліл)-4піридилкарбоксамід, N-(3-{[4-(2Н-бензо[3,4-d]1,3-діоксолан-5ілметил)піперазиніл]метил}-2-(4-хлофеніл)-5метилпіроліл)-4-піридилкарбоксамід, 4-(4-фторфеніл)-1-[(2-метил-5-феніл-1-(2піридил)пірол-3-іл)метил]піперазин, 4-(2-метоксифеніл)-1-[(2-метил-5-феніл-1-(2піридил)пірол-3-іл)метил]піперазин, 4-(3-трифторметилфеніл)-1-[(2-метил-5-феніл-1(2-піридил)пірол-3-іл)метил]піперазин, 4-(2-піридил)-1-[(2-метил-5-феніл-1-(2піридил)пірол-3-іл)метил]піперазин, 1-[(2-метил-5-феніл-1-(2-піридил)пірол-3-іл)метил]4-(2-піридил)піперазин, 5-({4-[(2-метил-5-феніл-1-(2-піридил)пірол-3іл)метил]піперазиніл}метил)-2Н-бензо[d]1,3діоксолан, 4-(4-фторфеніл)-1-[(5-метил-2-феніл-1-(2піридил)пірол-3-іл)метил]піперазин, 4-(2-метоксифеніл)-1-[(5-метил-2-феніл-1-(2піридил)пірол-3-іл)метил]піперазин, 4-(3-трифторметилфеніл)-1-[(5-метил-2-феніл-1(2-піридил)пірол-3-іл)метил]піперазин, 1-[(5-метил-2-феніл-1-(2-піридил)пірол-3-іл)метил]4-(2-піридил)піперазин, 5-({4-[(5-метил-2-феніл-1-(2-піридил)пірол-3 7 81640 іл)метил]піперазиніл}метил)-2Н-бензо[d]1,3діоксолан, 1-{[1,5-біс(4-хлорфеніл)-2-етилпірол-3-іл]метил}-4(3-трифторметилфеніл)піперазин, N-[5-(4-хлорфеніл)-2-метил-3-(1,4-тіазапергідроїн4-ілметил)піроліл]-4-піридилкарбоксамід, 2-[3-(гідроксиметил)-5-метил-2-феніл-4-(1,4тіазапергідроїн-4-ілметил)піроліл]бутан-1-ол і 2-[2-метил-5-феніл-3-(1,4-тіазапергідроїн-4ілметил)піроліл]бутан-1-ол. 3. Фармацевтична композиція, що містить: а) щонайменше одну або декілька сполук за п. 1 або 2, їх та утомери, енантіомери, діастереомери, Nоксиди, поліморфи і фармацевтично прийнятні солі; b) їх фармацевтично прийнятні носії. 4. Фармацевтична композиція за п. 3, яка є твердим або рідким препаратом. 5. Фармацевтична композиція за п. 3, що призначена для орального або парентерального введення. 6. Спосіб інгібування росту клітини мікроорганізму, при якому виконують контактування/вплив на клітину мікроорганізму щонайменше однією сполукою формули (І), її та утомерами, енантіомерами, діастереомерами, N-оксидами, поліморфами і їх фармацевтично прийнятними солями, з їх фармацевтичними носіями або без них. 7. Спосіб за п. 6, у якому клітиною мікроорганізму є Mycobacterium tuberculosis, резистентна до лікарських препаратів М.tuberculosis, M.Avium внутрішньоклітинний комплекс, М.Fortuitum і М.kansasii. 8. Спосіб лікування мікобактеріальних інфекцій у ссавців, що включає введення ефективної протимікобактеріальної кількості щонайменше однієї сполуки формули І, її та утомерів, енантіомерів, діастереомерів, N-оксидів, поліморфів і їх фармацевтично прийнятних солей, з їх фармацевтичними носіями або без них. 9. Спосіб за п. 8 лікування туберкульозу у ссавців, що включає введення ефективної протимікобактеріальної кількості щонайменше однієї сполуки формули І, її та утомерів, енантіомерів, діастереомерів, N-оксидів, поліморфів і їх фармацевтично прийнятних солей, з їх фармацевтичними носіями або без них. 10. Спосіб одержання сполуки формули (І) R4 R5 R3 N R1 R2 , (І) при якому дану сполуку одержують реакцією сполуки формули (V) R3 N R2 де 8 R1 - С1-С4 алкіл, С1-С4 алкокси, С1-С4 тіоалкокси, трифторалкіл, трифторалкокси або гідроксіалкіл; R2 вибраний із групи, що включає і) феніл, незаміщений чи заміщений одним або двома замісниками, кожний з яких незалежно вибраний із групи, що включає галоген, С1-С4 алкіл, С1-С4 алкокси, С1-С4 тіоалкокси, нітро, галоалкіл, галоалкокси, незаміщений чи заміщений піперазин, морфолін, тіоморфолін, піролідин і піперидин, або іі) гідроксіалкіл, або ііі) тіазол, або iv) тіадіазол, або v) піридин, або vi) нафталін, або vii) NHCOR6, де R6 - арил, гетероарил, гетероцикліл; R3 - феніл або заміщений феніл, арил, гетероарил, а один з R4 та R5 являє собою Н, а другий являє собою -(CH2)n-R7, де n = 1-3, з формальдегідом та аміном формули R7H, де R7 вибраний із групи ( )m N N R8 і N X , де R8 - феніл, незаміщений чи заміщений одним або двома замісниками, кожний з яких незалежно вибраний із групи, що включає галоген, С1-С4 алкіл, С1-С4 алкокси, С1-С4 тіоалкокси, нітро, аміно, галоалкіл, галоалкокси; бензил або бензил, заміщений 3,4-метилендіокси; гетероарил; гетероароїл; дифенілметил; m - 0-2, і Х є -NCH3, CH2, S, SO або SO2, якщо в сполуці формули І один з R4 і R5 є Н, іншій є -(СН2)n-R7, де n = 1-3 і R7 вибраний із групи ( )m N N R8 і N X , і так, що коли R2 зазначений в (і) або (у) ви ще, R7 являє собою N N R8 , де R8 - феніл, незаміщений чи заміщений одним або двома замісниками, кожний з яких незалежно вибраний із групи, що включає галоген, С1-С4 алкіл, С1-С4 алкокси, С1-С4 тіоалкокси, нітро, аміно, галоалкіл, галоалкокси; бензил або бензил, заміщений 3,4-метилендіокси; гетероарил; гетероароїл; дифенілметил; m = 0-2, і Х являється -NСН3, СН2, S, SO або SO 2; 11. Спосіб за п. 10, у якому сполуку формули (V) одержують реакцією сполуки формули (IV) R1 R3 , (V) O O R1 , (IV) де R1 - С1-С4 алкіл, С1-С4 алкокси, С1-С4 тіоалкокси, трифторалкіл, трифторалкокси або 9 81640 гідроксіалкіл; R3 - феніл або заміщений феніл, арил, гетероарил, з аміном формули R2-NH2, де R2 вибраний із групи, що включає і) феніл, незаміщений чи заміщений одним або двома замісниками, кожний з яких незалежно вибраний із групи, що включає галоген, С1-С4 алкіл, С1-С4 алкокси, С1-С4 тіоалкокси, нітро, галоалкіл, галоалкокси, незаміщений чи заміщений піперазин, морфолін, тіоморфолін, піролідин і піперидин, або іі) гідроксіалкіл, або ііі) тіазол, або iv) тіадіазол, або v) піридин, чи vi) нафталін, або vii) NHCOR6, де R6 - арил, гетероарил, гетероцикліл. 12. Спосіб за п. 11, у якому сполуку формули (IV) одержують реакцією сполуки формули (II) R3-Н, (ІІ) де R3 - феніл або заміщений феніл, арил, гетероарил, із сполукою формули (III) Даний винахід стосується нових 3- і/або 4-(4заміщених-піперазиніл)алкіл піролів формули (І), (I) і їх фармацевтично прийнятних кислотноадитивних солей, що проявляють протимікобактеріальну активність по відношенню до штамів Mycobacterium tuberculosis, як сприйнятливих, так і резистентних до лікарських препаратів. Протимікобактеріальна активність сполук за даним винаходом перевершує активність раніше відомих сполук. Даний винахід стосується також застосування нових сполук для лікування латентного туберкульозу, включаючи туберкульоз, що викликаний полірезистентними туберкульозними мікобактеріями. Винахід також стосується способів отримання нових сполук і фармацевтичних композицій, що містять згадані нові сполуки. Туберкульоз - інфекційна хвороба, що звичайно носить затяжний характер з поверненням загальних характерних проявів хвороби і завершується в більшості випадків летальним кінцем. Це захворювання є однією з найбільш важливих причин тривалої інвалідності і хронічної хвороби. Дана хвороба спричинюється туберкульозною паличкоподібною бактерією Mycobacterium tuberculosis, яку відносно важко контролювати. Лікарські препарати такі, як ізоніазид, рифампіцин, піразинамід, етамбутолу стрептоміцин, парааміносаліцилова кислота, етіонамід, циклосерин, капреоміцин, канаміцин, тіоацетазон та ін., застосовувалися і застосовуються в даний час у лікуванні 10 O R1 Cl O , (III) де R1 - С1-С4 алкіл, С1-С4 алкокси, С1-С4 тіоалкокси, трифторалкіл, трифторалкокси або гідроксіалкіл. 13. Спосіб за п. 12, у якому сполуку формули (IV) одержують реакцією сполуки формули (VI) O R3 CH3 , (VІ) де R3 - феніл або заміщений феніл, арил, гетероарил, із сполукою формули (VII) O R1 Br , (VII) де R1 – С1-С4 алкіл, С1-С4 алкокси, С1-С4 тіоалкокси, трифторалкіл, трифторалкокси або гідроксіалкіл. туберкульозу. Серед них: ізоніазид, рифамтцин, етамбутол і піразинамід - першочергові препарати вибору, що вводяться або як окремі лікарські композиції, або як композиції з двох чи більш вищевказаних лікарських препаратів у визначених пропорціях. Не дивлячись на те що, прийом кожного з вищезгаданих першочергових препаратів вибору має високу ефективність у лікуванні туберкульозу, ці препарати мають ряд недоліків, таких як неприємні побічні ефекти і відносно тривалий курс лікування. Останнє є результатом недотримання пацієнтом режиму лікування, призводить часто до невдач у лікуванні і, що особливо небезпечно, до розвитку лікарської резистентності туберкульозних мікобактерій. Розвиток лікарської резистентності є основною проблемою в лікуванні туберкульозу людини. Лікарські препарати другої черговості вибору, з однієї сторони менш ефективні, з другої сторони, більш дорогі і токсичні. Передбачається, що в наступні двадцять років більш ніж один мільярд людей на земній кулі можуть бути інфіковані туберкульозом, а 35 мільйонів людей загинуть від цієї хвороби (WHO Fact Sheet No.104, Global Alliance for ТВ Drug Development - Executive Summary of the Scientific Blueprint for ТВ De velopment). Сьогодні, з появою туберкульозу, що супроводжує вірус імунодефіциту людини, хвороба здобуває загрозливі розміри, як одна зі смертоносних хвороб у сві ті. Основний упор у вивченні протимікобактеріальних засобів в останнє десятиліття зроблено на розробку нових сполук для лікування хвороби, таких що a) широко варіюють за структурою, 11 81640 b) мають різні способи застосування/механізми дії; c) мають прийнятні фармакокінетичні властивості; d) безпечні і мають низьку частоту випадків побічних ефектів; е) забезпечують ефективний режим прийому. Кожний окремо новий клас сполук синтезовано і тестовано на активність щодо Mycobacterium tuberculosis, хімічні і біологічні особливості цих класів викладені в останньому огляді B.N. Roy [J. Ind Chem. Soc, April 2002, 79, 320-335] і в процитованих там джерелах. Заміщені похідні піролу складають окремий клас сполук, що перспективні в якості протимікобактеріальних засобів. Похідні піролу, що синтезовані і тестовані як на протитуберкулінову, так і на нетуберкулінову активність, розкриті в стаття х, приведених нижче. a) [D. Deidda et al. in Antimicrob. Agents and Chemother., Nov 1998, 3035-3037]. Ця стаття описує інгібуючу дію однієї зі сполук піролу, а саме ВМ 212, що має структурну формулу, приведену нижче, на Mycobacterium tuberculosis, включаючи полірезистентний до лікарських препаратів штам мікобактерії і деякі мікобактерії, що не викликають туберкульоз. Значення мінімальної інгібуючої концентрації (МІК) (мг/мл) щодо М. tuberculosis штаму 103471, яке продемонстровано сполукою ВМ 212, склало 0,70 у порівнянні з 0,25 у ізоніазиду. b) [М. Bia va et. al. in J. Med. Chem. Res., 1999,19-34] У цій статті повідомляється про синтез окремих аналогів ВМ 212, що мають загальну формулу 12 neoformans, грампозитивних або грамнегативних бактерій, ізолятів фітопатогенних грибів, Herpes simplex virus, штамів HSV1 і HSV2, Μ. tuberculosis, Μ. smegmatis,M. marinum і М. a vium. Проте, значення МІК (мг/мл) цих сполук щодо М. tuberculosis штаму 103471 гірше, ніж у ВМ 212 і знаходиться в діапазоні 4-16. c) [М. Bia va et. al. in Bioorg. & Med. Chem. Lett., 1999, 9,2983-2988]. Ця стаття описує синтез сполук піролу формули де Х-Н,абоСl; Υ -N, або СІ; R - N-метил піперазиніл чи тіоморфеніл, і їх відповідну активність in vitro щодо Μ. tuberculosis і видів mycobacteria, які не викликають туберкульоз. Проте, значення МІК (мг/мл) цих сполук проти М. tuberculosis штаму 103471 гірше, ніж у ВМ 212 і знаходиться в діапазоні 2-4. d) [F. Cerreto et. al. in Eur. J. Med. Chem., 1992, 27,701-708] У цій статті повідомляється про синтез конкретних похідних 3-аміно-1,5-діарил-2метилтролу і їх фунгіцидну активність in vitro проти Candida albicans і Candida sp. Проте, не повідомляється про активність таких сполук щодо М. tuberculosis. e) [С. Gillet et. al. in Eur. J. Med Chem.-Chimica Therapeutica, March-April 1976, 11 (2), 173-181]. У цій статті повідомляється про синтез окремих похідних піролу, що використовуються як протизапальні засоби і як антиалергени. f) [R. Ragno et. al, Bioorg. & Med. Chem., 2000, 8, 1423-1432]. Ця стаття повідомляє про синтез окремих біологічно активних похідних піролу, а також описує структур у взаємозв'язку між зазначеними сполуками піролу і протимікобактеріальною активністю. Сполуки, що синтезовані і тестовані авторами, приведені нижче: де Де і протимікробну активність сполук in vitro щодо Candida albicans, Candida sp, Cryptococcus 13 81640 14 іі) гідроксиалкіл, або ііі) незаміщений чи заміщений тіазол, або iv) незаміщений чи заміщений тіадіазол, або ν) незаміщений чи заміщений піридин, або vi) незаміщений чи заміщений нафталін, або vii) NHCOR6, де R6 - арил, незаміщений чи заміщений гетероарил, незаміщений чи заміщений гетероцикліл; R3 - феніл або заміщений феніл, арил, незаміщений чи заміщений гетероарил. Якщо один з R4 або R5 є воднем, тоді інший є (CH2)n-R7, де n=1-3 і R7 вибрано із групи де R - N, СІ, С2Н5 або ОСН 3 і R1 - Н, СІ, F, СН3 або ΝΟ2; A - N, R; Ζ - гр упа формули R2 - N, СІ, ОН або ОСН 3 і R3 - N або СІ. Жоден з вищезгаданих описів не повідомляє дію in vivo, включаючи токсичність будь-яких сполук, що описані тут, проти туберкульозу в експерименті на тваринній моделі. Крім того, більш високі значення МІК цих сполук говорять про те, що вони не можуть ефективно інгібувати Mycobacterium tuberculosis. Таким чином, основною метою даного винаходу є задоволення насущної потреби у нових протимікобактеріальних сполуках шляхом пропозиції нових похідних піролу, що a) показують більш істотну протимікобактеріальну активність, у порівнянні з існуючими лікарськими препаратами; b) забезпечують безпечний і специфічний лікувальний ефект при лікуванні туберкульозу, що спричиняється полірезистентними туберкульозними мікобактеріями; c) ефективні в лікуванні пацієнтів, які мають безсимптомну/латентну форму туберкульозу. Один з аспектів даного винаходу представляє сполуку формули (І), її та утомери, енантіомери, діастереомери, N-оксиди, поліморфи і їх фармацевтично прийнятні солі. (I) де R1 - С1-С4алкіл, С1-С4алкокси, С1-С4тіоалкокси, трифторалкіл, трифторалкокси, гідроксиалкіл; R2 вибраний із групи, що включає і) феніл, незаміщений чи заміщений одним чи двома замісниками, незалежно обраними з групи, яка включає галоген, С1-С4алкіл, С1-С4алкокси, С1С4тіоалкокси, нітро, галоалкіл, галоалкокси, незаміщений чи заміщений піперазин, морфолін, тіоморфолін, ігіролідин і піперидин, або де R8 - феніл, незаміщений чи заміщений 1-2 замісниками, що незалежно вибрані з групи, яка включає галоген, С1-С4алкіл, С1-С4алкокси, С1С4тіоалкокси, нітро, аміно, галоалкіл, галоалкокси і так далі; незаміщений чи заміщений бензил; незаміщений чи заміщений гетероарил; незаміщений чи заміщений гетероароїл; незаміщений чи заміщений дифенілметил, m=0-2 і X є -NCH3, CH2, S, SO або SO2; якщо R2 - феніл, незаміщений чи заміщений одним або двома замісниками, кожний з яких незалежно вибрано із групи, що включає галоген, С1-С4алкіл, С1-С4алкокси, С1-С4тіоалкокси, нітро, галоалкіл, галоалкокси, незаміщений чи заміщений піперазин, морфолін, тіоморфолін, піролідин і піперидин і R4 - N; R 8 не є С 1-С4алкілом, або X не є -NCH3, S, SO або SO2, якщо m=1, або X не є -СН2, якщо m=0. Сполука формули (І), що описана вище і її різні форми, включаючи їх фармацевтично прийнятні солі, безпечні і показують низький рівень токсичності. Наступний аспект даного винаходу представляє спосіб отримання сполуки формули (І) її та утомерів, енантіомерів, діастереомерів, Nоксидів, поліморф і їх фармацевтично прийнятних солей, при якому дану сполуку отримують реакцією сполуки формули (V) (V) де R1 - С1-С4алкіл, С1-С4алкокси, С1-С4тіоалкокси, трифторалкіл, трифторалкокси або гідроксиалкіл, R2 вибрано із групи, що включає і) феніл, незаміщений чи заміщений одним або двома замісниками, що незалежно вибрані з групи, яка включає галоген, С1-С4алкіл, С1-С4алкокси, С1С4тіоалкокси, нітро, галоалкіл, галоалкокси, незаміщений чи заміщений піперазин, морфолін, тіоморфолін, піролідин і піперидин, або іі) гідроксиалкіл, або ііі) незаміщений чи заміщений тіазол, або iv) незаміщений чи заміщений тіадіазол, або ν) незаміщений чи заміщений піридин, або vi) незаміщений чи заміщений нафталін, або vii) NHCOR6, де R6 - арил, незаміщений чи заміщений гетероарил, незаміщений чи заміщений гетероцикліл; 15 81640 R3 - феніл або заміщений феніл, арил, незаміщений чи заміщений гетероарил; с аміном формули R7H, де R7 вибрано із груп 16 У фармацевтично активної сполуки формули (І) за даним винаходом, (I) де R8 - феніл, незаміщений чи заміщений 1-2 замісниками, що вибрані з групи, яка включає галоген, С1-С4алкіл, С1-С4алкокси, С1-С4тіоалкокси, нітро, аміно, галоалкіл, галоалкокси і так далі; незаміщений чи заміщений бензил; незаміщений чи заміщений гетероарил; незаміщений чи заміщений гетероароїл; незаміщений чи заміщений дифенілметил, m=0-2 і X - -NCH3, CH2, S, SO або SO2, так що сполука формули (І), отримана таким чином, що якщо один з R4 або R5 - N, інший є -(CH2)n-R7, де n=1-3 і R7 вибрано із груп де R8 - феніл, незаміщений чи заміщений 1-2 замісниками, що незалежно вибрані з групи, яка включає галоген, С1-С4алкіл, С1-С4алкокси, С1С4тіоалкокси, нітро, аміно, галоалкіл, галоалкокси і так далі; незаміщений чи заміщений бензил; незаміщений чи заміщений гетероарил; незаміщений чи заміщений гетероароїл; незаміщений чи заміщений дифенілметил, m=0-2 і X є -NCH3, CH2, S, SO або SO2; так що, коли R2 - феніл, незаміщений чи заміщений одним або двома замісниками, що незалежно вибрані з групи, яка включає галоген, С1-С4алкіл, С1-С4алкокси, С1-С4тіоалкокси, нітро, галоалкіл, галоалкокси, заміщений чи незаміщений піперазин, морфолін, тіоморфолін, піролідин і піперидин, і R4 - Н; R8 не є С1С4алкілом, або X не є -NCH3, S, SO або SO2, коли m=1, або X не є -СН2, коли m=0. Наступний аспект даного винаходу представляє фармацевтичні композиції, застосовані у лікуванні мікобактеріальних станів, таких як туберкульоз, включаючи туберкульоз, що спричиняється полірезистентними туберкульозними мікобактеріями, які включають: а) щонайменше, одну сполук у формули (І), її таутомери, енантіомери, діастереомери, N-оксиди, поліморфи і їх фармацевтично прийнятні солі; b) фармацевтично прийнятні добавки. Подальший аспект даного винаходу представляє спосіб інгібування/впливу на мікроорганізм/стан сполуками, що вибрані із сполуки формули (І), її та утомерів, енантіомерів, діастереомерів, N-оксидів, поліморф, їх фармацевтично прийнятних солей, з фармацевтично прийнятними носіями або без них. Мікроорганізмом/станом може бути Mycobacterium tuberculosis, резистентна до ліків Mycobacterium tuberculosis, Mycobacterium avium внутрішньоклітинний комплекс, Mycobacterium fortuitum або Mycobacterium kansasii. визначення груп R1, R2, R3, R4 і R5 є наступним: R1 С1-С4алкіл, розгалужений чи нерозгалужений, С1-С4алкокси, С1-С4тіоалкокси, трифторалкіл, трифторалкокси або гідроксиалкіл. Прийнятними алкільними групами є метил, етил, n-пропіл, n-бутил, ізопропіл, ізобутил або трет-бутил. Метил є переважним. Прийнятними алкоксильними групами є метокси, етокси, nпропокси, ізо-пропокси, n-бутокси, ізо-бутокси і трет-бутокси. Прийнятними тіоалкільними групами є тіометил, тіоетил, 1-тіопропан, 2-тіопропан, 1тіобутан, 1-метил-1-тіопропан і 1-метил-2тіопропан. Прийнятними трифторалкільними групами є трифторметил і трифторетил. Прийнятними трифторалкоксильними групами є трифторметокси і трифторетокси. Прийнятними гідроксиалкильними групами є групи, що вибрані з трифторметокси і трифторетокси. R2 вибраний із групи, що включає: і) феніл, незаміщений чи заміщений одним або двома замісниками, що незалежно вибрані з групи, яка включає галоген, С1-С4алкіл, С1-С4алкокси, С1С4тіоалкокси, нітро, галоалкіл, галоалкокси, незаміщений чи заміщений піперазин, морфолін, тіоморфолін, піролідин і піперидин, або іі) гідроксиалкіл, або ііі) незаміщений чи заміщений тіазол, або iv) незаміщений чи заміщений тіадіазол, або ν) незаміщений чи заміщений піридин, або vi) незаміщений чи заміщений нафталін, або vii) NHCOR6, де R6 - арил, незаміщений чи заміщений гетероарил, незаміщений чи заміщений гетероцикліл. Заміщені фенільні групи вибрані з хлорбензолу, бромбензолу, фторбензолу, 1,2дихлорбензолу, 1,2-дибромбензолу, 1,2дифторбензолу, 1,3-дихлорбензолу, 1,3дибромбензолу, 1,3-дифторбензолу, 1,4дифторбензолу, 1,4-дибромбензолу, 1,4дифторбензолу, метилбензолу, етилбензолу, оксилолу, m-ксилолу, р-ксилолу, 2-етилтолуолу, 3етилтолуолу, 4-етилтолуолу, пропілбензолу, кумолу, бутилбензолу, втор-бутиленолу, ізобутилбензолу, трет-бутилбензолу, о-кумолу, mкумолу, р-кумолу, 1,2-діетилбензолу, 1,3діетилбензолу, 1,4-діетилбензолу, 1,3-ди-третбутилбензолу, 1,4-ди-трет-бутилбензолу, 4-третбутилтолуолу, анізолу, 2-метиланізолу, 3метиланізолу, 4-метиланізолу, 1,2бензолдиметанолу, 1,3-бензолдиметанолу, 1,4бензолдиметанолу, 1,2-диметоксибензолу, 2етоксианізолу, 3,5-діетокситолуолу, бензилмеркаптану, фенетилмеркаптану, 1,2бензолдиметанетіолу, 1,3-бензолдиметанетіолу, 1,4-бензолдиметанетіолу, нітробензолу, 1,2динітробензолу, 1,3-динітробензолу, 1,4динітробензолу, бензилхлориду, бензилброміду, 17 81640 трифторметокси, трифторетокси і т.п., і не обмежуються перерахованим. У групі R6, вираз "гетероарил" припускає будьяке арильне кільце, що містить один чи більш гетероатомів, вибраних з N, О і S, а вираз "гетероцикл" припускає будь-які гетероциклічні системи. R3 являється а) фенілом або заміщеним фенілом. Прийнятні заміщені фенільні групи вибрані з хлорбензолу, бромбензолу, фторбензолу, 1,2-дихлорбензолу, 1,2-дибромбензолу, 1,2-дифторбензолу, 1,3дихлорбензолу, 1,3-дибромбензолу, 1,3дифторбензолу, 1,4-дифторбензолу, 1,4дибромбензолу, 1,4-дифторбензолу, метилбензолу, етилбензолу, о-ксилолу, mксилолу, р-ксилолу, 2-етилтолуолу, 3-етилтолуолу, 4-етилтолуолу, пропілбензолу, кумолу, бутилбензолу, втор-бутиленолу, ізо-бутилбензолу, трет-бутилбензолу, о-кумолу, m-кумолу, р-кумолу, 1,2-діетилбензолу, 1,3-діетилбензолу, 1,4діетилбензолу, 1,3-ди-трет-бутилбензолу, 1,4-дитрет-бутилбензолу, 4-трет-бутилтолуолу, анізолу, 2-метиланізолу, 3-метиланізолу, 4-метиланізолу, 1,2-бензолдиметанолу, 1,3-бензолдиметанолу, 1,4-бензолдиметанолу, 1,2-диметоксибензолу, 2етоксианізолу, 3,5-діетокситолуолу, бензилмеркаптану, фенетилмеркаптану, 1,2бензолдиметанетіолу, 1,3-бензолдиметанетіолу, 1,4-бензолдиметанетіолу, нітробензолу, 1,2динітробензолу, 1,3-динітробензолу, 1,4динітробензолу, бензилхлориду, бензилброміду, трифторметокси, трифторетокси і т.п., і не обмежуються переліченими. Або b) арильною групою, або c) незаміщеним або заміщеним гетероарилом, як визначено раніше. R4 і R-5 кожен незалежно є воднем, -(CH2)n-R7, де n=1-3 і R7 вибраний із групи де R8 являється a) фенілом, незаміщеним або заміщеним одним або двома замісниками, що незалежно вибрані з групи, що включає галоген, С1-С4алкіл, С1-С4алкокси, С1-С4тіоалкокси, нітро, аміно, галоалкіл, галоалкокси, де замісники визначені вище, або b) незаміщеним чи заміщеним бензилом; незаміщеним чи заміщеним гетероарилом; незаміщеним чи заміщеним гетероароїлом; незаміщеним чи заміщеним дифенілметилом, m=0-2, і X є -NCH3, CH2, S, SO або SO2. До того ж, сполуки формули (І) за даним винаходом включають їх фармацевтично прийнятні нетоксичні кислотно-адитивні солі, утворені неорганічними або органічними кислотами способами, що добре відомі фахівцям у цій галузі. Ці солі можуть використовуватися замість вільних основ. Прикладами прийнятних кислот для утворення таких кислотно-адитивних солей є малеїнова, фумарова, бензойна, 18 аскорбінова, памова, бурштинова, бісметиленова, саліцилова, метансульфонова, етандисульфонова, оцтова, пропіонова, винна, лимонна, глюконова, аспаргінова, стеаринова, пальмітинова, ітаконова, гліколева, рамінобензойна, глутамінова, бензолсульфонова, ортофосфорна, бромоводнева, сірчана, хлороводнева, азотна кислоти і т.п. Даний винахід також включає можливі таутомери, енантіомери, діастереомери, N-оксиди, поліморфи сполук формули (І), що мають таку саму дію. Даний винахід також представляє фармацевтичні композиції, що містять сполуки формули (І), для лікування хвороби, що спричиняється М, tuberculosis. Ці композиції містять ефективну кількість сполук формули (І) або його таутомерів, енантїомерів, діастереомерів, N-оксидів, їх фармацевтично прийнятних солей або поліморфних форм, у поєднанні з фармацевтично прийнятними носіями і, необов'язково, у присутності наповнювача. Кілька переважних специфічних нових сполук (№1-91) формули (І), що названі відповідно до номенклатури Міжнародного союзу теоретичної і прикладної хімії (ИЮПАК) і складають частину даного винаходу, приведені нижче: 1. 1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3іл]метил}-4-(4-фторфеніл)піперазин; 2. 1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3іл]метил}-4-(2-метокси-феніл)піперазин; 3. 1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3іл]метил}-4-(3-трифтор-метилфеніл)піперазин; 4. 1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3іл]метил}-4-(2-піридил)піперазин; 5. 1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3іл]метил}-4-(2-піримідил)піперазин; 6. 1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3іл]метил}-4-(дифеніл-метил)піперазин; 7. 4-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3іл]метил}піперазиніл-2-фурил-кетон; 8. 5-[(4-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3іл]метил}піперазиніл)-метил]-2Н-бензо[d]1,3діоксолан; 9. 4-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3іл]метил}піперазинілоксолан-2-іл-кетон; 10. 1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3іл]метил}-4-5-хлорметилфеніл)піперазин; 11. N-(3-{[4-(4-фторфеніл)піперазиніл]метил}2-метил-5-фенілпіроліл)-4-піридилкарбоксамід; 12. N-(3-{[4-(3трифторметилфеніл)піперазиніл]метил}-2-метил5-феніл-піроліл)-4-піридилкарбоксамід; 13. N-(3-{[4-(2метоксифеніл)піперазиніл]метил}-2-метил-5фенілпіроліл)-4-піридилкарбоксамід; 14. N-(3-{[4-(2-піридил)піперазиніл]метил}-2метил-5-фенілпіроліл)-4-піридилкарбоксамід; 15. N-(2-метил-5-феніл-3-{[4бензилпіперазиніл]метил}піроліл)-4піридилкарбоксамід; 16. N-{2-метил-3-[(4-метилпіперазиніл)метил]5-фенілпіроліл}-4-піридилкарбоксамід; 19 81640 17. N-(3-{[4-(2Н-бензо[d]1,3-діоксолан-5-ілметил)піперазиніл]метил}-2-метил-5фенилпіроліл)-4-піридилкарбоксамід; 18. N-(2-метил-5-феніл-3(піперидинілметил)піроліл]-4-піридилкарбоксамід; 19. N-[2-метил-5-феніл-3(піролідилметил)піроліл]-4-піридилкарбоксамід; 20. N-[2-метил-3-(морфолін-4-іл-метил)-5фенілпіроліл]-4-піридилкарбоксамід; 21. N-[2-метил-5-феніл-3-(1,4-тіазапергідроїн4-іл-метил)піроліл]-4-піридилкарбоксамід; 22. N-(3-{[4-(4-фторфеніл)піперазиніл]метил}5-метил-2-фенілпіроліл)-4-піридилкарбоксамід; 23. N-(3-{[4-(3трифторметилфеніл)піперазиніл]метил}-5-метил2-феніл-піроліл)-4-піридилкарбоксамід; 24. N-(3-{[4-(2H-6erao[d]1,3-діоксолан-5-ілметил)піперазиніл]метил}-5-метил-2фенілпіроліл)-4-піридилкарбоксамід; 25. N-(3-{[4-(4-фторфеніл)піперазинщ]метил}2-метил-5-фенілпіроліл)піразин-2-іл-карбоксамід; 26. N-(3-{[4-(2метоксифеніл)піперазиніл]метил}-2-метил-5фенілпіроліл)піразин-2-іл-карбоксамід; 27. N-(3-{[4-(3трифторметилфеніл)піперазиніл]метил}-2-метил5-феніл-піроліл) піразин-2-іл-карбоксамід; 28. N-(3-{[4-(2-піридил)піперазиніл]метил}-2метил-5-фенілпіроліл)піразин-2-іл-карбоксамід; 29. N-(3-{[4-(2Н-бензо[d]1,3-діоксолен-5-ілметил)піперазиніл]метил}-2-метил-5фенілпіроліл)піразин-2-іл-карбоксамід; 30. N-(3{[4(дифенілметил)піперазиніл]метил}-2-метил-5фенілпіроліл)піразин-2-іл-карбоксамід; 31. N-(3-{[4-(4-фторфеніл)піперазиніл]метил}5-метил-2-фенілпіроліл)піразин-2-іл-карбоксамід; 32. N-(3-{[4-(2метоксифеніл)піперазиніл]метил}-5-метил-2фенілпіроліл)тразин-2-іл-карбоксамід; 33. N-(3-{[4-(3трифторметилфеніл)піперазиніл]метил}-5-метил2-феніл-піроліл)піразин-2-іл-карбоксамід; 34. N-(3-{[4-(2-піридил)піперазиніл]метил}-5метил-2-фенілпіроліл)піразин-2-іл-карбоксамід; 35. N-(3-{[4-(2Н-бензо[3,4-d]1,3-діоксолан-5-ілметил)тперазиніл]метил}-5-метил-2фенілпіроліл)піразин-2-іл-карбоксамід; 36. N-(3-{[4-(дифенілметил)піперазиніл]метил}5-метил-2-фенілпіроліл)піразин-2-іл-карбоксамід; 37. N-(5-(4-хлорфеніл)-3-{[4-(4фтор феніл)піперазиніл]метил}-2метилпіроліл)піразин-2-іл-карбоксамід; 38. N-(5-(4-хлорфеніл)-3-{[4-(2метоксифеніл)піперазиніл]метил}-2метилпіроліл)піразин-2-іл-карбоксамід; 39. N-(5-(4-хлорфеніл)-3-{[4-(3трифторметилфеніл)піперазиніл]метил}-2метилпіроліл)піразин-2-іл-карбоксамід; 40. N-(5-(4-хлорфеніл)-3-{[4-(2тридил)піперазиніл]метил}-2-метилпіроліл)піразин2-іл-карбоксамід; 41. N-(2-(4-хлорфеніл)-3-{[4-(4фтор феніл)піперазиніл]метил}-5метилпіроліл)піразин-2-іл-карбоксамід; 20 42. N-(2-(4-хлорфеніл)-3-{[4-(2метоксифеніл)піперазиніл]метил}-5метилпіроліл)піразин-2-іл-карбоксамід; 43. N-(2-(4-хлорфеніл)-3-{[4-(3трифторметилфеніл)піперазиніл]метил}-5метилпіроліл)піразин-2-іл-карбоксамід; 44. 1-{[1-(2,4-дифторфеніл)-5-(4-хлорфеніл)-2метилпірол-3-іл]метил}-4-(4-фторфеніл)піперазин; 45. 1-{[1-(2,4-дифторфеніл)-5-(4-хлорфеніл)-2метилпірол-3-іл]метил}-4-(2метоксифеніл)піперазин; 46. 1-{[1-(2,4-дифторфеніл)-5-(4-хлорфеніл)-2метилпірол-3-іл]метил}-4-(3трифторметилфеніл)піперазин; 47. 1-{[1-(2,4-дифторфеніл)-5-(4-хлорфеніл)-2метилпірол-3-іл]метил}-4-(2-піридил)піперазин; 48. 1-{[1-(2,4-дифторфеніл)-5-(4-хлорфеніл)-2метилпірол-3-іл]метил}-4-(4дифенілметил)піперазин; 49. 1-{[1-(2,4-дифторфеніл)-2-(4-хлорфеніл)-5метилпірол-3-іл]метил}-4(дифенілметил)піперазин; 50. 5-[(4-{[1-(2,4-дифторфеніл)-5-(4хлорфеніл)-2-метилпірол-3іл]метил}піперазиніл)метил]-2Н-бензо[а]1,3діоксолан; 51. 1-{[1-(2,4-дифторфеніл)-2-метил-5фенілпірол-3-іл]метил}-4-(4-фторфеніл)піперазин; 52. 1-{[1-(2,4-дифторфеніл)-2-метил-5фенілпірол-3-іл]метил}-4-(2метоксифеніл)піперазин; 53. 1-{[1-(2,4-дифторфеніл)-2-метил-5фенілпірол-3-іл]метил}-4-(3трифторметилфеніл)піперазин; 54. 1-{[1-(2,4-дифторфеніл)-2-метил-5фенілпірол-3-іл]метил}-4-(2-пїридил)піперазин; 55. 1-{[1-(2,4-дифторфеніл)-5-метил-2фенілпірол-3-іл]метил}-4-(4-фторфеніл)піперазин; 56. 1-{[1-(2,4-дифторфеніл)-5-метил-2фенілтрол-3-іл]метил}-4-(2метоксифеніл)піперазин; 57. 1-{[1-(2,4-дифторфеніл)-5-метил-2фенілпірол-3-іл]метил}-4-(3трифторметилфеніл)піперазин; 58. 1-{[1-(2,4-дифторфеніл)-5-метил-2фенілпірол-3-іл]метил}-4-(2-піридил)піперазин; 59. 1-{[5-(4-хлорфеніл)-2-метилнафтилпірол-3іл]метил}-4-(2-метоксифеніл)піперазин; 60. 1-{[5-(4-хлорфеніл)-2-метилнафтилпірол-3іл]метил}-4-(3-трифторметилфеніл)піперазин; 61. 1-{[5-(4-хлорфеніл)-2-метил-1нафтилпірол-3-іл]метил}-4-(2-піридил)піперазин; 62. 5-[(4-{[5-(4-хлорфеніл)-2-метил-1нафтилпірол-3-іл]метил}піперазиніл)метил]2Нбензо[d]1,3-діоксолан; 63. 1-{[2-(4-хлорфеніл)-5-метил-1нафтилпірол-3-іл]метил}-4-(2метоксифеніл)піперазин; 64. 1-{[2-(4-хлорфеніл)-5-метил-1нафтилпірол-3-іл]метил}-4-(3трифторметилфеніл)піперазин; 65. 1-{[2-(4-хлорфеніл)-5-метил-1нафтилпірол-3-іл]метил}-4-(2-піридил)піперазин; 21 81640 66. N-(5-(4-хлорфеніл)-3-{[4-(4фтор феніл)піперазиніл]метил}-2-метилпіроліл)-4піридилкарбоксамід; 67. N-(5-(4-хлорфеніл)-3-{[4-(2метоксифеніл)піперазиніл]метил}-2-метилпіроліл)4-піридилкарбоксамід; 68. N-(5-(4-хлорфеніл)-3-{[4-(3трифторметилфеніл)піперазиніл]метил}-2метилпіроліл)-4-піридилкарбоксамід; 69. N-(5-(4-хлорфеніл)-3-{[4-(2піридил)піперазиніл]метил}-2-метилпіроліл)-4піридилкарбоксамід; 70. N-(3-{[4-(2Н-бензо[d]1,3-діоксолан-5-ілметил)піперазиніл]метил}-5-(4-хлорфеніл)-2метилпіроліл)-4-піридилкарбоксамід; 71. N-(2-(4-хлорфеніл)-3-{[4-(4фтор феніл)піперазиніл]метил}-5-метилтроліл)-4піридилкарбоксамід; 72. N-(2-(4-хлорфеніл)-3-{[4-(2метоксифеніл)піперазиніл]метил}-5-метилпіроліл)4-піридилкарбоксамід; 73. N-(2-(4-хлорфеніл)-3-{[4-(3трифторметилфеніл)піперазиніл]метил}-5метилпіроліл)-4-піридилкарбоксамід; 74. N-(2-(4-хлорфеніл)-3-{[4-(2піридил)піперазиніл]метил}-5-метилпіроліл)-4піридилкарбоксамід; 75. N-(3-{[4-(2Н-бензо[-d]1,3-діоксолан-5-ілметил)піперазиніл]метил}-2-(4-хлорфеніл)-5метилпіроліл)-4-піридилкарбоксамід; 76. 4-(4-фторфеніл)-1-[(2-метил-5-феніл-1-(2піридил)пірол-3-іл)метил]піперазин; 77. 4-(2-метоксифеніл)-1-[(2-метил-5-феніл-1(2-піридил)пірол-3-іл)метил]піперазин; 78. 4-(3-трифторметилфеніл)-1-[(2-метил-5феніл-1-(2-піридил)пірол-3-іл)метил]піперазин; 79. 1-[2-метил-5-феніл-1-(2-піридил)пірол-3іл)метил]-4-(2-пірвдил)піперазин; 80. [(2-метил-5-феніл-1-(2-тридил)пірол-3іл)метил]піперазиніл}метил)-2Н-бензо[d]1,3діоксолан 81. 4-(4-фторфеніл)-1-[(5-метил-2-феніл-1-(2піридил)пірол-3-іл)метил]піперазин; 82. 4-(2-метоксифеніл)-1-[(5-метил-2-феніл-1(2-піридил)пірол-3-іл)метил]піперазин; 83. 4-(3-трифторметилфеніл)-1-[(5-метил-2феніл-1-(2-піридил)пірол-3-іл)метил]піперазин; 84. 1-[(5-метил-2-феніл-1-(2-піридил)шрол-3іл)метил]-4-(2-піридил)піперазин; 85. 5-({4-[(5-метил-2-феніл-1-(2-піридил)пірол3-іл)метил]піперазиніл}метил)2Н-бензо[d]1,3діоксолан; 86. 1-{[1,5-біс(4-хлорфеніл)-2-етилпірол-3іл]метил}-4-(3-трифторметилфеніл)піперазин; 87. 4-[(2-метил-1,5-дифенілпірол-3-іл)метил] 1,4-тіазапергідроїн-1-он; 88. 4-[(2-метил-1,5-дифенілпірол-3-іл)метил](1,4-тіазапергідроїн-1,1-діон; 89. N-[5-(4-хлорфеніл)-2-метил-3-(1,4тіазапергідроїн-4-іл-метил)піроліл]-4піридилкарбоксамід; 90. 2-[3-(гідроксиметил)-5-метил-2-феніл-4(1,4-тіазапергідроїн-4-іл-метил)піроліл]бутан-1-ол; 91. 2-[2-метил-5-феніл-3-(1,4-тіазапергідроїн4-іл-метил)піроліл]бутан-1-ол. 22 Сполуки формули (І), що згадані вище, їх фармацевтично прийнятні кислі солі, їх можливі таутомери, енантіомери, діастереомери, N-оксиди і їх поліморфи показують фармацевтичну активність особливо в лікуванні захворювань, що викликані Mycobacterium tuberculosis, резистентною до лікарських препаратів, Mycobacterium tuberculosis і Mycobacterium avium внутрішньоклітинний комплекс, Mycobacterium fortuitum або Mycobacterium kansasii. Фармацевтично активні сполуки формули (І) за даним винаходом можуть бути отримані будь-яким способом із тих, що приведені нижче. Спосіб І Схема І показує синтез сполуки формули (І), де R1 - СН3, R3 - заміщений чи незаміщений феніл і R2, R4 і R5 - визначені раніше. Спосіб отримання полягає у взаємодії сполук R3H формули (II) з кислою хлороводневою сіллю формули (II) у присутності АІСІ3 при температурі, що лежить у діапазоні 20-30°С, протягом 1-2 годин до отримання дикетонів формули (IV), що при конденсації з відповідними амінами (R2-NH2) з наступною циклізацією в присутності органічного розчинника при температурному діапазоні 80120°С протягом 2-3 годин дають відповідні піроли формули (V), як описано [М. Biava et. al. in Bioorg. & Med. Chem. Lett., 1999, 9, 2983-2988]. Сполуки формули (V) при реакції з різними гетероциклічними амінами (R7H) у присутності органічного розчинника при температурному діапазоні 20-30°С протягом 2-4 годин дають сполуки формули (І), де R1, R2, R3, R4 і R5 мають значення, що визначені вище. Вихідні кислі солі хлороводневої кислоти формули (III), відомі в даній області, можуть бути синтезовані по методиках, що описані [Bui-Hoi, N. P. in J. Org. СТгет.,1960, 25, 390]. Спосіб II У цьому способі, що коротко описаний схемою II, метилкетони формули (VI) взаємодіють з αбромметилкетонами формули (VII), у присутності основи та органічного розчинника при температурному діапазоні 20-30°С протягом 2-6 днів до отримання дикетонів формули (IV), що взаємодіють з відповідними амінами (R2-NH2) з наступною циклізацією в присутності органічного розчинника при температурному діапазоні 80120°С протягом 2-3 годин і дають відповідні піроли формули (V). Реакція сполук формули (V) з різними амінами (R7H) у присутності органічного 23 81640 розчинника при температурному діапазоні 20-30°С протягом 2-4 годин дає сполуки формули (І), де R1, R2, R3, R4 і R5 мають значення, що визначені вище. Варто розуміти, що в даних схемах, де згадуються визначені основи, кислоти, розчинники і т.д., можуть застосовуватися інші основи, кислоти, розчинники і т.д., що відомі фахівцю в цій галузі. Аналогічним образом, температура і час реакції можуть бути уточнені при необхідності. Винахід описаний посиланнями на певні приклади здійснення з метою ілюстрації. Численні альтернативні приклади здійснення будуть зрозумілі фахівцям цієї галузі і вважаються областю даного винаходу. Наступні приклади демонструють як загальні, так і специфічні варіанти отримання сполуки формули (І), які не мають на увазі обмеження області даного винаходу. Приклад 1 Одержання 1-{[1,5-біс(4-хлорфеніл)-2метилпірол-3іл]метил}-4-(3трифторметилфеніл)піперазину (Сполука №3 формули І) за способом І Етап 1: 1-(4-хлорфеніл)пентан-1,4-діон До добре перемішаної суспензії безводного хлориду алюмінію (29.66г, 0.223моль) у 154.7мл хлорбензолу додали 4-оксопентаноїлхлорид (25.0г, 0.187моль) по краплях з періодом у 30-35 хвилин при кімнатній температурі (25-30°С). Реакційну суміш перемішували при тій же температурі протягом 1 години. Після розкладання реакційної суміші шляхом додаванням твердого льоду і хлористоводневої кислоти (10мл) твердий осад, що утворився, відфільтрували і фільтрат випарили ротаційним випарюванням до видалення всіх розчинників. Осад розчинили етилацетатом (400мл), промили водою (2´100мл) і сольовим розчином (100мл). Органічний шар висушили на безводному сульфаті натрію і розчинник випарили. Неочищений продукт, що о тримали таким способом, хроматографували на силікагелі (з розміром комірок сита 100-200), елюент хлороформ: гексан (90:10), одержали 5.3г (13.60%) названої сполуки. Етап 2: 1,2-біс (4-хлорфеніл)-5-метилпірол Суміш 1-(4-хлорфеніл)пентан-1,4-діону (5.0г, 0.024моль), що отримали на Етапі 1, і 4хлораніліну (3.33г, 0.026моль) у бензолі (5.0мл) дифлегмірували з використанням молекулярних сит або апарату Дин-Старка. Через 3 години, 24 бензол зібрали під зменшеним тиском, і залишок розчинили етилацетатом, промили водою (2´100мл) і сольовим розчином (1´50мл). Шар етилацетату висушили на безводному сульфа ті натрію, і розчинник випарили. Тверду речовину, що отримали таким способом, промили гексаном і одержали 2.83г (39.45%) названої сполуки. Етап 3: 1-{[1,5-біс(4-хлорфеніл)-2-метжпірол3іл]метил}-4-(3-трифторметилфеніл)піперазин До перемішаного розчину 1,2-біс(4хлорфеніл)-5-метилпіролу (1.76г, 0.006моль), що отримали на Етапі 2, в ацетонітрилі (18мл) додали по краплях суміш 1-(3трифторметилфеніл)піперазину гідрохлориду (1.55г, 0.006моль), 40% формальдегіду (0.45мл, 0.006моль) і оцтової кислоти (5.23мл). Після додавання реакційну суміш перемішували при кімнатній температурі протягом 3-4 годин. Реакційну суміш нейтралізували NaOH (20% водяний розчин) і екстрагували етилацетатом (2´100мл). Об'єднаний етилацетатний екстракт промили водою (2´50мл), сольовим розчином (1´30мл), висушили на сульфа ті натрію і розчинник випарили. Неочищений продукт, отриманий таким чином, очистили колоночною хроматографією на силікагелі, елюент етилацетат: гексан (80:10), одержали 2.1г (66.24%) названої сполуки. Т.п. (Точка плавлення) 165-167°С, м-с (масспектрометрія): відношення маси до заряду (m/z) 544 (М+1) 1 H-ЯМР (CDCI3, δ): 2.05 (s, 3Н, СH3), 2.77 (br s, 4Н, 2´N-CH2), 3.31 (br s, 4Н, 2´N-СН2), 3.59 (s, 2Н, N-СH2), 6.34 (s, 1H, H-4), 6.85-7.31 (m, 12Н, Аr-H)· Приклад 2 Одержання Н-(3-{[4-(3трифторметилфеніл)піперазиніл]метил}-5-метил2-фенілпіроліл)-4-піридилкарбоксаміду (Сполука №23 формули І) і одержання N-(3-{[4-(3трифторметилфенїл)піперазиніл]метил}-2-метил5-фенілпіроліл)-4-піридилкарбоксаміду (Сполука №12 формули І)за способом І Етап 1: 1-(феніл)пентан-1,4-діон До добре перемішаної суспензії безводного хлориду алюмінію (27.0г, 205.9ммоль) у 126мл бензолу по краплях додали 4оксопентаноїлхлорид (23.0г, 171.6ммоль), з періодичністю в 30-35 хвилин при кімнатній температурі (25-30°С). Реакційну суміш перемішували при тій же температурі протягом 1 години. Після розкладання реакційної суміші шляхом додавання твердого льоду і хлористоводневої кислоти (10мл) осад профільтрували, і фільтрат випарили ротаційним випарюванням до видалення всіх розчинників. Осад розчинили етилацетатом (400мл), промили водою (2´100мл), сольовим розчином (100мл), висушили на безводному сульфаті натрію і розчинник випарили. Неочищений продукт, що отримали таким способом, хроматографували на силікагелі (з розміром комірок сита 100-200), елюент - хлороформ, одержали 8,6г (24,07%) названої сполуки. 25 81640 Етап 2: N-(5-метил-2-фенілпіроліл)-4піридилкарбоксамід Суміш 1-(феніл)пентан-1,4-діону (6.0г, 28.50ммоль), що отримали на Етапі 1, і ізоникотинового гідразиду (4.30г, 31.35ммоль) у бензолі (6.0мл) дифлегмірували за допомогою молекулярних сит. Через 2 години бензол зібрали зменшенням тиску, і залишок розчинили в етилацетаті, промили водою (2´100мл) і сольовим розчином(1´50мл). Шар етилацетату висушили на безводному сульфаті натрію і розчинник випарили. Неочищений продукт, що о тримали таким способом, хроматографували на силікагелі (з розміром комірок сита 100-200), елюент - 0,2% метанол у хлороформі, одержали 3,5г (39,42%) названої сполуки. Етап 3: N-(3-{[4-(3трифторметилфеніл)піперазиніл]метил}-5-метип-2фенілпіроліл)-4-піридилкарбокссшід (Сполука № 23 формули І) і N-(3-{[4-(3трифторметилфеніл)піперазиніл]метил}-2-метіиі-5фенілпіроліл)-4-піридипкарбоксамід (Сполука №12 формули І) До розмішаного розчину N-(5-метил-2фенілпіроліл)-4-піридилкарбоксамиду (0.300г, 1.083ммоль), що отримали на Етапі 2, в ацетонітрилі (5.0мл) додали по краплях суміш 1-(3трифторметилфеніл)піперазину гідрохлориду (0.288г, 1.083ммоль), 40% формальдегіду (0.032г, 1.083ммоль) і оцтової кислоти (0.09мл). Після додавання реакційну суміш розмішували при кімнатній температурі 4 години. Реакційну суміш нейтралізували гідроксидом натрію (20% водяний розчин) і екстрагували етилацетатом (2´50мл). Комбінований екстракт етилацетату промили водою (2´25мл), сольовим розчином (1´20мл), висушили на безводному сульфаті натрію і розчинник випарили. Тонкошарова хроматографія неочищеного продукту визначила дві зони, що були розділені колоночною хроматографією на силікагелі (з розміром комірок сита 100-200). Менш полярну сполуку елюювали з використанням 60% суміші етилацетатгексану, одержали сполуку, що складає 11.25% (0.060г) від продуктів реакції, визначену як N-(3-{[4-(3трифторметилфеніл)піперазиніл]метил}-5-метил2-фенілпіроліл)-4-піридилкарбоксамід (Сполука 23). Т.п. 105-107°С, мас-спектрометрія: m/z 520 (М+1) 1 Н-ЯМР (CDCI3, δ): 2.14 (s, 3Н, СH3), 2.49 (br s, 4Н, 2´N-CH2), 3.12 (br s, 4H, 2´N-СH2), 3.34 (s, 2H, N-CH2), 6.03 (s, 1H, H-3), 6.96-6.99 (m, 4H, ArH), 7.09-7.27 (m, 5H, ArH), 7.40 (d, 2H, J=6Hz, піридильне кільце), 8.60 (d, 2H, J=6Hz, піридильне кільце). Більш полярну сполуку елюювали з використанням 80% суміші етилацетату і гексану, одержали сполуку, що складає 24.34% (0.130г) від продуктів реакції, визначену як N-(3-{[4-(3трифторметилфеніл)піперазиніл]метил}-2-метил5-фенілпіроліл)-4-піридилкарбоксамід (Сполука 12). 26 Т. п. 80-82°С, мас-спектрометрія: m/z 520 (М+1) 1 H-ЯМР (CDCI3, δ) 2.13 (s, 3Н, СН3), 2.60 (br s, 4Н, 2´N-CH2), 3.18 (bs,4H,2´N-CH2),3.41 (s, 2H, NCH2), 6.24 (s, 1H, H-4), 6.97-7.03 (4H, m, Ar), 7.227.29 (m, 5H, Ar), 7.53 (d, 2H, J=6Hz, піридильне кільце), 8.50 (br s, 1H, NH D2O здатний заміщатися), 8.70 (d, 2H, J=6Hz, піридильне кільце). Приклад 3 Одержання 1-{[1,5-біс(4-хлорфеніл)-2етилпірол-3-іл]метил}-4-(3трифторметилфеніл)піперазину (Сполука №86 формули І)за способом II Етап 1: 1-(4-хлорфеніл)гексан-1,4-діон Безводний хлорид цинку (3.71г, 27.2ммоль) помістили в круглодонну колбу і плавили під вакуумом при температурі 250-350°С протягом 15 хвилин. Після охолодження під вакуумом до кімнатної температури послідовно додали бензол (15мл), триетиламін (2.7мл,19.42ммоль) і третбутанол (1.83мл, 19.42ммоль). Суміш перемішували до повного розчинення хлориду цинку (близько 2 годин), і послідовно додали 1-(4хлорфеніл)етан-1-он (3.0г, 19.42ммоль) і 1бромбутан-2-он (2.05г,13.6ммоль). Суміш перемішували протягом 1 години і залишили на 4 дні при кімнатній температурі, потім погасили 5% водним розчином сірчаної кислоти. Органічний шар зібрали, промили водою (2´50мл), сольовим розчином (1´25мл), висушили на безводному сульфаті натрію, розчинник випарили. Продукт очистили колоночною хроматографією на силікагелі (з розміром комірок сита 100-200), елюент - хлороформ, одержали 2.30г (75.63%) названої сполуки. Етап 2: 1,2-біс(4-хлорфеніл)-5-етилпірол Суміш 1-(4-хлорфеніл)гексан-1,4-діону (2.10г, 9.35ммоль), отриманого на Етапі 1, 4-хлораніліну (1.31г, 10.29ммоль) і р-толуол сульфокислоти (0.321г, 1.80ммоль) у толуолі (5.0мл) дифлегмірували на молекулярних ситах або з використанням апарату Дина-Старка. Хід реакції контролювали за допомогою тонкошарової хроматографії, через 3 години толуол зібрали при зменшеному тиску. Залишок розчинили етилацетатом (200мл), промили водним розчином бікарбонату натрію (2´75мл), потім водою (2´50мл) і сольовим розчином (1´25мл). Шар етилацетату висушили на безводному сульфа ті натрію і розчинник випарили. Отриману тверду речовину промили гексаном і одержали 2.39г (81%) названої сполуки. Етап 3: 1-{[1,5-біс(4-хлорфеніл)-2-етилпірол3іл]метил}-4-(3-трифторметгшфеніл)піперазин До перемішаного розчину 1,2біс(4-хлорфеніл)5-етилпіролу (1.20г, 3.80ммоль), що отримали на Етапі 2, в ацетонітрилі (15мл) Додали по краплях суміш 1-(3-трифторметилфеніл)піперазину гідрохлориду (1.01г, 3.80ммоль), 40% формальдегіду (0.114г, 3.80ммоль) і оцтової кислоти (3.6мл). Після додавання реакційну суміш перемішували при кімнатній температурі протягом 3 годин. Реакційну суміш нейтралізували гідроксидом натрію (20% водний розчин) і 27 81640 екстрагували етилацетатом (2´100мл). Комбінований етилацетатний екстракт промили водою (2´50мл), сольовим розчином (1´30мл), висушили на безводному сульфаті натрію і розчинник випарили. Отриманий продукт хроматографували на силікагелі, елюент етилацетат: гексан (80:10), одержали 1.05г (47.22%) 1-{[1,5-біс(4-хлорфеніл)-2-етилпірол-3іл]метил}-4-(3-трифторметилфеніл)піперазину (Сполука №86 формули І). Mac-спектрометрія: m/z 559 (М+1) 1 Н-ЯМР (CDCI3, δ) 1.05 (t, 3Н, СH3), 2.66 (q, 2H, J=8Hz, CH2CH3) 2.98-3.10 (br s, 4H, 2´N-CH 2), 3.503.55 (br s, 4H, 2´N-CH2), 3.94 (s, 2H, N-CH2), 6.50 (s, 1H, H-4), 7.20-7.38 (m, 12H, Ar-H). Приклад 4 Одержання хлороводневої солі Сполуки №3 формули І Сполуку №3 (1.1г), що отримали на Етапі 3 за Прикладом 1, розчинили в дихлорметані (3мл) при перемішуванні. До розчину по краплях при перемішуванні додали 6.43М НСІ-етанол (295.22мг, 8.08ммоль, 1.3мл, 4 еквівалент) при 10°С Реакційну суміш додатково перемішували 2 хвилини і розбавили діетиловим ефіром (10мл). Перемішування продовжували ще 15 хвилин при тій же температурі. Залишок випарили при зменшеному тиску, осад сушили під вакуумом протягом 1 години, одержали 1.22г названої хлороводневої солі. Т. п. 140-142°С 1 H-ЯМР (диметилсульфоксид d6, δ): 2.03 (s, 3Н, СH3), 3.10 (br s, 4H, 2´N-CH2), 3.91 (br s, 4H, 2´N-CH2) 4.17 (s, 2H, N-CH2), 6.57 (s, 1H, H-4), 6.91-7.48 (m, 12H, Аr). Приклад 5 Одержання хлороводневої солі Сполуки №12 формули І Сполуку №12 (0.405г), що отримали на Етапі 3 за Прикладом 2, розчинили в суміші діетилового ефіру (0.5мл) і дихлорметану (0.5мл) при перемішуванні. До цієї суміші по краплях при перемішуванні додали 1.20М НСІ-ефіру (142.35мг, 3.90ммоль, 3.25мл, 5 еквівалент) при 10°С Реакційну суміш додатково перемішували протягом 2 хвилин і розбавили діетиловим ефіром (10мл). Перемішування продовжували ще 15 хвилин при тій же температурі. Розчинник випарили при зменшеному тиску і осад сушили у вакуумі протягом 1 години, одержали 0.428г названої хлороводневої солі. Т.п. 174-176°С 1 H-ЯМР (диметилсульфоксид d6, δ) 2.10 (s, 3Н, СН3), 3.15 (br s, 4H, 2´N-CH2), 3.84 (br s, 4Н, 2´NCH2), 4.13 (s, 2H, N-CH2), 6.47 (s, 1H, H-4), 7.007.38 (m, 8H, Ar), 7.85 (d, 2H, J=6Hz, піридильне кільце), 8.76 (d, 2H, J=6Hz, піридильне кільце). Перелік сполук за винаходом, що синтезовані одним або декількома вищезгаданими способами, приведений нижче. Приклад 6 З використанням методик, описаних у Прикладах 1-3, були отримані Сполуки №1-2, 4-11, 13-22, 24-85 і 87-91, що докладно охарактеризовані тут: 28 1. 1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3іл]метил}-4-(4-фторфеніл)піперазин Т.п. 193195°С, м-с: m/z494 (M+1) 2. 1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3іл]метил}-4-(2-метоксифеніл)піперазин Т.п. 140142°С, м-с: m/z 506 (М+1) 4. 1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3іл]метил}-4-(2-піридил)піперазин Т.п. 152-154°С, мс: m/z 477 (M+1) 5. 1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3іл]метил}-4-(2-піримідил)піперазин Т.п. 184-186°С, м-с: m/z 478 (М+1) 6. 1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3іл]метил}-4-(дифенілметил)піперазин Т.п. 188190°С, м-с: m/z 566 (М+1) 7. 4-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3іл]метил}піперазиніл-2-фурилкетон Т.п. 84-86°С, мс: m/z 494 (М+1) 8. 5-[(4-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3іл]метил}піперазиніл)метил]-2Н-бензо[(І]1,3діоксолен Т.п. 135-137°С, м-с: m/z 534 (М+1) 9. 4-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3іл]метил}піперазинілоксолан-2-іл-кетонТ.п. 150152°С, м-с: m/z 498 (М+1) 10. 1-{[1,5-біс(4-хлорфеніл)-2-метилпірол-3іл]метил}-4-(5-хлоро-2-метилфеніл)піперазин Т.п. 156-158°С, м-с: m/z 524 (М+1) 11. N-(3-{[4-(4-фторфеніл)піперазиніл]метил}2-метил-5-фенілпіроліл)-4-піридилкарбоксамід Т.п. 98-100°С, м-с: m/z 470 (М+1) 13. N-(3-{[4-(2метоксифеніл)піперазиніл]метил}-2-метил-5фенілпіроліл)-4-піридилкарбоксамід Т.п. 125128°С, м-с: m/z 482 (М+1) 14. N-(3-{[4-(2-піридил)піперазиніл]піридил}-2метил-5-фенілпіроліл)-4-піридилкарбоксамід Т.п. 93-95°С, м-с: m/z 453 (М+1) 15. N-(2-метил-5-феніл-3-{[4бензилпіперазиніл]метил}піроліл)-4піридилкарбоксамід Т.п. 87-89°С, м-с: m/z 466 (М+1) 16. N-{2-метил-3-[(4-метилпіперазиніл]метил}5-фенілпіроліл)-4-піридилкарбоксамід в'язке маслом-с: m/z 390 (М+1) 17. N-(3-{[4-(2Н-бензо[d]1,3-діоксолан-5-ілметил)піперазиніл]метил}-2-метил-5фенілпіроліл)-4-піридилкарбоксамід Т.п. 95-97°С, м-с: m/z 510 (М+1) 18. N-[2-метил-5-феніл-3(піперидинілметил)піроліл]-4-піридилкарбоксамід Т.п. 98-100°С, м-с: m/z 376 (М+1) 19. N-[2-метил-5-феніл-3(піролідинілметил)піроліл]-4-піридилкарбоксамід Т.п. 72-73°C,M-c:m/z361(M+1) 20. N-[2-метил-3-(морфолін-4-іл-метил)-5фенілпіроліл]-4-піридилкарбоксамід Т.п. 160162°С, м-с: m/z 377 (М+1) 21. N-(2-метил-5-феніл-3-(1,4-тіазапергідроїн4-іл-метил)піроліл]-4-піридилкарбоксамід Т.п. 8789°С, м-с: m/z 393 (М+1) 22. N-(3-{[4-(4-фторфеніл)піперазиніл]метил}5-метил-2-фенілпіроліл)-4-піридилкарбоксамід Т.п. 98-99°С, м-с: m/z 470 (М+1) 24. N-(3-{[4-(2Н-бензо[-d]1,3-діоксолан-5-ілметил)піперазиніл]метил}-5-метил-2 29 81640 фенілпіроліл)-4-піридилкарбоксамід Т.п. 96-98°С, м-с: m/z 510 (М+1) 25. N-(3-{[4-(4-фторфеніл)піперазиніл]метил}2-метил-5-фенілпіроліл)піразин-2-іл-карбоксамід Т.п. 80-82°С, м-с: m/z 471 (М+1) 26. N-(3-{[4-(2метоксифеніл)піперазиніл]метил}-2-метил-5фенілпіроліл)піразин-2-іл-карбоксамід Т.п. 7678°С, м-с: m/z 483 (М+1) 27. N-(3-{[4-(3трифторметилфеніл)піперазиніл]метил}-2-метил5-фенілпіроліл) піразин-2-іл-карбоксамід Т.п. 8385°С, м-с: m/z 521 (М+1) 28. N-(3-{[4-(2-піридил)піперазиніл]метил}-2метил-5-фєнілпіроліл)піразин-2-іл-карбоксамід Т.п. 119-121°С, м-с: m/z 454 (M+1) 29. N-(3-{[4-(2Н-бензо[d]1,3-діоксолан-5-ілметил)піперазиніл]метил}-2-метил-5фенілпіроліл)піразин-2-іл-карбоксамід Т.п. 186188°С, м-с: m/z 511 (М+1) 30. N-(3-{[4-(дифенілметил)піперазиніл]метил}2-метил-5-фенілшроліл)піразин-2-іл-карбоксамід Т.п. 91-93°С, м-с: m/z 543 (М+1) 31. Н-(3-{[4-(4-фторфеніл)піперазиніл]метил}5-метил-2-фенілпіроліл)піразин-2-іл-карбоксамід Т.п. 200-202°С, м-с: m/z 471 (М+1) 32. N-(3-{[4-(2метоксифеніл)піперазиніл]метил}-5-метил-2фенілпіроліл)піразин-2-іл-карбоксамід Т.п. 7476°С, м-с: m/z 483 (М+1) 33. N-(3-{[4-(3трифторметилфеніл)піперазиніл]метил}-5-метил2-фенілпіроліл)піразин-2-іл-карбоксамід Т.п. 231233°С, м-с: m/z 521 (М+1) 34. N-(3-{[4-(2-піридил)піперазиніл]метил}-5метил-2-фенілпіроліл)піразин-2-іл-карбоксамід Т.п. 208-210°С, м-с: m/z 454 (М+1) 35. N-(3-{[4-(2Н-бензо[-d]1,3-діоксолан-5-ілметил)піперазиніл]метил}-5-метил-2фенілпіроліл)піразин-2-іл-карбоксамід; Т.п. 8183°С, м-с: m/z 511 (М+1) 36. N-(3-{[4-(дифенілметил)піпєразиніл]метил}5-метил-2-фенілпіроліл)піразин-2-іл-карбоксамід Т.п. 95-97°С, м-с: m/z 543 (М+1) 37. N-(5-(4-хлорфеніл)-3-{[4-(4фтор феніл)піперазиніл]метил}-2метилпіроліл)піразин-2-іл-карбоксамід Т.п. 110112°С, м-с: m/z 505 (М+1) 38. N-(5-(4-хлорфеніл)-3-{[4-(2метоксифеніл)піперазиніл]метил}-2метилпіроліл)піразин-2-іл-карбоксамід Т.п. 100102°С, м-с: m/z 517 (М+1) 39. N-(5-(4-хлорфеніл)-3-{[4-(3трифторметилфеніл)піперазиніл]метил}-2метилпіроліл)піразин-2-іл-карбоксамід Т.п. 9698°С, м-с: m/z 555 (M+1) 40. N-(5-(4-хлорфеніл)-3-{[4-(2піридил)піперазиніл]метил}-2метилпіроліл)піразин-2-іл-карбоксамід Т.п. 104106°С, м-с: m/z 488 (М+1) 41. N-(2-(4-хлорфеніл)-3-{[4-(4фтор феніл)піперазиніл]метил}-5метилпіроліл)піразин-2-іл-карбоксамид Т.п. 202204°С, м-с: m/z 505 (М+1) 30 42. N-(2-(4-хлорфеніл)-3-{[4-(2метоксифеніл)піперазиніл]метил}-5метилпіроліл)піразин-2-іл-карбоксамід Т.п. 9698°С, м-с: m/z 517 (М+1) 43. N-(2-(4-хлорфеніл)-3-{[4-(3трифторметилфеніл)піперазиніл]метил}-5метилпіроліл)піразин-2-іл-карбоксамід Т.п. 226228°С, м-с: m/z 555 (М+1) 44. 1-{[1-(2,4-дифторфеніл)-5-(4-хлорфеніл)-2метилпірол-3-іл]метил}-4-(4-фторфеніл)піперазин Т.п. 132-134°С, м-с: m/z 496 (М+1) 45. 1-{[1-(2,4-дифторфеніл)-5-(4-хлорфеніл)-2метилпірол-3-іл]метил}-4(2метоксифеніл)піперазин Т.п. 65-67°С, м-с: m/z 508 (М+1) 46. 1-{[1-(2,4-дифторфеніл)-5-(4-хлорфеніл)-2метилпірол-3-іл]метил}-4(3трифторметилфеніл)піперазин Т.п. 112-114°С, м-с: m/z 546 (М+1) 47. 1-{[1-(2,4-дифторфеніл)-5-(4-хлорфеніл)-2метилпірол-3-іл]метил}-4(2-піридил)піперазин Т.п. 124-126°С, м-с: m/z 479 (М+1) 48. 1-{[1-(2,4-дифторфеніл)-5-(4-хлорфеніл)-2метилтрол-3-іл]метил}-4(4дифенілметил)піперазин Т.п. 70-72°С, м-с: m/z 568 (М+1) 49. 1-{[1-(2,4-дифторфеніл)-2-(4-хлорфеніл)-5метилпірол-3-ил]метил}-4(дифенілметил)піперазин Т.п. 76-78°С, м-с: m/z 568 (М+1) 50. 5-[(4-{[1-(2,4-дифторфеніл)-5-(4хлорфеніл)-2-метилпірол-3іл]метил}піперазиніл)метил]-2Н-бензо[d]1,3діоксолан; в'язке масло м-с: m/z 536 (М+1) 51. 1-{[1-(2,4-дифторфеніл)-2-метил-5фенілпірол-3-іл]метил}-4-(4-фторфеніл)піперазин Т.п. 140-142°С, м-с: m/z 462 (М+1) 52. 1-{[1-(2,4-дифторфеніл)-2-мегил-5фенілпірол-3-іл]метил}-4-(2метоксифеніл)піперазин Т.п. 64-66°С, м-с: m/z 474 (М+1) 53. 1-{[1-(2,4-дифторфеніл)-2-метил-5фенілпірол-3-іл]метил}-4-(3трифторметилфеніл)піперазин Т.п. 122-124°С, м-с: m/z 512 (М+1) 54. 1-{[1-(2,4-дифторфеніл)-2-метил-5фенілпірол-3-іл]метил}-4-(2-піридил)піперазин Т.п. 144-146°С, м-с: m/z 445 (М+1) 55. 1-{[1-(2,4-дифторфеніл)-5-метил-2фенілпірол-3-іл]метил}-4-(4-фторфеніл)піперазин; в'язке масло, м-с: m/z 462 (М+1) 56. 1-{[1-(2,4-дифторфеніл)-5-метил-2фенілпірол-3-іл]метил}-4-(2метоксифеніл)піперазин; Т.п. 60-62°С, м-с: m/z 474 (М+1) 57. 1-{[1-(2,4-дифторфеніл)-5-метил-2фенілпірол-3-іл]метил}-4-(3трифторметилфеніл)піперазин; в'язке масло, м-с: m/z 512(M+1) 58. 1-{[1-(2,4-дифторфеніл)-5-метил-2фенілпірол-3-іл]метил}-4-(2-піридил)піперазин; в'язке масло, м-с: m/z 445 (М+1) 59. 1-{[5-(4-хлорфеніл)-2-метил-1нафтилпірол-3-іл]метил}-4-(2 31 81640 метоксифеніл)піперазин; Т.п. 65-67°С, м-с: m/z 552 (М+1) 60. 1-{[5-(4-хлорфеніл)-2метил-1-нафтилпірол3-іл]метил}-4-(3-трифторметилфеніл)піперазин; Т.п. 68-70°С, м-с: m/z 560 (М+1) 61. 1-{[5-(4-хлорфеніл)-2-метил-1нафтилпірол-3-іл]метил}-4-(2-піридил)піперазин; Т.п. 68-70°С, м-с: m/z 493 62. 5-[(4-{[5-(4-хлорфеніл)-2-метил-1нафтилпірол-3-іл]метил}-піперазиніл) метил]-2Нбензо[d]1,3-диоксолан; Т.п. 70-72°С, м-с: m/z 550 (М+1) 63. 1-{[2-(4-хлорфеніл)-5-метил-1нафтилпірол-3-іл]метил}-4-(2метоксифеніл)піперазин; в'язке масло, м-с: m/z 522 (М+1) 64. 1-{[2-(4-хлорфеніл)-5-метил-1нафтилпірол-3-іл]метил}-4-(3трифторметилфеніл)піперазин; Т.п. 78-80°С, м-с: m/z 560 (М+1) 65. 1-{[2-(4-хлорфеніл)-5-метил-1нафтилпірол-3-іл]метил}-4-(2-піридил)піперазин; в'язке масло, м-с: m/z 493 (М+1) 66. N-(5-(4-хлорфеніл)-3-{[4-(4фтор феніл)піперазиніл]метил}-2-метилпіроліл)-4піридилкарбоксамід; Т.п. 78-80°С, м-с: m/z 504 (М+1) 67. N-(5-(4-хлорфеніл)-3-{[4-(2метоксифеніл)піперазиніл]метил}-2-метилпіроліл)4-піридилкарбоксамід; Т.п. 175-177°С, м-с: m/z 516 (М+1) 68. N-(5-(4-хлорфеніл)-3-{[4-(3трифторметилфеніл)піперазиніл]метил}-2метилпіроліл)-4-піридилкарбоксамід; Т.п. 119121°С м-с: m/z 544 (М+1) 69. N-(5-(4-хлорфеніл)-3-{[4-(2піридил)піперазиніл]метил}-2-метилпіроліл)-4піридилкарбоксамід; в'язке масло, м-с: m/z 487 (М+1) 70. N-(3-{[4-(2H-бензо[d]1,3-діоксолан-5ілметил)піперазиніл]метил}-5-(4-хлорфеніл)-2метилпіроліл)-4-піридилкарбоксамід; Т.п. 69-71°С, м-с: m/z 544 (М+1) 71. N-(2-(4-хлорфеніл)-3-{[4-(4фтор феніл)піперазиніл]метил}-5-метилпіроліл)-4піридилкарбоксамід; Т.п. 70-72°С, м-с: m/z 504 (М+1) 72. N-(2-(4-хлорфеніл)-3-{[4-(2метоксифеніл)піперазиніл]метил}-5-метилпіроліл)4-піридилкарбоксамід; Т.п. 92-94°С, м-с: m/z 516 (М+1) 73. N-(2-(4-хлорфеніл)-3-{[4-(3трифторметилфеніл)піперазиніл]метил}-5метилпіроліл)-4-піридилкарбоксамід; Т.п. 144146°С, м-с: m/z 554 (М+1) 74. №(2-(4-хлорфеніл)-3-{[4-(2піридил)піперазиніл]метил}-5-метилпіроліл)-4піридилкарбоксамід; в'язке масло м-с: m/z 487 (М+1) 75. N-(3-{[4-(2Н-бензо[(і]1,3-ДІоксолан-5-ілметил)піперазиніл]метил}-2-(4-хлорфеніл)-5метилпіроліл)-4-піридилкарбоксамід; Т.п. 65-67°С, м-с: m/z 544 (М+1) 32 76. 4-(4-фторфеніл)-1-[(2-метил-5-феніл-1-(2піридил)пірол-3-іл)метил]піперазин; Т.п. 126128°С, м-с: m/z 427 (М+1) 77. 4-(2-метоксифеніл)-1-[(2-метил-5-феніл-1(2-піридил)пірол-3-іл)метил]піперазин Т.п. 92-94°С, м-с: m/z 439 (М+1) 78. 4-(3-трифторметилфеніл)-1-[(2-метил-5феніл-1-(2-піридил)пірол-3-іл)метил]піперазин; Т.п. 106-108°С, м-с: m/z 477 (М+1) 79. 1-[(2-метил-5-феніл-1-(2-піридил)пірол-3іл)метил]-4-(2-піридил)піперазин; Т.п. 128-130°С, м-с: m/z 410 (М+1) 80. 5-({4-[(2-метил-5-феніл-1-(2-піридил)пірол3-іл)метил]піперазиніл}метил)-2Н-бензо[d]1,3діоксолан; в'язке масло, м-с: m/z 467 (М+1) 81. 4-(4-фторфеніл)-1-[(5-метил-2-феніл-1-(2піридил)пірол-3-іл)метил]піперазин; в'язке масло, м-с: m/z 427 (М+1) 82. 4-(2-метоксифеніл)-1-[(5-метил-2-феніл-1(2-піридил)пірол-3-іл)метил]піперазин; Т.п. 120122°С, м-с: m/z 439 (М+1) 83. 4-(3-трифторметилфеніл)-1-[5-метил-2феніл-1-(2-піридил)пірол-3-іл)метил]піперазин; в'язке масло, м-с: m/z 477 (М+1) 84. 1-[(5-метил-2-феніл-1-(2-піридил)пірол-3іл)метил]-4-(2-піридил)піперазин; в'язке масло, мс: m/z 410 (М+1) 85. 5-({4-[(5-метил-2-феніл-1-(2-піридил)пірол3-іл)метил]піперазиніл}метил)-2Н-бензо[d]1,3діоксолан; в'язке масло, м-с: m/z 467 (М+1) 87. 4-[(2-метил-1,5-дифенілпірол-3-іл)метил]1,4-тіазапергідроїн-1-он; Т.п. 135-137°C,Mc:m/z365(M+1) 88. 4-[(2-метил-1,5-дифенІлпірол-3-іл)метил]1,4-тіазапергідроїн-1,1-діон; Т.п. 140-142°С, м-с: m/z 381 (М+1) 89. N-[5-(4-хлорфеніл)-2-метил-3-(1,4тіазапергідроїн-4-іл-метил)піроліл]-4піридилкарбоксамід; Т.п.220-222°С, м-с: m/z 427 (М+1) 90. 2-[3-(гідроксиметил)-5-метил-2-феніл-4(1,4-тіазапергідроїн-4-іл-метил)піроліл]бутан-1-ол; Т.п. 102-104°С, м-с: m/z 375 (М+1) 91. 2-[2-метил-5-феніл-3-( 1,4-тіазапергідроїн4-іл-метил)піроліл]бутан-1-ол; Т.п. 90-92°С, м-с: m/z 345 (М+1) Фармакологічне випробування Здатність сполук за винаходом демонструвати протимікобактеріальну активність може бути встановлена в дослідах з інгібуванням росту з використанням системи ВАСТЕС 460 ТВ і методом in vitro на рідкому агарі, як показано в прикладах, що приведені нижче. Інгібування росту in vitro і дослід на рідкому агарі для визначення МІК, які описані нижче, показали, що сполуки формули (І) за даним винаходом мають дуже низьке значення МІК стосовно штамів М. tuberculosis, Μ. avium, M. fortiutum і М. kansasii. Сполуки формули (І) за даним винаходом також інгібують ріст резистентних до лікарських препаратів штамів М. tuberculosis. Крім того, приклади, що приведені нижче, описують спосіб лікування експериментального туберкульозу у мишей. Сполуки за даним винаходом показують кращу дію 33 81640 при низьких дозах у порівнянні з відомими лікарськими препаратами, такими як ізоніазид. Сполуки можуть вводитися орально у складі фармацевтичних композицій. Дослід інгібування росту мікроорганізмів in vitro Здатність сполук за даним винаходом інгібувати ріст Mycobacterium species визначали за допомогою системи ВАСТЕС 460 ТВ. Штам М. tuberculosis H37Rv АТСС 27294 вирощували на рідкому середовищі Middlebrook 7H9, з додаванням 10% азодикарбонаміду, при 37°С на роторному шютель-апараті (150 оборотів у хвилину) протягом 7 днів. Мутність культури доводили до 1,0 по стандарту Макфарленда (McFarland). У пробірки із середовищем Middlebrook 7H12B висівали по 0.1мл культури М. tuberculosis з показником мутності приведеним до 0,1 по стандарту Макфарленда. У контрольні пробірки висівали по 0.1мл культури після 100 кратного розведення первісного інокулюма. Набір розчинів по 1мг/мл кожної сполуки в диметилсульфоксиді приготували в окремих стерильних пробірках. Сполуки булинадалі розведені до концентрації 25мг/100мл. По 0.1мл кожного розчину додали в пробірки, що містять мікобактеріальну культур у 7Н12В, так що остаточна концентрація сполук склала 6.25мг/мл. Ковпачки пробірок обробили ізопропіловим спиртом, пробірки помістили в штатив. Культури в пробірках інкубували при 37°С без перемішування. Дослідні пробірки тестували щодня на системі ВАСТЕС доки індекс росту (GI) в контрольних пробірках не досяг показника >30. Як тільки GI у контролі досяг 30, AGI (GI=GI(n) - GI( n-1)) визначили для всіх дослідних і контрольних пробірок. Якщо AGI для дослідної пробірки менше, ніж для контрольної, це означає, що культура чуттєва до сполуки, яку тестують. Таблиця 1 представляє експериментальні дані активності in vitro сполук формули (І) стосовно чуттєвих і резистентних до ліків штамів М. tuberculosis. № Сполука № Інгібування росту Μ. Tuberculosis 27294 01 02 03 04 05 06 07 08 09 10 11 12 13 14 15 1 89 6 2 4 7 8 10 3 9 5 21 87 88 14 + + + + + + + + + + + + + 34 16 90 >16.0 17 91 + 4.0 18 13 + 0.5 19 22 + 2.0 20 11 + 1.0 21 23 + 0.25 22 12 + 0.25 23 46 + 2.0 24 48 + >16.0 25 47 + 0.25 26 44 + 1.0 27 45 + 0.5 28 50 + 2.0 29 24 + 8.0 30 17 + 2.0 31 18 Не виявлено 32 19 16.0 33 20 + 2.0 34 16 + 2.0 35 15 + 0.5 36 60 + 4.0 37 62 + >16.0 38 25 + 2.0 39 32 >16.0 40 26 + 1.0 41 33 + 2.0 42 27 + 2.0 43 36 + 0.5 44 30 + 2.0 45 34 + 16.0 46 28 2.0 47 35 + >16.0 48 29 + >16.0 49 41 >16.0 50 37 16.0 51 43 >16.0 52 39 + 4.0 53 42 + 8.0 54 38 >16.0 55 55 >16.0 56 51 >16.0 57 56 + 8.0 Таблиця 1 58 52 + 8.0 59 57 + >16.0 60MIK (мкг/мл) по відношенню до 53 >16.0 клінічних ізолятів 61 + 8.0 Μ. Tuberculosis 27294 58 чуттєвих 62 54 + резистентних 2.0 0.5 0.5-2.0 2.0-4.0 63 64 >16.0 1.0 2.0-8.0 4.0-8.0 64 61 + 4.0 Не виявлено 65 59 Не виявлено - Не виявлено >16.0 0.25 0.25-1.0 66 63 0.125-0.25 + 8.0 0.5 0.5-4.0 67 Ізоніазид 0.25-1.0 + 0.25 4.0 2.0-4.0 68 Рифампіцин 1.0-4.0 + 0.25 1.0 0.5-1.0 1.0-4.0 1.0 Таблиця 2 представляє значення МІК сполук 1.0-2.0 1.0-4.0 0.125 формули (І) проти різних видів Mycobacteria. 0.125-0.25 0.25-0.5 He виявлено Не виявлено Не виявлено 0.25 0.5-1.0 0.5-2.0 0.5 0.5-1.0 1.0-4.0 МІК 8.0 Сполука 8.0-16.0 8.0->16.0 (мкг/мл) по відноше № М. М. avium-внутрі 0.5 1.0-4.0 tuberculosis2.0-8.0 № чуттєві (n=17) резистентні (n=26) клітинний комплек 4.0 4.0-8.0 4.0-8.0 35 1 2 3 4 2 3 5 Ізоніазид 0.125-0.25 0.125-0.25 0.5-1.0 0.25 81640 0.25-1.0 0.25-0.5 1.0-2.0 8.0->16.0 n: - номер штаму, що тестують. Дослід in vitro на рідкому агарі Визначення МІК сполук стосовно штамів Mycobacterium проводили методом вирощування культур на рідкому агарі за рекомендаціями стандартів тестування мікроорганізмів (NCCLSM24-T2). Сполуки розчинили в диметилсульфоксиді і послідовно розбавляли в два рази до одержання десяти серійних розведень кожної сполуки. Відповідні об'єми сполук помістили в чашки Петрі в двох повтореннях на агарове середовище Middlebrook 7H10 з додаванням 10% середовища Middlebrook, збагаченого олеїновою кислотою, альбуміном, декстрозою, каталазою (OADC) при концентраціях від 0.03мкг/мл до 16мкг/мл. Тест-організм (Mycobacterium strains) вирощували на середовищі Middle brook 7H9 (бульйон), що містить 0.05% Твін80 і 10% азодикарбонамід (АДК). Через 7 днів інкубації при 37°С бульйон довели до 1.0 по стандарту Макфарланда; культур у десятикратно розбавили стерильним сольовим розчином, що містить 0.10% Tween-80. Отриману в результаті мікобактеріальну суспензію висіяли плямами (35мл/пляма) у чашки Петрі на середовище 7Н10 з додаванням лікарських препаратів. Чашки Петрі герметично закупорили і інкубували при 37°С протягом 3-4 тижнів у вертикальному положенні. МІК вра ховували як найменшу концентрацію лікарського препарату, здатну цілком придушити ріст організму, що тестують. Ізоляти, що тестувалися, включали 10 виділених у хворих туберкульозом ізолятів, звичайно чуттєви х до загальновідомих протитуберкульозних препаратів, і 10 ізолятів, резистентних до одного і більш стандартних протитуберкульозних препаратів. Відповідні штами і контрольні лікарські препарати, що згадані вище, були включені в кожну групу тестів. Досліди in vivo Ефективність сполук за даним винаходом оцінювали на мишах, що були інфіковані легеневим туберкульозом. Культуру Mycobacterium tuberculosis H 37Rv вирощували на середовищі Middle brook 7H9 (бульйон), що містить 0.05% Твін-80 і 10% азодикарбонаміду, при 37°С протягом 7 днів на роторному шютельапараті при 150 оборотів у хвилину. Рідка культура для інокуляції тварин була аглютинована короткохвильовим ультразвуком, розведена відповідно до концентрації 1´107 колонієутворюючих одиниць (КУО)/0.2мл. Чотирьохтиждневих самок аутбредних швейцарських мишей-альбіносів помістили у вільні від патогенів, біологічно безпечні умови, в експерименті використовувалися ізольовані від мікроорганізмів клітки. Інфікування проводили внутрішньовенною інокуляцією 0.2мл 36 аглютинованої суспензії 8.0-16.0 М. tuberculosis 8.0 Rv У H37 4.0-8.0 хвостову вен у. Потім4.0-8.0 інфікованих 4.0 мишей 4.0-8.0 безсистемно розподілили на групи, по шість 4.0-8.0 8.0-16.0 8.0 мишей у кожній. 8.0->16.0 >16.0 >16.0 Лікування почали через 1 день після інфікування. Для лікування, сполуку №3 розчинили і розбавили до 50% поліетиленгліколем 400 (ПЕО400), ізоніазид розбавили стерильною водою. Лікарський препарат готували щоранку перед введенням. Терапія проводилася 5 разів у тиждень протягом 4 тижнів. Усі препарати вводилися через зонд дозою 50, 25, 12.5мг/кг маси тіла. Контрольні групи інфікованих мишей, але таких що не одержували лікування, були забиті на початку лікування (ранній контроль) і наприкінці лікування (пізній контроль). Миші були забиті перерізанням шийної артерії через 3-5 днів після введення останньої дози препарату. Цільові органи - селезінка і права легеня - виділили асептично і гомогенізували на тканинному гомогенізаторі. Принаймні, 4 серійні десятикратні розведення гомогенату зробили на бульйоні 7Н9 і помістили в чашки Петрі на агарізоване середовище Middlebrook 7H11 у двох повтореннях. Підрахунок колоній проводили після 4 тижневого інкубування при 37°С Значення КУО виразили в log 10. Зменшення вдвічі log 10 КУО для сполуки в порівнянні з раннім контролем вважали важливим показником. Активність in vivo сполуки №3 формули (І) проти М. tuberculosis H37Rv АТСС 27294аа у інфікованих швейцарських мишей-альбіносів показана в Таблиці 3. № Лікарський препарат і дози b (мг/кгдоба-1) або групи Середнє значення log10 КУ Легеня Селезінка 50 25 12.5 1.97 2.13 2.63 1.94 2.07 2.6 2 Ізоніазид 3 4 50 25 12.5 Ранній контроль Пізній контроль 1.95 2.16 2.93 4.48 6.68 2.12 2.21 2.91 4.63 6.67 1 Сполука №3 а - інокуляція 107КУО/миша: b - мишам вводили дози препаратів 5 днів у тиждень протягом 4 т с - розходження в середніх значеннях log10 КУО в порівнянні з ра Ефективність in vivo сполуки №12 формули І стосовно М. tuberculosis H 37Rv АТСС 27294а у мишей, що одержували лікування, через 14 днів після інфікування, і порівняння її з ефективністю ізоніазиду показані в Таблиці 4. № Лікарський препарат і дозиb (мг/кгдоба-1) або Середнє значення log10 КУО 37 групи 1 2 Сполука № 12 50 25 12.5 Ізоніазид 50 25 12.5 Ранній контроль Пізній контроль 81640 Легеня 2.74+0.36 2.87+0.15 4.18+0.38 38 3 Ранній контроль Селезінка Легеня 4 Пізній контроль 4.57+0.2 Селезінка 6.39+0.5 а - інокуляція 107КУО/миша 2.78+0.32 2.85 3.17 b - мишам 2.83+0.29 вводили дози препаратів 5 днів у тиждень протягом 4 т 2.72 3.12 с - розходження в1.41 середніх значеннях log10 КУО в порівнянні з ра 4.41+0.26 1.54 2.89+0.27 2.62 3.06 Не дивлячись на2.4 що даний 2.87 те, винахід був 3.08+0.44 описаний у специфічних варіантах 1.02 здійснення, 4.93+0.42 1.03 визначені модифікації та еквіваленти їх будуть 3 5.95+0.42 очевидні фахівцям у цій галузі і призначені, щоб 4 7.27+0.42 бути включеними в область даного винаходу. Дослідження гострої токсичності на мишах а - інокуляція 107КУО/миша Сполука №3 формули (І) вводилась як b - мишам вводили дози препаратів 5 днів у тиждень протягом 4 тижнів. Дні 1-28. одиночна раннім контролем. с - розходження в середніх значеннях log10 КУО в порівнянні з оральна доза швейцарським мишамальбіносам. Використовували дві дози 500 і 2000мг/кг. Мишей обстежували 14 днів. Не спостерігалися ні клінічні симптоми, ні летальні Ефективність in vivo сполуки №3 формули І кінці. Миші були забиті на 15 день, патологічні проти М. tuberculosis (резистентний до лікарських зміни в будь-яких органах не були виявлені. Таким препаратів штам) у мишей, що одержували чином, летальна доза 0% (LD0) перевищує лікування, через 1 день після інфікування, і 2000мг/кг при оральному способі введення у порівняння її з ефективністю ізоніазиду показані в мишей. Підтверджена летальна доза 50% (LD50) Таблиці 5. для ізоніазиду складає 139мг/кг при оральному введенні. Аналогічно, для сполуки №12 формули І, Таблиця 5 LD0>500мг/кг у мишей при оральному введенні. № 1 2 3 4 Лікарський препарат і дози b (мг/кгдоба-1) або групи Сполука №3 50 25 12.5 Ізоніазид 50 25 12.5 Ранній контроль Пізній контроль 2.97+0.46 3.19+0.6 4.56+0.24 5.59+0.29 7.3+0.2 Середнє значення log10 КУО Середнє значення log10 інгібування c Легеня Селезінка Легеня Селезінка 1.99+0.3 2.3+0.17 2.98+0.5 1.97+0.4 2.2+0.31 2.91+0.4 2.48 2.17 1.49 2.66 2.43 1.72 4.43+0.5 5.12+0.6 5.8+0.4 4.47+0.31 6.39+0.5 4.7+0.31 5.43+0.5 5.79+0.4 4.63+0.21 6.23+0.21 0.04 -0.65 -1.33 -0.07 -0.8 -1.16 а - інокуляція 107КУО/миша b - мишам вводили дози препаратів 5 днів у тиждень протягом 4 тижнів. Дні 1-28. с - розходження в середніх значеннях log10 КУО в порівнянні з раннім контролем. Ефективність in vivo Сполуки №12 формули І проти М. tuberculosis H37Rv АТСС 27294а у мишей, що одержували лікування, через 1 день після інфікування, і порівняння її з ефективністю ізоніазиду показані в Таблиці 6. Таблиця 6 № 1 2 Лікарський препарат і дози b (мг/кгдоба-1) або групи Сполука №3 50 25 12.5 Ізоніазид 50 25 12.5 4.69+0.21 6.2+0.32 Середнє значення log10 КУО Легеня Селезінка Середнє значення log10 інгібування c Легеня Селезінка 1.89+0.24 2.1+0.24 2.34+0.18 1.94+0.23 2.13+0.28 2.26+0.21 2.68 2.47 2.23 2.75 2.56 2.43 2.02+0.31 2.23+0.33 2.89+0.27 2.07+0.33 2.21+0.44 2.91+0.42 2.55 2.34 1.68 2.62 2.48 1.78
ДивитисяДодаткова інформація
Назва патенту англійськоюAntimycobacterial compounds, process for the preparation thererof, pharmaceutical composition based thereon
Автори англійськоюArora Sudershan Kumar, Sinha Neelima, Jain Sanjay, Upadhayaya Ram Shankar, Jana Gourhari, Ajay Shankar, Sinha Rakesh Kumar
Назва патенту російськоюПротивомикобактериальные соединения, способ их получения, фармацевтическая композиция на их основе
Автори російськоюАрора Судершан Кумар, Синха Неелима, Джаин Санджай, Упадхайайа Рам Шанкар, Джана Гурхари, Аджай Шанкар, Синха Ракеш Кумар
МПК / Мітки
МПК: C07D 401/14, A61P 31/06, C07D 401/12, C07D 417/06, C07D 403/12, A61K 31/4025, C07D 207/32, C07D 403/04, C07D 401/04, C07D 405/12, C07D 405/14
Мітки: композиція, основі, протимікобактеріальні, сполуки, одержання, фармацевтична, спосіб
Код посилання
<a href="https://ua.patents.su/19-81640-protimikobakterialni-spoluki-sposib-kh-oderzhannya-farmacevtichna-kompoziciya-na-kh-osnovi.html" target="_blank" rel="follow" title="База патентів України">Протимікобактеріальні сполуки, спосіб їх одержання, фармацевтична композиція на їх основі</a>
Попередній патент: Ліфт з канатопровідним шківом без противаги
Наступний патент: Спосіб одержання залеплону
Випадковий патент: Спосіб та пристрій для надавання декількох рівнів обслуговування для бездротового зв'язку












