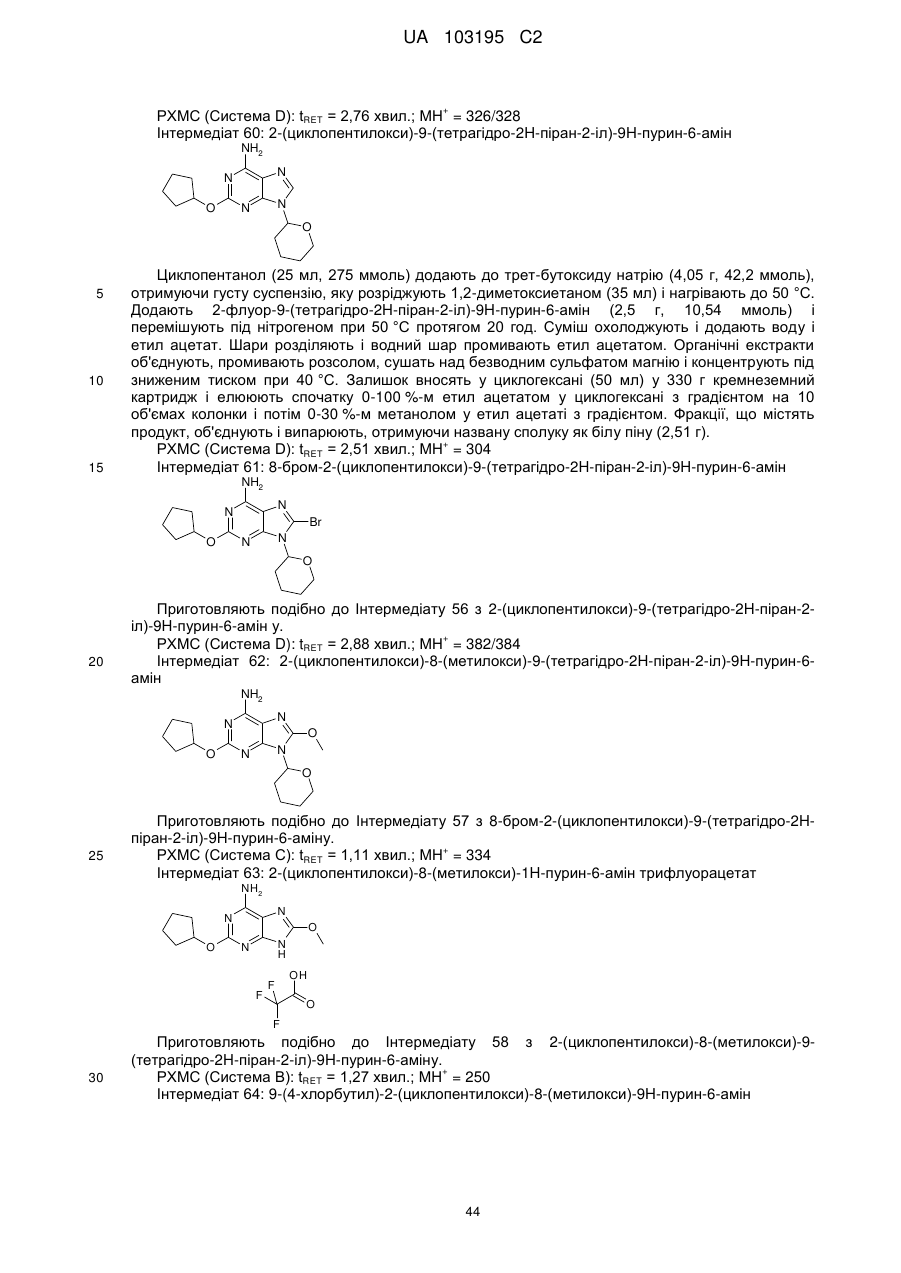
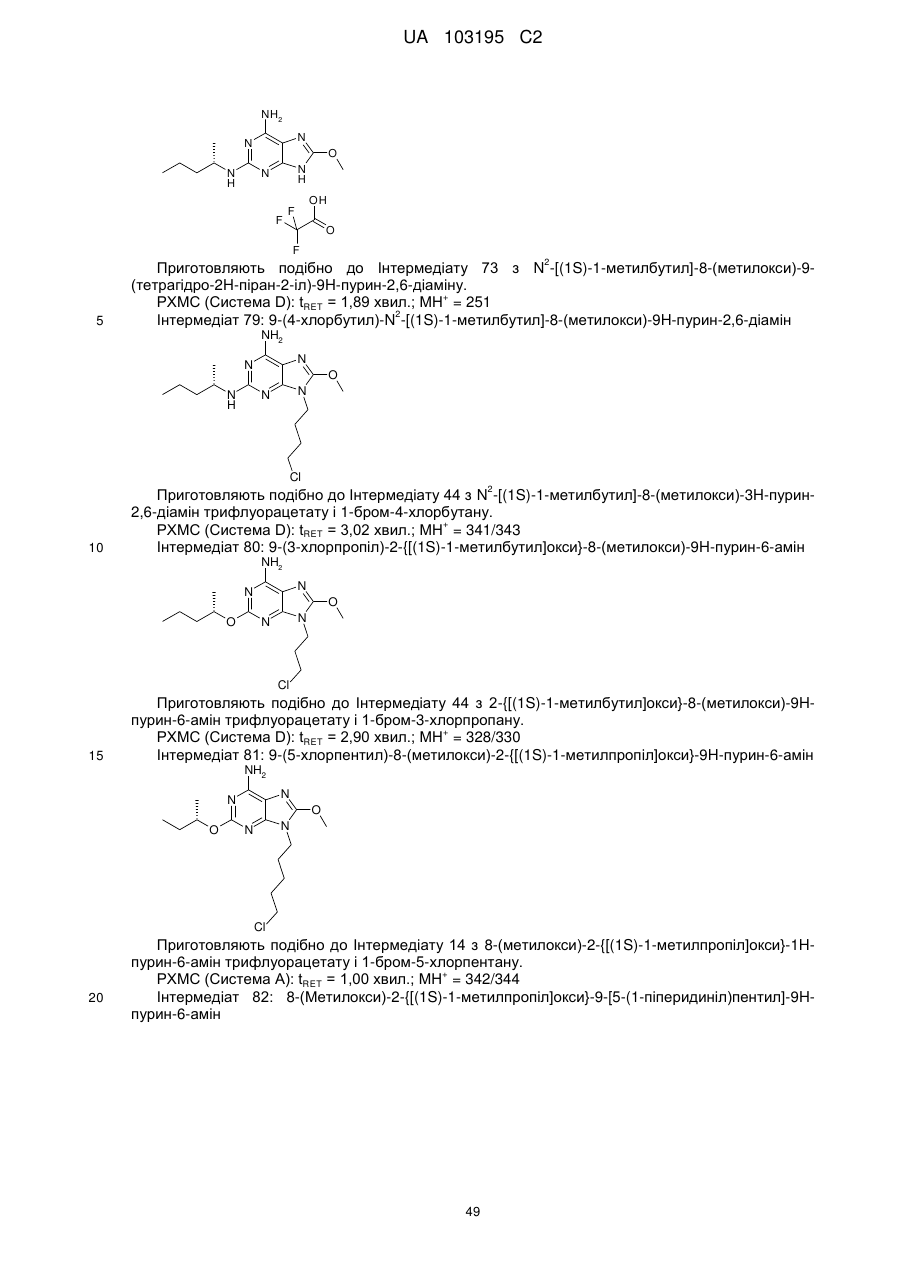
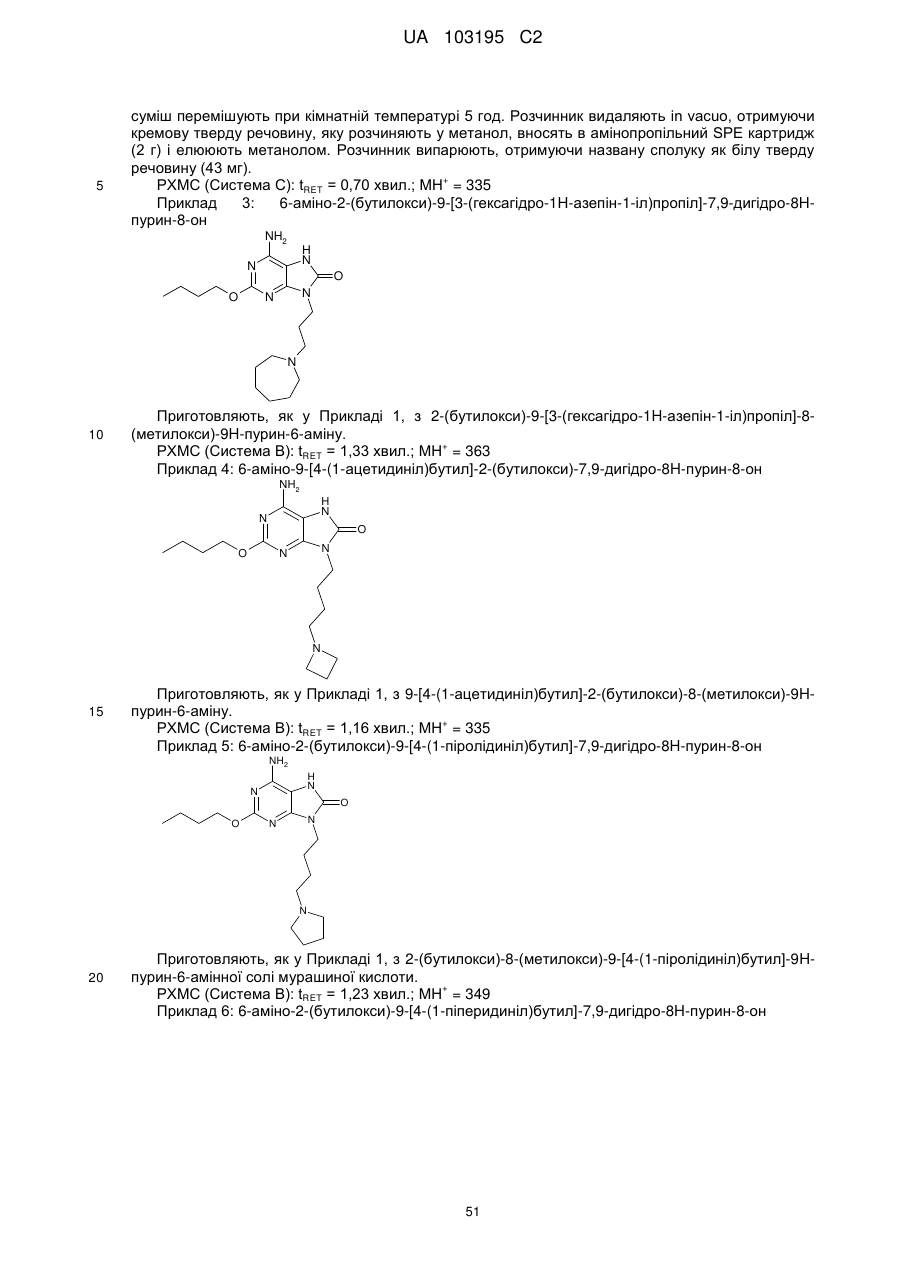
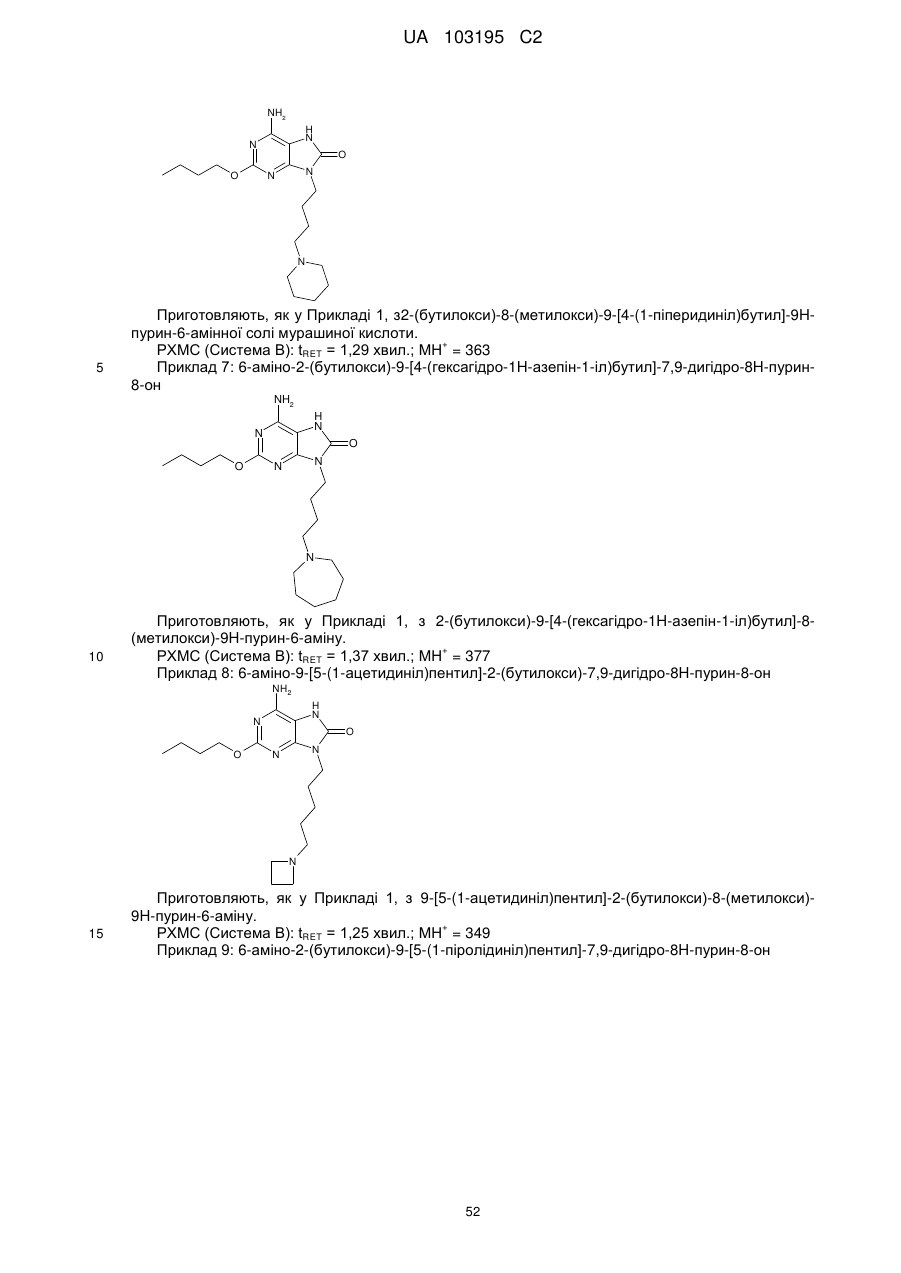
Похідні пурину для застосування у лікуванні алергій, запальних та інфекційних захворювань
Номер патенту: 103195
Опубліковано: 25.09.2013
Автори: Тріведі Найміша, Левелл Ціа К'юн, Сміт Стефан Аллан, Мітчелл Шарлотт Джейн, Біґґадік Кейт, Кое Даян Мері
Формула / Реферат
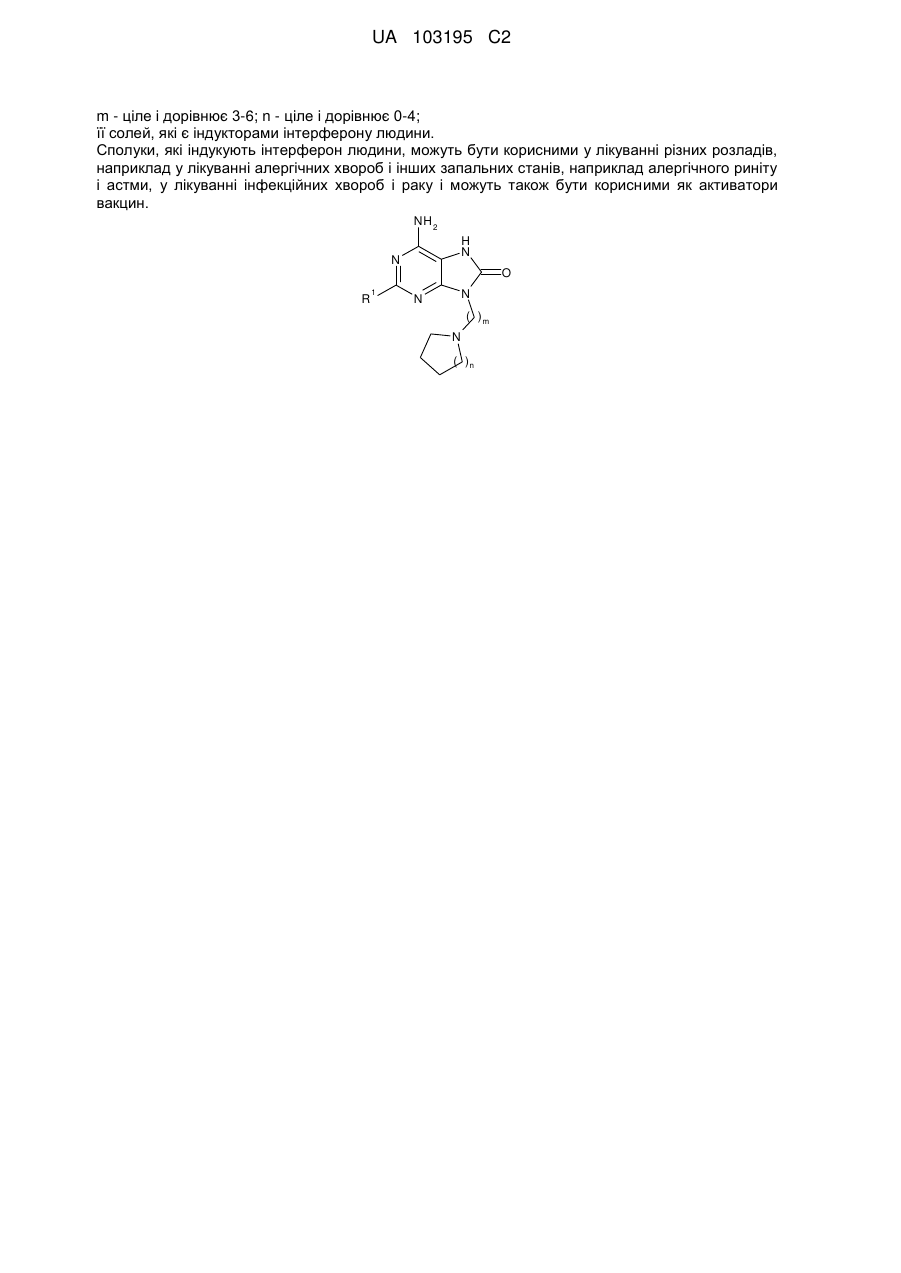
1. Сполука формули (І):
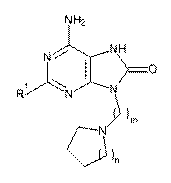 , (І)
, (І)
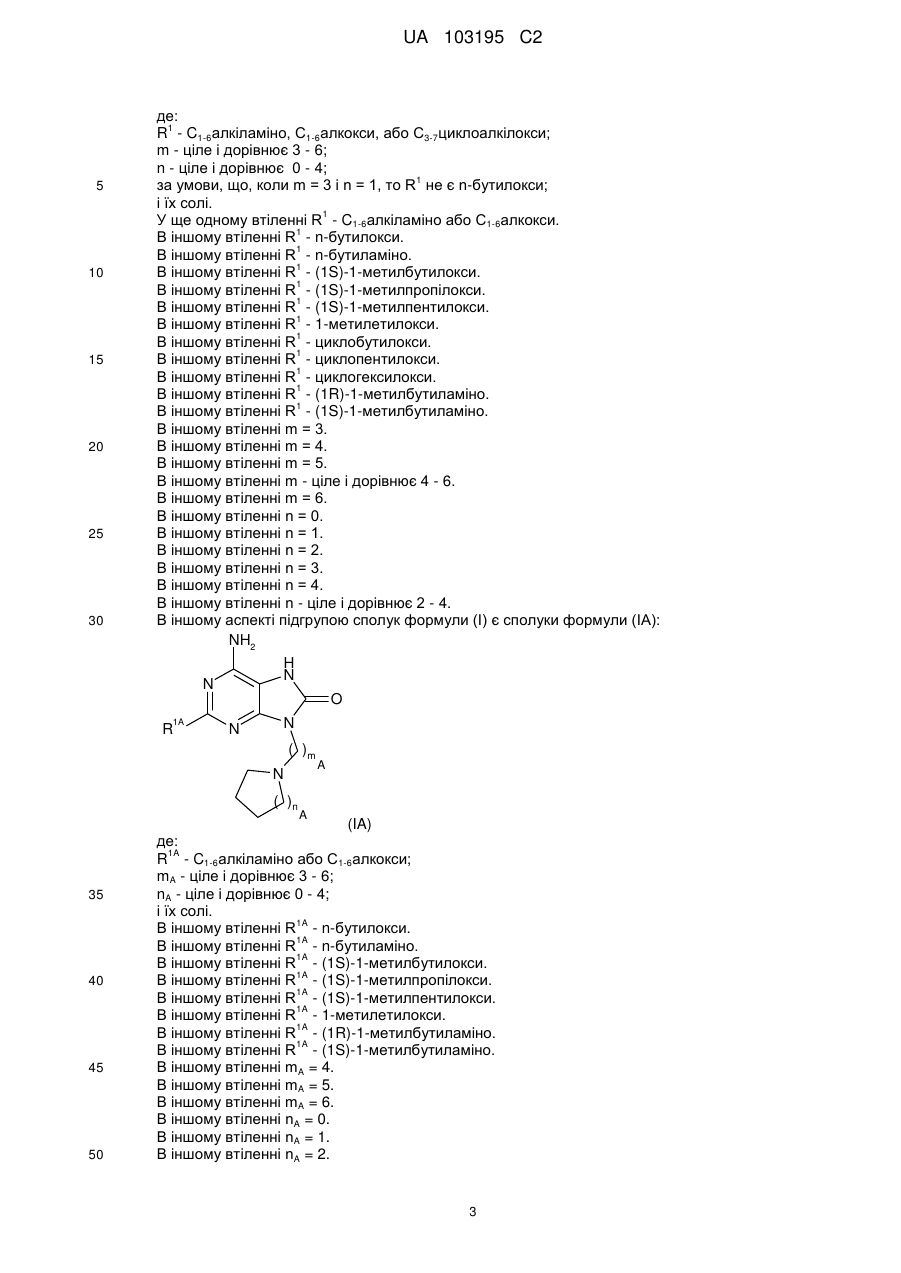
де:
R1 - С1-6алкіламіно, С1-6алкокси або С3-7циклоалкілокси;
m - ціле і дорівнює 3-6;
n - ціле і дорівнює 0-4;
за умови, що, коли m = 3 і n = 1, то R1 не є н-бутилокси;
або її сіль.
2. Сполука за п. 1 або її сіль, в якій R1 - н-бутилокси.
3. Сполука за п. 1 або її сіль, в якій R1 - (1S)-1-метилбутилокси.
4. Сполука за будь-яким з пп. 1-3 або її сіль, в якій m - ціле і дорівнює 4-6.
5. Сполука за будь-яким з пп. 1-4 або її сіль, в якій n - ціле і дорівнює 2-4.
6. Сполука або її сіль, вибрана з групи, яку складають:
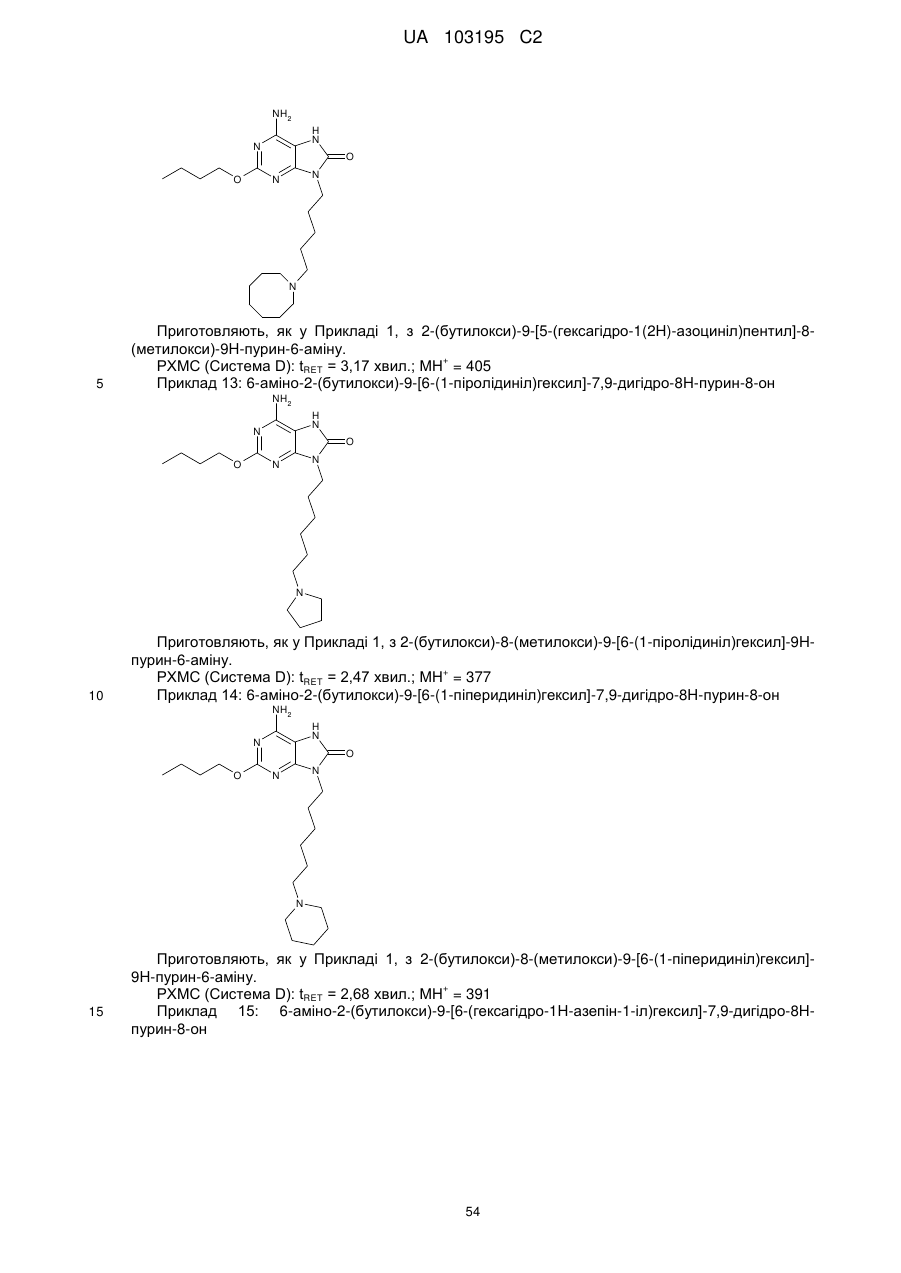
6-аміно-2-(бутилокси)-9-[6-(1-піролідиніл)гексил]-7,9-дигідро-8H-пурин-8-он;
6-аміно-2-(бутилокси)-9-[6-(гексагідро-1Н-азепін-1-іл)гексил]-7,9-дигідро-8Н-пурин-8-он;
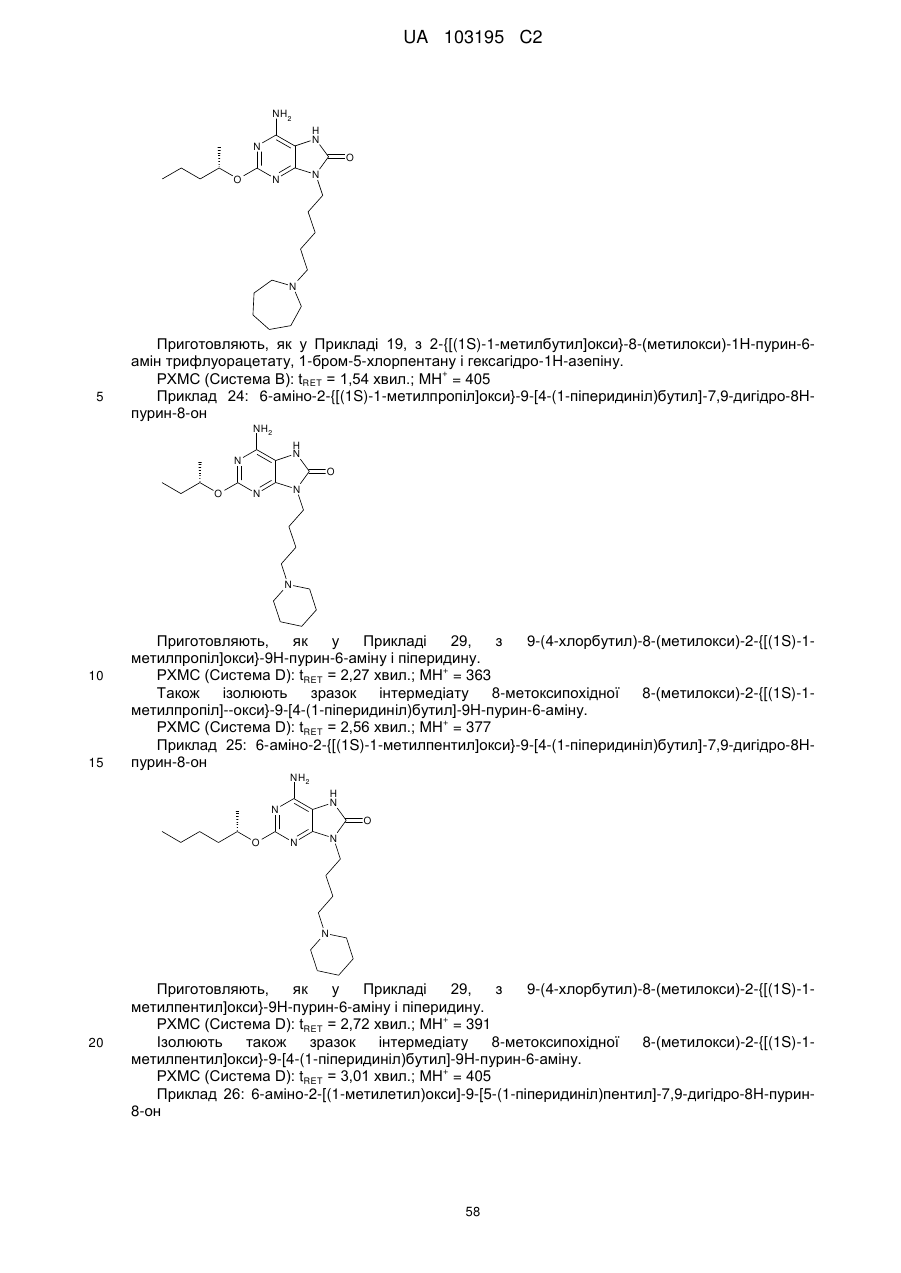
6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[4-(1-піперидиніл)бутил]-7,9-дигідро-8Н-пурин-8-он;
6-аміно-9-[4-(гексагідро-1Н-азепін-1-іл)бутил]-2-{[(1S)-1-метилбутил]окси}-7,9-дигідро-8Н-пурин-8-он;
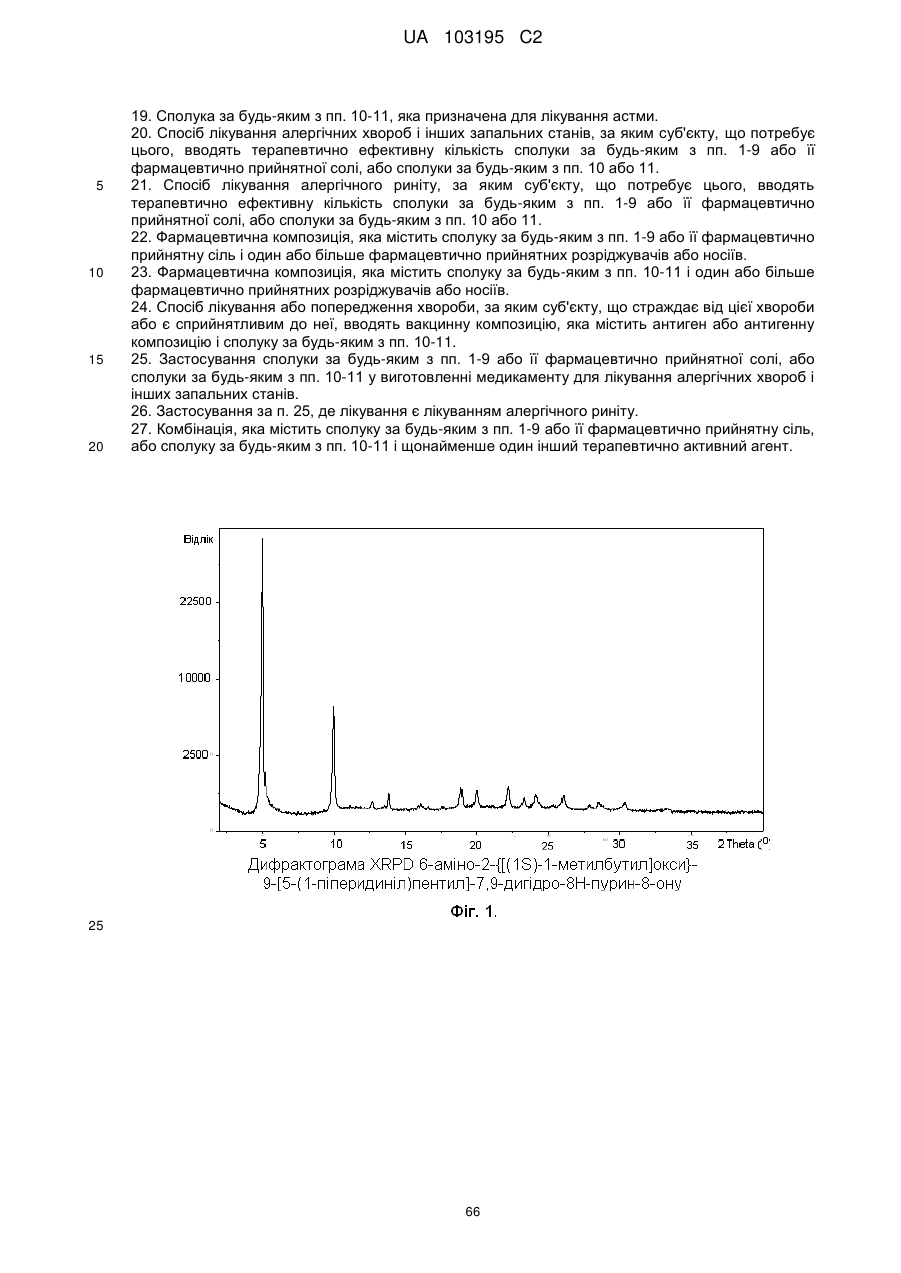
6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1-піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-он і
6-аміно-9-[5-(гексагідро-1H-азепін-1-іл)пентил]-2-{[(1S)-1-метилбутил]окси}-7,9-дигідро-8Н-пурин-8-он;
і їх солі.
7. Сполука за будь-яким з попередніх пунктів, яка має форму фармацевтично прийнятної солі.
8. Сполука, яка є 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1-піперидиніл)-пентил]-7,9-дигідро-8H-пурин-8-оном або його сіллю.
9. Сполука, яка є 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1-піперидиніл)-пентил]-7,9-дигідро-8H-пурин-8-оном або його фармацевтично прийнятною сіллю.
10. Сполука за будь-яким з пп. 1-6, яка має форму вільної основи.
11. Сполука, яка є 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1-піперидиніл)-пентил]-7,9-дигідро-8H-пурин-8-оном як вільною основою.
12. Сполука за будь-яким з пп. 1-9 або її фармацевтично прийнятна сіль, яка призначена для терапії.
13. Сполука за будь-яким з пп. 10-11, яка призначена для терапії.
14. Сполука за будь-яким з пп. 1-9 або її фармацевтично прийнятна сіль, яка призначена для лікування алергічних хвороб і інших запальних станів, інфекційних хвороб або раку.
15. Сполука за будь-яким з пп. 10-11, яка призначена для лікування алергічних хвороб і інших запальних станів, інфекційних хвороб або раку.
16. Сполука за будь-яким з пп. 1-9 або її фармацевтично прийнятна сіль, яка призначена для лікування алергічного риніту.
17. Сполука за будь-яким з пп. 10-11 або її фармацевтично прийнятна сіль, яка призначена для лікування алергічного риніту.
18. Сполука за будь-яким з пп. 1-9 або її фармацевтично прийнятна сіль, яка призначена для лікування астми.
19. Сполука за будь-яким з пп. 10-11, яка призначена для лікування астми.
20. Спосіб лікування алергічних хвороб і інших запальних станів, за яким суб'єкту, що потребує цього, вводять терапевтично ефективну кількість сполуки за будь-яким з пп. 1-9 або її фармацевтично прийнятної солі, або сполуки за будь-яким з пп. 10 або 11.
21. Спосіб лікування алергічного риніту, за яким суб'єкту, що потребує цього, вводять терапевтично ефективну кількість сполуки за будь-яким з пп. 1-9 або її фармацевтично прийнятної солі, або сполуки за будь-яким з пп. 10 або 11.
22. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-9 або її фармацевтично прийнятну сіль і один або більше фармацевтично прийнятних розріджувачів або носіїв.
23. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 10-11 і один або більше фармацевтично прийнятних розріджувачів або носіїв.
24. Спосіб лікування або попередження хвороби, за яким суб'єкту, що страждає від цієї хвороби або є сприйнятливим до неї, вводять вакцинну композицію, яка містить антиген або антигенну композицію і сполуку за будь-яким з пп. 10-11.
25. Застосування сполуки за будь-яким з пп. 1-9 або її фармацевтично прийнятної солі, або сполуки за будь-яким з пп. 10-11 у виготовленні медикаменту для лікування алергічних хвороб і інших запальних станів.
26. Застосування за п. 25, де лікування є лікуванням алергічного риніту.
27. Комбінація, яка містить сполуку за будь-яким з пп. 1-9 або її фармацевтично прийнятну сіль, або сполуку за будь-яким з пп. 10-11 і щонайменше один інший терапевтично активний агент.
Текст
Реферат: Винахід стосується сполуки формули (І) , (I) де: 1 R - С1-6алкіламіно, С1-6алкокси або С3-7циклоалкілокси; UA 103195 C2 (12) UA 103195 C2 m - ціле і дорівнює 3-6; n - ціле і дорівнює 0-4; її солей, які є індукторами інтерферону людини. Сполуки, які індукують інтерферон людини, можуть бути корисними у лікуванні різних розладів, наприклад у лікуванні алергічних хвороб і інших запальних станів, наприклад алергічного риніту і астми, у лікуванні інфекційних хвороб і раку і можуть також бути корисними як активатори вакцин. NH2 H N N O R 1 N N ( )m N ( )n UA 103195 C2 5 10 15 20 25 30 35 40 45 50 55 60 Винахід належить до сполук, способів їх приготування, композицій, що містять їх, їх використання у лікуванні різних розладів, зокрема, алергічних хвороб і інших запальних станів, наприклад, алергічного риніту і астми, інфекційних хвороб, раку і як активаторів вакцини. Хребці постійно знаходяться під загрозою інвазії мікроорганізмів і створили механізми імунного захисту для знищення інфекційних патогенів. У ссавців ця імунна система включає дві лінії: природний імунітет і набутий імунітет. Першою лінія захисту організму є природна система, опосередкована макрофагами і дендритними клітинами. Набутий імунітет забезпечує усунення патогенів на пізнішій стадії інфекції і забезпечує створення імунологічної пам'яті. Набутий імунітет є високоспецифічним внаслідок наявності широкого набору лімфоцитів з антигеноспецифічними рецепторами, які зазнали генної перебудови. Раніше вважали, що природна імунна реакція є неспецифічною, але тепер відомо, що існує дискримінація власними і іншими різними патогенами. Природна імунна система розпізнає мікроб за допомогою деякої кількості гермінативно кодованих розпізнавальних рецепторів (PRR), які мають ряд важливих характеристик. Толоподібні рецептори (TLR) є родиною десяти розпізнавальних рецепторів, описаних у людини. TLR експресовано головним чином природними імунними клітинами і їх роллю є моніторинг довкілля у пошуку ознак інфекції і, після активації, мобілізація захисних механізмів, спрямованих на знищення прониклих патогенів. Ранні природні імунні реакції, ініційовані TLR, обмежують розповсюдження інфекції, а прозапальні цитокіни і хемокіни, які вони індукують, викликають поповнення і активацію антигенних клітин, B клітин і T клітин. TLR можуть модулювати природу адаптивних імунних реакцій, отримуючи належний захист через активацію дендритних клітин і вивільнення цитокінів (Akira S. et al, Nat. Імуноl., 2001: 2, 675-680). Профіль реакції, забезпеченої різними агоністами TLR, залежить від типу активованих клітин. TLR7 є членом підгрупи TLR (TLR 3, 7, 8 і 9), локалізованим у ядерній частині клітини, де він спеціалізується на виявлення нуклеїнових кислот. TLR7 грає ключову роль у антивірусному захисті завдяки розпізнаванню ssРНК (Diebold S.S. et al, Science, 2004: 303, 1529-1531; і Lund J. M. et al, PNAS, 2004: 101, 5598-5603). TLR7 має обмежений профіль експресії у людини і експресується, головним чином, B клітинами і плазмацитоїдними дендритними клітинами (pDC) і, у меншій мірі, моноцитами. Плазмацитоїдні DC утворюють унікальну популяцію лімфоїдних дендритних клітин (0,2-0,8 % периферійних кров'яних мононуклеарних клітин (PBMC)), які належать до первинного типу I клітин, які продукують інтерферон і секретують високі рівні інтерферону-альфа (IFNα) і інтерферону-бета (IFNβ) у відповідь на вірусні інфекції (Liu Y-J, Annu. Rev. Імуноl., 2005: 23, 275-306). Алергічні хвороби пов'язані з зумовленою Th2 імунною реакцію на алергени. Реакції Th2 пов'язані з підвищеними рівнями IgE, які внаслідок їх дії на мастові клітин, сприяють гіперчутливості до алергенів, яка виявляється у симптомах, наприклад, в алергічному риніті. У здорових осіб імунна реакція на алергени є більш збалансованою з змішаною реакцією Th2/Th1 і регуляторних T клітин. Було показано, що ліганди TLR7 знижують вивільнення цитокінів Th2, поліпшують вивільнення цитокінів Th1 in vitro і знижують запальні реакції типу Th2 в алергічних легеневих моделях in vivo (Fili L. et al, J. All. Clin. Імуноl., 2006: 118, 511-517; Moisan J. et al, Am. J. Physiol. Lung Cell Mol. Physiol., 2006: 290, L987-995; Tao et al, Chin. Med. J., 2006: 119, 640648). Отже, ліганди TLR7 можуть відновлювати баланс імунної реакції у алергиків і модифікувати хворобу. Головними у ефективній природній імунній реакції у ссавців є механізми, які викликають індукування інтерферонів і інших цитокінів, які діють на клітини, породжуючи ряд явищ. Ці явища можуть включати активацію експресії антиінфекційного гену, активацію присутності антигену у клітинах для створення сильного специфічного до антигену імунітету і сприяння фагоцитозу у фагоцитних клітинах. Інтерферон бува вперше описаний як агент, здатний захистити клітину від вірусної інфекції (Isaacs & Lindemann, J. Virus Interference. Proc. R. Soc. Lon. Ser. B. Biol. Sci. 1957: 147, 258-267). У людини інтерферони типу І є родиною споріднених протеїнів, кодованих генами у хромосомах і з кодуванням щонайменше 13 ізоформ інтерферону-альфа (IFNα) і одної ізоформи інтерферону-бета (IFNβ). У рекомбінантний IFNα була вперше виявлена біологічна терапевтичність і його важливість у терапії вірусних інфекцій і раку. Забезпечуючи антивірусну активність у клітині, інтерферони, як відомо, є потужними модуляторами імунної реакції, діючи на клітини імунної системи. Першочерговою терапією проти вірусу гепатиту C (HCV) можуть бути комбінації інтерферонів, високоефективні у зниженні вірусного навантаження у деяких суб'єктів шляхом припинення реплікації вірусів. Однак, деякі пацієнти не показують постійної вірусної реакції і у цих пацієнтів вірусне навантаження є неконтрольованим. Крім того терапія з ін'єкціями 1 UA 103195 C2 5 10 15 20 25 30 35 40 45 інтерферону може бути пов'язана з рядом небажаних шкідливих явищ, які, як було показано, погано впливають на результати лікування (Dudley T, et al, Gut., 2006: 55(9), 1362-3). Введення низькомолекулярних сполук, здатних стимулювати природну імунну реакцію, включаючи активацію інтерферонів типу І і інших цитокінів, може стати важливою стратегією у лікуванні або відвертанні хвороб людини, включаючи вірусні інфекції. Такий тип імуномодуляційної стратегії дозволяє ідентифікувати сполуки, які можуть бути корисними не лише при інфекційних хворобах, але також у лікування раку (Krieg. Curr. Oncol. Rep., 2004: 6(2), 88-95), алергічних хвороб (Moisan J. et al, Am. J. Physiol. Lung Cell Mol. Physiol., 2006: 290, L987995), інших запальних станів, наприклад, хвороби подразненого кишечнику (Rakoff-Nahoum S., Cell., 2004, 23, 118(2): 229-41), і як активатори вакцини (Persing et al. Trends Microbiol. 2002: 10(10 Suppl), S32-7). У тваринних моделях імікімоди показали активаторну активність топічно (Adams S. et al, J. Imunol., 2008, 181:776-84; Johnston D. et al, Vaccine, 2006, 24:1958-65) або системно (Fransen F. et al, Infect. Immun., 2007, 75:5939-46). Ресиквінод і інші споріднені агоністи TLR7/8, як було показано, також мають активаторну активність (Ma R. et al, Biochem. Biophys. Res. Commun., 2007, 361:537-42; Wille-Reece U. et al, Proc. Natl. Acad. Sci. USA, 2005, 102:15190-4; Wille-Reece U. et al, US2006045885 A1). Механізми, які ведуть до індукування інтерферонів типу І, є зрозумілими лише частково. Одним механізмом, який може викликати індукування інтерферону у багатьох типах клітин, є розпізнавання двоспіральної вірусної РНК геліказами РНК RIG-I і MDA5. Цей механізм вважається первинним механізмом, яким інтерферони індукуються інфекцією клітин вірусом Сендаля (Sendai). Іншими механізмами індукування інтерферонів є залежні від TLR сигнальні явища. У людини плазмацитоїдні дендритні клітини (pDC), які є професійними клітинами, що виробляють інтерферон, можуть створити значну кількість інтерферонів у реакції, наприклад, на вірусну інфекцію. Було показано, що ці pDC здебільшого експресують TLR7 і TLR9 і стимуляція цих рецепторів вірусною РНК або ДНК може індукувати експресію інтерферону-альфа. Були описані олігонуклеотидні агоністи TLR7 і TLR9 і низькомолекулярні базовані на пурині агоністи TLR7, які можуть індукувати інтерферон-альфа з клітин цього типу у тварин і людини (Takeda K. et al, Annu. Rev. Імуноl., 2003: 21, 335-76). Агоністи TLR7 включають імідазохінолінові сполуки, наприклад, імікімод і ресикімод, аналоги оксоаденіну і аналоги нуклеозиду, наприклад, локсорибін і 7-тіа-8-оксогуанозин, які, як відомо, індукують інтерферон-альфа. У заявці WO 2008/114008 описано 9-заміщені-8-оксоаденінові сполуки як модулятори TLR7. Залишається незрозумілим, як низькомолекулярні пуриноподібні сполуки можуть індукувати інтерферони типу І і інші цитокіни, оскільки молекулярні об'єкти цих відомих індукторів не були ідентифіковані. Однак, були розроблені аналітичні стратегії для характеризації низькомолекулярних індукторів інтерферону IFNα людини (незалежно від механізм), які базуються на стимуляції первинних людських донорських клітин сполукам, які описані нижче. Було показано, що деякі сполуки винаходу є індукторами людського інтерферону і можуть мати поліпшений профіль порівняно відомими індукторами людського інтерферону, наприклад, більшу потужність кращу селективність до IFNα порівняно з TNFα. Наприклад, деякі сполуки винаходу показують більш, як 1000-разову селективність для індукування IFNα порівняно з індукуванням TNFα. Сполуки, які індукують людський інтерферон, можуть бути корисними у лікуванні різних розладів, наприклад, у лікуванні алергічних хвороб і інших запальних станів, наприклад, алергічного риніту і астми, у лікуванні інфекційних хвороб і раку і можуть також бути корисними як активатори вакцини. Деякі сполуки винаходу є потужними імуномодуляторами і тому потребують обережного використання. У першому аспекті запропоновано сполуки формули (I): NH2 H N N O 1 R N N ( )m N ( )n 50 (I) 2 UA 103195 C2 5 10 15 20 25 30 де: 1 R - C1-6алкіламіно, C1-6алкокси, або C3-7циклоалкілокси; m - ціле і дорівнює 3 - 6; n - ціле і дорівнює 0 - 4; 1 за умови, що, коли m = 3 і n = 1, то R не є n-бутилокси; і їх солі. 1 У ще одному втіленні R - C1-6алкіламіно або C1-6алкокси. 1 В іншому втіленні R - n-бутилокси. 1 В іншому втіленні R - n-бутиламіно. 1 В іншому втіленні R - (1S)-1-метилбутилокси. 1 В іншому втіленні R - (1S)-1-метилпропілокси. 1 В іншому втіленні R - (1S)-1-метилпентилокси. 1 В іншому втіленні R - 1-метилетилокси. 1 В іншому втіленні R - циклобутилокси. 1 В іншому втіленні R - циклопентилокси. 1 В іншому втіленні R - циклогексилокси. 1 В іншому втіленні R - (1R)-1-метилбутиламіно. 1 В іншому втіленні R - (1S)-1-метилбутиламіно. В іншому втіленні m = 3. В іншому втіленні m = 4. В іншому втіленні m = 5. В іншому втіленні m - ціле і дорівнює 4 - 6. В іншому втіленні m = 6. В іншому втіленні n = 0. В іншому втіленні n = 1. В іншому втіленні n = 2. В іншому втіленні n = 3. В іншому втіленні n = 4. В іншому втіленні n - ціле і дорівнює 2 - 4. В іншому аспекті підгрупою сполук формули (I) є сполуки формули (IA): NH2 H N N O 1A R N N ( )m N ( )n 35 40 45 50 A A (IA) де: 1A R - C1-6алкіламіно або C1-6алкокси; mA - ціле і дорівнює 3 - 6; nA - ціле і дорівнює 0 - 4; і їх солі. 1A В іншому втіленні R - n-бутилокси. 1A В іншому втіленні R - n-бутиламіно. 1A В іншому втіленні R - (1S)-1-метилбутилокси. 1A В іншому втіленні R - (1S)-1-метилпропілокси. 1A В іншому втіленні R - (1S)-1-метилпентилокси. 1A В іншому втіленні R - 1-метилетилокси. 1A В іншому втіленні R - (1R)-1-метилбутиламіно. 1A В іншому втіленні R - (1S)-1-метилбутиламіно. В іншому втіленні m A = 4. В іншому втіленні m A = 5. В іншому втіленні m A = 6. В іншому втіленні nA = 0. В іншому втіленні nA = 1. В іншому втіленні nA = 2. 3 UA 103195 C2 5 10 15 20 25 30 35 40 45 50 55 60 В іншому втіленні nA = 3. В іншому втіленні nA = 4. В іншому аспекті запропоновано сполуки формули (IA) і їх солі, визначені вище, де m - ціле і дорівнює 4 - 6. Іншим аспектом винаходу є сполуки формули (IA) і їх солі, визначені вище, за умови, що 6аміно-2-(бутилокси)-9-[3-(1-піролідиніл)пропіл]-7,9-дигідро-8H-пурин-8-он виключено. В іншому аспекті винахід включає сполуки формули (I) і їх солі за умови, що 6-аміно-2-{[(1S)1-метилбутил]окси}-9-[5-(1-піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-он і його солі виключено. В іншому аспекті винахід включає сполуки формули (IA) і їх солі, визначені вище, де m - ціле і дорівнює 4 - 6 і 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1-піперидиніл)пентил]-7,9-дигідро-8Hпурин-8-он і його солі виключено. В іншому аспекті винахід включає сполуки формули (IA) і їх солі, визначені вище, за умови, що 6-аміно-2-(бутилокси)-9-[3-(1-піролідиніл)пропіл]-7,9-дигідро-8H-пурин-8-он і 6-аміно-2-{[(1S)1-метилбутил]окси}-9-[5-(1-піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-он і їх солі виключено. Приклади сполук формули (I), перелічені далі, є ще одним аспектом винаходу: 6-аміно-9-[3-(1-ацетидиніл)пропіл]-2-(бутилокси)-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-(бутилокси)-9-[3-(1-піролідиніл)пропіл]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-(бутилокси)-9-[3-(гексагідро-1H-азепін-1-іл)пропіл]-7,9-дигідро-8H-пурин-8-он; 6-аміно-9-[4-(1-ацетидиніл)бутил]-2-(бутилокси)-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-(бутилокси)-9-[4-(1-піролідиніл)бутил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-(бутилокси)-9-[4-(1-піперидиніл)бутил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-(бутилокси)-9-[4-(гексагідро-1H-азепін-1-іл)бутил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-9-[5-(1-ацетидиніл)пентил]-2-(бутилокси)-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-(бутилокси)-9-[5-(1-піролідиніл)пентил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-(бутилокси)-9-[5-(1-піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-(бутилокси)-9-[5-(гексагідро-1H-азепін-1-іл)пентил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-(бутилокси)-9-[5-(гексагідро-1(2H)-азоциніл)пентил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-(бутилокси)-9-[6-(1-піролідиніл)гексил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-(бутилокси)-9-[6-(1-піперидиніл)гексил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-(бутилокси)-9-[6-(гексагідро-1H-азепін-1-іл)гексил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-(бутиламіно)-9-[3-(1-піперидиніл)пропіл]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-(бутиламіно)-9-[4-(1-піперидиніл)бутил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-(бутиламіно)-9-[4-(гексагідро-1H-азепін-1-іл)бутил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-(бутиламіно)-9-[5-(гексагідро-1H-азепін-1-іл)пентил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[4-(1-піперидиніл)бутил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-9-[4-(гексагідро-1H-азепін-1-іл)бутил]-2-{[(1S)-1-метилбутил]окси}-7,9-дигідро-8Hпурин-8-он; 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1-піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-9-[5-(гексагідро-1H-азепін-1-іл)пентил]-2-{[(1S)-1-метилбутил]окси}-7,9-дигідро-8Hпурин-8-он; 6-аміно-2-{[(1S)-1-метилпропіл]окси}-9-[4-(1-піперидиніл)бутил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-{[(1S)-1-метилпентил]окси}-9-[4-(1-піперидиніл)бутил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-[(1-метилетил)окси]-9-[5-(1-піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-(циклобутилокси)-9-[4-(1-піперидиніл)бутил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-(циклопентилокси)-9-[4-(1-піперидиніл)бутил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-(циклогексилокси)-9-[4-(1-піперидиніл)бутил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-{[(1R)-1-метилбутил]аміно}-9-[4-(1-піперидиніл)бутил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-{[(1S)-1-метилбутил]аміно}-9-[4-(1-піперидиніл)бутил]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[3-(1-піперидиніл)пропіл]-7,9-дигідро-8H-пурин-8-он; 6-аміно-2-{[(1S)-1-метилпропіл]окси}-9-[5-(1-піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-он, і 6-аміно-2-(бутилокси)-9-[3-(1-піперидиніл)пропіл]-7,9-дигідро-8H-пурин-8-он; і їх солі. В іншому втіленні винахід включає 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-он або його сіль. В іншому втіленні винахід включає 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-он або його фармацевтично прийнятну сіль. В іншому втіленні винахід включає 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-он як вільну основу. Ще одним аспектом винаходу є сполука формули (I) або її фармацевтично прийнятна сіль, призначені для використання у терапії. 4 UA 103195 C2 5 10 15 20 25 30 35 40 45 50 55 60 Винахід включає також 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1-піперидиніл)пентил]-7,9дигідро-8H-пурин-8-он або його фармацевтично прийнятну сіль, призначені для використання у терапії. Винахід включає також 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1-піперидиніл)пентил]-7,9дигідро-8H-пурин-8-он як вільну основу, призначений для використання у терапії. Коли сполука формули (I) або її фармацевтично прийнятна сіль використовуються у терапії, вони використовуються як активні терапевтичні агенти. Винахід включає також сполуку формули (I) або її фармацевтично прийнятну сіль для використання у лікуванні алергічних хвороб і інших запальних станів, інфекційних хвороб і раку. Винахід включає також 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1-піперидиніл)пентил]-7,9дигідро-8H-пурин-8-он або його фармацевтично прийнятну сіль для використання у лікуванні алергічних хвороб і інших запальних станів, інфекційних хвороб і раку. Винахід включає також 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1-піперидиніл)пентил]-7,9дигідро-8H-пурин-8-он як вільну основу для використання у лікуванні алергічних хвороб і інших запальних станів, інфекційних хвороб і раку. Винахід включає також сполуку формули (I) або її фармацевтично прийнятну сіль для використання у лікуванні алергічного риніту. Винахід включає також 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1-піперидиніл)пентил]-7,9дигідро-8H-пурин-8-он або його фармацевтично прийнятну сіль для використання у лікуванні алергічного риніту. Винахід включає також 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1-піперидиніл)пентил]-7,9дигідро-8H-пурин-8-он як вільну основу для використання у лікуванні алергічного риніту. Винахід включає також сполуку формули (I) або її фармацевтично прийнятну сіль для використання у лікуванні астми. Винахід включає також 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1-піперидиніл)пентил]-7,9дигідро-8H-пурин-8-он або його фармацевтично прийнятну сіль для використання у лікуванні астми. Винахід включає також 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1-піперидиніл)пентил]-7,9дигідро-8H-пурин-8-он як вільну основу для використання у лікуванні астми. Винахід включає також активатор вакцини, який містить сполуку формули (I) або її фармацевтично прийнятну сіль. Винахід включає також імуногенну композицію, яка містить антиген або антигенну композицію і сполуку формули (I) або її фармацевтично прийнятну сіль. Винахід включає також вакцинну композицію, яка містить антиген або антигенну композицію і сполуку формули (I) або її фармацевтично прийнятну сіль. Винахід включає також спосіб лікування або відвертання хвороби, який включає введення суб'єкту, що страждає від або має схильність до цієї хвороби, імуногенної композиції, яка містить антиген або антигенну композицію і сполуку формули (I) або її фармацевтично прийнятну сіль. Винахід включає також спосіб лікування або відвертання хвороби, який включає введення суб'єкту, що страждає від або має схильність до цієї хвороби, вакцинної композиції, яка містить антиген або антигенну композицію і сполуку формули (I) або її фармацевтично прийнятну сіль. Винахід включає також використання сполуки формули (I) або її фармацевтично прийнятної солі у виготовленні імуногенної композиції, яка містить антиген або антигенну композицію, для лікування або відвертання хвороби. Винахід включає також використання сполуки формули (I) або її фармацевтично прийнятної солі у виготовленні вакцинної композиції, яка містить антиген або антигенну композицію, для лікування або відвертання хвороби. Винахід включає також використання сполуки формули (I) або її фармацевтично прийнятної солі у виготовленні медикаменту для лікування алергічних хвороб і інших запальних станах, інфекційних хвороб і раку. Винахід включає також використання 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-ону або його фармацевтично прийнятної солі у виготовленні медикаменту для лікування алергічних хвороб і інших запальних станах, інфекційних хвороб і раку. Винахід включає також використання 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-ону як вільної основи у виготовленні медикаменту для лікування алергічних хвороб і інших запальних станих, інфекційних хвороб і раку. Винахід включає також використання сполуки формули (I) або її фармацевтично прийнятної солі у виготовленні медикаменту для лікування алергічного риніту. 5 UA 103195 C2 5 10 15 20 25 30 35 40 45 50 55 60 Винахід включає також використання 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-ону або його фармацевтично прийнятної солі у виготовленні медикаменту для лікування алергічного риніту. Винахід включає також використання 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-ону як вільної основи у виготовленні медикаменту для лікування алергічного риніту. Винахід включає також використання сполуки формули (I) або її фармацевтично прийнятної солі у виготовленні медикаменту для лікування астми. Винахід включає також використання 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-ону або його фармацевтично прийнятної солі у виготовленні медикаменту для лікування астми. Винахід включає також використання 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-ону як вільної основи у виготовленні медикаменту для лікування астми. Винахід включає також спосіб лікування алергічних хвороб і інших запальних станів інфекційних хвороб і раку, який включає введення суб'єкту, що потребує цього, терапевтично ефективної кількості сполуки формули (I) або її фармацевтично прийнятної солі. Винахід включає також спосіб лікування алергічних хвороб і інших запальних станів інфекційних хвороб і раку, який включає введення суб'єкту, що потребує цього, терапевтично ефективної кількості 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1-піперидиніл)пентил]-7,9-дигідро8H-пурин-8-ону або його фармацевтично прийнятної солі. Винахід включає також спосіб лікування алергічних хвороб і інших запальних станів інфекційних хвороб і раку, який включає введення суб'єкту, що потребує цього, терапевтично ефективної кількості 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1-піперидиніл)пентил]-7,9-дигідро8H-пурин-8-ону як вільної основи. Винахід включає також спосіб лікування алергічного риніту, який включає введення суб'єкту, що потребує цього, терапевтично ефективної кількості сполуки формули (I) або її фармацевтично прийнятної солі. Винахід включає також спосіб лікування алергічного риніту, який включає введення суб'єкту, що потребує цього, терапевтично ефективної кількості 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5(1-піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-ону або його фармацевтично прийнятної солі. Винахід включає також спосіб лікування алергічного риніту, який включає введення суб'єкту, що потребує цього, терапевтично ефективної кількості 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5(1-піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-ону як вільної основи. Винахід включає також спосіб лікування астми, який включає введення суб'єкту, що потребує цього, терапевтично ефективної кількості сполуки формули (I) або її фармацевтично прийнятної солі. Винахід включає також спосіб лікування астми, який включає введення суб'єкту, що потребує цього, терапевтично ефективної кількості 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-ону або його фармацевтично прийнятної солі. Винахід включає також спосіб лікування астми, який включає введення суб'єкту, що потребує цього, терапевтично ефективної кількості 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-ону як вільної основи. Винахід включає в іншому аспекті комбінацію, яка включає сполуку формули (I) або її фармацевтично прийнятну сіль разом з щонайменше одним іншим терапевтично активним агентом. Винахід включає в іншому аспекті комбінацію, яка включає 6-аміно-2-{[(1S)-1метилбутил]окси}-9-[5-(1-піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-он або його фармацевтично прийнятну сіль разом з щонайменше одним іншим терапевтично активним агентом. Винахід включає в іншому аспекті комбінацію, яка включає 6-аміно-2-{[(1S)-1метилбутил]окси}-9-[5-(1-піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-он як вільну основу разом з щонайменше одним іншим терапевтично активним агентом. Винахід, крім того, включає фармацевтичну композицію, яка містить сполуку формули (I) або фармацевтично прийнятну сіль і один або більше фармацевтично прийнятних розріджувачів або носіїв. Винахід, крім того, включає фармацевтичну композицію, яка містить 6-аміно-2-{[(1S)-1метилбутил]окси}-9-[5-(1-піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-он або його фармацевтично прийнятну сіль і один або більше фармацевтично прийнятних розріджувачів або носіїв. 6 UA 103195 C2 5 10 15 Винахід, крім того, включає фармацевтичну композицію, яка містить 6-аміно-2-{[(1S)-1метилбутил]окси}-9-[5-(1-піперидиніл)пентил]-7,9-дигідро-8H-пурин-8-он як вільну основу і один або більше фармацевтично прийнятних розріджувачів або носіїв. Винахід включає в іншому аспекті спосіб приготування фармацевтичної композиції, який включає змішування сполуки формули (I) або її фармацевтично прийнятної солі з одним або більше фармацевтично прийнятними розріджувачами або носіями. Винахід, крім того, включає спосіб приготування фармацевтичної композиції, який включає змішування 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1-піперидиніл)пентил]-7,9-дигідро-8Hпурин-8-ону або його фармацевтично прийнятної солі з одним або більше фармацевтично прийнятними розріджувачами або носіями. Винахід, крім того, включає спосіб приготування фармацевтичної композиції, який включає змішування 6-аміно-2-{[(1S)-1-метилбутил]окси}-9-[5-(1-піперидиніл)пентил]-7,9-дигідро-8Hпурин-8-ону як вільної основи з одним або більше фармацевтично прийнятними розріджувачами або носіями. Одним з аспектів винаходу є спосіб приготування сполук формули (I) і їх солей, описаний тут. Отже, винахід включає спосіб приготування сполуки формули (I), який включає зняття захисту сполуки формули (II): NH2 N N 2 OR 1 R N N ( )m N ( )n 20 25 30 35 40 45 50 (II) 1 2 де R , m, і n визначено вище для сполуки формули (I), а R - C1-6алкіл, і після цього, якщо потрібно, виконання, як варіант, одної або більше таких операцій: (i) видалення будь-якої необхідної захисних груп; (ii) приготування солі приготовленої у такий спосіб сполуки. Винахід включає усі комбінації втілень і аспектів, описаних тут. Винахід описано у термінах, відомих і схвалених фахівцями. Для кращого розуміння для деяких термінів наведено визначення. Ці визначення не слід розглядати як такі, що не є узгодженими з звичайним значенням, крім того, будь-який термін, що не був визначений, використовуються у звичайному загальноприйнятному значенні. Усі терміни, використані тут для опису винаходу, дозволяють звичайному фахівцю зрозуміти винахід у його повному об'ємі, не обмежуючи його. Термін "алкіл" включає як лінійні, так і і розгалужені ланцюгові аліфатичні ізомери відповідного алкілу, який має до 6 атомів карбону, наприклад, до 4 атомів карбону або до 2 атомів карбону. Це визначення придатне також, коли алкільна група є частиною іншої групи, наприклад, алкіламіно- або алкоксигрупи. Прикладами таких алкільних груп і груп, що містять алкільні групи, є C1-6алкіл, C1-6алкіламіно, і C1-6алкокси. Термін "циклоалкіл" стосується моноциклічних алкільних груп, які містять 3-7 атомів карбону, наприклад, 4 або 5 атомів карбону, або 6 атомів карбону. Цей термін придатен також, коли циклоалкільна група є частиною іншої групи, наприклад, циклоалкоксигрупи. Прикладами циклоалкільних груп є циклобутил, циклопентил і циклогексил. Терміни "гетероцикл" або "гетероцикліл" стосуються моноциклічного насиченого гетероциклічного аліфатичного кільця з 3-7 атомами карбону і одним гетероатомом, яким є нітроген. Такими гетероциклічними кільцями є ацетидин або ацетидиніл, піролідин або піролідиніл, піперидин або піперидиніл, гексагідроазепін або гексагідроазепініл і октагідроазоцин або гексагідро-(2H)-азоциніл. Термін "галоген" стосується йоду, брому, хлору або флуору, звичайно брому, хлору або флуору. Посилання на сполуки винаходу означають сполуку формули (I) як вільну основу або як сіль, наприклад, фармацевтично прийнятну сіль. Солі сполук формули (I) включають фармацевтично прийнятні солі і солі, які можуть не бути фармацевтично прийнятними, але можуть бути корисними у приготуванні сполук формули і їх 7 UA 103195 C2 5 10 15 20 25 30 35 40 45 50 55 60 фармацевтично прийнятних солей. Солі можуть походити від неорганічних або органічних кислот, або деяких неорганічних або органічних основ. Винах включає усі можливі стехіометричні і нестехіометричні форми солей сполук формули (I). Прикладами солей є фармацевтично прийнятні солі, які включають кислото-адитивні солі і осново-адитивні солі (див. Berge et al., J. Pharm. Sci., 66:1-19 (1977)). Приклади фармацевтично прийнятних кислото-адитивних солей сполуки формули (I) включають гідробромідні, гідрохлоридні, сульфатні, p-толуолсульфонатні, метансульфонатні, нафталінсульфонатні і фенілсульфонатні солі. Соли можуть бути отримані добре відомими способами, наприклад, осадженням з розчину з подальшою фільтрацією або випарюванням розчинника. Звичайно фармацевтично прийнятні кислото-адитивні солі можуть бути отримані реакцією сполуки формули (I) з належною сильною кислотою (наприклад, гідробромною, гідрохлорною, сульфуровою, p-толуолсульфоновою, метансульфоновою або нафталінсульфоновою кислотами), як варіант, у придатному розчиннику, наприклад, органічному розчиннику, з подальшою ізоляцією, наприклад, кристалізацією і фільтрацією. Деякі органічні сполуки можуть утворювати комплекси з розчинниками, у яких вони беруть участь у реакції або з яких вони осаджуються або кристалізуються. Ці комплекси є відомими як "сольвати". Наприклад, комплекс з водою є "гідратом". Розчинники з високою точкою кипіння і/або розчинники з високою здатністю утворювати гідрогенні зв'язки, наприклад, вода, етанол, ізо-пропіловий спирт і N-метил піролідинон, можуть бути використані для отримання сольватів. Способи ідентифікації сольватів включають (не лише) ЯМР і мікроаналіз. Сольвати сполук формули (I) входять в об'єм винаходу. Термін сольват включає сольвати сполук як вільних основ і будь-яких їх солей. Деякі з сполук винаходу можуть містити хіральні атоми і/або множинні зв'язки, і, отже, існувати в одній або більше стереоізомерних формах. Винахід включає усі стереоізомери сполук винаходу, включаючи оптичні ізомери, як індивідуально, такі і їх суміші, включаючи рацемічні модифікації. Будь-як стереоізомер може містити менше 10 %, наприклад, менше 5 % або менше 0,5 % за масою, будь-якого іншого стереоізомеру. Наприклад, будь-який оптичний ізомер може містити менше 10 %, наприклад, менше 5 % або менше 0,5 % за масою, його антиподу. Деякі з сполук винаходу можуть існувати у таутомерних формах. Винахід включає усі таутомери сполук винаходу як індивідуальні, так і їх суміші. Сполуки винаходу можуть мати кристалічну або аморфну форму. Деякі кристалічні форми сполук винаходу можуть існувати як поліморфи. Усі вони входять в об'єм винаходу. Заслуговують уваги термодинамічно стабільніt поліморфні форми або інші форми сполуки винаходу. Поліморфні форми сполук винаходу можуть бути характеризовані і розрізнені багатьма відомими аналітичними способами, включаючи (не лише) рентгенівську порошкову дифракцію (XRPD), ІЧ спектроскопію (IR), спектроскопію Рамана, дифіренційну сканувальну калориметрію (DSC), термогравіметричнийt аналіз (TGA) і твердотільний ядерно магнітний резонанс (ssЯМР). Отже, в об'єм винаходу включено сольвати, гідрати, ізомери і поліморфні форми сполук формули (I) і їх солей і сольватів. Приклад хворобливих станів, в яких сполук формули (I) і їх фармацевтично прийнятні солі можуть забезпечити потенційно сприятливу дію, включають алергічні хвороби і інші запальні стани, наприклад, алергічний риніт і астму, інфекційні хвороби, і рак. Сполуки формули (I) і їх фармацевтично прийнятні солі можуть бути потенційно використані як активатори вакцини. Сполуки формули (I) і їх фармацевтично прийнятні солі можуть також бути корисними як модулятори імунної реакція, як індивідуально, такі і у комбінації як активатори, у лікуванні і/або відвертанні імунно-опосередкованих розладів, включаючи (не лише) запальні або алергічні хвороби, наприклад, астму, алергічний риніт і ринокон'юнктивіт, харчові алергії, хвороби гіперчутливості легенів, еозинофільний пневмоніт, розлади гіперчутливості затриманого типу, атеросклероз, панкреатит, гастрит, коліт, остеоартрит, псоріаз, саркоїдоз, пульмонарний фіброз, синдром респіраторного дистресу, бронхоліт, хронічну обструктивну пульмонарну хворобу, синусит, цистозний фіброз, актинний кератоз, шкірну дисплазію, хронічнц уртикарію, екзему і усі типи дерматиту. Сполуки формули (I) і їх фармацевтично прийнятні солі можуть також бути корисними у лікуванні і/або відвертанні реакцій на респіраторні інфекції, включаючи (не лише) загострення вірусних хвороб дихальних шляхів і тонзиліт. Ці сполуки можуть також бути корисними у лікуванні і/або відвертанні аутоімунних хвороб, включаючи (не лише) ревматоїдний артрит, 8 UA 103195 C2 5 10 15 20 25 30 35 40 45 50 55 60 псоріазний артрит, системну червону вовчанку, хворобу Шегрена, анкілозний спондиліт, склеродерму, дерматоміозит, діабет, відторгнення трансплантату, включаючи гомологічну хворобу, запальні кишкові хвороби, включаючи (не лише) хворобу Крона і виразковий коліт. Cполуки формули (I) і їх фармацевтично прийнятні солі можуть також бути корисними у лікуванні інфекційних хвороб, включаючи (не лише) викликані вірусами гепатиту (наприклад, вірусом гепатиту B, вірусом гепатиту C), вірусом імунодефіциту людини, папіломавіруси, герпесвіруси, респіраторні віруси (наприклад, віруси інфлюенци, респіраторний синсиціальний вірус, риновірус, метамневмовірус, параінфлюенцавірус, SARS) і вірус Західного Нілу. Сполуки формули (I) і їх фармацевтично прийнятні солі можуть також бути корисними у лікуванні мікробних інфекцій, викликаних, наприклад, бактеріями, грибками або найпростішими. Вони включають (не лише) туберкульоз, бактеріальну пневмонію, аспергільйоз, гістоплазмоз, кандидозис, пневмоцистоз, лепру, хламідіоз криптококову хворобу, криптоспоридоз, токсоплазмоз, лейшманію, малярію і трипаносоміаз. Сполуки формули (I) і їх фармацевтично прийнятні солі можуть також бути корисними у лікуванні різних раків, зокрема, у лікуванні раків, чутливих до імунотерапії, включаючи (не лише) карциному клітин ниркового епітелію, рак легенів, рак грудей, колоректальний рак, рак сечового міхура, меланому, лейкемію, лімфоми і рак яєчника. Тут лікування або терапія можуть, залежно від стану, простягатись до профілактики, а також лікування встановлених станів. Сполуки формули (I) і їх фармацевтично прийнятні солі можуть бути корисними як терапевтичні агенти. Сполуки формули (I) і їх фармацевтично прийнятні солі можуть входити у рецептури, придатні для введення будь-яким відомим шляхом. Сполуки формули (I) і їх фармацевтично прийнятні солі можуть, наприклад, бути придатні для перорального, топічного, інгаляційного, інтраназального, букального, парентерального (наприклад, внутрішньовенного, підшкірного, інтрадермального або внутрішньом'язового введення) або ректального введення. В одному з аспектів сполуки формули (I) і їх фармацевтично прийнятні солі пристосовано для перорального введення. В іншому аспекті сполуки формули (I) і їх фармацевтично прийнятні солі пристосовано для топічного введення, наприклад, інтраназально або інгаляцією. Таблетки і капсули для перорального введення можуть містити звичайні ексципієнти, наприклад, зв'язуючі агенти, наприклад, сироп, гуміарабік, желатин, сорбітол, трагант, слиз крохмалю, целюлозу або полівініл піролідон; наповнювачі, наприклад, лактозу, мікрокристалічну целюлозу, цукор, кукурудзяний крохмаль, фосфат кальцію або сорбітол; змащувачі, наприклад, стеарат магнію, стеаринову кислоту, тальк, поліетилен гліколь або кремнезем; дезінтегратори, наприклад, картопляний крохмаль, кроскармелозний натрій або натрій крохмаль гліколат; або зволожувачі, наприклад, лаурилсульфат натрію. Таблетки можуть покриватись відомими способами. Пероральні рідкі препарати можуть мати форму, наприклад, водних або масляних суспензій, розчинів, емульсій, сиропів або еліксирів, або можуть бути презентовані як сухий продукт для змішування з водою або іншим придатним носієм перед використанням. Такі рідкі препарати можуть містити звичайнч добавки, наприклад, суспендуючі агенти, наприклад, сорбітольний сироп, метил целюлозу, глюкозний/цукровий сироп, желатин, гідроксиметил целюлозу, карбоксиметил целюлозу, гель стеарату алюмінію або гідрогеновані їстівні жири; емульгатори, наприклад, лецитин, сорбітан моноолеат або гуміарабік; неводні носії (які можуть включати їстівні масла), наприклад, миндальне масло, фракціоноване кокосове масло, масляні естери, пропілен гліколь або етиловий спирт; або консерванти, наприклад, метил- або пропіл pгідроксибензоати або сорбінову кислоту. Препарати можуть також містити буферні солі, смакові добавки, забарвлювачі і/або підсолоджувачі (наприклад, манітол). Композиції для інтраназального введення включають водні композиції для введення через ніс краплями або під тиском. Придатні композиції містять воду як розріджувач або носій. Композиції для введення у легені або ніс можуть містити один або більше ексципієнтів, наприклад, один або більше суспендуючих агентів, один або більше консервантів, одну або більше ПАР, один або більше коригентів тонусу, один або більше співрозчинників, і можуть включати компоненти для контролю pH композиції, наприклад, буферні системи. Крім того, композиції можуть містити інші ексципієнти, наприклад, антиоксиданти, наприклад, метабісульфіт натрію і агенти маскування смаку. Композиції можна також вводити у ніс або інші частини респіраторного тракту розпилюванням. Інтраназальні композиції можуть містити сполуки формули (I) або їх фармацевтично прийнятні солі для введення в усі частини носової порожнини і, крім того, можуть забезпечити 9 UA 103195 C2 5 10 15 20 25 30 35 40 45 50 55 60 тривале перебування сполук формули (I) або їх фармацевтично прийнятних солей у контакті з потрібною тканиною. Придатним режимом введення інтраназальної композиції є повільне вдихання пацієнтом через ніс після очищення носової порожнини. Композицію вводять в одну ніздрю, закриваючи іншу рукою. Цю процедуру потім повторюють для другої ніздрі. Звичайно одне або два уприскування у ніздрі повторюють один, два або три рази на день, бажано, щоденно. Зручними є інтраназальні композиції для введення один раз на день. Cуспендуючі агенти використовуються звичайно у кількості від 0,1 до 5 % (за масою), наприклад, від 1,5 % до 2,4 % (за масою) від повної композиції. Приклади фармацевтично ® прийнятних суспендуючих агентів включають (не лише) Avicel (мікрокристалічна целюлоза і карбоксиметилцелюлозний натрій), карбоксиметил-целюлозний натрій, гуму, трагант, бентоніт, метилцелюлозу, ксантанову гуму, карбопол і поліетилен гліколі. Композиції для введення у легені або ніс можуть містити один або більше ексципієнтів для захисту від мікробного абогрибкового зараження і його росту доданням одного або більше консервантів. Приклади фармацевтично прийнятних антимікробних агентів або консервантів включають (не лише) четверинні амонієві сполуки (наприклад, бензалконій хлорид, бензетоній хлорид, цетримід, цетилпіридинiй хлорид, лауралконій хлорид і міристил піколіній хлорид), ртутні агенти (наприклад, нітрат фенілмеркурію, ацетат фенілмеркурію і тимерозаль), спиртові агенти, (наприклад, хлорбутанол, фенілетиловий спирт і бензиловий спирт), антибактеріальні естери (наприклад, естери парагідроксибензойної кислоти), хелувальні агенти, наприклад, едетат динатрію (EDTA) і інші антимікробні агенти, наприклад, хлоргексидин, хлоркрезол, сорбінова кислота і її солі (наприклад, сорбат натрію) і поліміксин. Приклади фармацевтично прийнятних антигрибкових агентів або консервантів включають (не лише) бензоат натрію, сорбінову кислоту, пропіонат натрію, метилпарабен, етилпарабен, пропілпарабен і бутилпарабен. Консерванти можуть бути присутні у кількості від 0,001 до 1 %, наприклад, від 0,015 % до 0,5 % маси повної композиції. Композиції (де, наприклад, щонайменше одна сполука є у суспензії) можуть включати одну або більше ПАР, які сприяють розчиненню часток медикаменту у водній фазі композиції. Кількість ПАР не повинна створювати піну під час змішування. Приклади фармацевтично прийнятних ПАР включають жирні спирти, естери і етери, наприклад, поліоксиетилен (20) сорбітан моноолеат (Полісорбат 80), макрогольні етери і полоксамери. ПАР може бути присутня у кількості від приблизно 0,01 до 10 %, наприклад, від 0,01 до 0,75 %, наприклад, приблизно 0,5 % повної маси композиції. Можуть бути включені один або більше агентів корекції тонусу рідин тіла, наприклад, рідин носової порожнини, для зниження рівня подразнення. Приклади фармацевтично прийнятних агентів корекції тонусу включають (не лише) хлорид натрію, декстрозу, ксилітол, хлорид кальцію, глюкозу, гліцерин і собітол. Агент корекції тонусу, якщо він є, може бути у кількості від 0,1 до 10 % (w/w), наприклад, від 4,5 до 5,5 %, наприклад, приблизно 5,0 % повної маси композиції. Композиції винаходу можуть бути буферовані доданням придатного буферного агента, наприклад, цитрату натрію, лимонної кислоти, трометамолу, фосфатів, наприклад, фосфату динатрію (наприклад, додекагідрату, гептaгідрату, дигідратуі безводних форм), або фосфату натрію і їх сумішей. Буферний агент може бути включений у кількості від 0,1 до 5 %, наприклад, 1 до 3 % повної маси композиції. Приклади агентів маскування смаку включають цукралозу, сахарозу, сахарин або їх солі, фруктозу, декстрозу, гліцерол, кукурудзяний сироп, аспармат, ацесульфам-K, ксилітол, сорбітол, еритритол, гліциризинат амонію, тауматин, неотам, манітол, ментол, евкаліптове масло, камфору, природні смакові добавки, штучні смакові добавки і їх комбінації. Можуть бути включені один або більше співрозчинників для сприяння розчиненню медикаментозних сполук і/або інших ексципієнтів. Приклади фармацевтично прийнятних співрозчинників включають (не лише) пропілен гліколь, дипропілен гліколь, етилен гліколь, гліцерол, етанол, поліетилен гліколі (наприклад, PEG300 або PEG400) і метанол. В одному з втілень співрозчинником є пропілен гліколь. Кількість співрозчинників, якщо вони є, може становити від 0,05 до 30 %, наприклад, від 1 до 25 %, наприклад, від 1 до 10 % повної маси композиції. Композиції для інгаляційного введення включають водні, органічні або водні/органічні суміші, сухі порошкові або кристалічні композиції, які вводять у респіраторний тракт під тиском або інгалятором, наприклад, порошковими інгаляторами, однодозовими порошковими інгаляторами, заздалегідь дозованими багатодозовими порошковими інгаляторами, носовими інгаляторами або аерозольними інгаляторами під тиском, розпилювачами або інсуфляторами. Придатні 10 UA 103195 C2 5 10 15 20 25 30 35 40 45 50 55 60 композиції містять воду як розріджувач або носій і можуть містити звичайні ексципієнти, наприклад, буферні агенти, модифікатори тонусу тощо. Водні композиції можна вводити у ніс і інші місця респіраторного тракту розпилюванням. Такі композиції можуть бути водними розчинами або суспензіями або аерозолями, які вводять з пакетів під тиском, наприклад, дозованим інгалятором з використанням придатного зрідженого пропеленту. Композиції для топічного введення у ніс (наприклад, при лікуванні риніту) або у легені включають аерозольні композиції під тиском і водні композиції для введення у носові порожнини під тиском. Зручними є композиції, придатні для введення у носову порожнину без тиску. Придатні композиції містять воду як розріджувач або носій. Водні композиції для введення у легені або ніс можуть містити звичайні ексципієнти, наприклад, буферні агенти, модифікатори тонусу тощо. Водні композиції можна також вводити у ніс розпилюванням. Для подачі рідкої композиції у носову порожнину може бути використаний дозатор рідини. Рідка композиція може бути водною або неводною, частіше водною. Дозатор рідини може мати дозувальну форсунку або отвір, через який відмірена доза рідкою композиції вводиться після прикладання користувачем зусилля до нагнітального механізму дозатора рідини. Такий дозатор рідини взагалі має резервуар для багатьох доз рідких композиції, які вводяться активацією нагнітального пристрою. Дозувальна форсунка або отвір можуть бути пристосовані для введення у ніздрі для подачі рідкої композиції у носову порожнину. Дозатор рідини такого типу описано у міжнародній публікації WO 2005/044354. Дозатор має корпус, який містить пристрій подачі рідини з компресійний насосом, встановленим на контейнері рідкої композиції. Корпус має щонайменше один бічний важіль для пальця, який рухають усередину корпусу для пересування контейнера угору у корпусі кулачком, який стискає насос і відміряє дозу композиції для подачі через носову форсунку корпусу. В одному з втілень дозатор рідини є загального типу, ілюстрованого на фіг. 30-40 WO 2005/044354. Водні композиції, що містять сполуку формули (I) або її фармацевтично прийнятні солі, можна також вводити насосом, як це описано у заявці WO2007/138084 (фіг. 22-46) або у заявці GB0723418,0 (фіг. 7-32). Насос може приводитись у дію приводом (фіг. 1-6 GB0723418,0). Сухі порошкові композиції для топічного введення у легені інгаляцією можуть бути, наприклад, презентовані у капсулах і картриджах, наприклад, желатинових, або блістерах з ламінованої алюмінієвої фольги для використання в інгаляторі або інсуфляторі. Порошкові змішані композиції взагалі містять порошкову суміш для інгаляції сполуки формули (I) або її фармацевтично прийнятної солі і придатну порошкову основу (носій/розріджувач/ексципієнт), наприклад, моно-, ди-, або полісахариди (наприклад, лактозу або крохмаль). Сухі порошкові композиції можуть також включати, окрім ліків і носія, додатковий ексципієнт (наприклад, третинний агент, зокрема, цукровий естер, наприклад, октаацетат селобіозу, стеарат кальцію або магнію. В одному з втілень композиція, придатна для інгаляції, можу бути розміщена у декількох герметичних дозових контейнерах на пакеті медикаментів, встановленому у інгаляційному пристрої. Контейнери можуть бути розривними, шарованими або здатними розкриватись по одному і подавати дози сухої порошкової композиції у мундштук інгаляційного пристрою. Пакет медикаменту може мати різні форми, наприклад, форму диску або стрічки. Прикладами TM інгаляційних пристроїв є DISKHALER™ і DISKUS , від GlaxoSmithKline. Суха порошкова інгаляційна композиція може також бути розміщена повністю у інгаляційному пристрою, обладнаному дозувальним механізм для передачі дози композиції з резервуару у інгаляційний канал, з якого ця доза інгалюється пацієнтом через мундштук. Прикладами таких пристроїв є TURBUHALER™ (AstraZeneca), TWISTHALER™ (Scherin г) і CLІKKHALER™ (Innovata). Ще одним варіантом для сухої порошкової інгаляційної композиції є розміщення композиції у капсулах (ода доза у капсулі), які завантажують у інгаляційний пристрій, звичайно пацієнтом за потреби. Пристрій має засіб розривання, проколювання або іншого проникнення у капсул, завдяки чому доза може бути введена у легені пацієнта інгаляцією через мундштук. Прикладами таких пристроїв є ROTAHALER™ (GlaxoSmithKline) і HANDIHALER™ (Boehringer Ingelheim). Аерозольна композиція, придатна для інгаляції, може бути суспензією або розчином і може містити сполуку формули (I) або її фармацевтично прийнятну сіль і належний пропелент, наприклад, флуоркарбон або гідрогеновмісний хлорфлуоркарбон або їх суміші, зокрема, гідрофлуоралкани, особливо 1,1,1,2-тетрафлуоретан, 1,1,1,2,3,3,3-гептaфлуор-n-пропан або їх суміш. Аерозольна композиція може, як варіант, містити додаткові ексципієнти, наприклад, ПАР, зокрема, олеїнову кислоту, лецитин або олігомолочну кислот або її похідну, наприклад, описану у WO 94/21229 і WO 98/34596, і співрозчинники, наприклад, етанол. Композиції, що вводяться 11 UA 103195 C2 5 10 15 20 25 30 35 40 45 50 55 60 під тиском, утримують у каністрах (наприклад, алюмінієвих) з клапаном (наприклад, дозувальним) і з привідним механізмом з мундштуком. Мазі, креми і желе можуть, наприклад, бути приготовлені на водній або масляній основі з доданням придатного загущувача і/або желювального агента і/або розчинників. Такіоснови можуть, наприклад, включати воду і/або масло, наприклад, рідкий парафін або рослинне масло, наприклад, арахісове або касторове, або розчинник, наприклад, поліетилен гліколь. Загущувачі і желювальні агенти, які можуть бути використані, включають м'який парафін, стеарат алюмінію, цетостеариловий спирт, поліетилен гліколі, ланолін, бджолиний віск, карбоксиполіметилен і похідні целюлози і/або гліцерил моностеарат, і/або неіонні емульгатори. Лосьйони можуть бути приготовлені на водній або масляній основі і можуть також містити один або більше емульгаторів, стабілізаторів, диспергаторів, суспендуючих агентів або загущувачів. Порошки для зовнішнього застосування можуть бути приготовлені на будь-якій придатній порошковій основі, наприклад, тальку, лактози або крохмалю. Краплі можуть бути приготовлені на водній або неводній основі і містити також один або більше диспергаторів, солюбілізаторів, суспендуючих агентів або консервантів. Сполуки формули (I) і їх фармацевтично прийнятні солі можуть, наприклад, бути приготовлені для трансдермального введення композицією у накладки або інші засоби (наприклад, газові, під тиском), які вводять активний компонент у шкіру. Для букального введення композиції можуть мати форму таблеток або пастилок, приготовлених відомими способами. Сполуки формули (I) і їх фармацевтично прийнятні солі можуть також бути приготовлені як супозиторії, наприклад, на звичайній основі, наприклад, маслі какао або інших гліцеридах. Сполуки формули (I) і їх фармацевтично прийнятні солі можуть також пристосовані для парентерального введення болюсною ін'єкцією або інфузією і можуть мати дозовану форму, наприклад, в ампулах, флаконах, малих об'ємах для інфузії або у шприцах, або у багатодозових контейнерах з доданням консерванту. Композиції можуть мати форму розчинів, суспензій або емульсій у водних або неводних носіях і можуть містити рецептурні агенти, наприклад, антиоксиданти, буфери, антимікробні агенти і/або модулятори тонусу. Активний інгредієнт може також мати порошкову форму для змішування з придатним носієм, наприклад, стерильною апірогенною водою, перед використанням. Сухі тверді форми можуть бути приготовлені заповненням індивідуальних контейнерів стерильним порошком в асептичних умовах або заповненням контейнерів стерильним розчином з висушуванням виморожуванням. Сполуки формули (I) і їх фармацевтично прийнятні солі можуть також бути приготовлені з вакцинами як активатори для модуляції їх активності. Такі композиції можуть містити антитіла або фрагменти антитіл, або антигенні компоненти, включаючи (не лише) протеїн, ДНК, живі або мертві бактерії і/або віруси або вірусоподібні частки разом з одним або більше ад'ювантоподібними компонентами активатора, включаючи (не лише) солі алюмінію, масло і водні емульсії, протеїни теплового шоку, препарати ліпіду A і його похідні, гліколiпіди, інші агоністи TLR, наприклад, CpG ДНК або подібні агенти, цитокіни, наприклад, GM-CSF або IL-12 або подібні агенти. Cполуки формули (I) і їх фармацевтично прийнятні солі можуть бути використані індивідуально або у комбінації з іншими терапевтичними агентами. Сполуки формули (I) і їх фармацевтично прийнятні солі і інші фармацевтично активні агенти можуть бути введені разом або окремо, при введені окремо введення може бути одночасним або у послідовності, у будьякому порядку. Кількості сполук формули (I) або їх фармацевтично прийнятних солей і інших фармацевтично активних агентів і відносні часи введення вибирають таким чином, щоб досягти бажаної комбінованої терапевтичної дії. Введення комбінації сполуки формули (I) або її фармацевтично прийнятної солі з іншими лікувальними агентами може бути здійснене єдиною фармацевтичною композицією, яка включає обидві сполуки, або окремими фармацевтичними композиціями, кожна з яких включає одну з сполук. Комбінація також може бути введена у певній послідовності, де один лікувальний засіб вводять першим, а інший другим, або у зворотному порядку. Такі послідовні введення можуть бути близькими у часі або з значним інтервалом. Сполуки формули (I) і їх фармацевтично прийнятні солі можуть бути використані у комбінації з одним або більше агентами корисними у відвертанні або лікуванні вірусних інфекцій. Приклади таких агентів включають (без обмеження) інгібітори полімерази, наприклад, описані у WO 2004/037818-A1 і описані у WO 2004/037818 і WO 2006/045613; JTK-003, JTK-019, NM-283, HCV-796, R-803, R1728, R1626, а також описані у WO 2006/018725, WO 2004/074270, WO 2003/095441, US2005/0176701, WO 2006/020082, WO 2005/080388, WO 2004/064925, WO 12 UA 103195 C2 5 10 15 20 25 30 35 40 45 50 55 60 2004/065367, WO 2003/007945, WO 02/04425, WO 2005/014543, WO 2003/000254, EP 1065213, WO 01/47883, WO 2002/057287, WO 2002/057245 і подібні агенти; інгібітор реплікації, наприклад, aцикловір, фамцикловір, ганцикловір, цидофовір, ламівудин і подібні агентт; інгібітори протеази, наприклад, інгібітори протеази ВІЛ, сакінавір, ритонавір, індинавір, нелфінавір, ампренавір, фосампренавір, бреканавір, атазанавір, типранавір, палінавір, лазинавір і інгібітори протеази ВІЛ BILN2061, VX-950, SCH503034; і подібні агенти; інгібітор зворотної транскриптази нуклеозиду і нуклеотиду, наприклад, зидовудин, диданозин, ламівудин, зальцитабін, абпкавір, ставідин, адефовір, дипивоксил, фозивудин, тодоксил, емтрицитабін, аловудин, амдоксовір, ельвуцитабін і подібні агенти; ненуклеозидні інгібітори зворотної транскриптази (антиоксиданти, наприклад, імунокал, ольтипраз тощо.), наприклад, невірапін, делавірдин, ефавіренц, ловірид, імунокал, ольтипраз, каправірин, TMC-278, TMC-125, етравірин і подібні агенти; інгібітор входу, наприклад, енфувіртид (T-20), T-1249, PRO-542, PRO-140, TNX-355, BМС-806, 5-Helix і подібні агенти; інгібітори інтегрази, наприклад, L-870,180 і подібні агенти; інгібітор розгортання, наприклад, PA-344 і PA-457 і подібні агенти; інгібітори рецептора хемокіну, наприклад, вікриворок (Sch-C), Sch-D, TAK779, маравірок (UK-427,857), TAK449, а також описані у WO 02/74769, WO 2004/054974, WO 2004/055012, WO 2004/055010, WO 2004/055016, WO 2004/055011 і WO 2004/054581 і подібні агенти; інгібітори нейрамінідази, наприклад, CS-8958, занамівір, озельтамівір, перамівір і подібні агенти; блокери іонного каналу, наприклад, амантадин або римантадин і подібні агенти; і інтерфераційна РНК і антисенсні олігонуклеотиди, наприклад, ISIS-14803 і подібні агенти; антивірусні агенти невизначеного механізму дії, наприклад, описані у WO 2005/105761, WO 2003/085375, WO 2006/122011, рибавірин і подібні агенти. Сполуки формули (I) і їх фармацевтично прийнятні солі можуть також бути використан у комбінації з одним або більше іншими агентами, корисними у відвертанні або лікуванні вірусних інфекцій, наприклад, імунними терапіями (наприклад, інтерфероном або іншими цитокінами/хемокінами, модуляторами рецепторів цитокіну/хемокіну, агоністами або антагоністами цитокіну і подібними агентами); і терапевтичними вакцинами, антифіброзними агентами, антизапальними агентами, наприклад, кортикостероїдами або NSAID (нестероїдними антизапальними агентами) і подібними агентами. Сполуки формули (I) і їх фармацевтично прийнятні солі можуть бути використан у комбінації з одним або більше іншими агентами, корисними у відвертанні або лікуванні алергічної хвороби, запальної хвороби, аутоімунної хвороби, наприклад, антигенною імунотерапією, антигістамінами, стероїдами, NSAIDs, бронходилататорами (наприклад, агоністами бета 2, адренергічними агоністами, антихолінергічними агентами, теофіліном), метотрексатом, модуляторами лейкотрієну і подібними агентами; терапією моноклональними антитілами, наприклад, анти-IgE, анти-TNF, анти-IL-5, анти-IL-6, анти-IL-12, анти-IL-1 і подібними агентами; рецепторними терапіями, наприклад, ентанерцептом і подібними агентами; антигеннними неспецифічними терапіями (наприклад, інтерфероном або іншими цитокінами/хемокінами, модуляторами рецептора цитокіну/хемокіну, агоністами або антагоністами цитокіну, агоністами TLR і подібними агентами). Сполуки формули (I) і їх фармацевтично прийнятні солі можуть бути використані у комбінації з одним або більше іншими агентами, які можуть бути корисними у відвертанні або лікуванні раку, наприклад, хемотерапевтичними, наприклад, алкілувальними агентами, інгібіторами топоізомерaзи, антиметаболітами, антимітотичними агентами, інгібіторами кінази і подібними агентами; терапією моноклональними антитілами, наприклад, трастузимабом, гемтузимабом і іншими подібними агентами; і гормональними терапіями, наприклад, тамоксифеном, гозереліном і подібними агентами. Фармацевтичні композиції згідно з винаходом можуть також бути використані індивідуально або у комбінації з щонайменше одним іншим терапевтичним агентом в інших терапевтичних областях, наприклад, при шлунково-кишкових хворобах. Композиції згідно з винаходом можуть також бути використані у комбінації з генно-заміщуючими терапіями. Винахід включає в іншому аспекті комбінацію сполуки формули (I) або її фармацевтично прийнятної солі з щонайменше одним іншим терапевтично активним агентом. Описаним комбінаціям зручно надавати форму фармацевтичної композиції. Фармацевтичні композиції, які містять описані вище комбінації разом з щонайменше одним фармацевтично прийнятним розріджувачем або носієм, утворюють ще один аспект винаходу. Терапевтично ефективна кількість сполуки формули (I) або її фармацевтично прийнятної солі залежить від багатьох факторів. Наприклад, вид пацієнта, вік і мага реципієнта, конкретний стан, що потребує лікування і його важкість, природа композиції спосіб введення є факторами, які слід брати до уваги. Терапевтично ефективність кількість взагалі має визначатись лікарем. У будь-якому випадку ефективна кількість сполуки винаходу при лікуванні людини, що страждає 13 UA 103195 C2 5 10 15 20 25 30 від слабкості має становити 0,0001 - 100 мг/кг ваги реципієнта на день. Частіше ефективна кількість становить 0,001 - 10 мг/кг маси тіла на день. Отже, для дорослого вагою 70 кг, наприклад, щоденна доза має становити 7 - 700 мг. При інтраназальному і інгаляційному введеннях типові дози для дорослого вагою 70 кг мають становити 1 мкг - 1 мг на день. Цю кількість можна вводити одною дозою на день або декількома (наприклад, двома, трьома, чотирма, п'ятьма або більше) субдозами на день. Ефективна кількість фармацевтично прийнятної солі сполуки формули (I) може бути визначена через пропорцію ефективної кількості сполуки формули (I) або її фармацевтично прийнятної солі per se. Подібні дози можуть бути використані у лікуванні інших згаданих тут станів. Сполуки формули (I) і їх фармацевтично прийнятні солі можуть також бути введені з будьякою прийнятною частотою, наприклад, 1-7 разів на тиждень. Конкретний режим введення залежить від таких факторів, як терапевтичне показання, вік і стан пацієнта і спосіб введення. Фармацевтичні композиції можуть мати однодозові форми, які містять заздалегідь визначену кількість активного інгредієнта на дозу. Такі одиниці можуть містити, наприклад, 0,5 мг - 1 г сполуки формули (I) або її фармацевтично прийнятної солі, залежно від стану, що потребує лікування, способу введення і віку, ваги і стану пацієнта. Бажані однодозові композиції містять денну дозу або субдозу, згадані вище, або бажані частини активного інгредієнту. Такі фармацевтичні композиції можуть бути приготовлені будь-яким х відомих способів. Отже, винахід включає фармацевтичну композицію, яка містить сполуку формули (I) або її фармацевтично прийнятну сіль і один або більше фармацевтично прийнятних розріджувачів або носіїів. Винахід включає також спосіб приготування таких фармацевтичних композицій, який включає змішування сполуки формули (I) або її фармацевтично прийнятної солі з одним або більше фармацевтично прийнятними розріджувачами або носіями. У цьому описі і Формулі винаходу, якщо не зазначено інше, "включати" і, наприклад, "включає" і "включаючи" означають включення зазначеного числа або операції, або групи чисел без виключення будь-яких інших чисел або операцій, або груп операцій. Сполуки формули (I) і їх солі можуть бути приготовлені описаними далі способами, які входять в об'єм винаходу. Відповідно, винахід включає спосіб приготування сполуки формули (I), який включає позбавлення захисту сполуки формули (II): NH2 N N 2 OR 1 R N N ( )m N ( )n 35 40 (II) 1 2 де R , m, і n визначено вище для сполуки формули (I) і R - C1-6алкіл, після чого, якщо потрібно, виконання таких операцій: (i) видалення будь-якої необхідної захисної групи; (ii) приготування солі отриманої сполуки. Наприклад, сполуку формули (II) розчиняють у придатному розчиннику у присутності розчин придатної кислоти, наприклад, розчину гідрохлориду у 1,4-діоксані і перемішують при придатній температурі, наприклад, зовнішній температурі протягом придатного часу, наприклад, 12-24 год. Розчинник видаляють під зниженим тиском і залишок розчиняють у придатному розчиннику, наприклад, метанолі, і завантажують в іонообмінний картридж, наприклад, з амінопропілом SPE, потім елююють придатним розчинником, наприклад, метанол і розчинник видаляють, отримуючи сполуку формули (I). Сполука формули (II) може бути приготовлена введенням сполуки формули (III): 14 UA 103195 C2 NH2 N N 2 OR 1 R N N ( )m X (III) 2 де R і m визначено вище для сполуки формули (I), R визначено вище для сполуки формули (II), а X - відщеплювана група, наприклад, галогенна група, наприклад, бром або хлор, у реакцію з сполукою формули (IV): H N 1 ( )n 5 10 15 (IV) де n визначено для сполуки формули (I). Наприклад, сполуку формули (III), сполуку формули (IV) і придатну основу, наприклад, N,Nдіізопропілетиламін, розчиняють у придатному розчиннику, наприклад, ДМФ, і нагрівають при придатній температур, наприклад, 50-60 °C протягом придатного часу, наприклад, 46 - 50 год. Якщо потрібно, додають ще сполуки формули (IV) і основи і реакційну суміш нагрівають при придатній температурі, наприклад, 50-60 °C протягом належного часу, наприклад, 46 - 50 год. Продукт екстрагують з реакції звичайними засобами, наприклад, розділенням між придатним органічним розчинником і водою, з подальшою. ізоляцією органічної фази і видаленням розчинника і очищенням за потреби. Сполука формули (III) може бути приготовлена введенням сполуки формули (V), наприклад, солі сполуки формули (V), наприклад, трифлуорацетату: NH2 N N 2 OR 1 R 20 25 30 35 40 N N H (V) 1 2 де R визначено вище для сполуки формули (I) і R визначено вище для сполуки формули (II), у реакцію з сполукою формули (VI): X Br ( )m (VI) де m визначено вище для сполуки формули (I) і X визначено вище для сполуки формули (III). Наприклад, трифлуорацетатну сіль сполуки формули (V) і придатну основу, наприклад, карбонат калію, суспендують у придатному розчиннику, наприклад, ДМФ, і нагрівають до придатної температури, наприклад, 50-60 °C у придатній атмосфері, наприклад, нітрогену, протягом належного часу, наприклад, 20 - 120 хвил. Суміш охолоджують до придатної температури, наприклад, зовнішній температурі, додають сполуку формули (VI) і перемішування продовжують при зовнішній температурі протягом певного часу, наприклад, 18 24 год. Розчинник випарюють під зниженим тиском і залишок розділяють між придатними розчинниками, наприклад, ДХМ і водою. Сир продукт ізолюють від органічної фази і очищають звичайними способами, , наприклад, колонною хроматографією. В іншому варіанті сполука формули (II) може бути приготовлена реакцією сполуки формули (V), наприклад, солі сполуки формули (V), наприклад, трифлуорацетатної солі сполук формули (VI), де X - бром з сполукою формули (IV) у єдиному процесі. Наприклад, трифлуорацетатну сіль сполук формули (V) розчиняють у придатному розчиннику, наприклад, ДМФ, і додають і основу, наприклад, карбонат калію. Реакційну суміш перемішують при придатній температурі, наприклад, 45-60 °C у придатній атмосфері, наприклад, нітрогену, протягом певного часу, наприклад, 1-2 год. і потім охолоджують до придатної температури, наприклад, зовнішньої. Додають сполуку формули (VI), де X - бром, і після перемішування протягом придатного часу, наприклад, 40 - 60 хвил., додають сполуку формули (IV) і придатну основу, наприклад, тріетиламін, у придатному розчиннику, наприклад, 15 UA 103195 C2 5 ДМФ. Реакційну суміш перемішують протягом, наприклад, 12 - 24 год., розчинник видаляють і залишок розділяють між придатним органічним розчинником, наприклад, ДХМ і водою. Сирий продукт формули (II) ізолюють звичайними засобами і очищають, наприклад, хроматографією. Сіль сполуки формули (V) може бути приготовлена позбавленням захисту сполуки формули (VII): NH2 N N 2 OR 1 R N N P (VII) 2 де R визначено вище для сполуки формули (I), R визначено вище для сполуки формули (II) і P - захисна група, наприклад, тетрагідро-2H-піран-2-іл, у присутності придатної кислоти, наприклад, трифлуороцтової кислоти. Наприклад, придатну кислоту, наприклад, трифлуороцтову, додають до розчину сполуки формули (VII) у придатному розчиннику, наприклад, метанолі. Суміш перемішують при придатній температурі, наприклад, зовнішній, протягом придатного часу, наприклад, 48 - 72 год. Реакційну суміш концентрують під зниженим тиском, потім розріджують придатним розчинником, наприклад, етил ацетатом. Отриману суміш фільтрують і промивають невеликою кількістю придатного розчинника, наприклад, етил ацетату до знебарвлення фільтрату. Залишок сушать у повітрі і потім під зниженим тиском, отримуючи сіль сполуки формули (V). Фільтрат концентрують і концентрат розріджують невеликою кількістю придатного розчинника, наприклад, етил ацетату, і потім фільтрують і сушать, отримуючи другу порцію солі сполуки формули (V). Сіль сполуки формули (V), наприклад, трифлуорацетатну сіль, можна також приготовити, вводячи сполуку формули (IX): NH2 1 10 15 20 N N 1 R N N P (IX) де R визначено вище для сполуки формули (I) і P визначено вище для сполуки формули (VII), у реакцію з придатним галогенувальним агентом, наприклад, N-бромсукцинімідом, і потім реакцією з алкоксидним аніоном, наприклад, метоксидним аніоном, і ізолюють у присутності придатної кислоти, наприклад, трифлуороцтової кислоти. Наприклад, до розчину сирої сполуки формули (IX) у придатному сухому розчиннику, наприклад, сухому хлороформі, при придатні температурі, наприклад, зовнішній, додають придатний галогенувальний агент, наприклад, N-бромсукцинімід, порціями протягом придатного часу, наприклад, 5 хвил. Розчин перемішують при придатній температурі, наприклад, зовнішній, протягом придатного часу, наприклад, 25 - 35 хвил. Реакційну суміш промивають водою і органічну фазусушать, наприклад, пропускаючи через гідрофобну фриту і концентрують під зниженим тиском. Отриману тверду речовину розчиняють у придатному сухому розчиннику, наприклад, сухому метанолі, і додають придатний алкоксид, наприклад, розчин метоксиду натрію у метанолі, при придатній температурі, наприклад, зовнішній, в інертній атмосфері, наприклад, атмосфері нітрогену. Реакційну суміш нагрівають при придатній температурі, наприклад, 60-70 °C, з конденсатором, протягом придатного часу, наприклад, 12-18 год. Реакційну суміш охолоджують і концентрують під зниженим тиском. Залишок вносять у придатний розчинник, наприклад, етил ацетат, і вливають у придатне водне середовище, наприклад, насичений водний розчин хлориду амонію. Органічний шар відділяють і промивають водою, сушать, наприклад, над сульфатом магнію, фільтрують і концентрують під зниженим тиском. До розчину цього матеріалу у придатному сухому розчиннику, наприклад, сухому метанолі, при придатній температурі, наприклад, зовнішній температурі, додають придатну кислоту, наприклад, трифлуороцтову. Реакцію перемішують протягом придатного часу, наприклад, 25 - 35 год., і концентрують під зниженим тиском, отримуючи сполуку формули (V). 1 25 30 35 40 45 16 UA 103195 C2 Сполука формули (VII) може бути приготовлена реакцією сполуки формули (VIII): NH2 N N Q 1 R N N P (VIII) де R визначено вище для сполуки формули (I), P визначено вище для сполуки формули (VII) і Q - атом галогену, наприклад, брому, з алкоксидним аніоном, наприклад, метоксидним. Наприклад, розчин сполуки формули (VIII) у придатному розчиннику, наприклад, метанолі, нагрівають до температури флегми з розчином придатного алкоксиду, наприклад, метоксиду натрію, у придатному розчиннику, наприклад, метанолі, протягом придатного часу, наприклад, 4 - 5 год. Реакційну суміш концентрують під зниженим тиском і розділяють між придатним органічним розчинником, наприклад, етил ацетатом, і придатним водним середовищем, наприклад, насиченим водним розчином хлориду амонію. Органічну фазу відділяють, промивають, наприклад, розсолом, і сушать, наприклад, пропускаючи через гідрофобну фриту. Розчинник видаляють під зниженим тиском, отримуючи сполуку формули (VII). Сполуку формули (VIII) можна приготовити реакцією сполуки формули (IX) з придатним галогенувальним агентом, наприклад, N-бромсукцинімідом. Наприклад, сполуку формули (IX) розчиняють у придатному розчиннику, наприклад, хлороформі, і охолоджують до придатної температури, наприклад, 0-0,5 °C. До розчину додають придатний галогенувальний агент, наприклад, N-бромсукцинімід, при температур нижче приблизно 3 °C. Розчин перемішують при придатній температурі, наприклад, 2-3 °C протягом придатного часу, наприклад, 30 - 45 хвил. потім залишають нагрітись придатної температури, наприклад, зовнішної температури, і перемішують протягом придатного часу, наприклад, 5 - 7 год. Реакційну суміш промивають водою і органічну фазу сушать і відділяють від водної фази, використовуючи, наприклад, гідрофобну фриту. Органічний розчинник видаляють і сирий продукт очищають, наприклад, хроматографією, отримуючи сполуку формули (VIII). 1 Сполука формули (IX), де R - C1-6алкокси, може бути приготовлена реакцією сполуки формули (X): NH2 1 5 10 15 20 25 N N T 30 35 40 45 N N P (X) де P визначено вище для сполуки формули (VII) і T - придатна відщеплювана група, наприклад, атом галогену, атом хлору або атом флуору, з розчином сполуки формули (XIII): 1 R -M (XIII) 1 де R - C1-6алкокси і M придатний ліганд лужного металу, наприклад, натрію, приготовленого у розчиннику формули (ХIIIS): 1 R -H (XIIIS) 1 1 де R - група сполуки формули (XIII), є такою ж, як група R у розчиннику формули (XIIIS). Сполуку формули (XIII), наприклад, t-бутоксид натрію, додають до розчинника формули (XIIIS). Суміш перемішують до гомогенності, потім додають сполуку формули (VII). Реакційну суміш нагрівають до придатної температури, наприклад, 100 °C, протягом придатного часу, наприклад, 12 - 18 год. Розчинник видаляють під зниженим тиском і розділяють між придатним розчинником, наприклад, діетил етером, і водою. Органічну фазу відділяють і водну фазу екстрагують іншим розчинником. Органічні шар ізолюють, об'єднують, сушать, використовуючи придатний сушильний агент, наприклад, безводний сульфат магнію. Цей агент видаляють фільтрацією і розчинник видаляють з продукту під зниженим тиском, отримуючи сполуку 1 формули (IX), де R - C1-6алкокси. 1 Сполука формули (IX), де R - C1-6алкіламіно, може бути приготовлена реакцією сполук формули (X) з сполукою формули (XIV): 1 R -H (XIV), 1 де R - C1-6алкіламіно. 17 UA 103195 C2 5 10 Сполуку формули (XIV) додають до розчину сполуки формули (X) у придатному сухому розчиннику, наприклад, сухому етилен гліколі, при придатній температурі, наприклад, зовнішній температурі, у придатній інертній атмосфері, наприклад, атмосфері нітрогену. Реакційну суміш нагрівають при придатній температурі, наприклад, 110-130 °C, протягом придатного часу, наприклад, 12 - 18 год. Реакцію охолоджують до придатної температури, наприклад, зовнішньої температури, розріджують придатним розчинником, наприклад, етил ацетатом, і промивають водою. Органічний шар сушать з придатним сушильним агентом, наприклад, безводним сульфатом магнію, фільтрують і концентрують під зниженим тиском, отримуючи сполуку 1 формули (IX), де R - C1-6алкіламіно. Сполука формули (X) може бути приготовлена реакцією сполуки формули (XI): V N N T 15 20 25 N P (XI) де P визначено вище для сполуки формули (VII) і T визначен вище для сполук формули (X), а V - придатна відщеплювана група, наприклад, атом галогену, атом хлору, з спиртовим розчином амонію, наприклад, в ізо-пропіловому спирті. Сполуку формули (XI) нагрівають з спиртовим розчином амонію, наприклад, 2M розчином амонію в ізопропіловому спирті при придатній температурі, наприклад, 50-60 °C, протягом придатного часу, наприклад, 5 - 6 год. Реакційну суміш залишають відстоятись при придатній температурі, наприклад, зовнішній температурі, протягом придатного часу, наприклад, 12 - 18 год. Додають ще спиртового розчину амонію, наприклад, 2M розчину амонію в ізопропіловому спирті, щоб зруйнувати отриманий фільтрувальний залишок і реакційну суміш нагрівають протягом, наприклад, 8 - 10 год. до завершення реакції. Додають воду і тверду речовину видаляють фільтрацією, промивають придатним промивним середовищем, наприклад, сумішшю ізопропілового спирту і води, і потім сушать, наприклад, повітрям під всмоктуванням, отримуючи першу порцію сполук формули (X). Фільтрат відстоюють протягом, наприклад, 12 18 год. і отриману другу порцію сполуки формули (X) ізолюють фільтрацією і сушать. Сполуку формули (X) можна також приготовити реакцією сполуки формули (XII): V N N T 30 35 40 N N N H (XII) де T визначено вище для сполуки формули (X), і V визначено вище для сполуки формули (XI), з сполукою формули (XV): U P -H (XV) U де P - придатний попередник для захисної групи P, наприклад, 3,4-дигідро-2H-піранільної групи, і подальшою реакцією з спиртовим розчином амонію, наприклад, в ізопропіловому спирті. Моногідрат p-толуолсульфонової кислоти додають до розчину сполуки формули (XII) у придатному сухому розчиннику, наприклад, сухому етил ацетаті. Реакційну суміш нагрівають до придатної температури, наприклад, 50-60 °C, і додають сполуку формули (XV). Реакцію перемішують при придатній температурі, наприклад, 50-60 °C, протягом придатного часу, наприклад, 1 - 2 год., і розчинник видаляють під зниженим тиском. Суспензію отриманої твердої речовини у спиртовому розчині амонію, наприклад, 2M розчині амонію в ізопропіловому спирті нагрівають у придатній інертній атмосфері, наприклад, атмосфері нітрогену, при придатній температурі, наприклад, 60-70 °C, протягом придатного часу, наприклад, 4 - 5 год.з конденсатором. Реакційну суміш вливають у воду і залишають охолонути протягом придатного часу, наприклад, 12 - 18 год. Отриманий осад ізолюють фільтрацією і сушать, отримуючи сполуку формули (X). 18 UA 103195 C2 Сполуку формули (X) можна також приготовити реакцією сполуки формули (XIA): NH2 N N T 5 10 15 20 25 30 N N H (XIA) де T - атом флуору, з придатним захисним агентом, наприклад, силілувальним агентом, наприклад, N,O-біс(триметилсиліл)ацетамідом, і потім реакцією захищеної сполуки формули (XIA) з сполукою формули (XVE): U P -E (XVE) U де P - придатний попередник для захисної групи P, наприклад, 3,4-дигідро-2H-піранільнаl група і E - ацилоксигрупа, наприклад, ацетатна група. Придатний захисний агент, наприклад, N,O-біс(триметилсиліл)ацетамід додають з перемішуванням до суспензії сполук формули (XIA), наприклад, 2-флуор-1H-пурин-6-аміну, у придатному безводному розчиннику, наприклад, безводному ацетонітрилі, і отриману суміш нагрівають до температури флегми протягом придатного часу, наприклад, 2 - 3 год. Реакційну суміш охолоджують до придатної температури, наприклад, 0-5 °C. Повільно додають розчин сполуки формули (XVE), наприклад, тетрагідропіраніл ацетат, у придатному безводному розчиннику, наприклад, безводному ацетонітрилі і потім краплями додають кислоту Льюїса, наприклад, триметилсиліл трифлуорметансульфонат. Реакційну температуру доводять до придатної температури, наприклад, 8-15 °C, і перемішують протягом, наприклад, 1 - 2 год. Суміш гасять доданням 1M карбонату натрію. Органічний шар охолоджують до 0 °C з перемішуванням. Осаджену тверду речовину збирають, наприклад, фільтрацією, і сушать. Сполука формули (XI) може бути приготовлена реакцією сполуки формули (XII) з сполукою формули (XV). До сполуки формули (XII) додають придатний органічний розчинник, наприклад, етил ацетат, і потім p-толуолсульфонову кислоту. Суміш нагрівають до придатної температури, наприклад, 50-60 °C, і потім додають 3,4-дигідро-2H-піран. Реакційну суміш нагрівають до придатної температури, наприклад, 50-60 °C протягом придатного часу, наприклад, 4 - 5 год. Розчинник видаляють під зниженим тиском, отримуючи сполуку формули (XI). Абревіатури Далі неведено перелік деяких абревіатур, використаних тут. Абревіатури, не внесені у перелік, є добре відомими фахівцям. ДХМ Дихлорметан ДМФ N,N-диметилформамід ДМСО Диметилсульфоксид EtOAc Етил ацетат Et2O Діетил етер HCl Гідрохлорна кислота РХВЕ Рідинна хроматографія високої ефективності ISCO Companion Автоматизоване флеш-хроматографічне обладнання зфракційним аналізом через абсобцію УФ від Presearch Limited, Basingstoke, Hants., RG24 8PZ, UK MDAP РХВЕ Зворотно-фазова РХВЕ на колонці C18 з дворозчинниковим градієнтом і аналізом фракцій мас-спектроскопією з електророзпилюванням. SPE Екстракція твердої фази MeOH Метанол ТФК Трифлуороцтова кислот iPr Ізопропіл t-Bu Трет- бутил Ms Мезил Ac Ацетил n-Bu n-бутил Ph Феніл Процеси синтезу тут описано згідно з Схемою 1. 19 UA 103195 C2 Схема 1 A1 Cl N N Cl NH2 Cl N A N H N N N Cl B N N A R Z F N A N Br N N R Z O O NH2 N N N N N D O O NH2 N N C N N Cl NH2 NH2 N N H F E N N A2 N C N C1 NH2 O N N NH2 F A N H .TFA N G1 X ( )m N OMe R Z Br OMe N O N N A R Z NH2 N N OMe G A R Z N N ( )m (X=Br) X H N G2 ( )n NH2 N N OMe A R Z N N ( )m N ( )n H NH2 H N N O A R Z N N ( )m N (I) 5 10 ( )n Типові реакційні стани для кожної з операцій синтезу Схеми 1: A Дигідропіран/паратолуол-сульфонова кислота, наприклад, 50 °C протягом 3 - 6 год. A1 Дигідропіран/паратолуол-сульфонова кислота, наприклад, 50 °C протягом 1 год., потім амоній/iPrOH, наприклад, 60 °C протягом 4 год., потім додання води і охолодження до зовнішньої температури протягом 12 - 18 год. A2 BSA у MeCN, флегма, охолодження до 0 °C, потім THP ацетат у MeCN, нагрівання до 10 °C, потім NaHCO3 (водн.) B Амоній/iPrOH, наприклад, 50 °C протягом 5 год., потім зовнішня температура протягом 1218 год., потім 50°C протягом 9 год. A A C Для X = NH, R = C1-6алкіл: R NH2/етилен гліколь, наприклад, 120 °C протягом 12-18 год. 20 UA 103195 C2 A 5 10 15 20 25 30 35 40 45 50 55 A Для Z = O, R = C1-6алкіл: R ONa/BuOH/диметоксиетан, наприклад, 93-110 °C протягом 12-18 год. C1 NBS у CHCl3, наприклад, 0-5 °C протягом 30 хвил., потім зовнішня температура протягом 0,5 - 1 год., потім, наприклад, NaOMe/метанол під N2/60-70 °C /12-18 год., потім ТФК/MeOH, наприклад, зовнішня температура протягом 18-65 год. D NBS у CHCl3, наприклад, 0-5 °C протягом 30 хвил., потім зовнішня температура протягом 36-48 год. E NaOMe/MeOH, наприклад, флегма 4-6 год. F ТФК/MeOH, наприклад, зовнішня температура протягом 18-65 год. G K2CO3/ДМФ, потім 50 °C протягом 1-1,5 год., потім додання (VI), перемішування протягом 40 хвил., потім додання (IV)/Et3N, потім зовнішня температура протягом 18 год. G1 K2CO3/ДМФ, потім 50 °C під N2 протягом 30 хвил., потім зовнішня температура, додання (VI), перемішування протягом 20 год. G2 Розчин у ДМФ з N,N-діізопропілетиламіном, потім 50°C протягом 48 год., потім додання (IV), потім 50 °C протягом 48 год. H HCl/метанол, потім зовнішня температура протягом 18 год. Сполуки формул (IV), (VI), (XIA), (XII), (XIII), (XIV) і (XV) є відомими з літератури або є комерційно доступними, наприклад, від Sigma-Aldrich, UK, або можуть бути приготовлені по аналогії з відомими процедурами, наприклад, описаними у стандартних довідкових джерелах, наприклад, J. March, Advanced Organic Chemistry, 6th Edition (2007), WileyBlackwell, або Comprehensive Organic Synthesis (Trost B.M. і Fleming I., (Eds.), Pergamon Press, 1991), включених у цей опис посиланням. Приклади інших захисних груп, які можуть бути використані в описаному тут синтезі, засобів їх видалення можна знайти у T. W. Greene "Protective Groups in Organic Synthesis", 4th Edition, J. Wiley and Sons, 2006, включеному посиланням. Для будь-яких описаних тут реакцій або процесів можуть бути використані звичайні способи нагрівання і охолодження, наприклад, масляні ванни з регулюванням температури або нагрівні блоки з регулюванням температури і льодо-сольові ванни або сухі льодо-ацетонні ванни. Можуть бути використані звичайні способи ізоляції, наприклад, екстракція з водного або неводного розчинника. Можуть бути використані звичайні способи сушіння органічних розчинників, розчинів або екстрактів, наприклад, струшування з безводним сульфатом магнію або безводним сульфатом натрію, або проведення через гідрофобну фриту. Можуть бути використані звичайні способи очищення, наприклад, кристалізація і хроматографія, наприклад, кремнеземна хроматографія або зворотно-фазова хроматографія. Кристалізація може бути проведена з звичайних розчинників, наприклад, етил ацетату, метанолу, етанолу або бутанолу, або їх водних сумішей. Тривалість і температура конкретних реакцій можуть контролюватись звичайними способами, наприклад, тонкошаровою хроматографіє. і РХ-мС. За потреби індивідуальні ізомерні форми сполук винаходу можуть бути приготовлені як індивідуальні ізомери з використанням звичайних процедур, наприклад, фракційної кристалізації діастереоізомерних похідних або хіральною РХВЕ. Абсолютну стереохімію сполук можна визначати звичайними способами, наприклад, рентгенівською кристалографією. Аспекти винаходу ілюструються необмежуючими Прикладами, наведеними далі. Загальні експериментaльні деталі Сполуки іменовано з використанням програмного забезпечення ACD/Name PRO 6,02 від Advanced Chemistry Developments Inc., Toronto, Ontario, M5H2L3, Canada. Експериментaльні деталі систем РХМС A-D є такими: Система A Колонка: 50 мм x 2,1мм вн. д., 1,7 м Acquity UPLC BEH C18 Потік: 1 мл/ хвил. o Темп..: 40 C Межі виявлення УФ: 210 - 350 нм Мас-спектр: реєструють на мас-спектрометрі, переміжно використовуючи сканувальні позитивний і негативний режими електророзпилювальної іонізації. Розчинники: A: 0,1 % (об'єм/обє'м) мурашиної кислоти у воді B: 0,1 % (об'єм/обє'м) мурашиної кислоти в ацетонітрилі 21 UA 103195 C2 Градієнт: 5 10 20 30 B% 3 3 100 100 3 Час (хвил.) 0 0,1 4,2 4,8 4,9 5,0 A% 97 97 0 0 97 97 B% 3 3 100 100 3 3 Система C Колонка: 50 мм x 2,1мм вн. д., 1,7 мкм Acquity UPLC BEH C18 Потік: 1 мл/ хвил. Темп: 40 °C Межі виявлення УФ: 210 - 350 нм Мас-спектр: реєструють на мас-спектрометрі, переміжно використовуючи сканувальні позитивний і негативний режими електророзпилювальної іонізації. Розчинники: A: 10 мМ бікарбонат амонію, коригований до pH 10 B: ацетонітрил Градієнт: 25 A% 97 97 0 0 97 Система B Колонка: 30 мм x 4,6 мм вн. л., 3,5 мкм Sunfire колонка C18 Потік: 3 мл/ хвил. Темп.: 30 °C Межі виявлення УФ: 210 - 350 нм Мас-спектр: реєструють на мас-спектрометрі, переміжно використовуючи сканувальні позитивний і негативний режими електророзпилювальної іонізації. Розчинники: A: 0,1 % (об'єм/обє'м) розчин мурашиної кислоти у воді B: 0,1 % (об'єм/обє'м) розчин мурашиної кислоти в ацетонітрилі Градієнт: 15 Час (хвил.) 0 0,1 1,4 1,9 2,0 Час (хвил.) 0 1,5 1,9 2,0 A% 99 3 3 0 B% 1 97 97 100 Система D Колонка: 50 мм x 4,6 мм вн. д., 3,5 мкм колонка XBridge C 18 Потік: 3 мл/ хвил. Темп: 30 °C Межі виявлення УФ: 210-350 нм Мас-спектр: реєструють на мас-спектрометрі, переміжно використовуючи сканувальні позитивний і негативний режими електророзпилювальної іонізації. Розчинники: A: 10мМ бікарбонат амонію у воді, коригований до pH10 B: ацетонітрил Градієнт: Час (хвил.) 0 0,1 4,0 5,0 A% 99 99 3 3 35 22 B% 1 1 97 97 UA 103195 C2 5 10 15 20 25 30 35 40 45 Хроматографічне очищення проводять на заздалегідь пакованих силікагелевих картриджах. Flashmaster II є автоматизованою багатокористувацькою хроматографічною системою від Argonaut Techнолogies Ltd, яка використовує одноразову нормальну фазу і картриджи (2 г - 100 г) екстракції твердої фази (SPE). Він забезпечує четверинне змішування розчинників у потоці для здійснення градієнтних способів. Зразки встановлюють у чергу, використовуючи багатофункціональне відкрите програмне забезпечення, яке керує розчинниками, потоками, профілем градієнту і станом збирання. Систему обладнано УФ детектором Кнауера (Knauer) з змінною довжиною хвилі і двома колекторами фракцій Gilson FC204, що забезпечує зрізання піків, збирання і стеження. Видалення розчинника у потоці нітрогену проводять при 30-40 °C на системі ЗеленHouse Blowdown від Radleys Discovery Techноіogies Saffron Walden, Essex, CB11 3AZ, UK. 1 Спектри H ЯМР реєструють у CDCl3 або ДМСО-d6 на спектрометрі Bruker DPX 400 або Bruker Avance DRX, або Varian Unity 400 на 400 МГц. Внутрішній стандарт - тетраметилсилан або залишковий протонований розчинник при 7,25 1/млн для CDCl3 або 2,50 1/млн для ДМСОd6. Мас-орієнтовану РХВЕ проводять в умовах, визначених нижче. Виявленням через EA є усереднений сигнал з довжиною хвилі 210 - 350 нм і мас-спектр реєструють на масспектрометрі, переміжно використовуючи сканувальні позитивний і негативний режими електророзпилювальної іонізації. Спосіб A Спосіб A реалізують на колонці XBridge C18 A = 10 мМ водний бікарбонат амонію, коригований до pH 10. B = ацетонітрил. Спосіб B Спосіб B реалізують на колонці Sunfire C18 (звичайно 150 мм x 19 мм вн. д., пакувальний діаметр 5 мкм) при зовнішній температурі. Розчинники: A = 0,1 % (об'єм/обє'м) розчин мурашиної кислоти у воді B = 0,1 % (об'єм/обє'м) розчин мурашиної кислоти в ацетонітрилі. Спосіб C Спосіб С реалізують на колонці Sunfire C18 (звичайно 150 мм x 19 мм вн. д., пакувальний діаметр 5 мкм) при зовнішній температурі. Розчинники: A = 0,1 % (об'єм/обє'м) розчин трифлуороцтової кислоти у воді B = 0,1 % (об'єм/обє'м) розчин трифлуороцтової кислоти в ацетонітрилі. Спосіб D Спосіб D реалізують на колонці Atlанtis C18 (звичайно 100 мм x 30 мм вн. д., пакувальний діаметр 5 мкм) при зовнішній температурі. Розчинники: A = 0,1 % (об'єм/обє'м) розчин мурашиної кислоти у воді B = 0,1 % (об'єм/обє'м) розчин мурашиної кислоти в ацетонітрилі. Спосіб E Спосіб Е реалізують на колонці Supelcosil ABZ+Plus (звичайно 100 мм x 21,2 мм вн. д., пакувальний діаметр 5 мкм) при зовнішній температурі. Розчинники: A = 0,1 % (об'єм/обє'м) розчин мурашиної кислоти у воді B = ацетонітрил: вода 95:5 +0,05 % мурашиної кислоти ПРИКЛАДИ Інтермедіат 1: 2,6-дихлор-9-(тетрагідро-2H-піран-2-іл)-9H-пурин Cl N N Cl N N O 50 До 2,6-дихлорпурину (25,0 г) (від, наприклад, Aldrich, UK) додають етил ацетат (260 мл), потім p-толуолсульфонову кислоту (0,253 г). Суміш нагрівають до 50 °C і додають 3,4-дигідро2H-піран (16,8 г). Реакційну суміш нагрівають при 50 °C 4 год., потім випарюють in vacuo, отримуючи названу сполук як жовту тверду речовину (36,9 г). 1 H ЯМР (CDCl3): 8,35 (1H, s), 5,77 (1H, dd), 4,20 (1H, m), 3,79 (1H, m), 2,20-1,65 (6H, m). Інтермедіат 2: 2-хлор-9-(тетрагідро-2H-піран-2-іл)-9H-пурин-6-амін 23 UA 103195 C2 NH2 N N Cl N N O 5 10 15 2,6-дихлор-9-(тетрагідро-2H-піран-2-іл)-9H-пурин (36,9 г) нагрівають з 2M амонієм в ізопропанолі (250 мл) при 50 °C протягом 5 год. Після відстоювання при зовнішній температурі протягом ночі додають ще 2M амонію у ізопропанолі (100 мл) для руйнування отриманого фільтрувального залишку і реакційну суміш нагрівають ще 9 год. до завершення реакції. До реакційної суміші додають воду (70 мл) і жовту тверду речовину відфільтровують. Тверду речовину промивають ізопропіловим спиртом: вода (5:1 ((об'єм/обє'м)), 60 мл) і потім сушать повітрям з всмоктуванням, отримуючи першу порцію.. Фільтрат фільтрують після відстоюванняa протягом ночі для ізолювання осад і обидві тверді речовини сушать in vacuo. Перша частин є чистою, друга частина показує невелике забруднення (ізольований широкий сигнал 3,5 1/млн, відсутній у першій частині), але вони є в іншому ідентичними. Отримано першу частину (28,4 г) і другу частину (3,42 г). 1 H ЯМР (CDCl3): 8,01 (1H, s), 5,98 (2H, broad s), 5,70 (1H, dd), 4,16 (1H, m), 3,78 (1H, m), 2,151,60 (6H, перекриває m). Інтермедіат 2 (інший спосіб): 2-хлор-9-(тетрагідро-2H-піран-2-іл)-9H-пурин-6-амін NH2 N N Cl N N O 20 25 До розчину 2,6-дихлорпурину (25 г) (від, наприклад, Aldrich, UK) у сухому етил ацетаті (200 мл) додають p-толуолсульфонової кислоти моногідрат (235 мг). Реакцію нагрівають до 50 °C і додають 3,4-дигідро-2H-піран (18,1 мл). Реакцію залишають перемішуватись при 50 °C на 1 год. і розчинник видаляють під зниженим тиском, отримуючи жовту тверду речовину. Суспензію цієї твердої речовини (~36 г) у 2,0 M амонію в ізопропанолі (460 мл) нагрівають під нітрогеном при 60 °C 4 год. з конденсатором. Реакцію вливають у воду (50 мл) і залишають охолонути протягом ночі. Осад фільтрують і сушать на роторному випарювачі (60 °C) протягом 30 хвил. і отримують названу сполуку як білувату тверду речовину, 31 г (93 %, 2 операції). + МС, обчислений для (C10H12ClN5O) = 254, 256 + МС, отриманий (електророзпилювання): (M) = 254, 256 (3:1) 1 H ЯМР ((CD3)2SO): δ 8,43 (1H, s), 7,82 (2H, s), 5,55 (1H, dd), 4,00 (1H, m), 3,69 (1H, m), 2,21 (1H, m), 1,95 (2H, m), 1,74 (1H, m), 1,56 (2H, m). Інтермедіат 3: 2-(бутилокси)-9-(тетрагідро-2H-піран-2-іл)-9H-пурин-6-амін NH2 N N O N N O 30 35 40 До бутан-1-ол (76 мл) додають порціями трет-бутоксид натрію (15,2 г) (реакційна суміш розігрівається) і перемішують до гомогенності (прибл. 15 хвил.) потім додають 2-хлор-9(тетрагідро-2H-піран-2-іл)-9H-пурин-6-амін (10,0 г) і отримують блідожовтий розчин. Реакційну суміш нагрівають до 100 °C протягом ночі, потім видаляють максимальну кількість бутан-1-олу в потім розділяють між діетил етером і водою. Діетил етерну фазу відділяють і водну фазу екстрагують діетил етером. Об'єднані органічні шари сушать над сульфат магнію (безводним). Сульфат магнію відфільтровують і фільтрат видаляють, отримуючи коричневе в'язке масло, яке азеотропують з толуол (3 рази) і витримують у глибокому вакуумі протягом ночі, переносять у нову колбу з ДХМ і видаляють розчинник під зниженим тиском, вносять у глибокий вакуум і отримують названу сполуку як коричневе скло (9,45 г). 1 H ЯМР (CDCl3): 7,85 (1H, s), 5,92 (2H, broad s), 5,64 (1H, d), 4,32 (2H, t), 4,14 (1H, m), 3,75 (1H, m), 2,10–1,95 (3H, перекриває m), 1,81–1,58 (5H, перекриває m), 1,50 (2H, m), 0,97 (3H, t). 24 UA 103195 C2 Інтермедіат 4: 8-бром-2-(бутилокси)-9-(тетрагідро-2H-піран-2-іл)-9H-пурин-6-амін NH2 N N O Br N N O 5 10 2-(бутилокси)-9-(тетрагідро-2H-піран-2-іл)-9H-пурин-6-амін (9,45 г) розчиняють у хлороформі (50 мл) і охолоджують до 0 °C (лід-ванна). До розчину додають порціями N-бромсукцинімід (6,07 г) при температурі нижче 3 °C. Темнозелений розчин перемішують при 2,5 °C 30 хвил. потім залишають нагрітись до кімнатної температури і перемішують 6 год. Реакційну суміш промивають водою (100 мл, двічі). Органічну фазу сушать/відділяють, використовуючи гідрофобну фриту, і випарюють, отримуючи темнокоричневу гуму, яку очищають кремнеземною хроматографією (120 г) (ISCO) з градієнтом 0–50 % етил ацетат:циклогексан, отримуючи названу сполуку блідожовту тверду речовину (8,37 г). 1 H ЯМР (CDCl3): 5,61 (1H, dd), 5,49 (2H, broad s), 4,32 (2H, m), 4,17 (1H, m), 3,71 (1H, m), 3,04 (1H, m), 2,11 (1H, broad d), 1,89 –1,45 (6H, перекриває m), 1,50 (2H, m), 0,97 (3H, t). Інтермедіат 5: 2-(бутилокси)-8-(метилокси)-9-(тетрагідро-2H-піран-2-іл)-9H-пурин-6-амін NH2 N N O O N N O 15 20 25 8-бром-2-(бутилокси)-9-(тетрагідро-2H-піран-2-іл)-9H-пурин-6-амін (8,37 г) нагрівають до температури флегми з 25 % метоксиду натрію у метанолі (14,4 мл) і метанолі (65 мл) протягом 4,5 год. Реакційну суміш концентрують під зниженим тиском і розділяють між етил ацетатом і насиченим розчином хлориду амонію. Відділяють органічну фазу і екстрагують у етил ацетат. Об'єднані органічні фази промивають розсолом (двічі). Органічну фазупропускають через гідрофобну фриту і після відділення води випарюють, отримуючи світлокоричневу гуму, яку вносять у глибокий вакуум, отримуючи піну (7,52 г), яка стискається у гуму (7,34 г) під зовнішнім тиском і твердіє протягом ночі, і отримують названу сполуку жовту аморфну тверду речовину. + МС, обчислений для (C15H23N5O3) = 321 + МС, отриманий (електророзпилювання): (M+H) = 322 1 H ЯМР (CDCl3): 5,50 (1H, dd), 5,17 (2H, broad s), 4,29 (2H, t), 4,12 (3H, s і 1H, m), 3,70 (1H, m), 2,77 (1H, m), 2,05 (1H, m), 1,82–1,63 (6H, перекриває m), 1,50 (2H, m), 0,97 (3H, t). Інтермедіат 6: 2-(бутилокси)-8-(метилокси)-9H-пурин-6-амін трифлуорацетат salt NH2 N N O O N H N F F OH O F 30 35 40 До розчину 2-(бутилокси)-8-(метилокси)-9-(тетрагідро-2H-піран-2-іл)-9H-пурин-6-аміну (7,34 г) у метанолі (100 мл) додають трифлуороцтову кислоту (10 мл). Суміш перемішують при зовнішній температурі протягом доби, отримуючи суспензію. Реакційну суміш концентрують до невеликої кількості (густий шлам), потім розріджують етил ацетатом (50 мл). Отриманий шлам фільтрують і промивають невеликою кількістю етил ацетату до знебарвлення фільтрату. Тверду речовину сушать повітрям і потім in vacuo, отримуючи названу сполуку як білу тверду речовину (6,20 г). Фільтрат концентрують, отримуючи шлам, який розріджують невеликою кількістю етил ацетату (10 мл) і потім фільтрують і сушать, як описано вище. Цю другу частин ізолюють як білу тверду речовину (0,276 г). Обидві частини є ідентичними (ЯМР). + МС, обчислений для (C10H15N5O2) = 237 + МС, отриманий (електророзпилювання): (M+H) = 238 1 H ЯМР (CD3OD): 4,47 (2H, t), 4,15 (3H, s), 1,80 (2H, m), 1,50 (2H, m), 0,99 (3H, t) (взаємозамінні NH2, NH і COOH протони не помічено). 25 UA 103195 C2 2 Інтермедіат 7: N -бутил-9-(тетрагідро-2H-піран-2-іл)-9H-пурин-2,6-діамін NH2 N N N H 5 10 N N O До розчину 2-хлор-9-(тетрагідро-2H-піран-2-іл)-9H-пурин-6-аміну (10 г) у сухому етилен гліколі (50 мл) при кімнатній температурі під нітрогеном додають n-бутиламін (16 мл). Реакці нагрівають при 120 °C протягом ночі, потім охолоджують до кімнатної температури, розріджують етил ацетатом (150 мл) і промивають водою (2 x 50 мл). Органічний шар сушать над MgSO4, фільтрують і концентрують in vacuo, отримуючи названу сполуку як в'язке зелене масло (10,2 г), яке використовують без подальшого очищення. + МС, обчислений для (C14H22N6O) = 290 + МС, отриманий (електророзпилювання): (M+H) = 291 1 H ЯМР ((CD3)2SO): δ 7,8 (1H, s), 6,6 (2H, s), 6,2 (1H, t), 5,4 (1H, dd), 4,0 (1H, m), 3,6 (1H, m), 3,2 (2H, m), 2,2 (1H, m), 1,9 (1H, m), 1,8 (1H, m), 1,7 (1H, m), 1,5 (2H, m), 1,4 (2H, m), 1,3 (2H, m), 0,9 (3H, t). 2 Інтермедіат 8: N -бутил-8-(метилокси)-9H-пурин-2,6-діамін трифлуороцтов кислот salt NH2 N N N H 15 20 25 30 35 O N H N CF3CO2H 2 До розчину сирого N -бутил-9-(тетрагідро-2H-піран-2-іл)-9H-пурин-2,6-діаміну (прибл. 10,2 г) у сухому хлороформі (100 мл) при кімнатній температурі додають порціями N-бромсукцинімід (6,3 г) протягом 5 хвил. Темний розчин залишають перемішуватись при кімнатній температурі на 30 хвил. Реакційну суміш промивають водою. (20 мл). Органічну фазу пропускають через гідрофобну фриту і концентрують in vacuo, отримуючи бежеву тверду речовину, яку розчиняють у сухому метанолі (100 мл) і при кімнатній температурі під нітроген додають розчин метоксиду натрію (25 % (за масою) у метанол, 24 мл). Реакцію нагрівають при 65 °C, з конденсатором, протягом ночі, потім охолоджують і концентрують in vacuo. Отриманий оранжевий залишок вносять в етил ацетат (150 мл) і вливають у насичений водний хлорид амонію (50 мл). Органічний шар відділяють і промивають водою (50 мл), потім сушать над MgSO 4, фільтрують і концентрують in vacuo. Додають у сухому метанол (70 мл) при кімнатній температурі трифлуороцтову кислоту (7 мл). Реакці перемішують 30 год. і концентрують in vacuo, отримуючи темнокоричневу тверду речовину, яку вносять у діетил етер (20 мл) і перетирають. Тверду речовину фільтрують, отримуючи названу сполуку як бежеву тверду речовину (3,3 г, 35 %, 4 операції). + МС, обчислений для (C10H16N6O) = 236 + МС, отриманий (електророзпилювання): (M+H) = 237 1 H ЯМР ((CD3)2SO): δ 13,3-12,3 (1H, br.m), 8,6-7,3 (2H, m), 4,05 (3H, s), 3,28 (2H, m), 1,52 (2H, m), 1,33 (2H, m), 0,89 (3H, t) (залишковий взаємозамінний протон неясний). Інтермедіат 9: 2-{[(1S)-1-метилбутил]окси}-9-(тетрагідро-2H-піран-2-іл)-9H-пурин-6-амін NH2 N N O N N O 40 Спосіб A T-бутоксид натрію (48,5 г, 505 ммоль) додають порціями до (S)-2-пентанолу (185 мл) (від, наприклад, Julich Chiral Solutions, Germany) при кімнатній температурі і перемішують до гомогенності (реакція є екзогенною). Додають 2-хлор-9-(тетрагідро-2H-піран-2-іл)-9H-пурин-6амін (32 г, 126 ммоль) і реакційну суміш нагрівають при 70 °C 72 год. Реакці охолоджують до кімнатної температури і розділяють між етил ацетатом (500 мл) і водою (500 мл). Органічну 26 UA 103195 C2 5 10 15 20 фазу промивають насиченим розчином хлориду натрію (100 мл), сушать (MgSO 4), фільтрують і випарюють. Залишок перетирають з етер і тверду речовину фільтрують. Осад промивають етером і фільтрати об'єднують і випарюють. Сирий матеріал (прибл. 30 г) розчиняють у ДМСО:метанолі (1:1) і очищають хроматографією на зворотно-фазовій (C18) колонці (330 г) з градієнтом 25-65 % ацетонітрил (+0,1 %ТФК)-вода(+0,1 %ТФК) у 8 об'ємах колонки, фракції негайно нейтралізують насиченим водним розчином карбонату натрію. Відповідні фракції об'єднують і розділяють між ДХМ і насиченим водним гідрокарбонатом натрію. Органічну фазу сушать, пропускаючи через гідрофобну фриту, фільтрують і випарюють, отримуючи названу сполуку блідокремову піну (14,97 г). + РХМС (Система B): tRET = 2,21 хвил.; MH 306 Спосіб B T-бутоксид натрію (206 г, 2,144 моль) додають до (S)-2-пентанолу (720 мл, 6,58 моль) (від, наприклад, Julich Chiral Solutions, Germany) у 2-літровій круглодонній колбі. Суміш перемішують при 50 °C до розчинення усього t-бутоксиду натрію. Додають порціями 2-флуор-9-(тетрагідро2H-піран-2-іл)-9H-пурин-6-амін (130 г, 548 ммоль) протягом 5 хвил. Через 3 год. РХМС показує повне поглинання початкового матеріалу, і суміш вливають у лід/воду (3 л) і потім екстрагують метил t-бутил етером. Це дає емульсію, яку фільтрують через Celite і органічну фазу відділяють. Водний шар обробляють твердим NaCl і потім екстрагують метил t-бутил етером. Органічні екстракти об'єднують і промивають розсолом, сушать над сульфатом магнію, фільтрують і потім випарюють, отримуючи названу сполуку як блідокоричневу гуму (158,59 г). + РХМС (Система D): tRET = 2,65 хвил.; MH 306 Інтермедіат 10: 8-бром-2-{[(1S)-1-метилбутил]окси}-9-(тетрагідро-2H-піран-2-іл)-9H-пурин-6амін NH2 N N O Br N N O 25 30 35 N-бромсукцинімід (12,16 г, 68,3 ммоль) додають порціями протягом 5 хвил. до перемішаного розчину 2-{[(1S)-1-метилбутил]окси}-9-(тетрагідро-2H-піран-2-іл)-9H-пурин-6-аміну (14,9 г, 48,8 ммоль) у хлороформі (80 мл) при
ДивитисяДодаткова інформація
Назва патенту англійськоюPurine derivatives for use in the treatment of allergic, inflammatory and infectious diseases
Автори російськоюBiggadike, Keith, Coe, Diane, Mary, Lewell, Xiao, Qing, Mitchell, Charlotte, Jane, Smith, Stephen, Allan, Trivedi, Naimisha
МПК / Мітки
МПК: A61P 35/00, C07D 473/16, A61P 37/00, A61K 31/522, C07D 473/18
Мітки: алергій, захворювань, пурину, застосування, похідні, запальних, інфекційних, лікуванні
Код посилання
<a href="https://ua.patents.su/69-103195-pokhidni-purinu-dlya-zastosuvannya-u-likuvanni-alergijj-zapalnikh-ta-infekcijjnikh-zakhvoryuvan.html" target="_blank" rel="follow" title="База патентів України">Похідні пурину для застосування у лікуванні алергій, запальних та інфекційних захворювань</a>
Попередній патент: Підвісний туалетний контейнер із розподільним елементом для змивної води
Наступний патент: Літальний апарат з верхньорозташованим вхідним пристроєм
Випадковий патент: Мікроелектронний оптичний сенсор температури з частотним виходом