3- або 4-монозаміщені фенол і тіофенолпохідні, корисні як н3 ліганди
Номер патенту: 84748
Опубліковано: 25.11.2008
Автори: Лортіуа Едвіг, Дентон Стівен Мартін, Кемп Марк Ян, Деніс Алексіс, Бернарделлі Патрік, Якобеллі Анрі, Вернь Фабріс, Серрадеіл-Сіві Дельфін, Руссо Фіона, Кронін Ендрю Майкл
Формула / Реферат
1. Сполука формули (1) :
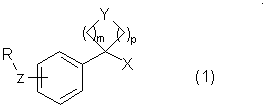
або її фармацевтично прийнятна сіль і/або сольват (включаючи гідрат), де:
замісник формули -Z-R знаходиться в мета або пара-положенні фенільної групи;
Х вибирають з -CN, -СН2ОН, -СН2-О-(С1-С4)алкілу, -С(О)ОН, -С(О)О(С1-С4)алкілу, -CH2-NR1R2, -C(O)NR3R4, -CH2-O-het2, -CH2-het1 і het1, група het1 і в -CH2-het1, і в het1 є, необов'язково, заміщеною одним або двома замісниками, що незалежно вибирають з гало, ціано, (С1-С4)алкілу, -S-(С1-С4)алкілу і (С1-С4)алкокси;
R1 є водень або (С1-С4)алкіл, необов'язково, заміщений (С3-С6)циклоалкілом;
R2 вибирають з групи, яка містить:
водень, (С1-С6)алкіл, необов'язково, заміщений одним або двома замісниками, що незалежно вибирають з (С3-С6)циклоалкілу, гідрокси, -S-(С1-С4)алкілу, -О-(С1-С4)алкілу, -SO2(С1-С4)алкілу, -SO-(С1-С4)алкілу, гало, het1, аміно, (С1-С4)алкіламіно, [(С1-С4)алкіл]2аміно і фенілу, згаданий феніл є, необов'язково, заміщеним одним або двома замісниками, що незалежно вибирають з гало, гідрокси, ціано, (С1-С4)алкілу і (С1-С4)алкокси, (С3-С6)циклоалкіл,
het2, необов'язково, заміщений одним або двома замісниками, що незалежно вибирають з гало, ціано, (С1-С4)алкілу, NH2 і (С1-С4)алкокси,
-SO2-R5, де R5 вибирають з групи, яка містить (С1-С4)алкіл, аміно, (С1-С4)алкіламіно, [(С1-С4)алкіл]2аміно, феніл і -(С1-С4)алкілфеніл, згаданий феніл є, необов'язково, заміщеним одним або двома замісниками, що незалежно вибирають з гало, ціано, (С1-С4)алкілу і (С1-С4)алкокси, і
-C(О)-R6, де R6 вибирають з групи, яка містить (С1-С4)алкіл, аміно, (С1-С4)алкіламіно, [(С1-С4)алкіл]2аміно, феніл і -(С1-С4)алкілфеніл, згаданий феніл є, необов'язково, заміщеним одним або двома замісниками, що незалежно вибирають з гало, ціано, (С1-С4)алкілу і (С1-С4)алкокси;
або R1 і R2 утворюють разом з атомом N, до якого вони приєднані, 3-, 4-, 5-, 6- або 7-членний насичений гетероцикл, де один атом С може бути замінений N, О, S, SO або SO2 і де згаданий насичений гетероцикл є, необов'язково, заміщеним однією або двома групами, що незалежно вибирають з гідрокси, гало, =O, (С1-С4)алкілу, -(С1-С4)алкіл(С3-С6)циклоалкілу, (С1-С4)алкокси, гідроксі(С1-С4)алкілу, (С1-С4)алкоксі(С1-С4)алкілу, -SO2(С1-С4)алкілу, -С(О)(С1-С4)алкілу, [(С1-С4)алкіл]2аміно, аміно, (С1-С4)алкіламіно, -C(О)NH2, С(О)O(С1-С4)алкілу і піролідинону;
R3 і R4 кожен, незалежно, вибирають з водню, (С3-С6)циклоалкілу і (С1-С4)алкілу, згаданий (С3-С6)циклоалкіл і (С1-С4)алкіл є, необов'язково, заміщеним аміно, (С1-С4)алкіламіно, [(С1-С4)алкіл]2аміно або (С3-С6)циклоалкілом, або
R3 і R4 утворюють разом з атомом N, до якого вони приєднані, 4-, 5-, 6- або 7-членний насичений гетероцикл, де один атом С може бути замінений N або О і де згаданий насичений гетероцикл є, необов'язково, заміщеним (С1-С4)алкілом, [(С1-С4)алкіл]2аміно, аміно, (С1-С4)алкіламіно або -С(О)(С1-С4)алкілом, згаданий -С(О)(С1-С4)алкіл є, необов'язково, заміщеним метокси або етокси,
Y вибирають з СН2, СН(ОН), О, С=O і N, згаданий N є заміщеним Н, (С1-С4)алкілом, С(О)(С1-С4)алкілом або (С1-С4)алкоксі(С1-С4)алкілом;
Z вибирають з О, S, SO і SO2;
m і р обидва є цілими числами, які є, незалежно, 1, 2 або 3, за умови, що m+р є еквівалентною або менше ніж 4, так що утворюється кільце:
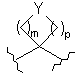 ,
,
яке є 4-, 5- або 6-членним кільцем;
і R є або групою формули:
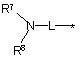 ,
,
де * позначає точку приєднання до Z, L є нерозгалуженим ланцюгом або розгалуженим (С2-С6)алкіленом і
R7 і R8 кожен, незалежно, вибирають з водню, (С1-С6)алкілу, (С3-С6)циклоалкілу, гідроксі(С1-С6)алкілу або R7 і R8 утворюють разом з атомом N, до якого вони приєднані, 4-, 5-, 6- або 7-членний насичений гетероцикл, де один атом С є, необов'язково, заміненим N, О, S, SO або SO2 і де згаданий насичений гетероцикл є, необов'язково, заміщеним однією або двома групами, що незалежно вибирають з (С1-С4)алкілу, (С1-С4)алкокси, (С1-С4)алкоксі(С1-С4)алкілу, гідроксі(С1-С4)алкілу, гідрокси, С(О)O(С1-С4)алкілу, -С(О)-(С1-С4)алкіл-NН2, -С(О)NН2, гало, аміно, (С1-С4)алкіламіно і [(С1-С4)алкіл]2аміно,
або R є групою формули:
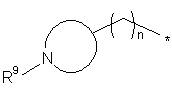 ,
,
де * позначає точку приєднання до Z,
N-вмісним кільцем є 4-7-членний насичений гетероцикл,
n є цілим числом еквівалентним 0, 1 або 2, і
R9 представляє замісник, що вибирають з водню, (С1-С4)алкілу, гідроксі(С1-С6алкілу) і (С3-С6)циклоалкілу;
het1 вибирають з моноциклічних або біциклічних гетероароматичних груп, що мають 5-10 кільцевих членів, які містять 1, 2, 3 або 4 гетероатом(и), що вибирають з азоту, кисню і сірки і het2 вибирають з моноциклічних або біциклічних гетероароматичних груп, що мають 5-10 кільцевих членів, які містять 1, 2, 3 або 4 гетероатом(и), що вибирають з азоту, кисню і сірки.
2. Сполука формули (1) згідно з пунктом 1, де Х вибирають з -CH2-NR1R2, -C(O)NR3R4, -CH2-het1 і het1, het1 є, необов'язково, заміщеним один раз або двічі (С1-С4)алкілом, де R1, R2, R3, R4 і het1 є такими як визначено вище в пункті 1.
3. Сполука формули (1) згідно з пунктом 2, де Х є -CH2-het1 або het1, і het1 вибирають з 5- або 6-членної моноциклічної гетероароматичної групи або 9-членної біциклічної гетероароматичної групи, кожна гетероароматична група, містить 1-3 атоми азоту, або 1-2 атоми азоту і 1 атом кисню, або 1 атом азоту і 1 атом сірки, і кожна гетероароматична група є, необов'язково, заміщеною один раз або двічі (С1-С4)алкілом.
4. Сполука формули (1) згідно з пунктом 3, де Х є тіазоліл, бензімідазолілметил-, піридиніл, оксазоліл, імідазопіридинілметил-, піримідиніл, імідазоліл, імідазолілметил- або триазолілметил-, згаданий тіазоліл, бензімідазолілметил-, піридиніл, оксазоліл, імідазопіридинілметил-, піримідиніл, імідазоліл, імідазолілметил- і триазолілметил- кожен є, необов'язково, заміщеним однією метильною групою.
5. Сполука формули (1) згідно з пунктом 1 або пунктом 2, де R1 є водень, метил або етил.
6. Сполука формули (1) згідно з пунктом 1, пунктом 2 або пунктом 5, де R2 вибирають з групи, яка містить водень, (С1-С6)алкіл, необов'язково, заміщений одним або двома замісниками, що незалежно вибирають з -S-(С1-С4)алкілу, -О-(С1-С4)алкілу, -SО2-(С1-С4)алкілу і фенілу, згаданий феніл є, необов'язково, заміщеним одним або двома замісниками, що незалежно вибирають з гало, гідрокси, ціано, (С1-С4)алкілу і (С1-С4)алкокси,
(С3-С6)циклоалкіл,
het2, необов'язково, заміщений одним або двома замісниками, що незалежно вибирають з гало, ціано, (С1-С4)алкілу і (С1-С4)алкокси, де het2 є таким як визначено у пункті 1,
-SO2-R5, де R5 вибирають з групи, яка містить (С1-С4)алкіл, [(С1-С4)алкіл]2аміно, феніл і -(С1-С4)алкілфеніл, де згаданий феніл є, необов'язково, заміщеним 1 замісником, що незалежно вибирають з гало і ціано, і
-C(О)-R6, де R6 вибирають з групи, яка містить (С1-С4)алкіл, [(С1-С4)алкіл]2аміно, аміно і -(С1-С4)алкілфеніл, згаданий феніл є, необов'язково, заміщеним одним або двома замісниками, що незалежно вибирають з гало, ціано, (С1-С4)алкілу і (С1-С4)алкокси.
7. Сполука формули (1) згідно з пунктом 6, де R2 вибирають з групи, яка містить (С1-С3)алкіл, необов'язково, заміщений -О-(С1-С3)алкілом, (С3-С5)циклоалкіл,
het2, де het2 вибирають з групи, яка містить 5- або 6-членні моноциклічні гетероароматичні групи, що містять 1-2 атоми азоту, або 1 атом азоту і 1 атом кисню, або 1 атом азоту і 1 атом сірки, згаданий het2 є, необов'язково, заміщеним (С1-С4)алкілом,
SO2-R5, де R5 є (С1-С4)алкіл і
C(О)-R6, де R6 (С1-С4)алкіл.
8. Сполука формули (1), згідно з пунктом 7, де R2 є (С1-С3)алкіл, необов'язково, заміщений метокси.
9. Сполука формули (1) згідно з пунктом 7, де R2 є het2, і het2 вибирають з групи, яка містить 5- або 6-членні моноциклічні гетероароматичні групи, що містять 1 або 2 атоми азоту.
10. Сполука формули (1) згідно з пунктом 9, де R2 є піридазинільною групою.
11. Сполука формули (1) згідно з пунктом 1 або пунктом 2, де R1 і R2 утворюють разом з атомом N, до якого вони приєднані, 4-, 5-, 6- або 7-членний насичений гетероцикл, де один атом С може бути замінений N, О, S, SO або SO2 і де згаданий насичений гетероцикл є, необов'язково, заміщеним однією або двома групами, що незалежно вибирають з гідрокси, гало, =O, (С1-С4)алкілу, -(С1-С4)алкіл(С3-С6)циклоалкілу, (С1-С4)алкокси, гідроксі(С1-С4)алкілу, (С1-С4)алкоксі(С1-С4)алкілу, -SO2(С1-С4)алкілу, -С(О)(С1-С4)алкілу, [(С1-С4)алкіл]2аміно, -C(О)NH2, С(О)O(С1-С4)алкілу і піролідинону.
12. Сполука формули (1) згідно з пунктом 11, де R1 і R2 утворюють разом з атомом N, до якого вониприєднані, морфолініл.
13. Сполука формули (1) згідно з пунктом 1 або пунктом 2, де R3 і R4 кожен, незалежно, вибирають з водню і (С1-С4)алкілу або R3 і R4 утворюють разом з атомом N, до якого вони приєднані, 4-, 5- або 6-членний насичений гетероцикл, де один атом С може бути замінений N або О і де згаданий насичений гетероцикл є, необов'язково, заміщеним (С1-С4)алкілом.
14. Сполука формули (1) згідно з пунктом 13, де R3 і R4 вибирають, незалежно, з водню, метилу і етилу, або R3 і R4 утворюють разом з атомом N, до якого вони приєднані, піролідиніл, піперидиніл, піперазиніл або азетидиніл, кожний піролідиніл, піперидиніл, піперазиніл і азетидиніл є, необов'язково, заміщеними метилом.
15. Сполука формули (1) згідно з будь-яким з попередніх пунктів, де Y вибирають з СН2, СН(ОН), О і С=O.
16. Сполука формули (1) згідно з пунктом 15, де Y є О.
17. Сполука формули (1) згідно з будь-яким з попередніх пунктів, де Z є О.
18. Сполука формули (1) згідно з будь-яким з попередніх пунктів, де m і р обидва є 2.
19. Сполука формули (1) згідно з будь-яким з попередніх пунктів, де R є група формули:
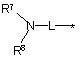 ,
,
де * позначає точку приєднання до Z, L є (С2-С5)алкілен і R7 і R8 кожен, незалежно, вибирають з водню, (С1-С6)алкілу, (С3-С6)циклоалкілу, гідроксі(С1-С6)алкілу або R7 і R8 утворюють разом з атомом N, до якого вони приєднані, 4-, 5-, 6- або 7-членний насичений гетероцикл, де один атом С є, необов'язково, заміненим N, О, S, SO або SO2 і де згаданий насичений гетероцикл є, необов'язково, заміщеним однією або двома групами, що незалежно вибирають з (С1-С4)алкілу, (С1-С4)алкокси, (С1-С4)алкоксі(С1-С4)алкілу, гідроксі(С1-С4)алкілу, гідрокси, С(О)O(С1-С4)алкілу, -С(О)-(С1-С4)алкіл-NН2, -С(О)NН2 і гало.
20. Сполука формули (1) згідно з пунктом 19, де R7 і R8 утворюють разом з атомом N, до якого вони приєднані, морфолініл або оксазепаніл.
21. Сполука формули (1) згідно з пунктом 19, де R7 і R8 утворюють разом з атомом N, до якого вони приєднані, 4-, 5- або 6-членний насичений гетероцикл, необов'язково, заміщений однією або двома (С1-С4)алкільними групами.
22. Сполука формули (1) згідно з пунктом 21, де насиченим гетероциклілом є піролідиніл, необов'язково, заміщений однією або двома метильними групами.
23. Сполука формули (1) згідно з пунктом 19, де R7 і R8 є (С1-С3)алкіл.
24. Сполука формули (1) згідно з будь-яким з пунктів 19-23, де L є пропілен.
25. Сполука формули (1) згідно з будь-яким з пунктів 1-18, де
R є група формули :
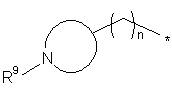 ,
,
де * позначає точку приєднання до Z, N-вмісним кільцем є 4- або 6-членний насичений гетероцикл, n є цілим числом еквівалентним 0 або 1, і R9 представляє замісник, що вибирають з водню, (С1-С4)алкілу і (С3-С6)циклоалкілу.
26. Сполука формули (1) згідно з пунктом 25, де R9 є ізопропіл або циклобутил.
27. Сполука формули (1) згідно з будь-яким з пунктів 1-26 або її фармацевтично прийнятна сіль і/або сольват, для використання як медикаменту.
28. Фармацевтична композиція, що містить сполуку формули (1) або її фармацевтично прийнятну сіль і/або сольват, як визначено в будь-якому з попередніх пунктів, разом з фармацевтично прийнятним екціпіентом.
29. Застосування сполуки формули (1), як визначено в будь-якому з пунктів 1-26, або її фармацевтично прийнятної солі і/або сольвату, для виготовлення медикаменту для лікування захворювань при яких показаний Н3 ліганд.
30. Застосування сполуки формули (1) згідно з пунктом 29, для виготовлення медикаменту для лікування розладів сну, мігрені, дискінезії, стресвикликаної тривоги, психотичних розладів, епілепсії, дефіциту пізнавальної здатності, такої як хвороба Альцгеймера або негострі погіршення когнітивної здатності, депресії, розладів настрою, шизофренії, тривоги, гіперактивного дефіциту уваги (ADHD), психотичних розладів ожиріння, запаморочення, епілепсії, нудоти, запальних захворювань, респіраторного дистрес-синдрому повнолітніх, гострого респіраторного дистрес-синдрому, бронхіту, хронічного бронхіту, хронічного обструктивного легеневого захворювання кістозно-фіброзної дегенерації, астми, емфіземи, риніту, хронічного синуситу, алергії, алергії, викликаної відповіддю дихальних шляхів, алергічного риніту, вірусного риніту, неалергічного риніту, річного і сезонного риніту, закупорювання носового каналу, алергічного закупорювання, сексуальної дисфункції у чоловіків або сексуальної дисфункції у жінок.
31. Спосіб лікування ссавця, включаючи людину, що страждає на захворювання при якому показаний Н3 ліганд, при якому вводять згаданому ссавцю ефективну кількість сполуки формули (1), як визначено в будь-якому з пунктів 1-26, або її фармацевтично прийнятної солі і/або сольвату, або її композиції.
32. Комбінація сполуки формули (1), як визначено в будь-якому з пунктів 1-26, і іншого фармакологічно активного агента, який вибирають з групи, що містить:
антагоністи рецептора гістаміна Н1, наприклад лоратидин, деслоратидин, фексофенадин і цетиризин,
антагоністи рецептора гістаміна Н4,
антагоністи рецептора гістаміна Н2,
антагоністи лейкотрієна, включаючи антагоністи LTB4, LTC4, LTD4 і LTE4, зокрема монтелукаст,
інгібітори фосфодіестерази, такі як інгібітори ФДЕ4 або інгібітори ФДЕ5,
інгібітори повторного захоплення нейротрансміттеру, наприклад, флуоксетин, сертралін, пароксетин, зипразидон,
інгібітори 5-ліпоксигенази (5-LO) або антагоністи 5-ліпоксигеназа-активуючого протеїну (FLAP),
антагоністи ![]() 1- і
1- і ![]() 2-адренорецептора або вазоконстрикторні симпатоміметичні агенти для протинабрякового застосування,
2-адренорецептора або вазоконстрикторні симпатоміметичні агенти для протинабрякового застосування,
антагоністи мускаринового М3 рецептора або антихолінергічні агенти,
антагоністи ![]() 2-адренорецептора,
2-адренорецептора,
теофілін,
хромоглікат натрію,
інгібітори СОХ-1 (НСПЗЗ) і селективні інгібітори СОХ-2,
пероральні і інгілюємі глюкокортикостероїди,
моноклональні антитіла активні проти ендогенних запальних проявлень,
агенти проти фактору некрозу пухлин (анти-TNF-![]() ),
),
інгібітори адгезії молекул, включаючи VLA-4 антагоністи,
антагоністи рецептора кініну-В1- і В2,
імуносупресивні агенти,
інгібітори матриксних металопротеїнкіназ (ММР),
антагоністи рецептора тахикініну NK1, NK2 і NK3,
інгібітори еластази,
антагоністи рецептора аденозину А2а,
інгібітори урокінази,
сполуки, що діють на допамінові рецептори, наприклад, агоністи D2,
модулятори NF![]() шляху, наприклад ІКК інгібітори,
шляху, наприклад ІКК інгібітори,
агенти, що можна класифікувати як муколітики або протикашлеві агенти,
антибіотики,
модулятори цитокінових сигнальних шляхів, такі як інгібітори р38 МАР кінази, syk кінази або JAK кінази,
інгібітори HDAC (гістондеацетилази) і
інгібітори РІЗ кінази.
33. Комбінація згідно з пунктом 32, де іншим фармакологічно активним агентом є антагоніст гістамінового Н1 рецептора.
34. Сполука формули (1), як визначено в будь-якому з пунктів 1-26, або її фармацевтично прийнятна сіль і/або сольват, для використання, як описано в пункті 29 або 30.
Текст
1. Сполука формули (1) : 2 (19) 1 3 84748 або R1 і R2 утворюють разом з атомом N, до якого вони приєднані, 3-, 4-, 5-, 6- або 7-членний насичений гетероцикл, де один атом С може бути замінений N, О, S, SO або SO2 і де згаданий насичений гетероцикл є, необов'язково, заміщеним однією або двома групами, що незалежно вибирають з гідрокси, гало, =O, (С1-С4)алкілу, -(С1С4)алкіл(С3-С6)циклоалкілу, (С1-С4)алкокси, гідроксі(С1-С4)алкілу, (С1-С4)алкоксі(С 1-С4)алкілу, SO2(С1-С4)алкілу, -С(О)(С1-С 4)алкілу, [(С1С4)алкіл]2аміно, аміно, (С1-С4)алкіламіно, C(О)NH2, С(О)O(С1-С4)алкілу і піролідинону; R3 і R4 кожен, незалежно, вибирають з водню, (С3С6)циклоалкілу і (С1-С4)алкілу, згаданий (С3С6)циклоалкіл і (С1-С4)алкіл є, необов'язково, заміщеним аміно, (С1-С4)алкіламіно, [(С1С4)алкіл]2аміно або (С3-С6)циклоалкілом, або R3 і R4 утворюють разом з атомом N, до якого вони приєднані, 4-, 5-, 6- або 7-членний насичений гетероцикл, де один атом С може бути замінений N або О і де згаданий насичений гетероцикл є, необов'язково, заміщеним (С1-С4)алкілом, [(С1С4)алкіл]2аміно, аміно, (С1-С4)алкіламіно або С(О)(С1-С4)алкілом, згаданий -С(О)(С1-С4)алкіл є, необов'язково, заміщеним метокси або етокси, Y вибирають з СН2, СН(ОН), О, С=O і N, згаданий N є заміщеним Н, (С1-С4)алкілом, С(О)(С1С4)алкілом або (С1-С4)алкоксі(С 1-С4)алкілом; Z вибирають з О, S, SO і SO 2; m і р обидва є цілими числами, які є, незалежно, 1, 2 або 3, за умови, що m+р є еквівалентною або менше ніж 4, так що утворюється кільце: Y ( )m ( )p , яке є 4-, 5- або 6-членним кільцем; і R є або групою формули: R7 N L * R8 , де * позначає точку приєднання до Z, L є нерозгалуженим ланцюгом або розгалуженим (С2С6)алкіленом і R7 і R8 кожен, незалежно, вибирають з водню, (С1С6)алкілу, (С3-С6)циклоалкілу, гідроксі(С 1-С6)алкілу або R7 і R8 утворюють разом з атомом N, до якого вони приєднані, 4-, 5-, 6- або 7-членний насичений гетероцикл, де один атом С є, необов'язково, заміненим N, О, S, SO або SO2 і де згаданий насичений гетероцикл є, необов'язково, заміщеним однією або двома групами, що незалежно вибирають з (С1-С4)алкілу, (С1-С4)алкокси, (С1-С4)алкоксі(С 1С4)алкілу, гідроксі(С 1-С4)алкілу, гідрокси, С(О)O(С1-С4)алкілу, -С(О)-(С1-С4)алкіл-NН2, С(О)NН2, гало, аміно, (С1-С4)алкіламіно і [(С1С4)алкіл]2аміно, або R є групою формули: n 9 R N * , де * позначає точку приєднання до Z, 4 N-вмісним кільцем є 4-7-членний насичений гетероцикл, n є цілим числом еквівалентним 0, 1 або 2, і R9 представляє замісник, що вибирають з водню, (С1-С4)алкілу, гідроксі(С 1-С6алкілу) і (С3С6)циклоалкілу; het1 вибирають з моноциклічних або біциклічних гетероароматичних гр уп, що мають 5-10 кільцевих членів, які містять 1, 2, 3 або 4 гетероатом(и), що вибирають з азоту, кисню і сірки і het2 вибирають з моноциклічних або біциклічних гетероароматичних груп, що мають 5-10 кільцевих членів, які містять 1, 2, 3 або 4 гетероатом(и), що вибирають з азоту, кисню і сірки. 2. Сполука формули (1) згідно з пунктом 1, де Х вибирають з -CH2-NR1R2, -C(O)NR3R4, -CH2-het1 і het1, het1 є, необов'язково, заміщеним один раз або двічі (С1-С4)алкілом, де R1, R2, R3, R4 і het1 є такими як визначено вище в пункті 1. 3. Сполука формули (1) згідно з пунктом 2, де Х є CH2-het1 або het1, і het1 вибирають з 5- або 6членної моноциклічної гетероароматичної групи або 9-членної біциклічної гетероароматичної групи, кожна гетероароматична група, містить 1-3 атоми азоту, або 1-2 атоми азоту і 1 атом кисню, або 1 атом азоту і 1 атом сірки, і кожна гетероароматична група є, необов'язково, заміщеною один раз або двічі (С1-С4)алкілом. 4. Сполука формули (1) згідно з пунктом 3, де Х є тіазоліл, бензімідазолілметил-, піридиніл, оксазоліл, імідазопіридинілметил-, піримідиніл, імідазоліл, імідазолілметил- або триазолілметил-, згаданий тіазоліл, бензімідазолілметил-, піридиніл, оксазоліл, імідазопіридинілметил-, піримідиніл, імідазоліл, імідазолілметил- і триазолілметил- кожен є, необов'язково, заміщеним однією метильною групою. 5. Сполука формули (1) згідно з пунктом 1 або пунктом 2, де R1 є водень, метил або етил. 6. Сполука формули (1) згідно з пунктом 1, пунктом 2 або пунктом 5, де R2 вибирають з групи, яка містить водень, (С1-С6)алкіл, необов'язково, заміщений одним або двома замісниками, що незалежно вибирають з -S-(С1-С4)алкілу, -О-(С1-С4)алкілу, -SО2-(С1-С4)алкілу і фенілу, згаданий феніл є, необов'язково, заміщеним одним або двома замісниками, що незалежно вибирають з гало, гідрокси, ціано, (С1-С4)алкілу і (С1-С4)алкокси, (С3-С6)циклоалкіл, het2, необов'язково, заміщений одним або двома замісниками, що незалежно вибирають з гало, ціано, (С1-С4)алкілу і (С1-С4)алкокси, де het2 є таким як визначено у пункті 1, -SO2-R5, де R5 вибирають з групи, яка містить (С1С4)алкіл, [(С1-С4)алкіл]2аміно, феніл і -(С1С4)алкілфеніл, де згаданий феніл є, необов'язково, заміщеним 1 замісником, що незалежно вибирають з гало і ціано, і -C(О)-R6, де R6 вибирають з групи, яка містить (С1С4)алкіл, [(С1-С4)алкіл]2аміно, аміно і -(С1С4)алкілфеніл, згаданий феніл є, необов'язково, заміщеним одним або двома замісниками, що незалежно вибирають з гало, ціано, (С1-С4)алкілу і (С1-С4)алкокси. 7. Сполука формули (1) згідно з пунктом 6, де R2 5 84748 вибирають з групи, яка містить (С1-С3)алкіл, необов'язково, заміщений -О-(С1-С3)алкілом, (С3С5)циклоалкіл, het2, де het2 вибирають з групи, яка містить 5- або 6-членні моноциклічні гетероароматичні групи, що містять 1-2 атоми азоту, або 1 атом азоту і 1 атом кисню, або 1 атом азоту і 1 а том сірки, згаданий het2 є, необов'язково, заміщеним (С1-С4)алкілом, SO2-R5, де R5 є (С1-С4)алкіл і C(О)-R6, де R6 (С1-С 4)алкіл. 8. Сполука формули (1), згідно з пунктом 7, де R2 є (С1-С3)алкіл, необов'язково, заміщений метокси. 9. Сполука формули (1) згідно з пунктом 7, де R 2 є het2, і het2 вибирають з групи, яка містить 5- або 6членні моноциклічні гетероароматичні групи, що містять 1 або 2 атоми азоту. 10. Сполука формули (1) згідно з пунктом 9, де R2 є піридазинільною групою. 11. Сполука формули (1) згідно з пунктом 1 або пунктом 2, де R1 і R2 утворюють разом з атомом N, до якого вони приєднані, 4-, 5-, 6- або 7-членний насичений гетероцикл, де один атом С може бути замінений N, О, S, SO або SO2 і де згаданий насичений гетероцикл є, необов'язково, заміщеним однією або двома групами, що незалежно вибирають з гідрокси, гало, =O, (С1-С4)алкілу, -(С1С4)алкіл(С3-С6)циклоалкілу, (С1-С4)алкокси, гідроксі(С1-С4)алкілу, (С1-С4)алкоксі(С 1-С4)алкілу, SO2(С1-С4)алкілу, -С(О)(С1-С 4)алкілу, [(С1С4)алкіл]2аміно, -C(О)NH2, С(О)O(С1-С4)алкілу і піролідинону. 12. Сполука формули (1) згідно з пунктом 11, де R1 і R2 утворюють разом з атомом N, до якого вони приєднані, морфолініл. 13. Сполука формули (1) згідно з пунктом 1 або пунктом 2, де R3 і R4 кожен, незалежно, вибирають з водню і (С1-С4)алкілу або R3 і R4 утворюють разом з атомом N, до якого вони приєднані, 4-, 5- або 6-членний насичений гетероцикл, де один атом С може бути замінений N або О і де згаданий насичений гетероцикл є, необов'язково, заміщеним (С1С4)алкілом. 14. Сполука формули (1) згідно з пунктом 13, де R3 і R4 вибирають, незалежно, з водню, метилу і етилу, або R3 і R4 утворюють разом з атомом N, до якого вони приєднані, піролідиніл, піперидиніл, піперазиніл або азетидиніл, кожний піролідиніл, піперидиніл, піперазиніл і азетидиніл є, необов'язково, заміщеними метилом. 15. Сполука формули (1) згідно з будь-яким з попередніх пунктів, де Y вибирають з СН2, СН(ОН), О і С=O. 16. Сполука формули (1) згідно з пунктом 15, де Y є О. 17. Сполука формули (1) згідно з будь-яким з попередніх пунктів, де Z є О. 18. Сполука формули (1) згідно з будь-яким з попередніх пунктів, де m і р обидва є 2. 19. Сполука формули (1) згідно з будь-яким з попередніх пунктів, де R є група формули: R7 N R8 L * , де * позначає точку приєднання до Z, L є (С2С5)алкілен і R7 і R8 кожен, незалежно, вибирають з 6 водню, (С1-С6)алкілу, (С3-С6)циклоалкілу, гідроксі(С1-С6)алкілу або R7 і R8 утворюють разом з атомом N, до якого вони приєднані, 4-, 5-, 6- або 7членний насичений гетероцикл, де один атом С є, необов'язково, заміненим N, О, S, SO або SO2 і де згаданий насичений гетероцикл є, необов'язково, заміщеним однією або двома групами, що незалежно вибирають з (С1-С4)алкілу, (С1-С4)алкокси, (С1С4)алкоксі(С 1-С4)алкілу, гідроксі(С 1-С4)алкілу, гідрокси, С(О)O(С1-С4)алкілу, -С(О)-(С1-С4)алкіл-NН2, -С(О)NН2 і гало. 20. Сполука формули (1) згідно з пунктом 19, де R7 і R8 утворюють разом з атомом N, до якого вони приєднані, морфолініл або оксазепаніл. 21. Сполука формули (1) згідно з пунктом 19, де R7 і R8 утворюють разом з атомом N, до якого вони приєднані, 4-, 5- або 6-членний насичений гетероцикл, необов'язково, заміщений однією або двома (С1-С4)алкільними групами. 22. Сполука формули (1) згідно з пунктом 21, де насиченим гетероциклілом є піролідиніл, необов'язково, заміщений однією або двома метильними групами. 23. Сполука формули (1) згідно з пунктом 19, де R7 і R8 є (С1-С3)алкіл. 24. Сполука формули (1) згідно з будь-яким з пунктів 19-23, де L є пропілен. 25. Сполука формули (1) згідно з будь-яким з пунктів 1-18, де R є гр упа формули : n 9 R N * , де * позначає точку приєднання до Z, N-вмісним кільцем є 4- або 6-членний насичений гетероцикл, n є цілим числом еквівалентним 0 або 1, і R9 представляє замісник, що вибирають з водню, (С1С4)алкілу і (С3-С6)циклоалкілу. 26. Сполука формули (1) згідно з пунктом 25, де R9 є ізопропіл або циклобутил. 27. Сполука формули (1) згідно з будь-яким з пунктів 1-26 або її фармацевтично прийнятна сіль і/або сольват, для використання як медикаменту. 28. Фармацевтична композиція, що містить сполуку формули (1) або її фармацевтично прийнятну сіль і/або сольват, як визначено в будь-якому з попередніх пунктів, разом з фармацевтично прийнятним екціпіентом. 29. Застосування сполуки формули (1), як визначено в будь-якому з пунктів 1-26, або її фармацевтично прийнятної солі і/або сольвату, для виготовлення медикаменту для лікування захворювань при яких показаний Н 3 ліганд. 30. Застосування сполуки формули (1) згідно з пунктом 29, для виготовлення медикаменту для лікування розладів сну, мігрені, дискінезії, стресвикликаної тривоги, психотичних розладів, епілепсії, дефіциту пізнавальної здатності, такої як хвороба Альцгеймера або негострі погіршення когнітивної здатності, депресії, розладів настрою, шизофренії, тривоги, гіперактивного дефіциту уваги (ADHD), психотичних розладів ожиріння, запаморочення, епілепсії, нудоти, запальних захворювань, респі 7 84748 8 раторного дистрес-синдрому повнолітніх, гострого респіраторного дистрес-синдрому, бронхіту, хронічного бронхіту, хронічного обструктивного легеневого захворювання кістозно-фіброзної дегенерації, астми, емфіземи, риніту, хронічного синуситу, алергії, алергії, викликаної відповіддю дихальних шляхів, алергічного риніту, вірусного риніту, неалергічного риніту, річного і сезонного риніту, закупорювання носового каналу, алергічного закупорювання, сексуальної дисфункції у чоловіків або сексуальної дисфункції у жінок. 31. Спосіб лікування ссавця, включаючи людину, що страждає на захворювання при якому показаний Н3 ліганд, при якому вводять згаданому ссавцю ефективну кількість сполуки формули (1), як визначено в будь-якому з пунктів 1-26, або її фармацевтично прийнятної солі і/або сольвату, або її композиції. 32. Комбінація сполуки формули (1), як визначено в будь-якому з пунктів 1-26, і іншого фармакологічно активного агента, який вибирають з групи, що містить: антагоністи рецептора гістаміна Н 1, наприклад лоратидин, деслоратидин, фексофенадин і цетиризин, антагоністи рецептора гістаміна Н4, антагоністи рецептора гістаміна Н2, антагоністи лейкотрієна, включаючи антагоністи LTB4, LTC4 , LTD4 і LTE 4, зокрема монтелукаст, інгібітори фосфодіестерази, такі як інгібітори ФДЕ4 або інгібітори ФДЕ5, інгібітори повторного захоплення нейротрансміттеру, наприклад, флуоксетин, сертралін, пароксетин, зипразидон, інгібітори 5-ліпоксигенази (5-LO) або антагоністи 5ліпоксигеназа-активуючого протеїну (FL AP), антагоністи a 1- і a 2-адренорецептора або вазоконстрикторні симпатоміметичні агенти для протинабрякового застосування, антагоністи мускаринового М3 рецептора або ан тихолінергічні агенти, антагоністи b 2-адренорецептора, теофілін, хромоглікат натрію, інгібітори СОХ-1 (НСПЗЗ) і селективні інгібітори СОХ-2, пероральні і інгілюємі глюкокортикостероїди, моноклональні антитіла активні проти ендогенних запальних проявлень, агенти проти фактору некрозу пухлин (анти-TNFa ), інгібітори адгезії молекул, включаючи VLA-4 антагоністи, антагоністи рецептора кініну-В1- і В2, імуносупресивні агенти, інгібітори матриксних металопротеїнкіназ (ММР), антагоністи рецептора тахикініну NK1, NK2 і NK3, інгібітори еластази, антагоністи рецептора аденозину А2а, інгібітори урокінази, сполуки, що діють на допамінові рецептори, наприклад, агоністи D2, модулятори NF kb шляху, наприклад ІКК інгібітори, агенти, що можна класифікувати як муколітики або протикашлеві агенти, антибіотики, модулятори цитокінових сигнальних шляхів, такі як інгібітори р38 МАР кінази, syk кінази або JAK кінази, інгібітори HDAC (гістондеацетилази) і інгібітори РІЗ кінази. 33. Комбінація згідно з пунктом 32, де іншим фармакологічно активним агентом є антагоніст гістамінового Н1 рецептора. 34. Сполука формули (1), як визначено в будьякому з пунктів 1-26, або її фармацевтично прийнятна сіль і/або сольват, для використання, як описано в пункті 29 або 30. Представлений винахід стосується 3- або 4монозаміщених фенол і тіофенолпохідних загальної формули: ри. (1) в якій R, X, Y, Z, m і р мають значення визначені нижче, і способів їх одержання, проміжних сполук, що використовуються при їх одержанні, композицій, що їх містять і застосування таких похідних. Рецептори гістаміну H3 з устрічаються на пресинаптичних закінченнях периферичних нервів, де вони модулюють автономну нейротрансмісію і модулюють різні відповіді рецептора, що знаходиться під контролем автономної нервової системи. Також вони є гетерорецепторами, що модулюють вивільнення ряду інших нейротрансмітерів, таких як допамін, глутамат, норадреналін, серотонін, GABA, ацетилхолін, деякі пептиди і співтрансміте Останнім часом було створено ряд лігандів рецептора гістаміну H3 Огляд досягнень в дослідженні ліганду H3 і патентні документи приводяться в Expert Opin. Ther. Patents (2003) 13(6). Приклади ліганду рецептора гістаміну H3 можна знайти в [WO 02/76925, WO 00/06254, WO 02/12190, WO 02/12214 і WO 02/06223]. Як відомо, ліганди H3 рецептора придатні для лікування різних захворювань включаючи як розлади центральної нервової системи, так і запальні розлади. Прикладами захворювань, при лікуванні яких, як відомо, корисні H3 ліганди є запальне захворювання кишечнику, хвороба Крона, виразковий коліт, розлади сну, мігрень, дискінезія, стресвикликана тривога, психотичні розлади, епілепсія, дефіцит пізнавальної здатності, такий як хвороба Альцгеймера або негострі погіршення когнітивної здатності, депресія, розлади настрою, шизофренія, тривога, гіперактивний дефіцит уваги (ADHD), психотичні розлади, ожиріння, запаморочення, епілепсія, нудота, запаморочення, респіраторні 9 84748 захворювання, такі як респіраторний дистрессиндром повнолітніх, гострий респіраторний дистрессиндром, бронхіт, хронічний бронхіт, хронічнеобструктивне легеневе захворювання, кістознофіброзна дегенерація, астма, емфізема, риніт, хронічний синусит, алергія, алергія викликана відповіддю дихальних шляхів, алергічний риніт, вірусний риніт, неалергічний риніт, річний і сезонний риніт, закупорювання носового каналу і алергічне закупорювання. Хоча відомі ліганди H3, все ще існує потреба в нових лігандах H3 що є добрими кандидатами в лікарські засоби. Зокрема, переважні сполуки повинні сильно зв'язувати рецептор H3 гістаміну і в той же час проявляти низьку спорідненість до інших рецепторів. Вони повинні добре абсорбуватись з гастроінтестинального тракту, бути метаболітично стабільними і проявляти відмінні фармакокінетичні властивості. Вони повинні бути нетоксичними і мати незначні побічні ефекти. В цьому контексті, представлений винахід стосується нових заміщених фенол і тіофенолпохідних загальної формула (1): (1) або їх фармацевтично прийнятної солі, де: замісник формули -Z-R знаходиться в мета або пара-положенні фенільної групи; X вибирають з -CN, -CH2OH, -СН2-О-(С1С4)алкілу, -C(O)OH, -С(О)О(С1-С4)алкілу, -CH2NR1R2, -C(O)NR3R4, -CH2-O-het2, -CH2-het1 і het1, група net1 і в -CH2-het1 і в het1 є, необов'язково, заміщеною одним або двома замісниками, що незалежно вибирають з гало, ціано, (С1-С4)алкілу, -S(С1-С4)алкілу і (С1-С4)алкокси; R1 є водень або (С1-С4)алкіл, необов'язково, заміщений (С3-С6)циклоалкілом; R2 вибирають з групи, яка містить: водень, (С1-С6)алкіл, необов'язково, заміщений одним або двома замісниками, що незалежно вибирають з (С3-С6)циклоалкілу, гідрокси, -S-(С1-С4)алкілу, -О(С1-С4)алкілу, -SO2-(С1-С 4)алкілу, -SО-(С1С4)алкілу, гало, het1, аміно, (С1-С4)алкіламіно, [(С1С4)алкіл]2аміно і фенілу, згаданий феніл є, необов'язково, заміщеним одним або двома замісниками, що незалежно вибирають з гало, гідрокси, ціано, (С1-С4)алкілу і (С1-С4)алкокси, (С3-С6)циклоалкіл, het2, необов'язково, заміщений одним або двома замісниками, що незалежно вибирають з гало, ціано, (С1-С4)алкілу, NH2 і (С1-С4)алкокси, -SO2-R5, де R5 вибирають з групи, яка містить (С1-С4)алкіл, аміно, (С1-С4)алкіламіно, [(С1С4)алкіл]2аміно, феніл і -(С1-С4)алкілфеніл, згаданий феніл є, необов'язково, заміщеним одним або двома замісниками, що незалежно вибирають з гало, ціано, (С1-С4)алкілу і (С1-С4)алкокси, і -C(O)-R6, де R6 вибирають з групи, яка містить (С1-С4)алкіл, аміно, (С1-С4)алкіламіно, [(С1С4)алкіл]2аміно, феніл і -(С1-С4)алкілфеніл, згаданий феніл є, необов'язково, заміщеним одним або 10 двома замісниками, що незалежно вибирають з гало, ціано, (С1-С4)алкілу і (С1-С4)алкокси; або R1 і R2 утворюють разом з атомом N, до якого вони приєднані, 3-, 4-, 5-, 6- або 7-членний насичений гетероцикл, де один атом C може бути замінений N, O, S, SO або SO2 і де згаданий насичений гетероцикл є, необов'язково, заміщеним однією або двома групами, що незалежно вибирають з гідрокси, гало, =O, (С1-С4)алкілу, -(С1С4)алкіл(С 3-С6)циклоалкілу, (С1-С4)алкокси, гідрокси (С1-С4)алкіл у, (С1-С4)алкокси(С 1-С4)алкілу, SO2(С1-С4)алкілу, -С(О)(С1-С 4)алкілу, [(С1С4)алкіл]2аміно, аміно, (С1-С4)алкіламіно, C(O)NH2, С(О)О(С 1-С4)алкілу і піролідинону; R3 і R4 кожен, незалежно, вибирають з водню, (С3-С6)циклоалкілу і (С1-С4)алкілу, згаданий (С3С6)циклоалкіл і (С1-С4)алкіл є, необов'язково, заміщеним аміно, (С1-С4)алкіламіно, [(С1С4)алкіл]2аміно або (С3-С6)циклоалкілом, або R3 і R4 утворюють разом з атомом N, до якого вони приєднані, 4-, 5-, 6- або 7-членний насичений гетероцикл, де один атом C може бути замінений N або O і де згаданий насичений гетероцикл є, необов'язково, заміщеним (С1-С4)алкілом, [(С1С4)алкіл]2аміно, аміно, (С1-С4)алкіламіно або С(O)(С1-С4)алкілом, згаданий -С(O)(С1-С4)алкіл є, необов'язково, заміщеним метокси або етокси, Y вибирають з CH2, CH(OH), O, C=O і N, згаданий N є заміщеним H, (С1-С4)алкілом, С(О)(С1С4)алкілом або (С1-С4)алкокси(С 1-С4)алкілом; Z вибирають з O, S, SO і SO 2; m і р обидва є цілими числами, які є, незалежно, 1, 2 або 3, за умови, що m+р є еквівалентною або менше ніж 4, так що утворюється кільце: є 4-, 5- або 6-членне кільце; і R є або групою формули: де * позначає точку приєднання до Z, L є нерозгалуженим ланцюгом або розгалуженим (С2С6)алкіленом і R7 і R8 кожен, незалежно, вибирають з водню, (C1-С6)алкілу, (С3-С6)циклоалкілу, гідрокси(С 1-С6)алкілу або R7 і R8 утворюють разом з атомом N, до якого вони приєднані, 4-, 5-, 6- або 7-членний насичений гетероцикл, де один атом C є, необов'язково, заміненим N, O, S, SO або SO2 і де згаданий насичений гетероцикл є, необов'язково, заміщеним однією або двома групами, що незалежно вибирають з (С1-С4)алкілу, (С1С4)алкокси, (С1-С4)алкокси(С 1-С4)aлкілу, гідрокси(С1-С4)алкілу, гідрокси, С(О)О(С1-С4)алкілу, C(O)-(С1-С4)алкіл-NH2, -C(O)NH2, гало, аміно, (С1С4)алкіламіно і [(С1-С4)алкіл]2аміно, або R є групою формули: де * позначає точку приєднання до Z, Nвмісним кільцем є 4-7-членний насичений гетероцикл, n є цілим числом еквівалентним 0, 1 або 2, і 11 84748 R9 представляє замісник, що вибирають з водню, (С1-С4)алкілу, гідрокси(С 1-С6алкіл) і (С3С6)циклоалкілу; het1 вибирають з моноциклічних або біциклічних гетероароматичних груп, що мають 5-10 кільцевих членів, які містять 1, 2, 3 або 4 гетероатом(и), що вибирають з азоту, кисню і сірки і het2 вибирають з моноциклічних або біциклічних гетероароматичних груп, що мають 5-10 кільцевих членів, які містять 1, 2, 3 або 4 гетероатом(и), що вибирають з азоту, кисню і сірки. Було знайдено, що ці сполуки є Н3 лігандами і, таким чином, є особливо корисними для лікування Н3-залежних захворювань, таких як неврологічні розлади, або запальні, респіраторні і алергійні захворювання, розлади і стани. В представленому описі використовуються наступні визначення, якщо не вказано інше. "гало" означає атом галогену, що вибирають з групи, яка містить фтор, хлор, бром і йод. "(С1-Сх)алкіл" означає насичену, нерозгалужену або розгалужену вуглеводневу груп у, що має від 1 до х атомів вуглецю і включає наприклад (коли х=4) метил, етил, пропіл, і-пропіл, н-бутил, ібутил, втор-бутил і т-бутил і далі (коли х=6) пентил, і-пентил, н-пентил і гексил. Це також вірно, якщо алкільна група несе замісники або є заміщеною іншою групою, наприклад, в -S-(С1-С4)алкіл, О-(С1-С4)алкіл, -SO2-(С1-С4)алкіл, -SO-(С1-С4)алкіл, -СН2-О-(С1-С4)алкіл, -С(О)О(С1-С4)алкіл, (С1С4)алкіламіно, [(С1-С4)алкіл]2аміно]-(С1С4)алкілфеніл, -(С1-С4)алкіл(С 3-С6)циклоалкіл, пдрокси(С 1-С4)алкт, (С1-С4)алкокси(С 1-С4)алкіл, С(О)(С1-С4)алкіл. "(С1-С4)алкокси" означає нерозгалужені і розгалужені алкоксигрупи і включає наприклад, метокси, етокси, н-пропокси, і-пропокси, н-бутокси, ібутокси, втор-бутокси і т-бутокси. "(С2-С6)алкілен" означає дивалентний радикал, що є похідним від нерозгалуженого або розгалуженого алкану, що містить від 2 до 6 атомів вуглецю. Прикладами (C2-С6)алкіленових радикалів є метилен, етилен (1,2-етилен або 1,1-етилен), триметилен (1,3-пропілен), тетраметилен (1,4бутилен), пентаметилен і гексаметилен. "гідрокси(С 1-С4)алкіл" радикали є алкільними радикалами заміщеними гідрокси. Вони можуть містити 1 або декілька гідроксизамісників, якщо не вказано інше. Прикладами придатних гідрокси(С 1С4)алкільних радикалів є гідроксиметил, 1гідроксиетил або 2-гідроксиетил. "(С3-С6)циклоалкіл" означає насичену моноциклічну карбоциклічну груп у, що містить 3-6 атоми вуглецю і включає наприклад циклопропіл, циклобутил, циклопентил і циклогексил. У випадку коли (С1-Сx)алкільні радикали є заміщеними гало, такий радикал може містити 1 або декілька атомів галогену, якщо не вказано інше. Згаданим гало, переважно, є фтор, хлор, бром або йод, зокрема, фтор або хлор. Наприклад у фторзаміщеному алкільному радикалі, метильна група може бути присутня як дифторметильна або трифторметильна група. "насичений гетероцикл" означає насичену моноціклічну групу, що містить 4-7 кільцевих членів, 12 яка містить 1 атом азоту і, необов'язково, ще гетероатом, який вибирають з азоту, кисню і сірки. Прикладами насичених гетероциклів є азетидиніл, піролідиніл, піперидиніл, морфолініл, піперазиніл, оксазепаніл і азепаніл. het1 і het2 є моноциклічними або біциклічними гетероароматичними групами, що мають 5-10 кільцевих членів, які містять 1, 2, 3 або 4 гетероатом(и), що вибирають з азоту, кисню і сірки. Зокрема, гетероароматична група містить або (а) 1-4 атоми азоту, (б) один атом кисню або один атом сірки або (в) 1 атом кисню або 1 атом сірки і 1 або 2 атоми азоту, het2 є, переважно, С-приєднаним, що означає, що гр упа є приєднаною до сусіднього атому через кільцевий атом вуглецю, het1 може бути С-приєднаним або N-приєднаним. Гетероарильна група може бути незаміщеною, монозаміщеною або дизаміщеною, як визначено у визначенні X і R2 тут ви ще загальної формули (1) згідно з представленим винаходом. Прикладами гетероарильних груп є, але необмежується, тіофеніл, фураніл, піроліл, піразоліл, імідазоліл, оксазоліл, ізоксазоліл, тіазоліл, ізотіазоліл, триазоліл, оксадіазоліл, тіадіазоліл, тетразоліл, піраніл, піридиніл, піразиніл, піримідиніл, піридазиніл, триазиніл, тіадіазиніл, ізобензофураніл, бензофураніл, хроменіл, індолізиніл, ізоіндоліл, індоліл, індазоліл, пуриніл, хінолініл, ізохіноліл, циннолініл, фталазиніл, нафтиридиніл, хіназолініл, хіноксалініл, бензоксазоліл, бензотіазоліл, бензімідазоліл, бензофураніл, бензотіофеніл, піролопіразиніл, піролопіридиніл і імідазопіридиніл. Переважні значення для net1 і net2 будуть тут розкриті далі. В загальній формулі (1) згідно з представленим винаходом, коли радикал є моно-або полізаміщеним, згаданий замісник(и) може бути розташований в будь-якому бажаному положенні(ях), якщо не вказано інше. Також, коли радикал є полізаміщеним, згадані замісники можуть бути однаковими або різними, якщо не вказано інше. Згідно з переважним аспектом винаходу, X вибирають з -CN, -CH2OH, -C(O)OH, -CH 2-NR1R2, C(O)NR3R4, -CH2-het1 і het1, het1 в -CH2-het1 і net1 є, необов'язково, заміщений один раз або двічі (С1С4)алкілом, більш переважно, X вибирають з -CH2NR1R2, -CONR3R4, -CH2-het1 і het1, het1 B-CH2-het1 і het1 є, необов'язково, заміщеним один раз або двічі (С1-С4)алкілом, де R1, R2, R3 , R4 і het1 є такими як визначено вище. het1, переважно, вибирають з 5 або 6 членної моноциклічної гетероароматичної групи, або 9 членної біциклічної гетероароматичної групи, кожна гетероароматична група містить 1-3 атоми азоту, або 1-2 атоми азоту і 1 атом кисню, або 1 атом азоту і 1 атом сірки, і кожна гетероароматична група є, необов'язково, заміщеною один раз або двічі (С1-С4)алкілом, і переважно, необов'язково заміщеною один раз або двічі (С1-С2)алкілом. Більш переважно, X є тіазоліл, бензімідазолілметил-, піридиніл, оксазоліл, імідазопіридинілметил-, піримідиніл, імідазоліл, імідазолілметил- або триазолілметил-, згаданий тіазоліл, бензімідазолілметил-, піридиніл, оксазоліл, імідазопіридинілметил-, піримідиніл, імідазоліл, імідазолілметил- і триазолілметил- є, необов'язково, заміщеним од 13 84748 нією метильною групою. R1 є переважно водень, метил або етил. R2, переважно, вибирають з групи, яка містить водень, (С1-С6)aлкіл, необов'язково, заміщений одним або двома замісниками, що незалежно вибирають з -S-(С1-С4)алкілу, -О-(С1-С4)алкілу, -SО2-(С1С4)алкілу і фенілу, згаданий феніл є, необов'язково, заміщеним одним або двома замісниками, що незалежно вибирають з гало, гідрокси, ціано, (С1С4)алкілу і (С1-С4)алкокси, (С3-С6)циклоалкіл, het2, необов'язково, заміщений одним або двома замісниками, що незалежно вибирають з гало, ціано, (С1-С4)алкілу і (С1-С4)алкокси, де het2 є таким як визначено вище, -SO2-R5, де R5 вибирають з групи, яка містить (С1-С4)алкіл, [(С1-С4)алкіл]2аміно, феніл і -(С1С4)алкілфеніл, де згаданий феніл є, необов'язково, заміщеним 1 замісником, що незалежно вибирають з гало і ціано, і -C(O)-R6, де R6 вибирають з групи, яка містить (С1-С4)алкіл, ((С1-С4)алкіл]2аміно, аміно, і -( С1С4)алкілфеніл, згаданий феніл є, необов'язково, заміщеною одним або двома замісниками, що незалежно вибирають з гало, ціано, (С1-С4)алкілу і (С1-С4)алкокси. Більш переважно R2 вибирають з групи, яка містить (С1-С3)алкіл, необов'язково, заміщений -O-(С1С3)алкілом, переважно метокси, (С3-С5)циклоалкіл, het2, де het2, переважно, вибирають з групи, яка містить 5 або 6 членні моноциклічні гетероароматичні кільцеві системи, що містять 1-2 атоми азоту або 1 атом азоту і 1 атом кисню або 1 атом азоту і 1 атом сірки, згаданий het2 є, необов'язково, заміщеним одним або двома замісниками, що незалежно вибирають з гало, ціано, (С1-С4)алкілу і (С1-С4)алкокси, переважно (С1-С4)алкілу, SO2-R5, де R5 вибирають з групи, яка містить (С1-С4)алкіл, [(С1-С4)алкіл]2аміно, феніл, і -(С1С4)алкілфеніл, де згаданий феніл є, необов'язково, заміщеним 1 замісником, що незалежно вибирають з гало і ціано і де R5 є переважно (С1С4)алкіл, C(O)-R6, де R6 вибирають з групи, яка містить (С1-С4)алкіл, ((С1-С4)алкіл]2аміно, аміно і -(С1С4)алкілфеніл, згаданий феніл є, необов'язково, заміщеною одним або двома замісниками, що незалежно вибирають з гало, ціано, (С1-С4)алкілу і (С1-С4)алкокси, і де R6 є переважно (С1-С4)алкіл. В іншому аспекті винаходу, R2 є переважно (С1-С3)алкіл, необов'язково, заміщений метокси. het2, переважно, вибирають з групи, яка містить 5 або 6 членні моноциклічні гетероароматичні кільцеві системи, що містять 1 або 2 атоми азоту. В іншому аспекті винаходу, R2 є, переважно, піридазинільною групою. Згідно з наступним переважним аспектом винаходу R1 і R2 утворюють разомз атомом N, до якого вони приєднані, 4-, 5-, 6- або 7-членний насичений гетероцикл, де один атом C може бути замінений N, O, S, SO або SO2 і де згаданий насичений гетероцикл є, необов'язково, заміщеним 14 однією або двома групами, що незалежно вибирають з гідрокси, гало, =O, (С1-С4)алкілу, -(С1С4)алкіл(С 3-С6)циклоалкілу, (С1-С4)алкокси, гідрокси(С1-С4)алкілу, (С1-С4)алкокси(С 1-С4)алкілу, SO2(С1-С4)алкілу, -C(O)(С1-С 4)алкілу, [(С1С4)алкіл]2аміно, -C(O)NH2, С(О)О(С1-С4)алкілу і піролідинону, більш переважно, R1 і R2 утворюють разом з атомом N, до якого вони приєднані, 5- або 6-членний насичений гетероцикл, що вибирають з необов'язково, заміщений однією або двома групами, що незалежно вибирають з гідрокси, фтор у, гідроксиметилу, метоксиметилу, SО2(С1С4)алкілу, -С(О)(С1-С4)алкілу, -CONH2 і піролідинону Навіть більш переважно, R1 і R2 утворюють разом з атомом N, до якого вони приєднані, морфолінільну гр упу. Переважно, R3 і R4 кожен, незалежно, вибирають з водню і (С1-С4)алкілу або R3 i R4 утворюють разом з атомом N, до якого вони приєднані, 4, 5 або 6 членний насичений гетероцикл, де один атом C може бути замінений N або O і де згаданий насичений гетероцикл є, необов'язково, заміщеним (С1-С4)алкілом. Більш переважно, R3 і R4 вибирають, незалежно, з водню, метилу і етилу, або R3 i R4 утворюють разом з атомом N, до якого вони приєднані, піролідинільне, піперидинільне, піперазинільне або азетидинільне кільце, (кожне піролідинільне, піперидинільне, піперазинільне або азетидинільне кільце є, необов'язково, заміщеним метилом). Переважно, Y вибирають з CH2, CH(OH), O і C=O, більш переважно, Y є O. Переважно, Z є O Переважно m є еквівалентним 1 або 2 і р є еквівалентним 2, більш переважно m і р бидва є 2. в іншому переважному аспекті винаходу R є групою формули: де * позначає точку приєднання до Z, L є (С2С5)алкілен і R7 і R8 кожен, незалежно, вибирають з водню, (С1-С6)алкілу, (С3-С6)циклоалкілу, гідрокси(С1-С6)алкілу або R7 і R8 утворюють разом з атомом N, до якого вони приєднані, 4-, 5-, 6- або 7членний насичений гетероцикл, де один атом C є, необов'язково, заміненим N, O, S, SO або SO2 і де згаданий насичений гетероцикл є, необов'язково, заміщеним однією або двома групами, що незалежно вибирають з (С1-С4)алкілу, (С1-С4)алкокси, (С1С4)алкокси(С 1-С4)алкілу, гідрокси(С 1-С4)алкілу, гідрокси, С(О)О(С1-С4)алкілу, -C(O)-(С1-С4)алкілNH2, -C(O)NH2 і гало. Прикладами 4-, 5-, 6- або 7 15 84748 членного насиченого гетероциклу є: Навіть більш переважно, R7 і R8 утворюють разом з атомом N, до якого вони приєднані, морфолінільну або оксазепанільну гр упу. В іншому переважному аспекті, R7 і R8 утворюють разом з атомом N, до якого вони приєднані, 4-, 5- або 6-членний насичений гетероцикл, необов'язково, заміщений одним або двома (С1С4)алкілами, переважно, метил. В іншому більш переважному аспекті, насиченим гетероциклом є піролідинільна група, необов'язково, заміщена однією або двома метильними групами. Переважно, L є пропілен. Згідно з іншим переважним аспектом винаходу R є гр упою формули де * позначає точку приєднання до Z, Nвмісним кільцем є 4- або 6-членний насичений гетероцикл, п є цілим числом еквівалентним O або 1, і R9 представляє замісник, що вибирають з водню, (С1-С4)алкілу і (С3-С6)циклоалкілу Переважно, R9 є ізопропіл або циклобутил. Коли одна з груп в сполуці формули (1) є заміщеною галогеном, переважно це є фтор або хлор, зокрема, фтор. Особливо переважними сполуками винаходу є такі, в яких кожну змінну в формулі (1) вибирають з придатних і/або переважних груп для кожної змінної. Навіть більш переважними сполуками винаходу є такі, в яких кожну змінну в формулі (1) вибирають з більш переважних або найбільш переважних груп для кожної змінної. Згідно з особливим аспектом винаходу наступні сполуки виключаються з винаходу: сполуки формули (1), де Y є O, Z є O, R є група формули: де R10 є водень або (С1-С4)алкіл, R11 є (С1С4)алкокси, гідрокси або N((С1-С4)алкіл)2 і X є -CN, -CH2OH, -СН2-О-(С1-С4)алкіл, -C(O)OH, -С(О)О(С1С4)алкіл, -CONR3R4 або CH2NR1R2 де R1 є водень або (С1-С4)алкільна група і R2 є або водень, (С1С4)алкіл (необов'язково заміщений фенілом), або С(О)(С1-С4)алкіл. 16 В іншому втіленні представленого винаходу, забезпечується сполука формули (1): 3-(4-{4-[(диметиламіно)метил]тетрагідро-2Нпіран-4-іл}фенокси)-N,N-диметилпропан-1-амін 1-ізопропіл-4-{4-[4-(4-метил-1,3-тіазол-2іл)тетрапдро-2Н-піран-4-іл]фенокси}піперидин 4-метил-2-{4-[4-(4-піролідин-1ілбутокси)феніл]тетрагідро-2Н-піран-4-іл}-1,3тіазол 2-{4-[4-(4-піролідин-1ілбутокси)феніл]тетрагідро-2Н-піран-4-іл}-1,3тіазол 4-(4-{3[етил(метил)аміно]пропокси}феніл)тетрагідро-2Нпіран-4-карбонітрил 4-[4-(4-піролідин-1-ілбутокси)феніл]тетрагідро2Н-піран-4-карбоксамід 1-({4-[4-(4-піролідин-1ілбутокси)феніл]тетрагідро-2Н-піран-4іл}карбоніл)піролідин N-етил-N',N'-диметил-N-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрапдро-2Н-піран-4іл}метил)етан-1,2-діамін 1-(4-{4-[4-(азетидин-1-ілкарбоніл)тетрагідро2Н-піран-4-іл]фенокси}бутил)піролідин N,N-димeтил-4-[4-(4-пipoлiдин-1iлбyтoкcи)фeнiл]тeтpaгiдpo-2H-пipaн-4-кapбoкcaмiд N-метил-1-піридин-2-іл-N-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрапдро-2Н-піран-4іл}метил)метанамін 1-циклoгeкcил-N-мeтил-N-({4-[4-(3-пipoлiдин-1iлпpoпoкcи)фeнiл]тeтpaгiдpo-2H-піран-4іл}метил)метанамін N,N-диметил-1-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}карбоніл)азетидин-3-амін N,N,N'-тpимeтил-N'-({4-[4-(3-пipoлiдин-1iлпpoпoкcи)фeнiл]тeтpaгiдpo-2H-пipaн-4іл}метил)етан-1,2-діамін N,N-диметил-1-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)азетидин-3-амін N-(3-{4-[4-(aмiнoмeтил)тeтpaгiдpo-2H-пipaн-4iл]фeнoкcи}пpoпiл)циклобутан амін 3-{4-[4-(aмiнoмeтил)тeтpariдpo-2H-пipaн-4iл]фeнoкcи}-N-eтил-N-мeтилпpoпaн-1-амін N-циклобутил-4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4карбоксамід N-циклопентил-4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4карбоксамід N-(циклопропілметил)-4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4карбоксамід N-циклогексил-4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4карбоксамід 1-(4-{4-[(2-піролідин-1ілетил)тіо]феніл}тетрагідро-2Н-піран-4іл)метанамін N,N-диметил-1-(4-{4-[(2-піролідин-1ілетил)тіо]феніл}тетрагідро-2Н-піран-4іл)метанамін 1-[3-(4-{4-[(диметиламіно)метил]тетрагідро-2Н 17 84748 піран-4-іл}фенокси)пропіл]піролідин-3-ол 1-[4-(4-{3-[(2R,6S)-2,6-диметилморфолін-4іл]пропокси}феніл)тетрагідро-2Н-піран-4-іл]-N,Nдиметилметанамін 1-[(4-{4-[(3-піролідин-1ілпропіл)тіо]феніл}тетрагідро-2Н-піран-4іл)карбоніл]піперидин 1-[3-({4-[4-(піролідин-1-ілкарбоніл)тетрагідро2Н-піран-4-іл]феніл}тіо)пропіл]піролідин (4-{4-[(3-піролідин-1ілпропіл)тіо]феніл}тетрапдро-2Н-піран-4іл)метанол N-етил-N-({4-[4-(3-тіоморфолін-4ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)ацетамід N,N-диметил-1-[4-(4-{3-[(3R)-3-метилморфолін4-іл]пропокси}феніл)тетрагідро-2Н-піран-4іл]метанамін N-[(4-{4-[(3-піролідин-1ілпропіл)тіо]феніл}тетрагідро-2Н-піран-4іл)метил]ацетамід N-[(4-{4-[(3-піролідин-1ілпропіл)тіо]феніл}тетрагідро-2Н-піран-4іл)метил]етанамін N-метил-N-[(4-{4-[(3-піролідин-1ілпропіл)тіо]феніл}тетрагідро-2Н-піран-4іл)метил]етанамін N-етил-N-[(4-{4-[(3-піролідин-1ілпропіл)тіо]феніл}тетрагідро-2Н-піран-4іл)метил]ацетамід N-метил-N-({4-[4-(3-тіоморфолін-4ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)етанамін N-етил-N-({4-[4-(3-тіоморфолін-4ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)етанамін 4-(3-{4-[4-(піролідин-1-ілкарбоніл)тетрагідро2Н-піран-4-іл]фенокси}пропіл)тіоморфолін N-етил-N-[(4-{4-[(3-піролідин-1ілпропіл)тіо]феніл}тетрагідро-2Н-піран-4іл)метил]етанамін N-({4-[4-(3-тіоморфолін-4ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)піридин-2-амін 4-[(4-{4-[(1-ізопропілпіперидин-4іл)окси]феніл}тетрагідро-2Н-піран-4іл)метокси]піридин 4-[3-(4-{1-[(4-метилпіперазин-1іл)карбоніл]циклогексил}фенокси)пропіл]морфолін 4-(3-{4-[1-(піперазин-1ілкарбоніл)циклогексил]фенокси}пропіл)морфолін (4-{4-[(1-ізопропілазетидин-3іл)метокси]феніл}тетрагідро-2Н-піран-4-іл)метанол 4-[3-(4-{4-[(4-метилпіперазин-1іл)карбоніл]тетрагідро-2Н-піран-4іл}фенокси)пропіл]морфолін 4-(3-{4-[4-(піперазин-1-ілкарбоніл)тетрагідро2Н-піран-4-іл]фенокси}пропіл)морфолін 4-[(4-{4-[(1-ізопропілазетидин-3іл)метокси]феніл}тетрагідро-2Н-піран-4іл)метокси]піридин 4-[(4-{4-[(1-ізопропілазетидин-3іл)метокси]феніл}тетрагідро-2Н-піран-4іл)карбоніл]морфолін 4-{4-[4-(1Н-імідазол-1-ілметил)тетрагідро-2Н 18 піран-4-іл]фенокси}-1-ізопропілпіперидин 4-[4-(1-метил-3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4карбонітрил 4-(4-{3-[(3R)-3-гідроксипіролідин-1іл]пропокси}феніл)тетрагідро-2Н-піран-4карбонітрил 4-{4-[(1-етилпіперидин-4іл)окси]феніл}тетрагідро-2Н-піран-4-карбонітрил 4-{4-[(1-пропілпіперидин-4іл)окси]феніл}тетрагідро-2Н-піран-4-карбонітрил (3R)-N,N-диметил-1-[3-(4-{4[(метиламіно)метил]тетрагідро-2Н-піран-4іл}фенокси)пропіл]піролідин-3-амін N-{[4-(4-{3-[(3R)-3-(диметиламіно)піролідин-1іл]пропокси}феніл)тетрапдро-2Н-піран-4-іл]метил}N-метилметансульфонамід (3R)-1-{3-[4-(4-{[(2метоксиетил)(метил)аміно]метил}тетрагідро-2Нпіран-4-іл)фенокси]пропіл}-N,N-диметилпіролідин3-амін N-{[4-(4-{3-[(3R)-3-(диметиламіно)піролідин-1іл]пропокси}феніл)тетрагідро-2Н-піран-4-іл]метил}N,N',N'-триметилсечовина (3R)-N,N-диметил-1-(3-{4-[4-(1,3-тiазол-2іл)тетрапдро-2Н-піран-4іл]фенокси}пропіл)піролідин-3-амін (3R)-N,N-диметил-1-(3-{4-[4-(морфолін-4ілкарбоніл)тетрагідро-2Н-піран-4іл]фенокси}пропіл)піролідин-3-амін N-{[4-(4-{3-[(3R)-3-(диметиламіно)піролідин-1іл]пропокси}феніл)тетрагідро-2Н-піран-4-іл]метил}N-метилпіримідин-2-амін (3R)-N,N-диметил-1-(3-{4-[4-(морфолін-4ілметил)тетрагідро-2Н-піран-4іл]фенокси}пропіл)піролідин-3-амін 1-ізопропіл-4-{4-[4-(піперидин-1ілкарбоніл)тетрагідро-2Н-піран-4іл]фенокси}піперидин 4-[(4-{4-[(1-ізопропілпіперидин-4іл)окси]феніл}тетрагідро-2Н-піран-4іл)карбоніл]морфолін N-ізопропіл-4-{4-[(1-ізопропілпіперидин-4іл)окси]феніл}-N-метилтетрагідро-2Н-піран-4карбоксамід N*4*-{4-[4-(3-Піролідин-1-ілпропокси)феніл]тетрагідропіран-4ілметил}піридин-3,4-діамін N*2*-{4-[4-(3-Піролідин-1-ілпропокси)феніл]тетрагідропіран-4ілметил}піридин-2,3-діамін Особливо переважними сполуками формули (1) є описані в розділі Приклади тут далі. Коли в Прикладах одержується сольова форма, сполука представленого винаходу включає її вільну основу, наприклад: {4-[4-(3-Піролідин-1ілпропокси)феніл]тетрагідропіран-4-іл}метиламін, {4-[4-(3-Піперидин-1ілпропокси)феніл]тетрагідропіран-4-іл}метиламін, і Диметил-{4-[4-(3-піперидин-1ілпропокси)феніл]тетрагідропіран-4-ілметил}амін. В іншому втіленні винаходу, особливо переважними прикладами є: {4-[4-(1-Ізопропілпіперидин-4 19 ілокси)феніл]тетрагідропіран-4ілметил}диметиламін Диметил-{4-[4-(4-піролідин-1ілбутокси)феніл]тетрагідропіран-4-ілметил}амін {4-[4-(3-Піролідин-1ілпропокси)феніл]тетрагідропіран-4-іл}метиламін Диметил-{4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідропіран-4-ілметил}амін {4-[4-(3-Піперидин-1ілпропокси)феніл]тетрагідропіран-4-іл}метиламін Диметил-{4-[4-(3-піперидин-1ілпропокси)феніл]тетрагідропіран-4-ілметил}амін 1-Метил-4-{4-[4-(3-піролідин-1-ілпропокси)феніл]тетрагідропіран-4ілметил}піперазин (R)-2-Метоксиметил-1-{4-[4-(3-піролідин-1-ілпропокси)феніл]тетрапдропіран-4ілметил}піролідин (S)-2-Метоксиметил-1-{4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідропіран-4ілметил}піролідин 1-{4-[4-(3-Піролідин-1ілпропокси)феніл]тетрагідропіран-4ілметил}піперидин метил-{4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідропіран-4-ілметил}амін ізопропіл-метил-{4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідропіран-4-ілметил}амін 1-{4-[4-(3-Піролідин-1ілпропокси)феніл]тетрагідропіран-4ілметил}піролідин 4-{4-[4-(3-Піролідин-1ілпропокси)феніл]тетрагідропіран-4-ілметил}морфолін (2-метоксиетил)-метил-{4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідропіран-4-ілметил}амін 4-[4-(1-Ізопропілпіперидин-4ілокси)феніл]тетрагідропіран-4-карбонітрил 4-[4-(3-Піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4карбонової кислоти амід N-метил-1-{1-[4-(3-піролідин-1ілпропокси)феніл]-циклогексил}метан амін N-етил-N-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)етанамін N-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)етан амін N-метил-N-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)етанамін 4-{4-[(1-циклобутил-4піперидиніл)окси]феніл}тетрагідро-2H-піран-4карбонітрил 4-{4-[(1-ізопропілпіперидин-4іл)окси]феніл}тетрагідро-2Н-піран-4-карбоксамід 4-{4-[(1-ізопропілпіперидин-4-іл)окси]феніл]N,N-диметилтетрагідро-2Н-піран-4-карбоксамід 4-{4-[(1-ізопропілпіперидин-4-іл)окси]феніл]N,N-діетилтетрагідро-2Н-піран-4-карбоксамід 4-{4-[(1-ізопропілпіперидин-4іл)окси]феніл)тетрагідро-2Н-піран-4іл]карбоніл}піролідин 4-метил-2-[4-(4-(3-піролідин-1 84748 20 ілпропокси)феніл)тетрагідро-2H-піран-4-іл]-1,3тіазол 2-[4-(4-(3-піролідин-1ілпропокси)феніл)тетрагідро-2Н-піран-4-іл]-1,3тіазол N-[(4-{4-[(1-ізопропілпіперидин-4іл)окси]феніл}тетрагідро-2Н-піран-4-іл)метил]-Nметиламін N-[(4-{4-[(1-ізопропілпіперидин-4іл)окси]феніл}тетрагідро-2H-піран-4-іл)метил]-Nетиламін N-{[4-(4-[(1-ізопропілпіперидин-4іл)окси]феніл)тетрагідро-2Н-піран-4іл]метил}піримідин-2-амін і N-{[4-(4-(3-Піролідин-1ілпропокси)феніл)тетрагідро-2Н-піран-4іл]метил}піримідин-2-амін. 1-(4-{4-[(1-циклопентилазетидин-3іл)метокси]феніл}тетрагідро-2Н-піран-4-іл)-N,Nдиметилметанамін 3-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4-іл}метил)3Н-імідазо[4,5-b]піридин 2-{[метил({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)аміно]метил}фенол N-метил-N-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)циклопентанамін 2-[метил({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)аміно]етанол N-метил-N-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)циклопропанамін 1-(3-{4-[4-(азиридин-1-ілметил)тетрагідро-2Нпіран-4-іл]фенокси}пропіл)піролідин N-({4-[4-(3-тіоморфолін-4ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)етанамін 1-(4-{4-[(1-циклобутилпіперидин-4іл)окси]феніл}тетрагідро-2Н-піран-4-іл)-N,Nдиметилметанамін N,N-диметил-1-(4-{4-[(3-піролідин-1ілпропіл)тіо]феніл}тетрагідро-2Н-піран-4іл)метанамін N-метил-N-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)циклогексанамін 1-[3-({4-[4-(піролідин-1-ілметил)тетрагідро-2Нпіран-4-іл]феніл}тіо)пропіл]піролідин 1-({1-[4-(3-піролідин-1ілпропокси)феніл]циклогексил}метил)піперидин-4ол 1-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4-іл}метил)1H-бензімідазол 4-{4-[(1-циклобутилпіперидин-4іл)окси]феніл}тетрагідро-2Н-піран-4-карбоксамід N-метил-N-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)гексан-1-амін 1-циклoпpoпiл-N-(циклoпpoпiлмeтил)-N-({4-[4(3-пipoлiдин-1-ілпропокси)феніл]тетрагідро-2Нпіран-4-іл}метил)метанамін 21 N-[2-(диметиламіно)етил]-N-етил-4-[4-(3піролідин-1-ілпропокси)феніл]тетрагідро-2Н-піран4-карбоксамід N-метил-N-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)бутан-1-амін 4-{4-[4-(4,5-диметил-1Н-імідазол-2іл)тетрагідро-2Н-піран-4-іл]фенокси}-1ізопропілпіперидин 3-{[метил({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)аміно]метил}фенол 4-[(4-{4-[(1-циклопентилазетидин-3іл)метокси]феніл}тетрагідро-2Н-піран-4іл)метил]морфолін N-метил-N-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)пентан-1-амін 4-{4-[(1-циклобутилпіперидин-4-іл)окси]феніл}N,N-диметилтетрагідро-2Н-піран-4-карбоксамід N,N-диметил-1-(4-{4-[3-(1,4-оксазепан-4іл)пропокси]феніл}тетрагідро-2Н-піран-4іл)метанамін N,3,3-триметил-N-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)бутан-1-амін 4-{4-[(1-циклобутилпіперидин-4-іл)окси]феніл}N-ізопропілтетрагідро-2Н-піран-4-карбоксамід 1-метил-4-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4-іл}метил)1,4-діазепан 1-циклобутил-4-{4-[4-(1,3-тіазол-2іл)тетрагідро-2Н-піран-4-іл]фенокси}піперидин N-[(4-{4-[(1-циклобутилпіперидин-4іл)окси]феніл}тетрагідро-2Н-піран-4іл)метил]піридин-2-амін N-метил-1-{4-[4-(3-морфолін-4ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метанамін 1-[(4-{4-[(1-ізопропілпіперидин-4іл)окси]феніл}тетрагідро-2Н-піран-4-іл)карбоніл]-4метилпіперазин 1-циклoпeнтил-N-мeтил-N-({4-[4-(3-пipoлiдин-1iлnpoпoкcи)фeнiл]тeтpaгiдpo-2H-піран-4іл}метил)метанамін 4-{4-[(1-циклобутилпіперидин-4-іл)окси]феніл}N-етилтетрагідро-2Н-піран-4-карбоксамід N-[(4-{4-[(1-циклобутилпіперидин-4іл)окси]феніл}тетрагідро-2Н-піран-4іл)метил]піримідин-2-амін N,N-діетил-4-[4-(3-піролідин-1ілпропокси)феніл]тетрапдро-2Н-піран-4карбоксамід 4-[(4-{4-[(1-циклобутилазетидин-3іл)метокси]феніл}тетрагідро-2Н-піран-4іл)метил]морфолін 4-{4-[(1-циклобутилпіперидин-4-іл)окси]феніл}N-метилтетрагідро-2Н-піран-4-карбоксамід 1-циклобутил-4-{4-[4-(4-метил-1,3-тіазол-2іл)тетрагідро-2Н-піран-4-іл]фенокси}піперидин 4-[(4-{4-[(1-ізопропілазетидин-3іл)метокси]феніл}тетрагідро-2Н-піран-4іл)метил]морфолін 1-ізопропіл-4-{4-[4-(1,3-тіазол-2-іл)тетрагідро2Н-піран-4-іл]фенокси}піперидин 84748 22 1-(4-{4-[(1-циклобутилазетидин-3іл)метокси]феніл}тетрагідро-2Н-піран-4іл)метанамін 1-етил-4-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрапдро-2Н-піран-4іл}карбоніл)піперазин N-етил-N-метил-4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4карбоксамід 1-(4-{4-[(1-ізопропілазетидин-3іл)метокси]феніл}тетрагідро-2Н-піран-4іл)метанамін 1-[(4-{4-[(1-ізопропілпіперидин-4іл)окси]феніл}тетрагідро-2Н-піран-4-іл)метил]-4метилпіперазин 1-(циклопропілметил)-4-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)піперазин N,N-диметил-1-{4-[4-(3-морфолін-4ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метанамін N-[2-(диметиламіно)етил]-N-метил-4-[4-(3піролідин-1-ілпропокси)феніл]тетрагідро-2Н-піран4-карбоксамід 1-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}карбоніл)піперазин 1-етил-4-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)піперазин 4-[(4-{4-[(1-циклобутилпіперидин-4іл)окси]феніл}тетрагідро-2Н-піран-4іл)карбоніл]морфолін N-[(4-{4-[(1-циклобутилпіперидин-4іл)окси]феніл}тетрагідро-2Н-піран-4іл)метил]піридин-3-амін 1-метил-4-({1-[4-(3-пірол ідин-1ілпропокси)феніл]циклогексил}карбоніл)піперазин 1-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4-іл}метил)1Н-імідазол N-[(4-{4-[(1-ізопропілпіперидин-4іл)окси]феніл}тетрагідро-2Н-піран-4іл)метил]піридин-2-амін 1-ізопропіл-4-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)піперазин 1-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4-іл}метил)1Н-імідазо[4,5-с]піридин N-({4-[4-(3-піперидин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)піридин-2-амін 1-пропіл-4-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}карбоніл)піперазин N-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)піридазин-4-амін N-етил-4-{4-[(1-ізопропілпіперидин-4іл)окси]феніл}-N-метилтетрапдро-2Н-піран-4карбоксамід 1-метил-4-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}карбоніл)піперазин 23 1-пропіл-4-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)піперазин N-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)піридин-2-амін 4-{4-[4-(азетидин-1-ілкарбоніл)тетрагідро-2Нпіран-4-іл]фенокси}-1-ізопропілпіперидин 1-(2-метоксиетил)-4-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)піперазин 2-{4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4-іл}піридин N-[(4-{4-[(1-ізопропілпіперидин-4іл)окси]феніл}тетрагідро-2Н-піран-4іл)метил]піридазин-4-амін N-[(4-{4-[(1-ізопропілазетидин-3іл)метокси]феніл}тетрагідро-2Н-піран-4іл)метил]піридин-2-амін 4-[(4-{4-[(1-ізопропілпіперидин-4іл)окси]феніл}тетрагідро-2Н-піран-4іл)метил]морфолін 1-метил-4-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}карбоніл)-1,4-діазепан 4-(3-{4-[4-(морфолін-4-ілметил)тетрагідро-2Нпіран-4-іл]фенокси}пропіл)-1,4-оксазепан 1-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}карбоніл)піперидин 1-метил-4-[4-(3-піролідин-1ілпропокси)феніл]піперидин-4-карбонітрил 1-(3-{4-[4-(піролідин-1-ілкарбоніл)тетрагідро2Н-піран-4-іл]фенокси}пропіл)піролідин 2-(метилтіо)-1-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4-іл}метил)1 Н-імідазол 4-[4-(3-піролідин-1ілпропокси)феніл]піперидин-4-карбонітрил N-[(4-{4-[(1-ізопропілпіперидин-4іл)окси]феніл}тетрагідро-2Н-піран-4іл)метил]піридин-3-амін 6-метил-N-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)піридин-3-амін N-[(4-{4-[(1-етилпіперидин-4іл)окси]феніл}тетрагідро-2Н-піран-4іл)метил]піридин-2-амін N,N-диметил-4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4карбоксамід 4-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4-іл}метил)4Н-1,2,4-триазол 1-({1-[4-(3-піролідин-1ілпропокси)феніл]циклогексил}метил)піперазин 1-ізопропіл-4-[4-(3-піролідин-1ілпропокси)феніл]піперидин-4-карбонітрил 5-{4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4-іл}-1,3оксазол 1-ацетил-4-({1-[4-(3-піролідин-1ілпропокси)феніл]циклогексил}метил)піперазин 4-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4 84748 24 іл}метокси)піридин 1-ацетил-4-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)піперазин N-({4-[4-(4-піролідин-1ілбутокси)феніл]тетрагідро-2Н-піран-4іл}метил)піридин-2-амін 1-[3-(4-{4-[(диметиламіно)метил]тетрагідро-2Нпіран-4нл}фенокси)пропіл]-N,N-диметилазетидин3-амін 1-(3-{4-[4-(азетидин-1-ілкарбоніл)тетрагідро2Н-піран-4-іл]фенокси}пропіл)піролі дин N-[(4-{4-[(1-циклобутилазетидин-3іл)метокси]феніл}тетрагідро-2Н-піран-4іл)метил]піридин-2-амін N-{[4-(4-{3[циклобутил(метил)аміно]пропокси}феніл)тетрагідро-2Нпіран-4-іл]метил}піридин-2-амін N-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)піридин-3-амін 4-(3-{4-[4-(морфолін-4-ілметил)тетрагідро-2Нпіран-4-іл]фенокси}пропіл)морфолін N,N-диметил-1-(4-{4-[3-(4-метил-1,4-діазепан1-іл)пропокси]феніл}тетрагідро-2Н-піран-4іл)метанамін 1-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4-іл}метил)1Н-імідазо[4,5-b]піридин 4-({4-[4-(3-азетидин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}метил)морфолін 2-{4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4-іл}-1Німідазол 4-(3-{4-[4-(піперазин-1-ілкарбоніл)тетрагідро2Н-піран-4-іл]фенокси}пропіл)-1,4-оксазепан 4-[3-(4-{4-[(4-метилпіперазин-1іл)карбоніл]тетрагідро-2Н-піран-4іл}фенокси)пропіл]-1,4-оксазепан 4-{4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4іл}піримідин 4-метил-1-({4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4-іл}метил)1Н-імідазол 4-{4-[4-(3-піролідин-1ілпропокси)феніл]тетрагідро-2Н-піран-4-іл}-1Німдазол 4-[4-(4-{3[етил(метил)аміно]пропокси}феніл)тетрагідро-2Нпіран-4-ілметил]морфолін Іншим втіленням винаходу є проміжна сполука описана тут. Фармацевтично прийнятними солями сполук формули (1) є їх кислотно-адитивні і основні солі. Придатні кислотно-адитивні солі утворюються з кислот, які утворюють нетоксичні солі. Прикладами солей є ацетатні, аспартатні, бензоатні, безплатні, бікарбонат/карбонатні, бісульфатні/сульфатні, боратні, камсилатні, цитратні, едисилатні, езилатні, форміатні, фумаратні, глуцептатні, глюконатні, глюкуронатні, гексафторфосфатні, гібензатні, гідрохлоридні/хлоридні, пдроб 25 84748 ромідні/бромідні, гідройодидні/йодидні, ізетюнатні, лактатні, малатні, малеатні, малонатні, мезилатні, метилсульфатні, нафтилатні, 2-напсилатні, нікотинатні, нітратні, оротатні, оксалатні, пальмітатні, памоатні, фосфатні/гідрофосфатні/дигідрофосфатні, са харатні, стеаратні, сукцинатні, тартратні, тозилатні і трифторацетатні солі. Придатні основні солі одержують з основ, які утворюють нетоксичні солі. Прикладами є солі алюмінію, аргініну, бензатину, кальцію, холіну, діетиламіну, діоламіну, гліцину, лізину, магнію, меглуміну, оламіну, калію, натрію, трометаміну і цинку. Також можуть бути одержані гемісолі кислот і основ, наприклад, гемісульфатні і гемікальцієві солі. Для ознайомлення з придатними солями, дивіться, "Handbook of Pharmaceutical Salts: Properties, Selection, and Use" by Stahl and Wermuth, (Wiley-VCH, Weinheim, Germany, 2002). Фармацевтично прийнятні солі сполук формули (1) можна одержати за допомогою одного або декількох з трьох методів: (і) за допомогою взаємодії сполуки формули (1) з бажаною кислотою або основою; (іі) шляхом видалення кислото- або основонестійкої захисної групи в придатному попереднику сполуки формули (1) або шляхом розмикання циклу придатного циклічного попередника, наприклад, лактону або лактаму, використовуючи бажану кислоту або основу; або (ііі) шляхом перетворення однієї солі сполуки формули (1) у іншу за допомогою реакції з прийнятною кислотою або основою або використовуючи придатну іонообмінну колонку. Всі три реакції типово проводять в розчині. Одержана сіль може випасти в осад і може бути зібрана фільтруванням або може бути виділена шляхом випаровування розчинника. Ступінь іонізації одержаної солі може змінюватись з повністю іонізованої до майже неіонізованої. Сполуки винаходу можуть існувати у несольватованій і сольватованій формах Термін 'сольват' використовується тут для опису молекулярних комплексів, що містять сполуку винаходу і сте хіометричну кількість однієї або декількох фармацевтично прийнятних молекул розчинника, наприклад, етанол. Термін 'гідрат' використовується, коли згаданий розчинник є водою. Включеними в межі винаходу є комплекси, такі як клатрати, комплекси включення лікарський засіб-хазяїн, в яких, на противагу згаданим вище сольватам, лікарський засіб і хазяїн присутні в стехіометричній або нестехіометричній кількості. Також включеними є комплекси лікарського засобу, що містять два або більше органічних і/або неорганічних компонентів, які можуть бути в сте хіометричній або нестехіометричній кількостях Одержані комплекси можуть бути іонізованими, частково іонізованими або неіонізованими. Огляд таких комплексів приводиться в [J Pharm Sci, 64 (8), 1269-1288 by Haleblian (August 1975).] Тут і далі всі посилання на сполуки формули (1) включають посилання на їх солі, сольвати і 26 комплекси і сольвати і комплекси їх солей. Сполуки винаходу включають сполуки формули (1), як тут визначено вище, включаючи всі їх поліморфи і кристали, їх пролікарські форми і ізомери (включаючи оптичні, геометричні і таутомерні ізомери), як тут визначено, і мічені ізотопами сполуки формули (1). Як вказується, так звані 'проліки' сполук формули (1) також включаються в рамки винаходу. Таким чином, деякі похідні сполук формули (1), які можуть мати малу або немати зовсім фармакологічної активності можуть, коли вводяться в або на тіло, перетворюватись у сполуки формули (1), що мають бажану активність, наприклад, шляхом гідролітичного розщеплення. Такі похідні відносяться до 'проліків' Додаткову інформацію по використанню проліків можна знайти в ['Pro-drugs as Novel Delivery Systems, Vol. 14, ACS Symposium Series (T. Higuchi and W. Stella) і 'Bioreversible Carriers in Drug Design', Pergamon Press, 1987 (ed. E. B Roche, American Pharmaceutical Association)]. Проліки у відповідності з винаходом можуть, наприклад, бути одержані шляхом заміни прийнятної групи присутньої в сполуці формули (1) деякими замісниками відомими спеціалістам в цій галузі як 'про-замісники', як описується, наприклад, в ["Design of Prodrugs" by H. Bundgaard (Elsevier, 1985)]. Деякими прикладами проліків у відповідності з винаходом є: (і) коли сполуки формули (1) містять карбоксильну групу (-СООН), її естер, наприклад, сполука, в якій водень карбонової кислоти сполуки формули (1) замінений (С1-С8)алкілом; (іі) коли сполуки формули (1) містять спиртову груп у (-OH), її е тер, наприклад, сполука, в якій водень спиртової групи сполуки формули (1) замінений (C1-С6)алканоїлоксиметилом; і (ііі) коли сполуки формули (1) містять первинну або вторинну аміногрупу (-NH2 або -NHR, де R¹Н), її амід, наприклад, сполука, в якій, в залежності відобставин, один абообидва водні аміногрупи сполуки формули (1) є заміненим(и) (С1С10)алканоїлом. Інші приклади заміщувальних груп у відповідності із згаданими вище прикладами і прикладами інших типів проліків можна знайти в приведених вище посиланнях Однак, деякі сполуки формули (1) можуть самі по собі виступати як проліки інших сполук формули (1). Також включені в рамки винаходу метаболіти сполук формули (1), що є сполуками, які утворюються in vivo після введення лікарського засобу. Деякими прикладами метаболітів згідно з винаходом є (і) коли сполука формули (1) містить метильну груп у, її гідроксиметильне похідне (-CH3→-CH2OH): (іі) коли сполука формули (1) містить алкоксигрупу, її гідроксипохідне (-OR→-OH); (ііі) коли сполука формули (1) містить третинну аміногрупу, її вторинний амін (-NR aRb→-NHRa або NHRb); (iv) коли сполука формули (1) містить вторинну аміногрупу, її первинне похідне (-NHRa→-NH2); 27 84748 (v) коли сполука формули (1) містить фенільний замісник, її фенольне похідне (-Ph→-PhOH); і (vi) коли сполука формули (1) містить амідну груп у, похідне карбонової кислоти (CONRcRd→COOH). Сполуки формули (1), що містять один або декілька асиметричних атомів вуглецю можуть існувати як два або більше стереоізомерів. Коли структурний ізомеризм є взаємозмінюваним завдяки низькій енергії бар'єру, може мати місце таутомерний ізомеризм ("таутомеризм"). Це може мати місце у формі протонової таутомерії в сполуках формули (1), що містять, наприклад, іміно, кето або оксимні групи, або так званий валентний таутомеризм в сполуках, які містять ароматичний замісник. Звідси випливає, що одна сполука може проявляти більше ніж один тип ізомеризму. Включеними в межі представленого винаходу є всі стереоізомери, геометричні ізомери і таутомерні форми сполук формули (1), включаючи сполуки, що проявляють більше ніж один тип ізомеризму і суміші одного або декількох. Також включеними є кислотноадитивні солі або основні солі, в яких протиіон є оптично-активним, наприклад, с/-лактат або /-лізин, або рацемічний, наприклад, dl-тартрат або dl-аргінін. Загальновідомі методики для одержання/виділення окремих енантіомерів включають хіральний синтез з придатного оптично чистого попередника або розділення рацемату (або рацемату солі або похідного) використовуючи, наприклад, хіральну високоефективну рідинну хроматографію (ВЕРХ). Альтернативно, рацемат (або рацемічний попередник) може реагувати з придатною оптичноактивною сполукою, наприклад, спиртом, або, у випадку, коли сполука формули (1) містить кислотний або основний замісник, кислотою або основою, такою як винна кислота або 1-фенілетиламін. Одержану діастереомерну суміш можна розділити використовуючи хроматографію і/або фракційну кристалізацію і один абообидва діастереоізомери перетворюють у відповідний чистий енантіомер(и) за способами добре відомими спеціалісту в цій галузі Хіральні сполуки винаходу (і їх хіральні попередники) можна одержати в енантюмернозбагаченій формі використовуючи хроматографію, типово ВЕРХ, на асиметричній смолі х рухомою фазою, що містить вуглеводень, типово гептан або гексан, що містить від 0 до 50% об'ємних ізопропанолу, типово від 2% до 20%, і від 0 до 5% об'ємних алкіламіну, типово 0,1% діетиламіну Концентрування елюенту дає збагачену суміш. Стереізомерні конгломерати можна розділити за допомогою звичайних методик відомих спеціалісту в цій галузі, дивіться, наприклад, ["Stereochemistry of Organic Compounds" by E. L. Eliel (Wiley, New York, 1994)]. Представлений винахід включає всі фармацевтично прийнятні ізотопічно-мічені сполуки формули (1), в яких один або декілька атомів замінена атомами, що мають теж саме атомне число, але атомну масу або масове число, що відрізняється від атомної маси або масового числа, яке домінує 28 в природі. Прикладами ізотопів для включення в сполуки винаходу є ізотопи водню, такі як 2H і 3H, вуглецю, такі як 11C, 13C і 14C, хлору, такі як 36CI, фтору, такі як 18F, йоду, такі як 123I i 125I, азоту, такі як 13N і 15N, кисню, такі як 15O,17O і 18O, фосфору, такі як 32P і сірки, такі як 35S. Деякі ізотопічно-мічені сполуки формули (1), наприклад, ті що включають радіоактивний ізотоп, є корисними в дослідженнях лікарського засобу і/або розподілення субстрату в тканині. Радіоактивні ізотопи тритію, тобто 3H, і вуглецю-14, тобто 14 C, є особливо корисними для цих цілей з огляду на легкість їх включення і легкість детектування. Заміщення тяжчими ізотопами, такими як дейтерій, тобто 2H, може давати деякі терапевтичні переваги внаслідок збільшення метаболітичної стабільності, наприклад, збільшення in vivo часу напіврозкладу або зменшення необхідної дози, і звідси може бути переважним в деяких випадках. Заміщення позитрон емітуючими ізотопами, такими як 11C, 18F, 15 O і 13N, може бути корисним в дослідженнях позитронноемісійної топографії (PET) для визначення блокування рецептора субстратом. Ізотопічно-мічені сполуки формули (1) загалом можна одержати за допомогою звичайних методик відомих спеціалісту в цій галузі або за допомогою процесів аналогічних тим, що описуються в супровідних Прикладах і Приготуваннях використовуючи прийнятні мічені ізотопами реагенти замість не мічених реагентів використовуваних раніше. Фармацевтично прийнятними сольватами у відповідності з винаходом є такі, в яких кристалізаційний розчинник може бути ізотопічно заміщеним, наприклад, D2O, d6-ацетон, d6-ДMCO. Фенол і тіофенолпохідні формули (1) можна одержати використовуючи звичайні методики, такі як наступні ілюстративні методики, в яких R, X, Y, Z, m, p, R 1, R 2, R3 , R4 , R5 , R6 , R7 , R8 і R9 є такими як визначено вище, якщо не вказано інше. Сполуки формули (1), де X є -CH2NR1R2, можна одержати з сполук формули (2): (2) Використовуючи стандартні методики для взаємного перетворення функціональних груп відомих спеціалісту в цій галузі, наприклад, як описано в [Comprehensive Organic Transformations, R.C. Larock, 1st Edition, 1989 VCH Publishers Inc]. Цими методиками є: 1) Відновне алкілування альдегідами або кетонами використовуючи відновлювальний агент (наприклад, мурашина кислота або NaHB(OAc)3) в придатному розчиннику (наприклад, дихлорметан, тетрапдрофуран), необов'язково, з додаванням оцтової кислоти, при температурі від кімнатної (приблизно 20°C) до температури кипіння; 2) Алкілування алкілгалоїдами в присутності основи (наприклад, карбонат калію, трет-бутоксид калію) в придатному розчиннику (наприклад, ацетонітрил, тетрагідрофуран) при температурі від 29 84748 кімнатної (приблизно 20°C) до температури кипіння; 3) Сульфонілювання сульфонілхлоридом в присутності основи (наприклад, триетиламін, Nетилдіізопропіламін) в придатному розчиннику (наприклад, дихлорметан) при температурі від кімнатної до температури кипіння; 4) Гетероарилювання галогетероароматичною або гетероароматичною сульфоновою кислотою в присутності основи (наприклад, карбонат калію) в придатному розчиннику (наприклад, ацетонітрил) при температурі від кімнатної (приблизно 20°C) до температури кипіння. Альтернативно, цю реакцію можна провести під дією мікрохвильового випромінювання, альтернативно, використовуючи Nетилдiiзопропіламін як основу, необов'язково в придатному розчиннику (наприклад, Nметилпіролідинон, ацетонітрил). 5) Утворення сечовини з діалкілкарбамоїлхлориду або ціанатної солі, необов'язково в присутності основи (наприклад, триетиламіну) або кислоти (наприклад, оцтової кислоти) в придатному розчиннику (наприклад, дихлорметан або вода) при температурі від кімнатної до температури кипіння; 6) Утворення сульфонілсечовини з діалкілсульфамоїлхлориду в присутності основи (наприклад, триетиламін) в придатному розчиннику (наприклад, дихлорметан) при температурі від кімнатної до температури кипіння; 7) Ацилювання активованої кислоти (наприклад, ацилхлорид або ангідрид) в присутності основи (наприклад, триетиламін) в придатному розчиннику (наприклад, дихлорметан) при температурі від кімнатної до температури кипіння. 8) Внутрішнє конденсування галогетероароматичної сполуки в присутності паладієвого каталізатору, використовуючи придатне джерело паладію (наприклад, тріс(дибензиліденацетон)паладію (O)), необов'язково, в присутності хелатуючого ліганду (наприклад, BINAP) і в присутності придатної основи (наприклад, трет-бутоксид натрію) в розчиннику (наприклад, толуол), при температурі від кімнатної до температури кипіння Ці трансформації можна проводити послідовно з одержанням сполук, в яких R1 і R2 є такими як тут визначено вище. Сполуки формули (2) можна одержати шляхом відновлення відповідних ціанопохідних формули (3): 30 (4) похідним формули R-RLG, де RLG є групою, що відходить, такою як гало, мезилат або тозилат, в присутності основи (наприклад, карбонат калію) і необов'язково, в присутності добавки (наприклад, йодид калію) в придатному розчиннику (наприклад, диметилформамід) при температурі від кімнатної до температури кипіння. Коли R є група формули: як визначено раніше, тоді похідне формули RRLG можна одержати шляхом алкілування відповідного амінопохідного формули NHR7R8 похідним формули RLG-L-RLG в присутності основи (наприклад, NaOH, Na 2CO3, K2CO 3, Cs 2CO3), необов'язково, в присутності добавки (наприклад, йодид калію) в придатному розчиннику (наприклад, N,Nдиметилформамід, ацетонітрил, ацетон/Н2О) при температурі від кімнатної до температури кипіння. Амінопохідне формули NHR7R8 є або комерційно доступним, або одержується використовуючи методики відомі спеціалісту в цій галузі. Коли R є група формули : як визначено раніше, тоді похідне формули RRLG є або комерційно доступним, або одержується використовуючи методики відомі спеціалісту в цій галузі з літератури. Сполуки формули (4) можна одержати шляхом зняття захисту з відповідних похідних формули (5), де Z є O: (5) де RP є захисною групою (наприклад, метил, знімається BBr3 в ди хлорметані при температурі від 0°C до кімнатної). Сполуки формули (5) є або комерційно доступними, або можна одержати шляхом подвійного алкілування сполуки формули (6): (3) Придатним відновлюючим агентом (наприклад, LiAIH 4 або водень в присутності каталізатору, такого як PtO2) в придатному розчиннику (наприклад, Еt2О/дихлорметан, тетрагідрофуран або ізопропанол) при температурі від кімнатної до температури кипіння. Сполуки формули (3), вище, фактично відповідають сполукам формули (1), де X є CN гр упа. Сполуки формули (3), де Z є O, можна одержати шляхом алкілування відповідних гідроксипохідних формули (4): (6) де RP є таким, як визначено раніше, сполукою формули (7): (7) LG де R є таким, як визначенораніше, в присутності основи (наприклад, NaH), необов'язково, в присутності добавки (наприклад, йодид калію) в придатному розчиннику (наприклад, N,Nдиметилформамід, N-метилпіролідинон) при температурі від кімнатної до температури кипіння. Сполуки формули (6) і (7)обидві є або комерційно доступним, або одержуються використовую 31 84748 чи методики добре відомі спеціалісту в цій галузі з літератури. Сполуки формули (3), де Z представляє S, можна одержати з сполук формули (5), де Z представляє S і RP є Me, за допомогою перегрупування Пуммерера, з наступним алкілуванням одержаної проміжної сполуки похідним формули R-RLG Реакцію проводять шляхом обробки сполуки формули (5) придатним окисником (наприклад, m-СРВА) в придатному розчиннику (наприклад, дихлорметан) при 0°C з одержанням відповідного сульфідуобробка цього проміжного продукту трифтороцтовим ангідридом в присутності придатної основи (наприклад, 2,6-лутидин) в придатному розчиннику (наприклад, ацетонітрил) приблизно при -15°C, з наступною реакцією з R-RLG, в присутності основи (наприклад, триетиламін, карбонат калію) в придатному розчиннику (наприклад, N,Nдиметилформамід) при температурі від 0°C до кімнатної дає сполуку формули (3). Альтернативно, сполуки формули (3), де Z є O, можна одержати шляхом алкілування сполуки формули (4) спиртом формули ROH, який є або комерційно доступним, або одержується використовуючи методики відомі спеціалісту в цій галузі з літератури, використовуючи реагенти Міцунобу, такі як PPh3 і ДІАД в придатному розчиннику (наприклад, ТГФ) при температурі від 0°C до температури кипіння. Спеціалістам в цій галузі повинно бути зрозуміло, що для того щоб одержати сполуки формули (1) альтернативним чином або більш зручним способом, окремі стадії згадані в цьому розділі можуть проводитись в іншому порядку Наприклад сполуки формули (1), де Z є O і X є -CH2NR1R2, можна одержати шляхом алкілування сполуки формули (8) 32 використовуючи умови аналогічні тим, що описані для одержання сполук формули (1) з сполук формули (2). Сполуки формули (10) можна одержати з сполук формули (5), де Z є O, використовуючи аналогічні умови відновлення, що описані для одержання сполук формули (2) з сполук формули (3). Наступний приклад проведення окремих стадії процесу описаного в цьому розділі в різному порядку забезпечує сполуки формули (1) альтернативним чином або більш зручним способом розкриває одержання сполук формули (1), де Z є O, шляхом подвійного алкілування сполук формули (11): (11) сполуками формули (7), як визначено раніше, використовуючи умови аналогічні описаним для одержання сполук формули (5) з сполук формули (6). Сполуки формули (11) можна одержати з відповідних гідроксипохідних формули (12): (12) використовуючи умови аналогічні описаним для одержання сполук формули (3) з сполук формули (4). Сполуки формули (12) є або комерційно доступними або одержуються використовуючи методики добре відомі спеціалісту в цій галузі з літератури. Приклад проведення окремих стадії процесу описаного в цьому розділі в різному порядку забезпечує сполуки формули (1), де Z є O і R є група формули: (8) похідним формули R-RLG або ROH як визначено раніше, використовуючи умови аналогічні тим, що описані для одержання сполук формули (3) Сполуки формули (8) можна одержати шляхом зняття захисту з сполуки формули (9): (9) де RР є таким, як визначено раніше, використовуючи умови прийнятні для захисної групи і природи R1 і R2 (наприклад, використовуючи NaSMe в диметилформаміді при 130°C, де RР є метил і R1 і R2 є (C1-С4)алкіл). Сполуки формули (9) можна одержати з відповідних амінопохідних формули (10): (10) забезпечує одержання цих сполук за допомогою реакції сполук формули (13): (13) де RLG є таким, як визначено раніше, з амінопохідними формули NHR7R8 використовуючи умови аналогічні описаним для одержання R-RLG. Альтернативно, ті ж самі трансформації можна провести шляхом нагрівання сполук формули (13) з амінопохідним формули NHR7R8 і основою (наприклад, діізопропілетиламін) в придатному розчиннику (наприклад, N-метилпіролідинон) при 150200°C протягом 5-10хв. використовуючи мікрохвильову піч. Альтернативно, сполуки формули (1), де Z є O, X є -CH2NR1R2 і R1 і R2 є водень або необов'язково заміщений (С1-С4)алкіл або разом з атомом N, до якого вони приєднані, утворюють необов'язково заміщений 4-, 5- або 6-членний насичений гетероцикл, де атом C може бути замінений N, O, S, SO або SO2, можна одержати шляхом відновного амінування сполук формули (14): 33 84748 (14) амінопохідним формули HNR1R2 і відновлюючим агентом (наприклад, NaHB(OAc)3), необов'язково, в присутності кислоти Люїса (наприклад, Ti(OіPr)4) в придатному розчиннику (наприклад, EtOH) при температурі від 0°C до температури кипіння. Сполуки формули (14) можна одержати шляхом відновлення сполуки формули (3), де Z є O, відновлюючим агентом (наприклад, гідрид діізобутилалюмінію) в придатному розчиннику (наприклад, толуол) при температурі від -78°C до кімнатної (приблизно 20°C). Альтернативно, сполуки формули (14) можна одержати шляхом окислення сполук формули (1), де Z є O і X є -CH2OH, використовуючи окисники (наприклад, хлорхромат піридинію) в придатному розчиннику (наприклад, дихлорметан) при температурі від 0°C до температури кипіння. Сполуки формули (1), де X є -CH 2OH, можна одержати шляхом відновлення сполук формули (1), де X є -С(О)О(С1-С4)алкіл, відновлюючим агентом (наприклад, LiAIH4) в придатному розчиннику (наприклад, тетрагідрофуран) при температурі від -78°C до температури кипіння. Сполуки формули (1), де X є -С(О)О(С1С4)алкіл, можна одержати шляхом естерифікації сполук формули (1), де X є COOH, використовуючи стандартні методики добре відомі спеціалісту в цій галузі. Наприклад, естерифікацію можна провести використовуючи реагент здатний активува ти карбонову кислота (наприклад, тюнілхлорид) і НО(С1-С4)алкіл, необов'язково, в присутності розчинника (наприклад, дихлорметан) при температурі від 0°C до температури кипіння. Сполуки формули (1), де X є C(O)OH, можна одержати шляхом гідролізу сполук формули (3), як визначено раніше, мінеральною кислотою (наприклад, концентрована водна HCI), необов'язково, в присутності придатного співрозчинника (наприклад, діоксан), при температурі від 0°C до температури кипіння. Сполуки формули (1), де m і р обидва є еквівалентними 2, Z є O і Y є CH(OH), можна одержати шляхом відновлення сполук формули (1), де m і р обидва є еквівалентними 2 і Y є C=O, відновлюючим агентом (наприклад, LiAIH4) в придатному розчиннику (наприклад, Et2O) при температурі від 0°C до температури кипіння. Сполуки формули (1), де m і р обидва є еквівалентними 2, Z є O і Y є C=O, можна одержати шляхом обробки сполук формули (15): (15) хлоридом натрію в придатному розчиннику (наприклад, диметилсульфоксид/вода) при температурі від 100°C до температури кипіння. 34 Сполуки формули (15) можна одержати шляхом обробки сполук формули (16): (16) основою (наприклад, NaH) в придатному розчиннику (наприклад, 1,2-диметоксиетан) при температурі від кімнатної до температури кипіння. Сполуки формули (16) можна одержати шляхом алкілування сполук формули (11), як визначено раніше, метилакрилатом і основою (наприклад, гідроксид бензилтриметиламонію) в придатному розчиннику (наприклад, метанол/ацетонітрил) при температурі від кімнатної до температури кипіння. Сполуки формули (1), де X є -CONH 2, можна одержати шляхом обробки сполук формули (3), як визначено раніше, поліфосфорною кислотою або комплексом трифторид бору-оцтова кислота при температурі від кімнатної до 100°C. Сполуки формули (1), де X є -CONR 3R4, можна одержати реакцією сполук формули (1), де X є COOH, послідовно з реагентом здатним активувати карбонову кислоту (наприклад, тіонілхлорид,) і потім з амінопохідним формули HNR3R4, в придатному розчиннику (наприклад, дихлорметан) при температурі від 0°C до температури кипіння. Альтернативно, кислоту можна обробити аміном формули HNR3R4, в присутності конденсувального агенту (наприклад, TBTU, O-бензотриазол-1-ілN,N,N',N'-тетраметилуронію гексафторфосфат, гідрохлорид 1-(3-диметиламінопропіл)-3етилкарбодііміду), необов'язково, в присутності придатної добавки (наприклад, 1гідроксибензотриазол) і основа (наприклад, триетиламін) в придатному розчиннику (наприклад, дихлорметан, N,N-диметилформамід) при кімнатній температурі. Сполуки формули (1), де X є CH2NR1R2, можна одержати шляхом відновлення сполук формули (1), де X є -CONR3R4 і NR1R2 еквівалентне NR3R4, відновлюючим агентом (наприклад, алюмогідрид літію) в придатному розчиннику (наприклад, тетрагідрофуран, ефір) при температурі від кімнатної до 50°C. Сполуки формули (1), де X є -СН2-О-(С1С4)алкіл, можна одержати шляхом алкілування сполук формули (1), де X є -CH2-OH, похідним формули RLG(C1-C4)алкіл, де RLG є таким, як визначено раніше, в присутності основи (наприклад, NaH) в придатному розчиннику (наприклад, диметилформамід) при температурі від кімнатної до температури кипіння. Сполуки формули (1), де X є -CH2-O-het2, можна одержати шляхом алкілування сполук формули (1), де X є -CH2-OH, похідним формули RLGHet2, в присутності паладієвого каталізатору з галогетероароматичною сполукою, використовуючи придатне джерело паладію (наприклад, тріс(дибензиліденацетон)паладій (0)), необов'язково, в присутності хелатуючого ліганду (наприклад, BINAP) і в присутності придатної основи (наприклад, трет-бутоксид натрію) в розчиннику 35 84748 (наприклад, толуол), при температурі від кімнатної до температури кипіння. Сполуки формули (1), де X є het1, можна одержати з сполук формули (1), де X є COOH, або альтернативно з сполук формули (3) або (14) використовуючи методики відомі спеціалісту в цій галузі, такі як ті, що описані в підручниках з хімії гетероциклічних сполук, таких як [Heterocyclic Chemistry, J.A. Joule and K. Mills, 4th Edition, Blackwell publishing, 2000 або Comprehensive Heterocyclic chemistry I and II, Pergamon Press]. Наприклад, сполуки формули (1), де X є необов'язково заміщеним 2-тіазолілом і Z є O можна одержати шляхом обробки сполук формули (17): (17) придатним реагентом (наприклад, бромацетальдегіддиметилацеталь, хлорацетон) і HCI в придатному розчиннику (наприклад, EtOH) при кип'я тінні. Сполуки формули (17) можна одержати реакцією сполук формули (3), де Z є O, з діетилдитіофосфа том і водою при 60°C. Сполуки формули (1), де X є -CH2-het1 , і де згаданий net1 є N-приєднаним, можна одержати з сполук формули (1), де X є -CH 2-NH2, використовуючи методики відомі спеціалісту в цій галузі, такі як ті, що описані в підручниках з хімії гетероциклічних сполук, таких як [Heterocyclic Chemistry, JA Joule and K. Mills, 4th Edition, Blackwell publishing, 2000 або Comprehensive Heterocyclic chemistry I and II, Pergamon Press]. Сполуки формули (1), де X є -CH2-het1 , і де згаданий het1 є С-приєднаним, можна одержати з сполук формули (1), де X є -COOH, використовуючи двостадійний процес CH2 гомологінування за допомогою синтезу Арндта-Ейстерта [Ad vanced Organic Chemistry, J March, 4th edition, Wileylnterscience publication, 1992] з наступним стандартним конструюванням гетероциклу з карбонової кислоти, що відоме спеціалісту в цій галузі Сполуки формули (1) і їх попередники, які містять сульфідн у груп у можна окислити до відповідних сульфоксидів або сульфонів використовуючи стандартні методики добре відомі спеціалісту в цій галузі, наприклад, як описано в [Comprehensive Organic TpaHcformations, R.C. Larock, 1st Edition, 1989 VCH Publishers Inc]. Спеціалісту в цій галузі повинно бути зрозуміло, що деякі сполуки формули (1) можна перетворити у альтернативні сполуки формули (1) використовуючи стандартні хімічні перетворення Прикладами таких перетворень є ацилювання і сульфонілювання аміногруп (наприклад, дивіться приклади 166, 229, 230), реакції відновного амінування (наприклад, дивіться приклади 167, 168), алкілування (наприклад, дивіться приклад 228) або гідрування атомів галогену (наприклад, дивіться приклади 202, 203). Спеціалісту в цій галузі повинно бути зрозуміло, що при звичайному проведенні процесів описаних вище, функціональні групи проміжних спо 36 лук можуть потребувати захисту захисними групами. Такими функціональними групами є гідроксил, аміно і карбоксильна група. Придатними захисними групами для гідроксилу є триалкілсиліл і диарилалкілсиліл (наприклад, третбутилдиметилсиліл, трет-бутилди фенілсиліл або триметилсиліл), алкіл (наприклад, метил або метоксиетил) і тетрагідропіраніл. Придатними захисними групами для аміно є трет-бутилоксикарбоніл, 9-флуоренілметоксикарбоніл або бензилоксикарбоніл. Придатними захисними групами для карбоксильної групи є (C1-С4)алкіл або бензилові естери. Захист і зняття захисту функціональних груп може мати місце до або після будь-якої стадії реакції описаної тут вище. Введення і видалення захисних груп повністю описується в [Protective Groups in Organic Chemistry, edited by J.W.F. McOmie, Plenum Press (1973), Protective Groups in Organic Synthesis, 2nd edition, T.W. Greene & P.G.M. Wutz, Wileylnterscience Publication, 1991) і Protecting Groups, PJ. Kocienski, Thieme, 1994]. Також, сполуки формули (1), також як і проміжні сполуки для їх одержання, можна очистити згідно з різними добре відомими методиками, такими як перекристалізація і хроматографія. Сполуки формули (1), їх фармацевтично прийнятні солі і/або похідні є цінними фармацевтично активними сполуками, які придатні для лікування і профілактики ряду розладів, в які включений рецептор гістаміну H3 або в яких агонізм або антагонізм цього рецептору може бути корисним. Сполуки винаходу призначені для фармацевтичного застосування можуть бути введенні як кристалічні або аморфні продукти. Вони можуть бути одержані, наприклад, як тверді речовини, порошки або плівки за методами, такими як осадження, кристалізація, сублімація, висушуванням розпиленням або упарюванням. Для цих цілей може бути використано висушування із використанням мікрохвильового або радіовипромінювання. Вони можуть бути введені окремо або в комбінації з іншими сполуками винаходу або в комбінації з одним або декількома іншими лікарськими засобами (або будь-яка їх комбінація). Загалом, вони будуть вводитись як рецептури у поєднанні з одним або більшою кількістю фармацевтично прийнятних екціпієнтів. Термін "екціпієнт" використовується тут для опису будь-якого інгредієнту іншого ніж сполука(и) винаходу. Вибір екціпієнту буде у великій мірі залежати від ряду факторів, таких як шлях введення, вплив екціпієнтів на розчинність і стабільність і природа дозованої форми. Згідно з наступним аспектом винаходу, забезпечується фармацевтична композиція, що містить сполуку формули (1) або її фармацевтично прийнятна сіль і/або сольват, як визначено в будь-якому з попередніх пунктів, разом з фармацевтично прийнятним екціпієнтом. Фармацевтичні композиції придатні для вивільнення сполук представленого винаходу і способи їх одержання добре відомі спеціалістам в цій 37 84748 галузі. Такі композиції і способи їх одержання можна знайти, наприклад, в ['Remington's Pharmaceutical Sciences", 19th Edition (Mack Publishing Company, 1995)]. Сполуки винаходу можуть бути введенні перорально. Пероральне введення може включати заточування, так що сполука потрапляє у шлунковокишковий тракт, або може бути використане букальне або сублінгвальне введення, при яких сполука потрапляє у потік крові безпосередньо з рота. Рецептурами придатними для перорального введення є тверді рецептури, такі як таблетки, капсули, що містять часточки, рідини або порошки, лозенги (включаючи наповнені рідиною), гумки, мульти- і нано-часточки, гелі, тверді розчини, ліпосоми, плівки, овули, спреї і рідкі рецептури. Рідкими рецептурами є суспензії, розчини, сиропи і еліксири Такі рецептури можуть бути використані як наповнювачі м'яких або твердих капсул і, типово, містять носій, наприклад, вода, етанол, поліетиленгліколь, пропіленгліколь, метилцелюлоза, або придатна олія, і один або декілька емульсифікаторів і/або суспендувальних агентів. Рідкі рецептури також можна одержати шляхом відновлення твердої речовини, наприклад, з маленького пакетику. Сполуки винаходу також можуть бути використані у швидкорозчинних, швидко-дезінтегруючих дозованих формах, таких як ті, що описані в [Expert Opinion in Therapeutic Patents, 11 (6), 981986, by Liang and Chen (2001)]. В таблетованих дозованих формах, в залежності від дози, лікарський засіб може складати від 1ваг.% до 80ваг.% дозованої форми, більш типово від 5ваг.% до 60ваг.% дозованої форми. На додаток до лікарського засобу, таблетки зазвичай містять дезінтегратор. Прикладами дезінтеграторів є крохмальгліколят натрію, натрій карбоксиметилцелюлоза, кальцій карбоксиметилцелюлоза, натрій кроскармелоза, кросповідон, полівінілпіролідон, метилцелюлоза, мікрокристалічна целюлоза, нижчий алкіл-заміщений гідроксипропілцелюлоза, крохмаль, прежелатинізований крохмаль і алгінат натрію. Зазвичай, дезінтегратор буде складати від 1ваг.% до 25ваг.%, переважно від 5ваг.% до 20ваг.% дозованої форми. Зв'язувальні агенти зазвичай використовуються для склеювання в єдине ціле рецептури таблетки Придатними зв'язувальними агентами є мікрокристалічна целюлоза, желатин, цукри, поліетиленгліколь, природні і синтетичні смоли, полівінілпіролідон, прежелатинізований крохмаль, гідроксипропілцелюлоза і гідроксипропілметилцелюлоза. Таблетки також можуть містити розріджувачи, такі як лактоза (моногідрат, висушений розпилюванням моногідрат, безводна і їм подібні), маніт, ксиліт, декстроза, цукроза, сорбіт, мікрокристалічна целюлоза, крохмаль і дигідрат диосновного фосфату кальцію. Таблетки також, необов'язково, можуть містити поверхнево-активні агенти, такі як лаурилсульфат натрію і полісорбат 80 і агенти, що покращують ковзкість, такі як діоксид кремнію і тальк. Коли присутні, поверхнево-активні агенти можуть скла 38 дати від 0,2ваг.% до 5ваг.% таблетки і агенти, що покращують ковзкість, можуть складати від 0,2 ваг % до 1ваг.% таблетки. Таблетки також зазвичай місять змащувальні агенти, такі як стеарат магнію, стеарат кальцію, стеарат цинку, стеаридфумарат натрію і суміші стеарату магнію з лаурилсульфатом натрію. Змащувальні агенти загалом складають від 0,25ваг.% до 10ваг.%, переважно від 0,5ваг.% до 3ваг.% таблетки. Іншими можливими інгредієнтами є антиоксиданти, барвники, ароматизатори, консерванти і агенти, що корегують смак фармацевтичного агенту. Типові таблетки містять до приблизно 80% лікарського засобу, від приблизно 10ваг.% до приблизно 90ваг.% зв'язувального агенту, від приблизно 0ваг.% до приблизно 85ваг.% розріджувача, від приблизно 2ваг.% до приблизно 10ваг.% дезінтегратора, і від приблизно 0,25ваг.% до приблизно 10ваг.% змащувального агенту. Таблеткову суміш можна спресувати безпосередньо або за допомогою валу у формі таблеток. Таблеткову суміш або частину суміші можна альтернативно перед таблетуванням піддати вологому-, сухому-гранулюванню або гранулюванню розплаву, заморожуванню розплаву або екструдуванню. Кінцева рецептура може містити один або декілька шарів і може бути покрита або непокрита; вонаможе бути навіть інкапсульована. Рецептури таблетокобговорюються [в Pharmaceutical Dosage Forms: Tablets, Vol.1, by H. Lieberman and L. Lachman (Marcel Dekker, New York, 1980)]. Використовуваними плавкими пероральними плівками для людей або ветеринарії є пластичні водорозчинні або водонабухаючі тонкоплівкові дозовані форми, які можуть швидко розчинятись або поглинатись слизовоюоболонкою і типово містять сполуку формули (1), плівкоутворюючий полімер, зв'язувальний агент, розчинник, вологопоглинач, пластифікатор, стабілізатор або емульсифікатор, агент, що модифікує в'язкість і розчинник. Деякі компоненти рецептури можуть виконувати більше ніж одну функцію. Сполука формули (1) може бути водорозчинною або нерозчинною Водорозчина сполука типово містить від 1ваг.% до 80ваг.%, більш типово від 20ваг.% до 50ваг.%, розчиненої речовини. Менш розчинні сполуки можуть складати більшу частину композиції, типово до 88ваг.% розчиненої речовини. Альтернативно, сполука формули (1) може бути у формі мілких часточок. Плівкоутворюючий полімер може бути вибраний з природних полісахаридів, протеїнів або синтетичних гідроколоїдів і типово присутній в інтервалі від 0,01 до 99ваг.%, більш типово в інтервалі від 30 до 80ваг.%. Іншими інгредієнтами є антиоксиданти, барвники, ароматизатори і підсилювачи аромату, консерванти, агенти, що стимулюють слиновиділення, хладогенти, співрозчинник (включаючи олії), пом'якшувачи, наповнювачи, протипінні агенти, поверхнево-активні речовини і агенти, що коригують смак фармацевтичного агенту. 39 84748 Плівки у відповідності з винаходом типово одержують шляхом сушіння випарюванням тонких водних плівок на носії з якого вона легко відшаровується або папері. Це можна здійснити у сушильній шафі або тунелі, типово поєднують висушувач покриттів або шляхом сушіння виморожуванням або вакуумуванням. Тверді рецептури для перорального введення можна сформувати для негайного і/або модифікованого вивільнення. Рецептури модифікованого вивільнення мають відстрочене-, тривале-, пульсуюче-, контрольоване-, цільове і програмоване вивільнення. Придатні рецептури з модифікованим вивільненням для цілей винаходу описуються в [патенті US 6,106,864]. Деталі інших придатних методик вивільнення, таких як високоенергійні дисперсії і осмотичні часточки і часточки з покриттям можна знайти в [Pharmaceutical Technology On-line, 25(2), 1-14, by Verma et al (2001)]. Використання жуйних гумок для досягнення контрольованого вивільнення описується в [WO 00/35298]. Сполуки винаходу також можна вводити безпосередньо в потік крові, в м'яз або у вн утрішній орган. Придатними шляхами для парентерального введення є внутрішньовенне, внутрішньоартеріальне, внутрішньоочеревинне, інтратекальне, інтравентрикулярне, інтрауретральне, інтрастернальне, інтракраніальне, внутрішньом'язове і підшкірне. Придатними пристроями для парентерального введення є голкові (включаючи мікроголки) ін'єктори, безголкові ін'єктори і засоби вливання. Парентеральні рецептури типово є водними розчинами, які можуть містити екціпієнти, такі як солі, карбогідрати і буфереючі агенти (переважно до рН від 3 до 9), але, для деяких застосувань, вони можуть бути більш придатно сформовані як стерильний неводний розчин або як суха форма, що використовується у поєднанні з придатним розчинником, таким як стерильна пірогенвільна вода. Одержання парентеральних рецептур в стерильних умовах, наприклад, шляхом ліофілізації, можна легко здійснити використовуючи стандартні фармацевтичні методики добре відомі спеціалісту в цій галузі. Розчинність сполук формули (1), що використовується при одержанні парентеральних розчинів, може бути збільшена шляхом використання прийнятних методик формування рецептур, таких як включення агентів, що збільшують розчинність. Рецептури для парентерального введення можуть бути сформовані для негайного і/або модифікованого вивільнення. Рецептури модифікованого вивільнення мають відстрочене-, тривале-, пульсуюче-, контрольоване-, цільове і програмоване вивільнення. Таким чином, сполуки винаходу можуть бути сформовані як тверда, напівтверда або тиксотропна рідина для введення як імплантуємого депо, для забезпечення модифікованого вивільнення активної сполуки Прикладами таких рецептур є покриті лікарським засобом стенти і мікросфери з полі(dІ-молочнаспівгліколева)кислоти (PGLA). 40 Сполуки винаходу також можуть бути нанесені на шкіру або слизовуоболонку, тобто дермально або трансдермально. Типовими рецептурами для цих цілей є гелі, гідрогелі, лосьйони, розчини, креми, мазі, порошки для обтрушування, пов'язки, піни, плівки, пластири, пластинки, імплантати, губки, волокна, бандажі і мікроемульсії'. Також можуть бути використані ліпосоми. Типовими носіями є спирт, вода, мінерально масло, рідкий вазелін, білий вазелін, гліцерин, поліетиленгліколь і пропіленгліколь. Можуть бути включені покращувачи проникнення - дивіться, наприклад, [J Pharm Sci, 88 (10), 955-958 by Finnin and Morgan (October 1999)]. Іншими засобами місцевого введення є доставка за допомогою електропорації, фонтофорез, фонофорез, сонофорез і мікроголкова або безтолкова методика (наприклад Powderject™, Bioject™, etc.) ін'єктування. Рецептури для місцевого введення можуть бути сформовані для негайного і/або модифікованого вивільнення. Рецептури модифікованого вивільнення мають відстрочене-, тривале-, пульсуюче, контрольоване-, цільове і програмоване вивільнення. Сполуки винаходу також можуть бути введені інтраназально або за допомогою інгаляції, типово у формі сухого порошку (або окремо, або як суміш, наприклад, суха суміш з лактозою, або як змішані часточки компонентів, наприклад, суміші з фосфоліпідами, такими як фосфатидилхолін) з інгалятору сухого порошку або як аерозоль з контейнеру під тиском, насосу, спрею, пульверизатору (переважно використовують електродинамічний пульверизатор для одержання тонкого туману) або розпилювачу, з або без використання придатного пропеланту, такого як 1,1,1,2-тетрафторетан або 1,1,1,2,3,3,3-гептафторпропан. Для інтраназального використання, порошок може містити біоадгезивні агенти, наприклад, хітозан або циклодекстрин. Контейнер під тиском, насос, спрей, пульверизатор або розпилювач містить розчин або суспензію сполук(и) винаходу, що включає, наприклад, етанол, водний етанол, або придатний альтернативний агент для диспергування, солюблізування або розтягування вивільнення активної речовини, пропелан(и) як розчинник і, необов'язково, поверхнево-активну речовину, таку як триолеат сорбіту, олеїнова кислота або олігомолочна кислота. Перед використанням сухого порошку або суспензії, лікарський продукт мікронізують до розміру придатного для вивільнення за допомогою інгалювання (типово менше ніж 5 мікрон). Це можна досягти будь-яким прийнятним методом подрібнення, таким як спіральний струминний млин, струминний млин з псевдо-зрідженим шаром, суперкритична рідинна обробка для одержання наночасточок, гомогенізація при високому тиску або висушування розпиленням. Капсули (виготовлені, наприклад, з желатину або гідроксипропілметилцелюлози), блістери і картриджі для використання в інгаляторі або інсуфлаторі можуть бути сформовані таким чином, що містять порошкову суміш сполуки винаходу, придатної порошкової основи, такі як лактоза або кро 41 84748 хмаль і модифікатор експлуатаційних якостей, таки як І-лейцин, маніт або стеарат магнію. Лактоза може бути безводною або у формі моногідрату, переважно остання. Іншими придатними екціпієнтами є декстран, глюкоза, мальтоза, сорбіт, ксиліт, фр уктоза, цукроза і трехалоза. Придатний розчин для використання в пульверизаторі, що використовує елеткродинамічну силу для одержання тонкого туману, може містити від 1мкг до 20мг сполуки винаходу і випускний об'єм може змінюватись від 1мкл до 100мкл. Типово рецептура може містити сполуку формули (1), пропіленгліколь, стерильну воду, етанол і хлорид натрію. Альтернативними розчинниками, які можуть бути використані замість пропіленгліколю є гліцерин гліцерин і поліетиленгліколь. В такі рецептури винаходу, що призначені для інгалювання/інтраназальнного введення можуть бути додані придатні ароматизатори, такі як ментол і левоментол, або підсолоджувачі, такі як сахарин або сахарин натрію. Рецептури для інгалювання/інтраназальнного введення можуть бути сформовані для негайного і/або модифікованого вивільнення використовуючи, наприклад, PGLA. Рецептури модифікованого вивільнення мають відстрочене-, тривале-, пульсуюче-, контрольоване-, цільове і програмоване вивільнення. У випадку інгалятору сухого порошку і аерозолю, одиниця дозування визначається за допомогою клапану, який вивільнює виміряну кількість. Одиниці у відповідності з винаходом типово готовляться для введення виміряної дози або "пшику", що містить від 1мкг до 4000мкг сполуки формули (1). Загальна добова доза зазвичай знаходиться в інтервалі від 1мкг до 20мг, яка може вводитись однією дозою або, що типовіше, як розподілені дози протягом дня. Сполуки винаходу можуть бути введені ректально або вагінально, наприклад, у формі супозиторію, песарію або клізми. Масло какао є традиційною супозиторійною основою, але можуть бути використані різні альтернативи, якщо прийнятно. Рецептури для ректального/інтравагінального введення можуть бути сформовані для негайного і/або модифікованого вивільнення. Рецептури модифікованого вивільнення мають відстрочене-, тривале-, пульсуюче-, контрольоване-, цільове і програмоване вивільнення. Сполуки винаходу також можуть бути введені безпосередньо у око або вухо, типово у формі крапель мікронізованої суспензії або розчину в ізотонічному, рН-коригованому, стерильному саліні. Іншими рецептурами придатним для окулярного або вушного введення є мазі, біодеградуємі (наприклад, абсорбуємі гелеві губки, колаген) і небіодеградуємі (наприклад, силікон) імплантати, пластинки, лінзи і часточкові або везикулярні системи, такі як ніосоми або ліпосоми. Можуть бути включені полімери, такі як поперечнозшиті поліакрилові кислоти, полівініловий спирт, гіалуронова кислота, полімери целюлози, наприклад, гідроксипропілметилцелюлоза, гідроксиетилцелюлоза, або метилцелюлоза, або гетерополісахаридні полімери, наприклад, геланова смола, разом з консерва 42 нтом, таким як бензалконійхлорид. Такі рецептури можуть бути вивільнені за допомогою іонтофорезу Рецептури для окулярного/вушного введення можуть бути сформовані для негайного і/або модифікованого вивільнення. Рецептури модифікованого вивільнення мають відстрочене-, тривале-, пульсуюче-, контрольоване-, цільове і програмоване вивільнення. Сполуки винаходу можуть бути об'єднані з розчинними макромолекулярними сполуками, такими як циклодекстрин і їх придатні похідні або поліетиленгліколь-вмісні полімери, для того щоб покращити їх розчинність, швидкість розчинення, замаскувати смак, біодоступність і/або стабільність для використання в будь-якому з вищезгаданих шля хів введення. Комплекси лікарський засіб-циклодекстрин, наприклад, знайшли застосування в більшості видів дозованих форм і шляхів введення. Можуть бути використані комплекси включення і невключення. Як альтернатива безпосередньому комплексуванню з лікарським засобом, циклодекстрин може бути використаний як допоміжна добавка, тобто, як носій, розріджувач або солюбілізатор. Найбільш часто для цих цілей використовується альфа-, бета- і гама-циклодекстрини, приклади яких можна знайти в [міжнародних заявках WO 91/11172, WO 94/02518 і WO 98/55148]. Оскільки може бути бажано ввести комбінацію активних сполук, наприклад, з ціллю лікування окремої хвороби або стану, в межах представленого винаходу, що дві або більше фармацевтичних композицій, принаймні, одна з яких містить сполуку у відповідності з винаходом, можуть легко бути об'єднані у формі набору придатного для спільного введення композицій. Таким чином, набір винаходу містить дві або більше окремі фармацевтичні композиції, принаймні, одна з яких містить сполуку формули (1) у відповідності з винаходом, і пристрої для окремого утримання згаданих композицій, такі як контейнер, окремі пляшечки або окремі пакетики з фольги. Прикладом такого набору є звичайна блістерна упаковка, що використовується для пакування таблеток, капсул і їм подібних. Набір винаходу є особливо придатним для введення різних дозованих форм, наприклад, парентерально, для введення окремих композицій з різними інтервалами дозування, або для титрування окремих композицій одна до одної Для сприяння відповідності, набір типово містить вказівки по введенню і може бути забезпечений так званою пам'яткою. Для введення людям, загальна добова доза сполуки винаходу типово знаходиться в інтервалі від 0,001мг до 2000мг, що звичайно залежить від шляху введення Наприклад, пероральне введення може потребувати загальної добової дози від 1мг до 2000мг, в той час як внутрішньовенна доза може потребувати тільки від 0,01мг до 100мг Загальна добова доза може бути введена за один раз або розподілена на декілька доз і може, на розсуд лікаря, випадати з типового інтервалу приведеного тут. Ці дози формуються виходячи з середньої 43 84748 людини, що має вагу приблизно 65-70кг. Лікар легко визначить дози для суб'єкта вага якого випадає з цього інтервалу, такого як дитина і людина похилого віку. Для уникнення сумнівів, посилання тут на "лікування" включає посилання на зцілююче, паліативне і профілактичне лікування. Згідно з іншим втіленням представленого винаходу, сполуки формули (1), або їх фармацевтично прийнятні солі, похідні або композиції, також можуть використовуватись в як комбінація з одним або декількома додатковими терапевтичними агентами для спільного введення пацієнтові з одержанням деякого особливо бажаного терапевтичного кінцевого результату. Др угим і подальшими додатковими терапевтичними агентами також може бути сполука формули (1), або її фармацевтично прийнятна сіль, похідні або композиції, або один або декілька лігандів рецептора гістаміну H3 відомих в цій галузі. Більш типово, другий і наступні терапевтичні агенти будуть вибирати з різних класів терапевтичних агентів. Як тут використовується, терміни "спільне введення", "спільно введенні" і "в комбінації з", стосовно сполук формули (1) і одного або більше інших терапевтичних агентів, призначені для означення, і віднесення, і включення наступного: - одночасне введення такої комбінації сполук(и) формули (1) і терапевтичного агенту(ів) пацієнтові, що потребує лікування, коли такі компоненти сформовані разом в одну дозовану форму, яка вивільнює згадані компоненти, по суті, в той же самий час у згаданому пацієнті, - по суті, одночасне введення такої комбінації сполук(и) формули (1) і терапевтичного агенту(ів) пацієнтові, що потребує лікування, коли такі компоненти сформовані окремо один від одного в різні дозовані форми, які приймаються, по суті, одночасно згаданим пацієнтом, де згадані компоненти вивільнюються, по суті, в той же самий час у згаданому пацієнті, - послідовне введення такої комбінації сполук(и) формули (1) і терапевтичного агенту(ів) пацієнтові, що потребує лікування, коли такі компоненти сформовані окремо один від одного в різні дозовані форми, які приймаються, по суті, послідовно згаданим пацієнтом із значним інтервалом часу між кожним прийомом, де згадані компоненти вивільнюються, по суті, в різний час у згаданому пацієнті; і - послідовне введення такої комбінації сполук(и) формули (1) і терапевтичного агенту(ів) пацієнтові, що потребує лікування, коли такі компоненти сформовані разом в одну дозовану форму, яка вивільнює згадані компоненти контрольовано, де вони одночасно, безперервно і/або з накладенням вивільнюються в той же самий час і/або в різний час в згаданому пацієнті, де кожна частина може бути введення одним або різними шляхами. Придатними прикладами інших терапевтичних агентів, які можуть бути використані в комбінації з сполукою(ами) формули (1), або фармацевтично прийнятними солями, похідними або композиціями, є, але необмежується ними: 44 - Антагоністи рецептора гістаміна Н 1, наприклад, лоратидин, деслоратидин, фексофенадин і цетиризин - Анта гоністи рецептора гістаміна H4 - Анта гоністи рецептора гістаміна H2 - Антагоністи лейкотрієна, включаючи антагоністи LTB4, LTC4, LTD4, і LTE4, зокрема монтелукаст - Інгібітори фосфодіестерази, такі як інгібітори ФДЕ4 або інгібітори ФДЕ5, - Інгібітори повторного захоплення нейротрансміттеру, наприклад, флуоксетин, сертралін, пароксетин, зипразидон - Інгібітори 5-ліпоксигенази (5-LO) або антагоністи 5-ліпоксигеназа-активуючого протеїну (FLAP), - Агоністи α1- і α 2-адренорецептору або вазоконстрикторні симпатоміметичні агенти для протинабрякового застосування, - Антагоністи мускаринового М3 рецептора або антихолінергічні агенти, - Агоністи β2-адренорецептора, - Теофілін, - Хромоглікат натрію, - Інгібітори СОХ-1 (НСПЗЗ) і селективні інгібітори СОХ-2, - Пероральні і інгілюємі глюкокортикостероїди, - Моноклональні антитіла активні проти ендогенних запальних проявлень, - Агенти проти фактору некрозу пухлини (антиTNF-α), - Інгібітори адгезії молекул включаючи VLA-4 антагоністи, - Анта гоністи рецептора кінінy-B1- і B2 , - Імуносупресивні агенти, - Інгібітори матриксних металопротеїназ (MMP), - Антагоністи рецептора тахикініну NK1, NK2 і NK3, - Інгібітори еластази, - Агоністи рецептора аденозину А2а, - Інгібітори урокінази, - Сполуки, що діють на допамінові рецептори, наприклад, агоністи D2, - Модулятори NFkβ шляху, наприклад IKK інгібітори - Агенти, що можна класифікувати як муколітики або протикашлеві агенти, - Антибіотики, - Модулятори цитокінових сигнальних шляхів, такі як інгібітори р38 МАР кінази, syk кінази або JAK кінази, - Інгібітори HDAC (гістондеацетилази) і - Інгібітори РІ3 кінази Згідно з представленим винаходом, комбінація сполуки формули (1) з: - Антагоністами рецептора гістаміна H1, наприклад, лоратидин, деслоратидин, фексофенадин і цетиризин - Анта гоністами рецептора гістаміна H4 - Анта гоністами рецептора гістаміна H2 - Антагоністами лейкотрієну, включаючи антагоністи LTB4, LTC4, LTD4 , і LTE4 , зокрема монтелукаст - Інгібіторами фосфодіестерази ФДЕ4, 45 84748 - Інгібіторами повторного захоплення нейротрансміттеру, наприклад, флуоксетин, сертралін, пароксетин, зипразидон э переважними. Сполуки формули (1) мають здатність взаємодіяти з H3 рецептором і тому мають широкий перелік терапевтичних застосувань, як описано тут нижче, оскільки H3 рецептор відіграє суттєву роль в фізіології всіх тварин. Згідно з цим винаходом під H3 лігандами розуміють антагоністи, агоністи і зворотні агоністи H3 рецептора. Для переважних показань при лікуванні згідно з винаходом, H3 антагоністи є найбільш придатними. В іншому аспекті винаходу забезпечується сполука формули (1), як тут визначено, або її фармацевтично прийнятна сіль і/або сольват, для використання як медикаменту. Наступний аспект представленого винаходу стосується сполук формули (1), або їх фармацевтично прийнятних солей, похідних або композицій, для використання при лікуванні захворювань, розладів і станів, в які втягнутий H3 рецептор Більш особливо, представлений винахід також стосується сполук формули (1), або їх фармацевтично прийнятних солей, похідних або композицій, для використання при лікуванні захворювань, розладів і станів, що вибирають з групи, яка містить: - захворювання центральної нервової системи: розлади сну, мігрень, дискінезія, стресвикликана тривога, психотичні розлади, епілепсія, дефіцит пізнавальної здатності, такий як хвороба Альцгеймера або негострі погіршення когнітивної здатності, депресія, розлади настрою, шизофренія, тривога, пперактивний дефиціт уваги (ADHD), психотичні розлади, ожиріння, запаморочення, запаморочення голови, епілепсія, нудота - запальні захворювання - респіраторні захворювання (респіраторний дистрес-синдром повнолітніх, гострий респіраторний дистрес-синдром, бронхіт, хронічний бронхіт, хронічнеобструктивне легеневе захворювання, кістозно-фіброзна дегенерація, астма, емфізема, риніт, хронічний синусит), алергія, алергія викликана відповіддю дихальних шля хів, алергічний риніт, вірусний риніт, неалергічний риніт, річний і сезонний риніт, закупорювання носового каналу і алергічне закупорювання - сексуальні дисфункції у жінок, включаючи гіпоактивне сексуальне бажання, розлад сексуального збудження, розлад оргазму і сексуальний біль - сексуальні дисфункції у чоловіків, включаючи розлади бажання у чоловіків, еректильна дисфункція у чоловіків, розлади оргазму у чоловіків, такі як передчасна еякуляція - серцеві дисфункції, такі як ішемія міокарда і аритмія - захворювання гастроінтестинального тракту, такі як запальне захворювання кишечнику, хвороба Крона і виразковий коліт - рак - гіпотензія - біль і - стани надактивної кровотечі Сполуки формули (1) винаходу є особливо придатними для лікування алергії, алергії виклика 46 ної відповіддю дихальних шляхів, алергічного риніту, вірусного риніту, неалергічного риніту, річного і сезонного риніту, закупорювання носового каналу і алергічного закупорювання. Наступний аспект представленого винаходу також стосується застосування сполук формули (1), або їх фармацевтично прийнятних солей, похідних або композицій, для виготовлення лікарського засобу, що є лігандом H3. Зокрема, представлений винахід стосується застосування сполук формули (1), або їх фармацевтично прийнятних солей, похідних або композицій, для виготовлення лікарського засобу для лікування H3опосередкованих захворювань і/або станів, зокрема, захворювань і/або станів приведених вище. Інший аспект винаходу стосується застосування сполуки формули (1), або її фармацевтично прийнятної солі, похідного або композиції, для виготовлення композиції для лікування сексуальної дисфункції у жінок, включаючи гіпоактивне сексуальне бажання, розлад сексуального збудження, розлад оргазму і сексуальний біль, або для лікування сексуальних дисфункції у чоловіків, включаючи розлади бажання у чоловіків, еректильна дисфункція у чоловіків, розлади оргазму у чоловіків, такі як передчасна еякуляція. Як результат, представлений винахід забезпечує особливо цікавий спосіб лікування ссавця, включаючи людину, використовуючи ефективну кількість сполуки формули (1), або її фармацевтично прийнятної солі, похідного або композиції. Більш особливо, представлений винахід забезпечує особливо цікавий спосіб лікування Н 3опосередкованих захворювань і/або станів у ссавця, включаючи людину, зокрема, захворювань і/або станів приведених вище , що полягає у введенні згаданому ссавцю ефективної кількості сполуки формули (1), її фармацевтично прийнятної солі і/або похідного. Приклади Наступні приклади ілюструють одержання фенол і тіофенолпохідних формули (1): XIAT Арбоцель® BINAP BOC Br CDI δ D D ДХМ ДІАД ДМФА ДМСО EDCI ECI+ ЕСl Словник хімічна іонізація при атмосферному тиску фільтрувальний агент 2,2'-біс(дифенілфосфіно)-1,1'бінафтил трет-бутокси карбоніл широкий карбонілдіімідазол хімічний зсув дуплет нагрівання дихлорметан діізопропілазодикарбоксилат N,N-диметилформамід диметилсульфоксид дивіться WSCDI електроспрейіонізація з позитивним скануванням електроспрейіонізація з негативним скануванням 47 84748 г HBTU годин O-(1H-бензотриазол-1-іл)-N,N,N',N'тетраметилуронію гексафторфосфат HOAT 1-гідрокси-7-азабензотриазол HOBT 1-гідроксибензотриазол ВЕРХ високоефективна рідинна хроматографія основа Хюні- діізопропілетиламін га m/z співвідношення маси до заряду xв хвилин MC масспектр NH3 0,88 водний розчин амонію NMM N-метилморфолін ЯМР ядерний магнітний резонанс к квартет с синглет STAB триацетоксиборгідридом натрію T триплет TBME трет-бутилметиловий етер TBTU 2-(1Н-бензотриазол-1-іл)-1,1,3,3тетраметилуронію тетрафторборат Tf трифторметансульфоніл ТФО трифтороцтова кислота ТГФ тетрагідрофуран ТШХ тонкошарова хроматографія TosMIC тозилметилізоціанід WSCDI гідрохлорид 1-(3диметиламінопропіл)-3етилкарбодііміду Проміжна сполука 1: 4-(4метоксифеніл)тетрагідро-2Н-піран-4-карбонітрил 4-Метоксифенілацетонітрил (10г, 67,9ммоль) в ДМФА (50мл) повільно додавали до суспензії NaH (5,04г, 150ммоль) в ДМФА (50мл) при 0°С в атмосфері N2. Реакцію залишали нагріватись до кімнатної температури і перемішували протягом 30хв. Реакцію охолоджували до 0°C і по краплям протягом 80хв. додавали біс(2-хлоретил)етер (10,7г, 74,7ммоль) в ДМФА (100мл). Реакцію залишали нагріватись до кімнатної температури і перемішували протягом 1 години. Реакцію гасили водою (200мл) і екстрагували етилацетатом (3´300мл).об'єднані органічні екстракти промивали водою (2´200мл), розсолом (200мл), сушили над MgSO4 , фільтрували, промивали етилацетатом і концентрували у вакуумі одержуючи вказану в заголовку сполуку (17,2г, 100%). Проміжна сполука 2: 4-(4-Гідроксифеніл)тетрагідропіран-4карбонітрил Трибромід бору (1М в ДХМ, 262мл) до розчину додавали 4-(4-метоксифеніл)тетрагідро2Н-піран-4-карбонітрилу (14,7г, 67,9ммоль) в ДХМ (294мл) при 0°C в атмосфері N2 підтримуючи температуру нижче 5°C. Реакцію залишали нагріватись до кімнатної температури і перемішували протягом 48 годин. Суміш охолоджували до -100°C сумішшю сухого льоду і ацетону і гасили насиченим водним бікарбонатом натрію (294мл). Суміш залишали нагріватись до кімнатної температури і перемішували протягом 1 години. Суміш відокремлювали і водну частину екстрагували ДХМ (3´250мл). Об'єднані органічні екстракти сушили 48 над MgSO4, фільтрували, промивали ДХМ і концентрували у вакуумі одержуючи вказану в заголовку сполуку (10,8г, 78%). Проміжна сполука 3: 4-(4-Диметиламінометилтетрагідропіран-4-іл)фенол Стадія 1: До суспензії, що перемішується, LiAIH4 (79г, 2,08моль, 5ек.) в ТГФ (900мл) при 0-5°C в атмосфері азоту протягом 25 хвилин додавали 4-(4метоксифеніл)тетрагідро-2Н-піран-4-карбонітрил (90г, 0,414моль) в ТГФ (900мл) підтримуючи температуру в межах 5-10°C. Реакційну суміш залишали нагріватись до кімнатної температури і перемішували до закінчення. По краплям додавали гідроксид натрію (2N, 850мл), одержані тверді речовини фільтрували і промивали ТГФ (2´800мл), органічні розчини концентрували у вакуумі при 40°C. Залишок розчиняли в EtOAc (300мл) і сушили над MgSO4 , фільтрували і концентрували у вакуумі при 40°C одержуючи {[4-(4метоксифеніл)тетрагідро-2Н-піран-4-іл]метил}амін як світло-жовте масло (92г, кількісно). Стадія 2: До розчину {[4-(4-метоксифеніл)тетрагідро-2Нпіран-4-іл]метил}аміну (60г, 0,271моль) в H2O (444мл) і AcOH (213мл) додавали формальдегід (37ваг.% розчин в H2O, 408мл) і суміш охолоджували до 0-5°С. Порціями додавали триацетоксиборпдрид натрію (345г, 1,626моль, 6ек.) підтримуючи температуру нижче 12°C. Суміш перемішували при кімнатній температурі до закінчення. Повільно додавали гідроксид натрію (2М, 1000мл) і суміш екстрагували ДХМ (4´250мл). Органічні екстракти сушили над MgSO 4, фільтр ували і концентрували у вакуумі при 30°C одержуючи {[4(4-метоксифеніл)тетрагідро-2Н-піран-4іл]метил}диметиламін як жовте масло (53,5г, 80%). Стадія 3: До суспензії тіометоксиду натрію (49,2г, 0,702моль, 5ек.) в ДМФА (140мл) додавали {[4(4метоксифеніл)тетрагідро-2Н-піран-4іл]метил}диметиламін (35г, 0,140моль) і одержану суміш нагрівали до 130°C. Завершевши додавання, залишали охолоджуватись до кімнатної температури і додавали насичений водний NH 4CI (525мл). Одержану суміш екстрагували EtOAc (3´500мл), сушили над MgSO4, фільтрували і концентрували у вакуумі при 35°С одержуючи 4-(4диметиламінометил-тетрагідропіран-4-іл)фенол (проміжна сполука 3) як жовту тверду речовину (35,7г, 108%), що містить залишковий ДМФА і EtOAc. Проміжна сполука 4: 3-(4[(диметиламіно)метил1тетрагідропіран-4-іл)фенол Стадія 1. 3-Метоксифенілацетонітрил (10г, 67,9ммоль) в ДМФА (50мл) повільно при 0°C в атмосфері N2 додавали до суспензії NaH (5,04г, 1 50ммоль) в ДМФА (50мл). Реакцію залишали нагріватись до кімнатної температури і перемішували протягом 30хв. Реакцію охолоджували до 0°C і по краплям додавали протягом 80хв. біс(2-хлоретил)етер (10,7г, 74,7ммоль) в ДМФА (100мл). Реакцію залишали нагріватись до кімнатної температури і перемішували протягом 1 години. Реакцію гасили 49 84748 водою (500мл) і екстрагували етилацетатом (3´100мл).об'єднані органічні екстракти промивали розсолом (3´50мл), сушили над MgSO4, фільтрували, промивали етилацетатом і концентрували у вакуумі. Неочищену суміш очищали колонковою хроматографією, елюювали гептаном збільшуючи полярність до гептан:етилацетат (90:10), одержуючи 4-(3-метоксифеніл)тетрагідропіран-4карбонітрил (4,1г, 28%). Стадія 2: До суспензії, що перемішується, LiAIH4 (3,7г, 96,7ммоль) в діетиловому етері (100мл) охолодженої до 0°С по краплям додавали розчин 4-(3метоксифеніл)тетрагідропіран-4-карбонітрилу (4,2г, 19,3ммоль) в діетиловому етері (100мл). Після перемішування при кімнатній температурі протягом 30хв., реакційну суміш кип'ятили ще 15хв. Суміш охолоджували до 10°С і по краплям послідовно додавали воду, гідроксид натрію (15% в/о у воді, 0,48мл) і знову воду. Після перемішування протягом 15хв. при кімнатній температурі, суміш фільтрували через діатомову землю і концентрували. Залишок очищали флеш хроматографією (ДХМ/МеОН: 95/5), одержуючи [4-(3метоксифеніл)тетрагідропіран-4-іл]метиламін (4г, 94%). Стадія 3: Суміш [4-(3-метоксифеніл)тетрагідропіран-4іл]метиламіну (0,51г, 2,3ммоль), оцтової кислоти (0,535мл, 9,2ммоль), триацетоксиборгідриду натрію (0,974г, 4,6ммоль), 37% розчину формальдегіду у воді (0,55мл) і ДХМ (40мл) перемішували 72г при кімнатній температурі. Органічну фазу двічі промивали водою. Додавали до водної фази концентрований NaOH (рН12) і суміш двічі екстрагували дихлорметаном. Органічні екстракти сушили над Na2SO4, фільтрували і концентрували у вакуумі одержуючи N-{[4-(3метоксифеніл)тетрагідропіран-4-іл]метил}-N,Nдиметиламін як масло (0,35г, 61%). Стадія 4: До суспензії тіометоксиду натрію (0,42г, 6ммоль) в ДМФА (1,2мл) додавали N-{[4-(3метоксифеніл)тетрагідропіран-4-іл]метил}-N,Nдиметиламін (0,3г, 1,2ммоль) і одержану суміш нагрівали при 65°C протягом 7г, залишали охолоджуватись до кімнатної температури і гасили насиченим водним NH4CI (6мл). Суміш екстрагували ДХМ, сушили над Na2SO4, фільтрували і концентрували у вакуумі одержуючи 0,25г неочищеного продукту. Суміш неочищеного продукту і HBr (3мл) нагрівали із зворотнім холодильником протягом 1г. після охолодження, додавали воду гасячи реакцію і суміш підлуговували NaHCO3 і екстрагували ДХМ. Органічні екстракти сушили над Na2SO4, фільтрували і концентрували. Залишок очищали за допомогою флеш-хроматографії (ДХМ/MeOH (10% NH3)), одержуючи 3-{4[(диметиламіно)метил]тетрагідропіран-4-іл}фенол (0,100г, 35,5%). Загальна методика А для синтезу хлоридів (RRLG, де RLG є хлорид): Амін (1ек.) додавали до реакційної колби після чого додавали ацетон (3об або 20об), 5М розчин NaOH (1,2ек.) і 1-бром-3-хлорпропан (1,5ек. або 50 3ек.). Реакцію перемішували протягом ночі при кімнатній температурі. Фази розділяли і ацетоновий шар концентрували у вакуумі. Водний шар підкислювали 2М розчином HCI до рН1 (~10об). Концентрат розводили TBME (30об) і промивали водою (15об). Водний шар екстрагували TBME (2´15мл).об'єднані TBME промивали 2М розчином HCI (15мл) іоб'єднували з першою кислою фазою.об'єднані кислі шари промивали TBME (15об) і підлуговували до рН14 4М розчином NaOH (~40мл). Водний шар екстрагували TBME (3´30мл).об'єднані органічні шари сушили над MgSO4 , фільтрували, промивали TBME (5об) і концентрували у вакуумі одержуючи необхідний хлорид. Загальна методика В: 4-(4-Диметиламінометил-тетрапдропіран-4іл)фенол (500мг, 2,13ммоль), хлорид (378мг, 2,13ммоль), ДМФА (10мл), воду (17мл) і K2CO3 (1,18г, 8,52ммоль) нагрівали при 130°C. Охолоджували до кімнатної температури, додавали воду (40мл), екстрагували EtOAc (3´25мл) іоб'єднані органічні екстракти промивали водою (2´25мл). Органічні розчини сушили над MgSO4, фільтрували і концентрували у вакуумі при 35°C. Очищали неочищений продукт хроматографією на силікагелі, елюент (4% MeOH, 1% NH3, в ДХМ), одержуючи вказані в заголовках сполуки. Проміжна сполука 5: 1-(3-Хлорпропіл)піролідин Піролідин (10г, 0,14моль), ацетон (28мл), 5М розчин NaOH (21мл) і 1-бром-3-хлорпропан (24,4г, 0,15моль) перемішували разом в атмосфері N2 протягом 8 годин. Органічний шар відокремлювали і концентрували у вакуумі. Неочищений продукт очищали перегонкою у вакуумі (Ткип. 90°С/30мбар), одержуючи вказану в заголовку сполуку (11,7г, 57%) як безбарвне масло. Приклад 1: Диметил-(4-[3-(3-піролідин-1ілпропокси)феніл]тетрагідропіран-4-ілметиліамін Алкілування 3-[4(диметиламіно)метилтетрагідро-2Н-піран-4іл]фенолу (0,1г, 0,425ммоль) 1-(3хлорпропіл)піролідином (0,125г, 0,85ммоль) згідно з загальною методикою В дає бажану сполуку після очищення 3Å допомогою флеш-хроматографії (0,030г, 20%) 1 H ЯМР (400МГц, CDCI3) δ 7,27-7,18 (м, 1Н), 6,92-6,84 (м, 2Н), 6,75 (дд, 1Н), 4,05 (т, 2Н), 3,8-3,7 (м, 2Н), 3,55 (т, 2Н), 2,65 (т, 2Н), 2,6-2,5 (м, 4Н), 2,4(с, 2Н), 2,15-1,85 (м, 6Н), 2,0 (с, 6Н), 1,85-1,75 (м, 4Н). Проміжна сполука 6: 1-(3-Хлорпропіл)2(R),5(R)-транс-диметил-піролідин 2(R),5(R)-транс-Диметил-піролідин (0,75г, 7,56ммоль), ацетон (15мл, 20об), 5М розчин NaOH 51 84748 (1,8мл, 1,2ек.) і 1-бром-3-хлорпропан (3,57г, 22,7ммоль, 3ек.) взаємодіяли разом згідно з загальною методикою А даючи вказану в заголовку сполуку (0,5г, 38%) як жовте масло. Приклад 2: (4-(4-[3-(2,5-Диметилпіролідин-1іл)пропокси]феніл}тетрагідропіран-4ілметил)диметиламін 4-(4-Диметиламінометил-тетрагідропіран-4іл)фенол (330мг, 1,43ммоль), 1-(3-хлорпропіл)-2,5транс-диметил-піролідин (221мг, 1,26ммоль), ДМФА (7,6мл) і K2CO3 (790мг, 5,72ммоль) взаємодіяли разом згідно з загальною методикою В. Виділений матеріал піддавали хроматографії на силікагелі, елюент 95:4:1 (ДХМ, MeOH, NH3), одержуючи вказану в заголовку сполук у як жовте масло (180мг, 34%). 1 H ЯМР (400МГц, CDCI3) δ 7,20 (д, 2Н), 6,87 (д, 2Н), 4,08-3,95 (м, 2Н), 3,79-3,70 (м, 2Н), 3,59-3,49 (м, 2Н), 3,11-3,00 (м, 2Н), 2,77 (м, 1Н), 2,54 (м, 1Н), 2,40 (с, 2Н), 2,14-1,81 (м, 8Н), 1,96 (с, 6Н), 1,441,31 (м, 2Н), 0,97 (д, 6Н). Проміжна сполука 7. 1-(3-Хлорпропіл)-2метил-піролідин 2-Метилпіролідин (0,9г, 10,6ммоль), ацетон (18мл, 20об), 5М розчин NaOH (2,50мл) і 1-бром-3хлорпропан (5г, 31,8ммоль, 3ек.) взаємодіяли разом згідно з загальною методикою А даючи вказану в заголовку сполуку (1г, 59%) як блідо-жовте масло. Приклад 3: Диметил-(4-(4-[3-(2-метилпіролідин-1-іл)пропокси]феніл)тетрагідропіран-4ілметил)-амін 4-(4-Диметиламінометил-тетрагідропіран-4іл)фенол (500мг, 2,13ммоль), 1-(3-хлорпропіл)-2метил-піролідин (344мг, 2,13ммоль), ДМФА (10мл) і K2CO3 (1,18г, 8,52ммоль) взаємодіяли разом згідно з загальною методикою В. Виділений матеріал піддавали хроматографії на силікагелі, елюент 95:4:1 (ДХМ, MeOH, NH 3), одержуючи вказану в заголовку сполуку як жовте масло (120мг, 16%). 1 H ЯМР (400МГц, CDCI3) δ 7,20 (д, 2Н), 6,87 (д, 2Н), 4,08-3,96 (м, 2Н), 3,75 (дт, 2Н), 3,55 (тд, 2Н), 3,18 (тд, 1Н), 2,98 (м, 1Н), 2,40 (с, 2Н), 2,29 (м, 1Н), 2,20 (м, 1Н), 2,16-1,62 (м, 10Н), 1,96(с, 6Н), 1,42(м, 1Н), 1,09 (д, 3H). Проміжна сполука 8: 1-(3-Хлорпропіл)-2.6-цисдиметил-піперидин Стадія 1: 2,6-цис-Диметил-піперидин (1,0г, 8,83ммоль), K2CO3 (1,52г, 1,25ек.) і 3-бромпропанол (6,14г, 44,2ммоль, 4об) взаємодіяли разом при 100°C протягом 2 годин. Реакцію залишали охолоджува 52 тись до кімнатної температури, розводили ДХМ (20мл) і гасили 2М розчином HCI (20мл). Водний шар екстрагували ДХМ (2 х 20мл) і підлуговували до рН14 2М розчином NaOH (~15мл). Водний шар екстрагували ДХМ (3´20мл).об'єднані ДХМ шари сушили над MgSO4, фільтрували промивали ДХМ і концентрували у вакуумі одержуючи 1-(пропан-1'ол)-2,6-цис-диметил-піперидин (1,22г, 81%) як блідо-жовте масло. Стадія 2: 1-(Пропан-1'-ол)-2,6-цис-диметил-піперидин (1,22г, 7,12ммоль) розчиняли в ДХМ (24мл) і охолоджували до 0-5°C в атмосфері N2. По краплям додавали тюнілхлорид (1,04мл, 14,25ммоль). Реакцію залишали нагріватись до кімнатної температури і перемішували протягом 30хв. Реакцію гасили 2М розчином HCI (25мл). Водний шар екстрагували ДХМ (25мл) і підлуговували до рН14 5М розчином NaOH (~25мл). Водний шар екстрагували TBME (3´25мл).об'єднані органічні шари сушили над MgSO 4, фільтрували промивали TBME і концентрували у вакуумі одержуючи вказану в заголовку сполуку (1,26г, 93%) як жовте масло. Приклад 4: (4-{4-[3-(2,6-Диметилпіперидин-1іл)пропокси]феніл)тетрагідропіран-4ілметил)диметиламін 4-(4-Диметиламінометил-тетрагідропіран-4іл)фенол (500мг, 2,13ммоль), 1-(3-хлорпропіл)-2,6цис-диметил-піперидин (410мг, 2,13ммоль), ДМФА (10мл) і K2CO3 (1,18г, 8,52ммоль) взаємодіяли разом згідно з загальною методикою В. Виділений матеріал піддавали хроматографії на силікагелі, елюент 95:4.1 (ДХМ, MeOH, NH3), одержуючи вказану в заголовку сполуку як жовте масло (280мг, 33,9%). 1 H ЯМР (400МГц, CDCI3) δ 7,20 (д, 2Н), 6,85 (д, 2Н), 3,93 (т, 2Н), 3,75 (дт, 2Н), 3,55 (тд, 2Н), 2,95 (т, 2Н), 2,51-2,36 (м, 2Н), 2,40 (с, 2Н), 2,14-2,04 (м, 2Н), 1,96 (с, 6Н), 1,93-1,82 (м, 4Н), 1,74-1,51 (м, 3H), 1,41-1,21 (м, 3H), 1,13 (д, 6Н). Проміжна сполука 9: 4-(3-Хлорпропіл)тіоморфолін Тіоморфолін (5г, 49ммоль), ацетон (15мл, 3об), 5М розчин NaOH (11,8мл) і 1-бром-3хлорпропан (11,6г, 73,5ммоль, 1,5ек.) взаємодіяли разом згідно з загальною методикою А даючи вказану в заголовку сполуку (8,5г, 96%) як блідожовте масло. Приклад 5: Диметил-{4-[4-(3-тіоморфолін-4ілпропокси)феніл]тетрагідропіран-4-ілметил}амін 4-(4-Диметиламінометил-тетрагідропіран-4іл)фенол (1000мг, 4,25ммоль), 4-(3-хлорпропіл) 53 84748 тіоморфолін (764мг, 2,13ммоль), ДМФА (20мл), і K2CO3 (2,34г, 17ммоль) взаємодіяли разом згідно з загальною методикою В. Виділений матеріал піддавали хроматографії на силікагелі, елюент ДXM:MeOH:NH3 (95:5:1), одержуючи вказану в заголовку сполуку (320мг, 20%). 1 H ЯМР (400МГц, CDCI3) δ 7,20 (д, 2Н), 6,86 (д, 2Н), 3,99 (т, 2Н), 3,75 (дт, 2Н), 3,55 (тд, 2Н), 2,792,64(м, 8Н), 2,55 (т, 2Н), 2,40 (с, 2Н), 2,16-2,04 (м, 2Н), 2,01-1,82 (м, 4Н), 1,97 (c, 6Н). Приклад 6: Диметил-(4-(4-[3-(1оксотіоморфолін-4-іл)пропокси]феніл)тетрагідропіран-4-ілметил)амін Диметил-{4-[4-(3-тіоморфолін-4ілпропокси)феніл]тетрагідропіран-4-ілметил}амін (300мг, 0,792ммоль) і ТФО (0,99мл) охолоджували до 0-5°C і додавали трифторпероцтову кислоту (4М, 0,77мл) [4М розчин одержували додаванням 27,5% H2O2 (0,94мл) до ТФО (1,56мл)] і реакцію перемішували протягом шести годин при 0-5°С. Суміш розводили ДХМ (6мл), підлуговували NaOH (2М, 8мл) і екстрагували ДХМ (2´20мл). ДХМ екстракти сушили над MgSO4, фільтрували і концентрували у вакуумі при 35°C. Очищали хроматографією на силікагелі, елюент ДХМ:МеОН:NН3 (96:4:1), одержуючи вказану в заголовку сполуку (200мг, 61%) як білу тверду речовину. 1 H ЯМР (400МГц, CDCI3) δ 7,21 (д, 2Н), 6,86 (д, 2Н), 4,01 (т, 2Н), 3,75 (дт, 2Н), 3,55 (тд, 2Н), 3,153,02 (м, 2Н), 2,93-2,79 (м, 4Н), 2,72 (дт, 2Н), 2,64 (т, 2Н), 2,40 (с, 2Н), 2,16-1,82 (м, 6Н), 1,97(с, 6Н). Приклад 7: (4-{4-[3-(1,1-Діоксо-тіоморфолін-4іл)пропокси]феніл}тетрагідропіран-4ілметил)диметиламін Диметил-{4-[4-(3-тіоморфолін-4ілпропокси)феніл]тетрагідропіран-4-ілметил}амін (300мг, 0,792ммоль) і ТФО (0,99мл) охолоджували до 0-5°С і додавали трифторпероцтову кислоту (4М, 0,77мл) і реакцію залишали нагріватись до кімнатної температури протягом ночі. Суміш розводили ДХМ (6мл), підлуговували NaOH (2М, 8мл) і екстрагували ДХМ (2 ´20мл). ДХМ екстракти сушили над MgSO 4, фільтрували і концентрували у вакуумі при 35°C. Очищали хроматографією на силікагелі, елюент ДXM:MeOH:NH3 (96:4:1), одержуючи вказану в заголовку сполуку (151мг, 46%) як білу тверду речовину. 1 H ЯМР (400МГц, CDCI3) δ 7,22 (д, 2Н), 6,85 (д, 2Н), 4,01 (т, 2Н), 3,75 (дт, 2Н), 3,55 (тд, 2Н), 3,102,97 (м, 8Н), 2,72 (т, 2Н), 2,40 (с, 2Н), 2,14-1,82 (м, 54 6Н), 1,97 (с, 6Н). Проміжна сполука 10: 1-(3Хлорпропіл)піперидин-4-ол 4-Гідроксипіперидин (3г, 30ммоль), ацетон (60мл, 20об), 5М розчин NaOH (7,2мл) і 1-бром-3хлорпропан (14,2г, 90ммоль, 3ек.) взаємодіяли разом згідно з загальною методикою А даючи вказану в заголовку сполуку (1,5г, 28%) як блідожовте масло. Приклад 8: 1-{3-[4-(4-Диметиламінометилтетрагідропіран-4-іл)фенікси]пропіл}-піперидин-4ол 4-(4-Диметиламінометил-тетрагідропіран-4іл)фенол (500мг, 2,13ммоль), 1-(3хлорпропіл)піперидин-4-ол (378мг, 2,13ммоль), ДМФА (10мл) і K2CO3 (1,18г, 8,52ммоль) взаємодіяли разом згідно з загальною методикою В. Виділений матеріал розчиняли в EtOAc (30мл), промивали NaOH (2М, 2´20мл) і водою (25мл), сушили над MgSO4 фільтрували і концентрували у вакуумі при 35°C одержуючи вказану в заголовку сполуку (411мг, 51%). 1 H ЯМР (400МГц, CDCI3) δ 7,20 (д, 2Н), 6,86 (д, 2Н), 4,00 (т, 2Н), 3,80-3,65 (м, 3H), 3,55 (тд, 2Н), 2,85-2,73 (м, 2Н), 2,52 (т, 2Н), 2,40 (с, 2Н), 2,221,82 (м, 10Н), 1,97 (с, 6Н), 1,66-1,54(м, 2Н), 1,52 (ш с, 1Н). Проміжна сполука 11: 1-(3-Хлорпропіл)-4метокси-піперидин 4-Метокси-піперидин (1,5г, 13ммоль), ацетон (30мл, 20об), 5М розчин NaOH (3,13мл) і 1-бром-3хлорпропан (6,14г, 39ммоль, 3ек.) взаємодіяли разом згідно з загальною методикою А даючи вказану в заголовку сполуку (1,5г, 60%) як блідожовте масло. Приклад 9: (4-{4-[3-(4-Метокси-піперидин-1іл)пропокси]феніл}тетрагідропіран-4ілметил)диметиламін 4-(4-Диметиламінометил-тетрагідропіран-4іл)фенол (500мг, 2,13ммоль), 1-(3-хлорпропіл)-4метокси-піперидин (410мг, 2,13ммоль), ДМФА (10мл) і K2CO3 (1,18г, 8,52ммоль) взаємодіяли разом згідно з загальною методикою В. Виділений матеріал піддавали хроматографії на силікагелі, елюент 95:4:1 (ДХМ:MeOH:NH3), одержуючи вказану в заголовку сполуку як жовте масло (415мг, 50%). 1 H ЯМР (400МГц, CDCI3) δ 7,20 (д, 2Н), 6,86 (д, 2Н), 4,00 (т, 2Н), 3,75 (дт, 2Н), 3,55 (тд, 2Н), 3,34 (с, 3H), 3,22 (м, 1Н), 2,83-2,71 (м, 2Н), 2,51 (т, 2H), 2,40 (с, 2H), 2,23-1,81 (м, 10Н), 1,97 (с, 6Н), 1,671,53 (м, 2Н). 55 84748 Проміжна сполука 12: 2-[1-(3Хлорпропіл)піперидин-4-іл]етанол 4-Піперидинетанол (0,9г, 7,5ммоль), ацетон (18мл, 20об), 5М розчин NaOH (1,8мл) і 1-бром-3хлорпропан (3,54г, 22,5ммоль, 3ек.) взаємодіяли разом згідно з загальною методикою А даючи вказану в заголовку сполуку (0,6г, 37%) як оранжеве масло. Приклад10: 2-(1-{3-[4-(4Диметиламінометилтетрагідропіран-4іл)фенокси]пропіл}піперидин-4-іл)етанол 4-(4-Диметиламінометил-тетрагідропіран-4іл)фенол (288мг, 1,22ммоль), 2-[1-(3хлорпропіл)піперидин-4-іл]етанол (252мг, 1,22ммоль), ДМФА (8мл) і K2CO 3 (674мг, 4,88ммоль) взаємодіяли разом згідно з загальною методикою В. Очищали хроматографією на силікагелі, елюент ДХМ:МеОН:NН3 (96:4:1), одержуючи вказану в заголовку сполук у (180мг, 36%) як майже білу тверду речовину. 1 H ЯМР (400МГц, CDCI3) δ 7,20 (д, 2Н), 6,86 (д, 2Н), 3,99 (т, 2Н), 3,75 (дт, 2Н), 3,70 (т, 2Н), 3,55 (тд, 2Н), 2,98-2,88 (м, 2Н), 2,49 (т, 2Н), 2,40 (с, 2Н), 2,14-1,82 (м, 6Н), 1,97 (с, 6Н), 1,75-1,15(м, 10Н). Проміжна сполука 13: 1-(3-Хлорпропіл)-4-(2метоксиетил)піперидин Стадія 1 N-Вос-4-(2-гідрокси-етил)піперидин (5г, 21,8ммоль) в ТГФ (25мл) додавали до суспензії NaH (1,47г, 43,7ммоль) в ТГФ (75мл) при 0°С в атмосфері N2 Реакцію перемішували протягом 1 години при 0°C і повільно додавали MeI (2,72мл, 43,7ммоль). Реакцію залишали нагріватись до кімнатної температури і перемішували протягом ночі. Реакцію гасили водою (100мл) і екстрагували ДХМ (3´100мл).об'єднані ДХМ шари сушили над MgSO4 , фільтрували, промивали ДХМ і концентрували у вакуумі. Неочищений продукт реакції (7,5г)обробляли 3М розчином HCI в EtOH (150мл) протягом 12 годин. Реакцію концентрували у вакуумі і азеотропували з толуолом (2´150мл), одержуючи 4-(2-метоксиетил)піперидину гідрохлорид (3,5г, 89%) як блідо-жовту тверду речовину. Стадія 2: 4-(2-Метоксиетил)піперидину гідрохлорид (1,5г, 8,4ммоль), ацетон (30мл, 20об), 5М розчин NaOH (6,03мл, 3,6ек.) і 1-бром-3-хлорпропан (3,96г, 25,1ммоль, 3ек.) взаємодіяли разом згідно з загальною методикою А даючи вказану в заголовку сполуку (1,6г, 88%) як блідо-жовте масло. Приклад 11 [4-(4-{3-[4-(2Метоксиетил)піперидин-1-іл]пропокси}феніл)тетрагідропіран-4-ілметил]-диметиламін 56 4-(4-Диметиламінометил-тетрагідропіран-4іл)фенол (500мг, 2,13ммоль), 1-(3-хлорпропіл)-4(2-метоксиетил)піперидин (466мг, 2,13ммоль), ДМФА (10мл) і K2CO3 (1,18г, 8,52ммоль) взаємодіяли разом згідно з загальною методикою В Очищали хроматографією на силікагелі, елюент ДХМ:MeOH:NH3 (96:4:1), одержуючи вказану в заголовку сполуку (409мг, 46%) як жовте масло. 1 H ЯМР (400МГц, CDCI3) δ 7,20 (д, 2Н), 6,86 (д, 2Н), 3,99 (т, 2Н), 3,75 (дт, 2Н), 3,55 (тд, 2Н), 3,41 (т, 2Н), 3,33 (с, 3H), 2,97-2,86 (м, 2Н), 2,49 (т, 2H), 2,40 (с, 2H), 2,15-1,78 (м, 8Н), 1,97(с, 6Н), 1,74-1,17(м, 7Н). Проміжна сполука 14: 1-(3Хлорпропіл)піперидин-4-карбоновоі кислоти амід Піперидин-4-карбоновоі кислоти амід (0,5г, 3,90ммоль), ацетон (1,5мл, 3об), 5М розчин NaOH (1,20мл, 1,2ек.) і 1-бром-3-хлорпропан (0,50мл, 5,04ммоль, 1ек.) взаємодіяли разом згідно з загальною методикою А даючи вказану в заголовку сполуку (0,16г, 20%) як блідо-жовте масло. Приклад 12: 1-{3-[4-(4-Диметиламінометилтетрагідропіран-4-іл)фенокси]пропіл}-піперидин-4карбоновоі кислоти амід 4-(4-Диметиламінометил-тетрагідропіран-4іл)фенол (500мг, 2,13ммоль), 1-(3хлорпропіл)піперидин-4-карбоновоі кислоти амід (436мг, 2,13ммоль) ДМФА (10мл) і K2CO3 (1,18г, 8,52ммоль) взаємодіяли разом згідно з загальною методикою В. Виділений матеріал піддавали хроматографії на силікагелі, елюент 95:4:1 (ДХМ: MeOH:NH3), одержуючи вказану в заголовку сполуку як білу тверду речовину (175мг, 20%). 1 H ЯМР (400МГц, CDCI3) δ 7,21 (д, 2Н), 6,86 (д, 2Н), 5,44 (ш с, 1Н), 5,25 (ш с, 1Н), 4,00 (т, 2Н), 3,75 (дт, 2Н), 3,55 (тд, 2Н), 3,03-2,93 (м, 2Н), 2,51 (т, 2Н), 2,40 (с, 2Н), 2,22-1,66 (м, 13Н), 1,97 (с, 6Н). Проміжна сполука 15: 4-(3-Хлорпропіл)піперазин-1-карбонової кислоти етиловий естер Піперазин-1-карбонової кислоти етиловий естер (3,0г, 18,9ммоль), K2CO3 (2,8г, 1,1ек.), ДМФА (30мл, 10об) і 1-бром-3-хлорпропан (1,8мл, 18,9ммоль, 1ек.) взаємодіяли разом при кімнатній температурі протягом ночі. Реакцію гасили водою (100мл) і екстрагували ДХМ (3´50мл).об'єднані ДХМ екстракти сушили над MgSO 4, фільтр ували промивали ДХМ і концентрували у вакуумі одержуючи вказану в заголовку сполуку (3,1г, 70%) як блідо-жовте масло. Приклад 13: {3-[4-(4Диметиламінометилтетрагідропіран-4 57 84748 58 іл)фенокси]пропіл}-піперазин-1-карбонової кислоти етиловий естер 4-(4-Диметиламінометил-тетрагідропіран-4іл)фенол (500мг, 2,13ммоль), 4-(3-хлорпропіл)піперазин-1-карбонової кислоти етиловий естер (499мг, 2,13ммоль), ДМФА (10мл) і K2CO3 (1,18г, 8,52ммоль) взаємодіяли разом згідно з загальною методикою В. Очищали хроматографією на силікагелі, елюент (10%МеОН в ДХМ) вказану в заголовку сполуку (276мг, 26%). 1 H ЯМР (400МГц, CDCI3) δ 7,21 (д, 2Н), 6,86 (д, 2Н), 4,14 (к, 2Н), 4,01 (т, 2Н), 3,75 (дт, 2Н), 3,603,42 (м, 6Н), 2,54 (т, 2Н), 2,47-2,36 (м, 4Н), 2,40 (с, 2Н), 2,16-1,82 (м, 6Н), 1,97 (с, 6Н), 1,26 (т, 3H). Проміжна сполука 16: (3-Хлорпропіл)діетиламін Діетиламін (7,27мл, 70ммоль), ацетон (15мл, 3об), 5М розчин NaOH (16,8мл, 1,2ек.) і 1-бром-3хлорпропан (16,5г, 105ммоль, 1,5ек.) взаємодіяли разом згідно з загальною методикою А даючи вказану в заголовку сполуку (6,2г, 59%) як безбарвне масло. Приклад 14: {3-[4-(4Диметиламінометилтетрагідропіран-4іл)фенокси]пропіл}-діетиламін 4-(4-Диметиламінометил-тетрагідропіран-4іл)фенол (500мг, 2,13ммоль), (3-хлорпропіл)діетиламін (319мг, 2,13ммоль), ДМФА (10мл) і K2CO3 (1,18г, 8,52ммоль) взаємодіяли разом згідно з загальною методикою В. Очищали хроматографією на силікагелі, елюент (3%ЕtOН:1%NH3 в ДХМ) одержуючи вказану в заголовку сполуку як блідо-жовте прозоре масло (160мг, 22%). 1 H ЯМР (400МГц, CDCI3) δ 7,20 (д, 2Н), 6,86 (д, 2Н), 4,00 (т, 2Н), 3,75 (дт, 2Н), 3,55 (тд, 2Н), 2,61 (т, 2Н), 2,54 (к, 4Н), 2,40 (с, 2Н), 2,15-1,82 (м, 6Н), 1,97 (с, 6Н), 1,02 (т, 6Н). Проміжна сполука 17: 2-[(3Хлорпропіл)етиламіно]етанол 2-Етиламіноетанол (6,2г, 70ммоль), ацетон (18мл, 3об), 5М розчин NaOH (16,8мл, 1,2ек.) і 1бром-3-хлорпропан (16,5г, 105ммоль, 1,5ек.) взаємодіяли разом згідно з загальною методикою А даючи вказану в заголовку сполуку (4,5г, 39%) як безбарвне масло. Приклад 15: 2-({3-[4-(4Диметиламінометилтетрагідропіран-4іл)фенокси]пропіл}етиламіно)етанол 4-(4-Диметиламінометил-тетрагідропіран-4іл)фенол (500мг, 2,13ммоль), 2-[(3хлорпропіл)етиламіно]етанол (353мг, 2,13ммоль), ДМФА (10мл) і K2CO3 (1,18г, 8,52ммоль) взаємодіяли разом згідно з загальною методикою В. Виділенийматеріал піддавали хроматографії на силікагелі, елюент 95:4:1 (ДХМ:MeOH:NH3), одержуючи вказану в заголовку сполуку як білу тверду речовину (150мг, 19%). 1 H ЯМР (400МГц, CDCI3) δ 7,21 (д, 2Н), 6,86 (д, 2Н), 4,00 (т, 2Н), 3,75 (дт, 2Н), 3,60-3,49 (м, 4Н), 2,68 (т, 2Н), 2,62 (т, 2Н), 2,59 (к, 2Н), 2,40 (с, 2Н), 2,14-1,82 (м, 6Н), 1,97 (с, 6Н), 1,62 (ш с, 1Н), 1,03 (т, 3H). Проміжна сполука 18: (3-Хлорпропіл)ізопропіл-метиламін Ізопропілметиламін (4г, 56ммоль), ацетон (12мл, 3об), 5М розчин NaOH (13,44мл, 1,2ек.) і 1бром-3-хлорпропан (13,22г, 84ммоль, 1,5ек.) взаємодіяли разом згідно з загальною методикою А даючи вказану в заголовку сполуку (4,8г, 66%) як безбарвне масло. Приклад 16: {3-[4-(4Диметиламінометилтетрагідропіран-4іл)фенокси]пропіл}ізопропілметиламін 4-(4-Диметиламінометил-тетрагідропіран-4іл)фенол (500мг, 2,13ммоль), (3-хлорпропіл)ізопропіл-метиламін (318мг, 2,13ммоль), ДМФА (10мл) і K2CO3 (1,18г, 8,52ммоль) взаємодіяли разом згідно з загальною методикою В. Очищали хроматографією на силікагелі, елюент ДХМ:MeOH:NH3 (96:3:1), одержуючи вказану в заголовку сполуку (200мг, 43%) як білу тверду речовину. 1 H ЯМР (400МГц, CDCI3) δ 7,20 (д, 2H), 6,87 (д, 2H), 4,00 (т, 2H), 3,75 (дт, 2H), 3,55 (тд, 2H), 2,83 (сеп, 1H), 2,55 (т, 2H), 2,40 (с, 2H), 2,22 (с, 3H), 2,14-2,05 (м, 2H), 1,96 (с, 6H), 2,00-1,82 (м, 4H), 1,00 (д, 6H). Проміжна сполука 19: 1-(2-хлоретил)піролідин Піролідин (10,4г, 0,15моль), ацетон (200мл), 5М розчин NaOH (35мл) і 1-бром-2-хлоретан (62,9г, 0,44моль) взаємодіяли разом згідно з загальною методикою А Неочищену суміш очищали колонковою хроматографією, елюювали етилацетатом, одержуючи вказану в заголовку сполуку (2,0г, 10%) як блідо-жовте масло. Приклад 17: Диметил-{4-[4-(2-піролідин-1ілетокси)феніл]тетрагідропіран-4-ілметил}амін 59 84748 4-(4-Диметиламінометил-тетрагідропіран-4іл)фенол (389мг, 1,65ммоль), 1-(2-хлоретил)піролідин (210мг, 1,57ммоль), ДМФА (4,5мл) і K2CO3 (885г, 6,40ммоль) нагрівали при 130°С протягом 30 хвилин. Суміш охолоджували до кімнатної температури; додавали воду (9мл) і суміш екстрагували EtOAc (3´4,5мл). Органічну фазу промивали розсолом (10мл), розчином NaOH (2М, 10мл) і водою (10мл). Органічний шар сушили над MgSO4 , фільтрували і концентрували у вакуумі при 35°С і залишок піддавали хроматографії на силікагелі, елюювали ДХМ:МеОН:NН3 (98:1:1), одержуючи вказану в заголовку сполуку як білу тверду речовину (150мг, 27%). 1 H ЯМР (400МГц, CDCI3) δ 7,21 (д, 2Н), 6,89 (д, 2Н), 4,10 (т, 2Н), 3,75 (дт, 2Н), 3,55 (тд, 2Н), 2,89 (т, 2Н), 2,67-2,58 (м, 4Н), 2,40 (с, 2Н), 2,13-2,05 (м, 2Н), 1,97 (с, 6Н), 1,88 (ддд, 2Н), 1,84-1,77 (м, 4Н). Проміжна сполука 20: 1-(3-Хлор-2-метилпропіл)піролідин Піролідин (3,0г, 42ммоль), ацетон (60мл), 5М розчин NaOH (10мл) і 1-бром-3-хлор-2-метилпропан (21,7г, 0,13моль) взаємодіяли разом згідно з загальною методикою А даючи вказану в заголовку сполуку (3,9г, 58%) як блідо-жовте масло. Приклад 18: Диметил-{4-[4-(2-метил-3піролідин-1-іл-пропокси)феніл]тетрагідропіран-4ілметил}-амін 4-(4-Диметиламінометил-тетрагідропіран-4іл)фенол (0,91г, 3,87ммоль), 1-(3-хлор-2-метилпропіл)піролідин (500мг, 3,10ммоль), ДМФА (5мл) і K2CO3 (2,14г, 15,50ммоль) взаємодіяли разом згідно з загальною методикою В. Органічну фазу промивали 2М NaOH (3´20мл), водою (2´20мл), сушили над MgSO4 фільтр ували і концентрували у вакуумі при 35°С. Неочищений продукт піддавали хроматографії на силікагелі, елюювали ДХМ:МеОН:NH3 (97:2:1), одержуючи вказану в заголовку сполуку (464мг, 42%) як блідо-жовте масло. 1 H ЯМР (400МГц, CDCI3) δ 7,20 (д, 2Н), 6,88 (д, 2Н), 4,00 (дд, 1Н), 3,80-3,70 (м, 3H), 3,55 (тд, 2Н), 2,59-2,43 (м, 5Н), 2,40 (с, 2Н), 2,33 (дд, 1Н), 2,212,04 (м, 3H), 1,97 (с, 6Н), 1,88 (ддд, 2Н), 1,82-1,70 (м, 4Н), 1,08 (д, 3H). Проміжна сполука 21: Метансульфонової кислоти 1-ізопропілпіперидин-4-іловий естер Стадія 1: 4-Гідроксипіперидин (2,13г, 21,1ммоль), K2CO3 (5,83г, 2ек.), 2-бромпропан (11,2г, 91ммоль, 4,3ек.) і MeOH (21,3мл) кип'ятили із зворотнім холодильником разом протягом ночі Реакцію залишали охолоджуватись до кімнатної температури і гасили 2М розчином HCI (40мл) і екстрагували TBME 60 (40мл). Водний шар підлуговували до рН14 2М розчином NaOH і екстрагували ДХМ (9´50мл).об'єднані органічні екстракти сушили над MgSO4 , фільтрували, промивали ДХМ і концентрували у вакуумі одержуючи 1-ізопропіл-4гідроксипіперидин (2,41г, 80%) як блідо-жовте масло. Стадія 2: 1-Ізопропіл-4-гідроксипіперидин (1г, 6,98ммоль), ДХМ (10мл) і триетиламін (1,08мл, 7,68ммоль) охолоджували до 0-5°C і по краплям в атмосфері N2 додавали мезилхлорид (0,54мл, 6,98ммоль). Реакцію залишали нагріватись до кімнатної температури і перемішували протягом 1 години. Реакцію гасили нас. NaHCO3 (20мл) і водну фазу екстрагували ДХМ (2´5мл).об'єднані органічні екстракти сушили над MgSO4, фільтрували, промивали ДХМ і концентрували у вакуумі одержуючи вказану в заголовку сполуку (1,55г, 100%) як блідо-жовте масло. Приклад 19: {4-[4-(1-Ізопропілпіперидин-4ілокси)феніл]тетрагідропіран-4ілметил}диметиламін 4-(4-Диметиламінометил-тетрагідропіран-4іл)фенол (532мг, 2,26ммоль) в ДМФА (2мл) до розчину додавали NaH (100мг, 2,5ммоль) в ДМФА (2мл) при кімнатній температурі в атмосфері N 2. Реакцію перемішували протягом 1г і повільно додавали розчин метансульфонової кислоти 1ізопропіл-піперидин-4-ілового естеру (400мг, 1,81ммоль) в ДМФА (1,3мл). Реакцію нагрівали при 75°C і перемішували протягом 6г. Реакцію залишали охолоджуватись до кімнатної температури і розводили TBME (20мл), водою (10мл) і 5М розчином NaOH (10мл). Органічний шар промивали 2,5М NaOH (2´20мл), розсолом (2´20мл), сушили над MgSO4, фільтрували і концентрували у вакуумі. Неочищений продукт реакції очищали колонковою хроматографією, елюювали ДXM:MeOH:NH3 (98:1:1), одержуючи вказану в заголовку сполуку як білу кристалічну речовину (113мг, 17%). 1 H ЯМР (400МГц, CDCl3) δ 7,20 (д, 2Н), 6,87 (д, 2Н), 4,27 (м, 1Н), 3,75 (дт, 2Н), 3,55 (тд, 2Н), 2,852,68 (м, 3H), 2,45-2,32 (м, 2Н), 2,40 (с, 2Н), 2,141,94 (м, 4H), 1,96 (с, 6H), 1,93-1,75 (м, 4Н), 1,06 (д, 6Н). Проміжна сполука 22: Метансульфонової кислоти 1-циклопентил-піперидин-4-іловий естер Стадія 1: 4-Гідроксипіперидин (2,08г, 21,2ммоль), K2CO3 (5,86г, 2ек.), циклопентилбромід (11,51г, 77,6ммоль, 3,7ек.) і MeOH (20,8мл) кип'ятили із зворотнім холодильником разом протягом ночі. Реакцію залишали охолоджуватись до кімнатної температури і гасили 2М розчином HCI (40мл) і
ДивитисяДодаткова інформація
Назва патенту англійською3- or 4-monosubstituted phenol derivatives useful as h3 ligands
Автори англійськоюBernardelli Patrick, Andrew Michael Cronin, Denis Alexis, Denton Stiven Martin, Jacobelli Henry, Kemp Mark Ian, Lorthiois Edwige, Rousseau Fiona, Serradeil-Civit Delphine, Vergne Fabrice
Назва патенту російською3- или 4-монозамещенные фенол и тиофенолпроизводные, полезные как н3 лиганды
Автори російськоюБернарделли Патрик, Кронин Эндрю Майкл, Денис Алексис, Дентон Стивен Мартин, Якобелли Анри, Кемп Марк Ян, Лортиуа Эдвиг, Руссо Фиона, Серрадеил-Сиви Дельфин, Вернь Фабрис
МПК / Мітки
МПК: C07D 417/04, C07D 405/14, C07D 417/06, C07D 309/06, C07D 405/06, C07D 405/12, A61P 25/06, C07D 309/08, A61K 31/55, C07D 405/04, C07D 295/14, C07D 295/12
Мітки: тіофенолпохідні, фенол, корисні, ліганди, 4-монозаміщені
Код посилання
<a href="https://ua.patents.su/102-84748-3-abo-4-monozamishheni-fenol-i-tiofenolpokhidni-korisni-yak-n3-ligandi.html" target="_blank" rel="follow" title="База патентів України">3- або 4-монозаміщені фенол і тіофенолпохідні, корисні як н3 ліганди</a>
Попередній патент: Трифазний трансформатор
Наступний патент: Антагоністи рецептора pgd2 для лікування запальних захворювань
Випадковий патент: Високотемпературне пластичне мастило (варіанти)












