Азабіциклічні похідні піридилоксиметилу і бензізоксазолу
Номер патенту: 78437
Опубліковано: 15.03.2007
Автори: Лодеккі Бішоп, Брайт Джен Майкл, Броудні Майкл Арон
Формула / Реферат
1. Сполука формули
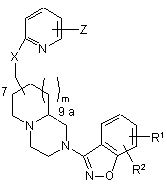 І
І
або її (R) або (S) енантіомер, або її цис- або трансізомер, або її фармацевтично прийнятна сіль, сольват або пролікарська форма або будь-яка з вищезгаданих, в якій m є О або 1; Z є
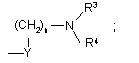 ,
,
Х є кисень;
Y є метилен, коли n є 0;
R1 і R2 є кожен, незалежно, водень, галоген або (С1-С6)алкіл, (С1-С6)алкокси або (С1-С6)алкоксі(С1-С6)алкіл, будь-яка з груп може бути незаміщена або заміщена одним або декількома галогенами;
R3 і R4 є кожен, незалежно, водень, (С1-С6)алкіл, (С3-С7)циклоалкіл або 5-6-членний гетероцикліл, будь-яка з груп може бути незаміщена або заміщена однією або декількома будь-якими наступними: (С1-С4)алкіл, (С3-С7)циклоалкіл, (С1-С4)алкокси, (С6-С10)арил, 5-6-членний гетероцикліл, аміно, галоген або гідрокси; або
R3 і R4 разом з атомом азоту, до якого вони приєднані, утворюють:
(і) 3-7-членне, необов'язково, ненасичене моноциклічне кільце; або
(іі) 4-10-членне, необов'язково, ненасичене поліциклічне кільце, де згадане моноциклічне або поліциклічне кільце, необов'язково, має один або два додаткові гетероатоми, що вибирають з азоту, кисню і сірки,
де будь-які згадані кільця (і) або (іі) можуть бути незаміщеними або заміщеними одним або декількома (С1-С4)алкілами, (С1-С4)алкокси, (С1-С4)алкоксі(С1-С4)алкілами, (С3-С7)циклоалкілами, (С6-С10)арилами, (С7-С13)аралкілами, 5-10-членними гетероарилами, гідрокси, аміно, ціано або галогенами; за умови, що в будь-якому кільці, утвореному NR3R4:
(а) в кільці не більше ніж один атом кисню;
(б) гідрокси, алкокси, ціано, аміно або алкіл аміногрупи є приєднані безпосередньо до будь-якого атома азоту; і
(в) відсутній вуглець кільця, що зв’язаний подвійним зв’язком з іншим вуглецем кільця і не є частиною ароматичної кільцевої системи, і який може бути зв’язаний з атомом кисню або азоту кільця {див. стор. 9, 5 абзац}.
2. Сполука згідно з пунктом 1, що має формулу
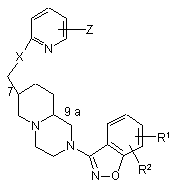 ,
,
в якій Z є
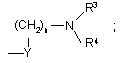 ,
,
Х є кисень; Y є метилен;
n є 0; і
R1 і R2 кожен є водень або галоген; і
R3 і R4 разом з атомом азоту, до якого вони приєднані, утворюють
і) насичене 3-7-членне моноциклічне кільце, згадане кільце і) є незаміщеним або заміщеним однією або декількома (С1-С4)алкілами, (С1-С4)алкоксі(С1-С4)алкілами або гідроксигрупами {див. стор. 8, останній абзац}.
3. Сполука згідно з пунктом 1, в якій Z є
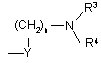 ,
,
в якій Y є метилен; Х є кисень; n є 0; R1 є водень; R2 є водень; і R3 і R4 разом з атомом азоту, до якого вони приєднані, утворюють і) насичене неароматичне 3-7-членне моноциклічне кільце, згадане кільце і) є незаміщеним або заміщеним одним або декількома (С1-С4)алкілами, (С1-С4)алкоксі(С1-С4)алкілами або гідроксигрупами.
4. Сполука згідно з пунктом 1, в якій Z є
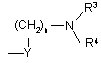 ,
,
в якій Y є метилен; Х є кисень; n є 0; R1 є водень; R2 є водень; і R3 і R4 разом з атомом азоту, до якого вони приєднані утворюють ііі) незаміщене 5-6-членне гетероциклічне кільце, де гетероциклічне кільце, на додаток до атома азоту, до якого приєднані R3 і R4, має додатковий атом азоту, атом сірки або атом кисню.
5. Сполука згідно з пунктом 1 або 2, в якій R2 є галоген; і R3 і R4 разом з атомом азоту, до якого вони приєднані утворюють
(і) насичене 3-7-членне моноциклічне кільце, де моноциклічне кільце може бути незаміщеним або заміщеним одним або декількома фенілами, (С1-С3)алкілами або (C1-С4)алкоксі(С1-С4)алкілами.
6. Сполука згідно з пунктом 1, де згадану сполуку вибирають з групи, що містить:
(7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-(6-морфолін-4-ілметилпіридин-2-ілоксиметил)октагідропіридо[1,2-а]піразин;
(7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-(5-піперидин-1-ілметилпіридин-2-ілоксиметил)октагідропіридо[1,2-а]піразин;
(7R,9аS)-транс-2-(5-фторбензо[d]ізоксазол-3-іл)-7-(5-піролідин-1-ілметилпіридин-2-ілоксиметил)октагідропіридо[1,2-а]піразин;
(7R,9аS)-транс-7-(5-азетидин-1-ілметилпіридин-2-ілоксиметил)-2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин;
(7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-[5-(2-метилазиридин-1-ілметил)піридин-2-ілоксиметил]октагідропіридо[1,2-а]піразин;
(7R,9аS)-транс-2-бензо[6]ізоксазол-3-іл-7-[5-(2-метоксиметилпіролідин-1-ілметил)піридин-2-ілоксиметил]октагідропіридо[1,2-а]піразин;
(7R,9аS)-цис-7-(5-азетидин-1-ілметилпіридин-2-ілоксиметил)-2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин;
(7R,9аS)-транс-1-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]-(S)-піролідин-3-ол;
(7R,9аS)-транс-1-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]-(R)-піролідин-3-ол;
(7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-[5-(2-метилпіролідин-1-ілметил)піридин-2-ілоксиметил]октагідропіридо[1,2-а]піразину;
(7R,9аS)-транс-1-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]піперидин-4-ол;
(7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-(6-піролідин-1-ілметилпіридин-2-ілоксиметил)октагідропіридо[1,2-а]піразину;
(7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-(5-піролідин-1-ілметилпіридин-2-ілоксиметил)октагідропіридо[1,2-а]піразину;
(7R,9аS)-цис-2-бензо[d]ізоксазол-3-іл-7-(5-піролідин-1-ілметилпіридин-2-ілоксиметил)октагідропіридо[1,2-а]піразин та
(7R,9аS)-транс-1-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]-піролідин-3-ол (див. Приклад 54).
7. Сполука згідно з пунктом 6, де згадану сполуку вибирають з групи, що містить:
(7R,9аS)-транс-1-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]-піролідин-3-ол (див. Приклад 54);
(7R,9аS)-транс-7-(5-азетидин-1-ілметилпіридин-2-ілоксиметил)-2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин (див. Приклад 55);
(7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-[5-(2-метилпіролідин-1-ілметил)піридин-2-ілоксиметил]октагідропіридо[1,2-а]піразин (див. Приклад 71);
(7R,9аS)-цис-7-(5-азетидин-1-ілметилпіридин-2-ілоксиметил)-2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин (див. Приклад 77);
(7R,9аS)-транс-1-[б-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]-(R)-піролідин-3-ол (див. Приклад 86);
(7R,9аS)-транс-1-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]-(S)-піролідин-3-ол (див. Приклад 87);
(7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-(5-піролідин-1-ілметилпіридин-2-ілоксиметил)октагідропіридо[1,2-а]піразин (див. Приклад 90);
(7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-(6-піролідин-1-ілметилпіридин-2-ілоксиметил)октагідропіридо[1,2-а]піразин (див. Приклад 97);
(7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-(5-піперидин-1-ілметилпіридин-2-ілоксиметил)октагідропіридо[1,2-а]піразин (див. Приклад 101);
(7R,9аS)-цис-2-бензо[d]ізоксазол-3-іл-7-(5-піролідин-1-ілметилпіридин-2-ілоксиметил)октагідропіридо[1,2-а]піразин (див. Приклад 104).
8. Сполука згідно з пунктом 1, де згадану сполуку вибирають з групи, що містить:
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]діетиламін (див. Приклад 53);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]диметиламін (див. Приклад 68);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]циклогексилметиламін (див. Приклад 67);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]етилметиламін (див. Приклад 69);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]циклопентилметиламін (див. Приклад 58);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]-(2-метоксіетил)метиламін (див. Приклад 57);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]-трет-бутиламін (див. Приклад 63);
(7R,9аS)-цис-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]етилметиламін (див. Приклад 74);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметил]диметиламін (див. Приклад 81);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметил]бензиламін (див. Приклад 98);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметил]циклопропілметиламін (див. Приклад 48) та
(7R,9аS)-цис-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]циклопентилметиламін (див. Приклад 75).
9. Сполука згідно з пунктом 1, де згадану сполуку вибирають з групи, що містить:
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметил]-(3-метилпіридин-4-іл)амін (див. Приклад 42);
(7R,9аS)-транс-1-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметил]піролідин-3-ол (див. Приклад 80);
(7R,9аS)-цис-1-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]піролідин-(S)-3-ол (див. Приклад 89);
(7R,9аS)-цис-1-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]піролідин-(Р)-3-ол (див. Приклад 93);
(7R,9аS)-транс-2-(5-фторбензо[d]ізоксазол-3-іл)-7-(6-піролідин-1-ілметилпіридин-2-ілоксиметил)октагідропіридо[1,2-а]піразин (див. Приклад 107);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]-(2-метокси-1-метилетил)амін (див. Приклад 70);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметил]-(2-метоксіетил)метиламін (див. Приклад 79);
(7R,9аS)-цис-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]циклогексилметиламін (див. Приклад 88);
(7R,9аS)-цис-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]диметиламін (див. Приклад 73);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметил]циклогексилметиламін (див. Приклад 82);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметил]тіазол-2-іламін) (див. Приклад 41);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметил]піридин-2-іламін (див. Приклад 47);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]-(2-морфолін-4-ілетил)амін (див. Приклад 30);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметил]-(2-морфолін-4-ілетил)амін (див. Приклад 49);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметил]-піримідин-4-іламін (див. Приклад 50);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметил]-(2-піролідин-1-ілетил)амін (див. Приклад 52);
(7R,9аS)-цис-[6-(2-бензо[6]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметил]диметиламін (див. Приклад 84);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметил]-(3-метилпіридин-4-іл)амін (див. Приклад 42);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]циклопропіламін (див. Приклад 32);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]циклопропілметиламін (див. Приклад 29);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]-(тетрагідрофуран-2-ілметил)амін (див. Приклад 36);
(7R,9аS)-транс-N-[6-(2-бензо[6]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил-N,N'-диметилетан-1,2-діамін (див. Приклад 59).
10. Сполука згідно з пунктом 1, де згадану сполуку вибирають з групи, що містить:
(7R,9аS)-транс-7-[6-(2,6-диметилпіперидин-1-ілметил)піридин-2-ілоксиметил]-2-(5-фторбензо[с1]ізоксазол-3-іл)октагідропіридо[1,2-а]піразин (див. Приклад 3);
(7R,9аS)-транс-2-(5-фторбензо[d]ізоксазол-3-іл)-7-[6-(4-метилпіперазин-1-ілметил)піридин-2-ілоксиметил]октагідропіридо[1,2-а]піразин (див. Приклад 10);
(7R,9аS)-транс-2-(5-фторбензо[d]ізоксазол-3-іл)-7-(6-піперидин-1-ілметилпіридин-2-ілоксиметил)октагідропіридо[1,2-а]піразин (див. Приклад 11);
(7R,9аS)-транс-7-[6-(2,5-диметилпіролідин-1-ілметил)піридин-2-ілоксиметил]-2-(5-фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2-а]піразин (див. Приклад 14);
(7R,9аS)-транс-7-(6-азепан-1-ілметилпіридин-2-ілоксиметил)-2-(5-фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2-а]піразин (див. Приклад 18);
(7R,9aS)-транс-7-(5-азепан-1-ілметилпіридин-2-ілоксиметил)-2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин (див. Приклад 61);
(7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-(5-тіазолідин-3-ілметилпіридин-2-ілоксиметил)октагідропіридо[1,2-а]піразин (див. Приклад 65);
(7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-(5-імідазол-1-ілметилпіридин-2-ілоксиметил)октагідропіридо[1,2-а]піразин (див. Приклад 66);
(7R,9аS)-цис-2-бензо[d]ізоксазол-3-іл-7-(5-піперидин-1-ілметилпіридин-2-ілоксиметил)октагідропіридо[1,2-а]піразин (див. Приклад 72);
(7R,9аS)-цис-2-бензо[d]ізоксазол-3-іл-7-[5-(2-метилазиридин-1-ілметил)піридин-2-ілоксиметил]октагідропіридо[1,2-а]піразин (див. Приклад 78);
(7R,9аS)-транс-7-(5-азетидин-1-ілметилпіридин-2-ілоксиметил)-2-(5-фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2-а]піразин (див. Приклад 94);
(7R,9аS)-цис-2-бензо[d]ізоксазол-3-іл-7-(6-морфолін-4-ілметилпіридин-2-ілоксиметил)октагідропіридо[1,2-а]піразин (див. Приклад 105);
(7R,9аS)-цис-2-бензо[d]ізоксазол-3-іл-7-(6-піролідин-1-ілметилпіридин-2-ілоксиметил)октагідропіридо[1,2-а]піразин (див. Приклад 106);
(7R,9аS)-транс-циклогексил-{6-[2-(5-фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2-а]піразин-7-ілметокси]піридин-2-ілметил}амін (див. Приклад 1);
(7R,9аS)-транс-2-(етил-{6-[2-(5-фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2-а]піразин-7-ілметокси]піридин-2-ілметил}аміно)етанол (див. Приклад 2);
(7R,9аS)-транс-(1,2-диметилпропіл)-{6-[2-(5-фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2-а]піразин-7-ілметокси]піридин-2-ілметил}амін (див. Приклад 5);
(7R,9аS)-транс-циклопропіл-{6-[2-(5-фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2-а]піразин-7-ілметокси]піридин-2-ілметил}амін (див. Приклад 6);
(7R,9аS)-транс-циклопропілметил-[6-[2-(5-фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2-а]піразин-7-ілметокси]піридин-2-ілметил}амін (див. Приклад 7);
(7R,9аS)-транс-{6-[2-(5-фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2-а]піразин-7-ілметокси]піридин-2-ілметил}диметиламін (див. Приклад 12);
(7R,9аS)-транс-{6-[2-(5-фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2-а]піразин-7-ілметокси]піридин-2-ілметил}-(тетрагідрофуран-2-ілметил)амін (див. Приклад 13);
(7R,9аS)-транс-{6-[2-(5-фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2-а]піразин-7-ілметокси]піридин-2-ілметил}-[3-(4-метилпіперазин-1-іл)пропіл]амін (див. Приклад 16);
(7R,9аS)-транс-{6-[2-(5-фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2-а]піразин-7-ілметокси]піридин-2-ілметил}піролідин-1-іламін (див. Приклад 17);
(7R,9аS)-цис-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметил]-(2-метоксіетил)метиламін (див. Приклад 85);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]піримідин-4-іламін (див. Приклад 31);
(7R,9аS)-транс-{6-[2-(5-фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2-а]піразин-7-ілметокси]піридин-3-ілметил]диметиламін (див. Приклад 95);
(7R,9аS)-транс-етил-[6-[2-(5-фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2-а]піразин-7-ілметокси]піридин-3-ілметил}метиламін (див. Приклад 96);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметил]-(6-метоксипіридин-3-іл)амін (див. Приклад 51);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]-(5-метилпіридин-2-іл)амін (див. Приклад 25);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]-(3-метилпіридин-4-іл)амін (див. Приклад 23);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]піридин-2-іламін (див. Приклад 28);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметил-(5-метил-2Н-піразол-3-іл)амін (див. Приклад 43);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]-(6-метоксипіридин-3-іл)амін (див. Приклад 33);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил-(6-метилпіридин-2-іл)амін (див. Приклад 27);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметил]-(6-метилпіридин-2-іл)амін (див. Приклад 46);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]-(2-піролідин-1-ілетил)амін (див. Приклад 34);
(7R,9аS)-транс-2-бензо[6]ізоксазол-3-іл-7-[5-(4-метил-[1,4]діазепан-1-ілметил)піридин-2-ілоксиметил]октагідропіридо[1,2-а]піразин (див. Приклад 35);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметил]-(5-метилпіридин-2-іл)амін (див. Приклад 44);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7'-ілметокси)піридин-3-ілметил]-(3-метилізоксазол-5-іл)амін (див. Приклад 22);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметил]-(1Н-піразол-3-іл)амін (див. Приклад 45);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]тіазол-2-іламін (див. Приклад 21);
(7R,9аS)-транс-{6-[2-(5-фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2-а]піразин-7-ілметокси]піридин-2-ілметил}-(2-морфолін-4-ілетил)амін (див. Приклад 109);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]-трет-бутилметиламін (див. Приклад 64);
(7R,9аS)-транс-(4-хлорбензил)-{6-[2-(5-фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2-а]піразин-7-ілметокси]піридин-2-ілметил}амін (див. Приклад 8);
(7R,9аS)-транс46-[2-(5-фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2-а]піразин-7-ілметокси]піридин-2-ілметил}-[2-(1-метилпіролідин-2-іл)етил]амін (див. Приклад 9);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]-(3-метилізоксазол-4-іл)амін (див. Приклад 20);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]-(1Н-піразол-3-іл)амін (див. Приклад 26);
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-ілметил]-(5-метил-2Н-піразол-3-іл)амін (див. Приклад 24).
11. Сполука формули
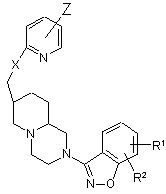
або її (R) або (S) енантіомер, або її цис- або трансізомер,
в якій Х є кисень або NR, де R є водень або (С1-С6)алкіл;
R1 і R2 є кожен, незалежно, водень, галоген або (С1-С6)алкіл, (С1-С6)алкокси або (С1-С6)алкоксі(С1-С6)алкіл, будь-яка з груп може бути незаміщена або заміщена одним або декількома галогенами; і
Z є
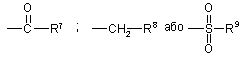 ,
,
де R7 є водень або (С1-С3)алкокси; R8 є водень, гідрокси або (С1-С3)алкокси; і R9 є (С1-С3)алкіл.
12. Сполука згідно з пунктом 7, де згадану сполуку вибирають з групи, що містить:
(7R,9аS)-транс-6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)нікотинової кислоти метиловий естер;
(7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3-іл]метанол;
(7R,9аS)-транс-метансульфонової кислоти 6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметиловий естер;
(7R,9аS)-транс-метансульфонової кислоти 6-[2-(5-фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2-а]піразин-7-ілметокси]піридин-2-ілметиловий естер;
(7R,9аS)-транс-6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-карбонової кислоти метиловий естер;
(7R,9аS)-транс-[6-(2-бензо[с1]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-іл]метанол;
(7R,9аS)-транс-{6-[2-(5-фторбензо[6]ізоксазол-3-іл)октагідропіридо[1,2-а]піразин-7-ілметокси]піридин-2-іл}метанол;
(7R,9аS)-транс-6-[2-(5-фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2-а]піразин-7-ілметокси]піридин-2-карбонової кислоти метиловий естер;
(7R,9аS)-цис-6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-карбонової кислоти метиловий естер;
(7R,9аS)-цис-[6-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-іл]метанол;
(7R,9аS)-цис-метансульфонової кислоти 6-(2-бензо[с1]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметиловий естер;
(7R,9аS)-транс-5-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-карбонової кислоти метиловий естер;
(7R,9аS)-транс-[5-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-іл]метанол і
(7R,9аS)-транс-метансульфонової кислоти 5-(2-бензо[d]ізокcaзон-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-2-ілметиловий естер.
13. Фармацевтична композиція, що містить сполуку згідно з будь-яким з пунктів 1-10 або її фармацевтично прийнятну сіль і фармацевтично прийнятний носій.
14. Спосіб лікування одного або декількох розладів центральної нервової системи, що включає введення ссавцю, який потребує такого лікування, терапевтичне ефективної
кількості сполуки згідно з будь-яким з пунктів 1-10.
15. Спосіб лікування розладу, яким є шизофренія, шизофреноподібний розлад, шизоафективний розлад, маревний розлад, речовиновикликаний психотичний розлад, психоз, розлад особистості параноїдального типу, розлад особистості шизоїдного типу, паніка, фобія, обсесивно-компульсивний розлад, стрес, генералізована тривога, розлади руху, включаючи хворобу Хантінгтона, дискінезію, пов'язану з терапією з використанням агоніста допаміну, хворобу Паркінсона, синдром неспокійних ніг, розлади, що включають, як їх симптом, дефіцит когнітивної функції, деменцію, розлади або напади настрою у ссавця; тривога або психотичні розлади, включаючи шизофренію параноїдального, дезорганізуючого, кататонічного, недиференційованого або залишкового типу; шизофреноподібний розлад; шизоафективний розлад типу марень або депресивного типу; маревний розлад; психоз, викликаний алкоголем, амфетаміном, канабінолом, кокаїном, галюциногенами, інгалянтами, опіоїдами або фенциклідином; розлад особистості параноїдального типу; і розлад особистості шизоїдного типу; агарофобія; специфічна фобія; соціальна фобія; посттравматичний стрес; гострий стресовий розлад; хімічна залежність: зловживання алкоголем, амфетаміном, кокаїном, героїном, фенобарбіталом, опіатами, нікотином та бензодіазепінами; розлади, що включають, як їх симптом, дефіцит когнітивної функції, субнормальне функціонування одного або декількох когнітивних аспектів; дефіцит пам'яті, розуму або навчальної і логічної здатності, зокрема, у індивідуума по відношенню до інших осіб в межах тієї ж самої загальної вікової групи; зниження будь-якого окремого функціонування індивідуума в одному або декількох когнітивних аспектах, вікозалежний когнітивний занепад; деменція, хвороба Альцгеймера, поліінфарктна деменція, алкогольна деменція або інша деменція, обумовлена хімічними речовинами, деменція, пов'язана з внутрішньочерепними пухлинами або церебральною травмою, деменція, пов'язана з хворобою Хантінгтона або хворобою Паркінсона, або СНІД-залежна деменція; деменція пов'язана з хворобою Альцгеймера; делірій; амнестичний розлад; посттравматичний стресовий розлад; затримка психічного розвитку; розлад навчання, наприклад розлад читання, математичний розлад або розлад письмового вираження; дефіцит уваги/гіперактивність; розлади настрою або напади настрою; основний депресивний напад слабкості помірного або жорсткого типу, маніакальний або змішаний напад настрою, напад гіпоманіакального настрою; напад депресії з атиповими ознаками; напад депресії з меланхолічними ознаками; напад депресії з кататонічними ознаками; напад настрою у післяпологовий період; постінсультна депресія; глибокий депресивний розлад; психічна депресія; малий депресивний розлад; передменструальний дисфоричний розлад; постпсихотична депресивна шизофренія; глибокий депресивний розлад, накладений на психотичний розлад, такий як марення або шизофренія; біполярний розлад, біполярний розлад І типу, біполярний розлад II типу, і циклотимічний розлад, гіпертензія, депресія, депресія у хворих на рак, депресія у хворих на хворобу Паркінсона, депресія після інфаркту міокарда, субсиндромально симптоматична депресія, депресія у безплідних жінок, депресія в педіатрії, глибока депресія, одиничний епізод депресії, рекурентна депресія, депресія у дітей, індукована зловживанням, та післяпологова депресія, проста фобія, замкнення у себе, передчасна еякуляція, розлади харчування, нервова анорексія та нервова булімія, ожиріння, нападоподібний головний біль з періодичними рецидивами, мігрень, біль, розлади пам'яті; паркінсонізм, індукований нейролептиками та пізня дискінезія, ендокринні розлади, гіперпролектинемія, вазоспазм, вазоспазм церебральних судин, мозочкова атаксія, розлади шлунково-кишкового тракту, включаючи зміни перистальтики та секреції, негативні симптоми шизофренії, манія, передменструальний синдром, синдром фіброміалгії, нетримання при стресі, хвороба Туретта, трихокриптоманія, клептоманія, чоловіча імпотенція, рак, дрібноклітинна легенева карцинома, хронічна пароксизмальна гемікранія та головний біль, пов'язаний з судинними розладами, що включає введення ссавцю, що потребує такого лікування, терапевтично ефективної кількості сполуки згідно з будь-яким з пунктів 1-10.
Текст
1. Сполука формули C2 2 UA 1 O R2 , 3 78437 в якій Z є R3 (CH 2)n N ; R4 Y Х є кисень; Y є метилен; n є 0; і R1 і R2 кожен є водень або галоген; і R3 і R4 разом з атомом азоту, до якого вони приєднані, утворюють і) насичене 3-7-членне моноциклічне кільце, згадане кільце і) є незаміщеним або заміщеним однією або декількома (С1-С4)алкілами, (С1С4)алкоксі(С 1-С4)алкілами або гідроксигрупами {див. стор. 8, останній абзац}. 3. Сполука згідно з пунктом 1, в якій Z є R3 (CH 2)n N R4 Y , в якій Y є метилен; Х є кисень; n є 0; R1 є водень; R2 є водень; і R3 і R4 разом з атомом азоту, до якого вони приєднані, утворюють і) насичене неароматичне 3-7-членне моноциклічне кільце, згадане кільце і) є незаміщеним або заміщеним одним або декількома (С1-С4)алкілами, (С1-С4)алкоксі(С 1С4)алкілами або гідроксигрупами. 4. Сполука згідно з пунктом 1, в якій Z є R3 (CH 2)n N R4 Y , в якій Y є метилен; Х є кисень; n є 0; R1 є водень; R2 є водень; і R3 і R4 разом з атомом азоту, до якого вони приєднані утворюють ііі) незаміщене 5-6членне гетероциклічне кільце, де гетероциклічне кільце, на додаток до атома азоту, до якого приєднані R3 і R4, має додатковий атом азоту, атом сірки або атом кисню. 5. Сполука згідно з пунктом 1 або 2, в якій R2 є галоген; і R3 і R4 разом з атомом азоту, до якого вони приєднані утворюють (і) насичене 3-7-членне моноциклічне кільце, де моноциклічне кільце може бути незаміщеним або заміщеним одним або декількома фенілами, (С1С3)алкілами або (C1-С4)алкоксі(С 1-С4)алкілами. 6. Сполука згідно з пунктом 1, де згадану сполуку вибирають з групи, що містить: (7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-(6морфолін-4-ілметилпіридин-2ілоксиметил)октагідропіридо[1,2-а]піразин; (7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-(5піперидин-1-ілметилпіридин-2ілоксиметил)октагідропіридо[1,2-а]піразин; (7R,9аS)-транс-2-(5-фторбензо[d]ізоксазол-3-іл)-7(5-піролідин-1-ілметилпіридин-2ілоксиметил)октагідропіридо[1,2-а]піразин; (7R,9аS)-транс-7-(5-азетидин-1-ілметилпіридин-2ілоксиметил)-2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин; (7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-[5-(2метилазиридин-1-ілметил)піридин-2ілоксиметил]октагідропіридо[1,2-а]піразин; 4 (7R,9аS)-транс-2-бензо[6]ізоксазол-3-іл-7-[5-(2метоксиметилпіролідин-1-ілметил)піридин-2ілоксиметил]октагідропіридо[1,2-а]піразин; (7R,9аS)-цис-7-(5-азетидин-1-ілметилпіридин-2ілоксиметил)-2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин; (7R,9аS)-транс-1-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(S)-піролідин-3-ол; (7R,9аS)-транс-1-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(R)-піролідин-3-ол; (7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-[5-(2метилпіролідин-1-ілметил)піридин-2ілоксиметил]октагідропіридо[1,2-а]піразину; (7R,9аS)-транс-1-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]піперидин-4-ол; (7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-(6піролідин-1-ілметилпіридин-2ілоксиметил)октагідропіридо[1,2-а]піразину; (7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-(5піролідин-1-ілметилпіридин-2ілоксиметил)октагідропіридо[1,2-а]піразину; (7R,9аS)-цис-2-бензо[d]ізоксазол-3-іл-7-(5піролідин-1-ілметилпіридин-2ілоксиметил)октагідропіридо[1,2-а]піразин та (7R,9аS)-транс-1-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-піролідин-3-ол (див. Приклад 54). 7. Сполука згідно з пунктом 6, де згадану сполуку вибирають з групи, що містить: (7R,9аS)-транс-1-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-піролідин-3-ол (див. Приклад 54); (7R,9аS)-транс-7-(5-азетидин-1-ілметилпіридин-2ілоксиметил)-2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин (див. Приклад 55); (7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-[5-(2метилпіролідин-1-ілметил)піридин-2ілоксиметил]октагідропіридо[1,2-а]піразин (див. Приклад 71); (7R,9аS)-цис-7-(5-азетидин-1-ілметилпіридин-2ілоксиметил)-2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин (див. Приклад 77); (7R,9аS)-транс-1-[б-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(R)-піролідин-3-ол (див. Приклад 86); (7R,9аS)-транс-1-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(S)-піролідин-3-ол (див. Приклад 87); (7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-(5піролідин-1-ілметилпіридин-2ілоксиметил)октагідропіридо[1,2-а]піразин (див. Приклад 90); (7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-(6піролідин-1-ілметилпіридин-2ілоксиметил)октагідропіридо[1,2-а]піразин (див. Приклад 97); (7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-(5піперидин-1-ілметилпіридин-2 5 78437 ілоксиметил)октагідропіридо[1,2-а]піразин (див. Приклад 101); (7R,9аS)-цис-2-бензо[d]ізоксазол-3-іл-7-(5піролідин-1-ілметилпіридин-2ілоксиметил)октагідропіридо[1,2-а]піразин (див. Приклад 104). 8. Сполука згідно з пунктом 1, де згаданусполуку вибирають з групи, що містить: (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]діетиламін (див. Приклад 53); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]диметиламін (див. Приклад 68); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3ілметил]циклогексилметиламін (див. Приклад 67); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]етилметиламін (див. Приклад 69); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3ілметил]циклопентилметиламін (див. Приклад 58); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(2метоксіетил)метиламін (див. Приклад 57); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-трет-бутиламін (див. Приклад 63); (7R,9аS)-цис-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]етилметиламін (див. Приклад 74); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]диметиламін (див. Приклад 81); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]бензиламін (див. Приклад 98); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2ілметил]циклопропілметиламін (див. Приклад 48) та (7R,9аS)-цис-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3ілметил]циклопентилметиламін (див. Приклад 75). 9. Сполука згідно з пунктом 1, де згадану сполуку вибирають з групи, що містить: (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]-(3-метилпіридин-4іл)амін (див. Приклад 42); (7R,9аS)-транс-1-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7 6 ілметокси)піридин-2-ілметил]піролідин-3-ол (див. Приклад 80); (7R,9аS)-цис-1-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]піролідин-(S)-3-ол (див. Приклад 89); (7R,9аS)-цис-1-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]піролідин-(Р)-3-ол (див. Приклад 93); (7R,9аS)-транс-2-(5-фторбензо[d]ізоксазол-3-іл)-7(6-піролідин-1-ілметилпіридин-2ілоксиметил)октагідропіридо[1,2-а]піразин (див. Приклад 107); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(2-метокси-1метилетил)амін (див. Приклад 70); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]-(2метоксіетил)метиламін (див. Приклад 79); (7R,9аS)-цис-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3ілметил]циклогексилметиламін (див. Приклад 88); (7R,9аS)-цис-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]диметиламін (див. Приклад 73); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2ілметил]циклогексилметиламін (див. Приклад 82); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]тіазол-2-іламін) (див. Приклад 41); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]піридин-2-іламін (див. Приклад 47); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(2-морфолін-4ілетил)амін (див. Приклад 30); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]-(2-морфолін-4ілетил)амін (див. Приклад 49); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]-піримідин-4-іламін (див. Приклад 50); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]-(2-піролідин-1ілетил)амін (див. Приклад 52); (7R,9аS)-цис-[6-(2-бензо[6]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]диметиламін (див. Приклад 84); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7 7 78437 ілметокси)піридин-2-ілметил]-(3-метилпіридин-4іл)амін (див. Приклад 42); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]циклопропіламін (див. Приклад 32); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3ілметил]циклопропілметиламін (див. Приклад 29); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(тетрагідрофуран-2ілметил)амін (див. Приклад 36); (7R,9аS)-транс-N-[6-(2-бензо[6]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил-N,N'-диметилетан1,2-діамін (див. Приклад 59). 10. Сполука згідно з пунктом 1, де згадану сполуку вибирають з групи, що містить: (7R,9аS)-транс-7-[6-(2,6-диметилпіперидин-1ілметил)піридин-2-ілоксиметил]-2-(5фторбензо[с1]ізоксазол-3-іл)октагідропіридо[1,2а]піразин (див. Приклад 3); (7R,9аS)-транс-2-(5-фторбензо[d]ізоксазол-3-іл)-7[6-(4-метилпіперазин-1-ілметил)піридин-2ілоксиметил]октагідропіридо[1,2-а]піразин (див. Приклад 10); (7R,9аS)-транс-2-(5-фторбензо[d]ізоксазол-3-іл)-7(6-піперидин-1-ілметилпіридин-2ілоксиметил)октагідропіридо[1,2-а]піразин (див. Приклад 11); (7R,9аS)-транс-7-[6-(2,5-диметилпіролідин-1ілметил)піридин-2-ілоксиметил]-2-(5фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2а]піразин (див. Приклад 14); (7R,9аS)-транс-7-(6-азепан-1-ілметилпіридин-2ілоксиметил)-2-(5-фторбензо[d]ізоксазол-3іл)октагідропіридо[1,2-а]піразин (див. Приклад 18); (7R,9aS)-транс-7-(5-азепан-1-ілметилпіридин-2ілоксиметил)-2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин (див. Приклад 61); (7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-(5тіазолідин-3-ілметилпіридин-2ілоксиметил)октагідропіридо[1,2-а]піразин (див. Приклад 65); (7R,9аS)-транс-2-бензо[d]ізоксазол-3-іл-7-(5імідазол-1-ілметилпіридин-2ілоксиметил)октагідропіридо[1,2-а]піразин (див. Приклад 66); (7R,9аS)-цис-2-бензо[d]ізоксазол-3-іл-7-(5піперидин-1-ілметилпіридин-2ілоксиметил)октагідропіридо[1,2-а]піразин (див. Приклад 72); (7R,9аS)-цис-2-бензо[d]ізоксазол-3-іл-7-[5-(2метилазиридин-1-ілметил)піридин-2ілоксиметил]октагідропіридо[1,2-а]піразин (див. Приклад 78); (7R,9аS)-транс-7-(5-азетидин-1-ілметилпіридин-2ілоксиметил)-2-(5-фторбензо[d]ізоксазол-3іл)октагідропіридо[1,2-а]піразин (див. Приклад 94); (7R,9аS)-цис-2-бензо[d]ізоксазол-3-іл-7-(6морфолін-4-ілметилпіридин-2ілоксиметил)октагідропіридо[1,2-а]піразин (див. Приклад 105); 8 (7R,9аS)-цис-2-бензо[d]ізоксазол-3-іл-7-(6піролідин-1-ілметилпіридин-2ілоксиметил)октагідропіридо[1,2-а]піразин (див. Приклад 106); (7R,9аS)-транс-циклогексил-{6-[2-(5фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2а]піразин-7-ілметокси]піридин-2-ілметил}амін (див. Приклад 1); (7R,9аS)-транс-2-(етил-{6-[2-(5фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2а]піразин-7-ілметокси]піридин-2ілметил}аміно)етанол (див. Приклад 2); (7R,9аS)-транс-(1,2-диметилпропіл)-{6-[2-(5фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2а]піразин-7-ілметокси]піридин-2-ілметил}амін (див. Приклад 5); (7R,9аS)-транс-циклопропіл-{6-[2-(5фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2а]піразин-7-ілметокси]піридин-2-ілметил}амін (див. Приклад 6); (7R,9аS)-транс-циклопропілметил-[6-[2-(5фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2а]піразин-7-ілметокси]піридин-2-ілметил}амін (див. Приклад 7); (7R,9аS)-транс-{6-[2-(5-фторбензо[d]ізоксазол-3іл)октагідропіридо[1,2-а]піразин-7ілметокси]піридин-2-ілметил}диметиламін (див. Приклад 12); (7R,9аS)-транс-{6-[2-(5-фторбензо[d]ізоксазол-3іл)октагідропіридо[1,2-а]піразин-7ілметокси]піридин-2-ілметил}-(тетрагідрофуран-2ілметил)амін (див. Приклад 13); (7R,9аS)-транс-{6-[2-(5-фторбензо[d]ізоксазол-3іл)октагідропіридо[1,2-а]піразин-7ілметокси]піридин-2-ілметил}-[3-(4метилпіперазин-1-іл)пропіл]амін (див. Приклад 16); (7R,9аS)-транс-{6-[2-(5-фторбензо[d]ізоксазол-3іл)октагідропіридо[1,2-а]піразин-7ілметокси]піридин-2-ілметил}піролідин-1-іламін (див. Приклад 17); (7R,9аS)-цис-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]-(2метоксіетил)метиламін (див. Приклад 85); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]піримідин-4-іламін (див. Приклад 31); (7R,9аS)-транс-{6-[2-(5-фторбензо[d]ізоксазол-3іл)октагідропіридо[1,2-а]піразин-7ілметокси]піридин-3-ілметил]диметиламін (див. Приклад 95); (7R,9аS)-транс-етил-[6-[2-(5фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2а]піразин-7-ілметокси]піридин-3ілметил}метиламін (див. Приклад 96); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]-(6-метоксипіридин-3іл)амін (див. Приклад 51); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(5-метилпіридин-2іл)амін (див. Приклад 25); 9 78437 (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(3-метилпіридин-4іл)амін (див. Приклад 23); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]піридин-2-іламін (див. Приклад 28); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил-(5-метил-2Н-піразол3-іл)амін (див. Приклад 43); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(6-метоксипіридин-3іл)амін (див. Приклад 33); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил-(6-метилпіридин-2іл)амін (див. Приклад 27); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]-(6-метилпіридин-2іл)амін (див. Приклад 46); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(2-піролідин-1ілетил)амін (див. Приклад 34); (7R,9аS)-транс-2-бензо[6]ізоксазол-3-іл-7-[5-(4метил-[1,4]діазепан-1-ілметил)піридин-2ілоксиметил]октагідропіридо[1,2-а]піразин (див. Приклад 35); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]-(5-метилпіридин-2іл)амін (див. Приклад 44); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7'ілметокси)піридин-3-ілметил]-(3-метилізоксазол-5іл)амін (див. Приклад 22); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]-(1Н-піразол-3-іл)амін (див. Приклад 45); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]тіазол-2-іламін (див. Приклад 21); (7R,9аS)-транс-{6-[2-(5-фторбензо[d]ізоксазол-3іл)октагідропіридо[1,2-а]піразин-7ілметокси]піридин-2-ілметил}-(2-морфолін-4ілетил)амін (див. Приклад 109); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-трет-бутилметиламін (див. Приклад 64); (7R,9аS)-транс-(4-хлорбензил)-{6-[2-(5фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2а]піразин-7-ілметокси]піридин-2-ілметил}амін (див. Приклад 8); (7R,9аS)-транс46-[2-(5-фторбензо[d]ізоксазол-3іл)октагідропіридо[1,2-а]піразин-7ілметокси]піридин-2-ілметил}-[2-(1-метилпіролідин2-іл)етил]амін (див. Приклад 9); 10 (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(3-метилізоксазол-4іл)амін (див. Приклад 20); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(1Н-піразол-3-іл)амін (див. Приклад 26); (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(5-метил-2Н-піразол3-іл)амін (див. Приклад 24). 11. Сполука формули Z N X N R1 N N O R2 або її (R) або (S) енантіомер, або її цис- або трансізомер, в якій Х є кисень або NR, де R є водень або (С1С6)алкіл; R1 і R2 є кожен, незалежно, водень, галоген або (С1-С6)алкіл, (С1-С6)алкокси або (С1-С6)алкоксі(С 1С6)алкіл, будь-яка з груп може бути незаміщена або заміщена одним або декількома галогенами; і Zє O O 9 8 або 7 ; С R CH R S R 2 O , де R7 є водень або (С1-С3)алкокси; R8 є водень, гідрокси або (С1-С3)алкокси; і R9 є (С1-С3)алкіл. 12. Сполука згідно з пунктом 7, де згадану сполуку вибирають з групи, що містить: (7R,9аS)-транс-6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)нікотинової кислоти метиловий естер; (7R,9аS)-транс-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-іл]метанол; (7R,9аS)-транс-метансульфонової кислоти 6-(2бензо[d]ізоксазол-3-ілоктагідропіридо[1,2а]піразин-7-ілметокси)піридин-2-ілметиловий естер; (7R,9аS)-транс-метансульфонової кислоти 6-[2-(5фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2а]піразин-7-ілметокси]піридин-2-ілметиловий естер; (7R,9аS)-транс-6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-карбонової кислоти метиловий естер; (7R,9аS)-транс-[6-(2-бензо[с1]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-іл]метанол; 11 78437 (7R,9аS)-транс-{6-[2-(5-фторбензо[6]ізоксазол-3іл)октагідропіридо[1,2-а]піразин-7ілметокси]піридин-2-іл}метанол; (7R,9аS)-транс-6-[2-(5-фторбензо[d]ізоксазол-3іл)октагідропіридо[1,2-а]піразин-7ілметокси]піридин-2-карбонової кислоти метиловий естер; (7R,9аS)-цис-6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-карбонової кислоти метиловий естер; (7R,9аS)-цис-[6-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-іл]метанол; (7R,9аS)-цис-метансульфонової кислоти 6-(2бензо[с1]ізоксазол-3-ілоктагідропіридо[1,2а]піразин-7-ілметокси)піридин-2-ілметиловий естер; (7R,9аS)-транс-5-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-карбонової кислоти метиловий естер; (7R,9аS)-транс-[5-(2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-іл]метанол і (7R,9аS)-транс-метансульфонової кислоти 5-(2бензо[d]ізокcaзон-3-ілоктагідропіридо[1,2а]піразин-7-ілметокси)піридин-2-ілметиловий естер. 13. Фармацевтична композиція, що містить сполуку згідно з будь-яким з пунктів 1-10 або її фармацевтично прийнятну сіль і фармацевтично прийнятний носій. 14. Спосіб лікування одного або декількох розладів центральної нервової системи, що включає введення ссавцю, який потребує такого лікування, терапевтичне ефективної кількості сполуки згідно з будь-яким з пунктів 1-10. 15. Спосіб лікування розладу, яким є шизофренія, шизофреноподібний розлад, шизоафективний розлад, маревний розлад, речовиновикликаний психотичний розлад, психоз, розлад особистості параноїдального типу, розлад особистості шизоїдного типу, паніка, фобія, обсесивно-компульсивний розлад, стрес, генералізована тривога, розлади руху, включаючи хворобу Хантінгтона, дискінезію, пов'язану з терапією з використанням агоніста допаміну, хворобу Паркінсона, синдром неспокійних ніг, розлади, що включають, як їх симптом, дефіцит когнітивної функції, деменцію, розлади або напади настрою у ссавця; тривога або психотичні розлади, включаючи шизофренію параноїдального, дезорганізуючого, кататонічного, недиференційованого або залишкового типу; шизофреноподібний розлад; шизоафективний розлад типу марень або депресивного типу; маревний розлад; психоз, викликаний алкоголем, амфетаміном, канабінолом, кокаїном, галюциногенами, інгалянтами, опіоїдами або фенциклідином; розлад особистості параноїдального типу; і розлад особистості шизоїдного типу; агарофобія; специфічна фобія; соціальна фобія; посттравматичний стрес; гострий стресовий розлад; хімічна залежність: зловживання алкоголем, амфетаміном, кокаїном, героїном, фенобарбіталом, опіатами, нікоти 12 ном та бензодіазепінами; розлади, що включають, як їх симптом, дефіцит когнітивної функції, субнормальне функціонування одного або декількох когнітивних аспектів; дефіцит пам'яті, розуму або навчальної і логічної здатності, зокрема, у індивідуума по відношенню до інших осіб в межах тієї ж самої загальної вікової групи; зниження будь-якого окремого функціонування індивідуума в одному або декількох когнітивних аспектах, вікозалежний когнітивний занепад; деменція, хвороба Альцгеймера, поліінфарктна деменція, алкогольна деменція або інша деменція, обумовлена хімічними речовинами, деменція, пов'язана з внутрішньочерепними пухлинами або церебральною травмою, деменція, пов'язана з хворобою Хантінгтона або хворобою Паркінсона, або СНІДзалежна деменція; деменція пов'язана з хворобою Альцгеймера; делірій; амнестичний розлад; посттравматичний стресовий розлад; затримка психічного розвитку; розлад навчання, наприклад розлад читання, математичний розлад або розлад письмового вираження; дефіцит уваги/гіперактивність; розлади настрою або напади настрою; основний депресивний напад слабкості помірного або жорсткого типу, маніакальний або змішаний напад настрою, напад гіпоманіакального настрою; напад депресії з атиповими ознаками; напад депресії з меланхолічними ознаками; напад депресії з кататонічними ознаками; напад настрою у післяпологовий період; постінсультна депресія; глибокий депресивний розлад; психічна депресія; малий депресивний розлад; передменструальний дисфоричний розлад; постпсихотична депресивна шизофренія; глибокий депресивний розлад, накладений на психотичний розлад, такий як марення або шизофренія; біполярний розлад, біполярний розлад І типу, біполярний розлад II типу, і циклотимічний розлад, гіпертензія, депресія, депресія у хворих на рак, депресія у хворих на хворобу Паркінсона, депресія після інфаркту міокарда, субсиндромально симптоматична депресія, депресія у безплідних жінок, депресія в педіатрії, глибока депресія, одиничний епізод депресії, рекурентна депресія, депресія у дітей, індукована зловживанням, та післяпологова депресія, проста фобія, замкнення у себе, передчасна еякуляція, розлади харчування, нервова анорексія та нервова булімія, ожиріння, нападоподібний головний біль з періодичними рецидивами, мігрень, біль, розлади пам'яті; паркінсонізм, індукований нейролептиками та пізня дискінезія, ендокринні розлади, гіперпролектинемія, вазоспазм, вазоспазм церебральних судин, мозочкова атаксія, розлади шлунково-кишкового тракту, включаючи зміни перистальтики та секреції, негативні симптоми шизофренії, манія, передменструальний синдром, синдром фіброміалгії, нетримання при стресі, хвороба Туретта, трихокриптоманія, клептоманія, чоловіча імпотенція, рак, дрібноклітинна легенева карцинома, хронічна пароксизмальна гемікранія та головний біль, пов'язаний з судинними розладами, що включає введення ссавцю, що потребує такого лікування, терапевтично ефективної кількості сполуки згідно з будь-яким з пунктів 1-10. 13 78437 Винахід стосується азабіциклічних сполук заміщених амінометилпіридилоксиметилом/бензізоксазолом, які, серед іншого, можуть бути придатні як ефективні інгібітори рецептора 5НТ1В, 5-НТ2А і D2, наприклад, антагоністи, зворотні агоністи і/або часткові агоністи. Винахід також стосується проміжної сполуки для одержання згаданих сполук; фармацевтичної композиції, що містить згадані сполуки; і застосування згаданих сполук або інших сполук, що мають згадану активність по зв'язуванню або інгібуванню 5-НТ1 В, 5-НТ2А і D2 рецептора в способі лікування деяких розладів ЦНС або інших розладів. Розлади центральної нервової системи (ЦНС) медично можуть лікуватись різними шляхами. Особливо важливими в цьому відношенні психотропічні лікарські засоби. Але окрім терапевтичної дії, вони також мають небажані і серйозні побічні проявлення. Наприклад, шизофренія може лікуватись так званими типовими лікарськими засобами, які відносяться до блоку деяких рецепторів допаміну (D2) в мозку відповідаючи за позитивні симптоми галюцинацій, розлади мислення і їм подібні. Однак, в той час як ці лікарські засоби можуть покращувати деякі позитивні симптоми, вони також можуть несприятливо впливати на моторну систему, викликаючи м'язові проблеми, такі як спазми, судоми, дрижання і Паркінсонізм. Оскільки такі типи побічних проявлень – зазвичай характеризуються як Екстрапірамідальні Симптоми (EPS) можуть бути доста тніми для руйнування добової активності, звертаються до так званих атипових лікарських засобів. Атипові антипсихотичні засоби зменшують випадки виникнення EPS і можуть полегшувати не тільки деякі позитивні симптоми шизофренії, але також деякі негативні симптоми, такі як емоційну несприйнятливість, соціальну самоізоляцію і їм подібні. Хоча антипсихотичні лікарські засоби, як припускають, є більш селективними за їх хімічною дією на мозок, таким чином зменшуючи EPS, вони також можуть мати побічні проявлення. Доки це зустрічається не часто як у випадку терапії з використанням типового лікарського засобу, вони можуть однак мати наслідки для пацієнта. Наприклад, атипові лікарські засоби можуть бути седативними і можуть викликати збільшення ваги. Ситуація надалі ускладнюється, коли у пацієнта присутні деякі розлади ЦНС. Наприклад, психоз, такий як шизофренія, може часто співіснувати з депресією, тривогою, обсесивно-компульсивним розладом (OCD) і іншими такими захворюваннями. В таких випадках, лікування часто включає введення комбінації лікарських засобів, наприклад, одного для лікування шизофренії і одного для лікування депресії або іншого співхворобливого розладу ЦНС. Оскільки кожен з таких лікарських засобів має власні побічні ефекти, спільне введення може призводити до їх збільшення або підвищення, і все це шкодить пацієнтові. Однак, припускають, що різні рецептори мозку, або комбінація або перестановка рецепторів, тим чи 14 іншим чином втягнуті в кожен з різноманітних розладів ЦНС; наприклад, з шизофренією, як припускають, пов'язані D2 і 5НТ-2А рецептори, в той час як депресія пов'язана з 5НТ-1В рецепторами. Азабіциклічні сполуки заміщені амінометилфеноксиметил/бензізоксазол корисні як селективні агоністи і антагоністи серотонін 1 (5-НТ1) рецепторів, і описуються в [WO 99/52907, Bright]. Донедавна доказувалась складність знайти один лікарський засіб, що може лікувати пацієнта, що страждає від різних розладів ЦНС, в якій втягнуті чисельні різноманітні рецептори. Відповідно, все ще існує потреба в психотропному лікарському засобі, що має доказані знижені побічні ефекти, і що може бути дієвим і сам по собі лікувати різноманітні розлади ЦНС, при яких показані антагоністи або агоністи різних рецепторів. Специфічно, бажаним є знайти лікарський засіб, що може конкурентно лікувати шизофренію і депресію, в які втягнуті D2, 5НТ-2А і 5НТ-1В рецептори. Представлений винахід спрямований на вирішення згаданих вище потреб, в одному з аспектів, винахід стосується сполуки, що має наступну формулу, позначену тут як Формула І: або її (R) або (S) енантіомер, або її цис або транс ізомер, або її фармацевтично прийнятна сіль, сольват або пролікарська форма або будьяка з вищезагаданих, в якій m є 0 або 1; Z є де R7 є водень або (С1-С3)алкокси; R8 є водень, гідрокси або (С1-С3)алкокси; і R9 є (С1С3)алкіл; X є кисень або NR, де R є водень або (С1С6)алкіл; Х є метилен, коли n є 0, 1 або 2; або кисень, азот або сірка, коли n є 2, 3 або 4; R1 і R2 є кожен, незалежно, водень, галоген або (С1-С6)алкіл, (С1-С6)алкокси або (С1С6)алкокси(С 1-С6)алкіл, будь-яка з груп може бути незаміщена або заміщена одним або декількома галогенами; R3 і R4 є кожен, незалежно, водень, (С1С6)алкіл, (С3-С7)циклоалкіл або 5-6 членний гетероцикліл, будь-яка з груп може бути незаміщена або заміщена однією або декількома будь-якими наступними: (С1-С4)алкіл, (С3-С7)циклоалкіл, (С1С4)алкокси, (С6-С10)арил, 5-6 членний гетероцикліл, аміно, галоген або гідрокси; або R3 і R4 разом з атомом азоту, до якого вони приєднані утворюють: 15 78437 (і) 3-7 членне, необов'язково, ненасичене моноциклічне кільце; або (іі) 4-10 членне, необов'язково, ненасичене поліциклічне кільце, де згадане моноциклічне або поліциклічне кільце, необов'язково, мають один або два додаткові гетероатоми, що вибирають з азоту, кисню і сірки, де будь-які згадані кільця (і) або (іі) можуть бути незаміщеними або заміщеними одним або декількома (С1-С4)алкілами, (С1-С4)алкокси, (С1С4)алкокси(С 1-С4)алкілами, (С3-С7)циклоалкілами, (С6-С10)арилами, (С7-С13)аралкілами, 5-10 членними гетероарилами, гідрокси, аміно, ціано або галогенами. В особливому втіленні, сполука винаходу має формулу: або її (R) або (S) енантіомер, або її цис або транс ізомер, або її фармацевтично прийнятна сіль, сольват або пролікарська форма або будьяка з вищезагаданих, в якій Z є де R7 є водень або (С1-С3)алкокси; R8 є водень, гідрокси або (С1-С3)алкокси; і R9 є (С1С3)алкіл; X є кисень або NR, де R є водень або (С1С6)алкіл; Х є метилен, коли n є 0, 1 або 2; або кисень, азот або сірка, коли n є 2, 3 або 4; R1 і R2 є кожен, незалежно, водень, галоген або (С1-С6)алкіл, (С1-С6)алкокси або (С1С6)алкокси(С 1-С6)алкіл, будь-яка з груп може бути незаміщена або заміщена одним або декількома галогенами; R3 і R4 є кожен, незалежно, водень, (С1С6)алкіл, (С3-С7)циклоалкіл або 5-6 членний гетероцикліл, будь-яка з груп може бути незаміщена або заміщена однією або декількома будь-якими наступними: (С1-С4)алкіл, (С3-С7)циклоалкіл, (С1С4)алкокси, (С6-С10)арил, 5-6 членний гетероцикліл, аміно, галоген або гідрокси; або R3 і R4 разом з атомом азоту, до якого вони приєднані утворюють: (і) 3-7 членне, необов'язково, ненасичене моноциклічне кільце; або (іі) 4-10 членне, необов'язково, ненасичене поліциклічне кільце, де згадане моноциклічне або поліциклічне кільце, необов'язково, мають один або два додаткові гетероатоми, що вибирають з азоту, кисню і сірки, де будь-які згадані кільця (і) або (іі) можуть бути незаміщеними або заміщеними одним або декількома (С1-С4)алкілами, (С1-С4)алкокси, (С1С4)алкокси(С 1-С4)алкілами, (С3-С7)циклоалкілами, (С6-С10)арилами, (С7-С13)аралкілами, 5-10 членни 16 ми гетероарилами, гідрокси, аміно, ціано або галогенами. В інших аспектах, винахід стосується фармацевтичної композиції, що містить згадану сполуку; і способу лікування одного або декількох розладів ЦНС, при якому потрібне застосування ліганду, наприклад, антагоністу, часткового агоністу (з 80% або більшим антагонізмом) або зворотного агоністу, до D2, 5НТ-2А і 5НТ-1В рецепторів, окремо або в будь-якій їх комбінації. Винахід також стосується частково сполуки, яка зв'язує рецептор D2:5HT1В, що виражається у співвідношенні приблизно 20 або менше; і/або інгібує активність кожного із згаданих D2, 5НТ1В і 5НТ2А рецепторів. Сполуки винаходу проявляють активність по зв'язуванню рецептора по відношенню до принаймні двох і переважно всіх трьох D2, 5НТ1В і 5НТ2А рецепторів. Рівень інгібування в цьому відношенні є таким, що сполуки винаходу є терапевтично ефективними при лікуванні розладу(ів) ЦНС у ссавця, при яких потрібна активність проти всіх трьох рецепторів. Це означає, що сполуки мають дію Кі менше ніж або еквівалентну 20нМ для всіх трьох рецепторів. Крім того, винахід переважно включає будьяку сполуку з властивою їй активністю антагоністу і/або зворотного агоністу по відношенню до рецепторів D2 людини, 5НТ1В і 5НТ2А людини. Властива активність, що вимірюється за допомогою активності аденилатциклази, круговороту фозоінозитолу або інших методів відомих в цій галузі. В попередньому рівні техніки відсутні згадки про сполуки, що проявляють активність антагоністу або зворотного агоністу проти всіх трьох рецепторів. Більш особливо, винахід переважно включає сполуки, яким властива активність антагоністу і/або зворотного агоністу рецепторів D2 і 5НТ2А людини і яким властива активність антагоністу >80% по відношенню до рецепторів 5НТ1В людини. Як згадувалось вище, властива активність може бути виміряна використовуючи активність аденілатциклази або по круговороту фозоінозитолу. Винахід переважно включає сполуки з функціональним значенням Кі для 5НТ1В менше ніж або еквівалентне 5нМ в комбінації з функціональним значенням Кі менше ніж або еквівалентне 20нМ для рецепторів D2 і 5НТ2А людини. Крім того, винахід переважно включає сполуки, що можуть самостійно проявляти in vivo активність в тваринних моделях антагонізму або зворотного агонізму 5НТ1В, D2 і 5НТ2А. Відповідні тваринні моделі приведені в наступних прикладах, але не обмежуються такими моделями. Сполуки досліджували на їх здатність антагонізувати гіпотермічну відповідь, що спричиняється 5-НТ1В агоністом, як міра in vivo 5-HT1B антагоністичної активності. Сполуки або розчинник вводять морським свинкам, за 0-60 хвилин до підшкірного (пш) введення 5-НТ1В агоністу і вимірюють температура тіла протягом чотирьох годин після введення агоністу. Представлений винахід переважно включає сполуки з ID50 менше ніж або еквівалентне 1мг/кг, пш при гіпотермії. В іншій тваринній моделі, сполуки досліджують на їх здатність антагонізувати DOI (лікарська вза 17 78437 ємодія) - викликані посмикування голови, яка міра in vivo 5-HT2 A антагоністичної активності. Введення 5-НТ2А агоністу, DOI, викликає характеристичні струшування (посмикування голови), що є атрибутом активування 5-НТ2А рецепторів. Сполуки або розчинник вводять тренованим щурам, за 30 до 60хв пш до введення 3,2мг/кг DOI, і підраховують посмикування голови протягом 30хв дослідження. Винахід переважно включає сполуки з ID50 менше ніж або еквівалентне 10мг/кг, пш при 5НТ2А посмикуванні голови. Крім того, сполуки досліджують на їх здатність антагонізувати d-амфетамін-індуковану гіперактивність, як міра in vivo антагоністичної активності по відношенню до допамін D2 рецептора. Безпосередньо вводять низькі дози агоністу допаміну, dамфетамін, що призводять до значного збільшення горизонтальної локомоторної активності у щурів, феномену, який є атрибутом активування мезолімбічної допамінової системи, і який тому забезпечує модель гіпердоамінергічної активності, що втягн ута в шизофренію. Сполуки або розчинник вводять тренованим щурам, за 30 до 60хв пш до введення 1,0мг/кг d-амфетаміну SO4 , і реєструють локомоторну активність в контрольованих комп'ютером клітках протягом 3 годин гіперактивної відповіді. Винахід включає сполуки з ID50 менше ніж або еквівалентне 10мг/кг, пш при dамфетамін локомоторній активності. В одному з втілень, винахід стосується сполуки, що має, inter alia, активність зв'язувати один або багато рецепторів, включаючи D2, 5НТ1В і 5НТ2А рецептори, окремо або в будь-якій їх комбінації. В переважному втіленні, сполук має зв'язувальну активність (ґрунтується на, наприклад, ІС50 або Кі) по відношенню до D2 і 5НТ1В рецепторів у співвідношенні D2:5HT1B приблизно 20 або менше; в більш практичних випадках, це співвідношення є приблизно 10 або менше; приблизно 5 або менше; більш переважно приблизно 1. Якщо не вказано інше, термін "інгібувальна активність" і його відповідні варіації, як тут використовується, означає, що сполука корисна, без обмеження, як антагоніст, зворотний агоніст і/або частковий агоніст (80% антагонізм або більше) і подібне по відношенню до будь-якого з рецепторів тут вказаних; наприклад, сполука проявляє спорідненість до зв'язування Кі приблизно 1 мікромоль або менше, з переважними випадками, що мають Кі приблизно 100 наномаль (нМ) або менше, приблизно 50нМ або менше, приблизно 20нМ або менше, і більш переважно приблизно 10нМ або менше, для будь-якого згаданого вище рецептора. В показових втіленнях, сполука винаходу має Формулу І, ви ще, включаючи її фармацевтчно прийнятні солі, наприклад, кислотноадитивні солі, основно-адитивні солі і їх проліки і сольвати. Без обмеження, прикладами фармацевтичноприйнтяних кислотно-адитивних солей сполук формули І є солі хлорводневої кислоти, птолуолсульфонової кислоти, фумарової кислоти, лимонної кислоти, бурштинової кислоти, саліцилової кислоти, щавлевої кислоти, бромводневої кислоти, фосфорної кислоти, метансульфонової кислоти, винної кислоти, малонової кислоти, ди-п 18 толуолвинної кислоти і манделової кислоти. Іншими можливими кислотно-адитивними солями є, наприклад, солі, що містить фармацевтично прийнятні аніони, такі як гідройодид, нітрат, сульфат або бісульфат, фосфат або гідрофосфа т, ацетат, лактат, глюконат, сахарат, бензоат, метансульфонат, етансульфонат, бензолсульфонат і памоат (тобто, 1,1¢-метилен-біс-(2-гідрокси-3-нафтоат) солі). Сполука формули І може мати оптичні центри (наприклад, в 7 і 9а положеннях) і таким чином може існувати в різних енантіомерних конфігураціях. Винахід включає всі такі енантіомери, діастереомери і інші стереомери і оптичні ізомери такої сполуки формули І, також як і рацемічні і інші їх суміші. Наприклад, сполука формули І включає (R) і (S) енантіомери і цис і транс ізомери. Представлений винахід також включає всі радіомічені форми сполуки Формули І. Переважними радіоміченими сполуками є сполуки, в яких радіомітку вибирають з 3Н, 11С, 14С, 18F, 123I і 125І. Такі радіомічені сполуки корисні для дослідження і як діагностичні інструменти при вивченні фармакокінетики метаболізму і в в дослідженнях зв'язування у тварин і людей. В іншому втіленні, винахід стосується сполуки Формули І, де в дослідженні зв'язування D2, 5НТ1В або 5НТ2А згадана сполука проявляє Кі приблизно при 1 мікромольабо менше; переважно проявляє Кі приблизно при 100 наномоль (нМ) або менше, приблизно 50нМ або менше, приблизно 20нМ або менше, і більш переважно приблизно 10нМ або менше. Такі дослідження є відомими або адаптуємими з відомого рівня техніки. В переважному втіленні, Z є в якій X є кисень; Y є метилен; n є 0; R 1 є водень; R2 є водень або галоген; і R 3 є водень або а (С1-С3)алкіл. В іншому переважному втіленні, R2 є водень; R3 є водень; і R4 є а) (С1-С6)алкіл; б) (С3С7)циклоалкіл; або в) 5-6 членний гетероцикліл, будь-яка з груп а), б) або в) може бути незаміщена або заміщена однією або декількома будь-якими наступними: (С1-С4)алкіл, (С3-С7)циклоалкіл, (С1С4)алкокси, (С6-С10)арил, 5-6 членний гетероцикліл, аміно, галоген або гідрокси. Більш переважно, R4 є а) (С1-С4)алкіл, який може незаміщений або заміщений однією з наступних: феніл, циклопропіл, метокси або заміщений 5-6 членний гетероцикліл, згаданий гетероцикліл, має принаймні один атом азоту або кисню; б) незаміщений (С3С7)циклоалкіл; або в) 5-6 членний гетероцикліл, який може бути незаміщений або заміщений (С1С3)алкілом або (С1-С3)алкокси, згаданий 5-6 членний гетероцикліл в) має принаймні один атом азоту і до одного іншого атому, що вибирають з азоту, кисню і сірки. Ще більш переважно, R4 є а) незаміщений С4 алкіл; С3 алкіл заміщений метокси; (С1С2)алкіл заміщений фенілом або циклопропілом; (С1-С2)алкілом заміщеним 5 членним гетероциклілом, що має атом азоту або кисню; або (С1С2)алкіл заміщений 6 членним гетероциклілом, що має принаймні один азот; б) незаміщений циклоп 19 78437 ропіл; або в) 5-6 членний гетероцикліл, який може бути незаміщений або заміщений метилом або метокси, згаданий 5-6 членний гетероцикліл в) має принаймні один атом азоту і до одного іншого атому, що вибирають з азоту, кисню і сірки, згаданим (С1-С3)алкілом є метил і згаданим (С1-С3)алкокси є метокси. В іншому переважному втіленні, Z є в якій X є кисень; Y є метилен; n є 0; R3 є (С1С3)алкіл; і R4 є а) (С1-С4) алкіл; або б) (С5С6)циклоалкіл, будь-яка з груп а) або б) може бути незаміщена або заміщена однією або декількома (С1-С3)алкокси або аміногрупами. Переважно, аміногрупа має формулу -NR5R6, де R5 і R6 є кожен, незалежно, водень або (С1-С4)алкіл; більш переважно, R4 є а) (С1-С4)алкіл незаміщений або заміщений однією або декількома метокси або аміногрупами, де R5 є водень і R6 є метил; або б) незаміщений (С5-С6)циклоалкіл. В ще одному іншому переважному втіленні, Z є де X є кисень; Y є метилен; n є 0; і R1 і R2 коджен є водень або галоген; і R і R4 разом з атомом азоту, до якого вони приєднані утворюють і) насичене 3-7 членне моноциклічне кільце, згадане кільце і) є незаміщеним або заміщеним однією або декількома (С1-С4)алкілами, (С1-С4)алкокси(С 1С4)алкілами або гідроксигрупами. Альтернативно, R3 і R4, разом з азотом до якого вони приєднані, утворюють незаміщену 5-6 членну кільце, яке має один додатковий атом азоту, сірки або кисню. Альтернативно, R1 є водень, R2 є галоген; і R4 є а) (С1С5)алкіл; б) (С3-С6) циклоалкіл, будь-яка з груп а) або б) може бути незаміщена або заміщена однією або декількома будь-якими наступними: циклопропіл; галоген; гідрокси; 5-6 членний гетероцикліл, де згаданий 5-6 членний гетероцикліл може бути незаміщений або заміщений однією або декількома метилами; або феніл, де згаданий феніл може бути незаміщений або заміщений одним або декількома галогенами; або R4 є в) 5 членний гетероцикліл. Переважно, R2 є фтор; і R3 є водень або метил. В іншому переважному втіленні, Z є в якій X є кисень; Y є метилен; n є 0; R 1 є водень, R2 є галоген; і R3 і R4 разом з атомом азоту, до якого вони приєднані утворюють і) насичене 3-7 членне моноциклічне кільце, яке може бути незаміщену або заміщену одним або декількома фенілами, (С1-С3)алкілами або (С1-С4)алкокси(С 1С4)алкілами; або іі) 5-6 членне кільце, яке може 20 бути незаміщене або заміщене однією або декількома (С1-С3) алкілами, і яке має додатковий атом азоту або кисню. В сполуках формули І, в будь-якому кільці утвореному NR3R4: (а) в кільці не більше ніж один атом кисню; (б) гідрокси, алкокси, алкоксиалкіл, ціано, аміно або алкіламіно групи є приєднані безпосередньо до будь-якого атому азоту; і (в) відсутній вуглець кільця що зв'язаний подвійним зв'язком з іншим вуглецем кільця і не є частиною ароматичної кільцевої системи і який може бути зв'язаний з атомом кисню або азоту кільця. Представлений винахід також стосується фармацевтичної композиції, що містить сполуку винаходу; і фармацевтично прийнятний носій. Якщо не вказано інше, наступні терміни і їх варіації, як тут використовуються, мають значення приведені далі: "Галоген" і "гало" і подібні включають фтор, хлор, бром і йод. "Алкіл" включає, як використовується в термінах "алкокси," "алкілоксиалкіл," і "аралкіл," насичені моновалентні вуглеводневі радикали, що мають нерозгалужену або розгалужену будову. Прикладами алкільних гр уп є, але не обмежується, метил, етил, н-пропіл, ізопропіл і т-бутил. "Метилен" стосується дивалентного радикалу (СН2)p-, де p є 1 (метилен), 2 (диметилен) або 3 (триметилен). "Циклоалкіл" включає не-ароматичні насичені циклічні алкільні замісники, де алкіл є таким як визначено вище. Прикладами циклоалкілу є, але не обмежується, циклопропіл, циклобутил, циклопентил, циклогексил і циклогептил; і біциклоалкільні і трициклоалкільні групи, що є неароматичними насиченими карбоциклічними групами, що складаються з двох або трьох кілець, відповідно, де згадані кільця мають, принаймні, один спільний атом вуглецю. Для цілей представленого винаходу, і якщо не вказано інше, біциклоалкільні групи включають спірогрупи і конденсовані групи. Прикладами біциклоалкільних гр уп є, але не обмежується, біцикло[3.1.0]гексил, біцикло[2.2.1]гепт-1-ил, норборніл, спіро[4.5]децил, спіро[4.4]ноніл, сліро[4.3]октил і спіро[4.2]гептил. Прикладом трициклоалкільної групи є адамантил. Циклоалкільними групами також є групи заміщені однією або декількома оксозамісниками. Прикладами таких груп з оксозамісниками є оксоциклопентил і оксоциклобутил. "Арил" включає органічний радикал, що є похідним від ароматичного вуглеводню після видалення одного водню, такий як феніл, нафтил, інденіл, інданіл і флуореніл; і конденсовані циклічні групи, де принаймні одне кільце є ароматичним. "Гетероцикліл" стосується циклічної групи, що містить один або або декілька гетероатомів, переважно від однго до чотирьох гетероатомів, і кожен вибирають з О, S і N. Гетероциклільні групи також включають циклічні системи заміщені однією або декількома оксозамісниками. Прикладами гетероциклільних груп є азиридиніл, азетидиніл, піролідиніл, піперидиніл, азепініл, піперазиніл, 1,2,3,6тетрагідропіридиніл, оксираніл, оксаетаніл, тетрагідрофураніл, тетрагідротієніл, тетрагідропіраніл, 21 78437 тетрагідротіопіраніл, морфоліно, тіоморфоліно, тіоксаніл, піролініл, індолініл, 2Н-піраніл, 4Нпіраніл, діоксаніл, 1,3-діоксоланіл, піразолініл, дигідропіраніл, дигідротієніл, дигідрофураніл, піразолідиніл, імідазолініл, імідазолідиніл, 3азабіцикло[3.1.0]гексаніл, 3азабіцикло[4.1.0]гептаніл, хінолізиніл, хінуклідиніл, 1,4-діоксаспіро[4.5]децил, 1,4діоксаспіро[4.4]ноніл, 1,4-діокса-спіро[4.3]октил і 1,4-діоксаспіро[4.2]гептил. "Гетероарил" стосується ароматичних гр уп, що містять один або декілька гетероатомів (О, S, або N), переважно, від одного до чотирьох гетероатомів. Багатоциклічна група, що містить один або декілька гетероатомів, де принаймні одне кільце групи є ароматичним є "гетероарильною" групою. Гетероарильні групи цього винаходу також можуть включати циклічні системи заміщені однією або декількома оксозамісниками. Прикладами гетероарильних груп є піридиніл, піридазиніл, імідазоліл, піримідиніл, піразоліл, триазоліл, піразиніл, хіноліл, ізохіноліл, 1,2,3,4-тетрагідрохіноліл, тетразоліл, фурил, тієніл, ізоксазоліл, тіазоліл, оксазоліл, ізотіазоліл, піроліл, індоліл, бензімідазоліл, бензофураніл, цинолініл, індазоліл, індолізиніл, фталазиніл, триазиніл, 1,2,4-триазиніл, 1,3,5триазиніл, ізоіндоліл, 1-оксоізоіндоліл, пуриніл, оксадіазоліл, тіадіазоліл, фуразаніл, бензофуразаніл, бензотіофеніл, бензотриазоліл, бензотіазоліл, бензоксазоліл, хіназолініл, хіноксалініл, нафтиридиніл, дигідрохіноліл, тетрагідрохіноліл, дигідроізохіноліл, тетрагідроізохіноліл, бензофурил, фуропіридиніл, піролопіримідиніл і азаіндоліл. Згадані вище групи, як похідні сполук згаданих вище, може бути приєднані через атом С або атом N, коли це можливе. Наприклад, похідне піролу може бути пірол-1-ілом (приєднане через N) або пірол-3-ілом (приєднане через С). Терміни приведені для груп також охоплюють всі можливі таутомери. "Аміно" включає замісники Формули -NR5R6, де R5 і R6 є кожен, незалежно, водень або (С1С4)алкіл. "Лікування" і "терапія" стосується обернення, полегшення, інгібування розвитку або профілактики розладу або стану, до якого такий термін застосовується, або одного або декількох симптомів такого стану або розладу. Як тут використовується, термін також охоплює, в залежності від стану пацієнта, профілактику розладу, включаючи профілактику початку розладу або будь-яких симптомів пов'язаних з ним, також як зменшення складності розладу або будь-яких його симптомів перед їх виникненням. "Лікування", як тут використовується, стосується також профілактики повторення розладу. Термін "терапія", як тут використовується, стосується акту лікування, де "лікування" є таким як визначено тут вище. Наприклад, "лікування шизофренії, або шизофреноподібного або шизоафективного розладу", як тут використовується також охоплює лікування одного або декількох симптомів (позитивних, негативних і інших пов'язаних рис) згаданих розладів, наприклад, лікування, маній і/або галюцинацій пов'язаних з ними. Іншими прикладами симптомів 22 шизофренії і шизофреноподібних або шизоафективних розладів є розлади мовлення, емоційна тупість, алогічність, ангедонія, неприйнятні дії, дисфоричний настрій (у формі, наприклад, депресії, тривоги або роздратування), і деякі ознаки когнітивної дисфункції. "Ссавець" стосується будь-якого члену класу "ссавець", включаючи, але не обмежується, люди, собаки і коти. "Модуляція серотонінергічної нейротрансмісії" стосується збільшення або покращення, або зменшення або уповільнення нейронного процесу, в ході якого серотонін виділяється пре-синаптичною клітиною при її збудженні, перетинає синапсис, таким чином стимулюючи або інгібуючи постсинаптичну клітину. "Хімічна залежність" означає анормальне бажання або сильне бажання, або звичку до наркотиків. Такі наркотики загалом вводяться особі, що знаходиться в залежності, будь-яким з багатьох способів введення, включаючи пероральний, парентеральний, назальний способи, або шляхом вдихання. Прикладами хімічних залежностей, які лікуються способами представленого винаходу є алкогольна залежність, залежність від нікотину, кокаїну, героїну, фенобарбіталу та бензодіазепінів (наприклад, Валіуму®). "Лікування хімічної залежності", як тут використовується, означає зменшення або ослаблення такої залежності і/або тяги. Винахід забезпечує спосіб лікування одного або декількох розладів ЦНС у ссавця, включаючи людину, що потребує такого лікування. Без обмеження, розлад ЦНС в цьому відношенні є розладом при якому показаним є ліганд D2, 5НТ1В і 5НТ2А рецептора, окремо або в будь-якій комбінації. В одному з аспектів, спосіб включає введення терапевтично ефективної кількості сполуки, що є інгібітором принаймні двох наступних рецепторів: D2, 5НТ-1В і 5НТ2А. В іншому аспекті винаходу, спосіб включає введення терапевтично ефективної кількості інгібітора D2/5HT1-В/5НТ-2А. В ще одному іншому аспекті, спосіб включає введення терапевтично ефективної кількості інгібітора D2/5HT1В, що має співвідношення D2:5HT1B інгібувальної активності приблизно 20 або менше, переважно, що згадане співвідношення дорівнює приблизно 10 або менше; приблизно 5 або менше; і більш переважно приблизно 1. В переважному випадку, інгібітор, що вводять для лікування у відповідності з способом винаходу, має структурну формулу І. Розлади ЦНС, що є об'єктом винаходу, відомі в цій галузі; і включають без обмеження розлади, при яких проказаний ліганд, наприклад, антагоніст, зворотний агоніст і/або частковий агоніст і їм подібні, D2, 5НТ1В, і 5НТ2А рецепторів, або окремо або в будь-яких їх комбінаціях. Таким чином в переважному випадку, у винаході може лікуватись один або декілька розладів ЦНС за допомогою однієї сполуки; наприклад, за допомогою винаходу може лікуватись шизофренія, при якій зазвичай показане інгібування D2 і 5НТ2А рецепторів, і депресія, при якій зазвичай показане інгібування 5НТ1В рецепторів. 23 78437 Сполуки винаходу також можуть бути використані в комбінації з іншими лікарськими засобами, наприклад, такими що зазвичай використовуються при лікуванні будь-яких розладів ЦНС описаних тут. Наприклад, сполуки винаходу можуть бути використані в комбінації з зипразидоном і подібними сполуками, що використовуються для лікування шизофренії; або з інгібіторами повторного поглинання 5НТ і подібними сполуками, що використовуються для лікування депресії. Розладами ЦНС, які планується лікувати з використанням представленого винаходу є, без обмеження: Тривога або психотичні розлади, такі як: шизофренія, наприклад, параноїдальна, дезорганізована, кататонічна, недиференційована або залишковий тип; шизофреноподібний розлад; шизоафективний розлад, наприклад, типу марень або депресивного типу; маревний розлад; речовиновикликаний психотичний розлад, наприклад, психоз викликаний алкоголем, амфетаміном, канабінолом, кокаїном, галюциногенами, інгалянтами, опіоїдами або фенциклідином; розлад особистості параноїдального типу; і розлад особистості шизоїдного типу. Прикладами тривоги є, але не обмежується, паніка; агарофобія; специфічна фобія; соціальна фобія; обсесивно-компульсивний розлад; пост-травматичний стрес-синдром; гострий стресовий розлад; і генералізована тривога. Розладами рухів є: хвороба Хантінгтона і дискінезія пов'язана з терапією з використанням агоністу допаміну; хвороба Паркінсона і синдром неспокійних ніг. Хімічні залежності: наприклад, зловживання спиртом, амфетаміном, кокаїном, опіатом, нікотином. Розлади, що включають, як їх симптом, дефіцит когнітивної функції: наприклад, субнормальне функціонування одного або декількох когнітивних аспектів, таких як пам'ять, розум або навчальна і логічна здатність, зокрема, у індивідуума по відношенню до інших осіб в межах тієї ж самої загальної вікової групи. Також, будь-яке зниження будь-якого окремого функціонування індивідууму в одному або декількох когнітивних аспектах, наприклад, як спостерігається при вікозалежному когнітивному занепаді. Прикладами розладів, що включають як симптом дефіцит когнітивних функцій, що можуть лікуватись згідно з представленим винаходом, є деменція, наприклад, хвороба Альцгеймера, поліінфарктна деменція, алкогольна деменція або інша деменція обумовлена хімічними речовинами, деменція пов'язана з внутрішньочерепними пухлинами або церебральна травма, деменція пов'язана з хворобою Хантінгтона або хворобою Паркінсона, або СНІД-залежна деменція; деменція пов'язана з хворобою Альцгеймера; делірій; амнестичний розлад; пост-травматичний стресовий розлад; затримка психічного розвитку; розлад навчання, наприклад, розлад читання, математичний розлад, постопераційний когнітивний занепад або розлад письмового вираження; дефіцит уваги/гіперактивність і вікозалежний когнітивний занепад. 24 Розлади настрою або приступи настрою, такі як: основний депресивний приступ слабкості, помірного або жорсткого типу, маніакальний або змішаний приступ настрою, гіпоманіакальний приступ настрою; приступ депресії з атипічними ознаками; приступ депресії з меланхолічними ознаками; приступ депресії з кататонічними ознаками; приступ настрою у післяпологовий період; постінсультна депресія; глибокий депресивний розлад; психічна депресія; малий депресивний розлад; лікування стійкої депресії, SSR1-стійка депресія, передменструальний дисфоричний розлад; постпсихотичний депресивна шизофренія; глибокий депресивний розлад накладений на психотичний розлад, такий як марення або шизофренія; біполярний розлад, наприклад, біполярний І розлад, біполярний II розлад, і циклотимічний розлад. Іншими розладами ЦНС є лікування стійкої депресії, SSR1 пошкоджень, аутизму і постопераційного занепаду. Іншими розладами суб'єктів, що лікуються за допомогою винаходу і на які впливає інгібування будь-якого або всіх рецепторів D2, 5НТ1В і 5НТ2А включаючи ті, що вибирають з: гіпертензії, аутизму, депресії (наприклад, депресії у хворих на рак, депресії у хворих на хворобу Паркінсона, депресії після інфаркту міокарда, субсиндромально симптоматичної депресії, депресії у безплідних жінок, депресії в педіатрії, глибокої депресії, одиничних епізодів депресії, рекурентної депресії, депресії індукованої зловживанням дітьми, та післяпологової депресії), стану загального неспокою, фобій (наприклад, агорафобії, соціальної фобії та простих фобій), посттравматичного стрес-синдрому, замкнення у себе, передчасної еяколяції, розладів харчування (наприклад, анорексії нервової та булімії нервової), ожиріння, хімічних залежностей (наприклад, залежності від алкоголю, кокаїну, героїну, фенобарбіталу, нікотину та бензодіазепінів), приступоподібного головного болі з періодичними рецидивами, мігрені, болю, хвороби Альцгеймера, обсесивно-компульсивного розладу, паніки, розладів пам'яті (наприклад, деменції, амнезії, та вікових змін когнітивних функцій (ВЗКФ)), хвороби Паркінсона (наприклад, деменції при хворобі Паркінсона, паркінсонізму індукованого нейролептиками та пізніх дискінезій), ендокринних розладів (наприклад, гіперпролектинемії), вазоспазму (особливо в церебральних судинах), мозочкової атаксії, розладів шлунково-кишкового тракту (включаючи зміни перистальтики та секреції), негативних симптомів шизофренії, шизоафективного розладу, обсесивно-компульсивного розладу, манії, передменструального синдрому, синдрому фіброміалгії, нетримання при стресі, хвороби Туретта, три хокриптоманії, клептоманії, чоловічої імпотенції, раку (наприклад, дрібноклітинної легеневої карциноми), хронічної пароксизмальної гемікранії та головного болю (пов'язаного з судинними розладами). Представлений винахід також стосується способу лікування розладу або стану, що лікується завдяки модулюванню серотонінергічної нейтротрасмісії у ссавця, переважно людини, що включає введення ссавцю, що потребує такого лікування, 25 78437 терапевтично ефективної кількості сполуки винаходу, включаючи переважно сполуки формули І. Інші розлади і стани суб'єкту, що лікуються представленим винаходом є стани згадані в [WO 99/52907, Bright], опис якого включений сюди як посилання. Представлений винахід також стосується фармацевтичної композиції для лікування згаданих вище розладів/станів, яка, між іншим, містить терапевтично ефективну кількість сполуки винаходу, включаючи переважно сполуку позначену Формулою І і фармацевтично прийнятний носій. Прикладами переважних сполук Формули І є сполуки, що мають абсолютну стереохімічну конфігурацію визначену як (7R,9aS)-Tpaнс або як (7S,9aS)-цис. Прикладами специфічних втілень сполук Формули І є сполуки приведені в Прикладах 1-110. В іншому більш специфічному втіленні, винахід стосується сполуки формули I¢ як показано далі: як її рацемат, або її (R) і (S) енантіомери, або її цис і транс ізомери, в якій X є кисень або NR, в якій R є водень або (С1-С6)алкіл; R1 і R2 є кожен, незалежно, такі як визначено вище і Zє де R7 є водень або (С1-С3)алкокси; R8 є водень, гідрокси, або (С1-С3)алкокси; і R9 є (С1С3)алкіл. Сполуки формули І¢ є особливо корисними при синтезі сполук Формули І. Прикладами специфічних сполук Формули I¢ є наступні і використовуються всі енантіомери і стереоізомери сполук: (7R,9aS)-Tpaнс-6-(2-BeH3o[d]iзоксазол-3ілоктагідропіридо[1,2-a]піразин-7ілметокси)нікотинової кислоти метиловий естер; (7R,9аS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-іл]метанол; (7R,9аS)-транс-Метансульфонової кислоти 6(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2а]піразин-7-ілметокси)піридин-2-ілметиловий естер; (7R,9аS)-транс-Метансульфонової кислоти 6[2-(5-фторбензо[d]ізоксазол-3іл)октагідропіридо[1,2-а]піразин-7ілметокси]піридин-2-ілметиловий естер; (7R,9аS)-транс-6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-карбонової кислоти метиловий естер; 26 (7R,9aS)-транс-[6-(2-Бензо[d]iзоксазол-3ілоктагідропіридо[1,2-a]піразин-7ілметокси)піридин-2-іл]метанол; (7R,9аS)-транс-{6-[2-(5-Фторбензо[d]ізоксазол3-іл)октагідропіридо[1,2-а]піразин-7ілметокси]піридин-2-іл}метанол; (7R,9aS)-транс-6-[2-(5-Фторбензо[d]ізоксазол3-iл)октагідропіридо[1,2-а]піразин-7ілметокси]піридин-2-карбонової кислоти метиловий естер; (7S,9аS)-цис-6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-карбонової кислоти метиловий естер; (7S,9аS)-цис-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-іл]метанол; (7S,9аS)-цис-Метансульфонової кислоти 6-(2бензо[d]ізоксазол-3-ілоктагідропіридо[1,2а]піразин-7-ілметокси)піридин-2-ілметиловий естер; (7R,9aS)-транс-5-(2-Бензо[d]iзоксазол-3ілоктагідропіридо[1,2-a]піразин -7ілметокси)піридин-2-карбонової кислоти метиловий естер; (7R,9aS)-тpaнc-[5-(2-Бeнзo[d]iзoкcaзoл-3iлoктaгiдpoпipидo[1,2-a]пipaзин-7ілметокси)піридин-2-іл]метанол; і (7R,9аS)-транс-Метансульфонової кислоти 5(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2а]піразин-7-ілметокси)піридин-2-ілметиловий естер. Наступні Схеми 1-5 ілюструють, без обмеження, можливі шляхи одержання сполук формули І. Повинно бути зрозуміло, що можуть бути використані або передбачені інші методики або варіації. 27 78437 28 Схема 1 ілюструє спосіб одержання сполук формули І, що мають (7R, 9aS)-транс або (7S,9aS)-цис стереохімію. Сполуки з (7S,9aR) стереохімію також можуть бути одержані використовуючи аналоги згаданому способу або інші розкриті способи. Стосовно Схеми 1, відому сполуку 29 78437 Формули II [наприклад, Bright, WO 99/52907] об'єднують з сполукою формули III, за умов конденсування Міцунобу, в присутності три фенілфосфіну і сполуки формули RO2CN=NCO2R, де R є метил або етил, з утворенням сполуки формули IV. [Дивіться О. Mitsunobu, Synthesis, 1 (1981)]. Придатними розчинниками для цієї реакції є тетрагідрофуран (ТГФ), інші етери і галогенвуглецеві розчинники, і ТГФ є переважним. Цю реакцію зазвичай проводять при температурі від приблизно кімнатної температури до приблизно 65°С, протягом від приблизно 1 до приблизно 24 годин. її переважно проводять приблизно при 50°С протягом приблизно 4-18 годин. Відновлення сполуки формули IV дає сполуку формули V. Це відновлення можна здійснити використовуючи літійалюмогідрид або інші гідриди алюмінію, як відновлюючий агент, в розчиннику, що вибирають з діетилового етеру і інших діалкілових етерів, переважно діетилового етеру, при температурі від приблизно -5°С до приблизно кімнатної температури, протягом від приблизно 0,5 до приблизно 18 годин. Сполуку формули V потім можна перетворити у сполуку формули VI піддаючи її взаємодії з метансульфонілхлоридом, в присутності третинної амінооснови, такої як триетиламін (TEA), в метиленхлориді або іншому галогенвуглецевому розчиннику, при температурі від приблизно -5°С до приблизно кімнатної температури, протягом від приблизно 10 хвилин до приблизно 2 годин. Реакція одержаної сполуки формули VI з сполукою формули HNR3R4, в якій R3 і R4, разом з азотом до якого вони приєднані утворюють кільце як зображено на Схемі 1, давала відповідну сполуку, що має Формулу VII. Типово, цю останню реакцію проводять в ТГФ, N,N-диметилформаміді (ДМФА) або ацетонітрилі, або суміші двох або більше згаданих розчинників, при температурі від приблизно кімнатної температури до приблизно 100°С, протягом від 1 до приблизно 18 годин. Схема 2 ілюструє спосіб одержання сполук формули І, що мають (7R, 9аS)-транс або (7S,9aS)-цис стереохімію. Стосовно Схеми 2, сполуку формули II можна перетворити у сполуку формули VIII за допомогою взаємодії її з метансульфонілхлоридом, в присутності третинної амінооснови, такої як триетиламін (TEA), в метиленхлориді або іншому галогенвуглецевому розчиннику, при температурі від приблизно -5°С до приблизно кімнатної температури, протягом від приблизно 10 хвилин до приблизно 2 годин. Сполуку Формули VIII об'єдн ують з сполукою формули III, за умов основного конденсування з утворенням сполуки формули IX. Придатними основами є гідрид натрію, гідрид калію, літійалкіл, бістриметилсиліламід натрію. Придатними розчинниками для цієї реакції є тетрагідрофуран (ТГФ), інші етери, диметилформамід і N-метилпіролідинон (NMP), і NMP є переважним. Цю реакцію зазвичай проводять при температурі від приблизно кімнатної температури до приблизно 100°С, протягом від приблизно 1 до приблизно 24 годин. її переважно проводять при температурі від приблизно 70°С до 30 приблизно 100°С. Зазвичай, реакція триває протягом приблизно 1-24 годин. Відновлення сполуки формули IX дає сполуку формули X. Це відновлення можна здійснити використовуючи літійалюмогідрид або інші гідриди алюмінію, як відновлюючий агент, в розчиннику, що вибирають з діетилового етеру і інших діалкілових етерів, переважно діетилового етеру, при температурі від приблизно -5°С до приблизно кімнатної температури, протягом від приблизно 0,5 до приблизно 18 годин. Сполуку формули X потім можна перетворити у сполуку формули XI, піддаючи її взаємодії з метансульфонілхлоридом, в присутності третинної амінооснови, такої як триетиламін (TEA), в метиленхлориді або іншому галоген вуглецевому розчиннику, при температурі від приблизно -5°С до приблизно кімнатної температури, протягом від приблизно 10 хвилин до приблизно 2 годин. Реакція одержаної сполуки формули XI з сполукою формули HNR3R4, в якій R3 і R4, разом з азотом до якого вони приєднані, утворюють кільце як зображено на Схемі 2, давала відповідну сполуку, що має Формулу XII. Типово, цю реакцію проводять в ТГФ, N,N-диметилформаміді (ДМФА) або ацетонітрилі, або суміші двох або більше згаданих розчинників, при температурі від приблизно кімнатної температури до приблизно 100°С, протягом від 1 до приблизно 18 годин. Схема 3 ілюструє спосіб одержання сполук Формули І, що мають (7R,9aS)-транс або (7S,9aS)цис стереохімію. Стосовно Схеми 3, сполуку формули II можна перетворити у сполуку формули XV за допомогою її реакції з сполукою формули XIV і придатною основою, такою як т-бутоксид калію в тетрагідрофурані, іншому етери або диметилформаміді, або галогенвуглецевому розчиннику. Придатними основами є гідрид натрію, гідрид калію, літійалкіл, бістриметилсиліламід натрію. Цю реакцію зазвичай проводять при температурі від приблизно кімнатної температури до приблизно 80°С, протягом від приблизно 1 до приблизно 24 годин. Її переважно проводять приблизно при 60°С протягом приблизно 1-12 годин. Сполуку Формули XIV можна одержати з сполуки формули XIII використовуючи сполуку формули HNR3R4, де R3 і R4, разом з азотом до якого вони приєднані утворюють кільце, як зображено на Схемі 3, і основи, такої як карбонат калію в розчиннику, такому як ацетонітрил. Придатними розчинниками для цієї реакції є тетрагідрофуран (ТГФ), інші етери, диметилформамід і галогенвуглецеві розчинники, і ацетонітрил є переважним. Придатними основами є гідрид натрію, карбонат калію, карбонат натрію, літійалкіл, бістриметилсиліламід натрію або літію, LDA. Цю реакцію зазвичай проводять при температурі від приблизно кімнатної температури до приблизно 80°С, протягом від приблизно 1 до приблизно 24 годин. її переважно проводять приблизно при 60°С протягом приблизно 1-12 годин. Схема 4 ілюструє спосіб одержання сполук Формули І, що мають (7R,9aS)-транс або (7S,9aS)цис стереохімію. Стосовно Схеми 4, сполуку формули XVI можна перетворити у сполук у формули XVII за допомогою її реакції з сполукою формули 31 78437 XIV і придатною основою, такою як т-бутоксид калію в тетрагідрофурані, інших етерах або диметилформаміді, або галогенвуглецевих розчинниках. Придатними основами є гідрид натрію, гідрид калію, літійалкіл, бістриметилсиліламід натрію. Цю реакцію зазвичай проводять при температурі від приблизно кімнатної температури до приблизно 80°С, протягом від приблизно 1 до приблизно 24 годин. Її переважно проводять приблизно при 60°С протягом приблизно 1-12 годин. Сполуку Формули XIV можна одержати з сполуки формули XIII використовуючи сполуку формули HNR 3R4, де R3 і R4, разом з азотом, до якого вони приєднані, утворюють кільце, як зображено на Схемі 4, і основу таку як карбонат калію в розчиннику, такому як ацетонітрил. Придатними розчинниками для цієї реакції є тетрагідрофуран (ТГФ), інші етери, диметилформамід і галогенвуглецеві розчинники, і ацетонітрил є переважним. Цю реакцію зазвичай проводять при температурі від приблизно кімнатної температури до приблизно 80°С, протягом від приблизно 1 до приблизно 24 годин. її переважно проводять приблизно при 60°С протягом приблизно 1-12 годин. З сполуки формули XVII потім знімають захист з утворенням кислотноадитивної солі з хлорводневою кислотою відповідної сполуки формули XVIII. Це можна здійснити використовуючи безводну хлорводневу кислоту (НСІ) в діетиловому етері, іншому діалкіловому етері або галогенвуглецевому розчиннику приблизно при кімнатній температурі. Цю реакцію також проводять без розчинника використовуючи трифтороцтову кислоту, в цьому випадку утворюється кислотноадитивна сіль бітрифтороцтової кислоти. Цю реакцію зазвичай протікає від приблизно 2 до приблизно 18 годин. Бажану відповідну сполуку формули XX можна одержати за допомогою взаємодії сполуки формули XVIII за вищезгаданою реакцією з прийнятною сполукою формули XIX, де R1 і R2 є такими як визначено вище для Формули І, і 1,8діазабіцикло[5.4.0]ундец-7-ен (DBU). Цю реакцію зазвичай проводять в піридині, при температурі від приблизно 50°С до приблизно 110°С, протягом від приблизно 1 до приблизно 48 годин. Схема 5 є альтернативним способом одержання сполук Формули І, що мають ту ж саму стереохімію в положеннях 7 і 9а як сполуки Формули XX і де амінометильний бічний ланцюг на феноксигрупі може бути приєднаним в будь-якому положенні (тобто орто, мета або пара) цієї групи. Стосовно Схеми 5, дигідрохлорид прийнятної сполуки Формули XVIII взаємодіє з син, анти або сумішшю син і анти ізомерів сполуки формули (тобто, прийнятно заміщеним бензогідроксиміноїлхлоридом), в присутності основи, такої як DBU, з утворенням відповідної сполуки формули XXI. Придатними розчинниками для цієї реакції є 32 хлорвуглеводні, такі як хлороформ і метиленхлорид. Придатна температура реакції знаходиться в інтервалі від приблизно -78°С до приблизно 50°С. Цю реакцію переважно проводять при температурі від приблизно 20°С до приблизно 40°С, протягом від приблизно 0,5 до приблизно 24 годин. Одержану сполуку формули XXI потім можна перетворити у бажану кінцеву сполуку формули XX шля хом взаємодії її з сильною нуклеофільною органічною основою (наприклад, н-бутиллітієм) або гідридом натрію. Цю реакцію типово проводять в розчиннику, такому як толуол, ДМФА або ТГФ, при температурі від приблизно кімнатної температури до приблизно 110°С, протягом від приблизно 1 до 48 годин. Переважно, розчинником є суміш толуолу і ТГФ і реакцію проводять при температурі від приблизно 80°С до приблизно 100°С. Якщо не вказано інше, тиск для кожної з вищезгаданих реакції не є критичним. Зазвичай, реакції проводять при тиску від приблизно одна до приблизно три атмосфери, переважно приблизно при нормальному тиску (приблизно, одна атмосфера). Сполуки формули І, які є основними за своєю природою, здатні утворювати велику кількість різних солей, з різними органічними та неорганічними кислотами. Не зважаючи на те, що такі солі повинні бути фармацевтично прийнятними для введення тваринам, на практиці часом бажано виділити сполуку формули І з реакційної суміші як фармацевтично неприйнятну сіль, та потім просто перетворити цю сіль у вільну основу, обробивши лужним реагентом, та потім перетворивши вільну основу на фармацевтично прийнятну кислотноадитивну сіль. Кислотно-адитивні солі основних сполук згідно з даним винаходом легко одержуються обробленням основної сполуки необхідною кількістю вибраної мінеральної або органічної кислоти у водному розчиннику або у придатному органічному розчиннику, такому як метанол або етанол. Шляхом ретельного випаровування розчинника, утворюють бажану тверду сіль. Кислотами, які використовуються для одержання фармацевтично прийнятних кислотно адитивних солей основних сполук згідно з даним винаходом, є такі, що утворюють нетоксичні кислотно-адитивні солі, тобто солі, що містять фармакологічно прийнятні аніони, такі як хлорводневу, гідробромідну, гідройодидну, нітратну, сульфатну або бісульфатну, фосфатну або кислотно фосфа тну, ацетатну, молочнокислу, цитратну або кислотну цитратну, виннокислу або бівиннокислу, сукцинатну, малеатну, фумаратну, глюконатну, сахаратну, бензоатну, метансульфонатну та памоатну [тобто, 1,1'-метилен-біс-(2-гідрокси-3нафтоат)] солі. Сполуки Формули І можуть переважно бути використаними у комбінації з одним або більше іншими терапевтичними агентами, наприклад, різними антидепресивними агентами такими як трициклічні антидепресанти (наприклад, амітриптилін, дотіепін, доксепін, триміпрамін, бутрипілен, кломпірамін, дезіпрамін, іміпрамін, іпріндол, лофепрамін, нортиптилін або протриптилін), інгібіторами моноаміноксидази (наприклад, ізокарбоксазид, фенелзін або транилциклопрамін), або з інгібіто 33 78437 рами повторного поглинання 5-НТ (наприклад, флувоксамін, сертралін, флуоксетин або пароксетин), та/або з агентами для лікування хвороби Паркінсона такими як допамінергічними агентами (наприклад, леводопа, переважно у комбінації з інгібітором периферійної декарбоксилази, наприклад, бензеразідом або карбідопою, або з агоністом допаміну, наприклад, бромкриптином, лізуридом або перголідом). Слід розуміти, що даний винахід включає використання сполуки загальної формули (І) або її фізіологічно прийнятної солі або сольвату у комбінації з одним або більше іншими терапевтичними агентами. Сполуки Формули І та їх фармацевтично прийнятні солі, у комбінації з інгібітором повторного поглинання 5-НТ (наприклад, флувоксаміном, сертраліном, флуоксетином або пароксетином), переважно сертраліном, або його фармацевтично прийнятною сіллю або поліморфом (комбінація сполуки Формули І з інгібітором повторного поглинання 5-НТ далі позначається як "активна комбінація"), корисні при фізіотерапії та можуть бути використані при лікуванні або попередженні розладів, лікуванню або попередженню яких сприяє модуляція серотонінергічної нейротрансмісії, таких як гіпертензія, депресії (наприклад, депресія у хворих на рак, депресія у хворих на хворобу Паркінсона, депресія після інфаркту міокарда, субсиндромально симптоматична депресія, депресія у безплідних жінок, педіатрична депресія, велика депресія, одиничні епізоди депресії, рекурентна депресія, депресія індукована ожирінням дітей, та післяпологова депресія), стан загального неспокою, фобії (наприклад, агорафобія, соціальна фобія та прості фобії), посттравматичний стрессиндром, аутизм, передчасна еяколяція, розлади харчування (наприклад, анорексія нервова та булімія нервова), ожиріння, хімічні залежності (наприклад, залежність від алкоголю, кокаїну, героїну, фенобарбіталу, нікотину та бензодіазепінів), "гістаміновий" головний біль, мігрень, біль, хвороба Альцгеймера, обесивно-компульсивний розлад, панічний розлад, розлади пам'яті (наприклад, деменція, амнезія, та вікові зміни когнітивних функцій (ВЗКФ)), хвороби Паркінсона (наприклад, деменція при хворобі Паркінсона, паркінсонізм індукований нейролептиками та пізні діскінезії), ендокринні розлади (наприклад, гіперпролектинемія), вазоспазм (особливо в церебральних судинах), мозочкова атаксія, розлади шлунково-кишкового тракту (перистальтики та секреції), негативні симптоми шизофренії, передменструальний синдром, синдроми фіброміалгії, нетримання при стресі, хвороба Туретта, тріхокриптоманія, клептоманія, чоловіча імпотенція, рак (наприклад, дрібноклітинна легенева карцинома), хронічна пароксизмальна гемікранія та головний біль (пов'язаний з судинними розладами). Дія інгібіторів повторного поглинання серотоніну (5-НТ), переважно сертраліну, направлена проти депресії; хімічних залежностей, станів неспокою, включаючи панічній розлад, станів загального неспокою, агорафобії, простих фобій, соціальної фобії, посттравматичного стрес-синдрому, обсесивно-компульсивного розладу, аутизму, пе 34 редчасної еякуляції у ссавців, включаючи людей, частково через їх здатність блокувати синаптосомальне поглинання серотоніну. Сертралін, (1S-цис)-4-(3,4-дихлорфеніл)1,2,3,4-тетрагідро-N-метил-1-нафталінамін, має хімічну формулу C17H17NCI2; його синтезописується в [патенті US 4,536,518] включеному сюди як посилання. Гідрохлорид сертраліну корисний як антидепресант і аноректичний агент, а також є корисним при лікуванні депресії, хімічної залежності, тривожних обсесисвно-компульсивних розладів, фобій, паніки, посттравматичого стрессиндрому і передчасної еяколяції. Активність активної комбінації як антидепресантів та пов'язаних фармакологічних властивостей може бути визначена нижчезазначеними способами (1)-(4), які описані у [Кое, В. et. al., Journal of Pharmacology and Experimental Therapeutics, 226 (3). 686-700 (1983)]. Зокрема, активність може бути визначена вивчивши (1) здатність вплинути на спроби мишей втекти від плаваючого баку (тест Порсолта на мишах "стан відчаю"), (2) здатність посилювати симптоми поведінки мишей in vivo, яка викликана 5-гідрокситриптофаном, (3) їх здатність антагонізувати активність, яка зменшує кількість серотоніну, гідрохлориду п-хлорамфетаміну в мозку пацюків in vivo, та (4) здатність блокувати поглинання серотоніну, норепінефрину та допаміну синаптосомальними клітинами мозку у пацюків in vitro. Здатність активної комбінації перешкоджати резерпіновій гіпотермії у мишей in vivo може бути визначена за допомогою способів описаних у [патенті US 4,029,731]. Сполуки винаходу можуть бути введені або окремо, або в комбінації з фармацевтично прийнятними носіями, в одиничній або розподіленій дозах. Придатними фармацевтичними носіями є інертні тверді розріджувачи або наповнювачі, стерильні водні розчини і різні органічні розчинники. Фармацевтичні композиції одержані таким чином можуть бути потім легко введені у вигляді різних дозованих форм, таких як таблетки, порошки, лозенги, рідкі рецептури, сиропи, ін'єктуємі розчини і їм подібні. Ці фармацевтичні композиції можуть, необов'язково, містити додаткові інгредієнти, такі як ароматизатори, зв'язувальні агенти, екціпієнти і їм подібні. Таким чином, сполуки винаходу може бути сформовані для перорального, букального, інтраназального, парентерального (наприклад, внутрішньовенного, внутрішньом'язового або підшкірного), трансдермального (наприклад, пластир) або ректального введення або у формі придатній для введення за допомогою інгаляції або вдування. Для перорального введення, фармацевтичні композиції можуть мати форму, наприклад, таблеток або капсул, що одержують загальновідомими шляхами використовуючи фармацевтично прийнятні екципієнти, такі як зв'язувальні агенти (наприклад, прежелатинізований кукурудзяний крохмаль, полівінілпіролідон або гідроксипропілметилцелюлозу); наповнювачі (наприклад, лактозу, мікрокристалічну целюлозу або фосфат кальцію); змащувальні агенти (наприклад, стеарат магнію, тальк або діоксид кремнію); дезінтегратори (наприклад, 35 78437 картопляний крохмаль або натрійгліколят крохмалю); або змочувальні агенти (наприклад, лаурилсульфат натрію). Таблетки можуть бути покриті, використовуючи способи добре відомі спеціалісту в цій галузі. Рідкі рецептури, для перорального введення, можуть мати форму, наприклад, розчинів, сиропів або суспензій, або вони можуть представляти собою сухий продукт, що розводиться водою або іншим придатним розчинником перед використанням. Такі рідкі рецептури можуть бути одержані використовуючи загальновідомі способи з фармацевтично прийнятних наповнювачів, таких як суспендувальні агенти (наприклад, сироп сорбіту, метилцелюлозу або гідрований їстівний жир); емульсифікуючі агенти (наприклад, лецетин або акацію); неводні розчинники (наприклад, мигдальну олію, естери жирів або етиловий спирт); і консерванти (наприклад, метил або пропіл пгідроксибензоати або сорбінова кислота). Для букального введення композиції можуть мати форму таблеток або коржиків і одержуватись з використанням загальновідомих методів. Сполуки згідно з винаходом можуть бути приготовані для парентерального введення шляхом ін'єкцій, включаючи використання відомих способів катетеризації або вливання. Рецептури для ін'єкцій можуть бути представлені у формах дозування, наприклад, в ампулах або в упаковці лікарських засобів для багаторазового прийому, з доданням консерванту. Композиції можуть мати форму суспензій, розчинів або емульсій у масляному або водному розчинниках, та можуть містити формуючі засоби такі як суспендувальні, стабілізувальні та/або диспергувальні засоби. Альтернативно, активний інгредієнт може бути у формі порошку для змішування з відповідним розчинником, наприклад, стерильною апірогенною водою, перед використанням. В наступному аспекті, цей винахід забезпечує композиції придатні для введення людині у вигляді розчину (наприклад, за допомогою ін'єкції або інтраназально), що містять комплекс включення солі сполук винаходу в матеріал, такий як циклодекстрин. Переважно, в переважному втіленні згаданий комплекс включення забезпечує кількість сполуки принаймні 2,5мгА/мл, коли кількість сполуки, що забезпечується згаданим комплексом вимірюється через концентрацію циклодекстрину 40% в/о у воді. Комплекс включення сполуки в циклодекстрин можна спочатку виділити висушуванням, зазвичай ліофілізацією. Виділений сухий комплекс включення можна зберігати при кімнатній температурі протягом часу до двох років і довше, і відновлювати у розчин продукт, коли необхідно. Коли потрібен розчин продукту, він може бути одержаний розчиненням виділеного комплексу включення у воді (або іншому водному середовищі) в кількості достатній для одержання розчину необхідної концентрації для перорального або парентерального введення пацієнтам. Якщо парентеральне введення є вибраним шляхом введення, внутрішньом'язова ін'єкція є переважною. Сполуки можуть бути сформовані у швидкодиспергуємі дозовані форми (шддф), які призначені для вивільнення активного інгредієнту в ротовій порожнині. Їх часто 36 одержують використовуючи швидкорозчинні матриці на основі желатину. Ці дозовані форми добре відомі і можуть бути використані для вивільнення широкого переліку лікарських засобів. Більшість швидкодиспергуємих дозованих форм використовують желатин як носій або структурноформуючий агент. Типово, желатин використовують для одержання достатньої стабільності дозованої форми для перешкоджання руйнування внаслідок виймання з упаковки, але негайно після поміщення в рот, желатин дозволяє негайне розчинення дозованої форми. Альтернативно, різні крохмалі використовуються для такої ж самої дії. Сполуки згідно з винаходом можуть мати форму ректальних композицій таких як супозиторії або клізми, що утримуються, наприклад які містять відомі супозиторні основи такі як масло какао або інші гліцериди. Для інтраназального введення або введення шляхом інгаляції, сполуки винаходу зазвичай вводяться у формі розчинів або суспензій з інгалятору, що здавлюється або накачується пацієнтом або у формі аерозольного спрею з герметичного контейнеру або розпилювача, з використанням придатного пропеланту, наприклад, дихлордифторметан, трихлорфторметан, дихлортетрафторетан, діоксид вуглецю або інші придатні гази. У випадку аерозолю у герметичному контейнері, дозована одиниця може бути визначена шляхом забезпечення клапаном, що вивільнює визначену кількість. Герметичний контейнер або розпилювач можуть містити розчин або суспензію активної сполуки. Капсули і картриджі (виготовляють, наприклад, з желатину) для використання в інгаляторі або інсульфлаторі можуть містити порошкоподібну суміш сполуки винаходу і придатну порошкоподібну основу, таку як лактоза або крохмаль. (Іншими рецептурами. Про які сліж згадати є: ІМ і швидкорозчинні FDDF Рекомендована доза активних сполук згідно з винаходом для перорального, парентерального або букального введення людині середнього віку для лікування вищеназваних станів (наприклад, депресії) є 0,1 - 200мг активного інгредієнта за один раз, який може призначатись, наприклад, від одного до 4 разів на день. Аерозольні рецептури для лікування вищезазначених станів (наприклад, мігрені) у людини середнього віку роблять таким чином, щоб кожна вимірюєма доза або "пшик" аерозолю, містила від приблизно 20мкг до приблизно 1000мкг сполуки винаходу. Повна добова доза аерозолю зазвичай буде знаходитися в інтервалі від приблизно 100мкг до 10мг. Призначатися вона може декілька разів на день, наприклад, 2, 3, 4 або 8 разів, одержуючи, наприклад, 1, 2 або 3 дози за раз. У зв'язку з використанням активної сполуки згідно з винаходом з інгібітором повторного поглинання 5-НТ, переважно сертраліном, для лікування хворих, у яких виявлено будь-який з вищеназваних станів, слід зазначити, що ці сполуки можуть бути призначені самостійно або у комбінації з фармацевтично прийнятними носіями, будь-яким з вищевказаних шля хів, і такі призначення можуть бути проведені в одноразовій або багаторазових 37 78437 дозах. Більш конкретно, активна комбінація може бути призначена у великій кількості різних форм дозування, тобто вони можуть бути скомбіновані з різними фармацевтично прийнятними інертними носіями у формі таблеток, капсул, пігулок, пастилок, твердих льодяників, порошків, спреїв, водних суспензій, розчинів для ін'єкцій, еліксирів, сиропів, і т.і. Такі носії включають тверді розріджувачі або наповнювачі, стерильні водні середовища та різні нетоксичні органічні розчинники, і т.д.. Більш того, такі оральні фармацевтичні композиції можуть бути відповідно підсолоджені та/або ароматизовані за допомогою різних засобів, які звичайно використовують для таких цілей. Загалом, сполуки формули І представлені у таких дозованих формах з рівнями концентрації, що лежать в межах приблизно від 0,5% до приблизно 90% від загальної ваги композиції, тобто, в кількості, достатній для забезпечення бажаної дози, та інгібітор повторного поглинання 5-НТ, переважно сертралін, представлений у таких дозованих формах з рівнями концентрації, що лежать в межах приблизно від 0,5% до приблизно 90% від загальної ваги композиції, тобто, в кількостях достатніх для забезпечення бажаного дозування. Рекомендована денна доза активної сполуки згідно з винаходом в комбінованій рецептурі (рецептурі, що містить активну сполук у згідно з винаходом та інгібітор повторного поглинання 5-НТ) для перорального, парентерального, ректального або букального введення людині середнього віку для лікування вищезазначених станів становить приблизно від 0,01мг до приблизно 2000мг, переважно приблизно від 0,1мг до приблизно 200мг активного інгредієнта Формули І на одноразову дозу, яка може бути введена, наприклад, від 1 до 4 разів на день. Рекомендована денна доза інгібітору повторного поглинання 5-НТ, переважно сертраліну, в композиціях для перорального, парентерального або букального призначення людині середнього віку для лікування вищезазначених станів становить приблизно від 0,1мг до приблизно 2000мг, переважно від приблизно 1мг до приблизно 200мг інгібітору повторного поглинання 5-НТ на одноразову дозу, яка може бути введена, наприклад, від 1 до 4 разів на день. Переважне відношення дози сертраліну до активної сполуки згідно з даним винаходом в композиції для перорального, парентерального або букального введення людині середнього віку для лікування вищезазначених станів становить приблизно від приблизно 0,00005 до приблизно 20000, переважно приблизно від 0,25 до приблизно 2000. Аерозольні комбіновані рецептури для лікування вищезазначених станів у людини середнього віку роблять таким чином, щоб кожна вимірюєма доза або "пшик" аерозолю, містила приблизно від 0,01мг до приблизно 100мг активної сполуки згідно з винаходом, переважно приблизно від 1мг до приблизно 10мг такої сполуки. Аерозольні рецептури можуть призначатися декілька разів на день, наприклад, 2, 3, 4 або 8 разів, приймаючи, наприклад, 1,2 або 3 дози кожного разу. 38 Аерозольні рецептури для лікування вищезазначених станів у людини середнього віку роблять таким чином, щоб кожна вимірюєма доза або "пшик" аерозолю містила приблизно від 0,01мг до приблизно 2000мг інгібітору повторного поглинання 5-НТ, переважно сертраліну, переважно приблизно від 1мг до приблизно 200мг сертраліну. Призначати можна декілька разів на день, наприклад, 2, 3, 4 або 8 разів, приймаючи 1, 2 або 3 дози кожного разу. Як було зазначено раніше, інгібітор повторного поглинання 5-НТ, переважно сертралін, у комбінації з сполуками Формули І легко пристосовується до терапевтичного використання у якості антидепресивних агентів. Загалом, ці антидепресивні композиції, які містять інгібітор повторного поглинання 5-НТ, переважно сертралін, та сполука формули І звичайно вводять у межах від приблизно 0,01мг до приблизно 100мг інгібітору повторного поглинання 5-НТ, переважно сертраліну, на кілограм маси тіла на день, переважно приблизно від 0,1мг до приблизно 10мг сертраліну на кілограм маси тіла на день; приблизно від 0,001мг до приблизно 100мг сполуки формули І на кілограм ваги тіла на день, переважно приблизно від 0,01мг до приблизно 10мг сполуки Формули І на кілограм ваги тіла на день, хоча можуть бути внесені зміни, враховуючи стан хворого, який проходить лікування, а також спосіб застосування. Наступні приклади ілюструють одержання різних сполук представленого винаходу. Точки плавлення некоригували. Дані ЯМР проводили в мільйонних частках відносно сигналу дейтерію з зразка розчинника (дейтерохлорофом, якщо не зазначено інше). Особливі ротації були виміряні при кімнатній температурі, використовуючи довжину хвилі натрію D (589нм). Комерційні реагенти використовували без подальшого очищення. ТГФ означає тетрагірофуран. ДМФА означає N,Nдиметилформамід. Під хроматографією розуміють колонкову хроматографію з використанням силікагелю з ступенем зернистості 47-61, яка виконувалась під тиском азоту (флеш-хроматографія). Кімнатна температура або температура навколишнього середовища - 20-25°С. Для зручності, усі неводні реакції проводили в атмосфері азоту для збільшення виходу. Концентрація при зменшеному тиску означає, що використовували роторний випаровувач. Приклади є тільки ілюстрацією; вони не повинні розглядатись як обмеження рамок, сутності і варіацій винаходу. Приклад 1 (7R,9аS)-транс-Циклогексил-{6-[2-(5фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2а]піразин-7-ілметокси]піридин-2-ілметил}амін Стадія 1 (7R,9аS)-транс-[2-(5-фторбензо[d]ізоксазол-3іл)октагідропіридо-1,2-а]піразин-7-іл]метанол (Октагідрохіназолін-3-іл)метанол (5,42г, 26,2ммоль), 1,8-діазобіцикло[5.4.0]ундец-7-ен (12,9мл, 85ммоль) і 3-хлор-5фторбензо[d]ізоксазол (5,54г, 32,3ммоль) розчиняли в піридині (16мл) і потім нагрівали (110°С) при перемішуванні протягом 18 годин. Додавали 10% водний бікарбонат натрію і метиленхлорид (250мл 39 78437 кожного) і суміш інтенсивно перемішували. Водну фазу потім екстрагували трьома 100мл порціями свіжого метиленхлориду. Об'єднані органічні екстракти сушили (безводний сульфат натрію) і концентрували у вакуумі до аморфної твердої речовини (4,88г). Флеш хроматографія всього зразка (силікагель, 47-61 мікрон меш; елюювали метанол/метиленхлорид=6,94 об'ємних) давала вказану в заголовку сполуку (3,46г, 43% вихід) як аморфну тверду речовину. МС m/z 306 (М+1). Стадія 2 (7R,9аS)-транс-6-[2-(5-Фторбензо[d]ізоксазол3-іл)октагідропіридо[1,2-а]піразин-7ілметокси]піридин-2-карбонової кислоти метиловий естер До розчину вказаної в заголовку попередньої стадії сполуки (3,05г, 10,0ммоль) в тетрагідрофурані (35мл) додавали 6-метил-2-гідроксипіколінат (1,91г, 12,5ммоль), діетилазодикарбоксилат (1,1мл, 12,0ммоль) і трифенілфосфін (3,14г, 12,0). Розчин нагрівали (50°С) і перемішували протягом 18 годин. Додавали 10% водний бікарбонат натрію і метиленхлорид (100мл кожного) і суміш інтенсивно перемішували. Водну фазу потім екстрагували трьома 50мл порціями свіжого метиленхлориду. Об'єднані органічні екстракти, в свою чергу, послідовно екстрагували 1N водним гідроксидом натрію і 10% водним бікарбонатом натрію. Відокремлену органічну фазу сушили (безводний сульфат натрію) і розчинник видаляли у вакуумі, одержуючи липку тверду речовину. Флеш хроматографія зразка давала вказану в заголовку сполуку (2,14г, 48% вихід) як білу тверду речовину. Діагностична 1Н ЯМР (400МГц, CDCI3) 1,18-1,78 (м, 3Н), 1,90-2,15 (м, 4Н), 2,41-2,58 (м, 1Н), 2,81-2,95 (м, 2Н), 3,013,08 (м, 1Н), 3,20-3,40 (м, 1Н), 3,74-3,88 (м, 2Н), 3,93 (с, 3Н), 4,17 (дд, 1Н, J=10,8 і 7,1Гц), 4,28 (дд, 1Н, J=10,8 і 5,4Гц), 6,87-6,92 (м, 1Н), 7,18-7,21 (м, 1Н), 7,29 (дд, 1Н, J=9,3 і 2,5Гц), 7,36 (дд, 1Н, J=9,1 і 3,8Гц), 7,63-7,69 (м, 2Н); МС m/z 441,3 (М+Н). Стадія 3 (7R,9аS)-транс-{6-[2-(5-Фторбензо[d]ізоксазол3-іл)октагідропіридо[1,2-а]піразин-7ілметокси]піридин-2-іл}метанол До добре перемішуваного охолоджуємого на льодяній бані розчину вказаної в заголовку попередньої стадії сполуки (440мг, 1,0ммоль) в тетрагідрофурані (10мл) по краплям додавали 1,0М тетрагідрофурановий розчин літійалюмогідриду (1,2мл, 1,20ммоль). Реакційну суміш потім інтенсивно перемішували при 0°С протягом 1 години і потім гасили обережно додаючи по краплям загалом 1мл 1N водного гідроксиду натрію. Після перемішування при кімнатній температурі протягом 30 хвилин, суміш сушили безводним сульфатом натрію і потім фільтрували крізь целіт. Розчинник видаляли у вакуумі одержуючи масло. Флеш хроматографія зразка давала вказану в заголовку сполуку як білу тверду речовину (162мг; 39% вихід). Діагностична С13 ЯМР (100МГц, CDCI3) 3,78 (д, 1Н, J=12,9Гц), 3,87 (д, 1Н, J=12,6Гц), 4,08-4,23 (м, 2Н), 4,63 (с, 2Н), 6,59 (д, 1Н, J=8,2Гц), 6,76 (д, 1Н, J=7,5Гц), 7,19-7,39 (м, 3Н), 7,53 (т, 1Н, J=7,4Гц); МС m/z 413,3 (М+Н). Стадія 4 40 (7R,9аS)-транс-Метансульфонової кислоти 6[2-(5-фторбензо[d]ізоксазол-3іл)октагідропіридо[1,2-а]піразин-7ілметокси]піридин-2-ілметиловий естер До добре перемішуваної суміші вказаної в заголовку попередньої стадії сполуки (162мг, 0,39ммоль) (частково розчинена) і триетиламіну (0,11мл, 0,79ммоль) в метиленхлориді (10мл), при кімнатній температурі, додавали метансульфонілхлорид (34мкл, 0,43ммоль). Реакцію перемішували протягом 12г і потім гасили 10% водним бікарбонатом натрію. Реакційну суміш екстрагували трьома 10мл свіжими порціями метиленхлориду. Об'єднані органічні екстракти сушили (безводний сульфат натрію) і концентрували у вакуумі. Масло очищали за допомогою флеш-хроматографії одержуючи вказану в заголовку сполуку як білу тверду речовину (58мг, 30%). Продукт використовували на наступній стадії без подальшого очищення. Діагностична 1Н ЯМР (400МГц, CDCI3) 5,16 (с, 3Н); МС m/z 491,4 (М+Н). Стадія 5 Загальна Методика: Реакційну суміш, що складається з мезилату вказаної в заголовку попередньої стадії сполуки (0,035ммоль, 17,2мг) і прийнятного аміну (0,15ммоль) в ацетонітрилі (1мл) перемішували в 2-горлій колбі при 90°С протягом 12 годин. Після охолодження, до кожної колби додавали 0,75мл гідроксиду натрію і 2,2мл етилацетату. Після перемішування, органічний шар відокремлювали і пропускали крізь Na2SO4 (6мл колонка SPE, 2г). Екстрагування повторювали більше 2 разів метиленхлоридом. Розчинник видаляли і залишок розчиняли в 1,0мл ДМСО і фільтрували крізь 0,45 MM N ylon Acrodisc в 12´32мм ВЕРХ колби для очищення аміну (0,15ммоль) в 2-горлі колби додавали мезилат і 0,9мл сухого ацетонітрилу. Реакцію збовтували і нагрівали при 80°С протягом 12г в закритій колбі. (7R9аS)-транс-Циклогексил-{6-[2-(5фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2а]піразин-7-ілметокси]піридин-2-ілметил}амін. Вказаний мезилат одержаний вище, (7R,9аS)транс-Метансульфонової кислоти 6-[2-(5фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2а]піразин-7-ілметокси]піридин-2-ілметиловий естер і циклогексиламін об'єднували після Стадії 5 вище. Очищали використовуючи препаративну ВЕРХ колонку одержуючи вказану в заголовку сполуку: Waters Symmetry (C18, 5мкМ, 30´150мм, потік 20мл/хв, 0,1% TFA/CH3CN), ЧУ=6,66хв. МС m/z 493,6. В Прикладах 2-18 вказані в заголовках сполуки одержували використовуючи Загальну Методику Прикладу 1, Стадія 5, очищали використовуючи препаративну ВЕРХ колонку і у всіх Waters Symmetry (C18, 5мкМ, 30´150мм, Потік 20мл/хв, 0,1% TFA/CH3CN). Ви хідний матеріал вказаний для кожного прикладу: Приклад 2 (7R,9аS)-транс-2-(Етил-{6-[2-(5фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2а]піразин-7-ілметокси]піридин-2ілметил}аміно)етанол. 41 78437 Вихідний матеріал: 2-етиламіноспирт. ЧУ=7,60хв. МС m/z 483,6 Приклад 3 (7R,9аS)-транс-7-[6-(2,6-Диметилпіперидин-1ілметил)піридин-2-ілоксиметил]-2-(5фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2а]піразин. Вихідний матеріал: 2,6-диметилпіперидин. ЧУ=7,76хв. МС m/z 507,7 Приклад 4 (7R,9aS)-транс-1-(1-{6-[2-(5Фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2а]піразин-7-ілметокси]піридин-2-ілметил}-4фенілпіперидин-4-іл)етанон. Вихідний матеріал: 4-ацетил-4фенілпіперидин. ЧУ=7,78хв. МС m/z 597,1. Приклад 5 (7R,9аS)-транс-(1,2-Диметилпропіл)-{6-[2-(5фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2а]піразин-7-ілметокси]піридин-2-ілметил}амін Вихідний матеріал: 1,2-диметилпропіламін. ЧУ=7,89хв. МС m/z 481,6. Приклад 6 (7R,9аS)-транс-Циклопропіл-{6-[2-(5фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2а]піразин-7-ілметокси]піридин-2-ілметил}амін. Вихідний матеріал: циклопропіламін. ЧУ=3,87хв. МС m/z 451,2. Приклад 7 (7R,9аS)-транс-Циклопропілметил-[6-[2-(5фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2а]піразин-7-ілметокси]піридин-2-ілметил}амін. Вихідний матеріал: циклопропілметиламін. ЧУ=3,91хв. МС m/z 465,3. Приклад 8 (7R,9аS)-транс-(4-Хлорбензил)-{6-[2-(5фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2а]піразин-7-ілметокси]піридин-2-ілметил}амін. Вихідний матеріал: 4-хлорбензиламін. ЧУ=4,11хв. МС m/z 535,2. Приклад 9 (7R,9аS)-транс-{6-[2-(5-Фторбензо[d]ізоксазол3-іл)октагідропіридо[1,2-а]піразин-7ілметокси]піридин-2-ілметил}-[2-(1-метилпіролідин2-іл)етил]амін. Вихідний матеріал: 2-(1-метилпіролідин-2іл)етиламін. ЧУ=3,77хв. МС m/z 522,3. Приклад 10 (7R,9аS)-транс-2-(5-Фторбензо[d]ізоксазол-3іл)-7-[6-(4-метилпіперазин-1-ілметил)піридин-2ілоксиметил]октагідропіридо[1,2-а]піразин. Вихідний матеріал: N-метилпіперазин МС m/z 494,3. Приклад 11 (7R,9aS)-транс-2-(5-Фторбензо[d]ізоксазол-3іл)-7-(6-піперидин-1-ілметилпіридин-2ілоксиметил)октагідропіридо[1,2-а]піразин. Вихідний матеріал: піперидин. ЧУ=3,88хв. МС m/z 479,3. Приклад 12 (7R,9aS)-транс-{6-[2-(5-Фторбензо[d]ізоксазол3-іл)октагідропіридо[1,2-а]піразин-7ілметокси]піридин-2-ілметил}диметиламін. Вихідний матеріал: диметиламін. ЧУ=3,82хв. МС m/z 439,2. 42 Приклад 13 (7R,9aS)-транс-{6-[2-(5-Фторбензо[d]ізоксазол3-іл)октагідропіридо[1,2-а]піразин-7ілметокси]піридин-2-ілметил}-(тетрагідрофуран-2ілметил)амін. Вихідний матеріал: тетрагідрофуран-2ілметиламін. ЧУ=3,89хв. МС m/z 495,3. Приклад 14 (7R,9aS)-транс-7-[6-(2,5-Диметилпіролідин-1ілметил)піридин-2-ілоксиметил]-2-(5фторбензо[d]ізоксазол-3-іл)октагідропіридо[1,2а]піразин. Вихідний матеріал: 2,5-диметилпіролідин ЧУ=3,92хв. МС m/z 493,3. Приклад 15 (7R,9aS)-транс-{6-[2-(5-Фторбензо[d]ізоксазол3-іл)октагідропіридо[1,2-а]піразин-7ілметокси]піридин-2-ілметил}-(2,2,2трифторетил)амін. Вихідний матеріал: 2,2,2-трифторетиламін. ЧУ=3,91хв. МС m/z 493,2. Приклад 16 (7R,9aS)-транс-{6-[2-(5-Фторбензо[d]ізоксазол3-іл)октагідропіридо[1,2-а]піразин-7ілметокси]піридин-2-ілметил}-[3-(4метилпіперазин-1-іл)пропіл]амін. Вихідний матеріал: 3-(4-метилпіперазин-1іл)пропіламін. ЧУ=3,74хв. МС m/z 551,3. Приклад 17 (7R,9aS)-транс-{6-[2-(5-Фторбензо[d]ізоксазол3-іл)октагідропіридо[1,2-а]піразин-7ілметокси]піридин-2-ілметил}піролідин-1-іламін. Вихідний матеріал: 1-амінопіролідин. ЧУ=3,84хв. МС m/z 480,3 Приклад 18 (7R,9aS)-транс-7-(6-Азепан-1-ілметилпіридин2-ілоксиметил)-2-(5-фторбензо[d]ізоксазол-3іл)октагідропіридо[1,2-а]піразин. Вихідний матеріал: цикпогептиламін. ЧУ=3,93хв. МС m/z 493,3. Приклад 19 Стадія 1 (7R,9aS)-транс-[2-бензо[d]ізоксазол-3іл)октагідропіридо-1,2-a]піразин-7-іл]метанол (Октагідро-хіназолін-3-іл)метанол (5,42г, 26,2ммоль), 1,8-діазобіцикло[5.4.0]-ундец-7-ен (12,9мл, 85ммоль) і 3-хлорбензо[d]ізоксазол (5,54г, 32,3ммоль) розчиняли в піридині (16мл) і потім нагрівали (110°С) при перемішуванні протягом 18 годин. Додавали 10% водний бікарбонат натрію і метиленхлорид (250мл кожного) і суміш інтенсивно перемішували. Водну фазу потім екстрагували трьома 100мл порціями свіжого метиленхлориду. Об'єднані органічні екстракти сушили (безводний сульфат натрію) і концентрували у вакуумі до аморфної твердої речовини (4,88г). Флеш хроматографія всього зразка (силікагель, 47-61 мікрон меш; елюювали метанол/метиленхлорид=6,94 об'ємних) давала вказану в заголовку сполуку (3,46г, 43% вихід) як аморфну тверду речовину. MC m/z 306(M+1). Стадія 2 (7R,9aS)-транс-5-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7 43 78437 ілметокси)піридин-2-карбонової кислоти метиловий естер До добре перемішуваної суміші вказаної в заголовку попередньої стадії сполуки (1,49г, 5,0ммоль) (частково розчинена) і триетиламіну (1,4мл, 10,0ммоль) в метиленхлориді (40мл), при кімнатній температурі, додавали метансульфонілхлорид (0,86мл, 5,5ммоль). Реакцію перемішували протягом 12г і потім гасили 10% водним бікарбонатом натрію. Реакційну суміш екстрагували трьома 10мл свіжими порціями метиленхлориду. Об'єднані органічні екстракти сушили (безводний сульфат натрію) і концентрували у вакуумі. Масло очищали за допомогою флеш-хроматографії одержуючи відповідний мезилат. Продукт використовували на наступній стадії без подальшого очищення. До 5-метил-2-гідроксинікотинату (0,92г, 17ммоль) в тетрагідрофурані (50мл) додають 0,18г (6,0ммоль) гідриду натрію (60% в мінеральному маслі). Реакцію нагрівали при 100°С протягом 1г. Мезилат одержаний вище розчиняли в 10мл тетрагідрофурану і додавали до реакційної суміші. Розчин нагрівали (100°С) і перемішували протягом 18 годин. Реакцію концентрували і фільтр ували етиловим етером. Відокремлену органічну фазу сушили (безводний сульфат натрію) і розчинник видаляли у вакуумі. Флеш хроматографія зразка давала вказану в заголовку сполуку (440мг, 21% вихід) як майже білу тверду речовину. Діагностична 1Н ЯМР (400МГц, CDCI3) 1,17-1,25 (м, 1Н), 1,291,39 (м, 1Н), 1,75-1,80 (м, 1Н), 1,85-1,98 (м, 2Н), 2,09-2,15 (м, 2Н), 2,51-2,59 (м, 1Н), 2,80-2,90 (м, 2Н), 3,08 (д, 1Н, J=8,8Гц), 3,20-3,35 (м, 1Н), 3,84 (с, 3Н), 3,78 (д, 1Н, J=13,3Гц), 4,12 (дд, 1Н, J=10,4 і 7,4Гц), 4,27 (дд, 1Н, J=10,4 і 5,4Гц), 6,72 (дц, 1Н, J=9,7 і 0,8Гц), 7,17-7,21 (м, 1Н), 7,41-7,48 (м, 2Н), 7,66 (д, 1Н, J=7,9Гц), 8,11 (дд, 1Н, J=8,7 і 2,4Гц), і 8,76-8,78 (м, 1Н). Стадія 3 (7R,9aS)-транс-[5-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-іл]метанол До добре перемішуваного охолоджуємого на льодяній бані розчину вказаної в заголовку попередньої стадії сполуки (991мг, 2,35ммоль) в тетрагідрофурані (30мл) по кралям при 0°С додавали 1,0М тетрагідрофурановий розчин літійалюмогідриду (4,7мл, 4,70ммоль). Реакційну суміш потім інтенсивно перемішували протягом 1 години і потім гасили обережно по краплям додаючи (при 0°С) загалом 1мл 1N водного гідроксиду натрію. Після перемішування при кімнатній температурі протягом 30 хвилин, суміш сушили безводним сульфатом натрію і потім фільтрували крізь целіт. Розчинник видаляли у вакуумі і флеш хроматографія зразка давала вказану в заголовку сполуку як білу тверду речовину (447мг; 48% вихід). Діагностична 1Н ЯМР (400МГц, CDCI3) 3,87 (д, 1Н, J=12,9Гц), 3,96 (д, 1Н, J=12,4Гц), 4,06 (дд, 1Н, J=10,8 і 5,4Гц), 4,59 (д, 2Н, J=5,4Гц), 6,70 (д, 1Н, J=8,8Гц), 7,17-7,21 (м, 1Н), 7,42-7,49 (м, 2Н), 7,59 (дд, 1Н, J=8,7 і 2,5Гц), 7,65 (д, 1Н, J=7,9Гц), 8,06 (д, 1 З, J=2,5Гц); МС m/z 395,2 (М+Н). 44 Стадія 4 (7R,9аS)-транс-Метансульфонової кислоти 5(2-бензо[d]ізоксазол-3-іл-октагідропіридо[1,2а]піразин-7-ілметокси)піридин-2-ілметиловий естер До добре перемішуваної суміші вказаної в заголовку попередньої стадії сполуки (148мг, 0,38ммоль) (частково розчинена) і триетиламіну (0,1мл, 0,75ммоль) в метиленхлориді (5мл), при кімнатній температурі, додавали метансульфонілхлорид (40мкл, 0,05ммоль). Реакцію потім перемішували протягом 1г і потім гасили 10% водним бікарбонатом натрію (додаючи 20мл метиленхлориду). Реакційну суміш екстрагували трьома 10мл свіжими порціями метиленхлориду. Об'єднані органічні екстракти сушили (безводний сульфат натрію) і концентрували у вакуумі одержуючи вказану в заголовку сполуку як в'язке масло. Продукт використовували на наступній стадії без подальшого очищення. Стадія 5 Загальна Методика є наступною: Реакційну суміш, що містить (7R,9aS)-транс-Метансульфонової кислоти 5-(2-бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин2-ілметиловий естер з попередньої стадії (0,03ммоль, 14,2мг) і прийнятного аміну (0,12ммоль) в ацетонітрилі (1мл) перемішували в 2-горлій колбі при 90°С протягом 12 годин. Після охолодження, розчинник видаляли і залишок розчиняли в 1,8мл ДМСО і фільтрували крізь 0,45 MM Nylon Acrodisc в 12´32мм ВЕРХ колби для очищення. Вказані в заголовках Прикладів 20-39 сполуки одержували використовуючи Загальну Методику Прикладу 19, Стадія 5, очищали використовуючи препаративну ВЕРХ колонку і всі з Waters Symmetry (C18, 5мкМ, 30´150мм, Потік 20мл/хв, 0,1% TFA/CH3CN). Ви хідний матеріал вказаний для кожного прикладу: Приклад 20 (7R,9аS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(3-метилізоксазол-4іл)амін. Вихідний матеріал: 3-метил-4-аміноізоксазол ЧУ=3,92хв. МС m/z 474,2. Приклад 21 (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]тіазол-2-іламін. Вихідний матеріал: 2-амінотіазол. ЧУ=4,15хв. МС m/z 476,2 Приклад 22 (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(3-метилізоксазол-5іл)амін. Вихідний матеріал: З-метил-5-аміноізоксазол. ЧУ=4,16хв. МС m/z 474,2 Приклад 23 (7П,9аЗ)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(3-метилпіридин-4іл)амін. 45 78437 Вихідний матеріал: 3-метил-4-амінопіридин. ЧУ=3,90хв. МС m/z 484,3 Приклад 24 (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(5-метил-2Н-піразол3-іл)амін. Вихідний матеріал: 5-метил-3-амінопіразол. ЧУ=3,85хв. МС m/z 473,3 Приклад 25 (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(5-метилпіридин-2іл)амін. Вихідний матеріал: 5-метил-2-амінопіридин. ЧУ=4,18хв. МС m/z 484,3 Приклад 26 (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(1Н-піразол-3іл)амін. Вихідний матеріал: 3-амінопіразол. ЧУ=3,35хв. МС m/z 459,2. Приклад 27 (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил-(6-метилпіридин-2іл)амін. Вихідний матеріал: 6-метил-2-амінопіридин. ЧУ=3,86хв. МС m/z 484,3 Приклад 28 (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]піридин-2-іламін. Вихідний матеріал: 2-амінопіридин. ЧУ=3,84хв. МС m/z 470,2 Приклад 29 (7R,9аS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3ілметил]циклопропілметиламін. Вихідний матеріал: цикпопропілетиламін. ЧУ=3,86хв. МС m/z 447,3 Приклад 30 (7R,9аS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(2-морфолін-4ілетил)амін. Вихідний матеріал: 2-(4-морфоліно)етиламін. ЧУ=3,98хв. МС m/z 506,3. Приклад 31 (7R,9аS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]піримідин-4-іламін. Вихідний матеріал: 4-амінопіримідин. ЧУ=3,66хв. МС m/z 471,2. Приклад 32 (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]циклопропіламін. Вихідний матеріал: циклопропіламін. ЧУ=3,88хв. МС m/z 433,2 Приклад 33 (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3ілокгагідропіридо[1,2-а]піразин-7 46 ілметокси)піридин-3-ілметил]-(6-метоксипіридин-3іл)амін. Вихідний матеріал: 6-метокси-2-амінопіридин. ЧУ=3,99хв. МС m/z 500,3 Приклад 34 (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(2-піролідин-1ілетил)амін. Вихідний матеріал: 1-(2-піролідино)етиламін ЧУ=3,89хв. МС m/z 490,3. Приклад 35 (7R,9aS)-транс-2-Бензо[d]ізоксазол-3-іл-7-[5-(4метил-[1,4]діазепан-1-ілметил)піридин-2ілоксиметил]октагідропіридо[1,2-а]піразин. Вихідний матеріал: 1-метилгомопіперазин. ЧУ=3,88хв. МС m/z 490,3. Приклад 36 (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(тетрагідрофуран-2ілметил)амін. Вихідний матеріал: 2(амінометил)тетрагідрофуран. ЧУ=3,89хв. МС m/z 477,2. Приклад 37 (7R,9аS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(1-фенілетил)амін Вихідний матеріал: 1-фенілетиламін. МС m/z 498,1 (М+1). Приклад 38 (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]піридин-3ілметиламін Вихідний матеріал: 3-піридилметиламін. МС m/z 485,1 (М+1). Приклад 39 (7R,9аЗ)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]піридин-3-іламін Вихідний матеріал: 3-піридилметиламін: преп. ВЕРХ колонка. МС m/z 471,1 (М+1). Приклад 40 (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]тіазол-2-іламін. Стадія 1 (7R,9aS)-транс-[2-бензо[R]ізоксазол-3іл)октагідропіридо-1,2-а]піразин-7-іл]метанол (Октагідро-хіназолін-3-іл)метанол (5,42г, 26,2ммоль), 1,8-діазобіцикло[5.4.0]-ундец-7-ен (12,9мл, 85ммоль) і 3-хлорбензо[d]ізоксазол (5,54г, 32,3ммоль) розчиняли в піридині (16мл) і потім нагрівали (110°С) при перемішуванні протягом 18 годин. Додавали 10% водний бікарбонат натрію і метиленхлорид (250мл кожного) і суміш інтенсивно перемішували. Водну фазу потім екстрагували трьома 100мл порціями свіжого метиленхлориду. Об'єднані органічні екстракти сушили (безводний сульфат натрію) і концентрували у вакуумі до аморфної твердої речовини (4,88г). Флеш хроматографія всього зразка (силікагель, 47-61 мікрон меш; елюювали метанол/метиленхлорид=6,94 47 78437 об'ємних) давала вказану в заголовку сполуку (3,46г, 43% вихід) як аморфну тверду речовину. МС m/z 306 (М+1). Стадія 2 (7R,9aS)-транс-6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-карбонової кислоти метиловий естер До розчину вказаної в заголовку попередньої стадії сполуки (4,07г, 14,18ммоль) в тетрагідрофурані (50мл) додавали 6-метил-2-гідроксипіколінат (3,25г, 21,3ммоль), діетилазодикарбоксилат (2,7мл, 17,0ммоль) і трифенілфосфін (4,46г, 17,0ммоль). Розчин нагрівали (50°С) і перемішували протягом 18 годин. Додавали 10% водний бікарбонат натрію і метиленхлорид (100мл кожного) і суміш інтенсивно перемішували. Водну фазу потім екстрагували трьома 50мл порціями свіжого метиленхлориду. Об'єднані органічні екстракти, в свою чергу, послідовно екстрагували 1N водним гідроксидом натрію і 10% водним бікарбонатом натрію. Відокремлену органічну фазу сушили (безводний сульфат натрію) і розчинник видаляли у вакуумі. Флеш хроматографія зразка давала вказану в заголовку сполуку (3,39г, 56% вихід) як білу тверду речовину. Діагностична 1Н ЯМР (400МГц, CDCI3) 1,21-1,29 (м, 1Н), 1,40-1,79 (м, 2Н), 1,951,99 (м, 1Н), 2,01-2,09 (м, 1Н), 2,20-2,40 (м, 2Н), 2,50-2,60 (м, 1Н), 2,80-3,02 (м, 2Н), 3,20-3,45 (м, 1Н), 3,87 (д, 1Н, J=12,5Гц), 3,92 (с, 3Н), 3,97 (д, 1Н, J=11,7Гц), 4,16-4,29 (м, 1Н), 4,20-4,31 (м, 1Н), 6,89 (дд, 1Н, J=7,1 і 2,5Гц), 7,17-7,21 (м, 1Н), 7,40-7,52 (м, 2Н), 7,61-7,68 (м, 3Н); С13 ЯМР 52,9, 60,9, 110,8, 115,5, 119,2, 121,9, 122,9, 130,1, 139,4, 145,5, 164,3. Стадія З (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-іл]метанол До добре перемішуваного охолоджуємого на льодяній бані розчину вказаної в заголовку попередньої стадії сполуки (2,76г, 6,54ммоль) в тетрагідрофурані (30мл) по краплям додавали 1,0М тетрагідрофурановий розчин літійалюмогідриду (7,0мл, 7,0ммоль). Реакційну суміш перемішували при 0°С протягом 1 годин і потім гасили обережно по краплям додаючи (при 0°С) загалом 1мл 1N водного розчину гідроксиду натрію. Після перемішування при кімнатній температурі протягом 30 хвилин, суміш сушили безводним сульфатом натрію і потім фільтрували крізь целіт. Розчинник видаляли у вакуумі одержуючи масло. Флеш хроматографія зразка давала вказану в заголовку сполуку як білу тверду речовину (2,05г; 50% вихід). Діагностична 1Н ЯМР (400МГц, CDCI3) 1,15-1,25 (м, 1Н), 1,40-1,60 (м, 1Н), 1,80-2,05 (м, 3Н), 2,202,40 (м, 2Н), 2,51-2,60 (м, 1Н), 2,93-3,05 (м, 2Н), 3,13-3,15 (м, 1Н), 3,39-3,42 (м, 2Н), 3,87 (д, 1Н, J=12,9Гц), 3,98 (д, 1Н, J=12,1Гц), 4,06-4,11 (м, 1Н), 4,20-4,24 (м, 1Н), 4,62 (д, 2Н, J=5,4Гц), 6,59 (д, 1Н, J=7,9Гц), 6,76 (д, 1Н, J=7,0Гц), 7,17-7,23 (м, 1Н), 7,42-7,55 (м, 3Н), 7,65 (д, 1Н, J=8,3Гц); С13 ЯМР 26,6, 58,5, 60,6, 64,1, 109,5, 110,8, 113,1, 122,1, 122,7, 129,9, 139,6, 164,2. 48 Стадія 4 (7R,9аS)-транс-Метансульфонової кислоти 6(2-бензо[d]ізоксазол-3-іл-октагідропіридо[1,2а]піразин-7-ілметокси)піридин-2-ілметиловий естер До добре перемішуваної суміші вказаної в заголовку попередньої стадії сполуки (2,05г, 5,2ммоль) (частково розчинена) і триетиламіну (1,09мл, 7,90ммоль) в метиленхлориді (20мл), при кімнатній температурі, додавали метансульфонілхлорид (0,45мл, 5,7ммоль). Реакцію перемішували протягом 3г при кт і потім гасили 10% водним бікарбонатом натрію (з 20мл метиленхлориду). Реакційну суміш екстрагували трьома 10мл свіжими порціями метиленхлориду. Об'єднані органічні екстракти сушили (безводний сульфат натрію) і концентрували у вакуумі одержуючи вказану в заголовку сполуку як в'язке масло (2,21г, 90%). Продукт використовували на наступній стадії без подальшого очищення. Діагностична 1Н ЯМР (400МГц, CDCI3) 5,15м.ч. Стадія 5 Загальна Методика Реакційну суміш, що містить вказаний в заголовку попередньої стадії мезилат (0,03ммоль, 14,2мг) і прийнятний амін (0,12ммоль) в ацетонітрилі (1мл) перемішували в 2-горлій колбі при 90°С протягом 12 годин. Після охолодження, розчинник видаляли і залишок розчиняли в 1,8мл ДМСО і фільтрували крізь 0,45 MM N ylon Acrodisc в 12´32мм ВЕРХ колби для очищення. Вказані в заголовках Прикладів 41-52 сполуки одержували використовуючи Загальну Методику Прикладу 40, Стадія 5, з Waters Symmetry (C18, 5мкМ, 30´150мм, Потік 20мл/хв, 0,1% TFA/CH 3CN). Вихідний матеріал вказаний для кожного прикладу: Приклад 41 (7R,9аS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]тіазол-2-іламін. Вихідний матеріал: 2-амінотіазол і мезилат з Стадії 4. ЧУ=8,50хв. МС m/z 476,2 Приклад 42 (7R,9аS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]-(3-метилпіридин-4іл)амін. Вихідний матеріал: 4-амінопіридин. ЧУ=8,58хв. МС m/z 484,3 Приклад 43 (7R,9аS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил-(5-метил-2Н-піразол3-іл)амін. Вихідний матеріал: 5-метил-2-амінопіразол. ЧУ=8,56хв. МС m/z 473,3. Приклад 44 (7R,9аS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]-(5-метилпіридин-2іл)амін. Вихідний матеріал: 5-метил-2-амінопіридин. ЧУ=8,66хв. МС m/z 484,3 49 78437 Приклад 45 (7R,9аS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]-(1Н-піразол-3іл)амін. Вихідний матеріал: 3-амінопіразол. ЧУ=8,60хв. МС m/z 459,2. Приклад 46 (7R,9аS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоістагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]-(6-метилпіридин-2іл)амін. Вихідний матеріал: 6-метил-2-амінопіридин. ЧУ=8,75хв. МС m/z 484,3. Приклад 47 (7R,9аS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]піридин-2-іламін. Вихідний матеріал: 2-амінопіридин. ЧУ=8,50хв. МС m/z 470,2. Приклад 48 (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2ілметил]циклопропілметиламін. Вихідний матеріал: амінометилциклопропан. ЧУ=8,65хв. МС m/z 447,3 Приклад 49 (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]-(2-морфолін-4ілетил)амін. Вихідний матеріал: 2-(4-морфоліно)етиламін. ЧУ=8,17хв. МС m/z 506,3. Приклад 50 (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]-піримідин-4-іламін. Вихідний матеріал: 4-аміно-піразин. ЧУ=8,40хв. МС m/z 471,2. Приклад 51 (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3ілокгагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]-(6-метоксипіридин-3іл)амін. Вихідний матеріал: 6-метокси-3-амінопіридин. ЧУ=8,88хв. МС m/z 500,3. Приклад 52 (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-2-ілметил]-(2-піролідин-1ілетил)амін. Вихідний матеріал: 2-піролідино-етиламін. ЧУ=8,16хв. МС m/z 490,3 Приклад 53 (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]діетиламін Стадія 1 (Октагідрохіназолін-3-іл)метанол (5,42г, 26,2ммоль), 1,8-діазобіцикло[5.4.0]ундец-7-ен (12,9мл, 85ммоль) і 3-хлорбензо[d]ізоксазол (5,54г, 32,3ммоль) розчиняли в піридині (16мл) і потім нагрівали (110°С) при перемішуванні протягом 18 годин. Додавали 10% водний бікарбонат натрію і 50 метиленхлорид (250мл кожного) і суміш інтенсивно перемішували. Водну фазу потім екстрагували трьома 100мл порціями свіжого метиленхлориду. Об'єднані органічні екстракти сушили (безводний сульфат натрію) і концентрували у вакуумі до аморфної твердої речовини (4,88г). Флеш хроматографія всього зразка (силікагель, 47-61 мікрон меш; елюювали метанол/метиленхлорид=6,94 об'ємних) давала (7R,9aS)-транс-[2бензо[d]ізоксазол-3-іл)октагідропіридо-1,2а]піразин-7-іл]метанол: (3,46г, 43% вихід) як аморфну тверду речовину. МС m/z 306 (М+1). До розчину 2-хлор-5-(хлорметил)піридину (0,28г, 1,7ммоль) в 3мл сухого ацетонітрилу додавали 0,36мл (3,46ммоль) діетиламіну після чого 240мг (1,73ммоль) карбонату калію. Реакцію нагрівали при 80°С протягом 20г. Після охолодження, реакційну суміш гасили 5мл води, три рази екстрагували метиленхлоридом і сушили над сульфатом натрію. Концентрування розчинника давало масло, яке очищали за допомогою хроматографії на силікагелі одержуючи 290мг (85% вихід) 1-(6Хлорпіридин-3-ілметил)-діетиламіну. Діагностична 1 Н ЯМР (400МГц, CDCI3) 1,01-1,15 (м, 6Н), 2,352,50 (м, 4Н), 3,45-3,65 (м, 2Н), 7,30 (д, 1Н, J=8,3Гц), 8,31 (д, 1Н, J=2,1Гц); МС 199,2 (М+Н). До (7R,9аS)-транс-[2-бензо[d]ізоксазол-3іл)октагідропіридо-1,2-а]піразин-7-іл]метанолу (336мг, 1,17ммоль) додавали 6мл тетрагідрофурану і потім 1,46мл 1,0М розчин трет-бутоксиду алію. Реакцію нагрівали протягом 30 хв при 50°С і додавали 1-(6-хлорпіридин-3-ілметил)діетиламін (290мг, 1,46ммоль). Розчин кип'ятили із зворотнім холодильником протягом 2г і гасили 5мл води і екстрагували метиленхлоридом. Органічний шар сушили сульфатом натрію, концентрували і одержану тверду речовину очи щали за допомогою хроматографії на силікагелі одержуючи вказану в заголовку сполуку 98мг (22% вихід). Діагностична С13 ЯМР (100МГц, CDCI3) 11,8, 27,2, 29,2, 36,3, 46,6, 48,5, 53,9, 54,2, 54,4, 59,0, 60,4, 68,9, 110,7, 110,9, 116,4, 122,4, 122,5, 127,7, 129,7, 140,0, 146,9, 161,3, 163,3, 164,2. МС m/z 405,4 (М+1). Приклад 54 (7R,9aS)-транс-1-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]піролідин-3-ол До розчину 2-хлор-5-(хлорметил)піридину (1,0г, 6,2ммоль) в 10мл сухого ацетонітрилу додавали 1,03мл (12,4ммоль) (S)-3-гідроксипіролідин після чого 858мг (6,2ммоль) карбонату калію. Реакцію нагрівали при 80°С протягом 2г. Після охолодження, реакційну суміш гасили 20мл води, три рази екстрагували метиленхлоридом і сушили над сульфатом натрію. Концентрування розчинника давало масло, яке очищали за допомогою хроматографії на силікагелі одержуючи 900мг (68% вихід) (S)-1-(6-Хлорпіридин-3-ілметил)піролідин-3олу. Діагностична С13 Я МР (100МГц, CDCI3) 35,1, 52,5, 56,7, 63,0, 71,4, 124,2, 133,4, 139,6, 149,9, 150,4; МС 213,2 (М+Н). До (7R,9aS)-транс-[2-бензо[d]ізоксазол-3іл)октагідропіридо-1,2-а]піразин-7-іл]метанолу (193мг, 0,67ммоль) одержаному на Стадії 1, прикладу 53 додавали 2,5мл тетрагідрофурану після 51 78437 чого 0,66мл 1,0М розчину трет-бутоксиду калію. Реакцію нагрівали протягом 30 хв при 50°С і додавали (S)-1-(6-Хлорпіридин-3-ілметил)піролідин-3ол (140мг, 0,66ммоль). Розчин кип'ятили із зворотнім холодильником протягом 2г і гасили 5мл води і екстрагували метиленхлоридом. Органічний шар сушили сульфатом натрію, концентрували і одержану тверду речовину очи щали за допомогою хроматографії на силікагелі одержуючи вказану в заголовку сполуку 52мг (17% вихід). Діагностична С13 ЯМР (100МГц, CDCI3) 27,1, 29,1, 35,1, 48,4, 52,4, 53,9, 54,4, 56,9, 59,0, 60,3, 62,8, 68,9, 71,3, 110,7, 111,0, 116,3, 122,3, 122,5, 126,9, 129,7, 139,9, 146,8, 161,2, 163,4, 164,1. МС m/z 464,5 (М+1). Приклад 55 (7R,9aS)-транс-1-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]піролідин-3-ол До розчину 2-хлор-5-(хлорметил)піридину (1,0г, 6,3ммоль) в 10мл сухого ацетонітрилу додавали 1,05мл (12,6ммоль) (R)-3-гідроксипіролідину після чого 858мг (6,2ммоль) карбонату калію. Реакцію нагрівали при 80°С протягом 2г. Після охолодження, реакційну суміш гасили 20мл води, три рази екстрагували метиленхлоридом і сушили над сульфатом натрію. Концентрування розчинника давало масло, яке очищали за допомогою хроматографії на силікагелі одержуючи 1,03г (77% вихід) (R)-1-(6-Хлорпіридин-3-ілметил)піролідин-3-олу. Діагностична С13 ЯМР (100МГц, CDCI3) 35,1, 52,5, 56,7, 63,0, 71,4, 124,2, 133,4, 139,6, 149,9, 150,4; МС 213,2 (М+Н). До (7R,9aS)-транс-[2-бензо[d]ізоксазол-3іл)октагідропіридо-1,2-а]піразин-7-іл]метанолу (189мг, 0,66ммоль) одержаному на Стадії 1, приклад 53, додавали 2,5мл тетрагідрофурану після чого 0,65мл 1,0М розчину трет-бутоксиду калію. Реакцію нагрівали протягом 30 хв при 50°С і додавали (R)-1-(6-Хлорпіридин-3-ілметил)піролідин-3ол (138мг, 0,65ммоль). Розчин кип'ятили із зворотнім холодильником протягом 2г і гасили 5мл води і екстрагували метиленхлоридом. Органічний шар сушили сульфатом натрію, концентрували і одержану тверду речовину очи щали за допомогою хроматографії на силікагелі одержуючи вказану в заголовку сполуку 40мг (13% вихід). Діагностична С13 ЯМР (100МГц, CDCI3) 27,1, 29,1, 35,1, 48,4, 52,4, 53,9, 54,4, 56,9, 59,0, 60,3, 62,8, 68,9, 71,3, 110,7, 111,0, 116,3, 122,3, 122,5, 126,9, 129,7, 139,9, 146,8, 161,2, 163,4, 164,1. МС m/z 464,5 (М+1). Приклад 56 (7R,9аS)-транс-7-(5-Азетидин-1ілметилпіридин-2-ілоксиметил)-2бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин До розчину 2-хлор-5-(хлорметил)піридину (0,34г, 2,1ммоль) в 4мл сухого ацетонітрилу додавали 389мг (4,14ммоль) гідрохлориду азетидину після чого 572мг (4,14ммоль) карбонату калію. Реакцію нагрівали при 80°С протягом 3г. Після охолодження, реакційну суміш гасили 5мл води, три рази екстрагували метиленхлоридом і сушили над сульфатом натрію. Концентрування розчинника давало масло, яке очищали за допомогою хро 52 матографії на силікагелі одержуючи 200мг (53% вихід) 1-(6-Хлорпіридин-3-ілметил)азетидину. Діагностична 1Н ЯМР (400МГц, CDCI3) 2,06-2,14 (м, 2Н), 3,23 (т, 4Н, J=7,0Гц), 3,55 (с, 2Н), 7,27 (д, 1Н, J=7,9Гц), 7,61 (дд, 1Н, J=8,3 і 2,5Гц), 8,26 (д, 1Н, J=2,5Гц); МС 183,2 (М+Н). До (7R,9aS)-транс-[2-бензо[d]ізоксазол-3іл)октагідропіридо-1,2-а]піразин-7-іл]метанолу (255мг, 0,88ммоль) одержаному на Стадії 1, приклад 53, додавали 2,5мл тетрагідрофурану після чого 1,10мл 1,0М розчину трет-бутоксиду калію. Реакцію нагрівали протягом 30хв. при 50°С і додавали 1-(6-Хлорпіридин-3-ілметил)азетидин (200мг, 1,10ммоль). Розчин кип'ятили із зворотнім холодильником протягом 5г і гасили 5мл води і екстрагували метиленхлоридом. Органічний шар сушили сульфатом натрію, концентрували і одержану тверду речовину очищали за допомогою хроматографії на силікагелі одержуючи вказану в заголовку сполуку 157мг (41% вихід). Діагностична С13 ЯМР (100МГц, CDCI3) 17,7, 25,0, 25,2, 33,5, 48,4, 53,8, 54,4, 55,1, 56,7, 60,6, 60,7, 66,9, 110,6, 110,9, 116,4, 122,4, 122,5, 126,4, 129,6, 139,5, 146,7, 161,3, 163,7, 164,1. МС m/z 434,5 (М+1). Приклад 57 (7R,9аS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3-ілметил]-(2метоксиетил)метиламін До розчину 2-хлор-5-(хлорметил)піридину (384мг, 2,37ммоль) в 4мл сухого ацетонітрилу додавали 0,51мл (4,74ммоль) 1-метил-2метоксиетиламіну після чого 328мг (2,37ммоль) карбонату калію. Реакцію нагрівали при 80°С протягом 3г. Після охолодження, реакційну суміш гасили 5мл води, три рази екстрагували метиленхлоридом і сушили над сульфатом натрію. Концентрування розчинника давало масло, яке очищали за допомогою хроматографії на силікагелі одержуючи 395мг (78% вихід) (6-Хлорпіридин-3ілметил)-(2-метоксиетил)метиламіну. Діагностична 1 Н ЯМР (400МГц, CDCI3) 2,25 (с, 3Н), 2,59 (т, 2Н, J=5,6Гц), 3,32 (с, 3Н), 3,49 (т, 2Н, J=5,6Гц), 7,26 (д, 1Н, J=8,5Гц), 7,68 (дд, 1Н, J=8,3 і 2,5Гц), 8,27 (д, 1Н, J=1,6Гц); МС 215,2 (М+Н). До (7R,9aS)-транс-[2-бензо[d]ізоксазол-3іл)октагідропіридо-1,2-а]піразин-7-іл]метанолу (344мг, 1,20ммоль) одержаному на Стадії 1, приклад 53, додавали 8мл тетрагідрофурану після чого 1,5мл 1,0М розчину трет-бутоксиду калію. Реакцію нагрівали протягом 30хв. при 50°С і додавали (6-Хлорпіридин-3-ілметил)-(2метоксиетил)метил-амін (325мг, 1,50ммоль). Розчин кип'ятили із зворотнім холодильником протягом 12г і гасили 5мл води і екстрагували метиленхлоридом. Органічний шар сушили сульфатом натрію, концентрували і одержану тверду речовину очищали за допомогою хроматографії на силікагелі одержуючи вказану в заголовку сполуку 308мг (55% вихід). Діагностична С13 ЯМР (100МГц, CDCI3) 27,2, 29,2, 36,3, 39,2, 42,6, 48,5, 53,9, 54,4, 56,2, 58,9, 59,0, 59,1, 59,3, 60,4, 68,9, 70,9, 110,7, 110,9, 116,4, 122,4, 122,5, 126,8, 129,7, 140,2, 147,2, 161,3, 163,5, 164,2. МС m/z 466,5 (М+1). 53 78437 Приклад 58 (7R,9аS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3ілметил]циклопентилметиламін До розчину 2-хлор-5-(хлорметил)піридину (318мг, 1,96ммоль) в 4мл сухого ацетонітрилу додавали 395мг (3,92ммоль) Nметилциклопентиламіну після чого 270мг (1,96ммоль) карбонату калію. Реакцію нагрівали при 80°С протягом 20г. Після охолодження, реакційну суміш гасили 5мл води, три рази екстрагували метиленхлоридом і сушили над сульфа том натрію. Концентрування розчинника давало масло, яке очищали за допомогою хроматографії на силікагелі одержуючи 340мг (77% вихід) (6Хлорпіридин-3-ілметил)циклопентилметиламіну. Діагностична 1Н ЯМР (400МГц, CDCl3) 1,40-1,90 (м, 4Н), 2,15 (с, 3Н), 2,78-2,89 (м, 1Н), 3,56 (с, 2Н), 7,29 (д, 1Н, J=8,3Гц), 7,70-7,80 (м, 1Н), 8,28 (д, 1Н, J=2,1Гц); МС 225,3 (М+Н). До (7R,9аS)-транс-[2-бензо[d]ізоксазол-3іл)октагідропіридо-1,2-а]піразин-7-іл]метанолу (350мг, 1,21ммоль) одержаному на Стадії 1, приклад 53, додавали 8мл тетрагідрофурану після чого 1,52мл 1,0М розчину трет-бутоксиду калію. Реакцію нагрівали протягом 30хв. при 50°С і додавали (6-Хлорпіридин-3-ілметил)-циклопентилметиламін (340мг, 1,52ммоль). Розчин кип'ятили із зворотнім холодильником протягом 5г і гасили 5мл води і екстрагували метиленхлоридом. Органічний шар сушили сульфа том натрію, концентрували і одержану тверду речовину очищали за допомогою хроматографії на силікагелі одержуючи вказану в заголовку сполуку 271мг (47% вихід). Діагностична С13 ЯМР (100МГц, CDCI3) 24,5, 27,2, 29,2, 30,6, 36,6, 39,9, 48,5, 53,9, 54,4, 57,3, 59,0, 60,4, 66,6, 66,9, 110,7, 110,9, 116,4, 122,4, 122,5, 127,3, 129,7, 140,2, 147,1, 161,2, 153,3, 164,1. МС m/z 476,5 (М+1). Приклад 59 (7R,9aS)-транс-N-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-a]піразин-7-ілметокси)піридин-3-ілметил-N,N'-диметилетан-1,2-діамін До розчину 2-хлор-5-(хлорметил)піридину (586мг, 3,62ммоль) в 8мл сухого ацетонітрилу додавали 756мг (7,24ммоль) N-N'диметилетилендіамінк після чого 500мг (3,62ммоль) карбонату калію. Реакцію нагрівали при 80°С протягом 1г. Після охолодження, реакційну суміш гасили 5мл води, три рази екстрагували метиленхлоридом і сушили над сульфа том натрію. Концентрування розчинника давало масло, яке очищали за допомогою хроматографії на силікагелі одержуючи 400мг (52% вихід) N-(6Хлорпіридин-3-ілметил)-N,N'-диметилетан-1,2діаміну. Діагностична 1Н ЯМР (400МГц, CDCI3) 2,18 (с, 3Н), 2,31 (ш с, 1Н), 2,48 (с, 3Н), 2,61 (т, 2Н, J=6,1Гц), 2,76 (т, 23, J=6,1Гц), 3,47 (с, 2Н), 7,28 (д, 1Н, J=7,9 і 2,5Гц), 8,31 (д, 1Н, J=1,6Гц); МС 214,2 (М+Н). До (7R,9aS)-транс-[2-бензо[d]ізоксазол-3-іл)октагідропіридо-1,2-а]піразин-7-іл]метанолу (273мг, 0,95ммоль) одержаному на Стадії 1, приклад 53, додавали 6мл тетрагідрофурану після чого 1,19мл 54 1,0М розчину трет-бутоксиду калію. Реакцію нагрівали протягом 30хв. при 50°С і додавали N-(6Хлорпіридин-3-ілметил)-N,N'-диметилетан-1,2діамін (253мг, 1,19ммоль). Розчин кип'ятили із зворотнім холодильником протягом 12г і гасили 5мл води і екстрагували метиленхлоридом. Органічний шар сушили сульфатом натрію, концентрували і одержану тверду речовину очи щали за допомогою хроматографії на силікагелі одержуючи вказану в заголовку сполук у 25мг (5% вихід). Діагностична С13 ЯМР (100МГц, CDCI3) 2,8, 27,1, 29,2, 31,8, 35,3, 36,3, 41,7, 48,2, 48,5, 53,9, 54,4, 54,9, 59,0, 59,4, 60,4, 68,9, 110,7, 111,1, 116,4, 122,3, 122,4, 126,8, 129,7, 140,1, 147,0, 161,3, 163,5, 164,1. МС m/z 465,5 (М+1). Приклад 60 (7R,9аS)-транс-2-Бензо[d]ізоксазол-3-іл-7-[5-(2метилазиридин-1-ілметил)піридин-2ілоксиметил]октагідропіридо[1,2-а]піразин До розчину 2-хлор-5-(хлорметил)піридину (352мг, 2,17ммоль) в 4мл сухого ацетонітрилу додавали 0,4мл (4,34ммоль) 2-метилазиридину після чого 300мг (2,17ммоль) карбонату калію. Реакцію нагрівали при 60°С протягом 20г. Після охолодження, реакційну суміш гасили 5мл води, три рази екстрагували метиленхлоридом і сушили над сульфатом натрію. Концентрування розчинника давало масло, яке очищали за допомогою хроматографії на силікагелі одержуючи 66мг (17% вихід) 2-Хлор-5-(2-метилазиридин-1-ілметил)піридин. Діагностична 1Н ЯМР (400МГц, CDCI3) 1,15 (д, 3Н, J=5,4Гц), 1,34 (д, 1Н, J=6,6Гц), 1,47-1,55 (м, 2Н), 3,35 (аbк, 2Н, J=5,8Гц), 7,25 (д, 1Н, J=6,3Гц), 7,65 (дд, 1Н, J=8,3 і 2,5Гц), 8,27 (д, 1Н, J=1,7Гц); МС 183,2 (М+Н). До (7R,9aS)-транс-[2-бензо[d]ізоксазол-3-іл)октагідропіридо-1,2-а]піразин-7-іл]метанолу (83мг, 0,29ммоль) одержаному на Стадії 1, приклад 53, додавали 2мл тетрагідрофурану після чого 0,36мл 1,0М розчину трет-бутоксиду калію. Реакцію нагрівали протягом 30хв. при 50°С і додавали 2-Хлор5-(2-метилазиридин-1-ілметил)піридин (66мг, 0,36ммоль). Розчин кип'ятили із зворотнім холодильником протягом 12г і гасили 5мл води і екстрагували метиленхлоридом. Органічний шар сушили сульфатом натрію, концентрували і одержану тверду речовину очищали за допомогою хроматографії на силікагелі одержуючи вказану в заголовку сполуку 20мг (16% вихід). Діагностична С13 ЯМР (100МГц, CDCI3) 18,5, 27,1, 29,1, 35,0, 35,2, 36,3, 48,4, 53,9, 54,4, 59,0, 60,4, 61,6, 68,8, 110,7, 111,0, 116,3, 122,3, 122,4, 127,9, 139,0, 146,0, 161,2, 163,3, 164,1. МС m/z 434,4 (М+1). Приклад 61 (7R,9aS)-транс-7-(5-Азепан-1-ілметилпіридин2-ілоксиметил)-2-бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин До розчину 2-хлор-5-(хлорметил)піридину (419мг, 2,59ммоль) в 5мл сухого ацетонітрилу додавали 512мг (5,18ммоль) азациклогептан, після чого 358мг (2,59ммоль) карбонату калію. Реакцію нагрівали при 80°С протягом 20г. Після охолодження, реакційну суміш гасили 5мл води, три рази екстрагували метиленхлоридом і сушили над сульфатом натрію. Концентрування розчинника 55 78437 давало масло, яке очищали за допомогою хроматографії на силікагелі одержуючи 340мг (59% вихід) 1-(6-Хлорпіридин-3-ілметил)-азепану. Діагностична 1Н ЯМР (400МГц, CDCI3) 1,40-1,70 (м, 8Н), 2,50-2,65 (м, 4Н), 3,65 (с, 2Н), 7,28 (д, 1Н, J=8,3Гц), 7,65-7,70 (м, 1Н), 8,30 (д, 1Н, J=2,1Гц); МС 225,3 (М+Н). До (7R,9aS)-транс-[2-бензо[d]ізоксазол-3іл)октагідропіридо-1,2-а]піразин-7-іл]метанолу (284мг, 0,99ммоль) одержаному на Стадії 1, приклад 53, додавали 6мл тетрагідрофурану після чого 1,24мл 1,0М розчину трет-бутоксиду калію. Реакцію нагрівали протягом 30хв. при 50°С і додавали 1-(6-Хлорпіридин-3-ілметил)азепан (278мг, 1,24ммоль). Розчин кип'ятили із зворотнім холодильником протягом 12г і гасили 5мл води і екстрагували метиленхлоридом. Органічний шар сушили сульфатом натрію, концентрували і одержану тверду речовину очищали за допомогою хроматографії на силікагелі одержуючи вказану в заголовку сполуку 37мг (8% вихід). Діагностична С13 ЯМР (100МГц, CDCI3) 27,1, 27,2, 28,1, 29,2, 36,3, 48,5, 53,9, 54,4, 55,5, 59,0, 59,4, 60,3, 68,9, 110,6, 110,9, 116,3, 122,4, 122,5, 127,8, 129,7, 139,9, 146,8, 161,3, 163,3, 164,2. МС m/z 476,5 (М+1). Приклад 62 (7R,9aS)-транс-2-Бензо[d]ізоксазол-3-іл-7-[5-(2метоксиметилпіролідин-1-ілметил)піридин-2-ілоксиметил]октагідропіридо[1,2-а]піразин До розчину 2-хлор-5-(хлорметил)піридину (369мг, 2,28ммоль) в 5мл сухого ацетонітрилу додавали 521мг (4,52ммоль) (S)-(+)-2(метоксиметил)піролідинону, після чого 314мг (2,28ммоль) карбонату калію. Реакцію нагрівали при 55°С протягом 20г. Після охолодження, реакційну суміш гасили 5мл води, три рази екстрагували метиленхлоридом і сушили над сульфа том натрію. Концентрування розчинника давало масло, яке очищали за допомогою хроматографії на силікагелі одержуючи 450мг (82% вихід) 2-Хлор-5-(2метоксиметилпіролідин-1-ілметил)піридину. Діагностична 1Н ЯМР (400МГц, CDCI3) 3,35 (с, 2Н), 7,28 (д, 1Н, J=7,9Гц), 7,40-7,50 (м, 1Н), 8,31 (д, 1Н, J=2,1Гц); МС 241,3(М+Н). До (7R,9aS)-транс-[2-бензо[d]ізоксазол-3іл)октагідропіридо-1,2-а]піразин-7-іл]метанолу (287мг, 1,00ммоль) одержаному на Стадії 1, приклад 53, додавали 6мл тетрагідрофурану після чого 1,25мл 1,0М розчину трет-бутоксиду калію. Реакцію нагрівали протягом 30хв. при 50°С і додавали 2-Хлор-5-(2-метоксиметилпіролідин-1ілметил)піридин (300мг, 1,25ммоль). Розчин кип'я тили із зворотнім холодильником протягом 5г і гасили 5мл води і екстрагували метиленхлоридом. Органічний шар сушили сульфатом натрію, концентрували і одержану тверду речовину очищали за допомогою хроматографії на силікагелі, одержуючи вказану в заголовку сполук у 177мг (36% вихід). Діагностична С13 ЯМР (100МГц, CDCI3) 22,8, 27,1, 28,5, 29,2, 36,3, 48,5, 53,9, 54,4, 56,1, 59,0, 59,3, 60,3, 62,9, 68,8, 76,6, 110,6, 110,8, 116,3, 122,3, 122,4, 129,7, 140,2, 146,9, 161,2, 163,3, 164,2. МС m/z 492,5 (М+1). 56 Приклад 63 (7R,9аS)-транс-[6-(2-Бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3ілметил]-трет-бутиламін До розчину 2-хлор-5-(хлорметил)піридину (537мг, 3,31ммоль) в 7мл сухого ацетонітрилу додавали 0,7мл (6,62ммоль) трет-бутиламіну після чого 457мг (3,31ммоль) карбонату калію. Реакцію нагрівали при 80°С протягом 12г. Після охолодження, реакційну суміш гасили 5мл води, три рази екстрагували метиленхлоридом і сушили над сульфатом натрію. Концентрування розчинника давало масло, яке очищали за допомогою хроматографії на силікагелі одержуючи 387мг (59% вихід) трет-бутил-(6-хлорпіридин-3-ілметил)аміну. Діагностична 1Н ЯМР (400МГц, CDCI3) 1,16 (с, 9Н), 1,60-1,80 (ш с, 1Н), 3,72 (с, 2Н), 7,26 (д, 1Н, J=8,3Гц), 7,71 (дд, 1Н, J=8,3 і 2,5Гц), 8,33 (д, 1Н, J=2,0Гц); МС 199,2 (М+Н). До (7R,9aS)-транс-[2-бензо[d]ізоксазол-3іл)октагідропіридо-1,2-а]піразин-7-іл]метанолу (222мг, 0,77ммоль) одержаному на Стадії 1, приклад 53, додавали 4мл тетрагідрофурану після чого 0,96мл 1,0М розчину трет-бутоксиду калію. Реакцію нагрівали протягом 30хв. при 50°С і додавали трет-бутил-(6-хлорпіридин-3-ілметил)амін (190мг, 0,96ммоль). Розчин кип'ятили із зворотнім холодильником протягом 12г і гасили 5мл води і екстрагували метиленхлоридом. Органічний шар сушили сульфатом натрію, концентрували і одержану тверду речовину очи щали за допомогою хроматографії на силікагелі одержуючи вказану в заголовку сполуку 150мг (43% вихід). Діагностична С13 ЯМР (100МГц, CDCI3) 27,2, 29,2, 29,3, 36,3, 44,1, 48,5, 51,1, 53,9, 54,4, 59,0, 60,3, 68,8, 110,6, 110,9, 116,3, 122,3, 122,4, 129,7, 139,5, 146,3, 161,2, 163,3, 164,2. МС m/z 450,5 (М+1). Приклад 64 (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3ілметил]-трет-бутилметиламін До розчину 2-хлор-5-(хлорметил)піридину (570мг, 3,52ммоль) в 7мл сухого ацетонітрилу додавали 608мг (7,04ммоль) N-метил-т-бутиламіну, після чого 486мг (3,52ммоль) карбонату калію. Реакцію нагрівали при 80°С протягом 12г. Після охолодження, реакційну суміш гасили 5мл води, три рази екстрагували метиленхлоридом і сушили над сульфатом натрію. Концентрування розчинника давало масло, яке очищали за допомогою хроматографії на силікагелі одержуючи 420мг (56% вихід) N-метил-трет-бутил-(6-хлорпіридин-3ілметил)аміну. Діагностична 1Н ЯМР (400МГц, CDCI3) 1,14 (с, 9Н), 2,06 (с, 3Н), 3,48 (с, 2Н), 7,26 (д, 1Н, J=6,2Гц), 7,68 (д, 1Н, J=6,6Гц), 8,28 (д, 1Н, J=2,5Гц); МС 213,3 (М+Н). До (7R,9aS)-транс-[2-бензо[d]ізоксазол-3іл)октагідропіридо-1,2-а]піразин-7-іл]метанолу (226мг, 0,79ммоль) одержаному на Стадії 1, приклад 53, додавали 4мл тетрагідрофурану після чого 0,98мл 1,0М розчину трет-бутоксиду калію. Реакцію нагрівали протягом 30хв. при 50°С і додавали N-метил-трет-бутил-(6-хлорпіридин-3ілметил)амін (206мг, 0,98ммоль). Розчин кип'ятили із зворотнім холодильником протягом 12г і гасили 57 78437 5мл води і екстрагували метиленхлоридом. Органічний шар сушили сульфатом натрію, концентрували і одержану тверду речовину очи щали за допомогою хроматографії на силікагелі одержуючи вказану в заголовку сполуку 111мг (30% вихід). Діагностична С13 ЯМР (100МГц, CDCI3) 26,4, 27,1, 29,2, 34,5, 36,3, 48,5, 52,0, 53,9, 54,4, 59,0, 60,4, 68,8, 110,7, 110,9, 116,3, 122,3, 122,4, 129,7, 139,8, 146,6, 161,2, 163,2, 164,1. MC m/z 464,5 (М+1). Приклад 65 (7R,9aS)-транс-2-Бензо[d]ізоксазол-3-іл-7-(5тіазолідин-3-ілметилпіридин-2ілоксиметил)октагідропіридо[1,2-а]піразин До розчину 2-хлор-5-(хлорметил)піридину (500мг, 3,08ммоль) в 4мл сухого ацетонітрилу додавали 0,42мл (6,17ммоль) тіазолідин, після чого 852мг (6,17ммоль) карбонату калію. Реакцію нагрівали при 80°С протягом 20г. Після охолодження, реакційну суміш гасили 5мл води, три рази екстрагували метиленхлоридом і сушили над сульфатом натрію. Концентрування розчинника давало масло, яке очищали за допомогою хроматографії на силікагелі одержуючи 275мг (42% вихід) 2-Хлор-5тіазолідин-3-ілметилпіридину. Діагностична С13 ЯМР (100МГц, CDCI3) 29,8, 53,6, 57,7, 60,3, 112,4, 124,4, 133,3, 139,6, 150,1; МС 215,2 (М+Н). До (7R,9aS)-транс-[2-бензо[d]ізоксазол-3іл)октагідропіридо-1,2-а]піразин-7-іл]метанолу (134мг, 0,47ммоль) одержаному на Стадії 1, приклад 53, додавали 2мл тетрагідрофурану після чого 0,58мл 1,0М розчину трет-бутоксиду калію. Реакцію нагрівали протягом 30хв. при 50°С і додавали 2-Хлор-5-тіазолідин-3-ілметилпіридин (124мг, 0,58ммоль). Розчин кип'ятили із зворотнім холодильником протягом 12г і гасили 5мл води і екстрагували метиленхлоридом. Органічний шар сушили сульфатом натрію, концентрували і одержану тверду речовину очищали за допомогою хроматографії на силікагелі одержуючи вказану в заголовку сполуку 184мг (84% вихід). Діагностична С13 ЯМР (100МГц, CDCI3) 27,1, 29,1, 29,7, 36,2, 48,4, 53,6, 53,9, 54,4, 57,5, 58,9, 60,1, 60,3, 68,9, 110,6, 111,2, 116,3, 122,3, 122,4, 126,9, 129,7, 139,9, 147,0, 161,2, 163,6, 164,1. МС m/z 466,5 (М+1). Приклад 66 (7R,9аS)-транс-2-Бензо[d]ізоксазол-3-іл-7-(5імідазол-1-ілметилпіридин-2ілоксиметил)октагідропіридо[1,2-а]піразин До розчину 2-хлор-5-(хлорметил)піридину (500мг, 3,08ммоль) в 4мл сухого ацетонітрилу додавали 420мл (6,17ммоль) імідазолу, після чого 852мг (6,17ммоль) карбонату калію. Реакцію нагрівали при 80°С протягом 20г. Після охолодження, реакційну суміш гасили 5мл води, три рази екстрагували метиленхлоридом і сушили над сульфатом натрію. Концентрування розчинника давало масло, яке очищали за допомогою хроматографії на силікагелі одержуючи 410мг (69% вихід) 2-Хлор-5імідазол-1-ілметилпіридину. Діагностична С13 ЯМР (100МГц, CDCI3) 47,7, 119,2, 124,9, 130,6, 131,1, 137,5, 137,8, 148,6, 151,8; МС 194,2 (М+Н). До (7R,9aS)-транс-[2-бензо[d]ізоксазол-3-іл)октагідропіридо-1,2-а]піразин-7-іл]метанолу (237мг, 0,83ммоль) одержаному на Стадії 1, приклад 53, додавали 4мл тетрагідрофурану після чого 1,03мл 58 1,0М розчину трет-бутоксиду калію. Реакцію нагрівали протягом 30хв. при 50°С і додавали 2-Хлор5-імідазол-1-ілметилпіридин (200мг, 1,03ммоль). Розчин кип'ятили із зворотнім холодильником протягом 12г і гасили 5мл води і екстрагували метиленхлоридом. Органічний шар сушили сульфатом натрію, концентрували і одержану тверду речовину очищали за допомогою хроматографії на силікагелі одержуючи вказану в заголовку сполуку 229мг (62% вихід). Діагностична С13 ЯМР (100МГц, CDCI3) 27,1, 29,0, 36,2, 48,0, 48,4, 53,8, 54,3, 58,9, 60,3, 69,1, 110,7, 111,8, 116,3, 119,0, 122,3, 122,5, 124,6, 129,7, 130,3, 137,3, 138,3, 146,1, 161,2, 164,1, 164,1. МС m/z 445,5 (М+1). Приклад 67 (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3ілоктагідропіридо[1,2-а]піразин-7ілметокси)піридин-3ілметил]циклогексилметиламін До розчину 2-хлор-5-(хлорметил)піридин (500мг, 3,08ммоль) в 8мл сухого ацетонітрилу додавали 384мг (3,39ммоль) Nметилциклогексиламін після чого 468мг (3,39ммоль) карбонату калію. Реакцію нагрівали при 80°С протягом 20г. Після охолодження, реакційну суміш гасили 5мл води, три рази екстрагували метиленхлоридом і сушили над сульфа том натрію. Концентрування розчинника давало масло, яке очищали за допомогою хроматографії на силікагелі одержуючи 700мг (95% вихід) (6Хлорпіридин-3-ілметил)циклогексилметиламін. С13 ЯМР 26,1, 26,6, 28,9, 37,7, 54,5, 62,8, 124,1, 135,1, 139,5, 149,9; МС 239,3 (М+Н). До (7R,9аS)-транс-[2-бензо[d]ізоксазол-3іл)октагідропіридо-1,2-а]піразин-7-іл]метанолу (263мг, 0,92ммоль) одержаному на Стадії 1, приклад 53, додавали 4мл тетрагідрофурану після чого 1,15мл 1,0М розчину трет-бутоксиду калію. Реакцію нагрівали протягом 30хв. при 50°С і додавали (6-Хлорпіридин-3-ілметил)циклогексилметиламін (274мг, 1,15ммоль). Розчин кип'ятили із зворотнім холодильником протягом 12г і гасили 5мл води і екстрагували метиленхлоридом. Органічний шар сушили сульфатом натрію, концентрували і одержану тверду речовину очи щали за допомогою хроматографії на силікагелі одержуючи вказану в заголовку сполуку 203мг (45% вихід). Діагностична С13 ЯМР (100МГц, CDCI3) 26,1, 26,5, 27,1, 28,7, 29,2, 36,3, 37,5, 48,5, 53,9, 54,4, 54,6, 59,0, 60,4, 62,5, 68,8, 110,7, 111,0, 116,3, 122,3, 122,4, 129,7, 139,9, 146,7, 161,3, 163,3, 164,1. МС m/z 490,6 (М+1). Приклад 68 (7R,9aS)-транс-[6-(2-Бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3ілметил]диметиламін До розчину 2-хлор-5-(хлорметил)піридину (509мг, 3,14ммоль) в 7мл сухого ацетонітрилу додавали 3,14мл (6,28ммоль) 2М розчин диметиламіну в ТГФ, після чого 434мг (3,14ммоль) карбонату калію. Реакцію нагрівали при 55°С протягом 20г. Після охолодження, реакційну суміш гасили 5мл води, три рази екстрагували метиленхлоридом і сушили над сульфатом натрію. Концентрування розчинника давало масло, яке очищали за допо 59 78437 могою хроматографії на силікагелі одержуючи 194мг (36% вихід) 1-(6-Хлорпіридин-3ілметил)диметиламіну. Діагностична С 13 ЯМР (100МГц, CDCl3) 45,5, 60,7, 124,2, 133,6, 139,7, 150,2, 150,4; МС 173,2 (М+Н). До (7R,9aS)-транс-[2-бензо[d]ізоксазол-3-іл)октагідропіридо-1,2-а]піразин-7-іл]метанолу (430мг, 1,50ммоль) одержаному на Стадії 1, приклад 53, додавали 10мл тетрагідрофурану після чого 1,87мл 1,0М розчину трет-бутоксиду калію. Реакцію нагрівали протягом 30хв. при 50°С і додавали 1-(6-Хлорпіридин-3-ілметил)диметиламін (320мг, 1,87ммоль). Розчин кип'ятили із зворотнім холодильником протягом 3г і гасили 5мл води і екстрагували метиленхлоридом. Органічний шар сушили сульфатом натрію, концентрували і одержану тверду речовину очищали за допомогою хроматографії на силікагелі одержуючи вказану в заголовку сполуку 270мг (43% вихід). Діагностична С13 ЯМР (100МГц, CDCI3) 27,2, 29,2, 36,3, 45,2, 48,5, 53,9, 54,4, 59,0, 60,3, 60,9, 68,9, 110,7, 111,0, 116,4, 122,3, 122,5, 126,8, 128,7, 140,1, 147,2, 161,3, 163,5, 164,2. МС m/z 422,4 (М+1). Приклад 69 (7R,9аS)-транс-[6-(2-Бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3ілметил]етилметиламін До розчину 2-хлор-5-(хлорметил)піридину (1,0г, 6,17ммоль) в 11мл сухого ацетонітрилу додавали 1,06мл (12,3ммоль) метилетиламіну, після чого 850мг (6,17ммоль) карбонату калію. Реакцію нагрівали при 80°С протягом 5г. Після охолодження, реакційну суміш гасили 5мл води, три рази екстрагували метиленхлоридом і сушили над сульфатом натрію. Концентрування розчинника давало масло, яке очищали за допомогою хроматографії на силікагелі одержуючи 1,0г (87% вихід) 1(6-Хлорпіридин-3-ілметил)метилетиламіну. Діагностична 1Н Я МР (400МГц, CDCI3) 1,06 (т, 3Н, J=7,1Гц), 2,14 (с, 3Н), 2,40 (к, 2Н, J=7,1Гц), 3,43 (с, 2Н), 7,25 (д, 1Н, J=8,2Гц), 7,62 (дд, 1Н, J=8,2 і 5,8Гц); МС (187,2 (М+Н). До (7R,9aS)-транс-[2-бензо[d]ізоксазол-3-іл)октагідропіридо-1,2-а]піразин-7-іл]метанолу (460мг, 1,60ммоль) одержаному на Стадії 1, приклад 53, додавали 10мл тетрагідрофурану після чого 2,0мл 1,0М розчину трет-бутоксиду калію. Реакцію нагрівали протягом 30хв. при 50°С і додавали 1-(6Хлорпіридин-3-ілметил)метилетиламін (370мг, 2,00ммоль). Розчин кип'ятили із зворотнім холодильником протягом 3г і гасили 5мл води і екстрагували метиленхлоридом. Органічний шар сушили сульфатом натрію, концентрували і одержану тверду речовину очищали за допомогою хроматографії на силікагелі одержуючи вказану в заголовку сполуку 400мг (57% вихід). Діагностична С13 ЯМР (100МГц, CDCI3) 12,5, 27,2, 29,2, 36,3, 41,5, 48,5, 51,1, 53,9, 54,4, 58,6, 59,0, 60,4, 68,9, 110,7, 110,9, 116,4, 122,4, 122,5, 127,0, 129,7, 140,1, 147,1, 161,3, 163,4, 164,2. МС m/z 436,5 (М+1). Приклад 70 (7R,9аS)-транс-[6-(2-Бензо[d]ізоксазол-3-ілоктагідропіридо[1,2-а]піразин-7-ілметокси)піридин-3ілметил]-(2-метокси-1-метилетил)амін 60 До розчину 2-хлор-5-(хлорметил)піридину (1,0г, 6,17ммоль) в 11мл сухого ацетонітрилу додавали 1,30мл (12,3ммоль) 2-аміно-1метоксипропану після чого 850мг (6,17ммоль) карбонату калію. Реакцію нагрівали при 80°С протягом 5г. Після охолодження, реакційну суміш гасили 5мл води, три рази екстрагували метиленхлоридом і сушили над сульфатом натрію. Концентрування розчинника давало масло, яке очищали за допомогою хроматографії на силікагелі одержуючи 640мг (48% вихід) (6-Хлорпіридин-3-ілметил)-(2метокси-1-метилетил)аміну. Діагностична С13 ЯМР (100МГц, CDCI3) 17,2, 48,0, 52,3, 59,1, 77,2, 124,1, 135,3, 138,9, 149,5, 150,1 МС (217,2 (М+Н). До (7R,9аS)-транс-[2-бензо[d]ізоксазол-3-іл)октагідропіридо-1,2-а]піразин-7-іл]метанолу (279мг, 0,98ммоль) одержаному на Стадії 1, приклад 53, додавали 7мл тетрагідрофурану після чого 1,22мл 1,0М розчину трет-бутоксиду калію. Реакцію нагрівали протягом 30хв. при 50°С і додавали (6Хлорпіридин-3-ілметил)-(2-метокси-1метилетил)амін (263мг, 1,22ммоль). Розчин кип'я тили із зворотнім холодильником протягом 3г і гасили 5мл води і екстрагували метиленхлоридом. Органічний шар сушили сульфатом натрію, концентрували і одержану тверду речовину очищали за допомогою хроматографії на силікагелі одержуючи вказану в заголовку сполуку 210мг (46% вихід). Діагностична С13 ЯМР (100МГц, CDCI3) 17,1, 27,2, 29,2, 36,3, 48,1, 48,5, 52,0, 53,9, 54,4, 59,0, 59,1, 60,4, 68,9, 110,7, 111,1, 116,4, 122,4, 122,5, 128,5, 129,7, 139,4, 146,5, 161,3, 163 А 164,2. МС m/z 466,5 (М+1). Приклад 71 (7R,9аS)-транс-2-Бензо[d]ізоксазол-3-іл-7-[5-(2метилпіролідин-1-ілметил)піридин-2-ілоксиметил] октагідропіридо[1,2-а]піразин До розчину 2-хлор-5-(хлорметил)піридину (498мг, 3,07ммоль) в 6мл сухого ацетонітрилу додавали 0,63мл (6,14ммоль) 2-метилпіролідинон після чого 424мг (3,07ммоль) карбонату калію. Реакцію нагрівали при 80°С протягом 2г. Після охолодження, реакційну суміш гасили 5мл води, три рази екстрагували метиленхлоридом і сушили над сульфатом натрію. Концентрування розчинника давало масло, яке очищали за допомогою хроматографії на силікагелі одержуючи 500мг (78% вихід) 2-Хлор-5-(2-метилпіролідин-1-ілметил)піридину. Діагностична 1Н ЯМР (400МГц, CDCI3) 1,15 (д, ЗН, J=5,8Гц), 1,41-1,78 (м, 3Н), 1,91-2,13 (м, 2Н), 2,41-2,45 (м, 1Н), 2,86 (т, 1Н, J=6,0Гц), 3,16 (д, 1Н, J=13,3Гц), 3,96 (д, 1Н, J=13,3Гц), 7,27 (д, 1Н, J=8,3Гц), 7,67 (д, 1Н, J=7,1Гц), 8,29 (д, 1Н, J=2,1Гц); МС 211,3 (М+Н). До (7R,9aS)-транс-[2-бензо[d]ізоксазол-3іл)октагідропіридо-1,2-а]піразин-7-іл]метанолу (177мг, 0,62ммоль) одержаному на Стадії 1, приклад 53, додавали 3мл тетрагідрофурану після чого 0,77мл 1,0М розчину трет-бутоксиду калію. Реакцію нагрівали протягом 30хв. при 50°С і додавали 2-Хлор-5-(2-метилпіролідин-1-ілметил)піридин (162мг, 0,77ммоль). Розчин кип'ятили із зворотнім холодильником протягом 3г і гасили 5мл води і екстрагували метиленхлоридом. Органічний шар сушили сульфа том натрію, концентрували і
ДивитисяДодаткова інформація
Назва патенту англійськоюAzabicyclic derivatives of pyridyloxymethyl and benzisoxazole
Назва патенту російськоюАзабициклические производные пиридилоксиметила и бензизоксазола
МПК / Мітки
МПК: A61P 25/00, A61K 31/496, C07D 471/04, A61K 31/495, C07D 413/04
Мітки: похідні, бензізоксазолу, азабіциклічні, піридилоксиметилу
Код посилання
<a href="https://ua.patents.su/40-78437-azabiciklichni-pokhidni-piridiloksimetilu-i-benzizoksazolu.html" target="_blank" rel="follow" title="База патентів України">Азабіциклічні похідні піридилоксиметилу і бензізоксазолу</a>
Попередній патент: Спосіб ригідифікації водних суспензій
Наступний патент: Осьовий асинхронний двигун
Випадковий патент: Різальний механізм пристрою для подрібнення харчової сировини












