Похідні формаміду, корисні як адренорецептори
Номер патенту: 86615
Опубліковано: 12.05.2009
Автори: Баннедж Марк Едвард, Льютвейт Расселл Ендрю, Глоссоп Пол Алан, Браун Алан Деніел, Лейн Шарлотт Еліс Луіз, Джеймс Кім, Прайс Девід Ентоні
Формула / Реферат
1. Сполука загальної формули (1)
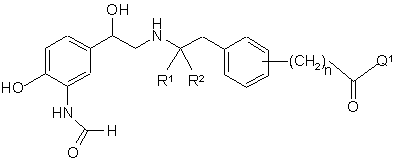 , (1)
, (1)
в якій (CH2)n-C(=O)Q1-група розташована в мета- або пара-положенні,
R1 і R2 кожний незалежно вибирають з водню та (С1-С4)алкілу;
n дорівнює 0, 1 або 2;
Q1 є групою, що вибирають з
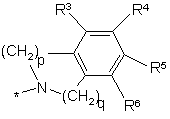 ,
,
в якій р дорівнює 1 або 2 і q дорівнює 1 або 2, згадана група є необов'язково місткованою із застосуванням одного атома вуглецю,
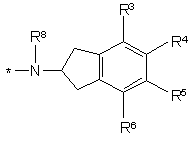 ,
,
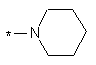 ,
,
і група *-NR8-Q2-А, в якій Q2 є С1-С4алкіленом, R8 є воднем або С1-С4алкілом і А є піридилом, С3-С10циклоалкілом, згаданий циклоалкіл є необов'язково місткованим із застосуванням одного або більше атомів вуглецю, тетрагідропіранілом, піперидинілом, тетрагідротіопіранілом або групою
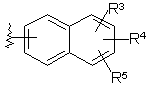
або
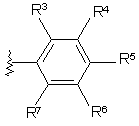 ,
,
R3, R4, R5, R6 і R7 є однаковими або різними і вибрані з водню, С1-С4алкілу, OR9, SR9, SOR9, SO2R9, гало, CO2R9, СF3, CN, ОСF3, SO2NR9R10, CONR9R10, NR9R10, NHCOR10 і фенілу, необов'язково заміщеного від 1 до 3 групами, вибраними з OR9, гало і С1-С4алкілу
R9 і R10 є однаковими або різними і вибрані з водню або С1-С4алкілу і * представляє місце приєднання до карбонільної групи;
або, якщо прийнятно, її фармацевтично прийнятні солі і/або ізомери, таутомери, сольвати або їх ізотопні модифікації.
2. Сполука за п. 1, в якій Q1 є групою *-NH-Q2-A, в якій А є циклогексилом або адамантилом.
3. Сполука за п. 1, в якій Q1 є групою *-NН-Q2-А, в якій А є групою
 ,
,
в якій R3, R4, R5, R6 і R7 є однаковими або різними і вибрані з водню, С1-С4алкілу, OR9, SR9, SOR9, SO2R9, гало, CN, CO2R9, СF3, ОСF3, SO2NR9R10, CONR9R10, NR9R10, NHCOR10 і фенілу, необов'язково заміщеного від 1 до 3 групами, вибраними з OR9, гало і С1-С4алкілу, за умови, що принаймні 2 з R3-R7 означають водень;
в якій R9 і R10 є однаковими або різними і вибрані з водню або С1-С4алкілу.
4. Сполука за п. 3, в якій Q1 є групою *-NH-Q2-A, в якій А є групою
 ,
,
де R3, R4, R5, R6 і R7 є однаковими або різними і вибрані з водню, ОН, СН3, ОСН3, ОСF3, OCH2-СН3, SСН3, N(CH3)2, N(C=O)CH3, C(=O)NH2, СООСН3, SО2СН3, SO2NH2, CN, гало, СF3 і фенілу, необов'язково заміщеного ОН.
5. Сполука за п. 1, в якій А є групою
 ,
,
де один з R3-R7 є ОН або фенілом, заміщеним ОН.
6. Сполука за п. 1, в якій А є нафтилом, необов'язково заміщеним ОН.
7. Сполука за будь-яким з пп. 1-6, в якій Q2 є -СН2-, -(СН2)2-, -(СН2)3-, -СН2-С(СН3)2- або -С(СН3)2-.
8. Сполука за п. 7, в якій Q2 є -СН2-.
9. Сполука за п. 1, в якій Q1 є
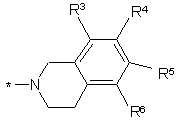 ,
,
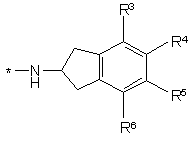 ,
,
в якій R3, R4, R5 і R6 є воднем.
10. Сполука за будь-яким з пп. 1-9, в якій R1 є воднем або С1-С4алкілом і R2 є С1-С4алкілом.
11. Сполука за п. 10, в якій R1 є воднем або СН3 і R2 є воднем або СН3.
12. Сполука за пп. 1-11, в якій n дорівнює 0 або 1.
13. Сполука за будь-яким з пп. 1-12, яка є (R,R)-стереоізомером.
14. Сполука за будь-яким з пп. 1-13, в якій (CH2)n-C(=O)Q1-група розташована в мета-положенні.
15. Сполука за п. 1, яку вибирають з групи, що включає:
N-бензил-2-(3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}феніл)ацетамід;
N-(3,4-диметилбензил)-2-(3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}феніл)ацетамід;
N-[2-(4-хлорфеніл)етил]-3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}бензамід;
N-[2-(2-хлорфеніл)етил]-3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}бензамід;
3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}-N-(2-нафтален-1-ілетил)бензамід;
N-[2-(2,6-диметилфеніл)етил]-3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}бензамід;
N-[2-(2,3-диметилфеніл)етил]-3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропілбензамід;
3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}-N-[2-(4-гідрокси-2,3-диметилфеніл)етил]бензамід;
3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}-N-[2-(4-метоксифеніл)етил]бензамід;
3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}-N-фенетилбензамід;
N-циклогексилметил-3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}бензамід;
N-[5-((1R)-2-{1,1-диметил-2-[3-(піперидин-1-карбоніл)феніл]етиламіно}-1-гідроксіетил)-2-гідроксифеніл]формамід;
3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}-N-[2-(3-трифторметилфеніл)етил]бензамід;
3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}-N-(3-фенілпропіл)бензамід;
3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}-N-індан-2-ілбензамід;
3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}-N-(2-піридин-2-ілетил)бензамід;
3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}-N-[2-(4-сульфамоїлфеніл)етил]бензамід;
N-(4-диметиламінобензил)-2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)ацетамід;
N-[5-(2-{(1R)-2-[3-(3,4-дигідро-1Н-ізохінолін-2-карбоніл)феніл]-1,1-диметилетиламіно}-1-гідроксіетил)-2-гідроксифеніл]формамід;
3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}-N-(4'-гідроксибіфеніл-3-ілметил)бензамід;
3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}-N-[2-(4-гідрокси-2,5-диметилфеніл)етил]бензамід;
3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}-N-[2-(4-гідрокси-3-метилфеніл)етил]бензамід;
N-(4-ацетиламінобензил)-2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)ацетамід;
4-{[2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)ацетиламіно]метил}бензамід;
N-адамантан-1-іл-3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}бензамід;
3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}-N-(2-гідроксинафтален-1-ілметил)бензамід;
3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}-N-(4-гідрокси-3,5-диметилбензил)бензамід;
3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}-N-(6-гідроксинафтален-2-ілметил)бензамід;
N-(3,6-дихлор-2-гідроксибензил)-3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}бензамід;
N-(3,4-диметилбензил)-2-(3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]етил}феніл)ацетамід;
3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}-N-[2-(4-гідроксифеніл)-2-метилпропіл]бензамід;
3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}-N-(4'-гідроксибіфеніл-4-ілметил)бензамід;
N-адамантан-1-іл-2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)ацетамід;
N-[5-(2-{2-[3-(10-азатрицикло[6.3.1.0*2,7*]додека-2(7),3,5-триєн-10-карбоніл)феніл]-1,1-диметилетиламіно}-1-гідроксіетил)-2-гідроксифеніл]формамід;
2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)-N-(4'-гідроксибіфеніл-3-ілметил)ацетамід;
метиловий естер 4-{[2-(3-{2-[(2R-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}феніл)ацетиламіно]метил}бензойної кислоти;
2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}феніл)-N-(4-трифторметоксибензил)ацетамід;
N-(2-хлор-4-гідроксибензил)-N-етил-2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}феніл)ацетамід;
N-(2-хлор-4-гідроксибензил)-2-(3-{(2R)-2-[(2R)-2-(3-форміламно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}феніл)ацетамід;
2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)-N-(4-гідрокси-3,5-диметилбензил)ацетамід;
2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)-N-(2-гідроксинафтален-1-ілметил)ацетамід;
N-(5-хлор-2-гідроксибензил)-2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)ацетамід;
N-(3,5-дихлор-2-гідроксибензил)-2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)ацетамід;
2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)-N-(6-гідроксинафтален-2-ілметил)ацетамід;
2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)-N-(4'-гідроксибіфеніл-4-ілметил)ацетамід;
N-(4-ціанобензил)-2-(3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}феніл)ацетамід;
2-(3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}феніл)-N-(4-метансульфонілбензил)ацетамід;
2-(3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}феніл)-N-(4-метилсульфанілбензил)ацетамід;
2-(3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}феніл)-N-(4-трифторметилбензил)ацетамід;
2-(3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}феніл)-N-(4'-гідроксибіфеніл-4-ілметил)ацетамід;
N-[2-(5-хлор-2-гідроксифеніл)етил]-3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}бензамід;
2-(3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}феніл)-N-(4'-гідроксибіфеніл-3-ілметил)ацетамід;
3-{2-[(2R)-2-(3-форміламіно-4-гідроксифенілі)-2-гідроксіетиламіно]пропіл}-N-[2-(4-гідроксифеніл)-2-метилпропіл]бензамід;
N-(2-хлор-4-гідроксибензил)-2-(3-{(2R)-2-[(2R)-(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)ацетамід;
N-[2-(5-хлор-2-гідроксифеніл)етил]-3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}бензамід;
3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]пропіл}-N-[2-(4-гідроксифеніл)-2-метилпропіл]бензамід;
2-(3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}феніл)-N-(тетрагідротіопіран-4-іл)ацетамід;
N-(5-хлор-2-гідроксибензил)-2-(3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}феніл)ацетамід і
N-{5-[(1R)-2-((1R)-2-{3-[3-(3,4-дигідро-1H-ізохінолін-2-іл)-3-оксопропіл]феніл}-1-метилетиламіно)-1-гідроксіетил]-2-гідроксифеніл}формамід.
16. N-(5-хлор-2-гідроксибензил)-2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)ацетамід або його фармацевтично прийнятна сіль або сольват.
17. 2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)-N-(4-гідрокси-3,5-диметилбензил)ацетамід або його фармацевтично прийнятна сіль або сольват.
18. 2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)-N-(6-гідроксинафтален 2-ілметил)ацетамід або його фармацевтично прийнятна сіль або сольват.
19. 2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)-N-(4'-гідроксибіфеніл-4-ілметил)ацетамід або його фармацевтично прийнятна сіль або сольват.
20. N-[2-(4-хлорфеніл)етил]-3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2-гідроксіетиламіно]-2-метилпропіл}бензамід або його фармацевтично прийнятна сіль або сольват.
21. Фармацевтична композиція, що містить принаймні ефективну кількість сполуки формули (1), як описано в будь-якому з пп. 1-20, або її фармацевтично прийнятну сіль або модифіковану форму і один або більше фармацевтично прийнятних екціпієнтів.
22. Сполука формули (1), як описано в будь-якому з пп. 1-20, або її фармацевтично прийнятна сіль, модифіковане похідне або композиція для використання як медикаменту.
23. Застосування сполуки формули (1), як описано в будь-якому з пп. 1-20, або її фармацевтично прийнятної солі, модифікованого похідного або композиції для виробництва лікарського засобу для лікування захворювань, розладів і станів, що вибирають з групи, яка включає:
астму будь-якого типу, етіології або патогенезу, зокрема астму, що є членом, який вибирають з групи, яка включає атопічну астму, неатопічну астму, алергічну астму, атопічну бронхіальну IgЕ-опосередковану астму, бронхіальну астму, ессенціальну астму, істинну астму, інфекційно-алергійну астму, викликану патофізіологічними розладами, зовнішню астму, викликану зовнішніми факторами, есенціальну астму невідомого або неочевидного походження, неатопічну астму, бронхітну астму, емфізематозну астму, астму, викликану фізичним навантаженням, астму, індуковану алергеном, астму, індуковану холодним повітрям, професійну астму, інфекційну астму, спричинену бактеріальною, фунгальною, протозойною або вірусною інфекцією, неалергійну астму, початкову астму, синдром задухи у немовлят і бронхіоліт,
хронічну або гостру бронхоконстрикцію, хронічний бронхіт, обструкцію малих дихальних шляхів та емфізему,
обструктивні або запальні захворювання дихальних шляхів будь-якого типу, етіології або патогенезу, зокрема обструктивне або запальне захворювання дихальних шляхів, що є членом, який вибирають з групи, що включає хронічну еозинофільну пневмонію, хронічне обструктивне легеневе захворювання (COPD), COPD, що включає хронічний бронхіт, легеневу емфізему або диспное, пов'язане або непов'язане з COPD, COPD, що характеризується незворотною прогресуючою обструкцією дихальних шляхів, респіраторний дистрессиндром повнолітніх (ARDS), загострення респіраторної гіперреактивності на фоні іншої фармакотерапії і захворювання дихальних шляхів, що пов'язані з легеневою гіпертензією,
бронхіт будь-якого типу, етіології або патогенезу; зокрема бронхіт, що є членом, що вибирають з групи, яка включає: гострий бронхіт, гострий ларинготрахеальний бронхіт, арахідоновий бронхіт, катаральний бронхіт, крупозний бронхіт, сухий бронхіт, інфекційний астматичний бронхіт, продуктивний бронхіт, стафілококовий або стрептококовий бронхіт і везикулярний бронхіт,
гостре ушкодження легень,
бронхоектазію будь-якого типу, етіології або патогенезу, зокрема бронхоектазія, що є членом, який вибирають з групи, що включає циліндричну бронхоектазію, осумковану бронхоектазію, веретеноподібну бронхоектазію, капілярну бронхоектазію, циститну бронхоектазію, суху бронхоектазію і фолікулярну бронхоектазію.
24. Спосіб лікування ссавця, включаючи людину, в якому згаданому ссавцеві вводять ефективну кількість сполуки формули (1), як описано в будь-якому з пп. 1-20, або її фармацевтично прийнятної солі, модифікованого похідного або композиції, що має b2 агоністичну активність.
25. Комбінація сполуки згідно з будь-яким з пп. 1-20 з іншим терапевтичним агентом(ами), що вибирають з наступного переліку:
(a) інгібітори 5-ліпоксигенази (5-LO) або антагоністи 5-ліпоксигенази активуючого протеїну (FLAP),
(b) антагоністи лейкотриєну (LTRAs), включаючи антагоністи L-ТВ4, L-TC4, LTD4 і LТЕ4,
(c) антагоністи рецептора гістаміну, включаючи Н1 і Н3 антагоністи,
(d) агоністи a1- і a2-адренорецептора, судинозвужувальні симпатоміметичні агенти для протизастійного застосування,
(e) антагоністи мускаринового М3 рецептора або антихолінергічні агенти,
(f) інгібітори PDE, наприклад, інгібітори PDE3, PDE4 і PDE5,
(g) теофілін,
(h) хромоглікат натрію,
(і) інгібітори СОХ як неселективні, так і селективні інгібітори СОХ-1 або СОХ-2 (NSAIDs),
(j) пероральні глюкокортикостероїди і глюкокортикостероїди, що інгалюються,
(k) моноклональні антитіла, активні проти ендогенного запалення,
(l) антипухлинні агенти фактора некрозу (анти-TNF-a),
(m) інгібітори адгезії молекули, включаючи VLA-4 антагоністи,
(n) антагоністи рецептора кініну-В1 і -B2,
(о) імуносупресивні агенти,
(р) інгібітори матриксних металопротеїназ (MMPs),
(q) антагоністи рецептора тахікініну NK1, NK2 і NK3,
(r) інгібітори еластази,
(s) агоністи рецептора аденозину А2а,
(t) інгібітори урокінази,
(u) сполуки, що діють як допамінові рецептори, наприклад, D2 агоністи,
(v) модулятори NFkb шляху, наприклад, ІКК інгібітори,
(w) модулятори цитокінових сигнальних шляхів, такі як р38 МАР кіназа або syk кіназа,
(х) агенти, що можуть класифікуватись як муколітики або протикашлеві агенти,
(у) антибіотики,
(z) інгібітори HDAC та
(аа) інгібітори РІЗ кінази.
Текст
УКРАЇНА (19) UA (11) 86615 (13) C2 (51) МПК (2009) C07C 233/43 (2006.01) C07C 217/60 (2006.01) A61K 31/135 МІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ ДЕРЖАВНИЙ ДЕПАРТАМЕНТ ІНТЕЛЕКТУАЛЬНОЇ ВЛАСНОСТІ ОПИС ДО ПАТЕНТУ НА ВИНАХІД (54) ПОХІДНІ ФОРМАМІДУ, КОРИСНІ ЯК АДРЕНОРЕЦЕПТОРИ 1 2 R8 R4 N * R5 R6 R1 R2 (CH2) n Q1 O HN H R5 або R3 R4 O , (1) в якій (CH2)n-C(=O)Q1-група розташована в метаабо пара-положенні, R1 і R2 кожний незалежно вибирають з водню та (С1-С4)алкілу; n дорівнює 0, 1 або 2; Q1 є групою, що вибирають з R3 R4 (CH2) p * N R5 (CH2)q R6 , R5 R7 R6 , R3, R4, R5, R6 і R7 є однаковими або різними і вибрані з водню, С1-С4алкілу, OR9, SR9, SOR9, SO2R9, гало, CO2R9, СF3, CN, ОСF3, SO2NR9R10, CONR9R10, NR9R10, NHCOR10 і фенілу, необов'язково заміщеного від 1 до 3 групами, вибраними з OR9, гало і С1-С4алкілу R9 і R10 є однаковими або різними і вибрані з водню або С1-С4алкілу і * представляє місце приєднання до карбонільної групи; (13) 86615 R4 (11) , і група *-NR8-Q2-А, в якій Q2 є С1-С4алкіленом, R8 є воднем або С1-С4алкілом і А є піридилом, С3С10циклоалкілом, згаданий циклоалкіл є необов'язково місткованим із застосуванням одного або більше атомів вуглецю, тетрагідропіранілом, піперидинілом, тетрагідротіопіранілом або групою R3 C2 N * H N HO , UA OH в якій р дорівнює 1 або 2 і q дорівнює 1 або 2, згадана група є необов'язково місткованою із застосуванням одного атома вуглецю, R3 (19) (21) a200610157 (22) 10.03.2005 (24) 12.05.2009 (86) PCT/IB2005/000619, 10.03.2005 (31) 0425054.4 (32) 12.11.2004 (33) GB (31) 04290767.5 (32) 23.03.2004 (33) EP (46) 12.05.2009, Бюл.№ 9, 2009 р. (72) БРАУН АЛАН ДЕНІЕЛ, БАННЕДЖ МАРК ЕДВАРД, ГЛОССОП ПОЛ АЛАН, ДЖЕЙМС КІМ, ЛЕЙН ШАРЛОТТ ЕЛІС ЛУІЗ, ЛЬЮТВЕЙТ РАССЕЛЛ ЕНДРЮ, ПРАЙС ДЕВІД ЕНТОНІ (73) ПФАЙЗЕР ІНК. (56) EP 1 235 787 A 04.09.2002 CH 686 869 A 31.07.1996 ES 2 005 492 A 01.03.1989 US 2004/006102 A1 08.01.2004 WO 03/042160 A 22.05.2003 (57) 1. Сполука загальної формули (1) 3 86615 або, якщо прийнятно, її фармацевтично прийнятні солі і/або ізомери, таутомери, сольвати або їх ізотопні модифікації. 2. Сполука за п. 1, в якій Q1 є групою *-NH-Q2-A, в якій А є циклогексилом або адамантилом. 3. Сполука за п. 1, в якій Q1 є групою *-NН-Q2-А, в якій А є групою R3 R4 4 R3 R4 * N H R5 R6 , в якій R , R , R і R6 є воднем. 10. Сполука за будь-яким з пп. 1-9, в якій R1 є воднем або С1-С4алкілом і R2 є С1-С4алкілом. 11. Сполука за п. 10, в якій R1 є воднем або СН3 і R2 є воднем або СН3. 12. Сполука за пп. 1-11, в якій n дорівнює 0 або 1. 13. Сполука за будь-яким з пп. 1-12, яка є (R,R)стереоізомером. 14. Сполука за будь-яким з пп. 1-13, в якій (CH2)nC(=O)Q1-група розташована в мета-положенні. 15. Сполука за п. 1, яку вибирають з групи, що включає: N-бензил-2-(3-{2-[(2R)-2-(3-форміламіно-4гідроксифеніл)-2-гідроксіетиламіно]-2метилпропіл}феніл)ацетамід; N-(3,4-диметилбензил)-2-(3-{2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}феніл)ацетамід; N-[2-(4-хлорфеніл)етил]-3-{2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}бензамід; N-[2-(2-хлорфеніл)етил]-3-{2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}бензамід; 3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}-N-(2-нафтален1-ілетил)бензамід; N-[2-(2,6-диметилфеніл)етил]-3-{2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}бензамід; N-[2-(2,3-диметилфеніл)етил]-3-{2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропілбензамід; 3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}-N-[2-(4-гідрокси2,3-диметилфеніл)етил]бензамід; 3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}-N-[2-(4метоксифеніл)етил]бензамід; 3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}-Nфенетилбензамід; N-циклогексилметил-3-{2-[(2R)-2-(3-форміламіно4-гідроксифеніл)-2-гідроксіетиламіно]-2метилпропіл}бензамід; N-[5-((1R)-2-{1,1-диметил-2-[3-(піперидин-1карбоніл)феніл]етиламіно}-1-гідроксіетил)-2гідроксифеніл]формамід; 3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}-N-[2-(3трифторметилфеніл)етил]бензамід; 3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}-N-(3фенілпропіл)бензамід; 3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}-N-індан-2ілбензамід; 3 R5 R6 R7 , в якій R , R , R5, R6 і R7 є однаковими або різними і вибрані з водню, С1-С4алкілу, OR9, SR9, SOR9, SO2R9, гало, CN, CO2R9, СF3, ОСF3, SO2NR9R10, CONR9R10, NR9R10, NHCOR10 і фенілу, необов'язково заміщеного від 1 до 3 групами, вибраними з OR9, гало і С1-С4алкілу, за умови, що принаймні 2 з R3-R7 означають водень; в якій R9 і R10 є однаковими або різними і вибрані з водню або С1-С4алкілу. 4. Сполука за п. 3, в якій Q1 є групою *-NH-Q2-A, в якій А є групою R3 R4 3 4 R5 R6 R7 , де R , R , R , R6 і R7 є однаковими або різними і вибрані з водню, ОН, СН3, ОСН3, ОСF3, OCH2-СН3, SСН3, N(CH3)2, N(C=O)CH3, C(=O)NH2, СООСН3, SО2СН3, SO2NH2, CN, гало, СF3 і фенілу, необов'язково заміщеного ОН. 5. Сполука за п. 1, в якій А є групою R3 R4 3 4 5 R5 R7 R6 , де один з R3-R7 є ОН або фенілом, заміщеним ОН. 6. Сполука за п. 1, в якій А є нафтилом, необов'язково заміщеним ОН. 7. Сполука за будь-яким з пп. 1-6, в якій Q2 є -СН2-, -(СН2)2-, -(СН2)3-, -СН2-С(СН3)2- або -С(СН3)2-. 8. Сполука за п. 7, в якій Q2 є -СН2-. 9. Сполука за п. 1, в якій Q1 є R3 R4 * R5 N R6 , 4 5 5 3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}-N-(2-піридин-2ілетил)бензамід; 3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}-N-[2-(4сульфамоїлфеніл)етил]бензамід; N-(4-диметиламінобензил)-2-(3-{(2R)-2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]пропіл}феніл)ацетамід; N-[5-(2-{(1R)-2-[3-(3,4-дигідро-1Н-ізохінолін-2карбоніл)феніл]-1,1-диметилетиламіно}-1гідроксіетил)-2-гідроксифеніл]формамід; 3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}-N-(4'гідроксибіфеніл-3-ілметил)бензамід; 3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}-N-[2-(4-гідрокси2,5-диметилфеніл)етил]бензамід; 3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}-N-[2-(4-гідрокси3-метилфеніл)етил]бензамід; N-(4-ацетиламінобензил)-2-(3-{(2R)-2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]пропіл}феніл)ацетамід; 4-{[2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4гідроксифеніл)-2гідроксіетиламіно]пропіл}феніл)ацетиламіно]метил}бензамід; N-адамантан-1-іл-3-{2-[(2R)-2-(3-форміламіно-4гідроксифеніл)-2-гідроксіетиламіно]-2метилпропіл}бензамід; 3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}-N-(2гідроксинафтален-1-ілметил)бензамід; 3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}-N-(4-гідрокси3,5-диметилбензил)бензамід; 3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}-N-(6гідроксинафтален-2-ілметил)бензамід; N-(3,6-дихлор-2-гідроксибензил)-3-{2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}бензамід; N-(3,4-диметилбензил)-2-(3-{2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]етил}феніл)ацетамід; 3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}-N-[2-(4гідроксифеніл)-2-метилпропіл]бензамід; 3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}-N-(4'гідроксибіфеніл-4-ілметил)бензамід; N-адамантан-1-іл-2-(3-{(2R)-2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]пропіл}феніл)ацетамід; N-[5-(2-{2-[3-(10-азатрицикло[6.3.1.0*2,7*]додека2(7),3,5-триєн-10-карбоніл)феніл]-1,1диметилетиламіно}-1-гідроксіетил)-2гідроксифеніл]формамід; 2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)N-(4'-гідроксибіфеніл-3-ілметил)ацетамід; метиловий естер 4-{[2-(3-{2-[(2R-2-(3-форміламіно4-гідроксифеніл)-2-гідроксіетиламіно]-2 86615 6 метилпропіл}феніл)ацетиламіно]метил}бензойної кислоти; 2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4гідроксифеніл)-2-гідроксіетиламіно]-2метилпропіл}феніл)-N-(4трифторметоксибензил)ацетамід; N-(2-хлор-4-гідроксибензил)-N-етил-2-(3-{(2R)-2[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}феніл)ацетамід; N-(2-хлор-4-гідроксибензил)-2-(3-{(2R)-2-[(2R)-2-(3форміламно-4-гідроксифеніл)-2-гідроксіетиламіно]2-метилпропіл}феніл)ацетамід; 2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)N-(4-гідрокси-3,5-диметилбензил)ацетамід; 2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)N-(2-гідроксинафтален-1-ілметил)ацетамід; N-(5-хлор-2-гідроксибензил)-2-(3-{(2R)-2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]пропіл}феніл)ацетамід; N-(3,5-дихлор-2-гідроксибензил)-2-(3-{(2R)-2-[(2R)2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]пропіл}феніл)ацетамід; 2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)N-(6-гідроксинафтален-2-ілметил)ацетамід; 2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)N-(4'-гідроксибіфеніл-4-ілметил)ацетамід; N-(4-ціанобензил)-2-(3-{2-[(2R)-2-(3-форміламіно-4гідроксифеніл)-2-гідроксіетиламіно]-2метилпропіл}феніл)ацетамід; 2-(3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}феніл)-N-(4метансульфонілбензил)ацетамід; 2-(3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}феніл)-N-(4метилсульфанілбензил)ацетамід; 2-(3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}феніл)-N-(4трифторметилбензил)ацетамід; 2-(3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}феніл)-N-(4'гідроксибіфеніл-4-ілметил)ацетамід; N-[2-(5-хлор-2-гідроксифеніл)етил]-3-{2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}бензамід; 2-(3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}феніл)-N-(4'гідроксибіфеніл-3-ілметил)ацетамід; 3-{2-[(2R)-2-(3-форміламіно-4-гідроксифенілі)-2гідроксіетиламіно]пропіл}-N-[2-(4-гідроксифеніл)-2метилпропіл]бензамід; N-(2-хлор-4-гідроксибензил)-2-(3-{(2R)-2-[(2R)-(2R)2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]пропіл}феніл)ацетамід; N-[2-(5-хлор-2-гідроксифеніл)етил]-3-{2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}бензамід; 3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]пропіл}-N-[2-(4-гідроксифеніл)-2метилпропіл]бензамід; 7 2-(3-{2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}феніл)-N(тетрагідротіопіран-4-іл)ацетамід; N-(5-хлор-2-гідроксибензил)-2-(3-{2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}феніл)ацетамід і N-{5-[(1R)-2-((1R)-2-{3-[3-(3,4-дигідро-1H-ізохінолін2-іл)-3-оксопропіл]феніл}-1-метилетиламіно)-1гідроксіетил]-2-гідроксифеніл}формамід. 16. N-(5-хлор-2-гідроксибензил)-2-(3-{(2R)-2-[(2R)2-(3-форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]пропіл}феніл)ацетамід або його фармацевтично прийнятна сіль або сольват. 17. 2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)N-(4-гідрокси-3,5-диметилбензил)ацетамід або його фармацевтично прийнятна сіль або сольват. 18. 2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)N-(6-гідроксинафтален 2-ілметил)ацетамід або його фармацевтично прийнятна сіль або сольват. 19. 2-(3-{(2R)-2-[(2R)-2-(3-форміламіно-4гідроксифеніл)-2-гідроксіетиламіно]пропіл}феніл)N-(4'-гідроксибіфеніл-4-ілметил)ацетамід або його фармацевтично прийнятна сіль або сольват. 20. N-[2-(4-хлорфеніл)етил]-3-{2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксіетиламіно]-2-метилпропіл}бензамід або його фармацевтично прийнятна сіль або сольват. 21. Фармацевтична композиція, що містить принаймні ефективну кількість сполуки формули (1), як описано в будь-якому з пп. 1-20, або її фармацевтично прийнятну сіль або модифіковану форму і один або більше фармацевтично прийнятних екціпієнтів. 22. Сполука формули (1), як описано в будь-якому з пп. 1-20, або її фармацевтично прийнятна сіль, модифіковане похідне або композиція для використання як медикаменту. 23. Застосування сполуки формули (1), як описано в будь-якому з пп. 1-20, або її фармацевтично прийнятної солі, модифікованого похідного або композиції для виробництва лікарського засобу для лікування захворювань, розладів і станів, що вибирають з групи, яка включає: астму будь-якого типу, етіології або патогенезу, зокрема астму, що є членом, який вибирають з групи, яка включає атопічну астму, неатопічну астму, алергічну астму, атопічну бронхіальну IgЕопосередковану астму, бронхіальну астму, ессенціальну астму, істинну астму, інфекційно-алергійну астму, викликану патофізіологічними розладами, зовнішню астму, викликану зовнішніми факторами, есенціальну астму невідомого або неочевидного походження, неатопічну астму, бронхітну астму, емфізематозну астму, астму, викликану фізичним навантаженням, астму, індуковану алергеном, астму, індуковану холодним повітрям, професійну астму, інфекційну астму, спричинену бактеріальною, фунгальною, протозойною або вірусною інфекцією, неалергійну астму, початкову астму, синдром задухи у немовлят і бронхіоліт, хронічну або гостру бронхоконстрикцію, хронічний бронхіт, обструкцію малих дихальних шляхів та емфізему, 86615 8 обструктивні або запальні захворювання дихальних шляхів будь-якого типу, етіології або патогенезу, зокрема обструктивне або запальне захворювання дихальних шляхів, що є членом, який вибирають з групи, що включає хронічну еозинофільну пневмонію, хронічне обструктивне легеневе захворювання (COPD), COPD, що включає хронічний бронхіт, легеневу емфізему або диспное, пов'язане або непов'язане з COPD, COPD, що характеризується незворотною прогресуючою обструкцією дихальних шляхів, респіраторний дистрессиндром повнолітніх (ARDS), загострення респіраторної гіперреактивності на фоні іншої фармакотерапії і захворювання дихальних шляхів, що пов'язані з легеневою гіпертензією, бронхіт будь-якого типу, етіології або патогенезу; зокрема бронхіт, що є членом, що вибирають з групи, яка включає: гострий бронхіт, гострий ларинготрахеальний бронхіт, арахідоновий бронхіт, катаральний бронхіт, крупозний бронхіт, сухий бронхіт, інфекційний астматичний бронхіт, продуктивний бронхіт, стафілококовий або стрептококовий бронхіт і везикулярний бронхіт, гостре ушкодження легень, бронхоектазію будь-якого типу, етіології або патогенезу, зокрема бронхоектазія, що є членом, який вибирають з групи, що включає циліндричну бронхоектазію, осумковану бронхоектазію, веретеноподібну бронхоектазію, капілярну бронхоектазію, циститну бронхоектазію, суху бронхоектазію і фолікулярну бронхоектазію. 24. Спосіб лікування ссавця, включаючи людину, в якому згаданому ссавцеві вводять ефективну кількість сполуки формули (1), як описано в будьякому з пп. 1-20, або її фармацевтично прийнятної солі, модифікованого похідного або композиції, що має b2 агоністичну активність. 25. Комбінація сполуки згідно з будь-яким з пп. 120 з іншим терапевтичним агентом(ами), що вибирають з наступного переліку: (a) інгібітори 5-ліпоксигенази (5-LO) або антагоністи 5-ліпоксигенази активуючого протеїну (FLAP), (b) антагоністи лейкотриєну (LTRAs), включаючи антагоністи L-ТВ4, L-TC4, LTD4 і LТЕ4, (c) антагоністи рецептора гістаміну, включаючи Н1 і Н3 антагоністи, (d) агоністи a1- і a2-адренорецептора, судинозвужувальні симпатоміметичні агенти для протизастійного застосування, (e) антагоністи мускаринового М3 рецептора або антихолінергічні агенти, (f) інгібітори PDE, наприклад, інгібітори PDE3, PDE4 і PDE5, (g) теофілін, (h) хромоглікат натрію, (і) інгібітори СОХ як неселективні, так і селективні інгібітори СОХ-1 або СОХ-2 (NSAIDs), (j) пероральні глюкокортикостероїди і глюкокортикостероїди, що інгалюються, (k) моноклональні антитіла, активні проти ендогенного запалення, (l) антипухлинні агенти фактора некрозу (антиTNF-a), (m) інгібітори адгезії молекули, включаючи VLA-4 антагоністи, 9 86615 10 (n) антагоністи рецептора кініну-В1 і -B2, (о) імуносупресивні агенти, (р) інгібітори матриксних металопротеїназ (MMPs), (q) антагоністи рецептора тахікініну NK1, NK2 і NK3, (r) інгібітори еластази, (s) агоністи рецептора аденозину А2а, (t) інгібітори урокінази, (u) сполуки, що діють як допамінові рецептори, наприклад, D2 агоністи, (v) модулятори NFkb шляху, наприклад, ІКК інгібітори, (w) модулятори цитокінових сигнальних шляхів, такі як р38 МАР кіназа або syk кіназа, (х) агенти, що можуть класифікуватись як муколітики або протикашлеві агенти, (у) антибіотики, (z) інгібітори HDAC та (аа) інгібітори РІЗ кінази. Даний винахід стосується b2 агоністів загальної формули: що швидко діють, в той час як форми довготривалої дії забезпечують уповільнене вивільнення і використовуються для тривалої терапії. Бронходилатація опосередковується через агонізм b2 адренорецептора, що експресується на клітинах гладких м'язів дихальних шляхів, що приводить до релаксації і, відповідно, бронходилатації. Таким чином, як функціональні антагоністи, b2 агоністи можуть попереджувати та регресувати вплив усіх бронхозвужувальних речовин, включаючи лейкотриєн D4 (LTD4), ацетилхолін, брадикінін, простагландини, гістамін та ендотеліни. Оскільки b2 рецептори так широко розповсюджені в дихальних шляхах, b2 агоністи можуть також впливати на інші типи клітин, що грають роль у перебігу астми. Наприклад, доповідалось, що b2 агоністи можуть стабілізувати тучні клітини. Інгібування вивільнення бронхозвужувальних речовин може показати, як b2 агоністи блокують бронхоконстрикцію, викликану алергенами, фізичними навантаженнями та холодним повітрям. Крім того, b2 агоністи інгібують холінергічну нейротрансмісію в дихальних шляхах людини, що може приводити до зменшення холінергічно-рефлекторної бронхоконстрикції. На додаток до дихальних шляхів, також було встановлено, що b2 адренорецептори також експресуються в інших органах та тканинах і, таким чином b2 агоністи, такі як описані в представленому винаході, можуть застосовуватися при лікуванні інших захворювань, що включають, але не обмежуються такими: захворювання нервової системи, передчасні пологи, застійна серцева недостатність, депресія, запальні та алергійні захворювання шкіри, псоріаз, проліферативні захворювання шкіри, глаукома та стани, для яких корисним є зниження кислотності шлунку, особливо, у випадку виразки шлунку та дванадцятипалої кишки. Однак, ряд b2 агоністів мають обмежене застосування завдяки їх низькій селективності або шкідливим побічним ефектам обумовленим високою системною дією і головним чином опосередковану через дію b2 адренорецепторів, що експресуються не в дихальних шляхах (м'язовий тремор, тахікардія, сильне серцебиття, неспокій). Тому існує потреба в покращенні агентів цього класу. Відповідно, все ще існує потреба в нових b2 агоністах, що будуть мати прийнятний фармакологічний профіль, наприклад, в одиницях активності, селективності, фармакокинетичних властивостей в якій R1, R2, n і Q1 мають значення, наведені нижче та способів їх одержання, композицій, що їх містять, та застосування таких похідних. Адренорецептори є членами великої надродини рецепторів, зв'язаних з G-білком. Підродина адренорецепторів сама підрозділяється на a та b підродини з b підродиною, що складається принаймні з 3 підтипів рецепторів: b1, b2 та b3. Ці рецептори проявляють характерні моделі експресії в тканинах різних систем та органів ссавців. b2 адренергічні (b2) рецептори експресуються, головним чином, в клітинах гладких м'язів (наприклад, гладких м'язів судин, бронхів, матки або кишечнику), в той час як b3 адренергічні рецептори, головним чином, експресуються в жирових тканинах (таким чином, b3 агоністи потенційно можуть бути придатними для лікування ожиріння та діабетів), а b1 адренергічні рецептори, головним чином, експресуються в тканинах серця (таким чином, b1 агоністи, головним чином, використовуються як серцеві стимулятори). Патофізіологія та лікування захворювань дихальних шляхів всебічно були розглянуті в літературі (як посилання дивіться Barnes, P. J. Chest, 1997, 111 : 2, pp.17S-26S та Bryan, S. А. та інші, Expert Opinion on investigational drugs, 2000, 9:1, pp.25-42) і тому лише короткі резюме будуть включені сюди для забезпечення певної інформації попереднього рівня техніки. Глюкокортикостероїди, анти-лейкотриєни, теофілін, хромони, антихолінергічні агенти та b2 агоністи складають класи лікарських засобів, що на даний час використовуються для лікування алергійних та неалергійних захворювань дихальних шляхів, таких як астма та хронічне обструктивне захворювання дихальних шляхів (COPD). Принципи лікування цих захворювань включають інгаляцію b2 агоністів як короткотривалої, так і довготривалої дії. Для "рятування" бронходилатації використовують b2 агоністи короткотривалої дії, 11 або тривалості дії. В цьому контексті, представлений винахід стосується нових b2 агоністів. Різні похідні формаміду вже були описані. Наприклад, в патентній заявці США 2004/0006112 описані сполуки, що мають активність b2 агоніста, формули: В патентній заявці США 2003/0229058 описані селективні b2 агоністи формули: Однак, ні одне з похідних формаміду, не виявляють фармакологічного профілю, який б дозволяв використовувати їх як ефективні лікарські засоби при лікуванні b2-опосередкованих захворювань та/або станів, зокрема, алергійних та неалергійних захворювань дихальних шляхів; зокрема, при введенні шляхом інгаляції. Винахід стосується сполук загальної формули (1): в якій (CH2)n-C(=O)Q1 група розташована в мета або пара положенні, - R1 і R2 кожний незалежно вибирають з водню та (С1-С4)алкілу; - n дорівнює 0, 1 або 2; - Q1 є групою, що вибирають з, в якій р дорівнює 1 або 2 і q дорівнює 1 або 2, згадана група необов'язково зв'язана містком з одного атому вуглецю, і група *-NR8-Q2-A, в якій Q2 є С1-С4 алкіленом, R є воднем або С1-С4 алкілом і А є піридилом, С3С10 циклоалкілом, згаданий циклоалкіл є необов'язково, зв'язаним містком з одного або більше атомів вуглецю, переважно 1, 2, 3 або 4, атомами 8 86615 12 вуглецю, тетрагідропіранілом, піперидинілом, тетрагідротіопіранілом або групою - R3, R4, R5, R6 і R7 є однаковими або різними і вибраними з водню, С1-С4 алкілу, OR9, SR9, SOR9, SO2R9, гало, CN, CO2R9, CF3, OCF3, SO2NR9R10, CONR9R10, NR9R10, NHCOR10 і фенілу необов'язково заміщеного від 1 до 3 групами вибраними з OR9, гало і С1-С4 алкілу - R9 і R10 є однаковими або різними і вибраними з водню або С1-С4 алкілу і * представляє місце приєднання до карбонільної групи; або, якщо прийнятно, їх фармацевтично прийнятні солі і/або ізомери, таутомери, сольвати або їх ізотопні модифікації. Сполуки формули (1) є агоністами b2 рецепторів, що є особливо корисними для лікування b2опосередкованих захворювань і/або станів і показують добру активність, зокрема, коли вводяться шляхом інгаляції. В наведеній вище загальній формулі (1), С1-С4 алкіл і С1-С4 алкілен означають нерозгалужену або розгалужену групу, що містить 1, 2, 3 або 4 атоми вуглецю. Це також використовується, якщо вони несуть замісники або зустрічаються як замісники на інших радикалах, наприклад, в О-(С1С4)алкільних радикалах, S-(С1-С4)алкільних радикалах і т. ін. Прикладами придатних (С1С4)алкільних радикалів є метил, етил, н-пропіл, ізо-пропіл, н-бутил, ізо-бутил, втор-бутил, третбутил і т. ін. Прикладами придатних О-(С1С4)алкільних радикалів є метокси, етокси, нпропілокси, ізо-пропілокси, н-бутилокси, ізобутилокси, втор-бутилокси та трет-бутилокси і т. ін. С3-С10 циклоалкіл, де 2 або більше атомів вуглецю є необов'язково, зв'язаними містком з одного або декількох атомів вуглецю, включає циклопропіл, циклобутил, циклопентил, циклогексил і циклогептил, адамантил, біцикло[3.1.1]гептан, біцикло[2.2.1]гептан, біцикло[2.2.2]октан. Переважними циклоалкільними групами є циклогексил і адамантил. Нарешті, гало означає атом галогену, вибраний з групи, яка включає фтор, хлор, бром та йод, особливо, фтор або хлор. Надалі, вільний зв'язок на фенільній групі, такій як структура показана нижче, означає, що феніл може бути заміщений в мета або пара положенні. Сполуки формули (1) 13 можна одержати використовуючи звичайні методики, такі як наступні ілюстративні методики, в яких Q1, Q2, R1, R2, А і n є такими, як визначено раніше для сполук формули (1), якщо не вказано інакше. Амідні похідні формули (1) можна одержати шляхом конденсування кислоти формули (2): 86615 14 метил і етил, згідно з будь-якою методикою добре відомою фахівцю в цій галузі для одержання кислоти з естеру, без модифікування залишку молекули. Наприклад, естер можна гідролізувати шляхом обробки водною кислотою або основою (наприклад, хлоридом водню, гідроксидом калію, гідроксидом натрію або гідроксидом літію), необов'язково в присутності розчинника або суміші розчинників (наприклад, води, 1,4-діоксану, тетрагідрофуран/вода), при температурі від 20°С до 100°С, протягом часу 1-40 годин. Альтернативно, якщо естер є бензильною групою, естер може бути гідрований в присутності придатного каталізатора (наприклад, паладію на вугіллі або гідроксиду паладію на вугіллі) в придатному розчиннику такому як (метанол, етанол, 2М аміак в метанолі) при температурі від 20°С до 50°С, протягом 1-48 годин в атмосфері водню, при тиску 1-4 атмосфери. Естер формули (4) можна одержати за допомогою реакції аміну формули (5): з аміном формули NHR8-Q2-A (3), в якій Ra і n є такими як визначено вище, з бромідом формули (6): Конденсування зазвичай проводять у надлишку згаданого аміну як акцептора кислоти, із звичайним конденсувальним агентом (наприклад, гідрохлоридом 1-(3-диметиламінопропіл)-3етилкарбодііміду, N,N'дициклогексилкарбодіімідом або гексафторфосфатом O-(1Н-бензотриазол-1-іл)-N,N,N',N'тетраметилуронію), необов'язково в присутності каталізатора (наприклад, гідрату 1гідроксибензотриазолу або 1-гідрокси-7азабензотриазолу) і необов'язково в присутності третинної амінової основи (наприклад, Nметилморфоліну, триетиламіну або діізопропілетиламіну). Реакцію можна проводити в придатному розчиннику, такому як піридин, диметилформамід, тетрагідрофуран, диметилсульфоксид, дихлорметан або етилацетат і при температурі від 10°С до 40°С (кімнатна температура) протягом періоду 124 години. Згаданий амін (3), (3'), (3") або (3''') або є наявним у продажу, або можна одержати за допомогою загальновідомих методик добре відомих фахівцю в цій галузі (наприклад, відновленням, окисленням, алкілуванням, конденсуванням медійованим перехідним металом, захистом, зняттям захисту і т. п.) з комерційно доступних матеріалів. Кислоту формули (2) можна одержати з відповідного естеру формули (4): в якій Ra є придатною кислото-захисною групою, переважно бензильною або (С1-С4)алкільною групою, яка включає, але не обмежується ними, В типовій методиці, амін формули (5) взаємодіє з бромідом формули (6), необов'язково, в присутності розчинника або суміші розчинників (наприклад, диметилсульфоксиду, толуолу, N,Nдиметилформамщу, ацетонітрилу), необов'язково, в присутності придатної основи (наприклад, триетиламіну, діізопропілетиламіну, карбонату калію) при температурі від 80°С до 120°С, протягом 12-48 годин. Бромід формули (6) можна одержати відповідно до способу, описаному в "Organic Process Research і Development 1998, 2, 96-99". Амін формули (5), де R1 є Me і R2 є воднем, можна одержати як або (R), або (S) енантіомер з відповідного захищеного аміну формули (7): в якій Ra і n є такими як визначено вище і Rb і Rc представляють будь-які придатні замісники, так що HNRbRc є хіральним аміном (наприклад, Rb може бути воднем і Re може бути aметилбензилом), за умови, що зв'язки між N і Rb і N і Rc можуть бути легко розщеплені, даючи вільний амін формули (5), використовуючи стандартні методики для відщеплення азот-захисних груп, таких як ті, що описані в книзі Protective Groups в Organic Synthesis Third Edition by T.W. Greene і P.G.M. Wuts, John Wiley і Sons Inc., 1999. 15 Амін формули (7) можна одержати як окремий діастереомер за допомогою реакції аміну формули HNRbRc з кетоном формули (8): в якій Ra, Rb, Rc і n є такими як визначено вище. В типовій методиці, реакція кетону формули (8) з аміном формули HNRbRc приводить до хіральної проміжної сполуки, яка в свою чергу відновлюється придатним відновлювальним агентом (наприклад, ціаноборгідридом натрію формули NaCNBH3 або триацетоксиборгідридом натрію формули Na(OAc)3BH), необов'язково, в присутності осушника (наприклад, молекулярні сита, сульфат магнію) і, необов'язково, в присутності кислотного каталізатора (наприклад, оцтової кислоти), з одержанням аміну формули (7) як суміші діастереомерів. Реакцію зазвичай проводять в розчиннику, такому як тетрагідрофуран або дихлорметан при температурі від 20°С до 80°С протягом 3-72 години. Одержаний продукт потім перетворюють у нітратну або гідрохлоридну сіль і селективно кристалізують з придатного розчинника або суміші розчинників (наприклад, ізопропанолу, етилацетату, етанолу, метанолу, діізопропілового етеру або діізопропілового етеру/метанолу), одержуючи (7) як окремий діастереомер. Кетон формули (8), в якому n=1, можна одержати шляхом конденсування, медійованого паладієм, з арилгалідом формули (9): в якій Ra є таким як визначено вище і Hal представляє атом галогену, який є, але не обмежується ними, бромом і йодом, з енолатом або еквівалентом енолату. В типовій методиці, арилгалід формули (9) взаємодіє з енолатом олова одержаним in situ шляхом обробки ізопропенілацетату метоксидом три-н-бутилолова формули Bu3SnOMe в присутності придатного паладієвого каталізатора (ацетат паладію/три-ортотолілфосфін формули Pd(OAc)2/P(o-ToI)3) в неполярному розчиннику (наприклад, толуолі, бензолі, гексані). Переважно, реакцію проводять при температурі від 80°С до 110°С протягом 6-16 годин. Арилгалід формули (9) можна одержати шляхом естерифікації відповідної кислоти формули (10): в якій Hal є таким як визначено вище, згідно з будь-якою методикою добре відомою фахівцю в цій галузі для одержання естеру з кислоти, без модифікування залишку молекули. В типовій методиці, кислота формули (10) взаємодіє із спиртовим розчинником формули RaOH, 86615 16 в якій Ra є таким як визначено вище, в присутності кислоти, такої як хлорид кислоти при температурі від 10°С до 40°С (кімнатна температура) протягом 8-16 годин. Альтернативно, кислоту формули (10) піддавали взаємодії з основою (наприклад, карбонатом цезію або калію) і обробляли за допомогою алкілгаліду (наприклад, метилйодиду, бензилброміду) в придатному розчиннику такому як N,Nдиметилформамід при температурі від 10°С до 40°С (кімнатна температура) протягом від 1 до 20 годин. Кислота формули (10) є комерційно доступним продуктом. Амін формули (5), де R1 і R2 обидва є С1-С4 алкілом, можна одержати відповідно до наступної схеми: в якій R1, R2 і Ra є такими як визначено вище. В типовій методиці, естер формули (11) піддають взаємодії з "активованим" алкілом (металоорганічним алкілом, таким як R2MgBr, R2MgCI або R2Li), одержуючи відповідний третинний спирт формули (12), використовуючи спосіб, описаний вище. Згаданий третинний спирт формули (12) потім обробляли за допомогою алкілнітрилу (наприклад, ацетонітрилу, хлорацетонітрилу), в присутності кислоти (наприклад, сірчаної кислоти, оцтової кислоти), одержуючи захищену проміжну сполуку, яку в свою чергу розщеплювали, використовуючи стандартні методики для відщеплення азот-захисних груп, таких як ті, що описані в підручниках. Одержану амінокислоту потім естерифікували, використовуючи описаний в цьому документі спосіб одержання аміну формули (5). Альтернативно, амін формули (5), в якій R1 і 2 R обидва є С1-С4 алкілом і n=0, можна одержати відповідно до наступної схеми: в якій R1, R2 і Ra є такими як визначено вище. В типовій методиці, естер формули (13) піддають взаємодії з "активованим" алкілом (металоорганічним алкілом, таким як R2MgBr, R2MgCI або R2Li), одержуючи відповідний третинний спирт формули (14), використовуючи спосіб, описаний вище. 17 Згаданий третинний спирт формули (14) потім обробляли за допомогою алкілнітрилу (наприклад, ацетонітрилу, хлорацетонітрилу), в присутності кислоти (наприклад, сірчаної кислоти, оцтової кислоти), одержуючи захищену проміжну сполуку, яку в свою чергу розщеплювали, використовуючи стандартні методики для відщеплення азот-захисних груп, таких як ті, що описані в підручниках, одержуючи бромамін (15). Одержаний бромамін (15) обробляли придатним паладієвим каталізатором (наприклад, [1,1'біс(дифенілфосфіно)фероцен]дихлорпаладію(ІІ), ацетат паладію (II), 1,1'біс(дифенілфосфін)фероцен], тріс(дибензилінденацетон)дипаладій(0), 2,2'біс(дифенілфосфін)-1,1'бінафтилдихлорпаладію(Іl)) в атмосфері монооксиду вуглецю, використовуючи RaOH як розчинник (наприклад, МеОН, EtOH, бензиловий спирт), або альтернативно використовуючи співрозчинник, такий як ДМФ, при підвищеній температурі (100°С) і тиску (100псі), одержуючи естер формули (5). Кетон формули (8), де n=2, можна одержати шляхом відновлення алкену формули (16): В типовій методиці, розчин олефіну формули (16) в придатному розчиннику (наприклад, метанолі, етанолі, етилацетаті) обробляли паладієвим каталізатором (наприклад, 10% паладієм на вугіллі) і витримували в атмосфері водню, необов'язково, при підвищеному тиску (наприклад, 60псі), при температурі від кімнатної до 60°С протягом 8-24 годин. Алкен формули (16) можна одержати шляхом конденсування, медійованого паладієм, активованого олефіну з арилгалідом формули (17): В типовій методиці, арилгалід (17) конденсували з вініловим естером (наприклад, метилакрилатом), в присутності придатного паладієвого каталізатора (наприклад, тетракис(трифенілфосфін)паладію (0) формули Pd(PPh3)4, ацетату паладію/три-орто-толілфосфіну формули Pd(OAc)2/P(o-Tol)3 або хлориду (дифенілфосфіно)фероценіл паладію формули dppfPdCI2), в придатному розчиннику (наприклад, ацетонітрилі, N,N-диметилформаміді, толуолі), необов'язково в присутності основи, такої як триетиламін при температурі від 40°С до 110°С протягом 8-24 години. Кетон формули (17) є комерційно доступним продуктом. Альтернативно сполуку формули (1) можна одержати за допомогою реакції броміду формули (6) та аміну формули (18): 86615 18 де R1, R2, Q1 і n є такими як визначено вище для сполук формули (1), якщо не вказано інакше. В типовій методиці, амін формули (18) піддають взаємодії з бромідом формули (6) необов'язково в присутності розчинника або суміші розчинників (наприклад, диметилсульфоксиду, толуолу, N,N-диметилформаміду, ацетонітрилу), необов'язково в присутності прийнятної основи (наприклад, триетиламіну, діізопропілетиламіну, карбонату калію) при температурі від 80°С до 120°С, протягом від 12 до 48 годин. Амід формули (18) можна одержати шляхом конденсування кислоти формули (19), залучаючи придатну аміно-захисну групу Р1: з аміном формули NHR8-Q2-A (3), Конденсування зазвичай проводять в надлишку згаданого аміну як акцептора кислоти, із звичайним конденсувальним агентом (наприклад, гідрохлоридом 1-(3-диметиламінопропіл)-3етилкарбодііміду або N,N'дициклогексилкарбодіімідом), необов'язково в присутності каталізатора (наприклад, гідрату 1гідроксибензотриазолу або 1-гідрокси-7азабензотриазолу) і необов'язково в присутності третинної амінової основи (наприклад, Nметилморфоліну, триетиламіну або діізопропілетиламіну). Реакцію можна проводити в придатному розчиннику, такому як піридин, N,Nдиметилформамід, тетрагідрофуран, диметилсульфоксид, дихлорметан або етилацетат і при температурі від 10°С до 40°С (кімнатна температура) протягом часу 1-24 години. Згаданий амін (3), (3'), (3") або (3''') або є наявним у продажу або можна одержати за допомогою загальновідомих методик добре відомих фахівцю в цій галузі (наприклад, відновленням, окисленням, алкілуванням, конденсуванням медійованим перехідним металом, захистом, зняттям захисту і т. п.) з комерційно доступних матеріалів. Кислоту формули (19) можна одержати з відповідного естеру формули (5). Кислоту формули (19), в якій R1 і R2 обидва є С1-С4 алкілом, можна одержати з естеру (5), залучаючи придатну амінозахисну групу Р1 перед утворенням кислоти або після цього: в якій Ra є придатною кислото-захисною групою, переважно (С1-С4)алкільною групою, яка включає, але не обмежується ними, метил і етил, згідно з будь-якою методикою добре відомою фахівцю в цій галузі для одержання кислоти з естеру, без модифікування залишку молекули. Наприклад, 19 естер можна гідролізувати шляхом обробки водною кислотою або основою (наприклад, хлоридом водню, гідроксидом калію, гідроксидом натрію або гідроксидом літію), необов'язково в присутності розчинника або суміші розчинників (наприклад, води, 1,4-діоксану, тетрагідрофурану/води), при температурі від 20°С до 100°С, протягом часу 1-40 годин. Амін формули (5), де R1 і R2 обидва є воднем, можна одержати відповідно до наступної схеми: в якій R1, R2 і Ra є такими як визначено вище. В типовій методиці, кислоту формули (20), переважно, відновлювали у відповідний спирт (21) в присутності естеру. Це можна здійснити шляхом утворення ацилімідазолу або змішаного ангідриду і подальшого відновлення боргідридом натрію або іншим придатним відновлювальним агентом. Згаданий первинний спирт формули (21) надалі перетворювали в групу, що відходить, таку як мезилат, тозилат, бромід або йодид і замінювали прийнятним нуклеофільним аміном. Переважним нуклеофілом є іон азиду, який можна відновити до первинного аміну шляхом гідрування або трифенілфосфін. Альтернативними нуклеофілами можуть бути аміак або алкіламіни, такі як бензиламін або аліламін і надалі відщеплювали алкільну групу для одержання аміну. 86615 20 одержанням сполуки формули 1 з використанням умов описаних раніше. Для деяких із стадій описаного вище способу одержання сполук формули (1), може бути необхідним захистити потенційно реакційноздатні функціональні групи, які небажано, щоб реагували, і потім відщепити згадані захисні групи. В такому випадку може використовуватися будь-який сумісний захисний радикал. Зокрема, можуть використовуватися способи захисту та зняття захисту, такі як описані Т.W. Greene і P.G.М. Wuts (Protective Groups в Organic Synthesis , John Wiley and Sons Inc. 1999) або by P.J. Kocienski (Protecting groups, Georg Thieme Verlag, 1994). Всі вищенаведені реакції та способи одержання нових вихідних сполук, використовуваних в згаданих методиках є традиційними придатними реагентами, а умови реакції для їх здійснення або одержання, також як методики виділення цільових продуктів, будуть добре відомими фахівцям з посиланням на попередні літературні джерела та приклади і препаративні приклади, наведені в них. До того ж сполуки формули (1), а також проміжні сполуки для їх одержання можуть бути очищені згідно з різними добре відомими способами, такими як, наприклад, кристалізація або хроматографія. Перевага надається підгрупам сполук формули (1), що включають наступні замісники: Переважно Q1 є групою *-NH-Q2-A, в якій А є циклогексилом або адамантилом. Переважно, Q1 є де R3, R4, R5 і R6 є воднем. Переважно Q1 є Альтернативно, амід формули 22, можна одержати як описано вище, використовуючи стандартні реакції утворення амідного зв'язку. Сполука формули 22 потім може взаємодіяти з захищеним вініламіном (наприклад, N-вінілфталімідом) в присутності придатного каталізатора (наприклад, ацетату паладію (II)) і фосфіну (наприклад, трифенілфосфіну, три-орто-толілфосфіну), в присутності основи (наприклад, N,N-діізопропілетиламіну), в розчиннику (наприклад, N,N-диметилформаміді, ацетонітрилі) при температурі в діапазоні 20°С 120°С і протягом від 1 до 48 годин. Алкен формули 23 потім може бути відновлений з одержанням алкану формули 24, використовуючи стандартні умови гідрування і стандартну методику для видалення захисної фталімідної групи. Амін формули 25 може взаємодіяти з бромідом формули 6, з де один з R3 - R6 є ОН, а інші є воднем. Переважно, Q1 є групою *-NH-Q2-A, в якій А є групою в якій R3, R4, R5, R6 і R7 є однаковими або різними і вибраними з водню, С1-С4 алкілу, OR9, SR9, SOR9, SO2R9, гало, CN, CO2R9, CF3, OCF3, SO2NR9R10, CONR9R10, NR9R10, NHCOR10 і фенілу необов'язково заміщеного від 1 до 3 групами вибраними з OR9, гало і С1-С4 алкілу, за умови, що 21 принаймні 2 з R3 - R7 означають водень; в якій R9 і R10 є однаковими або різними і вибраними з водню або С1-С4 алкілу. Більш переважно, Q1 є групою *NH-Q2-A, в якій А є групою в якій R3, R4, R5, R6 і R7 є однаковими або різними і вибраними з водню, ОН, СН3, ОСН3, OCF3, OCH2-CH3, SCH3, N(CH3)2, N(C=O)CH3, C(=O)NH2, COOCH3, SO2CH3, SO2NH2, гало, CN, CF3 і фенілу необов'язково заміщеного ОН, за умови, що принаймні 2 з R3 - R7 означають водень. В переважному втіленні, А є групою, в якій один з R3 - R7 є ОН або фенілом заміщеним ОН. В переважному втіленні, А є групою, в якій один з R3 - R7 є ОН або фенілом заміщеним ОН, а інші вибирають з водню, СІ або СН3, за умови, що принаймні 2 з R3 - R7 означають водень. Переважно А є нафтилом необов'язково заміщеним ОН. Переважно, А є нафтилом заміщеним ОН. В описаних вище групах сполук, особлива перевага надається наступним замісникам: Q2 є -СН2-, -(СН2)2-, -(СН2)3-, -СН2-С(СН3)2- або -С(СН3)2-, переважно -СН2- або - (СН2)2. R1 є воднем або С1-С4 алкілом і R2 є С1-С4 алкілом. Більш переважно, R1 є воднем або СН3 і R2 є воднем або СН3 n дорівнює 0 або 1. R1 є воднем і R2 є СН3 і n дорівнює 0 або 1. R1 є СН3, R2 є СН3 і n дорівнює 0 або 1. Особливо переважними є сполуки формули (1), які описані далі в розділі Приклади, тобто: N-Бензил-2-(3-{2-[(2R)-2-(3-форміламіно-4гідроксифеніл)-2-гідроксиетиламіно]-2метилпропіл}феніл)ацетамід; N-(3,4-Диметилбензил)-2-(3-{2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}феніл)ацетамід; N-[2-(4-Хлорфеніл)етил]-3-{2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}бензамід; N-[2-(2-Хлорфеніл)етил]-3-{2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}бензамід; 86615 22 3-{2-[(2R)-2-(3-Форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}-N-(2-нафтален1-ілетил)бензамід; 3-{2-[(2R)-2-(3-Форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}-N-[2-(4метилфеніл)етил]бензамід; N-[2-(2,6-Димeтилфeнiл)eтил]-3-{2-[(2R)-2-(3фopмiлaмiнo-4-гiдpoкcифeнiл)-2гідроксиетиламіно]-2-метилпропіл}бензамід; N-[2-(2,3-Диметилфеніл)етил]-3-{2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропілбензамід; 3-{2-[(2R)-2-(3-фopмiлaмiнo-4-гiдpoкcифeнiл)2-гiдpoкcиeтилaмiнo]-2-мeтилпpoпiл}-N-[2-(4гідрокси-2,3-диметилфеніл)етил]бензамід; 3-{2-[(2R)-2-(3-Фopмiлaмiнo-4-riдpoкcифeнiл)-2гiдpoкcиeтилaмiнo]-2-мeтилпpoпiл}-N-[2-(4метоксифеніл)етил]бензамід; 3-{2-[(2R)-2-(3-Фopмiлaмiнo-4-гiдpoкcифeнiл)-2гiдpoкcиeтилaмiнo]-2-мeтилпpoпiл}-Nфенетилбензамід; N-Циклoгeкcилмeтил-3-{2-[(2R)-2-(3фopмiлaмiнo-4-гiдpoкcифeнiл)-2гідроксиетиламіно]-2-метилпропіл}бензамід; N-[5-((1R)-2-{1,1-Диметил-2-[3-(піперидин-1карбоніл)феніл]етиламіно}-1-гідроксиетил)-2гідроксифеніл]формамід; 3-{2-[(2R)-2-(3-Форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}-N-[2-(3трифторметилфеніл)етил]бензамід; 3-{2-[(2R)-2-(3-Форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}-N-(3фенілпропіл)бензамід; 3-{2-[(2R)-2-(3-Форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}-N-індан-2ілбензамід; 3-{2-[(2R)-2-(3-Форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}-N-(2-піридин-2ілетил)бензамід; 3-{2-[(2R)-2-(3-Форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}-N-[2-(4сульфамоїлфеніл)етил]бензамід; N-(4-Диметиламінобензил)-2-(3-{(2R)-2-[(2R)-2(3-форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]пропіл}феніл)ацетамід; N-[5-(2-{(1R)-2-[3-(3,4-Дигідро-1Н-ізохінолін-2карбоніл)феніл]-1,1-диметилетиламіно}-1гідроксиетил)-2-гідроксифеніл]формамід; 3-{2-[(2R)-2-(3-Форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}-N-(4'гідроксибіфеніл-3-ілметил)бензамід; 3-{2-[(2R)-2-(3-Форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}-N-[2-(4гідрокси-2,5-диметилфеніл)етил]бензамід; 3-{2-[(2R)-2-(3-Форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}-N-[2-(4гідрокси-3-метилфеніл)етил]бензамід; N-(4-Ацетиламінобензил)-2-(3-{(2R)-2-[(2R)-2(3-форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]пропіл}феніл)ацетамід; 4-{[2-(3-{(2R)-2-[(2R)-2-(3-Форміламіно-4гідроксифеніл)-2гідроксиетиламіно]пропіл}феніл)ацетиламіно]метил}бензамід; 23 N-Адамантан-1-іл-3-{2-[(2R)-2-(3-форміламіно4-гідроксифеніл)-2-гідроксиетиламіно]-2метилпропіл}бензамід; 3-{2-[(2R)-2-(3-Форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}-N-(2гідроксинафтален-1-ілметил)бензамід; 3-{2-[(2R)-2-(3-Форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}-N-(4-гідрокси3,5-диметилбензил)бензамід; 3-{2-[(2R)-2-(3-Форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}-N-(6гідроксинафтален-2-ілметил)бензамід; N-(3,6-Дихлор-2-гідроксибензил)-3-{2-[(2R)-2(3-форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}бензамід; N-(3,4-Диметилбензил)-2-(3-{2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]етил}феніл)ацетамід; 3-{2-[(2R)-2-(3-Форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}-N-[2-(4гідроксифеніл)-2-метилпропіл]бензамід; 3-{2-[(2R)-2-(3-Форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}-N-(4'гідроксибіфеніл-4-ілметил)бензамід; N-Адамантан-1-іл-2-(3-{(2R)-2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]пропіл}феніл)ацетамід; N-[5-(2-{2-[3-(10Азатрицикло[6.3.1.0*2,7*]додека-2(7),3,5-триєн-10карбоніл)феніл]-1,1-диметилетиламіно}-1гідроксиетил)-2-гідроксифеніл]формамід; 2-(3-(2R)-2-[(2R)-2-(3-Форміламіно-4гідроксифеніл)-2-гідроксиетиламіно]пропіл}феніл)N-(4'-гідроксибіфеніл-3-ілметил)ацетамід; Метиловий естер 4-{[2-(3-{2-[(2R)-2-(3Форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2метилпропіл}феніл)ацетиламіно]метил}бензойної кислоти; 2-(3-{(2R)-2-[(2R)-2-(3-Форміламіно-4гідроксифеніл)-2-гідроксиетиламіно]-2метилпропіл}феніл)-N-(4трифторметоксибензил)ацетамід; N-(2-Хлор-4-гідроксибензил)-N-етил-2-(3-{(2R)2-[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}феніл)ацетамід; N-(2-Хлор-4-гідроксибензил)-2-(3-{(2R)-2-[(2R)2-(3-форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}феніл)ацетамід; 2-(3-{(2R)-2-[(2R)-2-(3-Форміламіно-4гідроксифеніл)-2-гідроксиетиламіно]пропіл}феніл)N-(4-гідрокси-3,5-диметилбензил)ацетамід; 2-(3-{(2R)-2-[(2R)-2-(3-Форміламіно-4гідроксифеніл)-2-гідроксиетиламіно]пропіл}феніл)N-(2-гідроксинафтален-1-ілметил)ацетамід; N-(5-Хлор-2-гідроксибензил)-2-(3-{(2R)-2-[(2R)2-(3-форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]пропіл}феніл)ацетамід; N-(3,5-Дихлор-2-гідроксибензил)-2-(3-{(2R)-2[(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]пропіл}феніл)ацетамід; 2-(3-{(2R)-2-[(2R)-2-(3-Форміламіно-4гідроксифеніл)-2-гідроксиетиламіно]пропіл}феніл)N-(6-гідроксинафтален-2-ілметил)ацетамід; 86615 24 2-(3-{(2R)-2-[(2R)-2-(3-Форміламіно-4гідроксифеніл)-2-гідроксиетиламіно]пропіл}феніл)N-(4'-гідроксибіфеніл-4-ілметил)ацетамід; N-(4-Ціанобензил)-2-(3-{2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}феніл)ацетамід; 2-(3-{2-[(2R)-2-(3-Форміламіно-4гідроксифеніл)-2-гідроксиетиламіно]-2метилпропіл}феніл)-N-(4метансульфонілбензил)ацетамід; 2-(3-{2-[(2R)-2-(3-Форміламіно-4гідроксифеніл)-2-гідроксиетиламіно]-2метилпропіл}феніл)-N-(4метилсульфанілбензил)ацетамід; 2-(3-{2-[(2R)-2-(3-Форміламіно-4гідроксифеніл)-2-гідроксиетиламіно]-2метилпропіл}феніл)-N-(4трифторметилбензил)ацетамід; 2-(3-{2-[(2R)-2-(3-Форміламіно-4гідроксифеніл)-2-гідроксиетиламіно]-2метилпропіл}феніл)-N-(4'-гідроксибіфеніл-4ілметил)ацетамід; N-[2-(5-Хлор-2-гідроксифеніл)етил]-3-{2-[(2R)2-(3-форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}бензамід; 2-(3-{2-[(2R)-2-(3-Форміламіно-4гідроксифеніл)-2-гідроксиетиламіно]-2метилпропіл}феніл)-N-(4'-гідроксибіфеніл-3ілметил)ацетамід; 3-{2-[(2R)-2-(3-Форміламіно-4-гідроксифенілі)2-гідроксиетиламіно]пропіл}-N-[2-(4гідроксифеніл)-2-метилпропіл]бензамід; N-(2-Хлор-4-гідроксибензил)-2-(3-{(2R)-2-[(2R)(2R)-2-(3-форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]пропіл}феніл)ацетамід; N-[2-(5-Хлор-2-гідроксифеніл)етил]-3-{2-[(2R)2-(3-форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}бензамід; 3-{2-[(2R)-2-(3-Форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]пропіл}-N-[2-(4-гідроксифеніл)2-метилпропіл]бензамід; 2-(3-{2-[(2R)-2-(3-Форміламіно-4гідроксифеніл)-2-гідроксиетиламіно]-2метилпропіл}феніл)-N-(тетрагідротіопіран-4іл)ацетамід; N-(5-Хлор-2-гідроксибензил)-2-(3-{2-[(2R)-2-(3форміламіно-4-гідроксифеніл)-2гідроксиетиламіно]-2-метилпропіл}феніл)ацетамід; і, N-{5-[(1R)-2-((1R)-2-{3-[3-(3,4-Дигідро-1Hізохінолін-2-іл)-3-оксопропіл]феніл}-1метилетиламіно)-1-гідроксиетил]-2гідроксифеніл}формамід. Згідно з одним з аспектів представленого винаходу, сполуки формули (1), в яких (CH2)nC(=O)Q1 група розташована в мета-положенні, є особливо переважними. Фармацевтично прийнятні солі сполук формули (1) включають їх кислотно-адитивні і основні солі. Придатні кислотно-адитивні солі утворюються з кислот, які утворюють нетоксичні солі. Приклади солей включають ацетат, адипат, аспартат, бензоат, безилат, бікарбонат/карбонат, бісульфат/сульфат, борат, камсилат, цитрат, цикламат, 25 едизилат, езилат, форміат, фумарат, глуцептат, глюконат, глюкуронат, гексафторфосфат, гібензат, гідрохлорид/хлорид, гідробромід/бромід, гідройодид/йодид, гідрофосфат, ізетіонат, D- і L-лактат, малат, малеат, малонат, мезилат, метилсульфат, 2-напсилат, нікотинат, нітрат, оротат, оксалат, пальмітат, памоат, фосфат/гідрофосфат/дигідрофосфат, піроглутамат, сахарат, стеарат, сукцинат, танат, D- і L-тартрат, 1-гідрокси-2-нафтоат, тозилат і ксинафоат. Придатні основні солі одержують з основ, які утворюють нетоксичні солі. Приклади включають солі алюмінію, аргініну, бензатину, кальцію, холіну, діетиламіну, діоламіну, гліцину, лізину, магнію, меглуміну, оламіну, калію, натрію, трометаміну і цинку. Також можуть бути одержані гемісолі кислот і основ, наприклад, гемісульфатні і гемікальцієві солі. Для ознайомлення з придатними солями, дивіться, "Handbook of Pharmaceutical Salts: Properties, Selection, and Use " by Stahl і Wermuth (Wiley-VCH, Weinheim, Germany, 2002). Фармацевтично прийнятні солі сполук формули (1) можна одержати за допомогою одного або декількох з трьох способів: (і) за допомогою взаємодії сполуки формули (1) з бажаною кислотою або основою; (іі) шляхом видалення кислото- або основонестійкої захисної групи з придатного попередника сполуки формули (1) або шляхом розмикання циклу придатного циклічного попередника, наприклад, лактону або лактаму, використовуючи бажану кислоту або основу; або (ііі) шляхом перетворення однієї солі сполуки формули (1) в іншу за допомогою реакції з прийнятною кислотою або основою, або використовуючи придатну іонообмінну колонку. Всі три реакції типово проводять в розчині. Одержана сіль може випасти в осад і може бути зібрана фільтруванням або може бути відновлена шляхом випаровування розчинника. Ступінь іонізації одержаної солі може змінюватись від повністю іонізованої до майже неіонізованої. Сполуки винаходу можуть існувати у несольватованій і сольватованій формах. Термін 'сольват' використовується тут для опису молекулярних комплексів, що містять сполуку винаходу і стехіометричну кількість однієї або декількох фармацевтично прийнятних молекул розчинника, наприклад, етанолу. Термін 'гідрат' використовується, коли згаданий розчинник є водою. Включеними в межі винаходу є комплекси, такі як клатрати, комплекси включення лікарський засіб-хазяїн, в яких, на противагу згаданим вище сольватам, лікарський засіб і хазяїн присутні в стехіометричній або нестехіометричній кількості. Також включеними є комплекси лікарського засобу, що містять два або більше органічних і/або неорганічних компонентів, які можуть бути в стехіометричній або нестехіометричній кількостях. Одержані комплекси можуть бути іонізованими, частково іонізованими або неіонізованими. Огляд таких комплексів наводиться в J Pharm Sci, 64 (8), 1269-1288 by Haleblian (August 1975). 86615 26 Тут і надалі всі посилання на сполуки формули (1) включають посилання на їх солі, сольвати і комплекси і сольвати і комплекси їх солей. Сполуки винаходу включають сполуки формули (1), як тут визначено вище, включаючи всі їх поліморфи і кристали, їх пролікарські форми і ізомери (включаючи оптичні, геометричні і таутомерні ізомери), як тут визначено, і мічені ізотопами сполуки формули (1). Як вказується, так звані 'проліки' сполук формули (1) також включаються в межі винаходу. Таким чином, деякі похідні сполук формули (1), які можуть мати малу або не мати зовсім фармакологічної активності можуть, коли вводяться в організм або на тіло, перетворюватися в сполуки формули (1), що мають бажану активність, наприклад, шляхом гідролітичного розщеплення. Такі похідні відносяться до 'проліків'. Додаткову інформацію по використанню проліків можна знайти в 'Pro-drugs as Novel Delivery Systems, Vol. 14, ACS Symposium Series (T. Higuchi and W. Stella) і 'Bioreversible Carriers в Drug Design', Pergamon Press, 1987 (ed. E. В Roche, American Pharmaceutical Association). Проліки у відповідності з винаходом можуть, наприклад, бути одержані шляхом заміни прийнятних функціональних груп, присутніх в сполуці формули (1), деякими замісниками відомими фахівцям в цій галузі як 'про-замісники' як описується, наприклад, в "Design of Prodrugs" by H. Bundgaard (Elsevier, 1985). Деякими прикладами проліків у відповідності з винаходом є: (і) коли сполука формули (1) містить карбоксильну групу (-СООН), її естер, наприклад, сполука, в якій водень карбонової кислоти сполуки формули (1) замінений (С1-С8)алкілом; (іі) коли сполука формули (1) містить спиртову групу (-ОН), її етер, наприклад, сполука, в якій водень спиртової групи сполуки формули (1) замінений (С1-С6)алканоїлоксиметилом; і (ііі) коли сполука формули (1) містить первинну або вторинну аміногрупу (-NH2 або -NHR, де R¹Н), її амід, наприклад, сполука, в якій, в залежності від обставин, одна або обидві водні аміногрупи сполуки формули (1) є заміненою(и) (С1С10)алканоїлом. Інші приклади заміщувальних груп у відповідності із згаданими вище прикладами і прикладами інших типів проліків можна знайти в наведених вище посиланнях. Однак, деякі сполуки формули (1) можуть самі по собі виступати як проліки інших сполук формули (1). Також включені в межі винаходу метаболіти сполук формули (1), що є сполуками, які утворюються in vivo після введення лікарського засобу. Деякими прикладами метаболітів згідно з винаходом є: (і) коли сполука формули (1) містить метильну групу, її гідроксиметильне похідне (-СН3®-СН2ОН): (іі) коли сполука формули (1) містить алкоксигрупу, її гідроксипохідне (-OR®-ОН); (ііі) коли сполука формули (1) містить третинну аміногрупу, її вторинний амін (-NR1R2®-NHR1 або NHR2); 27 (iv) коли сполука формули (1) містить вторинну аміногрупу, її первинне похідне (-NHR1®-NH2); (v) коли сполука формули (1) містить фенільний замісник, її фенольне похідне (-Ph®-PhOH); і (vi) коли сполука формули (1) містить амідну групу, похідне карбонової кислоти (CONH2®СООН). Сполуки формули (1), що містять один або декілька асиметричних атомів вуглецю можуть існувати як два або більше стереоізомерів. Коли сполука формули (1) містить алкенільну або алкеніленову групу, можлива геометрична цис/транс (або Z/E) ізомерія. Коли структурний ізомеризм є взаємозмінюваним завдяки низькій енергії бар'єру, може мати місце таутомерний ізомеризм ("таутомеризм"). Це може мати місце у формі протонової таутомерії в сполуках формули (1), що містять, наприклад, іміно, кето або оксимні групи, або так званий валентний таутомеризм в сполуках, які містять ароматичний замісник. Звідси випливає, що одна сполука може проявляти більше ніж один тип ізомеризму. Включеними в межі представленого винаходу є всі стереоізомери, геометричні ізомери і таутомерні форми сполук формули (1), включаючи сполуки, що проявляють більше ніж один тип ізомеризму і суміші одного або декількох. Також включеними є кислотноадитивні солі або основні солі, в яких протиіон є оптично-активним, наприклад, d-лактат або І-лізин, або рацемічним, наприклад, dl-тартрат або dl-аргінін. Цис/транс ізомери можуть бути розділені за допомогою загальновідомих методик добре відомих фахівцю в цій галузі, наприклад, хроматографії і фракційної кристалізації. Загальновідомі методики для одержання/виділення окремих енантіомерів включають хіральний синтез з придатного оптично чистого попередника або розділення рацемату (або рацемату солі або похідного) використовуючи, наприклад, хіральну високоефективну рідинну хроматографію (ВЕРХ). Альтернативно, рацемат (або рацемічний попередник) може реагувати з придатною оптичноактивною сполукою, наприклад, спиртом, або, у випадку, коли сполука формули (1) містить кислотний або основний замісник, кислотою або основою, такою як винна кислота або 1-фенілетиламін. Одержану діастереомерну суміш можна розділити використовуючи хроматографію і/або фракційну кристалізацію і один або обидва діастереоізомери перетворюють у відповідний чистий енантіомер(и) способами добре відомими фахівцю в цій галузі. Хіральні сполуки винаходу (і їх хіральні попередники) можна одержати в енантіомернозбагаченій формі, використовуючи хроматографію, типово ВЕРХ, на асиметричній смолі з рухомою фазою, що містить вуглеводень, типово гептан або гексан, що містить від 0 до 50% об'ємних ізопропанолу, типово від 2% до 20% і від 0 до 5% об'ємних алкіламіну, типово 0,1% діетиламіну. Концентрування елюенту дає збагачену суміш. Стереізомерні конгломерати можна розділити за допомогою звичайних методик відомих фахівцю в цій галузі, дивіться, наприклад, "Stereochemistry 86615 28 of Organic Compounds" by E. L. Eliel (Wiley, New York, 1994). Згідно з аспектом представленого винаходу, особливо переважним є (R,R)-стереоізомер формули наведеної нижче, в якій R1 є воднем і R2 є C1C4 алкілом, переважно метилом, а n і Q1 є такими як визначено вище: Представлений винахід включає всі фармацевтично прийнятні мічені ізотопами сполуки формули (1), в яких один або декілька атомів замінені атомами, що мають те ж саме атомне число, але атомну масу або масове число, що відрізняється від атомної маси або масового числа, які домінують в природі. Прикладами ізотопів для включення в сполуки винаходу є ізотопи водню, такі як 2Н і 3Н, вуглецю, такі як 11С, 13С і 14С, хлору, такі як 36СІ, фтору, такі як 18F, йоду, такі як 123І і 125І, азоту, такі як 13N і 15N, кисню, такі як 15O,17О і 18О, фосфору, такі як 32Р і сірки, такі як 35S. Деякі мічені ізотопами сполуки формули (1), наприклад, ті, що включають радіоактивний ізотоп, є корисними в дослідженнях лікарського засобу і/або розподілення субстрату в тканині. Радіоактивні ізотопи трітію, тобто 3Н, і вуглецю-14, тобто 14 С, є особливо корисними для цих цілей з огляду на легкість їх включення і легкість виявлення. Заміщення більш важкими ізотопами, такими як дейтерій, тобто 2Н, може давати деякі терапевтичні переваги внаслідок збільшення метаболітичної стабільності, наприклад, збільшення in vivo часу напіврозкладу або зменшення необхідної дози, і звідси може бути переважним в деяких випадках. Заміщення позитрон емітуючими ізотопами, такими як 11С, 18F, 15O і 13N, може бути корисним в дослідженнях позитронноемісійної топографії (PET) для визначення блокування рецептора субстратом. Мічені ізотопами сполуки формули (1) загалом можна одержати за допомогою звичайних методик відомих фахівцю в цій галузі або за допомогою процесів аналогічних тим, що описуються в супровідних Прикладах і Препаративних прикладах, використовуючи прийнятні мічені ізотопами реагенти, замість не мічених реагентів використовуваних раніше. Фармацевтично прийнятними сольватами у відповідності з винаходом є такі, в яких кристалізаційний розчинник може бути ізотопічно заміщеним, наприклад, D2O, d6-ацетон, d6-ДМСО. Сполуки формули (1), їх фармацевтично прийнятні солі і/або похідні є цінними фармацевтично активними сполуками, які є придатними для лікування і профілактики ряду розладів, в які залучений b2 рецептор або в яких агонізм цього рецептора може давати користь, зокрема, алергічних і 29 неалергічних захворювань дихальних шляхів, але також для лікування інших захворювань, таких як, але не обмежуючись ними, захворювання нервової системи, передчасні пологи, застійна серцева недостатність, депресія, запалення і алергічні захворювання шкіри, псоріаз, проліферативні захворювання шкіри, глаукома і при станах, при яких необхідне зменшення шлункової кислотності, особливо при виразці шлунку і дванадцятипалої кишки. Сполуки винаходу призначені для фармацевтичного застосування можуть бути введені як кристалічні або аморфні продукти. Вони можуть бути одержані, наприклад, як тверді речовини, порошки або плівки за допомогою способів, таких як осадження, кристалізація, сублімація, висушуванням розпиленням або випарюванням. Для цих цілей може використовуватися висушування з використанням мікрохвильового або радіовипромінювання. Вони можуть бути введені окремо або в комбінації з однією або більше сполуками винаходу або в комбінації з одним або декількома іншими лікарськими засобами (або у вигляді будь-якої їх комбінації). Загалом, вони будуть вводитись як рецептури у поєднанні з одним або більшою кількістю фармацевтично прийнятних ексціпієнтів. Термін "ексціпієнт" використовується тут для опису будьякого інгредієнта іншого ніж сполука(и) винаходу. Вибір ексціпієнта буде у великій мірі залежати від ряду факторів, таких як вибраний шлях введення, вплив ексціпієнта на розчинність і стабільність і природа дозованої форми. Фармацевтичні композиції придатні для вивільнення сполук представленого винаходу і способи їх одержання очевидні фахівцю в цій галузі. Такі композиції і способи їх одержання можна знайти, наприклад, в 'Remington's Pharmaceutical Sciences', 19th Edition (Mack Publishing Company, 1995). Сполуки, згідно з винаходом, можуть вводитися пероральним шляхом. Пероральне введення може включати ковтання, внаслідок чого сполука потрапляє в шлунково-кишковий тракт, або може застосовуватися букальнеабо сублінгвальне введення для того, щоб сполука потрапляла в кров безпосередньо з рота. Рецептури, придатні для перорального введення, включають тверді композиції, такі як таблетки, капсули, що містять частинки, рідини або порошки, лозенге (включаючи рідинно-наповнені), гумки, мульти- та наночастинки, гелі, тверді розчини, ліпосоми, плівки, овули, спреї і рідкі рецептури. Рідкі композиції включають суспензії, розчини, сиропи та еліксири. Такі композиції можуть застосовуватися як наповнювачі в м'яких або твердих капсулах і зазвичай містять носій, наприклад, воду, етанол, поліетиленгліколь, пропіленгліколь, метилцелюлозу або придатне масло, та один або декілька емульгаторів та/або суспенгаторів. Рідкі композиції можуть також одержуватися розведенням твердого складу, наприклад, з пакетику. Сполуки винаходу також можуть бути використані у швидкорозчинних, швидко-дезінтегруючих дозованих формах, таких як ті, що описані в Liang 86615 30 та Chen в Expert Opinion в Therapeutic Patents, 11 (6), 981-986, (2001). В таблетованих дозованих формах, в залежності від дози, лікарський засіб може складати від 1мас % до 80мас % дозованої форми, більш типово від 5мас % до 60мас % дозованої форми. На додаток до лікарського засобу, таблетки зазвичай містять дезінтегратор. Прикладами дезінтеграторів є крохмальгліколят натрію, натрій карбоксиметилцелюлоза, кальцій карбоксиметилцелюлоза, натрій кроскармелоза, кросповідон, полівінілпіролідон, метилцелюлоза, мікрокристалічна целюлоза, нижча алкіл-заміщена гідроксипропілцелюлоза, крохмаль, прежелатинізований крохмаль і алгінат натрію. Зазвичай, дезінтегратор буде складати від 1мас % до 25мас %, переважно від 5мас % до 20мас % дозованої форми. Зв'язувальні агенти зазвичай використовуються для склеювання в єдине ціле таблетованої рецептури. Придатними зв'язувальними агентами є мікрокристалічна целюлоза, желатин, цукри, поліетиленгліколь, природні і синтетичні смоли, полівінілпіролідон, прежелатинізований крохмаль, гідроксипропілцелюлоза і гідроксипропілметилцелюлоза. Таблетки також можуть містити розріджувачі, такі як лактоза (моногідрат, висушений розпилюванням моногідрат, безводна і їм подібні), маніт, ксиліт, декстроза, цукроза, сорбіт, мікрокристалічна целюлоза, крохмаль і дигідрат диосновного фосфату кальцію. Таблетки також можуть, необов'язково, містити поверхнево-активні агенти, такі як лаурилсульфат і полісорбат 80 і агенти, що підвищують ковзання, такі як діоксид кремнію і тальк. Коли присутні, поверхнево-активні агенти можуть складати від 0,2мас % до 5мас % таблетки, і агенти, що підвищують ковзання, можуть складати від 0,2мас % до 1мас % таблетки. Таблетки також зазвичай місять змащувальні агенти, такі як стеарат магнію, стеарат кальцію, стеарат цинку, стеаридфумарат натрію і суміші стеарату магнію з лаурилсульфатом натрію. Змащувальні агенти загалом складають від 0,25мас % до 10мас %, переважно від 0,5мас % до 3мас % таблетки. Іншими можливими інгредієнтами є антиоксиданти, барвники, ароматизатори, консерванти і агенти, що корегують смак фармацевтичних агентів. Типові таблетки містять приблизно до 80% лікарського засобу, від приблизно 10мас % до приблизно 90мас % зв'язувального агента, від приблизно 0мас % до приблизно 85мас % розріджувача, від приблизно 2мас % до приблизно 10мас % дезінтегратора і від приблизно 0,25мас % до приблизно 10мас % змащувального агента. Таблеткові суміші можна спресувати безпосередньо або за допомогою валу у формі таблеток. Таблеткову суміш або частини сумішей можна альтернативно перед таблетуванням піддати вологому-, сухому-гранулюванню або гранулюванню розплаву, заморожуванню розплаву або екструдуванню. Кінцева рецептура може містити один або декілька шарів і може бути покритою або непокритою; вона може бути навіть інкапсульованою. 31 Рецептури таблеток обговорюються в Pharmaceutical Dosage Forms: Tablets, Vol. 1, by H. Lieberman and L. Lachman (Marcel Dekker, New York, 1980). Використовуваними пероральними плівками для людей або ветеринарії є пластичні водорозчинні або здатні до набухання від води тонкоплівкові дозовані форми, які можуть швидко розчинятись або поглинатись слизовою оболонкою і типово містять сполуку формули (1), плівкоутворюючий полімер, зв'язувальний агент, розчинник, зволожувач, пластифікатор, стабілізатор або емульсифікатор, агент, що модифікує в'язкість і розчинник. Деякі компоненти рецептури можуть виконувати більше ніж одну функцію. Сполуки формули (1) можуть бути водорозчинними або нерозчинними. Водорозчина сполука типово містить від 1мас % до 80мас %, більш типово від 20мас % до 50мас %, розчиненої речовини. Менш розчинні сполуки можуть складати більшу частину композиції, типово до 88мас % розчиненої речовини. Альтернативно, сполука формули (1) може бути у формі дрібних частинок. Плікоутворюючий полімер може бути вибраний з природних полісахаридів, протеїнів або синтетичних гідроколоїдів і типово присутній в інтервалі від 0,01 до 99мас %, більш типово в інтервалі від 30 до 80 мас %. Іншими інгредієнтами є антиоксиданти, барвники, ароматизатори і підсилювачі аромату, консерванти, агенти, що стимулюють виділення слини, хладогенти, співрозчинники (включаючи олії), пом'якшувачі, наповнювачі, протиспінювачі, поверхнево-активні речовини і агенти, що коригують смак фармацевтичних агентів. Плівки у відповідності з винаходом типово одержують шляхом сушіння випарюванням тонких водних плівок на носії, з якого вона легко відшаровується або папері. Це можна здійснити у сушильній шафі або тунелі, типово у комбінованій сушарці для сушки покриттів або шляхом сушіння виморожуванням або вакуумуванням. Тверді рецептури для перорального введення можна сформувати для негайного і/або модифікованого вивільнення. Рецептури модифікованого вивільнення мають відстрочене-, тривале-, пульсуюче-, контрольоване-, цільове і програмоване вивільнення. Придатні рецептури з модифікованим вивільненням для цілей винаходу описані в патенті США 6,106,864. Деталі інших придатних методик вивільнення, таких як високоенергійні дисперсії і осмотичні частинки і частинки з покриттям можна знайти в Pharmaceutical Technology On-line, 25(2), 1-14, by Verma і інші (2001). Використання жувальних гумок для досягнення контрольованого вивільнення описані в WO 00/35298. Сполуки винаходу також можна вводити безпосередньо в потік крові, в м'яз або у внутрішній орган. Придатними шляхами для парентерального введення є внутрішньовенне, внутрішньоартеріальне, внутрішньочеревинне, інтратекальне, інтравентрикулярне, інтрауретральне, інтрастернальне, інтракраніальне, внутрішньом'язове і підшкірне. Придатними пристроями для парентерального 86615 32 введення є голкові (включаючи мікроголки) ін'єктори, безголкові ін'єктори і засоби вливання. Парентеральні рецептури типово є водними розчинами, які можуть містити ексціпієнти, такі як солі, карбогідрати і буферуючі агенти (переважно до рН від 3 до 9), але, для деяких застосувань, вони можуть бути більш придатносформовані як стерильний неводний розчин або як суха форма, що використовується у поєднанні з придатним розчинником, таким як стерильна пірогенвільна вода. Одержання парентеральних рецептур в стерильних умовах, наприклад, шляхом ліофілізації, можна легко здійснити, використовуючи стандартні фармацевтичні методики, добре відомі фахівцю в цій галузі. Розчинність сполук формули (1), що використовується при одержанні парентеральних розчинів, може бути збільшена шляхом використання прийнятних методик формування рецептур, таких як включення агентів, що збільшують розчинність. Рецептури для парентерального введення можуть бути сформовані для негайного і/або модифікованого вивільнення. Рецептури модифікованого вивільнення мають відстрочене-, тривале-, пульсуюче-, контрольоване-, цільове і програмоване вивільнення. Таким чином, сполуки винаходу можуть бути сформовані як тверда, напівтверда або тиксотропна рідина для введення у вигляді імплантованого депо, для забезпечення модифікованого вивільнення активної сполуки. Прикладами таких рецептур є покриті лікарським засобом стенти і мікросфери з полі(dІ-молочнаспівгліколева)кислоти (PGLA). Сполуки винаходу також можуть бути нанесені на шкіру або слизову оболонку, тобто дермально або трансдермально. Типовими рецептурами для цих цілей є гелі, гідрогелі, лосьйони, розчини, креми, мазі, порошки для обтрушування, пов'язки, піни, плівки, пластири, пластинки, імплантати, губки, волокна, бандажі і мікроемульсії. Також можуть бути використані ліпосоми. Типовими носіями є спирт, вода, мінеральне масло, рідкий вазелин, білий вазелин, гліцерин, поліетиленгліколь і пропіленгліколь. Можуть бути включені покращувачі проникнення - дивіться, наприклад, J Pharm Sci, 88 (10), 955-958 by Finnin and Morgan (October 1999). Іншими засобами місцевого введення є доставка за допомогою електропорації, фонтофорез, фонофорез, сонофорез і мікроголкова або безголкова методика (наприклад, Powderject™, Bioject™ і т. д.) ін'єктування. Рецептури для місцевого введення можуть бути сформовані для негайного і/або модифікованого вивільнення. Рецептури модифікованого вивільнення мають відстрочене-, тривале-, пульсуюче-, контрольоване-, цільове і програмоване вивільнення. Сполуки винаходу також можуть бути введені інтраназально або за допомогою інгаляції, типово у формі сухого порошку (або окремо, або як суміш, наприклад, суха суміш з лактозою, або як змішані частинки компонентів, наприклад, суміші з фосфоліпідами, такими як фосфатідилхолін) з інгалятору сухого порошку або як аерозоль з контейнеру під 33 тиском, насосу, спрею, пульверизатору (переважно використовують електродинамічний пульверизатор для одержання тонкого туману) або розпилювача, з або без використання придатного пропеланту, такого як 1,1,1,2-тетрафторетан або 1,1,1,2,3,3,3-гептафторпропан. Для інтраназального використання, порошок може містити біоадгезивні агенти, наприклад, цитозан або циклодекстрин. Контейнер під тиском, насос, спрей, пульверизатор або розпилювач містить розчин або суспензію сполук(и) винаходу, що включає, наприклад, етанол, водний етанол, або придатний альтернативний агент для диспергування, солюбілізування або розтягування вивільнення активної речовини, пропелант(и) як розчинник і, необов'язково, поверхнево-активну речовину, таку як триолеат сорбіту, олеїнову кислоту або олігомолочну кислоту. Перед використанням сухого порошку або суспензії, лікарський продукт мікронізують до розміру придатного для вивільнення шляхом інгаляції (типово, менше ніж 5 мікрон). Це можна досягти будь-яким прийнятним способом подрібнення, таким як з використанням спірального струминногомлина, струминногомлина з псевдо-зрідженим шаром, сусперкритичною рідинною обробкою для одержання наночастинок, гомогенізацією при високому тиску або висушуванням розпиленням. Капсули (виготовлені, наприклад, з желатину або гідроксипропілметилцелюлози), блістери і катриджі для використання в інгаляторі або інсуфлаторі можуть бути сформовані таким чином, що містять порошкову суміш сполуки винаходу, придатної порошкової основи, такої як лактоза або крохмаль і модифікатор експлуатаційних якостей, такий як І-лейцин, маніт або стеарат магнію. Лактоза може бути безводною або у формі моногідрату, останній надається перевага, іншими придатними ексціпієнтами є декстран, глюкоза, мальтоза, сорбіт, ксиліт, фруктоза, цукроза і трегалоза. Придатний розчин для використання в пульверизаторі, що використовує електродинамічну силу для одержання тонкого туману, може містити від 1мкг до 20мг сполуки винаходу і випускний об'єм може змінюватись від 1мкл до 100мкл. Типово рецептура може містити сполуку формули (1), пропіленгліколь, стерильну воду, етанол і хлорид натрію. Альтернативними розчинниками, які можуть бути використані замість пропіленгліколю є гліцерин і поліетиленгліколь. В такі рецептури винаходу, що призначені для інгалювання/інтраназального введення можуть бути додані придатні ароматизатори, такі як ментол і левоментол, або підсолоджувані, такі як сахарин або сахарин натрію. Рецептури для інгалювання/інтраназального введення можуть бути сформовані для негайного і/або модифікованого вивільнення використовуючи, наприклад, PGLA. Рецептури модифікованого вивільнення мають відстрочене-, тривале-, пульсуюче-, контрольоване-, цільове і програмоване вивільнення. У випадку інгалятору сухого порошку і аерозолю, одиниця дозування визначається за допомогою клапану, який вивільнює виміряну кількість. Одиниці у відповідності з винаходом типово виго 86615 34 товляються для введення виміряної дози або "пшику", що містить від 0,001мг до 10мг сполуки формули (1). Загальна добова доза зазвичай знаходиться в інтервалі від 0,001мг до 40мг, яка може вводитись однією дозою або, що типовіше, як розподілені дози протягом дня. Сполуки формули (1) є особливо придатними для введення шляхом інгаляції. Сполуки згідно з винаходом можуть бути введені ректально або вагінально, наприклад, у формі супозиторію, песарію або клізми. Масло какао є традиційною супозиторійною основою, але можуть бути використані різні альтернативи, якщо прийнятно. Рецептури для ректального/інтравагінального введення можуть бути сформовані для негайного і/або модифікованого вивільнення. Рецептури модифікованого вивільнення мають відстрочене-, тривале-, пульсуюче-, контрольоване-, цільове і програмоване вивільнення. Сполуки згідно з винаходом також можуть бути введені безпосередньо в око або вухо, типово у формі крапель мікронізованої суспензії або розчину в ізотонічному, рН-коригованому, стерильному саліні. Інші рецептури придатні для окулярного або вушного введення включають мазі, здатні до біорозщеплення (наприклад, здатні до абсорбування гелеві губки, колаген) і нездатні до біорозщеплення (наприклад, силікон) імплантати, пластинки, лінзи і частинкові або везикулярні системи, такі як ніосоми або ліпосоми. Можуть бути включені полімери, такі як поперечнозшита поліакрилова кислота, полівініловий спирт, гіалуронова кислота, полімери целюлози, наприклад, гідроксипропілметилцелюлоза, гідроксиетилцелюлоза або метилцелюлоза, або гетерополісахаридний полімер, наприклад, геланова смола, разом з консервантом, таким як бензалконійхлорид. Такі рецептури можуть бути вивільнені за допомогою іонтофорезу. Рецептури для окулярного/вушного введення можуть бути сформовані для негайного і/або модифікованого вивільнення. Рецептури модифікованого вивільнення мають відстрочене-, тривале-, пульсуюче-, контрольоване-, цільове і програмоване вивільнення. Сполуки винаходу можуть бути об'єднані з розчинними макромолекулярними сполуками, такими як циклодекстрин і їх придатні похідні або поліетиленглікольвмісні полімери, для того щоб покращити їх розчинність, швидкість розчинення, замаскувати смак, біодоступність і/або стабільність для використання в будь-якому з вищезгаданих шляхів введення. Комплекси лікарський засіб-циклодекстрин, наприклад, знайшли застосування в більшості видів дозованих форм і шляхів введення. Можуть бути використані комплекси включення і невключения. Як альтернатива безпосередньому комплексуванню з лікарським засобом, циклодекстрин може бути використаний як допоміжна добавка, тобто, як носій, розріджувач або солюбілізатор. Найбільш часто для цих цілей використовується альфа-, бета- і гама-циклодекстрини, приклади яких можна знайти в міжнародних патентних заяв 35 ках з номерами публікацій WO 91/11172, WO 94/02518 і WO 98/55148. Оскільки може бути бажано ввести комбінацію активних сполук, наприклад, з ціллю лікування окремого захворювання або стану, в межах представленого винаходу, що дві або більше фармацевтичних композицій, принаймні, одна з яких містить сполуку у відповідності з винаходом, можуть легко бути об'єднані у формі набору придатного для спільного введення композицій. Таким чином, набір згідно з винаходом містить дві або більше окремі фармацевтичні композиції, принаймні, одна з яких містить сполуку формули (1) у відповідності з винаходом, і пристрої для окремого утримання згаданих композицій, такі як контейнер, окремі пляшочки або окремі пакетики з фольги. Прикладом такого набору є звичайна блістерна упаковка, що використовується для пакування таблеток, капсул і їм подібних. Набір винаходу є особливо придатним для введення різних дозованих форм, наприклад, парентерально, для введення окремих композицій з різними інтервалами дозування, або для титрування окремих композицій одна до одної. Для сприяння відповідності, набір типово містить інструкції по введенню і може бути забезпечений так званою пам'яткою. Для введення людям, загальна добова доза сполуки винаходу типово знаходиться в інтервалі від 0,001мг до 5000мг, що звичайно залежить від шляху введення. Наприклад, внутрішньовенна добова доза може потребувати тільки від 0,001мг до 40мг. Загальна добова доза може бути введена за один раз або розподілена на декілька доз і може, на розсуд лікаря, не знаходитись у наведеному тут типовому інтервалі. Ці дози формуються, виходячи з середньої людини, що має вагу приблизно 65-70кг. Лікар легко визначить дози для суб'єкта, вага якого випадає з цього інтервалу, такого як дитина і людина похилого віку. Для уникнення сумнівів, посилання тут на "лікування" включає посилання на зцілююче, паліативне і профілактичне лікування. Згідно з іншим втіленням представленого винаходу, сполуки формули (1), або їх фармацевтично прийнятні солі, похідні або композиції, також можуть бути використані як комбінації з одним або декількома додатковими терапевтичними агентами для спільного введення пацієнтові для одержання деякого окремого терапевтичного кінцевого результату, такого як лікування патофізіологічнорелевантного захворювання, що включає, але не обмежується ним, (і) бронхоконстрикцію, (іі) запалення, (ііі) алергію, (iv) руйнування тканини, (v) ознаки і симптоми, такі як задуха, кашель. Другим і більше додатковим терапевтичним агентом також може бути сполука формули (1), або її фармацевтично прийнятна сіль, похідні форми або композиції, або один або більше b2 агоністів відомих в цій галузі. Більш типово, другий і більше терапевтичний агент будуть вибирати з різних класів терапевтичних агентів. Як використовується у даному контексті, під термінами "спільне введення", "спільно введені" і 86615 36 "в комбінації з", стосовно сполук формули (1) та один або декілька інших терапевтичних агентів, розуміють, посилаються та включають наступне: - одночасне введення такої комбінації сполук(и) формули (1) і терапевтичного агента(ів) пацієнтові, що потребує лікування, коли такі компоненти сформовані разом в одну дозовану форму, яка вивільнює згадані компоненти, по суті, в той же самий час у згаданому пацієнті, - по суті, одночасне введення такої комбінації сполук(и) формули (1) і терапевтичного агента(ів) пацієнтові, що потребує лікування, коли такі компоненти сформовані окремо один від одного в різні дозовані форми, які приймаються, по суті, одночасно згаданим пацієнтом, де згадані компоненти вивільнюються, по суті, в той же самий час у згаданому пацієнті, - послідовне введення такої комбінації сполук(и) формули (1) і терапевтичного агента(ів) пацієнтові, що потребує лікування, коли такі компоненти сформовані окремо один від одного в різні дозовані форми, які приймаються, по суті, послідовно згаданим пацієнтом із значним інтервалом часу між кожним прийомом, де згадані компоненти вивільнюються, по суті, в різний час у згаданому пацієнті; і - послідовне введення такої комбінації сполук(и) формули (1) і терапевтичного агента(ів) пацієнтові, що потребує лікування, коли такі компоненти сформовані разом в одну дозовану форму, яка вивільнює згадані компоненти контрольовано, де вони одночасно, безперервно і/або з накладенням вивільнюються в той же самий час і/або в різний час в згаданому пацієнті, де кожна частина може бути введена одним або різними шляхами. Придатними прикладами інших терапевтичних агентів, які можуть бути використані в комбінації з сполукою(ами) формули (1) або їх фармацевтично прийнятними солями, похідними або композиціями, є, але не обмежується ними: (a) інгібітори 5-ліпоксигенази (5-LO) або антагоністи 5-ліпоксигенази активуючого протеїну (FLAP), (b) антагоністи лейкотрієну (LTRAs), включаючи антагоністи LTB4, LTC4, LTD4 і LTE4, (c) антагоністи рецептора гістаміну, включаючи Н1 і НЗ антагоністи, (d) агоністи a1- і a2-адренорецептора, судинозвужувальні симпатоміметичні агенти для протизастійного застосування, (e) антагоністи мускаринового М3 рецептора або антихолінергічні агенти, (f) інгібітори PDE, наприклад, інгібітори PDE3, PDE4 і PDE5, (g) теофілін, (h) хромоглікат натрію, (і) інгібітори СОХ як неселективні, так і селективні інгібітори СОХ-1 або СОХ-2 (NSAIDs), (j) пероральні глюкокортикостероїди і глюкокортикостероїди, що інгалюються, (k) моноклональні антитіла активні проти ендогенного запалення, (І) антипухлинні агенти фактору некрозу (антиTNF-a), 37 (m) інгібітори адгезії молекули, включаючи VLA-4 антагоністи, (n) антагоністи рецептора кініну - Br і В2, (о) імуносупресивні агенти, (р) інгібітори матриксних металопротеїназ (MMPs), (q) антагоністи рецептора тахікініну NK1, NK2 і NK3, (r) інгібітори еластази, (s) агоністи рецептора аденозину А2а, (t) інгібітори урокінази, (u) сполуки, що діють як допамінові рецептори, наприклад, D2 агоністи, (v) модулятори NFkb шляху, наприклад, ІKK інгібітори, (w) модулятори цитокінових сигнальних шляхів, такі як р38 МАР кіназа або syk кіназа, (х) агенти, що можуть класифікуватись як муколітики або протикашлеві агенти і (у) антибіотики, (z) інгібітори HDAC та (аа) інгібітори РІ3 кінази. Згідно з представленим винаходом, комбінація сполуки формули (1) з: - Н3 антагоністами, - антагоністами мускаринового М3 рецептора, - інгібіторами ФДЕ4, - глюкортикостероїдами, - агоністами рецептора аденозину А2а, - модуляторами цитокінових сигнальних шляхів, такими як р38 МАР кіназа або syk кіназа, або - антагоністами лейкотрієну (LTRAs), включаючи антагоністи LTB4, LTC4, LTD4 і LTE4, є переважними. Згідно з представленим винаходом, комбінація сполуки формули (1) з: - глюкортикостероїдами, зокрема, глюкортикостероїдами, що інгалюються, із зменшеними системними побічними ефектами, включаючи преднізон, преднізолон, флунізолід, тріамцинолон ацетонід, беклометазону дипропіонат, будезонід, флутіказону пропіонат, циклезонід і мометазону фуроат, або - антагоністи мускаринового М3 рецептора або антихолінергічні агенти, включаючи, зокрема, солі іпратропію, а саме бромід, солі тіотропію, а саме бромід, солі окситропію, а саме бромід, перензепін і телензепін, є переважними. Зрозуміло, що всі посилання тут на лікування включають зцілююче, пом'якшуюче і профілактичне лікування. Опис, наведений далі, стосується терапевтичного застосування, в якому можуть бути застосовані сполуки формули (1). Сполуки формули (1) мають здатність взаємодіяти з b2 рецептором і таким чином мають широкий діапазон терапевтичних застосувань, як описано тут нижче, оскільки рецептор b2 відіграє суттєву роль в фізіології всіх ссавців. Тому, наступний аспект представленого винаходу стосується сполук формули (1), або їх фармацевтично прийнятних солей, похідних форм або композицій, для використання при лікуванні захворювань, розладів і станів, в які залучений b2 рецептор. Більш особливо, представлений винахід та 86615 38 кож стосується сполук формули (1) або їх фармацевтично прийнятних солей, похідних або композицій, для використання при лікуванні захворювань, розладів і станів, що вибирають з групи, яка включає: - астму будь-якого типу, етіології або патогенезу, зокрема, астму, що є членом, який вибирають з групи, яка включає атопічну астму, неатопічну астму, алергічну астму, атопічну бронхіальну lgE-опосередковану астму, бронхіальну астму, есенціальну астму, істинну астму, інфекційноалергійну астму, викликану патофізіологічними розладами, зовнішню астму, викликану зовнішніми факторами, есенціальну астму невідомого або неочевидного походження, неатопічну астму, бронхітну астму, емфізематозну астму, астму викликану фізичним навантаженням, астму індуковану алергеном, астму індуковану холодним повітрям, професійну астму, інфекційну астму, спричинену бактеріальною, фунгальною, протозойною або вірусною інфекцією, неалергійну астму, початкову астму, синдром задухи у немовлят і бронхіоліт, - хронічну або гостру бронхоконстрикцію, хронічний бронхіт, обструкцію малих дихальних шляхів та емфізему, - обструктивні або запальні захворювання дихальних шляхів будь-якого типу, етіології або патогенезу, зокрема, обструктивні або запальні захворювання дихальних шляхів, що є членами, які вибирають з групи, що включає хронічну еозинофільну пневмонію, хронічне обструктивне легеневе захворювання (COPD), COPD, що включає хронічний бронхіт, легеневу емфізему або диспное пов'язане або непов'язане з COPD, COPD, що характеризується незворотною прогресуючою обструкцією дихальних шляхів, респіраторний дистрессиндром повнолітніх (ARDS), загострення респіраторної гіперреактивності на фоні іншої фармакотерапії і захворювання дихальних шляхів, що пов'язані з легеневою гіпертензією, - бронхіт будь-якого типу, етіології, або патогенезу; зокрема, бронхіт, що є членом, вибирають з групи, яка включає: гострий бронхіт, гострий ларинготрахеальний бронхіт, арахідоновий бронхіт, катаральний бронхіт, крупозний бронхіт, сухий бронхіт, інфекційний астматичний бронхіт, продуктивний бронхіт, стафілококовий або стрептококовий бронхіт і везикулярний бронхіт, - гостре ушкодження легень, - бронхоектазію будь-якого типу, етіології або патогенезу, зокрема, бронхоектазію, що є членом, який вибирають з групи, що включає циліндричну бронхоектазію, осумковану бронхоектазію, веретеноподібну бронхоектазію, капілярну бронхоектазію, циститну бронхоектазію, суху бронхоектазію і фолікулярну бронхоектазію. Ще один наступний аспект представленого винаходу стосується застосування сполук формули (1), або їх фармацевтично прийнятних солей, похідних або композицій, для виготовлення лікарського засобу, що має b2 агоністичну активність. Зокрема, представлений винахід стосується застосування сполук формули (1) або їх фармацевтично прийнятних солей, похідних або композицій, для виготовлення лікарського засобу для лікуван 39 ня b2-опосередкованих захворювань і/або станів, зокрема, захворювань і/або станів наведених вище. Як результат, представлений винахід забезпечує особливо цікавий спосіб лікування ссавця, включаючи людину, що включає лікування згаданого ссавця ефективною кількістю сполуки формули (1) або її фармацевтично прийнятної солі, похідного або композиції. Більш особливо, представлений винахід забезпечує особливо цікавий спосіб лікування ссавця, включаючи людину, для лікування b2-опосередкованих захворювань і/або станів, зокрема, захворювань і/або станів наведених вище, що включає лікування згаданого ссавця ефективною кількістю сполуки формули (1) або її фармацевтично прийнятних солей або похідних. Наступні приклади ілюструють одержання сполук формули (1): Препаративний приклад 1: етиловий естер (3Етоксикарбонілметилфеніл)оцтової кислоти 2,2'-(1,3-Фенілен)діоцтову кислоту (10,0г, 51ммоль) розчиняли в етанолі (100мл) і розчин обробляли по краплях ацетилхлоридом (2,5мл). Реакційну суміш перемішували при кипінні протягом 18 годин перед тим як залишити іі охолоджуватись і концентрували у вакуумі. Залишок переносили в етилацетат (100мл) і екстрагували за допомогою розчину бікарбонату натрію (3´50мл) і насиченого сольового розчину (3´50мл). Органічну фазу сушили (MgSO4), концентрували у вакуумі і залишок розтирали з пентаном, одержуючи продукт (11,8г). 1 Н ЯМР (CDCI3, 400МГц) d: 1,31 (6Н, т), 3,65 (4Н, с), 4,20 (4Н, кв), 7,24-7,36 (4Н, м); НРМС ESI m/z 251 [М+Н]+ Препаративний приклад 2: (3Етоксикарбонілметилфеніл)оцтова кислота Розчин препаративного прикладу 1 (44,3г, 177ммоль) і 2,2'-(1,3-фенілен)діоцтової кислоти (59,2г, 308ммоль) в етанолі (24мл) і діоксані (290мл) обробляли по краплях хлорводневою кислотою (12М, 4,9мл, 58,8ммоль). Перед охолодженням реакційну суміш перемішували при кипінні протягом 18 годин і концентрували до незначного об'єму. Реакційну суміш розводили толуолом (125мл) і одержану суспензію фільтрували. Фільтрат концентрували у вакуумі і залишок переносили в воду і підлуговували бікарбонатом натрію до досягнення нейтрального значення показника рН. Суміш розводили етилацетатом (200мл) і органічний шар відокремлювали і промивали за допомогою розчину бікарбонату натрію (5´30мл) і насиченого сольового розчину (50мл). Об'єднані водні екстракти підкислювали до значення показника рН 3 за допомогою 6М хлорводневої кислоти і екстрагували за допомогою діети 86615 40 лового етеру (3´30мл). Органічні шари об'єднували, сушили (MgSO4) і концентрували у вакуумі. Залишок розтирали з пентаном, одержуючи безбарвну тверду речовину (10,8г). 1 Н ЯМР (CD3OD, 400мгц) d: 1,25 (3Н, т), 3,60 (2Н, м), 3,63 (2Н, м), 4,15 (2Н, кв), 7,18-7,32 (4Н, м); НРМС ESI m/z 245 [M+Na]+ Препаративний приклад 3: [3-(2-Гідрокси-2метилпропіл)феніл]оцтова кислота Метилмагнійхлорид (51мл 3М розчину в тетрагідрофурані, 153ммоль) додавали краплями до перемішуваного розчину препаративного прикладу 2 (11,6г, 51ммоль) International Journal of Peptide i Protein Research, 1987, 29 (3), 331 в тетрагідрофурані (300мл) при 0°С в атмосфері азоту. Реакційну суміш залишали нагріватися до кімнатної температури протягом ночі з утворенням тонкодисперсного білого осаду і потім обережно додавали воду (50мл) і 2N хлорводневої кислоти (80мл). Водний розчин екстрагували за допомогою етилацетату (2´300мл) і об'єднані органічні екстракти промивали за допомогою насиченого сольового розчину (50мл), сушили (сульфат натрію) і видаляли розчинник у вакуумі, одержуючи вказану в заголовку сполуку у вигляді золотавого масла (11,2г). 1 Н ЯМР (CDCI3, 400МГц) d: 1,22 (6Н, с), 2,75 (2Н, с), 3,63 (2Н, с), 7,12-7,30 (4Н, м); НРМС ESI m/z 209 [М+Н]+ Препаративний приклад 4: (3-{2[(Хлорацетил)аміно]-2-метилпропіл}феніл)оцтова кислота 2-Хлорацетонітрил (8,8мл, 140ммоль) додавали до розчину, одержаного в препаративному прикладі 3 (16,0г, 70ммоль) в оцтовій кислоті (33мл) і охолоджували до 0°С. Одержаний розчин обробляли концентрованою сірчаною кислотою (33мл) і залишали поступово нагріватися до кімнатної температури. Через 4 години реакційну суміш виливали на лід і підлуговували за допомогою твердого карбонату натрію. Розчин екстрагували за допомогою етилацетату (2´500мл) і об'єднані органічні екстракти сушили (MgSO4) і концентрували у вакуумі, одержуючи вказаний в заголовку продукт у вигляді безбарвної твердої речовини (19,0г). 1 Н ЯМР (CDCI3, 400МГц) d: 1,36 (6Н, с), 3,02 (2Н, с), 3,62 (2Н, с), 3,95 (2Н, с), 6,19 (1Н, м), 7,067,31 (4Н, м); НРМС ESI m/z 282 [M-H]Препаративний приклад 5: метиловий естер [3-(2-Аміно-2-метилпропіл)феніл]оцтової кислоти Розчин сполуки, одержаної в препаративному прикладі 4 (5,1г, 18ммоль), тіосечовини (1,6г, 21ммоль) і оцтової кислоти (18мл) в етанолі (80мл) нагрівали із зворотнім холодильником в атмосфері 41 азоту протягом 16 годин. Реакційну суміш залишали охолоджуватися до кімнатної температури і фільтрували і фільтрат концентрували у вакуумі. Залишок розчиняли в етанолі (150мл), насичували хлоридом водню і одержаний розчин нагрівали із зворотнім холодильником протягом 16 годин. Суміш концентрували у вакуумі і додавали етилацетат (200мл) і 5% водний розчин карбонату натрію (200мл). Органічну фазу промивали за допомогою насиченого сольового розчину (100мл), сушили (MgSO4) і концентрували у вакуумі. Залишок очищали, використовуючи сильну катіонобмінну смолу (метанол і потім 2М розчин аміаку в метанолі), одержуючи жовте масло (2,68г). 1 Н ЯМР (CDCI3, 400МГц) d: 1,14 (6Н, с), 2,68 (2Н, с), 3,62 (2Н, с), 3,69 (3Н, с), 7,08-7,16 (3Н, м), 7,23-7,27 (1 Н, м); НРМС ESI m/z 222 [М+Н]+ Препаративний приклад 6: метиловий естер [3-(2-трет-Бутоксикарбоніламіно-2метилпропіл)феніл]оцтової кислоти Розчин ди-трет-бутилдикарбоксилату (8,19г, 38,0ммоль) в дихлорметані (40мл) додавали до розчину препаративного прикладу 5 (8,4г, 38,0ммоль) і триетиламіну (5,2мл, 38,0ммоль) в дихлорметані (60мл) при 0-5°С. Суміш залишали нагріватися до кімнатної температури і перемішували протягом ночі. Розчинник видаляли і залишок обробляли за допомогою розчину карбонату натрію і екстрагували за допомогою етилацетату (3´30мл). Об'єднані органічні шари промивали за допомогою насиченого сольового розчину (3´20мл) і сушили (Na2SO4). Продукт очищали за допомогою хроматографії (0-80% етилацетат в гексані), одержуючи безбарвне масло, яке розчиняли в діетиловому етері (´3) і випаровували (10,1г). 1 Н ЯМР (CDCI3, 400мгц) d: 1,26 (6Н, с), 1,46 (9Н, с), 2,97 (2Н, с), 3,60 (2Н, с), 3,68 (3Н, с), 4,26 (1Н, шс), 7,05-7,07 (2Н, м), 7,13-7,17 (1Н, м), 7,227,26 (1 Н, м); НРМС ESI m/z 344 [M+Na]+ Препаративний приклад 7: [3-(2-третБутоксикарбоніламіно-2-метилпропіл)феніл]оцтова кислота Сполуку одержану в препаративному прикладі 6 (7,45г, 23,0ммоль), розчин гідроксиду натрію (5М, 4,6мл, 115ммоль), діоксан (30мл) і воду (8мл) перемішували при кімнатній температурі 18 годин. Розчинник видаляли і матеріал розчиняли в воді, охолоджували і підкислювали до рН 3, використовуючи хлорводневу кислоту (2М). Продукт екстрагували за допомогою етилацетату (3´30мл) і органічні екстракти промивали за допомогою насиченого сольового розчину (3´30мл) і сушили (Na2SO4). Одержане масло розчиняли в діетиловому етері і випаровували, одержуючи безбарвну смолу (7,0г). 86615 42 1 Н ЯМР (CD3OD, 400МГц) d: 1,23 (6Н, с), 1,48 (9Н, с), 2,96 (2Н, с), 3,57 (2Н, с), 7,04-7,06 (2Н, м), 7,11-7,13 (1Н, м), 7,18-7,22 (1Н, м); НРМС ХІАТ m/z 308 [М+Н]+ Препаративний приклад 8: трет-бутиловий естер (2-{3-[(3,4Дихлорбензилкарбамоїл)метил]феніл}-1,1диметилетил)карбамінової кислоти 3,4-Дихлорбензиламін (1,30мл, 9,76ммоль) додавали до розчину сполуки, одержаної в препаративному прикладі 7 (3,00г, 9,76ммоль), гідрату гідроксибензотриазолу (1,50г, 9,76ммоль), гідрохлориду 1-(3-диметиламінопропіл)-3етилкарбодііміду (1,87г, 9,76ммоль) і триетиламіну (4,07мл, 11,2ммоль) і одержаний розчин перемішували при кімнатній температурі 18 годин. Розчинник видаляли і неочищений матеріал переносили в етилацетат (50мл) і промивали водою (30мл), розчином карбонату натрію (2´30мл), насиченим сольовим розчином (30мл), хлорводневою кислотою (0,5М, 2´30мл) і насиченим сольовим розчином (30мл) і потім сушили (Na2SO4). Одержану тверду речовину білого кольору розтирали з діетиловим етером (3,1г). 1 Н ЯМР (CDCI3, 400мгц) d: 1,25 (6Н, с), 1,45 (9Н, с), 2,97 (2Н, с), 3,62 (2Н, с), 4,22 (1Н, шс), 4,34 (2Н, д), 5,78 (1Н, шс), 6,99-7,01 (1Н, дд), 7,04 (1Н, с), 7,07-7,09 (1Н, д), 7,12-7,14 (1Н, д), 7,22 (1Н, д), 7,27 (1Н, д), 7,32 (1Н, д); НРМС ХІАТ m/z 465 [М+Н]+ Препаративний приклад 9: трет-бутиловий естер (2-{3-[(3,4Диметилбензилкарбамоїл)метил]феніл}-1,1диметилетил)карбамінової кислоти Одержували, використовуючи кислоту з препаративного прикладу 7 і спосіб описаний для Препаративного прикладу 8 і 3,4диметилбензиламін. 1 Н ЯМР (CDCI3, 400МГц) d: 1,19 (6Н, с), 1,46 (9Н, с), 2,20 (6Н, д), 2,95 (2Н, с), 3,59 (2Н, с), 4,15 (1Н, шс), 4,32 (2Н, д), 5,59 (1Н, шс), 6,86-6,93 (2Н, м), 7,02-7,06 (3Н, м), 7,13-7,15 (1Н, д), 7,23-7,27 (1Н,м); НРМС ХІАТ m/z 425 [М+Н]+ Препаративний приклад 10: 2-[3-(2-Аміно-2метилпропіл)феніл]-N-(3,4-дихлорбензил)ацетамід Сполуку, одержану в препаративному прикладі 8 (3,0г, 6,50ммоль) в діоксані (5мл) обробляли за допомогою хлориду водню (4М в діоксані, 20мл) і одержаний розчин залишали перемішуватися при кімнатній температурі 18 годин. Розчинник вида 43 ляли і сполуку повторно розчиняли в метанолі (´2) і випаровували, потім одержану смолу суспендували в діетиловому етері (´2) і випаровували, одержуючи тверду речовину білого кольору (2,7г). Т. пл. (етилацетат-метанол) 214-216 (розкл.)°С. 1 Н ЯМР (CD3OD, 400МГц) d: 1,33 (6Н, с), 2,90 (2Н, с), 3,59 (2Н, с), 4,35 (2Н, с), 7,13-7,19 (3Н, м), 7,24-7,27 (1Н, м), 7,31-7,38 (2Н, м), 7,42 (1Н, д);. НРМС ESI m/z 365 [М+Н]+ Препаративний приклад 11: 2-[3-(2-Аміно-2метилпропіл)феніл]-N-(3,4-диметилбензил)ацетамід Одержували, використовуючи амід з препаративного прикладу 9 і спосіб описаний для препаративного прикладу 10. 1 Н ЯМР (CD3OD, 400МГц) d: 1,32 (6Н, с), 2,21 (6Н, с), 2,89 (2Н, с), 3,56 (2Н, с), 4,29 (2Н, с), 6,957,05 (3Н, м), 7,14-7,16 (2Н, м), 7,24-7,26 (1Н, м), 7,31-7,35 (1Н, м); НРМС ESI m/z 325 [М+Н]+ Препаративний приклад 12: N-{2-Бензилокси5-[(1R)-2-бром-1-(трет-бутилдиметилсиланілокси) етил]феніл}формамід До розчину N-[2-бензилокси-5-(2-бром-1гідроксиетил)феніл]формаміду (Organic Process Research і Development 1998, 2, 96-99) (4,12г, 11,8ммоль) в N,N-диметилформаміді (25мл) при кімнатній температурі в атмосфері N2 додавали трет-бутилдиметилсилілхлорид (3,50г, 23,2ммоль), імідазол (1,90г, 27,9ммоль) і 4(диметиламіно)піридин (40мг, 330мкмоль). Одержаний розчин перемішували при кімнатній температурі протягом ночі, розчинник видаляли і продукт переносили в етилацетат (70мл). Органічні шари промивали водою (100мл) і водні шари екстрагували за допомогою етилацетату (20мл). Об'єднані органічні екстракти промивали, використовуючи хлорводневу кислоту (2М, 50мл), насичений сольовий розчин (100мл) і сушили (MgSO4). Неочищений матеріал очищали, використовуючи колонкову хроматографію (5-25% етилацетат в пентані), одержуючи безбарвне масло (5,7г). 1 Н ЯМР (CDCI3, 400МГц) d: від -0,08 до -0,05 (3Н, м), 0,09-0,11 (3Н, с), 0,89-0,90 (9Н, м), 3,383,55 (2Н, м), 3,78-3,84 (1Н, м), 5,06-5,11 (2Н, м), 6,90-6,97 (1Н, м), 7,03-7,12 (1Н, м), 7,24 (м), 7,367,43 (5Н, м), 7,67-7,78 (м), 7,88 (д), 8,74 (д); НРМС ХІАТ m/z 464/466 [М+Н]+ 86615 44 Препаративний приклад 13: 2-(3-{2-[(2R)-2-(4Бензилокси-3-форміламінофеніл)-2-(третбутилдиметилсиланілокси)етиламіно]-2метилпропіл}феніл)-N-(3,4-дихлорбензил)ацетамід Сполуки, одержані в препаративному прикладі 12 (500мг, 1,08ммоль) і препаративному прикладі 10 (780мг, 216ммоль) нагрівали і перемішували при 90°С протягом 24 годин. Після охолодження матеріал розчиняли в метанолі і випаровували, матеріал суспендували в діетиловому етері і осад відфільтровували. Фільтрат випаровували і матеріал очищали, використовуючи колонкову хроматографію (0-5% метанол в дихлорметані) і потім суспендували в діетиловому етері (´3) і випаровували, одержуючи піну (425мг). 1 Н ЯМР (CD3OD, 400МГц) d: від -0,20 до -0,18 (3Н, м), -0,04 до 0,00 (3Н, м), 0,78-0,81 (9Н, м), 1,01-1,03 (3Н, м), 1,05 (3Н, шс), 2,62-2,74 (3Н, м), 2,83-2,88 (1Н, м), 3,52 (2Н, д), 4,31 (2Н, с), 4,684,71 (1Н, м), 5,17-5,19 (2Н, м), 7,00-7,23 (7Н, м), 7,29-7,41 (5Н, м), 7,44-7,49 (2Н, м), 8,57 (с); НРМС ESI m/z 748 [М+Н]+; ВРМС C41H51Cl2N3O4Si 748,3099 [М+Н]+ знайдено 748,3066. Препаративний приклад 14: 2-(3-{2-[(2R)-2-(4Бензилокси-3-форміламінофеніл)-2-(трет-бутилдиметилсиланілокси)етиламіно]-2-метилпропіл} феніл)-N-(3,4-диметилбензил)ацетамід Одержували, використовуючи амід з препаративного прикладу 13, бромід з препаративного прикладу 12 і спосіб описаний для препаративного прикладу 11. 1 Н ЯМР (CDCI3, 400МГц) d: -0,17, -0,16 (3Н, 2х с), від -0,05 до -0,01 (3Н, м), 0,78-0,82 (9Н, м), 0,971,01 (6Н, м), 2,19 (3Н, 2,20 (3Н, с), 2,56-2,90 (4Н, м), 3,54-3,63 (2Н, м), 4,28-4,35 (2Н, м), 4,67-4,74 (1Н, м), 5,06-5,09 (2Н, м), 5,58-5,62 і 5,99-6,03 (1Н, м), 6,87-7,25 (9Н, м), 7,35-7,44 (5Н, м), 7,68-7,79 (1Н, м), 8,30 (д), 8,43 (д), 8,71 (с), 8,74 (с); НРМС ESI m/z 748 [М+Н]+; ВРМС C43H57N3O4Si 708,4191 [М+Н]+ знайдено 708,4156. Препаративний приклад 15: N-Бензил-2-(3-{2[(2R)-2-(трет-бутилдиметилсиланілокси)-2-(3форміламіно-4-гідроксифеніл)етиламіно]-2метилпропіл}феніл)ацетамід 45 Сполуку, одержану в препаративному прикладі 13 (100мг, 134мкмоль) і паладій на вугіллі (10%, 20мг) в метанолі (10мл) гідрували при 50псі/кт протягом 6 годин. Суміш фільтрували крізь допоміжну фільтрувальну насадку і розчинник видаляли. Матеріал суспендували в розчині гідрокарбонату натрію і екстрагували за допомогою етилацетату (30мл). Органічний шар промивали, використовуючи розчин гідрокарбонату натрію, насичений сольовий розчин (2´ мл) і сушили (Na2SO4). Одержаний матеріал суспендували в діетиловому етері (´3) і випаровували, одержуючи плівку (24мг). 1 Н ЯМР (CD3OD, 400МГц) d: -0,19 (3Н, с), -0,02 (3Н, с), 0,79 (9Н, с), 1,04 (3Н, с), 1,07 (3Н, с), 2,622,89 (4Н, м), 3,48-3,56 (2Н, дд), 4,35 (2Н, с), 4,61 (1Н, шс), 4,69-4,72 (1Н, м), 5,17-5,19 (2Н, м), 6,796,85 (1Н, м), 6,91-6,94 (1Н, м), 7,04-7,06 (1Н, м), 7,11-7,28 (7Н, м), 8,12 (1Н, д), 8,27, 8,59 (1Н, 2х с); НРМС ESI m/z 590 [М+Н]+; ВРМС C34H47N3O4Si 590,3402 [М+Н]+ знайдено 590,3409. Препаративний приклад 16: 2-(3-{2-[(2R)-2(трет-Бутилдиметилсиланілокси)-2-(3-форміламіно-4-гідроксифеніл)етиламіно]-2-метилпропіл}феніл)-N-(3,4-диметилбензил)ацетамід Одержували, використовуючи амід з препаративного прикладу 14 і спосіб описаний для Препаративного прикладу 15. Продукт очищали, використовуючи колонкову хроматографію (0-3,5% метанол в дихлорметані + 0,3% аміак), одержуючи піну (85мг). 1 Н ЯМР (CD3OD, 400МГц) d: -0,20 до -18 (3Н, м), -0,03-0,00 (3Н, м), 0,79-0,81 (9Н, м), 1,02-1,05 (6Н, м), 2,19 (3Н, с), 2,20 (3Н, с), 2,61-2,73 (3Н, м), 2,83-2,88 (1 Н, м), 3,46 (2Н, дд), 4,27 (2Н, с), 4,65 (1Н, дд), 6,78-7,22 (8Н, м), 8,12 (д), 8,27 (с), 8,59 (с);. НРМС ESI m/z 618 [М+Н]+; ВРМС C36H51N3O4Si 618,3722 [М+Н]+ знайдено 618,3701. Препаративний приклад 17: Метил (3бромфеніл)ацетат Ацетилхлорид (0,7мл, 9,3ммоль) повільно додавали до розчину (3-бромфеніл)оцтової кислоти (20,0г, 93ммоль) в метанолі (500мл) при 0°С в атмосфері азоту і реакційну суміш залишали посту 86615 46 пово нагріватися до кімнатної температури протягом більше ніж 5 годин. Розчинник видаляли в вакуумі і маслоподібний залишок повторно розчиняли в дихлорметані, сушили над сульфатом натрію і концентрували у вакуумі, одержуючи вказану в заголовку сполуку у вигляді безбарвного масла (20,6г). 1 Н ЯМР (400МГц, CDCI3): d: 3,59 (2Н, с), 3,70 (3Н, с), 7,17-7,24 (2Н, м), 7,37-7,45 (2Н, м); НРМС ESI m/z 253 [M+Na]+ Препаративний приклад 18: Метил [3-(2оксопропіл)феніл]ацетат Метоксид трибутилолова (28,3мл, 98ммоль), продукт препаративного прикладу 17 (15,0г, 65ммоль), ізопропенілацетат (10,8мл, 98,0ммоль), ацетат паладію (II) (750мг, 3,30ммоль) і три-ортотолілфосфін (2,0г, 6,5ммоль) перемішували разом в толуолі (75мл) при 100°С протягом 5 годин. Після охолодження, реакційну суміш розводили етилацетатом (150мл) і 4М водного розчину фториду калію (90мл) і перемішували протягом 15 хвилин. Суміш фільтрували крізь Arbocele® і органічну фазу відокремлювали і концентрували у вакуумі. Залишок потім очищали за допомогою колонкової хроматографії на силікагелі, елююючи сумішшю діетиловий етер : пентан, з градієнтом від 0:100 до 25:75, потім за допомогою дихлорметану, одержуючи вказану в заголовку сполуку у вигляді блідожовтого масла з 94% виходом (12,6г). 1 Н ЯМР (400мгц, CDCI3): d: 2,15 (3Н, с), 3,61 (2Н, с), 3,69 (5Н, с), 7,10-7,13 (2Н, м), 7,19 (1Н, д), 7,30 (1Н, т); НРМС ESI : m/z 229 [M+Na]+ Препаративний приклад 19: гідрохлорид метил [3-((2R)-2-{[(1R)-1-фенілетил]аміно}пропіл)феніл] ацетату Розчин продукту препаративного прикладу 18 (8,5г, 41,2ммоль), (R)-a-метил бензиламіну (4,8мл, 37,2ммоль), триацетоксиборгідриду натрію (11,6г, 56ммоль) і оцтової кислоти (2,2мл, 38ммоль) в дихлорметані (400мл) перемішували при кімнатній температурі протягом 48 годин. Реакційну суміш гасили шляхом додавання насиченого розчину гідрокарбонату натрію (200мл) і залишали перемішуватися до відсутності кипіння. Водну фазу відокремлювали і екстрагували за допомогою дихлорметану (100мл). Об'єднаний органічний розчин потім сушили над сульфатом магнію і концентрували у вакуумі. Шляхом очищення за допомогою колонкової хроматографії на силікагелі, елююючи з використанням суміші дихлорметан : метанол : аміак, з градієнтом від 99:1:0,1 до 95:5:0,5, одержували 4:1 суміш діастереомерів (R,R основний) у вигляді блідо-жовтого масла (8,71г). Обробка хлоридом водню (40мл 1М розчину в метанолі, 40,0ммоль) після трьох послідовних кристалізацій (діізопропіловий етер/метанол) давала вказану в 47 86615 48 заголовку сполуку у вигляді кристалічної речовини білого кольору з 50% виходом, 5,68г. 1 Н ЯМР (400МГц, CD3OD): d: 1,18 (3Н, д), 1,68 (3Н, д), 2,60-2,66 (1Н, м), 3,15-3,26 (1Н, м), 3,253,30 (1Н, м), 3,31 (3Н, с), 3,62 (2Н, с), 4,59 (1Н, кв), 6,99-7,02 (2Н, м), 7,17 (1Н, м), 7,25-7,28 (1Н, м), 7,48-7,52 (5Н, м) НРМС ESI m/z 312 [М+Н]+ Препаративний приклад 20: Метил {3-[(2R)-2амінопропіл]феніл}ацетат сполуку у вигляді жовтого масла з 82% виходом (6,50г) 1 Н ЯМР (400МГц, CD3CI3): d: 1,07 (3Н, д), 1,40 (9Н, с), 2,61 (1Н, дд), 2,77-2,88 (1Н, шс), 3,62 (2Н, с), 3,89 (1Н, шс), 4,39 (1Н, шс), 7,07-7,16 (3Н,м), 7,22-7,27 (1 Н, м); НРМС ХІАТ m/z 292 [М-Н]' Препаративний приклад 23: Бензил (3-{(2R)-2[(трет-бутоксикарбоніл)аміно]пропіл}феніл)ацетат Розчин продукту препаративного прикладу 19 (7,69г, 22ммоль) і форміату амонію (6,94г, 110ммоль) нагрівали при 75°С в присутності 20% гідроксиду паладію на вугіллі (2,00г). Через 90 хвилин реакційну суміш охолоджували до кімнатної температури, фільтрували крізь Arbocele® і фільтрат концентрували у вакуумі. Залишок розподіляли між дихлорметаном (100мл) і 0,88 аміаком (100мл) і фази відокремлювали. Водну фазу екстрагували дихлорметаном (100мл) і об'єднаний органічний розчин сушили над сульфатом магнію і концентрували у вакуумі, одержуючи вказану в заголовку сполуку у вигляді безбарвного масла з кількісним виходом (4,78г) 1 Н ЯМР (400МГц, CD3OD): d: 1,06 (3Н, д), 2,572,67 (2Н, м), 3,05-3,12 (1Н, м), 3,63 (2Н, с), 3,67 (3Н, с), 7,09-7,13 (3Н, м), 7,23-7,27 (1Н, т); НРМС ESI m/z 208 [М+Н]+ Препаративний приклад 21: Метил (3-{(2R)-2[(трет-бутоксикарбоніл)аміно]пропіл}феніл)ацетат Продукт, одержаний в препаративному прикладі 22 (6,30г, 21,5ммоль), гідрохлорид 1-(3диметиламінопропіл)-3-етилкарбодііміду (4,14г, 21,5ммоль), гідрат 1-гідроксибензотриазолу (3,30г, 21,5ммоль) і триетиламін (4,85мл, 43ммоль) перемішували разом в дихлорметані (100мл) протягом 10 хвилин при кімнатній температурі. Потім додавали бензиловий спирт (2,2мл, 21,5ммоль) і суміш перемішували при кімнатній температурі протягом 18 годин. Реакційну суміш потім розводили дихлорметаном (50мл), промивали, використовуючи розчин гідрокарбонату натрію (100мл) і насичений сольовий розчин (100мл), сушили над сульфатом магнію і концентрували у вакуумі, одержуючи вказану в заголовку сполуку у вигляді прозорого масла з 50% виходом, 4,16г. 1 Н ЯМР (400МГц, CD3CI3): d: 1,04 (3Н, д), 1,44 (9Н, с), 2,59 (1Н, дд), 2,81 (1Н, дд), 3,64 (2Н, с), 3,87 (1Н, шс), 4,34 (1Н, шс), 5,13 (2Н, с), 7,07-7,11 (2Н, м), 7,13 (1Н, шд), 7,22-7,27 (1Н, м), 7,29-7,38 (5Н, м); НРМС ХІАТ m/z 382 [М-Н]Препаративний приклад 24: Бензил {3-[(2R)-2амінопропіл)]феніл}ацетат Вказану в заголовку сполуку одержували з продукту препаративного прикладу 20 і ди-третбутилдикарбоксилату, використовуючи методику подібну до описаної в препаративному прикладі 6, у вигляді жовтого масла з 97% виходом. 1 Н ЯМР (400МГц, CD3CI3): d: 1,07 (3Н, д), 1,43 (9Н, с), 2,61 (1Н, дд), 2,8 (1Н, дд), 3,60 (2Н, с), 3,69 (3Н, с), 3,89 (1Н, шс), 4,36 (1Н, шс), 7,06-7,19 (3Н, м), 7,22-7,27 (1Н, м); НРМС ХІАТ m/z 306 [М-Н]Препаративний приклад 22: (3-{(2r)-2-[(третбутоксикарбоніл)аміно]пропіл}феніл)оцтова кислота Суміш, одержану в препаративному прикладі 21 (8,31г, 27,1ммоль) і розчин гідроксиду літію (1М у воді, 54мл, 54ммоль) в тетрагідрофурані (100мл) перемішували при кімнатній температурі протягом 20 годин. Реакційну суміш потім концентрували у вакуумі і водний залишок підкислювали до рН 2, використовуючи 2М хлорводневу кислоту. Суміш потім екстрагували за допомогою етилацетату (3´75мл) і об'єднаний органічний розчин промивали за допомогою насиченого сольового розчину (100мл), сушили над сульфатом магнію і концентрували у вакуумі, одержуючи вказану в заголовку Хлорид водню (4М в діоксані, 5,43мл, 21,72ммоль) додавали до розчину продукту препаративного прикладу 23 (4,16г, 10,86ммоль) в діоксані (50мл) і одержаний розчин перемішували при кімнатній температурі протягом 72 годин. Розчинник видаляли в вакуумі і залишок розчиняли в дихлорметані і промивали, використовуючи розчин гідрокарбонату натрію (50мл) і насичений сольовий розчин (50мл). Органічний розчин потім сушили над сульфатом магнію і концентрували у вакуумі, одержуючи вказану в заголовку сполуку у вигляді жовтого масла з 93% виходом (2,85г). 1 Н ЯМР (400МГц, CD3CI3): d: 1,09 (3Н, д), 1,55 (2Н, шс), 2,48 (1Н, дд), 2,66 (1Н, дд), 3,10-3,18 (1Н, м), 3,65 (2Н, с), 5,17 (2Н, с), 7,09-7,13 (2Н, м), 7,147,18 (1 Н, шд), 7,24-7,38 (6Н, м); НРМС ХІАТ m/z 284 [М-Н]Препаративний приклад 25: Бензил (3-{(2R)-2[((2R)-2-[4-(бензилокси)-3-(форміламіно)феніл]-2{[трет-бутил(диметил)силіл]окси}етил)аміно]пропіл}феніл)ацетат 49 Вказану в заголовку сполуку одержували з продуктів препаративного прикладу 12 і препаративного прикладу 24, використовуючи методику подібну до описаної в препаративному прикладі 13, у вигляді коричневого масла з 25% виходом. НРМС ХІАТ m/z 667 [М+Н]+ Препаративний приклад 26: {3-[(2R)-2-({(2R)-2{[трет-Бутил(диметил)силіл]окси}-2-[3-(форміламіно)-4-гідроксифеніл]етил}аміно)пропіл]феніл}оцтова кислота 86615 50 кімнатній температурі протягом 10 хвилин. Потім додавали 4-(диметиламіно)бензиламін (31мг, 206мкмоль) і суміш перемішували при кімнатній температурі протягом 20 годин. Розчинник потім видаляли в вакуумі і залишок розводили дихлорметаном, промивали, використовуючи розчин гідрокарбонату натрію (20мл) і насичений сольовий розчин (20мл), сушили над сульфатом магнію і концентрували у вакуумі, одержуючи вказану в заголовку сполуку у вигляді коричневої смоли з 10% виходом, 131мг. 1 Н ЯМР (400МГц, CD3CI3): 0,17 (3Н, с), 0,00 (3Н, с), 0,83 (9Н, с), 1,08 (3Н, м), 2,80-3,00 (10Н, м), 3,47 (1 Н, м), 3,66 (2Н, м), 4,23 (2Н, м), 5,48(1 Н, м), 6,66 (1Н, д), 6,70-7,23 (10Н, м), 7,97 (м), 8,27 (с); НРМС ХІАТ m/z 504 [М+Н] Препаративні приклади 28-29 Наступні сполуки, загальної формули, наведені нижче, одержували з продукту препаративного прикладу 26 і прийнятного аміну, використовуючи методику подібну до описаної для препаративного прикладу 27. Реакційні суміші контролювали, використовуючи аналіз ТШХ і перемішували при кімнатній температурі протягом 18-72 годин. Продукт, одержаний в препаративному прикладі 25 (851мг, 1,27ммоль) і 10% Pd/C (50мг), суспендували в метанолі і суміш перемішували в атмосфері газоподібного водню при тиску 60псі, при кімнатній температурі протягом 72 годин. Реакційну суміш потім фільтрували через допоміжну фільтрувальну насадку і фільтрат концентрували в вакуумі, одержуючи вказаний в заголовку продукт у вигляді коричневої піни з 94% виходом, 580мг. 1 Н ЯМР (400МГц, CDCI3): d: -0,09 (3Н, с), 0,08 (3Н, с), 0,88 (9Н, с), 1,12, 1,24 (3Н, 2хд), 2,07-2,82 (2Н, м), 2,99 (1Н, дд), 3,18 (1Н, дд), 3,60 (2Н, с), 4,16-4,22 (1Н, м), 4,97-5,07 (1Н, м), 6,87 (1Н, д), 6,99-7,32 (6Н, м), 7,93 (с), 8,17 (д), 8,33 (с); НРМС ХІАТ m/z 487 [М+Н]Препаративний приклад 27: 2-{3-[(2R)-2-({(2R)2-{[трет-Бутил(диметил)силіл]окси}-2-[3-(форміламіно)-4-гідроксифеніл]етил}аміно)пропіл]феніл}-N[4-(диметиламіно)бензил]ацетамід Препаративний приклад 28: N-[4(амінометил)феніл]ацетамід можна одержати як описано в J. Med. Chem, 46, 3116; 2003. Препаративний приклад 29: 4(амінометил)бензамід можна одержати як описано в WO 02085860, стор. 239. Препаративний приклад 30: [3-((2R)-2-{[(1R)-1Фенілетил]аміно}пропіл)феніл]оцтова кислота Суміш продукту препаративного прикладу 26 (100мг, 206мкмоль), гідрату гідроксибензотриазолу (32мг, 206мкмоль), гідрохлориду 1-(3диметиламінопропіл)-3-етилкарбодііміду (40мг, 206мкмоль) і триетиламіну (58мкл, 412мкмоль) в N,N-диметилформаміді (2мл) перемішували при Розчин гідроксиду літію (1М в воді, 90мл, 90ммоль) додавали до розчину продукту препаративного прикладу 19 (13,50г, 43,5ммоль) в метанолі (200мл) і суміш перемішували при кімнатній температурі протягом 18 годин. Потім до реакційної суміші додавали 1М хлорводневу кислоту (90мл) і видаляли в вакуумі метанол. Одержаний осад відфільтровували і промивали водою (20мл) і сумішшю етанол/діетиловий етер, 20:80, одержуючи вказану в заголовку сполуку у вигляді твердої речовини з 91% виходом, 11,8г. 51 1 Н ЯМР (400МГц, CD3OD) d: 1,16 (3Н, д), 1,62 (3Н, д), 2,66-2,62 (1Н, м), 3,13-3,26 (2Н, м), 3,46 (2Н, с), 4,48-4,56 (1Н, кв), 6,92 (1Н, д), 7,19 (1Н, с), 7,18-7,22 (2Н, м), 7,45-7,52 (5Н, м); НРМС ESI m/z 298 [М+Н]+ Препаративний приклад 31: N-1-Адамантил-2[3-((2R)-2-{[(1R)-1-фенілетил]аміно}пропіл)феніл]ацетамід 1-Адамантиламін (5,44г, 36,0ммоль) і триетиламін (15мл, 108ммоль) додавали до розчину продукту препаративного прикладу 30 (10,7г, 36,0ммоль) в дихлорметані (200мл). Потім додавали гексафторфосфат 2-хлор-1,3диметилімідазолідинію (10,0г, 36,0ммоль) і суміш перемішували при кімнатній температурі протягом 2 годин. Реакційну суміш промивали водою і органічний розчин сушили над сульфатом магнію і концентрували у вакуумі. Шляхом очищення залишку за допомогою колонкової хроматографії на силікагелі, елююючи з використанням суміші дихлорметан : метанол : 0,88 аміак, 95:5:0,5, одержували продукт у вигляді піни з кількісним виходом, 17,6г. 1 Н ЯМР (400МГц, CD3OD) d: 0,89 (3Н, д), 1,35 (3Н, д), 1,65-1,75 (6Н, м), 1,98 (6Н, м), 2,04 (3Н, м), 2,37-2,42 (1Н, дд), 2,65-2,74 (1Н, м), 2,95-3,00 (1Н, дд), 3,36 (2Н, с), 3,98 (1Н, кв), 6,89 (1Н, д), 6,98 (1Н, с), 7,09 (1Н, д), 7,17 (1 Н, т), 7,22-7,27 (1 Н, м), 7,30-7,38 (4Н, м); НРМС ESI m/z 431 [М+Н]+ Препаративний приклад 32: N-1-Адамантил-2{3-[(2R)-2-амінопропіл]феніл}ацетамід Вказану в заголовку сполуку одержували з препаративного прикладу 31, використовуючи методику подібну до описаної в препаративному прикладі 20, у вигляді твердої" речовини з 92% виходом. 1 Н ЯМР (400МГц, CD3OD) d: 1,09 (3Н, д), 1,661,72 (6Н, м), 2,00 (6Н, м), 2,03 (3Н, м), 2,58-2,70 (2Н, м), 3,10-3,16 (1Н, кв), 3,40 (2Н, с), 7,05-7,28 (4Н, м); НРМС ESI m/z 327 [М+Н]+ Препаративний приклад 33: 2-(3-{(2R)-2-[((2R)2-[3-(Ацетиламіно)-4-(бензилокси)феніл]-2-{[третбутил(диметил)силіл]окси}етил)аміно]пропіл}феніл)-N-1-адамантилацетамід Суміш продуктів препаративного прикладу 12 (696мг, 1,5ммоль) і препаративного прикладу 32 86615 52 (978мг, 3,0ммоль) в дихлорметані (0,5мл) нагрівали при 90°С протягом 5 хвилин, залишаючи дихлорметан випаровуватися. Перед охолодженням до кімнатної температури реакційну суміш потім нагрівали у вигляді розплаву при 90°С протягом 18 годин. Неочищений продукт потім очищали за допомогою колонкової хроматографії на силікагелі, елююючи з використанням суміші дихлорметан : метанол : 0,88 аміак, 98:2:0,2, одержуючи вказану в заголовку сполуку у вигляді піни блідого кольору з 59% виходом, 630мг. 1 Н ЯМР (400МГц, CD3OD) d: -0,18 (3Н, с), 0,00 (3Н, с), 0,83 (9Н, с), 1,05-1,08 (д, 3Н), 1,66-1,72 (6Н, м), 2,00 (6Н, м), 2,02 (3Н, м), 2,52-2,71 (3Н, м), 2,84-2,96 (2Н, м), 3,36-3,41 (2Н, м), 4,68-4,72 (1Н, м), 5,20 (2Н, с), 6,92-7,18 (6Н, м), 7,30-7,50 (5Н, м), 8,22 (м), 8,36 (с), 8,54 (с); HPMC ESI m/z 710 [M+H]+ Препаративний приклад 34: N-Адамантан-1-іл2-(3-{2-[(2R)-2-({(2R)-2-(третбутилдиметилсиланілокси)-2-(3-форміламіно-4гідроксифеніл)етиламіно]пропіл}феніл)ацетамід Вказану в заголовку сполуку одержували з продукту 33, використовуючи методику подібну до описаної в препаративному прикладі 20, у вигляді прозорої піни з кількісним виходом. 1 Н ЯМР (400МГц, CD3OD) d: -0,17 (3Н, с), 0,00 (3Н, с), 0,83 (9Н, с), 1,04-1,06 (д, 3Н), 1,69-1,70 (6Н, м), 2,00 (6Н, м), 2,03 (3Н, м), 2,52-2,70 (3Н, м), 2,88-2,94 (2Н, м), 3,37-3,38 (2Н, м), 4,64-4,69 (1Н, м), 6,92-7,18 (6Н, м), 8,00 (1 Н, д), 8,30 (с), 8,56 (с); НРМС ESI m/z 620 [М+Н]+ Препаративний приклад 35: 1-(3-Бромфеніл)2-метилпропан-2-ол) Метилмагнійбромід (3М розчин в діетиловому етері, 51,6мл, 155ммоль) повільно додавали до розчину 1-(3-бромфеніл)пропан-2-ону (15,0г, 70ммоль) в сухому діетиловому етері (200мл) при 0°С і суміш перемішували протягом 3 годин. Реакційну суміш потім повторно охолоджували до 0°С і повільно гасили, використовуючи насичений водний розчин хлориду амонію. Органічний розчин промивали насиченим розчином солі, сушили над сульфатом натрію і концентрували у вакуумі. Маслоподібний залишок жовтого кольору потім очищали за допомогою колонкової хроматографії на силікагелі, елююючи з використанням суміші дихлорметан : пентан : метанол, 90:5:5, одержуючи блідо-жовте масло з 83% виходом, 13,26г. 1 Н ЯМР (400МГц, CDCI3) d: 1,22 (6Н, с), 1,42 (1Н, шс), 2,74 (2Н, с), 7,15 (2Н, м), 7,40 (2Н, м) 53 Препаративний приклад 36: N-[2-(3Бромфеніл)-1,1-диметилетил]-2-хлорацетамід До перемішуваного розчину продукту препаративного прикладу 35 (12,0г, 52,0ммоль) в оцтовій кислоті (25мл) додавали хлорацетонітрил (6,63мл, 105ммоль) при кімнатній температурі. Одержаний розчин охолоджували до 0°С і поки температура підтримувалася нижче 10°С, додавали концентровану сірчану кислоту (25мл). Одержаний розчин залишали перемішуватися протягом 1 години і потім виливали на лід і підлуговували шляхом додавання твердого карбонату калію. Продукт екстрагували за допомогою етилацетату (2´500мл) і об'єднаний органічний розчин промивали водою (50мл), сушили над сульфатом натрію і концентрували у вакуумі, одержуючи вказану в заголовку сполуку у вигляді твердої речовини оранжевого кольору з кількісним виходом, 16,08г. 1 Н ЯМР (400МГц, CDCI3) d: 1,37 (6Н, с), 3,02 (2Н, с), 3,94 (2Н, с), 6,17 (1Н, шс), 7,08-7,03 (1Н, д), 7,10-7,13 (1Н, т), 7,26 (1Н, с), 7,39-7,32 (1Н, д); НРМС ESI m/z 306 [М+Н]+; Мікроаналіз: C12H15BrCINO розраховано: С 47,32; Н 4,96; N 4,60; знайдено С 47,26; Н 4,87; N 4,65. Препаративний приклад 37: 2-(3-Бромфеніл)1,1-диметилетиламін Розчин продукту препаративного прикладу 36 (32,0г, 105ммоль), тіосечовини (9,60г, 126ммоль) і оцтової кислоти (50мл) в етанолі (250мл) нагрівали із зворотним холодильником протягом ночі. Реакційну суміш охолоджували до кімнатної температури і фільтрували. Фільтрат концентрували у вакуумі, підлуговували, використовуючи розчин гідроксиду натрію (1М, 450мл) і екстрагували за допомогою дихлорметану (2´500мл). Об'єднаний органічний розчин промивали за допомогою насиченого сольового розчину (50мл), сушили над сульфатом натрію і концентрували у вакуумі, одержуючи вказану в заголовку сполуку у вигляді чорного масла з 96% виходом, 23г. 1 Н ЯМР (400мгц, CDCI3) d: 1,12 (6Н, с), 1,84 (2Н, шс), 2,62 (2Н, с), 7,16-7,08 (2Н, м), 7,36-7,32 (2Н, м); НРМС ESI m/z 228 [М+Н]+ Препаративний приклад 38: трет-бутиловий естер [2-(3-Бромфеніл)-1,1диметилетил]карбамінової кислоти Продукт, одержаний в препаративному прикладі 37 (5,0г, 22ммоль) обробляли за допомогою ди-трет-бутилдикарбонату (5,26г, 24ммоль) в дихлорметані (50мл) і перемішували протягом 20 годин. Реакційну суміш промивали водою (50мл) і об'єднаний органічний розчин сушили над сульфа 86615 54 том натрію і концентрували у вакуумі. Неочищений матеріал очищали використовуючи іонообмінну колонку (використовуючи як елюент метанол, потім 2М аміак в метанолі), з наступним очищенням за допомогою колонкової флеш-хроматографії на силікагелі, елююючи з використанням дихлорметану, одержуючи вказану в заголовку сполуку у вигляді коричневого масла з кількісним виходом, 7,23г. 1 Н ЯМР (400МГц, CDCI3) d: 1,27 (6Н, с) 1,50 (9Н, с), 2,97 (2Н, с), 4,24 (1Н, шс), 7,05 (1Н, д), 7,15-7,11(14, т), 7,30 (1Н, с), 7,35 (1Н, д); НРМС ESI m/z 350 [M+NH4]+ Препаративний приклад 39: Бензил 3-{2-[(третбутоксикарбоніл)аміно]-2-метилпропіл}бензоат Розчин продукту препаративного прикладу 38 (3,9г, 12ммоль), [1,1'-біс(дифенілфосфін)фероцен] дихлорпаладію (II) (1,00г, 1,3ммоль) і триетиламіну (3,3мл, 24ммоль) в бензиловому спирті (60мл) нагрівали до 100°С в атмосфері монооксиду вуглецю при тиску 100псі протягом 5 годин. Охолоджену реакційну суміш потім фільтрували крізь Arbocele® і фільтрат концентрували у вакуумі. Залишок розчиняли в етилацетаті і промивали, використовуючи розчин гідрокарбонату натрію (50мл) і насичений сольовий розчин (2´50мл). Органічний розчин потім сушили над сульфатом натрію і концентрували у вакуумі, одержуючи темне масло. Це масло очищали за допомогою колонкової хроматографії на силікагелі, елююючи сумішшю гексан : етилацетат, з градієнтом від 100:0 до 84:16, одержуючи вказану в заголовку сполуку у вигляді блідо-жовтого масла з 61% виходом, 2,81г. 1 Н ЯМР (400МГц, CDCI3) d: 1,25 (6Н, с), 1,45 (9Н, с), 3,05 (2Н, с), 4,22 (1Н, шс), 5,35 (2Н, с), 7,32-7,45(7Н, м), 7,86 (1Н, с), 7,93-7,97 (1Н, м) Препаративний приклад 40: гідрохлорид Бензил 3-(2-аміно-2-метилпропіл)бензоату Вказану в заголовку сполуку одержували з продукту препаративного прикладу 39, використовуючи методику подібну до описаної в препаративному прикладі 24, у вигляді твердої речовини білого кольору з 91% виходом. 1 Н ЯМР (400МГц, CD3OD) d: 1,33 (6Н, с), 2,98 (2Н, с), 5,37 (2Н, с), 7,31-7,53 (7Н, м), 7,93 (1 Н, с), 8,00-8,04 (1 Н, м); НРМС ХІАТ m/z 284 [М+Н]+ Препаративний приклад 41: Бензил 3-{2-[((2R)2-[4-(бензилокси)-3-(форміламіно)феніл]-2-{[третбутил(диметил)силіл]окси}етил)аміно]-2-метилпропіл)бензоат 55 86615 56 3,30 (2Н, м), 4,91 (1Н, т), 6,89 (1Н, д), 7,02 (1Н, м), 7,37-7,49 (2Н, м), 7,85 (1Н, шс), 7,93-7,96 (1Н, д), 8,11 (с, 1Н), 8,32 (с), 61 (с); НРМС ESI m/z 487 [M+H]Препаративний приклад 43: (4-Гідрокси-2,5диметилфеніл)ацетонітрил Суміш продукту препаративного прикладу 40 (1,81г, 6,38ммоль), препаративного прикладу 12 (2,96г, 6,38ммоль) і карбонату калію (1,76г, 12,8ммоль) в диметилсульфоксиді (10мл) нагрівали при 95°С протягом 40 годин. Охолоджену реакційну суміш потім розводили водою (250мл) і екстрагували за допомогою етилацетату (3´50мл). Об'єднаний органічний розчин промивали, використовуючи розчин гідрокарбонату натрію (50мл) і насичений сольовий розчин (2´50мл), сушили над сульфатом натрію і концентрували у вакуумі, одержуючи оранжеве масло. Це масло очищали за допомогою колонкової хроматографії на силікагелі, елююючи з використанням суміші дихлорметан : гексан, 50:50, потім суміші дихлорметан : метанол, з градієнтом від 100:0 до 98:2. Придатні фракції випаровували при пониженному тиску і залишок потім очищали за допомогою колонкової хроматографії на силікагелі, елююючи з використанням суміші дихлорметан : метанол, з градієнтом від 100:0 до 98:2, одержуючи жовту смолу. Смолу азеотропували, використовуючи діетиловий етер (´3), одержуючи вказану в заголовку сполуку у вигляді жовтої смоли з 20% виходом, 0,83г. 1 Н ЯМР (400МГц, CDCI3): d: -0,15 до -0,17 (3Н, м), -0,03 (3Н, с), 0,79-0,82 (9Н, с), 1,01 (3Н, с), 1,04 (3Н, с), 2,62-2,86 (4Н, м), 4,66-4,74 (1Н, м), 5,065,07 (2Н, м), 5,36 (2Н, с), 6,88 (1Н, д), 7,01-7,05 (1Н, м), 7,27-7,50 (12Н, м), 7,74 (1Н, м), 7,87-7,96 (2Н, м), 8,39 (с), 8,40 (с), 8,76 (с), 8,78 (с); НРМС ХІАТ m/z 667 [М+Н]Препаративний приклад 42: 3-[2-({(2R)-2{[трет-Бутил(диметил)силіл]окси}-2-[3(форміламіно)-4-гідроксифеніл]етил}аміно)-2метилпропіл]бензойної кислоти Вказану в заголовку сполуку одержували з продукту препаративного прикладу 41, використовуючи методику подібну до описаної в препаративному прикладі 26. Неочищений продукт потім азеотропували, використовуючи діетиловий етер (´3), одержуючи вказану в заголовку сполуку у вигляді твердої речовини блідо-жовтого кольору з 97% виходом. 1 Н ЯМР (400МГц, CD3OD): d:-0,12 (3Н, с), 0,05 (3Н, с), 0,81 (9Н, с),1,24 (6Н, с), 2,98 (2Н, дд), 3,26 Розчин (4-метокси-2,5диметилфеніл)ацетонітрилу (0,5г, 2,9ммоль) в дихлорметані (10мл) охолоджували до -80°С і обробляли за допомогою бортриброміду (1Mb дихлорметані, 14,3мл, 14,3ммоль). Реакційну суміш перемішували при -80°С протягом наступних 30 хвилин і потім залишали нагріватися до кімнатної температури протягом періоду більше 2 годин. Реакційну суміш гасили, використовуючи насичений розчин гідрокарбонату натрію (20мл), і органічний шар відокремлювали. Органічний розчин промивали за допомогою насиченого сольового розчину (20мл), сушили над сульфатом натрію і концентрували у вакуумі, одержуючи тверду речовину блідо-коричневого кольору. Шляхом очищення за допомогою колонкової хроматографії на силікагелі, елююючи з використанням суміші етилацетат : пентан, з градієнтом від 20:80 до 33:67, одержували вказану в заголовку сполуку у вигляді безбарвної твердої речовини в 60% дисперсії в мінеральному маслі, вихід 0,28г. 1 Н ЯМР (400МГц, CD3OD) d: 2,13 (3Н, с), 2,23 (3Н, с), 3,66 (2Н, с), 6,60 (1 Н, с), 6,98 (1Н, с); НРМС ESI m/z 160 [М-Н]Препаративний приклад 44: (4-Гідрокси-2,3диметилфеніл)ацетонітрил Вказану в заголовку сполуку одержували з (4метокси-2,3-диметилфеніл)ацетонітрилу, використовуючи методику подібну до описаної в препаративному прикладі 43, у вигляді безбарвної твердої речовини з 94% виходом. 1 Н ЯМР (400МГц, CDCI3) d: 2,20 (3Н, с), 2,24 (ЗН, с), 3,62 (2Н, с), 6,64 (1 Н, д), 7,03 (1 Н, д); НРМС ХІАТ m/z 160 [М-Н]Препаративний приклад 45: (4-Гідрокси-3метилфеніл)ацетонітрил Вказану в заголовку сполуку одержували з (4метокси-3-метилфеніл)ацетонітрилу, використовуючи методику подібну до описаної в препаративному прикладі 43, у вигляді твердої речовини блідо-жовтого кольору. 57 1 Н ЯМР (400МГц, CDCI3) d: 2,25 (3Н, с), 3,65 (2Н, с), 4,98 (1Н, шс), 6,76 (1Н, д), 7,01 (1Н, д), 7,07 (1Н, с); НРМС ESI m/z 146 [М-Н]Препаративний приклад 46: 4-(2-Аміноетил)2,5-диметилфенол Розчин продукту препаративного прикладу 43 (0,28г, 1,74ммоль) в етанолі (15мл) гідрували при 60псі в присутності нікелю Ренея® (0,1г, 50% м/м) протягом 16 годин. Реакційну суміш потім фільтрували і розчинник видаляли в вакуумі. Залишок очищали використовуючи іоннообмінну смолу, елююючи з використанням метанолу і потім 1М аміаку в метанолі, одержуючи вказану в заголовку сполуку у вигляді безбарвного масла. 1 Н ЯМР (400МГц, CD3OD) d: 2,11 (3Н, с), 2,19 (3Н, с), 2,63-2,67 (2Н, м), 2,72-2,76 (2Н, м), 6,54 (1Н, с), 6,81 (1Н, с); НРМС ESI m/z 166 [М+Н]+ Препаративний приклад 47: 4-(2-Аміноетил)2,3-диметилфенол Вказану в заголовку сполуку одержували з продукту препаративного прикладу 44, використовуючи методику подібну до описаної в препаративному прикладі 46, у вигляді безбарвної твердої речовини з 95% виходом. 1 Н ЯМР (400МГц, CDCI3) d: 6,78 (1Н, д), 6,55 (1Н, д), 2,75-2,68 (4Н, м), 2,19 (3Н, с), 2,12 (3Н, с); НРМС ХІАТ m/z 166 [М+Н]+ Препаративний приклад 48: 4-(2-Аміноетил)-2метилфенол Вказану в заголовку сполуку одержували з продукту препаративного прикладу 45, використовуючи методику подібну до описаної в препаративному прикладі 46, у вигляді безбарвного масла. 1 Н ЯМР (400МГц, CD3OD) d: 2,15 (3Н, с), 2,602,64 (2Н, м), 2,79-2,83 (2Н, м), 6,66 (д,1Н), 6,82 (1Н, д), 6,90 (1Н, с); НРМС ESI m/z 152 [М+Н]+ Препаративний приклад 49: трет-Бутил (Зйодбензил)карбамат Суспензію гідрохлориду 3-йодбензиламіну (4,95г, 18,4ммоль) в дихлорметані (100мл) обробляли за допомогою триетиламіну (3,1мл, 22ммоль) і ди-трет-бутилдикарбонату (4,40г, 20ммоль) і одержаний розчин перемішували при кімнатній тем 86615 58 пературі протягом 1,5 годин. Реакційну суміш потім промивали, використовуючи 2М хлорводневу кислоту (30мл), воду (30мл), сушили над сульфатом натрію і концентрували у вакуумі, одержуючи вказану в заголовку сполуку у вигляді безбарвної твердої речовини з кількісним виходом, 6,43г. 1 Н ЯМР (400МГц, CDCI3) d: 1,46 (9Н, с), 4,214,30 (2Н, м), 4,79-4,89 (1Н, шс), 7,06 (1Н, дд), 7,25 (1Н, д), 7,60 (1Н, д), 7,63 (1Н, с); НРМС ESI m/z 332 [М-Н]Препаративний приклад 50: трет-Бутил [(4'гідроксибіфеніл-3-іл)метил]карбамат Розчин продукту препаративного прикладу 49 (0,75г, 2,25ммоль), 4-гідроксифенілборної кислоти (0,62г, 4,50ммоль) і хлориду 1,1'біс(дифенілфосфін)фероценілпаладію (II) (0,11г, 0,14ммоль) в N,N-диметилформаміді (14мл) обробляли за допомогою 2М водного розчину карбонату натрію (4мл) і одержану суміш нагрівали при 80°С протягом 16 годин. Розчинник видаляли в вакуумі і залишок очищали за допомогою колонкової хроматографії на силікагелі, елююючи з використанням суміші етилацетат : пентан, 25:75, одержуючи вказану в заголовку сполуку у вигляді кристалічної твердої речовини блідо-рожевого кольору з кількісним виходом, 0,73г. 1 Н ЯМР (400МГц, CDCI3) d: 1,47 (9Н, с), 4,334,41 (2Н, м), 4,87-4,94 (1Н, шс), 6,89 (2Н, д), 7,21 (1Н, д), 7,37 (1Н, дд), 7,43-7,45 (4Н, м); НРМС ESI m/z 298 [М-Н]Препаративний приклад 51: гідрохлорид 3'(Амінометил)біфеніл-4-олу Продукт, одержаний в препаративному прикладі 50 (0,73г, 2,43ммоль), обробляли за допомогою 4М хлорводневої кислоти в діоксані (6,1мл, 24,3ммоль) і одержаний розчин залишали перемішуватися при кімнатній температурі протягом 3 годин. Реакційну суміш потім концентрували у вакуумі, одержуючи вказану в заголовку сполуку у вигляді безбарвної твердої речовини. 1 Н ЯМР (400МГц, CD3OD) d: 4,17 (2Н, с), 6,87 (2Н, д), 7,34 (1Н, д), 7,45-7,50 (3Н, м), 7,61 (1Н, д), 7,65 (1Н, с); НРМС ESI m/z 198 [М-Н]Препаративний приклад 52: 2-Гідрокси-1нафтамід Розчин 2-гідрокси-1-нафтойної кислоти (5,0г, 26,6ммоль), гідрохлориду 1-(3диметиламінопропіл)-3-етилкарбодііміду (5,6г, 59 29,2ммоль) і 1-гідроксибензотриазолу (3,95г, 29,2ммоль) в тетрагідрофурані (70мл) перемішували при кімнатній температурі протягом 30 хвилин перед додаванням 0,88 аміаку (6мл). Одержану суспензію перемішували при кімнатній температурі протягом 2 годин. Реакційну суміш потім фільтрували і фільтрат розводили водою (80мл) і екстрагували за допомогою етилацетату (4´80мл). Об'єднані органічні екстракти промивали водою (2´50мл) і насиченим сольовим розчином (50мл), сушили над сульфатом натрію і концентрували у вакуумі, одержуючи оранжеве масло. Шляхом очищення масла за допомогою колонкової хроматографії на силікагелі, елююючи з використанням суміші дихлорметан : метанол : 0,880 аміак, 95:5:0,5, одержували вказану в заголовку сполуку у вигляді твердої речовини рожевого кольору з 37% виходом, 1,83г. 1 Н ЯМР (400МГц, CDCI3) d: 6,11-6,35 (2Н, шс), 7,17 (1Н, д), 7,36 (1Н, дд), 7,54 (1Н, дд), 7,79 (1Н, д), 7,84 (1Н, д), 8,22 (1Н, д), 11,70-11,88 (1Н, шс); HPMC ESI m/z 186 [M-H]Препаративний приклад 53: 3,5-Дихлор-Nетил-2-гідроксибензамід Вказану в заголовку сполуку одержували з 3,5дихлор-2-гідроксибензойної кислоти та етиламіну, використовуючи методику подібну до описаної в препаративному прикладі 52, одержуючи вказану в заголовку сполуку у вигляді твердої речовини блідо-жовтого кольору. 1 Н ЯМР (400МГц, CDCI3) d: 1,28 (3Н, т), 3,473,54 (2Н, м), 6,29-6,36 (1 Н, шс), 7,27 (1 Н, д), 7,48 (1 Н, д); НРМС ESI m/z 232 [М-Н]Препаративний приклад 54: гідрохлорид 4(Амінометил)-2,6-диметилфенолу Розчин борану в тетрагідрофурані (1Mb тетрагідрофурані, 27,1мл, 27,1ммоль) додавали краплями до розчину 3,5-диметил-4гідроксибензонітрилу (1,0г, 6,79ммоль) в тетрагідрофурані (70мл) і одержаний розчин нагрівали із зворотним холодильником протягом 16 годин. Реакційну суміш охолоджували до кімнатної температури, обробляли за допомогою 6N хлорводневої кислоти (20мл) і нагрівали із зворотним холодильником протягом наступних 30 хвилин. Реакційну суміш потім охолоджували до кімнатної температури і розчинник видаляли в вакуумі. Одержаний залишок очищали використовуючи сильну катіоннообмінну смолу, елююючи з використанням метанолу, потім 2М аміаку в метанолі, одержуючи оранжеве масло. Це масло потім обробляли за 86615 60 допомогою 1М хлориду водню в метанолі (20мл) і реакційну суміш концентрували у вакуумі, одержуючи вказану в заголовку сполуку у вигляді твердої речовини блідо-жовтого кольору з кількісним виходом, 1,12г. 1 Н ЯМР (400МГц, CDCI3) d: 2,22 (6Н, с), 3,75 (2Н, с), 6,90 (2Н, с). Препаративний приклад 55: гідрохлорид 2(Амінометил)-4-хлорфенолу Вказану в заголовку сполуку одержували з 5хлор-2-гідроксибензонітрилу, використовуючи методику подібну до описаної для препаративного прикладу 54. 1 Н ЯМР (400МГц, CDCI3) d: 4,08 (2Н, с), 6,87 (1Н, д), 7,27 (1Н, д), 7,35 (1Н, с); НРМС ХІАТ m/z 156 [M-H]Препаративний приклад 56: гідрохлорид 4'(Амінометил)біфеніл-4-олу Вказану в заголовку сполуку одержували з 4'гідроксибіфеніл-4-карбонітрилу, використовуючи методику подібну до описаної в препаративному прикладі 54. 1 Н ЯМР (400МГц, CD3OD) d: 4,10 (с, 2Н), 6,83 (д, 2Н), 7,44-7,46 (м, 4Н), 7,60 (д, 2Н). Препаративний приклад 57: 1-(Амінометил)-2нафтол Розчин борану в тетрагідрофурані (19,23мл 1М розчину, 19,23ммоль) додавали краплями до розчину аміду з препаративного прикладу 52 (0,90г, 4,81ммоль) в тетрагідрофурані (10мл) і реакційну суміш потім нагрівали із зворотним холодильником протягом 2 годин. Розчин охолоджували, обробляли за допомогою 6М хлорводневої кислоти (10мл) і нагрівали із зворотним холодильником протягом наступних 2 годин. Одержану суспензію охолоджували до кімнатної температури і шляхом додавання 0,88 аміаку доводили показник рН до значення рН 9 і екстрагували за допомогою етилацетату (3´50мл). Об'єднаний органічний розчин промивали за допомогою насиченого сольового розчину (20мл), сушили над сульфатом натрію і концентрували у вакуумі. Шляхом очищення залишку за допомогою колонкової хроматографії на силікагелі, елююючи з використанням суміші дихлорметан : метанол : 0,88 аміак, з градієнтом від 95:5:0,5 до 90:10:1, одержували вказану в заголовку сполуку у вигляді твердої речовини рожевого кольору з 23% виходом, 0,19г.
ДивитисяДодаткова інформація
Назва патенту англійськоюFormamide derivatives useful as adrenoceptor
Автори англійськоюBrown Alan Daniel, Bunnage Mark Edward, Glossop Paul Alan, James Kim, Lane Charlotte Alice Louise, Lewthwaite Russell Andrew, Price David Anthony
Назва патенту російськоюПроизводные формамида, полезные как адренорецепторы
Автори російськоюБраун Алан Дениэл, Баннедж Марк Эдвард, Глоссоп Пол Алан, Джеймс Ким, Лейн Шарлотт Элис Луиз, Льютвейт Расселл Эндрю, Прайс Девид Энтони
МПК / Мітки
МПК: C07C 217/60, C07C 233/43, A61K 31/135
Мітки: адренорецептори, корисні, формаміду, похідні
Код посилання
<a href="https://ua.patents.su/56-86615-pokhidni-formamidu-korisni-yak-adrenoreceptori.html" target="_blank" rel="follow" title="База патентів України">Похідні формаміду, корисні як адренорецептори</a>
Попередній патент: Сполука, що має активність інгібітора кіназ, фармацевтична композиція, що включає вказану сполуку, та їх застосування для приготування лікарського препарату
Наступний патент: Аміди карбонових кислот як інгібітори фактора xа
Випадковий патент: Котел благути












